Автор: Москвин А.В.
Теги: общая и неорганическая химия химия химическая промышленность справочник общая химия химические технологии химические реакции справочник химика технолога издательство профессионал
ISBN: 978-5-91259-013-9
Год: 2006
ЯОЪЬГЯ
СПРАВОЧНИК ХИМИКА и ТЕХНОЛОГА
— - Общие сведения _— Строение вещества
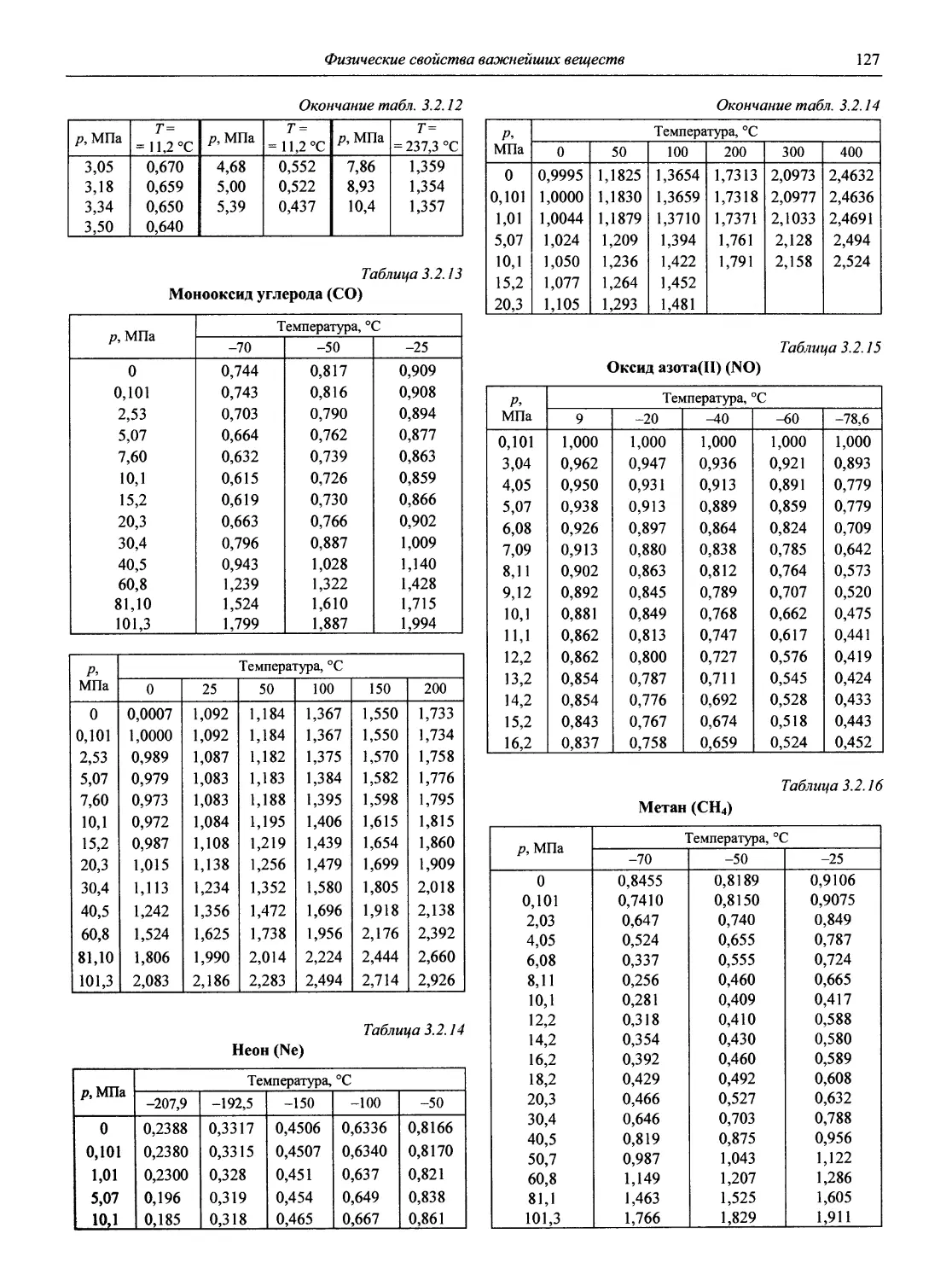
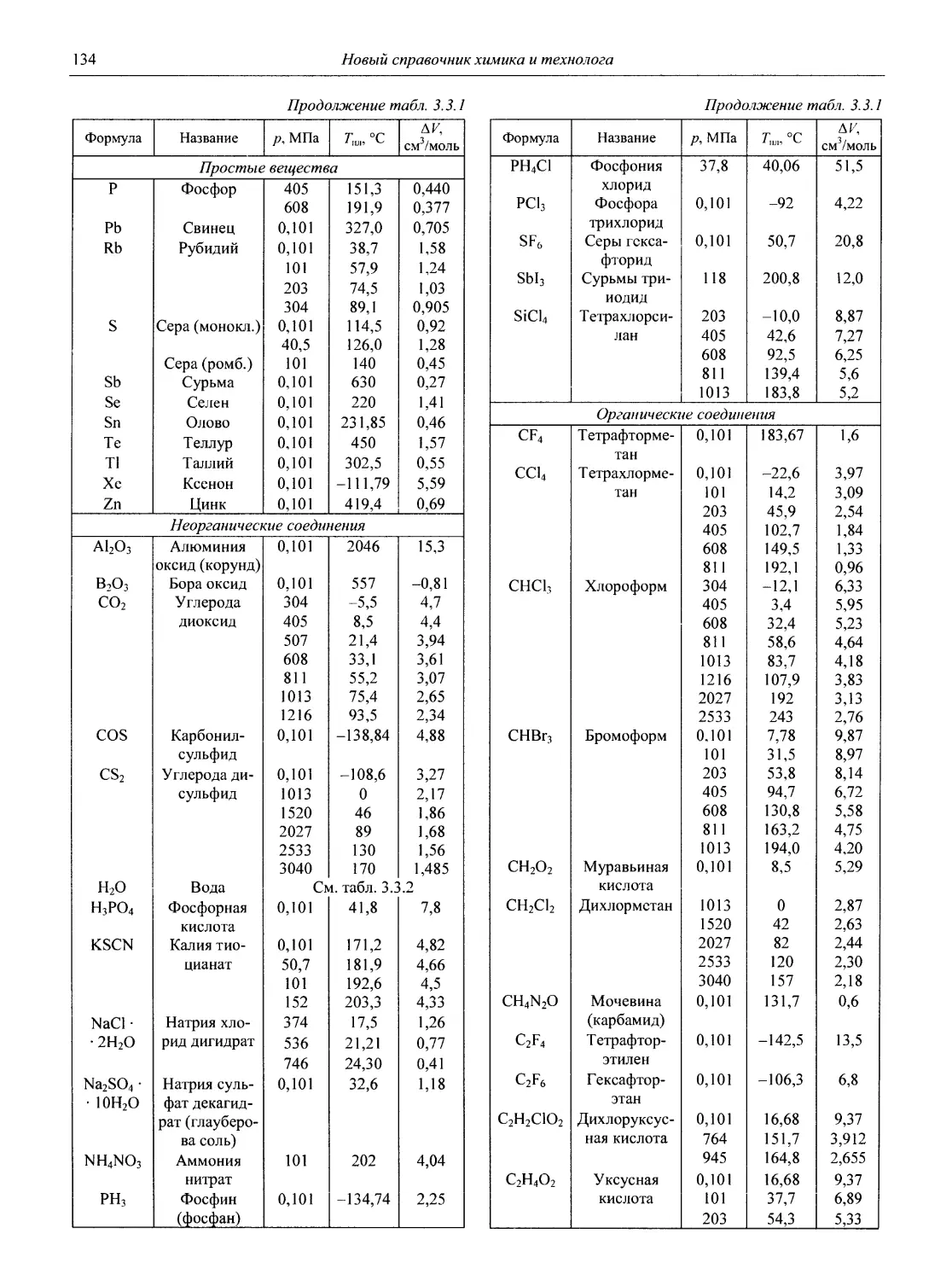
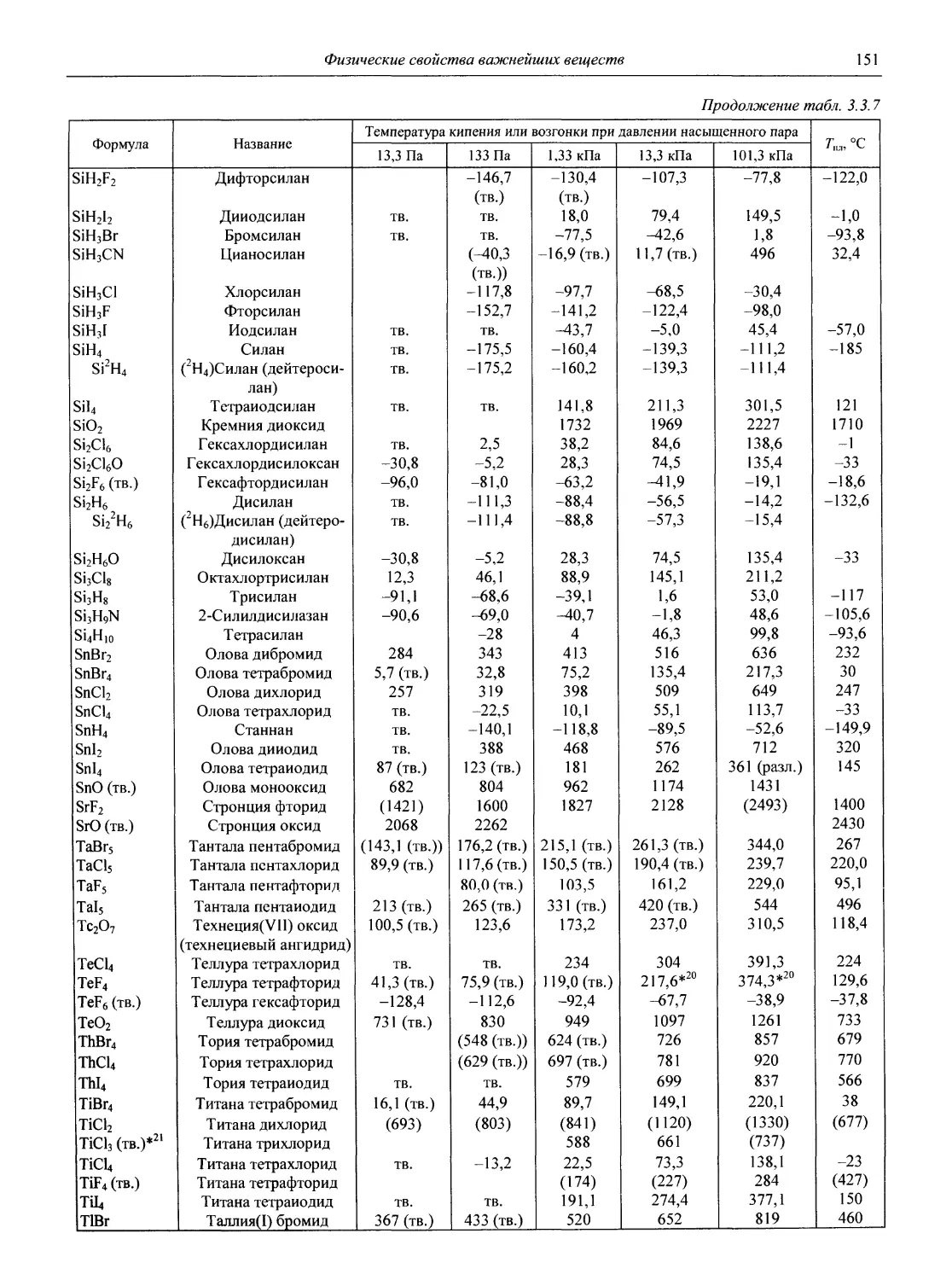
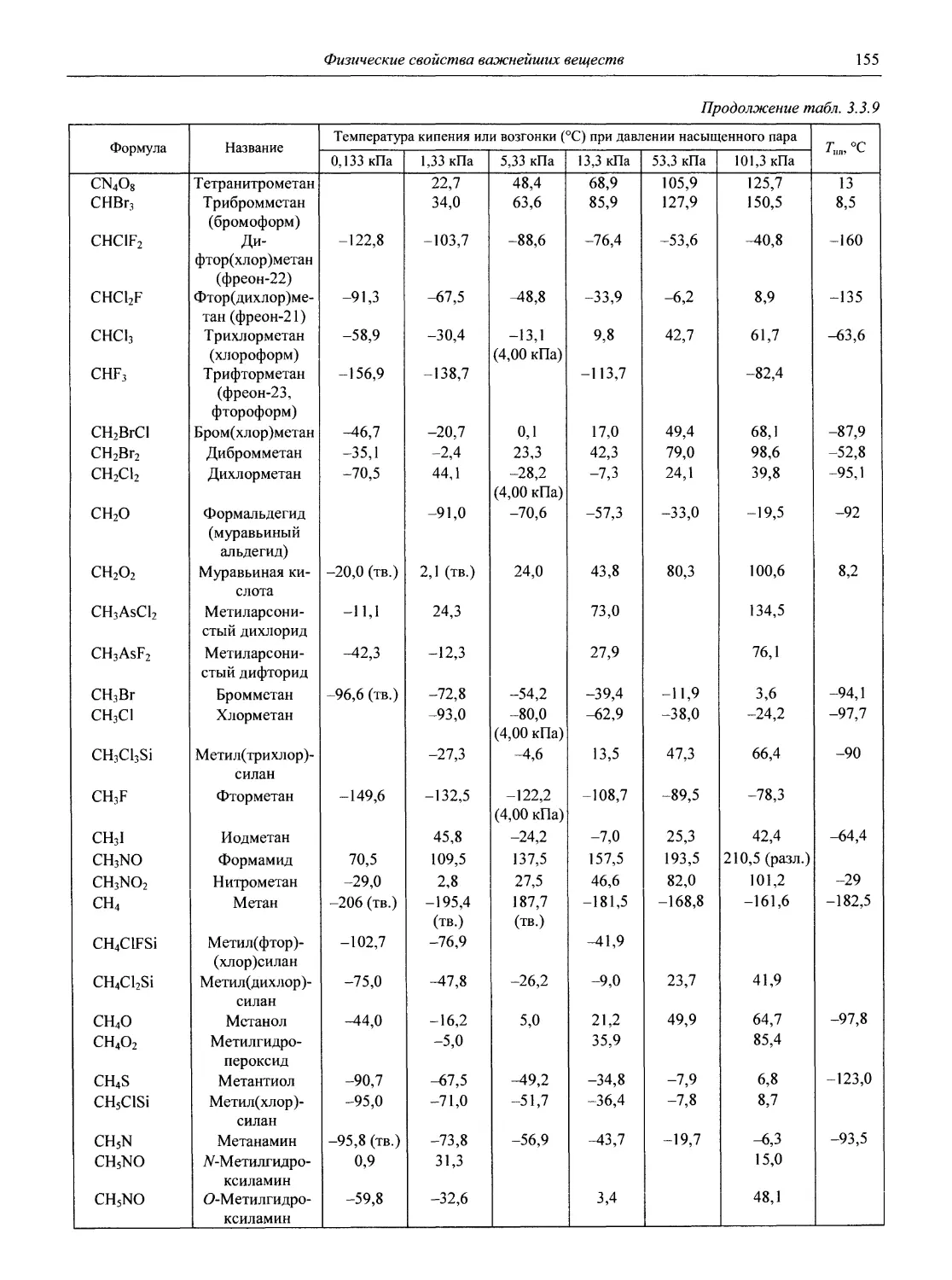
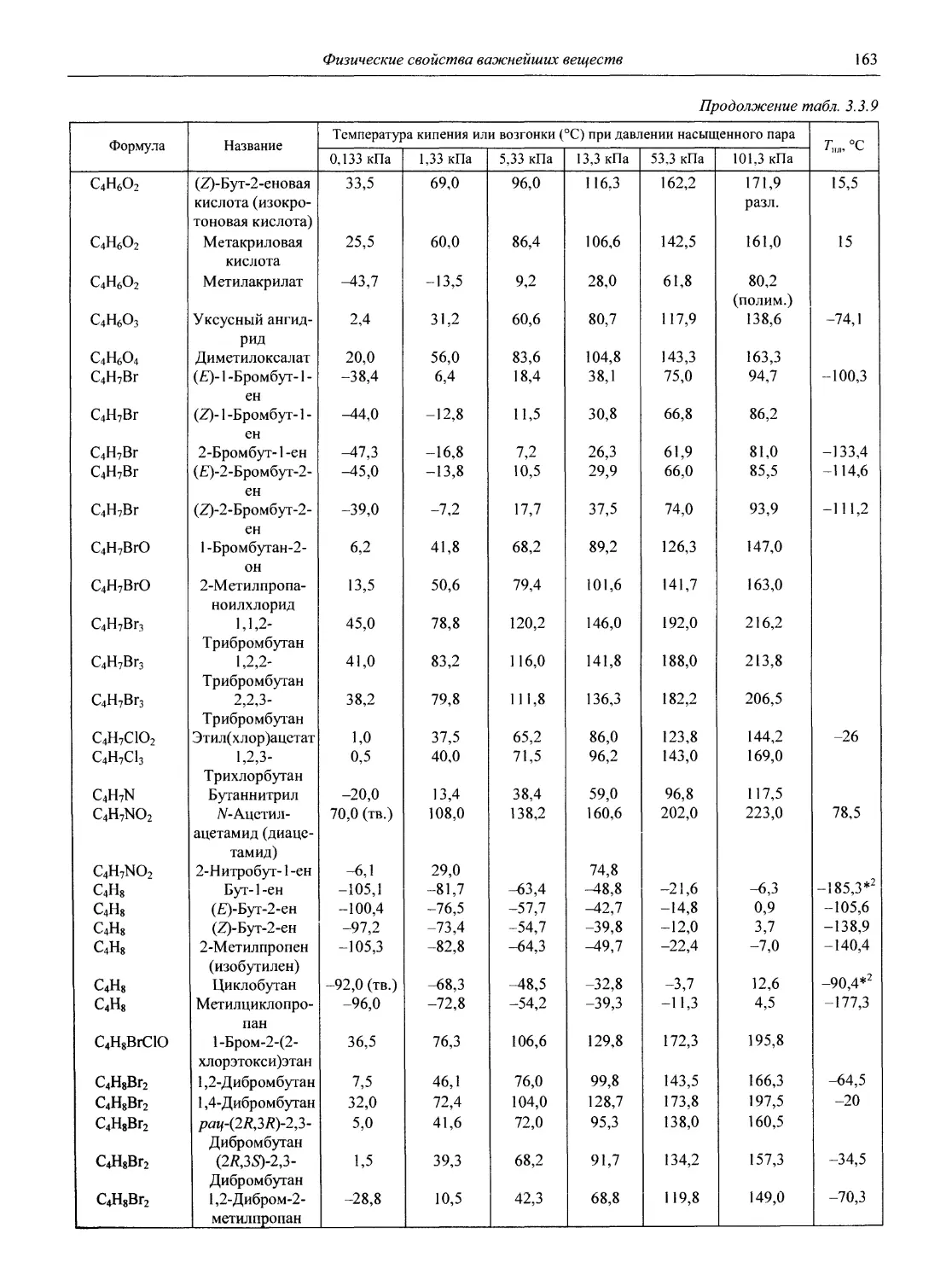
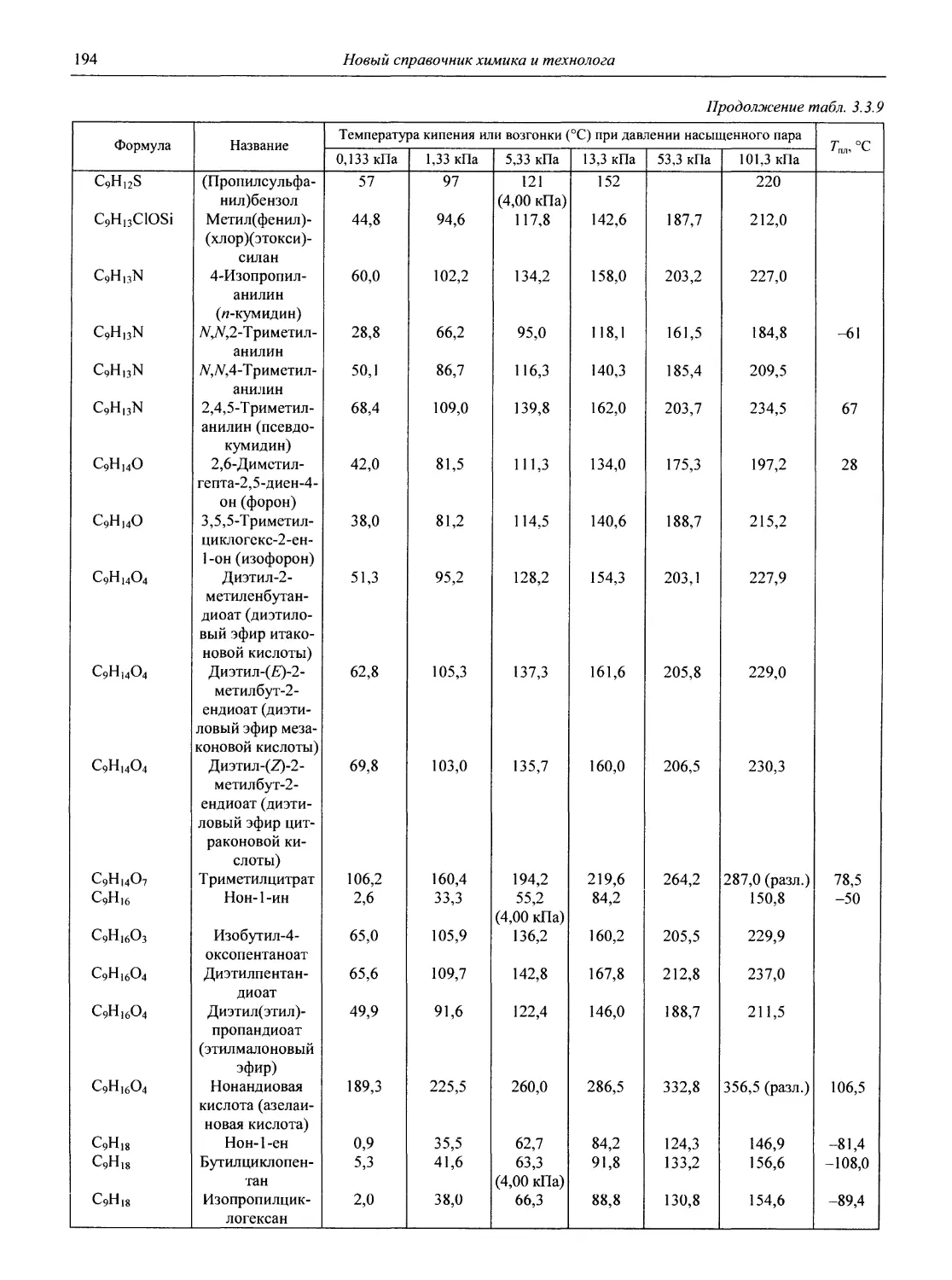
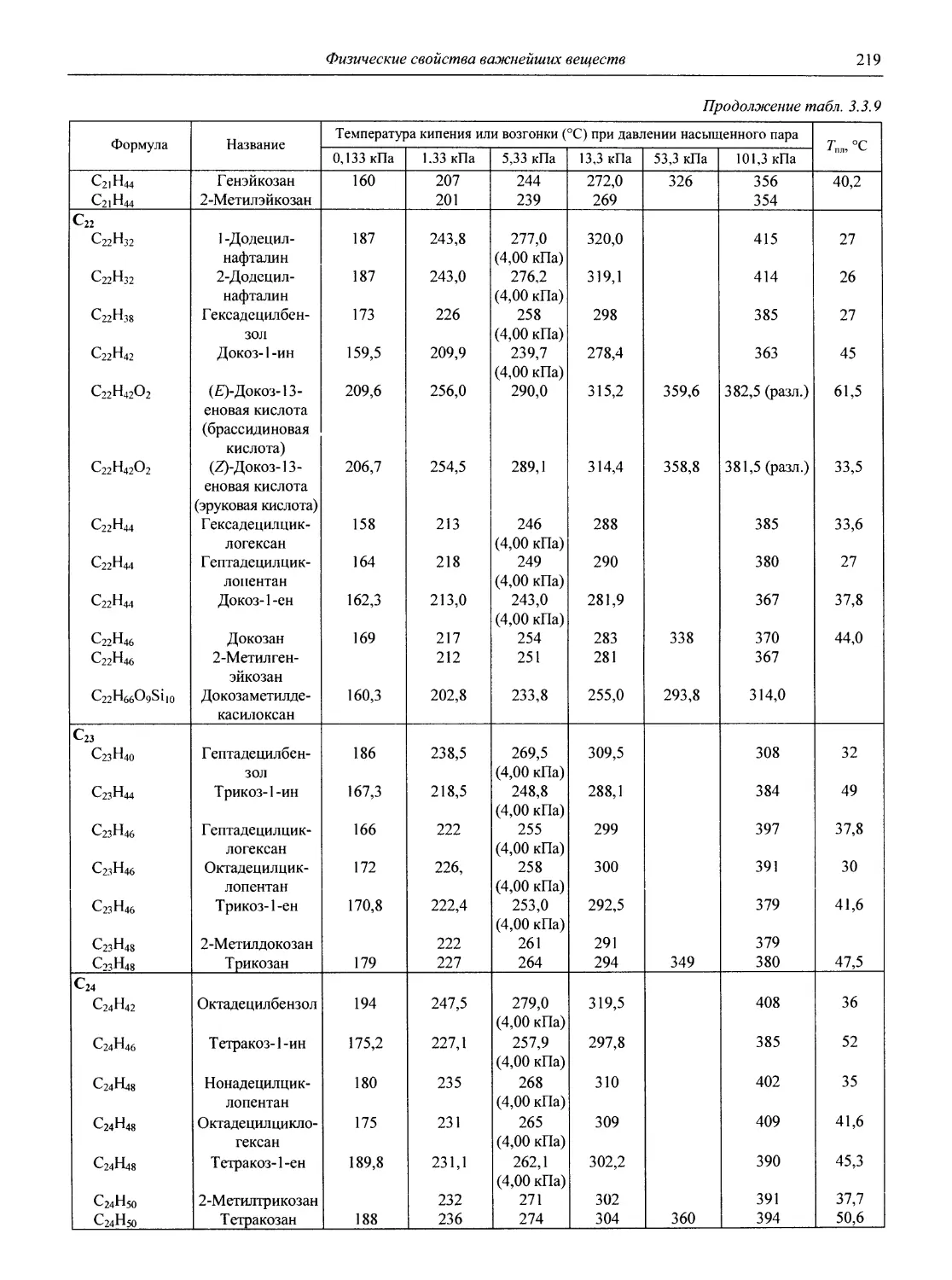
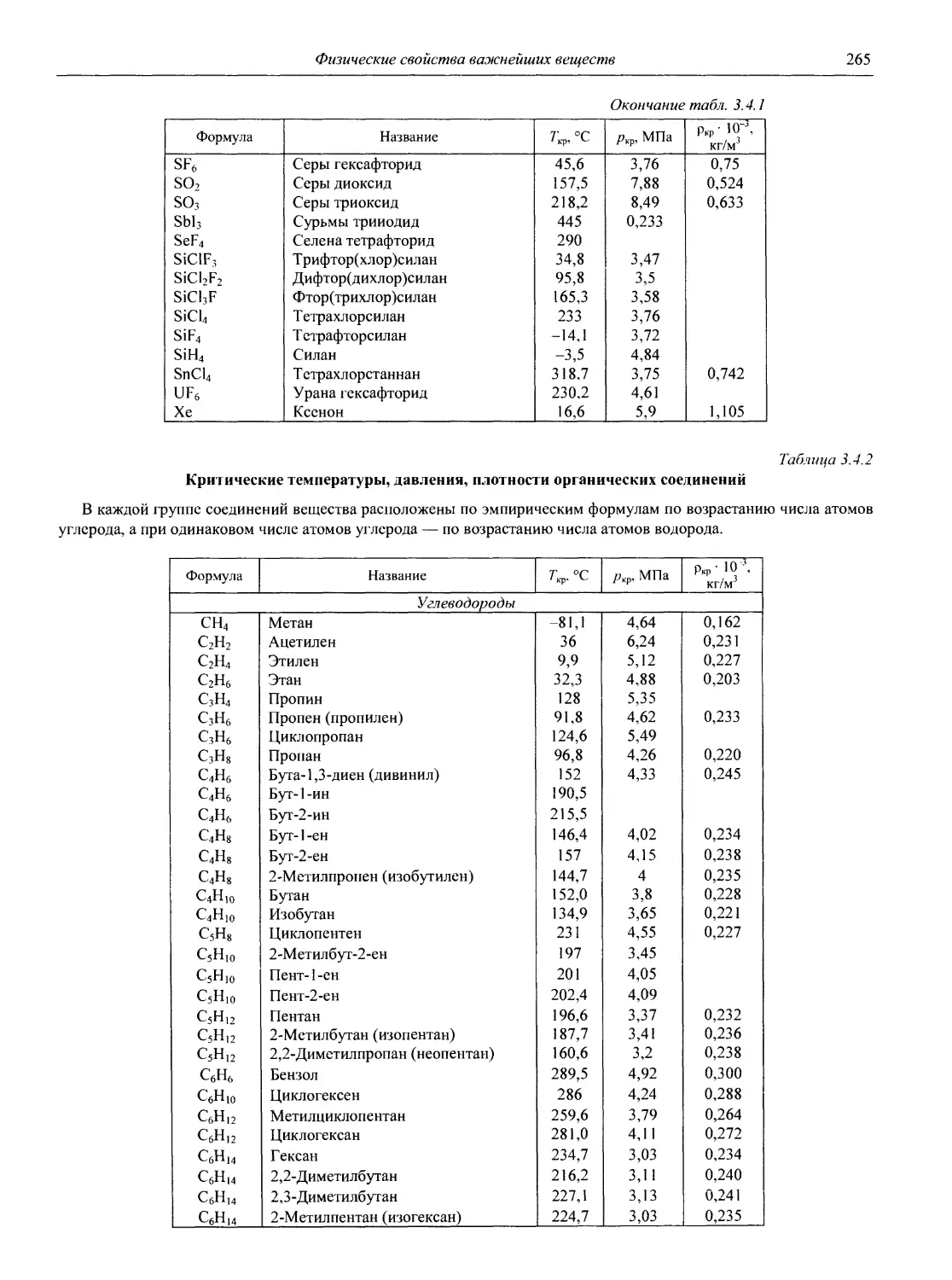
Физические свойства важнейших веществ
Ароматические соединения Химия фотографических процессов Номенклатура органических соединений Техника лабораторных работ Основы технологии
Интеллектуальная собственность
MMVI Санкт-Петербург 2006
ББК 24.1
24.2
30.6
35.62
67.404.3
Н72
Авторы:
д.х.н., проф. Ефим Ефимович Бибик к.х.н., доц. Лидия Михайловна Быкова к.т.н. Владимир Георгиевич Вавилов к.х.н. Светлана Георгиевна Изотова к.т.н. Алексей Михайлович Марков д.х.н., проф. Андрей Вадимович Москвин
Ольга Афанасьевна Пинчук
д.т.н., проф. Анатолий Владимирович Редько
д.т.н., проф. Борис Петрович Саушкин к.х.н., доц. Михаил Юрьевич Скрипкин Андрей Анатольевич Четвериков
Редактор: д.х.н., проф. Андрей Вадимович Москвин
Wil Новый справочник химика и технолога. Общие сведения. Строение вещества. Физические свойства важнейших веществ. Ароматические соединения. Химия фотографических процессов. Номенклатура органических соединений. Техника лабораторных работ. Основы технологии. Интеллектуальная собственность. — СПб.: НПО «Профессионал», 2006. — 1464 с., ил.
ISBN 978-5-91259-013-9
Справочник является последним томом многотомного издания «Новый справочник химика и технолога». В нем представлены общие сведения о строении вещества, физико-химических свойствах простых веществ и важнейших неорганических и органических соединений, а также единицы измерений, важнейшие физические константы. Большой раздел в справочнике посвящен ароматическим соединениям (бензолу, анилину и органическим красителям). Рассматриваются вопросы, связанные с галогенсеребряной и цветной фотографиями и, как следствие, фотолитографией. Впервые в справочной литературе представлен раздел «Номенклатура органических соединений». Приводится информация по технике лабораторных работ, основам технологии. Для разработчиков, исследователей и научных работников важен раздел посвященный вопросам интеллектуальной собственности.
Справочник предназначен для научного и инженерно-технического персонала отраслевых лабораторий, инженеров-химиков-технологов, исследователей, преподавателей и студентов университетов, химико-технологических, химико-фармацевтических вузов, а также для специалистов смежных профессий.
ББК 24.1
24.2
30.6
35.62
67.404.3
Все права защищены и принадлежат издателю.
ISBN 978-5-91259-013-9
© НПО «Профессионал», 2006
ОТ ИЗДАТЕЛЬСТВА
Петербургское издательство «Профессионал» предлагает специалистам-химикам и всем заинтересованным читателям 7-томный «Новый справочник химика и технолога» (Справочник). («Справочник химика» в 7 томах, под общей редакцией чл.-корр. АН СССР Б.П. Никольского, последний раз был переиздан в 1962-1966 гг.)
Название Справочника отражает основную задачу издателей и авторов: помимо базовых, «академических», публиковавшихся в научной и справочной литературе (например, в «Справочнике химика») сведений представить в максимально возможном объеме новую информацию, данные, полученные за последние 40 лет в области не только химической науки, но и химических технологий, — и таким образом сделать Справочник интересным, необходимым широкой «химической» аудитории — как ученым и студентам, так и производственникам-практикам.
В создании Справочника приняли участие крупные ученые и ведущие специалисты-химики из Москвы, Санкт-Петербурга, других городов страны (всего около 150 авторов); материалы являются оригинальными авторскими разработками либо подготовлены на основе современной литературы. Справочник обобщает опыт работы российских и зарубежных ученых и технологов второй половины XX в. и показывает перспективу развития химической и смежных областей науки и производства.
В процессе работы неоднократно возникала необходимость привлечения дополнительных материалов, разработки новых тем, более расширенного и углубленного изложения уже включенных в Справочник разделов. В связи с этим значительно увеличился, по сравнению с первоначально запланированным, объем издания (некоторые тома вышли в двух книгах).
Завершает издание том «Общие сведения. Строение вещества. Физические свойства важнейших веществ. Ароматические соединения. Химия фотографических процессов. Номенклатура органических соединений. Техника лабораторных работ. Основы технологии. Интеллектуальная собственность».
Основные темы изданных томов:
♦ основные свойства неорганических, органических и элементоорганических веществ;
♦ электродные процессы, химическая кинетика и диффузия, коллоидная химия;
♦ сырье и продукты промышленности;
♦ радиоактивные вещества, вредные вещества, гигиенические нормативы;
♦ аналитическая химия;
♦ химическое равновесие, свойства растворов;
♦ процессы и аппараты химических технологий.
Дирекция издательства выражает благодарность за самоотверженную работу всем принявшим участие в создании данного тома.
ПРЕДИСЛОВИЕ
Предлагаемый вниманию читателей заключительный (12-й) том Справочника по своему значению и важности занимает особое положение среди уже изданных томов.
Основу настоящего тома составляют фундаментальные, необходимые каждому специалисту-химику (технологу, инженеру, конструктору, решающему прикладные задачи) обширные справочные материалы по единицам физических величин, строению и свойствам веществ. Эти «ключевые» сведения, собранные в одном томе и представленные в удобном для использования виде (в виде таблиц), значительно упростят работу любого специалиста по быстрому и эффективному поиску нужных данных, послужат надежной базой инженерных и иных расчетов.
Настоящий том содержит также новую, представленную на современном уровне информацию по номенклатуре органических соединений, основам технологии и интеллектуальной собственности. В этих материалах могут быть заинтересованы как творческие коллективы, так и отдельные специалисты, принимающие участие в разработке новых материалов и технологий.
За многолетний период работы над предыдущими томами Справочника в них по разным причинам нс вошли очень важные материалы по ароматическим соединениям и химии фотографических процессов. В настоящем томе эти темы отражены по возможности наиболее полно и подробно.
Настоящий том имеет 9 разделов.
Раздел 1 содержит фундаментальные физические постоянные, системы единиц измерения и соотношения между ними.
В разделе 2 приводятся данные о строении вещества: свойствах и энергетических характеристиках элементарных частиц, изотопов и естественных радиоактивных семействах.
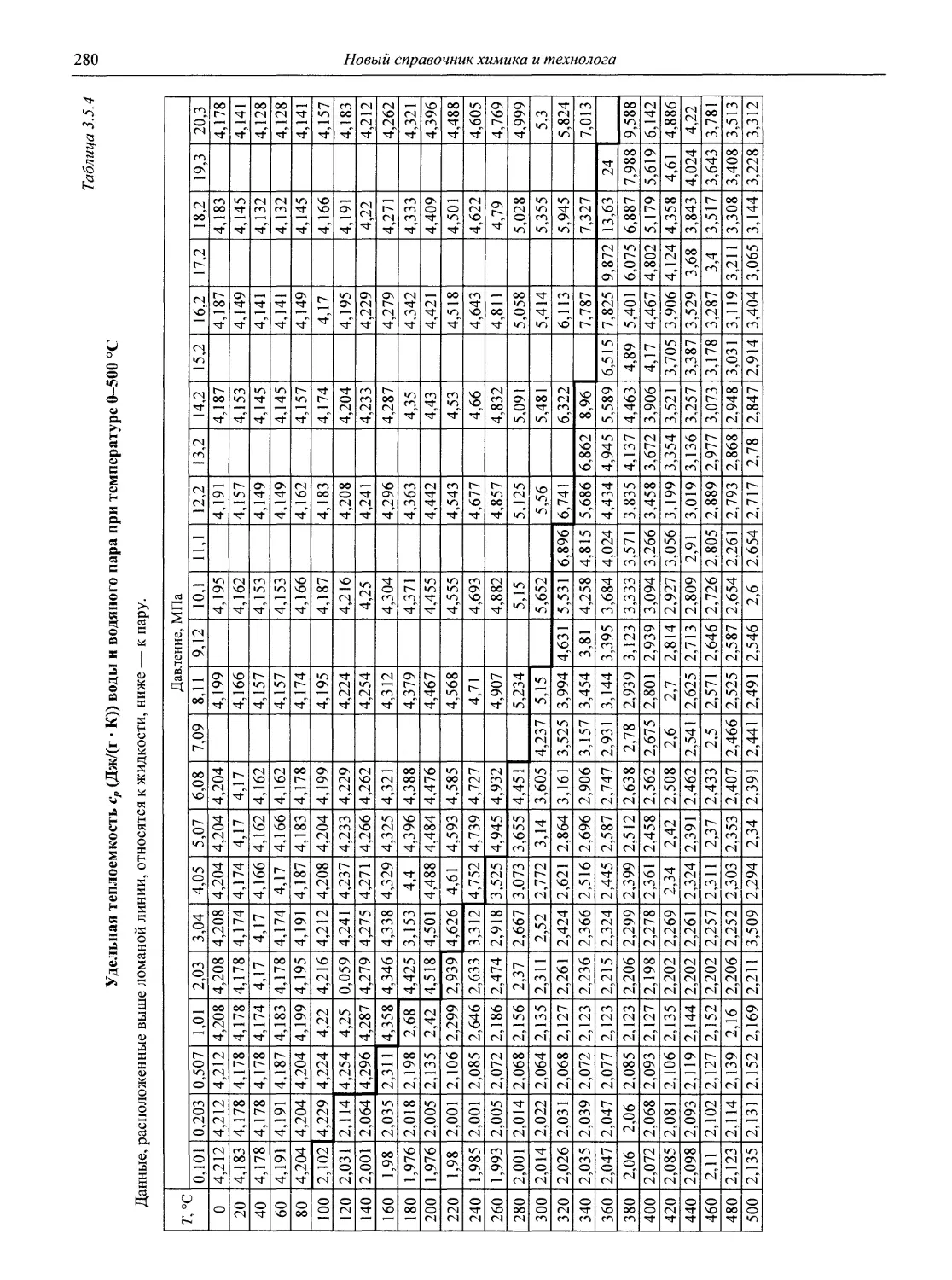
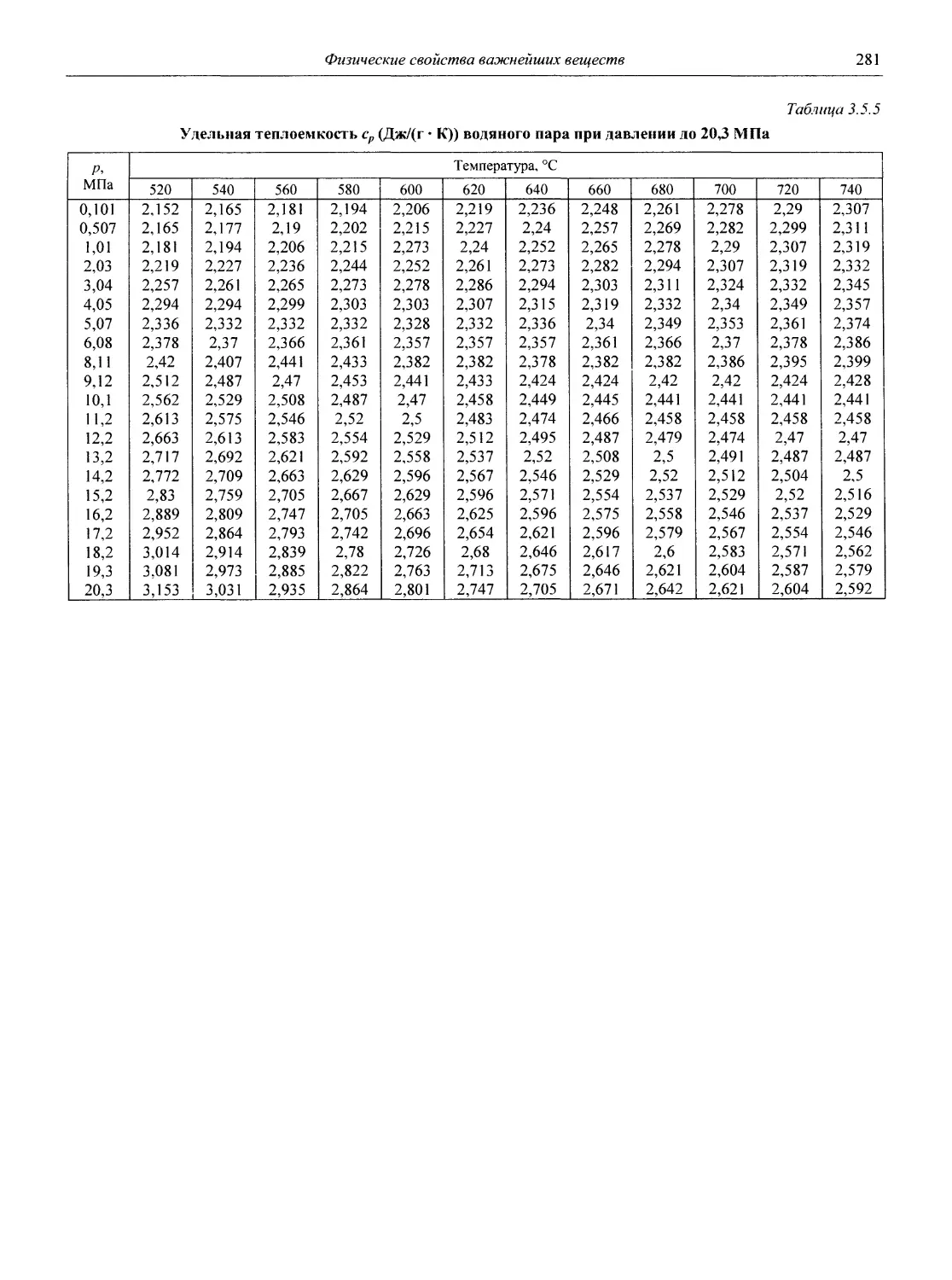
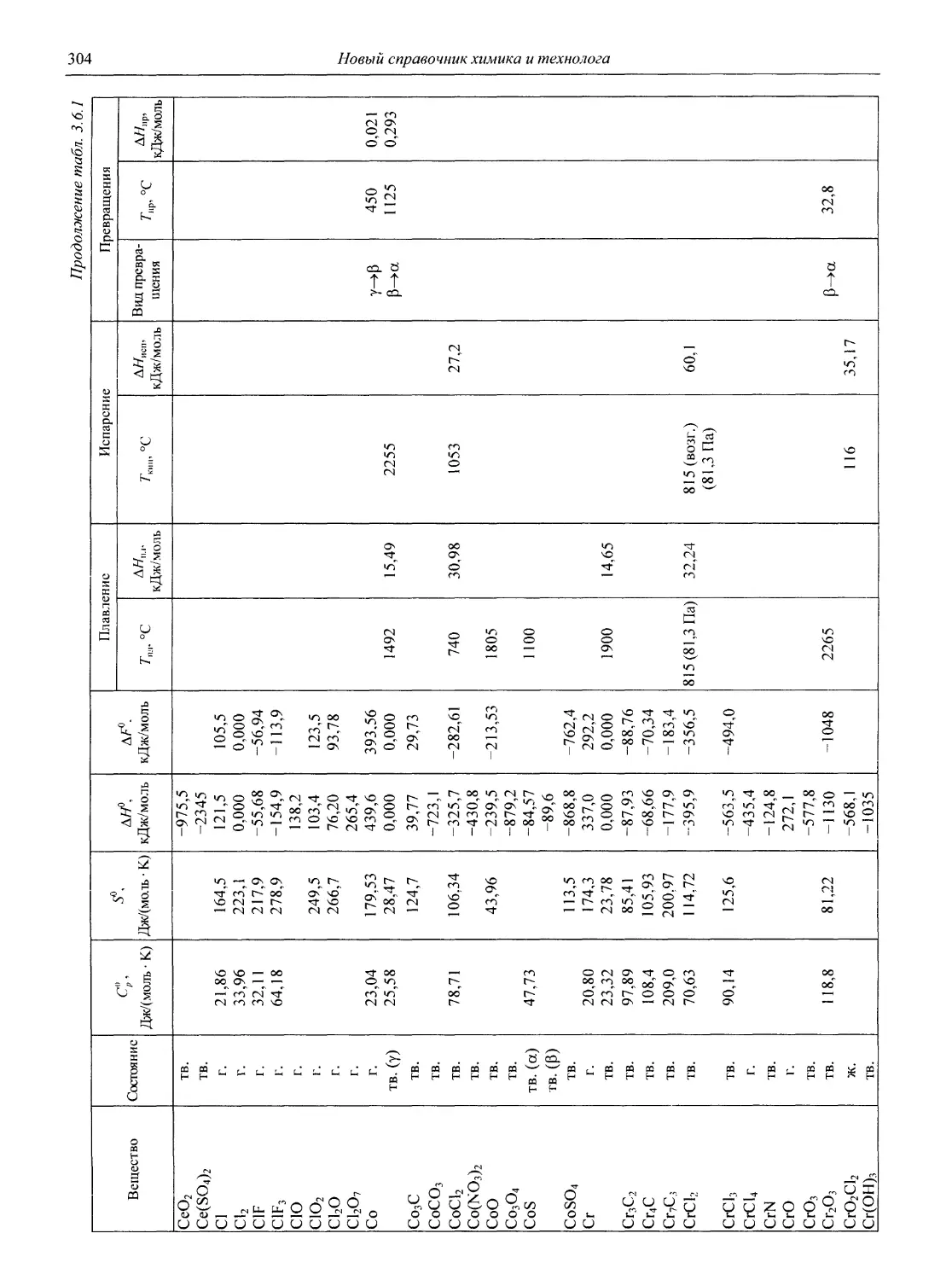
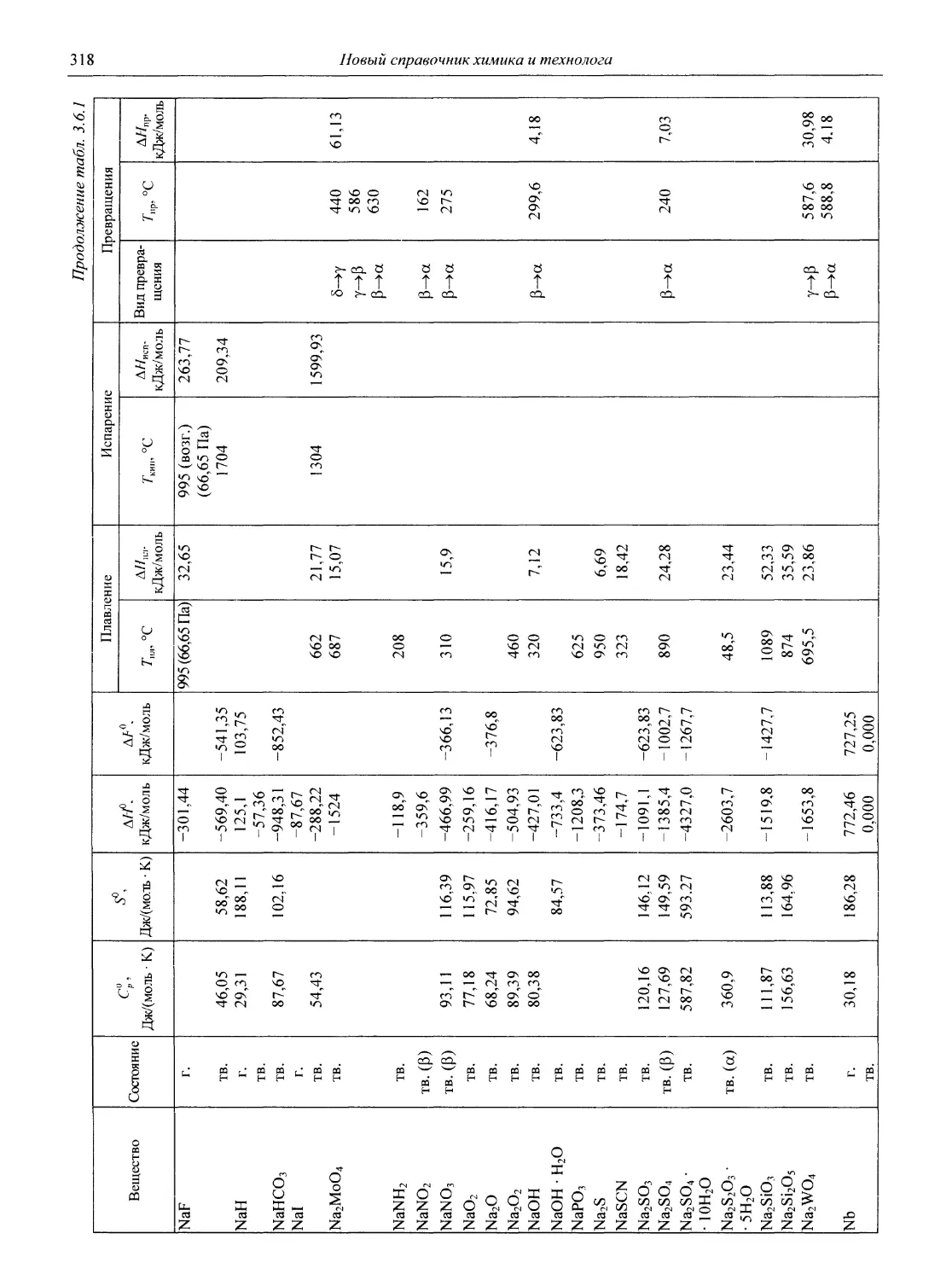
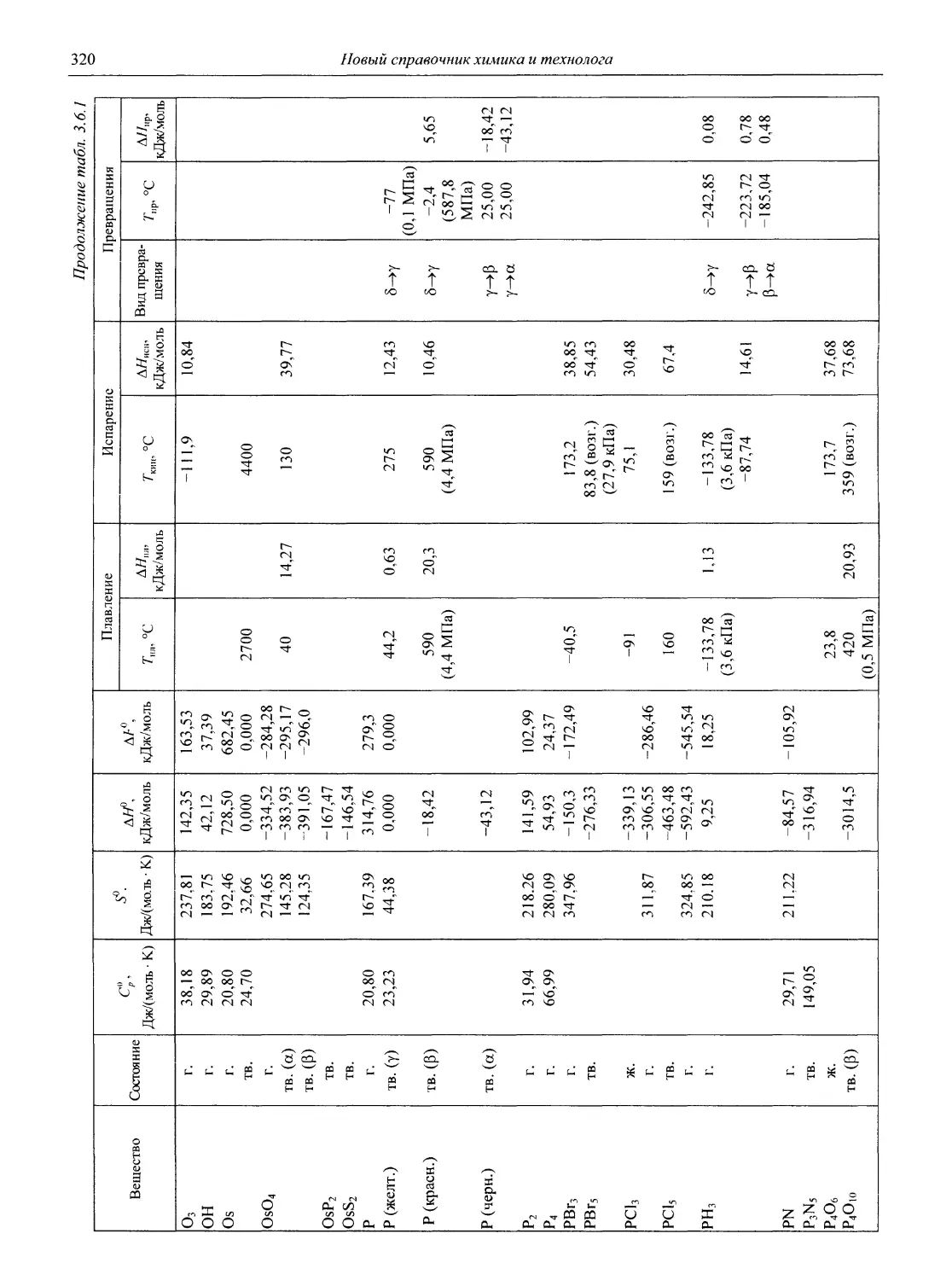
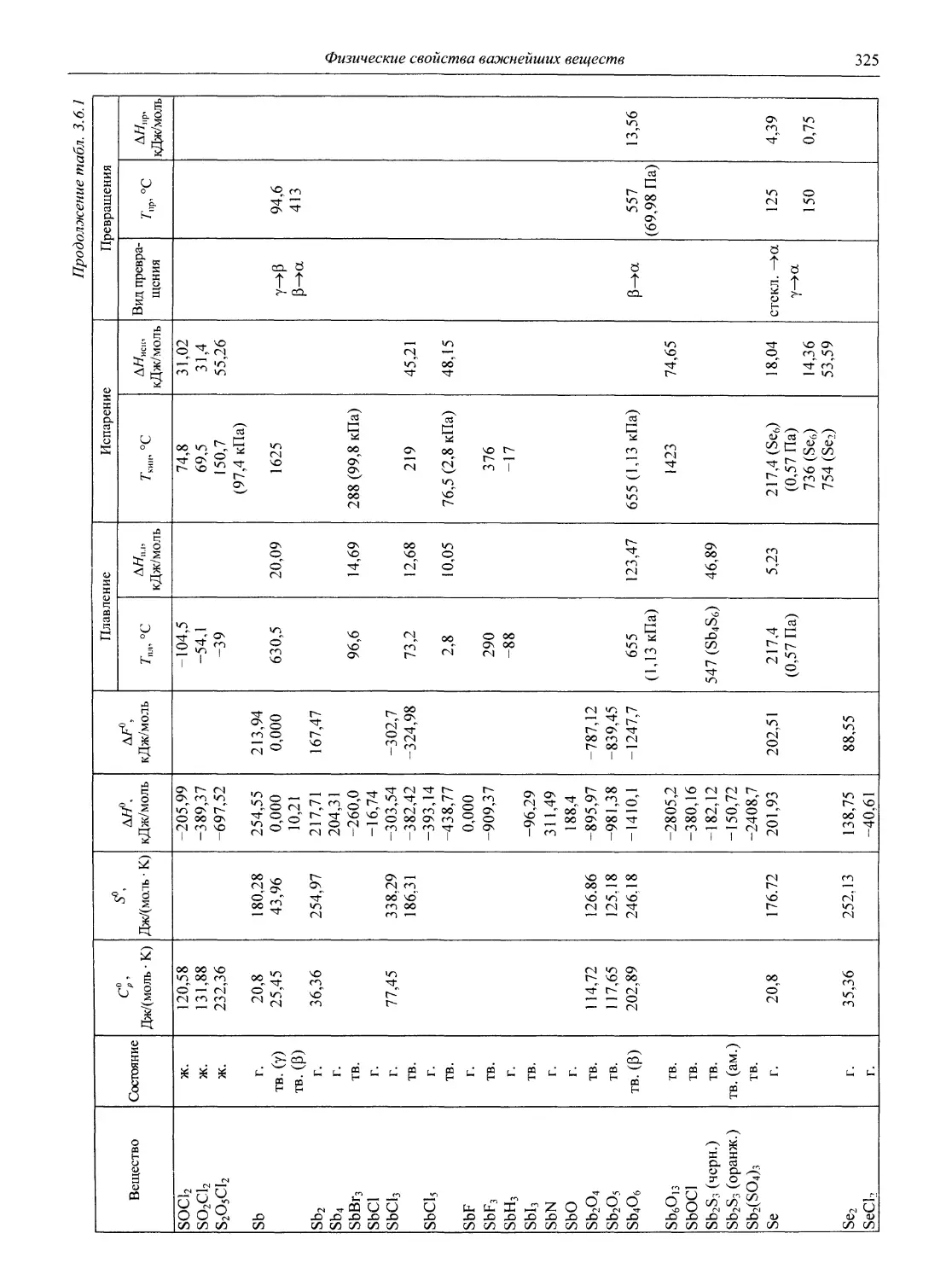
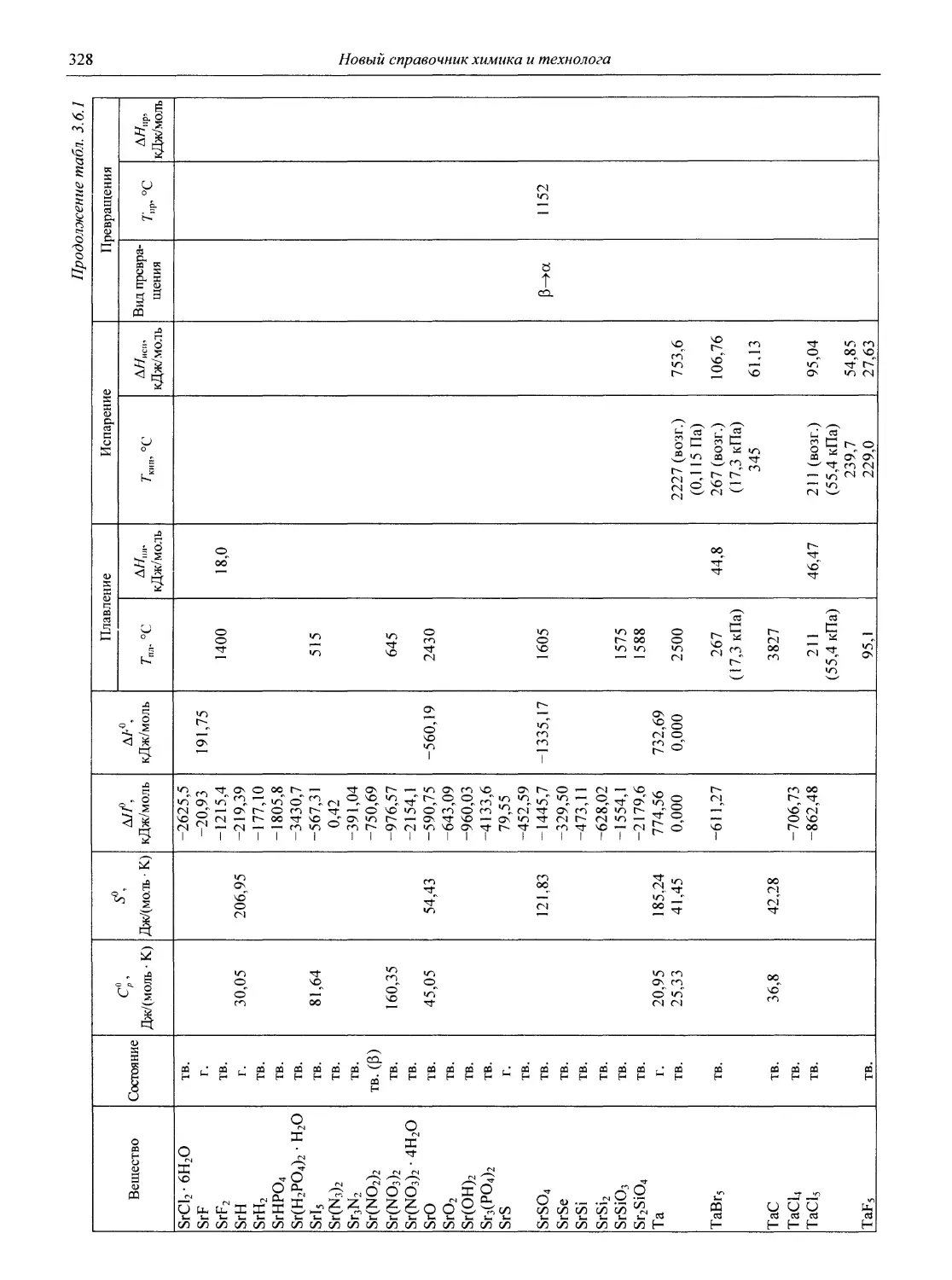
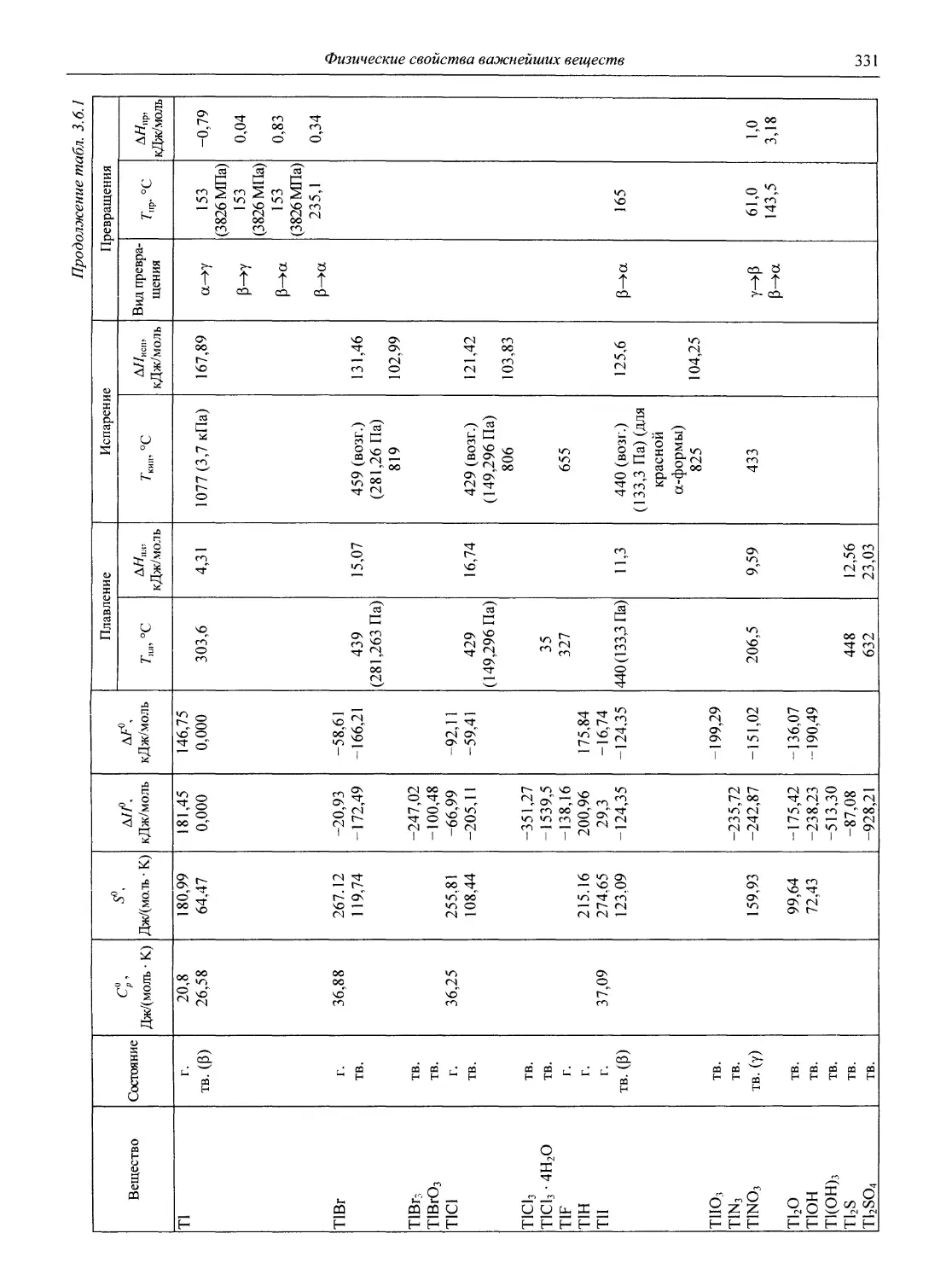
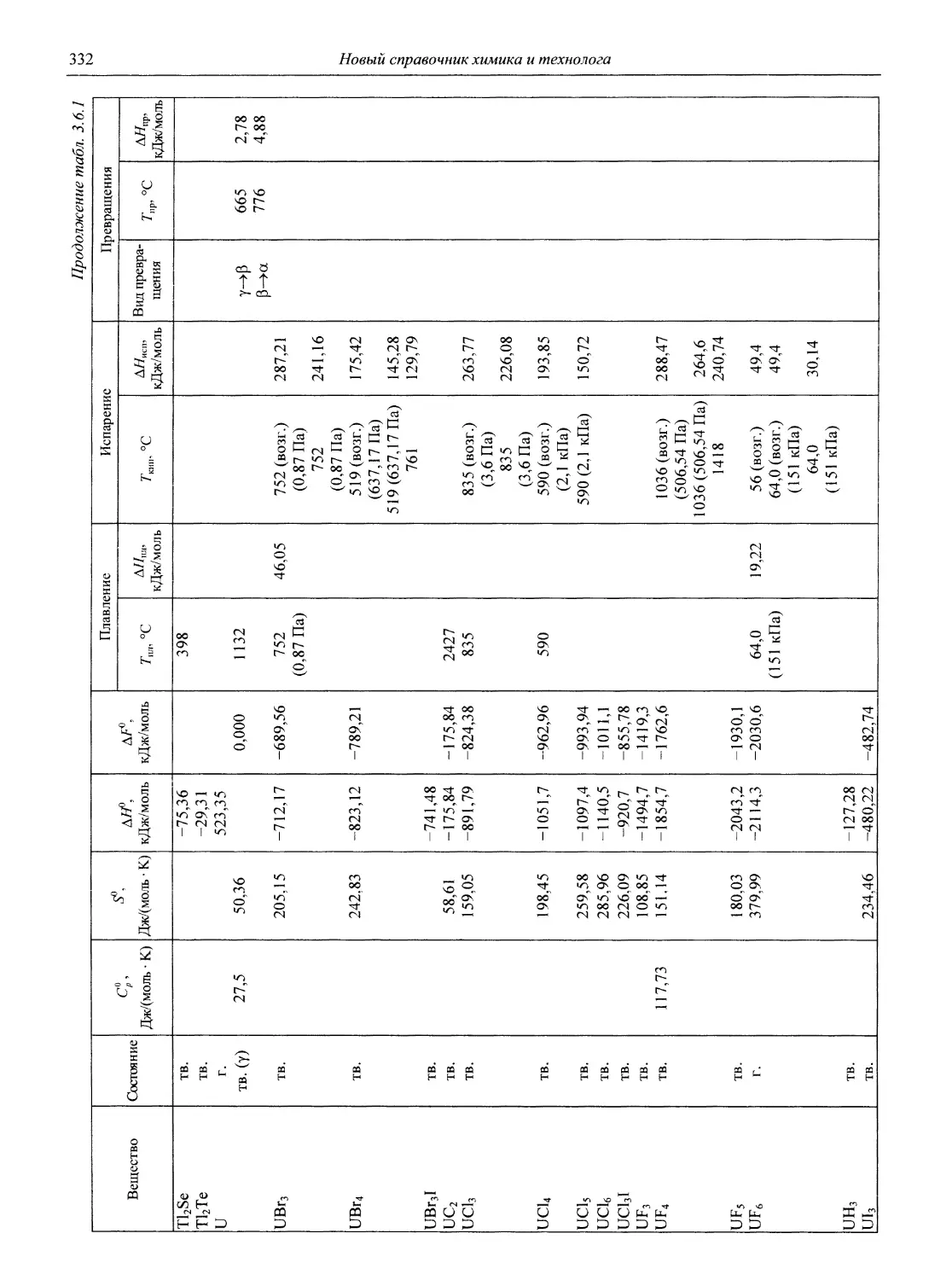
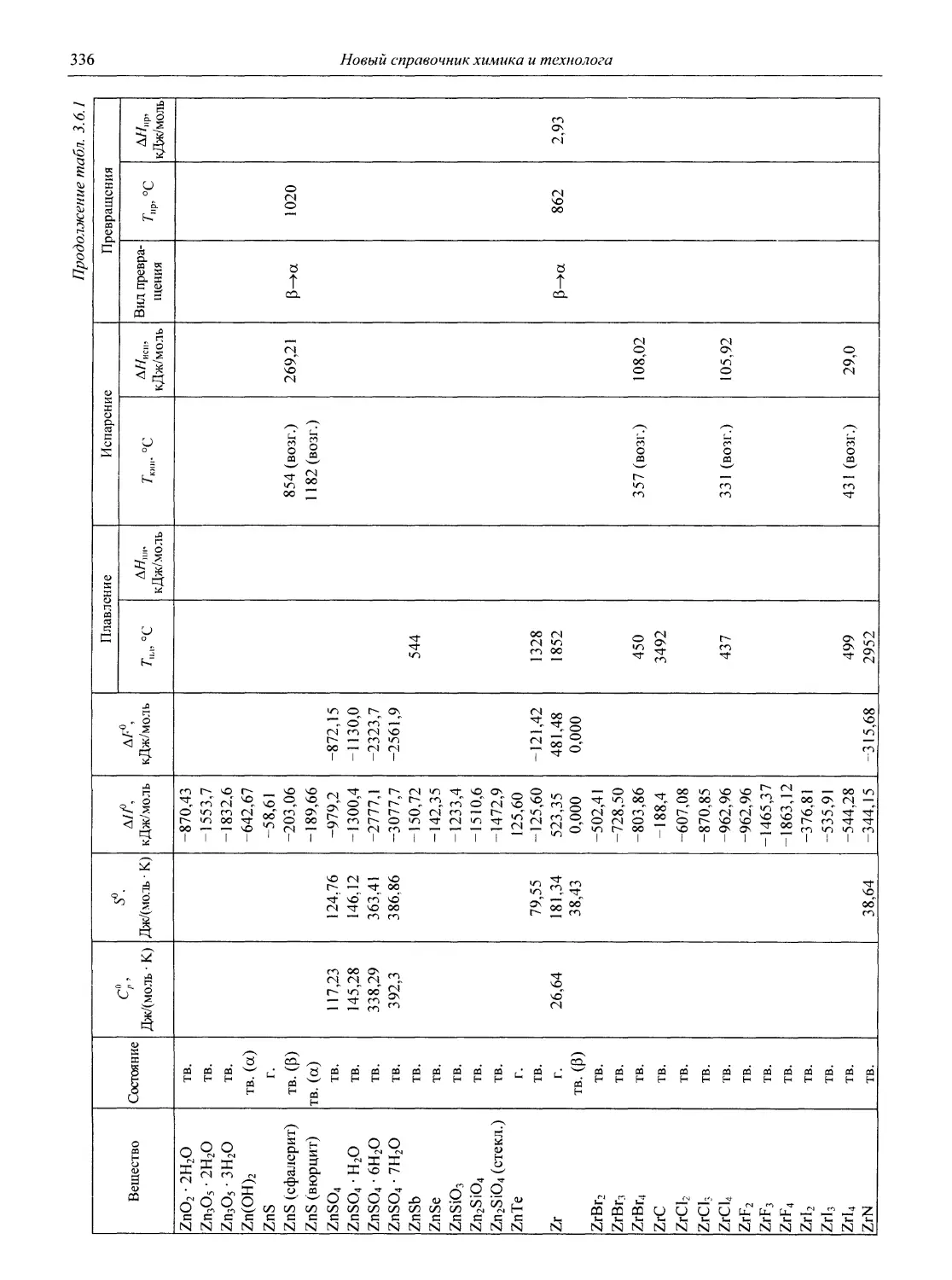
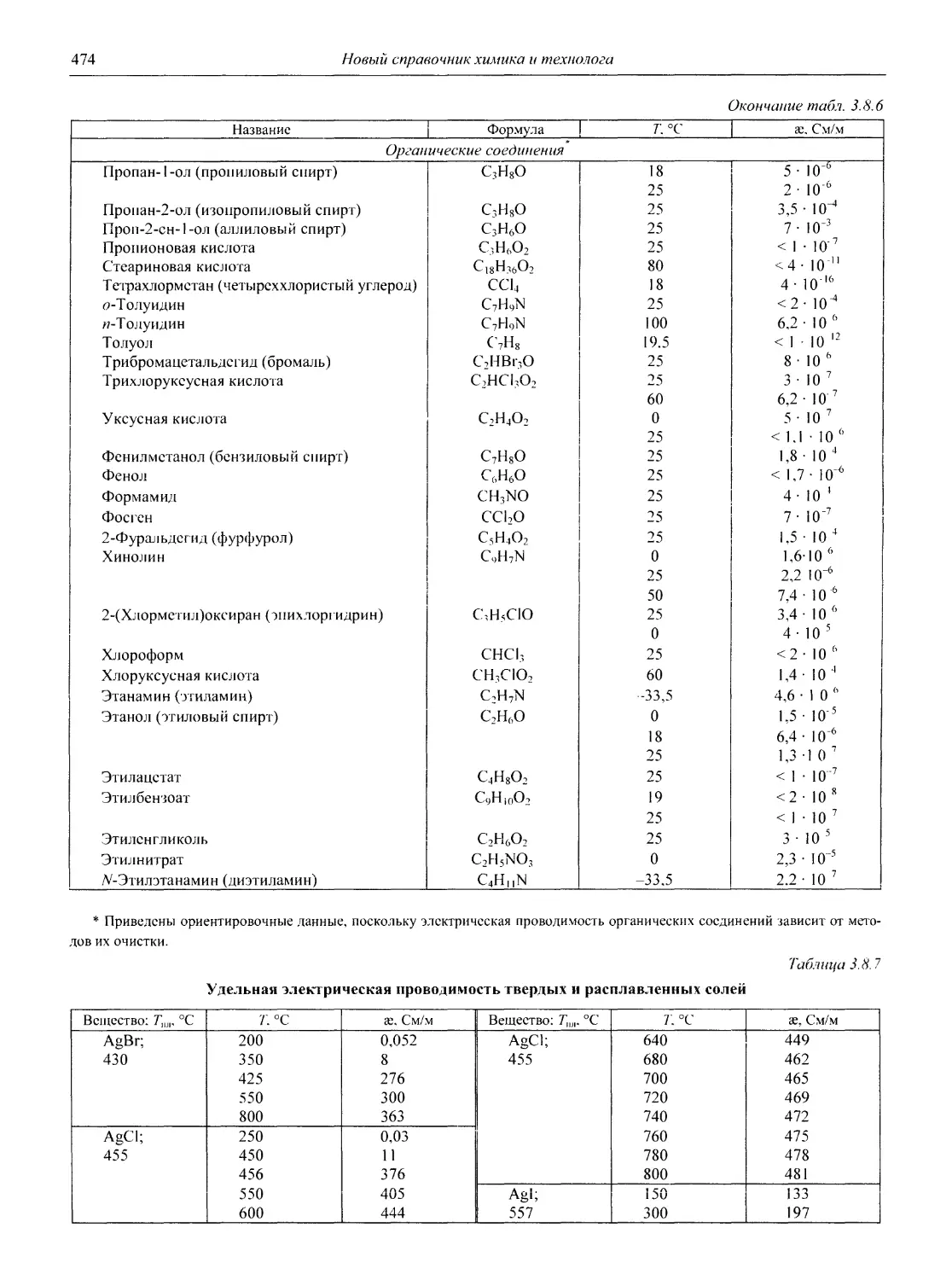
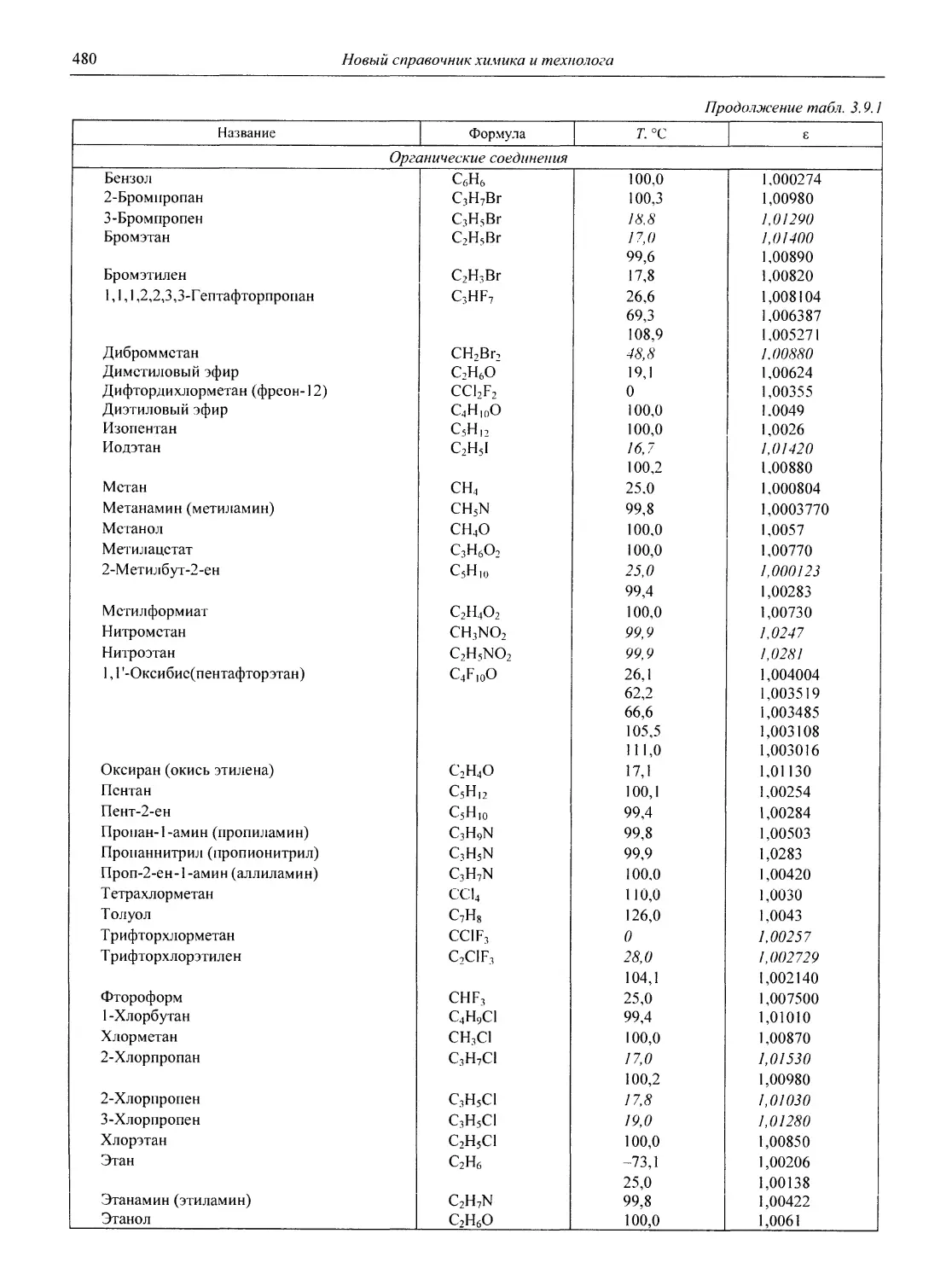
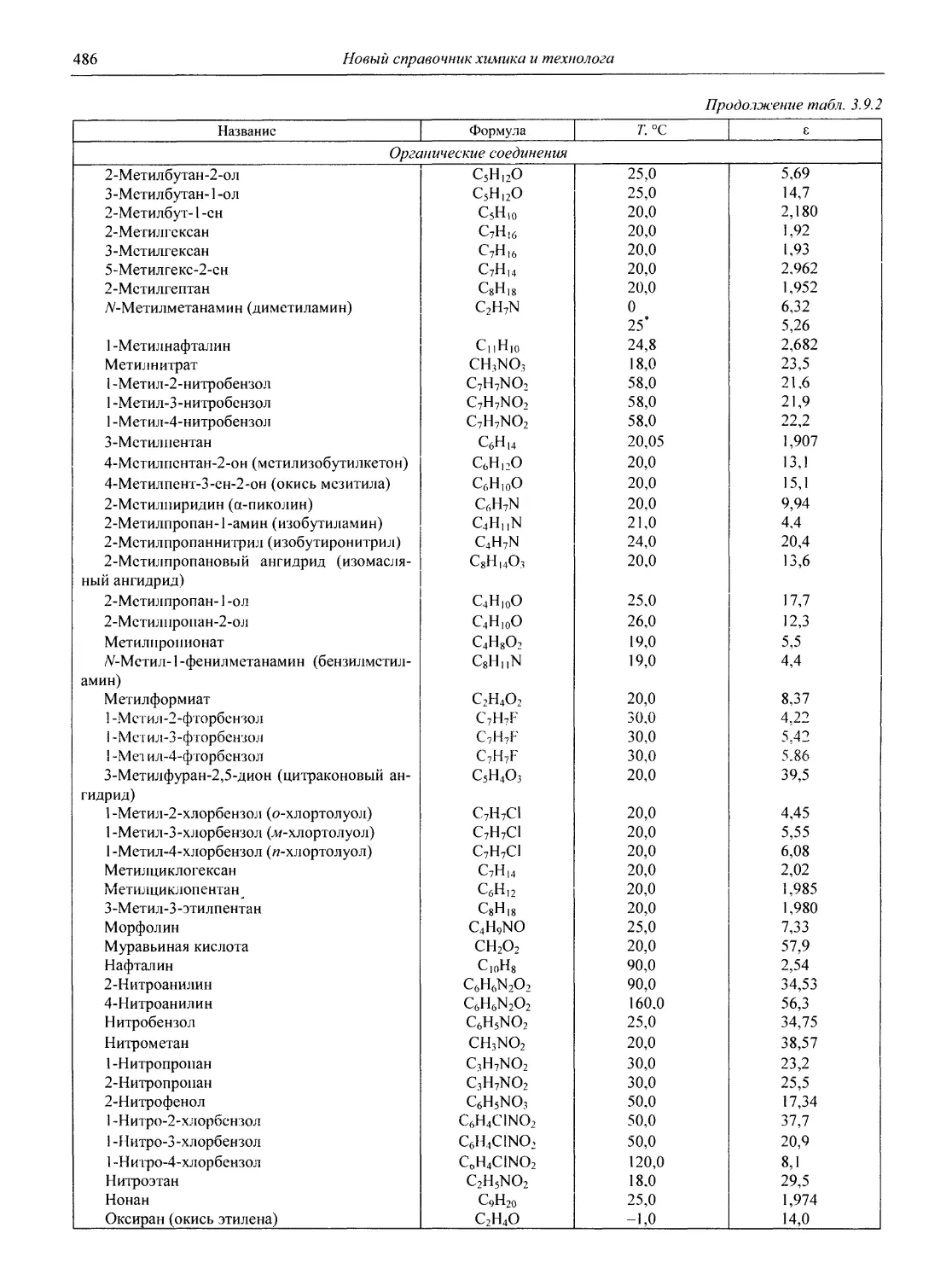
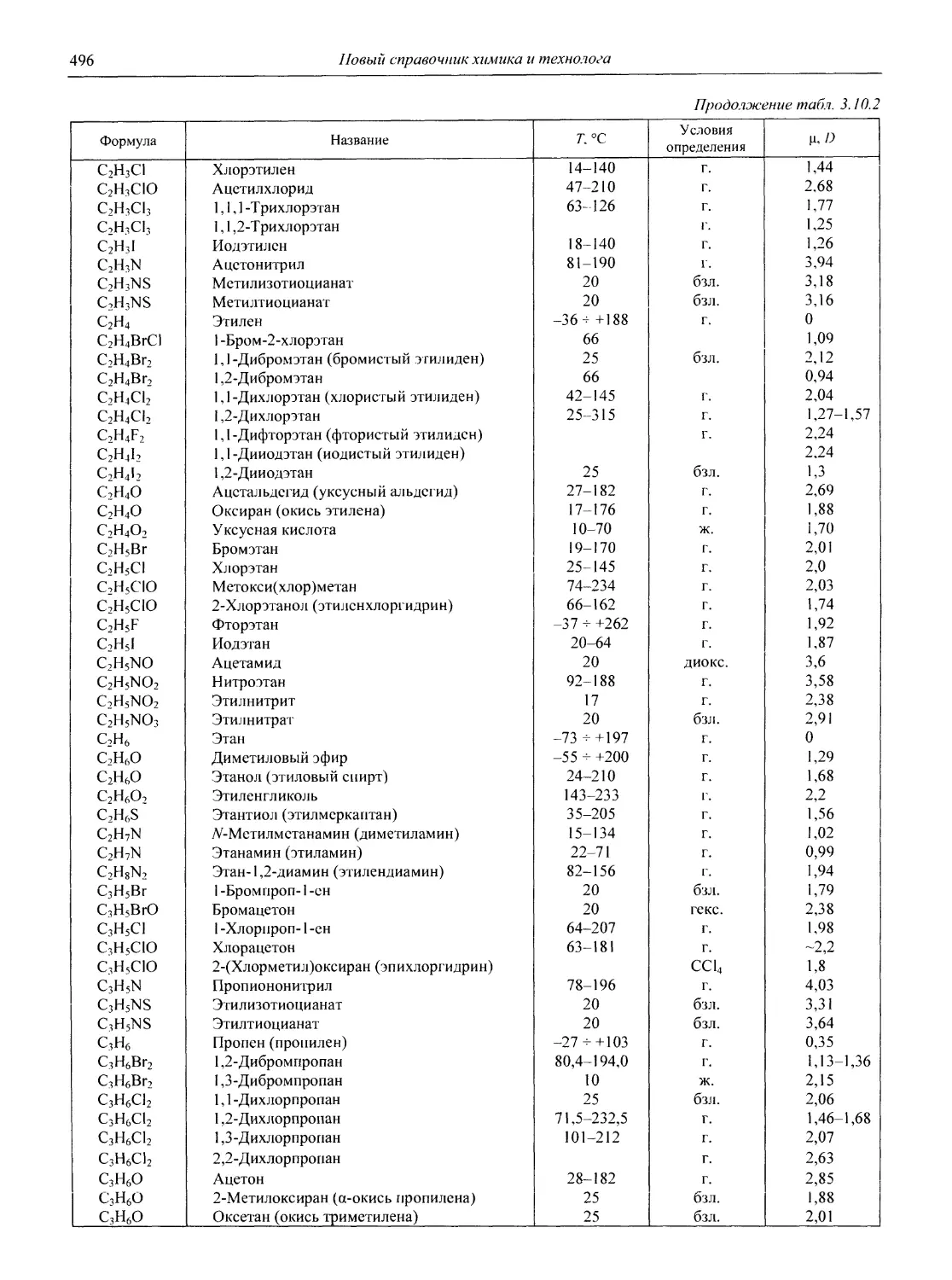
В разделе 3 представлены таблицы, отражающие физические свойства простых веществ и важнейших неорганических и элементоорганических соединений: плотность и сжимаемость жидкостей и газов; термическое расширение твердых тел, жидкостей и газов, равновесные температуры и давления (гетерогенное равновесие); теплоемкость, теплопроводность; электрическая проводимость и числа переноса, диэлектри-
ческая проницаемость, дипольные моменты; вязкость, поверхностное и межфазное натяжение веществ и растворов, их показатели преломления.
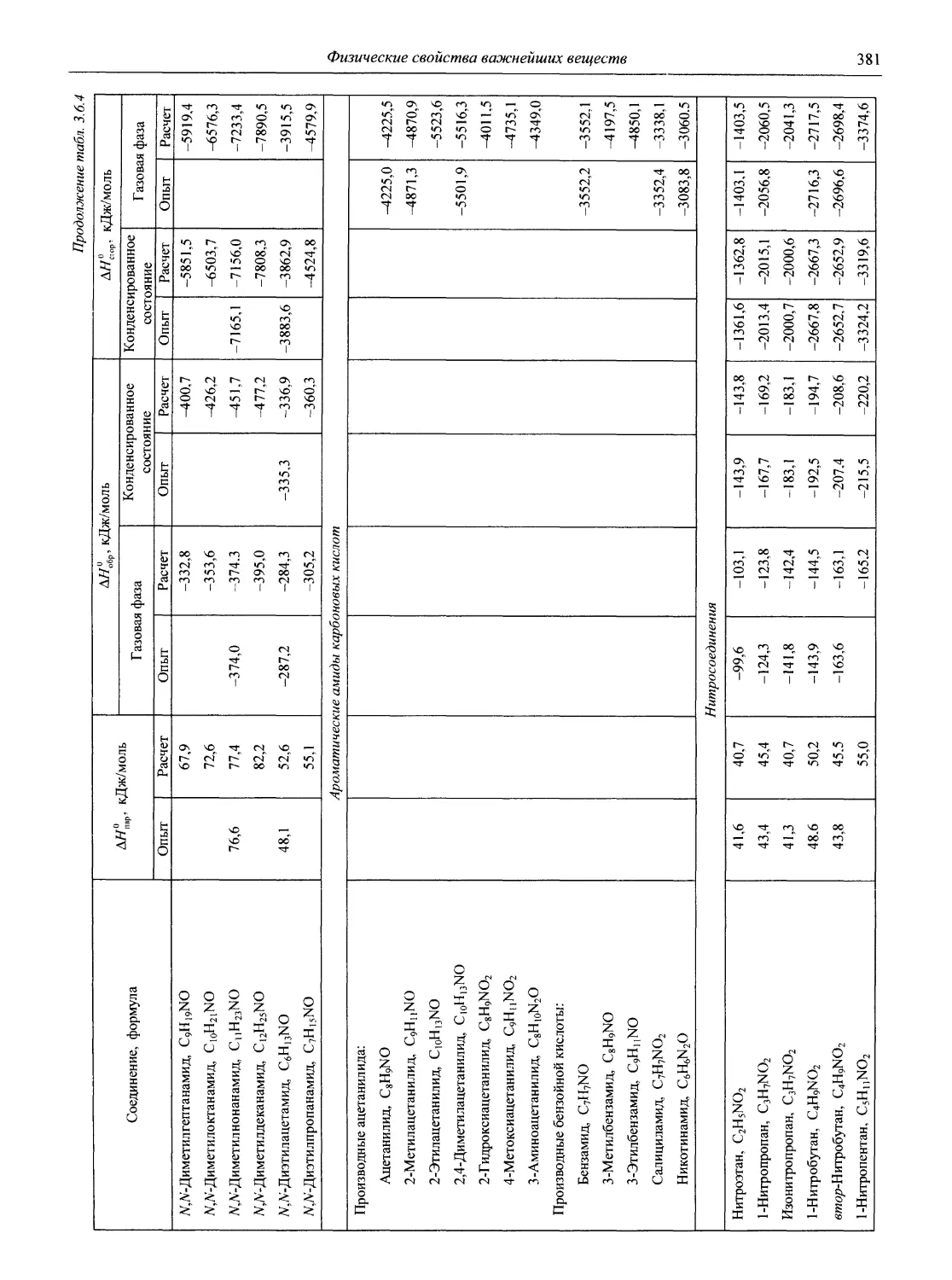
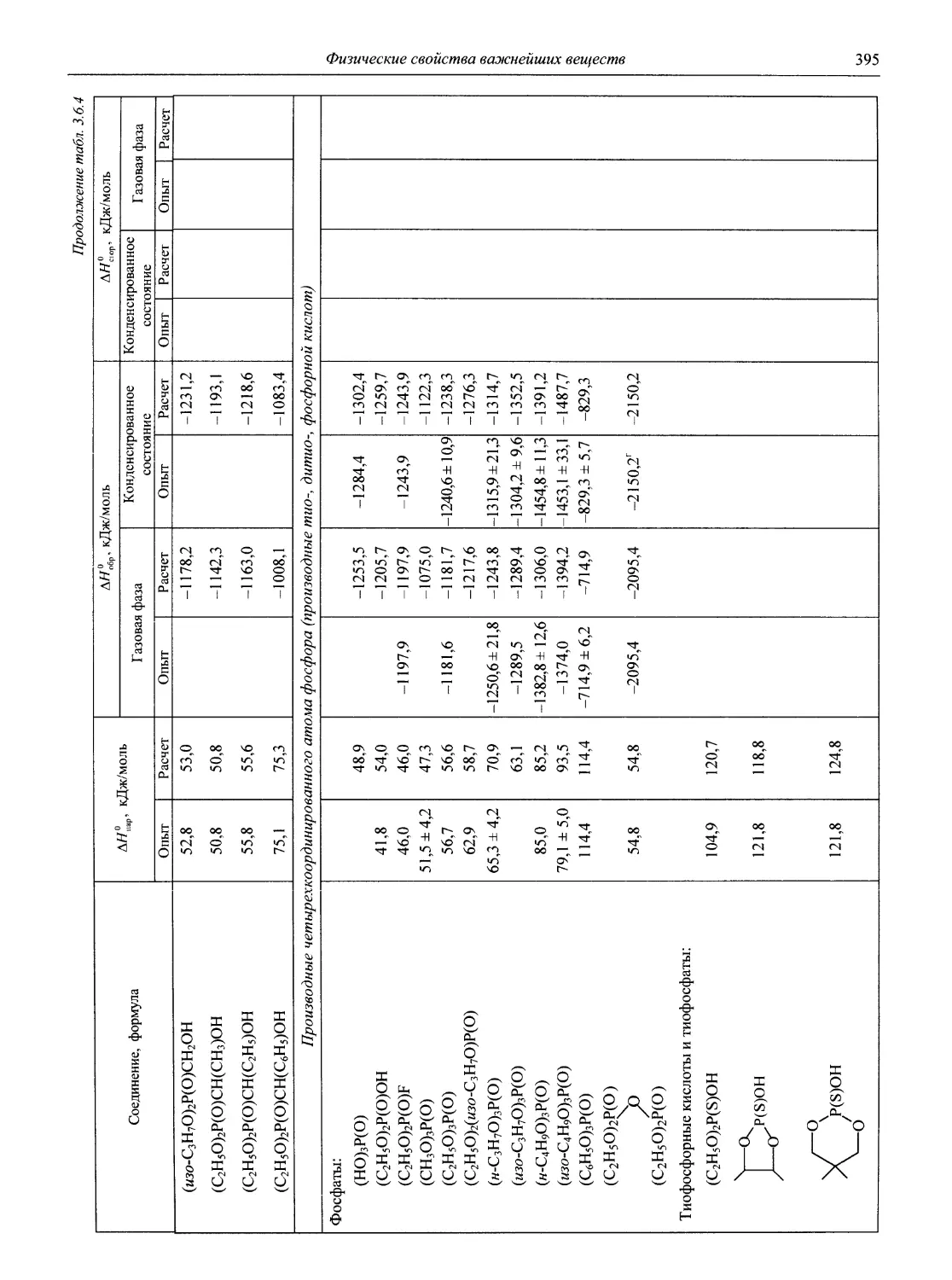
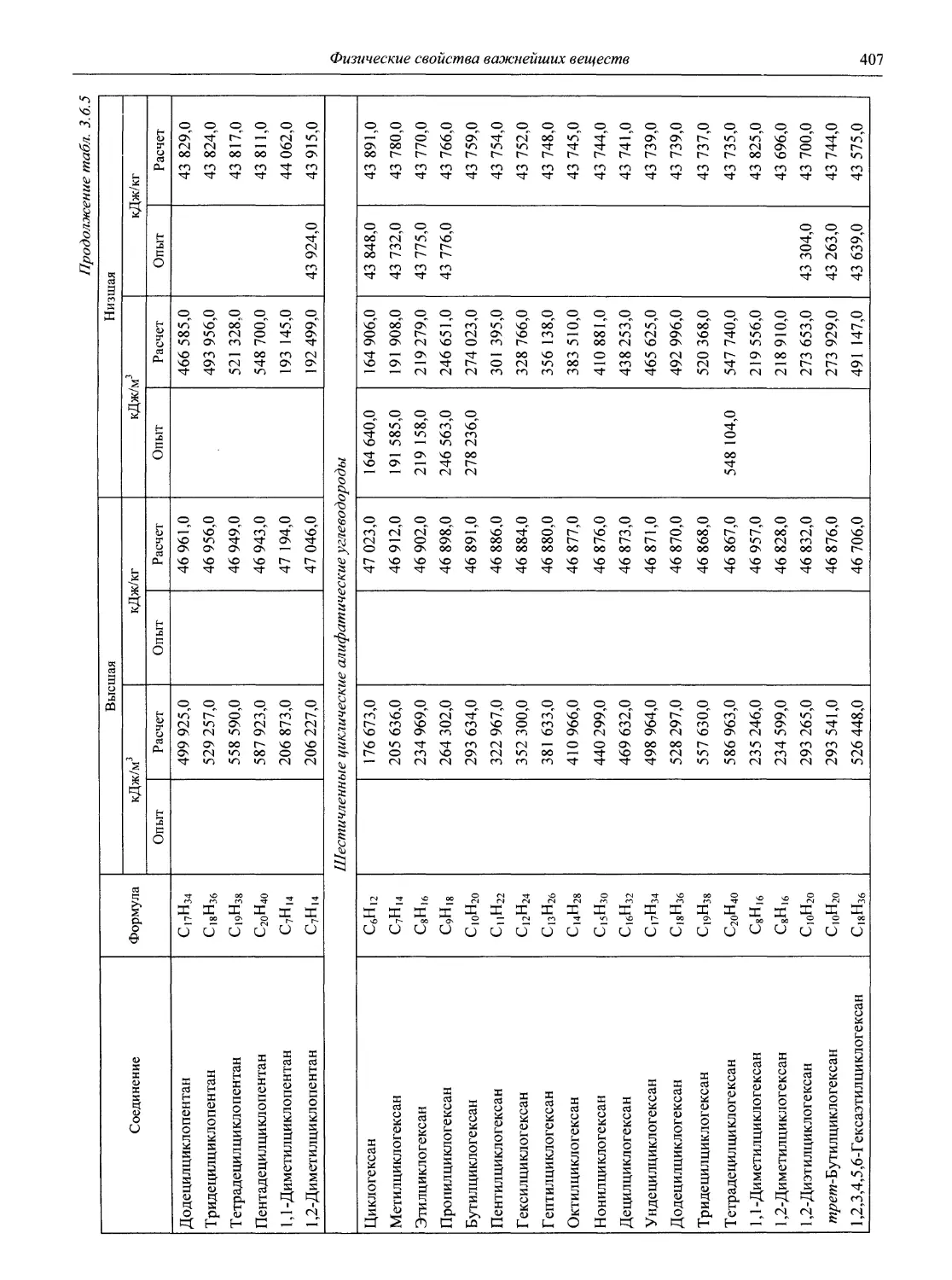
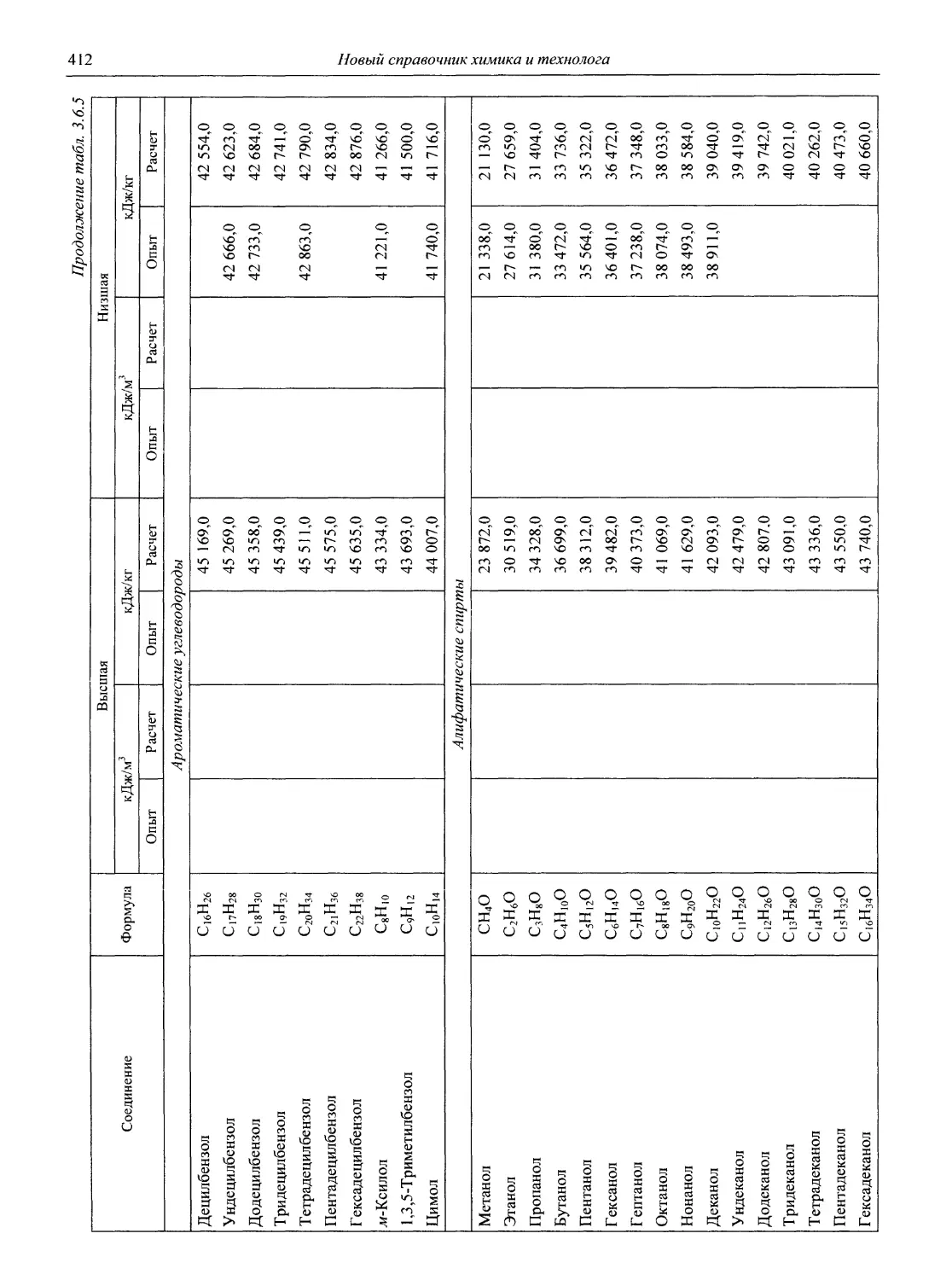
Для органических соединений впервые в справочнике приведены данные по расчету и экспериментальному определению стандартных энтальпий образования, парообразование и сгорание и обширная библиография по этому вопросу (более 300 источников).
Раздел 4 посвящен ароматическим соединениям: бензолу, анилину и органическим красителям, широко используемым в производстве синтетических полимеров, химических волокон, лакокрасочных материалов.
В разделе 5 представлена химия фотографических процессов и фотолитография, применяемая в микроэлектронных технологиях, связанных с получением систем обработки и передачи информации.
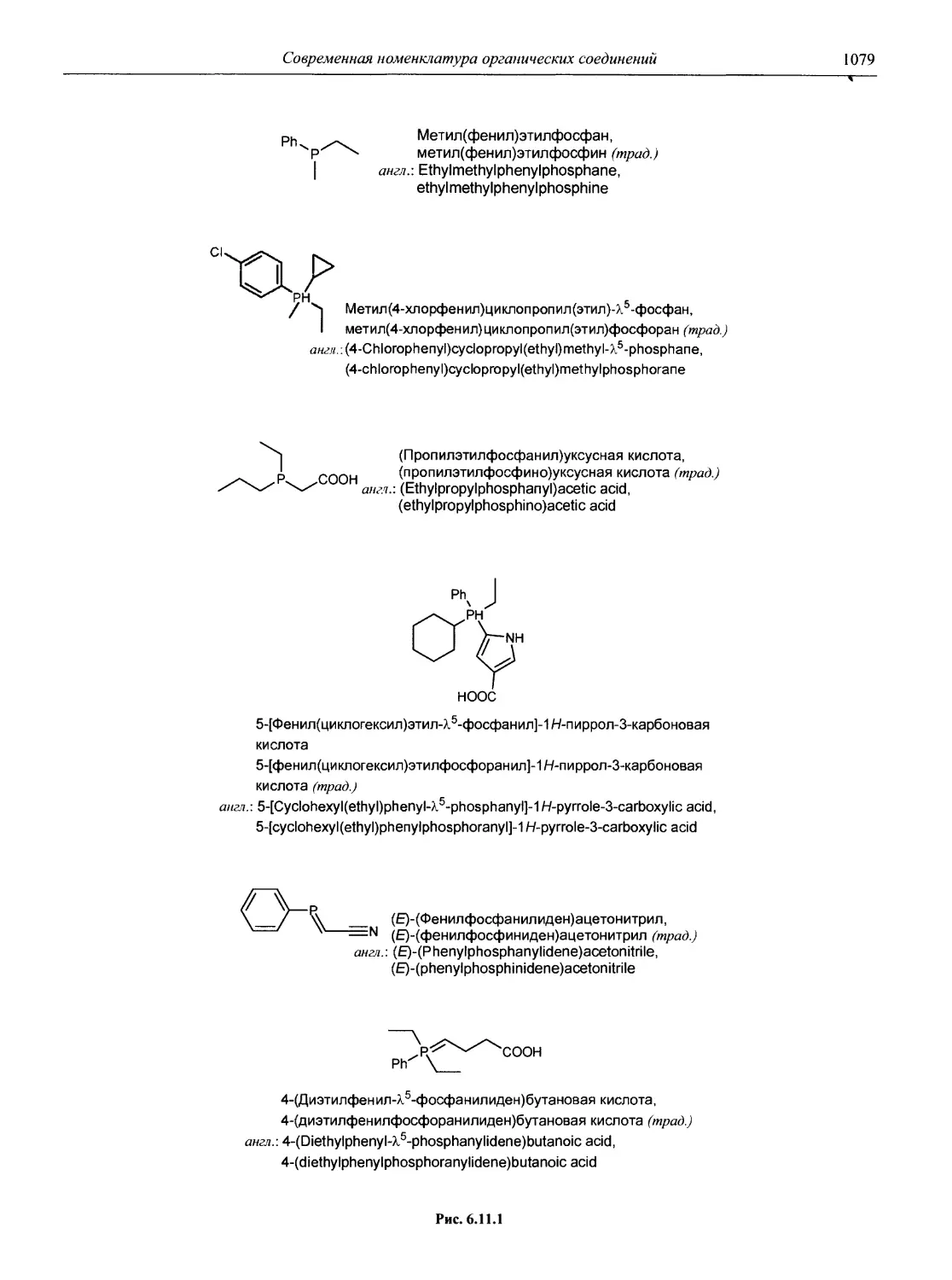
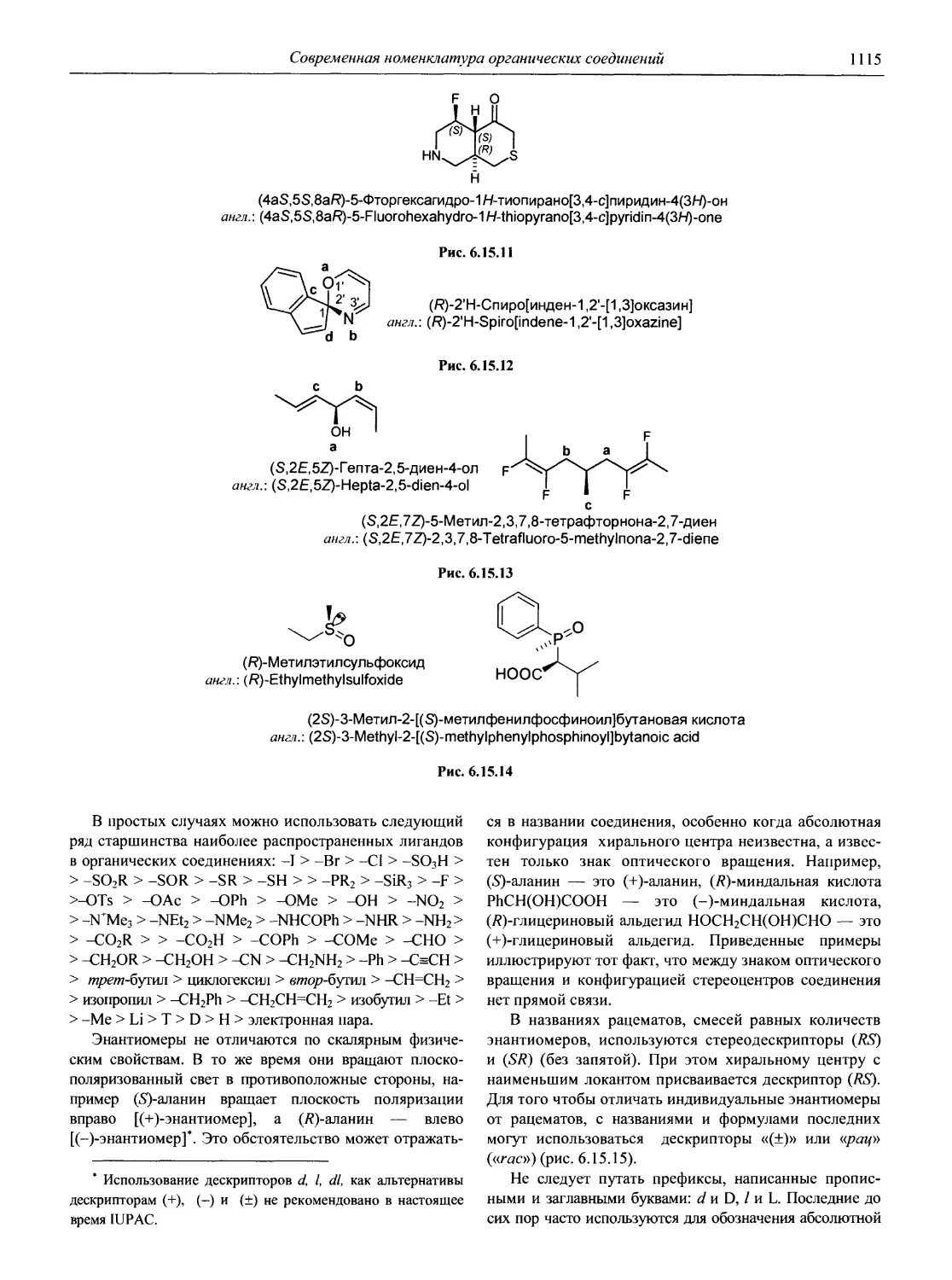
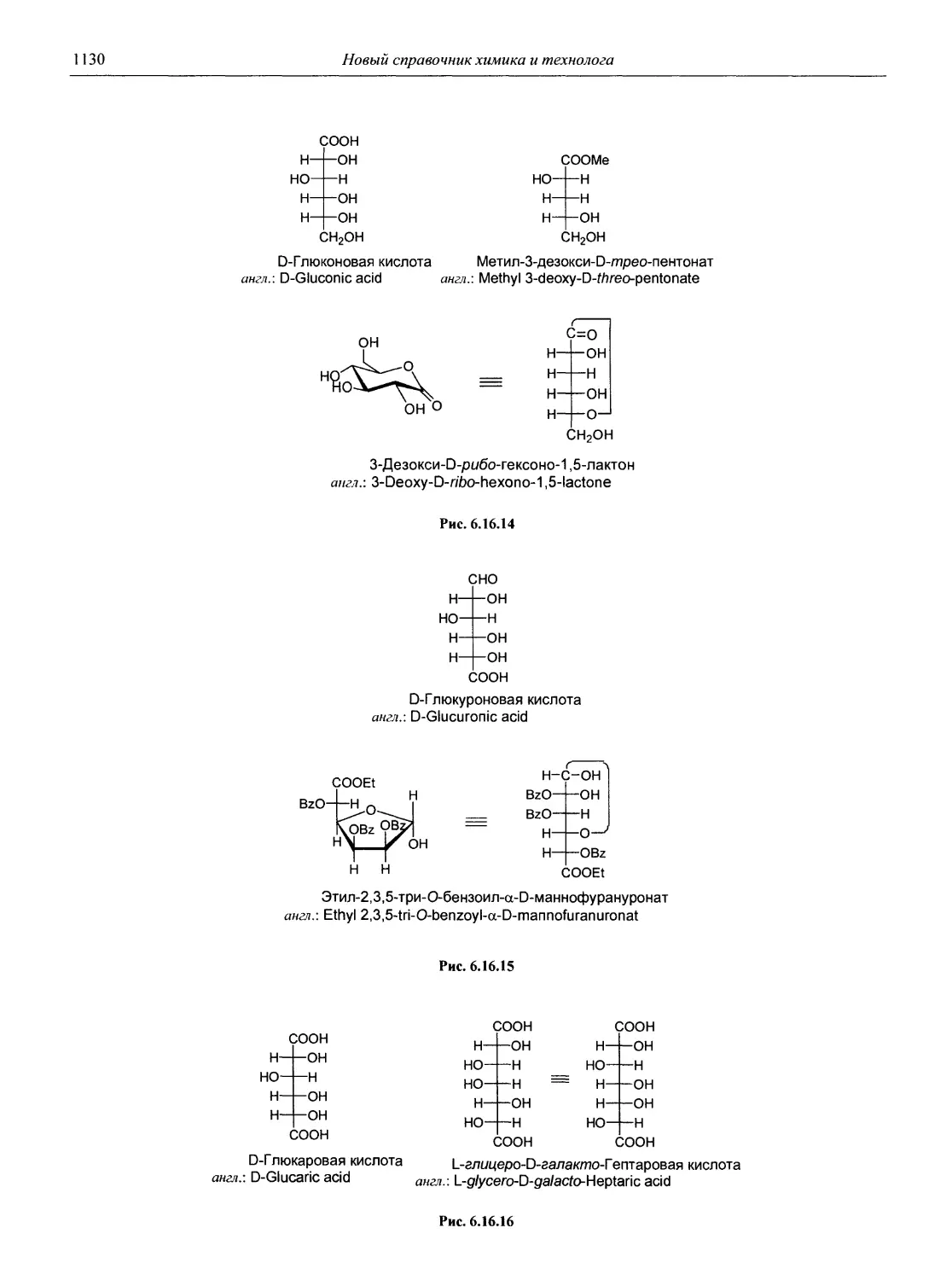
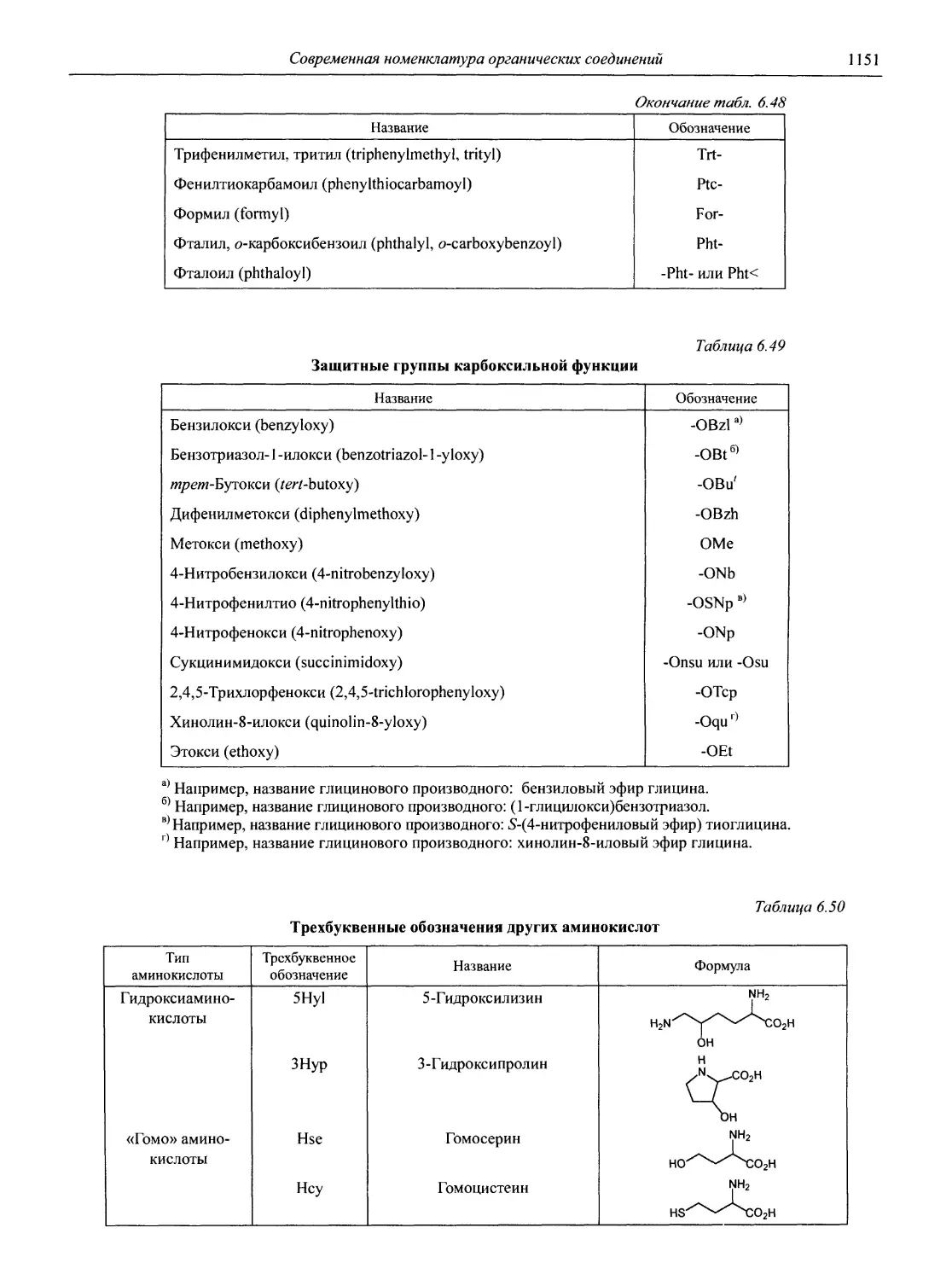
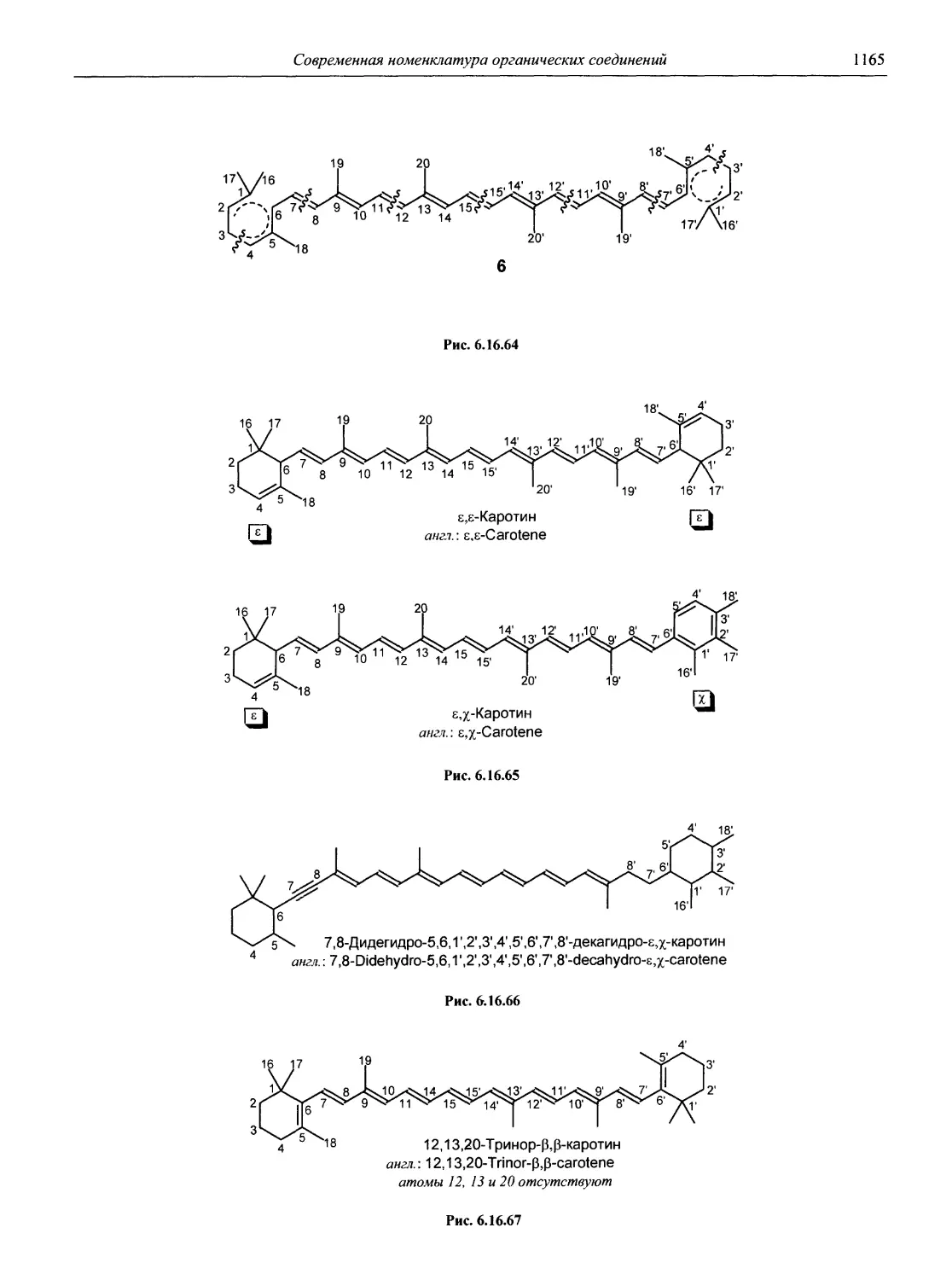
Раздел 6 является подробным справочным пособием по современной номенклатуре органических соединений, основанно на рекомендациях Международного союза теоретической и прикладной химии — ИЮПАК (IUPAC).
В разделе 7 приведены краткие сведения о лабораторной посуде и технике лабораторных работ. Описаны стеклянная и фарфоровая посуда, изготовляемая в соот-
ветствии с ГОСТами, а также газовые баллоны, индивидуальные средства защиты и пожаротушения в лаборатории.
Раздел 8 — новый раздел, посвященный основам технологии, — приводит информацию об анализе, проектировании и перспективных направлениях развития технологий.
В разделе 9 представлены сведения об интеллектуальной собственности: промышленной собственности, авторском праве, защите прав на интеллектуальную собственность, ее оценке. Во всех разделах тома использованы современная терминология и оценка физико-химических констант (в системе СИ).
В конце 12-го тома приведено содержание всех 11 -ти томов научного справочного издания «Новый справочник химика и технолога».
Информация, представленная в данном томе, может быть полезна химикам, занимающимся производственной, научно-исследовательской, учебно-методической и педагогической деятельностью, а также специалистам других отраслей промышленности, использующим новые материалы и технологии.
Канд. техн, наук В.А. Столярова
К ЧИТАТЕЛЯМ
Издательство с благодарностью примет и учтет при подготовке последующих изданий все ваши замечания, предложения и пожелания
Раздел 1. ОБЩИЕ СВЕДЕНИЯ
Составитель: д. х. н., проф. А.В. Москвин
Атом (от греч. atomos — неделимый) — наименьшая частица химического элемента, носитель его свойств. Каждому химическому элементу соответствует совокупность определенных атомов. Атом электронейт-рален и состоит из положительно заряженного ядра и отрицательно заряженных электронов.
Основная масса атома сосредоточена в ядре и характеризуется массовым числом, равным сумме чисел протонов и нейтронов. Заряд ядра соответствует атомному (порядковому) номеру элемента в периодической
системе. Атомная масса выражает относительное значение массы атома (по отношению к 1/12 атомной массы углерода 12С), выраженное в атомных единицах массы. За атомную массу природных элементов, состоящих из смеси изотопов принимают среднее значение массы изотопов с учетом их процентного содержания. В табл. 1.1 приведены относительные атомные массы элементов по данным на 2005 г. Элементы представлены в порядке увеличения их атомных номеров.
Относительные атомные массы элементов
Таблица 1.1
Атомный номер Символ Название Относительная атомная масса
русское латинское английское
1 Н Водород Hydrogen 1,007 94(7)*
2 Не Гелий Helium 4,002 602(2)*
3 Li Литий Lithium 6,941(2)*
4 Be Бериллий Beryllium 9,012 182(3)
5 В Бор Borum Boron 10,811(7)*
6 С Углерод Carboneum Carbon 12,0107(8)*
7 N Азот Nitrogenium Nitrogen 14,0067(2)*
8 О Кислород Oxygenium Oxygen 15,9994(3)*
9 F Фтор Ftorum Fluorine 18,998 403 2(5)
10 Ne Неон Neon 20,1797(6)*
11 Na Натрий Natrium Sodium 22,989 769 28(2)
12 Mg Магний Magnesium 24,3050(6)
13 Al Алюминий Aluminium 26,981 538 6(8)
14 Si Кремний Silicium Silicon 28,0855(3)
15 P Фосфор Phosphorum Phosphorus 30,973 762(2)
16 S Сера Sulfur 32,065(5)*
17 Cl Хлор Chlorum Chlorine 35,453(2)
18 Ar Аргон Argon 39,948(1)*
19 К Калий Kalium Potassium 39,0983(1)*
20 Ca Кальций Calcium 40,078(4)*
21 Sc Скандий Scandium 44,955 912(6)
22 Ti Титан Titanium 47,867(1)
23 V Ванадий Vanadium 50,9415(1)
24 Cr Хром Chromium 51,9961(6)
6
Новый справочник химика и технолога
Продолжение табл. /. /
Атомный номер Символ Название Относительная атомная масса
русское латинское английское
25 Мп Марганец Manganum Manganese 54,938 045(5)
26 Fe Железо Ferrum Iron 55,845(2)
27 Со Кобальт Cobaltum Cobalt 58,933 195(5)
28 Ni Никель Niccolum Nickel 58,6934(2)
29 Си Медь Cuprum Copper 63,546(3)
30 Zn Цинк Zincum Zinc 65,409(4)
31 Ga Галлий Gallium 69,723(1)
32 Ge Германий Germanium 72,64(1)
33 As Мышьяк Arsenicum Arsenic 74,921 60(2)
34 Se Селен Selenium 78,96(3)
35 Br Бром Bromum Bromine 79,904(1)
36 Kr Криптон Krypton 83.798(2)*
37 Rb Рубидий Rubidium 85,4678(3)*
38 Sr Стронций Strontium 87,62(1)*
39 Y Иттрий Yttrium 88,905 85(2)
40 Zr Цирконий Zirconium 91,224(2)*
41 Nb Ниобий Niobium 92,906 38(2)
42 Mo Молибден Molybdenum 95,94(2)*
43 Tc Технеций Technetium [98]
44 Ru Рутений Ruthenium 101,07(2)*
45 Rh Родий Rhodium 102,905 50(2)
46 Pd Палладий Palladium 106,42(1)*
47 Ag Серебро Argentum Silver 107,8682(2)*
48 Cd Кадмий Cadmium 112,411(8)*
49 In Индий Indium 114,818(3)
50 Sn Олово Stannum Tin 118,710(7)*
51 Sb Сурьма Stibium Antimony 121,760(1)*
52 Те Теллур Tellurium 127,60(3)*
53 I Иод lodum Iodine 126,904 47(3)
54 Xe Ксенон Xenon 131,293(6)*
55 Cs Цезий Caesium 132,905 451 9(2)
56 Ba Барий Barium 137,327(7)
57 La Лантан Lanthanum 138,905 47(7)*
58 Ce Церий Cerium 140,116(1)*
59 Pr Празеодим Praseodymium 140.907 65(2)
60 Nd Неодим Neodymium 144,242(3)*
61 Pm Прометий Promethium [145]
62 Sm Самарий Samarium 150,36(2)*
63 Eu Европий Europium 151,964(1)*
64 Gd Гадолиний Gadolinium 157,25(3)*
65 Tb Тербий Terbium 158,925 35(2)
66 Dy Диспрозий Dysprosium 162,500(1)*
67 Ho Гольмий Holmium 164,930 32(2)
68 Er Эрбий Erbium 167,259(3)*
69 Tm Тулий Thulium 168,934 21(2)
70 Yb Иттербий Ytterbium 173,04(3)*
71 Lu Лютеций Lutetium 174,967(1)*
72 Hf Гафний Hafnium 178,49(2)
73 Ta Тантал Tantalum 180,947 88(2)
74 W Вольфрам Wolfram ium Tungsten 183,84(1)
75 Re Рений Rhenium 186,207(1)
Общие сведения
7
Окончание табл. /. /
Атомный номер Символ Название Относительная атомная масса
русское латинское английское
76 Os Осмий Osmium 190,23(3)*
77 Ir Иридий Iridium 192,217(3)
78 Pt Платина Platinum 195,084(9)
79 Au Золото Aurum Gold 196,966 569(4)
80 Hg Ртуть Hiolrargirum Mercury 200,59(2)
81 T1 Таллий Thallium 204,3833(2)
82 Pb Свинец Plumbum Lead 207,2(1)*
83 Bi Висмут Bismuttum Bismuth 208,980 40(1)
84 Po Полоний Polonium [209]
85 At Астат Astatium Astatine [210]
86 Rn Радон Radon [222]
87 Fr Франций Francium [223]
88 Ra Радий Radium [226]
89 Ac Лстиний Actinium [227]
90 Th Торий Thorium 232,038 06(2)*
91 Pa Протактиний Protactinium 231,035 88(2)
92 U Уран Uranium 238,028 91(3)*
93 Np Нептуний Neptunium [237]
94 Pu Плутоний Plutonium [244]
95 Am Америций Americium [243]
96 Cm Кюрий Curium [247]
97 Bk Берклий Berkelium [247]
98 Cf Калифорний Californium [251]
99 Es Эйнштейний Einsteinium [252]
100 Fm Фермий Fermium [257]
101 Md Менделевий Mendelevium [258]
102 No Нобелий Nobelium [259]
103 Lr Лоуренсий Lawrencium [262]
104 Rf Резерфордий Rutherfordium [261]
105 Db Дубний Dubnium [262]
106 Sg Сиборгий Seaborgium [266]
107 Bh Борий Bohrium [264]
108 Hs Хассий Hassium [277]
109 Mt Мейтнерий Meitnerium [268]
НО Ds Дармштадтий Darmstadtium [281]
111 Kg Рентгений Roentgen ium [272]
112 (Jub Унунбий Ununbium [285]
ИЗ Uut Унунтрий Ununtrium [284]
114 (Juq Унунквадий Ununquadium [289]
115 (J up Унунпентий Ununpentium [288]
116 (Juh Унунгсксий Ununhexium [291]
117 (Jus Унунсептий Ununseptium
118 Uuo Унуноктий Ununoctium [294]
* В некоторых геологических образцах элемент имеет изотопный состав, отличающийся от обычного. В таких случаях могут иметь место существенные отклонения относительной атомной массы от приведенного значения.
Примечания: 1. Для элементов с атомными номерами 1-3, 5-8. 14, 16, 18, 29, 38 и 82 диапазон изменений изотопного состава, обычного земного образца не позволяет привести более точных значений относительной атомной массы; приведенные значения применимы к любым обычным образцам.
2. Для элементов с атомными номерами 1, 3, 5, 10, 17, 36, 54 и 92 иные изотопные составы могут быть представлены в коммерческих образцах, полученных при разделении изотопов. В таких образцах имеют место существенные отклонения относительных атомных масс от приведенных значений.
8
Новый справочник химика и технолога
3. Коммерчески доступные образцы Li имеют относительные атомные массы в диапазоне от 6,939 до 6,996; если необходимо более точное значение, то его следует определить для конкретного образца.
4. Элементы с атомными номерами 43, 61 и с 84 по 118 не имеют устойчивых нуклидов, поэтому для них в квадратных скобках приведено массовое число наиболее долгоживущего изотопа. Однако три таких элемента (Th. Ра и U) имеют характерный для земных условий изотопный состав, и для них приведены относительные атомные массы.
5. Названия и символы элементов с атомными номерами 112-118 находятся на рассмотрении. Для них рекомендована временная система (J. Chatt // Pure Appl. Chem. 1979. V. 51. P. 381-384). Названия элементов с атомными номерами 101-109 были согласованы в 1997 г. (Pure Appl. Chem. 1997. V. 69. Р. 2471-2473), элемента с номером 110 — в 2003 г. (Pure Appl. Chem. 2003. V. 75. Р. 1613-1615) и элемента 111 — в 2004 г. (Pure Appl. Chem. 2004. V. 76. Р. 2101-2103).
6. Описание обнаружения
элементов 113 и 115 см.: Phys. Bev. С. 2004. V. 69. 021601 (R);
элементов 116 и 118 см.: Pure Appl. Chem. 2006. V. 78. Р. 889-904.
В табл. 1.2 приведены значения фундаментальных физических постоянных.
Таблица 1.2
Фундаментальные физические постоянные
Наименование Символ Значение Единица измерения
У ниверсальные
Акустическое сопротивление в вакууме (импеданс акустический) Электрическая постоянная Магнитная постоянная Гравитационная постоянная Ньютона Планка постоянная Планка постоянная Планка время Планка длина Планка масса Планка температура Скорость света в вакууме 4 £о Цо G G/hc h h = h/2it he tp = Ip/c lp = Й/(Л7РС) m? = yjhc/G T? C-, Co 376,730 313 461... 8,854 187 817... • 10’12 4л- 10 7 = 12,566 370 614... • 10 7 6,742(10) • 10 11 6,7087(10) • 10 39 6,626 069 3(11)- 10’34 4,135 667 43(35)- 10 15 1,054 571 68(18)- 10 34 6,582 119 15(56) • 10 16 197,326 968(17) 5,391 21(40)- 10”44 1,616 24(12)- 10’35 2,176 45(16)- 10’8 1,4 1 6 79(11)- 1032 299 792 458 Ом «акустический» Ф • м’1 Гн • м’1 м’ • кг 1 • с 1 (ГэВ/с2)’2 Дж • с эВ • с Дж • с эВ • с МэВ • фм с м кг К м • с 1
Электромагнитные
Бора магнетон Квант проводимости Элементарный заряд Джозефсона постоянная Квант магнитного потока Ядерный магнетон фон Клитцинга постоянная Pb = eh/(2me) ^/hc Go 1/Go e e/h = 2e/h Фо = WO p.v = ehl(2mp) \\.N/hc \LNlk \)cNlh 927,400 949 (80)- 10 26 5,788 381 804 (39)- 10 5 13,996 245 8(12)- 109 46,686 450 7(40) 0,671 713 1(12) 7,748 091 733(26) • 10’5 12906,403 725 (43) 1,602 176 53(14)- 10 19 2,417 989 40(21)- 1014 483 597,879(41)- 109 2,067 833 72(18)- IO’15 5,050 783 43(43) • 10’27 3,152 451 259 (21)- 10’8 2,542 623 58(22)- 10’2 3,658 263 7(64)- 10’4 7,622 593 71(65) 25 812,807 449 (86) Дж • Тл 1 эВ • Тл’1 Гц • Тл’1 м’1 • Тл’1 К • Тл’1 См Ом Кл А • Дж’1 Гц • В’1 Вб Дж • Тл’1 эВ • Тл’1 “1 т-1 —1 м • Гл К • Тл”1 МГц • Тл’1 Ом
Атомные и ядерные
Тонкой структуры постоянная a = |Тосе2/(2/г) 1/a 7,297 352 568 (24)- 10 3 137,035 999 11(46)
Общие сведения
9
Продолжение табл. 1.2
Наименование Символ Значение Единица измерения
Ридберга постоянная /?х = теса2/{2И) 10 973 731,568 525 (73) -1 м
R^c 3,289 841 960 360 (22)- 1015 Гц
Rjhc 13,605 692 3(12) 2,179 872 09(37) • 10”18 эВ Дж
Бора радиус а0 = а/(4л7?ос) 0,529 177 210 8(18)- 10 ,0 м
Хартри энергия Ен = 2Rxhc 4,359 744 17(75) • 10”18 27,211 384 5(23) Дж эВ
Масса электрона те 9,109 382 6(16)- 10’31 5,485 799 094 5(24)- 10”4 кг а. е. м.
тсс2 8,187 104 7(14)- 10”14 0,510 998 918(44) Дж МэВ
Удельный заряд электрона е/те -1,758 820 12(15)- 10” Кл • кг 1
Молярная масса электрона Ме 5,485 799 094 5(24)- 10 7 кг • моль”1
Комптоновская длина волны электрона А< = h/(mec) 2,426 310 238 (16)- 1012 м
Классический радиус электрона гс = а2я0 2,817 940 325 (28)- 10’15 м
Сечение рассеяния электрона Томсона 8л 2 ое = —г 3 е 0,665 246 16(18)- 10 28 м2
Магнитный момент электрона Не Не/Цв -928,476 412 (80)- 10 26 -1,001 159 652 185 9(38) Дж • Тл 1
Аномалия магнитного момента электрона ае = 1 1,159 652 185 9(38)- 10 3
g-Фактор электрона ge = 2(1 + ас) -2,002 319 304 371 8(75)
Масса мюона 1,883 531 40(33)- 10”28 0,113 428 926 4(30) кг а. е. м.
/ИИС'2 1,692 833 60(29)- 10 11 105,658 369 2(94) Дж МэВ
Магнитный момент мюона Нц MHn -4,490 447 99(40) • 10 26 8,890 596 98(23) Дж • Тл”1
Аномалия магнитного момента мюона 2т ц _ ег ц 1 1 еп 1,165 919 81(62)- 10”3
g-Фактор мюона g^ = 2(l + аи) 2,002 331 839 6(12)
Масса протона тр 1,672 621 71(29)- 10 27 кг
трс2 1,503 277 43(26)- 10”10 938,272 029 (80) Дж МэВ
Отношение массы протона к массе электрона тр/те 1836,152 672 61(85)
Удельный заряд протона е/тр 9,578 833 76(82)- 107 Кл • кг’1
Комптоновская длина волны протона Xcp = h/(mpc) 1,321 409 855 5(88)- 10 15 м
Магнитный момент протона Mr Цр/Цл' 1,410 606 71(12)- 10”26 2,792 847 351(28) Дж • Тл”1
Магнитный момент протона без поправки на диамагнетизм 1,410 571 38(47) • 10 26 Дж • Тл”1
Гиромагнитное отношение Ур 2,675 222 05(23) • 108 с 1 • Тл”1
Масса нейтрона тп 1,674 927 28(29) • 10 27 1,008 664 904(14) кг а. е. м.
Отношение массы нейтрона к массе протона тп/тр 1,001 378 418 70(58)
10
Новый справочник химика и технолога
Окончание табл. 1.2
Наименование Символ Значение Единица измерения
Атомные и ядерные
Комптоновская длина волны нейтрона Магнитный момент нейтрона Хс, „ = hl(mnc) 1,319 590 906 7(88)- 10”15 0,966 236 45(24) -10 26 м Дж • Тл 1
Физико-химические
Атомная единица массы Энергетический эквивалент атомной единицы массы Авогадро постоянная Больцмана постоянная Фарадея постоянная Постоянная излучения первая Постоянная излучения вторая Лошмидта постоянная (273,15 К, 101,325 кПа) Молярная газовая постоянная Молярная постоянная Планка Молярный объем идеального газа (273,15 К, 100 кПа) Молярный объем идеального газа (273,15 К, 101,325 кПа) Стефана — Больцмана постоянная тис2 к k/h k/hc F=N^e С] = 2nhc2 С’ц = С]/л c2 - he!к no R N^hc vm a = л2А2/(60Й3с2) 1,660 538 86(28)- IO”27 1,492 417 90(26) -IO"10 8,6 • 10”8 6,022 141 5(10)- 1023 1,380 650 5(24)- 10 23 8,617 343 (15)- 10”5 2,083 664 4(36)- IO10 69,503 56(12) 96 485,3383(83) 3,741 771 38(64) • 10”16 1,191 042 82(20) • 10”16 1,438 775 2(25)- 10 2 2,686 777 3(47)- 1025 8,314 472(15) 3,990 312 716(27)- IO”10 0,119 626 565 72(80) 22,710 981 (40)- 10 3 22,413 996(39)- 10”3 5,670 400 (40)- 10”8 кг Дж МэВ моль’1 Дж • К”1 эВ • К 1 Гц • К ' м 1 • К”1 Кл • моль”1 Вт • м2 Вт • м2 • ср 1 м • К -3 м Дж • моль”1 • К 1 Дж • с • моль’1 Дж • м • моль”1 м3 • моль”1 м3 • моль 1 Вт • м 2-К”4
Примечание. В скобках указаны стандартные ошибки определения величины.
Международная система единиц СИ
(The International System of Units SI)
В СССР Международная система единиц введена с 1 января 1963 г. и с тех пор применяется как предпочтительная. В настоящее время применение Международной системы единиц в России устанавливается в соответствии с ГОСТ 8.417-2002.
Основными единицами Международной системы единиц (СИ) являются метр (L), килограмм (М), секунда (Т), ампер (I), Кельвин (К), моль (N) и кандела (J).
Кроме того, введены дополнительные единицы: плоский угол и телесный угол. Остальные единицы являются производными от основных и дополнительных единиц.
Ниже приведены: в табл. 1.3 — физические величины в системе СИ, в табл. 1.4 — внесистемные единицы, допускаемые к применению, в табл. 1.5 — соотношения между единицами физических величин, в табл. 1.6 — множители и префиксы, используемые для образования наименований десятичных кратных и дольных единиц.
Общие сведения
11
Физические величины и единицы СИ
Таблица 1.3
Физическая величина Символ Размерность Наименование единицы измерения Обозначение
международное русское
Основные
Длина Масса Время Сила электрического тока Т ермодинамическая температура Количество вещества Сила света / т t 1 Т п т L М т 1 0 N J метр килограмм секунда ампер кельвин моль кандела m kg s А К mol cd M кг c A К моль кд
Дополнительные
Плоский угол Телесный угол а _Q 1 1 радиан стерадиан rad sr рад ср
Производные
Пространственно-временны ые
Площадь Объем, вместимость Скорость Ускорение Угловая скорость Угловое ускорение A,S V V а со £ L2 L? LT 1 LT”2 Т 1 Т”2 квадратный метр кубический метр метр в секунду метр на секунду в квадрате радиан в секунду радиан на секунду в квадрате m2 m3 m • s’1 m • s 2 rad • s 1 rad • s 2 м2 м3 м • с”1 м • с 2 рад • с’1 рад • с’2
Периодические и связанные с ними явления
Фаза колебаний Период Частота периодического процесса Частота вращения Волновое число Коэффициент затухания Коэффициент ослабления Ф т fv п V 5 Н Т Т1 Т1 L 1 Т 1 L’1 секунда герц секунда в минус первой степени метр в минус первой степени секунда в минус первой степени метр в минус первой степени rad s Hz s’1 m 1 s 1 m”1 рад с Гц с 1 м 1 с 1 м 1
Механические
Плотность Удельный объем Количество движения (импульс) Момент количества движения (момент импульса) Момент инерции (динамический момент инерции) Сила Вес Момент силы Импульс силы Р V р L J F P,G М I L'3M L3M”’ LMT”1 L2MT 1 l2m LMT’2 LMT’2 l2mt 2 LMT’1 килограмм на кубический метр кубический метр на килограмм килограмм-метр в секунду килограмм-метр в квадрате на секунду килограмм-метр в квадрате ньютон ньютон ньютон-метр ньютон-секунда kg • m”3 m3•kg 1 kg • m • s’1 kg • m2 • s’1 kg • m2 N N N • m N • s кг • м 3 м3 • кг”1 кг • м • с”1 2 1 кг • м - с кг • м2 н н Н • м Н • с
12
Новый справочник химика и технолога
Продолжение табл. 1.3
Физическая величина Символ Размерность Наименование единицы измерения Обозначение
международное русское
Механические
Удельный вес Давление Работа Энергия Мощность Поверхностное натяжение Динамическая вязкость Кинематическая вязкость у р А Е N о П V L 2МТ 1 L 'МТ 2 L2MT 2 L2MT 2 l2mt 3 МТ’2 L 'МТ 1 L2T 1 ньютон на кубический метр паскаль джоуль джоуль ватт ньютон на метр паскаль-секунда квадратный метр на секунду N • m 3 Ра J J W N • т' Ра • s т2 • s ' Н • м 3 Па Дж Дж Вт Н • м 1 Па • с 2 -1 м • С
Электрические и магнитные
Электрический заряд, количество электричества Пространственная плотность электрического заряда Поверхностная плотность электрического заряда Линейная плотность электрического заряда Удельный заряд частицы-носителя заряда Электрический потенциал Электродвижущая сила Напряженность электрического ноля Поток напряженности электрического поля через элемент поверхности Электрическое смещение Поток электрического смещения Электрический момент электрического диполя Поляризованность Абсолютная диэлектрическая проницаемость Относительная диэлектрическая проницаемость Абсолютная диэлектрическая восприимчивость Q р о т 2уд С, Ф Е Е Ф/; D ¥ Р Р г, 8а 8Г X, Ха TI L’3TI L 2TI L 'Tl M 'TI L2MT 3I ' L2MT’3r' LMT 3I 1 L3MT”3r' L 2TI TI LT1 L 2TI L’3M'T4I2 1 L’3M’'T4!2 кулон кулон на кубический метр кулон на квадратный метр кулон на метр кулон на килограмм вольт вольт вольт на метр вольт-метр кулон на квадратный метр кулон кулон-метр кулон на квадратный метр фарад на метр фарад на метр С С • т”3 С • т 2 С • т ' С - kg 1 V V V • т' V • т С • т 2 С С • т С • гтГ2 F • т”1 F • т’1 Кл Кл • м ’ Кл • м 2 Кл • м ' Кл • кг’1 В В В • м”' В • м Кл • м ~ Кл Кл • м Кл • м”2 Ф • м 1 Ф • м”1
Общие сведения
13
Продолжение табл. 1.3
Физическая величина Символ Размерность Наименование единицы измерения Обозначение
международное русское
Относительная диэлектрическая восприимчивость Поляризуемость атома (иона, молекулы) Электрическая емкость Электрическое напряжение Плотность электрического тока Линейная плотность электрического тока Электрическое активное сопротивление Удельное электрическое сопротивление Активная электрическая проводимость Удельная электрическая проводимость Плотность электрического тока смещения Температурный коэффициент электрического сопротивления Магнитный поток Потокосцепление Магнитная индукция Магнитный момент плоского контура с током Намагниченность Магнитная восприимчивость Индуктивность Взаимная индуктивность Напряженность магнитного поля Абсолютная магнитная проницаемость Относительная магнитная проницаемость Магнитодвижущая сила Скалярный магнитный потенциал Магнитное сопротивление Хг а С и J А R Р G у, * Jcm а Ф Т В ш М X L н Ц, Ра Иг F Vm, фот Гт 1 М 'Т4!2 L”2M 'Т4!2 l2mt 3Г1 L 21 L 'I 1?МТ 31 2 L3MT 3Г2 L 2М“'Т312 L”3M 'Т3!2 L”2! О 1 l2mt 2г' l2mt 21 1 МТ 21 1 L2! L”1! 1 Ь2МТ"2Г2 L2MT 2I 2 L 'I LMT 2I 2 1 I I l2m’t2i2 кулон в квадра-те-квадратный метр на джоуль фарад вольт ампер на квадратный метр ампер на метр ом Ом-метр сименс сименс на метр ампер на квадратный метр кельвин в минус первой степени вебер вебер тесла ампер-квадратный метр ампер на метр генри генри ампер на метр генри на метр ампер ампер генри в минус первой степени С2 • т2 • Г1 F V А • т 2 А • т”1 От От • т S S • т 1 А • т 2 К 1 Wb Wb Т А • т2 А • т'1 Н Н А • т”1 Н • т 1 А А Н”1 Кл2 • м2 • Дж”1 Ф В А • м 2 А • м'1 Ом Ом • м См См • м”1 А • м 2 К"1 Вб Вб Тл А • м2 А • м”1 Гн Гн А • м 1 Гн • м 1 А А Гн”1
Тепловые
Количество теплоты Удельное количество теплоты Q q L2MT“2 I?T 2 джоуль джоуль на килограмм J J • kg 1 Дж Дж • кг”1
14
Новый справочник химика и технолога
Продолжение табл. 1.3
Физическая величина Символ Размерность Наименование единицы измерения Обозначение
международное русское
Тепловые
Внутренняя энергия Энтропия Удельная энтропия Теплоемкость Удельная теплоемкость Молярная теплоемкость Тепловой поток (тепловая мощность) Поверхностная плотность теплового потока Температуропроводность Коэффициент теплопроводности (теплопроводность) Коэффициент теплопередачи и S S С с Ст Ф ч а Т к L'MT “ L2MT 2O”‘ L2T 20 1 L2MT 20 1 L2T 20 1 L2MT 20 ’N 1 L2MT 3 MT ’ L2T 1 LMT 30”' MT 30 1 джоуль джоуль на кельвин джоуль на килограмм-кельвин джоуль на кельвин джоуль на килограмм-кельвин джоуль на моль-кельвин ватт ватт на квадратный метр квадратный метр на секунду ватт на метр-кельвин ватт на квадратный метр-кельвин J J • К 1 J • kg’1 • К’1 J • К 1 J • kg 1 • К 1 J • mol 1 • К 1 W W • m 2 m2 • s’1 W • m 1 • К 1 W • m 2 • К 1 Дж Дж-К 1 Дж • кг”1 • К"1 Дж-К 1 Дж • кг 1 • К 1 Дж • моль 1 • К"1 Вт Вт • м 2 2 -1 м • С Вт • м 1 • К 1 Вт•м 2 • К 1
Световые
Световой поток Световая энергия Освещенность Светимость (поверхностная плотность светового потока) Яркость Фг Q. Er Mr С- J TJ L 2J L 2 J L 2J люмен люмен-секунда люкс люмен на квадратный метр кандела на квадратный метр Im Im • s lx Im • m”2 cd • m 2 лм лм • с лк лм • м 2 кд • м”2
Физико-химические
Относительная атомная масса химического элемента Относительная молярная масса вещества Молярная масса вещества Молярный объем Коэффициент диффузии Молярная внутренняя энергия Молярная энтропия Концентрация молекул (частиц) Массовая концентрация Моляльность Ar Mr M ]/ r m D um Sm n Pb ^B 1 1 MN 1 L3N”' l2nt_1 L2MT”2N”’ L2MT 20-iN 1 L"3 L 3M M”’N килограмм на моль кубический метр на моль квадратный метр в секунду джоуль на моль джоуль на моль-кельвин метр в минус третьей степени килограмм на кубический метр моль на кило- грамм kg • mol ’1 m3 • mol”1 2 -1 m • s J • mol 1 J -mol”1 • K’1 m”J kg • m’3 mol • kg”1 кг • моль”1 м3 • моль”1 м2 • с 1 Дж • моль”1 Дж • моль'1 • К”1 -3 м кг • м 3 моль • кг”1
Общие сведения
15
Продолжение табл. 1.3
Физическая величина Символ Размерность Наименование единицы измерения Обозначение
международное русское
Массовая доля компонента Объемная доля компонента Молярная доля компонента Подвижность ионов (электронов) Молярное отношение растворенного вещества Парциальное давление Скорость химической реакции Тепловой эффект химической реакции Химический потенциал компонента Абсолютная активность компонента Относительная активность Летучесть (фугитивность) Осмотическое давление Зарядное число Ионная сила раствора Степень диссоциации Электрическая проводимость электролита Молекулярная рефракция WB <Рв b Ра V Q Цв fu и Z I а G R 1 1 1 М 'Т21 1 L 'МТ”2 L 3T”'N 1?МТ”2 L2MT’2N”' 1 1 L 'МТ 2 Ь'МТ”2 1 М 'N 1 L”3M 'Т3!2 М *T412N 1 квадратный метр на вольт-секунду паскаль моль на кубический метр в секунду джоуль джоуль на моль паскаль паскаль моль на килограмм сименс на метр кубический метр на моль т2 • V ' • s' Ра mol • m“3 • s’1 J J • mol ' Ра Ра mol • kg”' S • m”' m3 • mol ' m2 • B”' • c”' Па моль • м J • c”1 Дж Дж • моль ' Па Па моль • кг ' См • м”' м3 • моль '
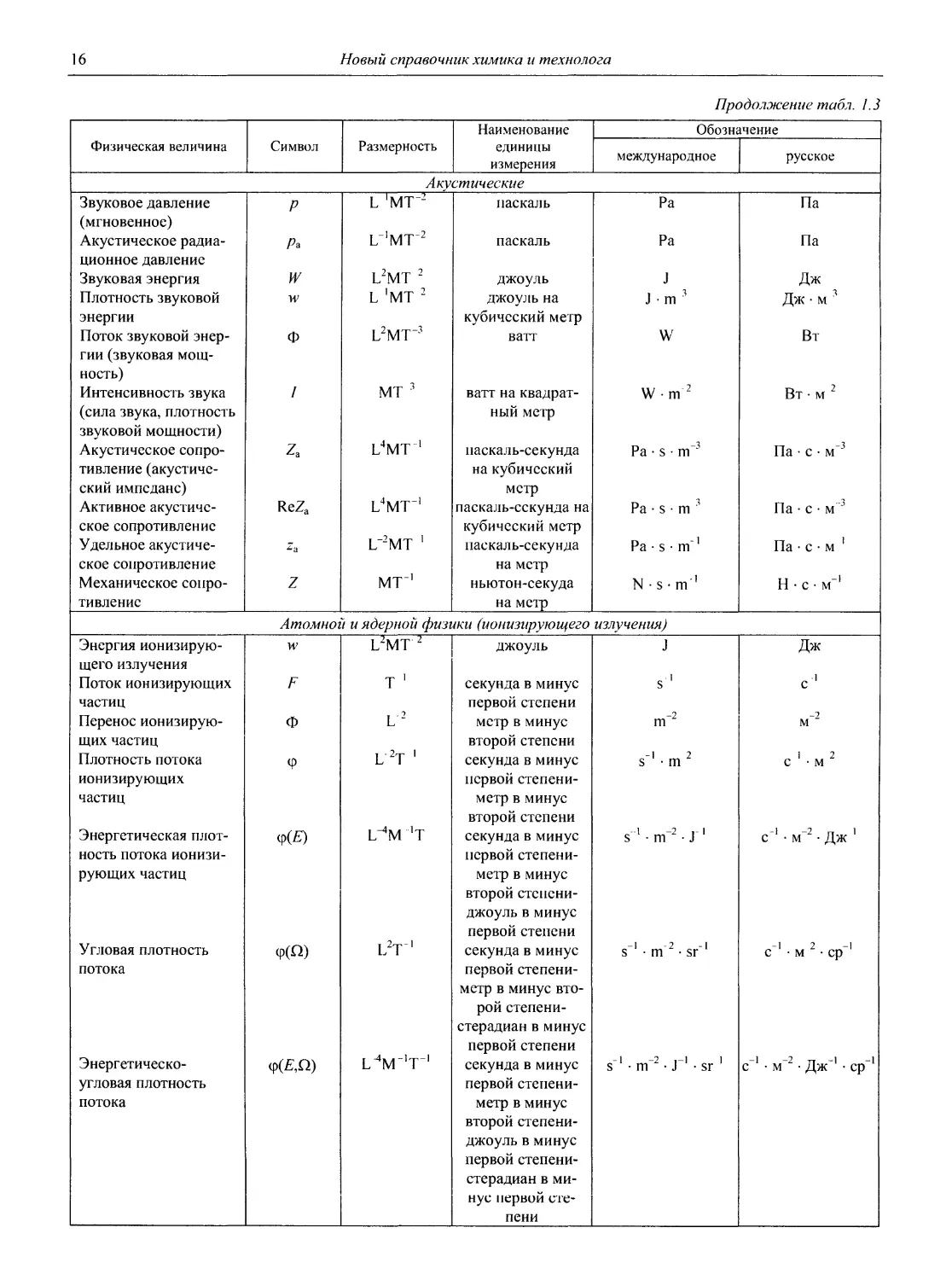
Акустические
Мгновенное колебательное смещение частицы Колебательное смещение частицы Пиковое колебательное смещение частицы Мгновенная колебательная скорость частицы Колебательная скорость частицы Объемная скорость Скорость звука(мгновенная) Статическое давление г о Лпах vK = drldt (V) Vjz V & L L L LT1 LT”1 LI1 LT”' L 'MT 2 метр метр метр метр в секунду метр в секунду кубический метр в секунду метр в секунду паскаль m m m m • s’1 m • s”' 3 -1 m • s m • s”1 Pa м м м м • с”' м • с’1 м3 • с”1 м • с 1 Па
16
Новый справочник химика и технолога
Продолжение табл. 1.3
Физическая величина Символ Размерность Наименование единицы измерения Обозначение
международное русское
Акустические
Звуковое давление (мгновенное) Акустическое радиационное давление Звуковая энергия Плотность звуковой энергии Поток звуковой энергии (звуковая мощность) Интенсивность звука (сила звука, плотность звуковой мощности) Акустическое сопротивление (акустический импеданс) Активное акустическое сопротивление Удельное акустическое сопротивление Механическое сопротивление Р Р* JT W Ф / 4 ReZa Z L 'МТ”2 L”'MT”2 l2mt 2 L 'МТ 2 L2MT”3 МТ 3 L4MT L4MT”' L”2MT 1 MT”1 паскаль паскаль джоуль джоуль на кубический метр ватт ватт на квадратный метр паскаль-секунда на кубический метр паскаль-сскунда на кубический метр паскаль-секунда на метр ньютон-секуда на метр Ра Ра J , 3 J • m W W • m 2 Ра • s • m”3 Ра • s • m ’ Pa • s • m‘1 N • s • m'1 Па Па Дж Дж • м 3 Вт Вт • м 2 Па • с • м”3 Па • с • м ’ Па • с•м 1 Н • с • м”1
Атомной и ядерной физики (ионизирующего излучения)
Энергия ионизирующего излучения Поток ионизирующих частиц Перенос ионизирующих частиц Плотность потока ионизирующих частиц Энергетическая плотность потока ионизирующих частиц Угловая плотность потока Энергетическо-угловая плотность потока W F Ф <Р <р(Е) (p(Q) <p(E,Q) L2MT 2 T 1 L 2 L 2T 1 l 4m 't l2t_| L^M-'T”1 джоуль секунда в минус первой степени метр в минус второй степени секунда в минус первой степени-метр в минус второй степени секунда в минус первой степени-метр в минус второй стспени-джоуль в минус первой степени секунда в минус первой степени-метр в минус второй степени-стерадиан в минус первой степени секунда в минус первой степени-метр в минус второй степени-джоуль в минус первой степени-стерадиан в минус первой степени J s' m”2 s”1 • m 2 s ' • m”2 • J"1 s”1 • m"2 • sr”1 s”1 • m”2 • J”1 • sr 1 Дж с 1 м”2 с 1 • м 2 с"1 • м”2 • Дж 1 с”1 • м 2 • ср”1 с”1 • м”2 • Дж”1 • ср”1
Общие сведения
17
Продолжение табл. 1.3
Физическая величина Символ Размерность Наименование единицы измерения Обозначение
международное русское
Поток ионизирующего излучения л.. LMT 3 ватт W Вт
Перенос энергии ионизирующего излучения Фи МТ 2 джоуль на квадратный метр J • m 2 Дж • м 2
Плотность потока ионизирующего излучения Фи мт 3 ватг на квадратный метр W • m 2 Вт • м 2
Сечение <5 L2 квадратный метр m“ м2
Сечение взаимодействия ионизирующих частиц о, L2 квадратный метр m2 м2
Полное сечение взаимодействия ионизирующих частиц <5 L2 квадратный метр m2 м2
Макроскопическое сечение взаимодействия ионизирующих частиц X, L’1 метр в минус первой степени m 1 м’1
Линейный коэффициент ослабления ц L 1 метр в минус первой степени m 1 М '
Массовый коэффициент ослабления Цт L2M-1 квадратный метр на килофамм m -kg 2 -1 м • кг
Атомный коэффициент ослабления Ца L2 квадратный метр m2 м2
Линейный коэффициент передачи энергии Ц/г L’1 метр в минус первой степени m”1 м’1
Массовый коэффициент передачи энергии №/г,т L2M ' квадратный метр на килограмм m2•kg 1 м2 • кг 1
Линейный коэффициент поглощения энергии L 1 метр в минус первой степени m 1 м”1
Массовый коэффициент поглощения энергии l2m квадратный метр на килограмм m2•kg 1 м2 • кг"1
Поглощенная доза ионизирующего излучения D L2t-2 грей Gy Гр
Мощность поглощенной дозы излучения Ь l2t 3 грей в секунду Gy • s’1 Гр • с"1
Керма К L2t-2 грей Gy Гр
Мощность кермы к L2T”3 грей в секунду Gy • s 1 Гр • с 1
Экспозиционная доза фотонного излучения X M 'TI кулон на килограмм C kg-' Кл • кг”1
Мощность экспозиционной дозы фотонного излучения X M ’1 ампер на килограмм A • kg’1 А • кг”1
Эквивалентная доза ионизирующего излучения н l2t-2 зиверт Sv Зв
Мощность эквивалентной дозы ионизирующего излучения н l2t-3 зиверт в секунду Sv • s'1 Зв • с’1
18
Новый справочник химика и технолога
Окончание табл. 1.3
Физическая величина Символ Размерность Наименование единицы измерения Обозначение
международное русское
Атомной и ядерной физики (ионизирующего излучения)
Активность радионуклида (изотопа) в источнике А Т1 беккерель Bq Бк
Удельная активность источника Ат м-'т-1 беккерель на килограмм Bq • kg’1 Бк • кг”1
Объемная активность источника Ау L 3Т"‘ беккерель на кубический метр Bq • m 3 Бк • м ’’
Молярная активность источника Ат Т 'N’1 беккерель на моль Bq • mol”1 Бк • моль”1
Поверхностная активность источника А, l2t-' беккерель на квадратный метр Bq • m 2 Бк • м 2
Постоянная мощность воздушной кермы (керма-постоянная) г5 L4t 2 грей-метр в квадрате на секунду-беккерель Gy • m2 • s’1 • Bq 1 Гр • м2 • с’1 • Бк”1
Керма-эквивалент источника ке l4t-3 грей-метр в квадрате в секунду Gy • m2 • s 1 Гр • м2•с 1
Постоянная радиоактивного распада радионуклида X Т 1 секунда в минус первой степени s 1 с 1
Средняя продолжительность жизни радионуклида т т секунда s с
Период полраспада ТС2 т секунда s с
Таблица 1.4
Внесистемные единицы, допускаемые к применению наряду с единицами СИ (ГОСТ 8.417-2002)
Наименование величины Единица Соотношение с единицей СИ
наименование обозначение
международное русское
Масса тонна t T 103 кг
атомная единица массы и a. e. m. 1,66 057 • 10 27 кг*
Время минута min мин 60 с
час h 4 3600 с
сутки d сут 86 400 с
Плоский угол градус О о (тс/180) рад = 1,745 329-• 10”2 рад
минута t t (д/10 800) рад = = 2,908 882... • Ю^рад
секунда ff If (л/64 8 000) рад = = 4,848 137... • 10* рад
Объем, вместимость литр 1 Л 10’3 м3
Длина астрономическая единица u. a. a. e. 1,495 98 • 1011 м*
световой год ly св. год 9,4605 • 1015 м*
парсек PC ПК 3,0857 • 101бм*
Оптическая сила диоптрия дптр 1 м”1
Площадь гектар ha га 104 м2
Энергия электрон-вольт eV эВ 1,60 219- 1019Дж*
Полная мощность вольт-ампер VA ВА
Реактивная мощность вар var вар
Приближенные данные.
Общие сведения
19
Таблица 1.5
Соотношения между единицами физических величин
Наименование единицы Обозначение Соотношение с единицей СИ
международное русское
Длина
Ангстрем Астрономическая единица Дюйм Икс-единица Кабельтов Микрон Миля морская Миля сухопутная Парсек Световой год Ферми Фут Ярд А и. а. in А М п. mile mile PC •у ft yd A a. c. ИКС-СД. MK ПК св. год 1 • 10 10м = 0,1 нм 1,495 978 70- 10й м 0,0254 м 1,002 06- 10”13м 185,2 м 1 • 10*м 1852 м 1609,344 м 3,085 678- 10,6 м 9,460 530 • 1015 м 1 • 10”15м 0,3048 м 0,9144 м
Площадь
Ар Барн Г ектар Квадратный дюйм Квадратный фут Квадратный ярд Акр ar b ha in2 ft2 yd2 acre ap 6 ra акр 100 м2 1 • 10”28м2 1 • 104 м2 6,4516 • 10"4 м2 9,290 30 • 1О”2м2 0,836 127 м2 4046,86 м2
Объем, вместимость
Баррель английский (для сыпучих веществ) Баррель нефтяной (США) Баррель сухой (США) Бушель (Великобритания) Бушель (США) Галлон (Великобритания) Галлон для жидкостей (США) Галлон для сыпучих веществ (США) Дюйм кубический Литр Лямбда Пинта(Великобритания) Пинта для жидкостей (США) Пинта для сыпучих веществ (США) Унция (Великобритания) Унция (США) Фут кубический Ярд кубический bbl (US) bu gal (UK) gal (US) in3 1, L T pt (UK) liq pt (US) dry pt (US) fl oz (UK) fl oz (US) ft3 yd3 л T 0,163 65 м3 0,158 988 м3 0,115 628 м3 3,636 87- 10 2 м3 3,523 93 • 10"2м3 4,546 09 • 10 3 м3 3,785 43 • 10 3м3 4,405 • 10 3 м3 1,638 71 • 10"5м3 1 • 10 3м3 1 • 10"9м3 5,682 61 • 10 4 м3 4,431 79- 10’4 м3 5,506 14- 10"4 м3 2,841 • 10 5 м3 2,957 37- 10”5м3 2,831 67 • 10 2 м3 0,764 55 м3
Объемный расход
Кубический дециметр в секунду dm3 • s 1 3 --1 ДМ • c 1 • 10 J mj • с '
20
Новый справочник химика и технолога
Продолжение табл. 1.5
Наименование Обозначение Соотношение
единицы международное русское с единицей СИ
Объемный расход
Кубический сантиметр в секунду Кубический метр в час Литр в минуту Кубический дюйм в секунду Кубический фут в секунду Литр в час ст3 • s 1 т3 • h’1 1 • min 1 in3 • s 1 ft3 • s’1 1-h’1 3 -1 CM • c 3 1 M • 4 л • мин’1 Л • 4 1 1 - Ю^м3 • с 1 0,277 78- 10’3 м3 • с’1 1,6667- 10 5 м3-с 1 1,6387- 105м3-с4 0,028 316 8 м3 - с 1 2,77(7)- 10“8 м3 • с’1
Массовый расход
Килограмм в минуту Килограмм в час kg • min 1 kg • h 1 кг • мин 1 кг • ч’1 1,6667- 10’2кг-с-1 2,7778- 10 3 кг-с 1
Плоский угол
Град, гон Градус Минута Оборот (полный угол) Прямой угол Румб в метеорологии Румб в морской навигации Секунда g о r r L ft град О f об L fl л/200 = 0,015 707 96 рад 0,017 453 29 рад 2,908 882 • 10 4 рад 2л рад = 6,283 185 рад 1,570 796 рад 0,392 699 рад 0,196 349 5 рад 4,848 137 • 10”6рад
Телесный угол
Квадратный градус Полный телесный угол ...□° Q ...□° Q 3,0462 • 10 4 ср 4л ср = 12,566 37 ср
Время
Год Минута Сутки Час a min d h год мин суг ч 3,155 692 597 47 • 107 с (на 1900 г.) 60 с 86 400 с 3600 с
Температура
Градус Ранкина °Ra °Ra 0,556 К = - К 9
Градус Реомюра Градус Фаренгейта °R °F °R °F 1,25 К 0,556 К = - К 9
Градус Цельсия °C °C 1 К
Скорость
Километр в час Миля в час Узел морской Фут в секунду km • h’1 mile • h”1 kn ft-s’1 км • ч 1 УЗ 0,277 78 м • с’1 0,447 04 м • с’1 0,514 444 м • с ’1 0,3048 м • с’1
Ускорение
Гал Gal Гл 0,01 м • с-2
Угловая скорость
Градус в секунду Оборот в минуту Оборот в секунду Прямой угол в секунду Радиан в минуту ° • s’1 r • min-1 r • s~’ L • s’1 rad • min 4 ° • с-1 об • мин-1 об • с”1 L • с 1 рад • мин’1 0,017 453 3 рад-с’1 0,104 719 7 рад • с”1 6,283 185 рад • с”1 1,570 80 рад • с”1 0,016(6) рад • с-1
Угловое ускорение
Градус на секунду в квадрате ...° • s 2 ...° • с 2 0,017 453 3 рад • с 2
Общие сведения
21
Продолжение табл. 1.5
Наименование единицы Обозначение Соотношение с единицей СИ
международное русское
Оборот на секунду _э Г • S “ об • с”2 6,283 185 рад • с 2
в квадрате
Оборот на минуту г • min 2 об • мин 2 0,104 719 7 рад-с”1
в квадрате
Частота вращения
Оборот в секунду Г • S 1 об • с 1 1 с”1
Оборот в минуту г • min 1 об • мин”1 0,016 66 с 1
Масса
Атомная единица массы и а. с. м. 1,660 538 86(28)- 10 '27 кг
Гамма Y — 1 • 10 9 кг
Грамм g г 1-10” кг
Гран gr — 6,479 891 • 10”5 кг
Карат — кар 2• 10 4 кг
Слаг slug — 14,5939 кг
Килограмм-сила-сскунда — кге • с2 • м 1 9,806 65 кг
в квадрате на метр
Тонна t т 1000 кг
Тонна (брит.) ton — 1016,05 кг
Тонна короткая (брит.) sh.ton — 907,185 кг
Унция аптекарская oz apoth — 31,1035 • 10 3 кг
Унция аптекарская русская — — 2,986 • 10 2 кг
У нция торговая oz — 28,3495 • 10”3 кг
Унция тройская oz tr — 31,1035 • 10 3 кг
Фунт торговый lb — 0,453 592 37 кг
Фунт в системе русских — — 0,409 512 41 кг
мер
Фунт (США) Ib(US) — 0,453 592 427 7 кг
Центнер, кратная q ц 100 кг
единица СИ Центнер (брит.) cwt — 50,8023 кг
Центнер короткий (брит.) sh.cwt — 45,3592 кг
Плотность
Грамм на кубический g • in'3 — 61,0 кг • м J
дюйм
Грамм на кубический g • m 3 г • м ’ 1 • 10”3 кг • м 3
метр
Грамм на кубический g • cm” г • см"3 1 • 103кг- м”3
сантиметр
Килограмм-сила-секунда kgf • s2 • m”4 кге • с2 • м 4 9,80665 кг • м”3
в квадрате на метр в четвертой степени Тонна на кубический t • m” т • м”3 1 • 103 кг-м 3
метр
Грамм на кубический фут g-ft3 — 3,53 • 10”2 кг-м”3
Грамм на литр g Г’ г • л 1 1
Унция на кубический oz • in 3 — 1,73 • 103 кг • м”
дюйм
Унция на кубический oz • cm 3 — 2,835 • 104кг- м 3
сантиметр
Унция на кубический фут oz • ft”3 — 1,0014 кг • м”3
Фунт на кубический фут lb • ft”3 — 16,0185 кг-м”3
Линейная плотность
Текс текс 1 • 10”6 кг/мН*
22
Новый справочник химика и технолога
Продолжение табл. 1.5
Наименование единицы Обозначение Соотношение с единицей СИ
международное русское
Сила
Дина Килограмм-сила Килопонд Паундаль Понд Стен Тонна-сила Фунт-сила dyn kgf kp pdl P sn Ibf ДИН кге CH тс 1 • 10”5 Н 9,806 65 Н* 9,806 65 Н* 0,138 255 Н* 9,806 65 • 10 3Н* 1 • 103 Н 9,806 65 • 103Н* 4,448 22 Н
Поверхностное натяжение
Килограмм-сила на метр kgf • m 1 кге • м 1 9,806 65 Н • м 1
Давление
Атмосфера Атмосфера техническая (килограмм-сила на квадратный сантиметр) Бар Дина на квадратный сантиметр Дюйм водяного столба Дюйм ртутного столба Килограмм-сила на квадратный метр Килограмм-сила на квадратный миллиметр Килопонд на квадратный санти метр Миллиметр водяного столба Миллиметр ртутного столба Паундаль на квадратный фут Пьеза Тонна-сила на квадратный метр Торр Фунт-сила на квадратный дюйм Фут водяного столба atm at bar dyn • cm’2 in H2O in Hg kgf • m 2 kgf • mm"2 kp • cm 2 mm H2O mm Hg pdl • ft 2 pz tf • m-2 torr Ibf • in-2 ft H2O атм ат бар дин•см 2 кге • м 2 кге • мм”2 мм вод. ст. мм рт. ст. из тс • м”2 1,013 25 • 105Па* 9,806 65 • 104Па* 1 • 105 Па 0,1 Па 249,089 Па 3386,39 Па 9,806 65 Па* 9,806 65 • 106Па 9,806 65 • 104 Па* 9,806 65 Па* 133,322 Па 148816 Па 1 • 103 Па 9,806 65 • 103 Па* 133,322 Па 6894,76 Па 2989,07 Па
Импульс (количество движения)
Г рамм-сантиметр в секунду Килограмм-сила-секунда Тонна-метр в секунду g • cm • s 1 kgf - s г • см • с 1 кге • с т • м • с”1 1 • 10 5 кг • м • с 1 9,806 65 Ki • м • с”1 1 • 103 кг • м • с”1
Импульс силы
Килограмм-сила-секунда kgf - s кге • с 9,806 65 Н • с
Момент силы
Дина-сантиметр Килограмм-сила-метр Килопонд-метр Стен-метр Фунт-сила-фут dyn • cm kgf • m kp • m sn • m Ibf - ft дин • см кге • м сн • м 1 • 10”7Н-м 9,806 65 Н • м* 9,806 65 Н • м* 1 • 103 Н • м 1,355 82 Н • м
Общие сведения
23
Продолжение табл. 1.5
Наименование Обозначение Соотношение
единицы международное русское с единицей СИ
Момент инерции
Грамм-сантиметр в квадрате Килограмм-сила-секунда в квадрате на метр g- cm2 kgf • s2 • m”1 2 г • CM КГС • c2• M 1 1 • 10 7 кг • м2 9,806 65 кг • м2
Момент импульса (момент количества движения)
Г рамм-квадратный сантиметр на секунду Килограмм-сила-метр-секунда Тонна-метр в квадрате на секунду 2 -1 g • cm • s kgf -ms 2 „ 1 Г•CM •c КГС • M • c 2 -1 T • M • c 1 • 10 7 кг • м2 • с 1 9,806 65 кг • м2 • с 1 1 • 103 кг • м2 • с 1
Напряжение (механическое)
Килограмм-сила на квадратный миллиметр Килопонд на квадратный миллиметр kgf • mm 7 kp • mm 2 2 КГС • MM 9,806 65 • 106Па* 9,806 65 • 106Па*
Работа, энергия
Ватг-час Киловатт-час Килограмм-сила-метр Килопонд-метр Литр-атмосфера Лошадиная сила-час Ридберг Фут-фунт-сила Фут-паундаль Электрон-вольт Эрг W • h kW • h kgf • m kp • m Ry ft - Ibf ft • pdl eV erg Вт • ч кВт • ч кге • м л • атм л.с. • ч эВ эрг 3600 Дж 3,6 • 106 Дж 9,806 65 Дж 9,806 65 Дж 101,328 Дж 2,647 80- 106Дж 2,1796 • 10 18Дж= 13,60 эВ 1,355 82 Дж 0,042 140 1 Дж 1,602 177 33 • 10’19Дж 1 • 10 7 Дж
Удельная работа технологических аппаратов
Лошадиная сила-час на килограмм л.с. • ч • кг 1 2,647 80- 106 Дж-кг 1
Мощность
Калория в секунду Килограмм-сила-метр в секунду Лошадиная сила Лошадиная сила (Брит.) Фут-паундаль на секунду Фут-фунт-сила на секунду Эрг в секунду cal • s 1 kgf• m • s 1 hp ft • pdl • s 1 ft - Ibf - s’1 erg • s 1 кал • с 1 кге • м • с "1 л.с. ЭРГ • с~' 4,1868 Вт 9,806 65 Вт 735,499 Вт 745,700 Вт 0,042 140 1 Вт 1,355 82 Вт 1 • 10”7 Вт
Динамическая вязкость
Килограмм-сила-секунда на квадратный метр Паундаль-секунда на квадратный фуг Пуаз Фунт-сила-секунда на квадратный фут kgf•s • m 2 pdl • s • ft”2 P Ibf - s • ft2 -2 КГС -с-м п 9,806 65 Па • с 1,488 16 Па - с 0,1 Па-с 47,8803 Па • с
Кинематическая вязкость
Квадратный метр на час Квадратный фут на секунду Квадратный фут на час m2 - h 1 ft2 • s 1 ft2 • h’1 2 1 м • ч 2,777- 10’4 м2-с 1 0,092 903 м2- с”1 2,580 64 • 10“5 м2- с”1
24
Новый справочник химика и технолога
Продолжение табл. 1.5
Наименование Обозначение Соотношение
единицы международное русское с единицей СИ
Кинематическая вязкость
Стокс St Ст 1 • 10”4 м2 • с”1
Ударная вязкость
Эрг на квадратный сантиметр erg • cm 2 эрг•см 2 1 • 10 3 Дж • м”2
Текучесть
Пуаз в минус первой степени Р”1 П'1 10 Па 1 • с”1
Количество теплоты
Британская тепловая единица Калория международная Калория пятнадцатиградусная Калория термохимическая Термия Эрг Btu cal cal 15 th erg кал кал]5 кал1х эрг 1,055 06- 103 Дж 4,1868 Дж* 4,1855 Дж 4,1840 Дж 4,1868- 103Дж 1 • 10”7Дж
Теплоемкость. Энтропия
Калория на градус Цельсия Эрг на кельвин cal • °C 1 erg • K”1 кал • °C 1 эрг • К”1 4,1868 Дж-К 1 1 • 10 7 Дж - К”1
Удельная теплоемкость
Калория на грамм-градус Цельсия Килокалория на килограмм-градус Цельсия Эрг на грамм-кельвин cal • g"1 • °C 1 kcal • kg 1 • °C’1 erg • g”1 • К 1 кал • г”1 • °C”1 ккал • кг”1 • °C 1 эрг • г”1 • К”1 4,1868- 103 Дж • кг”1 • К 1 4,1868- 103 Дж-кг”1-К 1 1-10”4 Дж-кг’-К”1
Молярная теплоемкость. Молярная энтропия
Калория на моль-градус Цельсия cal • mol 1 • °C 1 кал • моль 1 • °C 1 4,1868 Дж • моль"1 • К”1
Тепловой поток
Калория в секунду Килокалория в час Эрг в секунду cal • s ’1 kcal • h”1 erg • s'1 кал • с”1 ккал • ч 1 эрг • с”1 4,1868 Вт 1,163 Вт 1 • 10”7Вт
Теплопроводность
Британская тепловая единица в секунду на фут-градус Фаренгейта Калория в секунду на сантиметр-градус Цельсия Килокалория в час на метр-градус Цельсия Эрг в секунду на сантиметр-градус Цельсия Btu •s 1 • ft"1 • degF ! cal • s”1 • cm 1 • °C"1 kcal • h”1 • m 1 • °C"1 erg • s”1 • cm”1 • °C”1 кал • с"1 • см 1 • °C 1 ккал • ч"1 • м”1 • °C”1 эрг • с”1 • см”1 • °C”1 6,230 64- 10 3 В т • м ”1 • К”1 4,1868- 102 Вт-м'-К”1 1,163 Вт -м”1 - К 1 1 • 10"5 Вт - м”1 -КГ1
Электричество и магнетизм Электрический заряд
Фарадей Франклин Ампер-час F Fr Ah Ф Фр А • ч 96 484,56 Кл 3,335 64- Ю”10Кл 3,6- 103Кл
Электрический момент
Дебай D д 3,335 64- 1О”зоКл-м
Общие сведения
25
Продолжение табл. 1.5
Наименование Обозначение Соотношение
единицы международное русское с единицей СИ
Напряженность электрического поля
Вольт на сантиметр Киловольт на сантиметр V • ст kV • ст В • см кВ • см 100В • м 1 • 105 В • м
Плотность электрического тока
Ампер на квадратный миллиметр А • тт 2 А • мм 2 1 • 106А-м”2
Удельное электрическое сопротивление
Ом-квадратный миллиметр на метр Ом-сантиметр Q • тт2 • т 1 Q • ст Ом • мм2 • м 1 Ом • см 1 • 10"6 Ом • м 0,01 Ом • м
Удельная электрическая проводимость
Ом в минус первой сте-пени-сантиметр в минус первой степени Метр на ом-квадратный миллиметр Q 1 • ст 1 т • Q 1 • тт"2 Ом 1 • см 1 м•Ом1 •мм2 100 См • м"1 1 • 106См-м-1
Магнитная индукция
Гаусс Вебер на квадратный сантиметр Gs Wb • cm"2 Гс Вб • см"2 1 • 104 Тл 1 • 104Тл
Магнитный поток
Максвелл Мх Мкс 1 • 10"8 Вб
Напряженность магнитного поля
Ампер на сантиметр Ампер-виток на сантиметр Эрстед А • cm 1 Ое А • см 1 Ав • см"1 Э 100 А -м”1 100 А • м"1 79,5775 А • м"1
Магнитодвижущая сила. Разность магнитных потенциалов
Ампер-виток Гильберт Gb Ав Гб 1 А 0,795775 А
Акустика Звуковое давление
Дина на квадратный сантиметр dyn • cm'2 дин • см 2 0,1 Па
Акустическое сопротивление
Дина-секунда на сантиметр в пятой степени dyn • s • cm 5 дин • с • см 5 1 • 105 Па • с • м"3
Удельное акустическое сопротивление
Дина-секунда на сантиметр в кубе dyn • s • cm 3 -3 дин • с • см 10 Па • с • м 1
Механическое сопротивление
Дина-секунда на сантиметр dyn • s • cm 1 дин • с • см 1 1 • 10"3 Нс- м"1
Звуковая энергия
Эрг erg эрг 1 • 10“7 Дж
Плотность звуковой энергии
Эрг на кубический сантиметр -3 erg • cm -3 эрг • см 0,1 Дж • м 3
Поток звуковой энергии. Мощность звуковой энергии
Эрг в секунду erg • s 1 ЭРГ с"1 1 • 10’7 Вт
Интенсивность звука
Эрг в секунду на квадратный сантиметр erg • s 1 • cm 2 эрг • с 1 • см 2 1 • 10"3 Вт • м"2
26
Новый справочник химика и технолога
Продолжение табл. 1.5
Наименование единицы Обозначение Соотношение с единицей СИ
международное русское
Объемная скорость
Кубический сантиметр в секунду 3 -1 ст • s см3 • c 1 1 • 106м3-с'
Оптика Сила света
Свеча CB 1,005 кд
Световая энергия
Люмен-час 1т • h ЛМ • 4 3,6 • 10 3 лм • с
Светимость
Радфот radph радфот 1 • 104 лм • м 2
Освещенность
Фот ph Фот 1 • 104лк
Яркость
Стильб Апостильб Ламберт sb Asb L Сб Асб Лб 1 • 104 кд • м 2 0,319 кд • м”2 3,19- 103кдм”2
Световая экспозиция
Фот-секунда phs фот • с 1 • 104 лк • с
Объемная плотность световой энергии
Люмен-секунда на кубический сантиметр In • s • cm 3 ЛМ •с•см 3 1 • 106 лм • с • м 3
Энергия излучения
Эрг erg эрг 1 • 10”7 Дж
Поток излучения
Эрг в секунду erg • s”1 эрг • с 1 1 • 10”7Вт
Сила излучения
Эрг в секунду на стерадиан erg • s 1 • sr 1 эрг • с 1 • ср 1 1 • 10”7 Вт • ср”1
Энергетическая светимость. Энергетическая освещенность. Облученность
Эрг в секунду на квадратный сантиметр erg • s 1 • cm 2 эрг • с 1 • см 2 1 • 10”3 Вт • м”2
Энергетическое освечивание
Эрг на стерадиан erg • sr”1 эрг • ср”1 1 • 10”7Дж • ср”1
Энергетическая экспозиция
Эрг на квадратный сантиметр erg • cm 2 эрг • см 2 1 • 10”3 Дж • м”2
Энергетическая яркость
Эрг в секунду на стера-диан-квадратный сантиметр erg • s 1 • sr 1 • cm 2 эрг • с 1 • ср 1 • см 2 1 • 10”3 Вт • ср”1 • м’2
Объемная плотность силы излучения
Эрг в секунду на стера-диан-кубический сантиметр -1 -1 -3 erg • s • sr cm эрг • с 1 • ср 1 • см 3 0,1 Вт • ср 1 • м 3
Интегральная энергетическая яркость
Эрг на стерадиан-квадратный сантиметр erg • sr”1 • cm”2 эрг • ср 1 • см 2 1 • 10”3 Дж • ср”1 • м”2
Ионизирующее излучение Поглощенная доза ионизирующего излучения. Керма
Рад rad рад 1 • 10~2 Гр
Мощность поглощенной дозы ионизирующего излучения. Мощность кермы
Рад в секунду Грей в минуту rad • s 1 Gy • min”1 рад • с 1 Гр • мин”1 1 • 10”2 Гр • с”1 1,666 • 10”2 Гр • с”1
Общие сведения
27
Окончание табл. 1.5
Наименование единицы Обозначение Соотношение с единицей СИ
международное русское
Эквивалентная доза ионизирующего излучения
Бэр rem бэр 1 • 10’2 Зв
Мощность эквивалентной дозы ионизирующего излучения
Бэр в секунду rem • s’1 бэр • с 1 1 • 10’2 Зв • с"1
Микрозиверт в час pSv • h’1 мкЗв • ч”1 0,277 77 • Ю 93в - с 1
Экспозиционная доза фотонного излучения
Рентген R р 2,579 76 • 10 4 Кл • кг’1
Активность радионуклида в источнике
Кюри Ci Ки 3,70 • 1О10 Бк
Удельная активность источника
Кюри на килограмм Ci/kg"1 Ки • кг 1 3,70- Ю^Бккг’1
Поверхностная активность источника
Кюри на квадратный сантиметр Ci • cm 2 Ки • см 2 3,70- 1014 Бк • м”2
Объемная активность источника
Кюри на литр Ci • L’1 Ки • л 1 3,70 • 1013 Бк • м’3
Молярная активность источника
Кюри на моль Ci • mol 1 Ки • моль 1 3,70- 1010 Бк -моль’1
* Точные данные.
Приведенное соотношение между калорией и джоулем установлено 5-й Международной конференцией по свойствам водяного пара и является определением Международной калории.
Таблица 1.6
Множители и префиксы, используемые для образования наименований десятичных кратных и дольных единиц измерения физических величин
Множитель Префикс Буквенное обозначение Множитель Префикс Буквенное обозначение
международное русское международное русское
1024 иотта Y 10’1 деци d Д
1021 зетга Z 10’2 санти с С
1018 экса Е Э 10’3 милли m м
1015 пета Р П 104’ микро Р мк
1012 тера Т т 10’9 нано п н
109 гига G г 10’12 ПИКО Р п
106 мега М м 10’15 фемто f ф
103 кило к к Ю-is атто а а
102 гекто h г IO’21 зепто Z
101 дека da да 10’24 иокго У
Литература
Чертов А.Г. Физические величины (терминология, определения, обозначения, размерности, единицы). М.: Высшая школа, 1990. 335 с.
Раздел 2. СТРОЕНИЕ ВЕЩЕСТВА
Составители: к. х. н., доц. М.Ю. Скрипкин, А.А. Четвериков
2.1. Строение элементарных частиц
В табл. 2.1 содержатся сведения о свойствах основных элементарных частиц и соответствующих античастиц. В нее не включены короткоживущие частицы — резонансы, а также промежуточные векторные бозоны и глюоны. Массы покоя частиц и их заряды даны в единицах массы покоя электрона (9,11 • 10“31 кг) и заряда электрона (1,60 • 10~19Кл).
Спин — одна из основных характеристик элементарных частиц. Он может быть представлен (в некотором приближении) как момент собственного количества движения частицы (вращения вокруг собственной оси).
Странность — одна из характеристик элементарных частиц, не имеющая аналогов в макромире. Введена для объяснения протекания процессов распада элементарных частиц (при сильных взаимодействиях странность сохраняется, а при слабых — нет).
Барионный заряд — одна из характеристик элементарных частиц. Он равен единице для барионов, минус единице — для антибарионов, нулю — для лептонов и мезонов.
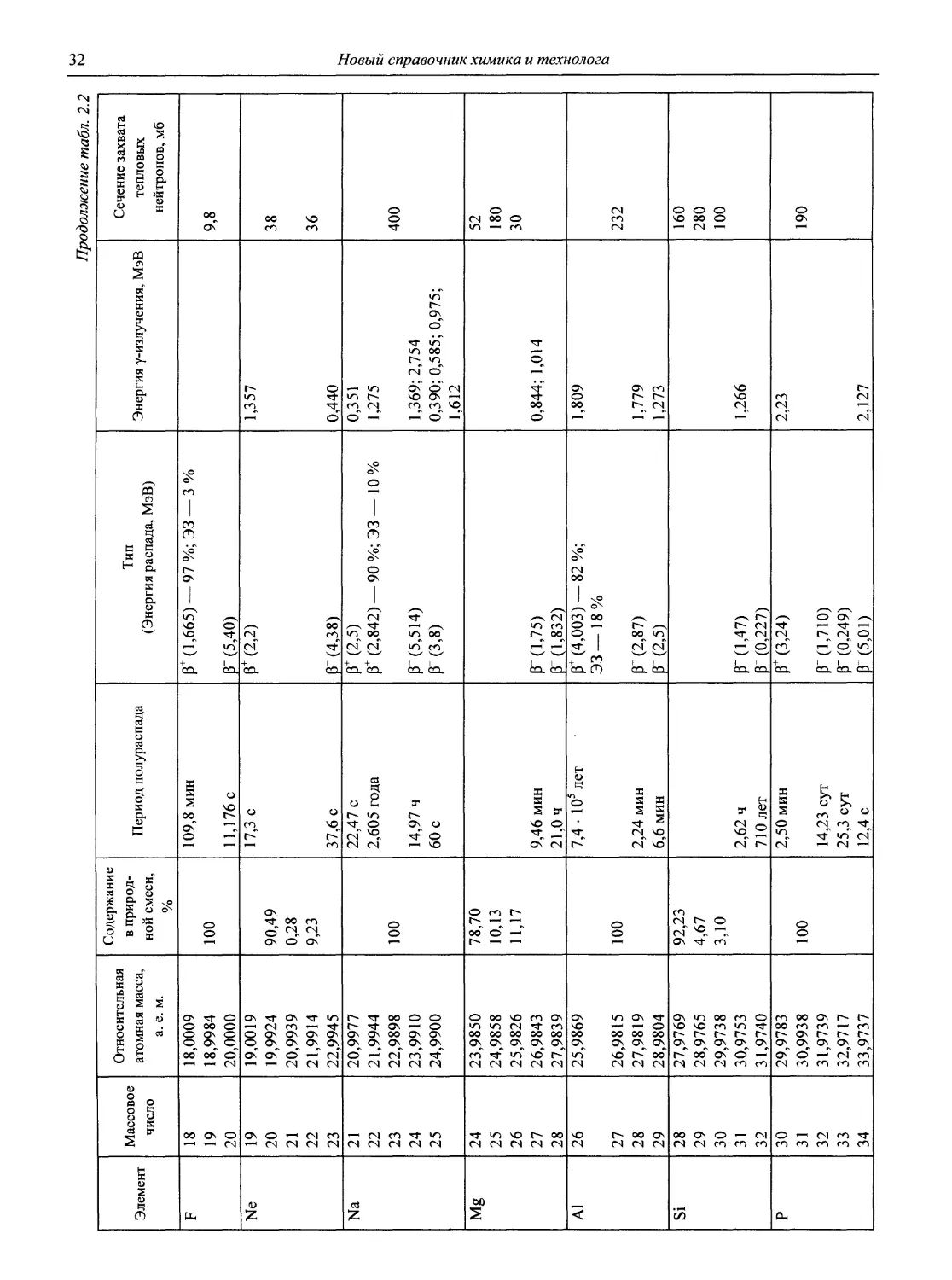
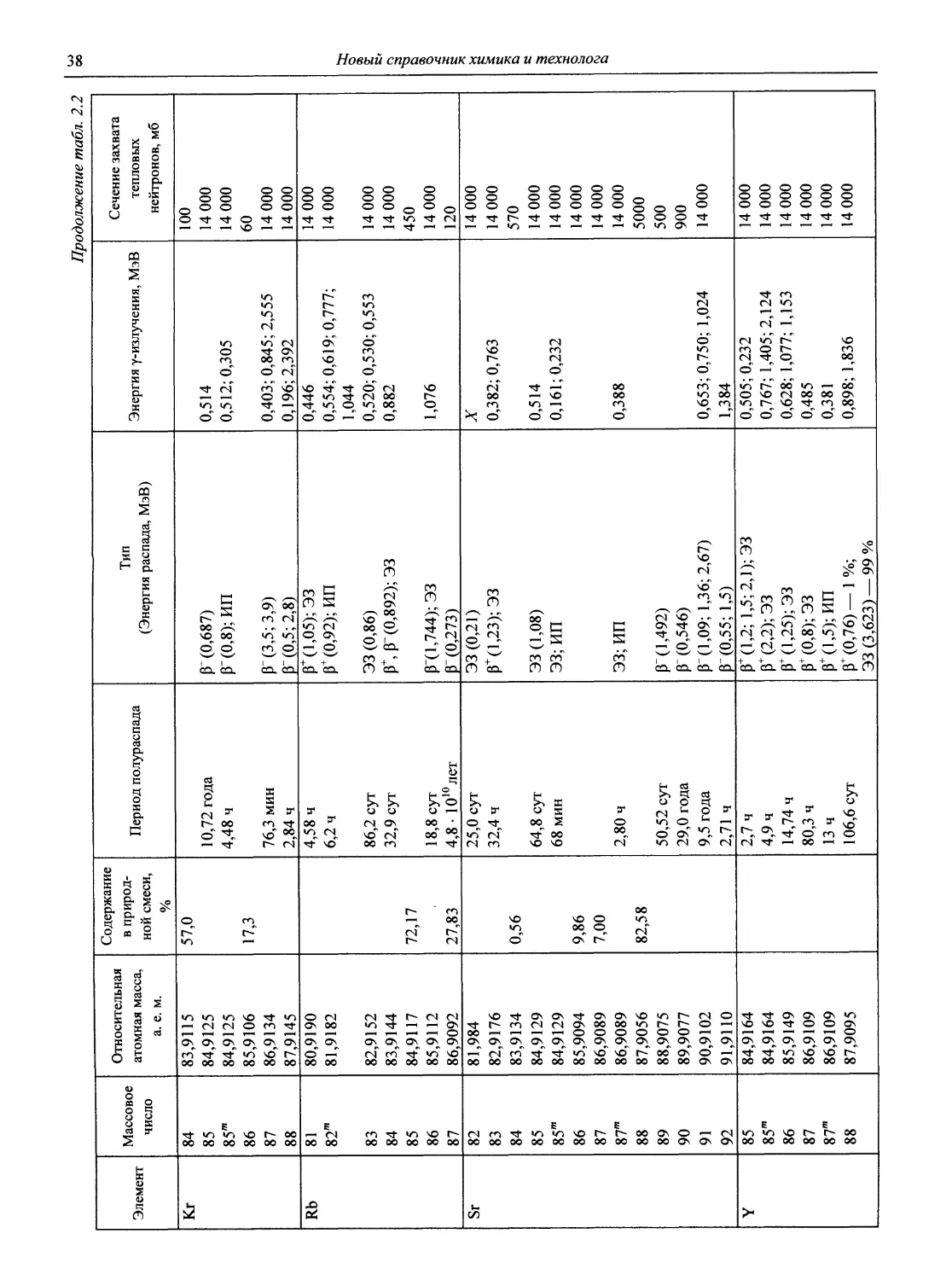
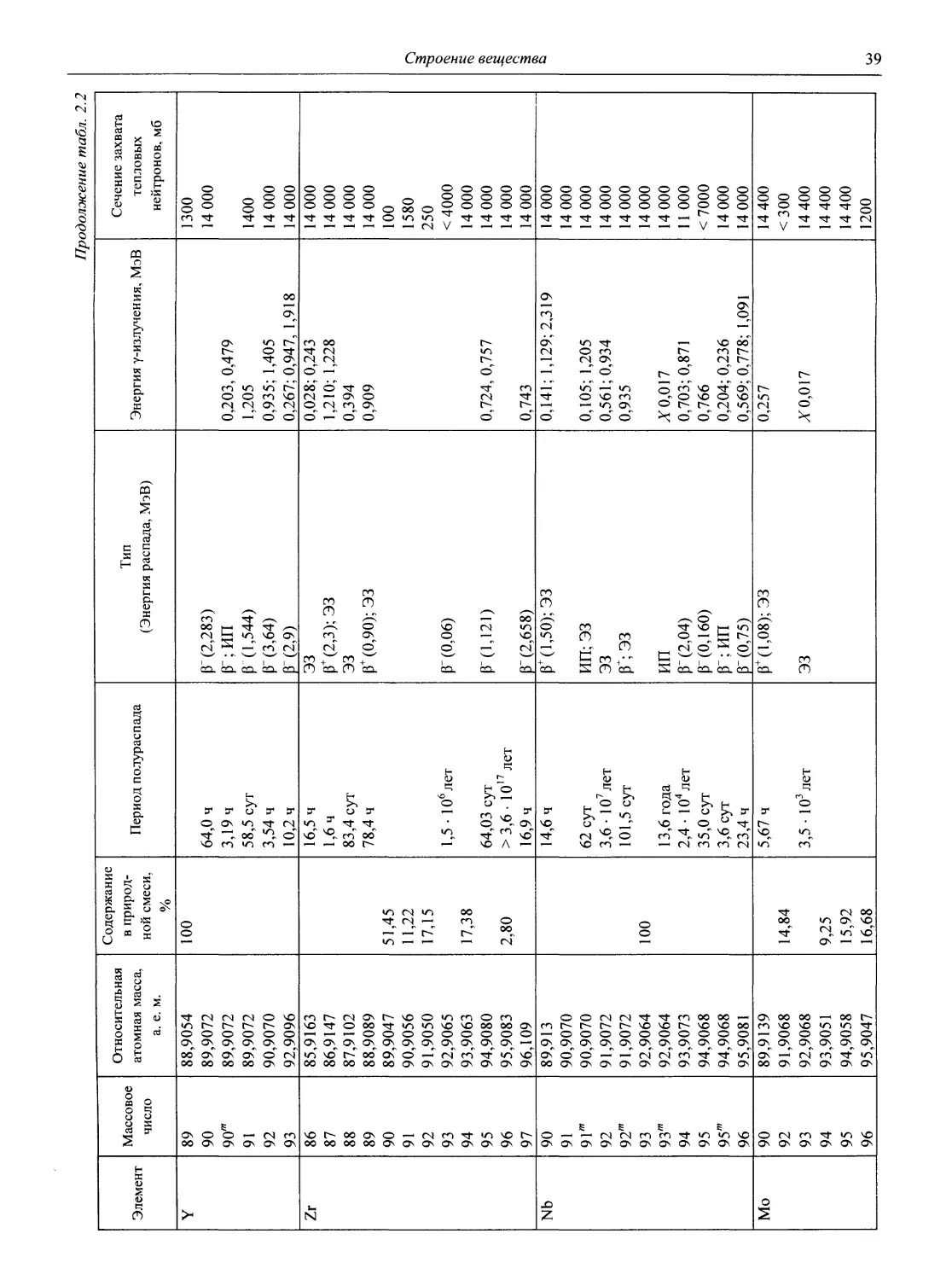
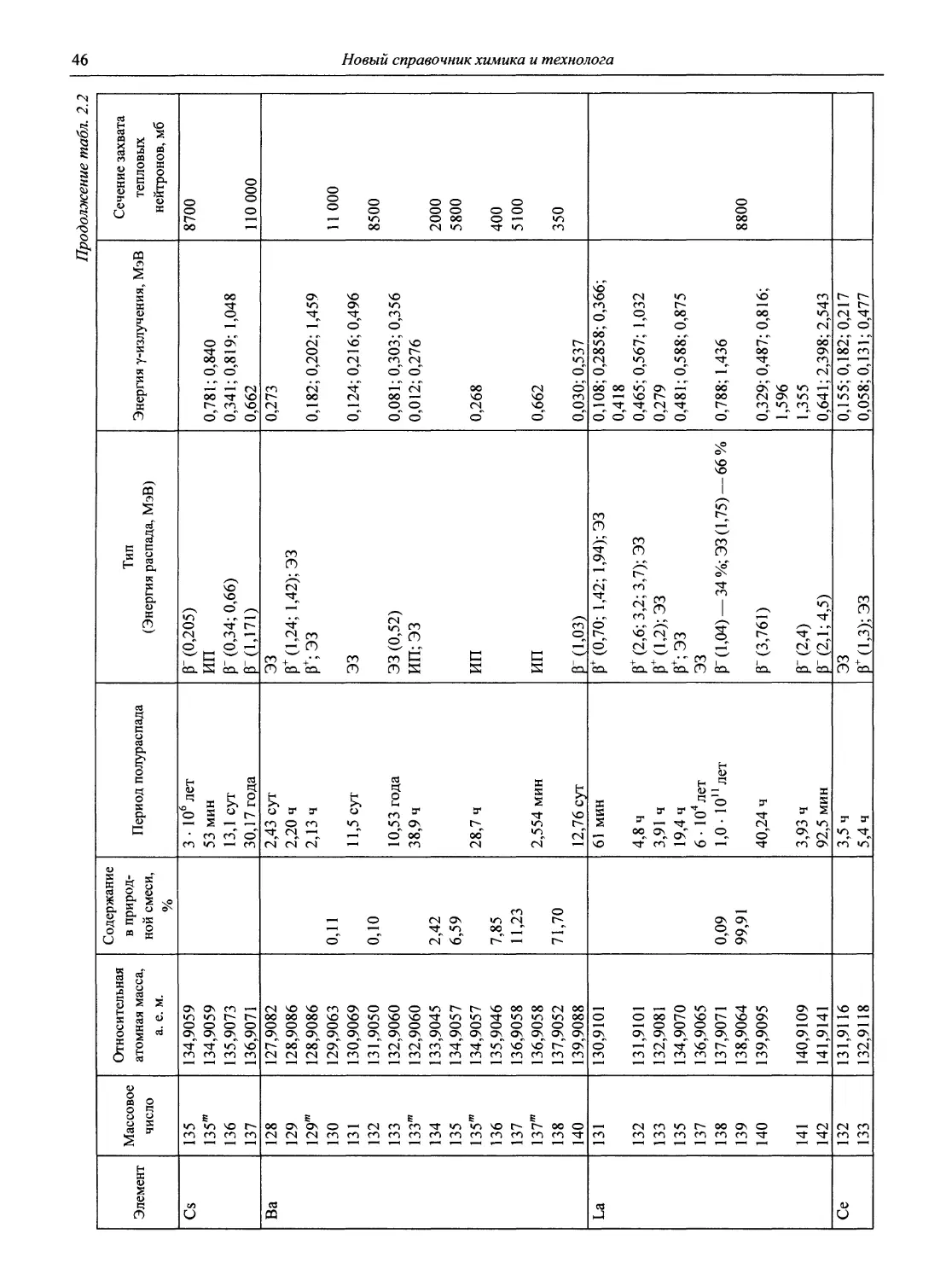
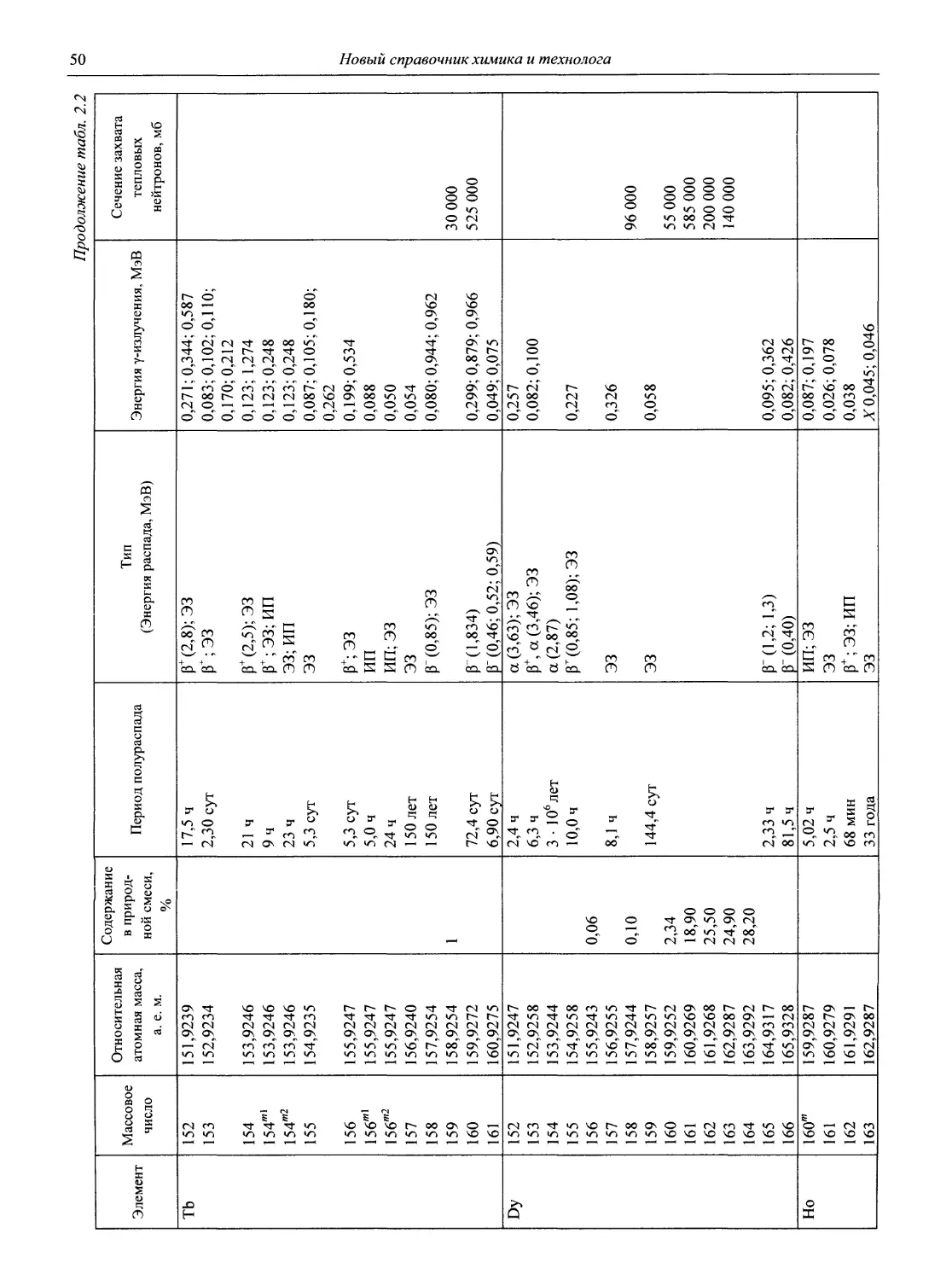
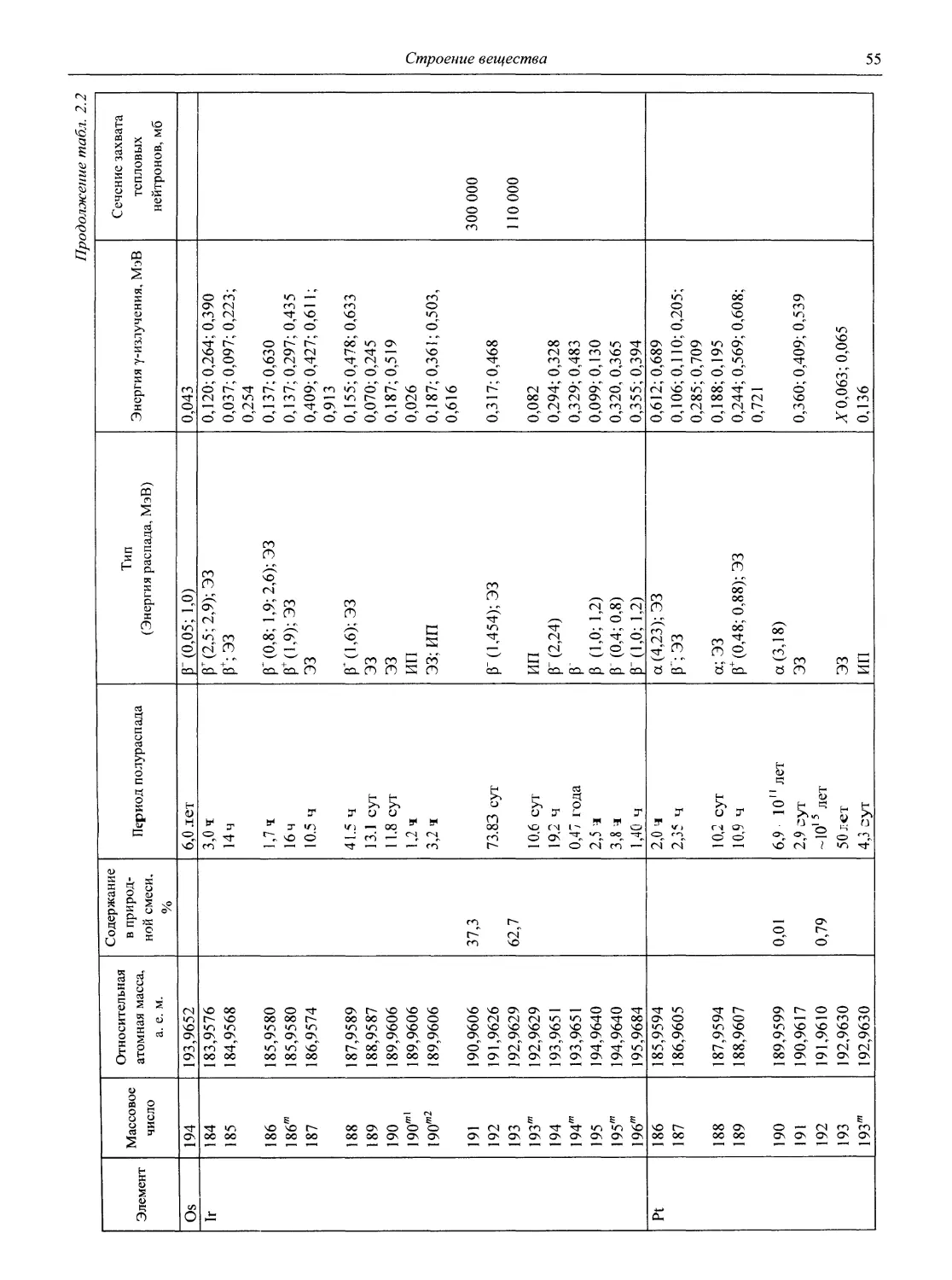
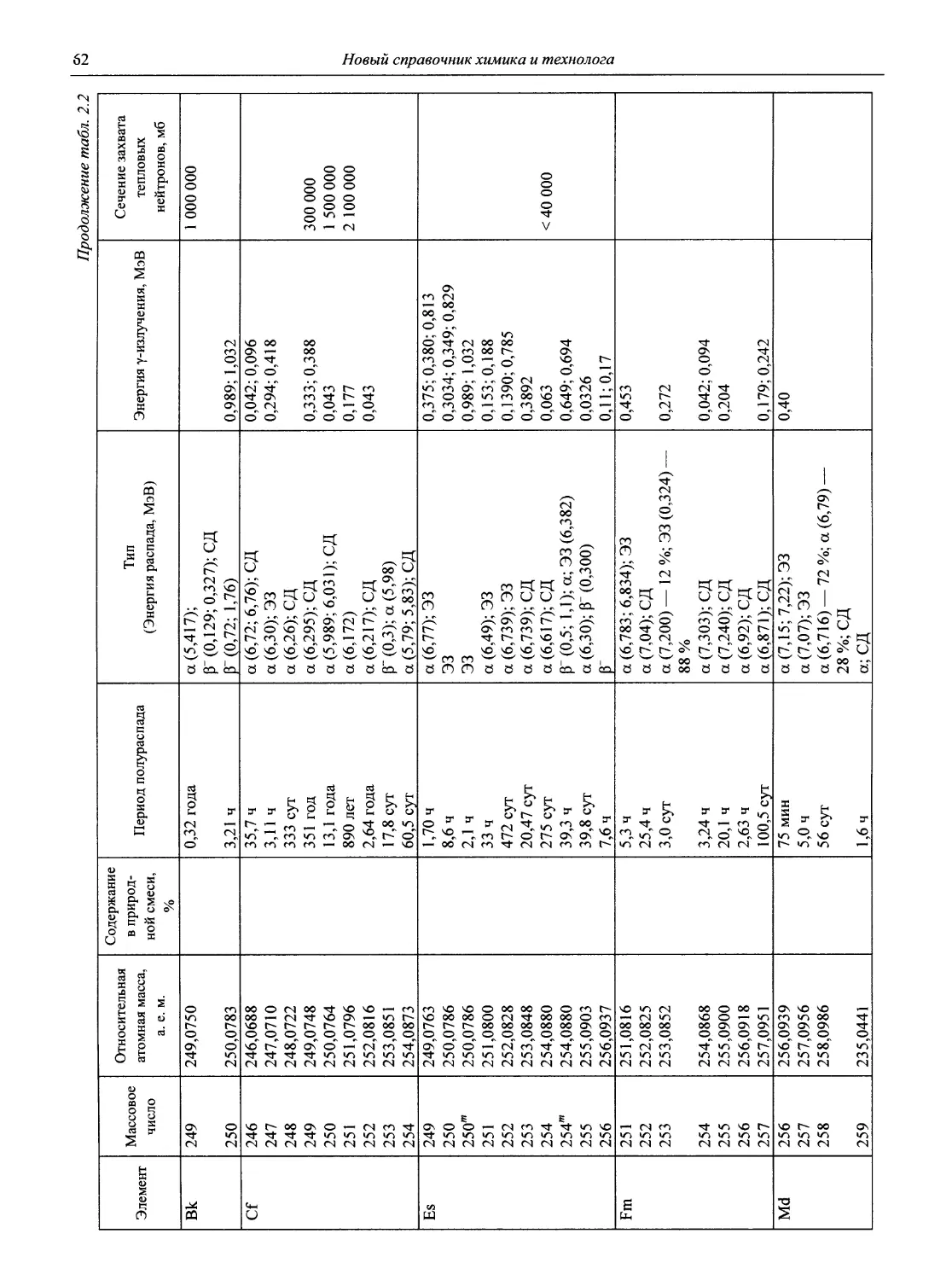
2.2. Свойства изотопов
В табл. 2.2 приведены важнейшие свойства основных стабильных и радиоактивных изотопов таблицы Д.И. Менделеева, вплоть до элемента № 116:
- массовое число — число нуклонов в ядре данного изотопа;
- относительная атомная масса в атомных единицах массы;
- содержание в природе',
- период полураспада — время, за которое количество данного изотопа уменьшается в два раза;
- тип и энергия распада', используемые сокращения: ЭЗ — электронный захват (ЛГ-захват), СД — самопроизвольное деление, ИП — изотопный переход (переход ядра из метастабильного («/и») состояния в стабильное;
- энергия у- (и рентгеновского —X) излучения',
- сечения захвата тепловых нейтронов — площади ядер изотопов, подверженные бомбардировке тепловыми нейтронами (нейтронами с энергией 0,025 эВ). Характеризуют вероятность протекания ядерной реакции под действием нейтронов. Измеряются в барнах (б), 1 б = Ю28 м2.
Свойства элементарных частиц
Таблица 2.1
Группа Название Символ Масса покоя, me Спин Заряд, <?e Время жизни, с Странность Барионный заряд Схема распада
Фотон Y 0 1 0 Стабилен 0 0
Нейтрино электронное Ve 0 1/2 0 Стабильно 0 0
Антинейтрино элек- Ve 0 1/2 0 » 0 0
тронное Нейтрино мюонное 0 1/2 0 » 0 0
Антинейтрино мюонное Vh 0 1/2 0 » 0 0
Нейтрино тау- vx 0 1/2 0 » 0 0
и лептонное
е Антинейтрино тау- V* 0 1/2 0 » 0 0
О лептонное
Электрон e" 1 1/2 -1 Стабилен 0 0
Позитрон e+ 1 1/2 1 » 0 0
Мюон Ц 206,7 1/2 -1 2,2 • 10^ 0 0 _> q~ + Vg + v*
Антимюон + 206,7 1/2 1 2,2 • 10^ 0 0 ц+ е+ + v‘ + ve
Тау-лептон 3528 1/2 -1 3,6 • Ю12 0 0 т-->|Г+ v* +vx
Анти-тау-лептон + T 3528 1/2 1 3,6 - 1012 0 0 ц++ vg+
Пи-мезоны Л° 264,1 0 0 8,0 • 10‘17 0 0 л° —> у + е+ + е~
о ~ к —> 2у
Л°* 264,1 0 0 8,0 • Ю17 0 0 0* + — к —► у + е + е
о* -> л —> 2у
Л+ 273,1 0 1 2,6 • 108 0 0 л+ -> ц+ + vM
Л~ 273,1 0 -1 2,6 • 10’8 0 0 v*
3 К-мезоны K+ 966,4 0 1 1,23 • 10’8 1 0 К+ —> е+ + ve + л°
и о м K" 966,4 0 -1 1,23 • 108 -1 0 К” —> е + v‘ + л °*
<и K° 973,1 0 0 К?, 8,6- 1011 1 0 К° —► л+ + л~
К° 2л°
1 0 К? —> л+ + л- + л°
KJ, 5,38 • 10’8
К° —> л+ + е + v‘
K°‘ 973,1 0 0 KJ*, 8,6 • 1О’П -1 0 К°’-+ л+* + л~*
К°; -> 2л°*
Строение вещества
Окончание табл. 2.1
Группа Название Символ Масса покоя, me Спин Заряд, <ye Время жизни, с Странность Барионный заряд Схема распада
К-мезоны К0’ 973,1 0 0 Kj‘,5,38- 10”8 -1 0 К. °* —► 71+* + 71* + 71°*
3 Я о К.,* —» п+* + е”* + ve
м <D Эта-нуль-мезон По 1074 0 0 1,0- IO”17 0 0 По “* 2у
Анти-эта-нуль-мезон По 1074 0 0 1,0- 10”17 0 0 По —* 2у
Протон р 1836,1 1/2 1 Стабилен 0 1
Антипротон р* 1836,1 1/2 -1 » 0 -1
Нейтрон п 1828,6 1/2 0 960 0 1 п —> р + е” + v‘
Антинейтрон п* 1828,6 1/2 0 960 0 -1 п* —> р* + е+ + ve
Гиперон лямбда А0 2184,1 1/2 0 2,5 • 1O“10 -1 1 А0 —> р + п~ А0 —» п + 71°
Антигиперон лямбда А0* 2184,1 1/2 0 2,5 • IO”10 1 -1 А0* —> р* + п+ А0* —♦ п* + 71°*
Гипероны сигма L+ 2327,6 1/2 1 8,0- 10H -1 1 L+ —> р + 71° L+ —> п + 71+
2327,6 1/2 -1 8,0- IO1' 1 -1 v+* * 1 0* 2 —+ 71
L+* —► п* + 7t”
3 L° 2333,6 1/2 0 1,0- IO14 -1 1 Х° А0 + у
S сх L°* 2333,6 1/2 0 1,0 -IO14 1 -1 S0* —> А0* + у
сЗ I-Q S" 2343,1 1/2 -1 1,49- IO”10 -1 1 Z” —» П + 7t”
S"* 2343,1 1/2 1 1,49 • 10”10 1 -1 Z”* —> п* + 7Г+
Гипероны кси ~o 2572,8 1/2 0 3,03 • IO”10 2 1 Е° -> А0 + 71°
—0* 2572,8 1/2 0 3,03 • IO10 -2 -1 Е°* —> А0* + л0*
77- 2585,6 1/2 -1 1,66 • IO”10 2 1 Е~ —> А0 + тг”
2585,6 1/2 1 1,66 • IO”10 -2 -1 E”*->A0*W
Омега-минус-частица Q 3373 3/2 -1 1,3 • IO”10 0 1 't=i + + + 0 । 0 [i] di < t t t cj a a
Анти-омега-минус- Q* 3373 3/2 1 1,3 • IO”10 0 -1 Q * —> E°* + ti+
частица a' -» л0’ + к'
Новый справочник химика и технолога
Литература
1. Справочник химика / Под ред. Б.П. Никольского. Л.: Химия, 1971. Т. 1.С. 177-179.
2. Полинг Л. Общая химия. М.: Мир, 1974. С. 703-726.
Свойства изотопов
Таблица 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Н 1 1,0078 99,985 0,332
2(D) 2,0140 0,015 0,51
3(Т) 3,0160 12,26 года Р~ (0,019) <0,0067
Не 3 3,0160 0,00014 <0,1
4 4,0026 100 ~0
6 6,0189 0,808 с 3(3,51)
8 8,0339 0,122 с р (10,66)
Li 6 6,0151 7,5 45
7 7,0160 92,5 37
9 9,0268 0,178 с Р" (13,5); п (0,76); а (2,9)
Be 7 7,0169 53,29 сут ЭЗ (0,862) 0,478
9 9,0122 100 9,2
10 10,0135 1,6 • 106 лет Р (0,555) <1
11 11,0217 13,8 с 3 (11,5); а(3) 2,125
В 8 8,0246 0,769 с Р+(14,1); а (1,6)
10 10,0129 19,9 500
11 11,0093 80,1 5
С 11 11,0114 20,3 мес Р" (1,982) 0,961
12 12,0000 98,90 3,4
13 13,0034 1,10 0,9
14 14,0032 Следы 5,73 • 103 лет р’ (0,156) <0,001
N 13 13,0057 9,97 мин Р+ (1,19)
14 14,0031 99,63 1810
15 15,0001 0,37 0,024
16 16,0061 7,13 с р (4,34; 10,5); а(1,6) 6,129
О 15 15,0031 122 с Р+(1,72)
16 15,9949 99,76 0,178
17 16,991 0,05 235
18 17,9992 0,19 0,21
19 19,0036 27 с р (3,25; 4,60) 0,197; 1,135
F 17 17,0021 64,8 с Р+(1,73)
Строение вещества
Продолжение табл. 2.2
N)
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
F 18 18,0009 109,8 мин 0+ (1,665) — 97 %; ЭЗ — 3 %
19 18,9984 100 9,8
20 20,0000 11,176 с 0(5,40)
Ne 19 19,0019 17,3 с 0+ (2,2) 1,357
20 19,9924 90,49 38
21 20,9939 0,28
22 21,9914 9,23 36
23 22,9945 37,6 с 0(4,38) 0,440
Na 21 20,9977 22,47 с 0+ (2,5) 0,351
22 21,9944 2,605 года 0+ (2,842) — 90 %; ЭЗ — 10 % 1,275
23 22,9898 100 400
24 23,9910 14,97 ч 0’ (5,514) 1,369; 2,754
25 24,9900 60 с 0(3,8) 0,390; 0,585; 0,975;
1,612
Mg 24 23,9850 78,70 52
25 24,9858 10,13 180
26 25,9826 11,17 30
27 26,9843 9,46 мин 0(1,75) 0,844; 1,014
28 27,9839 21,0 ч 0“ (1,832)
Al 26 25,9869 7,4 • 105 лет 0+ (4,003) — 82 %; 1,809
ЭЗ — 18%
27 26,9815 100 232
28 27,9819 2,24 мин 0 (2,87) 1,779
29 28,9804 6,6 мин 0(2,5) 1,273
Si 28 27,9769 92,23 160
29 28,9765 4,67 280
30 29,9738 3,10 100
31 30,9753 2,62 ч 0(1,47) 1,266
32 31,9740 710 лет 0’ (0,227)
P 30 29,9783 2,50 мин 0+ (3,24) 2,23
31 30,9938 100 190
32 31,9739 14,23 сут 0(1,710)
33 32,9717 25,3 сут 0 (0,249)
34 33,9737 12,4 с 0“(5,01) 2,127
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада. МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
S 32 31,9721 95,02 15
33 32,9715 0,75 200
34 33,9679 4,21
35 34,9690 87,2 сут Р’ (0,167)
36 35,9671 0,02 140
37 36,9711 5,0 мин Р (1,6) 3,103
38 37,9712 170 мин р-(1,00) 1,942
CI 35 34,9688 75,77 44 000
36 35,9797 3,1 • 105 лет |Г (0,709) — 98 %; ЭЗ — 2 % 100 000
37 36,9658 24,23 430
38 37,9680 37,3 мин Р“ (4,91) 1,642; 2,168
39 38,9680 56 мин Р (1,91) 0,250; 1,267; 1,517
40 39,9704 1,35 мин Р (3,2; 7,5) 1,461;2,622; 2,840
Аг 36 35,9675 0,34 6000
37 36,9667 34,8 сут ЭЗ
38 37,9627 0,06 800
39 38,9643 269 лет Р (3,44) 500 000
40 39,9624 99,60 650
41 40,9645 1,83 ч Р" (1,198; 2,48) 1,294
42 41,9631 33 года Р (0,6)
К 39 38,9637 93,26 2200
40 39,974 0,01 1,25 • 109лет Р" (1,32); ЭЗ 1,461 70 000
41 40,962 6,73 1300
42 41,963 12,36 ч Р’ (3,532) 1,525
43 42,9607 22,3 ч р-(1,82) 0,373; 0,618
Са 40 39,9626 96,04 430
41 1,03 • 105лет ЭЗ
42 41,9586 0,647 700
43 42,9588 0,135 6200
44 43,9555 2,09 1100
45 44,956 163,8 сут Р (0,257)
46 45,9537 0,003 250
47 46,954 4,536 ч Р’ (1,998) 1,297
48 47,9524 0,187 1100
Строение вещества
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Sc 43 3,89 ч 0+(1,2); ЭЗ 0,373
44 43,9594 3,93 ч 0+(3,655); ЭЗ 1,157
44w 43,9594 2,44 сут ЭЗ; ИП 0,271
45 44,9559 100 25 000
46 45,955 83,8 сут 0" (2,367) 5,889; 1,121 8000
47 46,9524 3,35 сут 0(0,601) 0,159
48 47,3 ч 0(0,66) 0,983; 1,038; 1,312
Ti 44 43,9596 47 лет 0,068; 0,078
45 44,9581 3,09 ч 0 0,04); ЭЗ 0,720
46 45,9526 8,00 ЭЗ (0,265) 600
47 46,9518 7,43 1700
48 47,9479 73,8 8300
49 48,9479 5,47 1900
50 49,9448 5,30 140
V 48 47,9523 15,974 сут 0+(4,О15);ЭЗ 0,983; 1,312
49 48,9485 331 сут ЭЗ (0,601)
50 49,9472 0,25 100 000
51 50,9440 99,75 4800
Cr 48 47,9540 21,56 ч ЭЗ 0,116; 0,305
49 48,9513 41,9 мин 0+(1,4); эз 0,091; 0,153; 0,511
50 49,9461 4,35 16 000
51 50,945 27,703 сут ЭЗ (0,751) 0,320
52 51,9405 83,79 760
53 52,9407 9,50 18 200
54 53,9389 2,36 380
Мп 52 51,9456 5,59 сут 0+(0,574); ЭЗ 0,744; 0,936; 1,434; 0,511
53 52,9413 3,7 • 106лет ЭЗ (0,596) 170 000
54 53,9402 312 сут ЭЗ (1,377) 0,835 <10 000
55 54,9381 100 13 300
56 55,9389 2,579 ч 0 (3,696) 0,847
Fe 52 51,9481 8,28 ч 0+(2,37) —57%; ЭЗ (2,37) — 43 % 0,169
54 53,9396 5,82 2800
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Fe 55 54,9383 2,72 года ЭЗ (0,231) X 0,006
56 55,9349 91,66 2500
57 56,9354 2,19 2500
58 57,9333 0,33 1230
59 58,935 44,5 сут Р(1,565) 1,099; 1,292
60 59,9340 ~105 лет Р (0,243) 0,586
Со 55 54,9662 17,5 ч р+(1,04); ЭЗ 0,477; 0,931
56 55,9398 77,7 сут р+ (4,566); ЭЗ 0,847; 1,238
57 56,9363 271 сут ЭЗ (0,836) 0,014; 0,136; 0,122
58 57,9358 70,91 сут р+(2,30); ЭЗ 0,811 1 700 000
58т 57,9358 9,2 ч ип 0,025
59 58,9332 100 19 900
60 59,9338 5,272 года р" (2,824) 1,173; 1,333 2000
61 60,9325 1,65 ч Р (1,22) 0,067
Ni 56 55,9421 6,10 сут ЭЗ 0,158; 0,270; 0,480; 0,750; 0,812
57 56,9398 36,0 ч р+(0,85); ЭЗ 0,127; 1,378; 1,919
58 57,9353 68,27 4400
59 58,9344 7,6 • 104 лет ЭЗ (1,072)
60 59,9332 26,10 2600
61 60,9310 1,13 2500
62 61,9283 3,59 15 000
63 62,9297 100,1 года Р' (0,065)
64 63,9280 0,91 1520
65 64,9301 2,52 ч Р’(0,65) 0,366; 1,116; 1,482
66 65,9291 54,8 ч Р (0,2)
Си 61 60,9335 3,41 ч Рч (1,21); ЭЗ 0,284; 0,656
63 62,9298 69,17 4500
64 63,9298 12,70 ч р+ (0,578) —39%; р'(1,675) — 19%; ЭЗ — 42% 1,346 <6000
65 64,9278 30,83 2300
67 66,9277 61,9ч Р (0,40) 0,091; 0,093; 0,185
Zn 62 61,9394 9,2 ч р+ (0,66); ЭЗ 0,041,0,508; 0,548; 0,597
Строение вещества
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Zn 64 63,9291 48,6 820
65 64,9292 243,8 сут Р+ (1,352) — 98 %; ЭЗ — 2 % 1,116
66 65,9260 27,9
67 66,9271 4,1
68 67,9249 18,8 90
69 68,9266 56 мин Р (0,9) 0,318
69m 68,9266 13,8 ч р' (0,439); ИП
70 69,9253 0,6
71 70,9277 2,4 мин Р"(2,1) 0,512; 0,910
7Г 70,9277 3,9 ч Р~(1,45) 0,386; 0,487; 0,620
72 71,9269 46,5 ч Р(0,30) 0,145; 0,192
Ga 66 65,9316 9,4 ч р+(4,15); ЭЗ 0,834; 1,039, 2,752
67 66,9282 78,25 ч ЭЗ (1,001) 0,093; 0,185; 0,300
68 67,9280 68,0 мин р+(1,90); ЭЗ 1,077
69 68,9257 60,11 1800
71 70,9249 39,89
72 71,9247 13,95 ч Р’(3,99) 0,630; 0,834; 2,202
73 72,9264 4,87 ч Р (1,2) 0,297; 0,326
Ge 66 65,9338 2,3 ч Р+(0,67);ЭЗ 0,044; 0,382
68 67,9281 288 сут ЭЗ (0,11) % 0,009
69 68,9280 39,0 ч р+(0,6); ЭЗ 0,574; 1,106
70 69,9243 20,5
71 70,9250 11,2 сут ЭЗ (0,236) % 0,009
72 71,9217 27,4 980
73 72,9234 7,8 14 000
74 73,9219 36,5 140
75 74,9229 82,8 мин Р (1,2) 0,199; 0,265
76 75,9214 7,8 90
77 76,9235 11,30 ч Р(2,70) 0,211
78 77,9316 1,45 ч Р (0,7) 0,277, 0,294
As 71 72 73 74 70,9271 71,9268 72,9238 73,9239 61 ч 26,0 ч 80,3 сут 17,78 сут Р+(0,81); ЭЗ Р+(2,50); ЭЗ ЭЗ (0,35) Р+(0,94), Р ( 1,36); ЭЗ 0,175 0,630; 0,834 0,0534 0,596
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия -у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
As 75 74,9216 100 4300
76 75,9224 26,3 ч Г (2,97) 0,559; 0, 657; 1,216
77 76,9206 38,8 ч Р"(0,7) 0,239; 0, 250; 0,521
78 77,9219 91 мин Р"(4,4) 0,614; 0, 695; 1,309
Se 72 71,9371 8,4 сут ЭЗ 0,046
73 72,9268 7,1 ч Р (1,32); ЭЗ 0,067; 0, 361 .
73т 72,9268 41 мин Р" (1,70); ИП 0,026; 0, 085; 0,254; 0,393
74 73,9225 0,9 55 000
75 74,9225 118,5 сут ЭЗ; Р’ (0,864) 0,136; 0, 265
76 75,9192 9,2 21 000
77 76,9199 7,6 42 000
78 77,9173 23,7 200
79 78,9185 <6,5-104 лет Р"(0,2)
80 79,9165 49,8
82 81,9167 8,8 6
Br 75 74,9258 98 мин Р+(1,7); эз 0,287
76 75,9192 16,1 ч Р’ (3,4); ЭЗ 0,559
77 76,9214 57,0 ч р+ (0,34); ЭЗ (1,365) 0,239; 0, 297; 0,521
79 78,9183 50,69 2600
80 79,9185 17,6 мин р+ (0,86); р- (1,4; 2,0); ЭЗ 0,616; 0, 666
8 О'” 79,9185 4,42 ч ИП 0,038
81 80,9193 49,31
82 81,9168 35,30 ч Р (0,44); р+(3,093) 0,554; 0, 619; 0,698; 0,777
83 82,9152 2,39 ч Р (0,92) 0,530
Кг 76 75,9258 14,8 ч ЭЗ 0,046; 0, 270; 0,316 14 000
78 77,9204 0,35 2000
79 78,9201 35,0 ч Р (0,92); ЭЗ 0,261; 0, 398; 0,606 14 000
80 79,9164 2,35 14 000
81 80,9166 2,1 • 105лет ЭЗ 14 000
82 81,9135 11,6 32 000
83 82,9141 11,5 180 000
83™ 82,9141 1,83 ч ИП 0,009 14 000
Строение вещества
Продолжение табл. 2.2
00
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Кг 84 83,9115 57,0 100
85 84,9125 10,72 года Г (0,687) 0,514 14 000
85м 84,9125 4,48 ч 0(0,8); ИП 0,512; 0,305 14 000
86 85,9106 17,3 60
87 86,9134 76,3 мин 0 (3,5; 3,9) 0,403; 0,845; 2,555 14 000
88 87,9145 2,84 ч 0(0,5; 2,8) 0,196; 2,392 14 000
Rb 81 80,9190 4,58 ч Р+(1,05);ЭЗ 0,446 14 000
82м 81,9182 6,2 ч Р+(0,92); ИП 0,554; 0,619; 0,777; 1,044 14 000
83 82,9152 86,2 сут ЭЗ (0,86) 0,520; 0,530; 0,553 14 000
84 83,9144 32,9 сут Р+, Р (0,892); ЭЗ 0,882 14 000
85 84,9117 72,17 450
86 85,9112 18,8 сут Р’( 1,744); ЭЗ 1,076 14 000
87 86,9092 27,83 4,8- Ю10лет Р’(0,273) 120
Sr 82 81,984 25,0 сут ЭЗ (0,21) X 14 000
83 82,9176 32,4 ч 0+(1,23); ЭЗ 0,382; 0,763 14 000
84 83,9134 0,56 570
85 84,9129 64,8 сут ЭЗ(1,08) 0,514 14 000
85м 84,9129 68 мин ЭЗ; ИП 0,161; 0,232 14 000
86 85,9094 9,86 14 000
87 86,9089 7,00 14 000
87м 86,9089 2,80 ч ЭЗ; ИП 0,388 14 000
88 87,9056 82,58 5000
89 88,9075 50,52 сут Р( 1,492) 500
90 89,9077 29,0 года Р“ (0,546) 900
91 90,9102 9,5 года 0 (1,09; 1,36; 2,67) 0,653; 0,750; 1,024 14 000
92 91,9110 2,71 ч 0(0,55; 1,5) 1,384
Y 85 84,9164 2,7 ч 0+(1,2; 1,5; 2,1); ЭЗ 0,505; 0,232 14 000
85м 84,9164 4,9 ч 0(2,2); ЭЗ 0,767; 1,405; 2,124 14 000
86 85,9149 14,74 ч Р+(1,25);ЭЗ 0,628; 1,077; 1,153 14 000
87 86,9109 80,3 ч Р+(0,8);ЭЗ 0,485 14 000
87м 86,9109 13 ч 0+(1,5); ИП 0,381 14 000
88 87,9095 106,6 сут 0+ (0,76) — 1 %; ЭЗ (3,623) — 99 % 0,898; 1,836 14 000
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Y 89 88,9054 100 1300
90 89,9072 64,0 ч Р" (2,283) 14 000
90'” 89,9072 3,19ч Р;ИП 0,203, 0,479
91 89,9072 58,5 сут Р (1,544) 1,205 1400
92 90,9070 3,54 ч Р’(3,64) 0,935; 1,405 14 000
93 92,9096 10,2ч Р (2,9) 0,267; 0,947, 1,918 14 000
Zr 86 85,9163 16,5 ч ЭЗ 0,028; 0,243 14 000
87 86,9147 1,6 ч Р+(2,3); ЭЗ 1,210; 1,228 14 000
88 87,9102 83,4 сут ЭЗ 0,394 14 000
89 88,9089 78,4 ч Р+(0,90);ЭЗ 0,909 14 000
90 89,9047 51,45 100
91 90,9056 11,22 1580
92 91,9050 17,15 250
93 92,9065 1,5 • 106лет Р(0,06) <4000
94 93,9063 17,38 14 000
95 94,9080 64,03 сут Р (1,121) 0,724, 0,757 14 000
96 95,9083 2,80 > 3,6 • 1017 лет 14 000
97 96,109 16,9ч Р’(2,658) 0,743 14 000
Nb 90 89,913 14,6ч Р+ (1,50); ЭЗ 0,141; 1,129; 2,319 14 000
91 90,9070 14 000
91'” 90,9070 62 сут ИП; ЭЗ 0,105; 1,205 14 000
92 91,9072 3,6 • 107лет ЭЗ 0,561; 0,934 14 000
92"1 91,9072 101,5 сут р"; эз 0,935 14 000
93 92,9064 100 14 000
93"1 92,9064 13,6 года ИП .¥0,017 14 000
94 93,9073 2,4 • 104 лет Р’(2,04) 0,703; 0,871 И 000
95 94,9068 35,0 сут Р’(0,160) 0,766 <7000
95m 94,9068 3,6 сут р;ИП 0,204; 0,236 14 000
96 95,9081 23,4 ч Р(0,75) 0,569; 0,778; 1,091 14 000
Mo 90 89,9139 5,67 ч Р+(1,08);ЭЗ 0,257 14 400
92 91,9068 14,84 <300
93 92,9068 3,5 • 103 лет ЭЗ Y 0,017 14 400
94 93,9051 9,25 14 400
95 94,9058 15,92 14 400
96 95,9047 16,68 1200
Строение вещества
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Мо 97 96,9060 9,55 2200
98 97,9054 24,13 14 400
99 98,9077 65,94 ч Р'(1,357) 0,181; 0,739; 0,778 14 400
100 99,9075 9,63 14 400
Тс 93 92,9102 2,7 ч Р+(0,81); ЭЗ 1,363; 1,520 14 400
94 93,9077 293 мин Р+(0,816); ЭЗ 0,703; 0,850; 0,871 14 400
95 94,9077 20,0 ч ЭЗ 0,766 14 400
95т 94,9077 61 сут р+(0,51; 0,71); ЭЗ; ИП 0,204; 0,582; 0,835 14 400
96 95,9079 4,3 сут ЭЗ 0,778; 0,813; 0,850 14 400
97 96,9064 2,6- 106лет ЭЗ (0,32) 14 400
97т 96,9064 90 сут ИП 0,097 14 400
98 97,9072 4,2 • 106лет 3(1,79) 0,652; 0,745
99 98,9062 2,13 • 105лет Р (0,293) 22 000
99« 98,9062 6,01 ч ИП 0,141 14 400
Ru 95 94,9104 1,65 ч Р(0,7; 1,0; 1,3); ЭЗ 0,336; 0,627; 1,097 14 400
96 95,9075 5,53 210
97 96,9076 2,89 сут ЭЗ (1,12) 0,216; 0,325 14 400
98 97,9053 1,87 <8000
99 98,9059 12,70 10 600
100 99,9042 12,60 10 400
101 100,9056 17,10 3100
102 101,9056 31,60 1400
103 102,9063 39,24 сут Р’(0,767) 0,497; 0,610 14 400
104 103,9054 18,60 470
105 104,9077 4,44 ч Р’(1,И; 1,19) 0,316; 0,469; 0,676; 0,724 14 400
106 105,9073 372,6 сут Р~ (0,039) 146 000
Rh 99 98,9082 15,0 сут Р+(0,5; 0,7; 1,1); ЭЗ 0,090; 0,353; 0,528 14 400
99« 98,9082 4,7 ч Р+(0,7); ЭЗ 0,341; 0,618; 1,261 14 400
100 99,9081 20,8 ч Р+(2,1; 2,6); ЭЗ 0,540; 0,823; 1,036; 1,553; 2,376 11 000
101 100,9062 3,3 года ЭЗ 0,127; 0,198; 0,325 11 000
10 Г 100,9062 4,34 сут ЭЗ; ИП 0,307 11 000
102 101,9043 2,9 года ЭЗ 0,475; 0,631; 0,697 11 000
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Rh 102w 101,9043 206 сут 0(0,8; 1,3), |Г (1,15); ЭЗ; ИП 0,475 11 000
103 102,9063 100
103™ 102,9063 56,1 мин 0’(0,040); ИП 11 000
105 104,9077 35,4 ч 0 (0,57) 0,306; 0,319 11 000
106 105,9073 30,0 с 0 (3,54) 0,512; 0,622 11 000
106й 105,9073 130 мин 0“ (0,73; 0,92) 0,451; 0,512; 0,717; 1,047 11 000
Pd 100 99,9085 3,6 сут ЭЗ 0,075; 0,084; 0,126 11 000
101 100,9083 8,5 ч 0+(О,5О; 0,78); ЭЗ 0,268; 0,296; 0,590 11 000
102 101,9056 1,02 4800
103 102,9061 16,97 сут ЭЗ (0,52) 0,357 11 000
104 103,9040 11,14 11 000
105 104,9051 22,33 11 000
106 105,9035 27,33 279
107 106,9051 6,5 • 106лет 0(0,04) 11 000
108 107,9039 26,46 12 000
109 108,9060 13,47 ч 0(1,116) 0,088 11 000
ПО 109,9052 11,72 11 000
111 110,9077 23,4 мин 0 (2,1) 0,580 11 000
11Г 110,9077 5,5 ч 0(1,1); ип 0,071; 0,172; 0,391 11 000
112 111,9073 21,1 ч 0(0,3) 0,019 11 000
Ag 105 104,9065 41,3 сут ЭЗ 0,064; 0,281; 0,345 X 0,021
106™ 105,9067 8,5 сут ЭЗ 0,451; 0,512; 0,717; 1,046 11 000
107 106,9051 51,84 35 000
108w 107,9060 127 лет 0+; ЭЗ; ИП 0,079; 0,434 11 000
109 108,9048 48,16 4200
110™ 109,9061 249,8 сут 0" (3,00) —99%; ИП — 1 % 0,658 82 000
111 110,9053 7,45 сут 0 (1,037) 0,246; 0,342 11 000
112 111,9070 3,14 ч 0(3,9) 0,617; 1,387 11 000
113 112,9066 5,37 ч 0 (2,0) 0,259; 0,298; 0,316 11 000
Cd 106 105,9065 1,25 1000
Строение вещества
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Cd 107 106,9066 6,50 ч р+(о,з); эз 0,829 11 000
108 107,9042 0,89 1500
109 108,9049 453 сут эз 0,088 X 0,022 11 000
ПО 109,9030 12,51 11 000
111 110,9042 12,81 11 000
111" 110,9042 48,6 мин ИП 0,151; 0,245 11 000
112 111,9028 24,13 11 000
113 112,9044 12,22 20 000 000
ПЗт 112,9044 14 лет ₽ (0,6); ИП 0,264 11 000
114 113,9034 28,72 360
115 114,9054 53,5 ч ₽’(1,45) 0,492; 0,528 11 000
IIS'” 114,9054 44,6 сут |Г(1,62) 0,934; 1,291 И 000
116 115,9048 7,47 11 000
117 116,9072 2,4 ч Р (1,3; 1,8; 2,2) 0,273; 0,345 11 000
\\Т 116,9072 3,4 ч Р (0,4; 0,7) 0,564; 1,029; 1,066; 1,433 11 000
In 109 108,9071 4,2 ч р+ (0,80); ЭЗ 0,203; 0,624
ПО 109,9072 69 мин Р(2,2);ЭЗ 0,658 11 000
ПО"*1 109,9072 4,9 ч ЭЗ 0,658; 0,885 11 000
110ю2 109,9072 4,1 ч ЭЗ 0,283 11 000
111 110,9051 2,81 сут ЭЗ 0,171; 0,245
113 112,9041 4,30
ИЗ7” 112,9041 99,5 мин р+; ЭЗ; ИП 0,391 X 0,024 11 000
114 113,9049 71,9с Р (1,99); ЭЗ 1,300 11 000
П4« 113,9049 49,51 сут ИП — 97 %; Э3(1,6) —3 % 0,190; 0,558; 0,725 11 000
115 114,9039 95,70 6 • 1014лет Р’(0,496) 11 000
115"* 114,9039 4,4 ч Р (0,8); ИП 0,336 11 000
Sn НО 109,9079 4,1 ч ЭЗ 0,283
112 111,9048 0,97 800
113 112,9052 115,1 сут ЭЗ(1,02) 0,255; 0,392 X 0,024
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Sn 114 113,9028 0,65
115 114,9033 0,36
116 115,9017 14530 6
117 116,9030 7,68
117"7 116,9030 14,0 сут ИП 0,156; 0,159
118 117,9016 24223
119 118,9033 8,58
119™ 118,9033 250 сут ИП 0,024 ЛГ 0,025
120 119,9022 32,59 ~1
121 120,9042 27,0 ч 0"(0,3 88)
121я* 120,9042 55 лет 0” (0,354) 0,037
122 121,9034 4,63 1
123 122,9057 129,2 сут 0 (0,3; 1,4) 1,030, 1,089
124 123,9053 5,79 4
125 124,9078 9,62 сут 0 (2,4) 0,823; 0,916; 1,067; 1,089
126 125,9077 1 • 105лет 0 (0,2) 0,088
127 126,9103 2,1 ч 0(1,4) 0,823; 1,096; 1,114
Sb 117 116,9048 2,80 ч 0+ (0,6); ЭЗ 0,158
118 117,9056 3,5 мин 0+ (2,7); ЭЗ 1,230; 1,267
118™ 117,9056 5,00 ч 0+; ЭЗ 0,254, 1,051, 1,230
119 118,9039 38,0 ч ЭЗ 0,024
120 119,9051 5,76 сут эз 0,090; 0,197; 1,023; 1,172
121 120,9038 57,30 6200
122 121,9052 2,71 сут 0" (1,982), 0+; ЭЗ 0,564, 0,693
123 122,9042 42,75 3400
124 123,9059 60,4 сут 0’(2,905) 0,603 6500
125 124,9053 2,76 года 0’(0,767) 0,428; 0,463; 0,601; 0,636
126 125,9072 12,4 сут 0 (1,9) 0,415; 0,666; 0,695
127 126,9069 3,9 сут 0’ (1,24; 1,49) 0,473; 0,686; 0,784
128 127,9090 9,1 ч 0 (2,3) 0,314, 0,526
Строение вещества
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Sb 129 128,9091 4,4 ч Р~(0,6; 2,2) 0,545; 0,813; 0,915
Те 116 115,9084 2,50 ч Р+ (0,4); ЭЗ 0,094; 0,103
117 116,9086 62 мин Р+ (1,8); ЭЗ 0,720; 1,716; 2,300
118 117,9059 6,00 сут ЭЗ X 0,026; 0,026
119 118,9064 16,05 ч Р+ (0,63); ЭЗ 0,644; 0,700
119м 118,9064 4,68 сут ЭЗ 0,154; 0,270; 1,213
120 119,9040 0,09 340
121 120,9050 16,8 сут ЭЗ 0,508; 0,573
121м 120,9050 154 сут Р+; ИП; ЭЗ 0,212
122 121,9031 2,57 1700
123 122,9043 0,89 1,3 • 10,3лет ЭЗ (0,052) 410 000
123м 122,9043 119,7 сут ИП 0,159
124 123,9028 4,76 6800
125 124,9044 7,10 1560
125м 124,9044 58,0 сут ИП 0,145 X 0,028
126 125,9033 18,89 125
127 126,9052 9,5 ч Р’ (0,697) 0,418
127м 126,9052 109 сут Р"(1,5); ИП 0,058; 0,088
128 127,9045 31,73 14
129 128,9066 69 мин [3 (0,29; 0,69; 0,99; 1,45) 0,028; 0,460
129м 128,9066 33,5 сут р" (1,60); ИП 0,151; 0,460; 0,699
130 129,9062 33,97 2,4 • 102,лет 20
131 130,9085 25,0 мин Р (1,35; 1,69; 2,14)
131м 130,9085 30 ч Р (0,216; 0,42; 0,57; 2,46); ИП 0,150; 0,774; 0,852
132 131,9085 78 ч Р" (0,22) 0,050; 0,228
I 120 119,9098 1,35 ч Р+ (4,0; 4,6) 0,560, 0,641; 1,523
120м 119,9098 53 мин Р+(3,1; 3,8) 0,560; 0,601; 0,615
121 120,9075 2,12 ч Р+ 0,213
123 122,9056 13,41 ч Э3(1,23) 0,159
124 123,9062 4,2 сут Р+ (0,81; 1,53; 2,13) 0,603; 0,723; 1,691
125 124,9046 59,9 сут ЭЗ (0,178) 0,035 X0,027; 0,028; 0,031 900
126 125,9056 13,0 сут Р“ (0,38; 0,86; 1,25), [Г 0,389; 0,666
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
I 127 126,9045 100 6200
129 128,9050 1,67 • 107лет р-(0,193) 0,040 9000
130 129,9067 12,36 ч Р (0,40; 0,62; 1,04) 0,536 18 000
131 130,9061 8,04 сут Р" (0,971) 0,365 -700
132 131,9080 2,28 ч Р"(2,1) 0,667; 0,773
132'" 131,9080 83 мин Р~ (1,47); ИП 0,600; 0,668
133 132,9078 20,9 ч Р (1>5) 0,530; 0,875
135 134,9100 6,61 ч Р" (0,9; 1,3) 1,132; 1,260
Хе 122 121,9086 20,1 ч ЭЗ 0,149; 0,350; 0,417
123 122,9084 2,08 ч Р+ (1,5); ЭЗ 0,149; 0,178; 0,330
124 123,9061 0,10 100 000
125 124,9065 17ч Р+ (0,47); ЭЗ 0,188; 0,243
126 125,9043 0,09 1500
127 126,9052 36,30 сут ЭЗ (0,66) 0,172; 0,203; 0,375
128 127,9035 1,91
129 128,9048 26,40 21 000
129'" 128,9048 8,89 сут ИП 0,040; 0,197
130 129,9035 4,10
131 130,9051 21,20 110 000
131'" 130,9051 11,77 сут ИП 0,164
132 131,9041 50
133 132,9059 5,25 сут р" (0,427) 0,081
133т 132,9059 2,19 сут ИП 0,233
134 133,9054 10,40 230
135 134,9071 9,10 ч р-(0,91) 0,2498; 0,6082
136 135,9072 8,90 280
Cs 127 126,9075 6,2 сут Р+ (0,68; 1,06); ЭЗ 0,125; 0,411; 0,462
129 128,9060 32,3 ч Р+; ЭЗ 0,372; 0,412; 0,549
131 130,9055 9,68 сут ЭЗ Х0,030; 0,298; 0,034
132 131,9064 6,48 сут Р+ (0,4), Р“ (0,8); ЭЗ 0,464; 0,506; 0,630; 0,668
133 132,9054 100 27 400
134 133,9067 2,065 года Р~ (2,06); ЭЗ 0,605; 0,796 134 000
134'" 133,9067 2,90 ч р-; ИП 0,128
Строение вещества
Продолжение табл. 2.2
О\
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Cs 135 134,9059 3 • 106 лет Р" (0,205) 8700
\35т 134,9059 53 мин ИП 0,781; 0,840
136 135,9073 13,1 сут Р (0,34; 0,66) 0,341; 0,819; 1,048
137 136,9071 30,17 года р-(1,171) 0,662 110 000
Ва 128 127,9082 2,43 сут ЭЗ 0,273
129 128,9086 2,20 ч Р+ (1,24; 1,42); ЭЗ
129'" 128,9086 2,13 ч Р+; ЭЗ 0,182; 0,202; 1,459
130 129,9063 0,11 11 000
131 130,9069 11,5 сут эз 0,124; 0,216; 0,496
132 131,9050 0,10 8500
133 132,9060 10,53 года ЭЗ (0,52) 0,081; 0,303; 0,356
133'" 132,9060 38,9 ч ИП; ЭЗ 0,012; 0,276
134 133,9045 2,42 2000
135 134,9057 6,59 5800
\35т 134,9057 28,7 ч ИП 0,268
136 135,9046 7,85 400
137 136,9058 11,23 5100
137'" 136,9058 2,554 мин ИП 0,662
138 137,9052 71,70 350
140 139,9088 12,76 сут Р(1,03) 0,030; 0,537
La 131 130,9101 61 мин Р+ (0,70; 1,42; 1,94); ЭЗ 0,108; 0,2858; 0,366;
0,418
132 131,9101 4,8 ч Р+ (2,6; 3,2; 3,7); ЭЗ 0,465; 0,567; 1,032
133 132,9081 3,91 ч Р+ (1,2); ЭЗ 0,279
135 134,9070 19,4 ч Р+; ЭЗ 0,481; 0,588; 0,875
137 136,9065 6 • 104лет эз
138 137,9071 0,09 1,0- 10й лет р- (1,04) — 34 %; ЭЗ (1,75) — 66 % 0,788; 1,436
139 138,9064 99,91 8800
140 139,9095 40,24 ч Р" (3,761) 0,329; 0,487; 0,816;
1,596
141 140,9109 3,93 ч Р (2,4) 1,355
142 141,9141 92,5 мин Р’ (2,1; 4,5) 0,641; 2,398; 2,543
Се 132 131,9116 3,5 ч ЭЗ 0,155; 0,182; 0,217
133 132,9118 5,4 ч Р+ (1,3); ЭЗ 0,058; 0,131; 0,477
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Се 133м 132,9118 97 мин Р+; эз 0,077; 0,097
134 133,9090 76 ч ЭЗ 0,301
135 134,9092 17,8ч Р+ (0,8); ЭЗ 0,266; 0,300; 0,518; 0,607
136 135,9071 0,19
137 136,9078 9,0 ч Р+; эз 0,447
137м 136,9078 34,4 ч ИП; ЭЗ 0,254
138 137,9060 0,25 1100
139 138,9066 140 сут ЭЗ (0,27) 0,166 % 0,033
140 139,9054 88,48 580
141 140,9083 32,5 сут (0,581) 0,145 29 000
142 141,9092 11,08 950
143 142,9124 33,0 ч Р (1,462) 0,057; 0,293; 0,665; 0,722
144 143,9137 284,4 сут Р’(0,318) 0,134 1000
Рг 137 136,9107 1,28 ч Р+ (1,7); ЭЗ 0,160; 0,434; 0,514; 0,837
138м 137,9108 2,1 ч р^ (1,6); ЭЗ 0,302; 0,511; 0,789; 1,038
139 138,9089 4,4 ч Р* (U); эз 1,347
141 140,9077 100 3900
142м 141,9100 19,13 ч р" (2,160); ЭЗ 1,576 18 000
143 142,9108 13,58 сут Р (0,934)
144 143,9133 17,28 мин Р’ (3,0) 0,697, 1,489; 2,186
145 144,9145 5,98 ч Р (1,8) 0,676; 0,748
Nd 138 137,9119 5,1 ч ЭЗ 0,200; 0,326
139м 138,9119 5,5 ч Р+(1,2; 3,3); ЭЗ; ИП 0,114; 0,231
140 139,9096 3,38 сут ЭЗ % 0,036
141 140,9096 2,5 ч Р+ (0,8); ЭЗ 1,127; 1,147; 1,293
142 141,9077 27,13 18 800
143 142,9098 12,18
144 143,9101 23,80 2,1 • 1015лет а(1,83) 4000
Строение вещества
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Nd 145 144,9126 8,30 50 000
146 145,9131 17,19 1400
147 146,9161 10,99 сут р' (0,895) 0,091; 0,531
148 147,9169 5,76 2500
149 148,9202 1,73 ч 3(1,4; 1,6) 0,114; 0,211; 0,270
150 149,9209 5,64 1300
Pm 143 142,9109 265 сут эз 0,742
144 143,9101 1,0 года эз 0,477; 0,618; 0,696
145 144,9126 17,7 года а (2,24); ЭЗ (0,161) 0,067; 0,072
146 145,9131 5,53 года Р’ (1,542) — 37 %; ЭЗ (1,48) — 63 % 0,454; 0,736; 0,747 8 400 000
147 146,9161 2,623 года р’ (0,224) 90 000
148 147,9169 5,37 сут Р (2,5) 0,550; 0,915; 1,465
148w 147,9169 41,3 сут Р’(0,4; 1,0) 0,550; 0,630; 0,726 25 000
149 148,9202 53,1 ч Р~ (1,073) 0,286
150 149,9209 2,7 ч Р~ (1,187) 0,334; 1,166; 1,325
151 150,9238 28,4 ч Р’ (0,8; 1,2) 0,168; 0,340
Sm 142 141,9152 72,4 мин Р+ (1,0); ЭЗ
144 143,9120 3,09 -700
145 144,9134 340 сут ЭЗ 0,061 %0,038; 0,039 -110 000
146 145,9131 1,03 • 108лет а (2,500)
147 146,9149 15,00 1,08 • 10й лет а (2,231) 75 000
148 147,9148 11,30 7 • 1015лет а (1,96) 2400
149 148,9172 13,80 1016 лет 41 000 000
150 149,9173 7,40 102 000
151 150,9199 90 лет Р~ (0,076) 0,022 15 000 000
152 151,9197 26,60 210 000
153 152,9221 46,7 ч Р" (0,810) 0,070; 0,103
154 153,9222 22,60 5500
156 155,9255 9,4 ч Р- (0,43; 0,72) 0,088; 0,166; 0,240
Eu 145 144,9163 5,93 сут Р+ (1,7); 0,654; 0,894; 1,659
146 145,9172 4,65 сут Р(1,5; 2,1); ЭЗ 0,633; 0,634; 0,747
147 146,9168 24 сут р+, а (2,91); ЭЗ 0,121; 0,197; 0,678
148 147,9182 54 сут Р+, а (2,63); ЭЗ 0,550; 0,611; 0,630
149 148,9179 93,1 сут ЭЗ 0,277, 0,328
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, a. e. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Ей 150 149,9197 36 лет ЭЗ 0,334; 0,439; 0,584
150™ 149,9197 12,6ч Г, Р (1,0);ЭЗ 0,334, 0,407
151 150,9199 47,82 5000
152 151,9218 13,64 года |Г (1,822) — 28 %;р+; 0,122; 0,344
Э3( 1,876) —72%
152wl 151,9218 9,3 ч р"(0,56; 1,55; 1,89); 0+; ЭЗ 0,842; 0,964
152w2 151,9218 96 мин ИП 0,090
153 152,9212 52,18 450 000
154 153,9230 8,5 года Р (0,27; 0,58); ЭЗ 0,123; 0,723 1 500 000
155 154,9229 4,7 года Р“(0,14; 0,16; 0,25) 0,087; 0,105 14 000 000
156 155,9248 15 сут Р" (0,30; 0,50; 1,2; 1,5) 0,089; 0,812; 1,231
157 156,9254 15,13 ч 3(0,9; 1,3) 0,064; 0,373, 0,413
Gd 146 145,9185 48,3 сут Р+; эз 0,115; 0,116; 0,155
147 146,9193 38,1 ч Р; эз 0,229; 0,396; 0,929
148 147,9181 98 лет а (3,183)
149 148,9193 9,5 сут а (3,01); ЭЗ 0,150; 0,299; 0,347
150 149,9187 1,8 • 106лст а (2,72)
151 150,9204 120 сут а (2,60); ЭЗ 0,022; 0,154; 0,175;
0,243
152 151,9198 0,20 1,1 • 1014лст ЭЗ; а (2,24) < 125 000
153 152,9215 241,6 сут ЭЗ (0,243) 0,097; 0,103
154 153,9209 2,18 102 000
155 154,9226 14,80 61 000 000
156 155,9221 20,47
157 156,9240 15,65 254 000 000
158 157,9241 24,84 3500
159 158,9264 18,6ч р“(0,6; 0,9; 0,95) 0,580; 0,363 770
160 159,9271 21,86
Tb 147w 146,9243 1,61 ч р+; эз 0,139; 0,694; 1,153
148w 147,9242 70 мин Р+(4,6); ЭЗ 0,489; 0,632; 0,784;
1,077
149w 148,9233 4,1 ч Р+(1,8), а (3,97); ЭЗ 0,165; 0,352; 0,388
150w 149,9237 3,5 ч Р+(3,7), а (3,49); ЭЗ 0,496; 0,638; 0,792
151 150,9231 17,6ч а(3,41);ЭЗ 0,108; 0,252; 0,287
Строение вещества
Продолжение табл. 2.2
<-Л о
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
ТЬ 152 151,9239 17,5ч Р+(2,8); ЭЗ 0,271; 0,344; 0,587
153 152,9234 2,30 сут Р\эз 0,083; 0,102; 0,110; 0,170; 0,212
154 153,9246 21 ч р+(2,5); ЭЗ 0,123; 1,274
154"” 153,9246 9 ч р+; ЭЗ; ИП 0,123; 0,248
154w2 153,9246 23 ч ЭЗ; ИП 0,123; 0,248
155 154,9235 5,3 сут ЭЗ 0,087; 0,105; 0,180; 0,262
156 155,9247 5,3 сут Р+; эз 0,199; 0,534
156"” 155,9247 5,0 ч ип 0,088
Иб"72 155,9247 24 ч ИП; ЭЗ 0,050
157 156,9240 150 лет ЭЗ 0,054
158 157,9254 150 лет р (0,85); ЭЗ 0,080; 0,944; 0,962
159 158,9254 1 30 000
160 159,9272 72,4 сут Р (1,834) 0,299; 0,879; 0,966 525 000
161 160,9275 6,90 сут Р' (0,46; 0,52; 0,59) 0,049; 0,075
Dy 152 151,9247 2,4 ч а (3,63); ЭЗ 0,257
153 152,9258 6,3 ч р+, а (3,46); ЭЗ 0,082; 0,100
154 153,9244 3 •106лет а (2,87)
155 154,9258 10,0 ч Рг (0,85; 1,08); ЭЗ 0,227
156 155,9243 0,06
157 156,9255 8,1 ч ЭЗ 0,326
158 157,9244 0,10 96 000
159 158,9257 144,4 сут ЭЗ 0,058
160 159,9252 2,34 55 000
161 160,9269 18,90 585 000
162 161,9268 25,50 200 000
163 162,9287 24,90 140 000
164 163,9292 28,20
165 164,9317 2,33 ч Р’(1,2; 1,3) 0,095; 0,362
166 165,9328 81,5 ч Р(0,40) 0,082; 0,426
Но 160"* 159,9287 5,02 ч ИП; ЭЗ 0,087; 0,197
161 160,9279 2,5 ч ЭЗ 0,026; 0,078
162 161,9291 68 мин р+; ЭЗ; ИП 0,038
163 162,9287 33 года ЭЗ X 0,045; 0,046
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Но 165 164,9303 100
166 165,9323 26,8 ч Р" (1,854) 0,081
166Л" 165,9323 1200 лет 3(0,07) 0,081
167 166,9331 3,1 ч Р“ (0,32; 0,61; 0,97) 0,321; 0,346
Ег 158 157,9302 2,4 ч ЭЗ 0,072; 0,387
160 159,9291 28,6 ч эз X 0,047
161 160,9300 3,24 ч р+ (0,82); ЭЗ 0,826
162 161,9288 0,14 160 000
163 162,9300 75,1 мин р+(0,30); ЭЗ 1,И
164 163,9292 1,61 13 000
165 164,9307 10,34 ч ЭЗ X 0,047
166 165,9303 33,60
167 166,9321 22,95 700 000
168 167,9324 26,80 1900
169 168,9346 9,4 сут р- (0,344; 0,352) 0,008; 0,110; 0,118
170 169,9355 14,90 6000
171 170,9380 7,5 ч р-(1,06; 1,49) 0,112; 0,296
172 171,9394 49,5 ч р“ (0,278; 0,358) 0,407; 0,610
Тт 163 162,9326 1,82 ч Р+(0,71; 1,5); ЭЗ 0,1043; 0,241
165 164,9324 30,06 ч Р+(0,30); ЭЗ 0,243
166 165,9336 7,70 ч р+(1,22; 1,93); ЭЗ 0,081; 0,186
167 166,9239 9,25 сут ЭЗ 0,208; 0,532
168 167,9342 93,1 сут р-; ЭЗ 0,918; 0,448; 0,816
169 168,9342 100 115 000
170 169,9358 128,6 сут Р’ (0,968) — 99,8 %; ЭЗ (0,314) — 0,2 % 0,084 92 000
171 170,9364 1,92 года р“ (0,030; 0,097) 0,067 4500
172 171,9384 63,6 ч р-(1,79; 1,87) 0,079; 1,094; 1,387
173 172,9336 8,2 ч 3(0,9; 1,3) 0,399; 0,461
Yb 164 163,9347 75,8 мин ЭЗ 0,445; 0,675
166 165,9339 56,7 ч эз 0,082
168 167,9339 0,13 3 200 000
169 168,9352 32,0 сут ЭЗ (0,908) 0,063; 0,1100
170 169,9348 3,05 9400
171 170,9363 14,01 50 000
Строение вещества
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
УЪ 172 171,9364 21,90 400
173 172,9382 16,12 19 000
174 173,9389 31,80
175 174,9413 4,19 сут Р" (0,467) 0,114; 0,283; 0,396
176 175,9426 12,70 5500
177 176,9453 1,88 ч Р(0,16; 1,4) 0,122; 0,150
178 177,9467 74 мин Р (0,25) 0,348; 0,391
Lu 169 168,9379 34,1 ч Р+(1,27); ЭЗ 0,191; 0,960; 1,450
170 169,9385 2,2 сут Р(2,39); ЭЗ 0,084
171 170,9379 8,22 сут Р+(0,667); ЭЗ
172 171,9391 6,7 сут ЭЗ 0,182
173 172,9389 499 сут ЭЗ 0,079
174 173,9404 3,3 года Р+(0,38); ЭЗ 0,076; 1,242
174м 173,9404 142 сут ИП; ЭЗ 0,067
175 174,9408 97,41 21 000
176 175,9427 2,59 2,2 • 1010 лет р-(1,02) 0,088 7000
176м 175,9427 3,68 ч р- (1,22; 1,32) 0,088
177 176,9438 6,71 сут Р (0,497) 0,11296
177м 176,9438 160,1 сут Р (0,2); ИП 0,1216
179 178,9473 4,6 ч Р~(М) 0,2143
Hf 170 169,9308 15,9 ч ЭЗ 0,165; 0,621
171 170,9406 12,1 ч Р+; эз 0,122; 0,662; 1,071
172 171,9395 1,87 года ЭЗ (0,35) 0,024; 0,067; 0,126
173 172,9407 23,6 ч эз 0,124; 0,140; 0,297; 0,311
174 173,9401 0,16 2,0 • 10,5лет а (2,55) 390 000
175 174,9408 70 сут ЭЗ (0,686) 0,344 X0,053; 0,054; 0,062
176 175,9414 5,21 15 000
177 176,9432 18,60 380 000
178 177,9437 27,30
178м 177,9437 31 год ИП 0,217; 0,495; 0,574
179 178,9458 13,63 65 000
179м 178,9458 25 сут ИП 0,123; 0,146; 0,363; 0,454
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Hf 180 179,9466 35,10 12 600
180"1 179,9466 5,5 ч ИП 0,057; 0,215; 0,332; 0,443
181 180,9491 42,4 сут р- (1,027) 0,133; 0,346; 0,482
182 181,9506 9 • 106лет 0(0,431) 0,114; 0,156; 0,270
182w 181,9506 62 мин 0 (0,5; 1,0); ИП 0,224; 0,344
183 182,9535 64 мин 0(1,0; 1,2; 1,5) 0,073; 0,459; 0,784
184 183,9555 4,12 ч P’(U) 0,139; 0,181,0,345
Та 173 172,9438 3,6 ч 0+(2,5); ЭЗ 0,070; 0,090; 0,160; 0,172
174 173,9442 1,1 ч Р+(2,5; 2,8); ЭЗ 0,091; 0,207, 1,206
175 174,9438 10,5 ч р+;эз 0,082; 0,207; 0,267; 0,349
176 175,9448 8,1 ч Р+; ЭЗ 0,088; 1,159; 1,225
177 176,9445 56,6 ч Р+; эз 0,113; 0,208
178 177,9458 2,4 ч р+(0,8; 0,9); ЭЗ 0,089; 0,213; 0,326; 0,426
179 178,9460 1,7 года ЭЗ X0,055; 0,056
180 179,9475 0,01 >1 • 1013лет р'; эз
180w 179,9475 8,1 ч р-(0,6; 0,7); ЭЗ 0,093; 0,104
181 180,9480 99,99 22 000
182 181,9502 114,5 сут р- (1,811) 0,068; 1,121; 1,221 8 200 000
183 182,9514 5,1 сут Р’ (0,47; 0,62) 0,108; 0,161; 0,246; 0,354
184 183,9540 8,7 ч Р"(1,19) 0,253; 0,414; 0,921
W 176 175,9457 2,3 ч ЭЗ 0,098; 0,133
177 175,9466 135 мин р+;эз 0,116; 0,186; 0,427; 1,036
178 177,9459 21,5 сут эз X0,056; 0,058
180 179,9467 0,12
181 180,9482 121,2 сут эз 0,136; 0,153
182 181,9482 26,30 20 700
183 182,9514 14,28 10 200
184 183,9540 30,70 1800
Строение вещества
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
W 185 186 187 188 184,9556 185,9586 186,9572 187,9585 28,60 74,8 сут 23,9 ч 69,4 сут ₽’ (0,433) Р(1,312) 0’ (0,35) 0,125 0,072; 0,480; 0,686 0,064; 0,227; 0,291 37 000 90 000
Re 181 182 182w 183 184 184'” 185 186 186w 187 188 189 190m 180,9502 181,9512 181,9512 182,9508 183,95261 183,9526 184,9530 185,9544 185,9544 186,9558 187,9581 188,9592 189,9619 37,40 62,60 20 ч 64 ч 12,7 ч 70 сут 38 сут 169 сут 88,9 ч 2 • 105лет 4,5 • Ю10лет 16,98 ч 24,3 ч 3,2 ч ЭЗ ЭЗ 0+(1,74); ЭЗ ЭЗ эз ИП; ЭЗ 0(1,071) — ип р- (0,031) Р"(2,Ю) • Р’ (0,8; 1,0) Р'(1,6) 92 %; ЭЗ — 8 % 0,361; 0,366; 0,639 0,100; 0,229; 1,121, 1,222 0,100, 1,121; 1,189; 1,222 0,046; 0,162 0,111,0,792 0,105; 0,217; 0,921 0,137 0,040; 0,059 0,155; 0,633 0,217; 0,219; 0,245 0,119; 0,187 110 000 <2000
Os 182 183 183й 184 185 186 187 188 189 190 191 19Г 192 193 181,9521 182,9533 182,9533 183,9525 184,9541 185,9539 186,9558 187,9553 188,9582 189,9585 190,9609 190,9609 191,9615 192,9642 0,02 1,58 1,64 13,3 16,1 26,4 41,0 22,0 ч 13 ч 9,9 ч 9,36 сут 2 • 1015 лет 15,4 сут 13,1 ч 30,6 ч ЭЗ 0+; ЭЗ ЭЗ; ИП ЭЗ (1,015) а (2,75) р-(0,313) ИП Р“ (1,0; 1,3) 0,056; 0,180; 0,263; 0,510 0,114; 0,168; 0,382 1,102; 1,108 0,646 0,130 0,074 0,073; 0,139; 0,461 < 200 000 12 000
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, a. e. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Os 194 193,9652 6,0 дет Р“ (0,05; 1,0) 0,043
Ir 184 183,9576 3,0 ч рт (2,5; 2,9); ЭЗ 0,120; 0,264; 0,390
185 184,9568 14ч р+; ЭЗ 0,037; 0,097; 0,223; 0,254
186 185,9580 1,7 ч р~(0,8; 1,9; 2,6); ЭЗ 0,137; 0,630
186w 185,9580 16 ч Р+(1,9); ЭЗ 0,137; 0,297; 0,435
187 186,9574 10.5 ч ЭЗ 0,409; 0,427; 0,611; 0,913
188 187,9589 41.5 ч р (1,6); ЭЗ 0,155; 0,478; 0,633
189 188,9587 13.1 сут ЭЗ 0,070; 0,245
190 189,9606 11.8 сут эз 0,187; 0,519
190"" 189,9606 1,2 ч ип 0,026
190"12 189,9606 3,2 ч ЭЗ; ИП 0,187; 0,361; 0,503, 0,616
191 190,9606 37,3 300 000
192 191,9626 73.83 сут р’ (1,454); ЭЗ 0,317; 0,468
193 192,9629 62,7 110 000
193"1 192,9629 10.6 сут ИП 0,082
194 193,9651 19.2 ч Р“ (2,24) 0,294; 0,328
194m 193,9651 0,47 года Р 0,329; 0,483
195 194,9640 2,5 ч Р (1,0; 1,2) 0,099; 0,130
195"1 194,9640 3,8 ч Р’ (0,4; 0,8) 0,320, 0,365
196™ 195,9684 1,40 ч Р“ (1,0; 1,2) 0,355; 0,394
Pt 186 185,9594 2,0 ч а (4,23); ЭЗ 0,612; 0,689
187 186,9605 2,35 ч Р'; эз 0,106; 0,110; 0,205; 0,285; 0,709
188 187,9594 10,2 сут а; ЭЗ 0,188; 0,195
189 188,9607 10,9 ч р+(0,48; 0,88); ЭЗ 0,244; 0,569; 0,608; 0,721
190 189,9599 0,01 6,9 10"лет а (3,18)
191 190,9617 2,9 сут ЭЗ 0,360; 0,409; 0,539
192 191,9610 0,79 -1015 лет
193 192,9630 50 лет ЭЗ X 0,063; 0,065
193™ 192,9630 4,3 сут ип 0,136
Строение вещества
Продолжение табл. 2.2
и» о\
Элемент Массовое ЧИСЛО Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Pt 194 193,9627 32,9 1200
195 194,9648 33,8 27 000
195м 194,9648 4,02 сут ИП 0,259
196 195,9649 25,3 900
197 196,9673 18,3 ч р“ (0,719) 0,077; 0,191
198 197,9679 7,22 4000
200 199,9714 12,6ч 0,076; 0,136
Аи 191 19,9636 3,2 ч ЭЗ 0,586; 0,674
192 191,9648 5,0 ч Р+(2,49); ЭЗ 0,296; 0,317; 0,612
193 192,9642 17,5ч ЭЗ 0,186; 0,256; 0,268
194 193,0654 39,5 ч р+(1,2; 1,5); ЭЗ 0,294, 0,329; 1,469
195 194,9650 186,1 сут ЭЗ (0,230) 0,099
196 195,9665 6,18 сут р- (0,26); ЭЗ 0,333
196м 195,9665 9,7 ч ИП 0,148
197 196,9666 100 98 800
198 197,9682 2,693 сут Р~ (1,372) 0,412 25 800 000
198м 197,9682 2,30 сут ИП 0,097; 0,180 25 800 000
199 198,9688 3,14 сут Р~ (0,453) 0,158; 0,208 30 000
200м 199,9707 18,7ч Р (0,56); ИП 0,256; 0,333; 0,368; 0,498; 0,579
Hg 192 191,9657 4,9 ч ЭЗ 1,157; 0,275; 0,307
193 192,9642 4 ч ЭЗ 0,187; 0,258
193м 192,9642 11ч Р+ (0,4; 1,2); ЭЗ 0,408; 0,573
194 193,9654 260 лет ЭЗ X 0,067; 0,069
195 194,9650 10ч ЭЗ 0,0612; 0,780
195м 194,9650 41 ч ЭЗ; ИП 0,388; 0,560
196 195,9665 0,15
197 196,9672 64,1 ч ЭЗ (0,600) 0,077; 0,191
197м 196,9666 23,8 ч ИП; ЭЗ 0,134
198 197,9682 10,10
199 198,9688 17,00 2 000 000
200 199,9707 23,10 < 60 000
201 200,9717 13,20 < 60 000
202 201,9706 29,60 4900
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Hg 203 202,9729 46,6 сут 0 (0,492) 0,279
204 203,9735 6,85 430
Т1 195 194,9701 1,16ч 0+ (1,8); ЭЗ 0,564; 0,885
196 195,9706 1,84 ч 0+; ЭЗ 0,426
196'" 195,9706 1,41 ч 0"; ЭЗ; ИП 0,426; 0,635; 0,695
197 196,9696 2,84 ч 0+ (1,2); ЭЗ 0,152; 0,426
198 197,9705 5,3 ч 0" (1,4; 2,1; 2,4); ЭЗ 0,412; 0,637
198"1 197,9705 1,87 ч 0’; ЭЗ; ИП 0,283; 0,412; 0,587; 0,637
199 198,9699 7,4 ч ЭЗ 0,158; 0,208; 0,247; 0,456
200 199,9710 26,1 ч 071,07; 1,44); ЭЗ 0,368; 0,579; 0,828; 1,206
201 200,9708 73 ч ЭЗ 0,135; 0,167
202 201,9721 12,2 сут эз 0,440
203 202,9723 29,52 10 000
204 203,9739 48 3,78 года 0" (0,763); ЭЗ 0,069; 0,071
205 204,9744 70,5 0“ (4,994) 500
208 207,9820 3,052 мин
РЬ 198 197,9722 2,4 ч ЭЗ 0,173; 0,290
199 198,9729 1,5 ч ЭЗ; 0+ (2,8) 0,353; 0,367
200 199,9719 21,5 ч ЭЗ 0,148; 0,236; 0,257; 0,268
201 200,9728 9,4 ч ЭЗ; 0+(0,6; 2,5)
202 201,9722 3 •1О5года ЭЗ 0,071; 0,073
203 202,9734 52,0 ч эз 0,279
204 203,9730 1,40 660
205 204,9745 1,1 • 107 года ЭЗ (0,052) X 0,071; 0,073
206 205,9745 24,10 30
207 206,9759 22,10 710
208 207,9766 52,40 20
209 208,9811 3,25 ч 0“ (0,64)
210 209,9842 22,3 года 0" (0,061) — 19 %; а (0,063) — 81 % 0,047
Строение вещества
Продолжение табл. 2.2
ел 00
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
РЬ 212 211,9919 10,64 ч (0,33; 0,57) 0,239; 0,300
214 213,9998 26,8 ч р (1,032) — 48 %; 0" (0,73) — 52% 0
Bi 201 200,9770 1,8 ч ЭЗ; 0+ 0,628; 0,902; 0,936; 1,326
202 201,9774 1,7 ч ЭЗ; 0+ 0,422; 0,658; 0,961
203 202,9768 11,8ч ЭЗ; 0+(О,7; 1,4) 0,820; 0,825; 0,897; 1,848
204 203,9777 11,2ч ЭЗ 0,375; 0,899; 0,984
205 204,9774 15,3 сут ЭЗ; 0+(1,ОО) 0,703; 0,988; 1,764
206 205,9785 6,243 сут ЭЗ (3,761); р+ 0,516; 0,803; 0,881
207 206,9785 32,3 года ЭЗ (2,40); р+ 0,570; 1,064
208 207,9797 3,68- 105 лет ЭЗ (2,878) 2,615
209 208,9804 100 19
210 209,9841 5,01 сут Р (1,16); а 54
21 О'” 209,9841 3,0- 106лет а (4,96); |Г 0,266; 0,305
212 211,9913 60,6 мин 0" (2,25); а (6,051; 6,090) 0,727; 1,621
Ро 204 203,9804 3,57 ч а (5,38); ЭЗ 0,270; 0,884; 0,016
205 204,9811 1,80 ч а (5,22); 0+; ЭЗ 0,837; 0,850; 0,872; 1,001
206 205,9805 8,8 сут а (5,22); ЭЗ 0,286; 0,511; 0,807; 1,032
207 206,9816 5,8 ч а (5,12); 0+; ЭЗ 0,743; 0,912
208 207,9812 2,90 года а (5,11); ЭЗ 9,292; 0,571
209 208,9824 105 года а (4,976); ЭЗ 0,261; 0,263
210 209,9829 138,38 сут а (5,407) 0,804
211 210,9866 0,52 с а (7,594)
212 211,9889 0,296 мкс а (8,784)
214 213,9987 163 мкс а (7,687) 0,800
216 216,0019 0,15 с а (6,906)
218 218,0089 3,11 мин а (6,114)
At 207 206,9857 1,8 ч а (5,759); р‘; ЭЗ 0,301; 0,588; 0,814
208 207,9864 1,63 ч а (5,641); 0+; ЭЗ 0,177; 0,660; 0,685
209 208,9862 5,4 ч а (5,647); ЭЗ 0,545; 0,782; 0,790
210 209,9871 8,1 ч а (5,63) <1 %; 0+; ЭЗ (3,98) 0,245; 1,181; 1,483
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
At 211 210,9875 7,21 ч а (5,981) — 41 %; ЭЗ (0,784) — 59% 0,687
Rn 210 209,9897 2,4 ч а (6,040); ЭЗ 0,458
211 210,9906 14,6ч а (5,78; 5,85); р+; ЭЗ 0,674; 0,678; 1,363
219 219,0095 3,96 с а (6,946)
220 220,0114 55,6 с а (6,404)
222 222,0176 3,82 сут а (5,590) 0,510 720
224 1,8 ч Р’ (0,2601; 0,2655)
Fr 212 212,9961 20 мин ЭЗ (5,070) — 57 %; а (6,529) — 43 %
218 218,0076 0,7 мкс а (7,56; 7,86)
223 223,0197 21,8 мин р- (1,47); а (5,34) 0,050; 0,080; 0,235
Ra 223 223,0185 11,43 сут а (5,979) 0,144; 0,154
224 224,0202 3,66 сут а (5,789) 0,2410
225 225,0236 14,8 сут Р‘ (0,32) 0,040
226 226,0254 1,608 • 103 лет а (4,780) 0,1862 20 000
228 228,0311 5,75 лет Р" (0,045); а (0,0135; 0,0162)
230 230,0371 93 мин Р’(0,5; 1,2) 0,072
Ac 224 224,0217 2,9 ч а (6,057; 6,139; 6,211); ЭЗ 0,133; 0,157; 0,217
225 225,0232 10,0 сут а (5,935) 0,100; 0,150
226 226,0261 29 ч р-(0,9; 1,1); ЭЗ 0,158; 0,230; 0,254
227 227,0278 21,773 года р (0,041) — 98,6 %; а (5,043) — 1,4% 0,100 810 000
228 228,0310 6,13 ч Р'(2,142) 0,338; 0,911; 0,964; 0,969
229 229,0330 62,7 мин Р’(1,1) 0,165; 0,569
Th 227 227,0277 18,718 сут а (5,757; 5,978; 6,038) 0,050; 0,236; 0,256
228 228,0287 1,913 года а (5,520) 0,084; 0,216 120 000
229 229,0318 7,3 • 103 лет а (5,168) 0,031; 0,125
230 230,0331 7,53 • 104лет а (4,771) 33 000
231 231,0363 25,52 ч р" (0,389) 0,026; 0,084
232 232,0381 100 1,40 • Ю10лет а (4,081) 7400
234 234,0436 24,10 сут р-(0,270) 0,063; 0,094
Строение вещества
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Ра 228 229 230 231 232 233 234 234"* 228,0310 229,0321 230,0345 231,0363 232,0381 233,0416 234,0436 234,0436 22 ч 1,4 сут 17,4 сут 3,27- 104лет 1,31 сут 27,0 сут 6,70 ч 1,18 мин а (5,80; 6,08); ЭЗ а (5,67); ЭЗ а (5,58); Р (0,40; 0,51); ЭЗ а (5,148) Р"(1,34) Р‘ (0,572) Р~ (2,199) Р(2,28) 0,463; 0,911; 0,965; 0,969 0,042 0,952 0,027 0,150; 0,894; 0,969 0,300; 0,312; 0,341 0,131 0,766; 1,001 200 000
и 230 231 232 233 234 235 236 237 238 239 240 230,0339 231,0363 232,0371 233,0396 234,0409 235,0439 236,0456 237,0487 238,0508 239,0543 240,0566 0,005 0,72 99,275 20,8 сут 4,2 сут 71,8 года 1,59- 105лет 2,45 • 105лет 7,04 • 108 лет 2,34 • 107лет 6,75 сут 4,46 • 109 лет 23,5 мин 14,1 ч а (5,818; 5,888) а (5,46); ЭЗ а (5,26; 5,32); СД а (4,784; 4,824) а (4,856) а (4,679); СД а (4,569) Р’ (0,24; 0,25) а (4,039); СД Р~ (1,2; 1,3) Р (0,4) 0,072 0,026; 0,084; 0,220 0,058 0,317 0,053 0,144; 0,186 0,049 0,060; 0,208 0,050 0,075 0,044 75 000 100 500 6000 2720
Np 234 235 236 236"* 237 238 239 240 234,0429 235,0441 237,0482 238,0509 239,0529 240,0561 4,4 сут 396 сут 22,5 ч 1,15 • 105 лет 2,14 • 106лет 2,117 сут 2,32 сут 67 мин Р’ (0,8); ЭЗ а (5,02); ЭЗ Р" (0,5); ЭЗ Р"; ЭЗ а (4,957) Р (0,25; 0,28 1,24) Р’ (0,33; 0,44) Р (0,9) 1,528; 1,559 0,084 0,642; 0,688 0,104; 0,160 0,029; 0,087 0,984; 1,026; 1,029 0,106; 0,228; 0,278 0,566, 0,974 170 000
Pu 234 236 237 238 239 240 241 234,0433 236,0466 237,0462 238,0509 239,0522 240,0561 241,0568 8,8 ч 2,85 года 45,4 сут 87,74 года 24,113 лет 6,57- 103 лет 14,6 лет а (6,15; 6,20); ЭЗ а (5,72; 5,77); СД а (5,36; 5,65); ЭЗ а (5,457; 5,499); СД а (5,244); СД а (5,124; 5,168) Р’ (0,0208); а (4,854; 4,897) 0,476 0,060 0,0435 0,052; 0,129 0,045; 0,104 0,104; 0,149 560 000 265 700 290 000 360 000
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Ри 242 242,0587 3,76 • 105лет а (4,983); СД 0,045 20 000
243 243,0620 4,96 ч Р (0,48; 0,58) 0,084 1800
244 244,0642 8,2- 107лет а (4,665); СД
245 245,0678 10,5 ч 0" (0,9; 1,2) 0,327; 0,560
246 246,0701 10,85 сут Г (0,2; 0,3) 0,044; 0,180; 0,224
Ат 237 237,0501 1,22 ч а (6,04); ЭЗ 0,280; 0,438
238 238,0530 1,63 ч а (5,94); ЭЗ 0,919; 0,963
239 239,0530 11,9ч а (5,776); ЭЗ 0,228; 0,278
240 240,0522 50,8 ч а (5,378); ЭЗ 0,889; 0,988
241 241,0568 432,2 года а (5,637); СД 0,060 70 000
242 242,0595 16,02 ч 0“ (0,619; 0,661); ЭЗ 0,042; 0,045
242т 242,0595 141 год а (5,207); СД 0,049; 0,067; 0,087 2 400 000
243 243,0615 7370 лет а (5,439); СД 0,075 180 000
244 244,0643 10,1 ч 0’ (0,39) 0,154; 0,746; 0,900
245 245,0664 2,05 ч 0(0,91) 0,253
Ст 238 238,0530 2,3 ч а (6,52); ЭЗ
239 239,0549 2,9 ч ЭЗ 0,19
240 240,0555 27 сут а (6,248; 6,291); СД
241 241,0576 32,8 сут а (5,939); ЭЗ 0,472
242 242,0588 162,9 сут а (6,126); СД 0,044 20 000
243 243,0614 28,5 года а (5,742; 5,784); ЭЗ; СД 0,210; 0,228; 0,278 250 000
244 244,0627 18,11 лет а (5,902); СД 0,043 13 000
245 245,0655 8500 лет а (5,623); СД 0,133; 0,174 250 000
246 246,0672 4,78 • 103 лет а (5,476); СД 0,045 8400
247 247,0703 1,56 • 107 лет а (5,352); СД 0,278; 0,402
248 248,0723 3,4 • 105 лет а (5,162); СД 6000
249 249,0760 65 мин 0(0,9) 0,634
250 250,0784 < 1,13 • 104лет СД
Вк 243 243,0630 4,5 ч а (6,542; 6,574); ЭЗ 0,755; 0,946
244 244,0651 4,4 ч а (6,625; 6,667); ЭЗ 0,218; 0,892; 0,922
245 245,0664 4,90 сут а (5,88; 6,15); ЭЗ 0,253; 0,381
246 246,0687 1,80 сут ЭЗ 0,799; 0,834; 1,081; 1,124
247 247,0703 1,4 • 103 лет а (5,889) 0,084; 0,265
248 248,0730 23,5 ч 0~ (0,65); ЭЗ 0,551
Строение вещества
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Вк 249 249,0750 0,32 года а (5,417); Р (0,129; 0,327); СД 1 000 000
250 250,0783 3,21 ч Р(0,72; 1,76) 0,989; 1,032
Cf 246 246,0688 35,7 ч а (6,72; 6,76); СД 0,042; 0,096
247 247,0710 3,11 ч а (6,30); ЭЗ 0,294; 0,418
248 248,0722 333 сут а (6,26); СД
249 249,0748 351 год а (6,295); СД 0,333; 0,388 300 000
250 250,0764 13,1 года а (5,989; 6,031); СД 0,043 1 500 000
251 251,0796 890 лет а (6,172) 0,177 2 100 000
252 252,0816 2,64 года а (6,217); СД 0,043
253 253,0851 17,8 сут р-(0,3); а (5,98)
254 254,0873 60,5 сут а (5,79; 5,83); СД
Es 249 249,0763 1,70 ч а (6,77); ЭЗ 0,375; 0,380; 0,813
250 250,0786 8,6 ч ЭЗ 0,3034; 0,349; 0,829
250m 250,0786 2,1 ч ЭЗ 0,989; 1,032
251 251,0800 33 ч а (6,49); ЭЗ 0,153; 0,188
252 252,0828 472 сут а (6,739); ЭЗ 0,1390; 0,785
253 253,0848 20,47 сут а (6,739); СД 0,3892
254 254,0880 275 сут а (6,617); СД 0,063 < 40 000
254™ 254,0880 39,3 ч Р’ (0,5; 1,1); а; ЭЗ (6,382) 0,649; 0,694
255 255,0903 39,8 сут а (6,30); Р’ (0,300) 0,0326
256 256,0937 7,6 ч ₽’ 0,11; 0,17
Fm 251 251,0816 5,3 ч а (6,783; 6,834); ЭЗ 0,453
252 252,0825 25,4 ч а (7,04); СД
253 253,0852 3,0 сут а (7,200) — 12 %; ЭЗ (0,324) — 88% 0,272
254 254,0868 3,24 ч а (7,303); СД 0,042; 0,094
255 255,0900 20,1 ч а (7,240); СД 0,204
256 256,0918 2,63 ч а (6,92); СД
257 257,0951 100,5 сут а (6,871); СД 0,179; 0,242
Md 256 256,0939 75 мин а (7,15; 7,22); ЭЗ 0,40
257 257,0956 5,0 ч а (7,07); ЭЗ
258 258,0986 56 сут а (6,716) — 72 %; а (6,79) — 28 %; СД
259 235,0441 1,6 ч а; СД
Новый справочник химика и технолога
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
No 251 252 253 254 255 256 257 258 259 259,1009 0,8 с 4,5 с 95 с 65 с 180 с 3,7 с 23 с 1,2 • 10 3 с 58 мин а (8,6); СД а (8,41); СД а (8,01); СД а (8,11); СД а (8,09); СД а (8,42); СД а (8,25); СД СД а (7,94) — 78 %; ЭЗ — 22 %
Lr 255 256 257 258 259 260 260,1054 21 с 33 с 0,6 с 4,2 с 5,4 с 3,0 мин а (8,37); СД а (8,42); СД а (8,87); СД а (8,62); СД а (8,45); СД а (8,04)
Rf 255 256 257 258 259 260 261 262 263 255,1015 256,1012 257,1030 258,1035 259,1055 260,1065 261,1087 262,1101 263,1125 1,7 с 0,007 с 4,8 с 0,012 с 3,1 с 0,02 с 65 с 1,2 с 10 мин а; СД СД а (9,20); СД; ЭЗ СД а (9,20); СД; ЭЗ а; СД а (8,60) СД а; СД 0,12
Db 255 256 257 258 259 260 261 262 263 255,1074 256,1081 257,1079 258,1093 259,1097 260,1114 261,1121 262,1138 263,1153 1,6 с 2,6 с 1,5 с 4,2 с 1,2 с 1,5 с 1,8 с 34 с - 30 с а; СД а; СД; ЭЗ а; СД; ЭЗ а (8,45; 9,02); СД; ЭЗ а а; СД; ЭЗ а; СД а; СД; ЭЗ а; СД
Sg 258 259 258,1132 259,1147 0,0029 с 0,9 с а; СД а
Строение вещества
Продолжение табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е. м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Sg 260 261 263 265 266 260,1144 261,1162 263,1182 265,1211 266,1219 0,0036 с 0,23 с 0,8 с 16 с 20 с а а; СД а а а; СД
Bh 260 261 262 263 264 265 266 267 260,1218 261,1218 262,1229 263,1231 264,1247 265,1251 266,1270 267,1277 0,0118 с 0,102 с 0,44 с а а; СД а; СД а а а
Hs 263 264 265 266 267 268 269 263,1287 264,1284 265,1302 266,1300 267,1318 268,1321 269,1341 1 с 0,00008 с 0,0018 с 0,033 с 9,3 с а а; СД а; СД а; СД а
Mt 265 266 267 268 269 270 271 265,1366 266,1376 267,1375 268,1388 269,1391 270,1407 271,1412 0,0034 с 0,70 с а; СД а
Ds 267 268 269 270 271 272 267,1440 268,1435 269,1451 270,1446 271,1461 272,1463 3 • 10“6 с 1,7 • 104 с 0,0011 с 0,00086 с а а а СД
Новый справочник химика и технолога
Окончание табл. 2.2
Элемент Массовое число Относительная атомная масса, а. е.м. Содержание в природной смеси, % Период полураспада Тип (Энергия распада, МэВ) Энергия у-излучения, МэВ Сечение захвата тепловых нейтронов, мб
Ds 273 273,1492 0,00018 с а
Rg 272 272,1535 0,0015 с а
UUb 277 285 -227 -285 0,00024 с 0,00028 с а а
Uut 283 284 -283 -284 0,147 с 0,376-1,196 с а а
Uuq 287 288 289 -287 -288 -289 -5,5 с 1,9 с 20-30 с а а
Uup 287 288 -287 -288 0,0466 с 0,0186-0,280 с а а
Uuh 292 -292 а
Литература
1. Справочник химика / Под ред. Б.П. Никольского. Л.: Химия, 1971. Т. 1. С. 180-299.
2. Ефимов А.И., Белорукова Л.П., Василькова И.В., Чечев В.П. Свойства неорганических соединений. Л.: Химия, 1983. С. 21-56.
3. Эмсли Дж. Элементы. М.: Мир, 1993. 256 с.
4. Lederer С.М., Shirley V.S. Tables of isotopes. N.-Y.: John Willey & Sons, 1978.
5. Fuller G.H. П J. of Phys. Chem. Ref. Data. 1976. Vol. 5. P. 835.
6. L’Annunziata M.F. Radionuclide tracers. N.-Y.; London: Academic Press, 1967.
Строение вещества
66
Новый справочник химика и технолога
2.3. Цепочки распада, периоды полураспада и выходы продуктов деления урана-235 на тепловых нейтронах
Ниже приведены цепочки распада осколков деления урана-235 под действием тепловых нейтронов, периоды полураспада каждого осколочного изотопа и выходы. Выход в процессе деления — доля делений, приводящая к рассматриваемому ядру непосредственно или в результате последующего 0-распада. Для каждого изотопа указан период полураспада и абсолютный выход в процентах, если он известен. Числа, обозначающие величину абсолютного выхода, напечатаны жирным шрифтом.
Если распад данного осколочного изотопа происходит двумя путями, то указываются относительные вероятности каждого распада.
В скобках указаны периоды полураспада изотопов, существование которых вероятно, но экспериментально не доказано.
Знак «*» обозначает изомер.
Выход последнего изотопа в цепочке обычно представляет собой выход цепочки. Более низкие значения выходов изотопов, стоящих ближе к началу цепочки распада, могут обусловливаться:
а) независимым выходом последующих членов цепочки;
б) ответвлениями цепочки;
в) неточностью экспериментальных данных.
^Zn-^-^Ga------> 3lGe
49 ч 14,1ч стабилен
1,6 • 10"5
30 Zn — > - > 32 Ge
(< 2 мин) 5,0 ч стабилен
1,1 • 10 4
77*/-
32 Ge
12 ч 38,7 ч стабилен
0,0031 0,0083
78 Ge___> 78 As_> 78 Se
32 * 33* 34 °C
86 мин 91 мин стабилен
0,019 0,021
^As ;49Se-----------------э-£вг
9,0 мин ~6 • 104 лет стабилен
0,056
81‘Са
34 Se
56,6 мин
0,0084
38’Se-^38’Br
17,6 мин стабилен
0,14
Строение вещества
67
85 Se
34 ОС
40 с
10,3г
0,293
збКг стабилен
2,02
SSe-^ 875Вг—38бКг-^-> 37Rb
17 с 55с^\о,о2 78 мин 6 1010лет
"Ч 2,49
зб Кг
стабилен
87 Кг
88Вг^^ 88Кг—> 878ИЬ-^-> SSr
15,5 с 2,8 ч' 17,8 мин стабилен
3,57
68
Новый справочник химика и технолога
*!Вг—> *9Кг—-
35 р- 36 р-
4,5 с 3,2 мин
4,59
37 Rb------->
15,4 мин
стабилен
1,4 с 33 с
5,0
v ЭД Qr ' 38ЙГ р- 90 у ? 391 р- -4 90Zr ' 40
2,7 мин 28 лет 64,3 ч стабилен
5,77 5,77
з>- -v^SRb- ——> «Sr-р- 38 > 92 у р- У 39* р- -4 92 Zr ' 40^'
3,0 с 80 с 2,7 ч 3,6 ч стабилен
1,87 5,3 6,03
2,0 с
₽-
37Rb —
короткоживущий
2кг- -V^'"Rb г -4 94 Qr 4 94 V ' 38°* р- ' 391 р- -4 94Zr ' 40
1,4 с коротко- ~2 мин 16,5 мин стабилен
живущий 5,4 6,40
Строение вещества
69
96 Zr стабилен
6,33
:*мо
стабилен
5,78
99 Zr________>
40 р- '
30 с
3 мин
2,1• 105 лет стабилен
72мо стабилен 6,30
v гТ'/> к ^Dn
42 Мо - > 43ТС - > 4Д Ru
14,4 мин 14,3 мин стабилен
~5,6 5,0
70
Новый справочник химика и технолога
(< 2,5 мин) 18 мин стабилен
1,8
105 Мо______> 105 Тс____
42iV1U * 43 1 С р-
(<2мин) 10 мин
Р"
35,3 ч
105 Pd
46 1 u
стабилен
106 т) . v lOOrjj
44RU““« Rh—у-> 46Pd
1,01г 30 c стабилен
22 мин 7 • 106 лет стабилен
0,19
‘«Тс *2Ru ’4°> ^Pd
(< 1 мин) 4,4 мин 18 с стабилен
Строение вещества
71
109
46
Pd
13,4ч
0,030
,о:;а8
39,2 сек
т
стабилен
«А8-Т-+ ~Cd
21,0 ч 3,14 ч стабилен
0,010
«Ag-------> ‘IJCd
2,4 мин 5 с стабилен
115r»j --- 115 а---------^-115^1 115т--------Н5е„
46 Pd р 47 Ag 4g Cd 49 In Р 50$^
45 с 21 мин 53 ч 6 • 1014 лет стабилен
0,0077 0,0097
116 л 116/~< j
47Ag-y-> 48Cd
2,5 мин
стабилен
72
Новый справочник химика и технолога
1,1 мин 50 мин 70 мин стабилен
«Cd—'"In—'J’Sn
10 мин 17,5 стабилен мин
^Sn-^’^Sb 21,5 ч стабилен
0,015
136 сут стабилен
123*С« v 123Ск
50Sn ~ р- ’ > 5! Sb
(40 мин) стабилен
9,6 сут 2,0 г стабилен
0,013 0,021
126 q . . 126qp_
50Sn—у» 51Sb--------> 52Те
50 мин 9 ч стабилен
0,05
Строение вещества
73
^Sn-^’^Sb-^^Sb
57 мин 10,3 мин стабилен
0,37
129*Те
Х521С
37 сут
0,35
129gu 0,64 ч 129т~_. 129 т . 129
51 Sb-р^~> 52Те—531—54 Хе
4,6 ч 72 мин 1,7-107 лет стабилен
0,9
v v 130 >т«
50Sn—р^-> 51Sb—52Те
2,6 мин 10,0 мин стабилен
2,0
132q '32qi_ v 132т . 132 j .
50Sn-y-> 51Sb~У"'> 52Те “У”•> Зз'-у-»
2,2 мин 2,1 мин 77 ч 2,30 ч ~4,7
'^Хе
стабилен
4,38
74
Новый справочник химика и технолога
'«Sb '«Те '*1--------------------> '“Хе
(0,8 мин) 44 мин 52,5 мин стабилен
6,9 7,8 8,06
’53бВа
стабилен
9,2 ч
6,3
86 с стабилен
3,1 6,46
24 с 3,9 мин 29 лет стабилен
6,15
я Хе
3,9 мин
138 т l-^V/х < 138
531—jF~> 54Хе——-> 55Cs—56Ва
5,8 с 17 мин 32,2 мин стабилен
5,74
139 j 53 1 2,7 с Г > 54АС 41 с 5,5 > l39Cs р- ? 55 Р- 9,5 мин -> '^Ва 56 р- 84 мин 6,55 -> '^7 La стабилен
“Хе- > l40Cs- Г ? 55^ . 1401") —-—> ч,Ва Р 56 р- -> ,4°Се JO
16 с 66 С 12,8 сут 40,2 ч стабилен
3,8 6,32 6,32 6,44
> 141 Cs р- > 55'""' р- -> l4jBa—— 56 р- -> 14'La - —--> '^Се—— Р 58 р- -> 141Рг ' 59Г1
1,7 с (коротко- 18 мин 3,7 ч 33 сут стабилен
1,34 живущий) 6,3 6,4 ~6,0
Строение вещества
75
-Ba^-^’^La^^'SCe
6 мин 75 мин стабилен
5,95
“Хе- 1 с > 143 Cs р- > 55 Р (короткоживущий) V D„ 56Ва р- (< 0,5 мин) V '43 Т > 57 La Р 18 мин -> 143 Се- ' 58VC 33 ч > 143 Рг р > 59 р- 13,7 сут 'SNd стабилен
0,051 5,7 5,98
144 Се—- 38 р —>|44рг ' 59Г1 р- '^Nd
285 сут 17,4 мин 5 • 1015 лет
~6,0 5,67
14gCe—- 58 р 145 рг ' 59Г1 р- ->'6oNd
3,0 мин 5,95 ч стабилен
3,95
146 Се 58 р _> 146 рг 59 Г1 р- -+14б>
13,9 мин 24,4 мин стабилен
3,07
,47Nd- 60 1>u Т-+“Рт- -^'б>
11,1 2,65 г 1,3 • 10" лет
-2,7 2,38
l48Nd
60 1>u
стабилен
0,67
149 Nd 60 р- (2,0 ч) -^Рт- 54 ч -V^Sm стабилен 1,13
150 Nd 60 1>u стабилен 0,67
«Nd 6 -^«Sm ₽ ->«Еи
(13 мин) 27,5 ч 80 лет стабилен
0,45
76
Новый справочник химика и технолога
'jSm стабилен 0,285
47 ч стабилен
0,15
«Sm
стабилен
0,077
24 мин 1,9 лет стабилен
0,033 -0,03
^Sm-^’^Eu-^^Gd
-10 ч 15,4 сут стабилен
0,013 0,014
'"Eu-^^Gd
15,4 ч стабилен
0,0078
1581-,, . 158z-j
бзЕи^—> 64 Gd
60 мин стабилен
0,002
’^Gd—> 15695ТЬ
18,0 ч стабилен
0,00107
161 (-J , 161 TL , 161
64Gd^-^ 65ТЬ^~> 66 Dy
(3,6 мин) 6,9 сут стабилен
7,6 - 10’5
Строение вещества
77
Естественные радиоактивные семейства
Ниже, в скобках, приведены периоды полураспада и энергии а-частиц (МэВ), выделенные полужирным шрифтом, для элементов естественных радиоактивных семейств: семейства тория (4л), нептуния (4 л + 1), ура
на (4л + 2) и актиния (4л + 3). Если распад какого-либо из изотопов происходит двумя путями, указана также доля ядер для каждого пути распада. Пунктиром отмечены маловероятные пути распада.
Семейство тория
23920Th (1,4- Ю10 лет; 4,0078)
22*Ra (6,7 г)
₽-v
2^Ас (6,13 ч)
₽-
Т
22^Th (1,9 г; 5,421)
f
224 Ra (3,64 сут; 5,682)
22°Rn (51,5 с; 6,282)
f
2^Ро (0,158 с; 6,775)
(11ч)
78
Новый справочник химика и технолога
Семейство нептуния
23J Np (2,2 • 108 лет; 4,872)
а“
т
239;Ра (27 сут)
₽-
2”и (1,6 • 105 лет; 4,8157)
а
т
2290Th (7340 лет; 5,02)
а“
V
288Ra (15 Сут)
₽-
V
28*Ас (10 сут; 5,818)
а“ V
22'Fr (4,8 мин; 6,33)
а*
т
2‘75At (0,018 с; 7,00)
а“
т
282Bi (47 мин; 5,86)
2^Ро (4,2 • 10^ с; 8,336) 2089,Т1 (2,2 мин)
2>
Строение вещества
79
Семейство урана
23 JU (4,5 • 109 лет; 4,180)
а"
23940Th (24 сут)
₽’
234^Ра (1,2 мин)
239> (6,7 ч) ₽-
2J4U (2 • 105 лет; 4,768)
а'
V
2390Th (8- 104 лет; 4,685)
а’
т
22*Ra (1620 лет; 4,779)
а"
V
222 Rn (3,8 сут; 5,486)
а"
у
2J8Po4 (3,05 мин; 5,998)
а '''^(0,0003)
282РЬ (19 лет)
₽-
V
28з^Н5 сут; 4>96)
а\5 • 1(Г7
!’°Ро (138 сут; 5,298) ,, ^Т1 (4,19 мин)
ctX. г'' Р"
80
Новый справочник химика и технолога
Семейство актиния
2J3U (7,2 • 108 лет; 4,58)
а"
т
239'Th (26 ч)
23]Ра (3,4 • 104лет; 5,049)
а
т
222 Ас (22 г; 4,942)
22970Th (18 сут: 6,0281) 223 Fr (22 мин; 5,34)
2^Ро (0,52 с; 7,43) 207 Т1 (4,79 мин)
207 РЬ
82 * u
Литература
1. Справочник химика / Под ред. Б.П. Никольского. Л.: «Химия», 1971. Т. 1. С. 300-314.
2.4. Ядерный магнитный резонанс и некоторые свойства ядер
Спектроскопия ядерного магнитного резонанса (спектроскопия ЯМР) — один из самых эффективных
физических методов исследования. Он основан на избирательном поглощении магнитного компонента радиочастотного электромагнитного поля системой ядер-ных магнитных моментов вещества. Говоря иными словами, в основе метода лежит тот факт, что однотипные магнитные ядра, находящиеся в различном химическом окружении, поглощаю ! радиочастотную энергию при различных частотах.
Строение вещества
81
Важнейшими характеристиками магнитных ядер являются ядерный спин, ядерный магнитный момент, ядерный квадруполъный момент и гиромагнитное (или магнитогирическое) отношение (см. табл. 2.3). Если ядро рассматривать как вращающуюся частицу, обладающую собственным угловым моментом количества движения, то максимальная величина углового момента описывается уравнением
где h — постоянная Планка.
Величина /, которая может принимать значения, кратные 1/2. называется ядерным спином. Проекция спина на ось напряженности магнитного поля (спиновое квантовое число) может принимать значения от -/ до +/ с шагом 1. В эксперименте ЯМР наблюдается резонансное поглощение энергии, необходимой для перехода ядер из состояния с одним значением спинового квантового числа в состояние с другим значением. Чаще всего применяют спекгроскопию ЯМР на ядрах со спином 1/2, поскольку в этом случае возможен единственный переход (-1/2 —> +1/2) и спектр является относительно простым. Ядра со спином, равным нулю, не обладают магнитными свойствами и непригодны для исследования методом ЯМР.
Гиромагнитное отношение — это отношение магнитного момента ядер к угловому моменту количества движения. Оно определяет силу воздействия магнитного поля на ядра.
Ядерный квадруполъный момент — величина, характеризующая отклонение распределения электрического заряда в атомном ядре от сферически симметричного. Наблюдается для ядер со спином / = 1 и / > 1.
Относительная чувствительность показывает, какое количество ядер данного изотопа дают такую же интенсивность сигнала ЯМР, как и одно ядро ’Н.
Восприимчивость — абсолютная чувствительность изотопа. Для изотопа 13С она принята равной единице.
Частота, при которой наблюдается сигнал в спектре ЯМР, и напряженность поля прямо пропорциональны друг другу. Поэтому приведенные в табл. 2.3 значения частоты (напряженности поля) легко могут быть приведены к другим условиям эксперимента.
2.5. Электронные конфигурации атомов
В табл. 2.4 приведено распределение электронов по энергетическим уровням и подуровням атомов в основном состоянии. Для электронных оболочек наряду с номерами, соответствующими значениям главного квантового числа п, приведены традиционные буквенные обозначения: К(п= 1), L (п = 2), М (п = 3), N (п = 4), О (п = 5), Р (п= 6), Q (п = 7). Для атомных орбиталей
приведены буквенные символы: 5 (соответствует орбитальному квантовому числу W/, равному 0), р (mt = 1), d (пц = 2),f(mt = 3).
В табл. 2.4 приведены также символы термов основного (обладающего минимальной энергией) состояния атома. Термом называется совокупность многоэлектронных конфигураций, характеризующихся общими для данного терма значениями квантовых чисел полных орбитального и спинового моментов (L = ^пц и S = соответственно). Значения квантовых чисел L обозначаются буквенными символами 5 (L = 0), Р (L = = 1), D (L = 2), F (L = 3), G (L = 4), Н (L = 5), / (L = 6), К (L = 7), L (L = 8). Слева вверху указывается спиновая мультиплетность терма (2S + 1), а справа внизу — мультиплетность состояния, т. е. значение 2J + 1, где J — квантовое число спин-орбитального взаимодействия J(J = L + S, L + S- 1,., L-S).
2.6. Энергия ионизации атомов и ионов
Энергией (или потенциалом) ионизации Е, называется энергия, затрачиваемая для отрыва электрона от атома (иона, молекулы или радикала) в газовой фазе. Это соответствует процессу, который можно записать в виде схемы:
Эгаз + Е,.1 —> э;, + е.
Первая энергия ионизации (E,j) — энергия, необходимая для отрыва одного электрона от нейтрального атома. Вторая энергия ионизации будет тогда соответствовать отрыву электрона от образовавшегося монокатиона и т. д. Например, пятая энергия ионизации будет соответствовать процессу:
Э4+ +Е,5 -> э5+ + ё.
газ га*
Ниже в табл. 2.5 приведены значения последовательных энергий ионизации атомов и одноатомных ионов. Оценочные величины приведены в скобках. Число значащих цифр соответствует точности определения величины. Все величины приведены в кДж/моль. Для перехода к широко используемой внесистемной единице энергии — электрон-вольтам (эВ) — приведенную величину следует делить на 96,486.
Литература
1. Справочник химика / Под ред. Б.П. Никольского. Л., Химия, 1971. Т. 1. С. 317-320.
2. Гордон А., Форд Р. Спутник химика. М.: Мир, 1976. 541 с.
3. Brevard С., Granger Р. Handbook of high resolution multinuclear NMR. N.-Y.: John Willey & Sons, 1981.229 p.
4. Harris R. K., Mann В. E. NMR and the periodic table. London: Academic Press, 1978. 459 p.
5. Mason J. Multinuclear NMR. N.-Y.-London: Plenum Press, 1987. 639 p.
Таблица 2.3
ЯМР и некоторые свойства ядер
Изотоп Ядерный спин Ядерный магнитный момент, цв Частота ЯМР, МГц, при магнитной индукции 2.3488 Тл Магнитная индукция. Тл, при частоте 10 МГц Относительная чувствительность при постоянной Восприимчивость Г иромагнитное отношение, 107рад/(Тл • с) Квадрупольный момент, 1О”32 м2
напряженности частоте
’Н + 1/2 +2,793 100,000 0,235 1,00 1,00 5,68 • 103 26,75
2Н +1 +0,857 15,351 1,530 9,65 • 10 3 0,409 8,2 • 106 4,11 27,3
3Н* + 1/2 +2,979 106,663 0,220 1,21 1,07 28,53
3Не + 1/2 -2,176 76,178 0,308 0,44 0,762 3,26- 10’3 -20,38
6Li + 1 +0,822 14,716 1,596 8,50 • 103 0,392 3,58 3,94 -8,0
7Li +3/2 +3,256 38,863 0,604 0,29 1,94 1,54- 103 10,40 -450
9Ве -3/2 -1,178 14,053 1,671 1,39- 10 2 0,703 78,8 3,76 520
10В +3 + 1,801 10,746 2,186 1,99 • 10’2 1,72 22,1 2,87 740
ИВ -3/2 +2,689 32,084 0,732 0,17 1,60 7,54- 102 8,58 355
13с -1/2 +0,702 25,144 0,934 1,59 • 10 2 0,252 1,00 6,73
13N + 1/2 ±0,3221 11,53 2,040 1,50- 10’3 0,115
14n + 1 +0,404 7,224 3,251 1,01 • 10’3 0,193 5,69 1,93 160
,5n +1/2 -0,283 10,133 2,318 1,04- 10’3 0,101 2,19- 10’2 -2,71
,7О +5/2 -1,894 13,557 1,730 2,91 • 10’2 1,58 6,10- 10’2 -3,63 -260
19f + 1/2 +2,689 94,077 0,250 0,83 0,941 4,73 • 103 25,17
21Ne +3/2 -0,662 7,894 2,975 2,50 • 10"3 0,395 3,59- 10"2 -2,11
22Na* +3 1,746 10,419 2,250 0,0181 1,67
23Na +3/2 +2,218 26,451 0,888 9,25 • 10’2 1,32 5,25 • 102 7,08 1200
25Mg +5/2 -0,855 6,1195 3,838 2,67 • 10 3 0,714 1,54 1,64 2200
27A1 +5/2 +3,642 26,057 0,901 0,21 3,04 1,17- 103 6,97 4193
29Si + 1/2 -0,555 19,865 1,182 7,84- 10 3 0,199 2,09 -5,32
3lp +1/2 +1,132 40,481 0,580 6,63 • 10 2 0,405 3,77- 102 10,83
33S +3/2 +0,644 7,760 3,062 2,26- 10 3 0,384 9,73 • 10’2 2,05 -500
35S* +3/2 1,00 11,932 1,970 8,50 • 10’3 0,597 400
35C1 +3/2 +0,822 9,798 2,397 4,70 • 10 3 0,490 20,2 2,62 -800
36сГ +2 1,285 11,493 2,044 0,0122 0,920 -170
37C1 +3/2 +0,684 8,156 2,88 2,71 • 10 3 0,408 3,8 2,17 -632
39K +3/2 +0,391 4,667 5,033 5,08 • 10 4 0,234 2,69 1,25 550
40K* +4 -1,298 5,801 4,05 5,23 • 10~3 1,55 -700
41K +3/2 +0,215 2,561 9,170 8,40 • 10’5 0,128 3,28 • 10 2 0,69 670
42K +2 -1,141 10,205 2,30 8,52 • 10 ' 0,817
43Ca -7/2 1,317 6,728 3,491 6,40 • 10’3 1,41 5,27 • 10’2 -1,80 -500
45Sc -7/2 +4,756 24,290 0,967 0,30 5,11 1,71 • 103 6,50 -2200
46Sc +4 3,03 13,55 1,730 0,0665 3,6 1200
47Ti -5/2 -0,789 5,637 4,167 2,09 • 10"3 0,659 0,864 1,51 +2900
49Ti -7/2 -1,042 5,638 4,166 3,76 • 10 3 1,18 1,18 1,51 +2400
49y +7/2 ±4,5 22,81 1,03 0,256 4,8
50у +6 3,347 9,970 2,356 5,55 • 10 2 5,59 0,755 2,65 2100
Новый справочник химика и технолога
Продолжение табл. 2.3
Изотоп Ядерный спин Ядерный магнитный момент, Цв Частота ЯМР, МГц, при магнитной индукции 2,3488 Тл Магнитная индукция, Тл, при частоте 10 МГц Относительная чувствительность при постоянной Восприим-чивость Гиромагнитное отношение, 107 рад/(Тл • с) Квадрупольный момент, 10“32 м2
напряженности частоте
51у -7/2 5,157 26,289 0,894 0,38 5,53 21,50 7,04 -520
53Сг +3/2 -0,475 5,652 4,155 9,03 • 10-4 0,283 0,49 -1,51 3000
52Мп +6 ±3,05 9,177 2,56 0,0422 5,1
53Мп +7/2 ±5,01 25,8 0,91 0,353 5,38
55Мп -5/2 +3,469 24,664 0,952 0,18 2,88 9,94 • 102 6,62 5500
57Fe -1/2 +0,090 3,231 7,269 3,37 • 10 5 3,2 • 10’2 4,2 • 10“3 0,87
56Со +4 ±3,83 17,24 1,36 0,134 4,6
57Со* +7/2 ±4,62 23,7 0,99 0,277 5,0
58Со* +2 4,03 36,2 0,65 0,376 2,9
59Со -7/2 +4,627 23,614 0,995 0,28 5,0 1,57 • 103 6,35 4000
60Со* +5 3,78 13,606 1,73 0,099 5,4
61Ni -3/2 -0,750 8,936 2,628 3,57 • 10 3 0,447 0,24 -2,39 1600
63Cu -3/2 +2,223 26,505 0,886 9,31 • 10’2 1,33 3,65 • 102 7,10 -2110
64Cu +1 -0,216 7,3 3,20 1,54 • 10 4 0,10
65Cu -3/2 +2,382 28,394 0,827 0,11 1,42 2,01 • 102 7,60 -1950
65Zn +5/2 0,769 5,508 4,26 1,95 • 10’3 0,64 -0,026
67Zn -5/2 +0,875 6,254 3,76 2,85 • 10 3 0,731 0,665 1,67 1500
68Ga + 1 ±0,0117 0,210 0,110 2,45 • 10’8 5,6 • 10 3 ±310
69Ga -3/2 +2,017 24,003 0,978 6,91 • 10’2 1,203 2,37 • 102- 6,42 1780
71Ga -3/2 +2,562 30,495 0,770 0,14 1,529 3,19 • 102 8,16 1120
72Ga +3 -0,1322 0,789 29,77 7,86 • 10’6 0,126 5900
71Ge 1/2 0,546 19,7 1,20 7,47 • 10“3 0,20
73Ge +9/2 -0,879 3,488 6,733 1,4 • 10‘3 1,15 0,617 -0,93 -2000
75As -3/2 + 1,439 17,126 1,371 2,51 • 10"2 0,859 1,43 • 102 4,58 3000
76As +2 -0,905 8,10 2,90 4,25 • 10 3 0,648
77Se -1/2 +0,536 19,092 1,23 6,93 • 10’3 0,191 2,98 5,10
79Se* +7/2 -1,02 5,21 4,5 2,98 • 10 3 1,1 8000
76Br + 1 ±0,548 9,82 2,4 2,52 • 10’3 0,26 ±2500
79Br -3/2 +2,106 25,053 0,938 7,86 • 10 3 1,26 2,26 • 102 6,70 3300
81Br -3/2 +2,271 27,006 0,870 9,85 • 10’2 1,35 2,27 • 102 7,22 2800
82Br +5 ±1,626 5,823 4,03 7,89 • 10’3 2,33 ±7000
83 Kr +9/2 -0,970 3,847 6,11 1,88 • 10 3 1,27 1,23 -1,03 1500
85Kr +9/2 ±1,005 3,983 5,898 2,11 • 10 3 1,32 4300
83Rb +5/2 1,4 10,17 2,3 0,01 1,2
84Rb +2 -1,32 11,81 2,0 0,013 0,95
85Rb -5/2 +1,353 9,655 2,433 1,05 • 10’2 1,13 43 2,58 2500
86Rb +2 -1,691 15,13 1,6 0,0277 1,21
87Rb -3/2 +2,75 32,721 0,718 0,17 1,64 2,77 • 102 8,75 1200
87Sr +9/2 -1,093 4,333 5,419 2,69 • 10 3 1,44 1,07 -1,16 3600
Строение вещества
00
Продолжение табл. 2.3
Изотоп Ядерный спин Ядерный магнитный момент, цв Частота ЯМР, МГц, при магнитной индукции 2,3488 Тл Магнитная индукция, Тл, при частоте 10 МГц Относительная чувствительность при постоянной Восприимчивость Гиромагнитное отношение, 107рад/(Тл • с) Квадрупольный момент, 10 32 м2
напряженности частоте
i^Y -1/2 -0,137 4,899 4,794 1,18 • 10 4 4,90 • 10’2 0,668 -1,31
90у +2 -1,63 14,49 1,6 0,025 1,17 -1500
91у + 1/2 ±0,164 5,85 4,0 2,0 • 10^ 0,059
91Zr +5/2 -1,303 9,330 2,517 9,48- 10 3 1,09 6,04 -2,49 -2100
93Nb +9/2 +6,171 24,442 0,961 0,48 8,10 2,74 • 103 6,55 -2000
95Мо +5/2 -0,913 6,514 3,60 3,23 • 103 0,763 2,88 1,74 1200
97Мо +5/2 -0,934 6,652 3,53 3,43 • Ж3 0,779 1,84 -1,78 И 000
99Тс* +9/2 +5,685 22,508 1,044 0,38 7,46 6,05 -1300
"Ru +5/2 -6,413 3,389 6,9 1,95 • 10^ 0,4 0,83 -1,23 760
101Ru +5/2 -0,719 4,941 4,8 1,41 • 10 3 0,6 1,56 -1,38 4400
103Rh -1/2 -0,088 3,172 7,462 3,11 • Ж5 3,16 • 10 2 0,177 -0,85
I05Pd +5/2 -0,642 4,576 5,1 1,12 • 103 0,54 1,41 -0,756 +8000
105 Ag + 1/2 ±0,101 3,62 6,5 4,7 • 10 5 0,036
,07Ag -1/2 -0,114 4,046 5,804 6,62 • Ж5 4,06 • 10 2 0,195 -1,08
109Ag -1/2 -0,131 4,652 5,049 1,01 • 10 4 4,67 • 102 0,276 -1,24
11()-Ag +6 3,604 10,703 2,19 0,0696 6,02
H1Ag + 1/2 -0,145 5,19 4,5 1,40 • 10^ 0,052
109Cd +5/2 -0,827 5,940 3,95 2,42 • 10 3 0,691 8 000
H,Cd + 1/2 -0,594 21,205 1,11 9,54 • 10 3 0,213 6,93 -5,67
113Cd +1/2 -0,622 22,182 1,06 1,09 • 10 2 0,222 7,6 -5,93
113mCd + 11/2 -1,087 3,55 6,6 2,11 • 103 1,69 -8000
115Cd + 1/2 -0,6477 23,163 1,01 0,0125 0,232
115mCd +11/2 -1,040 3,399 6,91 1,85 • 10 3 1,61 -6000
,13In +9/2 +5,523 21,866 1,074 0,34 7,25 83,8 5,85 11 400
113mIn + 1/2 -0,210 7,537 3,12 4,3 • 10^ 0,075
114mIn +5/2 4,7 16,9 1,4 0,2 6,7 11 400
”5и,1п* +9/2 +5,534 21,914 1,072 0,34 7,27 1,89 • 103 5,86 11 600
115Sn + 1/2 -0,918 32,699 0,715 3,5 • 10 2 0,329 0,693 -8,75
1,7Sn + 1/2 -1,000 35,625 0,659 4,52 • 10’2 0,358 19,54 -9,53
,19Sn + 1/2 -1,046 37,272 0,630 5,18 • 10 2 0,375 25,2 -9,98
121Sb +5/2 +3,359 23,930 0,982 0,16 2,81 5,20 • 102 6,40 -5300
122Sb +2 -1,90 17,00 1,4 0,0394 1,4 6900
I23Sb +7/2 +2,55 12,959 1,812 4,57 • 10 2 2,74 1,11 • 102 3,47 -6800
123Te + 1/2 -0,736 26,207 0,896 -1,80 • 10 2 0,264 0,89 -7,00
125Te + 1/2 -0,887 31,596 0,743 3,15 • 10“2 0,318 12,5 -8,44
125I +5/2 3,0 21 1,1 0,0320 0,318 -8900
127 j +5/2 +2,808 20,007 1,174 9,34 • 10“2 2,5 5,30 • 102 5,35 -7900
129j* +7/2 2,617 13,3160 1,764 0,050 2,81 -5500
131 j +7/2 2,74 14,006 1,68 0,0578 2,9 -4000
Новый справочник химика и технолога
Продолжение табл. 2.3
Изотоп Ядерный спин Ядерный магнитный момент, цв Частота ЯМР, МГц, при магнитной индукции 2,3488 Тл Магнитная индукция, Тл, при частоте 10 МГц Относительная чувствительность при постоянной Восприим-чивость Г иромагнитное отношение, 107рад/(Тл • с) Квадрупольный момент, 10’32 м2
напряженности частоте
129Хе + 1/2 -0,777 27,660 0,849 2,12 • 10’2 0,278 31,8 -7,40
131Хе +3/2 0,6908 8,199 2,864 2,76 • 10“3 0,412 3,31 2,19 -1200
131Cs +5/2 3,54 25,18 0,933 0,19 з,о -5700
132Cs +2 2,22 19,87 1,2 0,0628 1,6 4600
133Cs +7/2 +2,579 13,117 1,791 4,74 • 10’2 2,77 2,69 • 102 3,51 -30
134Cs* +4 2,990 13,308 1,76 0,0639 3,57 3600
135Cs +7/2 2,729 13,8802 1,692 0,0571 2,93 440
137Cs* +7/2 2,838 14,4352 1,627 0,0642 3,05 450
135Ba +3/2 +0,837 9,934 2,364 4,9 • 10 4 0,498 1,83 2,66 1800
,37Ba +3/2 +0,936 11,113 2,113 7,76- 10’4 0,558 4,41 2,97 2800
138La* +5 +3,707 13,193 1,780 9,19 • 10 2 5,31 0,43 3,53 —4700
139La +7/2 +2,778 14,126 1,663 5,92 • 10’2 2,98 3,36- 102 3,78 2100
l4,Ce* +7/2 ±0,9 4,9 4,8 2,05 • 10 3 1,0
141Pr +5/2 +4,3 29,291 0,80 0,29 3,6 1,62 • 103 7,77 -590
142Pr +2 ±0,25 2,6 9,1 9 • 10’5 0,18 ±300
,43Nd -7/2 -1,08 5,437 4,32 3,38 • 10 3 1,2 2,43 -1,47 4800
,45Nd -7/2 -0,66 3,346 7,0 7,86- 10’4 0,71 0,393 -0,91 -2500
147Nd +5/2 ±0,59 4,16 5,6 8 • Ю4 0,49
147Pm +7/2 +2,7 13,51 1,8 0,06 2,9 3,61 6700
148Pm + 1 2,0 38 0,63 0,1 1,0 2000
147Sm -7/2 -0,813 4,128 5,7 1,48 • 10’3 0,87 1,28 -1,11 -2080
149Sm -7/2 -0,670 3,289 7,1 7,47 • 10 4 0,72 0,665 -0,92 600
151Eu +5/2 +3,464 24,801 0,947 0,18 2,89 4,64 • 102 6,55 11600
152Eu +3 1,924 11,410 2,06 0,0242 1,84 ±30 000
,53Eu +5/2 + 1,530 10,951 2,145 1,52 • 10“2 1,28 45,7 2,94 29 000
154Eu +3 ±2,000 16,829 1,97 0,0272 1,91
155Gd -3/2 -0,27 3,819 6,3 2,79 • 10 4 0,15 0,124 -0,83 16 000
,57Gd -3/2 -0,36 4,774 5,0 5,44 • 10 4 0,20 0,292 -1,08 20 000
159Tb +3/2 + 1,95 22,678 1,0 5,83 • 10’2 1,2 3,94 • 102 6,43 13 000
i6°Tb +3 1,68 9,6 2,4 0,016 1,6 30 000
161Dy +5/2 -0,48 3,294 7,1 4,17 • 10"4 0,4 0,509 -0,92 14 000
163 Dy -5/2 +0,673 4,583 5,0 1,12 • 10 3 0,5 1,79 1,28 16 000
,65Ho -7/2 +4,173 20,513 1,1 0,18 4,4 1,16 • 103 5,71 28 200
,67Er +7/2 -0,567 2,890 8,1 5,07 • 10’4 0,61 0,665 -0,78 28 300
169Er + 1/2 0,513 18,3 1,3 6,2 • 10’3 0,18
169Tm + 1/2 -0,232 8,271 2,8 5,66 • Ю 4 0,083 3,21 -2,21
I70Tm + 1 ±0,246 4,7 5,0 2,3 • 10“4 0,12 ±5900
,7!Tm + 1/2 ±0,229 8,13 2,9 5,5 • 10 4 0,082
171Yb -1/2 +0,492 17,613 1,334 5,46- 10 3 0,176 4,05 4,72
Строение вещества
Продолжение табл. 2.3
Изотоп Ядерный спин Ядерный магнитный момент, |лв Частота ЯМР, МГц, при магнитной индукции 2,3488 Тл Магнитная индукция, Тл, при частоте 10 МГц Относительная чувствительность при постоянной Восприимчивость Г иромагнитное отношение, 107 рад/(Тл • с) Квадрупольный момент, 10“32 м2
напряженности частоте
173Yb -5/2 -0,678 4,852 4,841 1,33 • 10“3 0,566 1,14 1,31 22 000
175Lu +7/2 +2,233 11,407 2,1 3,12 • 10’2 2,4 1,56 • 102 3,05 56 800
176Lu* +7 3,18 8,0 2,9 0,040 6,1 80 000
177Lu +7/2 2,24 11,37 2,1 0,032 2,4 54 000
177Hf +7/2 +0,794 3,120 7,7 6,38 • 10 4 0,7 0,88 +0,95 45 000
179Hf +9/2 -0,641 1,869 13,0 2,16 • 10 4 0,6 0,27 -0,61 51 000
,81Ta +7/2 +2,370 11,970 1,96 3,60- 10“2 2,54 2,04- 102 3,21 30 000
183W -1/2 +0,118 4,161 5,645 7,20 • 10 4 0,042 5,89 • 10“2 1,11
185Re +5/2 +3,172 22,513 1,043 0,13 2,65 2,80 • 102 6,03 28 000
,86Re +1 ±1,73 30,93 0,759 0,079 0,83
,87Re +5/2 +3,220 22,744 1,033 0,13 2,68 4,90 • 102 6,09 26 000
,88Re +1 1,78 13,83 0,738 0,086 0,85
1870s -1/2 +0,065 2,282 10,2 1,22 • 10“5 0,023 1,14 • 10'3 0,61
1890s +3/2 +0,660 7,758 3,027 2,34 • 10 3 0,392 2,13 2,08 8000
191Ir +3/2 +0,146 1,718 13,7 2,53 • 10“5 0,087 2,30 • 10“2 0,54 15 000
,93Ir +3/2 +0,159 1,871 12,6 3,27 • 10 5 0,094 5,00 • 10’2 0,39 14 000
195Pt -1/2 +0,610 21,499 1,09 9,94 • 10’3 0,217 19,1 5,74
195 Au +3/2 ±0,147 1,743 13,5 2,7 • 10 5 0,088
196Au +2 +0,58 5,4 4,3 0,001 0,4
197Au +3/2 +0,148 1,712 13,7 2,51 • 10’5 0,086 6,00 • 10’2 0,36 5800
198Au +2 +0,590 5,231 4,49 1,2 • 10“3 0,42
199 Au +3/2 +0,270 3,190 7,36 1,3 • ю-4 0,16
197Hg + 1/2 0,524 18,6 1,3 6,6 • 10“3 0,19
199Hg -1/2 +0,506 17,827 1,318 5,67 • 10 3 0,180 5,42 4,79
201Hg -3/2 -0,560 6,599 3,559 1,44 • 10’3 0,332 1,08 -1,77 5000
203Hg +5/2 0,84 5,9 4,0 2,5 • 10 3 0,7
201^p| +1/2 1,6 56,6 0,41 0,19 0,57
203'tj + 1/2 +1,622 57,149 0,411 0,18 0,577 289 15,31
204'p । +2 ±0,089 0,80 29,0 4,1 • 10 6 0,06
205у| +1/2 + 1,638 57,708 0,407 0,19 0,583 7,69 • 102 15,46
2°7pb -1/2 +0,593 20,921 1,123 9,16 • 10 3 0,211 11,8 5,58
2°5Bi +9/2 5,5 21,8 1,1 0,35 7
209Bi -9/2 +4,110 16,069 1,462 0,13 5,35 7,77 • 102 4,30 -4000
210Bi + 1 0,0442 0,792 30,0 1,32 • 10“6 0,021 ±1300
207Po +5/2 0,27 1,93 12,0 8 • 10“5 0,2 2800
227Ac -3/2 +U 13,1 1,8 0,01 0,06 3,5 17 000
229Th +5/2 +0,46 1,5 8,3 2,3 • 10 4 0,3 0,40 44 000
231Pa +3/2 ±1,98 23,39 1,0 0,066 1,2
233Pa +3/2 3,4 40 0,6 0,33 2,0 -30 000
Новый справочник химика и технолога
Окончание табл. 2.3
Изотоп Ядерный спин Ядерный магнитный момент, Цв Частота ЯМР, МГц, при магнитной индукции 2.3488 Тл Магнитная индукция, Тл, при частоте 10 МГц Относительная чувствительность при постоянной Восприим-чивость Гиромагнитное отношение, 107рад/(Тл • с) Квадрупольный момент, 10“32 м2
напряженности частоте
™и‘ +5/2 0,54 3,8 6,3 6,7 • 10 4 0,5 35 000
235и* -7/2 -0,35 1,790 13,0 1,21 • 10“4 0,4 5,4 • 10 3 -0,49 45 500
237Np* +5/2 +3,14 11,25 0,56 0,15 3 3,1 42 000
239Pu* + 1/2 +0,203 3,63 3,3 3,7 • 10”4 0,072 0,97
24IPu* +5/2 -0,73 4,91 4,8 1,7 • 10 3 0,6
^Am +5/2 1,59 11,32 2,1 0,017 1,3 49 000
242Am + 1 ±0,382 6,81 3,4 8,5 • 10 4 0,18 ±28 000
243 Am -5/2 + 1,61 5,76 2,1 0,01 1,2 1,54 49 000
* Звездочка возле символа элемента указывает, что данный изотоп радиоактивен.
Таблица 2.4
Электронные конфигурации атомов
Z Элемент Оболочка 1 2 3 4 5 6 7 Терм основного состояния
К L M A О P Q
Орбиталь s s P s P d s P d f s P d f g s P d f g h s p
1 2 Н Не 1 2 -SV2 'So
3 4 5 6 7 8 9 10 Li Be В С N О F Ne 2 2 2 2 2 2 2 2 1 2 2 2 2 2 2 2 1 2 3 4 5 6 '-% 2PU2 >0 4 S3/2 >2 P 3/2 'So
И 12 13 14 15 16 17 18 Na Mg Al Si P S Cl Ar 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 2 6 6 6 6 6 6 6 6 1 2 2 2 2 2 2 2 1 2 3 4 5 6 2SU2 ‘So 3P1/2 >0 4S3/2 3P7 ^3/2 'So
19 20 21 22 К Ca Sc Ti 2 2 2 2 2 2 2 2 6 6 6 6 2 2 2 2 6 6 6 6 1 2 1 2 2 2 “Si/2 'S„ 4/2 +2
Строение вещества
00 00
Продолжение табл. 2.4
Z Элемент Оболочка 1 2 3 4 5 6 7 Терм основного состояния
К L M N О P Q
Орбиталь s s P s P d s P d f s P d f g s P d f g h s p
23 V 2 2 6 2 6 3 2 4^3/2
24 Сг 2 2 6 2 6 5 1 7S3
25 Мп 2 2 6 2 6 5 2 6-S5/2
26 Fe 2 2 6 2 6 6 2
27 Со 2 2 6 2 6 7 2 %2
28 Ni 2 2 6 2 6 8 2 3F,
29 Си 2 2 6 2 6 10 1 2Su2
30 Zn 2 2 6 2 6 10 2 'So
31 Ga 2 2 6 2 6 10 2 1 2p ‘ 1/2
32 Ge 2 2 6 2 6 10 2 2 3p 0
33 As 2 2 6 2 6 10 2 3 4^. «>3/2
34 Se 2 2 6 2 6 10 2 4 >2
35 Br 2 2 6 2 6 10 2 5 3P r 3/2
36 Kr 2 2 6 2 6 10 2 6 'So
37 Rb 2 2 6 2 6 10 2 6 1
38 Sr 2 2 6 2 6 10 2 6 2 'S„
39 Y 2 2 6 2 6 10 2 6 1 2 2T^3/2
40 Zr 2 2 6 2 6 10 2 6 2 2 3f2
41 Nb 2 2 6 2 6 10 2 6 4 1 eDi/2
42 Mo 2 2 6 2 6 10 2 6 5 1 7S,
43 Tc 2 2 6 2 6 10 2 6 6 1 %/2
44 Ru 2 2 6 2 6 10 2 6 7 1 5f5
45 Rh 2 2 6 2 6 10 2 6 8 1 4f9/2
46 Pd 2 2 6 2 6 10 2 6 10 0 'So
47 Ag 2 2 6 2 6 10 2 6 10 1 2-s1/2
48 Cd 2 2 6 2 6 10 2 6 10 2 'So
49 In 2 2 6 2 6 10 2 6 10 2 1 2PU2
50 Sn 2 2 6 2 6 10 2 6 10 2 2 ‘ 0
51 Sb 2 2 6 2 6 10 2 6 10 2 3 4^ ^3/2
52 Те 2 2 6 2 6 10 2 6 10 2 4 >2
53 I 2 2 6 2 6 10 2 6 10 2 5
54 Xe 2 2 6 2 6 10 2 6 10 2 6 ‘So
55 Cs 2 2 6 2 6 10 2 6 10 2 6 1 ^1/2
56 Ba 2 2 6 2 6 10 2 6 10 2 6 2 'S„
57 La 2 2 6 2 6 10 2 6 10 2 6 1 2 2Т>з/2
58 Ce 2 2 6 2 6 10 2 6 10 2 2 6 2 ’«4
Новый справочник химика и технолога
Продолжение табл. 2.4
Z Элемент Оболочка 1 2 3 4 5 6 7 Терм основного состояния
К L M N О P Q
Орбиталь s s P s P d s P d f s P d f g s P d f g h s P
59 Рг 2 2 6 2 6 10 2 6 10 3 2 6 2 4^9/2
60 Nd 2 2 6 2 6 10 2 6 10 4 2 6 2 S/4
61 Pm 2 2 6 2 6 10 2 6 10 5 2 6 2 6^5/2
62 Sm 2 2 6 2 6 10 2 6 10 6 2 6 2 7Fo
63 Eu 2 2 6 2 6 10 2 6 10 7 2 6 2 x2
64 Gd 2 2 6 2 6 10 2 6 10 7 2 6 1 2 9d2
65 Tb 2 2 6 2 6 10 2 6 10 9 2 6 2 6^15/2
66 Dy 2 2 6 2 6 10 2 6 10 10 2 6 2
67 Ho 2 2 6 2 6 10 2 6 10 11 2 6 2 15/2
68 Er 2 2 6 2 6 10 2 6 10 12 2 6 2
69 Tm 2 2 6 2 6 10 2 6 10 13 2 6 2 ^7/2
70 Yb 2 2 6 2 6 10 2 6 10 14 2 6 2 'So
71 Lu 2 2 6 2 6 10 2 6 10 14 2 6 1 2 2d3/2
72 Hf 2 2 6 2 6 10 2 6 10 14 2 6 2 2 3f2
73 Ta 2 2 6 2 6 10 2 6 10 14 2 6 3 2 4F3/2
74 W 2 2 6 2 6 10 2 6 10 14 2 6 4 2 ’Oo
75 Re 2 2 6 2 6 10 2 6 10 14 2 6 5 2 *’5/2
76 Os 2 2 6 2 6 10 2 6 10 14 2 6 6 2 5d4
77 Ir 2 2 6 2 6 10 2 6 10 14 2 6 7 2 4F9/2
78 Pt 2 2 6 2 6 10 2 6 10 14 2 6 9 1 3D,
79 Au 2 2 6 2 6 10 2 6 10 14 2 6 10 1 2S>/2
80 Hg 2 2 6 2 6 10 2 6 10 14 2 6 10 2 'So
81 TI 2 2 6 2 6 10 2 6 10 14 2 6 10 2 1 2PM2
82 Pb 2 2 6 2 6 10 2 6 10 14 2 6 10 2 2 3P«
83 Bi 2 2 6 2 6 10 2 6 10 14 2 6 10 2 3 453/2
84 Po 2 2 6 2 6 10 2 6 10 14 2 6 10 2 4 >2
85 At 2 2 6 2 6 10 2 6 10 14 2 6 10 2 5 >3/2
86 Rn 2 2 6 2 6 10 2 6 10 14 2 6 10 2 6 'So
87 Fr 2 2 6 2 6 10 2 6 10 14 2 6 10 2 6 1 >!/2
88 Ra 2 2 6 2 6 10 2 6 10 14 2 6 10 2 6 2 'So
89 Ac 2 2 6 2 6 10 2 6 10 14 2 6 10 2 6 1 2 2D3/2
90 Th 2 2 6 2 6 10 2 6 10 14 2 6 10 2 6 2 2 3f2
91 Pa 2 2 6 2 6 10 2 6 10 14 2 6 10 2 2 6 1 2 >11/2
92 U 2 2 6 2 6 10 2 6 10 14 2 6 10 3 2 6 1 2 5io
93 Np 2 2 6 2 6 10 2 6 10 14 2 6 10 5 2 6 2 >11/2
94 Pu 2 2 6 2 6 10 2 6 10 14 2 6 10 6 2 6 2 3F„
Строение вещества
Окончание табл. 2.4
Z Элемент Оболочка 1 2 3 4 5 6 7 Терм основного СОСТОЯНИЯ
К L M /V О P Q
Орбиталь s s P s P d 5 P d f s P d f g s P d f g h s P
95 Ат 2 2 6 2 6 10 2 6 10 14 2 6 10 7 2 6 2 ^7/2
96 Ст 2 2 6 2 6 10 2 6 10 14 2 6 10 7 2 6 1 2 ">В2
97 Вк 2 2 6 2 6 10 2 6 10 14 2 6 10 8 2 6 1 2 6WI5,2
98 Cf 2 2 6 2 6 10 2 6 10 14 2 6 10 10 2 6 2 4
99 Es 2 2 6 2 6 10 2 6 10 14 2 6 10 11 2 6 2 5/ /15/2
100 Fm 2 2 6 2 6 10 2 6 10 14 2 6 10 12 2 6 2
101 Md 2 2 6 2 6 10 2 6 10 14 2 6 10 13 2 6 2 2F7/2
102 No 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 2 '5o
103 Lr 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 1 2 2^5/2
104 Rf 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 2 2 3F2
105 Db 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 3 2 4F3/2
106 Sg 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 4 2
107 Bh 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 5 2 6o J5/2
108 Hs 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 6 2 SA
109 Mt 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 7 2 4F9/2
ПО Ds 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 8 2 t,
111 Rg 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 9 2 2^5/2
112 Uub 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 10 2 'So
113 Uut 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 10 2 1 3P>,2
114 Uuq 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 10 2 2 3Po
115 Uup 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 10 2 3 %2
116 Uuh 2 2 6 2 6 10 2 6 10 14 2 6 10 14 2 6 10 2 4 3P2
Новый справочник химика и технолога
Литература
1. Справочник химика / Под ред. Б.П. Никольского. Л.: Химия, 1971. Т. 1. С. 321-324.
2. Ефимов А.И., Белорукова Л.П., Василькова И.В., Чечсв В.П. Свойства неорганических соединений. Л.: Химия, 1983. С. 9-13.
3. Эмсли Дж. Элементы. М.: Мир, 1993. 256 с.
4. Fraga S., Karwowski J., Saxena K.M.S. Handbook of atomic data. Amsterdam: Elsevier, 1976. 554 p.
Энергии ионизации атомов и ионов
Таблица 2.5
Атомный номер Химический символ Е,Л ь;,2 £,.3 £/,4 £,,6 ь;,7 £.9 £/,10
1 Н 1312,0
2 Не 2372,3 5250,4
3 Li 513,3 7298,0 11 814,8
4 Be 899,4 1757,1 14 848 21 006
5 В 800,6 2427 3 660 25 025 32 822
6 С 1086,2 2352 4 620 6 222 37 827 47 270
7 N 1402,3 2 856,1 4 578,0 7 474,9 9 440,0 53 265,6 64 358,7
8 О 1313,9 3 388,2 5 300,3 7 469,1 10 989,3 13 326,2 71 333,3 84 076,3
9 F 1681 3 374 6 050 8 408 11 023 15 614 17 867 92 036 106 432
10 Ne 2080,6 3 952,2 6 122 9 370 12 177 15 238 19 998 23 069 1 15 377 131 429
11 Na 495,8 4 562,4 6912 9 543 13 353 16610 20 114 25 490 28 933 141 360
12 Mg 737,7 1 450,7 7 732,6 10 540 13 630 17 995 21 703 25 656 31 642 35 461
13 Al 577,4 1 816,6 2 744,6 11 575 14 839 18 376 23 293 27 457 31 857 38 459
14 Si 786,5 1 577,1 3 231,4 4 355,5 16 091 19 784 23 786 29 252 33 876 38 732
15 P 1011,7 1 903,2 2912 4 956 6 273 21 268 25 397 29 854 35 867 40 958
16 S 999,6 2 251 3 361 4 564 7013 8 495 27 106 31 699 36 578 43 138
17 Cl 1251,1 2 297 3 826 5 158 6 540 9 362 И 020 33 610 38 600 43 960
18 Ar 1520,4 2 665,2 3 928 5 770 7 238 8 811 12 021 13 844 40 759 46 186
19 К 418,8 3 051,4 4411 5 877 7 975 9 649 11 343 14 942 16 964 48 575
20 Ca 589,7 1 145 4910 6 474 8 144 10 496 12 320 14 207 18 191 20 385
21 Sc 631 1 235 2 389 7 089 8 844 10 720 13 320 15310 17 369 21 740
22 Ti 658 1 310 2 652 4 175 9 573 11 516 13 590 16 260 18 640 20 830
23 V 650 1 414 2 828 4 507 6 294 12 362 14 489 16 760 19 860 22 240
24 Cr 652,7 1 592 2 987 4 740 6 690 8 738 15 550 17 830 20 220 23 580
25 Mn 717,4 1 509,0 3 248,4 4 940 6 990 9 200 11 508 18 956 21 400 23 960
26 Fe 759,3 1 561 2 957 5 290 7 240 9 600 12 100 14 575 22 678 25 290
27 Co 760,0 1 646 3 232 4 950 7 670 9 840 12 400 15100 17 900 26 600
28 Ni 736,7 1 753,0 3 393 5 300 7 280 10 400 12 800 15600 18 600 21 660
29 Cu 745,4 1 958 3 554 5 326 7 709 (9940) (13400) (16000) (19 200) (22 400)
30 Zn 906,4 1 733,3 3 832,6 5 730 7 970 10 400 12 900 16 800 19 600 23 000
31 Ga 578,8 1 979 2 963 6 200 (8 700) (11 400) (14 400) (17 700) (22 300) (26 100)
32 Ge 762,1 1 537 3 302 4410 9 020 (11 900) (15 000) (18 200) (21 800) (27 000)
33 As 947,0 1 798 2 735 4 837 6 042 12 305 (15 400) (18 900) (22 600) (26 400)
34 Se 940,9 2 044 2 974 4 144 6 590 7 883 14 990 (19 500) (23 300) (27 200)
35 Br 1 139,9 2 104 3 500 4 560 5 760 8 550 9 940 18 600 (23 900) (28 100)
36 Kr 1 350,7 2 350 3 565 5 070 6 240 7 570 10710 12 200 22 229 (28 900)
Строение вещества
Продолжение табл. 2.5
Атомный номер Химический символ £,,i £,2 £),3 EtA £/,5 E/fo Е,л Et$ £,,9 Et jo
37 Rb 403,0 2 632 3 900 5 080 6 850 8 140 9 570 13 100 14 800 26 740
38 Sr 549,5 1 064,2 4210 5 500 6910 8 760 10 200 11 800 15 600 17 100
39 Y 616 1 181 1 980 5 963 7 430 8 970 11 200 12 400 14 137 18 400
40 Zr 660 1 267 2218 3 313 7 860 (9 500) (11 200) (13 800) (15 700) (17 500)
41 Nb 664 1 382 2416 3 695 4 877 9 899 12 100
42 Mo 685,0 1 558 2 621 4 480 5 900 6 560 12 230 14 800 (16 800) (19 700)
43 Tc 702 1 472 2 850 (4 100) (5 700) (7 300) (9 100) (15 600) (17 800) (19 900)
44 Ru 711 1 617 2 747 (4 500) (6 100) (7 800) (9 600) (11 500) (18 700) (20 900)
45 Rh 720 1 744 2 977 (4 400) (6 500) (8 200) (10 100) (12 200) (14 200) (22 000)
46 Pd 805 1 875 3 177 (4 700) (6 300) (8 700) (10 700) (12 700) (15 000) (17 200)
47 Ag 731,0 2 073 3 361 (5 000) (6 700) (8 600) (11 200) (13 400) (15 600) (18 000)
48 Cd 867,6 1 631 3 616 (5 300) (7 000) (9 100) (11 100) (14 100) (16 400) (18 800)
49 In 558,3 1 820,6 2 704 5 200 (7 400) (9 500) (11 700) (13 900) (17 200) (19 700)
50 Sn 708,6 1 411,8 2 943,0 3 930,2 6 974 (9 900) (12 200) (14 600) (17 000) (20 600)
51 Sb 833,7 1 794 2 443 4 260 5 400 10 400 (12 700) (15 200) (17 800) (20 400)
52 Те 869,2 1 795 2 698 3 610 5 668 6 822 13 200 (15 800) (18 500) (21 200)
53 I 1 008,4 1 845,9 3 200 (4 100) (5 000) (7 400) (8 700) (16 400) (19 300) (22 100)
54 Xe 1 170,4 2 046 3 097 (4 300) (5 500) (6 600) (9 300) (10 600) (19 800) (23 000)
55 Cs 375,5 2 420 (3 400) (4 400) (6 000) (7 100) (8 300) (11 300) (12 700) (23 700)
56 Ba 502,8 965,1 (3 600) (4 700) (6 000) (7 700) (9 000) (10200) (13 500) (15 100)
57 La 538,1 1 067 1 850 4 819 (6 400) (7 600) (9 600) (11 000) (12 400) (15 900)
58 Ce 527,4 1 047 1 949 3 547 (6 800) (8 200) (9 700) (11 800) (13 200) (14 700)
59 Pr 523,1 1 018 2 086 3 761 5 543
60 Nd 529,6 1 035 2 130 3 899
61 Pm 535,9 1 052 2 150 3 970
62 Sm 543,3 1 068 2 260 3 990
63 Eu 546,7 1 085 2 404 4 110
64 Gd 592,5 1 167 1 990 4 250
65 Tb 564,6 1 112 2 114 3 839
66 Dy 571,9 1 126 2 200 4 001
67 Ho 580,7 1 139 2 204 4 100
68 Er 588,7 1 151 2 194 4 115
69 Tm 596,7 1 163 2 285 4 119
70 Yb 603,4 1 176 2415 4 220
71 Lu 523,5 1 340 2 022 4 360
72 Hf 642 1 440 2 250 3 216
73 Ta 761 (1 500) (2 100) (3 200) (4 300)
Новый справочник химика и технолога
Окончание табл. 2.5
Атомный Химический Д.1 E,2 Д.З £,4 E.,, E, 6 E,i E, 8 £,9 Д.10
номер символ
74 W 770 (1 700) (2 300) (3 400) (4 600) (5 900)
75 Re 760 1 260 2510 3 640 (4 900) (6 300) (7 600)
76 Os 840 (1 600) (2 400) (3 900) (5 200) (6 600) (8 100) (9 500)
77 Ir 880 (1 680) (2 600) (3 800) (5 500) (6 900) (8 500) (10 000) (11 700)
78 Pt 870 1 791 (2 800) (3 900) (5 300) (7 200) (8 900) (10 500) (12 300) (14 100)
79 Au 890,1 1 980 (2 900) (4 200) (5 600) (7 000) (9 300) (11 000) (12 800) (14 800)
80 Hg 1 007,0 1 809,7 3 300 (4 400) (5 900) (7 400) (9 100) (11 600) (13 400) (15 300)
81 TI 589,3 1 971,0 2 878 (4 900) (6 100) (8 300) (9 500) (11 300) (14 000) (16 000)
82 Pb 715,5 1 450,4 3 081,5 4 083 6 640 (8 100) (9 900) (11 800) (13 700) (16 700)
83 Bi 703,2 1 610 2 466 4 372 5 400 8 520 (10 300) (12 300) (14 300) (16 300)
84 Po 812 (1 800) (2 700) (3 700) (5 900) (7 000) (10 800) (12 700) (14 900) (17 000)
85 At 930 1 600 (2 900) (4 000) (4 900) (7 500) (8 800) (13 300) (15 400) (17 700)
86 Rn 1 037 2 065 2 837
87 Fr 400 (2 100) (3 100) (4 100) (5 700) (6 900) (8 100) (12 300) (12 800) (29 300)
88 Ra 509,3 979,0 (3 300) (4 400) (5 700) (7 300) (8 600) (9 900) (13 500) (15 100)
89 Ac 499 1 170 1 900 (4 700) (6 000) (7300) (9200) (10500) (11 900) (15 800)
90 Th 587 1 110 1 978 2 780
91 Pa 568
92 U 584 1 420 1 910 3 541
93 Np 597
94 Pu 585
95 Am 578,2
96 Cm 581
97 Bk 601
98 Cf 608
99 Es 619
100 Fm 627
101 Md 635
102 No 642
Строение вещества
Литература
1. Справочник химика/Под ред. Б.П. Никольского. Л.: Химия, 1971. Т. 1. С. 325-327.
2. Ефимов А.И., Белорукова Л.П., Василькова И.В., Чечев В.П. Свойства неорганических соединений. Л.: Химия, 1983. С. 18-20.
3. Эмсли Дж. Элементы. М.: Мир, 1993. 256 с.
4. Ball М.С., Norbury А.Н. Physical Data for Inorganic Chemists. London: Longman, 1974. 175 p.
о
UJ
94
Новый справочник химика и технолога
2.7. Энергия сродства к электрону
Энергией сродства к электрону (Ееа) называется энергия, которая выделяется или поглощается при присоединении электрона к изолированному атому (или иону) в газовой фазе при температуре О К без передачи частице кинетической энергии. Это соответствует процессу, который можно записать в виде схемы:
Э + ё —> Э + F '-'газ v
Ниже в табл. 2.6 приведены значения энергии сродства к электрону атомов и некоторых одноатомных ионов. Оценочные величины приведены в скобках. Положительные значения энергии сродства к электрону означают, что при присоединении электрона энергия выделяется. Число значащих цифр соответствует точности определения величины. Все величины приведены в кДж/моль. Для перехода к широко используемой внесистемной единице энергии — электрон-вольтам (эВ) — приведенную величину следует делить на 96,486.
Таблица 2.6
Энергия сродства к электрону атомов и некоторых одноатомных ионов
Атомный номер Химический символ E^a ), кДж/моль
1 Н 72,8
2 Не 0,0
3 Li 59,6
4 Be -18
5 В 26,7
6 С 121,9
С +3ё -3163*
7 N -7
N“ + 2ё -2220**
8 О 141
О’ -877,1
9 F 328
10 Ne (-29)
11 Na 52,9
12 Mg -21
13 Al 44
14 Si 133,6
15 P 72,0
16 S 200,4
s -435,2
17 Cl 349,0
18 Ar (-35)
19 К 48,4
20 Ca -186
21 Sc 18,1
22 Ti 7,6
23 V 50,7
24 Cr 64,3
25 Mn <0
26 Fe 15,7
27 Co 63,8
28 Ni 156
29 Cu 118,5
Продолжение табл. 2.6
Атомный номер Химический символ Ea1 j. кДж/моль
30 Zn 9
31 Ga 30
32 Ge 116
33 As 78
34 Se 195,0
35 Br 324,7
36 Kr (-39)
37 Rb 46,9
38 Sr -146
39 Y 29,6
40 Zr 41,1
41 Nb 86,2
42 Mo 72,0
43 Tc 96
44 Ru 101
45 Rh 109,7
46 Pd 53,7
47 Ag 125,7
48 Cd -26
49 In 30
50 Sn 116
51 Sb 101
52 Те 190,2
53 1 259,2
54 Xe KI)
55 Cs 45,5
56 Ba -46
57 La 50
58 Ce <50
59 Pr <50
60 Nd <50
61 Pm <50
62 Sm <50
63 Eu <50
64 Gd <50
65 Tb <50
66 Dy
67 Ho <50
68 Er <50
69 Tm <50
70 Yb <50
71 Lu <50
72 Hf 0
73 Ta 14
74 W 78,6
75 Re 14
76 Os 106
77 Ir 151
78 Pt 205,3
79 Au 222,8
80 Hg -18
81 Tl 20
82 Pb 35,1
83 Bi 91,3
Строение вещества
95
Окончание табл. 2.6
Атомный номер Химический символ £еаj, КДЖ/МОЛЬ
84 Ро 183
85 At 270
86 Rn (-П)
87 Fr (44)
* Указанная величина является суммой трех последовательных значений энергии сродства к электрону и соответствует переходу С” + Зё —* С4”.
** Указанная величина является суммой двух последовательных значений энергии сродства к электрону и соответствует переходу N“ + 2ё —> N3-.
Литература
1. Справочник химика / Под ред. Б.П. Никольского. Л.: Химия, 1971. Т. 1.С. 328.
2. Ефимов А.И., Белорукова Л.П., Василькова И.В., Чечев В.П. Свойства неорганических соединений. Л.: Химия, 1983. С. 20.
3. Эмсли Дж. Элементы. М.: Мир, 1993. 256 с.
4. Hotop Н., Lineberger W.C. // J. Phys. Chem. Ref. Data. 1985. V. 14. P. 731.
2.8. Рентгено-спектральные свойства элементов
В табл. 2.7 приведены энергии связи электрон— ядро (electron binding energies) для элементов Периодической системы в их природных формах. Энергии приведены в эВ, для благородных газов, водорода, азота, кислорода, фтора и хлора— относительно уровня, соответствующего вакууму, для металлов — относительно уровня Ферми, для полупроводников — относительно валентной зоны.
В табл. 2.8 приведены энергии характеристических К-, L- и ЛУ-линий рентгеновских спектров элементов. Длина волны рентгеновского излучения может быть вычислена по его энергии с использованием соотношения:
12,398/Е, где Е — энергия в эВ.
Обозначения электронных уровней даны в принятой в рентгеновской спектроскопии системе обозначений; 1/2 (3/2, 5/2 и т. п.) — величина квантового числа спин-орбитального взаимодействия j.
Отнесение линий показано на рис. 2.1.
Таблица 2.7
Энергии связи электрон—ядро, эВ
Элемент £(15) Lx (2s) ^2 (2pi/2) /-3 (2рз/2) Mx (3s) У/2 (3pi/2) Mt, (Зрз/2) Л/4 (3<7з/2) Л/5(34/5/2> У] (45) У2 (4pi/2) Уз (4рз/г)
Н 13,6
Не 24,6
Li 54,7
Be 111,5
В 188
С 284,2
N 409,9 37,3
О 543,1 41,6
F 696,7
Ne 870,2 48,5 21,7 21,6
Na 1070,8 63,5 30,65 30,81
Mg 1303,0 88,7 49,78 49,50
Al 1559,6 117,8 72,95 72,55
Si 1839 149,7 99,82 99,42
P 2145,5 189 136 135
S 2472 230,9 163,6 162,5
Cl 2822,4 270 202 200
Ar 3205,9 326,3 250,6 248,4 29,3 15,9 15,7
К 3608,4 378,6 297,3 294,6 34,8 18,3 18,3
Ca 4038,5 438,4 349,7 346,2 44,3 25,4 25,4
96
Новый справочник химика и технолога
Продолжение табл. 2.7
Элемент К (Is) A,(2s) ^2 (2pi/2) ^3 (2/23/2) Mx (3s) A42(3pi/2) Мз (Зрз/г) .W4(3rf3/2) (Зс/5/2) A,(4s) A2 (4pV2) N3 (4p3/2)
Sc 4492 498,0 403,6 398,7 51,1 28,3 28,3
Ti 4966 560,9 460,2 453,8 58,7 32,6 32,6
V 5465 626,7 519,8 512,1 66,3 37,2 37,2
Cr 5989 696,0 583,8 574,1 74,1 42,2 42,2
Мп 6539 769,1 649,9 638,7 82,3 47,2 47,2
Fe 7112 844,6 719,9 706,8 91,3 52,7 52,7
Со 7709 925,1 793,2 778,1 101,0 58,9 59,9
Ni 8333 1008,6 870,0 852,7 110,8 68,0 66,2
Си 8979 1096,7 952,3 932,7 122,5 77,3 75,1
Zn 9659 1196,2 1044,9 1021,8 139,8 91,4 88,6 10,2 10,1
Ga 10367 1299,0 1143,2 1116,4 159,5 103,5 100,0 18,7 18,7
Ge 11103 1414,6 1248,1 1217,0 180,1 124,9 120,8 29,8 29,2
As 11867 1527,0 1359,1 1323,6 204,7 146,2 141,2 41,7 41,7
Se 12658 1652,0 1474,3 1433,9 229,6 166,5 160,7 55,5 54,6
Br 13474 1782 1596 1550 257 189 182 70 69
Kr 14326 1921 1730,9 1678,4 292,8 222,2 214,4 95,0 93,8 27,5 14,1 14,1
Rb 15200 2065 1864 1804 326,7 248,7 239,1 113,0 112 30,5 16,3 15,3
Sr 16105 2216 2007 1940 358,7 280,3 270,0 136,0 134,2 38,9 21,3 20,1
Y 17038 2373 2156 2080 392,0 310,6 298,8 157,7 155,8 43,8 24,4 23,1
Zr 17998 2532 2307 2223 430,3 343,5 329,8 181,1 178,8 50,6 28,5 27,1
Mb 18986 2698 2465 2371 466,6 376,1 360,6 205,0 202,3 56,4 32,6 30,8
Mo 20000 2866 2625 2520 506,3 411,6 394,0 231,1 227,9 63,2 37,6 35,5
Tc 21044 3043 2793 2677 544 447,6 417,7 257,6 253,9 69,5 42,3 39,9
Ru 22117 3224 2967 2838 586,1 483,5 461,4 284,2 280,0 75,0 46,3 43,2
Rh 23220 3412 3146 3004 628,1 521,3 496,5 311,9 307,2 81,4 50,5 47,3
Pd 24350 3604 3330 3173 671,6 559,9 532,3 340,5 335,2 87,1 55,7 50,9
Ag 25514 3806 3524 3351 719,0 603,8 573,0 374,0 368,3 97,0 63,7 58,3
Cd 26711 4018 3727 3538 772,0 652,6 618,4 411,9 405,2 109,8 63,9 63,9
In 27940 4238 3938 3730 827,2 703,2 665,3 451,4 443,9 122,9 73,5 73,5
Sn 29200 4465 4156 3929 884,7 756,5 714,6 493,2 484,9 137,1 83,6 83,6
Sb 30491 4698 4380 4132 946 812,7 766,4 537,5 528,2 153,2 95,6 95,6
Те 31814 4939 4612 4341 1006 870,8 820,0 583,4 573,0 169,4 103,3 103,3
I 33169 5188 4852 4557 1072 931 875 630,8 619,3 186 123 123
Xe 34561 5453 5107 4786 1148,7 1002,1 940,6 689,0 676,4 213,2 146,7 145,5
Cs 35985 5714 5359 5012 1211 1071 1003 740,5 726,6 232,3 172,4 161,3
Ba 37441 5989 5624 5247 1293 1137 1063 795,7 780,5 253,5 192 178,6
La 38925 6266 5891 5483 1362 1209 1128 853 836 274,7 205,8 196,0
Ce 40443 6549 6164 5723 1436 1274 1187 902,4 883,8 291,0 223,2 206,5
Pr 41991 6835 6440 5964 1511 1337 1242 948,3 928,8 304,5 236,3 217,6
Nd 43569 7126 6722 6208 1575 1403 1297 1003,3 980,4 319,2 243,3 224,6
Pm 45184 7428 7013 6459 1471 1357 1052 1027 242 242
Sm 46834 7737 7312 6716 1723 1541 1420 1110,9 1083,4 347,2 265,6 247,4
Eu 48519 8052 7617 6977 1800 1614 1481 1158,6 1127,5 360 284 257
Gd 50239 8376 7930 7243 1881 1688 1544 1221,9 1189,6 378,6 286 271
Tb 51996 8708 8252 7514 1968 1768 1611 1276,9 1241,1 396,0 322,4 284,1
Dy 53789 9046 8581 7790 2047 1842 1676 1333 1292,6 414,2 333,5 293,2
Ho 55618 9394 8918 8071 2128 1923 1741 1392 1351 432,4 343,5 308,2
Er 57486 9751 9264 8358 2207 2006 1812 1453 1409 449,8 366,2 320,2
Tm 59390 10116 9617 8648 2307 2090 1885 1515 1468 470,9 385,9 332,6
Yb 61332 10486 9978 8944 2398 2173 1950 1576 1528 480,5 388,7 339,7
Элемент 2V4 (4c/3/2) •Y5 (4<sZ5/2) ^(4/5/2) A7(4/7/2) Oi(5s) O2 (5pi/2) Оз (5рз/2) O4 (5<73/2) D5(5t/5/2) Pi(6s) P 2 (6pi/2) P3 (6p3/2)
Cd H,7 10,7
In 17,7 16,9
Sn 24,9 23,9
Sb 33,3 32,1
Строение вещества
97
Продолжение табл. 2.7
Элемент A4 (4d3/2) As (4d5/2) Л'б (4/s/2) (V7(4/7/2) O} (55) O2 (5/?i/2) Ct, (5/>3/2) о4 (5</j/2) O5 (5d5/2) Ps (65) P2 (6/21/2) P3 (6/?3/2)
Те 41,9 40,4
I 50,6 48,9
Хе 69,5 67,5 23,3 13,4 12,1
Cs 79,8 77,5 22,7 14,2 12,1
Ва 92,6 89,9 30,3 17,0 14,8
La 105,3 102,5 34,3 19,3 16,8
Се 109 0,1 0,1 37,8 19,8 17,0
Рг 115,1 115,1 2,0 2,0 37,4 22,3 22,3
Nd 120,5 120,5 1,5 1,5 37,5 21,1 21,1
Pm 120 120
Sm 129 129 5,2 5,2 37,4 21,3 21,3
Eu 133 127,7 0 0 32 22 22
Gd 142,6 8,6 8,6 36 28 21
Tb 150,5 150,5 7,7 2,4 45,6 28,7 22,6
Dy 153,6 153,6 8,0 4,3 49,9 26,3 26,3
Ho 160 160 8,6 5,2 49,3 30,8 24,1
Er 167,6 167,6 4,7 50,6 31,4 24,7
Tm 175,5 175,5 4,6 54,7 31,8 25,0
Yb 191,2 182,4 2,5 1,3 52,0 30,3 24,1
Элемент X(k) L\ (25) У (2д'2) ^3 (2/23/2) M\ (35) /W2(3^1/2) /W3 (3p3/2) 4/ (3d3/2) M/3d5/2) Y,(45) Y2 (4p1/2) Уз (4p3/2)
Lu 63314 10870 10349 9244 2491 2264 2024 1639 1589 506,8 412,4 359,2
Hf 65351 11271 10739 9561 2601 2365 2108 1716 1662 538 438,2 380,7
Ta 67416 11682 11136 9881 2708 2469 2194 1793 1735 563,4 463,4 400,9
W 69525 12100 11544 10207 2820 2575 2281 1872 1809 594,1 490,4 423,6
Re 71676 12527 11959 10535 2932 2682 2367 1949 1883 625,4 518,7 446,8
Os 73871 12968 12385 10871 3049 2792 2457 2031 1960 658,2 549,1 470,7
Ir 76111 13419 12824 11215 3174 2909 2551 2116 2040 691,1 577,8 495,8
Pt 78395 13880 13273 11564 3296 3027 2645 2202 2122 725,4 609,1 519,4
Au 80725 14353 13734 11919 3425 3148 2743 2291 2206 762,1 642,7 546,3
Hg 83102 14839 14209 12284 3562 3279 2847 2385 2295 802,2 680,2 576,6
T1 85530 15347 14698 12658 3704 3416 2957 2485 2389 846,2 720,5 609,5
Pb 88005 15861 15200 13035 3851 3554 3066 2586 2484 891,8 761,9 643,5
Bi 90524 16388 15711 13419 3999 3696 3177 2688 2580 939 805,2 678,8
Po 93105 16939 16244 13814 4149 3854 3302 2798 2683 995 851 705
At 95730 17493 16785 14214 4317 4008 3426 2909 2787 1042 886 740
Rn 98404 18049 17337 14619 4482 4159 3538 3022 2892 1097 929 768
Fr 101137 18639 17907 15031 4652 4327 3663 3136 3000 1153 980 810
Ra 103922 19237 18484 15444 4822 4490 3792 3248 3105 1208 1058 879
Ac 106755 19840 19083 15871 5002 4656 3909 3370 3219 1269 1080 890
Th 109651 20472 19693 16300 5182 4830 4046 3491 3332 1330 1168 966,4
Pa 112601 21105 20314 16733 5367 5001 4174 3611 3442 1387 1224 1007
U 115606 21757 20948 17166 5548 5182 4303 3728 3552 1439 1271 1043
Элемент A4(4d3/2) Ns (4d5/2) Nb (4/5/2) A7(4/7/2) 0,(55) O2 (5/?1/2) Оз (5рз/2) O4 (5d3/2) O5 (5d5/2) P,(65) P2 (6/2]/2) P3 (6/73/2)
Lu 206,1 196,3 8,9 7,5 57,3 33,6 26,7
Hf 220,0 211,5 15,9 14,2 64,2 38 29,9
Ta 237,9 226,4 23,5 21,6 69,7 42,2 32,7
W 255,9 243,5 33,6 31,4 75,6 45,3 36,8
Re 273,9 260,5 42,9 40,5 83 45,6 34,6
Os 293,1 278,5 53,4 50,7 84 58 44,5
Ir 311,9 296,3 63,8 60,8 95,2 63,0 48,0
Pt 331,6 314,6 74,5 71,2 101,7 65,3 51,7
Au 353,2 335,1 87,6 84,0 107,2 74,2 57,2
Hg 378,2 358,8 104,0 99,9 127 83,1 64,5 9,6 7,8
T1 405,7 385,0 122,2 117,8 136,0 94,6 73,5 14,7 12,5
Pb 434,3 412,2 141,7 136,9 147 106,4 83,3 20,7 18,1
Bi 464,0 440,1 162,3 157,0 159,3 119,0 92,6 26,9 23,8
98
Новый справочник химика и технолога
Окончание табл. 2.7
Элемент Ns (4б/5/2) N6 (4/s/2) A7(4/7/2) O, (55) O2 (5/? 1/2) O3 (5/?з/2) О4(5б/3/2) 05(5<s/2) Pi(65) P 2 (6^i/2) /’3 (6/?з/2)
Ро 500 473 184 184 177 132 104 31 31
At 533 507 210 210 195 148 115 40 40
Rn 567 541 238 238 214 164 127 48 48 26
Fr 603 577 268 268 234 182 140 58 58 34 15 15
Ra 636 603 299 299 254 200 153 68 68 44 19 19
Ac 675 639 319 319 272 215 167 80 80
Th 712,1 675,2 342,4 333,1 290 229 182 92,5 85,4 41,4 24,5 16,6
Pa 743 708 371 360 310 232 232 94 94
U 778,3 736,2 388,2 377,4 321 257 192 102,8 94,2 43,9 26,8 16,8
Таблица 2.8
Энергии фотонов для главных К-, L- и М-линий рентгеновского излучения, эВ
Элемент KaL Ka2 К Pi L di L a? A ₽i L P? PYi M dy
Li 54,3
Be 108,5
В 183,3
C 277
N 392,4
О 524,9
F 676,8
Ne 848,6 848,6
Na 1040,98 1040,98 1071,1
Mg 1253,60 1253,60 1302,2
Al 1486,70 1486,27 1557,45
Si 1739,98 1739,38 1835,94
P 2013,7 2012,7 2139,1
S 2307,84 2306,64 2464,04
Cl 2622,39 2620,78 2815,6
Ar 2957,70 2955,63 3190,5
К 3313,8 3311,1 3589,6
Ca 3691,68 3688,09 4012,7 341,3 341,3 344,9
Sc 4090,6 4086,1 4460,5 395,4 395,4 399,6
Ti 4510,84 4504,86 4931,81 452,2 452,2 458,4
V 4952,20 4944,64 5427,29 511,3 511,3 519,2
Cr 5414,72 5405,509 5946,71 572,8 572,8 582,8
Mn 5898,75 5887,65 6490,45 637,4 637,4 648,8
Fe 6403,84 6390,84 7057,98 705,0 705,0 718,5
Co 6930,32 6915,30 7649,43 776,2 776,2 791,4
Ni 7478,15 7460,89 8264,66 851,5 851,5 868,8
Cu 8047,78 8027,83 8905,29 929,7 929,7 949,8
Zn 8638,86 8615,78 9572,0 1011,7 1011,7 1034,7
Ga 9251,74 9224,82 10264,2 1097,92 1097,92 1124,8
Ge 9886,42 9855,32 10982,1 1188,00 1188,00 1218,5
As 10543,72 10507,99 11726,2 1282,0 1282,0 1317,0
Se 11222,4 11181,4 12495,9 1379,10 1379,10 1419,23
Br 11924,2 11877,6 13291,4 1480,43 1480,43 1525,90
Kr 12649 12598 14112 1586,0 1586,0 1636,6
Rb 13395,3 13335,8 14961,3 1694,13 1692,56 1752,17
Sr 14165 14097,9 15835,7 1806,56 1804,74 1871,72
Y 14958 4 14882,9 16737,8 1922,56 1920,47 1995,84
Zr 15775,1 15690,9 17667,8 2042,36 2039,9 2124,4 2219,4 2302,7
Nb 16615,1 16521,0 18622,5 2165,89 2163,0 2257,4 2367,0 2461,8
Mo 17479,34 17374,3 19608,3 2293,16 2289,85 2394,81 2518,3 2623,5
Tc 18367,1 18250,8 20619 2424 2420 2538 2674 2792
Ru 19279,2 19150,4 21656,8 2558,55 2554,31 2683,23 2836,0 2964,5
Rh 20216,1 20073,7 22723,6 2696,74 2692,05 2834,41 3001,3 3143,8
Строение вещества
99
Окончание табл. 2.8
Элемент К a! К a2 К Pi L a.! L a2 A Pi лр2 M СЦ
Pd 21177,1 21020,1 23818,7 2838,61 2833,29 2990,22 3171,79 3328,7
Ag 22162,92 21990,3 24942,4 2984,31 2978,21 3150,94 3347,81 3519,59
Cd 23173,6 22984,1 26095,5 3133,73 3126,91 3316,57 3528,12 3716,86
In 24209,7 24002,0 27275,9 3286,94 3279,29 3487,21 3713,81 3920,81
Sn 25271,3 25044,0 28486,0 3443,98 3435,42 3662,80 3904,86 4131,12
Sb 26359,1 26110,8 29725,6 3604,72 3595,32 3843,57 4100,78 4347,79
Те 27472,3 27201,7 30995,7 3769,33 3758,8 4029,58 4301,7 4570,9
1 Xe 28612,0 29779 28317,2 29458 32294,7 33624 3937,65 4109,9 3926,04 4220,72 4507,5 4800,9
Cs 30972,8 30625,1 34986,9 4286,5 4272,2 4619,8 4935,9 5280,4
Ba 32193,6 31817,1 36378,2 4466,26 4450,90 4827,53 5156,5 5531,1
La 33441,8 33034,1 37801,0 4650,97 4634,23 5042,1 5383,5 5788,5 833
Ce 34719,7 34278,9 39257,3 4840,2 4823,0 5262,2 5613,4 6052 883
Pr 36026,3 35550,2 40748,2 5033,7 5013,5 5488,9 5850 6322,1 929
Nd 37361,0 36847,4 42271,3 5230,4 5207,7 5721,6 6089,4 6602,1 978
Pm 38724,7 38171,2 43826 5432,5 5407,8 5961 6339 6892
Sm 40118,1 39522,4 45413 5636,1 5609,0 6205,1 6586 7178 1081
Eu 41542,2 40901,9 47037,9 5845,7 5816,6 6456,4 6843,2 7480,3 1131
Gd 42996,2 42308,9 48697 6057,2 6025,0 6713,2 7102,8 7785,8 1185
Tb 44481,6 43744,1 50382 6272,8 6238,0 6978 7366,7 8102 1240
Dy 45998,4 45207,8 52119 6495,2 6457,7 7247,7 7635,7 8418,8 1293
Ho 47546,7 46699,7 53877 6719,8 6679.5 7525,3 7911 8747 1348
Er 49127,7 48221,1 55681 6948,7 6905,0 7810,9 8189,0 9089 1406
Tm 50741,6 49772,6 57517 7179,9 7133,1 8101 8468 9426 1462
Yb 52388,9 51354,0 59370 7415,6 7367,3 8401,8 8758,8 9780,1 1521,4
Lu 54069,8 52965,0 61283 7655,5 7604,9 8709,0 9048,9 10143,4 1581,3
Hf 55790,2 54611,4 63234 7899,0 7844,6 9022,7 9347,3 10515,8 1644,6
Ta 57532 56277 65223 8146,1 8087,9 9343,1 9651,8 10895,2 1710
W 59318,24 57981,7 67244,3 8397,6 8335,2 9672,35 9961,5 11285,9 1775,4
Re 61140,3 59717,9 69310 8652,5 8586,2 10010,0 10275,2 1 1685,4 1842,5
Os 63000,5 61486,7 71413 8911,7 8841,0 10355,3 10598,5 12095,3 1910,2
Ir 64895,6 63286,7 73560,8 9175,1 9099,5 10708,3 10920,3 12512,6 1979,9
Pt 66832 65112 75748 9442,3 9361,8 11070,7 11250,5 12942,0 2050,5
Au 68803,7 66989,5 77984 9713,3 9628,0 11442,3 11584,7 13381,7 2122,9
Hg 70819 68895 80253 9988,8 9897,6 11822,6 11924,1 13830,1 2195,3
T1 72871,5 70831,9 82576 10268,5 10172,8 12213,3 12271,5 14291,5 2270,6
Pb 74969,4 72804,2 84936 10551,5 10449,5 12613,7 12622,6 14764,4 2345,5
Bi 77107,9 74814,8 87343 10838,8 10730,91 13023,5 12979,9 15247,7 2422,6
Po At Rn 79290 81520 83780 76862 78950 81070 89800 92300 94870 11130,8 11426,8 11727,0 11015,8 11304,8 11597,9 13447 13876 14316 13340,4 15744 16251 16770
Fr 86100 83230 97470 12031,3 11895,0 14770 14450 17303
Ra Ac 88470 90884 85430 87670 100130 102850 12339,7 12652,0 12196,2 12500,8 15235,8 15713 14841,4 17849 18408
Th 93350 89953 105609 12968,7 12809,6 16202,2 15623,7 18982,5 2996,1
Pa 95868 92287 108427 13290,7 13122,2 16702 16024 19568 3082,3
U Np Pu Am 98439 94665 111300 13614,7 13944,1 14278,6 14617,2 13438,8 13759,7 14084,2 14411,9 17220,0 17750,2 18293,7 18852,0 16428,3 16840,0 17255,3 17676,5 20167,1 20784,8 21417,3 22065,2 3170,8
Литература
1. Bearden J.A. // Rev. Modem Physics. 1967. V. 39. P. 78.
2. Bearden J.A., Burr A.F. П Rev. Modem Physics. 1967. V. 39. P. 125.
3. Cardona M., Ley L. Photoemission in Solids: General Principles. Berlin: Springer-Verlag, 1978. 290 p.
4. Krause M.O., Oliver J.H. H J. Phys. Chem. Ref. Data. 1979. V. 8. P. 329.
5. Fuggle J.C., Martensson N. П J. Electron Spectrosc. Relat. Phenom. 1980. V. 21. P. 275.
Раздел 3. ФИЗИЧЕСКИЕ СВОЙСТВА ВАЖНЕЙШИХ ВЕЩЕСТВ
Составитель: д. х. н., проф. А.В. Москвин
3.1. Плотность и сжимаемость жидкостей и газов
Плотностью тела р называется масса единицы объема, т. е. величина отношения массы тела в состоянии покоя т к его объему У:
Обратная величина v = — = — называется удельным р т
объемом тела.
В качестве единиц измерения плотности в СИ применяют: килограмм на кубический метр (кг/м3), килограмм на кубический дециметр (кг/дм3) и другие кратные и дольные единицы. Кроме того, часто используют единицы, не входящие в СИ: тонна на кубический метр (т/м3), килограмм на литр (кг/л), грамм на литр (г/л), грамм на миллилитр (г/мл), другие кратные и дольные единицы.
При исггользовании плотности, отнесенной не к 1 см3, а к 1 мл, следует иметь в виду, что 1 мл = 1,000028 см3, а 1 см3 = 0,999972 мл.
При всех измерениях, точность которых не превышает 0,01 %, миллилитр можно принять равным кубическому сантиметру. В пределах этой точности измерений числовые значения плотности, выраженные в г/см3 и г/мл, совпадают.
Относительной плотностью d называется величина отношения плотности рассматриваемого вещества р к плотности стандартного вещества р<> в определенных физических условиях:
d-2-.
ft
В качестве стандартного вещества обычно принимают воду при температуре 4 °C и давлении 101,3 кПа. В этом случае относительная плотность обозначается
d'A, где Т — температура рассматриваемого вещества в °C. Если за стандартное вещество принята вода, находящаяся при той же температуре Т, что и рассматриваемое вещество, то относительная плотность обозначается б7,'.
При определении относительной плотности газов в качестве стандартных веществ принимают сухой атмосферный воздух, водород или кислород.
Свойство тел уменьшать свой объем при всестороннем сжатии под действием сил гидростатического давления называется сжимаемостью. Количественно сжимаемость характеризуется коэффициентом сжимаемости.
Средний коэффициент сжимаемости 0 газа (жидкости) в интервале давлений от р\ до р2 определяется формулой:
У2-Ух \ _ W \
Р2-Р\ Ьр Г1 ’
где И] и Иг — объемы газа (жидкости) соответственно при давлениях р\ мр2.
Коэффициент сжимаемости выражается в Па
Истинным коэффициентом сжимаемости 0 газа (жидкости) называется предел, к которому стремится значение 0, когда Др стремится к нулю:
\dV
V
Коэффициент сжимаемости называется коэффициентом изотермической сжимаемости (0/), если процесс сжатия проводится при постоянной температуре:
1 pH Т~ v{dP)r
и коэффициентом адиабатической сжимаемости (0ад), если сжатие происходит в адиабатических условиях, т. е. без обмена теплотой с окружающей средой:
Физические свойства важнейших веществ
101
ад
if—
V I dP J6Q .0
Ру и рад связаны соотношением:
где ср — теплоемкость при постоянном давлении, а Су — теплоемкость при постоянном объеме.
В табл. 3.1.1-3.1.5 приведены плотность воды, свободной от воздуха, плотность, удельный и молярный
объемы воды и оксида дейтерия, плотность и удельный объем ртути и плотность абсолютного этанола при различных значениях температуры.
Плотности чистых веществ в состоянии жидкости и пара представлены в табл. 3.1.6-3.1.19 для неорганических соединений и в табл. 3.1.20-3.1.43 — для органических. Далее в табл. 3.1.44-3.1.46 содержится информация о среднем коэффициенте изотермической сжимаемости воды, ртути и простых неорганических и органических соединений. Для промышленных газов и паров плотность и сжимаемость при 0 °C и 101,3 кПа приведены в табл. 3.1.47.
Плотность воды (р • 10 3, кг/м3), свободной от воздуха, при 0-30 °C
Таблица 3.1.1
Температура, °C
Единицы Десятые доли
0 1 2 3 4 5 6 7 8 9
0 0,999841 0,999847 0,999854 0,999860 0,999866 0,999872 0,999878 0,999884 0,999889 0,999895
1 0,999900 0,999905 0,999909 0,999914 0,999918 0,999922 0,999926 0,999930 0,999934 0,999938
2 0,999941 0,999944 0,999947 0,999959 0,999953 0,999955 0,999958 0,999960 0,999962 0,999964
3 0,999965 0,999967 0,999968 0,999969 0,999970 0,999971 0,999972 0,999972 0,999973 0,999973
4 0,999973 0,999973 0,999973 0,999972 0,999972 0,999971 0,999970 0,999969 0,999968 0,999966
5 0,999965 0,999963 0,999961 0,999959 0,999957 0,999955 0,999952 0,999950 0,999947 0,999944
6 0,999941 0,999938 0,999935 0,999931 0,999927 0,999924 0,999920 0,999916 0,999911 0,999907
7 0,999902 0,999898 0,999893 0,999888 0,999883 0,999877 0,999872 0,999866 0,999861 0,999855
8 0,999849 0,999843 0,999837 0,999830 0,999824 0,999817 0,999810 0,999803 0,999796 0,999789
9 0,999781 0,999774 0,999766 0,999758 0,999751 0,999742 0,999734 0,999726 0,999717 0,999709
10 0,999700 0,999691 0,999682 0,999673 0,999664 0,999654 0,999645 0,999635 0,999625 0,999615
11 0,999605 0,999595 0,999585 0,999574 0,999564 0,999553 0,999542 0,999531 0,999520 0,999509
12 0,999498 0,999486 0,999475 0,999463 0,999451 0,999439 0,999427 0,999415 0,999402 0,999390
13 0,999377 0,999364 0,999352 0,999339 0,999326 0,999312 0,999299 0,999285 0,999272 0,999258
14 0,999244 0,999230 0,999216 0,999202 0,999188 0,999173 0,999159 0,999144 0,999129 0,999114
15 0,999099 0,999084 0,999069 0,999054 0,999038 0,999023 0,999007 0,998991 0,998975 0,998959
16 0,998943 0,998926 0,998910 0,998893 0,998877 0,998860 0,998843 0,998826 0,998809 0,998792
17 0,998774 0,998757 0,998739 0,998722 0,998704 0,998686 0,998668 0,998650 0,998632 0,998613
18 0,998595 0,998576 0,998558 0,998539 0,998520 0,998501 0,998482 0,998463 0,998444 0,998424
19 0,998405 0,998385 0,998365 0,998345 0,998325 0,998305 0,998285 0,998265 0,998244 0,998224
20 0,998203 0,998183 0,998162 0,998141 0,998120 0,998099 0,998078 0,998056 0,998035 0,998013
21 0,997992 0,997970 0,997948 0,997926 0,997904 0,997882 0,997860 0,997837 0,997815 0,997792
22 0,997770 0,997747 0,997724 0,997701 0,997678 0,997655 0,997632 0,997508 0,997585 0,998561
23 0,997538 0,997514 0,997490 0,997466 0,997442 0,997418 0,997394 0,997369 0,997345 0,997320
24 0,997296 0,997271 0,997246 0,997221 0,997196 0,997171 0,997146 0,997120 0,997095 0,997069
25 0,997044 0,997018 0,996992 0,996967 0,996941 0,996914 0,996888 0,996862 0,996836 0,996809
26 0,996783 0,996756 0,996729 0,996703 0,996676 0,996649 0,996621 0,996594 0,996567 0,996540
27 0,996512 0,996485 0,996457 0,996429 0,996401 0,996373 0,996345 0,996317 0,996289 0,996261
28 0,996232 0,996204 0,996175 0,996147 0,996118 0,996089 0,996060 0,996031 0,996002 0,995973
29 0,995944 0,995914 0,995885 0,995855 0,995826 0,995796 0,995766 0,995736 0,995706 0,995676
30 0,995646 0,995616 0,995586 0,995555 0,995525 0,995494 0,995464 0,995433 0,995402 0,995371
Новый справочник химика и технолога
Физические свойства важнейших веществ
103
Таблица 3.1.2
Плотность воды, свободной от воздуха, при 30-250 °C
7’, °C р • 10 3, кг/м3 Л °C р • 10 3, кг/м3
30 0,99565 55 0,98570
31 0,99534 60 0,98321
32 0,99502 65 0,98056
33 0,99470 70 0,97778
34 0,99437 75 0,97486
35 0,99403 80 0,97180
36 0,99368 85 0,96862
37 0,99333 90 0,96531
38 0,99296 95 0,96189
39 0,99266 100 0,95835
40 0,99221 ПО 0,9510
41 0,99183 120 0,9434
42 0,99144 130 0,9352
43 0,99104 140 0,9264
44 0,99063 150 0,9173
45 0,99022 160 0,9075
46 0,98979 170 0,8973
47 0,98936 180 0,8866
48 0,98893 190 0,8750
49 0,98849 200 0,8628
50 0,98804 210 0,850
51 0,98659 220 0,837
52 0,98612 230 0,823
53 0,98666 240 0,809
54 0,98618 250 0,794
Таблица 3.1.3
Плотность, удельный и молярный объемы воды и оксида дейтерия (тяжелой воды) при 0-34 °C
Т, °C р • 10 3, кг/м3 v • 103, м3/кг Кмол, СМ3/МОЛЬ
н2о d2o н20 d2o Н2О D2O
0 0,999841 1,1046 1,00016 0,9053 18,019 18,130
2 0,999941 1,1050 1,00006 0,9050 18,017 18,124
4 0,999973 1,1053 1,00003 0,9047 18,017 18,118
6 0,999941 1,1055 1,00006 0,9046 18,017 18,116
8 0,999849 1,1056 1,00015 0,9045 18,019 18,114
10 0,999700 1,1057 1,00030 0,9044 18,022 18,112
12 0,999498 1,1057 1,00050 0,9044 18,025 18,112
14 0,999244 1,1056 1,00076 0,9045 18,030 18,114
16 0,998943 1,1055 1,00106 0,9046 18,035 18,116
18 0,998595 1,1053 1,00141 0,9047 18,042 18,118
20 0,998203 1,1050 1,00180 0,9050 18,049 18,124
22 0,997770 1,1046 1,00223 0,9053 18,056 18,130
24 0,997296 1,1042 1,00271 0,9056 18,065 18,136
26 0,996783 1,1038 1,00322 0,9060 18,074 18,144
28 0,996232 1,1032 1,00378 0,9065 18,085 18,154
30 0,995646 1,1028 1,00327 0,9068 18,094 18,160
32 0,995025 1,1019 1,00500 0,9075 18,106 18,174
34 0,994371 1,1011 1,00566 0,9082 18,118 18,188
104
Новый справочник химика и технолога
Плотность и удельный объем ртути в зависимости от температуры
Таблица 3.1.4
Т, °C р • 10 3, кг/м3 V 103. л/кг Т. °C р • 10 3, кг/м3 V 103, л/кг
При давлении 101,325 кПа 31 13,5177 0,0739691
-20 13,6446 0,0732869 32 13,5163 0,0739825
-19 13,6421 0,0733002 33 13,5138 0,0739960
-18 13,6396 0,0733135 34 13,5114 0,0740094
-17 13,6371 0,0733269 35 13,5090 0,0740228
-16 13,6346 0,0733402 36 13,5065 0,0740362
-15 13,6322 0,0733535 37 13,5041 0,0740496
-14 13,6297 0,0733670 38 13,5016 0,0740630
-13 13,7282 0,0733805 39 13,4992 0,0740765
-12 13,6247 0,0733940 40 13,4967 0,0740898
-И 13,7222 0,0734074 41 13,4943 0,0741033
-10 13,7198 0,0734205 42 13,4918 0,0741167
-9 13,6173 0,0734338 43 13,4894 0,0741301
-8 13,6148 0,0734472 44 13,4869 0,0741435
-7 13,6023 0,0734608 45 13,4845 0,0741570
—6 13,6099 0,0734739 46 13,4821 0,0741704
-5 13,6074 0,0734873 47 13,4796 0,0741838
-4 13,6049 0,0735006 48 13,4772 0,0741972
-3 13,6025 0,0735140 49 13,4747 0,0742107
-2 13,6000 0,0735273 50 13,4723 0,0742241
-1 13,5975 0,0735407 51 13,4699 0,0742375
0 13,5951 0,0735540 52 13,4674 0,0742510
1 13,5926 0,0735674 53 13,4650 0,0742644
2 13,5901 0,0735808 54 13,4626 0,0742778
3 13,5876 0,0735943 55 13,4601 0,0742913
4 13,5852 0,0736075 56 13,4577
5 13,5827 0,0736209 57 13,4553
6 13,5802 0,0736342 58 13,4528
6 13,5778 0,0736476 59 13,4504
7 13,5778 0,0734376 60 13,4480 0,0743585
8 13,5753 0,0736610 61 13,4455
9 13,5728 0,0736746 62 13,4431
10 13,6704 0,0736877 63 13,4407
11 13,5679 0,0737011 64 13,4382
12 13,5654 0,0737145 65 13,4358 0,0744257
13 13,5630 0,0737278 66 13,4334
14 13,5605 0,0737412 67 13,4310
15 13,5580 0,0737550 68 13,4285
16 13,5556 0,0737680 69 13,4261
17 13,5531 0,0736713 70 13,4237
18 13,5507 0,0737947 71 13,4213
19 13,5482 0,0738081 72 13,4188
20 13,5457 0,0738215 73 13,4164
21 13,5433 0,0738348 74 13,4140
22 13,5408 0,0738487 75 13,4116 0,0745602
23 13,5384 0,0738617 76 13,4091
24 13,5359 0,0738753 77 13,4067
25 13,5335 0,0738888 78 13,4043
26 13,5310 0,0739022 79 13,4019
27 13,5286 0,0739153 80 13,3995 0,0746276
28 13,5261 0,0739289 81 13,3971
29 13,5237 0,0739423 82 13,3946
30 13,5212 0,0739558 83 13,3922
Физические свойства важнейших веществ
105
Продолжение табл. 3.1.4
Т, °с р • 10 3, кг/м3 v 103, л/кг Т, °C р • 10 3, кг/м3 v 103, л/кг
84 13,4898 290 12,899 0,077513
85 13,3874 0,0746949 300 12,876 0,077666
86 13,3850 При давлении 2,03 МПа
87 13,3826 200 13,114 0,076254
88 13,3902 210 13,090 0,076394
89 13,3777 220 13,066 0,076534
90 13,3753 0,0747623 230 13,043 0,076669
91 13,3729 240 13,019 0,076802
92 13,3705 250 12,995 0,076953
93 13,3681 260 12,971 0,077095
94 13,3657 270 12,948 0,077232
95 13,3633 0,0748294 280 12,924 0,077375
96 13,3609 290 12,900 0,077519
97 13,3585 300 12,877 0,077658
98 13,3561 310 12,853 0,077810
99 13,3537 320 12,829 0,077954
100 13,3514 0,0748971 330 12,805 0,078099
НО 13,328 0,075032 340 12,781 0,078245
120 13,304 0,075167 350 12,758 0,078391
130 13,280 0,075303 360 12,734 0,078538
140 13,256 0,075439 370 12,710 0,078685
150 13,232 0,075575 380 12,686 0,078834
160 13,208 0,075712 390 12,662 0,078993
170 13,184 0,075849 400 12,638 0,079133
180 13,160 0,075986 410 12,614 0,079277
190 13,137 0,076124 420 12,590 0,079349
200 13,113 0,076262 430 12,565 0,079586
210 13,089 0,076400 440 12,541 0,079738
220 13,065 0,076539 450 12,517 0,079897
230 13,042 0,076678 460 12,493 0,080045
240 13,018 0,076818 470 12,468 0,080205
250 12,994 0,076958 480 12,444 0,080360
260 12,970 0,077099 490 12,419 0,080522
270 12,947 0,077239 500 12,395 0,080686
280 12,923 0,077371
Таблица 3.1.5
Плотность абсолютного этанола при 0-39 °C
Т, °C р • 10 3, кг/м3 Т,°С р • 10 3, кг/м3 Л °C р • 10 J, кг/м3
0 0,80625 14 0,79451 28 0,78267
1 0,80541 15 0,79367 29 0,78182
2 0,80457 16 0,79283 30 0,78097
3 0,80374 17 0,79198 31 0,78012
4 0,80290 18 0,79114 32 0,77927
5 0,80207 19 0,79029 33 0,77841
6 0,80123 20 0,78945 34 0,77756
7 0,80039 21 0,78860 35 0,77561
8 0,79956 22 0,78775 36 0,77585
9 0,79872 23 0,78691 37 0,77500
10 0,79788 24 0,78606 38 0,77414
11 0,79704 25 0,78522 39 0,77329
12 0,79620 26 0,78437
13 0,79535 27 0,78352
106
Новый справочник химика и технолога
Плотность чистых веществ в состоянии жидкости (рж) и пара (р„), находящихся в равновесии
Величины, выделенные курсивом, относятся к критическому состоянию вещества. В конце некоторых таблиц приведены уравнения прямолинейного диаметра (правило Кальете — Матиаса), которые описывают зависимость средней плотности вещества в жидком и парообразном состоянии от температуры. Экстраполяция этой зависимости к критической температуре позволяет рассчитать плотность вещества при критической температуре. Недостаточно надежные данные заключены в скобки.
Простые вещества и неорганические соединения
Указатель таблиц плотности чистых веществ в состоянии жидкости и пара
Вещество № табл.
Аг 3.1.8
СО 3.1.16
со2 3.1.12
С12 3.1.19
Н2 3.1.9
Не 3.1.10
Кг 3.1.14
N2 3.1.6
NH3 3.1.7
Ne 13.1.17
о2 3.1.13
so2 3.1.11
SnCl4 3.1.18
Хе 3.1.15
В конце некоторых таблиц приведены уравнения, связывающие плотность веществ в жидком и парообразном состоянии с температурой.
Таблица 3.1.6
Азот (N2)
Т, °C рж • 10 3, кг/м3 рн • 10 3, кг/м3
-208,47 0,8622 0,00089
-205,45 0,8499 0,00136
-200,03 0,8265 0,00267
-195,09 0,8043 0,00490
-182,51 0,7433 0,01558
-173,73 0,6922 0,02962
-161,20 0,6071 0,06987
-153,65 0,5332 0,1177
-149,75 0,4799 0,1638
-148,61 0,4504 0,1862
-148,08 0,4313 0,2000
Таблица 3.1.7
Аммиак (NH3)
Т,°С рж • 10 3, кг/м3 рп • 10 3, кг/м3
0 0,6389 0,0034
45,0 0,5696 0,0150
78,7 0,5120 0,0322
Окончание табл. 3.1.7
Т, °C рж • 10 3, кг/м3 р„ • 10 3, кг/м3
98,75 0,4640 0,0533
109,25 0,4339 0,0691
116,4 0,4056 0,0873
121,3 0,3831 0,1024
123,2 0,3750 0,1085
125,45 0,3584 0,1220
129,6 0,3246 0,1509
132,4 0,235
-у-+ Рп = 0,32165 - 6,475 • 10’4 Т 2
Таблица 3.1.8
Аргон (Аг)
Т, °C рж • 10 3 кг/м3 р„ • 10'3 кг/м3
-183,15 1,37396 0,00801
-175,39 1,32482 0,01457
-161,23 1,22414 0,03723
-150,76 1,13851 0,06785
-140,20 1,03456 0,12552
-135,51 0,91499 0,19432
-125,17 0,77289 0,29534
-122,5 0,531
^-Рг-1' = 0,20956 - 0,00262357’
Таблица 3.1.9
Водород (Н2)
Г, °C рж • 10 3, кг/м3 Рн • 10“3, кг/м3
-258,27 0,07631 0,00020
-257,23 0,07538 0,00031
-256,76 0,07494 0,00038
-255,19 0,07344 0,00064
-253,76 0,07192 0,00101
-253,24 0,07137 0,00116
-252,68 0,07081 0,00135
-249,89 0,06724 0,00264
-247,79 0,06416 0,00405
-245,73 0,06050 0,00613
-244,30 0,05740 0,00806
-243,03 0,05402 0,01081
-241,83 0,05001 0,01366
-240,67 0,04316 0,01922
-239,9 0,031
Рп =0,063510-3,9402 • 1 О’4 Т
2
Таблица 3.1.10
Гелий (Не)
Г, °C рж • 10 3, кг/м3 р„ • 10 3, кг/м3
-270,79 0,1469 0,001159
-270,72 0,1466 0,001368
Физические свойства важнейших веществ
107
Окончание табл. 3.1.10
Г, °C рж • 10 3, кг/м3 рп • 10 3, кг/м3
-270,53 0,1457 0,002079
-269,79 0,1395 0,006435
-269,19 0,1311 0,01176
-268,87 0,1255 0,01618
-268,86 0,1253 0,01637
-268,50 0,1165 0,02389
-268,38 0,1139 0,02699
Рж +Рп = -0,40263 - 0,0017616Т
2
Таблица 3.1.11
Диоксид серы (SO2)
Т, °C рж • 10 3, кг/м3 рп • 10 3, кг/м3
145,0 0,8347 0,2388
154,4 0,6700 0,3747
154,8 0,6574 0,3847
155,4 0,6401 0,3997
156,0 0,6153 0,4194
156,3 0,6010 0,4319
156,55 0,5900 0,4414
Окончание табл. 3.1.13
Г, °C Рж-Ю’3, кг/м3 Г, °C Рж-Ю3, кг/м3
-195,5 1,2032 -187,0 1,1623
-195,0 1,2008 -186,5 1,1599
-194,5 1,1984 -186,0 1,1575
-194,0 1,1959 -185,5 1,1551
-193,5 1,1935 -185,0 1,1527
-193,0 1,1911 -184,5 1,1503
-192,5 1,1887 -184,0 1,1479
-192,0 1,1963 -182,0 1,1415
-191,5 1,1839 -154,51 0,9758
-191,0 1,1815 -140,20 0,8742
-190,5 1,1791 -129,9 0,7781
-190,0 1,1767 -123,3 0,6779
-189,5 1,1743 -120,4 0,6032
рж = 1,248874-0,0048(74 205)
Таблица 3.1.12
Диоксид углерода СО2
Г, °C рж • 10 3, кг/м3 рп • 10 3, кг/м3
-5,8 0,9604 0,0803
-1,8 0,9378 0,0940
1,2 0,9198 0,1029
6,2 0,8878 0,1217
11,2 0,8547 0,1309
15,2 0,8216 0,1607
17,2 0,8045 0,1621
22,9 0,7422 0,2163
31,0 0,468
Рж+Р^ = 0,4683 + 0,001442(Гкр - Г)
Таблица 3.1.14
Криптон (Кг)
т °C рж • 10 3, кг/м3 р„ • 10 3, кг/м3
-147,18 2,3707 0,01333
-139,02 2,3040 0,02196
-129,11 2,3202 0,003739
-119,81 2,1363 0,005774
-109,46 2,0350 0,09004
-102,22 1,9574 0,12014
-92,32 1,8338 0,17576
-84,76 1,7255 0,23501
-79,51 1,6379 0,2903
-73,51 1,5161 0,3774
-71,24 1,4590 0,4217
-67,15 1,3171 0,5404
-64,94 1,1926 0,6467
Таблица 3.1.13
Кислород (О2)
Г, °C Рж-10’3, кг/м3 Г, °C Рж • ЮЛ кг/м3
-210,4 1,2746 -201,5 1,2320
-205,9 1,2489 -201,0 1,2296
-204,5 1,2465 -200,5 1,2272
-204,0 1,2551 -200,0 1,2248
-203,5 1,2417 -199,5 1,2224
-203,0 1,2393 -199,0 1,2200
-202,5 1,2368 -198,5 1,2176
-202,0 1,2344 -198,0 1,2152
-198,5 1,2128 -189,0 1,1719
-197,0 1,2104 -188,5 1,1695
-196,5 1,2080 -188,0 1,1671
-196,0 1,2056 -187,5 1,1647
Таблица 3.1.15
Ксенон (Хе)
Г, °C рж • 10 3, кг/м3 рп • 10 3, кг/м3
-66,74 2,763 0,059
-59,24 2,694 0,078
-49,14 2,605 0,10
-39,24 2,506 0,139
-30,24 2,411 0,180
-20,19 2,297 0,235
-9,94 2,169 0,313
-4,94 2,074 0,363
0,06 1,987 0,421
10,06 1,750 0,602
15,06 1,528 0,770
Таблица 3.1.16
Монооксид углерода (СО)
Г, °C рж • 10 3, кг/м3 рн • 10 3, кг/м3
-204,97 0,84714 0,0008
-199,54 0,82554 0,00171
108
Новый справочник химика и технолога
Окончание табл. 3.1.16
Т,°С рж • 10 3, кг/м3 р„ • 10 3, кг/м3
-195,08 0,80640 0,00296
-190,86 0,79086 0,00477
-185,96 0,76904 0,00774
-182,83 0,75446 0,01019
-178,95 0,73408 0,01422
-172,18 0,69953 0,02389
-169,61 0,68560 0,02824
-165,50 0,66168 0,03681
-164,06 0,65262 0,04014
-152,21 0,56582 0,08202
-147,51 0,52083 0,11607
-145,40 0,49190 0,13601
-143,31 0,45640 0,16357
-142,26 0,43365 0,18462
Р1? = 0,03290 - 0,001912Т 2
Таблица 3.1.17
Неон (Ne)
Т, °C рж • 10 3, кг/м3 р„ • 10 3. кг/м3
-247,92 1,23824 0,00534
-245,94 1,20421 0,00939
-242,96 1,14960 0,02013
-240,00 1,08832 0,03831
-237,04 1,01750 0,06742
-235,26 0,96728 0,09310
-234,01 0,92803 0,11592
-232,02 0,85421 0,16563
-230,06 0,74866 0,23935
-227,7 0,484
Рж+Рп =-1,154406 - 0,071615Т 2
Таблица 3.1.18
Олова тетрахлорид (SnCl4)
Т, °C рж • 10 3, кг/м3 ри • 10 3, кг/м3
0 2,27875 (0,00009)
20 2,2262 (0,0002)
40 2,1749 (0,0007)
60 2,1231 (0,0015)
80 2,0717 (0,0031)
120 1,9639 0,009921
140 1,9073 0,01618
160 1,8481 0,02513
180 1,7873 0,03738
200 1,7224 0,04349
220 1,6488 0,07728
240 1,4557 0,1083
270 1,3628 0,1812
318,7 0,742
Рж +Рп = 1,1387 - 0,00127667 + 9,77 • 1О"8 Т1
2
Таблица 3.1.19
Хлор (С12)
Т, °C рж • 10 3, кг/м’ р„ • 10 3. кг/м3
-100 1,717
-90 1,694
-80 1,673
-70 1,646
-60 1,622
-50 1,598
^10 1,574
-30 1,550
-20 1,524
-10 1,496
0 1,468 0,0128
10 1,438 0,0175
20 1,408 0,0226
30 1,377 0,0300
40 1,344 0,0384
50 1,310 0,0486
60 1,275 0,0600
70 1,240 00740
80 1,199 0,0910
90 1,156 0,1125
100 1,109 0,1360
НО 1,059 0,1640
120 0,998 0,206
130 0,920 0,258
140 0,750 0,405
144 0,573
Органические соединения
Указатель таблиц плотности, чистых веществ в состоянии жидкости и пара
Соединение № табл. Соединение № табл.
СС14 3.1.36 С2Н5С1 3.1.40
СНС13 3.1.39 С2Н6О 3.1.27,
3.1.41
СН4 3.1.29 с3н6о 3.1.21
СН4О 3.1.30 с3н6о2 3.1.32
с2н2 3.1.20 с3н8о 3.1.35
с2н4 3.1.43 с4н8о2 3.1.32,
3.1.42
С2Н4О2 3.1.33, С4Ню 3.1.25
3.1.38
С4Н)0О 3.1.28 С7н8 3.1.37
С6Н5Вг 3.1.24 С8н18 3.1.34
с6н6 3.1.22 Cj2H ю 3.1.23
С6Н]4 3.1.26
Таблица 3.1.20
Ацетилен (С2Н2)
Г, °C рж • 10 3, кг/м3 рп • 103, кг/м3
-23,48 0,5185 0,0217
6,11 0,4476 0,0528
Физические свойства важнейших веществ
109
Окончание табл. 3.1.20
7, °C рж • 10 3, кг/м3 р„ • 10 3, кг/м3
12,05 0,4295 0,0632
17,07 0,4120 0,0740
20,40 0,3987 0,0831
23,42 0,3859 0,0925
24,11 0,3814 0,0958
28,98 0,3559 0,1160
29,07 0,3556 0,1163
31,43 0,3379 0,1305
32,09 0,3315 0,1361
32,88 0,3282 0,1393
33,74 0,3146 0,1490
36 0,231
Таблица 3.1.23
Бифенил ((С6Н5)2)
Таблица 3.1.21
Ацетон (СН3СОСН3)
Т, °C рж • 10 3, кг/м3 Рн • 10 3, кг/м3
211,0 0,4787
212,5 0,0834
212,6 0,0905
217,7 0,0930
224,1 0,4251
234,6 0,1713
235,0 0,3258
235,5 0,2980
235,5 0,273
Г, °C рж • 10 3, кг/м3 рп • 10 3, кг/м3
93,3 0,9749 0,000017
121,1 0,9525 0,000060
148,7 0,9304 0,000187
176,7 0,9074 0,000455
204,4 0,8849 0,000987
232,2 0,8620 0,001954
255,3 0,8424 0,003363
260,0 0,8381 0,003780
287,8 0,8126 0,00713
315,6 0,7865 0,01201
343,3 0,7577 0,01898
371,1 0,7269 0,02771
398,9 0,6933 0,03844
427,7 0,7660 0,05374
454,4 0,6103 0,07512
482,2 0,5539 0,10972
Таблица 3.1.24
Бромбензол (С6Н§Вг)
Таблица 3.1.22
Бензол (С6Н6)
Г, °C рж • 10 3, кг/м3 р„ • 10 3, кг/м3
0 0,90006 (0,00012)
20 0,8790 (0,0004)
40 0,8576 0,0008
60 0,8357 (0,0015)
70 0,8348 0,002040
80 0,8145 0,002732
90 0,8041 0,003610
100 0,7927 0,004704
ПО 0,7809 0,006042
120 0,7692 0,007675
130 0,7568 0,009551
140 0,7440 0,01176
150 0,7310 0,01437
170 0,7043 0,02087
200 0,6605 0,03546
230 0,6065 0,05977
260 0,5328 0,1034
280 0,4514 0,1660
286,1 0,4078
288,0 0,3856
289,5 0,300
Т °C рж • 10 3. кг/м3 Рн • 10 3, кг/м3
0 1,52182
20 1,4948
40 1,4682 (0,0001)
60 1,4411 (0,0002)
80 1,4142 (0,0005)
100 1,3864 (0,0010)
120 1,3583 (0,0019)
140 1,3293 (0,0031)
150 1,3146 (0,004125)
160 1,2994 0,005241
170 1,2847 0,006562
180 1,2697 0,008117
190 1,2534 0,009950
200 1,2385 0,01209
210 1,2210 0,01458
220 1,2037 0,01745
230 1,1876 0,02079
240 1,1689 0,02482
250 1,1510 0,02927
260 1,1310 0,03427
270 1,1099 0,04016
397 0,485
Рж + Рп- = 0,7609 + 6,655 • 1О4 Т
2
Рж + Рп = о, 4501 - 5,248 • 10"* Г + 6,93 • 108 Т2 2
Таблица 3.1.25
Бутан (С4Ню)
Г, °C рж • 10 3, кг/м3 рп • 10 3, кг/м3
0 0,5992
8,0 0,5907 0,00379
16,0 0,5820 0,00490
24,0 0,5725 0,00605
32,0 0,5635 0,00756
по
Новый справочник химика и технолога
Окончание табл. 3.1.25
Т,°С рж • 10 3, кг/м3 р„ • 10 3, кг/м3
40,0 0,5538 0,00948
48,0 0,5436 0,0120
56,0 0,5325
Таблица 3.1.26
Гексан (C6HJ4)
Т, °C рж • 10 3, кг/м3 ри • 10 3, кг/м3
0 0,6769 (0,0002)
10 0,6684 (0,0004)
40 0,6412 (0,0013)
50 0,6318 (0,0018)
60 0,6221 0,002488
70 0,6122 0,003367
80 0,6022 0,00446
90 0,5918 0,00585
100 0,5814 0,00754
ПО 0,5703 0,00956
120 0,5588 0,1202
130 0,5467 0,01504
140 0,5343 0,186
150 0,5207 0,02299
160 0,5063 0,02833
180 0,4751 0,04228
200 0,4365 0,06329
220 0,3810 0,1011
230 0,3329 0,1405
233 0,3040 0,1638
234 0,2883 0,1807
234,7 0,234
Окончание табл. 3.1.28
Т, °C рж • 10’3. кг/м3 р„ • 10 3, кг/м3
40 0,6894 0,003731
60 0,6658 0,006771
80 0,6402 0,01155
100 0,6105 0,01867
120 0,5764 0,02934
140 0,5385 0,04488
160 0,4947 0,06911
180 0,4268 0,1135
190 0,3663 0,1620
192 0,3300 0,2012
194 0,264
Рж+Рп = 0,3685 - 5,377 • 10’4 Т
2
Таблица 3.1.29
Метан СН4
Т. °C рж • 10"3. кг/мл Рн • 10 3, кг/м3
-107 0,3242 0,0412
-100 0,3024 0,0431
-95 0,2857 0,0532
-94 0,2810 0,0582
-90 0,2638 0,0679
-86 0,2382 0,0912
-85 0,2288 0,0992
-84 0,2156 0,1093
-82,1 0,162
Рж +Рп - о,11206-6,064-10 4Г
2
Рж+Р" =0,3388-4,445-10^7
2
Таблица 3.1.27
Диметиловый эфир ((СН3)2О)
Т, °C рж • 10'3, кг/м3 рп • 10 3, кг/м3
0,20 0,6903 0,0042
29,85 0,6458 0,0160
80,15 0,5522 0,0486
110,50 0,4550 0,1076
121,12 0,3950 0,1548
125,01 0,3518 0,1932
126,01 0,2393 0,2139
126,50 0,3098 0,2337
126,9 0,242
Рж +Рп = 0,3473 - 5,984 • 10 '4 Т
2
Таблица 3.1.28
Диэтиловый эфир ((С2Н5)2О)
Г, °C рж • 10 3, кг/м3 рн • 10 3, кг/м3
0 0,7362 0,000827
10 0,7248 0,001264
20 0,7135 0,001870
30 0,7019 0,002677
Метанол (СН3ОН)
Таблица 3.1.30
Г, °C рж • 10 3, кг/м3 Рн • 10"3, кг/м3
0 0,8100 0,00005620
10 0,8008 0,00009960
20 0,7915 0,0001695
30 0,7825 0,0002772
40 0,7740 0,0004394
50 0,7650 0,0006739
60 0,7555 0,001006
70 0,7460 0,001465
80 0,7355 0,002084
90 0,7250 0,002907
100 0,7140 0,003984
ПО 0,7020 0,005376
120 0,6900 0,007142
130 0,6770 0,009479
140 0,6640 0,01216
150 0,6495 0,01562
160 0,5340 0,01994
170 0,6160 0,02526
180 0,5980 0,03186
190 0,5770 0,04010
200 0,5530 0,05075
210 0,5255 0,06521
Физические свойства важнейших веществ
111
Окончание табл. 3.1.30
Т. °C рж • 10 3, кг/м3 ри • 10 3, кг/м3
220 0,4900 0,08635
225 0,4675 0,1003
230 0,4410 0,1187
232 0,4295 0,1277
234 0,4145 0,1381
236 0,3955 0,1505
238 0,3705 0,1681
239 — 0,1878
240 0,272
Окончание табл. 3.1.32
Г, °C рж • 10 3, кг/м3 р„ • 10 3, кг/м3
130 0,7705 0,01214
160 0,7221 0,02356
190 0,6657 0,04320
220 0,5938 0,07812
250 0,4655 0,1675
256 0,3982 0,2294
257,4 0,312
Рж+Рп = 0,4050 - 4,479 • 10 4 Т +1,330 • 10 7 Т1 -2
-2,776-10’9 Г3
Таблица 3.1.31
Метилацетат (СН3СООСН3)
Г, °C рж • 10 3, кг/м3 рп • 10 3, кг/м3
0 0,95932 (0,0003)
20 0,9338 (0,0007)
40 0,9075 (0,0015)
50 0,8939 0,002212
60 0,8800 0,003076
70 0,8662 0,004193
80 0,8519 0,005618
90 0,8374 0,007440
100 0,8221 0,009671
110 0,8060 0,01239
120 0,7893 0,01570
130 0,7715 0,1970
140 0,7532 0,02454
150 0,7339 0,03026
160 0,7133 0,03731
170 0,6907 0,04598
180 0,6671 0,05682
190 0,6410 0,06993
200 0,6100 0,08658
210 0,5741 0,1091
220 0,5281 0,1416
227 0,4818 0,1776
230 0,4527 0,2028
232 0,4226 0,2288
233 0,3995 0,2525
233,7 0,325
Рж+Рп = о,4624-5,992-10^7-7,64-10'7 Г2 2
Таблица 3.1.32
Метилпропаноат (С2Н5СООСНз)
Т,°С рж • 10 3, кг/м3 р„ • 10 3, кг/м3
0 0,93871 0,0001
20 0,9151 0,0003
60 0,8554 0,0016
80 0,8408 0,003199
100 0,8137 0,005714
Таблица 3.1.33
Метилформиат (НСООСН3)
Г, °с рж • 10 3, кг/м3 рп • 10 3, кг/м3
0 1,00319
30 0,9598 0,002291
50 0,9294 0,004456
80 0,8803 0,01049
100 0,8452 0,01723
120 0,8070 0,02688
150 0,7403 0,05063
180 0,6521 0,09434
210 0,4857 0,2188
213 0,4328 0,2681
213,5 0,4157 0,2865
214,0 0,349
Таблица 3.1.34
Октан С8Н18
Л °C рж • 10 3, кг/м3 Рп • 10 3, кг/м3
0 0,71848
20 0,7022 (0,0001)
40 0,6860 (0,0002)
60 0,6694 (0,0004)
80 0,6525 (0,0009)
100 0,6351 (0,0017)
120 0,6168 0,003247
140 0,5973 0,005405
160 0,5772 0,008591
180 0,5556 0,01316
200 0,5317 0,0196
220 0,5053 0,02874
240 0,4732 0,04237
260 0,3264 0,06223
280 0,3818 0,09833
290 0,3365 0,1346
296,7 0,233
^5—El = 03592-3,986-10 4Г-9,6-10 s72 2
Таблица 3.1.35
Пропан-1-ол (С3Н7ОН)
Т, °C рж • 10 3, кг/м3 рп • 10 3, кг/м3
0 0,8193
20 0,8035 (0,0001)
40 0,7875 (0,0002)
112
Новый справочник химика и технолога
Окончание табл. 3.1.35
7, °C рж • 10 3, кг/м3 р„ • 10 3, кг/м3
60 0,7700 (0,0004)
80 0,7520 0,00104
90 0,7425 0,00156
100 0,7325 0,00226
110 0,7220 0,00320
120 0,7110 0,00443
130 0,6995 0,00605
140 0,6875 0,00805
150 0,6740 0,01060
160 0,6600 0,01380
170 0,6450 0,01770
180 0,6285 0,0225
190 0.6110 0,0282
200 0,5920 0,0353
210 0,5715 0,0442
220 0,5485 0,0556
230 0,4230 0,0704
240 0,4920 0,0904
250 0,4525 0,1180
260 0,3905 0,1610
263,15 0,2340
253,5 0,3380
264 0,273
Окончание табл. 3.1.37
7, °C рж • 10 3. кг/м3 р„ • 10 3, кг/м3
240 0,614 0,048
250 0,594 0,057
260 0,574 0,066
270 0,554 0,076
280 0,534 0,085
Таблица 3.1.38
Уксусная кислота (СН3СООН)
Таблица 3.1.36
Тетрахлорметан (СС14)
7, °C рж • 10 3, кг/м3 р„ • 10 3, кг/м3
0 1,63255 (0,0003)
20 1,5939 (0,0008)
40 1,5557 (0,0017)
60 1,5165 (0,0033)
80 1,4705 0,006083
100 1,4343 0,01027
120 1,3902 0,01639
140 1,3450 0,02500
160 1,2982 0,03650
180 1,2470 0,05249
200 1,1888 0,07418
220 1,1227 0,1040
240 1,0444 0,1464
260 0,9409 0,2146
280 0,7634 0,3597
283,2 0,558
Рж +Рп = о 4624-5,992-10^7-7,64-Ю7Г2 2
7, °C рж • 10 3. кг/м3 Рн • 10 3, кг/м3
0 1,06970
10 1,0593
20 1,0491 0,0000764
30 1,0392 0,0001264
50 1,0175 0,00031
60 1,0060 0,0004621
70 0,9948 0,000673
80 0,9835 0,000959
90 0,9718 0,001338
100 0,9599 0,001833
ПО 0,9483 0,002468
120 0,9362 0,003271
130 0,9235 0,004275
140 0,9091 0,005515
150 0,8963 0,00703
160 0,8829 0,00887
170 0,8694 0,01084
180 0,8555 0,01370
190 0,8413 0,01681
200 0,8265 0,02052
210 0,8109 0,02488
220 0,7941 0,03021
230 0,7764 0,03626
240 0,7571 0,04327
250 0,7364 0,003626
260 0,7136 0,06165
270 0,6900 0,07365
280 0,6629 0,0883
290 0,6334 0,1073
300 0,5950 0,1331
310 0,5423 0,1718
320 0,4615
321,6 0,351
Рж + Рп = 0,5355-5,366-10^7-1,91-10~772 2
Таблица 3.1.37
Толуол (С6Н5СН3)
7, °C рж • 10 3, кг/м3 рп • 10 3, кг/м3
190 0,687 0,022
200 0,672 0,026
210 0,658 0,030
220 0,644 0,035
230 0,630 0,040
Таблица 3.1.39
Хлороформ (СНС13)
7, °C рж • 10 3, кг/м3 рп • 10 3, кг/м3
207,5 217,9 232,7 0,9306 0,1040 0,1184
Физические свойства важнейших веществ
113
Окончание табл. 3.1.39
7’, °C рж • 10”3. кг/м3 рп • 10 3, кг/м3
251,1 0,7988
251,3 0,8001
252,5 0,2370
260,8
261,6 0,6653
261,7 0,5812
262,2 0,5068
262,7 0,4872
262,8 0,5357 0,4579
263,4 0,50
Таблица 3.1.40
Хлорэтан (С2Н5С1)
Т, °C рж • 10 3, кг/м3 р„ • 10'3, кг/м3
-25 0,964
-15 0,942
-14,7 0,001078
-10 0,993 0,001228
0 0,919
10 0,907
10,7 0,002674
20 0,892
30 0,878
40 0,862
60 0,829
80 0,796
Таблица 3.1.42
Этилацетат (СН3СООС2Н5)
Т, °C рж • 10 3, кг/м3 ри • 10 3, кг/м3
0 0,92436 (0,000)
20 0,9005 (0,0003)
40 0,8762 (0,0008)
60 0,8508 (0,0018)
70 0,8376 0,002561
80 0,8245 0,003495
90 0,8112 0,004677
100 0,7972 0,006158
НО 0,7831 0,008006
120 0,7683 0,01030
130 0,7533 0,01314
140 0,7378 0,01650
150 0,7210 0,02070
160 0,7033 0,02577
170 0,6848 0,03165
180 0,6653 0,03883
190 0,6441 0,04751
200 0,6210 0,05797
210 0,5944 0,07128
220 0,5648 0,08905
230 0,5281 0,1131
240 0,4778 0,1499
247 0,4195 0,1996
249 0,3839 0,2288
250,1 0,308
Таблица 3.1.41
Этанол (С2Н5ОН)
Г, °C рж • 10 3, кг/м3 рп • 10 ’3, кг/м3
0 0,80625 3,3-10 5
10 0,7979 6,2-10 5
40 0,7722 0,000315
60 0,7541 0,000790
80 0,7348 0,00174
100 0,7157 0,00351
120 0,6925 0,00658
140 0,6631 0,01152
160 0,6329 0,01914
180 0,5984 0,03115
200 0,5568 0,0508
220 0,4958 0,0854
230 0,4550 0,1135
240' 0,3825 0,1715
241 0,3705 0,1835
242 0,3546 0,1990
242,5 0,3419 0,2164
243 0,276
Рж + р“ = о, 4624 - 5,992 • 10"4 Г - 7,64 • 10 7 Т2 2
Рж + = о, 4624 - 5,992 • 10~4 Г - 7,64 • 10 7 Т2
2
Таблица 3.1.43
Этилен (С2Н4)
Г, °C рж • 10 3. кг/м3 р„ • 10 3, кг/м3
-145,07 0,62465 9,363 • 10’5
-129,00 0,60449 0,00037586
-114,69 0,58380 0,0011127
-103,01 0,56740 0,0021928
-63,41 0,50588 0,012584
-48,15 0,47822 0,020407
-37,30 0,45610 0,029465
-24,33 0,42655 0,041865
-19,20 0,41313 0,051138
-14,18 0,39855 0,059942
-10,93 0,38818 0,067215
-7,70 0,37721 0,076050
5,84 0,30840 0,13266
6,50 0,30342 0,13716
7,98 0,28726 0,15268
114
Новый справочник химика и технолога
Таблица 3.1.44
Средний коэффициент изотермической сжимаемости воды Р7 -1О10, Па-1
Интервал Температура, °C
давлений МПа 0 5 10 15 20 30 40 50 60 70 80 90 100
0,101-2,53 5,18 4,93 4,85
2,53-5,07 5,09 4,86 4,70
0,101-10,1 5,04 4,87 4,77 4,67 4,62 4,54 4,43 4,43 4,49 4,56 4,72
10,1-20,3 4,86 4,69 4,55 4,45 4,36 4,30 4,23 4,19 4,21 4,33 4,62 7,96
20,3-30,4 4,74 4,56 4,47 4,37 4,28 4,16 4,09 4,08 4,10 4,19 4,30 4,53 7,59
30,4-40,5 4,60 4,43 4,35 4,27 4,18 4,08 4,91 4,86 4,90 4,06 4,16 4,40 7,21
40,5-50,7 4,49 4,38 4,24 4,16 4,10 4,01 3,99 3,94 3,89 3,93 4,03 4,28 6,73
50,7-60,8 4,32 4,24 4,13 4,06 3,99 3,87 3,85 3,85 3,83 3,86 3,94 4,11 6,51
60,8-70,9 4,23 4,04 4,00 3,93 3,89 3,82 3,77 3,72 3,78 3,75 3,82 4,02 6,19
70,9-81,1 4,13 4,02 3,93 3,85 3,83 3,7 3,69 3,66 3,64 3,69 3,73 3,84 6,05
81,1-91,2 4,01 3,88 3,84 3,75 3,68 3,63 3,57 3,57 3,58 3,61 3,63 3,77 5,81
91,2-101,3 3,63 3,60 3,55 3,48 3,48 3,55 3,56 3,57 3,66 5,58
Таблица 3.1.45
Средний коэффициент изотермической сжимаемости ртути р7.-10",Па"'
Интервал давлений р} -р2, МПа Температура, °C
22,8 52,8 84,8 ПО 150,3 191,8
0,101-50,7 3,8 3,8 3,9 4,0 4,3 4,5
50,7-101,3 3,8 3,8 3,9 3,9 4,3 4,5
101,3-152.0 3,7 3,8 3,9 3,9 4,3 4,4
152,0-202,7 3,6 3,8 3,8 3,8 4,2 4,3
202,7-253,3 3,5 3,8 3,8 3,8 4,2 4,3
253,3-304,0 3,4 3,8 3,7 3,7 4,1 4,1
Таблица 3.1.46
Средний коэффициент изотермической сжимаемости жидкостей
При наличии в графе «Интервал давлений» одного числа приводится значение истинного коэффициента сжимаемости
Название Формула Интервал давлений Р\~Ръ МПа Температура, °C Р, -1010, Па’1
Простые вещества и неорганические соединения
Бром Вг2 0-10 20 6,27
10-20 20 5,76
20-30 20 5,39
30^10 20 5,14
40-50 20 4,92
Серная кислота H2SO4 0,101-1,62 0 29,9
Углерода диоксид СО2 6,08 13 172
7,09 13 94,7
8,11 13 65,1
9,12 13 43,4
Углерода дисульфид cs2 0,101-0,203 20 8,00
0,101-50,7 0 6,51
50,7-101,3 0 5,23
101,3-152 0 4,24
152-202,7 0 3,65
202,7-253,3 0 3,26
Физические свойства важнейших веществ
115
Продолжение табл. 3.1.46
Название Формула Интервал давлений Р\~Р2, МПа Температура, °C ^•Ю'^Па’1
Фосфора трихлорид РС13 0,101-50,7 10,1 7,11
50,7-101,3 10,1 5,33
101,3-152 10,1 4,44
152-202,7 10,1 3,75
202,7-253,3 10,1 3,26
Хлор С12 1-10 29 11,7
10-20 20 10,9
20-30 20 10,1
30^10 20 8,95
40-50 20 8,34
Органические соединения
Анилин c6h5nh2 8,66 25 4,26
18,4 25 4,00
28,5 25 3,78
395 25 3,56
Ацетон (СНз)2СО 0,101-50,7 0 8,09
50,7-101,3 0 5,82
101,3-152 0 4,64
152-202,7 0 3,95
0,902-3,70 14,2 11,0
0,902-3,70 99,5 27,2
Бензол С6н6 0,0405-1,82 12,9 8,59
0,101-0,405 15,4 8,59
0,203-1,82 34,9 9,87
0,456-1,93 99,9 18,8
10-30 20 7,77
30-50 20 4,05
Бромоформ СНВгз 0-10 20 5,03
10-20 20 4,69
20-30 20 4,34
30-40 20 4,15
40-50 20 4,05
Бромэтан С2Н5Вг 0,101-50,7 10,1 8,88
50,7-101,3 10,1 6,22
101,3-152 10,1 4,93
202,7-253,3 10,1 3,55
0,101-1,87 13,7 11,2
Бутан-1-ол СН3(СН2)2СН2ОН 0,811 17,95 4,26
0,811 17,4 4,00
Бутилбензоат С6Н5СООС4Н9 0,101-0,532 10 3,78
Бутилбутаноат СзН7СООС4Н9 0,101-0,532 10 3,56
Бутилпентаноат С4Н9СООС4Н9 0,101-0,532 10 8,09
Гексан СНз(СН2)4СНз 0-0,101 23 5,82
Гексановая кислота С5НПСООН 2,03^40,5 30 4,64
Гептан СНз(СН2)5СНз 0-0,101 23 3,95
Глицерин СНОН(СН2ОН)2 0,101-1,01 14,8 11,0
Декан СНз(СН2)8СНз 0-0,101 23 27,2
1,2-Дибромэтан С2Н4Вг2 0,101-0,532 10 8,59
0,101-0,532 64 8,59
1,2-Дихлорэтан С2Н4С12 0,101-0,532 10 9,87
0,101-0,532 75 18,8
116
Новый справочник химика и технолога
Продолжение табл. 3.1.46
Название Формула Интервал давлений Pi р2, МПа Температура, °C Р,-1О1о,Па-'
Органические соединения
Диэтиловый эфир (С2н5)2о 101,3 -100,8 7,77
10,1 0 4,05
20,3 0 5,03
50,7 0 4,69
101,3 0 4,34
0,101-0,811 8,1 4,15
0,0405-1,77 12,2 4,05
0,854-2,57 13,5 8,88
0,203-1,93 34,8 6,22
0,101-202,7 35 4,93
0,871-3,48 63 3,55
0,871-3,48 78,5 11,2
0,871-3,70 99 4,26
10,1-20,3 185 4,00
10,1^10,5 185 3,78
Изопропилбензол (кумол) С6Н5СН(СНз)2 10-30 20 3,56
30-50 20 8,09
2-Изопропил-5-метил- С10Н14О 2,03-10,1 64 5,82
фенол (тимол) 2,03-40,5 64 4,64
2,03-40,5 100 3,95
2,03-40,5 310 11,0
Иодэтан С2Н51 0,101-50,7 10,6 27,2
50,7-101,3 10,6 8,59
101,3-152 10,6 8,59
152-202,7 10,6 9,87
202,7-253,3 10,6 18,8
Метанол СН3ОН 0,101-50,7 0 7,77
50,7-101,3 0 4,05
101,3-152 0 5,03
152-202,7 0 4,69
202,7-253,3 0 4,34
0,861-3,76 14,7 4,15
0,882-3,78 100 4,05
Мети л ацетат СН3СООСН3 0,821-3,80 14,3 8,88
Метилбутаноат C3II7COOCII3 0,101-0,532 10 6,22
Метилпентаноат С4Н9СООСН3 0,101-0,532 10 4,93
Нитробензол c6h5no2 8,76 25 3,55
19,5 25 11,2
30,7 25 4,26
42,5 25 4,00
Октан СНз(СН2)6СНз 0-0,101 23 3,78
Пальмитиновая кислота С15Н3!СООН 2,03-101,3 65 3,56
2,03-30,4 185 8,09
2,03—40,5 310 5,82
Парафин (ТПЛ = 55 °C) 20-10,1 64 4,64
2,03^40,5 100 3,95
2,03-40,5 185 11,0
2,03^40,5 310 27,2
Пентан СН3(СН2)зСНз 0,101-2,94 0 8,59
0,101-2,94 20 8,59
0 0 9,87
Физические свойства важнейших веществ
117
Продолжение табл. 3.1.46
Название Формула Интервал давлений р} -р2, МПа Температура, °C Р, -10'°, Па 1
Пентан 49,0 0 18,8
98,0 0 7,77
Пентан-1-ол С4Н9СН2ОН 0,811 17,7 4,05
0,861-3,76 13,8 5,03
Пропан-1 -ол С2Н5СН2ОН 0,101-50,7 0 4,69
50,7-101,3 0 4,34
101,3-152 0 4,15
253,3-304 0 4,05
Пропан-2-ол (СН3)2СНОН 0,811 5,6 8,88
0,811 17,85 6,22
Проп-2-ен-1 -ол СН2СНСН2()Н 0,101-50,7 9,6 4,93
50,7-101,3 9,6 3,55
101,3-152 9,6 11,2
152-202,7 9,6 4,26
Пропилбензол с6н5с3н7 10-30 20 4,00
30-50 20 3,78
Тетрахлорметан СС14 0,101-0,532 10 3,56
0-10 20 8,09
10-20 20 5,82
20-30 20 4,64
30-40 20 3,95
40-50 20 11,0
55,0 20 27,2
67,3 20 8,59
я-Толуидин ch3c6h4nh2 0,101-15,2 45 8,59
2,03-10,1 28 9,87
2,03-40,5 100 18,8
2,03-40,5 185 7,77
2,03-40,5 310 4,05
Толуол с6н6сн3 0,101-0,532 10 5,03
0,101-0,532 66 4,69
0,101-0,203 20 4,34
11,6 25 4,15
23,4 25 4,05
36,0 25 8,88
1,2,4-Триметилбензол С6Н3(СН3)3 10-30 20 6,22
(псевдокумол) 30-50 20 4,93
1,3,5-Триметилбензол С6Н3(СН3)3 10-30 20 3,55
(мезитилен) 30-50 20 11,2
Уксусная кислота СН3СООН 9,37 25 4,26
22,1 25 4,00
50 25 3,78
У-Фениланилин (C6H5)2NH 0-50,7 65 3,56
0-30,4 100 8,09
0-10,1 185 5,82
Фторбензол c6h5f 0,101-1,87 13,9 4,64
Хлорбензол С6Н5С1 0,0405-1,82 13,3 3,95
0,0405-1,82 35 11,0
0,101-0,203 80 27,2
0,0405-1,82 100 8,59
118
Новый справочник химика и технолога
Окончание табл. 3.1.46
Название Формула Интервал давлений Р\ -~ Ръ МПа Температура, °C р, • 10'°, Па 1
Органические соединения
Хлороформ СНС13 0,101-0,203 0 8,59
0-10 20 9,87
10-20 20 18,8
20-30 20 7,77
30-40 20 4,05
40-50 20 5,03
0,101-0,203 60 4,69
0,811-0,912 100 4,34
1,93-3,45 100 4,15
Хлорэтан С2Н5С1 0,101-50,7 0 4,05
50,7-101,3 0 8,88
101,3-152 0 6,22
202,7-253,3 0 4,93
0,882-3,77 15,2 3,55
1,29-3,49 99 11,2
Этанол СН3СН2ОН 0,101-5,07 0 4,26
10,1-20,3 0 4,00
30,4-40,5 0 3,78
50,7-60,8 0 3,56
60,8-70,9 0 8,09
91,2-101,3 0 5,82
0,101-5,07 20 4,64
5,07-10,1 20 3,95
10,1-20,3 20 11,0
20,3-30,4 20 27,2
30,4-40,5 20 8,59
40,5-50,7 20 8,59
50,7-60,8 20 9,87
15,2-40,5 28 18,8
0,101-5,07 40 7,77
15,2-40,5 65 4,05
15,2-40,5 100 5,03
15,2-40,5 185 4,69
15,2-40,5 310 4,34
Этилацетат СН3СООС2Н5 0,823-3,79 13,3 4,15
0,824-3,76 99,6 4,05
Таблица 3.1.47
Плотность и сжимаемость промышленных газов и паров при О °C и 101,3 кПа
Название Формула Плотность по воздуху Плотность, г/л Коэффициент адиабатической сжимаемости Рая' Ю9, Па’1
Простые вещества и неорганические соединения
Азот n2 0,96724 1,25055 -4,50
Азот атмосферный (с примесью аргона) n2 0,9721 1,2568 -4,50
Азота(1) оксид n2o 1,5297 1,9778 -71,3
Азота(П) оксид NO 1,0366 1,3402 -11,3
Аммиак NH3 0,5969 0,7710 -152
Аргон Ar 1,3796 1,7837 -9,76
Арсан (арсин) AsH3 2,695 3,484* -13,5
Бора трифторид BF3 2,37* 2,99*
Физические свойства важнейших веществ
119
Продолжение табл. 3.1.47
Название Формула Плотность по воздуху Плотность, г/л Коэффициент адиабатической сжимаемости Рад’ Ю9, Па 1
Вода (пар) Н2О 0,5941 0,768 -345
Водород Н2 0,06952 0,08988 6,01
Водорода бромид НВг 2,8189 3,6445 -из
Водорода иодид HI 4,4776 5,7891 -180
Водорода селенид H2Se 2,839 3,670
Водорода сульфид H2S 1,190 1,539 -103
(сероводород)
Водорода телланид Н2Те 4,49 5,81
Водорода хлорид НС1 1,2679 1,6391 -73,6
Воздух сухой ** 1,0000 1,2929 -6,01
Вольфрама гекса- WF6 9,98 12,9
фторид
Гелий He 0,13804 0,17847 5,26
Герман GeH4 2,645 3,420
Дигерман Ge2H6 5,2120* 6,74*
Диметилсилан SiH2(CH3)2 2,H 2,73
Дисилан Si2H6 2,204 2,85
Карбонилсульфид COS 2,10 2,72 -15
Кислород O2 1,1053 1,42895
Криптон Kr 2,868 3,708
Ксенон Xe 4,525 5,851 -68,3
Метилдихлорсилан SiHCl2CH3 4,1 5,3
Мети л си л ан SiH3CH3 1,61 2,08
Метилхлорсилан SiH2CICH3 2,82 3,64
Неон Ne 0,69638 0,90035 4,51
Нитрозилфторид NOF 1,683 2,176*
Нитрозилхлорид NOCI 2,314 2,992 -300
Озон o3 1,658 2,144 -451
Радон Rn 7,526 9,73
Серы гексафторид SF6 5,03* 6,50*
Серы диоксид so2 2,2638 2,9269 -15
Силан SiH4 1,114 1,44
Сульфурилдифторид SO2F2 2,88* 3,72*
Тетрафторсилан SiF4 3,623 4,684
Трифторсилан SiHF3 2 99 3,86
Углерода диоксид CO2 1,5290 1,9769 -69,1
Углерода монооксид CO 0,9671 1,2504 -4,51
Фосфан (фосфин) PH3 1,1899 1,5294 -95,4
Фосфора пентафто- pf5 4,494 5,81
рид
Фосфора трифторид PF3 3,022 3,907*
Фосфорил трифторид POF3 3,7 4,8
Фтор f2 1,312 1,696
Хлор ci2 2,486 3,214 4,3
Хлорсилан SiH3Cl 2,34 3,03
Органические соединения
Ацетилен C2H2 0,9073 1,1709 -88,6
Бутан CH3(CH2)2CH3 2,091 2,703 -406
Бутан-1-ол C3H7CH2OH 2,510 3,244 -691
Гептан CH3(CH2)5CH3 3,450 4,459 -901
Диметиловый эфир (CH3)2O 1,6 2,1098
120
Новый справочник химика и технолога
Окончание табл. 3.1.47
Название Формула Плотность по воздуху Плотность, г/л Коэффициент адиабатической сжимаемости Рад • Ю9, Па’1
Органические соединения
Дифтордихлорметан CC12F2 4,262 5,510 -267
(фреон-12)
Изобутан СН3СН(СН3)2 2,067 2,673 -282
Метан сн4 0,5545 0,7168 -21,8
Метанамин (метил- ch3nh2 1,080* 1,396
амин)
Метанол СН3ОН 1,103 1,426 -901
TV-Мети л метан амин (CH3)2NH 1,521 1,966
(диметиламин)
Октан СН3(СН2)6СН3 3,890 5,030 -766
Пентан СН3(СН2)3СН3 2,674 3,457 -1818
Пропан СН3СН2СН3 1,554 2,0096 -234
Пропен СН3СН=СН2 1,481 1,915 -198
Фторметан CH3F 1,1951 1,5452 -218
Хлорметан СН3С1 1,7848 2,3076 -243
Хлороформ СНС13 4,087 5,283 -751
Этан С2н6 1,049 1,356 -116
Этанамин (этиламин) c2h5nh2 0,706 2,0141
Этанол СН3СН2ОН 1,580 2,043 -856
Этилен С2Н4 0,9749 1,2604 -78,9
* При 20 °C.
** Объемные доли газообразных компонентов сухого атмосферного воздуха, %: N2 — 78,03; О2 — 20,99; Аг — 0,933; СО2 — 0,030; Н2 — 0,01; Ne — 0,0018; Не — 0,0005; Кг — 0,0001; Хе — 9 • 10”6.
Массовые доли газообразных компонентов сухого атмосферного воздуха, %: N2 — 75,47; О2 — 23,20; Аг — 1,28; СО2 — 0,046; Н2 — 0,001; Ne — 0.0018; Не — 7 • 10’5; Кг — 0,0003; Хе — 7 • I О-5.
3.2. Термическое расширение твердых тел, жидкостей и газов
Относительное изменение длины твердых тел и объема твердых, жидких и газообразных тел при повышении температуры на АТ характеризуется, с одной стороны, средним коэффициентом линейного расширения:
_ 1 А/ 1 1-L а =-----=------—,
/о АТ /0Т-Т0
с другой — средним коэффициентом объемного расширения:
1 АТ 1 Т-К
а =------=-------
V AT V Т-Т г о г О 1 1 0
Здесь /0 и Ио — длина и объем тела при температуре То, / и V-— те же величины при температуре Т.
Предельные значения ос и ос' при АТ—>0 называются истинным коэффициентом линейного расширения:
1 dl ат =----
/ dT
и истинным коэффициентом объемного расширения:
В табл. 3.2.1 приведены значения а2о для металлов и сплавов и коэффициенты уравнения 1Т = /0(1 + аТ + ЬТ2), где /0 — длина образца при 0 °C. Интервал температур, в котором применимо это уравнение, указан в третьей графе. В табл. 3.2.2 представлены средние коэффициенты линейного расширения некоторых материалов, в табл. 3.2.3 — данные по объемному термическому расширению неорганических и органических жидкостей, далее — произведение pv, отнесенное к р¥ при нормальных условиях: для газов — в табл. 3.2.4-3.2.18, для простых веществ и неорганических соединений — в табл. 3.2.19-3.2.22, для органических соединений — в табл. 3.2.23-3.2.26.
Размерность коэффициентов линейного и объемного расширения: К-1, °C”1.
Таблица 3.2.1
Линейное расширение металлов и сплавов
Металл или сплав а20- Ю6, (°C)-1 у; °с а - 105, (°C)-1 b 108, (°C)2
Алюминий Бронза 22,4 20-600 2,19 1,2
81,2 % Си + + 8,6 % Zn + + 9,9 % Sn 17,74 0-80 1,7552 0,469
96,0 % Си + + 2,6 % Zn + + 0,6 % Мп 16,92 16-100 1,678 0,36
Физические свойства важнейших веществ
121
Окончание табл. 3.2.1
Металл или сплав Й20 ’ 106, (осу! Г, °C а - 105, (°C)-1 Ь- 108. (°C)-2
Железо литое 11,79 0-750 1,1575 0,530
Золото 14,26 0-520 1,416 0,215
Кадмий 28,79 8-95 2,693 4,66
Латунь:
73,7 % Си + 18,12 0-80 1,7939 0,456
+ 24,2 % Zn +
+ 1,5 Sn
56,4 % Си + 19,31 16-100 1,910 0,52
+ 43,4 Zn
Магний 25,44 20-500 2,507 0,936
Медь 16,23 0-625 1,6070 0,403
Молибден 5,15 20-400 0,510 0,124
Никель 12,62 20-300 1,236 0,660
Олово 21,38 8-95 2,033 2,63
Платина 9,11 (-183)- 0,8911 0,491
16
Серебро 19,51 20-500 1,939 0,295
Свинец 27,56 14-94 2,726 0,74
Сталь литая 11,39 0-750 1,1181 0,526
Сурьма 9,76 11-98 0,923 1,32
Хром 8,24 20-500 0,811 0,323
Цинк 28,35 9-96 2,741 2,34
Чугун 10,02 0-625 0,9794 0,566
Таблица 3.2.2
Средний коэффициент линейного расширения некоторых материалов
При наличии в графе «Г, °C» одного числа приводится значение истинного коэффициента линейного расширения.
Материал Г, °C а • 106, (°C)-1
Алмаз 40 1,18
Алунд (искусственный 25-900 8,7
корунд)
Бакелит 20-60 22
Окончание табл. 3.2.2
Материал Г, °C а • 106, (°C)-’
Боксит 25-100 4,4
Воск белый 10-26 230
Графит 40 7,86
Известняк 25-100 9
Изумруд
|| оси 0-85 -1,35
± оси 0-85 1,00
Каменная соль 40 40,4
Карборунд 25-100 6,58
100-900 4,74
Каучук 16,7-25,3 77,0
Кварц
|| оси (—190)—16 5,21
0-80 7,97
-L оси 0-80 13,37
Лед (-20)-! 51
Парафин 0-16 106,62
0-38 130,30
38-49 477,07
Песчаник 20 7,12
Резина вулканизированная 0-18 63,60
Стекло
кварцевое (—191)—16 -0,26
16-500 0,57
16-1000 0,58
Уголь газовый (реторт- 40 5,40
ный)
Фарфор 0 2,5
20-790 4,13
1000-1400 5,53
Шпат
исландский
|| оси 0-80 26,31
± оси 0-80 5,44
плавиковый 0-100 19,50
Эбонит 25,3-35,4 84,2
Таблица 3.2.3
Объемное расширение жидкостей
В таблице приводятся значения а'2о и коэффициенты уравнения VT = Го(1 + аТ + ЬТ2 + cTJ), где Го — объем жидкости при О °C. Интервал температур, в котором применимо это уравнение, указан в четвертой графе.
Название Формула a'2O- 103, (°C)-1 T, °C a- Ю3, (°C)-1 b- 106, (°C)“2 с - 108, (°C)"1
Простые вещества и неорганические соединения
Бром Вг2 1,113 (-7H0 1,03819 1,711138 0,5447
Вода Н2О 0,207 0-33 -0,06427 8,5053 -6,7900
Мышьяка трихлорид AsC13 1,020 (-15)-130 0,97907 0,96695 0,17772
Ртуть Hg 0,13186 0-100 0,18169041 0,002951266 0,0114562
Серная кислота H2SO4 0-30 0,5758 -0,432
Тетрахлорсилан SiCl4 1,430 (-32)-59 1,29412 2,18414 4,08642
Т етрахлорстаннан SnCl4 1,178 (-19)-113 1,1328 0,91171 0,75798
Углерода дисульфид (сероуглерод) CS2 1,218 (-34)-60 1,13980 1,37065 1,91225
122
Новый справочник химика и технолога
Продолжение табл. 3.2.3
Название Формула а'2О • К)3, (°C)’1 Г, °C а- 103,(оСГ' b- 106. (°C)’2 с - 108, (°C)'1
Простые вещества и неорганические соединения
Фосфора трибромид РВг3 0,868 0-100 0,8472 0,43672 0,25276
Фосфора трихлорид РС13 1,154 (—36)—75 1,12862 0,87288 1,79236
Фосфорилтрихлорид РОС13 1,116 0-107 1,06431 1,12666 0,5299
Органические соединения
Анилин c6h5nh2 0,858 0-141 0,82349 0,43672 0,24276
Ацетон (СНз)2СО 1,487 0-54 1,3240 3,8090 -1,87983
Ацетонитрил CH3CN 1,301 6-66 1,2118 1,7780 1,5322
Бензоилхлорид С6Н5СОС1 0,880 12-^46 0,85893 0,44219 0,27139
Бензол с6н6 1,237 11-81 1,17626 1,27775 0,80648
Бромметан СНзВг 1,684 (—35)—28 1,41521 3,31528 1 1,3809
1 -Бромпентан С5НиВг 1,102 0-80 1,02321 1,90086 0,19756
З-Бромпропен СН2=СНСН2Вг 1,241 0-69 1,2275 -0.44365 2,5843
Бромэтан С2Н5Вг 1,418 (—32)—54 1,33763 1,50135 1,6900
Бутан-1-ол с3н7сн2он 0,950 6-108 0,83751 2,8634 -0,12415
Бутан-2-он СН3СОС2Н5 1,315 0-76 1,18654 3,37043 -0,53365
Гекса-1,5-диен (СН2=СНСН2)2 1,375 0-60 1,3423 -0,34339 3,8693
Гексановая кислота С5НИСООН 0,975 15-155 0,94413 0,68358 0,26586
Глицерин СНОН(СН2ОН)2 0,505 0,4853 0,3895
Диаллиловый эфир (СН2=СНСН2)2О 1,346 0-88 1,2519 2,2401 0,35775
Диизопропиловый эфир [(СНз)2СН]2О 1,452 0-67 1,2872 4,2923 -0,58573
Диметилсульфид (CH3)2s 1,082 0-111 1,01705 1,57606 0,19072
Дипропиловый эфир (СзН7)2О 1,354 0-88 1,2132 3,9318 1,3644
1,2-Дихлорэтан С2Н4С12 1,161 (-28)-84 1,11893 1,0469 0,10342
Диэтиловый эфир (С2Н5)2О 1,656 (—15)—38 1,51324 2,35918 4,00512
Диэтилоксалат (СООС2Н5)2 1,136 0-141 1,06031 1,0983 2,6657
Диэтил сульф ид (C2H5)2S 1,278 0-90 1,19643 1,80653 0,78821
Изомасляная кислота С3Н7СООН 1,068 16-118 0,97625 2,3976 -0,32145
Изопрен с5н8 1,567 0-33 1,4603 0,99793 5,60149
Иодметан СПз! 1,273 5-39 1,1440 4,0465 -2,7393
1 -Иодпентан С5Нн1 0,986 20-142 0,92658 1,4647 0,0596
1 -Иодпропан СзН71 1,102 10-98 1,0276 1,8658 -0,0051
З-Иодпропен СН2СНСН21 1,091 0-101 1,0539 0,63572 1,0036
Иодэтан с2н51 1,179 10-65 1,1520 0,26032 1,4181
Керосин (б/отн = 0,8467) 0,955 24-120 0,8994 1,396
лт-Крезол сн3с6н4он 65-194 0,77526 0,27102 0,3868
о-Крезол СН3С6Н4ОН 66-186 0,71072 1,1464 0,2242
«-Крезол СН3С6Н4ОН 66-186 0,86476 0,53912 0,64418
Масляная кислота С3Н7СООН 1,063 0-100 1,02573 0,83760 0,34694
Метанол СНзОН 1,259 (—38)—70 1,18557 1,56493 0,91113
Метилацетат СН3СООСН3 1,427 0-58 1,34982 0,87098 3,5562
2-Метилбутан (СНз)2СНС2Н5 1,680 0-27 1,46834 5,09626 0,6979
2-Метилпетан (СНз)2СНСзН7 1,445 0-55 1,37022 0,97649 2,9819
Метилпропионат С2Н5СООСНз 1,304 0-74 1,3049 -1,3275 4,6943
Метилформиат НСООСНз 1,563 0-10 0,35824 10,538 -1,8085
Муравьиная кислота нсоон 1,025 5-104 0,99269 0,62514 0,5965
Нитробензол c6h5no2 144-164 0,8263 0,52249 0,13779
Олеиновая кислота С17Н33СООН 0,721 0,68215 1,14053 -0,593
Пентан СНз(СН2)зСНз 1,656 (—190)—30 1,50697 3,435 0,975
Пентан-1-ол С4Н9СН2ОН 0,902 (-15)-80 0,9001 0,6573 1,18458
Пентан-З-он (С2Н5)2СО 1,233 0-95 1,15342 1,88396 0,32021
Пентилацетат СНзСООСзНц 1,162 0-124 1,1501 -0,09046 1,3015
Пентилбензоат С6Н5СООС5НИ 0,848 0-198 0,81711 0,7377 0,10593
Физические свойства важнейших веществ
123
Окончание табл. 3.2.3
Название Формула а 20 • Ю3, (°C) 1 Т, °C а - 103, (°C)’1 Ь- 10ь, (°C)’2 с • 108, (°C)’1
Петролейный эфир 2,26 (—190)—0 1,46 1,60
Пропан-1 -ол С2Н5СН2ОН 0,956 0-94 0,7743 4,9689 -1,4069
Пропан-2-ол (СН3)2СНОН 1,094 0-83 1,04345 0,44303 2,7274
Проп-2-ен-1-ол СН2=СНСН2ОН 1,049 0-94 0,97019 1,8725 0,36452
Пропионовая кислота С2Н5СООН 1,102 0-133 1,0396 1,5487 0,04301
Т етрахлорметан СС14 1,236 0-76 1,18384 0,89881 1,35135
Трихлорацетальдсгид СС13СНО 0,934 13-51 0,9545 -2,2139 5,6392
Уксусная кислота CH3COOH 1,071 16-107 1,063 -0,12636 1,0876
Фенол С6Н5ОН 36-157 0,8340 0,10732 0,4446
Хлороформ СНС13 1,273 0-63 1,10715 4,66473 -1,74328
1 -Хлорпентан С5НИС1 1,208 0-100 1,17155 0,50077 1,35368
1 -Хлорпропан С3Н7С1 1,447 0-42 1,3306 3,8313 -1,3859
2-Хлорпропан (СН3)2СНС1 1,591 0-34 1,3696 5,5287
З-Хлорпропен СН2С11СН2С1 1,475 9-44 1,3218 5,078 -4,1915
Хлорэтан С2Н5С1 1,706 (-32)-26 1,57458 2,81366 1,56987
Этанол СН3СН2ОН 0-39 0,7450 1,85 0,730
Этилацетат СН3СООС2Н5 1,389 (—36>—72 1,2585 2,95688 0,14922
Этилбензоат С6Н5СООС2Н5 0,900 0-159 0,86606 0,8229 0,12084
Этилбензол с6н5с2н5 0,961 24-131 0,86172 2,5344 -0,18319
Этиленгликоль НОСН2СН2ОН 0,6375 11-55 0,5657 1,7074 0,293
Этилнитрат C2H5ONO2 1,299 9-72 1.1290 4,7915 -1,8413
Этилформиат НСООС2Н5 1,417 0-63 0,36446 0,13538 3,9248
Указатель таблиц по произведениюpVдля газов, отнесенное KpV при нормальных условиях (О °C, 101,3 кПа)
Химическое соединение № табл. Химическое соединение № табл.
Аг 3.2.6 Кг 3.2.11
СО 3.2.13 n2 3.2.4
со2 3.2.9 NH3 3.2.5
СН4 3.2.16 NO 3.2.15
С2Н4 3.2.18 Ne 3.2.14
с2н6 3.2.17 о2 3.2.10
н2 3.2.7 Хе 3.2.12
Не 3.2.8
Простые вещества и неорганические соединения
Таблица 3.2.4
Азот (N2)
р, МПа Температура, °C
-130 -100 -50 0 50 100 150 200 300 400
0 0,101 1,01 2,03 4,05 6,08 8,11 10,1 20,3 40,5 60,8 81,1 101,3 0,5243 0,5208 0,4873 0,4466 0,3487 0,2482 Го^6342 0,6319 0,6109 0,5879 0,5406 0,4970 0,4631 0,4471 0,8173 0,8162 0,8059 0,7951 0,7767 0,7596 0,7476 0,7407 0,785 1,033 1,316 1,593 1,857 1,0005 1,0000 0,9961 0,9924 0,9840 0,9840 0,9838 0,9856 1,036 1,257 1,525 1,799 2,068 1,1836 1,1836 1,1837 1,1842 1,1866 1,1908 1,1967 1,2044 1,2692 1,483 1,741 2,009 2,276 1,3667 1,3670 1,3698 1,3732 1,3810 1,3901 1,4005 1,4123 1,490 1,704 1,957 2,221 2,486 1,5499 1,5503 1,5551 1,5606 1,5724 1,5851 1,5989 1,6136 1,700 1,920 2,171 2,432 2,696 1,7330 1,7336 1,7398 1,7470 1,7618 1,7773 1,7935 1,8105 1,912 2,146 2,396 2,656 2,921 2,0993 2,1000 2,1084 2,1177 2,1367 2,1560 2,1756 2,1956 2,313 2,551 2,804 3,062 3,317 2,4655 2,4664 2,4759 2,4865 2,5080 2,5300 2,5523 2,5748 2,697 2,945 3,198 3,459 3,722
124
Новый справочник химика и технолога
Таблица 3.2.5
Аммиак (NH3)
р, МПа Температура. °C
100 150 200 250 300
0 1,3886 1,5747 1,7608 1,9468 2,1329
0,101 1,3805 1,5679 1,7546 1,9420 2,1276
1,01 1,323 1,527 1,725 1,919 2,110
2,03 1,254 1,481 1,691 1,892 2,091
3,04 1,179 1,433 1,657 1,869 2,071
4,05 1,005 1,383 1,622 1,843 2,071
5,07 0,997 1,329 1,587 1,819 2,034
6,08 1,274 1,551 1,793 2,016
7,09 1,215 1,514 1,768 1,997
8,11 1,477 1,742 1,978
9,12 1,438 1,716 1,960
10,1 1,690 1,942
Таблица 3.2.6
Аргон (Аг)
р. МПа Температура, °C
-100 -50 0 50 100 200 300 400
0 0,6345 0,8178 1,0010 1,1842 1,4674 1,7339 2,1003 2,4668
0,101 0,6316 0,8161 1,0000 1,1837 1,3673 1,7341 2,1008 2,4675
1,01 0,6048 0,8010 0,9914 1,1795 1,3658 1,7361 2,1054 2,4736
2,03 0,5730 0,7843 0,9823 1,1651 1,3644 1,7385 2,1105 2,4804
4,05 0,5029 0,7518 0,9653 1,1673 1,3625 1,7440 2,1211 2,4941
6,08 0,4237 0,7206 0,9503 1,1611 1,3619 1,7504 2,1321 2,5078
8,11 0,3340 0,6919 0,9372 1,1563 1,3625 1,7517 2,1434 2,5214
10,1 0,6669 0,9262 1,1529 1,3648 1,7659 2,1550 2,5351
15,2 1,3741
20,3 1,3915
Таблица 3.2.7
Водород (Н2)
р, МПа Температура, °C
-207,9 -183 -150 -100
0 0,2388 0,3299 0,4506 0,6335
0,101 0,2379 0,3296 0,4507 0,6339
1,01 0,2308 0,3278 0,4521 0,6377
2,03 0,2238 0,3264 0,4540 0,6420
4,05 0,2134 0,3261 0,4591 0,6513
6,08 0,2126 0,3288 0,4657 0,6612
8,11 0,2186 0,3345 0,4739 0,6719
10,1 0,2300 0,3433 0,4838 0,6833
р, МПа Температура, °C
-50 0 50 100 200 300 400
0 0,8164 0,9994 1,1823 1,3652 1,7311 2,097 2,463
0,101 0,8170 1,0000 1,1830 1,3659 1,7318 2,097 2,463
1,01 0,8219 1,0056 1,1891 1,3721 1,7381 2,104 2,468
2,03 0,8274 1,0119 1,1959 1,3791 1,7451 2,111 2,473
4,05 0,8388 1,0247 1,2094 1,3930 1,7591 2,126 2,484
6,08 0,8506 1,0376 1,2229 1,4069 1,7731 2,141 2,495
Физические свойства важнейших веществ
125
Окончание табл. 3.2.7
р, МПа Температура, °C
-50 0 50 100 200 300 400
8,11 0,8628 1,0508 1,2364 1,4210 1,7872 2,156 2,505
10,1 0,8754 1,0641 1,2500 1,4352 1,8012 2,171 2,516
20,3 0,941 1,133 1,320 1,507 1,885 2,251 2,608
40,5 1,083 1,276 1,464 1,651 2,034 2,398 2,765
60,8 1,230 1,422 1,608 1,796 2,177 2,540
81,1 1,376 1,567 1,751 1,938 2,320 2,677
101,3 1,519 1,709 1,892 2,078 2,461 2,813
Таблица 3.2.8
Гелий (Не)
р, МПа Температура, °C
-252,8 -208 -183 -150 -100 -50
0 0,0745 0,2384 0,3299 0,4506 0,6336 0,8165
0,101 0,0745 0,2389 0,3305 0,4512 0,6342 0,8171
1,01 0,0744 0,2428 0,3348 0,4558 0,6390 0,8219
5,07 0,0891 0,2621 0,3547 0,4768 0,6606 0,8434
10,1 0,1206 0,2880 0,3816 0,5042 0,6884 0,8707
р, МПа Температура, °C
0 50 100 200 300 400
0 0,9995 1,1824 1,3654 1,7313 2,0972 2,4631
0,101 1,0000 1,1829 1,3658 1,7317 2,0975 2,4633
1,01 1,0047 1,1876 1,3704 1,7361 2,1017 2,4673
5,07 1,0257 1,2086 1,3907 1,7559 2,1204 2,4855
10,1 1,0519 1,2348 1,4161 1,7805 2,1439 2,5081
р, МПа Температура, °C
-70 -35 0 50 100 200
20,3 0,8490 0,9759 1,1036 1,2859 1,4660 1,8283
40,5 0,9491 1,0769 1,2026 1,3848 1,5635 1,9179
60,8 1,0481 1,1744 1,3003 1,4768 1,6553 2,0152
81,1 1,1417 1,2682 1,3924 1,5706 1,7481 2,0983
101,3 1,4838 1,6602 1,8359 2,1889
Таблица 3.2.9
Диоксид углерода (СО2)
р, МПа Температура, °C
0 10 20 30 40 50
0 1,0068 1,0437 1,0805 1,1174 1,1543 1,1911
5,07 0,105 0,115 0,680 0,775 0,850 0,920
7,60 0,153 0,163 0,180 0,219 0,620 0,747
10,1 0,202 0,213 0,229 0,255 0,309 0,491
15,2 0,295 0,309 0,326 0,346 0,377 0,419
20,3 0,385 0,401 0,419 0,440 0,468 0,500
30,4 0,560 0,578 0,599 0,623 0,649 0,677
40,5 0,728 0,748 0,771 0,795 0,823 0,852
50,7 0,991 0,913 0,938 0,963 0,990 1,021
60,8 1,050 1,073 1,100 1,128 1,157 1,187
70,9 1,206 1,232 1,259 1,289 1,319 1,350
81,1 1,358 1,387 1,417 1,448 1,479 1,510
91,2 1,509 1,539 1,569 1,633 1,633 1,665
101,3 1,656 1,685 1,716 1,780 1,780 1,814
126
Новый справочник химика и технолога
Окончание табл. 3.2.9
р, МПа Температура, °C
60 80 100 137 198 258
0 1,2280 1,3017 1,3754 1,5118 1,7366 1,9578
5,07 0,984 1,096 1,206 1,380 1,633 1,893
7,60 0,841 0,988 1,118 1,318 1,615 1,867
10,1 0,661 0,873 1,030 1,259 1,582 1,847
15,2 0,485 0,681 0,878 1,158 1,530 1,818
20,3 0,543 0,660 0,815 1,096 1,496 1,804
30,4 0,710 0,790 0,890 1,108 1,494 1,820
40,5 0,884 0,956 1,039 1,218 1,563 1,883
50,7 1,054 1,124 1,200 1,362 1,678
60,8 1,219 1,290 1,366 1,518 1,812
70,9 1,383 1,454 1,528 1,676 1,956
81,1 1,544 1,614 1,689 1,836 2,108
91,2 1,700 1,771 1,846 1,994 2,260
101,3 1,848 1,921 1,999
Таблица 3.2.10
Кислород (О2)
р. МПа Температура, °C
0 50 100
0 1,0010 1,1842 1,3674
0,101 1,0000 1,1837 1,3672
1,01 0,991 1,180 1,366
2,03 0,982 1,175 1,365
4,05 0,965 1,167 1,363
6,08 0,949 1,161 1,363
8,11 0,936 1,156 1,363
10,1 0,923 1,152 1,365
Окончание табл. 3.2.10
р. МПа Температура, °C
0 15,6
121,6 1,9620 2,0268
141,9 2,1798 2,2470
162,1 2,3960 2,4640
182,4 2,6073 2,6793
202,7 2,8160 2,8880
222,9 3,0217 3,0932
243,2 3,2244 3,2976
263,4 3,4229 3,4996
283,7 3,6176 3,6946
304,0 3,8880
р, МПа Температура, °C
0 100 200
20,3 0,91 1,40 1,82
30,4 0,96 1,45 1,89
40,5 1,05 1,53 1,96
50,7 1,16 1,62 2,05
60,8 1,27 1,72 2,14
70,9 1,39 1,83 2,24
81,1 1,50 1,93 2,34
101,3 1,74 2,15
р. МПа Температура, °C
15,6 199,50
10,1 1,0045
20,3 0,9945 1,8190
30,4 1,0420 1,8850
40,5 1,1250 1,9610
50,7 1,2270 2,0500
60,8 1,3370 2,1420
70,9 1,4515 2,2415
81,1 1,5660 2,3430
101,3 1,7980
Таблица 3.2.11
Криптон (Кг)
р, МПа Т= = 11,2 °C р, МПа Т = = 11,2 °C р, МПа Т= = 237,3 °C
2,63 1,012 5,44 0,937 5,16 1,882
2,83 1,008 5,86 0,918 5,55 1,880
3,07 1,000 6,39 0,901 6,01 1,874
3,36 0,993 7,04 0,884 6,60 1,868
3,71 0,980 7,31 0,863 7,21 1,862
4,14 0,968 8,85 0,841 8,03 1,859
4,69 0,953 10,3 0,821 9,07 1,856
5,02 0,940 10,5 1,877
Таблица 3.2.12
Ксенон (Хе)
р, МПа Т= = 11,2 °C р, МПа Т = = 11,2 °C р, МПа 7= = 237,3 °C
2,60 0,697 3,69 0,628 5,42 1,397
2,70 0,691 3,89 0,612 5,87 1,389
2,80 0,685 4,12 0,598 6,40 1,377
2,92 0,677 4,38 0,576 7,05 1,375
Физические свойства важнейших веществ
127
Окончание табл. 3.2.12
р, МПа Т= = 11,2 °C р, МПа Т = = 11,2 °C р, МПа Т= = 237,3 °C
3,05 0,670 4,68 0,552 7,86 1,359
3,18 0,659 5,00 0,522 8,93 1,354
3,34 0,650 5,39 0,437 10,4 1,357
3,50 0,640
Таблица 3.2.13
Монооксид углерода (СО)
Окончание табл. 3.2.14
Р, МПа Температура, °C
0 50 100 200 300 400
0 0,9995 1,1825 1,3654 1,7313 2,0973 2,4632
0,101 1,0000 1,1830 1,3659 1,7318 2,0977 2,4636
1,01 1,0044 1,1879 1,3710 1,7371 2,1033 2,4691
5,07 1,024 1,209 1,394 1,761 2,128 2,494
10,1 1,050 1,236 1,422 1,791 2,158 2,524
15,2 1,077 1,264 1,452
20,3 1,105 1,293 1,481
р, МПа Температура, °C
-70 -50 -25
0 0,744 0,817 0,909
0,101 0,743 0,816 0,908
2,53 0,703 0,790 0,894
5,07 0,664 0,762 0,877
7,60 0,632 0,739 0,863
10,1 0,615 0,726 0,859
15,2 0,619 0,730 0,866
20,3 0,663 0,766 0,902
30,4 0,796 0,887 1,009
40,5 0,943 1,028 1,140
60,8 1,239 1,322 1,428
81,10 1,524 1,610 1,715
101,3 1,799 1,887 1,994
Таблица 3.2.15
Оксид азота(П) (NO)
Р, МПа Температура, °C
0 25 50 100 150 200
0 0,0007 1,092 1,184 1,367 1,550 1,733
0,101 1,0000 1,092 1,184 1,367 1,550 1,734
2,53 0,989 1,087 1,182 1,375 1,570 1,758
5,07 0,979 1,083 1,183 1,384 1,582 1,776
7,60 0,973 1,083 1,188 1,395 1,598 1,795
10,1 0,972 1,084 1,195 1,406 1,615 1,815
15,2 0,987 1,108 1,219 1,439 1,654 1,860
20,3 1,015 1,138 1,256 1,479 1,699 1,909
30,4 1,113 1,234 1,352 1,580 1,805 2,018
40,5 1,242 1,356 1,472 1,696 1,918 2,138
60,8 1,524 1,625 1,738 1,956 2,176 2,392
81,10 1,806 1,990 2,014 2,224 2,444 2,660
101,3 2,083 2,186 2,283 2,494 2,714 2,926
Р, МПа Температура, °C
9 -20 ^10 -60 -78,6
0,101 1,000 1,000 1,000 1,000 1,000
3,04 0,962 0,947 0,936 0,921 0,893
4,05 0,950 0,931 0,913 0,891 0,779
5,07 0,938 0,913 0,889 0,859 0,779
6,08 0,926 0,897 0,864 0,824 0,709
7,09 0,913 0,880 0,838 0,785 0,642
8,11 0,902 0,863 0,812 0,764 0,573
9,12 0,892 0,845 0,789 0,707 0,520
10,1 0,881 0,849 0,768 0,662 0,475
11,1 0,862 0,813 0,747 0,617 0,441
12,2 0,862 0,800 0,727 0,576 0,419
13,2 0,854 0,787 0,711 0,545 0,424
14,2 0,854 0,776 0,692 0,528 0,433
15,2 0,843 0,767 0,674 0,518 0,443
16,2 0,837 0,758 0,659 0,524 0,452
Таблица 3.2.14
Неон (Ne)
р, МПа Температура, °C
-207,9 -192,5 -150 -100 -50
0 0,2388 0,3317 0,4506 0,6336 0,8166
0,101 0,2380 0,3315 0,4507 0,6340 0,8170
1,01 0,2300 0,328 0,451 0,637 0,821
5,07 0,196 0,319 0,454 0,649 0,838
10,1 0,185 0,318 0,465 0,667 0,861
Таблица 3.2.16
Метан (СН4)
р, МПа Температура, °C
-70 -50 -25
0 0,8455 0,8189 0,9106
0,101 0,7410 0,8150 0,9075
2,03 0,647 0,740 0,849
4,05 0,524 0,655 0,787
6,08 0,337 0,555 0,724
8,11 0,256 0,460 0,665
10,1 0,281 0,409 0,417
12,2 0,318 0,410 0,588
14,2 0,354 0,430 0,580
16,2 0,392 0,460 0,589
18,2 0,429 0,492 0,608
20,3 0,466 0,527 0,632
30,4 0,646 0,703 0,788
40,5 0,819 0,875 0,956
50,7 0,987 1,043 1,122
60,8 1,149 1,207 1,286
81,1 1,463 1,525 1,605
101,3 1,766 1,829 1,911
128
Новый справочник химика и технолога
Окончание табл. 3.2.16
р, МПа Температура, °C
0 25 50 100 150 200
0 1,0024 1,0942 1,1859 1,3694 1,5529 1,7365
0,101 1,0000 1,0922 1,1845 1,3686 1,5525 1,7363
2,03 0,954 1,056 1,156 1,351 1,543 1,732
4,05 0,907 1,020 1,128 1,335 1,536 1,731
6,08 0,861 0,986 1,102 1,321 1,530 1,731
8,11 0,819 0,966 1,080 1,310 1,526 1,732
10,1 0,784 0,930 1,062 1,302 1,524 1,735
12,2 0,858 0,910 1,048 1,296 1,525 1,740
14,2 0,743 0,898 1,039 1,294 1,527 1,747
16,2 0,740 0,893 1,035 1,295 1,532 1,755
18,2 0,746 0,894 1,036 1,298 1,539 1,765
20,3 0,761 0,903 1,043 1,305 1,548 1,776
30,4 0,889 1,006 1,129 1,379 1,623 1,853
40,5 1,049 1,150 1,261 1,493 1,727 1,959
50,7 1,209 1,306 1,411 1,628 1,854 2,080
60,8 1,371 1,466 1,565 1,773 1,994 2,213
Окончание табл. 3.2.16
Л МПа Температура, °C
0 25 50 100 150 200
81,1 1,689 1,780 1,878 2,074 2,283 2,495
101,3 2,000 2,089 2,185 2,376 2,580 2,786
Таблица 3.2.17
Этан (С2Н6)
Р, МПа Температура, °C
25 50 100 150 200 250
0 1,1044 1,1970 1,3822 1,5674 1,7526 1,9378
1,01 1,012 1,118 1,325 1,524 1,713 1,911
2,03 0,909 1,040 1,269 1,482 1,682 1,885
3,04 0,784 0,950 1,214 1,444 1,656 1,864
4,05 0,586 0,848 1,158 1,406 1,633 1,843
6,08 0,557 1,040 1,334 1,583 1,809
8,11 0,926 1,267 1,541 1,782
10,1 1,209 1,505 1,760
Таблица 3.2.18
Этилен (С2Н4)
МПа Температура, °C
0 20 40 60 80 100 137,5 198,5
0 1,0073 1,081 1,155 1,229 1,302 1,376 1,514 1,739
5,07 0,176 0,629 0,814 0,954 1,077 1,192 1,374 1,652
10,1 0,310 0,360 0,470 0,668 0,846 1,005 1,247 1,580
15,2 0,441 0,485 0,550 0,649 0,776 0,924 1,178 1,540
20,3 0,565 0,610 0,669 0,744 0,838 0,946 1,174 1,537
30,4 0,806 0,852 0,908 0,972 1,048 1,133 1,310 1,628
40,5 1,036 1,084 1,140 1,202 1,272 1,356 1,510 1,790
50,7 1,255 1,307 1,367 1,431 1,500 1,577 1,721 1,985
60,8 1,472 1,525 1,586 1,652 1,721 1,795 1,938 2,191
70,9 1,683 1,737 1,799 1,867 1,936 2,011 2,153 2,399
81,1 1,888 1,946 2,010 2,077 2,149 2,224 2,368 2,606
91,2 2,090 2,153 2,217 2,286 2,359 2,434 2,585 2,810
101,3 2,289 2,353 2,421 2,492 2,566 2,642 2,798
ПроизведениеpV(Дж/г) для веществ в газообразном состоянии, являющихся твердыми телами или жидкостями при О °C и 101,3 кПа
Простые вещества и неорганические соединения
Таблица 3.2.19
Бром (Вг2)
р, кПа Температура, °C
700 800 900 1000 1100 1200
50,7 60,8 50,531 50,531 56,053 62,001 61,960 68,85
70,9 50,531 56,033 61,930 68,688 76,602
81,1 50,531 56,012 61,889 68,526 76,298 85,995
91,2 55,972 61,859 68,364 76,085 85,346
101,3 111,5 121,6 55,931 61,818 68,202 68,04 75,913 75,751 75,599 84,931 84,708
Физические свойства важнейших веществ
129
Таблица 3.2.20
Вода (перегретый пар) (Н2О)
р, кПа Температура, °C
120 130 140 150
101 179,55 184,31 189,07 193,73
111 179,24 184,11 188,87 193,53
122 179,04 183,90 188,77 193,43
132 178,74 183,70 188,57 193,23
142 178,43 183,50 188,36 193,13
152 178,23 183,30 188,16 192,92
162 177,93 183,09 187,96 192,72
172 177,72 182,89 187,86 192,62
182 177,42 182,69 187,65 192,42
193 177,12 182,39 187,45 192,31
203 182,18 187,25 192,11
Окончание табл. 3.2.20
Р, кПа Т= 160 °C р, кПа Т= 170 °C р, кПа Т= 185 °C
456 193,13 608 195,86 1013 197,28
659 194,95 1064 196,27
709 194,14 1115 194,85
760 193,13
Таблица 3.2.21
Иод (12)
Л кПа Т= 160 °C р, кПа Т= 170 °C р, кПа Т= 185 °C
253 196,17 304 200,52 811 200,72
304 195,46 405 199,10 861 199,91
355 194,75 507 197,48 912 199,20
405 193,94 557 196,67 963 198,29
р, кПа Температура, °C
500 800 900 1000 1100 1200
50,7 25,281 37,673 43,965
60,8 25,281 37,581 43,701 52,030
70,9 37,470 43,448 51,503 62,001
81,1 37,328 43,195 51,007 61,261 73,359
91,2 37,136 42,931 50,531 60,582 72,458
101 42,678 50,075 59,964 71,475
111 49,639 59,397 70,755
122 49,214 58,829 69,975
132 58,282 69,256
Таблица 3.2.22
Сера (S)
р, кПа Температура, °C
400 450 500 550 600 650 850 950 1020
2,03 31,208 48,028 72,549
5,07 27,844 38,098 59,478 96,664 114,19 123,21 153,91
10,1 26,740 33,235 47,927 79,135 105,58 118,45 151,78 164,45 172,35
15,2 26,436 31,816 42,759 68,293 97,677 114,29 150,06 163,34 171,64
20,3 26,243 31,005 39,821 61,200 90,483 110,65 148,64 162,53 171,04
30,4 25,949 30,296 37,490 53,500 79,743 105,07 146,62 160,5 169,72
40,5 25,655 29,891 36,477 49,548 72,853 100,92 145,3 159,49 168,6
50,7 25,402 29,486 35,666 47,015 68,293 97,272 144,49 158,67 167,9
60,8 28,979 34,856 45,394 64,747 93,726 143,88
70,9 28,776 33,336 43,874 61,808 90,382 143,48
81,1 42,658 59,478 86,937
91,2 32,627 41,442 57,350 83,694
101 40,530 55,627 80,857
111 31,512 39,415 53,905 78,122
131 38,504 52,284 74,373
Органические соединения
Таблица 3.2.23
Метанол (СН3ОН)
р, кПа Температура, °C
120 160 180 200 230 240
203 10,041 11,217 12,200 13,081 13,304
405 9,5651 10,963 12,078 13,030 13,263
608 8,9470 10,7100 11,946 12,959 13,223
811 10,447 11,794 12,889 13,162
1013 9,1193 10,163 11,034 11,642 12,797 13,091
1216 9,8184 10,781 11,490 12,696 13,000
130
Новый справочник химика и технолога
Окончание табл. 3.2.23
р, кПа Температура, °C
120 160 180 200 230 240
1419 9,4334 10,507 11,328 12,585 12,899
1621 8,9470 10,234 11,156 12,453 12,858
1824 8,3188 9,9906 10,963 12,321 12,655
2027 9,5955 10,761 12,169 12,524
2229 9,2307 10,548 12,007 12,372
2432 8,8355 10,315 11,845 12,220
2634 8,4201 10,072 11,663 12,048
2837 9,8083 11,470 11,885
3040 9,5144 11,277 11,723
3242 9,2003 11,065 11,551
3648 8,4505 10,649 11,196
3850 8,0452 10,426 11,014
4053 10,203 10,832
/?, кПа Температура, С
220 225 232 234 236 238 239
2837 10,913 11,156 11,511 11,612 11,693 11,774 11,814
3040 10,690 10,963 11,338 11,429 11,521 11,612 11,642
3242 10,507 10,761 11,156 11,257 11,359 11,440 11,480
3445 10,295 10,558 10,963 11,075 11,186 11,267 11,308
3648 10,062 10,355 10,781 10,882 11,004 11,085 11,136
3850 9,8184 10,143 10,578 10,680 10,822 10,903 10,953
4053 9,5651 9,9096 10,366 10,487 10,629 10,710 10,761
4256 9,3016 9,6664 10,153 10,274 10,426 10,518 10,578
4458 9,0281 9,4131 9,9299 10,062 10,224 10,315 10,376
4661 8,7038 9,1496 9,6968 9,8387 10,001 10,112 10,163
4864 8,3796 8,8761 9,4536 9,5955 9,7880 9,8995 9,9501
5066 7,9945 8,5822 9,2003 9,3523 9,5448 9,6664 9,7272
5269 7,5892 8,2681 8,9369 9,0990 9,3016 9,4435 9,5043
5472 8,6532 8,8355 9,0483 9,1800 9,2611
5674 8,3593 8,5518 8,7849 8,9369 9,0179
5877 8,0452 8,2681 8,5012 8,6734 8,7646
6080 7,7007 7,9540 8,1871 8,3897 8,4910
6282 7,3258 7,6196 7,8831 8,0959 8,2276
6485 6,8901 7,2549 7,5183 7,7716 7,9236
6890 5,6945 6,3429 6,7077 7,0725 7,2650
7093 5,5931 6,1910 6,6571 6,8800
7295 5,5019 6,1707 6,4240
7498 5,5019 5,8667
7701 5,0663
Таблица 3.2.24
Пропан-1-ол (С3Н7ОН)
р, кПа Температура, °C
180 200 220 230 240 250 260 270 280
507 57,350 60,694 64,037 65,760 67,178 70,218 73,157
709 55,222 58,971 62,518 64,341 65,963 69,104 72,245
912 52,790 57,147 60,998 62,923 64,645 67,989 71,333
1115 55,222 59,376 61,403 63,328 66,875 70,320
1317 53,094 57,755 59,883 61,910 65,760 69,306
1520 50,663 56,033 58,262 60,491 64,544 68,293
1723 54,209 56,539 58,971 63,328 67,178
Физические свойства важнейших веществ
131
Окончание табл. 3.2.24
р, кПа Температура, °C
180 200 220 230 240 250 260 270 280
1925 52,284 54,716 57,350 62,011 66,165
2128 49,953 52,892 55,627 58,262 60,694 63,125 65,051
2330 47,420 50,764 53,905 56,641 59,376 61,910 63,835
2533 48,535 52,081 55,019 57,958 60,592 62,720
2736 45,799 50,055 53,196 56,438 59,275 61,504
2938 42.455 47,825 51,372 54,918 57,857 60,288
3040 46,610 50,460 54,108 57,147 59,680
3141 45,292 49.447 53,196 56,337 59,072
3242 43,772 48,332 52,284 55,627 58,363
3344 42,151 47,217 51,372 54,817 57,755
Таблица 3.2.25
Уксусная кислота (СН3СООН)
р, кПа Температура, °C
92 105,1 118,0 132,9 147.6 162.5 184,1
12,2 34,451 39,213 44,178 53,196 57,249 61,302
14,2 33,944 38,504 43,468 48,433 52,385 56,843 60,998
16,2 33,437 37,794 42,759 47,724 51,676 56,438 60,694
18,2 33,032 37,288 42,151 47,116 51,068 56,033 60,390
20,3 32,627 36,680 41,543 46,508 50,460 55,729 59,883
22,3 32,221 36,173 41,037 45,900 49,953 55,323 59,984
24,3 31,917 35,768 40,530 45,394 49,447 55,019 59,782
26,3 31,613 35,464 40,023 44,988 49,041 54,716 59,579
28,4 31,208 35,058 39,618 44,482 48,636 54,412 59,376
30,4 30,904 34,754 39,111 44,076 48,332 54,108 59,174
32,4 30,600 34,451 38,706 43,671 48,028 53,804 58,971
34,5 30,398 34,248 38,402 43,367 47,623 53,601 58,870
36,5 30,094 33,944 37,997 42,962 47,319 53,297 58,667
38,5 29,790 33,640 37,693 42,557 47,015 52,993 58,566
42,6 33,133 36,984 41,949 46,508 52,486 58,262
46,6 32,728 36,578 41,341 46,002 51,980 57,958
50,7 32,221 47,319 50,865 45,495 51,473 57,654
54,7 31,715 35,666 40,226 45,090 51,068 57,350
56,7 31,512 35,464 40,023 44,786 50,764 57,249
р, кПа Температура, °C
118 132,9 147,6 162.5 184,1
60,8 35,058 39,517 44,380 50,359 56,945
64,8 34,754 39,111 43,975 49,852 56,641
68,9 34,349 38,706 43,671 49,447 56,337
73 34,045 38,402 43,266 49,041 56,134
77 33,741 38,098 42,860 48,636 55,830
81,1 33,437 37,794 42,557 48,231 55,526
85,1 33,235 37,490 42,151 47,825 55,222
89,2 32,931 37,186 41,847 47,42 54,918
93,2 32,728 36,984 41,442 47,015 54,614
97,3 36,680 41,138 46,610
101 36,477 40,733
132
Новый справочник химика и технолога
Окончание табл. 3.2.25
р, кПа Температура, °C
240 280
405 59,478 69,205
507 57,553 67,989
608 55,729 66,773
709 54,006 65,659
811 52,486 64,443
912 50,966 63,227
1013 49,244 62,112
1115 47,724 60,998
1216 46,204 59,883
1317 44,786 58,769
1419 43,367 57,654
1520 41,847 56,539
2027 51,270
2533 45,900
2736 43,772
3040 40,125
3242 36,882
Таблица 3.2.26
Этанол (С2Н5ОН)
р. кПа Температура, ЭС
130 140 150 160 170 180 190
405 69,306 71,738 74,403 76,673 78,861 80,786
507 67,482 70,421 73,157 75,588 77,818 79,915 82,651
608 64,139 68,800 71,910 74,474 76,804 79,064 81,871
709 66,976 70,593 73,288 75,720 78,193 81,060
811 69,002 72,113 74,677 77,281 80,219
912 67,047 70,826 74,575 76,369 79,368
1013 64,139 69,479 72,447 75,436 78,496
1115 67,989 71,262 74,443 77,615
1216 66,094 70,087 73,390 76,673
1317 68,800 72,316 75,690
1419 67,330 71,181 74,707
1520 65,486 69,985 73,663
р, кПа Температура, °C
200 210 220 225 230 232 234
507 84,505 86,228 86,967 87,677 88,659 89,500 91,162
709 83,056 85,012 85,853 86,704 87,747 88,558 90,281
912 81,536 83,694 84,677 85,620 86,734 87,545 89,369
1115 79,945 82,347 83,390 84,404 85,620 86,461 88,254
1317 78,324 80,888 82,002 83,117 84,434 85,245 87,089
1520 76,602 79,337 80,584 81,769 83,157 83,998 85,822
1723 74,747 77,686 79,104 80,351 81,840 82,651 84,475
1925 72,751 75,943 77,544 78,861 80,523 81,263 83,087
2128 70,593 74,140 75,923 77,311 78,932 79,793 81,638
2330 68,242 72,245 74,241 75,720 77,412 78,253 80,118
2533 65,557 70,218 72,518 74,069 75,791 76,703 78,557
2736 62,416 68,121 70,725 72,376 74,140 75,082 76,906
2938 58,465 65,76 68,871 70,593 72,447 73,390 75,284
3141 63,095 66,875 68,769 70,654 71,667 73,613
3344 59,934 64,716 66,875 68,871 69,884 71,910
3546 55,830 62,315 64,848 66,976 68,090 70,188
Физические свойства важнейших веществ
133
Окончание табл. 3.2.26
р, кПа Температура. °C
200 210 220 225 230 232 234
3749 59,650 62,751 65,051 66,165 68,394
3952 56,438 60,491 63,024 64,210 66,571
4154 57,958 60,967 62,183 64,595
4256 56,509 59,853 61,099 63,561
4762 53,226 55,019 57,725
5168 46,204 51,341
5370 45,799
3.3. Равновесные температуры и давления (гетерогенные равновесия)
Ниже приведены данные по давлению, температуре плавления и изменению объема (ДГ --- Гж - К1В) некоторых веществ и воды (табл. 3.3.1 и 3.3.2).
Простые вещества и неорганические соединения представлены в табл. 3.3.1 в алфавитном порядке химических символов. Органические соединения расположены по эмпирическим формулам в соответствии с системой Хилла.
Таблица 3.3.1
Зависимость между давлением, температурой плавления и изменением объема некоторых веществ
Формула Название /?, МПа Т °C 1 пл* Л Г см3/моль
Простые вещества
А1 Алюминий 0,101 660 1,51
Аг Аргон 0,101 -189,25 3,16
101 -166,75 2,22
203 -146,69 1,7
304 -128,3 1,36
405 -111,2 1,02
608 -80,3 0,837
Bi Висмут 0,101 271,0 -0,72
101 267,5 -0,74
203 263,5 -0,76
405 256,0 -0,79
811 238,0 -0,85
1013 228,8 -0,87
Вг2 Бром 0,101 -7,0 4,08
Cd Кадмий 0,101 320,9 0,73
Cs Цезий 0,101 29,7 1,8
101 51,9 1,43
203 70,2 U7
304 85,7 1,035
Cs Цезий 405 98,5 0,955
Ga Галлий 0,101 29,85 -0,370
405 21,5 -0,407
811 12,6 -0,464
1216 2,5 -0,516
н2 Водород 0,007 -259,19 2,85
8,37 -266,72 2,30
15,4 -254,91 2,03
Продолжение табл. 3.3.1
Формула Название р, МПа Г11Л, °с дг, см3/моль
Н2Н (2Н])Водород 0,013 -256,6 2,65
(дейтероводо-
род)
ч (2Н2)Водород 0,018 -254,43 2,66
(дидейтерий)
10 -252,18 1,98
Не Гелий 3,12 -271,4 1,45
7,91 -270,2 1,19
10,3 -269,7 1,10
Hg Ртуть 0,101 -38,85 0,519
203 -28,66 0,506
406 -18,48 0,504
812 1,87 0,490
1017 12,07 0,477
1222 22,24 0,460
12 Иод 0,101 113,6 5,43
К Калий 0,101 62,5 1,05
101 78,7 0,926
203 92,4 0,820
405 115,8 0,656
811 152,5 0,420
1013 167,0 0,328
1216 179,6 0,252
Кг Криптон 0,101 -58,20 4,49
Li Литий 0,101 179 0,184
n2 Азот 0,101 -210,0 1,01
101 -190,9 0,81
203 -174,6 0,66
405 -147,4 0,46
608 -124,0 0,36
Na Натрий 0,101 97,6 0,641
101 105,9 0,587
203 114,2 0,54
405 128,8 0,477
811 155,1 0,394
1013 166,7 0,358
1216 177,5 0,322
Ne Неон 0,101 -248,59 2,19
o2 Кислород 0,101 -219 0,82
P Фосфор 0,101 44,2 0,597
101 72,7 0,555
203 99,3 0,516
304 124,4 0,479
134
Новый справочник химика и технолога
Продолжение табл. 3.3.1
Формула Название р, МПа Т °C 1 IU15 А К, см3/моль
Простые вещества
Р Фосфор 405 151,3 0,440
608 191,9 0,377
РЬ Свинец 0,101 327,0 0,705
Rb Рубидий 0,101 38,7 1,58
101 57,9 1,24
203 74,5 1,03
304 89,1 0,905
S Сера (монокл.) 0,101 114,5 0,92
40,5 126,0 1,28
Сера (ромб.) 101 140 0,45
Sb Сурьма 0,101 630 0,27
Se Селен 0,101 220 1,41
Sn Олово 0,101 231,85 0,46
Те Теллур 0,101 450 1,57
TI Таллий 0,101 302,5 0,55
Хе Ксенон 0,101 -111,79 5,59
Zn Цинк 0,101 419,4 0,69
Неорганические соединения
А120з Алюминия оксид (корунд) 0,101 2046 15,3
В2О3 Бора оксид 0,101 557 -0,81
СО2 Углерода 304 -5,5 4,7
диоксид 405 8,5 4,4
507 21,4 3,94
608 33,1 3,61
811 55,2 3,07
1013 75,4 2,65
1216 93,5 2,34
COS Карбонил-сульфид 0,101 -138,84 4,88
CS2 Углерода ди- 0,101 -108,6 3,27
сульфид 1013 0 2,17
1520 46 1,86
2027 89 1,68
2533 130 1,56
3040 170 1,485
Н2О Вода См. табл. 3.3.2
Н3РО4 Фосфорная 0,101 41,8 7,8
кислота
KSCN Калия тио- 0,101 171,2 4,82
цианат 50,7 181,9 4,66
101 192,6 4,5
152 203,3 4,33
NaCl • Натрия хло- 374 17,5 1,26
• 2Н2О рид дигидрат 536 21,21 0,77
746 24,30 0,41
Na2SO4 • Натрия суль- 0,101 32,6 1,18
• 10Н2О фат декагидрат (глауберо-
ва соль)
NH4NO3 Аммония 101 202 4,04
нитрат
РН3 Фосфин (фосфан) 0,101 -134,74 2,25
Продолжение табл. 3.3.1
Формула Название р, МПа тШ1, °с АТ, см3/моль
РН4С1 Фосфония 37,8 40,06 51,5
хлорид
РС13 Фосфора 0,101 -92 4,22
трихлорид
SF6 Серы гекса- 0,101 50,7 20,8
фторид
Sbl3 Сурьмы три- 118 200,8 12,0
иодид
SiCl4 Тетрахлорси- 203 -10,0 8,87
лан 405 42,6 7,27
608 92,5 6,25
811 139,4 5,6
1013 183,8 5,2
Органические соединения
cf4 Тетрафторме- 0,101 183,67 1,6
тан
СС14 Тетрахлорме- 0,101 -22,6 3,97
тан 101 14,2 3,09
203 45,9 2,54
405 102,7 1,84
608 149,5 1,33
811 192,1 0,96
СИСЬ Хлороформ 304 -12,1 6,33
405 3,4 5,95
608 32,4 5,23
811 58,6 4,64
1013 83,7 4,18
1216 107,9 3,83
2027 192 3,13
2533 243 2,76
СНВгз Бромоформ 0,101 7,78 9,87
101 31,5 8,97
203 53,8 8,14
405 94,7 6,72
608 130,8 5,58
811 163,2 4,75
1013 194,0 4,20
СН2О2 Муравьиная 0,101 8,5 5,29
кислота
СН2С12 Дихлормстан 1013 0 2,87
1520 42 2,63
2027 82 2,44
2533 120 2,30
3040 157 2,18
CH4N2O Мочевина 0,101 131,7 0,6
(карбамид)
c2f4 Тетрафтор- 0,101 -142,5 13,5
этилен
c2f6 Гексафтор- 0,101 -106,3 6,8
этан
С2Н2С1О2 Дихлоруксус- 0,101 16,68 9,37
ная кислота 764 151,7 3,912
945 164,8 2,655
С2Н4О2 Уксусная 0,101 16,68 9,37
кислота 101 37,7 6,89
203 54,3 5,33
Физические свойства важнейших веществ
135
Продолжение табл. 3.3.1
Формула Название р, МПа т,1Л. °C ДИ см3/моль
С2Н4О2 Уксусная 405 83 4,97
кислота 608 108,2 4,20
811 129,6 3,59
1013 148,3 3,21
С2Н4Вг2 1,2-Ди- 0,101 9,95
бромэтан 50,7 22,45 8,23
101 34,0 7,14
C2H5NO Ацетамид 0,101 81,5 6,486
101 93,1 5,033
203 103,1 3,946
405 119,0 2,534
608 133,1 3,597
811 151,1 2,906
1013 166,55 2,434
C2H5Br Бромэтан 0,101 -119 4,53
1520 5 2,06
2027 34 1,73
2533 58 1,45
3040 80 1,2
с2н6о Этанол 1520 -5 2,041
2027 25 2,00
2533 54 1,97
3040 82 1,93
С3Н4Вг2О2 2,3-Дибром- 0,101 64 2,351
пропановая
кислота
С3Н6О2 Пропионовая 0,101 -20,8 9,13
кислота
c3h7no2 Этилкарбамат 0,101 47,9 5,34
(уретан) 101 57,3 3,352
203 64,2 2,471
405 75,8 1,675
608 98,0 5,099
1013 138,4 3,875
С3Н7Вг 1 -Бромпропан 1520 34 2,82
2027 71 2,42
2533 105 2,14
3040 138 1,93
4053 197 1,61
С4Н6О4 Диметилокса- 0,101 54,24 17,16
лат 101 75,8 13,17
203 95,8 11,30
405 132,6 9,423
811 196,8 7,156
C4H8C12S Бис(2-хлор- 0,101 13,9 8,59
этил)сульфид 186 38,9 6,68
(иприт)
С4Н8О Этилацетат 0,101 -82,4
1226 25 2,14
2412 75 2,07
С4Н8О2 Масляная 0,101 -5,5 4,19
кислота
С4Н10О Бутан-1-ол 1013 12 3,54
1520 49 3,20
2027 80 2,96
Продолжение табл. 3.3.1
Формула Название р. МПа Tnjl. °C ДИ см3/моль
С4Н10О Бутан-1 -ол 2533 108 2,76
3040 132 2,61
С4Н10О 2-Метил-пропан-2-ол 0,101 24,9 6,51
С5н10о2 Пентановая 0,101 -34,5 10,90
кислота
С6Н4С12 1,4- 0,101 52,28 20,61
Дихлорбензол
C6H4N2O4 1,3-Ди-нитробснзол 0,101 89,8 15,75
c6h5no2 Нитробензол 0,101 5,67 10,01
101 27,9 9,019
203 48,1 8,173
405 87,6 6,835
608 122,3 6,014
811 153,8 5,435
1013 184,5 4,959
c6h5no3 4-Нитрофенол 0,101 112,4 12,39
50,7 125,5 11,29
101 137,7 10,29
203 159,8 8,54
405 198,8 6,19
С6Н5С1 Хлорбензол 0,101 -45,5 8,00
203 -12,0 6,36
405 16,7 5,28
608 41,9 4,50
811 64,8 3,93
1013 107,6 3,49
c6H6 Бензол 0,101 5,43 10,29
101 32,5 8,01
203 56,5 6,81
304 77,7 5,93
405 96,6 5,27
507 114,6 4,80
608 131,2 4,40
811 162,2 3,79
1013 190,5 3,30
с6116о Фенол 0,101 40,87 5,34
50,7 47,5 4,43
101 53,4 3,72
203 63,3 2,63
405 99,8 6,72
608 131,0 5,93
811 158,8 5,32
1013 184,6 4,83
1216 209,2 4,40
c6h7n Анилин 0,101 -6,4 7,95
101 13,1 7,30
203 31,6 6,74
405 64,5 5,87
608 93,2 5,22
811 119,1 4,67
1013 143,2 4,20
1216 165,3 3,77
С6Н12 Циклогексан 0,103 6,55 5,64
136
Новый справочник химика и технолога
Продолжение табл. 3.3.1
Формула Название р, МПа Т °C 1 !(Л> ди, см3/моль
Органические соединения
с6н12 Циклогексан 760 25 4,43
882 75 3,78
с6н12о Циклогекса- 0,101 25,45 2,52
НОЛ
С6Н12О2 Гексановая 0,101 -3,95 13,66
кислота
C6H)8OSi2 Гексаметил- 50,7 -52,5 13,64
дисилоксан 101 -37,7 12,11
203 -10,2 10,11
405 40,2 8,20
c7h7no2 1-Метил-4-нитробензол 0,101 51,65 14,08
С7Н8О о-Крезол 0,101 30,8 8,95
101 47,4 7,33
203 61,9 6,02
405 81,8 4,39
608 102,9 3,45
811 118,1 2,85
с7н8о м-Крезол 0,101 И,9 6,59
c7h9n и-Толуидин 0,101 43,6 15,14
101 69,0 12,80
203 91,5 11,11
405 131,3 9,13
608 168,4 7,89
811 204,6 6,93
с7н14 Метилцикло- 1398 25 3,47
гексан 1905 75 3,72
с8н6о2 2-Бснзофуран- 0,101 73 1,532
1(3//)-он (фталид)
с8н80 Ацетофенон (метилфенил- 0,101 19,2 12,54
кетон)
СвНю н-Ксилол 0,101 13,35 2,09
20,0 20 2,05
81,4 40 1,92
CsH16O2 Октановая 0,101 16,3 17,0
кислота
C8H24O2Si3 Октаметил- 50,7 -74,3 19,51
трисилоксан 101 -63,0 17,97
507 12,5 10,52
СюН8 Нафталин 0,101 80,01 18,74
28,9 90 18,2
43,6 95 17,8
58,8 100 17,5
Ск)Н12О 1 -Метокси-4-[(Е)-проп-1-ен- 0,101 22,3 11,80
1 -ил]бензол
(анетол)
СюН2оО 2-Изопропил- 0,101 42,4 10,2
5-метил-
циклогексанол
(ментол)
Окончание табл. 3.3.1
Формула Название р, МПа тип. °C ди, см3/моль
С10Н22О Дипентило- 760 25 9,62
вый эфир 1520 75 5,94
CioH3o03Si4 Декаметил- 50,7 -62,7 20,53
тетрасилоксан 101 -50,0 19,00
507 39,6 10,40
C12HnN А-Фенил- 0,101 54,0 16,21
анилин 101 79,1 13,66
203 103,0 11,98
405 144,9 9,92
608 180,9 8,53
811 212,9 7,58
C|2H24O2 Додекановая 0,101 42,5 24,72
кислота
С13Н,оО Бензофенон (дифенилке- 0,101 47,77 16,47
тон) 101 74,6 14,08
203 98,9 12,55
405 142,0 10,40
608 179,6 9,07
811 213,7 8,05
С13н12 Метилендибензол (дифс- 0,101 26,9 15,05
нилмстан)
с14н14 Этан-1,2- 0,101 51,3 20,59
диилдибензол 50,7 68,4 19,14
(1,2-дифенил- 101 83,2 17,50
этан) 152 97,3 16,04
С16Н32О2 Пальмитине- 0,101 61,2 4,321
вая кислота
С19н16 Метантриил-трибензол (трифснилмс- 0,101 92,8 18,15
тан)
В зависимости от давления жидкая вода может находиться в устойчивом равновесии лишь с определенными полиморфными видоизменениями льда, обозначаемыми в табл. 3.3.2 в порядке возрастания давления I, III, V, VI.
Таблица 3.3.2
Зависимость между давлением, температурой плавления и изменением объема воды
Твердая фаза р, МПа Температура равновесия, °C ДИ, см3/моль
Лед I 0,101 0,0 -1,62
61,8 -5,0 -1,83
115 -10,0 -2,02
161 -15,0 -2,195
200 -20,0 -2,365
Лед HI 214 -22,0 0,839
254 -20,0 0,668
Физические свойства важнейших веществ
137
Продолжение табл. 3.3.2
Твердая фаза р. МПа Температура равновесия, °C АГ, см3/моль
Лед III 295 -18,5 0,542
358 -17,0 0,416
Лед V 318 -20,0 1,48
385 -15,0 1,36
457 -10,0 1,225
551 -5,0 1,086
644 0,0 0,95
Лед VI 485 -15,0 1,765
535 -10,0 1,73
589 -5,0 1,69
644 0,0 1,65
Окончание табл. 3.3.2
Твердая фаза р, МПа Температура равновесия, °C АГ, см3/моль
Лед VI 709 5,0 1,59
774 10,0 1,52
842 15,0 1,435
912 20,0 1.355
1073 30,0 1,195
1248 40,0 1,065
1520 52,5 0,915
1824 66,0 0,764
2027 73,8 0,677
2270 81,6 0,595
Температуры кипения или возгонки индивидуальных веществ при различных давлениях
В табл. 3.3.3-3.3.7 и 3.3.9 приводятся температуры (в °C), при которых давление насыщенного пара достигает величины, указанной в головке таблицы. Каждый раздел таблиц (простые вещества, неорганические соединения, органические соединения) состоит из двух частей: в табл. 3.3.3, 3.3.4, 3.3.6-3.3.9 указаны температуры, при которых давление насыщенного пара ниже 101,3 кПа, в табл. 3.3.8 и 3.3.10 — температуры, при которых давление насыщенного пара выше 101,3 кПа. В связи с тем, что в точке плавления кривые давления
паров имеют излом, а в критической точке обрываются, в табл. 3.3.3-3.3.7 и 3.3.9 приводятся температуры плавления (в °C), а в табл. 3.3.8 и 3.3.10 — критические температуры (в °C) и критические давления (в МПа) соответствующих веществ. Вес температурные величины даются с точностью, не превышающей 0,1 °C.
Условные обозначения: ж. — жидкий; тв. — твердый; крист. — кристаллический; разл. — разлагается; полим. — полимеризуется; при отсутствии указания на агрегатное состояние подразумевается жидкость.
Простые вещества (см. также табл. 3.3.11)
Таблица 3.3.3
Температуры кипения или возгонки (°C) индивидуальных веществ при давлении пара от 1,33 • Ю7 до 1,33 • 10~4 Па
Вещество Температура кипения или возгонки при давлении насыщенного пара Т’нл, °C
1.33 • 10’7Па 1,33 • 10“6Па 1,33 • 10”5Па 1,33 • 10^ Па
Ag (тв.) 527 573 625 684 960,8
А1 595 (тв.) 644 (тв.) 701 766 660,1
As (крист.) 86 (тв.) 104 (тв.) 124 (тв.) 147 (тв.) 817
Au (тв.) 753 812 878 953 1063
В (тв.) 1270 1353 1445 1548 2075
Ва (тв.) 253 285 322 365 717
Be (тв.) 645 698 757 824 1280
Bi 228 (тв.) 248 (тв.) 270 (тв.) 296 271,3
Вг2 (тв.) -142 -137 -131 -125 -7,3
С (графит) 1591 (тв.) 1690 (тв.) 1800 (тв.) 1922 (тв.)
Са (тв.)*1 245 276 312 352 850
Cd (тв.) 54 73 95 120 321,0
Со (тв.) 657 705 760 822 1492
Сг (тв.) 764 821 885 956 1903
Cs (тв.) -32 -16 1 22 28,5
Си (тв.) 672 727 787 857 1083
Ей (тв.) 259 293 326 367 1150
Fe (тв.)*2 799 858 924 998 1530
Ga 519 567 620 681 29,7
Gd (тв.) 336 371 411 455 1350
Ge (тв.) 763 819 884 957 959
138
Новый справочник химика и технолога
Окончание табл. 3.3.3
Вещество Температура кипения или возгонки при давлении насыщенного пара Т„я. °с
1,33 • 10"7Па 1,33 • 10^ Па 1,33 • 10 5 Па 1,33 • 10"4 Па
Hf (тв.) 1507 1607 1717 1844 2230
Hg (тв.)*3 -84,0 -72,3 -59,1 -44,0 -38,9
12 (тв.) -104 -95 -85 -74 113,7
In 427 427 521 577 156,2
1г (тв.) 1375 1464 1562 1671 2443
К 4,9 (тв.) 22,4 (тв.) 41,9 (тв.) 65,3 63,6
La 919 990 1070 1212 887
Li 204 234 268 306 180
Lu (тв.) 613 664 720 784 1700
Mg (тв.) 157 182 211 244 651
Мп (тв.) 504 545 596 651 1220
Мо (тв.) 1491 1588 1696 1817 2625
N2 (тв.) -250,8 -249,5 -247,9 -246,2 -210,0
Na 54 (тв.) 74 (тв.) 97 (тв.) 124 97,8
Nb (тв.) 1677 1818 1987 2500
Nd (тв.) 673 731 797 871 1024
Ni (тв.) 625 673 727 788 1453
О2 (тв.) -246,5 -245,0 -243,2 -241,2 -218,8
Os (тв.) 1623 1723 1835 1961 2700
РЬ 310 (тв.) 346 387 435 327,3
Pd (тв.) 841 907 980 1063 1552
Ро (тв.) 102 123 148 175 252
Pt (тв.) 1202 1282 1371 1471 1769
Ra (тв.) 216 246 280 320 960
Rb (тв.) -20 -3 15 37 38,8
Re (тв.) 1812 1928 2059 2207 3150
Rh (тв.) 1194 1273 1362 1462 1960
Ru (тв.) 1468 1560 1663 1778 2430
S (ромб.)*4 -28 (тв.) -13 (тв.) 2 (тв.) 19 (тв.) 112,8, устойчива до 95,6
Sb (тв.) 243 274 307 344 630,5
Sc (тв.) 639 714 772 837 1400
Se (тв.) 67 84 104 121 220,5
Si (тв.) 747 802 863 931 1420
Sm (тв.) 337 373 414 460 1350
Sn 632 688 751 823 231,9
Sr (тв.) 210 239 272 309 777
Та (тв.) 1857 1964 2093 2238 2500
Тс (тв.) 1472 1567 1677 1797 2140
Ti (тв.)*5 997 1067 1146 1235 1725
Т1 250 (тв.) 282 (тв.) 318 356 303,5
Ти (тв.) 423 461 505 554 1500
и 1064 (тв.) 1136 1225 1326 1133
V (тв.) 1085 1158 1240 1331 1730
W (тв.) 1990 2110 2244 2394 3380
Y (тв.) 773 832 898 973 1475
Yb (тв.) 223 253 288 326 824
Zn (тв.) 104 126 151 180 419,5
Zr (тв.) 1389 1481 1585 1702 1852
*’ а-Модификация.
*2 Ниже 906 °C — p-модификация, выше 906 °C — у-модификация.
*3 См. также табл. 3.3.13 и 3.3.14.
*4 См. также табл. 3.3.18.
*5 Р-Модификация.
Физические свойства важнейших веществ
139
Таблица 3.3.4
Температуры кипения или возгонки (°C) простых веществ при давлении пара от 0,00133 Па до 101,3 кПа
Вещество Температура кипения или возгонки при давлении насыщенного пара Тпп. °C
0,00133 Па 0,0133 Па 0,133 Па 1,33 Па 13,3 Па 133 Па 1.33 кПа 13,3 кПа 101,3 кПа
Ag 751 (тв.) 828 (тв.) 918 (тв.) 1028 1163 1330 1543 1825 2163 960,8
Al 841 927 1028 1148 1299 1472 1700 1995 2348 660,1
Am 865 (тв.) 973 (тв.) 1103 (тв.) 1264 1472 1736 2173 2606 1200
Ar -241,3 -239,4 -235,0 -230,8 -225,8 -219,5 -211,3 -200,1 -185,9 -189,4
As (тв.) 178 (тв.) (тв.) 201 (тв.) (тв.) 234 (тв.) (тв.) 273 (тв.) (тв.) 317 (тв.) (тв.) 371 (тв.) (тв.) 437 (тв.) (тв.) 519 (тв.) 612 (тв.) 817
(крист.) At 23 42 65 92 123 160 206 262 334*'
Au 1038 (тв.) 1140 1260 1403 1574 1768 2055 2412 2847 1063
В 1666 (тв.) 1799 (тв.) 1953 (тв.) 2136 2358 2625 2957 3380 3860 2075
Ba 414 (тв.) 471 (тв.) 539 (тв.) 622 (тв.) 724 861 1044 1302 1634 717
Bi 327 365 415 487 614 767 947 1144 1430*2 271,3
Br2 -118,6 -110 (тв.) -99 (тв.) -87 (тв.) -71 (тв.) -51 (тв.) -26 (тв.) 8,6 57,9 -7,3
C (тв.) 2160 (тв.) 2217 (тв.) 2396 (тв.) 2543 (тв.) 2845 (тв.) 3214 (тв.) 3496 (тв.) 4373 (тв.) 4830
(графит) Ca*3 399 (тв.) 453,5 (тв.) 517,2 (тв.) 594 (тв.) 689,3 808 (тв.) 970 1199 (тв.) 1482 850
Cd 148,6 (тв.) 181 (тв.) 219 (тв.) 265 (тв.) (тв.) 321 (тв.) 394 488 615 770 321,0
Ce ci2 -171,7 -164,3 1187 -155,7 1292 -145,5 1442 -133,3 1602 -118,2 1860 -101,5 2170 -71,9 (2530) -34,1 785 -101,3
Co (тв.) 899 (тв.) (тв.) 1274 (тв.) (тв.) 1069 (тв.) (тв.) 1181 (тв.) (тв.) 1313 (тв.) (тв.) 1471 (тв.) (тв.) 1677 1940 2255 1492
Cr 1038 (тв.) ИЗО (тв.) 1238 (тв.) 1364 (тв.) 1513 (тв.) 1695 (тв.) 1922 2221 2570*4 1903
Cs 46 75 109,2 151 203 267 364 499 688 28,5
Cu 934 (тв.) 1025 (тв.) 1133 1264 1519 1617 1910 2312 2877 1083
Eu 414 (тв.) 468 (тв.) 532 (тв.) 608 (тв.) 702 (тв.) 820 (тв.) 980 (тв.) 1195 1470 1150
f2 Fe*5 1083 (тв.) 1180 (тв.) 1293 (тв.) -231,2 (тв.) 1425 (тв.) -226,6 (тв.) 1586 -221,0 (тв.) 1790 -213,7 2045 -202,6 2376 -188,1 2770 -219,6 1530
Ga 751 833 928 1042 1180 1352 1573 1871 2244 29,7
Gd 506 (тв.) 565 (тв.) 633 (тв.) 713 (тв.) 809 (тв.) 926 (тв.) 1074 (тв.) 1264 (тв.) 1497 1350
Ge 1046 1149 1270 1414 1588 1802 2074 2430 2850 959
H2 H2H 2h2 3h2 He Hf 1887(тв.) 2157 (тв.) -272,5 2354 -266,3 (тв.) -264,0 (тв.) -272,4 2587 -265,2 (тв.) -263,9 (тв.) -262,7 (тв.) -261,4 (тв.) -272,2 2870 -263,6 (тв.) -262,2 (тв.) -260,9 (тв.) -259,6 (тв.) -271,9 3205 -261,4 (тв.) -259,9 (тв.) -258,4 (тв.) -257,1 (тв.) -271,4 3700 -258,1 -256,4 -254,9 (тв.) -252,5 (тв.) -270,5 4440 -252,8 -251,0 -249,6 -248,1 -268,9 5700*6 -259,2 -256,6 -254,4 -252,5 2230
Hg” -26,7 -6,3 17,6 46,9 82,0 126,5 184,0 260,4 356,6 -38,9
h -61,3 (тв.) -46,9 (тв.) -30,2 (тв.) -10,8 12,1 (тв.) 39,4 (тв.) 73,2 (тв.) 115,8 182,8 113,7
In 641 716 805 (тв.) 912 1042 1205 1414 1688 2050 156,2
Ir 1798 (тв.) 1941 (тв.) 2106 (тв.) 2297 (тв.) 2525 2810 3160 3625 4180*8 2443
К 92,4 124,5 162,8 209,7 269 344 446 589 776 63,6
140
Новый справочник химика и технолога
Продолжение табл. 3.3.4
Вещество Температура кипения или возгонки при давлении насыщенного пара тнл, °C
0,00133 Па 0,0133 Па 0,133 Па 1,33 Па 13,3 Па 133 Па 1.33 кПа 13,3 кПа 101.3 кПа
Кг -213,7 (тв.) -206,9 (тв.) -198,3 (тв.) -187,2 (тв.) -172,4 (тв.) -153,4 -157,2
La 1267 1388 1530 1700 1904 2156 2474 2887 3370*9 887
Li 350 402 464 538 629 744 894 1098 1350 180
Lu 857 (тв.) 940 (тв.) 1037 (тв.) 451 (тв.) 1287 (тв.) 1453 (тв.) 1649 (тв.) 1938 2260 1700
Mg 281 (тв.) 325 (тв.) 376 (тв.) 437 (тв.) 510 (тв.) 602 (тв.) 723 892 1103 651
Мп*10 715 (тв.) 787 (тв.) 873 (тв.) 974 (тв.) 1096 (тв.) 1249 1462 1745 2120 1220
Mo 1955 (тв.) 2113 (тв.) 2300 (тв.) 2525 (тв.) 2775 3107 3540 4115 4800 2625
n2 -244,2 (тв.) -241,8 (тв.) -239,0 (тв.) -235,6 (тв.) -232,4 (тв.) -226,1 (тв.) -219,2 (тв.) -209,7 -195,8 -210,0
Na 155 192 236 289 355 439 550 704 900 97,8
Nb 2130 (тв.) 2290 (тв.) 2480 2710 2980 3300 3730 4240 4840*11 2500
Nd 958 (тв.) 1062 1190 1345 1535 1776 2090 2530 3110 1024
Ne -264,0 (тв.) -263,1 (тв.) -262,1 (тв.) -260,7 (тв.) -259,3 (тв.) -257,3 (тв.) -254,7 (тв.) -251.9 (тв.) -246,1 -248,7
Ni 856 (тв.) 934 (тв.) 1023 (тв.) 1123 (тв.) 1255 (тв.) 1408 (тв.) 1600 1850 2140 1453
o2 -239,0 (тв.) -263,1 (тв.) -262,1 (тв.) -260,7 (тв.) -259,3 (тв.) -257,3 (тв.) -254,7 (тв.) -251,0 (тв.) -246,1 -248,7
O3 -212,3 -207,4 -199,5 -194,6 -186,0 -172,1 -157,2 -137,0 -111,9 -251,4
Os 2102 (тв.) 2262 (тв.) 2446 (тв.) 2660 (тв.) 2920 3240 3630 4110 (4610) 2700
P (бел.) P (красн.) P (черн.) Pa -53 (тв.) -35 (тв.) -14 (тв.) 2000 9 (тв.) 2210 38 (тв.) 194 (тв.) 249 (тв.) 2460 75 235,9 (тв.) 290,0 (тв.) 2730 123 287,0 (тв.) 337,5 (тв.) 3080 190 349,2 (тв.) 393,8 (тв.) 3610 275 416,8 (тв.) 452,8 (тв.) 4230 44,1 590 1700
Pb 489 554 630 722 837 981 1171 1431 1751 327,3
Pd 1157 (тв.) 1266 (тв.) 1394 (тв.) 1547(тв.) 1738 1970 2270 2660 3110 1552
Po 206 (тв.) 242 (тв.) 287 343 411 498 612 768 962 252
Pt 1595 (тв.) 1715 (тв.) 1867 2049 2270 2530 2860 3270 3710*12 1769
Pu 1091 1224 1341 1463 1704 1955 2278 2710 3235 639
Ra 365 (тв.) 418 (тв.) 481 (тв.) 559 (тв.) 655 (тв.) 785 (тв.) 961 1206 1536 960
Rb 62 91 127 170 224 295 390 526 705 38,8
Re 2376 (тв.) 2571 (тв.) 2796 (тв.) 3060 (тв.) 3375 3760 4250 4880 5640 3150
Rh Rn 1574 (тв.) 1703 (тв.) 1951 (тв.) -176,2 (тв.) 2030 -165.7 (тв.) 2256 -152,5 (тв.) 2520 -135.6 (тв.) 2840 -113.2 (тв.) 3270 -81.7 (тв.) 3670 -61,9 1960 -71
Ru 1907 (тв.) 2055 (тв.) 2223 (тв.) 2419 (тв.) 2656 2940 3290 3730 (4200) 2430
S*13 37 (тв.) 57 (тв.) 79 (тв.) 104 (тв.) 137 182 243 331 444,6 112,8
Sb Sc 383 (тв.) 427 (тв.) 476 (тв.) 1282 (тв.) 533 (тв.) 1427 600 (тв.) 1597 731 1800 960 2160 1289 2380 1625 2700*14 630,5 1400
Se 144 (тв.) 169 (тв.) 198 (тв.) 231 287 350 428 534 657*15 220,5
Si 1009 (тв.) 1097 (тв.) 1202 (тв.) 1327 (тв.) 1477 1665 1910 2239 2620 1420
Sm 513 (тв.) 573 (тв.) 644 (тв.) 728 (тв.) 830 (тв.) 956 (тв.) 1117 (тв.) 1338 (тв.) 1600 1350
Sn 906 1002 1114 1248 1412 1617 1882 2245 (2720) 231,9
Sr 352 (тв.) 403 (тв.) 462 (тв.) 533 (тв.) 621 (тв.) 733 (тв.) 877 1097 1357 777
Ta 2402 (тв.) 2589 2804 3056 3352 3705 4135 4680 5300 2500
Tc 1930 (тв.) 2090 (тв.) 2270 2500 2800 3100 3500 4100 4700 2140
Те Th 254 (тв.) 289 (тв.) 329 (тв.) 2000 376 (тв.) 2207 432 (тв.) 2457 517 2730 632 3080 1792 3610 1012 4200 452,5 1830
Ti 1336 (тв.)*16 1453 (тв.)*16 1588 (тв.)*16 1748 1946 2191 2490 2833 3170 1725
Физические свойства важнейших веществ
141
Окончание табл. 3.3.4
Вещество Температура кипения или возгонки при давлении насыщенного пара Тп„ °C
0,00133 Па 0,0133 Па 0,133 Па 1,33 Па 13,3 Па 133 Па 1.33 кПа 13.3 кПа 101,3 кПа
Т1 408 463 528 608 706 828 988 1204 1472 303,5
Тт 612 (тв.) 680 (тв.) 752 (тв.) 848 (тв.) 964 (тв.) 2400 1500
и 1444 1581 1741 1933 2166 2456 2824 3205 3860*'7 1133
V 1435 (тв.) 1553 (тв.) 1690 (тв.) 1850 2044 2282 2590 2955 3390 1730
W 2564 (тв.) 2756 (тв.) 2976 (тв.) 3230 (тв.) 3525 3875 4295 4810 5370*18 3380
Хе -196,9 -189,0 -179,7 -168,0 -152,9 -132,9 -108,1 -111,8
(тв.) (тв.) (тв.) (тв.) (тв.) (тв.)
Y 1652 1847 2080 2470 2830 3200*19 1475
Yb 371 (тв.) 422 (тв.) 484 (тв.) 557 (тв.) 647 (тв.) 759 (тв.) 909 1121 1387 824
Zn 212 (тв.) 250 (тв.) 293 (тв.) 345 (тв.) 408 (тв.) 490 596 738 913 419,5
Zr 1836 (тв.) 1992 2174 2390 2645 2955 3335 3810 4225 1852
* ' По другим данным 227 °C.
* 2 По другим данным 1560 °C.
* 3 Р-Модификация.
* 4 По другим данным 2480 °C.
* 5 Ниже 1401 °C —у-модификация. от 1401 °C до температуры плавления — 5-модификация.
* 6 По другим данным 4300 °C.
* 7 См. также табл. 3.3.13 и 3.3.14.
* 8 По другим данным 4500 °C.
* 9 По другим данным 2730 °C.
* '° Ниже 835 °C — a-модификация, от 835 до 1044 °C — ^-модификация, от 1044 °C до температуры плавления — у-модификация.
* 11 По другим данным 5100 °C.
* 12 По другим данным 4120 °C.
* 13 Ниже 95,5 °C — ромбическая сера, от 95,5 °C до температуры плавления — моноклинная сера. См. также табл. 3.3.18.
* 14 По другим данным 2430 °C.
* 15 По другим данным 685 °C.
* 16 Р-Модификация.
* 17 По другим данным 3490 °C.
* 18 По другим данным 5900 °C.
* 19 По другим данным 2780 °C.
Таблица 3.3.5
Температуры кипения или возгонки (°C) простых веществ при давлении пара от 1013 кПа до 5,066 МПа
Вещество Температура кипения или возгонки при давлении насыщенного пара Критиче-с кая температура, °C Критическое давление, МПа
101.3 кПа 202,7 кПа 506,6 кПа 1,013 МПа 2,027 МПа 4,053 МПа 5.066 МПа
Аг -185,9 -178,8 -163,9 -156,4 -143,2 -124 -122,5 4,86
As 612 тв. 646 тв. 698 тв. 742 тв. 790
Вг2 57,9 78,8 110,3 139,8 174,0 216,0 *1 311 12,3
С12 -34,1 -17,7 10,4 35,0 63,6 101,6 109,3*2 144 7,71
н2 -252,8 -250,2 -245,7 -241,6 -239,9 1,3
Н2Н -251,0 -247,9 -243,9 -237,6 -237,2 1,48
Н3Н -249,6 -246,8 -242,6 -238,4 -234,9 1,66
2н2 -249,6 -247,0 -242,2 -238,3 -234,8 1,65
2Н3Н -248,8 -246,3 -241,8 -237,6 -233,7 1,75
’н2 -248,1 -245,7 -241,2 -236,9 -232,6 1,83
Не -268,9 -268,2 -267,9 0,23
Hg’ 356,6 399,1 461,6 519,2 587,4 668,0 *4 -1450
к 776 836 965
Кг -153,4 -143,8 -128,2 -113,7 -96,0 -74,5 -66,7 -63,8 5,5
142
Новый справочник химика и технолога
Окончание табл. 3.3.5
Вещество Температура кипения или возгонки при давлении насыщенного пара Критиче-екая температура, °C Критическое давление. МПа
101,3 кПа 202,7 кПа 506,6 кПа 1,013 МПа 2,027 МПа 4,053 МПа 5,066 МПа
n2 -195,8 -189,3 -179,1 -169,3 -157,3 -147,0 3,39
Na 900 964 1093
Ne -246,1 -243,5 -239,4 -235,5 -230,8 -227,7 2,73
о2 -183,0 -175,8 -164,2 -153,3 -140,1 -124,0 -118,5 -118,4 5,08
Оз -111,9 -101,0 -83,7 -67,8 48,6 -24,8 -15,8 -12,1 5,53
Р (красн.) 416,8 тв. 443,4 тв. 481,9 тв. 513,8 тв. 548,6 тв.
Р (черн.) 452,8 тв. 475,4 тв. 507,6 тв. 533,8 тв. 561,9 тв. 592,0 тв.
Rn -61,9 -45,5 -19,5 5,0 35,7 87,6 104,3 6,32
S 444,6 507,1 643,2 1040 11,8
Хе -108,1 -95,1 -73,9 -54,2 -30,2 -1,0 9,6 16,6 5,90
Zn 913 990 1090 1170 1280 1450
При 6,08 МПа Гкип = 243,5 °C. *2 При 6.08 МПа Гки1| =127,1 °C. *3 См. также табл. 3.3.13 и 3.3.14. *4 При 6.08 МПа ТКИ11 = 723,5 °C.
Неорганические соединения (см. также табл. 3.3.11)
В табл. 3.3.6-3.3.8 вещества расположены в алфавитном порядке химических символов. Соединения дейтерия помещены после соответствующих соединений водорода. Менее достоверные величины заключены в скобки.
Таблица 3.3.6
Температуры кипения или возгонки (°C) неорганических веществ при давлении пара от 1,33 • 10-4 до 1,33 Па
Формула Название Температура кипения или возгонки при давлении насыщенного пара FUJ1, °C
1.33 • КГ4 Па 0.00133 Па 0.0133 Па 0,133 Па 1,33 Па
AgCl Серебра хлорид 431 (тв.) 480 539 607 685 455
А1Вг3 (тв.) А1С13 (тв.) A1F3 (тв.) Алюминия бромид Алюминия хлорид Алюминия фторид 624 665 27,1 710 15,0 42,1 760 33.7 58,9 817 98 192,6
АП3 (тв.) Алюминия иодид 54,0 7U 90,4 112,1 137,1 191
AmF3 (тв.) Америция фторид 885 952 1029 1117 1220
As4O6 (тв.)*1 Мышьяка(Ш) оксид 65,5 83,6 103,8 126,3 151,8 313
ВаО (тв.) (мышьяковистый ангидрид) Бария оксид 1053 1150 1263 1395 1552 1920
ВеО (тв.) СО (тв.) Бериллия оксид Углерода монооксид -244,6 -242,7 1888 -240,4 2045 -237,9 2225 -234,9 -205,1
СО2 (тв.)*2 Углерода диоксид -186,4 -180,7 -174,3 -166,8 -158,0 -57,5
СаО (тв.) CdBr2 (тв.) Кальция оксид Кадмия бромид 1464 232 1582 264 1720 301 343 392 2600 568
CdCl2 (тв.) Кадмия хлорид 266 299 337 380 430 568
Cdl2 (тв.) Кадмия иодид 178 210 247 290 340 387
CdO (тв.) Кадмия оксид 551 603 662 729 809
CdS (тв.) Кадмия сульфид 440 486 615 605 679
СоС12 (тв.) Кобальта(П) хлорид 373 407 445 488 537 740
СгС12 (тв.) Хрома(П) хлорид 466 509 558 613 677 815
СгС12О2 Диоксидохрома ТВ. ТВ. -92,6 -79,1 -63,1 -95
CsBr (тв.) дихлорид (хромил-хлорид) Цезия бромид 355 394 439 490 549 632
Физические свойства важнейших веществ
143
Продолжение табл. 3.3.6
Формула Название Температура кипения или возгонки при давлении насыщенного пара г11Я. °C
1.33 • КГ4 Па 0.00133 Па 0,0133 Па 0,133 Па 1,33 Па
CsCl (тв.) Цезия хлорид (441,9) 497,2 561,7 642
CsI (тв.) Цезия иодид 340 378 421 471 528 621
FeCl3 (тв.) Железа(Ш) хлорид 76,9 92,6 110,0 129,2 150,8 304
GeS (тв.) Германия(П) сульфид 291 334 372 625
GeS2 (тв.) Германия(1У) 406 447 494
сульфид -114,2*3
HCI Водорода хлорид -200,7 (тв.) -196,5 -190,5 -183,5 -75,1
(тв.) (тв.) (тв.)
Н2О (тв.)*4 Вода -111,0 -100,4 -88,4 -74,7 -58,7 0,0
HgBr2 (тв.) Ртути(П) бромид 24,2 46,0 71,3 241
Hg2Br2 (тв.)*5 Ртути(1) бромид (49,0) 72,4 105,9
HgCl2 (тв.) Ртути(П) хлорид 4,0 22,8 44,5 69,7 277
Hg2Cl2 Ртути(1) хлорид 43,4 60,6 80,4 103,2 129,7 543
(тв.)*6 Hgl2 (тв.) Ртути(П) иодид 4,2 21,3 40,8 62,8 89,0 250
КВг (тв.) Калия бромид 387 429 477 532 598 735
КС1 (тв.) Калия хлорид 412 457 506 566 634 770
KF (тв.) Калия фторид 430 476 530 592 665 856
K.I (тв.) Калия иодид 358 397 442 494 553 682
КОН Калия гидроксид 402 459 527 400
KReO4 Калий перренат 491 (тв.) 529 (тв.) 581 550
МоОз (тв.) Молибдена триоксид 441 476 516 561 611 795
NH3 (тв.) Аммиак -180,2 -174,6 -168,4 -161,4 -153,2 -77,8*J
NO (тв.) Азота(П) оксид -216,2 -212,3 -207,8 -202,6 -163,7
N2O (тв.) Азота(1) оксид -192,1 -186,7 -180,6 -173,6 -165,2 -90,8*3
NaBr (тв.) Натрия бромид 402 445 495 552 618 750
NaCl (тв.) Натрия хлорид 442 487 539 599 670 800
NaF (тв.) Натрия фторид 556 606 666 738 820 995
NiCl2 (тв.) Никсля(П) хлорид 382 418 458 503 555 1001
NiO (тв.) Никеля(П) оксид 1133 1217 (1320)
РдОю (тв.) . Фосфора(У) оксид (фосфорный ангидрид (стабильная форма)) 171,9 197,3 225,8 257,9 294,4 565,6
Р40,о (тв.) Фосфора(У) оксид (фосфорный ангидрид (метастабильная фор- 22,5 41,4 62,8 87,3 115,7
ма))
РЬВг2 Свинца(П) бромид 226 (тв.) 256 (тв.) 290 (тв.) 329 (тв.) 377 370
РЫ2 (тв.) Свинца(П) иодид 214 242 275 312 354 412
РЬО (тв.) Свинца(П) оксид 500 549 605 669 745 890
PbS (тв.) Свинца(Н) сульфид 460 505 556 614 681 1114*J
PuBr3 Плутония трибромид 521,2 (тв.) 564 (тв.) 611 (тв.) 664 (тв.) 737 681
РиС13 Плутрония трихлорид 586 (тв.) 633 (тв.) 684 (тв.) 748 (тв.) 830 760
PuF3 (тв.) Плутония трифторид 874 938 1011 1096 1189 1410
Ри!3 (тв.) Плутония трииодид (457) (499) (546) (599) (661) (780)
РиО2 (тв.) Плутония диоксид 1586 1719 1872
RbBr (тв.) Рубидия бромид 377 420 468 524 590 682
RbCl (тв.) Рубидия хлорид 387 429 479 534 603 715
SbCl3 (тв.) Сурьмы трихлорид -39,8 -23,4 -14,3 73
Sb2O3 (тв.)*7 Сурьмы(Ш) оксид 296,9 329,9 367,0 409,0 456,8 655
SeO2 (тв.) Селена диоксид 37,3 55,0 74,9 97,6 123,6 340
Snl4 (тв.) Олова тетраиодид (Ю,2) 31,8 57,1 145
144
Новый справочник химика и технолога
Окончание табл. 3.3.6
Формула Название Температура кипения или возгонки при давлении насыщенного пара Т,.,, °C
1,33 • 10-4 Па 0,00133 Па 0,0133 Па 0.133 Па 1,33 Па
SrO (тв.) ТаВг5 (тв.) Стронция оксид Тантала пентабромид 1307 41,4 1404 57,9 (1514) 76,3 97,1 120,8 2430 267
ТаС15 (тв.) Та15 (тв.) Тантала пентахлорид Тантала пентаиодид 63 84 27,7 109 46,0 138 66,2 172 220,0 496
ТеО2 (тв.) Теллура диоксид 443 486 534 589 652 733
TiCl2 (тв.) TiO (тв.) Титана дихлорид Титана оксид 1328 1426 480 1538 539 1666 609 1811 (677)
TiO2 (тв.) Титана диоксид 1300 1391 1494 1608 1740
Т1Вг (тв.) Таллия(1) бромид 171 200 233 271 315 460
TIC1 (тв.) Таллия(1) хлорид 159 187 220 258 303 427
T1F (тв.) Таллия(1) фторид (160) (187) (219) (255) (297) 327
ТП (тв.) Таллия(1) иодид 166 195 229 268 314 440
UC13 (тв.) Урана трихлорид 554 602 658 724 699 835
UF5 (тв.) Урана пентафторид 177 200,3 227 257 291 400
ui3 Урана трииодид 508 (тв.) 556 (тв.) 611 (тв.) 674 (тв.) 748 (разл.) 680
UO2 (тв.) Урана диоксид 1508 1624 1748 1967 2107 2405
WO3 (тв.) Вольфрама триоксид 864 919 980 1047 1122 1470
ZnBr2 (тв.) (вольфрамовый ангидрид) Цинка бромид 147 175 207 245 288 392
ZnCl2 (тв.) Цинка хлорид 177 211 241 275 315 316
Znl2 (тв.) Цинка иодид 127 155 187 225 270 446
ZnS (тв.) ZrBr4 (тв.) Цинка сульфид Циркония тетрабро- 55 73 779 93 863 116 962 142 450
ZrCl4 (тв.) МИД Циркония тетрахло- 45 62 82 103 128 437
Zr 14 (тв.) рид Циркония тетраиодид 95 115 138 163 192 499
ZrO2 (тв.) Циркония диоксид 1495 1600 1718 1855 2014 (разл.) 2680
*' Орторомбическая модификация.
*2 См. также табл. 3.3.15 и 3.3.16.
Тройная точка.
*4 См. также табл. 3.3.19-3.3.22.
*5 В парах диспропорционирует на HgBr2 и Hg.
*6 В парах диспропорционирует на HgCl2 и Hg.
*7 Кубическая модификация.
Температуры кипения или возгонки (°C) неорганических веществ при давлении пара от 13,3 Па до 101,3 кПа
Таблица 3.3.7
Формула Название Температура кипения или возгонки при давлении насыщенного пара Т,1Л, °C
13,3 Па 133 Па 1,33 кПа 13,3 кПа 101,3 кПа
AgBr Серебра бромид (653) (797) (разл.) (1000) (разл.) (1322) (разл.) (1834) (разл.) 430
AgCI Серебра хлорид 789 914 1075 1294 1559 455
Agl Серебра иодид 697 (разл.) 819 (разл.) 981 (разл.) 1148 (разл.) 1503 (разл.) 557
А1(ВН4)3 Алюминия тетрагидри-доборат(1~) ТВ. ТВ. -43,3 -3,7 44,4 -64,5
А1Вг3 Алюминия бромид 55,6 (тв.) 81,1 (тв.) 118,0 176,1 256,3 98
Физические свойства важнейших веществ
145
Продолжение табл. 3.3.7
Формула Название Температура кипения или возгонки при давлении насыщенного пара М °C
13,3 Па 133 Па 1,33 кПа 13,3 кПа 101,3 кПа
А1С13 (тв.) Алюминия хлорид 77,6 98,7 123,1 151,0 179,7 192,6
A1F3 (тв.) Алюминия фторид 882 956 1043 1146 1256
А113 Алюминия иодид 147,2 (тв.) 177,7 (тв.) 225,0 295,7 387,9 191
AI2O3 Алюминия оксид ТВ. 2146 2380 2666 2980 2040
AsBr3 Мышьяка трибромид (20 (тв.)) (51) 93 152 221 31
AsCl3 Мышьяка трихлорид ТВ. (-6,0) 25,8 70,4 131,3 -16
AsF3 Мышьяка трифторид (-61 (тв.)) М3 (тв.)) -16 (тв.) 12,5 62,2 -5,9
AsF5 Мышьяка пентафторид -131,6 (тв.) -118,7 (тв.) -103,2 (тв.) -84,2 (тв.) -62,9 -80,8
Asl3 Мышьяка трииодид (121 (тв.)) (163) (220) 307 414 142
AsH3 Арсин (арсан) (-157,6 (тв.)) -143,4 (тв.) -125,2 (тв.) -98,1 -62,5 -116,9
As4O6*' Мышьяка(Ш) оксид (мышьяковистый ангидрид) 180,7 (тв.) 213,8 (тв.) 259,6 (тв.) 332,6 457,2 313
BBr3 Бора трибромид ТВ. —41,5 -10,4 33,2 90,9 46
BCI3 Бора трихлорид ТВ. -92,1 -67,7 -33,5 12,4 -107
BF3 Бора трифторид -166,7 (тв.) -155,5 (тв.) -141,6 (тв.) -123,6 -101,0 -128
BI3 B2CI4 Бора трииодид Дибора тетрахлорид (3 (тв.)) (31 (тв.)) -55,6 76,3 -24,8 134,2 16,2 (разл.) 209,5 (65,5 (разл.)) 44
B2H5Br Бромдиборан ТВ. -93,8 -66,5 -29,6 16,0 -104,2
B2H6 В20з (тв.) Диборан(б) Бора оксид ТВ. 1324 -162,5 1489 -145,7 (1694) -122,4 -92,6 -165,6
B4H10 Тстраборан(Ю) -112,2 -91,5 -64,6 -28,6 15,4 -119,9
B5H9 Пентаборан(9) ТВ. ТВ. -31,7 8,7 57,4 —47,0
b52h, (2Н9)Пентаборан(9) ТВ. ТВ. -32,6 8,0 59,0 —47,0
B5Hh Пентаборан(11) -50,7 -20,4 19,4 66,7 -123,3
B|oH]4 Декаборан(14) 36,6 (тв.) 61,0 (тв.) 89,6 (тв.) 141,2 (разл.) 211 (разл.) 99,6
BaCl2 Бария хлорид (985) (1080) (1240) (1505) 1825 960
BaF2 Бария фторид ТВ. 1436 1639 1905 (2224) 1353
Be(BH4)2 (тв.) Бериллия тетрагидри-доборат(1-) (-19) 2,0 27,6 58,4 91,2 123
BeBr2 (тв.)*2 Бериллия бромид (244) 288 340 404 471 488
BeCl2*3 Бериллия хлорид 262,0 (тв.) 303,2 (тв.) 351,4 (тв.) 409,3 481,3 404
BeF2 Бериллия фторид 693 (тв.) 775 (тв.) 880 1013 1159 803
Bel2 (тв.)*4 Бериллия иодид (234) 282 339 410 ж. 480
BeO (тв.) Бериллия оксид (2440) (2690) (3000) (3380) (3830)
BiBr3 Висмута трибромид (182 (тв.)) (222) 380 361 460 218
BiCl3 Висмута трихлорид (167 (тв.)) (207 (тв.)) 264 343 440 229
BrF3 Брома трифторид ТВ. ТВ. 29,2 72,7 125,7 8,8
BrF5 Брома пентафторид -89,3 (тв.) -69,9 (тв.) -39,9 -5,1 40,4 -61,4
CC14 Тетрахл орметан *5 -50,8 (тв.) -20,6 21,8 76,5 -23,0
CNBr Бромциан (-68,5 (тв.)) (-37,0 (тв.)) -10,8 (тв.) 22,1 (тв.) 61,5 52
CNC1 Хлорциан -95,8 (тв.) -77,2 (тв.) -54,2 (тв.) -25,2 (тв.) 12,5 -5
CNF (тв.) Фторциан -149,2 -135,7 -118,9 -97,0 -72,9
CNI (тв.) Иодциан -0,2 25,9 • 57,5 96,6 139,5 146*6
CO Углерода монооксид -231,3 (тв.) -226,9 (тв.) -221,5 (тв.) -205,9 (тв.) -191,6 -205,1
COC12 Фосген -119,8 -99,5 -72,9 -36,7 7,9 -127,8
cof2 Карбонилдифторид (-148,1 (тв.)) -139,9 (тв.) 114,8 (тв.) -83,4 -114,0
COS Карбонилсульфид (углерода сероокись) ТВ. -133,8 -113,9 -86,1 -50,3 -138,8
146
Новый справочник химика и технолога
Продолжение табл. 3.3.7
Формула Название Температура кипения или возгонки при давлении насыщенного пара Г„л, °C
13.3 Па 133 Па 1,33 кПа 13,3 кПа 101,3 кПа
COSe Карбонилселенид (углерода селеноокись) ТВ. (-117,1) (-95,0) -62,3 -21,7 -124,4
С02 (тв.)*7 Углерода диоксид -147,7 -135,2 -119,9 -100,5 -78,5 -57,5
c2N2 Оксалонитрил (дициан) -112,7 (тв.) -95,5 (тв.) -76,6 (тв.) -51,5 (тв.) -21,2 -34
C3O2 Прона-1,2-диен-1,3-дион (углерода недокись) ТВ. -94,8 -71,0 -36,9 6,3 -107
CSSe Углерода селенид-сульфид -71,2 -47,4 -16,1 27,5 85,3 -85
CS2 Углерода дисульфид (сероуглерод) -95,7 -73,8 -44,9 -4,8 46,2 -112,1
CSe2 Углерода диселенид (селеноуглерод) ТВ. -22,0 14,2 62,8 (122) -45,5
CaF2 Кальция фторид 1447 1625 1850 (2145) (2500) 1418
CdBr2 Кадмия бромид 450 (тв.) 519 (тв.) (607) (727) 863 568
CdCl2 Кадмия хлорид 488 (тв.) 558 (тв.) 543 794 968 568
Cdl2 Кадмия иодид 402 487 596 742 918 387
CdO (тв.) Кадмия оксид 883 1003 1153 1342 1559
CdS (тв.) Кадмия сульфид 767 885 1009 1182 1382
C1F Хлора фторид ТВ. -153,5 -139,3 -121,2 -100,8 -155
CIF3 Хлора трифторид ТВ. ТВ. -61,1 -18,7 11,3 -76,3
CIO3F Перхлорилфторид -145,1 -129,8 -109,8 -82,2 46.8 -146
C12O Хлора(1) оксид ТВ. -98,8 -73,3 -39,3 2,0 (разл.) -116
C12O7 Хлора(УП) оксид -71,4 -46,8 -14,6 28,3 79,8 (разл.) -91
CoCl2 Кобальта(П) хлорид 594 (тв.) 660 (тв.) 738 (тв.) 880 1053 740
CrBr3 (тв.) Хрома(П1) бромид 626 693 772 (864) (959) (ИЗО)
Cr(CO)6 (тв.) Гексакарбон и лхром 10,3 35,8 67,9 107,4 150,7 (разл.)
CrCl2 Хрома(П) хлорид 750 (тв.) 842 966 1124 1308 815
СгС13 (тв.) Хрома(Ш) хлорид 618 684 761 852 949 1152
СгО2С12 Диоксидохрома дихлорид -43,5 -19,1 12,8 57,2 116,0 -95
CrO2F2 (тв.) Диоксидохрома дифторид М4,3) -30,9 -14,4 6,0 29,6 31,6*6
CsBr Цезия бромид 642 748 885 1071 1303 632
CsCl Цезия хлорид 638,0 (тв.) 745 882 1068 1301 642
CsF Цезия фторид ТВ. 710 844 1025 1252 682
CsI Цезия иодид 633 737 872 1056 1280 621
CuBr CuCl2 (тв.) Меди(1) бромид Меди(П) хлорид ТВ. 570 714 368 946 435 1357 505 488 630
CuCl Меди(1) хлорид ТВ. 546 702 960 1490 430
Cui Меди(1) иодид ТВ. ТВ. 654 905 1339 588
F2O Кислорода дифторид -205,7 -196,3 -184,0 -166,9 -145,3 -223,9
f2o2 Дикислорода дифторид -155,8 -140,1 -119,7 -91,9 (разл.) -57,4 (разл.) -163,4
Fe(CO)5 Пентакарбонилжелезо ТВ. ТВ. 4,7 50,3 104,9 -21
FeCl2 Железа(П) хлорид (519 (тв.)) (582 (тв.)) 681 828 1012 677
FeCl3 Железа(Ш) хлорид 175 (тв.) 203 (тв.) 230 (тв.) 271 (тв.) 320 304
GaBr3*8 Галлия(Ш) бромид ТВ. ТВ. 140,6 203,8 277,8 122
GaCl3 Галлия(Ш) хлорид 23 (тв.) 48 (тв.) 78 (тв.) 133 204 78
GeBr4 Германия тетрабромид ТВ. ТВ. 56,1 111,3 188,7 26,1
GeCl4 Германия тетрахлорид ТВ. -44,2 -14,4 27,9 85,8 -49,6
GeF4 (тв.) Германия тетрафторид -109 -85 -61 -36 -15
GeH4 Герман ТВ. -163,5 -145,6 -120,8 -89,2 -165
Ge2H4 (2Н4)Герман (дейтерогерман) ТВ. (-161,5) -143,8 -119,5 -89,1 -166,2
Ge2H6 Дигерман -110,0 -88,6 -60,2 -20,5 31,0 109
Физические свойства важнейших веществ
147
Продолжение табл. 3.3.7
Формула Название Температура кипения или возгонки при давлении насыщенного пара r,L1, °C
13,3 Па 133 Па 1,33 кПа 13,3 кПа 101,3 кПа
Ge22H6 (2H6)Дигерман (дейте- (-86,2) -57,8 -19,2 29,1 -107,9
Ge3H8 родигерман) Тригерман -63,8 -37,2 -2,1 47,0 111,1 -105,7
Ge32H8 (2Н8)Тригерман (дейте- (-67,4) (-39,5) -2,7 47,6 110,7 -100,3
GeHCl3 ротригерман) Трихлоргерман -63,0 -41,3 -13,3 25,0 74,3 (разл.) -72,2
Gel4 Германия тетраиодид 93,4 (тв.) 125,6 (тв.) (195) (277) 377 (разл.) 146
GeS HBr Германия(П) сульфид (тв.) Водорода бромид 436 (-153,7 495 -139,7 -121,9 -98,0 (тв.) -66,8 625 -87,0
2HBr (2Н)Водорода бромид (тв.)) (тв.) (-140,4 (тв.) -122,2 -98,3 (тв.) -66,9 -87,5
HCN (дейтерия бромид) Водорода цианид -92,2 (тв.) (тв.)) -72,9 (тв.) (тв.) -49,0 (тв.) -18,6 (тв.) 25,6 -13,З*6
2HCN (2Н)Водорода цианид -91,2 (тв.) -72,0 (тв.) -48,2 (тв.) -18,1 (тв.) 25,9 -12
HC1 (дейтерия цианид) Водорода хлорид -164,9 (тв.) -151,8 -136,1 -114,5 (тв.) -85,1 —114,2*6
2HC1 (2Н)Водорода хлорид (тв.) -153,5 (тв.) -136,8 -113,8 -84,3 -115,О*6
HF (дейтерия хлорид) Водорода фторид ТВ. (тв.) ТВ. (тв.) -66,6 -28,1 19,9 -83,1
2HF (2Н)Водорода фторид ТВ. ТВ. (-69,9) -30,8 18,6
HI (дейтерия фторид) Водорода иодид -136,1 (тв.) -120,1 -99,6 (тв.) -72,0 (тв.) -35,4 -50,8
2HI (2Н)Водорода иодид -136,2 (тв.) (тв.) -120,3 -99,9 (тв.) -73,4 (тв.) -36,2 -51,7*6
HNO3 (дейтерия иодид) Азотная кислота ТВ. (тв.) ТВ. -4,4 34,2 83,8 -41,7
HN3 Водорода азид (азото- ТВ. -72,8 -44,9 -8,1 35,8 -80
HReO4 (тв.) водородная кислота) Рениевая кислота 4,3 40,5 87,4 150,9 (228,8)
HSO3C1 Хлорсульфоновая ки- 32,0 64,0 105,3 151,0 (разл.) -80
HTcO4 (тв.) слота Технециевая кислота (-13,1) 18,6 59,1 112,7 176,5
H2O Вода*9 -39,8 (тв.) -17,4 (тв.) 11,2 51,6 100,0 0,0
H2HO (2Н)Вода ТВ. ТВ. 12,4 52,5 100,7
H2,8O (,8О)Вода (вода тяжело- ТВ. ТВ. 11,3 51,7 100,1
2h2o кислородная) (2Н2)Вода (дидейтерия ТВ. ТВ. 13,1 54,0 101,4 3,8*6
H2O2 оксид) Водорода пероксид ТВ. (15,8) 50,1 95,4 150,0 -0,4
H2S Водорода сульфид -153,6 (тв.) -134,9 -116,5 -92,4 (тв.) -60,2 -85,7
H2SO4 (сероводород) Серная кислота (тв.) 145,8 (тв.) 194,2 257,0 330,0 (разл.) 10,5
H2Se Водорода селенид (-131,5 -108,9 -77,8 (тв.) -41,4 —66
H2SeO3 (тв.) H2SeO4 (тв.) Селенистая кислота Селеновая кислота 11,3 (тв.)) 31,4 (тв.) 40,9 (54,6) 92,0 (81,6) 153,0 (109,4)
H2Te Водорода телланид -114,3 (тв.) -96,8 (тв.) -74,9 (тв.) -45,3 -1,3 -49,0
Hf(BH4)4 Гафния тетрагидридо- -30,5 (тв.) -7,9 (тв.) 19,4 (тв.) 62,5 117,6 29
HfCl4 (та.) борат(1-) Гафния тетрахлорид 171 212 262 315,3 434*6
HgBr2 Ртути(П) бромид 100 (тв.) 137 (тв.) 181 (тв.) 327 (тв.) 321 241
HgCl2 Ртути(П) хлорид 100 (тв.) 135 (тв.) 179 (тв.) 235 (тв.) 305 277
Hgl2 Ртути(П) иодид 119,5 (тв.) 156 (тв.) 203 (тв.) 262 354 250
148
Новый справочник химика и технолога
Продолжение табл. 3.3.7
Формула Название Температура кипения или возгонки при давлении насыщенного пара ТПЯ, °C
13,3 Па 133 Па 1,33 кПа 13,3 кПа 101,3 кПа
HgS (тв.)*'° Hg2Br2 (тв.)*" Ртути(П) сульфид Ртути(1) бромид 142,6 (333) 187,1 (395) 242,2 (484) 312,5 392,5 407
Hg2Cl2 (тв.)*’2 Ртути(1) хлорид 161,1 199,2 246,8 309,0 383,6 543
IBr Иода бромид (-25 (тв.)) (0 (тв.)) (29 (тв.)) (73) 116 36
IC1 Иода хлорид (-40 (тв.)) (-19 (тв.)) 8 (тв.) 46,6 96,7 27,2
if5 Иода пентафторид -35,4 (тв.) -15,2 (тв.) 8,8 (тв.) 51,4 100,5 9,4
IF7 (тв.) Иода гептафторид -107,3 -88,2 -64,0 -32,6 4,1 6
InBr Индия(1) бромид (245) 312 398 502 658 220
InBr2 Индия(П) бромид 298 382 494 630 235
InBr3 (тв.) Индия(Ш) бромид (174) 212 257 312 371 436
InCi Индия(1) хлорид (240) 304 386 496 627 225
1пС12 Индия(П) хлорид (303) 341 485 436 488*13 235
1пС13 (тв.) Индия(1П) хлорид (292) 334 382 438 497 586
Ini Индия(1) иодид ТВ. ТВ. 433 557 710 369
К[А1С14] Калия тетрахлоридо- (435) 528 650 815 1017
KBr алюминат Калия бромид 674 (тв.) 794 939 1137 1386 735
КС1 Калия хлорид 716 (тв.) 819 965 1162 1406 770
KF Калия фторид 750 (тв.) 884 1038 1246 1503 857
KI Калия иодид 623 (тв.) 747 886 1079 1323 682
KOH Калия гидроксид 611 718 860 1060 1326 400
LiBr Лития бромид 640 747 886 1076 1311 552
LiCI Лития хлорид 674 785 934 ИЗО 1380 614
LiF Лития фторид 920 1048 1209 1427 1679 845
Lil Лития иодид 631 724 841 994 1170 446
Li2O (тв.) Лития оксид (869) 955 1056 1175 1298
MgCl2 Магния хлорид ТВ. 729 844 1017 1231 650
MgF2 Магния фторид (1271) (1434) 1641 1917 (2250) 1263
MnCl2 Марганца(Н) хлорид ТВ. 729 844 1017 1231 650
MnFO3 Марганца триоксид- ТВ. ТВ. -27 12 60 -38
Mo(CO)6 (tb.) фторид (фторангидрид марганцовой кислоты) Г ексакарбонилмолиб- (19,3) 45,5 76,9 115,0 156,2 (разл.)
MoO3 ден Молибдена триоксид 662 (тв.) 734 (тв.) 797 954 1155 795
NF3 Азота трифторид ТВ. ТВ. -171,1 -152,7 -129,0 -183,7
nh2oh Г идроксиламин ТВ. ТВ. (47,2) (77,5) (110.0) 34,0
NH3 Аммиак*14 -125,0 (тв.) -110,2 -94,9 (тв.) -67,4 -33,5 -77,8*6
N2H3 (2Н3)Аммиак (дейтеро- -122,3 (тв.) (тв.) -107,4 -89,3 (тв.) -64,8 -31,1 -74,0
NH4Br (tb.)*15 аммиак) Аммония бромид (тв.) (189,6) (248,6) 319,6 394,3 442
NH4CN (tb.) Аммония цианид -50,6 -28,6 -0,5 31,7 36
NH4C1 (tb.)*15 Аммония хлорид (160) (206,8) 270,6 337,6 (разл.) 520
NH4I (tb.)*15 Аммония иодид (219,7) (268,7) 331,4 404,7 541
NH4N3 (tb.) Аммония азид 4,9 29,5 58,8 94,4 132,8
nh4hs NO Аммония гидросульфид Азота(П) оксид -195,2 (тв.) -51,3 -187,6 -28,7 -178,3 0,0 -166,5 (тв.) 33,3 151,8 -163,7
NOCI Нитрозилхлорид (-113,1 (тв.) -96,0 (тв.) (тв.) -74,9 (тв.) -44,7 -4,4 -59,6
NOF Нитрозилфторид (тв.)) ТВ. (-131,3) -114,4 -91,2 -60,0 -132,5
NO2*16 Азота(1У) оксид -71,7 (тв.) -56,1 (тв.) -37,1 (тв.) -15,0 (тв.) 20,7 -П,2
no2f Нитроилфторид -156,0 -142,9 -126,0 -102,8 -72,6 -166,0
Физические свойства важнейших веществ
149
Продолжение табл. 3.3.7
Формула Название Температура кипения или возгонки при давлении насыщенного пара ТШ1, °C
13,3 Па 133 Па 1,33 кПа 13,3 кПа 101,3 кПа
N2H4 Гидразин ТВ. ТВ. 18,9 61,8 113,6 0,7
n2o Азота(1) оксид (азота -155,4 (тв.) -143,6 -129,1 -110,4 (тв.) -88,5 -90,8*6
N2O5 (тв.) закись, веселящий газ) Азота(У) оксид (азот- -54,4 (тв.) -37,5 (тв.) -18,5 7,8 32,3
NaBr ный ангидрид) Натрия бромид 697 (тв.) 805 950 1147 1392 750
NaCN Натрия цианид 687,3 816 984 1216 1497 562
NaCl Натрия хлорид 752 (тв.) 863 1014 1216 1467 800
NaF Натрия фторид 916 (тв.) 1075 1238 1452 1705 995
Nal Натрия иодид 597 (тв.) 768 903 1083 1304 662
NaOH Натрия гидроксид 618 738 896 1111 1378 320
NbCI4 (тв.) Ниобия тетрахлорид (244) 286 335 394 (456)*17
NbCl5 Ниобия пентахлорид (76,1 (тв.)) (106,5 142,6 (тв.) 186,3 (тв.) 250 204,7
NbF5 Ниобия пентафторид 45,0 (тв.) (тв.)) 67,1 (тв.) 103,8 163,0 233,0 78,9*6
NiBr2 (тв.) Никеля(П) бромид 587 653 730 822 919 963
NiCl2 (тв.) Никеля(П) хлорид 620 684 767 865 970 1001
OsO4 Осмия(УШ) оксид (а) -30,7 (тв.) -5,5 (тв.) 25,5 (тв.) 75,1 129,5 39,5
OsO4 Осмия(УШ) оксид (Р) -20,7 (тв.) 2,9 (тв.) 31,3 (тв.) 75,1 129,5 41,0
PBr3 Фосфора трибромид (2,5) 44,7 102,3 173,3 -40
PC13 Фосфора трихлорид -74,8 -51,8 -21,5 20,6 75,1 -91
PC15 (тв.) PF3 Фосфора пентахлорид Фосфора трифторид ТВ. ТВ. (77,8) -150,3 116,8 -128,2 158,9 -101,1 160,0 -151,3
pf5 Фосфора пентафторид (-136,4 -122,8 -106,3 (тв.) -84,5 -93,8
ph3 Фосфин (фосфан) (-172,1 (тв.)) (-159,3 (тв.) -142,7 -119,2 -87,8 -133,8
PH4Br (тв.) PH4C1 (тв.) Фосфания бромид Фосфания хлорид (тв.)) (тв.)) -43,7 -91,0 (тв.) -21,2 -74,0 7,4 -62,0 38,3 (разл.) -27,0 28,5
PH4I (ТВ.) PI3 Фосфания иодид Фосфора трииодид ТВ. -25,2 ТВ. -1,1 82 29,3 147 62,3 (227) 61,5
POC13 Фосфорилтрихлорид ТВ. ТВ. (2) 46,5 104,5 1,2
POF3 (тв.) (фосфора хлороксись) Фосфорил трифторид (-98,7) -81,9 -61,5 -39,6 -39, I*6
PSBr3 (фосфора фторокись) Тиофосфорилтрибро- ТВ. 50,0 83,6 126,3 175,0 38
Р40б МИД Фосфора(Ш) оксид ТВ. ТВ. 52,9 107,7 173,7 23,8
P4O10 (фосфористый ангидрид) Фосфора(У) оксид 331,5 (тв.) 381,5 (тв.) 440,4 (тв.) 510,9 (тв.) 603,1 565,б*6
P4Ojo (тв.) (фосфорный ангидрид (стабильная форма)) Фосфора(У) оксид 150,8 190,1 237,4 295,5 358,9
PbBr2 (фосфорный ангидрид (метастабильная форма)) Свинца(П) бромид 438 514 613 748 918 370
PbCl2 Свинца(П) хлорид 474 (тв.) 549 650 786 956 498
PbF2 Свинца(Н) фторид ТВ. ТВ. 904 1080 1297 824
Pbl2 Свинца(П) иодид 404 (тв.) 479 571 700 868 412
PbO Свинца(П) оксид 834 (тв.) 944 1085 1265 1473 890
PbS Свинца(П) сульфид 755 (тв.) 853 (тв.) 967 (тв.) 1108 (тв.) 1281 1114*6
PuBr3 Плутония трибромид 828 944 1087 1283 1531 681
150
Новый справочник химика и технолога
Продолжение табл. 3.3.7
Формула Название Температура кипения или возгонки при давлении насыщенного пара Ди, °C
13,3 Па 133 Па 1,33 кПа 13,3 кПа 101,3 кПа
РиС13 Плутония трихлорид 937 1070 1241 1476 1772 760
PuF3 Плутония трифторид 1304 (тв.) 1436 1629 1884 2196 1410
PuF6 Плутония гексафторид (-50,1 (тв.)) -30,9 (тв.) -7,4 (тв.) 20,8 (тв.) 62,3 54
Pul3 Плутония трииодид (733 (тв.)) 832 (970) (1156) (1390) (780)
RbBr Рубидия бромид 668 (тв.) 777 919 1112 1352 682
RbCl Рубидия хлорид 685 (тв.) 791 936 1134 1380 715
RbF Рубидия фторид ТВ. 827 972 1168 1409 775
Rbl Рубидия иодид 643 749 887 1073 1306 638
ReCl3 Рения трихлорид (135 (тв.)) (162 (тв.)) (202 (тв.)) (247 (тв.)) (327) 257
ReF4O Рения оксидтетрафторид (-46,4 (тв.)) -18,6 (тв.) 17,0 (тв.) 62,7 39,7
ReF6 Re2O8 (tb.) Рения гексафторид Рения(УШ) оксид -5,1 (-43,6 (тв.)) 43,8 -21,3 (тв.) 114,5 5,1 (тв.) 47,6 18,8 145*6
Re2O7 Рения(УП) оксид (рениевый ангидрид) 184,0 (тв.) 214,5 (тв.) 249,3 (тв.) 289,4 (тв.) 360,1 300
RuF5 Рутения пентафторид (60 (тв.)) (87 (тв.)) 134 (197) 272 101
SCI2 Серы дихлорид ТВ. -64 -33 9 60 -78
SF6 (тв.) Серы гексафторид -158,9 -141,1 -119,1 -92,2 -64,0 -50,0
SOC12 Т ионилдихлорид -81,3 -56,2 -23,6 20,6 74,8 -104,5
sof2 Т ионилдифторид ТВ. ТВ. -103,8 -77,1 -44,0 -129,5
so2 Серы диоксид -111,6 (ТВ.) -96,2 (тв.) -77,4 (тв.) -47,9 -10,1 -75,5*6
SO2C12 Сульфурилдихлорид ТВ. ТВ. -24,7 17,9 69,5 -54,1
so3 Серы триоксид (а-модификация) -57,8 (тв.) -38,9 (тв.) -16,5 (тв.) 10,7 (тв.) 44,9 17
so3 Серы триоксид (0-модификация) -52,5 (тв.) -34,1 (тв.) -12,3 (тв.) 13,9 (тв.) 44,9 32,3
SO3 (тв.) Серы триоксид (у-модификация) -32,7 -15,5 4,3 27,4 51,1 62,1
S2C12 Дисеры дихлорид -34,7 -8,2 26,5 74,3 136,8 -75
S2F10 Дисеры декафторид ТВ. (-80,7) -53,1 -16,1 28,6 94
SbBr3 Сурьмы трибромид (61 (ТВ.)) (92 (тв.)) (141) (208) 288 97
SbBr5 Сурьмы пентабромид 93,9 (тв.) 138,5 201,5 275,5 96,6
SbCl3 Сурьмы трихлорид 18,1 (тв.) 45,0 (тв.) 85,4 143,0 218,6 73
SbCl5 Сурьмы пентахлорид (-8 (тв.)) 22,2 61,2 112,2 (разл.) (разл.) 2,8
SbF5 Сурьмы пентафторид ТВ. ТВ. 39,2 (86,8) (142,6) 8,3
Sbl3 Сурьмы трииодид 163,6 (тв.) 223,3 302,8 397,2 167
Sb2O3*18 Сурьмы(Ш) оксид 512 (тв.) 577 (тв.) 660 953 1423 655
ScBr3 (тв.) Скандия трибромид (689) 761 844 930 960
ScCl3 Скандия трихлорид (715 (тв.)) 789 (тв.) 875 (тв.) 967 960
Scl3 (tb.) Скандия трииодид (669) 741 824 909 945
SeCl4 (tb.)*19 Селена тетрахлорид (7U) 105,5 146,6 191,1 305
SeF4 Селена тетрафторид ТВ. -12,9 17,9 57,0 101,3 -13
SeF6 (tb.) Селена гексафторид -134,1 -118,6 -99,2 -74,3 -45,7 -34,7
SeOCl2 Селенинилдихлорид 34,8 71,9 118,0 168,0 8,5
SeO2 (tb.) Селена диоксид 154,9 188,9 231,0 282,1 337,3 340
SiBr4 Т етрабромсилан ТВ. ТВ. 30,4 85,1 152,9 5,2
SiCl4 Тетрахлорсилан ТВ. -63,4 -34,6 5,3 57,3 -68,8
SiF4 (tb.) Т етрафторсилан -155,7 -144,4 -130,6 -113,7 -95,0
SiHBr3 Трибромсилан -61,8 -34,0 2,2 51,3 111,7 -73,5
SiHCl3 Трихлорсилан -101,3 -80,7 -53,8 -16,5 31,5 -126,6
SiHF3 Трифторсилан -152,0 (тв.) -138,2 (тв.) -118,7 -95,0 -131,4
SiH3SCN Т иоцианатосилан ТВ. -39,4 -7,5 (34,4) 84,0 -51,8
SiH2Br2 Дибромсилан ТВ. -59,3 -27,6 16,6 74,1 -70,1
Физические свойства важнейших веществ
151
Продолжение табл. 3.3.7
Формула Название Температура кипения или возгонки при давлении насыщенного пара тпл, °C
13,3 Па 133 Па 1,33 кПа 13,3 кПа 101,3 кПа
SiH2F2 Дифторсилан -146,7 -130,4 -107,3 -77,8 -122,0
(тв.) (тв.)
SiH2I2 Дииодсилан ТВ. ТВ. 18,0 79,4 149,5 -1,0
SiH3Br Бромсилан ТВ. ТВ. -77,5 -42,6 1,8 -93,8
SiH3CN Цианосилан (-40,3 -16,9 (тв.) 11,7 (тв.) 496 32,4
(тв.))
SiH3Cl Хлорсилан -117,8 -97,7 -68,5 -30,4
SiH3F Фторсилан -152,7 -141,2 -122,4 -98,0
SiH3I Иодсилан ТВ. ТВ. -43,7 -5,0 45,4 -57,0
SiH4 Силан ТВ. -175,5 -160,4 -139,3 -111,2 -185
Si2H4 (2Н4)Силан (дейтероси- ТВ. -175,2 -160,2 -139,3 -111,4
лан)
Sil4 Тетраиодсилан ТВ. ТВ. 141,8 211,3 301,5 121
SiO2 Кремния диоксид 1732 1969 2227 1710
Si2Cl6 Г ексахлордисилан ТВ. 2,5 38,2 84,6 138,6 -1
Si2Cl6O Г ексахлордисилоксан -30,8 -5,2 28,3 74,5 135,4 -33
Si2F6 (tb.) Г ексафтордисилан -96,0 -81,0 -63,2 -41,9 -19,1 -18,6
Si2H6 Дисилан ТВ. -111,3 -88,4 -56,5 -14,2 -132,6
Si22H6 (2Н6) Дисил ан (дейтеро- ТВ. -111,4 -88,8 -57,3 -15,4
дисилан)
Si2H6O Дисилоксан -30,8 -5,2 28,3 74,5 135,4 -33
Si3Cl8 Октахлортрисилан 12,3 46,1 88,9 145,1 211,2
Si3H8 Трисилан -91,1 -68,6 -39,1 1,6 53,0 -117
Si3H9N 2-Силилдисилазан -90,6 -69,0 -40,7 -1,8 48,6 -105,6
Si4H]o Тетрасилан -28 4 46,3 99,8 -93,6
SnBr2 Олова дибромид 284 343 413 516 636 232
SnBr4 Олова тетрабромид 5,7 (тв.) 32,8 75,2 135,4 217,3 30
SnCl2 Олова дихлорид 257 319 398 509 649 247
SnCl4 Олова тетрахлорид ТВ. -22,5 10,1 55,1 113,7 -33
SnH4 Станнан ТВ. -140,1 -118,8 -89,5 -52,6 -149,9
Snl2 Олова дииодид ТВ. 388 468 576 712 320
Snl4 Олова тетраиодид 87 (тв.) 123 (тв.) 181 262 361 (разл.) 145
SnO (tb.) Олова монооксид 682 804 962 1174 1431
SrF2 Стронция фторид (U21) 1600 1827 2128 (2493) 1400
SrO (tb.) Стронция оксид 2068 2262 2430
TaBr5 Тантала пентабромид (143,1 (тв.)) 176,2 (тв.) 215,1 (тв.) 261,3 (тв.) 344,0 267
TaCl5 Тантала пентахлорид 89,9 (тв.) 117,6 (тв.) 150,5 (тв.) 190,4 (тв.) 239,7 220,0
TaF5 Тантала пентафторид 80,0 (тв.) 103,5 161,2 229,0 95,1
Tal5 Тантала пентаиодид 213 (тв.) 265 (тв.) 331 (тв.) 420 (тв.) 544 496
Tc2O7 Технеция(УП) оксид (технециевый ангидрид) 100,5 (тв.) 123,6 173,2 237,0 310,5 118,4
TeCl4 Теллура тетрахлорид ТВ. ТВ. 234 304 391,3 224
TeF4 Теллура тетрафторид 41,3 (тв.) 75,9 (тв.) 119,0 (тв.) 217,6*20 374,3*20 129,6
TeF6 (tb.) Теллура гексафторид -128,4 -112,6 -92,4 -67,7 -38,9 -37,8
TeO2 Теллура диоксид 731 (тв.) 830 949 1097 1261 733
ThBr4 Тория тетрабромид (548 (тв.)) 624 (тв.) 726 857 679
ThCl4 Тория тетрахлорид (629 (тв.)) 697 (тв.) 781 920 770
Thl4 Тория тетраиодид ТВ. ТВ. 579 699 837 566
TiBr4 Титана тетрабромид 16,1 (тв.) 44,9 89,7 149,1 220,1 38
TiCl2 Титана дихлорид (693) (803) (841) (1120) (1330) (677)
TiCl3 (tb.)*21 Титана трихлорид 588 661 (737)
TiCl4 Титана тетрахлорид ТВ. -13,2 22,5 73,3 138,1 -23
TiF4 (tb.) Титана тетрафторид (174) (227) 284 (427)
Til4 Титана тетраиодид ТВ. ТВ. 191,1 274,4 377,1 150
TIBr ТаллияЦ) бромид 367 (тв.) 433 (тв.) 520 652 819 460
152
Новый справочник химика и технолога
Окончание табл. 3.3.7
Формула Название Температура кипения или возгонки при давлении насыщенного пара Г,., °C
13,3 Па 133 Па 1,33 кПа 13,3 кПа 101,3 кПа
Т1С1 Таллия(1) хлорид 357 (тв.) 422 (тв.) 515 645 805 427
T1F Таллия(1) фторид (346) (404) (474) (560) (655) 327
ТН Таллия(1) иодид 369 (тв.) 436 (тв.) 533 662 824 440
UBr3 Урана трибромид 840 977 1127 1332 (1586)
UBr4 Урана тетрабромид 428 (тв.) 476 (тв.) 538 643 761 519
UC13 Урана трихлорид 895 1023 1202 (1448) (1778) 835
UC14 Урана тетрахлорид 457 (тв.) 512 (тв.) 577 (тв.) 645 761 590
UC15 Урана пентахлорид (220 (тв.)) (262 (тв.)) (308 (тв.)) (374) (468) (330)
UC16 (ТВ.) Урана гексахлорид 73 104 142 ж. ж. 177 (разл.)
UF3 Урана трифторид (1294 (тв.)) (1447) (1657) (1944) (2307) 1427
uf4 Урана тетрафторид 872 (тв.) 973 1089 1243 1418 960
uf5 Урана пентафторид ТВ. ТВ. (463) (565) (696) 400 (разл.)
UF6 (тв.) Урана гексафторид -50,1 -30,2 -6,2 23,6 56,6 64,9*6
UI3 Урана трииодид (843) (974) (1148) 1402 1755 680
UI4 Урана тетраиодид 428 (тв.) 476 (тв.) 540 642 762 506
VC14 Ванадия тетрахлорид ТВ. -9,6 30,4 84,8 151,9 -25,7
VOC13 Оксидованадия трихлорид (ванадилхлорид) -52,4 -23,7 13,5 63,8 125,3 -78,9
W(CO)6 (тв.) Г ексакарбонилвольф-рам (36,0) 62,8 94,8 133,4 174,9 (разл.)
WC15 Вольфрама пентахлорид (114(тв.)) (160 (тв.)) (217 (тв.)) 286 230
WC16*22 Вольфрама гексахлорид 117,4 (тв.) 153,7 (тв.) 197,6 (тв.) 255,7 (тв.) 336,4 284
WF6 Вольфрама гексафторид -89,4 (тв.) -71,7 (тв.) -49,2 (тв.) -21,1 (тв.) 17,7 -0,5
WO3 (ТВ.) Вольфрама триоксид 1206 1301 1408 ж. ж. 1470
ZnBr2 Цинка бромид 340 (тв.) (385 (тв.)) (463) (574) 702 392
ZnCl2 Цинка хлорид 361 427 507 611 733 316
ZnF2 Цинка фторид (777 (тв.)) 922 1070 1266 1507 872
Znl2 ZnS (тв.) Цинка иодид Цинка сульфид 323 (тв.) 1080 390 (тв.) 1223 (487) (602) 730 446
Zr(BH4)4 Циркония тетрагидри-доборат(1-) -22,9 (тв.) 0,0 (тв.) 27,5 (тв.) 64,8 122,6 28,7
ZrBr4 (тв.) Циркония тетрабромид 172 208 250 301 357 450
ZrCl4 (тв.) Циркония тетрахлорид 157 189 230 279 331 437
ZrF4 (тв.) Циркония тетрафторид 586,3 651 725 813 903 (930)
Zrl4 (тв.) Циркония тетраиодид 226 265 312 369 431 499 (разл.)
* ' Ниже 233 °C — орторомбическая модификация, от 233 до 313 °C — моноклинная модификация.
* 2 В парах ВеВг2 + Ве2Вг4.
* 3 В парах ВеС12 + Ве2С14.
* 4 В парах Ве12 + Ве214.
* 5 Другие галогенпроизводные метана см. в табл. 3.3.9.
* 6 Тройная точка.
* 7 См. также табл. 3.3.15 и 3.3.16.
* 8 Пар состоит из GaBr3 + GaBr4 + Br2.
* 9 См. также табл. 3.3.19-3.3.22.
* 10 Ниже 386 °C — красная модификация, выше 386 °C — черная модификация.
* и В парах диспропорционирует на HgBr2 и Hg.
* 12 В парах диспропорционирует на HgCl2 и Hg.
* 13 Отчасти диспропорционирует на InCi и 1пС13
* 14 См. также табл. 3.3.17.
* 15 Пар состоит из NH3 и соответствующего галогеноводорода.
* 16 В парах NO2 + N2O4; при Т < -50 °C давлением NO2 можно пренебречь.
* 17 Выше 420 °C неустойчив.
* 18 Ниже 569 °C — кубическая модификация, от 569 до 655 °C — орторомбическая модификация.
Физические свойства важнейших веществ
153
* 19 В парах диссоциирует на SeCl2 и С12.
* 20 Выше 194 °C диспропорционирует.
* 21 В парах TiCl3 + Ti2Cl6.
* 22 Ниже 226,9 °C — a-модификация, от 226,9 до 284 °C — р-модификация.
Таблица 3.3.8
Температуры кипения или возгонки (°C) неорганических веществ при давлении пара выше 101,3 кПа
Формула Название Температура кипения или возгонки при давлении насыщенного пара Критическая температура,^ Критическое давление, МПа
101,3 кПа 202,7 кПа 506,6 кПа 1,01 МПа 2.03 МПа 4,05 МПа 6,08 МПа
AsH3 ВС13 BF3 Арсин (арсан) Бора трихлорид Бора трифторид -62,5 12,4 -101,0 -40 33,2 -87,8 -17 66,0 -71,1 4 96,7 -56,2 135,4 -39,0 -18,9 178,8 -12,3 3,87 4,99
В2Н6 СС14*’ Диборан(б) Т етрахлорметан -92,6 76,5 -73,3 102,0 -57,8 141,7 -37,4 178,0 -11,9 222,0 276,0 16,5 283,2 3,69 4,56
со cos Углерода монооксид Карбонилсульфид -191,6 -50,3 -184,9 -33 -174,4 -4 -164,0 20 -151,6 49 85 103 140,3 105 3,50 6,18
СО2*2 (углерода серо-окись) Углерода диоксид -78,5 (тв.) -69,8 -57,0 -39,8 -19,1 5,9 22,9 31,0 7,39
cs2 Углерода дисуль- 46,2 (тв.) 69,1 104,8 136,3 175,5 222,8 256,0 279 7,90
c2n2 фид (сероуглерод) Оксалонитрил -21,2 -4,4 21,4 44,6 72,6 106,5 126,6 5,90
C1O3F (дициан) Перхлорил фторид -46,8 -30,6 -5,0 18,2 45,9 79,4 95,2 5,37
GeCl4 HBr Германия тетрахлорид Водорода бромид 85,8 -66,8 120 -51,5 147 -29,1 202 -8,4 242 16,8 48,1 76,6 276,9 90,0 3,85 8,51
HCN Водорода цианид 25,6 44,5 75,7 104,5 142,1 169,9 183,5 5,39
HC1 Водорода хлорид -85,1 -71,4 -50,5 -31,7 -8,8 17,8 36,2 51,4 8,26
HF HI Водорода фторид Водорода иодид 19,5 -35,4 40,1 -18,9 70,4 7,3 98,3 32,0 62,2 100,7 127,5 188 151,0 6,93 8,31
H2O*3 Вода 100,0 120,1 152,4 180,5 213,1 251,1 276,5 374,2 22,1
H2HO 2H2O (2Н)Вода (2Н2)Вода (дидей- 100,7 101,4 120,5 120,9 152,7 153,0 180,7 180,8 213,1 213,2 251,1 251,1 273,4 370,9 22,1
H2O2 H2S терия оксид) Водорода пероксид Водорода сульфид 150,0 -60,2 173,5 -45,9 208,3 -22,3 240,7 -0,4 25,5 55,8 76,3 100,4 9,01
H2Se (сероводород) Водорода селенид -41,4 -25,2 0,0 23,4 50,8 84,0 108,7 137 9,22
NH3 Аммиак -33,5 -18,7 4,7 25,7 50,1 78,9 98,3 132,4 11,3
NO Азота(П) оксид -151,8 -145,1 -135,8 -127,1 -117,0 -104,8 -96,4 -92,9 6,55
no2*4 Азота(1У) оксид 20,7 37,3 59,8 79,4 100,3 121,4 132,2 158 10,0
n2h4 Гидразин 113,6 131 157 182 227 272 302 380 14,7
n2o Азота(1) оксид -88,5 -74,7 -54,5 -36,4 -14,9 10,8 28,3 36,5 7,27
PF3 (азота закись, веселящий газ) Фосфора трифто- -101,1 -82 -62 -46 -28 -10 -10 4,05
PH3 рид Фосфин (фосфан) -87,8 -69 -43 -19 7 33 50 51,3 6,54
SF6 so2 Серы гексафторид Серы диоксид -64,0 -10,1 (-53,2) 6,3 (-29,4) 32,1 -7,7 55,5 18,1 83,8 118,0 141,7 45,6 157,5 3,76 7,88
so3 Серы триоксид 44,9 57,9 77,9 94,7 113,2 133,6 146,6 218,2 8,49
154
Новый справочник химика и технолога
Окончание табл. 3.3.8
Формула Название Температура кипения или возгонки при давлении насыщенного пара Кри-тиче-ская температура,^ Критическое давление, МПа
101,3 кПа 202,7 кПа 506,6 кПа 1,01 МПа 2.03 МПа 4,05 МПа 6,08 МПа
SiH4 Силан -111,2 -97 -75 -57 -34 -И 3,5 4,84
SnCl4 Олова тетрахлорид 113,7 141,3 184,3 223,0 270,0 318,7 3,75
UF6 Урана гексафторид 56,6 (тв.) 74,4 107,9 139,6 222,6 230,2 4,61
*’ Другие галогенпроизводные метана см. табл. 3.3.10.
*2 См. также табл. 3.3.15 и 3.3.16.
*3 См. также табл. 3.3.19-3.3.22.
*4 В парах NO2 + N2O4.
Органические соединения (см. также табл. 3.3.12)
В табл. 3.3.9 соединения расположены по эмпирическим формулам в порядке возрастания числа атомов углерода, а при одинаковом числе атомов углерода — в порядке возрастания числа атомов водорода. Остальные элементы в эмпирических формулах размещены по системе Хилла. Эмпирические формулы с одинаковым числом атомов углерода и водорода расположены в порядке возрастания числа атомов каждого элемента с соблюдением указанной выше последовательности элементов. Численные значения, помеченные звездочкой, расшифрованы в конце табл. 3.3.9.
Таблица 3.3.9
Температуры кипения или возгонки органических веществ при давлении пара от 0,133 до 101,3 кПа
Пояснение. Для ряда веществ в графе «5,33 кПа» в скобках указано давление (4,00 кПа); это означает, что приведенная здесь температура соответствует давлению насыщенного пара 4,00 кПа.
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Д,л, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
Ci
СВгС13 Бром(трихлор)ме-тан -31,5 (тв.) 0,6 20 (4,00 кПа) 45,9 104,7 -5,7
CBrF3 Бром(трифтор)ме-тан -143,7 -122,6 -106,4 -93,7 -70,6 -57,9 -174,5
CBr2F2 Дибром(ди-фтор)метан -88,7 -61,8 -41,0 -24,5 5,8 22,8
CBr4 Т етрабромметан 29,1 (тв.) 67,9 (тв.) 96,3 119,7 163,5 189,5 90,1
CC1F3 Трифтор-(хлор)метан (фреон-13) -149,5 -134,1 -121,9 -111,7 -92,7 -81,2 -181
CC12F2 CC12O Дифтор(ди-хлор)метан (фреон-12) Карбонилдихлорид (фосген) -118,5 -99,5 -97,8 -72,9 -81,6 -68,6 -36,7 -43,9 -29,8 7,9 -160 -118
CC13F Фтор(трихлор)ме-тан (фреон-11) -84,3 -59,0 -39,0 -23,0 6,8 23,7 -111
CC13NO2 Нитро(трихлор)-метан (хлорпикрин) -25,5 7,8 33,8 53,8 91,8 111,9 -64
CC14 Т етрахлор метан -50,8 (тв.) -20,6 -2,3 (4,00 кПа) 21,8 76,5 -23,0
cf4 Т етрафторм етан -184,6 (тв.) -169,3 -158,8 -150,7 -135,5 -127,7
Физические свойства важнейших веществ
155
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Гпл, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
cn4o8 Тетранитрометан 22,7 48,4 68,9 105,9 125,7 13
СНВг3 Триброммстан (бромоформ) 34,0 63,6 85,9 127,9 150,5 8,5
CHC1F2 Ди- -122,8 -103,7 -88,6 -76,4 -53,6 -40,8 -160
фтор(хлор)метан
(фреон-22)
chci2f Фтор(дихлор)ме- -91,3 -67,5 48,8 -33,9 -6,2 8,9 -135
тан (фреон-21)
СНС13 Трихлорметан -58,9 -30,4 -13,1 9,8 42,7 61,7 -63,6
(хлороформ) (4,00 кПа)
CHF3 Трифторметан -156,9 -138,7 -113,7 -82,4
(фреон-23, фтороформ)
CH2BrCl Бром(хлор)метан -46,7 -20,7 0,1 17,0 49,4 68,1 -87,9
CH2Br2 Дибромметан -35,1 -2,4 23,3 42,3 79,0 98,6 -52,8
CH2C12 Дихлорметан -70,5 44,1 -28,2 (4,00 кПа) -7,3 24,1 39,8 -95,1
CH2O Формальдегид (муравьиный -91,0 -70,6 -57,3 -33,0 -19,5 -92
альдегид)
CH2O2 Муравьиная ки- -20,0 (тв.) 2,1 (тв.) 24,0 43,8 80,3 100,6 8,2
слота
CH3AsC12 Метиларсони-стый дихлорид -1U 24,3 73,0 134,5
CH3AsF2 Метиларсони-стый дифторид -42,3 -12,3 27,9 76,1
CH3Br Бромметан -96,6 (тв.) -72,8 -54,2 -39,4 -11,9 3,6 -94,1
CH3C1 Хлорметан -93,0 -80,0 (4,00 кПа) -62,9 -38,0 -24,2 -97,7
CH3Cl3Si Метил(трихлор)- -27,3 -4,6 13,5 47,3 66,4 -90
силан
CH3F Фторметан -149,6 -132,5 -122,2 (4,00 кПа) -108,7 -89,5 -78,3
CH3I Иодметан 45,8 -24,2 -7,0 25,3 42,4 -64,4
CH3NO Формамид 70,5 109,5 137,5 157,5 193,5 210,5 (разл.)
CH3NO2 Нитрометан -29,0 2,8 27,5 46,6 82,0 101,2 -29
CH4 Метан -206 (тв.) -195,4 187,7 -181,5 -168,8 -161,6 -182,5
(тв.) (тв.)
CH4ClFSi Метил(фтор)-(хлор)силан -102,7 -76,9 -41,9
CH4Cl2Si Метил(дихлор)- -75,0 -47,8 -26,2 -9,0 23,7 41,9
силан
CH4O Метанол -44,0 -16,2 5,0 21,2 49,9 64,7 -97,8
CH4O2 Мети л гидро- -5,0 35,9 85,4
пероксид
CH4S Метантиол -90,7 -67,5 -49,2 -34,8 -7,9 6,8 -123,0
CH5ClSi Метил(хлор)- -95,0 -71,0 -51,7 -36,4 -7,8 8,7
силан
CH5N Метанамин -95,8 (тв.) -73,8 -56,9 -43,7 -19,7 -6,3 -93,5
ch5no А-Метилгидро- 0,9 31,3 15,0
ксиламин
ch5no О-Метилгидро- -59,8 -32,6 3,4 48,1
ксиламин
156
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Т °C
0,133 кПа 1,33 кПа 5,33 кПа 13.3 кПа 53,3 кПа 101.3 кПа
ch6n2o2 CH6Si CH9NSi2 Карбамат аммония Метилсилан 2-Метилди-силазан -26,1 (тв.) -138,5 -76,3 -2,9 (тв.) -120,0 -50,1 14,0 (тв.) -104,8 -29,6 26,7 (тв.) -93,0 -13,1 48,0 (тв.) -70,3 17,2 58,3 (тв.) -56,9 34,0
С2 C2BrCl3O c2cif3 c2ci2f2 c2ci2f4 c2ci3f3 C2C14 C2C14F2 C2C14O СД*1 c2f4 c2f6 c2n2 C2HBr3O C2HC13 C2HCI3O C2HC13O2 C2HC15 c2H2 C2H2AsC13 C2H2AsC13 C2H2Br2Cl2 C2H2Br4 Трихлорацетил-бромид Трифтор(хлор)-этилен 1,2-Дифтор-1,2-дихлорэтилен 1,1,2,2-Тетра-фтор-1,2-дихлорэтан 1,1,2-Трифтор-1,2,2-трихлор-этан (фреон-113) Т етрахлорэтилен 1,2-Дифтор-1,1,2,2-тетра-хлорэтан Трихлорацетил-хлорид Г ексахлорэтан Т етрафторэтилен Гексафторэтан Оксалонитрил (дициан) Трибромацетальдегид (бромаль) Трихлорэтилен Т рихл орацетал ь-дегид (хлораль) Т рихлоруксусная кислота Пентахлорэтан Ацетилен Дихлор[(£)-2-хлорвинил]арсин (люизит) Дихлор[(7)-2-хлорвинил]арсин 1,2-Дибром-1,1-дихлорэтан 1,1,1,2-Тетрабромэтан -7,4 -116,0 -82,0 -96,1 (тв.) -68,0 (тв.) -20,1 (тв.) -37,5 (тв.) -21,2 33,4 (тв.) -146,4 (тв.) -95,5 (тв.) 18,5 -42,9 -37,8 53,6 (тв.) 1.0 -144,7 (тв.) 32,0 20,6 58,0 29,3 -95,9 -57,3 -72,1 -40,3 (тв.) 14,0 -5,0 (тв.) 12,0 72,9 (тв.) -132,4 -132,8 (тв.) -76,6 (тв.) 58,0 -11,9 -5,0 88,7 39,8 -128,6 (тв.) 72,1 57,3 58,8 95,7 57,2 -79,7 -38,2 -53,7 -18,5 34,4 (4,00 кПа) 19,8 (тв.) 37,9 -62,5 (тв.) 87,8 6,9 (4,00 кПа) 20,2 115,7 69,9 -126,8 (тв.) (4,00 кПа) 81,5 (4,00 кПа) 123,2 79,5 -66,7 -23,0 -39,1 -1,7 61,0 38,6 58,5 116,8 (тв.) -107,3 -111,1 (тв.) -51,5 (тв.) 110,2 31,5 40,2 137,8 93,9 -107,8 (тв.) 125,1 109,3 111,3 144,0 120,2 -41,7 5,0 -12,0 30,2 100,0 73,1 96,7 -33,0 151,6 67 77,5 176,0 137,2 -92,0 (тв.) 181,0 143,0 -27,9 20,9 3,5 47,6 121,0 92,0 118,2 183,9 (тв.) -76,5 -78,3 -21,2 174,0 (разл.) 87,1 97,7 198,6 161,5 83,6 (тв.) 196,6 169,8 178,3 200,0 (разл.) -157,5 -112 -94 -35 -19,0 26,5 -56,9 187 -100,6 -34 -73 -57 59,2 -22 -81 -66,9 0
Физические свойства важнейших веществ
157
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Тпл, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С2Н2ВГ4 1,1,2,2- 65,0 110,0 144,0 170,0 217,5 243,5 0,1
С2Н2С12 Тстрабромэтан 1,1-Дихлор- -77,2 -51,2 -31,1 -15,0 14,8 31,7 -122,5
С2Н2С12 этилен (£)-1,2-Дихлор- -65,4 (тв.) -38,0 -17,0 -1,9 30,8 47,9 -50,0
С2Н2С12 этилен (2)-1,2- -58,4 -31,4 -7,9 9,4 41,0 60,8 80,5
C2H2CI2O Дихлорэтилен Хлорацетилхло- -20,5 10,0 33,6 52,3 86,7 106,0 -21,3
С2Н2С12О2 рид Дихлоруксусная 44,0 82,6 111,8 134,0 173,7 194,4 9,7
С2Н2С14 кислота 1,1,1,2-Тетра- -16,3 19,3 46,7 68,0 108,2 130,5 -68,7
С2Н2С14 хлорэтан 1,1,2,2-Тетра- -3,8 33,0 60,8 83,2 124,0 145,9 -36
С2НЗВГО2 хлорэтан Бромуксусная 54,7 94,1 124,0 146,3 186,7 208,0 49,5
С2Н3ВГ3 кислота 1,1,2-Трибром- 28,0 67,2 90,2 120,4 188,9 -29,2
С2Н3С1 этан Хлорэтилен -109,4 -87,5 (4,00 кПа) -74,0 -55,8 -28,0 -13,4 -153,8
С2Н3С1О С2Н3С1О2 Ацетилхлорид Хлоруксусная -95,8 43,0 (тв.) -67,6 83,1 (4,00 кПа) 109,7 -28,8 130,5 168,3 51,5 189,1 61,6
C2H3C13 кислота 1,1,1-Трихлор- -50,8 (тв.) -21,2 -3,3 20,3 54,6 74,1 -30,4
C2H3C13 этан 1,1,2-Трихлор- -20,5 11,0 (4,00 кПа) 30,4 55,8 93,0 113,8 -36,6
C2H3C13O2 этан Хлоральгидрат -9,8 (тв.) 19,5 (тв.) (4,00 кПа) 39,7 (тв.) 55,0 82,1 96,2 (разл.) 51,7
C2H3Cl3Si C2H3Cl5Si C2H3F (2,2,2-трихлор-этан-1,1-диол) Винил(трихлор)-силан (1,2-Дихлор-этил)трихлор-силан Фторэтилен -149,3 -10,7 61,1 -132,2 14,5 91,6 -118,0 34,2 115,2 -106,2 70,5 157,6 -84,0 90,6 180,6 -72,2 -160,5
C2H3FO2 C2H3F3 C2H3N Фторуксусная кислота 1,1,1-Трифтор-этан Ацетонитрил -^47,0 (тв.) 64,9 -110,1 -16,3 7 113,5 -82,5 25,8 61 168,3 -^47,5 80,0 -41
C2H3NS Метилизотио- -34,7 (тв.) 5,4 (тв.) 38,2 59,3 97,8 119,0 35,5
C2H3NS цианат Метилтиоцианат -14,0 21,6 49,0 70,4 110,8 132,9 -51
С2Н4 Этилен -168,4 -153,3 -141,3 -131,8 -113,9 -103,7 -169,2*2
C2H4BrCl 1-Бром-1- -36,0 (тв.) -9,4 (тв.) 10,4 (тв.) 28,0 63,4 82,7 16,6
С2Н4ВгС1 хлорэтан 1-Бром-2- -28,8 (тв.) 4,1 29,7 49,5 86,0 106,7 -16,6
С2Н4ВГ2 хлорэтан 1,2-Дибромэтан -12,7 (тв.) 22,2 43,0 70,2 110,0 131,4 9,9
С2Н4С12 1,1 -Дихлорэтан -60,7 -32,3 (4,00 кПа) -10,2 7,2 39,8 57,4 -96,7
158
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Tnsl, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53.3 кПа 101,3 кПа
С2Н4С12 1,2-Дихлорэтан -43,1 (тв.) -12,5 5,8 (4,00 кПа) 29,8 65 83,5 -35,7
C2H4F2 1,1 -Дифторэтан -112,5 -91,7 -75,8 -63,2 -39,5 -26,5 -117
С2Н4О Ацетальдегид (уксусный альдс- -81,5 -56,8 -37,8 -22,6 4,9 20,2 -123,5
гид)
С2Н4О Оксиран (окись -90,6 -66,0 -47,1 -32,2 -4,8 10,4 -112,5
этилена)
с2н4о2 Метилформиат -74,2 -48,6 -28,7 -12,9 16,0 32,0 -99,8
С2Н4О2 Уксусная кислота -17,2 (тв.) 17,1 42,4 62,2 98,1 117,9 16,3
С2Н32НО2 (О-2Н)Уксусная 16,0 61,2 116,5
кислота
C2H4O2S Сульфанилук- 60,0 101,5 131,8 154,0 -16,5
сусная кислота (меркаптоуксус- (разл.)
ная кислота,
тиогликолевая
кислота)
С2Н4Оз Этанпероксовая кислота(надуксусная кислота) -13,9 18,9 61,2 110
C2H4S Тиран -62,1 -34,2 -17,4 4,8 54,9 -109
(этиленсульфид) (4,00 кПа)
C2H5AsF2 Дифтор(этил)- -1,3 53,4 93,9
арсин
C2H5Br Бромэтан -74,1 -47,5 -26,7 -10,0 21,0 38,4 -119,3
С2Н5С1 Хлорэтан -90,9 -66,4 -47,0 -32,0 -3,9 12,3 -139
С2Н5С1О 2-Хлорэтанол -4,0 30,3 56,0 75,0 110,0 128,8 -69
C2H5Cl3OSi Т рихлор(этокси)- -32,4 0,0 25,3 45,2 82,2 102,4
силан
C2H5Cl3Si Трихлор(этил)- -1,6 22,3 41,5 77,9 98,8 -40
силан
c2h5f Фторэтан -117,0 -97,7 -81,8 -69,3 -45,5 -32,0
C2H5F3Si Три- -95,4 -73,7 -56,8 -43,6 -19,1 -5,4
фтор(этил)силан
C2H5I Иодэтан -54,4 -24,3 -0,9 18,0 52,3 72,4 -105
C2H5NO Ацетальдегидок- -5,8 (тв.) 25,8 (тв.) 48,6 66,2 98,0 115,0 47
сим
c2h5no Ацетамид 65,0 (тв.) 105,0 135,8 158,0 200,0 222,0 81
c2h5no2 Нитроэтан -21,0 12,5 38,0 57,8 94,0 114,0 -90
c2h5no2 Этилнитрит -108,8 -62,0 -16,1 17,4
c2h5no3 Этилнитрат -38,7 -7,8 34,7 86,7
c2H6 Этан -159 -142,9 -129,8 -119,3 -99,7 -88,6 -182,8*2
C2H6Be Диметилберил- 107,6 140,6 178,4
ЛИЙ
C2H6Cd Диметилкадмий 5,8 49,6 105,6
C2H6ClFSi Диметил(фтор)- -47,2 -10,3 36,2
(хлор)силан
C2H6Cl2Si Диметил-(дихлор)силан -53,5 -23,8 -0,8 17,4 51,4 70,3
C2H6Cl2Si Дихлор-(этил)силан -24,4 0,8 20,4 56,0 75,5
C2H6O Диметиловый -115,7 -93,3 -76,2 -62,7 -37,8 -23,7 -138,5
эфир
C2H6O Этанол -31,3 -2,3 19,9 34,9 63,5 78,4 -112
Физические свойства важнейших веществ
159
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Т11Л, °с
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
с2н6о2 С2Н6О2 Этилгидропероксид Этиленгликоль -21,0 53,0 11,2 92,1 120,0 52,8 141,8 178,5 101,1 197,3 -15,6
c2H6s (этан-1,2-диол) Диметилсульфид -75,6 -49,2 -28,4 -12,0 18,7 36,0 -83,2
c2H6s Этантиол -76,7 -50,2 -29,8 -13,0 17,7 35,0 -147,9
c2H6s2 C2H6Zn C2H7As c2h7n Диметилдисульфид Диметилцинк Димстиларсин А-Мстилметан- -81,6 -87,7 6,0 -43,9 -52,3 -64,6 -46,7 51,5 -4,3 -12,4 -32,6 -7,1 109,7 43,8 37,1 7,4 -84,7*2 -96
c2h7n амин (димстил-амин) Этанамин -82,3 (тв.) -58,3 -39,8 -25,1 2,0 16,6 -80,6
c2h7no 2-Аминоэтанол 37,6 70,8 96,1 115,6 151,0 170,4 10,3
c2h7p c2h8n2 Диметилфосфин Этан-1,2-диамин -11,0 (тв.) -63,7 21,5 45,8 -25,9 62,5 99,0 20,9 117,2 8,5
C2H8Si Диметилсилан -115,0 -93,1 -75,7 -61,4 -35,0 -20,1
C2H10B2 Диметилдиборан -106,5 -82 -62,4 -47,0 -18,8 -2,6 -150,2
C2HHNSi2 Этилдисилазан -62,0 -32,2 -8,3 10,4 45,9 65,9 -127
C3 C3C16 Г ексахлорпропен 43,5 84,5 109,0 141,1 214,1 -57,1
C3H3N Акрилонитрил -51,0 -20,3 (4,00 кПа) 3,8 22,8 58,3 78,5 -82
C3H4 Аллен (пропадиен) -122,2 -100,8 -84,3 -71,3 -47,5 -34,3 -135,З*2
C3H4 Пропин -110,6 -90,9 -74,3 -61,1 -36,7 -23,0 -102,7
C3H4Br2 2,3-Дибром- (тв.) -6,0 30,0 57,8 79,5 119,5 141,2
C3H4C12O2 пропен Метил(дихлор)- 3,2 38,1 64,7 85,4 122,6 143,0
C3H4O ацетат Акриловый -64,5 -36,7 -15,0 2,5 34,5 52,5 -87,7
c3H4o2 альдегид Акриловая 3,5 (тв.) 39,0 66,2 86,1 122,0 141,0 14
C3H4O3 кислота Пировиноград- 21,4 57,9 85,3 106,5 144,7 165,0 (разл.) 13,6
C3H5Br3 ная кислота 1,2,3-Трибром- 50,0 91,8 116,7 149,2 222,2 16,2
C3H5C1 C3H5C1 C3H5C1 пропан (Е)-1-Хлор-пропен (Z)-l-Хлор-пропен З-Хлорпропен -70,0 -48,7 -52,1 -42,9 (4,00 кПа) -32,6 (4,00 кПа) -36,2 (4,00 кПа) -21,2 -Н, -15,1 -4,5 27,5 37,4 32,8 44,6 -99,0 -134,8 -136,4
C3H5C1O 2-(Хлорметил)- -16,5 16,6 42,0 62,0 98,0 117,9 -25,6
C3H5C1O2 оксиран (эпихлоргидрин) Метил(хлор)- -2,9 30,0 54,5 73,5 109,5 130,3 -31,9
C3H5O3 ацетат 1,1,1-Трихлор- -28,8 4,2 29,9 50,0 87,5 108,2 -77,7
C3H5C13 пропан 1,2,3-Трихлор- 9,0 46,0 74,0 96,1 137,0 158,0 -14,7
C3H5Cl3Si пропан Аллил(трихлор)- -20,7 13,2 39,2 59,3 97,1 118,0
силан
160
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Д1Л, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
c3h5n Пропаннитрил -35,2 -3,2 21,5 40,6 77 97,3 -91,9
c3h5no З-Гидрокси-пропаннитрил 58,7 102.0 134,1 157,7 200,0 221,0
c3h5ns c3h5n309 Этилизотиоцианат Пропан-1,2,3-триилтринитрат (нитроглицерин) -13,2 (тв.) 127 22,8 188 50,8 235 71,9 (разл.) 110,1 131,0 -5,9 11
c3H6 Пропен(пропилен) -132,1 -112,2 -96,6 -84,2 -60,9 -47,7 -185,2*2
c3H6 Циклопропан -101,1 -84,5 -71,3 -46,7 -32,8 -127,4
C3H6BrCl 1-Бром-3 -хлорпропан -3,0 32,4 53,6 (4,00 кПа) 81,2 143,4 -58,9
C3H6BrNO 2-Бром-2-нитро-зопропан -33,5 -4,3 17,9 35,2 66,2 83,0
С3НбВг2 1,2-Дибром-пропан -6,8 28,9 50,2 (4,00 кПа) 78,2 118,5 142,0 -55,5
C3H6Br2 1,3-Дибром-пропан 10,4 48,6 71,3 (4,00 кПа) 100,8 144,1 166,7 -34,2
C3H6Br2O 2,3-Дибром-пропан-1 -ол 57,0 98,2 129,8 153,0 196,0 219,0
C3H6C12 1,2-Дихлор-пропан -35,0 -3,7 15,2 (4,00 кПа) 40,0 76,0 96,4 -100,4
C3H6C12O 1,3-Дихлор-пропан-2-ол 28,0 64,7 93,0 114,8 153,5 174,3
c3H6o Ацетон -59,4 -31,1 -9,4 7,7 39,5 56,5 -94,6
c3H6o 2-Метилоксиран -73,5 -47,8 -27,8 -11,9 17,6 34,8 -112,1
c3H6o Проп-2-ен-1 -ол -20,0 10,5 33,4 50,0 80,2 96,6 -129
c3H6o2 Метилацетат -57,2 -29,3 -7,9 9,4 40,0 57,8 -98,7
c3n6o2 Пропионовая кислота 4,6 39,7 65,8 85,1 122,0 141,1 -22
c3H6o2 Этилформиат -60,5 -33,0 -11,5 5,4 37,1 54,3 -79
c3H6o3 Метил-(гидрокси)ацетат (метилгликолят) 9,6 45,3 72,3 93,7 131,7 151,5
C3H6O3 c3H6o3 Метоксиуксус -ная кислота Пропанпероксо-вая кислота (надпропионовая кислота) 52,5 -11,6 92,0 22,7 122,0 144,5 67,4 184,2 204,0 119,7
c3H6s 2-Мет илтииран -47,9 -18,6 -1,0 (4,00 кПа) 22,2 74,4 -91
c3H6s Тиетан -36,2 -14,9 14,0 (4,00 кПа) 38,9 95,0 -73,3
C3H7Br 1 -Бромпропан -53,0 -23,3 -0,3 18,0 52,0 71,0 -109,9
C3H7Br 2-Бромпропан -61,8 -32,8 -10,1 8,0 41,5 60,0 -89,0
C3H7C1 1-Хлорпропан -68,3 -41,0 -19,5 -2,5 29,4 46,4 -122,8
C3H7CI 2-Хлорпропан -74,7 -48,7 -32,9 (4,00 кПа) -12,2 34,8 -117,2
C3H7Cl3Si C3H7CI3Si Изопропил-(трихлор)силан Пропил-(трихлор)силан -24,3 9,9 16,1 36,5 57,8 63,0 96,8 118,5 122,7
Физические свойства важнейших веществ
161
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара TnJ1, °с
0.133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С3Н71 1 -Иодпропан -36,0 -2,4 23,6 43,8 81,8 102,5 -98,8
С3Н71 2-Иодпропан -43,3 -11,7 13,2 32,8 69,5 89,5 -90
C3H7NO Пропанамид 65,0 (тв.) 105,0 134,8 156,0 194,0 213,0 79
c3h7no2 1 -Нитропропан -9,6 25,3 51,8 72,3 110,6 131,6 -108
c3h7no2 2-Нитропропан -18,8 15,8 41,8 62,0 99,8 120,3 -93
c3h7no2 Этилкарбамат 77,8 105,6 126,2 164,0 184,0 49
c3H8 Пропан -129 -108,5 -92,5 -79,6 -55,6 -42,1 -187,7*2
C3H8Cl2OSi Метил(дихлор)-(этокси)силан -33,8 -1,3 24,4 44,1 80,3 100,6
c3H8o Метоксиэтан -91,0 -67,8 -49,4 -34,8 -7,8 7,5
c3H8o Пропан-1-ол -15,0 14,7 36,4 52,8 82,0 97,8 -127
c3H8o Пропан-2-ол -26,1 2,4 23,8 39,5 67,8 82,5 -89
С3н8о2 2-Метоксиэтанол -13,5 22,0 47,8 69,8 104,3 124,5
с3н8о2 Пропан-1,2-диол 45,5 83,2 111,2 132,0 168,1 188,2
С3Н8О2 Пропан-1,3-диол 59,4 100,6 131,0 153,4 193,8 214,2
с3н8о3 Глицерин 125,5 167,2 198,0 220,1 263,0 290,0 17,9
c3H8s (Метилсульфа- -54,4 -25,7 14,7 66,5
нил)этан
c3H8s Пропан-1 -тиол -53,9 -25,1 -3,2 15,4 49,3 67,7 -113,1
c3H8s Пропан-2-тиол -64,2 -36,7 2,1 52,5 -130,7
С3Н9А1 Триметилалюман 21,9 68,9 124,7
C3H9As Триметиларсин -70,5 -40,3 0,4 50,4
с3н9в Триметилборан -118,0 -92,4 -74,7 -60,8 -34,7 -20,1
С3Н9ВО Диметил-(метокси)боран -85,4 -58,3 -22,1 21,0
С3Н9В3О3 2,4,6-Триметил-1,3,5,2,4,6-три-оксатриборинан -139,2 -121,1 -106,6 -95,3 -74,8 -64,0
C3H9Bi Триметилвисму- -0,6 47,5 106,7
тан
C3H9ClSi Триметил-(хлор)силан -62 -34,9 -12,3 5,6 38,9 57,6
C3H9FSi Триметил -(фтор)силан -64,5 -28,1 16,4
C3H9Ga Т риметилгаллан -62,3 (тв.) -31,7 (тв.) -9,0 8,0 39,0 55,6 -19
c3h9n /У,/У-Диметил-метанамин (три- -97,1 -73,8 -55,2 -40,3 -12,5 2,9 -117,1
метиламин)
c3h9n Пропан-1-амин -64,4 -37,2 -16,0 0,5 -31,5 48,5 -83
C3H9O4P Триметилфосфат 26,0 69,7 100,0 123,8 191,0
c3H9p Триметилфосфин -77,7 -48,6 -9,5 38,4
C3H10OSi Триметилсила- 3,9 41,7 84,7
НОЛ
C3H12B2 Триметилдибо- -74,0 -44,8 -22,0 -4,4 27,8 45,5 -122,9
ран
C4
C4C16O3 Трихлоруксусный ангидрид 56,2 99,6 131,2 155,2 199,8 223,0
c4H2 Бута-1,3-диин -83,3 (тв.) -61,2 (тв.) -45,9 -34,9 -6,1 10,3 -36,4
(диацетилен) (тв.)
C4H2C12O2 Фумароилдихло- 15,0 51,8 79,5 101,0 140,0 160,0
рид
162
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара г,„„ °с
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С4Н2О3 Фуран-2,5-дион 44,0 (тв.) 79,8 111,8 135,8 179,5 202,0 58
C4H3NO2S (малеиновый ангидрид) 2-Нитротиофен 48,2 92,0 125,8 151,5 199,6 224,5 46
С4Н4 Бут-1-ен-З-ин -86,1 -66,1 -49,7 -36,3 -10,1 5,4
C4H4CI2O2 (винилацетилен) Сукцинилдихло- 39,0 78,0 107,5 130,0 170,0 192,5 17
C4H4CI2O3 рид Хлоруксусный 67,2 108,0 138,2 159,8 197,0 217,0 46
С4Н4О ангидрид Фуран -75,6 -50,2 -35,1 -14,1 31,4 -85,7
С4Н4О3 Дигидрофуран- 92,0 (тв.) 128,2 (4,00 кПа) 163,0 189,0 237,0 261,0 119,6
С4Н4О4 2,5-дион (янтарный ангидрид) 1,4-Диоксан-2,5- 116,6 148,6 173,2 217,0 240,0 87
C4H4S дион (гликолид) Тиофен -42 (тв.) -12,3 12,5 29,9 64,7 84,2 -38,2
C4H4Se Селенофсн -39,0 -4,0 24,1 47,0 89,8 114,3
С4Н5С1О2 (7)-2-Хлорбут-2- 70,0 108,0 135,6 155,9 193,2 212,0
C4H5CI3O2 еновая кислота Этилтрихлораце- 20,7 57,7 85,5 107,4 146,0 167,0
c4h5n тат (£)-Бут-2- -19,5 15,0 41,8 62,8 101,5 122,8
c4h5n еннитрил (7)-Бут-2- -29,0 4,0 30,0 50,1 88,0 108,0
c4h5n еннитрил Бут-З-еннитрил -19,6 14,1 40,0 60,2 98,0 119,0
c4h5n Метакрилонит- -44,5 -12,5 12,8 32,8 70,3 90,3
c4h5no2 рил Пиррол-2,5-дион 115,0 (тв.) 157,0 192,0 217,4 263,5 287,5 125,5
c4h5ns (сукцинимид) Аллилизотио- -2,0 38,3 67,4 89,5 129,8 150,7 -100
c4H6 цианат Бута-1,2-диен -94,5 -69,1 -49 -33,8 -5,2 10,9 -136,2
c4H6 (метлаллен) Бута-1,3-диен -103,2 -79,9 -61,6 47,0 -19,8 -4,4 -108,9
c4H6 (дивинил) Бут-1 -ин (этил- -75,1 59,3 -45,4 -33,4 -7,9 8,5 -125,7
c4H6 ацетилен) Бут-2-ин (диме- -80,0 (тв.) -54,5 (тв.) -39,0 -18,7 10,7 26,2 -32,3
c4H6 тилацетилен) Циклобутен -99,1 -75,4 (тв.) (4,00 кПа) -56,4 -41,1 -13,2 2,5
c4H6ci2o2 C4H6C12O2 C4H6O2 (2-Хлорэтил)-хлорацетат Этил(дихлор)аце-тат (Е)-Бут-2-еновая 46,0 9,6 86,0 46,3 80,0 107,8 140,0 96,1 128,0 165,5 205,0 156,5 189,0 72
c4H6o2 кислота(кротоновая кислота) Винилацетат -48,0 -18,0 5,3 23,3 55,5 72,5
Физические свойства важнейших веществ
163
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Е,л, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
с4н6о2 (7)-Бут-2-еновая кислота(изокро-тоновая кислота) 33,5 69,0 96,0 116,3 162,2 171,9 разл. 15,5
с4н6о2 Метакриловая кислота 25,5 60,0 86,4 106,6 142,5 161,0 15
С4Н6О2 Метилакрилат -43,7 -13,5 9,2 28,0 61,8 80,2 (полим.)
С4Н60з Уксусный ангидрид 2,4 31,2 60,6 80,7 117,9 138,6 -74,1
С4Н6О4 Диметилоксалат 20,0 56,0 83,6 104,8 143,3 163,3
С4Н7Вг (Е)-1-Бромбут-1 -ен -38,4 6,4 18,4 38,1 75,0 94,7 -100,3
С4Н7Вг (2)-1 -Бромбут-1 -ен -44,0 -12,8 11,5 30,8 66,8 86,2
С4Н7Вг 2-Бромбут-1-ен -47,3 -16,8 7,2 26,3 61,9 81,0 -133,4
С4Н7Вг (Е)-2-Бромбут-2-ен -45,0 -13,8 10,5 29,9 66,0 85,5 -114,6
С4Н7Вг (7)-2-Бромбут-2-ен -39,0 -7,2 17,7 37,5 74,0 93,9 -111,2
С4Н7ВгО 1-Бромбутан-2-он 6,2 41,8 68,2 89,2 126,3 147,0
С4Н7ВгО 2-Метилпропа-ноилхлорид 13,5 50,6 79,4 101,6 141,7 163,0
С4Н7Вг3 Ы,2-Трибромбутан 45,0 78,8 120,2 146,0 192,0 216,2
С4Н7Вг3 1,2,2-Трибромбутан 41,0 83,2 116,0 141,8 188,0 213,8
С4Н7Вг3 2,2,3-Трибромбутан 38,2 79,8 111,8 136,3 182,2 206,5
С4Н7С1О2 Этил(хлор)ацстат 1,0 37,5 65,2 86,0 123,8 144,2 -26
С4Н7С13 1,2,3-Трихлорбутан 0,5 40,0 71,5 96,2 143,0 169,0
c4h7n Бутаннитрил -20,0 13,4 38,4 59,0 96,8 117,5
c4h7no2 c4h7no2 У-Ацстил-ацетамид (диацетамид) 2-Нитробут-1-ен 70,0 (тв.) -6,1 108,0 29,0 138,2 160,6 74,8 202,0 223,0 78,5
c4H8 Бут-1-е н -105,1 -81,7 -63,4 48.8 -21,6 -6,3 -185,3*2
c4H8 (Е)-Бут-2-ен -100,4 -76,5 -57,7 -42,7 -14,8 0,9 -105,6
с4н8 (2)-Бут-2-ен -97,2 -73,4 -54,7 -39,8 -12,0 3,7 -138,9
с4н8 2-Метилпропен (изобутилен) -105,3 -82,8 -64,3 -49,7 -22,4 -7,0 -140,4
с4н8 Циклобутан -92,0 (тв.) -68,3 48,5 -32,8 -3,7 12,6 -90,4*2
с4н8 Метилциклопропан -96,0 -72,8 -54,2 -39,3 -11,3 4,5 -177,3
С4Н8ВгС1О 1-Бром-2-(2-хлорэтокси)этан 36,5 76,3 106,6 129,8 172,3 195,8
С4Н8Вг2 1,2-Дибромбутан 7,5 46,1 76,0 99,8 143,5 166,3 -64,5
С4Н8Вг2 1,4-Дибромбутан 32,0 72,4 104,0 128,7 173,8 197,5 -20
С4Н8Вг2 рац-(2И., 3 Е)-2,3 -Дибромбутан 5,0 41,6 72,0 95,3 138,0 160,5
С4Н8Вг2 (2E,3S)-2,3-Дибромбутан 1,5 39,3 68,2 91,7 134,2 157,3 -34,5
С4Н8Вг2 1,2-Дибром-2 -метилпропан -28,8 10,5 42,3 68,8 119,8 149,0 -70,3
164
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Тш„ °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С4Н8Вг2 1,3-Дибром-2-метилпропан 14,0 53,0 83,5 107,4 150,6 174,6
С4Н8Вг2О 1 -Бром-2-(2-бромэтокси)этан 47,7 88,5 119,8 144,0 188,0 212,5
С4Н8С12 1,2-Дихлорбутан -23,6 11,5 37,7 60,2 100,8 123,5
С4Н8С12 2,3 - Дихлорбутан -25,2 8,5 35,0 56,0 94,2 116,0 -80,4
С4Н8С12 2-Метил-1,1-дихлорпропан -31,0 2,6 29,3 50,0 85,8 105,0 (разл.)
С4Н8С12 2-Метил-1,2-дихлорпропан -25,8 6,7 32,0 51,7 87,8 108,0
С4Н8С12 2-Метил-1,3-дихлорпропан -3,0 32,0 58,6 78,8 115,4 135,0
С4Н8С12О C4H8Cl2Si 1-Хлор-2-(2-хл орэтокс и)этан Винил(дихлор)-(этил)силан 23,5 62,0 15,5 91,5 42,1 114,5 63,1 155,4 102,0 178,3 123,7
С4Н8О 2,2-Диметилоксиран -69,0 -49,3 -17,3 1,2 36,0 55,5
С4Н8О Бутанон -48,3 -17,7 6,0 25,0 60,0 79,6 -85,9
с4н8о2 1,4-Диоксан -35,8 (тв.) -1,2 (тв.) 25,2 45,1 81,8 101,1 10
с4н8о2 Изомасляная кислота 14,7 51,2 77,8 98,0 134,5 154,5 -47
с4н8о2 Изопропилфор-миат -62,0 -22,7 -0,2 17,8 50,5 68,3
с4н8о2 Масляная кислота 25,5 61,5 88,0 108,0 144,5 163,5 -4,7
С4Н8О2 Метилпропионат -42,0 -11,8 11,0 29,0 61,8 79,8 -87,5
С4Н8О2 Пропилформиат -43,0 -12,6 10,8 29,5 62,6 81,3 -92,9
с4н8о2 С4Н8О3 Этилацетат Бутанпероксовая кислота (надмасляная кислота) -43,4 -4,1 -13,5 30,2 9,1 27,0 74,7 59,3 77,1 126,2 -82,4
С4Н8Оз 2-Гидрокси-2-метилпропановая кислота 73,5 (тв.) 110,5 138,0 157,7 193,8 212,0 79
С4Н8Оз c4H8s Этил(гидрокси)-ацетат (этилгли-колят) 2,2-Диметилтииран 14,3 -36,7 50,5 -8,8 78,1 9,2 (4,00 кПа) 99,6 32,8 138,0 158,2 86
c4H8s c4H8s Тетрагидротиофен (тетрамети-ленсульфид) 2-Этилэтил-тииран -19,4 -24,1 14,5 7,3 34,7 (4,00 кПа) 25,9 (4,00 кПа) 61,2 50,2 121,1 105 -96,2
C4H9Br 1 -Бромбутан -33,0 -0,3 24,8 44,7 81,7 101,6 -112,4
C4H9Br 2-Бромбутан -40,0 -9,1 9,7 (4,00 кПа) 34,6 91,4 -112,7
C4H9BrO 1-Бромбутан-2-ол 23,7 55,8 79,5 97,6 128,3 145,0
C4H9C1 C4H9CI 2-Метил-1-хлорпропан 2-Метил-2-хлорпропан -53,8 -24,5 -1,9 -19,0 16,0 -1,0 50,0 32,6 68,9 51,0 -131,2 -26,5
Физические свойства важнейших веществ
165
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Т °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53.3 кПа 101,3 кПа
С4Н9С1 1 -Хлорбутан -47,2 -17,4 0,7 (4,00 кПа) 24,5 59 78,4 -123,2
С4Н9С1 2-Хлорбутан -60,2 -29,2 -5,0 14,2 50,0 68,0 -131,3
C4H9NO Морфолин 24,9 44,7 (4,00 кПа) 70,5 128,3 -4,8
c4h9no2 1 -Нитробутан 7,0 42,0 89,9 152,9
c4h9no2 2-Нитробутан -3,5 29,9 78,3 139,6
c4h9no2 Пропилкарбамат 90,0 117,7 138,3 175,8 195,0 60
c4h9no2 Этил(метил)кар- 26,5 63,2 91,0 112,0 149,8 170,0
бамат
C4Hio Бутан -101 -77,8 -59,1 -44,2 -16,3 -0,5 -138,3
C4H|0 Изобутан -109,6 -86,6 -68,5 -54,1 -27,0 -Н,7 -159,6
C4H10Cl2Si Дихлор-(диэтил)силан -9,2 21,0 47,9 69,1 108,4 130,4
C4H10F2Si Дифтор-(диэтил)силан -56,8 -28,8 -7,3 9,8 40,5 58,0
C4HioO Бутан-1-ол -1,2 30,2 53,4 70,1 100,8 117,5 -79,9
C4H10O Бутан-2-ол -12,2 16,9 38,1 54,1 83,9 99,5 -114,7
C4HioO Диэтиловый эфир (этиловый -74,3 -48,0 -27,7 -11,5 17,9 34,6 -116,3
эфир)
C4H]0O 2-Метилиропан- -9,0 21,7 44,1 61,5 91,4 108,0 -108
1-ол
C4HioO 2-Метилпропан- -20,4 (тв.) 5,5 (тв.) 24,5 (тв.) 39,8 68,0 82,9 25,3
2-ол
C4H10O Метилпропило- -72,2 -45,4 -24,3 -8,1 22,5 39,1
вый эфир
C4H10O2 Бутан-1,3-диол 22,2 (тв.) 85,3 117,4 141,2 183,8 206,5 77
C4H]0O2 Бутан-2,3-диол (псевдобути-ленгликоль) 44,0 80,3 107,8 127,8 164,0 182,0 22,5
C4H10O2 1,2- -48,0 -15,3 31,8 93,0
Диметоксиэтан
C4H10O2 /и/?е/и-Бутил-гидропероксид 0,3 35,0 79,7 131,4
C4H 10o2 Диэтилпероксид -34,5 10,0 65,8
C4H10O2S 42,0 128,0 210,0 285
Сульфандиилди- разл. разл.
этанол
C4H10O3 Бутан-1,2,3- 102,0 146,0 178,0 202,5 243,5 264,0
триол
С4Н1оОз 2,2'- 91,8 133,8 164,3 187,5 226,5 224,8 -10,5
Оксидиэтанол (диэтиленгли-
коль)
c4H10o3s Диэтилсульфит 10,0 46,4 74,2 96,3 137,0 159,0
C4H10O4S Диэтил сульф ат 47,0 87,7 118,0 142,5 185,5 209,5 (разл.) -24,5
C4HioS Диэтилсульфид -39,6 -8,0 16,1 35,0 69,7 88,0 -103,9
c4H10s2 Диэтилдисуль- з,з 39,9 89,7 154,1 -101,5*2
фид
C4Hi0Se Диэтилселенид -25,7 7,0 31,2 51,8 88,0 108,0
C4H10Zn Диэтилцинк -22,4 11,7 38,0 59,1 97,3 118,0 -28
166
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Т °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
C4HhN 2-Метилпропан-1 -амин (изобутил- -50,0 -21,0 1,3 18,8 50,7 68,6 -85,0
амин)
C4HhN /V-Этилэтанамин -33,0 -11,3 6,0 38,0 55,5 -38,9
(диэтиламин)
c4hhno2 2,2'-Иминодиэтанол (диэта- 111,7 151,7 181,8 204,9 246,1 268,4 28,0
ноламин)
C4H12BC1N2 Бис(диметилами- -4,1 33,8 83,9 146,0
но)хлорборан
C4H]2Cl2OSi2 1,1,з,з- -7,4 28,3 55,7 76,9 116,3 138,0 -37
Тетраметил-1,3-дихлордисилок-
сан
C4H12Ge Тетрамстилгер- -73,2 -45,2 -23,4 -6,3 26,0 44,0 -88
ман
c4h12n2 Т етраметилги д- -51,1 -19,5 20,3 73,0
разин
C4H12Pb Тетраметил- -29,0 (тв.) 4,4 30,3 50,8 89,0 110,0 -27,5
плюмбан
C4H12Sb2 Тетраметилди- 44,0 86,0 143,5 211,0
стибан
C4H12Si Т етраметилсилан -83,8 -58,0 -37,4 -20,9 10,0 27,0 -102,1
C4H]2Sn Т етраметилстан- -51,3 -20,6 3,5 23,2 58,5 78,0
нан
C4H14B2 Т етраметилдибо- -59,6 -27,4 -3,4 15,3 49,8 68,6 -72,5
ран
C5
C5H4BrN З-Бромпиридин 16,8 55,2 84,1 107,8 150,0 173,4
C5H4C1N 2-Хлорпиридин 13,3 51,7 81,7 104,6 147,7 170,2
c5h402 2-Фуральдегид 49,7 99,5 161,6 -36,5
(ФУРФУРОЛ)
c5h403 3-Метил фуран-2,5-дион (цитраконовый ангид- 47,1 88,9 120,3 145,4 189,8 213,5
рид)
c5h5n Пиридин -18,9 13,2 38,0 57,8 95,6 115,2 -42
c5h6ci202 Пентандиоилди- 56,1 97,8 128,3 151,8 195,3 217,0
хлорид
c5h6n2 Пентандинитрил (глутаронитрил) 91,3 140,0 176,4 205,5 257,3 286,2
c5H6o2 2-Фурилметанол 31,8 68,0 95,7 115,9 151,8 170,0
c5H6o3 Дигидро-2//-пиран-2,6(3//)-дион (глутаровый ангидрид) 100,8 149,5 185,5 212,5 261,0 287,0
c5H6o3 3-Метилдигидрофуран-2,5-дион (метилянтарный ангид- 69,7 114,2 147,8 173,8 221,0 247,4
рид)
c5H6s 2-Метилтиофен -23,3 9,2 28,6 (4,00 кПа) 54,3 91,8 112,6 -63,4
Физические свойства важнейших веществ
167
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Гпл, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
c5H6s 3-Метилтиофен -22,2 11,0 30,8 (4,00 кПа) 56,8 93,8 115,4 -69,0
С5Н7С1О3 Пропил(оксо)-(хлор)ацетат 9,7 43,5 68,8 88,0 123,0 150,0
C5H7N (£)-2-Метилбут-2-еннитрил (нитрил тиглиновой кислоты) -25,5 9,2 36,7 58,2 99,7 122,0
c5h7n (7)-2-Метилбут-2-еннитрил (нитрил ангеликовой кислоты) -8,0 28,0 55,8 77,5 117,7 140,0
c5h7n 2-Этилакрило-нитрил -29,0 5,0 31,8 53,0 92,2 114,0
c5h7no2 Этилцианоацетат 67,8 106,0 133,8 152,8 187,8 206,0
с5н8 Изопрен -78,1 -51,6 -30,8 -14,2 16,7 34,1 -146,0
С5н8 с5н8 З-Метилбута-1,2-диен З-Мстилбут-1-ин -72,7 -46 -55 -25 -39,5 (4,00 кПа) -8 -19,4 23 40 26,4 -89,7
с5н8 Пента-1,2-диен -70,0 -42,6 -21,2 -4,3 27,2 44,9 -137,3
с5н8 (£)-Пента-1,3-диен (транс-пиперилен) -71,1 -45,1 -23,9 -7,1 24,3 42,0 -87,5
с5н8 (2)-Пента-1,3-диен (цис-пиперилен) -70,2 -43,1 -21,9 -5,0 26,4 44,1 -140,8
С5н8 Пента-1,4-Диен -82,7 -57,1 -37,0 -21,0 9,0 26,9 -148,3
С5н8 Пента-2,3-диен -65,2 -38,4 -17,4 -0,6 30,6 48,3 -125,7
С5н8 Пент-1-ин -70 -44 -28 (4,00 кПа) -7 40,2 -105,7
С5н8 Пент-2-ин -61 -32,8 -16,0 (4,00 кПа) 6,2 56,1 -109,3
С5н8 Спи-ро[2.2]пентан -73,5 46,9 -26,0 -9,4 21,5 39,0 -107,О*2
С5Н8 СзН8Вг4 Циклопентен 1,3-Дибром-2,2-бис(бромметил)-пропан -71,4 118,3 (тв.) -44,0 154,8 (тв.) -22,5 -5,5 222,5 26,3 44,2 301,2 -135,1
С5Н8О (Е)-2-Метилбут-2-еналь (тигли-новый альдегид) -25,0 10,0 37,0 57,7 95,5 116,4
с5н8о2 5-Метилдигид-рофуран-2(3 Н)-он (у-валеролактон) 37,5 79,8 101,9 136,5 182,3 207,5
С5Н8О2 Метилметакрилат -29,8 1,5 25,5 45,6 82 101,2
с5н8о2 4-Оксопентаналь (левулиновый альдегид) 28,2 68,0 98,3 121,8 164,0 187,0
С5Н8О2 (Е)-2-Метилбут-2-еновая кислота (тиглиновая кислота) 52,0 (тв.) 90,2 119,0 140,5 179,2 198,5 64,5
168
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Г11Л. °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
с5н8о2 Этилакрилат -29,5 2,0 26,0 44,5 80,0 99,5 -71,3
с5н8о2 2-Этилакриловая кислота 47,0 82,0 108,1 127,5 160,7 179,2
С5Н8Оз 4-Оксопентановая кислота (левулиновая кислота) 102,0 141,8 169,5 190,2 226,4 245,8 (разл.) 33,5
с5н8о4 Пентандиовая кислота (глутаровая кислота) 155,5 196,0 226,3 247,0 283,5 303,0 97,5
с5н8о4 Диметилмалонат 35,0 72,0 100,0 121,9 159,8 180,7 -62
С5Н9С1О2 Изопро-пил(хлор)ацетат 3,8 40,2 68,7 90,3 128,0 148,6
С5Н9С1О2 Этил-2-хлорпропаноат 6,6 41,9 68,2 89,3 126,2 146,5
c5h9n Пентаннитрил (валеронитрил) -6,0 30,0 57,8 78,6 118,7 140,8
С5Н,о 2-Метилбут-1 -ен -79,5 -64,5 -37,5 (4,00 кПа) -16,5 13,9 31,2 -137,6
С5Н,о 2-Метилбут-2-ен -74,5 -47,7 -26,7 -10,1 21,0 38,6 -133,8
С5Н,о 3-Метил бут-1-ен -88,3 -62,9 -42,8 -26,8 3,1 20,1 -168,5
С5Н,о Пент-1-ен (амилен) -80,3 -54,5 -34,1 -17,8 12,7 30,0 -165,2
с5н10 (2)-Пент-2-ен -75,2 -48,8 -28,0 -11,4 19,5 36,9 -151,4
С5Н,о (£)-Пент-2-ен -76,0 -49,4 -28,6 -12,0 18,9 36,3 -140,2
С5Н,о Циклопентан -68,0 -40,3 -18,6 -1,3 31,0 49,3 -93,8
С5Н10С12О 2-Хлор-1-(2-хлорэток-си)пропан 29,8 70,0 101,5 125,6 169,8 194,1
С5Н10С12О 1-Хлор-2-(2-хлорэток-си)пропан 24,7 63,0 92,4 115,8 156,5 180,0
С5Н10С12О2 1-Хлор-2-[(2-хлорэток-си)метокси]этан 53,0 94,0 125,5 149,6 192,0 215,0
с5н|0о З-Метилбутан-2-он -19,9 8,3 29,6 45,5 73,8 88,9 -92
с5н10о Пентан-2-он -12,0 17,9 39,8 56,8 85,8 103,3 -77,8
С5н10о Пентан-З-он -12,7 17,2 39,4 56,2 86,3 102,7 -42
CsHio02 Бутилформиат -26,4 6,1 31,6 51,0 86,2 106,0
CsHi0O2 втор-Бутилформиат -34,4 -3,1 21,3 40,2 75,2 93,6
CsHio02 трет-Бутилформиат -32,7 -1,2 23,4 42,8 78,2 98,0
c5H10o2 4-Гидрокси-З-метилбутан-2-он 44,6 81,0 108,2 129,0 165,5 185,0
c5H10o2 Изобутилформи-ат -32,7 -0,8 24,1 43,4 79,0 98,2 -95,3
CsHio02 Изопропилацетат -38,3 -7,2 17,0 35,7 69,8 89,0
CsH]o02 Метил бутират -26,8 5,0 29,6 48,0 83,1 102,3
CsHI0O2 З-Метилбутано-вая кислота (изо-валериановая кислота) 34,5 71,3 98,0 118,9 155,2 175,1 -37,6
Физические свойства важнейших веществ
169
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара °с
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С5Н10О2 Метил-2 -метилпропаноат (метилизобутират) -34,1 -2,9 21,0 39,6 73,6 92,6 -84,7
С5Н|о02 Пентановая кислота (валериановая кислота) 42,2 79,8 107,8 128,3 165,0 184,4 -34,5
С5Н10О2 Пропилацетат -26,7 5,0 28,8 47,8 82,0 101,8 -92,5
С5Н10О2 Этилпропаноат -28,0 3,4 27,2 45,2 79,8 99,1 -72,6
СзНюОз С5Н10О4 Диэтилкарбонат (2,3-Дигидрокси-пропил)ацетат (моноацетин) -10,1 109,2 23,8 151,2 49,5 69,7 203,6 105,8 125,8 261,7 -43
C5HI0S 2-Метилтетрагидротиофен -12,0 22,9 43,8 (4,00 кПа) 71,2 133,2 -100,7
C5H10S З-Метилтетра-гидротиофен -8,6 27,0 48,1 (4,00 кПа) 75,9 138,7 -81,2
c5H10s Т етрагидро-(2//)-тиопиран (пен-таметиленсуль-фид) -6,3 (тв.) 29,1 50,3 (4,00 кПа) 78,3 141,8 19,0
С5НиВг 1-Бром-З-метилбутан -20,4 13,6 39,8 60,4 99,4 120,4
C5HHI 1-Иод-3-метилбутан -2,5 34,1 62,3 84,4 125,8 148,2
C5HhN Пиперидин 3,9 29,2 49,0 85,7 106,0 -9
с5нико2 Изобутилкарба-мат 96,4 125,3 147,2 186,0 206,5 67
c5hhno3 3-Метил -бутилнитрат (изоамилнитрат) 5,2 40,3 67,6 88,6 126,5 147,5
c5H12 Изопентан (2-метилбутан) -82,8 -56,9 -36,5 -20,1 10,5 27,8 -159,9
C5H12 Неопентан (2,2-диметилпропан) -102 (тв.) -76 (тв.) -56 (тв.) -39 (тв.) -7 9,5 -16,6
С5н12 Пентан -76 -50,1 -29,3 -12,6 18,5 36,1 -129,7
С5Н12О З-Метилбутан-1-ол 10,0 40,8 63,4 80,7 113,7 130,6 -117,2
С5н12о Пентан-1-ол 13,6 44,9 68,0 85,8 199,8 137,8
С5Н12О Пентан-2-ол 1,5 32,2 54,1 70,7 102,3 199,7
С5н12о 2-Метилбутан-2-ол -12,9 (тв.) 17,2 38,8 55,3 85,7 101,7 -11,9
С5н12о 1 -Этоксипропан (этилпропиловый эфир) -64,3 -35,0 -12,0 6,8 41,6 61,7
с5н12о3 Пентан-2,3,4-триол 155,0 204,5 239,6 263,5 307,0 327,2
C5Hi4OSi Триме-тил(этокси)силан -50,9 -20,7 3,7 22,1 56,3 75,7
C5Hi4Si Триме-тил(этил)силан -60,6 -31,8 -9,0 9,2 42,8 62,0
c5Hl4sn Триме-тил(этил)станнан -30,0 3,8 30,0 50,0 87,6 108,8
170
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара г„л, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
с6 C6CI4O2 2,3,5,6- 70,7 (тв.) 97,8 (тв.) 116,1 129,5 151,3 162,6 (тв.) 290
C6F12 C&F и Т етрахлорбензо-1,4-хинон (хлоранил) Додекафторциклогексан Т етрадекафтор- -55,5 (тв.) -87,1 -27,1 (тв.) -57,8 (тв.) -30,1 (тв.) 9,8 (тв.) -13,5 (тв.) 52,8 (тв.) 8,3 62,9*2 -87,1
CeFu С6С16 гексан 2-(Трифтор-метил)ундека-фторпентан Г ексахлорбензол -58,3 144,4 (тв.) -30,5 166,4 (тв.) (4,00 кПа) -13,7 (4,00 кПа) 206,0 8,3 235,5 283,5 57,7 309,4 227
С6НС15 Пентахлорбензол 98,6 144,3 (тв.) 178,5 205,5 251,0 276,0 85,5
С6НС15О Пентахлорфенол ТВ. ТВ. 209,5 236,7 284,1 309,2 189,6
С6Н2ВгС13О З-Бром-2,4,6- 112,4 163,2 200,5 (разл.) 229,3 (разл.) 289,0 (разл.) 305,8
С6Н2С14 трихлорфенол 1,2,3,4- 68,5 114,7 149,2 175,7 225,5 254,0 46,5
С6Н2С14 Т етрахлорбензол 1,2,3,5- 58,2 104,1 140,0 168,0 220,0 246,0 54,5*2
С6Н2С14 С6Н2С14О Т етрахлорбензол 1,2,4,5- Т етрахлорбензол 2,3,4,6- 100,0 145,3 146,0 179,1 173,5 205,2 220,5 250,4 245,0 275,0 139 69,5
С6Н3ВгС12О Т етрахлорфенол 2-Бром-4,6- 84,0 130,8 165,8 193,2 242,0 268,0 68
С6Н3С13 дихлорфенол 1,2,3-Трихлор- 40,0 (тв.) 85,6 119,8 146,0 193,5 218,5 52,5
С6Н3С13 бензол 1,2,4-Трихлор- 43,1 84,8 109,5 141,7 187,7 213,5 16,9
С6Н3С13 бензол 1,3,5-Трихлор- 49,9 (тв.) 78,0 (4,00 кПа) 110,8 136,0 183,0 208,4 63,5
С6Н3С13О бензол 2,4,5-Трихлор- 72,0 117,3 151,5 178,0 226,5 251,8 62
С6Н3С13О фенол 2,4,6- 76,5 120,4 152,2 177,8 222,5 246,0 68,5
С6Н4ВгС1 Трихлорфенол 1-Бром-4- 32,0 72,7 103,8 128,0 162,5 196,9
СбЩВгг хлорбензол 1,2-Дибром- 49,2 91,1 117,6 150,8 225,5 7,1
СбРЦВгг бензол 1,4-Дибром- 61,0 (тв.) 87,7 (4,00 кПа) 120,8 146,5 192,5 218,6 87,5
C6H4C1F С6Н4С12 бензол 1-Фтор-3-хлорбензол 1,2-Дихлор- -21,2 20,0 16,1 58,4 88,4 66,3 112,0 155,9 127,5 180,6 -17,0
С6Н4С12 бензол 1,3-Дихлор- 16 53,3 75,9 105,6 149,0 173,1 -24,8
С6Н4С12 бензол 1,4-Дихлор- 16,7 (тв.) (4,00 кПа) 83,4 106,6 149,8 174,1 53,0
С6Н4С12О бензол 2,4-Дихлорфенол 53,0 92,8 123,4 146,0 187,5 210,0 45,0
С6Н4С12О 2,6-Дихлорфенол 59,5 101,0 131,6 154,6 197,7 220,0
Физические свойства важнейших веществ
171
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Г,|л, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
c6h4ci3n 2,4,6- 134,0 170,0 195,8 214,6 246,4 262,0 78
С6Н4О2 C6H5AsC12 Трихлоранилин Бензо- 1,4-хинон Фенил(дихлор)- 47,0 (тв.) 61,8 78,5 (тв.) 116,0 151,0 118,9 178,9 228,8 181,8 256,5 112,9
С6Н5Вг арсин Бромбензол 3,7 42,1 61,7 90,5 132,3 145,1 -30,8
С6Н5С1 Хлорбензол 13,0 21,6 (4,00 кПа) 42,4 69,8 110,0 131,7 -45,6
С6Н5С1О 2-Хлорфенол 18,5 56,4 (4,00 кПа) 79,0 108,5 149,8 174,9 7
С6Н5С1О 3-Хлорфенол 44,2 86,1 (4,00 кПа) 118,0 1434,0 188,7 214,0 32,5
С6Н5С1О 4-Хлорфенол 49,8 92,2 125,0 150,0 196,0 220,0 42
C6H5C1O2S Бензолсульфо- 65,9 112,0 147,7 174,5 224,0 251,5 (разл.) 14,5
С6Н5С12О2Р нилхлорид Фенилдихлор- 66,7 110,0 143,4 168,0 213,0 239,5
C6H5Cl3Si фосфат Фенил(трихлор)- 32 75,3 105,9 130,3 175,5 201,0
c6h5f силан Фторбензол -10,7 7,5 31,3 65,7 85,1 -41,9
C6H5F3Si Фенил(трифтор)- -31,0 0,8 (4,00 кПа) 25,4 44,2 78,7 98,3
с6н51 силан Иодбензол 24,9 64,0 94,4 118, 163,9 188,3 -31,3
c6h5no2 Нитробензол 43,1 83,9 108,2 139,8 185,8 210,8 5,7
c6h5no3 2-Нитрофенол 49,3 90,4 (4,00 кПа) 122,1 146,4 191,0 214,5 45
c6H6 Бензол -45 (тв.) -11,6 (тв.) 7,5 26,1 60,6 80,1 5,5
c6H6 Гекса-1,5-диен-З- -46,5 -14,4 10,2 29,3 64,3 83,5
C6H6C1N ин (дивинилацетилен) 2-Хлоранилин 44,3 84,6 108,4 139,5 183,7 208,8 -3,5
C6H6C1N З-Хлоранилин 59,3 101,2 (4,00 кПа) 126,0 158,2 204 229,9 -10,3
C6H6C1N 4-Хлоранилин 49,3 (тв.) 102,1 (4,00 кПа) 135,0 159,9 206,6 230,5 70,5
C6H6C16 (Ir, 2R, 35,4г, 57?, 130 176,1 204,0 240,5 323,4 112,5
c6h6n2o2 65)-1,2,3,4,5,6-Г ексахлорцикло-гексан (у-гексахлор-циклогексан) 2-Нитроанилин 104,0 150,4 (4,00 кПа) 186,0 213,0 260,0 284,5 (разл.) 71,5
c6h6n2o2 3-Нитроанилин 119,3 167,8 204,2 232,1 280,2 305,7 (разл.) 114
c6h6n2o2 4-Нитроанилин 142,4 (тв.) 194,4 234,2 261,8 310,2 336,0 (разл.) 146,5
c6H6o Фенол 33,6 (тв.) 70,9 92,8 120,7 (разл.) 160,0 181,8 40,9
c6H6o2 Пирокатехин 118,3 (4,00 кПа) 150,6 176,0 221,5 245,5 105
C6H6O2 Резорцин 108,4 (тв.) 152,1 185,3 209,8 253,4 276,5 110,7
c6H6o2 Гидрохинон 132,4 (тв.) 163,5 (тв.) 192,0 216,5 262,5 286,2 170,3
c6H6o3 c6H6s Пирогаллол Бензолтиол 98,8 (тв.) 8,4 177,3 46,4 69,3 238,6 99,5 309,0 (разл.) 168,7 133 -14,8
c6h7n (тиофенол) Анилин 31,0 68,2 (4,00 кПа) 96,9 119,4 160,9 184,0 -6,3
172
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара л, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
c6h7n 2-Метилпиридин -11,1 24,4 51,2 71,4 108,4 128,8 -70
(а-пиколин)
c6h7no 4-Аминофенол 139,2 (тв.) 169,5 (тв.) 284,0 (разл.) 185
C6H8CI2O4 Этан-1,2-диилбис- 112,0 158,0 191,0 215,0 259,5 283,5
(хлорацетат)
c6h8n2 Бензол-1,2-диамин (м-фе-нилендиамин) 99,8 147,0 182,5 209,9 259,0 285,5 62,8
c6h8n2 Фенилгидразин 72,8 115,0 139,9 (4,00 кПа) 172,1 218 243,1 (разл.) 19,6
C6H8O3 З-Метилдигидро-2/7-пиран-2,6(3//)-дион (а-метилглутаровый 93,8 141,8 177,5 205,0 255,5 282,5
ангидрид)
c6H8o3 3,3-Дигидро-фуран-2,5-дион 61,4 102,0 132,3 155,3 197,5 219,5
C6H8O4 Диметилма- 45,7 86,4 117,2 140,3 182,2 205,0
леинат
c6H8o4 Диметил фумарат 44,7 85,3 137,8 198,6
c6H8s 2,3-Диметил- -6,2 29,3 50,5 78,4 141,6 -49,0
тиофен (4,00 кПа)
c6H8s 2,4-Диметил- -5,3 29,9 51,0 78,5 140,7
тиофен (4,00 кПа)
c6H8s 2,5-Диметил- -8,8 26,2 47,1 74,6 136,7 -62,6
тиофен (4,00 кПа)
c6H8s 3,4-Диметил- -4 32 53,4 81 145
тиофен (4,00 кПа)
c6H8s 2-Этилтиофен -10 24 45,3 (4,00 кПа) 72 134
c6H8s 3-Этилтиофен -9 26 46,5 (4,00 кПа) 74 136 -89,1
СбНю Гекса-1,2-диен -47,1 -17,7 0,1 (4,00 кПа) 23,4 76
СбН,о (£)-; (2)-Гекса- -49,2 -20,0 -2,4 20,8 73
1,3-диен (4,00 кПа)
c6H10 (£)-; (2)-Гекса- -54,7 -26,2 -8,9 13,8 65
1,4-диен (4,00 кПа)
СбН1о Гекса-1,5-диен -58,6 -30,4 -13,4 9,0 59,5 -140,7
(диаллил) (4,00 кПа)
СбНю Гекса-2,3-диен -52,7 -23,9 -6,5 16,4 68,0
(4,00 кПа)
С6н1о (2Z,4Z)-; (2Z,4£)-; -44,3 -14,6 -3,3 26,9 80
(2Е,4£)-Гекса-2,4- (4,00 кПа)
диен
СбН10 Гекс-1-ин (бу- -52,2 -22,9 -5,2 18,2 71,3 -132,1
тилацетилен) (4,00 кПа)
С6н]о 2,3-Диметил- -52,1 -23,2 -5,8 17,1 68,8 -76,0
бута-1,3-диен (4,00 кПа)
СбНю (£)-; (Z)-3- -46,4 -16,9 0,9 24,3 77
Метилпента-1,3- (4,00 кПа)
диен
СбНю З-Метилпента- -61,6 -33,8 -17,0 5,1 55
1,4-диен (4,00 кПа)
Физические свойства важнейших веществ
173
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
с6н10 СбНю С6Н10 1 -Метилцикло-пентен З-Метилцикло-пентен 4-Метилцикло-пентен -50,3 -57,4 -50,7 -20,6 -28,5 -21,0 -2,5 (4,00 кПа) -11,0 (4,00 кПа) -2,9 (4,00 кПа) 21,4 12,2 20,9 75,8 65,0 75,2 -127
СбНю СбН]0 Циклогексен 2-Этилбута-1,3-диен -45,5 -47,8 -15,1 -18,5 8,7 -0,7 (4,00 кПа) 27,6 22,5 63,0 83,0 75 -103,5
С6Н10С12О2 с6н]0о Изобутил-(дихлор)ацетат 4-Метилпент-З-ен-2-он (окись мезитила) 28,6 67,5 23,6 96,7 119,8 70,9 160,0 109 183,0 129,6 -59
с6н10о Циклогексанон 1,4 38,7 67,8 90,4 132,5 155,6 -45,0
СбН10О2 4-Изопропил оксетан-2-он (изокапролактон) 38,3 80,3 112,3 137,2 182,1 207,0
С6Н10Оз Метил-4-оксопентаноат 39,8 79,7 109,5 133,0 175,8 197,7
С6Н10О3 Пропионовый ангидрид 20,6 57,7 85,6 107,2 146,0 167,0 -45
С6Н10О3 Этил-3-оксо-бутаноат(ацетоуксусный эфир) 28,5 67,3 96,5 118,5 158,2 180,8 (разл.) -45
С6Н10О4 с6н10о4 Адипиновая кислота Диэтилоксалат 159,5 30,0 205,5 70,1 240,5 265,0 115,6 312,5 337,5 183,9 152 -40,6
с6н10о4 Этан-1,2-диилдиацетат 38,3 77,1 106,1 128,0 168,3 190,5 -31
с6н10о5 Диметил-(5)-2-гидроксибутан-диоат 75,4 118,3 150,1 175,1 219,5 242,6
С6Н10О6 Диметил-(2/?,3/?)-тартрат (диметиловый эфир L-винной кислоты) 102,1 148,2 182,4 208,8 255,0 280,0 61,5
С6НюО6 Диметил -рац-(2/?,37?)-тартрат (диметиловый эфир DL-винной кислоты) 100,4 147,5 182,4 209,5 257,4 282,0 89
c6H10s Диаллилсульфид -9,5 26,6 54,2 75,8 116,1 138,6 -83
C6H10Cl2Si Диаллилдихлор-силан 9,5 47,4 76,4 99,7 142,0 165,3
C6HnBr Бромциклогексан 7,3 45,5 68,3 (4,00 кПа) 98,3 164 -56,5
C6HUC1O2 в/иор-Бутил-(хлор)ацетат 17,0 54,6 83,6 105,5 146,0 167,8
C6HUN Гексаннитрил (капронитрил) 9,2 47,5 76,9 99,8 141,0 163,7
c6H12 Гекс-1-ен -57,9 -29,3 -6,8 11,1 44,6 63,5 -139,8
СбН12 (Е)-Гекс-2-ен -54,9 -25,9 8,3 (4,00 кПа) 15,0 48,9 67,9 -133,0
174
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара 7™, °с
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53.3 кПа 101.3 кПа
с6н12 (2)-Гекс-2-ен -54,2 -25,1 -7,5 (4,00 кПа) 15,9 49,9 68,9 -141,1
С6н12 (Е)-Гекс-З-ен -55,5 -26,5 -8,9 (4,00 кПа) 14,3 48,2 67,1 -113,4
С6Н|2 (2)-Гекс-3-ен -55,9 -27,0 -9,4 (4,00 кПа) 13,8 47,5 66,4 -137,8
С6н12 2,2-Диметилбут- 2-ен -73,4 -46,4 -30,0 (4,00 кПа) -8,3 23,0 41,2 -115,2
С6н,2 2,3-Диметилбут-2-ен -51,3 -21,8 -4,0 (4,00 кПа) 19,6 54,1 73,2 -74,3
С6Н12 (Е)-3-Метил пент-2-ен -53,2 -24,0 -6,2 (4,00 кПа) 17,2 51,4 70,4 -138,4
С6н12 (2)-3-Мстилпент-2-ен -55,1 -26,1 -8,5 (4,00 кПа) 14,8 48,7 67,7 -134,8
С6н12 4-Метилпент-1-ен -64,5 -36,6 -19,6 (4,00 кПа) 2,8 35,2 53,9 -153,6
С6н12 Метилциклопентан -53,2 -23,7 -0,6 17,9 52,3 71,8 -142,4
С6Н12 2-Этилбут-1 -ен -57,1 -28,3 -10,8 (4,00 кПа) 12,2 45,9 64,7 -131,5
С6н12 Циклогексан -47,0 (тв.) 17,0 (тв.) 6,7 25,5 60,8 80,7 6,6
С6Н12С12О2 1-Хлор-2-[2-(2-хлорэток-си)этокси]этан 56,2 97,6 127,8 150,7 190,5 212,6
С6Н12О Гексан-2-он 7,7 38,8 62,0 79,8 111,0 127,5 -56,9
С6н12о С6н12о С6н12о З-Изо-пропоксипроп-1-ен 2-Метилпентан-3-он 4-Метилпентан-2-он -43,7 -12,9 10,0 13,0 10,9 29,0 56,9 58,2 61,7 79,5 113,4 115,5 -84,7
С6Н12О З-Пропоксипроп- 1-ен -39,0 -7,9 16,4 35,8 71,4 90,5
С6н12о Циклогексанол 21,0 (тв.) 56,0 83,0 103,7 141,4 161,0 23,9
С6н12о2 Гексановая кислота (капроновая кислота) 71,4 99,5 125,0 144,0 181,0 202,0 -1,5
С6Н12О2 4-Г идрокси-4-метилпентан-2-он (диацетоновый спирт) 22,0 58,0 86,7 108,2 147,5 167,9 -47
СбН12О2 Изобутилацстат -21,2 12,8 39,2 59,7 97,5 118,0 -98,9
С6н12о2 (3 -Мети лбутил)-формиат (изо-амилформиат) -17,5 17,1 44,0 65,4 102,7 123,3
С6Н12О2 Метил-3-метил-бутаноат (метилизовалерат) -19,2 14,0 39,8 59,8 96,7 116,7
С6н12о2 4-Метилпентановая кислота (изокапроновая кислота) 66,2 94,0 120,4 141,4 181,0 207,7 -35
С6Н12О2 Пропилпропио-нат -14,2 19,4 45,0 65,2 102,0 122,4 -76
С6н12о2 Этилбутират -18,4 15,3 41,5 62,8 100,0 121,0 -93,3
Физические свойства важнейших веществ
175
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара г„л, °C
0,133 кПа 1.33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С6н|2о2 Этилизобутират -24,3 8,4 33,8 53,5 90,0 110,1 -88,2
С6Н12О3 ewo/j-Бутил- 28,3 66,0 94,2 116,4 155,6 177,5
С6н12о3 (гидрокси)ацетат {втор-бутилгликолят) 2,4,6-Триметил- -9,4 (тв.) 24,1 (тв.) 49,5 (тв.) 69,0 (тв.) 104,3 122
C6H12S 1,3,5-триоксан (паральдегид) (27?,55)-2,5- -5,5 29,9 51,5 79,0 (тв.) 142,3 -89,4
c6H12s Диметилтетрагидротиофен /яп/-(2/?,5/?)-2,5- -7,0 28,8 (4,00 кПа) 50,3 78,3 142,0 -76,4
c6H12s Диметилтетрагидротиофен 2-Метилтетра- -0,3 36,4 (4,00 кПа) 58,4 87,2 153,0 -58,1
c6H12s гидро-2//-тиопиран 3-Метилтетра- 2,7 40,0 (4,00 кПа) 62,4 91,7 158,0 -60,2
c6H12s гидро-2//-тиопиран 4-Метилтетра- 3,4 40,6 (4,00 кПа) 52,8 92,1 158,6 -28,1
c6H12s c6H12s C6H14 гидро-2//-тиониран 2-Этилтетрагидротиофен 3-Этилтетра-гидротиофен Г ексан 4 8,9 -54 41 46,4 -25,0 (4,00 кПа) 63 (4,00 кПа) 68,8 (4,00 кПа) -2,3 91 98,2 15,8 49,6 157 165 68,7 -95,3
C6H14 2,2-Диметил- -69,3 -41,5 -19,5 -2,0 31,0 49,7 -99,7
C6H14 бутан 2,3-Диметил- -63,4 -34,9 -12,5 5,4 38,9 58,0 -128,4
C6H,4 бутан 2-Метилпентан -60,6 -32,1 -9,8 8,1 41,4 60,3 -153,7
c6H14 (изогексан) З-Метилпентан -58,9 -30,1 -7,5 10,5 44,2 63,3 -118
C6H14O Гексан-1-ол 24,4 58,2 83,7 102,8 138,0 157,0 -51,6
C6H14O Гексан-2-ол 14,6 45,0 67,9 87,3 121,8 139,9
C6H14O Гексан-З-ол 2,5 36,7 62,2 81,8 117,0 135,5
C6H14O Диизопропило- -57,0 -27,4 -4,5 13,8 49 68,4 -60
СбН14О вый эфир Дипропиловый -43,3 -11,8 13,2 33,0 69,5 89,5 -122
СбН14О эфир 2-Метилпентан- 15,4 49,6 74,7 94,2 129,8 147,9
C6H14O 1-ол 2-Метилпентан- -4,5 27,6 51,3 69,2 102,6 121,1
СбН14О 2-ол З-Метилпентан- -0,3 33,3 58,2 78,0 113,5 131,7
СбН14О2 1-ол 1,1 -Диэтоксиэтан -23,0 8,0 31,9 50,1 84,0 102,2
С6Н14О2 (ацеталь) 1,2-Диэтоксиэтан -33,5 1,6 29,7 51,8 94,1 119,5
176
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки ( °C) при давлении насыщенного пара Т °C
0,133 кПа 1,33 кПа 5.33 кПа 13.3 кПа 53.3 кПа 101.3 кПа
СбНиОз 1 -Метокси-2-(2- 5,4 44,7 97,0 159,6
метоксиэток-
си)этан (диметиловый эфир диэтиленгликоля)
С6Н14О3 1 -(2-Этоксиэток- 45,3 85,8 116,7 140,3 180,3 201,9
си)этанол
С6Н]4О3 1,1'- 73,8 116,2 147,4 169,9 210,5 231,8
Оксидипропан-2-
ол (дипропи-ленгликоль)
С6Н|4О4 2,2’-[Этан-1,2- 114,0 158,1 191,3 214,6 256,6 278,3
ди ил-
бис(окси)]диэта-нол (триэтилен-
гликоль)
C6H14Zn Дипронилцинк -9,8 28,0 78,5
С6Н15А1 Триэтилалюман 48,7 90,1 143,7
C6H15ClSi Триэтилхлорси- -4,9 32,0 60,2 82,3 123,6 146,3
лан
C6H15Ga Триэтилгаллан -5,7 32,0 82,2 142,4
c6h15n H,N- -45,1 -12,8 30,2
Диэтилэтанамин
(триэтилами н)
с6н15о4р Триэтилфосфат 84,4 116 142,1 187,0 210,8
C6H15Sb Триэтилстибан 3,0 43,0 96,5 161,4
С6Н15Т1 Триэтилталлан 9,3 51,7 85,4 1121 163,5 192,1 (разл.) -63,0
C6H16OSi Т риэтилсиланол 18,7 54,9 101,4 154,0
C^H^C^Si Диметил(ди-этокси)силан -19,1 13,3 38,0 57,6 93,2 113,5
C6H16Si Триметил-(пропил)силан -46,0 -13,9 11,3 31,6 69,2 90,0
C6H16Sn Триметил-(пропи л)стан нан -12,0 21,8 48,5 69,8 109,6 131,7
c6h18bn3 Г ексаметилбор- 0,6 37,9 86,6 147,6
ный гриамид
C6H18Cl2O2Si3 Тексам ети л-1,5-дихлортрисилок- 26,0 56,1 94,8 118,2 160,2 184,0 -53
сан
C6H18OSi2 Г ексаметилдиси- -20,0 2,8 45,6 99,2
локсан
СбН18О3813 2,2,4,4,6,6-Гекса-метил-1,3,5,2,4,6-триоксатрисили- 35,7 (тв.) 78,7 114,7 134,0 64
нан
c7
C7H3C1F3NO2 2-Нитро-4- 58,2 98,3 122,1 153,2 222,6 -2,5
(трифторметил)- (4,00 кПа)
1-хлорбензол
c7h3cif3no2 4-Нитро-2- 63,1 104,4 128,9 160,7 231,9 21,7
(трифторметил)- (4,00 кПа)
1 -хлорбензол
c7h3ci2f3 4-(Трифтор-метил)-1,2-дихлорбензол 11,0 52,2 84,0 109,2 150,5 172,8 -12,1
Физические свойства важнейших веществ
177
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53.3 кПа 101,3 кПа
С7Н3С15 3-(Трихлор-метил)-1,2-дихлорбензол 95 140,1 167,3 (4,00 кПа) 202,9 283,1 25,8
C7H4C1F3 1-(Трифтор-метил)-2-хлорбензол 0,0 37,1 65,9 88,3 130,0 162,2 -6,0
С7Н4С14 1-(Трихлор-метил)-3-хлорбензол 77,0 122,6 149,7 (4,00 кПа) 185,0 264,3 29,4
C7H4F3NO2 1 -Нитро-3 -(трифтормс-тил)бензол 42 81,6 104,8 (4,00 кПа) 135,1 202,8 -132
С7Н5ВгО Бензоилбромид 47,0 89,8 122,6 147,7 193,7 218,5 0
С7Н5С1О Бензоилхлорид 32,1 73,0 103,8 128,0 172,8 197,2 -0,5
С7Н5С1О 2-Хлорбснзаль-дсгид 43,5 84,3 108,6 (4,00 кПа) 140,4 211,9 12,2
С7Н5С1з 2,4-Дихлор-1-(хлорме-тил)бензол 69,4 113,0 138,9 (4,00 кПа) 172,6 248,0 -2,6
С7Н5С1з (Трихлорме-тил)бензол (бензотрихлорид) 45,8 87,6 119,8 144,3 189,2 213,5 -21,2
c7h5f3 (Трифторме-тил)бензол (бензотрифторид) -30,6 (тв.) 1,0 20,2 (4,00 кПа) 45,3 82,0 102,1 -29,1
c7h6f3n 3-(Трифтор-метил)анилин 35,8 73,8 96,3 (4,00 кПа) 125,6 191,1 5,7
c7h5n Бензонитрил 28,2 69,2 99,6 123,5 166,7 190,6 -12,9
c7h5n Изоцианобензол 12,0 49,7 78.3 101,0 142,3 165,0 (разл.)
c7h5no Фенилизоцианат 10,6 48,5 77,7 100,6 142,7 165,6
c7h5no3 2-Нитробенз-альдегид 85,8 133,4 168,8 196,2 246,8 273,5 40,9
c7h5no3 З-Нитробенз-альдегид 96,2 142,8 177,7 204,3 252,1 278,3 58
c7h5ns c7h5n3o6 Фенилизотиоцианат 2-Метил-1,3,5-тринитробензол (тротил) 47,2 149,7 89,8 195,8 122,5 147,3 267,8 194,0 218,5 -21,0
C7H6C12 (Дихлорме-тил)бензол (бензальхлорид) 35,4 78,7 112,1 138,3 187,0 214,0 -16,1
C7H6C12 4-Метил-1,2-дихлорбензол 41,4 81,8 105,9 (4,00 кПа) 134,5 208,9 -15,3
c7H6o Бензальдегид 26,2 62,0 90,1 112,5 154,1 179,0 -26
c7H6o2 Бензойная кислота 96,0 (тв.) 132,1 162,6 186,2 227,0 249,2 121,7
c7H6o2 2-Гидрокси-бензальдегид (салициловый альдегид) 33,0 73,8 105,2 129,4 173,7 196,5 -7
c7H6o2 4-Гидрокси-бензальдегид 121,2 169,7 206,0 233,5 282,6 310,0 115,5
178
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Т11Л, °с
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С7Н6О3 2-Гидрокси-бензойная кислота (салициловая кислота) 113,7 (тв.) 146,2 (тв.) 172,2 193,4 230,5 256,0 159
С7Н7Вг (Бромме-тил)бензол 32,2 73,4 104,8 129,8 175,2 198,5 —4
С7Н7Вг 1-Бром-2-метилбензол 20,5 59,1 82,3 (4,00 кПа) 112,7 157,3 181,7 -27,7
С7Н7Вг 1-Бром-3 -метилбензол 14,8 64,0 93,9 117,8 160,0 183,7 -39,8
С7Н7Вг 1 -Бром-4-метилбензол 22,9 (тв.) 61,9 85,2 (4,00 кПа) 115,6 160 184,4 24,8
С7Н7ВгО 1 -Бром-4-метоксибензол 48,8 91,9 125,0 150,1 197,5 223,0 12,5
С7Н7С1 1 -Метил-2-хлорбензол 5,4 43,2 65 (4,00 кПа) 94,7 137 159,3 -35,1
С7Н7С1 1-Метил-З-хлорбензол 4,8 43,2 73,0 96,3 139,7 162,3
С7Н7С1 1 -Метил-4-хлорбензол 5,5 (тв.) 43,8 73,5 96,6 139,8 162,3 7,3
С7Н7С1 (Хлорме-тил)бензол 22,0 60,8 90,7 114,2 155,8 179,4 -39
c7h7f 1 -Метил-2 -фторбензол -24,2 8,9 34,7 55,3 92,8 114,0 -80
c7h7f 1-Метил-З-фторбензол -22,4 11,0 37,0 57,5 95,4 116,0 -110,8
c7h7f 1 -Метил-4-фторбензол -21,8 11,8 37,8 58,1 96,1 117,0
c7h7i 1-Иод-2 -метилбензол 37,2 79,8 112,4 138,1 185,7 211,0
c7h7no2 1 -Метил-2 -нитробензол 50,0 93,8 126,3 151,5 197,7 222,3
c7h7no2 c7h7no2 1-Метил-3 -нитробензол 1 -Метил-4-нитробензол 50,2 96,0 98,9 130,7 156,9 159,9 206,8 231,9 233,1 15,5 51,9
c7H8 Толуол -26,1 6,4 31,8 51,9 89,5 110,6 -95,0
c7H8o Анизол (метилфениловый эфир) 5,4 42,2 70,7 93,0 133,8 155,5 37,3
c7H8o о-Крезол 36,8 74,9 97,4 (4,00 кПа) 126,5 168 190,9 30,9
c7H8o .w-Крезол 47,2 86,0 108,7 (4,00 кПа) 138,0 179 202,2 11,5
c7H8o и-Крезол 46,9 85,7 108,4 (4,00 кПа) 137,7 179 201,9 34,8
c7H8o C7H8O2 Фенилметанол (бензиловый спирт) 2-Метокс ифенол (гваякол) 50,5 89,2 83,0 111,9 (4,00 кПа) 141,2 136,0 183 205,1 205,0 -15,2 28,3
C7H8O3 c7h8s Этил-2-фуроат (Метилсульфа-нил)бензол (ме-тилфенилсуль-фид) 37,6 35 77,1 74 107,5 97 (4,00 кПа) 130,4 127 172,5 195,0 193 34
Физические свойства важнейших веществ
179
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара т1Ш, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
c7H8s 2-Метилбензол- 27,2 67,1 91,0 122,5 194,2 15
тиол (4,00 кПа)
c7H8s З-Метилбензол- 27,8 67,8 91,8 123,3 195,1
тиол (4,00 кПа)
c7H8s 4-Метилбензол- 27,6 (тв.) 67,6 91,6 123,1 194,9 44
тиол (4,00 кПа)
C7H8Cl2Si Бензилдихлорси- 45,3 83,2 133,5 194,3
л ан
C7H8Cl2Si Метил(фенил) (дихлор)силан 35,7 77,4 145,2 205,5
C7H8Cl2Si л-Т ол ил(дихлор)- 46,2 84,2 135,5 196,3
силан
C7H9N А'-Метиланилин 36,0 76,2 106,0 129,8 172,0 195,5 -57
c7h9n 2-Метиланилин 41,0 80,1 103,3 133,4 177 200,2
(о-толуидин) (4,00 кПа)
c7h9n З-Метиланилин 42,9 82,3 105,7 136,0 181 203,4 -30,4
(л/-толуидин) (4,00 кПа)
c7h9n 4-Метиланилин 40,3 (тв.) 79,6 102,9 133,2 177 200,6 45
(и-толуидин) (4,00 кПа)
c7h9n Фенилметанамин 29,0 67,7 97,3 120,0 161,3 184,5
(бензиламин)
c7h9no 2-Метокси- 61,0 101,7 132,0 155,2 197,3 218,5 5,2
анилин
(о-анизидин)
c7h10n2 4-Метилбензол- 106,5 151,7 185,7 211,5 256,0 280,0 99
1,3-диамин
c7h10n2 л-Т олилгидразин 82,0 123,0 154,1 189,0 219,5 242,0 (разл.) 65,5
C7H,o03 3,3,4-Триметил-дигидрофуран- 53,5 97,4 131,0 156,5 205,5 231,0
2,5-дион
c7H10o4 Диметил-(Е)-2-метилбут-2-ендиоат (диметиловый эфир мезаконовой ки- 46,8 87,8 118,0 141,5 183,5 206,0
слоты)
С7Н]о04 Диметил-(7)-2-метилбут-2-ендиоат (диметиловый эфир цитраконовой 50,8 91,8 122,6 145,8 188,0 ?10 5 — - - 5-
кислоты)
С7НюО4 Диметил-2-метиленбутан-диоат (диметиловый эфир ита- 69,3 106,6 133,7 153,7 189,8 208,0 38
коновой кислоты)
c7H10s 2-Изопропил- 1 38 59,5 88 153
тиофен (4,00 кПа)
c7H10s 3-Изопропил- 4 41 62,5 91 157
тиофен (4,00 кПа)
c7H10s 2-Метил-З- 4 41 62,5 91 157
1 этилтиофен (4,00 кПа)
180
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Г,„„ °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
c7H10s 2-Метил-4- 8 45 67,1 96 163 -59
этилтиофен (4,00 кПа)
c7H10s 2-Метил-5- 5,7 42,8 64,9 94,0 160,1 -68,5
этилтиофен (4,00 кПа)
c7H10s 3-Метил-2- 7 44 65,8 95 161
этилтиофен (4,00 кПа)
c7H10s 2-Пропилтиофен 4,8 41,6 63,7 92,7 158,5
(4,00 кПа)
c7H10s 3-Пропилтиофен 6 43 65,6 95 161
(4,00 кПа)
c7H10s 2,3,4-Триметил- 13,5 51,6 74,5 104,5 172,7
тиофен (4,00 кПа)
c7H10s 2,3,5-Триметил- 9,6 46,8 69,0 98,2 164,5
тиофен (4,00 кПа)
c7H12 Гепт-1-ин -38,0 -6,0 13,6 39,6 99,7 -80,9
(4,00 кПа)
c7H12 1,2-Диметил- -30,7 1,5 21,0 46,9 105,8 -90,4
циклопентен (4,00 кПа)
C7H12 1,3-Диметил- -39,7 -8,6 10,2 35,2 92
циклопентен (4,00 кПа)
c7H12 1,4-Диметил- -40,2 -9,0 10,1 35,4 93,2
циклопентен (4,00 кПа)
c7H12 1,5-Диметил- -32,8 -1,0 18,4 43,9 102 -118
циклопентен (4,00 кПа)
c7H12 3,3-Димстил- 43,0 -12,2 6,5 31,3 88
циклопентен (4,00 кПа)
c7H12 4,4-Диметил- 43,0 -12,2 6,5 31,3 88
циклопентен (4,00 кПа)
c7H12 1 -Метилцикло- -27,6 4,9 24,6 50,7 110,0 -121
гексен (4,00 кПа)
c7H12 З-Метилцикло- -31,5 0,5 19,9 45,6 104,0
гексен (4,00 кПа)
c7H12 4-Метилцикло- -32,2 -0,4 19,0 44,5 102,7 -115,5
гексен (4,00 кПа)
c7H12 1 -Этил цикло- -30,3 1,9 21,5 47,4 106,3 -118,4
пентен (4,00 кПа)
c7H12 З-Этилцикло- -35,7 -42 15,0 40,3 98,1
пентен (4,00 кПа)
c7H12 4-Этилцикло- -31,0 1,2 20,8 46,8 106
пентен (4,00 кПа)
C7H12O2 Бутилакрилат -0,5 35,5 63,4 85,1 125,2 147,4 -64,6
C7H12O3 Этил-4-оксопен- 47,3 87,3 117,7 141,3 183,0 206,2
таноат
C7H12O4 Гептандиовая 163,4 212,0 247,0 272,0 318,5 342,1 103
кислота (пиме-
линовал кислота)
C7H12O4 Диэтилмалонат 40,0 81,3 113,3 136,2 176,8 198,9 -49,8
(малоновый
эфир)
с7н13сю Гептаноилхло- 34,2 64,6 86,4 102,7 130,7 145,0
рид
c7h13n Гептаннитрил 21,0 61,6 92,6 116,8 160,0 184,6
(энантонитрил)
С7Н14 Гепт-1-ен -36,9 -6,1 18,1 37,4 73,4 93,6 -119,0
Физические свойства важнейших веществ
181
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара гпл, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С7Н,4 (Е)-Г епт-2-ен -34,3 -3,0 16,1 (4,00 кПа) 41,1 98,0 -109,5
С7Н,4 (7)-Гепт-2-ен -33,9 -2,6 16,5 (4,00 кПа) 41,6 98,5
С7Н,4 (Е)-Гепт-З-ен -35,9 -4,7 14,0 (4,00 кПа) 39,1 95,7 -136,6
С7н14 (7)-Гепт-3-ен -35,8 -4,6 14,3 (4,00 кПа) 39,2 95,8
с7н14 2,3-Диметил- -47,4 -16,7 2,1 27,0 84,3 -134,3
пент-1 -ен (4,00 кПа)
С7Н,4 2,3-Диметил- -38,4 —6,6 12,8 38,5 97,5 -118,3
пент-2-ен (4,00 кПа)
С7Н,4 4,4-Диметил- -55,9 -26,1 -7,9 16,4 72,5 -136,6
пент-1-ен (4,00 кПа)
С7Н,4 (Е)-4,4-Диметил- -52,8 -22,7 -4,3 20,2 76,8 -115,2
пент-2-ен (4,00 кПа)
С7Н,4 (7)-4,4-Диметил- -50,2 -19,8 -1,2 23,5 80,4 -135,5
пент-2-ен (4,00 кПа)
с7н14 1,1 -Диметил-циклопентан -43,1 -12,3 11,9 31,2 67,4 87,8 -69,7
С7Н,4 (1/?,25)-1,2-Диметилцикло- -34,9 -3,3 21,6 41,5 78,6 99,5 -53,9
пентан
С7н14 paq-(]R,2R)-l,2-Диметилцикло- -40,1 -9,0 15,4 34,9 71,3 91,9 -117,6
пентан
с7н14 (1/?,35)-1,3-Диметилцикло- -40,3 -9,2 15,2 34,7 71,1 91,7 -133,7
пентан
С7н14 рац-{ 1 R,3R)~ 1,3-Диметилцикло- -41 -10,0 14,4 33,8 70,2 90,8 -133,9
пентан
С7н14 2-Метилгекс-2- -36,0 -4,8 14,0 38,9 95,4 -130,4
ен (4,00 кПа)
С7н14 4-Метилгекс-1 - -42,0 -11,5 7,0 31,4 86,7 -141,5
ен (4,00 кПа)
с7н14 (Е)-5-Метилгекс- -46,0 -15,2 3,6 28,6 86
2-ен (4,00 кПа)
с7н14 (Z)-5-Метилгекс - -42,5 -11,3 7,8 33,0 91
2-ен (4,00 кПа)
С7н14 Метилциклогек- -35,2 -3,2 22,0 42,1 79,6 100,9 -126,6
сан
с7н14 3-Метил-2- -43,9 -12,9 6,1 31,2 89
этилбут-1 -ен (4,00 кПа)
С7н14 2-Этилпент-1 -ен -40,2 -8,8 10,3 (4,00 кПа) 35,7 94
С7н14 З-Этилпент-1-ен -47,3 -16,5 2,3 (4,00’кПа) 27,4 85,1 -127,5
с7н14 З-Этилпент-2-ен -38,8 -7,3 12,0 (4,00 кПа) 37,5 96,0
с7н14 Этилциклопен- -32 -0,1 25,0 45,0 82,4 103,5 -138,4
тан
С7Н14О Гептаналь (энан-товый альдегид) 12,0 43,0 66,3 84,0 125,5 155,0 -42
С7Н14О Гептан-2-он 19,3 55,5 81,2 100,0 133,2 150,2
С7Н14О Г ептан-4-он 23,0 55,0 78,1 96,0 127,3 143,7 -32,6
182
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Т °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С7Н14О С7Н14О С7Н14О2 С7Н14О2 C7Hi4O2 С7Н]4О2 С7Н14О2 С7Н]4О2 С7Н14О2 С7Н14О2 С7н16 С7н16 С7н16 С7н16 С7н16 С7н16 С7н16 С7н16 С7н16 С7Н16О С7Н16О3 C7H18O3Si C7H18Si C7H18Si 2,4-Диметилпен-тан-3-он 2-Метилгексан-3-он Гептановая кислота (энантовая кислота) Изобутилпро-пионат Изопропил-2-метилпропаноат (изопропилизобутират) (З-Метил-бутил)ацетат (изоамилацетат) Метилгексаноат (метилкапронат) Пропилбутират Пропил-2-метилпропаноат (пропилизобутират) Этил-3-метил-бутаноат(этилизовалерат) Гептан 2,2-Диметил-пентан 2,3-Диметил-пснтан 2,4-Диметил-пентан 3,3-Диметил-пснтан 2-Метилгексан З-Мстилгсксан 2,2,3-Триметил-бутан 3-Этилпентан Гептан-1-ол Т риэтоксиметан (ортомуравьи-ный эфир) Метил-(триэтокси)силан Бутил-(триметил)силан Метил-(триэтил)силан 5,2 81,4 -2,3 -16,3 0,0 5,0 -1,6 -6,2 -6,1 -33 -48,7 -41,2 -47,0 -45,3 -39,7 -38,6 -49,3 (тв.) -37,8 42,4 5,5 -1,5 -23,4 36,7 27,1 113,2 32,3 17,0 35,2 42,0 34,0 28,3 28,7 -2,0 -18,6 -10,3 -17,0 -14,4 -9,1 -7,9 -18,8 -6,8 74,7 40,5 34,6 9,9 16,6 59,6 140 58,5 42,4 62,1 70,0 61,5 54,3 55,2 22,4 5,0 13,9 6,5 9,9 14,9 16,3 5,3 17,5 99,8 67,5 61,7 35,9 44,0 77,0 75,6 160,7 79,5 62,3 83,2 92,4 82,6 73,9 75,9 41,8 23,9 33,2 25,4 29,2 34,1 35,6 24,5 36,9 119,5 88,0 82,7 56,3 65,6 108,0 199,6 116,4 100,0 121,5 129,8 121,7 112,0 114,0 78,0 59,2 69,4 60,6 65,5 69,8 71,5 60,5 73,0 115,6 125,7 121,8 93,8 105,3 123,7 133,4 220,5 136,8 120,5 142,0 150,0 (разл.) 142,7 133,9 134,3 98,4 79,2 89,8 80,5 86,1 90,1 91,9 80,9 93,5 175,8 146,0 143,5 115,0 127,0 -10 -71 -95,2 -99,3 -90,6 -123,8 -135 -119,2 -134,5 -118,3 -119,4 -24,9 -118,6 34,6
С8 С8Н4С12О2 C8H4NO Фталоилдихлорид Бензоилцианид 44,5 134,2 85,5 170,0 116,6 197,8 141,0 248,3 185,0 281 208,0 16 33,5
Физические свойства важнейших веществ
183
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Twl, °с
0,133 кПа 1,33 кПа 5,33 кПа 13.3 кПа 53,3 кПа 101,3 кПа
С8Н40з 2-Бензофуран-1,3-дион (фталевый ангидрид) 96,5 (тв.) 134,0 172,0 202,3 256,8 284,5 130,8
C8H5C12N Фенил(ди-хлор)ацето-нитрил 56,0 98,1 130,0 154,5 199,5 223,5
С8Н5С15 Пентахлорэтил-бензол 96,2 148,0 186,2 216,0 269,3 299,0
С8Н6С12 1-Винил-2,3-дихлорбензол 61,0 104,6 137,8 163,5 210,0 235,0
С8Н6С12 1-Винил-2,4-дихлорбензол 53,5 97,4 129,2 153,8 200,0 225,0
С8Н6С12 1-Винил-3,5-дихлорбензол 53,5 97,4 129,2 153,8 200,0 225,0
С8Н6С12 2-Винил-1,3-дихлорбензол 47,8 90,0 122,4 147,6 193,5 217,0
С8Н6С12 2-Винил-1,4-дихлорбензол 55,5 98,2 131,0 155,8 202,5 227,0
С8Н6С12 4-Винил-1,2-дихлорбснзол 57,2 100,4 133,7 158,2 205,7 230,0
С8Н6С14 1,2-Диметил-3,4,5,6-тетрахлорбензол 94,4 140,3 174,2 200,5 248,3 273,5 I
С8Н6С14 1,2,3,5-Теграхлор-4-этилбензол 77,0 126,0 162,1 191,6 243,0 270,0
С8Н6О2 Оксо(фенил)ацет-альдегид (фе-нилглиоксаль) 87,8 115,5 136,2 173,5 193,5 73
С8Н6О2 2-Бензофуран-1 (3/7)-он (фта-лид) 95,5 144,0 181,0 210,0 261,8 290,0 73
С8Н60з 1,3-Бензоди-оксол-5-карбаль-дегид (пиперональ) 87,0 132,0 165,7 191,7 238,5 263,0 37
С8Н7Вг 1 -Бром-2 -винилбензол 40,2 80,9 105,2 (4,00 кПа) 137,2 209,8 -52,8
С8Н7Вг 1 -Бром-4-винилбензол 44,0 84,6 108,8 (4,00 кПа) 140,5 212,0 7,7
С8Н7С1 1 -Винил-2-хлорбензол 25,6 64,6 88,0 (4,00 кПа) 118,7 188,7 -63,2
С8Н7С1 1-Винил-З-хлорбензол 25,3 65,2 96,5 121,2 165,7 190,0
С8Н7С1 1 -Винил-4-хлорбензол 27,0 66,3 90,0 (4,00 кПа) 121,1 166 192,0 -15,9
С8Н7С1О 1 -(4-Хлор-фенил)этанон 63,4 105,8 131,1 (4,00 кПа) 163,9 237,2 18,4
С8Н7С1О Фенилацетил-хлорид 48,0 89,0 119,8 143,5 186,0 210,0
c8h7n 1-Изоциано-2-метилбензол 25,2 64,0 94,0 117,7 159,9 183,5
c8h7n 2-Метилбен-зонитрил 36,7 77,9 110,0 135,0 180,0 205,2 -13
c8h7n 4-Метилбен-зонитрил 42,5 85,8 145,2 193,0 217,6 29,5
184
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Т1Ш, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
c8h7n Фенилацетонитрил (бензилциа-нид) 60,0 103,5 136,3 161,8 208,5 233,5 -23,8
c8h7no4 (2-Нитрофенил)-ацетат 100,0 142,0 172,8 194,1 233,5 253,0 (разл.)
c8h7ns c8h7ns Бензилизотиоцианат 2-Метил-1,3-бензотиазол 79,5 70,0 121,8 111,2 153,0 177,7 163,9 220,4 243,0 225,5
c8H8 Стирол -1,6 32,8 60,6 82,5 122,7 145,2 -30,6
c8H8 Циклоокта-1,3,5,7-тетраен -6,3 (тв.) 29,3 56,6 78,2 140,6 -4,7
C8H8Br2 (1,2-Дибром-этил)бензол 86,0 129,8 161,8 186,3 230,0 254,0
С8Н8С12 1,4-Диметил-2,5-дихлорбензол 55 (тв.) 96,3 120,9 (4,00 кПа) 152,8 224,3 68,2
С8Н8С12 1,2-Дихлор-З-этилбензол 46,0 90,0 123,8 149,8 197,0 222,1 -40,8
С8Н8С12 1,2-Дихлор-4-этилбензол 47,0 92,3 127,5 153,3 201,7 226,6 -76,4
С8Н8С12 1,4-Дихлор-2-этилбензол 38,5 83,2 118,0 144,0 191,5 216,3 -61,2
С8н8о Ацетофенон 39,0 78,8 102,4 (4,00 кПа) 133,2 177,6 202,0 19,7
с8н8о2 Метилбензоат 38,0 77,1 107,8 130,9 174,7 199,4 -12,4
С8Н8Оз Мети л-2 -гидроксибензоат (метилсалици-лат) 54,0 95,3 126,2 150,0 197,5 223,2 -8,3
с8н8о2 4-Метоксибенз-альдегид (анисовый альдегид) 73,2 117,8 150,5 176,7 223,0 248,0 2,5
с8н8о2 Фенилацетат 38,2 78,0 108,1 131,6 173,5 195,9
с8н8о2 Фенилуксусная кислота 97,0 141,3 173,6 198,2 243,0 265,5 76,5
С8Н8Оз 4-Гидрокси-З-метоксибензаль-дегид (ванилин) 107,0 154,0 188,7 215,6 260,0 285,0 81,5
с8н8о4 З-Ацетил-6-метил-2Н-пиран-2,4(3//)-дион (дегидрацетовая кислота) 91,7 137,3 171,0 197,5 244,5 269,0
С8Н9Вг 2-Бром-1,4-диметилбензол 37,5 78,8 110,6 135,7 181,0 206,7 9
С8Н9Вг 1 -Бром-2 -этилбензол 34,1 73,8 97,6 (4,00 кПа) 128,8 199,3 -67,9
С8Н9Вг 1-Бром-4-этилбензол 40 79,8 103,6 (4,00 кПа) 134,7 181 205,1 -43,5
С8Н9Вг (2-Бром-этил)бензол 46,8 89,5 121,8 146,7 191,4 215,7 -55,0
С8Н9С1 1-Хлор-2-этилбензол 21 59,0 81,7 (4,00 кПа) 111,3 153 178,4 -83,3
С8Н9С1 1-Хлор-3 -этилбензол 24,9 63,2 86,1 (4,00 кПа) 116,0 183,8 -55,0
Физические свойства важнейших веществ
185
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара тпл, °с
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С8Н9С1 1 -Хлор-4-этилбензол 25 63,5 86,4 (4,00 кПа) 116,5 160 184,4 62.6
С8Н9С1О 2-(4-Хлорфенил)-этанол 84,1 127,5 153,1 (4,00 кПа) 186,2 234,5 259,2
С8Н9С1О 1-Хлор-2-этоксибензол 45,8 86,5 117,8 141,8 185,5 208,0
C8H9NO А-Фс ни л аистам ид (ацетанилид) 114,0 162,0 199,6 227,2 277,0 303,8 113,5
c8h9no2 Метил-2-аминобензоат (метиловый эфир антраниловой кислоты) 80,0 124,2 150,2 (4,00 кПа) 184,2 259,8 24,4
c8h9no2 1 -Нитро-2-этилбензол 59,4 101,6 126,7 (4,00 кПа) 159,4 232,5 -12,3
c8h9no2 2,4-Диметил-1-нитробензол 65,6 109,8 143,3 168,5 217,5 244,0 2
c8H10 о-Ксилол -3,7 32,1 59,6 81.3 121,7 144,4 -25,2
c8H10 л/-Ксилол -7,2 28,2 55,3 76,8 116,7 139,1 -47,9
c8H10 и-Ксилол -8,1 (тв.) 27,3 54,4 75,9 115,9 138,4 13,3
С8Н,о Этилбензол -0,2 25,9 52,8 74,1 113,8 136,2 -95,0
C8H10Cl2OSi Фенил(дихлор)-(этокси)силан 52,4 94,6 126,2 151,4 197,2 222,2
C8H10Cl2Si Фенил(дихлор)-(этил)силан 48,5 92,4 126,7 153,3 203,5 230,0
c8H10o 2,3-Диметил-фенол 55,1 (тв.) 95,4 119,2 (4,00 кПа) 150 195 218 75
С8Н,оО 2,4-Диметил-фснол 49,6 89,3 112,7 (4,00 кПа) 143,0 183 210,0 27
с8н10о 2,5-Диметил-фенол 49,6 (тв.) 89,3 112,7 (4,00 кПа) 143,0 183 210,0 73,5
С8Н10О 2,6-Диметил-фснол 51,4 91,2 114,7 (4,00 кПа) 145 212 49,0
с8н10о 3,4-Диметилфенол 67,0 106,8 130,1 (4,00 кПа) 160,0 203 225 62,5
с8н10о 3,5-Диметил-фенол 62,8 (тв.) 102,3 125.4 (4,00 кПа) 155,0 197 219,5 68
с8н10о с8н10о 1 -Фенилэтанол 2-Фенилэтанол 48,5 57,4 87,3 97,4 110,0 (4,00 кПа) 120,9 (4,00 кПа) 139,3 151,3 180 203,4 218,2
с8н10о 2-Этилфенол 44,2 84,1 107,7 (4,00 кПа) 138,5 207 -45
с8н10о 3-Этилфенол 60,0 99,3 122,0 (4,00 кПа) 151,0 193 214 -4,0
с8н10о 4-Этилфенол 59,7 99,5 122,9 (4,00 кПа) 153,0 197 219 47,0
с8н10о Этоксибензол (фенетол) 18,1 57,4 86,6 108,4 149,8 172,0 -30,2
С8Н10О2 C8HiqS 2-Феноксиэтанол 2,4-Диметил-бензолтиол 67,0 37 121,2 78 152,2 102,3 (4,00 кПа) 176,5 135 221,0 245,3 208 11,6
186
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара тип, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
C8H10S C8H]0S CgHjoS c8H10s c8H10s C8H]0S C8HnClSi C8HhN c8h,,n c8h,,n C8HhN c8h,,n c8h,,no C8HhNO C8H12AsNO3 C8H12C12O5 C8Hi2O4 C8H12O4 C8H12Si C8H]4 c8H14 C8H14 C8Hi4 C8H14 C8Hi4 2,5-Диметил-бензолтиол 1 -Метил-4-(метилсульфа-нил)бензол (ме-тил-ц-толил-сульфид) 2-Этилбензол- тиол З-Этилбензол- тиол 4-Этилбензол-тиол (Этилсульфа-нил)бензол (этилфенилсуль-фид) Диметил(фенил)-(хлор)силан /У,7У-Димстил-анилин 2,4-Диметил-анилин 2,6-Диметил-анилин А-Этиланилин 4-Этиланилин 2-Этоксианилин (о-фенетидин) 4-Этоксианилин (ц-фенетидин) Диметил(4-аминофе-нил)арсонат Этан-1,2-диилбис-(хлорацетат) Диэтилмалеинат Диэтилфумарат Диметил-(фенил)силан 1,2-Диметил-циклогексен 1,3-Диметилциклогексен 1,4-Диметил-циклогексен 1,5-Диметил-циклогексен 1,6-Диметил-циклогексен 3,3-Диметил-циклогексен 35 54 39 40 40 44 29,8 29,5 50,7 44,0 38,5 51,6 67,0 83,1 15,0 148,3 57,3 53,2 5,3 -10,5 -10,5 -16,5 -16,5 -13,2 -22,4 76 94 80 81 81 84 70,0 70,0 90,9 87,0 80,6 92,3 108,6 123,8 51,8 195,8 100,0 95,3 42,6 24,8 24,8 18,1 18,1 21,8 11,5 100,2 (4,00 кПа) 118 (4,00 кПа) 104,3 (4,00 кПа) 105,3 (4,00 кПа) 105,3 (4,00 кПа) 107 (4,00 кПа) 101,2 101,6 114,6 (4,00 кПа) 129,2 113,2 116,4 (4,00 кПа) 139,9 147,8 (4,00 кПа) 79,7 229,0 131,8 126,7 71,4 46,0 (4,00 кПа) 47,0 (4,00 кПа) 38,8 (4,00 кПа) 38,8 (4,00 кПа) 42,8 (4,00 кПа) 31,7 (4,00 кПа) 132 149 137 138 138 138 124,7 125,8 145,5 146,0 137,3 147,8 163,5 178,9 101,0 252,0 156,0 151,1 94,2 73,8 73,8 66,0 66,0 70,3 58,4 168,6 169,2 188 193,7 180,8 194 107,0 140,3 291,8 201,7 195,8 136,4 205 217 210 211 211 205 193,5 193,1 214,0 217,9 204,0 216,8 228,0 248,6 160,5 313,0 225,0 118,5 159,3 137 137 128 128 133 119 2,5 -63,5 4,7 0,6 -59
Физические свойства важнейших веществ
187
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара т„л, °C
0.133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С8Н14 4,4-Диметил-циклогексен -23,8 9,9 30,1 (4,00 кПа) 45,5 117,0 -80,5
С8Н14 С8Н]4 С8Н]4 C8H|4 Окт-1-ин 1-Этилциклогексен З-Этилцикло-гексен 4-Этилцикло-гексен -13,7 -11,0 -12,8 -13,2 19,7 24,2 22,3 21,8 39,9 (4,00 кПа) 45,3 (4,00 кПа) 43,4 (4,00 кПа) 42,8 (4,00 кПа) 66,4 72,9 71,0 70,3 126,2 136 134 133 -79,5
c8H14o3 Изопропил-4-оксопентаноат 48,0 88,0 118,1 141,8 185,2 208,2
С8Н14О3 Пропил-4-оксопентаноат 59,7 99,9 130,1 154,0 198,0 221,2
С8Н14О3 Этил-З-оксо-2-этилбутаноат 40,5 80,2 110,3 133,8 175,6 198,0
С8Н]4О4 Диизопропилок-салат 43,2 81,9 110,5 132,6 171,8 193,5
с8н1404 Дипропилокса-лат 53,4 93,9 124,6 148,1 190,3 213,5
С8Н]4О4 Диэтил(метил)-пропандиоат(диэтиловый эфир изоянтарной кислоты, метилмалоновый эфир) 39,8 80,0 111,0 134,8 177,7 201,3
С8Н14О4 Диэтилсукцинат 54,6 96,6 127,8 151,1 193,8 216,5 -20,8
С8Н]4О4 Октандиовая кислота(пробковая кислота) 172,8 219,5 254,6 279,0 322,8 345,5 142
С8Н14О5 Диэтил-2-гидроксибутан-диоат (диэтиловый эфир яблочной кислоты) 102,0 148,0 182,3 208,5 254,8 280,0
с8н14о6 Диэтил-(2/?,3/?)-тартрат(диэтиловый эфир L-винной кислоты) 102,0 148,0 182,3 208,5 254,8 280,0
с8н14о6 Диэтил-раг/-(27?,3/?)-тартрат (диэтиловый эфир DL-винной кислоты) 100,0 147,2 181,7 208,0 254,3 280,0
С8Н15Вг (2-Бромэтил)-циклогексан 39,6 81,3 106,3 (4,00 кПа) 138,8 186 212,1 -57,3
c8h15n Октаннитрил (каприлонитрил) 43,0 80,4 110,6 134,8 179,5 204,5
c8h15no3 Этил(диэтилами-но)(оксо)ацетат 76,0 121,7 154,4 180,3 226,5 252,0
c8H16 С8н16 (2)-2,2-Диметил-гекс-3-ен (Е)-2,2-Диметил-гекс-3-ен -29,2 -32,3 2,7 -0,7 22,1 (4,00 кПа) 18,4 (4,00 кПа) 47,6 43,6 105,4 100,9 -137,4
188
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Т11Л, °с
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101.3 кПа
с8н16 2,3-Диметилгекс- -18,8 15,1 35,3 61,8 121,8 -115,0
2-ен (4,00 кПа)
С8н16 3,4-Диметилгекс- -22,5 7,6 27,4 53,3 112
1-ен (4,00 кПа)
С8н16 (Z)- или (£)-3,4- -18,6 15,3 35,3 62,0 122
Диметилгекс-3- (4,00 кПа)
ен
с8н16 5,5-Диметилгекс- -31,2 0,5 19,7 45,1 102,5
1-ен (4,00 кПа)
С8н16 (7)-5,5-Диметил- -28,2 3,9 23,3 48,9 106,9
гекс-2-ен (4,00 кПа)
С8Н16 (Е)-5,5-Диметил- -30,1 1,7 21,0 46,5 104,1
гекс-2-сн (4,00 кПа)
С8Н16 2,2-Диметил-З- -26,9 6,1 25,8 51,6 ПО
метиленпентан (4,00 кПа)
С8н16 2,4-Диметил-З- -30.2 1,7 20,9 46,4 104
метиленпентан (4,00 кПа)
С8н16 1,1 -Диметил- -23,4 10,1 36,5 57,6 97,1 119,5 -33,5
циклогексан
С8н16 pay-(\R,2R)-\,2-Димстилцикло- -21.0 13,0 39,7 61,0 100,9 123,4 -88,2
гексан
С8н16 (17?,25)-1,2-Диметилцикло- -15,9 18,4 45,3 66,8 107,0 129,7 -50,0
гексан
С8Н16 2-Изопропил- -24,8 8,4 28,2 54,2 ИЗ
пент-1 -ен (4,00 кПа)
С8н16 Изопропилцик- -17,7 16,4 43,1 64,3 104,0 126,4 -111,4
лопентан
с8н16 2-Метилгепт-1 - -22,5 11,4 31,7 58,4 119,3 -90,0
ен (4,00 кПа)
с8н16 2-Метилгепт-2- -18,2 15,7 36,0 62,5 122,6
ен (4,00 кПа)
С8н16 (Z)-; (Е)-2- -25,5 7,6 27,4 53,3 112
Мстилгепт-З-ен (4,00 кПа)
С8н16 З-Метилгепт-1- -27,8 4,8 24,7 51,0 111
ен (4,00 кПа)
с8н16 (Z)-; (£)-4- -24,1 9,2 29,0 55,1 114
Метилгепт-2-ен (4,00 кПа)
с8н16 (Z)-; (7Д-4- 18,6 15,3 35,5 62,0 122
Метилгспт-З-ен (4,00 кПа)
С8н16 2-Метил-З- -22,1 11,4 31,4 57,6 117,0
этилпент-2-ен (4,00 кПа)
с8н16 З-Метил-2- -25,2 8,0 27,8 53,7 112,5
этилпент-1 -ен (4,00 кПа)
с8н16 4-Метил-З- -27,8 4,3 23,8 49,4 107,5
этилпент-1-ен (4,00 кПа)
С8н16 z/wc-4-Метил-З- -22,8 10,7 30,6 56,8 116
этилпент-2-ен (4,00 кПа)
С8н16 тряно4-Метил- -23,9 9,4 29,3 55,3 114,3
З-этилпент-З-ен (4,00 кПа)
С8н16 pay-(\R,2S)-l- -16,6 18,2 44,9 66,1 105,7 128,0 -106,0
Метил-2-
этилциклопентан
Физические свойства важнейших веществ
189
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки ( 3С) при давлении насыщенного пара £пл, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
с8н16 р«г/-(1£,2£)-1-Метил-2-этилциклопентан 21,2 12,8 33,3 (4,00 кПа) 60,1 99,2 121,2
с8н16 Окт-1 -ен -17,5 15,4 41,2 61,6 99,8 121,3 -101,7
С8н!6 (7)-Окт-2-ен -17,8 16,5 37,9 (4,00 кПа) 64,1 125,6 -100,3
С8н16 С8н16 (£)-Окт-2-ен (7)-Окт-3-ен -18,3 -19,9 16,0 14,3 36,6 (4,00 кПа) 34,8 (4,00 кПа) 63,6 61,7 125,0 122,9 -87,7
С8н16 (£)-Окт-3-ен -19,6 14,6 35,1 (4,00 кПа) 62,0 123,3 -110
С8н16 (7)-Окт-4-ен -10,2 14,0 34,5 (4,00 кПа) 61,3 122,5 -118,7
С8н16 С8н16 (£)-Окт-4-ен 2-Пропилпент-1-ен -20,4 -21,6 13,7 12,0 34,2 (4,00 кПа) 32,0 (4,00 кПа) 61,1 58,3 122,3 117,7 -93,8
С8н16 Пропилциклопентан -12,6 21,3 47,9 69,1 108,6 130,9 -117,3
С8н16 2,3,3-Триметилпент-1 -ен -27,2 5,0 24,5 (4,00 кПа) 50,1 108,3 -69
С8н16 2,3,4-Триметил-пент-2-ен -22,5 10,9 30,9 (4,00 кПа) 57,0 116,3 -113,3
С8н16 2,4,4-Триметил-пент-1-ен -31,9 -0,3 18,9 (4,00 кПа) 44,1 101,4 -93,5
С8н16 2,4,4-Триметил-пент-2-ен -29,6 2,3 21,7 (4,00 кПа) 47,2 104,9 -106,3
С8н16 (1 R,2s,3S)~ 1,2,3-Триметилцикло-пентан -21 13,6 34,2 (4,00 кПа) 61,2 100,7 123,0 -116,4
С8н16 С8н,6 С8н16 С8н16 С8н16 С8н16 pay-(\R,3R)-1,2,3-Триметил-циклопентан 2-Этилгекс-1-ен З-Этилгекс-1-ен (Z)-; (£)-3-Этилгекс-2-ен З-Этилгекс-З-ен (Z)-; (£)-4-Этилгекс-2-ен -24 -20,0 -26,7 -19,3 -22,8 -24,8 9,5 13,7 6,3 14,5 10,7 8,4 29,8 (4,00 кПа) 33,9 (4,00 кПа) 26,0 (4,00 кПа) 34,7 (4,00 кПа) 30,6 (4,00 кПа) 28,2 (4,00 кПа) 56,5 60,3 51,8 61,1 56,8 54,2 95,5 117,5 120 110,3 121 116 113 -112
С8н16 Этилциклогексан -13,7 20,6 47,6 69,0 109,1 131,8 -111,3
с8н17сю4 2-{2-[2-(2-Хлорэтокси)-этокси]этокси}-этанол 110,1 156,1 190,0 214,7 258,2 281,5
c8h16no2 с8н16о Этил-Ь-лейцинат (этиловый эфир L-лейцина) 2-Метилгеитан-3-он 27,8 72,1 43,1 106,0 131,8 94,3 167,3 184,0 155,3
190
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С8н16о 6-Метилгепт-З-ен-2-ол 41,6 76,7 102,7 122,6 156,6 175,5
С8н16о 6-Метилгепт-5-сн-2-ол 41,9 77,8 104,0 123,8 156,6 174,3
С8н16о Октаналь (каприловый альдегид) 73,4 101,2 120,0 133,9 156,5 168,5
С8н16о2 Октановая кислота (каприловая кислота) 92.3 124,0 150,6 172,2 218,9 237,5 16
с8н16о Октан-2-он 23,6 60,9 89,8 111,7 151,0 172,9 -16
С8н16о 2,2,4-Триметил-пентан-3-он 14,7 46,4 69,8 87,6 118,4 135,0
С8н16о2 Изобутилбутират 4,6 42,2 71,7 94,0 135,7 156,9
С8Н|6О2 Изобутилизобутират 4,1 39,9 67,2 88,0 126,3 147,5 -80,7
С8н16о2 Пентилпропионат 8,5 46,3 75,5 97,6 138,4 160,2
С8н16о2 Пропил-З-метилбутаноат (пропилизовалерат) 8,0 45,1 72,8 95,0 135,0 155,9
с8н1602 Этил-4-метил-пентаноат(этил-изокапронат) 11,0 48,0 76,3 98,4 139,2 160,4
с8н171 1 -Иодоктан 45,8 90,0 123,8 150,0 199,3 225,5 45,9
с8н18 2,2-Диметил-гексан -28,8 3,1 28,2 48,2 85,7 106,8 -121,2
С8н18 3,4-Диметил-гексан -21,5 11,3 37,1 57,7 96,0 117,7
с8н18 2-Метилгептан -20,3 12,3 37,9 58,3 96,2 117,6 -109,0
С8н18 2-Метил-З-этилпентан 23,3 9,5 35,2 55,7 94,0 115,6 -115,0
с8н18 Октан -14 19,2 45,1 65,7 104,0 125,7 -56,8
с8н18 Т етраметилбутан -18,0 (тв.) 13,1 (тв.) 36,6 (тв.) 54,7 (тв.) 87,5 (тв.) 106,5 100,8
С8н18 2,2,4-Триметилпентан (изооктан) 36,1 20,7 40,7 78,0 99,2 -107,4
С8н18 2,3,4-Триметил-пентан -25,7 7,1 32,9 53,4 91,8 113,5 -109,2
с8н18 З-Этилгексан -19,9 12,8 38,5 58,9 97,0 118,5
c8h18n2 2,3,5,6-Тетра-метилпиперазин 23,7 61,7 90,0 113,8 157,8 183,5
с8н]80 Октан-1 -ол 54,0 88,3 115,2 135,2 173,8 195,2 -15,4
С8н18о С8н18о2 Октан-2-ол АИ/2вАИ-БуТИЛ-пероксид 32,8 70,0 -9,2 98,0 119,8 42,4 157,5 178,5 107,4 -38,6
с8н1802 1,1'-[Этан-1,2-диилбис(окси)]-дипропан(дипропиловый эфир этиленгликоля) -38,8 5,0 42,3 74,2 140,0 180,0
Физические свойства важнейших веществ
191
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара TnJ„ °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
СЛ с75 с/5 с/5 сч с/5 Чч ООО <z> сл N JZ О О £ £ ’сл ‘сл О О ОО QO 00 00 00 00 00 QS ООООООГЧ Tf rfrf — — >— — -- -н гч сч еч еч гч сч еч гч еч еч XXX X X X X ХХХХХХХ X XX 00 00 00 00 00 00 00 00 00 00 00 00 00 00 00 00 00 ООО ОООО ООООООО О ОО 2-(2-Бутокси-этокси)этанол Винил(три-этокси)силан 2,2'-[Оксибис-(этан-2,1 -диилокси)]-диэтанол (тетраэтиленгликоль) Дибутилсульфид Дибутилдисульфид Дибутилцинк 7У-Изобутил-2-метилпропан-1-амин (диизобу-тиламин) Этил(триэтокси)-силан Тетраэтоксисилан Тетраэтилплюм-бан Т етраэтилдисти-бан Тетраэтилсилан Триметил-(пентил)силан Тетраметил-1,3 -диэтоксидисилоксан Октаметил-1,7-дихлортетраси-локсан Октаметилтрисилоксан 2,2,4,4,6,6,8,8-Октаметил-1,3,5,7,2,4,6,8-тетраоксатетра-силоксан(октаметил циклотетрасилоксан) 70,0 153,9 21,7 34,6 21,4 -5,1 8,8 38,4 97,0 -1,0 -9,2 14,8 53,3 7,4 21,7 107,8 49,4 197,1 66,4 94,0 65,9 30,6 50,5 49,3 75,8 151,2 36,3 26,7 51,2 95,8 43,1 59,0 135,5 77,2 228,0 96,0 145,1 57,8 77,7 102,4 193,2 65,3 54,4 78,7 127,8 70,0 87,4 159,8 98,9 250,0 118,6 188,0 126,2 79,2 99,2 103,4 123,8 225,6 88,0 76,2 100,3 152,7 91,1 110,0 205,0 138,6 288,0 159,0 275,5 118,0 138,8 146,2 161,8 286,2 130,2 116,6 139,8 197,8 129,4 149,6 231,2 160,5 307,8 182,0 330,5 139,5 160,9 168,6 183,0 320,3 153,0 139,0 160,7 222,0 150,2 171,2 -79,7 -70 -136 -62 17,4
с9 с9н6о2 c9h7n c9h7n c9H8 С9Н8О с9н8о2 2/7-Хромен-2-он (кумарин) Изохинолин Хинолин Инден 3-Фенил проп-2-еналь (коричный альдегид) (£)-3-Фенил-проп-2-еновая кислота(коричная кислота) 106,0 63,5 59,7 16,4 76,1 127,5 (тв.) 153,4 107,8 103,8 58,0 120,0 173,0 189,0 141,6 136,7 89,5 152,2 207,1 216,5 167,6 163,2 113,9 177,7 232,4 264,7 214,5 212,3 157,7 222,4 276,7 291,0 240,5 237,7 181,6 246,0 300,0 70 24,6 -15 -1,5 -7,5 133
192
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Twl, °C
0,133 кПа 1,33 кПа 5.33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
C9H9N 3-Метил индол (скатол) 95,0 139,6 171,9 197,4 242,5 266,2 95
c9h9no4 Этил-З-нитро-бензоат 108,1 155,0 192,6 220,3 270,6 298,0 47
С9Ню 1-Винил-2 -метилбензол 16 54 76 (4,00 кПа) 105 169,8 -68,6
С9Н]о 1-Винил-3 -метилбензол 15 53 76 (4,00 кПа) 105 171,6 -86,3
С9Ню 1-Винил-4-метилбензол 16 54,1 76,6 (4,00 кПа) 106,1 172,8 -34,2
с9н10 C9Hio Изопропенил-бензол (а-метилстирол) (£)-Проп-1-ен-1-илбензол (транс-р-метилстирол) 11,6 17,5 48,5 57 70,6 (4,00 кПа) 99,6 111,7 143 165,4 179,0 -23,2
С9Н]о (7)-Проп-1-ен-1-илбензол (уис-$-метилстирол) 15 52 74 (4,00 кПа) 104 170 -52,2
с9н10о 1-Винил-2 -метоксибензол 41,9 81,0 110,0 132,3 172,1 194,0
с9н10о 1-Винил-З-метоксибензол 43,4 83,0 112,5 135,3 175,8 197,5
С9Н10О 1-Винил-4-метоксибензол 45,2 85,7 116,0 139,7 18,0 204,5
С9Нк)О 2,4-Диметил-бензальдегид 59,0 (тв.) 99,0 129,7 152,2 194,1 215,5 75
С9Н10О Пропиофенон 50,9 91,6 115,8 (4,00 кПа) 147,3 217,5 18,6
С9Н1оО (Е)-З-Фенил-проп-2-ен-1-ол (коричный спирт) 72,6 117,8 151,0 177,8 224,6 250,0 33
С9Н10О2 Бензилацетат 45,0 87,6 119,6 144,0 189,0 213,5 -51,5
С9Н]о02 Этилбензоат 44,0 86,0 118,2 143,2 188,4 213,4 -34,6
С9НюО2 З-Фенил-пропановая кислота (гидроко-ричная кислота) 102,2 148,7 18,3 209,0 255,0 279,8 48,5
С9Н10О3 Этил-2 -гидроксибензоат (этил сали цилат) 61,2 104,2 136,7 161,5 207,0 231,5 1,3
С9НцВг 1-Бром-2-изопропилбензол 42,5 83,0 107,1 (4,00 кПа) 138,8 210,2 -59,3
С9НцВг 1-Бром-4-изопропилбензол 48,1 89,5 114,1 (4,00 кПа) 146,4 219,0 -22,4
С9НИС1 1-Изопропил-2 -хлорбензол 30,0 68,8 92,1 (4,00 кПа) 122,4 191,1 -74,4
СЛпС! 1-Изопропил-4-хлорбензол 34,5 74,0 97,6 (4,00 кПа) 128,5 198,3 -12,3
C9HhNO /У-Метил-/У-фенилацетамид 118,6 152,2 179,8 227,4 253,0 102
C9HhNO2 Этил-2 -аминобензоат 90,1 133,2 159,0 (4,00 кПа) 192,8 268,8 14,3
Физические свойства важнейших веществ
193
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Ttul, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
C9HnNO2 Этил(фенил)кар-бамат (фенилуре-тан) 107,8 143,7 168,8 187,9 220,0 237,0 52,5
с9н12 Изопропилбензол (кумол) 2,8 38,3 66,1 88,1 129,2 152,4 -96,0
с9н12 Мезитилен (1,3,5-триметил-бензол) 12,3 48,8 77,2 99,7 141,4 164,7 -44,7
с9н12 1 -Метил-2 -этилбензол 11,9 48,5 77,0 99,6 141,6 165,1 -80,8
с9н12 1-Метил-3-этилбензол 9,4 45,7 74,0 96,4 137,9 161,3 -95,5
с9н12 1 -Метил-4-этилбензол 9,3 45,7 74,1 96,6 138,5 162,0 -62,4
с9н12 Пропилбензол 7,4 43,4 71,6 94,0 135,7 159,2 -99,5
с9н)2 1,2,3-Триметил-бензол (гемелли-тол) 19,3 56,8 86,0 109,1 152,0 176,1 -25,4
с9н12 1,2,4-Триметил-бензол (псевдокумол) 14,8 51,7 80,5 103,4 145,6 169,3 -43,8
С9Н12О 2-Изопропил-фенол 56,6 97,0 127,5 (4,00 кПа) 150,3 192,6 214,5 15,5
С9Н12О 3-Изопропилфенол 62,0 104,1 136,2 160,2 205,0 228,0 26
С9Н12О 4-Изопропил-фенол 67,0 108,0 139,8 163,3 206,1 228,2 61
С9Н12О 1 -Метокси-2-этилбензол 29,7 69,0 98,8 122,3 164,2 187,1
С9Н12О 1-Метокси-З-этилбензол 33,7 73,9 104,8 129,2 172,8 196,5
С9Н12О С9Н|2О 1 -Метокси-4-этилбензол 2-Пропилфенол 33,5 67,8 73,9 106,7 104,7 129,2 (4,00 кПа) 128,4 158 172,3 196,5 220
С9Н12О З-Пропилфенол 71,5 111,2 134,4 (4,00 кПа) 163,9 228 26,0
С9Н12О 4-Пропилфенол 71,0 111,7 135,4 (4,00 кПа) 166,0 232,6 22,0
С9Н12О C9H12S C9HJ2S C9H12S C9HI2S (Этокси метил )бензол (этилбензиловый эфир) (Изопропил-сульфа-нил)бензол 1 -(Метил-сульфанил)-2-этилбензол 1-Метил-З-(этилсульфа-нил)бензол 1-Метил-4-(этилсульфа-нил)бензол 26,0 47 63 56 57 65,0 87 104 96 97 95,4 ПО (4,00 кПа) 128 (4,00 кПа) 120 (4,00 кПа) 121 (4,00 кПа) 118,9 141 159 151 152 161,5 185,0 208 228 219 220
194
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Гпл, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
C9H12S (Пропилсульфа-нил)бензол 57 97 121 (4,00 кПа) 152 220
C9H13C10Si Метил(фенил)-(хлор)(этокси)-силан 44,8 94,6 117,8 142,6 187,7 212,0
c9h13n 4-Изопропил-анилин (и-кумидин) 60,0 102,2 134,2 158,0 203,2 227,0
c9h13n МЛ,2-Триметил-анилин 28,8 66,2 95,0 118,1 161,5 184,8 -61
c9h13n МЛ,4-Т риметил-анилин 50,1 86,7 116,3 140,3 185,4 209,5
c9h13n 2,4,5-Триметил-анилин (псевдокумидин) 68,4 109,0 139,8 162,0 203,7 234,5 67
C9H14O 2,6-Димстил-гепта-2,5-диен-4-он (форон) 42,0 81,5 111,3 134,0 175,3 197,2 28
C9H)4O 3,5,5-Триметил-циклогекс-2-ен-1 -он (изофорон) 38,0 81,2 114,5 140,6 188,7 215,2
C9H14O4 Диэтил-2-метиленбутан-диоат(диэтиловый эфир итаконовой кислоты) 51,3 95,2 128,2 154,3 203,1 227,9
C9H]4O4 Диэтил-(Е)-2-метилбут-2-ендиоат(диэтиловый эфир мезаконовой кислоты) 62,8 105,3 137,3 161,6 205,8 229,0
C9H]4O4 Диэтил-(7)-2-метилбут-2-ендиоат(диэтиловый эфир цитраконовой кислоты) 69,8 103,0 135,7 160,0 206,5 230,3
C9H14O7 Т риметил цитрат 106,2 160,4 194,2 219,6 264,2 287,0 (разл.) 78,5
c9H16 Нон-1-ин 2,6 33,3 55,2 (4,00 кПа) 84,2 150,8 -50
C9H16O3 Изобутил-4-оксопентаноат 65,0 105,9 136,2 160,2 205,5 229,9
c9H16o4 Диэтилпентан-диоат 65,6 109,7 142,8 167,8 212,8 237,0
c9H16o4 Диэтил(этил)-пропандиоат (этилмалоновый эфир) 49,9 91,6 122,4 146,0 188,7 211,5
c9H16o4 Нонандиовая кислота (азелаи-новая кислота) 189,3 225,5 260,0 286,5 332,8 356,5 (разл.) 106,5
C9H18 Нон-1-ен 0,9 35,5 62,7 84,2 124,3 146,9 -81,4
C9H18 Бутилциклопентан 5,3 41,6 63,3 (4,00 кПа) 91,8 133,2 156,6 -108,0
C9H18 Изопропилциклогексан 2,0 38,0 66,3 88,8 130,8 154,6 -89,4
Физические свойства важнейших веществ
195
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Д,л, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
с9н18 Пропилциклогексан 4,2 40,2 68,5 91,0 133,0 156,7 -94,9
С9Н18 1,1,3-Триметил-циклогексан -11,8 23,1 50,6 72,5 113,4 136,6 -65,7
С9Н18О Нонаналь (пеларгоновый альдегид) 33,3 71,6 100,2 123,0 163,4 185,0
С9Н18О Нонан-2-он 32,1 72,3 103,4 127,4 171,2 195,0 -19
С9н|8о2 Изобутил-3 -метилбутаноат (изобутилизовалерат) 16,0 53,8 82,7 105,2 146,4 168,7
С9Н18О2 (3-Метил -бутил)бутират (изоамилбутират) 21,2 59,9 90,0 113,1 155,3 178,6
С9н18о2 (3 -М ети л бутил )-2-метил npoi 1аноат (изоамилизобутират) 14,8 52,8 81,8 104,4 146,0 168,8
С9н18о2 Метилоктаноат (метилкаприлат) 34,2 74,9 105,3 128,0 170,0 193,0 (разл.) -40
С9н18о2 Нонановая кислота (пеларгоновая кислота) 108,2 137,4 163,7 184,4 227,5 253,5 12,5
С9Н191 1 -Иоднонан 70,0 109,0 138,1 159,8 199,3 219,5
С9Н20 2,2-Диметил-гептан -11 23 50 71 110,4 132,7 -113,0
С9Н20 3,4-Диметил-гептан -5,1 29 56 78 118,0 140,6
С9Н20 2,3-Диметил-3-этилпентан -7,1 28 55 77 119 142
С9Н20 3,3-Диэтилпен-тан -5,0 30,7 58,7 81,0 122,7 146,2 -33,1
С9Н20 З-Метилоктан -2,1 33 60 81 121,5 144,2 -107,6
с9н20 2-Метил-4-этилгексан -9,2 24 50 72 111,3 133,8
С9Н20 З-Метил-4-этилгексан -5,2 29 56 77,0 117,6 140,4
с9н20 Нонан 4 39,1 66,3 87,9 128,1 150,8 -53,5
С9Н2о 2,2,3,4-Тетра-метилпентан -13,0 20,8 48,0 69,6 110,1 133,0 -121,1
С9Н20 2,2,4,4-Тетра-метилпентан -24,7 12,5 39,0 60,1 99,8 122,3 -66,5
С9Н20 2,3,3,4-Тетра-метилпентан -8,4 27,2 54,9 77,0 118,2 141,5 -102,1
С9Н20 2,2,5-Триметил-гексан -17,0 16,2 42,3 63,1 102,0 124,1 -105,8
С9Н20 2,3,4-Триметил-гексан -7 27 54 76 116,1 139,0
С9Н20 4-Этилгептан -3,4 31 57 79 118,7 141,2
С9Н20О Нонан-1 -ол 59,5 99,7 129,0 151,3 192,1 213,5 -5
196
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара ТШ1, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С9Н20О3 1 -(2-Изопро-поксипропок- 46,0 86,2 117,0 140,3 183,1 205,6
си)пропан-2-ол (изопропиловый эфир дипропи-
ленгликоля)
С9Н20О4 Трипропилен- 96,0 140,5 173,7 199,0 244,3 267,2
гликоль
с9н21в Триизопропил- -7,2 31,5 83,4
боран
С9Н21В Т рипропилборан -1,1 39,8 95,0
C9H22S1 Гексил(три-метил)силан 6,7 44,8 74,0 97,2 139,9 163,0
C9H22Si Пропил(три-этил)силан 15,2 54,0 83,7 107,4 149,8 173,0
Сю
С10Н7ВГ 2-Бромнафталин 84,2 133,6 170,2 198,8 252,0 281,1 6,2
С1ОН7С1 1 -Хлорнафталин 80,6 118,6 153,2 180,4 230,8 259,3 -20
CioHg Нафталин 50,1 (тв.) 85,8 119,4 144,0 191,5 218,0 80,3
С]оН80 1 -Нафтол 94,0 (тв.) 142,0 177,8 206,0 255,8 282,5 96
С10Н8О 2-Нафтол 145,5 181,7 209,8 260,6 288,0 122,5
C10H8Cl2Si 1 -Нафтил-(дихлор)силан 106,2 149,2 181,7 205,9 249,7 273,3
c10h9n 2-Метилхинолин 75,3 119,0 150,8 176,2 211,7 246,5 -1
(хинальдин)
c10h9n Нафталин-1-амин (а-нафтиламин) 104,3 153,8 191,5 20,0 272,2 300,8 50
c10h9n Нафталин-2-амин (0-нафтиламин) 108,0 (тв.) 157,6 195,7 224,3 277,4 306,1 111,5
C10H10 1,3- 32,7 73,8 105,5 130,0 175,2 199,5 -66,9
Дивинилбензол
C10H10O 4-Фенилбут-З-ен-2-он (бензи-лиденацетон) 81,7 127,4 161,3 187,8 235,4 261,0 41,5
CioH]002 5-Аллил-1,3- 63,8 107,6 140,1 165,1 210,0 233,0 11,2
бензодиоксол
(сафрол)
СюНюОг (£)-2-Метил-3-фенилпроп-2- 125,7 169,8 201,8 224,8 266,8 288,0
еновая кислота
(а-метилкорич-
ная кислота)
CioH]o02 Метилциннамат 77,4 123,0 157,9 185,8 235,0 263,0 33,4
CioH|004 Диметил фталат 100,3 147,6 182,8 210,0 257,8 283,7
CioH1004 1,2-Фенилен-диацетат (диацетат пирокатехина) 98,0 145,7 179,8 206,5 253,3 278,0
C10H12 1-Винил-2,4-диметилбензол 34,2 75,8 107,7 132,3 177,5 202,0
CioH12 2-Винил-1,4-диметил бензол 29,0 69,0 100,2 124,7 168,7 193,0
C10H12 1-Винил-3- 30,5 69,1 92,2 122,3 167 190,1 -101,3
этилбензол (4,00 кПа)
Физические свойства важнейших веществ
197
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Т„л, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С,оН12 1-Винил-4-этилбензол 28,9 68,1 91,6 (4,00 кПа) 122,6 192,8 -49,7
С,оН12 1,2,3,4-Тетра-гидронафталин (тетралин) 38,7 79,4 103,7 (4,00 кПа) 135,7 181,7 207,6 -35,8
С10н12о 1 - Аллил-4-метоксибензол (эстрагол) 52,6 93,7 124,6 148,5 192,0 215,0
С10Н12О 1-Винил-4-этоксибензол 64,0 105,6 136,3 169,8 202,8 225,0
С]0Н]2О 4-Изопропил-бензальдегид (кумоловый альдегид) 58,0 102,0 135,2 160,0 206,7 232,0
С|0Н12О 1 -(4-Метилфе-нил)пропан-1-он 59,6 103,8 138,0 164,2 212,7 238,5
СюН12О 1 -Метокси-4-[(Е)-проп-1-енил]бензол (анетол) 62,6 106,0 139,3 164,2 210,5 235,3 22,5
Ск)Н]2О2 4-Аллил-2-метоксифенол (эвгенол) 78,4 123,0 155,8 182,2 228,3 253,5
С10Н]2О2 5-Аллил-2-метоксифенол (хавибетол) 83,6 127,0 159,8 185,5 229,8 254,0
СюН12О2 2-Метокси-4-(нроп-1 -енил)-фенол (изоэвгенол) 86,3 132,4 167,0 194,0 242,3 267,5 -10
С]0Н|2О2 Пропилбензоат 54,6 98,0 131,8 157,4 205,2 231,0 -51,6
Ск)Н120з (2-Фе-ноксиэтил)ацетат 82,6 128,0 162,3 189,2 235,0 259,7 -6,7
С1он13сю [(1-Метил-2-хлорэток-си)метил]бензол 62,3 106,0 139,6 164,8 210,8 235,0
С10Н14 Бутилбензол 24,6 62,4 91,9 115,3 158,8 183,3 -88,0
С10Н|4 ewop-Бутил-бензол 16,5 53,7 82,8 106,0 149,0 173,3 75,5
CioHi4 7И/76ЛЛ-БуТИЛ-бензол 14,1 50,8 79,6 102,5 145,1 169,1 -57,9
СюН]4 1,2-Диметил-З-этилбензол 31,7 71,1 101,2 125,0 169,2 193,9 -49,5
С1оН14 1,2-Диметил-4-этилбензол 28,9 68,0 97,8 121,4 165,2 189,8 -67,0
С(оН14 1,3-Диметил-2-этилбензол 28,0 68,0 97,9 121,6 165,4 190,0 -16,3
Ск)Н14 1,3-Диметил-5-этилбензол 24,4 63,1 92,7 116,1 159,4 183,7 -84,3
Ск)Н14 1,4-Диметил-2-этилбензол 25,9 65,0 94,8 118,5 162,3 186,9 -53,7
CioHI4 2,4-Диметил-1-этилбензол 27,5 66,6 96,4 120,0 163,8 188,4 -63,0
СюН14 1,2-Диэтил-бензол 25,2 62,9 92,3 115,6 159,0 183,4 -31,2
198
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара /’..л, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
СюН14 1,3-Диэтилбензол 24,0 61,4 90,7 113,9 156,9 181,1 -83,9
С]0Н14 1,4-Диэтил-бензол 25,0 62,8 92,4 115,8 159,3 183,8 -42,9
СюН]4 Изобутилбензол 16,1 53,2 82,3 105,4 148,5 172,8 -51,5
С]оН14 1 -Изопропил-2-метилбензол (о-цимол) 17,3 56,8 87,1 110,9 154,3 178,3 -71,5
СюН14 1-Изопропил-3 -метилбензол (л/-цимол) 16,6 57,2 84,9 108,3 151,1 174,9 -63,9
СюН]4 1 -Изопропил-4-метилбензол (и-цимол) 19,6 53,1 87,8 111,1 153,6 177,2 -67,9
СюН14 1 -Метил-2-пропилбензол 24,9 63,6 93,2 166,7 160,3 184,8 -60,2
СюН]4 1-Метил-3 -пропилбензол 23,1 61,5 90,9 114,2 157,5 181,8
С]оН]4 1 -Метил-4-пропилбензол 23,3 62,0 91,6 115,1 158,8 183,3 -63,6
С10Н,4 1,2,3,4-Тетра-метилбензол (пренитол) 39,2 79,5 110,3 134,6 179,8 205,0 -6,2
С|оН14 1,2,3,5-Тетра-метилбснзол (изодурол) 34,8 74,5 106,2 129,2 173,0 198,1 -23,7
СюН14 C10H14N2 1,2,4,5-Тетра-метилбензол (Дурол) Анабазин (3-пиперидин-2-илпиридин) 34,0 (тв.) 59,7 73,5 (тв.) 113,3 103,7 127,7 187,6 172,0 196,8 280,8 79,2
C10H14N2 (5)-(-)-Никотин 61,8 107,2 142,1 169,5 219,8 247,3
С10Н14О С10Н14О 2-Бутилфенол 3-Бути л фенол 64,6 80,9 106,5 122,8 131,3 (4,00 кПа) 147,4 (4,00 кПа) 163,5 179 235 248 -20
C]oHj40 4-Бутил фенол 80,4 122,4 147,0 (4,00 кПа) 179,0 248,0 22
С10Н14О 2-втор-Бутилфенол 57,4 100,8 133,4 157,3 203,8 228,0
СюН|4О 4-втор-Бутилфенол 71,4 114,8 147,8 172,4 217,6 242,1
СюН14О 2-трет-Бутилфенол 55,1 96,4 128,2 153,1 198,8 224,1 —5,6
С10Н)4О 3-трет-Бутилфенол 75,4 116,7 140,9 (4,00 кПа) 172 240 41
с10н14о 4-трет-Бутилфенол 72,2 113,9 146,0 170 214 239,5 100
С10Н14О С10Н14О 4-Изобу-тилфенол 5-Изопропенил-2-метил-циклогекс-2-ен-1 -он (карвон) 72,1 57,4 115,5 100,4 147,2 171,2 157,3 214,7 237,0 227,5
Физические свойства важнейших веществ
199
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Г1Ш, °с
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С10Н14О 2-Изопропил-5-метилфенол (тимол) 64,3 107,4 139,8 164,1 209,2 231,8 51,5
СюН14О 5-Изопропил-2-метилфенол (карвакрол) 70,0 113,2 145,2 169,7 213,8 237,0 0,5
CioH]40 СюНмО 4-(Изопропил-фенил)метанол (куминовый спирт) 2-(2-Этил-фенил)этанол 74,2 80,1 118,0 122,5 150,3 147,3 (4,00 кПа) 176,2 179,4 221,7 246,6 249,7
СюН14О 2-(4-Этил-фенил)этанол 79,5 122,0 146,9 (4,00 кПа) 179,1 250,0 7,9
С10н14о Ci0H15N 1-Этил-4-этоксибензол 4-Бутиланилин 48,5 69,6 89,5 И 1,7 119,8 136,7 (4,00 кПа) 143,5 169,3 185,7 208,0 241,6
c10h15n С]оН]6 МЛ-Диэтил-анилин 2,2-Диметил-З-метиленбицик-ло[2.2.1]гептан (камфен) 49,7 91,9 47,2 123,6 69,8 147,3 92,9 192,4 135,5 215,5 159,2 -34,4
C10H16 6,6-Диметил-2-метиленбицик-ло[3.1.1]гептан (Р-пинен) 4,2 42,2 75,0 94,0 136,1 158,3
C10H16 (/?)-4-Изопро-пенил-1 -метилциклогексен ((+)-лимонен) 14,0 53,8 84,3 108,2 151,4 175,0 -96,9
СюН ]б (/?5)-4-Изопро-пенил-1 -метилциклогексен (дипентен, (±)-лимонен) 14,0 53,8 86,0 109,2 152,4 176,6
с10н16 5-Изопропил-2-метилциклогек-са-1,3-диен (а-фелландрен) 20,0 58,0 87,8 110,6 152,0 175,0
CioH16 7-Метил-З-метиленокта-1,6-диен (мирцен) 14,5 53,2 82,6 106,0 148,3 171,5
С1оН16 1-Метил-4-(1-метилэтили-ден)циклогексен (терпинолен) 32,3 70,6 100,0 122,7 153,5 185,0
СюН1б 2,6,6-Триметил-бицик-ло[3.1.1]гепт-2-ен (а-пинен) -1,0 37,3 68,1 90,6 132,4 155,9 -55
200
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Г,,.,, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
CioHjgAsNOj Диэтил(4-аминофе-нил)арсонат (диэтиловый эфир арсаниловой кислоты) 38,0 74,8 102,6 123,8 161,0 181,0
С10н16о (Е)-3,7-Д имети л-окта-2,6-диеналь (цитраль) 61,7 103,9 135,9 160,0 205,0 228,0 (разл.)
СюН16О (25,5S)-5-Изопропенил-2-метилциклогек-санон ((-)-дигидрокарвон) 46,6 90,0 123,7 149,7 197,0 223,0
С]0Н]бО 1 -Изопропил-4-метилицик-ло[3.1.0]гексан-3-он (туйон) 38,3 79,3 110,0 145,0 177,8 201,0
С,оН160 5-Метил-2-(1-метилэтили-ден)циклогек-санон (пулегон) 58,3 94,0 121,7 143,1 189,8 221,0
С10Н|6О (15,4/?)-1,3,3-Триметилбицик-ло[2.2.1]гептан-2-он ((+)-фенхон) 28,0 68,3 99,5 123,6 166,8 191,0 5
С10н16о (1Я,4Я)-1,7,7- Триметилбицик-ло[2.2.1]гептан-2-он ((+)-камфора) 41,5 (тв.) 82,3 (тв.) 114,0 (тв.) 138,0 (тв.) 182,0 209,2 178,5
C10H16OSi Диметил-(фенил)(этокси)-силан 36,3 76,2 107,2 131,4 175,0 199,5
CioHi602 З-Изопропил-6-метилциклогек-сан-1,2-дион (бу-кокамфора, ди-осфенол) 66,7 109,0 141,2 165,6 209,5 232,0
С10Н18 /ироне-Декагидронафталин (транс- декалин) 24 63 84,9 115,5 161,0 187,3 -30,4
с10н18 г/мс-Декагидро-нафталин (цис-декалин) 29,5 69,4 99,7 123,4 169,0 195,7 -43,0
CioHis Дец-1-ин 20,0 57,0 79,3 (4,00 кПа) 108,5 174 -44
С10н18о (5)-3,7-Диметил-окта-1,6-диен-3-ол (кориандрол, (+)-линалоол) 40,0 79,8 109,9 133,3 175,6 198,0
С10н18о (Е)-3,7-Диметилокта-2,6-диен-1-ол (гераниол) 69,2 110,0 141,8 165,3 207,8 230,0
Физические свойства важнейших веществ
201
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Тал, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
с10н18о (Z)-3,7-Диметилокта-2,6-диен-1 -ол (нерол) 61,7 104,0 136,1 159,8 203,5 226,0
С]оН180 (Я)-3,7-Диметилокт-6-еналь ((+)-цитронеллаль) 44,0 84,8 116,1 140,1 183,8 206,5
С10Н]8О (1Я,2Я,5Я)-5-Изопропенил-2-метилциклогек-санол(дигидро-карвсол) 63,9 105,0 136,1 159,8 202,8 225,0
СюН]8О 2-[раг/-(/?)-4-Метилциклогекс-З-ен-1-ил]-пропан-2-ол ((±)-а-терпинеол) 52,8 94,3 126,0 150,1 194,3 217,5 35
С10н18о рш/-(1/?,2/?,45)-1,3,3-Триметил-бицикло[2.2.1]-гептан-2-ол ((±)-фенхол) 34,8 82,1 110,8 132,3 173,2 201,0 35
С]оН]80 1,3,3-Триметил-2-оксабицикло-[2.2.2]октан (цинеол) 15,0 54,1 84,2 108,2 151,6 176,0 -1
СюН|8О2 3,7-Диметилокт-6-еновая кислота (цитронелловая кислота) 99,5 151,4 171,9 195,4 236,6 257,0
С10Н18Оз (3 -Мети лбутил)-4-оксопентаноат 75,6 118,8 151,7 177,0 222,7 247,9
СюН180з Пентил-4-оксопентаноат 81,3 124,0 155,8 180,5 227,4 253,2
СюН18О4 Декандиовая кислота (себаци-новая кислота) 183,0 232,0 268,2 294,5 332,8 352,3 (разл.) 134,5
СюН18О4 Диизобутилокса-лат 63,2 105,3 137,5 161,8 205,8 229,5
СюН18О4 Дипропилсукци-нат 77,5 122,2 154,8 180,3 226,5 250,8
С]0Н)8О4 Диэтилгексан-диоат(диэтиладипат) 74,0 123,0 154,6 179,0 219,1 240,0 -21
СюН18О4 Диэтил(метил)-(этил)малонат (метилэтилмало-новый эфир) 44,7 85,7 116,7 140,8 184,1 207,5
СюН]8О6 Диизопропил-(27?,37?)-тартрат (диизопропиловый эфир L-винной кислоты) 103,7 148,2 181,8 207,3 251,8 275,0
202
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Тпп, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
СюН^Ое Дипропил-(27?,3/?)-тартрат (дипропиловый эфир L-винной кислоты) 115,6 163,5 199,7 127,0 275,6 303,0
C10H19N 2-(2,3,3-Три-метилциклопент-1 -енил)этиламин ф-камфиламин) 45,3 83,7 112,5 134,6 173,8 195,0
С10Н20 Бутилциклогексан 21,8 59,5 89,0 112,5 156,3 180,9 -74,7
С10Н20 втор-Бутилциклогек-сан 19,8 57,5 87,0 110,6 154,5 179,3
СюНго трет-Бутилциклогек-сан 12,9 50,3 79,7 103,1 146,8 171,6 -41,2
С10Н20 Дец-1-ен 18,2 54,4 82,7 105,2 147,0 170,6 -66,3
С10Н20 Изобутилциклогексан 14,2 51,3 80,4 103,6 146,8 171,3 -94,8
С]оН2о 1 -Изопропил-4-метилциклогек-сан ф-ментан) 9,7 48,3 78,3 102,1 146,0 169,5
С10Н20 Пентилциклопентан 22 60 89 ИЗ 156 180 -83
СюН2оВГ2 1,2-Дибромдекан 96,7 137,3 167,4 190,2 229,8 250,4
С10Н20О Деканаль (каприновый альдегид) 51,9 92,0 122,2 145,3 186,3 208,5
с10н20о Декан-2-он 44,2 85,8 117,1 142,0 186,7 211,0 3,5
С10н20о (/?)-3,7-Диметилокт-6-ен-1 ол ((+)-цитронеллол) 66,4 107,0 137,2 159,8 201,0 221,5
С10Н20О (1Я,25,5Я)-2- Изопропил-5-метилциклогек-сапол ((-)-ментол) 56,0 96,0 126,1 149,4 190,2 212,0 42,5
С10Н20О2 Декановая кислота (каприновая кислота) 109,9 149,9 180 203,7 267,3 31,5
С10Н20О2 (З-Метилбутил)-3-метилбутаноат (изопентилизовалерат) 27,0 68,6 100,6 125,1 169,5 194,0
С10Н22 СюН22 С10Н22 СюН22 С10Н22 Декан 2,4-Диметил-октан 3,4-Диметил-октан 2,2-Диметил-4-этилгексан 3,4-Диметил-3-этилгексан 21 1,9 И,1 -3,2 12,0 57,7 38,3 48,4 32,8 49,8 86,0 60,0 (4,00 кПа) 70,7 (4,00 кПа) 54,4 (4,00 кПа) 72,5 (4,00 кПа) 108,6 88,5 99,9 82,7 102,3 150,5 174,1 153 166 147 170 -29,7
Физические свойства важнейших веществ
203
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Т °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа 1 пл>
С10Н22 С10Н22 С]0Н22 С10Н22 С]оН22 С1ОН22 С]()Н22 С10Н22 С10Н22 С10Н22 С1ОН22 С]0Н22 С1()Н22 С]оН22 с10н22 С]0Н22 СюН22 С10Н22 С1ОН22 С1()Н22О с10н22о С10Н22О С10Н22О2 3,4-Д иэтилгексан 4-Изопропил-гептан З-Изопропил-2,4-диметилпентан З-Изопропил-2-метилгексан 2-Мстил-3,3-диэтилпентан 2-Метилнонан З-Метилнонан 2-Метил-5-этилгептан 4-Метил-З-этилгептан 2,2,3,3,4-Пентаметилпен-тан 2,2,3,4,4-Пентаметилпен-тан 4-Пропилгептан 2,2,5,5-Тетраметил-гексан 3,3,4,4-Тетра-метилгексан 2,3,4-Триметил-гептан 2,4,6-Триметил-гептан 2,2,4-Триметил-3-эти л пентан 2,3,4-Триметил-3-этилпентан З-Этилоктан Бис(3-метил-бутиловый) эфир (диизопентиловый эфир) Декан-1-ол 3,7-Диметил-октан-1 -ол (дигидроцитронеллол) 2-Бутил-2-этилбутан-1,3-диол 8,3 6,9 3,2 9,0 14,9 13,6 15,8 6,6 11,7 9,0 4,2 8,3 -11,3 11,9 9,0 -5,3 1,4 И,4 15,9 18,6 69,5 68,0 94,1 45,3 43,8 40,0 46,1 53,0 51,0 52,5 43,5 49,2 46,6 41,3 45,3 24,1 49,7 46,1 30,6 38,2 49,3 52,6 57,0 111,3 103,0 136,8 67,5 (4,00 кПа) 65,8 (4,00 кПа) 62,1 (4,00 кПа) 68,3 (4,00 кПа) 75,9 (4,00 кПа) 79,3 74,4 (4,00 кПа) 65,5 (4,00 кПа) 71,5 (4,00 кПа) 69,1 (4,00 кПа) 63,5 (4,00 кПа) 67,5 (4,00 кПа) 45,4 (4,00 кПа) 72,4 (4,00 кПа) 68,3 (4,00 кПа) 52,1 (4,00 кПа) 60,2 (4,00 кПа) 71,9 (4,00 кПа) 74,5 (4,00 кПа) 86,3 142,1 127,6 167,8 96,4 94,7 91,1 97,3 105,9 101,8 103,1 94,4 100,8 98,7 92,7 96,4 73,4 102,2 97,3 80,4 89,2 101,7 103,2 109,6 165,8 145,9 191,9 143,5 150,3 208,8 176,8 233,5 162 160 157,0 163 174 167,0 167,8 159,7 167 166,1 159,3 162 137,5 170,0 163 144,8 155,3 169,4 168 173,4 231,0 193,5 255,0 -81,7 -74,5 -84,7 -36,5 -38,8 -12,6 7
204
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки ( °C) при давлении насыщенного пара Т °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С10Н22О3 c10H22s CioI^Si Cjob^Si CioH2804Si3 CioH3o03Si4 CioH3o05Si5 1 -(2-Бутокси-пропокси)-пропан-2-ол (мо-нобутиловый эфир дипропи-ленгликоля) Бис(3-метил -бутил)сульфид (диизопентилсульф ид) Бутил(триэтил)-силан Гептил (три-метил)силан Гексаметил-1,5-диэтокситриси-локсан Декаметилтетрасилоксан Декаметилциклопентасилоксан 64,7 43,0 27,1 22,3 41,8 35,3 45,2 106,0 87,6 67,5 62,1 80,7 74,3 86,2 136,3 120,0 98,3 92,4 110,0 104,0 117,7 159,8 145,3 123,2 116,5 133,2 127,3 142,0 203,8 191,0 167,5 159,8 174,0 169,8 186,0 227,0 216,0 192,0 184,0 196,6 193,5 210,0 -38,0
Cn c,,h8o2 C,iH8O2 C] ]H]o СцН.о СцН12О2 СцН12О2 СцН^Оз СиН120з СцН14 СИН14 син14 СцН14 Син14 СцН14 1 -Нафтойная кислота 2-Нафтойная кислота 1 -Метил-нафталин 2-Метил-нафталин 1-Фенилпентан-1,3-дион Этилциннамат (этил-3-фенил-пропеноат) 6-Аллил-4-метокси-1,3-бензодиоксол (миристицин) Этил-3-оксо-3-фенилпропаноат 1-Винил-4-изопропилбензол 1-Винил-2,4,5-триметилбензол 2-Винил-1,3,5-триметилбензол 1-Метил-1,2,3,4-тетрагидронаф-талин 2-Метил-1,2,3,4-тетрагидронаф-талин 5-Метил-1,2,3,4-тетрагидронаф-талин 156,0(тв.) 160,8 (тв.) 63,5 61,1 98,0 87,6 95,2 107,6 41,4 48,1 37,5 47 46 58,1 196,8 202,8 107,5 104,8 144,0 134,0 142,0 150,3 80,9 91,6 79,7 88 87 100,7 225,0 231,5 141,2 138,2 178,0 169,2 177,7 181,8 104,5 (4,00 кПа) 124,2 111,8 113 (4,00 кПа) 112 (4,00 кПа) 126,1 (4,00 кПа) 245,8 252,7 167,8 164,7 204,5 196,0 205,0 205,0 135,2 149,8 136,8 146 145 159,8 281,4 289,5 217,0 213,6 251,2 245,0 253,5 244,7 196,1 182,3 207,5 300,0 308,5 244,7 251,1 276,5 271,0 280,0 265,0 (разл.) 204,1 221,2 207,0 219 218 234,3 160,5 184 -30,5 34,6 12 -44,7 -22,9
Физические свойства важнейших веществ
205
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки ( °C) при давлении насыщенного пара Т °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа 1 ПЛ9
СцН]4 СпН^О СцН14О СцН14О CiiH]4O2 СцН]4О2 СцН]6 СцН16 СцН|6 Син16 СнН16 СцН16 СцН16 С.1Н16 СцН16 СИН16 СцН16 СцН1б СцН1б СИН16 Ci]H16 спн16 С„Н16 СцН16 СцН1б СцН1б С] 1 н16 СцН16 6-Метил-1,2,3,4-тетрагидронаф-талин 2,2-Диметил-1 -фенилпропан-1 -он 3-Метил-1-фенилбутан-1 -он 1-(2,3,5-Триметил )этанон 4-Аллил-1,2-диметоксибензол Изобутилбензоат 1 -Бутил-2-метилбензол 1 -в/ио/?-Бутил-2-метилбензол 1 -/и/?вАИ-Бутил-2-метилбензол 1 -я7/?еи7-Бутил-3-метилбензол 1 -АИ/?вАИ-БуТИЛ-4-метилбензол (1,1 -Диметил-пропил)бензол (1,2-Диметил-пропил)бензол 1,2-Диметил-З-пропилбензол 1,3-Диметил-5-пропилбензол 1-Изобутил-2-метилбензол 1-Изопропил-2,3-д и метил бензо л 1-Изопропил-3,5-диметилбензол 1-Изопропил-2-этилбензол (1-Метил-бутил )бензол (2-Метил-бутил)бензол (З-Метил-бутил)бензол 1-Метил-3,5-диэтилбензол 2-Метил-1,3-диэтилбензол Пентаметилбен-зол Пентилбензол 1-Пропил-2 -этилбензол 1,2,3-Триметил-4-этилбензол 54 57,8 58,3 79,0 85,0 64,0 41 33 35,9 28,4 30,7 31 28 34 37 33 37 32 31 31 34 35 36 41 57 40,7 38 49 96 99,0 101,4 122,3 127,0 108,6 81,4 72,3 75,6 67,2 69,8 69,5 66,2 83,5 77,0 72,3 77,3 71,5 70,0 70 73,0 74,5 76 82 100 80,6 77,6 91 122 (4,00 кПа) 130,4 133,8 154,2 158,3 141,8 105,2 (4,00 кПа) 95,8 (4,00 кПа) 99,4 (4,00 кПа) 90,4 (4,00 кПа) 93,2 (4,00 кПа) 92,9 (4,00 кПа) 89,3 (4,00 кПа) 107,7 (4,00 кПа) 100,8 (4,00 кПа) 95,8 (4,00 кПа) 101,1 (4,00 кПа) 94,9 (4,00 кПа) 93,4 (4,00 кПа) 93,4 (4,00 кПа) 96,6 (4,00 кПа) 98,1 (4,00 кПа) 100,0 (4,00 кПа) 106,2 (4,00 кПа) 125,0 (4,00 кПа) 104,3 (4,00 кПа) 101,5 (4,00 кПа) 115,6 (4,00 кПа) 154,8 154,0 158,0 179,7 183,7 166,4 137,0 126,6 130,4 120,7 123,7 123,4 119,6 139,4 132,0 126,6 132,3 125,5 123,9 123,9 127,4 129,1 130,7 137,7 157,9 135,4 132,7 147,9 202,4 197,7 204,2 224,3 226,2 212,8 176 229,0 220,0 228,0 247,5 248,0 237,0 208 196 200,5 189,3 192,8 192,4 188 210,7 202,2 196 202,6 194,5 193 193 197 198,9 200,7 208,8 231,8 205,4 203 220,4 -39,7 -50,3 -41,4 -52,5 -59,1 -74,1 54,3 -75
206
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Гнл, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53.3 кПа 101,3 кПа
син16 СцН16 СцН16О 1,2,4-Триметил-5-этилбензол (1 -Этил-пропил)бензол 2-в/ио/?-Бутил-4-метилфенол 44 29,5 72,6 85 68,5 113,8 109,6 (4,00 кПа) 91,7 (4,00 кПа) 137,9 (4,00 кПа) 141,4 122,2 169,0 213,0 191 237,0 -13,5
СцН16О 2-/и/?е?/и-Бутил-4-метилфенол 69,1 110,7 135,3 (4,00 кПа) 167 237 51,7
СцН16О 4-/и/?е?/и-Бутил-2-метилфенол 74,3 118,0 150,8 176,2 221,8 247,0
СцН16О 4-( 1,1 -Диметил-пропил)фенол 92,5 135,3 160,3 (4,00 кПа) 192,5 262,5 92
СцН)6О 4-Пентилфенол 83,3 125,3 149,9 (4,00 кПа) 181,5 250,5 23
СцН18О2 [(£)-3,7-Диметилокта-2,6-диен-1-ил]формиат (ге-ранилформиат) 61,8 104,3 136,2 160,7 205,8 230,0
СцН18О2 [(2)-3,7-Диметилокта-2,6-диен-1-ил]формиат (не-рилформиат) 57,3 99,7 131,5 155,6 200,0 224,5
СцН|8О2 (1,7,7-Триме-тилбицик-ло[2.2.1]гепт-2-ил)формиат (борнилформиат) 47,0 89,3 121,2 145,8 190,2 214,0
С11Н ]8O2Si СцН20 С]]Н20 СнН20 Метил(фенил)-(диэтокси)силан транс-1 -Метилдекагидронафталин транс-4а.-Метилдекагид-ронафталин цис-4а~ Метилдекагидронафталин 56,5 58 36 44 97,2 101 77 85 127,5 126,6 (4,00 кПа) 101 (4,00 кПа) НО (4,00 кПа) 151,2 160 133 142 193,8 216,5 235 205 215
СцН20 Ундец-1-ин 34,6 73,2 96,4 (4,00 кПа) 126,8 195 -25
СцН20О2 (2-Изопропил-5 -метилциклогек-сил)формиат (ментилформиат) 47,3 90,0 123,0 148,0 194,2 219,0
СцН20О2 Октилакрилат 58,5 102,0 135,6 159,1 204 227,0
СцН20О2 У ндец-10-еновая кислота 114,0 156,3 188,7 213,5 254,0 275,0 24,5
СцН20Оз Гексил-4-оксопентаноат 90,0 134,7 167,8 193,6 241,0 266,8
СцН22 Г ексилциклопен-тан 39 79 109 133 178 203 -73
СцН22 Пентилциклогексан 34,9 75,3 99,4 (4,00 кПа) 131,1 202,8 -57,5
Физические свойства важнейших веществ
207
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Гпл, °C
0.133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
СцН22 С,,н22о СцН22О2 СцН22О2 СцН24 СИН24 син24о CHH26Si C,.H26Si Ундец-1-ен Ундекан-2-он Метилдеканоат (метилкапринат) Ундекановая кислота Ундекан 2-Метилдекан Ундекан-2-о л Пентил(триэтил)-силан Триме-тил(октил)силан 34,5 68,2 63,7 101,4 37 71,1 41,8 41,8 72,1 108,9 108,0 149,0 75,1 68,5 112,8 83,8 82,3 101,5 139,0 139,0 185,6 104,6 98,1 143,7 116,0 113,0 124,9 161,0 161,5 212,5 127,9 121,5 167,2 141,2 136,5 168,2 202,3 202,9 262,8 171,4 164,9 209,8 186,3 179,5 192,7 224,0 224,0 (разл.) 290,0 195,9 189,2 232,0 211,0 202,0 -49,2 15 -18 29,5 -25,6 -48,9
С12 с12н8о С12Н9Вг С12Н9ВгО С12Н9ВгО С12Н9С1 С12Н9С1 С12Н9СЮ С12Н9С1О c12h9n С]2Н ю С12Н ю C12H10Cl2Si C12H10F2Si Ci2H10N2 С12н10о С12Н10О С12н10о С12н10о С12н10о c12H10s C12H10S2 C}2H)oSe C12HhN Ci2H12 Дибен-3o[Z>,<7] фуран (окись дифенилена) 4-Бромбифенил З-Бромбифенил-4-ол 1 -Бром-4-феноксибензол 2-Хлорбифенил 4-Хлорбифенил 2-Хлорбифенил-З-о л З-Хлорбифенил-2-ол Карбазол Аценафтен Бифенил Дифенил-(дихлор)силан Дифенил-(дифтор)силан (£)-Дифенил-диазен (транс-азобензол) Бифенил-2-ол Бифенил-4-ол Дифениловый эфир 1-(1-Нафтил)-этанон 1-(2-Нафтил)-этанон Дифенилсульфид Дифенилдисульфид Дифенилселенид У-Фениланилин (дифениламин) 1,3-Диметил-нафталин 98,0 100,0 118 89,3 96,4 118,0 119,8 70,6 109,5 68,4 103,5 100,0 66,1 115,6 120,2 96,1 131,6 105,7 108,3 81 125,2 150,6 152,3 163 134,7 146,0 169,7 170,7 131,2 117,0 158,4 115,5 151,5 146,2 176,2 114,0 161,5 168,5 145,0 180,0 154,4 157,0 125 190,8 193,8 190,7 (4,00 кПа) 169,9 183,8 207,4 208,2 168,2 152,5 194,0 149,8 187,9 180,3 213,0 150,0 196,8 203,8 182,8 214,8 192,2 194,3 151,4 (4,00 кПа) 197,0 221,8 224,5 226,8 197,0 212,5 237,0 237,1 265,0 197,5 178,4 222,2 176,3 216,0 205,9 240,9 178,8 223,8 229,8 211,8 241,3 220,8 222,8 185,7 277,7 280,2 243,8 264,5 289,4 289,5 323,0 250,0 228,0 274,8 225,4 266,1 251,8 285,5 230,7 270,5 275,8 263,9 285,8 273,2 274,1 285,1 310,0 311,0 310,1 267,5 292,9 317,5 317,0 354,8 277,5 255,5 304,4 252,5 293,0 275,0 308,0 258,5 295,5 301,0 292,5 310,0 301,5 302,0 263 90,5 95 18,7 34 75,5 6 244,8 95 69,8 681 56,5 164,5 27 55,5 61 2,5 52,9 -4,0
208
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара ТП1„ °с
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53.3 кПа 101,3 кПа
С12Н12 2,3-Диметил-нафталин 84,1 (тв.) 128,7 155,2 (4,00 кПа) 189,9 268 105,0
С]гН12 2,6-Диметил-нафталин 80,4 (тв.) 124,4 150,6 (4,00 кПа) 184,8 262 112,0
с12н12 1-Этилнафталин 76 120,0 153,8 180,6 230,4 258,7 -13,8
С12Н12 2-Этилнафталин 74 119,1 153,1 180,1 230,0 257,9 -7
C12HI2N2 1,1 -Дифенил-гидразин 126,0 176,1 213,5 242,5 294,0 322,2 44
C12H|4N2O5 2,4-Динитро-6-циклогексилфе-нол 132,8 175,9 206,7 229,0 269,8 291,5
С]2Н140з (4-Аллил-2-метоксифе-нил)ацетат (ацетэвгенол) 101,6 148,0 183,0 209,7 257,4 282,0 30
С12Н14О4 5-Аллил-4,7-диметокси-1,3-бензодиоксол (апиол) 116,0 160,2 193,7 218,0 262,1 285,0 30
С12Н14О4 Диэтил фталат 108,8 156,0 192,1 219,5 267,5 294,0
С12Н,6 С12н16 2-Винил-1,4-диэтилбензол 1,1 -Диметил-1,2,3,4-тетра-гидронафталин 49,7 48 92,6 90 125,8 115 (4,00 кПа) 151,0 147 198,0 223,0 221
С12н16 2,6-Диметил- 1,2,3,4-тетра-гидронафталин 60 103 129 (4,00 кПа) 162 238 20
С12н16 5,7-Диметил- 1,2,3,4-тетра-гидронафталин 71,7 115,7 142,0 (4,00 кПа) 176,2 253,1
С12Н16 1-Изопропенил-4-изопропил-бензол 55,1 95,8 119,9 (4,00 кПа) 151,1 220,8 -30,6
С12Н16 С12Н16 Циклогексилбен-зол 1-Этил-1,2,3,4-тстрагидронаф-талин 67,5 59 111,3 102 137,2 127 (4,00 кПа) 163,3 161 212,2 240,1 236 7,5
С12н16 5-Этил-1,2,3,4-тетрагидронаф-талин 64 107 133 (4,00 кПа) 166 242 -44,5
С12Н16О2 (3 -Метилбути л )-бензоат (изопентилбензоат) 72,0 121,6 158,3 186,8 235,8 262,0
c12h17no С12Н18 У-Бутил-jV-фенилацетамид Гексаметилбен-зол 95,7 141,4 168,4 (4,00 кПа) 203,4 187,2 236,5 281,1 263,5 24,5 165,5
С12Н18 Г ексилбензол 56,2 97,7 122,4 (4,00 кПа) 154,5 226,1 -55,2
С12Н18 1,2-Диизопро-пилбензол 38,6 78,7 109,8 133,9 178,6 203,8 -56,5
С12н18 1,3-Диизопропилбензол 38,4 78,4 109,4 133,4 178,1 203,2 -63,0
С12Н18 1,4-Диизопро-пилбензол 43,8 83,3 114,7 139,3 184,8 210,4 -17,0
Физические свойства важнейших веществ
209
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара 7Ш1, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С]2Н18 1,2,4-Триэтил-бензол 46,0 88,5 121,7 146,8 193,7 218,0
С12Н18 1,3,5-Триэтил-бснзол 47,9 90,2 122,6 147,7 193,2 217,5 -66,5
с12н18о 2-^е^г-Бутил-4,5-диметил-фенол 86,1 129,1 154,4 (4,00 кПа) 187,0 258,5 46,0
с12н18о 2-/д/?е/д-Бутил-4,6-диметил-фенол 81,8 123,8 138,1 (4,00 кПа) 180 249 22,3
с12н18о 4-т/?е/д-Бутил-2,5-диметил-фенол 93,0 136,0 161,1 (4,00 кПа) 193,5 240 264 71,2
О о о 00 ОС 00 X X X о о <5 4-7И/?е7?г-Бутил-2,6-диметил-фенол 2-/д/?е/д-Бутил-4-этилфенол 4-/д/?е/д-Бутил-2-этил фенол 76,5 (тв.) 80,8 87,4 119,0 122,9 130,0 144,1 (4,00 кПа) 147,7 (4,00 кПа) 154,9 (4,00 кПа) 176,5 179 187 248 250 257 82,4
С|2Н18О С)2Н18О С12Н18О 2-( 1,1 -Диметил-пропил)-4-мстилфенол 4-(1,1-Диметил-пропил)-2-метилфенол 4-( 1,1 -Диметил-пропил)-3-метилфенол 84,8 102,2 101,4 126,7 145,5 144,7 151,3 (4,00 кПа) 170,7 (4,00 кПа) 170,1 (4,00 кПа) 183 203 202,5 252 273 273 Т1
С12Н2о02 (1-Винил-1,5-диметилгекс-4-ен-1ил)ацетат (линалилацетат) 55,4 96,0 126,6 151,8 196,2 220,0 (разл.)
С]2Н2о02 [(£)-3,7- Диметилокта-2,6-диен-1-и л] ацетат(геранилацетат) 73,5 117,9 150,0 175,2 219,8 243,3 (разл.)
С12Н20О2 {(1/?,25,4/?)-1,7,7-Триметилбицик-ло[2.2.1]гепт-2-ил} ацетат ((+)-борнилацетат) 46,9 90,2 123,8 149,8 197,5 223,0 29
С12Н20Оз81 Фенил(три-этокси)силан 71,0 112,6 143,5 167,5 210,5 233,5
Ci2H20O7 Триэтилцитрат 107,0 144,0 190,4 217,8 267,5 294,0 (разл.)
С12Н210дР С12Н22 Трис(2-метилпроп-2-ен-1 -ил)фосфат 1,Г-Би(циклогексил) 93,7 149,8 192,0 134,7 225,7 161,3 288,5 210,7 324,0 238,5
С12Н22 С12Н22 Додец-1-ин транс-'Ха-Этилдекагидро-нафталин 49,1 51,1 89,1 93,1 113,2 (4,00 кПа) 118,1 (4,00 кПа) 160,7 150,9 234 225 -5
210
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара тпл, °C
0,133 кПа 1,33 кПа 5.33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С12Н22 С12Н22 С]2Н22 г/«с-4а-Этилдекагидро-нафталин цис-\, 10-Диметилдека-гидронафталин транс-\, 10-Диметилдска-гидронафталин 57 47,4 45 99 89,0 83 125 (4,00 кПа) 113,9 (4,00 кПа) 108 (4,00 кПа) 158 146,4 140 233 220 213
С12Н22О2 (3,7-Диметилокт-6-ен-1-ил)ацетат (цитронеллил-ацетат) 74,7 113,0 140,5 161,0 197,8 217,0
С12Н22О2 (2-Изопропил-5-метилциклогек-сил)ацетат (ментил ацетат) 57,4 100,0 132,1 156,7 202,8 227,0
С12Н22О4 Бис(3-метил-бутил)оксалат (диизопентил-оксалат) 85,4 131,4 165,7 192,2 240,0 265,0
С12Н22О4 Диметилдекан-диоат (диметил-себацинат) 104,0 156,2 196,0 222,6 269,6 293,5 38
С12Н22О6 Диизобутил-(2/?,37?)-тартрат (диизобутиловый эфир L-винной кислоты) 117,8 169,0 208,5 239,5 294,0 324,0 73,5
С12Н24 Г ексилциклогек-сан 50,1 92,0 117,1 (4,00 кПа) 149,9 224,0 -43,0
С12Н24 Г ептилциклопен-тан 55 96 127 152 198 224 -53
Ci2H24 Додец-1 -ен 49 88,8 119,2 143,3 188,1 213,4 -35,2
С12Н24 1,1,3,3,5,5- Г ексаметилцик-логексан (триизобутилен) 18,0 56,5 86,8 110,0 153,0 179,0
С12Н24О С12Н24О2 Додеканаль (лауриновый альдегид) Додекановая кислота (лауриновая кислота) 77,7 129,3 123,7 172,4 157,8 184,5 225,9 231,8 257,0 299,0 44,5 48
С]2Н24О Додекан-2-он 77,1 120,4 152,4 177,5 222,5 246,5
С]2Н26 C12H26 Додекан 2-Метилундекан 52 91,6 85,0 122,0 115,6 146,1 139,9 191,0 184,8 216,3 210,0 -9,6
С12Н2бО Додекан-1 -ол 91,0 134,7 167,2 192,0 235,7 259,0 24
С12Н2бО4 Изопропокси-трипропилен-гликоль (моноизопропиловый эфир трипропи-ленгликоля) 82,4 127,3 161,4 187,8 232,8 256,6
Физические свойства важнейших веществ
211
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Т °C
0,133 кПа 1.33 кПа 5.33 кПа 13.3 кПа 53,3 кПа 101,3 кПа
о о п р рр р Ю Ю Ю Ю bJ Ю bj XX X X X X X UJ IzJ W Ю bJ bj Os O' -t» Ф 00 О ~U О О О p Й Z Z СЛ & GO i I z А,А-Диизобутил-2-метилпропан-1 -амин (триизо-бутиламин) Додекан-1 -амин Г ексил(триэтил)-силан Г ексаэтилтриси-локсан Октаметил-1,7-диэтокситетра-силоксан Додекаметилпентасилоксан Додекаметил-циклогексаси-локсан 32,3 82,8 52,4 67,7 56,6 67,3 69,8 127,8 96,4 123,0 108,6 98,0 110,0 97,8 158,4 130,0 152,9 139,0 128,8 141,8 119,7 182,1 156,0 177,1 162,0 162,8 166,3 157,8 225,0 204,6 223,5 204,0 196,5 210,6 179,0 248,0 230,0 250,3 227,5 220,5 236,0 -21,8 -28 -3,0
c13 c13h9n Cj3H10 СвНюО С1зН]о02 C13H10O3 C13H12 С,зН12О C13H12O С13Н12О C13H13ClSi C)3Hl3N С13Н14 С]3Н14 С13Н14 С1зН)4 C13H14Si С1зН]8О С1зН2о Акридин Флуорен Бензофенон (ди-фенилкетон) Фенилбензоат Фенил-2-гидроксибензоат (салол, фенилса-лицилат) Мстилендибен-зол (дифенилме-тан) (Бензилок-си)бснзол Дифенилметанол (бензгидрол) 1-(1-Нафтил )-пропан-1 -он Метил(дифенил)-(хлор)силан А-Метил-А-фениламин 1 -Изопропил-нафталин 2-Изопропил-нафталин 1 -Пропилнафта-лин 2-Пропилнаф-талин Метил(дифенил)-силан 1 -Фенилгептан-1-он Гептилбензол 129,4 112,7 106,8 117,8 80,6 95,4 110,0 124,0 105.0 103,5 76,0 86,9 87,6 88,0 100,0 69,4 184,0 146,0 159,9 157,8 167,0 125,5 144,0 162,0 171,0 152,7 149,7 129,3 128,5 131,9 132,6 132,8 145,5 112,5 224,2 183,6 188,0 (4,00 кПа) 197,6 205,0 152,1 (4,00 кПа) 180,1 200,0 206,9 189,2 184,0 162,9 162,0 158,7 (4,00 кПа) 159,5 (4,00 кПа) 166,4 178,9 138,0 (4,00 кПа) 256,0 213,4 224,4 227,8 233,8 186,7 209,2 227,5 233,5 216.0 210,1 189,7 188,8 193,7 194,6 193,7 204,2 171,3 314,3 267,8 276,8 283,5 284,8 237,5 259,8 275,6 280,2 266,5 257,0 239,7 239,4 241,5 248,3 346,0 297,9 306 314,0 313,0 264,3 287,0 301,0 306,0 295,5 282,0 267,9 268,2 272,5 273,5 266,8 271,3 245,5 110,5 114,2 70,5 42,5 25,2 68,5 -7,6 -15,5 -8,5 -3 -48
212
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Т °C
0,133 кПа 1.33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С13Н20О • 4-(2,6,6- 79,5 123,0 155,6 181,2 225,2 250,0
Триметил цикло-гекс-2-енил)бут-
З-ен-2-он (а-ионон)
С13Н22О2 (1,7,7-Тримстил-бицикло[2.2.1]- 64,6 108,0 140,4 165,7 211,2 235,0
гепт-2-ил)-пропионат
(борнилпропио-
нат)
С13Н24 Тридец-1-ин 61,3 103,0 128,0 (4,00 кПа) 160,7 234,0 -5
С13Н26 Г ептилциклогек- 64 107 133 167 244 -40,4
сан (4,00 кПа)
С,зН26 Октилциклопен- 69 111 143 169 216 243 -44
тан
С13Н26 Тридец-1 -ен 63,9 104,5 135,9 160,7 206,8 232,8 -23,1
С13Н26О Тридекан-2-он 86,8 131,8 165,7 191,5 238,3 262,5 28,5
С]зН2бО2 Метилдодекано-ат (метиллаурат) 87,8 133,2 166,0 190,8 (разл.) 5
С13Н26О2 Тридекановая 137,8 181,0 212,4 236,0 276,5 299,0 41
кислота
С13Н28 Тридекан 67 107,1 138,4 163,3 209,5 235,4 -5,4
С13Н28 2 -Метилдодекан 59,6 100,5 132,2 157,3 203,6 229,5
С13Н28О4 Бутокситрипро- 101,5 147,0 179,8 204,4 247,0 269,5
пилснгликоль
(монобутиловый эфир трипропи-
ленгликоля)
C13H30Si Г ептил(триэтил)- 70,0 114,6 148,0 174,0 221,0 247,0
силан
С1зНзо81 Децил(три-метил)силан 67,4 111,0 144,0 169,5 215,5 240,0
С]4
С14Н8О2 Антра-9,10- 190,0 (тв.) 234,2 (тв.) 264,3 285,0 346,2 379,9 286
хинон (тв.) (тв.)
С14Н8О4 1,4-Дигидрокси- 196,7 259,8 307,4 344,5 413,0 450,0 (разл.) 194
антра-9,10-хинон (разл.)
(хинизарин)
СиНю Антрацен 145,0 (тв.) 187,2 (тв.) 218,4 250,1 309,1 342,3 216,0
С^Ню Фенантрен 118,2 173,0 218,0 249,0 307,1 340,1 99,1
С14НюО2 Бензил 128,4 183,0 224,5 255,8 314,3 347,0 95
(дибензоил)
С14Н10Оз Бензойный ан- 143,8 198,0 239,8 270,4 328,8 360,0 42
гидрид
С14Н12 1,Г-Этен-1,1-диилдибензол 87,4 135,0 170,8 198,6 249,8 277,0
С14Н12 1, Г-Этен-1,2-диилдибензол 113,2 (тв.) 161,0 199,0 227,4 287,3 306,5 124
(стильбен)
С14Н12О 1,2-Дифенил-этанон (дезокси- 123,3 173,5 212,0 241,3 293,0 321,0 60
бензоин)
Физические свойства важнейших веществ
213
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара т„л, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С14Н12О2 2-Гидрокси-1,2-дифенилэтанон (бензоин) 135,6 188,0 227,6 258,0 313,5 343,0 132
С14Н14 1,1'-Этан-1,2-диилдибензол (дибензил) 86,8 136,0 173,7 202,8 255,0 284,0 51,2
с14н14о 2-Метил-1-(2-нафтил)пропан-1-он 133,2 181,0 215,6 242,3 288,2 313,0
C,4H15N c14h15n TV-Бензил-1 -фенилметанамин (дибензиламин) /У-Фенил-УУ-этиланилин 118,3 98,3 165,6 146,0 200,2 227,3 209,8 274,3 300,0 286,0 -26
Ci4H|6 1 -Бутилнафталин 97,5 144,1 171,8 (4,00 кПа) 208,0 289,3 -19,7
Ci4H16 2-Бутилнафталин 99,2 146,0 173,9 (4,00 кПа) 210,2 292 -5
С14Н20С12 1,2-Дихлор- 3,4,5,6-тетра-этилбензол 105,6 155,0 192,2 220,7 272,8 302,0
С14Н20С12 1,4-Дихлор-2,3,5,6-тетра-этилбензол 91,7 143,8 183,2 212,0 265,8 296,5
С]4Н22 Октилбензол 84 127,6 153,8 (4,00 кПа) 187,9 264,5 -36
С14Н22О 2,4-Ди-трет-бутилфенол 89,0 132,4 158,0 (4,00 кПа) 191 263,5 56,5
С14Н24О2 [(£>3,7-Диметилокта-2,6-диен-1 -ил]бутират(геранилбутират) 96,8 139,0 170,1 193,8 235,0 257,4
С14Н24О2 [(£)-3,7-Диметилокта-2,6-диен-1-ил]изобутират (геранилизобутират) 90,7 133,0 164,0 187,7 228,5 251,0
С14Н24О2 (1,7,7-Триметилбицик-ло[2.2.1]гепт-2-ил)бутират(борнилбутират) 74,0 118,0 150,7 176,4 222,2 247,0
С14Н24О2 (1,7,7-Триметил-бицикло[2.2.1]-гепт-2-ил)изо-бутират (борнилизобутират) 70,0 114,0 147,2 172,2 218,2 243,0
С14Н26 Тстрадец-1-ин 75,5 118,3 144,0 (4,00 кПа) 177,4 252 0
С14Н26О4 Диэтилдекандио-ат (диэтилсеба-цинат) 125,3 172,1 207,5 234,4 280,3 305,5 1,3
214
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки ( °C) при давлении насыщенного пара Т °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101.3 кПа
С14Н28 с14н28 С14н28 с14н280 с14н280 С14Н28О2 С14Н29С1 С14Нзо С14Н30 c14h31n C14H32Si C|4H40O6Si5 C]4H42C>7Si6 Ci4H42O7Si7 Нонилциклопентан Октилциклогексан Тетрадец-1-ен Тетрадеканаль (миристиновый альдегид) Тетрадекан-2-он Тетрадекановая кислота (миристиновая кислота) 1 -Хлортетрадекан 2-Метилтридекан Тетрадскан Тетрадекан-1-амин Октил(триэтил)-силан Декаметил-1,10-диэтоксипента-силоксан Т етрадекаметил-гексасилоксан Т етрадекаметил-циклогептаси-локсан 83 77 74,5 99,0 99,3 149,3 98,5 80 102,6 73,7 89,0 73,7 86,3 126 122 119,0 148,3 145,5 192,4 148,2 115,2 121,9 152,0 120,6 131,5 117,6 131,5 159 149 (4,00 кПа) 144,4 (4,00 кПа) 186,0 179,8 223,5 187,0 147,9 154 189,0 155,7 162,2 149,8 165,3 186 184,3 177,1 214,5 206,0 248,7 215,5 173,7 197,5 215,7 184,3 187,0 175,2 191,8 235 224,5 267,9 253,3 294 267,5 226,9 264,6 235,0 230,0 220,5 239,2 262 264 251,1 297,8 278,0 318 296,0 247,9 253,6 291,2 262,0 253,3 245,5 264,0 -29 -19,7 -12,8 23,5 59,9*2 0,9 5,5 -32
C15 C,5H14O C15H18 c15H18 c15h180 Ci5HI8OSi C15H24 c15H24 C15H24O CisH24O Ci5H24O C15H26O 1,3-Дифенил-ацетон 1 -Пентилнаф-талин 2-Пентилнаф-талин 2,4,6-Триаллил-фенол Метил(дифенил)-(этокси)силан Нонилбензол а-Кадинен 2,4-Ди-АП/?вАИ-бутил-5-метилфенол 2,4-Ди-7и/?ети-бутил-6-метил фенол 2,6-Ди-7и/?ети-бутил-4-метилфенол Цедран-8-ол (кедровая камфора, цедрол) 125,5 112 113,2 116,2 109,0 96 101,3 108,8 94,9 93,0 100,0 177,6 159,1 160,9 161,1 152,7 141,5 146,0 152,6 138,5 136,2 148,0 216,6 187,3 (4,00 кПа) 189,3 (4,00 кПа) 187,4 (4,00 кПа) 186,0 168,5 (4,00 кПа) 179,8 178,2 (4,00 кПа) 164,1 (4,00 кПа) 161,5 (4,00 кПа) 184,0 246,6 224,1 226,4 221 211,8 203,6 205,6 211 194 194 211,9 301,7 256,8 250,7 257 261,2 330,5 307 310 294 282,0 282,0 275,0 282 265 265 288,0 34,5 -24,4 -24 62,1 70 91
Физические свойства важнейших веществ
215
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Тпл, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С15Н28 Пентадец-1 -ин 85,7 129,8 156,3 (4,00 кПа) 190,8 268 10
С15Н30 Децилциклопен- 96,6 140,7 174,5 201,8 251,3 279,4 -22,1
тан
С15Н3о Нонилциклогек- 89 136 164 200 282 -10,2
сан (4,00 кПа)
С15Н30 Пентадец-1 -ен 91,2 133,7 166,5 192,7 241,2 268,4 -3,7
С15Нз2 Пентадекан 93 136 168,7 195,0 243,4 270,6 9,9
С15Н32 2-Метилтетра- 86,1 129,3 162,8 189,3 265,4
декан
С15Н3о02 Метилтетрадеканоат (метилми- 115,0 160,8 195,8 222,6 269,8 295,8 18,5
ристинат)
с15н32о5 13-Метил-3,6,9,12-тетра- 116,6 163,0 197,7 223,3 268,3 292,7
оксадекан-1 -ол
(моноизопропиловый эфир тетраэтиленгликоля)
C15H34Si Додецил(три-метил)силан 91,2 137,7 172,1 199,5 248,0 273,0
С16
С1бН14О2 Бензилциннамат 173,8 221,5 255,8 281,5 326,7 350,0 39
С16н18о 1,1 '-(Оксидиэтан- 96,7 144,0 179,6 206,8 254,8 281,0
1,1 -диил)-дибензол
С16Н20 1-Гексил- 121,4 170,2 199,2 237,0 322 -18
нафталин (4,00 кПа)
С,бН20 2-Гексил- 122,8 171,7 200,9 238,8 324 -3
нафталин (4,00 кПа)
C16H20O2Si Дифенил(ди-этокси)силан 111,5 157,6 193,2 220,0 259,7 296,0
С16Н22О4 Дибутилфталат 148,2 198,2 235,8 263,7 313,5 340,0
С16Н25С1 1-Хлор-2,3,4,5,6-пентаэтилбензол 90,0 140,7 178,2 208,0 257,2 285,0
С16н26 Децилбензол 109 156 184 217,8 269,1 297,9 -14,4
С16н26 Пентаэтилбензол 96,0 135,8 171,9 200,0 250,2 277,0
С16Н26О 4,6-Ди-гарега- 110,6 154,4 180,2 213 284 85,5
бутил-2,3-димстилфенол (4,00 кПа)
С16Н26О 2,4-Ди-гарега- 115,2 159,4 185,1 218 264 289 80,5
бутил-5-этилфенол (4,00 кПа)
С16Н26О 2,4-Ди-т/?ет- 100,4 144,3 170,0 203,0 275 30
бутил-6-этилфенол (4,00 кПа)
С16Н26О 2,6-Ди-трет- 95,9 139,9 165,7 199,0 272 44,0
бутил-4-этил фенол (4,00 кПа)
С1бНзо Гексадец-1-ин 103,3 147,8 174,2 (4,00 кПа) 208,6 284 15
C16H31N Пальмитонитрил 134,3 185,8 223,8 251,5 304,5 332,0 31
С16Н32 Гексадец-1-ен 103,9 147,3 180,7 207,6 257,1 284,9 4,1
С1&Н32 Децилциклогек- 101 148 177 217,0 268,6 297,6 -1,7
сан (4,00 кПа)
216
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара г11Л, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С1бН32 С16Н32 с16н32о с16н32о С16Н32О2 С16Нз4 С16Нз4 Ci6H34O CI6H35N C16H36Si C16H46O7Si6 Ci6H4sO6Si7 Ci6H480gSi8 1,1,3,3,5,5,7,7-Октаметилцикло-октан (тетраизобутилен) Ундецилциклопентан Г ексадекан-2-он Пал ьм итальдегид Пальмитиновая кислота 2-Метилпентадекан Гексадекан Гексадекан-1-ол (цетиловый спирт) Гексадекан-1-амин (цетиламин) Дсцил(триэтил)-силан Додскаметил-1,11 -диэтоксигексасилоксан Г ексадекаметил-гептасилоксан Г ексадекаметил-циклооктасилок-сан 63,8 108 109,8 121,6 165,2 98,4 105 122,7 123,6 108,5 103,6 93,2 103,5 108,5 153 167,3 171,8 211,8 142,6 149,0 177,8 176,0 155,6 147,5 138,5 150,5 142,2 188 203,7 210,0 244,4 176,9 182,8 219,8 215,7 191,7 180,0 171,8 186,2 167,5 216 230,5 239,5 272,2 294,0 209,5 251,7 245,8 218,3 205,5 198,0 213,8 214,6 267 279,8 292,3 326 259,0 312,7 300,4 267,5 250,0 244,7 263,0 240,0 296 307,0 321,0 351,8 281,9 186,8 344,0 330,0 293,0 273,5 270,0 290,0 -10 34 61,9*2 18,2 49,3 46 31,5
C17 C17H10O C17H22 С17И22 C17H24O2 C17H28 C17H28O C17H32 C17H34 Q7H34 C17H34 C17H34O С17Н34О2 C17H36 СрНзб 10-Бензантрон 1-Гептил-нафталин 2-Гептил-нафталин (2-Изопропил-5-метилциклогек-сил)бензоат (метилбензоат) Ундецилбензол 2,6-Бис(1,1-диметилпропил)-4-метилфенол Гептадец-1-ин Гептадец-1-ен Додецилциклопентан Ундецил циклогексан Г ептадекан-2-он Метилпальмитат Гептадекан 2-Метилгексадекан 225,0 133,9 134,6 123,2 121 106,0 114,0 116 120 112 129,6 134,3 117 297,2 184,2 185,0 170,0 169 150,5 159,6 160 166 161 178,0 184,3 162 155,4 350,0 214,1 (4,00 кПа) 214,9 (4,00 кПа) 204,3 197 (4,00 кПа) 176,5 (4,00 кПа) 186,7 (4,00 кПа) 186,3 (4,00 кПа) 202 191 (4,00 кПа) 214,3 (разл.) 195,9 190,6 390,0 253,0 253,9 230,4 234 210 221,8 221,0 230 229 242,0 223,3 218,3 277,1 271,3 282 291,7 273,8 340 341 301,0 316 283 299 299,7 312 316 319,5 302,1 297,7 174 -8 1 54,5 -5 22 11,2 -5 5,8 30 22,0
Физические свойства важнейших веществ
217
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки ( ЭС) при давлении насыщенного пара Т °C
0,133 кПа 1,33 кПа 5,33 кПа 13.3 кПа 53,3 кПа 101,3 кПа
C17H36Si Т римети л(тетра-децил)силан 120,0 166,2 201,5 227,8 275,0 300,0
р п р ppp р р р рр р р р р р рр р ррр“ ОО 00 ОФ 00 00 ОС 00 00 00 00 00 ОООООООООСОООООООООС х х ill х х х II х х х х х хх х iii 4^ hj \О 00 00 ОС О'- О' О'- О' иДА.ОООДД'-'’'-'’ 0020 ОО ОО о о > ОС bJ N) Ю -U (/) (Z) (Z) "С 00 Трифениларсин Трифенилфосфат 1 -Октилнафталин 2-Октилнафталин Г ексаэтилбснзол Додецилбензол 2,4,6-Tpn-wpew-бутилфенол Октадец-1-ин Олеиновая кислота (£)-0ктадец-9-еновая кислота (элаидиновая кислота) Додецилциклогексан Октадец-1-ен Т ридецилцикло-нентан Стеариновый альдегид (октаде-каналь) Стеариновая кислота 2-Метилгепта-декан Октадекан Октадекан-1-ол тУ-Этилгексадс-кан-1 -амин Т етрадекамети л-1,13-диэтокси-гептасилоксан Октадекаметилоктасилоксан 168,3 193,5 146,0 145,8 132 103,2 (тв.) 123,8 176,5 171,3 122 128 131 140 181,8 120 129 150,3 133,2 119,0 105,8 223,8 249,8 198 197,2 150,3 181 147,2 170,5 223,0 223,5 172 172 179 192,1 229,9 168 173,6 202,0 186,0 163,5 152, 290,3 228 (4,00 кПа) 227,6 (4,00 кПа) 187,7 210 (4,00 кПа) 172,9 (4,00 кПа) 198,3 (4,00 кПа) 257,2 198,8 (4,00 кПа) 203 (4,00 кПа) 207 215 230,8 263,3 204 208,8 240,4 226,5 197,0 187,5 295,2 322,5 268 267,3 216,0 248 206 234,2 286,0 288,0 242 234,2 244 260,0 291,6 232 236,6 269,4 256,8 223,2 214,5 379,2 268,5 334,7 337,0 285,3 297 313,8 343,2 280 288,4 320,3 313,0 268,3 263,5 413,5 356 357 298,3 331 278 313 360,0 (разл.) 362,0 331 314,2 327 342,5 370 (разл.) 313 317 349,5 342,0 (разл.) 293,5 290,0 49,4 -2 12 130 3 131 27 14 51,5 12,5 18 5 63,5 68,7*2 28,2 58,5
С19 С19Н16 С]9Н26 С19Н26 С19Н32 Ci9H36 1, Г, 1 "-Метантри-илтрибензол (трифенилметан) 1-Нонил-нафталин 2-Нонил-нафталин Т ридецилбензо л Нонадец-1-ин 169,7 157 157 143 133,9 197,0 209,7 209,7 194 181,6 215,5 240,9 (4,00 кПа) 240,9 (4,00 кПа) 223 (4,00 кПа) 209,9 (4,00 кПа) 228,4 281,5 281,5 262 246,5 249,8 259,2 372 372 346 327 92,1 8 12 10 33
218
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Д.л, °C
0,133 кПа 1.33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С19Н38 Нонадец-1 -ен 138,8 184 211,2 (4,00 кПа) 247 298,6 328,0 23,4
С19Н38 Тетрадецилцик-лопентан 142 190 227 256 310 341 9
С]9Н38 С19Н40 Т ридецилцикло-гексан 2-Метилоктадекан 132 184 179 215 (4,00 кПа) 216 255 245 346 327 18,5
С19Н40 Нонадекан 139 185 220,8 249,2 302 330 31,8
Сю
СгоНгоОЗ! Трифенил-(этокси)силан 167,0 213,5 247,0 273,5 319,5 344,0
С20Н28 1 -Децилнафталин 168 222 253 (4,00 кПа) 295 387 15
С20Н28 2-Д еци л нафтал и н 168 221,6 253,5 (4,00 кПа) 294,9 387 20
С2()Н34 Тетрад ецилбен-зол 153 204 235 (4,00 кПа) 274 359 16
СгоН38 Эйкоз-1-ин 143,2 191,8 220,7 (4,00 кПа) 258,0 340 36
С20Н40 Эйкоз-1-ен 149 195 222,9 (4,00 кПа) 259 311,4 341,2 28,6
С20Н40 Пентадецилциклопентан 152 201 239 269 324 355 17
С20Н40 С20Н42 Т етрадецил циклогексан 2-Метилнонадекан 141 194 191 226 (4,00 кПа) 228 267 257 360 341 24,0
С20Н42 Эйкозан 150 196 232,5 261 314 343 36,4
C2oH43N У,У-Диэтил-гексадскан-1-амин 139,8 194,0 235,0 265,5 324,6 355,0
C20H58O9Si8 Г ексадекаметил -1,15-диэтокси-октасилоксан 133,7 179,7 213,8 240,0 286.0 311,5
C2oH6o08Si9 Эйкозаметилнонасилоксан 144,0 189,0 220,5 244,3 286,0 307,5
с2!
С21Н21О4Р Три(2-метил-фенил)фосфат (три-о-толил фосфат) 154,6 198,0 229,7 252,2 292,7 313,0
C21H3O 1-Ундецил-нафталин 177 232,6 265,2 (4,00 кПа) 307,4 401 23
C2lH30 2-Ундецил-нафталин 177 232,6 265,2 (4,00 кПа) 307,4 401 20
C2iH36 Пентадецилбен-зол 163 216 247 (4,00 кПа) 287 373 22
C21H40 Генэйкоз-1-ин 151,7 201,2 230,6 (4,00 кПа) 268,6 352 41
C21H42 Генэйкоз-1-ен 153,8 203,5 233,1 (4,00 кПа) 271,3 355 33,4
C21H42 Гексадецилцик-лопентан 162 212 250 280 336 368 21
C21H42 Пентадецилциклогексан 150 204 236 (4,00 кПа) 278 373 29,0
Физические свойства важнейших веществ
219
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара тпл, °C
0,133 кПа 1.33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С21Н44 С21Н44 Генэйкозан 2-Метилэйкозан 160 207 201 244 239 272,0 269 326 356 354 40,2
с22
С22Н32 1 -Додецил-нафталин 187 243,8 277,0 (4,00 кПа) 320,0 415 27
С22Н32 2-Додецил-нафталин 187 243,0 276,2 (4,00 кПа) 319,1 414 26
С22Н38 Гексадецил бензол 173 226 258 (4,00 кПа) 298 385 27
С22Н42 Докоз-1 -ин 159,5 209,9 239,7 (4,00 кПа) 278,4 363 45
С22Н42О2 (Е)-Докоз-13-еновая кислота (брассидиновая кислота) 209,6 256,0 290,0 315,2 359,6 382,5 (разл.) 61,5
С22Н42О2 (Z)-Докоз-13-еновая кислота (эруковая кислота) 206,7 254,5 289,1 314,4 358,8 381,5 (разл.) 33,5
С22Н44 Гексадецилцик-логексан 158 213 246 (4,00 кПа) 288 385 33,6
С22Н44 Гептадецилцик-лопентан 164 218 249 (4,00 кПа) 290 380 27
С22Н44 Докоз-1-ен 162,3 213,0 243,0 (4,00 кПа) 281,9 367 37,8
С22Н46 С22Н46 Докозан 2-Метилген-эйкозан 169 217 212 254 251 283 281 338 370 367 44,0
C22H66O9S110 Докозаметилдекасилоксан 160,3 202,8 233,8 255,0 293,8 314,0
С2з
С23Н40 Гептадецилбен-зол 186 238,5 269,5 (4,00 кПа) 309,5 308 32
С23Н44 Трикоз-1-ин 167,3 218,5 248,8 (4,00 кПа) 288,1 384 49
С23Н46 Гептадецилцик-логексан 166 222 255 (4,00 кПа) 299 397 37,8
С2зН46 Октадецилциклопентан 172 226, 258 (4,00 кПа) 300 391 30
С23Н46 С23Н48 Трикоз-1-ен 2-Метилдокозан 170,8 222,4 222 253,0 (4,00 кПа) 261 292,5 291 379 379 41,6
С23Н48 Трикозан 179 227 264 294 349 380 47,5
С24
С24Н42 Октадецилбензол 194 247,5 279,0 (4,00 кПа) 319,5 408 36
С24Н46 Тетракоз-1-ин 175,2 227,1 257,9 (4,00 кПа) 297,8 385 52
С24Н48 Нонадецилциклопентан 180 235 268 (4,00 кПа) 310 402 35
С24Н48 Октадецил циклогексан 175 231 265 (4,00 кПа) 309 409 41,6
С24Н48 С24Н50 Тетракоз-1-ен 2-Метилтрикозан 189,8 231,1 232 262,1 (4,00 кПа) 271 302,2 302 390 391 45,3 37,7
С24Н50 Тетракозан 188 236 274 304 360 394 50,6
220
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Тпл, °C
0.133 кПа 1,33 кПа 5,33 кПа 13.3 кПа 53,3 кПа 101,3 кПа
C^O^Si., Т етракозаметил-ундекасилоксан 185,2 216,7 246,2 266,3 303,7 322,8
С25
С25Н44 Нонадецилбензол 202 256,6 288,5 (4,00 кПа) 329,5 419 40
С25Н48 Пентакоз-1-ин 182,3 235,0 266,2 (4,00 кПа) 306,6 305 55
С25Н50 Нонадецилциклогексан 180 237 272 (4,00 кПа) 318 420 45,2
С25Н5О Пентакоз-1-он 186,5 239,7 271,2 (4,00 кПа) 311,9 401 48,7
С25Н50 Эйкозил цикло-пентан 190 246 297 (4,00 кПа) 321 413 38
С25Н52 Пентакозан 196 245 283 313 370 401 53,5
с26
С26Н46 Эйкозилбензол 209 264,9 297,2 (4,00 кПа) 338,7 429 44
С2бН50 Гексакоз-1-ин 189,4 242,9 274,5 (4,00 кПа) 315,5 405 57
с26н52 Гексакоз-1-ен 193,6 247,5 279,5 (4,00 кПа) 320,7 411 51,8
С2бН52 Гснэйкозилцик-лопентан 195 252 285 (4,00 кПа) 328 423 42
с26н52 Эйкозилциклогексан 188 246 281 (4,00 кПа) 327 430 48,5
С2бН54 Гексакозан 205 254 292 322 379 412 56,3
С27
с27н48 Генэйкозилбен-зол 217 273,2 305,9 (4,00 кПа) 347,9 439 48
С27Н52 Гептакоз-1-ин 196,6 250,7 282,8 (4,00 кПа) 324,3 415 60
С27Н54 Генэйкозил циклогексан 195 254 289 (4,00 кПа) 335 440 51,5
С27Н54 Гептакоз-1-он 200,8 255,4 287,8 (4,00 кПа) 329,6 421 54,7
С27Н54 Докозилциклопентан 202 260 294 (4,00 кПа) 337 433 45
с27н56 Гептакозан 212 262 300 331 389 422 58,9
С28
с28н50 Докозилбензол 224 280,7 313,8 (4,00 кПа) 356,2 448 51
С28Н54 Октакоз-1 -ин 203,0 257,8 290,3 (4,00 кПа) 332,3 424 62
С28Н56 Докозилциклогексан 200 260 296 (4,00 кПа) 343 449 54,4
С28Н56 Октакоз-1-ен 207,1 264,4 295,2 (4,00 кПа) 337,5 430 57,5
С28Н36 Трикозил циклопентан 208 267 301 (4,00 кПа) 345 442 49
с28н58 Октакозан 220 270 309 340 398 432 61,3
С29
СгэНзг Т рикозилбензол 231 288,3 321,7 (4,00 кПа) 364,5 457 54
С29Н56 Нонакоз-1-ин 208,7 264,1 296,9 (4,00 кПа) 339,3 432 65
Физические свойства важнейших веществ
221
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
С29Н58 Нонакоз-1-ен 214,3 270,3 303,5 (4,00 кПа) 346,4 440 60,0
С29Н58 Т етракозилцик-лопентан 219 277 310 (4,00 кПа) 354 451 51
С29Н58 Т рикозил циклогексан 207 268 304 (4,00 кПа) 352 459 57,0
С29Н60 Нонакозан 227 277 316 348 406 441 63,4
С30
С30Н54 Тетракозилбен-зол 238 295,9 329,7 (4,00 кПа) 372,8 466 57
С30Н58 Триаконт-1-ин 215,1 271,2 304,4 (4,00 кПа) 327,3 443 67
СзоНбо Пентакозилциклопентан 225, 284 318 (4,00 кПа) 363 460 54
СзоНбо Т етракозилцик-логексан 213 274 310 (4,00 кПа) 359 467 59,5
СзоНбо Триаконт-1-ен 220,0 276,6 310,1 (4,00 кПа) 353,4 448 62,4
СзоН62 Триаконтан 234 284 324 356 414 450 66,0
с31
С3,Н56 Пентакозил бензол 244 302,7 336,8 (4,00 кПа) 380,3 474 59
С31Нбо Г ентриаконт-1 -ин 220,7 277,4 311,0 (4,00 кПа) 354,4 449 69
Сз,Н62 Гексакозилциклопентан 231 290 325 (4,00 кПа) 370 468 56
с31н62 Г ентриаконт-1 -ен 226,4 283,7 317,6 (4,00 кПа) 361,4 347 64,6
Сз 1Н62 Пентакозилциклогексан 218 280 317 (4,00 кПа) 366 476 61,9
С31Нб4 Гентриаконтан 240 291 331 363 422 458 67,3
С32
С32Н58 Г ексакозилбензол 250 309 344 (4,00 кПа) 388 482 62
С32Нб2 Дотриаконт-1 -ин 226,5 283,7 317,5 (4,00 кПа) 361,4 347 71
С32Н64 Гексакозилциклогексан 224 287 324 (4,00 кПа) 373 484 64,0
С 32^64 Гептакозилциклопентан 237 297 332 (4,00 кПа) 377 476 59
СзгНб4 Дотриаконт-1 -ен 232,1 290,0 324,2 (4,00 кПа) 368,5 465 66,7
СзгНбв Дотриаконтан 247 298 338 371 430 467 69,2
С33
СззНбо Гептакозилбензол 262 320,3 354 (4,00 кПа) 397,4 490 64
СззНб4 Тритриаконт-1-ин 231,4 289,2 323,4 (4,00 кПа) 367,6 464 73
С33Нбб Гептакозилциклогексан 229 292 330 (4,00 кПа) 380 492 66,1
СззНбб Октакозилциклопентан 243 301 338 (4,00 кПа) 384 483 61
СззНбб Тритриаконт-1 -ен 237,8 296,2 330,9 (4,00 кПа) 275,5 473 68,7
222
Новый справочник химика и технолога
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Г„л, °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
с33н68 Тритриаконтан 253 305 345 378 437 375 71,1
С34
С34н62 Октакозилбснзол 268 327 361 (4,00 кПа) 405 498 66
С34н66 Т етратриаконт-1 -ин 237,2 295,6 330,1 (4,00 кПа) 374,7 472 74
С34Н68 Нонакозилциклопентан 249 309 345 (4,00 кПа) 391 491 63
С34Н68 Октакозилциклогексан 234 298 336 (4,00 кПа) 386 499 68,0
с34н68 Тетратриаконт-1 -ен 243,5 302,5 337,5 (4,00 кПа) 382,6 481 70,5
с34н70 Т етратриаконтан 259 311 352 384 444 482 72,7
С35
C3sH(>4 Нонакозилбензол 274 333 368 (4,00 кПа) 411 505 68
с35н68 Пентатриаконт-1 -ин 242, 301,0 335,9 (4,00 кПа) 380,8 479 76
С35Н7О Нонакозилцикло-гсксан 239 304 342 (4,00 кПа) 393 507 69,9
С35Н7О Пентагриаконт-1 -ен 249,2 308,8 344,1 (4,00 кПа) 389,7 489 72,3
С35Н7о Т риаконтилцик-лопентан 254 315 351 (4,00 кПа) 497 498 65
Q5H-72 Пентатриаконтан 25 317 358 391 451 490 74,5
С36
С36н66 Триаконтилбсн-зол 279 339 374 (4,00 кПа) 418 512 70
с36н70 С3бН72 Г ексатриаконт-1 -ин Г ексатриаконт-1 -ен 274,4 307,2 314,4 342,3 (4,00 кПа) 349,9 (4,00 кПа) 387,5 395,8 486 496 77 73,9
С36н72 Гентриаконтилциклопентан 259 321 357 (4,00 кПа) 404 505 67
С36Н72 Триаконтилцик-логексан 244 309 348 (4,00 кПа) 399 514 71,6
С36н74 Г ексатриаконтан 270 323 364 297 457 497 75,9
С37
с37н68 Гентриаконтил-бензол 285 345 380 (4,00 кПа) 425 519 72
С37Н72 Г ептатриаконт-1 -ин 252,2 312,1 347,5 (4,00 кПа) 393,2 493 79
с37н74 Гентриаконтилциклогексан 248 314 353 (4,00 кПа) 404 520 73,3
с37н74 Г ептатриаконт-1 -ен 259,2 319,9 355,7 (4,00 кПа) 402,0 503 75,5
с37н74 Дотриаконтилциклопентан 265 327 363 (4,00 кПа) 410 512 69
С37н76 Г ептатриаконтан 276 329 370 403 463 504 77,7
С38
с38н70 Дотриаконтил-бензол 290 351 386 (4,00 кПа) 430 525 74
с38н74 Октатриаконт-1-ин 256,4 316,8 352,5 (4,00 кПа) 398,5 499 80
С38н76 Дотриаконтилциклогексан 253 319 358 (4,00 кПа) 410 527 74,8
Физические свойства важнейших веществ
223
Продолжение табл. 3.3.9
Формула Название Температура кипения или возгонки (°C) при давлении насыщенного пара Тш„ °C
0,133 кПа 1,33 кПа 5,33 кПа 13,3 кПа 53,3 кПа 101,3 кПа
СзвНуб Октатриаконт-1 -ен 264,1 325,3 361,5 (4,00 кПа) 408,2 510 77,0
С38Н76 Тритриаконтилциклопентан 269 332 369 (4,00 кПа) 416 518 70
С38Н78 Октатриаконтан 281 384 376 409 469 511 79,0
С39
С39Н72 Т ритр иаконтил-бензол 295 357 392 (4,00 кПа) 437 532 75
^39^76 Нонатриаконт-1 -ин 260,7 321,5 357,4 (4,00 кПа) 403,8 505 82
С39Н78 Нонатриаконт-1 -ен 269,1 330,8 367,3 (4,00 кПа) 414,4 517 78,4
С39Н78 Тетратриаконтилциклопентан 274 338 375 (4,00 кПа) 422 525 72
С39Н78 Т ритриаконтил-циклогексан 257 323 363 (4,00 кПа) 415 533 76,3
С39Н8О Нонатриаконтан 286 339 381 414 475 518 80,3
С40
С40Н74 Тетратриаконтил бензол 300 362 397 (4,00 кПа) 442 538 77
С40Н78 Тетраконт-1-ин 265,6 327,0 363,2 (4,00 кПа) 410,0 512 83
С40Н80 Пентатриаконтилциклопентан 279 343 380 (4,00 кПа) 428 531 74
С40Н80 Тетраконт-1-ен 273,3 335,5 372,3 (4,00 кПа) 419,7 523 79,8
QoHsO Тетратриаконтилциклогексан 262 329 369 (4,00 кПа) 421 540 77,7
С40Н82 Тетраконтан 291 344 386 420 480 525 81,5
С41
С41Н76 Пентатриаконтил бензол 305 367 403 (4,00 кПа) 448 544 79
с4,н82 Гексатриаконтилциклопентан 284 348 385 (4,00 кПа) 433 537 75
С41Н82 Пснтатриакон-тилциклогексан 266 333 374 (4,00 кПа) 427 546 79,1
С42
с42н78 Гексатриаконтил бензол 309 372 407 (4,00 кПа) 453 549 80
с42н84 Гексатриаконтилциклогексан 269 337 378 (4,00 кПа) 431 551 80,4
*' Ниже 72 °C — кубическая модификация, от 72 до 187 °C — триклинная модификация.
*2 Тройная точка.
Таблица 3.3.10
Температуры кипения или возгонки (°C) органических веществ при давлении пара выше 101,3 кПа
Формула Название Температура кипения или возгонки при давлении насыщенного пара Критическая температура, °C Критическое давление, МПа
0,101 МПа 0,203 МПа 0,507 МПа 1,013 МПа 2,027 МПа 5,066 МПа
Ct CCIF3 Трифтор хлорме-тан (фреон-13) -81,2 -66,7 -42,7 -18,5 12,0 28,8 3,95
CC12F2 Дифтордихлор-этан (фреон-12) -29,8 -12,2 16,1 42,4 74,0 111,5 4,01
224
Новый справочник химика и технолога
Продолжение табл. 3.3.10
Формула Название Температура кипения или возгонки при давлении насыщенного пара Критическая температура, °C Критическое давление. МПа
0,101 МПа 0,203 МПа 0,507 МПа 1,013 МПа 2,027 МПа 5,066 МПа
СС12О Фосген 7,9 27,3 57,2 84,6 119,0 174,0 182 5,67
CC13F Фтортрихлормс- 23,7 44,1 77,3 108,2 146,7 198,0 4,38
СС14 тан (фреон-11) Т етрахлормстан 76,5 102,0 141,7 178,0 222,0 283,2 4,56
CHC1F2 Дифторхлорметан -40,8 -24,7 0,4 24,0 52,0 96,4 4,91
chci2f (фреон-22) Фтордихлорметан 8,9 29,4 59,0 87,0 121,2 177,5 178,5 5,17
CHCh CH3Br (фреон-21) Хлороформ Бромметан 61,7 3,6 23,3 120,0 54,8 152,3 84,0 191,8 121,7 190,0 191
СН3С1 Хлормстан -24,2 -6,4 22,0 47,3 77,3 126,0 143,1 6,68
CH3F Фторметан -7,3 -64,5 -42,0 -21,0 2,6 36,0 44,6 5,88
CH3I Иодметан 42,4 65,5 101,8 138,0 176,5 248,1 255
сн4 Метан -161,6 -153,0 -137,5 -123,6 -107,0 -82,1 4,64
СН4О Метанол 64,7 83,7 111,7 137,3 166,5 212 240 7,95
CH4S Метантиол 6,8 26,1 55,9 83,4 117,5 172,0 196,8 71,4
ch5n Метанамин -6,3 10,1 36,0 59,5 87,8 133,7 156,9 7,23
С2 c2cif3 Трифторхлорэти- -27,9 -1U 15,5 40,0 71,1 106 4,05
c2ci2f4 c2ci2f4 лен 1,1,1,2-Тетрафтор- 2,2-дихлорэтан 1,1,2,2-Тетрафтор- 3,0 3,5 22,8 54,5 54,0 83,1 82.3 117,2 117,5 145,7 3,27
c2ci3f3 1,2-дихлорэтан 1,1,2-Трифтор- 47,5 70,0 105,5 138,0 177,7 214,1 3,41
c2f4 c2n2 1,2,2-трихлорэтан (фреон-113) Т етрафторэтилсн Оксалонитрил -76,5 -21,2 -14 -39,6 21,4 -19,2 44,6 4,9 72,6 118,2 127 5,98
c2hcif2 c2h2 (дициан) 1,1 -Дифтор-2 -хлорэтилен Ацетилен -58,6 -83,6 -72,2 -15,7 -51,2 9,4 -32,3 39,9 -10,0 104,5 26,3 36 6,24
C2H2Ci2 (£)-1,2-Дихлор- (тв.) 47,9 69,8 104,0 135,7 173,7 236,5 243,3 5,52
C2H2C12 этилен (Z)-1,2-Дихлор- 60,8 83 119,5 152,5 193,4 260,5 271,0 5,87
c2h2f2 c2h3cif2 c2h3f3 c2h4 этилен 1,1 -Дифторэтилен 1,1 -Дифтор-1 -хлорэтан 1,1,1-Трифторэтан Этилен -85,7 -47,5 -103,7 -91,0 -49,4 38,7 -6,2 -70,5 -28,9 65,5 17,8 -51,4 -4,4 97,4 44,1 -28,4 8,9 9,9 5,12
C2H4Br2 1,2-Дибромэтан 131,4 157,7 200,0 237,0 269,0 300,0 309,8 7,15
C2H4C12 1,1-Дихлорэтан 57,4 80,2 117,3 150,3 192,7 250 250 5,07
C2H4C12 1,2-Дихлорэтан 83,5 108,1 147,8 183,5 226,5 285,0 288 5,37
c2h4f2 C2H4O C2H4O2 1,1 -Дифторэтан Оксиран (окись этилена) Метилформиат -26,5 10,4 32,0 51,9 19,5 57,7 83,5 44,0 83,6 112,0 72,9 114,0 147,2 213,0 214,0 6,00
C2H4O2 Уксусная кислота 117,9 143,5 180,3 214,0 252,0 312,5 321,6 5,79
Физические свойства важнейших веществ
225
Продолжение табл. 3.3.10
Формула Название Температура кипения или возгонки при давлении насыщенного пара Критическая температура, °C Критическое давление, МПа
0,101 МПа 0,203 МПа 0,507 МПа 1,013 МПа 2.027 МПа 5,066 МПа
С2Н5Вг Бромэтан 38,4 60,2 95,0 126,8 164,3 220,0 230,7 6,23
С2Н5С1 Хлорэтан 12,3 32,5 64,0 92,6 127,3 180,5 187,2 5,27
C2H5F Фторэтан -32,0 -16,7 7,7 30,2 57,5 102,2 4,66
С2н6 Этан -88,6 -75,5 -52,1 -31,0 -6,6 32,3 4,88
c2H6Hg с2н6о Диметилртуть Диметиловый 21,9 -23,7 -6,4 88,9 20,8 128,1 45,5 75,7 125,2 126,9 5,37
с2н6о эфир Этанол 78,4 97,5 126,0 151,8 183,0 230,0 243 6,38
c2H6s Диметилсульфид 36,0 57,8 92,3 124,5 163,8 224,5 229,9 5,53
c2H6s Этантиол 35,0 56,6 90,7 121,9 159,5 220,0 226 5,49
c2h7n А-Метил- 7,4 25,0 53,9 80,8 111,7 162,6 164,5 5,31
c2h7n метанамин Этанамин 16,6 35,7 65,3 91,8 124,0 176,0 183 5,62
Сз
C3H4 Аллен -34,3 -18,4 8,0 33,2 64,5 118,0 120,7 5,25
C3H4 Пропин -23,0 -7,1 19,5 43,8 74,0 125,0 128 5,35
СзН6 Пропен -47,7 -31,3 -47 20,1 49,4 91,8 4,62
СзН6О Ацетон 56,5 89,6 113,0 144,5 181,0 235,5 4,72
СзН6О2 Мстилацетат 57,8 97,5 113,1 144,2 181,0 233,7 4,69
СзН6О2 СзН6О2 Пропионовая кислота Этилформиат 141,1 54,3 76,0 186,0 110,5 203,5 142,2 220,0 180,0 235,3 4,74
С3н8 Пропан -42,1 -26,1 2,5 28,0 57,9 96,8 4,26
СзН8О Метоксиэтан 7,5 26,5 56,4 84,0 108,0 164,7 4,4
СзН8О Пропан-1 -ол 97,8 117,0 149,0 177,0 210,8 264 5,09
СзН8О Пропан-2-ол 82,5 101,3 130,2 155,7 186,0 232,0 235,6 5,37
c3h9n c3h9n А,А-Диметил-мстанамин Пропан-1-амин 2,9 48,5 70 54,2 103 83,5 134 118,4 170 223,8 4,74
С4
c4h5n Пиррол 130 156 195 232 275 342 352 5,67
с4н6 Бута-1,3-диен -4,4 14,5 44,7 73,0 114,0 152 4,33
С4Н60з (дивинил) Уксусный ангид- 138,6 162,0 194,0 221,5 253,0 296 4,68
С4н6о4 С4н8 С4н8 С4н8 С4н8 рид Диметилоксалат Бут-1-ен (И)-Бут-2-ен (£)-Бут-2-ен 2-Метилпропен 163,3 6.3 3,7 0,9 -7,0 189,6 43,5 23,4 12,5 228,7 71,8 54,9 52,0 43,2 105,5 84,3 80,5 71,4 114,5 105,2 260 146 144,7 0,96 4,05 4,00
С4Н8О С4н8о2 Бутан-2-он 1,4-Диоксан 79,6 101,1 125 139,5 164 173,3 200 213,0 242 308 312 5,14
С4Н8О2 Изомасляная 154,5 179,8 217,0 250,0 289,0 336 4,05
С4н8о2 кислота Масляная кислота 163,5 188,3 225,0 257,0 295,0 352,0 355 5,27
С4н8о2 Пропилформиат 81,3 104,3 142,0 176,4 217,5 264,9 4,06
с4н802 Этилацетат 77,1 100,6 136,6 169,7 209,5 250,1 3,83
с4н8о2 Метилпропионат 79,8 103,0 139,8 172,6 212,5 257,4 3,98
С4Н10 Бутан -0,5 18,1 51,2 80,7 115,3 152,0 3,8
С4Н10 Изобутан -И,7 7,5 39,0 69,3 108,7 134,9 3,65
с4н10о Бутан-1-ол 117,5 139,8 172,5 203,0 237,0 287,0 4,92
226
Новый справочник химика и технолога
Продолжение табл. 3.3.10
Формула Название Температура кипения или возгонки при давлении насыщенного пара Критическая температура, °C Критическое давление, МПа
0,101 МПа 0,203 МПа 0,507 МПа 1,013 МПа 2,027 МПа 5,066 МПа
с4н10о Бутан-2-ол 99,5 118,2 147,5 172,0 204,0 265
с4н10о 2-Метилпропан-1 -ол 108,0 127,3 156,2 182,0 212,5 265
с4н10о 2-Метилпропан-2-ол 82,9 102,0 130,0 154,2 184,5 235 4,86
с4н10о Диэтиловый эфир 34,6 55,5 89,0 119,8 156,4 194 3,61
c4H10s Диэтилсульфид 88,0 11,0 153,8 190,2 234,0 284 3,96
C4HhN Бутан-1-амин 70 100 136 167,5 205,5 251 4,15
C4HnN Л'-Эгилэтанамин 55,5 77,8 113,0 145,3 184,5 223 3,71
C4H]2Si Т етрамети лсил ан 27,0 48,0 82,0 113,0 152,0 185 3,34
C5
c5H10 2-Метилбут-1 -ен 31,2 88,1 119,9 157,8
C5HI0 Пент-1-ен 30,0 86,0 118,0 156,1
c5H10 Циклопентан 49,3 72,1 109,3 142,6 182,2 238,6 4,52
c5H10o З-Метилбутан-2-он 88,9 153,4 189,6 232,7
c5H10o Пентан-2-он 103,3 165,0 200,9 243,3
c5H10o Пентан-3-он 102,7 164,7 200,8 243,4
C5H,o02 Изобутилформиат 98,2 121,8 157,8 192,4 234,0 278,2 3,88
C5H10O2 Пропилацетат 101,8 126,8 165,7 200,5 242,8 276,2 3,33
c5H10o2 Этилпропионат 99,1 123,8 162,7 197,8 240,0 272,9 3,34
c5H10o2 Мети л бутират 102,3 127,5 166,7 203,0 244,5 281,3 3,48
c5H10o2 Метилизобутират 92,6 116,7 155,2 190,2 232,0 267,6 3,43
c5H12 Изопентан 27,8 49,8 84,7 114,5 154,0 187,8 3,33
c5H12 Неопентан 9,5 29,5 61,1 90,7 127,6 160,6 3,2
c5H12 Пентан 36,1 56,7 93,4 124,7 164,3 196,6 3,37
c5H12o 1 -Этоксипропан 61,7 85,3 123,1 156,2 197,2 227,4 3,25
C6
C6H5Br Бромбензол 156,1 186,2 232,5 274,5 327,0 397 4,52
C6H5C1 Хлорбензол 131,7 160,2 205,0 245,3 292,8 359,2 4,52
c6h5f Фторбензол 85,1 109,9 148,5 184,4 227,6 286,6 4,52
c6h5i Иодбензол 188,3 220,0 270,0 315,7 371,5 448 4,52
c6H6 Бензол 80,1 104,4 143,3 178,8 221,5 289,5 4,92
c6H6o Фенол 181,8 208,0 248,2 283,8 328,7 400,0 419,2 6,13
C6H7N Анилин 184,0 212,8 254,8 292,7 342,0 422,4 426 5,31
c6H10o Циклогексанон 155,6 185 229 265 308 356 3,85
c6H)2 Метилциклопентан 71,8 96,2 135,9 171,4 213,8 259,6 3,79
c6HI2 Циклогексан 80,7 105,7 145,7 183,2 228,4 281,0 4,11
c6H12o Циклогексанол 161,0 188 230 266 308 352 3,75
c6H12o 4-Метилпентан-2-он 115,5 180,8 218,3 262,6
c6H12o2 Этилизобутират 110,1 135,5 174,2 210,0 253,0 280 3,04
c6H14 Гексан 68,7 92,6 131 167 209 234,7 3,03
c6HI4 2,2-Диметилбутан 49,7 73,2 111,2 145,6 186,7 216,2 3,11
c6H14 2,3-Диметилбутан 58,0 81,8 120,3 155,7 198,7 227,1 3,13
c6H14 2-Метилпентан 60,3 83,9 122,1 156,5 197,4 224,7 29,9
c6H14 З-Метилпентан 63,3 87,1 125,4 160,1 201,3 231,5 3,12
C7
c7H6o Бензальдегид 179,0 212 256 298 348 352 2,18
c7H8 Толуол 110,6 137,0 179,0 215,8 262,5 320,8 4,22
C7H8O Метоксибензол 155,5 184 224 265 312 369 4,18
(анизол)
C7H8O о-Крезол 190,9 220 263 303 352 422 5,01
C7H8O jw-Крезол 202,2 232 276 317 366 426 4,8
C7H8O «-Крезол 201,9 230 274 315 362 426,0 4,66
Физические свойства важнейших веществ
227
Окончание табл. 3.3.10
Формула Название Температура кипения или возгонки при давлении насыщенного пара Критическая температура, °C Критическое давление, МПа
0,101 МПа 0,203 МПа 0,507 МПа 1,013 МПа 2,027 МПа 5,066 МПа
C7H9N о-Толуидин 200,2 232 280 322 372 421 3,75
c7h9n л/-Толуидин 203,4 233 281 322 372 436 4,15
c7h9n «-Толуидин 200,6 229,5 276 319 368 394 2,38
c7H14 Метилциклогексан 100,9 171,0 209,9 256,3
c7H14 Этилциклопентан 103,5 172,4 210,6 25,8
С7н16 Г ептан 98,4 122,3 164,7 202,4 246,8 267,0 2,74
С8
С8Н!0 Этилбензол 136,2 164,0 208,5 246,3 294,5 346,4 3,75
с8н10 о-Ксилол 144,4 172,6 217,6 259 307 359,0 3,65
С8Н10 л/-Ксилол 139,1 167 211 253 303 346,0 3,55
С8Н|о «-Ксилол 138,4 166 211 253 303 345,0 3,45
С8НюО 2,4-Диметилфенол 210,0 241 290 334 386 (496,4) (65)
С8н10о 3,4-Диметилфенол 225 253 300 342 390 (545) (Ю,13)
С8Н10О 3,5-Диметилфенол 219,5 250 299 344 398 (493) (5,57)
С8н18 Октан 125,7 150,9 195,6 235,3 281,5 296,7 2,49
с9
c9h7n Хинолин 237,7 270 322 369 424 (527) (5,78)
С9н12 Изопропилбензол 152,4 187 232 275 326 362,7 3,24
(кумол)
С9Н12 1,2,4-Триметил- 169,3 199 246 302 381,2 3,34
бензол
(псевдокумол)
С9Н20 Нонан 150,8 177,2 224,0 265,5 313,6
Сю
СюН18 цис- Декагидронафталин (цис- декад ин) 195,7 227 275 319 370 404 2,49
Сн)Н22 Декан 174,1 204,3 274,7 319,1
Сн
СцН24 Ундекан 195,9 224,3 274,7 319,1
с12
с12н10 Бифенил 255,5 292 345 398 454 496 3,12
С12Н10О Дифениловый 258,5 299 354 407 (515) (3,14)
эфир
c12h„n У-Фениланилин 302,0 339 397 445 499 (658) (8,41)
С12н18 1,4-Диизопропилбензол 210,4 241 287 328 374 449 (521) (9,78)
С12Н26 Додекан 216,3 247,7 300,0 345,8 386 1,81
Св
С13н12 1,1 '-Метилен- 264,3 298 353 401 460 (572,5) (5,98)
дибензол
Примечание. Недостаточно надежные данные заключены в скобки.
Давление пара в зависимости от температуры (см. также табл. 3.3.3-3.3.8)
В табл. 3.3.11 приводятся значения констант А и В уравнения
1 л В
р — давление насыщенного пара, мм рт. ст., Т — абсолютная температура, К.
Это уравнение справедливо в температурном интервале, указанном для каждого вещества. Для перехода от мм рт. ст. к атм значение константы А следует уменьшить на 2,88081, а для перехода к Па — увеличить на 2,1249.
Данные, относящиеся к широкому температурному интервалу, предназначены для ориентировочных расчетов; соответствующие величины выделены курсивом.
228
Новый справочник химика и технолога
Таблица 3.3.11
Давление пара простых веществ и неорганических соединений
Формула Название Температурный интервал, °C А В
от до
Ag Серебро 762 960 9,208 14 700
936 2240 8,25 13 700
961 1353 8,66 1409
AgBr Серебра бромид 967 1224 8,714 10 367
AgCl Серебра хлорид 1028 1260 8,597 10 386
1255 1442 8,179 9688
Al Алюминий 724 1279 8,99 15 630
887 2200 8,23 13 300
А1Вгз Алюминия бромид 0 40 12,18 4292
AlCh Алюминия хлорид 0 40 17,77 6536
70 190 16,24 6006
180 197,5 16,115 6000
197,5 230 7,678 2070
A1F3 Алюминия фторид 707 850 14,44 16 967
А120з Алюминия оксид 2040 2970 11,296 27 320
Am Америций 830 1380 7,563 13162
Ar Аргон -208 -289,4 7,5344 403,91
-17,2 -183 6,9605 356,52
As Мышьяк 311 790 10,559 6777
800 860 6,692 2460
AsCh Мышьяка трихлорид 50 100 7,953 2043
AsF5 Мышьяка пентафторид -117 -83 10,952 1692,2
-83 -52,9 7,8449 1093,7
AsH3 Арсин (арсан) -138 -116,9 8,141 1057
AS2O3 Мышьяка(Ш) оксид 65,5 233 13,70 6672
233 313 10,15 4875
313 457 7,16 3126
Au Золото 1083 1867 8,65 18 520
1316 2900 8,82 18 900
В Бор 1052 1648 11,13 21 370
1239 2700 8,60 17,200
BBr3 Бора трибромид -40 90 7,655 1740
BF3 Бора трифторид -166,7 -128 9,47 1115
-128 -100 8,75 1010
-50 -12 7,9808 889,6
B2C14 Дибора тетрахлорид -63 23 8,057 1753
b2f4 Дибора тетрафторид -95 -64 10,82 1856
-55 -35 9,009 1466
B2O3 Бора оксид 1058 1535 9,623 16 960
В4Ню Тетраборан(Ю) -119,9 15,4 7,78 1414
b5h9 Пентаборан(9) -47 57 7,97 1683
BioHi4 Декаборан(14) 36 99,6 12,69 4241
99,6 170 8,12 2536
Ba Барий 418 858 7,88 8908
625 1670 8,00 9900
BaO Бария оксид 930 1200 8,69 19 400
Be Бериллий 942 1284 9,99 18 220
1284 1582 8,95 16 590
ИЗО 2550 8,40 16 000
BeBr2 Бериллия бромид 351 422 11,68 6550
BeCl2 Бериллия хлорид 365 404 12,977 7480
BeF2 Бериллия фторид 746 803 11,822 12 385
Физические свойства важнейших веществ
229
Продолжение табл. 3.3.11
Формула Название Температурный интервал, °C А В
от до
BeF2 Бериллия фторид 803 1025 10,466 10 943
Ве12 Бериллия иодид 305 430 10,64 5900
ВеО Бериллия оксид 1830 2300 11,037 33 240
Bi Висмут 206 259 7,213 8397
457 575 9,39 10 500
538 788 8,743 10 339
609 1650 7,95 9600
BiCl3 Висмута трихлорид 98 195 12,83 6200
Bil3 Висмута трииодид 410 490 8,170 4310
BrF Брома фторид -33 20 7,280 1303,4
BrF5 Брома пентафторид -90 -61,4 9,490 1929
-61,4 24 8,0716 1627,7
C Углерод 1590 2845 10,900 37 100
2470 4500 10,7 37 700
CBrN Бромциан 0 35 9,993 2360
CC1N Хлорциан -96 -5 9,525 1867
-5 40 7,840 1415
CFN Фторциан -149 -70 9,19 1264
CIN Иодциан 64 146 10,46 3129
CO Углерода монооксид -218 -211,7 8,3509 424,94
-211,7 -205,1 7,8469 393,91
COS Углерода оксид-сульфид -80 -50 7,383 1004
COSe Углерода оксид-селенид -53 -23 7,45 1150
CO/1 Углерода диоксид -135 -54,7 9,9082 1367,3
CSe2 Углерода диселенид 0 50 7,9153 1987,4
c2n2 Оксалонитрил (дициан) -93 -32 9,6553 1695,1
-32 —6 7,808 1240,5
c3o2 Аллен-1,3-дион (недокись углерода) -100 6 7,640 1330
C3s2 Аллен-1,3-дитион 20 90 8,01 2296
Ca Кальций 25 850 8,10 9600
475 670 7,790 8524
528 1480 7,80 8650
CaO Кальция оксид 1360 1480 9,77 27 400
Cd Кадмий 142 291 8,748 5766
500 840 7,897 5218
Cd3 As2 Кадмия арсенид 142 291 11,123 8292,5
CdBr2 Кадмия бромид 450 568 9,38 7380
568 725 8,252 6011
CdCl2 Кадмия хлорид 487 549 11,575 9472
602 753 8,537 6229
Cdl2 Кадмия иодид 385 450 9,269 6383
500 655 8,812 6012
CdO Кадмия оксид 321 1250 9,560 12310
CdS Кадмия сульфид 503 704 7,572 10 500
950 1175 9,64 11 163
CdTe Кадмия теллурид 450 650 9,218 9500
Ce Церий 1004 1600 11,74 20 100
C1F Хлора фторид -154 -103 9,950 1530
C1O2 Хлора диоксид -40 20 8,35 1552
Cl2 Хлор -15 -103 9,950 1530
C12O Дихлора оксид -100 15 7,87 1373
C12O6 Дихлора гексаоксид -160 3,5 9,3 2690
3,5 20 7,1 2070
230
Новый справочник химика и технолога
Продолжение табл. 3.3.1 /
Формула Название Температурный интервал, °C А В
от до
С12О7 Дихлора гептаоксид -75 80 8,03 1818
Со Кобальт 1249 2056 9,43 21 960
1494 3160 9,15 21 400
Сг Хром 1010 1288 10,296 20 434
907 1900 9,88 17 560
СгВг3 Хрома трибромид 665 800 13,35 12 900
Сг(СО)6 Гексакарбонилхром 35 130 10,63 3285
-34 29 7,692 4036
Cs Цезий 45 277 6,86 3774
200 350 6,949 3834
CsBr Цезия бромид 978 1305 7,990 8022,5
CsCl Цезия хлорид 327 577 9,446 9620
507 635 9,942 9970
986 1295 8,340 8524
CsF Цезия фторид 1033 1255 7,703 7359
CsI Цезия иодид 1052 1280 9,124 9699
Cu Медь 970 1083 9,232 17 260
1083 1290 8,907 16 820
1140 2610 8,50 16 600
Cu2Br2 Меди(1) бромид 997 1351 5,460 4137
Cu2Cl2 Меди(]) хлорид 989 1369 5,454 4215
Cu2I2 Меди([) иодид 991 1154 5,570 4215
f2 Фтор -221,3 -186,9 8,23 430,1
f2o Кислорода дифторид -195 -145 7,224 555,4
f2o2 Дикислорода дифторид -132 -95 7,515 1000
Fe Железо 1094 1535 9,63 20 000
1310 2850 8,80 18 700
2220 2450 7,482 16 140
FeBr2 Железа дибромид 350 445 11,88 10 300
670 740 11,95 10 220
Fe(CO)5 Пентакарбонилжелезо -21 105 8,09 1970
FeCl2 Железа дихлорид 670 740 11,10 9890
700 930 8,33 7061
Ga Галлий 771 1443 7,79 13 360
965 2300 8,26 14 000
GaBr3 Галлия трибромид 112 275 8,554 3126
GaCl3 Галлия трихлорид 23 78 11,70 3760
Gal3 Галлия трииодид 51 109 11,208 4950
Ge Германий 959 1635 7,94 15 150
1112 2600 8,45 16 300
GeClF3 Т рифторхлоргерман -64 -20 11,05 2062
GeCI2F2 Дифтордихлоргерман -47 -2 8,22 1441
GeCl3F Фтортрихлоргерман -31 43 8,76 1825
GeCl4 Т етрахлоргерман 10,4 86 7,340 2011
GeH4 Герман -165 -89 7,135 782,7
Ge2H4 (2Н4)Герман (дейтерогерман) -144 -89 7,327 818,5
GeO Германия монооксид 642 705 15,53 13 770
GeO2 Г ермания диоксид 880 980 10,16 15 620
1040 1100 16,245 25 517
GeS Германия моносульфид 300 500 10,78 8350
525 615 10,05 7579
615 662 8,70 6398
GeS2 Германия дисульфид 460 650 12,44 10 970
Физические свойства важнейших веществ
231
Продолжение табл. 3.3.11
Формула Название Температурный интервал, °C А В
от до
НВг Водорода бромид -114 -86 8,734 1171
-86 -66 8,427 938,05
2НВг (2Н)Водорода бромид -99 -87,5 8,306 1103
-87,5 -67 7,517 956,5
HCN Водорода цианид -37 -13,3 9,372 1877
0 46 7,752 1456
2HCN (2Н)Водорода цианид -37 -12 9,476 1907
НС1 Водорода хлорид -158 -ПО 8,4430 1023,1
HF Водорода фторид -66 19 7,3739 1316,8
2HF (2Н)Водорода фторид -33 17 7,2026 1261,2
HI Водорода иодид -97 -51 8,259 1262
-50 -34 7,630 1127
HN3 Азотистоводородная кислота -94 36 8,19 1643
HReO4 Рениевая кислота 30 70 7,680 2409
HTcO4 Технециевая кислота 89 256 8,207 2395
H2 Водород -259,2 -249 5.394 51,26
-252,9 -240,0 5,753 58,59
H2H (2Н1)Водород (дейтероводород) -256,4 -247 5,539 59,55
-250,8 -236,8 5,947 68,67
H3H (3Н])Водород (тритийводород) -254,7 -246 5,730 67,23
-249,6 -234,9 6,046 74,70
2h2 (2Н2)Водород (дидейтерий) -254,7 -246 5,730 67,23
-249,6 -134,9 6,046 74,70
2H3H (2Н3Н)Водород (дейтеротритий) -253,6 -245 5,989 75,53
-248,9 -233,7 6,098 78,18
3h2 (3Н2)Водород (дитритий) -259,2 -251,6 6,4773 88,002
-252,7 -244 6,068 79,35
-248,3 -232,6 6,131 80,98
2H2O (2Н2)Вода (тяжелая вода) 4 101,4 8,986 2286
H2O2 Водорода пероксид 10 90 8,853 2534.7
H2s Водорода сульфид (сероводород) -145 -131 8,5005 1175,3
-110 -83 7,880 1080,6
H2s2 Водорода дисульфид 0 45 9,041 2077
H2Se Водорода селенид -109 -66 8,96 1380
-66 105 7,48 1067
H2SeO3 Селенистая кислота 71 153 8,150 2246
H2SeO4 Селеновая кислота 11 31 14,130 4304
H2Te Водорода телланид -114 -49 9,07 1600
-49 -1,3 7,44 1240
Hf Гафний 1530 2330 9,46 30 200
Hf(BH4)4 Гафния(4+) тетрагидридоборат(1-) -30 29 10,719 2844
29 118 8,247 2097
HfCl4 Гафния тетрахлорид 203 408 11,712 5197
Hg*2 Ртуть -80 -38,87 10,383 3813
18 360 7,20 2760
400 1300 7,752 3066
HgBr2 Ртути(П) бромид 111 235 10,818 4168
238 331 8,284 3199
Hg2Br2 Ртути(1) бромид 99 394 9,338 4298
HgCl2 Ртути(П) хлорид 11 59 10,693 4358
60 130 10,888 4441
130 270 10,094 4118
232
Новый справочник химика и технолога
Продолжение табл. 3.3.11
Формула Название Температурный интервал, °C А В
от до
Hgl2 Ртути(П) иодид 100 250 10,057 4301
266 360 8,115 3278,5
IC1 Иода хлорид 0 27,2 10,4 2660
27,2 97 8,504 2080
IF5 Иода пентафторид -5 9,4 11,764 3035
9,4 60 8,659 2159
if7 Иода гептафторид -63 -26 8,660 1603
In Индий 564 1080 8,003 12 180
840 2080 8,18 12 600
InBr Индия бромид 317 648 7,74 4525
InBr2 Индия дибромид 335 611 7,84 4480
InBr3 Индия трибромид 149 221 12,945 7232
InCi Индия хлорид 300 590 8,03 4635
InCl2 Индия дихлорид 340 478 14,98 9205
InCl3 Индия трихлорид 209 291 12,654 8086
390 486 13,62 8265
Ini Индия иодид 397 688 7,66 4700
Inl3 Индия трииодид 99 132 12,097 6038
Ir Иридий 1993 3118 10,06 34 НО
2340 4400 10,4 35 400
К Калий 91 338 7,36 4503
260 760 7,183 4434
587 1007 6,977 4207
KBr Калия бромид 906 1063 8,247 8780
1095 1375 7,936 8555
KC1 Калия хлорид 438 597 10,451 11 310
582 751 10,151 И 070
906 1105 8,3526 9114
1116 1418 8,130 8863
KF Калия фторид 128 1500 9,000 10 840
KI Калия иодид 843 1028 8,0957 8231
1063 1333 7,949 8132
KOH Калия гидроксид 1170 1327 7,330 7103
Kr Криптон -207 -158 7,722 578
La Лантан 1023 1754 8,88 18 000
Li Литий 325 725 7,50 7480
439 1330 7,65 7750
LiBr Лития бромид 1010 1265 8,068 7975,5
LiCl Лития хлорид 535 616 9,911 1020
1045 1325 7,939 8143
LiF Лития фторид 653 779 10,366 12 733
1387 1666 8,753 11 407
Lil Лития иодид 940 1140 8,011 7500
Li2O Лития оксид 960 1300 13,19 16 200
Mg Магний 287 605 8,82 7741
383 ИЗО 7,50 6689
475 600 7,790 8524
Mn Марганец 717 1244 9,25 14 100
878 2130 8,20 12 900
MnCl2 Марганца дихлорид 826 943 8,559 8448
Mo Молибден 1923 2533 8,80 30 310
2295 4300 10,2 34 700
Mo(CO)6 Г ексакарбонилмолибден 53 147 11,174 3561
MoCl5 Молибдена пентахлорид 70 160 10,623 3991
Физические свойства важнейших веществ
233
Продолжение табл. 3.3.11
Формула Название Температурный интервал, °C А В
от до
MoF6 Молибдена гексафторид -88 17 9,01 1858
17 36 7,12 1312
МоОз Молибдена триоксид 680 797 18,172 19 045
797 860 13,228 12 680
n2 Азот -221 -210,1 7,65894 459,093
NH3 Аммиак -97 -78 10,00593 1630,70
N2H3 (2Н3)Аммиак (дейтероаммиак) -122 -74 10,0164 1680,4
NH4Br Аммония бромид 250 400 9,9404 4711,6
NH4CI Аммония хлорид 100 400 10,0164 4360,5
NH4HS Аммония гидросульфид 6 40 10,750 2404
NH4I Аммония иодид 300 400 10,270 5000
NH4N3 Аммония азид 15 134 11,325 3428
NO Азота(П) оксид -200 -161 10,048 851,8
-163,7 -148 8,440 681,1
N2O Азота(1) оксид -144 -90 9,579 1232
12 36 7,5064 858,63
n2o3 Азота(П1) оксид -25 0 10,30 2058
n204 Диазота тетраоксид -71,7 -11,2 12,65 2750
-11,2 103 8,82 1746
-8 43,2 8,814 1746
n2o5 Азота(У) оксид -54,4 32 12,77 3017
NOCI Н итроз илхлорид -97 -59,6 9,37 1660
-59,6 -7 7,922 1347
NSF Азота сульф ид-фторид (азот тиофтористый) -60 0 7,06 1160
Na Натрий 180 883 7,553 5395
620 1135 7,402 5220
NaBr Натрия бромид 870 ИЗО 8,957 9687
1138 1394 7,948 8440
NaCN Натрия цианид 685 1500 7,45 8150
NaCl Натрия хлорид 976 1155 8,3297 9417
1156 1439 8,548 9704
NaF Натрия фторид 1562 1701 8,640 11 397
Nal Натрия иодид 1063 1307 8,371 8623
NaOH Натрия гидроксид 618 1380 7,434 7519
Nb Ниобий 2194 2500 11,37 40 400
2539 4600 11,0 39 200
NbBr5 Ниобия пентабромид 268 360 9,33 4085
NbCl4 Ниобия тетрахлорид 304 374 12,30 6870
NbCl5 Ниобия пентахлорид 76 204,7 11,51 4370
204,7 250 8,37 2870
NbF5 Ниобия пентафторид 27 78,9 14,397 4900
78,9 260 8,3716 2779,3
Ne Неон -268 -253 7,0424 111,76
Ni Никель 1157 1455 10,28 21 840
1371 3000 9,00 19 700
1455 1884 9,55 20 600
Ni(CO)4 Тетракарбонилникель 0 25 7,878 1574,5
NiCl2 Никеля дихлорид 700 783 12,051 И 499
NiF2 Никеля дифторид 753 1076 9,7 13 100
Os Осмий 2101 3221 10,59 37 000
OsO4 Осмия тетраоксид (белый) -31 39,5 9,63 2578
OsO4 Осмия тетраоксид (желтый) -21 41 10,70 2954
OsO4 Осмия тетраоксид (жидкий) 41 130 8,01 2066
234
Новый справочник химика и технолога
Продолжение табл. 3.3.11
Формула Название Температурный интервал, °C А В
от до
Р Фосфор (желтый) 20 44,1 9,6511 3296,9
Р Фосфор (красный) 230 550 10,996 5600
РВг3 Фосфора трибромид 60 173 7,53 2076
РВг5 Фосфора пентабромид 32,5 75 10,1173 2895,7
РС13 Фосфора трихлорид 0 70 7,681 1664
РС13О Фосфора оксид-трихлорид 1,2 105 7,73 1832
РС15 Фосфора пентахлорид 101 158 11,034 3523
PF3 Фосфора трифторид -151,3 -101 7,58 8090
PF3O Фосфора оксид-трифторид -85 -39,1 11,3755 1984,7
-39,1 -18 8,0524 1207
pf5 Фосфора пентафторид -126 -93,8 11,101 1519
-93,8 -84 7,646 898,9
РН3 Фосфин (фосфан) -145 -133,8 7,8643 895,7
РН4Вг Фосфония бромид -80 40 10,9561 2513
РН41 Фосфония иодид 10 60 10,950 2708
Р1з Фосфора трииодид 61,5 227 7,43 2300
Р4О6 Фосфора(Ш) оксид 23,8 174 7,960 2257
Р4О10 Фосфора(У) оксид (а-модификация) 172 294 12,54 8253
РдОю Фосфора(У) оксид (метастабильная модифи- 22 115 10,74 4940
кация) 151 360 10,792 5000
Р4ОЮ Фосфора(У) оксид (жидкий) 565,6 603 7,809 4320
РЬ Свинец 483 975 7,69 9600
625 1700 8,11 10 000
РЬВг2 Свинца дибромид 563 860 8,8467 6953,6
РЬС12 Свинца дихлорид 500 950 8,961 7411
PbF2 Свинца дифторид 519 715 8,350 9096
1078 1289 8,391 8623
РЬО Свинца(П) оксид 614 878 11,58 13 900
PbSe Свинца(П) селенид 501 688 10,084 11 032
РЬТе Свинца(П) теллурид 511 679 10,827 11 636
Pd Палладий 1156 2000 8,46 19 230
1405 3100 9,12 20 000
Ро Полоний 438 745 7,2345 5377,8
Pt Платина 1426 1765 7,786 25 380
1770 3700 8,44 25 000
Pu Плутоний 1065 1565 7,895 17 587
PuCi3 Плутония трихлорид 580 760 12,726 15910
760 834 9,509 12 590
PuF3 Плутония трифторид 1110 1410 12,468 21 120
1410 1790 11,273 19 400
PuF6 Плутония гексафторид -33 21 11,45 2778
Pul3 Плутония трииодид 592 780 13,386 15 280
780 1380 10,321 12 360
Rb Рубидий 59,4 283 7,42 4132
250 370 6,976 3970
RbBr Рубидия бромид 1050 1365 8,223 8618
RbCl Рубидия хлорид 558 675 9,643 10 200
1142 1395 9,111 10 370
RbF Рубидия фторид 1142 1400 8,570 9569
Rbl Рубидия иодид 1075 1325 8,067 8179
Re Рений 2200 2725 10,4045 40 865
ReO2 Рения диоксид 480 660 5,345 4742
ReO3 Рения триоксид 300 440 7,745 4966
Физические свойства важнейших веществ
235
Продолжение табл. 3.3.11
Формула Название Температурный интервал. °C А В
от до
Re2O7 Дирения гептаоксид 220 300 15,010 7320
301 350 8,989 3868
ReO4 Рения тстраоксид 100 220 5,4851 1738,7
Rh Родий 1681 2607 10,55 30 400
1971 3850 9,9 29 100
Rn Радон -71 -62 7,031 876,9
Ru Рутений 1913 2046 10,50 33 800
2230 4250 10,2 33 300
S Сера (ромб.) 59 95,5 11,866 5267
S Сера (монокл.) 95,5 119,3 11,364 5082
s Сера (жидкая) 119,3 300 6,0489 4087,8
300 1040 4,5758 3288,5
SBr2O Т ионилдибромид -86 40 8,03 1610
SC12 Серы дихлорид -78 60 7,74 1620
SC12O Тионилдихлорид -104 75 7,65 1660
SC12O2 Сульфурилдихлорид -53 70 7,84 1700
S2C12 Дисеры дихлорид 0 138 7,455 1880
S2C12O5 Дисульфурилдихлорид 0 90 8,397 2323
90 152 8,021 2184
SF2O2 Сульфурилдифторид -155 -56 7,593 1023
SF6 Серы гексафторид 0 45,6 7,2593 899,46
so2 Серы диоксид -112 -75,5 10,45 1850
so3 Серы триоксид (а-модификация) -58 17 11,44 2680
SO3 Серы триоксид ((^-модификация) -52,5 13,9 11,96 2860
SO3 Серы триоксид (у-модификация) -33 51 14,01 3610
SO3 Серы триоксид (жидкий) 62 219 9,89 2230
Sb Сурьма 345 457 11,044 10 509
500 560 9,815 9655
860 1242 6,29 6500
SbBr3 Сурьмы трибромид 235 324 8,005 2870
SbBr5 Сурьмы пентабромид 96,6 275 8,53 3100
SbCl3 Сурьмы трихлорид 170 253 8,090 2582
SbCl5 Сурьмы пентахлорид 3 112 8,565 2530
SbF5 Сурьмы пентафторид 9 50 8,567 2364
Sbl3 Сурьмы трииодид 167 400 8,25 3600
Sb2O3 Сурьмы(Ш) оксид (кубическая модификация) 197 569 12,26 10410
Sb2O3 Сурьмы(Ш) оксид (орторомбическая 569 655 11,53 9800
модификация)
Sc Скандий 1058 1804 8,94 18 570
1280 2800 8,70 18 200
ScBr3 Скандия трибромид 800 960 14,35 13 800
ScCl3 Скандия трихлорид 800 960 14,37 14 200
Scl3 Скандия трииодид 740 905 14,17 13 350
Se Селен 184 220 12,78 7440
272 687 8,089 4990
SeCl4 Селена тетрахлорид 109 227 11,204 3864
SeF2O2 Селенонилдифторид -08 -5 8,474 1480,6
SeF4 Селена тетрафторид 20 70 9,44 2457
SeF6 Селена гексафторид -145 -45 8,99 1390
Si Кремний 1025 1410 10,20 19 720
1410 1670 9,55 18 550
1223 2730 8,60 17 900
SiBrF3 Бромтрифторсилан -69 -40 7,0415 962,7
SiBrCl2F Бромфтордихлорсилан -112 35 7,098 1301
236
Новый справочник химика и технолога
Продолжение табл. 3.3.11
Формула Название Температурный интервал, °C А В
от до
SiBr2ClF Дибромфторхлорсилан -99 55 7,567 1558
SiBr2F2 Дибромдифторсилан -9 21 7,408 1298
SiBr3F Трибромфторсил ан 32 84 7,672 1710
SiClF3 Т рифторхл орсил ан -85 -66 7,4563 929,3
SiCl2F2 Дифтордихлорсилан -50 -26 7,425 1095
SiCl3CN Трихлорцианосилан —45 20 7,751 1687
SiCl3F Фтортрихлорсилан -30 15 7,353 1278
SiCl3SCN Т иоцианатотрихлорсилан 68 130 7,9985 2060
SiCI4 Тетрахлорсилан -68,8 57 7,6414 1572,3
Si2CI6 Г ексахлордисилан -1 139 8,719 2404
Si3Cl8 Октахлортрисилан 12,3 211 8,45 2698
SiF4 Т етрафторс илан -156 -95 10,40 1340
SiHBr3 Трибромсилан 0 120 7,608 1819,5
SiH3CN Цианосилан -20 32,4 10,951 2550
32,4 46 7,735 1567
SiH3SCN Т иоцианатосилан -33 10 8,340 1950
SiH4 Силан -160 -112 6,996 662,8
Si2H6 Дисилан -115 -14,6 7,258 1133
Si3H8 Трисилан -70 52 7,675 1559
SiO2 Кремния диоксид 1860 2230 13,43 26 430
Sn Олово 1042 2330 8,28 14 400
1151 1367 8,352 15 730
1970 2270 9,423 16 630
SnBr2 Олова дибромид 456 610 8,76 5360
SnCl2 Олова дихлорид 404 629 7,73 4480
SnCl4 Олова тетрахлорид -52 -38 9,824 2441
3 109 7,5968 1824,9
SnH3Cl Хлорстаннан -100 -50 7,8381 1520,4
SnH4 Станнан -149 -52 7,26 966,3
Snl2 Олова дииодид 480 713 8,42 5470
Snl4 Олова тетраиодид 87 145 10,08 3990
145 361 7,63 ЗОЮ
SnO Олова(П) оксид 670 1425 7,82 8420
SnS Олова(П) сульфид 677 802 9,969 10 470
Sr Стронций 400 600 7,435 7548
475 1380 7,67 8100
Ta Тантал 730 1730 10,154 40 550
1930 3000 9,859 39 780
TaBr5 Тантала нентабромид 144 267 12,571 5650
267 345 8,171 3265
TaCl5 Тантала пентахлорид 220 240 8,68 2975
TaF5 Тантала пентафторид 96 232 8,524 2834
Tal5 Тантала пентаиодид 496 544 7,72 3995
Tc2C>7 Дитехнеция гептаоксид 89 118,4 18,279 7205
118,4 256 8,999 3571
Те Теллур 208 427 9,753 7600
550 750 7,977 6196
TeCl2 Теллура дихлорид 204 304 8,52 3350
TeF4 Теллура тетрафторид 25 129,6 9,0934 3174,3
129,6 194 5,6397 1786,4
TeF6 Теллура гексафторид -79 9,161 1471
TeO2 Теллура диоксид 573 733 10,948 12 000
733 938 10,248 И 300
Th Торий 1827 2715 9,52 28 440
Физические свойства важнейших веществ
237
Продолжение табл. 3.3.11
Формула Название Температурный интервал, °C А В
от до
ThBr4 Тория тетрабромид 630 677 11,73 9630
680 800 9,56 7550
ThCl4 Тория тетрахлорид 700 760 14,30 12 900
780 910 9,57 7980
ThF4 Тория тетрафторид 780 1026 11,986 16 860
1160 1325 10,821 15 270
Thl4 Тория тетраиодид 580 830 9,09 6890
ThO2 Тория диоксид 1775 1975 11,53 37 100
Ti Титан 1134 1727 8,25 18 640
1727 3260 9,136 22 110
TiBr4 Титана тетрабромид 38 220 8,11 2580
TiCl2 Титана дихлорид 480 610 9,593 10 230
610 680 9,30 8500
680 1300 8,80 9470
TiCl3 Титана трихлорид 620 680 13,74 10 970
TiCl4 Титана тетрахлорид 40 85 8,0015 2077,5
Til4 Титана тетраиодид 160 370 7,577 3054
TI Таллий 405 821 8,15 8920
527 1450 7,75 8450
950 1200 6,140 6270
TIBr Таллия(1) бромид 634 817 7,940 5505
T1C1 Таллия(1) хлорид 665 807 7,974 5495
T1F Таллия(1) фторид 282 298 12,52 5484
TH Таллия(1) иодид 693 822 7,902 5505
TISe Таллия(П)селенид 160 350 12,443 6742
T12O Таллия(1) оксид 180 315 11,51 6612
T12S Таллия(1) сульфид 800 1000 7,82 8100
Tl2Se Таллия(1) селенид 175 440 9,805 5881
Tl2Se3 Таллия(Ш) селенид 240 400 9,248 7425,5
Tm Туллий 536 946 9,176 12 550
U Уран 1350 1700 8,583 23 330
1730 3500 9,34 25 000
UBr4 Урана тетрабромид 450 519 14,56 10 900
519 650 9,71 7060
uf4 Урана тетрафторид 875 969 12,945 1644
969 1000 8,003 1000
UF6 Урана гексафторид 0 69 9,521 2180
UO2 Урана диоксид 1330 1530 14,056 38 220
V Ванадий 1465 2207 10,32 26 120
1725 3500 9,34 25 000
VC14 Ванадия тетрахлорид 30 80 7,581 1998
vf5 Ванадия пентафторид -20 19,5 11,049 2608
19,5 45 10,430 2423
VC13O Ванадия оксид-трихлорид 19 100 7,50 1921
W Вольфрам 2554 3309 9,24 40 260
3016 5100 11,8 49 300
W(CO)6 Г ексакарбонилвольфрам 85 154 11,523 3872
WC15 Вольфрама пентахлорид 114 230 9,55 3700
230 286 9,03 3440
WC16 Вольфрама гексахлорид (а-модификация) 152 226,9 10,732 4582
WC16 Вольфрама гексахлорид (Р-модификация) 226,9 284 9,255 3837
WC16 Вольфрама гексахлорид (жидкий) 284 362 8,352 3335
wo3 Вольфрама триоксид 865 1470 15,63 24 600
1100 1250 17,973 27 295
Xe Ксенон -189 -111 8,00 841,7
238
Новый справочник химика и технолога
Окончание табл. 3.3.11
Формула Название Температурный интервал. °C А В
от до
Y Иттрий 149 2056 9,43 21 970
Zn Цинк 150 350 9,664 7198
550 650 8,011 6079
600 985 8,108 6163
Zn3As2 Цинка арсенид 328 478 9,053 8658
ZnBr2 Цинка бромид 428 650 9,547 6193
ZnCl2 Цинка хлорид 470 690 9,529 6613
ZnS Цинка сульфид 370 1000 9,795 13 390
1150 1310 9,78 13 380
ZnTe Цинка теллурид 520 720 9,539 10 627
Zr Цирконий 1527 2127 9,38 25 870
1816 3700 9,5 26 300
Zr(BH4)4 Циркония(4+) тетрагидридоборат( 1 -) -20 28,7 10,919 2983
28,7 122,6 8,032 2039
ZrCl4 Циркония тетрахлорид 207 416 11,766 5400
437 468 9,088 3427
ZrF4 Циркония тетрафторид 616 881 13,3995 12 376
*’ См. также табл. 3.3.15 и 3.3.16.
*2 См. также табл. 3.3.13 и 3.3.14.
В табл. 3.3.12 приводятся значения констант Л, В и С уравнений:
Igp = /l-p (1)
= Л---^7, (2)
1 + С
гдер — давление насыщенного пара, мм рт. ст.; Т — абсолютная температура, К; г — температура, °C.
В каждом случае указано, какое из этих уравнений имеется в виду и в каком температурном интервале оно сохраняет свою справедливость для данного вещества. Для перехода от мм рт. ст. к атм следует значение константы А уменьшить на 2,88081, а для перехода к Па — увеличить на 2,1249.
Таблица 3.3.12
Давление пара органических соединений (см. также табл. 3.3.9 и 3.3.10)
Формула Название Уравнение Температурный интервал,°C А В С
от до
Ci СВгС13 Бромтрихлорметан 2 20 170 6,86625 1294,08 220
CBrF3 Бромтрифторметан 2 2 170 -144 318 -58 7,29174 7,46062 1647,18 1018,31 269,99 280,24
CBr2F2 Дибромдифторметан 2 -89 6 7,15971 1185,48 254,26
CBr4 Т етрабромметан 1 3 90 8,782 2655
CC1F3 Трифторхлорметан 1 -138 -81 7,347 857,3
CC12O (фреон-13) Карбонилдихлорид 1 -120 8 7,54 1310
CC13F (фосген) Фтортрихлорметан 1 -89 24 7,540 1385
CC13NO2 (фреон-11) Нитротрихлорметан 1 -20 35 8,2424 2045,1
CC14 (хлорпикрин) Т етрахлорметан 1 -70 -19 8,540 1910,8
2 2 -15 138 138 283 6,93390 7,3703 1242,43 1584 230,0 277
Физические свойства важнейших веществ
239
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал, °C А В С
от до
cf2o Карбонилдифторид 1 -150 -80 7,3231 843,05
cf4 T етрафторметан 1 -165 -117 7,596 685,4
cn4o8 Тетранитрометан 1 -18 13 9,464 2464
chci2f Фтордихлорметан 1 -67 -38 8,185 1476
(фреон-21)
СНС1з Хлороформ 2 -15 135 6,90328 1163,0 227
2 135 263 7,3362 1498 276
CH2BrCI Бромхлорметан 2 —6 297 6,86624 1132,3 216
CH2C12 Дихлорметан 2 -28 121 7,07138 1134,6 231
2 121 237 7,50819 1462,59 278,60
CH2O2 Муравьиная кислота 1 -5 8,2 1,486 3160
1 8,2 110 7,884 1860
CH3C1 Хлорметан 2 -80 40 6,99445 902,45 243,60
2 40 143,1 7,81148 1433,6 317,5
CH3F Фторметан 2 -122 -20 7,09761 740,22 253,89
2 -20 44,6 7,81764 1113,00 306,57
ch3no2 Нитрометан 2 55 136 7,28050 1446,19 227,52
CH3AsC12 Метилдихлорарсин 1 0 134,5 8,3397 2331,1
CH3Br Броммстан 2 -58 53 6,95965 986,59 238,32
CH3CI3Si Метилтрихлорсилан 2 13,7 64 6,87213 1167 226
CH3I Иодметан 1 0 34 7,56 1475
CH4 Метан 2 -200 -182,5 6,30181 320,30 255,84
2 -182,5 -161,6 6,56430 380,22 264,80
2 -161,6 -118,1 6,81554 437,08 272,66
2 -118,1 -82,1 7,31603 600,17 298,42
CH32H (2Н)Метан 1 -181,4 -161,6 6,927 421,8
(монодейтерометан)
ch22h2 (2Н2)Метан (дидейтерометан) 1 -181,4 -161,6 6,947 453,8
CH2H3 (2Н3)Метан (тридейтерометан) 1 -181,4 -161,7 6,967 455,5
c2h4 (2Н4)Метан 1 181,3 -161,9 6,981 456,6
(тетрадейтерометан)
CH4O Метанол 1 -62 -44 8,9547 2049,2
1 7 153 8,349 1835
CH4ClFSi Метил фторхлорсилан 1 -75 1,2 7,6066 1296,6
CH4F2Si Метилдифторсилан 1 -75 -35,6 7,7655 1160,4
CH4Ci2Si Метилдихлорсилан 1 -40 40,4 7,6304 1489,4
CH5N Метанамин (метиламин) 1 3 34 8,911 1577
CH6Si Мети л силан 2 -130 -57 7,0590 868,94 265
C2
C2C12F4 Тетрафтор-1,2-дихлорэтан 1 -94 4 7,658 1300
c2ci2f4 Т етрафтор-2,2-дихлорэтан 1 30 140 7,3245 1227,0
C2C13N Трихлорацетонитрил 1 16,8 83,4 7,853 1783
С2СЦ Тетрахлорэтилен 2 34 187 7,02003 1415,5 221
2 187 340 7,4489 1787 271
C2C14O Т р ихлор ацетилхлорид 2 -21 -119 6,98442 1386,68 219,70
C2C16 Гексахлорэтан (куб.) 1 1,9 72 8,731 2677
C2C16 Гексахлорэтан (трикл.) 1 72 184 9,890 3077
c2F4 Т етрафторэтилен 1 -142,7 -76,5 7,618 931,9
C2HC13 Трихлорэтилен 2 7 155 7,02808 1315,0 230
2 155 298 7,3675 1675 280
C2HC13O2 Трихлоруксусная кислота 2 59,2 198 7,31057 1618,97 167,88
C2HC15 Пентахлорэтан 1 15 165 7,80304 2129,6
240
Новый справочник химика и технолога
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал. °C А В С
от до
С2Н2 Ацетилен 2 -180 -81,8 8,7371 1084,9 268,85
2 -81,8 35,3 7,5716 925,59 283,05
С2Н2Вг2 (£)-1,2-Дибромэтилен 1 4 70,5 7,71 1840
С2Н2Вг2 (Z)-1,2-Дибромэтилен 1 26 78 8,40 2120
С2Н2С1О2 Дихлоруксусная кислота 2 62,7 190 7,56597 1733,96 181,00
С2Н2С12 (£)-1,2-Д ихлорэтилен 1 -31 14 7,890 1598
С2Н2С12 (Z)-1,2-Дихлорэтилен 1 27 59 7,752 1619,4
С2Н2С12О Хлорацетилхлорид 2 -21 106 7,13411 1331,94 207,18
С2Н2С14 1,1,1,2-Тетрахлорэтан 1 105 145 7,605 1906,8
С2Н2С14 1,1,2,2-Тетрахлорэтан 1 20 146 8,06938 2167,83
c2h2f2 1,1 -Дифторэтилен 1 -40 25 7,1766 805
С2Н212 (£)-1,2-Дииодэтилсн 1 77 130 7,62 2210
С2Н212 (Z)-1,2-Дииодэтилен 1 29 152 8,18 2430
С2Н2О4 Щавелевая кислота 1 37 52 12,57 4875
(монокл.) 1 55 105 12,229 4726,95
С2Н2О4 Щавелевая кислота 1 37 52 13,17 5130
(ромб.) 1 14 112 7,586 1511
С2Н3Вг Бромэтилен 2 -60 60 6,66715 953,4 236,0
С2Н3Вг3 1,1,2-Трибромэтан 1 90 270 6,94373 1562,12 196
2 270 451 7,3511 1964 262
С2Н3С1 Хлорэтилен 2 -100 50 6,49712 783,4 230,0
2 50 156,5 10,71749 4927,2 652
C,H3C1F2 1,1 -Дифтор-1 -хлорэтан 1 25 117 7,3776 1184,5
С2Н3С13 1,1,1-Трихлорэтан 2 -3 131 6,90160 1202,60 225
2 131 266 7,32605 1524,70 269,86
С2Н3С13 1,1,2-Трихлорэтан 2 30 186 6,84165 1262,6 205
2 186 339 7,2567 1599 254
C2H3Cl3Si Винилтрихлорсилан 2 17,7 90 7,32284 1513 250
c2h3f3 1,1,1 -Трифторэтан 1 -42 72 7,3799 1014,7
c2h3n Ацетонитрил 1 -41 23 8,151 1838
с2н4 Этилен 2 -169,2 -103,7 6,76503 590,34 255,68
2 -103,7 -70,0 6,87477 624,24 260,01
2 -70,0 9,5 7,2058 768,26 282,43
С2Н4Вг2 1,2-Дибромэтан 1 10,3 44,3 8,376 2181
2 43 215 7,06245 1469,7 220
2 215 377 7,4959 1871
С2Н4С12 1,1 -Дихлорэтан 1 0 30 7,909 1656
С2Н4С12 1,2-Дихлорэтан 2 6 161 7,18431 1358,5 232
2 161 288 7,6284 1730 283
c2h4f2 1,1 -Дифторэтан 1 -40 105 7,4785 1140,95
c2h4n206 Этан-1,2-диилдинитрат 1 75 199 9,73 3200
С2Н4О Ацетальдегид 1 -24,3 27,5 7,8206 1447,14
С2Н4О Оксиран (окись этилена) 2 -91 10,5 6,25100 1115,10 244,14
С2Н4О2 Метилформиат 1 -23 27 8,103 1587
С2Н4О2 Уксусная кислота 1 -35 10 8,502 2177,4
(2Н4)Уксусная кислота 2 16,4 118 7,55716 1642,54 233,39
с22н4о2 2 25 125 7,4397 1556,17 224,82
(тетрадейтероуксусная
кислота)
C2H4S Тииран (этиленсульфид) 2 -17 147 6,98816 1166,2 229
2 147 287 7,42828 1520,8 282
C2H5AsBr2 Этилдибромарсин 1 0 82,5 8,49558 2608,7
C2H5AsC12 Этилдихлорарсин 1 0 60 8,4497 2331,1
C2H5Br Бромэтан 2 -32 110 6,91995 1090,81 231,71
2 НО 230,7 7,59098 1545,3 290,0
C2H5C1 Хлорэтан 2 -50 70 6,94914 1012,77 236,67
Физические свойства важнейших веществ
241
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал, °C А В С
от до
C2H5Cl3Si Этилтрихлорсилан 2 28,5 96 6,58174 1102 199
c2h5f Фторэтан 1 -72 66 7,707 1162
c2h5fo 2-Фторэтанол 1 0 103 9,06 2304
(этиленфторгидрин)
c2h5no Ацетальдегидоксим 1 —6 47 9,471 2531
c,h5no Ацетамид 1 66 158 9,213 3110
c2h5no3 Этилнитрат 1 0 60 8,4497 2331,1
2 15 99 8003 1945
c2h5no4 2-Г идроксиэтилнитрат 1 75 199 9,73 3200
c2H6 Этан 2 -182,8 -142 6,81882 661,09 256,50
2 -142 -44 6,80266 656,40 256,00
2 -44 32,3 7,67290 1096,9 320,54
C2H6Cd Диметилкадмий 1 -6,2 16,6 7,52 1486
C2H6CbSi Диметилдихлорсилан 2 28 72 7,14354 1328 241
C2H6Cl2Si Этилдихлорсилан 2 6 73 7,51426 1664 276
c2H6Hg Диметилртуть 1 30 127 6,662 1116
C2H6O Диметиловый эфир 1 -70 -20 7,720 1202,6
c2H6o2 Этиленгликоль 1 25 90 8,863 2694,7
1 90 130 9,7423 3193,6
1 130 197 9,2477 2994,4
c2H6s Этантиол 1 8 45 7,572 1473,4
c2H6s2 Диметилдисульфид 1 72 129 7,677 1837
C2H6Zn Диметилцинк 2 37 171 7,73800 1732,11 186,21
c2h7n Этанамин (этиламин) 1 75 177 7,603 1358
c2h8n2 Этан-1,2-диамин 1 -11,0 50 9,3539 2468,1
1 50 117,2 8,100 2038,2
C3
C3C16 Г ексахлорпропен 2 20 109 7,2664 1863,7 212,95
2 109 267 6,92329 1649,33 193,87
2 267 447 7,3256 2041 245,7
c3H4 Аллен (пропадиен) 2 -150 -136,2 14,4941 3002,3 331,95
2 -136,2 -34,3 7,3256 2041 245,7
2 -45,4 75 7,4068 1066,4 269,96
c3H4 Пропин 2 -104,7 -23,3 7,0760 920,72 242,48
2 -23,3 60,0 7,4583 994,78 250,37
C3H4Cl2Cb Метилдихлорацетат 1 25 131 8,4073 2222,2
c3H4o Акрилальдегид (акролеин) 1 -3 140 7,655 1558
C3H5Br3 1,2,3-Трибромпропан 2 117 322 7.09534 1779,2 200
2 322 550 7,5173 2246 264
C3H5C1 (£)-1 -Хлорпропен 2 -40 217,8 7,26279 1322,0 270
2 100 225 7,28034 1349 270
C3H5C1 (Z)-1 -Хлорпропен 2 -^0 96 6,88871 1065,3 233
2 95 217,8 7,26279 1322,0 270
C3H5Cl3Si Аллилтрихлорсилан 2 46 115 6,60390 1116 183
c3h5n Пропиононитрил 1 -79 -35 8,893 2116
c3h5no Акриламид 1 7 77 12,34 4321
1 87 137 9,341 3250
c3H6 Пропен 2 -182,2 47,7 6,85658 798,46 248,58
2 -47,7 0,0 6,64808 712,19 236,80
2 0,0 91,4 7,57958 1220,33 309,80
c3H6 Циклопропан 2 -120 30 6,90530 863,62 247,39
1 3 115 7,261 1063,8
C3H6BrCl 1 -Бром-З-хлорпропан 2 53 215 7,03215 1475,23 212
2 215 379 7,32546 1760,2 252
C3H6Br2 1,2-Дибромпропан 2 50 210 6,89105 1419,6 212
2 210 371 7,3109 1796 265
242
Новый справочник химика и технолога
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал. °C А В С
от до
С3Н6Вг2 1,3-Дибромпропан 2 71 242 7,19874 1678,3 222
2 242 414 7,6370 2110 278
С3Н6С12 1,2-Дихлорпропан 2 15 160 6,96395 1295,9 221
2 160 304,3 7,35053 1610,6 265,2
С3Н6О 2-Метилоксиран 2 -74 35 6,96997 1065,27 226,28
С3Н6О2 Пропионовая кислота 1 20 140 8,715 2410
С3Н6О2 Этилформиат 1 -28 48 8,190 1730
C3H6S Тиетан (триметиленсульфид) 2 -15 210 7,01667 1321,33 224,51
C3H7AsC12 Пропилдихлорарсин 1 0 99 8,8516 2572,0
C3H7Br 1 -Бромпропан 1 0 30 7,821 1693,8
C3H7Br 2-Бромпропан 1 0 30 7,722 1606,6
C3H7CI 1 -Хлорпропан 1 0 50 7,593 1509,1
C3H7C1 2-Хлорпропан 2 -32 90 6,96540 1081,6 230
2 90 212 7,39133 1372,3 270,6
C3H7C1S 1 -(Метилсульфанил)-2- 1 0 60 8,28937 2215,7
хлорэтан
C3H7I 1 -Иодпронан 1 0 30 7,826 1845,4
C3H7I 2-Иодпропан 1 0 30 7,629 1722,4
С3Н8 Пропан 2 -188,6 -130 6,83054 813,86 248,12
2 -130 5 6,82973 813,20 248,00
2 5 96,8 7,56290 1096,9 320,54
С3Н8О Метоксиэтан 1 -1 68 7,644 1377
С3Н8О Пропан-1 -ол 1 -45 -10 9,5180 2469,1
С3Н8О2 2-Метоксиэтанол 1 -13 124 8,3077 2157
С3Н8О2 Пропан-1,2-диол 1 80 130 9,5157 3039,0
c3H8s Пропан-1 -тиол 1 И 67,4 7,7190 1647
c3H8s Пропан-2-тиол 2 И 86 6,87734 1113,86 226,16
С3Н9А1 Триметилалюман 1 40 125 8,279 2148
C3H9AS Триметиларсин 1 -25 25 7,3836 1456
СзН9В Триметилборан 1 -118 -20 7,4595 1158,0
C3H9Bi Т риметилвисмутан 1 -25 15 7,6280 1816
C3H9ClSi Триметилхлорсилан 2 2,6 55,6 6,95054 1191 235
C3H9Ga Триметилгаллан 1 -35,5 55,7 8,07 1705
c3h9n А,А-Диметил метанам ин 1 -67 0 7,7580 1342
(триметиламин)
C3H9P Триметилфосфин 1 -25 25 7,7627 1518
C3H9Sb Триметилстибан 1 -25 25 7,7068 1697
C3Hl2B2 Триметилдиборан 1 -78,5 45,5 7,673 1527
c4
c4H2 Бута-1,3-диин 2 -80 -36,5 12,8322 3362,9 345,36
2 -36,5 10,3 6,1718 692,50 200,09
c4h2n2o4s 2,5-Динитротиофен 1 115 292 8,385 3116,1
С4Н20з Фуран-2,5-дион 1 60 160 7,825 2420
(малеиновый ангидрид)
C4H3NO2S 2-Нитротиофен 1 105 224,5 8,334 2679,0
C4H4 Бут-1-ен-З-ин 2 -50 30 6,08797 620,16 187,96
C4H4O Фуран 2 -35 90 6,97523 1060,85 227,74
C4H4O3 Дигидрофуран-2,5-дион 1 -8 19 11,905 4348
(янтарный ангидрид)
C4H4S Тиофен 2 5 155 6,95926 1246,04 221,46
2 155 297 7,13243 1378,58 241
C4H5NO2 Пирролидин-2,5-дион 1 143 288 9,109 3491
(сукцинимид)
c4h5n 2-Метилакрилонитрил 1 —6 25 7,697 1743
c4H6 Бута-1,2-диен 2 -54 68 7,1619 1121,0 251,00
Физические свойства важнейших веществ
243
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал, °C А В С
от до
с4н6 Бута-1,2-диен 2 68 170,6 7,62883 1438,26 293,28
С4н6 Бута-1,3-диен (дивинил) 2 -66 46 6,85941 935,53 239,55
2 46 152 7,29710 1202,54 277,80
с4н6 Бут-1-ин 2 -67 63 6,97497 986,46 238,85
С4н6 Бут-2-ин 2 -32 91 7,07871 1104,72 236,19
2 91 212 7,34794 1354,8 277,8
с4н6 Циклобутен 2 -80,0 2,4 7,0892 1061,4 249,70
2 2,4 50 7,5494 1319,5 280,11
С4Н6О2 Винилацетат 1 0 72,5 8,091 1797,44
С4Н6О3 Уксусный ангидрид 2 2 139 7,12165 1427,77 198,04
С4Н7С1О2 Этилхлорацетат 1 25 146 8,3893 2291,6
с4н8 Бут-1-ен 2 -67 40 6,84290 926,10 240,00
2 40 146 7,2793 1186 277
с4н8 (Е)-Бут-2-ен 2 -62 49 6,86952 960,8 240
2 49 155 7,3082 1231 278
с4н8 (7)-Бут-2-ен 2 -59 41 6,89926 960,1 237
2 41 155 7,3023 1229 275
с4н8 2-Метилпропен 2 -68 39 6,84134 923,2 240
2 39 144,7 7,2777 1183 277
с4н8 Циклобутан 2 -80 12,6 7,0127 1068,07 245,01
2 12,6 60 7,6348 1400,0 281,90
С4Н8С12О Бис(2-хлорэтиловый) эфир 1 45 180 8,1040 2359,6
C4H8Cl2Si Винил(дихлор)(этил)силан 2 45 122 7,11466 1489 228
С4Н8О Бутан-2-он 1 -15 85 7,764 1725,0
с4н8о Бутиральдегид 1 -15 80 7,959 1768,4
С4н8о2 1,4-Диоксан 1 10 105 7,8642 1866,7
С4Н8О2 Изомасляная кислота 1 30 155 8,819 2533
С4Н8О2 Изопропилформиат 1 25 72 7,8909 1710,5
С4Н8О2 Масляная кислота 1 80 165 9,010 2669
С4Н8О2 Метилпропионат 1 85 257 7,617 1667
С4Н8О2 Пропилформиат 1 26 82 7,9925 1806,5
C4H8S Т етрагидротиофен 1 -65 -20 9,084 2296
(тетраметиленсульфид) 2 10 35 7,34491 1576,6 234
2 35 200 6,9518 1372,4 216
2 200 358 7,37677 1748,6 270
С4Н9Вг 1 -Бромбутан 1 -75 -33 9,483 2278
С4Н9Вг 2-Бромбутан 2 10 146 6,82724 1229,08 220
2 146 286 7,2470 1555,6 266
С4Н9С1 1 -Хлорбутан 2 0 123 6,93790 1227,43 224,10
2 123 269 7,13392 1410,8 255,0
C4H9C1S 1 -Хлор-2-(этилсульфанил)этан 1 0 72 8,92455 2318,8
C4H9NO Морфолин 2 0 44 7,71813 1745,8 235,0
2 44 170 7,16030 1447,70 210,0
c4H10 Бутан 2 -138,3 -60 6,88032 968,10 242,56
2 -60 45 6,83029 945,9 240,0
2 45 152 7,39949 1299 289,1
С4Н10 Изобутан 2 -159,4 -85 6,82285 916,05 243,78
2 -75 30 6,74804 882,80 240,00
2 30 134,9 7,42067 1288,1 296,7
С4Н]оВе Диэтилбериллий 1 -80 8,5 7,59 2299
C4H10Cl2Si Диэтил(дихлор)силан 2 102,2 180,5 7,07712 1483 223
c4H10Hg Диэтилртуть 1 64 80 7,975 2200
С4Н10О Бутан-1-ол 1 75 117,5 9,136 2443
C4HioO 1 -Метоксипропан 1 -0,5 40 7,729 1512,2
С4Н10О2 Бутан-1,3-диол 1 100 150 9,389 3116,7
С4Н10О2 Бутан-2,3-диол 1 -20 30 9,552 3024
244
Новый справочник химика и технолога
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал,°C А В С
от до
С4Н10О2 1,2-Диметоксиэтан 1 -1 68 7,719 1748
СдНюОг 2-Этоксиэтанол 2 50 135 8,416 2135 253
С4Н|0Оз 2,2 '-Окси диэтанол (диэтиленгликоль) 1 80 165 8,1527 2727,3
СдНюЗ 2-Метилпропан-2-тиол 1 20 53 7,664 1612
1 53 99 7,447 1542
C4H10S2 Диэтилдисульф ид 2 0 115 6,97792 1346,34 218,86
C4H10Se Диэтилселенид 1 22 108 7,905 1924
C4H10Zn Диэтилцинк 1 1 91 8,280 2109
C4HhN TV-Этилэтанамин 1 -33,0 55,5 8,103 1709
(диэтиламин)
C4HhNO2 2,2'-Иминодиэтанол 2 111 269 8,13968 2328,56 174,40
(диэтаноламин)
C4H12Pb Тетраметилплюмбан 1 -20 49 8,021 1950
C4H12Sn Тетраметилстаннан 1 18 78,9 7,495 1620
C4H14B2 Т страметилдиборан 1 -51,2 0 7,687 1643
C5
C5F10 Декафторциклопентан 1 22 57 7,579 1389
c5F12 Додекафторпентан 1 9 65 7,675 1452
c5f12 2-(Трифторме-тил)нонафторбутан 1 22 50 7,655 1448
C5H4O2 2-Фур альдегид 1 120 -252 7,959 2209
(ФУРФУРОЛ)
c5h5n Пиридин 2 -20 130 6,8827 1281,3 205
c5H6s 2-Метилтиофен 2 0 28 7,14504 1428,6 233,3
2 28 180 6,93897 1326,47 214,31
2 180 337,6 7,40824 1724,0 266,7
c5H6s 3-Метилтиофен 2 0 30 7,33318 1541,1 232,38
2 30 185 6,98611 1363,86 216,78
2 185 333,0 7,35668 1677,7 263,6
C5H7AsC12 Метилбис(2-хлорвинил)арсин 1 0 91 9,0918 2908,5
c5H8 Изопрен 2 -50 84 6,90334 1081,00 234,67
2 84 202 7,33735 1374,92 275,34
c5H8 З-Метилбута-1,2-диен 2 -30 90 7,005 ИЗО 234
2 90 212 7,43814 1428,51 274,34
c5H8 З-Метилбут-1 -ин 2 -40 73 6,88971 1017,50 227,46
2 73 188 7,34037 1329,4 272,6
c5H8 Пента-1,2-диен 2 -60 97 7,01100 1154,42 234,65
2 97 221 7,44719 1462,26 276,31
c5H8 (Е)-Пента-1,3-диен 2 -60 92 6,92257 1108,94 232,34
2 92 214 7,35341 1406,44 273,32
c5H8 (2)-Пента-1,3-диен 2 -60 96 6,94179 1118,37 231,33
2 96 219 7,37139 1417,55 272,55
c5H8 Пента-1,4-диен 1 -60 72 6,83880 1025,02 232,35
2 72 198 7,27510 1301,04 270,91
c5H8 Пента-2,3-диен 2 -40 101 6,88603 1086,64 223,04
2 101 226 7,30054 1372,39 263,23
c5H8 Пент-1-ин 2 -50 70 6,97263 1095,42 227,53
C5H8 Пент-2-ин 2 -19 113 7,05189 1193,05 229,96
2 113 243 7,22935 1424,6 272,6
c5H8 Спиро[2.2]пентан 2 -60 120 6,91794 1090,59 231,16
C5H8 Циклопентен 2 -50 105 6,92066 1121,82 233,45
2 105 231 7,35778 1436,9 278
c5H8o 3 -Мети лбут-3 -ен-2 -он 1 47 97,7 7,24656 1430,7
Физические свойства важнейших веществ
245
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал. °C А В С
от до
с5н8о 2-Метилбут-3-ин-2-ол 1 21 106 8,964 2291
с5н8о2 З-Пропилоксиран-2-он 1 70 160 8,2059 2540,4
С5Н9ВгО З-Бромпентан-2-он 1 0 60 8,4256 2359,4
с5н9сю2 Изопропил(хлор)ацстат 1 35 153 8,3321 2298,6
С5Н,о 2-Мстилбут-1-ен 2 -60 60 6,82618 1013,47 236,82
2 75 191 7,3005 1334 271
С5Н,о 2-Мстилбут-2-ен 2 -60 85 6,91562 1095,09 232,84
2 85 197 7,3453 1385 272
с5н10 З-Метилбут-2-ен 2 -60 60 6,82618 1013,47 236,82
2 85 197 7,3453 1385 272
С5Н,о Пент-1 -сн (амилен) 2 -60 100 6,78568 1014,29 229,78
2 100 188 7,2651 1324 272
С5Н10 (Е)-Пент-2-ен 2 -60 81 6,90575 1083,99 232,97
2 81 199 7,3347 1370 272
с5н10 (7)-Пент-2-ен 2 -60 82 6,87540 1069,47 230,79
2 82 202 7,2973 1350 270
С5Н10 Циклопентан 2 -60 130 6,87998 1119,21 230,74
2 130 238,6 7,4333 1529,36 288,10
С5Н10О З-Метилбутан-2-он 1 8 82 7,872 1831
с5н10о Пентан-2-он 1 17 103,3 7,8642 1870,4
CsHio02 Бутилформиат 1 18 114 8,121 1984
СзН10О2 в/ио/?-Бутилформиат 1 15 103 8,042 1894
CsHi0O2 Изобутилформиат 1 18 107 7,962 1887
СзНюО2 Метилбутират 1 89 315 7,629 1783
CsH10O2 М етилизобутират 1 95 187 7,582 1715
CsH|o02 1 -Метоксибутан-2-он 2 25 135 7,11187 1429,5 205
CsH]0O2 Этилпропионат 1 87 198 7,644 1770
c5H10s Т страгидротиопиран 2 0 50 7,18029 1570,3 225
2 50 210 6,90518 1422,47 211,72
c5H12 Пентан 2 -30 120 6,87372 1075,82 233,36
2 120 196,6 7,47480 1520,66 297,09
c5H12 Изопентан (2-мстилбутан) 2 -30 100 6,78967 1020,01 233,10
2 100 187,8 7,51725 1547,32 308,24
c5H12o 1-Этоксипропан 1 —4 72 7,835 1667
C5H14SI1 Триметил(этил)станнан 1 0 63 7,994 1934
C6
C6C14O2 2,3,5,6-Тетрахлорбензо- 1 70 163 13,666 4700
1,4-хинон (хлоранил)
C6C16 Г ексахлорбензол 1 114 227 8,368 3242
C&F14 Т етрадекафторгексан 2 -14 66 7,12338 1205,37 227,0
C&F 14 2-(Трифторметил)- 2 -14 73 7,08320 1198,63 227,5
ундекафторпентан
C6HC15O Пентахлорфенол 2 189,7 309 9,073 3606 273,15
C6H3C13 1,2,4-Трихлорбензол 2 20 НО 7,5553 2064,4 230,1
2 НО 280 7,19508 1827,0 210
2 280 461,8 7,19792 1829,7 200,4
C6H3N3O6 1,3,5-Тринитробензол 1 80 122 11,832 5077
СбН4Вг2 1,2-Дибромбензол 2 20 120 7,45706 2013,06 227,4
2 115 295 7,10265 1825,77 207,0
2 295 486,6 7,52773 2279,0 266,1
C6H4Br2 1,4-Дибромбензол 1 -45 74 8,80 3850
C6H4C12 1,2-Дихлорбензол 2 20 181 7,07028 1649,55 213,31
2 176 366 7,1123 1651,1 212,2
246
Новый справочник химика и технолога
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал. °C А В С
от до
С6Н4С12 1,3-Дихлорбензол 2 10 75 7,22086 1690,7 218,4
2 75 240 6,88045 1496,2 201
2 240 410,8 7,28934 1878,8 254,2
С6Н4С12 1,4-Дихлорбензол 2 0 75 7,23948 1703,2 218
2 75 240 6,89797 1507,3 201
2 240 411,6 7,30658 1889,6 254
c6h4n2o5 2,3-Динитрофенол 1 30 70 12,58 5171
c6h4n205 2,4-Динитрофенол 1 20 60 13,95 5466
c6h4n2o5 2,5-Динитрофенол 1 5 60 12,45 4876
c6h4n2o5 2,6-Динитрофенол 1 20 60 15,38 5860
c6h4n2o5 3,4-Динитрофенол 1 55 НО 14,25 6451
C6H5Br Бромбензол 2 0 60 7,35311 1696,4 227
2 60 190 6,91444 1474,06 199,4
2 190 397 7,35936 1853,57 258,2
C6H5C1 Хлорбензол 2 0 40 7,49823 1654,0 232,3
2 40 200 6,94504 1413,12 216,0
2 200 359,2 7,58977 2001,9 295,3
C6H5C1O 2-Хлорфенол 2 20 80 7,42442 1808,0 225
2 80 300 7,05272 1589,1 206
C6H5Cl3Si Фснил(трихлор)силан 2 102 197 6,98346 1641 199
c6h5f Фторбензол 2 0 145 7,04659 1283,5 223
2 145 286,6 7,0756 1305 226
c6h5i Иодбензол 2 0 85 7,23639 1765,99 219
2 85 270 6,89506 1562,87 201
c6h5no2 Нитробензол 2 15 108 7,55755 2026 225
2 108 300 7,08283 1722,2 199
c6H6 Бензол 1 -75 -37 10,454 2466
2 -20 5,5 6,48898 902,28 178,10
2 5,5 160 6,91210 1214,64 221,20
2 160 289,4 7,42912 1628,32 279,56
c6H6 Г екса-1,5-диен-З-ин 2 -50 100 7,51221 1569,91 255,47
C6H6C1N 2-Хлоранилин 2 25 110 7,55246 1991,84 219,4
2 110 330 7,19240 1762,74 200,0
C6H6C1N З-Хлоранилин 2 25 125 7,59884 2099,20 216,96
2 125 265 7,23603 1857,75 196,64
c6h6n2o2 2-Нитроанилин 1 0 50 12,50 4701
1 150 260 8,868 3337
c6h6n2o2 З-Нитроанилин 1 15 70 13,00 5095
1 170 260 8,819 3441
c6h6n2o2 4-Нитроанилин 1 30 90 13,69 5707
1 190 260 9,560 4040
c6H6o Фенол 2 0 40 11,5638 3586,36 273
2 41 93 7,86819 2011,4 222
2 93 240 7,57893 1817,0 205
2 240 419 7,9398 2219,3 257,6
c6H6o2 Гидрохинон 1 52 72 16,46 5420
1 132 170 14,071 5701
C6H6O2 Резорцин 1 10 50 12,30 4876
с6н6о3 Бензол-1,2,3-триол 1 2 27 12,923 4808
(пирогаллол)
c6H6o4 Диметилбут-2-индиоат 1 0 60 9,204 2941
c6H6s Бензолтиол 2 25 70 7,11854 1657,1 224
(тиофенол)
2 70 205 6,78419 1466,5 207
Физические свойства важнейших веществ
247
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал,°C А В С
от до
С6Н6С16 (lr,2fl,3S,4r,5fl,6S)- 2 ИЗ 205 7,23920 2097,4 160
1,2,ЗД5,6- 2 205 450 6,92309 1873,3 140
гексахлорциклогексан
(у-гексахлорциклогексан)
c6h7n Анилин 2 15 90 7,63851 1913,8 220
2 90 250 7,24179 1675,3 200
2 250 426 7,75568 2140,4 258,8
c6h7n 2-Метилпиридин 2 64,4 130,0 7,03450 1417,58 211,87
(а-пиколин)
c6h7n З-Метилпиридин 2 81,3 145,1 7,03247 1469,89 209,91
(0-пиколин)
c6h7n 4-Метилпиридин 2 76,9 145,5 7,04250 1481,20 210,56
(у-пиколин)
c6h7no 4-Аминофенол 1 145 189 12,190 4955
c6h8n2 Фенилгидразин 2 25 140 7,78509 2232,5 214
2 140 335 7,41124 1975,68 193
2 335 АфИТ 7,8233 2434,5 251
c6h8s 2,3-Диметилтиофен 2 25 80 7,2681 1615,9 229
2 80 200 6,9249 1430,0 212
2 200 362,0 7,3425 1797,9 262
c6H8s 2,4-Диметилтиофен 2 25 50 7,3415 1639,2 229
2 50 220 6,9939 1450,7 212,0
2 220 358 7,4100 1814 261
c6H8s 2,5-Диметилтиофен 2 25 50 7,3066 1613,3 230
2 50 195 6,9611 1427,7 213,2
2 195 352 7,3785 1789,6 262
c6H8s 3,4-Диметилтиофен 2 25 55 7,2830 1634,7 228
2 55 205 6,9389 1446,7 211,5
2 205 367 7,3562 1817,0 262
c6H8s 2-Этилтиофен 2 15 45 7,30149 1598,0 229
2 45 195 6,9563 1515,2 213,0
2 195 350,0 7,37327 1774,2 261,9
c6H8s 3-Этилтиофен 2 15 45 7,2980 1606,8 229
2 45 200 6,9530 1422,0 213,2
2 200 354 7,3711 1786,2 262,8
C6H10 Гекса-1,5-диен 2 -13 102 7,00740 1184,99 227,7
СбНю Гекс-1-ин 2 -8 118 6,91212 1194,6 225
2 118 248 7,16827 1453,8 268,5
СбНю 2,3-Диметилбута-1,3-диен 2 —6 116 7,02388 1220,88 225,9
СбНю 1 -Метилциклопентен 2 -5 130 6,86884 1199,6 225
2 130 269 7,29519 1524,9 271
СбНю 3 -М етилцикл опентен 2 -10 119 6,87259 1165,6 227
2 119 250 7,29924 1479,7 271
СбНю 4-Метилциклопентен 2 -2 130 6,87015 1197,6 225
2 130 268 7,29635 1522,2 271
СбНю Циклогексен 2 3 146 6,88617 1229,97 224,10
2 146 286 7,31379 1566,7 272
СбНюО 4-Метилпент-3-ен-2-он 2 0 129,8 7,01266 1399,09 208,85
(окись мезитила)
C6H10O4 Этан-1,2-диилдиацетат 1 128 197 8,566 2632
СбНцВг Бромциклогексан 2 0 68 7,34139 1778,81 235
2 68 205 6,97980 1572,19 217,38
C6HnC102 вто/?-Бутил(хлор)ацетат 1 62 164 8,361 2410
248
Новый справочник химика и технолога
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал, °C А В С
от до
C6HnNO Азепан-2-он (s-капрол актам) 1 80 140 6,78 2344
С6Н12 Гекс-1-ен 2 -60 103 6,86572 1152,97 225,85
2 103 228 7,2845 1445 265
С6н12 (£)-Гекс-2-ен 2 -8 108 6,89830 1181,0 226
2 108 236 7,3188 1479 266
С6н12 (2)-Гекс-2-ен 2 -7 110 6,89962 1184,6 226
2 110 238 7,32029 1484 266
С6н12 (£)-Гекс-3-ен 2 -9 107 6,89575 1177,7 226
2 107 234 7,3162 1475 266
С6Н12 (7)-Гекс-3-ен 2 -9 107 6,89493 1175,4 226
2 107 233 7,3156 1472 266
С6Н12 2,3-Диметилбут-2-ен 2 -15 94 6,8820 1136,7 228,4
2 94 217 7,3038 1425 267
С6н12 2-Метилпент-1 -ен 2 -14 100 6,88772 1154,7 227
2 100 255 7,30907 1447 267
С6н12 2-Метилпент-2-ен 2 -9 108 6,89488 1178,1 226
2 108 235 7,3157 1476 266
С6Н12 З-Метилпент-1 -ен 2 -19 92 6,87729 1130,4 229
2 92 213 7,2989 1417 267
С6н12 Метилциклопентан 2 -60 125 6,86283 1186,06 226,04
2 125 259,6 7,34080 1549,9 276,1
С6Н12 Циклогексан 2 -20 142 6,84498 1203,53 222,86
2 142 281,0 7,32217 1577,42 275,8
C6H12C13N 2-Хлор-А,А-бис(2-хлорэтил)этанамин 1 0 60 9,41621 3393,4
с6н12о Г ексан-2-он 1 7 127,5 8,1852 2117,2
С6Н12О 2-Метил пентан-3 -он 1 10 113,3 8,0277 1989,7
С6Н12О 4-Метилпснтан-2-он 1 -1 119 8,0590 2009,5
С6Н12О2 Бутилацетат 2 0 126,5 8,099 1964 253
С6Н12О2 4-Гидрокси-4-метилпентан-2-он 2 22 168 8,091 2188 253
(диацетоновый спирт)
С6н12о2 Пропилпропионат 1 45 125 8,0525 2048,5
С6н12о2 Этилбутират 1 45 121 8,903 2053,6
c6h13ci2n 2-Хлор-У-(2-хлорэтил)-7У- 1 0 60 9,01892 2868,9
этилэтанамин
С6Н14 Г ексан 2 -60 ПО 6,87776 1171,53 224,37
2 НО 234,7 7,31938 1483,1 265,9
С6н14 2,2-Диметилбутан 2 -80 95 6,75483 1081,18 229,34
2 95 216,2 7,34293 1494,7 286,2
С6н14 2,3-Диметилбутан 2 -60 100 6,80983 1127,19 228,90
2 100 227,1 7,30917 1481,8 277,4
С6н14 2-Метилпентан 2 -60 100 6,83910 1135,41 226,57
2 100 224,7 7,31635 1468,9 271,5
С6н14 3-Метил пентан 2 -60 105 6,84887 1152,37 227,13
2 105 231,2 7,36387 1520,0 276,46
С6Н14О Дипропиловый эфир 1 8 90 7,821 1791,2
С6н14о2 2,3-Диметилбутан-2,3- 1 190 235 10,886 4649
диол
(пинакон)
С6н14о2 1 -Метокси-2-(2-метокси- 1 25 159,8 8,0837 2251,5
этокси)этан
С6Н 14О4 2,2'-[Этан-1,2- 1 140 210 9,6396 3726,2
диилбис(окси)]диэтанол
(триэтиленгликоль)
Физические свойства важнейших веществ
249
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал, °C А В С
от до
с6н15в Триэтилборан 1 -137 -107 5,707 581,9
c6h15n УД-Диэтилэтанамин 1 -40 120 8,059 1838
(триэтиламин)
с6н15р Триэтилфосфин 1 18 78,2 7,86 2000
С6Н15Т1 Триэтилталлий 1 0 74 7,466 2107
C6Hi6Sn Триметил(пропил)станнан 1 13 55 8,338 2164
СбН]8О3813 Г сксаметилциклотриси- 1 24 62 10,335 2884
локсан 1 70 115 7,984 2080
с7
C7F14 (Трифторме- 2 32,6 111 6,82184 1132,49 211,07
тил)ундекафторцикло-
гексан
c7f 16 Г сксадекафторгептан 1 37 81 7,966 1807
C7H4C12O 2-Хлорбензоилхлорид 1 100 122 8,396 2755
С7Н4СЬО З-Хлорбензоилхлорид 1 94 117 8,086 2605
С7Н4С12О 4-Хлорбензоил хлорид 1 97 126 8,619 2813
С7Н4С14 1 -(Трихлорметил)-2- 2 15 150 7,47331 2205 218,1
хлорбензол 2 150 315 7,11794 1951,37 196,27
3 315 511,0 7,5302 2395,6 251,6
c7h4f4 1 -(Трифторметил)-З- 2 40,5 137 7,00795 1305,69 215,77
фторбензол
С7Н5С1О Бензоилхлорид 1 140 200 7,9245 2372
с7н5сю 2-Хлорбензальдегид 2 25 109 7,38896 1925,0 217
2 109 290 7,06216 1718,10 199
С7Н5С13 2,4-Дихлор-1- 2 20 140 7,50457 2125,90 213,8
(хлорметил)бензол 2 140 305 7,14735 1881,38 192,93
2 305 498,1 7,5540 2308,4 246,6
c7h5f3 (Трифторметил )бензол 2 0 150 7,00708 1331,3 220,58
2 150 289,5 7,42586 1658,7 263,5
С7Н6С12 4-Метил-1,2- 2 25 105 7,32588 1870,60 214,0
дихлорбензол 2 105 270 6,97925 1655,44 195,0
2 270 451,2 7,3839 2053,3 247,9
c7h6n2o5 2-Метил-3,5-динитрофенол 1 17 51 14,140 5400
С7н6о2 Бензойная кислота 1 60 121 11,956 4409
с7н6о2 4-Г идроксибензальдегид 1 244 311 8,716 3397
с7н6о3 Салициловая кислота 1 104 148 11,300 4292
С7Н7Вг 1 -Бром-4-метилбснзол 2 25 85 7,35604 1821,91 224,7
2 85 250 7,00762 1612,35 206,36
2 250 419,7 7,4238 2011,3 259,3
С7Н7С1 1 -Метил-2-хлорбензол 2 0 65 7,29227 1691,79 226,2
2 65 220 6,94763 1497,2 209,0
2 220 385,9 7,3637 1876,5 260,4
С7Н7С1 (Хлорметил)бензол 1 0 60 8,804 2601
С7Н7С1О 1 -Метокси-4-хлорбензол 2 115 201,8 7,54073 2012,4 230
C7H7NO2 1 -Метил-2-нитробензол 1 55 225 7,97285 2513,0
c7h7no2 1 -Метил-3-нитробензол 1 85 235 8,06553 2618,2
c7h7no2 1 -Метил-4-нитробензол 1 100 245 7,98149 2608,9
C7H7Br о-Бромтолуол 2 20 80 7,25065 1750,76 221,0
2 80 245 6,90847 1459,39 203,0
2 245 419,7 7,3209 1942,3 256,8
c7H8 Толуол 1 -92 15 8,330 2047,3
2 20 200 6,95334 1343,94 219,38
2 200 320,8 7,45657 1796,9 284,62
250
Новый справочник химика и технолога
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал, °C А В С
от до
с7н8о о-Крезол 2 0 30,9 12,7778 3970,17 273
2 30,9 97 7,7696 1984,7 220
2 97 250 7,39476 1777,8 203
2 250 422 7,7327 2098 242,3
с7н8о .м-Крезол 2 15 ПО 7,9424 2138,2 220
2 110 240 7,53185 1875,3 201
2 240 426 7,73634 2064 223,3
с7н8о л-Крезол 2 0 35 12,0298 3861,98 273
2 35 97 7,9375 2134,5 222
2 97 250 7.52871 1872,4 201
2 250 426,0 7,8594 2241,2 250
с7н80 Фенилметанол 2 20 112 7,93428 2130,42 218
(бензиловый спирт) 2 112 330 7,58200 1904,3 200
c7H8s 2-Метилбснзолтиол 2 25 90 7,20649 1784,6 220
2 90 235 6,86693 1579,3 202
c7H8s 3 -М ети л бснзолтиол 2 25 90 7,20945 1789,0 221
2 90 235 6,86972 1593,2 202
c7H8s 4-М етилбензолтиол 2 25 90 7,20945 1789,0 221
2 90 235 6,86972 1593,2 202
c7h9n 2,5-Димстилпиридин 2 85,1 157,3 7,05816 1524,02 207,82
c7h9n 2,6-Диметилпиридин 2 79,3 144,3 7,05246 1467,36 207,70
c7h9n о-Толуидин 2 20 103 7,63271 1984,1 219
2 103 320 7,28896 1768,7 201
c7h9n л/-Толуидин 2 20 105 7,61573 1986,9 218
2 105 320 7,27435 1772,06 200
c7h9n и-Толуидин 2 20 103 7,61234 1981,3 220
2 103 330 7,25137 1755,0 201
c7H12 Гепт-1-ин 2 14 142 6,68593 1216,6 220
2 142 280 7,10459 1538,4 265,0
c7H12 1 -Метилциклогексен 2 25 165 6,86861 1308,10 218
2 165 311 7,28846 1649,7 265
c7HI2 3 -М ети л циклогексен 2 20 158 6,86718 1287,6 219
2 158 301 7,28693 1622,9 265
c7H12 4-М ети л ци клогексен 2 19 156 6,86881 1283,1 219
2 156 299 7,28813 1616,5 265
c7H12 Циклогептен 2 -50 160 7,36948 1615,00 245,44
c7H14 Гепт-1-ен 2 -60 128 6,90069 1257,51 219,18
2 128 262 7,3119 1560 259
c7H14 1,1 -Диметилциклопентан 2 -60 140 6,81724 1219,47 221,95
2 140 277 7,61456 1863,9 307,3
c7H14 Этилциклопентан 2 -60 155 6,88709 1298,60 220,68
2 155 296,3 7,33306 1654,1 268,9
c7H14 (1/?,2S)-1,2- 2 -50 150 6,85008 1269,14 220,21
Диметилциклопентан 2 150 292 7,44124 1745,6 284,3
c7H14 рац-( 1 R,2R}-1,2- 2 -60 145 6.84422 1242,75 221,69
Диметилциклопентан 2 145 282 7,36128 1648,7 277,1
c7H14 (1/?,3S)-1,3- 2 -60 145 6,83817 1240,02 221,62
Диметилциклопентан 2 145 282 7,21251 1528,2 261,8
c7Hl4 рац-{ \R,3R}-1,3- 2 -60 145 6,83715 1237,46 222,01
Диметилциклопентан 2 145 282 7,48224 1753,6 291,5
c7Hl4 Метилциклогексан 2 -40 160 7,82689 1272,86 221,63
2 160 299,1 7,56476 1929,24 313,64
c7H14 Циклогептан 2 60 160 6,85271 1330,74 216,24
C7H14O Гептан-2-он 2 0 75 7,36537 1650,47 218,68
C7H14O 2,4-Диметилпентан-З-он 1 15 123,7 7,9752 2021,4
C7H14O 2-Метилгексан-З -он 1 27 133,6 8,1930 2159,5
Физические свойства важнейших веществ
251
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал, °C А В С
от до
С7Н]4О2 Пентилацетат 2 0 147 8,078 2077 253
с7н16 Гептан 2 -60 130 6,90027 1266,87 216,76
2 130 267 7,3270 1581,7 257,6
С7н16 2,2-Диметилпентан 2 -60 115 6,81479 1190,03 223,30
2 115 247,7 7,50352 1705,8 290,5
с7н16 2,3-Диметилпентан 2 -60 130 6,85382 1238,02 221,82
2 130 264,6 7,40013 1652,5 276,5
с7н16 2,4-Диметилпентан 2 -60 115 6,82621 1192,04 221,63
2 115 247,1 7,33247 1559,5 270,5
с7н16 3,3-Диметилпентан 2 -60 130 6,82668 1228,66 235,32
2 130 263 7,55060 1795,1 299,3
с7н16 2-Метилгексан 2 -60 125 6,87319 1236,03 219,55
2 125 257,9 7,31001 1555,4 261,5
С7н16 З-Метил гексан 2 -60 130 6,86764 1240,20 219,22
2 130 262,4 7,39633 1635,1 270,8
с7н16 3-Этилпентан 2 -60 130 6,87565 1251,83 219,89
2 150 267,6 7,29098 1561,6 261,0
с7н,6 2,2,3-Триметилбутан 2 -25 125 6,79230 1200,56 226,05
2 125 258,3 7,40100 1666,5 288,7
С8
C8F16 (Пентафторэтил)- 2 38 138 6,85194 1217,73 205,17
ундекафторциклогексан
c8h5no2 1 //-Изоиндол-1,3(2//)- 1 105 150 10,014 4326
ДИОН
(фталимид)
c8h6n2o2 5-Амино-1 //-изоиндол- 1 110 185 11,865 5655
1,3(2//)-дион
С8Н4О3 2-Бензофуран-1,3-дион 1 30 60 12,249 4632
(фталевый ангидрид) 1 90 145 9,209 3410
1 160 285 8,022 2868
c8H6o4 Терефталевая кислота 1 119 152 12,15 5130
С8Н7Вг 1 -Бром-2-винилбензол 2 20 105 7,25268 1834,2 214
2 105 270 6,91038 1631,2 195
2 270 453,0 7,3159 2031,5 249
С8Н7Вг 1 -Бром-4-винилбензол 2 20 НО 7,36378 1901,2 214
2 НО 270 7,01490 1682,5 195
2 270 453,4 6,8754 1554,8 177
С8Н7С1 1 -Винил-2-хлорбснзол 2 15 90 7,20597 1741,4 216
2 90 250 6,86644 1541,1 198
2 250 423,6 7,2622 1925,6 251
С8Н7С1 1 -Винил-4-хлорбензол 2 25 90 7,18050 1745,8 216
2 90 250 6,84248 1545,00 198
2 250 427,4 7,24901 1932,8 251
С8Н7С1О 1 -(4-Хлорфенил)этанон 2 25 131 7,49315 2063,8 212
2 131 350 7,17747 1852,9 194
с8н8 Стирол 2 10 55 7,26725 1604,6 222
2 55 205 6,92409 1420,0 206
2 205 363,7 7,33218 1774,8 254
с8н8 Циклоокта-1,3,5,7-тетраен 2 0 75 7,01490 1682,5 195
С8Н8О 1 -Фенилэтанон 2 15 102 7,51308 1946,1 220
(ацетофенон) 2 102 330 7,15738 1723,46 201
С8Н8О2 Метилбензоат 2 25 100 7,4312 1871,5 213,9
2 100 260 7,07832 1656,25 195,23
2 260 438 7,3186 1866 218,7
С8Н80з Метилсалицилат 1 175 215 8,008 2542,0
С8НдВг (2-Бромэтил)бензол 2 46 216 7,94437 2359,07 250,19
252
Новый справочник химика и технолога
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал, °C А В С
от до
С8Н9С1 1 -Метил-4- 1 0 60 8,862 2762
(хлорметил)бензол
С8Н9С1О 1 -Хлор-4-этоксибензол 2 122 211,9 7,56470 2070,0 230
C8H9NO2 1 -Нитро-2-этилбензол 2 15 125 7,50205 2058,9 215,0
2 125 290 7,14960 1825,0 195
с8н|0 о-Ксилол 2 25 50 7,35638 1671,8 231,0
2 50 200 6,99891 1474,68 213,69
2 200 359,0 7,4175 1842,1 262,4
с8н10 ^-Ксилол 2 25 45 7,36810 1658,23 232,3
2 45 195 7,00908 1462,27 215,11
2 195 346,0 7,4281 1824,1 262,8
с8н10 и-Ксилол 2 25 45 7,32611 1635,74 231,4
2 45 190 6,99052 1453,43 215,31
2 190 345,0 7,4096 1814,3 263,0
С8Н10 Этилбензол 2 20 45 7,32525 1628,0 230,7
2 45 190 6,95719 1424,26 213,21
2 190 346,4 7,3729 1779,0 260,6
с8н10о 1 -Фенилэтанол 2 20 НО 7,90607 2115,01 219
2 ПО 230 7,55432 1889,9 201
С8Н,оО 2-Фенилэтанол 2 20 121 7,80851 2126,92 215
2 121 340 7,46926 1905,1 197
с8н10о 2-Этилфенол 2 25 105 7,57011 1984,8 218
2 105 245 7,23343 1771,5 200
с8н10о З-Этилфенол 2 25 120 8,11966 2245,0 216
2 120 250 7,74624 1999,7 197
с8н10о 4-Этил фенол 2 25 125 7,89361 2167,9 215
2 125 255 7,55177 1943,1 197
c8h,,n 2,4-Диметиланилин 2 20 115 7,63281 2035,4 216
C8HhNO 4-Этоксианилин 2 20 148 7,87653 2216,5 198,6
2 148 300 7,16534 1750,62 160,0
С8Н,4 Окт-1 -ин 2 25 170 7,02447 1514,8 215,0
с8н14 Циклооктен 2 8 160 6,99615 1506,36 221,52
с8н|4о 1 -Циклогексилэтанон 1 21 178 8,2238 2418,7
с8н16 рац-( 1 R,2R)~ 1,2- 2 10 155 6,82180 1332,61 218,79
Диметилциклогексан 2 155 299 7,23940 1663,83 262,8
с8н16 (1/?, 25)-1,2- 2 15 165 6,83699 1347,79 216,36
Диметилциклогексан 2 165 309 7,2522 1681,8 260,8
с8н16 Изопропилциклопентан 2 10 40 7,22699 1558,70 234,0
2 40 165 6,88622 1379,42 217,97
2 165 312,1 7,30422 1718,9 262,6
С8н16 Окт-1 -ен 2 -50 151 6,93262 1353,49 212,76
2 151 292 7,3370 1664 252
с8н16 Пропилциклопентан 2 20 40 7,24581 1564,31 229,2
2 40 170 6,90392 1384,39 213,16
2 170 317,1 7,3143 1716,3 256,6
С8Н16 Циклооктан 2 100 190 6,86173 1437,68 210,00
с8н16 Этилциклогексан 2 10 40 7,21019 1563,9 231,3
2 40 170 6.87041 1384,04 215,13
2 170 321,3 7,2853 1724,55 260,2
с8н16о 2,5-Диметилгексан-З-он 1 -1 145 8,1873 2221,9
с8н16о 2-Метилгептан-З -он 1 50 155 8,1827 2271,9
с8н18 2,5-Диметилгексан 2 -50 140 6,85984 1287,27 214,41
2 140 276,8 7,23831 1570,2 251,5
С8Н18 4-Метилгептан 2 25 150 6,89098 1327,88 212,60
2 150 290 7,31607 1645,2 253,5
Физические свойства важнейших веществ
253
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал, °C А В С
от до
с8н18 3 -Метил-3 -этил пентан 2 0 30 8,17016 2077,18 280,10
2 30 160 6,86731 1347,21 219,68
2 160 305 7,49210 1864,1 286,7
С8н18 Октан 2 15 40 7,47175 1641,52 234,5
2 40 155 6,92377 1355,23 209,52
2 155 296,2 7,30712 1648,0 246,9
с8н18 2,2,3,3-Тетраметилбутан 2 -20 100,7 7,92864 1709,43 233,63
2 100,7 160 6,87665 1327,8 226,0
2 160 305 7,49210 1864,1 286,7
С8н18 2,2,3-Триметилпентан 2 20 150 6,82546 1294,88 218,42
2 150 294 7,29189 1663,7 267,9
С8н18 З-Этилгексан 2 0 25 7,30017 1529,6 230
2 25 150 6,89098 1327,88 212,60
2 150 294 7,29602 1639,8 253,2
с8н18о Октан-1-ол 2 101 195 6,596 1170 120
с8н18о Октан-2-ол 2 88 178,5 6,434 1066 120
с8н18о Октан-3-ол 2 76 173 6,089 940 120
с8н180 Октан-4-ол 2 81 176 6,229 992 120
С8н,8о Дибутиловый эфир 1 50 150 8,002 2106
С8Н18О2 1,1 '-[Этан-1,2-диилбис- 1 13 66 5,977 1381
(окси)]дипропан (дипроииловый эфир
этиленгликоля)
C8H18O3Si Винил(триэтокси)силан 2 61,1 148 7,44079 1735 220
C8H20O3Si Этил(триэтокси)силан 2 64,5 153 7,13148 1530 199
C8H20Pb Т етраэтилплюмбан 1 0 70 9,428 2938
с9
c9h7n Хинолин 1 180 240 7,969 2597
c9H8 Инден 1 56 181,8 7,919 2291
c9H10 1 -Винил-2-метилбензол 2 15 75 7,44611 1788,4 224
2 75 220 7,09235 1582,7 206
2 220 384,4 7,5014 1950 253
С9Ню 1-Винил-3-метилбензол 2 15 75 7,34229 1755,3 224
2 75 225 6,99468 1553,4 206
2 225 389,0 7,4053 1926 255
с9н10 1 -Винил-4-метилбензол 2 10 75 7,35420 1765,6 223,8
2 75 225 7,00589 1562,5 206
2 225 392,5 7,4170 1938,0 255
с9н10 Изопропенилбензол 2 15 70 7,26679 1680,13 219,6
(а-метилстирол) 2 70 220 6,92366 1486,88 202,4
2 220 381,7 7,3284 1847 250
С9Н]о Прон-1 -ен-1 -илбензол 2 25 75 7,26651 1694,73 218,3
ф-метил стирол) 2 75 225 6,92339 1499,80 201,0
2 225 389,5 7,3273 1862,6 250
С9Н,оО 1 -(4-Метилфенил)этанон 1 100 224,4 8,347 2719
С9Н10О Пропиофенон 2 25 115 7,54342 2012,9 216
2 115 350 7,21435 1800,5 198
С9НцВг 1 -Бром-4-изопропилбензол 2 131 210,2 7,41652 1996,8 230
С9н12 Кумол (изопропилбензол) 2 25 65 7,26890 1669,28 222,9
2 60 200 6,93666 1460,79 207,78
2 200 363 7,3445 1809,9 253,6
с9н12 Мезитилен 2 25 70 7,42169 1770,47 227,0
(1,3,5-триметилбензол) 2 70 210 7,07437 1569,62 209,58
2 210 368 7,4868 1935,7 256,0
254
Новый справочник химика и технолога
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал, °C А В С
от до
с9н12 1 -Метил-2-этилбензол 2 25 70 7,22202 1659,41 218,3
2 70 215 7,00314 1535,37 207,30
2 215 380 7,4134 1900,3 254,7
с9н12 1 -Метил-3-этилбензол 2 25 65 7,29569 1687,63 222,5
2 65 210 7,01582 1529,18 208,51
2 210 363 7,4264 1889,8 254,9
с9н12 1 -Мстил-4-этилбензол 2 25 70 7,30339 1700,72 224,2
2 65 210 6,99801 1527,11 208,92
2 210 363 7,4095 1889,3 255,7
с9н12 Пропил бензол 2 25 65 7,26890 1669,28 222,9
2 65 205 6,95142 1491,30 207,14
2 205 365 7,3599 1847,0 253,7
С9Н)2 1,2,3-Триметилбензол 2 25 80 7,37775 1792,86 224,4
(гемеллитол) 2 75 230 7,04082 1593,96 207,08
2 230 395 7,4536 1973,5 256,1
с9н12 1,2,4-Триметилбензол 2 25 75 7,38166 1770,01 225,7
(псевдокумол) 2 70 220 7,04383 1573,27 208,56
2 220 381,2 7,4565 1944,8 256,2
С9Н12О 2-(4-Метилфенил)этанол 1 67 204 9,908 3352
С9Н12О Пропоксибензол 2 101 189,9 7,45465 1920,0 230
С9Н12О 2-Фенилпропан-2-ол 2 118 192,6 8,01461 2212,0 230
С9Н|6 Нон-1-ин 2 50 223 6,77410 1404,7 210
С9Н16О 1 -Циклогексилпропан-1 -он 1 76 196 8,2379 2512,5
с9н18 Бутилциклопентан 2 10 65 7,2617 1649,8 221,9
2 65 190 6,9189 1460,0 205,0
2 190 346,0 7,30759 1814,5 253,5
С9Н18 Изопропилциклогексан 2 25 60 7,3199 1706,4 230
2 60 185 6,87257 1452,82 209,39
2 185 343 7,30519 1805,47 254
С9Н]8 Нон-1-ен 2 -70 173 6,95389 1435,36 205,54
2 173 321 7,1708 1518 211
С9Н|8 Пропилциклогексан 2 25 60 7,3199 1706,4 230
2 60 190 6,88866 1461,72 207,99
2 190 346,0 7,30759 1814,5 253,5
С9Н)8О 2,6 - Д и м ети л гептан -4 -он 2 60 180 6,94539 1476,40 195,0
С9Н18О Нонан-5-он 2 86 168,2 6,94539 1476,20 209,39
С9Н)8О2 Изобутилпентаноат 1 90 170 8,143 2323
С9Н20 Нонан 2 20 60 7,30801 1630,71 219,5
2 60 185 6,93513 1528,81 201,62
2 185 322 7,43583 1842,3 254,0
С9Н20О 2,6-Диметилгептан-4-ол 2 90 190 6,53806 1144,81 235,0
Сю
СюН8 Нафталин 1 -36 0 12,275 4000
2 10 НО 7,18400 1815,3 206,1
2 ПО 280 6,84577 1606,53 187,23
2 280 469,0 8,04266 2930,8 352,3
СюН8О 1 -Нафтол 1 99 203 8,907 3322
С10Н10О4 Диметилфталат 1 -20 30 11,50 4122
1 104 283,7 11,06 4113
СюН]2 1 -Винил-2-этилбензол 2 100 190 7,42883 1897,7 230
с мН i2 1 -Винил-3-этилбензол 2 100 190 7,44297 1917,9 230
СюН12 1 -Винил-4-этилбензол 2 ПО 200 7,45524 1931,6 230
СюН]2 1,2,3,4-Тетрагидро- 2 25 105 7,31568 1878,46 218
нафталин 2 105 265 6,96965 1662,4 199
(тетралин) 2 265 446 7,37894 2064,90 252
Физические свойства важнейших веществ
255
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал, °C А В С
от до
CioH^Br 2-Бром-1 -изопропил-4- 1 100 234,1 7,860 2525
метилбензол
С]оН|зВг 2-Бром-4-изопропил-1 - 1 53 234,3 8,053 2625
метилбензол
С10Н13С1 1 -Изопропил-4-метил-2- 1 100 216,5 7,906 2463
хлорбензол
С10Н13С1 4-Изопропил-1 -метил-2- 1 100 217,6 8,138 2579
хлорбензол
С]оН]4 Бутилбензол 2 25 85 7,33005 1783,05 219,4
2 85 220 6,98318 1557,97 201,38
2 220 386,1 7,38707 1937,9 257,1
СюН14 в/иор-Бутилбснзол 2 25 75 7,29582 1740,35 222,8
2 75 210 6,93033 1526,38 204,17
2 210 372,0 7,3566 1896,0 250,6
С10Н14 /ире/и-Бутилбензол 2 25 75 7,26343 1700,12 220,7
2 75 205 6,92050 1540,17 205,10
2 205 366,6 7,3229 1952,7 248,3
С]оН]4 1,2-Диэтилбензол 2 20 85 7,3375 1783,0 218,6
2 85 225 6,99016 1577,89 200,55
2 225 389,6 7,3918 1937,3 246,4
С10Н,4 1,3-Диэтилбензол 2 25 85 7,35433 1781,13 219,0
2 85 225 6,99016 1577,89 200,55
2 225 389,6 7,3918 1937,3 246,4
С)0Н|4 1,4-Диэтилбензол 2 25 85 7,34852 1795,83 220,1
2 85 225 7,00054 1589,27 202,02
2 225 387,3 7,4037 1949,7 247,7
С10Н14 Изобутилбензол 2 25 75 7,27388 1724,77 221,8
2 75 210 6,93033 1526,38 204,17
2 210 368,8 7,3324 1876,1 249,0
СюН]4 1 -Изопропил-2-метилбензол 2 17 179 7,41674 1880,47 236,27
(о-цимол)
СюН]4 1 -Изопропил-З-метилбензол 2 16 175 7,31903 1784,78 227,23
(jw-цимол)
С]оН]4 1 -Изопропил-4-метилбензол 2 19 178 7,03724 1599,29 207,66
(и-цимол)
С1оН]4 1,2,3,4-Тетраметилбензол 2 25 100 7,4100 1908,6 218,3
(пренитол)
2 100 250 7,0584 1689,10 199,28
2 250 426,9 7,4638 2074,7 248,1
С]оН]4 1,2,3,5-Тетраметилбензол 2 25 95 7,42969 1891,57 219,8
(изодурол) 2 95 240 7,0769 1674,00 200,94
2 240 413,6 7,48236 2052,4 248,4
С1оН14 1,2,4,5-Тетраметилбензол 2 25 95 7,4319 1888,21 220,0
(ДУРОЛ) 2 95 240 7,0790 1671,0 201,23
2 240 411,4 7,4845 2048,21 248,5
С10Н14О 2-/ирети-Бутилфенол 2 55 224 7,35275 1928,57 207,18
CjoHuO Бутоксибензол 2 118 210,2 7,51370 1916,0 230
С10Н14О 5-Изопропенил-2-метил- 1 82 230,8 8,247 2694
циклогекс-2-ен-1 -он
(карвон)
С10Н14О 2-Изопропи л-5-метилфенол 1 0 40 14,201 4766
(тимол)
СюН14О 2-(2-Этилфенил)этанол 2 20 147 7,85529 2279,03 210
2 147 380 7,53399 2055,2 192
256
Новый справочник химика и технолога
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал, °C А В С
от до
С10Н14О 2-(4-Этилфенил)этанол 2 20 147 7,80242 2251,25 209
2 147 380 7,48252 2029,3 191
C10H14N2 Никотин 1 102 247 8,0935 2695,5
c10h15n 4-Бутиланилин 2 25 140 7,43364 2011,5 201
2 140 370 7,29253 1917,28 193
С]оН16 2,2-Диметил-З-метилсн- 2 60 160 7,2159 1902,88 233,58
бицикло[2.2.1 ]гептан
(камфен)
С10Н |6 6,6-Диметил-2-метилсн- 2 50 90 8,1504 2280 273,2
бицикло[3.1,1 ]гентан
(0-пинен)
СюН]б 7,7-Диметил-З-метилен- 2 80 180 6,9895 1525,52 200,88
бицикло[4.1.0]гептан
(0-карен)
С мН if, (7?5)-4-Изопропенил-1 - 2 80 180 6,9858 1573,66 205,80
метилциклогексен
(дипентен, (±)-лимонен)
С10Н16 2,6,6-Триметилбицикло- 2 70 160 6,9619 1503,51 212,46
[3.1.1]гепт-2-сн
(а-пинен)
С10Н16О 1,7,7-Триметилбицикло- 1 -3 179 8,440 2652
[2.2.1]гсптан-2-он
(камфора)
С]ОН18 транс- Декагидро- 2 25 85 7,24657 1774,4 221
нафталин 2 85 225 6,90464 1570,3 203
(транс- декалин) 2 225 391 7,31068 1937,4 250
С]()Н |8 цис- Декагидронафталин 2 25 100 7,2780 1823 221
(г/ис-декалин) 2 100 235 6,92860 1609,6 202
2 235 404 7,16561 1921 260
С юН 18 Дсц-1 -ин 2 78 246 7,10870 1606,6 206,0
CjoHisO 2-(4-Метилциклогекс-3- 1 77 229 8,466 2740
ен-1 -ил)пропан-2-ол
(а-терпинеол)
С10Н20 Бутил циклогексан 2 20 82 7,29925 1776,1 223
2 82 240 6,91261 1539,45 200,88
2 240 372,6 7,58996 2187,8 285
С10Н20 Дец-1 -ен 2 25 233 6,96634 1501,87 197,58
2 233 343 7,8050 2317 302
С10Н20 Пентилциклопентан 2 15 85 7,272 1725 215
2 85 220 6,929 1526 197
2 220 366,0 7,405 1948 251
С10Н22 Декан 2 25 75 7,33883 1719,86 213,8
2 75 210 6,95367 1501,27 194,48
2 210 346 7,3363 1809,1 232,0
Си
СцН1о 1 -Метилнафталин 2 10 130 7,42128 2093,5 218,6
2 130 305 7,06899 1852,67 197,72
2 305 496 7,48224 2290,2 253,8
СцН1о 2-Метилнафталин 2 15 130 7,42076 2079,4 219,1
2 130 300 7,06850 1840,27 198,40
2 300 488,7 7,48161 2273,4 253,8
СцН[4 5-Метил-1,2,3,4- 2 25 125 7,38379 2010,1 214
тетрагидронафталин 2 125 280 7,03372 1778,9 194
2 280 470 7,43238 2187,1 246
Физические свойства важнейших веществ
257
Продолжение табл. 3.3.12
Формула Название Уравнение Температурный интервал, °C А В С
от до
син14 6-Метил-1,2,3,4- 2 25 120 136159 1982,5 215
тетрагидронафталин 2 120 270 7,01848 1754,5 195
2 270 460 7,42299 2156,8 246
СцН|6 Пентаметилбензол 2 20 125 7,49417 2072,1 219,4
2 125 280 7,13756 1833,8 199
2 280 452,1 7,5838 2284,2 252,4
СцН16 Пентилбензол 2 25 105 7,39800 1887,82 214,5
2 105 270 7,04709 1670,68 195,6
2 270 405,9 7,69926 2333,3 280,3
СцН22 Пентилциклогексан 2 20 99 7,28882 1850,6 219
2 99 260 6,96030 1647,3 201
2 260 394 7,62691 2319,2 287
СцН24 Ундекан 2 25 98 7,3225 1776,4 206
2 98 258 6,97674 1572,48 188,02
2 258 367 7,9352 2543,8 309,3
с12
c12h9n Карбазол 1 244 352 8,280 3380
c12h9ns Фенотиазин 1 40 140 9,265 4490
С|2Н ю Аценафтен 1 147 288 8,033 2835
С12Н10 Бифенил 2 160 325 7,2825 2037,0 207,23
С12н10о Дифениловый эфир 2 25 147 7,4531 2115,2 206,8
2 147 325 7,09894 1871,92 185,84
Ci2HioAsC1 Дифенил(хлор)арсин 1 25 75,0 7,8930 3288
C12H10CI2Si Дифенил(дихлор)силан 2 192,1 281 6,95480 1884 158
С]2Н i2 1-Этилнафталин 2 0 145 7,30532 2024,2 201,1
2 145 310 6,9599 1791,4 180,5
2 310 502,4 7,35228 2195.7 232,9
Ci2H12 2-Этилнафталин 2 15 145 7,4350 2131,1 212,2
2 145 305 7,0819 1886 191,0
2 305 498,0 7,3859 2308,7 243,8
с12н14о4 Диэтилфталат 1 17 50 11,712 4433
С]2Н]8 Гексилбензол 2 20 125 7,54230 2049,47 215,5
2 120 290 7,18284 1813,74 195,5
2 290 423,6 7,88933 2561,8 286,7
С12Н18 Г ексаметилбензол 2 165 265 7,7520 2427,70 234,88
С|2Н24 Г ексилциклогексан 2 20 117 7,32035 1940,4 215
2 117 275 7,00361 1735,7 197
2 275 412 7,66201 2412,9 282
С12Н24О2 Додекановая кислота (лауриновая кислота) 1 164 205 9,768 3885
Ci2H26 Додекан 2 25 150 7,3157 1830,0 198,3
2 150 280 6,98059 1625,93 180,31
2 280 386 8,0653 2780,0 322,0
С12НзоОз81з Г ексаэтилтрисилоксан 2 161,5 242,8 7,38317 1276 114
с13 С13Н ю Флуорен 2 150 300 7,3770 2321,23 218,27
С1зН)0О Бензофенон (дифенилке- 2 25 190 7,57278 2358,9 199
тон) 2 190 600 7,28937 2144,6 181
С]зНюО2 Фенилбензоат 1 106 228 8,328 3125
С.зНнС! 1,Г-(Хлор- 1 0 60 9,631 3680
метилен)дибензол (дифенил(хлор)метан)
258
Новый справочник химика и технолога
Продолжение табл. 3.3.12
Формула Название Уравнение Т емпературный интервал, °C А В С
от до
с13н12 1,1 '-(Метилен)дибензол 2 25 150 7,51935 2197,1 211,6
(дифенилметан) 2 150 310 7,16125 1944,42 190
2 310 494,4 7,60249 2410,9 246,8
С13н14 1 -Пропилнафталин 2 20 155 7,41108 2136,5 201,3
2 155 335 7,0594 1890,8 180
2 335 508 7,58084 2467,5 253,5
С13Н14 2-Пропилнафталин 2 20 160 7,41227 2141,9 201,4
2 160 335 7,0605 1895,5 180
2 335 506,9 7,58130 2470,1 252,9
Ci3H2o Гептилбензол 2 15 140 7,55112 2310,86 212,8
2 135 305 7,19114 1885,77 192,0
2 305 439,7 7,19109 2528,2 270,4
С]3Н28 Тридекан 2 25 131 7,3147 1881,7 190,9
2 131 302 6,9887 1677,34 172,90
2 302 404 8,1985 3013,2 333,4
с14
С14Н8О2 Антра-9,10-хинон 1 217 289 11,676 5405
1 289 370 8,002 3342
с14н10 Антрацен 1 30 100 11,15 5401
2 100 216,1 11,8345 4967,30 267,69
2 216,1 350 6,9645 2121,24 177,15
С14Н|о Фенантрен 2 200 340 6,7883 1934,64 155,02
С14Н12О2 Бензилбензоат 1 25 82 10,115 4057
с14н18о4 Дипропилфталат 1 23 217 11,66 4634
С]4Н22 Октилбензол 2 25 155 7,4693 2126,3 201
2 155 320 7,11415 1881,7 180,0
2 320 453,5 7,85374 2690 277
С)4Н28О2 Тетрадекановая кислота 1 30 80 20,35 7828
(миристиновая кислота) 1 190 244 9,541 3958
С14Н30 Тетрадекан 2 25 147 7,3143 1930,4 183,8
2 147 325 6,9957 1725,46 165,75
2 325 422 8,36982 3312,8 352,5
С15
Ci5H14O 1,3-Дифенилацетон 1 262 344 8,226 3226
С15н16о Ди(4-метилфенил)метанол 1 146 305 10,264 4267
с15н24 Нонилбензол 2 25 165 7,5503 2249,8 202
2 165 330 7,19041 1991,0 180
2 330 467,5 7,9653 2863 282
С15Н32 Пентадекан 2 25 160 7,3123 1973,3 176,6
2 160 338 7,0017 1768,82 158,60
2 338 437 8,5317 3600,5 369,1
с16
С]бНю Пирен 1 25 90 12,00 5248
С16Н22О4 Ди-ви?о/?-бутилфталат 1 134 210 12,15 4899
с,6н26 Децилбензол 2 25 185 7,6368 2381,6 203
2 185 345 7,27177 2107,7 180
С16Н32О2 Пальмитиновая кислота 1 45 100 22,65 8878
С16н34 Гексадекан 2 70 175 7,33309 2036,4 172,5
2 175 358 7,03044 1831,32 154,53
2 358 452 8,7725 4015,9 397,6
С17
С17Н36 Гептадекан 2 85 188 7,3095 2052,2 163,5
2 188 374 7,0115 1847,82 145,52
2 374 462 8,9220 4310,1 414,4
Физические свойства важнейших веществ
259
Окончание табл. 3.3.12
Формула Название Уравнение Температурный интервал, °C А В С
от до
С18 CisH|5As С18Н26О4 С|8Н38 Трифениларсин Дипснтилфталат Октадекан 1 1 2 2 2 220 160 25 201 387 290 246 201 387 477 8,954 12,04 7,3094 7,0156 9,1876 3953 5191 2088,9 1883,73 4810,2 157,5 139,46 449,57
С19 с19н40 Нонадекан 2 2 2 25 212 403 212 403 487 7,31561 7,0192 9,4412 2127,54 1917,0 5302 152 133,5 482
С20 С20Н30О4 С2оН38 С20Н40 С20Н42 Дигексилфталат ЭЙКОЗ-1-ИН Эйкоз-1-ен Эйкозан 1 2 2 2 2 2 2 176 219 223 405 25 224 417 265 431 405 486 224 417 502 11,98 7,52336 6,859 9,50720 7,30970 7,0225 9,6945 5381 2386,3 1807,9 5591 2155,78 1948,7 5807 174 113 505 146 127,8 513
с21 С2|Н2]О4Р С21Н21О4Р Трис(3-метилфенил)фосфат Трис(4-метилфенил)фосфат 1 1 210 210 243 266 12,22 12,22 5895 5826
с24 С24Н42 Г ексапропилбензол 2 180 335 8,7550 3556,78 272,17
С26 C26H]8 С2бН4б 9,10-Дифенилантрацен Эйкозилбензол 1 2 2 75 25 295 145 295 500 13,283 8,0889 7,69708 6024 3178,3 2812,7 183,5 155
Сзо С30Н58 СзоНбо Триаконт-1-ин Триаконт-1-ен 2 2 304 313 545 545 7,60053 7,61184 2813,0 2850,4 155 154,5
Сзб СзбЩб Т риаконтилбензол 2 2 25 375 375 580 8,52362 8,10600 3849,6 3406,8 172 140
Сзв С38Н30 Этан-1,1,1,2,2,2-гексаил-гексабензол (гексафенилэтан) 1 75 120 12,87 5987
Давление насыщенного пара ртути
В табл. 3.3.13 и 3.3.14 приведены данные по давлению насыщенного пара ртути при Т = 1004-358 °C и при Т — 350-4-675 °C соответственно.
Таблица 3.3.13
Давление насыщенного пара ртути (кПа) при температуре от 100 до 358 °C
Температура, °C
Десятки Единицы
0 2 4 6 8
100 0,036 0,04 0,045 0,049 0,053
110 0,06 0,067 0,074 0,081 0,09
120 0,098 0,108 0,119 0,13 0,266
260
Новый справочник химика и технолога
Окончание табл. 3.3.13
Температура, °C
Десятки Единицы
0 2 4 6 8
130 0,156 0,171 0,187 0,204 0,223
140 0,243 0,264 0,288 0,313 0,34
150 0,369 0,4 0,434 0,47 0,508
160 0,562 0,594 0,508 0,692 0,746
170 0,804 0,866 0,932 1,003 1,075
180 1,157 1,241 1,332 1,427 1,529
190 1,637 1,751 1,872 2,001 2,137
200 2,282 2,434 2,596 2,766 2,946
210 3,136 3,337 3,553 3,769 4,008
220 4,256 4,516 4,79 5,078 5,381
230 5,7 6,033 6,386 6,751 7,138
240 7,542 7,971 8,415 8,879 9,37
250 9,882 10,42 10,97 11,56 12,17
260 12,8 13,46 14,15 14,88 15,63
270 16,42 17,24 18,08 18,97 19,92
280 20,87 21,88 22,92 24,01 25,13
290 26,31 27,52 28,78 30,1 31,46
300 32,87 34,33 35,85 37,42 39,06
310 40,75 42,49 44,32 46,21 48,14
320 50,16 52,22 54,38 56,58 58,89
330 61,26 66,38 54,22 68,69 71,53
340 74,34 77,19 80,15 83,22 86,34
350 89,63 92,98 96,41 99,95 103,6
Таблица 3.3.14
Давление насыщенного пара ртути при температуре от 350 до 675 °C
Температура, °C Давление, МПа Температура, °C Давление, МПа Температура, °C Давление, МПа
350 0,09 465 0,529 575 1,81
355 0,098 470 0,564 580 1,904
360 0,107 475 0,601 585 1,991
365 0,117 480 0,639 590 2,087
370 0,128 485 0,68 595 2,186
375 0,139 490 0,723 600 2,288
380 0,152 495 0,767 605 2,394
385 0,164 500 0,814 610 2,505
390 0,179 505 0,863 615 2,617
395 0,193 510 0,914 620 2,733
400 0,209 515 0,968 625 2,853
405 0,226 520 1,021 630 2,977
410 0,244 525 1,079 635 3,106
415 0,263 530 1,142 640 3,238
420 0,284 535 1,205 645 3,374
425 0,305 540 1,268 650 3,514
430 0,329 545 1,34 655 3,658
440 0,378 550 1,41 660 3,807
445 0,405 555 1,484 665 3,96
450 0,434 560 1,561 670 4,117
455 0,464 565 1,641 675 4,277
460 0,495 570 1,724
Давление насыщенного пара диоксида углерода
В табл. 3.315-3.3.18 представлена информация по давлению диоксида углерода (твердого и жидкого), аммиака и серы в зависимости от температуры; в табл.
3.3.19-3.3.22 приведены данные по давлению насыщенного пара в равновесии с водой, переохлажденной водой и со льдом, а также данные по температуре кипения воды при высоких давлениях.
Физические свойства важнейших веществ
261
Таблица 3.3.15
Давление насыщенного пара твердого диоксида углерода
Температура, °C
Десятки Единицы
-8 -6 I 4 _ -2 0
Давление, Па
-180 6,67 • 10”5 1,47 • 10"4 4,00- 10 4 8,00 • 10 4 0,00173
-170 0,00347 0,00693 0,0133 0,0267 0,0493
-160 0,0893 0,159 0,28 0,48 0,787
-150 1,31 2,11 3,35 5,23 8,07
-140 12,3 18,4 27.2 39,7 57,5
-130 0,0813 0,116 0,163 0,224 0,308
-120 0,417 0,563 0,751 0,995 1,31
-110 1,71 2,21 2,85 3,64 4,62
-100 5,83 7,31 9,12 11,3 14,0
-90 17,2 21,0 25,5 31,0 37,3
-80 44,8 53,5 63,8 75,8 89,6
-70 105 124 146 170 198
-60 230 267 309 356 410
-50 471
Давление насыщенного пара (МПа) жидкого диоксида углерода
Таблица 3.3.16
Температура, °C
Десятки Единицы
-8 -6 -4 -2 0 2 4 6 8
-50 -40 -30 -20 -10 0 10 20 30 0,487* 0,741 1,08 1,53 2,1 2,8 0,532 0,802 1,16 1,63 2,22 2,96 0,579 0,866 1,25 1,74 2,36 3,0 0,63 0,934 1,34 1,85 2,5 3,3 0,684 1,01 1,43 1,97 2,65 3,49 4,5 5,73 7,21 3.67 4,5 5,73 7,21 3,87 4,73 6,0 4,07 4,96 6,29 4,28 5,21 6,58
* Переохлажденная жидкость.
Давление насыщенного пара (МПа) аммиака
Таблица 3.3.17
Ткр = 132,4 °C; дкр = 11,67 МПа; = 4,26 см3/г.
Температура, ЭС
Десятки Единицы
-9 -8 -7 —6 -5 —4 -3 -2 -1 0
-70 0,0059 0,00639 0,00692 0,00748 0,00808 0,00872 0,00941 0,0101 0,0109
-60 0,0117 0,0126 0,0136 0,0146 0,0156 0,0167 0,0179 0,0192 0,0205 0,0219
-50 0,0234 0,0249 0,0266 0,0283 0,0302 0,0321 0,0341 0,0363 0,0385 0,0409
-40 0,0434 0,046 0,0487 0,0515 0,0545 0,0577 0,061 0,0644 0,068 0,0718
-30 0,0757 0,0798 0,0841 0,0885 0,0932 0,199 0,103 0,108 0,114 0,12
-20 0,126 0,132 0,138 0,145 0,152 0,159 0,166 0,174 0,182 0,19
-10 0,199 0,208 0,217 0,226 0,236 0,247 0,257 0,268 0,279 0,293
0 0,303 0,315 0,328 0,341 0,355 0,369 0,383 0,398 0,414 0,429
Десятки 0 1 2 3 4 5 6 7 8 9
0 0,429 0,446 0,462 0,48 0,497 0,516 0,534 0,554 0,574 0,594
10 0,615 0,636 0,657 0,681 0,704 0,728 0,753 0,778 0,804 0,83
20 0,857 0,885 0,913 0,942 0,972 1,0 1,03 1,07 1,1 1,13
262
Новый справочник химика и технолога
Окончание табл. 3.3.17
Десятки 0 1 2 3 4 5 6 7 8 9
30 1,17 1,2 1,24 1,27 1,31 1,35 1,39 1,43 1,47 1,51
40 1,55 1,6 1,64 1,69 1,73 1,78 1,83 1,88 1,93 1,98
50 2,03 2,09 2,14 2,2 2,25 2,31 2,37 2,43 2,49 2,55
60 2,63 2,68 2,74 2,81 2,88 2,95 3,02 3,09 3,16 3,24
70 3,31
80 4,14
90 5,12
100 6,26
110 7,58
120 9,12
130 10,9
Таблица 3.3.18
Давление насыщенного пара (Па) серы и ее модификаций
Температура, К S S2 S4 S6 s8 is
300 7,85 • 10 5 3,05 • 10" 3,84- 10"
320 9,33 • 10" 0,00328 0,00421
340 0,00853 0,0295 0,0393
360 0,0627 0,213 0,279
380 0,313 1,33 1,64
400 1,16 • 10"9 0,048 0,0012 1,55 4,84 6,39
450 3,0 • 10"6 0,212 0,00964 26,1 77,3 103
500 1,59 • 10"3 0,724 1,81 189 511 700
550 2,65 • 10” 9,88 20,8 1080 2610 3730
600 1,87- 10’9 81,7 147 3450 7650 11 300
650 6,73 • 10’8 453 720 10 800 21 600 33 600
700 1,44 • 10* 2200 3000 26 100 47 300 78 700
Таблица 3.3.19
Давление насыщенного водяного пара (Па) в равновесии с водой
Температура, °C
Де-сят-ки Единицы
0 1 2 3 4 5 6 7 8 9
0 0,8371 0,8923 0,9595 1,0295 1,1049 1,1850 1,2704 1,3610 1,4572 1,5595
10 1,6680 1,7830 1,9050 1,9875 2,1713 2,3162 2,4696 2,6320 2,8033 2,9846
20 3,1765 3,3778 3,5911 3,8164 4,0536 4,3042 4,5668 4,8441 5,1360 5,4426
30 5,7652 6,1051 6,4610 6,8356 7,2288 7,6421 8,0740 8,5285 9,0041 9,5030
40 10,024 10,571 11,438 11,742 12,369 13,025 13,708 14,424 15,172 15,952
50 16,766 17,617 18,503 19,428 20,392 21,396 22,441 23,532 24,666 25,847
60 27,073 28,353 29,686 31,059 32,498 33,992 35,538 37,151 38,817 40,550
70 42,349 44,216 46,162 48,161 50,241 52,400 54,626 56,946 59,332 61,811
80 64,371 67,023 69,769 72,608 75,541 78,567 81,670 84,939 88,285 91,737
90 95,296 98,975 102,77 106,69 110,73 114,89 119,20 123,62 128,18 132,89
100 127,73 142,72 147,86 153,15 158,60 164,20 169,97 175,90 182,00 189,62
НО 195,82 201,36 208,19 215,20 222,40 229,80 238,47 245,19 253,20 261,43
120 269,86 278,53 287,41 296,53 305,88 315,47 325,30 335,38 345,71 356,31
130 367,16 378,28 389,68 401,37 414,70 425,49 438,02 450,82 463,88 477,48
140 491,21 505,21 519,60 534,40 549,46 564,79 580,52 596,65 613,05 629,84
150 647,04 664,50 682,50 700,76 719,42 738,48 757,94 777,94 798,33 819,00
160 840,06 861,65 883,78 906,17 795,80 952,56 976,42 1000,7 1025,5 1050,8
170 1076,5 1102,9 1129,7 1156,9 1184,7 1213,16 1241,96 1271,4 1301,4 1331,9
180 1363,0 1394,6 1426,7 1459,6 1493,1 1527,08 1561,61 1596,8 1632,6 1669,2
190 1706,2 1743,9 1782,4 1821,4 1861,1 1901,5 1942,6 1981,6 2026,7 2069,9
Физические свойства важнейших веществ
263
Окончание табл. 3.3.19
Де-сят-ки Единицы
0 1 2 3 4 5 6 7 8 9
200 2113,7 2158,4 2203,7 2249,7 2296,5 2344,1 2392,5 2441,5 2491,4 2542,0
210 2593,5 2645,7 2698,8 2752,8 2807,4 2862,9 2919,4 2970,0 3034,8 3093,8
220 3153,7 3214,5 3276,1 3338,8 3402,2 3466,7 3532,1 3598,4 3665,6 3733,9
230 3803,2 3873,3 3944,5 4016,7 4089,9 4164,2 4239,3 4315,6 4392,9 4471,4
240 4550,8 4631,5 4713,1 4795,9 4888,1 4964,6 5050,7 5138,0 5226,4 5316,0
250 5406,6 5498,6 5592,0 5686,6 5781,2 5878,5 5975,8 6075,8 6175,8 6277,1
260 6381,1 6485,0 6590,3 6697,0 6804,9 6915,6 7026,2 7138,2 7251,5 7366,2
270 7483,5 7600,8 7719,4 7840,7 7962,0 8086,0 8211,3 8337,9 8465,9 8595,2
280 8725,8 8857,8 8992,4 9127,1 9264,4 9403,0 9542,9 9662,4 9828,2 9973,5
290 10 120 10 268 10417 10 570 10 723 10 877 11 035 11 193 И 353 11 512
300 И 678 11 843,7 12012 12 181 12 352 12 524 12 698 12 875 13 054 13 234
310 13 415 13 599 13 786 13 974 14 163 14 355 14 550 14 746 14 944 15 144
320 15 347 15 550,8 15 758 15 965 16 176 16 389 16 566 16 821 17 041 17 262
330 17 486 17 713 17 982 18 173 18 502 18 642 18 837 19 121 19 363 19 608
340 19 856 20 107 20 359 20 615 20 874 21 133 21 397 21 664 21 932 22 204
350 22 478 22 755,6 23 036 23 317 23 603 23 838 24 185 24 480 24 778 25 078
360 25 383 25 689,6 26 002 26 315 26 633 26 955 27 278 27 608 27 940 28 276
370 28617 28 960,8 29310 29 663 30 022
Таблица 3.3.20
Давление насыщенного водяного пара (кПа) в равновесии с переохлажденной водой
Температура, °C
Десятки Единицы
-9 -8 -7 -6 -5 -4 -3 -2 -1 0
-10 0 0,3092 0,3344 0,3615 0,1753 0,3903 0,1905 0,4209 0,2067 0,4537 0,2245 0,4891 0,2434 0,5268 0,2638 0,5673 0,2857 0,6104
Таблица 3.3.21
Давление насыщенного водяного пара (Па) в равновесии со льдом
Температура. °C
Десятки Единицы
-9 -8 -7 -6 -5 -4 -3 -2 -1 0
-50 1,0664 1,1997 1,4663 1,7329 1,9995 2,2661 2,5327 2,9326 3,3325 3,8657
-40 4,3989 4,9321 5,5986 6,2651 6,9316 7,7314 8,7978 9,8642 11,0639 12,3969
-30 13,996 15,862 17,862 19,995 22,261 24,660 27,326 30,259 33,592 37,324
-20 41,456 45,988 51,054 56,626 62,784 69,449 76,781 84,779 93,443 102,908
-10 113,305 124,635 136,899 149,696 165,025 180,888 198,084 216,879 237,274 259,402
0 283,262 309,389 337,516 368,041 400,966 436,691 475,348 517,071 561,993 610,381
Таблица 3.3.22
Температура кипения воды при высоких давлениях
Давление, МПа Т’кип, °C Давление, МПа ткип, °C Давление, МПа тКИ11, °C Давление. МПа ткип, °C Давление, МПа Тки.,, °C Давление, МПа Гк„„, °C
0,049 80,9 0,490 151,1 0,980 179,0 1,470 197,4 1,960 211,4 2,450 222,9
0,098 99,1 0,588 158,1 1,078 183,2 1,568 200,4 2,058 213,9 2,548 225,0
0,196 119,6 0,686 164,2 1,176 187,1 1,666 203,4 2,156 216,2 2,646 227,0
0,294 132,9 0,784 169,6 1,274 190,7 1,764 206,1 2,254 218,5
0,392 142,9 0,882 174,5 1,372 194,1 1,862 208,8 2,352 220,8
264
Новый справочник химика и технолога
3.4. Критические величины и константы Ван-дер-Ваальса
В табл. 3.4.1 и 3.4.2 приведены критические значения температур Т^, давлений ркр и плотностей ркр простых веществ, неорганических и органических соединений.
Таблица 3.4.1
Критические температуры, давления, плотности простых веществ и неорганических соединений
Формула Название ?;Р, °с /?кр. МПа Ркр • Ю-3. кг/м3
Аг Аргон -122,5 4,86 0,531
ВВг3 Бора трибромид 300 0,90
ВС13 Бора трихлорид 178,8 3,87
BF3 Бора трифторид -12,3 4,99
В2Н6 Диборан 16,5 3,69
Вг> Бром 311 10,3 1,18
(CN)2 Оксалонитрил (дициан) 126,6 5,9
со Углерода монооксид -140,3 3,5 0,301
со2 Углерода диоксид 31,0 7,39 0,468
cos Углерода оксид-сульфид 105 6,18
cs2 Углерода дисульфид 279 7,9 0,44
(сероуглерод)
С12 Хлор 144 7,71 0,573
f2 Фтор -129 5,57
GeCl4 Т етрахлоргерман 276,9 3,85
HBr Водорода бромид 90,0 8,51 0,807
HCN Водорода цианид 183,5 5,39 0,195
HC1 Водорода хлорид 51,4 8,26 0,42
HF Водорода фторид 188 6,93
HI Водорода иодид 151,0 8,31
H2 Водород -239,9 1,3 0,031
H2H (2Н)Водород (дейтероводород) -237,2 1,48
H3H (3Н)Водород -234,9 1,66
2H, СН2)Водород (дидейтерий) -234,8 1,65
’H2 (3Н2)Водород (дитритий) -232,6 1,83
2H3H (2Н3Н)Водород (дейтеротритий) -233,7 1,75
H2O Вода 374,2 22,1 0,32
2H2O (2Н2)Вода (тяжелая вода) 370,9 22,2
H2S Водорода сульфид 100,4 9,01 0,349
H2Se Водорода селенид 137 9,22
He Г слий -267,9 0,229 0,0693
3He (3Не)Гелий -269,8 0,117
Hg Ртуть 1450
12 Иод 553
Kr Криптон -63,8 5,5 0,908
NH3 Аммиак 132,4 и,з 0,235
NO Азота(П) оксид -92,9 6,55 0,52
NOCI Нитрозилхлорид 165 9,36
n2 Азот -147,0 3,39 0,311
n2h4 Г идразин 380 14,7
n2o Азота(1) оксид 36,5 7,27 0,452
n204 Диазота тетраоксид 158 10,0 0,56
Ne Неон -227,7 2,73 0,484
o2 Кислород -118,4 5,08 0,41
O3 Озон -12,1 5,53 0,54
PF3 Фосфора трифторид -10 4,05
PH3 Фосфин (фосфан) 51,3 6,54 0,30
PH4C1 Фосфония хлорид 49,1 7,37
Rn Радон 104,3 6,32
s Сера 1040 11,8 0,403
Физические свойства важнейших веществ
265
Окончание табл. 3.4.1
Формула Название 7’кр, °C ркр, МПа Ркр- кг3, кг/м3
SF6 Серы гексафторид 45,6 3,76 0,75
so2 Серы диоксид 157,5 7,88 0,524
so3 Серы триоксид 218,2 8,49 0,633
Sbl3 Сурьмы трииодид 445 0,233
SeF4 Селена тетрафторид 290
SiClF3 Т рифтор(хл ор)сил ан 34,8 3,47
SiCl2F2 Дифтор(дихлор)силан 95,8 3,5
SiCl3F Фтор (трихл ор)с и л ан 165,3 3,58
SiCl4 Тетрахлорсилан 233 3,76
SiF4 Тетрафторсилан -14,1 3,72
SiH4 Силан -3,5 4,84
SnCl4 Т страхлорстаннан 318,7 3,75 0,742
UF6 Урана гексафторид 230,2 4,61
Xe Ксенон 16,6 5,9 1,105
Таблица 3.4.2 Критические температуры, давления, плотности органических соединений
В каждой группе соединений вещества расположены по эмпирическим формулам по возрастанию числа атомов углерода, а при одинаковом числе атомов углерода — по возрастанию числа атомов водорода.
Формула Название Т °C ' кр* Ркрч МПа Ркр ' Ю \ кг/м3
Углеводороды
СН4 Метан -81,1 4,64 0,162
с2н2 Ацетилен 36 6,24 0,231
с2н4 Этилен 9,9 5,12 0,227
С2н6 Этан 32,3 4,88 0,203
С3н4 Пропин 128 5,35
С3н6 Пропен (пропилен) 91,8 4,62 0,233
С3н6 Циклопропан 124,6 5,49
С3н8 Пропан 96,8 4,26 0,220
С4н6 Бута-1,3-диен (дивинил) 152 4,33 0,245
С4н6 Бут-1-ин 190,5
с4н6 Бут-2-ин 215,5
С4н8 Бут-1 -ен 146,4 4,02 0,234
С4н8 Бут-2-ен 157 4,15 0,238
с4н8 2-Метилпропен (изобутилен) 144,7 4 0,235
с4н]0 Бутан 152,0 3,8 0,228
с4н10 Изобутан 134,9 3,65 0,221
с5н8 Циклопентен 231 4,55 0,227
С5Н1О 2-Метилбут-2-ен 197 3,45
CjHjo Пент-1-ен 201 4,05
С5Н,о Пент-2-ен 202,4 4,09
с5н12 Пентан 196,6 3,37 0,232
С5н12 2-Метилбутан (изопентан) 187,7 3,41 0,236
С5Н12 2,2-Диметилпропан (неопентан) 160,6 3,2 0,238
С6н6 Бензол 289,5 4,92 0,300
с6н10 Циклогексен 286 4,24 0,288
С6н12 Метилциклопентан 259,6 3,79 0,264
С6н)2 Циклогексан 281,0 4,11 0,272
С6н14 Г ексан 234,7 3,03 0,234
С6н14 2,2-Диметилбутан 216,2 3,11 0,240
СбН14 2,3 - Димети лбутан 227,1 3,13 0,241
С6Н14 2-Метилпентан (изогексан) 224,7 3,03 0,235
266
Новый справочник химика и технолога
Продолжение табл. 3.4.2
Формула Название Т °C 1 кр* /4р, МПа Ркр- Ю 3, кг/м3
Углеводороды
с7н8 Толуол 320,8 4,22 0,29
с7н14 Этилциклопентан 296,3 3,39 0,262
С7Н14 1,1 -Диметилциклопентан 277 3,55 0,28
С7н14 рац-( 1 R,2R)-1,2-Диметилциклопентан 282 3,45 0,27
С7н]4 (1 R,2S)~ 1,2-Диметилциклопентан 282 3,45 0.27
С7Н14 рац-( 1 R,3 R)-1,3 -Димети лци клопентан 282 3,55 0,28
с7н14 (1 /?,3S)-1,3-Диметилциклопентан 282 3,45 0,27
С7н14 Метилциклогексан 299,1 3,48 0,285
С7н16 Гептан 267,0 2,74 0,235
С7н16 2,2-Диметилпентан 247,7 2,88 0,248
С7н16 2,3-Диметилпентан 264,6 2,96 0,247
С7н16 2,4-Д и мети л пе нта н 247,1 2,78 0,239
С7Н16 3,3-Димстилпентан 263 3,04
С7н|6 2-Мстилгексан 257,9 2,83 0,234
С7Н16 З-Метилгексан 262,4 2,85 0,240
С7Н16 2,2,3-Триметилбутан 258.3 2,82 0,254
С7н16 3-Этилпентан 267,6 2,9 0,241
С8Н1О л/-Ксилол 346,0 3,55 0,27
с8н10 о-Ксилол 359,0 3,65 0,28
С8Н|о и-Ксилол 345,0 3,45 0,29
С8Н,0 Этилбензол 346,4 3,75 0,29
С8н18 2,2-Диметилгексан 279 2,59 0,245
С8н18 2,3-Диметилгексан 293 2,7 0,248
с8н18 2,4-Диметилгсксан 282 2,61 0,245
с8н18 2,5 - Д иметилгексан 276,8 2,49 0,237
с8н18 3,3 - Димети л ге кс ан 291 2,76 0,254
с8н|8 3,4-Д иметилгексан 298 2,78 0,253
с8н18 2-Метилгептан 288 2,51 0,234
С8н18 З-Метилгептан 292 2,59 0,239
С8н18 4-Метилгептан 290 2,59 0,240
С8н18 2-Мстил-З-этилпентан 295 2,78 0,254
С8н18 3 -Метил-3 -этилпентан 305 2,93 0,263
с8н18 Октан 296,7 2,49 0,233
с8н|8 2,2,3,3 -Т етраметилбутан 270,8 2,48 0,238
с8н18 2,2,3-Триметилпентан 294 2,86 0,261
с8н]8 2,2,4-Триметилнентан 271,1 2,58 0,24
c8Hi8 2,3,3-Триметилпентан 303 2,94 0,264
С8н18 2,3,4-Триметилпентан 295 2,8 0,256
с8н18 З-Этилгексан 294 2,67 0,245
с9н12 Кумол (изопропилбензол) 362,7 3,24 0,28
с9н12 Мезитилен (1,3,5-триметилбензол) 368 3,34 0,28
С9Н12 1 -Метил-2-этилбензол 380 3,14 0,28
С9н12 1 -Метил-З-этилбензол 363 3,14 0,28
С9Н12 1 -Метил-4-этилбснзол 363 3,14 0,28
С9н,2 Пропилбензол 365,6 3,24 0,28
с9н12 1,2,3-Триметилбензол (гемеллитол) 395 3,14 0,28
С9н12 1,2,4-Триметилбензол (псевдокумол) 381,2 3,34 0,28
С9Н20 Нонан 322 2,28 0,236
С10Н8 Нафталин 469,0 3,98 0,314
С1оН]2 1,2,3,4-Тетрагидронафталин 446 3,52 0,309
(тетралин)
СюН]4 Бутилбензол 386,1 2,83 0,268
С1он14 ewop-Бутилбензол 273,0 2,73 0,263
С1он14 wpew-Бутилбе нзол 366,6 2,73 0,274
Физические свойства важнейших веществ
267
Продолжение табл. 3.4.2
Формула Название 7’кр, °C Р^, МПа Ркр - ЮЛ кг/м3
с10н14 1,2-Диэтилбензол 389,6 2,96 0,274
С10Н14 1,3-Диэтилбензол 383,9 3,93 0,287
СюН14 1,4-Диэтилбензол 387,3 2,87 0,281
С1он,4 Изобутилбензол 377 3,14 0,274
С10Н14 1,2,3,4-Тетраметилбензол (пренитол) 426,9 3,27 0,308
С10Н14 1,2,3,5-Тетраметилбензол (изодурол) 413,6 3,21 0,308
с10н14 1,2,4,5-Тетраметилбензол (дурол) 411,4 3,2 0,306
СюН18 транс-Декагидронафталин 391 2,61 0,254
(трш/с-декалин)
С1оН18 цис-Декагидронафталин 404 2,49 0,24
(г/мс-декалин)
С10Н22 Декан 346 2,11 0,236
СцН16 Пентилбензол 405,9 2,65 0,284
СИН24 Ундекан 367 1,95 0,237
с12н26 Додекан 386 1,81 0,237
С1зН28 Тридекан 404 1,72 0,24
С]4Нзо Тетрадекан 422 1,62 0,24
С15Н32 Пентадскан 437 1,52 0,24
с16н34 Гсксадекан 452 1,42 0,24
С17Н36 Гептадекан 462 1,32 0,24
с18н38 Октадекан 477 1,32 0,24
С19Н40 Нонадекан 487 1,22 0,24
C2qH42 Эйкозан 502 1,11 0,24
Галогенпроизводные углеводородов
CCIF3 Трифторхлорметан (фреон-13) 28,8 3,95 0,58
cci2f2 Дифтордихлорметан (фреон-12) 111,5 4,01 0,555
cchF Фтортрихлорметан (фреон-11) 198,0 4,38 0,554
СС14 Т етрахлорметан 283,2 4,56 0,558
CHC1F2 Дифторхлорметан (фреон-22) 96,4 4,91 0,525
chci2f Фтордихлорметан (фрсон-21) 178,5 5,17 0,552
СНС13 Хлороформ 263.4 5,47 0,50
СН2С12 Дихлорметан 237 6,08
СН3Вг Бромметан 191
СН3С1 Хлорметан 143,1 6,68 0,353
CH3F Фторметан 44,6 5,88 0,300
CH3I Иодметан 255
C2C1F3 Трифторхлорэтилен 106 4,05 0,55
c2ci2f4 1,1,1,2-Т етрафтор-2,2-дихлорэтан 145,5 3,3 0,582
C2HC1F2 1,1 -Дифтор-2-хлорэтилсн 127,4 4,46 0,499
c2h2f2 1,1 -Дифторэтилен 30,1 4,44 0,417
C2H3C1F2 1,1 -Дифтор-1 -хлорэтан 137,1 4,12 0,435
C2H3F3 1,1,1-Трифторэтан 73,1 3,76 0,434
C2H4C12 1,1 -Дихлорэтан 250 5,07
С2Н4СЬ 1,2-Дихлорэтан 288 5,37 0,44
C2H4F2 1,1 -Дифторэтан 113,5 4,5 0,365
C2H5Br Бром этан 230,7 6,23 0,507
C2H5C1 Хлорэтан 187,2 5,27 0,33
C2H5F Фторэтан 102,2 4,66
C3H7C1 1 -Хлорпропан 230 4,58
С6Н3С1з 1,2,4-Трихлорбензол 461,8 3,98 0,472
C6H4Br2 1,2-Дибромбензол 486,6 4,22 0,645
С6Н4С12 1,2-Дихлорбензол 424,1 4,1 0,408
С6Н4С12 1,3-Дихлорбензол 410,8 3,88 0,415
С6Н4С12 1,4-Дихлорбензол 411,6 3,9 0,395
С6Н5Вг Бромбензол 397 4,52 0,485
С6Н5С1 Хлорбензол 359,2 4,52 0,365
268
Новый справочник химика и технолога
Продолжение табл. 3.4.2
Формула Название Т °C 1 кр* v р^, МПа Ркр- 10-’, кг/м3
Галогенпроизводные углеводородов
c6h5f Фторбензол 286,9 4,55 0,357
С6Н51 Иодбензол 448 4,52 0,581
c7h5f3 (Трифторметил)бензол 289,5 3,56 0,427
Спирты и простые эфиры
СН4О Метанол 240 7,95 0,272
С2Н6О Диметиловый эфир 126,9 5,37 0,242
с2н6о Этанол 243 6,38 0,276
С3Н8О Метоксиэтан 164,7 4,4 0,272
С3Н8О Пропан-1 -ол 264 5,09 0,273
С3Н8О Пропан-2-ол 235,6 5,37 0,274
с4н10о Бутан-1 -ол 287,0 4,92
С4Н]оО Бутан-2-ол 265
С4Н10О Диэтиловый эфир 194 3,61 0,264
С4И10О 2-Метилпропан-1 -ол 265 4,86
С4Н10О 2-Метилпропан-2-ол 235
С5Н12О 1-Этоксипропан 227,4 3,25 0,260
С6н6о Фенол 419,2 6,13 0,401
с7н8о о-Крсзол 422 5,01 0,375
с7н8о .м-Крезол 426 4,8 0,357
с7н8о н-Крсзол 426,0 4,66 0,347
с7н8о Анизол 369 4,18
c8Hi0o Этоксибензол (фенетол) 374 3,42
Альдегиды и кетоны
С9Н4О Ацетальдегид 188
С3Н6О Ацетон 235,5 4,72 0,273
С4Н8О Бутан-2-он 260 4 0,25
Карбоновые кислоты, сложные эфиры, ангидриды и нитрилы
c2h3n Ацетонитрил 274,7 4,83 0,237
с2н4о2 Метилформиат 214,0 6,0 0,349
С2Н4О2 Уксусная кислота 321,6 5,79 0,351
c3h5n Пропиононитрил 291,2 4,19 0,240
С3Н6О2 Метилацетат 33,7 4,69 0,325
СзН6О2 Пропионовая кислота 339 5,37 0,32
СзН6О2 Этилформиат 235.3 4,74 0,323
С4Н6О3 Уксусный ангидрид 296 4,68
С4Н6О4 Диметилоксалат 260 0,963
c4h7n Бутиронитрил 309,1 3,79
С4Н8О2 Изомасляная кислота 336 4,05 0,302
С4Н8О2 Масляная кислота 355 5,27 0,304
с4н8о2 Метилпропионат 257,4 3,98 0,312
С4Н8О2 Пропилформиат 264,9 4,06 0,309
С4Н8О2 Этилацетат 250,1 3,83 0,308
С5Н10О2 Изобутилформиат 278,2 3,88
С5Н10О2 Метилбутират 281,3 3,48 0,300
с5н10о2 Пентановая кислота 378
(валериановая кислота)
CsHkjO? Пропилацетат 276,2 3,33 0,296
С5Н10О2 Этилпропионат 272,9 3,34 0,296
c5hun Пентаннитрил (капронитрил) 348,8 3,25
С6Н12О2 Изобутилацетат 288 3,14 0,281
С6Н12О2 Метилпентаноат 294 3,24 0,279
С6Н12О2 Этилизобутират 280 3,04 0,276
С6Н12О2 Этилбутират 293 3,04 0,276
Физические свойства важнейших веществ
269
Окончание табл. 3.4.2
Формула Название Ткр,°С ркр, МПа Ркр’ ЮЛ кг/м3
C7H5N Бензонитрил 426,2 4,22
N-содержащие соединения
CH3NO2 Нитрометан 315 6,31 0,352
ch5n Метанамин (метиламин) 156,9 7,46
c2h7n УУ-Метилметанамин (диметиламин) 164,5 5,31
c2h7n Этанамин (этиламин) 183 5,62
C3H9N N,N- Диметилметанамин (триметиламин) 160,1 4,07 0,233
c3h9n Пропан-1-амин (пропиламин) 223,8 4,74
C4H]]N ДУ-Этил этанам ин (диэтиламин) 223 3,71 0,246
c5h5n Пиридин 344,2 6,08
c6h7n Анилин 426 5,31 0,314
c6h15n А,А-Диэтилэтанамин (триэтиламин) 259 3,04 0,251
c6h15n А-Пропилпропан-1 -амин (дипропиламин) 277 3,14
S-содержащие соединения
CH4S Метантиол 196,8 7,23 0,323
C2H6S Димстилсульфид 229,9 5,53 0,309
C2H6S Этантиол 226 5,49 0,300
c3H8s (Метилсульфанил)этан 260 4,26
C4H4S Тиофен 317 4,86 0,34
c4HI0s Диэтилсульфид 284 3,96 0,279
Прочие соединения
CC12O Карбонилдихлорид (фосген) 182 5,67 0,52
C2H4O Оксиран (окись этилена) 195 7,19 0,32
C4H8O2 1,4-Диоксан 312 5,14 0,36
Уравнение Ван-дер-Ваальса:
\(V-b) = RT.
В табл. 3.4.3 приведены значения констант а (см3 • атм) и b (см3), вычисленные из критических данных для объема, занимаемого моль при давлении 1 атм и температуре О °C (1 см’ для идеального газового состояния).
Таблица 3.4.3
Константы Ван-дер-Ваальса
Название Формула a b
Простые вещества и неорганические соединения
Азот n2 0,00277 0,001747
Азота(1) оксид n2o 0,00754 0,001971
Азота(П) оксид NO 0,00267 0,001245
Аммиак NH3 0,00831 0,001655
Аргон Ar 0,00268 0,001437
Вода H2O 0,01089 0,001362
Водород H2 0,00487 0,001188
Водорода бромид HBr 0,00887 0,001978
Водорода селенид H2Se 0,01050 0,002070
Водорода сульфид (сероводород) H2S 0,00883 0,001914
Водорода хлорид HC) 0,00731 0,001822
Гелий He 0,000068 0,001058
Диазота тетраоксид N2O4 0,01053 0,001975
270
Новый справочник химика и технолога
Продолжение табл. 3.4.3
Название Формула a b
Простые вещества и неорганические соединения
Кислород о2 0,00271 0,001421
Криптон Кг 0,00462 0,001776
Ксенон Хе 0,00816 0,002279
Неон Ne 0,000422 0,000763
Радон Rn 0,01293 0,002770
Ртуть Hg 0,01613 0,000757
Серы диоксид so2 0,01338 0,002516
Силан SiH4 0,00861 0,002583
Т етрахлоргерман GeCl4 0,04504 0,006630
Тетрахлорсилан SiF4 0,00836 0,002487
Т етрахлорстаннан SnCl4 0,05363 0,007332
Углерода диоксид co2 0,00716 0,001905
Углерода монооксид co 0,00296 0,001779
Углерода дисульфид (сероуглерод) cs2 0,02316 0,003431
Фосфин (фосфан) PH3 0,00923 0,002302
Фосфония хлорид PH4C1 0,00808 0,002029
Хлор ci2 0,01294 0,002510
Органические соединения
Анилин c6h7n 0,05282 0,006113
Ацетилен C,H2 0,00875 0,002293
Ацетон c3H6d 0,02774 0,004437
Ацетонитрил c2h3n 0,03277 0,005216
Бензол c6H6 0,03588 0,005150
Бромбензол C6H5Br 0,05692 0,006872
Бутан c4H10 0,02884 0,005472
Бутан-1 -ол C4H10O 0,03394 0,005103
Бутиронитрил c4h7n 0,05125 0,007126
Г ексан c6H14 0,04928 0,007850
Гептан c7H16 0,06280 0,011850
А,А-Диметиланилин C8HhN 0,02069 0,003826
А,А-Диметилметанамин c3h9n 0,02594 0,004841
(триметиламин)
Диметиловый эфир c2H6o 0,02381 0,004369
Диэтиловый эфир C4HWO 0,03464 0,006002
А,А-Диэтилэтанамин (триэтиламин) c6h15n 0,05415 0,008176
Изобутан C4H,o 0,02564 0,005098
Изобутилацетат C6H12O2 0,05680 0,008185
Иодбензол C6H5I 0,06592 0,007395
л/-Крезол c7H8o 0,6592 0,007395
Метан CH4 0,00449 0,001910
Метанамин (метиламин) ch5n 0,01421 0,002675
Метанол CH4O 0,02998 0,002992
Метантиол CH4S 0,02564 0,004113
Метилацетат C3H6O2 0,03047 0,004870
2-Метилбутан (изопентан) C5H12 0,03651 0,006409
Метилбутират c5h]0o2 0,05083 0,007407
Метилизобутират CsHi0O2 0,004883 0,007308
А-Метилметанамин (диметиламин) c2h7n 0,02069 0,003826
Метил пропионат C4H8O2 0,04027 0,006145
Метилформиат C2H4O2 0,02266 0,003764
Нафталин C10H8 0,07923 0,008648
Оксалонитрил (дициан) C2N2 0,01528 0,003081
Октан CsHjg 0,07440 0,010570
Пентан C5H12 0,03788 0,006516
Нентилформиат c6H12o2 0,05496 0,007724
Пропан c3H8 0,001727 0,003693
Физические свойства важнейших веществ
271
Окончание табл. 3.4.3
Название Формула а b
Пропан-1-амин (пропиламин) c3h9n 0,02988 0,004865
Пропан-1-ол С3Н8О 0,02395 0,03753
Пропан-2-ол с3н8о 0,02747 0,004377
Пропен с3н6 0,01670 0,003693
Пропилацетат С5Н10О2 0,05144 0,007577
У-Пропилпропан-1 -амин c6hI5n 0,05524 0,008124
(дипропиламин)
Пропилформиат С4Н8О2 0,04086 0,006144
Пропионовая кислота СзН6О2 0,04008 0,005297
Пропиононитрил c3h5n 0,03277 0,004750
Т етрахлорметан СС14 0,03892 0,005661
Тиофен C4H4S 0,04130 0,005670
Толуол с7н8 0,04795 0,006533
Уксусная кислота С2Н4О2 0,03505 0,004767
Уксусный ангидрид С4Н60з 0,03967 0,005639
Фторбензол c6h5f 0,03972 0,005742
Хлорбензол С6Н5С1 0,05068 0,006485
Хлорметан CH3C1 0,01489 0,002894
Хлороформ СНС13 0,03023 0,004562
1 -Хлорпропан СзН7С1 0,03170 0,005098
Хлорэтан С2Н5С1 0,02174 0,003862
Циклогексан С6Н,2 0,04347 0,006359
Этан С2Н6 0,01074 0,002848
Этанамин (этиламин) c2h7n 0,02113 0,003754
Этанол С2н6о 0,02395 0,03753
Этилацетат С4Н8О2 0,04776 0,006303
Этилбутират СбН12О2 0,05993 0,008567
Этилен С2Н4 0,00891 0,002551
Этилизобутират С6Н12О2 0,05754 0,008410
Этилпропионат С5Н10О2 0,04861 0,007209
Этилформиат СзН6О2 0,02949 0,004714
У-Этилэтанамин (диэтиламин) С4Н]^ 0,03816 0,006216
3.5. Теплоемкость
Во всех таблицах настоящего раздела приняты следующие условные обозначения:
ам. — аморфный
бел. — белый
возг. — возгоняется
г. — газообразный
ж. — жидкий
желт. — желтый
кр. — критический
красн. — красный
крист. — кристаллический
куб. — кубический
металл. — металлический
монокл. — моноклинный
октаэдр. — октаэдрический
оранж. — оранжевый
переохл. — переохлажденный
плавл. — плавленый
разл. — разлагается
раств. — растворимый
ромб. — ромбический
сер. — серый
стекл. — стеклообразный
тв. — твердый
тетрагон. — тетрагональный
черн. — черный
Удельная теплоемкость ср простых веществ и неорганических соединений
Теплоемкость тела (системы) — отношение количества теплоты, поглощенного системой, к соответствующему повышению температуры.
Истинную теплоемкость с определяют при условии, что повышение температуры бесконечно мало:
с^.
dl
Среднюю теплоемкость с определяют при условии повышения температуры на конечную величину:
272
Новый справочник химика и технолога
Теплоемкость единицы массы вещества называют удельной теплоемкостью (Дж/(г • К), одного моля — молярной теплоемкостью (Дж/моль • К).
Различают теплоемкость при постоянном объеме cv и теплоемкость при постоянном давлении ср", в первом случае в процессе нагревания вещества поддерживается постоянным его объем, во втором случае — давление; ср всегда больше cv, т. к. в случае нагревания при постоянном давлении часть теплоты идет на работу расширения вещества, а часть — на увеличение его внутренней энергии, в то время как в случае нагревания при постоянном объеме вся теплота расходуется только на увеличение внутренней энергии. Для твердых и жидких веществ разность между ср и cv мала. Для идеальных
газов Ср - cv = R, где R — универсальная газовая постоянная.
В табл. 3.5.1 приведены удельные теплоемкости ср простых веществ и неорганических соединений при температурах 10-298,15 К. Табл. 3.5.2 содержит коэффициенты уравнения ср = а + ЬТ- сТ2, позволяющего вычислить ср простых веществ и неорганических соединений при более высоких температурах.
В отдельных таблицах приведены удельные теплоемкости воды и водяного пара (табл. 3.5.3-3.5.6), органических соединений в твердом и жидком агрегатном состояниях (табл. 3.5.7 и 3.5.8), некоторых веществ в газообразном состоянии (табл. 3.5.9-3.5.22), а также удельная и молярная теплоемкости ртути (табл. 3.5.23).
Таблица 3.5.1
Удельная теплоемкость ср (Дж/(г • К)) простых веществ и неорганических соединений при температуре 10-298,15 К
Значения ср относятся к веществам, находящимся в твердом состоянии, за исключением случаев, отмеченных индексами «ж» (для жидкостей) и «г» (для газов).
Вещество Температура, К
10 25 50 100 150 200 298,15
Ag 0,0021 0,0193 0,108 0,187 0,213 0.225 0,237
AgBr 0,0126 0,0829 0,179 0,243 0,26 0,257 0,279
AgCl 0,0118 0,0862 0,193 0,292 0,327 0,347 0,355
Agl 0,026 0,0729 0,134 0,195 0,213 0,222 0,232
AgIO3 0,0067 0,0498 0,127 0,226 0,287 0,328 0,372
AgNO2 0,0176 0,0942 0,21 0,351 0,42 0,466 0,52
AgNO3 0,0184 0,0888 0,211 0,332 0,419 0,47 0,553
Ag2CO3 0,0075 0,0599 0,155 0,257 0,315 0,355 0,408
Ag2CrO4 0,014 0,0762 0,162 0,266 0,332 0,377 0,429
Ag2O 0,0195 0,095 0,153 0,196 0,225 0,252 0,285
Ag2SO4 0,0117 0,0754 0,17 0,265 0,318 0,361 0,422
Al 0,0017 0,0178 0,143 0,481 0,691 0,8 0,904
A1Cs(SO4)2 • 12H,0 0,0147 0,0879 0,2386 0,4605 0,6866 0,8164 1,0928
A12O3 0,0004 0,0021 0,018 0,132 0,329 0,509 0,775
Ar 0,0754 0,393 0,649 0,519г 0,519г 0,519г 0,519г
As 0,0017 0,0197 0,105 0,223 0,276 0,304 0,329
As2O3 0,0054 0,0456 0,101 0,206 0,308 0,386 0,481
As2O5 0,0004 0,0092 0,048 0,172 0,289 0,38 0,508
Au 0,0026 0,0261 0,073 0,108 0,121 0,125 0,128
BF3 0,046 0,244 0,53 0,787 1,521ж 0,62г 0,746г
B4C < 0,0004 < 0,0004 0,008 0,093 0,266 0,498 0,952
Ba(BrO3)2 • H2O 0,0067 0,054 0,154 0,291 0,384 0,448 0,539
BaCO3 0,0028 0,0344 0,115 0,256 0,325 0,37 0,432
BaCl2 • 2H2O 0,0063 0,0544 0,175 0,364 0,468 0,542 0,636
BaF2 0,0021 0,026 0,103 0,252 0,333 0,377 0,407
Ba(NO3)2 0,0071 0,0645 0,197 0,365 0,439 0,491 0,579
BaSO4 0,0031 0,0356 0,129 0,247 0,311 0,381 0,438
Be <0,0021 0,0042 0,025 0,188 0,586 1,105 1,98
BeO < 0,0008 0,0033 0,017 0,117 0,318 0,574 1,017
Bi 0,0105 0,0465 0,085 0,109 0,117 0,12 0,122
Bi2O3 0,0046 0,0265 0,065 0,135 0,175 0,208 0,244
Br2 0,0389 0,2156 0,494 0,55 0,615 0,674 0,461ж
С (алмаз) <0,0021 <0,0021 < 0,0021 0,021 0,088 0,201 0,507
С (графит) <0,0021 0,0126 0,039 0,138 0,264 0,419 0,72
Физические свойства важнейших веществ
273
Продолжение табл. 3.5.1
Вещество Температура, К
10 25 50 100 150 200 298,15
c2n2 0,0234 0,2181 0,565 0,921 1,164 1,412 1,048г
СО 0,1172 0,8164 1,549 l,043r l,043r 1,043, 1,043,
со2 0,0172 0,2035 0,582 0,904 1,093 0,737r 0,846г
cos 0,0356 0,2659 0,528 1,048 1,205ж 1,182ж 0,695г
cs2 0,0331 0,2206 0,435 0,608 0,733 0,9672ж 0,9889ж
Са 0,0046 0,0628 0,2721 0,4857 0,5736 0,6196 0,6573
СаСО2, (арагонит) 0,0017 0,0264 0,1231 0,3936 0,5635 0,6703 0,8131
СаСОз (кальцит) 0,0021 0,0322 0,1562 0,3915 0,5568 0,6665 0,8194
СаС2О4 • Н2О 0,0031 0,0418 0,1746 0,44 0,6389 0,7926 1,0463
CaF2 0,0004 0,0109 0,0858 0,3823 0,5937 0,7176 0,0852
СаО < 0,0004 0,0042 0,0461 0,2889 0,4857 0,6196 0,9002
CaS 0,0013 0,0197 0,1172 0,3584 0,5066 0,5862 0,6594
CaSO4 (ангидрит) 0,0017 0,0193 0,1189 0,3404 0,4815 0,5878 0,7335
CaSO4 • 2Н2О (гипс) 0,0034 0,0389 0,1851 0,4647 0,6691 0,8114 1,0881
Са3(РО4)2 (а) 0,0011 0,0247 0,1164 0,283 0,4752 0,5887 0,7469
Са3(РО4)2 (₽) 0,0013 0,0212 0,1101 0,2793 0,4664 0,5811 0,7415
Cd 0,0084 0,0636 0,1453 0,198 0,2135 0,2211 0,2307
CdO 0,0008 0,0167 0,0783 0,1892 0,2625 0,3061 0,3287
Cl2 0,0188 0,2135 0,4145 0,5945 0,7197 0,9412ж 0,4773г
СоС12 0,0092 0,1214 0,1507 0,3563 0,4639 0,5296 0,605
Сг 0,0008 0,0042 0,0377 0,1926 0,3174 0,3873 0,448
СгС12 0,0205 0,0984 0,1758 0,2952 0,3701 0,4111 0,4455
СгС13 0,1302 0,3165 0,4367 0,5074 0,569
Сг2О3 0,0004 0,0039 0,0303 0,1591 0,3362 0,4953 0,7947
CsCIO3 0,0159 0,1034 0,2219 0,304 0,3504 0,3831 0,4605
Си 0,0008 0,0155 0,098 0,2525 0,3211 0,3546 0,3835
СиО 0,0008 0,0147 0,0795 0,2102 0,3291 0,4438 0,5317
CuS (ковелин) 0,0038 0,0553 0,1591 0,2973 0,3898 0,4438 0,5024
Си2О 0,0167 0,1013 0,1909 0,278 0,332 0,3747 0,4291
Cu2S 0,0147 0,0804 0,1834 0,3148 0,3898 0,4325 0,4798
Fe 0,0008 0,0084 0,0511 0,211 0,3236 0,3869 0,448
FeCO3 (сидерит) 0,0017 0,0366 0,1323 0,3462 0,4869 0,5778 0,7097
FeCl2 0,0272 0,0971 0,1947 0,399 0,5141 0,5799 0,6557
FeO 0,0013 0,0138 0,0846 0,3412 0,5828 0,6837 0,7252
FeS 0,0025 0,0348 0,1344 0,3408 0,4689 0,5401 0,6222
FeS2 (пирит) 0,0004 0,0029 0,0251 0,1612 0,3483 0,4107 0,5179
Fe2O3 0,0013 0,0176 0,0749 0,201 0,3525 0,479 0,5254
Fe3C 0,0008 0,0109 0,0745 0,2437 0,3714 0,4953 0,5903
Fe3O4 0,0013 0,0155 0,0674 0,2453 0,4049 0,5037 0,6209
Ga 0,0088 0,0502 0,1499 0,2801 0,3291 0,3521 0,373
HBr 0,0327 0,175 0,291 0,1280 0,5807 0,7369ж 0,3638,
HCN 0,0184 0,2081 0,6573 1,2435 1,5575 1,8548 2,6293ж
HC1 0,027 0,2441 0,5234 1,0886 1,3105 0,7997, 0,7997,
HI 0,0335 0,1319 0,2177 0,3421 0,355 0,3743 0,2278г
H2O 0,1717 0,4396 0,8834 1,2225 1,5659 4,191ж
2H2O 0,1758 0,4312 0,8918 1,344 1,7668 4,3459ж
H2S 0,0234 0,2311 0,5652 1,1514 1,6538 1,9929ж 1,0006,
Hf 0,0006 0,0071 0,0913 0,1269 0,1361 0,1407 0,144
Hg 0,023 0,0657 0,1047 0,1231 0,1298 0,1369 0,1386ж
HgO 0,0037 0,0375 0,0833 0,1331 0,162 0,1784 0,2114
Hg2SO4 0,0067 0,0569 0,1089 0,1595 0,1943 0,2227 0,2659
h 0,0155 0,0846 0,1453 0,1813 0,1959 0,2056 0,2173
К 0,0544 0,3232 0,5359 0,6322 0,6699 0,695 0,7453
KBr 0,2935 0,3542 0,3902 0,4157 0,4518
KBrO3 0,0064 0,0687 0,2177 0,3898 0,4815 0,5434 0,6289
KCI 0,0059 0,0729 0,2834 0,5275 0,6117 0,6506 0,6912
274
Новый справочник химика и технолога
Продолжение табл. 3.5. /
Вещество Температура, К
10 25 50 100 150 200 298,15
КС1О3 0,0071 0,0932 0,3031 0,52 0,6184 0,7 0,8248
КС1О4 0,0138 0,0896 0,2868 0,4727 0,5585 0,6439 0,8018
КЮ3 0,0058 0,0565 0,1712 0,3065 0,3848 0,4338 0,4982
КМпОз 0,0155 0,1143 0,2751 0,4459 0,5552 0,636 0,7444
KNO3 0,0075 0,0862 0,3195 0,5983 0,6682 0,7909 0,9584
Кг 0,0729 0,2215 0,3006 0,3776 0,2487r 0,2487,. 0,2487r
Li 0,0167 0,0963 0,5987 1,8506 2,5707 2,9852 3,4122
LiH <0,0021 0,0167 0,1214 0,875 2,1227 3,0522 0,1675
Ы2СО3 0,0025 0,0289 0,1738 0,5234 0,8332 1,0861 1,4578
Mg 0,0017 0,0327 0,2428 0,649 0,8457 0,9253 0,9839
MgCO3 (магнезит) 0,0004 0,0084 0,0565 0,2948 0,5217 0,6883 0,8968
MgO < 0,0004 0,0029 0,023 0,2119 0,4647 0,6783 0,9378
Mg(OH)2 0,0013 0,013 0,0846 0,3701 0,7034 0,978 1,3251
MgSiO3 0,0017 0,0163 0,0842 0,219 0,3592 0,5229 0,8081
Mn 0,0013 0,013 0,0892 0,2721 0,3655 0,4271 0,4773
MnCO3 0,0013 0,0218 0,1043 0,3153 0,4672 0,5694 0,7105
(родохрозит)
MnCl2 0,0084 0,0528 0,1758 0,3961 0,497 0,5581 0,6314
MnO 0,0025 0,0318 0,1478 0,4647 0,4731 0,5359 0,6071
MnO2 0,0013 0,0142 0,0934 0,2872 0,3864 0,4986 0,6582
MnSe 0,0025 0,0382 0,1583 0,3278 0,371 0,3957 0,3818
MnTe 0,0034 0,0388 0,1256 0,2311 0,2767 0,3065 0,3994
МП3О4 0,0021 0,0197 0,1017 0,2834 0,4317 0,538 0,659
Mo 0,0004 0,0059 0,041 0,1394 0,1964 0,2223 0,2453
MoS2 0,0004 0,0088 0,0486 0,1499 0,2567 0,3287 0,3973
n2 0,1587 0,9713 1,4863 l,0383r l,0383r 1,0383r l,0383r
NH3 0,0147 0,1633 0,6531 1,5366 2,2902 4,1868ж 2,1561,
NH4CI 0,0398 0,0502 0,2927 0,718 0,9818 1,3063 1,6509
NO 0,0389 0,3295 0,7118 1,2016 1,0383, 1,0132, 0,9965r
N2O 0,0218 0,2165 0,6238 0,9462 1,1597 0,762r 0,8792r
n2o4 0,0151 0,1465 0,4007 0,6619 0,8353 0,9994 1,5470ж
n2o5 0,198 0,8386 1,009 1,323
Na 0,0255 0,2621 0,6992 0,9839 1,0802 1,1388 1,2393
Na2CO3 0,0063 0,0729 0,2437 0,5702 0,7712 0,8813 1,0438
NaCl 0,0029 0,0414 0,2734 0,6029 0,7218 0,7942 0,8537
NaHCO3 0,0025 0,0322 0,2026 0,5489 0,7398 0,8675 1,0442
NaNO3 0,0057 0,0758 0,2864 0,6129 0,7792 0,8901 1,1053
Na2SO4 0,0021 0,036 0,1876 0,4698 0,6322 0,7453 0,8964
Na2SO4 • 10H2O 0,0092 0,0955 0,3215 0,7327 1,0383 1,2895 1,838
Ne 0,3098 l,0341r
Ni 0,0008 0,0092 0,0712 0,2311 0,3308 0,3839 0,4396
NiCl2 0,008 0,0494 0,1746 0,3722 0,4827 0,5393 0,6008
NiO 0,0004 0,0063 0,0435 0,1922 0,3295 0,4522 0,5945
o2 0,0795 0,695 1,4403 0,9085r 0,9085r 0,9085, 0,9085r
PH3 0,0394 0,3278 1,3314 1,3775 1,792ж 0,9965r l,0928r
PH4I 3,295 0,4291 0,4936 0,5472
Pb 0,0134 0,0678 0,1034 0,1181 0,1223 0,1256 0,1294
PbBr2 0,0162 0,0791 0,1717 0,234 0,2575 0,2675 0,2793
PbCO3 (церуссит) 0,0092 0,0536 0,1181 0,2068 0,252 0,2801 0,3274
РЬС12 0,0117 0,0657 0,152 0,216 0,2449 0,2604 0,2763
PbO 0,0043 0,0366 0,0749 0,1269 0,1608 0,1846 0,2177
PbO2 0,0013 0,0182 0,0678 0,1323 0,183 0,2198 0,2709
PbS 0,0063 0,0502 0,108 0,165 0,1867 0,1972 0,2077
PbSO4 0,005 0,0481 0,1218 0,2018 0,2491 0,286 0,3433
Pb3O4 0,1888 0,2441 0,283 0,3174
Pb3(PO4)3 0,0062 0,0409 0,1034 0,1792 0,2286 0,2663 0,3157
Физические свойства важнейших веществ
275
Окончание табл. 3.5.1
Вещество Температура, К
10 25 50 100 150 200 298,15
Pt 0,0013 0,0138 0,0544 0,1009 0,1185 0,1273 0,1365
RbC103 0,0075 0,0745 0,2366 0,3785 0,4656 0,5434 0,6117
S (ромб.) 0,013 0,113 0,2311 0,3998 0,515 0,6071 0,7034
S (монокл.) 0,2311 0,4044 0,5275 0,628 0,7369
SF6 0,0448 0,2031 0,3308 0,4007 0,5137 0,7155 0,6619г
so2 0,0184 0,1784 0,4815 0,7486 0,9035 1,3147ж 0,628г
Sb 0,0021 0,0276 0,103 0,1691 0,1909 0,198 0,2077
Sb2O3 0,0033 0,031 0,0791 0,1725 0,2412 0,2927 0,3479
Sb2O4 0,0036 0,0315 0,0733 0,152 0,2353 0,2747 0,3726
Sb2O5 0,0008 0,0133 0,0511 0,1641 0,2391 0,2943 0,3634
Se 0,0096 0,059 0,134 0,2311 0,2755 0,2977 0,3144
Si < 0,0008 0,0084 0,0712 0,26 0,4291 0,5594 0,7076
SiC < 0,0004 < 0,0004 0,0059 0,1068 0,2533 0,407 0,6657
SiO2 (а-кварц) 0,0021 0,0264 0,0963 0,2596 0,4166 0,5455 0,7411
SiO2 (кристобалит) 0,0033 0,0406 0,1089 0,265 0,4208 0,5485 0,7369
SiO2 (плавл.) 0,0042 0,0394 0,1139 0,2692 0,4111 0,5409 0,074
SiO2 (тридимит) 0,0033 0,0406 0,1118 0,2721 0,4271 0,5568 0,744
Sm2(SO4)3 • 8H2O 0,004 0,044 0,1566 0,3559 0,5024 0,6238 0,8277
Sn (бел.) 0,008 0,0582 0,1298 0,1888 0,2068 0,2148 0,2223
Sn (cep.) 0,0105 0,0435 0,116 0,165 0.1922 0,2052 0,2177
SnCl4 0,3877 0,461 0,5074 0,6343ж
SnO 0,0017 0,0188 0,0837 0,1825 0,2466 0,2897 0,3295
SnO2 0,0004 0,0071 0,0431 0,1386 0,2186 0,2805 0,3496
SrCO3 (стронцианит) 0,0017 0,0205 0,1114 0,3006 0,404 0,4677 0,5518
SrO 0,0013 0,0155 0,0846 0,2336 0,3303 0,3864 0,4346
Ta 0,0013 0,0138 0,0603 0,111 0,1269 0,1336 0,1398
TaC 0,0006 0,008 0,0427 0,0967 0,1256 0,1516 0,1909
Ta2O5 0,0008 0,0115 0,0502 0,1315 0,1955 0,2433 0,3061
Те 0,0067 0,0507 0,1164 0,1696 0,1859 0,1934 0,2014
TI (a) 0,0167 0,0699 0,1026 0,1197 0,1239 0,1264 0,129
T1C1 0,0109 0,0754 0,1407 0,1863 0,2022 0,211 0,2202
T1NO3 0,0197 0,0804 0,1624 0,2449 0,2801 0,3094 0,3735
V 0,0008 0,0105 0,0795 0,2659 0,3797 0,4354 0,4857
V2O3 0,0008 0,0096 0,0519 0,1918 0,4078 0,5388 0,6891
v2o4 0,0008 0,01 0,0586 0,2223 0,4015 0,5112 0,7063
v2o5 0,0013 0,018 0,1047 0,286 0,4425 0,556 0,7013
W 0,0004 0,0046 0,0335 0,0888 0,1139 0,1256 0,1361
Xe 0,062 0,1507 0,1909 0,2156 0,2567 0,1583г 0,1583,
Zn 0,0033 0,0494 0,17 0,2939 0,3446 0.3718 0,3806
ZnCO3 (смитсонит) 0,0008 0,0167 0,0867 0,2742 0,4145 0,5091 0,6351
ZnO 0,0008 0,0184 0,0955 0,2181 0,3178 0,3969 0,494
ZnS 0,0021 0,031 0,1189 0,2529 0,3542 0,4078 0,4731
Таблица 3.5.2
Удельная теплоемкость ср(Дж/(г • К)) простых веществ и неорганических соединений при температуре выше О °C
В таблице приведены коэффициенты уравнения ср = а + b - сТ2 (Т — абсолютная температура), температурный интервал его применимости и погрешность результатов, получаемых при расчетах по этому уравнению.
Вещество Состояние а - 102 Ь- 105 с- 10 3 Погрешность, % Интервал температур, °C
Ag AgBr ТВ. ж. ТВ. ж. 22,32 31,82 19,13 33,24 4,91 31,40 0,23 0,5 3 5-7 5 0-961 961-1300 0^30 430-563
276
Новый справочник химика и технолога
Продолжение табл. 3.5.2
Вещество Состояние а - 102 ь- ю5 с - 10 3 Погрешность. % Интервал температур, °C
AgCl ТВ. 28,05 27,13 2 0^455
ж. 41,03 5 455-533
Agl ТВ. 15,28 25,12 5-7 0-150
AgNO3 тв. (а) 46,47 39,44 2 0-160
тв.(Р) 63,43 5 160-209
ж. 74,52 5 209-268
Ag2S тв. (а) 22,32 28,43 2 1-175
тв. (Р) 32,95 5,73 2 175-572
Al ТВ. 74,52 49,82 1 0-658,6
ж. 108,86 5 658,6-10000
AlBr3 ТВ. 29,39 29,26 3 0-97,5
ж. 46,26 5 97,5-134
A1C13 ТВ. 41,57 87,92 3 0-192,5
ж. 97,97 3 192,5-231
ai2f6 ТВ. 77,04 55,26 3 0-927
A1I3 ТВ. 17,33 23,28 3 0-191
A12O3 ТВ. 107,93 17,37 30,39 1 0-1500
Al2SiO5 (андалузит) ТВ. 113,67 4,97 28,09 3 0-1300
AI2SiO5 (дистен) ТВ. 108,02 13,65 31,32 2 0-1400
Al2SiO5 (силлиманит) ТВ. 105,38 12,33 25,66 3 0-1300
Ar г. 5,19 0 Все температуры
выше 0
As ТВ. 28,93 13,06 5 0-895
Au ТВ. 12,06 2,68 1 0-1063
ж. 14,86 5 1063-1300
В ТВ. 59,45 169,98 5 0-900
BN ТВ. 54,30 134,81 5 0-900
BaCO3 ТВ. 42,41 19,59 3 0-810
BaF2 ТВ. 40,61 9,55 5 0-1000
BaSO4 ТВ. 37,80 25,16 5 0-1050
Be ТВ. 217,84 72,14 56,14 1 0-900
BeO ТВ. 139,84 58,69 50,41 5 0-902
Bi ТВ. 11,01 4,89 1 0-271
ж. 15,24 5 271-1000
Bi2O3 ТВ. 20,89 9,92 2 0-504
Br2 г. 23,28 0,43 0,74 0,5 27-1327
С (алмаз) ТВ. 73,69 148,67 45,47 3 0-1040
С (графит) ТВ. 93,36 91,27 40,74 2 0-1100
CO г. 98,81 17,96 2 0-2200
CO2 г. 98,35 25,12 18,58 1,5 0-900
Ca тв. (а) 55,39 34,83 2 0^400
ТВ. (Р) 65,69 14,61 2 400-600
CaCO3 ТВ. 82,39 49,78 12,88 3 0-760
CaF2 ТВ. 92,95 20,64 13,14 5 0-1217
CaO ТВ. 88,51 5,73 12,28 2 0-1500
CaO • A12O3 • 2SiO2 ТВ. 101,36 15,78 28,38 1 0-700
(стекло)
CaO • MgO • SiO2 ТВ. 137,66 25,89 34,75 1 0-700
(стекло)
CaSiO3 (волластонит) ТВ. 100,69 7,40 26,85 1 0-1300
CaSiO3 (псевдоволла- ТВ. 92,11 14,90 17,59 1 0-1400
стонит)
CaSiO3 (стекл.) ТВ. 83,31 34,82 17,56 1 0-700
Ca3(PO4)2 тв. (а) 65,56 54,89 8,41 2 0-1100
ТВ.(Р) 113,33 5 1100-1298
CaSO4 ТВ. 56,94 25,62 4,81 5 0-1100
Физические свойства важнейших веществ
277
Продолжение табл. 3.5.2
Вещество Состояние а - 102 ь- ю5 с - 10 3 Погрешность, % Интервал температур. °C
Cd ТВ. 18,25 9,17 1 0-321
ж. 26,54 5 321-700
CdCl2 ТВ. 41,78 9,73 3,99 3 0-598
Cl2 г. 51,83 1,47 3,56 1 0-1200
Со ТВ. 36,42 23,69 5 0-1490
Сг ТВ. 38,98 23,74 5 0-1550
Си ТВ. 38,68 6,58 1,90 1 0-1084
ж. 49,32 3 1084-1300
СиС12 ТВ. 52,33 26,46 5 0-500
СиО ТВ. 56,81 17,42 6,79 2 0-977
Cu2S тв. (а) 24,70 82,06 3 0-103
тв. (Р) 55,01 2 103-900
CuSO4 ТВ. 67,57 11,30 5,65 5 0-600
F2 г. 98,55 3,31 9,92 1,5 0-1700
Fe тв. (а) 30,94 47,94 3 0-777
тв. (р) 86,25 89,89 2 777-908
ТВ.(у) 52,46 29,98 2 908-1401
тв.(8) 82,48 5 1401-1530
FeO ТВ. 73,48 8,70 4,44 2 0-900
Fe2O3 ТВ. 64,73 42,08 11,09 2 0-824
Fe3O4 ТВ. 74,52 34,08 17,73 2 0-792
Ge ТВ. 26,67 13,06 5 0-440
H2 г. 1381,64 143,19 1,5 0-3200
HBr г. 33,95 5,73 1 0-1700
HCN г. 157,13 32,24 38,39 1 0-1500
HC1 г. 75,57 11,25 1,5 0-1700
HF г. 138,58 14,65 2 0-1700
HI г. 21,48 3,93 1 0-1200
H2O ж. 422,86 0,5 0-100
г. 167,47 62,80 1 100-1700
H2S г. 85,20 46,05 1 0-1000
He г. 520,42 0 Все температуры
выше 0°
Hg ж. 13,77 1 0-357
г. 10,34 0 Все температуры
выше 0°
In ТВ. 20,55 11,39 1 0-232,3
Ir ТВ. 11,93 3,21 1 0-1600
IrO2 ТВ. 17,12 28,30 5 0-950
h ТВ. 9,29 0,76 2 -73-113,6
ж. 16,12 2 113,6-160
г. 14,86 2 0-1200
К ТВ. 56,10 59,45 5 0-63,5
KBr ТВ. 40,40 12,68 2 0-270
KC1 ТВ. 71,05 7,58 3,77 2 0-777
K2Cr2O7 ТВ. 60,83 58,19 5 0-398
KF ТВ. 89,89 78,67 8,58 2 0-857
Kr г. 24,87 0 Все температуры
выше 0°
Li ТВ. 198,87 494,88 2 0-186
Li3N ТВ. 139,42 278,42 2 0-500
LiNO3 ТВ. 55,81 21,89 5 0-250
Mg ТВ. 106,89 22,94 11,69 4 0-650
MgCI2 ТВ. 72,47 23,49 2 0-718
MgF2 ТВ. 80,68 57,15 5 0-1000
MgO ТВ. 112,83 12,45 21,66 2 0-1800
278
Новый справочник химика и технолога
Продолжение табл. 3.5.2
Вещество Состояние а - 102 Ь- 105 с - 10’3 Погрешность, % Интервал температур, °C
Мп тв. (a) 28,68 57,19 5 0-835
тв. (p) 38,60 30,14 5 835-1044
ТВ. (у) 36,63 32,19 5 1044-1220
Мо ТВ. 25,37 5,02 15,15 2 0-1550
n2 г. 99,64 14,99 2 0-2200
NH3 г. 175,42 149,89 9,79 1 0-1100
NH4C1 тв. (а) 78,29 293,91 5 0-184,5
тв. (р) 39,94 271,72 5 184,5-250
NO г. 93,36 18,71 1 0-1200
no2 г. 98,26 25,04 20,55 1 0-1200
Na ТВ. 91,27 97,55 1,5 0-98
NaBr ТВ. 47,81 9,49 2 0-250
NaCl ТВ. 85,41 19,01 3,72 2 0-800
NaC103 ТВ. 37,64 185,5 3 0-275
NaF ТВ. 97,22 43,84 3 0-992
NaNO3 ТВ. 22,44 28,55 5 0-310
Nb ТВ. 25,67 4,245 1 0-1554
Ne г. 103,4 0 Все температуры
выше 0 °C
Ni тв. (а) 30,4 45,64 2 0-351
тв. (Р) 49,82 6,297 5 351-1452
o2 г. 98,39 10,61 11,79 1 0-1700
Os ТВ. 12,52 1,926 1 0-1604
P (желт.) ТВ. 74,36 5 0—44
P (красн.) ТВ. 2,839 243,3 10 0-199
P ж. 89,3 10 44-100
P4O10 ТВ. 23,19 161,2 2 0-358
г. 108,4 3 358-1098
Pb ТВ. 11,58 4,354 0,5 0-327,4
ж. 13,75 5 327,4-1000
PbBr2 ТВ. 20,89 3,538 2 0 488
PbCl2 ТВ. 23,95 12,57 2 0 438
Pbl2 ТВ. 16,96 2,663 2 0-375
PbO ТВ. 19,59 5,975 2 0-271
PbS ТВ. 18,63 7,021 3 0-600
Pd ТВ. 23,03 5,275 1 0-1554,5
PdO ТВ. 11,26 48,48 5 0-730
Pt ТВ. 12,69 2,491 1 0-1600
Rb ТВ. 16,04 64,04 2 0-39
Re ТВ. 12,85 2,52 2 0-1200
Rh ТВ. 21,98 8,918 2 0-1604
Ru тв. (а) 20,98 7,076 1 0-1035
ТВ. (Р) 19,68 7,076 1 1035-1500
ТВ. (у) 22,4 4,187 1 1500-1604
S (ромб.) ТВ. 46,89 81,64 1 0-95,5
S (монокл.) ТВ. 46,56 91,06 1 95,5-119
S г. 56,52 1,696 5,485 1 0-1700
SO? г. 74,44 11,18 13,33 2 0-1700
so3 г. 66,19 33,49 5 0-627
Sb ТВ. 18,97 6,113 2 0-630
ж. 20,43 5 630-1000
Se ТВ. 24,03 29,18 2 0-217
ж. 44,38 3 217-497
Si ТВ. 85,83 9,24 15,11 2 0-900
SiO2 (кварц) тв. (а) 75,86 60,79 16,83 1 0-575
Физические свойства важнейших веществ
Т1Ч
Окончание табл. 3.5.2
Вещество Состояние а - 102 Ь- 105 с - 10’3 Погрешность, % Интервал температур, °C
SiO2 (кварц) тв. (P) 94,2 20,93 3,5 575-1600
Sn ТВ. 17,79 16,96 2 0-231,8
ж. 23,28 10 231,8-1000
Та ТВ. 13,4 1,909 1 0-1400
Те ТВ. 17,08 7,997 3 0-327
ТеС14 ТВ. 51,5 2 25-224
ж. 85,41 2 224-265
Ti ТВ. 77,96 9,965 37,89 3 0^40
TiO2 ТВ. 61,96 39,52 2,194 3 0-440
Tl тв. (а) 11,43 5,359 1 0-232,3
тв. (р) 14,7 3 232,3-302,1
ж. 13,8 3 302,1-354
TIBr ТВ. 18,46 1,474 10 0-460
T1C1 ТВ. 21,94 1,541 5 0-427
V ТВ. 44,46 17,21 1,252 1,5 0-1553
W ТВ. 12,9 1,976 1 0-1800
Xe г. 15,83 0 Все температуры
выше 0° С
Zn ТВ. 33,6 17,29 1 0-419,5
ж. 48,57 3,521 3 419,5-850
ZnO ТВ. 58,62 5,882 9,429 1 0-1300
ZnS ТВ. 55,43 4,086 8,357 5 0-900
Удельная теплоемкость ср воды и водяного пара
Таблица 3.5.3
Удельная теплоемкость ср (Дж/(г • К)) воды и водяного пара при температуре кипения
р, МПа Т. °C с„. Дж/(г • К) /?, МПа Т. °C су. Дж/(г • К) /?, МПа 7’, °C ср. Дж/(г • К)
воды пара воды пара воды пара
0,101 99,09 4,229 2,04 4,05 249,18 4,836 3,75 14,2 335,09 7,704 11,0
0,203 119,62 4,245 2,12 5,07 262,70 5,003 4,12 16,2 345,74 8,792 14,3
0,507 151,11 4,3 2,29 6,08 274,29 5,171 4,61 18,2 355,35 10,05 19,4
1,01 179,04 4,384 2,55 8,11 293,62 5,589 5,65 20,3 364,08 11,43 27,6
2,03 211,38 4534 2,95 10,1 309,53 6,071 6,95
3,04 232,76 4,689 3,37 12,2 323,15 6,783 8,5
Таблица 3.5.4
Удельная теплоемкость ср (Дж/(г • К)) воды и водяного пара при температуре 0-500 °C
Данные, расположенные выше ломаной линии, относятся к жидкости, ниже — к пару.
Т,°С Давление, МПа
0,101 0,203 0,507 1,01 2,03 3,04 4,05 5,07 6,08 7,09 8,11 9,12 10,1 Н,1 12,2 13,2 14,2 15,2 16,2 17,2 18,2 19,3 20,3
0 4,212 4,212 4,212 4,208 4,208 4,208 4,204 4,204 4,204 4,199 4,195 4,191 4,187 4,187 4,183 4,178
20 4,183 4,178 4,178 4,178 4,178 4,174 4,174 4,17 4,17 4,166 4,162 4,157 4,153 4,149 4,145 4,141
40 4,178 4,178 4,178 4,174 4,17 4,17 4,166 4,162 4,162 4,157 4,153 4,149 4,145 4,141 4,132 4,128
60 4,191 4,191 4,187 4,183 4,178 4,174 4,17 4,166 4,162 4,157 4,153 4,149 4,145 4,141 4,132 4,128
80 4,204 4,204 4,204 4,199 4,195 4,191 4,187 4,183 4,178 4,174 4,166 4,162 4,157 4,149 4,145 4,141
100 2,102 4,229 4,224 4,22 4,216 4,212 4,208 4,204 4,199 4,195 4,187 4,183 4,174 4,17 4,166 4,157
120 2,031 2,114 4,254 4,25 0,059 4,241 4,237 4,233 4,229 4,224 4,216 4,208 4,204 4,195 4,191 4,183
140 2,001 2,064 4,296 4,287 4,279 4,275 4,271 4,266 4,262 4,254 4,25 4,241 4,233 4,229 4,22 4,212
160 1,98 2,035 2,311 4,358 4,346 4,338 4,329 4,325 4,321 4,312 4,304 4,296 4,287 4,279 4,271 4,262
180 1,976 2,018 2,198 2,68 4,425 3,153 4,4 4,396 4,388 4,379 4,371 4,363 4,35 4.342 4,333 4,321
200 1,976 2,005 2,135 2,42 4,518 4,501 4,488 4,484 4,476 4,467 4,455 4,442 4,43 4,421 4,409 4,396
220 1,98 2,001 2,106 2,299 2,939 4,626 4,61 4,593 4,585 4,568 4,555 4,543 4,53 4,518 4,501 4,488
240 1,985 2,001 2,085 2,646 2,633 3,312 4,752 4,739 4,727 4,71 4,693 4,677 4,66 4,643 4,622 4,605
260 1,993 2,005 2,072 2,186 2,474 2,918 3,525 4,945 4,932 4,907 4,882 4,857 4,832 4,811 4,79 4,769
280 2,001 2,014 2,068 2,156 2,37 2,667 3,073 3,655 4,451 5,234 5,15 5,125 5,091 5,058 5,028 4,999
300 2,014 2,022 2,064 2,135 2,311 2,52 2,772 3,14 3,605 4,237 5,15 5,652 5,56 5,481 5,414 5,355 5,3
320 2,026 2,031 2,068 2,127 2,261 2,424 2,621 2,864 3,161 3,525 3,994 4,631 5,531 6,896 6,741 6,322 6,113 5,945 5,824
340 2,035 2,039 2,072 2,123 2,236 2,366 2,516 2,696 2,906 3,157 3,454 3,81 4,258 4,815 5,686 6,862 8,96 7,787 7,327 7,013
360 2,047 2,047 2,077 2,123 2,215 2,324 2,445 2,587 2,747 2,931 3,144 3,395 3,684 4,024 4,434 4,945 5,589 6,515 7,825 9,872 13,63 24
380 2,06 2,06 2,085 2,123 2,206 2,299 2,399 2,512 2,638 2,78 2,939 3,123 3,333 3,571 3,835 4,137 4,463 4,89 5,401 6,075 6,887 7,988 9,588
400 2,072 2,068 2,093 2,127 2,198 2,278 2,361 2,458 2,562 2,675 2,801 2,939 3,094 3,266 3,458 3,672 3,906 4,17 4,467 4,802 5,179 5,619 6,142
420 2,085 2,081 2,106 2,135 2,202 2,269 2,34 2,42 2,508 2,6 2,7 2,814 2,927 3,056 3,199 3,354 3,521 3,705 3,906 4,124 4,358 4,61 4,886
440 2,098 2,093 2,119 2,144 2,202 2,261 2,324 2,391 2,462 2,541 2,625 2,713 2,809 2,91 3,019 3,136 3,257 3,387 3,529 3,68 3,843 4,024 4,22
460 2,11 2,102 2,127 2,152 2,202 2,257 2,311 2,37 2,433 2,5 2,571 2,646 2,726 2,805 2,889 2,977 3,073 3,178 3,287 3,4 3,517 3,643 3,781
480 2,123 2,114 2,139 2,16 2,206 2,252 2,303 2,353 2,407 2,466 2,525 2,587 2,654 2,261 2,793 2,868 2,948 3,031 3,1 19 3,211 3,308 3,408 3,513
500 2,135 2,131 2,152 2,169 2,211 3,509 2,294 2,34 2,391 2,441 2,491 2,546 2,6 2,654 2,717 2,78 2,847 2,914 3,404 3,065 3,144 3,228 3,312
280 Новый справочник химика и технолога
Физические свойства важнейших веществ
281
Таблица 3.5.5
Удельная теплоемкость ср (Дж/(г • К)) водяного пара при давлении до 20,3 МПа
р, МПа Температура, °C
520 540 560 580 600 620 640 660 680 700 720 740
0,101 2,152 2,165 2,181 2,194 2,206 2,219 2,236 2,248 2,261 2,278 2,29 2,307
0,507 2,165 2,177 2,19 2,202 2,215 2,227 2,24 2,257 2,269 2,282 2,299 2,311
1,01 2,181 2,194 2,206 2,215 2,273 2,24 2,252 2,265 2,278 2,29 2,307 2,319
2,03 2,219 2,227 2,236 2,244 2,252 2,261 2,273 2,282 2,294 2,307 2,319 2,332
3,04 2,257 2,261 2,265 2,273 2,278 2,286 2,294 2,303 2,311 2,324 2,332 2,345
4,05 2,294 2,294 2,299 2,303 2,303 2,307 2,315 2,319 2,332 2,34 2,349 2,357
5,07 2,336 2,332 2,332 2,332 2,328 2,332 2,336 2,34 2,349 2,353 2,361 2,374
6,08 2,378 2,37 2,366 2,361 2,357 2,357 2,357 2,361 2,366 2,37 2,378 2,386
8,11 2,42 2,407 2,441 2,433 2,382 2,382 2,378 2,382 2,382 2,386 2,395 2,399
9,12 2,512 2,487 2,47 2,453 2,441 2,433 2,424 2,424 2,42 2,42 2,424 2,428
10,1 2,562 2,529 2,508 2,487 2,47 2,458 2,449 2,445 2,441 2,441 2,441 2,441
11,2 2,613 2,575 2,546 2,52 2,5 2,483 2,474 2,466 2,458 2,458 2,458 2,458
12,2 2,663 2,613 2,583 2,554 2,529 2,512 2,495 2,487 2,479 2,474 2,47 2,47
13,2 2,717 2,692 2,621 2,592 2,558 2,537 2,52 2,508 2,5 2,491 2,487 2,487
14,2 2,772 2,709 2,663 2,629 2,596 2,567 2,546 2,529 2,52 2,512 2,504 2,5
15,2 2,83 2,759 2,705 2,667 2,629 2,596 2,571 2,554 2,537 2,529 2,52 2,516
16,2 2,889 2,809 2,747 2,705 2,663 2,625 2,596 2,575 2,558 2,546 2,537 2,529
17,2 2,952 2,864 2,793 2,742 2,696 2,654 2,621 2,596 2,579 2,567 2,554 2,546
18,2 3,014 2,914 2,839 2,78 2,726 2,68 2,646 2,617 2,6 2,583 2,571 2,562
19,3 3,081 2,973 2,885 2,822 2,763 2,713 2,675 2,646 2,621 2,604 2,587 2,579
20,3 3,153 3,031 2,935 2,864 2,801 2,747 2,705 2,671 2,642 2,621 2,604 2,592
Таблица 3.5.6
Удельная теплоемкость ср (Дж/(г • К)) водяного пара при давлении выше 20,3 МПа
р, МПа Температура. °C
400 420 440 460 480 500 520 540 560 580 600 620 640 660 680 700 720 740
21,3 6,824 5,2 4,434 3,931 3,622 3,4 3,224 3,509 2,985 2,906 2,834 2,776 2,73 2,696 2,667 2,642 2,621 2,608
22,3 7,645 5,58 0,481 4,095 3,739 3,488 3,295 3,144 3,035 2,952 2,876 2,809 2,759 0,650 2,688 2,663 2,642 2,625
23,3 8,683 6,05 0,733 0,084 3,864 3,58 3,37 3,207 3,09 2,994 2,91 2,839 2,784 2,742 2,709 2,684 2,659 2,642
24,3 10,08 6,59 5,196 4,459 3,998 3,676 3,446 3,274 3,144 3,04 2,948 2,872 2,814 2,772 2,734 2,7 2,675 2,659
25,3 11,91 7,11 5,493 4,66 4,137 3,776 3,525 3,341 3,199 3,09 2,994 2,914 2,847 2,797 2,755 2,721 2,696 2,675
26,3 14,54 7,8 5,828 4,878 4,283 3,881 3,609 3,408 3,253 3,14 3,04 2,952 2,876 2,818 0,664 2,742 2,713 2,692
27,4 18,62 8,62 6,201 5,108 4,438 3,99 3,684 3,475 2,889 2,726 2,659 2,985 2,91 2,847 2,801 2,763 2,73 2,705
28,4 23,7 9,57 6,611 5,342 4,585 4,095 3,768 3,546 3,366 3,232 3,119 3,023 2,943 2,876 2,826 2,784 2,751 2,726
29,4 28,61 10,7 7,072 5,602 4,752 4,212 3,856 3,617 3,421 3,278 3,161 3,061 2,977 2,901 2,847 2,805 2,772 2,742
30,4 28,89 12 7,561 5,87 4,932 4,333 3,944 3,684 3,475 3,324 3,622 3,098 3,006 2,931 2,872 2,826 2,788 2,759
31,4 8,055 6,184 5,12 4,459 4,036 3,756 3,538 3,375 3,245 3,136 3,04 2,952 2,897 2,847 2,809 2,776
32,4 8,579 6,502 5,321 4,597 4,128 3,827 3,596 3,425 3,287 3,174 3,073 2,985 2,922 2,872 2,83 2,793
33,4 9,123 6,833 5,531 4,735 4,229 3,902 3,659 3,479 3,329 3,207 3,102 3,019 2,952 2,893 2,847 2,809
34,5 9,68 7,176 5,753 4,882 4,333 3,977 3,722 3,529 3,375 3,245 3,136 3,048 2,977 2,918 2,868 2,83
35,5 10,23 7,524 5,983 5,033 4,438 4,061 3,781 3,58 3,416 3,282 3,169 3,077 3,002 2,939 2,889 2,847
36,5 7,875 6,222 5,196 4,547 4,141 3,852 3,63 3,462 3,316 3,203 3,107 3,027 2,96 2,906 2,445
37,5 8,235 6,469 5,363 4,664 4,224 3,923 3,684 3,504 3,358 3,236 3,136 3,052 2,985 2,931 2,885
38,5 8,575 6,72 5,535 4,781 4,312 3,99 3,743 3,555 3,4 3,274 3,165 3,081 3,01 2,952 2,901
39,5 8,889 6,967 5,711 4,903 4,392 4,057 3,802 3,601 3,442 3,308 2,738 3,107 3,035 2,973 2,918
40,5 9,148 7,21 5,895 5,028 4,48 4,12 3,856 3,655 3,488 3,345 3,228 3,136 3,061 2,994 2,939
282 Новый справочник химика и технолога
Физические свойства важнейших веществ
283
Удельная теплоемкость ср органических соединений
В табл. 3.5.7 и 3.5.8 приведены значения теплоемкостей органических соединений в твердом и жидком агрегатном состояниях для указанных температур или значения средних теплоемкостей для интервалов температур.
Данные по удельной теплоемкости органических соединений в газообразном состоянии см. в табл. 3.5.9, 3.5.18,3.5.21 и 3.5.22.
Таблица 3.5.7
Удельная теплоемкость ср (Дж/(г • К)) органических соединений в твердом состоянии
Название Формула Г, °C ср
2-Аминобензойная C7H7NO2 85 1,063
кислота
(антраниловая
кислота)
З-Аминобензойная c7h7no2 120 1,059
кислота
4-Аминобензойная c7h7no2 128 1,202
кислота
Анилин c6h7n 0 3,102
Антра-9,10-хинон C14H8O2 0 1,08
Антрацен СиНю 50 1,29
Ацетон c3H6o -210 2,261
Бензойная кислота с7н6о2 20 1,202
Бензол с6н6 -250 0,167
-200 0,519
-180,6 0,62
-159,4 0,691
-122,5 0,837
-100 0,95
-50 1,252
-33,7 1,31
-13,7 1,486
Бензофенон С13н10о -150 0,481
-50 0,921
0 1,151
20 1,269
Бензо-1,4-хинон с6н4о2 -250 0,13
-200 0,473
-150 1,181
Бифенил С12н ю 30 1,285
50 1,394
60 1,444
1 -Бром-2- С6Н4Вг1 -50 0,599
иодбензол
1-Бром-3- С6Н4Вг1 -75 - —15 0,599
иодбензол
1 -Бром-4- С6Н4Вг! -40 0,486
иодбензол
2-Бромнафталин С10Н7Вг 41 1,089
1 -Бром-2- С6Н4ВгС1 -34 0,804
хлорбензол
1-Бром-3- С6Н4ВгС1 -52 0,628
хлорбензол
1 -Бром-4- С6Н4ВгС1 -40 0,628
хлорбензол 0 0,712
Продолжение табл. 3.5.7
Название Формула Т, °C ср
(£)-Бут-2-еновая с4н6о2 38 2,177
кислота
(кротоновая кислота) Г ексан С6н14 -179,8 0,917
-158,0 1,051
-127,7 1,235
-109,7 1,373
Гексан-1-ол С6Н14О -254,9 0,07
-242,5 0,196
-228,3 0,355
-212,2 0,52
-178,6 0,767
-127,4 1,057
-101,5 1,169
Гидрохинон С6н6о2 -250 0,103
-150 1,122
Глицерин с3н8о3 -250 0,197
-200 0,481
-100 0,909
0 1,382
Глутаровая с5н8о4 20 1,252
кислота
D-Глюкоза (декст- С6Н12О6 -250 0,065
роза) 0 1,16
20 1,151
1,2-Дибромбензол С6Н4Вг2 -36 1,043
1,3-Дибромбензол С6Н4Вг2 -25 0,561
1,4-Дибромбензол С6Н4Вг2 -50 0,582
2,3-Дигидрокси- с4н6о6 -36 1,202
янтарная кислота 0 1,29
(винная кислота) 50 1,532
1,3-Дииодбензол с6н412 -52 0,419
1,4-Дииодбензол с6н412 -50 0,423
2,2-Диметил-З- CioH]6 35 1,591
метилен-
бицик-ло[2.2.1]гептан (камфен) Диметилоксалат с4н6о4 10 0,888
1,2-Динитро-бензол C6H4N2O4 -160 1,055
1,3-Динитро-бензол C6H4N2O4 -160 1,038
1,4-Динитро-бензол c6h4n2o4 -119 1,084
Дифенилдиазен (азобензол) C12H,oN2 28 1,382
1,2-Дихлорбензол C6H4C12 -48,5 0,775
1,3-Дихлорбензол C6H4C12 -52 0,779
1,4-Дихлорбензол С6Н4С12 -50 0,917
Дихлоруксусная С2Н2С12О2 0 1,7
кислота
Диэтиловый эфир с4н10о -193,7 0,858
-181,6 0,967
-167,7 1,051
284
Новый справочник химика и технолога
Продолжение табл. 3.5.7
Название Формула Г, °C Ср
Диэтиловый эфир С4Н10О -144,7 1,185
-136,0 1,256
Додекановая с12н24о2 -30 1,8
кислота
(лауриновая
кислота)
Дульцит С6Н14О6 20 1,181
2-Изопропил-5- с10н14о 0 1,319
метилфенол
(тимол)
Малоновая С3Н4О4 20 1,151
кислота
Маннит с6н14о6 0 1,31
Метанол СН4О -254,4 0,145
-242,5 0,37
-213,7 0,895
-180,0 1,299
-139,5 1,652
-119,2 1,846
Метантриилтри- С]9Н]6 0 0,791
бензол
(трифенилметан)
2-Метилбензойная С8Н8О2 54 1,16
кислота
(о-толуиловая
кислота)
З-Метилбензойная с8н8о2 54 1,001
кислота
(jw-толуиловая
кислота)
4-Метилбензойная с8н8о2 130 1,135
кислота
(и-толуиловая
кислота)
2-Мстилбут-2-сн С5Н,0 -180,5 0,996
-172 1,063
-165,7 1,114
Метилендибензол с13н12 -171,3 0,528
(дифенилметан)
-27,2 1,105
0 1,243
25,3 1,39
2-Метилпропан-2-ол С4Н10О —4 2,34
Метилянтарная с5н8о4 20 1,26
кислота
Мочевина CH4N2O 20 1,34
Муравьиная СН2О2 -22 1,62
кислота
Нафталин С,оН8 -258 0,046
-80,5 0,806
0 1,172
26,5 1,294
50 1,465
70 1,612
Нафталин-1 -амин
(1-нафтиламин) c10h9n 0 1,13
Продолжение табл. 3.5.7
Название Формула T. °C Cp
1 -Нафтол С10н8о 50 1,005
2-Нафтол С|0Н8О 61 0,971
2-Нитроанилин C6H6N2O2 -160 1,126
З-Нитроанилин c6h6n2o2 -160 1,151
4-Нитроанилин c6h6n2o2 -160 1,156
2-Нитробснзойная c7h5no4 -163 1,072
кислота
З-Нитробензойная c7h5no4 -160 1,034
кислота
Октановая кислота c8H16o2 -2 2,617
(каприловая кислота) Пальмитиновая C16H32O2 -180 0,699
кислота -100 1,051
-50 1,281
0 1,599
20 1,8
Пентан c5H12 -180,4 0,976
-164,6 1,093
-146,5 1,239
Пирокатехин C6H6O2 -163 1,164
Пропан-1-ол C3H8O -200 0,712
-130 2,081
Пропан-2-ол C3H8O -200 0,212
Пропионовая C3H6O2 -33 3,04
кислота
Резорцин C6H6O2 -160 1,126
Стеариновая c18H36o2 15 1,671
кислота
Т етрадекановая кислота (миристиновая кислота) C14H28O2 0 1,595
Тетрахлорметан CC14 -200 0,34
(углерод четырех- -80 0,762
хлористый) -10 0,842
и-Толуидин c7h9n 0 1,411
20 1,62
Толуол c7h8 -195,0 0,603
-147,1 0,749
-125,8 0,837
-105,2 0,938
1,3,5-Триазин- 2,4,6-триамин (меламин) C3H6N6 40 1,47
1,3,5-Триазин- 2,4,6-триол(циа- C3H3N3O3 40 1,331
нуровая кислота) 2,4,6-Тринитро- c6h3n3o7 -100 0,691
фенол(пикрино- 0 1,005
вая кислота) Т рихлоруксусная 50 1,101
кислота C2HC13O2 0 1,922
2,2,2-Три-хлорэтан-1,1 -диол (хлоральгидрат) C2H3C13O2 32 0,892
Физические свойства важнейших веществ
285
Окончание табл. 3.5.7
Название Формула Т, °C ср
Уксусная кислота С2Н4О, 0 2,039
А-Фениланилин C12HhN 26 1,411
(дифениламин) Фенилсалицилат С13Н10О3 32 1,21
(салол) Фталевая кислота с8н6о4 20 0,971
Хингидрон С6Н4О2 -250 0,069
• С6Н4(ОН)2 -200 0,41
0 1,072
2-Хлорбензойная с7н5сю2 80 1,013
кислота
З-Хлорбензойная с7н5сю2 94 0,971
кислота
4-Хлорбензойная С7Н5СЮ2 80 0,955
кислота
Хлоруксусная С2Н3С1О2 60 1,52
кислота
А-Цианогуанидин (дициандиамид) c2h4n4 0-204 1,909
Циклогексан С6Н12 -160,4 0,758
-129,1 0,904
-95,7 1,101
-64 1,323
-44 1,377
-28,4 1,432
-7,6 1,516
Циклогексен С6Н10 -141,1 0,833
-126,7 1,172
-116,1 1,231
Циклопентан С5Н,о -180 0,808
-159,1 0,917
-144,8 1,331
-140,5 1,319
-128,9 1,264
-107 1,252
-101,9 1,252
Щавелевая кисло- С2Н2О4 • 0 1,415
та дигидрат • 2Н2О
Эритрит C4Hi 0О4 60 1,47
Этан-1,2-диилдибензол С]4Н14 28 1,52
(дибензил) Этанол (крист.) с2н6о -190 0,971
Этанол (стекл.) с2н6о -190 1,089
Этилацетат С4Н8О2 -181 0,833
-148 0,992
-121,3 1,101
-105,9 1,193
Янтарная кислота С4Н6О4 -179,8 0,561
-147,7 0,678
-116,5 0,783
-88,1 0,883
-58,2 0,992
-13,2 1,16
2,8 1,21
16,6 1,269
Таблица 3.5.8
Удельная теплоемкость ср (Дж/(г • К)) органических соединений в жидком состоянии
Название Формула Г, °C ср
Аллилацетат с5н8о2 0 1,805
Аллилбензоат CjoH|o02 20 1,624
Аллилбутират с7н1202 20 1,888
Аллилизобутират С7Н12О2 20 1,876
Аллилпентаноат С8Н14О2 20 1,888
Аллилпропионат С6Н10О2 20 1,888
2-Аминобензойная C7H7NO2 145 1,821
кислота
(антраниловая
кислота)
З-Аминобензойная c7h7no2 174 1,821
кислота
4-Аминобензойная c7h7no2 186 1,859
кислота
Анизол (метилфс- c7H8o 20-152 2,022
ниловый эфир)
Анилин c6h7n 0 2,001
50 2,181
100 2,403
Ацетилхлорид С2Н3С1О 0 1,419
Ацетон c3H6o 0 2,119
20 2,211
Ацетонитрил c2h3n 21-76 2,265
Бензальдегид c7H6o 22-172 1,792
Бензол с6н6 8 1,629
20 1,7
60 1,859
Бензонитрил c7h5n 22-186 1,846
Бифенил С]2Н10 80 1,767
100 1,834
Бромбензол С6Н5Вг 20 0,967
1 -Бром-2-иодбензол С6Н4Вг! 5-100 0,67
1 -Бром-З-иодбензол С6Н4Вг! 5-100 0,662
1 -Бром-2- С6Н4ВгС1 0
хлорбензол 0,9
1-Бром-3- С6Н4ВгС1 0
хлорбензол 0,888
Бромэтан С2Н5Вг 5-10 0,904
15-20 0,9
Бутан С4Ню ~0 2,303
Бутан-1 -ол С4Н10О 2,3 2,202
19,2 2,357
Бутан-2-он С4Н8О 20-78 2,299
Бутан-2-оноксим C4H9NO 22-152 2,721
Бутилбутират с8н1602 20 1,922
Бутилпентаноат С9Н18О2 20 1,922
Бутилпропионат С7Н14О2 20 1,922
Бутилформиат СзНюОг 20 1,922
Бутиронитрил c4h7n 21-113 2,29
Гекса-1,5-диен СбНю 0 1,704
Г ексан с6н14 -84,4 1,976
-55,5 2,018
2,2 2,181
20,3 2,244
|Гексаннитрил C6HnN 18-156 2,269
286
Новый справочник химика и технолога
Продолжение табл. 3.5.8
Название Формула Т, °C ср
Гексановая кислота С6Н12О2 32-105 2,232
(капроновая кислота)
Гексан-1-ол С6н14о -43,6 1,904
-22,5 2,001
-2,6 2,123
16,8 2,278
Гексан-2-он с6н12о 21-127 2,315
Гекс-1-ен С6Н12 0-50 2,119
Гептан с7н16 20 2,052
Гептаналь С7Н14О 0 1,528
(энантовый
альдегид)
Гептановая кислота С7н,4о2 0 1,323
(энантовая кислота)
Гсптан-4-он С7Н14О 20-140 2,311
Гепт-1-ен С7Н14 0-50 2,043
Глицерин (переохл.) С3Н8О3 0 2,261
Глицерин С3Н8О3 50 2,512
100 2,801
Дец-2-сн СюН20 0-50 1,964
Диаллилоксалат С8н10о4 20 1,784
Диаллилсукцинат СюН]4О4 20 1,892
1,2-Дибромбензол С6Н4Вг2 0 0,754
(переохл.)
1,3-Дибромбензол С6Н4Вг2 0 0,628
1,2-Дибром этан С2Н4Вг2 20 0,729
Дибутилоксалат СюН|8О4 20 1,846
Диизобутилсук- С]2Н22О4 0 1,851
цинат
1,3-Дииодбензол с6н412 34,2-99,6 0,586
А(Л-Диметиланилин C8HnN 2,5-20 1,75
Ди(3-метил- С]2Н22О4 20 1,88
бутил)оксалат
Ди(3-метил- с14н26о4 0 1,88
бутил)сукцинат
Диметилкарбонат С3Н60з 19,88-88 1,892
2,7-Диметилоктан СюН22 21,5-155 2,47
1,3-Динитробензол С6Н4М2О4 90 1,696
Дипропилмалонат С9Н16О4 20 1,813
Дипроп илоксалат С8Н14О4 20 1,813
Дипропилсукцинат С]0Н]8О4 20 1,892
Дифениловый эфир С12НюО 50 1,671
1,2-Дихлорбензол С6Н4С12 0 1,13
1,3-Дихлорбензол С6Н4С12 0 1,13
1,4-Дихлорбензол С6Н4С12 53-99 1,248
Дихлорметан СН2С12 15-40 1,206
(хлористый мети-
лен)
Дихлоруксусная С2Н2С12О2 21-106 1,465
кислота
1,2-Дихлорэтан С2Н4С12 20 1,26
?У,?У-Диэтиланилин C10H15N 20 1,892
Диэтилкарбонат С5Н10Оз 20-100 1,943
Диэтилмалонат с7н1204 24-186 1,989
(малоновый эфир)
Продолжение табл. 3.5.8
Название Формула Т. °C
Диэтиловый эфир С4Н|оО -113,9 1,989
-79,9 2,102
-50 2,165
-35,4 2,186
0 2,215
30 2,29
Диэтилмалат с8н1405 24-186 1,913
Диэтилоксалат С6Н|0О4 20 1,813
Диэтилсукцинат С8Н14О4 20 1,892
Диэтилсульфид c4H10s 0 1,968
15-20 1,997
Додекан с12н26 0-50 2,093
Додекановая кисло- С|2Н24О2 57 2,156
та (лауриновая кислота) Додец-1 -ен С|2Н24 0-50 1913
Изобутилацетат С6НрОэ 20 1,922
Изобутилбутират С8н16о2 20 1,922
А/-Изобутил-2-метилпропан-1- c8h19n 22-130 2,391
амин
(диизобутиламин) Изомасляная С4Н8О2 20 1,884
кислота
Изопентан С5н)2 8 2,206
(2-метилбутан) 5-Изопропил-2-метилфенол (карвакрол) С]оН|40 24-233 2,416
Иодэтан С2Н51 0 0,678
о-Ксилол С8Н1О 30 1,721
.и-Ксилол с8н10 16-35 1,62
н-Ксилол С8Н1О 30 1,662
Масляная кислота С4Н8О2 20-100 2,156
Мезитилен с9н|2 0
(1,3,5-триметил-бензол) 1,645
Метанол СН4О -88,1 2,177
-51,5 2,232
-16,9 2,311
0 2,37
12,8 2,445
20 2,512
/V-Метил анилин c7h9n 20-197 2,148
Метил ацетат СзН6О2 15 1,959
Метилбензоат с8н8о2 0 1,52
2-Метилбензойная С8Н8О2 0 1,767
кислота
(о-толуиловая кислота)
3 -Мети лбензойная с8н802 0 2,106
кислота
(м-толуиловая кислота)
Физические свойства важнейших веществ
287
Продолжение табл. 3.5.8
Название Формула Г, °C ср
4-Метилбензойная с8н8о2 0 1,323
кислота
(«-толуиловая кислота) 3-Метил бутан-1 - c5h13n 22-91 2,571
амин
(изопентиламин) З-Метилбутановая С5Н]0О2 23-98 2,177
кислота
(изовалериановая кислота) 2-Метилбутан-1 -ол С5Н12О 22-125 2,981
2-Мстилбутан-2-ол С5Н12О 20-99 3,153
З-Метилбутан-1 -ол С5Н12О 0 2,102
20 2,24
75,7 2,881
3-М стал бутан-2-о н с5н10о 20-91 2,198
2-Метилбут-2-ен С5Н1О -129,3 1,876
-71,8 1,922
-40,2 1,976
2,2 2,085
20,7 2,144
(З-Метил-бутил)ацетат C7Hi4O2 20 1,922
(З-Метил-бутил)бутират с9н18о2 20 1,922
(З-Метил-бутил)изобутират с9н18о2 20 1,922
(З-Метил-бутил)пентаноат СюН20О2 20 1,922
(3-М ети лбутил )-пропионат С8н16о2 20 1,922
(3-М ети л бутил )-формиат С6Н12О2 20 1,922
Метилбутират С5н10о2 20 1,922
2-Метил гексан С7н16 0-50 2,098
Метил(дихлор)- С3Н4С12О2 20 1,302
ацетат Метилендибензол с13н12 37,5 1,633
(дифенилметан) 49,4 1,645
1-Метил-4-метоксибензол с8н10о 0 1,696
Метилпентаноат С6Н12О2 20 1,922
4-М ети лпентан-2 -он с6н12о 20 1,922
4-Метилпент-З-ен- СбНюО 21-121 2,181
2-он (окись мезитила) 2-Метилпропан-1 -ол с4н10о 21-108 2,998
Метилпропионат С4Н8О2 20 1,922
2-Метил-1,3,5-тринитробензол c7h5n3o6 20 1,403
Метил(трихлор)- С3Н3С13О2 20 1,118
ацетат Метилформиат С2Н4О2 13-29 2,16
Метил(хлор)ацетат с3н5сю2 20 1,599
2-Метилцикло- С7Н14О 15-18 1,75
гексанол
Продолжение табл. 3.5.8
Название Формула Г, °C с/>
З-Мстилцикло- С7Н14О 15-18 1,767
гексанол
4-Метилцикло- С7Н14О 15-18 1,771
гексанол
2-Метилцикло- С7Н12О 15-18 1,825
гексанон
З-Мстилцикло- С7Н|2О 15-18 1,846
гексанон
4-Метилцикло- с7н120 15-18 1,846
гексанон
1 -Метокси-4-(проп- С10Н12О 22^18 2,307
1-ен-1-ил)бензол
(анетол)
Муравьиная кислота СН2О2 15,5 2,139
20-100 2,202
Нафталин СюН8 90 1,788
Нафталин-1 -амин c10h9n 53,2 1,989
(1-нафтиламин)
Нитробензол c6h5no2 30 1,419
100 1,491
120 1,65
Нитрометан ch3no2 17 1,725
1 -Нитронафталин c10h7no2 58,6 1,528
Нонан C9H2o 0-50 2,106
Нон-1-ен C9H18 0-50 2,031
Октан c8H18 20-123 2,42
Октан-2-он с8н16о 22-168 2,311
Окт-1 -ен с8н16 0-50 2,035
Пальмитиновая С16н32о2 65-104 2,734
кислота
Пентадекан С15н32 10-50 2,081
Пентадец-1 -ен с15н30 5-50 1,972
Пентан с5н12 -123,3 1,947
-87,7 1,98
-42,0 2,068
1,6 2,211
18 2,261
Пентаннитрил c5h9n 23-121 2,177
Пентан-З-он с5н10о 20-98,5 2,332
Пент-1-ен (амилен) С5Н,о 0 1,181
Пиперидин c5h,,n 20-98 2,19
Пиридин c5h5n 21-108 1,805
Пропан-1 -ол c3H8o -100 1,821
0 2,202
25 2,453
Проп-2-ен-1-ол с3н6о 21-96 2,784
Пропилацетат CsHi0O2 20 1,922
Пропилбензоат С)0Н12О2 20 1,666
Пропилбензол c9H)2 0 1,675
Пропилбутират С7Н14О2 20 1,922
Пропилизобутират С7Н]4О2 20 1,922
Пропилпентаноат С8Н16О2 20 1,922
N-Пропилпропан-1 - С6н15™ 22-100 2,5
амин
(дипропиламин)
Пропилпропионат с6н12о2 20 1,922
288
Новый справочник химика и технолога
Продолжение табл. 3.5.8
Название Формула Г, °C ср
Пропилформиат С4н8о2 20 1,922
Пропил(хлор)ацетат С5Н9С1О2 20 1,733
Пропиональдегид СзН6О 0 2,186
Пропионовая СзН6О2 20-137 2,345
кислота
Пропиононитрил c3h5n 19-95 2,252
Пропоксибензол С9Н12О 0 1,796
Салицилальдегид с7н6о2 18 1,599
Стеариновая кислота С]8НзбО2 74-137 2,303
Т етрадекан С14Нзо 6-50 2,081
Тетрадей-1-ен С14Н28 0-50 1,897
Тетрадекановая ки- С|4Н28О2 58-100 2,257
слота(миристино-
вая кислота)
Т етрахлорметан СС14 0 0,829
20 0,842
Т етрахлорэтиле н С2С14 20 0,883
Толуол С7н8 -88,8 1,44
-78,0 1,486
-45,4 1,549
-13,4 1,574
0 1,62
25,3 1,758
50 1,763
100 1,968
Тридекан С13н28 0-50 2,089
Тридец-1-ен С)зН2б 0-50 1,913
1,2,4-Тримстил- С9н12 20 1,733
бензол
(псевдокумол)
Т рихлорацетальде- С2НС13О 17-53 1,047
гид (хлораль)
2,2,2-Трихлорэтан- С2Н3С13О2 55-88 1,968
1,1 -диол
(хлоральгидрат)
Трихлорэтилен С2НС1з 20 0,934
У ндекан СцН24 0-50 2,098
Ундец-1-ен СцН22 0-50 2,018
У-Фсниланилин c12h„n 53 1,943
(дифениламин)
Фенилметанол с7н8о 20-100 2,139
Фени лсалици лат C13H10O3 44,1 1,637
(салол)
1-Фенилэтанон с8н8о 20-196 1,985
(ацетофенон)
Фенол С6Н6О — 2,349
Формамид CH3NO 19 2,307
2-Фуральдегид С5Н4О2 20-100 1,75
(Фурфурол)
Хинолин c9h7n 0-20 1,474
Хлорбензол С6Н5С1 20 1,294
1 -Хлорбутан С4Н9С1 20 1,888
(Хлорметил)бензол С7Н7С1 0 1,352
Продолжение табл. 3.5.8
Название Формула Г, °C ср
Хлороформ СНС13 0 0,971
15 0,946
20 0,942
30 0,95
40 0,959
2-Хлорпропен С3Н5С1 0 1,31
2-Хлорфснол С6Н5С1О 0-20 1,679
Хлорэтан С2Н5С1 0 1,541
Циклогексан с6н12 9,9 1,767
17,5 1,8
25,7 1,842
Циклогексанон с6н|0о 15-18 1,813
Циклогексен СбН,0 -96,1 1,411
-76,1 1,461
-46,2 1,541
2,6 1,704
20,0 1,771
Циклопентан с5н10 -87 1,419
-59,1 1,478
-21,6 1,599
2,2 1,704
20,5 1,796
Этанол с2н6о -100 1,909
0 2,24
25 2,433
30 2,525
35 2,571
45 2,357
50 2,801
55 2,881
65 3,027
70 3,153
Этилацетат с4н8о2 -77,5 1,821
-28,4 1,834
1,7 1,884
20,4 1,922
Этилбензоат С9Н]о02 20 1,629
Этилбензол C8HW 30 1,712
Этилбутират с6н12о2 20 1,922
Этил(дихлор)ацетат С4Н6С12О2 20 1,377
Этиленгликоль С2НбО2 0 2,278
14,9 2,391
Этилизобутират С6НрО, 20 1,922
Этил-3-оксобу- С6Н10О3 20-100 1,997
таноат(ацетокусус-
ный эфир)
Этилпентаноат с7н14о2 20 1,922
Этилпропионат С5Н,о02 20 1,922
Этил(трихлор)ацетат С4Н5С13О2 10-81 1,235
Этилформиат с3н6о2 14-49 2,135
Этил(хлор)ацетат С4Н7С162 9-138 1,75
У-Этил этанам ин C4H,jN 20 1,331
(диэтиламин)
60 1,336
Этоксибензол С8Н,оО 20 1,867
Физические свойства важнейших веществ
289
Удельная теплоемкость ср веществ в газообразном ср состоянии и отношение —
Cv
Значения теплоемкостей ср приведены при давлении 101,3 кПа (за исключением специально отмеченных случаев).
с,
Теоретические значения отношения —: для одно-cv
атомных газов — 1,66; для двухатомных — 1,40; для трехатомных — 1,28.
Таблица 3.5.9
Удельная теплоемкость веществ в газообразном состоянии
Название Формула T. °C c,„ Дж/(г • К)
Простые вещества и неорганические соединения
Азот n2 -181 1,072 1,47
15 1,163 1,404
300 1,384
Азота(1) n2o -70 0,795 1,45
оксид -30 0,837 1,32
0 1,31
15 0,839 1,303
25-100 0,888
100 1,277
300 1,209
Азота(П) NO -80 1,024 1,38
оксид -45 1 1,39
15 0,975 1,40
10-180 0,971
300 1,319
Азота(1У) no2 27-67 6,783
оксид Аммиак NH3 15 2,227 1,310
100 1,28
300 1,319
Аргон Ar -180 0.557 1,76
0 1,67
15 0,517 1,668
Бром Br2 19-388 (10,1- 152 кПа) 20-350 (ЗОЛ- 152 кПа) 0,23 1,32
Вода (пар) H2O 100 1,324
200 1,310
300 1,304
400 1,301
500 1,296
Водород H2 -185 1,605
-181 11,05 1,597
-118 1,480
-76 13,19 1,453
-21 1,420
15 14,19 1,410
Продолжение табл. 3.5.9
Название Формула T. °C cp. Дж/(г • К) s Cv
Водород Н2 100 14,36 1,404
200 14,5 1,398
400 14,79 1,387
600 15,08 1,377
800 15,37 1,367
1000 15,66 1,358
2000 17,12 1,318
Водорода НВг 11-110 0,343
бромид 18-25 1,42
Водорода HI 20-100 1,40
иодид
Водорода H2S -57 1,223 1,29
сульфид -A5 1,168 1,30
(ссроводо- 15 1,059 1,32
РОД) 10-190 1,017
300 1,28
Водорода НС1 15 0,812 1,41
хлорид 10-190 0,775
100 1,40
Водорода HCN 65 1,31
цианид
Воздух -180 1,448
0 1,4032
100 1,399
400 1,017 1,393
1000 1,076 1,365
1400 1,13 1,341
1800 1,193 1,316
Гелий Нс -180 5,234 1,660
15 5,234 1,66
Иод h 185 1,30
206-377 0,142
Иода(1) хло- IC1 100 1,31
рид
Калий К 800 1,64
850 1,77
760-1000 1,7
Кислород О2 -181 0,957 1,45
-76 0,897 1,415
15 0,912 1,401
100 0,913 1,399
200 0,916 1,396
400 0,927 1,391
600 0.938 1,383
800 0,954 1,375
1000 0,973 1,365
2000 1,117 1,303
Криптон Kr 15 0,251 1,67
Ксенон Xe 15 1,7
Неон Ne 15 1,038 1,68
Ртуть Hg 360 1,666
(50,7-
101,3 кПа)
Серы диок- so2 15 0,216 1,29
сид 10-190 0,561
20 1,27
290
Новый справочник химика и технолога
Продолжение табл. 3.5.9
Название Формула Т,°С ср, Дж/(г • К) с.
Простые вещества и неорганические соединения
Тетрахлор- SiCl4 90-230 0,553
силан
Тетрахлор- SnCl4 149-273 0,394
станнан
Углерода СО2 -15 0,879 1,28
диоксид 0 1,307
100 1,27
300 1,216
Углерода cs2 80-190 0,657
дисульфид
(сероугле-
РОД)
Углерода со -180 1,084 1,41
монооксид 15 1,037 1,404
300 1,379
Фосфор р 300 1,17
Фосфора РС13 110-250 0,565
трихлорид
Хлор С12 15 0,481 1,355
300 1,297
Органические соединения
Ацетальде- С2Н4О 30 1,14
гид
Ацетилен С2Н2 -71 1,469 1,31
15 1,604 1,26
Ацетон СзН6О 130-230 1,725
Бензол С6н6 100 1,10
120-220 1,549
Бромэтан С2Н5Вг 38-116 0,674
14 1,19
(30,4 кПа)
У,У- c3h9n 18-25 1,184
Диметилме-
танамин
(триметил-
амин)
Диметило- c2Hbo 6-30 1,П
вый эфир
1,2-Дихлор- С2Н4С12 111-121 0,963
этан
Диэтиловый С4Н10О 35 1,863 1,08
эфир 35-189 1,934
Метан сн4 -115 1,885 1,41
-74 2,085 1,35
15 2,212 1,31
Окончание табл. 3.5.9
Название Формула Т, °C Ср, Дж/(г • К) с_^ су
Метан СН4 10-200 2,483
Метанамин ch5n 18-25 1,149
(метиламин) Метанол CH3OH 77 1,633 1,203
100 1,26
У-Метил- c2h7n 18-25 1,149
метанамин
(диметиламин) Оксалонит- c2n2 15 1,714 1,256
рил(дициан) Пент-1-ен С5Н,о 210 2,642
Пропан С3Н8 16 1,13
(50,7 кПа)
Пропан-1-ол С3Н8О 100-223 1,918
100 1,27
Пропан-2-ол С3Н8О 100 1,59
Пропионо- c3h5n 114-223 1,784
нитрил Тетрахлор- СС14 20(10,1 кПа) 1,13
метан 30(10,1 кПа) 0,553
70(10,1 кПа) 0,481
Уксусная С2Н4О2 118-140 6,28
кислота 136 140-180 5,317 1,15
Хлороформ СНС13 100 120-230 0,657 1,15
Хлорэтан С2Н5С1 16 1,19
100-170 (30,4-50,7 кПа) 1,151
Этан с2н6 -82 1,455 1,28
15 1,617 1,22
50 1,21
Этанамин c2h7n 18-25 1,135
(этиламин) Этанол С2н6о 90 1,7 1,13
100-223 1,901
Этилацетат С4Н8О2 80-189 1,554
Этилен с2н4 -91 1,292 1,35
15 1,504 1,255
15-100 1,671
100 25-200 1,8 1,18
Физические свойства важнейших веществ
291
Удельная теплоемкость ср газов в зависимости от температуры и давления
В табл. 3.5.10-3.5.22 приведены более подробные данные для некоторых газов.
Таблица 3.5.10
Удельная теплоемкость ср (Дж/(г • К)) азота (N2) при давлении до 10,1 МПа
Г, °C Давление, МПа
0,00101 0,0101 0,0405 0,0709 0,101 0,405 0.709 1.01 4.05 7,09 10,1
-150 1,0397 1,0409 1,0421 1,0495 1,054 1,107
-100 1,0397 1,0402 1,0419 1,0437 1,0472 1,0637 1,0833 1,1043
-50 1,0397 1,04 1,041 1,0419 1,0428 1,0524 1,0623 1,0724 1,1795 1,3063 1,4319
0 1,04 1,0401 1,0412 1,0413 1,0419 1,0478 1,0956 1,0598 1,1218 1,1836 1,2393
50 1,0408 1,041 1,0413 1,0418 1,0421 1,0461 1,0501 1,0542 1,0943 1,1325 1,1677
100 1,0429 1,043 1,0433 1,0436 1,0439 1,0467 1,0496 1,0525 1,0807 1,1075 1,1321
150 1,0468 1,0468 1,047 1,0472 1,0475 1,0496 1,0517 1,0539 1,075 1,0948 1,1131
200 1,0526 1,0527 1,0528 1,053 1,0531 1,0549 1,0565 1,0582 1,0745 1,0897 1,104
250 1,0604 1,0605 1,0606 1,0607 1,0609 1,0622 1,0635 1,065 1,0777 1,0899 1,1013
300 1,0699 1,0699 1,07 1,0701 1,0702 1,0713 1,0724 1,0835 1,0923 1,1005 1,1082
350 1,0806 1,0806 1,0807 1,0808 1,0809 1,0818 1,0827 1,0835 1,0923 1,1005 1,1082
400 1,0921 1,0921 1,0503 1,0923 1,0924 1,0931 1,0939 1,0946 1,1019 1,1088 1,1154
450 1,1041 1,1041 1,1042 1,1043 1,1043 1,1049 1,1056 1,1062 1,1124 1,1183 1,1239
500 1,1162 1,1163 1,1163 1,1164 1,1165 1,117 1,1176 1,1181 1,1234 1,1285 1,1334
600 1,1399 1,1399 1,1399 1,14 1,1401 1,1405 1,1409 1,1413 1,1424 1,1493 1,153
700 1,162 1,162 1,1621 1,1621 1,1622 1,1625 1,1628 1,1632 1,1663 1,1694 1,1723
800 1,1821 1,1821 1,1821 1,1822 1,1822 1,1825 1,1827 1,183 1,1855 1,188 1,1903
900 1,2 1,2 1,2 1,2 1,2 1,2002 1,2004 1,2006 1,2069 1,2047 1,2066
1000 1,2156 1,2156 1,2157 1,2157 1,2157 1,2159 1,2161 1,2163 1,2179 1,2221 1,2212
1200 1,2415 1,2415 1,2415 1,2415 1,2415 1,2416 1,2418 1,2419 1,2431 1,2441 1,2453
1400 1,2613 1,2613 1,2613 1,2614 1,2614 1,2614 1,2615 1,2616 1,2625 1,2633 1,2641
1600 1,2768 1,2768 1,2768 1,2768 1,2768 1,2769 1,2769 1,277 1,2776 1,2782 1,2788
1800 1,289 1,289 1,289 1,289 1,2891 1,2891 1,2892 1,2892 1,2897 1,2901 1,2906
2000 1,2989 1,2989 1,2989 1,2989 1,2989 1,299 1,299 1,2991 1,2994 1,2998 1,3001
2200 1,3071 1,3071 1,3071 1,3071 1,3071 1,3071 1,3071 1,3072 1,3075 1,3077 1,308
2400 1,3138 1,3138 1,3138 1,3138 1,3138 1,3139 1,3139 1,3139 1,3142 1,3144 1,3145
2600 1,3196 1,3196 1,3196 1,3196 1,3196 1,3196 1,3196 1,3197 1,3198 1,32 1,3201
Таблица 3.5.11
Удельная теплоемкость ср (Дж/(г • К)) азота (N2) при давлении выше 20,3 МПа
Т, °C Давление, МПа
20.3 30,34 40,5 50,7 60,8 81.1 10! 111 122
-70 1,809 1,813 1,8 1,788 1,784 1,779 1,771 1,767 1,758
-50 1,595 1,612 1,608 1,599 1,587 1,583 1,574 1,566 1,557
-25 1,474 1,503 1,482 1,47 1,453 1,44 1,432 1,424 1,411
0 1,382 1,411 1,403 1,39 1,377 1,361 1,352 1,344 1,331
25 1,34 1,382 1,382 1,373 1,365 1,352 1,34 1,336 1,331
50 1,252 1,298 1,315 1,319 1,315 1,31 1,302 1,298 1,294
100 1,189 1,239 1,264 1,281 1,29 1,294 1,302 1,315 1,331
200 1,13 1,164 1,185 1,197 1,214 1,239 1,256 1,26 1,269
300 1,105 1,126 1,143 1,156 1,172 1,185 1,197 1,197 1,202
400 1,097 1,114 1,122 1,13 1,139 1,147 1,156 1,156 1,16
500 1,084 1,097 1,105 1,И 1,118 1,126 1,135 1,135 1,135
Таблица 3.5.12
Удельная теплоемкость ср (Дж/(г • К)) аммиака (NH3) при давлении до 2,03 МПа
Т,°С Давление, МПа
0 0,101 0,203 0,304 0,405 0,507 0,608 0,709 0,811 0,912 1,01 1,11 1,22 1,32 1,42 1,52 1,62 1,72 1,82 1,93 2,03
-30 2,022 2,307
-20 2,035 2,236
-10 2,047 2,198 2,386
0 2,06 2,173 2,315 2,483 2,675
10 2,072 2,165 2,273 2395 2537 2,696 2,872
20 2,089 2,16 2,244 2,34 2,449 2,567 2,696 2,839 2,989
30 2,102 2,165 2,232 2,307 2,391 2,479 2,579 2,684 2,797 2,918 3,052 3,195
40 2,119 2,169 2,227 2,286 2,353 2,843 2,5 2,579 2,667 2,759 2,86 2,964 3,077 3,195 3,329 3,471
50 2,135 2,177 2,223 2,273 2,328 2,386 2,445 2,512 2,579 2,65 2,726 2,805 2,889 2,981 2,659 3,178 3,287 3,408 3,538 3,684 3,839
60 2,152 2,19 2,227 2,269 2,315 2,361 2,412 2,462 2,516 2,575 2,633 2,696 2,763 2,83 2,901 2,981 3,061 3,148 3,241 3,341 3,45
70 2,169 2,202 2,236 2,269 2,307 2,349 2,386 2,433 2,474 2,52 2,571 2,621 2,671 2,726 2,78 2,839 2,901 2,968 3,04 3,111 3,19
80 2,186 2,215 2,244 2,273 2,307 2,34 2,374 2,458 2,445 2,487 2,525 2,567 2,608 2,65 2,696 2,742 2,793 2,843 2,897 2,952 3,01
90 2,202 2,227 2,257 2,282 2,311 2,336 2,366 2,399 2,428 2,462 2,495 2,529 2,562 2,596 2,633 2,671 2,713 2,751 2,797 2,839 2,885
100 2,223 2,244 2,265 2,29 2,315 2,34 2,366 2,391 2,416 2,445 2,474 2,5 2,529 2,562 2,592 2,621 2,7 2,688 2,721 2,759 2,793
ПО 2,24 2,261 2,282 2,303 2,324 2,345 2,366 2,391 2,412 2,437 2,458 2,483 2,508 2,533 2,558 2,587 2,613 2,642 2,671 2,7 2,73
120 2,257 2,278 2,294 2,315 2,332 2,353 2,37 2,391 2,412 2,433 2,453 2,474 2,495 2,516 2,537 2,562 2,583 2,608 2,633 2,659 2,68
130 2,278 2,294 2,311 2,328 2,345 2,361 2,378 2,395 2,412 2,433 2,449 2,466 2,487 2,504 2,525 2,546 2,562 2,583 2,604 2,625 2,646
140 2,299 2,311 2,328 2,34 2,357 2,37 2,386 2,403 2,42 2,433 2,449 2,466 2,483 2,5 2,516 2,533 2,55 2,567 2,592 2,604 2,621
150 2,315 2,328 2,345 2,357 2,37 2,382 2,399 2,412 2,424 2,441 2,453 2,47 2,483 2,5 2,512 2,529 2,541 2,558 2,575 2,592 2,604
Давление, МПа 0,101 0,203 0,304 0,405 0,507 0,608 0,709 0,811 0,912 1,01 1,11 1,22 1,32 1,42 1,52 1,62 1,72 1,82 1,93 2,03
Т °C 1 кип? -33,35 -18,57 -8,91 -1,54 4,50 9,67 14,21 18,27 21,96 25,34 28,47 31,40 34,15 37,74 39,19 41,52 43,75 45,88 47,92 49,89
Ср ПрИ Т'кип 0,559 0,594 0,621 0,646 0,668 0,668 0,707 0,724 0,741 0,758 0,773 0,789 0,804 0,820 0,836 0,851 0,867 0,884 0,901 0,919
Таблица 3.5.13
292 Новый справочник химика и технолога
Удельная теплоемкость ср (Дж/(г • К)) аммиака (NH3) при давлении выше 2,03 МПа
Г, °C Давление, МПа
2,03 4,05 6,08 8,11 10,1 12,7 15,2 17,7 20,3 25,3 30,4 40,5 50,7 60,8 70,9 81,1 91,2 101,3
150 2,604 2,906 3,479 4,266 5,175 8,374 11,01 10,55 8,541 7,168 6,498 5,568 4,999 4,853 4,559 4,312 4,141 4,091
175 2,587 2,855 3,224 3,643 4,141 4,903 6,971 10,3 10,59 8,457 6,791 5,686 5,2 4,823 4,559 4,312 4,166 4,091
200 2,587 2,759 3,027 3,349 3,693 4,266 4,702 5,79 6,971 7,733 6,992 5,736 5,146 4,806 4,509 4,283 4,166 4,091
225 2,587 2,734 2,952 3,153 3,425 3,693 4,015 4,434 5,049 6,155 6,326 5,635 5,07 4,752 4,48 4,283 4,166 4,065
250 2,613 2,759 2,881 3,052 3,224 3,45 3,668 3,915 4,212 4,878 5,443 5,443 4,999 4,702 4,459 4,283 4,166 4,065
275 2,633 2,759 2,881 3,002 3,153 3,303 3,45 3,668 3,818 4,283 4,773 5,024 4,853 4,631 4,459 4,283 4,166 4,065
300 2,659 2,382 2,437 2,977 3,077 3,224 3,349 3,475 3,622 3,94 4,283 4,702 4,652 4,53 4,384 4,266 4,141 4,065
Физические свойства важнейших веществ
293
Таблица 3.5.14
Удельная теплоемкость ср (Дж/(г • К)) водорода (Н2) при давлении до 1,01 МПа
р, МПа Температура, °C
-250 -200 -150 -100 -50 0 50 100 150 200 250 300
0 10,32 10,57 11,89 13,1 13,82 14,21 14,39 14,47 14,5 14,52 14,53 14,55
0,101 10,93 10,64 11,91 13,11 13,82 14,21 14,39 14,47 14,51 14,52 14,53 14,55
1,01 — 11,26 12,07 13,19 13,88 14,24 14,41 14,48 14,52 14,53 14,54 14,56
Таблица 3.5.15
Удельная теплоемкость ср (Дж/(г • К)) водорода (Н2) при давлении выше 2,53 МПа
р, МПа Температура, °C
-75 -50 -25 0 25 50 100 200 300 400 500
2,53 13,69 14 14,15 14,32 14,4 14,44 14,53 14,57 14,57 14,61 14,7
5,07 13,86 14,1 14,24 14,36 14,44 14,49 14,57 14,57 14,61 14,65 14,7
7,6 13,98 14,2 14,32 14,44 14,53 14,57 14,61 14,61 14,61 14,65 14,7
10,1 14,11 14,3 14,4 14,49 14,57 14,61 14,61 14,61 14,61 14,65 14,7
15,2 14,36 14,5 14,57 14,61 14,65 14,65 14,7 14,65 14,65 14,65 14,74
20,3 14,57 14,7 14,65 М,7 14,74 14,74 14,74 14,65 14,65 14,7 14,74
30,4 14,86 14,9 14,86 14,86 14,86 14,82 14,82 14,74 14,7 14,7 14,74
40,5 15,03 15 14,95 14,95 14,95 14,91 14,86 14,74 14,74 14,74 14,78
50,7 15,11 15,1 15,03 15,03 14,99 14,95 14,91 14,78 14,74 14,74 14,78
60,8 15,2 15,2 15,07 15,07 15,03 14,99 14,95 14,82 14,78 14,78 14,78
81,1 15,32 15,2 15,16 15,11 15,07 15,07 14,99 14,86 14,78 14,78 14,82
101 15,41 15,3 15,24 15,2 15,11 15,07 15,03 14,86 14,82 14,82 14,82
111 15,49 15,4 15,24 15,2 15,16 15,07 15,03 14,86 14,82 14,82 14,82
122 15,49 15,4 15,24 15,2 15,16 15,11 15,03 14,86 14,82 14,82 14,82
Таблица 3.5.16
Удельная теплоемкость ср (Дж/(г • К)) диоксида углерода (СОД
Г, °C Давление, МПа
0,00101 0,0101 0,0405 0,0709 0,101 0,405 0,709 1,01 4,05 7.09 10,1
-50 0,7619 0,7639 0,7706 0,7777 0,7854
0 0,8178 0,8188 0,8216 0,8245 0,8273 0,8562 0,8855 0,9157
50 0,8698 0,8703 0,8719 0,8735 0,875 0,89137 0,95 0,9253 1,2058 1,6496 2,5791
100 0,9585 0,9169 0,9179 0,9189 0,9198 0,92989 0,9314 0,9508 1,0718 1,2351 1,457
150 0,9585 0,9587 0,9593 0,96 0,9605 0,96757 0,9743 0,9814 1,0588 1,1463 1,2405
200 0,996 0,9962 0,9967 0,9971 0,9977 1,00232 1,0073 1,0124 1,0634 1,1087 1,1371
250 1,03 1,03 1,0304 1,0307 1,0312 1,03456 1,0383 1,0421 1,0815 1,1229 1,161
300 1,0607 1,0607 0,9857 1,0613 1,0614 1,06428 1,0672 1,0701 1,0999 1,1325 1,166
350 1,0886 1,0887 1,0889 1,0891 1,0894 1,09192 1,094 1,0961 1,1472 1,1443 1,2351
400 1,1141 1,1142 1,1144 1,1146 1,1145 1,11662 1,1183 1,12 1,1388 1,1585 1,1794
450 1,1375 1,1376 1,1377 1,1378 1,138 1,13923 1,1409 1,1426 1,1577 1,1736 1,1899
500 1,1588 1,1588 1,1589 1,1591 1,1593 1,16016 1,1618 1,1631 1,1757 1,1882 1,2012
600 1,1958 1,1959 1,196 1,196 1,1962 1,19701 1,1978 1,1987 1,2079 1,2167 1,2255
700 1,2271 1,2272 1,2272 1,2273 1,2272 1,22799 1,2284 1,2292 1,2364 1,2426 1,2489
800 1,2535 1,2535 1,2535 1,2535 1,2535 1,25395 1,2548 1,2552 1,2606 1,2657 1,2703
900 1,2753 1,2753 1,2753 1,2753 1,2753 1,27614 1,2766 1,277 1,2812 1,2853 1,2891
1000 1,2946 1,2946 1,2946 1,2946 1,2946 1,29498 1,295 1,2958 1,2992 1,3025 1,3054
1100 1,3105 1,3105 1,3105 1,3105 1,3105 1,31047 1,3109 1,3113 1,3142 1,3172 1,3197
1200 1,3239 1,3239 1,3239 1,3239 1,3239 1,32428 1,3243 1,3247 1,3272 1,3297 1,3318
294
Новый справочник химика и технолога
Таблица 3.5.17
Удельная теплоемкость ср (Дж/(г • К)) кислорода (О2)
Г, °C Давление, МПа
0,00101 0,0101 0,0405 0,0709 0,101 0,405 0,709 1,01 4,05 7,09 10,1
-150 0,9104 0,9118 0,9163 0,921 0,9257
-100 0,9105 0,911 0,9128 0,9146 0,9164 0,93529 0,9561 0,9789 1,4235
-50 0,9116 0,9119 0,9128 0,9138 0,9147 0,92436 0,9343 0,9493 1,0681 1,2364 1,457
0 0,915 0,9156 0,9158 0,9167 0,9173 0,92319 0,9177 0,9352 0,9997 1,0685 1,1376
50 0,9231 0,9231 0,9235 0,9239 0,9243 0,92821 0,9322 0,9362 0,9772 1,0182 1,0559
100 0,9343 0,9344 0,9347 0,9349 0,9352 0,93801 0,9408 0,9437 0,9724 1,0006 1,0266
150 0,9482 0,9484 0,9486 0,9488 0,949 0,95107 0,9532 0,9553 0,9765 0,9973 1,0166
200 0,9638 0,9638 0,964 0,9641 0,9643 0,96594 0,9673 0,969 0,9856 1,0016 1,0136
250 0,9797 0,9798 0,9799 0,98 0,9802 0,98147 0,9828 0,984 0,997 1,0098 1,022
300 0,9954 0,9955 0,9956 0,9957 0,9958 0,99684 0,9979 0,999 1,0094 1,0199 1,03
350 1,0104 1,0104 1,0105 1,0106 1,0107 1,01157 1,0125 1,0133 1,022 1,0306 1,0392
400 1,0244 1,0244 1,0245 1,0246 1,0246 1,02539 1,0261 1,0269 1,0342 1,0413 1,0484
450 1,0373 1,0373 1,0374 1,0374 1,0375 1,03816 1,0388 1,0394 1,0456 1,0516 1,0576
500 1,0491 1,0491 1,0492 1,0492 1,0493 1,04984 1,0504 1,0511 1,0562 1,0614 1,0668
600 1,0695 1,0695 1,0696 1,0696 1,0696 1,07002 1,0704 1,0709 1,0749 1,0789 1,0827
700 1,0865 1,0865 1,0865 1,0866 1,0866 1,08694 1,0872 1,0876 1,0907 1,0938 1,0953
800 1,1007 1,1007 1,1007 1,1008 1.1008 1,101 1,1013 1,1015 1,104 1,1065 1,1087
900 1,1127 1,1127 1,1127 1,1127 1,1128 1,11298 1,1132 1,1134 1,1 154 1,1133 1,1196
1000 1,1232 1,1232 1,1232 1,1232 1,1232 1,12336 1,1236 1,1237 1,1254 1,1271 1,1288
1200 1,1411 1,1411 1,1412 1,1412 1,1412 1,14128 1,1414 1,1415 1,1427 1,1438 1,1451
1400 1,157 1,157 1,157 1,157 1,157 1,15706 1,1572 1,1573 1,1581 1,159 1,1597
1600 1,172 1,172 1,172 1,172 1,172 1,17209 1,1721 1,1722 1,1726 1,1735 1,174
1800 1,1866 1,1866 1,1866 1,1867 1,1867 1,18671 1,1867 1,1868 1,1873 1,1878 1,1882
2000 1,201 1,201 1,201 1,201 1,201 1,20107 1,2011 1,2012 1,2016 1,2019 1,202
2200 1,2151 1,2151 1,2151 1,2151 1,2151 1,21518 1,2152 1,2152 1,2156 1,2158 1,2158
2400 1,2287 1,2287 1,2287 1,2287 1,2287 1,22874 1,2288 1,2288 1,2291 1,2293 1,2297
2600 1,2417 1,2417 1,2417 1,2417 1,2417 1,24176 1,2418 1,2418 1,242 1,2422 1,2426
Таблица 3.5.18
Удельная теплоемкость ср (Дж/(г • К)) метана (СН4)
р, МПа Температура. °C
-70 -50 -25 0 25 50 100 150 200
1,01 2,252 2,252 2,252 2,252 2,252 2,303 2,462 2,617 2,801
2,03 2,328 2,328 2,328 2,328 2,328 2,328 2,487 2,613 2,801
3,04 2,826 2,617 2,437 2,407 2,382 2,407 2,537 2,617 2,801
4,05 3,977 2,931 2,667 2,093 2,462 2,462 2,562 2,667 2,826
5,07 4,396 3,479 2,881 2,617 2,537 2,537 2,617 2,696 2,851
6,08 5,074 3,793 3,165 2,772 2,617 2,617 2,667 2,721 2,851
8,11 5,259 4,237 3,609 3,165 2,772 2,696 2,747 2,801 2,906
10,1 4,317 4,237 4,082 3,479 2,931 2,826 2,772 2,851 2,931
12,2 3,295 3,793 4,396 3,663 3,115 2,931 2,906 2,906 3,006
14,2 2,801 3,349 4,551 3,793 3,375 3,035 2,956 2,981 3,01
16,2 2,587 3,086 4,421 3,818 3,534 3,14 3,01 3,035 3,061
18,2 2,437 2,956 4,107 3,818 3,689 3,245 3,086 3,086 3,086
20,3 2,303 2,826 3,584 3,768 3,743 3,295 3,115 3,115 3,115
25,3 2,093 2,587 3,295 3,663 3,663 3,429 3,19 3,19 3,19
30,4 1,959 2,407 3,086 3,504 3,534 3,454 3,22 3,22 3,22
40,5 1,805 2,227 2,851 3,245 3,295 3,295 3,245 3,245 3,245
50,7 1,75 2,119 2,721 3,115 3,22 3,245 3,245 3,245 3,245
60,8 1,725 2,119 2,696 3,035 3,165 3,22 3,22 3,22 3,22
81,1 1,725 2,119 2,667 2,931 3,061 3,14 3,14 3,14 3,14
101 1,725 2,093 2,617 2,881 3,01 3,086 3,086 3,086 3,086
Физические свойства важнейших веществ
295
Таблица 3.5.19
Удельная теплоемкость ср (Дж/(г • К)) монооксида углерода (СО) при давлении до 1,01 МПа
р, МПа Температура, °C
-50 0 50 100 150 200 250 300 350 400 450 500
0,00101 1,04 1,0404 1,0421 1,0454 1,0513 1,0593 1,0693 1,081 1,0936 1,1066 1,12 1,1329
0,0101 1,0404 1,0408 1,0421 1,0454 1,0513 1,0593 1,0693 1,081 1,0936 1,1066 1,12 1,1329
0,101 1,0438 1,0429 1,0434 1,0467 1,0521 1,0597 1,0697 1,081 1,0936 1,1066 1,12 1,1329
1,01 1,0764 1,063 1,0576 1,0567 1,0597 1,066 1,0743 1,0852 1,0969 1,1095 1,1225 1,1376
Таблица 3.5.20
Удельная теплоемкость ср (Дж/(г • К)) монооксида углерода (СО) при давлении выше 2,58 МПа
р, МПа Температура, °C
-70 -50 -25 0 25 50 100 150 200 300 400
25 1,1346 1,1137 1,1011 1,0886 1,0802 1,076 1,0718 1,0718 1,076 1,0928 1,1137
50 1,2435 1,2016 1,1639 1,1388 1,1221 1,0969 1,0886 1,0886 1,0886 1,1011 1,1221
75 1,3691 1,2895 1,2309 1,1891 1,1639 1,143 1,1221 1,1053 1,1053 1,1095 1,1262
100 1,5031 1,3816 1,2937 1,2393 1,2016 1,1765 1,143 1,1262 1,1 179 1,1179 1,1346
150 1,725 1,5324 1,3942 1,3188 1,2602 1,2225 1,1765 1,1514 1,1388 1,1346 1,143
200 1,8464 1,6161 1,4528 1,3607 1,2979 1,256 1,2016 1,1723 1,1556 1,1472 1,1514
300 1,905 1,6622 1,4905 1,3942 1,3314 1,2853 1,2309 1,2016 1,1849 1,1681 1,1723
400 1,8631 1,6412 1,4779 1,3942 1,3314 1,2937 1,2435 1,2184 1,2016 1,1388 1,1849
500 1,8254 1,6161 1,5072 1,3858 1,3314 1,2937 1,2477 1,2225 1,21 1,1932 1,1974
600 1,8338 1,6203 1,4654 1,3816 1,323 1,2895 1,2435 1,2267 1,2142 1,2016 1,21
800 1,8631 1,6412 1,4654 1,3691 1,3105 1,277 1,2351 1,2267 1,2184 1,2184 1,2309
1000 1,8799 1,6496 1,4696 1,3649 1,2979 1,2644 1,2267 1,2225 1,2225 1,2309 1,2435
1100 1,8841 1,6538 1,4696 1,3649 1,2937 1,2602 1,2225 1,2184 1,2225 1,2309 1,2477
1200 1,8882 1,6538 1,4738 1,3607 1,2895 1,2519 1,2184 1,2184 1,2225 1,2351 1,2519
Таблица 3.5.21
Удельная теплоемкость ср (Дж/(г • К)) хлорметана (СН3С1)
Таблица 3.5.23
Удельная и молярная теплоемкости ртути при постоянном давлении
р, МПа Температура, °C
-30 0 30 70 НО
0,0689 0,846 0,879 0,9 0,95 0,892
0,276 0,929 0,959 1,001
0,553 0,959 1,001 1,03
0,831 1,009 1,043 1,072
Таблица 3.5.22
Удельная теплоемкость ср (Дж/(г • К)) хлорэтана (С2Н5С1)
р, МПа Температура, °C
-30 0 30 70 НО
0,0139 0,879 0,921 1,001 1,059
0,139 1,022 1,093 1,13
0,278 1,03 1,13 1,172
Температура. °C Удельная теплоемкость, Дж/(г • К) Молярная теплоемкость, Дж/(моль • К)
Твердое состояние
-75,6 0,13356 26,7934
-73,9 0,13565 27,2134
-65,4 0,13565 27,2134
-69,5 0,13565 27,2134
-44,9 0,14068 28,2211
-42,2 0,14068 28,2211
-40,0 0,1411 28,3053
Жидкое состояние
-38,88 0,14104 28,2936
-20 0,1404 28,1654
0 0,13976 28,0377
20 0,13917 27,9188
25 0,13903 27,8904
40 0,13862 27,8083
60 0,13811 27,7066
80 0,13765 27,6136
100 0,13723 27,529
296
Новый справочник химика и технолога
Окончание табл. 3.5.23
Температура, °C Удельная теплоемкость, Дж/(г • К) Молярная теплоемкость, Дж/(моль • К)
120 0,13685 27,4533
140 0,13651 27,3859
160 0,13622 27,3272
180 0,13597 27,277
200 0,13576 27,2351
220 0,13559 27,2016
240 0,13547 27,1765
260 0,13538 27,1594
280 0,13534 27,1501
300 0,13533 27,1485
320 0,13536 27,1547
340 0,13543 27,1681
360 0,13553 27,1891
380 0,13567 27,2163
400 0,13584 27,2506
420 0,13605 27,2921
440 0,13628 27,339
460 0,13655 27,3926
480 0,13684 27,4516
500 0,13717 27,5169
Газообразное состояние
0 0,1037 20,8
100 0,1037 20,8
200 0,1037 20,8
300 0,1038 20,83
400 0,1042 20,9
500 0,105 21,06
3.6. Термодинамические свойства
В табл. 3.6.1 приведены: молярная теплоемкость и стандартная энтропия простых веществ и неорганических соединений, изменение энтальпии и свободной энергии при их образовании, изменение энтальпии при плавлении, испарении и фазовых превращениях.
Соединения расположены в алфавитном порядке химических символов.
В графе «Состояние» указано агрегатное состояние вещества в стандартных условиях, к которым относятся данные последующих четырех граф. В качестве стандартного состояния во всех случаях принято состояние чистого вещества при температуре 298,15 К (25 °C) и давлении 0,1 МПа (1 атм) Для твердых веществ стандартному состоянию обычно соответствует состояние устойчивой модификации. Температуры плавления и кипения приведены при нормальном давлении, за ис
ключением отдельных случаев, для которых соответствующие давления указаны в скобах.
В таблице приняты следующие обозначения:
С? — молярная теплоемкость вещества в стандартном состоянии, Дж / (моль • К);
5° — энтропия вещества в стандартном состоянии, Дж / (моль • К) ;
А 77° — стандартная теплота образования, т. е. изменение энтальпии при реакции образования данного соединения из простых веществ, когда каждое из реагирующих веществ находится в стандартном состоянии, кДж/моль ;
AF0 — стандартная свободная энергия образования, т. е. изменение изобарного потенциала при реакции образования данного соединения из простых веществ, когда каждое из реагирующих веществ находится в стандартном состоянии, кДж/моль;
Тпп — температура плавления, °C;
А//пл — изменение энтальпии при плавлении (теплота плавления), кДж/моль;
Гпр — температура фазового превращения, °C;
А//„р — изменение энтальпии при соответствующем фазовом превращении (теплота превращения), кДж/моль.
В тех случаях, когда в соответствующих графах приведены одинаковые значения температуры и давления как для равновесия между жидким и газообразным состоянием, так и для равновесия между твердым и газообразным состоянием, все величины относятся к тройной точке (равновесие твердой, жидкой и газообразной фаз данного вещества).
В табл. 3.6.2 приведены термодинамические свойства воды и перегретого водяного пара для интервала температур 0-750 °C и давлений от 1,01 кПа до 40,5 МПа.
Данные, расположенные выше горизонтальной прямой, относятся к жидкости, ниже — к пару.
Условные обозначения:
р — давление; Т — температура, °C; v — удельный объем, м3/кг; А/?0 — удельная энтальпия, кДж/кг; 5° — удельная энтропия, кДж/(кг • К).
В литературе встречаются также следующие названия и обозначения термодинамических функций: энтропия — ц; энтальпия (теплосодержание, тепловая функция Гиббса) — X, /; свободная энергия (изобарный потенциал, изобарно-изотермный потенциал, свободная энергия Гиббса) — Q, Z, G, Ф.
Термодинамические показатели
Таблица 3.6.1
Вещество Состояние с°, ДжДмоль • К) 5°, Дж/(моль • К) Д//°, кДж/моль Д/< кДж/моль Плавление Испарение Превращения
Тп11, °C A7/HJ1, кДж/моль гКИ1„ °C А7/11С11, кДж/моль Вид превращения Г11р. °C А7/пр, кДж/моль
Ag г. 20,80 173,0 289,4 250,5
ТВ. 25,06 28,97 0,000 0,00 960,8 11,30 2163 254,2
AgBr тв. (р) 52,42 107,2 -99,56 -96,00 430 9,13 1533 154,9 Р~>а 259
AgCN ТВ. 83,74 146,3 164,13 350 11,72
Ag2CO3 ТВ. 112,2 167,5 -506,6 -437,5
AgCl г. 35,76 244,9 97,26 70,3
ТВ. 50,83 96,17 -127,1 -109,8 455 13,23 1559 182,9
AgC102 ТВ. 87,38 134,7 0,00 66,99
AgC103 ТВ. -23,99 231
AgC104 ТВ. -32,45
Ag2CrO4 ТВ. 142,4 216,9 -712,4 -662,0
AgF ТВ. 83,74 -203,1 -185,1 435
AgF • H2O ТВ. -504,1
AgF • 2H2O ТВ. 159,1 -800,5 -665,7
AgF • 4H2O ТВ. -1388
AgF2 ТВ. -370,53
AgH ТВ. 29,27 204,6 283,4 254,6
Agl ТВ. (р) 54,47 114,3 -62,42 -66,35 557 9,42 1503 144,0 Р~>а 147 6,16
AgN3 ТВ. 279,4
AgNO2 ТВ. 78,71 128,2 -44,42 19,86
AgNO3 ТВ. (Р) 93,11 141,0 -123,2 -32,2 210 11,56 Р~>а 160 2,76
Ag2O ТВ. 65,61 121,8 -30,59 -10,83
Ag2O2 ТВ. -26,38
Ag2S (ромб.) ТВ. (Р) 145,7 -31,82 -40,28 842 14,07 Р~>а 179 4,40
тв. (а) 150,3 -29,35 -39,19
AgSCN ТВ. 87,92
Ag2SO4 ТВ.(Р) 131,5 200,1 -713,8 -616,2 660 16,75 Р~»а 412 7,96
Ag2Se ТВ.(Р) -12,14 Р~»а 133 7,12
Ag2SeO4 ТВ. 202,2 -396,5 -287,0
Al г. 21,4 164,6 314,0 273,4
ТВ. 24,36 28,34 0,000 0,000 660,1 10,88 2348 284,3
AlBr г. 7,54
AlBr3 ТВ. 102,6 184,2 -526,7 -505,4
A14C3 ТВ. 140,7 104,7 -129,4 -121,4
A1C1 г. -20,52
Физические свойства важнейших веществ 297
Продолжение табл. 3.6.1
Вещество Состояние с°^ Дж/(моль • К) 5°, Дж/(мо.ть • К) Д/7°, кДж/моль Д/Л кДж/моль Плавление Испарение Превращения
Тпп, °C А//и1. кДж/моль Гки„, °C А//иС11’ кДж/моль Вид превращения Т °C 7 нр^ А//,1р. кДж/моль
А1С13 ТВ. 89,18 167,5 -696,8 -637,2
А12С16 г. -1271 192 70.76 192 (возг.) 111,0
(0,2166 МПа) (0,2166 МПа) 180,1 (возг.) 111,8
А1С13 • 6Н2О ТВ. 376,8 -2684 -2271
A1F г. 215,2
A1F3 ТВ. 96,3 -1302 -1231 1256 (возг.) 322,4
A1F3- 1/2 Н2О ТВ. 117,2 -1496 -1397
A1F3 • ЗН2О ТВ. 209,3 -2299 -2053
А1Н г. 247,8
АП г. 128,1
АП3 ТВ. 202,0 -314,8 -314,0
A1N ТВ. 32,13 20,93 -241,6 -209,8 2200
(0,4052 МПа)
Al (NO3)3 • 6Н2О ТВ. 433,3 468,1 -2850 -2202
Al (NO3)3 • 9Н2О ТВ. 569,4 -3757 -2932
А12О3 (корунд) ТВ. 79,05 51,02 -1671 -1577 2700 108,8 2250
А12О3 • Н2О ТВ. 131,3 96,92 -1972 -1821
А12О3 • ЗН2О ТВ. 188,0 140,3 -2569 -2294
(гидраргиллит) A12S3 ТВ. 96,30 -509,0 -492,4
A12(SO4)3 ТВ. 259,6 239,4 -3437 -3094
A12(SO4)3 • 6Н2О ТВ. 493,2 469,3 -5309 -4627
Al2SiOs (андалузит) ТВ. 134,6 104,7 -2689 -2545
Al2SiO5 (дистен) ТВ. 121,4 86,68 2691 -2541
Al2SiO5 (силли- ТВ. 127,5 113,0 2717 -2575
манит) Аг г. 20,8 154,8 0,000 0,000
Аг • 5Н2О ТВ. -1489
As г. 20,8 174,3 253,9 212,4
As (металл) ТВ. 25,00 35,17 0,000 0,000
AsCl3 г. 327,4 -299,4 -285,1
ж. 233,6 -335,8 -295,2
AsF3 г. 289,3 -914,0 -898,9
ж. 126,9 181,3 -949,6 -902,2
298 Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние Дж/(моль • К) 5°, Дж/(моль • К) А//0, кДж/моль Д/Л кДж/моль Плавление Испарение Превращения
Т °C 7 ПЛ’ АН,,,,. кДж/моль гкип. °C ^Нпсп, кДж/моль Вид превращения 7пР, °C А7/„р, кДж/моль
AsH3 г. 38,55 222,6 66,99 -116,3 (3,28 кПа) 2,34 -62,5 17,53 0—>а -167,6 0,548
AS2O5 ТВ. 116,6 105,5 -915,2 -772,9
As4O6 (октаэдр.) тв.(0) 191,4 214,4 -1314 -1153 274 (3,73 49,83 274 (возг.) 109,3
кПа) (3,73 кПа)
As4O6(mohokji.) тв. (а) -1310 313 (8,93 36,84 313 (возг.) 92,30
кПа) (8,93 кПа)
457,2 59,45
ASS2 г. 35,03 239,9 123,9 73,27
As2S2 ТВ. -133,6 307 565 р—>а 267
AS2S3 ТВ. -146,5 300 р—>а 170
AsS4 г. 288,9 149,5 105,5
Au г. 20,8 180,5 344,5 304,9
ТВ. 25,25 47,73 0,000 0,000 1063,0 12,69 2847 310,7
AuBr ТВ. -18,42
AuBr3 ТВ. -54,43
AuCl ТВ. -35,17
AuCl3 ТВ. -11,85
Aul ТВ. 0,84
Au2O3 ТВ. 125,6 80,80 163,3
Au(OH)3 ТВ. 121,4 -418,7 -290,1
AuSb2 ТВ. (у) 79,55 -20,1 у->р 355 4,689
р—>а 405
AuSri ТВ. 52,34 418 25,62
В г. 20,81 153,4 407,0 361,4
ТВ. 11,97 6,53 0,000 0,000 2075 3860
BBr3 г. 68,04 324,4 -186,7 -213,5
ж. 229,0 -221,1 -219,4 -46 90,9 30,56
BC13 г. 62,67 290,1 -395,6 -380,6
ж. 209,3 -418,7 -379,3 -107 12,4 23,86
BF3 г. 50,49 254,1 -ни -1094 -128,7 4,19 -128,7 (7,20 кПа) 19,68
(7,20 кПа) -128,7 (возг.) 22,19
(7,20 кПа)
-101 18,00
BH г. 29,1 165,9 309,0 280,9
Физические свойства важнейших веществ 299
Продолжение табл. 3.6.1
Вещество Состояние с" ^р ’ Дж/(моль • К) S0. Дж/(моль • К) Д/Д кДж/моль М*. кДж/моль Плавление Испарение Превращения
г,,.,, °с кДж/моль 7’кип, °C ^НИсп, кДж/моль Вид превращения гпр. °C кДж/моль
в2н6 г. 56,44 233,0 31,40 82,90 -165,6 4,44 -92,53 14,44
В5н9 г. 79,55 275,8 62,80 165,8
ж. 149,89 184,9 32.66 162,4 -46,9 57,4 32,24
BN ТВ. 20,01 15,36 -254,1 -228,2
ВО г. 29,10 197,7 -22,19 -48,56
В2О3 ТВ. 62,30 54,05 -1264 -1185 450 22,06 1250 (266 Па) 322,4
В2О3 (стекл.) ТВ. 61,13 78,71 -1246 -1174
B2S3 ТВ. -238,7 310
Ва г. 20,80 170,4 175,7 144,8
ТВ. (Р) 26,38 66,99 0,000 0,000 717 1634 149,5 Р—>ос 375
704 (возг.) 172,1
(0,84 Па)
ВаСО3 (витерит) ТВ. (Р) 85,41 112,2 -1220 -1139 Р—>а 810 14,80
ВаС12 ТВ. 75,36 125,6 -860,6 -811,4 960 22,61 1189 (839,8 Па) 238,6 Р^а 925
ВаС12 Н2О ТВ. 118,07 167,5 -1166 -1060
ВаС12 • 2Н2О ТВ. 155,33 203,1 -1463 -1297
ВаСгО4 ТВ. -1433
BaF2 ТВ. 71,26 96,30 -1201 -1149 1353 12,56 1799(5,6 кПа) 374,8
ВаН г. 29,31 221,8 217,71 192,6
Ba(NO3)2 ТВ. 151,1 213,0 -992,5 -795,4 595 25,12
ВаО ТВ. 47,48 70,34 -558,5 -528.8 1920 1377 (возг.) 372,6
(0,1013 Па)
ВаО2 ТВ. -630,1
Ва3(РО4)2 ТВ. -4178 1727 77,87
BaS ТВ. —443,80
BaSO3 ТВ. -1183
BaSO4 ТВ. 101,8 132,3 -1466 -1354 1350 40,61 Р—>а 1 149
Be г. 20,80 136,3 320,83 283,0
ТВ. 17,84 9,55 0,00 0,000 1283 9,63 1283 (возг.) 314,8
(4,53 Па) (4,53 Па)
ВеС12 ТВ. -512,0 405 (2,67 Па) 109,7
BeH г. 29,12 171,0 327,0 298,52
ВеО г. 29,15 197,5 49,40 23,86
ТВ. 25,41 14,11 -611,3 -582,0 2550 2550 (возг.) 608,8
(26,13 Па) (26,13 Па)
Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние с° Дж/(молъ • К) 5ю, Дж/(моль • К) А//0, кДж/моль д/Л кДж/моль Плавление Испарение Превращения
Л.1- °C кДж/моль Лип, °C кДж/моль Вид превращения ЛР, °с кДж/моль
BeSO4 ТВ. 87,93 -1 197
Bi г. 20,80 187 208,1 169,2
ТВ. 25,54 56,94 0,00 0,00 271,3 11,01 1430
Bi2 г. 36,97 273,8 248,6 201,0
BiBr г. 257,9 53,17 15,91
BiCi г. 264,6 44,80 21,77
BiCl3 г. 79,63 355,5 -270,9 -260,4
ТВ. 189,7 -379,4 -319,2 229 10,88 440 72,64
Bil г. 265,4 66,99 46,06
Bi2O3 ТВ. 113,9 151,6 -577,4 -497,0 817 28,47
BiOCl ТВ. 86,25 -365,5 -322,4
Bi2S3 ТВ. 147,8 -183,4 -165,0 685 (разл.)
Br г. 20,80 175,0 111,8 82,40
Br2 г. 36,00 245,5 30,73 3,144 -7,3 10,55 25,00 (0,028 МПа) 30,73
BrCl г. 240,1 14,70 -0,879
C г. 20,85 158,1 718,9 673,4
С (алмаз) ТВ. 6,07 2,44 1,90 2,868
С (графит) ТВ. 8,65 5,70 0,00 0,00 4830 (возг.)
CBr4 г. 91,27 358,1 50,24 36,01 90,1 4,10 187 43,54 Р—^ос 46,9 6,280
CC14 г. 83,48 310,0 -106,8 -64,06 4,19
ж. 131,8 214,6 -139,4 -68,66 -22,9 2,51 76,7 30,02 Р—^ос -47,7 4,564
cf4 г. 61,25 262,2 -681,6 -635,6 -183,69 0,699 -128,02 12,60 Р—^ос -196,93 1,465
(CN)2 г. 15,07 242,2 -308,2 296,5 -34 8,11 -21,15 23,35
CNCI г. 44,80 235,8 144,4 137,7
CNI г. 48,32 256,5 228,6 199,71
ТВ. 129,0 169,2 178,36
CO г. 29,16 198,0 -110,6 -137,4 -205,06 0,84 -205,06 Р—^ос -211,63 0,628
(0,015 (0,015 МПа)
МПа) -191,5 6,046
CO2 г. 37,15 213,8 -393,8 -394,6 -52,6 (265,3 Па) -78,48 (возг.) 25,25
COS г. 41,53 230,7 -137,3 -169,4 -138,82 4,73 -50,24 18,52
CS2 г. 45,68 238,0 115,4 65,10
ж. 75,78 151,1 87,93 63,64 -112,1 4,40 46,25 26,80
Физические свойства важнейших веществ
Продолжение табл. 3.6.1
Вещество Состояние Дж/(моль • К) 5ю, Дж/(моль • К) Mf, кДж/моль Д/Л кДж/моль Плавление Испарение Превращения
Д.л. °C кДж/моль Лип. °C Д^ИСМ* кДж/моль Вид превращения Тпр, °C кДж/моль
Са г. 20,80 154,9 192,76 159,0
ТВ. 26,29 41,66 0,000 0,000 850 9,20 850 (46,66 Па) 184,2 Р->а 450 0,837
СаВь ТВ. 129,8 -675,3 -656,5
СаС2 ТВ. 62,38 70,34 -62,80 -67,83 Р~»а 447 5,57
СаСО3 (кальцит) ТВ. 81,94 92,95 -1208 -изо
СаСОз ТВ. 81,31 88,76 -1208 -1129
(арагонит)
СаС12 ТВ. 72,68 113,9 -795,5 -750,6 782 28,39 661,4 (возг.) 226,1
(2,4 Па)
СаСгО4 ТВ. 134,0 -1380 -1278 2160
CaF2 ТВ. 67,07 68,92 -1215 -1163
СаН2 ТВ. 41,87 -188,8 -150,0
СаНРО4 ТВ. 87,92 -1822 -1681
СаНРО4 • 2Н2О ТВ. 167,5 -2412 -2155
Са12 ТВ. 142,4 -535,1 -530,0
Ca3N2 ТВ. 94,20 104,7 -432,1 -368,9 1195
Ca(NO3)2 ТВ. 149,4 193,4 -937,8 -742,5 561 22,19
Ca(NO3)2 • 2Н2О ТВ. 269,2 -1541 -1229
Ca(NO3)2 • ЗН2О ТВ. 309,8 -1830 -1461 51,1
Ca(NO3)2 • 4Н2О ТВ. 339,1 -2133 -1702 39,7
CaO ТВ. 42,83 39,78 -636,0 -604,6 2600 5,02
CaO B2O3 ТВ. 104,0 105,1 -2023 -1916 1162 73,98
CaO • 2В2О3 ТВ. 158,0 134,8 -3344 -3150 987 113,3
2CaO • В2О3 ТВ. 147,2 145,3 -2728 -2590 1312 100,9 Р->а 531 4,606
ЗСаО • В2О3 ТВ. 188,0 183,0 -3424 -3254 1487 148,6
Са(ОН)2 ТВ. 84,57 76,20 -987,2 -897,4
Са3(РО4)2 тв. (а) 231,7 241,2 -4129 -3892
ТВ.(Р) 228,0 236,13 -4140 -3902
CaS ТВ. 47,44 56,52 -482,7 -477,7
CaSC)3 • 2Н2О ТВ. 178,8 184,2 -1764 -1566
CaSO4 ТВ. 99,65 106,8 -1434 -1321 1400 28,05 Р->а 1193
(ангидрит)
CaSO4 (раство- тв. (а) 100,1 108,4 -1425 -1312
римый) ТВ.(Р) 99,65 108,4 -1420 -1308
CaSO4 • */2 Н2О тв. (а) 119,7 130,6 -1576 -1436
тв.(р) 123,9 134,4 -1574 -1435
302 Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние с Дж/(моль • К) 5ю, Дж/(мо.1ь • К) Д/7°, кДж/моль Д/Л кДж/моль Плавление Испарение Превращения
Тпл, °C Д//[|Л1 кДж/моль Гкии, °C Д7/исп, кДж/моль Вид превращения Л,р, °с ДЯПр. кДж/моль
CaSO4 • 2Н2О ТВ. 186,31 194,1 -2022 -1797
CaSe ТВ. 66,99 -312,8 -307,7
CaSiO3 (волла- ТВ. 85,33 82,06 -1585 -1500
стонит)
CaSiO3(псевдо- ТВ. 86,54 87,50 -1580 -1496 1530 р—>а 1190
волластонит)
Cd г. 20,80 167,71 112,9 78,25 1400 99,90
ТВ. 25,92 51,50 0,000 0,000 320,9 6,11 320,9 (возг.) 110,0
(14,7 Па) (14,7 Па)
CdBr2 ТВ. 133,6 -314,6 -293,7 568 20,93 365 (возг.) 159,9
(0,43 Па)
CdBr2 • 4Н2О ТВ. 363,6 -1492 -1246
CdCO3 ТВ. 105,5 -748,2 -670,7
CdCl2 ТВ. 118,5 -389,4 -342,8 568 22,19 568 (возг.) 172,5
(128,8 Па) (128,8 Па)
CdCl2 • H2O ТВ. 170,8 -687,2 -586,7 968 123,1
CdCl2 • 2!4 H2O ТВ. 232,8 -ИЗО -944,0
CdF2 ТВ. 113,04 -690,4 -648,1 1100 22,61 1747 234,5
Cdl2 ТВ. 80,00 168,3 -201,0 -201,0 387 33,49 387 (возг.) 134,0
(63,98 Па) (63,98 Па)
Cd(NO3)2 • 4H2O ТВ. -1650 59,5 32,66
CdO ТВ. 43,46 54,85 -254,8 -225,2 1559 (возг.) 225,2
Cd (OH)2 ТВ. 95,46 -557,9 -470,8
CdS ТВ. 71,18 -144,4 -140,7 685 (возг.) 215,2
(1,68 Па)
CdSO4 ТВ. 137,3 -926,8 -820,6 1000
CdSO4 • H2O ТВ. 172,1 -1232 -1067
CdSO4 • % H2O ТВ. 242,4 -1724 -1464
Cd3Sb2 ТВ. 329,9 32,78 6,657 421
CdTe ТВ. 94,62 -101,7 -99,73 1042
Ce г. 355,9
ТВ.(у) 25,92 57,78 0,000 0,000 785 8,792 8—>у -133
у->р 393
р—>а 440
CeCl3 ТВ. -1090 822 33,49
Cel3 ТВ. -688,3 752
CeN ТВ. 46,89 -327,8
Физические свойства важнейших веществ 303
Продолжение табл. 3.6.1
Вещество Состояние л*0 ^р ’ Дж/(мопь • К) 5°, Дж/(моль • К) Д/7°, кДж/моль кДж/моль Плавление Испарение Превращения
Л,л- °C AM,.,-кДж/моль FK„„, °C А7/исп, кДж/моль Вид превращения Т’пр, °C АМ,Р, кДж/моль
СеО2 ТВ. -975,5
Ce(SO4)2 ТВ. -2345
Cl г. 21,86 164,5 121,5 105,5
ci2 г. 33,96 223,1 0,000 0,000
C1F г. 32,11 217,9 -55,68 -56,94
C1F3 г. 64,18 278,9 -154,9 -113,9
CIO г. 138,2
C1O2 г. 249,5 103,4 123,5
C12O г. 266,7 76,20 93,78
C12O7 г. 265,4
Co г. 23,04 179,53 439,6 393,56 у->Р 450 0,021
тв.(у) 25,58 28,47 0,000 0,000 1492 15,49 2255 Р~>а 1125 0,293
Co3C ТВ. 124,7 39,77 29,73
СоСОз ТВ. -723,1
CoCl2 ТВ. 78,71 106,34 -325,7 -282,61 740 30,98 1053 27,2
Co(NO3)2 ТВ. -430,8
CoO ТВ. 43,96 -239,5 -213,53 1805
CO3O4 ТВ. -879,2
CoS тв. (а) 47,73 -84,57 1100
тв.(р) -89,6
COSO4 ТВ. 113,5 -868,8 -762,4
Cr г. 20,80 174,3 337,0 292,2
ТВ. 23,32 23,78 0,000 0,000 1900 14,65
Cr3C2 ТВ. 97,89 85,41 -87,93 -88,76
Cr4C ТВ. 108,4 105,93 -68,66 -70,34
Cr7C; ТВ. 209,0 200,97 -177,9 -183,4
CrCl;> ТВ. 70,63 1 14,72 -395,9 -356,5 815(81,3 Па) 32,24 815 (возг.) 60,1
(81,3 Па)
CrCl3 ТВ. 90,14 125,6 -563,5 -494,0
CrCl4 г. -435,4
CrN ТВ. -124,8
CrO г. 272,1
CrO3 ТВ. -577,8
Cr2O3 ТВ. 118,8 81,22 -1130 -1048 2265 Р— 32,8
CrO2Cl2 ж. -568,1 116 35,17
Cr(OH)3 ТВ. -1035
Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние Дж/(моль • К) 5ю, Дж/(моль • К) Д/7°, кДж/моль Д/Л кДж/моль Плавление Испарение Превращения
Лы- °с ьнц11. кДж/моль Т °C 1 кип* кДж/моль Вид превращения F„p, °C ДМ,р, кДж/моль
Cs г. 20,80 175,6 78,84 51,25 р->а 783
ТВ. 31,07 82,90 0,000 0,000 28,7 2,0934 28,7 (возг.) 78,80
(0,16 мПа) (0,16 мПа)
690 68,33
CsA1(SO4)2 • ТВ. 620,1 686,6 -6069 -5102
• 12Н2О
CsBr ТВ. 51,92 121,4 -394,8 -383,5 642 15,07 1300 149,4 р->а 445 7.54
CsCl тв. (р) -433,3
CsC104 ТВ. 107,6 175,4 -434,8 -306,8 682 10,26 1252
CsF ТВ. -531,2
CsH г. 29,86 214,6 121,4 101,7
CsI ТВ. 51,91 127,6 -253,3 -333,7 417 13,61 р->а 156
CsNO3 ТВ.(Р) -494,5 490
Cs2O ТВ. -317,8
CsO2 ТВ. -260,0
Cs2O2 ТВ. -402,8 272,3 6,74 р->а 223 6,11
CsOH ТВ. (Р) -407,0 1019 р->а 660
Cs2SO4 ТВ. (Р) -1421
Cu г. 20,8 166,4 341,3 301,6 1083 13,02 2877 304,8
ТВ. 24,48 33,33 0,000 0,000
CuBr г. 36,05 247,9 159,1 117,2 488
ТВ. 91,72 -105,1 -99,69
CuCO3 ТВ. 87,92 -595,4 -518,3
CuCl г. 35,17 236,6 134,0 104,7
ТВ. 91,69 -134,8 -118,9 430 10,05
CuCl2 ТВ. -206,0
CuF г. 184,2
CuF2 ТВ. -531,2
CuF2 • 2H2O ТВ. 151,6 -1149 -984,7
CuH г. 29,22 196,3 297.3 268,0
Cui г. 36,42 256,6 259,6 209,34 588
ТВ. 54,09 96,72 -67,83 -69,57
Cul2 ТВ. (Р) -7,118 р->а 590
CuO г. -146,5
ТВ. 44,38 43,54 -155,3 -127,3
Cu2O ТВ. 69,92 100,9 -166,8 -146,4 1229 56,10
Физические свойства важнейших веществ
Продолжение табл. 3.6.1
Вещество Состояние с°, р ’ Дж/(моль • К) 5°, Дж/(моль • К) Д/Л кДж/моль д/Л кДж/моль Плавление Испарение Превращения
гпл, °C АНпп, кДж/моль 7’кин, °C А7/ИС|1, кДж/моль Вид превращения Д,р, °C А7/„Р, кДж/моль
Си(ОН)2 ТВ. -448,8
CuS ТВ. 47,86 66,57 -48,57 -48,99
Cu2S ТВ. 76,37 121,0 -79,55 -86,25 1127 23,03 Р— 103 5,61
CuSO4 ТВ. 100,9 113,5 -770,4 -662,4
CuSO4 • н2о ТВ. 131,0 149,9 -1084 -917,8
CuSO4 • 3H2O ТВ. 205,2 225,2 -1684 -1401
CuSO4 • 5H2O тв.(р) 281,4 305,6 -2280 -1881 Р— 54
Cu2Se ТВ. (3) 88,76 -23,03 1113 Р— 110 4,73
CuWO4 ТВ. -1047
CuWO4 • 2H2O ТВ. -1645
Dy г. 364,2
ТВ. 0,000 0,000
DyBr3 ТВ. 881
DyCl3 ТВ. 655
Dyl3 ТВ. 955
Er ТВ. 0,000 0,000
ErBr3 ТВ. 950
ErCl3 ТВ. -970,5 774
Erl3 ТВ. -586,2 1020
F г. 22,76 158,8 76,62 59,45
f2 г. 31,48 203,5 0,000 0,000 Р— -227,6 0,73
f2o г. 246,8 23,03 40,61
Fe г. 25,66 180,5 404,8 363,2
ТВ. 25,25 27,17 0,000 0,000 1530 15,07 2270 сс—^Р 760 0,0
1200 (возг.) 387,3 рн>у 907 0,91
(0,28 мПа) у—>6 1400 0,63
Fe3C (цементит) ТВ. 105,9 107,6 20,93 14,65
FeCO3 (сидерит) ТВ. 82,19 92,95 -748,2 -674,4
Fe(CO)5 ж. -786,3 -21 13,61 105 37,26
FeCl2 ТВ. 76,41 119,7 -341,2 -302,3 677 43,04 1012 126,5
FeCl3 ТВ. -405,3 304 (0,776 Па) 43,12 304 (0,776 Па) 26,12
304 (возг.) (0,776 Па) 69,08
319 25,04
FeCl3 • 6H2O ТВ. -2227 37
306 Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние хчО Дж/(моль К) 5°, Дж/(моль • К) Д/7°, кДж/моль AF0, кДж/моль Плавление Испарение Превращения
гШ1, °C А//„л, кДж/моль Гкип, °C А7/ИС11, кДж/моль Вид превращения 7’11р, °C АЯпр, кДж/моль
FeN ТВ. 156,6 4,606
Fe2N ТВ. 70,34 101,3 -3,768 10,89
Fe4N ТВ. 122,7 156,2 -10,68 3,726
Fe0,95O (вюстит) ТВ. 54,00 -266,7 -244,5 1368 31,40
Fe2O3 (гематит) ТВ. 104,7 90,01 -822,7 -741,5 Р—>а 1030
Fe3O4 (магнетит) ТВ. 146,5 -1118 -1015 1594 138,2
Fe(OH)2 ТВ. 79,55 -568,6 -483,9
Fe(OH)3 ТВ. -824,8
FeS ТВ. 54,85 67,41 -95,12 -97,64 Р^а 138 4,40
FeS2 (пирит) ТВ. 61,96 53,17 -178,0 -166,8
FeSO4 ТВ. -923,2
FeSO4 • 7H2O ТВ. -3009 64
FeTiF6 ТВ. 99,56 105,9 -1208 -1126 1367
(2,9 кПа)
FeWO4 ТВ. -1148
FeWO4 • 3H2O ТВ. -2038
Fe2(WO4)3 • 8H2O ТВ. -5664
Ga г. 27,86 169,1 276,3 238,6
тв. (а) 25,59 42,70 0,000 0,000 2,4 1,23 937 63,8 а^Р 2,4 2,14
(1181 МПа) (80 мПа) (1181 МПа)
29,780 5,594
тв. (р) 2,4 3,015
(1181 МПа)
GaBr г. 46,06
GaBr3 ТВ. -386,9
GaCl2 ТВ. 170,5
GaCl3 ТВ. -525,0 78 204
Gal г. 113,0
Gal3 ТВ. -214,4
GaN ТВ. -104,7
GaO г. 276,3
Ga2O ТВ. -343,3
Ga2O3 ТВ. 83,74 -1080 1740
Ga(OH)3 ТВ. -833,2
Ge г. 30,76 167,9 326,6 328,4
ТВ. 26,13 42,45 0,000 0,000 960 34,75
GeBr г. 36,17 145,7
Физические свойства важнейших веществ 307
Продолжение табл. 3.6.1
Вещество Состояние х'.О - Дж/(моль • К) 5°, ДжДмоль • К) ДЯ°. кДж/моль А/Л кДж/моль Плавление Испарение Превращения
Тнл, °C кДж/моль 7’кип, °C А77ИС11, кДж/моль Вид превращения 7„р, °C А7/нр, кДж/моль
GeCl г. 35,21 135,9
GeCl4 ж. -544,3 -49,6 85,8 33,08
GeH4 г. 45,05 214,4 Y~>P -200,0 0,209
Ge3N4 ТВ. -61,96 -165 0,837 -89,2 14,07 Р^а -196,7 0,360
GeO г. 30,94 220,1 -95,46 -118,1
GeO2 тв. (а) 710 (возг.)
тв.(р) 1116
GeO2 (стекл.) тв. (ам.) -537,17 1086 Р^а 1033
GeS г. 33,70 5,65 625
H г. 20,80 114,7 218,1 203,4
D г. 20,80 123,4 221,8 206,6
H2 г. 28,86 130,7 0,000 0,000 -259,20 0,117 -259,20
(7,2 кПа) (7,2 кПа)
-252,77 0,904
d2 г. 29,22 144,9 0,000 0,000 -254,44 0,197 -254,44
(17,1 кПа) (17,1 кПа)
-249,59
HD г. 29,22 143,8 0,155 -1,637 -256,56 0,160 -256,56
(2,2 кПа) (2,2 кПа)
-251,03
HAsO4 ТВ. -896,0
hbo2 ТВ. 46,06 -782,5 -713,8 236
НЗВО3 ТВ. 82,10 89,64 -1089 -963,8 185 разл.
HBr г. 29,14 198,6 -36,26 -53,25 -86,82 2,407 -66,73 17,63
HCN г. 35,92 202,1 130,6 120,2
HC1 г. 29,14 186,9 -92,37 -95,32
HC1O4 ж. -46,05
HC1O4 • H2O ТВ. -385,6
HCIO4 • 2H2O ж. -681,6
HF г. 29,09 173,6 -268,8 -270,9
HI г. 29,18 206,5 25,96 1,298 -50,80 2,872 -35,36 19,78
HIO3 ТВ. -238,8
H5IO6 ТВ. -772,0
HN3 г. 41,95 237,6 294,3 328,7 -80 36 29,73
HNO3 г. 266,4 -133,9 -73,50
ж. 109,9 155,7 -173,35 -79,96 -41,60 10,48 20 (6,4 кПа) 39,48
308 Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние с° Дж/(моль • К) 5ю, Дж/(молъ • К) А//0, кДж/моль Д/Л кДж/моль Плавление Испарение Превращения
Тш>, °C Д//Ш1. кДж/моль Гки„, °C кДж/моль Вид превращения Лф, °с кДж/моль
HNO3 • Н2О ж. 182,5 217,0 -472,9 -328,3 -37,63 17,52
HNO3 • ЗН2О ж. 325,4 347,2 -1055,9 -811,0 -18,47 29,11
Н2О г. 33,60 188,9 -242,0 -228,8
ж. 75,34 70,00 -286,0 -237,4 0,00 6,013 0,00 (0,6 кПа) 45,08
25,00 44,02
(3,2 кПа)
100,00 40,68
25,00 44,04*
HDO г. 33,74 199,5 -245,9 -233,7
ж. 78,92 79,34 -290,5 -242,5 25,00 44,6
(2,9 кПа)
D2O г. 34,29 198,4 -249,4 -234,7 3,82 6,28 25,00 42,68
ж. 82,48 76,04 -294,8 -243,7 (2,8 кПа)
25,00 45,43*
Н2О2 г. 233,5 -133,3 -0,4 10,55 25,00 54,47
ж. -187,7 (2,8 кПа)
НРО3 ТВ. -955,4
Н3РО2 ТВ. -609,2 26,5 9,71
ж. -599,6
Н3РО3 ТВ. -972,2 70,1 12,85
ж. -959,2
Н3РО4 ТВ. -1282 42,35 10,55
н4р2о7 ТВ. -2252 61 9,21
H2PtCl6 • 6Н2О ТВ. -2399
H2S г. 33,99 205,8 -20,16 -33,04 -85,53 2,39 -85,53 -169,62 1,53
(23,2 кПа) (23,2 кПа)
-60,2 18,68 5—>а -146,92 0,45
H2S • 6Н2О ТВ. -1805,3
H2s2 ж. -23,03 -89,8 7,54 70,3 (99,7 кПа) 35,17
H2s3 ж. -53 69
H2SO4 ж. -811,86 10,5 9,88
H2SO4 • H2O ж. -1126 8,53 19,38
H2S2O7 ж. -1267 34,9 13,35
HSO3C1 ж. -597,4
H2Se г. 221,5 85,83 71,17 -65,73 2,52 -65,73 22,36 -190,9 1,293
(27,4 кПа) (27,4 кПа)
-41,4 19,34 5—>а -100,62 1,118
Физические свойства важнейших веществ 309
Продолжение табл. 3.6.1
Вещество Состояние Дж/(моль • К) 5е, Дж/(моль • К) кДж/моль МЛ кДж/моль Плавление Испарение Превращения
Г,,л, °C кДж/моль 7™„, °C А^сп-кДж/моль Вид превращения 7'„p, °C АЯпр, кДж/моль
H2SeO3 ТВ. -529,6
H2SeO4 ТВ. -538,4 60 14,44
H2SeO4 • Н20 ТВ. -849,9 26 19,89
H2SiO3 ТВ. -1133
H4SiO4 ТВ. -1426
H2Te г. 234,5 154,5 138,6 -49,0 4,2 -1,з 23,24
H2TeO3 ТВ. 199,7 -605,8 -484,4
Н2ТеО4 • 2Н2О ТВ. 196,8 -1284 -1027
H2WO4 ТВ. -1171
Hg г. 20,8 175,0 61,04 31,78
ж. 27,84 77,45 0,000 -38,87 2,33 -38,87 (возг.) 63,64
(0,33 мПа) (0,33 мПа)
25,00 60,88
(2,8 Па)
356,57 58,15
HgBr г. 36,93 272,14 96,30 75,36
HgBr2 ТВ. -169,6 241 16,58 241 (возг.) 78,79
(15,5 кПа) (15,5 кПа)
321 58,95
Hg2Br2 ТВ. 213,1 -206,9 -178,83
HgCl г. 36,21 260,4 79,55 58,61
HgCb ТВ. 76,62 -230,3 277 17,37 277 77,45
(55,7 кПа) (55,7 кПа)
304 58,95
Hg2ci2 ТВ. 101,74 195.94 -265,1 -210,8
Hg(CN)2 ТВ. -261,7
Hg(SCN)2 ТВ. 201,0
HgH г. 29,92 219,47 243,1 220,2
Hgl г. 37,22 280,9 138,2 96,29
Hgl2 ТВ.(р) -105,5 257 18,96 257 (1,17 кПа) 83,15 Р—>а 129 2,52
тв. (а) -102,8 (1,17 кПа) 354 59,7 (25,99 Па)
Hg2I2 ТВ. 105,92 239,48 -121,0 -111,37
Hg2(N3)2 ТВ. 556,8
HgNO3 • ’ЛН2О ТВ. -389,4
Hg2(NO3)2-2H2O ТВ. -866,3
HgO (красн.) ТВ. (р) 45,76 72,01 -90,77 -58,57
HgO (желт.) тв. (а) 73,27 -90,27 -58,44
Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние с°, р > Дж/(моль • К) 5ю, Дж/(мо.ть • К) А//0, кДж/моль лЛ кДж/моль Плавление Испарение Превращения
гпл, °C кДж/моль °C А7/Исп, кДж/моль Вид превращения 7иР, °C ая1!Р. кДж/моль
Hg2O ТВ. 91,27
HgS тв.(p) 77,87 -58,20 -48,86 р—>а 386 4,2
тв. (a) 83,32 -54,01 -46,26 (10,6 кПа)
Hgso4 ТВ. -704,6
Hg2SO4 ТВ. 132,13 200,9 -742,5 -624,33
In г. 25,18 173,8 243,7 207,66
ТВ. 27,42 52,33 0,00 0,000 156,2 3,26 927 (0,9 Па) 233,2
InBr г. 36,72 259,58 41,87 4,2 220 656 92,1
InBr3 ТВ. -404,0 436 371 105,1
(0,65 МПа)
InCi г. 36,0 248,28 -75,36 -111,96
ТВ. (Р) -186,3 225 627 90,0 р—>а 120
InCI2 ТВ. -363,4 235 488 192,6
InCl3 ТВ. -537,6 586 442 (возг.) 159,1
(13,3 МПа) (13,3 МПа)
InH г. 29,56 207,66 213,5 188,4
Ini г. 34,88 267,12 83,74 37,68 369 710 90,85
Inl3 ТВ. -230,27 210
Ir г. 20,8 193.64 690,82 644,77
ТВ. 24,7 36,42 0,000 0,000 2443 4180
IrCl ТВ. -93,35
IrCI2 ТВ. -179,2
IrCl3 ТВ. -257,5
IrF6 ж. -544,3 53 36,0
IrO2 ТВ. 57,36 -167,9
I г. 20,8 180,8 106,7 70,19
ь г. 36,88 260,75 62,28 18,0
ТВ. 55,01 116,81 0,000 0.000 113,6 15,66 25,00 (возг.) 62,3
(41,32 Па)
IBr г. 36,38 258,7 40,82 3,8
IC1 г. 35,42 247,5 17,58 -5,53 27,3 (4,4 кПа) 7,66 27,3 (4,4 кПа) 41,57
IC13 ТВ. 172,1 -88,34 -22,4
12O5 ТВ. -177,27
К г. 20,80 160,4 90,06 61,21
ТВ. 29,18 63,64 0,000 0,000 63,6 2,48 776
K2 г. 249,9 128,9 92,53
KAg(CN)2 ТВ. -16,33
Физические свойства важнейших веществ
Продолжение табл. 3.6.1
5°. Дж/(моль • К) Плавление Испарение Превращения
Вещество Состояние с° р ’ Дж/(моль • К) Д/7°, кДж/моль Д/^. кДж/моль Тпп. °C А//,,.., кДж/моль т °C д//ИС11. кДж/моль Вид превращения Г11р, °C А//цр, кДж/моль
KA1(SO4)2 KA1(SO4)2 • • 12Н2О КВг КВгОз KCN KCNO К2СО3 К2С2О4 КС! КС1О3 КС1О4 К2СгО4 К2Сг2О7 KF K4[Fe(CN)6] • •ЗН2О КН KH2AsO4 КНСОз khf2 КН2РО4 KHS KHSO4 KI ТВ. ТВ. г. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. г. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. г. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. г. ТВ. 193,09 651,46 36,63 53,67 104,96 36,26 51,54 100,32 110,24 49,11 126,82 76,91 36,76 55,10 204,7 687,89 250,66 96,51 149,26 239,65 82,73 143,06 151,14 66,61 598,7 198,0 155,2 104,3 258,07 104,4 -2467 -6061 -392,43 -332,43 -112,62 -412,40 -1147 -1343 -216,0 -436,2 -391,5 -433,8 -1383,7 -2034,4 -562,96 -1424,7 125,60 -56,94 -1136,7 -960,03 -921,01 -1569 -264,61 -1158,9 -327,87 -2237 -5141 -379,5 -243,7 -235,3 -408,6 -290,1 -304,4 -533,48 105,09 992,27 -853,0 -322,5 91 735 (39,99 Па) 610 896 772 (53,32 Па) 980 398 856 238,7 218,6 682 28,05 29,3 14,65 32,66 25,54 28,89 35,39 28,47 6,61 735 (возг.) (39,99 Па) 1386 772 (возг.) (53,32 Па) 1406 1502 1323 204,7 155,3 207,25 162,42 172,9 Р—>а (3—>а 8— у->р Р^а Р^а Р^а Р~>а Р~>а Р-»а Р—>а Y->p Р^а -215,3 -104,9 250 428 622 299,5 665 241,6 -177,59 196,0 180 164,2 180,5 0,197 1,256 13,77 10,26 0,35 11,13 2,3 2,05 0,39
312 Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние Дж/(моль • К) 5°, Дж/(мо.ть • К) Д/У°, кДж/моль AF0, кДж/моль Плавление Испарение Превращения
°C ДЯ1Ь1, кДж/моль 7к„„, °C А7/исп, кДж/моль Вид превращения Д.Р, °с кДж/моль
КЮз ТВ. 106,43 151,56 -508,69 -425,8 560
КМпО4 ТВ. 119,32 171,83 -813,91 -714,3 >200 (разл.)
kno2 ТВ. -370,53 440
KNO3 ТВ. 96,34 133,01 -493,04 -393,4 337 11,72 Р->а 127,7 5,44
К2О ТВ. -361,74 1300 154,9
К2О4 ТВ. -561,03 400
кон ТВ. -426,13 400 7,53 1327 128,95 Р—>а 249 6,36
K2PtCl4 ТВ. -1064,3
K2PtCl6 ТВ. 205,57 334,11 -1260,2 -1109,9
K2S ТВ. -418,68 Р—>а 146,4 0,355
KSCN ТВ. -203,56 177 10,46 Р—>а 140,6 0,125
K2so3 ТВ. -1117,5
K2SO4 ТВ. (Р) 130,2 175,84 -1434,6 -1317,3 1069 36,67 Р—>а 583 8,12
K2S2O5 ТВ. -1518,1
Kr г. 20,80 164,08 0,000 0,000 -157,21 1,63 -157,21
(73,2 кПа) (73,2 кПа)
-153,4 9,03
Kr • 5H2O ТВ. -1495,1
La г. 22,76 182,4 368,4 330,76
ТВ. (у) 27,63 57,36 0,000 0,000
LaCl? ТВ. -1103,6 870 5->у -163
у->р 548
Р—>а 709
Lal3 ТВ. -700,9
La2O3 ТВ. 101,32 -1917,6 2305
La(OH)3 ТВ. -1309,6
La2(SO4)3 • 9H2O ТВ. 636,39 -5875
Li г. 20,80 138,76 155,20 122,21
ТВ. 23,65 28,05 0,000 0,000 180 4,187 1350 Р—>а -196
Li? г. 35,67 197,03 199,3 157,42
LiBr г. 33,99 225,16 -171,65 -209,34
ТВ. 51,91 -350,52 552 12,14 1310 148,21
Li2CO3 ТВ. 97,47 90,43 -1216,43 -1133,2 735
LiCl г. 32,99 213,57 -221,9 -242,83 610 (возг.) 193,43
(1,87 кПа)
ТВ. 51,08 -409,05 614 13,39 1380 150,72
Физические свойства важнейших веществ
Продолжение табл. 3.6.1
Вещество Состояние с(| Дж/(моль • К) 5°, Дж/(моль • К) даД кДж/моль д/Д кДж/моль Плавление Испарение Превращения
Д.. °C ДДь.-кДж/моль Дип, °C Д7/исп, кДж/моль Вид превращения ДР. °C А//пр, кДж/моль
LiCl • Н2О ТВ. 97,97 103,83 -713,05 -214,36
LiF ТВ. 42,03 35,88 -612,53 -584,48 845 10,05 1680 213,53
LiH г. 29,56 170,7 128,53 105,5
ТВ. 34,75 24,70 -90,48 -70,0
Lil г. 34,83 233,12 -66,99 -108,85
ТВ. 54,42 -267,95 446 1170 170,82
LiNO3 ТВ. -482,65 254 25,54
Li2O ТВ. -596,20
Li2O2 ТВ. -635,14
LiOH ТВ. 50,24 -487,55 -444,22 471 20,9 Р—>а 413
LiOH • H2O ТВ. 92,11 -790,34 -705,05
Li2SO4 тв. (р) -1435,4 859 12,56 [3—>а 575 28,47
Mg г. 20,80 148,65 150,31 115,55
ТВ. 23,91 32,53 0,000 0,000 650 (0,4 кПа) 9,21 1103 131,88
MgBr2 ТВ. -517,9 711 34,75
MgBr2 • 6H2O ТВ. 397,74 -2409,1 -2055,7 172,4
MgCO3 ТВ. 75,57 65,73 -1113,7 -1030,0
MgCl2 ТВ. 71,34 89,60 -642,25 -592,72 714 43,12 1417 136,9
MgCl2 • H2O ТВ. 115,05 137,32 -967,78 -862,94
MgCl2 • 2H2O ТВ. 159,18 180,03 -1281,12 -1119,21
MgCl2 • 4H2O ТВ. 241,58 264,19 -1900,8 -1634,9
MgCl2 • 6H2O ТВ. 315,94 366,34 -2501,3 -2117,05 117 34,33
MgF г. 32,74 229,64 -83,73 -113,04
MgF2 ТВ. 61,63 57,27 -1103 -1050 1263 58,19 2227 272,14
MgH г. 29,51 199,3 171,66 142,35
Mg3N2 ТВ. 104,63 -461,55 Р—>а 788 1,09
у-»р 550 0,92
Mg(NO3)2 ТВ. 142,10 164,1 -790,13 -588,8
Mg(NO3)2 • 6H2O ТВ. -2614,1 89,9 41,03
MgO ТВ. 37,43 26,79 -602,23 -569,95
Mg(C)H)2 ТВ. 77,08 63,18 -925,28 -834,3
Mg(OH)Cl ТВ. 82,90 -800,93 -732,7
MgSO4 ТВ. 96,34 91,69 -1279,1 -1174,4 1127 14,65
MgSO4 • 2H2O ТВ. -1599
MgSO4 • 4H2O ТВ. -2493
MgSO4 • 6H2O ТВ. -3084
MgSO4 • 7H2O ТВ. -3385,9
314 Новый справочник химика и технолога
Продолжение табл. 3.6.1
5°, Дж/(моль • К) Плавление Испарение Превращения
Вещество Состояние Ср ' Дж/(моль • К) АЯ°, кДж/моль Д/Л кДж/моль Г„л, °C Ж.., кДж/моль Л,„„ °C А7/ИС11. кДж/моль Вид превращения Кг °C кДж/моль
Mg2Si ТВ. -77,87 1102
MgSiO3 ТВ. 81,89 67,82 -1498,5 -1411,8 1525 61,54
Mg2SiO4 ТВ. 118,1 95,04 -2044 -1925,1 1885
Мп г. 20,80 173,72 286,12 243,8 8—>у 727 2,26
тв. (5) 26,33 31,78 0,000 0,000 1220 14,56 2120 224,8 у-*Р 1101 2,26
тв. (р) 27,59 32,32 1,55 1,38 Р—>ot 1137 1,80
MnBr2 ТВ. -379,74 698
Мп3С ТВ. (Р) 93,53 98,8 -4,19 -4,19 Р— 1310 12,97
МпСОз ТВ. 81,56 85,82 -895,55 -818,1
МпС12 ТВ. 72,93 117,23 -482,74 -441,7 650 37,68 1231 120,6
MnF2 тв. (а) 67,99 92,94 -791,3 -749,44 856
Mn(NO3)2 ТВ. -696,35
MnO тв. (а) 42,99 60,28 -385,2 -363,41 1780
МпО2 тв. (а) 54,05 53,17 -521,25 -466,41
Мп2О3 тв. (Р) 108,02 -971,8 Р— 600
Мп3О4 тв. (а) 139,38 148,63 -1387,5 -1281,16 1560 Р— 1172 18,84
Мп(ОН)2 тв. (ам.) 88,34 -694,2 -610,85
MnS тв. (а) 49,99 78,29 -204,31 -208,9 1615
MnSO4 ТВ. 100,23 112,2 -1064,5 -956,6 700
MnSe тв. (а) 51,08 90,85 -117,23 -122,25
MnSiO3 ТВ. 86,41 89,18 -1266,5 -1186,12 1272 33,49 у-*р 1120
MnSiO3 (стекл.) ТВ. -1231 Р— 1208
Mo г. 20,80 181,96 651,05 603,74 2610
ТВ. 23,49 28,59 0,000 0,000
MoBr2 ТВ. -230,27
MoBr3 ТВ. -272,14
MoBr4 ТВ. -305,63
Mo2C ТВ. 82,48 18,00 12,14 2672
MoCl2 ТВ. -288,9
MoCl3 ТВ. -393,56
MoCl4 ТВ. -479,8
MoCl5 ТВ. -529,63 194 7,53 268 58,19
Mo02 ТВ. 76,62 -589,5
Физические свойства важнейших веществ
Продолжение табл. 3.6.1
Вещество Состояние с'1. Дж/(моль • К) 5°, Дж/(моль • К) Д/У°, кДж/моль ДЛ°. кДж/моль Плавление Испарение Превращения
Тпл, °C кДж/моль Т °C 1 кип* кДж/моль Вид превращения 7’нр, °C А/7пр, кДж/.моль
МоО3 ТВ. 73,64 78,2 -755,0 -678,05 795 52,5 700 (возг.) 272,14
(1,33 кПа) (39,99 Па)
1155 138,16
МоО2Вг2 ТВ. -622,16
МоОС14 ТВ. -644,77
МоО2С12 ТВ. -724,31
MoS2 ТВ. 63,51 63,22 -232,36 -225,25
MoS3 ТВ. -256,23
N г. 20,80 153,29 358,24 341,1
n2 г. 29,14 191,62 0,000 0,000 -210,01 0,72 -210,01 Р^а -237,54 0,23
(12,5 кПа) (12,5 кПа)
-195,82 5,58
NH3 г. 35,68 192,63 -46,22 -16,65 -77,76 5,65 -77,76
(6,1 кПа) (6,1 кПа)
-33,43 23,36
n2h4 ж. 50,45 0,7 113,5 41,86
(0,1 МПа)
n2h4 • НС1 ТВ. -196,5 92,6 15,24
N2H4 • 2HC1 ТВ. -376,81 198
N2H4 • H2O ж. -242,62 -40 118,5
N2H4 • H2SO4 ТВ. -969,66 254
NH4A1(SO4)2 ТВ. 226,6 216,45 -2349,8 -2034,6
NH4A1(SO4)2 • ТВ. 683,7 697,52 -5942,7 -4936,3 95 Р—>а -202,2 0,81
• 12H2O
nh4ci ТВ. (Р) 84,15 94,62 -315,60 -204,02 520 520 Р—>ос 184.4 4,18
(3,5 МПа) (3,5 МПа)
NH4H2AsO4 ТВ. 172.16 -1052,8 -825,80
nh4h2po4 ТВ. 142,35 152.06 -1451,8 -1216,1
nh4no3 ТВ. 182,12 —365,38 169,6 5,44 £—>8 -18 0,54
8— 32,1 1,59
Y~>P 84,2 1,34
Р—>а 125,2 4,23
nh2oh ТВ. -106,76 33,1 58 (2,9 кПа)
nh2oh • HC1 ТВ. 92,1 -309,82 157
(NH4)2SO4 ТВ. 187,61 220,43 -1180,1 -900,95 513
nh4vo3 ТВ. 129,41 140,67 -1051,7 -886,76
316 Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние с° Дж/(моль • К) 5ю, Дж/(моль • К) Д/Д кДж/моль ДЛ°, кДж/моль Плавление Испарение Превращения
Т'.и,- °с Д//и.„ кДж/моль Гки... °C А7/исп, кДж/моль Вид превращения Др. °с кДж/моль
NO г. 29,88 210,76 90,43 86,74 -163,65 2,3 -163,65
(21,9 кПа) (21,9 кПа)
-151,77 13,78
no2 г. 37,93 240,61 33,87 51,87
n2o г. 38,73 220,14 81,60 103,66 -90,86 6,43 -90,86
(87,8 кПа) (87,8 кПа)
-88,48 16,56
n2o3 г. 83,73 -111 2 39,35
n204 г. 79,13 304,5 9,66 98,35 -11,20 14,66 -11,20(18,6 кПа)
(18,6 кПа) 20,7 38,14
n205 ТВ. -41,87 32,4 (возг.) 56,94
NOBr г. 272,81 81,89 82,48 -55,5
NOCI г. 263,77 52,63 66,40 -61,5 -61,5
(5,14 кПа) (5,14 кПа)
-4,4 25,12
Na г. 20,80 153,72 108,77 78,16
ТВ. 28,43 51,08 0,000 0,000 98 2,63 900
Na2 г. 230,35 142,23 104,04
NaBH4 тв. (а) 86,66 104,75 -183,46 -119,61
NaBO2 ТВ. 69,08 -1059,3
Na2B4O7 ТВ. 200,96 -3256,1 742
NaBr г. -152,1 750 25,54 750 (возг.) 206,4
(5,3 кПа)
ТВ. 52,33 -360,19 1392 162,03
Na2C2 ТВ. 17,16
NaC2H3O2 ТВ. -710,92 Р—>а 198
NaCN ТВ.(у) -89,85 562 16,74 1497 154,91 у->Р -101,1 0,63
Р—>а 15,3 2,93
Na2CO3 ТВ. 110,57 136,07 -1131,69 -1048,37 854 33,49 8—>у 356
у->Р 486
Р—>а 618
NaCl г. -182,12 808 28,47 808 (возг.) 215,62
ТВ. 49,74 72,43 -411,27 -384,28 (66,65 Па) (66,65 Па)
1465 170,82
NaC103 ТВ. -358,93 255 22,6
NaC104 ТВ. (Р) -385,93 308
Физические свойства важнейших веществ
Продолжение табл. 3.6.1
Вещество Состояние с°, р ’ Дж/(моль • К) 5°, Дж/(молъ • К) д/А кДж/моль Д/А кДж/моль Плавление Испарение Превращения
°с A//1l.,. кДж/моль Т °C А7/Исп. кДж/моль Вид превращения Л,Р, °C А^пр-кДж/моль
NaF г. -301,44 995 (66,65 Па) 32,65 995 (возг.) 263,77
(66,65 Па)
ТВ. 46,05 58,62 -569,40 -541,35 1704 209,34
NaH г. 29,31 188,11 125,1 103,75
ТВ. -57,36
N аНСОз ТВ. 87,67 102,16 -948,31 -852,43
Nal г. -87,67
ТВ. 54,43 -288,22 662 21,77 1304 1599,93
Na2MoO4 ТВ. -1524 687 15,07 6->у 440 61,13
у-»р 586
Р~>а 630
NaNH2 ТВ. -118,9 208
NaNO2 тв.(р) -359,6 р—>а 162
NaNO3 ТВ.(Р) 93,11 116,39 -466,99 -366,13 310 15,9 Р~>а 275
NaO2 ТВ. 77,18 115,97 -259,16
Na2O ТВ. 68,24 72,85 -416,17 -376,8
Na2O2 ТВ. 89,39 94,62 -504,93 460
NaOH ТВ. 80,38 -427,01 320 7,12 Р~>а 299,6 4,18
NaOH • H2O ТВ. 84,57 -733,4 -623,83
NaPO3 ТВ. -1208,3 625
Na2S ТВ. -373,46 950 6,69
NaSCN ТВ. -174,7 323 18,42
Na2SO3 ТВ. 120,16 146,12 -1091,1 -623,83
Na2SO4 ТВ.(Р) 127,69 149,59 -1385,4 -1002,7 890 24,28 р->а 240 7,03
Na2SO4 • ТВ. 587,82 593.27 -4327,0 -1267,7
• 10H2O
Na2S2O3 • тв. (а) 360,9 -2603,7 48,5 23,44
• 5H2O
Na2SiO3 ТВ. 111,87 113,88 -1519,8 -1427,7 1089 52,33
Na2Si2O5 ТВ. 156,63 164,96 874 35,59
Na2WO4 ТВ. -1653,8 695,5 23,86 Y->p 587,6 30,98
Р~>а 588,8 4.18
Nb г. 30,18 186,28 772,46 727,25
ТВ. 0,000 0,000
318 Новый справочник химика и технолога
Продолжение табл. 3.6. ]
Вещество Состояние с" Дж/(моль • К) 5°, Дж/(мо.ть • К) Д/Д кДж/моль д/Д кДж/моль Плавление Испарение Превращения
Тп11, °C кДж/моль г °C Д/7цС1Г кДж/моль Вид превращения 7„Р, °C Д77цр, кДж/моль
NbCl5 ТВ. 34,75 -798,00 210 35,59 210 (возг.) 85,41
(44 кПа) (44 кПа)
250 52,75
NbF5 ТВ. 78,9 233 46,47
NbO ТВ. -418,26
NbO2 ТВ. -797,16
Nb2O4 ТВ. -1623,6
Nb2O5 ТВ. 126,86 -1904,2 1512 102,95
NbOCl3 ТВ. -880,06
Nd г. 364,25 6—>у -164
ТВ.(у) 30,14 0,000 0,000 у->Р 508
Р—>а 714
NdCl3 ТВ. -1064,7 760
Ndl3 ТВ. -665,28 775
Nd2O3 ТВ. -1850,6
Nd2(SO4)3 • ТВ. -6383,6 -5587,3
• 8H2O
Ne г. 20,80 146,32 0,000 0,000 -248,59 0,33 -248,59 1,8
(43,2 кПа) (43,2 кПа)
Ni г. 23,44 182,51 425,42 380,03
ТВ.(р) 26,00 30,14 0,000 0,000 1455 17,58 2140 380,99 Р—>а 353 0,38
NiBr2 ТВ. -219,39 963
NiCb ТВ. 77,87 107,18 -316,10 -272,56 1001 987 (возг.) 202,47
NiCl2 • 6H2O ТВ. 314,84 -2117,7 -1718,7
Nil2 ТВ. -85,83 797
NiO г. 238.65 248,28 216,87
ТВ. 44,38 38,60 -244,51 -216,45 1950 1227 (возг.) 466,41
(1,52 мПа)
Ni(OH)2 ТВ. 79,55 -538,42 -453,43
NiS тв. (а) -73,27 797
ТВ. (Р) -77,87
NiSO4 ТВ. 139,84 77,87 -891,79 -774,14
NiSO4 - 6H2O ТВ. (Р) 343,32 306,05 -2690 -2223,2 Р—>а 53,3
О г. 21,92 161,06 247,68 230,25
O2 г. 29,38 205,16 0,000 0,000 -218,7 0,44 -218,76 у->р -249,50 0,09
(146,63 Па) (146,63 Па)
-182,97 6,82 Р->а -229,39 0,74
Физические свойства важнейших веществ 319
Продолжение табл. 3.6.1
Вещество Состояние Дж/(моль • К) S0. Дж/(моль • К) Д//°, кДж/моль лЛ кДж/моль Плавление Испарение Превращения
Тпя, °C АМь., кДж/моль Т'кип, °C кДж/моль Вид превращения °с А7/.,р, кДж/моль
Оз г. 38,18 237,81 142,35 163,53 -111,9 10,84
ОН г. 29,89 183,75 42,12 37,39
Os г. 20,80 192,46 728,50 682,45
ТВ. 24,70 32,66 0,000 0,000 2700 4400
OsO4 г. 274,65 -334,52 -284,28
тв. (а) 145,28 -383,93 -295,17 40 14,27 130 39,77
тв.(3) 124,35 -391,05 -296,0
OsP2 ТВ. -167,47
OsS2 ТВ. -146,54
P г. 20,80 167,39 314,76 279,3
P (желт.) ТВ. (у) 23,23 44,38 0,000 0,000 44,2 0,63 275 12,43 8->у -77
(0,1 МПа)
P (красн.) ТВ. (р) -18,42 590 20,3 590 10,46 8->у -2,4 5,65
(4,4 МПа) (4,4 МПа) (587,8
МПа)
P (черн.) тв. (а) -43,12 у->р 25,00 -18,42
у—>а 25,00 -43,12
P2 г. 31,94 218.26 141,59 102,99
P4 г. 66,99 280,09 54,93 24,37
PBr3 г. 347,96 -150,3 -172,49 -40,5 173,2 38,85
PBr5 ТВ. -276,33 83,8 (возг.) 54,43
(27,9 кПа)
PC13 ж. -339,13 -91 75,1 30,48
г. 311,87 -306,55 -286,46
PCl5 ТВ. -463,48 160 159 (возг.) 67,4
г. 324,85 -592,43 -545,54
PH3 г. 210.18 9,25 18,25 -133,78 1,13 -133,78 8—>у -242,85 0,08
(3,6 кПа) (3,6 кПа)
-87,74 14,61 у->р -223,72 0,78
[3—>ct -185,04 0,48
PN г. 29,71 211,22 -84,57 -105,92
P3N5 ТВ. 149,05 -316,94
P4O6 ж. 23,8 173,7 37,68
P4Oio ТВ. (р) -3014,5 420 20,93 359 (возг.) 73,68
(0,5 МПа)
Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние С° '-'р ’ Дж/(моль • К) 5°, Дж/(моль • К) ЛН°, кДж/моль д/Л кДж/моль Плавление Испарение Превращения
7’,и1, °C Д/7цл, кДж/моль /ки..- °C Д//иси, кДж/моль Вид превращения 7„р, °C д//„Р, кДж/моль
Р4Ою тв. (a) 572 48,5 572 70,34
(75,98 кПа) (75,98 кПа)
тв. (ам.) -3073,1
РОВг3 ТВ. -479,8 55 191,7 38,02
РОС13 ж. -632,21 1,17 13,02 105 34,37
г. 324,85 -592,43 -545,54
РЬ г. 20,8 175,38 194,01 161,06
ТВ. 26,84 64,94 0,000 0,000 327,4 5,1 1750 180,03
РЬВг2 ТВ. 80,17 161,61 -277,21 -260,58 370,0 20,93 918 115,97
РЬСОз ТВ. 87,5 131,05 -700,45 -626,76
РЬСЬ ТВ. 77,03 136.49 -359,43 -314,17 498 23,86 956 123,93
РЬСгО4 ТВ. -911,46 у->Р 707
PbF2 ТВ. 121,41 -663,6 -620,6 824 7,53 1297 160,35
РЫ2 ТВ. 177,1 -175,21 -173,88 412 21,77 868 103,83
Pb(N3)2 ТВ. 436,68
Pb(NO3)2 ТВ. -449,45
PbO г. 240,32 890 11,72 1472 213,52 Р^а 489
ТВ. (Р) 67,82 -219,39 -189,45
тв.(а) 48,56 69,5 -218,0 -188,61
PbO2 ТВ. 64,47 76,62 -276,83 -219,13
Pb3O4 ТВ. 147,12 211,43 -735,2 -617,97
Pb(OH)2 ТВ. 87,92 -514,97 -421,19
PbO • PbCO3 ТВ. 134,81 203,05 -921,09 -818,94
2PbO • PbCO3 ТВ. 272,14 -1143,0 -1013,2
Pb3(PO4)2 ТВ. 256,23 353,57 -2597,1 -2434,2 1014
PbS ТВ. 49,53 91,27 -94,37 -92,73 1114 17,58 965 (возг.) 230,27
(1,3 кПа)
PbSO4 ТВ. (Р) 104,25 147,37 -919,00 -811,78 1087 40,19 Р^а 866 16,99
PbSiO3 ТВ. 113,04 -1083,5 -1000,6
тв. (ам.) -1075,6
PbSiO4 ТВ. 180,03 -1309,21 -1196,17
тв. (ам.) -1293,72
Pd г. 20,8 167,09 389,37 351,69
ТВ. 26,37 37,26 0,000 0,000 1552 16,74 3110
PdBr2 ТВ. -104,25
PdCI, ТВ. -190,08 970
Физические свойства важнейших веществ
Продолжение табл. 3.6.1
Вещество Состояние с Дж/(моль • К) 5е, Дж/(мо.ть • К) Д/7°, кДж/моль д/Л кДж/моль Плавление Испарение Превращения
Г,,.,,, °C кДж/моль Гки-р °C Д7/исп, кДж/моль Вид превращения Т'нр, °с Д77.,р, кДж/моль
Pdl2 • 2Н2О ТВ. -365,51
PdO ТВ. 31,4 -85,41
Рг г. 364,25
ТВ. 28,47 0,000 932 11,3
РгС13 ТВ. -1079,4 823
РПз ТВ. -678,26 733
РгО2 ТВ. -979,71
Рг2О3 ТВ. -1861,0
Pt г. 25,55 192,42 509,11 464,31
ТВ. 26,58 41,87 0,000 0,000 1769,3 21,77
PtBr4 ТВ. -172,91
PtCl ТВ. -74,11
PtCl2 ТВ. -148,63
PtCl3 ТВ. -208,92
PtCl4 ТВ. -263,35
Ptl4 ТВ. -90,43
PtO1;39 ТВ. -58,61
Pt(OH)2 ТВ. 110,95 -365,09 -285,54
PtS ТВ. -87,09
Pts2 ТВ. -116,39
Ra г. 20,8 176.47 129,79 96,29
ТВ. 71,17
RaCl2 ТВ. 133,98
RaCl2 • 2H2O ТВ. 209,34 -1469,6 -1305,0
Ra(NO3)2 ТВ. 217,71 -992,27 796,75
RaO ТВ. -523,35
RaSO4 ТВ. 142,35 -1473,75 -1364,9
Rb г. 20,8 170,1 85,87 55,89
ТВ. 30,44 69,5 0,000 0,000 38,8 2,18 38,8 (возг.) 85,7 Р^а -30
(1,3 Па)
705 75,82
RbBr ТВ. 53,09 108.35 -389,49 -378,4 682 15,49 1352 155,41
Rb2CO3 ТВ. 118,9 -1128,8 835
RbCl ТВ. 51,49 -430,86 715 18,42 1380 154,57
RbClO3 ТВ. 103,24 151,98 -392,72 -292,24
RbClO4 ТВ.(3) 160,77 -434,88 -304,43
322 Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние с° Дж/(моль • К) 5°, Дж/(моль • К) А//0, кДж/моль А/Л кДж/моль Плавление Испарение Превращения
гпл, °C д/4,. кДж/моль /кип. °C Д//иС1Н кДж/моль Вид превращения 'Л,р, °C д//„Р, кДж/моль
RbF ТВ. 51,08 -549,64 775 17,29 1408 165,42
RbF • HF ТВ. -909,79 205
RbH г. 138,16
Rbl ТВ. 52,33 118,14 -328,66 -325,73 638 12,52 1306 150,55
RbNO3 тв.(Р) -490,02 316 5,61 5—>у 165
7~>Р 225
Р—^01 291
Rb2O ТВ. -330,34
Rb2O4 ТВ. -528,37
RbOH ТВ.(Р) -414,07 301 6,78 Р—^01 245 7,12
Rb2S ТВ. -348,34
Rb2SO4 ТВ. -1425,60 1074 Р—^01 650
RbSH ТВ. -261,25 Р—^01 130 1,67
Rb2SiF6 ТВ. -2840,3
Re г. 20,8 188,95 791,30 749,43
ТВ. 25,54 41,87 0,000 0,000 3150
ReF6 г. -1143,0 18,8 20,93 48 28,89
ReO3 ТВ. -347,50 160
Re2O7 ТВ. -1245,6 300 64,04 360,1 75,78
Re2O8 ТВ. -620,90
ReS2 ТВ. -185,47
Rh г. 20,94 185,85 577,78 531,72
ТВ. 25,54 31,82 0,000 0,000 1960 3670
RhCl ТВ. -66,99
RhCl2 ТВ. -150,72
RhCl3 ТВ. -234,46
RhO ТВ. 48,15 -90,85
Rh2O ТВ. 73,27 -95,04
Rh2O3 ТВ. 104,25 -285,96
Rn г. 20,8 176,26 0,000 0,000 -71 2,9 -62 16,41
Ru г. 186,6 669,89 623,83
тв. (8) 23,44 28,89 0,000 0,000 2430 4200 8—>у 1035 0,14
у->Р 1200
р—>а 1500 0,96
RuBr3 ТВ. -184,22
Rul3 ТВ. -159,10
Физические свойства важнейших веществ
Продолжение табл. 3.6.1
Вещество Состояние Дж/(моль • К) S0, Дж/(моль • К) Д/7°, кДж/моль дл°, кДж/моль Плавление Испарение Превращения
7',,.,, °C кДж/моль ТК1Ю. °C Д7/ИС11, кДж/моль Вид превращения Л,р, °C ДЯ11Р. кДж/моль
RuCl3 ТВ. 162,86 -205,15 -146,54 870 969
RuO? ТВ. 69,08 -305,63 -253,72
RuS2 ТВ. -201,38
S г. 23,69 167,83 222,94 182,42
ж. (X) 1,06 444,60 10,46
ж. (ц) 2,8
S (ромб.) ТВ.(р) 22,6 31,9 0,000 0,000 95,4 (возг.) 12,6 Р—>а 95,4 0,37
(6,265 Па) (626 мПа)
S (монокл.) тв. (а) 23,65 32,57 0,29 0,09 119 1,23 95,4 (возг.) (6,265 Па) 12,22
s2 г. 125,02
S6 г. 105,92
S8 г. 100,90
S2Br2 ж. -15,07 -46 54 (23,99 Па)
SC14 ж. -56,94
S2C12 ж. -60,29 -75 136,8 36,05
S2C14 ж. -100,48
SF6 г. 290,98 -1096,94 -992,27 -50,7 5,02 -63,7 (возг.) 22,86 Р—>а -178,9 1,6
(0,2 МПа) -50,7 (0,2 МПа) 17,08
SO г. 222,06 79,63 53,5
so2 г. 39,81 248,69 -297,09 -300,57 -75,48 7,4 -75,48
(167,42 Па) (167,42 Па)
-10,02 24,93
SO2 • 7H2O ТВ. -2379,2
SO3 г. 50,66 256,39 -395,44 -370,61
SO3 (легкоплавк. ТВ. (Р) -449,87 16,8 1,96 16,8 (возг.) 49,23
волокнист.) (21,3 кПа) (21,3 кПа)
(ледяной) (ледяной)
SO3 (тугоплавк. тв. (а) -462,72 32,5 (53,3 кПа) 10,34 32,5 (возг.) 54,26
волокнист.) (волок- (53,3 кПа)
НИСТЫЙ р) (волокнистый р)
ж. -438,23 62,2 25,49 62,2 (возг.) 66,61
(0,2 МПа) (0,2 МПа)
(волок- (волокнистый а)
нистый а) 51,6 (возг.) (волокнистый а) 41,82
43,3
324 Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние с° р ’ Дж/(молъ • К) 5й, Дж/(мо.ть • К) А/Д кДж/моль д/Д кДж/моль Плавление Испарение Превращения
гп.,„ °C дм,.„ кДж/моль °C кДж/моль Вид превращения Г„р, °C д//„Р, кДж/моль
SOC12 ж. 120,58 -205,99 -104,5 74,8 31,02
SO2C12 ж. 131,88 -389,37 -54,1 69,5 31,4
S2O5CI2 ж. 232,36 -697,52 -39 150,7 (97,4 кПа) 55,26
Sb г. 20,8 180,28 254,55 213,94
тв.(у) 25,45 43,96 0,000 0,000 630,5 20,09 1625 Y~>P 94,6
тв. (р) 10,21 Р->а 413
Sb2 г. 36,36 254,97 217,71 167,47
Sb4 г. 204,31
SbBr3 ТВ. -260,0 96,6 14,69 288 (99,8 кПа)
SbCl г. -16,74
SbCl3 г. 77,45 338,29 -303,54 -302,7
ТВ. 186,31 -382,42 -324,98 73,2 12,68 219 45,21
SbCl5 г. -393,14
ТВ. -438,77 2,8 10,05 76,5 (2,8 кПа) 48,15
SbF г. 0,000
SbF3 ТВ. -909,37 290 376
SbH3 г. -88 -17
Sbi3 ТВ. -96,29
SbN г. 311,49
SbO г. 188,4
Sb2O4 ТВ. 114,72 126.86 -895,97 -787,12
Sb2O5 ТВ. 117,65 125,18 -981,38 -839,45
Sb4O6 ТВ.(р) 202,89 246,18 -1410,1 -1247,7 655 123,47 655 (1,13 кПа) Р->а 557 13,56
(1,13 кПа) (69,98 Па)
Sb6O]3 ТВ. -2805,2 1423 74,65
SbOCl ТВ. -380,16
Sb2S3 (чсрн.) ТВ. -182,12 547 (Sb4S6) 46,89
Sb2S3 (оранж.) тв. (ам.) -150,72
Sb2(SO4)3 ТВ. -2408,7
Se г. 20,8 176.72 201,93 202,51 217,4 5,23 217,4 (Se6) 18,04 стскл. —>а 125 4,39
(0,57 Па) (0,57 Па) 736 (Se6) 14,36 у->а 150 0,75
754 (Se,) 53,59
Se2 г. 35,36 252,13 138,75 88,55
SeCl2 г. -40,61
Физические свойства важнейших веществ
Продолжение табл. 3.6.1
Вещество Состояние с° Дж/(молъ • К) 5ю, Дж/(моль • К) Д/7°. кДж/моль Д/Л кДж/моль Плавление Испарение Превращения
Т11Л, °C А//цЛ, кДж/моль Т °C 1 КИП’ ч-' А7/ИС11, кДж/моль Вид превращения г1ф, °C АН,Ф, кДж/моль
SeCl4 ТВ. -188,4 305 161 (возг.)
SeF6 г. 314,43 -1030,0 -929,47 34,6 7,12 46,6 (возг.) 26,25
(0,2 МПа) 34,6 (0,2 МПа) 18,34
SeO г. 39,69
SeO2 ТВ. -230,27 337 (возг.) 86,34
Se(0H)3C104 ТВ. -623,83 33
SeO2SO3 ТВ. -699,61
Si г. 22,26 167,97 368,60 324,1
ТВ. 19,89 18,71 0,000 0,000 1420 46,05
тв. (ам.) 4,19
SiBr4 ж. -398,16 5,2 152,8 38,1
Si2Br6 ТВ. 95 265
SiC ТВ. 26,67 16,47 -111,79 -109,27
SiCl4 г. 90,85 331,59 -610,01 -570,24 -68,8 7,7 57,3 29,3
ж. 145,28 239,48 -640,58 -573,17
SiF4 г. 76,2 284,7 -1549,1 -1507,3 -90,3 7,07 -95,0 (возг.) 25,75
(0,18 МПа) -90,3 (0,18 МПа) 18,67
SiH4 г. 42,87 203,9 -61,96 -39,35 -184,7 0,66 -111,2 12,14 Р— -209,7 0,61
Sil4 ТВ. -132,3
Si3N4 ТВ. 42,87 93,78 -750,69 -647,7
SiO г. 29,89 206,24 -111,87 -137,2
SiO2 (кварц-Р) ТВ. 44,46 41,89 -859,97 -805,54 КВ.у—>кв.р -182
SiO2(кристо-балит-у) ТВ. 44,21 42,66 -858,3 -804,28 кв.р—>кв.а 573 0,63
SiO2 (тридимит-у) ТВ. 44,63 43,37 -857,45 -803,44 1610 8,54 кв.а—>тр.5 867 0,50
SiO2 (стекл.) ТВ. 44,38 46,89 -847,83 -799,26 1728 7,7 гр.5—>тр.у тр.у—> тр.р тр.р—>тр.а тр.а—>кр.а кр.р—>кр.а (кв.— кварц, 117 163 225 1470 0,29 0,17 0,20 0,20
тр.— три- 242 1,3
димит,
кр.— кристобалит)
326 Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние Дж/(моль • К) 5°, Дж/(моль • К) А//0, кДж/моль д/Л кДж/моль Плавление Испарение Превращения
Т„„, °C кДж/моль /’кии, °C А//иСИ, кДж/моль Вид превращения /’„р, °с кДж/моль
SiS2 ТВ. -145,28
Sm г. 30,37 183,13 364,25
ТВ. 0,000 0,000 1350
SmCl3 тв. (а) -1045,9 682
Sml3 тв. (р) -642,25 820
Sm2O3 ТВ. -1800,5
Sm(C)H)3 ТВ. -1292,88
Sm2(SO4)3 • 8H2O ТВ. -5579,33
Sn г. 21,27 168,49 301,45 267,95
Sn (сер.куб.) ТВ. (у) 25,79 44,8 2,51 4,6 у->Р 18 2,51
Sn (бел. тет- ТВ. (Р) 26,37 51,49 0,000 0,000 231,9 7,07 р—>а 202,8 0,008
рагон.)
SnBr2 ТВ. -266,28 232 7,12 636 92,11
SnBr4 тв. (а) -406,54 30 12,56 217,3 41,86 р—>а 267 -25,12
SnCb ТВ. -350,01 247 12,56 649 87,92
SnCl4 ж. 165,38 258,74 -515,54 -474,36 -33,3 9,17 113,7 34,75
SnF4 ТВ. 705
Snl2 ТВ. -144,02 320 712 100,48
Snl4 ТВ. 144,5 18,76 344 56,94
SnO г. 88,13 230.19
ТВ. 44,38 56,52 -286,38 -257,49
SnO2 ТВ. 52,63 52,33 -581,13 - 520,0 р—>а 410 1,88
Sn(OH)2 ТВ. 96,71 -579,03 -492,36
Sn(OH)4 ТВ. -1132,5
SnS ТВ. 98,8 -77,87 -82,48 880
Sn(SO4)2 ТВ. -1647,1
SnSe ТВ. 860
SnTe ТВ. 800
Sr г. 20,8 164,64 164,12 110,11
ТВ. 25,12 54,43 0,000 0,000 777 9,21 1357 141,51
SrBr2 ТВ. -716,36 643 20,09
SrCO3 ТВ. (Р) 81,47 97,13 -1219,2 -1138,4 1497 р—>а 925
Sr(C2H3O2)2 ТВ. -1531,1
SrCl г. 37,68
SrCl2 ТВ. 79,13 117,23 -828,98 -781,67 875 17.16
SrCl2 • H2O ТВ. 120,16 -1137,6
SrCl2 • 2H2O ТВ. 160,35 -1439,0
Физические свойства важнейших веществ 327
Продолжение табл. 3.6.1
Вещество Состояние Дж/(моль • К) 5ю, Дж/(моль • К) Д/Д кДж/моль кДж/моль Плавление Испарение Превращения
Гпл. °C АН,.. кДж/моль Т °C ^НИСЦ, кДж/моль Вид превращения Гнр, °C ДЯ11р, кДж/моль
SrCb • 6Н2О ТВ. -2625,5
SrF г. -20,93 191,75
SrF2 ТВ. -1215,4 1400 18,0
SrH г. 30,05 206,95 -219,39
SrH2 ТВ. -177,10
SrHPO4 ТВ. -1805,8
Sr(H2PO4)2 • H2O ТВ. -3430,7
Srl5 ТВ. 81,64 -567,31 515
Sr(N3)2 ТВ. 0,42
Sr3N2 ТВ. -391,04
Sr(NO2)2 ТВ.(Р) -750,69
Sr(NO3)2 ТВ. 160,35 -976,57 645
Sr(NO3)2 • 4H2O ТВ. -2154,1
SrO ТВ. 45,05 54,43 -590,75 -560,19 2430
SrO2 ТВ. -643,09
Sr(OH)2 ТВ. -960,03
Sr3(PO4)2 ТВ. -4133,6
SrS г. 79,55
ТВ. -452,59
SrSO4 ТВ. 121,83 -1445,7 -1335,17 1605 Р—>а 1152
SrSe ТВ. -329,50
SrSi ТВ. -473,11
SrSi2 ТВ. -628,02
SrSiO3 ТВ. -1554,1 1575
Sr2SiO4 ТВ. -2179,6 1588
Ta г. 20,95 185,24 774,56 732,69
ТВ. 25,33 41,45 0,000 0,000 2500 2227 (возг.) 753,6
(0,115 Па)
TaBr5 ТВ. -611,27 267 44,8 267 (возг.) 106,76
(17,3 кПа) (17,3 кПа)
345 61,13
TaC ТВ. 36,8 42,28 3827
TaCl4 ТВ. -706,73
TaCl5 ТВ. -862,48 211 46,47 211 (возг.) 95,04
(55,4 кПа) (55,4 кПа)
239,7 54,85
TaF5 ТВ. 95,1 229,0 27,63
328 Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние Дж/(моль • К) S0, Дж/(моль • К) Д/7°, кДж/моль Д/Л кДж/моль Плавление Испарение Превращения
Т.л, °с кДж/моль Тки,,. °C Д77НС11, кДж/моль Вид превращения 7'пр- °C Д/7пр, кДж/моль
TaN ТВ. -243,67 3067
Та2О3 ТВ. 135,23 143,19 -2046,5 -1923,83 1890
Те г. 20,8 182,71 199,29 159,52
тв.(р) 25,75 49,74 0,000 0,000 450 (23,994 Па) 17,92 450 (23,994 Па) 55,68 Р—>а 348 0,54
1012 49,82
Те2 г. 36,5 268,25 171,66 121,42
ТеВг4 ТВ. -208,50
ТеС14 ТВ. -323,22 224,1 18,88 391,3 77,04
TeF6 г. 337.75 -1318,8 -1222,5 -37,7 8,79 -38,9 (возг.) 27,09 Р—>а -73,5 2,09
(106,6 кПа) -37,7 18,0 (8 кПа)
(106,6 кПа)
ТеО г. 180,03
ТеО2 ТВ. 66,53 71,13 -325,27 -270,46
(TeO2)2SO3 ТВ. -1225,9
Th г. 190,2
ТВ. 32,24 56,94 0,000 0,000
ThBr4 ТВ. -950,82 679 679 (возг.) 188,4
(5,7 кПа)
857 127,28
ThBr4 • 7H2O ТВ. -3155,59
ThBr4 • 10H2O ТВ. -4067,9
ThBr4 • 12H2O ТВ. -4672,5
ThF4 ТВ. -1997,1
ThCl2 ТВ. - 188,4
ThCl4 • NH4C1 ТВ. -1564,2
ThCl4 • 2NH4C1 • ТВ. 4909,4
• 10H2O
ThH4 ТВ. -180,03
Thl4 ТВ. -548,47 566 837 120,58
Th3N4 ТВ. -1289,5
Th(NO3)4 • ТВ. -1867,3
• NH4NO3 • H2O
ThO2 ТВ. -1222,5 3050
ThOBr2 ТВ. -1058,4
ThOCl2 ТВ. -1150,5
Th(OH)4 (раств.) ТВ. -1764,7
Физические свойства важнейших веществ 329
Продолжение табл. 3.6.1
Вещество Состояние с°, р ’ Дж/(моль • К) 5°, Дж/(моль • К) Л А/0, кДж/моль д/Л кДж/моль Плавление Испарение Превращения
Tnjl, °C А/Ды, кДж/моль °с А7/исп, кДж/моль Вид превращения т„Р, °C Д//ПР, кДж/моль
ThOl2 ТВ. -955,4
ThOSO4 ТВ. -2039,0
Th2S3 ТВ. -1096,9
Th(SO4)2 ТВ. -2520,5
Th(SO4)2 • 4H2O ТВ. -3695,7
Th(SO4)2 • 8H2O ТВ. -4892,7
Ti г. 24,44 180.32 468,92 422,86
тв.(Р) 25,16 30,31 0,000 0,000 1812 (возг.) (4,799 Па) 445,89 Р—>а 882
TiBr2 ТВ. -397,74
TiBr3 ТВ. -552,66
TiBr4 ТВ. -648,95 38,5 8,79 220 Р—>а -15
TiC ТВ. 33,66 24,28 -226,09 -221,9 3127
TiCl2 г. 275,91 -290,56
ТВ. 103,41 -504,93
TiCl3 г. 313,59 -538,84
ТВ. 144,02 -714,68
TiCl4 г. 95,79 353,36 -760,32
ж. 157,0 252,88 -800,51 -724,73 -23 9,38 138 35,17
TiF2 ТВ. -828,98
TiF3 ТВ. -1318,8
TiF4 ТВ. -1549,1 284
Til2 -255,39
Til3 -334,94
Til4 -427,05 150 377,1 56,94
TiN ТВ. 37,09 30,14 -305,64 -276,75 2927
TiO г. 180,03
ТВ. 39,98 34,79 -525,02
TiO2 (рутил-у) ТВ. 55,1 50,28 -941,61 -882,16 1835 Р~>а 991 3,43
(рутил-а)
TiO2 (анатаз-у) ТВ. 55,34 49,95 -866,67
тв. (ам.)
Ti2O3 ТВ.(Р) 97,43 78,84 -1519.0 -1431,0 р->а 200 0,92
Ti3O5 ТВ.(Р) 154,91 129.45 -2457,7 -2315,3 Р—>а 177 0,92
TiOCl2 ТВ. 73,27 -761,99
330 Новый справочник химика и технолога
Продолжение тпабл. 3.6.1
Вещество Состояние ДжДмолъ • К) 5ю, ДжДмоль • К) А//0, кДж/моль AF0, кДж/моль Плавление Испарение Превращения
гШ1, °C ДМ.л, кДж/моль гКИ1„ °C Д7/ИС11, кДж/моль Вид превращения °с ДТ7Пр, кДж/моль
Т1 г. 20,8 180,99 181,45 146,75
тв.(р) 26,58 64,47 0,000 0,000 303,6 4,31 1077 (3,7 кПа) 167,89 а—>у 153 -0,79
(3826 МПа)
р->у 153 0,04
(3826 МПа)
р—>а 153 0,83
(3826 МПа)
р—>а 235,1 0,34
Т1Вг г. 36,88 267.12 -20,93 -58,61
ТВ. 119,74 -172,49 -166,21 439 15,07 459 (возг.) 131,46
(281,263 Па) (281,26 Па)
819 102,99
Т1Вг3 ТВ. -247,02
Т1ВгО3 ТВ. -100,48
Т1С1 г. 36,25 255,81 -66,99 -92,11
ТВ. 108,44 -205,11 -59,41 429 16,74 429 (возг.) 121,42
(149,296 Па) (149,296 Па)
806 103,83
Т1С13 ТВ. -351,27
Т1С13 • 4Н2О ТВ. -1539,5 35
T1F г. -138,16 327 655
Т1Н г. 215.16 200,96 175,84
ТП г. 37,09 274,65 29,3 -16,74
ТВ. (Р) 123,09 -124,35 -124,35 440(133,3 Па) и,з 440 (возг.) 125,6 р—>а 165
(133,3 Па) (для
красной
а-формы)
825 104,25
ТПОз ТВ. -199,29
™3 ТВ. -235,72
T1NO3 ТВ. (у) 159,93 -242,87 -151,02 206,5 9,59 433 у->р 61,0 1,0
р—>а 143,5 3,18
Т12О ТВ. 99,64 -175,42 -136,07
тюн ТВ. 72,43 -238,23 -190,49
Т1(ОН)з ТВ. -513,30
T12S ТВ. -87,08 448 12,56
T12SO4 ТВ. -928,21 632 23,03
Физические свойства важнейших веществ
Продолжение табл. 3.6.1
Вещество Состояние Х"»0 Дж/(моль • К) 5°, Дж/(моль • К) ДЯ°, кДж/моль Д/Л кДж/моль Плавление Испарение Превращения
ТП1„ °C А7/пл, кДж/моль т °су * КИП’’ А/7ИСП, кДж/моль Вид превращения 7’.,Р, °C Д7/Пр, кДж/моль
Tl2Se ТВ. -75,36 398
Т12Те ТВ. -29,31
и г. 523,35
тв.(у) 27,5 50,36 0,000 1132 у->(3 665 2,78
р-НХ 776 4,88
иВг3 ТВ. 205,15 -712,17 -689,56 752 46,05 752 (возг.) 287,21
(0,87 Па) (0,87 Па) 752 (0,87 Па) 241,16
UBr4 ТВ. 242,83 -823,12 -789,21 519 (возг.) (637,17 Па) 175,42
519 (637,17 Па) 145,28
761 129,79
UBr3I ТВ. -741,48
ис2 ТВ. 58,61 -175,84 -175,84 2427
UC13 ТВ. 159,05 -891,79 -824,38 835 835 (возг.) 263,77
(3,6 Па) 835 (3,6 Па) 226,08
исц ТВ. 198,45 -1051,7 -962,96 590 590 (возг.) (2,1 кПа) 193,85
UC15 ТВ. 259,58 -1097,4 -993,94 590 (2,1 кПа) 150,72
исц ТВ. 285,96 -1140,5 -1011,1
UC13I ТВ. 226,09 -920,7 -855,78
UF3 ТВ. 108,85 -1494,7 -1419,3
uf4 ТВ. 117,73 151,14 -1854,7 -1762,6 1036 (возг.) (506,54 Па) 288,47
1036 (506,54 Па) 264,6
1418 240,74
uf5 ТВ. 180,03 -2043,2 -1930,1
UF6 г. 379,99 -2114,3 -2030,6 64,0 19,22 56 (возг.) 49,4
(151 кПа) 64,0 (возг.) 49,4
(151 кПа) 64,0 (151 кПа) 30,14
UH3 ТВ. -127,28
UI3 ТВ. 234,46 -480,22 -482,74
332 Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние с°, р ’ Дж/(моль • К) 5°, Дж/(моль • К) ДЯ°, кДж/моль д/Л кДж/моль Плавление Испарение Превращения
7-„л. °C ДНпл, кДж/моль 7кии. °C Д^ИСП’ кДж/моль Вид превращения г.,р, °C Д^пр, кДж/моль
UI4 ТВ. 272,14 -531,72 -527,95
UN ТВ. 75,36 -334,94 -314,01
U2N3 ТВ. 121,42 -891,79 -812,24
uo2 ТВ. 77,87 -1085,2 -1030,8
UO3 ТВ. 98,68 -1264,4 -1184,9
u308 ТВ. -3759,7
UOBr3 ТВ. -979,29
UO2Br2 ТВ. -1146,76
UO2(C2H2O2)2 • ТВ. -2616,3
• 2H2O
UO2(C2H2O2) • ТВ. -4378,5
• NH4(C2H2O2) •
• 6H2O
UOC12 ТВ. -1081,5
UOC13 ТВ. -1186,5
UOCrO4 • ТВ. -3511,9
• 5'/2H2O
UO2(NO3)2 ТВ. 276,33 -1378,3 -1143,4
UO2(NO3)2 • ТВ. 505,97 -3200,0 -2616,7
•6H2O
UO2SO4 • 3H2O ТВ. 263,77 -2800,1 -2453,5
U(SO4)2 ТВ. -2357,2
V г. 26,03 182,32 502,41 456,36
ТВ. 24,49 29,52 0,000 0,000 1730
VBr3 ТВ. -447,99
VC ТВ. 33,37 6,77 2770
VC12 ТВ. 72,26 97,13 -452,17 -406,12 1350
VC13 ТВ. 93,24 131,05 -573,59 -502,41
VC14 ж. -577,78 -25,7 152 38,1
VN ТВ. 38,01 37,3 -171,66 -146,54 2027
VO г. 217,71
ТВ. -427,05
V2o2 ТВ. -837,36
v203 ТВ. 103,96 98,72 -1256,04 -1176,49 1977
V2O4 ТВ.(Р) 118,48 103,2 -1440,26 -1331,4 1542 113,92 Р—>а 72 8,58
V2O5 ТВ. 129,79 131,05 -1561,67 -1440,3 670 65,14
v305 ТВ. -1574,23
Физические свойства важнейших веществ
Продолжение табл. 3.6.1
5ю. Дж/(моль • К) Плавление Испарение Превращения
Вещество Состояние с", Дж/(моль • К) д/Л кДж/моль д/Л кДж/моль Ди- °C Д//„;1. кДж/моль Лип- °C А/Дсп-кДж/моль Вид превращения /;,Р, °C А//„р, кДж/моль
VOC13 VOSO4 W WBr6 WC W2C WC12 WC14 WCh WC16 WI2 WI4 WI5 wo2 WO3 (желт.) W3O8 WOCI4 WO2C12 Y YC13 YI3 Y2o3 Y(OH)3 Y2(SO4)3 • 8H2O Yb YbCl3 Yb2(SO4)3 • 8H2O ТВ. ТВ. г. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. г. ТВ. ТВ. ТВ. ТВ. ТВ. ТВ. г. ТВ. ТВ. ТВ. 21,31 24,99 81,56 25,88 96,29 577,78 20,8 173.97 33,49 83,81 179,49 172,91 -720,13 -1307,12 844,06 0,000 -387,69 -38,06 -251,2 -506,6 -573,59 -682,45 -4,18 0,000 113,04 -570,66 -840,87 -2198,1 -745,25 -837,36 0,000 -983,06 -599,55 -1413,5 -6333.0 364,25 0,000 -957,52 802,19 0,000 -783,96 431,24 0,000 -1290,8 -5557,2 0,000 -5479,7 -79 3380 2867 2857 230 284 (31,1 кПа) (а-форма) 1102 (0,77 Па) 210 1475 700 1000 854 20,93 9,63 458,92 7,53 125 286 226,9 (возг.) (5,06 кПа) 284,0 (возг.) (31,1 кПа) 336,5 3200 34,75 61,54 87,92 72,85 62,38 0-»а 0—>газ. а-» газ. 169 226,9 (5,06 кПа) 226,9 284 14,23 87,92 72,85
334 Новый справочник химика и технолога
Продолжение табл. 3.6.1
Вещество Состояние хЧ) Р 5 Дж/(моль • К) 5ю, Дж/(моль • К) АЯ°, кДж/моль Д/Л кДж/моль Плавление Испарение Превращения
Т[1Л, °C ДЯпл, кДж/моль Гкип, °C Д7/,1СП, кДж/моль Вид превращения Т °C 1 пр? АЯпр, кДж/моль
Zn г. 20,8 160,98 130,58 94,99 419,5 6,68 913 114,84
ТВ. 25,08 41,66 0,000 0,000
ZnBr г. 35,88 254,55
ZnBr2 ТВ. 137,49 -327,28 -310,42 392 269 (возг.) (0,43 Па) 126,02
702
ZnBr2 • 2H2O ТВ. 235,3 -924,86 -798,0 37
Zn(CHO2)2 ТВ. -942,03
Zn(CHO2)2 • ТВ. -1536,6
2H2O Zn(C2H3O2)2 ТВ. -1080,2
Zn(C2H3O2)2 • ТВ. -1377,5
• H2O Zn(C2H3O2)2 • ТВ. — 1666,3
2H2O Zn(CN)2 ТВ. 77,04
Zn(CN)2 • ZnO ТВ. -138,58
ZnCO3 ТВ. 82,02 82,48 -813,07 -731,85
ТВ. (Р) -640,99
ZnCl г. 35,38 244,09 4,18 -20,93
ZnCl2 ТВ. 76,62 108,44 “416,17 -369,5 316 23,02 733 129,37
ZnF2 ТВ. 872 1507 180,45
ZnH г. 32,28 203,89 227,76 198,87
Znl г. 36,67 263,77 62,80 12,56
Znl2 ТВ. 159,1 -209,25 -209,38 446 245 (возг.) (0,43 Па) 115,55
2Znb • Pbl2 ТВ. -598,29
Zn(N3)2 ТВ. 107,6 212,69
Zn3N2 ТВ. -28,89
Zn(NH4)2(SO4)2 • ТВ. “4000,9
•6H2O Zn(NO3)2 ТВ. -481,98
Zn(NO3)2 • H2O ТВ. -803,82 70,7
Zn(NO3)2 • 2H2O ТВ. -1109,3 55,4
Zn(NO3)2 • 4H2O ТВ. -1698,8 44,7
Zn(NO3)2 - 6H2O ТВ. -2306,6 36,1
ZnO ТВ. 40,27 43,96 -348,21 -318,4 1975
Физические свойства важнейших веществ 335
Продолжение табл. 3.6.1
Вещество Состояние с° Дж/(моль • К) 5°. Дж/(моль • К) д/Л кДж/моль д/Л кДж/моль Плавление Испарение Превращения
ТиА, °C Д7/,иг кДж/моль Ли,,. °C А//ИСц, кДж/моль Вид превращения ЛР, °с кДж/моль
ZnO2 • 2Н2О ТВ. -870,43
Zn3O5 • 2Н2О ТВ. -1553,7
Zn3O5 • ЗН2О ТВ. -1832,6
Zn(OH)2 тв. (а) -642,67
ZnS г. -58,61
ZnS (сфалерит) тв. (р) -203,06 854 (возг.) 269,21 Р^а 1020
ZnS (вюрцит) тв. (а) -189,66 1182 (возг.)
ZnSO4 ТВ. 117,23 124,76 -979,2 -872,15
ZnSO4 • н2о ТВ. 145,28 146,12 -1300,4 -1130,0
ZnSO4 • 6H2O ТВ. 338,29 363,41 -2777,1 -2323,7
ZnSO4 • 7H2O ТВ. 392,3 386,86 -3077,7 -2561,9
ZnSb ТВ. -150,72 544
ZnSe ТВ. -142,35
ZnSiO3 ТВ. -1233,4
Zn2SiO4 ТВ. -1510,6
Zn2SiO4 (стекл.) ТВ. -1472,9
ZnTe г. 125,60
ТВ. 79,55 -125,60 -121,42 1328
Zr г. 26,64 181,34 523,35 481,48 1852 Р^а 862 2,93
ТВ.(Р) 38,43 0,000 0,000
ZrBr2 ТВ. -502,41
ZrBr3 ТВ. -728,50
ZrBr4 ТВ. -803,86 450 357 (возг.) 108,02
ZrC ТВ. -188,4 3492
ZrCl2 ТВ. -607,08
ZrCl3 ТВ. -870,85
ZrCl4 ТВ. -962,96 437 33 1 (возг.) 105,92
ZrF2 ТВ. -962,96
ZrF3 ТВ. -1465,37
ZrF4 ТВ. -1863,12
Zrl2 ТВ. -376,81
Zrl3 ТВ. -535,91
Zrl4 ТВ. -544,28 499 43 1 (возг.) 29,0
ZrN ТВ. 38,64 -344,15 -315,68 2952
336 Новый справочник химика и технолога
Окончание табл. 3.6.1
Вещество Состояние С° Дж/(моль • К) S°, Дж/(моль • К) дя°, кДж/моль AF0, кДж/моль Плавление Испарение Превращения
7™ °C АНпл, кДж/моль Т °C 2 кип? кДж/моль Вид превращения 7)1р, °C АНпр, кДж/моль
ZrO2 ZrO2 • 5Н2О Zr(OH)4 ZrO(OH)2 Zr(SO4)2 Zr(SO4)2 • 4H2O ZrSiO4 ТВ. тв. (ам.) ТВ. ТВ. ТВ. ТВ. ТВ. 111,79 98,51 50,36 84,15 -1081,0 -2618,0 -1721,6 -1415,1 -2501,2 -3739,2 -1023,25 2677 2420 225 (возг.) 643,09 у->Р р^а 1000 1900
Физические свойства важнейших веществ
338
Новый справочник химика и технолога
Таблица 3.6.2
Термодинамические показатели воды и перегретого водяного пара
Т V ДЛ° 5й
р = 1,01 кПа
0 0,0010002 0,0 0,0000
30 142,6 2556 9,1285
60 156,7 2613 9,3043
90 170,8 2669 9,4668
120 185,0 2726 9,6175
150 199,1 2783 9,7582
180 213,2 2840 9,8901
210 227,3 2899 10,014
240 241,4 2957 10,132
270 255,6 3017 10,24
300 269,7 3076 10,351
330 283,8 3136 10,454
360 297,9 3197 10,552
390 312,0 3259 10,647
420 326,1 3321 10,738
450 340,3 3383 10,827
480 354,4 3447 10,913
510 368,5 3511 10,996
540 382,6 3575 11,077
570 396,7 3640 11,155
600 410,8 3706 11,232
630 425,0 3773 11,307
660 439,1 3840 11,38
690 453,2 3908 11,452
720 467,3 3976 11,522
750 481,4 4045 11,59
р - 2,03 кПа
0 0,0010002 0,0 0,0000
30 71,29 2556 8,8078
60 78,36 2612 8,9836
90 85,42 2669 9,1469
120 92,48 2725 9,2976
150 99,54 2783 9,4383
180 106,6 2840 9,5702
210 113,7 2899 9,6945
240 120,7 2957 9,8126
270 127,8 3017 9,9244
300 143,8 3076 10,031
330 141,9 3136 10,134
360 149,0 3197 10,232
390 156,0 3259 10,327
420 163,1 3321 10,418
450 170,1 3383 10,507
480 177,2 3447 10,593
510 184,2 3511 10,676
540 191,3 3575 10,757
570 198,4 3640 10,835
600 205,4 3706 10,912
630 212,5 3773 10,987
660 219,5 3840 11,06
690 226,6 3908 11,132
720 233,7 3976 11,202
750 240,7 4045 11,27
Продолжение табл. 3.6.2
Т V ДЛ° 5й
р = 3,04 кПа
0 0,0010002 0,0 0,0000
30 47,49 2556 8,6164
60 52,21 2612 8,7923
90 56,93 2669 8,9556
120 61,64 2725 9,1063
150 66,35 2783 9,2486
180 71,06 2840 9,3826
210 75,77 2899 9,504
240 80,48 2957 9,625
270 85,18 3017 9,7368
300 89,89 3076 9,844
330 94,59 3136 9,9466
360 99,30 3197 10,045
390 104,0 3259 10,14
420 108,7 3321 10.231
450 113,4 3383 10,32
480 118,1 3447 10,406
510 122,8 3511 10,489
540 127,5 3575 10,57
570 132,2 3640 10,649
600 136,9 3706 10,725
630 141,6 3773 10,8
660 146,4 3840 10,873
690 151,1 3908 10,945
720 155,8 3976 11,015
750 160,5 4045 6,8961
р - 4,05 кПа
0 0,0010002 0,0 0,0000
30 35,61 2556 8,4871
60 39,15 2612 8,6629
90 42,69 2669 8,8262
120 46,23 2725 8,9773
150 49,76 2783 9,118
180 53,30 2840 9,2499
210 56,82 2899 9,3742
240 60,36 2957 9,4923
270 63,89 3017 9,6041
300 67,42 3076 9,7113
330 70,95 3136 9,8139
360 74,47 3197 9,9118
390 78,00 3259 10,007
420 81,53 3321 10,099
450 85,06 3383 10,187
480 88,59 3447 10,273
510 92,12 3511 10,356
540 95,65 3575 10,437
570 99,18 3640 10,516
600 102,7 3706 10,593
630 106,2 3773 10,668
660 109,8 3840 10,74
690 113,3 3908 10,812
720 116,8 3976 10,882
750 120,4 4045 10,95
р = 5,07 кПа
0 0,0010002 0,0 0,0000
Физические свойства важнейших веществ
339
Продолжение табл. 3.6.2
Т V ДЛ° 5°
30 0,0010044 125,6 0,4367
60 31,31 2612 8,5578
90 34,15 2668 8,7228
120 36,98 2725 8,8739
150 39,81 2783 9,015
180 42,63 2840 9,1469
210 45,46 2899 9,2712
240 48,28 2957 9,3893
270 51,11 3016 9,5011
300 53,93 3076 9,6083
330 56,75 3136 9,7109
360 59,58 3197 9,8088
390 62,40 3259 9,9039
420 65,22 3321 9,9956
450 68,05 3383 10,084
480 70,87 3447 10,17
510 73,70 3511 10,253
540 76,52 3575 10,334
570 79,34 3640 10,413
600 82,17 3706 10,49
630 84,99 3773 10,565
660 87,82 3840 10,637
690 90,64 3908 10,709
720 93,46 3976 10,779
750 96,29 4045 10,847
р = 6,08 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 26,08 2612 8,4749
90 28,45 2668 8,6382
120 30,81 2725 8,7898
150 33,17 2783 8,9309
180 35,52 2840 9,0627
210 37,88 2899 9,1871
240 40,23 2957 9,3052
270 42,59 3016 9,417
300 44,94 3076 9,5241
330 47,29 3136 9,6267
360 49,65 3197 9,7247
390 52,00 3259 9,8197
420 54,35 3321 9,9114
450 56,71 3383 10
480 59,07 3447 10,086
510 61,41 3511 10,169
540 63,77 3575 10,25
570 66,12 3640 10,329
600 68,47 3706 10,405
630 70,83 3773 10,481
660 73,18 3840 10,554
690 75,53 3908 10,625
720 77,88 3976 10,695
750 80,24 4045 10,763
р = 7,09 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 22,35 2611 8,4037
Продолжение табл. 3.6.2
Т V дл° &
90 24,38 2668 8,567
120 26,41 2725 8,7186
150 28,43 2783 8,8597
180 30,45 2840 8,9916
210 32,47 2899 9,1159
240 34,48 2957 9,234
270 36,50 3016 9,3458
300 38,52 3076 9,453
330 40,54 3136 9,5555
360 42,55 3197 9,6535
390 44,57 3259 9,7485
420 46,59 3321 9,8402
450 48,61 3383 9,929
480 50,62 3447 10,015
510 52,64 3511 10,098
540 54,66 3575 10,179
570 56,67 3640 10,258
600 58,69 3706 10,334
630 60,71 3773 10,41
660 62,72 3840 10,482
690 64,74 3908 10,554
720 66,76 3976 10,624
750 68,78 4045 10,692
р = 8,11 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 19,55 2611 8,3418
90 21,33 2668 8,5051
120 23,10 2725 8,6566
150 24,87 2783 8,7977
180 26,64 2840 8,93
210 28,41 2899 9,0544
240 30,17 2957 9,172
270 31,94 3016 9,2842
300 33,70 3076 9,3914
330 35,47 3136 9,494
360 37,23 3197 9,592
390 39,00 3259 9,687
420 40,76 3321 9,7787
450 42,53 3383 9,8675
480 44,29 3447 9,9533
510 46,06 3511 10,037
540 47,83 3575 10,117
570 49,59 3640 10,196
600 51,35 3706 10,273
630 53,12 3773 10,348
660 54,88 3840 10,421
690 56,65 3908 10,493
720 58,41 3976 10,562
750 60,18 4045 10,631
р = 9,12 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 17,37 2611 8,2869
90 18,96 2667 8,4502
120 20,53 2725 8,6022
340
Новый справочник химика и технолога
Продолжение табл. 3.6.2
Т V ДЛ° S0
150 22,11 2782 8,7433
180 23,68 2840 8,8756
210 25,25 2898 8,9999
240 26,82 2957 9,1176
270 28,39 3016 9,2298
300 29,96 3076 9,337
330 31,52 3136 9,4396
360 33,10 3197 9,5375
390 34,67 3259 9,6326
420 36,23 3321 9,7243
450 37,80 3383 9,813
480 39,37 3447 9,8989
510 40,94 3511 9,9822
540 42,51 3575 10,063
570 44,08 3640 10,142
600 45,65 3706 10,218
630 47,22 3773 10,294
660 48,79 3840 10,367
690 50,36 3908 10,438
720 51,92 3976 10,508
750 53,49 4045 10,576
р = 10,1 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 15,63 2611 8,2379
90 17,06 2667 8,4012
120 18,48 2725 8,5532
150 19,89 2782 8,6947
180 21,31 2840 8.8266
210 22,72 2898 8,951
240 24,14 2957 9,069
270 25,55 3016 9,1812
300 26,96 3076 9,2884
330 28,37 3136 9,391
360 29,79 3197 9,489
390 31,20 3259 9,5844
420 32,61 3321 9,6757
450 34,02 3383 9,7645
480 35,43 3447 9,8503
510 36,85 3511 9,9336
540 38,26 3575 10,014
570 39,67 3640 10,093
600 41,08 3706 10,17
630 42,50 3773 10,245
660 43,91 3840 10,318
690 45,32 3908 10,39
720 46,73 3976 10,459
750 48,14 4045 10,528
р = 20,3 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 7,796 2609 7,916
90 8,514 2666 8,0797
120 9,229 2724 8,2312
150 9,939 2781 8,374
180 10,65 2839 8,5063
Продолжение табл. 3.6.2
Т V ДЛ° S0
210 11,36 2898 8,6307
240 12,06 2957 8,7487
270 12,77 3016 8,8609
300 13,48 3076 8,9681
330 14,18 3136 9,0711
360 14,89 3197 9,1691
390 15,60 3259 9,2641
420 16,30 3321 9,3558
450 17,01 3383 9,4446
480 17,72 3447 9,5304
510 18,42 3511 9,6137
540 19,13 3575 9,6945
570 19,84 3640 9,7732
600 20,54 3706 9,8499
630 21,25 3773 9,9252
660 21,95 3840 9,9981
690 22,66 3908 10,07
720 23,36 3976 10,14
750 24,07 4045 10,208
р = 30,4 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 0,0010171 250,8 0,8311
90 5,666 2664 7,8892
120 6,145 2722 8,0424
150 6,621 2781 8,1852
180 7,095 2839 8,3179
210 7,568 2897 8,4431
240 8,039 2956 8,5612
270 8,512 3016 8,6734
300 8,983 3076 8,781
330 9,455 3136 8,884
360 9,926 3197 8,9819
390 10,40 3258 9,077
420 10,87 3321 9,1687
450 11,34 3383 9,2574
480 11,81 3447 9,3433
510 12,28 3511 9,4266
540 12 75 3575 9,5074
570 13,22 3640 9,5861
600 13,69 3706 9,6627
630 14,16 3772 9,7381
660 14,63 3839 9,8109
690 15,10 3908 9,8825
720 15,58 3976 9,9524
750 16,04 4045 10,021
р = 40,5 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 0,0010171 250,8 0,8311
90 4,242 2664 7,7544
120 4,604 2721 7,9084
150 4,961 2780 8,0508
180 5,318 2838 8,1844
210 5,673 2897 8,3095
240 6,028 2956 8,4284
Физические свойства важнейших веществ
341
Продолжение табл. 3.6.2
Т V Д/г° S0
270 6,382 3015 8,5407
300 6,736 3075 8,6478
330 7,090 3135 8,7508
360 7,443 3197 8,8488
390 7,797 3258 8,9443
420 8,150 3320 9,0355
450 8,503 3383 9,1247
480 8,857 3447 9,2105
510 9,210 3510 9,2934
540 9,563 3575 9,3747
570 9,916 3640 9,4534
600 10,27 3706 9,53
630 10,62 3772 9,6049
660 10,98 3839 9,6782
690 11,33 3907 9,7494
720 11,68 3976 9,8193
750 12,03 4044 9,888
р = 50,7 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 0,0010171 250,8 0,8311
90 3,388 2662 7,6489
120 3,679 2721 7,8034
150 3,966 2779 7,9465
180 4,252 2838 8,0805
210 4,536 2896 8,2061
240 4,821 2955 8,3246
270 5,105 3015 8,4372
300 5,388 3075 8,5448
330 5,671 3135 8,6474
360 5,954 3197 8,7454
390 6,236 3258 8,8408
420 6,519 3320 8,9325
450 6,802 3383 9,0213
480 7,085 3446 9,1075
510 7,367 3510 9,1904
540 7,650 3575 9,2717
570 7,932 3640 9,35
600 8,215 3706 9,427
630 8,497 3772 9,5019
660 8,780 3839 9,5752
690 9,062 3907 9,6464
720 9,345 3975 9,7167
750 9,628 4044 9,785
р - 60,8 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 0,0010171 250,8 0,8311
90 2,818 2661 7,5609
120 3,062 2720 7,7171
150 3,303 2779 7,8611
180 3,541 2837 7,9955
210 3,779 2896 8,1211
240 4,016 2955 8,24
270 4,252 3015 8,3527
300 4,488 3075 8,4603
Продолжение табл. 3.6.2
Т V АА° S0
330 4,724 3135 8,5633
360 4,960 3196 8,6612
390 5,196 3258 8,7567
420 5,432 3320 8,8484
450 5,668 3383 8,9371
480 5,903 3446 9,023
510 6,139 3510 9,1063
540 6,374 3575 9,1875
570 6,610 3640 9,2658
600 6,845 3706 9,3428
630 7,081 3772 9,4178
660 7,316 3839 9,4911
690 7,551 3907 9,5627
720 7,788 3975 9,6322
750 8,023 4044 9,7008
р = 70,9 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 0,0010171 251,2 0,8311
90 2,411 2660 7,486
120 2,622 2719 7,643
150 2,828 2778 7,7887
180 3,033 2837 7,9235
210 3,237 2896 8,0495
240 3,441 2955 8,1684
270 4,644 3014 8,2811
300 3,846 3075 8,3891
330 4,049 3135 8,4921
360 4,251 3196 8,5905
390 4,453 3258 8,6855
420 4,655 3320 8,7772
450 4,858 3383 8,866
480 5,060 3446 8,9518
510 5,262 3510 9,0351
540 5,463 3575 9,1 159
570 5,665 3640 9,1946
600 5,867 3706 9,2721
630 6,069 3772 9,3466
660 6,270 3839 9,4199
690 6,472 3907 9,4915
720 6,675 3975 9,561
750 6,877 4044 9,6296
р = 81,1 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 0,0010171 251,6 0,8311
90 0,0010359 377,2 1,1928
120 2,291 2718 7,5815
150 2,473 2777 7,7259
180 2,652 2836 7,8611
210 2,831 2895 7,9872
240 3,009 2955 8,1065
270 3,187 3014 8,2191
300 3,364 3074 8,3267
330 3,542 3135 8,4301
360 3,719 3196 8,5281
390 3,896 3258 8,6236
342
Новый справочник химика и технолога
Продолжение табл. 3.6.2
Т V дл° S0
420 4,073 3320 8,7152
450 4,250 3383 8,804
480 4,427 3446 8,8903
510 4,604 3510 8,9736
540 4,780 3575 9,0544
570 4,957 3640 9,1331
600 5,134 3706 9,2097
630 5,310 3772 9,2851
660 5,486 3839 9,3583
690 5,663 3907 9,4295
720 5,840 3975 9,4994
750 6,017 4044 9,5681
р = 91,2 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 0,0010171 251,6 0,8311
90 0,0010359 377,2 1,1928
120 2,034 2716 7,5245
150 2,196 2776 7,6702
180 2,356 2836 7,8059
210 2,515 2895 7,9323
240 2,674 2954 8,0516
270 2,832 3014 8,1647
300 2,990 3074 8,2723
330 3,147 3135 8,3753
360 3,305 3196 8,4737
390 3,463 3257 8,5691
420 3,620 3320 8,6608
450 3,777 3383 8,7496
480 3,935 3446 8,8358
510 4,092 3510 8,9191
540 4,249 3574 8,9999
570 4,406 3640 9,0787
600 4,563 3705 9,1553
630 4,720 3772 9,2306
660 4,877 3839 9,3039
690 5,034 3907 9,3751
720 5,191 3975 9,445
750 5,348 4044 9,489
р = 101 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 0,0010171 251,6 0,8311
90 0,0010359 377,2 1,1928
120 1,829 2716 7,4734
150 1,975 2775 7,6204
180 2,119 2835 7,756
210 2,263 2894 7,8829
240 2,406 2954 8,0022
270 2,548 3014 8,1157
300 2,690 3074 8,1157
330 2,832 3135 8,3263
360 2,974 3196 8,4247
390 3,116 3257 8,5201
420 3,258 3320 8,6118
450 3,399 3382 8,701
Продолжение табл. 3.6.2
Т V Д/7° S0
480 3,541 3446 8,7868
510 3,682 3510 8,8702
540 3,824 3574 8,9514
570 3,965 3640 9,0301
600 4,106 3705 9,1067
630 4,248 3772 9,1821
660 4,389 3839 9,2553
690 4,530 3907 9,3265
720 4,672 3975 9,3964
750 4,813 4044 9,4651
р = 122 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 0,0010171 251,6 0,8311
90 0,0010359 377,2 1,1928
120 1,520 2714 7,3859
150 1,643 2774 7,5337
180 1,764 2834 7,6702
210 1,884 2893 7,7975
240 2,004 2953 7,9172
270 2,123 3013 8,0307
300 2,251 3074 8,1387
330 2,359 3134 8,2417
360 2,478 3195 8,3409
390 2,596 3257 8,4356
420 2,714 3319 8,5273
450 2,832 3382 8,6164
480 2,950 3445 8,7027
510 3,068 3509 8,786
540 3,186 3574 8,8668
570 3,304 3640 8,9459
600 3,422 3705 9,0226
630 3,539 3772 9,0979
660 3,657 3839 9,1716
690 3,775 3907 9,2424
720 3,893 3975 9,3123
750 4,011 4044 9,3809
р = 142 кПа
0 0,0010002 0,0 0,0000
30 0,0010044 125,6 0,4367
60 0,0010171 251,6 0,8311
90 0,0010359 377,2 1,1928
120 1,300 2712 7,3106
150 1,406 2773 7,46
180 1,510 2833 7,5974
210 1,613 2893 7,7255
240 1,716 2953 7,8452
270 1,818 3012 7,9587
300 1,920 3073 8,0667
330 2,022 3134 8,1701
360 2,123 3195 8,2689
390 2,224 3256 8,3644
420 2,326 3319 8,4561
450 2,427 3382 8,5453
480 2,528 3445 8,6315
510 2,629 3509 8,7148
Физические свойства важнейших веществ
343
Продолжение табл. 3.6.2
Т V АЛ0
540 2,731 3574 8,7956
570 2,832 3639 8,8743
600 2,933 3705 8,9514
630 3,033 3772 9,0267
660 3,134 3839 9,0996
690 3,235 3907 9,1712
720 3,337 3975 9,2411
750 3,438 4044 9,3098
р = 162 кПа
0 0,0010001 0,0 0,0000
30 0,0010043 125,6 0,4367
60 0,0010170 251,6 0,8311
90 0,0010358 377,2 1,1928
120 1,135 2711 7,2461
150 1,228 2771 7,396
180 1,320 2832 7,5341
210 1,410 2892 7,6623
240 1,500 2952 7,7828
270 1,590 3012 7,8963
300 1,679 3072 8,0043
330 1,768 3133 8,1082
360 1,857 3195 8,2074
390 1,946 3256 8,3024
420 2,035 3318 8,3941
450 2,123 3382 8,4833
480 2,212 3445 8,5695
510 2,300 3509 8,6529
540 2,389 3574 8,7337
570 2,477 3639 8,8128
600 2,566 3705 8,8894
630 2,654 3771 8,9648
660 2,742 3839 9,038
690 2,830 3907 9,1096
720 2,920 3975 9,1796
750 3,008 4044 9,2482
р = 182 кПа
0 0,0010001 0,0 0,0000
30 0,0010043 125,6 0,4367
60 0,0010170 251,6 0,8311
90 0,0010358 377,2 1,1928
120 1,006 2708 7,1879
150 1,090 2770 7,3386
180 1,172 2831 7,4776
210 1,252 2891 7,6066
240 1,333 2951 7,7272
270 1,412 3012 7,841
300 1,493 3072 7,9495
330 1,571 3133 8,0529
360 1,650 3194 8,1521
390 1,729 3256 8,2476
420 1,808 3318 8,3393
450 1,887 3381 8,4284
480 1,966 3445 8,5147
510 2,045 3509 8,598
540 2,123 3574 8,6792
570 2,202 3639 8,7584
Продолжение табл. 3.6.2
Т V л/?° 5ю
600 2,280 3705 8,835
630 2,359 3771 8.9103
660 2,437 3838 8,9836
690 2,516 3906 9,0552
720 2,595 3975 9,1251
750 2,674 4044 9,1938
р = 203 кПа
0 0,0010001 0,0 0,0000
30 0,0010043 125,6 0,4367
60 0,0010170 251,6 0,8311
90 0,0010358 377,2 1,1928
120 0,9030 2706 7,1347
150 0,9791 2768 7,2867
180 1.053 2830 7,427
210 1,126 2890 7,5568
240 1,198 2950 7,6778
270 1,270 ЗОН 7,7921
300 1,342 3072 7,9005
330 1,413 3133 8,0039
360 1,485 3194 8,1031
390 1,556 3256 8,1986
420 1,627 3318 8,2907
450 1,698 3381 8,3799
480 1,769 3444 8,4661
510 1,840 3509 8,5494
540 1,911 3573 8,6307
570 1,982 3639 8,7094
600 2.052 3705 8,7864
630 2,123 3771 8,8618
660 2,193 3838 8,935
690 2,264 3906 9,0066
720 2,336 3975 9,0766
750 2,406 4044 9,1448
р = 304 кПа
0 0,0010001 0,4187 0,0000
30 0,0010043 125,6 0,4367
60 0,0010170 251,6 0,8307
90 0,0010358 377,2 1,1924
120 0,0010602 503,7 1,5278
150 0,6469 2761 7,0866
180 0,6976 2824 7,2298
210 0,7471 2886 7,3625
240 0,7960 2947 7,4852
270 0,8444 3008 7,6007
300 0,8926 3069 7,7104
330 0,9405 3130 7,8147
360 0,9883 3192 7,9139
390 1,036 3254 8,0093
420 1,083 3317 8,1023
450 1,131 3380 8,1915
480 1,178 3444 8,2777
510 1,226 3508 8,3615
540 1,273 3573 8,4427
570 1,320 3638 8,5218
600 1,367 3704 8,5988
630 1,414 3771 8,6742
344
Новый справочник химика и технолога
Продолжение табл. 3.6.2
Т V ДЛ° S0
660 1,462 3838 8,7475
690 1,509 3906 8,8191
720 1,557 3975 8,889
750 1,604 4044 8,9577
р = 405 кПа
0 0,0010000 0,4187 0
30 0,0010042 125,6 0,4367
60 0,0010169 251,6 0,8307
90 0,0010357 377,2 1,1924
120 0,0010602 504,1 1,5273
150 0,4806 2753 6,94
180 0,5197 2818 7,0878
210 0,5576 2881 7,2231
240 0,5947 2944 7,3474
270 0,6314 3005 7,4642
300 0,6678 3067 7,5743
330 0,7040 3128 7,679
360 0,7400 3190 7,7795
390 0,7758 3252 7,8754
420 0,8116 3315 7,9683
450 0,8473 3379 8,0575
480 0,8830 3442 8,1442
510 0,9186 3507 8,2279
540 0,9541 3572 8,3091
570 0,9896 3637 8,3883
600 1,025 3703 8,4653
630 1,060 3770 8,5411
660 1,096 3837 8,6143
690 1,131 3905 8,6859
720 1,167 3974 8,7559
750 1,203 4043 8,8245
р = 507 кПа
0 0,0009999 0,4187 0,0000
30 0,0010042 125,6 0,4367
60 0,0010168 251,6 0,8307
90 0,0010357 377,2 1,1924
120 0,0010601 504,1 1,5273
150 0,0010906 632,2 1,8418
180 0,4130 2812 6,9744
210 0,4438 2877 7,113
240 0,4740 2940 7,2394
270 0,5036 3002 7,3575
300 0,5329 3064 7,4684
330 0,5621 3126 7,5735
360 0,5910 3188 7,674
390 0,6198 3251 7,7707
420 0,6485 3314 7,8636
450 0,6772 3377 7,9532
480 0,7058 3441 8,0399
510 0,7343 3506 8,1241
540 0,7628 3571 8,2053
570 0,7913 3636 8,2848
600 0,8197 3702 8,3619
630 0,8481 3769 8,4372
660 0,8765 3837 8,5109
690 0,9049 3905 8,5825
Продолжение табл. 3.6.2
Т V ДА° S0
720 0,9332 3973 8,6524
750 0,9616 4043 8,7211
р = 608 кПа
0 0,0009999 0,4187 0,0000
30 0,0010041 126 0,4367
60 0,0010168 251,6 0,8307
90 0,0010356 377,6 1,1924
120 0,0010601 504,1 1,5273
150 0,0010906 632,2 1,8418
180 0,3417 2806 6,8793
210 0,3680 2873 7,0213
240 0,3935 2936 7,1498
270 0,4184 2999 7,2691
300 0,4430 3062 7,3809
330 0,4674 3124 7,4873
360 0,4917 3187 7,5882
390 0,5158 3249 7,6849
420 0,5398 3313 7,7778
450 0,5638 3376 7,8678
480 0,5877 3440 7,9549
510 0,6115 3505 8,0391
540 0,6353 3570 8,1207
570 0,6590 3636 8,1998
600 0,6828 3702 8,2773
630 0,7065 3769 8,3527
660 0,7302 3836 8,4264
690 0,7538 3904 8,4979
720 0,7774 3973 8,5683
750 0,8011 4042 8,6369
р = 709 кПа
0 0,0009999 0,8374 0
30 0,0010041 126,4 0,4367
60 0,0010168 251,6 0,8307
90 0,0010356 377,6 1,1924
120 0,0010600 504,1 1,5273
150 0,0010904 632,2 1,8414
180 0,2908 2800 6,7977
210 0,3138 2868 6,9426
240 0,3358 2933 7,0732
270 0,3575 2996 7,1938
300 0,3788 3059 7,3068
330 0,3998 3122 7,4131
360 0,4207 3185 7,5149
390 0,4415 3248 7,612
420 0,4622 3311 7,705
450 0,4827 3375 7,7954
480 0,5033 3439 7,8825
510 0,5237 3504 7,9666
540 0,5442 3569 8,0491
570 0,5646 3635 8,1283
600 0,5849 3701 8,2053
630 0,6053 3768 8,2811
660 0,6256 3836 8,3548
690 0,6459 3904 8,4264
720 0,6662 3972 8,4967
750 0,6864 4042 8,5654
Физические свойства важнейших веществ
345
Продолжение табл. 3.6.2
Т V дл° 5ю
/7 = 811 кПа
0 0,0009998 0,8374 0
30 0,0010040 126,4 0,4363
60 0,0010167 251,6 0,8307
90 0,0010355 377,6 1,192
120 0,0010600 504,1 1,5273
150 0,0010904 632,6 1,8414
180 0,2524 2793 6,7257
210 0,2730 2863 6,8731
240 0,2928 2929 7,0066
270 0,3118 2993 7,128
300 0,3306 3057 7,2419
330 0,3492 3120 7,3491
360 0,3675 3183 7,4508
390 0,3858 3246 7,5484
420 0,4039 3310 7,6422
450 0,4220 3374 7,7326
480 0,4400 3438 7,8201
510 0,4579 3503 7,9043
540 0,4759 3568 7,9863
570 0,4937 3634 8,0659
600 0,5116 3700 8,1433
630 0,5294 3767 8,2191
660 0,5472 3835 8,2924
690 0,5650 3903 8,3644
720 0,5827 3972 8,4347
750 0,6005 4041 8,5034
р = 912 кПа
0 0,0009997 0,8374 0
30 0,0010040 126,4 0,4363
60 0,0010167 251,6 0,8307
90 0,0010355 377,6 1,192
120 0,0010599 504,5 1,5269
150 0,0010903 632,6 1,8414
180 0,2225 2786 6,6595
210 0,2414 2858 6,8107
240 0,2591 2925 6,9463
270 0,2762 2990 7,0698
300 0,2930 3054 7,1841
330 0,3097 3117 7,2921
360 0,3261 3181 7,3943
390 0,3424 3244 7,4923
420 0,3586 3308 7,5865
450 0,3747 3372 7,6769
480 0,3908 3437 7,7644
510 0,4068 3502 7,849
540 0,4227 3567 7,9311
570 0,4386 3633 8,0106
600 0,4545 3699 8,0881
630 0,4704 3767 8,1643
660 0,4862 3834 8,2379
690 0,5020 3903 8,3095
720 0,5178 3972 8,3799
750 0,5336 4041 8,449
р= 1,01 МПа
0 0,0009997 0,8374 0
Продолжение табл. 3.6.2
т V дл° 5ю
30 0,0010040 126,4 0,4363
60 0,0010166 251,6 0,8307
90 0,0010354 377,6 1,192
120 0,0010599 504,5 1,5269
150 0,0010902 632,6 1,8414
180 0,1986 2779 6,5984
210 0,2160 2853 6,7537
240 0,2322 2922 6,8919
270 0,2479 2987 7,0167
300 0,2632 3052 7,1322
330 0,2782 3115 7,2411
360 0,2930 3179 7,3436
390 0,3078 3243 7,442
420 0,3223 3307 7,5362
450 0,3369 3371 7,6271
480 0,3514 3436 7,715
510 0,3658 3501 7,7996
540 0,3802 3566 7,8817
570 0,3945 3632 7,9616
600 0,4089 3699 8,0391
630 0,4232 3766 8,1149
660 0,4374 3834 8,1885
690 0,4517 3902 8,2606
720 0,4659 3971 8,3309
750 0,4801 4040 8,4
р = 2,03 МПа
0 0,0009992 2,093 0
30 0,0010035 127,3 0,4363
60 0,0010164 252,5 0,8298
90 0,0010349 378,5 1,1911
120 0,0010593 504,9 1,5261
150 0,0010896 633 1,8401
180 0,0011267 763,7 2,1378
210 0,0011726 897,6 2,4246
240 0,1109 2879 6,508
270 0,1197 2955 6,6512
300 0,1281 3025 6,7772
330 0,1361 3093 6,8936
360 0,1440 3160 7,0016
390 0,1517 3226 7,1037
420 0,1593 3292 7,2009
450 0,1668 3358 7,2942
480 0,1742 3424 7,3838
510 0,1816 3491 7,4705
540 0,1889 3558 7,5538
570 0,1962 3625 7,6346
600 0,2034 3692 7,7129
630 0,2107 3759 7,79
660 0,2179 3828 7,8641
690 0,2251 3897 7,9369
720 0,2323 3966 8,0077
750 0,2394 4036 8,0768
р = 3,04 МПа
0 0,0009987 2,931 0
30 0,0010031 128,1 0,4358
60 0,0010157 253,3 0,8294
346
Новый справочник химика и технолога
Продолжение табл. 3.6.2
Т V АЛ0 S0
90 0,0010344 379,3 1,1903
120 0,0010588 505,8 1,5253
150 0,0010890 633,9 1,8388
180 0,0011259 764,1 2,1357
210 0,0011715 898,1 2,4225
240 0,06976 2827 6,24
270 0,07670 2917 6,4104
300 0,08290 2996 6,5519
330 0,08869 3070 6,2538
360 0,09423 3141 6,791
390 0,09961 3209 6,8973
420 0,1049 3277 6,9978
450 0,1100 3345 7,0937
480 0,1151 3413 7,1854
510 0,1201 3480 7,2737
540 0,1251 3548 7,3583
570 0,1301 3616 7,4404
600 0,1350 3684 7,5199
630 0,1398 3753 7,5974
660 0,1447 3822 7,6723
690 0,1495 3891 7,7456
720 0,1544 3961 7,8168
750 0,1592 4031 7,8867
р = 4,05 МПа
0 0,0009982 4,187 0,0004
30 0,0010027 129,4 0,4354
60 0,0010152 254,1 0,8286
90 0,0010339 380,2 1,1895
120 0,0010582 506,6 1,5244
150 0,0010883 634,3 1,838
180 0,0011251 764,5 2,1336
210 0,0011704 898,5 2,4204
240 0,0012281 1037 2,7009
270 0,05491 2874 6,2149
300 0,0616 2964 6,3765
330 0,06488 3044 6,5117
360 0,06931 3119 6,6331
390 0,07355 3192 6,7441
420 0,07765 3262 6,8488
450 0,08164 3332 6,9472
480 0,08556 3401 7,0414
510 0,08942 3470 7,131
540 0,09322 3539 7,2176
570 0,09699 3608 7,3005
600 0,1007 3677 7,3809
630 0,1044 3746 7,4592
660 0,1081 3816 7,535
690 0,1117 3886 7,6087
720 0,1154 3956 7,6807
750 0,1190 4026 7,7506
р = 5,07 МПа
0 0009977 5,024 0,0004
30 0,0010022 130,2 0,4354
60 0,0010148 255 0,8281
90 0,0010334 381 1,1886
120 0,0010577 507,4 1,5236
Продолжение табл. 3.6.2
Т V Л/7° 5°
150 0,0010877 635,1 1,8367
180 0,0011243 764,9 2,1323
210 0,0011694 898,9 2,4187
240 0,0012265 1037 2,698
270 0,04167 2825 6,0374
300 0,04637 2930 6,2258
330 0,05052 3017 6,3748
360 0,05431 3097 6,5034
390 0,05788 3173 6,6202
420 0,06130 3246 6,7286
450 0,06460 3318 6,8303
480 0,06782 3390 6,9266
510 0,07098 3460 7,0183
540 0,07408 3530 7,1063
570 0,07715 3600 7,1904
600 0,08018 3670 7,2721
630 0,08317 3740 7,3512
660 0,08614 3810 7,4274
690 0,08911 3880 7,5015
720 0,09205 3951 7,5739
750 0,09498 4022 7,6447
р = 6,08 МПа
0 0,0009972 5,862 0,0004
30 0,0010018 131 0,435
60 0,0010144 255,8 0,8277
90 0,0010329 381,8 1,1878
120 0,0010572 507,9 1,5227
150 0,0010870 635,6 1,8359
180 0,0011235 765,8 2,1307
210 0,0011683 898,9 2,4166
240 0,0012250 1037 2,6959
270 0,0013013 1185 2,9751
300 0,03705 2890 6,0872
330 0,04088 2989 6,2534
360 0,04426 3074 6,3916
390 0,04741 3154 6,5142
420 0,05038 3231 6,6269
450 0,05323 3305 6,732
480 0,05599 3377 6,8303
510 0,05868 3450 6,9241
540 0,06132 3521 7,0133
570 0,06392 3591 7,0991
600 0,06648 3662 7,1816
630 0,06900 3733 7,2616
660 0,07151 3804 7,3386
690 0,07401 3875 7,4131
720 0,07647 3946 7,486
750 0,07893 4017 7,5572
р = 7,09 МПа
0 0,0009967 7,118 0,0004
30 0,0010014 131,9 0,4346
60 0,0010139 256,7 0,8269
90 0,0010325 382,3 1,187
120 0,0010566 508,7 1,5219
150 0,0010864 678,3 1,8347
180 0,0011226 766,2 2,129
Физические свойства важнейших веществ
347
Продолжение табл. 3.6.2
Т V лл° 5й
210 0,0011673 899,3 2,4149
240 0,0012235 1038 2,6938
270 0,0012988 1185 2,9718
300 0,03025 2845 5,9511
330 0,03393 2957 6,1399
360 0,03706 3050 6,2911
390 0,03992 3135 6,4205
420 0,04258 3214 6,5377
450 0,04510 3290 6,6457
480 0,04753 3365 6,747
510 0,04990 3439 6,8429
540 0,05220 3511 6,9333
570 0,05446 3583 7,0204
600 0,05669 3655 7,1042
630 0,05888 3726 7,185
660 0,06106 3797 7,2624
690 0,06322 3874 7,3382
720 0,06353 3941 7,4115
750 0,06746 4013 7,4826
р = 8,Н МПа
0 0,0009962 7,955 0,0004
30 0,0010009 132,7 0,4342
60 0,0010135 261,7 0,8265
90 0,0010320 383,1 1,1861
120 0,0010561 509,5 1,5211
150 0,0010858 636,8 1,8338
180 0,0011219 766,6 2,1277
210 0,0011662 899,7 2,4129
240 0,0012220 1038 2,6917
270 0,0012964 1185 2,9689
300 0,02497 2794 5,8142
330 0,02864 2922 6,0323
360 0,03162 3024 6,1965
390 0,03427 3113 6,335
420 0,03670 3197 6,4573
450 0,03899 3276 6,5691
480 0,04119 3353 6,6729
510 0,04330 3428 6,7709
540 0,04536 3502 6,8634
570 0,04737 3575 6,9518
600 0,04935 3648 7,0359
630 0,05130 3720 7,1176
660 0,05322 3792 7,1963
690 0,05512 3864 7,2725
720 0,05700 3936 7,3462
750 0,05887 4008 7,4178
р = 9,12 МПа
0 0,0009957 9,211 0,0004
30 0,0010005 133,6 0,4342
60 0,0010130 258,3 0,8256
90 0,0010315 383,9 1,1857
120 0,0010556 510 1,5198
150 0,0010851 679,5 1,8326
180 0,0011211 767 2,1261
210 0,0011652 900,2 2,4112
240 0,00112205 1080 2,6892
Продолжение табл. 3.6.2
Г V лл° 5й
270 0,0012941 1184 2,9659
300 0,0014023 1344 3,2531
330 0,02446 2885 5,9281
360 0,02736 2996 6,1081
390 0,02987 3092 6,2555
420 0,03213 3179 6,3832
450 0,03425 3261 6,4992
480 0,03625 3340 6,6059
510 0,03818 3417 6,706
540 0,04005 3492 6,8002
570 0,04187 3566 6,8898
600 0,04365 3640 6,9752
630 0,04539 3713 7,0577
660 0,04712 3786 7,1372
690 0,04882 3858 7,2139
720 0,05051 3931 7,288
750 0,05218 4003 7,3604
р = 10,1 МПа
0 0,0009952 10,05 0,0004
30 0,0010001 134,4 0,4333
60 0,0010126 259,2 0,8252
90 0,0010311 384,8 1,1849
120 0,0010550 510,8 1,519
150 0,0010845 638,1 1,8317
180 0,0011203 767,4 2,1248
210 0,0011642 900,6 2,4095
240 0,0012191 1038 2,6867
270 0,0012918 1184 2,963
300 0,0013978 1344 3,2485
330 0,02102 2843 5,8222
360 0,02390 2967 6,0235
390 0,02631 3069 6,1806
420 0,02845 3161 6,3141
450 0,03043 3246 6,4343
480 0,03228 3327 6,5444
510 0,03407 3406 6,6461
540 0,03578 3482 6,7424
570 0,03744 3558 6,8333
600 0,03908 3632 6,9199
630 0,04067 3706 7,0037
660 0,04224 3779 7,0836
690 0,04379 3853 7,1611
720 0,04523 3926 7,2356
750 0,04684 3999 7,3085
р= 15,2 МПа
0 0,0009929 15,07 0,0008
30 0,0009981 139 0,4321
60 0,0010104 263,3 0,8227
90 0,0010288 388,5 1,1815
120 0,0010524 514,1 1,5152
150 0,0010814 641 1,8267
180 0,0011165 770 2,1185
210 0,0011591 902,3 2,4011
240 0,0012121 1039 2,6762
270 0,00128010 1183 2,9492
300 0,0013781 1338 3,2272
330 0,001542 1519 3,5353
348
Новый справочник химика и технолога
Продолжение табл. 3.6.2
Т V АЛ0 S0
360 0,01307 2780 5,589
390 0,01546 2940 5,8356
420 0,01730 3072 6,0143
450 0,01892 3165 6,1596
480 0,02037 3259 6,2877
510 0,02171 3347 6,4029
540 0,02298 3432 6,5084
570 0,02419 3513 6,6072
600 0,02536 3593 6,6997
630 0,02649 3671 6,7881
660 0,02760 3748 6,8718
690 0,02868 3824 6,9522
720 0,02975 3900 7,0296
750 0,03080 3975 7,105
р = 20,3 МПа
0 0,0009905 19,68 0,0013
30 0,0009960 143,6 0,4304
60 0,0010083 267,1 0,8198
90 0,0010265 392,3 1,1782
120 0,0010498 517,9 1,5106
150 0,0010784 644,3 1,8217
180 0,0011128 772,5 2,1122
210 0,0011543 903,9 2,3932
240 0,0012054 1040 2,6662
270 0,0012711 1182 2,9362
300 0,0013611 1334 3,2083
330 0,001501 1505 3,5002
360 0,001828 1743 3,8849
390 0,00957 2761 5,4742
420 0,01153 2938 5,7355
450 0,01305 3071 5,9226
480 0,01434 3184 6,0763
510 0,01550 3285 6,2082
540 0,01656 3378 6,3254
570 0,01755 3467 6,4326
600 0,01850 3552 6,5318
630 0,01940 3635 6,6256
660 0,02029 3716 6,714
690 0,02113 3796 6,7977
720 0,02197 3874 6,8781
750 0,02278 3952 6,9551
р = 25,3 МПа
0 0,0009882 24,7 0,0013
30 0,0009940 147,8 0,4296
60 0,0010062 271,3 0,8177
90 0,0010242 396,1 1,1748
120 0,0010473 521,3 1,5068
150 0,0010754 647,7 1,8171
180 0,0011092 774,6 2,1064
210 0,0011497 905,6 2,3856
240 0,0011992 1040 2,6561
270 0,0012619 1182 2,9232
300 0,0013460 1331 3,1908
330 0,001471 1496 3,4734
360 0,001690 1698 3,8016
390 0,00512 2446 4,9459
420 0,00782 2787 5,45
Продолжение табл. 3.6.2
Т V АЛ° 5°
450 0,00944 2964 5,6999
480 0,01066 3100 5,8854
510 0,01173 3217 6,0378
540 0,01269 3322 6,168
570 0,01356 3419 6,2852
600 0,01438 3510 6,392
630 0,01515 3599 6,4921
660 0,01589 3684 6,5846
690 0,01661 3766 6,6721
720 0,01731 3848 6,7554
750 0,01798 3928 6,835
р = 30,4 МПа
0 0,0009859 29,73 0,0013
30 0,0009920 152,4 0,4279
60 0,0010042 275,5 0,8156
90 0,0010220 399,8 1,1723
120 0,0010448 525 1,5026
150 0,0010726 650,6 1,812
180 0,0011057 777,9 2,1009
210 0,0011452 907,3 2,42
240 0,0011932 1041 2,6465
270 0,0012533 1181 2,9102
300 0,0013327 1328 3,174
330 0,001446 1488 3,4474
360 0,001634 1675 3,7484
390 0,00220 1962 4,1893
420 0,00521 2580 5,1058
450 0,00697 2840 5,4738
480 0,00822 3009 5,7041
510 0,00922 3145 5,8804
540 0,01010 3262 6,0265
570 0,01091 3367 6,1546
600 0,01163 3467 6,2702
630 0,01230 3560 6,3761
660 0,01296 3650 6,4732
690 0,01361 3737 6,5649
720 0,01421 3821 6,6516
750 0,01479 3903 6,7336
р - 35,5 МПа
0 0,0009836 34,33 0,0013
30 0,0009900 156,6 0,4271
60 0,0010022 279,7 0,8139
90 0,0010198 403,6 1,1698
120 0,0010423 528,4 1,4993
150 0,0010698 654,4 1,8079
180 0,0011023 780,8 2,0959
210 0,0011408 909,4 2,3718
240 0,0011875 1043 2,6385
270 0,0012455 1181 2,8998
300 0,001321 1327 3,1602
330 0,001424 1484 3,4273
360 0,001584 1658 3,7099
390 0,00194 1887 4,062
420 0,00329 2323 4,706
450 0,00514 2695 5,2343
480 0,00646 2910 5,5249
510 0,00743 3068 5,7317
Физические свойства важнейших веществ
349
Продолжение табл. 3.6.2
Т V дл° S0
540 0,00827 3199 5,8954
570 0,00901 3315 6,0353
600 0,00969 3421 6,1596
630 0,01031 3522 6,2714
660 0,01090 3616 6,374
690 0,01146 3707 6,4694
720 0,01200 3794 6,5599
750 0,01252 3879 6,6445
р = 40,5 МПа
0 0,0009813 38,94 0,0013
30 0,0009880 161,2 0,4258
60 0,0010002 283,9 0,8122
90 0,0010177 407,4 1,1673
120 0,0010401 532,1 1,4959
150 0,0010672 656,9 1,8037
180 0,0010991 783,4 2,0909
210 0,0011367 911,9 2,3655
240 0,0011821 1044 2,6306
Окончание табл. 3.6.2
Т V дл° 5ю
270 0,0012379 1182 2,8901
300 0,001309 1325 3,1468
330 0,001407 1477 3,4072
360 0,001548 1645 3,6798
390 0,00180 1851 3,9976
420 0,00243 2155 4,4435
450 0,00386 2540 4,989
480 0,00512 2801 5,3424
510 0,00610 2988 5,586
540 0,00690 3135 5,7711
570 0,00760 3261 5,9235
600 0,00822 3375 6,0558
630 0,00880 3482 6,1751
660 0,00935 3581 6,2835
690 0,00987 3676 6,3832
720 0,01036 3766 6,477
750 0,01083 3854 6,5649
3.6.1. Термодинамические показатели органических соединений
В табл. 3.6.3 приведены: молярная теплоемкость и стандартная молярная энтропия органических соединений, изменения молярной стандартной энтальпии и энергии Гиббса при их образовании, изменение молярной стандартной энтальпии при сгорании, плавлении и испарении веществ.
Соединения расположены по эмпирическим формулам в соответствии с системой Хилла (в порядке возрастания числа атомов С, Н, Br, Cl, F, I. N, О, S).
В графе «Состояние» указано агрегатное состояние вещества в стандартных условиях, к которым относятся данные последующих четырех граф. В качестве стандартных условий во всех случаях приняты температура 25 °C (298,15 К) и давление 1,01325 • 105 Па. Температуры плавления и кипения приведены при стандартном давлении (1,01325 • 105 Па).
В таблице приняты следующие обозначения:
С® — стандартная молярная теплоемкость вещества, Дж/(моль • К);
5° — стандартная молярная энтропия вещества, Дж/(моль • К);
AfH° — стандартная молярная энтальпия образования, т. е. изменение энтальпии при образовании 1 моль данного соединения из простых веществ, когда все вещества этой реакции находятся в стандартном состоянии, кДж/моль;
AfC70 — стандартная молярная энергия Гиббса образования, т. е. изменение энергии Гиббса при образовании 1 моль данного соединения из простых веществ, когда все вещества этой реакции находится в стандартном состоянии, кДж/моль;
Ас//° — стандартная молярная энтальпия сгорания вещества, кДж/моль;
Гпл — температура плавления, °C;
Afus//° — стандартная молярная энтальпия плавления (теплота плавления), кДж/моль;
Гисп — температура испарения, °C;
АуарЯ° — стандартная молярная энтальпия испарении (теплота испарения), кДж/моль.
Энтальпия сгорания Ас//° относится к указанному слева агрегатному состоянию вещества при 20 °C; если указания на состояние отсутствует, АСН° относится к стандартному состоянию вещества в газовой фазе. В качестве продуктов сгорания приняты: СО2, N2, галогениды водорода, SO2 в газообразном состоянии, Н2О в жидком состоянии.
Новый справочник химика и технолога
Термохимические характеристики органических соединений
Таблица 3.6.3
Формула Название Состояние Ф Дж/(моль • К) 5°, Дж/(моль • К) Af/7°, кДж/моль AfG°, кДж/моль Сгорание Плавление Испарение
Состояние дс#°. кДж/моль Д1Л, °C AfiX-кДж/моль гнс„, °C Avaptf°, кДж/моль
CBrClF2 Бром(дифтор)хлорметан г. 74,61 331,3
CBrCl2F Бром(фтор)дихлорметан г. 80,47 331
СВгС13 Бромтрихлорметан г. 85,33 333,1
CBrF3 Бромтрифторметан г. 74,94 297,6
CBr2ClF Дибром(фтор)хлорметан г. 82,61 343,1
CBr2Cl2 Дибромдихлорметан г. 87,42 348,6
CBr2F2 Дибромдифторметан г. 78,71 325,1
CBr3Cl Трибромхлорметан г. 89,39 357,4
CBr3F Трибромфторметан г. 84,49 346
CBr4 Т етрабромметан г. 91,27 358,1 50,2 36 90,1 4,1 187 43,54
CC1F3 Трифторхлорметан (фреон-13) г. 67,53 286,3 81,2 15,16
Продолжение табл. 3.6.3
Формула Название Состояние с° Дж/(моль • К) 5°, Дж/(моль • К) Af/7°, кДж/моль Af<70, кДж/моль Сгорание Плавление Испарение
Состояние АСЯ°, кДж/моль Тпп, °C АпХ, кДж/моль 7„с„, °C AvapH°, кДж/моль
CC12F2 Дифтордихлорметан (фреон-12) г. 73,06 301,5 -15,5 4,14 -30,5 20,31
CC13F Фтортрихлорметан (фреон-11) г. 77,96 309,7 -110,68 6,9 23,6 24,95
СС14 Т етрахлорметан г. 83,48 309,9 -106,76 -64,06 ж. 156,2 -22,9 2,51 76,7 30,02
CF3I Иодтрифторметан г. 70,76 307
CF4 Т етрафторметан г. 61,25 262,2 -681,61 -635,6 -183,69 0,7 -128,02 12,6
CHBrCIF Бром(фтор)хлорметан г. 63,26 305,1
CHBrF2 Бромдифторметан г. 57,69 291,9
CHBr2CI Дибромхлорметан г. 69,21 327,9
C2HBr2Cl (2Н)Дибромхлорметан г. 72,52 329,5
CHBr2F Дибромфторметан г. 65,19 316,9
СНВгз Бромоформ г. 71,13 330,9 25,121 15,91 8,05 11,1 50 43,54
C2HBr3 (2Н)Бромоформ г. 74,4 332,2
CHC1F2 Дифторхлорметан (фреон-22) г. 55,89 281,1 -40,8 21,35
chci2f Фтордихлорметан (фреон-21) г. 61 293,1 8,9 26,8
CHCI3 Хлороформ г. 65,02 295,7 -100,48 -66,99 ж. 373,5 -63,5 9,21 61,2 29,39
C2HC13 (2Н)Хлороформ г. 68,54 297,1
CHF3 Фтороформ (фреон-23) г. 51,12 259,7 -84,2 18,42
c2hf3 (2Н)Фтороформ г. 53,59 261,1
CHN3O6 Тринитрометан ж. 78
CHN Циановодород г. 35,92 201,9 130,63 120,16 -13,24 8,41 25,70 25,23
CH2BrCl Бромхлорметан г. 52,75 287,5
CH2BrF Бромфторметан г. 49,24 276,2 -87,923 -58,62
CH2BrI Бромиодметан г. 56,4 307,7
CH2Br2 Дибромметан г. 54,89 293,4 -4,1868 -5,862 -52,7 4,19 97,2 36,01
CH2C1F Фторхлорметан г. 47,1 264,4 -9 23,45
CH2C1I Иодхлорметан г. 54,51 296,3
CH2C12 Дихлорметан г. 51,16 270,4 г. 447,2 -97 4,61 40 28,01
ch2f2 Дифторметан г. 43,04 288,6
CH212 Дииодметан г. 57,9 309,3 ж. 746,9 6,10 12,1
CH2O Формальдегид г. 35,38 218,9 -115,97 -113,8 г. 561,4 -19,3 24,49
C2H2O (2Н2)Формальдегид г. 38,23 225,2 -362,87 -335,9
CH2O2 Муравьиная кислота г. 47,57 251,2 -376,94 -350,2 ж. 262,9 8,30 12,7 100,5 22,27
CH3Br Бромметан г. 42,45 246,3 -35,588 -25,96 г. 770,4 -93,68 5,98 3,56 23,93
Физические свойства важнейших веществ
Продолжение табл. 3.6.3
Формула Название Состояние с° Дж/(моль • К) 5°, Дж/(моль • К) кДж/моль AfC°, кДж/моль Сгорание Плавление Испарение
Состояние Дс/7, кДж/моль Г,,, °C AfiX-кДж/моль Г,fcn, °C Avap/7°, кДж/моль
СН22НВг (2Н)Бромметан г. 44,67 257,5
СН2Н2Вг (2Н2)Бромметан г. 47,44 260,6
СН3С1 Хлорметан г. 40,78 234,6 <82,06 -58,62 г. 687,5 -97,72 6,44 -24,22 21,56
CH3F Фторметан г. 37,43 222,9 -78,1 17,71
СН31 Иодметан г. 44,13 254 20,515 22,19 ж. 815,2 42,4 28,05
С2Н31 (2Н3)Иодметан г. 50,53 261,8
CH3NO Формамид г. 45,38 249,2 2,55 6,7
CH3NO2 Нитрометан г. 57,36 275,2 -74,776 -6,95 ж. 709,2 -28,38 9,71 25,00 38,3
СН4 Метан г. 35,74 186,3 -74,898 -50,83 891 -182,49 0,94 -161,58 8,202
CH4N2O Мочевина ТВ. 93,2 104,7 -333,41 -197,3 ТВ. 634,7 132,6 15,07
СН4О Метанол г. 43,92 239,9 -201,3 -162 ж. 715,5 97,90 3,17 64,7 35,29
CH4S Метантиол г. 50,74 254,8 -12,435 -37,34 -123,00 5,91 5,96 24,58
ch5n Метанамин (метиламин) г. 54,01 241,7 -28,052 27,633 ж. 1072 -93,46 6,14 -6,32 25,83
ch6n2 Метилгидразин г. 71,18 278,9
ch6n2o3 Метанаминия нитрат ТВ. 337,46
(метиламмония нитрат)
c2ci3n Трихлорацетонитрил г. 96,13 336,2
C2C16 Гексахлорэтан г. 136,5 396,8 ТВ. 460,5 184,4 51,08
C2HC15 Пентахлорэтан г. 117,9 380,7 -29,0 11,3 159,3 40,61
C2HBrF2 2-Бром-1,1 -дифторэтилен г. 73,81 315
C2H2 Ацетилен г. 43,96 201 226,9 209,3 1300,5 -81,5 3,77 -83,6 17,29
C2H2Br2 (£)-1,2-Дибромэтилен г. 71,05 313,6
C22H2Br2 (£)-1,2-Дибромэтилен-б/2 г. 76,24 318,5
C2H2Br2 (Z)-1,2-Дибромэтилен г. 68,83 311,4
C22H2Br2 (Z)-1,2-Дибромэтилен-б/2 г. 75,24 316,4
C2H2C14 1,1,1,2-Тетрахлорэтан г. 102,9 356,3 130,5 36,84
C2H2C14 1,1,2,2-Тетрахлорэтан г. 100,9 363 145 38,52
C2H2O4 Щавелевая кислота ТВ. 108,9 120,2 -827,31 -698,4 ТВ. 252 100 90,85
C2H3C13 1,1,1 -Трихлорэтан г. 93,49 322,8 -32,8 3,35 13,37 33,33
C2H3C13 1,1,2-Трихлорэтан г. 89,05 337,3 113,9 36,84
c2h3f3 1,1,1 -Трифторэтан г. 78,5 286,7 -111,34 6,2 -48,76 19,19
c2h3n Ацетонитрил г. 52,29 243,5 ж. 1266,1 -44,9 8,92 81,5 32,78
c2H4 Этилен г. 43,58 219,6 52,318 68,17 1411,9 -169,15 3,35 -103,70 13,52
C2H4C12 1,1 -Дихлорэтан г. 76,28 304,5 ж. 1202 -96,7 5,44 57,4 30,56
C2H4C12 1,2-Дихлорэтан г. 79,55 309 г. 1134,6 -35,7 8,83 83,5 32,24
C2H4O Ацетальдегид г. 54,68 264,4 -166,09 -133 ж. 1168,1 -118 3,22 20,1 27,21
C2H4O Оксиран (окись этилена) г. 48,19 243,4 -51,037 -11,68 ж. 1264,8 112,45 5,16 10,56
Новый справочник химика и технолога
Продолжение табл. 3.6.3
Формула Название Состояние с°, р Дж/(моль • К) 5°, Дж/(моль • К) Д/Л кДж/моль Af€7°, кДж/моль Сгорание Плавление Испарение
Состояние дХ кДж/моль г„л, °C кДж/моль Гис.,, °C ДхаХ кДж/моль
с2н4о2 Уксусная кислота г. 72,43 293,5 -436,68 -381,8 16,61 11,72 118,2 24,41
ж. 123,5 159,9 -487,34 -392,7 ж. 876,7
C2H4S Тииран г. 53,72 255,4 131,09 16,45
С2Н5С1 Хлорэтан г. 62,38 275 г. 1326 -138,33 4,46 12,27 24,7
c2h5no2 Глицин ж. 99,23 109,3 -528,92 -371 ТВ. 981,8
c2h5no2 Нитроэтан ж. 140,17 20 38,1
c2H6 Этан г. 52,69 229,6 -847,24 -32,91 1560,9 -182,81 2,86 -88,63 14,64
c2h6n2o5 Глицина нитрат ТВ. 726,83
С2Н6О Этанол г. 73,65 278,2 -235,47 -167,6 ж. 1371,6 -114,6 5,02 78,5 38,6
С2Н6О2 Этиленгликоль г. 323,8 -398,16 -313,3 ж. 1180,3 -15,6 11,64 197,2 56,94
C2H6S Димети л сульф ид г. 74,15 286 -102,16 -33,12
c2H6s Этантиол г. 72,72 296,3 -110,74 44,8 34,4 28,89
c2h7n У-Метилметанамин (ди метиламин) г. 69,42 273,4 -27,633 -59,03 ж. 1744,6 -92,19 5,95 6,8 26,5
c2h8n2o3 У-Метилмстанаминия ТВ. 330,76
нитрат (диметиламмония нитрат)
c2h8n2o3 Этанаминия нитрат (этиламмония нитрат) ТВ. 363,83
c2h8n2o4 2-Г идроксиэтанаминия нитрат (этаноламина нитрат) ТВ. 576,1
C2HhB2N Диметиламинодиборан г. 117,8 313,7
c3h2n2 Малононитрил г. 72,52 289,1
C3H3N Акрилонитрил г. 63,81 274,1
c3H4 Аллен (пропадиен) г. 59,03 244,1 192,26 202,5 1945,6 -135,25 4,405 -34,42 20,52
c3H4 Пропин г. 60,71 248,3 185,55 193,9 1938,9 -23,23 22,06
c3h5n Пропиононитрил г. 72,12 283,9 ж. 1910,9 -91,9 6,071 97,16 30,98
c3H6 Пропен г. 63,93 267,1 20,427 62,76 2059,9 -185,25 3,004 -47,75 18,48
c3H6 Циклопропан г. 55,27 237,9 70,715 104,4 -127,42 5,447 -32,8 20,1
c3h6n2o4 1,1 -Динитропропан ж. -170,74
c3h6n2o4 1,3-Динитропропан ж. -224,04
c3h6n2o4 2,2-Динитропропан ТВ. -187,86
c3H6o Ацетон г. 74,94 295,1 -216,54 -152 ж. 1786,9 -94,6 5,719 27,5 32,29
c3H6s Тиетан г. 69,38 285,3 68,329 -2,596
c3h7no2 1-Нитропропан ж. -167,68
c3h7no2 2-Нитропропан ж. -183,3
Физические свойства важнейших веществ
Продолжение табл. 3.6.3
Формула Название Состояние с°, ^р' Дж/(моль • К) 5°, Дж/(моль • К) кДж/моль AfG°, кДж/моль Сгорание Плавление Испарение
Состояние Ас/Г, кДж/моль r,UI, °C Afus^0, кДж/моль 7иС1„ °C Avap/7°, кДж/моль
С3Н8 Пропан г. 73,56 270,1 -103,92 -23,5 2221,5 -187,65 3,526 -42,06 18,79
С3Н8О Пропан-1-ол г. 322 -260,54 -163,8 ж. 2011,8 -127 5,196 25 46,26
С3н8о Пропан-2-ол г. 306,5 -275,61 -175,5 ж. 1987,9 -89,5 5,376 82,3 40,19
С3Н8О3 Глицерин ж. 223,2 208,1 -659,84 469,3 ж. 1662,2 17,9 18,48 195 76,07
c3H8s (Метилсульфанил)этан г. 95,12 333,4
c3H8s Пропан-1 -тиол г. 94,83 336,6 -131,72 -37,14
c3H8s Пропан-2-тиол г. 96,05 324,5 -140,09 -41,87
C3H10N2O3 2У,7У-Диметилметанаминия ТВ. 297,68
нитрат
(триметиламмония нитрат)
C4H2 Бута-1,3-диин г. 73,69 250,2 10,3 23,36
c4H2o3 Фуран-2,5-дион ТВ. 469,88
(малеиновый ангидрид)
С4Н4О Фуран г. 59,54 261,9 31,2 27,2
с4н6 Бута-1,2-диен г. 80,18 293,2 162,32 198,6 2595,5 -136,190 6,966 10,84 24,07
с4н6 Бута-1,3-диен (дивинил) г. 79,59 278,9 110,24 150,8 2543,4 -108,915 7,99 —4,6 22,5
с4н6 Бут-1-ин г. 81,48 291 165,71 244,1 2596 -125,720 6,033 8,07 24,55
с4н6 Бут-2-ин г. 78 283,5 146,41 185,6 2579,6 -32,260 9,241 26,99 26,54
с4н6 Циклобутен г. 67,11 263,7 2,4 23,57
С4Н6О2 Бутан-2,4-дион (диацетил) ж. -366,76
c4h7n Бутиронитрил г. 96,05 324,1 ж. 2567,8 -112,6 5,024 20 40,49
с4н8 Бут-1-ен г. 85,7 305,8 -0,1256 71,55 2719,1 -185,35 3,851 -6,25 21,96
с4н8 (Е)-Бут-2-ен г. 87,88 296,7 -11,179 63,01 2708,1 -105,550 9,763 0,88 22,77
с4н8 (2)-Бут-2-ен г. 78,96 301 -6,992 65,9 2712,3 -138,910 7,314 3,72 24,19
С4н8 2-Метилпропен г. 89,18 293,8 -16,915 58,11 2702,3 -140,350 5,935 -7,01 22,27
с4н8 Циклобутан г. 72,26 258,4 6,1965 110,2 -90,35 1096 12,6 23,99
(285,67 К)
С4Н8О Бутанон ж. 276,33
С4Н8О2 1,4-Диоксан ж. 152,8 196,8 -398,08 -233 11,3 12,6 100,3 31,78
С4Н8О2 Этилацетат ж. 259,6 463,48 -315,7 ж. 2247,9
C4H8S Т етрагидротиофен г. 90,94 309,4 -98,39 -5,862 1910,9
c4h9n Пирролидин г. 82,31 309,9 -3,4332 114,9 2059,9
c4h9no2 1 -Нитробутан ж. -192,72
c4h9no2 2-Нитробутан ж. -207,71
C4H]Q Бутан г. 97,51 310,3 -126,23 -17,17 2879,1 -138,350 4,663 -0,5 224,2
С4Ню Изобутан г. 96,88 294,8 -134,61 -20,93 2870,7 -159,600 4,544 -11,7 21,27
C4H10O Бутан-1 -ол г. 355 -284,24 -157,9 ж. 2673,7 -79,9 9,274 117 43,84
354 Новый справочник химика и технолога
Продолжение табл. 3.6.3
Формула Название Состояние Дж/(моль • К) 5°. Дж/(моль • К) кДж/моль кДж/моль Сгорание Плавление Испарение
Состояние дл°, кДж/моль 7’пл. °с ДяХ-кДж/моль ГИС11, °с A W0 £Avap-'7 9 кДж/моль
СдНюО Диэтиловый эфир ж. 253,3 -273,4 -116,7 ж. 2728,5 -116,3 7,536 34 26,71
СдНюО 2-Метилпропан-2-ол г. 324,1 -324,38 -189,2 ж. 2634,8 25,5 6,783 82,86 39,69
c4H10s Бутан-1-тиол г. 118,2 375,5 -151,94 -28,26
c4H10s Бутан-2-тиол г. 121 338,3
c4H10s 2-Метилпропан-1 -тиол г. 118,4 363,1 -161,11 -33,75
c4H10s Диэтилсульфид г. 117,1 368,3
c4H10s 1 -(Метилсульфанил)пропан г. 117,4 372 -145,62 -20,89
c4H10s2 Диэтилдисульфид г. 143,4 414,5
c4h12n2o3 jV-Этилэтанаминия нитрат ТВ. 413,24
(диэтиламмония нитрат)
c5h5n Пиридин г. 140,8 ж. 2757 -42 8,227 114,1 35,55
C5H6S 3-Метилтиофен г. 94,91 321,5 19,008 82,56
c5H8 Изопрен г. 104,7 315,9 75,781 146 3188,7 -145,950 4,827 34,07 25,71
c5h8 З-Метилбута-1,2-диен г. 105,5 319,9 129,79 198,7 3242,7
c5h8 2-Метилбут-2-ин г. 104,8 319,2 136,49 210 3249,5
c5h8 Пента-1,2-диен г. 105,5 333,7 145,7 210,6 3258,6 44,86 27,21
c5h8 (£)-Пента-1,3-диен г. 103,4 319,9 77,874 146,8 3190,8 42,03 26,75
c5H8 (2)-Пента-1,3-диен г. 94,62 324,5 78,293 146 3191,2 44,07 27,13
c5h8 Пента-1,4-диен г. 105,1 333,7 105,51 170,4 3218,4 148,275 6,146 25,97 25,04
c5h8 Пента-2,3-диен г. 101,3 324,9 138,58 206,1 3251,5 48,26 27,93
c5H8 Пент-1-ин г. 105,4 330 144,44 194,3 3257,5 40,25 27,21
c5h8 Пент-2-ин г. 98,77 332 128,95 205,7 3242
c5h8 Спиро[2.2]пентан г. 88,17 282,4 -174,84 265,3 -107,02 6,438 38,98 26,75
c5H8 Циклопентен г. 75,15 289,9 32,95 110,9 -135,070 3,366 44,24 27,38
c5h9n Пентаннитрил г. 118,8 363
c5H10 2-Метилбут-1 -ен г. 111,7 342,2 -36,341 64,94 3362,7 -137,560 7,916 31,16 25,53
c5H10 2-Метилбут-2-ен г. 105,1 338,8 -42,58 59,7 3356,5 -133,768 7,602 38,57 26,33
c5H10 З-Метилбут-1 -ен г. 118,7 333,7 -28,973 74,82 3370,1 -168,528 5,363 10,00 24,07
c5H10 Пент-1 -ен г. 109,7 346 -20,934 79,38 3378,1 -165,220 5,811 29,97 25,23
c5H10 (Е)-Пент-2-ен г. 108,5 340,6 -31,778 70,17 3367,3 -140,244 8,357 36,35 26,13
c5H10 (2)-Пент-2-ен г. 101.8 346,5 -28,093 71,89 3371,8 -151,390 7,116 36,94 27
c5H10 Циклопентан г. 82,98 293,1 -77,288 38,64 3321,8 93,879 0,609 49,26 27,47
c5H10o Циклопентанол ж. 300,49
СзНшОг 2,2-Диметилпропановая ТВ. 565,22
кислота
C5H)0O2 2-Метилбутановая кислота ж. 556,84
Физические свойства важнейших веществ
Продолжение табл. 3.6.3
Формула Название Состояние Дж/(моль • К) 5°, Дж/(моль • К) Af//°, кДж/моль AfG°, кДж/моль Сгорание Плавление Испарение
Состояние Ас//3, кДж/моль гШ1, °с А^/Л кДж/моль 7’иси, °C AVap/7°, кДж/моль
С5Н10О2 З-Метилбутановая кислота (изовалериановая кислота) ж. 565,22
С5НЮО2 Пентановая кислота (валериановая кислота) ж. 548,47 ж. 2853,7
c5H10s Тетрагидротиопиран г. 108,3 323,5 -127,19 13,69
с5н12 Изопентан г. 118,9 343,8 -154,58 -14,82 3530,5 -159,890 5,134 27,85 24,7
С5н12 Неопентан г. 121,7 306,6 -166,09 -15,24 3519 -16,550 3,258 9,50 22,65
с5н12 Пентан г. 120,3 349,2 -146,54 -8,374 3538,5 -129,723 8,42 36,07 25,81
с5н12о 2-Метил бутан-2 -ол г. 3555 -352,9 -186,3 -Н,9 4,497 20 46,05
С5н12о Пентан-1-ол г. 381,8 -307,39 -148,4 ж. 3323,1 -78,5 9,835 25 52,13
c5H12s Пентан-1-тиол г. 141,8 415,3
С6Н4С12 1,2-Дихлорбензол г. 113,5 341,6 ж. 2812,7
С6Н4С12 1,3-Дихлорбензол г. 114,5 343,9
С6Н4С12 1,4-Дихлорбензол г. 114,1 334,7
С6Н4О2 Бензо-1,4-хинон ТВ. -184,64 115,7 18,46 25 62,8
С6Н5С1 Хлорбензол г. 97,13 313,4 -45 7,536 130,56 36,55
C6H5F Фторбензол г. 94,5 302,8 -110,87 -63,3
c6h5no2 Нитробензол ж. 224,4 15,91 146,3 ж. 3094,9 5,7 12,12 209,6 48,86
c6H6 Бензол г. 81,73 269,4 82,982 129,7 3303,7 5,533 9,843 80,10 30,77
С6Н6О Фенол ТВ. -162,87 ТВ. 3065,6 42 11,26 183 48,15
СбН6О2 Гидрохинон ТВ. -363,2 ТВ. 2862,5 170,3 27,13 78,5 99,23
C6H6S Бензолтиол (тиофенол) г. 100,8 338,8 47,06 107,6
c6h7n Анилин ж. 199,7 191,8 35,337 153,3 ж. 3398,4 -6,2 10,55 184 40,65
c6h7n 2-Метилпиридин (а-пи колин) г. 102,07
c6h7n 3-Метил пиридин (0-пиколин) г. 113,71
c6h7n 4-Метил пир идин (у-пиколин) г. 102,28
c6h8n2o3 Бензоламиния нитрат (анилиния нитрат) ТВ. 726,83
СбНю Гекс-1-ин г. 128,3 369 123,72 218,4 3916,5 71,4 29,31
СбНю 1 -Метилциклопентен г. 100,9 326,6
СбНю 3-Метил циклопентен г. 100,1 330,8
СбНю 4-Мет илциклопентен г. 100,1 329,1
СбНю Циклогексен г. 105,1 311 -7,1176 105,2 -103,500 2,353 82,98 30,69
C6HnN Гексаннитрил г. 141,7 402,5
Новый справочник химика и технолога
Продолжение табл. 3.6.3
Формула Название Состояние Дж/(моль • К) 5°, Дж/(моль • К) кДж/моль AfG°. кДж/моль Сгорание Плавление Испарение
Состояние Дс#°. кДж/моль 7'„л. °C кДж/моль Тисп, °C AvaX кДж/моль
с6н12 Гекс-1-ен г. 132,4 384,9 -41,701 87,76 4037,2 63,48 28,43
С6н12 (£)-Гекс-2-ен г. 132,5 380,9 -52,586 78 4026,3
С6н]2 (7)-Гекс-2-ен г. 125,8 386,7 48,399 80,22 4030,5
С6н12 (£)-Гекс-3-ен г. 132,9 375,1 -52,586 79,72 4026,3
С6н12 (7)-Гекс-3-ен г. 86,04 379,9 ^48,399 82,31 4030,5
С6Н12 2,3-Диметилбут-1 -ен г. 143,6 365,9 -61,881 72,98 4017
С6н12 2,3-Диметилбут-2-ен г. 127,6 362,9 -66,612 69,17 4012,3 -74,280 5,464
С6Н12 3,3-Диметилбут-1 -ен г. 126,6 344 -59,662 81,77 4019,2 -115,20 1,097
С6н12 З-Метиленпентан г. 133,6 376,9 -54,093 77,5 4024,8
С6Н12 2-Метилпент-1 -ен г. 134,4 382,4 -56,773 73,14 4022,1
С6н12 2-Метилпент-2-ен г. 126,7 378,7 -62,635 68,41 4016,2
С6Н12 З-Метилпент-1 -ен г. 145 377,1 ^46,139 85,41 4032,7
С6н12 (Е)-3-Метилпент-2-ен г. 126,7 382,1 -59,955 70,09 4018,9
С6Н12 (7)-3-Метилпент-2-ен г. 126,7 378,7 -59,955 71,09 4018,9
С6н12 4-Метилпент-1 -ен г. 126,6 368 48,818 85,62 4030
С6н12 (Е)-4-Метилпент-2-ен г. 141,5 368,5 -59,704 74,4 4019,2
С6н12 (7)-4-Метилпент-2-ен г. 133,6 373,6 -55,517 77,04 4023,3
С6н12 Метилциклонентан г. 109,9 340,1 -106,76 35,8 3972,1 -142,445 6,933
С6н12 Циклогексан г. 106,3 298,4 -123,22 31,78 3955,6 6,554 2,679 81 30,73
с6н12о Циклогексанол ж. -352,9 -186,3 ж. 3729,2 23,9 1,788 158,7 45,51
С6Н12О2 Метил-2,2-диметил-пропаноат ж. 552,66
С6Н12О2 Метил-2-мети л бутаноат ж. 535,91
С6Н12О2 Метил-3 -метилбутаноат ж. 540,1
С6Н12О2 Метилпентаноат ж. 527,54
С6Н14 Гексан г. 143,2 388,7 -167,3 -0,293 4197,6 -95,348 13,04 68,74 28,89
СбН14 2,2-Диметилбутан г. 142 358,5 -185,68 -9,923 4179,1 -99,87 0,58 49,74 26,38
С6Н14 2,3 - Диметил бутан г. 140,6 366 -177,9 -4,103 4187 -128,538 0,812 57,99 27,3
С6н14 2-Метилпентан г. 144,3 380,8 -174,42 -5,024 4190,4 -153,67 6,28 60,21 27,8
С6н14 З-Метилпентан г. 143,2 380 -171,74 -2,135 4193,1 63,28 27,7
С6Н14О Г ексан-1 -ол г. 415,7 -330,5 -140,9 -51,6 15,37 20 64,9
c6H14s Гексан-1-тиол г. 164,8 454,4
C6H16N2O3 УУ,А\Диметилметанаминия ТВ. 407,38
нитрат (триэтиламмония нитрат)
c7H6o2 Бензойная кислота ТВ. 167,6 ТВ. 3228,9 121,7 23,32 110 86,16
С7Н8 Толуол г. 103,8 320 50,032 122,4 3950,6 -94,991 6,624 110,63 33,54
Физические свойства важнейших веществ 357
Продолжение табл. 3.6.3
Формула Название Состояние с°, Дж/(моль • К) 5°, Дж/(моль • К) Af/7°, кДж/моль кДж/моль Сгорание Плавление Испарение
Состояние АСЯ\ кДж/моль 7’ил, °C кДж/моль гисп, °C AvapH°, кДж/моль
С7Н8О С7Н9Ы c7h9n c7h10n2o3 с7н12 с7н12 с7н12 С7н12 C7Hi2 С7н12 с7н12 с7н12 С7Н12 с7н12 c7h13n Фенилметанол 2,5 - Диметил пири ди н 2,6-Диметилпиридин 1 -Фенилметанаминия нитрат (бензиламмония нитрат) Гепт-1-ин 1,2-Диметилциклопентен 1,3-Диметилциклопентен 1,4-Диметилциклопентен 1,5-Диметилциклопентен 3,3 - Дим ети л циклопе нте н paif-(3R,^R)-3,4-Диметилциклопентен /?аг/-(37?,45)-3,4-Диметил-циклопентен paif-(3R,5R)-3,5-Диметил-циклопентен (3 R, 5S)-3,5-Диметилциклопентен Г ептаннитрил ж. г. г. ТВ. г. г. г. г. г. г. г. г. г. г. г. 151,2 126,9 126 125,6 126 123,1 124,8 125,6 125,6 125,6 164,7 408 351,7 361,7 365,5 361,7 347,9 361,7 363,4 354,2 354,2 441,9 -161,15 65,607 56,229 239,48 103,08 226,8 ж. 3744,3 4575,7 -15,3 8,972 204,25 50,49
с7н14 Гепт-1-ен г. 155,3 423,9 -62,341 96,09 4696,3 -119,035 12,67 93,04 31,36
с7н14 1,1 -Диметилциклопентан г. 133,4 359,5 -138,37 39,06 4620,3 -69,795 1,079 87,85 30,69
С7н14 рац-( 1 R,2R)-1,2-Диметил-циклопентан г. 134,6 367,1 -136,78 38,39 4621,9 -117,58 6,448 91,78 31,07
с7н14 (1 R,2S)-1,2-Диметилциклопентан г. 134,2 366 -129,62 45,76 4629 -53,856 1,658 99,53 31,74
с7н14 рац-(\ R,3R)-\ ,3-Диметилциклопентан г. 134,6 367,1 -135,95 39,23 4622,7 -133,702 7,403 91,72 31,19
с7н14 (1 R,3S)~ 1,3 -Диметилциклопентан г. 134,6 367,1 -133,68 41,49 4624,9 -133,975 7,277 90,77 31,02
с7н14 Метилциклогексан г. 135,1 343,6 -154,87 27,3 4603,8 -126,593 6,755 100,93 31,74
с7н14 С7Н]4О2 C7Hi4O2 С7Н14О2 C7Hi4O2 Этилциклопе нтан Этил-2,2-диметилпропаноат Этил-2-метилбутаноат Этил-3 -метилбутаноат Этилпентаноат г. ж. ж. ж. 131,8 378,6 -127,15 577,78 565,22 569,4 552,66 44,63 ж. 4631,5 4260,1 -138,446 6,874 103,45 32,36
358 Новый справочник химика и технолога
Продолжение табл. 3.6.3
Формула Название Состояние Дж/(моль • К) 5°, Дж/(моль • К) Aftf0, кДж/моль Д^0. кДж/моль Сгорание Плавление Испарение
Состояние ДСЯ°. кДж/моль Г„л, °с Afus/Л кДж/моль Д,сп, °C Avap^°, кДж/моль
с7н16 Гептан г. 166,1 428,1 -187,95 8,122 4856,7 -90,610 14,04 98,43 31,74
с7н16 2,2 - Дим ети лпе нтан г. 390,8 -206,37 0,084 4838,3 -123,811 5,828 79,20 29,35
с7н16 2,3-Диметилпентан г. 414,3 -199,38 0,67 4845,3 89,78 30,48
с7н16 2,4-Диметилпентан г. 396,9 -202,22 3,014 4842,5 -119,242 6,845 80,50 29,64
с7н16 3,3-Диметилпентан г. 400 -201,68 2,638 4843 -134,46 7,072 86,06 29,77
с7н)б 2-Метил гексан г. 420,1 -195,1 3,224 4849,6 -118,276 9,19 90,05 30,69
с7н16 З-Метилгексан г. 424,4 -192,43 4,605 4852,2 91,85 30,81
С7н16 2,2,3-Триметилбутан г. 164,7 383,5 -204,99 4,271 4839,7 -24,919 2,263 80,88 28,97
с7н16 З-Этилпентан г. 411,6 -189,83 10,76 4854,8 -118,604 9,554 93,47 31,02
С7Н16О Гептан-1-ол г. 187,8 443,8 -352,98 -131,1 ж. 4626 176,1 51,08
C7H16S Гептан-1-тиол г. 187,8 493,5
С8Н4О3 2-Бензофуран-1,3-дион ТВ. 460,67
(фталевый ангидрид)
С8Н6О4 Фталевая кислота ТВ. 782,43 ТВ. 3228
с8н8 Стирол г. 118 345,3 147,46 213,9 4441,8 30,628 10,96 145,1 37,3
с8н8 Циклоокта-1,3,5,7-тетраен г. 122,1 325,6 297,77 370,1 4,68 11,28 140,6 36,72
с8н10 о-Ксилол г. 133,3 353 19,008 122,2 4598,9 -25,182 13,61 144,41 36,84
с8н10 л/-Ксилол г. 127,7 357,9 17,25 118,9 4597,6 -47,872 11,58 139,10 36,59
C8Hio п-Ксилол г. 126,9 352,7 17,961 121,2 4598,3 13,263 17,12 138,25 36,31
с8н10 Этилбензол г. 128,5 360,7 29,81 130,7 4618,6 -94,975 9,169 136,85 35,92
с8н14 Окт-1-ин г. 174,1 446,9 82,48 235,3 5234,9
c8h15n Октаннитрил г. 187,5 480,9
С8н16 1,1 -Диметилциклогексан г. 154,5 365,3 -181,12 35,25 5257,3 -33,495 2,024 119,54 33,03
с8н16 рац-{ 1 /?,27?)-1,2-Диметил- г. 159,1 371,2 -180,12 34,5 5258,3 -88,194 10,43 123,42 33,41
циклогексан
с8н16 (1 R,2S)~1,2-Диметил- г. 156,6 374,8 -172,29 41,24 5266,2 -50,023 1,646 129,73 34,25
циклогексан
С8Н16 (1 R,3S)~1,3-Диметил- г. 157,4 370,7 -184,89 29,85 5253,6 -75,573 10,83 120,09 33,24
циклогексан
С8Н16 рац-( 1 R,3R)-1,3-Диметил- г. 157,4 376,5 -176,68 36,34 5261,8 -90,108 9,872 124,45 33,95
циклогексан
С8Н16 транс-1,4-Диметил- г. 157,8 365 -184,72 31,74 5253,7 -36,962 12,34 119,35 33,08
циклогексан
С8Н16 цис-\ ,4-Диметил- г. 157,42 370,7 -176,77 37,97 5261,7 -87,436 9,313 124,32 33,79
циклогексан
с8н16 Окт-1-ен г. 178,19 462,85 -82,982 104,5 5355,3 121,28 34,29
с8н16 Пропилциклопентан г. 154,74 417,55 -148,17 52,59 5290,3 130,45
Физические свойства важнейших веществ 359
Продолжение табл. 3.6.3
Формула Название Состояние Дж/(моль • К) 5°, Дж/(моль • К) Af/7°, кДж/моль д^°, кДж/моль Сгорание Плавление Испарение
Состояние АСЯ°, кДж/моль °C АлХ, кДж/моль Т’исп, °C AvapH°, кДж/моль
с8н16 Этилциклогексан г. 158,93 382,84 -171,87 39,27 5266,6 -111,323 8,339 131,78 34,75
с8н)8 2,2-Диметилгексан г. 431,49 -224,87 10,72 5499,6 -121,18 6,783 106,84 32,41
с8н18 2,3 -Диметил гексан г. 444,26 -214,07 17,71 5485,3 115,61 33,58
с8н)8 2,4-Диметилгексан г. 445,94 -219,56 11,72 5504,9 109,43 32,74
с8н18 2,5 - Д иметилгексан г. 439,32 -222,78 10,47 5501,7 -91,200 12,85 109,10 32,87
с8н18 3,3-Диметилгексан г. 438,36 -220,27 13,27 5504,2 -126,10 7,118 111,97 32,78
с8н18 3,4-Диметилгексан г. 448,62 -213,15 17,33 5511,3 117,72 33,75
с8н18 2-Метилгептан г. 455,57 -215,62 12,81 5508,8 -109,040 10,26 117,65 33,7
С8Н18 З-Метилгептан г. 461,89 -212,77 13,77 5511,7 -120,50 11,39 118,92 34,08
с8н18 4-Метилгептан г. 453,64 -212,23 16,75 5512,2 -120,955 10,84 117,71 34,04
с8н18 2-Метил-З-этилпентан г. 441,41 -211,35 21,27 5513,1 -114,960 11,35 115,65 33,37
С8Н]8 З-Метил-З-этилпентан г. 433,25 -215,12 19,93 5509,3 -90,870 10,84 118,26 33,16
С8Н18 Октан г. 188,99 467,04 -208,59 16,54 5515,9 -56,795 20,75 125,66 34,62
с8н18 2,2,3,3-Тетраметилбутан г. 192,72 389,62 -225,79 22,06 5498,4 100,89 7,545 106,3 31,44
С8Н]8 2,2,3-Триметилпентан г. 425,46 -220,27 17,12 5504,2 109,84 32,28
с8н18 2,2,4-Триметилпентан г. 423,49 -224,29 13,69
ж. 239,48 328,25 -259,46 6,908 5500,2 -107,360 9,219 99,24 31,07
с8н18 2,3,3-Триметилпентан г. 431,83 -216,58 18,92 5507,9 -100,70 1,549 114,76 32,57
с8н18 2,3,4-Триметилпентан г. 423,49 -217,59 18,92
ж. 247,86 329,54 -255,31 10,63 5506,9 -109,210 9,274 113,47 32,74
С8Н18 З-Этилгексан г. 458,5 -211,01 16,54 5513,5 118,53 34,33
C8H]8S Октан-1-тиол г. 210,76 532,64
С9Н10 1 -Винил-2-метилбензол г. 145,28 383,93 118,49 214,1 5092,6 169,80 40,4
С9Н10 1-Винил-3-метилбензол г. 145,28 389,79 115,56 209,4 5089,7 171,6 40,19
С9Н10 1 -Винил-4-метилбензол г. 145,28 383,93 114,72 210,3 5088,8 172,78 40,19
С9Н10 Изопропенилбензол г. 145,28 383,93 113,04 208,7 5087,2
С9НЮ (Е)-Проп-1 -ен-1 -илбензол г. 146,12 377,19 117,23 213,9 5091,4
С9Н10 (2)-Проп-1 -ен-1 -илбензол г. 145,28 383,93 121,42 217 5091,4
С9Н10О 1 -Фенилацетон ж. -163,12
С9н12 Изопропилбензол (кумол) г. 151,81 388,83 3,94 137,1 5264,1 -96,035 7,118 152,39 37,93
С9н12 Мезитилен г. 150,35 385,81 -16,08 118 5244,1 -44,720 9,63 164,72 39,15
С9н12 1 -Метил-2-этилбензол г. 158,01 399,5 1,21 133,7 5261,4 -80,833 10,63 165,15 39,15
С9н12 1 -Метил-3-этилбензол г. 152,32 404,44 -1,93 126,5 5258,3 -95,55 7,62 161,31 38,77
С9н12 1 -Метил-4-этилбензол г. 151,65 399,17 -3,27 126,8 5256,9 -62,350 12,73 161,99 38,6
С9н12 Пропил бензол г. 152,44 400,93 7,83 137,3 5268 -99,500 8,541 159,22 38,48
С9н12 1,2,3-Триметилбензол (гемеллитол) г. 154,28 391,47 -9,59 122,8 5250,6 -25,375 8,374 176,08 40,36
360 Новый справочник химика и технолога
Продолжение табл. 3.6.3
Формула Название Состояние Дж/(моль • К) 5°, Дж/(моль • К) дХ, кДж/моль Д(6°. кДж/моль Сгорание Плавление Испарение
Состояние Ас/Г, кДж/моль Тил, °C ДгЖ кДж/моль гисп, °с AvaX’ кДж/моль
с9н12 1,2,4-Триметилбснзол (псевдокумол) г. 155,33 396,62 -13,94 116,9 5246,2 -43,80 12,35 169,35 39,57
С9н16 Нон-1-ин г. 196,95 485,92 61,84 243,7 5894,1
c9h17n Нонаннитрил г. 210,39 519,83
С9н18 Бутилциклопентан г. 177,6 456,53 -168,39 61,42 5949,9
c9Hi8 Нон-1-ен г. 201,09 501,83 -103,58 112,9 6014,7 146,87 37,6
с9н18 Пропилциклогексан г. 184,34 419,81 -193,43 47,35 5924,8 156,72 37,76
с9н20 Нонан г. 211,85 506,02 -229,19 24,95 6175,1 -53,519 15,48 150,80 37,89
c9H20s Нонан-1-тиол г. 233,79 571,75
С1он8 Нафталин г. 134,31 336,74 152,11 224,5
ТВ. 165,8 167,51 78,503 201,4 ТВ. 5160,2 80,284 19,3 218,0 43,54
С10Н14 Бутилбензол г. 175,22 439,78 -13,82 144,8 5926,2 -87,970 10,99 183,27 40,19
C]oHi8 транс-Декагидронафталин (транс-декалин) г. 167,64 374,8 182,42 73,48 ж. 6278,1 187,3 38,94
С1он18 цис-Декагидронафталин (г/мс-декалин) г. 166,8 377,98 169,06 85,87 ж. 4406,6 195,7 39,77
С10Н18 Дец-1-ин г. 219,85 524,86 41,24 252 6553,3
C,oH19N Деканнитрил г. 233,29 558,81
СюН2о Бутилциклогексан г. 207,25 458,79 -213,32 56,48 6584,7 180,95 39,36
С1оН2о Дец-1-ен г. 223,95 540,81 -124,22 121,3 6673,8 170,57 40,19
С1ОН2О Пентилциклопентан г. 200,51 495,51 -189,03 69,84 6609
С1оН22 Декан г. 234,75 545 -249,83 33,37 6834,3 29,661 28,73 174,12 39,77
c10H22s Декан-1 -тиол г. 256,78 610,9
СцН10 2-Метилнафталин ТВ. 196,11 221,82 33,45 181,3 34,58 11,93
С । ]Н 16 Пентилбензол г. 198,12 479,26 -34,46 153 6585,3 232 48,78
СцН2о Ундец-1-ин г. 242,75 563,84 20,6 260,5 7212,5
CnH21N Ундеканнитрил г. 256,15 597,79
СПН22 Г ексилциклопентан г. 223,37 534,49 -209,63 78,25 7268,2
СцН22 Пентилциклогексан г. 230,11 497,77 -233,96 64,9 7243,9
СцН22 У ндец-1 -ен г. 246,85 579,79 -144,86 129,7 7333
СцН24 Ундекан г. 257,61 583,97 -270,47 41,78 7493,5 -25,594 22,19 195,88 41,53
C11H24S Ундекан-1-тиол г. 279,8 650
с12н10 Бифенил ТВ. 197,2 205,99 102,7 256,5 ТВ. 6253,4 70,5 18,59 255,3 48,02
С12Н18 Г ексилбензол г. 221,02 518,24 -55,06 161,4 7244,5
С]2Н22 Додец-1-ин г. 265,61 602,82 -0,04 268,9 7871,6
С12Н220ц Сахароза (тростниковый сахар) ТВ. 431,24 360,06 -2222,4 -1531 ТВ. 5650,5
Физические свойства важнейших веществ
Продолжение табл. 3.6.3
Формула Название Состояние с% р Дж/(моль • К) 5°. Дж/(моль • К) дХ, кДж/моль дХ кДж/моль Сгорание Плавление Испарение
Состояние ДСЯ°, кДж/моль тпл, °C Д(Х< кДж/моль Тис,,, °C А ^vap77 9 кДж/моль
cI2h23n Додекан нитрил г. 277,38 636,77
С12Н24 Г ексилциклогексан г. 253,01 536,75 -254,56 73,31 7903,1
С12Н24 Г ептилциклопентан г. 246,27 573,42 -230,27 86,67 7927,4
С]2Н24 Додец-1-ен г. 269,76 618,73 -165,46 138,1 7992,2
С12Н26 Додекан г. 280,52 622,91 -291,07 50,16 8152,7 -9,587 36,86 216,278 43,71
c12h26s Додекан-1-тиол г. 302,79 689,11
С13Н10О Бензофенон ТВ. 32,91 ТВ. 6516,8 36 78,29
Ci3Hi2 Метилендибензол ж. 233,2 239,48 88,97 277,1 ТВ. 6929,2 25,24 1,859
(дифенилметан)
С13Н12О Дифен илметанол ТВ. -105,34 ТВ. 6763,4
С1зН20 Гептилбензол г. 243,88 557,22 -75,7 169,8 7903,7
С13н24 Тридец-1-ин г. 288,51 641,79 -20,64 277,3 8530,8
Ci3H25N Тридеканнитрил г. 301,91 675,75
С1зН2б Г ептил циклогексан г. 284,24 575,73 -275,2 81,73 8562,3 -40,4 22,24
СвН2б Октилциклопентан г. 269,17 612,4 -250,87 95,08 8586,6
С13Н26 Тридец-1-ен г. 292,62 657,7 -186,1 146,5 8651,4
С1зН28 Тридекан г. 303,42 661,89 -311,71 58,57 8811,8 -5,392 28,52 235,47 45,64
c13h28s Тридекан-1 -тиол г. 325,77 728,25
С14Н10 Антрацен ТВ. 208,08 207,67 106,89 263,6 ТВ. 7119,2 217 28,85
CuHjo Фенантрен ТВ. 234,46 211,85 111,58 267 ТВ. 7086,2
С14н12 Этен-1,2-диилдибензол г. 214,36 251,21 135,95 124 30,14
(стильбен)
С14Н14 Этан-1,2-диилдибензол ТВ. 251,21 270,47 53,59 52,2
С14Н22 Октилбензол г. 266,78 596,2 -96,3 178,2 8562,9
Ci4H26 Тетрадец-1-ин г. 311,37 680,77 -41,28 285,7 9190
c14h27n Тетрадеканнитрил г. 324,81 714,73
С14Н28 Нонилциклопентан г. 292,03 651,38 -271,51 103,5 9245,8
С14Н28 Октил циклогексан г. 298,77 614,71 -295,8 90,14 9221,5
С14н28 Тетрадец-1-ен г. 315,52 696,68 -206,66 155 9310,6
С14Н30 Тетрадекан г. 326,28 700,87 -332,35 66,99 9471 5,863 45,1 253,59 47,73
CI4H30S Тетрадекан-1 -тиол г. 348,8 767,36
С15Н24 Нонилбензол г. 289,64 635,18 -116,94 186,6 9222,1
CisH28 Пентадец-1-ин г. 334,27 719,75 -61,88 294,1 9849,2
c15h29n П ентаде кан нитр ил г. 347,71 753,71
С15Н30 Децилциклопентан г. 314,93 690,36 -292,15 111,9 9905
С15Н30 Нонилциклогесан г. 321,67 653,64 -316,44 98,56 9880,7
С15Н30 Пентадец-1-ен г. 338,38 735,66 -227,39 163,4 9969,7
362 Новый справочник химика и технолога
Продолжение табл. 3.6.3
Формула Название Состояние Дж/(моль • К) 5°, Дж/(моль • К) д^°, кДж/моль AfG°, кДж/моль Сгорание Плавление Испарение
Состояние дся, кДж/моль 7™ °C кДж/моль 7исп, °C А ^vap-** , кДж/моль
С15н32 Пентадекан г. 349,18 739,85 -352,99 75,4 10130,2 9,926 34,61 270,74 49,4
C15H32S Пентадекан-1 -тиол г. 371,79 806,46
С1бНю Пирен ТВ. 227,76 215,2 112,62
с16н12о2 1,4-Дифенилбут-2-ен-1,4- ТВ. -115,35
ДИОН
Ci6Hl4O2 1,4-Д ифенилбутан-1,4-дион ТВ. -256,4
с16н26 Децилбензол г. 312,54 674,16 -137,58 195 9881,3
С1бНзо Гексадец-1-ин г. 357,18 758,73 -82,52 302,6 10 508,8
C16H3IN Пальмитонитрил г. 370,57 792,69
С16Н32 Гексадец-1-ен г. 361,28 774,64 -247,98 171,8 10 628,9 4,120 28,29
С16Нз2 Децилциклогексан г. 344,53 692,62 -337,08 106,9 11 377,2
С16Н32 У ндецилциклопентан г. 337,79 729,34 -312,75 120,3 10 564,1
С1бН34 Гексадекан г. 372,04 778,83 -373,59 83,82 10 789,4 18,165 53,38 287,05 51,5
С16Нз4О Гексадекан-1-ол (цетиловый спирт) ТВ. 684,75 ТВ. 10 485,8
C16H34S Г ексадекан-1 -тиол г. 394,82 845,61
с17н28 Ундецилбензол г. 335,45 713,1 -158,18 203,4 10 540,4
С17Нз2 Гептадецин-1 г. 380,04 797,71 -103,16 311 11 167,5
Ci7H33N Г ептадеканнитрил (маргаринонитрил) г. 393,48 831,67
С17Нз4 Г ептадец-1 -ен г. 384,18 813,62 -268,58 180,2 11 288,2
С)7Нз4 Додецилциклопентан г. 360,69 768,32 -333,39 128,7 11 223,3
С17Нз4 У ндецилциклогексан г. 367,43 731,6 -357,68 115,3 11199
С17Нзб Гептадекан г. 394,94 817,81 -394,19 92,24 11 448,6 21,980 40,51 302,56 53,17
c17H36s Г ептадекан-1 -тиол г. 417,8 884,71
С18Нзо Додецилбензол г. 358,31 752,07 -178,82 211,9 И 199,6
С18Нз4 Октадец-1-ин г. 402,94 836,69 -123,76 319,4 11 826,7
c18h35n Стеаронитрил г. 416,34 870,65
С18Нзб Додецилциклогексан г. 390,29 770,58 -378,32 123,8 11 858,2 12,6 45,87
С]8Нзб Октадец-1-ен г. 407,04 852,6 -289,22 188,6 11 947,3
С18Н36 Т ридецил циклопентан г. 383,59 807,3 -353,99 137,1 11 882,5
Ci8H38 Октадекан -414,83 100,7 12 107,7 28,180 62,03 317,38 54,85
c18H38s Октадекан-1 -тиол г. 440,79 923,82
С19н16 Метантриилтрибензол (трифенилметан) ТВ. 295,17 312,34 162,07 412,8 ТВ. 10 001 92,1 21,56
С19Н16О Трифенилметанол ТВ. -3,35
С19Нз2 Тридецилбензол г. 381,21 791,05 -199,42 220,3 1 1 858,8
Физические свойства важнейших веществ
Окончание табл. 3.6.3
Формула Название Состояние р ’ Дж/(моль • К) 5°, Дж/(моль • К) ДХ кДж/моль АХ, кДж/моль Сгорание Плавление Испарение
Состояние АХ, кДж/моль Тил, °C А&Х кДж/моль т„сп, °C AVapH°, кДж/моль
с19н36 Нонадец-1-ин г. 425,8 875,67 -144,4 327,8 12 485,9
c19h37n Нонадеканнитрил г. 439,24 909,62
С19Н38 Нонадец-1-ен г. 429,94 891,58 -309,82 197 12 606,5
С19Н38 Т етрадецилциклопентан г. 406,45 846,28 -374,63 145,5 12 541,7
С19Н38 Тридецилциклогексан г. 413,2 809,56 -398,92 132,2 12 517,4
С19Н40 Нонадекан г. 440,7 895,77 —435,43 109,1 12 766,9 32,1 50,24 331,55 56,52
C19H4OS Нонадекан-1 -тиол г. 463,81 933,61
С2оН34 Т етрадецилбензол г. 404,07 830,03 -220,06 228,7 12518
С2оН34 Эйкоз-1-ин г. 448,7 914,65 -165 339,1 13 145,1
c20h39n Эйкозаннитрил (арахинонитрил) г. 462,14 948,6
С2оН4о Пентадецилциклопентан г. 429,36 885,26 -395,28 153,9 13 200,9
С2оН4о Т етрадецилциклогексан г. 436,1 848,54 419,56 140,6 13 176,6
С2оН4о Эйкоз-1-ен г. 452,8 930,56 -330,46 205,4 13 265,7
с20н42 Эйкозан г. 463,6 934,74 —456,07 120 13 426,1 36,8 70,34 345,12 57,78
C2oH42S Эйкозан-1-тиол г. 486,8 1002,1
С21Н36 Пентадецилбензол г. 426,97 869,01 -240,7 237,1 13 177,2
C2iH41N Г енэйкозаннитрил г. 485 991,77
с21н42 Г ексадецилциклопентан г. 452,22 924,24 -415,87 162,4 13 860,1
C2iH42 Пентадецилциклогексан г. 458,96 887,52 -440,2 149,4 13 835,7
с22н38 Г ексадецилбензол г. 449,87 907,99 -261,3 245,5 13 836,4
С22н44 Г ексадецилциклогексан г. 481,86 926,5 460.8 157,4 14 453,1
С25Н20 Метантетраилтетрабензол (тетрафенилметан) ТВ. 368,02 383,51 279,8 597,5 ТВ. 12 989,1 285 21,98
364 Новый справочник химика и технолога
Физические свойства важнейших веществ
365
3.6.2. Расчет и экспериментальное определение термохимических характеристик органических соединений (к. х. н., доц. Е.В. Сагадеев, д. х. н., проф. В.П. Барабанов)
Термохимические характеристики, и в первую очередь стандартные энтальпии парообразования, а также сгорания и образования (как в конденсированном состоянии, так и в газовой фазе), являются важнейшими константами органических соединений. В основе экспериментального определения энтальпий сгорания органических соединений лежит калориметрия сгорания в стационарной или вращающейся калориметрической бомбе, а для определения энтальпий образования в ряде случаев используют различные методы реакционной калориметрии. Экспериментальное определение энтальпии парообразования органических соединений основано главным образом на уравнении Клапейрона — Клаузиуса (по давлению пара). В элементоорганических соединениях основным способом получения экспериментальных данных по энтальпии парообразования является эмпирическое уравнение Б.Н. Соломонова.
Непосредственное получение термохимических данных в области органических, и особенно элементоорганических, соединений в силу целого ряда объективных причин связано с большими экспериментальными трудностями, а в исключительных случаях вообще невозможно. Поэтому надежность определения некоторых термохимических характеристик соединений может вызывать определенные сомнения, а для модельных, гипотетических, или перспективных органических производных термохимические данные могут отсутствовать. В связи с этим все более возрастает роль теоретических способов расчета в области термохимии органических соединений, которые в большинстве случаев являются эмпирическими. Многие из существующих методов предназначены для расчета термохимических характеристик только отдельных классов органических соединений, и, кроме того, получаемые расчетные данные далеко не всегда удовлетворительно согласуются с экспериментальными результатами.
В настоящем Справочнике для расчета термохимических характеристик органических соединений ис
пользован аддитивный метод групповых вкладов по атомам с учетом их ближайшего атомарного окружения. Метод групповых вкладов является более универсальным и в большей степени позволяет учитывать химическую специфику соединений. В основе расчетов лежит многопараметровое аддитивное уравнение:
Y = т}Х\ + W2A2 + ... + тХ,
где т, — число фрагментов /-го вида в молекуле; X, — инкремент, описывающий групповой вклад /-го фрагмента.
К настоящему времени с учетом имеющихся литературных данных рассчитана система групповых вкладов (инкрементов) в энтальпии парообразования, сгорания и образования, охватывающая большинство классов органических соединений алифатического и ароматического рядов, а также ряд основных классов элементоорганических соединений. Для обозначения инкрементов используется модифицированная символика Бенсона — Басса. В данном Справочнике приведены рассчитанные на основе аддитивной схемы термохимические характеристики семисот органических и элементоорганических соединений (табл. 3.6.4, 3.6.5), причем отклонение расчетных значений от экспериментальных в среднем не превышает 1-5 %. Значительная часть полученных расчетных результатов неоднократно подтверждена экспериментально. Для большого числа важных в практическом плане органических веществ термохимические характеристики приведены впервые. Кроме того, получены используемые в теплоэнергетике расчетные данные по высшим и низшим теплотворным способностям (теплотам сгорания) органических соединений, и в первую очередь углеводородов различного строения.
В табл. 3.6.4 приняты следующие обозначения: — стандартная энтальпия парообразования, кДж/моль; Д//“бр — стандартная энтальпия образования, кДж/моль; Д//“ор — стандартная энтальпия сгорания. кДж/моль. Все термохимические характеристики относятся к стандартным условиям — температуре 298,15 К (25 °C) и давлению 101,325 кПа (760 мм. рт. ст).
Таблица 3.6.4
Экспериментальные и расчетные термохимические характеристики
Соединение, формула Д//"ар, кДж/.моль А/7'бР- кДж/моль ДЯс°1ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Алифатические углеводороды (алканы)
Метан, СН4 -74,9 -890,4
Этан, С21-Ц -84,7 -844 -1559,8 -1559.8
Пропан, С3Н8 -104,7 -105.1 -2220,0 -2212,1
Бутан, С4Н]о -126,1 -125,8 -2876,7 -2864,4
Изобутан, С4Н10 -134,5 -134,5 -2868,7 -2858,1
Пентан, C5Hi2 26,7 27,0 -146,4 -146.5 -173,1 -173,5 -3511,9 -3516,7 -3536,1 -3543,7
Изопентан, С5Н]2 25.2 25,0 -154,5 -155,2 -179,3 -180,2 -3507,4 -3510,4 -3531,2 -3535,4
Гексан, С6Н14 31.5 31,8 -167,2 -167,2 -198.8 -199.0 -4163,1 -4168,9 -4194,8 -4200.7
Гептан, С7Н16 36,6 36,6 -187,8 -187,9 -224,4 -224,5 -4816,9 -4821,2 -4853,5 -4857,8
Октан, С8Н]8 41,5 41,3 -208,4 -208.6 -250,0 -249,9 -5470,7 -5473.5 -5512,2 -5514,8
Нонан, С9Н20 46,4 46,1 -229,3 -274,7 -275,4 -6124.0 -6125,8 -6171,0 -6171,9
Декан, С10Н22 51,4 50,9 -249,7 -250.0 -301,0 -300.9 -6777,8 -6778,1 -6829,7 -6829,0
Ундекан, СИН24 56,3 55,7 -270,3 -270.8 -327,2 -326,5 -7431.5 -7430,4 -7488,4 -7486,1
Додекан, С12Н26 61,3 60,4 -290,9 -291.5 -352,1 -351,9 -8085,3 -8082.7 -8147,2 -8143,1
Тридекан, С)3Н28 66,2 65,2 -311,5 -312,2 -377,7 -377,4 -8739,0 -8734,9 -8805,9 -8800,1
Тетрадекан, С14Н30 71,2 70,0 -332,1 -332,9 -403,3 -402,9 -9392,8 -9387,2 -9464,7 -9457.2
Пентадекан, С15Н32 74,0 74,7 -354,8 -353,6 -428,8 -428,3 -10046,5 -10 039,5 -10 123,4 -10114,2
Гексадекан, С16Н34 80,4 79,5 -374.3 456.1 -453,8 -10 700,3 -10 691,8 -10 782,2 -10 771,3
Гептадекан, С17Н36 85,6 84.3 -393,9 -395,0 -479.5 -479,3 -11 354.0 -11 344,1 -11 440,9 -11 428,4
Октадекан, С18Н38 90.8 89,0 -414,6 -415,7 -505,4 -504.7 -12007,8 -11 996,4 -12 099,6 -12 085,4
Нонадекан, С19Н40 95.8 93,8 -435.1 -436,4 -531,0 -530,2 -12661,5 -12 648,7 -12 758,4 -12 742,5
Эйкозан, С20Н42 100,8 98,6 -455,8 -457,1 -556.5 -555,7 -13 315,3 -13 300.9 -13 417,1 -13 399,5
Пятичленные циклические алифатические углеводороды
Циклопентан, С5Ню 29,3 30,3 -77,2 -78,5 -105,9 -108,8 -3291,6 -3291,6 -3319.5 -3321,9
Мезилциклопентан, С6Н12 31,8 33.1 -106,7 -107,9 -141,1 -141,0 -3937,7 -3937.7 -3969,4 -3970.8
Этилциклопентан, С7Н14 36,5 37,8 -127,1 -128,6 -165,8 -166,4 -4589.6 -4589,9 -4628.4 -4627,7
366 Новый справочник химика и технолога
Продолжение табл. 3.6.4
’ Соединение, формула Д//„аР, кДж/моль Д//О°бр, кДж/моль Д7/С°1ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Пропилциклопентан, С8Н16 41,1 42,6 -148,1 -149,3 -189,2 -191,9 -5245,6 -5242,2 -5286,7 -5284,8
Бутилциклопентан, С9Н18 45,9 47,4 -168,3 -170,0 -214,3 -217,4 -5899.9 -5894,5 -5945,9 -5941,9
Пентилциклопентан, СюН20 52,1 -188,9 -190,7 -242,8 -6546,8 -6604,6 -6598,9
Гексилциклопентан, СцН22 56,9 -209,5 -211,4 -268,3 -7199,1 -7263,4 -7256,0
Гептилциклопентан, С12Н24 61,7 -230,1 -232,1 -293,8 -7851,4 -7922,1 -7913,1
Октилциклопентан, С]3Н26 66,4 -250,7 -252,8 -319,2 -8503,7 -8580,8 -8570.1
Нонилциклопентан, С]4Н28 71,2 -271,3 -273,6 -344,8 -9155,9 -9239,6 -9227,1
Децилциклопентан, Ci5H30 76,0 -294,3 -368.2 -370,3 -9822,1 -9808,2 -9898,3 -9884,2
Ундецилциклопентан, С16Н32 80,8 -312,5 -315,0 -395,8 -10 460,5 -10 557,1 -10 541,3
Додецилциклопентан, С)7Н34 85,5 -333,2 -335,7 —421,2 -11 112.8 -11 215,8 -11 198,3
Тридецилциклопентан, С18Н36 90,3 -353,8 -356,4 —446,7 -11 765,1 -11 874,6 -11 855,4
Тетрадецилциклопентан, С19Н38 95,1 -374,4 -377,1 -472,2 -12 417,4 -12 533,3 -12 512,5
Пентадецилциклопентан, С20Н40 99.8 -397,8 -497,6 -13 069,6 -13 192,0 -13 169,4
1,1-Диметилциклопентан, С7Н14 33,8 35,9 -138,3 -140,0 -172,1 -175,9 —4583,3 -4598,1 —4617,2 -4634,0
1,2-Диметилциклопентан, С7Н14 34,6 35,8 -136,7 -137,3 -171,3 -173,1 —4584,2 -4583,7 -4618.8 -4619,5
Шестичленные циклические алифатические углеводороды
Циклогексан, С6Н12 34,0 35,1 -123,1 -120,1 -157,7 -155,2 -3919.8 -3922,4 -3953,0 -3957,5
Метилциклогексан, С7Н]4 35,4 37,8 -154,8 -149,5 -190,2 -187,3 -4564,3 -4568,4 —4600,7 -4606,2
Этилциклогексан, С8Н|6 40,6 42,6 -171,8 -170,2 -212,5 -212,8 -5222,6 -5220,7 -5263,1 -5263,3
Пропилци клогексан, С9Н; 8 45,2 47,4 -193,3 -190,9 -238,4 -238,3 -5875,8 -5873,0 -5920,9 -5920,4
Бутилциклогексан, С10Н20 50,0 52,1 -213,2 -211,6 -263,2 -263,7 -6525,3 -6580,3 -6577,4
Пентилциклогексан, С ]! Н22 54,1 56,9 -233,8 -232,3 -289,2 -7177,6 -7239,1 -7234,5
Гексилциклогексан. С12Н24 59,0 61,7 -254,4 -253,1 -314,8 -7829,9 -7897,8 -7891,6
Гептилциклогексан, С]3Н26 64,8 66,4 -275,0 -273,8 -353,0 -340,2 -8478,5 -8482,1 -8556,6 -8548,6
Октилциклогексан, С14Н28 71,2 -295,6 -294,5 -365,7 -9134,4 -9215,3 -9205,6
Нонилциклогексан, С15НЗО 76,0 -316,2 -315,2 -391,2 -9786,7 -9874,1 -9862,7
Децилцикло гексан, С16Н32 78,8 80.8 -336,9 -335,9 -418,4 -416,7 -10451,1 -10 439,0 -10 532,8 -10 519,8
Ундецилциклогексан, С17Н34 85.5 -357,4 -356,6 -442,1 -И 091,3 -11 191,5 -11 176,8
Физические свойства важнейших веществ 367
Продолжение табл. 3.6.4
Соединение, формула Д//“ар, кДж/моль А//0°бр, кДж/моль Д//';.ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Шестичленные циклические алифатические углеводороды
Додецилциклогексан, С18Н36 88.9 90,3 -378.1 -377.3 -467,6 -467,6 -11 760,6 -11 743,6 -11 850,3 -11 833,9
Тридецилциклогексан, С19Н38 95,1 -398,7 -398,0 -493,1 -12 395,9 -12 509,0 -12 491,0
Тетрадецилциклогексан, С20Н40 99,8 -419,3 -418,7 -518,5 -13 048,1 -13 167,8 -13 147,9
1,1 -Диметилциклогексан, С8Н16 38,0 40,7 -181,0 -181,6 -222,3 -5216,0 -5228,8 -5253,8 -5269,5
1,2-Диметилциклогексан, С8Н16 38,4 40,6 -180.0 -178,9 -219,5 -5216,5 -5214,4 -5254,8 -5255,0
1,2-Диэтилциклогексан, С]ОН2о 50,1 -220,3 -270,4 -6519,0 -6513,6 -6569,1
/ире/тг-Бутилциклогексан, С1ОН2о 47,0 48,2 -231,8 -280.0 -6527,1 -6575,3
1,2,3,4,5,6-Гексаэтилциклогексан, С]8Н36 80,3 -420.8 -501,1 -11 587,8 -11 712,2 -11 792,5
Шестичленные бициклические алифатические углеводороды
1,1-Бициклогексил, С12Н22 58,0 62,9 -218,4 -214,6 -276,4 -277,5 -7589,9 -7577,1 -7647,9 -7640,0
2-Метил-1,1-бициклогексил, С13Н24 65,7 -244,1 -309,8 -7824,0 -8223,1 -8288,8
2-Этил-1,1-бициклогексил, С14Н26 70,5 -264,8 -335,3 -8431,0 -8875,4 -8945,9
4-Этил-1,1-бициклогексил, С)4Н26 70,5 -264,8 -335,3 -8875,4 -8945,9
2-Пропил-1,1 -бициклогексил, С 15Н28 75.2 -285,5 -360,7 -9037,0 -9527,6 -9602,8
2-Изопропил-1,1 -бициклогексил, С]5Н28 73,2 -294,2 -367,4 -9521,4 -9594,6
2,4,6,2',4',6'-Гексаметил-1,1 -бициклогексил, С ] 8Н34 79.5 -391,1 -470,6 -11389,9 -И 453,1 -11 532,6
4-Гептил-1,1 -бициклогексил, С19Н36 94,3 -368,3 -462,6 -12 136,8 -12231,1
4-Нонил-1,1 -бициклогексил, С2|Н40 103,9 -409.7 -513.6 -13 441,4 -13 545,3
2,2-Диметил-1,1 -бициклогексил, С]4Н26 68,5 -276,2 -344,7 -8883.5 -8952,0
Дициклогексилметан, С13Н24 67,7 -235,4 -303,1 -8250,8 -8229,3 -8297,0
Циклогексил(3-метилциклогексил)метан, С!4Н26 70,5 -264,8 -3.35,3 -8326,0 -8875,4 -8945,9
Циклогексил(2-этилциклогексил)метан. С15Н28 75,2 -285,5 -360,7 -9539,3 -9527,6 -9602,8
Бис-(этилциклогексил)метан, С i7H32 82,8 -335,6 -418,4 -10 825,9 -10 908,7
Циклогексил(4-изопропилциклогексил)метан, С16Н30 78,0 -314,9 -392,9 -10 180,0 -10 173,7 -10 251,7
Бис-(2,4,6-триметилциклогексил)метан, С19Н36 84.3 -411,8 -496,1 -12 105,4 -12 189,7
1,1 -Дициклогексилэтан, С14Н26 70,5 -264,8 -335,3 -8929,1 -8875,4 -8945.9
1 -Циклогексил-1 -изопропилциклогексилэтан, С17Н32 80.8 -344,3 -425,1 -10 819,7 -10 900,5
368 Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула AH",,,, кДж/моль Д//‘’6р, кДж/моль Д//с°10р, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
1, 1-Бис-(4-метилциклогексил)этан, С)6Н30 76,0 -323,6 -399,6 -10 167,4 -10 243,4
1,1 -Бис-(диметилциклогексил)этан, С|8Н34 81,5 -382,4 -463,9 -11 459,4 -11 540,9
1, 1-Бис-(этилциклогексил)этан, С18Н34 85,5 -365,0 -450,5 -11 471,9 -11 557,4
2,2-Бис-(метилциклогексил)пропан, С17Н32 78,8 -355,7 -434,5 -10 827,8 -10906,6
1,1 * Дициклогексил-2 -метил пропан, С]6Н30 78,0 -314,9 -392,9 -10 173,7 -10251,7
1,1-Дициклогексилгептан, С]9Н36 94,3 -368,3 -462.6 -12 030,5 -12 136,8 -12231,1
1,2-Дициклогексилэтан, С14Н26 72,5 -256,1 -328,6 -8881,6 -8954,1
1 -Циклопентил-З-циклогексилпропан, СМН26 72,5 -235,1 -307,6 -8903,1 -8975,6
1,3-Дициклогексилбутан, Ci6H30 80,0 -306.2 -386,2 -10 179,9 -10259,9
Бис-(циклогексилметил)циклогексан, С20Н36 100,3 -350,6 -450.9 -12 536,3 -12 636,6
1,3,5-Трициклопентилциклогексан, С211 Ьб 104,4 -278,9 -383,3 -12 994,0 -13 098,4
1,1,3-Трициклогексилпропан, С21Н38 105,1 -371,3 -476,4 -13 188,6 -13 293,7
Конденсированн ые алициклические углеводороды
транс-Декалин, С10Н18 48.5 53,4 -182,2 -173.2 -230,7 -226,6 -6277,0 -6272,5 -6325,5 -6325,9
транс-2 -Метилдекалин, СиИ20 56,2 -202.6 -258,8 -6922,0 -6918,5 -6974,7
трсшс-9-Метилдекалин, СцН20 56,2 -205,4 -249,8 -261,6 -6937,2 -6932,9 -6989,1
1-Этилдекалин, С)2Н22 60,9 -223,3 -284.2 -7493.3 -7570,8 -7631,7
2-Этилдекалин, С12Н22 60,9 -223,3 -284,2 -7495,0 -7570.8 -7631,7
1-Пропилдекалин, С13Н24 65,7 -244,1 -309.8 -8223,1 -8288,8
1-Изопропилдекалин, С13Н24 63,7 -252,8 -316,5 -8147,0 -8216,8 -8280,5
1-Бутилдекалин, С14Н26 70,5 -264,8 -335,3 -8875,4 -8945,9
1 -Изобутилдекали н, С! 4Н26 68,5 -273,5 -342,0 -8869,1 -8937,6
1-emop-Бутилдекалин, С14Н26 68,5 -273,5 -342,0 -8869,1 -8937,6
l-mpew-Бутилдекалин, С14Н26 66.5 -284,9 -351,4 -8877,2 -8943,7
1,1-Диметилдекалин. С]2П22 59,0 -234,8 -293,8 -7578,9 -7637,9
транс-Гидриндан, С9Н16 44,8 48.6 -131,6 -131,6 -176.4 -180.2 -5634,7 -5641,7 -5679,5 -5690.3
1-Этилгидриндан, СцН20 56,2 -181,7 -237,9 -6940,0 -6996,2
I-Изопропилгидриндан, С12Н22 58,9 -211,1 -270,0 -7586,0 -7644,9
Физические свойства важнейших веществ
Os чО
Продолжение табл. 3.6.4
Соединение, формула АН“ар, кДж/моль Д//0°6р, кДж/моль А77"ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт | Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Конденсированные алициклические углеводороды
1,2-Диизопропилгидриндан, С15Н28 69,2 -290,7 -359,9 -9530,3 -9599,5
1 -Циклогексил-3-метил-«?/>анс-гидриндан, Ci6H28 79,2 -255,6 -334,8 -9942,4 -10 021,6
1 -Циклогексил-1,3,3-триметилгидриндан, С18Н32 84,9 -319,8 -404,7 -11 263,2 -11 348,1
Этиленовые углеводороды (олефины, алкены)
Этилен (этен), С2Н4 52,5 52,4 -1411,1 -1411,0
Пропен, С3Нб 20,4 20,0 -2058,4 -2058,7
Бут-1-ен, С4Н8 -0,1 -0,1 -2716,8 -2711,0
Пент-1-ен, С5Н10 25,5 26,2 -20,9 -20,7 -46,9 -46.9 -3361,4 -3363,3 -3375,9 -3389.5
Гекс-1-ен, C6Hi2 30,7 31,0 -41,7 -41,4 -72,3 -72,4 -4015,6 -4034,5 -4046,6
Гепт-1-ен, С7Н14 35,6 35.7 -62,3 -62,1 -97,7 -97,8 -4658,3 -4667,8 -4693,2 -4703,5
Окт-1-ен, С8Н16 40,6 40,5 -82,9 -82,8 -121,8 -123,3 -5312,9 -5320,1 -5351,9 -5360,6
Нон-1-ен, С9Н18 45,3 -103,5 -148,8 -5972,4 -6010,7 -6017,7
Дец-1-ен, С10Н20 50,5 50,0 -124,6 -124,2 -173,8 -174,2 -6619,6 -6624,7 -6669,4 -6674,7
Ундец-1-ен, СцН22 54,8 -144,9 -199,7 -7277,0 -7328,1 -7331,8
Додец-1-ен, С12Н24 60,8 59,6 -165,4 -165,6 -226,2 -225,2 -7925,8 -7929,3 -7986,9 -7988,9
Тридец-1-ен, С13Н26 64,4 -186,4 -250,8 -8581,6 -8645,6 -8646,0
Тетрадец-1-ен, Ci4H28 69,1 -207,1 -276,2 -9233,8 -9304,3 -9302,9
Пентадец-1-ен, Ci5H3O 73,9 -227,8 -301,7 -9886,1 -9963,1 -9960,0
Гексадец-1-ен, Ci6H32 80,1 78,7 -248,4 -248,5 -327,3 -327,2 -10 539,0 -10 538,4 -10 621,8 -10617,1
Гептадец-1-ен, С[7Н34 83,4 -269,2 -352,6 -И 190,7 -11 280,6 -11 274.1
Октадец-1-ен, С18Н36 88,2 -289,9 -378,1 -11 843,0 -11 939,3 -11931,2
Нонадец-1-ен, С19Н38 93,0 -310,6 -403,6 -12 495,3 -12 598,1 -12 588,3
Эйкоз-1-ен, С20Н40 97,7 -331,3 -429,0 -13 147,6 -13 256,8 -13 245,3
З-Метилбут-1-ен, С5Н10 24,1 24,2 -29,0 -28,4 -51,6 -52,6 -3345,1 -3357,0 -3367,8 -3381,2
А цетиленовые углеводороды (алкины)
Ацетилен (этан), С2Н2 226,7 225.4 -1299,6 -1299,3
Пропин, С3114 185,4 185,8 -1937.6 -1928,2
Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула ЛН°ар, кДж/моль Д/7‘’бр. кДж/моль ДЯ'’,ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Бут-1-ин, С4Н6 165,2 166,0 -2596,8 -2580,5
Пент-1-ин, С5Н8 27,2 28,1 144,3 145,3 117,2 -3232,8 -3255,3 -3260,9
Гекс-1-ин, С6Н10 29.3 32,8 122,3 124,6 91,8 -3885,1 -3913,9 -3917,9
Гепт-1-ин, С7Н]2 41,0 37,6 103,8 103,9 62.8 66.3 -4570,6 -4537,3 -4572,7 -4574,9
Окт-1-ин, С8Н14 42,3 42,4 80,7 83,1 40,7 -5189.6 -5231.4 -5232,0
Нон-1-ин, С9Н16 47.2 62,3 62,4 15,2 -5841.9 -5890,2 -5889,1
Дец-1-ин, С10Н]8 51.9 41.9 41,7 -10,2 -6494,2 -6548,9 -6546,1
Ундец-1-ин, иН20 56,7 21,0 -35,7 -7146,5 -7207,7 -7203,2
Додец-1-ин, С12Н22 61.5 0,3 -61,2 -7798,8 -7866,4 -7860,3
Тридец-1-ин, С13Н24 66,2 -20,4 -86,6 -8451,1 -8525,1 -8517,3
Тетрадей-1-ин, С14Н26 71.0 -41.1 -112,1 -9103.3 -9183,8 -9174,3
Пентадец-1-ин, Ci5H28 75,8 -61.8 -137,6 -9755,6 -9842,6 -9831,4
Гексадец-1-ин, С16Н30 80,5 -82.6 -16.3,1 -10 407,9 -10 501,8 -10488,4
Гептадец-1-ин, С17Н32 85,3 -103,3 -188,6 -11 060.2 -И 160,1 -11 145,5
Октадец-1-ин, С18Н34 90,1 -124,0 -214,1 -11 712,5 -И 818,8 -11 802,6
Нонадеи-1 -ин, С]9Н36 94,9 -144,7 -239,6 -12 364,8 -12 477,6 -12 459.7
Эйкоз-1-ин, С20Н38 99,6 -165.4 -265,0 -13 017,1 -13 136,3 -13 116,7
Бут-2-ин, С4Н6 26.9 26,6 145,1 146,2 119.6 -2557,1 -2576.7 -2583,7
Ароматические углеводороды
Бензол, С6Н6 33.8 31,9 82,9 82,8 49.0 50,9 -3267,6 -3267,5 -3301,5 -3299,4
Толуол, С7Н8 37,8 37,2 50,0 49,9 12,0 12,7 -3910,0 -3912,9 -3947,9 -3950,1
Этилбензол, C8Ht0 42,3 42,0 29,8 29,6 -12,5 -12,4 -4564,9 -4565,6 -4607,1 -4607.6
Пропилбензол, С9Н12 46,2 46.7 7,8 8,9 -38,4 -37,8 -5218,3 -5217,9 -5264,5 -5264,6
Бутилбензол, С10Н14 51,4 51,5 -13,8 -11,8 -62,9 -63,3 -5872,1 -5870,2 -5922,2 -5921,7
Пентилбензол, СцН16 56,3 -32,6 -88,9 -6522,4 -6580,9 -6578,7
Гексилбензол, С]2Н18 61,0 -53,3 -114,3 -7174,7 -7239.7 -7235,7
Гептилбензол, С13Н2О 65.8 -74,0 -139,8 -7827,0 -7898,4 -7892,8
Октилбензол, С14Н22 70,6 -94.7 -165,3 -8479.3 -8557,2 -8549,9
Физические свойства важнейших веществ
Продолжение табл. 3.6.4
Соединение, формула ДЯ,^р, кДж/моль АЯобр, кДж/моль кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Ароматические углеводороды
Нонилбензол, С15Н24 75,4 -115,4 -190,8 -9131,6 -9215,9 -9207,0
Денилбензол, С]6Н26 79,8 80,1 -136,1 -219,1 -216,2 -9793,0 -9783,9 -9874,7 -9864,0
Ундецил бензол, С17Н28 84,9 -156,8 -241,7 -10 436,2 -10 533,4 -10521,1
Додецилбензол, С18Н30 89,7 -177,5 -267,2 -11 088,4 -И 192,1 -11 178,1
Тетрадецилбензол, С20Н34 99,2 -219,0 -318,2 -12 393,0 -12 509,6 -12 492.2
Тридецилбензол, С19Н32 94,4 -198,2 -292,6 -11 740,7 -11 850,9 -11 835,1
Пентадецилбензол, С21Н36 104,0 -239,7 -343,7 -13 045,3 -13 168,3 -13 149.3
Гексадецилбензол, С22Н38 108,7 -260,4 -369,1 -13 697,6 -13 827,1 -13 806,3
jw-Ксилол (1,3-диметилбензол), С8Ню 42,7 42,5 17,2 17,0 -25,4 -25,5 -^4551,9 -^4558,3 -^4594,5 -^4600,8
1,3,5-Триметилбензол, С9Н|2 47,5 47,8 -16,1 -15.9 -63,7 -5193,1 -5203,7 -5240,6 -5251,5
Цимол, С10Н14 50,0 -29,3 -78,4 -79,3 -5857,6 -5856,6 -5906,6
Производные нафталина
Нафталин, С]0Н8 72,8 72,6 151,7 152,0 78,5 79,4 -5165,6 -5166.8 -5238,4 -5239,4
1-Метилнафталин, СПН1О 77,9 116,9 119,0 41,1 -5814,0 -5812,2 -5890.1
2-Метилнафталин, СцНю 81,1 77,9 116,1 119,0 44,9 41,1 -5802,7 -5812.2 -5883,8 -5890,1
1-Этилнафталин, С]2Н12 82,6 98,7 16,1 -6171,4 -6464.9 -6547,5
1-Пропилнафталин, С13Н|4 87,4 78.0 -9.4 -6819,9 -7117,2 -7204,6
2-Изопропилнафталин, С13Н14 85,4 72,8 -12,6 -6819,9 -7110,5 -7195,9
1 -Бутилнафталин, С14Н16 92,2 57,3 -34,9 -7426,6 -7769,4 -7861,6
1-Изобутилнафталин, Ci4H]6 90,2 48,6 -41,6 -7763.2 -7853,4
1-Пентилнафталин, С]5Н18 96,9 36.6 -60,3 -8033,3 -8421,7 -8518,6
1-Гексилнафталин, С16Н20 101,7 15,9 -85.8 -9074,0 -9175,7
1-Гептилнафталин, С)7Н22 106.5 -4,9 -111,4 -9726,3 -9832,8
1,8-Диметилнафталин, Ci2H12 82,8 83,2 86,1 2,9 -6463,0 -6457,6 -6545,8 -6540,8
2,3-Диметилнафталин, С]2Н12 82,0 83,2 86,1 2,9 -6434,8 -6457,6 -6516.8 -6540,8
2,6-Диметилнафталин, Ci2Hl2 83,2 86,1 2,9 -6431,4 -6457,6 -6540.8
2,7-Диметилнафталин, С)2Н12 83,3 83,2 79,5 86,1 2,9 -6431,7 -6457,6 -6515,0 -6540,8
372 Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула кДж/моль А//О°6р, кДж/моль ДЯс°1ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
1,4,5,8-Тетраметилнафталин, С]4Н)6 100,0 93,8 20,3 -73,5 -7777,6 -7748,4 -7877,6 -7842,2
1 -Этил-8-метилнафталин, С)3Н]4 88,0 65,8 -22,2 -7142,1 -7110,3 -7198,3
1 -(1 -Метилпропил)-нафталин, Ci4Hi6 90,2 52,1 -38,1 -7405,7 -7762,8 -7853,0
1 -Изопропил-8-метил-нафтали н, С14Н j 6 90,7 39,8 -50,9 -7798,6 -7755,9 -7846,6
4-Изопропил-1,6-диметилнафталин, С15Н18 96,0 6,9 -89.1 -8340,4 -8401,3 -8497,3
Производные антрацена
Антрацен, С14Н10 104,5 113,2 230,8 221,1 106.8 107,9 -7063,8 -7066,1 -7168,3 -7179,3
Фенантрен, Ci4H10 113,2 206,9 221,1 109,7 107,9 -7054,5 -7066,1 -7179.3
4-Метилфенантрен, С]5Н12 118,5 195,8 188,2 69,7 -7720,1 -7711,5 -7830,0
2,3-Бензантрацен (нафтацен), C]8Hi2 142,3 153,9 290,2 136,3 -8956,9 -8965,4 -9099,2 -9119,3
1,2-Бензантрацен, С18Н12 153,9 290,2 136,3 -8969,0 -8965,4 -9119,3
1,2-Бензофенантрен (хризен), С18Н12 153,9 290,2 136,3 -8943,4 -8965,4 -9119,3
9,10-Диметил-1,2-бензофенантрен, С20Н |6 164,5 224,4 59,9 -10289,3 -10 256,2 -10420,7
3,4-Бензофенантрен, С18Н12 153,9 290,2 136,3 -8983.0 -8965,4 -9119,3
2,9-Диметил-3,4-бензофенантрен, С20Н16 164,5 224,4 59,9 -10265,0 -10 256,2 -10420,7
1,2,3,4-Дибензонафталин (трифенилен), С]8Н12 153,9 290,2 141,0 136,3 -8950,0 -8965.4 -9119,3
Алифатические спирты нормального строения (алканолы)
Метанол, СН4О 37,4 38,7 -200,8 -200,7 -239.5 -239,4 -726,6 -726.1 -764,0 -764,8
Этанол, С2Н6О 42,3 41,8 -235,3 -236,2 -277,6 -278,0 -1366,9 -1364,2 -1409,2 -1406,0
Пропан-1-ол, С3Н8О 47,9 46,6 -256,5 -256,9 -303,0 -303,5 -2021,4 -2016,5 -2069,3 -2063,1
Бутан-1-ол, С4Н10О 51,9 51,4 -276,6 -277,7 -328.4 -329,1 -2674,9 -2668,8 -2726,8 -2720,2
Пентан-1-ол, С5Н12О 56,9 56,2 -300,6 -298,4 -352,6 -354,6 -3330,0 -3321,1 -3386,9 -3377,3
Гексан-1-ол, СбН14О 62.8 60.9 -321,1 -319,1 -379,4 -380,0 -3978,1 -3973,3 -4040.9 4034,2
Гептан-1-ол, С7Н)6О 67,8 65,7 -341,6 -339,8 —403.3 -405.5 -4631,9 -4625,6 4699,7 4691,3
Октан-1-ол, С8Н18О 72.8 70,5 -362,2 -360,5 —428,0 -431,0 -5285,7 -5277,9 -5358,5 -5348,4
Нонан-1-ол, С9Н20О 77,8 75,2 -382,7 -381,2 -453,5 —456,4 -5939,5 -5930,2 -6017,3 -6005,4
Декан-1-ол, СюН22О 82,9 80,0 —403.2 -401,9 479.7 —481,9 -6593,3 -6582.5 -6676,2 -6662,5
Ундекан-1-ол, СИН24О 84,8 —422.6 -505,0 -507,4 -7253,8 -7234,8 -7319,6
Физические свойства важнейших веществ
Продолжение табл. 3.6.4
Соединение, формула ДН“ар, кДж/моль Д/7"бр, кДж/моль Д/7с°гор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Алифатические спирты нормального строения (алканолы)
Додекан-1-ол, С12Н2бО 91,8 89,5 -443,3 -528,4 -532.8 -7909,4 -7887,1 -7976,6
Тридекан-1-ол, С13Н28О 94,3 -464,1 -558,4 -8517,8 -8539,3 -8633,6
Тетрадекан-1-ол, С14Н30О 102,2 99,1 -474,9 -484,8 -583,9 -9167,1 -9191,6 -9290,7
Пентадекан-1-ол, С15Н32О 103,9 -505,5 -609,4 -9817,8 -9843,9 -9947,8
Гексадекан-1-ол, С16Н34О 109,4 108,6 -517,6 -526,2 -634.8 -10486,3 -10 496,2 -10 604,8
Гептадекан-1-ол, С17Н36О 113,4 -546,9 -660,3 -И 148,5 -11 261,9
Октадекан-1-ол, С18Н38О 118,2 -567,6 -685,8 -11 824,0 -11 800,8 -11 919,0
Нонадекан-1-ол, С19Н40О 122,9 -588,3 -711,2 -12 453,1 -12 576,0
Эйкозан-1-ол, С20Н42О 127,7 -609,0 -736,7 -13 129,4 -13 105,3 -13 233,0
Алифатические спирты (многоатомные и разветвленного строения)
Пропан-2-ол, С3Н8О 45,2 44,0 -272,8 -272,1 -317,0 -316,1 -2011,2 -2010,2 -2054,2
Бутан-2-ол, С4Н10О 49.5 48,8 -292,0 -292,8 -342,7 -341,6 -2660,6 -2662,5 -2710,1 -2711,3
Пентан-2-ол, С5Н)2О 54,2 53,6 -313,8 -313.6 -367,1 -367,2 -3315,4 -3314,7 -3368,3
Гексан-2-ол, С6Н14О 58,5 58,3 -334,3 -392,0 -392,6 -3967,0 -4025,3
Гептан-2-ол, С7Н16О 63,1 -355,0 -416,9 -418,1 -4619,3 -4682,4
Пентан-З-ол, С5Н12О 54,0 53,6 -314,7 -313,6 -368,9 -367,2 -3312,3 -3314,7 -3368.3
3-Метилбутан-2-ол, С5Н12О 53,0 51,6 -316,4 -322,3 -369,9 -373,9 -3315,1 -3308,5 -3360,1
Пропан-1,2-диол, С3Н8О2 73,1 -424,0 -497,1 -1839,3 -1814.6 -1887,7
Этиленгликоль (этан-1,2-диол), С2Н6О2 72,0 71,0 -386.6 -388,1 -459,8 -459,1 -1179.5 -1168,6 -1256.6 -1239,6
Глицерин, С3Н8О3 102,3 -577,8 -575,9 -669,4 -678,2 -1654,1 -1619,0 -1721,3
Производные фенола
Фенол, С6Н6О 62,3 -96,7 -97,1 -162,8 -159,4 -3053.6 -3053,5 -3115,8
2-Метилфенол (о-крезол), С7Н8О 67,7 -128,6 -130,0 -202,1 -197,7 -3695,7 -3698,9 -3766,6
З-Метилфенол (м-крезол), С7Н8О 61,7 67,7 -132,2 -130,0 -194,1 -197,7 -3703,9 -3698,9 -3765,6 -3766,6
З-Этилфенол, С8Н10О 68,2 72,4 -146,2 -150,3 -214,3 -222,7 -4362,9 -4351,6 -4431,1 -4424.0
4-Этилфенол, С8Н10О 72,4 -144,3 -150,3 -224,4 -222,7 -4352,8 -4351,6 -4424,0
2-Пропилфенол, С9Н12О 77,2 -171,0 -248,2 -5003,9 -5081,1
Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула АН"ар, кДж/моль А/70°бр. кДж/моль АЯ'’10р, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
2,6-Диметилфенол, С8Н10О 75,3 73,0 -161,9 -162,9 -233,1 -235,9 -4344,2 —4344,3 -4417,3
Резорцин, С6Н6О2 95,4 92,8 -274,9 -277,0 -368,0 -369,8 -2847,9 -2839,5 -2932,3
Гидрохинон, С6Н6О2 94,1 92,8 -277,0 -277,0 -371,1 -369,8 -2847,5 -2839,5 -2941,6 -2932,3
3,5-Дигидроксифенол, С6Н6О3 131.7 123,3 -452,7 -456.9 -584,5 -580,2 -2633,8 -2625,5 -2765,5 -2748.8
Алифатические и ароматические альдегиды
Этаналь, С2Н4О 26,1 26,1 -166,1 -166,0 -196,4 -192,1 -1166,6 -1169,1 -1192,4 -1195,2
Пропаналь, C3HgO 29,6 28,5 -186,0 -186,9 -215,7 -215,4 -1816,5 -1831,0 -1859,5
Бутаналь, С4Н8О 33,9 33,3 -204,6 -207,7 -240,3 -241,0 -2478,7 -2483,3 -2516,6
Пентаналь, С5Н10О 38,0 -228,4 -266.4 -3135,6 -3173,6
Гексаналь, С6Н12О 42,8 -249,1 -291,9 -3787,9 -3830,7
Гептаналь, С7Н14О 47,7 47,6 -264,0 -269,8 -311.7 -317,4 -4443,8 -4440,1 -4491,5 —4487,7
Октаналь, С8Н!6О 52,3 -291,9 -290,5 -342,8 -5100,0 -5092.4 -5144,7
Нонаналь, С9Н)8О 57,1 -311,2 -368,3 -5744,7 -5801,8
Деканаль, С10Н20О 61,9 -331,9 -393,8 -6397,0 -6458,9
2-Метилпропаналь, С4Н8О 31,5 31.3 -215,8 -215,7 -247,2 -247,0 -2469.4 -2478,6 -2509,9
2-Этилгексаналь, C8Ht6O 50,4 -298.6 -348,6 -349,0 -5086,2 -5087.7 -5138,1
Бензальдегид, С7Н6О 49,8 49,5 -37.2 -37,2 -87,0 -86,7 -3528.8 -3525,4 -3578,6 -3574,9
Алифатические кетоны
Ацетон, С3Н6О 31,3 31,0 -216,3 -216,2 -249,4 -247.2 -1787,0 -1787,8 -1821,4 -1818,8
Диэтилкетон, С5Н|0О 38,5 35,8 -257,9 -258,0 -296.5 -293,8 -3104,5 -3111,6 -3147,4
Дипропилкетон, С7Н14О 45,4 -298,3 -299,4 -344,8 -4416,2 —4461,6
Дибутил кетон, С9Н18О 53,3 54.9 -344,9 -340,8 -398,2 -395,7 -5715,8 -5720,8 -5769,1 -5775,7
Бутан-2-он, С4Н8О 34,7 33,4 -238,5 -237,1 -273,3 -270,5 -2444,2 -2449,7 -2483,1
Пентан-2-он, С5Н10О 38,4 38,2 -259,0 -257,8 -297,3 -296,0 -3099,5 -3102.0 -3155,6 -3140,2
Гексан-2-он, С6Н12О 42.2 42,9 -279,8 -278,5 -322,0 -321,4 -3754,0 -3754.3 -3796,2 -3797,2
Гексан-3-он, СбН12О 42,5 40,6 -278,2 -278,7 -320,1 -319,3 -3755,9 -3763,9 -3804,5
Октан-2-он, С8Н)6О 52,5 -319,9 -372,4 -5050.1 -5058,9 -5111,4
Октан-3-он, С8Н16О 50,1 -338.6 -320.1 -383.0 -370,2 -5052.0 -5068,5 -5118,6
Физические свойства важнейших веществ
Продолжение табл. 3.6.4
Соединение, формула А/7п°ар. кДж/моль А/7"бр, кДж/моль ДЯ”ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Карбоновые кислоты
Уксусная, С2Н4О2 51,5 53,9 -434,3 -434,2 -487,0 -488,1 -875,2 -875,3 -919,7 -929,2
Пропановая, С3Н6О2 54,4 56,4 -455,1 -510,8 -511,5 -1528,0 -1537,2 -1593,6
Бутановая, С4Н8О2 58,6 61,1 -475,9 -533,9 -537,0 -2183,5 -2189,5 -2250,6
Пентановая, С5Н10О2 69,3 65,9 -496.6 -560,2 -562,5 -2838,8 -2841,8 -2907,7
Гексановая, СбН12О2 71,1 70,7 -512,5 -517,3 -585,7 -588,0 -3492,4 -3494,1 -3563,5 -3564,8
Гептановая, С7Н14О2 72,0 75,4 -538,0 -611,5 -613,4 -4146,8 -4146,3 -4221,7
Октановая, С8Н16О2 80,3 80,2 -558,7 -636,9 -638,9 -4800,0 -4798,6 -4878.8
Нонановая, C9Hi8O2 82,4 85,0 -579,4 -664,4 -5452,3 -5450,9 -5535,9
Декановая, С10Н2о02 89,8 -600,1 -689,9 -6079,4 -6103,2 -6193,0
Ундекановая, СИН22О2 94,5 -620,8 -715,3 -6736,7 -6755,5 -6850,0
Додекановая, С12Н24О2 99,3 -641,5 -740,8 -7423,7 -7407,8 -7507,1
Тридекановая, С13Н26О2 104,1 -662.2 -766,3 -8024,1 -8060,1 -8164,2
Тетрадекановая, С14Н28О2 108,8 -683,0 -791,8 -8676,8 -8712,3 -8821,1
Пентадекановая, С15Н30О2 113,6 -703,7 -817.3 -9327,8 -9364,6 -9478,2
Гексадекановая (пальмитиновая), С16Н32О2 118,4 -724,4 -841,0 -842,8 -10028,6 -10 016,9 -10 135,3
Гептадекановая, С17Н34О2 123,1 -745,1 -868,2 -10624,4 -10 669,2 -10 792,3
Октадекановая (стеариновая), С18Н36О2 127,9 -765,8 -891,6 -893,7 -11316,0 -И 321,5 -11 449,4
Нонадекановая, С19Н38О2 132,7 -786,5 -919,2 -11 923,4 -11 973,8 -12 106,5
Эйкозановая, С2оН4о02 137,4 -807,2 -944,6 -12 574,2 -12 626,1 -12 763,5
Адипиновая, С6Н10О4 109,5 -867,3 -998,2 -976,8 -2802,4 -2819,2 -2928,7
Простые алифатические эфиры
Диметиловый (диметоксиметан), С2Н6О -184,1 -180,6 -1460,4 -1448,9
Диэтиловый (диэтоксиэтан), C4HWO 27,4 26,7 -252,2 -251,7 -271,2 -278,4 -2732,1 -2725,0 -2751,1 -2751,7
Дипропиловый (дипропоксипропан), С6Н14О 36,5 36,2 -292,9 -293,1 -328,8 -329,3 -4028,9 -4029,6 -4065,4 -4065,8
Метилэтиловый (метоксиэтан), С3Н8О -216,4 -216,2 -2107,4 -2086,9
Метилпропиловый (метоксипропан), С4Н10О 27,9 28,4 -237,7 -236,9 -266.0 -265,3 -2737,2 -2739,2 -2765,5 -2767,6
Метилбутиловый (метоксибутан), C5Hi2O 32,5 33,1 -258,1 -257,6 -290,5 -290,7 -3392.0 -3391,5 -3424,5 -3424,6
376 Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула кДж/моль Д//О°бр, кДж/моль Д//”ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Метилпентиловый (метоксипентан), C6Hi4O 36,9 37,9 -278,3 -316,2 -4043,8 -4081,7
Метилгексиловый (метоксигексан). С7Н16О 42,3 42,7 -299,0 -341,7 -4696,1 -4738,8
Метилдециловый (метоксидекан), СИН24О 62,3 61,8 -381,1 -381,8 -443,4 -443.6 -7315,2 -7305,2 -7377,5 -7367,0
Этилпропиловый (этоксипропан), С5Н12О 31,4 31,5 -272,2 -272,4 -303,6 -303,9 -3379,0 -3377,3 -3410,4 -3408,8
Сложные алифатические эфиры
Метилацетат, С3Н6О2 30,4 30,9 -410,0 -410.0 -445,9 -440,9 -1596.6 -1600,2 -1664,0 -1631,1
Этилацетат, С4Н8О2 35,1 34,0 -445,4 -445,6 -478,8 -479,6 -2238,5 -2238,3 -2277,8 -2272,3
Пропилацетат, С5Н10О2 39,1 38,7 -466,3 -505,0 -2890,6 -2929,3
Бутилацетат, С6Н)2О2 43.6 43,5 -487,0 -530,5 -3542,6 -3542,8 -3586,3
Пентилацетат, С7Н14О2 48,3 -507,7 -556,0 -4351,4 -4195,1 -4243,4
Метилпропаноат, С4Н8О2 34,3 33,3 -430,9 -464,2 -2246,4 -2262,1 -2295,4
Этилпропаноат, С5Н10О2 37,8 36.4 -466,5 -466,5 -502,5 -502,9 -2894,0 -2900,2 -2936,6
Пропилпропаноат, С6Н12О2 43.5 41,2 -487,2 -528,4 -3545,1 -3552,5 -3593,7
Бутилпропаноат, С7Н14О2 45.9 -507,9 -553,8 -4200,3 -4204,8 -4250,7
Метилбутаноат, С5Н10О2 39,3 38,1 -451,6 -489,7 -2899,5 -2914,4 -2952,5
Этилбутаноат, С6Н12О2 42,0 41.2 -484,9 -487.2 -528,4 -528,4 -3544,7 -3552,5 -3593,7
Пропилбутаноат, С7Н14О2 45,9 -507,9 -553,8 -4187,8 -4204,8 -4250,7
Бутилбутаноат, С8Н)6О2 50.7 -528,6 -579,3 -4844,2 -4857,0 -4907,7
Метилпентаноат, С6Н12О2 42,7 42,8 -471,5 -472,3 -514,2 -515,1 -3561,8 -3566,7 -3604,5 -3609,5
Этилпентаноат, С7Н14О2 46,0 45.9 -507,1 -507,9 -553,1 -553,8 -4202,4 -4204,8 -4248,4 -4250,7
Пропилпентаноат, С8Н) 6О2 50,7 -528,6 -579,3 -4851,8 -4857,0 -4907,7
Метилгексаноат, С7Н14О2 46.4 47,6 -493,7 -493,0 -540,2 -540,6 -4215,0 -4219,0 -4261,4 -4266,6
Метилгептаноат, C8H]6O2 50,2 52,4 -516,7 -513,8 -567,1 -566,2 -4867,2 -4871,3 -4917.5 -4923,7
Метилоктаноат, С9Н18О2 56.4 57,2 -534,5 -591,7 -5523,3 -5523,6 -5580,8
Метилнонаноат, С10Н20О2 62,0 61,9 -555,2 -617,1 -6176,8 -6175,8 -6237,7
Кислородсодержащие гетероциклы
Тетрагидрофуран, С4Н8О 31,8 30,0 -184,2 -183,7 -216,0 -213,7 -2502,0 -2500,0 -2533,2 -2530,0
1,3-Диоксолан, С3Н6О2 35,6 29,4 -301,8 -312.5 -337,2 -341,9 -1700,8 -1702,1 -1736,4 -1731,5
Физические свойства важнейших веществ 377
Продолжение табл. 3.6.4
Соединение, формула , кДж/моль А77"бр. кДж/моль А//“ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Кислородсодержащие гетероциклы
2-Метил-1,3-диоксолан, С4Н8О2 34,9 32,5 -350,2 -352,6 -385,1 -385,1 -2332,3 -2330,9 -2367,2 -2363,4
Тетрагидропиран, С5Н|0О 34,7 34,7 -223,8 -225,3 -254,8 -260,0 -3137,6 -3130,8 -3173,3 -3165,5
1,3-Диоксан, С4Н8О2 35,6 34.2 -349,8 -354,2 -385,3 -388,4 -2332.8 -2332,8 -2378,9 -2367,0
2-Метил-1,3-диоксан, С5Н)0О2 38,5 37,3 -399,2 -394,3 -436,5 -431,6 -2960,3 -2961,7 -2998,8 -3000.0
4-Метил-1,3-диоксан, С5Н10О2 39,3 36,4 -378,4 -390,1 -417,6 -426,5 -2979,1 -2978,8 -3018,4 -3015.2
4,5-Диметил-1,3-диоксан, С6Н12О2 39,1 -419,5 -451,7 -458,6 -3624,4 -3624,8 -3663,9
1,4-Диоксан, С4Н8О2 34,1 34,4 -318,0 -330,5 -355,1 -364,9 -2346,2 -2339.1 -2380,3 -2373,5
Первичные алифатические амины
Метиламин, CH5N -23,0 -22,1 -1071,5 -1073,2
Этиламин, C2H7N -46,0 -49.7 -1715,0 -1714,4
Пропиламин, C3H9N 31,3 31,3 -70,2 -70,4 -101.5 -101,7 -2365,3 -2366.7 -2396,6 -2398,0
Изопропиламин, C3H9N 28,7 28,7 -83,8 -86,0 -112,3 -114,7 -2354,5 -2356,8 -2383,0 -2385,5
Бутиламин, C4HhN 35,8 36,0 -91,2 -91,1 -127,7 -127.1 -3018,5 -3019.0 -3055.0
ewop-Бутиламин, C4H]]N 32.8 33,5 -106.3 -106,7 -137,5 -140,2 -3008.6 -3009.1 -3040,0 -3042,6
Пентиламин, C5H13N 40,1 40.8 -111,8 -152,6 -3671,3 -3712,1
Гексиламин, C6H|5N 45,1 45,6 -132.6 -178.2 -4292,8 -4323,6 -4369.2
Гептиламин, C7H17N 50,0 50,3 -153,3 -203.6 -4949.7 ^4975,9 -5026,2
Октиламин, C8H]9N 54,6 55,1 -173,5 -174,0 -228,1 -229,1 -5635,4 -5628,2 -5690,0 -5683,3
Нониламин, C9H21N 59,9 -194,7 -254,6 -6280,4 -6340,3
Дециламин, C10H23N 64,6 -215,4 -280,0 -6932,7 -6997,3
2-Метил-1-пропиламин, C4H]]N 33,9 34,0 -98,6 -99,8 -132,5 -133,8 -3013,5 -3012,7 -3047,4 -3046,7
3-Метил-1-бутиламин, C5H13N 38,8 -120,5 -159,3 -3639,2 -3665,0 -3703,8
Этилендиамин, C2H8N2 40,3 -17,0 -15,1 -55,4 -1867,3 -1869.1 -1909,4
Вторичные алифатические амины
Диметиламин, C2H7N -19,5 -19,9 -1749,7 -1763,2
Диэтиламин, C4HtlN 31,2 30,3 -72,0 -75,1 -105,4 -3035.5 -3045.7 -3076,0
Дипропиламин, C6H15N 38,1 39,8 -116,5 -116.6 -156,2 —156,4 -4350,1 -4350,2 -4388,2 -4390,0
Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула ДЯ°ар, кДж/моль АА0°бр, кДж/моль АА'’ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Диизопропиламин, C6H15N 34,7 34.8 -147,8 -178,4 -182,6 -4333,8 -4330,4 -4368,5 -4365,2
Дибутиламин, C8H19N 49,5 49,3 -158,0 -206,1 -207,3 -5657,4 -5654,8 -5692,5 -5704,1
Диизобутиламин, C8H19N 44,8 45,3 -180,8 -175,4 -218,6 -220,7 -5637,9 -5642,3 -5682,7 -5687,6
Ди-втор-бутиламин, C8H19N 43,9 44,3 -183,6 -189,2 -227.7 -233.5 -5635,8 -5635,0 -5679,8 -5679,3
Дипентиламин, CiOH23N 58,9 -199,4 -258,3 -6959,4 -7018,3
Диизопентиламин, C10H23N 54,9 -216,8 -271,7 -6974,3 -6946,8 -7001,7
Изобутилбутиламин, C8H19N 47,3 -168,2 -166,7 -215,9 -214,0 -5647,7 -5648,5 -5688,7 -5695.8
З-Метиламинопропиламин, C4H]2N2 45,7 -33,6 -80,2 -79,3 -3208,9 -3211,4 -3257,1
Третичные алифатические амины
Триметиламин, C3H9N -23,7 -20,6 -2430,1 -2454,3
Триэтиламин, C6H15N 34.9 32,7 -100,0 -103,5 -127,8 -136,2 -4377,1 -4378,0 -4410,7
Трипропиламин, C9H21N 46,1 47,0 -165.6 -206,9 -212,6 -6335,7 -6334,8 -6381,8
Триизопропиламин, C9H2]N 39,5 -212,4 -251,9 -6305,1 -6344,6
Трибутиламин, CI2H27N 61,3 -227.7 -281.8 -289,0 -8299,2 -8291,7 -8353,0
Триизобутиламин, C12H27N 55,3 -253,8 -331.8 -309,1 -8249,2 -8272,9 -8328,2
Трипентиламин, C15H33N 75,7 -289,9 -365,6 -10 248.5 -10 324,2
Триизопентиламин, C]5H33N 69.6 -316,0 -385,6 —10277,2 -10 229,7 -10 299,3
Тригексиламин, C18H39N 90,0 -352,0 -442,0 -12 205,4 -12 295,4
А,А'-Диметил-1,3-пропандиамин, С5Н14N2 45,0 -34,7 -34,3 -77,4 -79,3 -3891,5 -3902,4 -3947,4
Ароматические амины
Анилин, C6H7N 52,7 52,2 87,0 87,0 33,5 34,8 -3391,3 -3391,1 -3441,5 -3443,3
2-Метиланилин, C7H9N 57,7 57,5 54,8 54,1 -4,7 -3,4 -4036,1 -4036,4 -4093.8 -4093,9
2-Этиланилин, C8HhN 62,3 33,8 -28,5 -4689,1 -4751,4
2,4-Диметиланилин, C8H]]N 62,8 21,2 -41,6 4655,5 4681.8 -4744,6
2,4,5-Триметиланилин, C9H13N 68,1 -11,8 -79,9 -5318,7 -5327,2 -5395,3
А-Метиланилин, C7H9N 53,1 53,1 90,4 87,1 33,5 34,0 -4076,9 -4076,9 -4130,0
А-Этиланилин, C8H]jN 52,3 56,3 56,1 59.5 3,8 3,2 -4724,2 -4718,1 -4776,5 -4774,4
А,А-Диметиланилин, C8HhN 52,8 52,8 95,4 92,2 34,3 39,4 -4767,7 -4767,7 -4820,5 -4820,5
Физические свойства важнейших веществ 379
Продолжение, табл. 3.6.4
Соединение, формула ДЯп°ар, кДж/моль ДЯ''6р, кДж/моль Д//С°,ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Ароматические амины
А,А-Диэтиланилин, C10Hi5N 60,2 59,1 40,2 37,0 -16,3 -22,1 -6062,6 -6050,2 -6119,1 -6109,3
4-Аминоанилин, C6H8N2 72,5 91,2 18,7 -3510,8 -3514,6 -3587,1
Первичные алифатические амиды карбоновых кислот
Ацетамид, C2H5NO 71,3 -238,3 -237,9 -310,1 -309,2 -1184,6 -1182,9 -1254,2
Пропанамид, C3H7NO 73,8 -258,9 -258,9 -338,2 -332,7 -1842,8 -1844,8 -1918,6
Бутанамид, C4H9NO 78.5 -279,2 -279,6 -364,0 -358,1 -2496,2 -2497,1 -2575,6
Изобутанамид, C4H9NO 76,6 -282,4 -287.7 -368,6 -364,3 -2491,6 -2492,4 -2569,0
Пентанамид, C5HhNO 83,3 -300,3 -383,6 -3157,1 -3149,4 -3232,7
Изопентанамид, C5Hi]NO 81,3 -309,0 -390,0 -390,3 -3149,7 -3143,1 -3224,4
Гексанамид, C6Hi3NO 88,1 -321,0 -423,0 -409.1 -3796,0 -3801,7 -3889,8
Гептанамид, C7H15NO 92,8 -341,7 -434,5 -4454,0 -4546,8
Октанам ид, C8H17NO 97,6 -362.4 -460,0 -5104,5 -5106,2 -5203,8
Нонанамид, C9H19NO 102,4 -383,1 -485,5 -5758,5 -5860,9
Деканамид, C10H21NO 107,2 -403,8 -511.0 -6410,8 -6518,0
Вторичные алифатические амиды карбоновых кислот
А-Метилацетамид, C3H7NO 63.0 -248,1 -248,1 -313,3 -311.1 -1862,3 -1880,5 -1943,5
А-Этилацетамид, C4H9NO 66,2 -275,7 -341,9 -2521,7 -2587,9
А-Пропилацетамид, С5НцМО 70,9 -296,4 -367,3 -3174,0 -3244,9
А-Бутилацетамид, C6H13NO 76,1 75,7 -317,2 -392,9 -3826,3 -3902,0
А-Метилпропанамид, C4H9NO 65,4 -269.0 -334.4 -2539,7 -2542.4 -2607,8
А-Бутилпентанамид, C9HI9NO 87,7 -379.5 -467,2 -5793.6 -5792,8 -5880,5
Третичные алифатические амиды карбоновых кислот
А, А-Диметил ацетамид, C4H9NO 45,6 46,4 -229,1 -278,3 -275,5 -2582,0 -2580.4 -2626,8
А,А-Диметилпропанамид, C5HtlNO 52,9 48.8 -250,2 -250,0 -298.8 -3236,6 -3242,3 -3291,1
А,А-Диметилбутанамид, C6H13NO 55,2 53,6 -270,9 -270.7 -324,3 -3893,0 -3894,6 -3948,2
А,А-Диметилпентанамид, С7Н15NО 58,3 -291.4 -349.7 -4546.9 -4605,2
А,А-Диметилгексанамид, С8Н, 7NO 63,1 -312,1 -375,2 -5199,2 -5262,3
380 Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула Д/7"ар, кДж/моль А//Ои6р, кДж/моль А//с°10р, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Л^А-Диметилгептанамид, C9H19NO 67,9 -332,8 -400,7 -5851,5 -5919,4
А^А’-Диметилоктанамид, C10H2iNO 72,6 -353,6 —426,2 -6503,7 -6576,3
AJV’-Диметилнонанамид, СцН23МО 76,6 77,4 -374,0 -374.3 451,7 -7165,1 -7156,0 -7233,4
А^А'-Диметилдеканамид, C12H25NO 82,2 -395,0 -477,2 -7808,3 -7890,5
А^А-Диэтилацетамид, C6H13NO 48,1 52,6 -287,2 -284,3 -335,3 -336,9 -3883,6 -3862,9 -3915,5
А^А’-Диэтилпропанамид, C7Hi5NO 55,1 -305,2 -360,3 -4524,8 -4579.9
Ароматические амиды карбоновых кислот
Производные ацетанилида:
Ацетанилид, C8H9NO —4225,0 -4225,5
2-Метилацетанилид, C9HhNO -4871,3 -4870,9
2-Этилацетанилид, C10H13NO -5523,6
2,4-Диметилацетанилид, C10H13NO -5501,9 -5516,3
2-Гидроксиацетанилид, C8H9NO2 -4011,5
4-Метоксиацетанилид, C9HhNO2 4735,1
3-Аминоацетанилид, C8H10N2O 4349,0
Производные бензойной кислоты:
Бензамид, C7H7NO -3552,2 -3552,1
З-Метилбензамид, C8H9NO 4197,5
3-Этилбензамид, C9HhNO 4850,1
Салициламид, C7H7NO2 -3352,4 -3338,1
Никотинамид, С6НбМ2О -3083,8 -3060.5
Нитросоединения
Нитроэтан, C2H5NO2 41,6 40,7 -99,6 -103,1 -143,9 -143,8 -1361,6 -1362,8 -1403,1 -1403,5
1-Нитропропан, C3H7NO2 43,4 45,4 -124,3 -123,8 -167,7 -169,2 -2013,4 -2015,1 -2056,8 -2060,5
Изонитропропан, C3H7NO2 41,3 40,7 -141,8 -142,4 -183,1 -183,1 -2000,7 -2000,6 -2041,3
1-Нитробутан, C4H9NO2 48.6 50,2 -143,9 -144,5 -192,5 -194,7 -2667,8 -2667,3 -2716,3 -2717,5
ewpp-Нитробутан, C4H9NO2 43,8 45.5 -163,6 -163,1 -207,4 -208,6 -2652,7 -2652,9 -2696,6 -2698,4
1-Нитропентан, C5HuNO2 55,0 -165,2 -215,5 -220,2 -3324,2 -3319,6 -3374,6
Физические свойства важнейших веществ
Продолжение табл. 3.6.4
Соединение, формула ДЯ”ар, кДж/моль ЛТ/'обр, кДж/моль Д/7"гор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Нитросоединения
Нитробензол, C6H5NO2 46,0 46,2 58.6 58,6 12,6 12,4 -3088,1 -3088,6 -3134,8
1-Метил-3-нитробензол, C7H7NO2 51,5 51,5 26,0 25,7 -25,5 -25,8 -3734,2 -3733,9 -3785,4
1-Этил-2-нитробензол, C8H9NO2 56,3 5,3 —48,7 -51,0 -4385,7 —4386,6 -4442,9
1-Этил-4-нитробензол, C8H9NO2 56,3 5,3 -55,3 -51,0 —4379,0 -4386,6 -4442,9
1,3-Диметил-2-нитробензол, C8H9NO2 59,4 56,8 -7,3 -64,1 —4383,6 —4379.3 —4436,1
1,3,5-Триметил-2-нитробензол, C9Hi !NO2 62,1 -43,3 —40,2 -105,4 -102,3 -5008,2 -5024,7 -5086,8
1,3-Динитробензол, C6H4N2O4 60,8 60,5 33,6 34,3 -27,2 -26,2 -2910,0 -2909,6 -2970,8 -2970,1
1,4-Динитробензол, C6H4N2O4 60,5 34,3 -26,2 -2902.4 -2909,6 -2970,1
1-Метил-2,4-динитробензол, C7H6N2O4 65,8 1,4 -66,4 -64.4 -3551,2 -3554,9 -3620,7
1,3,5-Тринитробензол, C6H3N3O6 77,4 74,8 10,0 -48.4 -64.8 -2745,9 -2730,6 -2805,4
2,4,6-Тринитротолуол, C7H5N3O6 80,1 -22.9 -80.5 -103,0 -3388,6 -3375,9 -3456,0
2,4,6-Тринитроксилол, C8H7N3O6 85,4 -55,8 -109,6 -141,2 -4044,4 -4021,3 —4106,7
2,4,6-Тринитрофенол, C6H3N3O7 105,3 -169,9 -237,9 -275,2 -2560.2 -2516,6 -2621,9
2,4,6-Тринитрорезорцин, C6H3N3O8 135,7 -349,8 -467.4 —485,5 -2322,1 -2302,5 -2438,2
Производные гидразина
Гидразин, H4N2 44,8 44,8 95,4 95,4 50,5 50,6 -622,1 -622,1 -666,9
Метилгидразин, CH6N2 40.4 40.2 93,3 93,1 53,0 52.9 -1304,2 -1303,4 -1344.6 -1343,6
Этилгидразин, C2H8N2 43,3 65,5 22,2 -1944,6 -1987,9
Пропилгидразин, C3H10N2 48,1 44,8 -3,3 -2596,9 -2645,0
1,1-Диметилгидразин, C2H8N2 35,2 37,9 85,4 85,4 48,3 47,5 -1978.7 -1979,2 -2017,1
1,1-Диэтилгидразин, C4H12N2 44,1 30,1 -14,0 -3261,6 -3305.7
1,1-Дипропилгидразин, C6HI6N2 53,7 -11,3 -65,0 —4566,2 —4619,9
1,2-Диметилгидразин, C2H8N2 35,1 35,6 90,4 90,8 55,3 55,2 -1983,0 -1984,7 -2020,3
1,2-Диэтилгидразин, C4H(2N2 41,8 35,5 -6,3 -3267,2 -3309,0
1,2-Дипропилгидразин. C6H16N2 51,4 -5,9 -57,3 -4571,8 —4623,2
1,2-Дибутилгидразин, C8H20N2 60.9 -59.4 —47,3 -108,2 -5876,3 -5937,2
Триметилгидразин, C3H10N2 33,3 33,3 83,1 49,8 -2660,5 -2693,8
Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула Д/7"ар, кДж/моль Д//0°6р. кДж/моль ЛЯСПГОР’ кДж/моль
Газовая фаза Конденсированное состояние Конден сированнос состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Триэтилгидразин, C6H16N2 42,7 0,2 —42,5 —4584,2 —4626,9
Трипропилгидразин, C9H22N2 57,0 -61,9 -118,9 -6541,1 -6598.1
Тетраметилгидразин, C4H)2N2 31.0 75.3 44,3 -3336,2 -3367,2
Тетраэтил гидр азин, C8H20N2 43,5 -35,2 -78,7 -5901,2 -5944,7
Фенилгидразин, C6H8N2 61,9 61,7 209,6 210,2 142,2 148,5 -3646,6 -3646,4 -3708,1
1-Метилфенилгидразин, C7Ht0N2 63,2 63,2 210,8 210,8 147,6 147,6 —4331,3 —4331,3 —4394,5 —4394,5
1,2-Дифенилгидразин, C)2H12N2 78,7 325,9 324.9 221,3 246,2 -6658,4 -6670,6 -6749,3
Тетрафенилгидразин, C24H20N2 452,7 -12755,5 -12 754,2
Производные пиридина, пиримидина и пиразина
Пиридин, C5H5N 40,2 40,0 140,2 138,9 100,0 98,9 -2782,2 -2775,9 -2822.4 -2815,9
2-Метилпиридин, C6H7N 42,5 42,4 102,0 103,4 59,0 61,0 -3418,0 -3414,7 -3460,5 -3457,1
З-Метилпиридин, C6H7N 45,2 45,3 106,1 106,0 61,1 60,7 -3423,2 -3421,3 -3467,7 -3466,6
4-Метилпиридин, C6H7N 45,3 45,3 103,8 106,0 59,2 60,7 -3420,7 -3421,3 -3465.2 -3466,6
2,3-Диметилпиридин, C7H9N 47,7 47,7 70,5 22,8 —4060,2 —4060,1 —4107,8
2,4-Диметилпиридин, C7H9N 47,8 47.7 70,5 22,8 —4056,9 —4060,1 -4107,8
2,5-Диметилпиридин, C7H9N 47,8 47,7 70.5 22,8 -4059,4 —4060,1 —4107,8
2,6-Диметилпиридин, C7H9N 45,4 44,8 68,0 23.2 —4053,5 —4053,5 —4098,3
3,4-Диметилпиридин, C7H9N 50,5 50,6 73,1 22,5 —4059,1 -4066,7 —4117,3
3,5-Диметилпиридин, C7H9N 50,4 50,6 72,8 73,1 22,4 22,5 —4063,2 -4066.7 —4117,3
2,3,6-Триметилпиридин, С8НцК 50,6 50,1 35,0 -15,1 -4698,8 —4748,9
2,4,6-Триметилпиридин, C8Ht)N 50,1 35,0 -15,1 -4689,0 -4698,8 -4748,9
2-Этилпиридин, C7H9N 47,2 83,1 35,9 —4042,3 —4067,4 —4114.6
2-Метил-5-этилпиридин, С8Нц\ 52,5 50,2 -2,3 —4708.7 —4712,7 —4755,1 —4765,2
Пиримидин, C4H4N2 50,0 50,0 195,8 195,9 143,2 145,9 -2288,9 -2290,6 -2338,8 -2340,6
5-Метилпиримидин, C5H6N2 55,3 162.9 107,6 -2936,0 -2991,3
Пиразин, C4H4N2 48,0 196,1 195,0 139,8 147,0 -2285,5 -2284,3 -2341,8 -2332,3
2,3-Диметилпиразин, C6H8N2 52,7 52,9 126,0 124,0 73,3 71,1 -3577,8 -3561,8 -3630,5 -3614,7
2,3,5-Триметилпиразин, C7Hi0N2 54,0 55.3 88,5 33,2 —4204,1 —4200,6 —4258,1 —4255,9
2,3,5,6-Тетраметилпиразин, C8H12N2 57,7 54,8 53,1 -4,6 -4823,3 -4839,4 —4917,9 —4897,1
ОО
Физические свойства важнейших веществ
Продолжение табл. 3.6.4
Соединение, формула АЯ^р, кДж/моль ДЯ'йр. кДж/моль А//с°10р, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Производные пиррола и имидазола
Пиррол, C4H5N 45,2 45,3 108,3 108,7 63,1 63,4 -2351,7 -2352,4 -2396,9 -2397,7
1-Метилпиррол, C5H7N 40,8 42,8 103,1 103,1 62.3 60,3 -3030,3 -3030,4 -3071,1 -3073,2
2-Метилпиррол, C5H7N 47,7 73,2 25,5 -2991,1 -3038,8
2-Этилпиррол, C6H9N 52,5 52,8 0,3 -3643,8 -3696.3
2,5-Диметилпиррол, C6H9N 50,1 38.1 37.7 -12,4 -3630,5 -3629,9 -3680,0
3,4-Диметилпиррол, C6H9N 55,9 42,8 -13,1 -3643,1 -3699.0
Имидазол, C3H4N2 55.3 165,6 110,3 -1812,2 -1867.1 -1922,4
1-Метилимидазол, C4H6N2 52,8 160,1 107,3 -2545,0 -2597,8
2-Метилимидазол, C4H6N2 88,3 86,7 90,0 89,2 2,5 -2433.0 -2435,0 -2521.3 -2521,7
2-Этилимидазол, C5H8N2 89,5 91,5 68.2 68.9 -21,3 -22.6 -3089,6 -3087,6 -3179,1 -3179.1
Азотистые основания, нуклеотиды ДНК и АТФ
Пурин, C5H4N4 87,5 243,6 156,1 -2708,6 -2690,1 -2777,6
Аденин, C5H5N5 126,3 126,3 223,4 222,8 97,1 96,5 -2779,0 -2778,6 -2904,9
9-Метиладенин, C6H7N5 121.3 123.8 217.3 93,5 -3456,6 -3580,4
8,9-Диметиладенин, C7H9N5 155,3 141.0 -14.3 -4024,5 -4179,8
Гуанин, C5H5N5O 186,2 186,2 2,3 2,3 -183,9 -183,9 -2498.2 -2498.2 -2684,4
Ксантин, C5H4N4O2 166,2 -247,9 -414,1 -2159.7 -2115,9 -2282,1
Цитозин, C4H5N3O 119,3 -95,4 -221,3 -214,7 -2067.3 -2067,6 -2186.9
Тимин, C5H6N2O2 134,1 134,0 -328,7 -328,6 -462.8 -462,6 -2362,2 -2361,7 -2496,3 -2495,7
Урацил, C4H4N2O2 126,5 128,7 -295,6 -295,7 -422,1 -424,4 -1716,1 -1716,4 -1842,6 -1845,1
6-Метилурацил, C5H6N2O2 131,0 131,1 -331.2 -462,3 -2356.9 -2355,1 -2486,2
Аденозинтрифосфорная кислота (АТФ), C10H16N5O13P3 227,7 -3351,1 -3578,8
384 Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула Л//П°ар, кДж/моль Д//0°6р. кДж/моль Д/7“ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт | Расчет Опыт | Расчет Опыт | Расчет Опыт | Расчет Опыт | Расчет
Производные трехкоординированного атома фосфора
Первичные алкилфосфины:
СН3РН2 22,2 22,3
\ / РН2 52,5 45,2
Н2Р(СН2)2РН2 38,1 38,1
Н2Р(СН2)3РН2 40,3 42,8
Вторичные алкилфосфины:
(СН3)2РН 26,2 26,5
СН3(С2Н5)РН 31,0 29,6
CH3(h-C3H7)PH 35,2 34,4
CH3(h-C4H9)PH 34,3 39,2
PH 29,2 29,7
PH 37,8 36,0
Третичные алкилфосфины:
(СНз)зР 29,0 29,6 -97,1 -96,7 -126,1 -126,3
(СН3)2С2Н5Р 32,7 32,7 -107,0 -139,7
(С2Н5)3Р 39,5 38,9 -137,2 -127,7 -176,7 -166,6
(н-С3Н7)3Р 46,7 53,2 -189,8 -243,0
(н-С4Н9)3Р 53,6 67,5 -251,9 -319,4
(шо-С4Н9)зР 49,5 61,5 -278,0 -339,5
(С6Н13)зР 96,2 -376,2 -492,9 ±45,2 -472,4
(СН2=СН)3Р 37,2 37,2
(С6Н5)3Р 113,2 113,2 318,0 323,2 221,8 ± 12,6 210,0
Физические свойства важнейших веществ
оо СЛ1
Продолжение табл. 3. б. 4
Соединение, формула ДЯ,^р, кДж/моль АН'бр, кДж/моль ДЯс°10р, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт | Расчет
Производные трехкоординированного атома фосфора
(CF3)3P 24,6 24,7
(CF3)2CH3P 26,4 26,4
(CH3)2CF3P 29,1 28,0
Алкилдихлорфосфины:
С2Н5С12Р* 34,9 34,7 -261,9 -261,9 -296,8 -296,6
н-С3Н7С12Р* 39,2 39,5 -282,6 -322,1
н-С4Н9С12Р* 42,1 44,2 -303,3 -347,5
н-С5НцС12Р* 42,2 49,0 -324,1 -373,1
н-С6Н]3С12Р* 45,3 53,8 -344,8 -398,6
«-С7Н15С12Р* 47,9 58,5 -365,5 -424,0
н-С8Н17С12Р* 51,3 63,3 -386,2 -449,5
Ал кил(арил)фосфиты:
(СН3О)3Р 40,6 40,8 -704,2 ±6,3 -703,0 -741,0 ±4,6 -743,8
(С2Н5О)3Р 53,0 50,1 -809,6 -809,7 -851,4 -859,8
(н-С3Н7О)3Р 46,0 64,4 -937,2 -871,9 -983,2 -936,3
0/?о-С3Н7О)3Р 61,4 56,7 -928,0 -917,4 -980,3 ± 8,4 -974,1
(н-С4Н9О)3Р 80,5 78,7 -1015,3 -934,0 -1095,8 ±163 -1012,7
| ^РОСН3 41,6 40,8 -664,7 -705,5
^РОС2Н5 50,1 48,2 -772,1 -820,3
Производные трехкоординированного атома фосфора
^РОС2Н5 51,4 53,9 -853,1 -907,0
386 Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула ЛН°лр, кДж/моль АЯ“бр, кДж/моль ДЯс°гор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
( —О юс2н5 —О 48,6 48,6 -742,0 ± 10,6 -741,9 -790,6 -790,5
( —о ХРОС4Н9 —О 58,1 58,2 -783,3 -841,5
—О ЧРОСН3 —о 47,8 47,7 -742,2 -789,9
—О ЮС2Н5 —О 51,6 50,8 -774,0 ± 12,5 -777,8 -825,6 -828,6
/—° ' ХРОСН3 \—о 48,2 51,1 -767,9 -819,0
/ОС2Н5 52,8 54,2 -803,5 -857,7
Г /ос2н5 57,7 57,3 -610,6 -610,6 -668,3 -667,9
1) 4 || POC4H9-mpem 61,9 62,3 -687,0 -749,3
Силилфосфиты: ((CH3)3SiO)3P 92,6 92,6
^>OSi(CH3)3 61,6 60,0
Физические свойства важнейших веществ
Продолжение табл. 3.6.4
Соединение, формула ДЯ“ар, кДж/моль ДЯ"бр. кДж/моль Д//С°гор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт | Расчет
Производные трехкоординированного атома фосфора
/—° У ¥oSKCH3)3 '—О Г Г '₽OSi(CH3)3 Фосфониты: (С2Н5О)2РС6Н5 /с6н5 \—0 Алкил(арил)хлорфосфиты: (С2Н5О)2РС1 | ^РС1 64,5 70,9 71,3 78,2 48,5 40,5 41,4 44,9 66,1 70,9 72,7 76,8 46,7 40,4 42,6 44,8 -€35,0 ± 8,4 -557,8 ± 4,2 -588,8 ± 5,4 -640,0 ± 6,7 -664,8 -555,4 -591,3 -627,2 -683,5 -598,3 -630,2 -684,9 -711,5 -595,8 -633,9 -672,0
^pci
,РС1
/
Производные трехкоординированного атома фосфора
Sei 48,0 50,5 -695,0 ± 8,4 -708,2 -743,0 -758,7
388 Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула A//n°ap, кДж/моль кДж/моль Д//С°гор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
/—о
/ РС1 W у-О 44,5 45,2 -611,0 ±7,5 -597,0 -655,5 -642,2
( РС1 \—о 47,1 47,4 -647,0 ± 8,4 -632,9 -694,1 -680,3
>С/рс| 4—О 47,0 50,8 -666,0 ± 10,0 -658,6 -713,0 -709,4
Г L 'РС1 1 I /рвг Алкил(арил)дихлорфосфиты: 52,8 57,6 52,8 57,6 -431,0 ±5,0 -431,0 -483,8 -483,8
СН3С12ОР* 37,3 37,3 -418,0 ± 7,1 -429,4 -455,3 -466,7
С2Н5С12ОР* 40,4 40,4 -461,1 ±2,1 465.0 -501,5 -505,4
н-С3Н7С12ОР* 45,2 45,2 488,0 ± 7,0 -485,7 -533,2 -530,9
н-С4Н9С12ОР* 48,9 50,0 -508,0 ± 10,6 -506,4 -556,9 -556,4
С6Н5С12ОР* Амидофосфиты: 57,4 57,4 -310,0 ±8,3 -310,0 -367,4 -367,4
((CH3)2N)3P 54,4 54,4 -133,9 -133,9 -188,3 -188,3
((C2H5)2N)3P 60,7±4,2 73,2 -228,9 ± 10,9 -299,6 -289,6 ± 10,0 -372,8
((C2H5)2N)2PC1 С4Н9 1 1 N\ PCI 1 nX 1 C4H9 71,7 82,4 70,7 83,5 -263,4 -263,4 -236,8 -335,1 ±7,5 -334,1 -320,3
Физические свойства важнейших веществ 389
Продолжение табл. 3.6.4
Соединение, формула кДж/моль Д/7'йр, кДж/моль Д//"ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт | Расчет
Производные четырехкоординированного атома фосфора (производные фосфористой и фосфоновой кислот)
Фосфористые кислоты: (СН3О)2Р(О)Н (С2Н5О)2Р(О)Н (н-С3Н7О)2Р(О)Н (мзо-С3Н7О)2Р(О)Н (СбН5о)2р(О)н (С1СН2СН2О)2Р(О)Н 39,5 49,3 57,0 51,3 82,1 65,7 39,8 43,1 39,5 45,7 55,2 50,0 86,7 67,9 41,6 43,8 -877,4 -806,0 ±33,0 -866,0 ± 28,0 -811,9 -883,0 -924,4 -954,8 -604,5 -929,2 -809,4 -845,3 -926,7 -845,8 -909,1 -851,4 -928,7 -979,6 -1004,8 -691,2 -997,1 -851,0 -889,1
^Р(О)Н
Р(О)Н
/
67,3 32,1 60,7 60,3 49,5 44,2 46,4 49,8 -845,0 ± 35,0 -844,0 ±31,0 -867,0 ± 45,0 -926,3 -815,2 -851,1 -876,7 -877,1 -904,7 -927,3 -975,8 -859,4 -897,5 -926,5
< —о /(О)Н —о —О /(О)Н —О /—° ( /Р(О)Н '—о
390 Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула A/7'’ap, кДж/моль Д//0°бр, кДж/моль Д/7с°|ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
О''Р<О)Н 95,9 106,1 -590,6 -696,7
Фосфоновые кислоты и фосфонаты:
(НО)2Р(О)СН3 48,1 46,9 -1006,3 ±26,4 -1002,4 -1054,4 ±25,9 -1049,3
(НО)2Р(О)С2Н5 50,6 51,7 -1007,9 ±14,6 -1016,6 -1058,5 ±14,2 -1068,3
(НО)2Р(О)С10Н21-« 89,9 -1182,3 -1235,9 ± 14,2 -1272,2
(НО)2Р(О)С6Н5 71,4 -826,8 -889,5 ±10,9 -898,2
(НО)(Мзо-С3Н7О)Р(О)СН3 60,7 51,7 -1014,4 -1066,1
(СН3О)2Р(О)СН3 42,4 45,9 -883,4 -929,3
(С2Н5О)2Р(О)СН3 52,2 52,1 -969,8 ± 27,6 -954,5 1026,3 ±27,2 -1006,6
(С2Н5О)2Р(О)С2Н5 56,0 56,8 -968,8 -1025,6
(«-С3Н7О)2Р(О)СН3 61,6 61,6 -996,0 -1057,6
(пзо-С3Н7О)2Р(О)С2Н5 60,7 61,2 -1056,0 ±17,1 -1040,6 -1116,7 ±16,3 -1101,8
(С6Н5О)2Р(О)СН3 84,2 93,1 -676,1 -769,2
(С1СН2СН2О)2Р(О)СН3 67,4 74,2 -1000,7 -1074,9
| ^Р(О)СН3 46,0 45,8 -874,0 ± 32,0 -845,1 -920,0 -890,9
^Р(О)СН3 50,6 48,0 -911,0 ±29,0 -881,0 -961,6 -929,0
J ^>(О)СН3 49,8 50,1 -962,0 ± 29,0 -916,9 -1011,8 -967,0
Физические свойства важнейших веществ
Продолжение табл. 3.6.4
ДЯ,^р, кДж/моль Д/70°бр, кДж/моль ДЯс°1Ор, кДж/моль
Соединение, формула Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт | Расчет
Производные четырехкоординированного атома фосфора (производные фосфористой и фосфоновой кислот)
< (С6 ^Р(О)СН3 —О /(О)СН3 —О —О /(О)СН3 —о /~°ч ZP(O)CH3 '—О °ХР(О)СН3 Н5О)2Р(О)СН(С6Н5)2 ^>(О)СН(С6Н5)2 ^>(О)СН(С6Н5)2 /—° ' zP(O)CH(C6H5)2 '—О 53,9 40,6 39,9 72,0 94,9 55,8 50,5 52,7 56,2 112,5 149,5 106,6 112,3 112,6 -1006,0 ±25,0 -901,0 ±30,0 -926,0 ±31,0 -960,0 ±32,0 -471,9 -746,4 -811,5 -720,9 -997,9 -886,7 -922,6 -948,3 -662,2 -457,7 -698,5 -779,5 -729,9 -1059,9 -941,6 -965,9 -1032,0 -1053,7 -937,2 -975,3 -1004,5 -774,7 -607,2 -805,1 -891,8 -842,5
392 Новый справочник химика и технолога
Продолжение табл. 3.6.4
ЛН"ар, кДж/моль zV7'бр, кДж/моль Д//"ор, кДж/моль
Соединение, формула Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Хлорангидриды фосфоновой кислоты:
(мзо-С3Н7О)С1Р(О)СН3 58,6 58,6 -797,1 -797,2 -855,7 -855,8
С12Р(О)СН3 (СН3С12ОР)* 62,3 62,3 -556,9 ± 26,4 -556,8 -619,2 + 25,9 -619,1
С12Р(О)С2Н5 (С2Н5С12ОР)* 42,7 67,1 -570,7 ± 14,6 -571,0 -613,4 ±13,8 -638,1
а-Аминофосфонаты:
(C2H5O)2P(O)CH(C6H5)NHCH3 89,4 93,2 -819,8 -913,0
(h-C3H7O)2P(O)CH(C6H5)NHCH3 99,3 102,7 -861,2 -963,9
(m3O-C3H7O)2P(O)CH(C6H5)N нсн3 94,2 97,5 -891,6 -989,1
Хлорангидриды фосфоновой кислоты:
О II (н-С5Н1]О)2Р—с—nhch2c6h5 138,7 138,1 -978,9 -1117,0
О II (»-C5H||O)2P-^C^NHCH2C6H5 143,4 142,9 -1020,5 -1163,4
(C2H5O)2P(O)C(CH3)2NHCH2C6H5 103,2 102,7 -881,2 -983,9
(C2H5O)2P(O)C(CH3)2N Н(мзо-С3Н7) 80,0 80,5 -1051,8 -1132,3
Г~ Р(О)СНСН(СН3)2
/ & N ("1 99,2 87,6 -1070,1 -1105,1 -1169,3 -1192,7
Физические свойства важнейших веществ
Продолжение табл. 3.6.4
Соединение, формула кДж/моль А/7'’6р, кДж/моль Д/7'’[ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт | Расчет
Производные четырехкоординированного атома фосфора (производные фосфористой и фосфоновой кислот)
/—° У 'рсоюнсщснзЬ "О ч) ] °У(О)С(С6Н5)СН3 / & N с: О .—о У \(О)С(С6Н5)СН3 "О О (С2Н5О)2Р(О)СНСН(СН3)2 0 О (CH3O)2P(O)CHHN— 99,0 96,3 93,6 104,9 -1030,7 -952,3 -1136,5 -954,5 -1129,7 -1048,6 -1230,1 -1059,4
107,0 88,4 89,8 111,0 89,5 94,9 -930,6 -1037,0 -903,9 -985,9 -1142,7 -890,0 -1037,6 -1125,4 -993,7 -1096,9 -1232,2 -984,9
сн=сн-сн3
а-Г идроксифосфонаты:
(С2Н5О)2Р(О)СН2ОН 48,3 48,7 -1106,4 -1155,1
(н-С3Н7О)2Р(О)СН2ОН 58,2 58,2 -1147,8 -1206,0
394 Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула АЯ“ар, кДж/моль АЯ''бр, кДж/моль А/7с°10р, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
(шо-С3Н7О)2Р(О)СН2ОН 52,8 53,0 -1178,2 -1231,2
(С2Н5О)2Р(О)СН(СН3)ОН 50,8 50,8 -1142,3 -1193,1
(С2Н5О)2Р(О)СН(С2Н5)ОН 55,8 55,6 -1163,0 -1218,6
(С2Н5О)2Р(О)СН(С6Н5)ОН 75,1 75,3 -1008,1 -1083,4
Производные четырехкоординированного атома фосфора (производные тио-, дитио- , фосфорной кислот)
Фосфаты:
(НО)зР(О) 48,9 -1253,5 -1284,4 -1302,4
(С2Н5О)2Р(О)ОН 41,8 54,0 -1205,7 -1259,7
(C2H5O)2P(O)F 46,0 46,0 -1197,9 -1197,9 -1243,9 -1243,9
(СН3О)зР(О) 51,5 ±4,2 47,3 -1075,0 -1122,3
(С2Н5О)3Р(О) 56,7 56,6 -1181,6 -1181,7 -1240,6 ±10,9 -1238,3
(С2Н5О)2(м5о-СзН7О)Р(О) 62,9 58,7 -1217,6 -1276,3
(к-С3Н7О)зР(О) 65,3 ± 4,2 70,9 -1250,6 ±21,8 -1243,8 -1315,9 ±21,3 -1314,7
(м5о-С3Н7О)3Р(О) 63,1 -1289,5 -1289,4 -1304,2 ±9,6 -1352,5
(н-С4Н9О)3Р(О) 85,0 85,2 -1382,8 ±12,6 -1306,0 -1454,8 ±11,3 -1391,2
(м5о-С4Н9О)3Р(О) 79,1 ±5,0 93,5 -1374,0 -1394,2 -1453,1 ±33,1 -1487,7
(С6Н5О)3Р(О) 114,4 114,4 -714,9 ±6,2 -714,9 -829,3 ± 5,7 -829,3
(С2Н5О)2Р(О) 54,8 54,8 -2095,4 -2095,4 —2150,2г -2150,2
(С2Н5О)2Р(О)
Тиофосфорные кислоты и тиофосфаты:
(C2H5O)2P(S)OH 104,9 120,7
^P(S)OH 121,8 118,8
/—°
Д P(S)OH 121,8 124,8
—о
Физические свойства важнейших веществ
Продолжение табл. 3.6.4
Соединение, формула A/7°ap, кДж/моль AH“6p, кДж/моль А//'’10р, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт ] Расчет
Производные четырехкоординированного атома фосфора (производные тио-, дитио-, фосфорной кислот)
(C2H5O)3P(S) 66,6 67,4 -906,2 -906,2 -972,8 ± 4,6 -973,6
J^P(S)OC2H5 66,2 65,4 -868,5 -933,9
/—о \ / х
X /(S)OC2H5 88,4 71,5 -899,9 -971,4
Дитиофосфорные кислоты и дитиофосфаты:
(CH3O)2P(S)SH 56,3 57,4 -540,9 ± 19,9 -580,3 -597,2 ± 17,8 -637,7
(C2H5O)2P(S)SH 67,7 63,6 -647,3 ± 12,5 -651,5 -715,0 -715,1
(h-C3H7O)2P(S)SH 74,2 73,1 -633,6 ± 18,6 -692,9 -707,8 ± 16,0 -766,0
(mjo-C3H7O)2P(S)SH 68,8 67,9 -727,4 ± 14,8 -723,3 -796,2 -791,2
(h-C4H9O)2P(S)SH 81,8 82,6 -734,3 -816,9
(m3o-C4H9O)2P(S)SH 77,8 78,6 -751,7 -830,3
(emop-C4H9O)2P(S)SH 78,1 77,5 -764,7 -842,2
^P(S)SH 66,0 61,6 -646,2 ± 16,0 -613,8 -712,2 -675,4
^>(S)SH 81,0 67,3 -694,8 -762,1
X°\
< P(S)SH 64,4 64,2 -619,5 -683,7
0
Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула кДж/моль ДЯ”6р, кДж/моль Д/7"ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт | Расчет
—о 4P(S)SH —о 72,3 66,4 -655,4 -721,8
/—°
( P(S)SH 81,4 67,7 -645,2 -712,9
V-oz
”°\ 4P(S)SH —0 87,5 69,3 -695,9 -765,2
/“Ч < ZP(S)SH r° 72,9 77,4 -731,2 -808,6
(C2H5O)2P(S)SC2H5 71,8 71,1 -696,6 -697,9 -768,4 -769,0
(w3o-C3H7O)2P(S)SCH3 71,5 71,9 -746,0 -817,9
(ewo^-C4H9O)2P(S)SC2H5 84,7 85,0 -811,1 -896,1
_^>(S)SC2H5 64,9 69,2 -675,3 -660,2 -740,2 -729,4
^P(S)SCH3 84,6 71,3 -717,6 -788,9
—о
4P(S)SC2H5 80,0 73,9 -703,0 -701,8 -783,0 -775,7
—o'
Физические свойства важнейших веществ 397
Продолжение табл. 3.6.4
Соединение, формула ДН"ар, кДж/моль ДЯ"бр, кДж/моль ДНс°.ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт | Расчет
Производные четырехкоординированного атома фосфора (производные тио-, дитио-, фосфорной кислот)
/—о
У ZP(S)SCH3 88,9 71,7 -667,9 -739,6
'—о
У~О
< P(S)SCH3 87,7 73,3 -718,7 -792,0
У
V p(s>sch3 У° 75,1 81,4 -754,0 -835,4
(С4Н9О)2Р(8)8Д 0 109,7 111,6 -893,1 -964,0 -1002,8 -1075,6
сн}—'
(Мдо-С4Н9О)2Р(8)8Д О 104,9 107,5 -912,0 -981,4 -1016,9 -1088,9
сн}—'
(ветор-С4Н9О)2Р(8)8Д О 108,1 106,4 -924,2 -994,3 -1032,3 -1100,7
сн?—
(CH3O)2P(S)SCHCOOCH3 СН2СООСН3 142,3 180,8 -1210,2 ±24,4 -1209,1 -1352,5 ±28,4 -1389,9
(C3H7O)2P(S)SCHCOOCH3 СН2СООСН3 196,1 196,5 -1302,1 ±23,8 -1321,6 -1498,2 ±27,8 -1518,1
(w3t>-C3H7O)2P(S)SCHCOOCH3 СН2СООСН3 191,7 191,3 -1350,9 ±22,4 -1352,0 -1542,6 ±25,9 -1543,3
(C4H9O)2P(S)SCHCOOCH3 СН2СООСН3 208,8 206,1 -1351,8 ±22,5 -1363,0 -1560,6 ±26,3 -1569,1
398 Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула ДЯ^р, кДж/моль Д//"бр. кДж/моль ДНс°10р, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
| Qxp(S)schcooch3 / СН2СООСН3 \—О / /P(S)SCHCOOCH3 '—о сн2соосн3 169,2 164,5 185,1 187,7 -1319,9 ±22,6 -1259,3 ±21,0 -1242,5 -1248,3 -1489,1 ±26,9 -1423,8 ±25,0 -1427,6 -1436,0
Производные пятикоординированного атома фосфора (алкоксифосфораны)
(С2Н5О)5Р /°—1 (С2Н5О)3РХ о—1 о^СЛ (С2Н5О)3Р' о—L хс6н5 ОС2Н5 1—.V\ хс6н5 ос2н5 Н3С\ ] /С6н5 H3CZ ХСбН5 ОС2Н5 < х Ч Х О О к ХС6Н5 QSi(CH3)3 Н3СХ ] /С6Н5 4fc( H3cz хс6н5 154,1 115,0 115,3 142,5 98,6 92,3 154,1 147,8 152,2 154,8 142,5 -911,8 -852,2 -874,6 -1349,8 -1240,4 -909,2 -799,7 -871,5 -877,3 -1484,7 ±5,5 -1065,9 -967,2 -989,9 -1448,4 -1332,7 -1063,3 -947,5 -1023,7 -1032,1
Физические свойства важнейших веществ 399
Продолжение табл. 3.6.4
Соединение, формула Д/7п°ар, кДж/моль ДЯ"6р, кДж/моль ДЯ“ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт | Расчет
Производные трехкоординированного атома мышьяка
Третичные алкил(арил)арсины: (CH3)3As (C2H5)3As (w3O-C5Hh)3As (C2H5)2AsC6H5 (C6H5)2AsC2H5 28,9 ± 1,3 43,1 ±4,2 66,6 90,6 69,0 86,3 43,4 52,6 67,7 89,5 69,0 91,8 11,7 ± 10,5 56,1 ± 17,6 11,7 -95,0 -195,2 -307,5 -16,3 ± 10,0 13,0 ± 16,7 -31,7 -147,6 -262,9 -397,0
isCH, 81,6 82,0
0 AsC,H, 95,6 94,6
^AsC6H13 106,2 104,1
400 Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула A//^ , кДж/моль АЯ"6р, кДж/моль д^сюр’ кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
О AsC8H17 113,0 113,7
(C6H5)3As 123,6 123,6 491,6 ± 18,8 491,6 393,3 ± 16,7 368,0
Диарилхлорарсины:
с/ y\sCI 90,8 90,8
~AsCl 85,8 123,3
Арилдихлорарсины:
C6H5AsC12 58,4 58,4
— Asc12 95,4 109,7
Физические свойства важнейших веществ
Продолжение табл. 3.6.4
Соединение, формула Zk//“ap, кДж/моль ДН0°бр, кДж/моль ДНс°10р. кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт 1 Расчет
Производные трехкоординированного атома мышьяка
Диарилбромарсин:
AsBr 90,7 90,7
Алкиларсениты:
(CH3O)3As 42,3 ± 1,2 51,3 -548,5 ± 1,7 -551,9 -590,8 ± 1,3 -603,2
(C2H5O)3As 59,9 60,5 -656,1 ±4,6 -658,6 -706,7 ± 1,2 -719,1
(h-C3H7O)3As 74,8 74,9 —726,7 ± 10,0 -720,7 -785,3 ± 5,0 -795,6
(h-C4H9O)3As 89,8 89,2 -782,9 -872,1
(mjo-C4H9O)3As 86,5 83,1 -809,0 -892,1
Алкил(арил)хлорарсениты:
^AsCl 60,4 57,2 -497,0 ± 8,0 -495,0 -557,4 -552,2
1 (>XAsCi 59,8 59,3 -528,9 ± 7,3 -530,9 -588,7 -590,2
(>XAsC! 61,0 61,5 -581,0 ±7,6 -566,8 -642,0 -628,3
^ASC1 97,3 67,2 -630,6 ± 12,1 -647,8 -727,9 -715,0
402 Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула ДЯ,«Р, кДж/иоль ДЯ"6Р' кДж/моль ДЯС°П,Р, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
< AsCl '—О 62,0 61,9 -503,4 ± 8,3 -536,6 -565,4 -598,5
/л < AsCl '—О 59,4 64,1 -543,4 ± 7,4 -572,5 -602,8 -636,6
Г Г \sCI 125,8 125,8 -331,4 ± 10,0 -331,4 -457,2 -457,2
Ал килдихлорарсениты:
CH3OAsC12 43,8 44,1 -490,8 ±8,1 -470,8 -534,6 -514,9
C2H5AsC12O* 47,1 47,2 -511,6 ±9,8 -506,4 -558,7 -553,6
h-C3H7AsC12O* 52,2 51,9 -521,8 ±10,5 -527,1 -574,0 -579,0
h-C4H9AsCI2O* 55,7 56,7 -535,1 ± 12,0 -547,8 -590,8 -604,5
Алифатические тиолы (меркаптаны)
Метантиол (метилмеркаптан), CH4S -22,8 -22,8 -1518,8 -1519,8
Этантиол, C2H6S 27,3 26,9 -46,1 -46,5 -73,7 -73,4 -2173,2 -2173,6 -2200,7 -2200,5
Пропантиол, C3H8S 32,0 31,7 -67,2 -67,2 -100,6 -98,9 -2825,3 -2825,8 -2857,5
Изопропантиол, C3H8S 29,6 29,5 -76,1 -76,1 -106,6 -105,6 -2819,3 -2820,5 -2850,0
Бутантиол, C4H10S 36,4 36,4 -87,9 -87,9 -124,3 -3478,1 -3514,5
Изобутантиол, C4Hi0S 34,7 34,4 -96,5 -96,6 -131,2 -131,0 -3472,8 -3471,8 -3507,5 -3506,2
ewop-Бутантиол, C4H|0S 34,1 34,3 -96,1 -96,8 -131,0 -131,1 -3473,9 -3472,8 -3507,1
Пентантиол, C5H12S 41,1 41,2 -108,3 -108,6 -150,9 -149,8 -4132,6 -4130,4 -4171,6
Изопентантиол, C5H)2S 39,4 39,2 -114,6 -117,3 -154,1 -156,5 4130,0 -4124,1 -4169,4 -4163,3
Гексантиол, C6H14S 46,0 -129,0 -129,3 -175,3 -4782,7 -4828,7
Физические свойства важнейших веществ
Продолжение табл. 3.6.4
Соединение, формула АН'ар, кДж/моль АН"бр. кДж/моль АН'’ор, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт I Расчет
Алифатические тиолы (меркаптаны)
Гептантиол, C7Hi6S 50,8 -149,2 -150,0 -200,8 -5435,0 -5485,8
Октантиол, C8Hi8S 55,5 -170,8 -226,3 -6087,3 -6142,8
Нонантиол, C9H20S 60,3 -191,5 -251,8 -6739,6 -6799,9
Декантиол, C10H22S 65,1 -211,6 -212,2 -277,3 -7391,8 -7456,9
З-Метил-2-бутантиол, C5Hi2S 37,5 37,0 -121,0 -126,2 -158,4 -163,2 -4125,4 4118,8 -4162,9 -4155,8
Алифатические сульфиды (тиоэфиры)
Диметил сульфид, C2H6S 28,0 28,0 -37,4 -36,2 -65,4 -64,2 -2180,2 -2180,2 -2208,1 -2208,2
ДиЭТИЛСуЛьфИД, C4H10S 35,9 35,0 -83,3 -83,5 -118,6 -118,5 -3486,1 -3487,7 -3522,7
Дипропилсульфид, C6Hi4S 44,6 -125,2 -124,9 -169,5 -4792,2 -4836,8
Метилэтилсульфид, C3H8S 32,0 31,5 -59,5 -59,8 -92,3 -91,3 -2833,6 -2833,9 -2865,4
Метилпропилсульфид, C4H]0S 36,3 -81,6 -80,5 -116,8 -3486,2 -3522,5
Метилбутилсульфид, C5H12S 41,0 41,1 -101,3 -101,3 -142,3 -142,4 -4142,1 -4138,5 -4183,1 -4179,6
Этилпропилсульфид, C5HI2S 40,0 39,8 -104,5 -104,2 -144,6 -144,0 -4139,9 4139,9 -4180,0 -4179,7
Этилбутилсульфид, C6H14S 44,6 -126,8 -124,9 -169,5 -4792,2 4836,8
Метилизопропилсульфид, C4H10S 34,2 34,1 -90,3 -89,4 -123,9 -123,5 -3480,8 -3480,8 -3514,9
Этилизопропилсульфид, C5H]2S 38,9 37,6 -117,2 -113,1 -156,1 -150,7 -4128,3 -4134,6 -4167,2 -4172,2
Хлор- и дихлоралканы
1-Хлорэтан, С2Н5С1 -107,7 -107,5 -1413,1 -1395,7
1-Хлорпропан, C3H7CI 28,6 28,6 -129,5 -128,2 -156,8 -2025,0 -2048,0 -2072,1 -2076,6
1-Хлорбутан, С4Н9С1 33,6 33,4 -154,6 -148,9 -188,2 -182,3 -2695,8 -2700,3 -2729,4 -2733,7
1-Хлорпентан, С5НцС1 38,2 38,1 -175,2 -169,6 -212,0 -207,7 -3349,9 -3352,6 -3388,1 -3390,7
1-Хлороктан, С8Н]7С1 52,4 52,4 -238,9 -231,7 -291,3 -284,1 -5310,0 -5309,5 -5362,4 -5361,9
1-Хаор-2-метилпропан, С4Н9С1 31,7 31,3 -157,6 -188,9 -2692,8 -2694,0 -2725,3
1-Хлор-3-метилбутан, С5НцС1 37,0 36,1 -171,0 -178,3 -208,0 -214,4 -3355,4 -3346,3 -3392,4 -3382,4
1,2-Дихлорэтан, С2Н4С12 35,2 34,9 -129,0 -130,5 -169,7 -165,4 -1236,4 -1231,7 -1266,6
404 Новый справочник химика и технолога
Продолжение табл. 3.6.4
Соединение, формула ДЯ”ар, кДж/моль Д/70°бр, кДж/моль A/7"op, кДж/моль
Газовая фаза Конденсированное состояние Конденсированное состояние Газовая фаза
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
1,3-Дихлорпропан, С3Н6С12 40,8 39,7 -151,3 -191,0 -1885,3 -1884,0 -1923,7
1,4-Дихлорбутан, С4Н8С12 46,4 44,4 -183,4 -172,0 -229,5 -216,4 -2534,8 -2536,3 -2581,2 -2580,7
Хлорбензолы
Хлорбензол, С6Н5С1 41,0 40,8 52,3 53,1 11,8 12,3 -3107,2 -3107,5 -3148,3
4-Метилхлорбензол, С7Н7С1 46,1 20,2 -25,9 -3753,0 -3752,8 -3798,9
2-Этилхлорбензол, С8Н9С1 50,8 -0,2 -54,0 -51,0 -4403,2 -4405,5 -4456,3
4-Этилхлорбензол, С8Н9С1 50,8 -0,2 -51,6 -51,0 -4405,6 -4405,5 -4456,3
4-Пропилхлорбензол, С9НИС1 55,6 -20,8 -76,4 -5057,8 -5113,4
2-Изопропилхлорбензол, С9НцС1 53,6 -26,1 -79,5 -79,7 -5051,1 -5104,7
3,4-Диметилхлорбензол, С8Н9С1 51,4 -12,7 -64,1 -4398,2 -4449,6
2,4,6-Триметилхлорбензол, С9Н ] ] С1 56,7 -45,7 -102,4 -5043,6 -5100,3
1,3-Дихлорбензол, С6Н4С12 48,6 49,6 24,7 23,4 -26,2 -2953,9 -2947,4 -3008,9 -2997,0
1,4-Дихлорбензол, С6Н4С12 49,6 24,6 23,4 -26,2 -2939,9 -2947,4 -2997,0
* Эмпирические формулы по Хиллу.
Таблица 3.6.5
Экспериментальные и расчетные значения теплотворной способности (теплоты сгорания)
Соединение Формула Высшая Низшая
кДж/м3 кДж/кг кДж/м3 кДж/кг
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Алифатические углеводороды
Метан СН4 39 731,0 39 748,0 55 508,0 35 807,0 35 826,0 50 031,0 50 031,0
Этан С2Н6 69 622,0 69 634,0 51 872,0 63 727,0 63 750,0 47 503,0 47 489,0
Пропан С3н8 99 077,0 98 754,0 50 161,0 91 211,0 90 909,0 46 366,0 46 176,0
Бутан С4Ню 128 407,0 127 874,0 49 284,0 118 595,0 118 068,0 45 735,0 45 504,0
Изобутан С4Ню 127 593,0 49 176,0 117 788,0 45 396,0
Пентан С5н12 157 800,0 158 200,0 49 115,0 146 022,0 146 433,0 45 406,0 45 462,0
Изопентан С5н12 157 830,0 49 001,0 146 063,0 45 347,0
Гексан С6Н14 187 533,0 48 744,0 173 636,0 173 805,0 44 769,0 45 176,0
Физические свойства важнейших веществ 405
Продолжение табл. 3.6.5
Соединение Формула Высшая Низшая
кДж/м3 кДж/кг кДж/м3 кДж/кг
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Алифатические углеводороды
Гептан С7н16 216 866,0 48 481,0 200 260,0 201 176,0 44 769,0 44 974,0
Октан с8н18 246 199,0 48 278,0 228 028,0 228 548,0 44 769,0 44 817,0
Нонан С9Н20 275 531,0 48 120,0 256 341,0 255 920,0 44 769,0 44 695,0
Декан С10Н22 304 864,0 47 997,0 283 675,0 283 291,0 44610,0 44 600,0
Ундекан СцН24 334 197,0 47 892,0 310 663,0 44 520,0
Додекан С12Н26 363 530,0 47 805,0 338 035,0 44 452,0
Тридекан С]зН28 392 863,0 47 731,0 365 407,0 44 395,0
Тетрадекан С14Н30 422 196,0 47 670,0 392 778,0 44 348,0
Пентадекан С15Н32 451 529,0 47 614,0 418 400,0 420 150,0 44 338,0 44 305,0
Гексадекан С16Нз4 480 861,0 47 566,0 447 521,0 44 268,0
Гептадекан С1?Нз6 510 194,0 47 525,0 474 893,0 44 237,0
Октадекан Ci8H38 539 527,0 47 487,0 503 892,0 502 265,0 44 207,0
Нонадекан С19Н40 568 860,0 47 453,0 529 637,0 44 181,0
Эйкозан С20Н42 598 192,0 47 424,0 552 288,0 557 008,0 44217,0 44 158,0
Пятичленные циклические алифатические углеводороды
Циклопентан с5н10 148 300,0 47 368,0 138 323,0 138 495,0 44 214,0 44 236,0
Метилциклопентан с6н12 177 263,0 47 180,0 165 352,0 165 496,0 44 042,0 44 048,0
Этилциклопентан С7Н,4 206 596,0 47 131,0 192 799,0 192 868,0 44 013,0 43 999,0
Пропилциклопентан С8Н16 235 929,0 47 093,0 220 204,0 220 240,0 43 984,0 43 962,0
Бутилциклопентан С9н18 265 262,0 47 068,0 247 611,0 43 936,0
Пентилциклопентан С]оН2о 294 595,0 47 044,0 275 726,0 274 983,0 43 913,0
Г ексилциклопентан СцН22 323 927,0 47 025,0 302 354,0 43 893,0
Г ептилциклопентан С12Н24 353 260,0 47012,0 329 726,0 43 880,0
Октилциклопентан С13Н26 382 593,0 46 998,0 357 098,0 43 866,0
Нонилциклопентан С]4Н28 411 926,0 46 986,0 384 470,0 43 854,0
Децилциклопентан С15Нзо 441 259,0 46 978,0 414 216,0 411 842,0 43 846,0
У ндецилциклопентан С16Н32 470 592,0 46 969,0 439 213,0 43 837,0
406 Новый справочник химика и технолога
Продолжение табл. 3.6.5
Высшая Низшая
Соединение Формула кДж/м3 кДж/кг кДж/м3 кДж/кг
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Додецилциклопентан С17Н34 499 925,0 46 961,0 466 585,0 43 829,0
Тридецилциклопентан с18н36 529 257,0 46 956,0 493 956,0 43 824,0
Т етрадецилциклопентан С19Н38 558 590,0 46 949,0 521 328,0 43 817,0
Пентадецилциклопентан С20Н40 587 923,0 46 943,0 548 700,0 43 811,0
1,1 -Диметилциклопентан с7н14 206 873,0 47 194,0 193 145,0 44 062,0
1,2-Диметилциклопентан с7н14 206 227,0 47 046,0 192 499,0 43 924,0 43 915,0
Шестичленные циклические алифатические углеводороды
Циклогексан С6н12 176 673,0 47 023,0 164 640,0 164 906,0 43 848,0 43 891,0
Метилциклогексан с7н14 205 636,0 46912,0 191 585,0 191 908,0 43 732,0 43 780,0
Этилциклогексан С8н16 234 969,0 46 902,0 219 158,0 219 279,0 43 775,0 43 770,0
Пропилциклогексан С9Н18 264 302,0 46 898,0 246 563,0 246 651,0 43 776,0 43 766,0
Бутилциклогексан СюНэо 293 634,0 46 891,0 278 236,0 274 023,0 43 759,0
Пентилциклогексан С|]Н22 322 967,0 46 886,0 301 395,0 43 754,0
Г ексилциклогексан С]2Н24 352 300,0 46 884,0 328 766,0 43 752,0
Г ептилциклогексан Ci3H26 381 633,0 46 880,0 356 138,0 43 748,0
Октилциклогексан Ci4H28 410 966,0 46 877,0 383 510,0 43 745,0
Нонилциклогексан С15Н30 440 299,0 46 876,0 410 881,0 43 744,0
Децилциклогексан С16Н32 469 632,0 46 873,0 438 253,0 43 741,0
У н деци лциклогексан С17Н34 498 964,0 46 871,0 465 625,0 43 739,0
Додецилциклогексан с18н36 528 297,0 46 870,0 492 996,0 43 739,0
Тридецилциклогексан С19Н38 557 630,0 46 868,0 520 368,0 43 737,0
Т етрадецил циклогексан С2оН4о 586 963,0 46 867,0 548 104,0 547 740,0 43 735,0
1,1 -Диметилциклогексан С8н16 235 246,0 46 957,0 219 556,0 43 825,0
1,2-Диметилциклогексан С8Н16 234 599,0 46 828,0 218 910,0 43 696,0
1,2-Диэтилциклогексан С]оН2о 293 265,0 46 832,0 273 653,0 43 304,0 43 700,0
>и/2в/и-Бутилциклогексан С]оН2о 293 541,0 46 876,0 273 929,0 43 263,0 43 744,0
1,2,3,4,5,6-Гексаэтилциклогексан С18н36 526 448,0 46 706,0 491 147,0 43 639,0 43 575,0
Физические свойства важнейших веществ
Продолжение табл. 3.6.5
Высшая Низшая
Соединение Формула кДж/м3 кДж/кг кДж/м3 кДж/кг
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Шестичленные бициклические алифатические углеводороды
1,1 -Бициклогексил 2-Метил-1,1 -бициклогексил 2-Этил-1,1 -бициклогексил 4-Этил-1,1 -бициклогексил 2-Пропил-1,1 -бициклогексил 2-Изопропил-1,1 -бициклогексил 2,4,6,2',4',6'-Г ексаметил-1,1-би циклогексил 4-Г ептил-1,1 -бициклогексил 4-Н они л-1,1 -бициклогексил 2,2-Диметил-1,1 -бициклогексил С12Н22 С13Н24 С14Н26 С14Н26 С15Н28 С15Н28 CisH34 С19Н36 С21Н40 С14Н26 45 938,0 45 964,0 46 027,0 46 027,0 46 081,0 46 041,0 46 044,0 46 244,0 46 300,0 46 059,0 42 886,0 42 844,0 42 949,0 42 928,0 42 949,0 42 865,0 43 095,0 43 074,0 43 074,0 42 907,0 43 033,0 43 041,0 43 089,0 43 089,0 43 130,0 43 090,0 43 062,0 43 254,0 43 297,0 43 121,0
Производные шестичленных бициклических алифатических углеводородов
Дициклогексилметан Циклогексил(3 -метилцикло-гексил)метан Циклогексил(2-этилцикло-гексил)метан Бис(этилциклогексил)метан Циклогексил(4-изопропилцикло-гексил)метан Бис(2,4,6-триметилцикло-гексил)метан 1,1 -Д ициклогексилэтан 1 -Циклогексил-1 - изопропилциклогексилэтан 1,1 -Бис(4-метилциклогексил)этан 1,1 -Бис(диметилциклогексил)этан 1,1 -Бис(этилциклогексил)этан С1зН24 С14Н26 С15Н28 С17Н32 С]бНзо С19Н36 С14Н26 С17Н32 С1бН30 С18Н34 С18Н34 46 010,0 46 027,0 46 081,0 46 137,0 46 093,0 46 087,0 46 027,0 46 102,0 46 056,0 46 077,0 46 143,0 42 970,0 42 970,0 43 012,0 42 970,0 42 991,0 43 095,0 42 899,0 42 949,0 42 928,0 43 074,0 42 769,0 43 087,0 43 089,0 43 130,0 43 164,0 43 131,0 43 098,0 43 089,0 43 129,0 43 093,0 43 095,0 43 161,0
408 Новый справочник химика и технолога
Продолжение табл. 3.6.5
Соединение Формула Высшая Низшая
кДж/м3 кДж/кг кДж/м3 кДж/кг
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
2,2-Бис(метилциклогексил)пропан с17н32 46 128,0 42 907,0 43 156,0
1,1 -Дициклогексил-2-метилпропан С1бНзо 46 093,0 43 032,0 43 131,0
1,1 -Дициклогексилгептан С19Н36 46 244,0 43 095,0 43 254,0
1,2-Дициклогексилэтан С14Н26 46 070,0 42 698,0 43 131,0
1-Циклопентил-3-циклогексил пропан С14н26 46 180,0 42 719,0 43 242,0
1,3-Дициклогексил бутан С1бНзо 46 131,0 42 899,0 43 168,0
1,1,3-Трициклогексилпропан С21н38 45 757,0 42 593,0 42 884,0
Бис(циклогексилметил)ци клогексан С2оН3б 45 700,0 42 635,0 42 841,0
1,3,5-Трициклопентил циклогексан С21Нзб 45 398,0 42 468,0 42 658,0
Конденсированные алициклические углеводороды
транс-Декалин С1он18 45 757,0 42 593,0 42 897,0
транс-2-Метилдекалин СцН2о 45 801,0 42 468,0 42 917,0
транс-9-Метилдекалин СцН2о 45 897,0 43 012,0
1 -Этилдекалин С]2Н22 45 888,0 42 614,0 42 983,0
2-Этилдекалин С]2Н22 45 888,0 42 635,0 42 983,0
1 -Пропилдекалин С,зН24 45 964,0 42614,0 43 041,0
1 -Изопропилдекалин С]зН24 45 918,0 42 886,0 42 995,0
1-Бутилдекалин С.4н26 46 027,0 42 802,0 43 089,0
1 -Изобутилдекалин С14Н26 45 984,0 42 698,0 43 046,0
1 -втор-Бутилдекалин С14н26 45 984,0 42 802,0 43 046,0
1 -тире/и-Бутилдекалин С14Н26 46016,0 42 886,0 43 078,0
1,1 -Диметилдекалин С)2Н22 45 926,0 42 781,0 43 020,0
транс-V и дрин дан С9Н16 45 805,0 42 593,0 42 976,0
1 -Этилгидрин дан СцН2о 45 943,0 42 802,0 43 058,0
1 -Изопропилгидриндан С]2Н22 45 968,0 42 543,0 43 062,0
1,2-Диизопропилгидриндан CisH28 46 065,0 42 928,0 43 114,0
1 -Циклогексил-3 -метил-транс-гидриндан С16н28 45 470,0 42 551,0 42 680,0
Физические свойства важнейших веществ 409
Продолжение табл. 3.6.5
Соединение Формула Высшая Низшая
кДж/м3 кДж/кг кДж/м3 кДж/кг
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Конденсированные алициклические углеводороды
1 -Циклогексил-1,3,3-триметил-гидриндан С18Н32 45 676,0 42 635,0 42 847,0
Этиленовые углеводороды (олефины)
Этилен С2Н4 62 969,0 62 991,0 50 303,0 59 036,0 59 069,0 47 180,0 47 171,0
Пропилен С3Н6 91 906,0 48 923,0 85 981,0 86 023,0 45 797,0 45 792,0
Бутил-1-ен с4н8 121 026,0 48 315,0 ИЗ 432,0 113 181,0 45 322,0 45 184,0
Пент-1 -ен С5н]о 151 315,0 48 331,0 141 001,0 141 509,0 45 008,0 45 199,0
Гекс-1-ен С6Н12 180 648,0 48 081,0 168 881,0 44 949,0
Гепт-1-ен с7н14 209 981,0 47 903,0 196 253,0 44 771,0
Окт-1 -ен с8н16 239 313,0 47 769,0 223 624,0 44 637,0
Нон-1-ен СдН|8 268 646,0 47 669,0 250 996,0 44 537,0
Дец-1-ен С]оН2о 297 979,0 47 585,0 298 738,0 278 367,0 44 453,0
Ундец-1-ен СцН22 327 312,0 47 516,0 305 739,0 44 385,0
Додец-1-ен С]2Н24 356 645,0 47 462,0 333 1 1 1,0 44 330,0
Тридец-1-ен С1зН26 385 978,0 47414,0 360 483,0 44 282,0
Тетрадец-1-ен Ci4H28 415 311,0 47 372,0 387 854,0 44 240,0
Пентадец-1 -ен С15Н30 444 643,0 47 338,0 416 308,0 415 226,0 44 207,0
Гексадец-1-ен С1бНз2 473 976,0 47 307,0 442 598,0 44 175,0
Гептадец-1-ен СпНз4 503 309,0 47 279,0 469 969,0 44 147,0
Октадец-1-ен с18н36 532 642,0 47 256,0 497 341,0 44 124,0
Нонадец-1-ен С19Н38 561 975,0 47 234,0 524 713,0 44 102,0
Эйкоз-1-ен С20Н40 591 308,0 47 214,0 589 944,0 552 084,0 44 082,0
З-Метилбутил-1 -ен с5н10 150 945,0 48 213,0 141 139,0 45 081,0
Ацетиленовые углеводороды
Ацетилен С2Н2 57 969,0 58 004,0 49 896,0 56 036,0 56 043,0 48 203,0 48 209,0
Пропин С3Н4 86 080,0 48 133,0 82 559,0 82 158,0 46 164,0 45 940,0
Бут-1-ин с4н6 115 200,0 47 707,0 110 017,0 109 317,0 45 561,0 45 271,0
410 Новый справочник химика и технолога
Продолжение табл. 3.6.5
Соединение Формула Высшая Низшая
кДж/м3 кДж/кг кДж/м3 кДж/кг
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Пент-1-ин с5н8 145 573,0 47 869,0 137 474,0 137 729,0 45 206,0 45 289,0
Гекс-1-ин СбНю 174 906,0 47 692,0 165 119,0 165 100,0 45 023,0 45 018,0
Гепт-1-ин С7н12 204 239,0 47 571,0 192 389,0 192 472,0 44 811,0 44 831,0
Окт-1-ин c8HJ4 233 571,0 47 477,0 219 847,0 219 843,0 44 688,0 44 687,0
Нон-1-ин С9Н16 262 904,0 47 404,0 247 304,0 247 215,0 44 592,0 44 576,0
Дец-1 -ин С1ОН18 292 238,0 47 350,0 274 575,0 274 587,0 44 488,0 44 490,0
Ундец-1-ин СцН2о 321 570,0 47 302,0 301 958,0 44 417,0
Додец-1-ин с12н22 350 903,0 47 263,0 329 330,0 44 357,0
Тридец-1-ин С1зН24 380 236,0 47 232,0 356 702,0 44 308,0
Тетрадей-1-ин С14Н26 409 569,0 47 203,0 384 074,0 44 265,0
Пентадец-1 -ин Ci5H28 438 901,0 47 178,0 411 863,0 411 445,0 44 271,0 44 227,0
Гексадец-1-ин СюНзо 468 234,0 47 158,0 438 817,0 44 195,0
Гептадец-1-ин С1?Нз2 497 567,0 47 139,0 466 188,0 44 166,0
Октадец-1-ин С18Н34 526 900,0 47 122,0 493 560,0 44 140,0
Нонадец-1-ин С19Н36 556 233,0 47 108,0 520 932,0 44 118,0
Эйкоз-1-ин СгоНз8 585 566,0 47 094,0 547 282,0 548 304,0 44 015,0 44 097,0
Бут-2-ин С4Н6 115 344,0 47 767,0 109 460,0 45 330,0
Ароматические углеводороды
Бензол с6н6 42 241,0 40 281,0 40 553,0
Толуол С7Н8 42 871,0 40 959,0 40 964,0
Этилбензол с8н10 43 398,0 41 340,0 41 329,0
Пропилбензол С9н12 43 802,0 41 600,0 41 609,0
Бутилбензол СюН]4 44 119,0 41 828,0
Пентилбензол СцНю 44 376,0 42 023,0 42 005,0
Гексилбензол С1гН18 44 591,0 42 183,0 42 154,0
Гептилбензол С]зН20 44 769,0 42315,0 42 277,0
Октилбензол С]4Н22 44 921,0 42 427,0 42 382,0
Нонилбензол С15н24 45 053,0 42 503,0 42 473,0
Физические свойства важнейших веществ
Продолжение табл. 3.6.5
Соединение Формула Высшая Низшая
кДж/м3 кДж/кг кДж/м3 кДж/кг
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Ароматические углеводороды
Децилбензол Ci6H26 45 169,0 42 554,0
Ундецилбензол С17Н28 45 269,0 42 666,0 42 623,0
Додецилбензол С18Н30 45 358,0 42 733,0 42 684,0
Т ридецилбензол С19Н32 45 439,0 42 741,0
Тетрадецил бензол С20Н34 45 511,0 42 863,0 42 790,0
Пентадецилбензол С21Н36 45 575,0 42 834,0
Г ексадецилбензол С22Н38 45 635,0 42 876,0
jw-Ксилол С8Н10 43 334,0 41 221,0 41 266,0
1,3,5-Т риметилбензол с9н12 43 693,0 41 500,0
Цимол С]0Н14 44 007,0 41 740,0 41 716,0
Алифатические спирты
Метанол СН4О 23 872,0 21 338,0 21 130,0
Этанол с2н6о 30 519,0 27 614,0 27 659,0
Пропанол С3Н8О 34 328,0 31 380,0 31 404,0
Бутанол С4Н10О 36 699,0 33 472,0 33 736,0
Пентанол с5н12о 38 312,0 35 564,0 35 322,0
Гексанол СбН^О 39 482,0 36 401,0 36 472,0
Гептанол С7Н16О 40 373,0 37 238,0 37 348,0
Октанол с8н18о 41 069,0 38 074,0 38 033,0
Нонанол С9Н20О 41 629,0 38 493,0 38 584,0
Деканол С10Н22О 42 093,0 38 911,0 39 040,0
Ундеканол СцН24О 42 479,0 39419,0
Додеканол С12Н26О 42 807,0 39 742,0
Тридеканол С1зН28О 43 091,0 40 021,0
Тетрадеканол С14Н30О 43 336,0 40 262,0
Пентадеканол С15Н32О 43 550,0 40 473,0
Гексадеканол С16Н34О 43 740,0 40 660,0
412 Новый справочник химика и технолога
Окончание табл. 3.6.5
Соединение Формула Высшая Низшая
кДж/м3 кДж/кг кДж/м3 кДж/кг
Опыт Расчет Опыт Расчет Опыт Расчет Опыт Расчет
Гептадеканол с17н36о 43 911,0 40 828,0
Октадеканол с18н38о 44 063,0 40 977,0
Нонадеканол С19н40о 44 199,0 41 111,0
Эйкозанол С20Н42О 44 324,0 41 234,0
Карбоновые кислоты
Уксусная С2Н4О2 15 474,0 14 644,0 14011,0
Пропановая с3н6о2 21 511,0 19 732,0
Бутановая С4Н8О2 25 543,0 23 012,0 23 549,0
Пентановая с5н10о2 28 470,0 26 320,0
Гексановая с6н1202 30 688,0 28419,0
Гептановая с7н14о. 32 428,0 30 066,0
Октановая с8н160. 33 831,0 31 394,0
Нонановая С9Н18О2 34 984,0 32 486,0
Декановая СюН2о02 35 949,0 33 054,0 33 399,0
Ундекановая СцН22О2 36 771,0 34 177,0
Додекановая С12Н24О2 37 475,0 34 844,0
Тридекановая с13н2602 38 088,0 35 424,0
Т етрадекановая С14Н28О2 38 625,0 35 932,0
Пентадекановая CisH30O2 39 102,0 36 383,0
Гексадекановая (пальмитиновая) С,6Н32О2 39 525,0 36 784,0
Г ептадекановая Ci7H34O2 39 904,0 37 142,0
Октадекановая (стеариновая) с18н3602 40 247,0 37 238,0 37 467,0
Нонадекановая С]9Н38О2 40 556,0 37 760,0
Эйкозановая С2оН4о02 40 838,0 38 027,0
Адипиновая с6н10о4 20 041,0 18 537,0
Физические свойства важнейших веществ
414
Новый справочник химика и технолога
Литература к табл. 3.6.4 и 3.6.5
1. Алемасов В.Е., Дрегалин А.Ф., Тишин А.П., Худяков В.А. Термодинамические и теплофизические свойства продуктов сгорания. В 10 т. Т. 10 (часть 1). М.: Изд-во АН СССР, 1980. 380 с.
2. Брусько В.В. Термохимия циклических производных дитиофосфорной, фосфористой и метилфосфоновой кислот: Дис. ... канд. хим. наук. Казань, 1994. 112 с.
3. Бузников Е.Ф., Роддатис К.Ф., Спсйшер В.А. Перевод котлов ДКВ и ДКВР на газообразное топливо. М.; Л.: Энергия, 1964. 192 с.
4. Ван Везер Дж. Р. Фосфор и его соединения. М.: Изд-во ин. лит., 1962. 687 с.
5. Васильева Т.Ф. Энтальпия образования А,А-диэтил-ацстамида и тепловые эффекты реакции синтеза ди-алкилзамещенных амидов И Журн. прикл. химии. 1984. Т. 57, вып. 8. С. 1890-1892.
6. Васильева Т.Ф., Жильцова Е.Н. Энтальпии сгорания двух монометиламидов И Термодинамика органических соединений: межвуз. сб. научн. тр. / Горьк. ун-т. Горький, 1982. С. 108-110.
7. Васильева Т.Ф., Жильцова Е.Н., Введенский А.А. Энтальпии сгорания алкиленкарбонатов И Журн. физ. химии. 1972. Т. 46, вып. 2. С. 541-542.
8. Васильева Т.Ф., Котов В.И. Энтальпии сгорания диметилзамещенных амидов и диметилалкиламинов И Тез. докл. 7-й Всесоюз. конфер. по калориметрии. 1977. Т. ЕС. 102-106.
9. Вдовченко В.С., Мартынов М.И. Энергетическое топливо СССР (ископаемые угли, горючие сланцы, торф, мазут и горючий природный газ): Справ. М.: Энергоатомиздат, 1991. 183 с.
10. Герасимов П.А., Губарева А.И., Тарбесва Н.А., Кундерснко В.М. Физико-химические свойства Р-пиколина // Журн. прикл. химии. 1992. Т. 65, № 2. С. 460-462.
11. Губарева А.И., Герасимов П.А. Физико-химические свойства изомасляного альдегида И Журн. прикл. химии. 1990. Т. 63, № 4. С. 905-907.
12. Козина М.П., Скуратов С.М., Штехер С.М., Соснина И.Е., Турова-Поляк М.Б. Теплоты горения некоторых бицикланов И Журн. физ. химии. 1961. Т. 35, № 10. С. 2316-2321.
13. Лебедев Ю.А., Мирошниченко Е.А. Термохимия парообразования органических веществ. М.: Наука, 1981.215с.
14. Лебедева Н.Д. Теплоты сгорания ряда монокарбоновых кислот // Журн. физ. химии. 1964. Т. 38, № 11. С.2648-2649.
15. Лебедева Н.Д., Катин Ю.А. Теплоты сгорания некоторых монозамещенных бензола // Журн. физ. химии. 1972. Т. 46, № 7. С. 1888-1889.
16. Лебедева Н.Д., Катин Ю.А. Энтальпии образования амидов монокарбоновых кислот // Журн. прикл. химии. 1973. Т. 46, вып. 9. С. 2009-2011.
17. Лебедева Н.Д., Катин Ю.А., Ахмедова Г.Я. Стандартная энтальпия образования нитробензола И Журн. физ. химии. 1971. Т. 45, № 8. С. 2103.
18. Лебедева Н.Д., Катин Ю.А., Ахмедова Г.Я. Энтальпии образования дипропиламина, диизопропиламина, дибутиламина и диизобутиламина И Журн. физ. химии. 1971. Т. 45, №6. С. 1357-1359.
19. Лебедева Н.Д., Ряднснко В.Л. Энтальпии образования некоторых мононитроалканов И Журн. физ. химии. 1973. Т. 47, № 9. С. 2442.
20. Лебедева Н.Д., Ряднснко В.Л., Кузнецова И.Н. Теплоты сгорания и энтальпии образования некоторых ароматических нитропроизводных // Журн. физ. химии. 1971. Т. 45, № 4. С. 980-981.
21. Макеева Т.Б. Термохимия циклических и ациклических алкил(арил)арсинов и хлорангидридов ал-кил(алкилен)мышьяковистой кислоты: Дис. ... канд. хим. наук. Казань, 1996. 104 с.
22. Николаев А.В., Афанасьев Ю.В., Старостин А.Д. Термохимия некоторых фосфорорганических соединений //Докл. АН СССР. 1966. Т. 168. С. 351-353.
23. Николаев А.В., Афанасьев Ю.В., Старостин А.Д. Термохимия фосфорорганических соединений // Изв. Сиб. отд. АН СССР. Сер. хим. 1968. № 14. Вып. 6. С. 3-7.
24. Пурдела Д., Вылчану Р. Химия органических соединений фосфора. М.: Химия, 1972. 752 с.
25. Равич М.Б. Упрощенная методика теплотехнических расчетов. М.: Изд-во АН СССР, 1961.304 с.
26. Рыскалиева А.К., Абрамова Г.В., Еркасов Р.Ш., Ну-рахметов Н.Н. Энтальпии сгорания и образования производных салициловой кислоты // Журн. физ. химии. 1992. Т. 66, вып. 3. С. 797-799.
27. Рыскалиева А.К., Абрамова Г.В., Нурахметов Н.Н., Еркасов Р.Ш. Энтальпии сгорания и образования о-фенилацетамида и изовалсрамида И Изв. вузов. Химия и хим. технология. 1990. Т. 33, вып. 9. С. 17-19.
28. Рыскалиева А.К., Еркасов Р.Ш., Абрамова Г.В., Нурахметов Н.Н. Термохимия о-метилацета-нилида и 2',4'-диметилацетанилида // Изв. вузов. Химия и хим. технология. 1991. Т. 34, вып. 9. С. 25-28.
29. Рыскалиева А.К., Еркасов Р.Ш., Абрамова Г.В., Нурахметов Н.Н. Энтальпии сгорания никотинамида и его нитрата И Изв. вузов. Химия и хим. технология. 1993. Т. 36, вып. 4. С. 112-114.
30. Сагадеев Е.В. Термохимия производных фосфоновой кислоты с a-функциональными группами: Дис. ... канд. хим. наук. Казань, 1997. 184 с.
31. Сагадеев Е.В., Барабанов В.П. Расчет теплот сгорания производных бензола И Изв. вузов. Химия и хим. технология. 2003. Т. 46, вып. 3. С. 155-157.
32. Сагадеев Е.В., Барабанов В.П. Расчет теплот сгорания углеводородов ряда ацетилена И Изв. вузов. Химия и хим. технология. 2003. Т. 46, вып. 1. С. 157-159.
Физические свойства важнейших веществ
415
33. Сагадеев Е.В., Барабанов В.П. Энтальпии испарения и образования азоторганических соединений // Журн. физ. химии. 2005. Т. 79, № 11. С. 1955-1960.
34. Сагадеев Е.В., Кафиатуллин Р.А., Сагадеев В.В., Сагадеев В.И. Расчет теплот сгорания углеводородов ряда этилена // Теорет. основы хим. технологии. 2003. Т. 37, №5. С. 558-560.
35. Сагадеев Е.В., Сагадеев В.В. Расчет теплот сгорания предельных углеводородов, входящих в энергетические топлива // Теплофизика высоких температур. 2002. Т. 40, № 4. С. 581-585.
36. Сагадеев Е.В., Сагадеев В.В. Расчет теплоты сгорания углеводородных компонентов топлив И Теплофизика высоких температур. 2004. Т. 42, № 3. С. 421—425.
37. Сагадеев Е.В., Сафина Ю.Г. Использование функции «состав—свойство» для определения термохимических характеристик производных трехкоординированного атома фосфора И Журн. физ. химии. 2004. Т. 78, № 12. С. 2147-2153.
38. Сагадеев Е.В., Сафина Ю.Г. Термохимия производных фосфорной кислоты: эмпирический подход // Журн. физ. химии. 2005. Т. 79, № 3. С. 427-^132.
39. Сагадеев Е.В., Сафина Ю.Г. Энтальпии испарения и образования производных фосфоновой и фосфористой кислот И Журн. физ. химии. 2002. Т. 76, №9. С. 1565-1571.
40. Сагадеев Е.В., Сафина Ю.Г., Черкасов Р.А. Исследование внутри- и межмолекулярных взаимодействий с участием а-фосфорилированных аминов и спиртов в растворителях различной природы И Журн. орг. химии. 2004. Т. 40, вып. 7. С. 981-986.
41. Сагадеев Е.В., Сафина Ю.Г., Черкасов Р.А. О возможностях расчета базовых термохимических характеристик фосфоранов на основе применения аддитивной схемы // Журн. орг. химии. 2005. Т. 41, вып. 10. С. 1557-1560.
42. Сафина Ю.Г. Циклические триметилсилилфосфи-ты. Особенности строения, сольватации и химического поведения в реакциях присоединения по связям С=О и C=N: Дис. ... канд. хим. наук. Казань, 1987.209 с.
43. Ситникова Е.Ю. Термохимия некоторых моно-, ди-, и тетратиопроизводных четырекхкоординирован-ного атома фосфора: Дис. ... канд. хим. наук. Казань, 2000. 125 с.
44. Скуратов С.М., Бонецкая А.К. Энтальпия образования амидной связи // Высокомол. соед. 1966. Т. 8, №9. С. 1591-1593.
45. Скуратов С.М., Стрепихеев А.А., Козина М.П. О реакционной способности пяти- и шестичленных гетероциклических соединений И Докл. АН СССР. 1957. Т. 117, №3. С. 452-454.
46. Старостин А.Д., Николаев А.В., Афанасьев Ю.А. Стандартные теплоты образования некоторых фосфорорганических соединений /7 Изв. АН СССР. Сер. хим. 1966. № 8. С. 1303-1307.
47. Стрепихеев А.А., Скуратов С.М., Качинская О.Н., Муромова Р.С., Брыкина Е.П., Штехер С.М. О напряженности лактамов // Докл. АН СССР. 1955. Т. 102, № ЕС. 105-108.
48. Фикре Маммо Демиссие. Термохимия и реакционная способность хлорангидридов кислот трехкор динированного атома фосфора: Дис. ... канд. хим. наук. Казань, 1993. 104 с.
49. Хмельницкий Л.И. Справочник по взрывчатым веществам. Ч. II. М., 1962. 842 с.
50. Черкасова Р.И., Рожнов А.М., Нестерова Т.Н. Равновесие изомеризации 1,2-, 1,3-, 1,4-дихлорбутанов И Журн. физ. химии. 1974. Т. 48, № 1. С. 234.
51. Чертков Я.Б. Современные и перспективные углеводородные реактивные и дизельные топлива. М.: Химия, 1968. 356 с.
52. Abboud J.-L.M., Jimenez Р., Roux M.V., Turrion С., Lopez-Mardomingo С. Structural Effects on the Thermochemical Properties of Carbonyl Compounds. I. Enthalpies of Combustion, Vapour Pressures and Enthalpies of Sublimation and Enthalpies of Formation of 2-Methylpropanamide, 2,2-Dimethylpropanamide and 1-Adamantyl Carboxamide // J. Chem. Thermodyn. 1989. V.21.P. 859-865.
53. Acree W.E. Jr., Tucker S.A., Pilcher G., Chowdhary A., Ribeiro da Silva M.D.M., Monte M.J.S. Enthalpies of Combustion of 2,2',4,4',6,6'-Hexamethylazobenzene-A,A-dioxide, 2,2',6,6'-Tetramethylazobenzene-V,A-dio-xide, 2,4,6-Trimethylnitrobenzene, and 2,6-Dimethyl-nitrobenzene: the Dissociation Enthalpies of the N=N and N-O Bonds 11 J. Chem. Thermodyn. 1993. V. 25. P. 1253-1261.
54. Adriaanse N., Dekker H., Coops J. Heats of Combustion of Normal Saturated Fatty Acids and their Methyl Esters // Rec. Trav. Chim. Pays/Bas. 1965. V. 84. P. 393-407.
55. Ambrose D., Connett J.E., Green J.H.S., Hales J.L., Head A.J., Martin J.F. Thermodynamic Properties of Organic Oxygen Compounds. 42. Physical and Thermodynamic Properties of Benzaldehyde // J. Chem. Thermodyn. 1975. V. 7. P. 1143-1157.
56. An X., He J., Hu R. Study on the Electrostatic Interaction in Organic Chlorocompounds. Enthalpies of Combustion and Formation of 1,3- and 1,4-Dichlorobutanes 11 Ther-mochim. Acta. 1990. V. 169. P. 331-337.
57. Anderson C.M., Gilbert E.C. The Apparent Energy of the N-N Bond as Calculated from Heats of Combustion //J. Am. Chem. Soc. 1942. V. 64. P. 2369-2372.
58. Andon R.J.L., Biddiscombe D.P., Cox J.D., Handley R., Harrop D., Herington E.F.G., Martin J.F. Thermodynamic Properties of Organic Oxygen Compounds. Part I. Preparation and Physical Properties of Pure Phenol, Cresols and Xylenols // J. Chem. Soc. 1960. P. 5246-5254.
59. Andon R.J.L., Cox J.D., Herington, E.F.G., Martin J.F. The Second Virial Coefficients of Pyridine and Benzene, and Certain of their Methyl Homologues П Trans. Faraday Soc. 1957. V. 53. P. 1074.
416
Новый справочник химика и технолога
60. Arshad М., Beg A. Correlation of the Physical Properties of Organophosphorus Compounds. Ill // Bull. Chem. Soc. Japan. 1967. V. 40. N 1. P. 15-18.
61. Aston J.G., Fink H.L., Janz G.J., Russell K.E. The Heat Capacity, Heats of Fusion and Vaporization, Vapor Pressures, Entropy and Thermodynamic Functions of Methyl Hydrazine // J. Am. Chem. Soc. 1951. V. 73. P. 1939-1943.
62. Aston J.G., Rock E.J., Isserow S. The Heats of Combustion of the Methyl Substituted Hydrazines and Some Observations on the Burning of Volatile Liquids // J. Am. Chem. Soc. 1952. V. 74. P. 2484-2486.
63. Aston J.G., Wood J.L., Zolki T.P. The Thermodynamic Properties and Configuration of Unsymmetrical Dimethylhydrazine // J. Am. Chem. Soc. 1953. V. 75. N 24. P. 6202-6204.
64. Aston J.G., Zolki T.P., Wood J.L. The Thermodynamic Properties and Configuration of Trimethylhydrazine Identification and Correction for a Major Impurity // J. Am. Chem. Soc. 1955. V. 77. P. 281-284.
65. Baccanari D.P., Novinski J.A., Pan Y., Yevitz M.M., Swain H.A. Jr. Heats of Sublimation and Vaporization at 25 °C of Long Chain Fatty Acids and Methyl Esters // Trans. Faraday Soc. 1968. V. 64. P. 1201.
66. Badoche M.M. Determinations des Chaleurs de Combustion de Derives Nitres de la Serie Benzenique // Bull. Soc. Chim. France. 1939. V. 6, N 5. P. 570-579.
67. Barnes D.S., Pilcher G. Enthalpies of Combustion of Ethanamide, Propanamide and Butanamide //.J. Chem. Thermodyn. 1975. V. 7. P. 377-382.
68. Baroody E.E., Carpenter G.A. Heats of Formation of Propellant Compounds (U), Rpt. Naval Ordnance Systems Command Task N 331-003/067-1/UR2402-001 for Naval Ordance Station // Indian Head. MD. 1972. P. 1-9.
69. Bastos M., Nilsson S.O., Ribeiro da Silva M.D.M.C., Ribeiro da Silva M.A.V., Wadso I. Thermodynamic Properties of Glycerol Enthalpies of Combustion and Vaporization and the Heat Capacity at 298,15 K. Enthalpies of Solution in Water at 288,15, 298,15 and 308,15 К 11 J. Chem. Thermodyn. 1988. V. 20. P. 1353-1359.
70. Beak P., Lee J.-K., Zeigler J.M. Equilibration Studies: Amide-imidate and Thioamide-thioimidate Functions // J. Org. Chem. 1978. V. 43. P. 1536-1538.
71. Bedford A.F., Edmondson, P.B., Mortimer C.T. Heats of Formation and Bond Energies. Part VI. и-Buty-lisobutyraldimine, и-Butylisobutylamine, Pyrazole and Imidazole // J. Chem. Soc. 1962. P. 2927-2931.
72. Bedford A.F., Mortimer C.T. Heats of Formation and Bond Energies. Part II // J. Chem. Soc. 1960. P. 1622— 1624.
73. Benson S.W., Quickshank F.R., Golden D.M., Haugen G.R., O'Neal H.E., Rodgers A.S., Shaw R., Walsh R. Additivity Rules for the Estimation of Thermochemical Properties // Chemical Reviews. 1969. V. 69, N 3. P. 279-324.
74. Biddiscombe D.P., Handley R., Harrop D., Head A.J., Lewis G.B., Martin J.F., Sprake C.H.S. Thermodynamic Properties of Organic Oxygen Compounds. Part XIII. Preparation and Physical Properties of Pure Ethylphenols // J. Chem. Soc. 1963. P. 5764-5768.
75. Birr K.H. Bildungswarmen von Triphenylarsine und Triphenylwismut// Z. Anorg. Allge. Chem. 1961. Bd. 311, N 1-2. S. 92-96.
76. Bjellerup L., Smith L. Heats of Combustion of Some Organic Chlorocompounds 11 Kgl. Fysiograph. Sall-skap. Lund Forh. 1954. V. 24. P. 1-13.
77. Bretschneider E., Rogers D.W. A New Microcalorimeter: Heats of Hydrogenation of Four Monoolefins // Mikrochim. Acta. 1970. P. 482 490.
78. Browne C.C., Rossini F.D. Heats of Combustion, Formation, and Isomerization of the cis- and /rans-Isomers of Hexahydroindan // J. Phys. Chem. 1960. V. 64. P. 927-931.
79. Bqckley E., Cox J.D. Chemical Equilibria. Part 2. Dehydrogenation of Propanol and Butanol // Trans. Faraday Soc. 1967. V. 63. P. 895-01.
80. Buckley E., Herington E.F.G. Equilibria in Some Secondary Alcohol + Hydrogen + Ketone Systems // Trans. Faraday Soc. 1965. V. 61. P. 1618-1625.
81. Burlot E. Etude Relative a la Calorimetrie des Ex-plosifs 11 Mem. Poudres. 1939. V. 29. P. 226-260.
82. Bystrm K., Mansson M. Enthalpies of Formation of Some Cyclic 1,3- and 1,4-Di- and polyethers: Thermochemical Strain in the -O-C-O- and -O-C-C-O-groups // J. Chem. Soc. Perkin Trans. 1982. V. 2. P. 565.
83. Carson A.S., Skinner H.A. Carbon-halogen Bond Energies in the Acetyl Halides // J. Chem. Soc. 1949. P. 936-939.
84. Cass R.C., Fletcher S.E., Mortimer C.T., Quincey P.G., Springall H.D. Heats of Combustion and Molecular Structure. Part IV. Aliphatic Nitroalkanes and Nitric Esters//J. Chem. Soc. 1958. P. 958-962.
85. Cass R.C., Fletcher S.E., Mortimer C.T., Springall H.D., White T.R. Heats of Combustion and Molecular Structure. Part V. The Mean Bond Energy Term for the C-0 Bond in Ethers, and the Structures of Some Cyclic Ethers//J. Chem. Soc. 1958. P. 1406-1410.
86. Chao J., Rossini F.D. Heats of Combustion, Formation, and Isomerization of Nineteen Alkanols // J. Chem. Eng. Data. 1965. V. 10. P. 374-379.
87. Chao J., Zwolinski BJ. Ideal Gas Thermodynamic Properties of Propanone and 2-Butanone // J. Phys. Chem. Ref. Data. 1976. V. 5. P. 319-328.
88. Chamley T., Mortimer C.T., Skinner H.A. The Thermochemistry of Organoarsenic Compounds. Part II. Esters of Arsenious Acid // J. Chem. Soc. 1953. N 4. P.1181-1184.
89. Chase M.W. Jr. NIST-JANAF Themochemical Tables. Fourth Edition // J. Phys. Chem. Ref. Data. Monograph 9. 1998. P. 1951.
90. Chemick C.L., Pedley J.D., Skinner H.A. Thermochemistry of Organophosphorus Compounds. Part III /7 J. Chem. Soc. 1957. P. 1851-1853.
Физические свойства важнейших веществ
417
91. Ciocazanu I., Dogaru V., Zavoianu D. Structure and Reactivity of Amides. Concerning the Heats of Combustion and Formation of Some Unsaturated Amides Derived from Acetamide П Rev. Chim. (Bucharest). 1976. V. 27. P. 4-6.
92. Chirico R.D., Hossenlopp I.A., Nguyen A., Steele W.V., Gammon B.E. The Thermodynamic Properties of 4-Methylphenanthrene // J. Chem. Thermodyn. 1989. V.21. P. 179-201.
93. Chirico R.D., Knipmeyer S.E., Nguyen A., Steele W.V. The Thermodynamic Properties to the Temperature 700 К of Naphthalene and of 2,7-Dimethylnaphthalene П J. Chem. Thermodyn. 1993 V. 25. P. 1461-1494.
94. Clark L.B., Peschel G.G., Tinoco I. Jr. Vapor Spectra and Heats of Vaporization of Some Purine and Pyr-midine Bases// J. Phys. Chem. 1965. V. 69. P. 3615.
95. Cole L.G., Gilbert E.C. The Heats of Combustion of Some Nitrogen Compounds and the Apparent Energy of the N-N Bond 11 J. Am. Chem. Soc. 1951. V. 73. P. 5423-5427.
96. Coleman D.J., Pilcher G. Heats of Combustion of Biphenyl, Bibenzyl, Naphthalene, Anthracene and Phenanthrene // Trans. Faraday Soc. 1966. V. 62. P. 821-827.
97. Colomina M., Jimenez P., Roux M.V., Turrion C. Thermochemical Properties of Naphthalene Derivatives. V. Formation Enthalpies of 2,3-Dimethylna-phthalene and 2,3-Dihydroxynaphthalene П An. Quim. 1979. V. 75. P. 620-624.
98. Colomina M., Pell A.S., Skinner H.A., Coleman D.J. Heats of Combustion of Four Dialkylethers H Trans. Faraday Soc. 1965. V. 61. P. 2641.
99. Connett J.E. Chemical Equilibria 6. Measurement of Equilibrium Constants for the Dehydrogenation of 2-Methylpropan-l-ol by a Vapour-flow Technique 11 J. Chem. Thermodyn. 1975. V. 7. P. 1159-1162.
100. Connett J.E. Chemical Equilibria. Part III. Dehydrogenation of Pentan-l-ol, Pentan-2-ol and 3-Methylbutan-2-ol//J. Chem. Soc. A. 1970. P. 1284-1286.
101. Connett J.E. Chemical Equilibria. 5. Measurement of Equilibrium Constants for the Dehydrogenation of Propanol by a Vapour Flow Technique 11 J. Chem. Thermodyn. 1972. V. 4. P. 233-237.
102. Contineanu I., Wagner L., Stanescu L., Marchidan D.I. Combustion and Formation Enthalpies of o-Phe-nylenediamine, Urea and 2-Benzimidazolone // Rev. Roum. Chim. 1982. V. 27. P. 205-209.
103. Cox J.D. The Heats of Combustion of Phenol and the Three Cresols 11 Pure Appl. Chem. 1961. V. 2. P. 125— 128.
104. Cox J.D., Chailoner A.R., Meetham A.R. The Heats of Combustion of Pyridine and Certain of its Derivatives // J. Chem. Soc. 1954. P. 265-271.
105. Cox J.D., Gundry H.A. Heats of Combustion. Part II. The Six Lutidines 11 J. Chem. Soc. 1958. P. 1019-1022.
106. Cox J.D., Pilcher G., Thermochemistry of Organic and Organometallic Compounds. N. Y.: Academic Press., 1970. 636 p.
107. Cox J.D. The Second Virial Coefficients, Latent Heats of Vaporization and Heats of Formation of the Lutidines 11 Trans. Faraday Soc. 1960. V. 56. P. 959.
108. Dauben W.G., Rohr O. The Heat of Isomerization of the cis- and trans- Isomers of 9-Methyldecahydronaphtha-lene //J. Phys. Chem. 1960. V. 64. P. 283-284.
109. Davies J., Lacher J.R., Park J.D. Reaction Heats of Organic Compounds. Part 4. Heats of Hydrogenation of n- and Isopropyl Bromides and Chlorides П Trans. Faraday Soc. 1965. V. 61. P. 2413-2416.
110. Desai P.D., Wilhoit R.C., Zwolinski B.J. Heat of Combustion of Resorcinol and Enthalpies of Isomerization of Dihydroxybenzenes H J. Chem. Eng. Data. 1968. V. 13. P. 334-335.
111. Donovan T.M., Shomate C.H., McBride W.R. The Heat of Combustion of Tetramethyltetrazene and 1,1-Dimethylhydrazine 11 J. Phys. Chem. 1960. V. 64. P. 281-282.
112. Douslin D.R., Scott D.W., Good W.D., Osborn A.G. Thermodynamic Properties of Organic Compounds and Thermodynamic Properties of Fluids П Gov. Rep. Announce. Index U.S. 1976. V. 76. P. 97.
113. Draeger J.A. Chemical-thermodynamic Properties of Molecules that Undergo Inversion. II. The Methylanilines // J. Chem. Thermodyn. 1984. V. 16. P. 1067— 1073.
114. Dubois J.-E., Herzog H. Heats of Formation of Aliphatic Ketones: Structure Correlation Based on Environment Treatment H J. Chem. Soc. Chem. Commun. 1972. P. 932-933.
115. Engel P.S., Owens W.H., Wang C. The Heat of Oxidation of 1,2-Di-w-butylhydrazine to Azo-w-butane П J. Phys. Chem. 1993. V. 97. P. 10486-10488.
116. Evans D.P., Davies W.C., Jones W.J. The Lower Try-alkil-or/o-phosphates. Part I // J. Chem. Soc. 1930. P. 1310-1313.
117. Evans F.W., Fairbrother D.M., Skinner H.A. The Heats of Combustion of Organic Compounds of Nitrogen. Part 3. Butylamines and the cA-Dimer of Nitrosoisobutane // Trans. Faraday Soc. 1959. V. 55. P. 399-403.
118. Evers E.C., Street E.H., Jung S.L. The Alkali Metal Phosphides. II. Certain Chemical Properties of Tetrasodium Diphosphide// J. Am. Chem. Soc. 1951. V. 73, N 11. P. 5088-5091.
119. Fenwick J.O., Harrop D., Head A.J. Thermodynamic Properties of Organic Oxygen Compounds. 41. Enthalpies of Formation of Eight Ethers П J. Chem. Thermodyn. 1975. V. 7. P. 943-954.
120. Fenwick J.O., Harrop D., Head A.J. Thermodynamic Properties of Organic Oxygen Compounds. 46. Enthalpies of Formation of Ethyl Acetate and 1-Hexanoix Acid H J. Chem. Thermodyn. 1978. V. 10. P. 687-690.
121. Finke H.L., Hossenlopp I.A., Berg W.T. 1-Pentanethiol: Heat of Vaporization and Heat Capacity of the Vapor H J. Phys. Chem. 1965. V. 69. P. 3030.
418
Новый справочник химика и технолога
122. Finke H.L., Messerly J.F., Todd S.S. Thermodynamic Properties of и-Propyl-, «-Butyl- and «-Decylsubstituted Cyclohexane from 10 to 370 К // Ber. BunsenGes.Phys. Chem. 1965. V. 69. S.2094.
123. Finch A., Gardner P.J., Hussain V.S., Melaugh R.A. The Standard Enthalpies of Combustion and Formation of Crystalline Phenilphosphonic, Phenil-phosphinic and Diphenilphosphinic acids // J. Chem. Thermodynamics. 1975. V. 7, N. 9. P. 881-886.
124. Finch A., Payne J. Thermochemistry of Nitroresorcinols. I. 2,4,6-Trinitroresorcinol (styphnic acid) // Thermochim. Acta. 1990. V. 170. P. 209-212.
125. Fletcher S.E., Mortimer C.T., Springall H.D. Heats of Combustion and Molecular Structure. Part VII. 1,3-Dioxa-and 1,3,5-Trioxacycloalkanes // J. Chem. Soc. 1959. P. 580-584.
126. Fletcher R.A., Pilcher G. Measurements of Heats of Combustion by Flame Calorimetry. Part 7. Chloromethane, Chloroethane, 1-Chloropropane, 2-Chloro-propane 11 Trans. Faraday Soc. 1971. V. 67. P. 3191— 3201.
127. Fraser F.M., Prosen E.J. Heats of Combustion of Liquid «-Hexadecane, 1-Hexadecene, «-Decylbenzene, «-Decylcyclohexane, «-Decylcyclopentane and the Variation of Heat of Combustion with Chain Length // J. Res. NBS. 1955. V. 55. P. 329-333.
128. Freeman B., Bagby M.O. Heats of Combustion of Fatty Esters and Triglycerides // J. Am. Oil Chem. Soc. 1989. V. 66. P. 1601-1605.
129. Fuchs R., Peacock L.A. Heats of Vaporization of Monoalkylcyclohexanes by the Gas Chromatographycalorimetry Method // Can. J. Chem. 1978. V. 56. P. 2493-2496.
130. Frisch M.A., Barker C., Margrave J.L., Newman M.S. Strain Energies in Hydrocarbons from Heats to Combustion. I. 4,5-and 2,7-Dimethylphenanthrenes, 1,12-and 5,8-Benzo(c)phenanthrenes and Г,9- and 3',6-Benzanthracenes 11 J. Am. Chem. Soc. 1963. V. 85. P. 2356-2357.
131. Furukawa J., Sakiyama M., Seki S., Saito Y., Kusano K. Standard Enthalpies of Combustion and Vaporization of MA-dimethylaniline // Bull. Chem. Soc. Jpn. 1982. V. 55. P. 3329-3330.
132. Gardner P.J., Hussain K.S. The Standard Enthalpies of Formation of Some Aliphatic Diols // J. Chem. Thermodyn. 1972. V. 4. P. 819-827.
133. Gamer W.E., Abernethy C.L. Heats of Combustion and Formation of Nitrocompounds. Part I. Benzene, Toluene, Phenol and Methylaniline Series // Proc. Roy. Soc. London A. 1921. P. 213-235.
134. Geiseler V.G., Quitzsch K., Rauh H.J., Schaffemicht H., Walther HJ. Bildungsenthalpien und Mesomerieener-gien von A-Bindungssystemen. 1. Mitteilung: Bildungsenthalpien und Mesomerieenergien Einiger Mehrkemiger Aromaten und Verschiedener Pseudoazulene H Ber. BunsenGes. Phys. Chem. 1966. Bd. 70. S. 551-556.
135. Geiseler V.G., Ratzsch M. Bildungsenthalpien Stel-lungsisomerer «-Alkanderivate. 1. Mitteilung: Bildungsenthalpien des Octanals und der Drei Isomeren Octanone // Ber. BunsenGes. Phys. Chem. 1965. Bd. 69. S. 85-88.
136. Glaser F., Ruland H. Untersuchungsen der Dampfdruckkurven und Kritische Daten Einiger Tech-nisch Wichtiger Organischer Substanzen // Chem. Ing. Techn. 1957. V. 29. P. 772.
137. Gollis M.H., Belenyessy L.I., Gudzinowicz B.J., Koch S.D., Smith J.O., Wineman RJ. Evaluation of Pure Hydrocarbons as jet Fuels // J. Chem. Eng. Data. 1962. V. 7. P. 316-331.
138. Good W.D. The Enthalpies of Combustion and Formation of 1,8-Dimethylnaphthalene, 2,3-Dimethylna-phthalene, 2,6-Dimethylnaphthalene and 2,7-Dimethyl-naphthalene // J. Chem. Thermodyn. 1973. V. 5. P. 715— 720.
139. Good W.D. Enthalpies of Combustion and Formation of 11 Isomeric Nonanes 11 J. Chem. Eng. Data. 1969. V. 14. P. 231-235.
140. Good W.D. Enthalpies of Combustion of Nine Organic Nitrogen Compounds Related to Petroleum // J. Chem. Eng. Data. 1972. V. 17. P. 28-31.
141. Good W.D. Enthalpies of Combustion of 18 Organic Sulfur Compounds Related to Petroleum // J. Chem. Eng. Data. 1972. V. 17. P. 158-162.
142. Good W.D. The Standard Enthalpies of Combustion and Formation of «-Butylbenzene, the Dimethylethylbenzenes and the Tetramethylbenzenes in the Condensed State //J. Chem. Thermodyn. 1975. V. 7. P. 49-59.
143. Good W.D., Lacina J.L., McCullough J.P. Methanethiol and Carbon Disulfide: Heats of Combustion and Formation by Rotating-bomb Calorimetry // J. Phys. Chem. 1961. V. 65. P. 2229-2231.
144. Good W.D., Smith N.K. The Enthalpies of Combustion of the Isomeric Pentenes in the Liquid State. A Warning to Combustion Calorimetrists about Sample Drying // J. Chem. Thermodyn. 1979. V. 11. P. 111-118.
145. Good W.D., Moore R.T. Enthalpies of Formation of Ethylenediamine, 1,2-Propanediamine, 1,2-Butane-diamine, 2-Methy 1-1,2-propanediamine and Isobutylamine C-N and N-F Thermochemical Bond Energies//}. Chem. Eng. Data. 1970. V. 15. P. 150-154.
146. Goodman LA., Wise P.H. Dicyclic Hydrocarbons. 11. 2-Alkylbicyclohexyls // J. Am. Chem. Soc. 1951. V. 73. P. 850-851.
147. Green J.H.S. Revision of the Values of the Heats of Formation of Normal Alcohols // Chem. Ind. (London). 1960. P. 1215-1216.
148. Guinchant MJ. Etude Sur la Fonction Acide Dans les Derives Metheniques et Methiniques // Ann. Chem. 1918. V. 10. P. 30-84.
149. Gundry H.A., Harrop D., Head A.J., Lewis, G.B. Thermodynamic Properties of Organic Oxygen Compounds. 21. Enthalpies of Combustion of Benzoic
Физические свойства важнейших веществ
419
Acid, Pentan- l-ol, Octan-l-ol and Hexadecan-l-ol 11 J. Chem. Thermodyn. 1969. V. 1. P. 321-332.
150. Guthrie J.P. Hydratation and Dehydratation of Phosphoric Acid Derivation. Free Energies of Formation of the Pentacoordinate Intermediates for Phosphate Ester Hydrolysis and Monomeric Metapnosphate П J. Am. Chem. Soc. 1977. V. 99. N 12. P. 3991-4001.
151. Guthrie J.P. Tautomerization Equilibria for Phosphorus Acid it's Ethyl Esters, Free Energies, and pKA Values for Ionization of the P-H Bond in Phosphoric and Phosphonic Esters // Can. J. Chem. 1979. V. 57, N 2. P. 236-239.
152. Guthrie J.P., Barker J., Cullimore P.A., Lu J., Pike D.C. The Tetrahedral Intermediate from the Hydration of A-Methylformanilide // Can. J. Chem. 1993. V. 71. P. 2111-2122.
153. Guthrie J.P., Cullimore P.A. Effect of the Acyl Substituent on the Equilibrium Constant for Hydration of Esters // Can. J. Chem. 1980. V. 58. P. 1281-1294.
154. Hall H.K. Jr., Baldt J.H. Thermochemistry of Strained-ring Bridgehead Nitriles and Esters // J. Am. Chem. Soc. 1971. V. 93. P. 140-145.
155. Handrick G.R. Report of the Study of Pure Explosive Compounds. Part IV. Calculation of Heat of Combustion of Organic Compounds from Structural Features and Calculation of Power of High Explosives. Rpt. C-58247 for the Office of the Chief of Ordnance, contract DA-19-020-ORD-47 by the Arthur D. Little. Inc. Cambridge. MA. 1956. P. 467-573.
156. Harrop D., Head A.J., Lewis G.B. Thermodynamic Properties of Organic Oxygen Compounds. 22. Enthalpies of Combustion of Some Aliphatic Ketones H J. Chem. Thermodyn. 1970. V. 2. P. 203-210.
157. Hartley S.B., Holmes W.S., Jaques J.K., Mole M.P., McCoubrey J.C. Thermochemical Properties of Phosphorus Compounds // Quart. Reviews Chem. Soc. 1963. V. 17. N 2. P. 204-223.
158. Hatton W.E., Hildenbrand D.L., Sinke G.C., Stull D.R. Chemical Thermodynamic Properties of Aniline П J. Chem. Eng. Data. 1962. V. 7. P. 229-231.
159. Hipsher H.F., Wise P.H. Dicyclic Hydrocarbons VIII. 1-Alkylnaphthalenes and Some of Their Tetrahydroderivatives // J. Am. Chem. Soc. 1954. V. 76. P. 1747— 1748.
160. Holcomb D.E., Dorsey C.L. Jr. Thermodynamic Properties of Nitroparaffins // Ind. Eng. Chem. 1949. V. 41. P. 2788-2792.
161. Hu A.T., Sinke G.C. Combustion Calorimetry of Some Chlorinated Organic Compounds // J. Chem. Thermodyn. 1969. V. l.P. 507-513.
162. Huckel W., Kamenz E., Gross A., Тарре W. Zur Kenntnis der Waldenschen Umkehrung // Ann. Chim. 1937. Bd. 533. S. 1—45.
163. Hubbard W.N., Good W.D., Waddington G. The Heats of Combustion, Formation and Isomerization of the Seven Isomeric C4Hi0S Alkane Thiols and Sulfides /7 J. Phys. Chem. 1958. V. 62. P. 614-617.
164. Hubbard W.N., Frow F.R., Waddington G. The Heats of Combustion and Formation of Pyridine and Hippu-ric Acid//J. Phys. Chem. 1961. V. 65. P. 1326-1328.
165. Hubbard W.N., Katz C., Waddington G. A Rotating Combustion Bomb for Precision Calorimetry. Heats of Combustion of Some Sulfur-containing Compounds I I J. Phys. Chem. 1954. V. 58. P. 142.
166. Hubbard W.N., Knowlton J.W., Huffman H.M. Combustion Calorimetry of Organic Chlorine Compounds. Heats of Combustion of Chlorobenzene, the Dichlorobenzenes and o- and p-Chloroethylbenzene 11 J. Phys. Chem. 1954. V. 58. P. 396.
167. Hubbard W.N., Waddington G. The Heat of Combustion, Formation and Isomerization of Propanethiol-l, Propanethiol-2 and 2-Thiabutane П Rec. Trav. Chim. Pays/Bas. 1954. V. 73. P. 910.
168. Johnson W.H., Prosen E.J., Rossini F.D. Heats of Combustion and Isomerization of the Eight C8H16 Alkylcyclohexanes 11 J. Res. NBS. 1947. V. 39. P. 49-52.
169. Johnson W.H., Prosen E.J., Rossini F.D. Heats of Combustion and Isomerization of the Six C7Hi4 Alkylcyclopentanes // J. Res. NBS. 1949. V. 42. P. 251-255.
170. Johnson W.H., Prosen E.J., Rossini F.D. Heats of Combustion and Isomerization of the Eight C9H12 Alkylbenzenes//J. Res. NBS. 1945. V. 35. P. 141-146.
171. Irving R.J. The Standard Enthalpy of Sublimation of Naphthalene 11 J. Chem. Thermodyn. 1972. V. 4. P. 793-794.
172. Issoire J., Long C. Etude de la Thermodynamique Chimi-que de la Reaction de Formation des Methylamines // Bull. Soc. Chim. France. 1960. P. 2004-2012.
173. Jimenez P., Roux M.V., Turrion C. Thermochemical Properties of A-Heterocyclic Compounds IV. Enthalpies of Combustion, Vapour Pressures and Enthalpies of Sublimation, and Enthalpies of Formation of 2-Methylimidazole and 2-Ethylimidazole and 2-Ethy-limidazole // J. Chem. Thermodyn. 1992. V. 24. P.1145-1149.
174. Kaarsemaker S., Coops J. Thermal Quantities of Some Cycloparaffins. Part HI. Results of measurements 11 Rec. Trav. Chim. Pays-Bas. 1952. V. 71. P. 261.
175. Knauth P., Sabbah R. Energetics of Intra- and Intermo-lecular Bonds in Alkanediols (II). Thermochemical Study of 1,2-Ethanediol, 1,3-Propanediol, 1,4-Buta-nediol and 1,5-Pentanediol at 298,15 К 11 Struct. Chem. 1990. V. 1. P. 43-46.
176. Kirkbride F.W. The Heats of Chlorination of Some Hydrocarbons and their Chloro-derivatives // J. Appl. Chem. 1956. V. 6. P. 11-21.
177. Kirklin D.R., Domalski E.S. Enthalpy of Combustion of Purine//J. Chem. Thermodyn. 1984. V. 16. P. 633-641.
178. Kirklin D.R., Domalski E.S. Enthalpy of Combustion of Adenine 11 J. Chem. Thermodyn. 1983. V. 15. P. 941-947.
179. Kirklin D.R., Domalski E.S. Energy of Combustion of Triphenilphosphale // J. Chem. Thermodyn. 1989. V. 21.N5. P. 449-456.
420
Новый справочник химика и технолога
180. Kirklin D.R., Domalski E.S. Enthalpies of Combustion of Triphenylphosphine and Triphenylphosphine Oxide // J. Chem. Thermodyn. 1988. V. 20. P. 743.
181. Kruif C.G. Enthalpies of Sublimation and Vapour Pressures of 11 Polycyclic Hydrocarbons // J. Chem. Thermodyn. 1980. V. 12. P. 243-248.
182. Kruif C.G., Oonk H.A.J. Enthalpies of Vaporization and Vapour Pressures of Seven Aliphatic Carboxylic Acids // J. Chem. Thermodyn. 1979. V. 11. P. 287-290.
183. Lacher J.R., Emery E., Bohmfalk E., Park J.D. Reaction Heats of Organic Compounds. IV. A High Temperature Calorimeter and the Hydrogenation of Methyl Ethyl and Vinyl Chlorides // J. Phys. Chem. 1956. V. 60. P. 492-495.
184. Lacher J.R., Walden C.H., Lea K.R., Park J.D. Vapor Phase Heats of Hydrobromination of Cyclopropane and Propylene //J. Am. Chem. Soc. 1950. V. 72. P. 331-333.
185. Lamneck J.H. Jr., Wise P.H. Dicyclic Hydrocarbons. IX. Synthesis and Physical Properties of the Monomethyldiphenylmethanes and Monomethyldicyclo-hexylmethanes // J. Am. Chem. Soc. 1954. V. 76. P. 1104-1106.
186. Lamneck J.H.Jr., Wise P.H. Dicyclic Hydrocarbons. X. Synthesis and Physical Properties of Some Propyl-and Butyldiphenylmethanes and 4-Isopropyldicyclo-hexylmethane // J. Am. Chem. Soc. 1954. V. 76. P. 3475-3476.
187. Lautsch W., Trober F., Zimmer W. et al. Energetische Daten des Metalloorganicher Verbindungen. I TeiL Verbrennugs und Bildungsenthalpien // Z. Chem. 1963. Bd. 3, N 11. S. 415-421.
188. Lemoult M.P. Recherches Theoriques et Experimentales sur les Chaleurs de Combustion et de Formation des Composes Organiques // Ann. Chim. Phys. 1907. V. 12. P. 395-432.
189. Lenchitz C., Velicky R.W., Silvestro G., Schlosberg L.P. Thermodynamic Properties of Several Nitrotoluenes // J. Chem. Thermodyn. 1971. V. 3. P. 689-692.
190. Loeffler S.M.C., Rossini F.D. Heats of Combustion and Formation of the Higher Normal Alkylcyclopentanes, Cyclohexanes, Benzenes and 1-Alkenes in the Liquid State at 25 °C // J. Phys. Chem. 1960. V. 64. P. 1530-1533.
191. Long L.H., Sackman J.F. The Heat of Formation of Trimethylarsine // Trans. Faraday Soc. 1956. V. 52, N9. P. 1201-1206.
192. Mackie H., Mayrick R.G. Studies in the Thermochemistry of Organic Sulfides. Part 2. The Gas-phase Heats of Formation of Ten Aliphatic Sulfides // Trans. Faraday Soc. 1962. V. 58. P. 230-237.
193. Magnus A., Hartmann H., Becker F. Verbren-nungswarmen und Resonanzenergien von Mehrkemi-gen Aromatischen Kohlenwasserstoffen // Z. Phys. Chem. 1951. Bd. 197. S. 75-91.
194. Majer V., Svoboda V. Enthalpies of Vaporization of Organic Compounds: A Critical Review and Data
Compilation. Oxford: Blackwell Scientific Publications, 1985. 300 p.
195. Mansson M. A Calorimetric Study of Peri Strain in 1,8-Dimethylnaphthalene and 1,4,5,8-Tetramethylnaphtha-lene // Acta Chem. Scand. Ser. B. 1974. V. 28. P. 677-680.
196. Mansson M. Enthalpies of Combustion and Formation of Ethyl Propionate and Diethyl Carbonate // J. Chem. Thermodyn. 1972. V. 4. P. 865-871.
197. Mansson M., Sellers P., Stridh G., Sunner S. Enthalpies of Vaporization of Some 1-Substituted «-Alkanes // J. Chem. Thermodyn. 1977. V. 9. P. 91.
198. Mathews J.H. The Accurate Measurement of Heats of Vaporization of Liquids // J. Am. Chem. Soc. 1926. V. 48. P. 562-576.
199. McCullough J.P., Finke H.L., Hubbard W.N., Todd S.S., Messerly J.F., Douslin D.R., Waddington G. Thermodynamic Properties of Four Linear Thioalkanes // J. Phys. Chem. 1961. V. 65. P. 784-791.
200. McCullough J.P., Finke H.L., Messerly J.F., Pennington R.E., Hossenlopp I.A., Waddington G. 3-Methyl-2-thiabutane: Calorimetric Studies from 12 to 500 K, the Chemical Thermodynamic Properties from 0 to 1000 КI I J. Am. Chem. Soc. 1955. V. 77. P. 6119-6125.
201. McCullough J.P., Hubbard W.N., Frow F.R., Hossenlopp I.A., Waddington G. Ethanethiol and 2-Thiapropane: Heats of Formation and Isomerization; the Chemical Thermodynamic Properties from 0 to 1000 К//J. Am. Chem. Soc. 1957. V. 79. P. 561-566.
202. McCullough J.P., Scott D.W., Finke H.L., Gross M.E., Williamson K.D., Pennington R.E., Waddington G., Huffman H.M. Ethanethiol (Ethylmercaptan): Thermodynamic Properties in the Solid, Liquid and Vapor States. Thermodynamic functions to 1000 К // J. Am. Chem. Soc. 1952. V. 74. P. 2801-2804.
203. McDougall L.A., Kilpatrick J.E. Entropy and Related Thermodynamic Properties of «-Valeric Acid // J. Chem. Phys. 1965. V. 42. P. 2307-2310.
204. Medard L. La Chaleur de Combustion de la Diphenylamine et L'energie de la Liaison N-N // J. Chem. Phys. 1955. V. 52. P. 467-472.
205. Medard L., Thomas M. Chaleur de Combustion de onze Substances Explosives ou Apparentees a des Ex-plosifs//Mem. Poudres. 1957. V. 39. P. 195-208.
206. Medard L., Thomas M. Determination des Chaleurs de Combustion de Douze Composes Organiques Utilises Dans les Poudres et Enplosies // Mem. Poudres. 1952. V. 34. P. 421-442.
207. Metzger R.M., Kuo C.S., Arafat E.S. A Semi-micro Rotating-bomb Combustion Calorimeter // J. Chem. Thermodyn. 1983. V. 15. P. 841-851.
208. Miles C.B., Hunt H. Heats of Combustion. I. The Heat of Combustion of Acetone // J. Phys. Chem. 1941. V. 45. P. 1346-1359.
209. Montgomery R.L., Rossini F.D., Mansson M. Enthalpies of Combustion, Vaporization, and Formation of Phenylbenzene, Cyclohexylbenzene and Cyclohexyl
Физические свойства важнейших веществ
421
cyclohexane; Enthalpy of Hydrogenation of Certain Aromatic Systems 11 J. Chem. Eng. Data. 1978. V. 23. P. 125-129.
210. Moore G.E., Parks G.S. New Thermodynamic Data for the Cyclohexane—Methylcyclopentane Isomerization // J. Am. Chem. Soc. 1939. V. 61. P. 2561-2562.
211. Moore G.E., Renquist M.L., Parks G.S. Thermal Data on Organic Compounds. XX. Modem Combustion Data for Two Methylnonanes, Methyl Ethyl Ketone, Thiophene and Six Cycloparaffins // J. Am. Chem. Soc. 1940. V. 62. P. 1505-1507.
212. Mosselman C., Dekker H. Enthalpies of Formation of и-Alkan-l-ols 11 J. Chem. Soc. Faraday Trans. 1975. V. 1. P. 417-424.
213. Murrin J.W., Goldhagen S. Determination of the C-0 Bond Energy from the Heats of Combustion of Four Aliphatic Ethers H NAVORD Report N 5491. U.S. Naval Powder Factory Res. & Dev. Dept. 1957. P. 1-14.
214. Moureu C., Andre E. Thermochimie des Composes Acety-leniques//Ann. Chim. Phys. 1914. V. 1. P. 113-145.
215. Nabavian P.M., Sabbah R., Chastel R., Laffitte M. Thermodynamique de Composes Azotes. II. Etude Thermochimique des Acides Aminobenzoiques, de la Pyrimidine, de L'uracile et de la Thymine П J. Chim. Phys. 1977. V. 74. P. 115-126.
216. Neale E., Williams L.T.D. The Thermochemistry of Organic Phosphorus Compounds. Part I. Heats of Hydrolysis and Oxidation // J. Chem. Soc. 1955. P. 2485-2490.
217. Neale E., Williams L.T.D., Moors V.T. The Thermochemistry of Organic Phosphorus Compounds. Part 11. Ester and Anilide Formation from Halides and Combustion of Anilides // J. Chem. Soc. 1956. P. 422^127.
218. Nesterova T.N., Rozhnov A.M., Malova T.N., Kov-zel E.N. Molar Enthalpies of Formation of Isopropylchlorobenzenes Derived from Equilibrium Measurements 11 J. Chem. Thermodyn. 1985. V. 17. P.649-656.
219. Nicholson G.R. The Heats of Combustion of Butanal and Heptanal 11 J. Chem. Soc. 1960. P. 2377-378.
220. Osborn A.G., Douslin D.R. Vapor Pressure and Derived Enthalpies of Vaporization for Some Condensed Ring Hydrocarbons 11 J. Chem. Eng. Data. 1975. V. 20. P. 229-231.
221. Parks G.S., West T.J., Naylor B.F., Fujii P.S., McClaine L.A. Thermal Data on Organic Compounds. XXIII. Modem Combustion Data for Fourteen Hydrocarbons and Five Polyhydroxy Alcohols // J. Am. Chem. Soc. 1946. V. 68. P. 2524-2527.
222. Parks G.S., Manchester K.E. The Heats of Solution of Erythritol, Mannitol and Dulcitol; Combustion Values for Liquid Polyhydroxy Alcohols // J. Am. Chem. Soc. 1952. V. 74. P. 3435-34.
223. Parks G.S., Manchester K.E., Vaughan L.M. Heats of Combustion and Formation of Some Alcohols, Phenols and Ketones 11 J. Chem. Phys. 1954. V. 22. P. 1089-1090.
224. Patent N 3.113.425 to Monsanto Research Corp. Everett, MA, USA. Ortho-substituted Bicyclohexyl Hydrocarbons as High Energy fuels / J.O. Smith, K.W. Easley. 12.10.63. 1963.
225. Pedley J.B., Naylor R.D., Kirby S.P. Thermochemical Data of Organic Compounds. N. Y.: Chapman and Hall, 1986. 792 p.
226. Pell A.S., Pilcher G. Measurements of Heats of Combustion by Flame Calorimetry. Part 3. Ethylene Oxide, Trimethylene Oxide, Tetrahydrofuran and Tetrahydropyran // Trans. Faraday Soc. 1965. V. 61. P. 71-77.
227. Pennington R.E., Kobe K.A. The Thermodynamic Properties of Acetone // J. Am. Chem. Soc. 1957. V. 79. P. 300-305.
228. Pennington R.E., Scott D.W., Finke H.L., McCullough J.P., Messerly J.F., Hossenlopp I.A., Waddington G. The Chemical Thermodynamic Properties and Rotational Tautomerism of 1-Propanethiol // J. Am. Chem. Soc. 1956. V. 78. P. 3266-3272.
229. Perrottet E., Taub W., Briner E. Sur Etats Energeti-ques Comparatifs des Noyaux Azulenique et Naph-talenique // Helv. Chim. Acta. 1940. Bd. 23. S. 1260— 1268.
230. Pihlaja K., Heikkila J. Enthalpies of Formation of Cyclic Acetals, 1,3-Dioxolane, 2-Methyl-l,3-dioxolane, and 2,4-Dimethyl-l,3-dioxolanes 11 Acta Chem. Scand. 1969. V. 23. P. 1053-1055.
231. Pihlaja K., Heikkila J. Heats of Formation of Cyclic Vinyl Ethers. A Correction H Suom. Kemistilehti. 1972. P. 148.
232. Pihlaja K., Heikkila J. The Configurations of Isomeric 2,2,4,6-Tetramethyl-l,3-dioxanes 11 Acta Chem.
Scand. 1967. V. 21. P. 2430-2434.
233. Pihlaja K., Luoma S. Heats of Formation and Conformational Energies of 1,3-Dioxane and its Methyl Homologues П Acta Chem. Scand. 1968. V. 22. P. 2401-2414.
234. Pilcher G., Pell A.S., Coleman D.J. Measurements of Heats of Combustion by Flame Calorimetry. Part 2. Dimethyl Ether, Methyl Ethyl Ether, Methyl w-Propyl Ether, Methyl Isopropyl Ether H Trans. Faraday Soc. 1964. V. 60. P. 499-505.
235. Pilcher G., Skinner H.A., Pell A.S., Pope A.E. Measurements of Heats of Combustion by Flame Calorimetry. Part 1. Diethyl Ether, Ethyl Vinyl Ether and Divinyl Ether//Trans. Faraday Soc. 1963. V. 59. P. 316-330.
236. Pittam D.A., Pilcher G. Measurements of Heats of Combustion by Flame Calorimetry. Part 8. Methane, Ethane, Propane, «-Butane and 2-Methylpropane // J. Chem. Soc. Faraday Trans. 1.1972. V. 68. P. 2224-2229.
237. Prosen E.J., Rossini F.D. Heats of Combustion and Formation of the Paraffin Hydrocarbons at 25 °C // J. Res. NBS. 1945. V. 35. P. 263-267.
238. Prosen E.J., Gilmont R., Rossini F.D. Heats of Combustion of Benzene, Toluene, Ethylbenzene, o-Xylene, m-Xylene, ^-Xylene, «-Propylbenzene and Styrene // J. Res. NBS. 1945. V. 34. P. 65-70.
422
Новый справочник химика и технолога
239. Prosen E.J., Johnson W.H, Rossini F.D. Heats of Combustion and Formation at 25 °C of the Alkylbenzenes Through Ci0HI4 and of the Higher Normal Monoalkylbenzenes // J. Res. NBS. 1946. V. 36. P. 455-461.
240. Prosen E.J., Johnson W.H., Rossini F.D. Heats of Formation and Combustion of the Normal Alkylcyclopentanes and Cyclohexanes and the Increment per CH2 Group for Several Homologous Series of Hydrocarbons // J. Res. NBS. 1946. V. 37. P. 51-56.
241. Prosen E.J., Maron F.W., Rossini F.D. Heats of Combustion, Formation, and Insomerization of Ten C4 Hydrocarbons//J. Res. NBS. 1951. V. 46. P. 106-112.
242. Pushin N.A. Heats of Combustion and Heats of Formation of Isomeric Organic Compounds H Bull. Soc. Chim. Belg. 1954. V. 19. P. 531-547.
243. Redemann C.E., Chaikin S.W., Fearing R.B., Benedict D. The Volatility and Vapor Pressure of Nine Organic Arsines // J. Am. Chem. Soc. 1948. V. 70, N 2. P. 639-640.
244. Ribeiro da Silva M.A.V., Ribeiro da Silva M.D.M.C., Luisa M., Gomes A.C.N.; Johnson M., Pilcher G. Enthalpies of Combustion of Di-n-propylamine, Diisopropylamine, Diisobutylamine and Di-sec-butylamine // J. Chem. Thermodyn. 1997. V. 29. P. 1025-1030.
245. Ribeiro da Silva M.A.V., Matos M.A.R., do Rio C.M.A. Standard Molar Enthalpy of Formation of 2,4,6-Trimethylpyridine // J. Chem. Thermodyn. 1997. V. 29. P. 901-906.
246. Ribeiro da Silva M.A.V., Ribeiro da Silva M.D.M.C., Monteiro M.F.B.M., Gomes M.L.A.C.N., Chickos J.S., Smith A.P., Liebman J.F. Thermochemical Studies for Determination of the Molar Enthalpy of Formation of Aniline Derivatives // Struct. Chem. 1996. V. 7. P. 367-373.
247. Ribeiro da Silva M.A.V., Morais V.M.F., Matos M.A.R., Rio C.M.A., Piedade G.M.G.S. Thermochemical and Theoretical Study of Some Methyldiazines // Struct. Chem. 1996. V. 7. P. 329-336.
248. Ribeiro da Silva M.D.M.C., Ribeiro da Silva M.A.V., Pilcher G. Enthalpies of Combustion of the Three Trihydroxybenzenes and of 3-Methoxycatechol and 4-Nitrocatechol 11 J. Chem. Thermodyn. 1986. V. 18. P. 295-300.
249. Richardson J.W., Parks G.S. Thermal Data on Organic Compounds. XIX. Modem Combustion Data for Some Non-volatile Compounds Containing Carbon, Hydrogen and Oxygen // J. Am. Chem. Soc. 1939. V. 61. P. 3543-3546.
250. Rockenfeller J.D., Rossini F.D. Heats of Combustion, Isomerization and Formation of Selected C7, C8 and Сю Monoolefin Hydrocarbons // J. Phys. Chem. 1961. V. 65. P. 267-272.
251. Rogers D.W., Dagdagan O.A., Allinger N.L. Heats of Hydrogenation and Formation of Linear Alkynes and a Molecular Mechanics Interpretation // J. Am. Chem. Soc. 1979. V. 101. P. 671-676.
252. Rosenbaum E.J., Sandberg C.R. Vapor Pressures of Trimethylphosphine, Trimethylarsine and Trimethyl-stibine // J. Am. Chem. Soc. 1940. V. 62, N 6. P. 1622-1624.
253. Roth W.A., Meyer I. Einige Physikalisch-chemische Konstanten des Dioxans 11 Z. Electrochem. 1933. Pt. 39. P. 35-37.
254. Roth W.A., Rist-Schumacher E. Beitrag zur Thermo-chemie der Sulfonsauren und Saurechlorid // Z. Electrochem. 1944. V. 50. P. 7-9.
255. Roux M.V., Jimenez P., Davalos J.Z., Castano O., Molina M.T., Notario R., Herreros M., Abboud J.-L.M. The First Direct Experimental Determination of Strain in Neutral and Protonated 2-Azetidinone // J. Am. Chem. Soc. 1996. V. 118. P. 12735-12737.
256. Sabbah R., Buluku E.N.L.E. Thermodynamic Study of Three Isomers of Dihydroxybenzene // Can. J. Chem. 1991. V. 69. P. 481488.
257. Sato-Toshima T., Kamagughi A., Nishiyama K., Saki-yama M., Seki S. Enthalpies of Combustion of Organic Compounds. IV. Acetanilide and Nicotinic Acid // Bull. Chem. Soc. Japan. 1983. V. 56. P. 51-54.
258. Schjanberg E. Die Verbrennungswarmen und die Re-fraktionsdaten Einiger Chlorsubstituierter Fettsauren und Ester 11 Z. Phys. Chem. Abt. A. 1935. V. 172. P. 197-233.
259. Schjanberg E. Die Verbrennungswarmen und die Re-fraktionsdaten einiger pentensaureeste // Z. Phys. Chem. 1937. Bd. 178. S. 274-281.
260. Schuls P.S. Calor de Combustion del Heido n-De-kanofosfonico // Bol. Soc. quim. Peru. 1978. V. 44, N 2. P. 92-93.
261. Scott D.W., Berg W.T., Hossenlopp LA., Hubbard W.N., Messerly J.F., Todd S.S., Douslin, D.R., McCullough J.P., Waddington G. Pyrrole: Chemical Thermodynamic Properties //J. Phys. Chem. 1967. V. 71. P. 2263-2270.
262. Scott D.W., Finke H.L., McCullough J.P., Messerly J.F., Pennington R.E., Hossenlopp LA., Waddington G. 1-Butanethiol and 2-Thiapentane. Experimental Thermodynamic Studies between 12 and 500 K, Thermodynamic Functions by a Refined Method of Increments// J. Am. Chem. Soc. 1957. V. 79. P. 1062-1068.
263. Scott D.W., Finke H.L., Hubbard W.N., McCullough J.P., Oliver G.D., Gross M.E., Katz C., Williamson K.D., Waddington G., Huffman H.M. 3-Thiapentane: Heat Capacity, Heats of Fusion and Vaporization, Vapor Pressure, Entropy, Heat of Formation and Thermodynamic Functions // J. Am. Chem. Soc. 1952. V. 74. P. 4656-4662.
264. Scott D.W., Good W.D., Guthrie G.B., Todd S.S., Hossenlopp LA., Osborn A.G., McCullough J.P. Chemical Thermodynamic Properties and Internal Rotation of Methylpyridines. II. 3-Methylpyridine H J. Phys. Chem. 1963. V. 67. P. 685-689.
265. Scott D.W., Hubbard W.N., Messerly J.F., Todd S.S., Hossenlopp LA., Good W.D., Douslin D.R., McCullough J.P. Chemical Thermodynamic Properties and
Физические свойства важнейших веществ
423
Internal Rotation of Methylpyridines. I. 2-Methyl-pyridine // J. Phys. Chem. 1963. V. 67. P. 680-685.
266. Sinke G.C., Getting F.L. The Chemical Thermodynamic Properties of Methyl Ethyl Ketone // J. Phys. Chem. 1964. V. 68. P. 1354-1358.
267. Skinner H.A., Snelson A. The Heats of Combustion of the Four Isomeric Butylalcohols 11 Trans. Faraday Soc. 1960. V. 56. P. 1776-1783.
268. Smith L., Bjellerup L., Krook S., Westermark H. Heats of Combustion of Organic Chlorocompounds Determined by the «Quartz Wool» Method // Acta Chem. Scand. 1953. V. 7. P. 65.
269. Smith N.K., Gammon B.E., Good W.D. Thermodynamics of Organic Compounds // Gov. Rep. Announce. Index (U.S.). Avail. NTIS AD-A110430. 1982. V. 82. P. 2252.
270. Smith N.K., Good W.D. Enthalpies of Combustion and Formation of Propylamine, Isopropyl amine and tert-Butylamine // J. Chem. Eng. Data. 1967. V. 12. P. 572-574.
271. Snelson A., Skinner H.A. Heats of Combustion: sec-Propanol, 1,4-Dioxan, 1,3-Dioxan and Tetrahydropyran// Trans. Faraday Soc. 1961. V. 57. P. 2125-2131.
272. Speros D.M., Rossini F.D. Heats of Combustion and Formation of Naphthalene, the Two Methylnaphthalenes, cis- and trans- Decahydronaphthalene and Related Compounds//J. Phys. Chem. 1960. V. 64. P. 1723-1727.
273. Spitzer R., Huffman H.M. The Heats of Combustion of Cyclopentane, Cyclohexane, Cycloheptane and Cyclooctane // J. Am. Chem. Soc. 1947. V. 69. P. 211-213.
274. Steele W.V., Chirico R.D., Cowell A.B., Knipmeyer S.E., Nguyen A. Thermodynamic Properties and Ideal-gas Enthalpies of Formation for 2-Aminoisobutyric Acid (2-Methylalanine), Acetic Acid (4-Methyl-3-penten-2-one), 4-Methylpent-1-ene, 2,2'-Bis(phenylthio)propa-ne, and Glycidylphenyl Ether (l,2-Epoxy-3-phenoxypropane) // J. Chem. Eng. Data. 1997. V. 42. P. 1052— 1066.
275. Steele W.V., Chirico R.D., Nguyen A., Hossenlopp I.A., Smith N.K. Determination of Ideal-gas Enthalpies of Formation for key Compounds // Am. Inst. Chem. Eng. Symp. Ser. (AIChE Symp. Ser.) 1990. P. 138-154.
276. Steele W.V., Chirico R.D., Nguyen A., Hossenlopp I.A., Smith N.K. Determination of Some Pure Compound Ideal-gas Enthalpies of Formation 11 AIChE Symp. Ser. 1989. V. 85. P. 140-162.
277. Steele W.V., Chirico R.D., Knipmeyer S.E., Nguyen A., Smith N.K., Tasker I.R. Thermodynamic Properties and Ideal-gas Enthalpies of Formation for Cyclohexene, Phthalan (2,5-Dihydrobenzo-3,4-fiiran), Isoxazole, Octylamine, Dioctylamine, Trioctylamine, Phenylisocyanate, and 1,4,5,6-Tetrahydropyrimidine П J. Chem. Eng. Data. 1996. V. 41. P. 1269-1284.
278. Steele W.V., Chirico R.D., Nguyen A., Knipmeyer S.E. The Thermodynamic Properties of 2-Methylaniline and /ram-(7?,S)-Decahydroquinoline H J. Chem. Thermodyn. 1994. V. 26. P. 515-544.
279. Steele W.V., Chirico R.D., Nguyen A., Hossenlopp LA., Smith N.K. DIPPR PROJECT 871: Determination of Ideal-gas Enthalpies of Formation for Key Compounds: The 1989 Project Results // J. Chem. Thermodyn. 1991. P. 101-134.
280. Stephenson R.M., Malanowski S. Handbook of the Thermodynamics of Organic Compounds. N. Y.: Elsevier, 1987.
281. Stiehler R.D., Huffman H.M. Thermal Data. IV. The Heats of Combustion of Adenine, Hypoxanthine, Guanine, Xanthine, Uric Acid, Allantoin and Alloxan // J. Am. Chem. Soc. 1935. V. 57. P. 1734-1740.
282. Stridh G. Enthalpies of Formation of 1-Dodecene and 1-Hexadecene and the CH2-Increment in the 1-Alkene Series // J. Chem. Thermodyn. 1976. V. 8. P. 895-899.
283. Stridth G., Sunner S. Enthalpies of Formation of Some 1-Chloroalkanes and the CH2-Increment in the 1-Chloroalkanes Series // J. Chem. Thermodyn. 1975. V. 7. P. 161-168.
284. Sunner S. Corrected Heat of Combustion and Formation Values for a Number of Organic Sulfur Compounds // Acta Chem. Scand. 1963. V. 17. P. 728-730.
285. Sunner S., Svensson Ch., Zelepuga A.S. Enthalpies of Vaporization at 298,15 К for Some 2-Alkanoles and Methylalkanes // J. Chem. Thermodyn. 1979. P. 11; P. 491 495.
286. Suradi S., Hacking J.M., Pilcher G., Gumrukcu 1., Lappert M.F. Enthalpies of Combustion of Five Steri-cally Hindered Amines 11 J. Chem. Thermodyn. 1981. V. 13. P. 857-861.
287. Svensson Ch. Enthalpies of Vaporization of 1-Decanol and 1-Dodecanol and their Influence on the CH2-Increment for the Enthalpies of Formation // J. Chem. Thermodynam. 1979. V. 11. P. 593-596.
288. Swarts M.F. Sur la Chaleur de Formation de L'aniline et de Quelquesuns de ses Derives // Reel. Trav. Chim. Pays/Bas. 1909. V. 28. P. 155-165.
289. Текас V., Majer V., Svoboda V., Hynek V. Enthalpies of Vaporization and Cohesive Energies for Six Monochlorinated Alkanes // J. Chem. Thermodyn. 1981. V. 13. P. 659-662.
290. Tjebbes J. Heats of Combustion of Butannal and Some Related Compounds 11 Acta Chem. Scand. 1960. V. 14. P. 180-88.
291. Tjebbes J. Heats of Combustion of Propanal and 2-Methyl Propanal П Acta Chem. Scand. 1962. V. 16. P. 953-57.
292. Tjebbes J. The Heats of Combustion and Formation of the Three Diazines and Their Resonance Energies // Acta Chem. Scand. 1962. V. 16. P. 916-921.
293. Uchytilova V., Majer V., Svoboda V., Hynek V. Enthalpies of Vaporization and Cohesive Energies for Seven Aliphatic Ketones // J. Chem. Thermodyn. 1983. V. 15. P. 853-858.
294. Verkade P.E., Hartman H., Coops J. Calorimetric researches. X. Heats of Combustion of Successive Terms of Homologous Series: Dicarboxylic Acids of
424
Новый справочник химика и технолога
the Oxalic Acid Series // Rec. Trav. Chim. Pays/Bas. 1926. V. 45. P. 373-393.
295. Vriens G.N., Hill A.G. Equilibria of Several Reactions of Aromatic Amines // Ind. Eng. Chem. 1952. V. 44. P. 2732-27.
296. Wadso I. Enthalpies of Vaporization of Organic Compounds // Acta Chem. Scand. 1969. V. 23. P. 2061.
297. Wadso I. Heats of Vaporization of Organic Compounds II. Chlorides, Bromides and Iodides // Acta Chem. Scand. 1968. V. 22. P. 2438.
298. Wadso I. Thermochemical Properties of Diacetimide, A-Butyldiacetimide and /V-Phenyldiacetimide // Acta Chem. Scand. 1965. V. 19. P. 1079-1087.
299. Wagman D.D., Kilpatrick J.E., Pitzer K.S., Rossini F.D. Heats, Equilibrium Constants and Free Energies of Formation of the Acetylene Hydrocarbons Through the Pentynes to 1500 К // J. Res. NBS. 1945. V. 35. P. 467-496.
300. Westrum E.F. Jr., Wong S. Strain Energies and Thermal Properties of Globular and Polynuclear Aromatic Molecules // AEC Rept. Coo-1149-92. Contract AT(11-1)-1149. 1967. P. 1-7.
301. Wiberg K.B., Crocker L.S., Morgan K.M. Thermochemical Studies of Carbonyl Compounds. 5. Enthalpies of Reduction of Carbonyl Groups // J. Am. Chem. Soc. 1991. V. 113. P. 3447-3450.
302. Wiberg K.B., Waldron R.F. Lactones. 2. Enthalpies of Hydrolysis, Reduction and Formation of the C4-C13 Monocyclic Lactones, Strain Energies and Conformations//J. Am. Chem. Soc. 1991. V. 113. P. 7697-7705.
303. Wiberg K.B., Wasserman D.J. Enthalpies of Hydration of Alkenes. 1. The «-Hexenes // J. Am. Chem. Soc. 1981. V. 103. P. 6563-6566.
304. Wiberg K.B., Wasserman D.J., Martin E. Enthalpies of Hydration of Alkenes. 2. The п-Heptenes and «-Pentenes // J. Phys. Chem. 1984. V. 88. P. 3684-3688.
305. Wilson S.R., Watson I.D., Malcolm G.N. Enthalpies of Formation of Solid Cytosine, L-Histidine and Uracil // J. Chem. Thermodyn. 1979. V. 11. P. 911-912.
306. Wise C.H., Serijan K.T., Goodman LA. // NACA Technical Report 1003. 1951. P. 1-10.
307. Wrede F. Uber die Bestimmung von Berbren-nungswarmen Mittels der Kalorimetrischen Bombe unter Benutzung des Platinwiderstandsthermometers // Z. Phys. Chem. (Leipzig). 1911. S. 81-94.
308. Young J.A., Keith J.E., Stehle P., Dzombak W.C., Hunt H. Heats of Combustion of Some Organic Nitrogen Compounds // Ind. Eng. Chem. 1956. V. 48. P. 1375-1378.
309. Yost D.M., Osborne D.W., Gamer C.S. The Heat Capacity, Entropy and Heats of Transition, Fusion and Vaporization of Dimethylacetylene. Free Rotation in the Dimethylacetylene Molecule // J. Am. Chem. Soc. 1941. V. 63. P. 3492-3496.
310. Zaheeruddin M., Lodhi Z.H. Enthalpies of Formation of Some Cyclic Compounds // Phys. Chem. (Peshawar Pak.). 1991. V. 10. P. 111-118.
3.6.3. Термодинамические свойства насыщенных паров чистых веществ
Термодинамические свойства насыщенных паров чистых неорганических веществ (аммиака, воды, диоксидов серы и углерода, ртути, дисульфида углерода) приведены в табл. 3.6.6-3.6.11, органических веществ (метана, этана, пропана, бутана, изобутана, галогенпро-изводных углеводородов, диэтилового эфира и этилена) — в табл. 3.6.12-3.6.27.
Условные обозначения
Т — температура, °C; р — давление, МПа; v — удельный объем жидкости, л/кг; v' — удельный объем пара, м3/кг; р —- плотность жидкости, кг/л; р' — плотность пара, кг/м3; h — удельная энтальпия жидкости, кДж/кг (энтальпия жидкости при 0 °C принимается равной 0 или 100); h' — удельная энтальпия пара, кДж/кг; kvaph — удельная энтальпия парообразования, кДж/кг (&vaph = h' - h); s — удельная энтропия жидкости, кДж/(кг • К) (энтропия жидкости при 0 °C принимается равной 0 или 1); s' — удельная энтропия пара, кДж/(кг • К).
Курсивом выделены данные, относящиеся к критическому состоянию вещества.
Таблица 3.6.6
Термодинамические свойства насыщенного пара аммиака (NH3)
т Р V v' Р Р' h IT ^vaph s s'
-75 0,00773 1,387 12,85 0,731 0,0778 87,504 1563,8 1476,3 2,777 10,23
-70 0,01129 1,379 9,01 0,725 0,1110 108,44 1573 1464,5 2,88 10,09
-65 0,01613 1,390 6,45 0,719 0,1550 129,79 1582,2 1452,4 2,982 9,962
-60 0,02263 1,401 4,70 0,714 0,213 151,14 1591 1439,8 3,084 9,841
-55 0,03126 1,413 3,48 0,708 0,287 172,5 1599,8 1427,3 3,182 9,727
-50 0,04225 1,425 2,62 0,702 0,381 193,43 1608,1 1414,7 3,279 9,62
-45 0,05634 1,437 2,003 0,696 0,500 215,62 1616,5 1400,9 3,377 9,52
-40 0,07417 1,449 1,550 0,690 0,645 237,81 1624,9 1387,1 3,473 9,424
-35 0,09626 1,462 1,215 0,684 0,823 260 1632,9 1372,9 3,567 9,334
-30 0,1235 1,476 0,963 0,678 1,038 282,19 1640,8 1358,6 3,66 9,249
-25 0,1567 1,490 0,771 0,671 1,297 304,38 1648,3 1344 3,751 9,167
-20 0,1966 1,504 0,624 0,665 1,604 327,41 1655,9 1328,5 3,841 9,09
Физические свойства важнейших веществ
425
Окончание табл. 3.6.6
7' Р V v' Р Р' h h' ^vai>h 5 s'
-15 0,2442 1,519 0,509 0,659 1,97 350,02 1662,6 1312,6 3,929 9,015
-10 0,3005 1,534 0,418 0,652 2,39 372,63 1669,3 1296,7 4,016 8,944
-5 0,3667 1,550 0,347 0,645 2,88 395,65 1675,1 1279,5 4,102 8,876
0 0,4437 1,566 0,290 0,639 3,45 418,68 1681 1262,3 4,187 8,809
5 0,5329 1,583 0,244 0,632 4,11 441,71 1686,4 1244,7 4,271 8,746
10 0,6354 1,601 0,206 0,625 4,86 465,15 1691 1225,9 4,353 8,673
15 0,7525 1,619 0,175 0,618 5,72 488,6 1695,7 1207,1 4,435 8,624
20 0,8857 1,639 0,1494 0,610 6,69 512,46 1699,4 1187 4,515 8,566
25 1,0361 1,659 0,1283 0,603 7,80 536,33 1703,2 1166,9 4,595 8,509
30 1,2053 1,680 0,1107 0,595 9,03 560,19 1705,7 1145,5 4,675 8,454
35 1,3947 1,702 0,0969 0,588 10,43 584,9 1708,2 1123,3 4,753 8,399
40 1,606 1,726 0,0833 0,580 12,00 609,18 1709,9 1100,7 4,831 8,346
45 1,8401 1,750 0,0726 0,581 13,77 633,88 1710,7 1076,8 4,908 8,293
50 2,1005 1,777 0,0635 0,563 15,76 659 1711,1 1052,1 4,984 8,24
Таблица 3.6.7
Термодинамические свойства насыщенного пара воды (Н2О)
T Р V v' Р Р' h h' ^vaph 5 s'
0 0,000631 1,0001 206,3 0,9999 0,004847 0 2500,8 2500,8 0 9,1544
1 0,000678 1,0001 192,7 0,9999 0,005189 4,229 2502,5 2498,3 0,0155 9,1281
2 0,000729 1,0000 180,0 1,0000 0,005555 8,415 2504,5 2496,2 0,0306 9,1017
3 0,000783 1,0000 168,2 1,0000 0,005945 12,64 2506,2 2493,7 0,0456 9,0757
4 0,00084 1,0000 157,3 1,0000 0,006357 16,83 2508,3 2491,6 0,0611 9,0498
5 0,000901 1,0000 147,2 1,0000 0,006793 21,06 2510 2489,1 0,0762 9,0242
6 0,000966 1,0000 137,8 1,0000 0,007256 25,25 2511,7 2486,5 0,0913 8,9987
7 0,001035 1,0001 129,1 0,9999 0,007746 29,43 2513,8 2484,4 0,1063 8,9731
8 0,001108 1,0001 121,0 0,9999 0,008265 33,66 2515,4 2481,9 0,1214 8,9484
9 0,001185 1,0002 113,4 0,9998 0,008815 37,85 2517,1 2479,4 0,1365 8,9237
10 0,001268 1,0003 106,42 0,9997 0,009398 42,04 2519,2 2477,3 0,1511 8,8995
И 0,001355 1,0004 99,91 0,9996 0,01001 46,22 2520,9 2474,8 0,1658 8,8752
12 0,001448 1,0005 93,84 0,9995 0,01066 50,41 2523 2472,7 0,1805 8,8513
13 0,001546 1,0006 88,18 0,9994 0,01134 54,6 2524,6 2470,2 0,1951 8,8274
14 0,00165 1,0007 82,90 0,9993 0,01206 58,78 2526,7 2468,1 0,2098 8,804
15 0,001761 1,0009 77,97 0,9991 0,01282 62,97 2528,4 2465,6 0,2244 8,7806
16 0,001877 1,0010 73,38 0,9990 0,01363 67,16 2530,1 2463,1 0,2391 8,7571
17 0,002 1,0013 69,10 0,9988 0,01447 71,34 2531,8 2460,6 0,2533 8,7341
18 0,00213 1,0015 65,09 0,9986 0,01536 75,53 2533,4 2458,1 0,2675 8,7111
19 0,00227 1,0016 61,34 0,9984 0,01630 79,72 2535,5 2456 0,2818 8,6884
20 0,00241 1,0018 57,84 0,9982 0,01729 83,9 2537,2 2453,5 0,2964 8,6663
21 0,00257 1,0020 54,56 0,9980 0,01833 88,09 2538,9 2451 0,3107 8,6441
22 0,00273 1,0022 51,49 0,9978 0,01942 92,28 2541 2448,9 0,3249 8,6223
23 0,0029 1,0024 48,62 0,9976 0,02057 96,46 2542,6 2446,3 0,3391 8,6005
24 0,00308 1,0027 45,93 0,9973 0,02177 100,6 2544,7 2444,3 0,3529 8,5788
25 0,00327 1,0029 43,40 0,9971 0,02304 104,8 2546,4 2441,7 0,3672 8,557
26 0,00347 1,0023 41,03 0,9968 0,02437 109 2548,1 2439,2 0,381 8,5356
27 0,00368 1,0035 38,82 0,9965 0,02576 113,2 2550,2 2437,1 0,3948 8,5147
28 0,0039 1,0037 36,74 0,9963 0,02722 117,4 2551,9 2434,6 0,4091 8,4938
29 0,00414 1,0040 34,78 0,9960 0,02875 121,5 2553,9 2432,5 0,4229 8,4728
30 0,00438 1,0043 32,93 0,9957 0,03036 125,7 2555,6 2430 0,4367 8,4523
31 0,00464 1,0046 31,20 0,9954 0,03205 129,9 2557,3 2427,5 0,4505 8,4322
32 0,00491 1,0050 29,58 0,9950 0,03381 134,1 2559,4 2425,4 0,4643 8,4117
426
Новый справочник химика и технолога
Продолжение табл. 3.6.7
Т Р V v' Р Р' h /?' \vltph 5 5'
33 0,0052 1,0053 28,05 0,9947 0,03565 138,2 2561,1 2422,9 0,4777 8,3916
34 0,00549 1,0056 26,61 0,9944 0,03758 142,4 2562,7 2420,4 0,4911 8,3715
35 0,00581 1,0059 25,25 0,9941 0,03960 146,6 2564,8 2418,3 0,5049 8,3518
36 0,00614 1,0063 23,97 0,9937 0,04172 150,8 2566,5 2415,8 0,5183 8,3326
37 0,00648 1,0066 22,77 0,9934 0,04393 155 2568,2 2413,3 0,5321 8,3133
38 0,00684 1,0070 21,63 0,9930 0,04523 159,1 2570,3 2411,2 0,5455 8,2941
39 0,00722 1,0073 20,56 0,9927 0,04864 163,3 2572 2408,7 0,5589 8,2748
40 0,00762 1,0079 19,55 0,9922 0,05115 167,5 2573,6 2406.2 0,5723 8,256
41 0,00804 1,0082 18,60 0,9919 0,05376 213,5 2575,7 2404,1 0,5857 8,2371
42 0,00847 1,0086 17,70 0,9915 0,05649 175,8 2577,4 2401,5 0,5987 8,2187
43 0,00893 1,0090 16,85 0,9911 0,05935 180 2579,1 2399 0,6121 8,2003
44 0,0094 1,0094 16,04 0,9907 0,06234 184,2 2580,7 2396,5 0,6251 8,1818
45 0,0099 1,0098 15,28 0,9903 0,06545 188,4 2582.4 2394 0,6385 8,1638
46 0,01042 1,0103 14,56 0,9898 0,06868 192,6 2584,1 2391,5 0.6515 8,1458
47 0,01096 1,0107 13,88 0,9894 0,07205 196,7 2586,2 2389.4 0,6644 8,1278
48 0,01153 1,0112 13,23 0,9890 0,07557 200,9 618,1 2386,9 0,6778 8,0927
49 0,01213 1,0116 12,62 0,9885 0.07923 205,1 2589,5 2384,4 0,6908 8,0927
50 0,01274 1,0121 12,05 0,9881 0,08302 209,3 2591,6 2382,3 0,7038 8,0751
51 0,01339 1,0125 11.50 0,9876 0,08696 213,5 2593,3 2379,8 0,7168 8,0575
52 0,01406 1.0130 10,98 0,9872 0,09107 217,7 2595 2377,3 0,7293 8,0403
53 0,01477 1,0135 10,49 0,9857 0,09535 221,9 2597,1 2375.2 0,7423 8,0236
54 0,0155 1,0140 10,02 0,9862 0,09980 226 2598,7 2372,7 0,7549 8,0068
55 0,01626 1,0145 9,578 0,9857 0,1044 230,2 2600,4 2370,1 0,7679 7.9901
56 0,01706 1,0150 9,158 0,9852 0,1092 234,4 2602,5 2368,1 0,7804 7,9733
57 0,01789 1,0155 8,759 0,9847 0,1142 238,6 2604,2 2365,5 0,7934 7,9566
58 0,01875 1,0160 8,380 0,9842 0,1193 242,8 2605,9 2363 0,806 7,9403
59 0,01965 1,0166 8.020 0,9836 0,1247 246,9 2607,5 2360,5 0,8185 7.9244
60 0,02058 1,0171 7,678 0,9831 0,1302 251,1 2609,2 2358 0,8311 7,9084
61 0,02155 1,0177 7,352 0,9825 0,1360 255,3 2610,9 2355,5 0,8436 7,8925
62 0,02257 1,0182 8,042 0,9820 0,1420 259,5 2612,6 2353 0,8562 7,8766
63 0,02361 1,0187 6,748 0,9816 0,1482 263,7 2614,2 2350,5 0,8688 7,8607
64 0,0247 1,0193 6,468 0,9811 0,1546 267,9 2615,9 2264,2 0,8809 7,8452
65 0,02584 1,0199 6,201 0,9805 0,1613 272,1 2617,6 2345,4 0,8935 7,8297
66 0,02701 1,0204 5,947 0,9801 0,1682 276,2 2619,3 2342,9 0,9056 7,8147
67 0,02824 1,0210 5,705 0.9796 0,1753 280,4 2620,9 2340,4 0,9182 7,7996
68 0,02951 1,0216 5,474 0,9789 0,1827 276,2 2622,6 2337,9 0,9303 7,7845
69 0,03082 1,0222 5,254 0,9783 0,1903 288,8 2624,7 2335,8 0,9424 7,895
70 0,03219 1,0228 5,045 0,9777 0,1982 293 2626,4 2333,3 0,955 7,7544
71 0,03361 1,0234 4,846 0,9772 0,2064 297,2 2628,1 2330,8 0,9672 7,7397
72 0,03509 1,0240 4,655 0,9766 0,2148 301,4 2629,7 2328,3 0,9793 7,7251
73 0,03661 1,0246 4,473 0,9760 0,2236 305,6 2631,4 2325,8 0,9914 7,7104
74 0,03799 1,0252 4,299 0,9756 0,2326 309,8 2633,1 2323,3 1,0036 7,6962
75 0,03983 1,0258 4,133 0,9750 0,2420 314 2634,8 2320,7 1,0157 7,6819
76 0,04152 1,0264 3,975 0,9744 0,2516 318,2 2636,4 2318,2 1,0274 7,6677
77 0,04329 1,0270 3,824 0,9738 0,2615 322,3 2638,1 2315,7 1,0396 7,6535
78 0,0451 1,0277 3,679 0,9731 0,2718 326,6 2639,8 2313,2 1,0513 7,6392
79 0,04698 1,0283 3,541 0,9725 0,2824 330,8 2641,5 2310,7 1,0634 7,6254
80 0,04893 1,0290 3,409 0,9718 0,2933 334,9 2643,1 2308,2 1,0752 7,6116
81 0,05095 1,0296 3,282 0,9712 0,3047 339,1 2644,8 2305,7 1,0873 7,5978
82 0,05303 1,0303 3,161 0,9705 0,3164 343,4 2646,5 2303,2 1,099 7,5844
83 0,05519 1,0310 3,045 0,9699 0,3284 347,5 2648,2 2300,6 1,1108 7,571
84 0,0574 1,0317 2,934 0,9693 0,4508 351,7 2649,8 2298,1 1,1225 7,5572
85 0,0597 1,0324 2,828 0,9686 0,3536 356 2651,5 2295,6 1,1304 7,5438
86 0,0621 1,0331 2,625 0,9680 0,3668 360,1 2653,2 2293,1 1,1036 7,5304
Физические свойства важнейших веществ
427
Продолжение табл. 3.6.7
Т Р V v' Р Р' h h’ \vaph 5 s’
87 0,0646 1,0338 2,629 0,9673 0,3804 364,4 2654,8 2290,6 1,153 7,517
88 0,0671 1,0345 2,536 0,9666 0,3943 368,6 2656,5 2288,1 1,169 7,504
89 0,0697 1,0352 2,447 0,9660 0,4087 372,8 2657,8 2285,2 1,1807 7,491
90 0,0724 1,0359 2,361 0,9653 0,4235 377 2659,5 2282,6 1,1924 7,4785
91 0,0752 1,0366 2,279 0,9648 0,4388 383,1 2661,1 2280,1 1,2037 7,4659
92 0,0781 1,0373 2,200 0,9641 0,4545 385,4 2663,2 2277,6 1,2154 7,4533
93 0,0811 1,0381 2,125 0,9633 0,4706 389,6 2664,9 2275,1 1,2272 7.4408
94 0,0842 1,0388 2,052 0,9627 0,4873 393,8 2666,6 2272,6 1,2389 7,4282
95 0,0873 1,0396 1,982 0,9619 0,5045 398 2667,8 2269,7 1,2502 7,4157
96 0,0906 1,0404 1,915 0,9611 0,522 402,2 2669,5 2267,2 1,2615 7,4031
97 0,094 1,0412 1,851 0,9604 0,5403 406,5 2671,2 2264,6 1,2732 7,3905
98 0,0974 1,0419 1,789 0.9598 0,5590 410,7 2672,9 2262,1 1,2845 7,3784
99 0,101 1,0427 1,730 0,9591 0,5781 414,9 2674,1 2259,2 1,2958 7,3663
100 0,1047 1,0435 1,673 0,9584 0,5977 419,1 2675,8 2256,7 1,3071 7,3545
101 0,1085 1,0443 1,618 0,9576 0,6180 423,3 2677,5 2254,2 1,3184 7,3428
102 0,1124 1,0451 1,565 0,9569 0,6389 427,6 2678,7 2251,2 1,3297 7,3311
103 0,1164 1,0458 1,515 0,9562 0,6602 431.7 2680,4 2248,7 1,3406 7,3194
104 0,1206 1,0466 1,466 0,9555 0,6821 436 2681,6 2245,8 1,3519 7,3076
105 0,1248 1,0474 1,419 0,9548 0,7047 440,2 2683,3 2243,3 1,3632 7,2959
106 0,1292 1,0482 1,374 0,9540 0,7278 444,4 2685,4 2240,8 1,3745 7,2842
107 0,1337 1,0490 1,331 0,9533 0,7514 448,7 2686,7 2237,8 1,3854 7,2725
108 0,1383 1,0498 1,289 0,9525 0,7757 452,9 2688,3 2235,3 1,3967 7,2612
109 0,1431 1,0507 1,249 0,9517 0,8007 457,1 2689,6 2232,4 1,4076 7,2499
110 0,148 1,0515 1,210 0,9510 0,8263 461,3 2691,3 2229,9 1,4185 7,2386
111 0,1531 1,0523 1,173 0,9503 0,8525 465,6 2692,9 2227,4 1,4298 7,2273
112 0,1582 1,0531 1,137 0,9496 0,8794 469,8 2694,2 2224,4 144,07 7,2159
113 0,1636 1,0540 1,102 0,9488 0,9070 474 2695,9 2221,9 1,4516 7,2051
114 0,1691 1,0549 1,069 0,9479 0,9354 478,3 2697,1 2219 1,4624 7,1942
115 0,1747 1,0558 1,037 0,9472 0,9647 482,5 2698,8 2216,5 1,4733 7,1833
116 0,1804 1,0566 1,005 0,9465 0,9950 486,8 2700,5 2213,6 1,4842 7,1724
117 0,1864 1,0575 0,9756 0,9457 1,025 491 2702,2 2211 1,4951 7,1615
118 0,1925 1,0584 0,9466 0.9449 1,056 495,2 2288,9 2208,1 1,506 7,1506
119 0,1987 1,0593 0,9186 0,9441 1,089 499,5 2704,7 2205,2 1,5169 7,1398
120 0,2051 1,0603 0,8917 0,9431 1,122 503,7 2706,3 2202,7 1,5278 7,1289
121 0,2117 1,0612 0,8658 0,9423 1,155 507,9 2708 2200,2 1,5386 7,1184
122 0,2185 1,0621 0,8407 0,9416 1,189 512 2709,3 2197,2 1,5495 7,1092
123 0,2254 1,0630 0,8164 0,9407 1,225 516,2 2710,5 2194,3 1,56 7,0987
124 0,2325 1,0639 0,7930 0,9400 1 П4 1 1 1 520,8 2712,2 2191,4 1,5709 7,0883
125 0,2398 1,0649 0,7704 0,9391 1,298 525 2713,5 2188,4 1,5814 7,0778
126 0,2473 1,0658 0,7485 0,9383 1,336 529,2 2714,7 2185,5 1,5922 7,0673
127 0,2549 1,0668 0,7274 0,9374 1,375 533,4 2716 2182,6 1,6027 7,0573
128 0,2628 1,0678 0,7070 0,9365 1,415 537,6 2717,7 2180,1 1,6136 7,0472
129 0,2708 1,0687 0,6873 0,9358 1,455 542,2 2719,3 2177,1 1,6241 7,0372
130 0,2791 1,0697 0,6683 0,9349 1,496 546,4 2720,6 2174,2 1,6345 7,0271
131 0,2875 1,0707 0,6499 0,9340 1,539 550,6 2721,8 2171,3 1,645 7,0171
132 0,2962 1,0717 0,6321 0,9331 1,582 554,8 2723,1 2168,3 1,6555 7,007
133 0,3051 1,0727 0,6148 0,9323 1,626 558,9 2724,4 2165,4 1,6659 6,9974
134 0,3142 1,0737 0,5981 0,9314 1,672 563,5 2726 2162,5 1,6764 6,9878
135 0,3234 1,0747 0,5820 0,9306 1,718 567,7 2727,3 2159,6 1,6869 6,9781
136 0,333 1,0757 0,5664 0,9299 1,765 571,9 2728,5 2156,6 1,6973 6,9685
137 0,3427 1,0767 0,5513 0,9289 1,814 576,1 2729,8 2153,7 1,7078 6,9589
138 0,3527 1,0777 0,5366 0,9279 1,864 580,7 2731,5 2150,8 1,7183 6,9493
139 0,3629 1,0787 0,5224 0,9271 1,914 584,9 2732,7 2147,8 1,7287 6,9396
140 0,3734 1,0798 0,5087 0,9261 1,966 589,1 2734 2144,9 1,7392 6,9304
428
Новый справочник химика и технолога
Продолжение табл. 3.6. ~
Т Р V V ' Р р' h h' 5 5 '
141 0,384 1,0808 0,4954 0,9254 2,018 593,3 2735,2 2142 1,7497 6,9212
142 0,395 1,0819 0,4825 0,9244 2,072 597,9 2736,9 2139 1,7597 6,9116
143 0,4062 1,0829 0,4700 0,9235 2,128 602,1 2738,2 2136,1 1,7702 6,9024
144 0,4177 1,0840 0,4579 0.9226 2,184 606,2 2739 2132,8 1,7802 6,8931
145 0,4293 1,0851 0,4461 0,9216 2,242 610,4 2740,3 2129,8 1,7907 6,8839
146 0,4413 1,0862 0,4347 0,9207 2,300 615 2741,5 2126,5 1,8012 6.8747
147 0,4535 1,0873 0,4237 0,9197 2,360 619,2 2742,8 2123,5 1,8112 6,8655
148 0,466 1,0884 0,4130 0,9187 2,421 623,4 2744 2120,6 1,8213 6,8563
149 0,4788 1,0895 0,4026 0,9179 2,484 628 2745,3 2117,3 1,8313 6,8475
150 0,4918 1,0906 0,3926 0,9169 2,547 632,2 2746,5 2114,3 1,8418 6.8383
151 0,5051 1,0917 0,3829 0,9160 2,612 636,4 2747,8 2111,4 1,8476 6,8291
152 0,5188 1,0928 0,3734 0,9151 2,678 641 2749,1 2108,1 1,8623 6,8203
153 0,5327 1,0939 0,3642 0,9142 2,746 645,2 2750,7 2105,5 1,8723 6,8115
154 0,5469 1,0950 0.3552 0,9133 2,815 649,4 2751,6 2102,2 1,8824 6,8027
155 0,5613 1,0962 0,3465 0,9123 2,886 653,6 2752.4 2098,8 1,8924 6,7939
156 0,5761 1,0973 0,3381 0,9114 2,958 658,2 2753,7 2095.5 1,9025 6,7855
157 0,5913 1,0985 0,3299 0,9105 3,031 662,4 2754,5 2092,1 1,9125 6,7768
158 0,6068 1,0997 0,3220 0,9094 3,106 667 2755,8 2088,8 1,9226 6,768
159 0,6225 1,1009 0,3143 0,9085 3.182 671,1 2757 2085,9 1.9326 6,7592
160 0,6386 1,1021 0,3068 0,9074 3,259 675.3 2757,8 2082,5 1,9427 6,7508
161 0,655 1,1033 0,2996 0,9064 3,338 679,9 2759,1 2079,2 1,9527 6,742
162 0,6718 1,1044 0,2925 0,9055 3,418 684,1 2760,4 2076,2 1,9628 6,7332
163 0,6888 1,1056 0,2857 0,9046 3,500 688,7 2761,6 2072,9 1,9728 6,7248
164 0,7062 1,1069 0,2790 0,9035 3.584 692,9 2762,5 2069,5 1,9829 6,7165
165 0,7241 1,1081 0.2725 0,9025 3.670 697,5 2763,7 2066,2 1,9925 6,7081
166 0,7422 1,1093 0,2662 0,9016 3,757 701,7 2764,5 2062,8 2,0025 6,6997
167 0,7606 1,1106 0,2601 0,9005 3,845 705,9 2765,4 2059,5 2,0122 6,6918
168 0,7795 1.1118 0,2541 0,8995 3,935 710,5 2766,6 2056,1 2,0222 6,683
169 0,7987 1,1131 0,2483 0,8984 4,027 714,7 2767,5 2052,8 2,0319 6,675
170 0,8183 1,1144 0,2426 0,8974 4,122 719,3 2768,7 2049,4 2,0419 6,6666
171 0,8384 1,1156 0,2371 0,8965 4,218 723,5 2769,6 2046,1 2,0515 6,6583
172 0,8587 1,1169 0,2318 0,8953 4,315 728,1 2770,8 2042,7 2,0616 6,6499
173 0,8794 1,1182 0,2266 0,8945 4,414 732,7 2771,7 2039 2,0712 6,6415
174 0,9006 1,1195 0,2215 0,8933 4,515 736,9 2772,5 2035,6 2,0813 6,6336
175 0,9222 1,1208 0,2166 0,8923 4,617 741,1 2773,3 2032,3 2,0909 6,6256
176 0,944 1,1221 0,2118 0,8913 4,721 745,7 2774,6 2028,9 2,1005 6,6177
177 0,9664 1,1235 0,2071 0,8901 4,828 749,9 2775,4 2025,6 2,1106 6,6097
178 0,9892 1,1248 0,2026 0,8891 4,936 754,5 2776,7 2022,2 2 1202 6,6017
179 1,0124 1,1261 0,1982 0,8880 5,045 758,6 2777,5 2018,9 2,1298 6,5938
180 1,036 1,1275 0,1939 0,8869 5,157 763,3 2778,4 2015,1 2,1395 6,5858
181 1,0601 1,1289 0,1897 0,8858 5,271 767,4 2778,8 2011,3 2,1491 6,5779
182 1,0845 1,1303 0,1856 0,8848 5,388 772 2779,6 2007,6 2,1587 6,5699
183 1,1095 1,1316 0,1816 0,8838 5,507 776,7 2780,5 2003,8 2,1683 6,562
184 1,1349 1,1330 0,1777 0,8827 5,627 780,8 2781,3 2000,5 2,178 6,554
185 1,1608 1,1344 0,1739 0,8816 5,750 785,4 2782,5 1997,1 2,1876 6,5465
186 1,187 1,1358 0,1702 0,8806 5,875 789,6 2783 1989,1 2,1972 6,5385
187 1,2138 1,1372 0,1666 0,8795 6,002 794,2 2783,8 1989,6 2,2069 6,5306
188 1,241 1,1386 0,1631 0,8784 6,131 756,6 2784,6 1986,2 2,2165 6,523
189 1,2688 1,1400 0,1597 0,8773 6,262 803 2785,5 1982,4 2,2261 6,5151
190 1,297 1,1415 0,1564 0,8761 6,395 807,6 2786,3 1978,7 2,2358 6,5075
191 1,3256 1,1430 0,1531 0,8750 6,532 812,2 2787,2 1974,9 2,2454 6,5
192 1,3548 1,1445 0,1499 0,8738 6,671 816,4 2787,6 1971,1 2,255 6,4925
193 1,3845 1,1459 0,1468 0,8728 6,812 821 2788,4 1967,4 2,2646 6,4849
194 1,4147 1,1474 0,1438 0,8716 6,954 825,6 2789,2 1963,6 2,2743 6,4774
Физические свойства важнейших веществ
429
Продолжение табл. 3.6.7
Т Р V у' Р р' h h ’ Avaph Л’ 5 '
195 1,4454 1,1489 0,1409 0,8704 7,098 829,8 2789,7 1959,8 2,2835 6,4699
196 1,4766 1,1504 0,1380 0,8693 7,246 834,4 2790,5 1956,1 2,2931 6,4623
197 1,5083 1,1519 0,1352 0,8682 7,396 839 2791,3 1952,3 2,3027 6,4548
198 1,5405 1,1535 0,1325 0,8669 7,548 843,2 2791,8 1948,5 2,312 6,4468
199 1,5734 1,1550 0,1298 0,8658 7,704 847,8 2792,2 1944,3 2,3216 6,4393
200 1,6067 1,1565 0,1272 0,8647 7,863 852,4 2793 1940,6 2,3308 6,4318
201 1,6407 1,1581 0,1246 0,8635 8,024 857 2793,4 1936,4 2,3404 6,4242
202 1,6751 1,1596 0,1221 0,8624 8,188 861,2 2793,4 1932,2 2,3496 6,4167
203 1,7101 1,1612 0,1197 0,8612 8,355 865,8 2794,3 1928,4 2,3588 6,4092
204 1,7456 1,1628 0,1173 0,8600 8,525 870,4 2795,1 1924,7 2,3685 6,4016
205 1,7818 1,1644 0,1150 0,8588 8,696 875 2795,5 1920,5 2,3777 6,3945
206 1,8186 1,1660 0,1128 0,8577 8,869 879,6 2796,4 1916,7 2,3873 6,3874
207 1,8559 1,1676 0,1106 0,8565 9,044 884,3 2796,8 1912,5 2,3965 6,3798
208 1,8938 1,1693 0,1085 0,8553 9,220 888,9 2797,2 1908,3 2,4057 6,3723
209 1,9323 1,1709 0,1064 0,8541 9,398 893 2797,6 1891,6 2,4149 6,3648
210 1,9714 1,1726 0,1044 0,8528 9,578 897,6 2798 1900,4 2,4246 6,3577
211 2,0111 1,1743 0,1024 0,8515 9,765 902,3 2798,5 1896,2 2,4338 6,3505
212 2,0514 1,1760 0,1004 0,8503 9,960 906,9 2798,9 1892 2,443 6,343
213 2,0925 1,1778 0,09836 0,8490 10,17 911,5 2799,3 1887,8 2,4526 6,3359
214 2,134 1,1795 0,09649 0,8479 10,36 916,1 2799,7 1883,6 2,4618 6,3283
215 2,1762 1,1812 0,09465 0,8466 10,56 920,7 2800,1 1879,5 2,4715 6,3212
216 2,2191 1,1829 0,09285 0,8454 10,77 925,3 2800,6 1875,3 2,4807 6,3141
217 2,2627 1,1846 0,09109 0,8441 10,98 929,9 2801 1871,1 2,4903 6,3066
218 2,3069 1,1864 0,08937 0,8429 11,19 934,5 2801 1866,5 2,4995 6,2995
219 2,3517 1,1882 0,08770 0,8416 11,40 939,1 2801,4 1862,3 2,5087 6,2919
220 2,3972 1,1900 0,08606 0,8403 11,62 943,7 2801,4 1857,7 2,5179 6,2848
221 2,4435 1,1918 0,08445 0,8390 11,84 948,3 2801,8 1853,5 2,5272 6,2777
222 2,5004 1,1936 0,08288 0,8378 12,06 952,9 2801,8 1848,9 2,5364 6,2706
223 2,5379 1,1955 0,08134 0,8365 12,29 957,5 2802,2 1844,7 2,5456 6,263
224 2586,1 1,1973 0,07984 0,8352 12,52 962,1 2802,2 1840,1 2,5548 6,2559
225 2,6352 1,1992 0,07837 0,8339 12,76 967,2 2802,6 1835,5 2,564 6,2488
226 2,6848 1,2011 0,07693 0,8325 13,00 971,8 2802,6 1830,9 2,5728 6,2417
227 2,7353 1,2029 0,07552 0,8312 13,24 976,4 2802,6 1826,3 2,5824 6,2346
228 2,7863 1,2048 0,07414 0,8299 13,48 981 2802,6 1821,7 2,5916 6,2274
229 2,8382 1,2068 0,07279 0,8286 13,74 985,6 2803,1 1817,5 2,6008 6,2279
230 2,8909 1,2087 0,07147 0,8273 13,99 990,2 2803,1 1812,9 2,6101 6,2132
231 2,9442 1,2107 0,07018 0,8260 14,25 995,2 2803,5 1808,3 2,6193 6,2061
232 2,9983 1,2127 0,06891 0,8246 14,51 999,8 2803,5 1803,7 2,6285 6 199
233 3,0532 1,2147 0,06767 0,8233 14,78 1004,4 2803,5 1799,1 2,6377 6,1923
234 3,1089 1,2167 0,06646 0,8220 15,05 1009 2803,5 1794,5 2,6469 6,1852
235 3,1653 1,2187 0,06527 0,8206 15,32 1014 2803,5 1789,4 2,6561 6,178
236 3,2224 1,2207 0,06410 0,8192 15,60 1018,6 2803,5 1784,8 2,6653 6,1709
237 3,2804 1,2227 0,06296 0,8179 15,88 1023,3 2803,5 1780,2 2,6745 6,1638
238 3,3392 1,2248 0,06184 0,8165 16,17 1028,3 2803,5 1775,2 2,6837 6,1567
239 3,3988 1,2269 0,06074 0,8151 16,46 1032,9 2803,5 1770,6 2,6929 6,1496
240 3,4592 1,2291 0,65967 0,8136 16,76 1037,5 2803,1 1765,6 2,7022 6,1425
241 3,5205 1,2313 0,05862 0,8122 17,06 1042,5 2803,1 1760,5 2,7114 6,1353
242 3,5825 1,2334 0,05759 0,8108 17,36 1047,1 2803,1 1755,9 2,7206 6,1282
243 3,6455 1,2356 0,05658 0,8094 17,67 1052,1 2803,1 1750,9 2,7294 6,1211
244 3,7092 1,2377 0,05559 0,8080 17,99 1056,7 2802,6 1745,9 2,7386 6,1144
245 3,7737 1,2399 0,05462 0,8066 18,31 1061,8 2802,6 1740,9 2,7478 6,1073
246 3,8392 1,2421 0,05367 0,8051 18,63 1066,4 2802,2 1735,8 2,757 6,1002
247 3,9056 1,2444 0,05274 0,8036 18,96 1071,4 2801,8 1730,4 2,7662 6,0931
248 3,9728 1,2477 0,05183 0,8022 19,29 1076 2801,4 1725,4 2,775 6,0864
430
Новый справочник химика и технолога
Продолжение табл. 3.6.7
Т Р V v' Р р' h h' ky(lph s 5'
249 4,0408 1,2489 0,05093 0,8007 19,63 1081 2801,4 1720,4 2,7842 6,0792
250 4,1097 1,2512 0,05005 0,7992 19,98 1086,1 2801 1714,9 2,7934 6,0721
251 4,1797 1,2536 0,04919 0,7977 20,33 1090,7 2800,6 1709,9 2,8026 6,065
252 4,2506 1,2560 0,04835 0,7962 20,68 1095,7 2800,1 1704,4 2,8119 6,0579
253 4,3225 1,2583 0,04752 0,7947 21,04 1100,7 2799,7 1699 2,8211 6,0508
254 4,3945 1,2607 0,04671 0,7932 21,41 1105,3 2799,3 1694 2,8303 6,0436
255 4,4684 1,2631 0,04591 0,7917 21,78 1110,3 2798,9 1688,5 2,8395 6,0365
256 4,5424 1,2655 0,04523 0,7901 22,16 1115,4 2798,5 1683,1 2,8487 6,0294
257 4,5171 1,2679 0,04436 0.7886 22,54 1120 2797,6 1677,7 2,8579 6,0223
258 4,6944 1,2704 0,04361 0,7871 22,93 1125 2797,2 1672.2 2,8667 6,0152
259 4,7714 1,2729 0,04287 0,7856 23,33 1130 2796,8 1666,8 2,8759 6,0085
260 4,8504 1,2755 0,04215 0,7840 23,72 1135 2796,4 1661,3 2,8851 6,0014
261 4,9295 1,2781 0,04144 0,7824 24,13 1140,1 2795,5 1655,5 2,8939 5,9942
262 5,0095 1,2807 0,04074 0,7808 24,54 1145,1 2795,1 1650 2,9031 5,9871
263 5,0906 1,2834 0,04005 0,7792 24,96 1150,1 2794,3 1644,2 2,9123 5,98
264 5,1726 1,2860 0,03938 0,7776 25,39 1155,1 2793,9 1638,7 2,9215 5,9729
265 5,2567 1,2886 0,03872 0,7760 25,83 1160,2 2793,4 1633,3 2,9308 5,9658
266 5,3408 1,2913 0,03807 0,7744 26,27 1165,2 2792,6 1627,4 2,94 5,9587
267 5,426 1,2940 0,03744 0,7728 26,71 1170,2 2792,2 1622 2,9492 5,9515
268 5,5121 1,2967 0,03682 0,7712 27,16 1175,2 2791,3 1616,1 2,9584 5,9444
269 5,5992 1,2995 0,03620 0,6795 27,62 1180,3 2790,5 1610,2 2,9672 5,9369
270 5,6884 1,3023 0,03560 0,7679 28,09 1185,3 2789,7 1604,4 2,9764 5,9298
271 5,7776 1,3051 0,03501 0,7662 28,56 1190,3 2788,8 1598,5 2.9856 5,9226
272 5,8677 1,3080 0,03443 0,7645 29,04 1195,3 2746,1 1592,7 2,9948 5,9155
273 5,9599 1,3109 0,03386 0,7628 29,53 1200.4 2787,2 1586,8 3,004 5,9084
274 6,0521 1,3138 0,03330 0,7611 30,03 1205,8 2786,3 1580,5 3,0132 5,9009
275 6,1464 1,3168 0,03275 0,7595 30,53 1210,8 2785,1 1574,2 3,0225 5,8938
276 6,2619 1,3198 0,03221 0,7578 31,05 1215,8 2783,8 1568 3,0317 5,8866
277 6,3379 1,3228 0,03167 0,7561 31,58 1221,3 2783 1561,7 3,0409 5,8791
278 6,4352 1,3259 0,03114 0,7543 32,1 1 1226,3 2781,7 1555,4 3,0501 5,872
279 6,5334 1,3290 0,03063 0,7525 32,65 1224,2 2780,9 1549,1 3,0593 5,8649
280 6,6327 1,3321 0,03013 0,7507 33,19 1236,8 2779,6 1542,8 3,0685 5,8573
281 6,733 1,3353 0,02964 0,7489 33,74 1242,2 2778,8 1536,6 3,0777 5,8498
282 6,8354 1,3385 0,02915 0,7471 34,30 1247,2 2777,5 1530,3 3,0869 5,8427
283 6,9377 1,3417 0,02867 0,7453 34,88 1252,7 2776,3 1523,6 3,0961 5,8351
284 7,0421 1,3450 0,02820 0,7435 35,46 1257,7 2774,6 1516,9 3,1053 5,8276
285 7,1475 1,3483 0,02774 0,7417 36,05 1263,2 2773,3 1510,2 3,1146 5,8201
286 7 2539 1,3516 0,02729 0,7399 36,65 1268,6 2772,1 1503 5 3,1238 5,8125
287 7,3613 1,3550 0,02684 0,7380 37,26 1273,6 2770,4 1496,8 3,133 5,8054
288 7,4707 1,3585 0,02639 0,7361 37,89 1279,1 2769,1 1490,1 3,1422 5,7979
289 7,5811 1,3620 0,02595 0,7342 38,53 1284,5 2767,5 1483 3,1518 5,7903
290 7,6926 1,3655 0,02553 0,7323 39,17 1290 2766,2 1476,3 3,161 5,7824
291 7,8051 1,3691 0,02512 0,7303 39,81 1295,4 2765 1469,6 3,1707 5,7749
292 7,9185 1,3727 0,02471 0,7284 40,47 1300,8 2763,3 1462,4 3,1807 5,7673
293 8,0341 1,3764 0,02430 0,7265 41,15 1306,3 2761,6 1455,3 3,1895 5,7598
294 8,1506 1,3801 0,02390 0,7246 41,84 1311,7 2759,9 1448,2 3,1987 5,7518
295 8,2681 1,3839 0,02351 0,7226 42,54 1317,2 2758,3 1441,1 3,2079 5,7443
296 8,3877 1,3877 0,02312 0,7206 43,25 1322,6 2756,6 1434 3,2171 5,7368
297 8,5083 1,3916 0,02274 0,7186 43,97 1328,1 2754,9 1426,9 3,2263 5,7288
298 8,6299 1,3956 0,02237 0,7166 44,70 1333,9 2753,2 1419,3 3,236 5,7208
299 8,7525 1,3996 0,02200 0,7145 45,45 1339,4 2751,1 1411,8 3,2452 5,7129
300 8,8771 1,4036 0,02164 0,7125 46,21 1344,8 193,47 1404,3 3,2548 5,7049
301 9,0027 1,408 0,02129 0,7102 46,98 1350,7 2747 1396,3 3,264 5,697
302 9,1304 1,412 0,02094 0,7082 47,76 1356,1 2744,9 1388,8 3,2737 5,689
Физические свойства важнейших веществ
431
Продолжение табл. 3.6.7
Т Р V у' Р р' !г h' ^vaph S’ S’'
303 9,2591 1,416 0,02060 0,7062 48,55 1362 2743,2 1381,2 3,2833 5,6811
304 9,3888 1,420 0,02026 0,7042 49,36 1367,4 2741,1 1373,7 3,2929 5,6727
305 9,5195 1,425 0,01992 0,7017 50,20 1373,3 2701,3 1365,7 3,3025 5,6647
306 9,6522 1,429 0,01959 0,6998 51,05 1378,7 2736,5 1359 3,3122 5,6564
307 9,787 1,434 0,01926 0,6973 51,92 1384,6 2734,4 1349,8 3,3218 5,6484
308 9,9228 1,438 0,01894 0,6954 52,80 1390,4 2732,3 1341,9 3,3314 5,64
309 10,06 1,443 0,01862 0,6930 53,70 1396,3 2729,8 1333,5 3,3411 5,6317
310 10,197 1,447 0,01831 0,6911 54,61 1402,2 2727,3 1325,1 3,3507 5,6233
311 10,337 1,452 0,01801 0.6887 55,53 1408 2724,8 1316,7 3,3603 5,6149
312 10,479 1,457 0,01771 0,6863 56,47 1413,9 2722,3 1308,4 3,37 5,6061
313 10,622 1,462 0,01741 0,6840 57,43 1419,7 2719,7 1300 3,38 5,5978
314 10,766 1,467 0,01712 0,6817 58,41 1426 2717,2 1291,2 3,3896 5,589
315 10,912 1,472 0,01683 0,6794 59,42 1431,9 2714,3 1282,4 3,3997 5,5802
316 11.06 1,477 0,01654 0,6771 60,45 1438,2 2711,4 1273,2 3,4097 5,5714
317 11,209 1,482 0,01626 0,6748 61,50 1444 2708,4 1264,4 3,4194 5,5626
318 11,36 1,488 0,01598 0,6720 62,57 1449,9 2705,5 1255,6 3,4294 5,5534
319 1 1,512 1,493 0,01571 0,6698 63,65 1455,8 2702,6 1246,8 3,4395 5,5446
320 11,666 1,499 0,01545 0,6671 64,74 1462 2699,6 1237,6 3,4495 5,5354
321 11,821 1,505 0,01519 0,6645 65,85 1468,3 2696,7 1228,4 3,4596 5,5262
322 11,978 1,511 0,01493 0,6627 66,99 1474,6 2693,8 1219,2 3,4696 5,5169
323 12,136 1,517 0,01467 0,6592 68,16 1480,9 2690,4 1209,6 3,4796 5,5077
324 12,296 1,523 0,01442 0,6566 69,35 1487,2 2687,1 1199,9 3,4897 5,4985
325 12,458 1,529 0,01417 0,6532 70,56 1493,4 2683,3 1189,9 3,5002 5,4893
326 12,621 1,536 0,01393 0,6511 71,79 1500,1 2680 1179,8 3,5102 5,4797
327 12,786 1,542 0,01369 0,6486 73,05 1506,4 2676,2 1169,8 3,5207 5,4701
328 12,953 1,548 0,01345 0,6460 74,35 1512,7 2672,4 1159,7 3,5307 5,4562
329 13,122 1,555 0,01321 0,6431 75,70 1519,4 2669,1 1149,7 3,5412 5,4508
330 13,292 1,562 0,01297 0,6402 77,09 1526,1 2665,7 1139,6 3,5521 5,4412
331 13,464 1,569 0,01273 0,6373 78,51 1532,8 2662 1129,2 3,5625 5,4315
332 13,637 1,576 0,01250 0,6345 79,96 1539.5 2657,8 1118,3 3,5734 5,4215
333 13,814 1,584 0,01228 0,6313 81,44 1546,2 2654 1107,8 3,5839 5,4114
334 13,991 1,591 0,01206 0,6285 82,94 1552,9 2649,8 1096,9 3,5948 5,401
335 14,17 1,599 0,01184 0,6254 84,47 1559,6 2645,2 1085,6 3,6057 5,3905
336 14,351 1,607 0,01162 0,6223 86,05 1566,3 2640,6 1074,3 3,6166 5,38
337 14,534 1,615 0,01141 0,6192 87,66 1573,4 2636 1062,6 3,6274 5,3692
338 14,718 1,623 0,01120 0,6162 89.30 1580,5 2631,4 1050,9 3,6387 5,3583
339 14,905 1,631 0,01099 0,6139 91,01 1587,6 2626,8 1039,2 3,6496 5.3474
340 15,093 1,639 0,01078 0,6102 92,77 1594,8 2634,3 1027 3,6605 5,3361
341 15,284 1,648 0,01057 0,6068 94,58 1601,9 2616,8 1014,9 3,6718 5,3248
342 15,475 1,657 0,01037 0,6035 96,43 1609,4 2611,7 1379,1 3,6831 5,313
343 15,67 1,666 0,01017 0,6002 98,33 1616,9 2606,3 989,34 3,6949 5,3013
344 15,866 1,676 0,009970 0,5966 100,3 1624,5 2600.8 976,36 3,7066 5,2892
345 16,064 1,686 0,009771 0,5931 102,3 1632 2595,4 963,38 3,7183 5,277
346 16,265 1,696 0,009574 0,5896 104,4 1639,6 2589,5 949,98 3,73 5,2641
347 16,467 1,707 0,009379 0,5858 106,6 1647,1 2583,7 936,59 3,7417 5,2511
348 16,671 1,728 0,009186 0,5821 108,9 1654,6 2577,4 922,77 3,7539 5,2381
349 16,878 1,729 0,008995 0,5783 111,2 1663 2571,1 908,12 3,766 5,2251
350 17,086 1,741 0,008805 0,5744 113,6 1671,4 2564,4 893,04 3,7786 5,2117
351 17,297 1,752 0,008616 0,5708 116,1 1679,3 2557,3 877,97 3,7911 5,1979
352 17,51 1,764 0,008427 0,5669 118,7 1687,7 2550,2 862,48 3,8037 5,1854
353 17,724 1,777 0,008240 0,5628 121,4 1696,1 2542,6 846,57 3,8167 5,169
354 17,942 1,792 0,008054 0,5581 124,2 1704,9 2535,1 830,24 3,8301 5,154
355 18,161 1,807 0,007869 0,5534 127,1 1714,1 2527,2 813,08 3,8439 5,1385
356 18,383 1,822 0,007683 0,5489 130,2 1723,3 2518,8 795,49 3,8581 5,123
432
Новый справочник химика и технолога
Окончание табл. 3.6.7
Т Р V v’ Р Р' h h' .S’ 5
357 18,607 1,838 0,007498 0,5441 133,4 1732,5 2510 777,49 3,8728 5,1071
358 18,834 1,855 0,007313 0,5391 136,7 1741,7 2500,8 759,07 3,887 5,0903
359 19,062 1,874 0,007128 0,5336 140,3 1751,3 2491,1 739,81 3,9017 5,0719
360 19,294 1,894 0,006943 0,5280 144,1 1761,4 2481,1 719,71 3,9163 5,053
361 19,527 1,916 0,00675 0,5219 148,1 1771,9 2470,2 698,36 3,9322 5.0338
362 19,764 1,939 0,00656 0,5158 152,4 1782,7 2458,9 676,17 3,9486 5,0137
363 20,003 1,964 0,00637 0,5092 156,9 1793,6 2446,8 653,14 3,9657 4,9923
364 20,245 1,991 0,00619 0,5023 161,6 1805,3 2434,2 628,86 3,9829 4,9702
365 20,489 2,02 0,00600 0,495 166,7 1817,5 2420,8 603,32 4,0009 4,9463
366 20,735 2,05 0,00580 0,488 172,4 1830,5 2406,2 575,69 4,0202 4,9212
367 20,985 2,08 0,00559 0,481 178,9 1844,3 2390,2 545,96 4,0411 4,894
368 21,238 2.12 0,00538 0,471 186,0 1858,9 2372,7 513,72 4,0633 4,8646
369 21,493 2,17 0,00516 0,461 193,8 1874,8 2353 478,13 4.0872 4,832
370 21,752 2,22 0,00493 0,451 202,4 1892,4 2330,8 438,36 4.1135 4,7951
371 22,014 2,29 0,00468 0,437 214,0 1912,5 2304,8 392,3 4,1441 4,7529
372 22,279 2,38 0,00440 0,420 227,0 1936,8 2273 336,2 4,1809 4,7018
373 22,548 2,51 0,00409 0,398 244,0 1969,1 2236,2 267,12 4,2295 4,6427
374 22,82 2,80 0,00361 0,375 277,0 2031,9 2171,7 139,84 4,3258 4,5418
Таблица 3.6.8
Термодинамические свойства насыщенного пара диоксида серы (SO2)
T P V v' P P' h h' ^vaph 5 5
-50 0,012 0,642 2,491 1,557 0,401 350,4 774,1 423,7 3,9151 5,81
-45 0,0165 0,647 1,844 1,545 0,542 357,1 776,7 419,5 3,9406 5,7811
-40 0,0223 0,652 1,387 1,534 0,721 367,2 779,6 415,3 3,9712 5,7527
-35 0,0298 0,658 1,059 1,520 0,944 371 782,1 411,1 4.0009 5,7275
-30 0,0393 0,663 0,818 1,508 1,223 378,1 785 407 4,0294 5,7028
-25 0,0511 0,668 0,641 1,497 1,560 384,8 787,5 402,8 4,0574 5,6802
-20 0,0657 0,674 0,507 1,484 1,972 391,5 790 398,6 4,0842 5,658
-15 0,0834 0,680 0,406 1,470 2,46 398,6 792,6 394 4,111 5,6379
-10 0,1048 0,686 0,328 1,458 3,05 405,3 795,1 389,8 4,1361 5.6178
-5 0,1303 0,692 0,268 1,445 3,73 412 797,6 385,6 4,1625 5,5998
0 0,1606 0,697 0,2200 1,435 4,55 418,7 799,7 381 4,1868 5,5818
5 0,1962 0,704 0,1824 1,420 5,48 425,4 802,2 376,8 4,2119 5,5488
10 0,2378 0,710 0,1523 1,408 6,57 432,1 804,3 372,2 4,2349 5,5488
15 0,286 0,716 0,1280 1,397 7,81 438,8 806,4 367,6 4,2592 5,5341
20 0,3415 0,723 0,1084 1,383 9,23 445,5 808,5 363 4,2818 5,5195
25 0,405 0,730 0,0923 1,370 10,84 452,2 810,1 358 4,3049 5,5056
30 0,4772 0,738 0,0790 1,355 12,66 458,9 812,2 353,4 4,3262 5,4918
35 0,5591 0,745 0,0680 1,342 14,71 466 814,3 348,3 4,3484 5,4793
40 0,6512 0,754 0,0588 1,326 17,01 472,3 816 82.1 4,3685 5,4667
45 0,7546 0,763 0,0511 1,311 19,57 479 817,7 338,7 4,3903 5,455
50 0,8697 0,772 0,0446 1,295 22,4 485,7 819,4 333,7 4,4104 5,4433
Таблица 3.6.9 Термодинамические свойства насыщенного пара диоксида углерода (СО2)
Выше черты находятся данные, относящиеся к равновесию твердое тело—пар, а ниже ее — к равновесию жидкость—пар.
T P V v' P P' h h' ^vaph 5 5'
-100 0,0144 0,627 2,336 1,595 0,428 45,64 631 585,3 2,5104 5,8908
-95 0,0239 0,629 1,442 1,589 0,693 51,08 633,9 582,8 2,5431 5,815
-90 0,0384 0,632 0,920 1,582 1,087 56,94 637,2 580,3 2,5749 5,7435
Физические свойства важнейших веществ
433
Окончание табл. 3.6.9
т р V v' Р Р' h h' 8-vaph S s'
-85 0,0604 0,635 0,598 1,575 1,672 62,8 640,2 577,4 2,6059 5,6748
-80 0,0926 0,639 0,398 1,566 2,51 68,66 642,7 574 2,6373 5,6095
-75 0,1388 0,634 0,269 1,557 3,71 74.94 645,2 569,8 2,6695 5,5467
-70 0,2047 0,637 0,1854 1,546 5,39 82,06 646,9 564,8 2,7043 5,486
-65 0,2969 0,652 0,1293 1,535 7,74 90,02 648,5 562,7 2,7428 5,4261
-60 0,4235 0,657 0,0912 1,522 10,97 99,23 649,4 550,1 2,7863 5,3671
-56,6 0,535 0,661 0,0722 1,512 13,84 105,5 649,4 543,9 2,8156 5,3273
-56,6 0.535 0,849 0,0722 1,178 13,84 301.4 649,4 347,9 3,72 5,3273
-55 0,5735 0,853 0,0676 1,172 14,79 304,4 649,8 345,4 3,7334 5,3172
-50 0,688 0,867 0,0554 1,154 18,05 314 651,5 337,5 3,7765 5,2883
-45 0,8602 0,881 0,0458 1,135 21,8 323,6 652,7 329,1 3,8184 5,2607
-40 1,039 0,897 0,0382 1,115 26,2 333,3 654 320,7 3,8594 5,2348
-35 1,242 0,913 0,0320 1,095 31,2 342,9 654,8 311,5 3,8996 5,2096
-30 1,474 0,931 0,0270 1,074 37,0 352,5 655,7 303,1 3,9389 5,1854
-25 1,737 0,950 0,0229 1,053 43,8 362,2 656,1 293,5 3,9779 5,1615
-20 2,033 0,971 0,0195 1,030 51.4 372,2 656,1 283,9 4,0168 5,138
-15 2,365 0,994 0,0166 1,006 60,2 382,7 656,1 273,4 4,057 5,1154
-10 2,735 1,019 0,01419 0,981 70,5 394 655,7 261,7 4,0976 5,0924
-5 3,146 1,048 0,01214 0,954 82,4 405,7 654,8 249,1 4,1407 5,0698
0 4,707 1,081 0,01038 0,925 96,3 418,7 653,6 234,9 4,1868 5,0472
5 4,104 1,120 0,00885 0,893 113,0 431,7 651 219,4 4,2299 5,0179
10 4,656 1.166 0,00752 0,858 133,0 445.9 647.3 201,4 4,2781 4.9894
15 5,262 1,223 0,00632 0,818 158,0 461 641,4 180,5 4,3292 4,9551
20 5,924 1.298 0,00526 0,771 190,2 477,3 632,6 155,3 4,3827 4,9128
25 6,646 1,417 0,00417 0,706 240 497,4 616,7 119,3 4,4497 4,8504
30 7,431 1,677 0,00299 0,596 334 527,1 590,8 63,22 4,5444 4.7524
31 7,595 2,156 0,002156 0,468 468 558,9 558,9 0 4,6465 4,6465
Термодинамические свойства насыщенного пара ртути (Hg)
При Т = О °C удельная энтальпия h = 0 кДж/кг и удельная энтропия 5 = 0 кДж/(кг • К).
Таблица 3.6.10
Т Р у' Р' h /?' Aw/?/7 S’'
205,56 0,003 7,1480 0,1399 32,12 330,2 298,08 0,0875 0,7101
228,89 0,006 3,728 0,2682 35,73 331,69 295,96 0,095 0,6845
236,67 0,007 3,025 0,3306 36,96 332,18 295,22 0,0976 0,6766
251,67 0,011 2,069 0,4833 39,31 333,15 293,84 0,1022 0,6619
262,78 0,014 1,581 0,6324 41,06 333,88 292,82 0,1051 0,6515
292,22 0,028 0,8278 1,2080 45,64 335,74 290,1 0,1135 0,6268
310,56 0,043 0.5678 1,7609 48,53 336,95 288,4 0,1185 0,6121
325,00 0,057 0,4347 2,3003 50,74 337,83 287,1 0,1223 0,6025
336,11 0,071 0,3534 2,8294 52,5 338,57 286,05 0,1252 0,5945
357,78 0,106 0,2430 4,1152 55,94 339,97 284,05 0,1306 0,5807
374,44 0,153 1,1862 5,369 58,49 341,01 282,52 0,1348 0,5711
387,78 0,178 0,1516 6,595 60,58 341,88 281,28 0,1382 0,5635
399,44 0,191 0,1282 7,802 62,34 342,6 280,24 0,1407 0,5573
409,44 0,249 0,11122 8,991 63,93 343,25 279,31 0,1432 0,5522
418,33 0,285 0,09840 10,160 65,31 343,81 278,49 0,1449 0,5476
426,11 0,32 0,08832 11,320 66,57 344,34 277,77 0,147 0,5443
433,33 0,355 0,08016 12,470 67,7 344,81 277,09 0,1486 0,5405
446,67 0,426 0,06780 14,740 69,75 345,65 275,88 0,1511 0,5342
458,33 0,496 0,05891 16,974 71,51 346,34 274,82 0,1537 0,5296
468,33 0,567 0,05212 19,185 73,14 347,01 273,89 0,1557 0,525
477,78 0,638 0,04680 21,365 74,57 347,6 273,03 0,1578 0,5221
434
Новый справочник химика и технолога
Окончание табл. 3.6.10
Т Р у' Р' h /?' &vclph 5 5 '
486,11 0,712 0,04252 23,518 75,91 348,16 272,26 0,1595 0,5179
493,89 0,783 0,03897 25,661 77,12 348,67 271,54 0,1612 0,515
501,11 0,855 0,03600 27,775 78,29 349,13 270,84 0,1629 0,5125
508,33 0,926 0,03346 29,883 79,38 349,58 270,21 0,1641 0,51
514,44 0,997 0,03129 31,959 80,34 350 269,63 0,1654 0,5079
520,76 1,064 0,02938 34,04 81,31 350,36 269,05 0,1666 0,5053
537,78 1,287 0,02491 40,14 83,95 351,46 267,51 0,17 0,4999
Таблица 3.6.11
Термодинамические свойства насыщенного пара дисульфида углерода (CS2)
Т Р у' р' h h' ts.vaph
-17,78 0,00783 3,356 0,2979 398,67 783,63 384,93
-12,22 0,0104 2,714 0,3684 405,66 788,28 382,63
-6,67 0,0135 2,175 0,4597 411,69 791,31 379,62
-1,11 0,0168 1,841 0,5430 417,51 794.79 377,27
4,44 0,0216 1,468 0,6808 423,45 798,4 374,97
10,00 0,0278 1,286 0,7721 428,56 800,7 372,16
15,56 0,0352 1,124 0,8890 435,43 805,73 370,28
21,11 0,0416 0,824 1,214 441,46 809,22 367,73
26,67 0,052 0,649 1,539 445,89 810,84 364,96
32,22 0,0652 0,518 1,929 450,79 812,7 361,91
37,78 0,0789 0,439 2,193 456,24 815,38 359,14
43,33 0,0962 0,362 2,762 461,26 817,59 356,34
48,89 0,1147 0,318 3,140 465,24 776,91 353,53
Таблица 3.6.12
Термодинамические свойства насыщенного пара метана (СН4)
Энтальпия жидкости при 100 К принята равной 0 кДж/кг.
Т Р V у' Р Р' h IT AVUph
-170 0,0456 2,30 0,435 10,718 538,51 527,79
-160 0,1216 2,37 0,480 0,421 2,08 45,343 556,13 510,79
-150 0,2523 2,46 0,251 0,406 3,98 80,47 574,05 493,58
-140 0,46 2,56 0,144 0,390 6,94 116,77 591,26 474,49
-130 0,8126 2,68 0,0887 0,373 11,27 154,45 606,88 452,43
-120 1,281 2,82 0,0562 0,354 17,8 194,23 619,19 424,96
-НО 1,888 3,02 0,0377 0,331 26,5 236,81 626,43 389,62
-100 2,571 3,27 0,0244 0,306 41,0 284,7 626,18 341,48
-90 3,839 3,88 0,0127 0,258 78,6 344,03 605,96 261,93
-82,1 4,793 6,17 0,00617 0,162 162,0 478,68 478,68 0
Таблица 3.6.13
Термодинамические свойства насыщенного пара пропана (С3Н8)
Т Р V у' Р р' h h' ^vaph
-56,67 0,0525 1,669 0,805 0,5991 1,24 290,15 731,06 440,87
-51,11 0,0692 1,687 0,620 0,5927 1,78 301,87 736,88 435,01
-45,56 0,0898 1,706 0,483 0,5863 2,07 314,85 743,87 429,15
-40,00 0,1155 1,725 0,383 0,5797 2,61 326,15 748,52 422,03
-34,44 0,1449 1,745 0,308 0,5731 3,25 339,13 755,47 416,34
-28,89 0,1814 1,765 0,250 0,5666 4,00 350,85 760,16 409,39
-23,33 0,2239 1,786 0,204 0,5600 4,92 363,41 767,1 1 403,57
-17,78 0,2726 1,807 0,169 0,5533 5,91 376,39 772,93 396,57
Физические свойства важнейших веществ
435
Окончание табл. 3.6.13
7’ Р V v' Р р' h h'
-12,22 0,3273 1,830 0,142 0,5465 7,06 388,95 779,92 390,75
-6,67 0,3952 1,854 0,119 0,5393 8,43 401,93 785,74 383,8
-1,11 0,4722 1,880 0,0999 0,5318 10,0 415,75 792,69 376,81
4,44 0,5553 1,907 0,0855 0,5243 11,7 429,98 799,68 369,82
10,00 0,6535 1,936 0,0737 0,5164 13,6 443,8 806,67 362,87
15,56 0,763 1,966 0,0631 0,5086 16,9 457,62 813,62 355,88
21,11 0,8836 1,998 0,0551 0,5004 18,1 471,85 819,44 347,76
26,67 1,017 2,033 0,0481 0,4918 20,8 486,92 826,43 339,59
32,22 1,168 2,071 0,0420 0,4829 23,9 502 833,42 331,47
37,78 1,332 2,1 11 0,0369 0,4738 27,1 517,07 839,03 322,13
43,33 1,518 2,164 0,0324 0,4621 31,4 532,14 844,06 311,67
48,89 1,709 2,206 0,0287 0,4533 34,9 547,21 847,41 300,07
Таблица 3.6.14
Термодинамические свойства насыщенного пара бутана (С4Н]0)
Т Р V v' Р р' h h' &vaph
-17,78 0,052 1,618 0,693 0,6181 1,44 378,65 775,27 396,57
-12,22 0,066 1,633 0,559 0,6125 1,79 391,47 783,39 391,93
-6,67 0,083 1,648 0,451 0,6069 2,21 403,19 791,56 388,45
-1,11 0,102 1,663 0,368 0,6013 2,71 415,87 800,85 384,93
4,44 0,126 1,679 0,305 0,5957 3,28 428,73 808,97 380,29
10,00 0,154 1,695 0,254 0,5898 3,94 441,29 817,14 375,64
15,56 0,187 1,713 0,212 0,5839 4,71 455,44 826,43 370,99
21,11 0,225 1,731 0,180 0,5776 5,56 468,08 834,55 366,35
26,67 0,267 1,751 0,154 0,5710 6,52 482,32 842,8 360,53
32,22 0,317 1,771 0,131 0,5645 7,62 497,39 850,76 353,53
37,78 0,372 1,792 0,113 0,5581 8,84 511,21 859,13 347,76
43,33 0,433 1,814 0,0986 0,5512 10,1 526,28 868,34 341,94
48,89 0,505 1,838 0,0862 0,5440 11,6 541,35 875,46 333,77
54,44 0,58 1,864 0,0755 0,5364 13,2 556,43 883,41 326,82
60,00 0,66 1,893 0,0668 0,5283 15,0 572,75 892,63 319,83
Таблица 3.6.15
Термодинамические свойства насыщенного пара изобутана (С4Н10)
Т Р V v’ Р р' h И'
-28,89 0,0534 1,628 0,665 0,6143 1,52 359,23 744,33 384,93
-23,33 0,0661 1,645 0,556 0,6079 1,79 369,69 748,98 379,16
-17,78 0,0827 1,660 0,448 0,6023 2,23 380,29 753,62 373,34
-6,67 0,1297 1,696 0,292 0,5895 3,43 403,61 766,44 362,87
-1,Н 0,1591 1,715 0,241 0,5831 4,15 416,34 773,39 357,05
4,44 0,1915 1,734 0,201 0,5866 4,98 429,15 780,38 351,23
10,00 0,231 1,754 0,169 0,5702 5,91 443,09 788,5 345,41
15,56 0,2756 1,774 0,142 0,5638 7,03 457,07 796,66 339,59
21,11 0,3263 1,794 0,121 0,5574 8,25 472,27 805,96 333,77
26,67 0,384 1,817 0,104 0,5502 9,64 488,6 815,25 326,82
32,22 0,4509 1,842 0,886 0,5430 11,3 504,93 824,55 319,83
37,78 0,5249 1,866 0,0768 0,5358 13,0 522,09 835,02 312,84
43,33 0,6059 1,892 0,0668 0,5286 15,0 540,93 845,31 304,72
48,89 0,6981 1,921 0,0578 0,5206 17,3 559,36 855,78 296,55
54,44 0,7974 1,951 0,0506 0,5126 19,7 580,29 868,76 288,43
60,00 0,9033 1,963 0,0447 0,5094 21,1 601,22 881,74 280,26
436
Новый справочник химика и технолога
Таблица 3.6.16
Термодинамические свойства насыщенного пара дифтордихлорметана (фреона-12) (CCI2F2)
Т Р V v’ Р Р' И h' \aph 5 5 '
-80 0,00643 0,6150 2,124 1,626 0,471 349,2 534,2 185 3,8879 4,8458
-75 0,00914 0,6202 1,531 1,612 0,653 353,4 536,7 183 3,9092 4,8345
-70 0,01267 0,6255 1,125 1,598 0,888 357,6 539,3 182 3.9301 4,824
-65 0,01743 0,6309 0,841 1,585 1,188 361,7 541,8 180 3.9507 4,8148
-60 0,02341 0,6364 0,639 1,571 1,564 366,3 544,3 178 3,9708 4,8064
-55 0,03101 0,6421 0,493 1,557 2,028 370,5 546,8 176 3,9904 4,7993
-50 0,04043 0,6479 0,385 1,543 2.60 374,7 549,3 175 4,0097 4,7926
-45 0,05218 0,6538 0,305 1,529 3,28 378,9 551,8 173 4,029 4,7863
-40 0,06637 0,6600 0,244 1,515 4,10 383,5 554,3 171 4,0478 4,7809
-35 0,08349 0,6662 0,1972 1,501 5,07 387.7 556,8 169 4,0654 4,7763
-30 0,1039 0,6728 0,1633 1,486 6,20 391,9 559,4 167 4,083 4,7717
-25 0,1279 0,6794 0,1331 1,472 7,52 396,1 561,9 165 4,1006 4,7679
-20 0,156 0,6864 0,1106 1,457 9,04 400,7 564 164 4,1181 4,7646
-15 0,1888 0,6936 0,0927 1,442 10,79 404,9 566,5 162 4,1357 4,7616
-10 0,2266 0,7011 0,0781 1,426 12,80 409,5 569 160 4,1529 4,7587
-5 0,26983 0,7091 0,0663 1,410 15,09 414,1 571,5 157 4,1701 4,7566
0 0,3191 0,7174 0,0566 1,394 17,66 418,7 573,6 155 4,1868 4,7541
5 0,3748 0,7259 0,0486 1,378 20,56 423,3 576,1 152 4,2035 4,7524
10 0,4375 0,7348 0,0420 1,361 23,8 428,3 578,2 150 4.2203 4,7503
15 0,5078 0,7439 0,0365 1,344 27,4 432,9 580,3 147 4,2408 4,7487
20 0,5862 0,7534 0,0317 1,327 31,5 437,9 582,4 145 4,2538 4,7474
25 0,6732 0,7637 0,0277 1,310 36,1 442,5 584,5 142 4,2701 4,7457
30 0,7693 0,7742 0,0243 1,292 41,2 448 586,6 139 4,2869 4,7445
35 0,8751 0,7855 0,0214 1,273 46,8 453 588,2 136 4,3032 4,7428
40 0,9914 0,7976 0,0188 1,254 53,1 458 590,3 132 4,3195 4,7416
45 1,119 0,8104 0,0166 1,234 60,4 463,5 592 129 4,3359 4,7399
50 1,257 0,8244 0,0146 1,213 68,7 468,5 593,3 125 4,3518 4,7378
Таблица 3.6.17
Термодинамические свойства насыщенного пара дифторхлорметана (фреона-22) (CHCIF2)
Т Р V v' Р Р' h h' ^vaph
-100 0,00208 0,643 8,33 1.55 0,120 310,53 577,44 267,4
-90 0,00495 0,651 3,63 1,63 0,275 320,88 582,38 261,5
-80 0,01074 0,661 1,79 1,51 0,558 331,34 587,32 256
-70 0,02118 0,671 0,941 1,49 1,061 341,81 592,35 250,5
-60 0,03871 0,682 0,534 1,47 1,87 352,32 597,41 245,1
-50 0,06687 0,695 0,323 1,44 3,10 362,91 602,44 239,5
-40 0,109 0,709 0,205 1,41 4,88 373,76 607,42 233,7
-30 0,1702 0,724 0,135 1,38 7,41 384,81 612,28 227,5
-20 0,2543 0,740 0,093 1,35 10,76 395,95 617,01 221,1
-10 0,3678 0,759 0,065 1,32 15,4 407,12 621,45 214,3
0 0,5168 0,779 0,0471 1,28 21,2 418,68 625,72 207
10 0,7083 0,800 0,0346 1,25 28,9 431,28 629,57 198,3
20 0,9474 0,824 0,0258 1,21 38,7 444,35 632,75 188,4
30 1,243 0,851 0,0194 1,175 51,5 458,12 635,35 177,2
40 1,6 0,883 0,0148 1,133 67,6 472,19 636,94 164,8
50 2,025 0,992 0,0113 1,008 88,5 486,67 637,94 151,3
Физические свойства важнейших веществ
437
Таблица 3.6.18
Термодинамические свойства насыщенного пара дихлорметана (СН2С12)
Г Р v' р' h h' Avaph .S’ x'
-30 0,0036 6,81 0,1469 384,8 751,1 366,3 4,0558 5,5626
-25 0,00491 5,08 0,1969 390,6 754,9 364,3 4,0788 5,5479
-20 0,00662 3,85 0,260 396,1 758,6 362,6 4,101 5,5337
-15 0,00878 2,95 0,339 401,5 762 360,5 4,1232 5,5199
-10 0,0116 2,28 0,439 407,4 765,8 358,4 4,1449 5,5069
-5 0,015 1,79 0,559 413,2 769,1 355,9 4,1663 5,4943
0 0,0193 1,416 0,706 418,7 772,5 353,8 4,1868 5,4822
5 0,0244 1,131 0,884 424,1 775,4 351,3 4,2073 5,4705
10 0,0308 0,912 1,096 430 778,7 348,8 4,227 5,4592
15 0,0385 0,741 1,349 435,4 781,3 345,8 4,2471 5,4479
20 0,0476 0,608 1,645 441,3 784,2 342,9 4,2663 5,4374
25 0,0585 0,502 1,99 446,7 786,7 340 4,2856 5,4265
30 0,0712 0,417 2,40 452.6 789,6 337 4,304 5,4165
35 0,0861 0,349 2,86 458 791,7 333,7 4,3225 5,4064
40 0,1034 0,295 3,39 463,9 794,2 330,3 4,3409 5,3964
Таблица 3.6.19
Термодинамические свойства насыщенного пара диэтилового эфира (С4Н10О)
T P V P' h h' Д,ч„/г
-17,78 0,0092 2,37 0,4213 376,81 774,56 397,7
-12,22 0,013 2,03 0,5318 390,75 787,19 396,4
-6,67 0,018 1,69 0,5959 403,57 798,98 395,4
-1,11 0,024 1,34 0,7496 415,2 809,22 394
4,44 0,031 1,06 0,9419 427,97 819,68 391,7
10,00 0,04 0,82 1,213 440,95 830,78 389,8
21,11 0,063 0,49 2,050 465,28 850 384,7
26,67 0,078 0,39 2,595 480,1 862,02 381,9
32,22 0,095 0,32 3,140 491,95 871,11 379,2
37,78 0,113 0,28 3,556 503,59 878,06 375,6
Таблица 3.6.20
Термодинамические свойства насыщенного пара 1.1,2-трифтор-1,2,2-трихлорэтана (фреона-113) (C2CI3F.O
T P V v' P P' h h' Ayap/z
-30 0,0028 0,594 3,910 1,68 0,256 393,27 561,2 167,93
-20 0,0053 0,601 2,204 1,66 0,453 401,64 567,14 165,5
-10 0,0091 0,609 1,309 1,64 0,764 410,14 573,13 162,99
0 0,0153 0,617 0,813 1,62 1,23 418,68 579,16 160,48
10 0,0244 0,626 0,526 1,60 1,90 427,39 585,27 157,88
20 0,0376 0,634 0,362 1,58 2,76 436,26 591,39 155,12
30 0,0559 0,644 0,243 1,56 4,12 445,31 597,54 152,23
40 0,0809 0,654 0,172 1,53 5,82 454,52 603,74 149,22
50 0,1137 0,665 0,125 1,50 8,00 463,9 609,93 146,04
60 0,1674 0,676 0,0931 1,48 10,73 473,49 616,09 142,6
70 0,21 0,688 0,0704 1,45 14,2 483,28 622,24 138,96
80 0,2774 0,701 0,0545 1,43 18,3 493,29 628,31 135,02
90 0,3592 0,715 0,0423 1,40 23,6 503,5 634,34 130,84
100 0,4574 0,730 0,0334 1,37 30,0 513,22 640,33 127,11
438
Новый справочник химика и технолога
Таблица 3.6.2!
Термодинамические свойства насыщенного пара трифторхлорметана (фреона-13) (CC1F3)
Т Р V V ' Р Р' ^vapk
-140 0,00088 0,576 12,380 1,760 0,0808 173,3
-130 0,00275 0,587 4,270 1,704 0,258 170
-120 0,00723 0,599 1,733 1,699 0,577 166,6
-НО 0,01665 0,612 0,798 1,634 1,253 162,4
-100 0,03435 0,626 0,407 1,596 2,45 158,3
-90 0,06485 0,642 0,226 1,558 4,43 154,1
-80 0,1135 0,658 0,1342 1,519 7,45 149,1
-70 0,1865 0,675 0,0844 1,480 11,85 144
-60 0,2911 0,695 0,0555 1,438 18,0 138,6
-50 0,4344 0,717 0,0379 1,394 26,4 132,7
-40 0,6242 0,741 0,02643 1,348 37,8 125,6
-30 0,8704 0,769 0,01890 1,300 53,0 118,1
-20 1,182 0,802 0,01374 1,246 72,7 109,7
-10 1,566 0,842 0,01010 1,187 99 100,1
0 2,036 0,894 0,00749 1,118 146 90
10 2,604 0,962 0,00547 1,040 182 77
20 3,284 1,079 0,00383 0,927 261 57,8
25 3,672 1,193 0,00302 0,838 335 42,7
28,8 3,988 1,721 0,00172 0,581 581 0
Таблица 3.6.22
Термодинамические свойства насыщенного пара фтортрихлорметана (фреона-11) (CC13F)
Т Р V V ' Р Р' h /?' 5 s'
-30 0,00993 0,623 1,530 1,604 0,653 393,6 587,4 193,8 4,0892 4,8868
-25 0,013 0,628 1,196 1,592 0,836 397,7 590,8 193 4,106 4,8847
-20 0,0167 0,633 0,944 1,580 1,059 401,9 594,5 192,6 4,1223 4,8835
-15 0,0213 0,638 0,753 1,568 1,328 406,1 597,9 191,8 4,1387 4,8822
-10 0,027 0,643 0,606 1,556 1,651 410,3 601,2 190,9 4,155 4,881
-5 0,0337 0,648 0,492 1,544 2,03 414,5 604,6 190,1 4,1709 4,8801
0 0,042 0,653 0,402 1,532 2,49 418,7 607,9 189,2 4,1868 4,8797
5 0,0517 0,658 0,332 1,520 3,02 422,9 611,3 188,4 4,2027 4,8797
10 0,0631 0,663 0,275 1,508 3,63 427,5 614,6 187,1 4,2182 4,8793
15 0,0766 0,638 0,230 1,496 4,34 431,7 617,6 185,9 4,2337 4,8793
20 0,0923 0,674 0,194 1,484 5,17 436,3 620,9 184,6 4,2488 4,8789
25 0,1104 0,679 0,164 1,472 6,11 440,9 624,3 183,4 4,2638 4,8789
30 0,1317 0,685 0,139 1,460 7,18 445,1 626,8 181,7 4,2789 4,8789
35 0,1550 0,691 0,119 1,448 8,40 449,7 629,7 180 4,294 4,8785
40 0,1824 0,696 0,102 1,436 9,77 454,3 632,6 178,4 4,3086 4,8785
45 0,2128 0,702 0,088 1,424 11,3 458,9 635,6 176,7 4,3233 4,8785
50 0,2483 0,708 0,077 1,412 13,1 463,5 638,1 174,6 4,3379 4,878
Таблица 3.6.23
Термодинамические свойства насыщенного пара хлорметана (СН3С1)
Т р V V ' Р Р' h h' ^vapk 5 s'
-60 0,0161 0,936 2,26 1,068 0,442 328,7 789,2 460,5 3,8142 5,975
-55 0,0219 0,944 1,715 1,059 0,583 335,8 792,1 456,4 3,8481 5,9407
-50 0,029 0,953 1,297 1,050 0,771 342,9 795,1 452,2 3,8812 5,908
-45 0,038 0,961 1,008 1,041 0,992 350,4 798,4 448 3,9142 5,877
-40 0,049 0,970 0,794 1,031 1,259 357,6 801,4 443,8 3,9461 5,8485
-35 0,0627 0,978 0,632 1,023 1,583 365,1 804,3 439,2 3,9775 5,8213
-30 0,0793 0,986 0,508 1,014 1,97 372,6 807,2 434,6 4,0089 5,7958
Физические свойства важнейших веществ
439
Окончание табл. 3.6.23
Т Р V У Р Р' И h' &mph 5 5 '
-25 0,0992 0,995 0,412 1,005 2,43 380,2 810,1 430 4,0394 5,7719
-20 0,1228 1,003 0,338 0,997 2,96 387,7 813,1 425,4 4,0696 5,7493
-15 0,1507 1,013 0,279 0,988 3,58 395,7 816 420,4 4,0997 5,7284
-10 0,1832 1,022 0,233 0,979 4,30 403.2 818,5 415,3 4,129 5,7079
-5 0,2209 1,032 0,195 0,970 5,13 410,7 821 410,3 4,1579 5,6882
0 0,2644 1,042 0,1648 0,960 6,07 418,7 824 405,3 4,1868 5,6698
5 0,314 1,053 0,1402 0,950 7,13 426,6 826,1 399,4 4,2153 5,6518
10 0,3703 1,064 0,1198 0,940 8,34 434,6 828,6 394 4,2433 5,635
15 0,4341 1,075 0,1031 0,930 9,70 442,1 830,7 388,5 4,271 5,6187
20 0,5059 1,086 0,0891 0,921 11,22 450,1 832,8 382,7 4,2986 5,6032
25 0,586 1,098 0,0774 0,911 12,93 458,5 834,8 376,4 4,3254 5,5881
30 0,6746 1,110 0,0675 0,901 14,82 466,4 836,5 370,1 4,3522 5.5735
35 0,7726 1,123 0,0591 0,891 16,92 474,4 838,2 363,8 4,379 5,5592
40 0,8805 1,135 0,0520 0,881 19,2 482,3 839,9 357,6 4,4049 5,5463
45 0,9991 1,149 0,0460 0,870 21,8 490,7 841,5 350,9 4,4309 5,5329
50 1,1288 1,164 0,0408 0,859 24,5 499,1 842,8 343,7 4,4568 5,5211
Таблица 3.6.24
Термодинамические свойства насыщенною пара тетрахлорметана (СС14)
Т Р у' Р' h h'
-6,67 0,0028 4,34 0,2303 414,03 633,71 219,68
-1,11 0,0043 3,31 0,3021 418,09 636,06 217,96
4,44 0,006 2,50 0,4005 422,4 639,2 216,79
15,56 0,0101 1,50 0,6673 432,54 646,99 214.45
21,11 0,0132 1,22 0,8214 437,77 650,17 212,61
26,67 0,0171 0,999 1,016 441,46 650,96 209,51
32,22 0,0222 0,812 1,232 445,66 655,07 209,38
37,78 0,0285 0,624 1,602 449,85 657,79 207,96
43,33 0,0349 0,530 1,884 455,43 661,77 206,33
48,89 0,0424 0,470 2,135 460,67 664,99 204,44
Таблица 3.6.25
Термодинамические свойства насыщенного пара этана (С2Н6)
Т Р V у' Р Р' /г /г' &vaph 5 5'
-100 0,0542 1,789 0,889 0,559 1,125 148,6 649,4 500,7 2,9915 5,882
-95 0,0733 1,808 0,673 0,553 1,486 160,8 654,8 494 3,4792 5,833
-90 0,0973 1,825 0,518 0,548 1,932 173,3 660,3 486,9 3,1284 5,7874
-85 0,1268 1,844 0,405 0,542 2,47 185,5 665,7 480,2 3,1954 5,746
-80 0,1627 1,863 0,321 0,537 3,12 197,6 670,7 472,7 3,2594 5,7074
-75 0,2064 1,884 0,257 0,531 3,89 210,2 675,7 465,6 3,3218 5,671
-70 0,2583 1,905 0,208 0,525 4,80 222,7 680,8 458 3,3834 5,6379
-65 0,3196 1,927 0,171 0,519 5,86 234,9 685,4 450,5 3,4428 5,6061
-60 0,3912 1,951 0,1409 0,513 7,10 247,4 690 442,5 3,5018 5,5768
-55 0,4744 1,976 0,1173 0,506 8,53 260 694,2 434,2 3,5588 5,5488
-50 0,5701 2,003 0,0983 0,499 10,17 272,6 698,4 425,8 3,6149 5,5224
-45 0,6793 2,032 0,0830 0,492 12,05 285,5 702,1 416,6 3,6706 5,4973
-40 0,8034 2,062 0,0705 0,485 14,19 298,5 705,5 407 3,7267 5,473
-35 0,9432 2,093 0,0601 0,478 16,63 311,9 708,8 396,9 3,7836 5,4495
-30 1,1 2,128 0,0515 0,470 19,41 326,2 711,8 385,6 3,8406 5,4269
-25 1,275 2,167 0,0444 0,462 22,5 340,4 714,7 374,3 3,8992 5,4068
-20 1,47 2,209 0,0383 0,453 26,1 355,5 716,8 361,3 3,9549 5,383
-15 1,685 2,255 0,0332 0,444 30,2 371 718,9 347,9 4,0135 5,3612
440
Новый справочник химика и технолога
Окончание табл. 3.6.25
т Р V v' Р р' h IT s s'
-10 1,921 2,305 0,0288 0,434 34,7 386,4 720,5 334,1 4,0708 5,3403
-5 2,181 2,364 0,0250 0,423 40,0 402,4 721,4 319 4,1286 5,3189
0 2,464 2,429 0,0218 0,412 46,0 418,7 721,8 303,1 4,1868 5,2971
5 2,775 2,503 0,0188 0,400 53,2 435,8 721 285,1 4,2463 5,2712
10 3,1 16 2,586 0,0161 0,387 62,0 454,3 718,5 264,2 4,3082 5,2415
15 3,489 2,706 0,0137 0,370 73,2 46,47 712,6 239,1 4,3731 5,2025
20 3,9 2,856 0,01143 0,350 87,5 494,9 705,1 210,2 4,4003 5,1594
25 4,355 3,07 0,00937 0,326 106,7 518,3 693,3 175 4,518 5,105
30 4,864 3,49 0,00706 0,286 142 553,1 666,1 113 4,6273 5,0003
31 4,975 3,69 0,00643 0,271 156 565,2 654,8 89,6 4,6662 4,9605
32,3 5,097 4,70 0,00470 0,203 203 610,4 610,4 0 4,8123 4,8123
Таблица 3.6.26
Термодинамические свойства насыщенного пара хлорэтана (С2Н5С1)
T P V v' P p' h h' &.vaph
-30 0,016 1,034 2,24 0,9670 0,446 365,1 786,7 421,6
-20 0,026 1,050 1,331 0,9526 0,751 382,7 798 415,3
-10 0,042 1,068 0,859 0,9382 1,163 400,7 808,9 408,2
0 0,064 1,081 0,575 0,9236 1,740 418,7 819,8 401,1
10 0,095 1,100 0,397 0,9089 2,520 436,7 830.2 393,6
20 0,138 1,118 0,2818 0,8941 3,549 454,7 840,7 386
30 0,194 1,139 0,2053 0,8794 4,876 472.3 850,3 378,1
40 0,264 1,158 0,1524 0,8643 6,554 490,3 860 369,7
50 0,356 1,177 0,1159 0,8492 8.624 508.3 869,6 361,3
Таблица 3.6.27
Термодинамические свойства насыщенного пара этилена (С2Н4)
T P V v' P P' h IT
-116 0,0481 1,71 1,004 0,585 0,996 76,74 574,72 497,98
-110 0,0712 1,73 0,693 0,578 1,44 89 578,7 489,6
-100 0,1294 1,78 0,378 0,571 2,65 110,49 585,44 474,95
-90 0,2199 1,82 0,233 0,550 4,30 132,81 592,68 459,88
-80 0,3516 1,87 0,150 0,535 6,67 156,29 600,81 444,51
-70 0,535 1,93 0,101 0,518 9,90 180,95 608,72 427,77
-60 0,7812 2,00 0,0712 0,500 14,05 206,79 616,63 409,85
-50 1,098 2,08 0.0516 0,480 19,4 234,46 624,54 390,08
-40 1,499 2,16 0,0378 0,463 26,4 263,77 628,02 364,25
-30 1,995 2,27 0,0277 0,440 36,1 295,17 628,94 333,77
-20 2,807 2,41 0,0202 0,415 49,5 329,84 624,08 294,25
-10 3,339 2,60 0,0146 0,384 68,4 369,82 617,3 247,48
0 4,226 2,90 0,0100 0,345 100 418,68 602,48 183,8
9,9 5,213 4,63 0,00463 0,227 227 527,96 527,96 0
3.6.4. Термодинамические функции Дебая
для кристаллических веществ
Функции Дебая предназначены для вычисления атомной теплоемкости (при постоянном объеме) кристал-
U-U. A-U.
лических веществ, а также величин --, ------ и 5.
Т Т
В табл. 3.6.28 и 3.6.29 приведены следующие параметры:
0 — характеристическая температура, К (параметр, связанный с частотой собственных колебаний):
Q _ ^^собств к
где h — постоянная Планка, равная 6,6260755 • 10”34 Дж • с; Мсобств — частота, с '; к — постоянная Больцмана, равная 1,380658 • 10”23 Дж/К. Из спектра собственных час
Физические свойства важнейших веществ
441
тот твердого тела для вычисления 0 берут максималь-
с , 1
ную частоту. Так как сособггв = —, а л = —, то:
А. ®
@ = 4o6cnL = ^£==^£^ = ] 439й)
к кк к
где с — скорость света; w — волновое число, м
Условные обозначения:
Т — абсолютная температура, К; С,. — функция Дебая, Дж/(моль • К); U — внутренняя энергия, Дж/моль; С — молярная теплоемкость при постоянном объеме, Дж/(моль • К); А — энергия Гельмгольца, Дж/моль; S— энтропия, ДжДмоль • К).
Таблица 3.6.28
Термодинамические функции Дебая
0 Т с„ 11 -11 т = - \cdt тJ 0 ‘ 0 5 = ^ 7
0 24,95 24,958
0,1 24,95 24,028 66,7 90,73
0,2 24,91 23,136 50,33 73,48
0,3 24,87 22,261 41,11 63,39
0,4 24,79 21,415 34,83 56,27
0,5 24,66 20,586 30,14 50,74
0,6 24,53 19,787 26,46 46,26
0,7 24,37 19,008 23,47 42,5
0,8 24,2 18,263 20,98 39,24
0,9 24,03 17,543 18,87 36,42
1,0 23,78 16,835 17,09 33,92
U 23,53 16,153 15,49 31,64
1,2 23,24 15,487 14,1 29,59
1,3 22,99 14,859 12,89 27,75
1,4 22,69 14,243 11,82 26,06
1,5 22,4 13,657 10,86 24,51
1,6 22,06 13,088 9,99 23,08
1,7 21,73 12,539 9,215 21,75
1,8 21,35 12,004 8,512 20,52
1,9 20,98 11,48 7,871 19,35
2,0 20,6 10,995 7,298 18,29
2,1 20,22 10,534 6,77 17,3
2,2 19,85 10,086 6,293 16,38
2,3 19,47 9,6589 5,857 15,52
2,4 19,05 9,2403 5,451 14,69
2,5 18,59 8,8341 5,083 13,92
2,6 18,17 8,4531 4,744 13,2
2,7 17,75 8,0847 4,43 12,51
2,8 17,33 7,7288 4,145 7,687
2,9 16,91 7,3939 3,877 11,27
3,0 16,52 7,0715 3,631 10,7
3,1 16,08 6,7617 3,404 10,17
3,2 15,66 6,4644 3,193 9,659
3,3 15,28 6,1839 2,999 9,182
3,4 14,86 5,9159 2,821 8,738
Продолжение табл. 3.6.28
0 Т С„ т 1 0 т 'гсгг'г J 2 jf <7/ 0 1 0 5 = ^ т
3,5 14,44 5,6647 2,65 8,315
3,6 14,07 5,4219 2,495 7,917
3,7 13,69 5,1874 2,352 7,54
3,8 13,31 4,9614 2,216 7,176
3,9 12,94 4,7436 2,092 6,837
4,0 12,56 4,5343 1,973 6,506
4,1 12,18 4,3417 1,864 6,205
4,2 11,85 4,1617 1,764 5,924
4,3 11,85 3,99 1,67 5,661
4,4 11,18 3,8225 1,582 5,405
4,5 10,84 3,6593 1,499 5,158
4,6 10,51 3,5044 1,42 4,924
4,7 10,17 3,3536 1,346 4,702
4,8 9,839 3,2071 1,276 4,484
4,9 9,504 3,0647 1,209 0,088
5,0 9,211 2,9391 1,148 4,087
5,2 8,625 2,6963 1,037 3,734
5,4 8,122 2,4911 0,943 3,434
5,6 7,62 2,2944 0,858 3,152
5,8 7,118 2,1101 0,78 2,89
6,0 6,615 1,9343 0,707 2,641
6,2 6,196 1,7836 0,644 2,428
6,4 5,778 1,6454 0,59 2,235
6,6 5.443 1,5324 0,544 2,076
6,8 5,108 1,4193 0,501 1,92
7,0 4,765 1,3105 0,46 1,77
7,2 4,472 1,2184 0,425 1,643
7.4 4,191 1,1304 0,393 1,523
7,6 3,927 1,0551 0,364 1,419
7,8 3,684 0,9797 0,337 1,317
8,0 3,479 0,9211 0,315 1,236
8,2 3,312 0,8709 0,297 1,168
8,4 3,144 0,8206 0,281 1,101
8,6 2,985 0,7787 0,264 1,043
8,8 2,826 0,7327 0,247 0,98
9,0 2,667 0,6866 0,232 0,919
9,2 2,508 0,6448 0,217 0,862
9,4 2,349 0,6029 0,202 0,805
9,6 2,194 0,561 0,188 0,749
9,8 2,039 0,5192 0,175 0,694
10 1,888 0,4815 0,162 0,643
11 1,436 0,363 0,121 0,484
12 1,118 0,2814 0,094 0,375
13 0,879 0,2206 0,073 0,294
14 0,703 0,1758 0,059 0,234
15 0,574 0,1436
16 0,473
17 0,394
18 0,331
19 0,281
20 0,243
21 0,209
22 0,181
442
Новый справочник химика и технолога
Окончание табл. 3.6.28
0 Т с„ 7 0 4-Ц, г. Т ''dr1?, 0 1 0 5 = ^ Т
23 24 25 26 27 28 29 30 0,159 0,14 0,124 0,11 0,098 0,088 0,079 0,072
Таблица 3.6.29
Характеристические температуры по Дебаю 0 некоторых простых веществ в кристаллическом состоянии
Вещество p • 10 ’. кг/м’’ С.,, “c 0
Ag 10,5 960 215
Al 2,7 660 390
Au 19,3 1063 170
В 2,3 2075 1150
Ba 3,5 717 115
Bi 9,8 271 80
Ca 1,55 850 230
Cd 8.6 321 135
Co 8,9 1492 385
Cr 6,9 1890 415
Cu 8,9 1083 315
Fe 7,9 1530 400
Ge 5,4 959 400
К 0,9 63 110
Mg 1,7 651 350
Mo 10,2 2625 280
Na 1,0 97,8 190
Ni 8,9 1453 360
Pb 11,3 327 88
Pt 21,5 1769 210
Sb 6,7 630 140
Sn 7,3 232 110
Ti 4,5 1725 410
U 18,7 1133 140
W 19,3 3380 300
Zn 7,1 419 210
3.6.5. Термодинамические функции Эйнштейна для линейного гармонического осциллятора
Функции Эйнштейна СЕ предназначены для вычисления колебательной составляющей теплоемкости таза Q кол по формуле:
3/V-5(6)
Q, кол = Z СЕ • К),
1
где N — число атомов в молекуле газа; (3N - 5) — число видов колебаний в линейных молекулах; (3N - 6) —
число видов колебаний в нелинейных молекулах, а СЕ определяется по формуле:
Дж/(моль • К).
Остальные обозначения в табл. 3.6.30 те же, что и в табл. 3.6.28.
Таблица 3.6.30
Функции Эйнштейна для линейного гармонического осциллятора
0 T CE T 1 0 S = - T = 0 1 0
0 8,315 8,315 oc 00
0,10 8,302 7,905 27,47 19,55
0,15 8,294 7,708 23,99 16,29
0,20 8,286 7,331 21,73 14,19
0,25 8,273 7,314 19,85 12,52
0,30 8,265 7,126 18,38 1 1,22
0,35 8,235 6,946 17,08 10,13
0,40 8,206 6,762 15,99 9,211
0,45 8,173 6,582 15,07 8,457
0,50 8,143 6,41 14,15 7,746
0,55 8,114 6,238 13,4 7,155
0,60 8,072 6,067 12,69 6,619
0,65 8,03 5,903 12,05 6,142
0,70 7,988 5,74 11,46 5,71 1
0,75 7,938 5,585 10,9 5,317
0,80 7,888 5,43 10,39 4,961
0,85 7,834 5,275 9,919 4,639
0,90 7,779 5,125 9,471 4,342
0,95 7,721 4,987 9,052 4,07
1,00 7,658 4,84 8,658 3,814
1,05 7,595 4,702 8,286 3,584
1,10 7,494 4,564 7,934 3,366
1,15 7,461 4,4296 7,599 3,165
1,20 7,39 4,3 7,285 2,981
1,25 7,314 4,174 6,984 2,809
1,30 7,239 4,053 6,699 2,646
1,35 7,164 3,931 6,427 2,495
1,40 7,084 3,814 6,016 2,357
1,45 7,005 3,697 5,92 2,223
1,50 6,946 3,584 5,686 2,102
1,55 6,837 3,471 5,46 1,985
1,60 6,749 3,366 5,242 1,876
1,65 6,665 3,262 5,037 1,775
1,70 6,573 3,161 4,84 1,679
1,75 6,485 3,061 4,652 1,587
1,80 6,393 2,964 4,467 1,503
1,85 6,301 2,872 4,296 1,424
1,90 6,209 2,78 4,128 1,348
1,95 6,117 2,65 3,969 1,277
Физические свойства важнейших веществ
443
Продолжение табл. 3.6.30
0 Т 7 = — [Cdt Т J Т T ’rdT'r. 0 1 о
2,00 6,025 2,604 3,814 1,21
2,10 5,832 2,437 3,525 1,084
2,20 5,644 2,282 3,257 0,976
2,30 5,451 2,135 3,01 0,879
2,40 5,259 1,993 2,784 0,791
2,50 5,066 1,859 2,571 0,712
2,60 4,873 1,733 2.378 0,641
2,70 4,685 1,616 2,198 0,578
2,80 4,497 1,507 2,031 0,523
2,90 4,312 1,407 1,876 0,469
3,00 4,128 1,306 1,733 0,427
3,10 3,948 1,218 1,599 0,385
3,20 3,772 1,13 1,478 0,348
3,30 3,601 1,051 1,365 0,314
3,40 3,433 0,9755 1,26 0,281
3,50 3,27 0,9085 1,16 0,255
3,60 3,115 0,8415 1,072 0,23
3,70 2,96 0,7829 0,988 0,209
3,80 2,814 0,7243 0,913 0,188
3,90 2,667 0,6699 0,842 0,172
4,00 2,529 0,6196 0,775 0,155
4,20 2,269 0,5317 0,657 0,126
4,40 2,026 0,4564 0,557 0,105
4,60 1,805 0,3881 0,473 0,084
4,80 1,625 0,3308 0,402 0,067
5,00 1,419 0,2818 0,339 0,059
5,20 1,256 0,2399 0,285 0,046
5,40 1,097 0,2039 0,243 0,038
5,60 0,9713 0,1729 0,205 0,029
5,80 0,8541 0,1478 0,172 0,025
6,00 0,7453 0,1243 0,147 0,021
Окончание табл. 3.6.30
0 T T 1 , ~p\cdt 1 0 5 = ^-^-Т 0 1 0
6,40 0,5694 0,1051 0,1 0,013
6,80 0,4312 0,0632 0,071 0,008
7,20 0,3224 0,0448 0,059 0,004
7,60 0,2386 0,0318 0,038 0,004
8,00 0,1788 0,0222 0,025 0,004
8,40 0,134 0,0159 0,017
8,80 0,0963 0,0126 0,013
9,20 0,0712 0,0075 0,008
9,60 0,0502 0,0054 0,004
10,00 0,0377 0,0038 0,004
11 0.0167 0,0017
12 0,0071 0,0004
13 0,0029
3.6.6. Эмпирические данные и зависимости для вычисления термодинамических параметров
Ниже приведены эмпирические зависимости, которые дают возможность приближенно определять некоторые термодинамические величины и параметры, если в литературе отсутствуют точные данные.
Теплоемкости (см. также расчет Az//2°98, С/? и S^g органических веществ в идеализированном газовом состоянии).
Твердые и жидкие неорганические вещества:
CI> =YjC>n‘ ДжАмоль • к)
где п, — число атомов в молекуле; Cz — атомные теплоемкости, Дж/(моль • К) — см. табл. 3.6.31.
Таблица 3.6.31
Атомные теплоемкости С, твердых и жидких веществ, Дж/(моль • К)
Элементы С Н N в Be О Si }’ S Р Остальные элементы
С, твердых веществ С, жидких веществ 7,54 11,72 9,63 18,0 11,3 11,72 19,68 15,91 16,75 25,12 20,1 24,28 20,93 29,31 22,61 30,98 23,02 29,31 25,94-26,78 33,47
Газообразные алканы:
Ср = 4,0 + 1,3и + 0,0\2пТ кал/(моль • К) (от 400 до 800 К);
Ср = 2,56 + 0,51 и + (0,0013и2 + 0,0044и - 0,00065пт + + 0,00495w - 0,0057)7" кал/(моль • К),
где п — число атомов углерода в молекуле (и > 3); т — число атомов водорода в молекуле; Т—температура, К. Для перехода в систему СИ — Дж/(моль • К) — полученную величину следует умножить на 4,1868.
Сплавы, шлаки, стекла, растворы:
С = )Т,С,+)Т2С2+... .
100
где W|, w2 — массовые доли компонентов, %; ct, c-i — их удельные теплоемкости, Дж/(кг • К).
Примечание. При значительных теплотах смешения (растворения) расчет по приведенной формуле дает завышенные результаты.
444
Новый справочник химика и технолога
Стандартные энтальпии образования газообразных органических соединений (см. также расчет
&fH^,C и 5208 органических веществ
в идеализированном газовом состоянии).
А/^298 =^^2(Ч£/)исх вещ + Si Qi во ir j ~ р-ции кДж/моль,
где п, и mt — число связей данного вида в исходных веществах и в продуктах реакции; — энергия разрыва данной связи, кДж/моль (табл. 3.6.32); я, — число атомов твердых элементов; (7, возг — теплота возгонки твердых исходных веществ.
Примечание. Формула наиболее точна для алифатических углеводородов и спиртов.
Примеры.
1. Расчет стандартной энтальпии образования СН3СООН(г.).
2Н?(г.) + О2(г.) + 2С(графит) = СН3СООН(г.).
При образовании СН3СООН(г.) из простых веществ разрываются две связи Н—Н, одна связь 0=0, возгоняются два грамм-атома С и образуются три связи Н—С, связь С—С и группа СООН. Поэтому (табл. 3.6.32):
A , = 2s(H—Н) + 8(0=0) + 2£>ВОЗГ(С) -
- 38(Н—С) - 8(С—С) - 8(С00Н) -
= 2 • 432,1 + 490,7 + 2 • 523,4 - 3 • 358,4 - 262,9 -
- 1507 = -443,8 кДж/моль
По литературным данным A f Н^ = -436,7 кДж/моль.
2. Расчет стандартной теплоты образования СН31(г.).
С(графит) + 1,5Н2 + 0,512(тв.) = СН31(г.)
A f = 22воДС) + 1,58(Н—Н) + О,50возг(12) +
+ 0,58(1-1) 38(Н - С)-8(С-1) =
= 523,4 + 1,5 • 432,1 + 0,5 • 62,3* + 0,5 • 149,1 -
-3 -358,4- 180 = 21,8 кДж/моль
По литературным данным A f H°9i = 20,5 кДж/моль.
Таблица 3.6.32
Энергии связей и групп
Связь 8, кДж/моль
н-н 432,1
н-с 358,4
Н-N (в NH3) 348,8
н-о 418,7
H-F 561
* См. табл. 3.6.1.
Продолжение табл. 3.6.32
Связь 8. кДж/моль
Н-С1 427,5
Н-Вт 359,6
H-I 295,6
Н-Р 263,8
H-S 343,3
С(графит) —» С(г.) 523,4
с-с 262.9
с=с 423,7
с=с 536,7
C-N -224
C=N -351,7
C=N (в HCN) 611,3
C=N (в нитрилах) 623,8
C=N (в изоцианидах) 582
С—0 (в спиртах) 314
С—0 (в эфирах) 314
С=О (в Н2С=О) 602,9
С=О (в других альдегидах) -628
С=О (в кетонах) 653.1
С=О (в СО) - 937,8
С=О (в СО2) 703,4
СООН (в НСООН)* 1457
СООН (в других кислотах)* 1507
СООС (в формиатах)* 1310
СООС (в других эфирах)* 1369
C-F -435,4
С-С1 293,1
С-Вг 238,6
С-1 180
c-s 226,1
C=S(bCS2) 491,9
с—Si 241,2
N-N -113
N=N -334,9
N=N 712,6
N-0 -255,4
N=O -452,2
N=O(bNO) 626,3
no2* 707,6-778,7
N-Cl 160,8
0=0 490,7
o-ci 206,4
P=P 485,7
s-ci 239,5
s=o 386
s-s 429,6
s=s -422,9
F-F -154,9
Cl-Cl 239,5
Cl—Br 220,6
CI-1 213,5
Br—Br 190,2
I-I 149,1
Na—Na 74,53
Физические свойства важнейших веществ
445
Окончание табл. 3.6.32
Связь £. кДж/моль
к-к 49,4
Na-Cl 408,2
Na—Вг 367,2
Si-0 425
в-с 293,1
* Имеется в виду разрыв всех связей. См. пример расчета.
Энтальпии сгорания органических соединений в газообразном состоянии
А с //'од -(204,2/7 + 44,4т + Lx) кДж/моль, где п — число атомов кислорода, необходимое для полного сгорания вещества; т — число молекул воды, образующейся при сгорании молекулы вещества; х — термическая характеристика (поправка) для соответствующей группы атомов или типа связи, кДж/моль.
На основании приведенных в табл. 3.6.33 значений термических характеристик отдельных групп атомов и связей могут быть вычислены термические характеристики самых разнообразных органических соединений. Для этой цели, руководствуясь структурной формулой, суммируют значения х отдельных групп и связей, входящих в соединение.
Пример.
Вычисление энтальпии сгорания газообразного коричного альдегида С6Н5СН=СНСНО.
Термическая характеристика коричного альдегида складывается из значений х:
Фенильная группа 100,5
Двойная связь 87,9
Альдегидная группа 75,4
х = 263,8 кДж/моль
Реакция сгорания:
С6Н5СН=СНСНО + 10,5О2 = 9СО2 + 4Н2О; п = 21; т = 4.
Дс//298 = -(204,2 • 21 + 44,4 • 4 + 263,8) =
= -4727,9 кДж/моль.
Таблица 3.6.33
Числовые значения термической характеристики
Группы атомов и типы связей Термическая характеристика х. кДж/моль
Ординарная связь С—С 0
Двойная связь С—С 87,9
Тройная связь С=С 213,4
Фенильная группа R—С6Н5 100,5
Спиртовая группа R—СН2ОН 50,2
Простые эфиры R—О—R 87,9
Альдегидная группа R—СПО 75,4
Кетогруппа R—СО—R 50,2
Окончание табл. 3.6.33
Группы атомов и типы связей Термическая характеристика х, кДж/моль
Кислотная группа в одноосновной кислоте R—СООН Кислотные группа в двухос- 0
новной кислоте HOOC-R-COOH Алкилциклогексаны 12,6
0
Алкилциклопентаны
R 25,1
Энтальпии сгорания органических соединений в жидком состоянии
Расчет основан на ряде допущений:
1. При сгорании происходит перемещение валентных электронов от атомов органического соединения к атомам кислорода.
2. От каждого атома углерода переходит 4 электрона, от каждого атома водорода — 1 электрон.
Энтальпия перемещения 1 моль электронов:
А//=-109,07 кДж/моль.
Таким образом:
А с //n98 = -109,07 (4с + И) кДж/моль, где с — число атомов углерода; h — число атомов водорода в молекуле вещества.
3. Если водород в соединении замещен другим атомом или 1руппой атомов, то изменяется электронная структура молекулы и энтальпия сгорания соединения увеличивается или уменьшается на величину структурной поправки а (табл. 3.6.34). При этом число перемещенных к кислороду электронов уменьшается на величину р, равную числу электронов, прочно связанных с атомами, замещающими в соединении атомы водорода (например, с атомами кислорода, галогенов и г. п.). Тогда:
Ас//2°98 = [-109,07 (4с + h- р) + La] кДж/моль.
Примеры.
1. Расчет энтальпии сгорания проп-2-ен-1-ола (аллилового спирта) СН2=СНСН2ОН:
4с+ h- p = 4- 3 + 6- 2= 16
(два электрона в молекуле спирта связаны с атомом кислорода, поэтому р = 2).
Структурные поправки:
а) на двойную (этиленовую) связь:
a = -54,4 кДж/моль;
446
Новый справочник химика и технолога
б) на связь первичного алифатического радикала с гидроксильной группой (первичный спирт):
а = -54,4 кДж/моль.
Таким образом:
Ас/Л°98 =-109,07- 16-54,4-54,4 = -1853,9 кДж/моль.
По литературным данным А^^ =-1853,1 кДж/моль.
2. Расчет теплоты сгорания 1-метил-2-нитробснзола
CH3C6H4NO2:
4с + Z? — /? = 4 • 7 + 7 — 1 =34
{один электрон углерода связан с атомом азота и оста-
Структурные поправки:
а) на связь ароматического радикала с группой -NO?:
а = -54,4 кДж/моль;
б) на связь ароматического и алифатического радикалов Rap~Ra/
а = +14,7 кДж/моль.
Ас//2°98 =- -109,07 • 34 - 54,4 + 14,7 = -3748 кДж/моль.
По литературным данным А с = -3764,8 кДж/моль.
ется у него после сгорания, поэтому р = 1).
Таблица 3.6.34
Числовые значения структурной поправки
Характер группировок, заместителей и связей Структурная поправка а, кДж/моль Примечания
Связь между алифатическим и ароматическим радикалами Rai—Rap Связь между ароматическими радикалами Rap-Rap Двойная связь С—С Двойная связь в г/г/с-сосдинсниях С=С Двойная связь в ш^ш/с-сосдинениях С=С Связь между ароматическим радикалом и винильным Rap—СП—СП? или ацетиленильным Rap—С^СН радикалами Двойная связь в замкнутом цикле Тройная связь — С=СН Группировка —С=С—, не связанная с водородом Связь между первичным алифатическим радикалом и гидроксильной группой (первичный спирт) Связь между вторичным алифатическим радикалом и гидроксильной группой (вторичный спирт) Связь между третичным алифатическим радикалом и гидроксильной группой (третичный спирт) Связь между ароматическим радикалом и гидроксильной группой 14,7 27,2 -54,4 -69,1 -54,4 27,2 -27,2 -193 -138,6 -54,4 -27,2 -14,7 -14,7 При сгорании атомов углерода, один из которых принадлежит к ароматическому, а другой — к алифатическому радикалам, будут перемещаться все электроны, имеющиеся у этих атомов; р = 0 При сгорании перемещаются все электроны у атомов углерода. Число структурных поправок для многядерных соединений равно числу «спаек» ядер При сгорании углерода, связанного с гидроксильной группой, перемещаются не все электроны, а только три. Нс перемещается электрон, участвующий в образовании связи между углеродом и кислородом, а также электрон водорода, находящегося в гидроксильной группе, р = 2 То же » То же, что и для алифатических спиртов
Физические свойства важнейших веществ
447
Продолжение табл. 3.6.34
Характер группировок, заместителей и связей Структурная поправка а, кДж/моль Примечания
Простые эфиры алифатические и ароматические RM(Rap) — О-(Rap)Ra., Сложные алифатические эфиры R^-COO-Raa Альдегидная группа в алифатических и ароматических соединениях Кетонная группа в алифатических и ароматических соединениях а-Оксокислоты R—С(=О)—СООН а-Гидроксикислоты ^С(ОН)—СООН Группировка R—С(=О)—С(=О)—R Фрагменты циклопропана в карбоновых кислотах Фрагменты циклобутана в карбоновых кислотах Лактоны типа ЧУ^О Ангидриды карбоновых кислот Первичные алифатические амины r,-nh2 Вторичные алифатические амины Ran-Nil — Ral Третичные алифатические амины Первичные ароматические амины Rap-NH2 Вторичные ароматические амины Rap-NH-Rap Третичные ароматические амины (RaphN Амиды и гидразины ^N—С(=О)—Rap и-NH-NC Ацетанилиды Rap—NH—С(=О)—СН3 Связь между углеродом и цианогруппой —C=N в алифатических и ароматических соединениях Ароматические нитрилы -81,6 -69,1 -54,4 -27,2 -54,4 -27,2 -54,4 -54,4 -54,4 -54,4 -41,9 -54,4 -81,6 -108,9 -27,2 -54,4 -81,6 -27,2 14,7 -69,1 27,2 Углерод, связанный с кислородом, перемещает при сгорании только три электрона; р = 1 • 2 р = 4 В альдегидной группе углерод, связанный с кислородом, перемещает при сгорании два электрона; р = 2 То же Если радикал R—СО— связан с группой —СООН, то на эту связь вводят указанную поправку, вообще же группа —СООН такой поправки не имеет. При сгорании углерод карбоксильной группы перемещает только один электрон Поправка вводится только при связи группы ^С(ОН)— с группой —СООН. Остальное см. выше (в н. «а-Оксокислоты») Поправку вводят только в том случае, если радикал R—С(=О)— связывается с подобным радикалом Углерод, связанный с аминогруппой, перемещает при сгорании все свои электроны. При подсчете числа перемещающихся электронов учитывают также электроны, имеющиеся у водорода, связанного непосредственно с азотом То же » » » То же. Жирноароматические третичные амины рассматривают как третичные ароматические Углерод, связанный с азотом в цианогруппе, при сгорании перемещает все четыре электрона При расчете Ас//2°98 вводят две поправки: на связь между углеродом и группой —C=N и на наличие самой нитрильной группы
448
Новый справочник химика и технолога
Окончание табл. 3.6.34
Характер группировок, заместителей и связей Структурная поправка а. кДж/моль Примечания
Изоцианогруппа RM—N=C в алифатическом ряду HnTpoipyinia — NO2 в алифатических -138,6 -54,4 При сгорании углерод, связанный с нитро^уп-
и ароматических соединениях Хлор в ароматических соединениях -27,2 пой, перемещает не все электроны, а на один меньше, 1. к. этот электрон при сгорании соединения остается у азота нитрогруппы, восстанавливающегося в процессе сгорания; р 1 В галогенсодержащих соединениях при сгора-
Rap-Cl Хлор в алифатических соединениях -54,4 нии атом углерода, связанный с галогеном, перемещает нс все электроны, а на один меньше; Р= 1 То же
R^-Cl Бром в ароматических соединениях -54,4 »
Rap-Br Бром в алифатических соединениях -54,4 »
Raj, —Вг Иод в ароматических соединениях Rap—I -167,9 »
Иод в алифатических соединениях Ra., —1 -167,9 »
Энтальпии испарения неполярных жидкостей
(Дж/моль) при нормальной температуре кипения
\Н
-а'- ~ 36,61 +19,141g ТК1Ш Дж/(моль • К)
ЛиП
Д И
«89,12 Дж/(моль • К)
^кип
При расчете по этим уравнениям погрешность, как правило, не превышает 7 %.
Энтальпии плавления, Дж/моль
bf„H
Простые вещества: —; « 10,5 ± 2,1 Дж/(моль • К) Ап
Неорганические соединения:
Д, н
«(25,1 ±4,2) Дж/(моль • К).
^ПЛ
Органические соединения:
Л.Н
* (54,4 ± 12,6) Дж/(моль • К).
^пл
Стандартные энергии Гиббса образования веществ
A fG^ = АА fH29S+В,
где Д f Н2(№ — стандартная энтальпия образования соединения; А и В — постоянные величины для данной группы соединений (см. табл. 3.6.35).
Пример.
Расчет Д fG^ для K2SO4, CdSO4 и A12(SO4)3.
Реакции образования сульфатов записывают, в соответствии с табл. 3.6.35, в следующей форме:
уК(тв.) + Б(ромб.) + 20, (г.) = |K2(SO4)t (тв.);
|-Сб(тв.) + 8(ромб.) + 20,(г.) = ^-Cd2(SO4)2 (тв.);
2 I
уА1(тв.) + Б(ромб.) + 2О2(г.) = -A12(SO4), (тв.).
Энтальпии образования Д f Л/298 следует взять соответственно для K2SO4, CdSO4 и ^A12(SO4)3, т. е.
-1434,65;-926,79 и —(-3437,28) кДж/моль (см. табл. 3.6.1).
Тогда:
Для K2SO4: ДуО2°98 = 0,990 • (-1434,65)+ 98,52 = = -1321,77 кДж/моль.
Для CdSO4: ДГО298 = 0,990 • (-926,79) + 98,52 = = -819,02 кДж/моль.
Для 1a1,(SO4)3 : ДГО298 = 0,990- -—I28 +
3 4 7 J Z?O 7 I 3 /
+ 98,52 = -1035,77 кДж/моль.
Для A12(SO4)4: Д f O2Q8 = 3 • (-1035,77) = 3107,32 кДж/моль.
По литературным данным значения Д 7<j298 соответственно равны: -1317,25; -820,57 и -3094,00 кДж/моль.
Физические свойства важнейших веществ
449
Таблица 3.6.35
Константы А и В уравнения A f - АЛ f + В для реакций образования различных веществ Условные обозначения: М — металл; Э — элемент; п — валентность металла.
Реакция А В
2 1 — М(тв.) + 8(ромб.) + 2О,(г.) = — M2(SO4)„(tb.) п ~ п 0,990 98,52
113 1 -М(тв.) + - N2 (г.) + —О2 (г.) = - М2 (NO, )п (тв.) п 2 2 п 0,981 89,68
2 3 1 — М(тв.) + С(графит) + —О2(г.) = —М2(СО3)н(тв.) п 2 п 0,985 65,06
2 3 1 - М(тв.) + Si(TB.) + -О2 (г.) = - М, (SiO3 )„ (тв.) п 2 п 0,993 75,03
- М( тв.) + 1о? (г.) -Дн2 (г.) = 1 М(ОН)„ (тв.) п 2 “ 2 п 0,994 41,45
- М(тв.) + -J-О, (г.) = - М,О„ (тв.) п 2 п ~ 0,990 25,46
М(тв.) + |о2(г.) = МО(г.) 0,998 -26,7
3 1 1 - М (тв.) + - N 2 (г.) = - М 3 N „ (тв.) п 2 п 0,96 16,24
— М(тв.) + —F2(r.) = — MF/;(tb.) п 2 п 0,980 14,82
- М(тв.) + -С1, (г.) = - МС1„ (тв.) п 2 " п 0,985 18,3
М(тв.) + |ci(F)2(r.) = MCl(F)(r.) 0,980 -25,2
— М(тв.) + — Вг,(ж.) = — МВгДтв.) п 2 п 0,983 4,61
— М(тв.) + —1,(тв.) = — М1н(тв.) п 2 п 0,982 -2,34
— M(tb.) + S(dom6J = — M,S..(tb.) п 1 д 0,990 0.71
М(тв.) + уН2(г.) = МН(г.) 0,965 -18,6
1мг(г.) = М(г.) 0,995 -15,1
Э (ТВ.) = Э (г.) 0,980 -32,8
Гидратация иона 0,956 0
Стандартные энтропии (см. также расчет А^Я^, Ср и "^298 органических веществ в идеализированном газовом состоянии)
Твердые неорганические вещества:
iS^ = A 1g М + В Дж/(моль • К),
где М — относительная молекулярная масса; А и В — константы, характерные для каждого типа соединений (см. табл. 3.6.36).
Например, каждому типу оксидов (ЭО, Э2О3, ЭО2 и т. п.) отвечают свои значения А и В, которые определяют по известным энтропиям двух веществ данного типа.
450
Новый справочник химика и технолога
Таблица 3.6.36
Константы А и В для некоторых типов соединений
Условные обозначения: Э — металл, X — галоген.
Тип соединения А В
Э2О 87,5 -87,5
эо 60,71 -70,76
Э2О3 138,6 -227,8
эо2 64,06 -68,66
э2о5 133,1 -209,3
эх 62,8 -38.1
эх2 136,9 -185,5
ЭХОз 36,01 68,24
3S 69,92 -73,27
ЭЫОз 90,85 -60,71
Газообразные неорганические вещества:
\^=А\%М + \£В
или
= ВМА Дж/(моль • К),
где М — относительная молекулярная масса; А и В — константы, определяемые в основном числом атомов в молекуле (см. табл. 3.6.37).
Таблица 3.6.37
Константы А и В для некоторых газов
Атомность газа А В 1g в
2 0,136 124,68 2,096
3 0,211 101,67 2,007
4 0,221 101,25 2,005
5 0,213 102,51 2,011
6 0,294 82,42 1,916
Твердые неразветвленные алканы:
S°2W = 75,31 + 24,27/7 Дж/(моль • К),
где п — число атомов углерода в молекуле.
Жидкие алканы (в том числе с разветвленной цепью), алициклические и ароматические углеводороды (в том числе с боковыми цепями):
52°98 = 104,60 + 32,22п - 18,83(г - 2) +
+ 81,59/?! + 110,88/72 Дж/(моль • К),
где п — число атомов углерода вне кольца; р\ — число фенильных групп; /?2 — число насыщенных циклов (циклопентана или циклогексана); г — число разветвлений на прямой цепи или число углеводородных групп (алифатических, ароматических или алициклических), присоединенных к какому-либо углеродному атому алифатической цепи.
Примеры.
Для трифенилметана п= 1, г = 3 - 2 = 1, /?1 = 3; для /и/?е/77-бутилбензола /7 = 4, r = 4- 2 = 2,/?] = 1.
Газообразные неразветвленные алканы:
Х298 = 142,3 +41,8/7 Дж/(моль • К),
где п — число атомов углерода в молекуле.
Твердые органические вещества:
Х298 = 1,1С;, ДжДмоль • К),
где Ср — молярная теплоемкость при постоянном давлении.
Жидкие органические вещества:
Я298 = 1,4С/; Дж/(моль • К),
где Ср — молярная теплоемкость при постоянном давлении.
Одноатомные ионы в водных растворах:
S?98 = 28,71g.4 - + 155 Дж/(моль • К),
{r + xY
где А — атомная масса; z — формальный заряд иона; г— радиус иона в кристаллическом веществе, А ; х — постоянная, равная 2,0 для положительных и 1,0 для отрицательных ионов.
Приближенный расчет стандартных энтальпий образования, теплоемкостей и энтропий органических веществ в идеализированном газовом состоянии
Расчет строится на основе значений A f H29g, 5298 и коэффициентов а, b и с уравнения Ср = а + ЬТ + сТ2 {Ср в Дж/(моль • К)) для веществ, являющихся основой соответствующего гомологического ряда (для ациклических углеводородов — метан, для ароматических — бензол, для первичных аминов — метанамин и т. д.). В эти основные величины вводят, согласно изложенным ниже правилам, поправки на удлинение углеродной цени, замещение простых связей двойными или тройными и т. д., пользуясь для этого табл. 3.6.38-3.6.43. Расчет производят следующим образом.
1. Выбирают основное вещество, из которого минимальным числом замещений можно получить структурную формулу рассматриваемого соединения (практическую возможность того или иного замещения не принимают во внимание). По табл. 3.6.39 определяют для основного вещества &fH2W, или S298 , или коэффициенты а, b и с уравнения Ср = а + ЬТ + сТ2 — в зависимости от того, какую величину вычисляют. Дальнейшее изложение дано для расчета A z//298 . Энтропии и теплоемкости рассчитывают по тем же правилам.
2. Последовательным введением в основное вещество групп -СН3 строят углеродный скелет искомого соединения, учитывая, что введение галогенов, спиртовых, кислотных и других функциональных групп возможно только взамен одной или нескольких групп СН3. Рекомендуется сначала строить наиболее длинную основную цепь, затем наиболее длинные боковые
Физические свойства важнейших веществ
451
цепи (см. примеры 2 и 3). На каждую введенную группу -СН3 вносят поправки (см. ниже, п. 3) в основную величину найденную по табл. 3.6.39. Если одно
и то же соединение может быть получено различными замещениями (например, введением боковых групп -СН3 по часовой или против часовой стрелки), то берут средний результат.
3. При введении поправок на группы -СН3 различают первичные и вторичные замещения атомов водорода группами -СН3.
Под первичным замещением подразумевают введение одной группы -СПз вместо атома водорода у данного атома углерода основного вещества. Так, например, в СН4, CH3NH2, HCONH2 можно сделать только по одному первичному замещению, в (CH3)2NH — два, в (CH3)3N — три. Каждое первичное замещение в димс-тиламине и в тримстиламинс является равноценным. Первичные замещения атома водорода группами -СН3 в циклопснтанс, бензоле и нафталине неравноценны. Каждому из них приписана определенная поправка (табл. 3.6.40). Для димстилового эфира поправка на первичное замещение атома водорода группой -СН3 нс предусмотрена. Введение даже одной группы -СН3 в
диметиловый эфир считается вторичным замещением (табл. 3.6.41).
Введение второй или последующих групп -СН3 вместо атома водорода у одного и того же атома углерода называют вторичным замещением. Для определения соответствующих поправок необходимо знать так называемые «типовые числа» того атома углерода, у которого производят замещение (атом А) и соседнего с ним атома углерода (атом В). Если таких соседних атомов углерода у атома А несколько, то поправки берут для максимального типового числа. Типовое число определяют, руководствуясь числом и видом связей данного атома углерода с другими атомами углерода (табл. 3.6.38).
В случае простых и сложных эфиров типовое число атома В принимают равным нулю.
4. После построения углеродного скелета соединения замещают простые связи сложными и вводят соответствующие поправки (табл. 3.6.42). Для введения поправок также следуеч знать типовые числа атомов, между которыми заменяют связь.
5. Замещают одну или несколько ipyim -СН3 другими группами и вводят соответствующие поправки (табл. 3.6.43).
Типовые числа атомов углерода
Таблица 3.6.38
Группа -СН3 ^СН2 СН —f— С в бензольном или нафталиновом кольце
Типовое число 1 2 3 4 5
Примеры.
1. Расчет энтальпии образования газообразного бензальдегида (см. табл. 3.6.41 и 3.6.43):
= 82,9кДж/моль
(А)= 1
(В)= 1
A(Af ) = -18,8 кДж/моль
(А) = 2
(В) = 5
A(Af/7°98 ) = - 24,3 кДж/моль
С СН(СН3)2
II
Д(ДгЯ°,з) = - 54 кДж/моль
AzH2°Q8 = 82,9 - 18,8 - 25,5 - 24,3 - 54 = -39,7 кДж/моль.
По литературным данным A f //°98 = 1,9 кДж/моль.
452
Новый справочник химика и технолога
2. Составление уравнения Ср =f(T) для 2,2,4-триметилпентана (см. табл. 3.6.39-3.6.41):
сп4 ► (А) - 1 (В) (А) (В) 1 Н3С—СН3 ►
Ал -- 8,54 Дж/(моль • К) а 14,3 Дж7(моль • К) ? АЛ • 103 = 100,5 Дж/(моль • К2) Л - 10’’= 74,7 ДжДмоль • КД Ас- 10 - -40.49 Дж/(.моль • К ) с • 10й -17,4 Дж/(моль • К ) Да = -3.88 Дж/(моль • К) Д6 • 103 -95,71 Дж'(моль- КД /\с 10й 36,63 Дж-'(моль • К )
(А) - 1 (В)-2
(А) - 1
(В) 2
(В) (А)
Н3С—СН2-СП2—СП3
(В) (А)
----► Н3С—СН2— СИ3
Ди 4,65 Дж/(моль • К)
АЛ • 10' 77,3 Дж/(моль • К")
Ас • 106 = -28,68 Дж'(моль • К3)
А« 4,65 Дж'(моль • К)
АЛ • К)’’ = 77.3 ДжДмоль • К2)
Ас • 106 28,68 Дж/(моль • К )
(В) (А) (В)
(В) 2
(А) - 3 (В)-2
----► СПз—СН2-СН2-СП2—СПз -----------------►
А</ 6,36 ДжДмоль • К)
АЛ • 10 = 83,53 Дж/(моль • КД
Ас • 10й : -35,88 Дж (моль • К')
Н3С—СП—СН2— СН2—СПз
СПз
Д</ - -5 Дж/(моль • К)
АЛ-103 120,5 Дж'( моль- КД
Ас-10й 53,21 Дж'(моль-К’)
V13 (В) (А) (В)
Н3С--С—сн2—сп2-сн3
СПз
(А)- 2
(Вр2
-------------------------► П3С-
Л</ 6,36 Дж'(моль • К)
АЛ • 103 = 83,53 Дж/(моль • КД
Ас- • 10й =" -35,88 Дж/(моль • К')
СПз
С—СП2—СП—СНз
СП3 СП3
а = 14,3 - 8,54 - 3,88 + 4,65 + 4,65 + 6,36 - 5 + 6,36 = 18,9 Дж/(моль • К);
b • 103 = 74,7 + 100,5 + 95,71 + 77,3 + 77,3 + 83,53 4 120,5 + 83,53 - 713,07 Дж/(моль • К2);
с • 106 = -17,4 - 40,49 - 36,63 - 28,68 - 28,68 - 35,88 - 53,21 - 35,88 = -276,85 Дж/(моль • К3);
Ср = 18,9 + 713,07- 10 3 Т-276,85- 10 6 Т2 Дж/(моль • К).
Согласно найденному уравнению, теплоемкость вещества при Т = 298 К равна 280,01 Дж/(моль • К); по литературным данным теплоемкость равна 268,8 Дж/(моль • К).
3. Расчет энтропии газообразного ацетона (см. табл. 3.6.39-3.6.41 и 3.6.43):
(А) = 1
(В) (А) (в) = 1
СН4 ----------------------► Н3С—СН3 --------------------------►
ДСЙ -43,5Дж/(моль-К)
= 18б,ЗДж/(моль -К)
Д5’98 = 41Дж/(моль -К)
(В) (А)
Н3С—сн2—сн3
(А) “2
(В)=1
Д5°98 = 24,ЗДж/(моль - К)
(В) (А) Н3С----СН----СН3
СНз
(А)=3
(В)=1
Д5^ -11,ЗДж/(моль -К)
СН3
------► Н3С-----С-----СНз
СН3
Н3С---С-----СНз
Д5°98 10Дж/(моль - К)
S°98 - 186.3 + 43.5 + 41 + 24,3 + 1 1.3 - 10 = 296,4 Дж/(моль • К).
По литературным данным = 295,2 Дж/(моль • К).
Физические свойства важнейших веществ
453
Таблица 3.6.39
Термодинамические свойства основных веществ
Вещество А/<8-кДж/моль Коэффициенты уравнения С„ ~ J\T) 5° ‘•’298 ’ Дж/(моль • К)
а, Дж/(моль • К) Ь- 10’, Дж/(моль • К2) с-106. Дж/(моль • К')
Бензол 82,9 1 325,9 -113,7 269,2
^yV-Димстил- -45,6 16,5 275,7 —81,6
метанамин
(триметиламин)
Димстиловый эфир -192,6 26,9 166 -47,9 266,7
Метан -74,9 14,3 74,7 -17,4 186,3
Метанамин -28,1 16,8 128,6 -36,4 241,6
(метиламин)
/V-Мстил метанам ин -27,6 16,4 202,3 -59 273,4
(диметиламин)
Нафталин 151 13,2 458 -145,7 336,6
Формамид -207,3 27,3 105,4 -31,3 249,1
Циклопентан -77,5 11 346,1 -103,5 293,1
Таблица 3.6.40
Поправки на первичное замещение водорода группами -СН3
Основная группа A(AZC8). кДж/моль Коэффициенты уравнения Ср - f (Т) 5° 1?298 " Дж/(моль • К)
/Ха. Дж/(моль • К) АЛ- 10’, Дж/(моль • К2) Ac - 106. Дж/(моль • К3)
Бензол и нафталин:
первое замещение -18,8 1,51 73,9 -24,62 50,2
второе замещение:
в положение 2 -26,4 21,8 25,2 4,94 33,9
в положение 3 -27,2 7,2 59,37 -15,74 38,5
в положение 4 -33,5 5,36 61 -16,66 32,7
третье замещение 2,39 69,17 -21,73 33,5
/V,/V-Диме гил метанам ин -17,2
(триметиламин)
Метан -9,21 -8,54 100,5 -40,49 43,5
Метанамин -23,9
(метиламин)
УУ-Метилметанамин -26,4 -0,42 73,35 -22,4
(диметиламин)
Циклопентан:
увеличение кольца -39,4 -4,35 80,81 -24,24 2,93
первое замещение -21,8 -0,29 77,75 -24,16 48,1
второе замещение:
в положение 2 -51,1
в положение 3 -35,2 -1 194,9 -21,14
в положении 4 -29,7
третье замещение -29,3
Формамид -37,7 25,58 -7,33 19,89
Поправки на вторичное замещение водорода группами -СН3
Таблица 3.6.41
Типовые числа кДж/моль Коэффициенты уравнения Ср ~ f(T) AV0 ZAO 298 , Дж/(моль • К)
(А) (В) /Ха, Дж/(моль • К) АЛ • 103, Дж/(моль • К2) Ac - 106. Дж/(моль • К3)
1 1 -18,8 -3,88 95,71 -36,63 41
1 2 -21,8 4,65 77,33 -28,68 38,5
1 3 -23 4,19 83,23 -33,62 39,8
1 4 -20,9 5,82 71,68 -24,62 46,1
454
Новый справочник химика и технолога
Окончание табл. 3.6.41
Типовые числа A(AzC8), Коэффициенты уравнения ср - ДТ) Д5°
(А) (В) Да. Д/> • 103. Дс • 106. ^>298 '
кДж/моль Дж/(моль • К) Дж/(моль • К2) Дж/(моль • К3) Дж/(моль • К)
1 5 -25,5 0,42 71,93 -21,77 41,9
2 1 -27,6 7,91 73,69 -26 24,3
2 2 -28,5 6,36 83,53 -35,88 29,3
2 3 -28,5 4,23 82,44 -32,78 26,4
2 4 -21,4 10,6 67,45 -24,62 25,1
2 5 -24,3 0,04 72,93 -22,32 11,3
3 1 -33,9 ~4 115 -51,83 11,3
3 2 -33,5 -5 120,5 -53,21 20,1
3 3 -28,9 -14 129,6 -58,87 24,3
3 4 -23,9 -0.6 102,9 -43 7.12
3 5 -38,5 1,76 67,83 -19,59 5,44
Замена водорода в сложных или 29,3 0,04 73,6 -22,32 60,3
простых эфирах
Замена водорода в кислоте с образованием сложного эфира -39,8 1,84 69,63 -20,72 69,9
Таблица 3.6.42
Поправки на замещение простых связей сложными
Цифры в первой графе обозначают типовые числа атомов углерода.
Тип связи между атомами углерода А и В д(дХД кДж/моль Коэффициенты уравнения Ср / (Г) д с0 ZV>298’ Дж/(моль • К)
Да, Дж/(моль • К) Д/> • 103. Дж/(моль • К2) Дс • 106, Дж/(моль • К3)
1 = 1 137,3 5.57 -53,13 19,97 -8,8
1=2 125,6 6,53 -62,26 23,32 3,3
1=3 118,1 2,64 -99,02 54,85 9,2
2-2 117,2 1,67 -79 41,41 -3,8
2=2, z/wc-положение 118,9 1,67 -79 41,41 -2,5
2=2, т/?ш/с-положение 115,1 1,67 -79 41,41 -5
2=3 111,8 2,64 -99,02 54,85 -6,7
3=3 106,8 -19,4 -74,69 49,74
Дополнительная поправка на ка- -15,9 ~0 -43,5
ждую пару сопряженных связей
1 = 1 311,5 23,4 -130,59 46,85 -28,5
1=2 251,6 26,9 -152,44 60,83 -32,7
2=2 272,6 19,5 -151,14 63,97 -26,4
Поправка на двойную связь, -21,4 ~0 -18
смежную с ароматическим
кольцом
*См. п. 3 приближенного расчета Ду /7298, и *^298 органических веществ в идеализированном газовом состоянии.
Поправки на группы, замещающие группу -СН3
Таблица 3.6.43
Группа Д(Ду//2°98), кДж/моль Коэффициенты уравнения Ср f(T) дс° Дж/(моль • К)
Да, Дж/(моль • К) Д/>- 103, Дж/(моль • К2) Дс • 106. Дж/(моль • К3)
-Вг 41,87 11,76 -81,27 26,5 12,6*
-CN 163,3 15,24 -58,28 18,97 16,7
-соон -364 35,59 -63,1 33,24 64,5
-С6Н5 135,2 3,31 224,54 -80,4 90,9
Физические свойства важнейших веществ
455
Окончание табл. 3.6.43
Группа АСА/СД кДж/моль Коэффициенты уравнения Ср - /\Т) дс° Дж/(моль • К)
Аа, Дж/(моль • К) Д6•10\ Дж/(моль • К2) Дс • 106. Дж/(моль • KJ)
-CI 0 для первого атома С1 у атома углерода: 18,8 — для каждого последующего 9,17 -78,92 26,21 0*
-F -147 9,38 -98,85 49,36 -4,2*
-I 103,8 11,43 -72,73 17,12 20,9*
-nh2 51,5 5,28 -30,65 9,34 -20,1
-no2 5 26,38 -81,77 43,38 8,4
=0 (альдегид) -54 15,11 -233,29 95,12 -51,5
=0 (кетон) -55,3 21,02 -276,66 126,5 -10
-ОН (алифатические и ароматические в положениях 3 и 4) -ОН (ароматические в положении 2) -137 -199,7 13,27 -62,22 23,4 10,9
-SH 66,2 17,04 -104,5 51,79 21,8
* К вычисленным поправкам на энтропию галогенов для метильных производных следует прибавить 4.2 Дж/(моль • К): например, энтропия хлорметана:
S°Q)j = 186.3 (основная группа) + 43.5 (первичное замещение) + 0 (замещение атомом CI) + 4.2 = 234 Дж/(моль • К).
По литературным данным = 234,6. Дж/(моль • К).
Расчет критических параметров жидкостей
Критические температуры, К.
1. Для всех соединений (неорганических и органических), кипящих ниже 235 К, и для всех простых веществ:
Т = 1 70 Т
2. Для соединений, кипящих выше 235 К.
а) все соединения, содержащие галогены и серу:
Дкр=1,41 7;тк+66-11Г;
б) ароматические соединения и нафтены, не содержащие галогенов и серы:
Т’кр- 1,41 +66 -г (0,383 , к -93);
в) все соединения, не содержащие галогенов и серы, кроме ароматических и нафтеновых:
Гкр= 1,027 Д1Л к + 159,
где Ткр — критическая температура, К; Д, г к — нормальная температура кипения, К; F — число атомов фтора в молекуле; г — отношение числа нециклических атомов углерода к их общему числу.
Погрешность расчета обычно не превышает ±5 %. Критический объем, мл/моль.
Для всех веществ:
^ = (0,377 Р + 11,0)1’25,
где Икр — критический объем, моль; Р — парахор.
Парахор вычисляют по уравнению:
Рж ~ Рп
где М — молекулярная масса: о — поверхностное натяжение жидкости, дин/см; рж — плотность жидкости, г/см3; ри — плотность пара, г/см3.
Парахор можно также вычислить как сумму парахоров атомов и связей, образующих молекулу.
Средняя погрешность при определении Икр составляет ±3 %.
Критическое давление, Па.
Для всех веществ:
_ 2,108-10”^
Лр ~ V -8 ’
кр
где ркр — критическое давление, атм; Тк? — критическая температура, К; Икт,— критический объем, мл/моль.
Максимальная погрешность расчета не превышает 11 %.
3.7. Теплопроводность
Коэффициент теплопроводности X обозначает количество тепла, передаваемого в единицу времени через единицу поверхности при единичном температурном градиенте, т. е. при перепаде температур в один градус на единицу длины стенки по нормали к тепловому потоку.
456
Новый справочник химика и технолога
Размерность коэффициента теплопроводности: Вт/(м • К).
В табл. 3.7.1 приведены коэффициенты теплопроводности металлов и сплавов.
Для каждого значения X указана температура, которой это значение соответствует. В тех случаях, когда такое указание отсутствует, данные относятся к комнатной температуре.
Таблица 3. Z /
Коэффициенты теплопроводности металлов и сплавов
Состав сплавов указан в массовых долях (кроме особо оговоренных случаев).
Металл или сплав, масс. % 7 . °C А.. Вт/(м • K)
Алюминий 99 18 211
30 208,1
100 205,2
400 318,2
600 422,9
Висмут -186 10,47
-77 10,76
0 7,411
100 6,866
96 Bi -г 3,5 Pb (объемн.) 44 5,401
90 Bi + 3,5 Sn (объемн.) 44 5,401
80 Bi + 20 Sb 0 6,364
100 8,583
50 Bi + 50 Sn 12,5 23,45
50 Bi + 25 Pb 4 25 Sn 20 16,24
48 Bi 4 26 Pb + 13 Sn + I3 Cd 7 13,36
Вольфрам 0 160,4
2227 148,2
Железо кованое чистое 0 59,45
100 56,94
99,92 (армко) 20 73,27
100 67,41
Золото 0 311,5
97 312,3
90 Au 4 lOPd 25 97,97
50 Au + 50 Pd 25 36,01
Иридий 17 59,03
Кадмий 0 92,65
100 85,62
Калий 5 97,97
20,7 97,13
57,6 90,85
62,9 К + 37,1 Na 6,0 22,99
42,9 25,92
Кобальт (97,12 Со + 0,24 С + 1,4 Fe + 1,1 Ni + 0,14 Si) 30 487,8
Латунь красная 0 103
100 118,5
желтая 0 85,45
100 106,3
Литий 0 71,18
101,3 75,36
Магний 0-100 157,4
92 Mg + 8 Al 20-200 62,8-79,55
92 Mg + 8 Си 20-200 125,6-132,3
88 Mg+ 10 Al + 2 Si 20-200 121,4-133,1
Марганец 18 21,77
Физические свойства важнейших веществ
457
Продолжение табл. 3.7. /
Металл или сплав, масс. % Г °C X, Вт/(м • К)
Медь -183 465,2
0 385,2
100 385,2
99,37 Си + 0,63 Р 30 104,7
98,02 Си + 1,98 Р 30 52,34
96 Си + 3 Si + 1 Мп (эвердюр) 20 33,08
84 Си + 4 Ni + 12 Мп (манганин) 18 21,73
100 26,42
60 Cu + 40Ni 18 22,61
100 26,8
54 Cu + 46Ni 18 20,26
89 Си + 11 Zn 18 115,1
87 Си + 13 Zn 18 126
82 Си + 18 Zn 18 131
68 Си + 32 Zn 18 108,9
62 Си+ 22 Zn + 15 Ni 18 24,91
52 Си л 26 Zn + 22Ni 0 29,31
100 36,43
95 Си + 5 Al (бронза алюминиевая) 20 82,48
90 Си + 10 Sn 20 41,87
75 Си + 25 Sn (бронза оловянная) 20 25,54
92,8 Си + 5 Sn + 2 Zn + 0,15 Р (бронза фосфористая) 20 79,13
Молибден 17 144,9
Натрий 5,7 134,4
21,2 132,7
88,1 120,6
Никель 99 -160 54,01
18 58,62
Ni + (2ч-3)Со 300 52,75
79,5 Ni + 13 Сг + 6,5 Fe (никонель) 70 15,07
Олово -170 81,64
0 64,06
100 59,45
91 Sn + 8,9 Zn 44 65,73
Палладий 100 76,2
90 Pd+ 10 Pt 25 56,1
50 Pd + 50 Pt 25 36,84
90 Pd + 10 Ag 25 47,73
50 Pd + 50 Ag 25 31,82
Платина -252,8 389,4
-183 76,2
0-200 69,92
90 Pt+ 10 Ir 17 30,98
90 Pt+ 10 Rh 17 30,14
90 Pt+ 10 Pd 25 43,12
Родий 17 87,92
Ртуть твердая -269,3 167,5
-44,2 27,8
жидкая 0 8,081
50 8,75
Свинец 18 34,62
100 34,12
Серебро 99,9 -160 417,8
0 458,9
10-97 403,2
458
Новый справочник химика и технолога
Окончание табл. 3.7.1
Металл или сплав, масс. % 7'. °C А. Bt/(m • K)
Серебро 99,98 18 421,2
100 415,3
90 Ag + 10 Pd 25 141,1
90 Ag + 10 Pt 25 97,97
70 Ag + 30 Pt 25 30,98
Сталь См. таб л. 3.7.2
Сурьма 0 18,42
0-30 17,58
100 16,75
70 Sb ь 30 Bi 0 9,797
100 11.76
66,7 Sb + 33,3 Cd 0 1,252
50 Sb + 50 Cd 0 2,173
Тантал 17 54,43
1827 82,9
Цинк -170 117,2
18 111
100 109.7
70 Zn + 30 Sn 44 93,78
Чугун 18 45,64
100 45.22
В табл. 3.7.2 3.7.7 приведены коэффициенты тенлонроводноети некоторых сталей, чистых веществ в твердом состоянии, термоизоляционных, строительных и некоторых других материалов, жидкометаллических теплоносителей, чистых органических жидкостей и хладагентов в жидком состоянии.
Таблица 3.7.2
Коэффициенты теплопроводности Z (Вт/(м • К)) некоторых сталей
Группа стали Температура. °C
100 200 300 400 500 600 700 800
Углеродистая:
марка 15 54,4 50,2 46,1 41,9 37,7 33,5
марка 30 50,2 46.1 41,9 37,7 33,5 29,3
Молибденовая 41,9
Хромистая Хромомолибденовая: 22,4 21,2 23,5 22
Х10С2М (ЭИ107) 18,4 0 21,7 24,7 22
1 О VN4 1 Z, yYlVi 37,7 35,6 33,5
Хромоникелевая 16,9 19,2 21,5 24,4 26,7 29,7 32,6 36,1
Хромоникельвольфрамовая 15,5 0 18,1 21,2 22
Таблица 3.7.3
Коэффициенты теплопроводности некоторых чистых веществ в твердом состоянии
Название Формула Г. °C А., Вт/(м • К)
Алюминия оксид: А12О3
порошок 46,8 0,678
плавленый Графит (плотность 1580 кг/м3): С 650-1350 3,349
Цоси 50 44,17
-L оси 142 555 17,84 116,8
Графич (порошок, плотность 700 кг/м3) С 40 1,193
Физические свойства важнейших веществ
459
Окончание табл. 3.7.3
Название Формула 7; °C X, Bt/(m • K)
Кадмия оксид (прессов, порошок) CdO 46,5 0,682
Калия иодид KI 0 5,024
Калия хлорид КС1 0 6,95
Кобальта(Ш) оксид (прессов, порошок) Со2О3 48,5 0,419
Кремния карбид (карборунд) SiC 650-1350 15,57
Кремния диоксид (кварц): SiO2
Цоси 0 13,61
100 9,002
± оси 0 7,247
100 5,581
Магния оксид MgO 47,6 0,607
(прессов, порошок, плотность 797 кг/м3)
Меди(П) оксид (прессов, порошок) CuO 45,6 1,013
Натрия хлорид NaCl 0 1,116
Нафталин C10H8 0 0,377
1-Нафтол c10H8o 35 0,293
2-Нафтол c10h8o 35 0,335
Никеля(Ш) оксид Ni2O3 46,2 0,938
(прессов, порошок, плотность 1445 кг/м’)
Сера: S
ромбическая 0 0,293
пластическая 20-100 0,264
Серебра бромид AgBr 0 1,03
Серебра хлорид AgCl 0 1,089
Таблица 3.7.4
Коэффициенты теплопроводности термоизоляционных, строительных и некоторых других материалов
Материал 7’, °C X. Вт/(м • К)
Асбестовая ткань 20 0,279
Асбестовое волокно 0 0,112
100 0,121
Асбестовый картон 100 0,144
Асфальт 20 0,744
Баз алы 20 2,175
Бетон 20 0,922
Боксит 600 0,557
Войлок шерстяной 40 0,073
Гипс 0 1,297
Глина огнеупорная 300-600 0,875-0,925
Г ранит 20 3,419
Дерево:
береза (10,8 % влажности), волокнам 29 0,172
дуб (плотность 825 кг/м3), волокнам 15 0,209
дуб (плотность 819 кг/м3), || волокнам 20 0,349
Диатомитовая земля 20 0,055
Древесный уголь 81 0,076
Известняк 0 2,07
Известь глинистая 20 3,256
Каменный уголь 20 0,186
Картон гофрированный 0,064
460
Новый справочник химика и технолога
Окончание табл. 3.7.4
Материал 7, °C X, Вт/(м • К)
Кирпич:
изоляционный 100 0,14
огнеупорный 200 1,006
строительный 20 0,233-0,291
Клинкер 30 0,163
Кокс порошкообразный 100 0,191
Лсд 0 2,25
-95 3,954
Магнезит 1000 1,663
Мрамор:
белый 3,268
черный 30 2,861
Накинь котельная 65 1,31-3,14
Оникс 30 2,34
Опилки древесные 20 0,07
Парафин 20 0,267
Песок:
сухой 20 0,326
влажный 20 1,13
Песчаник (плотность 2259 кг/м3) 40 1,84
Портландцемент 30 0,302
Пробка гранулированная 20 0,038
Пробковая пластина 30 0,042
Резина мягкая 20 0,167
Сланец 100 1,49
Слюда 0,582
Снег:
свежевыпавший 0,105
уплотненный 0,048
Стеклянная вата 0 0,037
Текстолит 20 0,645-0,93
Торфоплиты 50 0,064
Фарфор 95 1,04
Фибра (пластины) 20 0,049
Флюорит 0 10,4
Шерсть минеральная 50 0,047
Шлакобетон 0,93
Шлаковая вата 100 0.07
Штукатурка 20 0,779
Хлопок (плотность 81 кг/м3) 0 0,057
Эбонит 0 0,158
Таблица 3.7.5
Коэффициенты теплопроводности к (Вт/(м • К)) некоторых жидкометаллических теплоносителей
Теплоноситель Температура, °C
0 50 100 150 200 250 300 400 500 600 700
Висмут' (ТШ1 = 271,3 °C; ТКИ11 = 1560 °C) 14,7 15,6 16,5 17,3 18,3
Калий 46,5 46,4 45,9 44,9 43,4 39,5 34,9 30,9 28,3
(Тпл = 63,6 °C; Ткип = 776 °C) Литий 46,1 46,3 46,6 47,1 47,6 48 48,5
(ТШ1= 180 °С;Ткип= 1350 °C) Натрий (Тпл = 97,8 °C; Гкип = 900 °C) 86,1 84,1 81,6 78,7 75,5 68,7 63,8 60,6 59,1
Физические свойства важнейших веществ
461
Окончание табл. 3.7.5
Теплоноситель Температура, °C
0 50 100 150 200 250 300 400 500 600 700
Олово (7k, = 231,9 °C; Ткип = 2720 °C) Ртуть (Тпл = -38,9 °C; 7"кип - 356,6 °C) Свинец (Тпл = 327,3 °C; Гкип= 1751 °C) Сплав натрий—калий: 25 % Na + 75 % К (Т„;, = 11 °C; Тки„ = 784 °C) Сплав свинец—висмут: 44 % РЬ + 55,5 % Bi (Гпл= 123,5 °C; Ткт= 1670 °C) 7,79 8,43 22,7 9,07 23,3 9,71 23,8 11,2 10,4 24,5 11,7 30,7 11 25,1 12,2 31,6 11,6 25,8 12,7 33,6 12,6 15,1 27,1 13,7 35,5 13,3 15,5 28,4 14,7 37,4 15,9 29,7 15,8 39,4 17,7 30,9 16,7
Таблица 3.7.6
Коэффициенты теплопроводности чистых органических жидкостей
Название Формула 7 . °C X.. Вт/(м • К)
Анилин c6h7n 16,5 0,1774
Ацетальдегид С2Н4О 21 0,1712
Ацетон СзН6О 16 0,1902
Бензол с6н6 16 0,1902
Бромбензол С6Н5Вг 20 0,1115
2-Бромбутан С4Н9Вг 12 0,1164
1 -Бромпентан СзНнВг 18 0,0984
1 -Бромпропан С3Н7Вг 12 0,1076
Бромэтан С2Н5Вг 30 0,1198
Бутан-1 -о л С4Н,0О 20 0,1534
Бутилацетат С6Н i2O-> 20 0,1369
Г ексан с6н14 30-100 0,1376
Гексан-1-ол С6Н|4О 30-100 0,1615
Гептан С7н16 30 0,1404
Гептан-1-ол с7н16о 70-100 0,1625
Глицерин С,Н8О3 20 0,2943
Декан С,оН22 30 0,1402
Диизопропиловый эфир с6н|4о 20 0,1097
Дифтордихлорметан (фреон-12) CC12F2 20 0,08248
Дифторхлорметан (фреон-22) CHCIF? 20 0,09295
Дихлорметан (хлористый метилен) СН2СЬ 0 0,1218
1,2-Дихлорпропан СзН6С12 20-50 0,1254
1,2-Дихлорэтан (хлористый этилен) С2Н4С12 20 0,1264
Диэтиловый эфир С4Н|0О 30 0,1375
А,А-Диэтилэтанамин c6h15n 20 0,121
(триэтиламин)
Изомасляная кислота С4Н8О2 12 0,1424
Изопропилацетат С5Н]о02 20 0,1344
1 -Изопропил-4-метилбензол С|()Н]4 30 0,1347
(н-цимол)
2-Изоиропил-5-метилфснол (тимол) С]оН140 13 0,1311
Иодбензол с6н51 30-100 0,1203
2-Иодбутан С4Н91 12 0,08709
1 -Иодпентан с5н,,1 12 0,08499
1-Иодпропан С3н71 12 0,09211
Иодэтан С2Н51 30 0,111
jw-Крезол С7н8о 20 0,1499
н-Крезол с7н80 20 0,1444
о-Ксилол С8Н,о -20-80 0,1428
462
Новый справочник химика и технолога
Окончание табл. 3.7.6
Название Формула Т. °C X. Вт/(м • К)
.w-Ксилол с8н1() 25 0,1577
Масляная кислота с4н8о2 12 0,1507
Мезитилсн С| Jн 12 20 0,1359
Метанол СН4О 20 0,2023
Метилацетат с3н6о2 12 0,1612
З-Метилбутан-1 -ол С5Н|2О 0 0,1478
(3 -Мстил бутш i )ацетат с7н|4о? 20 0,1298
2-Метилнропан-1 -ол с4н10о 20 0,1424
1 -Метил-З-хлорбензол С7Н7С1 20 0,1298
Метилциклогексан с7н|4 30 0.1278
Муравьиная кислота СН2О2 12 0,2713
Нитробензол c6h5no2 30-100 0.1636
Нитрометан CH3NO, 30 0,2153
Нонан С9Н2о 30-100 0,1413
Нонан-1-ол с9н?0о 30-100 0,1681
Октан с8н18 30 0,1452
Октан-1-ол с8н|80 30-100 0,1663
Олеиновая кислота С|8Н34О2 26.5 0,2309
Пальмитиновая кислота С16Н32О2 72,5 0,1715
Пентан С5н|21 30 0,1349
Пентан-1 -ол С<Н12О 30-100 0,1622
Пентахлорэтан С2НС15 20 0.1254
Пентилацетат С7Н14О2 20 0.1292
Пропан-1,2-диол с3н8о2 20-80 0,2009
Пропан-1 -ол С3н8о 12 0,1562
Пронан-2-ол с3н8о 20 0,1408
Проп-2-ен-1-ол С3Н6О 30 0,1798
Прон ил ацетат С5Н10О2 12 0,1369
Пронилформиат с4н802 12 0,1537
Пропионовая кислота С3н6о2 12 0,1633
Стеариновая кислота С18н36о2 72,5 0,1601
1,1,2,2-Т етраф гор-1,2-дихлорэтан C2C12F4 30 0,0775
(фреон-114)
Т етрахлорметан СС14 20 0,1034
1,1,2,2-Т етрахлорэтан С2Н2С14 20 0,1139
Т етрахлорэтилен СС12=СС12 20 0,1619
Толуол С7н8 20 0,1349
1,1,2-Трифтор-1,2,2-трихлорэ 1 ан c2ci3f3 30 0,09085
(фреон-113)
Трихлорэтилен СНС1=СС12 20 0,1162
Уксусная кислота С2Н4О2 20 0,172
Уксусный ангидрид С4н6о3 21 0,2213
Фтордихлорметан (фреон-21) chci2f 0,108
Фтортрихлорметан (фреон-11) CC13F 20 0,09546
Хлорбензол С6Н5С1 30-100 0,1447
2-Хлорбутан С4Н9С1 12 0,1164
Хлорметан СН3С1 -15-30 0,1925
Хлороформ СНС13 20 0,103
1-Хлорпентан С5НнС1 12 0,1185
1 -Хлорпропан С3Н7С1 12 0,1185
Этанол с2н6о 20 0,1673
Этилацетат с4н8о2 16 0,1491
Этилбензол С8Н1О 20 0,1323
Этиленгликоль С2Н6О2 20 0,2611
Физические свойства важнейших веществ
463
Таблица 3.7.7
Коэффициенты теплопроводности А. (Вг/(м • К)) некоторых хладагентов в жидком состоянии
Хладагент Формула Температура. °C
-30 -20 -10 0 10 20 30
Аммиак NH3 0,57 0,57 0,558 0,547 0,518
Дифтордихлорметан CC12F2 0,106 0,101 0,097 0,092 0,087 0,083 0,078
(фреон-12) Серы диоксид SO2 0,223 0,207 0,212 0,205 0,199 0,193
У глсрода диоксид со2 0,151 0,14 0,128 0,116 0,093 0,07
Фтортр и х л ор м стан CC13F 0,12 0,115 0,1 1 0,106 0,101 0,095 0,091
(фреон-11) Хлорметан CH3CI 0,188 0,179 0,171 0,162 0,154
В табл. 3.7.8 приведены коэффициенты теплопроводности газов и паров при давлении р = 101,3 кПа или в области давлений, в которой А. не зависит от р (т. е. при таких давлениях, когда средний свободный путь молекул весьма мал по сравнению с толщиной проводящего теплоту слоя).
Звездочкой отмечены вещества, дополнительные сведения о которых представлены в табл. 3.7.9. В табл. 3.7.10 приведены коэффициенты теплопроводности воды и водяного пара.
Таблица 3.7.8
Коэффициенты теплопроводности газов и паров
Газ или пар Формула T, °C X. Вт/(м • K)
Простые вещества и неорганические соединения
Азот* n2 -191,4 0,007658
-78,4 0,01802
0 0,02428
Азота(1) оксид n2o -71,8 0,01135
0 0,01472
100 0,02119
Азота(П) оксид NO -71,4 0,01742
0 0,02324
Азота(1У) оксид no2 55 0,03718
Аммиак NH3 -57,6 0,01599
0 0,0215
100 0,02968
Аргон* Ar -182,6 0,005945
0 0,01625
Вода (пар) H2O См. табл. 3.7.10
Водород* H2 -252,2 0,01348
-78,4 0,1283
0 0,1742
Водорода сульфид (сероводород) H2S 0 0,01275
Гелий He -252,2 0,02169
-191,7 0.06213
0 0,1407
100 0,1668
Кислород* o2 -191,4 0,007205
-78,4 0,01797
0 0,02466
Неон Ne -181,4 0,02089
-74,4 0,0368
0 0,04551
Ртуть Hg 203 0,007729
Серы диоксид so2 0 0,008164
Углерода диоксид* co2 -78,5 0,01066
0 0,01373
Углерода дисульфид (сероуглерод) cs2 0 0,006762
464
Новый справочник химика и технолога
Окончание табл. 3.7.8
Газ или пар Формула г, °C к Вт/(м • К)
Простые вещества и неорганические соединения
Углерода монооксид* СО -191 0,006908
0 0,02152
Хлор С12 0 0,007658
Органические соединения
Ацетилен с2н? 0 0,01842
Ацетон С3Н6О 100 0,01658
184 0,0247
Бензол с6н6 100 0,01735
212,5 0,02964
Бромметан СНзВг 4,6 0,007285
Бутан-1-амин (бутиламин) C4HnN 6,5 0,01257
Гексан с6н14 20 0,01195
Гептан С7Н16 100 0,01732
Диэтиловый эфир c4Hl0o 0 0,01298
100 0,0221
212,5 0,03517
Изопентан с5н12 0 0,01219
100 0,02137
184 0,03149
Подметан сн31 0 0,004597
100 0,007553
Метан* сн4 -181,6 0,009412
-75,6 0,02068
0 0,02939
Метанол СН4О 0 0,01406
100 0,02161
Пентан С5Н12 20 0,01368
Тетрахлорметан СС14 46 0,006975
100 0,008575
184 0,01088
Хлорметан СН3С1 0 0,009278
100 0,01608
212,5 0,02559
Хлороформ CHCI3 0 0,006376
100 0,009768
184 0,01299
Этан* CH3CH3 -70,4 0,01142
0 0,01803
Этанол С2Н6О 20 0,015
100 0,02085
Этилацетат С4н8о2 46 0,01206
100 0,01617
184 0,02382
Этилен* С2н4 -7U 0,01077
0 0,01641
Таблица 3.7.9
Коэффициенты теплопроводности к(Вт/(м • К)) некоторых газов при различных температурах
Газ Температура, °C
0 100 200 300 400 500 600 700 800 900 1000
Азот 0,0243 0,0315 0,0385 0,0449 0,0507 0,0558 0,0603 0,0643 0,0674 0,07 0,0724
Аргон 0,0162 0,021 0,0258 0,0304 0,0348 0,0391 0,0435 0,0486 0,0511 0,0548 0,0583
Водород 0,1742 0,216 0,2579 0,2998 0,3416 0,3835 0,4262 0,4677 0,51 0,5518 0,5937
Воздух (сухой) 0,0244 0,0321 0,0394 0,046 0,052 0,0574 0,0623 0,0671 0,0721 0,0762 0,0795
Физические свойства важнейших веществ
465
Окончание табл. 3.7.9
Газ Температура, °C
0 100 200 300 400 500 600 700 800 900 1000
Кислород 0,0247 0.0329 0,0407 0,048 0,055 0,0615 0,0674 0,0729 0,0778 0,0821 0,0858
Метан 0,0294 0,0481 0,07 0,0929 0,1181 0,1431 0,1708 0,1972 0,2202 0,25 0,2767
Углерода диоксид 0,0137 0,0214 0,0288 0,0367 0,0443 0,0513 0,0579 0,0645 0,0707 0,0766 0,0821
Углерода моно- 0,0215 0,0275 0,033 0,0384 0,0441 0,0495 0,0549 0,0602 0,0652 0,0698 0,0742
оксид
Этан 0,018 0,0309 0,0466 0,064 0,0829 0,1024 0,1214 0,14 0,1585
Этилен 0,0164 0,0295 0,0441 0,0595 0,0758 0,0923 0,1082 0,1195 0,1349
Таблица 3.7. /6
Коэффициенты теплопроводности Z • 1()2 (Вт/(м • К)) воды и водяного пара
Коэффициенты теплопроводности воды расположены по правую сторону ломаной линии; по левую сторону этой линии расположены коэффициенты теплопроводности перепетого пара, а также воды и пара на линии насыщения.
Т. °C На линии насыщения Давление. МПа
вода пар 0,101 2,03 4,05 6,08 8,11 10,1 15,2 20,3 25,3 30,4
0 55,1 55,1 55,1 55,2 55,4 55,4 55,5 55,6 55,8 56,1 56,3
10 57,5 57,5 57,5 57,6 57,7 57,8 57,9 58,2 58,4 58,6 59
20 59,9 59,9 59,9 60 60,1 60,2 60,4 60,6 60,8 61,1 61,4
30 61,8 61,8 61,8 61,9 62 62,1 62,2 62,5 62,8 63 63,4
40 63,4 63,4 63,4 63,5 63,6 63,7 63,8 64,1 64,4 64,7 65
50 64,8 64,8 64,8 64,9 65 65,1 65,2 65,5 65,7 65,9 66,3
60 65,9 65,9 65,9 66,1 66,2 66,3 66,4 66,6 66,9 67,1 67,5
70 66,8 66,8 66,8 66,9 67 67,1 67,2 67,5 67,8 68 68,4
80 67,5 67,5 67,5 67,6 67,7 67,8 67,9 68,2 68,5 68,7 69,1
90 68 68 68 68,2 68,3 68,4 68,5 68,7 69,1 69,3 69,7
100 68,3 2,37 2,79 68,4 68.5 68,6 68,7 69 69,2 69,5 69,8 70,1
НО 68,5 2,49 2,47 68,5 68,6 68,7 69 69,2 69,4 69,8 70 70,4
120 68,6 2,59 2,57 68,6 68,7 68,8 69,1 69,3 69,7 70 70,4 70,7
130 68,6 2,69 2,66 68,6 68,7 68,8 69,1 69,3 69,7 70 70,4 70,8
140 68,5 2,79 2,76 68,5 68,6 68,8 69,1 69,3 69,7 70 70,4 70,7
150 68,4 2,88 2,84 68,4 68,6 68,8 69,1 69,3 69,5 69,9 70,2 70,7
160 68,3 3,01 2,94 68,3 68,4 68,5 68,7 69 69,3 69,7 70,1 70,5
170 67,9 3,13 3,04 67,9 68 . 68,3 68,5 68,7 69,1 69,4 69,8 70,1
180 67,5 3,27 3,15 67,5 67,6 67,8 68 68,3 68,6 69 69,3 69,8
190 67 3,42 3,26 67 67,1 67,3 67,6 67,8 68,2 68,5 69 69,4
200 66,3 3,55 3,35 66,3 66,5 66,8 67 67,2 67,6 67,9 68,4 69
210 65,5 3,72 3,47 65,5 65,7 65,9 66,2 66,5 67 67,5 67,8 68,3
220 64,5 3,9 3,57 3,8 64,8 65 65,2 65,6 66,1 66,5 67,1 67,7
230 63,7 4,09 3,68 3,93 63,8 64,1 65,5 64,7 65,1 65,7 66,2 66,8
240 62,8 4,29 3,77 4 62,8 63 63,3 63,6 64,2 64,8 65,4 65,9
250 61,8 4,51 3,87 4,09 4,5 61,8 62 62,5 63 63,6 64,2 64,8
260 60,5 4,8 3,99 4,2 4,57 60,6 60,8 61,2 61,8 62,3 62,9 63,6
270 59 5,11 4,11 4,33 4,69 59 59,3 59,8 60,5 61,2 61,8 62,5
280 57,5 5,49 4,22 4,42 4,75 5,26 57,6 58,2 58,8 59,5 60,4 61,2
290 55,8 5,83 4,31 4,52 4,85 5,21 55,8 56,3 57 57,8 58,7 59,7
300 54 6,27 4,42 4,59 4,92 5,35 5,98 54,2 55 55.8 56,5 57,2
310 52,3 6,84 4,55 4,75 5,05 5,45 6,01 6,8 53,3 54,1 54,9 55,7
320 50,6 7,51 4,66 4,86 5,15 5,52 6,05 6,72 51,3 52,5 53,4 54,1
330 48,4 8,26 4,77 4,95 5,31 5,61 6,09 6,71 48,8 50,5 51,5 52,6
340 45,7 9,3 4,88 5,07 5,35 5,7 6,14 6,71 45,7 48,1 49,5 50,8
466
Новый справочник химика и технолога
Окончание табл. 3.7.10
7’, °C На линии насыщения Давление, МПа
вода пар 0,101 2,03 4,05 6,08 8,11 10,1 15,2 20,3 25,3 30,4
350 43 10,7 5 5,16 5,43 5,77 6,2 6,71 8,89 45,2 47,3 48,7
360 39,5 12,8 5,11 5,27 5,54 5,86 6,27 6,76 8,61 41,2 44,5 46,4
370 33,7 17,1 5,23 5,4 5,65 5,98 6,35 6,8 8,46 12,3 40,5 43,7
380 5,36 5,51 5,76 6,07 6,44 6,87 8,37 11.1 32,1 40,1
390 5,49 5,64 5,87 6,16 6,54 6,95 8,34 10,6 17,1 34,8
400 5,59 5,75 5,98 6,26 6,62 6,99 8,28 10,3 14.2 25,7
410 5,71 5,86 6,09 6.37 6,7 7,07 8,28 10 13 20
420 5,84 5,99 6,22 6,49 6,8 7,16 8,3 9,92 12,4 16,9
430 5,95 6,11 6,33 6,59 6,9 7,25 8,33 9,83 12 15,4
440 6,08 6,23 6,44 6,71 6,99 7,34 8,37 9,75 11,7 14,4
450 6,2 6,35 6,56 6,84 7,09 7,42 8,41 9,71 11.4 13,8
460 6,34 6,49 6,7 6,97 7,21 7,52 8,48 9,71 11,3 13,4
470 6,47 6,62 6,83 7,08 7,32 7,63 8,55 9,7 11,2 13,1
480 6,61 6,75 6,94 7,19 7,44 7,73 8,62 9,72 11,1 12,9
490 6,72 6,86 7,05 7,28 7,54 7,83 8,68 9.73 11,1 12,7
500 6,84 6,98 7,16 7,39 7,64 7,92 8,75 9,76 11 12,6
3.8. Электрическая проводимость и числа переноса {С.Г. Изотова)
Электрическое сопротивление — характерная для данного проводника величина, определяющая силу тока, проходящего по проводнику и вызываемого приложенным к его концам напряжением. При этом напряжение U, сила тока / и сопротивление R связаны между собой законом Ома:
Если U выражено в вольтах, а / в амперах, то R выражается в омах.
Величина, обратная электрическому сопротивлению, называется электрической проводимостью (или проводимостью) и выражается в сименсах (1 См = = 1 Ом’1).
Зависимость электрического сопротивления постоянному току от длины проводника / (в м) и площади его поперечного сечения 5 (в м2) выражается формулой
Зависимость электрического сопротивления металлических проводников от температуры может быть выражена (в ограниченном интервале температур) формулой
R, = /?о(1 + а 7),
где Ro и Rt — сопротивления при 0 и Г °C, Ом, а а — температурный коэффициент электрического сопротивления.
Числом переноса z-ro иона, называется доля общего количества электричества, проходящего через электролит (расплав, раствор), переносимая данным ионом:
где р — удельное сопротивление проводника, Ом • м, т. е. сопротивление проводника длиной 1 м и площадью поперечного сечения 1 м2.
В технической литературе удельное сопротивление проводника часто выражается в Ом • мм2/м, т. е. как сопротивление проводника длиной 1 м и площадью поперечного сечения 1 мм2.
Величина ае, обратная удельному сопротивлению, называется удельной электрической проводимостью и выражается в См/м.
где q, — количество электричества, перенесенное ионами z-ro рода, Кл; Q — общее количество электричества, прошедшее через электролит, Кл.
Сумма чисел переноса всех ионов равна единице.
В случае бинарного электролита
и р =-----:---
(и+ + и__)
и
и 1_ =----=—,
(и± + и )
где /Т и t — числа переноса катиона и аниона; и+ и м_ — подвижности соответственно катиона и аниона, м2/(В • с). Подвижностью иона z-ro рода называется скорость его движения в электрическом поле напряженностью 1 В/м.
Физические свойства важнейших веществ
467
В табл. 3.8.1-3.8.3 приведены удельное сопротивление р и температурный коэффициент сопротивления а простых веществ, чистых металлов и сплавов, в табл. 3.8.4 — удельное сопротивление металлов и сплавов, применяемых в нагревательных устройствах. Информация об
удельной электрической проводимости воды, органических и неорганических веществ, твердых и расплавленных солей, а также о числах переноса катиона и аниона в твердых солях содержится в табл. 3.8.5-3.8.8 соответственно.
Таблица 3.8. /
Удельное сопротивление р и температурный коэффициент сопротивления а простых веществ Значения а приведены для интервала температур 0-100 °C.
Вещество 7'. °C p- 10s, Ом • м a • 10’ Вещество T. °C p- 108. Ом • м a • 103
Ag 20 1,6 4,1 Mn 0 185
Al 20 2,69 4,2 Mo 0 5,17 4,6
As 20 35 Na 0 4,34 5,0
Au 0 2,19 Nb 18 13,1 3,95
20 2,3 3,9 Nd 18 79
В 0 1,8- 1012 Ni 20 6,84 6,81
Ba 20 50 Os 20 9,5 4,2
Be 20 4-6 6,0 P (бел.) 11 1017
Bi 0 106,8 Pa 20 10.8
20 116 4,2 Pb 20 20,6 3,36
C 0 1375 Pd 20 10,8 3,77
Ca 20 4,37 4,6 Pr 18 88
Cd 0 6,83 Pt 0 9,81 3,92
20 7,4 4,3 Rb 0 11,3 5,53
Ce 18 78 Re 0 19,8
Co 20 6,24 6,04 Rh 0 4,3 4,57
Cr 0 18,9 5,88 Ru 0 7,6
Cs 0 18,83 S (ам.) 20 2 • 1023
20 21 4,8 Sb 20 42 5,1
Cu 20 1,673 4,3 Si 0 1015
Fe 20 9,71 6,51 Sn 20 12,8 4,2
Ga 0 53,4 Sr 0 24,8 0,0038
Ge 0 ~89• 10’ Ta 20 13,5 3,8
Hf 0 30 Tc 19,6 2- 105
Hg 20 95,8 0,9 Th 20 18,62 2,3
In 0 8,37 4,7 Ti 0 43,5 0,0054
Ir 20 5,3 3,9 T1 0 15,0 5,2
I2 20 1,3 • 1015 U 0 30,6 3,4
К 0 6,15 5,8 V 20 26 2,8
La 18 59 w 20 5.5
Li 0 8,55 4,75 Zn 20 5,92 4,2
Mg 20 4,4 4,2 Zr 0 41,0 4,4
Таблица 3.8.2
Удельное сопротивление р и температурный коэффициент сопротивления а сплавов
Значения а даны для интервала температур 0-100 °C (если взят другой интервал, то он указывается в скобках).
Сплавы расположены в алфавитном порядке химических символов (по преобладающему компоненту).
Сплав Состав, масс. % T, °C p • 108. Ом • м a - 104
Ag—Cd—Zn—Cu 50 Ag; 18 Cd; 16,5 Zn; 15,5 Cu 0 7,0
Ag—Cu—Zn 60 Ag; 25 Cu; 15Zn 0 8,3
Al—-Cu 94,0 Al; 6,0 Cu 0 3,1 38
Al—Cu—Mg—Mn 94,8 Al; 4,0 Cu; 0,6 Mg; 0,6 Mn 20 5,0-5,3 23
Al—Mg 90 Al; 10 Mg 0 8,0
Al—Mg—Si 99 Al; 0,5 Mg; 0,5 Si 20 3,25 36
Al—Mn 98,75 Al; 1,25 Mn 20 3,4-4,4
468
Новый справочник химика и технолога
Продолжение табл. 3.8.2
Сплав Состав, масс. % T. °C p • i О8. Ом • м a - 104
Al—Si 88 Al; 12 Si 0 4,5
Al—Zn—Mg—Си 90,3 Al; 5,6 Zn; 2,5 Mg; 1,6 Си 0 3,7-5,0
Au—Ag 90 Au; 10 Ag 0 6,3 12
67 Au; 33 Ag 0 10,8 6,5
Au—Си—Ag 66,5 Au; 15,4 Си; 18,1 Ag 0 14,6 5,3
(см. также 58,3 Au; 26,5 Си; 15,2 Ag 0 13,2 5,7
Си—Ag—Au)
Bi—Sn 98 Bi; 2 Sn 0 24,4
(см. также Sn—Bi)
Bi—Sn—Pb 72 Bi; 14 Sn; 14 Pb 0 52 20
49 Bi; 23 Sn; 28 Pb 0 64 20
Си—Ag—Au 78,3 Си; 14,3 Ag; 7,4 Au 0 3,6 18
Си—Al 97 Си; 3 Al 0 8,26 10,2
90 Си; 10 Al 0 12,6 32
Си—Be 98 Си; 2 Be 0 6,8-7,4 13
Си—Mn 99,02 Си; 0,98 Mn 0 4,83
98,51 Си; 1,49 Mn 0 6,66
95,8 Си; 4,2 Mn 20 17,9 1,7(20-100 °C)
92,6 Си; 7,4 Mn 20 19,7 2,5 (20-100 °C)
Си—Mn—Fe 91,0 Си; 7,1 Mn; 1,9 Fe 0 20 1,2
95,68 Си; 3,0 Mn; 1,32 Fe 0 107,3 0,4
84,91 Си; 14,76 Mn; 0,33 Fe 22,5 53,46
70,6 Си; 23,2 Mn; 6,2 Fe 0 77 0,22
Си—Mn—Ni 84 Си; 12 Mn; 4 Ni 20 44 0,0 (при 25 °C)
(см. также Mn—Ni—Си) 73 Си; 24 Mn; 3 Ni 0 48 -0,3
Си—Ni 90 Си; 10 Ni 20 14,1 5,24 (20-100 °C)
80 Си; 20 Ni 20 26,6 2,37(20-100 °C)
70 Си; 30 Ni 20 36.3 0,48 (20-100 °C)
55 Си; 45 Ni 20 49 ±0,18
Си—Zn—Ni 61 Си; 25 Zn; 14 Ni 20 33 4
60 Си; 32 Zn;8Ni 0 72
58 Си; 24 Zn; 18 Ni 0 30,9 0,43
44 Си; 26 Zn; 30 Ni 0 47,6 0,43
Си—P 99,52 Си; 0,48 P 20 8,4 8,43 (20-100 °C)
99,07 Си; 0,93 P 20 15,2 5,03 (20-100 °C)
Си—Pb—Sn—Zn 85 Си; 5 Pb; 5 Sn; 5 Zn 0 10,5
Си—Sn 95 Си; 5 Sn 0 9,5
88 Си; 12 Sn 20 18 5
С и—S n—N i—Zn 88 Си; 5 Sn; 5 Ni; 2 Zn 0 10,5-14
Си—Sn—Zn 90 Си; 6 Sn; 4 Zn 15 13,5
Си—Zn 85 Си; 15Zn 0 4,65
70 Си; 30 Zn 0 6,87 16
60 Си; 40 Zn 0 6,81 17
Си—Zn—Fe—Sn 59 Си; 39 Zn; 1 Fe; 1 Sn 0 7,03
Fe—C 96,6 Fe; 3,4 C 20 66,0
Fe—C—Si 97,2 Fe; 1 C; 1,8 Si 18 12,0
Fe—Cr 88 Fe; 12Cr 20 60
80 Fe; 20 Cr 20 62
Fe—Cr—Ni 74 Fe; 18Cr;8Ni 20 73
63 Fe; 25 Cr; 12 Ni 20 87
55 Fe; 25 Cr; 20 Ni 20 88
45 Fe; 18Cr;37Ni 20 108
Fe—Si 96 Fe; 4 Si 20 62 80
75 Fe; 25 Si 20 45
Fe—Ti—C 97,35 Fe; 2,5 Ti; 0,15 C 20 16
Fe—V—C 93,9 Fe; 5 V; 1,1 C 20 121
Физические свойства важнейших веществ
469
Окончание табл. 3.8.2
Сплав Состав, масс. % 71 °C p • 108, Ом • м a 104
Fe—W—С 94,8 Fe; 5 W; 0,2 C 20 20
79,8 Fe; 20 W; 0,2 C 20 24
Mg—Al—Zn 94,3 Mg: 4,8 Al; 0,9 Zn 0 11,3
89 Mg; 9 Al; 2 Zn 0 16
Mn—Ni—Си 72 Mn; 10 Ni; 18 Си 25 175 14,1 (25-150 °C)
Ni—Al—Мп—Si—Fe 94 Ni; 2 Al; 2,5 Mn; 1 Si; 0,5 Fe 0 33,3 12
Ni—Cr 80Ni;20 Cr 0 98-103 1,8
Ni—Cr—Fe 78 Ni; 15Cr;7Fe 0 98
75-70 Ni; 20 Cr;5-10Fe 20 109
Ni—Си—Fe—Mn 67,6 Ni; 30 Си; 1,4 Fe; 1,0 Mn 0 48 20
Ni—Mn 95 Ni; 5 Mn 0 18
Ni—Mo—Fe 62 Ni; 32 Mo; 6 Fe 0 135
Pb—Sb 94 Pb; 6 Sb 0 23
Pb—Sn 66,7 Pb; 33,3 Sn 15 16
(см. также Sn—Pb)
Pb—Те—Си 99,9 Pb; 0,04 Те; 0,06 Си 0 20
Pt—I г 90 Pt; 10 Ir 0 24 12
Pt—Rh 90 Pt; 10 Rh 0 21,14 13
Sn—Bi 90,5 Sn; 9,5 Bi 12 16
Sn—Pb 90 Sn; 10 Pb 15 13,5
60 Sn; 40 Pb 0 15
Zn—Си 98,95 Zn; 1,05 Си 0 6
Таблица 3.8.3
Отношение удельных сопротивлений — чистых металлов при различных значениях температуры Ро
(р, и ро — удельное сопротивление (Ом • м) при Г и О °C соответственно).
Металл Ро - 108 Температура, °C
-253 -192 -78 100 200 300 400 500
Ag 1,49 0,009 0,207 0,684 1,410 1,829 2,263 2,710 3,168
Al 2,41 0,008 0,144 0,646 1,45 1,89
Au 2,19 0,007 0,238 0,696 1,398 1,809 2,232 2,680 3,144
Bi 106,8 0,223 0,395 0,715 1,446 2,071
Ca 4,3 0,354
Cd 6,83 0,021 0,253 0,693 1,424 1,886
Co 5,06 0,046 0,151 1,658 2,478 3,527 4,564 5,605
Cs 18,83 0,067
Си 1,55 0,006 0,148 0,649 1,433 1,866 2,308
Fe 8,7 0,011 0,085 0,579 1,648 3,474
Ge ~89 • 10' 1,30 1,35
Hf 30 0,100 0,263
Hg 94,07 0,064 0,282
In 8,37 0,026 0,218
Ir 4,58 0,054 0,225 0,694 1,393 1,795 2,197 2,631 3,070
Li 8,55 0,007
Mg 4,18 0,034 0,285 0,707 1,37 1,76 2,21 2,76
Mo 5,17 0,045 0,137 0,667 1,435 1,885 2,342 2,285
Na 4,34 0,007
Nb 13 0,338 0,499
Ni 6,05 0,086 0,178 0,615 1,672 2,532 3,660 4,914
Pb 18,8 0,031 0,263 0,691 1,422 1,877 2,379
Pd 10,8 0,010 0,173
Pt 9,81 0,001 0,206 0,686 1,392 1,772 2,141 2,498 2,844
Rb 11,3 0,081
Re 19,8 0,110 0,162 0,659 1,443 1,903 2,382 2,888 3,414
Rh 4,3 0,004 0,007 0,685 1,377 1,728 2,058 2,368
470
Новый справочник химика и технолога
Окончание табл. 3.8.3
Металл Po- 108 Температура. °C
-253 -192 -78 100 200 300 400 500
Ru 7,6 0,083 0,176
Sb 38,6 0,032 0,204
Sn 9,3 0,011 0,23 0,665
Sr 24,8 0,116
Та 12,4 0,014 0,296 0,730 1,347 1,661
Th 12,0 0,031 0,245 1,24
Ti 43,5 0,215 1,47
T1 15,0 0,030 0,245
U 30,6 0,597 0,684
V 19,0 0,954 0,967
W 4,91 0,001 0,156 0,652 1,465 1,957 2,479 3,026
Zn 4,8 0,009 0,211 0,686 1,415 1,856 2,341
Zr 41,0 0,044 1,44
Таблица 3.8.4
Удельное сопротивление р (Ом • мм2/м) металлов и сплавов, применяемых в нагревательных устройствах
Металл или сплав Состав, масс. % I Наивысшая I допустимая температура, °C Температура, °C
20 100 200 300 400 500 600 700 800 900 1000 1100 1200 1300 1500
Алюминиевая 93Си; 7 А1 450 0,142
бронза
Вольфрам* 100 W 2000 0,055 0,074 0,098 0,125 0,153 0,182 0,211 0,241 0,271 0,301 0,332 0,394 0,425 0,49
Изабеллин А1, Мп, Си 400 0,50 0,498 0,495 0,495 0,496
Кантал 60 Fe; остальное Сг, 1300 1,45
А1, Со
Константан 54 Си; 46 Ni 400 0,50 0,504 0,505 0,506 0,506
Кремнистая 96 Fe; 4 Si 200 0,50 0,55 0,59
сталь
Манганин 86 Си; 12Mn;2Ni 300 0,43 0,429 0,422 0,426
Мегапир 65 Fe; 30 Cr; 5 Al 1300 1,40 1,40 1,41 1,41 1,42 1,42 1,42 1,42 1,43 1,43 1,43 1,43 1,43 1,43
Молибден** 100 Mo 1500 0,055 0,075 0,23 0,265 0,288 0,315 0,345 0,374 0,403 0,462
Нейзильбер 60 Cu; 20 Ni; 20 Zn 300 0,55 0,562 0,579 0,589
Никелин 67 Cu; 30-31 Ni; 300 0,40 0,408 0,415 0,422
2-3 Mn
Никель 100 Ni 400 0,06 0,16 0,22 0,30 0,37
Нирезист Fe, Ni, Cu, Cr 700 1,18 1,26 1,34 1,40 1,46 1,51 1,56 1,62
Нихром 80 Ni; 20 Cr 1150 1,10 1,12 1,14 1,17 1,17 1,17 1,17 1,16 1,16 1,16 1,17 1,18
Платина 100 Pt 1500 0,10 0,137 0,174 0,21 0,245 0,28
Хромоалюми- 65 Fe; 30 Cr; 5 Al 1300 1,5
ниевая сталь
* Предохранительный газ — Н2 или смесь Н2 + N2.
** Предохранительный газ — пары СН3ОН.
Физические свойства важнейших веществ
472
Новый справочник химика и технолога
Таблица 3.8.5
Удельная электрическая проводимость воды
Данные относятся к предельно чистой воде, перегнанной в вакууме.
Удельная электрическая проводимость воды, перегнанной в присутствии воздуха, при 20-25 °C составляет (1-2)- 10”6 См/м.
7’. °C ж • 1()6. См/м Т. °C ж • 106, См/м
-2 1,47 20 4,85
0 1,58 26 6,70
2 1,80 30 8,15
4 2,12 34 9,62
10 2,85 50 18,9
18 4,41
Таблица 3.8.6
Удельная элект рическая проводимость жидкостей
Название Формула T. °C ж. См/м
Простые вещества и неорганические соединения
Аммиак NH3 -79 1,3 • 10 5
Бром Br? -17,2 1,33 • 10’"
Водорода бромид HBr -80 8 • 10~7
Водорода иодид Hl -35,4 10630
Водорода хлорид HC1 -96 1 • 10 6
Водорода цианид HCN 0 3,3 • 10 4
Ртуть Hg 0 1 • 10 10
Селена дибромид-оксид SeOBr2 45-50 6 • 10’3
Селена оксид-дихлорид SeOCl2 25 2 • 10 3
Серная кислота H2SO4 25 1
Серы диоксид SO2 -15 9 • 10 5
Серы диоксид-дихлорид (сульфурил хлори- SO2C12 25 3 • 10 6
стый)
Серы оксид-дихлорид (тионил хлористый) SOC12 25 2 • 104
Сульфан (сероводород) H2S -61,8 1 • 10’9
Трихлорарсан AsCl3 25 1,2 • 10 4
Фосфора оксид-трихлорид POCI3 25 2,2 • 10”5
Хлор ci2 -70 < 1 • 10 14
Хлорссрная кислота (хлорсульфоновая C1SO2OH 25 1,6 • 10-2
кисло»а
Органические соединения
Анилин c6h7n 25 2,4 • 10 6
Антрацен C14H10 230 3 • 10’8
Ацетальдегид (уксусный альдегид) C2H4O 15 1,7 • 10 4
Ацетилбромид C2H3BrO 25 2,4- 10 4
Ацетилхлорид C2H3C1O 25 4 • 10’5
Ацетон c3H6o -15 1,1 • 10 7
0 6 • 10"6
18 2 • 10 “6
20 1,2 • 10”5
25 6 • 10 6
Ацетофенон C8H8O 25 6 • IO'7
Бензальдегид c7H6o 20 4 • 10 5
25 1,5 • 10’5
Бензилбензоат C14H12O2 25 < 1 • 10 7
Бензойная кислота c7H6o2 125 3 • 10’7
Бензол c6H6 < 1 • 10 16
Физические свойства важнейших веществ
473
Продолжение табл. 3.8.6
Название Формула /’. °C аз, См/м
Бензонитрил c7h5n 25 5 • 10‘6
Бромбснзол С6Н5Вг 25 <2 • 10 9
Бромоформ (трибром метан) СНВгз 25 <2 • 10’6
Бромциан CBrN 55 ~2
Бромэтан C2H5Br 25 <2 • 10 6
Бутан-2-он С4Н8О 25 1 • 10 5
Гексан С6Н14 18 < 1 • 10 16
Гептан С7Н16 19,5 < 1 • 10’"
Глицерин С3Н8О3 25 6,4 • 10 6
1,2-Дибромэтан С2Н4Вг2 19 <2 • 10 8
МА'-Диметилметанамин (триметиламин) c3h9n -33,5 2,2 • 10 8
Димстилсульфат c2h6o4s 0 1,6 • 10 5
25 3 • 10 5
Дихлоруксусная кислота С2Н2С12О2 0 4 • 10 6
25 7 • 10-6
1,2-Дихлорэтан С2Н4С12 25 3 • 10 6
Диэтиловый эфир С4Н|0О 25 <4 • 10’11
Диэтилоксалат С(,Н]о04 25 7,6 • 10 5
И од метан СН31 25 <2 • 10 6
Иодэтан С2Н<1 25 <2 • 10 6
м-Крезол С7Н8О 25 < 1,7 • 10 6
Ксилол С8Н,о 19,5 <1-10 '
л-Мента-1,3-диен (тсрпинен) С,оН16 25 1,7 • 10 6
Метанамин (метиламин) ch5n ~7 - 10 5
Метанол (метиловый спирт) СН4О 18 4,4 105
20 5,8 • 10 4
25 2,2 • 10 5
Метилацетат С3н6о2 25 3,4 • 10 4
З-Метилбутан-1-ол (изоамиловый спирт) С5Н12О 18 5 • 10 6
Метилнитрат CH3NO3 25 4,5 • 10’4
1-Метил-2-нитробензол или 1-метил-З-нит- C7H7NO2 25 <2 • 10 5
робензол
4-Метилпентановая кислота (изовалсриано- С3НюО2 80 <4 • IO'"
вая кислота)
2-Мстилниридин (а-пиколин) c6h7n 25 5,5 • 10 5
2-Метилпропан-1-ол (изобутиловый спирт) c4H10o 18 1 • 10 5
25 8 • 10 6
Муравьиная кислота CH2O2 18 5,6 • 10 3
25 6,4 • 10 ’
Нафталин С10Н8 82 4 • 10 8
Нитробензол c6h5no2 0 5 • 10 7
25 <2 • 10’6
Нитрометан ch3no2 0 4,4 • 10 6
Нонан C9H2Q 25 1,7 • 10 6
Оксонитрил (дициан 2n2 <7 • 10 ‘5
Олеиновая кислота cI8H34o2 15 <2 • 10’8
Пентан C5H12 19,5 <2 • 10’8
Пентан-2,4-дион (ацетилацетон) C5H8O2 0 2 • 10 5
Пентилнитрат (амилнитрат) C5HnNO3 25 2,8 • 10"5
Пентилнитрит (амилнитрит) C5HhNO2 25 1 • 10 5
Пин-2-ен C,0Hl6 23 <2 • 10 8
Пиперидин C5HhN 25 6,8 • 10‘8
Пиридин c5h5n 18 5,3 • 10’6
25 <2 • 10 5
Пропаналь c3H6o 25 8,5-10 5
474
Новый справочник химика и технолога
Окончание табл. 3.8.6
Название Формула Г. °C ж. См/м
Органические соединения
Пропан-1-ол (пропиловый спирт) С3Н8О 18 5 • 10’6
25 2 • 10 0
Пропан-2-ол (изопропиловый спирт) С3Н8О 25 3,5 • Ж4
Проп-2-сн-1-ол (аллиловый спирт) С3Н6О 25 7 • 10’3
Пропионовая кислота СзН6О, 25 < 1 • 10 7
Стеариновая кислота С18Нз6О2 80 <4 • 10 "
Теграхлормстан (четыреххлористый углерод) СС14 18 4 • 10 16
о-Толуидин c7h9n 25 <2 • 10 4
«-Толуидин c7h9n 100 6,2 • 10 6
Толуол c7H8 19.5 < 1 - 10 12
Трибромацетальдегид (бромаль) С2НВГ3О 25 8 • 10 6
Трихлоруксусная кислота С2НС13О2 25 ЗЮ7
60 6,2 • 10 7
Уксусная кислота С2Н4О2 0 5 • 10 7
25 < 1,1 • 10 6
Фенилмстанол (бензиловый спирт) С7Н8О 25 1,8 • 10 4
Фенол с6н6о 25 < 1,7 • 10*
Формамид CH3NO 25 4 • 10 *
Фосген СС12О 25 7 • 10 "7
2-Фуральдсгид (фурфурол) С5Н4О2 25 1,5 • 10 4
Хинолин c9h7n 0 1,6-10 6
25 2,2 10”6
50 7,4 • 10 6
2-(Хлорметил)оксиран (эпихлоргидрин) С;Н5С1О 25 3,4 • 10 6
0 4 • 10 5
Хлороформ СНС13 25 <2 • 10 6
Хлоруксусная кислота СН3СЮ2 60 1,4 • 10 4
Этанамин (этиламин) c2h7n -33,5 4,6 • 1 0 6
Этанол (этиловый спирт) С2Н6О 0 1,5 • 10 5
18 6,4 • 10’6
25 1,3 -1 0 7
Этилацстат с4н8о2 25 < 1 • 10 7
Этилбензоат C9Hi0O2 19 <2 • 10 8
25 < 1 •10 7
Этиленгликоль С2Н6О2 25 ЗЮ5
Этилнитрат C2H5NO3 0 2,3 • 10”5
А-Этилэтанамин (диэтиламин) c4h,,n -33,5 2.2 • 10 7
* Приведены ориентировочные данные, поскольку электрическая проводимость органических соединений зависит от методов их очистки.
Таблица 3.8.7
Удельная электрическая проводимость твердых и расплавленных солей
Вещество: Тпп, °C Т. °C ж, См/м Вещество: Т„„. °C 7- оС ж, См/м
AgBr; 200 0,052 AgCl; 640 449
430 350 8 455 680 462
425 276 700 465
550 300 720 469
800 363 740 472
AgCl; 250 0,03 760 475
455 450 и 780 478
456 376 800 481
550 405 Agl; 150 133
600 444 557 300 197
Физические свойства важнейших веществ
475
Продолжение табл. 3.8.7 Продолжение табл. 3.8.7
Вещество: Т1П|. °C T, °C ae, Cm/m Вещество; Tnj), °C T. °C <E, Cm/m
Agi; 500 252 CuBr; 500 252
557 600 243 (жидк.) 550 267
800 230 CuCl; 45 5,3 • 10“6
AgNO3; 230 74 430 213 0,015
209 260 88 366 6,15
300 105 404 23,7
330 117 450 330
350 125 550 360
А1Вг3; 195 9- 10 6 CuCl2: 440 20,8
98 201 1,0 • 10 4 630 460 22,5
243 1,8 • 104 480 34,1
270 2,6 • 10”4 490 39,4
A1CI3; 189 ~4 - 10 4 HgBr2; 128 7,6 • 10“5
192,6 200 5,6 • 10“5 241 132 1,5 • 10 3
227 8,6 • 10 5 HgCl2; 294 8,2 • 10“3
245 1,1 • 104 277 311 0,01
A1I3; 209 2,6 • 10’4 441 0,0112
191 246 5,2 • 10 4 Hgi2; 92 1 • 10’6
270 7,4 • 10 4 250 167 1 • 10 5
BaCl2; 900 171 220 8 • 10 5
960 1000 205 260 0,85
1050 219 320 0,66
1100 231 lnBr3; 445 17
BeCl2; 451 0,319 436 480 17
404 460 0,572 540 16
472 0,868 InCi; 242 97
BiCl3; 266 44 225 272 114
229 315 51 310 138
350 56 351 166
CaCl2; 795 199 392 54
765 851 211 466 67
888 234 496 71
966 259 InCl3; 594 42
CdBr2; 571 106 586 625 39
568 597 112 633 38
617 115 673 35
CdCl2; 576 193 694 33
568 668 212 Inl3; 221 5,4
755 230 210 250 6,6
801 237 319 8,5
Cdl2; 388 19 372 9,6
387 418,6 25 KBr; 760 166
442,9 30 735 860 186
466,4 35 900 195
CsCl; 660 114 950 205
642 711 126 KC1; 440 4,4 • 10“ъ
775 139 770 540 1,91 • 10 4
831 148 640 1,01 • 10“3
CsNO3; 446,6 59 740 9,8 - IO’3
407 494,1 66 800 219
556,3 74 850 230
y-CuBr 137 3,3 • 10 4 900 240
359 7,5 930 246
p-CuBr 400 148 K2CO3; 900 193
450 200 897 950 212
a-CuBr; 480 354 1000 226
488 KF; 857 863,0 295
476
Новый справочник химика и технолога
Продолжение табл. 3.8.7 Продолжение табл. 3.8.7
Вещество; Тпл. °C Г, °C ж. Cm/m Вещество; Г)1Л, °C °C ae. Cm/m
KF; 857 881,1 311 NaCl; 800 950 388
903,4 329 Na2CO3; 850 237
916,3 342 850 900 310
971,6 392 NaF; 988 305
KI; 691,5 123 995 1000 315
682 742,9 132 1010 324
779,8 138 1020 332
813,0 148 1030 340
KNO3; 350 67 1040 348
308 410 85 Nal; 700 256
450 97 662 750 263
500 111 850 276
КОН; 450 281 950 290
400 500 310 NaNO3; 240 7,6 • 10 3
550 340 312 260 1,65 • 10”4
600 369 275 3,2 • IO”4
K2SO4; 1100 184 290 5,8 • 10 4
1096 1150 194 305 1,15 • 10 •’
LaCh; 872 114 320 102,7
872 895 123 350 1 17,3
1005 155 380 130,5
LiCl; 620 587 400 138,4
614 681 614 440 152,8
746 640 480 165,8
786 653 500 171,6
801 659 NaOH; 320 212,3
LiF; 905 2030 318 350 238
845 950 2340 400 282
LiNO3; 250 79 450 327
260 300 107 NaPO3; 700 55
320 118 619 800 80
350 132 900 105
400 160 1000 130
440 180 1100 154
MgCI2; 729 105 Na2SO4; 900 223
714 750 106 884 950 237
774 113 1000 250
800 118 1050 264
909 139 1100 277
1013 158 NdCi3; 775 69
MoCl5; 216 1,8 • 10 4 761 827 84
194 234 4,1 • 10 4 873 97
258 7,5 • 10"4 900 104
NaBr; 420 6 • 10 3 PbCl2; 94 2,50 • 10”4
750 500 3,1 • 10”4 498 123 6,35 • 10”4
540 7,4 • 10”4 169 2,54 • 10”3
600 3,15 • 10”3 193 4,57 • 10”3
640 6,91 • 10 3 249 1,72 • 10 2
700 1,74 • 10 2 289 4,23 • 10‘2
740 2,76 • 10 2 323 6,57 • 10”2
NaCl; 590 8,7 • 10 4 363 0,111
800 650 3,05 • 10”3 390 0,161
700 8,72 -10 3 438 0,291
750 2,46 • 10”2 466 0,466
790 5,70 • 10 2 484 0,92
850 366 508 147,8
900 377 Pbl2; 412 155 1,82 • 10”6
Физические свойства важнейших веществ
477
Продолжение табл. 3.8.7 Окончание табл. 3.8.7
Вещество: °C T, °C a?. Cm/m Вещество; 7^, °C T, °C зе. Cm/m
РЫ2; 209 6,92 • 10 6 TIBr; 250 0,004
412 280 3,63 • 10 5 457 447 0,47
307 1,00 • 10 4 460 81
370 1,10 • 10’3 550 102
РгС13; 824 90 600 113
780 902 120 T1C1; 250 0,005
965 140 427 421 0,61
RbCl; 733 149 431 109
715 780 162 500 133
873 181 600 170
915 187 Til; 250 1 • 10 3
RbNO3; 318,8 44 438 429 0,48
305 377,7 57 439 53
435,9 69 550 75
493 80 600 84
SbCl3; 100 7,35 -10 2 UC14; 598 42
73 120 8,09 • 10’2 590 620 48
140 8,78 • 10’2 WC15; 250 6,7 • 10’5
160 9,51 • 10 2 230 270 1,22 • IO-4
180 0,1026 290 1,70 • 10’4
200 0,1073 300 1,84 • 10 4
210 0,1128 WC16; 300 2,60 • 10 4
ScCl3; 959 56 284 320 4,05 • 10’4
940 991 65 330 6,94 • 10 4
SnCl2; 253 78 YC13; 714 40
247 263 89 721 793 53
314 118 875 73
411 172 ZnCl2; 319 0,03
SrCl2; 900 198 316 340 0,28
872 1000 229 460 5,09
1050 243 581 21
1110 256 650 31
ThCl4; 843 74
770 889 84
922 86
Таблица 3.8.8
Числа переноса катиона и аниона в твердых солях при различных температурах
Вещество Температура. °C C t_
AgBr 20-300 1,00 0,00
AgCl 20-350 1,00 0,00
Agl 20-400 1,00 0,00
a-Ag2S 200
a-Ag2Se 200 Электронная проводимость
a-Ag2Te 200
BaBr2 350—450 0,00 1,00
ВаС12 400-700 0,00 1,00
BaF2 500 0,00 1,00
y-CuBr* 390 1,00 * * 0,00
308 0,92 0,08**
272 0,39 0,6 Г*
223 0,14 0,86**
181 0,036 0,964**
52 0,005 0,995**
478
Новый справочник химика и технолога
Окончание табл. 3.8.8
Вещество Температура. °C t- t.
y-CuBr* 27 0,00 1,00’*
СиС1* 366 1,00 0,00**
315 1,00 0,00**
254 0,90 0,10**
218 0,29 0,71**
178 0,05 0,95*’
40 0,02 0,98*’
18 0,00 1,00**
Си! 400-500 1,00 0,00
Си2О 1000 1,00 -4 • 10“4
Cu2S 220 1,00 0,00
КВг 605 0,5 0,5
660 0,4 0.6
КС1 435 0,956 0,044
500 0,941 0,059
550 0,917 0,083
600 0,884 0,116
KI 610 0.9 0.1
NaCl 400 1,000 0,000
500 0,983 0,017
550 0,937 0,063
580 0,919 0,081
620 0,883 0,113
NaF 500 1,000 0,000
550 0,996 0.004
600 0,916 0,084
625 0,816 0,184
PbBr2 250-365 0,00 1,00
PbCI2 90 1 • 10“10 1,00
270 1 - 10 5 1,00
484 1 • 10 3 1,00
PbF2 200 0,00 1,00
Pbl2 376 0,93-1,00 0,07-0,00
338 0,79-0,85 0,21-0,15
290 0,67 0,33
255 0,39 0,61
194 0,03 0,97
155 0,004 0,996
Натриевое стекло (30 % Na2O, 70 % SiO2) 400-500 1,00 0,00
* Электрическая проводимость осуществляется катионом и электроном.
** Приведенные значения соответствуют числу переноса электрона.
3.9. Диэлектрическая проницаемость
(С.Г. Изотова)
Диэлектрическая проницаемость £ численно равна отношению силы взаимодействия точечных электрических зарядов в вакууме к силе их взаимодействия в однородном диэлектрике. Для изотропных тел диэлектрическая проницаемость является скалярной величиной, для анизотропных кристаллов — тензорной. Диэлектрическая проницаемость зависит от поляризуемости
молекул (атомов, ионов), от их числа в единице объема, а также от температуры и частоты изменения электрического поля.
Предел, к которому стремится диэлектрическая проницаемость, когда частота стремится к 0, называется статической диэлектрической проницаемостью.
В табл. 3.9.1-3.9.3 приведены данные по диэлектрической проницаемости газов и паров, жидкостей и твердых веществ.
Физические свойства важнейших веществ
479
Приведенные в табл. 3.9.1 данные относятся к давлению 101,3 кПа и частоте < 1 МГц. Курсивом выделены величины, полученные экстраполяцией.
Таблица 3.9. /
Диэлектрическая проницаемость газов и паров
Название Формула T, °C E
Простые вещества и неорганические соединения
Азот n2 0 1,000580
25,0 1,000528
Азота оксид NO 25,0 1,00059
Аммиак NH3 16,0 1,0066
Аргон Ar 0 1,000554
25,0 1,000504
Арсан (арсин) AsH3 16,0 1,00191
Вода H2O 110,0 1,0126
140,0 1,00785
Водород H2 0 1,000270
25,0 1,000252
Водорода бромид HBr 21,2 1,00280
Водорода иодид Hl 21,9 1,00212
Водорода хлорид HC1 21,0 1,00380
Водорода цианид HCN 15,0 1,0238
29.8 1,0159
Воздух 0 1,00057
Гелий He 0 1,000068
Дидейтерий (103,5 кПа) d2 20,1 1,000250
Диазота оксид n2o 25,0 1,00103
Дисилан Si2H6 25,0 1,00354
Иода пентафторид if5 119,5 1,009108
150,3 1,007973
172,8 1,007135
Кислород 02 0 1,000532
25,0 1,000486
Криптон Kr 25,0 1,000768
Ксенон Xe 25 1,001238
Неон Ne 0 1,000127
Озон Оз 0 1,00190
Ртуть Hg 0 1,00170
400,0 1,00074
Серы гексафторид 0 25,0 1,002049
Серы диоксид so2 -7,7 1,0100
Серы триоксид so3 79,8 1,001270
Сульфан (сероводород) H2S 27,8 1,00331
Углерода диоксид co2 0 1,00099
Углерода дисульфид (сероуглерод) cs2 28,4 1,00290
151,1 1,00206
Углерода монооксид co 25,0 1,00634
Урана гексафторид UF6 20,0 1,00380
83,1 1,00322
Фосфин PH3 100,0 1,00146
16,0 1,00238
Органические соединения
Ацетилен C2H2 -76,9 1,00189
25,0 1,001217
Ацетилхлорид C2H3C1O 16,8 1,0219
Ацетон c3H6o 100,0 1,0159
480
Новый справочник химика и технолога
Продолжение табл. 3.9.1
Название Формула Т. °C £
Органические соединения
Бензол с6н6 100,0 1,000274
2-Бромнропан С3Н7Вг 100,3 1,00980
З-Бромпропен С3Н5Вг 18,8 1,01290
Бромэтан С2Н5Вг 17,0 1,01400
99,6 1,00890
Бромэтилен С2Н3Вг 17,8 1,00820
1,1,1,2,2,3,3-Г ептафторпропан C3HF7 26,6 1,008104
69,3 1,006387
108,9 1,005271
Дибром метан СН2Вг2 48,8 1,00880
Димстиловый эфир С2Н6О 19,1 1,00624
Дифтордихлорметан (фреон-12) CC12F2 0 1,00355
Диэтиловый эфир СдНюО 100,0 1.0049
Изопентан С5Н!2 100,0 1,0026
Иодэтан С2Н51 16,7 1,01420
100,2 1,00880
Метан сн4 25.0 1,000804
Метанамин (метиламин) ch5n 99,8 1,0003770
Метанол СНдО 100,0 1,0057
Метил ацетат с3н6о2 100,0 1,00770
2-Метилбут-2-ен С5н1о 25,0 1,000123
99,4 1,00283
Мсти л формиат С2НдО2 100,0 1,00730
Нитрометан CH3NO2 99,9 1,0247
Нитроэтан c2h5no2 99,9 1,0281
1,1 '-Оксибис(пентафторэтан) C4F,oO 26,1 1,004004
62,2 1,003519
66,6 1,003485
105,5 1,003108
111,0 1,003016
Оксиран (окись этилена) С2НдО 17,1 1,01130
Пентан c5H12 100,1 1,00254
Пент-2-ен С5Н,о 99,4 1,00284
Пропан-1-амин (пропиламин) c3h9n 99,8 1,00503
Пропаннитрил(пропионитрил) c3h5n 99,9 1,0283
Проп-2-ен-1-амин (аллиламин) c3h7n 100,0 1,00420
Т етрахлорметан СС1д 110,0 1,0030
Т олуол c7H8 126,0 1,0043
Трифторхлорметан CC1F3 0 1,00257
Трифторхлорэтилен C2C1F3 28,0 1,002729
104,1 1,002140
Фтороформ CHF3 25,0 1,007500
1 -Хлорбутан СдН9С1 99,4 1,01010
Хлорметан CH3C1 100,0 1,00870
2-Хлорпропан С3Н7С1 17,0 1,01530
100,2 1,00980
2-Хлорпропен С3Н5С1 17,8 1,01030
З-Хлорпропен С3Н5С1 19,0 1,01280
Хлорэтан С2Н5С1 100,0 1,00850
Этан с2н6 -73,1 1,00206
25,0 1,00138
Этанамин (этиламин) c2h7n 99,8 1,00422
Этанол с2н6о 100,0 1,0061
Физические свойства важнейших веществ
481
Окончание табл. 3.9.1
Название Формула Т. °C 8
Этилен с2н4 -35,8 1,001680
25.0 1,001328
Этилнитрит c2h5no2 17,2 1,0183
А-Этилэтанамин (диэтиламин) c4hI(n 99,8 1,00380
Таблица 3.9.2
Диэлектрическая проницаемость жидкостей
Измерения производились при таких частотах, чтобы получить статическое значение диэлектрической проницаемости.
Название Формула T. °C £
Простые вещества и неорганические соединения
Азот n2 -198,4 1,445
Азота диоксид no2 18,0 2,42
Аммиак NH3 -77,7 25,0
-50,0 22,7
-33,35 22,38
15,0* 15,9
25,0* 16,9
Аргон Ar -184,4* 1,516
Арсан (арсин) AsH3 -50,0 2,58
15,0 2,05
Бора грибромид BBr3 0 2,6
Бром Br2 15,0 3,22
Ванадия тетрахлорид vci4 25,0 3,05
Ди азота оксид n2o 15,0* 1,52
Вода H2O 25,0 78,3
200,0* 34,6
364,0* 10,1
Водород H2 -252,85 1,225
Водорода бромид HBr -80,0 6,3
24,7* 3,8
Водорода иодид HI -50,0 2,88
21,7* 2,90
Водорода пероксид H2O2 0 84,2
Водорода фторид HF 0 83,6
Водорода хлорид HC1 -113,2 11,80
-90,42 9,12
-15.0* 6,32
27,7* 4,6
Водорода цианид HCN 0 158,1
20,0 114,9
Гелий He -269,0 1,048
Германия тетрахлорид GeCl4 25,0 2,43
Гидразин n2h4 0** 51,7
25,0 58,5
Диборан(б) B2H6 -92,5 1,872
-164,9 2,073
-128,13 1,970
Дидейтерий d2 -252,85 1,277
Дидейтерия оксид (вода тяжелая, 99,95 %) d2o 25,0 78,2
Дисеры декафторид s2f10 20,0 2,02
Иод h 118,1 11,08
Кислород O2 -213,67 1,556
-192,4 1,505
-182,9 1,463
482
Новый справочник химика и технолога
Продолжение табл. 3.9.2
Название Формула r.°c e
Простые вещества и неорганические соединения
Мышьяка трибромид AsBr3 35,0 8,8
Мышьяка трихлорид AsCl3 17,0 12,6
Нитрозилбромид NOBr 15,2* 13,4
Нитрозилхлорид NOCI -27,5 22,5
12,0* 18,2
Олова тетрахлорид SnCl4 22,0 3,2
Пентаборан(9) B5H9 -46,8 53,1
-12,2 32,6
24,8 21,1
Пентакарбон илжелезо Fe(CO)5 20,0 2,60
Свинца тетрахлорид PbCl4 20,0 2,78
Селен Se 237,5 5,44
Сера S 118,0 3,52
231,0 3,48
Серы оксид-дибромид (тионилбромид) SBr2O 20,0 9,06
Серы диоксид SO2 -21,0 17,73
0* 15,1
20,0* 14,0
Серы оксид-дихлорид (тионилхлорид) SC12O 20,0 9,25
Серы триоксид sd3 18,0 3,11
Стибан SbH3 -80,0 2,93
-50,0 2,58
-15,0* 1,81
Сульфан (сероводород) H2S -85,5 9,26
-78,6 8,99
-61,2 8,04
10,0* 5,93
Сурьмы пентахлорид SbCI5 21,5 3,78
Сурьмы трихлорид SbCl3 75,0 33,2
Тетрахлорсилан SiCl4 16,0 2,40
Титана тетрахлорид TiCI4 20,0 2,79
У глерода диоксид co2 10,0* 2,644
Углерода дисульфид (сероуглерод) cs2 25,0 2,625
Фосфин PH3 -50,0* 2,6
15* 2,9
Фосфора нентахлорид PC15 165,0* 2,7
Фосфора трибромид PBr3 20,0 3,9
Фосфора трихлорид PC13 22,0 4,7
Фтор f2 -215,78 1,576
-189,97 1,517
Хлор C12 -65,2 2,147
-60,0 2,150
-33,2 2,048
-20,0* 2,030
10,0* 1,970
Органические соединения
5-(Аллил)-1,3-бензодиоксол (сафрол) СюН10О2 21,0 3,1
4-Аллил-2-метоксифенол (эвгенол) C10H12O2 30,0 10,5
Анизол C7H8O 25,0 4,30
Анилин c6h7n 25,0 6,99
50,0 6,30
Ацетальдегид (уксусный альдегид) C2H4O 20,0 14,8
Ацетальдегидоксим C2H5NO 25,0** 3,0
Ацетон c3H6o 25,0 20,74
50,0 17,00
Физические свойства важнейших веществ
483
Продолжение табл. 3.9.2
Название Формула Т, °C £
Ацетонитрил c2h3n 20,0 37,4
Ацетофенон С8Н8О 25,0 17,39
Бензальдегид с7н60 18,0 17,6
/V-Бензил-!-фенилметанамин (дибензиламин) cI4H15N 20,0 3,45
Бензойный ангидрид С14Н|0Оз 95,0 13,0
Бензол С6н6 10,0 2,302
25,0 2,2747
Бифенил (дифенил) С l2H jo 75,0 2,53
Бромбензол С6Н5Вг 25,0 5,39
1 -Бромбутан С4Н9Вг 20,0 7,09
2-Бромбутан С4Н9Вг 25,0 8,64
1 -Бромгексан С6Н13Вг 25,0 5,82
Броммстан СН3Вг 0 10,6
1 -Бром-2-мстилбензол (о-бромтолуол) С7Н7Вг 58,0 4,28
1 -Бром-З-метилбензол (лг-бромтолуол) С7Н7Вг 58,0 5,36
1 -Бром-4-метилбензол (и-бромтолуол) С7Н7Вг 58,0 5,49
1 -Бром-4-метоксибснзол (и-броманизол) С7Н7ВгО 30,0 7,06
1-Бромнафталин С10Н7Вг 25,0 4,83
Бромоформ (триброммстан) СНВгз 50,0 4,385
1 -Бромпентан С5НнВг 25,0 6,31
1-Бромпропан С,Н7Вг 25,0 8,09
2-Бромпронан С3Н7Вг 25,0 9,46
З-Бромпропен С3Н5Вг 20,0 7,0
Бромциклогексан С6НнВг 25,0 7,845
Бромэтан С2Н5Вг 25,0 9,01
Бутаналь (масляный альдегид) с4н8о 26,0 13,4
Бутан-1-амин (бутиламин) C4H]|N 21,0 5,3
Бутан-1,4-диол с4н10о2 30,0 30.16
Бутан-1 -ол С4Н10О 25,0 17,7
Бутан-2-ол С4Н,оО 25,0 16,35
Бутан-2-он (метилэтилкетон) с4н8о 20,0 18,50
Бутан-1-тиол (бутилмеркаптан) C4Ht0S 25,0 4,95
Бутилацетат С6Н12О2 30,0 4,87
/V-Бутилбутан-1 -амин (дибутиламин) c8h19n 20,0 3,00
Бутиронитрил c4h7n 21,0 20,3
Гексадекан Ск,Нз4 20,0 2,052
Гекса-2,4-диен С6Н,0 25,0 2,224
Гексан С6Н12 25,0 1,90
75,0 1,84
Гексановая кислота (капроновая кислота) С'бН i2O2 71,0 2,63
Гексан-1-ол с6н14о 25,0 12,5
Гексан-2-он (метилбутилкетон) с6н|2о 14,5 14,6
(1 r,2R,3S,4s,5R,6S)~ 1,2,3,4,5,6-Г ексахлор- С6Н6С16 156,0 4,8
циклогексан (а-гексахлорциклогексан)
Гекс-1-ен с6н12 20,0 2,051
Гекс-2-ен С6Н12 20,0 2,06
(£)-Гекс-3-ен с6н12 25,0 2,00
(2)-Гекс-3-ен С6н12 25,0 2,062
Гептадекан С17н36 25,0 2,052
Гептан С7н16 25,0 1,927
Гептановая кислота (энантовая кислота) С7Н14О7 71,0 2,59
Гептан-1-ол С7Н16О 25,0 П,1
Гептан-4-он (дипропилкетон) С7Н14О 20,0 12,6
Гепт-1-ен с7н14 20,0 2,071
1 -Г идроксиацетон С3Н6О2 21,0 3,59
2-Гидроксибензальдегид (салициловый с7н6о2 30,0 17,09
альдегид)
484
Новый справочник химика и технолога
Продолжение табл. 3.9.2
Название Формула г °C
Органические соединения
4-Г идрокси-4-метилпентан-2-он С6Н12О2 25,0 18,2
Глицерин С3Н8О3 -50,0** 64,1
0 48,2
25,0 42,4
75,0 42,8
/и/?анс-Дскагидронафталин (га/дгг/одекалин) С1он18 20,0 2,18
г/z/с-Декагидрона фтал ин (z/г/с-декалин) С)оН|8 20,0 2,22
Декан СюН22 20,0 1,956
Декан-1-ол С|0Н22О 20,0 8,1
Дибензо[/>,г/]фуран с12н8о 100,0 3,0
1,2-Дибромбензол С6Н4Вг2 20,0 7,50
1,3-Дибромбензол С6Н4Вг2 23,0 4,74
1,4-Дибромбензол С6Н4Вг2 95,0 2,57
Дибромметан СН2Вг2 20,0 7,04
1,2-Дибромэтан С2Н4Вг2 55,0 4,58
Дивиниловый эфир С4Н6О 20,0 3,94
125,0* 2,37
Диизопропиловый эфир с6н14о 25,0 4,04
Дииодметан СН212 25,0 5,31
7У,7У-Диметиланилин C8HhN 20 5,02
2,3-Диметилбута-1,3-диен СбНю 25,0 2,099
2, З-Д и мети л бутан С6Н14 19,06 1,960
3,3-Диметилбутан-2-он (пинаколин) с5н12о 17,5 12,6
2,2-Димстилгексан С8Н18 20,0 1,950
2,5-Диметилгексан С8н18 20,8 1,962
3,3-Диметилгсксан с8н!8 20,0 1,964
3,4-Диметилгсксан С8Н|8 18,94 1,981
Диметималонат с5н8о4 20,0 10,3
N,N- Ди метилметанамин (триметиламин) c3h9n 0 2,57
25,0 2,44
Диметиловый эфир с2н6о 25,0* 5,02
2,2-Диметилпентан с7н16 20,0 1,915
2,3-Диметил пентан С7н16 20,0 1,953
2,4-Димстилпентан с7н16 20,0 1,919
3,3 - Димети лпентан с7н|6 20,0 1,94
Диметилсульфат c2H6o2s 20,0 55,0
ТУ,7У-Диметилформамид C3H7NO 20,0 37,6
1,2-Диметоксибензол (всратрол) c8H,0o2 23,0 4,5
1,3-Динитробензол c6h4n204 90,0 20,6
2,2-Динитропропан c3h6n204 20,0 35,0
1,4-Диоксан c4H8o2 25,0 2,21
Дипропиловый эфир c6H14o 25,7 3,39
TV,ТУ-Дипропил пропан-1 -амин (трипропил- c9h21n 20,0 2,28
амин)
1,2-Дихлорбензол С6Н4С12 20,0 9,82
1,3-Дихлорбензол С6Н4С12 50,0 9,90
Дихлорметан СН2С12 25,0 8,93
Дихлоруксусная кислота С2Н2С12О2 60,0 7,8
1,1 -Дихлорэтан С2Н4С12 25,0 10,46
1,2-Дихлорэтан С2Н4С12 25,0 10,16
ТУ,/У-Диэтиланилин c10h15n 20,0 5,20
Диэтиловый эфир с4н10о 25,0 4,22
75,0* 3,70
Ди эти л ртуть c4H10Hg 20,0 2,1
Физические свойства важнейших веществ
485
Продолжение табл. 3.9.2
Название Формула Т. °C Е
Диэтилцинк C4H]()Zn 20,0 2,55
M/V-Диэтилэтанамин (триэтиламин) c6h15n 25,0 2,42
1,1-Диэтоксиэтан С6Н14О2 25,0 3,80
Додекан С12Н26 20,0 2,016
Додекан-1-амин (додециламин) C12bb7N 29,5 3,13
А^-Изобутил-2-метил пропан-1 -амин (диизо-бутиламин) c8h)9n 22,0 2,65
Изомасляная кислота С4Н8О, 25,0 2,58
Изопентан С5Н,2 0 1,870
Изопентилацстат (изоамилацетат) с7н,4о2 25,0 4,79
УУ-Изопентил-З-метилбутан-1 -амин (диизо-пентиламин) C10H23N 18,0 2,5
Изопрен С5Н8 25,0 2,098
5-Изопропенил-2-метил циклогексанон (дигидрокарвон) С,оН160 19,0 8,5
Изохинолин c9h7n 25,0 10,7
Иодбензол с6н51 20,0 4,62
75,0 4,87
1-Иодбутан С4Н91 20,0 6,29
2-Иодбутан С4и91 20,0 7,87
1 -Иодгексан С6н131 20,0 5,37
Иодметан СНз! 20,4 7,1
1-Иодпснтан C5HJ 20,0 5,81
З-Иодпентан CsH.,1 20,0 7,43
1 -Иодпропан СзН71 20,0 7,00
2-Иодпропан С3Н71 20,0 8,19
З-Иодпропен C3H51 19,0 6,1
Иодэтан C2H5I 25,0 7,64
о-Крезол с7н8о 58,0 6,02
.и-Крезол с7н8о 25,0 11,75
58,0 9,68
и-Крезол С7н8о 58,0 9,91
о-Ксилол С8Н,о 25,0 2,51
лг-Ксилол с8н10 25,0 2,368
и-Ксилол С8Н|о 25,0 2,265
Кумол (изопропилбензол) С9Н12 20,0 2,384
Масляная кислота С4Н8О2 25,0 2,90
Масляный ангидрид С8Н140з 20,0 12,9
Мезитилен (1,3,5-триметилбензол) С9Н ]2 20,0 2,279
(4/?)-и-Мента-1,8-диен ((+)-лимонсн) с10н16 25,0 2,375
(45)-и-Мента-1,8-диен ((-)-лимонсн) С10Н16 25,0 2,374
(4/?5)-и-Мента-1,8-диен ((±)-лимонсн) С10Н16 25,0 2,381
и-Ментан-З-он (ментон) С10Н18О 18,0 8,8
и-Мент-З-ен-2-он (карвенон) С|0Н|6О 20,0 18,8
и-Мент-4(8)-сн-3-он (пулегон) С|()Н1бО 19,0 9,50
Метан сн4 -161,5 1,68
Метанамин (метиламин) ch5n -10,0 11,41
0* 11,3
25,0* 9,4
Метанол СН4О 0 37,92
10,0 34,05
25,0 32,65
N-Метиланилин C7H9N 20,0 5,96
Метилацетат С3Н6О2 25,0 6,68
3-Метилбутановая кислота (изовалериано-вая кислота) С5Н10О2 20,0 2,74
486
Новый справочник химика и технолога
Продолжение табл. 3.9.2
Название Формула T. °C £
Органические соединения
2-Метилбутан-2-ол С5н12о 25,0 5,69
З-Метилбутан-1 -ол С5н12о 25,0 14,7
2-Метилбут-1-сн с5н10 20,0 2,180
2-Метилгсксан с7н!6 20,0 1,92
З-Мстилгексан С7н16 20,0 1,93
5-Метилгекс-2-сн с7н14 20,0 2,962
2-Мстилгептан с8н18 20,0 1,952
TV-Метилметанамин (диметиламин) c2h7n 0 6,32
25* 5,26
1 -Метилнафталин СцН|о 24,8 2,682
Метил нитрат CH3NO3 18,0 23,5
1 -Метил-2-нитробензол C7H7NO2 58,0 21,6
1 -Метил-3-нитробензол c7h7no2 58,0 21,9
1 -Метил-4-нитробензол c7h7no2 58,0 22,2
З-Мстилнентан c6H14 20,05 1,907
4-Мстилпснтан-2-он (мстилизобутилкетон) с6н12о 20,0 13,1
4-Метилпент-3-ен-2-он (окись мезитила) с6н10о 20,0 15,1
2-Мстилпиридин (а-пиколин) c6h7n 20,0 9,94
2-Метилпропан-1 -амин (изобутиламин) c4h1(n 21,0 4,4
2-Мстилпропаннитрил (изобутироиитрил) c4h7n 24,0 20,4
2-Мстилпропановый ангидрид (изомасля- С8Н|40з 20,0 13,6
ный ангидрид)
2-Метилпропан-1 -ол С4Н10О 25,0 17,7
2-Мстилпропан-2-ол С4Н10О 26,0 12,3
Метилпропионат с4н8о2 19,0 5,5
У-Метил-1 -фенилметанамин (бензилмстил- c8h,,n 19,0 4,4
амин)
Метилформиат С2Н4О2 20,0 8,37
1 -Метил-2-фторбензол c7h7f 30,0 4,22
1-Метил-З-фторбензол c7h7f 30,0 5,42
1 -Mei ил-4-фторбснзол c7h-f 30,0 5.86
З-Метилфуран-2,5-дион (цитраконовый ан- С5Н40з 20,0 39,5
гидрид)
1 -Метил-2-хлорбензол (о-хлортолуол) С7Н7С1 20,0 4,45
1 -Метил-3-хлорбензол (л/-хлортолуол) С7Н7С1 20,0 5,55
1 -Метил-4-хлорбензол (и-хлортолуол) С7Н7С1 20,0 6,08
Метилциклогексан С7н14 20,0 2,02
Метилциклопентан с6н12 20,0 1,985
З-Метил-З-этилпентан с8н18 20,0 1,980
Морфолин c4h9no 25,0 7,33
Муравьиная кислота СН2О2 20,0 57,9
Нафталин С,оН8 90,0 2,54
2-Нитроанилин с6н6м,о2 90,0 34,53
4-Нитроанилин c6h6n2o2 160,0 56,3
Нитробензол c6h5no2 25,0 34,75
Нитрометан CH3NO2 20,0 38,57
1-Нитропропан C3H7NO2 30,0 23,2
2-Нитропропан c3h7no2 30,0 25,5
2-Нитрофенол c6h5no3 50,0 17,34
1 -Нитро-2-хлорбензол c6h4cino2 50,0 37,7
1 -Нитро-З-хлорбензол c6h4cino2 50,0 20,9
1 -Ни гро-4-хлорбензол c6h4cino2 120,0 8,1
Нитроэтан c2h5no2 18,0 29,5
Нонан C9H20 25,0 1,974
Оксиран (окись этилена) C2H4O -1,0 14,0
Физические свойства важнейших веществ
487
Продолжение табл. 3.9.2
Название Формула Т. °C £
Октан С8Н)8 25,0 1,946
Октан-1 -ол С8Н18О 25,0 9,85
Олеиновая кислота С18Н34О2 21,9 2,43
Пальмитиновая кислота с16н32о2 75,0 2,40
Пентадекан С|5Н32 20,0 2,045
Пента-1,3-дисн С5Н8 25,0 2,319
Пентан с5н12 25,0 1,843
Пснтаналь(валериановый альдегид) с5н10о 17,0 10,1
Пентан-1-амин (пентиламин) c5h13n 22,0 4,50
Пентан-2,4-дион (ацетилацетон) с5н8о2 20,0 23,0
Пентановая кислота (валериановая кислота) с5н10о2 20,0 2,67
Пентан-1-ол (амиловый спирт) С5НрО 25,0 14,4
Пентан-2-ол с5н120 20,0 14,17
Пентан-З-ол С5Н12О 20,0 14,02
Пентахлорэтан С2НС15 20,0 3,83
Пент-1-ен (а-амилен) С5Н,о 20,0 2,017
Пент-2-сн (0-амилен) с5н|0 25,0 1,889
Пснтилацетат (амилацетат) С7Н14О2 19,0 4,81
Пиперидин CsHhN 20,0 5,8
Пиридин c5h5n 25,0 12,3
Пиррол C4H5N 25,0 8,31
Пропаналь (пропионовый альдегид) С3Н6О 17,0 18,5
Пропан-1-амин (пропиламин) c3h9n 20,0 5,31
Пропан-2-амин (изопропиламин) c3h9n 20,0 5,45
Пропан-1,2-диол (а-пропиленгликоль) c3H8o2 20,0 29,46
Пропан-1,3-диол (0-пропиленгликоль) c3H8o2 20,0 35,0
Пропан-1-ол с3н8о 25,0 19,7
Пропан-2-ол С3Н8О 25,0 18,3
Пропан-1,2,3-триилтринитрат (нитроглицерин) C3H5N3O9 20,0 19,2
5-(Проп-1 -ен-1 -ил)-1,3-бензодиоксол (изо- СюН|0О2 21,0 3,3
сафрол)
Проп-2-ен-1-ол с3н6о 21,0 20,6
N-Пропиланилин c9h13n 20,0 5,48
Пропилнитрат c3h7no3 18,0 13,9
/V-Пропилпропан-1 -амин (дипропиламин) c6h15n 20,0 3,07
Пропилформиат с4н8о2 23,1 9,02
Пропионитрил c3h5n 20,0 27,7
Пропионовая кислота с3н6о2 17,0 3,15
Пропионовый ангидрид c6H10d3 16,0 18,3
Стеариновая кислота С|8Н36О2 100,0 2,26
Стирол c8H8 25,0 2,431
75,0 2,321
1,1,2,2-Т етрабромэтан С2Н2Вг4 20,0 6,70
1,2,3,4-Тетрагидронафталин (тетралин) с юН 12 20,0 2,773
Т етрагидрофуран с4н8о 25,0 7,39
Тетрадекан С14нзо 20,0 2,037
Тетрадекан-1 -амин C14H31N 39,4 2,90
Тетраметилсилан C4Hl2Si 20,0 1,92
Тетрахлорметан СС14 0 2,288
25,0 2,230
1,1,1,2-Т етрахлорэтан С2Н2С14 -40,0 7,93
1,1,2,2-Тетрахлорэтан С2Н2С14 20,0 8,08
Тетрахлорэтилен С2С14 7,5 2,36
Тетраэтилсилан C8H20Si 20,0 2,09
Тиофен C4H4S 20,0 2,73
о-Толуидин c7h9n 18,0 6,34
58,0 5,71
488
Новый справочник химика и технолога
Продолжение табл. 3.9.2
Название | Формула Т, °C £
Органические соединения
.и-Толуидин C7H9N 18,0 5,95
58,0 5,45
«-Толуидин c7h9n 58.0 4,88
Т олуол c7H8 0 2,435
25,0 2,378
75,0 2,275
Триацетилглицерин (триацетин) С9н|4о6 20,0 7,19
Трибромацетальдегид (бромаль) С2НВг3О 20,0 7,6
Тридекан с13н28 20,0 2,026
1,2,3-Тримстилбснзол (гемеллитол) С9н12 20,0 2,636
1,2,4-Триметилбснзол (псевдокумол) С9Н12 20,0 2,378
1,3,3-Тримстилбицикло[2.2.1 ]гептан-2-он с!Они,Ь 21,0 12,8
(фенхон)
2,2,3-Триметилбутан С7н,6 20,0 1,93
2,2,3-Триметилпентан С8н18 20,0 1,96
2,2,4-Триметилпентан С8Н18 20,0 1,943
2,3,3-Триметилпентан С8н|8 20,0 1,978
2,3,4-Триметил пентан С8н18 20,0 1,973
2,4,6-Тримстил-1,3,5-гриоксан (паральдегид) С6Н12О3 20,0 15,06
1,3,5-Тринитробснзол C6H3N3O6 127,0 7,21
Трифторуксусная кислота C2HF3O2 25,0 8,2
Трихлорацетальдсгид (хлораль) С2НС13О 20,0 6,7
1,2,4-Т рихлорбензол С6Н3С13 25,0 3,94
2,2,3-Трихлорбутаналь С4Н5С13О 18,0 10,0
Трихлоруксусная кислота С2НС13О2 61,0 4,55
1,1,1-Трихлорэтан С2Н3С13 20,0 5,64
1,1,2-Трихлорэтан С2Н3С13 20,0 7,29
Трихлорэтилен С2НС13 20,0 3,409
Т риэтилалюман с6н15А1 20,0 2,9
Уксусная кислота С2Н4О2 25,0 6,19
Уксусный ангидрид С4н6о3 20,0 20,5
Ундекан Син24 20,0 2,005
Фенантрен С|4Ню 110,0 2,72
(Фенил-М N, О-азокси)бснзол (азоксибензол) C12H10N2O 36,0 5,2
Фенилацетальдегид с8н8о 20,0 4,78
Фенилгидразин c6h8n2 25,0 7,106
1-Фенилметанамин (бензиламин) c7h9n 20,0 5,18
Фенилметанол c7H8o 20,0 16,3
Фенол С6Н6О 50,0 10,28
Формамид CH3NO 20,0 111,5
Фосген СС12О 0 4,79
22,0* 4,34
Фторбензол c6h5f 25,0 5,42
60,0 4,76
1 -Фторпентан C5Ht!F 20,0 4,24
2-Фуральдегид (фурфурол) c5H4o2 20,0 41,7
Фуран С4Н4О 25,0 2,95
Фуран-2,5-дион (малеиновый ангидрид) с4н2о3 60,0 50,0
Хинолин C9H7N 25,0 9,22
З-Хлоранилин C6H6CIN 19,0 13,4
Хлорбензол С6Н5С1 0 6,08
25,0 5,61
75,0 4,90
1 -Хлорбутан С4Н9С1 -90,0 12,2
20 7,39
Физические свойства важнейших веществ
489
Окончание табл. 3.9.2
Название Фор,мула T, °C £
Хлормстан СН3С1 -20,0’ 12,6
(Хлормстил)бензол С7Н7С1 13,0 7,0
2-(Хлормстил)оксиран (эпихлоргидрин) C3H5C10 20,0 23,0
1-Хлорнаф талин С10Н7С1 25,0 5,04
Хлороформ СНС13 25,0 4,724
1 -Хлорпентан С5НИС1 11,0 6,6
1-Хлорпропан C3H7C1 20,0 8,13
З-Хлорпропсн C3H5C1 20,0 8,2
2-Хлорфенол С6Н5С1О 30,0 6,16
58,0 5.41
4-Хлорфснол С6Н5С1О 58,0 9,46
Хлорциклогексан С6НИС1 25,0 7,6
Хлорэтан С2Н5С1 170,0* 6,29
2-Хлорэтанол (этиленхлоргидрин) С2Н5С1О 25,0 25,8
132,0* 13,2
Циклогексан С6Н12 20,0 2,02
Циклогсксанамин (циклогексиламин) С6Н13М 20,0 4,73
Циклогексанол С6Н12О 25,0 16,8
Циклогексанон с6н|0о 20,0 18,3
Циклогексен С6Н,о 25,0 2,220
Циклопентан С5Н10 20,0 1,965
Циклопентанол с5н10о 20,0 18,0
Циклопентанон с5н8о 20,0 13,45
Циклопентен С5Н8 20,0 2,095
Эритрит C4HJ0O4 120,0 28,5
Этанамин (этиламин) c2h7n 25,0* 6,17
Этан-1,2-диамин (этилсндиамин) c2h8n2 26,5 13,5
Этанол С2Н6О 10,0 26,4
25,0 25,2
75,0 23,2
Этантиовая кислота (тиоуксусная кислота) C2H4OS 20,0 12,8
Этантиол (этилмеркаптан) C2H6S 15,0 6,912
А-Этиланилин C8HhN 20,0 5,87
4-Этиланилин C8HnN 25,0 4,84
Этилацетат c4H8o2 25,0 6,00
Этилбензол C8H,o 20,0 2,403
Этилбутират c6H12o2 18,0 5,08
З-Этилгексан c8H18 20,0 1,962
Этиленгликоль C2H6O2 20,0 38,7
Этилнитрат c2h5no3 20,0 19,4
З-Этилпентан c7H16 20,0 1,94
З-Этилпент-2-ен C7H14 20,0 2,051
Этилформиат C3H6O2 25,0 7,2
А-Этилэтанамин (диэтиламин) C4HhN 25,0 3,78
Этоксибензол (фенетол) CsHioO 20,0 4,22
* Вещество находилось под давлением.
** Переохлажденная жидкость.
Таблица 3.9.3
Диэлектрическая проницаемость твердых веществ
Название Формула Г, °C Частота, Гц £
Простые вещества и неорганические соединения
Аммония бромид NH4Br 1 • 1012 7,3
Аммония хлорид NH4CI 1 • 1012 6,8
Бериллия карбонат ВеСО3 18,0 1,67 • 105 9,7
490
Новый справочник химика и технолога
Продолжение табл. 3.9.3
Название Формула T. °C Частота, Гц 8
Простые вещества и неорганические соединения
Бор В 5 • IO5 -12,0
Вода (лед) Н2О -70,0 1 • 10’ 3,33
-50,0 1 • 103 3,82
-30.0 1 • 103 14.6
-10,0 1 • 103 69,4
-3,0 1 • I03 72,4
-i,o 1 • 103 72,5
Германий Ge -196,0 1 • I06 15,8
Кадмия бромид CdBr2 20,0 0,51 • 106-3 • 106 8,6
Калия бромид KBr 25,0 1 • 102-l • 10'° 4,9
Калия гидрокарбонат КНСОз 25,0 1 • 104 4,3
Калия иодид Ki 5,6
Калия карбонат К2СО3 18,0 1,66 • 105 5,0
Калия-натрия тартрат тетрагидрат KNaC4H4O6 • 4Н2О 1,6 • 106 6,8
(сегнстова соль)
Калия нитрат KNO3 20,0 1,65 • 106 4,37
Калия хлорид КС1 29,5 1 • 106 4,68
Кальция нитрат Ca(NO3)2 19,0 1,67 • 105 6,5
Кремний Si -196,0 1 • 106 H,7
Кремния диоксид (кварц, | оптич. оси) SiO2 1,6 • 106 4,6
Кремния диоксид (кварц, ± оптич. оси) SiO2 1,6 • 106 4,45
Лития бромид LiBr 2 • 106 10,95
Лития иодид Lil 2 • 106 8,2
Лития карбонат Li2CO3 18,0 1,66 • 105 4,9
Лития фторид LiF 25,0 1 • 103 9,00
Лития хлорид LiCI 19,0 1,66 • 105 10,62
Магния оксид MgO 25,0 1 -103-l • 104 9,65
Магния сульфат MgSO4 20,0 1,6 • 105 82,0
Меди(1) бромид CuBr 20,0 3 • 106 8,0
Меди(1) оксид Cu2O 21,0 1 • 106 10,5
Меди(П) хлорид CuCl2 20,0 3 106 10.0
Мышьяка трибромид AsBr3 20,0 3,75 • 108 3,3
Мышьяка трииодид Asl3 18,0 3,75 • 108 5,4
Мышьяка трифторид AsF3 1 • 106 5,7
Мышьяка трихлорид AsCl3 -50,0 3,75 • 108 3,6
Натрия бромид NaBr 2 • 106 6,1
Натрия гидрокарбонат NaHCO3 25,0 1 • 104 4,4
Натрия иодид Nal 6,6
Натрия карбонат Na2CO3 20,0 1 • 103 7,1
Натрия карбонат декагидрат Na2CO3 • 10H2O 20,0 1 • 103 5,5
Натрия нитрат (| оптич. оси) NaNO3 18,0 1 • IO12 17,8
Натрия нитрат (1 оптич. оси) NaNO3 18,0 1 • 1012 6,5
Натрия сульфат Na2SO4 -20,0 1 • 103 7,9
Натрия сульфат дскагидрат Na2SO4 • 10H2O 20,0 1 • 103 5,0
Натрия фторид NaF 19,0 8,6 • 105 6,00
Натрия хлорид NaCl 25,0 1 • 102-l • 104 5,90
Рубидия бромид RbBr 19,0 8,6 • 105 4,87
Рубидия иодид Rbl 19,0 8,6 • 105 5,58
Рубидия карбонат Rb2CO3 19,0 1,67 • 105 6,7
Рубидия хлорид RbCl 19,0 8,6 • 105 4,95
Свинца дибромид PbBr2 20,0 5 • 105 30,0
Свинца дииодид Pbl2 20,0 5 • 105 20,8
Свинца динитрат Pb(NO3)2 20,0 5 • 105 16,8
Свинца дихлорид PbCl2 20,0 5 • 105 33,5
Селен Se 18,0 1 • IO10 6,0
Физические свойства важнейших веществ
491
Продолжение табл. 3.9.3
Название Формула T. °C Частота, Гц c
Сера S 25,0 1 • 103 3,7
Серебра бромид AgBr 20,0 1 • 106 13,1
Серебра нитрат AgNO3 20,0 3 • 106 9,0
Серебра оксид Ag2O 54,0 9,7 • 105 8,8
Серебра хлорид AgCI 20,0 1 • 106 12,3
Стронция карбонат SrCO3 18,0 1,67 • 105 8,85
Стронция нитрат Sr(blO3)2 19,0 1,67 • 105 5,33
Сурьмы(Ш) оксид Sb2O3 2 • 106 12,8
Сурьмы трибромид SbBr3 20,0 3,75 • 108 5,1
Сурьмы трииодид Sbl3 20,0 3,75 • 108 9,1
Сурьмы трихлорид SbCI3 18,0 3,6 • 108 5,4
Таллия бромид TIBr 20,0 5 • 105-5 • 106 30,0
Таллия нитрат T1NO3 20,0 5 • 105—5 • 106 16,5
Таллия сульфат T12SO4 20,0 5 • 10-5 • 106 25,5
Таллия хлорид T1C1 20,0 5 • 10-5 • 106 32,0
Теллур (|| онтич. оси) Те 5,0
Теллур (± оптич.оси) Те 2,2
Трижелеза тетраоксид Fe3O4 25,0 1,72 • 108 -100,0
Углерод (алмаз) C 26,0 1,60 • 106 5,68
Фосфор (белый) P 20,0 3,75 • 106 4,1
Цезия бромид CsBr -20,0 9,7 • 105 6,5
Цезия иодид Csl 25,0 9,7 • 105 5,7
Цезия хлорид CsCl -51,0 9,7 • 105 7,2
Органические соединения
Антрацен c14H10 17,0 8 • 105 3,46
Ацетамид C2H5NO 20,0 4 • 108 4,0
Ацетанилид c8h9no 22,0 4 • 108 ~3,0
Бензидин c12h12n2 17,0 8 • 105 3,6
Бензо-1,4-хинон c6h4o2 17,0 3,6
Бифенил (дифенил) C12H,o 17,0 2,57
Бромциклогсксан C6H„Br -70,0 1 • 105 2,82
Винная кислота c4H6o6 15,0 2,5 • 106 35,9
(1 г,2/?,35,4s,5/?,6S)-1,2,3,4,5,6-Гекса- C6H6C16 156,0 1 • 105 2,91
хлорциклогексан (а-гексахлорциклогексан)
(1 /?,45)-2,2-Димстил-3 -метилен- C,oH16 39,5 1 • 105 2,36
бицикло[2.2.1]гептан ((+)-камфен)
(+)-Кокаин cl7H21NO4 20,0 4 • 108 3,05
(-)-Кокаин c17h21no4 20,0 4- 108 3,10
Метилциклогексан c7H14 -129,0 1 • 105 2,28
2-(4-Метилциклогекс-3-ен-1 -ил)про- CioH.sO 20,0 4- 108 2,75
пан-1-ол (а-терпинеол)
Муравьиная кислота CH2o2 2,0 4 • 108 19,0
Нафталин C]oH8 25,0 1 • 103 2,85
Пикриновая кислота c6h3n3o7 17,0 8 • 105 3,6
Пирен C16H10 17,0 8 • 105 3,21
Пропиофенон (этилфенилкетон) c9HI0o 17,0 4- 108 15,5
Резорцин c6H6o2 21,8 4 • 108 3,2
1,1,1,2-Тетрахлорэтан C2H2C14 -66,0 2 • 106 9,22
1,1,2,2-Тетрахлорэтан C2H2C14 -45,0 2 • 106 3,15
1,3,5-Т ринитробензол C6H3N3O6 17,0 8 • 105 3,0
Фенантрен C14H,o 17,0 8 • 105 3,0
А-Фениланилин (дифениламин) Ci2HhN 25,0 2,97
Фенилуксусная кислота C8H8O2 20,0 4 • 108 ~3,2
492
Новый справочник химика и технолога
Окончание табл. 3.9.3
Название Формула ? °C Частота. Гц Е
Органические соединения
Хлорциклогексан С6НИС1 -47,0 1 • 105 10,5
Циклогексан С6н12 -105,0 1 • 105 2,52
Циклопентанол С5Н,оО -20,0 1 • 105 27,1
Циклопентанон С5н8о -51,0 1 • 105 2,84
3.10. Дипольные моменты некоторых веществ
(С.Г. Изотова)
Дипольный момент — основная векторная характеристика диполя, численно равная произведению заряда полюса диполя на расстояние между полюсами. Дипольный момент сложных молекул представляет собой векторную сумму дипольных моментов групп, из которых состоят эти молекулы.
В табл. 3.10.1-3.10.3 приводятся постоянные дипольные моменты молекул ц, выраженные во внесистемных единицах — дебаях (D): \D ~ 3,33 • 10 ?0 Кл • м.
Простые вещества и неорганические соединения расположены в табл. 3.10.1 в алфавитном порядке химических символов.
Органические вещества (табл. 3.10.2) размещены в порядке возрастания числа атомов углерода в эмпирических формулах, а при одинаковом числе атомов углерода — в порядке возрастания числа атомов водорода.
Данные по элементоорганическим соединениям приведены в табл. 3.10.3.
Условные обозначения
г. — газ
ж. — жидкость
тв. — твердое тело
бзл. — раствор в бензоле
гекс. — раствор в гексане
гепт. — раствор в гептане
диокс. — раствор в диоксане
дек. — раствор в декалине
СС14 — раствор в тстрахз юр метане
м.п. — метод молекулярного пучка
м.р. — метод радиоспектроскопии
Штарк — метод Штарка
Таблица 3.10.!
Дипольные моменты молекул простых веществ и неорганических соединений
Формула Название Т °C Условия определения Ц,/7
AgC104 Перхлорат серебра 25 бзл. 10,7
А1Вг3 Трибромид алюминия 20 бзл. 5,2
Аг Аргон -210-+25 г. <0,03
AsBr3 Трибромид мышьяка 25 бзл. 3,3
AsCl;, Трихлорид мышьяка 25 бзл. 2,17
AsF3 Трифторид мышьяка 25 бзл. 2,65
AsH3 Арсан 16-100 г. 0,18
AsH22H (2Н|)Арсан Штарк 0,22
Asl3 Трииодид мышьяка 25 диокс. 1,83
As2O3 Триоксид димышьяка 525 г. 0,13
BBr3 Трибромид бора -70-+180 ж. 0
BC13 Трихлорид бора 35-169 г. 0,60
BF3 Трифторид бора -80-+199 г. 0
B2H6 Диборан(б) (бороэтан) -120-+95 ж. 0
B3H6N3 Т риазатриборан 25 г. 0
B5H9 Пентаборан(9) Штарк 2,1
B10H)4 Дскаборан(14) 25 бзл. 3,52
BeBr2 Бромид бериллия бзл. 0
BeCl2 Хлорид бериллия бзл. 0
Br2 Бром 20-129 г. <0,1
COC12 Фосген 30-152 г. 1,18
CO Монооксид углерода 0,11
COS Оксид-сульфид углерода -71 - +92 г. 0,65
co2 Диоксид углерода 0
CSC12 Тиофосген 30-111 г. 0,28
Физические свойства важнейших веществ
493
Продолжение табл. 3.10.1
Формула Название Т. °C Условия определения и,/2
CS2 Дисульфид углерода (сероуглерод) 49-216 г. 0
С12 Хлор -65 - +8 ж. 0,23
С1О2 Диоксид хлора СС14 0,89
С12О Оксид дихлора СС14 1,7
С12О7 Гептаоксид дихлора (хлорный ангидрид) СС14 0,72
СгС12О2 Диоксид-дихлорид хрома (хлористый 25 СС14 0,47
хромил)
CsI Иодид цезия 600 м. п. 10,2
GeH2Cl2 Дихлоргерман 25 СС14 2,21
HBr Бромид водорода -67 - +300 г. 0,79
HCN Цианид водорода 2,9
HCI Хлорид водорода -84 - +300 г. 1,03
2HC1 (“Н)Хлорид водорода (хлорид дейтерия) 18-244 г. 1,09
HF Фторид водорода 23-101 г. 1,91
HI Иодид водорода -28 - +73 г. 0,42
H2 Водород -210- +25 г. <0,015
H2O Вода 100-210 г. 1,84
H2HO (2Н,)Вода 20 бзл. 1,78
2H2O (2Н2)Вода (оксид дидейтерия, тяжелая 91-200 г. 1,86
вода)
H2O2 Пероксид водорода 25 диокс. 2.13
H2N2O2 Нитрамид 20 диокс. 3,75
H2S Сульфан (сероводород) 0,93
H2HS (2Н|)Сульфан (монодейтеросероводород) Штарк 1,02
He Гелий -210-+25 г. <0,015
Hg Ртуть 301-370 г. 0
HgBr. Дибромид ртути 341-122 г. 0
HgCl2 Дихлорид ртути 326-428 г. 0
Hgi2 Дииодид ртути 295-428 г. 0
ь Иод 15-70 бзл. 0
IBr Бромид иода Вг2 1,21
1C1 Хлорид иода 61-162 г. 0,54
IF5 Пентафторид иода г. 2,28
К Калий г. 0
KBr Бромид калия 647 М. 11. 9,1
KC1 Хлорид калия 676 м. п. 8,0
KF Фторид калия Штарк 7,3
KI Иодид калия 625 м. п. 9,2
Kr Криптон -210-+25 г. <0,03
LiC104 Перхлорат лития 25 диокс. 7,8
NF3 Трифторид азота -80 - +95 г. 0,21
NH3 Аммиак 1-150 г. 1,46
N2H3 (2Н3)Аммиак (тридейтероаммиак) 1-152 г. 1,50
NO Монооксид азота -80 - +25 г. 0,16
no2 Диоксид азота 24-124 г. 0,33
n2 Азот -189-+289 г. 0
N2H4 Гидразин 1,83
n2o Оксид диазота 20-181 г. 0,14
n2o5 Пентаоксид диазота 25 СС14 1,39
Na Натрий г. 0
Nal Иодид натрия 653-703 м. п. 4,9
Ne Неон -210-+25 г. <0,015
O2 Кислород 0-25 г. 0
O3 Озон -79 - +85 г. 0,52
p Фосфор ж. 0
PBr3 Трибромид фосфора 18 СС14 0,61
494
Новый справочник химика и технолога
Окончание табл. 3.10.1
Формула Название Г °C Условия определения д. 1)
РС13 Трихлорид фосфора 33-190 г 0,78
РС15 Пентахлорид фосфора 9-32 СС14 0
PF.3 Трифторид фосфора 10-107 г. 0
pf5 Пентафторид фосфора 10-115 г. 0
РН3 Фосфин 0,55
рн22н (2Н])Фосфин (монодейтерофосфин) м. р. 0,579
рн2н2 (2Н2)Фосфин (дидейтсрофосфин) м. р. 0.565
Р13 Трииодид фосфора СС14 1,6
РОС13 Оксид-трихлорид фосфора (фосфорилтрихлорид) 20 бзл. 2,40
POF3 Оксид-трифторид фосфора (фосфорилтрифторид) Штарк 1,7
S Сера 118-350 ж. 0
SF6 Гексафторид серы -80 - +25 г. 0
SOBr2 Дибромид-оксид серы (тионилдибромид) 20 бзл. 1,47
SOCI2 Оксид-дихлорид серы (тионилдихлорид) 15—134 г. 1.4
sof2 Оксид-дифторид серы (тион и л дифторид) 1,62
so2 Диоксид серы (сернистый ангидрид) -7 - +171 г. 1,61
SO2CI2 Диоксид-дихлорид серы (сульфурилдихлорид) 20-143 г. 1,8
SO2F2 Диоксид-дифторид серы (сульфурилдифторид) Штарк 0,23
SO2(NH2)2 Сульфамид 20 диокс. 3,9
SO3 Триоксид серы (серный ангидрид) -80-+160 г. 0
S2C12 Дихлорид дисеры 25 бзл. 0,60
s2F10 Декафторид дисеры 25 г. 0
SbBr3 Трибромид сурьмы 25 бзл. 3,3
SbCI3 Трихлорид сурьмы 25 бзл. 3,75
SbCl5 Пентахлорид сурьмы 7-47 СС14 0
SbF, Трииодид сурьмы 25 бзл. 0,4
Se2CI2 Дихлорид дисслсна 25 бзл. 2,1
SiCl4 Тетрахлорсилан 25 диокс. 0
SiF4 Тетрафторсилан -80 - +25 г. 0
SiHBr.3 Трибромсилан 25 гепт. 0,79
SiHCl3 Трихлорсилан 12-141 г. 0,85
SiHF3 Трифторсилан Штарк 1,26
SiH2Cl2 Дихлорсилан 18-124 г. 1,17
SiH2F2 Дифторсилан Штарк 1,52
SiH3Br Бромсилан Штарк 1,31
SiH3CI Хлорсилан 15-129 г. 1,28
SiH3F Фторе ил ан Штарк 1,27
SiH4 Силан -33 - +25 г. 0
Si2H6 Дисилан 25 г. 0
SnBr4 Тетрабромид олова 130-231 г. 0
SnCl4 Тетрахлорид олова 90-200 г. 0
Snl4 Тетраиодид олова 25 бзл. 0
TaCl5 Пентахлорид тантала 25 СС14 1,2
TeCI4 Теграхлорид теллура 25 бзл. 2,57
TeF6 Гексафторид теллура 50 диокс. 0
TiBr4 Тетрабромид титана 20 диокс. 5,05
TiCI4 Тетрахлорид титана 100 г. 0
Xe Ксенон -210-+25 г. <0,05
Физические свойства важнейших веществ
495
Таблица 3.10.2
Дипольные моменты молекул органических соединений
Формула Название Т, °C Условия определения
СВгС13 Бромтрихлорметан бзл. 0
CBr3F T рибромфтормстан бзл. 0
CC12F2 Дифтордихлорметан (фреон-12) 32-197 г. 0,51
CC13F Фторгрихлормстан (фреон-11) 26-103 г. 0,45
CC13NO2 Нитро(трихлор)метан (хлорпикрин) 30-152 г. 1,18
CCI4 Тетрахлормстан 23-95 г. 0
cf4 Тстрафторметан -80 - +95 г. 0
cn4o8 Т етранитромстан 82 г. 0
CHBr3 Бромоформ (трибромметан) г. 0,99
CHC1F2 Дифторхлорметан 31-206 г. 1,41
CHCbF Фтордихлорметан 32-151 г. 1,29
CHC13 Хлороформ 25 ж. 1,06
CHF3 Фтороформ (фреон-23) 25-95 г. 1,6
CHI3 Йодоформ (трииодметан) 25 бзл. 0,99
CH2Br2 Диброммстан (бромистый метилен) 49-147 г. 1,91
CH2CI2 Дихлорметан (хлористый метилен) 30-153 г. 1,62
CH2I2 Дииодметан (иодистый метилен) 25 бзл. 1,10
ch2n2 Цианамид 20 бзл. 3,8
CH2O Муравьиный альдегид (формальдегид) 147-247 г. 2,27
CH2O2 Муравьиная кислота 37-74 г. 1,4
CH3Br Бромметан 18-143 г. 1,79
CH3CI Хлорметан 25-145 г. 1,86
CH3F Фторметан -49 - +225 г. 1,81
CH3I Иодмстан 22-64 г. 1,64
CH3NO Формамид (амид муравьиной кислоты) 153-176 г. 3,22
CH3NO2 Нитрометан 64-181 г. 3,54
CH3NO3 Метили итрат 20 бзл. 2,85
CH4 Метан 19-142 г. 0
CH4O Метанол (метиловый спирт) 25-206 г. 1,706
ch5n Метанамин (метиламин) 15-144 г. 1,32
ch6n2 Метилгидразин 15 бзл. 1,7
C2C14 Т сграхлорэтилсн 25 бзл. 0
C2C16 Гексахлорэтан 15-20 бзл. 0
c2F6 Гексафторэтан 23 г. 0
C2I6 Гексаиодэтан 0 СС14 0,33
c2N2 Оксалони грил (дициан) -80 - +25 г. 0
C2HC13 Трихлорэтилен 25 бзл. 0,94
C2HC15 Пентахлорэтан г. 0,092
C2H2 Ацетилен -77-+188 г. 0
C2H2BrCl (£)-1 -Бром-2-хлорэтилен 0
C2H2BrCl (Z)-1 -Бром-2-хлорэтилсн 1,57
C2H2Br2 (£)-1,2-Дибромэтилен бзл. 0
C2H2Br2 (Z)-1,2-Дибромэтилен бзл. 1,35
C2H2C1I (£)-1 -Иод-2-хлорэтилен бзл. 1,27
C2H2CU (Z)-1 -Иод-2-хлорэтилен бзл. 0,57
C2H2C12 1,1 - Дихлорэтилен 25 бзл. 1,30
C2H2C12 (£)-1,2-Дихлорэтилен 25 бзл. 0,70
C2H2C12 (Z)-1,2-Дихлорэтилен г. 2,95
C2H2C14 1,1,1,2-Т етрахлорэтан бзл. 1,2
C2H2C14 1,1,2,2-Тетрахлорэтан 128-163 г. 1,36
C2H2I2 (£)-1,2-Дииодэтилен бзл. 0
C2H2I2 (Z)-1,2-Дииодэтилен бзл. 0,75
C2H3Br Бромэтилен 21-140 г. 1,41
C2H3BrO Ацетилбромид 20 бзл. 2,43
496
Новый справочник химика и технолога
Продолжение табл. 3.10.2
Формула Название Т. °C Условия определения р,/2
С2Н3С1 Хлорэтилен 14-140 г. 1,44
С2Н3С1О Ацетилхлорид 47-210 г. 2,68
С2Н3С1з 1,1,1-Трихлорэтан 63-126 г. 1,77
С,НзС1з 1,1,2-Трихлорэтан Г. 1,25
С2Н31 Иодэтилсн 18-140 г. 1,26
c2h3n Ацетонитрил 81-190 г. 3,94
c2h3ns Метилизотиоцианат 20 бзл. 3,18
C,H3NS Метилтиоцианат 20 бзл. 3,16
c2H4 Этилен -36+ +188 г. 0
C2H4BrCl 1 -Бром-2-хлорэтан 66 1,09
C2H4Br2 1,1-Дибромэтан (бромистый этилиден) 25 бзл. 2,12
C2H4Br2 1,2-Дибромэтан 66 0,94
C2H4C12 1,1-Дихлорэтан (хлористый этилиден) 42-145 г. 2,04
C2H4CI2 1,2-Дихлорэтан 25-315 г. 1,27-1,57
c2h4f2 1,1-Дифторэтан (фтористый этилиден) г. 2,24
C2H412 1,1 -Дииодэтан (иодистый этилиден) 2,24
C2H4I2 1,2-Дииодэтан 25 бзл. 1,3
c2h4o Ацетальдегид (уксусный альдегид) 27-182 г. 2,69
C2H4O Оксиран (окись этилена) 17-176 г. 1,88
C2H4O2 Уксусная кислота 10-70 ж. 1,70
C2H5Br Бромэтан 19-170 г. 2,01
C2H5C1 Хлорэтан 25-145 г. 2,0
C2H5CIO Метокси(хлор)метан 74-234 г. 2,03
C2H5CIO 2-Хлорэтанол (этиленхлоргидрин) 66-162 г. 1,74
c2h5f Фторэтан -37 + +262 г. 1,92
c2h5i Иодэтан 20-64 г. 1,87
c2h5no Ацетамид 20 диокс. 3,6
c2h5no2 Нитроэтан 92-188 г. 3,58
c2h5no2 Этилнитрит 17 г. 2,38
c2h5no3 Этилнитрат 20 бзл. 2,91
c2h6 Этан -73 + +197 г. 0
C,H6O Диметиловый эфир -55 + +200 г. 1,29
c2H6o Этанол (этиловый спирт) 24-210 г. 1,68
C2H6O2 Этиленгликоль 143-233 г. 2,2
C2H6S Этантиол (этилмеркаптан) 35-205 г. 1,56
c2h7n А-Метилмстанамин (диметиламин) 15-134 г. 1,02
c2h7n Этанамин (этиламин) 22-71 г. 0,99
c2h8n2 Этан-1,2-диамин (этилендиамин) 82-156 г. 1,94
c3H5Br 1-Бромпроп-1-ен 20 бзл. 1,79
C3H5BrO Бромацетон 20 гекс. 2,38
C3H5C1 1-Хлорнроп-1-ен 64-207 г. 1,98
C3H5CIO Хлорацетон 63-181 г. -2,2
СзН5С1О 2-(Хлорметил)оксиран (эпихлоргидрин) СС14 1,8
c3h5n Пропиононитрил 78-196 г. 4,03
c3h5ns Этилизотиоцианат 20 бзл. 3,31
C3H5NS Этилтиоцианат 20 бзл. 3,64
C3H6 Пропен (пропилен) -27 ++103 г. 0,35
СзН6Вг2 1,2-Дибромпропан 80,4-194,0 г. 1,13-1,36
СзН6Вг2 1,3-Дибромпропан 10 ж. 2,15
СзН6С12 1,1 -Дихлорпропан 25 бзл. 2,06
С3Н6С12 1,2-Дихлорпропан 71,5-232,5 г. 1,46-1,68
С3Н6С12 1,3-Дихлорпропан 101-212 г. 2,07
СзН6С12 2,2-Дихлорпропан г. 2,63
С3н6о Ацетон 28-182 г. 2,85
С3Н6О 2-Метилоксиран (а-окись пропилена) 25 бзл. 1,88
СзН6О Оксетан (окись триметилена) 25 бзл. 2,01
Физические свойства важнейших веществ
497
Продолжение табл. 3.10.2
Формула Название Т. °C Условия определения
С3Н6О Пропаналь (пропионовый альдегид) 81-236 г. 2,73
С3Н6О2 Метилацстат 35-209 г. 1,72
с3н6о2 Пропионовая кислота 83-213 г. 1,74
с3н6о2 Этилформиат 19-162 г. 1,92
С3Н7Вг 1-Бромпропан 29-143 г. 2,01
С3Н7Вг 2-Бромпропан 14-107 г. 2,19
С3Н7С1 1-Хлорпропан 65-185 г. 2,04
С3Н7С1 2-Хлорпропан 15-110 г. 2,15
c3h7no2 Пропилнигрит 20 бзл. 2,28
c3h7no3 Пропилнитрат 20 бзл. 2,98
с3н8 Пропан -46- +213 г. 0
с3н8о Пропан-1-ол 103-232 г. 1,64
С3н8о Пропан-2-ол 27-190 г. 1,68
c3h9n А^/У-Диметилметанамин (тримстиламин) 16-145 г. 0,65
С4Н4О Фуран г. 0,72
C4H4S Тиофен 54-201 г. 0,55
c4h5n Пиррол г. 1,8
c4h6n2o2 Этилдиазоацетат 25 бзл. 2,03
С4Н6О (£)-Бут-2-еналь (кротоновый альдегид) 139-246 г. 3,67
с4н6о3 Уксусный ангидрид 47-267 г. 2,8
С4н8 Бут-1 -ен (бутилен) 25-95 г. 0,3
С4н8 Бут-2-ен (псевдобутилен) 25-95 г. 0
С4н8 2-Метилпропен (изобутилен) 25-95 г. 0
С4Н8О2 1,4-Диоксан 64-214 г. 0
С4Н8О2 Масляная кислота 22 бзл. 0,93
С4Н8О2 Метилпропионат 149 г. 1,73
с4н8о2 Пропил формиат г. 1,89
С4Н8О2 Этилацетат 29-194 г. 1,81
C4H9CJ 1 -Хлорбутан 15-102 г. 2,11
С4Н10 Бутан 25-95 г. 0
С4Н10 Изобутан 25-95 г. 0
С4Н,оО Бутан-1 -ол 35-206 г. 1,63
С4н10о Бутан-2-ол 30 бзл. 1,65
С4н10о Диэтиловый эфир (этиловый эфир) 15-203 г. 1,17
с4н10о 2-Метилпропан-1 -ол 50-208 г. 1,63
С4Н10О 2-Метилпропан-2-ол 30 бзл. 1,66
C4H10S Диэтилсульфид 36-201 г. 1,51
С5Н4О2 2-Фуральдегид (фурфурол) 25 бзл. 3,6
c5h5n Пиридин 25 бзл. 2,20
c5h7n 1 -Метилпиррол 25 бзл. 1,92
c5H8 Изопрен (2-мстилбута-1,3-дисн) 85-204 г. 0,38
с5н8 Пента-1,3-диен 113-186 г. 0,68
с5н8 Циклопентен 25 0,97
с5н8о Циклопентанон г. 3,00
с5н8о2 Пентан-2,4-дион (ацетилацетон) 149-204 г. 3,00
С5Н10 Пент-1-ен 20 ж. 0,47
С5Н10О Пентан-З-он (диэтилкетон) 15 бзл. 2,72
С5н10о2 Бутилформиат 1,8
CsHio02 Изобутилформиат 22 бзл. 1,88
С5Н10О2 Изопропилацетат 22 бзл. 1,85
СзНюОг З-Метилбутановая кислота (изовалериановая 22 бзл. 0,89
кислота)
CsH10O2 Метилбутират 22 бзл. 1,71
CsHi0O2 Пропилацетат 22 бзл. 1,78
^sHio02 Этилпропионат 22 бзл. 1,74
C5HhNO2 Пентилнитрит 25 бзл. 2,27
498
Новый справочник химика и технолога
Продолжение табл. 3.J0.2
Формула Название Т, °C Условия определения
с5н12 Пентан -90 - +30 ж. 0
c5h12n2s 1,3-Диэтилтиомочсвина 20 диокс. 4,9
с5н12о 2-Мстилбутан-2-ол (шрет-амиловый спирт) 18 бзл. 1,66
С5Н12О З-Метилбутан-1-ол (изоамиловый спирт) г. 1,85
С5Н12О Пентан-1-ол (амиловый спирт) 30 бзл. 1,65
С5Н12О4 Пентаэритрит г. ~2
С5Н12О4 Тетраметоксиметан (тстраметиловый эфир 108-183 г. ~0
ортоугольной кислоты)
С6С16 Г сксахлорбснзол 50 бзл. 0,2
С6Н2Вг4 1,2,4,6-Тетрабромбензол бзл. 0,7
С6Н2С14 1,2,3,4-Тстрахлорбензол 25 бзл. 1,90
С6Н2С14 1,2,4,6-Тетрахлорбензол бзл. 0,65
С6Н3Вг3 1,3,5-Трибромбензол 20 бзл. 0,28
С6Н3Вг3О 2,4,6-Трибромфенол бзл. 1,56
С6Н3С13 1,2,3-Трихлорбензол 20 бзл. 2,31
С6Н3С13 1,2,4-Трихлорбензол 1,25
С6Н3С13 1,3,5-Трихлорбснзол 0
С6Н,С13О 2,4,6-Трихлорфенол бзл. 1,62
с6н313 1,3,5-Трииодбензол 20 бзл. 0,24
C6H3N3O6 1.3,5-Тринитробензол бзл. 0,7
C6H4BrNO2 1 -Бром-2-нитробензол 20 бзл. 4,20
C6H4BrNO2 1-Бром-З-нитробензол 20 бзл. 3,41
C6H4BrNO, 1 -Бром-4-нитробензол 20 бзл. 2,65
C6H4Br2 1,2-Дибромбснзол 2,0
C6H4Br2 1,3-Дибромбснзол 1,5
C6H4Br2 1,4-Дибромбснзол 0
C6H4C1NO2 1 -Нитро-2-хлорбензол 203 г. 4,59
c6h4cino2 1 -Нитро-З-хлорбензол 210 г. 3,69
c6h4cino2 1 -Нитро-4-хлорбензол 210 г. 2,78
C6H4C12 1,2-Дихлорбензол 147-175 г. 2,16
C6H4C12 1,3-Дихлорбензол 20 бзл. 1,48
C6H4Cb 1,4-Дихлорбензол 161 г. 0
c6h4f2 1,2-Дифторбензол 22 бзл. 2,38
c6h4f2 1,3-Дифторбензол г. 1,58
c6h4ino2 1 -Иод-2-нитробензол 22 бзл. 3,92
c6h4ino2 1 -Иод-3-нитробензол 22 бзл. 3,43
c6h4ino2 1 -Иод-4-нитробензол 22 бзл. 3,05
c6h4i2 1,2-Дииодбензол 20 бзл. 1,69
C6H4I2 1,3-Дииодбензол 20 бзл. 1,27
C6H4I2 1,4-Дииодбензол 20 бзл. 0,19
c6h4n2o4 1,2-Динитробензол бзл. 6,00
c6h4n2o4 1,3-Динитробензол бзл. 3,70
c6h4n,o4 1,4-Динитробензол бзл. 0,8
c6H4o2 Бензо-1,2-хинон (о-хинон) бзл. 5,1
C6H4O2 Бензо-1,4-хинон (и-хинон) г. 0
C6H5Br Бромбензол г. 1,77
C6H5BrO 2-Бромфенол 1,36
C6H5BrO 4-Бромфенол 2,12
C6H5C1 Хлорбензол 87-212 г. 1,69
C6H5C1O 2-Хлорфенол 1,31
C6H5C1O З-Хлорфенол 2,10
C6H5C1O 4-Хлорфенол 2,22
C6H5C12N 2,5-Дихлоранилин 20 бзл. 1,68
c6h5f Фторбензол 71-234 г. 1,57
C6H5I Иодбензол 25 бзл. 1,40
c6h5no2 Нитробензол 129-250 г. 4,23
Физические свойства важнейших веществ
499
Продолжение табл. 3.10.2
Формула Название Г, °C Условия определения
c6h5no3 2-Нитрофенол 25 бзл. 3,10
c6h5no3 3-Нитрофенол 25 бзл. 3,90
c6h5no3 4-Нитрофенол 25 бзл. 5,05
c6H6 Бензол 20-249 г. 0
C6H6C1N 2-Хлоранилин 20 бзл. 1,77
C6H6CIN З-Хлоранилин 20 бзл. 2,66
C6H6C1N 4-Хлоранилин 20 бзл. 2,97
c6h6n2o2 2-Нитроанилин 4,96
c6h6n2o2 З-Нитроанилин 4,85
C6H6N2O-> 4-Нитроанилин 6,17
c6H6o Фенол 177 г. 1,40
c6H6o2 Гидрохинон 0
c6H6o2 Пирокатехин 27 бзл. 2,62
c6H6s Бснзолтиол (тиофснол) 20 бзл. 1,33
c6h7n Анилин 186 г. 1,48
c6h7n 2-Мстилпиридин 10^10 бзл. 1,72
c6h7n З-Метилпиридин 10^10 бзл. 2,30
c6h8n2 Бензол-1,2-диамин (о-фенилендиамин) 150-320 г. 1,5
c6h8n2 Бензол-1,3-диамин (л/-фенилендиамин) 150-325 г. 1,70
c6h8n2 Бензол-1,4-диамин (и-фенилендиамин) 150-325 г. 1,46
c6h8n2 Фенил гидразин 18-19 бзл. 1,7
C6H,o 2,3-Диметилбута-1,3-диен 75-50 гекс. 0
СбНю 2-Мстилпента-1,3-диен 126-224 г. 0,65
СбНю З-Метилпента-1,3-диен 126-214 г. 0,63
СбНю 4-Метилпента-1,3-диен -75 - +50 гекс. 0,52
C6HioO 4-Метилпснт-3-ен-2-он (окись мезитила) 25 бзл. 2,84
СбНюО Циклогексанон 25 диокс. 2,9
СбН10О3 Этил-З-оксобутаноат (ацетоуксусный эфир) 121 г. 2,95
СбНюОд Диэтилоксалат 25 бзл. 2,49
С6Н12 Циклогексан 25 бзл. 0
С6н12о Гексан-2-он (метилбутилкетон) 22 бзл. 2,16
С6н12о 3,3-Диметилбутан-2-он (нинаколин) 15 бзл. 2.79
с6н120 Циклогексанол 25 бзл. 1,9
С6Н]2О2 Бутилацетат 30—40 ж. 1,83
С6Н]2О2 трет-Бутилацетат 22 бзл. 1,91
С6Н12О2 Изобутилацетат 22 бзл. 1,85
С6Н12О2 Метилпентаноат (метилвалерат) 1,61
С6Н12О2 Пентилформиат 103-243 г. 1,90
С6Н12О2 Пропилпропионат 22 бзл. 1,77
С6Н12О2 Этилбутират 22 бзл. 1,74
С6Н12О3 2,4,6-Тримстил-1,3,5-триоксан (паральдегид) г. 1,44
C6H13N 1 -Метилнипсридин 10^10 бзл. 0,91
С6Н14 Г ексан 65-285 г. 0
С6Н]4О Гексан-1-ол 25 бзл. 1,64
С7Н5ВгО Бензоилбромид 20 бзл. 3,37
С7Н5С1О Бензоилхлорид 20 бзл. 3,33
С7Н5С13 (Трихлорметил)бензол (бензогрихлорид) 25 бзл. 2,07
c7h5n Бензонитрил 110-250 г. 4,39
c7h5no Изоцианатобензол (фенилизоцианат) 20 бзл. 2,28
c7h5no3 2-Нитробснзальдегид 25 бзл. 4,3
c7h5no3 З-Нитробензальдсгид 25 бзл. 3,28
c7h5no3 4-Нитробензальдегид 25 бзл. 2,4
c7h5no4 4-Нитробензойная кислота 25 бзл. 3,5
C7H5NS Изотиоцианатобснзол (фенилизотиоцианат) 20 бзл. 3,00
С7НбС12 (Дихлорметил)бензол (бензальхлорид) 25 бзл. 2,03
c7H6o Бензальдегид 25 бзл. 3,0
500
Новый справочник химика и технолога
Продолжение табл. 3.10.2
Формула Название Т. °C Условия определения
С7Н6О2 Бензойная кислота 25 бзл. 1,0
С7Н7С1 1 -Метил-2-хлорбензол (о-хлортолуол) 139 г. 1,56
С7Н7С1 1 -Метил-3-хлорбензол (л/-хлортолуол) 1,8
С7Н7С1 1 -Метил-4-хлорбензол («-хлортолуол) 162 г. 2,19
С7Н7С1 (Хлорметил)бензол (хлористый бензил) 20 бзл. 1,85
C7H7NO Бензамид (амид бензойной кислоты) 20 диокс. 3,6
c7h7no2 1 -Метил-2-нитробензол (о-нитротолуол) 22 бзл. 3,66
c7h7no2 1 -Метил-З-нитробснзол (jw-нитротолуол) 4,17
c7h7no2 1 -Метил-4-нитробензол («-нитротолуол) 25 бзл. 4,44
c7h7no3 1 -Мстокси-2-нитробснзол (о-нитроанизол) 20 бзл. 4,83
c7h7no3 1-Метокси-3-нитробензол (л/-нитроанизол) 20 бзл. 3,86
c7h7no3 1 -Метокси-4-нитробензол («-нитроанизол) 20 бзл. 4,74
c7h8 Толуол 357^482 г. 0,37
c7H8o Анизол (метоксибензол) 130 г. 1,35
C7H8O о-Крсзол 25 бзл. 1,41
c7H8o л/-Крезол 25 бзл. 1,54
c7H8o «-Крезол 25 бзл. 1,57
c7H8o Фенилметанол (бензиловый спирт) г. 1,71
C7HqN А'-Мстиланилин 25 бзл. 1,61
c7h9n о-Толуидин бзл. 1,58
c7h9n л/-Толуидин бзл. 1,43
c7h9n «-Толуидин бзл. 1,27
c7h9no 2-Метоксианилин 150-325 г. 1,62
c7h9no 4-Метоксианилин 25 бзл. 1,80
c7H12o Циклогептанон бзл. 3,04
C7H|4O 2-Мстил циклогексанол 25 бзл. 1,95
C7H14O З-Метилциклогексанол 25 бзл. 1,9
C7H14O 4-Мстил циклогексанол 25 бзл. 1,9
c7H16 Г ептан 65-285 г. 0
c7H16 2-Метилгексан 20-30 ж. 0
c7H16 3-Метил гексан 20-30 ж. 0
c7H16 3-Этилпентан -120- +90 ж. 0
c7H16 2,2-Диметилпентан -120-+90 ж. 0
c7H16 2,3-Диметилпентан 20-30 ж. 0
c7H16 2,4-Диметилпентан 20-30 ж. 0
c7HI6 3,3-Диметилпентан 20-30 ж. 0
c7H16 2,2,3-Тримстилбутан 20-30 ж. 0
c8h7n Индол 20 бзл. 2,05
c8h7n Фенилацетонитрил (бензилцианид) 25 бзл. 3,47
c8H8 Стирол 169-189 г. <0,2
c8H8o Ацетофенон 137-220 г. 3,00
C8H,o Этилбензол 76-182 г. 0,59
C8H,o о-Ксилол г. 0,62
C8H]0 Af-Ксилол -40- +120 ж. 0,34
C8H10 «-Ксилол г. 0
C8H10BrN 4-Бром-/У,А-диметиланилин 25 бзл. 3,37
c8h10cin А,А'-Диметил-4-хлоранилин 25 бзл. 3,29
C8HioN202 /У,А-Диметил-4-нитроанилин 25 бзл. 6,87
C8H10O2 1,2-Диметоксибензол (вератрол) 25 СС14 1,38
C8H,0O2 1,3-Диметоксибензол (диметиловый эфир 25 бзл. 1,59
резорцина)
C8Hi0O2 1,4-Диметоксибензол (диметиловый эфир 25 бзл. 1,81
гидрохинона)
c8h„n А,А-Диметиланилин 25 бзл. 1,58
C8HhN 2,4,6-Триметилпиридин (у-коллидин) 10^10 бзл. 1,93
c8h„n А'-Этиланилин 20 бзл. 1,68
Физические свойства важнейших веществ
501
Продолжение табл. 3.10.2
Формула Название Г, °C Условия определения щ/7
с8н12о4 Диэтилмалсат г. 2,55
с8н12о4 Диэтил фумарат 25 бзл. 2,39
С8Н|4О4 Диэтилсукцинат 157-246 г. 2,3
с8н,4о6 Диэтил-(2/?*,3/?*)-дигидроксисукцинат ((±)-диэтилтартрат) 22 бзл. 3,12
С8Н14О6 Диэтил-(2/?,ЗХ)-дигидроксисукцинат (диэтилмезотартрат) 25 бзл. 3,66
С8н18 Октан -50-+110 ж. 0
C9H7N Изохинолин 10^10 бзл. 2,54
C9H7N Хинолин 10^10 бзл. 2,16
С9Н8О (2Е)-3-Фенилакрилальдегид (коричный альдегид) 25 бзл. 3,63
с9н8о, Коричная кислота 25 диокс. 1,78
с9н10д2 Бензилацетат 25 бзл. 1,8
СдНюОт (2-Метилфенил)ацстат (о-крезилацетат) 22 бзл. 1,68
С9Н|о02 (З-Метилфенил)ацстат (л/-крезилацетат) 22 бзл. 1,60
С9н10о2 (4-Мстилфенил)ацетат (я-крсзилацстат) 22 бзл. 1,53
С9н10о2 Этилбензоат 132-232 г. 1,95
С9Н12 Мезитилен (1,3,5-гриметилбензол) 25 бзл. 0,2
с9н,4о 2,6-Димстилгепта-2,6-дисн-4-он (форон) 25 бзл. 2,36
с9н14о 3,5,5-Триметилциклогекс-2-сн-1 -он (изофорон) 25 диокс. 3,96
С9Н20О4 Тетраэтоксимстан (тетраэтиловый эфир ортоугольной кислоты) бзл. >0
С1ОН6С12 1,2-Дихлорнафталин 25 бзл. 2,47
С1ОН6С12 1,3-Дихлорнафталин 25 бзл. 1,78
С]оН6С12 1,4-Дихлорнафталин 25 бзл. 0,50
С,оН6С12 1,5-Дихлорнафталин 25 бзл. 0
С)0Н6С12 1,6-Дихлорнафталин 25 бзл. 1,44
С10Н6С12 1,7-Дихлорнафталин 25 бзл. 2,55
С10Н6С12 1,8-Дихлорнафталин 25 бзл. 2,82
С1ОН6С12 2,3-Дихлорнафталин 25 бзл. 2,55
С10Н6С12 2,6-Дихлорнафталин 25 бзл. 0
С1ОН6С12 2,7-Дихлорнафталин 25 бзл. 1.53
С1ОН7С1 1 -Хлорнафталин 19 бзл. 1.50
С1ОН7С1 2-Хлорнафталин 25 бзл. 1,65
C10H7F 1 -Фторнафталин 20 бзл. 1,42
C10H7F 2-Фторнафталин 19 бзл. 1,49
c10h7no2 1 -Нитрозо-2-нафтол бзл. 4,39
c10h7no, 2-Нитрозо-1 -нафтол бзл. 4,36
c10h7no2 1 -Нитронафталин 20 бзл. 3,68
c10h7no2 2-Нитронафталин 25 бзл. 4,4
СюН8 Нафталин 25 бзл. 0
Ci0H8O 1 -Нафтол 21 бзл. 1,0
CioH80 2-Нафтол 18 бзл. 1,3
CioHi004 Диметилтерефталат 25 бзл. 2,2
CioH]004 Дим ети л фтал ат 25 бзл. 2,8
CioHi2 C]oH]402 1,2,3,4-Тетрагидронафталин (тетралин) 1,2-Диэтоксибензол (диэтиловый эфир пирокатехина) 25 бзл. 0,52 1,37
CioH]402 1,3-Диэтоксибензол (диэтиловый эфир резорцина) 25 бзл. 1,7
CioHi402 1,4-Диэтоксибензол (диэтиловый эфир гидрохинона) 25 бзл. 1,7
C10H16 (4/?)-н-Мента-1,8-диен ((+)-лимонен) 25 бзл. 1,56
СюН1бО Камфора 22 бзл. 2,95
СюН1бО н-Мент-4(8)-ен-3-он (пулегон) 25 бзл. 3,02
502
Новый справочник химика и технолога
Продолжение табл. 3.10.2
Формула Название Т, °C Условия определения р.Г>
С10н16о Фенхан-2-он (фенхон) 22 бзл. 2,92
СюН]8 трш/с-Декагидронафталин (тмрднс-дскалин) 20-175 ж. 0
Cj0Hi8 цис-Декагидронафталин (г/ис-дскалин) 20-175 ж. 0
с10н18о (1 .S',27?,45)-1,7,7-Триметилбицикло[2.2.1 ]-гептан-2-ол ((-)-борнеол) 22 1,56
С10н18о 1,7,7-Триметилбицикло[2.2.1 ]гептан-2-ол ((±)-борнсол) 35 бзл. 1,85
С]оН180 и-Ментан-З-он (ментон) 22 бзл. 2,82
С1(>н2оо (1/?,37?,45)-л-Ментан-3-ол ((±)-мснтол) 7 бзл. 1,62
С]()Н22 Декан -30- +-170 ж. 0
С|]Н24 Ундекан -1 -4-190 ж. 0
с12н8о Дибснзо[/>,<Дфуран (окись дифенилена) 25 бзл. 0,88
CI2H9NO2 2-Н итробифенил бзл. 3,79
C12H9NO2 З-Нитробифенил бзл. 3,90
c12h9no2 4-Нитробифенил бзл. 4,28
С12Н ] о Бифенил (дифенил) 75-155 ж. 0
C|2H|oN2 C12Hi0N2O C|2h10n2o C12H10N2O Дифенилдиазен (азобензол) 2-Нитрозо-У-фениланилин 4-Нитрозо-У-фениланилин [(Е)-Фснил-У N, О-азокси]бензол (z/wc-азоксибензол) 24 бзл. 0 4,13 5,82 4,68
C12H,oN20 [(2)-Фенил-У,У, (9-азокси]бензол (/и/хздоазоксибензол) бзл. 1,71
c12H10o Дифениловый эфир 172-210 г. 1,14
Ci2H|0S Дифенилсульфид 25 бзл. 1,50
Ci2H]0S2 Дифснилдисульфид 24 бзл. 1,81
C |2H ] |N У-Фениланилин (дифениламин) 20 ТВ. 1,3
C]2H|2N2 1,1 -Дифенилгидразин 20 бзл. 1,87
c12h12n2 1,2-Дифенилгидразин (гидразобензол) 25 бзл. 1,79
С12Н14О4 Диэтил терефталат бзл. 2,3
C12H14O4 Диэтилфталат бзл. 2,4
CI2H22O2 (2-Изопропил-5-метилциклогексил)ацетат (ментилацетат) 22 1,83
c13h8o Флуорсн-9-он 18 бзл. 3,3
C13H9C1 9-Хлорфлуорен 14 бзл. 1,76
c13h9n Акридин 14 бзл. 1,95
C|3H]o Флуорен 20 бзл. 0,28
C|3H10O Бензофенон (дифенилкетон) 100 г. 2,5
C]3Hjo03 Фенил-2-гидроксибензоат (салол, фснилсалицилат) 40 бзл. 3,15
C13H12N2O 1,3-Дифенилмочевина 20 диокс. 4,6
c13h12n2s 1,3-Дифенилтиомочевина 20 диокс. 4,85
C14H12O 2,3-Дифенилоксиран (окись 1,2-дифенилэтилена) 14 бзл. 1,73
c14H12o2 2-Гидрокси-1,2-дифенилэтанон (бензоин) 18 бзл. 3,57
C]4H|4 1,1 '-Этан-1,2-диилдибензол (дибензил) 57-178 ж. 0
c14h14n2o 1 -Метил-2-[(Е)-(2-метилфенил)-У N, 0-азокси]бензол (тцис-о,о -азокситолуол) бзл. 4,37
c14h14n2o 1-Метил-4-[(Е)-(4-метилфснил)-У,У,(9-азокси]бензол (г/цс-л,н'-азокситолуол) бзл. 5,06
Ci4H14N2O 1 -Метил-2-[(2)-(2-метилфенил)-У N, 0-азокси]бензол (транс-о,о -азокситолуол) бзл. 1,73
c14h14n2o 1 -Метил-4-[(2)-(4-метилфенил)-У N, 0-азокси]бензол (транс-п,п -азокситолуол) бзл. 1,74
С14Н14О Дибензиловый эфир 21 бзл. 1,38
Физические свойства важнейших веществ
503
Окончание табл. 3.10.2
Формула Название Г. °C Условия определения ц, D
С]4Н28О2 Тетрадекановая кислота 25 бзл. 0,76
(миристиновая кислота)
С;5Н|4О 1,3-Дифенилацстон (дибензилкетон) 18 бзл. 2,65
Ci5H14O3 Бис(4-метоксифенил )мсганон (ди-я-анизилкетон) 25 бзл. 3,90
c18h15n М?/-Дифениланилин (трифениламин) 15 бзл. 0,26
С]8Н36О2 Стеариновая кислота 25 диокс. 1,74
с19н|6 1, Г, 1 "-Метантриилтрибснзол (трифенилмстан) 94-175 ж. 0
Таблица 3.10.3
Дипольные моменты элементоорганических соединений
Формула Название у; °с Условия определения М
CH3Br3Si Трибром(мстил)силан 25 бзл. 1,86
CH6Si Мстилсилан Штарк 0,73
CH6Sn Мстилстаннан Штарк 0,68
C2H2AsCI3 Дихлор(2-хлорвинил)арсан 20 бзл. 1,77
((2-хлорвинил)арсонистый дихлорид)
C2H5AsC12 Дихлор(этил)арсан (этиларсонистый дихлорид) 20 бзл. 2,51
C2H5BrHg Бром идо(этил )ртуть бзл. 2,76
C2H5Br3Si Трибром(этил)силан 25 бзл. 1,99
C2H5Cl3Ge Трихлор(этил)! ерман 25 бзл 2,3
C2H5Cl3Si Т рихлор(этил)силан 25 бзл. 2,04
C2H5Li Этиллитий бзл. >1,50
C2H6Br2Si Дибром(димстил)силан 25 бзл. 2,45
C2H6Cl2Si Дихлор(этил)силан 25 бзл. 2,04
C2H6I2Te Дииодидо(диметил)теллур 25 бзл. 2,26
C2H8BN М?/-Диметил боранамин 1,5
C3H7AuBr2 Дибром идо(пропил)золото 25 6,0
C3H9BrPt Бромидо(тримстил)платина 1
C3H9BrSi Бром(триметил)силан 25 бзл. 2,36
C3H9ClPb Триметил(хлор)плюмбан 25 бзл. 4,47
C3H9ClPt Триметил(хлоридо)платина 1
C3H9IPt Иодидо(триметил)платина 1
C3H9ISi Иод(триметил)силан 2,46
C4H4AsC13 Хлорбис(2-хлорвинил)арсан 20 бзл. 1,45
(бис(2-хлорвинил)арсинистый хлорид)
C4H9BrHg Бром и до(бути л )ртуть 25 диокс. 3,45
C4H9Li Бутиллитий 1,43
C4H10AuBr Бромидо(диэтил)золото 25 СС14 1,32
C4H10Br2Si Дибром(диэтил)силан 25 бзл. 2,51
C4H10Br2Sn Дибром(диэтил)станнан гепт. 4,0
C4H10Cl2Pb Дихлор(диэтил)илюмбан 25 бзл. 4,70
C4H10Cl2Si Дихлор(диэтил)силан 25 бзл. 2,39
C4H10Cl2Si (Дихлорметил)(триметил)силан 30 бзл. 2,28
C4H10Hg Диэтилртуть 15 бзл. 0,39
C4H10Zn Диэтилцинк бзл. 0,53
C5HHBrHg Бромидо(пснтил)ртуть 25 бзл. 3,47
C4HnClSi Триметил(хлорметил)силан 30 бзл. 2,03
C4HnClSi Хлор(диэтил)силан 25 бзл. 2,01
C4Hi2BN А,А'-Диметил(диметил)боранамин 1,40
C4H]2Si Т етраметилсилан 25 ж. 0
504
Новый справочник химика и технолога
Продолжение табл. 3.10.3
Формула Название Т. °C Условия определения И
C5H14Si T риметил(этил)силан 30 бзл. 1,18
C6H4BrClHg Бромидо(4-хлорфенил)ртуть 25 диокс. 1,57
C6H5BrHg Бромидо(фенил)ртуть 50 диокс. 3,06
C6H5Br3Si Трибром(фснил)силан 25 бзл. 2,36
C6H5ClHg Фенил(хлоридо)ртуть 20 диокс. 2,99
C6H5Cl3Si Фенил(трихлор)силан 25 бзл. 2,41
C6H5F3Si Фенил(трифтор)силан 25 бзл. 2,77
C6H6AsCl3 Трис(2-хлорвинил)арсан 20 бзл. 0,39
C6H6Br2Si Дибром(фснил)силан 25 бзл. 2,33
C6H7BrSi Бром(фенил)силан 25 бзл. 2,07
C6H15A1 Триэтилалюминий бзл. 0,63
C^H^As Триэтиларсан 20 бзл. 1,04
c6h15b Триэтилборан бзл. 0,2
C6H|5BrPb Бром(триэтил)нлюмбан 25 бзл. 4,46
C6H15BrSi Бром(триэтил)силан 25 бзл. 2,42
C6H15BrSn Бром(триэтил)станнан 25 СС14 3,32
C6Hl5ClPb Хлор(триэтил)плюмбан 25 бзл. 4,36
C6H15ClSi Хлор(триэтил)силан 25 бзл. 2,07
C6HI5CISn Хлор(триэтил)станнан 25 СС14 3,44
C6H15FSi Фтор(триэтил)силан 25 бзл. 1,72
C6HI5Ga Триэтилгаллий бзл. 0,67
C6Hl5Ill Триэтилиндий бзл. 1,38
C6H16Si Триэтилсилан 25 бзл. 0,75
C6HI5T1 Триэтилталлий бзл. 0,5
C7H5NHg Фснил(цианидо)ртуть 20 диокс. 3,92
C7H7BrHg Бромидо(4-метилфснил)ртуть 25 диокс. 3,39
C7H7ClHg Бензил(хлоридо)ртуть 25 бзл. 3,05
C7H14AuN Дииропил(цианидо)золото СС14 1,47
C8H20Si Тетраэтилсилан 20 СС14 0
C8H20Sn Т етраэтилстаннан 22 бзл. 0
C9H13BrSi (4-Бромфенил)(триметил)силан 25 бзл. 1,79
C9H13ClSi Диметил(фенил)(хлорметил)силан 30 бзл. 1,93
C9H13ClSi Триметил(3-хлорфенил)силан 30 бзл. 1,83
C9H13CISi Триметил(4-хлорфенил)силан 25 бзл. 1,70
C9H13FSi Триметил(4-фторфенил)силан 25 бзл. 1,69
C9H13NO2Si Триметил(3-нитрофенил )силан 30 бзл. 4,28
C9H i4Si Триметил(фенил)силан 25 бзл. 0,44
C9H21 As Трипропиларсан 20 бзл. 1,00
C]oHIOFe Ферроцен (бис(циклопентадиенил)железо) 25 бзл. 0
C10H10Pb Бис(циклоиентадиснил)свинец 25 бэл. 1,63
CjoHjoSn Бис(циклопентадиенил)олово 25 бзл. 1,02
CI0H15NO2Si Т риметил(4-нитробензил)силан 25 бзл. 4,94
C)0H16Si Диметил(фенил)(этил)силан 30 бзл. 1,30
C10H16Si Триметил(2-метилфенил)силан 25 бзл. 0,57
Ci0Hi6Si Т риметил(3 -метилфенил)силан 25 бзл. 0,46
CioHjfcSi Триметил(4-метилфенил)силан 25 бзл. 0,46
C10H17NSi 2-[(Триметилсилил)метил]анилин 25 бзл. 1,73
C|0H17NSi 4-[(Т риметилсилил)метил]анилин 25 бзл. 1,33
CHH19NSi МЛ-Диметил-4-(триметилсилил)анилин 25 бзл. 1,83
C„H26Si (3 -Метилбутил)(триэтил)силан 27 СС14 0
Ci2H8Br2Hg Ди(4-бромфенил)ртуть 142 дек. 0,92
C12H8Cl2Hg Ди(4-хлорфенил)ртуть 142 дек. 1,15
Физические свойства важнейших веществ
505
Окончание табл. 3.10.3
Формула Название Т. °C Условия определения р
C12H8F2Hg Ди(4-фторфенил)ртуть 112 дек. 0,87
C12H10AsC1 Дифенил(хлор)арсан (дифениларсинистый хлорид) 20 гепт. 2,70
C12H10AS2 Дифснилдиарссн (арсснобензол) 25 бзл. 0
C|2H10Br2Si Дибром(дифенил)силан 25 бзл. 2,77
Ci2H10CI2Si Дифенил(дихлор)силан 25 бзл. 2,56
Ci2H|0Cd Дифенилкадмий бзл. 0,66
Ci2H|0F2Si Дифенил(дифтор)силан 25 бзл. 2,57
C,2H10Hg Дифенилртуть 25 бзл. 0,41
C12H10Mg Дифснилмагний диокс. 4,94
C12H10Te Дифенилтелланид 21 бзл. 1,13
C^HioZn Дифенилцинк бзл. 0,85
Ci2H!0Zr Дифенилцирконий бзл. 0,85
C12H20Pb Фснил(триэтил)плюмбан 22 бзл. 0,86
Ci2H2oSi Фенил(триэтил)силан 27 СС14 0,7
C]2H2(jSn Фенил(триэтил)станнан 22 СС14 0,5
C)2H25BrHg Бромидо(додецил)ртуть бзл. 2,76
C12H25ClHg Додецил(хлоридо)ртуть диокс. 3,0
Ci2H27As Т рибутиларсан 20 бзл. 0,92
Ci3H21As Бутил(4-метилфенил)(этил)арсан 20 бзл. 1,29
C14H 14Br2Te Дибромидоди(4-метилфснил)тсллур 25 бзл. 3,21
C|4Hl4Cl2Te Дихлоридоди(4-метилфенил)теллур 25 бзл. 2,98
C14H14Hg Ди(4-мстилфенил)ртуть 142 дек. 0,74
Ci4H16Si Диметил(дифенил)силан 30 бзл. 0,34
CibFbaBrHg Бромид о(гексадецил)ртуть бзл. 2,31
CjgHisAl Т рифснилалюминий бзл. 1,17
CigHisAs Трифсниларсан 18 бзл. 1,07
CisH^AsCF Т рифенил(дихлор)-Х5-арсан 25 бзл. 0
c18h15b Трифенилборан бзл. 0
CisHisBi Т рифснилвисмут 16 бзл. 0
C18H15BrGe Бром(трифенил)гсрман 25 бзл. 2,35
C18H15BrPb Бром(трифенил)плюмбан 25 бзл. 4,21
C18H15BrSn Бром(трифенил)станнан 22 бзл. 3,15
Cl8H15ClPb Трифенил(хлоридо)свинец 25 бзл. 4,21
CjsHijdSn Трифснил(хлор)станнан 25 бзл. 3,28
C18H15Cl2Sb Трифенил(дихлоридо)сурьма 25 бзл. 1,19
Ci8Hi5Ga Т рифснилгалл ий бзл. 0,4
C18H15IPb Иод(трифенил)плюмбан 25 бзл. 3,73
C18H15In Трифенилиндий бзл. 0,79
CisHisSb Трифснилсурьма 14 бзл. 0,57
C18H15T1 Трифенилталлий бзл. 0.67
c18H]6si Трифенилсилан 25 СС14 1
CisIbvBrHg Бромидо(октадецил)ртуть диокс. 2,0
C19H15Na (Трифснилмстил)натрий 25 диокс. 7,П
C2OH2oPb Трифенил(этил)плюмбан 22 бзл. 0,81
C2oH2oSi Трифенил(этил)силан 30 бзл. 1,25
C2oH2OSn Т рифенил(этил)станнан 22 бзл. 0,73
C21H21AS Три(4-метилфенил)арсан 20 бзл. 1,74
C22H16Cl2Fe 1,1 '-Бис(4-хлорфенил)ферроцен (бис[ 1 -(4-хлорфенил)-г|5-циклопентадиенил]железо) 25 бзл. 3,12
506
Новый справочник химика и технолога
3.11. Вязкость веществ и растворов
(Е.Е. Бибик)
Общие понятия
Понятием «вязкость» обозначается хорошо известное и как будто не требующее пояснений свойство жидкостей, проявляющееся в процессе их течения. На самом деле это свойство характеризует лишь одну, хотя и важную, сторону поведения веществ под воздействием механических сил. В связи с этим необходимо выяснить границы применимости указанного понятия и адекватные характеристики поведения веществ за границами его применимости. К числу свойств и явлений, указывающих на такую необходимость, относятся известная условность деления веществ на жидкие и твердые, «неньютоновскис» свойства некоторых жидкостей, наличие жидкостей которые могут течь также и в направлении, перпендикулярном к действующей силе (эффект Вайссснберга), и др.
Основные понятия, которые используются при описании поведения веществ под действием механических сил, — это интенсивность механического воздействия на вещество (нагрузка), характеризуемая величиной напряжения, и уровень геометрических изменений формы образца, вызванных этим напряжением, характеризуемый величиной деформации.
Напряжение — это удельная (на единицу площади) сила, действующая на поверхность образца или в произвольном сечении внутри его. Размерность напряжения Н/м2 (ньютон на квадратный метр). Величина напряжения, равная 1 Н/м2, называется паскалем (Па).
Деформация — обратимое или необратимое изменение формы образца или любой его части без разрыва сплошности образца. Деформация является безразмерной величиной и выражается отношением приращения некоторого размера образца (или его части) к самому этому размеру, например, отношением удлинения образца к его длине. Существенно, что деформируемый образец считается при этом сплошным телом вне зависимости от того, что он представляет собой на самом деле. Это может быть действительно образец сплошного материала (меди, эпоксиолигомера, воды), а может быть дисперсной системой — взвесью частиц твердого вещества, например той же меди, в смоле, воде или даже в газовой среде (порошком). Испытуемые жидкие материалы и дисперсные материалы (на жидкой основе), как правило, помещаются в некоторую форму (сосуд). Понятие «вещество» не подразумевает наличия у него способности сохранять сплошность при деформации, поэтому объектами при изучении и описании деформационных свойств являются не вещества, а материалы, в качестве которых могут выступать и различные индивидуальные вещества в виде монолитных образцов, и их гомогенные (растворы) и гетерогенные смеси (дисперсные системы), причем свойства последних наиболее разнообразны.
Процесс увеличения необратимой деформации во времени называется течением. Материалы, способные
к такого рода деформациям, называются жидкостями или флюидами. Последний термин относится и к жидкостям, и к газам. Поведение флюидов под нагрузкой характеризуется скоростью деформации — отношением приращения деформации к интервалу времени, за который это приращение возникло. Размерность скорости деформации с '.
Жидкости в практическом отношении можно считать несжимаемыми. Для них наиболее характерна деформация сдвига. При простом сдвиге (параллельном перемещении слоев жидкости в одном направлении) скорость деформации совпадает по величине с градиентом скорости течения — отношением разности скоростей движения двух произвольных слоев жидкости к расстоянию между этими слоями. При однородном сдвиге градиент скорости одинаков во всех частях деформируемого образца.
Наиболее общие вопросы деформационных свойств материалов изучает реология [1 ]. Основная задача реологии — установление законов (уравнений), которые описывают поведение материалов под нагрузкой, и значений коэффициентов этих уравнений для каждого конкретного вещества или материала. В частности, поведение жидкостей описывается законом внутреннего трения Ньютона:
т = ПУ'.
Здесь т — напряжение сдвига (сдвиговое усилие), действующее на единицу площади поверхности или внутреннего сечения испытуемого образца (Па) и у' — скорость сдвиговой деформации материала (с1). Коэффициент г| в этом уравнении называется вязкостью, которая является характеристикой реологических свойств жидкостей любого типа (индивидуальных жидких веществ, гомогенных растворов, дисперсных систем с жидкой средой). Этот коэффициент может быть константой данного уравнения, т. е. не зависящей от напряжения (или скорости сдвига) величиной, или может быть функцией напряжения (или скорости сдвига). Жидкости, у которых вязкость является константой уравнения Ньютона, называются ньютоновскими. Жидкости, у которых вязкость зависит от напряжения (скорости сдвига), не вполне удачно называются неньютоновскими. Неудачность названия заключается в том, что оно часто понимается излишне буквально и создает ошибочное впечатление, что неньютоновские жидкости — это жидкости, течение которых не подчиняются закону внутреннего трения Ньютона. Парадоксальнось ситуации в том, что основанием для возникновения такого впечатления служит зависимость вязкости от напряжения, полученная именно путем применения закона Ньютона к результатам измерения, т. е. путем
т вычисления величины г| = — . у'
Размерность вязкости Па • с. В системе единиц СГС вязкость имеет размерность дин • с/см2, причем вязкось величиной 1 дин • с/см2 имеет наименование «пуаз» (П).
Физические свойства важнейших веществ
507
Вязкость воды при 20 °C составляет 0,01 П или 1 сП (сантипуаз). В системе СИ вязкость воды при тех же условиях равна 0,001 Па • с, т. е. 1 мПа • с. Таким образом, обе формы обозначения единиц при краткой записи величин вязкостей (сП и мПа • с) эквивалентны: 1 сП = 1 мПа • с. Первая обладает преимуществами, как величина, имеющая наименование и более короткое обозначение, поэтому может употребляться наряду со второй. Для получения значения вязкости, пригодного к использованию в расчетных формулах в системе СИ (т. е. в Па • с), величины, выраженные в сП или в мПа • с, следует умножить на 0,001.
V П
Кинематическая вязкость v = —, применяемая в нс-Р
которых уравнениях, равна отношению вязкости жидкости г| к ее плотности р. Размерность кинематической вязкости в системе СГС см2/с и ее величина, равная 1 см2/с, имеет наименование «стокс» (Ст). Кинематическая вязкость воды при 20 °C равна приближенно 0,01 Ст или 1 сСт (сантистокс). В системе СИ кинематическая вязкость имеет размерность м2/с и для воды при тех же условиях равна приближенно 106м7с. Не рекомендуется использовать десятичные приставки (санти-, милли-, микро- и др.) в размерностях величин типа м7с, в которых степень основных единиц измерения (кг, м, с) отличается от единицы, т. к. это не исключает возможность неоднозначного толкования величины. Например, значение, равное 1 мкм2/с, может быть истолковано и как 10'6 м2/с, и как 10 12 м2/с (т. е. как мкм2/с).
Реологическим антиподом жидкостей являются твердые тела. В них деформация у существует только до тех пор, пока действует напряжение т. Снятие напряжения приводит к полному восстановлению первоначальной формы образца, т. е. к исчезновению деформации. Поэтому поведение твердых материалов описывается законом упругих деформаций Гука, утверждающего пропорциональность напряжения и деформации:
т = Gy.
Реологической характеристикой материала является его модуль упругости G, имеющий ту же размерность, что и напряжение.
Завершая серию реологических определений основных типов материалов (веществ), отметим, что газ — это материал, который может существовать только под действием механического напряжения (давления), а из геометрических характеристик его состояния имеет значение только одна — объем газа (сосуда). Газ, как и жидкость, способен неограниченно деформироваться (течь) и также характеризуется вязкостью т|.
Деление веществ на жидкие и твердые в известной мере условно. Принадлежность материала к тому или иному реологическому типу сильно зависит от величины и длительности воздействия деформирующего усилия. Имеются в виду как экстремальные условия деформирования типичных жидкостей и твердых веществ, так и материалы с особыми свойствами уже при нормаль
ных условиях их существования и деформирования. Например, струйка воды раскалывается, как стеклянная палочка, при попадании в нее пули, а ледники и даже континенты движутся (текут) в геологическом масштабе времени. Сталь, медь, свинец способны течь (необратимо деформироваться) при напряжениях порядка тысячи атмосфер (108Па). Кусок битума заметно расплывается за несколько дней под действием слабой силы собственного веса и он же хрупко разрушается при ударе молотка. В справочной литературе это находит свое отражение в том, что приводятся данные о вязкости типичных твердых веществ, которая на много порядков превышает вязкость жидкостей. Вязкость газов, наоборот, на несколько порядков ниже вязкости жидкостей. Особенностью газов является то, что их вязкость слабо зависит от концентрации (давления).
Относительная условность деления материалов на твердые и жидкие делает актуальным поиск более универсальных способов описания реальных материалов, чем это возможно с помощью законов Ньютона и Гука. Один из них считает реальные материалы вязкоупругими, а другой — вязкопластичными (пластичными).
Вязкоупругость означает, что реальный материал сочетает в себе свойства твердого вещества и жидкости так, что или напряжения, или деформации реального материала аддитивно складываются из величин, определяемых законами Ньютона и Гука. Материал, следовательно, характеризуется модулем упругости и вязкостью одновременно или обобщающим параметром —
временем релаксации
п
tr = —. По размерности он сов-G
падает со временем, но смысл его зависит от способа формального сочетания элементов упругого и вязкого сопротивления (от аддитивности по напряжениям или по деформациям) и может представлять собой или время релаксации (уменьшения) напряжения, необходимого для поддержания заданной величины деформации, или время релаксации (восстановления) формы при изменении (в частности уменьшении до нуля) деформирующего усилия. С точки зрения концепции вязко
упругости, одно и то же идеальное твердое тело можно считать жидкостью, но с бесконечно большим временем релаксации напряжений, или же твердым телом с нулевой величиной времени релаксации формы. Суть этого замечания в том, что время релаксации зависит от формальной модели материала и поэтому в справочную литературу может включаться только вместе с описанием модели. Выбор модели может быть субъективным, поэтому сведения о временах релаксации не имеют статуса справочного материала.
Пластичность (вязкопластичность) означает, что
вплоть до некоторого характерного напряжения т, каждый материал ведет себя как упругий, а при превышении его начинает течь со скоростью, пропорциональной величине превышения (т-тЛ) напряжения т над указанной характерной его величиной:
т = т5 + т| *у'.
508
Новый справочник химика и технолога
Это уравнение реологии пластичных материалов известно как эмпирический закон Шведова — Бингама, который, однако, позднее был получен и теоретически [2]. Величина т|* называется пластической вязкостью, а тЛ — предельным напряжением сдвига или просто прочностью материала (на сдвиг). Свойства материала в рамках этого закона исчерпывающе характеризуются этими двумя константами. Их смысл вполне определен уравнением Шведова — Бингама. Однако эквивалентным образом свойства пластичного материала описываются и одной переменной величиной — вязкостью т
г| = —, которая выражается через константы уравнения У'
пластического течения: г| =----. Эта формула —
T-Ts
конкретный пример применения закона Ньютона к типичной «нсньютоновской» жидкости — пластичному материалу.
В большинстве случаев и пластическая вязкость не остается постоянной (обычно уменьшается) с увеличением напряжения (скорости) сдвига. Материалы с таким свойством называются нелинейно-пластичными. В общем случае может иметь место крайне медленное течение (ползучесть) и при напряжениях, меньших предельного напряжения сдвига. Вязкость ц в режиме ползучести на несколько порядков превышает вязкость при высоких скоростях течения. Кроме того, при достаточно высоких скоростях течения вязкость может уменьшиться до некоторой минимальной и постоянной величины, так что скорость сдвига в этом режиме деформирования становится пропорциональной напряжению, т. е. материал начинает вести себя как ньютоновская жидкость (переходит в режим квазиньютонов-ского течения). Таким образом, в общем случае имеются гри разных режима деформирования неньютоновского материала пластического типа: режим ползучести, режим пластического течения и режим ква-зиньютоновского течения, каждый из которых имеет свой набор реологических констант и уравнений течения. В технологической практике обычно приходится иметь дело с пластическим режимом деформирования.
По характеру зависимости вязкости от напряжения (скорости) деформации неньютоновскис материалы делят также на тиксотропные и дилатантные. Первым присуще снижение вязкости с увеличением напряжения, а вторым — увеличение. Заметим, что понятие тиксотропии и дилатансии относился не к типу зависимости вязкости от напряжения, а к структуре материалов дисперсного типа.
Под структурой подразумевается характер взаимного расположения элементов (частиц, молекул), образующих данную среду. В структурированных системах существуют некоторые предпочтительные способы взаимного расположения частиц (корреляция их координат и импульсов), в неструктурированных системах координаты и импульсы частиц не связаны между собой. Структура системы определяет характер реологических законов и
значения коэффициентов соответствующих уравнений, и именно на основе этой концепции теоретически получены все известные к настоящему времени уравнения реологии неньютоновских систем [2, 3]. Их сводка приводится ниже. Она относится только к дисперсным системам (коллоидным растворам, суспензиям, эмульсиям, пенам), в том числе неструктурированным, которые являются ньютоновскими жидкостями.
Особое место в теоретической и прикладной реологии занимает формула Эйнштейна для вязкости г| разбавленных, неструктурированных коллоидных растворов:
г| = По( 1 + аср )•
Здесь г|о — вязкость растворителя, (р — объемная доля дисперсной фазы во взвеси и а — числовой коэффициент, равный 2,5 для частиц сферической формы. Формула дает приемлемые но точности результаты при концентрации (р не более 0,1. При этом должно быть
гарантировано отсутствие слипания частиц.
Структура дисперсной системы определяется взаимодействием частиц и их концентрацией. Неструктурированные системы — это суспензии, эмульсии и более тонкие взвеси (золи), в которых полностью исключено слипание частиц при малой или умеренной их концентрации. Они же при большой концентрации переходят в кристаллоподобнос состояние, т. е. частицы вследствие
взаимного отталкивания располагаются в узлах пра-(1 у3 вильнои решетки с периодом, равным примерно — ,
у п )
где п — число частиц в единице объема взвеси. Системы с периодической структурой склонны к дилатантному типу течения. Системы с выраженной склонностью частиц к слипанию образуют коагуляционную структуру (гель) — более или менее рыхлую сетку из взаимосцепленных частиц. Им присущ тиксотропный тип поведения под нагрузкой.
К настоящему времени не выявлено фактов, которые бы дали повод усомниться в справедливости сформулированного П.А. Ребиндером основополагающего принципа теоретической реологии: вязкость определяется структурой и остается неизменной до тех пор, пока неизменна структура материала. Продуктивность структурных представлений в реологии дисперсных
систем заметно выше, чем в теории вязкости индивидуальных жидких веществ или истинных растворов. Этим предопределена ведущая роль коллоидов в формировании общих представлений реологии, особенно коллоидных ферромагнетиков (феррожидкостей) благодаря возможности контролируемым образом изменять их структуру воздействием магнитного поля [2].
Свойства индивидуальных жидких веществ (воды, ртути, спиртов и др.), в том числе вязкость, также определяются их структурой, которая достаточно сильно меняется при изменении температуры и состава растворов. Тем не менее, жидкости и истинные растворы (за исключением полимерных) строго следуют закону
Физические свойства важнейших веществ
509
внутреннего трения Ньютона с постоянной (при данных температуре, составе, давлении) вязкостью. Это обусловлено определяющей ролью термических флуктуаций в формировании структуры жидкости, тогда как в дисперсных системах структурное состояние определяется величиной механических напряжений в лабильных структурных элементах системы.
Справочные данные о вязкости индивидуальных веществ, растворов и газов в основном упорядочены по признаку усложнения (удлинения) их химических формул [4, 5]. Такой способ систематизации подразумевает отсутствие у веществ других свойств, определяющих их вязкость. На самом деле такие свойства существуют, что следует из приводимых ниже основных теоретических положений, комментариев и пояснений к ним, которые могут служить ориентиром в поисках взаимосвязи строения и вязкости веществ и растворов. Следует иметь в виду, что экспериментальный справочный материал и теория предполагают принадлежность обычных жидкостей к ньютоновским, хотя в случае водных растворов некоторых солей появление неньютоновских свойств нс исключено вследствие их гидролиза с образованием коллоидных частиц или высокомолекулярных гидроксоком-плексов, сходных по свойствам с полимерами.
Важную роль в технологии материалов композиционного типа занимают полимеры и их растворы. Характерным реологическим свойством полимерных систем является вязкоупругость. Соответствующие сведения можно найти в специализированных изданиях [6]. Здесь же ограничимся основными данными о вязкости разбавленных растворов, которые используются, в частности, в аналитических целях — для определения молярной массы М полимеров по вязкости их растворов с помощью формулы Куна:
[Г|] КЬГ,
где Кип — эмпирические константы, индивидуальные для каждого гомологического ряда полимеров, а [т|] — характеристическая вязкость растворенного вещества. Она определяется экспериментально как предел удель-
Г|-Г|о нои вязкости ------ растворов разной концентрации с
при ее устремлении к нулю. Здесь т|0 — вязкость растворителя. В соответствии с формулой Эйнштейна характеристическая вязкость растворенного вещества сир равна —L.
с
В случае анизотропных материалов (их свойства различны в разных направлениях) направление деформации может не совпадать с направлением действующего напряжения. При этом напряжение, деформация и скорость деформации могут быть разложены на компоне-ты, направленные вдоль трех осей координат. Каждый компонет деформации и скорости деформации зависит от всех трех компонентов напряжения (является частью тензора). Некоторые материалы способны приобретать
наведенную анизотропию, т. е. возникающую только при их деформировании (течении). В частности она присуща полимерам и их растворам и является вероятной причиной эффектов Вайссенберга, сводящихся к возникновению градиента всестороннего (пуазейлево-го) давления при неоднородной сдвиговой деформации раствора. Один из них — подъем жидкости по стержню, опущенному во вращающийся сосуд с раствором подходящего полимера [1]. Данные справочного типа о таких эффектах и общее мнение об их природе отсутствуют, однако совокупность эффектов указывает на определяющую роль растяжения полимерных клубков в потоке. Если потоки жидкости замкнуты, то упругие напряжения клубков создают в среде усилия, направленные на уменьшение длины линий тока (натяжение линий тока) и, следовательно, на повышение давления в тех областях, которые охватываются этими линиями.
При проектировании и подборе технологической аппаратуры знание характера зависимости параметров того или иного процесса от условий его осуществления оказывается, как правило, важнее, чем знание точных, но не имеющих адекватного математического выражения эмпирических зависимостей. Последние к тому же далеко не всегда имеются в распоряжении технолога или конструктора. В связи с этим уместно располагать уравнениями и формулами, которые хотя бы на качественном уровне правильно передавали бы связь между различными величинами, определяющими ход технологического процесса. С этой целью ниже приводятся основные теоретические зависимости.
Теоретические положения
Вязкость газов [7]
Вязкость идеального газа не зависит от его давления (концентрации).
где d— диаметр, т — масса молекулы, к — постоянная Больцмана (1,38 • 10“23 Дж/К) и Г— температура.
Вязкость реальных газов хорошо описывается этой формулой в части ее зависимости от массы молекул. Зависимость же от температуры в реальности несколько сильнее. Объясняется это влиянием неидеальности газа (притяжения молекул) на частоту столновений молекул, посредс твом которых и происходит торможение взаимного движения соседних слоев газа. Поправка на этот эффект учитывается формулой Сазерленда:
7 V>l/2
d = d 1+- .
A Т)
В ней эмпирическая константа 5 имеет размерность температуры, а константа dVj соответствует размеру молекул при бесконечно большой температуре, когда взаимодействие молекул не сказывается на поведении
510
Новый справочник химика и технолога
газа. Для ряда газов имеются справочные данные о величине константы S (см. справочные таблицы). Комбинирование приведенных выше формул дает выражение, удобное для вычисления вязкости г| при некоторой температуре Т но вязкости т|о при другой температуре То:
3
Вязкость жидкостей [7]
Имеется ряд формул для вычисления вязкости простых жидкостей, полученных теоретически на основе различных моделей их строения. Наиболее популярна следующая формула
п = — ^2пткТ ехр—— , v RT
выведенная на основе активационной модели течения, согласно которой течение возникает в результате тепловых перемещений молекул преимущественно в направлении действующей на них силы. В отсутствие сдвиговых напряжений перемещения имеют характер хаотично направленных скачков на расстояние s порядка диаметра молекул <7, а их частота определяется вероятностью флуктуационного возникновения в жидкости полостей (вакансий) с объемом v, достаточным для размещения в ней молекулы. Тот и другой параметры по порядку величины равны соответствующим размерам молекул, так что — ~ . Количественно эта веро-
v d
ятность описывается экспоненциальным множителем формулы через энергию Ua образования полости, которая в эксперименте воспринимается как энергия активации течения и является одной из основных характеристик жидкостей. В формуле энергия активации отнесена к молю вещества и R — газовая постоянная (8,31 Дж/(моль • К)). В целом предсказываемая формулой зависимость вязкости жидкости от массы молекул выполняется удовлетворительно. Проверка этой и других закономерностей сильно осложняется тем, что в реальности с изменением одного параметра, например массы молекул, изменяются и другие параметры, входящие в формулу, в первую очередь — энергия активации.
Вязкость растворов [7]
Теория пока не может предложить формул, пригодных хотя бы для ориентировочных расчетов вязкости истинных (неколлоидных) растворов по вязкости их компонентов. Проблема заключается в нахождении энергии активации течения смеси. Можно утверждать, что зависимость вязкости от состава будет в определенной мере повторять зависимость энергии активации от состава. Замечено также, что вязкость физической смеси (раствора) двух углеводородов практически совпадает с вязкостью индивидуального вещества, со
стоящего из тех же компонентов что и раствор, но в химически связанном состоянии.
Вязкость расплавов солей [7]
Заслуживает внимания тот факт, что вязкость расплавленных ионных соединений оказывается примерно такой же, как вязкость одинаковых по составу недиссоциирующих соединений. Это означает, что кинетическими единицами расплавов являются не ионы, а молекулы, и их можно считать обычными полярными жидкостями.
Вязкость расплава металла при температуре плавления [7]
Вязкость расплава металла при температуре плавления зависит от температуры Дебая 0 — энергетической характеристики кристаллической решетки.
Здесь h — постоянная Планка. Отношение --- име-
А0
к© ет размерность времени, так что величина — в этой h
формуле отражает частоту тепловых скачков атомов расплава на расстояние порядка их диаметра d.
Вязкость растворов полимеров
Роль частиц в растворе полимера выполняют свернутые в клубки длинные полимерные молекулы. Теория таких молекул [8] позволяет найти гидродинамический объем клубка а и, следовательно, эффективную объемную долю гр/? полимера в растворе, и таким путем выразить характеристическую вязкость растворенного вещества через параметры его молекул:
/ . , \(3-ф)/ф
[pl = — £>3(ф_|)/ф _ j Р )
Отсюда следует, что в уравнении Куна ар’|ф " * 3-ф
А = и п =------L. Здесь р — плотность поли-
рт,3”ф)/ф ф
мера; т — молярная масса его элементарного химического звена; р — число таких звеньев в эффективном жестком сегменте Куна; ф — фрактальная размерность клубка. Последняя представляет собой показатель сте-
( L У
ггени фундаментального соотношения v = — фрак-\pd )
тальной геометрии [9], связывающего размер клубка L М хх
с числом v = — эффективных жестких звеньев и их тр
длиной pd, из которых как бы состоит гибкая полимерная цепь. Фрактальная размерность любых объектов
Физические свойства важнейших веществ
511
находится в пределах от 1 до 3. Если считать, что вращательная подвижность жестких сегментов цепи никак не офаничена, то тогда ф = 2, и в формуле остается только один подгоночный (эмпирический) параметр молекулярной цепи — число р мономерных звеньев в виртуальном жестком сегменте Куна при фиксированном значении п = 0,5. Фактически имеются, как минимум, стерические ограничения возможных конфигураций цепи, поэтому показатель степени оказывается несколько большим, чем 0,5. Систематизация экспериментальные данных о вязкости растворов полимеров в основном ограничена нахождением значений констант уравнения Куна Кип для некоторых полимерго-мологических рядов.
Вязкость ньютоновских суспензий и коллоидных растворов [ 1 ]
В дополнение к приведенной выше формуле Эйнштейна создано большое число ее модификаций с целью расширения диапазона концентраций дисперсной фазы, при которых можно вычислять вязкость взвесей. Чаще всего модифицированные формулы представляют собой степенные ряды но концентрациям (р с очень разной у различных авторов величиной коэффициентов при высших степенях концентрации. В обобщенном виде формула имеет вид:
г| = г|о(1 + аср + £1(а(р)2 + А2(сф)3 + •••),
где к\, к.2 — коэффициенты порядка единицы, значение которых различно у разных авторов [1]. При оценочных вычислениях, не делая грубой ошибки, их можно считать равными единице. Вместе с тем следует обратить внимание на то, что при конечном числе членов ряда эта формула в любом варианте нс может дать значение вязкости, равное бесконечности, которое, естественно, должно получаться при концентрации твердой дисперсной фазы (р = 1.
Из других форм привлекательно своей простотой уравнение Бринкмена:
которое также выведено на основе уравнения Эйнштейна и дает очевидный результат: г| = оо при (р = 1, т. е. при переходе к монолитному твердому веществу.
Вязкость высококонцентрированных суспензий с периодической структурой [2]
Классический подход к описанию течения таких суспензий аналогичен тому, что принят в активационных теориях течения обычных жидкостей и в общем дает тот же результат. Отличие в том, что энергия упругих напряжений, действующих на частицу суспензии, может существенно превышать энергию теплового
движения частиц, и поэтому в окончательном результате приходится сохранять экспоненциальную зависимость скорости сдвига от напряжения, а не ее упрощенную линейную функцию. В итоге это ведет к появлению зависимости тиксотропного типа, что совершенно не характерно для рассматриваемых здесь дисперсных систем. Корректная теория их течения учитывает наличие вакантных (не занятых частицами) узлов периодической структуры и уменьшение их концентрации при увеличением скорости течения вследствие «размазывания» вакансий по межчастичному просгранству. В итоге получается уравнение, которое правильно описывает экспериментальные данные [2]:
_ со 2пкТ
где с0 — концентрация вакансий в состоянии покоя; п— конценграция частиц (1/м3); f = /оехр|| — частота перескоков частицы между двумя ее положениями в решетке при наличии соседнего с ней вакантного узла (она определяется частотой/0 свободных тепловых колебаний частицы в узле решетки и потенциальным барьером Ua, отделяющим ее от вакантного узла); tr — время релаксации вакансий. В оригинале [2] и других работах [10,11] имеются соотношения для расчета этих параметров, однако по ряду причин, в том числе вследствие полидисперсности реальных суспензий, их следует воспринимать как подгоночные параметры уравнения. В сущности их два: время релаксации вакансии и частота перескоков частиц. Величина, обратная этой частоте, известна как время оседлой жизни частицы в узле решетки рядом с вакансией. Варьируя эти параметры можно, получить все разнообразие наблюдаемых зависимостей вязкости от напряжения, в том числе тиксотропно-дилатантную (очень характерную для грубодисперсных суспензий). Минимум вязкости при этом приходится на безразмерное напря-т
жение £ =-----, величина которого зависит от одного
2пкТ
единственного параметра — произведения ftr и находится решением уравнения:
- е)+ she - sche = 0.
Минимум существует при ftr < 0,5 и смещается в сторону больших напряжений при уменьшении величины Д..
Вязкость тиксотропных суспензий [3]
В суспензиях этого типа частицы связаны между собой силами сцепления, образуя или сплошную рыхлую сетку (гель), или отдельные ее фрагменты — более или менее рыхлые флокулы, гидродинамический размер L
512
Новый справочник химика и технолога
которых связан с размером частиц d и их числом р во флокуле основным соотношением фрактальной геомет-< мф
рии флокул [9]: р = — . Здесь ф — фрактальная раз-\d )
мерность — эмпирическая величина, лежащая в пределах от 1 до 3. Общая гидродинамическая объемная доля флокул (р/, много больше совокупной объемной ДОЛИ (р всех частиц суспензии, поэтому вязкость флокулированной взвеси может на порядки превышать вязкость взвеси нс склонных к слипанию частиц. Сплошная структурная сетка (гель) представляет собой совокупность плотно упакованных и связанных между собой флокул, так что их объемная доля во взвеси ф/, равна 1. При течении сплошная сетка разрушается на отдельные флокулы. Чем выше напряжение, тем меньше гидродинамически равновесный размер флокул и, соответственно, их объемая доля (р/, во взвеси. В гидродинамическом отношении флокулы подобны сплошным телам, и поэтому вязкость взвеси флокул может вычисляться по тем же формулам, что и вязкость взвеси сплошных частиц, в частности по формуле Бринкмсна. Принципиальное же отличие флокул от сплошных частиц в том, что их гидродинамический объем уменьшается с увеличением напряжения сдвига, и поэтому вязкость нс остается постоянной. Количественно ее зависимость от напряжения описывается системой уравнений, включающей следующие формулы:
I. Закон внутреннего трения Ньютона, определяю-т щии смысл вязкости: г| = — .
У’
2. Уравнение, описывающее зависимость вязкости от концентрации взвешенных в среде включений, создающих дополнительное сопротивление движению соседних слоев среды. В качестве такового может быть выбрано уравнение Бринкмена, в котором объемная доля дисперсной фазы ср заменена на объемную долю
флокул (рА: г| =
По
3. Уравнение структурного состояния взвеси, раскрывающее зависимость гидродинамически существенного параметра взвешенных в среде включений от напряжения сдвига. Согласно выбранному выше уравнению, это концентрация (объемная доля) флокул (р/;. Определяющими параметрами суспензии при этом являются объемная доля ср дисперсной фазы (частиц), размер d (диаметр) и сила сцепления F частиц. Комбинация
двух последних дает прочность хт структурного каркаса
при плотной упаковке частиц (при ср= 1): tw=tw/
3F ~dr'
При произвольной концентрации дисперсной фазы ср в структурированной взвеси ее прочность
£ , 2
т, = т,„Ф •, £, = -—- .
3 - ф
Каждому режиму течения (ползучесть, пластичность, квазиньютоновость) соответствует свое уравнение структурного состояния:
т < т„ ср = 1 (ползучесть или упругость);
, , (Т, У I
т„, < т < т„ ф/, = — ; ц = — (пласт ичность);
V. т )
т > т,„, <р/7 = (р (квазиньютоновость)
Эта система уравнений дает типичные для тиксотропных систем зависимости скорости сдвига и вязкости от напряжения, в частности нелинейно-пластическое течение в интервале напряжений от т„ до хт с переходом к квазиньютоновскому течению при т > тт. Сила сцепления частиц может быть вычислена на основе уравнений теории устойчивости дисперсных систем [10, 11]. Однако на практике надежнее использовать ее как эмпирическую характеристику дисперсной системы. Фрактальная размерность имеет аналогичный статус. Стандартная обработка экспериментальных данных для пластического участка течения позволяет вычислить оба парамета системы уравнений. Уравнения для
По
вязкости г| =----------- следует предварительно пре-
I Э; J
образовать в уравнение прямой:
Далее в табл. 3.11.1-3.11.5 приведены для воды: текучесть, вязкость и относительная вязкость при Т = = 0-г100 °C, вязкость при Т > 100 °C и давлении насыщенного пара при указанной температуре, вязкость и кинематическая вязкость при различных значениях температуры и давления, относительная вязкость при различных значениях температуры и давления, вязкость переохлажденной воды и оксида дейтерия (тяжелой воды). В табл. 3.11.6-3.11.13 представлена вязкость при различных значениях температуры для простых веществ, неорганических соединений, некоторых твердых веществ, углеводородов, органических соединений, некоторых газов, сжиженных газов и хладонов; в табл. 3.11.14 — вязкость водяного пара в зависимости от давления и температуры, в табл. 3.11.15 — вязкость газов и паров при давлении 0,1 МПа и константы Сазерленда для них.
Таблица 3.11.1
Текучесть f, вязкость Т| и относительная вязкость Г воды в интервале температур 0—100 °C
Текучесть/= —, относительная вязкость г = — отношение вязкости г|(7) при данной температуре Т к вязкости ц(0) при 0 °C и давлении 101,3 кПа. П П(0)
Национальное бюро стандартов США (NBS) предлагает для целей калибровки в качестве абсолютной величины вязкость 1,002 • 10“3 Па • с для воды при 20 °C и давлении
101,3 кПа.
Т, °C f, Па"’ • с’1 п • 103, Па • с г Т,°С Па’1 • с 1 п • 103, Па • с г Т. °C Па ' •с 1 ц • 103. Па • с г Г. °C / Па’1 • с 1 п • ю3, Па • с г
0 558 1,7921 1 26 1144,5 0,8737 0,4875 51 1850,5 0,5404 0,3015 76 2666,7 0,375 0,2093
1 577,6 1,7313 0,9661 27 1170,3 0,8545 0,4768 52 1881,4 0,5315 0,2966 77 2701,2 0,3702 0,2066
2 597,8 1,6728 0,9334 28 1196,2 0,836 0,4665 53 1912,3 0,5229 0,2918 78 2735,7 0,3655 0,204
3 617,6 1,6191 0,9035 29 1222,5 0,818 0,4564 54 1943,4 0,5146 0,2871 79 2770,4 0,361 0,2014
4 638 1,5674 0,8746 30 1248,9 0,8007 0,4468 55 1974,5 0,5064 0,2826 80 2805,3 0,3565 0,1989
5 658,4 1,5188 0,8475 31 1275,4 0,784 0,4375 56 2006,2 0,4985 0,2782 81 2840,3 0,3521 0,1965
6 679 1,4728 0,8218 32 1302,2 0,7679 0,4285 57 2037,8 0,4907 0,2738 82 2875,3 0,3478 0,1941
7 700,1 1,4284 0,7971 33 1329,3 0,7523 0,4198 58 2069,5 0,4832 0,2696 83 2910,3 0,3436 0,1917
8 721,5 1,386 0,7734 34 1356,6 0,7371 0,4113 59 2101,3 0,4759 0,2656 84 2945,4 0,3395 0,1894
9 742,8 1,3462 0,7512 35 1384 0,7225 0,4032 60 2133,3 0,4688 0,2616 85 2980,6 0,3355 0,1872
10 764,7 0,3077 0,7297 36 1411,5 0,7085 0,3953 61 2165,4 0,4618 0,2577 86 3016,3 0,3315 0,185
И 786,6 0,2713 0,7094 37 1439,5 0,6947 0,3876 62 2198 0,455 0,2539 87 3052,7 0,3276 0,1828
12 808,9 0,2363 0,6899 38 1467,6 0,6814 0,3802 63 2230,7 0,4483 0,2502 88 3087,8 0,3239 0,1807
13 831,4 0,2028 0,6712 39 1496 0,6685 0,373 64 2263,4 0,4418 0,2465 89 3123,5 0,3202 0,1787
14 854 0,1709 0,6534 40 1524,5 0,656 0,3661 65 2296,4 0,4355 0,243 90 3159,2 0,3165 0,1766
15 876,9 0,1404 0,6363 41 1553 0,6439 0,3593 66 2329,4 0,4293 0,2396 91 3195,3 0,313 0,1747
16 900 1,1111 0,62 42 1582 0,6321 0,3527 67 2362,5 0,4233 0,2362 92 3231,3 0,3095 0,1727
17 923,5 1,0828 0,6042 43 1611,1 0,6207 0,3464 68 2395,7 0,4174 0,2329 93 3267,4 0,306 0,1707
18 947,1 1,0559 0,5892 44 1640,2 0,6097 0,3402 69 2429,1 0,4117 0,2297 94 3303,8 0,3027 0,1689
19 971 1,0299 0,5747 45 1670 0,5988 0,3341 70 2462,6 0,4061 0,2266 95 3340,1 0,2994 0,1671
20 995 1,005 0,5608 46 1699,7 0,5883 0,3283 71 2496,3 0,4006 0,2235 96 3376,5 0,2962 0,1653
21 1019,4 0,981 0,5474 47 1729,5 0,5782 0,3226 72 2530,2 0,3952 0,2205 97 3413 0,293 0,1635
22 1044 0,9579 0,5345 48 1759,5 0,5683 0,3171 73 2564,2 0,39 0,2176 98 3449,6 0,2899 0,1618
23 1068,6 0,9358 0,5222 49 1789,5 0,5588 0,3118 74 2598,2 3849 0,2148 99 3486,3 0,2868 0,16
24 25 1093,8 1119,1 0,9142 0,8937 0,5101 0,4987 50 1820 0,5494 0,3066 75 2632,5 0,3799 0,212 100 3523 0,2838 0,1584
Физические свойства важнейших веществ
514
Новый справочник химика и технолога
Таблица 3.11.2
Вязкость воды при температуре выше 100 °C и давлении насыщенного пара при указанной температуре*
Г, °C т| • 103, Па • с Г, °C т| • 10?, Па • с Г, °C г] • 10’, Па • с
101 0,282 109 0,259 160 0,178
102 0,279 НО 0,256 170 0,166
103 0,276 120 0,232 180 0,155
104 0,273 130 0,212 190 0,146
105 0,27 140 0,196 200 0,139
106 0,267 150 0,184 210 0,134
107 0,264 160 0,174 220 0,129
108 0,262 225 0,128
* Данные из другого источника выделены курсивом.
Таблица 3.11.3
Вязкость 1] и кинематическая вязкость v воды при различных значениях температуры и давления
Кинематическая вязкость v (м2/с) равна отношению вязкости жидкости р (Па • с) к се плотности р (кг/м3).
В таблице приведены значения вязкости, соответствующие рекомендованному национальным бюро стандартов США (NBS) значению вязкости воды 1,002 • 10 3 Па • с при 20 °C при давлении 101.3 кПа.
Т°С Давление, МПа
0,101 5.07 101 2.03 3,04
р • К)3. Па • с v • 106, м2/с р • К)3. Па • с v • 106. м2/с р • 103. Па • с v • 106. м2/с п • ю3, Па • с v • 10°, м2/с р • Ю3, Па • с v • 106, м2/с
0 1,792 1,792 1,781 1,776 1,77 1,761 1,748 1,731 1,726 1,702
10 1,307 1,307 1,301 1,299 1,296 1,29 1,289 1,276 1,281 1,266
20 1,002 1,004 1,001 1,001 1 0,997 0,998 0,991 0,995 0,984
30 0,797 0,801 0,797 0,799 0,798 0,798 0,798 0,795 0,8 0,792
40 0,653 0,658 0,653 0,657 0,654 0,656 0,656 0,656 0,658 0,655
50 0,546 0,553 0,547 0,553 0,549 0,553 0,552 0,554 0,555 0,555
60 0,466 0,474 0,468 0,475 0,469 0,475 0,472 0,476 0,476 0,478
70 0,404 0,413 0,406 0,414 0,408 0,415 0,411 0,418 0,416 0,42
80 0,355 0,365 0,358 0,367 0,361 0,37 0,366 0,373 0,372 0,377
90 0,315 0,326 0,319 0,329 0,324 0,334 0,33 0,339 0,337 0,345
100 0,282 0,295 0,287 0,299 0,293 0,304 0,301 0,311 0,309 0,318
200 0,139 0,161 0,141 0,162 0,145 0,165 0,149 0,169
300 0,094 0,132 0,096 0,131 0,099 0,132
400 0,043 0,13
Таблица 3.11.4
Относительная вязкость воды г при различных значениях температуры и давления
Давление, МПа Температура, °C
0 10.3 30 75
0,101 1 (0,779) (0,488) (0,222)
50,7 0,938 0,755 0,5 0,23
101,3 0,921 0,743 0,514 0,239
152,0 0,932 0,745 0,53 0,247
202,7 0,957 0,754 0,55 0,258
304,0 1,024 0,791 0,599 0,278
405,3 1,111 0,842 0,658 0,302
506,7 1,218 0,908 0,72 0,333
608,0 1,347 0,981 0,786 0,367
709,3 1,064 0,854 0,404
Физические свойства важнейших веществ
515
Окончание табл. 3.11.4
Давление. МПа Температура. °C
0 10,3 30 75
810,6 1,152 0,923 0,445
912,0 0,989 0,494
1013 1,058
1115 1,126
Таблица 3.11.5
Вязкость переохлажденной воды и окида дейтерия (тяжелой воды)
Переохлажденная вода Оксид дейтерия
7'. °C г] • 103, Па • с Т, °C г] • 10’, Па • с Т, °C т] • 10\ Па-с
-2 1,91 30 0,969 100 0,323
~4 2,05 45 0,713 125 0,252
-5 2,14 60 0,552 150 0,208
-6 2,22 75 0,445 175 0,175
-8 2,4 90 0,365 200 0,151
-10 2,6
Таблица 3.11.6
Вязкость простых веществ при различных значениях температуры
Т,°С т] 103, Па-с T. °C Г] • 103. Па • с Т °C г] • 103, Па • с Т. °C г] • 1 О ’, Па • с
Ag Cu 30 1,499 50,5 1,6
1167 3,02 1085 3,36 40 1,45 53,65 1,55
1200 2,98 1100 3,33 50 1,407 60,2 1,45
Bi 1150 3,22 60 1,367 69,7 1,32
304 1,662 1200 3,12 70 1,331 79,9 1,21
451 1,271 Fe 80 1,298 РЬ
600 1 97,5 Fe; 2,5 С 90 1,268 350 2,648
601 0,996 1350 2,65 100 1,24 400 2,315
Br2 1400 2,25 НО 1,214 450 2,057
0 1,253 97 Fe; 3 С 120 1,191 500 1,85
5 1,178 1300 2,8 130 1,169 550 1,681
10 1,107 1350 2,375 140 1,149 600 1,54
15 1,045 1400 2,025 150 1,13 650 1,438
20 0,991 96,5 Fe; 3,5 С 200 1,052 700 1,356
25 0,942 1250 2,9 250 0,995 750 1,29
30 0,897 1300 2,4 300 0,95 800 1,23
35 0,855 1350 2 340 0,921 850 1,18
40 0,817 1400 1,75 К S*
45 0,78 96 Fe; 4 С 100 0,466 123 10,94
50 0,746 1250 2,1 150 0,382 135,5 8,66
55 0,715 1300 1,75 200 0,324 149,5 7,09
60 0,686 1350 1,55 Na 156,3 7,19
Cd 1400 1,45 100 0,814 158,2 7,59
349 1,44 Hg 132 0,742 159,2 9,48
406 1,34 -20 1,855 183 0,635 159,5 14,45
466 1,27 -10 1,764 Р 160 22,83
506 1,18 0 1,685 43,2 1,73 160,3 77,32
550 1,15 10 1,615 45,05 1 7 165 500
603 1,1 20 1,554 48,1 1,64 171 4500
516
Новый справочник химика и технолога
Окончание табл. 3.11.6
Г, °C т] • 10\ Па • с Т. °C тр Ю3, Па с Т,°С г] • 1 О’, Па • с Г, °C г| • 10J. Па • с
S* 700 1,26 400 1,38 Zn
184 16000 750 1,16 450 1,27 450 3,168
190,5 19700 800 1,08 500 1,18 500 2,779
197,5 21300 850 1,05 550 1,11 550 2,476
200 21500 Sn 600 2,233
210 20500 240 1,91 600 1,05 650 2,033
217 19100 260 1,82 650 0,99 700 1,865
220 18600 280 1,74 700 0,94
Sb 300 1,67 750 0,91
650 1,5 350 1,51 800 0,87
* Значения до 160.3 °C (выделены курсивом) определены для очищенной, но содержащей газообразные вещества серы, остальные — для серы, нс содержащей газообразных веществ.
Таблица 3.11.7
Вязкость неорганических соединений при различных значениях температуры
Т, °C r| • 103, Па • c T, °C r| • 103, Па • c T, °C r| • 103, Па • c T, °C r| • 103, Па • c
AgBr HgBr2 410 12,41 15,36 0,4401
609 1,863 240 3,31 420 11,71 NaBr
649 1,661 247 2,97 430 11,05 762 1,42
688 1,487 258 1,97 440 10,42 766 1,35
770 1,217 KBr 450 9,8 780 1,28
803 1,192 745 1,48 460 9,2 NaCl
AgCI 775 1,34 470 8,62 825 1,432
603 1,606 805 1,19 480 8,06 850 1,275
632 1,466 KCI 490 7,52 875 1,138
669 1,372 790 1,42 500 6,99 900 1,017
734 1,186 835 1,21 510 6,49 925 0,912
Agl 920 0,99 LiNO3 950 0,82
605 3,026 1035 0,71 260 6,477 975 0,752
630 2,748 KNO3 270 6,26 1000 0,704
698 2,375 350 2,728 291 5,476 NaNO3
730 2,123 360 2,578 300 5,058 315 2,916
792 1,854 380 2,312 310 4,696 320 2,826
827 1,556 400 2,094 322 4,318 340 2,527
AgNO3 420 1,905 330 4,24 360 2,283
244 3,77 440 1,738 354 3,63 NaNO3
265 3,27 460 1,596 390 2,49 380 2,077
275 3,04 480 1,476 429 2,054 400 1,895
309 2,61 500 1,38 MgCl2 420 1,741
342 2,29 520 1,301 808 4,12 440 1,616
BiCl3 540 1,239 n2h4 460 1,518
260 32 550 1,211 5 1,21 NaOH
270 29,5 KOH 10 1,12 350 4
280 27 400 2,3 15 1,04 400 2,8
290 25 450 1,7 20 0,97 450 2,2
300 23 500 1,3 25 0,91 500 1,8
320 20,5 550 1 N2O4 550 1,5
340 18 600 0,8 0,72 0,522 NaPO3
CaCI2 K2Cr2O7 5,09 0,4954 650 1250
800 4,94 400 13,16 9,15 0,472 700 700
Физические свойства важнейших веществ
517
Окончание табл. 3.11.7
Т, °C г| • 103, Па • с Т, °C г| • 103, Па • с Т, °C г| • 103, Па • с Г, °C г| • 103, Па • с
750 440 412 6,97 538 4,02 50 0,668
800 300 432 6,13 558 3,59 UF6
850 210 452 5,38 578 3,28 70 0,91
Na3AIF6 472 4,7 598 3,06 80 0,86
1000 2,8 492 4,07 608 2,95 90 0,76
РЬВг2 РЬС12 SnCI4
372 392 10,2 8,06 498 518 5,53 4,66 30 40 0,806 0,725
Таблица 3.11.8
Вязкость некоторых твердых веществ при различных значениях температуры
Т, °C т|, Па • с
Алюминий
9 7,50 • 1012
Глюкоза
22 9,10 • 10,()
30 6,60 • 108
40 2,80 • 106
50 3,00 • 104
60 930
70 63,0
80 6,60
90 1,05
100 0,25
НО 0,08
120 0,032
130 0,0145
Окончание табл. 3.11.8
Г, °C г|, Па • с
140 0,0076
Лед
-14 8,50 • 10'°
0 1,00 • ю'°
Ментол
14,9 2,00 • 10У
26,1 3,12 • 108
34 6,15 • 1.07
37,2 2,41 • 107
Олово
9 2,40 • 1012
Сахароза
109 2800
125 190
Цинк
9 3,30 • 101’
Таблица 3.11.9
Вязкость углеводородов (р • 103, Па • с) при различных значениях температуры
Алканы
Формула Название Температура, °C
-90 -50 -20 0 10 20 40 60 80 100 120 150
с4н10 Бутан 0,63 0,355 0,252 0,207 0,191 0,174 0,146
С4Н]о 2-Метилпропан (изобутан) 0,392 0,267 0,214 0,195 0,176 0,146
С5н12 2,2-Диметилпропан (неопентан) 0,327 0,28
С5н12 2-Мстилбутан (изопентан) 0,55 0,353 0,277 0,248 0,224
С5Н12 Пентан 0,948 0,474 0,341 0,283 0,259 0,24
С6Н]4 Гексан 1,82 0,742 0,479 0,381 0,343 0,307 0,253 0,222
Сбн14 2-Метилпентан (изогексан) 0,37 0,331 0,298 0,246 0,206
С7н16 Г ептан 3,85 1,18 0,689 0,526 0,466 0,417 0,339 0,283 0,241 0,209
с7н16 2-Метилгсксан (изогептан) 0,476 0,424 0,379 0,309 0,257 0,216
С8н18 Октан 1,83 0,967 0,714 0,622 0,546 0,435 0,356 0,298 0,255 0,22
С9Н20 Нонан 2,99 1,4 0,968 0.827 0,714 0,555 0,445 0,366 0,308 0,264 0,213
СюН22 Декан 1,93 1,27 1,07 0,907 0,701 0,552 0,448 0,372 0,314 0,244
СцН24 Ундекан 2,779 1,742 1,425 1,182 0,871 0,671 0,535 0,437 0,365 0,288
Продолжение табл. 3.11.9
Алканы
Формула Название Температура, °C
0 10 20 40 60 80 100 120 150 200 250 300
С12Н26 Додекан 2,264 1,827 1,492 1,064 0,803 0,632 0,51 429 334 0,231
СыН28 Тридекан 2,962 2,339 1,878 1,312 0,969 0,751 0,598 0,494 0,38 0,262
С14Нзо Тетрадекан 2,96 2,322 1,56 1,135 0,868 0,685 0,565 0,431 0,294 0,207
С]зНз2 Пентадекан 3,663 2,841 1,873 1,335 1,01 0,786 0,64 0,483 0,326 0,231
с16н34 Гексадскан 3,451 2,232 1,56 1,161 0,892 0,716 0,532 0,349 0,242
С]7Нзб Гептадекан 4,209 2,652 1,829 1,34 1,014 0,794 0,598 0,392 0,277 0,203
С]8Нз8 Октадекан 3,06 2,06 1,484 0,952
С|9Н4о Нонадекан 3,588 2,379 1,693 1,269 989 0,719 0,468 0,327 0,24
С2оН42 Эйкозан 4,072 2,665 1,88 1,403 1,094 0,789 0,505 0,353 0,26
Новый справочник химика и технолога
Продолжение табл. 3.11.9
Алкены и алкадиены
Формула Название Температура, °C
0 10 20 30 40 50 60 70 80 90 100 115
с5н8 2-Метилбута-1,3-диен (изопрен) 0,26 0,236 0,216 0,198
С6н12 Гекс-1-ен 0,33 0,29 0,26 0,24 0,22 0,2 0,19
с7н14 Гепт-1-ен 0,44 0,39 0,35 0,32 0,29 0,27 0,25 0,23 0,22 0,2
С8н16 Окт-1 -ен 0,613 0,533 0,47 0,425 0,383 0,347 0,317 0,292 0,271 0,251 0,235 0,22
С9н18 Нон-1-ен 0,839 0,715 0,62 0,552 0,492 0,441 0,399 0,364 0,336 0,307 0,285 0,26
СюН2о Дец-1-ен 1,13 0,945 0,803 0,7 0,613 0,547 0,488 0,442 0,399 0,371 0,342 0,3
С15Н30 Пентадец-1 -ен 4,161 3,21 2,52 2,052 1,694 1,432 1,224 1,064 0,937 0,826 0,735 0,62
С2оН4о Эйкоз-1 -ен 4,77 3,77 3,05 2,52 2,12 1,81 1,55 1,35 1,1
Продолжение табл. 3.11.9
Циклоалканы
Формула Название Температура, °C
-20 -10 0 10 20 30 40 50 60 80 100 ПО
с5н10 Циклопентан 0,72 0,631 0,555 491 0,439 0,393 0,354 0,323
С6Н12 Метилциклопентан 0.86 0,745 0,648 0,569 0,505 0,45 0,404 0,365 0,33
с6н12 Циклогексан 1,18 979 0,826 0,704 0,608 0,531 0,411
с7н14 Метилциклогексан 1,41 1,175 0,991 0,847 0,731 0,639 0,562 0,5 0,446 0,36 0,3
с7н14 Этилциклопентан 0,96 0,829 0,725 0,637 0,565 0,506 0,456 0.412 0,376 0,32 0,27
С8Н16 Пропилциклопентан 1,24 1,049 0,886 0,772 0,679 0,603 0,538 0,488 0,444 0,38 0,33 0,3
с8н16 Этилциклогексан 1,63 1,356 1,142 0,976 0,843 0,737 0,651 0,581 0,523 0,43 0,37 0,34
C2iH42 Г ексадецилциклопентан 9,63 7,28 5,56 4,43 3,55 2,45 1.84 1,58
C2iH42 Пентадецилциклогексан 8,91 6,69 5,21 4,15 2,74 1,87 1,57
Продолжение табл. 3.11.9
Арены
Формула Название Температура. °C
-20 -10 0 10 20 30 40 60 80 100 120 150
С6Нб Бензол 0,755 0,649 0,559 0,489 0,389 0,318 0,261 0,22 0,169
С7н8 Толуол 0,989 0,863 0,77 0,667 0,584 0,517 0,469 0,381 0,318 0,269
СзНю Этилбензол 1,17 1,021 0,873 0,757 0,671 0,596 0,53 0,436 0,363 0,308 0,265
С8Н10 о-Ксилол 1,447 1,232 1,055 0,917 0,804 0,707 0,623 0,5 0,417 0,345 0,294
Физические свойства важнейших веществ 519
Окончание табл. 3.11.9
Формула Название Температура, °C
-20 -10 0 10 20 30 40 60 80 100 120 150
с8н10 л/-Ксилол 0,805 0,699 0,615 0,548 0,49 0,405 0,34 0,29 0,25
С8Н1О и-Ксилол 0,648 0,571 0,514 0,416 0,354 0,293 0,25
СюН14 Бутилбензол 2,23 1,79 1,466 1,204 1,02 0,88 0,767 0,608 0,492 0,411 0,35 0,28
Ci2Hi8 Гексилбензол 5,17 3,66 2,6 1,98 1,63 1,362 1,162 0,909 0,712 0,574 0,47 0,36
С16Н26 Децилбензол 16 9,81 6,72 4,94 3,8 3,02 2,46 1,73 1,275 0,977 0,77 0,56
С20Н34 Т етрадецилбензол 10,63 7,65 5,66 4,43 2,9 2,06 1,507 1,14 0,79
Примечания: 1. Курсивом выделены значения вязкости при давлении насыщенного пара выше нормальной точки кипения.
2. Дифенил, нафталин, тетралин и декалин см. в табл. 3.11.10
520 Новый справочник химика и технолога
Физические свойства важнейших веществ
521
Таблица 3.11.10
Вязкость органических соединений*
т °с т| • 103, Па • с Т °с т| • 103, Па • с Т, °C т| • I О3, Па • с Т, °C г| • 103, Па • с
СС14 Тетрахлорметан (четыреххлористый углерод) СН2Вг2 Дибромметан 15 20 30 40 0,518 0,500 0,460 0,424 10 20 25 30 40 50 60 80 100 120 5,000 3,750 3,300 2,940 2,430 2,040 1,710 1,170 0,830 0,630
15 30 0,109 0,092
-10 0 10 15 20 30 40 50 60 70 80 90 100 120 140 160 180 1,680 1,330 1,130 1,038 0,969 0,840 0,739 0,651 0,585 0,524 0,468 0,426 0,384 0,323 0,276 0,234 0,201
СН2С12 Дихлорметан CH3NO2 Нитрометан
-20 -10 0 10 15 20 30 40 0,680 0,602 0,537 0,481 0,449 0,435 0,393 0,363 0 10 15 20 25 30 40 50 60 70 80 85 0,850 0,740 0,697 0,660 0,627 0.595 0,530 0,478 0,433 0,392 0,357 0,343
С2С14 Тетрахлорэтилен
0 10 20 30 40 50 60 80 100 120 1,140 1,000 0,880 0,800 0,720 0,660 0,600 0,510 0,441 0.383
СН2О2 Муравьиная кислота
7,59 10 15 20 30 40 50 60 70 80 100 2,387 2,262 1,970 1,804 1,460 1,219 1,025 0,890 0,780 0,680 0,549
СН4О Метанол
-100 -80 -70 -60 -50 -40 -30 -20 -10 0 10 15 20 25 30 40 50 60 16,000 5,700 4,020 2,980 2,260 1,750 1,400 1,160 0,970 0,817 0,690 0,623 0,597 0,547 0,510 0,450 0,396 0,350
Ди суды cs2 >ид углерода
-10 0 15 20 30 40 50 0,495 0,433 0,381 0,365 0,341 0,319 0,297
С2НС13 Трихлорэтилен
-10 0 10 20 25 30 40 50 60 75 0,790 0,710 0,640 0,580 0,550 0,530 0,480 0,446 0,410 0,371
СН3С1 Хлорметан
0 10 20 30 40 50 60 70 80 90 100 120 130 0,221 0,202 0,183 0,166 0,152 0,140 0,129 0,118 0,108 0,099 0,089 0,072 0,063
СНВгз Трибромметан (бромоформ)
25 1,890
СНС13 Трихлорметан (хлороформ)
-13 0 10 15 20 30 40 50 60 0,860 0,700 0,630 0,596 0,570 0,514 0,466 0,426 0,390
С2Н2С14 1,1,2,2-Тетрахлорэтан
ch5n Метанамин (метиламин)
15 30 1,840 1,460
0 0,236 С2Н3С13 1,1,1-Трихлорэтан
СН31 Иодметан ch5no Формамид
15 30 0,910 1,010
0 0,606 0 7,500
522
Новый справочник химика и технолога
Продолжение табл. 3.11.10
Т, °C г| • 103, Па • с Т, °C т| • 103, Па • с Т, °C т| • 103, Па • с Г, °C т| • 103, Па • с
с 2Н3С13 0 0,320 С2Н5С1 75 0,471
1,1,2-Трихлорэтан С2Н4О2 Хл орэтан С2н6о2
15 1,230 Метилформиат -20 0,392 Этиленгликоль
30 1,010 0 0,429 -10 0,354 20 19,900
c2h3n 10 0,385 0 0,320 30 13,200
Ацетонитрил 15 0,362 10 0,291 40 9,130
0 0,442 20 0,348 20 0,266 60 4,950
15 0,375 25 0,330 30 0,244 80 3,020
30 0,325 30 0,318 40 0,224 100 1,990
С2Н4Вг2 С 2Н4О2 с2н51 120 1,400
1,2-Дибромэтан Уксусная кислота Иодэтан 130 1 200
0 2,422 10 1,450 0 0,727 140 1,040
10 2,030 15 1,310 15 0,617 —
20 1,710 20 1,210 20 0 592 С2Н6э
Диметилсульфид
30 1,470 30 1,040 30 0,540 —
0 0,361
40 1,280 40 0,900 40 0,495
10 0,329
50 1,120 50 0,790 70 0,391
20 0,301
60 0,995 60 0,700 С, Hz О
30 0,277
80 0,800 70 0,620 Этанол
100 0,670 80 0,560 -98,1 44,000 c2h7n
120 0,560 90 0,500 -90 28,500 ^V-Метил метанамин
С гН4С12 100 0,460 -80 18,100 (диме тилам ин)
1,2-Дихлорэтан 110 0,420 -70 12,500 -33 0,437
0 1,123 С2Н5Вг -60 8,700 0 0,236
10 0,962 Бромэтан -50 6,400 C2H7NO
15 0,887 -120 5,600 -40 4,790 Ацетамид
20 0,832 -100 2,890 -30 3,650 105 1,320
30 0,730 -90 2,250 -20 2,780 120 1,060
40 0,644 -80 1,810 -10 2,230 С3Н5Вг
50 0,568 0 0,487 0 1,773 З-Бромпроп-1 -ен
60 0,519 10 0.441 5 1,623 0 0,626
70 0,469 15 0,418 10 1,466 20 0,504
80 0,417 20 0,400 15 1,332 40 0,419
С2Н4О 30 0,348 20 1,200 70 0,328
Ацетальдегид 40 0,321 25 1,096 С3Н5С1
— З-Хлорпроп-1-ен
0 0,276 50 0,293 30 1,003 —
0 0,413
10 0,253 60 0,268 35 0,914
15 0,347
20 0,225 70 0,248 40 0,834 20 0 337
С2Н4О 80 0,230 45 0,764 30 0,300
Оксиран 90 0,213 50 0,702 40 0,282
(окись этилена) 100 0,199 55 0,644 г
-49,8 0 577 120 0,173 60 0,592
З-Иодпроп-1-ен
-38,2 0,488 140 0,149 65 0,551 0 0,936
-21 0,394 160 0,126 70 0,504 20 0,734
Физические свойства важнейших веществ
523
Продолжение табл. 3.11.10
Г, °C т] • 103, Па • с Т, °C т] • 103, Па • с Г, °C т] • 10J, Па • с Т,°С т] • 103, Па • с
40 100 0,597 0,365 10 15 20 25 30 40 50 60 70 80 90 100 ПО 120 130 140 0,425 0,402 0,381 0,362 0,344 0,312 0,284 0,258 0,237 0,217 0,198 0,182 0,166 0,154 0,142 0,130 С3Н7Вг 1-Бромпропан 70 80 1,810 1,460
C3H5N3O9 Пропан-1,2,3-триилтринитрат (нитроглицерин) 0 15 20 30 40 0,651 0,539 0,524 0,459 0,433 с3н8о Пропан-1-ол
-60 -50 -40 -30 -20 -10 0 10 15 20 30 40 50 60 70 80 90 100 31,600 20,200 13,500 9,500 6,900 5,100 3,883 2,897 2,520 2,720 2,234 2,400 1,129 0,921 0,758 0,628 0,526 0,443
10 20 30 40 50 60 69,200 36,000 21,000 13,600 9,400 6,800
С3Н7Вг 2-Бромпропан
0 15 20 30 40 50 0,605 0,536 0,482 0,437 0,394 0,359
с3н6о Ацетон
-90 -80 -70 -60 -50 -40 -30 -20 -10 0 10 20 30 40 50 60 2,075 1,507 1,205 0,982 0,822 0,713 0,612 0,513 0,447 0,397 0,361 0,325 0,296 0,271 0,249 0,228
С3Н7С1 1-Хлорпропан
с3н6о2 Пропионовая кислота
0 10 15 20 25 30 40 45 0,436 0,390 0,370 0,352 0,335 0,319 0,231 0,278
0 10 15 20 30 40 50 60 70 80 90 100 120 140 1,520 1,289 1,180 1,100 0,958 0,840 0,746 0,662 0,601 0,545 0,496 0,452 0,379 0,322
С3Н8О Пропан-2-ол
-60 -50 -40 -30 -20 -10 0 10 15 20 30 40 50 60 70 80 66,100 37,600 23,200 14,900 10,100 6,800 4,600 3,260 2,860 2,390 1,770 1,330 1,030 0,800 0,650 0,520
С3Н7С1 2-Хлорпропан
0 10 15 20 30 0,402 0,358 0,335 0,322 0,286
С3Н6О Проп-2-ен-1-ол
0 15 20 30 40 70 90 2,145 1,490 1,363 1,070 0,914 0,553 0,410 С3Н71 1-Иодпропан
с3н6о2 Этилформиат
0 20 40 100 0,943 0,744 0,607 0,371
0 10 15 20 25 30 40 50 0,510 0,450 0,419 0,402 0,382 0,358 0,329 0,308
с3н71 2-Иодпропан
С3Н6О Пропиональдегид
0 20 40 80 0,884 0,697 0,568 0,400
С3Н8О3 Глицерин
0 20 40 0,470 0,410 0,330
С3н6о3 2-Гидроксипропановая кислота (молочная кислота) -42 -36 -25 -20 -15,4 6 710 000 2 050 000 262 000 134 000 66 500
с3н6о2 Метилацет ат c3h7no2 Этилкарбамат (уретан)
0 5 0,479 0,450
25 40,330 60 2,360
524
Новый справочник химика и технолога
Продолжение табл. 3.11.10
Т, °C т| • 103, Па • с Т, °C т| • 103, Па • с Т, °C т| • 103, Па • с Т, °C т| • 103, Па • с
С3Н8О3 80 0,248 10 0,512 30 0,363
Глицерин с4н8о2 15 0,473 С4Н91
-10,8 35 500 1,4-Диоксан 20 0,458 1-Иодбутан
-4,2 14 900 20 1,255 30 0,403 15 0,918
0 12 110 30 1,063 40 0,360 30 0,777
10 3950 40 0,917 50 0,324 С4Н91
15 2330 50 0,778 60 0,294 1-Иод-2-метил пропан
20 1490 60 0,685 70 0,269 15 0,945
25 954 70 0,606 80 0,246 30 0,777
30 629 80 0,539 90 0,226 С 4Н]оО
c3h9n С лНеОт 100 0,208 Бутан-1-ол
Л,Л-Ди\1е1ил\1етана\1ин Изомасляная кислота 120 0,178 -50 34,700
(триметиламин) 0 1 887 140 0 153 -40 22,400
-33,5 0,321 10 1,568 160 0 129 -30 14,600
c3h9n 15 1,440 180 0,109 -20 10,300
Пропан-1-амин 20 1,318 190 0,100 -10 7,400
(пропиламин) 5,190
О 30 1,129 С4Н9Вг 0
V,3 3 3 40 0,980 1-Бромбутан 10 3,870
Тиофен 50 0,862 15 0,626 15 3,379
0 0,871 70 0,683 30 0,532 20 2,950
10 0,753 100 0,501 С4Н9Вг 30 2,280
20 0,658 150 0,326 2-Бр омбутан 40 1,780
30 0,582 С дН8О2 15 0,618 50 1,410
40 0,520 Масляная кислота 30 0,526 60 1,133
50 0,468 0 2,260 С4Н9Вг 70 0,926
60 0 424 10 1,875 1 -Бром-2-метил пропан 80 0,762
70 0,386 20 1,560 15 0,679 90 0,634
80 0,352 30 1,303 30 0,567 100 0,532
С 4Н6О3 40 1,114 С4Н9Вг 120 0,394
Уксусный ангидрид 50 0,972 2-Бром-2-метилпропан С 4HioO
0 1,245 60 0,851 15 0,883 Бутан-2-ол
10 1,058 70 0,756 30 0,702 15 4,210
15 0,975 90 0,605 С4Н9С1 30 3,180
20 0,907 100 0,545 2-Метил-1-хлорпропан С 4Н10О
30 0,787 ПО 0,493 15 0,471 Диэтиловый эфир
40 0,699 120 0,449 30 0,395 -110 2,560
50 0,623 140 0,373 C4Hi)CI -100 1,690
60 0,550 160 0,319 2-Метил- 2-хлорпропан -90 1,240
70 0,507 С дН8О2 15 0,543 -80 0,958
80 0,453 Метил пропионат 30 0,439 -60 0,637
100 0,387 0 0,586 С4Н9С1 -40 0,461
120 0,320 20 0,460 1-Х. юрбутан -30 0,410
С 4Н8О 40 0,375 15 0,469 -20 0,362
Бутан-2-он 70 0,286 30 0,405 -10 0,323
0 0,543 С 4н8о2 С4Н9С1 0 0,284
20 0,428 Этилацстат 2-Хлорбутан 17 0,240
40 0,349 0 0,582 15 0,439 20 0,233
Физические свойства важнейших веществ
525
Продолжение табл. 3.11.10
Т,°С т| • 103, Па-с Т, °C т| • 103, Па • с Г, °C т| • 10J, Па • с Г, °C т| • 103, Па • с
25 30 40 60 80 100 0,222 0,213 0,197 0,166 0,140 0,118 с5н4о 2-Фуральдегид (фурфурол) 70 90 0,986 0,753 10 20 30 40 50 0,346 0,313 0,284 0,260 0,239
С5НюО2 Пропилацет ат
0 25 2,480 1,490
0 10 20 30 40 50 60 70 80 90 100 0,769 0,664 0,585 0,510 0,455 0,408 0,368 0,333 0,303 0,276 0,252
c5h5n Пиридин С5Н12О Пентан-1-ол
С4н10о 2-Метилпропан-1-ол
0 10 20 30 40 50 60 70 80 90 1,330 1,120 0,974 0,830 0,735 0,651 0,580 0,528 0,482 0,443 15 30 4,650 2,990
-40 -30 -20 -10 0 10 20 30 40 50 60 80 100 51,300 29,900 18,400 12,300 8,300 5,650 3,950 2,880 2,120 1,610 1,240 0,780 0,520
С5Н12О 1-Этоксипропан
0 10 20 30 40 50 0,402 0,360 0,324 0,294 0,268 0,245
CsHjo02 Этилпропионат
с5н8о2 Пентан-2,4-дион (ацетилацетон) 0 15 20 30 40 90 0,696 0,564 0,537 0,473 0,428 0,270 c5h,3n З-Метилбутан-1-амин
25 0,724
0 25 1,090 0,788 С6Н5Вг Бромбензол
С4н10о 1 -Метоксипропан
с5н10о Пентан-2-он 0 10 15 20 30 40 50 60 80 100 142,5 1,520 1,310 1,196 1,130 0,990 0,890 0,790 0,720 0,600 0,520 0,370
Q5H10O3 Диэтилкарбонат
0 10 20 30 0,314 0,285 0,260 0,237 0 20 40 100 0,648 0,500 0,410 0,247
15 30 0,868 0,698
С5Н10О3 Этил-2-гидрокси-пропаноат
c4H10s Диэтилсульфид с5н10о Пентан-З-он
0 10 20 30 40 60 80 100 5,300 3,680 2,680 2,040 1,610 1,080 0,780 0,560
0 10 20 30 40 50 70 0,563 0,501 0,450 0,407 0,369 0,338 0,287 15 30 0,493 0,423
с5н10о2 З-Метилбутановая кислота (изовалериано-вая кислота)
С6Н5С1 Хлорбензол
0 10 15 20 30 40 50 60 70 80 90 100 1,056 0,915 0,844 0,802 0,708 0,635 0,573 0,520 0,476 0,437 0,400 0,370
15 30 2,730 1.970
C4HnN 2-Метилпропан-1-амин (изобутиламин)
c5HnF 1-Фторпентан
CsHio02 Пентановая кислота (валериановая кислота)
20 30 40 50 60 0,372 0,335 0,304 0,278 0,253
25 0,553
C4HnN Л-Этилэтанамин (диэтиламин)
15 20 25 30 50 2,360 2,300 2,050 1,770 1,310
-33,5 25 35 0,824 0,350 0,279 С5Н12О 2-Мегил-1 -ме1 оксибутан
0 0,387
526
Новый справочник химика и технолога
Продолжение табл. 3.11.10
Т,°С г| • 103, Па • с Т,°С г| • 10J, Па • с Т, °C г| • 103, Па • с Т, °C г| • 10?, Па • с
С6Н5С1 Хлорбензол 140 0,510 30 40 50 60 2,090 1,700 1,410 1,200 С6Н10О3 Пропионовый ангидрид
c6h5no2 Нитробензол
НО 120 140 160 180 200 220 240 0,339 0,313 0,274 0,239 0,209 0,185 0,163 0,144 0 10 20 30 40 50 60 80 100 120 140 160 1,610 1,330 1,120 0.960 0,830 0,730 0,650 0,520 0,430 0,360 0,306 0,246
0 3 5 10 15 20 30 40 50 60 70 80 90 100 125 150 175 200 207,6 3,090 2,907 2,771 2,483 2,239 2,034 1,682 1,438 1,251 1,094 0,970 0,875 0,779 0,718 0,573 0,472 0,397 0,339 0,324
C6H6FN 3-Фгора нилин
25 30 40 50 60 2,480 2,200 1,750 1,480 1,250
с6н5сю 2-Хлофенол
C6H6FN 4-Фторанилин
25 50 4,110 2,015
20 30 40 50 60 3,030 2,370 1,930 1,580 1,340
с6н5сю З-Хлофенол С6н|0о4 Диэтилоксалат
25 50 11,550 3,980
15 30 2,310 1,620
с6н5сю 4-Хлофенол С6Н6О Фенол
с6н12о Циклогексанол
50 4,990 20 30 40 50 60 70 80 90 100 120 140 11,600 7,000 4,770 3,420 2,600 2,000 1,600 1,310 1,050 0,780 0,690
15 20 30 40 50 60 80 97,000 68,000 36,100 20,300 12,100 7,800 3,500
c6h5f Фторбензол
c6h5no3 2-Нитрофенол
0 10 20 30 40 50 60 80 100 120 140 160 180 0,745 0,646 0,584 0,519 0,471 0,427 0,388 0,327 0,275 0,231 0,198 0,168 0,144
45 23,430
C6H6BrN 2-Броманилин
40 60 80 100 3,190 2,160 1,540 1,190
С6н12о2 Бутилацетат
0 10 20 30 40 60 80 100 1,004 0,851 0,732 0,637 0,563 0,448 0,366 0,304
C6H6BrN З-Броманилин с6н7х Анилин
20 30 40 60 80 100 6,810 4,900 3,700 2,380 1,700 1,310 -5 0 10 20 30 40 50 60 70 80 90 100 ПО 120 13,400 10,200 6,460 4,400 3,200 2,350 1,820 1,520 1,280 1,100 0,940 0,825 0,730 0,657
с6н51 Иодбензол
10 20 30 40 50 60 80 100 120 1,970 1,690 1,450 1,260 1,120 0,990 0,810 0,690 0,580 С6н12о2 Гексановая кислота (капроновая кислота)
C6H6BrN 4-Броманилин
70 80 100 2,130 1,810 1,380 20 25 40 50 70 90 3,230 2,840 2,120 1,750 1,290 0,980
C6H6FN 2-Фторанилин
20 2,580
Физические свойства важнейших веществ
527
Продолжение табл. 3.11.10
Т, °C г| • 103, Па • с Г, °C г| • 10J, Па • с Т, °C r| • 103, Па • с Г, °C г| • 103, Па • с
с6н12о2 Изобутилацетат С7н6о3 2-Гидроксибензойная кислота (салициловая кислота) 10 20 30 40 60 80 100 1,010 0,880 0,760 0,680 0,550 0,460 0,390 C7H7NO2 1-Метил-З-нитробензол
20 78 100 130 0,710 0,370 0,290 0,220 20 30 40 60 80 100 2,330 1,910 1,600 1,180 0,920 0,750
10 20 40 3,200 2,710 1,810
С6н12о2 Этилбутират
С7Н7Вг 1 -Бром-2-метилбензол
С7Н7С1 1 -Метил-4-хл орбензол
C7H7NO2 1-Метил-4-нитробензол
15 25 30 50 70 0,711 0,628 0,595 0,466 0,381 0 10 20 30 40 60 80 100 2,210 1,810 1,510 1,290 1,120 0,870 0,710 0,590
10 20 30 40 60 80 100 1,030 0,890 0,780 0,700 0,560 0,470 0,400
60 80 100 1,200 0,940 0,760
с7н8о о-Крезол
С6Н14О Дипропиловый эфир
0 10 20 30 40 60 80 ПО 39,700 17,900 9,560 6,120 4,100 2,240 1,430 0,890
0 10 15 20 30 40 50 70 0,544 0,479 0,448 0,425 0,381 0,344 0,311 0,260
c7h7f 1 -Метил-2-фторбензол
С7Н7Вг 1 -Бром-З-метилбензол
20 30 40 50 60 0,680 0,601 0,538 0,481 0,434
0 10 20 30 40 60 80 100 1,730 1,450 1,250 1,080 0,960 0,760 0,630 0,530
с7н8о м-Крезол
с6н14о 2-Метил-1-этоксипропан c7h7f 1 -Метил-З-фторбензол
0 10 20 30 40 50 70 0,487 0,430 0,384 0,345 0,311 0,284 0,237 20 30 40 50 60 0,608 0,534 0,481 0,434 0,400 0 10 20 30 40 60 80 НО 84,400 34,600 16,900 9,470 5,920 2,990 1,800 1,020
С7Н7Вг 1 -Бром-4-метил бензол
30 40 60 80 100 1,095 0,964 0,768 0,630 0,531
c7h7f 1 -Метил-4-фторбензол
c6h15n АТУ-Диэтил этанам ин (триэтиламин) 20 30 40 50 60 1,340 1,110 0,950 0,820 0,720
с7н8о w-Крезол
С7Н7С1 1-Метил-2-хлорбензол
-33,5 25 0,773 0,363 0 10 20 30 40 60 80 НО 98,400 39,600 18,900 10,500 6,540 3,280 1,930 1,080
0 10 20 30 40 60 80 100 1,400 1,190 1,020 0,890 0,790 0,630 0,520 0,440
c7h5n Бензонитрил C7H7NO2 1 -Метил-2-нитробензол
0 25 40 50 70 1,950 1,240 1,000 0,876 0,666 0 10 20 30 40 60 80 100 3,830 2,960 2,370 1,940 1,630 1,210 0,940 0,760
с7н8о Фенилметанол (бензиловый спирт)
С7Н6О Бензальдегид С7Н7С1 1-Метил-З-хлорбензол
25 1,390 0 1,180 20 5,800
528
Новый справочник химика и технолога
Продолжение табл. 3.11.10
Т, °C т| • 1 О’, Па • с Т, °C г| • 103, Па • с Г, °C г| • 10’, Па • с Т, °C г| • 1 О ’, Па • с
С7н8о Фенилметанол (бензиловый спирт) 130 150 175 0,520 0,490 0,420 С7н14о2 Этилпентаноат 90 98 0,579 0,537
0 10 20 30 40 60 80 100 1,150 0,966 0,832 0,724 0,635 0,504 0,414 0,346 C8HhN /V-Этиланилин
25 30 35 40 45 50 5,054 4,326 3,739 3,288 2,906 2,574 c7h9n 1-Фенил метанамин (бензиламин)
10 20 40 60 80 90 100 2,979 2,251 1,434 1,013 0,766 0,674 0.603
25 130 1,590 0,442
с7н12о4 Диэтилмалонат (малоновый эфир)
c7h9n /V-Метиланилин
С7н16о Гептан-1-ол
0,3 10 20 30 40 50 70 4,265 3,065 2,303 1,811 1,466 1,215 0,886 15 30 2,380 1,750 С8н16о2 Бутилбутират
20 30 50 80 90 6,600 4,800 2,500 1,200 1,000
С7Н14О Гептаналь (энантовый альдегид) 0 10 20 30 40 60 80 100 1,440 1,200 1,010 0,871 0,760 0,594 0,478 0,395
15 30 0,977 0,791
С8н8о 1-Фенил этанон (ацетофенон)
c7h9n «-Толуидин с7н14о2 Бутилпропионат
0 10 20 30 40 50 60 80 100 10,200 6,400 4,350 3,200 2,440 1,940 1,570 1,110 0,830 0 10 20 30 40 60 80 100 1,155 0,975 0,835 0,726 0,639 0,510 0,413 0,343 16 25 50 95 1,990 1,670 1,240 0,653
С8н18о Дибутиловый эфир
С8н8о2 Метилбензоат 0 10 20 30 40 60 80 100 0,940 0,800 0,690 0,610 0,540 0,429 0,350 0,293
20 2,060
С8н8о2 Фенил ацет ат
С7н14о2 Гептановая кислота (энантовая кислота)
c7h9n jw-Толуидин
45 1,800
C8H9NO /V-Фенилацетамид (ацетанилид)
0 10 20 30 40 60 80 100 8,660 5,510 3,810 2,790 2,140 1,400 1,000 0,770 10 20 30 40 60 80 100 120 5,620 4,340 3,400 2,740 1,890 1,380 1,056 0,820
С8н18о Октан-Пол
120 130 2,220 1,900 15 30 10,600 6,100
c8HnN АТУ-Диметиланилин С9н10о2 Бензилацет ат
0 10 20 30 40 50 60 70 80 2,020 1,690 1,410 1,200 1,020 0,905 0,800 0,714 0,642 45 1,399
c7h9n и-Толуидин С7н14о2 (З-Метилбутил)ацетат С9Нк)О2 Этилбензоат
40 50 60 80 100 125 2,080 1,800 1,330 1,020 0,770 0,580 0 20 1,030 0,870 10 15 20 25 50 75 2,880 2,550 2,240 2,000 1,280 0,950
С7н14о2 Пентилацетат
11 45 1,580 0,805
Физические свойства важнейших веществ
529
Продолжение табл. 3.11.10
Т,°С т| • 10 ’, Па • с Т, °C п • 103, Па-С Т, °C г] • 103, Па • с Т, °C г| • 103, Па • с
С9Н10Оз Этил-2-гидроксибензоат (этил сап и цил ат) 25 50 75 2,000 1,300 0,970 43,4 56,9 55,6 74,6 82,2 99 13,680 6,890 6,280 2,470 1,850 1,040 C12HnN А-Фениланилин (дифениламин)
СюН12О 1 -Фенилбутан-1 -он 55 130 4,660 1,040
45 1,800
С9Н14О6 Триацетин
0 10 20 30 40 60 80 100 4,070 3,030 2,360 1,890 1,560 1,130 0,870 0,690 С12Н24О2 Додекановая кислота (лауриновая кислота)
С10н22о Бис(З-метилбутиловый) эфир
17 28,000
С9Н18О2 Бутилпентаноат 50 60 80 100 120 140 160 6,880 5,370 3,510 2,460 1,790 1,350 1,040
0 10 20 30 40 60 80 100 1,790 1,470 1,230 1,050 0,910 0,700 0,560 0,460 0 10 20 30 40 60 80 100 1,460 1,200 1,010 0,870 0,750 0,580 0,470 0,380
CjoHi202 4-Аллил-2-метоксифенол (эвгенол)
c12h27n А,А-Дибутилбутан-1-амин (трибутиламин)
0 10 20 30 40 60 80 100 29,900 15,200 9,220 5,990 4,220 2,430 1,590 1,150
С9Н18О2 Гептилацетат Сн)Н22О Дипентиловый эфир 0 10 20 30 40 60 80 100 2,240 1,740 1,410 1,170 0,990 0,740 0,570 0,460
0 10 20 30 40 60 80 100 2,320 1,850 1,520 1,270 1,090 0,830 0,650 0,540
0 10 20 30 40 60 80 100 1,580 1,290 1,080 0,920 0,800 0,620 0,490 0,410
C10H15N А, А-Д иэти л ан ил и н
С13Н10О Бензофенон
С9Н]8О2 Пентилбутират 0,5 10 20 40 60 80 98 3,841 2,850 2,185 1,425 1,021 0,777 0.630
СцН20О4 Дибутилмалонат 55 75 120 155 180 250 4,790 2,900 1,380 0,910 0,720 0,420
0 10 20 30 40 60 80 100 1,770 1,450 1,210 1,030 0,890 0,690 0,550 0,450 15 30 3,870 2,680
С]2Ню Бифенил
СюН18 Декагидронафталин (декалин) 70 80 90 100 НО 120 140 160 180 200 220 240 254 1,490 1,240 1,080 0,970 0,850 0,760 0,615 0,510 0,430 0,370 0,321 0,280 0,256 C13H13N А-Бензиланилин
55 130 5,390 1,200
СюН8 Нафталин 20 25 50 75 2,600 2,420 1,580 1,090
с14н12о2 Бензилбензоат
80 90 150 152 0,890 0,760 0,217 0,196
5 15 25 40 60 80 90 19,280 12,120 8,292 5,243 3,259 2 245 1,912
С10н20о** 2-Изопропил-5-метилциклогексанол (ментол)
с10н12 1,2,3,4-Тетрагидронаф-талин (тетралин)
34,9 37,8 25,050 20,360
20 2,200
530
Новый справочник химика и технолога
Продолжение табл. 3.11.10
Т,°С т| • 103, Па • с Т, °C т| • 103, Па • с Т, °C т| • 1 О ’, Па • с Г, °C т| • 103, Па • с
С14Н12О2 Бензилбензоат 10 20 30 40 60 80 100 3,430 2,620 2,060 1,670 1,170 0,870 0,680 35 12,000 60 10,300
С16Н34О Гексадекан-1-ол (цетиловый спирт) с18н36о2 Стеариновая кислота
100 1,655
с14н14о Дибензиловый эфир 70 80 100 120 140 160 180 200 11,600 7,950 5,120 3,370 2,380 1,780 1,370 1,090
50 60 75 13,400 8,420 5,380
0 10 20 30 40 60 80 100 10,500 7,250 5,330 4,060 3,210 2,160 1,570 1,200
Ci5H33N 3-Метил-А,А-бис(3-ме-тил бути л)бутан-1 -амин (триизопентиламин) С]8Н30О2 Октадека-9,12,15-триеновая кислота (линоленовая кислота)
0 10 20 30 40 60 80 100 4,980 3,580 2,690 2,100 1,700 1,170 0,870 0,670
20 40 60 17,600 10,300 6,300 Сз1Н98Об Трипальмитин
70 75 80 85 16,800 14,700 12,900 11,400
С^НгбОб Трибутирин
С18Н32О2 Октадека-9,12-д иеновая кислота(линолевая кислота)
-40 20 543,000 11,600
С57Н110О6 Тристеарин
С15Н28О2 Дибутилгептандиоат
20 40 60 23,400 12,300 7,500
15 30 8,210 5,260 C16H22O4 Дибутилфтал ат 75 80 85 18,500 16,200 14,300
c15h33n А,А-Д и пентил пентан-1-амин (трипентиламин) 15 20 25 30 29,000 20,700 16,900 14,000 С18Н34Ог Олеиновая кислота
20 40 36,200 18,200
0 4,720
Вязкость углеводородов см. в табл. 11.9.
** Курсивом выделены данные другого ряда измерений.
Таблица 3.11.11
Вязкость (ц • 107 Па • с) некоторых газов при низкой температуре
Т, К Аг СО Не Ne 7'. К Аг СО Не Ne
80 68,8 53,3 82 119,8 220 173,8 137,8 159,4 254,3
100 83 9 66,8 94,7 143 4 240 187,8 148,6 169,1 270,8
120 99,2 79,6 106,8 164,6 260 201,4 158,9 178,8 286,6
140 114,6 91,9 118,1 184 273,1 210 165,5 185,3 296,7
160 129,7 103,8 129 202,5 280 214,5 168,8 188,7 302
180 144,7 115,4 139,5 220,4 300 226,9 178,4 198,7 317,2
200 159,4 126,8 149,6 237,5
Таблица 3.11.12
Вязкость сжиженных газов при различных значениях температуры
т К т| • 103, Па • с Г, К т| • 103, Па • с Т, К т| • 103, Па • с Т, К т] • 103, Па • с
Аг 72 0,244 99,6 0,116 16,35 0,01849
84,2 0,28 75,2 0,203 111,6 0,1 17,77 0,01593
86,25 0,262 77,8 0,186 129,6 0,066 18,78 0,01448
87,3 0,252 80,9 0,17 н2 20,43 0,013
СО 82,8 0,165 14,85 0,02162 Не*
68,55 0,287 90,1 0,146 15,89 0,01932 1,282 1,54 • 10 4
Физические свойства важнейших веществ
531
Т к П • Ю3, Па • с Т. К П ' 103, Па • с
1,304 1,24 • 10"4 104,1 0,085
1,335 1,79 • 10 4 105,3 0,084
1,586 2,33 • 10 4 111,7 0,074
1,762 3,56 • 10 4 о2
1,906 6,75 • 10 4 54,4 0,873
1,973 8,11 • 104 56,4 0,717
1,988 9,60- 10^ 59,7 0,631
2,086 1,15 • 10 3 61,7 0,521
2,111 1,26 • 10 3 63,5 0,476
2,116 1,35 • 10’3 65,4 0,435
2,145 1,55 • 10 3 68,9 0,377
2,159 1,77 • 10“3 72,3 0,323
2,171 2,02 • 10 3 79,2 0,279
2,174 1,95- 10 3 84 0,253
2,178 2,30 • 10"3 90,1 0,218
2,29 1,87- 10 3 111,8 0,124
2,315 1,97 10 3 125,6 0,108
2,642 2,35 • 10’3 138,4 0.1
2,934 2,40 • 10"3 145,6 0,0965
3,738 2,75 • 10 3 154,2 0,0915
3,81 2,87 • 10 3 СН4
3,97 2,88 • 10 3 91,1 0,21
4,021 2,98 • 10’3 93,5 0,188
n2 94,6 0,179
63,9 0,292 98,3 0,162
64,8 0,284 102,4 0,144
66,2 0,247 108,8 0,125
69 0,217 111,2 0,098
71,1 0,201 125,9 0,09
73,3 0,184 130,6 0,084
75,4 0,171 134,2 0,082
77,4 0,158 148,6 0,068
90,1 0,116 154,6 0,067
Окончание табл. 3.11.12
7 ’, К П • 103, Па-с Т, К 7] • 103, Па • с
с2н4 С3Н6
105 0,66 88,7 14,46
110,4 0,553 89,8 12,73
126 0,402 90,1 12,4
134,1 0,333 94,3 7,84
148,8 0,231 98 5,37
160 0,207 102,6 3,58
169,3 0,167 111,1 2,15
183,8 0,135 119 1,55
204,6 0,115 123 1,31
226,4 0,092 134,2 0,9
233,9 0,0775 141,9 0,67
240,9 0,075 150 0,55
252,2 0,072 159,8 0,45
273,1 0,064 174,8 0,37
280,9 0,0625 С3Н8
с2н6 85,1 11,54
101,2 0,878 88,1 8,66
103,3 0,787 93,1 6,09
105,7 0,729 96,8 4,59
108 0,675 101.6 3,58
0,179 0,624 106.7 2,57
150,3 0,271 111,6 2,1
159,8 0,236 119,4 1,49
166,8 0,207 133,2 0,98
172,3 0,175 141,8 0,97
186 0,137 144,4 0,74
201,2 0,114 149,8 0,72
215,4 0,097 160 0,56
230 0,09 169,6 0,38
243,4 0,082
270 0,067
288 0,055
* Обращает на себя внимание отклонение от монотонной зависимости значений вязкости гелия при некоторых температурах (выделены курсивом). В [4] и других источниках пояснения по этому поводу отсутствуют. Возможно, эти данные ошибочны.
Таблица 3.11.13
Вязкость некоторых хладонов т] • 106, кг • с/м2*
Величины, выделенные курсивом, относятся к жидкому состоянию вещества.
Давление, атм Температура, °C
-15 -10 0 1 ‘0 20 30 40
СО2
5 1,38 1,4 1,42 1,45 1,49 1,52 1,6
10 1,43 1,45 1,45 1,47 1,51 1,54 1,62
20 1,58 1,56 1,53 1,51 1,55 1,58 1,67
532
Новый справочник химика и технолога
Продолжение табл. 3.1 /. 13
Давление, атм Температура, °C
-15 -10 0 .1 10 20 30 40
СО2
30 12,04 11,44 1,63 1,59 1,61 1,65 1,72
40 12,33 11,85 10,56 1,71 1,7 1,73 1,8
50 12,6 12,16 11,06 9,14 1,82 1,82 1,9
60 12,82 12,43 11,47 9,73 7,27 1,96 2,01
70 13,04 12,66 11,83 10,22 8,01 2,24 2,18
80 13,23 12,9 12,16 10,66 8,6 5,61 2,47
90 13,44 13,12 12,43 11,06 9,1 6,51 3,32
100 13,62 13,33 12,67 11,41 9,54 7,21 4,7
НО 13,81 13,53 12,9 11,72 9,93 7,82 5,72
120 13,47 13,72 13,11 12,01 10,28 8,35 6,44
Продолжение табл. 3.11.13
Давление, атм Температура, °C
-20 -10 0 10 20 45 80
NH3
1 0,88 0,92 0,95 0,99 1,02 1,12 1,24
2 25,78 0,98 0,98 1,01 1,04 1,12 1,24
6 27,04 26,16 24,98 1,2 1,16 1,15 1,26
10 27,89 27,1 26,07 24,64 22,81 1,23 1,31
14 28,45 27,75 26,77 25,43 23,72 1,39 1,41
18 28,85 28,18 27,24 25,93 24,28 — 1,6
22 29,16 28,52 27,57 26,3 24,66 — 1,89
26 29,4 28,76 27,82 26,57 24,97 — —
SO2
0,5 1,07 1,Н 1.15 1,21 1,26 1,32 1,39
1 50 1,14 1,19 1,24 1,28 1,33 1,4
2 51,2 45,85 40,03 1,33 1,36 1,36 1,43
3 52 46,8 41,05 34,48 1,48 1,42 1,47
4 52,55 47,55 41,83 35,35 28,4 1,55 1,54
5 53,02 48,15 42,43 36 29,24 — 1,65
6 53,35 48,65 42,92 36,5 29,88 — 1,8
7 53,65 49,05 43,32 36,9 30,37 — —
с 53,85 49 44 43,65 37 25 30,8
CH3CI
0,5 0,89 0,96 0,99 1,04 1,09 1,13 —
1 0,95 0,99 1,02 1,05 1,1 1,13 —
2 32,15 30,91 1,09 1,08 1,Н 1,14 —
3 32,74 31,55 30,15 1,15 1,15 1,16 —
4 33,18 32,03 30,65 28,9 1,22 1,21 —
5 33,53 32,4 31,05 29,36 27,53 1,29 —
6 33,77 32,67 31,32 29,7 27,87 1,43 —
7 33,9 32,84 31,5 29,9 28,06 25,9 —
* Принятая в таблице размерность вязкости (кг • с/м2) обусловлена тем. что удельные силы (нормальная р — давление и касательная т — напряжение сдвига) выражены в кг/м2, т. е. в атмосферах (атм). Это оправдано спецификой расчетов холодильных агрегатов, в основе которых лежит, в частности, формула Пуазейля для расхода газа v = яг4р/8г|/ через трубопровод радиусом г и длиной / под действием давления р, в которой размерности вязкости и давления должны быть согласованы. Последнее же традиционно выражается в атмосферах. Для перехода к стандартным единицам следует воспользоваться соотношением I атм- 0,1 МПа, 1 П-0.1 Па • с = 0,0101972 кг • с/м2.
Физические свойства важнейших веществ
533
Таблица 3.11.14
Вязкость (1] * 1()7, Па с) водяного пара в зависимости от давления и температуры
Г °C Давление, МПа
Давление насыщенного пара 0.101 2,03 4,05 6,08 8.11 10,1 15.2 20,3
100 124 124
120 133 132
140 142 140
160 152 148
180 163 155
200 175 163
220 188 171 184
240 201 179 190
260 217 186 196 211
280 235 194 203 217 232
300 257 202 210 223 236 250
320 282 209 217 230 242 255 268
340 318 217 225 236 248 261 272 318
360 365 225 232 243 254 266 278 308
380 232 240 250 261 272 283 311 361
400 240 247 257 268 279 289 316 354
420 247 254 264 275 284 295 322 354
440 254 262 271 282 291 302 329 358
460 262 269 279 288 298 308 335 363
480 269 277 285 294 304 315 342 370
500 277 284 292 301 311 322 349 380
Т’кип 124 182 209 231 249 267 318 379
Таблица 3.11.15
Вязкость газов и паров (т| • 107 Па • с) при давлении 0,1 МПа и константы Сазерленда S для них
Курсивом выделены величины, полученные экстраполяцией.
Название Формула Вязкость при температуре t. °C 5 Интервал 7', °C
0 20 50 100 150 200 250 300 400 600 800
Простые вещества и неорганические соединения
Азот n2 165 175 188 208 228 246 263 280 311 366 413 104 25-280
Азота(1) оксид n2o 137 146 160 183 204 225 245 265 303 260 25-280
Азота(П) оксид NO 179 188 204 227 247 268 287 128 20-250
Аммиак NH3 93 100 111 198 146 165 181 503 20-300
Аргон Ar 210 221 241 269 296 321 344 368 411 487 554 142 20-827
Бром Br2 146 158 194 219 244 269 294 342 533 > 187
Водород H2 85 88 94 103 113 191 130 138 154 183 210 73* 20-100
Бромид HBr 171 237 375 0-100
Иодид HI 173 186 202 232 263 292 319 390 0-100
Фосфид PH3 107 145 290
Хлорид HC1 133 143 158 183 208 230 253 360 0-250
Гелий He 188 (196) 208 229 249 269 288 307 342 407 466 83 100-200
Ди циан (CN)2 94 107 198 330
Иод I2 123 175 198 220 242 264 308 568 106-523
Кислород 02 192 202 218 244 267 290 310 330 369 435 493 125 15-830
Криптон Kr 233 246 306 210,4 0-100
Ксенон Xe 211 226 247 282 317 349 379 290 0-100
Неон Ne 298 311 365 425 453 478 531 625 710 61 20-100
Серы(1У) оксид SO2 116 125 140 163 186 207 227 246 282 346 404 306 300-825
Сероводород H2S 116 130 161 331
Сероуглерод cs2 (89) 125 142 160 177 194 499,5 114-310
Углерода(1У) оксид co2 137 146 160 183 204 225 245 265 299 360 414 л _ Л*** 254 25-280
Углерода(П) оксид co 166 175 188 208 228 246 263 101,1 (-78)277
Хлор C12 123 133 147 168 189 209 229 249 287 351 20-500
Новый справочник химика и технолога
Окончание табл. 3.11.15
Название Формула Температура, °C 5 Интервал Т. °C
0 20 50 100 120 150 200 250 300
Органические соединения
Ацетилен с2н2 94 102 1 1 1 125 132 198,2 20-120
Ацетон (СН3)2СО (66) 93 99 108 121 134 147 541,5 119-306
Бензол С6н6 70 75 83 95 100 107 119 131 380 15-250
Бутан СН3(СН2)2СН3 69 73,9 82 95 100 377,4 20-120
Гексан СН3(СН2)4СН3 59 87 93 104 115 125 436,1 121-307
Изобутан (СНз)зСН 69 74 89 95 100 335,5 20-120
Метан сн4 104 109 118 133 139 147 160 173 185 162 20-500
Бромметан (метил бромистый) СН3Вг 104 133 146 180 379,2 20-120
Хлорметан (мстил хлористый) СН3С1 98 103 115 134 141 152 170 187 204 441 20-300
Дихлорметан (метилен хлористый) СН2С12 91 99 109 127 91 144 160 176 192 425 22-309
Пентан СН3(СН2)зСН3 62 66 85 91 98 109 119 130 383 122-306
Пропан СН3СН2СНз 75 80 90 103 108 113 125 136 (147) 278 20-250
Пропилен СН2-СНСН; 78 84 93 107 112 121 134 146 362
Пропан-2-ол (спирт изопропиловый) (СНз)2СНОН 70 103 1 11 125 138 150 460 119-308
Метанол (спирт метиловый) СНзОН 87 129 139 156 173 188 486,9 111-312
Пропан-1-ол (спирт пропиловый) С2Н5СН2ОН 68 102 110 124 138 515,6 122-273
Этанол (спирт этиловый) С2Н5ОН 109 1 14 123 137 151 165 407,3 130-309
Тетрахлормстан (четыреххлори-стый углерод) СС14 90 108 120 137 152 170 335 50-250
Трихлорметан (хлороформ) СНС13 95 100 НО 195 132 142 158 175 191 462 14-345
Этан СН3СН3 86 91 100 114 1 19 128 141 153 252 20-250
Дихлорэтан (этил хлористый) С2Н5С1 94 105 411
Этилен сн2=сн2 94 101 110 196 132 140 154 167 225 20-250
Эфир диметиловый (СН3)2О 85 91 101 117 123 344,9 20-120
Эфир диэтиловый (С2н5)2о 68 95 106 118 130 141 404 122-309
Физические свойства важнейших веществ
* S = 86 при 100 °C; S = 105 при 200-250 °C; 5 = 234 при 713-822 °C.
* * S = 95 при 200-250 °C; S = 173 при 682-815 °C.
* **5 = 213 при 300-824 °C.
536
Новый справочник химика и технолога
Литература
1. Реология. Под ред. Ф. Эйриха. М.: ИЛ, 1962. 824 с.
2. Бибик Е.Е. Реология дисперсных систем. Л.: Изд-во ЛГУ, 1981. 172 с.
3. Бибик Е.Е., Гамов Н.С., Грибанов Н.М. Фрактальные агрегаты и реологические свойства феррожидкостей. // V Всесоюзное совещание по физике магнитных жидкостей. Пермь: ИМСС УрО АН СССР, 1990. 152 с.
4. Справочник химика. Л.: Госхимиздат, 1962. Т. 1. 1072 с.
5. Справочник химика. Л.: Химия, 1964. Т. 3. 1008 с.
6. Виноградов Г.В., Малкин А.Я. Реология полимеров. М.: Химия, 1977. 440 с.
7. Мелвин-Хьюз Э.А. Физическая химия. М.: ИЛ, 1962. Т. 1,2. 1148 с.
8. Гросберг А.Ю., Хохлов А.Р. Статистическая физика макромолекул. М.: Наука, 1989. 344 с.
9. Смирнов Б.М. Фрактальные кластеры. // УФН. 1986. Т. 149, №2. С. 177-219.
10. Дерягин Б.В., Чурасв Н.В., Муллер В.М. Поверхностные силы. М.: Наука, 1985. 398 с.
11. Бибик Е.Е. // Журн. прикл. химии. 1997. Т. 70, №8. С. 1258-1262.
3.12. Поверхностное и межфазное натяжение
(Е.Е. Бибик)
Реально вещества существуют в среде некоторой другой по природе субстанции и отделены от нее границами, т. с. образуют гетерогенную систему. Чаще всего в качестве среды выступает воздух, иногда — вакуум, а также собственный пар вещества, если оно достаточно летуче, или какая-либо жидкость или даже твердое вещество. Протяженность границ является одним из параметров состояния вещества и количественно характеризуется площадью S' контакта вещества со средой. В случае контакта вещества со своим собственным паром или расплавом уместно говорить о границе между фазами одного и того же вещества. Понятие межфазной границы относится и к поверхности контакта веществ разной химической природы в одинаковом или разном агрегатном состояниях. Межфазная граница не возникает только при контакте газообразных или неограниченно растворимых веществ.
Граница раздела двух фаз это нс только непременный атрибут реально существующих веществ, но и объект, который сам по себе важен практически. Существует множество технологических задач, цель которых — придание нужных свойств именно границе раздела фаз, а природа веществ, являющихся носителем этой границы при этом может иметь второстепенное значение. Отражение и преломление света, адсорбция, внешнее трение, возникновение разности электрических потенциалов двух фаз, вентильный и другие эффекты в полупроводниковых приборах и многое другое происходит именно на границе фаз.
Фундаментальными характеристиками любой межфазной границы является ее площадь S и поверхностное
натяжение о. Поверхностное натяжение границы двух фаз — это работа, которую необходимо совершить для увеличения поверхности их контакта на единицу площади в обратимом изохорно-изотермическом процессе. Энергия, подведенная при этом к гетерогенной системе, запасается в ней на межфазных границах, так что натяжение имеет смысл энергии Гиббса единицы поверхности. Произведение oS представляет собой избыток энергии Гиббса гетерогенной системы с хорошо развитой поверхностью контакта со средой по сравнению с энергией того же количества вещества системы в монолитном состоянии, т. е. с поверхностью S близкой к нулю. В силу известного стремления любой системы к состоянию с минимальной величиной энергии наличие ее избытка является движущей силой разнообразных процессов, направленных на уменьшение как площади межфазных границ S, так и величины их натяжения о. Этим и определяется исключительно важная роль границ и натяжения в управлении свойствами и поведением реальных материалов. Поверхностное натяжение проявляет себя и как сила, действующая вдоль поверхности на единицу длины произвольного контура на поверхности и направленная на сокращение се площади. Именно в таком качестве его легко наблюдать на поверхности жидкостей.
В литературе термин «поверхностное натяжение» вещества принято применять к границе раздела этого вещества с газовой фазой и термины «межфазное» или «пограничное» натяжение — к границам между конденсированными фазами. Фактически же от такой терминологии приходится неизбежно отказываться, как только речь заходит о конкретных веществах или гетерогенных системах. Например, самое обычное суждение типа «поверхностное натяжение границы воды и воздуха практически равно поверхностному натяжению границы воды и ее пара» грамматически некорректно. Слово «поверхностное» здесь лишнее, поскольку словосочетания «поверхностное натяжение» и «натяжение границы» означают одно и то же, причем слово «границы» из этой фразы не может быть удалено без искажения ее смысла. В дальнейшем будут применяться термины типа «натяжение» и «натяжение границы воды и стекла» наряду с классическими терминами, если последние не будут создавать грамматически неприемлемых словесных конструкций.
Прямые измерения натяжения возможны только на границах флюидных, т. е. текучих фаз: жидкость/газ и жидкость/жидкость. Тем не менее, поверхность твердых веществ также характеризуется величиной натяжения и его роль в гетерогенных системах типа твердое/газ и особенно твердое/жидкость не менее значительна, чем в системах флюидных фаз. Однако натяжение твердых веществ определяется только косвенно (чаще всего по смачиваемости жидкостью с известным натяжением) причем не всегда однозначно и потому оно не получило статуса справочных сведений. О величине натяжения твердых веществ можно судить по величине
Физические свойства важнейших веществ
537
натяжения их расплавов вблизи температуры плавления, так как плавление вещества нс сильно изменяет его натяжение.
Величину поверхностного и межфазного натяжения можно регулировать в достаточно широких пределах. На границе двух жидкостей оно может быть уменьшено практически до нуля. Дробление капель одной жидкости в среде другой при исчезающе малом натяжении практически не требует затрат энергии и потому оно происходит самопроизвольно с образованием практически гомогенной смеси (мицеллярного раствора) двух взаимно нерастворимых веществ. Этот эффект называется солюбилизацией и играет важную роль в действии моющих средств, в добыче нефти, пищеварении и других процессах. Основное средство воздействия на величину натяжения — это поверхностно активные вещества (ПАВ). ПАВ — это вещества, способные изменять (уменьшать) поверхностное натяжение раствора или натяжение границы раствора с другой конденсированной фазой при изменении (увеличении) концентрации ПАВ в растворе. Основной характеристикой ПАВ является его поверхностная активность G — отношение отрицательной величины приращения натяжения, к приращению концентрации ПАВ в пределе, когда концентрация стремится к нулю. Разумеется, что натяжение раствора может быть понижено только введением в растворитель вещества с меньшим натяжением, чем у растворителя. По отношению к воде поверхностную активность проявляют водорастворимые органические вещества с меньшим, чем у воды натяжением, а это практически все органические водорастворимые вещества. Неорганические водорастворимые вещества (соли, кислоты, щелочи) проявляют отрицательную поверхностную активность, т е. увеличивают натяжение раствора при увеличении их концентрации.
Связь между концентрацией и натяжением раствора существенно нелинейна (не аддитивна по отношению к натяжениям компонентов раствора). Объясняется это адсорбцией — изменением состава поверхностного слоя раствора по сравнению с составом раствора в целом. Поверхностный слой обогащается менее полярным компонентом раствора, т. е. тем, который имеет меньшее натяжение. В растворах веществ с высокой поверхностной активностью (например, солей щелочных металлов жирных кислот) поверхностный слой раствора состоит практически только из молекул растворенного вещества, хотя его концентрация в растворе может составлять доли процента. О поверхностном слое в этом случае говорят, что он представляет собой насыщенный мономолеку-лярный адсорбционный слой ПАВ.
Имеющиеся данные о поверхностной активности и о веществах этого типа относятся исключительно к водным растворам, что и нашло свое отражение в содержании приводимых ниже справочных данных. Более того, система понятий и определений в этой области науки о веществах и поверхностных явлениях сложилась именно с ориентацией на водные системы. Между тем роль натяжения и ПАВ в неводных средах не менее
существенна, чем в водных. Достаточно указать в связи с этим на противоизносную и моющую роль присадок в моторных маслах, на роль присадок в металлах и сплавах, которые через механизм адсорбции в процессе кристаллизации регулируют структуру и свойства сплавов.
Общие вопросы теории (термодинамики) растворов ПАВ разработаны глубоко и разносторонне [1]. Вместе с тем теория пока нс в состоянии решать многие актуальные практические вопросы. Так, для описания зависимости натяжения раствора ПАВ от его концентрации до сих пор используются эмпирическое уравнения Шишковского:
о0- ° = Z?1 n( 1 + Ас),
где о0 — натяжение растворителя, а к и В — эмпирические константы, причем первая близка по смыслу к поверхностной активности, а В — к разности натяжений растворителя и ПАВ. Уравнение в большинстве случаев довольно фубо передает зависимость натяжения от состава раствора, однако в силу исторических заслуг не вытеснено более точными. Таковым является. например, также эмпирическое уравнение Малова [2]:
Вкс о0 - о =----.
I + кс
Другая практически важная задача химии ПАВ — установление связи между строением их молекул и активностью. Опять же на основе опыта установлено, что молекулы ПАВ должны быть дифильными, т. е. обладать сродством и к полярным, и к неполярным средам за счет наличия в их составе полярных и неполярных фрагментов. В качестве последних часто выступаю! углеводородные группы. Эмпирическое же правило Траубе гласит, что увеличение длины углеводородной группы на один метиленовый фрагмент ведет к увеличению поверхностной активности вещества данного гомологического ряда примерно в 3,2 раза. Эти представления о природе ПАВ справедливы только по отношению к водорастворимым веществам. Как следствие описанного выше сосюяния вопроса в соогвеюгвую-щих разделах справочника приводятся только результаты прямых измерений натяжения растворов различных концентраций.
Следует различать простейшие ПАВ (типа водорастворимых спиртов) и вещества, предназначенные для практического применения (технические ПАВ) типа солей высших жирных кислот или оксиэтилированных эфиров. Многие из них характеризуются критической концентрацией мицеллообразования (ККМ), выше которой раствор становится коллоидным (мицеллярным). По этой и другим причинам технические ПАВ далеко не во всем следуют классическим закономерностям [3]. Например, производная da/de может иметь максимум не при минимальной, а при некоторой средней концентрации; активность ПАВ может увеличиваться с ростом температуры и в присутствии электролита (в случае ионогенных ПАВ).
538
Новый справочник химика и технолога
Справочные данные о натяжении веществ и межфазных натяжениях представлены в табл. 3.12.1-3.12.9 [3-11].
Поверхностное натяжение о существенно зависит от температуры Т. Состав газовой фазы мало влияет на величину поверхностного натяжения, но, тем не менее, он обычно указывается. Если состав газа нс указан, то подразумевается, что это воздух при атмосферном давлении. В закрытых сосудах — это смесь пара вещества и одного из газов.
Обозначения газовой фазы, граничащей с веществом:
взд — воздух, насыщенный паром;
пар — насыщенный пар вещества;
СО? — диоксид углерода;
Н2 — водород;
Нс — гелий;
N2 — азот.
Обозначения температур фазовых переходов:
Тпл — температура плавления;
Т’кпп — температура кипения.
Поверхностное натяжение на границе раздела между двумя жидкостями называется межфазным натяжением. Размерность натяжения: Дж/м2 или Н/м. Т. к. 1 Н = Дж/м, то 1 мН/м = 1 мДж/м2 = 0,001 Дж/м2.
Таблица 3.12.1
Поверхностное натяжение воды на границе с воздухом
Т, °C СУ. мДж/м2 Т. °C СУ. мДж/м2 Т °C СУ, мДж/м2
-10 77,1 16 73,34 30 71,15
-5 76,4 17 73,2 35 70,35
0 75,62 18 73,05 40 69,55
5 74,9 19 72,89 45 68,73
6 74,76 20 72,75 50 67,9
7 74,62 21 72,6 60 66,17
8 74,48 22 72,44 70 64,41
9 74,34 23 72,28 80 62,6
10 74,2 24 72,12 90 60,74
И 74,07 25 71,96 100 58,84
12 73,92 26 71,8 ПО 56,89
13 73,78 27 71,64 120 54,89
14 73,64 28 71,47 130 52,84
15 73,48 29 71,31
Таблица 3.12.2
Поверхностное натяжение смесей воды и оксида дейтерия (тяжелой воды) на границе с собственным паром при 20 °C
Состав смеси, % СУ, мДж/м2 Состав смеси. % о, мДж/м2
Н2О 2Н2О Н2О 2Н2О
100 0 72,75 8 92 68,1
69 31 71,5 0 100 67,8
34,5 65,5 69,8
Таблица 3.12.3
Поверхностное натяжение простых веществ
Символ Название Газ /'. °C су, мДж/м2
Ag Серебро взд 970 800
Н2 995 923
н? 1050 916
н? 1100 909
н? 1163 902
Al Алюминий взд 700 840
Au Золото взд 700 1207
взд 800 1177
Н? 1120 1128
Н? 1200 1120
Н? 1300 1110
Bi Висмут Н? 300 388
н? 583 354
н? 779 343,9
СО? 700-800 346
Br2 Бром взд -21 62,1
взд 13 44,1
Cd Кадмий Н2 330 570
н? 400 597
Н? 600 585
Cu Медь Н2 1140 1120
Н? 1200 1160
н? 1300 1226
Fe Железо н? 1267 936
н? 1310 917
Ga Галлий СО2 30 358
Ge Германий 959 600
(7k?)
Hg Ртуть пар, взд 0 479,5
пар, взд 10 477
пар, взд 20 475
пар, взд 25 473,5
пар, взд 30 472,5
пар, взд 40 470
пар, взд 50 467,5
пар, взд 100 456
пар, взд 150 444
пар, взд 200 433
пар, взд 250 416
пар, взд 300 400
пар, взд 350 381
К Калий пар 110 95
Na Натрий пар 100 222
пар 250 211
СО2 90 294
P . Фосфор взд 50 69,7
Физические свойства важнейших веществ
539
Окончание табл. 3.12.3
Символ Название Газ 71 °C ст, мДж/м2
взд 54 68,53
взд 60,2 66,95
взд 68,7 64,95
РЬ Свинец н2 350 442
Н2 400 438
н2 500 431
н2 600 424
н2 800 410
н2 1000 401
Pt Платина взд 2000 1819
Rb Рубидий 39,5 77
S Сера взд 119 42
пар 445 (ТКИ11) 33
Sb Сурьма н2 750 368
н2 1000 355
Se Селен взд 217 92,5
Si Кремний Не 1450 725
Sn Олово пар 250 575
пар 500 525
пар 600 505
н2 253 526
н2 800 520
н2 1000 497
TI Таллий пар 300-320 375-
496
Zn Цинк пар 470 772,2
пар 635 728,1
н2 510 785
н2 640 761
Таблица 3.12.4
Поверхностное натяжение неорганических соединений
Формула Название Газовая фаза T. °C CT. мДж/м2
AgBr Бромид серебра взд 434 121,4
(7™)
AgCl Хлорид серебра взд 450 125
взд 494 121,6
взд 501 119
взд 550 113
AsBr3 Трибромид n2 49,6 49,6
мышьяка n2 121 41
n2 179,7 36,1
AsCl3 Трихлорид n2 -21 43,8
мышьяка n2 0 41,4
Продолжение табл. 3.12.4
Формула Название Газовая фаза 7', °C о, мДж/м2
BC13 ВаС12 CS2 H2S2 H2O 2H2O кво2 KBr KCN KC1 KF Трихлорид бора Хлорид бария Дисульфид углерода (сероуглерод) Дисульфид диводорода (дисульфан) Вода Оксид дидейтерия (тяжелая вода) Метаборат калия Бромид калия Цианид калия Хлорид калия Фторид калия n2 n2 n2 пар взд взд взд взд взд взд взд взд взд взд взд взд взд взд взд взд взд взд n2 n2 n2 n2 взд взд n2 n2 n2 n2 n2 взд n2 n2 n2 20,8 50,2 110 20 962 (7™) -30 -20 0 10 20 30 50 -20,5 -0,3 14,6 20,5 См. таб; 15 20 25 30 35 99 110,8 216 992 775 886,5 920 730 (^л) 634 (7ko 800 885 986 1088 1167 776 (7^,) 913 1185 1310 39,4 36,6 31 16,7 150,5 40 38,5 35,5 33,9 32,4 30,9 27,8 53,7 50 47,4 46,2 . 3.12.1 73,35 72,6 71,8 71.1 70,3 58,5 56 32,8 123,5 85,7 77,8 75,4 91 96,1 95,8 89,7 82,2 75,2 69,6 98,4 138,4 116,1 104,9
540
Новый справочник химика и технолога
Продолжение табл. 3.12.4
Формула Название Газовая фаза T, °C CT. мДж/м2
KI Иодид калия n2 737 75,2
n2 812 69,2
n2 873 66,5
KNO3 Нитрат калия n2 380 110,4
n2 578 95,2
n2 771,6 80,2
n2 414 100,7
K2SO4 Сульфат калия n2 1070 143,7
n2 1306 128,8
n2 1400 122,4
n2 1656 106,8
n2h4 Г идразин 25 66,7
40 60,1
n2o2 Диоксид диазота ВЗД 1,6 29,5
ВЗД 19,8 26,6
NaBO2 Метаборат натрия n2 1016 193,7
n2 1192 166,1
n2 1441 126,2
Na2B4O7 Тсграборат натрия n2 1000 211,9
NaBr Бромид натрия n2 761 105,8
n2 941 92,9
n2 1073,5 84
n2 1166 78
Na2CO3 Карбонат натрия ВЗД 851 179
(TkO
NaCl Хлорид натрия n2 803 113,8
n2 960 102,7
n2 1080 94
n2 1172 88
Nal Иодид натрия n2 705,5 85,6
n2 815,5 80,5
n2 861 77,6
NaNO3 Нитрат натрия ВЗД 661 93,9
(7™)
n2 321,5 119,7
n2 513 108,9
n2 602 103,4
n2 738 93,7
Na2SO4 Сульфат натрия n2 900 194,8
n2 990 188,2
n2 1077 184,7
Ni(CO)4 Тетракарбонилни- 0 17,4
кель 20 15,1
50 11,6
PBr3 Трибромид фосфора IN 2 -20 45,8
Окончание табл. 3.12.4
Формула Название Газовая фаза T. °C CT. мДж/м2
PBr3 Трибромид N, 0 44,7
фосфора n2 20,8 43,2
n2 99,8 36
n2 170 26,3
PC13 Трихлорид n2 -70 37,4
фосфора n2 0 29,3
n2 35,2 25,8
n2 75,1 21,9
Pl3 Трииодид n2 75,3 56,5
фосфора n2 150 51,4
POCI3 Оксид-три хлорид ВЗД 15 32,77
фосфора ВЗД 49 28,36
ВЗД 65 26,57
S2C12 Дихлорид дисеры n2 0 45,4
n2 75 34,6
n2 121 29,4
SbCl3 Трихлорид n2 74,5 49,6
сурьмы n2 137 42,6
n2 178 38,3
SeF4 Тетрафторид -7,6 39,06
селена 17,8 36,33
89,2 27,51
SiCl4 Тетрахлорид n2 20 19,71
кремния
(тетрахлорсилан)
SnCl2 Дихлорид олова n2 307 97
n2 405 89
n2 480 81,6
TINO3 Нитрат таллия(1) n2 210 117,3
n2 312 109,8
n2 430 99,5
UF6 Гексафторид взд 70 16,8
урана ВЗД 80 15,6
ВЗД 90 14,3
ВЗД 100 13,1
Таблица 3.12.5
Поверхностное натяжение органических соединений
В каждой группе соединений вещества расположены в соответствии с системой Хилла (в порядке возрастания числа атомов углерода в молекуле, затем — числа атомов водорода и других элементов в алфавитном порядке в эмпирических формулах веществ).
Формула Название Газовая фаза 7’, °C ст, мДж/м2
Углеводороды
Г ” C4riio Бу тан взд —20 17,34
взд 0 14,84
Физические свойства важнейших веществ
541
Продолжение табл. 3.12.5
Формула Название Газовая фаза г °C ст, мДж/м2
СдНю Изобутан взд 10 14,07
С5н8 Изопрен взд 22 22,05
С5Н10 Циклопентан взд 15 23,28
взд 20 22,65
взд 30 21,32
с5н12 Изопентан взд 20 15
взд 30 13,93
с5н12 Пентан взд 20 16,09
взд 30 15
взд 40 13,8
СбН? Бензол взд 10 30,24
взд 20 28,87
взд 30 27,5
взд 40 26,13
взд 80 21,2
с6н8 Циклогекса-1,3- взд 20 27,32
диен взд 60 22,22
С6н|2 Циклогексан взд 20 24,95
взд 30 23,75
взд 60 21,35
СбН14 Г ексан взд 20 18,41
взд 30 17,37
взд 40 16,32
взд 60 14,33
С6Н,4 2,2-Диметилбутан взд 20 16,3
взд 40 14,33
С6Н,4 2,3-Димстилбутан взд 20 17,37
взд 40 15,37
С6н14 2-Метилпентан взд 20 17,38
взд 40 15,36
С6н14 З-Метилпентан взд 20 18,12
взд 40 16,03
с7н8 Толуол взд 0 30,93
взд 20 28,53
взд 30 27,33
взд 40 26,13
взд 100 18,93
С7н16 Гептан взд 20 20,29
взд 30 19,27
взд 40 18,26
взд 90 13,6
С7н16 2,2-Диметилпентан взд 20 18,03
С7н16 2,3-Диметилпентан взд 20 19,82
С7н16 2,4-Диметилпентан взд 20 18,12
С7н16 3, З-Д имети л пентан взд 20 19,61
С7н16 2-Метилгексан взд 20 19,21
Продолжение табл. 3.12.5
Формула Название Г азовая фаза Т, °C (7, мДж/м2
с7н16 3-Метил гексан взд 20 19,82
взд 20 20,46
с7н16 2,2,3-Триметил-бутан взд 20 18,76
с8н10 о-Ксилол взд 20 30,03
взд 30 28,93
взд 40 27,84
взд 100 21,27
С8Н1О л/-Ксилол взд 20 28,63
взд 30 27,53
взд 40 26,44
взд 100 19,87
С8Н1О и-Ксилол взд 20 28,31
взд 30 27,22
взд 40 26,13
взд 100 19,59
С8Н,о Этилбензол взд 20 29,04
взд 30 27,91
взд 40 26,78
взд 100 20
С8н18 Октан взд 20 21,78
взд 30 20,8
взд 40 19,82
взд 120 12,6
С9Н|2 Изопропилбензол (кумол) взд 20 28,2
с9н12 Пропил бензол взд 20 29
взд 30 27,91
взд 40 26,83
взд 100 20,32
С9Н]2 1,2,3-Триметил-бензол (гемеллитол) взд 20 31,27
с9н20 Нонан взд 20 22,96
взд 30 22,01
взд 150 11,6
С10Н8 Нафталин взд 80 32,26
СюН]2 1,2,3,4- Т етрагидронафта-лин (тетралин) взд 19,3 36,28
С 10н 18 Декагидронафталин (декалин) взд 19,8 29,89
CjoH22 Декан взд 20 23,89
взд 30 22,97
взд 150 12,8
СИН24 Ундекан взд 20 24,78
взд 30 23,89
взд 150 13,7
С ]2Н ю Бифенил пар 129,2 28,64
пар 179,7 24,04
542
Новый справочник химика и технолога
Продолжение табл. 3.12.5
Формула Название Газовая фаза 7 . °C ст. мДж/м2
Углеводороды
С]2Н26 Додекан взд 20 25,48
взд 30 24,6
взд 150 14,7
С13Н28 Тридекан взд 20 26,13
взд 150 15,6
с14н14 1,1 '-Этан-1,2-диилдибензол (дибензил) пар 108,3 27,86
С14Н3(> Тстрадекан взд 20 26,69
взд 150 16,2
С15Н32 Пентадекан взд 20 27,17
взд 150 16,9
С)6н34 Г сксадекан взд 20 27,64
взд 150 17,4
С17Нз6*2 Гептадекан взд 20 28,06
взд 100 21,35
С18Н38*2 Октадекан взд 20 28,42
взд 100 21,75
С19Н16 1.Г, Г'-Метан- No 156 32,7
триилтрибензол (трифснилмстан)
С20Н42 Эйкозан взд 40 27,2
взд 100 23
Галогенпроизводные углеводородов
СС14*' Т страхлормстан (четыреххлористый нар 20 25,68
углерод) нар 100 16,48
СНВг3 Бромоформ (трибромметан) 20 51
СНС13*‘ Хлороформ взд 20 27,14
(трихлорметан) пар 10,2 27,62
пар 45,5 23,03
СН2С12 Дихлорметан взд 15 28,83
взд 20 28,12
взд 30 26,54
CH3CI Хлор метан взд 20 16,26
C2C13F3 1,1,2-Трифтор- 1,2,2-трихлорэтан (фреон-113) взд 20 17,75
С2С14 Т страхлорэтилсн пар 20 31,74
С2НС13 Трихлорэтилен взд 15 29,73
взд 20 29,1
взд 30 27,76
С2Н2Вг4*' 1,1,2,2-Тетра-бромэтан взд 20 49,6
С2Н2С14 1,1,2,2-Тстра- n2 0 36,7
хлорэтан взд 22,5 36,03
С2Н3С1з 1,1,1-Трихлорэтан взд 15 26,17
взд 20 25,56
Продолжение табл. 3.12.5
Формула Название Г азовая фаза 7; °C ст, мДж/м2
С2Н3С13 1,1,1-Трихлорэтан взд 30 24,25
С2Н3С13 1,1,2-Трихлорэтан взд 15 34,37
взд 20 33,83
взд 30 32,78
С2Н4Вг2 1,2-Дибромэтан пар 12,2 38,91
пар 45 34,5
С2Н4С12 1,1 -Дихлорэтан N, 0 25,7
n2 30 22,4
С2Н4С12 1,2-Дихлорэтан n2 0 34,1
n2 30 30,1
С2Н5Вг Бромэган пар 20 24,15
С2Н51 Иодэган n2 20 28,1
С5Г К) Дскафторцикло- 20 11,09
пентан
C5F12 Додскафторнснтан 20 9,87
C5F12 2-(Т рифторметил)- 20 10,48
1,1,1,2,3,3,4,4,4-
нонафторпентан
C6H5Br Бромбензол взд 25 35,75
n2 35,6 35,2
n2 71,5 31
С6Н5С1 Хлорбензол взд 20 33,19
взд 30 31,98
n2 25 32,9
n2 50 29,6
С6н51 Иодбензол n2 0 39,1
n2 25,1 37,1
C7F16 Г ексадекафторгеп- 20 12,6
тан
C8F18 Октадекафторок 1 ан 20 13,6
Спирты, фенолы, тиолы
СН4О*! Метанол ВЗД 15 22,99
ВЗД 20 22,55
ВЗД 30 21,69
с2н6о Этанол n2 -79 30,6
n2 -24 25,2
nap 20 22,03
nap 40 20,2
nap 60 18,43
nap 80 16,61
nap 100 14,67
nap 200 3,99
С2НбО2 Этиленгликоль nap 20 46,1
C2H6S Этантиол (этилмеркаптан) взд 20 22,4
С3н6о Проп-2-сн-1-ол взд 15 26,15
(аллиловый спирт) взд 20 25,68
взд 30 24,92
Физические свойства важнейших веществ
543
Продолжение табл. 3.12.5
Формула Название Газовая фаза 7 . °C о, мДж/м2
с3н8о Пропан-1 -ол 25 22,9
с3н8о Пропан-2-ол пар 18 21,2
СзНЛ*' Глицерин (99,19 %) взд 18 62,47
взд 30 62,08
взд 90 57,65
с4н10о Бутан-1ол пар, 0 26,2
взд
пар, 20 24,6
взд
пар, 50 22,1
взд
С4н10о 2-Мстил npoi 1ан-1 -ол пар 18 22,7
С4Н,оО 2-Метилпропан-2-ол нар, 20 20,7
взд
с5н12о З-Мстилбутан-1-ол взд 18 24
с5н120 Пентан-1-ол взд 15 26,03
(амиловый спирт) взд 20 25,6
взд 30 24,72
С6Н6О Фенол взд 50 37,66
взд 60 36,57
взд 70 35,51
С6Н12О Циклогексанол взд 20 26,54
взд 30 25,22
взд 60 21,54
с7н8о Фенилметанол (бензиловый спирт) взд 20 42,76
С8н18о Октан-1 -ол взд 20 27,53
Простые эфиры, альдегиды, кетоны
С2НС13О Т рихлорацетал ьде-гид (хлораль) пар 20 24,4
С2Н4О Ацетальдегид пар 20 21,2
с3н6о*' Ацетон пар, 20 23,7
взд
с4н8о Бутан-2-он пар, 20 24,6
взд
пар 75 17,8
с4н8о2 1,4-Диоксан 20 35,42
30 33,97
90 25,97
с4н10о*’ Диэтиловый эфир пар 20 16,49
пар 30 15,27
пар 40 14,05
С5Н4О2 2-Фуральдегид n2 0 43,5
(ФУРФУРОЛ) n2 58,3 37
С5Н8О2 Пентан-2,4-дион n2 0 31,6
(ацетилацетон) 25 29,2
с5н10о Пентан-3-он взд 15 25,87
взд 20 25,26
взд 30 24,37
Продолжение табл. 3.12.5
Формула Название Газовая фаза 7’, °C о, мДж/м2
С6Н12О3 2,4,6-Триметил- пар 15 26,77
1,3,5-триоксан (паральдегид) взд 20 25,9
С6н14о Дипропиловый эфир взд 20 20,55
С7н6о Бензальдегид пар 15 39,2
C8OF |8 Бис(нонафторбути-ловый) эфир 20 12,2
CsHsO’1 1 -Фенилэтанон взд 15 40,09
(ацетофенон) взд 30 39,15
с8н180 Дибутиловый эфир взд 20 22,93
С13н10о Бензофенон пар 33,5 42,38
Карбоновые кислоты и их производные
СН2О2’‘ Муравьиная взд 15 38,13
кислота взд 20 37,58
взд 30 36,48
CH5NO*' Формамид пар 20 58,2
n2 0 59,6
n2 105 50,1
QHCIA*1 Трихлоруксусная n2 80 27,8
кислота
С2Н3С1О Ацетил хлорид пар 14,8 25,8
С2Н3С1О2 Хлоруксусная n2 80 33,3
кислота n2 150 26,6
С2Н4О2*' Уксусная кислота взд 15 28,26
взд 20 27,79
взд 30 26,87
с3н6о2 Пропионовая взд 15 27,21
кислота взд 20 26,7
взд 30 25,71
С4Н6О3 Уксусный взд 15 33,37
ангидрид взд 20 32,65
взд 30 31,22
с4н8о2 Изомасляная пар 16 24,99
кислота
С4Н8О2 Масляная кислота взд 15 27,32
взд 20 26,74
взд 30 25,57
CsHio02 3 -Метил бутановая взд 15 25,78
кислота взд 20 25,3
(изовалсриановая кислота) взд 30 24,45
CsH]o02 Пентановая кислота взд 15 27,83
(валериановая взд 20 27,36
кислота) взд 30 26,35
С6Н12О2 Гексановая кислота пар 25,7 27
(капроновая кислота) пар 100 21,3
544
Новый справочник химика и технолога
Продолжение табл. 3.12.5
Формула Название Газовая фаза Г. °C ст, мДж/м2
Карбоновые кислоты г их производные
с8н16о2 Октановая кислота пар 20 28,3
(каприловая кислота) пар 100 21,6
С10Н20О2 Декановая кислота пар 31,9 27,7
(каприновая кислота) пар 90 23,4
С12Н24О2 Додекановая пар 45 28,5
кислота(лауриновая кислота) пар 103,3 23,9
С|4Н28О2 Тстрадекановая пар 56,8 28,6
кислота (миристиновая кислота) пар 150 21,3
С|6Н32О2 Пальмитиновая пар 65 28,6
кислота пар 100 26,9
С18Н34О2 Олеиновая взд 20 33,3
кислота пар 65 28,6
пар 100 26,9
С18Н36О2 Стеариновая 70 28,9
кислота 150 22,9
Сложные эфиры
С2Н4О, Метилформиат пар 20 24,62
пар 50 20,05
пар 100 12,9
пар 200 0,87
с3н6о2 Этилформиат взд 20 23,84
взд 30 22,38
с3н6о2 Мстилацетат взд 15 25,2
взд 20 24,49
взд 30 23,44
С4Н8О2 Этилацетат взд 15 24,36
взд 20 23,75
взд 30 22,25
V- 5 Н 10^2 Метилбутират пар 10 25,56
пар 210 5,09
С5Н10ОЭ Метилизобутират пар 10 24,09
С5Н10О2 Этилпропионат взд 15 24,83
взд 20 24,27
взд 30 23,16
С5н10о3 Диэтилкарбонат взд 20 26,44
взд 30 25,47
С5н10о3 Этил-2- взд 18 28,8
гидроксипропаноат
с6н10о3 Этил -3 -о ксобутаноат n2 25 32
(ацетоуксусный эфир) n2 125 21,7
С6Н10О4 Диэтилоксалат взд 15 32,83
взд 20 32,22
взд 30 31,03
Продолжение табл. 3.12.5
1 Формула Название Г азовая фаза T,°C ст, мДж/м2
С6Н12О2 Бутилацетат взд 20 24,81
С6Н12О2 Этилбутират взд 25 24,3
взд 15 25,09
взд 20 24,58
взд 30 23,26
С6Н12О2 Этилизобутират n2 0 24,6
С7н)2о4 Диэтилмалонат (малоновый эфир) взд 30 30,56
с7н14о2 Пентилацетат взд 15 26,36
взд 20 25,85
взд 30 24,8
с8н8о2 Метилбензоат n2 25 37,3
с9н10о2 Этилбензоат n2 25 34,6
с9н|0о3 Этил-2-гидроксибензоат (этилсалицилат) n2 0 39,1
С9Н14О6 Триацстин взд 20 35,15
взд 100 27,03
с|5н26о6 Трибутирин взд 20 27,98
взд 100 21,57
с18н36о2 Этилпальмитат 22 31,54
100 24,3
С19н38о4 Пальмитоилглице-рин взд 100 20,78
С21Н38О6 Тригексаноилгли- взд 20 26,32
церин (триканроин) взд 100 21,68
С2|Н42О4 Стеароил гл и цер и н взд 100 18,64
с27н50о6 Триоктаноилгл и цс- взд 20 25,68
рин (трикаприлин) взд 100 20,68
С5|Н98О6 Трипальмитин взд 100 22,57
С57НЮ4О6 Триолеин взд 20 28,71
взд 100 23,17
С57Н||0О6 Тристеарин взд 100 24,18
Амины
c2h7n /V-Мсти лметанами н (диметиламин) n2 0 18,1
c2h7n Этанамин n2 —33 24,6
(этилами и) n2 0 21,4
n2 10 20,4
c3h7n Проп-2-ен-1 -амин n2 0 26
(аллиламин) n2 20 23,6
n2 40 21,5
c3h9n Пропан-1 -амин (пропиламин) n2 20 22,4
С4Н]^ Бутан-1-амин n2 0 23,8
(бутиламин) n2 25 21,2
n2 70 17,4
C4HhN 2-Мстилиропан-1 - n2 0 22,4
амин
(изобутиламин) n2 55,8 17,7
Физические свойства важнейших веществ
545
Продолжение табл. 3.12.5
Формула Название Газовая фаза T. °C а, мДж/м2
C4HnN А-Этилэтанамин n2 0 20,8
(диэтиламин) n2 25 18,2
n2 45 16,6
c5h13n Пентан-1-амин n2 25 21,9
(пентиламин) n2 55 19,2
n2 99,8 4,67
c6h7n Анилин*’ взд 17,5 44,1
взд 20 43,66
c6h15n А,А-Диэтил- взд 15 21,25
этанамин взд 20 20,66
(триэтиламин) взд 30 19,62
c6h15n А-Пронилпропан- n2 0 23,5
1- амин
(дипропиламин) n2 50 18,2
C7H9N А-Метиланилин взд 20 39,89
c7h9n о-Толуидин взд 20 40,8
c7h9n .м-Толуидин ВЗД 20 38,3
c7h9n н-Толуидин ВЗД 50 34,9
c7h9no 1,3-Метоксианилин (анизидин) взд 20 44,1
c8hun А,А-Диметил- nap, 20 36,6
анилин взд
nap 99 26,8
c9h13n А-Мстил-А-этил- взд 20 35,48
анилин
c9h13n А-Пропиланилин взд 20 34,17
C1oH,5N А-Бутиланилин взд 20 33,76
ChH17N 2-Метил-А,А-ди- взд 20 30,19
этиланилин
c12hhn А-Фениланилин (дифениламин) nap 77,2 36,66
c14h15n А-Бензил-1 - n2 25 38,5
фенилметанамин (дибензиламин) n2 100 31.7
c14h23n A-Октил анилин ВЗД 20 32,9
c22h39n А,А-Диоктилани- ВЗД 20 31,7
лин
Другие азотсодержащие соединения
cn4o8 Т етранитрометан ВЗД 15 30,9
взд 20 30,41
взд 30 29,21
ch3no2 Нитрометан ВЗД 15 37,74
ВЗД 20 36,98
ВЗД 30 35,51
n2 0 38,1
n2 100 25,4
Продолжение табл. 3.12.5
Формула Название Г азовая фаза Г, °C о, мДж/м2
c2n2 Оксалонитрил пар -20 21,9
(дициан) взд -10 20,2
0 18,5
10 16,8
20 15,1
c2h3n Ацетон итр ил взд 15 29,76
взд 20 29,1
взд 30 27,8
c2h5no2 Нитроэтан пар 16,6 31,96
c4h5n Пиррол взд 15 38,06
взд 20 37,52
взд 30 36,23
C5H5N Пиридин n2 25 34,9
c5hun Пиперидин пар 16,5 29,89
c6f15n А,А-Бис(нента-фторэтил)-1,1,2,2,2-1 ю нтафторэтанамин 20 13,6
c6h5no2 Нитробензол взд 18 42,58
N2 35 41,7
n2 100 34,4
c6h7n 2-Метилпиридин взд 15 33,87
(а-пиколин) взд 20 33,25
взд 30 31,96
c7h7no2 1 -Метил-2 -нитробензол n2 25 40,9
c7h7no2 1-Метил-4-нитробензол n2 60 35,5
c9f21n А,А-Бис(гепта-фторпропил)-1,1,2,2,3,3,3-гепта-фторпропан-1 -амин 20 15
c9h7n Хинолин n2 25 44,7
n2 230 23
c10h14n2 Никотин взд 20,5 38,61
взд 93,5 30,99
c12f27n А,А-Бис(нонафтор-бутил)- 1,1,2,2,3,3,4,4,4- нонафторбутан-1 - 20 16,8
амин
Ci2H|0N2O Фенил-А, А, О-азоксибснзол (азоксибензол) n2 55,8 39,3
Прочие органические вещества и масла
С]2Н220ц Тростниковый сахар (расплавленный) взд 160 66,9
С18н15р Трифенилфосфин (Тпл = 80 °C) взд 45,7 40,69
Керосин взд 0 28,9
( р = 846,7 kiVmj) взд 25 26,4
взд 50 24,2
546
Новый справочник химика и технолога
Окончание табл. 3.12.5
Формула Название Газовая фаза Д °C о, мДж/м"
П рочие органические вещества и масла
Масло вазелиновое (чистое) взд 20 31,8
Масло касторовое (р = 961,2 кг/м3) взд 18 36,4
Масло оливковое (р = 915,1 кг/м3) Масло сезамовое DAB взд 18 33,06
(р = 921,2 кг/м3) Скипидар (масло терпентинное) взд 18 31,78
(р = 853,3 кг/м’) взд 18 26,79
Для этих веществ, зависимость поверхностного натяжения от температуры показана графически (рис. 13.12.1).
*2 Для переохлажденной жидкости.
Рис. 13.12.1. Зависимость поверхностного натяжения некоторых жидкостей от температуры: / — ацетон—азот; 2 — ацетофенон—азот;
3 — /,/,2,2-тетрабромэтан—азот; 4 — муравьиная кислота— азот; 5 — формиатамид (амид муравьиной кислоты)—азот;
6 — анилин—азот; 7 — бензол—пар; 8 — хлороформ—азот; 9 — диэтиловый эфир—пар; 10 — уксусная кислота—пар; / / — глицерин—азот; 12 — этиленгликоль—пар;
13 — метанол—пар; 14 — четыреххлористый углерод—пар; 15 — трихлоруксусная кислота—азот; 16 — вода—влажный воздух
Таблица 3.12.6
Поверхностное натяжение сжиженных газов на границе с собственным паром
Формула Название д °с о. мДж/м2
Простые вещества и органические соединения
Аг Аргон -188,1 13,2
-183,1 11,9
В2Н6 Диборан(б) -120 17,9
-110 16,25
-100 14.6
СО Монооксид углерода -203,1 12,11
-193,1 9,83
-188,1 8,74
СО2 Диоксид углерода -52,2 16,54
-25 9,13
0 4,62
20 1,37
25 0,5
СН4 Метан -180 18
-170 15,8
-160 13,7*
CH5N Метанамин -70 29,2
(метиламин) -20 23,6
-12 22,2
С2Н2 Ацетилен -78,1 18,2
-70 16,4
-63,1 14,7
С2Н4О Оксиран -50,1 35,8
(окись этилена) -0,1 27,6
19,9 24,3
с2н6 Этан -160 28,08
-120 21,23
-90 16,31
С2Н6О Диметиловый эфир -40,1 21
-20,1 17,9
-10,1 16,4
c2h7n /V-Метилметанамин -78 25,2
(диметиламин) 0 18,1
5 17,5
c2h7n Этанамин -74 28,9
(этиламин) 0 21,3
9,9 20,3
c3H8 Пропан -130 27,8
-90 22
-60 17,85
-40 15,15*
c3h9n М?/-Диметилметанамин -73 24,8
(триметиламин) -19 18,7
-4 П,4
c4H10 Бутан -100 27,2
-50 20,88
-20 17,22
0 14,84*
Физические свойства важнейших веществ
547
Продолжение табл. 3.12.6
Формула Название 7 . °C с>, мДж/м2
СдНю Изобутан -100 25,2
С12 Хлор(дихлор) -72 33,0
-60 31,2
-50 29,2
-40 27,3
-30 25,4
-0,1 21,7
19,9 18,4
49,9 13,4
F2 Фтор (дифтор) -210 13,6
-200 11,9
-190 10,2
НВг Бромид водорода -91,3 30,19
-77,8 27,02
-69,2 25,4
НС1 Хлорид водорода -НО 27,87
-101,4 26,25
-89,9 24,05
-80,5 22,41
HF Фторид водорода -81,8 17,6
-16,3 11,19
19,2 8,92
HI Иодид водорода -47,8 29,06
-36,6 26,96
н2 Водород(диводород) -258,1 2,83
-255,1 2,32
-253,1 1,98
H2S Сульфид водорода -84,1 33,42
(сероводород) -71,6 30,81
-62,3 28,78
H3N Аммиак -50 37,95
-40 35,6
-30 33,3
-20 31
0 26,55
10 24,25
20 22
50 15,05
Н3Р Фосфин (фосфан) -106 22,78
-94,2 20,8
3Не Гелий -271,9 0,12
-271 0,07
4Не Гелий -271,6 0,354
-270,1 0,224
-268,9 0,098
NO Оксид азота(П) -163 27,79
-156 24,12
-153,6 22,11
Окончание табл. 3.12.6
Формула Название Г. °C о, мДж/м2
n2 Азот (диазот) -203,1 10,53
-193,1 8,27
-183,1 6,16
n2o Оксид азота(1) -89,3 26,3
-50 14,39
-20 9,13
0 5,4
20 2,01
30 0,55
Ne Неон -248,4 5,61
-246,6 4,99
-244,9 4,44
О2 Кислород (дикислород) -203,1 18,3
-193,1 15,7
-183,1 13,2
so2 Диоксид серы -50,57 37,2
0,23 26,66
20 22,72
50 16,85
-50 18,9
-20 15,28
-10 14,Г
* При давлении насыщенного пара.
Таблица 3.12.7
Межфазное натяжение ртути на границе с водными растворами
Растворенное вещество Раствор Т °C с>, мДж/м2
формула название с, масс. % р- 10’3. кг/м3
С2Н4О2 Уксусная 5,3 1,006 20 344
кислота
с2н6о Этанол 20 0,969 19-20 363,2
44,5 0,927 19-20 361,1
87,8 0,825 0 366,6
98,3 0,795 19-20 364
CuSO4 Сульфат 1,3 1,012 19-20 343,2
меди(П) 6,5 1,067 19-20 334,9
9,6 1,103 19-20 331,7
НС1 Хлорово- 1,15 1,004 19-20 362,8
дородная 6,85 1,032 19-20 356,1
кислота 24,7 1,122 19-20 342,4
37,8 1,19 19-20 335,7
Н2О Вода 100 1 20 375
H2SO4 Серная 2,15 1,015 19-20 337,5
кислота 10,6 1,071 19-20 319,7
КВг Бромид _ * 1 20 318,5
калия
548
Новый справочник химика и технолога
Окончание табл. 3.12.7
Растворенное вещество Раствор Т, °C (У. мДж/м2
формула название с, масс. % р - 10 3, кг/м3
К2СО3 Карбонат 1* 20 381,6
калия
к2с2о4 Оксалат Г 1,145 19-20 353,6
калия
КС! Хлорид 1* 20 357,5
калия
KI Иодид 1* 20 318,5
калия
кмо2 Нитрит г 20 379
калия
КМОз Нитрат 1* 20 338,5
калия
NaC2H3O2 Ацетат натрия 3,1 1,014 19-20 379
NaOH Гидро- 0,7 1,006 19-20 407,1
ксид на- 7,3 1,079 19-20 423
трия 27 1,296 19-20 429,4
Ma2SO4 Сульфат 1,3 1,01 19-20 371,8
натрия 6,4 1,057 19-20 371
10,7 1,098 19-20 377,3
ZnCl2 Хлорид 10,4 1,094 19-20 359
цинка 40,6 1,426 19-20 328,7
56,3 1,683 19-20 304,7
Молярная концентрация, моль/л.
Окончание табл. 3.12.8
Формула Название Т. °C о. мДж/м2
с4н10о Диэтиловый эфир 20 379
с4н10о 2-Метилпропан-1 -ол 20 343
с5н12о З-Метилбутан-1 -ол 25 373,7
c6h5no2 Нитробензол 20 350
25 349,5
с6н6 Бензол 20 357
25 364,3
c6h7n Анилин 20 341
С6Н)4 Гексан 20 378
25 379,9
с7н8 Толуол 20 359
25 363,6
С7Н16 Гептан 25 378,7
С8Н10 (Э-КСИЛОЛ 20 359
С8Н,о .w-Ксилол 20 357
С8Н,о /7-Ксилол 20 361
С8н18 Октан 20 375
25 376
С8н|8о Октан-1-ол 20 352
с9н12 Пропилбензол 25 363,1
С|оН|4 Бутилбензол 25 362,5
С|оН2з1Ч /V-Пентилпентан-1 - 20 371
амин (дипентиламин)
СцН22О2 Ундекановая кислота 20 353
Ci8H34O2 Олеиновая кислота 20 322
Оливковое масло 20 301.8
Таблица 3.12.8
Межфазное натяжение ртути на границе с органическими жидкостями
Таблица 3.12.9
Межфазное натяжение воды на границе с органическими жидкостями
Формула Название 7’, °C су, мДж/м2
СС14 Тетрахлорметан 20 362
CS2 Дисульфид углерода (сероуглерод) 20 339
СНС13 Хлороформ 20 357
СН2С12 Дихлорметан 20 441
С2Н2Вг4 1,1,2,2-Тетрабромэтан 20 307
С2Н4Вг2 1,2-Дибромэтан 20 326
С2Н4С12 1,1 -Дихлорэтан 20 337
С2н51 Иодэтан 20 306
с2н5мо2 Нитроэтан 20 378
С2Н6О Этанол 20 364
25 376,9
с3н6о Ацетон 20 390,1
СзН8О Пропан-1-ол 20 368
25 376,5
с4н10о Бутан-1-ол 25 372,8
Формула Название Т. °C <т, мДж/м2
СС14 Тетрахлорметан 25 43,4
30 42,75*
СНС13 Хлороформ 30 31,39
С2Н4Вг2 1,2-Дибромэтан 20 37,2
40 35,03
С4Н6О3 Уксусный ангидрид 30 3,6
С4Н8О2 Этилацетат 25 6,8
30 6,8*
с4н10о Бутан-1 -ол 25 1,8
с4н10о Диэтиловый эфир 10 10,19
18 10,6
20 9,7*
30 11,13
С4Н,0О 2-Метилпропан-1 -ол 17 1,78
27 1,86
37 1,8
Физические свойства важнейших веществ
549
Продолжение табл. 3.12.9
Формула 11азвание 7 . °C о. мДж/м‘
С5Н4О2 2-Фуральдегид (фурфурол) 30 5,13
С5Н10О2 З-Метилбутановая кислота (изовалериановая кислота) 20 2,7
с5н120 З-Метилбутан-1 -ол 18 4,42
20 5,4*
с5н120 Пентан-1-ол 30 40,11
С6Н5С1 Хлорбензол 25,13 37,93
c6h5no2 Нитробензол 15,13 26,65
25,13 25,51
30 23,9*
С6н6 Бензол 25 34,1*
30 33,1
c6h7n Анилин 26 4,8
30 5,69
С6Н12 Циклогексан 20 51,01
40 50,15
С6Н i2O2 Бутилацетат 25 14,5
С6Н12О2 Гексановая кислота (капроновая кислота) 20 5,2
С6Н12О2 Этилбутират 30 13,31
СбН|2О3 2,4,6-Триметил-1,3,5-триоксан (паральдегид) 30 9,6
С6Н,4 Гексан 10 51,25
20 51,1*
30 50,66
40 50,48
С7Н7С1 (Хлорметил)бензол 30 27,1
с7н8 Толуол 25 35,7
30 34,4*
с7н14о Гептаналь 0 10,78
(энантовый альдегид) 20 13,74
40 14,82
60 12,13
с7н1402 Гептановая кислота (энантовая кислота) 20 6,6
С7Н]4О2 Пентилацетат 30 12,04
70 10*
С7н16 Гептан 25 50,85
с8н8о 1 -Фенилэтанон (ацетофенон) 30 12,08
С8Н8О2 Метилбензоат 30 16,91
с8н8о3 Метил-2-гидроксибензоат (метилсалицилат) 30 22,3
С8Н1О Этилбензол 25,13 38,26
c8h„n У,У-Диметиланилин 25 25,57
с8п16о2 Октановая кислота 18 8,2
(каприловая кислота) 60 8
Продолжение табл. 3.12.9
Формула 11азвание Г, °C о, мДж/м2
с8н1602 Этилгексаноат 0 21,03
20 21,29
30 21,15
40 21,02
С8Н18 Октан 10 51,01
20 50,98
25 50,2*
40 49,58
с8н18 2,2,4-Триметилпентан (изооктан) 25 49,3
С8Н|8О Октан-1-ол 0 7,75
16 8,7
30 8,97
40 9,32
c9h7n Хинолин 30 2,87
С9Н,о02 Бензилацетат 30 15,15
С9Н|2 Изопропилбензол (кумол) 25 38,7
С9Н|2 Пропилбензол 25,13 39,98
С9Н14О6 Триацетин 25 3,23
С9Н18О2 Пентилбутират 30 21,92
с юН 12 1,2,3,4-Тетрагидронафталин (тетралин) 25 38,6
С]оН14 Бутилбензол 25,13 38,26
С,оН18 транс-Де каги дро нафтал и н 20 51,3
(трш/с-декад ин) 40 50,44
с юН |8 цис-Де каги дро нафтал и н 20 51,74
(г/мс-декалин) 40 51,12
CioH2002 Пентилпентаноат 30 21,1
С]оН22 Декан 20 51,24
30 50,71
СцН2о02 Ундец-10-еновая кислота (ундециленовая кислота) 25 10,1
СцН24О Ундекан-1-ол 25 8,61
СцН24О 1-Этоксинонан 20 23,9
С12Н16О3 Пентил-2-гидроксибензоат (пентилсалицилат) 30 29,83
С|2Н24О2 Додекановая кислота (лауриновая кислота) 60 10,5
с12п2402 Этилдеканоат 60 22
С)4Н|2О2 Бензилбензоат 30 23,82
С14Н28О2 Этилдодеканоат 60 25
С15н26о6 Трибутирин 25 11,9
С!8Н34О2 Олеиновая кислота 20 15,7
60 15
550
Новый справочник химика и технолога
Окончание табл. 3.12.9
Формула Название 7’. °C <т, мДж/м2
С18Н34О3 12-Г идроксиоктадец-9-ено- 16 14,2
вая кислота
(рицинолевая кислота)
с18н3602 Этилпальмитат 60 26,5
С21Н42О4 Стеароилглицерин 70 1
С57Н104О6 Триолеин 16 20,4
Бензин 20 48
Керосин 20 48,3
30 46,3
Масло оливковое 20 18,2
Масло парафиновое 25 52,5
Масло хлопковое 30 20,8
70 28*
Масло эвкалиптовое 30 16,1
* Данные другого ряда измерений.
Литература
1. Русанов А.И. Фазовые равновесия и поверхностные явления. Л.: Химия, 1967. 388 с.
2. Малов В.А. Математическое обеспечение некоторых коллоидно-химических расчетов на ЭВМ. Методические указания. Л.: ЛТИ им. Ленсовета, 1988. 36 с.
3. Поверхностно-активные вещества и моющие средства: Справ. / Под ред. А.А. Абрамзона. М.: ТОО НТР «Гиперокс», 1993. 270 с.
4. Справочник химика. Л.: Госхимиздат, 1962. Т. 1. 1072 с.
5. Справочник химика. Л.: Химия, 1964. Т. 3. 1008 с.
6. Тропинина Л.В. Автореферат дис. ... канд. хим. наук. / ЛТИ им. Ленсовета. Л., 1986. 20 с.
7. Абрамзон А.А., Яковлев В.Д., Мерзликина З.К. Толкачев С.П. // Журн. прикл. химии. 1985. Т. 58, № 5. С. 1018-1022.
8. Голубятникова А.Л., Пассет Б.В., Абрамзон А.А. // Журн. прикл. химии. 1984. Т. 57, № 4. С. 874-879.
9. Кучерова Н.Л. Автореферат дис. ... канд. хим. наук. / ЛТИ им. Ленсовета. Л., 1988. 21 с.
10. Wesniewsky М., Novak В., Kedrina В., Szyma-nowsky J. // Tenside Deterg. 1987. Bd 24, N 1. S. 46-50.
И. Дашдисв P.A., Геокчаев T.B. // Охрана окружающей среды при поисках, разведке морских месторождений нефти и газа. Рига, 1986. С. 29-37.
3.13. Показатели преломления
(Е.Е. Бибик)
Показатель преломления является универсальной характеристикой индивидуальных веществ, их растворов, а также газов. Он представляет собой отношение скорости света в вакууме, к скорости света в веществе [1] и связан с поляризуемостью вещества в поле световой частоты. Последняя сложным образом зависит
от частоты (длины волны) электромагнитных волн. Эта зависимость определяется частотами резонансных колебаний электронов и ионов в веществе [2]. Длина волн видимой части спектра много больше электронных резонансных длин, принадлежащих к рентгеновскому диапазону, и значительно меньше длины волн инфракрасного диапазона, характерного для колебаний ионов. По этой причине частотная зависимость показателя преломления в видимой части спектра сравнительно проста и характеризуется его монотонным увеличением с уменьшением длины волны. Наглядной демонстрацией этой зависимости является разложение белого света на цветовые составляющие стскляной призмой.
В табл. 3.13.2-3.13.5 приводятся показатели преломления веществ [3] и растворов [4] для разных длин световых волн, соответствующих определенным спектральным линиям излучения стандартных веществ — источников излучения (водород, ртуть и др.), что гарантирует высокую точность фиксации длины волны. Это даст возможность с большой точностью измерять показатели преломления (обычно 5 знаков после запятой), атак же их дисперсию — разность показателей преломления при различных длинах волн. В таблицах приводится средняя дисперсия, найденная как разность показателей преломления на краях видимой части спектра. Она более наглядно, чем сам показатель, характеризует принадлежность веществ к тем или иным классам химических соединений. Например, ароматические соединения отличаются большей дисперсией.
Доступность точного измерения показателя преломления делает его одним из важнейших способов контроля чистоты веществ, а также состава растворов. Неспецифичность преломления света нс позволяет использовать показатели преломления для качественного анализа (идентификации) веществ. Для этой цели применяются другие оптические методы исследования, в частности, спектроскопия — зависимость величины поглощения (пропускания) световых волн от их длины.
В табл. 3.13.2-3.13.5 нижний индекс при символе показателя преломления п указывает длину волны X, а верхний — температуру Т для данной величины показателя. Вместо значения длины волны может указываться ее обозначение, принятое для некоторых линий спектра стандартных источников излучения (табл. 3.13.1).
Таблица 3.13.1
Длиня волн А и обозначения соответствующих линий спектров излучения некоторых стандартных источников
X, нм Обозначение X, нм Обозначение X, нм Обозначение
Ртуть Водород 501,6
404,7 Н 486,1 F 587,6 D
435,8 G 656,3 С 667,8
546,1 Е Гелий 706,5
577,0 447,1 Натрий
471,3 589,3 О
Физические свойства важнейших веществ
551
Таблица 3.13.2
Показатели преломления дистиллированной воды для желтой линии натрия в зависимости от температуры
7 . °C /’. °C ft/-. Т. °C ftp
0 1,33395 21 1,33290 41 1,33046
1 1,33395 22 1,33280 42 1,33031
2 1,33394 23 1,33271 43 1,33016
3 1,33393 24 1,33261 44 1,33001
4 1,33391 25 1,33250 45 1,32985
5 1,33388 26 1,33240 46 1,32969
6 1,33385 27 1,33229 47 1,32953
7 1,33382 28 1,33217 48 1,32937
8 1,33378 29 1.33206 49 1,32920
Окончание табл. 3.13.2
/'. °C Т. °C n'l> 7', °C
9 1,33374 30 1,33194 50 1,32904
10 1,33369 31 1,33182 51 1,32887
11 1,33364 32 1,33170 52 1,32870
12 1,33358 33 1,33157 53 1,32852
13 1,33352 34 1,33144 54 1,32835
14 1,33346 35 1,33131 55 1,32817
15 1,33339 36 1,33117 56 1,32799
16 1,33331 37 1,33104 57 1,32781
17 1,33324 38 1,33090 58 1,32762
18 1,33316 39 1,33075 59 1,32744
19 1,33307 40 1,33061 60 1,32725
20 1,33299
Абсолютные показатели преломления газов при нормальных условиях для зеленой линии ртути Е
Таблица 3.13.3
Газ («/..-!)• 106 Газ («/..-I) - 106 Газ («/.-!)• 106 Газ («/..-!)• 106
Воздух 293,6 n2 299,8 НВг 614,9 CO 336
Аг 283 Ne 67,2 HI 925,8 co2 450,6
Вг2 1185 о2 271,2 SO2 664 CH4 443
сь 784 Оз 520 H2S 644 (CN)2 854
н2 139,7 Хе 705,5 NO 295,5 c2H2 605
2Н; 137,9 Н2О 252,7 N2O 510 C2H4 720
Кг 429 НС1 448 NH3 379 c2H6 757
Таблица 3.13.4
Показатели преломления дистиллированной воды для спектральных линий водорода, гелия и ртути
T,°C Длина волны спектральной линии, нм
706.5 гелия 667.8 гелия 656,3 водорода (Q 587.6 гелия (D) 577.0 ртути 546.1 ртути (£) 501,6 гелия 486.1 водорода 471.3 гелия 447.1 гелия 435.8 ртути (С) 404.7 ртути (Н)
0 1,33095 1,33182 1,33209 1,334 1,33435 1,33544 1.33734 1,33811 1,33893 1,34042 1,34121 1,34376
5 1,33089 1,33175 1,33203 1,33394 1,33428 1,33537 1,33727 1,33804 1,33885 1,34035 1,34114 1,34368
10 1,33070 1,33157 1,33184 1,33374 1,33408 1,33518 1,33707 1,33784 1,33865 1,34015 1,34093 1,34348
15 1,33041 1,33127 1,33155 1,33344 1,33378 1,33487 1,33676 1,33753 1,33834 1,33983 1,34062 1,34316
20 1,33002 1,33088 1,33115 1,33304 1,33338 1,33447 1,33635 1,33712 1,33793 1,33942 1,34021 1,34274
25 1,32954 1,3304 1,33067 1,33256 1,33289 1,33398 1,33586 1,33663 1,33743 1,33892 1,33971 1,34239
30 1,32899 1,32984 1,33016 1,33199 1,33233 1,33341 1,33529 1,33606 1,33686 1,33835 1,33913 1,34166
35 1,32837 1,32922 1,32949 1,33136 1,33170 1,33277 1,33465 1,33541 1,33621 1,3377 1,33848 1.34100
40 1,32768 1,32853 1,32880 1,33066 1,33100 1,33207 1,33394 1,33470 1,33550 1,33698 1,33776 1,34028
45 1,32694 1,32778 1,32805 1,3299 1,33024 1,33131 1,33317 1,33393 1,33473 1,33621 1,33699 1,33950
50 1,32614 1,32697 1,32724 1,32909 1,32942 1,33049 1,33235 1,33310 1,33390 1,33537 1,33615 1,33866
55 1,32528 1,32611 1,32638 1,32822 1,32855 1,32962 1,33147 1,33222 1,33302 1,33449 1,33526 1,33776
60 1,32437 1,3252 1,32547 1,3273 1,32763 1,32869 1,33054 1,33129 1,33208 1,33355 1,33432 1,33681
552
Новый справочник химика и технолога
Таблица 3.13.5
Показатели преломления, их температурные коэффициенты и дисперсии органических жидкостей
В таблице приведены показатели преломления п (при 20 °C) для желтой (/7) линии натрия, для красной (С) и голубой (/•)
Аг?.. Дил 20
линий водорода; ---- и ----- — температурные коэффициенты показателей преломления; &п1С — средняя дисперсия
ДГ ДГ
( п\ - -) • 104 при температуре Т.
Название Формула 20 "с 1 ЛГ J «20 Г11) дг) Д/?“
Алканы
Гексадекан (ГГ1Л = 18,14 °C) С16н34 1,43235 4,06 1,43453 4,06 75,8
Гексан С6Н,4 1,37300 5,32 1.37499* 5,40 65,0
Гептан с7н16 1,38572 5,04 1,38764 5,06 66,9
2,2-Диметилбутан С6Н,4 1,36695 5,64 1,36887* 5,52 64,9
2,3-Диметил бутан С6Н,4 1,37313 5,38 1,37509* 5,40 65,2
2,2-Диметилиентан С7Н16 1,38023 5,18 1,38215 5,20 67,6
2,3-Диметилпентан с7н16 1,39005 5,00 1,39196 5,02 66,9
2,4-Диметилпентан С7н16 1,37954 5,24 1,38145 5,26 66,4
3.3-Диметилпентан С7н16 1,38897 4,96 1,39092 5,00 67,5
3,3-Диэтилпентан с9н20 1,41845 4,24 1,42051 4,28 71,3
2-Метилбутан С5н12 1,35218 5,80 1,35396* 5,90 60,9
2-Метилгексан С7н,6 1,38293 5.14 1,38485 5,16 66,8
З-Метилгексан С7н16 1,38671 5,08 1,38864 5,10 67,1
2-Метилпентан С6н|4 1,36961 5,38 1,37156* 5,42 64,8
З-Метилпентан С6н14 1,37470 5,46 1,37662* 5,46 64,4
Нонан с9н20 1,40342 4,60 1,40542 4,62 69,9
Октан с8н18 1,39562 4,82 1,39770* 4,80 69,0
Пентан С9Н20 1,35587 5,58 1,35769* 5,78 61,3
2,2,3,3-Тетраметилпентан С9Н20 1,42152 4,38 1,42360 4,40 72,7
2,2,3,4-Тетраметилпентан С9Н20 1,41266 4,50 1,41472 4,52 71,5
2,2,4,4-Тетраметилпентан С9Н20 1,40487 4,70 1,40694 4,70 72,5
2,3,3,4-Тетраметилпентан С9Н20 1,42016 4,36 1,42222 4,38 72,1
2,2,3-Триметилбутан С7н16 1,38746 5,00 1,38944 5,04 68,6
2,2,5-Триметилгексан С9Н20 1,39771 4,86 1,39972 4,88 69,9
2,4,4-Триметилтексан с9н20 1,40540 4,58 1,40745 4,60 71,1
2,2,4-Триметилпентан с8н18 1,38945 4,93 1,39145 4,95 69,4
З-Этилпентан С7н16 1,39147 5,08 1,39339 5,10 66,7
Циклоалканы
Бутилциклогексан С]оН2о 1,43852 4,40 1,44075 4,40 77,5
вто/?-Бутил циклогексан СюН20 1,44446 4,36 1,44673 4,38 77,3
wpew-Бутилциклогексан С1оН2О 1,44467 4,40 1,44694 4,42 78,5
Децилциклогексан С16н32 1,45108 3,94 1,45338 3,94 80,0
Децилциклопентан С15Н30 1,44637 4,06 1,44862 4,06 78,3
1,1 -Диметилциклогексан С8н16 1,42676 4,72 1,42900 4,76 77,0
1,1 -Диметилциклопентан с7н14 1,41144 5,28 1,41356 5,30 73,4
рац-{ 1 R,2R)-1,2-Диметилциклопентан с7н|4 1,40992 5,14 1,41200 5,18 72,5
(1 /?,25)-1,2-Диметилциклопентан с7н14 1,41997 5,04 1,42217 5,08 75,4
рац-{ 1 R,3R)-1,3-Диметилциклопентан с7н14 1,40686 5,18 1,40894 5,22 72,5
Физические свойства важнейших веществ
553
Продолжение табл. 3.13.5
Название Формула -|ЭЦю‘ Л Г ) л20 < AT J Ал2?,
(1 R,3S)-1,3-Диметилциклопентан С7Н,4 1,40865 5,18 1,41074 5,22 72,1
Изобутилциклогексан СюН2о 1,43637 4,48 1,43861 4,50 77,5
Изопропилциклогексан С9Н18 1,43862 4,48 1,44087 4,52 77,5
Изопропилциклопентан с8н16 1,42369 4,63 1,42582 4,64 74,3
Метилциклогексан С7Н14 1,42094 5,03 1,42312 5,06 75,3
Метилциклопентан С6Н12 1,40764 5,42 1,40983 5,40 72,4
1 - Метил-1 -этил циклопентан С8н16 1,42501 4,80 1,42718 4,84 75,0
рац-( 1 R,2S)-1 - Метил-2- с8н16 1,42719 4,76 1,42933 4,76 74,2
этилциклопентан
Пропилциклогексан С9Н]8 1,43481 4,52 1,43705 4,54 77,3
Пропилциклопентан С8н|6 1,42412 4,70 1,42626 4,74 74,4
1,1,3-Триметилциклогексан с9н18 1,42734 4,58 1,42955 4,60 77,0
1,1,2-Триметилциклопентан С8н16 1,42081 4,90 1,42298 4,94 74,9
1,1,3-Триметилциклопентан С8н16 1,40904 4,94 1,41119 4,98 74,0
(1/?,25,45)-1,2,4- с8н|6 1,41644 4,82 1,41855 4,86 73,2
Триметилциклопептан
^г/-(1/?,2/?)-1,2,4- С8н16 1,40851 4.92 1,41060 4,96 72,3
Триметилциклопентан
Циклогексан (Тпл = 6,55 °C) С6н12 1,42405 5,42 1,42630* 5,44 75,2
Циклопентан СзНю 1,40442 5,70 1,40649* 5,58 70,3
Этилцикло г i е нтан с7н14 1,41769 4,98 1,41981 5,02 73,2
Ароматические углеводороды
Бензол (ТПЛ = 5,53 °C) с6н6 1,49643 6,28 1,50112 6,35 167,0
Бутилбензол С|оН|4 1,48591 4,73 1,48979 4,77 137,2
ewop-Бутилбензол С10Н]4 1,48633 4,79 1,49020 4,82 137,1
трет-Бутиябензол СюН|4 1,48877 4,85 1,49266 4,90 137,9
Децилбензол С,бН26 1,47986 4,16 1,48319 4,20 117,2
1,2-Диэтилбензол С10Н,4 1,49935 4,77 1,50346 4,81 146,3
1,3-Диэтилбензол С]0Н|4 1,49146 4,80 1,49552 4,85 144,2
1,4-Диэтил бензол С]оН14 1,49075 4,76 1,49483 4,80 145,0
Изобутилбензол С|оН]4 1,48260 4,86 1,48646 4,92 137,1
Изопропилбензол С9Н12 1,48744 4,94 1,49145 4,99 142,7
о-Ксилол С8Ню 1,50100 5,07 1,50545 5,13 158,8
jw-Ксилол с8н10 1,49283 5,18 1,49722 5,24 156,4
n-Ксилол (Тпл = 13,26 °C) С8Ню 1,49141 5,22 1,49582 5,28 157,1
1 -Метил-2-этилбензол С9Н)2 1,50028 4,89 1,50456 4,93 151,8
1 -Метил-3-этилбензол С9Н|2 1,49238 5,01 1,49660 5,06 150,0
1 -Метил-4-этил бензол С9Н12 1,49079 4,96 1,49500 5,01 149,7
Пропилбензол С9Н]2 1,48799 4,96 1,49202 5,00 143,6
1,2,3-Триметилбензол С9Н12 1,50952 4,79 1,51393 4,82 157,2
1,2,4-Триметилбензол С9Н12 1,50047 4,88 1,50484 4,93 156,0
1,3,5-Триметилбензол с9н,2 1,49507 4,96 1,49937 5,00 153,6
Толуол С7н8 1,49243 5,61 1,49693 5,67 160,4
Этилбензол С8Н1О 1,49162 5,34 1,49588 5,38 151,6
554
Новый справочник химика и технолога
Продолжение табл. 3.13.5
Название Формула 20 «с -Ню1 1 ЬТ ) 20 < АГ )
Галогенпроизводные углеводородов
Бромбензол С6Н5Вг 1,5546 4,8 1,5601 4,9 193,6
1 -Бромбутан С4Н9Вг 1,4369 5,0 1,4398 5.0 93,5
1-Бромнафталин (ГШ| = 6,2 °C) С10Н7Вг 1,6494 4,4 1,6582 4,4 325,5
1 -Бромнронан С3Н7Вг 1,4318 5,2 1,4344 5,2 94,4
2-Бромпропан С3Н7Вг 1,4229 5,6 1,4256 5,7 95,4
Бром этан С2Н5Вг 1,4220 5.5 1,4248 5,6 95,0
1,2-Дибромэтан С2Н4Вг2 1,5345 5,8 1,5387 5,8 142,5
Дииодметан СН212 1,7310 6,1 1,7411 6,4 275,8
1,2-Дихлорэтан С2Н4С12 1,4427 5,0 1,4450 5,1 85,8
Иодбензол с6н51 1,6129 5,3 1,6202* 5,5 253,9
Иодметан СН31 1,5257 6,5 1,5312 6,5 183,3
Иодэтан С2Н51 1,5090 6,2 1,5137 6,3 165,7
2-Метил-1 -хлорпронан С4Н9С1 1,3962 5,2 1,3984 5,2 72,5
2-Метил-2-хлорпропан С4Н9С1 1,3830 5,2 1,3852* 5,2 73,2
Т етрахлорметан СС14 1,4574 5,4 1,4603 5,5 96,5
Трибромметан (бромоформ) СНВг3 1,5924 5,6 1,5977 5,7 181,5
Трихлометан (хлороформ) СНС13 1,4430 5,8 1,4456 5,9 90,4
Хлорбензол С6Н5С1 1,5197 5,4 1,5248 5,4 172,3
1 -Хлорбутан С4Н9С1 1,4003 5,0 1,4024* 5,1 70,2
1 -Хлорпропан С3Н7С1 1,3866 5,2 1.3887* 5,4 72,1
2-Хлорпропан С3Н7С1 1,3762 5,5 1,3783 5,6 72,0
Кислородсодержащие соединения
Ацетон С3Н6О 1,3571 4,9 1,3591 0,5 67,5
Ацетофенон (Гпл = 19,6 °C) С8н8о 1,5285 4,5 1,5340 4,6 200,5
Бутан-1 -ол с4н10о 1,3972 3,9 1,3993 3,9 69,9
Бутан-2-ол с4н10о 1,3950 4,6 1,3970 4,9 70,4
Глицерин С3н8о3 1,4721 2,2 1,4744 2,2 80,7
1,4-Диоксан (Гпл = 11,8°С) с4н8о2 1,4202 4,2 1,4223 4,3 73,3
Диэтиловый эфир С4н10о 1,3510 5,6 1,3528 5,6 62,4
Диэтилоксалат СбН]о04 1,4081 4,1 1,4103* 4,2 75,0
Изомасляная кислота С4н8о2 1,3913 4,0 1,3965* 4,0 70,6
Масляная кислота С4Н8О2 1,3959 4,2 1,3980 4,3 70,7
Метанол СН4О 1,3270 4,0 1,3286 3,9 54,9
З-Метилбутановая кислота С5Н10О2 1,4010 4,1 1,4033* 4,1 75,1
2-Метил пропан-1 -ол С4н10о 1,3938 3,8 1,3958 3,9 70,1
Муравьиная кислота (Д1Л = 8,4 °C) СН2О2 1,3695 3,8 1,3716 3,8 71,0
Пентановая кислота С5Н10О2 1,4061 4,2 1,4084* 4,2 75,5
Пентан-2-он С5н|0о 1,3905 4,5 1,3927* 4,5 71,1
Пропан-1 -ол С3н8о 1,3832 3,7 1,3854 3,8 67,7
Пропан-2-ол С3н8о 3,4 1,3773 3,9
Проп-2-ен-1-ол С3Н6О 1,4097 4,1 1,4125* 4,1 96,6
Пропионовая кислота С3н6о2 1,3846 3,8 1,3869* 3,8 69,7
Уксусная кислота (ГП1 = 16,6 °C) С2Н4О2 1,3698 3 7 1,3720* 3,8 68,6
Уксусный ангидрид С4Н6О3 1,3881 3,9 1,3902 4,1 71,6
Физические свойства важнейших веществ
555
Продолжение табл. 3.13.5
Название Формула \ЬТ ) L at)
Фенилметанол С7н8о 1,5358 4,0 1,5405 4,0 172,5
Циклогексанон С6Н|0О 1,4478 3,6 1,4502 3,7 86,2
Циклонентанон С5Н8О 1,4348 4,0 1,4372 4,2 81,9
Этанол С2н6о 1,3613 4,0
Этилацетат С4Н8О2 1,3707 4,8 1,3726 4,9 65,6
Этилбензоат с9н10о2 1,5010 3,9 1,5055 4,1 163,5
Этиленгликоль С2н6о2 1,4296 2,6 1,4318 2,6 73,9
Этилформиат С3Н6О2 1,3583 4,4 1,3603 4,4 63,8
Азотсодержащие соединения
Анилин (Tnj, = -6,1 °C) c6h7n 1,5792 5,1 1,5861 5,2 250,7
Ацетонитрил c2h3n 1,3422 4,6 1,3437 4,6 57,9
Бензонитрил c7h5n 1,5229 4,8 1,5284 4,8 193,5
N,N- Ди метил ан ил ин (Тпл = 2,45 °C) c8h,,n 1,5516 4,8 1,5583 5,0 246,2
2,6-Диметилпиридин c7h9n 1,49334 1,4977 156,1
А,А-Диэтилэтанамин (триэтиламин) c6h15n 1,3986 5,4 1,4010 5,4 83,6
А-Метиланилин c7h9n 1,5641 5,2 1,571 5,3 250,5
2-Метилпиридин c6h7n 1,49657 5,19 1,50101 5,20
З-Метилпиридин c6h7n 1,50232 1,50682 161,3
4-Метилпиридин c6h7n 1,50144 1,50584 157,6
Нитробензол (Тп11 = 5,7 °C) c6h5o2n 1,5455 4,6 1,5524 4,6 254
Нитрометан ch3o2n 1,3793 4,2 1,3820 4,2 91,3
Пиперидин C5HhN 1,4501 4,7 1,4529 4,8 92,6
Пиридин c5h5n 1,50556 5,51 1,51020 5,50 166,5
Пиррол c4h5n 1,50569 4,69 1,51015 4,7 157,8
Пирролидин c4h9n 1,44045 5,32 1,44283 5,3 83,8
Хинолин c9h7n 1,6193 1,6269 4,8
Сераорганические соединения
Бутан-1 -тиол c4H10s 1,44022 5,74 1,44298 5,48 96,0
Бутан-2-тиол C4H|oS 1,43399 5,51 1,43673 5,59 94,5
Диметилдисульфид c2h6s2 1,52163 5,88 1,52592 5,94 152,0
Диметилсульфид c2H6s 1,43249 6,42 1,43547 6,47 93,7
Диэтилдисульфид c4H10s2 1,50354 5,28 1,50731 5,33 132,6
Диэтилсульфид C4H10S 1,44015 5,62 1,44298 5,64 98,3
2-Метилпропан-2-тиол C4H,0S 1,42046 6,35 1,42046 6,23 94,5
1 -(Метилсульфанил)проиан c4H10s 1,44158 5,49 1,44435 5,47 97,1
2-(Метилсульфанил)пропан c4H10s 1,43631 5,56 1,43914 5,60 97,7
(Метилсульфанил)этан c3H8s 1,43747 5,94 1,44035 5,98 101,2
2-Метилтиофен C5H6S 1,51570 5,82 1,52035 5,84 164,8
3-Метилтиофен C5H6S 1,51585 5,78 1,52042 5,87 162,5
Пентан-1 -тиол c5H12s 1,44420 5,08 1,44692 5,12 94,0
Пропан-2-тиол c3H8s 1,42277 6,17 1,42554 6,27 97,1
Тетрагидро-2//-тиопиран c5H10s 1,50358 5,08 1,50684 5,11 112,6
556
Новый справочник химика и технолога
Окончание табл. 3.13.5
Название Формула 20 n(. ( An.. . - —- -10 AT ) < AT )
Сераорганические соединения
Тетрагидротиофен C4H8S 1,50154 5,20 1,50483 5,21 114,1
Тиетан C3H6S 1,50660 5,67 1,51020 5,78 126,2
Тиофен C4H4S 1,52403 6,25 1,52890 6,33 173,2
Углерода дисульфид (сероуглерод) CS2 1,6182 7,70 1,6277 7,8 341,4
Этантиол C2H6S 1,42810 6,48 1,43105 6,52 102,6
Для линии I) гелия.
Литература
1. Яворский Б.М., Детлаф А.А. Справочник по физике. М.: Наука, 1964. 848 с.
2. Калитеевский Н.И. Волновая оптика. М.: Наука, 1971.376 с.
3. Справочник химика. Л.: Госхимиздат, 1962. Т. 1. 1072 с.
4. Справочник химика. Л.: Химия, 1964. Т. 3. 1008 с.
Раздел 4. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
Автор: к. х. н., доц. Л.М. Быкова
4.1. Бензол
Бензол в органической химии является столь же важным веществом, как и серная кислота в неорганической химии. И если последняя известна химикам еще с древнейших времен, то бензол был открыт лишь в начале XIX в., на заре рождения новой химии — той химии, которая лидирует в наши дни, с которой связано появление различных полимеров, искусственных тканей и волокон, синтетических красителей и др. И путь к многообразию продуктов химии лежит именно через бензол — ничем не примечательную, прозрачную жидкость с резким запахом, которой и название дали не сразу, формулу не могли определить, а строение было загадкой и предметом многочисленных научных дискуссий.
Бензол (бензен) — это простейший представитель класса ароматических' соединений (аренов). Фактически бензол является родоначальником ароматических углеводородов — наиболее многочисленного класса органических соединений. Быстрое развитие химии ароматических соединений в течение последующих десятилетий после открытия бензола стимулировалось успехами первых попыток создания теории строения бензола.
1 Название «ароматические» (от греч. aroma, род. падеж aromatos — благовоние) появилось в связи с тем, что первые соединения этого ряда были выделены из природных смол и бальзамов и обладали приятным ароматным запахом. Так. еще в XVI в. из бензойной смолы были выделены бензойная кислота и бензиловый спирт, из масла горького миндаля — бензальдегид, из сосновой смолы — цимол и т. д. Позднее появилось понятие «ароматичность», характеризующее совокупность структурных, энергетических свойств и особенностей реакционной способности циклических структур, обладающих системой сопряженных связей и замкнутой электронной оболочкой. Термин был введен немецким химиком Ф.А. Кекуле в 1865 г. для описания свойств соединений, структурно близких к бензолу, который по своему строению оказался простейшим представителем ароматических соединений.
Бензол преимущественно использовали для получения нитро- и динитросоединений, а также бензолдисульфокислоты. В настоящее время бензол применяется в основном в производстве циклогексана, кумола, этилбензола и других алкилбензолов, используемых для получения синтетических каучуков, пластических масс, синтетических волокон, красителей, поверхностно-активных веществ и др. Бензол широко применяется также в качестве растворителя и экстрагента в производстве лаков и красок, используется как высокоактивная добавка к моторным топливам.
4.1.1. Мировой рынок бензола
Бензол — один из самых распространенных нефтехимических продуктов и самое распространенное ароматическое соединение. В настоящее время спрос на бензол во всем мире определяется производством этилбензола, кумола (изопропилбензола) и циклогексана. В 2004 г. доля этих веществ в общем потреблении бензола тремя самыми активными регионами: Северной Америкой, Западной Европой и Японией, — составила 88 %. В последнее время особенно вырос спрос на кумол, являющийся сырьем для получения фенола, производство которого, а соответственно и фенолформальдегидных смол, растет в связи с их новым применением в процессе получения поликарбонатов (термостойких полимеров).
Мировой спрос на бензол, по прогнозам аналитиков, будет расти в среднем на 5,2 % в год до 2008 г. и составит в 2008 г. ~42 млн т. Наиболее быстрый рост будет наблюдаться в Азии (за исключением Японии), а также в других регионах мира (главным образом на Ближнем Востоке и в Южной Америке), в среднем — 13,6% в год. С учетом более долгосрочных прогнозов консалтинговой фирмы CMAI (Chemical Market Associates, Inc), спрос на бензол будет расти до 2020 г. в среднем на 2,8 % в год и к концу этого срока составит 57 млн т.
В 2004 г. мировые мощности по производству бензола составляли более 40 млн. т/год. Доли США и Западной Европы равнялись 23 и 22 % от общего объема мировых мощностей соответственно. За ними следовала
558
Новый справочник химика и технолога
Япония (13 %). К началу 2007 г. ожидается снижение объема мощностей этих доминирующих регионов с 58 до 54 %. Наибольший прирост мощностей до 2007 г. будет происходить в Азии (исключая Японию) и на Ближнем Востоке: их доля увеличится с 16 до 19% и с 23 до 24 % соответственно. Большинство новых предприятий будет построено на Ближнем Востоке, где планируемый рост мощностей должен составить 12 % в год.
С учетом планов строительства новых мощностей и расширения имеющихся к 2008 г. основными импортерами бензола будут страны Северной Америки (-860 тыс. т/г) и Западной Европы (-560 тыс. т/г). Экспортные поставки бензола будут осуществляться в основном из Южной Америки (166 тыс. т/г), Саудовской Аравии и Индии (-300 тыс. т/г). К 2008 г. Юго-Восточная Азия станет экспортировать, а не импортировать бензол (объем экспорта уже достигает 200 тыс. т/г).
Во всех странах цены на бензол в последнее время выросли. Прогнозы аналитиков звучат неутешительно: до тех пор, пока не подешевеет сырье, а объемы производства не увеличатся, оптовая цена на бензол останется высокой. Большинство экспертов основной причиной неустойчивости цен на бензол называют высокие цены на сырую нефть. По другим сведениям, внутренний рынок бензола уже в значительной степени освободился от «энергетической зависимости», т. е. от высокой цены на сырье. Даже в то время, когда цена на нефть оставалась постоянной, цены на бензол продолжали неуклонно расти.
Самая высокая стоимость бензола в мире — на рынках США. Ежегодно США не хватает -600 тыс. т бензола, который раньше без проблем импортировался из Южной Америки и северо-западной Азии. Но сейчас эти регионы обзавелись собственными потребителями бензола, и США приходится вести ожесточенную борьбу за контракты на поставку бензола.
На рынках Европы в 2005 г. самая высокая цена на бензол (с отгрузкой) составляла 860 долларов за т. Однако, когда из-за плановых и неплановых остановок некоторых производств в Германии, Голландии и Англии Европа не досчиталась 55 тыс. т бензола, цена на бензол доходила до 900 и более долларов за т.
Необычайно резкий рост цен на бензол во всем мире произошел в середине 2004 г. Это было вызвано рядом причин, среди которых следует отметить дефицит свободных мощностей, увеличивающийся спрос на топливные ресурсы, рост цен на нефтепродукты, появление новых проблем у производителей бензола и пр. К августу 2004 г. контрактные цены на бензол достигли максимального уровня: 1160 долларов за т в США и 1140 долларов за т в Западной Европе, хотя на начало года эти цифры составляли -500-600 долларов за т. Хотя такая ситуация была кратковременной, по прогнозам аналитиков, она может иметь далеко идущие последствия. Возможно, потребители сделают ряд «защитных» инвестиций. Весьма вероятно, что в глобальной торговле бензолом повысится уровень участия торгующих по
требителей. Ожидается также существенный рост форвардных и финансовых рынков по мере того, как прямые и косвенные потребители бензола будут приспосабливаться к ценам.
Азиатские цены на бензол ниже европейских. Однако доставка бензола из Азии в Европу связана не только с большими расходов, но и с большим риском. Поэтому азиатский бензол все чаще оседает на внутреннем рынке и используется собственными потребителями, число которых возрастает с каждым годом.
По данным российских аналитиков, Россия производит бензола почти в 10 раз меньше, чем США и Европа. Производство бензола в России ведется на предприятиях нефтеперерабатывающей (нефтяной бензол) и металлургической и коксохимической промышленности (каменноугольный бензол). В общем объеме производимого в России бензола доля нефтяного бензола составляет -75 %.
Среди предприятий нефтехимического комплекса наиболее крупными производителями нефтяного бензола являются: ОАО «Нижнекамскнефтехим» (Татарстан), ОАО «Сибнефть-Омский НПЗ» (г. Омск) и ОАО «Салаватнефтеоргсинтез» (Башкортостан). На долю этих предприятий в общероссийском производстве нефтяного бензола приходится -50 %. Крупными производителями бензола являются также предприятия: «Ставролен» (г. Буденовск), ООО «Киришинефтеорг-синтез» (Ленинградская обл.), ОАО «Сибур-Нефтехим» (г. Нижний Новгород), ОАО «Славнефть-Ярославнефтеоргсинтез» (г. Ярослав). Бензол производится также ОАО «Череповецкий «Азот» (г. Череповец).
Основной объем (49,5 %) каменноугольного бензола производится тремя предприятиями Кемеровской области: ОАО «Западно-Сибирский металлургический комбинат» (г. Новокузнецк), ОАО «Кокс» (г. Кемерово) и ОАО «Кузнецкий металлургический комбинат (г. Новокузнецк). Каменноугольный бензол для синтеза выпускается также ОАО «Западно-Сибирский МК» (г. Новокузнецк), ОАО «Новолипецкий МК» (г. Липецк)), ОАО «Северсталь» (г. Череповец) и ОАО «Мечел» (г. Челябинск), ОАО «Алтай-Кокс» (г. Заринск), Губахинский коксохимический завод (г. Губаха).
Более 95 % производимого в России бензола используется внутри страны. Наиболее крупным импортером российского бензола является Финляндия, в основном закупая у металлургических компаний бензол сырой (неочищенный). Ежегодно Россией импортируется -15 тыс. т бензола, в основном из Украины и Казахстана, что составляет менее 2 % российского потребления.
Ситуация на российском рынке бензола характеризуется неизменным дефицитом этого продукта. Рост производства бензола в России в настоящее время находится на уровне 7,5-8 %, а рост производства продуктов его переработки — 10-25 %. Большинство предприятий, производящих бензол, имеют долгосрочные договоры о его поставках или используют бензол для собственных нужд. Так, ОАО «Салаватнефтеоргсинтез» в связи
Ароматические соединения
559
с пуском собственного производства стирола полностью прекратил поставки бензола на рынок, а это ~8,5 тыс. т в месяц. В последнее время не поставляют на рынок бензол такие предприятия, как «Ставролен» и ОАО «Сибнефть-Омский НПЗ».
Некоторые крупные потребители бензола, испытывая острый дефицит в сырье, планируют организовать производство собственного бензола. Уже принято решение о создании производства бензола на ЗАО «Куй-бышевазот» (г. Тольятти, Самарская обл.) — крупнейшем производителе капролактама в России (бензол является основным сырьем для производства капролактама). Начать производство бензола на новом предприятии планируется в начале 2009 г. Объем производства составит —100 тыс. т бензола в год. Решение сырьевой проблемы позволит «Куйбышевазоту» сохранить свое лидирующее положение на рынке капролактама.
Крупный нефтехимический инвестиционный проект реализуется в Татарстане. Проект предусматривает строительство комплекса, в состав которого войдут три завода по переработке нефти с производством ароматических соединений, в том числе бензола.
Ряд инвестиционных проектов по модернизации и запуску новых производств, тесно связанных с бензолом, планирует осуществить в период 2005-2008 гг. компания ОАО «Казаньоргсинтез», в частности, планируется строительство производства бензола мощностью 35 тыс. т / год.
Один из реальных путей уменьшения дефицита бензола в России — это выпуск отечественного бензина в соответствии со стандартом «Евро-3». Содержание ароматических соединений в таком бензине не должно превышать 1 % (в настоящее время содержание ароматических соединений составляет 5 %). Извлеченный из бензина нефтяной бензол будет заметным вкладом в общий объем производимого в России бензола.
Бывшие республики СНГ также испытывают дефицит бензола и пытаются найти решение этой проблемы. В Белоруссии в 2006 г. введена в эксплуатацию установка по производству бензола мощностью 55 тыс. т/год на Мозырском нефтеперерабатывающем заводе. Будет также внедрена технология извлечения бензола из высокооктановых бензинов, что позволит улучшить качество и конкурентоспособность бензина и дополнительно получить чистый бензол. После проведения этих мероприятий Мозырский нефтеперерабатывающий завод сможет заполнить нехватку бензола для белорусских предприятий. В настоящее время около 60 тыс. т бензола импортируются из России. Предварительные расчеты показывают, что собственное производство позволит снизить цену на бензол на 30 %. Основным потребителем бензола на сегодняшний день является ОАО «Гродно Азот», который из этого сырья производит широкий спектр химической продукции, в том числе растворители, компоненты для парфюмерии и косметики.
Более подробную информацию о мировом рынке бензола можно получить на сайтах:
www.chembz.ru;www.rccnews.ru;www.rcc.ru; www.himtrade/ruwww.tyumen.sibneft.ru;www.lh.ru; research.rbc.ru; www.3plp.ru;www.avias.com;
www.cmna.ru;neft.tatcenter.ru; www.i63.ru; vestnik.zos-v.ru; www.rccgroup.ru;www.infogeo.ru; www.merchantconsult.com;www.rusenergy.com;
e-news.com; business.dp.ua
4.1.2. История бензола
В 2005 г. исполнилось 180 лет со дня открытия бензола, именно в 1825 г. английский физик и химик Майкл Фарадей выделил его из каменноугольной смолы. На это открытие Фарадея подтолкнул простой случай. В начале XIX в. в Лондоне для уличного освещения стали использовать так называемый «светильный газ», получаемый из каменноугольной смолы. Жители были недовольны новым освещением (Вальтер Скотт писал: «мир перевернулся, Лондон будет освещаться угольным дымом»), производители свечей открыто громили новые фонари. Сам же «светильный газ» имел существенный недостаток: со временем он утрачивал свою горючесть, а на дне баллонов оседала неизвестная маслянистая жидкость. Особенно обильным было ее выделение в холодную погоду. Этой проблемой, чисто из практических соображений, и решил заняться М. Фарадей.
Исследуя конденсированные остатки коксового газа, М. Фарадей получил неизвестный ранее углеводород. Выделив соединение в чистом виде и подвергнув его элементному анализу, Фарадей обнаружил, что оно содержит только два элемента: углерод и водород в соотношении 11,4 : 1. Поэтому Фарадей определил состав нового вещества как СП и изучил его некоторые физические и химические свойства. Истинная формула вещества С6Н6 была установлена позже, когда была определена его молекулярная масса.
Открытие нового вещества не вызвало большого интереса, и лишь в 1834 г. вспомнили об открытии Фарадея. Немецкий химик Э. Митчерлих, нагревая негашеную известь СаО с бензойной кислотой С6Н5СООН (она содержится во многих ягодах, в частности, в клюкве и бруснике, и препятствует их гниению), получил неизвестную легкокипящую жидкость с резким запахом. Анализ ее показал, что это то же соединение, которое получил Фарадей.
Митчерлих признал приоритет Фарадея, и назвал вещество бензином, т. к. получил соединение из бензойной кислоты. Против этого названия выступил ряд ведущих химиков во главе с немецким химиком Ю. Либихом. Они полагали, что суффикс «-ин» указывает на присутствие в молекуле атомов азота, и поэтому предложили заменить его суффиксом «-ол», исходя из маслянистости вещества (от англ, oil — «масло»), а соединение, соответственно, называть бензолом. Однако это название также не было вполне корректным, т. к. суффикс «-ол» уже стал атрибутом спиртов (этиловый спирт — этанол). Споры о названии продолжались
560
Новый справочник химика и технолога
довольно долго, в результате, вещество С6Н6 в английском языке получило название «бензен» («-ен» — суффикс, указывающий на двойную связь), а в остальном мире авторитет Либиха был настолько силен, что закрепилось название «бензол».
В 1845 г. немецкий химик А. Гофман доказал присутствие бензола в каменноугольной смоле, а ученик Гофмана Мансфильд в 1848 г. выделил бензол из смолы и показал, что выход бензола зависит не только от состава каменноугольной смолы, но и от способов ее обработки и хранения. Синтетическим путем бензол был получен в 1870 г. французским химиком М. Вертело, который при исследовании химических свойств ацетилена обнаружил, что это вещество тримеризуется в бензол.
Долгое время строение бензола было предметом многочисленных дискуссий и споров. Всему виной были удивительные противоречия в свойствах бензола. Если сравнить бензол с гексаном QHu — насыщенным углеводородом, то видно, что бензол С6Н6 — «ненасыщенное» соединение, в его молекуле не достает 8 атомов водорода. Поэтому вначале предлагались ненасыщенные структуры, например, СН2=С=СН—СН=С=СН2 и, соответственно, предполагалось, что бензол, как все ненасыщенные соединения, будет обесцвечивать бромную воду и раствор перманганата калия, т. е. будет веществом довольно активным. Но все оказалось совсем не так: бензол не обесцвечивал ни бромную воду, ни раствор перманганата калия. А «насытить» бензол водородом или хлором удавалось с большим трудом, реакции проходили только при высокой температуре, давлении или требовали интенсивного ультрафиолетового облучения. И даже в этом случае при гидрировании получался не гексан, а циклогексан С6Н]2. Химики об этом не знали, поскольку не предполагали существование циклических молекул.
Анализируя различные экспериментальные данные, химики всех стран искали ключ к разгадке строения бензола. Успеха добился немецкий химик Август Кеку-ле, и легенда гласит, что идея пришла к нему во сне. Однажды, размышляя о строении бензола, Кекуле задремал и увидел во сне змею, которая вцепилась в собственный хвост. Этот сон послужил толчком к гипотезе, которая впоследствии блестяще подтвердилась, гипотезе о циклическом строении бензола.
В 1865 г. Кекуле предложил для бензола циклическую гексатриеновую структуру, в которой атомы углерода, замкнутые в шестичленное кольцо, связаны между собой попеременно простыми и двойными связями, а каждый атом углерода еще соединен с водородом — до насыщения валентности.
Н
Н
Предполагаемая циклическая структура бензола вызвала у химиков большой интерес, и они с усиленной энергией принялись изучать свойства бензола и его производных. И сразу же натолкнулись на трудности. Формула Кекуле предусматривала для производных бензола существование изомеров — веществ одинакового состава, но разного строения, например, таких:
На практике же любые попытки получить два разных вещества приводили к одному и тому же соединению. Поэтому уже в 1867 г. для бензола было предложено несколько десятков разнообразных структур. Среди них наиболее интересными являются структуры К. Дьюара (а), А. Клауса (б) и А. Ладенбурга (в):
Продолжая отстаивать свой вариант циклического строения бензола, Кекуле, чтобы теория не расходилась с практикой, в 1872 г. выдвинул гипотезу об осцилляции между возможными положениями двойных связей в молекуле бензола. Он предположил, что атомы углерода в бензоле быстро колеблются — «осциллируют» и каждые два соседних атома попеременно соединены то простой, то двойной связью:
Кекуле полагал, хотя и не мог этого строго доказать, что все шесть атомов углерода в кольце эквивалентны. С учетом дополнительной симметрии молекулы, обусловленной осцилляцией, формула Кекуле позволяла объяснить, почему бензол образует только один изомер при монозамещении С6Н5Х и три изомерных продукта C6H4XY при дизамещении.
Однако и эта гипотеза не удовлетворила химиков. Многочисленные факты подталкивали их к мысли, что в бензоле нет ни простых, ни двойных связей, а есть... «полуторные». Эту идею впервые высказал немецкий химик И. Тиле на рубеже XIX и XX вв. Он предположил, что атомы углерода в молекуле бензола соединены простыми связями, а остаточные валентности равномерно распределяются по всему кольцу. Таким образом, Тиле утверждал, что в кекулевской структуре бен
Ароматические соединения
561
зола сопряжение происходит по замкнутому кольцу и вследствие этого молекула бензола имеет гексагональную симметрию. Поскольку цепь сопряжения не имеет концов, именно этим объясняется относительно невысокая реакционная способность бензола по сравнению с ненасыщенными соединениями. С учетом этих представлений формулу бензола стали изображать в виде правильного шестиугольника с кольцом посередине.
В настоящее время для изображения бензола (7) принято использовать структурные формулы Кекуле (/«) или Тиле (16)
4.1.3. Строение бензола
В настоящее время на основе рентгенографических и спектральных исследований было установлено, что молекула бензола совершенно плоская и все связи С-С в бензоле имеют одинаковую длину. Было доказано, что молекула бензола представляет собой правильный шестиугольник с внутренними углами 120° и расстояниями между соседними атомами углерода 0,139 нм. Это среднее значение между длинами простой (0,154 нм) и двойной (0,133 нм) связей. Порядок связи в молекуле бензола 1,672. Шесть атомов водорода, связанных по одному с каждым из атомов углерода, лежат на расстоянии 0,109 нм от кольца, в плоскости кольца и на радиусах, направленных от кольца.
Н
0,139 нм
В этой формуле три валентных электрона каждого из углеродных атомов входят в состав связей, каждая из которых образована двумя электронами. Однако у каждого атома углерода остается еще по одному свободному валентному электрону. Если эти электроны локализовать в пары, как в классической структуре цикло-гексатриена, получится формула, предложенная для бензола Кекуле (1а). Если электроны распределить по всему кольцу, получим формулу Тиле (16).
2 Порядок связи может варьировать от 1 до 3. Порядок простой связи С—С в этане принимают равным 1, связи С=С в этилене — 2, связи С=С в ацетилене — 3.
В полной объеме особенности физических и химических свойств бензола удалось объяснить только в рамках квантовой химии.
В квантовохимической модели молекулы бензола каждый атом углерода рассматривается как находящийся в состоянии л/22-гибридизации3 и образующий три копланарных (расположенных в одной плоскости) 5/22-гибридных о-связи4 с валентными углами, равными 120°. На образование трех связей (двух С—С и одной С—Н) каждый углеродный атом затрачивает три из четырех своих валентных электронов. Оставшиеся шесть электронов углеродных атомов располагаются на гантелеподобных /2-орбиталях (по одному у каждого атома углерода). Оси /2-орбиталей взаимно параллельны и расположены под прямым углом к плоскости бензольного кольца. Эти электроны образуют л-связи4. Особенность бензола состоит в том, что каждый из /2-электронов взаимодействует с /2-электронами смежных углеродных атомов, образуя общую л-систему — ароматический секстет («секста» в переводе с греческого шесть). Поэтому все /2-электроны распределяются симметрично вокруг кольца и могут перемещаться по кольцу в том или ином направлении, т. е. л-систему молекулы бензола можно рассматривать как непрерывную.
Таким образом, в молекуле бензола достигается идеальное сопряжение всех двойных связей, поскольку электроны, образующие эти связи, принадлежат всеми шести атомам углерода. Такие электроны называют делокализованными.
Другой способ описания делокализации — представление структуры молекулы бензола (7) как промежуточной между различными структурными формулами (каноническими структурами). Для бензола приняты пять канонических структур: две структуры Кекуле (1а и la') и три структуры Дьюара (1 в, г, д). Как показывает расчет, вклад этих структур в резонансную гибридизацию молекулы бензола неравноценный: 0,39 для каждой ке-кулевской структуры и 0,07 для каждой дьюаровской
? В валентных состояниях углеродных атомов электроны распределены не на свободных 5- и р-орбиталях, а на смешанных, или так называемых гибридных орбиталях. Гибридные орбитали имеют более высокую энергию, чем 5- и /2-орбитали,
но они выгоднее геометрически для образования связи, т. к. эффективнее перекрываются с орбиталями других атомов и, следовательно, образуют более прочные связи.
4 о-Связь — это связь, образованная электронной парой в результате перекрывания 5- и р-атомных орбиталей, обладающих цилиндрической симметрией относительно линии связи. л-Связь — это связь, образованная электронной парой в результате перекрывания р-атомных орбиталей, антисимметричных относительно плоскости, проходящей через связь. Простая связь образована только о-молекулярными орбиталями. Двойная связь состоит из одной о- и одной л-связи. Систему чередующихся простых и двойных связей называют системой сопряженных двойных связей.
562
Новый справочник химика и технолога
структуры. Поэтому бензол нередко рассматривают как резонансный гибрид5 двух структур Кекуле (1а и la').
На рис. 4.1.1. представлена модель молекулы бензола. Бензольное кольцо, представляющее собой плоский шестиугольник, находится в центре (все о-связи: С-С и С-Н — светлые). л-Электронные облака (ароматический секстет), расположенные выше и ниже кольца, слегка затемнены.
Рис. 4.1.1. Модель молекулы бензола
Так как делокализация электронов всегда приводит к выигрышу энергии, бензольное кольцо отличается большой устойчивостью6. Нарушение сопряжения
в каком-либо месте бензольного кольца сразу же приводит к потере устойчивости. Поэтому очень трудно получить продукты присоединения к бензолу каких-либо веществ с разрывом только одной связи.
Доказано, что молекула бензола имеет ось симметрии шестого порядка, следовательно, и ядра и электроны в ней располагаются совершенно симметрично. Молекула неполярна и не имеет магнитного момента. Если приложить к молекуле бензола магнитное поле, перпендикулярное плоскости кольца, электроны на /7-орбиталях будут двигаться в одном направлении, что вызовет заметный диамагнетизм7 (подтверждено экспериментально), т. е. бензольное кольцо можно рассматривать как замкнутый сверхпроводник, в котором электроны движутся свободно, не испытывая сопротивления:
5 Метод резонанса использует для описания реальной молекулы некоторые гипотетические валентные схемы, которые могут быть для этой молекулы составлены. Валентные схемы называют резонансными структурами, однако реально эти структуры не существуют. К каноническим структурам относят так называемые «независимые» валентные схемы, которые не могут быть получены комбинацией других. Для бензола — это две структуры Кекуле и три структуры Дьюара. Было бы ошибкой считать, что молекула бензола осциллирует между этими каноническими структурами. Осцилляция невозможна, т. к. ни одна из канонических структур в действительности не существует. Это лишь способ наглядного изображения молекулы.
6 В квантовохимической модели молекулы бензола, в рамках метода молекулярных орбиталей, л-электроны сопряженной системы рассматриваются как общие для всех углеродных атомов и находящиеся на общих молекулярных орбиталях. Число таких молекулярных орбиталей равно числу атомов, принимающих участие в образовании сопряженной системы.
Молекулярные орбитали бывают связывающие — энергия электронов на этих орбиталях меньше, чем на атомных, и, следовательно, нахождение электронов на них делает систему более устойчивой; несвязывающие— энергия электронов на этих орбиталях равна энергии электронов на атомных орбиталях; разрыхляющие — энергия электронов на этих орбиталях больше, чем на атомных, и поэтому переход электронов на них энергетически невыгоден. На каждой молекулярной орбитали, согласно принципу Паули, может размещаться не более двух электронов с антипараллельными спинами.
Расчет показывает, что в молекуле бензола имеются три связывающие молекулярные орбитали и три разрыхляющие.
Уровни энергии этих орбиталей: а + 2(3, <х <- 0, а + 0 для связывающих и а - 2р, а - р, а Р для разрыхляющих (рис. 4.1.2).
(р-20 (р-0
Рис. 4.1.2. Диаграмма энергетических уровней л-молекулярных орбиталей молекулы бензола
В основном состоянии бензола его 6 л-электронов занимают наиболее выгодные низшие электронные уровни, т. е. три связывающие орбитали. Из этого следует, что в бензоле образуется устойчивая «замкнутая» система из 6 л-электро-нов. Ее устойчивость и «замкнутость» определяются тем, что все л-электроны находятся на связывающих орбиталях и занимают их полностью. Таким образом, и приобретение новых электронов, и отдача уже имеющихся должны требовать затраты энергии. В этом отношении л-электронная система бензола подобна электронной оболочке благородных газов.
7 Диамагнетизм — явление ослабления внешнего магнитного поля. Вещества, которые создают это поле и ослабляют его, называются диамагнетиками. Например, серебро, свинец, кварц. Ампула с бензолом, помещенная в магнитное поле, будет из него выталкиваться.
Ароматические соединения
563
4.1.4. Получение бензола
4.1.4.1. Источники бензола
В настоящее время основными источниками ароматических соединений, в том числе и бензола, являются продукты коксования каменного угля (коксовый газ и каменноугольная смола) и продукты переработки нефти.
Продукты коксования каменного угля
Коксование каменного угля проводится с целью получения кокса для металлургической промышленности. Измельченные до зерен размером 3 мм и тщательно перемешанные угли (шихту) нагревают в специальных коксовых печах или коксовых батареях без доступа воздуха при 1000-1250 °C в течение 14-16 ч. В процессе коксования уголь разлагается с образованием твердого остатка — кокса (75-80 %) и летучих веществ, так называемого прямого коксового газа (схема 4.1.1).
В выделяющихся летучих продуктах содержатся пары каменноугольной смолы (80-130 г/м3), низкоки-пящие ароматические углеводороды, в основном бензол и его ближайшие гомологи — толуол и ксило
лы (30^40 г/м3), а также пары воды, сероводород, аммиак, оксид и диоксид углерода, метан, этан и др. Обычно из 1 т сухой шихты образуется 340-350 м3 коксового газа.
Полученный коксовый газ пропускают через эффективную систему конденсаторов и скрубберов для разделения продуктов, входящих в его состав (рис. 4.1.3.)
Летучие продукты коксования (прямой коксовый газ) из печи 1 попадают по стоякам в газосборную трубу 2. Там происходят первичное охлаждение и конденсация газа за счет испарения аммиачной воды, которая впрыскивается в трубу через специальные разбрызгиватели. Продукты коксования при этом охлаждаются до 85-90 °C, и некоторая их часть конденсируется. Из газосборной трубы коксовый газ поступает в холодильник 3, в котором охлаждается до 30-35 °C, при этом конденсируется дополнительное количество смолы. Выходящий из холодильника газ содержит смоляной туман и для его отделения проходит электрофильтр 4, после чего газодувкой 5 направляется на установку 7 для улавливания аммиака и пиридиновых оснований.
Уголь
Коксование
Прямой коксовый газ Кокс
Охлаждение, конденсация
V
Каменноугольная смола
Разгонка
V
Легкая фракция Фенольная фракция Нафталиновая фракция Поглотительная фракция Антраценовая фракция Пек
▼
Сырой бензол
Промывка H2SO4, гидроочистка, ректификация
▼
Бензол
Толуол
Ксилолы
Сольвент (этил бензол, мезитилен, этилтолулы и др.)
Схема 4.1.1. Коксование каменного угля
564
Новый справочник химика и технолога
Рис. 4.1.3. Технологическая схема конденсации и улавливания летучих продуктов коксования каменного угля:
1 — коксовая печь; 2 — газосборная труба; 3, 8. 12 — холодильники; 4 — электрофильтр;
5 — газодувка; 6 — сепаратор; 7 — установка для улавливания аммиака и пиридиновых снований; 9 — абсорбер; 10 — теплообменник; 11 — десорбер
Конденсат из газосборной трубы 2, холодильника 3 и электрофильтра 4 разделяют в сепараторе 6 на органический и водный слои. Органический слой представляет собой каменноугольную смолу, содержащую более высококипящие органические вещества; ее направляют на переработку в «смолоперегонный» цех. Водный слой (аммиачная вода) частично возвращается в газосборную трубу 2 для первичного охлаждения продуктов коксования, а частично направляется туда же, куда попадает и коксовый газ после электрофильтра: на установку 7. На этой установке имеются испаритель аммиака из аммиачной воды, сатуратор для поглощения азотистых оснований серной кислотой, кристаллизатор для сульфата аммония и аппарат для вытеснения пиридиновых оснований аммиаком из их сульфатов.
Газ после установки 7 еще содержит пары летучих органических соединений (бензол, толуол). Для их улавливания газ охлаждают водой в холодильнике 8 непосредственного смешения и направляют в абсорбер 9, орошаемый поглотительным маслом. Выходящий из абсорбера так называемый обратный коксовый газ используют для обогревания коксовых печей. Значительная часть газа направляется на химическую переработку. Насыщенное поглотительное масло, выходящее из нижней части абсорбера, проходит теплообменник 10, в котором подогревается обратным регенерированным маслом, и поступает в десорбер 11. Там происходит ректификация, в результате которой отгоняется смесь легких ароматических соединений (сырой бензол). Освобожденное от сырого бензола поглотительное масло отдает тепло насыщенному маслу в теплообменнике 10, дополнительно охлаждается в холодильнике 12 и вновь используется для абсорбции бензольных углеводородов из коксового газа.
Ароматические соединения, образовавшиеся при коксовании, находятся в каменноугольной смоле и сы
ром бензоле. Выход каменноугольной смолы составляет 32-34 кг, а сырого бензола 10-11 кг на 1 т сухого угля.
Каменноугольная смола. Выход и состав каменноугольной смолы зависят от характера угля и условий сухой перегонки, причем важнейшими факторами являются форма и размеры аппаратуры, скорость нагревания, температура и продолжительность процесса. В целом выход смолы небольшой (~3-4 %), однако она вырабатывается в огромных количествах, т. к. масштабы коксохимического производства, обслуживающего металлургию, достаточно велики.
Каменноугольная смола представляет собой вязкую жидкость черного цвета с запахом фенола (плотность 1200-1300 кг/м3). Она является сложной смесью органических соединений, в основном ароматических. Состав ее до конца не изучен. В настоящее время идентифицировано около 500 соединений (~60 % от общей массы смолы). Большое количество соединений образуется также в процессе переработки смолы.
Переработка каменноугольной смолы состоит в разделении ее ректификацией на отдельные фракции с последующей кристаллизацией, экстракцией и повторной ректификацией полученных фракций. Ректификацию осуществляют таким образом, чтобы получить фракции, содержащие максимально возможное количество подлежащего выделению вещества. В результате смолу разделяют на ряд следующих первичных фракций:
1) до 170 °C — легкая (0,6 % от массы смолы), состоит преимущественно из низкокипящих ароматических углеводородов (сырой бензол);
2) 170-210 °C — фенольная (2,5 % от массы смолы), содержит в больших количествах фенолы;
3) 210-230 °C — нафталиновая (10 % от массы смолы), содержит 80-85 % нафталина;
4) 230-290 °C — поглотительная (9,5 % от массы смолы), содержит большое количество различных аро
Ароматические соединения
565
матических веществ. Эту фракцию после отделения фенольных соединений и пиридиновых оснований используют как поглотительное масло для извлечения сырого бензола из коксового газа.
5) 290-410 °C — антраценовая (25,4 % от массы смолы), содержит преимущественно полициклические соединения;
6) остаток — пек (около 52 % от массы смолы).
Каждую из фракций обрабатывают щелочью для удаления кислых составных частей (преимущественно фенолов) и кислотой для выделения азотистых оснований. После этого очищенные фракции вновь перегоняют. Твердые углеводороды (нафталин, антрацен) отжимают от масла. Из легкой фракции (после обработки щелочью для удаления фенолов и экстракции оснований серной кислотой) отделяют перегонкой сырой бензол, который объединяют с выделенным из коксового газа.
Сырой бензол. Сырой бензол представляет собой в основном смесь низкокипящих ароматических углеводородов. Его подвергают переработке с целью выделения бензола, толуола, ксилолов и сольвента (сольвент-нафты). Переработка сырого бензола осложнена присутствием в нем непредельных соединений и соединений, содержащих серу (тиофен и его гомологи), температуры кипения которых близки к температурам кипения основных веществ. Поэтому переработка сырого бензола состоит из двух основных процессов: 1) очистки ароматических углеводородов от примесей непредельных и содержащих серу соединений и 2) разделения смеси очищенных ароматических соединений ректификацией.
Основным методом очистки является промывка концентрированной серной кислотой с последующей нейтрализацией раствором щелочи. При этом в результате процессов полимеризации, сополимеризации, конденсации и сульфирования образуются так называемая кислая смолка, продукты, растворимые в воде и серной кислоте и легко отделяемые от углеводородов, и вещества, частично растворимые в углеводородах ряда бензола и выделяющиеся при последующей ректификации в виде кубовых остатков.
С целью сокращения потерь очистке подвергают не весь сырой бензол, а выделяемые из него в результате предварительной ректификации более или менее узкие фракции ароматических углеводородов: так называемые фракции ВТК (бензол—толуол—ксилол) и БТКС (бензол—толуол—ксилол—сольвент).
Широкое распространение получил также метод каталитической гидроочистки, который заключается в обработке сырого бензола и его фракций водородом или коксовым газом. При этом ароматические углеводороды освобождаются от примесей непредельных соединений; соединений, содержащих серу; азот и кислород, из которых в результате гидрирования и гидрогенолиза образуются насыщенные углеводороды, сероводород, аммиак и вода. Каталитическая гидроочистка протекает при 300-500 °C и давлении водо
рода 2-2,5 МПа. При дальнейшей ректификации сырого бензола получают бензол, толуол, ксилолы, сольвент.
Коксохимическая промышленность в течение длительного времени являлась единственным поставщиком ароматического сырья. Она сохраняет свое монопольное положение и в настоящее время по производству полициклических ароматических соединений, используемых в промышленности, хотя из каменноугольной смолы извлекается не более 0,1 % их общего количества. Однако в производстве бензола и его гомологов в послевоенные годы на первое место выдвинулась нефтехимическая промышленность.
Продукты переработки нефти
Нефть является важным источником ароматических соединений. Некоторые нефти, например уральские и среднеазиатские, содержат значительные количества ароматических углеводородов, которые могут быть выделены перегонкой или химическими способами. Однако во многих нефтях содержание ароматических соединений крайне низкое. И тем не менее, ароматические углеводороды можно получать из любой нефти, т. к. углеводороды других классов при высоких температурах, и особенно в присутствии катализаторов, могут частично превращаться в ароматические. Особенно легко образуются ароматические соединения из полиметиленовых углеводородов с шестичленными циклами, которые в больших количествах содержатся, например, в кавказских нефтях.
Ароматические углеводороды образуются в процессе высокотемпературного крекинга нефтепродуктов при 650-750 °C и давлении, близком к атмосферному. В процессе крекинга образуются: 1) газообразные продукты (до 50 % от массы сырья), содержащие до 30 % этилена, водород и предельные углеводороды; 2) жидкие продукты — смола (40-60 %, а в некоторых случаях 80-90 % от массы сырья), содержащая бензол, толуол, ксилолы и др.; 3) кокс (небольшое количество). Недостатком этого способа является сравнительно малый выход ароматических углеводородов.
Использование катализаторов при крекинге нефтепродуктов позволяет снизить температуру процесса и увеличить выход ароматических соединений.
Каталитический риформинг. Наибольшее количество ароматических углеводородов в настоящее время получают методом каталитического риформинга. Промышленный процесс протекает при 470-550 °C. В этих условиях все углеводороды, присутствующие в исходном сырье, претерпевают те или иные превращения. Ароматические углеводороды образуются в основном в результате дегидрирования шестичленных циклоалканов (уравнение (4.1.1)) и дегидроизомеризации пятичленных алкилциклоалканов (уравнение (4.1.2)). В меньшей степени они образуются вследствие дегидроциклизации парафиновых углеводородов (уравнение (4.1.3)). Одновременно протекают и другие реакции. Выход и состав продуктов риформинга зависит от природы
566
Новый справочник химика и технолога
используемого катализатора, состава исходного сырья, а также параметров процесса.
Как видно из рис. 4.1.4, превращение циклогексана (2) в бензол (/) термодинамически возможно уже при 520-570 К (250-300 °C), причем равновесие реакции в значительной степени смещается вправо при дальнейшем повышении температуры.
Пятичленные углеводороды сначала превращаются в циклогексан и его гомологи, а при последующем дегидрировании также образуют ароматические соединения (уравнение (4.1.2)).
Термодинамические данные показывают, что равновесие данной изомеризации при высокой температуре неблагоприятно для образования циклогексана (2). Однако, благодаря последующему дегидрированию и превращению циклогексана в бензол, циклогексан непрерывно выводится из системы, что способствует высокой степени конверсии метилциклопентана (3).
При более жестком режиме риформинга в образовании циклических соединений возрастает роль реакции дегидроциклизации парафинов (уравнение (4.1.3)).
Первоначально процесс риформинга проводили на алюмосиликатном катализаторе, который в основном
способствовал дегидрированию. Выход ароматических углеводородов был низким (25-30 %). Затем перешли к использованию платиновых катализаторов на алюмооксидных носителях (платформинг). Это привело к увеличению доли реакции дегидроциклизации парафиновых углеводородов и повышению выхода ароматических углеводородов до 35-40 %. В последнее время стали использовать платинорениевый катализатор на носителе кислотного типа (рениформинг). Состав смеси, образующейся при каталитическом риформинге на алюмоплати-новых и платинорениевых катализаторах, значительно отличается от состава исходной смеси (табл. 4.1.1).
Таблица 4.1.1
Углеводородный состав исходной смеси и продуктов риформинга
Углеводороды Сырье Полученные продукты
Парафиновые 62,2 34,4
Циклопарафиновые 29,0 3,2
Ароматические 8,7 61,6
Непредельные 0,1 0,8
£ 500
| 400
1 300
% 200
<1
100
О'
100
Температура, К
Рис. 4.1.4. Температурная зависимость изобарно-изотермического потенциала (AG0) образования углеводородов из простых веществ
В настоящее время риформинг применяют в промышленности для двух главных целей: для повышения октанового числа моторных топлив и для получения индивидуальных ароматических углеводородов. В первом случае сырьем служат лигроиновая фракция или
тяжелые прямогонные бензины, октановое число которых в результате риформинга увеличивается с 35—40 до 80-90. Во втором случае риформингу подвергают более узкие фракции нефти, содержащие парафины и нафтены с тем же числом атомов углерода, что и целевой
Ароматические соединения
567
ароматический углеводород. Сырьем для риформинга служат бензиновые фракции прямой перегонки нефти. Для получения бензола используется фракция с температурой кипения 62-85 °C, для получения толуола — фракция с /кип = 85-И 05 °C, для получения ксилолов — фракция с /кип = 105-Н40 °C; причем для образования бензола необходим более жесткий режим риформинга, чем для образования его гомологов.
Благодаря давлению водорода катализатор риформинга может работать длительное время без значительного закоксовывания и дезактивирования. При давлении 3,5-5 МПа, когда отложение кокса практически исключается, регенерацию катализатора вообще не проводят (безрегенерационный процесс), а после 1-2 лет службы из отработанного катализатора извлекают платину, используя ее для приготовления новых катализаторов. Недостатком этой схемы является невысокая степень ароматизации сырья. В схеме с регенерацией катализатора (улътраформинг) применяют более низкое давление водорода (1,5-2 МПа) и через каждые 5-7 суток с поверхности катализатора выжигают кокс.
При рениформинге катализатор более стабилен, способен работать при более низком давлении (1 МПа) и высоких нагрузках, обеспечивая повышенную степень ароматизации сырья. При этом в ароматические углеводороды превращается свыше 90 % нафтенов и примерно 50 % парафинов.
Катализатор риформинга чувствителен к отравлению сернистыми соединениями, причем чувствительность тем больше, чем ниже давление водорода. Поэтому бензин или другую узкую прямогонную фракцию сернистой нефти предварительно очищают от сернистых соединений, обычно гидрированием на катализаторах, стойких к сере (оксиды или сульфиды кобальта, вольфрама и молибдена, их смеси):
RSH + Н2 -+ RH + H2S
Технологическая схема платформинга изображена на рис. 4.1.5. Исходную нефтяную фракцию подогревают в теплообменнике 5, смешивают с водородом и нагревают в трубчатой печи 6 до температуры, необходимой для очистки от серы. Гидроочистка проводится в контактном аппарате 4 на катализаторе, стойком к сернистым соединениям. Горячие газы из аппарата 4 отдают свое тепло исходной нефтяной фракции в теплообменнике 5 и охлаждаются водой (и частично конденсируются) в холодильнике 2. В сепараторе 1 конденсат отделяют от водорода и сероводорода, затем очищенную от серы нефтяную фракцию насосом 3 подают на стадию риформинга (платформинга).
Перед платформингом нефтяную фракцию смешивают с циркулирующим водородом, а затем подогревают в теплообменнике 10 и в трубчатой печи 6. Платформинг осуществляют в реакторах 7, 8 и 9 адиабатического типа. Ввиду высокой эндотермичности процесса реакционную массу из аппаратов 7 и 8 приходится подогревать в печи 6. В последнем контактном аппарате 9 платформинг завершается. Тепло горячих газов используют в теплообменнике 10 для подогрева смеси, идущей на риформинг, а затем для охлаждения газов в холодильнике 11. Полученный конденсат отделяют от водорода в сепараторе 13 и направляют на стабилизацию.
Водород (с примесью низших парафинов) из сепаратора 13 разделяют на три потока. Один циркуляционным компрессором 12 подают на смешение с очищенной нефтяной фракцией, направляемой на риформинг, другой смешивают с исходной фракцией и подают на гидроочистку, а остальное выводят.
Рис. 4.1.5. Технологическая схема платформинга:
1, 13 — сепараторы; 2, 11 — холодильники; 3 — насос; 4 — реактор гидроочистки;
5, 10, 17 — теплообменники; 6 — трубчатая печь; 7-9 — реакторы риформинга; 12 — циркуляционный компрессор;
14 — стабилизационная колонна; 15 — конденсатор; 16 — сборник
568
Новый справочник химика и технолога
Стабилизация жидкого продукта риформинга заключается в отгонке низших углеводородов (С4Ню, С3Н8 и отчасти С2Н6), растворившихся в жидком продукте при повышенном давлении. Для этой цели служит специальная, так называемая, стабилизационная колонна. Конденсат поступает в стабилизационную колонну 14 из сепаратора 13, предварительно подогреваясь в теплообменнике 77. В стабилизационной колонне 14 низшие углеводороды отгоняются, их пары конденсируются в конденсаторе 15, а конденсат стекает в емкость 16. Часть конденсата подается на верхнюю тарелку колонны в качестве флегмы, а остальное количество отводится с установки в виде сжиженного газа. Очищенный от низших углеводородов продукт из куба колонны 14 поступает в теплообменник 17, в котором отдает тепло конденсату, и направляется на дальнейшую переработку.
Полного превращения всех углеводородов в ароматические не происходит, поэтому после риформинга необходимо выделить ароматические соединения. Для этой цели применяют жидкостную экстракцию. Освоенные промышленностью процессы экстракции продуктов риформинга различаются природой применяемых растворителей. Наибольшее применение в качестве экстрагентов получили гликоли, сульфолан (тетрагидротиофендиоксид), диметилсульфоксид (ДМСО), N-метил-пирролидон (в смеси с этиленгликолем и водой). Первоначально в больших количествах использовали диэтиленгликоль, который в последнее время заменяется триэтиленгликолем и тетраэтиленгликолем.
Продукты пиролиза нефти. Кроме риформинга, ценным источником получения бензола и его гомологов являются жидкие продукты пиролиза, образующиеся при кратковременном крекинге нефти с целью получения этилена. На каждые 1000 кг этилена приходится 600-900 кг жидких продуктов, содержащих 60-70 % ароматических углеводородов (-20-40 % бензола, 15-20 % толуола, 10-15 % ксилолов), которые разделяют в основном методом дистилляции.
4.1.4.2. Деалкилирование гомологов бензола
Большие масштабы потребления бензола наряду с наличием избыточных количеств толуола обусловили практическое значение процесса деалкилирования (деметилирования) последнего. В основе деметилирования толуола (7) лежит процесс гидрогенолиза (деструктивной гидрогенизации) с расщеплением углеродуглеродной связи между ароматическим ядром и метильной группой (уравнение (4.1.4)).
Реакцию можно проводить как без катализатора (термическое деалкилирование), так и с катализатором (каталитическое деалкилирование).
Термическое деалкилирование толуола успешно протекает при 700-760 °C. Чтобы избежать чрезмерного образования кокса и увеличить выход целевого продукта, процесс необходимо проводить при 4-5 МПа и избытке водорода (4 : 1) по отношению к толуолу. В этих условиях предотвращаются реакции дегидроконденсации ароматических соединений, являющиеся причиной коксообразования. Степень конверсии толуола составляет -50 %, и при рециркуляции непрореагировавшего сырья выход бензола доходит до 98 % от теоретического.
Каталитическое деалкилирование толуола осуществляется с такими дегидро-гидрирующими катализаторами, которые активны в отношении деструктивного гидрирования и не затрагивают ароматическое ядро. К таким катализаторам относятся оксиды молибдена, кобальта и хрома, из них практическое значение имеет оксид хрома, нанесенный на активный оксид алюминия. Чтобы избежать дезактивации катализатора в результате отложения кокса на его поверхности, процесс проводят при давлении водорода 3-10 МПа. Температура при каталитическом деалкилировании лишь немного ниже, чем при термическом, и составляет 580-620 °C. Выход бензола из толуола в этом случае составляет -95 % от теоретического.
В последнее время успешную конкуренцию процессу деалкилирования составило диспропорционирование (переалкилирование) толуола (уравнение (4.1.5)).
Реакция протекает с гетерогенным катализатором при температуре 350-530 °C и давлении 1-1,2 МПа в присутствии водорода, препятствующего коксообразо-ванию и удлиняющего срок службы катализатора. Продуктами реакции являются бензол и изомеры ксилола: -52 % л/е/ла-изомера (наиболее термодинамически стабильного), 23 % пара- и 25 % o/w/o-изомера.
При более жестком режиме происходит гидродеалкилирование (уравнение (4.1.4)), что дает возможность регулирования относительного выхода бензола и ксилолов.
Совершенствование методов переработки нефти и выделения ароматических углеводородов привело к тому, что в настоящее время основное количество ароматических углеводородов производится из нефти. Так, в США уже в 1977 г. 91 % бензола производили из нефтяного сырья. В Западной Европе для производства ароматических углеводородов преимущественное значение имеет процесс пиролиза; получаемый при этом избыточный толуол выгодно перерабатывать на бензол и ксилолы.
C61U—С И3
СбН6 + СбН4(СН3)2 (4.1.5)
Ароматические соединения
569
В зависимости от технологии получения и назначения бензол подразделяют на бензол нефтяной и каменноугольный «высшей очистки», «для синтеза», «высшего сорта», «первого сорта», «для нитрации», «технический», «сырой». Эти бензолы отличаются друг от друга степенью чистоты, составом присутствующих примесей. Бензол любого сорта, поступающий в продажу, не представляет химически чистого соединения, а содержит в виде примеси, главным образом, толуол и ксилол, углеводороды жирного ряда, сероуглерод, тиофен и другие вещества. Большинство этих примесей удаляется фракционированной перегонкой в сложных аппаратах путем обработки едкой щелочью и концентрированной серной кислотой, кристаллизацией на холоду и отжиманием затвердевшего продукта. После такой обработки в бензоле еще остается примесь тиофена (—0,15 %). Тиофен кипит при 84 °C, поэтому и не отделяется от бензола при самой тщательной фракционированной перегонке. Соединение легко обнаруживается при помощи очень чувствительной реакции с раствором изатина в серной кислоте; бензол, содержащий даже следы тиофена, окрашивается упомянутым реактивом в интенсивный голубой цвет.
В лаборатории часто требуется бензол, не содержащий никаких примесей (по классификации: «химически чистый для анализа»), В этом случае для удаления тиофена к 1 л бензола добавляют 80 мл концентрированной серной кислоты, энергично перемешивают 30 мин при комнатной температуре и отделяют темный слой кислоты. Эту операцию повторяют до тех пор, пока кислота не начнет окрашиваться достаточно слабо. Бензол тщательно отделяют и перегоняют. Для полного обезвоживания бензола в него добавляют небольшими порциями металлический натрий (до прекращения выделения водорода), затем перегоняют.
4.1.4.3. Синтез бензола из ацетилена
Кроме рассмотренных основных источников ароматических соединений следует упомянуть еще один, пока не имеющий существенного значения. Это — ацетилен. Пропуская ацетилен через раскаленные трубки (-500 °C), французский химик М. Бертло в 1866 г. впервые получил бензол синтетическим методом (уравнение (4.1.6)), однако выход бензола был очень низким.
В присутствии катализаторов эта реакция проходит при значительно более низких температурах и с хорошим выходом бензола.
Например, при пропускании ацетилена под давлением над никельорганическим катализатором бензол образуется с удовлетворительным выходом уже при температуре 70 °C. В последние годы, в связи с исключи
тельным развитием промышленности ацетилена, синтез бензола на его основе может представить интерес.
4.1.4.4. Получение бензола из природного газа
Ароматические углеводороды всегда были отходом производства ацетилена, получаемого пиролизом природного газа. В последнее десятилетие в Казахстане были разработаны катализаторы, позволяющие получать бензол и другие ароматические соединения одностадийным методом непосредственно из природного газа. Технологический процесс получения бензола был осуществлен на установке проточного типа, представляющей собой каскад параллельных реакторов, при небольшом избыточном давлении 0,15 МПа (1,5 атм.) и температуре 500-600 °C. Параллельно с бензолом образуется водород, представляющий большой интерес для химической промышленности. Катализаторы представляют собой шарики диаметром 1,5-2 мм. Срок службы катализаторов -5 лет, химический состав является научным и коммерческим секретом. Производство катализаторов налаживается на опытно-экспериментальной установке Института органического катализа и электрохимии из сырья, имеющегося в Казахстане, в частности, цеолитов.
Для увеличения объемов производимого бензола химики и технологи ищут не только новые способы производства, но и активно занимаются реконструкцией уже имеющихся. Более подробную информацию об этом можно получить на сайтах:
www.uran.donetsk.ua;
www.advis.ru;
www.ukrgiap.com.ua;
www.chemindustry.ru;
www.fpnp.org;
www.kataliz.ru;
www.programs-gov.ru;
www.geo.kz;
www.chembz.ru;
news.opthim.ru;
4.1.4.5. Лабораторные методы получения бензола
Обычно бензол в лаборатории не получают, но иногда возникает необходимость заменить функциональную группу в бензольном ядре на водород. Так, при сплавлении соли бензойной кислоты (5) со щелочью происходит декарбоксилирование бензойной кислоты и образуется бензол (уравнение (4.1.7)).
При перегонке фенола (б) с цинковой пылью, в результате замещения гидроксильной группы водородом, также происходит образование бензола (уравнение (4.1.8)).
При нагревании соли бензолдиазония (7) со спиртом диазониевая группа замещается водородом (уравнение (4.1.9)). Если реакцию проводить в ацетатном буферном растворе бензол получается практически с количественным выходом.
570
Новый справочник химика и технолога
(4-1.7)
нагревание
+ ZnO
(4.1.8)
(б)
С2Н5ОН
+ N2 + НС1 +СН3СНО
(4.1.9)
4.1.5. Физические и химические свойства бензола
4.1.5.1. Физические свойства бензола
Бензол — бесцветная, прозрачная, легкоподвижная жидкость с характерным «ароматическим» запахом, горит ярким коптящим пламенем и образует легковоспламеняющиеся пары. На холоду застывает в кристаллическую массу, плавящуюся при 6 °C. Молекулярная масса 78,12. В табл. 4.1.2 приведены важнейшие физические константы бензола.
Присутствие в молекуле бензола единой сопряженной системы делает его термодинамически более устойчивым, чем гипотетический циклогексатриен. Если бы в молекуле бензола были три независимые двойные связи, его теплота гидрирования до циклогексана составляла бы 359,1 кДж/моль (теплота гидрирования циклогексена до циклогексана составляет 119,7 кДж/моль). В действительности при гидрировании бензола выделяется на 150,7 кДж/моль меньше. На эту же величину меньше вычисленной и найденная экспериментально теплота сгорания бензола. Эти данные свидетельствуют о том, что бензол стабильнее циклогексатриена на 150,7 кДж/моль. Эту величину называют энергией стабилизации (энергией резонанса) молекулы бензола. Энергия резонанса является мерой стабилизации основного состояния молекулы. Чем больше величина энергии резонанса, тем менее активно вступает молекула в химические реакции.
В табл. 4.1.3 приведены важнейшие термодинамические характеристики бензола.
Бензол практически не смешивается с водой: при 22 °C растворяется не более 0,08 % (растворимость воды в бензоле при 25 °C — 0,05 %). Бензол хорошо растворяется во многих органических растворителях: неограниченно — в углеводородах, эфирах, достаточно хорошо — в метаноле, этаноле, ацетоне, трихлорметане (хлороформе). Бензол и сам является прекрасным растворяющим средством для жиров, смол, масел, асфальта, алкалоидов, серы, фосфора, иода и др. С некоторыми растворителями бензол образует азеотропные смеси (табл. 4.1.4).
Электронный спектр бензола (рис. 4.1.6) имеет три характерных полосы поглощения, соответствующие трем различным возбужденным состояниям молекулы. Наиболее коротковолновая полоса, принадлежащая единственному разрешенному л—переходу, имеет максимум при 184 нм и достаточно высокую интенсивность. Полоса при 203 нм соответствует запрещенному переходу, и ее интенсивность меньше. Наиболее характерным поглощением для бензола является полоса при 230-260 нм с ярко выраженной колебательной структурой (так называемая «бензольная полоса»). В шкале длин волн расстояние между максимумами этой полосы составляет 5-6 нм, а в шкале волновых чисел 900 см”1, что соответствует частоте колебания бензольного ядра. Интенсивность полосы небольшая, поскольку соответствующий переход запрещен по симметрии.
В ИК спектре бензола (рис. 4.1.7) полосы поглощения обнаруживаются в нескольких областях. В области —3000 см 1 полосы поглощения относятся к валентным
Ароматические соединения
571
колебаниям связей С—Н, эти полосы имеют среднюю интенсивность. В области 1500 см-1 умеренно интенсивная полоса поглощения относится к скелетным колебаниям ароматических углерод-углеродных связей (С—С), и самая интенсивная полоса поглощения при
670 см-1 соответствует деформационным колебаниям связей С—Н.
В ПМР спектрах ароматические соединения имеют сигналы в области 6-8 м. д. Сигнал протонов бензола находится при 7,27 м. д. (рис. 4.1.8).
Важнейшие физические константы бензола
Таблица 4.1.2
Наименование константы, размерность Величина
Температура кипения (при атм. давл.) Ткип, °C Температура плавления (затвердевания) Т^, °C Относительная плотность d\ Показатель преломления n‘D (для £)-линии Na) Температура вспышки в воздухе Твсп, °C Температура самовоспламенения ТСВС|1Л, °C Критическая температура Ткр, °C Критическое давление р^, МПа Критическая плотность ркр, 103 кг/м3 Диэлектрическая проницаемость £ Дипольный момент молекулы ц, D Динамическая вязкость т|, мПа • с Поверхностное натяжение о, мН/м Криоскопическая константа Давление насыщенного пара р, кПа Октановое число 80,1 5,53 0,88954°; 0,8790'°- 0,868534° 1,5011220; 1,4947830 -12 534 (пары в воздухе) 289,41 4,92 0,307 2,28425 0 0,60025; О,32980 28,8820; 27,5630 5,12 3,48°; 9,9720; 35,7250; 178100 113
Таблица 4.1.3
Термодинамические константы бензола (для жидкого состояния)
Наименование константы, размерность Величина
Удельная теплоемкость при постоянном давлении ср, кДж/(кг • К) Стандартная теплоемкость*, С° Дж/(моль • К) Стандартная энтальпия образования А//°, кДж/моль Стандартная энтропия S0, Дж/(моль • К) Стандартная энтальпия плавления А//пл, кДж/моль Стандартная энтальпия испарения АЯИСП. кДж/моль Теплота сгорания при постоянном давлении Qp, кДж/моль 1,73421’8 81,6 (ж) 82,93 (ж) 269,2 (ж) 9,95 33,8525; 30,7680 3273,1
* Стандартные термодинамические величины (С", ЛЯ °, 5°) приводятся в расчете на один моль вещества, находящегося в стандартном состоянии при температуре 298,15 К (25 °C). Величины (ДЯИЛ, ДЯИС1|) приводятся в расчете на один моль вещества, находящегося в стандартном состоянии, для температур кипения и плавления соответственно. В качестве стандартного состояния принято устойчивое состояние чистого вещества при нормальном атмосферном давлении (101,325 кПа).
Таблица 4.1.4
Характеристика азеотропных смесей бензола
Второй компонент смеси TKmt смеси, °C Содержание бензола, масс. %
Вода 69,8 91,0
Муравьиная кислота 71,0 67,0
Метанол 58,0 62,0
Этанол 67,9 67,5
Пропанол 77,1 83,1
Изопропанол 71,9 66,2
572
Новый справочник химика и технолога
Рис. 4.1.6. Электронный спектр поглощения бензола в гептане:
Хмакс! = 184 нм (Ige = 4,77); = 203,5 нм (Ige = 3,87); Амакс3 = 254,5 нм (Ige = 2,31)
Длина волны, мкм
Волновое число, см
Рис. 4.1.7. ИК спектр раствора бензола (капиллярная кювета)
__1_I__I_I_। ।_। । । । ।
§ 10 9876 54 321 0
М.Д.
Рис. 4.1.8. ПМР спектр бензола в тетрахлорметане (эталон — тетраметилсилан)
4.1.5.2. Химические свойства бензола
Бензол как представитель ароматических соединений (см. 4.1.3) обладает особыми «ароматическими» свойствами. К этим свойствам относятся высокая устойчивость, способность образовываться даже в жестких пиролитических процессах и сравнительная трудность протекания реакций окисления. Для бензола характерна устойчивость к действию высоких температур. Лишь при температуре выше 650 °C он частично
превращается в дифенил, выше 750 °C разлагается на углерод и водород.
Для бензола наиболее типичными являются реакции электрофильного замещения атомов водорода, приводящие к образованию различных производных бензола, в которых структура бензольного кольца полностью сохраняется, однако происходит некоторое перераспределение электронной плотности под влиянием индукционного и мезомерного эффектов заместителя.
Ароматические соединения
573
Реакции электрофильного замещения
Реакции электрофильного замещения — это основной метод превращения бензола в его производные. В качестве электрофильного реагента может выступать как положительно заряженная частица X , так и нейтральная молекула с пониженной электронной плотностью на атоме, который образует ковалентную связь с атомом углерода ароматического кольца, например молекула SO3. Наибольшее практическое значение имеют алкилирование, галогенирование, нитрование, сульфирование и ацилирование бензола.
Алкилирование. Для алкилирования бензола используются алкилгалогениды, олефины и спирты. Алкилирование алкилгалогенидами и олефинами ведут в присутствии катализаторов Фриделя—Крафтса, представляющих собой безводные галогениды ряда металлов, например, А1С13, А1Вг3, FeCl3, TiCl4, SnCl4, ZnCl2 и др. При алкилировании спиртами в качестве катализаторов используют сильные протые кислоты, например, фосфорную, пирофосфорную, серную, хлорсульфоновую, олеум.
Активной электрофильной частицей, атакующей бензол при алкилировании, является алкил-катион (карбкатион) в свободном состоянии или в виде ион
ной пары. Из алкилгалогенидов карбкатион образуется по уравнению (4.1.10).
Образование карбкатионов из олефинов при действии катализаторов Фриделя—Крафтса требует так называемых сокатализаторов, которыми являются протонные кислоты, чаще всего хлороводородная. Хлороводород, присоединяясь по двойной связи олефина, образует соответствующий алкилхлорид, который взаимодействует с А1С13 (уравнение (4.1.11)) по аналогичной схеме с образованием карбкатиона.
При алкилировании спиртами карбкатион образуется при взаимодействии спирта с кислотой, используемой в качестве катализатора (уравнение (4.1.12)).
При алкилировании бензола в присутствии любых катализаторов происходит последовательное замещение атомов водорода с образованием продуктов разной степени алкилирования, при этом каждая последующая реакция алкилирования идет с большей скоростью, чем предыдущие, т. к. реакционная способность бензольного кольца возрастает по мере накопления в нем алкильных групп. Так, метилирование и этилирование бензола идут вплоть до получения гексаалкилбензолов, пропилирование — до получения тетраизопропилбензола и т. д.
1Т СН,=СН2 СН2=СН2 СН2=СН, гтт/г ТГА
С6Н6 ------- 2~» С6н5-С2н5 ---------. > С6Н4(С2Н5)2 -------. - » С6Н3(С2Н5)з и т. д.
«/ к2 «3
Каждая из реакций при умеренной температуре является практически необратимой. Так, константы равновесия при синтезе этилбензола из этилена и бензола при 0, 200 и 500 °C равны соответственно 6- 10", 2,2- 104и 1,9.
Из алкилпроизводных бензола важнейшее практическое значение имеют этилбензол (8) и кумол (9); изо
пропилбензол). Их получают сотнями тысяч т при действии на бензол этилена или пропилена соответственно в присутствии хлорида алюминия и хлороводорода (уравнение (4.1.13)).
Галогенирование. При действии на бензол хлора или брома в присутствии катализаторов, например железа, атом водорода замещается галогеном (уравнение (4.1.14)).
5+ 5-
RC1 + А1С13 R—►С1—>• AICI3—
±2 R+ + AICI4
(4.1.10)
+
RCH=: СН2 + НС1 + А1С13--------------► RCH—СН3 + AlClf (4.1.11)
ROH + HX ± ROH2+X~ ...................— R+ + H2O + X (4.1.12)
C2H5
(<S)
CH2=CH2
CH2=CHCH3
CH(CH3)2
(?)
(4.1.13)
574
Новый справочник химика и технолога
Х2 ----->. -нх
X
(4.1.14)
(70) X = С1; (77)Х=Вг
В качестве катализаторов галогенирования чаще всего используют хлорид железа(Ш), иод, серную кислоту. Катализаторами являются также хлориды алюминия, титана(1У), сурьмы и ряд других соединений, которые относятся к кислотам Льюиса.
Из галоген производных бензола наибольшее практическое значение имеет хлорбензол (70). Получить его в чистом виде при хлорировании бензола практически не удается, т. к. по мере образования хлорбензола начинается дальнейшее его хлорирование, причем скорость этого процесса растет с повышением концентрации хлорбензола. Вследствие этого при хлорировании бензола неизбежно получаются полихлориды, количество которых возрастает с увеличением глубины превращения (см. ниже). Полихлориды разделяют, комбинируя методы кристаллизации и дистилляции при пониженном давлении. Например, дихлорбензолы выделяют в виде смеси, содержащей 55 % пара-, 40 % орто- и 5 % л/е/ид-изомера, затем разделяют. Если необходимо получить хлорбензол в чистом виде, реакцию прерывают задолго до полного израсходования бензола. На схеме 4.1.2 показаны соединения, получаемые при хлорировании бензола.
При фотохимическом хлорировании бензола (уравнение (4.1.15)) образуется гексахлорциклогексан (27). Технический продукт (гексахлоран) является смесью восьми стереоизомеров, отличающихся пространственной ориентацией атомов хлора. Практическое значение имеет у-изомер (у-ГХЦГ). Его выход (11-18 %) зависит от температуры проведения реакции хлорирования и выбора растворителя. При проведении процесса в органическом растворителе (кроме бензола) оптимальной является температура (-20)-^(-30) °C; при проведении реакции в избытке бензола рекомендуется поддерживать температуру в пределах 20-30 °C. При более низ
кой температуре значительно уменьшается скорость реакции и, следовательно, снижается выход у-изомера. На рис. 4.1.9 приведена зависимость выхода у-изомера от температуры хлорирования бензола.
Из технического продукта у-изомер обычно выделяют экстракцией метанолом или другим подходящим растворителем. Выделенный из экстракта продукт содержит более 90 % основного вещества. После перекристаллизации продукта экстракции получают чистый у-изомер.
Рис. 4.1.9. Зависимость содержания у-изомера гексахлорциклогексана в техническом продукте от температуры хлорирования бензола
При бромировании бензола в среде олеума (уравнение (4.1.16)) получают гексабромбензол (22).
Бромировать бензол можно также в среде нейтрального органического растворителя в присутствии катализатора: например, FeCl3.
С12
T]V
(4.1.15)
Ароматические соединения
575
Схема 4.1.2. Хлорирование бензола
Вг2
H2SO4
(4.1.16)
(22)
576
Новый справочник химика и технолога
Нитрование. Нитрованием бензола (уравнение (4.1.17)) получают нитробензол (23) и jw-динитробензол (24). Для получения нитробензола на бензол при 40-50 °C действуют нитрующей смесью, содержащей 35-36 % HNO3, 52-53 % H2SO4 и 11-13% воды. Нитрующим агентом являются продукты превращения азотной кислоты, которая берется в количестве 0,97-1,01 моль на 1 моль бензола. По окончании нитрования с высоким выходом образуется нитробензол; содержание H2SO4 в отработанной кислоте не менее 69 %. Если азотная ки
слота берется в недостатке, непрореагировавший бензол отгоняют с водяным паром.
Введение второй нитрогруппы в бензольное кольцо происходит со скоростью в 105—107 раз меньшей, чем скорость введения первой нитрогруппы, и проходит в более жестких условиях.
Более глубокое нитрование бензола не имеет практического применения, т. к. требует чрезмерно жестких условий, сильно снижающих выход 1,3,5-гринитро-бензола.
HNO3
H2SO4 s40°C
HNO3 ----—>
H2SO4
= 90 °C
(4.1.17)
Сульфирование. При действии на бензол концентрированной серной кислоты образуется бензолсульфокислота (25). По мере течения реакции, в результате уменьшения содержания сульфирующего агента и увеличения количества бензолсульфокислоты, последняя может вступать в реакцию с бензолом, при этом происходит образование побочного продукта — дифенил-сульфона (26). Поэтому серную кислоту необходимо брать в достаточном избытке.
При действии на бензол 65%-го олеума образуется бензол-1,3-дисульфокислота [jw-бензолдисульфокислота (27)].
При длительном нагревании л/етя-изомера с 90% серной кислотой при 235 °C получается равновесная смесь, содержащая 66 % м- и 34 % ц-бензолдисульфокислоты (28) (уравнение (4.1.18)).
При действии на бензол сульфонилхлоридом получают бензолсульфонилхлорид (29) и бензол-1,3-дисуль-фонилхлорид (30) — ценные промежуточные продукты, на основе которых получают вспенивающие агенты для полимерных материалов.
SO2C1
(29)
Ароматические соединения
577
Хлорметилирование. Это введение группы СН2С1 в молекулу органического соединения. Реакцию проводят, действуя на вещество одновременно формальдегидом и хлороводородом в присутствии катализаторов: H2SO4, Н3РО4, ZnCl2, AICI3, SnCl4. Вместо формальдегида можно применять триоксиметилсн, параформ (параформальдегид) и ацетали формальде-гида.Для хлорметилирования бензола (уравнение (4.1.19)) используют формалин или параформ, а в качестве катализатора ZnCl2, при этом образуется бен-зилхлорид (37).
Так как бензилхлорид (37) алкилируется почти с такой же скоростью, как исходный бензол в процессе реакции образуются о- и, в большей степени, и-бис-хлормстильныс производные. Чтобы уменьшить образование этих соединений, степень превращения бензола поддерживают в пределах 20-25 %.
В процессе реакции бензол может взаимодействовать с бензилхлоридом (уравнение (4.1.20)), следствием чего является образование побочного продукта-дифенилметана (32). При температуре выше 60 °C количество дифенилметана заметно возрастает.
Ацилирование. Для ацилирования бензола используются галогенангидриды и ангидриды кислот. Обычно эти реакции проводятся с катализаторами Фриделя— Крафтса (см. алкилирование), чаще всего с хлоридом алюминия.
В производстве промежуточных продуктов метод ацилирования широко используется для синтеза жирноароматических и ароматических кетонов. Так, конденсацией бензола с ацетилхлоридом в присутствии хлорида алюминия или хлорида железа(Ш) получается ацетофенон [(33); метилфенилкетон] (уравнение (4.1.21)).
Хлорид алюминия, введенный в реакцию, нс регенерируется, т. к. остается связанным с карбонильной группой. Поэтому он расходуется в стехиометрических количествах, и его необходимо брать не менее чем 1 моль на 1 моль хлорангидрида.
Вместо ацетилхлорида можно применять уксусный ангидрид. В этом случае необходимо брать удвоенное количество катализатора, т. к. образующаяся при реакции уксусная кислота связывает еще 1 моль хлорида алюминия.
Аналогично получают пропиофенон и кетоны с более длинной углеводородной цепью.
При взаимодействии бензола с бензоилхлоридом (34) в присутствии А1С13 (уравнение (4.1.22)) получают бензофенон [(35); дифенилкетон].
Бензофенон (35) можно также синтезировать из бензола и фосгена (СОС12) в присутствии А1С13. Реакцию обычно ведут под давлением.
В промышленности бензофенон получают взаимодействием бензола с тетрахлорметаном (четыреххлори-стым углеродом) (уравнение (4.1.23)) с последующим гидролизом дифснилдихлорметана (36) (С6Н5СС12С6Н5).
При взаимодействии бензола с фталевым ангидридом (37) в присутствии А1С13 (уравнение (4.1.24)) образуется о-бензоилбензойная кислота (38). Хлорид алюминия в этой реакции вводится из расчета 2-2,5 моль на 1 моль фталевого ангидрида. Растворителем служит избыток бензола. При нагревании о-бензоилбензойной кислоты в среде концентрированной серной кислоты происходит внутримолекулярная циклизация и образуется антрахинон [(39); антрацендион-9,10].
О
(55)
О
(34)
578
Новый справочник химика и технолога
С6Н6 + со, А1С'3 >(С6Н5)2СС12—(С6Н,)СО (4.1.23)
(36) (35)
А1С13
(^)
IbSO^
(4.1.24)
Формилирование. При действии на бензол безводных оксида углерода и хлороводорода в присутствии стандартного катализатора этих реакций (А1С13) происходит образование бензальдегида (40), однако с очень низким выходом (уравнение (4.1.25)). Основной причиной низкого выхода бензальдегида оказалась нерастворимость А1С13 в бензоле. В лаборатории это препятствие удалось преодолеть, используя вместо хлорида алюминия его бромид (А1Вг3) или применяя в качестве растворителя нитробензол.
Техническое решение задачи было найдено проведением реакции бензола с оксидом углерода и хлорово
дородом под давлением. В автоклаве при 6-7 МПа и 20-60 °C формилирование бензола идет, как правило, с выходом не менее 90 % от теоретического, причем в качестве катализатора используется А1С13, который значительно дешевле бромида алюминия. Высокий выход бензола в этих условиях объясняется тем, что давление смещает равновесие СО + НС1 НСОС1 вправо. Формилхлорид взаимодействует с хлоридом алюминия, образуя ионную пару ( НС=О+ || А1С14") которая и является активным реагентом.
+ СО + НС1
А1С13
+ НС1
(4.1.25)
Восстановление
Основной метод восстановления ароматических углеводородов, в том числе и бензола, — каталитическое гидрирование. Катализаторами гидрирования могут быть все металлы VIII группы, но в промышленности применяют главным образом никель, нанесенный на оксид хрома(Ш). С этим катализатором реакцию ведут при температуре 120-200 °C и под давлением 1-5 МПа, которое необходимо для увеличения степени конверсии.
При гидрировании бензола образуется циклогексан [(2); гексагидробензол]. Процесс гидрирования протекает через ряд стадий (уравнение (4.1.26)). Наиболее медленной является первая стадия — образование циклогексадиена (41); на этой стадии происходит поглощение тепла (23,8 кДж/моль), которое расходуется на преодоление энергии стабилизации бензола. Остановиться на стадии получения циклогексадиена не удается, т. к. соединение (41), не стабилизированное энергией
резонанса, гидрируется значительно легче бензола, причем в процессе гидрирования происходит выделение тепла (110,4 кДж/моль). Второй продукт гидрирования — циклогексен (42) гидрируется еще легче, при этом также выделяется тепло (119,5 кДж/моль). Поскольку скорости гидрирования возрастают в этой цепи последовательных реакций, в реакционной массе не обнаруживается циклических олефинов.
При восстановлении бензола щелочными металлами в жидком аммиаке конечным продуктом реакции является 1,4-циклогексадиен (41).
Дегидрирование бензола
При нагревании бензола до 750-800 °C в присутствии катализатора (например, РЬО2) происходит дегидрирование бензола (уравнение (4.1.27)) и образуется дифенил (43).
(41) (42) (2)
Ароматические соединения
579
(43)
(4.1.27)
Окисление
Окислением ароматических колец могут быть получены фенолы, хиноны и карбоновые кислоты, весьма важные для синтеза промежуточных продуктов, красителей и полимеров. Из ароматических углеводородов бензол, в котором электронная плотность полностью выровнена, окисляется труднее всего.
Получить фенол прямым окислением бензола особенно перспективно, т. к. потребность в феноле продолжает неуклонно возрастать. В этом направлении ведутся многочисленные исследования, но практически ценных результатов пока не получено.
Хиноны прямым окислением бензола также нс получают. Например, бензо-1,2-хинон, имеющий высокий редокс-потенциал, можно получить только окислением пирокатехина оксидом серебра в безводном растворителе. Находящий промышленное применение и значительно более устойчивый бензо-1,4-хинон (44) образуется при окислении бензола (уравнение (4.1.27)) в особых условиях, например электрохимическим окис
лением эмульсии бензола в растворе сульфата и ацетата натрия, или при действии пероксида водорода в уксусной кислоте.
При глубоком окислении бензола происходит деструкция ароматического кольца и образуется малеиновый ангидрид (45). Предполагается, что процесс окисления идет через образование промежуточного продукта — бензо-1,4-хинона (уравнение (4.1.28)).
Фотоизомеризация бензола
При кратковременном облучении бензола коротковолновым УФ-светом (254 нм, ртутная лампа низкого давления) происходит изомеризация бензола (уравнение (4.1.29)) с образованием фульвена (46) и бензвалена (47). При продолжительном фотолизе бензол превращается в призман (48). Продукты изомеризации бензола являются его валентными изомерами и отличаются от последнего прежде всего неплоским строением. Они обладают высокой термической стабильностью.
4.1.6. Применение бензола
Бензол является важнейшим сырьем для химической промышленности, поскольку, он используется и как исходный реагент для синтеза самых разнообразных соединений, и как растворитель для других реакций (бензол растворяет практически все органические соединения, это своего рода «органическая вода»).
В первой половине XX в. бензол преимущественно использовали для получения нитро- и динитросоединений, а также для бензолдисульфокислоты. В настоящее время бензол применяется в основном в производстве этилбензола, кумола и циклогексана. На основе бензола по-прежнему получают различные полупродукты (сульфо-, нитро-, галоген-, алкил-,
580
Новый справочник химика и технолога
арил-, ацетилбензолы и др.), используемые в дальнейшем для получения синтетических каучуков, пластических масс, синтетических волокон, красителей, поверхностно-активных веществ, инсектицидов, лекарственных веществ и др. Сам бензол также используется для получения некоторых инсектицидов, вспенивающих агентов, антипиренов. Бензол широко применяется также в качестве растворителя и экстрагента в производстве лаков и красок, используется как высокоактивная добавка к моторным топливам. В России основная часть бензола востребована отечественными производителями этилбензола, капролактама и фенола. По результатам 2004 г. удельный вес этих производных в структуре потребления бензола составил 38 %, 32 %, и 21 % соответственно (рис. 4.1.10).
(См.: www.tyumen.sibneft.ru;www.tybet.ru;
www.textilmarket.ru).
Рис. 4.1.10. Структура потребления бензола по основным производным в РФ
4.1.6.1. Алкилбензолы
Более 60 % бензола используется для получения этилбензола и кумола. Небольшое количество бензола
применяется для получения алкилбензолов с длинной алифатической цепью, бензилхлорида и дифенилметана.
Этилбензол (8) используется в основном как промежуточный продукт при производстве стирола и как добавка к моторному топливу.
Наиболее дешевый этилбензол получают выделением из ксилольной фракции продуктов риформинга или пиролиза нефти, где он содержится в количестве 10-15%. Но основную массу этилбензола получают алкилированием бензола этиленом в присутствии хлорида алюминия и хлороводорода (уравнение (4.1.13)). При каталитическим дегидрировании этилбензола (уравнение (4.1.30)) образуется стирол [(49); винилбензол].
Практический интерес представляет новый метод использования бензола для получения стирола, а именно: окислительное сочетание бензола с этиленом в присутствии Pd-катализатора (уравнение (4.1.31)).
Стирол имеет большое практическое значение: на его основе получают полистирол, применяемый в автомобилестроении, электро- и радиотехнической промышленности, в производстве бытовых товаров и упаковок, ионообменных смол (катализаторов процесса получения кислородсодержащих добавок при производстве реформулированных бензинов). Стирол используется также для получения бутадиенстирольных латексов, каучуков, термоэластопластов, сополимеров с акрилонитрилом, винилхлоридом и др., является модификатором алкидов, реакционноспособным растворителем полиэфирных олигомеров.
Побочным продуктом при получении этилбензола является диэтилбензол [С6Н4(С2Н5)2], представляющий собой смесь мета- и пара-изомеров. Диэтилбензол приобрел значение для получения дивинилбензола [С6Н4(СН=СН2)2] — ценного мономера для производства ионообменных смол.
(4.1.30)
С6Н6 + С2Н4 + 0,5О2 > с6Н5- СН= СН2
— Н2О
(4.1.31)
Кумол [(9); изопропилбензол] — это полупродукт, используемый для получения фенола — соединения, имеющего большое практическое значение. Из изопропилбензола получают также ацетон и а-метилстирол.
Кумол получают при взаимодействии бензола с пропиленом в присутствии хлорида алюминия и хлороводорода (схема 4.1.13). При окислении кумола кислородом воздуха (уравнение (4.1.32)) образуется а,а-ди-метилбензилгидропероксид (50), который в присутст
вии каталитических количеств серной кислоты подвергается изомеризации с образованием полуацеталя (57), распадающегося на фенол (6) и ацетон (52). Выход фенола и ацетона ~90 %.
Фенол используется для получения феноло-альде-гидных смол (в основном, феноло-формальдегидных), анилина, £-капролактама, фотохимикатов, красителей, лекарственных препаратов, изоцианатов (сырья для получения полиуретанов), крезолов и г. д. Эфиры
Ароматические соединения
581
фенола используются в качестве присадок к топливам и смазочным маслам.
При синтезе кумола побочно образуются диизопропилбензолы (преимущественно мета- и пара-кзо-меры). Из диизопропилбензолов можно получать дешевые резорцин и гидрохинон, потребность в которых неуклонно возрастает. Резорцин [(53); 1,3-дигидрок-
сибензол] применяется в производстве красителей, резорцино-формальдегидных смол, как антисептик. Эфиры резорцина являются стабилизаторами и пластификаторами полимеров. Гидрохинон [(54); 1,4-ди-гидроксибензол] используется как проявляющее вещество в фотографии, антиоксидант жиров и масел, ингибитор полимеризации.
Алкилбензолы: С6Н5С„Н2„ . । (/7=10 18). Большое значение имеют алкилбензолы, содержащие достаточно длинную алифатическую цепь. Для получения этих соединений используют 1-алкены (а-олефины) с нераз-ветвленной цепью, получаемые крекингом парафина или синтезом на катализаторах Циглера. При взаимодействии их с бензолом получаются длинноцепочечные алкилбензолы, которые являются промежуточными продуктами для синтеза анионных поверхностно-активных веществ (ПАВ) — сульфонолов: С„Н2„^ ]С6Н48О3Ка (и = 10^-18) [(55); алкилбензолсульфонаты]. Сульфоно-лы являются основой моющих композиций, используются как пенообразователи, эмульгаторы, смачиватели.
Бензилхлорид (37) — продукт хлорметилирования бензола (уравнение (4.1.19)) — применяется в производстве бензилового спирта, сложных эфиров бензойной кислоты, красителей, четвертичных аммониевых оснований.
Дифенилметан (32) получают при взаимодействии бензола с бензилхлоридом или формальдегидом. Применяется в парфюмерии как душистое вещество (запах герани), растворитель лакокрасочных материалов.
4.1.6.2. Циклогексан
Циклогексан (2) — продукт полного гидрирования бензола (уравнение (4.1.26)) — используется в основном как сырье для синтеза адипиновой кислоты и е-ка-пролактама.
Адипиновая кислота [(56); гександиовая кислота] получается при окислении циклогексана в присутствии катализатора — стеарата кобальта (уравнение (4.1.33)). Используется в производстве полиамидных волокон, пластификаторов, инсектицидов.
е-Капролактам [(5<3); лактам е-аминокапроновой кислоты] получают из циклогексана через промежуточный продукт — циклогексаноноксим (57). Один из промышленных способов получения циклогексанонокси-ма — это фотонитрозирование циклогексана (уравнение (4.1.34)). При действии концентрированной серной кислоты циклогексаноноксим перегруппировывается в капролактам {58). Капролактам используется для получения поли-е-капроамида и лизина.
*• НООС—(СН2)4-СООН
(4.1.33)
(4.1.34)
{58)
(2)
582
Новый справочник химика и технолога
4.1.6.3. Малеиновый ангидрид
Малеиновый ангидрид (45) — продукт окисления бензола — применяется в производстве ненасыщенных полиэфиров (~50 %), янтарной кислоты. Янтарная кислота НООС(СН2)2СООН [(60); бутандиовая кислота] образуется при гидролизе янтарного ангидрида [(59);
тетрагидрофуран-2,5-дион], который является продуктом восстановления малеинового ангидрида (уравнение (4.1.35)). Янтарная кислота применяется в производстве алкидных олигомеров, пестицидов, присадок к смазочным маслам, красителей, лекарственных веществ, фотоматериалов.
НС"""
II
НС^
н2
О
н2о
II о
о
II
Н2С"""С °И
Н2С^-с—он
II о
(4.1.35)
(45)
(59)
(60)
4.1.6.4. Галогенбензолы
Из галогенпроизводных бензола многие соединения имеют важное практическое значение.
Хлорбензол (10) применяется как растворитель и промежуточный продукт для синтеза некоторых нитрохлорбензолов, хлоранилинов, нитрофенолов. Раньше из хлорбензола получали фенол и известный инсектицид ДДТ.
Дихлорбензолы: 1,2-дихлорбензол (12), 1,3-дихлор-бензол (13) и 1,4-дихлорбензол (14) являются промежуточными продуктами для получения красителей, пестицидов, лекарственных веществ. 1,2-Дихлорбензол используется как флотореагент, теплоноситель, растворитель, а также как промежуточный продукт для получения пирокатехина, 1,2-фенилендиамина, 3,4-дихлор-нитробензола. 1,3-Дихлорбензол применяется в производстве 2,4-дихлорнитробензола, 1,3-дихлорантрахино-на. 1,4-Дихлорбензол используется как репеллент (против моли), дезодорант, является промежуточным продуктом для получения гидрохинона, 2,5-дихлор-анилина, 2-амино-4-хлорфенола, 1,4-фенилендиамина.
Трихлорбензолы: 1,2,3-трихлорбензол (15), 1,2,4-три-хлорбензол (16) и 1,3,5-трихлорбензол (17) используются как ускорители вулканизации и растворители в производстве кубовых красителей. 1,2,3-Трихлорбензол применяется в производстве пирогаллола, 1,2,4-три-хлорбензол — в производстве 2,4,5-трихлорнитробен-зола, синтетического трансформаторного масла, 1,3,5-три-хлорбензол — в производстве флороглюцина.
1,2,4,5-Тетрахлорбензол (18) используется как им-прегнант против огня и влаги, в качестве промежуточного продукта для получения 2,4,5-трихлорфенола, 2,4,5-трихлоранилина, полихлорзамещенных 1,2-амино-фенолов и других полупродуктов для красителей, гербицидов и дефолиантов.
Пентахлорбензол (19) используется для получения фунгицида — пентахлорнитробензола.
Гексахлорбензол (20) — продукт полного хлорирования бензола. Соединение является активным избирательным фунгицидом, применяется главным образом
для протравливания семян злаков с целью предохранения их от головни. Используется также как полупродукт для получения пентахлорфенола, пентахлортиофенола, гексафторбензола.
Гексахлорциклогексан [(21)', у-ГХЦГ, линдан] является инсектицидом. Соединение используется для борьбы с саранчой, клещами и другими вредными насекомыми, применяется также в качестве инсектицидной добавки к протравителям семян с целью предохранения всходов от повреждения почвообитающими вредителями.
Бромбензол (11) преимущественно используется в качестве растворителя.
Гексабромбензол (22) используется как антипирен для полиолефинов, эпоксидов, полиэфиров, поливинилхлорида, полиуретанов, полиамидов, полистирола и АБС-пластиков, бутадиенстирольных пеноматериалов, поликарбонатов, сополимеров этилена с винилацетатом. Выпускная форма гексабромбензола имеет различные торговые наименования:
Торговое наименование Фирма (страна)
ГББ (Россия)
Adine 061 Billault (Франция)
НВВ Teijin (Япония)
Sumiguard НВВ Sumitomo (Япония)
Практически значимыми соединениями являются некоторые гидрокси- и нитрогалогенпроизводные бензола. Так, 2,4,5-трихлорфенол (61) — продукт гидролиза 1,2,4,5-тетрахлорбензола в водно-метанольном растворе NaOH — используется как антисептик для древесины и фунгицид. Нитропентахлорбензол (62) — продукт нитрования пентахлорбензола — является фунгицидом, используется для обработки почвы, протравливания семян, а также применяется для защиты от обрастания морских судов (совместно с бис(трибутилолово)оксидом). Пентахлорфенол (63) — продукт гидролиза гексахлорбензола в метаноле водным раствором NaOH-применяется как инсектицид, фунгицид, гербицид, а также как антисептик для древесины и других неметаллических материалов.
Ароматические соединения
583
(67)
4.1.6.5 Сульфопроизводные бензола
Сульфопроизводные бензола используются в основном как промежуточные продукты для получения более сложных промежуточных веществ. На основе некоторых бензолсульфокислот получают практически значимые соединения, например, гидразиды бензолсульфокислот, использующиеся как вспенивающие агенты (порообразователи) в производстве полимеров. И лишь одно сульфопроизводное бензола (дифенилсульфон) непосредственно применяется на практике.
Дифенилсульфон (26) находит практическое применение как акарицид, его используют для борьбы с личинками растительноядных клещей. Дифенилсульфон получают сульфированием бензола 65%-м олеумом при 60 °C (уравнение (4.1.36)) или триоксидом серы SO3 в токе SO2 при 150-200 °C.
Бензолсульфокислота (25) в виде натриевой соли используется в основном для получения фенола.
Бензол-1,3-дисульфокислота (27) является промежуточным продуктом для получения резорцина, азокрасителей.
Бензолсульфонилхлорид (29) является промежуточным продуктом для получения бензолсульфамида, бензолсульфоногидразида, метилового эфира бензолсульфокислоты. Бензолсульфамид [(64); бензолсульфо-намид] является продуктом взаимодействия бензол-сульфонилхлорида с водным раствором аммиака в присутствии оснований (уравнение (4.1.37)). При действии хлора на щелочной раствор бензолсульфамида получают монохлорамин Б [(65); натриевая соль моно-хлорамида бензолсульфокислоты] и дихлорамин Б [(66); дихлорамид бензолсульфокислоты] — дезинфицирующие и дегазирующие средства.
При взаимодействии бензолсульфонилхлорида и гидразингидрата в присутствии оснований образуется бензолсульфонилгидразид [(67); бензолсульфонилгид-разин]. Метилбензолсульфонат (68) является продуктом взаимодействия бензолсульфонилхлорида с метанолом.
мальдегидных и эпоксидных олигомеров, нитроцеллюлозы, бутилкаучука, силоксановых и бутадиенстирольных каучуков, сополимеров стирола с акрилонитрилом или бутадиеном, сополимеров винилхлорида и винилацетата, антиоксидант. Его производят во многих странах:
(67)
SO2NHNH2
(68)
SO2OCH3
Торговое наименование ЧХЗ-9 (Гидразид СБ) Genitron BSH Cellogen BSH
Porofor BSH Alveofer BS1
Фирма (страна)
(Россия)
Fisons, Whiffen (Англия) Uniroyal (США)
Bayer, Didier (Германия) Bozzetto (Италия)
Бензолсульфонгидразид (67) применяется как вспенивающий агент для поливинилхлорида, полиэфиров, полиамидов, полистирола, полиолефинов, фенолофор-
Метилбензолсульфонат (68) применяется в производстве лекарственных веществ, дисперсных и кубовых красителей.
584
Новый справочник химика и технолога
Бензолсульфазид [(69); С6Н58О2Кз] — продукт взаимодействия бензолсульфагидразида (67) с азотистой кислотой-используется в качестве вспенивающего агента для силоксановых и других каучуков. Его торговые названия: Азид СБ и Порофор ДФ-8.
Бензол-1,3-Дисульфонилхлорид (50) является промежуточным продуктом для получения бензол-1,3-дисульфонилгидразида (70) (уравнение (4.1.38)).
Бензол-1,3-дисул ьфонилгидразид (70) используется в качестве вспенивающего агента для поливинилхлорида, полистирола, полиолефинов, каучуков и резин; имеет различные торговые названия:
Торговое наименование
Порофор ДФ-9 (Дигидразид СБ)
PoroforB 13
PoroforB 13/СР 50
Фирма (страна) (Россия)
Bayer, Didier (Германия) Bayer (Германия)
4.1.6.6. Нитропроизводные бензола
Из нитропроизводных бензола наибольшее значение имеют нитробензол и 1,3-динитробензол.
Нитробензол (25) применяется в основном для получения анилина (7/) (уравнение (4.1.39)) и других азотсодержащих соединений: бензидина, хинолина, азобензола; используется также как растворитель, является компонентом полировальных составов для металлов.
1,3- Динитробензол (25) является промежуточным продуктом для получения 3-нитроанилина (72) и 1,3-фе-нилендиамина (75) (уравнение (4.1.40)).
З-Нитроанилин (72) применяется как азоамин (торг, назв. Азоамин оранжевый К) в производстве азокрасителей, является промежуточным продуктом для получения азотолов, основных, дисперсных, протравных, сернистых красителей, красителей для анодированного алюминия. 1,3-Фенилендиамин (75) используется в качестве отвердителя эпоксидных смол, применяется в производстве азокрасителей, для получения полиуретанов, полиамидов; реагент для обнаружения моносахаридов, нитроаминов, фурфурола.
(4.1.39)
(4.1.40)
(73)
Ароматические соединения
585
4.1.6.7. Ацилпроизводные бензола
Из продуктов ацилирования бензола практическое значение имеют ацетофенон, бензофенон, о-бензоил-бензойная кислота.
Ацетофенон [(55); метилфенилкетон] — продукт взаимодействия бензола с ацетилхлоридом — применяется как душистое вещество в мыле (запах черемухи), в производстве лекарственных веществ.
Бензофенон [(55); дифенилкетон] — продукт взаимодействия бензола с бензоилхлоридом — применяется в производстве душистых веществ.
о-Бензоилбензойная кислота [(5<5); бензофенон-2-карбоновая кислота] — продукт взаимодействия бензола с фталевым ангидридом — является промежуточным продуктом для получения антрахинона и антрона.
Бензальдегид (40) — продукт формулирования бензола — применяется в парфюмерии как душистое вещество (запах горького миндаля), в пищевой промышленности, является промежуточным продуктом для получения арилметановых красителей, некоторых душистых веществ (жасминальдегида, коричного альдегида и др.).
4.1.6.8. Продукты пиролиза бензола
Единственным продуктом пиролиза бензола, имеющим практическое значение, является дифенил (43). Дифенил применяется как высокотемпературный теплоноситель (в смеси с дифенилоксидом). Используется
в качестве фунгицида для предохранения цитрусовых от поражения грибами при хранении (обычно плоды заворачивают в бумагу, пропитанную сплавом дифенила с парафином).
Чтобы подвести итоги практического использования бензола, ниже приведены две таблицы и схема. В табл. 4.1.5 представлены соединения, которые получают непосредственно из бензола. Эти соединения обладают полезными свойствами, благодаря которым используются в народном хозяйстве в качестве различных препаратов.
Эти же соединения, используются в качестве промежуточных продуктов для получения других, как правило, более сложных веществ. В состав таблицы не вошли соединения, которые используются только как промежуточные продукты, например динитробензол (24), бензолсульфокислота (25), бензилхлорид (57) и др.
В табл. 4.1.6 представлены полезные соединения, полученные на основе производных бензола, большинство из которых используются также в качестве промежуточных продуктов для получения красителей, лекарственных препаратов, пестицидов и пр. В состав таблицы не вошли соединения, которые используются только как полупродукты.
На схеме 4.1.3 показано промышленное использование бензола.
Таблица 4.1.5
Полезные соединения, получаемые непосредственно из бензола
Номер соединения Название соединения Применение
8 Этилбензол Добавка к моторному топливу
10 Хлорбензол Растворитель
11 Бромбензол Растворитель
12 1,2-Дихлорбензол Флотореагент, теплоноситель, растворитель
14 1,4-Дихлорбензол Репеллент, дезодорант
15 1,2,3-Трихлорбензол Ускоритель вулканизации, растворитель
16 1,2,4-Трихлорбензол Ускоритель вулканизации, растворитель
17 1,3,5-Трихлорбензол Ускоритель вулканизации, растворитель
18 1,2,4,5-Тетрахлорбензол Импрегнант против огня и влаги
20 Гексахлорбензол Фунгицид
21 Гексахлоран (ГХЦГ) Инсектицид
22 Гексабромбензол (ГББ) Антипирен для полимерных материалов
23 Нитробензол Растворитель, компонент полировальных составов
для металлов
26 Дифенилсульфон Акарицид
32 Дифенилметан Душистое вещество (парфюмерия), растворитель
лакокрасочных материалов
33 Ацетофенон Душистое вещество (мыло)
40 Бензальдегид Душистое вещество (парфюмерия, пищевая про-
мышленность)
43 Дифенил Высокотемпературный теплоноситель, фунгицид
586
Новый справочник химика и технолога
Таблица 4.1.6
Полезные соединения, получаемые из производных бензола
Номер соединения Торговое название соединения Применение
53 Резорцин Антисептик
54 Гидрохинон Антиоксидант, ингибитор полимеризации, проявляющее вещество в фотографии
55 Сульфонолы Пенообразователи, эмульгаторы, смачиватели, основа моющих композиций
61 2,4,5-Трихлорфенол Фунгицид, антисептик для древесины
62 Нитропентахлорбензол Фунгицид
63 Пентахлорфенол Инсектицид, фунгицид, гербицид, антисептик для древесины
65 Монохлорамин Б Дезинфицирующее и дегазирующее средство, отбеливатель в текстильной промышленности
66 Дихлорамин Б Дезинфицирующее, хлорирующее, дегазирующее средство
67 Гидразид СБ Вспенивающий агент для полимерных материалов
69 Бензолсульфазид Вспенивающий агент для силоксановых и других каучуков
70 Порофор ДФ-9 (Дигидразид СБ) Вспенивающий агент для полимерных материалов
72 Азоамин оранжевый К Компонент азокрасителей
73 1,3-Фенилендиамин Отвердитель эпоксидных олигомеров
скк
(бу|адиенетирольный синтетический каучук)
-► Полистирол
сн2=сн2
Алкилирование
С6Н5- С2Н5 С6Н5СН=СН2
Этилбензол Стирол
Ю|
СН2=СН2 СН3
С6Н5-СН(СН3)2
Кумол
н2
Окисление „ и рахюжснис гидропсроксидов
Фенол
Ацет он
НС^С\
II О — НС< /
со
Малеиновый ангидрид
НоС'С\ I р н2сх;о/
Янтарный ангидрид
Гидролиз Янтарная кислота
Полиэфиры (лаки, олигомеры)
Красители
HNO, (H2SO4)
|Н|
C6H5NO2 --------► СбНзМНг--------
Нитробензол Анилин
Лекарственые вещества
Пестициды, гербициды
Взрывчатые вещества
|Ц|
- С6Н12 ------
Циклогексан
Фото-питрозиповаии^
=N-OH
Капролактам
Полиамиды (капрон)
10]
Циклогексаноноксим
(СН2)4(СООН)2 Адипиновая кислота
H2N(CH2)6NH2 -
Гексаметилеидиамин
Полиамиды (найлон) Полиуретаны
СбНбС1б Гексахлоран (инсектицид)
NH3
Анилин
Хлорирование
сч3с снр
ДДТ (инсектицид)
н2о
СбН5С1
С1
С1 и-Дихлорбензол (инсектицид)
Фенол
Сульфирование Щелочное
---------------► C6H5SO3H-----------------► Фенол и J J плавление
Бензолсульфо-
кислота
Схема 4.1.3. Промышленное применение бензола
Ароматические соединения
587
4.1.7. Промышленные способы получения основных производных бензола
4.1.7. 1. Получение алкилпроизводных бензола
В промышленности при синтезе алкилпроизводных бензола в качестве алкилирующих агентов применяют главным образом алкилгалогениды (в основном хлор-производные) и олефины. В качестве катализатора при алкилировании алкилгалогенидами используют только хлорид алюминия, отличающийся наибольшей активностью из всех доступных апротых кислот. Он же может применяться при алкилировании бензола олефинами, но в этом случае пригодны и другие катализаторы кислотного типа (H2SO4, безводный HF, BF3, фосфорная кислота на носителях, алюмосиликаты, цеолиты).
Использование спиртов в качестве алкилирующих агентов менее эффективно, потому что при алкилировании спиртами А1С13 разлагается, а протые кислоты разбавляются образующейся водой. В обоих случаях происходит дезактивирование катализатора, что обусловливает его большой расход.
При реакции с хлорпроизводными или олефинами A1CI3 расходуется только в каталитических количествах. В первом случае он активирует атом хлора, образуя сильно поляризованный комплекс или ион карбония (уравнение (4.1.10)), что с олефинами происходит только в присутствии сокатализатора — хлороводорода (уравнение (4.1.11)).
В твердом виде хлорид алюминия практически нерастворим в бензоле и является слабым катализатором. Однако в присутствии хлороводорода хлорид алюминия начинает превращаться в темное жидкое вещество, так называемый комплекс Густавсона, обладающий высокой каталитической активностью, и реакция алкилирования постепенно ускоряется. Комплекс Густавсона можно приготовить, пропуская HCI при нагревании через суспензию А1С13 в ароматическом углеводороде. Комплекс представляет собой соединение А1С13 и НС1 с 1-6 молекулами ароматического углеводорода, одна из которых находится в особом структурном состоянии положительно заряженного иона (о-комплекс), а остальные образуют сольватную оболочку:
Во избежание медленного катализа твердым хлоридом алюминия этот активный каталитический комплекс целесообразно готовить предварительно и потом подавать в реакцию. Кроме НС1 его образованию способствуют небольшие добавки воды или соответствующего хлорпроизводного, роль которых состоит в генерации НС1. Более приемлемо использовать НС1 или RC1, т. к. вода дезактивирует часть катализатора, разлагая его. По этой же причине необходимо хорошо осушать реагенты
и следить, чтобы в реакционную смесь не попадала вода, способная вызвать бурное разложение комплекса. Другими катализаторными ядами являются многие сернистые соединения и аммиак, в меньшей степени — диены и ацетилен. Следовательно, жидкая реакционная масса при алкилировании с хлоридом алюминия состоит из двух фаз: каталитического комплекса и углеводородного слоя.
При использовании в качестве катализаторов:
H2SO4 и HF процесс алкилирования проводят в жидкой фазе при 10-40 °C и давлении 0,1-1 МПа;
Н3РО4 — в газовой фазе при 225-275 °C и 2-6 МПа;
алюмосиликатов и цеолитов — в жидкой или газовой фазе при 200-400 °C и том же давлении.
В недавнем прошлом широко применялся при алкилировании твердый фосфорно-кислотный катализатор, в настоящее время больше внимание уделяется цеолитам, но преобладающее промышленное значение все же имеет хлорид алюминия, обладающий перед другими катализаторами рядам существенных преимуществ.
Из алкилпроизводных бензола важнейшее практическое значение имеют этилбензол (8) и кумол [(9); изопропилбензол]. Их получают сотнями тысяч т при действии на бензол этилена или пропилена соответственно в присутствии хлорида алюминия и хлороводорода (уравнение (4.1.13)).
Синтез ведут в аппаратах непрерывного действия, представляющих собой эмалированные или футерованные графитовой плиткой многосекционные колонны. Хлорид алюминия вводится в аппараты в виде заранее приготовленного раствора, содержащего 10-12 % А1С13, 50-60 % бензола и 25-30 % соответствующего диал-килбензола, т. к. в бензоле А1С13 растворяется плохо. Для образования хлороводорода, который является со-катализатором, в раствор добавляют воду (2 % от массы А1С13). В нижнюю часть колонны через распылитель подается алкен.
Так как этилбензол (8) и кумол (9) алкилируются быстрее бензола, в процессе реакции неизбежно образование диалкилбензолов (преимущественно мета- и wapa-изомеров). Основным фактором, влияющим на соотношение образующихся продуктов, является степень конверсии («глубина алкилирования»). Чтобы предотвратить образование нежелательных диалкилбензолов, глубину алкилирования в этих процессах поддерживают на уровне 10 %. Однако наряду с целевыми продуктами образуются заметные количества диалкилпроизводных, которые отделяются при ректификации; не вступивший в реакцию бензол возвращается в реактор.
На рис. 4.1.11 изображена технологическая схема производства этил- или изопропилбензола алкилированием бензола газообразным олефином в присутствии А1С13.
Свежий бензол вместе с бензолом, возвращенным со стадии разделения, поступает в колонну 5, предназначенную для осушки бензола азеотропной ректифика
588
Новый справочник химика и технолога
цией. Низкокипящая азеотропная смесь бензола с водой конденсируется в конденсаторе 4 и разделяется в сепараторе 5 на два слоя. Воду с растворенным в ней бензолом отводят (ее можно использовать для промывки реакционной массы), а бензольный слой стекает на верхнюю тарелку колонны 3, создавая орошение. Осушенный бензол из куба колонны 3 в теплообменнике 2 подогревает бензол, идущий на осушку, и попадает в сборник 8, откуда насосом непрерывно закачивается в алкилатор 9.
Каталитический комплекс готовят в аппарате б с мешалкой и рубашкой для обогрева паром. В него загружают полиалкилбензолы (ПАБ) или смесь бензола и
полиалкилбензола (примерно в отношении 1 : 1) и хлорид алюминия (I моль на 2,5-3 моль ароматических углеводородов), после чего при нагревании и перемешивании подают хлорпроизводное. Приготовленный комплекс периодически вводят в алкилатор.
Реакция проводится в непрерывно действующей ко-лонне-алкилаторе 9 с горячим сепаратором 12 для отделения каталитического комплекса и обратным конденсатором 10 для возвращения испарившегося бензола и отвода тепла. Олефин поступает в низ колонны, предварительно проходя расходомер. Бензол из емкости 8 поступает в низ алкилатора, как и конденсат из обратного холодильника 10.
Рис. 4.1.11. Технологическая схема производства этилбензола или изопропилбензола:
/ — насосы; 2 — теплообменник; 3 — колонна осушки бензола; 4, 10— конденсаторы; 5 — сепаратор; 6 — аппарат для получения каталитического комплекса; 7 — кипятильник; 8 — сборник; 9 — алкилатор; // — газоотделитель; 12, 16 — сепараторы; 13 — абсорбер; 14 — водяной скруббер; 15— холодильник;
17, 18 — промывные колонны
Газы, отходящие после конденсатора 10, содержат значительное количество паров легколетучего бензола (особенно при использовании разбавленных фракций олефинов). Для улавливания бензола эти газы направляют в абсорбер 13, который орошается полиалкилбен-золами, выделенными из реакционной массы на стадии разделения. Собирающийся в нижней части абсорбера раствор бензола в полиалкилбензолах поступает в реакционный аппарат 9 для переалкилирования. Газы после абсорбера 13 промывают водой в скруббере 14 для удаления НС1 и сбрасывают в атмосферу или используют в качестве топочного газа.
Углеводородный слой, отбираемый после сепаратора 12, состоит из бензола, моно- и по лиалки л бензолов.
В нем присутствуют также в небольшом количестве другие гомологи бензола, получившиеся за счет примесей олефинов в исходной фракции или путем частичной деструкции алкильной группы под действием AICI3.
При синтезе этил- и изопропилбензола реакционная масса содержит: 45-55 масс. % бензола, 35-40 масс. % моноалкилбензола, 8-12 масс. % диалкил бензола и до 3 масс. % более высокоалкилированных соединений, побочных продуктов и смол. Вся эта смесь проходит водяной холодильник 75 и дополнительно отстаивается в холодном сепараторе 16, откуда каталитический комплекс периодически возвращают в алкилатор. Алкилат направляют после этого на очистку от растворенного хлороводорода и следов хлорида алюминия. С этой це
Ароматические соединения
589
лью смесь промывают в системе противоточных колонн 17 и 18 вначале водой, а затем водной щелочью. Нейтрализованная смесь углеводородов (алкилат) поступает на ректификацию.
Продукты реакции разделяют в нескольких непрерывно действующих ректификационных колоннах (на схеме не показаны). В первой колонне отгоняют бензол и воду, растворившуюся в углеводородах на стадии промывки. В следующей колонне в вакууме отгоняют фракцию, содержащую главным образом целевой продукт, но с примесью ближайших гомологов бензола. Затем ее подвергают дополнительной ректификации с выделением технического этил- или изопропилбензола. Кубовая жидкость второй колонны содержит полиалкилбензолы с примесью продуктов осмоления, которые образуются под действием А1С13. Полиалкилбензолы отгоняют в вакууме от смол и используют для абсорбции бензола из отходящих газов и приготовления каталитического комплекса. Через эти промежуточные операции полиалкилбензолы снова возвращают в аппарат 9, где их подвергают деалкилированию. Выход целевого продукта с учетом всех потерь достигает 94-95 % при расходе 10 кг А1С13 на 1 т моноалкилбензола.
Данная технология алкилирования бензола имеет ряд недостатков и в последнее время непрерывно совершенствуется. Так, для уменьшения количества сточных вод предлагалось разлагать кислотный алкилат небольшим количеством воды, при этом получается концентрированный раствор гексагидрата А1С13, находящий разнообразное применение. Предлагалось проводить неодинаковые по скорости процессы алкилиро
вания бензола и переалкилирования полиалкилбензолов в разных аппаратах, что снижает количество рецирку-лята и энергетические затраты и позволяет работать при меньшем избытке бензола по отношению к олефину.
Один из вариантов усовершенствованного процесса алкилирования состоит в применении небольшого количества каталитического комплекса, растворяющегося в алкилате (гомогенное алкилирование). В этом случае, ввиду отсутствия больших масс катализатора, проводят реакцию при 160-200 °C и соответствующем давлении, необходимом для поддержания смеси в жидком состоянии. Схема гомогенного алкилирования бензола представлена на рис. 4.1.12.
В алкилатор 1 подают этилен, бензол и небольшое количество каталитического комплекса, снимая выделяющееся тепло кипящим водным конденсатом и генерируя технологический пар (при обычной технологии это тепло не утилизируется). Полученный алкилат поступает в переалкилатор 2, куда подают полиалкилбензолы (ПАБ) со стадии разделения; взаимодействуя с бензолом, они образуют дополнительное количество целевого продукта. Алкилат из аппарата 2 дросселируют до атмосферного давления и подают в сепаратор 3, при этом выделяющуюся энергию полезно утилизируют для испарения части бензола, который конденсируют и возвращают на алкилирование. Жидкий алкилат из сепаратора 3 охлаждают и направляют на нейтрализацию и последующее разделение. По этой технологии уже работают несколько установок большой единичной мощности.
Рис. 4.1.12. Технологическая схема процесса гомогенного алкилирования бензола: / — алкилатор; 2 — переалкилатор; 3 — сепаратор; 4 — конденсатор; 5 — холодильник
4.1.7.2. Гидрирование бензола
При гидрировании бензола получают циклогексан (2) — один из трех основных продуктов, определяющих спрос на бензол. Условия гидрирования бензола зависят от степени его чистоты. Гидрирование бензола, очищенного от тиофена, проводят при 140-200 °C и давлении 1-5 МПа; катализатором является никель, на
несенный на оксид хрома(Ш) или алюминия. При наличии в бензоле примесей, содержащих серу, в качестве катализатора используют сульфиды никеля, кобальта, молибдена или вольфрама, нечувствительные к сернистым соединениям. Эти катализаторы требуют значительно более жестких условий гидрирования: процесс ведут при температуре 320-360 °C и давлении ~30 МПа.
590
Новый справочник химика и технолога
В качестве сырья используют нефтяной или каменноугольный бензол. При использовании нефтяного бензола циклогексан получается высокого качества. Однако в последнее время все чаще используется каменноугольный бензол, который характеризуется повышенным содержанием примесей, и циклогексан, полученный из каменноугольного бензола, нуждается в дополнительной очистке.
На рис. 4.1.13 приведена схема процесса производства циклогексана, разработанного Французским институтом нефти. Циклогексан получается высокой степени чистоты. Процесс гидрирования протекает в две стадии: на первой происходит гидрирование основной части бензола на суспендированном непирофорном
никеле Ренея, на второй — дегидрирование на стационарном катализаторе Ni / А12О3.
Бензол и водород поступают в основной реактор жидкофазного гидрирования 1, в который предварительно насосом в виде суспензии подается катализатор. Однородность распределения катализатора обеспечивается барботированием газа через жидкость и интенсивной циркуляцией реакционного раствора через выносной теплообменник 3, в котором генерируется технический пар низкого давления. Температура в реакторе регулируется за счет испарения циклогексана. Гидрирование проводится при 200 °C и давлении 4 МПа (парциальное давление водорода ~0,3 МПа).
Рис. 4.1.13. Технологическая схема процесса производства циклогексана:
/ — основной реактор гидрирования; 2 — вспомогательный реактор гидрирования; 3 - - 5, 8 - теплообменники; 6 — сепаратор высокого давления; 7 — колонна стабилизации; 9 — сепаратор; 10 — насосы
Продукты реакции из верхней части основного реактора гидрирования поступают во вспомогательный реактор 2, в котором реализуется практически 100%-я степень превращения бензола в циклогексан. Затем продукты через теплообменники отводятся в сепаратор высокого давления 6 и подвергаются фракционированию в колонне стабилизации 7. Газообразные продукты из сепаратора частично возвращаются на рецикл, а из колонны стабилизации через холодильник 8 поступают в сепаратор 9, из которого отводят готовый продукт. Газы отдувки из сепаратора и колонны стабилизации используются в качестве топлива.
Расход суспендированного катализатора составляет 1 кг на 2,3 т циклогексана. Активность катализатора зависит от содержания оксида углерода в водороде — максимально 0,002 масс. %. Длительность работы катализатора обусловливается содержанием серы в бензоле, которой должно быть не более 0,0001 масс. %. При нормальном режиме установка работает 5-6 месяцев до полной смены катализатора.
Лимитирующими факторами производительности реактора гидрирования являются мощность жидкостных насосов и предельно допустимая скорость барботирования газа, при превышении которой начинается
унос жидкости и катализатора с отходящими парами. При использовании бензола 99,9%-й чистоты и насыщенного водой водорода при давлении 3,0-3,4 МПа выход циклогексана практически стехиометрический — 99 %, чистота > 99,8 масс. %.
4.1.7.3. Окисление бензола
При глубоком окислении бензола происходит деструкция ароматического кольца и образуется малеиновый ангидрид (45). Предполагается, что процесс окисления идет через образование промежуточного продукта — 1,4-бензохинона.
В промышленности этот способ получения малеинового ангидрида используется в больших масштабах. Процесс ведут путем контактно-каталитического окисления бензола в паровой фазе кислородом воздуха, катализаторами являются модифицированные смеси оксидов ванадия и молибдена. Модифицирующими добавками служат соли кобальта, никеля, фосфора, натрия, вольфрама, титана и т. д. Каталитическая масса формуется в гранулы или наносится на носитель, в качестве которого чаще всего используется а-А12О3. Окисление в этих условиях идет благодаря активации кислорода, хемосорбированного поверхностью катали
Ароматические соединения
591
затора с последующим его взаимодействием с углеводородом.
В основе различных технологических схем получения малеинового ангидрида лежит схема процесса, разработанная фирмой «Scientific Design D» в 1960 г. (рис. 4.1.14).
Смесь бензола с воздухом подогревается контактными газами в теплообменнике / до 120-150 °C и поступает в реактор 4 — аппарат, содержащий большое количество реакционных трубок, в которых находится катализатор. Окисление происходит при температуре 370-450 °C. Для отвода тепла реакции в межтрубном пространстве циркулируют расплавы нитрита натрия и нитрата калия. Нагретые соли, в свою очередь, отдают тепло воде, образуя пар высокого давления. Бензол в реакторе окисляется практически полностью.
Контактные газы, выходящие из реактора 4, поступают в теплообменник /, затем в холодильник 2, в котором охлаждаются водой до 160-170 °C, после чего
направляются в сепаратор 5, где из них выделяется часть малеинового ангидрида. Затем газы через сепаратор 5 поступают в скруббер 6, в котором улавливается водой оставшийся малеиновый ангидрид и другие растворимые в воде продукты реакции; малеиновый ангидрид при этом растворяется в воде, образуя малеиновую кислоту. Выходящий газ выбрасывается в атмосферу. Полученный 40%-й раствор малеиновой кислоты проходит стадию дегидратации в аппарате 7 и вместе с малеиновым ангидридом, выделенным из сепаратора 5, подвергается химической очистке и вакуумной ректификации в колонне 9. Выход малеинового ангидрида составляет 68-72 %.
В настоящее время более совершенными считаются конвертеры с гранулированным катализатором в псевдоожиженном слое. В них эффективно работает весь катализатор, и создаются условия, позволяющие значительно легче отводить тепло и точнее поддерживать необходимую температуру. Это повышает выход продукта на стадии контактирования.
Рис. 4.1.14. Технологическая схема производства малеинового ангидрида:
/ — теплообменник; 2 — холодильник; 3 — котел-утилизатор; 4 — контактный аппарат; 5 — сепаратор;
6 — скруббер; 7 — дегидрататор; 8 — емкость для малеинового ангидрида-сырца; 9 — ректификационная колонна
4.1.7.4. Получение хлорпроизводных бензола
Из хлорпроизводных бензола в промышленности в больших масштабах получают хлорбензол (10) и гексахлорбензол (20).
Промышленное производство хлорбензола — это крупнотажный непрерывный процесс. В качестве катализатора используют хлорид железа(Ш), получающийся при взаимодействии хлора и металлического железа, загружаемого в аппарат в виде обрезков листового железа. Образующийся безводный хлорид железа(Ш) растворяется в бензоле и продуктах его хлорирования, благодаря чему реакция идет как гомогенно-каталитическая. Очень важно применять осушенные бензол и хлор, т. к. гидратированный хлорид железа(Ш) нерастворим в органической фазе и реакция может приобрести менее выгодный гетерогенно-каталитический характер. Кроме того, образующийся при этом хлороводо
род, растворяясь в воде (соляная кислота), агрессивно действует на металлы.
По мере образования хлорбензола начинается дальнейшее его хлорирование, и неизбежно получаются полихлориды, причем скорость этого процесса растет с повышением концентрации хлорбензола. Чтобы уменьшить количество нежелательных продуктов, реакцию приходится вести с «обратным» бензолом, т. е. обрывать ее задолго до полного израсходования бензола. Например, при периодическом способе производства реакцию заканчивают, когда в смеси содержится около 50 % бензола, 30-40 % хлорбензола и 20-30 % полихлоридов. Использование более прогрессивного непрерывного процесса хлорирования позволяет сократить образование полихлорпроизвод-ных до 1,5—4 %, при этом в реакционной массе остается до 65 % бензола.
592
Новый справочник химика и технолога
В настоящее время в промышленности хлорбензол получают непрерывным методом (рис. 4.1.15) в специальных аппаратах — хлораторах, представляющих собой трубу, заполненную перемешанными стальными и керамическими кольцами. В верхней части хлоратора имеется сепарационный объем, не заполненный насадкой. Бензол и хлор подают в нижнюю часть аппарата. Подачу реагентов регулируют таким образом, чтобы полностью использовать хлор, и чтобы температура в аппарате поддерживалась за счет теплоты реакции (32 кДж/моль) на уровне 76-83 °C. Пары бензола и, в небольшой степени, хлорбензола вместе с выделяющимся хлороводородом из верхней части аппарата поступают в теплообменник, конденсируются, отделяются от хлороводорода и после
осушки возвращаются в процесс. Хлороводород направляется на абсорбцию. Реакционная масса, вытекающая из сепарационной части хлоратора, поступает на непрерывную ректификацию, в процессе которой хлорбензол и полихлориды отделяются, а бензол возвращается в цикл.
Выделяющийся хлороводород улавливается водой и в виде соляной кислоты используется в промышленности.
В условиях непрерывного процесса реакционная масса представляет собой газопарожидкостную эмульсию плотностью 200-300 кг/м3. Реактор работает в режиме полного вытеснения, благодаря чему достигается мольное соотношение хлорбензола к дихлорбензолу в реакционной массе, близкое к 40. Лучшего соотношения пока не удалось достичь.
Рис. 4.1.15. Технологическая схема процесса непрерывного хлорирования бензола: / — колонна с катализатором (хлоратор); 2 — конденсаторы-холодильники;
3 — приемник обратного бензола; 4 — холодильник
Из полихлоридов, комбинируя кристаллизацию и вакуум-перегонку, выделяют о- и w-дихлорбензолы, 1,2,3-и 1,2,4-грихлорбензолы, а также 1,2,4,5-тетрахлорбензол, которые находят значительное по объему промышленное применение. В меньших масштабах выделяют и используют также пента- и гексахлорбензолы.
Для получения хлорбензола в промышленности применяется также парофазный каталитический метод — так называемый метод окислительного хлорирования. Реакцию осуществляют, пропуская пары бензола и хлороводород при 200-250 °C над катализатором, содержащим медь(П). В присутствии кислорода воздуха идет окисление хлороводорода и одновременное хлорирование бензола по суммарному уравнению (4.1.41).
С6Н6+ НС1 + 0,5О2 -► С6Н5С1 + Н2О (4.1.41)
Степень превращения бензола за проход — около 10 %, выход хлорбензола — 90 % от теоретического. Одно из преимуществ этого метода заключается в практическом отсутствии полихлоридов, а основной его
недостаток — трудность подбора материалов для аппаратуры, которая должна работать в среде хлороводорода и воды при высокой температуре.
Гексахлорбензол (20) в промышленности получают хлорированием бензола при 300 °C (в присутствии катализатора (1гС12 или RhCl3 на А12О3)) или при 600 °C, а также окислительным хлорированием бензола смесью НО с воздухом при 200-250 или 300-400 °C в зависимости от катализатора (соли меди, активированные А1 или Fe).
4.1.7.5. Получение нитропроизводных бензола
Из нитропроизводных бензола, полученных прямым нитрованием бензола, практическое значение имеют нитробензол и л/-динитробензол. Нитробензол (23) в основном используется для получения анилина, потребность в котором постоянно возрастает; производство нитробензола крупнотоннажное и осуществляется непрерывным методом. л/-Динитробензол (24) используется в значительно меньших масштабах, поэтому производится преимущественно периодическим способом. Из jw-динитробензола получают л/-нитроанилин
Ароматические соединения
593
ил^-фенилендиамин. В настоящее время потребность в jw-фенилсндиамине значительно возросла в связи с его применением для производства термостойких полимеров и волокон.
Нитробензол в промышленности получают нитрованием бензола нитрующей смесью, в которой количество нитрующего агента несколько меньше теоретического. Это необходимо для того, чтобы азотная кислота была использована полностью и в продукте нитрования не было примеси динитросоединений. Небольшое количество не вступившего в реакцию бензола легко отделяется при перегонке.
На рис. 4.1.16 представлена схема получения нитробензола методом непрерывного нитрования бензола.
Непрерывное нитрование бензола проводится в нит-раторс 5 — стальном аппарате, снабженном рубашкой,
двумя внутренними змеевиками для охлаждения водой и двумя мешалками — турбинной и пропеллерной, посаженными на один вал. Верхняя мешалка (турбинная) служит для интенсивного смешения подаваемых на нее реагентов: бензола, кислотной нитросмеси и отработанной кислоты; нижняя мешалка (пропеллерная) работает как осевой насос. Бензол, нитрующая смесь и отработанная серная кислота вводятся в нитратор непрерывно через дозирующие устройства из напорных баков 2, 3, 4 соответственно. Подача бензола и нитросмеси автоматически регулируется по заданному соотношению, а количество отработанной кислоты — по температуре в реакторе, которая поддерживается на уровне 65-68 °C. Нитратор работает в режиме полного смешения. При установившемся процессе концентрация нитробензола в смеси постоянна и равна 5 %.
Рис. 4.1.16. Технологическая схема процесса непрерывного нитрования бензола:
1 — емкость для бензольного экстракта; 2, 3, 4 — напорные баки для бензола, кислотной смеси и отработанной кислоты; 5 — ни тратор; 6 — теплообменники; 7 — насосы; 8 — сепаратор; 9 — сборник отработанной кислоты
Из нитратора реакционную массу подают с помощью насоса 7 в два расположенных последовательно спиральных теплообменника 6. В первом из них завершается реакция нитрования, во втором температура реакционной массы снижается до 25-30 °C. Охлажденную реакционную массу подают в сепаратор непрерывного действия 8, в котором происходит разделение нитробензола и отработанной кислоты. Так как разность плотностей нитробензола и отработанной кислоты велика, расслаивание происходит быстро (время пребывания реакционной массы в сепараторе 5-10 мин). Сырой нитробензол промывают водой, нейтрализуют аммиачной водой или раствором карбоната натрия; при этом легко удаляются минеральные кислоты. Нитрофенолы, образующиеся в качестве примеси, отмываются с трудом и при большом расходе воды. При нейтрализации аммиачной водой аммониевые соли нитрофенолов
выпадают в осадок, который отделяют и утилизируют. В ряде случаев нитробензол без очистки передают на дальнейшую переработку — восстановление или сульфирование. Если нитробензол необходим в чистом виде, его очищают перегонкой в вакууме.
С каждой той товарного нитробензола из производственного цикла выводится 900-1000 кг 70-73% отработанной серной кислоты, содержащей 1,5-2,2 % нитробензола и 0,25-0,50 % азотной кислоты. Перед утилизацией этой кислоты из нее экстрагируют нитробензол. Экстракцию ведут бензолом, который при этом частично нитруется азотной кислотой, содержащейся в отработанной серной кислоте. В результате двухступенчатой экстракции полуторным по массе количеством бензола и последующего разделения слоев нитробензол практически полностью извлекается, а азотная кислота расходуется на нитрование бензола. Бензол
594
Новый справочник химика и технолога
со следами нитробензола собирают в емкость 7, а затем направляют в нитратор 5. Циркуляция нитробензола вызывает образование и накопление заметных количеств динитробензола. Наличие в нитробензоле даже 0,3 % динитробензола представляет опасность для процесса парофазного каталитического восстановления нитробензола до анилина, т. к. взрывоопасный динитробензол может накапливаться в испарителе. Отработанная серная кислота идет на регенерацию или используется для получения суперфосфата.
Получение нитробензола по непрерывному методу требует точного соблюдения технологического режима. Повышение температуры ускоряет процессы окисления. Сравнительно небольшой избыток азотной кислоты в нитраторе, появившийся в результате нарушения соотношения подаваемых реагентов, может привести к увеличению примеси динитробензола. Несоблюдение режима промывки и нейтрализации сырого нитробензола приводит к образованию стойких эмульсий и увеличению примесей нитрофенолов в готовом продукте и т. д. Лишь надежная автоматизация всего процесса может гарантировать высокую производительность синтеза и получение нитробензола высокого качества.
1,3-Динитробензол (ж-динитробензол) получают в относительно небольшом количестве, поэтому производство его ведется периодическим способом в специальных стальных аппаратах (нитраторах) с большой поверхностью теплообмена в виде рубашек, змеевиков или полых цилиндров, в которые подается вода или холодильный рассол. Нитратор снабжается также быстроходной мешалкой, термопарой для непрерывной регистрации температуры и автоматическим устройством, закрывающим подачу нитрующего агента при прекращении размешивания массы или ее перегреве. Для получения 1,3-динитробензола используют нитрующую
смесь, содержащую 33-34 % HNO3 и 66-67 % H2SO4. Азотную кислоту берут с небольшим избытком (на 1 моль бензола 2,05-2,10 моля HNO3). Нитрование начинают при 10-30 °C, а заканчивают при 90 °C. При этой же температуре производят отстаивание реакционной массы и отделение отработанной кислоты. Динитробензол промывают горячей водой, разбавленным раствором гидроксида натрия до нейтральной реакции и выделяют гранулированием в холодной воде. В полученном продукте содержится около 90 % мета-, 8-9 % орто- и 1-2% ия/?а-изомера. Для выделения jw-дини-тробензола нитропродукт при 65-70 °C обрабатывают раствором сульфита натрия. При этом орто- и пара-изомеры превращаются в соли соответствующих нит-робензолсульфокислот и переходят в раствор. jw-Ди-нитробензол в этих условиях не взаимодействует с сульфитом натрия.
.и-Д и нитробензол можно выделить также с использованием кристаллизации. После отделения мета-изомера образовавшуюся эвтектическую смесь обрабатывают серной кислотой; при последующем охлаждении из нее можно выделить также о-динитробензол.
4.1.7.6. Получение сульфопроизводных бензола
При сульфировании бензола получают бензолсульфокислоту (25) и бензол-1,3-дисульфокислоту (27).
Производство бензолсульфокислоты крупнотоннажное, бензол-1,3-дисульфокислота производится в значительно меньших масштабах.
Бензолсульфокислота — основной продукт сульфирования бензола. Существует много промышленных способов получения бензолсульфокислоты, из них наиболее экономичным является сульфирование бензола «в парах». Технологическая схема сульфирования приведена на рис. 4.1.17.
Рис. 4.1.17. Технологическая схема процесса сульфирования бензола «в парах»:
1 — испаритель; 2 — сульфуратор; 3 — кольцевой барботер; 4 — брызгоуловитель;
5 — холодильник-конденсатор; 6 — отстойник-сепаратор; 7 — нейтрализатор
Ароматические соединения
595
Бензол из хранилища насосом подают во внутренние трубы испарителя 1 (типа «труба в трубе» или кожух отру бчатого). Во внешние трубы испарителя (в рубашку) подается греющий пар давлением 0,8 МПа. В испарителе бензол нагревается, испаряется, а пары его перегреваются до 150-160 °C (давление паров бензола на выходе из испарителя 0,05-0,08 МПа). Перегретые пары бензола, взятого в большом избытке (6-8-кратном), с помощью кольцевого барботера 3 поступают в сульфуратор 2, в котором барботируются через слой предварительно загруженной 94-96% серной кислоты (купоросное масло). Температура в сульфураторе поддерживается -150 °C (обогревают через рубашку паром). Избыток бензола с парами воды через брызгоуло-витель 4 поступает в холодильник-конденсатор 5, в котором смесь бензола и воды конденсируется и охлаждается. Охлажденная до 30-35 °C смесь поступает в отстойник-сепаратор 6, где расслаивается на составные части. Бензол после нейтрализации в колонне 7 возвращается на сульфирование.
Так как избыток бензола уносит из аппарата воду (как образовавшуюся при сульфировании, так и внесенную с купоросным маслом), концентрация серной кислоты в сульфураторе не снижается до значения л-сульфирования. Теоретически можно было бы использовать эквимольное количество серной кислоты, однако этому препятствует образование сульфонов. Чтобы их количество не превышало 1 %, сульфирование прекращают при содержании в реакционной массе 4-5 % непрореагировавшей серной кислоты.
По окончании сульфирования в сульфомассе остается 1,5-2 % бензола, который удаляют отдувкой воздухом, после чего сульфомасса, содержащая бензолсульфокислоту (88,5-91,5 %), бензол-1,3-дисульфокислоту (0,4-0,6 %), H2SO4 (3,0-3,5 %), дифенилсульфон (1,0 %) и бензол (0,2 %), поступает на нейтрализацию. Нейтрализация проводится непрерывным способом в стальном футерованном кислотоупорной плиткой аппарате с помощью водного раствора сульфита натрия, после чего реакционная масса поступает в колонну для удаления выделяющегося диоксида серы (его используют для выделения фенола).
После нейтрализации и удаления диоксида серы получается водный раствор, содержащий бензол сульфонат натрия (-50 %), сульфат натрия (-4 %), сульфоны (0,7%) и бензол-1,3-дисульфонат натрия (0,5 %). Этот раствор может быть направлен для щелочного плавления и получения фенола. Если необходимо, упариванием этого раствора можно получить сухой бензолсуль-фонат натрия.
При сульфировании бензола «в парах» расход серной кислоты снижается в 1,8-1,9 раза по сравнению с жидкофазным сульфированием. Недостатком сульфирования «в парах» является замедление сульфирования вследствие уменьшения содержания серной кислоты в реакционной массе.
Жидкофазное сульфирование бензола осуществляют действием двукратного количества моногидрата в периодически действующих сульфураторах при температуре -60 °C в начале процесса и до 105 °C в конце процесса. Реакционную массу после разбавления водой частично нейтрализуют сульфитом натрия, а затем карбонатом кальция. Раствор бензолсульфоната натрия после фильтрации упаривают досуха.
Известны и другие методы сульфирования бензола. Один из непрерывных методов состоит в том, что жидкий бензол пропускают через серную кислоту (противотоком). Образующаяся бензолсульфокислота растворима в бензоле и вымывается затем из бензольного слоя водой.
Описано сульфирование бензола до бензолсульфокислоты слабым олеумом при 190-250 °C и давлении 1-3 МПа; образование сульфонов может быть подавлено добавлением бензолсульфоната натрия. В качестве сульфирующего агента для получения бензолсульфокислоты используют также 100%-й триоксид серы.
Промышленные методы сульфирования бензола были разработаны в основном для производства фенола: полученную бензолсульфокислоту действием NaOH и последующим подкислением превращали в фенол. В настоящее время эти методы потеряли свое прежнее значение в связи с развитием производства фенола из изопропилбензола.
Бензол- 1,3-дисульфокислота производится в значительно меньших масштабах, поэтому получают ее в промышленности периодическим способом в специальных чугунных или стальных аппаратах (сульфураторах) со специфическим днищем и крышкой. Сульфуратор снабжен рубашкой для обогрева и охлаждения, мешалкой, термометром в гильзе, трубой для передавливания массы, в крышке имеются загрузочные отверстия. При прямом сульфировании бензола олеумом до бензол-1,3-дисульфокислоты получается значительное количество сульфонов, поэтому процесс обычно ведут в два этапа: вначале бензол сульфируют моногидратом при 50-60 °C, а затем 65% олеумом при той же температуре. Иногда применяется одностадийный способ получения бензол-1,3-дисульфокислоты, в этом случае сульфирование бензола 65% олеумом проводится в присутствии сульфата натрия, подавляющего образование дифенилсульфона. По окончании сульфирования сульфомассу передавливают в аппарат, содержащий раствор сульфата натрия, и нейтрализуют серную кислоту гидроксидом кальция (известковым молоком) или карбонатом кальция (мелом). После отделения сульфата кальция (гипса) и перевода кальциевой соли бензолдисульфокислоты в натриевую последнюю выделяют, выпаривая воду. Если бензол-1,3-дисульфокислота необходима для получения резорцина, после фильтрации раствор ее натриевой соли выпаривают до 60%-й концентрации и в этом виде используют для щелочного плавления.
596
Новый справочник химика и технолога
4.1.7.7. Хлорметилирование бензола
Хлорметилирование бензола — один из промышленных методов получения бензилхлорида (31). Для хлорметилирования бензола используют параформ (параформальдегид), а в качестве катализатора ZnCl2. Хлорид цинка вводят в смесь бензола и пароформа в виде концентрированного раствора в соляной кислоте и во время реакции, которую ведут при температуре не выше 50-60 °C, через реакционную массу барботируют хлороводород. Синтез проводят периодическим способом в стальных или эмалированных аппаратах, снабженных рубашкой для обогрева и охлаждения, мешалкой и обратным холодильником.
4.1.7.8. Ацилирование бензола
В производстве ацилирование бензола используется для синтеза жирноароматических [ацетофенон (35)] и ароматических кетонов [бензофенон (55), о-бензоил-бензойная кислота (55)].
Ацетофенон. При синтезе в качестве ацилирующих агентов обычно используют хлорангидриды и ангидриды кислот, в качестве катализатора хлорид алюминия. Важным условием для проведения процесса с высоким выходом продукта реакции является использование сухих реагентов, в частности бензола и хлорида алюминия. Бензол должен быть также очищен от тиофена, иначе выход уменьшается на 5-10 %. Проводят ацилирование периодическим способом в эмалированных аппаратах, снабженных рубашкой для обогрева и охлаждения, мешалкой и обратным холодильником. Контроль процесса обычно осуществляют по скорости, с которой выделяется хлороводород. После завершения процесса реакционную массу сжатым азотом передавливают в футерованный стальной аппарат на предварительно загруженную подкисленную воду. При разбавлении реакционной массы происходит разложение алюминиевого комплекса с выделением большого количества тепла, за счет которого отгоняется часть бензола с водой. Затем органический слой отделяют от водного, в котором остаются соли алюминия. Для выделения целевого продукта бензол отгоняют с водяным паром или весь органический слой подвергают фракционированной вакуум-перегонке.
Бензофенон (55) чаще получают взаимодействием бензола с тетрахлорметаном (четыреххлористым углеродом) с последующим гидролизом дифенилди-хлорметана (С6Н5СС]2СбН5). Бензол легко взаимодействует с СС14 в присутствии безводного хлорида алюминия. Температуру реакции необходимо поддерживать в интервале 5-10 °C, т. к. при температуре меньше 5 °C скорость реакции очень мала, а при температуре больше 10 °C происходит образование смолообразных веществ и уменьшается выход продукта реакции — дифенилдихлорметана. После завершения процесса реакционную массу разбавляют водой и отгоняют с паром СС14, при этом проходит гидролиз дифенилди
хлорметана и образуется бензофенон, выход которого обычно составляет 80-89 %.
Бензальдегид (40) получают взаимодействием бензола с оксидом углерода и хлороводородом под давлением. Синтез ведут в автоклаве при 6-7 МПа и 20-60 °C, в качестве катализатора используется А1С13 Формилирование бензола идет, как правило, с выходом не менее 90 % от теоретического.
4.1.8. Методы определения бензола
Промышленность выпускает бензолы различного сорта. Эти бензолы отличаются друг от друга степенью чистоты и составом присутствующих примесей. Бензол любого сорта, поступающий в продажу, не представляет собой химически чистого соединения, а содержит в виде примеси главным образом толуол и ксилол, углеводороды жирного ряда, сероуглерод, меркаптаны, тиофен, а также другие вещества.
Существуют различные методы анализа бензола, но в любом случае вначале определяют, какие примеси присутствуют в бензоле. В зависимости от состава примесей применяют различные методы определения содержания чистого бензола в техническом продукте. Существуют физические и химические методы анализа.
В некоторых случаях содержание чистого бензола можно определить по температуре плавления образца. Совершенно чистый бензол плавится при +5,483 °C, при наличии примесей температура плавления уменьшается. Была предложена формула, позволяющая сразу же рассчитать процентное содержание (X) бензола в образце: X = 90,68 + 1,7377, где Т— температура плавления образца.
Существует весовой метод определения содержания бензола, основанный на взаимодействии бензола с цианидом никеля в присутствии аммиака, при этом образуется комплексное соединение состава Ni(CN)2NH3(C6H6), которое можно выделить и взвесить (1 г соединения соответствует 0,378 г бензола). Образование светло-сиреневого осадка [Ni(CN)2NH3(C6H6)] может быть качественной реакцией на бензол.
Фотометрический метод основан на способности бензола образовывать окраску в ацетоне в присутствии щелочей (необходимо иметь калибровочные кривые, с которыми сравнивают интенсивность окраски).
Существует способ определения бензола, основанный на его переводе в нитросоединение Для этого исследуемый образец обрабатывают нитрующей смесью до получения л/-динитробензола. Полученное нитросоединение смешивают со щелочным раствором метилэ-тилкетона, при этом образуется пурпурная окраска, по интенсивности которой фотометрическим методом определяют содержание бензола.
Метод определения содержания бензола по коэффициенту рефракции является базисным для анализа известных смесей бензола с органическими растворителями (дихлорэтан, н-гексан, циклогексан, ацетон, трихлорметан (хлороформ), метиловый, этиловый и
Ароматические соединения
597
изопропиловый спирты и др.) и водой. Результаты анализа искусственно приготовленных смесей бензола оформлены в виде таблиц и диаграмм, сравнение с которыми позволяет определить содержание бензола в исследуемом образце. Провести определение бензола в подобных смесях можно также, измеряя удельную плотность образца.
Иногда необходимо определить, присутствует ли бензол как примесь в каком-либо растворителе или смеси, а если присутствует, превосходит ли содержание бензола допустимую для безопасности здоровья норму. Самый распространенный метод обнаружения бензола— это реакция с цианидом никеля (способ Гофмана и Арнольди, см. выше). Можно также определить присутствие бензола, получив его комплекс с трифенилметаном или 2,4,6-тринитрофенолом (пикриновой кислотой).
При наличии бензола в воде, начиная с 5 мкг/л, его можно обнаружить по запаху, т. к. вода приобретает бензольный запах задолго до того, как станет опасной для здоровья.
При проведении работ, связанных с использованием бензола или смесей, в состав которых входит бензол, необходимо контролировать содержание последнего в воздухе помещения, в котором проводится работа. Для этой цели служат газоанализаторы, использующие различные способы определения бензола. Например, в газоанализаторе «URAS» фирмы «BASF» (Германия) для определения содержания бензола в газах используется метод ИК-спектроскопии.
Наиболее современным способом определения содержания бензола является хроматографический метод. Именно этим методом определяют содержание бензола в бензинах. Фирма «Метахром» предлагает для решения этих задач программно-аппаратный комплекс на базе автоматизированного многоканального газового хроматографа «Кристаллюкс-4000М». На рис. 4.1.18 приведены результаты исследования образца бензина: отчетливо видны пики ароматических углеводородов, по интенсивности пиков определяют содержание соединений.
Рис. 4.1.18. Анализ бензина по ГОСТ Р 51941-2002 (неароматические углеводороды выходят отрицательным пиком в начале хроматограммы до переключения колонок)
Наличие бензола в воздухе и его концентрацию можно определить с помощью универсального газоанализатора У Г-2, принцип действия которого основан на изменении окраски слоя порошка в индикаторной трубке после просасывания через нее воздуха рабочей зоны производственных помещений. Длина окрашенного столбика порошка пропорциональна концентрации анализируемого газа в воздухе и измеряется по шкале, отградуированной в мг/м3. Погрешность измерений -10 %.
Для анализа бензола в воздухе используются также газоанализаторы УПГК «и Колион-1», отградуированные специально по бензолу.
4.1.9. Техника безопасности при работе с бензолом
4.1.9.1. Токсические свойства бензола и защита от отравления
Бензол относится к числу токсичных продуктов второго класса опасности по ГОСТ 12.1.005. Однако ток
сические свойства бензола до сих пор до конца не изучены. Нет другого такого вещества, для которого за весь период санитарно-токсикологических исследований предельно допустимые концентрации были бы уменьшены в тысячу раз, как это было с бензолом. Это говорит о том, что со временем открываются все новые и новые токсические свойства и негативные стороны воздействия бензола на организм человека.
Чаще всего бензол попадает в организм человека с воздухом (через органы дыхания). Вдыхание паров бензола вызывает шум в ушах, ощущение металлического вкуса, головокружение, нарушение координации движений, тошноту, рвоту и в итоге потерю сознания. При высоких концентрациях бензола возможны мышечные подергивания, переходящие в судороги, зрачки расширяются и не реагируют на свет, дыхание сначала учащается, затем замедляется. Температура тела резко снижается, кожа и слизистые оболочки бледнеют. Артериальное давление понижается, известны случаи
598
Новый справочник химика и технолога
сильной сердечной аритмии. При очень высоких концентрациях (от ~60 г/м3) — почти мгновенная потеря сознания и смерть в течение нескольких минут. Если бензол попал человеку в рот, минимальная смертельная доза составляет 50 мг/кг.
При непосредственном контакте бензол попадает в организм человека не только через легкие, но и через кожу (неповрежденную), т. к. обладает поразительной проникающей способностью. Вызывая набухание резины, бензол проникает через латексные перчатки и всасывается в кожу со скоростью 0,4 мг/час (на площади 1 см2). При этом наблюдаются такие же симптомы отравления, как и в случае ингаляционного воздействия, но дополнительно к этому возникают различные заболевания кожи. Так, соприкосновение бензола с кожей вызывает сухость, трещины, зуд, кожа краснеет, появляется просовидная пузырьковая сыпь.
При многократном воздействии бензола (даже низких концентраций) могут развиваться хронические заболевания, в частности наблюдаются изменения в периферической крови и кроветворных органах, поражения центральной и периферической нервной системы, желудочно-кишечного тракта. Исследования, проведенные среди китайских рабочих одной из обувных фабрик Пекина сотрудниками Калифорнийского Университета (США) и Китайского Центра Контроля и Предупреждения Болезней, показали, что воздействие бензола приводит к общему снижению количества клеток крови и даже к их разрушению. Было отмечено также снижение содержания гранулоцитов и лимфоцитов. Причем этот эффект наблюдается даже в тех случаях, когда концентрация бензола ниже допустимого уровня (по американским стандартам) и составляет 1 ppm (одна часть на миллион). У рабочих, подвергавшихся воздействию высоких концентраций бензола (свыше 10 ppm), было обнаружено на 24 % меньше эритроцитов, чем у их коллег, работавших на фабрике одежды. Когда концентрация бензола была менее 1 ppm, это различие составляло около 15 %.
Бензол обладает слабым (по сравнению с другими химическими токсикантами), но все-таки заметным кумулятивным действием. При длительной работе в атмосфере, содержащей бензол, он обнаруживается в крови еще в течение 5-6 суток после прекращения работы. Содержание бензола в органах или соответствует концентрации бензола в крови, или превышает ее, но не более, чем в 3 раза. В жировой ткани и костном мозге содержание бензола может быть в 20 раз больше, чем в крови. При хроническом отравлении бензол обнаруживается в костном мозге спустя 14-20 месяцев после прекращения работы с этим веществом. Бензол лишь частично выделяется из организма через легкие в неизменном виде, частично же он окисляется в фенол и дигидроксибензолы (пирокатехин и гидрохинон) и выводится с мочой. После тяжелых отравлений бензолом наблюдаются длительные расстройства здоровья: легочные заболевания, плевриты, катары верхних дыха
тельных путей, заболевания роговицы и сетчатки, поражения печени, сердечные расстройства и т. д.
В настоящее время бензол подозревают (и небезосновательно) в канцерогенных свойствах. Метаболизм бензола с образованием других токсичных продуктов (основным метаболитом бензола является фенол) проходит в костном мозге и печени. Поэтому первой страдает кровеносная система человека. Уменьшается число эритроцитов, катастрофически падает гемоглобин. При воздействии бензола в клетках костного мозга происходит ряд хромосомных нарушений, причем наблюдается картина, сходная с симптомами поражения радиацией. Существуют данные, что около 15 % от общего числа заболевших лейкемией работали или как-то контактировали с бензолом. Исследования, проведенные на 233 предприятиях Китая с обследованием 28 460 рабочих, подвергавшихся воздействию бензола, показали, что смертность от лейкемии у рабочих резинового производства, контактирующих с бензолом, составила 701 на 100 тыс. человек в год. Концентрации бензола были от 10 до 1000 мг/м3, но в основном составляли 50-500 мг/м3.
Опасность бензола, так же как и радиации, в том, что последствия могут проявиться спустя месяцы и даже годы после отравления. При сильном отравлении улучшение состояния больного происходит через несколько месяцев, а восстановление кроветворной системы человека — через 5-7, иногда 9-12 лет. По материалам Промышленной Группы МАИР доказательств канцерогенности бензола вполне достаточно для того, чтобы отнести соединение в группу 1 (безусловно канцероген для человека). Обнаружено и мутагенное действие бензола: были замечены хромосомные аномалии у людей, работающих с бензолом в производственных условиях. В последнее время появились сообщения о том, что мутагенные свойства бензола могут быть причиной развития лейкемии.
Почему бензол токсичен? Каков механизм его негативного влияния? На эти вопросы нет однозначного ответа. Следует сказать, что бензол хорошо растворяет жиры, а жиры хорошо всасывают бензол. Попадая в клеточные структуры, бензол нарушает обменные процессы.
Для человека, подвергшегося воздействию бензола, так же как и для объектов природы, нет уникального противоядия. Вывести частично бензол из организма может специальная диета. При хроническом отравлении лечение, после прекращения работы с бензолом, состоит в усиленном питании пищей, богатой витаминами (особенно витамином С), приеме препаратов, содержащих железо, препаратов для поддержания печени и др. Существует ряд веществ, ускоряющих как вывод бензола, так и его метаболизм в организме. Одним из них является метионин — аминокислота, которая ускоряет метилирование бензола и его превращение в менее токсичные вещества. При хроническом отравлении рекомендуется лечение тиосульфатом натрия. Существу
Ароматические соединения
599
ют данные об успешном применении сульфаниламидных препаратов.
Первая помощь при отравлениях бензолом: при вдыхании — свежий воздух, покой, тепло; при попадании на кожу — тщательно вымыть водой с мылом; при попадании в глаза — промывать проточной водой в течение 10-15 мин; при попадании через рот — обильное питье воды, активированный уголь, сульфат натрия (1 ст. ложка на стакан воды), ни в коем случае не давать касторовое масло, молоко или спирт. Обратиться за медицинской помощью.
4.1.9.2. Охрана труда при работе с бензолом
Бензол — бесцветная, летучая, огнеопасная легковоспламеняющаяся жидкость (ЛВЖ) с характерным запахом — относится к классу AI. Испаряется бензол при комнатной температуре, пары его в 2,69 раза тяжелее воздуха. Взрывоопасные концентрации бензола в смеси с воздухом 3-6 %, по другим данным 5-8 %. Температура вспышки бензола: -11,1 °C, температурные пределы распространения пламени: (-15)-(+13) °C, концентрационные пределы распространения пламени: 1,43-8,0 г/м3. По пожарной опасности относится к первой категории.
Бензол должен храниться в металлической таре, исправной и герметически закрытой, в специальных помещениях для хранения ЛВЖ, обеспеченных приточновытяжной вентиляцией, или на открытой площадке, под навесом с металлическим ограждением, исключающим доступ посторонних лиц, вдали от открытого огня. В помещениях, где хранится или используется бензол, запрещается применение открытого огня, а также использование инструментов, дающих при ударе искру. Металлические контейнеры для хранения бензола необходимо заземлять, чтобы избежать возгорания от искр, вызываемых статическим электричеством. Электрооборудование и искусственное освещение должны быть выполнены во взрывобезопасном исполнении.
Транспортируется бензол в железнодорожных и автоцистернах с внутренним маслобензостойким и паростойким защитным покрытием. Цистерны снабжены оборудованием для разогрева продукта в зимнее время. В настоящее время разработаны и внедрены в производство новые вагоны-цистерны для транспортировки бензола, содержащие по 4 теплообменника для разогрева продукта и имеющие устройства с тройной степенью защиты для слива бензола по обе стороны вагона. При транспортировке на контейнерах с бензолом должен быть обозначен класс опасности 3 (воспламеняемые жидкости).
Главный аспект безопасности при работе с бензолом в химической промышленности — отсутствие утечки бензола из аппаратов и арматуры. По оценке Американского агентства по охране окружающей среды, типичный нефтеперерабатывающий завод имеет 11 000 единиц арматуры, которая из-за утечек в местах соединения аппаратуры выделяет в воздух 3,3 т летучих ор
ганических веществ в сутки. Особую опасность с учетом тенденций развития нефтехимии в будущем представляет бензол, вдыхание паров которого наносит большой вред здоровью. Традиционные методы испытания герметичности арматуры (например, «пузырьковая» проба с использованием мыльного раствора) могут оказаться в будущем недостаточными.
В 1984 г. Агентством по охране окружающей среды были опубликованы правила безопасности для арматуры на трубопроводах бензола. Правила предусматривают периодические проверки, взятие проб воздуха, регистрацию и устранение утечек, систематическую отчетность о состоянии трубопроводов.
Отравления бензолом возможны в различных отраслях промышленности. Острые отравления наблюдаются чаще всего при чистке цистерн из-под бензола, дистилляционных аппаратов, при применении бензола в составе быстросохнущих красок, при переливании бензола в замкнутых помещениях (подвалы, трюмы и пр.). Особенно опасны: пневматическая окраска нитролаками, в состав которых входит бензол, изготовление лаков и красок, растворимых в бензоле, производство гранитоля, где применяются очень большие количества бензола, и вообще все производства, в которых герметизация производственного процесса затруднительна, а поверхность испарения бензола велика. Возможны отравления и в химических лабораториях, а также у шоферов при применении бензола в качестве горючего.
При производственной аварии, утечке бензола при хранении и транспортировке опасную зону следует немедленно изолировать, удалив посторонних. Разлившуюся жидкость, не прикасаясь к ней, необходимо оградить земляным валом. При разливе бензол выделяет воспламеняющиеся пары, которые скапливаются в низинах, подвалах, телях. Поэтому необходимо соблюдать меры пожарной безопасности, устранить источники огня и искр. Небольшие утечки бензола следует засыпать песком, землей или другим негорючим материалом, затем собрать в герметичную тару и отнести в специально отведенное место для дальнейшего уничтожения. Для осаждения паров бензола в воздухе используют воду. При больших разливах бензол смывают водой в дренажную емкость или химический сток. Категорически запрещается сливать бензол в канализационную систему, т. к. это может привести к взрыву. Крупные утечки бензола должны ликвидироваться специалистами пожарного отделения.
Порог восприятия запаха бензола — около 5 мг/м3. Предельно допустимая концентрация (ПДК) бензола в атмосферном воздухе населенных мест (среднесуточная) равна 0,8 мг/м3, в рабочем помещении промышленного предприятия — 5 мг/м3.
Если концентрация бензола выше максимально допустимой или неизвестна, аварийные работы следует проводить только с использованием индивидуальных средств защиты, к которым относятся защитные кремы и пасты, фильтрующий противогаз, фартук из прорези
600
Новый справочник химика и технолога
ненной ткани или защитный костюм, резиновые сапоги и резиновые перчатки. При работе с бензолом рекомендуется использовать фильтрующий противогаз марки А, который применяется для органических растворителей с температурой кипения ~65 °C (коробка коричневого цвета) или БКФ. При концентрациях бензола более 0,5 об. % и кислорода менее 18 об. % применяют шланговые изолирующие противогазы типа ПШ-1 или ПШ-2.
Для защиты рук рекомендуются перчатки из фтор-эластомера «Viton», наиболее устойчивого к действию бензола. Запачканную бензолом одежду следует немедленно заменить, чтобы избежать проникновения вещества через кожу.
При работе с бензолом нельзя курить, принимать пищу. Категорически запрещается применение бензола для мытья рук, тары, промывки деталей. Использовать бензол следует только по прямому назначению.
При возгорании бензола в качестве средств пожаротушения необходимо применять инертный газ, химическую и воздушно-механическую пену. Для тушения небольших очагов загорания применяют ручные пенные или углекислотные огнетушители. Отходы бензола направляются на утилизацию (сжигание).
4.1.10. Проблемы экологии
Сотни тысяч тонн бензола, ежегодно выпускаемых промышленными предприятиями всего мира и используемые в самых различных целях, оказывают негативное влияние на экологию окружающей среды.
Бензол является одним из самых неприятных органических загрязнителей воды. Его допустимая концентрация составляет 0,01 мг/л. Бензол поступает в поверхностные воды с предприятий и производств основного органического синтеза, нефтехимической, химико-фармацевтической промышленности, при производстве пластмасс, взрывчатых веществ, ионообменных смол, лаков и красок, искусственных кож, а также со сточными водами мебельных фабрик. В стоках коксохимических заводов бензол содержится в концентрациях 100-160 мг/л, в сточных водах производства капролактама — 100 мг/л, производства изопропилбензола — до 20000 мг/л. Источником загрязнения акваторий может быть и транспортный флот, т. к. бензол применяется в моторном топливе для повышения октанового числа. Бензол используется также в качестве ПАВ.
Так как бензол имеет плотность гораздо меньшую, чем плотность воды, и растворимость его в воде невелика (0,073 масс. % при 25 °C), то, попадая в водоем, бензол изначально будет перемещаться в виде своеобразной линзы, находящейся на поверхности воды, растворяясь постепенно по мере увеличения объема воды.
Если концентрация бензола в воде не превышает 5 мг/л, то процессы биологического потребления кислорода не изменяются, т. к. под влиянием биохимических процессов в воде бензол окисляется слабо. При концентрациях 5-25 мг/л бензол не задерживает минерализации органических веществ и не влияет на про
цессы бактериального самоочищения водоемов. Однако при концентрации 1000 мг/л бензол тормозит самоочищение разведенных сточных вод, при концентрации 100 мг/л тормозит процесс очистки сточных вод в аэротенках, при концентрации 885 мг/л задерживает брожение осадка в метантенках.
Порог ощущения запаха бензола в воде 0,5 мг/л при 20 °C. При содержании бензола в воде 2,9 мг/л интенсивность его запаха оценивается в 1 балл, при 7,5 мг/л — 2 балла. Мясо рыб приобретает неприятный запах, если концентрация бензола в воде составляет 10 мг/л.
По нормам Евросоюза 1995 г., ПДК бензола в питьевой воде составляет 0,7 мкг/л, причем бензол обозначен как канцероген. По намного менее требовательным отечественным нормам бензол является санитарнотоксикологическим веществом с ПДК 0,5 мг/л (в -1000 раз больше европейских норм).
Вода, содержащая бензол, имеет своеобразный привкус, интенсивность которого оценивается в баллах: 1 балл — при концентрации бензола 1,2 мг/л, 2 балла — при концентрации 2,5 мг/л. Большинство людей может чувствовать запах бензола в воде при концентрациях 2 мг/л (примерно одна капля на 100 л) и ощущать на вкус в диапазоне концентраций 0,5-4,5 мг/л. Однако существенный риск получить онкологическое заболевание возникает уже в том случае, если человек на протяжении всей жизни употребляет воду с концентрацией бензола 0,01 мг/л.
Из водоемов бензол испаряется в атмосферу (период полуиспарения составляет 37,3 мин при 20 °C). При концентрации бензола в воде 5 мг/л запах бензола исчезает через сутки, при концентрации 10 мг/л интенсивность запаха снижается до 1 балла за сутки, при концентрации 25 мг/л — через двое суток.
Имея температуру плавления 5,5 °C, бензол может вмерзнуть в лед, увеличив таким образом срок своего вредного воздействия на окружающую среду. Благодаря устойчивости своих молекул, бензол не сразу деградирует, активно же начинает разрушаться лишь при нагревании выше 650 °C.
Техногенные аварии всегда тяжело влияют на состояние окружающей среды, особенно когда в эту среду попадают токсичные вещества в большом количестве. Взрыв на химическом заводе в провинции Цзилинь в Китае привел к выбросу токсичных веществ, в том числе бензола, в реку Сунгари. Максимальная отмеченная концентрация бензола в воде превышала норму более чем в 100 раз. Несомненно, что бензол, попавший в реку, надолго сохранит свои токсические свойства, и использовать такую воду надо с большой осторожностью, так же как и рыбу, обитающую в таких водоемах, которая способна накапливать ядовитые вещества.
Средств противостоять бензолу практически нет. Бензол можно осадить, выловить, собрать из воды, сорбировать на уголь или цеолит, но все эти мероприятия достаточно дороги. Остается надежда на то, что будучи
Ароматические соединения
601
подвижной жидкостью с низкой температурой кипения и малой плотностью, бензол не будет накапливаться в донном грунте реки и в живых организмах, т. к. кумулятивные свойства бензола не настолько велики, как у некоторых химических токсикантов. Спустя некоторое время воды рек, в которые попал бензол, унесут его в океан, и огромный объем океана поглотит бензол, добавив его к тем тысячам тонн бензола, которые человек ежегодно сбрасывает в океан.
В наш техногенный век бензол не так уж редок и в объектах окружающей среды. Он используется как промышленный растворитель, входит в состав многих материалов, используемых как в строительстве, так и в быту (полимерные покрытия для полов, панели, клеи, мастики, латексы и др.). При нарушении технологии изготовления или применения таких материалов бензол выделяется в окружающую среду, т. е. он присутствует и в атмосфере квартиры. Наиболее интенсивно выделение токсичных веществ из отделочных материалов происходит в первые недели эксплуатации (выделяются продукты неполной полимеризации). С течением времени интенсивность выделения веществ падает. Бензол является одним из основных продуктов горения такого известного всем материала как поливинилхлорид. Выделяется бензол и из горящей полиэтиленовой бутылки.
Бензол — важный компонент бензина, повышающий октановое число, но поскольку бензол является канцерогенным веществом, его содержание в бензине регламентируется специальными нормативными документами. Бензины, выпускаемые в России, по содержанию бензола не соответствуют европейским нормативам (не более 1 %), нормативные документы России допускают содержание бензола в бензине до 5 %. Однако нередко бензин, продаваемый на АЗС, не соответствует и российским нормам. Так, при проверках АЗС Санкт-Петербурга в 2004 г. были обнаружены бензины, содержащие бензол в количестве ~8 % (при норме не более 5 %). Выхлопные газы автомобилей, использующих такой бензин, содержат заметное количество бензола, который рассеивается в воздухе. Таким образом, невидимый и необнаруживаемый бензол соседствует с нами в городском воздухе и, пусть в малых дозах, поступает в организм каждого городского жителя.
Когда бензол был обнаружен в газированных напитках, правительственные агентства, контролирующие пищевые продукты в США, Англии, Германии и других странах, были очень обеспокоены устрашающей находкой. Понять их озабоченность можно, ведь бензол способен вызывать злокачественные заболевания крови (лейкозы) и лимфатической системы (лимфомы). По словам Ю. Остапенко, руководителя научно-практического токсикологического центра Росздрава, в газированных напитках содержатся такие дозы бензола, которые оказывают не острое токсическое действие, а хроническое. В этом тоже нет ничего хорошего, хроническое влияние бензола может приводить к онкологическим заболеваниям, заболеваниям печени и по
чек, угнетает процесс кроветворения. Чтобы точно определить риск, необходимы дальнейшие исследования.
В настоящее время установлено, что многие напитки, в том числе и российские, содержат до 25-50 мкг бензола в 1 л напитка. Это в 2,5-5 раз больше верхнего предела, разрешенного Всемирной организацией здравоохранения для питьевой воды, и в 20-25 раз превышает нормы ПДК в странах Евросоюза. Если бы такая бензольная вода текла из крана на кухне, чиновники должны были бы забить тревогу и предупредить население об опасности ее потребления. В случае же с напитками все иначе — их названия даже не разглашаются.
Впервые большие дозы бензола были обнаружены в газированных напитках еще в 1990 г. в США. Полтора десятка лет проблему замалчивали так умело, что в Европе о ней не знали даже специалисты. И когда в 1998-1999 гг. в Бельгии, Франции и Германии в газированных напитках случайно обнаружили бензол, производители убеждали чиновников в том, что их подвели поставщики, подсунув загрязненный бензолом углекислый газ. В российском НИИ питания эту версию считают правильной и не исключают, что нынешний бензол в напитках имеет такое же происхождение. Однако американские химики еще в 1990 г. установили, что бензол под влиянием света и тепла может образоваться из бензоата натрия, используемого в качестве консерванта, и аскорбиновой кислоты (витамин С). Оба эти компонента входят в состав любого безалкогольного газированного напитка. В секретных документах одной из компаний, попавших в прессу, приводятся такие цифры: в бутылке диетического низкокалорийного газированного напитка было 25 мкг бензола, а после того, как бутылка постояла при 30 °C на свету, канцерогена стало в три с лишним раза больше — 82 мкг. И самыми канцерогенными оказались именно диетические газированные напитки, сделанные на заменителях сахара. По иронии судьбы, такие напитки пользуются все большим спросом среди людей, ведущих здоровый образ жизни. Но, избегая лишних калорий, эти люди потребляют больше ядовитого бензола.
Многие западные специалисты считают, что необходимо менять рецептуру газированных напитков. Однако подобрать такой же эффективный консервант, как бензоаты, будет непросто. Известно, что бензойная кислота и витамин С встречаются и во многих других продуктах — в недорогих соках, консервированных овощах и фруктах, рыбопродуктах, маргаринах, майонезах и т. д. Все эти продукты в настоящее время находятся в зоне внимания специалистов, и, возможно, скоро появится новая информация на эту тему.
В 1971 г. Международной Организацией Труда на Генеральной конференции в Женеве была принята Конвенция «О защите от опасности отравления бензолом». Конвенция содержит 22 статьи, в которых всесторонне рассматриваются мероприятия, обеспечивающие защиту трудящихся, подвергающихся воздействию бензола или продуктов, содержание бензола в которых
602
Новый справочник химика и технолога
превышает один объемный процент. Конвенция предписывает во всех возможных случаях заменять бензол другими менее вредными веществами. (Полный текст Конвенции приводится в Приложении 4.1.)
Таким образом, несмотря на отличные технические качества, невысокую стоимость, хорошие растворяющие свойства бензола, от него стремятся отказаться из-за высокой токсичности и вместо бензола использовать менее вредные вещества.
Более подробную информацию о токсических свойствах бензола, мерах безопасности, принимаемых при работе с бензолом, и проблемах экологии можно получить на сайтах:
www.rosinvest.com;
www.businesspravo.ru;
himia.studentu.ru;
nv.vspb.ru;
www.nntu.ru;
www.autoua;
www.rg.ru;
www.aquaexpert.ru;
www.ngv.ru;
www.medlenta.ru;
www.news.bv;
www.line-red.spb.ru;
www.rg.ru;
www.laborant.ru;
www.rpohbv.ru;
uglehim.hl.ru;
www.bvt-s.ru;
www.naukakaz.kz/ru;
www.kentos.ru;
www.erudition.ru;
biology.krc.karelia.ru;
base.safework.ru;
www.himtrade.ru;
www.agroline.ru;
www.epochimes.ru;
www.cocacola.ru;
www.podrobnostu.ua.
Литература
1. Лебедев Н.П. Химия и технология основного органического и нефтехимического синтеза. М.: Химия, 1988.588 с.
2. Справочник нефтехимика / Под род. С.К. Огородникова. Л.: Химия, 1978. Т. 2, 592 с.
3. Ворожцов Н.П. Основы синтеза промежуточных продуктов и красителей. Изд. 4-с. М.: Госхимиздат, 1955.
4. Эфрос Л.С., Горелик М.В. Химия и технология промежуточных продуктов. Л.; Химия, 1980. 544 с.
5. Чекалин М.А., Пасет Б.В., Иоффе В.А. Технология органических красителей и промежуточных продуктов. Л.; Химия, 1980. 472 с.
6. Маслова И.П., Золотарева К.А., Глазунова Н.А. и др. Химические добавки к полимерам: Справ. М.: Химия, 1973.272 с.
7. Мельников Н.П. Пестициды. Химия, технология и применение. М.: Химия, 1987. 712 с.
8. Беккер Г.О. Введение в фотохимию органических соединений / Пер. с нем.; Под ред. А.В. Ельцова. Л.: Химия, 1976. 384 с.
9. Добрянский А.Ф. Анализ нефтяных продуктов. Л.; М.: ОНТИ НКТП СССР, Гл. ред. горно-топливной лит., 1936. 453 с.
10. Губен-Вейль. Методы органической химии. М.: Госхимиздат. 1032 с.
11. Вредные вещества в промышленности: Справ. / Под ред. Н.В. Лазарева и Э.Н. Левиной. Изд.7 -е Л.: Химия, 1976. Т. 2,456 с.
12. Химический энциклопедический словарь / Гл. ред. И.Л. Кнунянц. М.: Советская энциклопедия, 1983. 792 с.
Приложение 4.1
О ЗАЩИТЕ ОТ ОПАСНОСТИ ОТРАВЛЕНИЯ БЕНЗОЛОМ
КОНВЕНЦИЯ
МЕЖДУНАРОДНАЯ ОРГАНИЗАЦИЯ ТРУДА
2 июня 1971 г.
N 136(Д)
Генеральная Конференция Международной Организации Труда, созванная в Женеве Административным Советом Международного Бюро Труда и собравшаяся 2 июня 1971 года на свою пятьдесят шестую сессию, постановив принять ряд предложений о защите трудящихся от опасностей, связанных с использованием бензола, что является шестым пунктом повестки дня сессии, решив придать этим предложениям форму международной конвенции, принимает сего двадцать третьего дня июня месяца тысяча девятьсот семьдесят
первого года нижеследующую Конвенцию, которая будет именоваться Конвенцией 1971 года о бензоле:
Статья 1
Настоящая Конвенция применяется ко всем видам деятельности, при которых трудящиеся подвергаются воздействию: а) ароматического углеводорода бензола (С6Н6), именуемого ниже «бензол»; Ь) продуктов, содержание бензола в которых превышает один объемный процент, именуемых ниже: «продукты, содержащие бензол».
Ароматические соединения
603
Статья 2
1. Всякий раз, когда имеются безвредные или менее вредные продукты-заменители, они применяются вместо продуктов, содержащих бензол.
2. Пункт 1 настоящей статьи не применяется:
а) к производству бензола;
Ь) к использованию бензола в химическом синтезе;
с) к использованию бензола в моторных топливах;
d) к выполняемым в лабораториях работам, связанным с проведением анализов и научных исследований.
Статья 3
1. Компетентный орган власти в каждой стране может допускать временные изъятия из положения о процентном содержании бензола, изложенного в пункте Ь) статьи 1, и из положений пункта 1 статьи 2 настоящей Конвенции при условиях и на срок, которые определяются по консультации с наиболее представительными заинтересованными организациями предпринимателей и трудящихся, если таковые существуют.
2. В таком случае соответствующие Члены Организации в своих докладах о применении настоящей Конвенции, которые они обязаны представлять согласно статье 22 Устава Международной Организации Труда, сообщают о состоянии их законодательства и практики в вопросах, являющихся предметом таких, изъятий, и о достигнутых ими успехах на пути к полному применению положений Конвенции.
3. По истечении трехлетнего срока с момента первоначального вступления в силу настоящей Конвенции Административный Совет Международного Бюро Труда представляет Конференции специальный доклад о применении пунктов 1 и 2 настоящей статьи, с такими предложениями, какие он сочтет целесообразными для принятия дальнейших мер в этой области.
Статья 4
1. Использование бензола и продуктов, содержащих бензол, запрещается при некоторых работах, определяемых национальным законодательством или правилами.
2. Эго запрещение касается, как минимум, использования бензола и продуктов, содержащих бензол, в качестве растворителей или разбавителей, за исключением операций, выполняемых в герметизированных устройствах или посредством других столь же безопасных методов работ, когда таковые имеются.
Статья 5
В целях эффективности защиты трудящихся, подвергающихся воздействию бензола или продуктов, содержащих бензол, применяются технические меры предупреждения и меры промышленной санитарии.
Статья 6
1. В помещениях, где бензол или продукты, содержащие бензол, производятся, используются или с ними выполняются какие-либо операции, принимаются все необходимые меры для предотвращения выделения паров бензола в воздух рабочего помещения.
2. Когда трудящиеся подвергаются воздействию бензола или продуктов, содержащих бензол, предприниматель принимает меры для того, чтобы концентрация бензола в воздухе рабочего помещения не превышала максимальной концентрации, которая устанавливается компетентным органом власти на уровне, не превышающем верхнего предела в 25 частей на миллион (80 мг/м3).
3. Способы определения концентрации бензола в воздухе рабочих помещений устанавливаются инструкциями компетентного органа власти.
Статья 7
1. Работы, связанные с использованием бензола или продуктов, содержащих бензол, выполняются, насколько это возможно, в герметизированных устройствах.
2. Когда нет возможности применять герметизированные устройства, места работы, на которых используются бензол или продукты, содержащие бензол, оборудуются эффективными средствами, обеспечивающими удаление паров бензола в той мерс, в какой это необходимо для охраны здоровья трудящихся.
Статья 8
I. Трудящиеся, которые могут иметь контакт с жидким бензолом или с жидкими продуктами, содержащими бензол, снабжаются средствами индивидуальной защиты от опасности проникновения бензола через кожные покровы.
2. Трудящиеся, которые по особым причинам могуз подвергаться воздействию концентраций бензола в воздухе рабочих помещений, превышающих максимальную концентрацию, указанную в пункте 2 статьи 6 настоящей Конвенции, снабжаются соответствующими средствами индивидуальной защиты, предохраняющими от вдыхания паров бензола; продолжительность пребывания под воздействием паров бензола по возможности ограничивается.
Статья 9
1. Трудящиеся, которые должны выполнять работы, связанные с воздействием бензола или продуктов, содержащих бензол, проходят:
а) тщательный предварительный медицинский осмотр в целях определения пригодности к работе, включая исследование крови;
Ь) последующие периодические осмотры, включающие биологические исследования, в том числе исследование крови, периодичность которых определяется национальным законодательством или правилами.
2. Компетентный орган власти в каждой стране, по консультации с наиболее представительными заинтересованными организациями предпринимателей и трудящихся, если таковые существуют, может разрешить изъятия из обязательств, предусмотренных в пункте 1 настоящей статьи, в отношении отдельных категорий трудящихся.
604
Новый справочник химика и технолога
Статья 10
1. Медицинские осмотры, предусмотренные в пункте 1 статьи 9 настоящей Конвенции:
а) проводятся под ответственностью квалифицированного врача, назначенного по согласованию с компетентным органом власти, с помощью, при необходимости, компетентных лабораторий;
Ь) документально подтверждаются надлежащим образом.
2. Эти медицинские осмотры нс могут приводить к каким-либо расходам для трудящихся.
Статья 11
1. Женщины в период медицински установленной беременности и кормящие матери не могут быть заняты на работах, связанных с воздействием бензола или продуктов, содержащих бензол.
2. Подростки моложе 18 лет не могут быть заняты на работах, связанных с воздействием бензола или продуктов, содержащих бензол; однако это запрещение может не применяться к подросткам, проходящим обучение или подготовку, если они находятся под должным техническим и медицинским наблюдением.
Статья 12
Надпись «Бензол» и необходимые символы опасности должны быть ясно видны на любой таре, в которой находятся бензол или продукты, содержащие бензол.
Статья 13
Каждый Член Организации принимает все соответствующие меры, для того чтобы любой трудящийся, подвергающийся воздействию бензола или продуктов, содержащих бензол, получал надлежащий инструктаж о мерах по охране здоровья и по предупреждению несчастных случаев, а также о мерах, которые следует принимать в случае появления симптомов отравления.
Статья 14
Каждый Член Организации, ратифицирующий настоящую Конвенцию:
а) принимает в законодательном порядке или любым иным путем, соответствующим национальной практике и условиям, необходимые меры для осуществления положений настоящей Конвенции;
Ь) указывает, в соответствии с национальной практикой, лицо или лиц, на которых лежит обязанность обеспечивать применение положений настоящей Конвенции;
с) обязуется возложить на соответствующие службы инспекции контроль за применением положений настоящей Конвенции или следить за осуществлением надлежащей инспекции.
Статья 15
Официальные документы о ратификации настоящей Конвенции направляются Генеральному Директору Международного Бюро Труда для регистрации.
Статья 16
1. Настоящая Конвенция связывает только тех Членов Международной Организации Труда, чьи докумен
ты о ратификации зарегистрированы Генеральным Директором.
2. Она вступает в силу через двенадцать месяцев после того, как Генеральный Директор зарегистрирует документы о ратификации двух Членов Организации.
3. Впоследствии настоящая Конвенция вступает в силу в отношении каждого Члена Организации через двенадцать месяцев после даты регистрации его документа о ратификации.
Статья 17
1. Любой Член Организации, ратифицировавший настоящую Конвенцию, может но истечении десятилетнего периода с момента се первоначального вступления в силу денонсировать ее посредством акта о денонсации, направленного Генеральному Директору Международного Бюро Труда и зарегистрированного им. Денонсация вступает в силу через год после регистрации акта о денонсации.
2. Каждый Член Организации, ратифицировавший настоящую Конвенцию, который в годичный срок по истечении упомянутого в предыдущем пункте десятилетнего периода не воспользуется своим правом на денонсацию, предусмотренным в настоящей статье, будет связан на следующий период в десять лет и впоследствии сможет денонсировать настоящую Конвенцию но истечении каждого десятилетнего периода в порядке, установленном в настоящей статье.
Статья 18
1. Генеральный Директор Международного Бюро Труда извещает всех Членов Международной Организации Труда о регистрации всех документов о ратификации и актов о денонсации, полученных им от Членов Организации.
2. Извещая Членов Организации о регистрации полученного им второго документа о ратификации, Генеральный Директор обращает их внимание на дату вступления настоящей Конвенции в силу.
Статья 19
Генеральный Директор Международного Бюро Труда направляет Генеральному Секретарю Организации Объединенных Наций для регистрации в соответствии со статьей 102 Устава Организации Объединенных Наций полные сведения относительно всех документов о ратификации и актов о денонсации, зарегистрированных им в соответствии с положениями предыдущих статей.
Статья 20
Каждый раз, когда Административный Совет Международного Бюро Труда считает это необходимым, он представляет Генеральной Конференции доклад о применении настоящей Конвенции и решает, следует ли включать в повестку дня Конференции вопрос о ее полном или частичном пересмотре.
Статья 21
1. В случае, если Конференция примет новую конвенцию, полностью или частично пересматривающую
Ароматические соединения
605
настоящую Конвенцию, и если в новой конвенции не предусмотрено обратное, то:
а) ратификация каким-либо Членом Организации новой, пересматривающей конвенции влечет за собой автоматически, независимо от положений статья 17, немедленную денонсацию настоящей Конвенции при условии, что новая, пересматривающая конвенция вступила в силу:
Ь) начиная с даты вступления в силу новой, пересматривающей конвенции настоящая Конвенция закрыта для ратификации ее Членами Организации.
2. Настоящая Конвенция остается во всяком случае в силе по форме и содержанию в отношении тех Членов Организации, которые ее ратифицировали, но не ратифицировали новую, пересматривающую конвенцию.
Статья 22
Английский и французский тексты настоящей Конвенции имеют одинаковую силу.
/подписи/
4.2. Анилин
Анилин является простейшим ароматическим амином, одним из первых органических продуктов, который в значительных количествах начали получать еще в XIX в. Получали анилин путем восстановления нитробензола железом в уксусной кислоте. Синтез анилина на несколько десятилетий определил направление развития органической химии и послужил основой для создания промышленности органических красителей.
Более 60 лет анилин использовался исключительно в анилинокрасочной промышленности. В этот период производство красителей в промышленно развитых странах в среднем увеличивалось в год на -4 %.
В начале XX в. было обнаружено, что анилин ускоряет вулканизацию каучука, и с этого времени потребность в анилине стала неуклонно возрастать. Однако до 1930 г. основным потребителем анилина по-прежнему оставалась промышленность синтетических красителей.
После второй мировой войны значительно возрастает доля анилина, расходуемого на производство химикатов для резины, прежде всего ускорителей вулканизации резины: каптакса, альтакса, дифенилгуанидина. В 1961 г. уже 2/3 всего произведенного анилина расходовалась на нужды промышленности резиновых изделий (получение химических добавок для резины).
В 1960-е гг. производство анилина значительно возросло, благодаря созданию полиуретанов — полимеров, получаемых из полупродуктов на основе анилина и широко используемых для конструкционных материалов. С 1960 по 1975 г. мировое производство анилина увеличилось почти в 5 раз, причем среднегодовой прирост производства составлял 25 %. С тех пор мировое производство анилина, подстегиваемое ростом спроса на полиуретаны, продолжает расти, и анилин является одним из самых востребованных органических полупродуктов.
4.2.1. Мировой рынок анилина
В ближайшем будущем движущей силой роста спроса на анилин будет расширение производства ди-фенилметандиизоцианата, для получения которого необходим анилин. Такая тенденция наблюдается
с 1982 г. В 2000 г. на долю дифенилметандиизоцианата приходилось 84 % потребления анилина в США, 80 % — в Западной Европе, 87 % — в Японии.
Дифснилметандиизоцианат используется, в первую очередь, для изготовления жесткого полиуретана и полиуретановых эластомеров (например, пластмасс для реакционного инжекционного формования). Главным потребителем жесткого полиуретана является строительство, а самым крупным потребителем мягких и жестких пенопластов и пластмасс для реакционного инжекционного формования — автомобильная промышленность.
В настоящее время, по данным агентства «DeWitt», производство полиуретанов потребляет 85 % производимого анилина, и если рынок полиуретанов будет продолжать расти в таком же темпе, то к 2008 г. будет ощущаться нехватка анилина, т. к. (по прогнозам того же агентства) рост производства анилина до 2008 г. составит 5,2 % в год. В связи с этим на некоторых заводах планируется увеличить производство анилина. Так, португальская компания «Quimigal» намерена расширить производство анилина на своем заводе до 30-40 тыс. т/г. Германский концерн «Bayer» планирует к 2006 г увеличить мощности на заводе в Антверпене (Бельгия) на 25 тыс. т/г. Чешская «Borsodchem-MCHZ» с середины 2005 г. планирует довести уровень производства анилина до 150 тыс. т/г.
Основной объем анилина производят 10 корпораций США, Японии и Западной Европы. Крупнейшими производителями анилина являются корпорации «Huntsman» (с заводами в Великобритании и США, например, Rubicon), «Bayer AG» (с заводами в Бельгии, Германии и США) и «BASF» (с заводами в Бельгии, Германии и США). В табл. 4.2.1 приведены основные фирмы, производящие анилин.
В России крупнейшим производителем анилина (более 80 % всего объема) является АО «Волжский орг-синтез». Анилин выпускают также на предприятиях: АО «Химпром» (г. Новочебоксарск), АО «Бератон» (г. Березники) и АО «Анилинокрасочный завод» (г. Кемерово). В 2000 г. -13% выпускаемого анилина экспортировались, однако в последние годы экспорт ани
606
Новый справочник химика и технолога
лина резко сократился в связи с высоким спросом на анилин со стороны российских потребителей. Конъюнктура рынка анилина в России в основном зависит от конъюнктуры рынка сырья, в первую очередь бензола.
Таблица 4.2.1
Основные фирмы, производящие анилин
Страна Фирма
США ФРГ Великобритания Португалия Франция Швейцария Япония American Cyanamid Du Pont (E. 1.) de Nemours First Chemical Mobay Chemical Rubicon Chemicals Bayer AG Bayer Antwerpen NY BASF ICI Quimigal Pechiney-Ugine-Kuhlmann Lonza Мицун сэкию кагаку Сумитомо кагаку Шин Ниппон Рика Мицун Тоатсу Кемикалз Ниппон Пориуретан
Цены на анилин и его производные за последние годы демонстрировали самые высокие темпы роста по сравнению с остальным сырьем на основе бензола.
Более подробную информацию о мировом рынке анилина можно найти в Интернете на сайтах:
www.rcc.ru;
www.advis/ru;
www.avias.com;
www.polymers-money.com;
www.lh.ru;
www.plastinfo.ru;
www.chemprice.ru;
www.chemmarket.info;
www.himvestnik.ru;
www.himtek.ru;
www.usetender.com;
www.chembz.ru.
4.2.2. История анилина
Анилин был впервые получен в 1826 г. немецким аптекарем О. Унфердорбеном. Унфердорбен, перегоняя индиго, выделил маслянистое вещество, способное образовывать кристаллические соли с серной и фосфорной кислотами, и назвал это соединение «кристаллином».
В 1834 г. немецкий химик Ф. Рунге обнаружил это же соединение в продуктах сухой перегонки каменноугольной смолы и назвал «кианолом» от греческого «кианос» — лазурный и латинского «олеум» — масло,
поскольку маслянистый продукт давал голубое окрашивание с раствором хлорной извести.
В 1840 г. немецкий химик и ботаник, академик Петербургской АН К. Фрицше, обрабатывая индиго горячей концентрированной щелочью, выделил антраниловую кислоту, распадающуюся при нагревании на диоксид углерода и соединение, содержащее азот, которое он назвал «анилином» от испанского названия индиго — «анил».
В 1842 г. анилин впервые был получен синтетическим путем выдающимся русским химиком Н.Н. Зининым. Н.Н. Зинин, восстанавливая нитробензол сульфидом аммония, получил маслянистый продукт, который назвал бензидамом. В этом же году К. Фрицше, исследуя свойства бензидама и анилина, установил их идентичность и определил брутто-формулу соединений C6H7N.
В 1843 г. немецкий химик А. Гофман, исследуя и сравнивая «бензидам» Зинина с «анилином» Фрицше и «кианолом» Рунге, установил полную идентичность всех трех соединений.
Синтез анилина имел огромное значение для химической науки и промышленности. «Если бы Зинин не сделал ничего более, кроме превращения нитробензола в анилин, то его имя и тогда осталось бы записанным золотыми буквами в истории химии» — эти слова крупнейшего немецкого химика А. Гофмана, одного из создателей промышленности красителей в Германии, подтверждают огромное значение открытия Зинина. За прошедшее столетие справедливость этих слов выдержала испытание временем: синтез анилина, а также других ароматических аминов по этому же методу, именуемому в литературе реакцией Зинина, на несколько десятилетий определил направления развития органический химии и послужил основой для создания промышленности синтетических красителей. Был открыт путь к получению дешевых и доступных красящих веществ (взамен природных красителей) для текстиля, бумаги, кожи и других материалов.
В 1856 г., после того как английский химик У. Перкин создал промышленное производство первого синтетического красителя — мовеина (образуется при взаимодействии анилина с бихроматом калия), французским химиком А. Бешаном было организовано полупромышленное производство анилина. Получали анилин путем восстановления сырого нитробензола железом в уксусной кислоте. Позднее уксусная кислота была заменена на соляную.
Производство анилина в промышленном масштабе было организовано в 1866 г. шотландским химиком А. Купером. Анилин получали из очищенного нитробензола по схеме А. Бешана.
В 1872 г. русским ученым М.М. Зайцевым была открыта реакция восстановления нитросоединений водородом в присутствии катализаторов. Превращение нитробензола в анилин было осуществлено путем пропускания смеси паров нитробензола и водорода над
Ароматические соединения
607
палладиевой чернью, помещенной в нагретую до 150 °C стеклянную трубку.
В начале XX в. французские химики П. Сабатье и Ж. Сандеран показали, что и многие другие металлы, имеющие большую удельную поверхность, например получаемые восстановлением их оксидов при нагревании в струе водорода, оказываются эффективными катализаторами восстановления нитробензола в анилин. Однако прежде чем процесс газофазного восстановления нитробензола был реализован в промышленности, прошло около 50 лет. С середины 1950-х гг. получение анилина каталитическим восстановлением нитробензола водородом занимает прочное место среди промышленных методов синтеза анилина, а к началу 1960-х гг. этот способ почти повсеместно вытесняет другие методы.
В незначительных количествах анилин содержится в каменноугольной смоле.
4.2.3. Методы получения анилина
4.2.3.1. Восстановление нитробензола
c6h5-no2 > c6h^nh2
(/) У)
Это самый распространенный метод получения анилина. В качестве восстановителей могут быть использованы самые разнообразные неорганические и органические вещества. Применение в технике нашли соединения, наиболее доступные по цене и удобные для практического использования: металлы (железо, цинк, олово), соли (хлорид олова, сульфиды щелочных металлов, гидросульфиты), сероводород. Кроме того, вое-
I |_|
C6H5-NO2 —► C6H5-NO --------------
—Н2О
(/) (3)
становление можно вести каталитическим или электрохимическим методом. В лабораторной, а в последние годы — ив заводской практике все большее значение приобретает восстановление нитробензола смешанными гидридами металлов: алюмогидридом лития, бор-гидридом натрия.
Восстановление нитросоединений протекает ступенчато и в общем виде может быть выражено уравнением (4.2.1).
Конечный продукт реакции зависит от природы восстановителя и характера среды. В кислой среде конечным продуктом восстановления всегда является анилин (2), а нитрозобензол (3) и фенилгидроксиламин (4) образуются в качестве промежуточных продуктов. Однако в нейтральной среде нитрозобензол и фенилгидроксиламин могут быть получены как конечные продукты восстановления нитробензола. В щелочной среде процесс идет более сложно (уравнение (4.2.2)), т. к. фенилгидроксиламин (4), являясь весьма реакционноспособным соединением, в этих условиях активно взаимодействует с нитро- (7) или нитрозобензолом (3), образуя азоксибензол (5). При дальнейшем восстановлении азоксибензол превращается в азобензол (6), далее в гидразобензол (7) и, наконец, в анилин.
Обычно восстановление нитробензола металлами и их солями в щелочной среде приводит к образованию азобензола (SnCl2; NaOH) или гидразобензола (Zn; NaOH); анилин в этих условиях не получают. Однако при восстановлении нитробензола в щелочной среде сульфидами щелочных металлов образуется анилин. Таким образом, варьируя восстановитель и условия восстановления, можно регулировать процесс, получая тот или иной целевой продукт.
C6H5-NHOH C6H5-NH2 (4.2.1)
(4) (2)
СбН5-ЫО (или C6H5-NO2 ) + C6H5-NHOH
* c6h5-n=n-c6h5
I о
(5)
(4.2.2)
c6h5-n=n-c6h5 c6h5nh-nhqh5 c6h5nh2
—Н7О
(6) (7) (2)
Восстановление нитробензола железом в присутствии электролитов
В 1854 г. французским химиком Антуаном Бешаном была открыта реакция восстановления нитробензола железом в слабокислой среде. Этот метод получения анилина, известный как метод Вешана, оказался про
стым и доступным. Как промышленный метод получения анилина он существует с 1856 г. Достоинствами этого метода являются высокий выход анилина, отсутствие побочных продуктов, дешевизна восстанавливающего агента и простота технологического оформления процесса.
608
Новый справочник химика и технолога
Механизм восстановления нитросоединений железом, в частности чугунными стружками, был обстоятельно изучен В.О. Лукашевичем, который показал, что реакция протекает в две стадии. На первой стадии происходит восстановление нитросоединения железом, при этом железо окисляется и образуется гидроксид железа(П) (уравнение (4.2.3)). Гидроксид желс-за(П) также способен восстанавливать нитросоединение до амина, превращаясь при этом в гидроксид жслеза(Ш) (уравнение (4.2.4)). Реакция идет с большой скоростью.
Соотношение скоростей первой и второй стадий определяет соотношение в реакционном шламе оксидов железа, образующихся из гидроксидов путем дегидратации. На соотношение образующихся оксидов железа влияет также наличие избытка чугунной стружки (уравнение (4.2.5)), степень ее измельчения и природа применяемого элскгролита. При восстановлении в присутствии хлорида аммония, например, в шламе содержится 49,7 % оксида железа (111), а в присутствии хлорида железа (III) содержание оксида железа (III) составляет 74,7 %.
C6H5NO2 + 3Fe + 4Н2О C6H5NH2 + 3Fe(OH)2 (4.2.3)
C6H5NO2 + 6Fe(OH)2 + 4H2O -» C6H5NH2 + 6Fe(OH)3 (4.2.4)
Fe + 8Fe(OH)3 3Fe3O4 + 12H2O (4.2.5)
Суммарном уравнением реакции восстановления ароматических нитрососдинений железом в присутствии электролитов является уравнение (4.2.6).
4C6H5NO2 + 9Fe + 4Н2О -> 4C6H5NH2 + 3Fe3O4 (4.2.6)
Как видно из приведенных уравнений, восстановление протекает только за счет железа и воды. Однако чтобы реакция шла успешно, необходимо обеспечить условия влажной коррозии железа. Такие условия создаются при наличии в реакционной массе электролитов. В качестве электролитов применяют растворимые соли железа (хлорид, ацетат, формиат), соли аммония (сульфат, хлорид), реже хлорид натрия и сульфат железа (II).
Было показано, что скорость коррозии железа, которая в растворах солей в несколько раз (до 10) больше, чем в воде, зависит от природы и концентрации электролита. Наивысшая скорость процесса наблюдается при использовании хлоридов аммония и жслеза(П), несколько меньшая — при использовании сульфата аммония. Количество применяемого электролита обычно составляет 0,1 -0,2 моль / 1 моль нитробензола.
Электролиты вводят в реакционную массу готовыми или (чаще) получают в самом аппарате взаимодействием чугунных стружек с разбавленными кислотами: соляной, серной, уксусной, муравьиной.
Этот процесс носит название протравливания чугуна (железа) и производится обычно до добавления нитросоединения.
Для восстановления лучше всего использовать стружку серого чугуна — отход металлообрабатывающих заводов. Серый чугун по химической природе представляет собой железо, в котором растворен углерод, образующий обнаруживаемые в микроструктуре чугуна
углеродсодержащие компоненты: феррит и перлит, а также графит. Кроме того, в чугуне в небольших количествах содержатся соединения других элементов: Mn, Р, Si, S. Химическая неоднородность чугуна является причиной его активности в отношении окисления во влажной среде (влажная коррозия), т. к. обусловливает возможность возникновения элементарных гальванических пар, например, феррит—графит. Выделяющийся при этом на аноде кислород способствует окислению железа. Вследствие зернистого строения серого чугуна его стружка очень хрупка и легко ломается, поэтому при размешивании в процессе восстановления она распадается на мелкие частицы. При этом значительно увеличивается ее поверхность соприкосновения с жидкостью, что ведет к ускорению восстановления. Часто перед употреблением стружку специально измельчают и просеивают.
Для восстановления ни тробензола в анилин в промышленных масштабах были разработаны два способа: периодический и непрерывный.
Периодический способ. Восстановление нитробензола в анилин в аппаратах периодического действия осуществляется в промышленном масштабе более 100 лет без существенных усовершенствований (рис. 4.2.1).
Для восстановления нитробензола применяют цилиндрические реакционные аппараты (редукторы), стальные или чугунные, емкостью 10-20 м3, защищенные изнутри от коррозии и истирания кислотоупорной плиткой. Аппараты снабжены мощными тихоходными мешалками, необходимыми для размешивания тяжелого осадка, состоящего из чугунных стружек и оксидов железа. Через полый вал мешалки в аппарат подают острый пар для нагрева массы в начальный период восстановления. Редукторы некоторых конструкций имеют паровую рубашку для обогрева.
Ароматические соединения
609
Вода (или возвратная анилиновая вода)
Рис. 4.2.1. Схема установки для получения анилина восстановлением нитробензола:
/ — редуктор; 2 — грубчатый холодильник; 3 — змеевиковый холодильник; 4 — холодильник для легких углеводородов;
5 — штуцер для загрузки реагентов; 6 — труба для загрузки чугунных сгружск; 7 — краны
Порядок загрузки реагентов может быть различным. Обычно сначала в аппарат загружают воду (или возвратную анилиновую воду) и часть чугунной стружки, нагревают острым паром и добавляют готовый электролит или кислоту для протравливания стружки. Затем постепенно порциями добавляют нитробензол и оставшееся количество чугунной стружки.
Восстановление нитробензола в анилин сопровождается выделением большого количества тепла (548 кДж/моль), поэтому реакционная масса в редукторе находится постоянно в состоянии кипения, которое поддерживается за счет теплоты реакции. При этом испаряется большое количество воды и образующегося анилина. Пары воды и анилина конденсируются в обратном холодильнике и возвращаются в редуктор. Отгоняющийся анилин содержит некоторое количество непрореагировавшего нитробензола. После окончания загрузки нитробензола проводят небольшую выдержку до полного восстановления. Конец реакции определяют по исчезновению окраски конденсата, возвращающегося в редуктор, или по концентрации образовавшегося анилина, которую определяют с помощью титрования нитритом натрия.
После нейтрализации реакционной массы анилин из смеси выделяют. Применяется несколько методов выделения: отгонка анилина из редуктора острым паром, вакуум-отгонка анилина из реакционной массы, сифо-нирование анилина из редуктора. Из-за сложности аппаратурного оформления первый и второй методы не нашли широкого применения. Наиболее распространенным является третий метод — сифонирование, основанный на том, что при комнатной температуре плотность анилина больше, чем воды, но уже при 71 °C его плотность меньше. Разность в плотностях еще больше увеличивается при добавлении в редуктор хлорида натрия. Анилин всплывает наверх и может быть отделен сифонированием. Около половины анилина остается
в водном слое и железном шламе и отгоняется с острым паром. Так как анилин частично растворим в воде (~3 %), водный слой после отделения анилина вновь возвращают в процесс или экстрагируют нитробензолом. Общий выход анилина ~97 % от теоретического.
Образующийся в процессе реакции шлам состоит из смеси оксидов железа: FeO и Fe2O3. Его промывают, сушат и прокаливают, при этом получают искусственные железооксидные пигменты красного, коричневого и черного цветов. Если проводить восстановление в присутствии хлорида алюминия, образуется гидрат оксида железа FeO(OH) или Fe2O3 • Н2О находящий применение в качестве желтого пигмента.
Этот промышленный метод восстановления нигро-соединений до аминов практически потерял свое значение для анилина. В настоящее время он используется лишь для получения малотоннажных аминов: о- и «-толуидинов, ксилидинов, w-фенилендиамина, охлор-анилина, 2,5-дихлоранилина.
Непрерывный способ. При непрерывном восстановлении нитробензола применяют редуктор той же конструкции, что и при периодическом. Для ускорения реакции восстановления в процесс вводят самый активный электролит — хлорид аммония и чугунную стружку, обладающую повышенной активностью, равномерно измельченную и очищенную от примесей.
Нитробензол, раствор хлорида аммония и «анилиновая вода» из напорных емкостей поступают в смеситель / (рис. 4.2.2), смешиваются там и насосом 2 подаются в редуктор 3 под слой чугунной стружки, которая непрерывно подается в редуктор шнековым питателем 4. Острым паром через барботер реакционную массу нагревают до кипения, а затем кипение поддерживается за счет теплоты реакции. Подача в редуктор нитробензола, раствора хлорида аммония, анилиновой воды, а также чугунной стружки регулируется автоматически.
610
Новый справочник химика и технолога
При постоянной подаче этих компонентов ход реакции зависит только от количества загружаемой в редуктор чугунной стружки, активность которой может в известных пределах колебаться.
Электродвигатели питателя и мешалки сблокированы. При избыточной загрузке редуктора стружкой возрастает потребляемая мощность электродвигателя мешалки. В этом случае автоматически временно прекращается подача стружки шнековым питателем.
Полнота реакции восстановления контролируется фотоколориметрически: остаточное содержание нитробензола не должно быть выше 0,05 %. При увеличении содержания нитробензола в анилине выше 0,05 % поток жидкости, вытекающей из конденсатора 5, автоматически с помощью исполнительных механизмов направляется в аварийные емкости, а подача реагентов в редуктор снижается.
Основное количество полученного анилина отгоняется из редуктора с водяным паром, часть которого образуется вследствие теплоты реакции, а часть подается в редуктор через барботер. Пары анилина и воды на
правляются в конденсатор 5. Шламовая жидкость, в которой остается более 40 % анилина, непрерывно удаляется из редуктора через верхний боковой штуцер и перетекает в аппарат 6, из которого острым паром отгоняют оставшийся анилин. Анилин и водяной пар конденсируются в аппарате 7, охлаждаемом водой. Конденсат попадает в отстойник шлама 8, холодильник 9 и сепаратор 10, в котором водный анилин отделяется от анилиновой воды.
Сырой анилин собирается в сборнике //, из которого подается на вакуум-перегонку для получения товарного продукта. Анилиновая вода собирается в сборнике 12, а затем перегоняется в насадочной колонне. Разбавленная анилиновая вода после охлаждения возвращается в редуктор, а смесь анилина с водой — в сепаратор 10. Если баланс анилиновой воды почему-либо нарушился, то перед сбросом ее в канализацию анилин экстрагируют нитробензолом.
Непрерывный способ восстановления нитробензола чугунной стружкой в среде электролита впервые был разработан и внедрен в промышленность в Советском Союзе.
Рис. 4.2.2. Схема непрерывного восстановления нитробензола чугунной стружкой:
1 — смеситель; 2 — насос; 3 — редуктор; 4 — шнековый питатель; 5,7 — конденсаторы; 6 — аппарат для отгонки анилина; 8 — отстойник шлама; 9 — холодильник; 10 — сепаратор; 11 — сборник сырого анилина; 12 — сборник анилиновой воды
Этот метод позволил несколько улучшить условия труда, но технико-экономические показатели производства существенно не улучшились. Непрерывный метод используется до сих пор, хотя и он фактически утратил свое значение из-за большого количества сточных вод, содержащих анилин и нитробензол, громоздкости аппаратуры и трудоемкости. Важной проблемой является также утилизация образующегося железного шлама.
Каталитическое восстановление нитробензола
В настоящее время этот способ восстановления нитробензола с целью получения анилина в промышленности является основным, т. к. отличается высокой скоростью, чистотой получаемых продуктов, простотой
технологии, возможностью автоматизации технологического процесса.
Направление реакции и степень восстановления нитросоединения часто зависят от условий процесса и природы применяемых катализаторов. Роль катализатора в процессах каталитического восстановления заключается в активации реагентов — восстанавливаемого соединения и молекулярного водорода. При сорбции водорода на активных центрах катализатора (К) ослабляются или даже полностью разрываются химические связи в молекулах водорода (уравнение (4.2.7)).
К + Н2-+К Н2->К-Н Н->2К-Н (4.2.7)
Нитросоединения также сорбируются на катализаторе, но в меньшей степени. Дальнейшее взаимодейст-
Ароматические соединения
611
вис происходит между двумя сорбированными молекулами, находящимися на соседних активных центрах. При этом образуется продукт гидрирования, обладающий меньшей сорбционной способностью, вследствие чего он вытесняется с активных центров катализатора новой молекулой нигросоединения.
Активность катализаторов, применяемых в реакциях гидрирования нитросоединений, зависит от их химического состава и физического состояния. Чаще всего применяются металлические катализаторы, особенно металлы VIII группы периодической системы — платина, палладий, родий, никель, кобальт, а также сплавы никеля и хрома, никеля и меди и др. Показано, что активность катализатора увеличивается, если он содержит примеси некоторых веществ — загрязнения или же специальные добавки — так называемые активаторы. Большое значение имеет также степень измельчения катализатора. Максимальное раздробление достигается осаждением каталитически активного вещества на так называемый носитель.
Роль активаторов и носителей до настоящего времени полностью не выяснена. Известно, что тс и другие вызывают изменения структуры поверхности катализатора, носители, кроме того, значительно увеличивают поверхность катализатора. В результате уменьшается склонность катализатора к спеканию при повышенных
СбН5-МО2 + ЗН2
Восстановление в паровой фазе. В условиях парофазного процесса нитросоединсние испаряется, смешивается с избытком водорода и пропускается через контактный аппарат, заполненный твердым катализатором. Процесс восстановления идет на поверхности катализатора до полного превращения нитросоединения в амин. Реакционное тепло отводится либо избытком водорода, либо высококипящим органическим теплоносителем (ВОТ). Реакционные газы охлаждаются, амин конденсируется, а избыток водорода возвращается в цикл. Преимущество метода в том, что катализатор нс увлекается реакционными газами.
Катализаторами этого процесса являются активные сплавы никеля, алюминия, вольфрама, медь, нанесенная на оксид кремния. Наиболее подходящим катализатором для восстановления нитробензола является медь, т. к. ее действие распространяется только на нитрогруппу, не затрагивая ароматического ядра. В присутствии медного катализатора превращение нитробензола в анилин начинается при 230 °C, между 300 и 400 °C реакция проходит быстро. При избытке водорода выход анилина достигает 98 %, причем в получаемом продукте содержатся лишь следы азобензола. Водород может быть заменен водяным газом (смесь СО и Н2О), при этом монооксид углерода также играет роль восстановителя, превращаясь в диоксид.
Медь, полученная восстановлением гидроксида меди (II), более активна как катализатор восстановления, чем полученная из нитрата меди (II). Медь, нанесенная
температурах. Вероятно, добавление активатора или носителя увеличивает количество активных центров, а также их характер. В качестве активаторов применяются чаще всего оксиды и гидроксиды различных металлов, реже некоторые их соли, причем для каждой пары катализатор—активатор существует оптимальное количественное соотношение, при котором катализатор имеет максимальную активность.
В качестве носителей применяют различные пористые материалы, такие, как активированный уголь, асбест, пемза.
Способ приготовления катализаторов оказывает огромное влияние на их активность и область применения. Чувствительность катализаторов к небольшим изменениям условий их получения очень велика, вследствие чего даже катализаторы, полученные, казалось бы, при одинаковых условиях, обычно обнаруживают различную активность.
Реакция восстановления нитросоединений водородом идет по уравнению (4.2.8).
Реакция, как видно из уравнения, идет с уменьшением объема. Поэтому ее проводят при сравнительно низкой температуре и преимущественно под давлением.
Каталитическое восстановление нитробензола проводят в паровой или жидкой фазе.
С6Н5НЧН2 + 2Н2О (4.2.8)
на асбест, более активна, чем нанесенная на пемзу или приготовленная без носителя. Однако медь, нанесенная на асбест, скорее теряет активность.
В промышленности катализатором служит карбонат меди, нанесенный в виде суспензии в растворе силиката натрия на пемзу и восстановленный водородом. Катализатор хорошо работает около года, но за этот период дважды подвергается регенерации.
Схема производства анилина каталитическим восстановлением нитробензола в паровой фазе изображена на рис. 4.2.3.
Нитробензол из резервуара проходит через экстрактор, в котором извлекает полученный анилин из воды, образующейся в результате реакции, и поступает в напорный бачок б, а затем в трубчатый испаритель 5. Испарение нитробензола происходит в тонкой пленке, нагрев осуществляется горячим водородом, нагнетаемым газодувкой 2 и проходящим через теплообменники 3 и 4. Пары нитробензола смешиваются с водородом и проходят в два соединенных последовательно контактных аппарата 7 и 8 (конвекторы), содержащих катализатор. В качестве катализатора наиболее часто используют медь на носителях, т. к. при использовании этих катализаторов не идет гидрирование ароматического кольца. Реакция начинается в первом аппарате при 170 °C, при выходе из второго аппарата температура смеси доходит до 350— 370 °C. Давление в аппаратах 0,15-0,20 МПа.
Из реакторов контактные газы проходят через теплообменник 3, нагревая водород, а затем поступают
612
Новый справочник химика и технолога
в конденсатор 9, где конденсируются пары анилина и воды. Для полного улавливания анилина газы проходят через теплообменник 10 с развитой охлаждающей поверхностью и сепаратор 11. Избыток водорода возвращается в цикл, конденсат стекает в отстойник 12, из которого «анилиновая вода» поступает на экстракцию нитробензолом, а анилин — на вакуум-перегонку. Выход анилина составляет 98 % от теоретического. Побочно образуется 0,3-0,4 % о-аминофенола, который можно выделить из кубового остатка, остающегося после перегонки анилина.
По мерс потери активности катализатора температура газов на входе в контактный аппарат должна повышаться до 280 °C, причем производительность установки снижается. Катализатор регенерируют 4-5 раз за
время работы (регенерацию проводят в токе воздуха с последующим восстановлением оксида меди водородом). Возможна также пропитка катализатора медно-аммиачным раствором. После прохождения через реакторы 4000 т нитробензола катализатор подлежит замене. Расход меди — 1 кг на 1000 кг анилина.
При описанном методе восстановления нитробензола для регулирования температуры в контактном аппарате применяется большой избыток водорода, возвращаемого в процесс после отделения продуктов реакции. При этом во много раз увеличивается объем контактных газов, выходящих из аппарата, и уменьшается концентрация в них анилина. Большой объем газов вызывает необходимость использования громоздких аппаратов на всех стадиях процесса и больших поверхностей теплообмена.
Нитробензол с анилином
вакуум-перегонку
Рис. 4.2.3. Схема производства анилина гидрированием нитробензола:
/ — гидравлический затвор; 2 — газодувка; 3, 4, 10 — теплообменник; 5 — испаритель; 6 — напорный бачок; 7, 8 — конвекторы;
9 — конденсатор; 11 — сепаратор; 12 — отстойник
В настоящее время в производстве анилина в качестве реактора используют также кожухотрубчатые контактные аппараты, в трубки которых загружают катализатор. В этом случае регулирование температуры и отвод тепла обеспечиваются высококипящим органическим теплоносителем, которым заполняют межтрубное пространство. Тепло, выделяющееся в процессе восстановления нитробензола, вызывает кипение ВОТ, пары которого поступают в межтрубное пространство парового котла-утилизатора, где теплоноситель конденсируется и стекает обратно в контактный аппарат. Высокий коэффициент теплопередачи от кипящего ВОТ к газам позволяет поднять температуру газов на входе в контактный аппарат значительно выше 170 °C, что, наряду с уменьшением объема газов, повышает производительность контактного аппарата. Такой метод отвода теплоты реакции приводит к снижению капитальных и эксплуатационных расходов.
Парофазное каталитическое восстановление нитробензола является основным методом получения анилина во всем мире. При сравнении технико-экономических показателей производства анилина этим методом и непрерывным методом восстановления нитробензола чугунными стружками в среде электролита было установлено, что метод парофазного каталитического восстановления более экономичен: затраты на 1 т готовой продукции уменьшаются примерно на 15 %, уменьшается также расход энергии. Основной статьей расходов в обоих методах являются расходы на сырье; для улучшения технико-экономических показателей необходимо в первую очередь снижение этих затрат. Использование более селективных катализаторов, уменьшение потерь на каждой стадии процесса, уменьшение осмоления анилина приводят к повышению выхода анилина.
С высоким выходом (97-99 % от теоретического) получается анилин при использовании в качестве
Ароматические соединения
613
катализатора никеля, комбинированного с оксидами ванадия и алюминия. Катализатор работает в относительно широком интервале температур (240-300 °C) и легко регенерируется при окислении воздухом. Описано также производство анилина с использованием подвижного слоя катализатора (медь на силикагеле). Метод позволяет легко отводить выделяющееся при реакции тепло посредством контактных аппаратов с межтрубным пространством, заполненным органическим теплоносителем. В других случаях для отвода тепла используется кипящая вода, дающая перегретый пар.
Если в исходном нитробензоле присутствуют каталитические яды, например сернистые соединения, гидрирование можно вести на сульфидах никеля и молибдена при 350-370 °C и давлении 20-30 МПа, что значительно усложняет аппаратуру.
Восстановление в жидкой фазе. Каталитическое восстановление нитробензола водородом в жидкой фазе имеет не меньшее значение, чем парофазное восстановление. Этот процесс проходит при более низкой температуре, чем газофазный. Так как один из ингредиентов реакции (водород) газообразен, то для увеличения его концентрации в системе процесс ведут под давлением в автоклавах. В условиях периодического жидкофазного процесса нитросоединение, смешанное с твердым катализатором, обрабатывают водородом под давлением до прекращения поглощения последнего. После отстаивания образовавшегося амина его сифонируют и очищают от катализатора. Через несколько циклов катализатор отфильтровывают и регенерируют. Гидрирование проводят при энергичном перемешивании реакционной массы для равномерного распределения катализатора по всему объему.
Как правило, жидкофазное гидрирование нитросоединений проводят в присутствии растворителя, которым может служить и образующийся в результате реакции амин. Свойства растворителя существенно влияют на скорость гидрирования. Гидрирование быстрее протекает в спиртах и в воде и медленнее — в ароматических углеводородах вследствие их сорбции на активных центрах катализатора. Испытано гидрирование нитросоединений также в водной эмульсии.
Катализаторами жидкофазного гидрирования являются металлический никель (в технике), платина и палладий (в лабораторной практике). Никелевые катализаторы получают восстановлением водородом оксидов никеля, образующихся при прокаливании нитрата, карбоната или оксалата никеля. Активный и стойкий никелевый катализатор может быть получен нагреванием формиата никеля в смеси парафина и парафинового масла до 250 °C с последующей промывкой спиртом и петролейным эфиром. В производственных условиях удобно работать с катализаторами в виде гранул достаточно крупных, чтобы их не уносили потоки жидкости
или газа. В этом случае исключается необходимость фильтрования продуктов восстановления и легче организуется непрерывный процесс.
Широкое применение как катализатор гидрирования получил скелетный никелевый катализатор, так называемый никель Ренея. Его получают, обрабатывая никелевоалюминиевый сплав едкой щелочью при нагревании до полного выщелачивания алюминия. Остающийся при этом мелко раздробленный никель обладает очень большой поверхностью и весьма активен. Катализатор сохраняют под водой или под спиртом — сухой катализатор пирофорен. В катализаторе содержится значительное количество водорода, поэтому многие органические соединения можно гидрировать таким катализатором без введения водорода извне. Применение скелетного никелевого катализатора позволяет получать из нитросоединений амины при атмосферном давлении и комнатной температуре. На рис. 4.2.4 представлена одна из промышленных схем восстановления нитробензола в жидкой фазе в присутствии растворителя.
Нигробензол, растворитель (метанол) и катализатор (никель Ренея) смешивают в аппарате 1 и подают в систему реакторов 2-5, одновременно в реакторы подается водород. Реакторы 2-4 имеют высоту около 6 м, в каждом аппарате есть три ряда охлаждающих трубок, в которых циркулирует вода. В реакторе 5, меньшем по размеру, происходит окончательное восстановление нитробензола. Давление в системе 15-20 МПа. Благодаря движению водорода катализатор находится в суспендированном состоянии, а реакционная смесь транспортируется через реакторы. Из сепаратора 8 часть катализаторной суспензии в метанольном растворе анилина насосом 9 направляют на рециркуляцию через смеситель /. Основное количество реакционной смеси после отстаивания направляют в ректификационную колонну 10, где отгоняют метанол (дефлегматоры и кипятильники колонн на рисунке не показаны). После отгонки метанола в сепараторе 11 расслаивают кубовую жидкость на водный и анилиновый слои. Водный слой поступает в колонну 12, где сверху выводится азеотропная смесь анилина с водой, а из куба выходит вода, направляемая на биохимическую очистку перед спуском в водоем. В колонне 13 отгоняют воду из органического слоя. Водная фракция направляется обратно в сепаратор 11, а органический слой — в колонну 14, где в виде дистиллята отгоняют товарный анилин, а кубовые остатки направляют на сжигание. Выход анилина составляет 99 %.
Жидкофазное гидрирование нитробензола используется и в лабораторной практике, реакцию проводят при относительно невысоких температурах (начиная с комнатной), что благоприятно сказывается на выходе и качестве целевого продукта. Наиболее употребительные катализаторы для жидкофазного гидрирования
614
Новый справочник химика и технолога
Рис. 4.2.4. Схема восстановления нитробензола в жидкой фазе в присутствии растворителя: / — смеси!ель; 2-5 — реакторы; 6,9 — насосы; 7 — дросселирующий клапан;
8, II —сепараторы; 10,12 -14— ректификационные колонны
в лаборатории: никель Ренея и палладий на угле. При проведении гидрирования через жидкую реакционную массу (раствор нитробензола в спирте или его эмульсия в воде), находящуюся в контакте с твердым катализатором, барботируют водород. Для увеличения скорости процесса его практически всегда ведут под давлением водорода. Чтобы обеспечить наилучший контакт водорода, раствора нигросоединения и твердого катализатора, что является важнейшим условием успешного проведения гидрирования, необходимо энергичное перемешивание реакционной массы. Для этого прибегают к специальным размешивающим устройствам или усиленному барботажу водорода, который берут со значительным избытком, а затем рециркулируют.
4.2.3.2. Аммонолиз фенола
При действии на фенол (8) аммиаком гидроксигруппа замещается на аминогруппу (уравнение (4.2.9)). Эта реакция требует достаточно жестких условий: при пропускании паров фенола и аммиака над катализатором при 425 °C выход анилина составляет 88 %.
Реакция аминирования фенола слабо экзотермична: -Д//2°98=+10 кДж/моль; энергия активации реакции -117 кДж/моль. Аминирование фенола сопровождается побочными реакциями (уравнения (4.2.10), (4.2.11)) образования дифениламина (9), которые эндотермичны. При температуре более 450 °C происходит диссоциация аммиака на азот и водород (уравнение (4.2.12)).
С6Н5ОН + NH3 C6H5NH2 + Н2О (4.2.9)
(5)
С6Н5ОН + c6h5nh2 (C6h5)2nh + Н2О (4.2.10)
(3) (2) (9)
2C6H5NH2 (QH5)2NH + NH3 (4.2.11)
(2) (9)
NH3 :>450^ > N2 + ЗН2 (4.2.12)
Несмотря на то, что реакция аминирования фенола известна давно, в промышленности этот способ долгое время не был реализован в основном из-за проблем, связанных с созданием экономичного катализатора, защитой аппаратуры от коррозии и повышением качества готового продукта.
Аминирование фенола чаще всего проводят на кислотных катализаторах; обычно это оксиды алюминия,
кремния, титана или циркония, алюмосиликаты, а также фосфорная кислота. Особенно активна система: оксид алюминия (10-20 %) + оксид кремния (90-80 %) — в форме природных или синтетических цеолитов. Чтобы облегчить регенерацию, в катализаторы вводят церий, ванадий, вольфрам или их оксиды, катализирующие процессы окисления. Работают катализаторы при 300-600 °C. Оптимальными условиями считаются
Ароматические соединения
615
400^180 °C и давление 0,7 МПа и выше. Для предотвращения образования дифениламина при аминировании фенола нужен избыток аммиака, который составляет от 1 до 20 моль на 1 моль фенола. Выход анилина от 88 до 95 %.
Аммонолиз фенола в жидкой фазе проводят в присутствии хлорида, сульфата и нитрата аммония, хлоридов алюминия, железа, меди, ртути, свинца и лития, а также оксида, сульфата и хлорида олова. Процесс ведут в автоклаве при 300-350 °C. Наиболее активен хлорид олова, в присутствии которого получают анилин с выходом 55-56 %.
В первой промышленной установке получения анилина из фенола, пущенной в Японии в 1970 г. фирмой «Halcon International» (США) по технологии, разработанной фирмой «Scientific Design» (США), в качестве катализатора использовался оксид алюминия, полученный из соответствующего геля с содержанием не более 1 % щелочного металла, а также алюмосиликат, содержащий 35-55 % оксида алюминия. Катализатор проработал без замены до 1976 г.
Серьезные затруднения при разработке технологии аминирования фенола были связаны с разделением фенола и анилина, которые образуют азеотропную смесь,
содержащую 42 % фенола и кипящую при 186 °C при атмосферном давлении. Это означает, что весь не вступивший в реакцию фенол должен рециркулировать через реактор в виде азеотропной смеси. Поскольку такая смесь содержит большое количество анилина, неизбежно образование дифениламина и потери анилина. Эта проблема в основном была решена за счет высокой степени конверсии фенола.
Смеси, содержащие фенол, являются очень коррозионными при высоких температурах. Поэтому аминирование фенола проводят при относительно низких температурах. Кроме того, при низких температурах продлевается время работы катализатора и уменьшается диссоциация аммиака. Смеси фенола и анилина разделяют при пониженном давлении в колоннах из нержавеющей стали.
Промышленный процесс получения анилина из фенола состоит из следующих основных стадий: 1) аминирование фенола в газовой фазе в присутствии катализатора; 2) отделение избытка аммиака от продуктов реакции и возврат аммиака в реактор; 3) отделение воды от продуктов реакции; 4) разделение анилина и фенола и возврат фенола в реактор. Схема аммонолиза фенола приведена на рис. 4.2.5.
Рис. 4.2.5. Схема аммонолиза фенола:
/- смеситель; 2 — реактор; 3 — холодильник; 4 — колонна для отгонки аммиака;
5 — кипятильники; 6 — дефлегматоры; 7 — осушительная колонна; 8 — колонна выделения анилина;
9 — сепаратор; 10 — компрессор
Фенол и жидкий аммиак испаряют частично за счет утилизации теплоты реакции, а частично за счет тепла, подводимого в смеситель 7, и подают в адиабатический трубчатый реактор 2 с неподвижным слоем катализатора. В этот же реактор подают смесь фенола и анилина со стадии выделения азеотропной смеси. Проходя через слой катализатора, фенол, реагируя с аммиаком, превращается в анилин. Процесс проводят при 300-400 °C и давлении 1 МПа. Соотношение фенола и аммиака от
1 : 5 до 1 : 20. Степень превращения фенола 98-99 %.
Продукты реакции частично конденсируются в теплообменнике 3. Жидкую фазу, состоящую в основном из анилина и растворенного аммиака, отделяют и подают в систему ректификационных колонн. В колонне 4 отгоняют аммиак, который возвращается в реактор 2 компрессором 10, некоторое количество аммиака при этом диссоциирует на водород и азот. По мере накопления примесей циркулирующий аммиак сбрасывают
616
Новый справочник химика и технолога
в систему очистки отходящих газов. Кубовая жидкость колонны 4 поступает в осушительную колонну 7, в которой отгоняют реакционную воду, а затем в колонну 8. Из колонны 8 анилин отгоняют в виде дистиллята, а с нижних тарелок колонны отбирают азеотропную смесь фенола и анилина, которую возвращают в реактор 2. Из куба колонны 8 выводят остатки, содержащие дифениламин, и направляют их на сжигание. Разделение фенола и анилина для увеличения их относительной летучести проводят в вакууме. Полученный анилин не нуждается в дополнительной очистке.
Расход фенола и аммиака на 1 т анилина составляет соответственно 1,035 и 0,185 т, что соответствует выходу 97,6 % от теоретического.
4.2.3.3. Получение анилина из толуола
В начале 1970-х гг. фирма «American Cyanamid» (США) разработала оригинальную технологию получения анилина аммонолизом бензойной кислоты (77). В промышленности бензойную кислоту получают путем жидкофазного окисления толуола (70) в присутствии солей кобальта (уравнение (4.2.13)).
2С6Н5СН3 + ЗО2 -► 2С6Н5СООН + Н2О (4.2.13) (70) (77)
При действии на бензойную кислоту водным раствором аммиака в присутствии оксида меди(П) при 215 -220 °C и 3,5-4,2 МПа образуется анилин. Выход анилина составляет 37 %.
Процесс аммонолиза бензойной кислоты состоит из двух стадий:
1) взаимодействие оксида меди(П), бензойной кислоты и аммиака с образованием анилина (уравнение (4.2.14));
2) регенерация оксида меди(П), т. е. окисление оксида меди(1) кислородом воздуха (уравнение (4.2.15)).
Превращение бензойной кислоты в анилин проходит через стадию образования промежуточного соединения — амида бензойной кислоты (C6H5CONH2; бензамид). В результате внутримолекулярной перегруппировки (реакция Гофмана) образуется анилин и оксид углерода, который окисляется в диоксид.
СбН5СООН + NH3 + 2CuO -► СбН5МН2 + Си2О + СО2 + Н2О
(4.2.14)
2Cu2O + О2 4СиО (4.2.15)
На производстве при получении анилина из толуола (рис. 4.2.6) процесс начинается с приготовления суспензии катализатора в толуоле в аппарате 7, снабженном мешалкой. Катализатором обычно служит нафтенат кобальта. Суспензию направляют в реактор 2, в нижнюю часть которого подают воздух. Окисление толуола проводят при 130-140 °C и 0,21-0,22 МПа. Так как реакция окисления сопровождается большим экзотермическим эффектом, необходимо постоянно отводить тепло. Степень конверсии толуола в бензойную кислоту 30-40 %.
Выходящие из реактора 2 газы направляются в конденсатор 3, в котором конденсируются органические продукты, унесенные отработанным воздухом. Из конденсатора конденсат направляется в жидкостный сепаратор 4 для расслоения на водный и органический слои. Органическую фазу, богатую толуолом, возвращают в реактор, а водную направляют на биохимическую очистку. Газы, выходящие из конденсатора 3, очищаются в угольных адсорберах (на схеме не показаны), где улавливается большая часть органических примесей. Для десорбции уловленных продуктов через адсорберы продувают водяной пар. Полученную смесь расслаивают. Органический слой, содержащий толуол, возвращают в реактор, а воду направляют на биохимическую очистку.
Реакционная масса из реактора 2 после отделения катализатора (методом фильтрования) поступает в отгонную колонну 5, работающую при атмосферном давлении. Дистиллятом является толуол, возвращаемый в реактор. Кубовая жидкость поступает в вакуум-отгонную колонну 6, в которой бензойная кислота отделяется от высококипящих примесей. Бензойная кислота в расплавленном состоянии направляется на стадию аммонолиза для получения анилина.
В абсорбере 7 готовят водный раствор аммиака. Бензойную кислоту, суспензию оксида меди(П) и аммиачную воду подают в реактор 8, снабженный мешалкой и обратным холодильником. Мольное соотношение бензойной кислоты, воды, аммиака и оксида меди составляет 1,5 : 1,8 : 3,4 : 1. Хотя вода и не участвует в реакции, показано, что ее избыток тормозит образование промежуточного соединения — бензамида.
Реакцию аммонолиза проводят при 220 °C и 3,5 МПа, при этом в реакцию вступает 35 % всей поступающей бензойной кислоты, из которой 88 % превращается в анилин. Кроме того, образуется около 10 % фенола и 2 % дифениламина. После аммонолиза реакционную массу отфильтровывают от катализатора и направляют в каскад ректификационных колонн.
Осадок с фильтра 10 поступает в реактор 77 для окисления образовавшегося Си2О в СиО. Реакция протекает в среде аммиака. В нижнюю часть реактора подают воздух, и там при обычной температуре и атмосферном давлении протекает эндотермическая реакция с полным превращением Си2О в СиО. Суспензия СиО из реактора 7 7 возвращается в реактор 8.
Из фильтрата в колонне 12 десорбируют аммиак, который улавливают в абсорбере 7 и возвращают в реакцию. В колонне 13 удаляют воду и возвращают ее на стадию абсорбции аммиака. Небольшая часть воды используется для промывки СиО на фильтрах. В колонне 14 при пониженном давлении отгоняют анилин. Из куба колонны (аппарат 15) при более глубоком вакууме выделяют некоторое количество фенола, анилина, а также бензойную кислоту, возвращаемую в реактор 8, и дифениламин. Кубовые остатки направляют на сжигание.
Суммарный выход анилина в расчете на толуол составляет 79,2 %.
Ароматические соединения
617
Рис. 4.2.6. Схема получения анилина из толуола:
1 — аппарат для приготовления суспензии катализатора; 2 — реактор окисления толуола; 3 —- конденсатор;
4 — сепаратор;5, 6, 12 — отгонные колонны; 7 — абсорбер; 8 — реактор аммонолиза; 9 — обратный холодильник;
10 — фильтр;// — реактор окисления Си2О; 13 — колонна осушки анилина; 14 — колонна дистилляции товарного анилина;
15 — аппарат для разделения реакционной смеси
4.2.3.4. Получение анилина из хлорбензола
Анилин можно получить из хлорбензола реакцией нуклеофильного замещения хлора на аминогруппу (уравнение (4.2.16)).
С6Н;С1 + 2NH3 C“;O> C6H5NH2 + NH4CI (4.2.16)
Вследствие малой подвижности галогена, связанного с ароматическим ядром, реакция протекает гладко при температуре около 200 °C и давлении 6-10 МПа лишь в присутствии соединений меди. Особенно эффективным катализатором являются соли меди(1). Скорость реакции прямо пропорциональна концентрации хлорбензола и катализатора и не зависит от концентрации аммиака.
Промышленный процесс проводят в трубчатом аппарате из хромоникелевой стали. Степень коррозии аппаратуры зависит от скорости движения реакционной массы и резко возрастает при Re > 150 000. Реакция хорошо идет уже при скорости, которая обеспечивает устойчивый турбулентный режим (Re * 10 000). При расходе на 1 моль хлорбензола 5 моль аммиака, который берется в виде 34%-ного раствора, и 0,2 моль оксида меди(1) реакция заканчивается через 2-3 ч при 200-230 °C и 7 МПа. В результате образуется около 90 % анилина, 4—5 % фенола и 1 -2 % дифениламина. Анилин, полученный из хлорбензола, легко выделяется из реакционной массы путем перегонки и отличается большой стойкостью при хранении.
Этот метод синтеза анилина не получил широкого распространения в промышленности. Лишь одна фирма— «Dow Chemical» (США) — в течение ряда лет
получала анилин таким способом, что в основном объясняется наличием у фирмы дешевого хлора. Этот способ получения анилина известен как способ Доу (Dow process). В 1966 г. промышленное производство анилина из хлорбензола фирмой было закрыто.
4.2.3.5. Замещение сулъфогруппы аминогруппой
Сульфогруппу в бензолсульфокислоте {12) можно заменить аминогруппой (уравнение (4.2.17)). В качестве реагента необходимо взять амид щелочного металла, г. к. с аммиаком эта реакция не идет. В условиях сплавления бензолсульфокислоты и амида натрия получается анилин, но выход продукта небольшой.
C6H5SO3Na + NH2Na -► C6H5NH2 + Na2SO3 (4.2.17) (/2)
Значительно с большим выходом идет реакция, если она проводится между солью сульфокислоты и пиперидином натрия в избытке пиперидина, но в промышленности этот метод синтеза анилина практического применения не получил.
4.2.4. Физические и химические свойства анилина
4.2.4.1. Физические свойства анилина
Анилин (аминобензол, фениламин) — бесцветная маслянистая жидкость со слабым запахом, горит ярким коптящим пламенем. Молекулярная масса 93,12. Важнейшие физические константы анилина приведены в табл. 4.2.2. Значения констант даны для нормальных условий: температуры — 20 °C и давлении — 101,325 кПа.
618
Новый справочник химика и технолога
Электронный спектр анилина (рис. 4.2.7) имеет две характерные полосы поглощения (молярный коэффициент поглащения Igs), максимумы которых в водном растворе находятся на 230 нм и 280 нм.
В ИК спектре анилина (рис. 4.2.8) наиболее характерными являются полосы поглощения в области -3100 см"1 (валентные колебания связей С—Н) и в области -3500 см"1 (валентные колебания связей N—Н).
В ПМР спектре анилина (рис. 4.2.9) отчетливо видны сигналы протонов бензольного кольца (8 = 6,5^-7,5 м. д.) и интенсивный сигнал неразличимых протонов аминогруппы (8 = 3,6 м. д.).
При низких температурах анилин в растворах углеводородов дает голубовато-фиолетовую фосфоресценцию. В табл. 4.2.4 приведены некоторые фотохимические константы анилина.
Анилин частично растворяется в воде (3,3 % при 20 °C; 4,5 % при 60 °C; 6,4 % при 90 °C). Добавление в воду минеральных солей, как правило, уменьшает растворимость анилина вводе (рис. 4.2.10). Однако
бромиды лития и цезия практически не изменяют растворимость, а добавка иодида цезия даже повышает растворимость анилина в воде.
Анилин хорошо растворяется и смешивается в любых соотношениях с этанолом, метанолом, диэтиловым эфиром, ацетоном, бензолом, толуолом, три- и тетра-хлорметаном (четыреххлористым углеродом), хлороформом, пиридином, этилацетатом и др.
С большинством углеводородов и галогенуглеводородов анилин образует азеотропные смеси с минимумом температуры кипения, а с такими веществами, как фенол и крезол — азеотропные смеси с максимумом температуры кипения. С водой анилин образует расслаивающуюся азеотропную смесь (ГКИГ1 = 98,5 °C при атмосферном давлении), содержащую 18 % анилина.
ПДК = 0,1 мг/м3. Пары анилина токсичны. Чистота анилина определяется по температуре застывания продукта, содержанию влаги, наличию нитробензола и производных серы.
Таблица 4.2.2
Важнейшие физические константы анилина
Наименование константы (размерность) Величина
Температура кипения при атм. давлении Ткип, °C 184,4
Температура плавления (затвердевания) ТПЛ, °C -5,89
Относительная плотность d4 1,О2220; О,98860
Показатель преломления п™ 1,5863
Температура вспышки Твсп, °C 79
Температура самовоспламенения Тсвспл, °C 562 (пары в возд.)
Критическая температура Т^, °C 425,65
Критическое давление /?кр, МПа 5,31
Критический объем Укр, см3/моль 274
Динамическая вязкость г|, мПа • с 10,2°; 4,420; 0,8100
Поверхностное натяжение о20, Н/м 4,33 • 10"2
Диэлектрическая проницаемость £ 6,8925; 5,9370
Дипольный момент молекулы ц, D 1,5625
Криоскопическая константа 5,87
Эбулиоскопическая константа 3,69
Таблица 4.2.3
Термодинамические свойства анилина (для жидкого состояния)
Наименование константы, размерность Величина
Станд. теплоемкость при постоянном давлении с°р , Дж/(моль • К) 191
Энтальпия образования анилина А/7°, кДж/моль 29,7
Стандартная энтропия AS0, Дж/(моль • К) 191,42
Стандартная энергия образования (изменение энергии Гиббса) AG0, кДж/моль 149,18
Стандартная энтальпия испарения А/7ИСП, кДж/моль 55,83
Стандартная энтальпия плавления АЯП1, кДж/моль 10,56
Теплота диссоциации Qwcc, кДж/моль 21,73
Теплота сгорания (?сг, кДж/моль 3410
Ароматические соединения
619
Рис. 4.2.7. Электронный спектр поглощения анилина в воде:
Лмакс! = 230 нм (Ige = 3,93); Х„акс2 = 280 нм (Ige = 3,16)
2800 3200 3600
тт -1
Частота, см
Рис. 4.2.8. ИК спектр раствора анилина в тетрахлорметане (четыреххлористом углероде)
Рис. 4.2.9. ПМР спектр анилина в тетрахлорметане (эталон — тетраметил с ил ан)
Рис. 4.2.10. Зависимость растворимости анилина в воде от концентрации минеральных веществ при 25 °C: 7 — КОН; 2 — K2SO4; 3 — NaCl; 4 — LiCl; 5 — NaBr; 6 — KBr; 7 — NH4C1; 8 — LiBr; 9 — CsBr; 10 — Csl
Таблица 4.2.4
Фотохимические характеристики анилина
Наименование константы, размерность Величина
Энергия триплетного состояния ЕТ, кДж/моль 321
Энергия синглетного состояния Е$, кДж/моль 396
Выход флуоресценции в неполярных растворителях <рфл 0,08
Время жизни флуоресценции тфл, нс 3,9
Время жизни фосфоресценции при 77 °К тф, с 4,7
Потенциал фотоионизации, эВ 7,7
Анилин быстро темнеет при хранении, особенно под влиянием кислорода воздуха и света, и становится более вязким. Этот процесс, известный как «аутооксидация» анилина, может быть заторможен добавлением специальных веществ — антиоксидантов, в качестве
которых могут быть использованы гидросульфит и тиосульфат натрия, а также щавелевая кислота.
В то же время диамины бензольного ряда и аминотиофенол или продукты его разложения являются типичными «прооксидантами», т. е. веществами, увеличи
620
Новый справочник химика и технолога
вающими скорость окисления анилина. Поэтому стойкость анилина при хранении может быть увеличена снижением содержания примесей динитробензола и нитротиофена в нитробензоле, из которого получают анилин.
4.2.4.2. Химические свойства анилина
Анилин имеет менее выраженный основной характер по сравнению с алифатическими аминами, его константа диссоциации равна 3,8 • 1О”10 (рК„ = 4,98), тогда как константа диссоциации метиламина 4,4 • 10 5 (рК„ = 10,62). Растворы анилина в воде не окрашивают ни лакмус, ни фенолфталеин. Анилин не образует солей с такими слабыми кислотами, как угольная или синильная.
Уменьшение основности анилина по сравнению с алифатическими аминами объясняется взаимодействием (сопряжением) неподеленной пары электронов азота с л-электронами ароматического ядра. Следствием такого взаимодействия является изменение электронной плотности бензольного кольца и появление в орто- и иа/?а-положениях отрицательного заряда. Смещение электронной плотности можно представить с помощью резонансных структур (2а) и (26). Квантовохимические расчеты подтверждают наличие повышенной электронной плотности в этих положениях (цифрами показаны величины электронной плотности на атомах углерода).
(2) (2а) (26)
Протонирование аминогруппы выводит се из сопряжения с бензольным кольцом, при этом изменяется распределение электронной плотности в кольце и его реакционная способность: наиболее активным в реакциях электрофильного замещения становится мета-положение (показано звездочкой).
Анилин является химически активным соединением, химические реакции происходят как с участием аминогруппы, так и ароматического кольца.
Взаимодействие с неорганическими веществами
Взаимодействие с кислотами. С сильными неорганическими кислотами (соляная, серная, фосфорная) анилин образует соли. Наибольшее практическое значение имеет гидрохлорид анилина (C6H5NH2 • НС1), так называемая анилиновая соль, которая используется в промышленности органических красителей и в текстильной промышленности. Соли анилина и фосфорной кислоты применяются для очистки анилина в лабораторных условиях. Их получают кристаллизацией из воды или из органических растворителей.
Взаимодействие со щелочными металлами. При нагревании анилина с металлическим калием водород аминогруппы замещается на калий с выделением молекулярного водорода, при этом образуется анилид калия
C6H5NHK. Анилид натрия C6H5NHNa образуется при нагревании анилина с металлическим натрием в присутствии металлической меди, никеля или кобальта, а также в присутствии солей или оксидов этих металлов. Реакция протекает при 140 °C с выделением газообразного водорода. При нагревании анилина с кальцием под давлением (при 200 °C) в потоке водорода образуется дианилид кальция.
Взаимодействие с серой. При нагревании анилина с избытком серы (сплавление) образуется 2,2'-диамино-дифенилсульфид (/2).
При добавлении оксида свинца в смесь анилина с серой при сплавлении получают 4,4'-диаминоди-фенилсульфид (13) — отвердитель эпоксидных олигомеров, антиоксидант, промежуточный продукт в синтезе красителей и лекарственных веществ.
Если смесь анилина, гидрохлорид анилина и серы (мольное соотношение 4:2: 3,5) выдержать при 195 °C в течение 5-6 ч, образуется гетероциклическое соединение — фенотиазин (14) и несколько побочных продуктов: 4-амино-4'-анилино дифенилдисульфид (15), 4,4'-диаминодифенилсульфид (13) и совсем немного 2,4'-диаминодифенилсульфида.
Взаимодействие с сероуглеродом. При конденсации анилина с сероуглеродом в щелочной среде в присутствии NaHSO3 получают тиокарбанилид [(76); А,А'-дифенилтиомочевина] — ускоритель вулканизации резиновых смесей, ценный промежуточный продукт в синтезе красителей и лекарственных средств.
При взаимодействии анилина с серой и сероуглеродом в присутствии нитробензола образуется каптакс [(77); 2-меркаптобензотиазол] — ускоритель вулканизации каучуков, ценный промежуточный продукт,
Ароматические соединения
621
используемый в синтезе цианиновых красителей и химических добавок к полимерам.
Взаимодействие с трифторидом фосфора. При
взаимодействии анилина с трифторидом фосфора в
присутствии триэтиламина образуется три(фенил-амид)фосфористой кислоты (18) — эффективный стабилизатор каучуков.
S
-H2S
S;[PbO] -------►
-H2S
(/5)
(/4)
(/5)
cs2
-----►
-H2S
(/6)
CS2; S
------►
-H2S
(/7)
pci3
-HCl
Взаимодействие с фосгеном. При взаимодействии анилина с фосгеном в зависимости от условий образуются различные продукты. Реакция в газовой фазе при эквимольных соотношениях приводит к образованию фенилизоцианата (19) — ценного промежуточного про
дукта, применяемого для синтеза уретанов, гербицида фенурона, дисперсных красителей.
C6H5NH2 + СОС12 -► C6H5NCO + 2НС1
(/9)
622
Новый справочник химика и технолога
N-Алкилирование анилина
А-Алкилирование анилина проходит по общей схеме алкилирования аминов:
C6H5NH2 -> C6H5NHR C6H5NR2 C6H5 NR3
На промежуточных этапах реакции образуются вторичные и третичные амины, а на завершающем — соли полностью замещенного четвертичного аммония. В общем случае, когда алкил R не вызывает больших пространственных препятствий для дальнейшего течения реакции, скорости отдельных ее этапов мало отличаются друг от друга, и в результате алкилирования образуются смеси продуктов. Из них соли триалкил-аммония легко отделить благодаря их растворимости в воде или же превратить в третичные амины при нагревании в щелочной среде под давлением (уравнение (4.2.18)).
Наибольшие трудности связаны с получением вторичных аминов; в обычных условиях они неизбежно образуются в смеси с первичными и третичными аминами. Разделение таких смесей, как правило, затруднительно, т. к. их компоненты имеют близкие температуры кипения.
В качестве алкилирующих агентов применяются алифатические спирты (в присутствии кислот), алкил-галогсниды, простые эфиры, алкиловые эфиры серной кислоты и ароматических сульфокислот, непредельные соединения.
Алкилирование спиртами. Алкилирование ароматических аминов спиртами проводят обычно с добавлением небольших количеств кислых агентов: минеральная кислота, хлорид фосфора(Ш), при 200 °C в автоклавах под давлением (до 3 МПа и выше). Обычно используют метанол и этанол, реже бутанол и высшие
C6Hs NR3X + NaOH C6H5NR2 + ROH + NaX
спирты; в качестве минеральной кислоты применяют хлороводородную и серную кислоты (0,05-0,3 моль на 1 моль амина). Когда введение в реакционную массу воды нежелательно, то вместо хлороводородной кислоты применяют гидрохлориды соответствующих ароматических аминов.
Под действием кислоты происходит протонирование спирта, например метанола, с образованием меток-сониевого иона, который далее диссоциирует с образованием метил-катиона, проявляющего электрофильные свойства и способного атаковать атом азота аминогруппы (уравнения (4.2.19) и (4.2.20)).
Первоначально образующийся вторичный амин подвергается действию метил-катиона с образованием третичного амина, который также атакуется метил-катионом с образованием катиона четвертичной аммониевой соли (схема 4.2.1).
Реакцию алкилирования трудно остановить на какой-то определенной стадии. Изменяя количество исходного спирта, можно сдвинуть реакцию в сторону образования вторичного или третичного амина. Так, для получения А,А-диметиланилина (20) применяют 3-4 моль метанола спирта на 1 моль анилина и добавляют 0,1-2 моль серной кислоты (уравнение (4.2.21)); реакцию ведут при 205-215 °C и давлении 3 МПа. В этих условиях образуется также соль четвертичного аммониевого основания (2/) и в незначительном количестве монометиланилин [(22); А-метиланилин].
Для превращения образовавшейся соли четвертичного аммониевого основания (21) в целевой продукт-А,А-димстиланилин (20) — после окончания алкилирования содержимое автоклава обрабатывают щелочью (уравнение (4.2.22)) и нагревают при 130-170 °C. Продукт реакции отделяют от водного слоя и очищают перегонкой.
(4.2.18)
CH3OH 1 H ^ CH3'()H2 +CH3 + H2O (4.2.19)
ArNH2 + "CH3 Аг>4Н2СН3 ArNHCH3 + H+ (4.2.20)
+CH3 4- -Hb +CH3 +
ArNHCH3 -7-^ ArNH(CH3)2 ArN(CH3)2 ArN(CH3)3
Схема 4.2.1
CH3OH +
C6H5-NH2 -----------► C6H5N(CH3)2 + C6H5N(CH3)3X- + C6H5NHCH3 (4.2.21)
nr
(2) (20) (21) (22)
+
C6H5N(CH3)3X" + NaOH --------► C6H5N(CH3)2 + CH3OH + NaX (4.2.22)
(27) (20)
Ароматические соединения
623
Изучение кинетики алкилирования ароматических аминов спиртами показало, что реакция обратима. Значение константы равновесия, например, при метилировании анилина и А-метиланилина при 200 °C очень велико (>200), поэтому в этих условиях реакция протекает практически до конца — до образования N,N-au-метиланилина. N, А-Диметиланилин используется в производстве основных красителей и как проявитель для цветной фотографии. А'-Метиланилин применяется для получения красителей и ВВ (тетрила).
Ценными промежуточными продуктами являются и TV-этил производные анилина, они используются для получения красителей, пестицидов, лекарственных веществ. При этилировании анилина получить А,А-диэти-ланилин (23), свободный от А-этиланилина (24), практически не удается, однако смесь продуктов со значительным содержанием А-этиланилина образуются легко. Так, равновесная смесь, получаемая при алкилировании анилина при 200 °C этанолом (3 моль на 1 моль анилина), содержит около 11 % анилина, 29 % А^этиланилина и 60 % А,А-диэтиланилина (уравнение (4.2.23)). Это объясняется тем, что константы равновесия при этилировании анилина и особенно А-этила-нилина значительно меньше, чем при метилировании, и равны соответственно 30 и 2,7.
При уменьшении количества спирта и увеличении продолжительности реакции повышается выход моно-алкиланилина (24). Иногда алкилирование анилина ведут, используя около 2 моль спирта на 1 моль анилина, до исчезновения в реакционной массе анилина. В ряде случаев количество применяемого спирта составляет менее 1 моль; при этом реакционная масса содержит анилин и моноалкиланилин и не содержит третичный амин.
Для получения N, N- диэтил анилина (23) процесс ведут при 180-200 °C и давлении около 3 МПа. В качестве кислотного агента обычно вводят гидрохлорид анилина.
Вместо соляной или серной кислоты при алкилировании спиртами можно с успехом пользоваться трихлоридом фосфора (РС13), который добавляют в количестве 0,8-0,9 % от взятого амина. Использование этого катализатора позволяет значительно сократить время реакции и получить вторичные и третичные амины с хорошим выходом.
В промышленности используют в качестве катализатора РС13 при получении А'-этиланилина (24) непрерывным методом, алкилирующим агентом является этанол. Смесь анилина, этанола и РС13 (0,9 %) подают под давлением 7-10 МПа в систему из трех автоклавов. Процесс ведут так, чтобы температура в первом автоклаве поддерживалась 200 °C, а в третьем автоклаве 280-290 °C; время пребывания реакционной массы в каждом из автоклавов составляет 1 ч. Образующаяся смесь содержит 20 % анилина, 65 % А-этиланилина и 15 % А,А-диэтиланилина. А,А-Ди-этиланилин (23) возвращают в процесс (вместо эта
нола) и при его взаимодействии с анилином в результате диспропорционирования (уравнение (4.2.24)) получается А-этиланилин (24).
Алкилирование ароматических аминов спиртами может быть осуществлено в паровой фазе, как гетеро-генно-каталитический процесс. В качестве катализаторов используют обычно А12О3, а также его смеси с ThO2, TiO2, ZrO2. Пары амина и спирта пропускают над катализатором при 300 ^400 °C. Следует отметить, что при парофазном алкилировании ароматических аминов спиртами возможно С-алкилирование — вступление алкильной группы в ароматическое кольцо.
Алкилирование алкилгалогенидами. Алкилгало-гениды применяют для алкилирования ароматических аминов (уравнение (4.2.25)) в тех случаях, когда последние не могут быть проалкилированы спиртами или когда алкилгалогениды более доступны, чем соответствующие спирты.
Для связывания выделяющегося галогеноводорода берут избыток амина или добавляют в реакционную массу вещества основного характера (гидроксид натрия, карбонат натрия или кальция, гидроксид кальция и др.). При использовании низкокипящих алкилгалоге-нидов (например, метилхлорида, этилхлорида) реакцию проводят под давлением в автоклавах. Если применяют алкилгалогениды с Гкип > 100 °C (например, бензил-хлорид, монохлоруксусную кислоту), то реакцию ведут при атмосферном давлении в аппаратах, снабженных обратными холодильниками.
В качестве алкилгалогенидов обычно используют более дешевые и доступные алкилхлориды. Так, действием этилхлорида на анилин при 190-200 °C получают А,А-диэтиланилин (23) с небольшой примесью А-эти-ланилина (24). Дополнительная обработка этилброми-дом позволяет получать А,А-диэтиланилин практически в чистом виде.
С помощью бензилхлорида в аминогруппу вводят бензильный остаток С6Н5СН2. Так, при действии 1 моль бензилхлорида (25) на 2 моль анилина при 140 °C получают А-бензиланилин (26) (уравнение (4.2.26)).
Увеличивая количество бензилхлорида в реакционной массе, можно получить А,А-дибензиланилин [C6H5N(CH2C6H5)2], однако из-за стерических затруднений второе бензилирование идет значительно медленнее первого.
Алкилирование бензилхлоридом вторичных аминов позволяет получать несимметричные третичные жирноароматические амины. Например, при взаимодействии А-этиланилина (24) с бензилхлоридом (уравнение (4.2.27)) образуется А-бензил-А-этиланилин (27), применяющийся в синтезе трифенилметановых красителей. Для связывания хлороводорода в этом случае в реакционную массу добавляют щелочные агенты (карбонат натрия или кальция, гидроксид кальция).
При алкилировании смеси А-этиланилина (24) и А,А-диэтиланилина (23) бензилхлоридом образуется смесь третичных аминов: А, А-диэтил анилина (23)
624
Новый справочник химика и технолога
и TV-бензил-А-этиланилина (27), которую разделить легче, чем смесь исходных вторичного и третичного аминов, т. к. разница в температурах кипения данных третичных аминов значительно больше.
Действием на анилин монохлоруксусной кислоты вводят карбоксиметильную группу СН2СООН, в результате получают фенилглицин [(28); А-фенил-аминоуксусная кислота] — ценный промежуточный продукт, используемый в синтезе Индиго. Однако при взаимодействии анилина и хлоруксусной кислоты с большой легкостью образуется также не находящее практического применения диалкильное производное — А-фенилиминодиуксусная кислота (29).
Чтобы избежать образования диалкильного производного (29), реакцию ведут в присутствии гидроксида железа(П). В этих условиях образуется плохо растворимая в воде железная соль А-фениламиноуксусной кислоты, которая выпадает в осадок, что препятствует введению второй карбоксиметильной группы. Гидроксид железа(П) связывает также и выделяющийся хлороводород. Железную соль А-фениламиноуксусной кислоты отфильтровывают и обрабатывают КОН. Образующуюся при этом калиевую соль /V-фениламиноуксусной кислоты фильтруют для отделения гидроксида железа(П) и упаривают. Ее и используют в производстве Индиго; гидроксид железа (II) возвращают в процесс.
C6H^NH2 -------—► C6H5N(C2H5)2 + C6H5NHC2H5 (4.2.23)
(23) (24)
C6H5N(C2H5)2 + C6H5NH2 - 2C6H5NHC2H5
(23) (24)
ArNH2 + R_X —> ArNHR + HX X = CI, Br
(4.2.24)
(4.2.25)
2C6H5NH2 + C6H5CH2CI -► C6H5NHCH2C6H5 + C6H5NH2-HCI (4.2.26)
(25) (26)
C6H5NHC2H5 + C6H5CH2C1 -► C6H5N(C2H5)CH2C6H5 + HC1 (4.2.27)
(24) (25) (27)
c6h^nh2 .™^содн^ c6h5nhch2cooh —c6h5n(ch2cooh)2
(28) (29)
Алкилирование эфирами. В качестве алкилирующих агентов могут быть использованы простые эфиры (например, диметиловый эфир СН3ОСН3, побочно образующийся в производстве метанола), алкиловые эфиры серной кислоты (диметилсульфат, диэтилсульфат) или метиловые эфиры ароматических сульфокислот (например, метиловый эфир бензолсульфокислоты C6H5SO2OCH3 или метиловый эфир и-толуолсульфо-кислоты h-CH3C6H5SO2OCH3).
В промышленности процесс алкилирования анилина диметиловым эфиром осуществляется в паровой фазе, как гетерогенно-каталитический. В испарителе пары анилина смешиваются с парами (диметилового эфира) смесь паров поступает в контактный аппарат трубчатого типа, в который загружен катализатор (активный
оксид алюминия); процесс ведут при 230-295 °C. Из контактного аппарата выходит смесь аминов, содержащая 94-96 % А,А-диметиланилина и метанол (уравнение (4.2.28)). После отделения метанола смесь аминов с диметиловым эфиром поступает во второй контактный аппарат. В результате двукратного контактирования получают N,А-диметиланилин с выходом 99,5-99,6 %.
Алкилирование анилина эфирами серной кислоты (уравнение (4.2.29)) или ароматических сульфокислот (уравнение (4.2.30)) применяется сравнительно редко.
Синтез А-гидроксиэтильных производных анилина. Алкилирование анилина этиленхлоргидрином (30) и этиленоксидом (32) используют для получения моно-(31) и бис-2-гидроксиэтильных (33) производных (уравнения (4.2.31) и (4.2.32)), применяющихся в синтезе дис
Ароматические соединения
625
персных азокрасителей. Реакции алкилирования легко проходят в водных растворах. При использовании этиле-ноксида в основном образуется третичный амин — N,N-ди(2-гидроксиэтил)анилин (33) с небольшой примесью вторичного амина — А-(2-гидроксиэтил)анилина (31). Продукты реакции разделяют перегонкой, используя большую разницу в температурах кипения.
Алкилирование акрилонитрилом. Алкилирование анилина акрилонитрилом с целью получения А-(2-ци-аноэтил)анилина (34) ведут при нагревании до 120-140 °C в присутствии уксусной кислоты (уравнение (4.2.33)). При более высокой температуре образуется смесь продуктов моно- и дицианэтилирования. Соединения используются в синтезе дисперсных и катионных красителей.
C6H5NH2 + 2(СН3)2О -> C6H5N(CH3)2 + 2СН3ОН (4.2.28)
C6H5NH2 + (CH3)2SO4-> C6H5NHCH3 + CH3OSO3H
(4.2.29)
C6H5NH2 + C6H5SO2OCH3 -> C6H5NHCH3 + C6H5SO3H
(4.2.30)
C6H5NH2 + C1CH2CH2OH -> C6H5NH(CH2CH2OH)
(4.2.31)
(30) (31)
p—NH2 + 2 H2C-CH2 ---------► C N(CH2CH2OH)2 (4.2.32)
(32)
(33)
C6H5NH2 + CH2 CHCN c6h5nhch2ch2cn
(4.2.33)
(34)
14-Ацилирование анилина
А-Ацилирование анилина — часто используемая реакция. Ее применяют как для временной защиты аминогруппы при сульфировании, нитровании или галогенировании анилина, так и для получения соединений, обладающих определенными практически важными свойствами. В первом случае чаще всего в качестве ацилирующих реагентов применяют муравьиную или уксусную кислоту и их ангидриды, во втором — самые разнообразные карбоновые кислоты и их производные — чаще всего хлорангидриды.
Формилирование и ацетилирование анилина обычно проводят, нагревая анилин с некоторым избытком муравьиной или уксусной кислоты (уравнение (4.2.34)).
Реакция обратима, но образующаяся вода отгоняется с избытком кислоты и благодаря этому процесс доходит до конца. Эти реакции используются в основном для временной защиты аминогруппы, т. к. и А-формиланилин (35) и А-ацетиланилин (36) легко гидролизуются при нагревании с разбавленными растворами щелочи или сильной кислоты. А'-Ацетиланилин
применяется также как полупродукт для получения азокрасителей.
Реакция анилина с альдегидами
Анилин легко (особенно в присутствии щелочи) взаимодействует с альдегидами (уравнение (4.2.35)), образуя азометины [(37); основания Шиффа)]. При действии разбавленных кислот азометины расщепляются на исходные амин и альдегид, причем реакция начинается уже на холоду.
Реакция образования азометинов используется для временной защиты аминогруппы и как промежуточная стадия при синтезе вторичных аминов, которые трудно получить в чистом виде прямым алкилированием анилина. Для получения вторичного амина азометин гидрируют над катализатором, например над никелем Ренея или палладием на угле.
C6H5-N=CHR —C6H5-NHCH2R
При взаимодействии гидрохлорида анилина с водным раствором формальдегида образуется 4,4'-диами-
626
Новый справочник химика и технолога
и одновременно несколько увеличивает скорость ос-, новной реакции.
[ Нитрит натрия применяют в количестве, близком [ к теоретическому, следя за тем, чтобы в конце реакции в растворе обнаруживался очень небольшой избыток i азотистой кислоты. Для этого используются индикато-i ры или редоксметр.
I Соли фенилдиазония и сильных кислот неустойчивы и легко разлагаются, особенно при повышении температуры. Поэтому диазотирование ведут с охлаждением (при 0-10 °C), добавляя лед непосредственно в реакционную массу или охлаждая с помощью змеевиков, [ через которые циркулирует охлажденный рассол. Полученные диазосоединения сразу же используются в последующих синтезах.
Соль фенилдиазония (39) является ценным промежуточным продуктом, используемым в синтезе красителей, лекарственных соединений, пестицидов и пр.
При диазотировании анилина с уменьшенным вдвое против теоретического количеством нитрита натрия получают диазоаминобензол (40) — ускоритель вулканизации каучуков, инициатор полимеризации диеновых углеводородов.
Кислотный гидролиз анилина
Для гидролиза аминосоединений обычно используют разбавленную серную или фосфорную кислоту. В присутствии кислоты образуется ион аммония. При । наличии аммонийной группы электронная плотность на реакционном центре понижается, что облегчает нуклеофильную атаку молекулой воды.
Кислотный гидролиз анилина приводит к образованию фенола (5), (уравнение (4.2.37)).
Реакция проходит в достаточно жестких условиях: при 35СМ40 °C и давлении 2-5 МПа. На 1 моль анилина берется 1 моль фосфорной кислоты или дигидрофосфата аммония и 50 моль воды. С увеличением кислотности среды скорость гидролиза возрастает. Реакция обратима, причем в зависимости от температуры в равновесной смеси содержится от 50 до 65 % фенола. Практического применения эта реакция не получила.
-► C6H5NHCOR + Н2О (4.2.34)
(35) R = Н
(36) R = СН3
нодифенилметан (38) — ценный промежуточный продукт, используемый в производстве диизоцианатов, полиамидов, красителей. 4,4'-Диаминодифенилметан используется также как ингибитор коррозии металлов и отвердитель эпоксидных олигомеров.
Существуют два основных промышленных способа получения 4,4'-диаминодифенилметана. По одному из них формальдегид нагревают с избытком анилина под давлением в присутствии катализатора, представляющего собой минеральную кислую соль или обработанную кислотой глину. По второму способу, получившему более широкое распространение, анилин обрабатывают определенным количеством формальдегида и соляной кислоты в реакторе с мешалкой при сравнительно низкой температуре. По окончании реакции повышают температуру до 100 °C, чтобы разложить высокомолекулярные продукты конденсации до первичных аминов.
Диазотирование анилина
Диазотированием называется взаимодействие анилина с азотистой кислотой. Эта реакция имеет большое практическое значение, в результате ее образуется соль бензолдиазония (39) — диазосоединения, отличающегося высокой реакционной способностью. На практике обычно используют не саму азотистую кислоту, а ее натриевую соль (NaNO2). Действуя на нитрит натрия сильной минеральной кислотой (например, соляной), получают азотистую кислоту, которая немедленно вступает в реакцию с амином (уравнение (4.2.36)).
Соляной кислоты, как видно из приведенного уравнения, должно быть два эквивалента. Фактически кислоту надо брать с небольшим избытком (~2,2-3 эквивалента), чтобы в конце реакции pH находился в пределах 0,5-1,5. При недостаточной кислотности реакционной массы диазотирование не проходит до конца главным образом из-за побочной реакции, в которой участвуют диазосоединение и еще не успевший вступить в реакцию диазотирования исходный амин (образуется диазоаминосоединение C6H5NH—N=N— С6Н5)). Избыток кислоты тормозит течение побочной реакции
C6H5NH2 + RCOOH
он-C6H5-NH2 + ОСН-R C6H5-N=CH-R
н+
2
NH2 • HC1 + CH2O
(57) R = Aik, Ar
{38)
C6H5NH2 + NaNO2 + 2HC1 -► C6H5N2+Cr + NaCl + 2H2O {39)
(4.2.36)
Ароматические соединения
627
NaNO2; Н+
(40)
C6H5NH2
с6н5^н3 с6н5он
(8)
(4.2.37)
Реакция с трихлорметаном (хлороформом) и щелочью
При нагревании анилина с грихлорметаном (хлороформом) и спиртовой щелочью (уравнение (4.2.38)) образуется фенилизоцианид (41) — вещество с исключительно неприятным тошнотворным запахом.
Эта реакция применяется для обнаружения первичных аминов, к которым относится и анилин.
Реакции электрофильного замещения
Для ароматического кольца анилина, имеющего повышенную электронную плотность, характерны реакции электрофильного замещения: сульфирование, нитрование, галогенирование. Предварительно аминотруп-пу анилина защищают (чаще всего ацилированием), если: 1) в условиях проведения реакций замещения аминогруппа окисляется; 2) при проведении реакции в кислой среде аминогруппа протонируется и переходит в аммониевую, что приводит к изменению ориентации при замещении. Факторами, определяющими направление электрофильного замещения, являются величины электронной плотности на атомах углерода и стабильность о-комплексов, образующихся в реакциях замещения.
Сульфирование анилина. Сульфированием анилина получают ценный промежуточный продукт — сульфаниловую кислоту (44), используемую в синтезе красителей и лекарственных веществ.
При действии серной кислоты на анилин аминогруппа протонируется, образуя аммониевую группу — электроноакцепторный заместитель. Поэтому при прямом сульфировании анилина неизбежно образование изомеров, и этим методом пользуются достаточно редко. Чаще используют обходные пути, временно защищая аминогруппу ацильным остатком или применяя «реакцию запекания».
C6H5-NH2 + CHCI3 + ЗКОН C6H5-N=C + ЗН2О + ЗКС1
(41)
Реакция запекания позволяет получать сульфаниловую кислоту при минимальном расходе серной кислоты. Эту реакцию осуществляют путем длительного нагревания заранее приготовленного бисульфата анилина [(42); соль анилина с эквимольным количеством серной кислоты)] при 180-190 °C. Бисульфат анилина, теряя молекулу воды, превращается в фенилсульфаминовую кислоту (43), которая при дальнейшем нагревании изомеризуется, образуя сульфаниловую кислоту (44).
Этот метод получения сульфаниловой кислоты применяется в промышленности. Раньше запекание соли анилина проводили на металлических противнях в специальных печах, иногда при пониженном давлении. В настоящее время эту операцию проводят, нагревая бисульфат анилина в высококипящих органических растворителях, например в полихлоридах бензола. Это обеспечивает значительно более равномерный обогрев и исключает возможность подгорания твердого продукта.
Нитрование анилина. Нитрованию обычно подвергают ацетильное производное анилина — /V-ацетил-анилин [(36): ацетанилид]. Нитрование ацетанилида проводят нитрующей смесью, состоящей из азотной и серной кислот. Вначале ацетанилид растворяют в концентрированной H2SO4 и при охлаждении (до 0 °C и ниже) добавляют HNO3. При этом в основном образуется и-нитроацетанилид (45) с примесью до 10 % орто-изомера (46). Разбавлением реакционной массы выделяют нитропродукт и при последующей кристаллизации разделяют изомеры.
В полученных нитроацетанилидах ацетильную труппу удаляют нагреванием с разбавленной кислотой или щелочью и получают соответственно п- (47) и о-нигроанилины (48). В настоящее время эти соединения чаще получают аминированием соответствующих нитрохлорбензолов.
(4.2.38)
SO3H
(43) (44)
628
Новый справочник химика и технолога
Галогенирование анилина. Из галогенпроизвод-ных анилина широко применяются хлорпроизводные. Бромпроизводные имеют меньшее значение, что в первую очередь связано со значительно более высокой стоимостью брома и его дефицитом. Иодпроизвод-ные практически не используются.
Анилин под влиянием электронодонорной аминогруппы легко хлорируется. Действие хлора на анилин в неводном растворителе приводит к образованию симметричного 2,4,6-трихлоранилина. При проведении реакции в водном растворе кроме 2,4,6-трихлоранилина образуются окрашенные продукты окисления (индули-новые красители).
При действии хлора на анилин в водных растворах серной кислоты образуется хлоранил [(49); 2,3,5,6-тет-рахлор-н-бензохинон].
С12 ---------->
H2SO4; Н2О
(49)
Хлорирование гидрохлорида анилина в растворе или суспензии индифферентного растворителя при полном отсутствии влаги приводит к образованию полихлорированного соединения, восстановление которого, например, сульфидом натрия в спирте, приводит к образованию пентахлоранилина (59).
(59)
Для получения монохлорпроизводных анилин предварительно ацилируют по аминогруппе, а затем хлорируют хлором в среде органического растворителя (хлорбензол, нитробензол, диметилформамид). Реакция начинается с образования А-хлорпроизводного (5/), которое в результате перегруппировки превращается в С-галогензамещенный А-ацетанилид: орто- (52) или яд/7<7-изомер (53). Изомеры разделяют и ацильную защиту снимают, нагревая соединения с разбавленной кислотой.
C-Алкилирование анилина
Анилин легко алкилируется в ядро, но реакция идет в две стадии: вначале образуются А-алкильные производные, которые затем перегруппировываются с перемещением алкила в ароматическое кольцо (перегруппировка Гофмана—Марциуса). Примером может служить синтез 4-бутиланилина (55), используемого для получения кислотных антрахиноновых красителей. При нагревании анилина с бутанолом в присутствии минеральной кислоты сначала образуется А-бутилани-
лин (54), который при нагревании до 200-250 °C в присутствии катализатора (хлорид цинка или кобальта) превращается в 4-бутиланилин (55).
Внутримолекулярное С-алкилирование А-алкил-производных анилина приводит к образованию новых циклов. Практически важной реакцией этого типа является синтез хинолиновых производных по Скраупу.
Для получения хинолина в реакционную массу вводятся анилин, глицерин, серная кислота и окислитель, в качестве которого в данном синтезе целесообразнее
Ароматические соединения
629
всего применять нитробензол. Серная кислота, отнимая воду от глицерина, превращает его в акролеин (56).
(54) (55)
H2SO4
СН2ОНСНОНСН2ОН • - > сн2=снсно
(56)
По двойной связи акролеина присоединяется анилин, и далее идет циклизация за счет альдегидной группы. Затем происходит дегидратация, в результате которой образуется 1,2-дигидрохинолин (57). При дегидрировании 1,2-дигидрохинолина за счет введенного окислителя (нитробензола) образуется хинолин (58); нитробензол при этом восстанавливается в анилин, который также реагирует с акролеином.
Реакция сопровождается выделением большого количества тепла, поэтому нафев реакционной массы до температуры взаимодействия (-130 °C) надо вести очень осторожно (при резком повышении температуры реакция начинается внезапно и так бурно, что вся масса может превратиться в смолу). Если вместо глицерина вводить в реакцию готовый акролеин, из-за слишком бурного взаимодействия также может произойти ос моление реакционной массы. Скорость реакции можно уменьшить путем дополнительного введения в смесь железного купороса.
При взаимодействии анилина с ацетальдегидом в среде концентрированной серной кислоты или с кротоновым альдегидом в среде концентрированной соляной кислоты получают хинальдин [(59); 2-метил-хинолин], при взаимодействии с винилметилкетоном — лепидин [(60); 4-метилхинолин]. Оба вещества являются ценными промежуточными продуктами, используемыми для получения красителей, гербицидов, лекарственных веществ.
(61)
Хорошие результаты при гидрировании анилина получены также при использовании в качестве катализатора кобальта, активированного известью.
Моно- и дициклогексиламин используются как промежуточные продукты для синтеза ускорителей вулканизации каучука, а также для синтеза некоторых красителей.
Окисление анилина
Анилин в отличие от метиламина легко окисляется, поэтому при хранении обычно темнеет. При контролируемом окислении анилина в кислой среде образуется п-бензохинон (62).
Гидрирование анилина
При гидрировании анилина образуется циклогекси-ламин (61). Гидрирование ведут водородом в присутствии катализатора (никеля Ренея) при давлении 9,5 МПа и температуре 30-150 °C, В верхнем пределе указанного интервала температур образуется также дициклогексиламин с выходом до 25 %. Добавка к исходному анилину дициклогексиламина устраняет образование последнего и увеличивает выход цикло-гексиламина.
Na2Cr2O7, Н+
(62)
Этот метод получения и-бензохинона находит промышленное применение. В качестве окислителя приме-
630
Новый справочник химика и технолога
няют Na2Cr2O7 или МпО2 (пиролюзит) в серной кислоте. Выход продукта обычно составляет 85-90 %. «-Бензохинон применяется для получения красителей, гидрохинона; дубящее вещество.
При окислении анилина хромовой кислотой получается черный краситель «анилиновый черный» (см. подраздел 4.2.5.3). При окислении гидропероксидом трифторацетила анилин с хорошим выходом образует нитробензол (уравнение (4.2.39)).
C6H5NH2 + ЗСБзСО-ООН ->
-> C6H5NO2 + 3CF3COOH + Н2О (4.2.39)
4.2.5. Применение анилина
Анилин (иногда называемый анилиновым маслом) — один из наиболее широко применяемых в технике полупродуктов. Он имеет большое значение в производстве более сложных промежуточных продуктов, красителей, химических добавок к полимерам, фармацевтических препаратов, пестицидов и др.
Анилин имеет некоторое значение как ингибитор коррозии. Особенно хорошо он зарекомендовал себя для защиты металлов в среде влажного тетрахлормета-на (четыреххлористого углерода). Фосфаты анилина при добавлении к растворам сильных электролитов замедляют коррозию углеродистых сталей.
Аддукты анилина с трифторидом бора, а также продукты конденсации анилина с альдегидами могут быть использованы в качестве катализаторов и отвердителей эпоксидных олигомеров.
Различные соли и реактивы на основе анилина используются в качестве добавок к топливам и смазочным маслам в процессах очистки топлива. Американская фирма «Gulf Research a. Development» предложила использовать производное анилина — о-азидоанилин в качестве антидетонационной добавки к моторным топ
ливам. Это предложение вызвало большой интерес в связи с жесткими ограничениями на применение свинцовых и марганцевых антидетонаторов.
В лабораторной практике анилин находит применение как растворитель и реагент.
В настоящее время ~85 % производимого анилина потребляет производство полиизоцианатов.
4.2.5.1. Полиизоцианаты
Это соединения, на основе которых получают ценные полимерные материалы — полиуретаны, широко используемые для конструкционных материалов и прочной тепло- и звукоизоляции. Современная технология получения полиуретанов базируется на толуи-лендиизоцианатах и дифенилметандиизоцианатах. Для получения толуилендиизоцианатов анилин не требуется. Дифснилметандиизоцианат (63) получают фосгени-рованием 4,4'-диаминодифенилметана (38) — продукта конденсации анилина с формальдегидом.
Технический продукт представляет собой смесь, известную под названием «МДИ для полимеризации», которая содержит 50 % 4,4'-изомера, 5-10 % 2,4'-изо-мера и ряд полифенилполиизоцианатов, имеющих в молекуле метиленовые мостики.
При дальнейшей конденсации 4,4'-диаминодифе-нилмстана с анилином и формальдегидом образуется полиметиленполифениленамин (64).
При фосгенировании полиамина (64) в среде хло-рорганического растворителя получают полиизоцианат (полиметиленполифениленполиизоцианат). В промышленной практике наиболее широко применяются полиамины, содержащие от 2,6 до 2,9 аминогрупп на 1 молекулу полиамина. Таким образом, на получение 100 кг полиизоцианата расходуется от 75 до 80 кг анилина (теоретический расход при 2,7 аминогрупп составляет 73,5 кг).
(35)
(63)
(64)
Полиметиленполифениленполиизоцианат применяется в производстве полимеров (полиуретанов), полиуретановых лакокрасочных материалов, является модификатором резиновых смесей и клеевых составов.
4.2.5.2. Химические добавки к полимерам
К вспомогательным веществам, которые используются в производстве полимерных материалов, относятся стабилизаторы полимеров, ускорители и агенты
Ароматические соединения
631
вулканизации, инициаторы полимеризации, пластификаторы, антиоксиданты, антиозонанты, модификаторы, порообразователи.
На производство химических добавок к полимерам расходуется ~7 % анилина. Эти соединения можно условно разделить на три группы: 1) химические добавки, получаемые непосредственно на основе анилина; 2) химические добавки, получаемые с использованием анилина и других полупродуктов; 3) химические
добавки на основе полупродуктов, полученных из анилина.
Химические добавки к полимерам, получаемые на основе анилина
На схеме 4.2.2 представлены соединения, получаемые непосредственно из анилина, которые эффективно используются на практике как вспомогательные вещества в производстве полимеров.
Схема 4.2.2
Дифениламин (9)
Известно много способов получения дифениламина. В промышленности его получают (по непрерывной технологии) методом жидкофазной конденсации анилина при 300-340 °C и 1,5-2 МПа в присутствии катализатора (смесь фторида и дифторида аммония с борной кислотой).
Дифениламин более ста лет применяется для стабилизации порохов и некоторых пищевых продуктов (рыбные консервы). Стабилизатор многих полимеров, эффективный ингибитор фотодеструкции полихлоропреновой пленки, окислительно-восстановительный индикатор. Является одним из основных полупродуктов для получения различных стабилизаторов полимерных материалов, органических красителей.
4,4'-Диаминодифенилсульфид (73)
Синтез см. подраздел 4.2.4.2. Отвердитель эпоксидных олигомеров, антиоксидант, промежуточный продукт в синтезе органических красителей.
/ЧТУ'-Дифенилтиомочевина (76)
Синтез см. подраздел 4.2.4.2. Ускоритель вулканизации резиновых смесей на основе натурального и синтетических каучуков общего назначения; стабилизатор поливинилхлорида; флотореагент для экстракции, вы
деления и фотометрического определения платиновых металлов. Промежуточный продукт в синтезе красителей и лекарственных средств.
2-Меркаптобензотиазол (77)
Синтез см. подраздел 4.2.4.2. Широко распространенный ускоритель вулканизации смесей на основе натурального и синтетических каучуков (требует применения активаторов), повышает сопротивление вулканизатов тепловому старению. В виде водной дисперсии применяется для стабилизации латексов. Является промежуточным продуктом для синтеза других ускорителей вулканизации, цианиновых красителей.
Три(фениламид) фосфористой кислоты (18)
Синтез см. подраздел 4.2.4.2. Эффективный стабилизатор бутадиен-стирольных, особенно маслонаполненных каучуков. Антиоксидант для резин.
4,4'-Диаминодифенилметан (38)
Синтез см. подраздел 4.2.4.2. Эффективный стабилизатор резин на основе каучуков общего назначения, антиоксидант, активатор вулканизации, отвердитель эпоксидных олигомеров. Мономер для синтеза термостойких полимеров и полиизоционатов, полупродукт для органических красителей.
632
Новый справочник химика и технолога
Диазоаминобензол (40)
Синтез см. подраздел 4.2.4.2. Порообразователь, ускоритель вулканизации каучуков, инициатор полимеризации диеновых углеводородов.
Ди(2-бензотиазолил)дисульфид (65)
Получают окислением Na-соли 2-меркаптобенз-тиазола нитритом натрия в присутствии серной кислоты. Широко распространенный ускоритель вулканизации смесей на основе натурального и синтетических каучуков диенового типа, а также бутилкаучука. Замедляет процесс вулканизации хлоропренового каучука.
А,Л'-Дифенилгуанидин (66)
Получают взаимодействием анилина с CS2 с последующим окислением РЬО в присутствии NH3; взаимодействием /V,/V'-дифенилтиомочевины с NH3 Ускоритель вулканизации для смесей на основе натурального и
синтетических каучуков, применяется в основном в сочетании с другими ускорителями. Окрашивает светлые резины. Применяется в производстве шин, резинотехнических изделий, резиновой обуви. Аналитический реагент для экстракции, осаждения и соосаждения ряда элементов.
Химические добавки к полимерам, получаемые с использованием анилина и других полупродуктов
На схеме 4.2.3 представлены соединения, которые используются на практике, в основном как химические добавки к полимерам. Все вещества получены с использованием анилина в качестве одного из основных полупродуктов.
Схема 4.2.3
УУ-Фенил-1-нафтиламин (67)
Получают взаимодействием анилина с 1-нафтиламином в присутствии сульфаниловой кислоты. Стабилизатор синтетических каучуков (бутадиеновых, бутадиенстирольных, изопреновых, хлоропреновых). Термостабилизатор резин на основе натурального и синтетических каучуков, полиэтилена. Используется в качестве стабилизатора смазочных масел и противокоррозионных жидкостей для двигателей внутреннего сгорания (антидетонатор). Промежуточный продукт в синтезе азокрасителей.
Л-Фенил-2-нафтиламин (68)
Получают взаимодействием анилина с 2-нафтолом в присутствии гидрохлорида анилина или бензолсульфокислоты. Широко распространенный стабилизатор различных видов синтетических каучуков (бутадиеновых,
бутадиен-стирольных, бутадиен-нитрильных, изопреновых, хлоропреновых, бутилкаучука и др.). Термостабилизатор полиэтилена, полиизобутилена и сополимеров этилена с винилацетатом; стабилизатор смазочных масел. Применяется в производстве триарилметановых красителей.
4-Гидроксидифениламин (69)
Получают конденсацией анилина с гидрохиноном или с и-аминофенолом в присутствии сульфаниловой кислоты или хлорида аммония соответствено. Стабилизатор синтетических каучуков общего назначения, ингибитор полимеризации бутадиена, антиоксидант бензина, турбинного и трансформаторного масел. Один из важнейших полупродуктов в производстве стабилизаторов, органических красителей, фармацевтических препаратов.
Ароматические соединения
633
Ацетан (70)
Получают конденсацией анилина с ацетальдегидом. Ускоритель вулканизации для смесей на основе натурального и синтетических каучуков диенового типа, а также бутилкаучука. Обладает термостабилизирующим действием.
Бутиран (77)
Получают конденсацией анилина с масляным альдегидом Ускоритель вулканизации для резиновых смесей на основе натурального и синтетических каучуков. Применяется в производстве шин и резинотехнических изделий, обуви, эбонитовых и латексных изделий; оказывает стабилизирующее действие.
/V,7У'-Дифенил-1,4-фенилендиамин (72)
Получают конденсацией анилина с гидрохиноном или с и-аминофенолом. Широко распространенный стабилизатор синтетических каучуков общего назначения. Термостабилизатор резин на основе натурального и синтетических каучуков. Термо- и светостабилизатор полипропилена, пентапласта, полиоксипропилена, полиацетальдегида. Повышает стабильность химических волокон к атмосферным воздействиям. Ингибитор полимеризации эфиров ненасыщенных карбоновых кислот, антиокислительная присадка для жидкоготоплива и смазочных масел.
У,Л'-Дифенилэтилендиамин (73)
Получают взаимодействием анилина с 1,2-дихлорэтаном в присутствии катализатора (СаСО3 и др.). Стабилизатор бутадиен-стирольных и олефиновых каучуков и латексов. Термостабилизатор сополимеров этилена с пропиленом. Защищает резины от термоокис-литсльного старения и разрушения при многократных деформациях. Отвердитель полиуретанов, антиоксидант для эпоксидных олигомеров. Предохраняет окраски дисперсными красителями на ацетатном шелке от воздействия оксидов азота.
7У,7У'-Дифенилпропилендиамин (74)
Получают взаимодействием анилина с 1,2-дихлор-пропаном. Антиоксидант для резин.
Бис(о-бензамидофенил)дисул ьфид (75)
Получают взаимодействием анилина с элементарной серой и последующей обработкой полученного соединения бензоилхлоридом. Эффективный ускоритель пластикации резиновых смесей на основе натурального и синтетических каучуков. Несколько ускоряет процесс вулканизации.
Химические добавки к полимерам на основе полупродуктов, полученных из анилина
Многие вспомогательные вещества для полимерной промышленности получают на основе соединений, синтезированных из анилина. Большое практическое значение имеют такие соединения, как 2-меркаптобензотиазол, дифениламин, 4-аминодифениламин, 4-гидроксидифениламин. Так, 2-меркаптобензтиазол (17) является основой группы ускорителей вулканизации резиновых
смесей на основе натурального и синтетических каучуков различного назначения (табл. 4.2.5).
(76Н<?7)
При взаимодействии 2-меркаптобензотиазола с хлором и циклогексиламином получают эффективный ускоритель высокотемпературной вулканизации резиновых смесей на основе натурального и синтетических каучуков — Сульфенамид 2Ц [(52); Л-?,Л-бис(2-бензо-тиазол илтио)ци клогексил амин].
Конденсацией 2-меркаптобензтиазола с формальдегидом и последующим взаимодействием продукта конденсации с фенотиазином получают соединение (83) — стабилизатор натурального и бутадиеновых каучуков, антиоксидант для резин.
БТФ (83)
На основе дифениламина (9) получают ряд соединений (84)-(86), которые используются как стабилизаторы синтетических каучуков и антиоксиданты для резин (табл. 4.2.6).
(54Н56)
Нитрозированием дифениламина получают А-нитро-зодифениламин (87), который используется как замедлитель подвулканизации и структурирования резиновых смесей.
(57)
4-Аминодифениламин [(55); R=H; М-фенил-1,4-фенилендиамин], так же как дифениламин, является основой для синтеза ряда соединений (89)-(92), которые используются как стабилизаторы синтетических каучуков и антиоксиданты для резин (табл. 4.2.7).
634
Новый справочник химика и технолога
(89)-{92)
На основе 4-гидроксидифениламина (69) получают соединения (93)-(95), которые используются в качестве термостабилизаторов полимерных материалов (табл. 4.2.8).
Нитрозированием У-метиланилина (22) нитритом натрия в кислой среде получают Нитрозан к [(96); У,4-динитрозо-А-метиланилин], которое используется как активатор вулканизации резиновых смесей, модификатор, антиструктурирующий агент.
(96)
Конденсацией /V-этиланилина (24) с сероуглеродом и последующим взаимодействием продукта конденсации с хлоридом цинка получают карбамат ЭФЦ [(97); N,N-диэтил-А,А'-дифенилтиокарбамат цинка] — активный ускоритель вулканизации (ультраускоритель). Применяется для получения прозрачных, белых и цветных резин из натурального и синтетических каучуков.
(97)
(93)-(95)
Таблица 4.2.5
Ускорители вулканизации резиновых смесей, полученные на основе 2-меркаптобензотиазола (МБТ)
R Название: торговое, [химическое] Способ синтеза
-nh-c-nh2 II О /С2Н5 -N\c и ХС2Н5 \О -S-N// \) —N=CH-\ У О БТСМ, [(76); А-(2-бензотиазолилтио)мочевина] Сульфенамид БТ, [(77); А,А-диэтилбензотиазолсульфе-намид-2] Сульфенамид Ц, [(75); тУ-циклогексилбснзотиазол-сульфенамид-2] Сульфенамид М, [(79); (бензотиазолил-2)морфолино-сульфид] Сульфенамид ТМ, [(50); (бензтиазолил-2)морфолиноди-сульфид] Сульфенамид Ф, [(5/); А-фурфурилиденбензотиазол-сульфенамид-2] Взаимодействие МБТ с хлором и мочевиной Взаимодействие Na-соли МБТ с диэтилами-ном в присутствии H2SO4 и окисление промежуточного соединения NaOCI Взаимодействие МБТ с циклогексиламином и окисление промежуточного соединения NaOCI Конденсация Na-соли МБТ с А'-хлор-морфолином Взаимодействие МБТ с морфолином и серой в присутствии NaOCI Взаимодействие МБТ с NH3 в присутствии NaOCI, затем конденсация с фурфуролом
Таблица 4.2.6
Стабилизаторы синтетических каучуков, полученные на основе дифениламина
R Название: торговое, [химическое] Способ синтеза
СН3 -5 СНз4^7 Дифенам ДМБ, {(84); 4,4 '-бис(а,а- диметилбензил)-дифениламин] Алкилирование дифениламина метилстиролом в присутствии серной кислоты или алюмосиликатов
Ароматические соединения
635
Окончание табл. 4.2.6
R Название: торговое, [химическое] Способ синтеза
-СН-^ СН3 или один из R=H СН3 СН3 —С—СН2—С—СН3 СН3 СНз или один из R=H Дифенам С, [(55); 4,4'- бис(а-метилбензил)-дифениламин; 4-(а-метилбснзил)-дифениламин (смесь)] Дифенам ДИБ, [(56); 4,4'-бис( 1,1,3,3-тетрамстил-бутил)-дифениламин; 4-(1,1,3,3-тетраметилбутил)дифениламин (смесь)] Алкилирование дифениламина стиролом в присутствии катализатора (А1С13, ZnCl2 или алюмосиликаты) Алкилирование дифениламина диизобутиленом в присутствии катализатора (А1С13, природные алюмосиликаты)
Таблица 4.2.7
Стабилизаторы синтетических каучуков, полученные на основе 4-аминодифениламина
R Название: торговое, [химическое] Способ синтеза
-so2-^ У~сн3 /СН3 -СН^ Х СНз /СН3 -сн-сн2-сн^ 1 ХСН3 СНз Алкилы: С7Н15—С9Н19 Диафен ФСТ, [(59); 4-(4-толилсульфониламидо)-дифениламин] Диафен ФП, [(90); А-изопропил-А'-фенил-1,4-фенилендиамин] Диафен ФДМБ, [(97); А-(1,3-диметилбутил)-А'-фе-нил-1,4-фенилендиамин] С-789, [(92); А-алкил-А'-фенил-и-фени-лендиамин] Взаимодействие 4-аминодифениламина с толилсульфохлоридом Восстановительное алкилирование 4-аминодифениламина ацетоном Восстановительное алкилирование 4-аминодифениламина 4-метил-пентано ном-2 Алкилирование 4-аминодифениламина смесью жирных спиртов (С7-С9)
Таблица 4.2.8
Термостабилизаторы полимерных материалов, полученные на основе 4-гидроксидифениламина
R Название: торговое, [химическое] Способ синтеза
-(СН2)-О-(СН2)- —CHj-CH—СИОН СНз "Г СН3 Н-1, [(93); 2,2'-бис(4-фениламино-фенокси)диэтиловый эфир] С-47, [(94); 2-гидрокси-1,3-бис(4-фениламинофенокси)пропан] С-1, [(95); диметил-бис(4-фениламино-фенокси)силан] Алкилирование Na-соли 4-гидроксидифениламина дихлордиэтиловым эфиром Взаимодействие 4-гидроксидифениламина с 1,3-дихлоргидрином глицерина в присутствии щелочи Конденсация 4-гидроксидифениламина с дихлордиметилсиланом в присутствии аммиака
4.2.5.3. Красители на основе анилина
Открытие Зининым реакции получения анилина из нитробензола явилось основой развития анилинокрасочной промышленности. Более 60 лет анилин использовался практически полностью для нужд анилинокрасочной промышленности. Синтетические красители даже получили общее название — анилиновых.
В настоящее время в международном справочнике «Color Index» содержится 163 красителя, получаемых из анилина, и еще больше — из производных анилина. В последние годы для нужд промышленности синтетических красителей используется ~3 % производимого анилина.
Красители, получаемые с использованием анилина, можно условно разделить на три группы:
636
Новый справочник химика и технолога
1) красители, получаемые из анилина;
2) красители, в состав которых, кроме анилина, входят другие соединения;
3) красители на основе промежуточных продуктов, полученных из анилина.
Для нужд текстильной промышленности выпускается хлоргидрат анилина СбН5МН2 • НС1, так называемая анилиновая соль.
Красители, получаемые из анилина
Полидиазиновые (Анилиновый черный,
Пигмент глубоко-черный)
(И. водорастворимый, И. спирторастворимый,
И. жирорастворимый)
Нигрозины (Н. водорастворимый, Н. спирторастворимый. Н. жирорастворимый)
Полидиазиновые красители. Краситель Анилиновый черный образуется при окислении анилина непосредственно на волокне (так называемое окислительное крашение). Окислительное крашение проводят на текстильных отделочных фабриках. Для получения черной окраски ткань пропитывают смесью гидрохлорида анилина, окислителей (хлорат натрия или дихромат калия) и катализаторов (соли меди, железа или ванадия) и обрабатывают при повышенной температуре (-100 °C) паром. Если окисление анилина произошло недостаточно, то образовавшаяся черная окраска зеленеет на воздухе. Для предотвращения этого ткань дополнительно обрабатывают раствором дихромата. Опасность образования зеленой окраски уменьшается при добавлении к анилину w-фенилендиамина, который облегчает процесс окисления.
Образование Анилинового черного {104) проходит через ряд стадий, представляющих собой чередующиеся реакции окисления и конденсации, при этом последовательно образуются промежуточные продукты — индамины [(98)-{103)], строение которых все более усложняется, а окраска углубляется от фиолетового [(100); Протоэмеральдин] до синего [(101); Эмераль-дин], темно-синего [(102); Нигранилин], зелено-черного [(/03); Псрнигранилин] и черного (104) цветов.
Окраски, образованные Анилиновым черным (104) на целлюлозных волокнах, отличаются глубоким,
«сочным», черным цветом, на фоне которого особенно ярко выглядят расцветки другими красителями. Ни один из черных красителей других классов не может сравниться с ним в этом отношении. Окраски отличаются высокой устойчивостью к действию кислот, окислителей, восстановителей, света, погоды, горячим мыльно-содовым обработкам, но недостаточно устойчивы к глажению. Рыболовные сети, окрашенные Анилиновым черным методом окислительного крашения, устойчивы к гниению.
Недостатком использования Анилинового черного является то, что в процессе окислительного крашения происходит ослабление волокна и сам процесс крашения весьма неудобен из-за высокой токсичности анилина.
На анилинокрасочных заводах Анилиновый черный получают под названием Пигмент глубоко-черный, окисляя разбавленный водный раствор гидрохлорида анилина дихроматом калия в присутствии H2SO4 и CuSO4 при 25-30 °C. Окисление можно проводить и кислородом воздуха, если процесс вести в присутствии w-фенилендиамина (до 15 % от массы анилина) и CuSO4 при температуре выше 70 °C и pH «2. Пигмент глубоко-черный устойчив к свету, действию кислот, щелочей и органических растворителей. Он применяется для крашения пластических масс, изготовления копировальной бумаги, краски для лент пишущих машин, лаков и т. п.
[О]
(98)
* штохг -
(99)
Ароматические соединения
637
Нигрозины (красители черного цвета) получают нагреванием анилина, гидрохлорида анилина и нитробензола (краситель можно получить, не используя нитробензол) с чугунной стружкой при 170-180 °C («нигрозиновая плавка»). Химизм нигрозиновой плавки сложен и до конца не изучен. Предполагают, что на первой стадии процесса происходит окисление анилина нитробензолом в и-хинонимин (7 05) или восстановление нитробензола чугунной стружкой в фенилгидроксиламин, который перегруппировывается в и-аминофе-нол (106). При взаимодействии этих веществ с анилином образуется индоанилин (107).
Индоанилин (107) претерпевает обычные для хинониминовых красителей превращения (присоединение к хиноидному ядру, замыкание циклов и т. д.). В результате образуется сложная смесь красителей с диазиновыми и оксазиновыми кольцами. Красители имеют различные оттенки: от красновато-черных до синеваточерных, в зависимости от условий проведения плавки. Главной составной частью нигрозинов являются соеди
нения с одним диазиновым и одним оксазиновым кольцами [(70$) и (110)] и соединения с двумя диазиновыми кольцами [(109) и (7/7)]. Красители (110) и (777), являющиеся главной составной частью синевато-черных нигрозинов, отличаются от красновато-черных нигрозинов (108) и (109) наличием еще одной фениламиногруппы.
Нигрозины выпускают в виде Нигрозинов спирторастворимого, жирорастворимого и водорастворимого. Нигрозин спирторастворимый образуется в результате «плавки» и применяется для крашения пластмасс, дерева и изготовления спиртовых лаков. Нигрозин жирорастворимый получают обработкой Нигрозина спирторастворимого 40% раствором NaOH при нагревании; его применяют для изготовления сапожных кремов, краски для лент пишущих машин, типографских красок и т. д. Сульфированием Нигрозина спирторастворимого 100% серной кислотой получают Нигрозин водорастворимый, применяемый в качестве кислотного красителя для кожи, шелка и шерсти, а также для изготовления чернил.
638
Новый справочник химика и технолога
[О]
----►
{105)
(108) R = Н
(НО) R = NHC6H5
(109) R = Н (///)R = NHC6H5
Индулины. Это красители синего цвета, которые получают взаимодействием и-аминоазобензола (112) с анилином и его гидрохлоридом при 150-200 °C («инду-линовая плавка»). и-Аминоазобензол [продукт азосочетания бензолдиазония с анилином] реагирует с анилином в хинонгидразонной форме (112а), при этом сначала образуется индамин (113).
Индамин (113), взаимодействуя с гидрохлоридом анилина, образует Феносафранин (114), отличающийся от Сафранина отсутствием метильных групп.
(114)
Дальнейшая плавка с анилином приводит к арили-рованию Феносафранина и к присоединению новых ариламиногрупп к продукту арилирования. В результате образуется сложная смесь красителей, например, фениламинофеносафранины (115) с различным числом фениламиногрупп. В зависимости от условий индули-
новой плавки (соотношение реагентов, температура, продолжительность реакции) получаются красители различной степени араминирования и, соответственно, различных оттенков: от красновато-синего до зеленовато-синего.
Фениламинофеносафранины находятся в плаве в форме хлоридов, нерастворимых в воде, но растворимых в спирте. Их выпускают под названием Индулин спирторастворимый и применяют для изготовления спиртовых лаков.
При обработке индулинового плава разбавленным раствором NaOH при 100 °C образуются соответствующие основания, растворимые в спирте, восках, жирах, маслах, углеводородах (парафин, бензин и др.). Их выпускают под названием Индулин жирорастворимый и применяют для изготовления типографских красок, черного лака для резиновой обуви, а также для крашения пластических масс.
Сульфированием Индулина спирторастворимого или жирорастворимого 100% серной кислотой получают сульфокислоты, натриевые соли которых растворимы в воде и являются кислотными красителями. Под названием Индулин водорастворимый их применяют для крашения кожи, шелка, шерсти и для приготовления чернил.
Ароматические соединения
639
(772)
(772а)
c6h5nh3ci
(773)
Красители, получаемые на основе анилина и других соединений
Это красители, в состав которых, кроме анилина, входят и другие полупродукты, часто имеющие достаточно сложное строение. Ниже показано, к каким техническим классам относятся подобные красители.
Ниже представлены азокрасители, которые получают, используя анилин в качестве одного из полупродуктов: диазо- или азосоставляющей.
Азокрасители
Органические
Кислотные
красители
(получены на основе анилина и других полупродуктов)
Прямые Дисперсные
Жирорастворимые
Азокрасители
Н итрокрасители
Антрахиноновые Триарилметановые
Азокрасители
Азокрасители получают по общей схеме:
1) диазотирование ароматического амина с образованием диазосоединения (уравнение (4.2.40));
ArNH2 + NaNO2 + 2НХ ArN2X + 2Н2О + NaX
(4.2.40)
2) взаимодействие (азосочетание') диазосоединения с веществами, содержащими активный атом водорода (уравнение (4.2.41)). В результате этого взаимодействия образуются азосоединения.
ArN2X + R YArN-N R + Y+X (4.2.41)
Амин, из которого образуется активный компонент реакции — диазосоединение, называется диазосоставляющей, а вещество, с которым реагируют диазосоединение, — азосоставляющей (пассивный компонент реакции или азокомпонент).
Красители, полученные с использованием анилина как диазосоставляющей. Это наиболее обширная группа красителей. При синтезе этих красителей из анилина получают активное диазосоединение [(39); хлорид бензолдиазония], которое немедленно вводится в реакцию азосочетания.
Анилин диазотируется легко, быстро и при достаточно высокой концентрации в растворе. Синтез проводят следующим образом: анилин растворяют в 10-15% хлороводородной кислоте (на 1 моль амина 2,5 моль НС1) и охлаждают до 0 °C. к охлажденному раствору при перемешивании добавляют 30% раствор нитрита натрия (на 1 моль амина 1,1 моль NaNO2) с такой скоростью, чтобы температура реакционной массы не превышала 2 °C. Так как реакция отличается высоким экзотермическим эффектом, выделяющееся тепло надо постоянно отводить. По окончании диазотирования реакционная масса должна иметь pH «2 и содержать небольшой избыток азотистой кислоты. Раствор хлорида бензолдиазония используют сразу же после приготовления.
Диазосоединение на основе анилина отличается высокой реакционной способностью и легко взаимодействует с соединениями, имеющими повышенную электронную плотность у атома углерода. Поэтому подавляющее большинство азосоставляющих, используемых
640
Новый справочник химика и технолога
для синтеза азокрасителей, — это соединения с электронодонорными заместителями, практически амино- и гидроксисоединения. При взаимодействии хлорида бензолдиазония с аминосоединениями азосочетание проводят в кислой среде (уравнение (4.2.42)), чтобы
избежать образования побочных продуктов (диазоаминосоединений), при взаимодействии с гидроксисоединениями азосочетание проводят в щелочной среде (уравнение (4.2.43)), чтобы повысить активность азосоставляющей.
С6Н5-К2+СГ +
(4.2.42)
C6H5-N2+Cr +
(4.2.43)
Процесс азосочетания является экзотермическим, и выделяющееся тепло необходимо отводить. Для каждой реакции существует оптимальная температура. При азосочетании с аминосоединениями температура реакционной массы может подниматься до 5-10 °C, что практически нс влияет на качество продукта реакции. При азосочетании с гидроксисоединениями температура реакции не должна превышать 2 °C, т. к. в щелочной среде при повышении температуры диазосоединенис активнее разлагается, чем сочетается, что отрицательно влияет как на выход, так и на качество продуктов реакции. Лишь в конце азосочетания температура реакционной массы может подняться до 4-5 °C.
Азосочетанис проводят следующим образом: готовят раствор азосоставляющей, который в зависимости от соединения может быть кислым, щелочным или нейтральным, и охлаждают его до необходимой температуры. к охлажденному раствору азокомпонента при перемешивании добавляют кислый раствор хлорида бензолдиазония. Такой порядок ведения процесса называют прямым. При сочетании в щелочной среде необходимая щелочность среды обычно поддерживается добавлением соды и ацетата натрия.
Если азосочетанис необходимо вести в слабокислой среде, а азосоставляющая растворяется только в ще
лочной среде, то применяют так называемый обратный порядок сочетания. В этом случае раствор азосоставляющей, содержащий ацетат натрия или соду, приливают к кислому раствору диазососдинения; таким образом, в течение всего процесса обеспечивается необходимая кислотность среды.
В табл. 4.2.9 приведены практически значимые азокрасители, полученные при использовании анилина в качестве диазосоставляющей. Все эти красители получены при азосочетании хлорида бензолдиазония (39) с различными азосоставляющими (см. уравнения (4.2.42), (4.2.43)).
В табл. 4.2.10 приведены наиболее значимые азокрасители (125-127), полученные при азосочетании диазотированного анилина с производными 4-гидрокси-нафталин-2,7-дисульфокислоты (среда сочетания щелочная).
Таблица 4.2.9
Азокрасители, полученные при использовании анилина в качестве диазосоставляющей
Структурная формула красителя Название красителя: торговое, [химическое] Азосоставляющая (кислотность среды при азсочетании)
у>—N = N —N Н2 nhT N=N —N(CH3)2 —N = N —N(C2H5)2 Хризоидин, [(776); 3-амино-1-фенилазоанилин] Жирорастворимый желтый 2Ж, [(777); 4-фенилазо-А, А-диме-тиланилин] Жирорастворимый желтый Е, [(118); 4-фенилазо-А,А-диэтил-анилин] jw-Фенилендиамин (кислая среда) N, А-Диметиланилин (кислая среда) N, А-Диэтиланилин (кислая среда)
Ароматические соединения
641
Окончание табл. 4.2.9
Структурная формула красителя Название красителя: торговое, [химическое] Азосоставляющая (кислотность среды при азсочетании)
СН3 // \ /^N , , // \\ N=N / । zX \ / \ / OH 4=7 CH3 // \ /^N tv \ 7—N=N—G | f/ \ \_/ VN \ 4— SO3H OH HO\ ^-N=N— N=N— ho3s HO3S N=N— ^г^у^Ч^ОН H03S/k4x'^Xj^ n=n~/ HO3S /^^Чх^Х^ХзОзН Жирорастворимый желтый 3, [(119); 5-гидрокси-3-метил-1-фенил-4-фенилазопиразол] Кислотный желтый светопрочный, [(120)', 5-гидрокси-3-метил-1-(4-сульфофенил)-4-фенил-азопиразол] Жирорастворимый оранжевый, [(121); 2-гидрокси-1 -фенилазонафталин] Кислотный ярко-оранжевый Ж, [(122); 6-гидрокси-5-фенилазо-нафталин-2-сульфокислота] Кислотный оранжевый светопрочный, [(123); (7-гидроксинафталин-8-фенилазонафталин-1,3-дисульфокислота] Кислотный оранжевый Ж, [(124); (З-гидрокси-1-фенилазонафталин-2,7-дисульфо-кислота] З-Метил-1 -фенил-5-пи-разолон (щелочная среда) З-Метил-1 -(4-сульфо-фенил)-5-пиразолон (щелочная среда) 2-Г идроксинафталин (щелочная среда) 6-Гидроксинафталин-2-сульфокислота (щелочная среда) Г-кислота (7-гидроксинафталин-1,3-дисульфокислота) Р-кислота (З-гидроксинафталин-2,7-дисульфокислота)
Кислотные азокрасители на основе анилина и производных 4-гидроксинафт алин-2,7-дисульфокислоты
Таблица 4.2.10
R Название красителя Азосоставляющая
ОН NHCOCH3 nh2 Хромотроповый 2Р (125) Кислотный ярко-красный (126) Кислотный прочный фуксиновый 2Б (127) 4,5-Дигидроксинафталин-2,7-дисульфокислота 5-Ациламино-4-гидроксинафталин-2,7-дисульфокислота 5-Амино-4-гидроксинафталин-2,7-дисульфо-кислота
642
Новый справочник химика и технолога
Красители Прямой красный 4С (128) и Прямой ярко-оранжевый (129) являются первичными дисазокра-сителями. Их получают по схеме:
М->С^М',
где М и М' — моноамины (диазосоставляющие; они могут быть одинаковыми и разными), С — центральная азосоставляющая (сочетается больше одного раза). Для данных красителей и М и М' — это анилин.
Используя различные диазосоставляющие, можно варьировать цвет красителя, например, краситель Прямой алый (130).
В красителе Кислотном сине-черном (131) центральной азосоставляющей является Аш-кислота (5-ами-но-4-гидрокси нафтали н-2,7-дисульфокислота), которая сочетается дважды (цифры над азофуппами указывают последовательность проведения реакций азосочетания). Первой диазосоставляющей является и-нитроанилин, второй — анилин.
[анилин—>4,4'-дигидрокси-7,7'-динафтиламин-2,2'-дисульфокислота«— анилин] (129) (R = NHCONH)
[анилин—>7V, А'-бис(4-гидрокси-2-сул ьфонафтил-7)мочевина<— анилин]
[анилин—>А,А"-бис(4-гидрокси-2-сульфонафтил-7)мочевина«— и-аминоацетанилид]
(737)X = NO2;
[и-нитроанилин—> Аш-кислота*—анилин]
При восстановлении нитрогруппы в (131) сульфидом натрия образуется кислотный азокраситель Ацилан темно-зеленый Б [(732); X - NH2].
Красители Дисперсный оранжевый О (133) и Дисперсный оранжевый 4К (134) относятся к вторичным дисазокрасителям. Их получают по схеме:
М—>А—>К
где М — моноамин (диазосоставляющая), А — азосо-ставляющая-амин (применяется сначала как азосоставляющая, но после сочетания аминогруппа диазотируется и сочетается с новой азосоставляющей), К — конечная азосоставляющая (соединение, которое сочетается один раз).
СН3О
(755)
[анилин—> 1 -аминонафталин—>фенол]
(734)
[анилин—>2,5-диметоксианилин—>фенол]
Ароматические соединения
643
Красители, при получении которых анилин используется в качестве диазосоставляющей и азосоставляющей одновременно. Это вторичные дисазо-красители, которые также получают по схеме:
М—>А—>К
Однако в данном случае и М и А, т. е. и диазосоставляющая и азосоставляющая — амин, являются анилином.
При использовании анилина в качестве азосоставляющей аминогруппу предварительно защищают, что
бы избежать образования диазоаминосоединения. Обычно в таких случаях практикуется предварительная обработка анилина формальдегидом и гидросульфитом натрия, при этом получается А-фениламинометан-сульфокислота (135). А-Фениламинометансульфокис-лота сочетается с диазосоединением обычным образом, образуя азосоединение, после чего сульфометильную группу удаляют гидролизом в щелочной среде. Полученный 4-аминоазобензол (112) диазотируют обычным способом и сочетают с азосоставляющей.
C6H5NH2+ СН2О + NaHSO3 C6H5NHCH2SO3Na + Н2О
(/35)
(39) + (/35) -► C6H5-N=N-C6H4NHCH2SO3Na
C6H5-N=N-C6H5NH2 + СН2О + Na2SO3 (//2)
Продукт азосочетания диазотированного анилина с анилином выпускается под названием Дисперсный диазо-бордо [(//2); 4-аминоазобензол]. Красителем окрашивают химические волокна в водной суспензии, а затем на волокне диазотируют и сочетают с азосоставляющими, которые называют проявителями. В названии красителя указывается окраска, возникающая после проявления на волокне.
4-Аминоазобензол является полупродуктом для получения вторичных дисазокрасителей (136)-(140). В табл. 4.2.11 приведены практически значимые азокрасители, полученные сочетанием диазотированного 4-аминоазобензола с различными азосоставляющими.
(136)-{140)
(112)
Дисазокрасители, полученные на основе 4-аминоазобензола
Таблица 4.2.11
Аг (конечная азосоставляющая) Название красителя Диазо- и азокомпоненты (конечные)
—ОН Дисперсный желтый 7 (136) 4-Аминоазобензол —> фенол
zCH3 —ОН Дисперсный желтый прочный 4К (/37) 4-Аминоазобензол —> о-крезол
Жирорастворимый красный Ж (138) 4-Аминоазобензол —> 2-нафтол
^\Д^/ОН ^^A^^^CONH-fl \ Дисперсный красный 4 полиэфирный (139) 4-Аминоазобензол —> Азотол ОФ [3-гидрокси-2-(2-этокси-фенил)карбамоил-нафталин]
н5с2о/ HO3S /Ах/Ах^ОН г I т HOsS^^X^ Кислотный красный 2Ж (140) 4-Аминоазобензол—>7-гид-роксинафталин-1,3-дисульфо-кислота
644
Новый справочник химика и технолога
В качестве первой диазосоставляющей могут быть использованы различные амины, которые после диазотирования сочетают с анилином. Например, краситель Дисперсный оранжевый Ж {141} получают сочетанием с анилином диазотированного «-нитроанилина.
Азосоединение, содержащее первичную аминогруппу, можно вновь диазотировать и сочетать с новой азо
составляющей. Так получают красители Хромовый оранжевый {142} и Прямой красный светопрочный 2С {143}.
{141}
{142}
[сульфаниловая кислота—>анилин—>салициловая кислота]
[сульфаниловая кислота—>анилин—>7-бензоиламино-4-гидрокси-нафталин-2-сульфокислота]
Полиазокрасители. Это красители, в которых содержится три и более азогрупп. Чаще всего их получают на основе диаминов.
Красители {144}-{146} получены по схеме:
К«—Д—>С«—М, где Д — диамин, значения М, С, и К см. красители {128} и {134}. Цифры над азогруппами указывают на последовательность реакций сочетания, при необходимости указывается также среда сочетания.
{144} Прямой черный 3 (R^ = R2 = NH2, R3 = Н) [лг-феиилецдиамшк—бензидин—>Лш-кислота<—анилин]
{145} Прямой черный к (Rj = R2 = NH2, R3 = CH3) [л/-толуилендаамин«—бензидин—>Аш-кислота«—анилин] {146} Прямой темно-зеленый (Ri = R3 NH2, R2= ОН) [2,5-диаминофенол«—бензидин—>Аш-кислота«—анилин]
Азокрасители с триазиновым кольцом
Краситель Прямой зеленый светопрочный {147} получают, последовательно вводя в реакцию с цианур-хлоридом (7) синий дисазокраситель [Аш-кислота—> —жрезидин—>Аш-кислота], (2) желтый моноазокраситель [«-нитроанилин—«-салициловая кислота; восстановление нитрогруппы] и {3} анилин.
Краситель Прямой ярко-зеленый светопрочный 4Ж {148} получают, последовательно вводя в реакцию с цианурхлоридом (7) голубой антрахиноновый краситель (1 -амино-4-(4-амино-2-сульфофенил)аминоантра-хинон-2-сульфокислота), (2) желтый моноазокраситель и {3} анилин.
Антрахиноновые красители
Практически значимые антрахиноновые красители {{149}-(753)], полученные с использованием анилина как одного из основных полупродуктов, приведены в табл. 4.1.12.
{149}-{153}
Ароматические соединения
645
(/45)
Таблица 4.2.12
Антрахиноновые красители
R R1 R2 Название красителя: торговое, [химическое] Способ синтеза
ОН Н H Дисперсный фиолетовый, [(149); 1-гидрокси-4-фениламино-антрахинон] Взаимодействие анилина с Хи-низарином
NHCH3 Н H Дисперсный голубой, [(/50); 1-метиламино-4-фенил-аминоантрахинон] Взаимодействие анилина с 4-бром-1-метил-амино-антрахиноном
nh2 so3H Н Кислотный чисто-голубой антрахиноновый 3, [(151); 1-амино-4-фениламино-антрахинон-2-сульфокислота] Взаимодействие 1 -амино-4-бромантрахинон-2-сульфо-кислоты с водно-щелочным раствором анилина
nh2 ОСиН2и+] («= 104-12) SO3H Кислотный фиолетовый антрахиноновый НК, [(152); 1-амино-2-алкокси-4-(4-сульфофениламино)антрахинон] Замена сульфогруппы в (151) смесью высших спиртов С10-С|2 с последующим сульфированием соединения
он SO3H Хромовый сине-черный антрахиноновый С, [(153); 1-гидрокси-2,4-ди(4-сульфо-фениламино)-антрахинон] Взаимодействие анилина с Пурпурином и последующее сульфирование соединения
Триарилметановые красители
Окислением смеси анилина, о- и «-толуидинов нитробензолом получают смесь красителей красного цвета, выпускаемую под названием «Фуксин» [(/54)-(/57)].
Простейшим из этих красителей является Парарозанилин {154). Остальные соединения являются его метильными гомологами.
646
Новый справочник химика и технолога
полиэфирных волокон Дисперсный желтый ПЭ [(158);
А-фенил-З-нитро-4-фениламинобензолсульфамид].
(755)
(154) R = R' = R" = Н; (155) R = СН3, R' = R" = Н;
(156) R = R' = СН3, R" = Н; (157) R = R' = R" = СН3;
Hump о красит ели
При взаимодействии анилина с З-нитро-4-хлор-бензол-1-сульфонилхлоридом получают краситель для
Красители на основе полупродуктов, полученных из анилина
На схеме 4.2.3 представлены промежуточные продукты, которые получаются на основе анилина и используются в дальнейшем для синтеза красителей. В табл. 4.2.13 приведены названия соединений, синтез и области применения.
Схема 4.2.3
Таблица 4.2.13
Полупродукты, полученные на основе анилина и используемые для синтеза красителей
Название соединения Метод получения Применение
Дифениламин (9) Жидкофазная конденсация анилина в присутствии катализатора 1. Азокрасители (Кислотный желтый метаниловый, Дисперсный оранжевый К); 2. Стабилизатор пластмасс и порохов
Ароматические соединения
647
Продолжение табл. 4.2.13
Название соединения Метод получения Применение
А,А-Диметил-апилин (20) А,А-Диэтил-анилин (23) А-Этил-А-бензиланилин (27) Алкилирование анилина метиловым спиртом Алкилирование анилина этиловым спиртом Взаимодействие А-этиланилина с бензилхлоридом 1. Красители: арилметановые (Малахитовый зеленый, Основной бирюзовый, Основной фиолетовый, Основной синий К, Кислотный фиол. С, Аурамин); ариламиновые (Зеленый Биндшедлера, а-Нафтоловый синий); тиазиновые (Метиленовый голубой); диазиновые (Толуиленовый красный); сернистые (Серный чисто-голубой К); азокрасныйи-тели (Метиловый оранжевый, Жирный желтый 2Ж, Катионовый красный С, Катионовый фиолетовый 2С); 2. ВВ (тетрил); 3. Проявитель для цветной фотографии 1. Красители: триарилметановые (Кислотный зеленый Ж, Кислотный ярко-голубой 3, Основной фиолетовый С, Основной ярко-зеленый); оксазиновые (Катионовый бирюзовый 23); азокрасители (Катионовый красный 2С); 2. Лекарственные вещества (акрихин) Красители: триарилметановые (Кислотный зеленый, Кислотный зеленый для кожи, Кислотный ярко-синий, Кислотный фиолетовый С)
Фениламино-уксусная кислота (28) Взаимодействие анилина с монохлоруксусной кислотой Красители: индигоидные (Индиго, Индигокармин, Бро-миндиго)
А,А-Ди-(2-гидрокси-этил)анилин (33) Взаимодействие анилина с этилен-оксидом Азокрасители (Дисперсный фиолетовый 4К)
Сульфаниловая кислота(44) Нагревание бисульфата анилина при 180-190 °C 1. Красители: азокрасители (Метиловый оранжевый, Хромовый желтый К, Хромовый оранжевый, Хромовый ярко-красный 2С, Кислотный оранжевый, Кислотный светло-коричневый для кожи, Кислотный коричневый 2К для кожи, Кислотный сине-черный, Прямой красный светлый 2С, Прямой коричневый ЖХ, Лак оранжевый); антрахиноновые (Хромовый сине-черный антрахиноновый С); 2. Лекарственные вещества (см. табл. 4.2.16)
л-Нитроанилин (47) Нитрование ацетанилида нитрующей смесью с последующим разделением изомеров и гидролизом 1. Красители: азокрасители (Дисперсный оранжевый, Дисперсный алый Ж, Дисперсный рубин, Кислотный синечерный, Кислотный коричневый К для кожи, Прямой зеленый ЖХ, Пигментный красный Ж, Азоамин черный К). 2. я-Фенилендиамин (Черный для меха Д) 3. Стабилизатор газолина, ингибитор коррозии
Хинальдин [2-метилхинолин (59)] Взаимодействие анилина с ацетальдегидом в среде H2SO4 1. Красители: полиметиновые (Псевдоцианин, Пинациа-нол), хинофталоновые
Лепидин [4-метилхинолин ОТ] Взаимодействие анилина с винилметилкетоном 1. Красители: полиметиновые (Криптоцианин, Хеноциа-нин)
А-Этил-А-(2-гидроксиэтил)-анилин (159) Взаимодействие А-этиланилина с этиленхлор-гидрином Азокрасители (Дисперсный алый Ж, Дисперсный бордо С, Дисперсный красно-коричневый, Катионный синий О)
648
Новый справочник химика и технолога
Окончание табл. 4.2.13
Название соединения Метод получения Применение
А-Этил-А-(2-цианоэтил)-анилин (160) Взаимодействие А-этилани-лина с акрилонитрилом Азокрасители (Дисперсный оранжевый, Дисперсный рубиновый 1, Дисперсный красный полиэфирный)
2-Мер капто-4-хлоранилин (161) Взаимодействие анилина с S2C12 с последующим гидролизом Тиоиндиго иды (Тиоиндиго розовый 2С)
4-Амино-дифениламин-2-сульфокислота (/62) Конденсация анилина с 3 -нитро-5 -хлорбензолсульфо-кислотой с последующим восстановлением нитрогруппы Оксазиновые (Прямой ярко-голубой светлый), азиновые, азокрасныйители, нитрокрасныйители
А-Фенил-пери-кислота [(/63); 8-фениламино-нафталинсуль-фокислота] Взаимодействие анилина с 8-аминонафталинсульфокислотой Азокрасители (Кислотный синий 2К, Кислотный темно-синий, Кислотный черный С)
А-Фенил-И-кислота [(/64); 4-гидрокси-7-фениламино-нафталин-2-сульфокислота] Взаимодействие анилина с 4-гидрокси-7-аминонаф-талин-2-сульфокислотой Азокрасители (Прямой фиолетовый С, Прямой синий светопрочный, Прямой синий светопрочный ЗУ, Прямой синий светопрочный 23М, Прямой голубой светопрочный)
А-Фенил-Г амма-кислота [(/65); 4-гидрокси-6-фениламино-нафталин-2-сульфокислота] Взаимодействие анилина с 4-гидрокси-6-аминонаф-талин-2-сульфокислотой Азокрасители (Кислотный коричневый К, Кислотный коричневый Ж для кожи, Кислотный коричневый МШ, Кислотный черный 2С)
Фенилгидразин (/66) Восстановление хлорида бензолдиазония гидро сульфатом натрия в щелочной среде 1.2-Метилиндол (красители: Катионный желтый 43, Катионный оранжевый Ж, Катионный оранжевый К, Катионный красно-фиолетовый, Катионный розовый 2С); 2. З-Метил-1-фенилпиразолон-5 (азокрасители: Жирорастворимый желтый 3, Кислотный желтый светлый, Спирторастворимый бордо). Лекарственные вещества
4.2.5.4. Пестициды
Практически значимых пестицидов, получаемых с использованием анилина как промежуточного продукта, немного. Тем не менее, производство пестицидов потребляет ~4 % производимого анилина. Ниже показано, какие группы пестицидов получают на основе анилина.
Пестициды
(на основе анилина)
Г ербициды
Фунгициды Дефолианты (системные)
Гербициды
В качестве гербицидов широко применяются анилиды хлоруксусной кислоты (в основном замещенные), производные мочевины, алкиловые эфиры ^арил-карбаминовых кислот. В каждой из этих групп гербицидов есть производные анилина. В табл. 4.1.14 приведены практически значимые гербициды, полученные на основе анилина.
Фунгициды
Анилиды некоторых ароматических и гетероарома-тических кислот используются в качестве системных фунгицидов. Их получают взаимодействием анилина с хлорангидридами соответствующих кислот. В табл. 4.1.15 приведены структурные формулы, названия и
Ароматические соединения
649
(/55)
способ синтеза практически значимых фунгицидов, 2-меркаптобензотиазола [(/7); см. стр. 23] с бутилхло-полученных с использованием анилина. ридом в присутствии гидроксида натрия.
Из этих соединений наибольшей фунгицидной активностью обладает витавакс.
Дефолианты
Дефолиантом является бутилкаптакс [(/55); 2-бу-тилтиобензотиазол]. Получают его взаимодействием
Таблица 4.1.14
Гербициды, полученные на основе анилина
Структурная формула Название: торговое, [химическое] Способ синтеза
/=\ /COCHjCI Y_/N4CH(CH3)2 Пропахлор (рамрод), [(/67); А-изопропил-А (фенил)хлорацетамид] А-Алкилирование анилина 2-пропилхлоридом с последующим ацилированием хлораце-тилхлоридом
/СОСН2С1 \\ /)— N< \/ ХСН(СН3)СЕСН Принахлор, [(/65); А-бутин-З-ил-2-А-(фенил)хлорацетамид] А-Алкилирование анилина с последующим ацилированием А-алкильного производного хлорацетилхлоридом
NHCON(C Н3)2 Фенурон (фенидим), [(/69); А,А-диметил-А-фенил-мочевина] Взаимодействие фенилизоцианата (19) с диметиламином
\-NHCONH(CH3)2 ссьсоо- Фенурон-трихлор-ацетат (ураб), [(/ 70); А, А-диметил-А'-фенилмочеви-на, трихлорацетат] Взаимодействие фенурона с трихлоруксусной кислотой
^—NHCON Н— СН3 Сидурон (туперсан), [(171); А-(2-метилциклогексил- А-фенилмочевина] Взаимодействие фенилизоцианата с 2-метилциклогексил-амином
СН3 NHCO— Роутат, [(172); 2,5-диметил-1-(А-фенил)-карбамоил)пирролидин] Взаимодействие фенилизоцианата с пирролидином
СН3
N Н-СООСН(С Н3)2 Профам (ИФК), [(173); изопропил-А-фенилкарбамат] Взаимодействие фенилизоцианата с изопропанолом
NH-<OOCHCONHC2H5 '—' (^Н3 Карбетамид (карбетамекс, легурам), [(174); 2-(А-(фенилкарбамоилокси)-А'-этилпропионамид] Взаимодействие фенилизоцианата с 2-гидрокси-А-этил-пропионамидом
H2N-^ so2nhcooch3 Азулам, [(/75); А-(4-аминофенилсульфонил)-Ометилкарбамат] Взаимодействие натриевого производного сульфаниламида с метилхлоркарбонатом
650
Новый справочник химика и технолога
Фунгициды, полученные с использованием анилина
Таблица 4.2.15
Структурная формула Название: торговое, [химическое] Способ синтеза
^\.СН3 [ |Г /=\ Мебенил, [(776); анилид о-толуиловой кислоты] Взаимодействие анилина с хлоран-гидридом о-толуиловой кислоты
^x^CONH—d /°х/СН3 Пиракарболит(сикарол), Взаимодействие анилина с хлор-
II /=\ ^X^CONH—d /°\/снз [(777); анилид 5,6-дигидро-2-метил-пиран-3-карбоновой кислоты] Витавакс (карбоксин), ангидридом 5,6-дигидро-2-метилниран-3-карбоновой кислоты Взаимодействие бисф-гидрокси-
ГТ /=\ X^cONH-h' Л /(к/СН3 [(178); 2,3-дигидро-6-метил-5-фенилкарбомоил-1,4-оксатиин] Плантвакс, этил)дисульфида с анилидом ацетоуксусной кислоты с последующей циклизацией Окисление витавакса пероксидом
Г Т /=\ [(779); оксид витавакса] водорода
Sof^CONH-Z \ zCONH—/ \ < >— Спз о zCON Н—(^ СНз-Л СНз О H2N—SCN Фенфурам (панорам), [(180); анилид 2-метилфуран-З-карбоновой кислоты] Фуркарбанил(бенодил), [(181); анилид 2,5-диметилфуран-З-карбоновой кислоты] Родан, [(182); 4-тиоцианатоанилин] Конденсация анилида ацетоуксусной кислоты с ацетоксипропионовым альдегидом в присутствии H2SO4 То же Взаимодействие анилина с хлором и тиоцианатом аммония в метаноле
/^\zN=NSO3Na (ch3)2n/L4/ Дексон, [(183); 4-(А,А-диметиламино)фенил-ди-азосульфонат натрия] Диазотирование А,А-ди-мстил-и-фе-нилсндиамина и взаимодействие с NaHSO3
/С1 o2n-Z nh2 ДХНА (дихлоран, ботран), [(184); 2,6-дихлор-4-нитроанилин] Прямое хлорирование 4-нитро-анилина хлором
4.2.5.5. Лекарственные вещества
Практически важные лекарственные вещества, получаемые на основе анилина, можно разделить на три группы.
Анилин
Производные пиразолина (обезболивающие,
жаропонижающие)
Производные
сульфониламида (антимикробные)
Производные фенотиазина (нейролептические)
Производные пиразолина
Анилин является основой для получения противовоспалительных и обезболивающих лекарственных веществ, относящихся к производным пиразолина. Это антипирин [(186); феназон], амидопирин [(188); пирамидон] и анальгин {190}.
Синтез соединений проводят следующим образом. Анилин переводят в диазосоединение (39), которое восстанавливают смесью сульфита и гидросульфита натрия, при этом получается фенилгидразин (166). При
Ароматические соединения
651
конденсации фенилгидразина с ацетоуксусным эфиром образуется 3-метил-1-фснилпиразолон-5, алкилированием (метилированием) которого иодистым метилом (или метилбензолсульфонатом) получают антипирин [(756); 2,3-диметил-1-фенилпиразолон-5].
Антипирин нитрозируют, нитрозогруппу восстанавливают гидросульфитом натрия до аминогруппы, получая аминопроизводное [(/£7); 4-амино-2,3-диметил-1-фенилпиразолин-5-он], которое метилируют в системе формальдсгид/муравьиная кислота (метод Лейкарта—
Валлаха), при этом получается амидопирин [(755); 2,3-диметил-4-диметиламино-1-фенилпиразолин-5-он].
Для получения анальгина [(790); 2,3-диметил-4-(А-метил-А-сульфонатометиламино)-1 -фенилпиразолин-5-он натриевая соль] промежуточное аминосоединение {187} метилируют диметилсульфатом до А-моноамино-производного (759), в которое действием смеси формальдегида с гидросульфитом натрия вводят метилсульфонатную группу.
1. NaNO2, HCJ
2 NaHSO3, H f
{166)
1. СН3СОСН2СООС2Н5
2 СН31 (СбН58О2ОСН3)
Производные сульфаниламида
Анилин является промежуточным продуктом для получения большой группы антимикробных лекарственных препаратов. Простейшим представителем этого
класса соединений является белый стрептоцид [(792); сульфаниламид; и-аминобензолсульфонамид]. Получают стрептоцид по схеме 4.2.4:
1. СН3СООН
2. HOSO2C1
(797) (792)
Схема 4.2.4
Анилин переводят в ацетанилид для защиты аминогруппы от окисления. Действуя на ацетанилид (36) хлорсульфоновой кислотой, получают ц-ацетамино-бензолсульфонхлорид (191). При обработке соединения (191) аммиаком замещают хлор на аминогруппу и гидролизом снимают ацильную защиту.
ц-Ацетаминобензолсульфонхлорид (191) является
общим полупродуктом для получения группы лекарственных соединений [(193)-(208), табл. 4.2.16].
h2n
so2nh-r
(193)-(208)
652
Новый справочник химика и технолога
Сульфаниламидные лекарственные соединения
Таблица 4.2.16
R Название: торговое, [химическое] Способ синтеза
^NH -C^nh2 -C\NH2 N^/CH3 /^/СНз N^° CH3 ~VN s-^c2H5 к zOCH3 /ГЛ N N sx \\ /) N—" N=\ N—" N=/CH3 42# N—< \CH3 /ОСН3 N=/ ZOCH3 N=Z "A /N %CH3 Сульгин, [(/93); и-аминобензолсульфонилгуанидин] Уросульфан, [(194); и-аминобензолсульфонилмочевина] Норсульфазол, [(195); 2-(и-аминобензолсульфонами-до)тиазол] Сульфазол, [(196); 2-(я-аминобензолсульфонамидо)-4-метилтиазол] Сульфаметоксазол, [(197); З-(я-аминобензолсульфонамидо)- 5-метилизоксазол] Сульфафуразол, [(198); 5-(и-аминобснзолсульфонамидо)-3,4-диметилизоксазол] Этазол, [(199); 2-(и-аминобензолсульфонамидо)-5-этил-1,3,4-тиадиазол] Сульфаметрол, [(200); 3-(и-аминобензолсульфонамидо)-4-метокси-1,2,5-тиадиазол] Сульфидин, [(201); 2-(и-аминобензолсульфонамидо-пиридин] Сульфазин, [(202); 2-(и-аминобензолсульфон-амидо)ниримидин] Сульфадимезин, [(203); 2-(и-аминобензолсульфонамидо)-4,6-диметилпиримидин] Сульфамонометоксин, [(204); 4-(и-аминобензолсульфонамидо)-2-метоксипиримидин] Сульфадиметоксин, [(205); 4-(и-аминобензолсульфонамидо)-2,6-диметоксипиримидин] Взаимодействие сульфонхлорида (191) с гуанидином в присутствии карбоната натрия Взаимодействие сульфаниламида с мочевиной в присутствии карбоната натрия Взаимодействие сульфонхлорида (191) с 2-аминотиазолом с последующим гидролизом ацильной группы Взаимодействие сульфонхлорида (191) с 2-амино-4-метилтиазолом с последующим гидролизом ацильной группы Взаимодействие сульфонхлорида (191) с З-амино-6-метилизооксазолом с последующим гидролизом ацильной группы Взаимодействие сульфонхлорида (191) с 5-амино-3,4-диметилизооксазолом с последующим гидролизом ацильной группы Взаимодействие сульфонхлорида (191) с 2-амино-5-этил-1,3,4-тиадиазолом с последующим гидролизом ацильной группы Взаимодействие сульфонхлорида (/9/) с З-амино-4-метокси-1,2,5-тиадиазолом с последующим гидролизом ацильной группы Взаимодействие сульфонхлорида (191) с 2-аминопиридином с последующим гидролизом ацильной группы Взаимодействие сульфонхлорида (191) с 2-аминопиримидином с последующим гидролизом ацильной группы Взаимодействие сульфонхлорида (191) с 2-амино-4,6-диметилпиримидином с последующим гидролизом ацильной группы Взаимодействие сульфонхлорида (191) с 4-амино-2-метоксипиримидином с последующим гидролизом ацильной группы Взаимодействие сульфонхлорида (191) с 4-амино-2,6-диметоксипиримидином с последующим гидролизом ацильной группы
Ароматические соединения
653
Окончание табл. 4.2.16
R Название: торговое, [химическое] Способ синтеза
^-°СН3 N-N Н3СОЧ N—/ ^>0 ~c\nhc4h9 Сульфапиридазин, [(206); 6-(л-аминобензолсульфонамидо)-3-метоксипиридазин] Сульфален, [(207); 2-(и-аминобензолсульфонамидо)-3-метоксипиразин] Букарбан, [(208); А-(и-аминобензолсульфонил)- N'-h-6yiил мочевина] (противодиабетическое средство) Взаимодействие сульфонхлорида (191) с З-амино-6-метоксипиридазином с последующим гидролизом ацильной группы Взаимодействие сульфонхлорида (191) с 2-амино-З-метоксипиразином с последующим гидролизом ацильной группы Взаимодействие сульфаниламида с мочевиной в присутствии карбоната натрия
Производные фенотиазина
Анилин является промежуточным продуктом при получении лекарственных препаратов [(209)-(217), табл. 4.2.17] группы фенотиазина (14).
(14) R1 = R2 = Н
Таблица 4.2.17
Лекарственные соединения группы фенотизина
R' R2 Название: торговое, [химическое]
Н -(СНгШСНзЬ • НС1 Пропазин, [(209); А-(3-диметиламинопропил)-фенотиазина гидрохлорид]
CI -(CH2)3N(CH3)2 • HC1 Аминазин, [(210); А-(3-диметиламинопропил)-2-хлор-фенотиазина гидрохлорид]
Н -СН2СН(СНз)^(СНз)2 Дипрозин, [(211); А-(2-диметиламинопропил)-фенотиазин] — антигистаминное действие
Н -СН2СН(СНз)СН2Ы(СНз)2 • C4H6O6 Алимемазин, (212); [А-(3-диметиламино-2-метилпропил)-фенотиазина гидротартрат]
ОСН3 -СН2СН(СНз)СН2Ы(СНз)2 • HC1 Левомепразин, [(213); А-(3-диметиламино-2-метилпропил)-2-метоксифенотиазина гидрохлорид]
С1 -CH2CH2CH2-N^ \-CH3 • 2C4H4O4 Метеразин, [(214); А-(3-(4-метилпиперазинил-1)-пропил)-2-хлорфенотиазина дималеат]
CF3 -СН2СН2СН2-т/ CH3* 2HC1 Трифтазин, [(215); А-(3-(4-метилпиперазинил-1)-пропил)-2-(трифторметил)-фенотиазина дигидрохлорид]
CF3 -(СН2)3-т/ \-CH2CH2OH-2HC1 Фторфеназин, [(216); А-(3-(4-([3-гидроксиэтил)пиперазинил-1 )пропил)-2-(трифторметил)-фенотиазина дигидрохлорид]
Cl -(CH2)3- >/ CH2CH2OH*2HCI Этаперазин, [(217); А-(3-(4-([3-гидроксиэтил)пиперазинил-1 )пропил)-2-хлорфенотиазина дигидрохлорид]
654
Новый справочник химика и технолога
Незамещенный фенотиазин (74) получают при нагревании смеси анилина, гидрохлорида анилина и серы (см. подраздел 4.2.4.1). N-Алкилированием фенотиазинового ядра хлоралкиламинами в присутствии щелочных агентов получают соединения, не содержащие заместители в бензольных фрагментах фенотиазинового цикла: пропазин (209), дипрозин (217), алимемазин (212).
При синтезе фенотиазинов, содержащих заместители в бензольных кольцах [Аминазин (210), Левомепра-зин (213) и др.], главными реакциями являются А-арилирование анилина и последующая гетероциклизация замещенного дифениламина.
4.2.6. Методы анализа анилина
Основным методом анализа анилина, позволяющим определить содержание различных примесей в анализируемом продукте, является метод газожидкостной хроматографии.
Для проведения анализа пригоден любой прибор, имеющий систему программирования температуры, например «Цвет 100». Для анализа используется колонка длиной 2 м и диаметром 2 мм. Температура колонки, 120-220 °C (скорость подъема температуры 4 град/мин). Температура испарителя 300 °C. Газом-носителем служит азот, расход которого составляет 20 мл/мин. Объем анализируемой пробы 0,3 мкл.
В техническом анилине присутствуют вещества, относящиеся к различным классам органических соединений и обладающие разной летучестью, поэтому основной и наиболее ответственной операцией в выборе оптимальных условий разделения является подбор неподвижной фазы. Эта фаза, наряду с высокой селективностью, должна обладать еще и высокой термостойкостью, т. к. для хроматографирования аминофенолов и многоядерных аминов требуется высокая температура. Этим требованиям удовлетворяет лишь очень ограниченное число неподвижных фаз (полиэтиленгликоль-сукцинат, нитрилсилоксаны, полифениловый эфир). Однако при испытании они не дали положительных результатов.
Полного разделения всех примесей в анилине и их отделения от основного компонента удалось добиться только при использовании в качестве неподвижной фазы полимера группы карборансилоксанов — карборансилоксанового эластомера КБС-2. Было обнаружено, что в различных партиях анилина-сырца, полученного газофазным восстановлением нитробензола, содержатся примеси бензола, толуола, циклогексана, циклогек-силамина, А-фенилциклогексиламина, толуидинов, нитробензола, 3,4-ксилидина, лг-фенилендиамина, дифенила, дифениламина, азобензола, «-нитроанилина, карбазола. Содержание всех неидентифицируемых примесей в анилине составляет менее 0,05 %. В товарном анилине примеси отсутствуют.
Хроматографические методы определения анилина в виде его производных нашли меньшее распространение. В ряде случаев для определения содержания ани
лина в смесях применяют спектрофотометрические методы, основанные на измерении светопоглощения в видимой или УФ-области спектра.
Несмотря на то, что применение физических методов позволило повысить точность анализа и ускорить его выполнение, до настоящего времени широко применяются классические потенциометрические методы, основанные на титровании анилина в виде кислого водного раствора смесью бромата и бромида калия с образованием триброманилина или нитритом натрия с образованием диазобензола. Находит применение также кулонометрическое титрование анилина.
Определение нитробензола в анилине обычно осуществляют полярографическим методом. Этот метод более чувствителен, чем газохроматографический при определении именно этой примеси. Полярографический метод определения содержания нитробензола в анилине вошел во все действующие стандарты на анилин.
Анализ содержания анилина в атмосфере производственных помещений обычно проводят, пропуская воздух через растворы соляной кислоты. Затем определяют содержание солянокислого анилина в растворе потенциометрическим или кулонометрическим методом.
Гораздо менее трудоемким является способ, основанный на пропускании проб воздуха через индикаторную трубку, заполненную смесью пероксодисульфата (персульфата) калия и комплексного нитрата церия, нанесенного на фарфоровый порошок. Концентрацию паров анилина определяют по длине слоя индикаторной массы, изменившей свою окраску после пропускания пробы воздуха. На этом принципе основаны пассивные дозиметры анилина, устанавливаемые в производственных помещениях.
4.2.7. Техника безопасности и охрана труда в производстве анилина
4.2.7.7. Токсические свойства анилина и защита от отравления
Анилин является высокотоксичным веществом. Отравления им возможны как при вдыхании паров, так и при попадании жидкого анилина на кожу. Высокие температура и влажность усиливают его токсическое действие, вызывая изменения в крови. Одновременно нарушаются функции всех органов и центральной нервной системы. При приеме алкоголя отравление анилином усиливается.
Токсическое действие анилина на человека в легких случаях проявляется в посинении губ и ногтей, небольшой слабости, головной боли, головокружении и потере аппетита. При отравлениях средней тяжести, кроме того, наблюдаются тошнота, иногда рвота, учащается пульс, возможно повышение кровяного давления. В более тяжелых случаях — учащенное дыхание, подергивания и судороги, общее возбуждение, падение температуры, нарушение сознания, расширение зрач
Ароматические соединения
655
ков. Нарушения центральной нервной системы и расстройство желудочно-кишечного тракта сохраняются в течение долгого времени после отравления.
Хронические отравления анилином даже при малых ежедневных дозах могут приводить к расстройствам пищеварения, общей слабости, неврозам.
Минимально ощутимая по запаху концентрация анилина в воздухе для наиболее чувствительных лиц равна 0,37 мг/м3. Максимально разовая предельно допустимая концентрация анилина в атмосферном воздухе населенных мест составляет 0, 05 мг/м3, а среднесуточная предельно допустимая концентрация — 0,03 мг/м3.
Адсорбция паров анилина через дыхательные пути составляет 5-11 мг/ч. Жидкий анилин всасывается в кожу со скоростью 0,2-0,7 мг/(см2 • ч). Считается, что в условиях производства 60-70 % анилина проникает в организм через кожу. Поэтому необходимо строгое соблюдение мер личной гигиены. В производстве анилина должна быть организована ежедневная обязательная стирка спецодежды и нательного белья. В цехе должен храниться комплект чистой спецодежды и белья на всю смену работающих. Рядом с рабочими местами рекомендуется установка кабины аварийного душа.
Для защиты органов дыхания в производстве анилина применяется фильтрующий промышленный противогаз марки А, для защиты кожи — спецодежда, белье, защитные перчатки и герметичные очки. При работе внутри аппаратов необходимы гидрокостюм и шланговый или изолирующий противогаз. Загрязненные анилином спецодежду, обувь и перчатки необходимо сразу же снять. При попадании анилина на кожу его необходимо смывать вначале слабой (пищевой) уксусной кислотой, а затем водой с мылом.
Токсичным веществом в производстве анилина является нитробензол, представляющий значительную опасность из-за своего наркотического действия. Нитробензол имеет сильный специфический запах, напоминающий запах миндаля. Порог восприятия запаха около 0,01 мг/л. Токсические концентрации и дозы для нитробензола очень малы.
Нитробензол является кроветворным ядом, тем не менее его токсическое действие во многом сходно с действием анилина, т. к. в организме нитробензол восстанавливается в анилин через промежуточное образование нитрозобензола и фенилгидроксиламина.
Производственные отравления нитробензолом выражаются обычно в легкой анемии, желтизне белков. Возможны внезапные обострения, особенно при попадании в организм несколько больших доз. В более тяжелых случаях появляются изменения в крови. Даже при самых легких отравлениях наблюдаются усталость, головные боли, отсутствие аппетита, реже тошнота, заболевания кожи.
Во всех случаях отравления нитробензолом следует немедленно обратиться к врачу. В первые часы после отравления пострадавшему необходимы покой и тепло
(грелка). Нельзя давать ему молоко и жиры, т. к. нитробензол хорошо растворим в них.
Индивидуальная защита такая же, как для анилина. Особое внимание следует обратить на применение двойных резиновых перчаток, фартуков, нарукавников, резиновых сапог.
В производстве анилина из фенола основными токсичными веществами кроме анилина являются фенол и аммиак.
Фенол — сильный нервный яд, вызывающий общее отравление организма; на кожу действует обжигающе. Острые отравления происходят главным образом при попадании фенола на кожу. Тяжесть их зависит от степени поражения кожи и быстроты оказания первой помощи. При попадании фенола на кожу необходимо немедленно удалить пострадавшего с рабочего места (даже при кажущемся хорошем его состоянии), сменить одежду и вымыть все тело водой с мылом. Рекомендуется обтирание пораженных мест 10-40% этанолом или растительным маслом. Индивидуальные средства защиты такие же, как для анилина.
Аммиак оказывает сильное раздражающее действие на верхние дыхательные пути, вызывает раздражение роговицы глаз, действует на кровь. Высокие концентрации аммиака приводят к обильному слезотечению и боли в глазах, удушью, сильным приступам кашля, головокружению, болям в желудке, рвоте. Порог восприятия запаха 5 • 10 4 мг/л. Индивидуальные средства защиты — промышленный противогаз марки КД, защитные очки, перчатки, спецодежда из плотной ткани.
4.2.7.2. Охрана труда в производстве анилина
Оздоровление условий труда в производстве анилина достигается за счет исключения контакта работающих с указанными вредными веществами и предотвращения их проникания в атмосферу рабочих помещений. Это достигается путем герметизации оборудования и коммуникаций, комплексной автоматизации и механизации технологического процесса, расположения аппаратов на открытых площадках и очистки отходящих газов перед выводом их в атмосферу. Чтобы исключить загазованность производственных помещений парами анилина, нитробензола и других токсичных веществ, устанавливают вентиляционные системы с соответствующей кратностью воздухообмена, а также принимают меры предосторожности против переполнения емкостей и хранилищ путем установки уровнемеров с сигнальными устройствами (при заполнении хранилища подается звуковой и световой сигналы). Ректификационные колонны должны иметь емкости аварийного опорожнения.
Современное производство анилина полностью автоматизировано. Центральный пульт, с которого осуществляется управление производством, отделен от технологического оборудования.
Главными источниками поступления в атмосферу токсичных паров являются газы, выделяющиеся при
656
Новый справочник химика и технолога
заполнении анилином и нитробензолом цистерн и хранилищ, а также выхлопные газы вакуум-насосов. Все выделяющиеся газы направляют на стадию угольной адсорбции. Кубовые остатки, образующиеся при дистилляции анилина, направляют на сжигание.
Анилин является горючей жидкостью. Минимальное содержание кислорода в воздухе, необходимое для поддержания диффузионного горения, составляет 13,8 об. %. Анилин необходимо гасить водой со смачивателями, распыленной водой или воздушно-механической пеной с кратностью 90-100.
Кубовые остатки, образующиеся при дистилляции анилина и нагретые выше 180 °C, пирофорны, поэтому снятие вакуума на колоннах дистилляции необходимо осуществлять, подавая в куб азот или другой инертный газ.
Расплав солей, применяемый в производстве анилина в качестве теплоносителя в контактных аппаратах и представляющий собой смесь нитритов и нитратов калия и натрия, в некоторых случаях может явиться источником возгорания. При контакте расплава, нагретого до 450 °C, с органическими веществами последние могут воспламениться. Поэтому особое внимание необходимо обращать на обеспечение герметичности аппаратов, в которых находится расплав, и коммуникаций, по которым его транспортируют.
Производство анилина восстановлением нитробензола водородом является взрывопожароопасным и относится действующими строительными нормами к категории А. Это определяется пожароопасностью водорода. Для обеспечения безопасной работы в помещениях, где возможно выделение водорода, устанавливают датчики автоматических газоанализаторов, которые отключают подачу электроэнергии и дают аварийный сигнал при превышении допустимой концентрации водорода в воздухе. В цехе имеется и система релейной защиты, предупреждающая возможность одновременного включения газодувки водорода и воздуходувки.
4.2.8. Перспективы развития производства анилина
В настоящее время мировое производство анилина продолжает расти, и пристальное внимание химиков направлено на улучшение технико-экономических показателей этого производства.
Основными промышленными методами получения анилина являются газофазное гидрирование нитробензола и газофазный аммонолиз фенола. В табл. 4.2.18 приведены экономические показатели производства анилина этими способами по сравнению с первым непрерывным промышленным методом получения анилина путем восстановления нитробензола чугунной стружкой.
Сравнение экономических данных показывает, что основные расходы приходятся на сырье. Следовательно, мероприятия, направленные на снижение затрат сырья, могли бы дать наибольший экономический эф
фект. к подобным мероприятиям в первую очередь относятся поиски селективных катализаторов с целью увеличения степени конверсии продукта. Поскольку в настоящее время выход анилина по стадии контактирования доведен до 99 %, этот путь практически исчерпал себя.
Важным резервом повышения выхода анилина является борьба с его потерями на стадии дистилляции. Перегонка анилина при более низкой температуре, которая достигается понижением давления в дистилляторе, позволяет уменьшить осмоление анилина и, соответственно, снизить его потери.
Таблица 4.2.18
Сравнительные экономические показатели производства анилина
Статья расхода Восстановление нитробензола чугунной стружкой Восстановление нитробензола водородом Аммонолиз фенола
Стоимость 84,9 70,9 66,9
сырья
Стоимость 2,6 2,1 4,2
энергии
Остальные 12,5 12,3 Н,7
расходы
Всего, % 100 85,3 82,8
*В настоящее время метод получения анилина путем восстановления нитробензола чугунной стружкой не используется. На действующих производствах этим методом получают различные производные анилина: ксилидины, толуидины и др.
При использовании колонн с высокой разделяющей способностью (с увеличенной исчерпывающей частью) анилин полнее извлекается из кубовых остатков, при этом качество продукта не ухудшается. Было показано, что снижение содержания анилина в сточных водах с 0,1 до 0,02 % за счет более эффективной отгонки анилина из анилиновой воды позволяет увеличить выход анилина на 0,04 %.
Оба промышленных способа получения анилина в качестве основного сырья используют бензол. Экономические показатели процесса получения анилина через нитробензол зависят в основном от цен на азотную кислоту и водород, для процесса получения анилина через фенол определяющими являются цены на фенол и ацетон. В обоих процессах выход анилина доведен до высокого уровня и в расчете на бензол составляет ~98 и ~97 % соответственно для нитробензольного и для фенольного способов.
В настоящее время 90 % современного производства анилина основано на технологии гидрирования нитробензола и только 10 % анилина получают из фенола. Основные проблемы при традиционном способе получения анилина из нитробензола существуют на стадии производства самого нитробензола, т. к. процесс полу
Ароматические соединения
657
чения его сопровождается образованием большого количества трудноутилизируемых жидких и газообразных отходов. Так, на 1 т товарного нитробензола образуется около 1 т 70% серной кислоты и примерно 1 т сточных вод, содержащих нитрофенолы. Решение данной проблемы может быть связано как с регенерацией серной кислоты, так и с использованием экономичных нитрующих агентов (если их удастся найти), применение которых позволит уменьшить количество отработанной серной кислоты.
Метод получения анилина каталитическим аммонолизом фенола имеет существенные экологические преимущества, т. к. получение фенола кумольным методом сопровождается значительно меньшим количеством сточных вод, чем получение эквивалентного количества нитробензола. Кроме того, параллельно с анилином образуется ацетон, использование которого позволяет снизить себестоимость анилина. Однако затраты энергии по фенольному способу значительно выше, чем по нитробензольному.
Среди методов получения анилина, которые нс вышли еще из стен лаборатории, но в будущем смогут представить промышленный интерес, наиболее перспективным является окислительный аммонолиз бензола. Если будет найден катализатор, обеспечивающий выход анилина больше 50 %, этот метод может конкурировать как с классическим нитробензольным методом, так и с получением анилина через фенол.
Представляет интерес также метод получения бензола аминированием бензойной кислоты, т. к. в данном случае сырьем является толуол. Этот метод сможет конкурировать с получением анилина через нитробензол особенно в том случае, если прогнозируемая цена бензола существенно увеличится по причине его дефицитности или если цена на толуол снизится на 40 % при сохранении существующей цены на бензол.
Литература к 4.2
1. Николаев Ю.Т., Якубсон А.М. Анилин. М.: Химия, 1984. 152 с.
2. Беркман Б.Е. Промышленный синтез ароматических нитросоединений и аминов. М.: Химия, 1964. 344 с.
3. Николаев Ю.Т. и др. // Хим. пром-сть. 1981. № 10. С. 625.
4. Маслова И.П., Золотарева К.А., Глазунова Н.А. и др. Химические добавки к полимерам: Справ. М.: Химия, 1973. 272 с.
5. Горбунов Б.Н., Гурвич Я.А., Маслова И.П. Химия и технология стабилизаторов полимерных материалов. М.: Химия, 1981. 368 с.
6. Блок Г.А. Органические ускорители вулканизации и вулканизирующие системы для эластомеров. Л.: Химия, 1978. 240 с.
7. Венкатараман К. Химия синтетических красителей / Пер. с англ.; Под ред. Б.А. Порай-Кошица. Л.: ГХИ, 1956. Т. 1.С. 100-114.
8. Ворожцов Н.Н. (мл.) Химия синтетических красителей / Под ред. К. Венкатарамана; Пер. с англ.; Под ред. Л.С. Эфроса, Л.: Химия, 1974. Т. 3. С. 1773-1786.
9. Ворожцов Н.Н. Основы синтеза промежуточных продуктов и красителей. 4-е изд. М.: Госхимиздат, 1955.
10. Эфрос Л.С., Горелик М.В. Химия и технология промежуточных продуктов. Л.: Химия, 1980. 544 с.
11. Чекалин М.А., Пасет Б.В., Иоффе В.А. Технология органических красителей и промежуточных продуктов. Л.: Химия, 1980. 472 с.
12. Мельников Н.Н. Пестициды. Химия, технология и применение. М.: Химия, 1987. 712 с.
13. Системные фунгициды / Пер. с англ.; Под ред. Н.Н. Мельникова. М.: Мир, 1975, 304 с.
14. Солдатенков А.Т., Колядина Н.М., Шендрик И.В. Основы органической химии лекарственных веществ. М.: Мир, 2003. 192 с.
15. Машковский М.Д. Лекарственные средства. М.: Медицина, 1993. Ч. 1, 736 с., Ч. 2, 688 с.
16. Беккер Г.О. Введение в фотохимию органических соединений / Пер. с нем.; Под ред. А.В. Ельцова. Л.: Химия, 1976. 384 с.
17. Вредные вещества в промышленности: Справ. / Под ред. Н.В. Лазарева и Э.Н. Левиной, 7-е изд. Л.: Химия, 1976. Т. 2. 456 с.
Приложение 4.2
Торговые названия некоторых производных анилина, используемых в качестве химических добавок к полимерам
Торговое название Фирма (страна)
Дифениламин (9)
Фенам (Россия)
4,4'-Диаминодифенилметан (38)
Диамет Tonox, Tonox, D Robac 4,4' Epikure DDM (Россия) Rubb. Regen (Англия) Robinson (Англия) Shell (Англия)
4,4'-Диаминодифенилметан (38)
DADM Caytur22, Na-11 Man. Land (Франция) Du Pont (США)
Торговое название Фирма (страна)
Tonox, Tonox D, Tonox R Resistox В Uniroyal (США) Monsanto (США)
Диазоаминобензол (40)
ДАБ, Азобензол (Россия)
Диазоаминобензол (40)
Vulcacel AN Porofor DB, Cellofor DAB Porofor DB Unicel ICI (Англия) Didier (Германия) Bayer (Германия) Du Pont (США)
658
Новый справочник химика и технолога
Торговое название | Фирма (страна)
4-Гидроксидифениламин (69)
Дифенам О, Фенам О Good-Rite АО 3920 (Россия) Goodrich (США)
Л,Л'-Дифенилэтилендиамин (73)
Nonox DED Stab i lite ICI (Англия) Hall(CLUA)
Бис(#-бензамидофенил)дисульфид (75)
Амифенс Б (Россия)
N,N -Диэтилбензтиазолсульфенамид-2 (77)
Сульфенамид БТ Accelerateur 400 Vulkancit AZ (Россия) Kuhlmann (Франция) Bayer (Германия)
УУ-Фурфурилиденбензотиазолсульфенамид-З (81)
Сульфенамид Ф (Россия)
А,А7-Дифенилтиомочевина (76)
Тиокарбанилид, Тиомал ФД Vulcafor ТС, Vulcafor ТС IV А-1 Anchorace 1 Stabilisator С, Vulkacit СА Accelerateur LL, Ekagom LL Eveite TC Activit Interstab C 27 Przyspieszacz DFT Accelerateur 15, Vulkanol NCA Accelerateur BB NCC, Exellerex NCC Thip J-172 Sumilizer C, Soxinol A Nocceler C (Россия) ICI (Англия) Monsanto (Англия) Anchor Chemical (Англия) Bayer (Германия) Ugine Kiihlmann (Франция) ACNA (Италия) Union Chem. (Бельгия) AKZO (Нидерланды) (Польша) Du Pont (США) Goodrich (США) Naugatuck (США) Monsanto (США) Heveatex (США) Sumitomo (Япония) Ouchi Shinko (Япония)
2-Меркаптобензотиазол (17)
Каптакс, Тиазол BM Mertax, Mercapto F, Mercapto FP, Thiotax Vulcadote M Ancap Captax Kuracap МВТ Vulcafor МВТ Accelerateur M, Accelerateur G, Ekagom G Accelerateur 200 МВТ, МВТ XXX Vulkacit Mercapto, Mercapto Dispersion (Россия) Monsanto (Англия) ICI (Англия) Anchor Chemical (Англия) Greeff (Англия) Dickinson (Англия) Vulnax (Англия, Франция) Kuhlmann (Франция) Rhone Poulenc (Франция) Man. Land (Франция) Bayer (Германия)
2-Меркаптобензотиазол (17)
Eveite M Accelerante МВТ Przyspieszacz M, Vulka-tor PX Accicure МВТ ACNA (Италия) Gen. Quimica (Испания) (Польша) Alkali (Индия)
Торговое название Фирма (страна)
Croydax Captax, Rotax, Rotax Dispersion Rubbacure 6031 МВТ Vulcaid МВТ Paracure AC-50, AC-51, AC-61 PMD-75 Poly-Dispersion Poly Zole МВТ Amizem M, Accelerateur CX, Accel M, M-R Soxinol M Diacceler M Nocceler M, Mitsui M Rapidex KB Belger M Pennsalt (США) Vanderbilt (США) Rubb. Corp. (США) Du Pont, Cyanamid, Uniroyal (США) Binney (США) Testworth (США) Wyrough (США) Nat. Polychem. (США) Kawaguchi (Япония) Sumitomo (Япония) Nippon (Япония) Ouchi Shinko (Япония) Gomu Jakaschui (Япония) Yanaginuma (Япония)
Ди(2-бензотиазолил)дисульфид (65)
MBTS Eveite DM Bawox AC, Mercasulf MBTS Gequisa MBTS Beschleuniger DM, Vulkator DX, Przyspieszacz DM, Przyspieszacz F Accicure MBTS, Vulcarite 121 Altax, Rodform Altax Rubbacure 6032 MBTS Vulcaid MBTS Paracure AC-52 PMD-60 Poly-Dispersion Poly Zole MBTS Accel DM, Accelerateur DM Soxinol DM Diacceler DM Nocceler DM Rapidex KY Belger DM Hebei u. Frengle (Германия) ACNA (Италия) Bozzetto (Италия) Gen. Quimica (Исландия) (Польша) Alco (США) Vanderbilt (США) Rubb. Corp. (США) Du Pont, Naugatuck, Cyanamid, Uniroyal (США) Binney (США) Testworth (США) Wyrough (США) Nat. Polychem. (США) Kawaguchi (Япония) Sumitomo (Япония) Nippon (Япония) Ouchi Shinko (Япония) Gomu Jakaschui (Япония) Yanaginuma (Япония)
А^УУ'-Дифенилгуанидин (66)
Гуанид Ф, ДФГ DPG Vulcafor DPG Ekagom D' (Россия) Monsanto (Англия) Vulnax (Англия, Франция) Kuhlmann (Франция)
Л,/У'-Дифенилгуанидин (66)
DPG Accelerateur D Vulkacit D Eveite D Rhone Poulenc (Франция) Mat. Col. (Франция) Bayer (Германия) ACNA (Италия)
Ароматические соединения
659
Торговое название Фирма (страна)
Accelerante DPG, Gequisa DPG Beschleuniger D Accelerateur 12 DPG Vulcaid DPG Accelerateur D Soxinol D Nocceler D Gen. Quimica (Испания) (Польша) Du Pont (CHIA) Cyanamid (США) Binney (США) Kawaguchi (Япония) Sumitomo (Япония) Ouchi Shinko (Япония)
7У-Фенил-1-нафтиламин (67)
Нафтам-1, Неозон A Nonox AN, Nonoxol AN Antioxidant PAN Additin PAN, ASM PAN Antioxygene A Antioxygene MCA, Altofane A Neozone A Antiage PAN Neozone A Naugard PAN Antigene PA Nocrac PA, Nocceler PA Antigene A Россия ICI (Англия) Monsanto (Англия) Bayer (Германия) Mat. Col. (Франция) Ugine Kiihlmann (Франция) ACNA (Италия) Franc. Donders (Нидерланды) Du Pont (США) Uniroyal (США) Sumitomo (Япония) Ouchi Shinko (Япония) Dyestuffs (Япония)
УУ-Фенил-2-нафтиламин (68)
Нафтам-2, Неозон Д Antioxidant 116 Nonox D, Nonox DN, Nonoxol D PBN, Wettable PBN ASM PBN, Vulkanox PBN PBN Antioxygene MC Altofane MC Rionox Inhibitor OD Stabilizator AR Antioxidant PBN Neozone D Good-Rite AO-3100 PBN STD Antage B, Antage D Antigene D Antioxidant D, Nonflex D Nocrac D (Россия) Anchor Chemical (Англия) ICI (Англия) Monsanto (Англия) Bayer (Германия) BASF (Германия) Mat. Col. (Франция) Ugine Kuhlmann (Франция) Man. Land. (Франция) ACNA (Италия) (Польша) (Венгрия) Du Pont (США) Goodrich (США) Naugatuck (США) Benson (США) Kawaguchi (Япония) Sumitomo (Япония) Seiko Chemical (Япония) Ouchi Shinko (Япония)
Ацет ан (70)
Ускоритель К-1, Ацетан Vulcafor RN (Россия) ICI (Англия)
Ацетан (70)
А-7, А-19, А-40, А-77 Accelerateur S, Ekagom S Anti-Age 55 Monsanto (Англия) Ugine Kuhlmann (Франция) Binney (США)
Торговое название Фирма (страна)
EA, H-50 D, Vulcone Crilene Base, Crilene VGB Nocceler К Du Pont (США) Naugatuck (США) Ouchi Shinko (Япония)
М2У'-Дифенил-1,4-фенилендиамин (72)
Дифен ФФ, Дифсн Ф DPPD Nonox DPPD Permanax DPPD Permanax 18 Antioxygene DIP Altofane DIP DPPD Good-Rite AO 3152, Good-Rite Caromax Age Rite DPPD JZF Naugard J Perflectol X Nocrac DP Antage DP Antigene H, P Antioxidant H (Россия) Monsanto (Англия) ICI (Англия) Vulnax (Англия, Франция) Rhone Poulenc (Франция) Mat. Col. (Франция) Ugine Kiihlmann (Франция) ACNA (Италия) Goodrich (США) Vanderbilt (США) Naugatuck (США) Uniroyal (США) Monsanto (США) Ouchi Shinko (Япония) Kawaguchi (Япония) Sumitomo (Япония) Seiko Chemical (Япония)
7У-Циклогексилбензотиазолсульфенамид-2 (78)
Сульфонамид Ц CBS, Cydac, Furbac Santocure PSANNSD-70 PolyDispersion Vulcafor HBS Vulcafor CBS Ekagom CBS, CBS 101 Rhodifax 16 Sulfen 1 Accelerateur 400 Vulkazit CZ, CZ/GR Beschleuniger BSD Eveite MS Mercamid C Przyspieszacz Tiohexam Accicure HBS Conac S Grains Durax, Vandure DA Cydac Delac S Vulcaid МВТ Nocceler CZ Accelerator FC, Accel CZ, CZ-R Soxinol CZ (Россия) Anchor Chemical (Англия) Monsanto (Англия) Wilkins (Англия) ICI (Англия) Vulnax (Англия, Франция) Kiihlmann (Франция) Rhone Poulenc (Франция) Man. Land (Франция) Kiihlmann (Франция) Bayer (Германия) Hebei u. Frengle (Германия) ACNA (Италия) Bozzetto (Италия) (Польша) Alkali (Индия) Du Pont (США) Vanderbilt (США) Cyanamid (США) Uniroyal (США) Binney (США) Ouchi Shinko (Япония) Kawaguchi (Япония) Sumitomo (Япония)
(Бензотиазолил-2)морфолиносульфид (79)
Сульфенамид М NOBS Accelerateur, NOBS special Accelerateur Santocure MOR (Россия) Anchor Chemical (Англия) Monsanto (Англия)
660
Новый справочник химика и технолога
Торговое название Фирма (страна)
Vulcafor BSM Vulcafor MBS Rhodifax 12, Rhodifax 19 Vulkacit MOZ Amax Delac MOR Nocceler MSA, Nocceler NOBS Accel NOS Soxinol NBS ICI (Англия) Vulnax (Англия, Франция) Rhone Poulenc (Франция) Bayer (Германия) Vanderbilt (США) Uniroyal (США) Ouchi Shinko (Япония) Kawaguchi (Япония) Sumitomo (Япония)
Смесь: 4,4'-бис(1,1,33-тетраметилбутил)-дифениламин (£б);4-(1,1ДЗ~ тетраметилбутил)-дифениламин
Дифенам ДИБ, Дифенам ДМБ Nonox OD Irganox LO-1 Age Rite Stalite S Cyanox 8 Octamine (Россия) ICI (Англия) Ciba-Geigy (Швейцария) Vanderbilt (США) Cyanamid (США) Uniroyal (США)
/V-Нитрозодис >ениламин (87)
Дифенам H Curetard A Vulcatard A Diphene SD Vulkalent A Retarder AN Accitard A Good-Rite Vultrol, Vultrol Retarder 2N Antifix D, Delac Y, Re-dax, Retarder J (Россия) Monsanto (Англия) Vulnax (Англия, Франция) Kuhlmann (Франция) Bayer (Германия) ACNA (Италия) Alkali (Индия) Goodrich (США) Cyanamid (США) Naugatuck (США)
А-Нитрозоди< >ениламин (87)
Naugard TJB Uniroyal (США)
Торговое название Фирма (страна)
Vultrol N Sconoc Retarder NDPA Nat. Polychem. (США) Ouchi Shinko (Япония) Kawaguchi (Япония)
А-Изопропил-А-фенил-1,4-фенилендиамин (90)
Диафен ФП Nonox ZA Antiozonant IP Santoflex 36 Permanax IPPD Permanax 115 Vulkanox 4010 NA Ipognox 44 Cyzone IP Flexzone 3C Antioxidant 420 Eastozone 34 Nocrac 810-NA Antage 3C Antigene 3C Ozonone 3C (Россия) ICI (Англия) Anchor Chemical (Англия) Monsanto (Англия) Vulnax (Англия, Франция) Rhone Poulenc (Франция) Bayer (Германия) (Польша) Cyanamid (США) Uniroyal (США) Naugatuck (США) Eastman (США) Ouchi Shinko (Япония) Kawaguchi (Япония) Sumitomo (Япония) Seiko Chemical (Япония)
А-(1,3-Диметилбутил)-А'-фенил-1,4-фенилен-диамин (91)
Диафен 13, Диафен ФДМБ, Диафсн ДММД Nonox ZC Permanax 6PPD Permanax 120 ASM 4020, Bayer 4020 Ipognox 45 Antozite 67 Santoflex 13 Elexzone 7L UOP 588 (Россия) ICI (Англия) Vulnax (Англия, Франция) Rhone Poulenc (Франция) Bayer (Германия) (Польша) Vanderbilt (США) Monsanto (США) Uniroyal (США) Univ. Oil (США)
4.3. Органические красители
4.3.1. Основные понятия
Красителями называются органические соединения, обладающие способностью интенсивно поглощать и преобразовывать энергию электромагнитных излучений (световую энергию) в видимой и ближних ультрафиолетовой и инфракрасной областях спектра и сохраняющие эту способность при нанесении на различные тела. Поглощая часть световых лучей определенной длины волны в видимой области спектра, эти соединения становятся цветными. От характера преобразования поглощенной энергии зависит специфика практического использования красителей.
Красители, преобразующие поглощенную световую энергию в тепловую и передающие ее в окружающую среду в виде тепла, используются именно как красители (в узком смысле этого слова).
Красители, преобразующие поглощенную световую энергию в энергию химического процесса превращения веществ (например, галогенидов серебра в фотоэмульсии), используются в производстве кинофотоматериалов в качестве оптических сенсибилизаторов — веществ, повышающих чувствительность фотопленки к световым лучам определенной части спектра.
Красители, преобразующие частично поглощенную световую энергию в тепловую, а частично излучающие ее в виде световых лучей иной (большей) длины волны, используются в качестве люминофоров и флуоресцентных (оптических) отбеливателей.
Термин «краситель» был введен А.Е. Порай-Коши-цем в 1908 г. взамен ранее применявшихся терминов «краска» и «пигмент», которым в настоящее время придается иное, более ограниченное значение.
Ароматические соединения
661
4.3.2. История красителей
4.3.2.1. Красители растительного и животного про исхожден ия
Применение веществ, способных придавать тот или иной цвет различным предметам (тканям, одежде, посуде и пр.), было известно в самые отдаленные эпохи. Для этого использовались цветные глины, оксиды металлов, а также органические вещества, которые добывали из растений (деревья, травы, лишайники) и животных (насекомые, моллюски). Природные красители использовались несколько тысячелетий, но не более десятка из них сохранили свое значение до настоящего времени, т. к. большая часть этих красителей давала неяркие цвета, прочность окрасок была невысокой, а процесс крашения — длительным и сложным.
Наиболее прочный и яркий из природных красителей — Индиго. Само слово «индиго» происходит от «ин-дикус», что значит индийский. В Индии и Египте краситель был известен более 4000 лет назад, о чем свидетельствуют образцы тканей, найденных археологами в египетских пирамидах и при разных раскопках. В VIII в. Индиго был завезен в Европу арабскими купцами. Этот синий краситель добывали из стеблей и листьев растений рода индигофера (Indigofera tinctoria L.), произрастающих в странах жаркого и влажного климата (Индия, Индонезия и др.). Для получения 3 кг красителя необходимо было переработать 100 кг листьев растений. В Англии этот же краситель, но менее интенсивного цвета и худшего качества, добывали из местного растения вайды.
Наиболее распространенным и значимым красителем красного цвета был Ализарин (другое название — Марену), который добывали из корней растения марена (корни растения Rubia tinctoria, известные под названием alizari). Этот краситель использовался для крашения обмундирования во французской и английской армиях. В XIX в. Луи Филипп одел свою пехоту в рейтузы, окрашенные Ализарином, но наиболее знамениты были английские красные плащи. Сам Ализарин имеет желтый цвет и образует красную окраску только после протравы ткани солями алюминия. Обычно для этого применялись алюминиевые квасцы. С солями других металлов Ализарин образует иные цвета, например, с солями железа — фиолетовый, с солями хрома — коричневый.
Другие красители красного цвета были животного происхождения. Алый краситель Кармин (другое название — Кошениль) добывали из высушенных тел самок червеца карминоносного (Coccus cacti) — насекомого, живущего на одном из видов мексиканского кактуса (для получения 1 кг красителя необходимо было высушить 150 тысяч насекомых). Другой краситель красного цвета Кермес извлекали из высушенных самок червеца кермессового (Coccus ilicis) — насекомого, поражающего кермесовый дуб.
Главным желтым красителем древности был Шафран, извлекаемый из цветов растения шафрана (Crocus sativus). Чтобы получить 1 кг красителя, надо было переработать свыше 40 тысяч цветков. В средние века
наиболее известным желтым красителем был Резеда — краситель, получаемый из семян, стеблей и листьев растения резеда (Reseda luteola L.). Использовались и другие природные красители желтого цвета: Кверцитрон — краситель, содержащийся в экстракте коры североамериканского дуба (Guercus tinctoria nigra), Сафлор — краситель, извлекаемый из высушенных лепестков сафлора красильного (Carthamus tinctorius). В желтый цвет ткани окрашивали также экстрактом незрелых плодов крушины.
Для получения черного цвета использовали экстракт древесины кампешевого дерева (Haematoxylon сатре-chiancum L.). Природный краситель — Кампешевый черный был известен еще в XV в., однако приобрел свою настоящую ценность лишь в 1812 г., когда французский химик Шеврель открыл его свойство образовывать с солями металлов окрашенные лаки.
Некоторые красители были дороже золота, например, Тирийский (античный) пурпур. Его добывали из особой улитки-багрянки, обитающей в Средиземном море. Сама улитка не окрашена в пурпурный цвет. Обычно ее измельчали с водой и полученным соком пропитывали ткань, которую развешивали на воздухе. При окислении кислородом воздуха сок багрянки и окрашивался в пурпурный цвет. Из 10 тысяч улиток удавалось получить только 1 г красителя. Название Тирийского пурпура происходит от древнего средиземноморского города Тира, в котором начиналось и развивалось производство этого красителя. Окрашенные пурпурные изделия ценились очень дорого еще в Древнем Риме.
Многие из естественных красителей растительного и животного происхождения добывались в значительных количествах, удовлетворявших потребности общества. Фактически до конца XIX в. преимущественно использовались красители, добытые из природных источников.
4.3.2.2. Первые синтетические красители
Бурное развитие текстильной промышленности в XVIII в. и переход к машинному производству текстильных изделий резко повысили спрос на дешевые красители. Становилась неотложной задача замены дорогих природных красителей дешевыми и доступными синтетическими красителями.
В XIX в. на мировом рынке было единственное синтетическое красящее вещество (пикриновая кислота), открытое Вульфом в 1771 г., и его производство составляло лишь 1 % от мирового производства красителей.
Первый синтетический краситель был получен в 1855 г. польским ученым Я. Натансоном. Работая в г. Юрьев (ныне г. Тарту), он, нагревая анилин с дихлорэтаном в запаянной трубке, получил соединение красного цвета, способное окрашивать шерсть и шелк в более красивый красный цвет, чем Кармин. В 1858 г. французский химик Верген получил то же вещество окислением технического анилина (содержащего примесь толуидинов) и назвал его Фуксином, т. к. краситель напоминал окраской цветок фуксии.
662
Новый справочник химика и технолога
В 1856 г., полугодом позже Натансона, английский химик В. Перкин, окисляя технический анилин хромовой смесью, получил красновато-фиолетовое вещество, интенсивно окрашивающее шелк. Позднее краситель получил название Мовеина за сходство с окраской цветка мальвы. Шелк цвета мальвы пользовался большим спросом, и в короткий срок было организовано промышленное производство красителя. Так возникла новая отрасль химического производства — анилинокрасочная промышленность, названная так потому, что все первые синтетические красители были получены либо из анилина, либо из его технических смесей с аналогичными продуктами.
Первые синтетические красители были получены случайно. Лишь после создания А.М. Бутлеровым в 1861 г. теории строения органических соединений — теоретического фундамента органической химии — стал возможным целенаправленный синтез красителей. Синтез Ализарина был первым направленным синтезом промышленно важного красителя. Краситель синтезировали немецкие химики Гребе и Либерманн после того, как в 1868 г. они исследовали структуру Ализарина, извлеченного из корней марены, и определили, что он является 1,2-дигидроксиантрахинином.
4.3.3. Теория цветности
4.3.3.1. Физические основы
Цвет красителей является следствием их взаимодействия со светом, в результате которого происходит поглощение части световых лучей определенной длины волны. Процессы поглощения световых лучей органическими соединениями изучает теория цветности.
Световой луч представляет собой поток фотонов — отдельных порций (квантов) электромагнитной энергии, величина которых Е (кДж) выражается уравнением Планка
E = hv, (4.3.1)
где v — частота электромагнитных колебаний, с '; h — постоянная Планка, 6,62 • 10”37 кДж • с.
Каждому фотону соответствует определенная длина электромагнитной волны, связанная с частотой колебаний уравнением
c = vX, (4.3.2)
где X — длина волны, выражаемая обычно в метрах или нанометрах (м, нм); с — скорость света, равная в вакууме 3 • 108 м/с = 3 • 10’7 нм/с.
Волновое число v — величина, обратная длине волны; фактически это число волн, помещающихся в единице длины, например, в 1 см (если v выражена в см”'), vX = 1.
Электромагнитный спектр охватывает диапазон длин волн X от 10”'4 до 106 м. Этим длинам волн соответствуют частоты колебаний v от 3 • 1022 до 3 • 102см”', энергии фотонов Е от 2 • 10”14 до 2 • Ю’4 кДж. Из всего этого огромного диапазона электромагнитной энергии
зрительный аппарат человека способен воспринимать как ощущение света воздействие фотонов лишь в узком интервале энергий: ~ от 2,5 • 10”22 до 5 • 10”22 кДж. Этим фотонам соответствуют световые лучи с частотами колебаний v от 4 • 1014 до 7,5 • 10,4см”' и длинами волн X от 760 до 400 нм (видимая часть спектра). Световые лучи, выходящие за пределы этого интервала, не вызывают у нас зрительных ощущений. Невидимые лучи с длинами волн меньше 400 нм называются ультрафиолетовыми, больше 760 нм — инфракрасными.
Особенностью зрительного восприятия человека является то, что при совместном действии всех световых лучей с длинами волн от 400 до 760 нм возникает ощущение так называемого белого неокрашенного света. Раздельное действие на зрительный аппарат световых лучей в более узких интервалах длин волн (монохроматический свет) производит ощущение окрашенного света {спектральные цвета), причем характер окраски (цвет) строго зависит от длин волн лучей, входящих в эти узкие интервалы.
При взаимодействии белого цвета с различными веществами могут наблюдаться следующие явления:
1. Все лучи видимой части спектра полностью отражаются непрозрачной поверхностью или полностью проходят сквозь прозрачное вещество; в этом случае непрозрачное вещество кажется белым, а прозрачное — бесцветным.
2. Все лучи видимой части спектра полностью поглощаются веществом; вещество кажется черным.
3. Все лучи видимой части спектра частично поглощаются веществом, а частично отражаются им; вещество имеет серый цвет.
4. Вещество избирательно поглощает некоторые лучи видимой части спектра, остальные лучи проходят сквозь вещество или отражаются от него; вещество представляется окрашенным (цветным).
Цвета, ощущение которых возникает в результате воздействия на зрительный аппарат всех световых лучей видимой части спектра за вычетом поглощенных лучей, называются дополнительными. Совместное действие дополнительных и спектральных цветов производит ощущение белого цвета (дополнительные цвета «дополняют» спектральный цвет до белого). Цвета предметов в естественных условиях, как правило, являются дополнительными.
Например, тело избирательно поглощает лучи с длинами волн от 500 до 560 нм; при действии на зрительный аппарат эти лучи вызывают ощущение спектрального зеленого цвета. Поскольку эти лучи поглощаются, то воздействие оставшихся лучей видимой части спектра, т. е. лучей с длинами волн от 400 до 500 нм и от 560 до 760 нм, вызывает ощущение дополнительного цвета, и окраска предмета нам кажется пурпурной. Как и все дополнительные цвета, пурпурный цвет является смешанным, т. к. ощущение его вызывается совместным действием монохроматических лучей, порознь произ
Ароматические соединения
663
водящих ощущение фиолетового, синего, оранжевого, желтого и др.
В табл. 4.3.1 приведена зависимость спектральных и дополнительных цветов от длины волны.
Таблица 4.3.1
Соотношение между основными и дополнительными цветами
Длина волны, нм Спектральный цвет (поглощенное излучение) Дополнительный цвет (цвет тела)
400-435 Фиолетовый Зеленовато-желтый
435-480 Синий Желтый
480-490 Зеленовато-синий Оранжевый
490-500 Синевато-зеленый Красный
500-560 Зеленый Пурпурный
560-580 Желтовато-зеленый Фиолетовый
580-595 Желтый Синий
595-605 Оранжевый Зеленовато-синий
605-730 Красный Синевато-зеленый
730-760 Пурпурный Зеленый
Таким образом, причиной окраски (цвета) предмета является избирательное поглощение им части световых лучей из общего светового потока в видимой области электромагнитного спектра.
Поглощение и отражение света окрашенными телами может быть измерено. Для этого используют специальные приборы — спектрофотометры. В спектрофотометрах свет лампы с помощью кварцевых призм разлагается на отдельные составляющие этот свет монохроматические излучения, которые поочередно пропускают через исследуемый объект. Объектами исследования могут быть растворы красителей, цветные прозрачные пленки (поглощение света) и окрашенные непрозрачные поверхности (отражение света). Краситель поглощает некоторую часть направленного на него светового потока, в результате чего интенсивность прошедшего или отраженного излучения уменьшается. Уменьшение интенсивности светового луча регистрируется фотоэлементом.
Поглощение света для достаточно разбавленных растворов красителя, в которых отсутствует ассоциация частиц растворенного вещества, подчиняется закону Бугера — Ламберта — Бера. Согласно этому закону
Igf-y-) = ес/= £>, (4.3.3)
где /о и / — интенсивности светового луча до и после прохождения раствора соответственно; £ — мольный коэффициент поглощения (коэффициент погашения, коэффициент экстинкции), характерный для данного вещества; с — концентрация вещества в растворе, моль/л; / — толщина слоя раствора, см; D — оптиче
ская плотность.
Определив изменение интенсивности светового потока для каждой длины волны, строят график зависимости с от X, откладывая по оси абсцисс длины волн X, а по оси ординат — мольные коэффициенты поглощения £ или lg£. Полученный график называется спектральной кривой поглощения или спектром поглощения (рис. 4.3.1). Положение максимума на кривой по оси абсцисс характеризует цвет (окраску) вещества, по оси ординат — интенсивность поглощения (интенсивность окраски). Изменение цвета, соответствующее сдвигу максимума поглощения в сторону лучей с большей длиной волны, называется углублением цвета или батохромным сдвигом (от греческих слов «батос» — глубина и «хрома» — цвет). Изменение цвета в обратном направлении называется повышением цвета или гипсохромным сдвигом (греч. «гипсос» — высота). Увеличение интенсивности поглощения называется гиперхромным эффектом (греч. «гипер» — над, возвышение), уменьшение — гипохромным эффектом (греч. «гипо» — под, снижение).
Если цвет вещества определяется положением максимума поглощения на оси длин волн, то оттенки этого цвета зависят от общего характера кривой поглощения. Красители, отличающиеся чистым, ярким оттенком, имеют узкие полосы поглощения, которые изображаются кривой с четко выраженными максимумами и круто падающими склонами, например фиолетовый краситель (рис. 4.3.2). Чем более пологи склоны кривой, т. е. чем шире полоса поглощения, тем менее чист и ярок оттенок красителя. Так, желтый, оранжевый и красный цвета приобретают коричневый оттенок, синий — черноватый, зеленый переходит в оливковый и г. д. Для красителей «нечистых» тонов (оливковых, коричневых, серых, черных) — характерно отсутствие четкого максимума на кривой поглощения (рис. 4.3.3).
Многие красители имеют сложную кривую поглощения с несколькими максимумами или с дополнительными нечеткими максимумами в виде изгиба («плеча») кривой поглощения. В этих случаях цвет вещества является результатом суммарного действия дополнительных цветов. Так, наличие двух максимумов (одного в области 400-430 нм, а другого в области 600-700 нм) обусловливает результирующий зеленый цвет (сложение дополнительных цветов: желтого и голубого, рис. 4.3.4).
Рис. 4.3.1. Спектральная кривая поглощения
664
Новый справочник химика и технолога
Рис. 4.3.2. Кривая поглощения фиолетового красителя
ла переходит в результате поглощения света, через Е*, то разность ЛЕ = Е* - Eq, называемая энергией возбуждения, будет соответствовать энергии фотона, избирательно поглощаемого данной молекулой.
Так как Е = hv, a vX = с, то связь между длиной волны избирательно поглощаемого света и энергией возбуждения для одной молекулы можно выразить уравнением
he
ЬЕ = —- (4.3.4)
X-
для моля вещества — уравнением
Рис. 4.3.3. Кривая поглощения коричневого красителя
300 400 500 600 700 X, нм
Рис. 4.3.4. Кривая поглощения зеленого красителя
4.3.3.2. Энергия возбуждения молекул и цвет
Причиной избирательного поглощения световых лучей определенных длин волн, т. е. фотонов определенной энергии, является квантованность внутренней энергии молекул. Поскольку каждому виду молекул свойственны строго определенные значения (уровни) внутренней энергии, переход от одного значения к другому совершается скачкообразно, путем поглощения или выделения только такого кванта (порции) энергии, который сразу переводит молекулу с одного, присущего ей энергетического уровня, на другой. Вследствие этого молекула способна поглотить из светового потока только такие фотоны, энергия которых соответствует разности характерных для нее уровней энергии. Все остальные фотоны большей или меньшей энергии не будут поглощаться данным веществом.
Если энергию молекулы в обычном, нормальном состоянии, называемом основным, обозначить через Eq, а энергию в состоянии возбуждения, в которое молеку
где N а — число Авогадро.
Подставляя значения NA = 6,02 • 1023 моль-1, h = 6,62 • 10“37 кДж • с, с = 3 • 1017 нм/с, получим:
ЛЕ ~ 12 • 104 / X (кДж/моль).
Расчет по этой формуле показывает, что на границах видимой части спектра (X равно 400 и 760 нм) энергия возбуждения ЛЕ соответствует 300 и 158 кДж/моль. Следовательно, окраской обладают только те вещества, которые переходят в возбужденное состояние от поглощения порций энергии в пределах 158-300 кДж/моль. Если энергия возбуждения ДЕ >300 кДж/моль, вещество поглощает в ультрафиолетовой (УФ) области спектра, если ЛЕ < 158 кДж/моль, вещество поглощает в инфракрасной (ИК) области спектра. В обоих случаях вещество кажется нам бесцветным.
Таким образом, в спектре поглощения соединения величина Хмакс, характеризующая цвет (окраску) вещества, является мерой энергии возбуждения его молекул, а величина емакс, характеризующая интенсивность окраски (интенсивность поглощения), — мерой вероятности того, что при взаимодействии со светом с длиной волны Хмакс молекула вещества захватит соответствующий фотон и перейдет в возбужденное состояние.
4.3.3.3. Ранние химические теории цветности
Уровни энергии молекул в основном и возбужденном состояниях, от которых зависит энергия возбуждения и равная ей энергия фотона, избирательно поглощаемого данным веществом и обусловливающего его цвет, определяются химическим строением вещества.
Основоположник теории строения органических соединений А.М. Бутлеров впервые предпринял попытку найти зависимость между химическим строением молекул и их способностью избирательно поглощать световые лучи. В 1864 г. во «Введении к полному изучению органической химии» он отмечал, что введение в бесцветные органические соединения некоторых групп, способных восстанавливаться (нитро-, нитрозо-, например) сообщает веществу окраску, а при восста
Ароматические соединения
665
новлении этих групп окраска исчезает. Таким образом, Бутлеров установил фундаментальный для теории цветности факт — ненасыщенность молекул веществ, обладающих цветом.
Хромофорно-ауксохромная теория. В 1868 г. немецкие химики Гребе и Либерманн подтвердили и развили идеи Бутлерова о связи ненасыщенности органических соединений с их окраской. В 1876 г. русский ученый П.П. Алексеев отмечал, что интенсивно окрашенные соединения наряду с ненасыщенными группами должны содержать и такие заместители, как гидрокси- и аминогруппы. Эти идеи получили законченное выражение в хромофорно-ауксохромной теории цветности, сформулированной в 1876 г. немецким ученым О. Виттом. Согласно этой теории, причиной окраски органических соединений является присутствие в их молекулах ненасыщенных: нитро- (~NO2), нитрозо-(-N=O), карбонильной (-С(О)-), азо- (-N=N-), виниленовой (-СН=СН-) и др. Эти группы были названы хромофорными дуплами, или хромофорами, т. е. носителями цветности (от греч. слов «хрома» — цвет, «форео» — ношу). Окрашенные соединения, содержащие хромофоры, были названы хромогенами. Эти соединения еще не являются красителями, т. к. обладают неинтенсивной окраской и не имеют сродства к волокнам. Для превращения хромогена в краситель в его молекулу необходимо ввести ауксохромные группы, или ауксохромы — усилители цветности (от греч. слова «ауксо» — увеличиваю). К ауксохромам относятся группы: гидрокси-(-ОН), амино-(-МН2), меркапто-(-SH) и др.
Схема красителя по О. Витту:
хромоген
Хромофорно-ауксохромная теория цветности оказала большое влияние на развитие химии красителей, позволила предсказать возможность синтеза большого числа новых окрашенных соединений и систематизировать их. На основе этой теории была создана классификация красителей (по типу хромофор).
Теория координационно-ненасыщенных атомов. После открытия свободных радикалов, оказавшихся окрашенными соединениями, Пфейфер (1911) включил в число хромофоров трехвалентный углерод, аДилтей (1920) все многообразие хромофорных групп свел к нескольким хромофорным атомам. По мнению Дилтея, координационная ненасыщенность атома является признаком его хромофорного характера. Ненасыщенность выражается в том, что атом связан с меньшим числом других атомов, чем это соответствует его максимальному координационному числу. Например, атомы углерода, координационное число которого 4, в алмазе и
парафине не являются хромофорами, т. к. каждый связан с четырьмя другими атомами и, следовательно, координационно насыщен. Однако в графите, этилене, бензоле и подобных соединениях атомы углерода являются хромофорами, т. к. связаны только с тремя другими атомами. Если хромофорных атомов в соединении достаточно много, оно становится окрашенным, причем окраска соединения усиливается в результате ионизации молекул. Теория Дилтея была дополнена Вицинге-ром (1926), который преобразовал понятие об ауксохромах и дал новую классификацию красителей.
Хиноидная теория. Хромофорно-ауксохромная теория и теория координационно-ненасыщенных атомов объясняли окраску соединений только наличием хромофорных и ауксохромных групп. Эти теории не принимали в расчет остальную часть молекулы, которая рассматривалась лишь как пассивный носитель этих групп, и не учитывали, в частности, сильнейшее влияние, которое оказывали некоторые заместители на реакционную способность и другие свойства ароматических соединений. В 1888 г. Армстронг и Нецкий создали хиноидную теорию цветности, в которой появление окраски соединения объяснялось перестройкой обычного ароматического (бензоидного) ядра в хиноидное. Эта теория утверждала, что само по себе ни наличие ароматического ядра, ни наличие хромофоров и ауксохромов Витта не делают вещество окрашенным. Например, 1,4-циклогексадион (/), содержащий две карбонильные группы — хромофоры Витта, и гидрохинон [бензолдиол-1,4 (2)], имеющий ароматическое кольцо и две гидроксигруппы — ауксохромы Витта, бесцветны. Однако л-бензохинон [циклогексадиен-2,5-дион-1,4 (5)], обладающий хиноидным ядром, окрашен в желтый цвет.
О ОН О
О ОН О
(/) (2) (5)
Сторонники хиноидной теории считали, что все окрашенные органические соединения имеют хиноидное строение. На основе этой теории была создана классификация красителей (по типу хиноидных систем).
Осцилляционная теория. Хромофорно-ауксохромная и хиноидная теории цветности по-разному объясняли причины окраски органических соединений. Однако обе теории рассматривали молекулу окрашенного вещества как нечто неизменное и совершенно не учитывали, что эта молекула взаимодействует со светом. Между тем новые факты свидетельствовали о подвижности связей между атомами в молекуле; в результате появились теории, которые пытались установить зависимость между изменениями связей в молекуле и поглощением света.
666
Новый справочник химика и технолога
Согласно осцилляционной теории А.Е. Порай-Кошица (1910 г.), избирательное поглощение света происходит в результате интерференции между колебаниями световых лучей и осцилляцией (перемещением) связей внутри молекул ненасыщенных соединений. Чем больше скорость осцилляции связей, тем больше частота колебаний поглощаемых лучей и, следовательно, меньше длина волны этих лучей. Таким образом, теория А.Е. Порай-Кошица связывала поглощение света с процессами изменения связей в молекуле. Когда появилась электронная теория валентности, раскрывшая физическую природу связей между атомами, эта идея получила полное признание.
Переход к электронной теории цветности. Основы современной электронной теории цветности органических соединений были заложены в многочисленных работах В.А. Измаильского, начатых с 1913 г. Основная идея Измаильского заключается в том, что способность органических соединений поглощать свет определяется особым электронным состоянием их молекул. Это состояние возникает при наличии достаточно длинной цепочки сопряженных двойных связей и присоединенных к ней электронодонорных (поставляющих электроны) и электроноакцепторных (принимающих электроны) заместителей. Развитие и уточнение представлений В.А. Измаильского привело к созданию принятой в настоящее время теории цветности органических соединений.
4.3.3.4. Энергетические уровни молекул
Энергия фотонов электромагнитных излучений, поглощаемая молекулой, идет на увеличение ее внутренней энергии, т. с. на перевод молекулы из основного состояния в возбужденное. Поскольку полная энергия молекулы складывается из вращательной энергии Еа, колебательной энергии Ек и энергии электронов Еэ (Е = = Ев + Ек + Еэ), энергия поглощенных фотонов может расходоваться на увеличение каждого из этих слагаемых. Наибольший вклад в эту сумму вносит энергия электронных переходов.
Диапазон энергии электронных переходов достаточно широк: от значений —110 кДж/моль, соответствующих излучению с длиной волны А. = 1100 нм, что характерно для ближней ИК-области спектра, до (4-103)-(4 • 106) кДж/моль, соответствующих излучениям с длинами волн порядка 30-0,03 нм, что характерно для рентгеновских лучей. В этих границах находятся и световые лучи видимой части спектра (ДЕ = 158^300 Дж/моль, А, = 760^-400 нм), поглощение которых сопровождается возникновением окраски. Этой энергии недостаточно для перевода в возбужденное состояние электронов внутренних электронных слоев атомов, которые прочно удерживаются притяжением атомного ядра, и поэтому эти электроны не участвуют в поглощении света в видимой и ближних УФ- и ИК-областях спектра. Электроны наружного электронного слоя атомов (валентные электроны) слабее удерживаются ядром и переходят
в возбужденное состояние значительно легче — при поглощении порций энергии порядка 110-1050 кДж/моль. Конкретная величина энергии возбуждения определяется характером электронных переходов, в которых участвуют валентные электроны.
Современная теория электронных спектров основывается на квантово-механических представлениях, и наиболее широко в этом случае применяется метод молекулярных орбиталей (МО). Метод МО предполагает, что энергетические уровни, на которых располагаются валентные электроны, — это молекулярные орбитали, которые образуются как линейные комбинации атомных орбиталей (принцип МО ЛКАО). Каждая молекула имеет свой набор молекулярных орбиталей со своими волновыми функциями. В органических соединениях это связывающие а- и л-орбитали, несвязывающая /7-орбиталь и разрыхляющие (антисвязывающие) а -и л -орбитали, причем каждым связывающим а- и л-ор-биталям соответствуют разрыхляющие а - и л -орбитали. Относительное расположение энергетических уровней валентных электронов показано на рис. 4.3.5.
Е
а
б
Рис. 4.3.5. Энергетические уровни и типы электронных переходов в простых (а) и сложных (о) молекулах
В соответствие с принципом Паули на каждой орбитали может размещаться не более двух электронов. Обычно в основном состоянии все связывающие и несвязывающие орбитали заняты. Связывающие орбитали заняты валентными электронами, образующими химическую связь между атомами. Образование связи всегда сопровождается выигрышем энергии, вследствие чего уровень энергии связывающих орбиталей значительно ниже уровня энергии атомных орбиталей. Несвязывающие орбитали занимают валентные электроны, не участвующие в образовании связей с другими атомами. Это неподеленные пары электронов, локализованные в поле одного ядра; они имеют энергию того же порядка, что и валентные электроны в атоме.
Переход молекулы в возбужденное состояние означает переход валентных электронов на свободные орбитали с более высокими уровнями энергии, т. е. разрыхляющие орбитали. Различают переходы: ст—, Л~*Л , П~^><5 И п-*л .
В большинстве случаев по уровню энергии орбитали располагаются в ряд: ст < л < п < л*< а . Однако
Ароматические соединения
667
в случае сложных молекул с достаточно большими сопряженными системами энергия некоторых л-орбита-лей может быть больше энергии /7-орбиталей, и тогда последовательность меняется: <з < п < п < л. < о .
4.3.3.5. Основные положения современной теории цветности
Электронные переходы в молекулах углеводородов
Молекулы органических соединений могут иметь о-, л- и /7-электроны. Простую, одинарную связь образуют о-электроны. Они прочно удерживаются атомом, и для их возбуждения необходима большая энергия. Например, в молекулах насыщенных углеводородов связи а-С-Н и о-С-С переходят в возбужденное состояние от порций энергии более 800 кДж/моль, что соответствует энергии фотонов дальней ультрафиолетовой части спектра, поэтому молекулы насыщенных углеводородов бесцветны.
В ненасыщенных углеводородах двойная связь образуется л-электронами. л-Электроны более подвижны, легче возбуждаются, и их переход на высший энергетический уровень требует меньших затрат энергии. Однако углеводороды с одной двойной связью или с несколькими изолированными (разобщенными) двойными связями бесцветны, т. к. для их возбуждения также необходима энергия фотонов ультрафиолетовой части спектра.
Сопряжение двойных связей повышает подвижность л-электронов. В органическом соединении с длинной цепочкой сопряженных двойных связей л-элсктроны образуют единое электронное облако, принадлежащее уже не отдельным атомам, а всей молекуле в целом. Чем длиннее цепочка сопряженных двойных связей, тем подвижнее л-электроны и тем меньшие порции энергии нужны для их возбуждения и перевода на высший энергетический уровень. Эту закономерность можно проследить на примере ненасыщенных алифатических углеводородов:
Соединение 1 л'макс^ НМ ДЕ, кДж/моль
Бутадиен СН2=СН-СН=СН2 217 553
Гексатриен СН2=СН-СН=СН-СН=СН2 260 461
Оксатетраен СН2=СН-СН=СН-СН=СН-СН=СН2 302 397
Полосы поглощения, появление которых вызывается электронными (л-*л*)-переходами, обусловленными наличием сопряженной системы в целом, получили название К-полос (от слова «конъюгация» — сопряжение). Отличительной особенностью Х'-полос является
высокая интенсивность (емакс =10 00(Н200 ООО). При дальнейшем удлинении цепи сопряжения энергия возбуждения снижается до значений, соответствующих энергии фотонов видимой части спектра (Х-полоса смещается в длинноволновую часть спектра), и соединение воспринимается человеческим глазом как окрашенное. Например, в молекуле ликопина — красящего вещества томатов — содержится цепочка из одиннадцати сопряженных двойных связей, и длина волны поглощаемого света (Хмакс = 506 нм) обусловливает ярко-красный цвет с синеватым оттенком.
Особое значение для химии красящих веществ имеют замкнутые системы сопряженных двойных связей — ароматические ядра. В молекуле бензола двойные облака шести л-электронов перекрываются друг с другом и образуют единое электронное облако, состоящее из двух кольцеобразных частей, расположенных по обе стороны плоскости ароматического ядра. Это создает дополнительные возможности электронных переходов и соответственно вызывает появление дополнительных полос поглощения. Увеличение числа л-электронов в молекулах ароматических соединений оказывает на цвет такое же влияние, как удлинение сопряженной цепочки в алифатических соединениях: энергия возбуждения снижается и поглощение смещается в длинноволновую область.
Первое положение теории цветности
При наличии в молекулах углеводородов только ординарных (простых) и изолированных (разобщенных) двойных связей, независимо от их числа, поглощение света происходит в дальней ультрафиолетовой части спектра. Поглощение смещается в длинноволновую часть спектра лишь при наличии в молекулах органических соединений открытых или замкнутых систем (цепочек) сопряженных двойных связей. Удлинение сопряженной системы приводит к сдвигу полосы поглощения в сторону более длинных волн (т. е. к углублению цвета, если поглощение происходит в видимой части спектра).
Исключение составляют неальтернантные углеводороды, характеризующиеся специфическим электронным строением молекул.
Электронные переходы в молекулах с гетероатомами
Замена атомов углерода на гетероатомы в молекулах с сопряженными двойными связями оказывает определенное влияние на электронный спектр соединения. Так как гетероатомы (азот, кислород, сера и др.) имеют не-поделенные электронные пары, в молекулах возникает возможность иных (помимо су ^о* и л—*л*) электронных переходов. Неподеленные электроны в основном состоянии молекулы занимают несвязывающие /7-орбитали, энергетический уровень которых является промежуточным для простых молекул между уровнями связывающих и разрыхляющих орбиталей. Вследствие
668
Новый справочник химика и технолога
этого переход одного электрона с несвязывающей п-орбитали на разрыхляющую орбиталь требует значительно меньших затрат энергии, чем соответствующий переход со связывающих а- и л-орбиталей. Наиболее длинноволновая полоса поглощения, возникающая в результате (/7 >л*)-псрсхода, называется /?-полосой (от слова «радикал»). Отличительной особенностью R-полос является низкая интенсивность: обычно £макс 100 и не бывает больше 2000. Причиной этого является различная симметрия орбиталей /7-электронов гетероатома и л-элсктронов связи: оси симметрии этих орбиталей взаимно перпендикулярны, и нет условий для взаимного перекрывания орбиталей. В таких случаях вероятность электронного перехода мала (запрет по симметрии), а следовательно, мала и интенсивность полосы поглощения.
В отличие от гетероароматических соединений, поглощение которых сравнительно мало отличается от поглощения соответствующих ароматических соединений, замена атомов углерода гетероатомами в алифатических участках сопряженных систем часто весьма сильно сказывается на положении полосы поглощения. Это видно, например, при сравнении гидрола Михлера [4,4'-бис(Л( А-диметиламино)дифенилкарбоний хлорид (4)]; и красителя Зеленый Биндшедлера [4,4'-бис(МА-диметиламино)дифениламмоний хлорид (5)].
(H3C)2N—/ У-СН=/ V=N(CH3)2 VzzV \=/ ci Хмакс = 603,5 нм (синий)
(4)
(h3c)2n—# 7~n=\ /^n(ch3)2
\=/ \=/ С1 Хмакс = 726 нм (зеленый) (5)
В подобных случаях проявляется одно из свойств нечетных альтернантных систем. Однако батохромное смещение длинноволновой полосы поглощения происходит лишь в том случае, если гетсроатом, замещающий данный атом углерода, более электроотрицателен по сравнению с углеродом. Если электроотрицательность гетероатома меньше, чем у углерода, полоса поглощения смещается в коротковолновую часть спектра.
Второе положение теории цветности
Включение в молекулы соединений с сопряженными двойными связями гетероатомов изменяет уровни энергии их связывающих и разрыхляющих молекулярных орбиталей и приводит к появлению несвязывающих молекулярных орбиталей. Эти изменения сопровождаются большим или меньшим батохромным или гипсо-хромным сдвигом полос поглощения в электронных спектрах и появлением новых полос, обусловленных электронными переходами с участием несвязывающих молекулярных орбиталей. Характер всех изменений
зависит от природы гетероатома и от положения гетероатома в сопряженной системе.
Поляризующие заместители
Переход молекулы с сопряженными двойными связями в возбужденное состояние связан с ее поляризацией, т. е. с появлением положительного заряда на одном конце молекулы и отрицательного — на другом. Введение в такую молекулу заместителей вызывает постоянное, нс зависящее от поглощения света, смещение л-электронов.
Заместители делятся на две группы: электронодонорные (ЭД) и электроноакцепторные (ЭА). Электронодонорные заместители обладают неподеленными электронами (р-электронами), способными вступать во взаимодействие с л-электронами цепочки сопряженных двойных связей, отталкивая их и, в конечном счете, включаясь в общую л-электронную систему молекулы, например:
бутадиен
(H5C2)2NX^X^CH2
диэтиламинобутадиен
В случае диэтиламинобутадиена полярная структура вносит значительный вклад уже в основном состоянии. Следовательно, переход молекулы диэтиламинобутадиена в возбужденное состояние, в котором полярная структура становится главной, требует меньших энергетических затрат (ДЕ = 428 кДж/моль), чем в случае незамещенного бутадиена (553 кДж/моль), что соответствует поглощению света с Хмакс = 281 нм (у бутадиена ^макс = 217 НМ).
В молекулах ароматических соединений, содержащих сильные ЭД-заместители, возможны электронные переходы, сопровождающиеся переносом неподеленных электронов заместителя на ароматическое кольцо; соответствующие полосы поглощения называются полосами переноса заряда (ПЗ). Эти переходы для молекул анилина и фенола можно представить следующим образом:
П30Н 7-макс = 210,5 нм, 6200 (в воде)
Ароматические соединения
669
Символ ПЗэд означает перенос заряда с ЭД-группы на кольцо (к). Полосы ПЗ часто сливаются с полосами (л—>-71*)-11ереходов в ароматическом кольце, которые под влиянием заместителей сами претерпевают батохромный сдвиг по сравнению с незамещенным соединением.
Наиболее важными ЭД-заместителями являются свободные и замещенные амино-, гидрокси- и меркаптогруппы.
ЭА-Заместителями называют такие заместители, которые способны притягивать к себе электроны. Они содержат двойную связь, и их влияние на углубление окраски органических соединений особенно сильно сказывается в том случае, если они связаны с сопряженной системой двойных связей. К этим заместителям относятся: нитрогруппа (—NO2), нитрозогруппа (—N=O), карбонильная группа [—С(О)~], кетониминная (хинониминная) группа [—C(O)NH—] и др. Подобно ЭД-заместителям, они создают некоторое постоянное, не зависящее от действия света смещение л-электронов в сопряженной системе, усиливают их делокализацию в основном состоянии молекулы и увеличивают вклад полярной структуры. Это приводит к уменьшению энергии возбуждения и соответственно к сдвигу полосы поглощения в длинноволновую область. При введении сильных ЭА-заместителей в ароматическое кольцо возникает возможность электронных переходов с переносом тт-электронов ароматического кольца на ЭА-группу, и в электронном спектре появляются соответствующие полосы ПЗ.
Особенно сильное влияние на электронный спектр оказывают ЭД- и ЭА-заместители при одновременном действии, если они находятся на противоположных концах цепи сопряжения. Совместное действие поляризующих заместителей противоположного характера приводит обычно к резкому сдвигу полосы поглощения в сторону более длинных волн не только по сравнению с незамещенным соединением, но и с любым из соответствующих монозамещенных. При одновременном введении сильных ЭД- и ЭА-заместителей в сопряженные положения ароматического кольца (например, в «дря-положение) появляются полосы переноса заряда с донора на акцептор (ПЗ ). Это интенсивные длинноволновые полосы, обычно перекрывающие длинноволновые полосы локальных (л^л*)-псрсходов в ароматическом кольце. Перенос электронной плотности в молекулах «-нитроанилина (6) и «-нитрофенола (7) можно представить следующим образом, см. схему 4.3.1.
Делая Ti-электронную систему более подвижной, ЭД- и ЭА-заместители увеличивают вероятность электронных переходов, т. е. вероятность избирательного поглощения фотонов, переводящих молекулу из основного состояния в возбужденное. Это приводит к увеличению интенсивности поглощения света, т. е. увеличивается интенсивность окраски соединения. Высокая интенсивность поглощения (высокий мольный коэффициент поглощения, Емакс) является типичным признаком красителей, отличающим их от других соединений, обладающих окраской.
n3NH^ Чакс = 286 нм’ ^макс = 14 000 (в гексане)
Схема 4.3.1
Третье положение теории цветности
Введение в молекулы органических соединений с сопряженными двойными связями поляризующих ЭД-и ЭА-заместителей, обусловливающих постоянное, не зависящее от действия света смещение электронов в сопряженной системе, приводит к сдвигу полос поглощения в длинноволновую область спектра (т. е. к углублению окраски) и к увеличению интенсивности поглощения (т. е. интенсивности окраски) и может привести к появлению в спектре дополнительных полос переноса заряда.
Ионизация молекул
Влияние поляризующих ЭД- и ЭА-заместителей в молекулах органических соединений может быть усилено или ослаблено ионизацией. Для красителей наибольшее значение имеет ионизация таких ЭД-замес-тителей, как гидроксигруппа (-ОН), аминогруппа (-NH2), меркаптогруппа (-SH), и таких ЭА-замести-телей, как карбонильная группа (-С(О)-) и кетониминная группа (-С(МН)-).
Ионизация гидроксигруппы и меркаптогруппы происходит в щелочной среде, в результате протон удаляется от атома кислорода или серы:
-ОН + ОН" -О + Н2О
-SH + ОН“ -S" + Н2О
У атомов кислорода и серы появляется еще одна не-поделенная пара электронов, и они приобретают отрицательный заряд. Превращение нейтральной молекулы в анион значительно усиливает электронодонорность этих групп. Если эти группы входят в состав молекулы красителя, при ионизации происходит сдвиг А.макс в длинноволновую часть спектра и увеличение интенсивности поглощения.
670
Новый справочник химика и технолога
Ионизация аминогруппы происходит в кислой среде и заключается в присоединении протона к атому азота за счет его неподелснной пары электронов, при этом нейтральная молекула превращается в катион:
~NH2 + H ->-NH3+
В результате исчезновения неподеленной пары электронов аминогруппа перестает быть ЭД-замес-тителем; она как бы «выключается» из соединения, и молекула взаимодействует со светом так, как будто этого заместителя вообще нет.
Ионизация ЭА-групп происходит в кислой среде и заключается в присоединении протона к атому кислорода или азота за счет имеющихся у них неподеленных пар электронов, при этом нейтральная молекула превращается в катион:
^С=О + Н+
;с-он
>C=NH + H"-> >C=NH2
Возникновение у ЭА-заместителей эффективного положительного заряда усиливает их электроноакцепторное действие, т. к. увеличивает способность групп -С(О)- и -C(NH)- притягивать электроны.
В молекулах красителей эти свойства заместителей приводят к углублению цвета и усилению интенсивности окраски. Действительно, ионизация 4-амино-фуксонимина (8) сопровождается углублением цвета от желтого до фиолетового: краситель Фиолетовый Дейб-нера [4,4'-диаминотрифенилкарбоний хлорид (9)].
HN
В молекулах соединений, содержащих как ЭД-, так и ЭА-заместители, возможность ионизации увеличивается и соответственно возрастает зависимость окраски от pH среды.
Так, краситель Феноловый красный [(10); Хмакс= 430 нм (желтый)] углубляет цвет в кислой среде за счет ионизации ЭА-заместителя [(11); Хмакс = 503 нм (красный)], а в щелочной среде — ЭД-заместителя [(72); Хмакс= 556 нм (красный)], причем в первом случае интенсивность окраски в 2,2 раза, а во втором — в 2,7 раза больше интенсивности окраски неионизированного соединения.
Четвертое положение теории цветности
Ионизация молекул органических соединений, приводящая к усилению электронодонорности ЭД-замести-телей или электроноакцепторности ЭА-заместителей, сопровождается сдвигом максимума поглощения в длинноволновую область спектра и увеличением интенсивности поглощения. Ионизация молекул, приводящая к уменьшению электронодонорнасти ЭД-заместителей, оказывает противоположное действие.
Конкурирующие и перекрещивающиеся сопряженные системы
Сопряженные системы с одним ЭД- и одним ЭА-за-местителем на концах являются простейшими. Введение в цепь сопряжения второго ЭД-заместителя приводит к тому, что на более близком расстоянии от ЭА-заместителя появляется новая пара подвижных неподеленных электронов. Эти электроны вступают во взаимодействие с ЭА-заместителем по более короткой сопряженной цепочке, чем та, по которой с ним взаимодействует пара электронов первого ЭД-заместителя. Возникающая конкуренция уменьшает постоянное (не зависящее от действия света) смещение электронов на участке между концевым и новым ЭД-заместителями. По своему действию это равносильно укорочению цепи сопряжения и, соответственно, приводит к сдвигу полосы поглощения в коротковолновую область спектра, т. е. к повышению окраски.
Так, присоединение аминогруппы к центральному атому углерода гидрола Михлера [(4); Хмакс = 603,5 нм] повышает цвет от синего до желтого: краситель Аура-мин [амино-4,4'-бис(7У,7У-диметиламино)дифенилкарбо-ний хлорид (13), Хмакс = 420 нм].
Однако введение фенильной группы к центральному атому углерода гидрола Михлера обогащает л-электро-нами сопряженную систему между ЭД- и ЭА-за-местителями, и это приводит к сдвигу максимума полосы поглощения в длинноволновую область. Одновре
Ароматические соединения
671
менно возникает разветвленная сопряженная система, и появляется возможность электронных переходов в конкурирующей цепочке, приводящая к появлению новой полосы поглощения. Вследствие отсутствия в этой цепочке ЭД-замсстителя данный электронный переход требует больших энергетических затрат и сопровождается поглощением света в более коротковолновой части спектра. Вероятность такого перехода меньше, что находит отражение и в меньшей интенсивности второй полосы. В результате разветвления сопряженной системы и возникновения конкурирующей системы в видимой части спектра соединения появляются две полосы поглощения с Хмакс = 621 и 430 нм (рис. 4.3.4). Первая обусловливает дополнительный синевато-зеленый (голубой) цвет, вторая — зеленовато-желтый; результирующий цвет соединения — зеленый: краситель Малахитовый зеленый [4,4'-бис(А,А-диметил-амино)трифенилкарбоний хлорид (14)].
характерной для гидрола Михлера, возможны переходы и в двухзвенной сопряженной системе между атомом кислорода в гетероцикле и тем же ЭА-заместителем. В результате длинноволновая полоса поглощения гидрола Михлера (Хмакс = 603,5 нм) в молекуле Пиронина смещается гипсохромно — до Хмакс = 550,5 нм, и появляется вторая полоса поглощения с Хмакс = 510 нм.
(H3C)2N:
(H3C)2N:
(/5)
Если новый ЭД-заместитель или новая сопряженная цепочка присоединяются к молекуле в таком положении, что между ними и имеющимися заместителями или отдельными участками молекулы сопряжение невозможно, возникает перекрещивающаяся сопряженная система. Эта система характеризуется тем, что отдельные участки ее одновременно входят в несколько ква-зиавтономных сопряженных систем. В этих случаях возможные электронные переходы по затратам энергии мало отличаются друг от друга, и в спектре появляются близко расположенные полосы, сливающиеся в одну широкую полосу. В результате получаются неяркие оттенки («с примесью серого») — коричневатые, черноватые.
Так, в молекуле красителя (16) азогруппы и связанные с ними нафталиновое и бензольное ядра не сопряжены друг с другом, тогда как центральное бензольное ядро и обе гидроксигруппы в нем находятся в сопряжении с каждой из азогрупп и связанным с нею ароматическим остатком. Вследствие этого в центральном бензольном ядре перекрещиваются две квазиавтономные сопряженные системы, причем л-электроны этого ядра и неподеленные электроны гидроксигрупп участвуют в обеих сопряженных системах. В результате возникает возможность ряда электронных переходов с образованием различных возбужденных предельных структур, и в спектре красителя появляются близко расположенные полосы, сливающиеся в одну широкую полосу (рис. 4.3.3), характерную для светло-коричневого красителя (оранжевый с примесью серого).
Конкурирующие сопряженные системы могут возникнуть и при замыкании новых гетероциклов. Например, молекула Пиронина (15) отличается от молекулы гидрола Михлера наличием кислородного мостика между бензольными ядрами, поэтому наряду с электронным переходом в пятизвенной сопряженной системе,
(/6)
672
Новый справочник химика и технолога
Пятое положение теории цветности
При введении в молекулы органических соединений новых заместителей, введении или замыкании новых ароматических или гетероароматических циклов могут возникать конкурирующие разветвленные или перекрещивающиеся сопряженные системы. В первом случае полоса поглощения смещается в коротковолновую часть спектра, и появляются новые полосы поглощения; если новые полосы находятся в видимой части спектра, образующаяся окраска является результатом сложения всех дополнительных цветов. Во втором случае происходит расширение полосы поглощения и образование окраски, отличающейся неярким оттенком.
Влияние пространственных факторов
Большое влияние на поглощение света органическими соединениями оказывает пространственное расположение атомов в их молекулах. Если молекула расположена в одной плоскости (копланарна), то происходит перекрывание облаков л-электронов, облегчается их смещение по цепочке сопряженных двойных связей. Нарушение плоскостности молекулы затрудняет взаимодействие л-электронов. Для перевода такой молекулы в возбужденное состояние требуются дополнительные энергетические затраты для восстановления плоской структуры, вследствие чего возрастает уровень энергии молекулы в возбужденном состоянии, а следовательно, и энергия возбуждения, что сказывается на поглощении света: максимум поглощения сдвигается в сторону более коротких волн (цвет повышается).
Чаще всего копланарность молекулы нарушается вследствие свободного вращения отдельных частей молекулы вокруг простой С-С-связи. Например, в молекуле бинафтила (77) возможен поворот двух нафталиновых ядер вокруг о-связи С-С, что нарушает сопряжение л-электронов ароматических ядер, поэтому бинафтил — бесцветное соединение. Перилен (18) отличается от бинафтила наличием второй связи между ароматическими ядрами, молекула его имеет плоскую
форму, вследствие чего все л-электроны беспрепятственно взаимодействуют друг с другом, и соединение окрашено в желтый цвет.
Хмя = 291 нм
MdKv
(бесцветный)
(/7)
Иногда из-за поворота вокруг связи Сар—Сар цепь сопряжения фактически разрывается, и каждая независимая сопряженная часть молекулы поглощает «свои» фотоны. В этом случае в красителях наблюдается так называемый эффект внутримолекулярного смешения цветов. Например, зеленый цвет азокрасителя (19), в молекуле которого вращение вокруг связи Сар—Сар между бензольными кольцами нарушает единую цепь сопряжения, соответствует цвету смеси желтого (20) и темно-синего (21) красителей, которые образуются при фактическом разрыве молекулы (19) по месту этой связи.
Если искажение формы молекулы происходит без значительного нарушения се плоской структуры и заключается в изменении нормальных углов между направлениями связей атомов, то сопряжение л-электронов существенно не нарушается, т. к. оси симметрии их облаков остаются параллельными. Однако возникающее в молекуле напряжение приближает уровень ее энергии в основном состоянии к уровню энергии возбужденного состояния, снижая тем самым энергию возбуждения, и в электронном спекгре наблюдается сдвиг полосы поглощения в длинноволновую область, т. е. углубление цвета. Это, в частности, отмечается при введении метильной группы в молекулу красителя [(22); ZMaKC = 521 нм], у образовавшегося красителя [(23); лмакс = 542 нм].
HO3S
no2
Ароматические соединения
673
Шестое положение теории цветности
Нарушение плоскостности молекул в результате свободного вращения вокруг простой связи приводит к частичному или полному разобщению отдельных участков сопряженной системы, что сопровождается сдвигом полосы поглощения в коротковолновую область спектра (т. е. повышением цвета). Изменение валентных углов атомов под влиянием пространственных затруднений, происходящее без нарушения плоскостности молекулы, сопровождается сдвигом полосы поглощения в длинноволновую область (т. е. углублением цвета).
Комплексообразование с металлами
Любые изменения в хромофорной системе красителя влияют на окраску соединения. Довольно часто в молекулу красителя вводится ион металла, образующий с красителем комплексное соединение.
Атом металла связывается с кислородом гидроксигруппы или азотом аминогруппы, замещая атом водорода, а с карбонильным кислородом или азотом в азогруппе, имеющим неподсленную пару электронов, образует координационную (донорно-акцепторную) связь.
Поскольку атомы кислорода или азота, отдающие свою неподеленную пару электронов металлу, включены в цепочку сопряженных связей, то изменение их электронных оболочек приводит к изменению поглощения света. Возникающая окраска зависит от природы металла-комплексообразователя, т. к. он, включаясь в сопряженную систему, влияет на нее своей электронной оболочкой и зарядом ядра. Например, 1-нитрозо-2-нафтол (24) — соединение оранжево-желтого цвета, образуя комплексное соединение с солями железа, становится зеленым, с солями хрома — оливковым, с солями кобальта — красно-коричневым.
Если при комплексообразовании электронная оболочка атомов, входящих в сопряженную систему, существенно не изменяется, то углубления цвета не происходит. Так, азокрасители — производные салициловой кислоты, например (25), образуют комплекс с металлом за счет неподеленных электронов кислорода карбоксильной группы, не входящей в главную цепь сопряжения, и окраска соединения при комплексообразовании фактически не меняется.
Седьмое положение теории цветности
Если при образовании внутрикомплексного соединения с металлом координационная связь возникает за счет неподеленной пары электронов атома, который входит в систему сопряженных двойных связей, ответственную за поглощение света, комплексообразование приводит к углублению света.
Таким образом, ответственной за цвет красителя является его хромофорная система. Основой хромофорной системы является в простых случаях достаточно длинная цепь сопряженных двойных связей, а в более сложных — несколько (две и больше) изолированных, конкурирующих или перекрещивающихся цепей сопряженных двойных связей в составе единой молекулы. В хромофорную систему входят все присоединенные к сопряженным цепям ЭД- и ЭА-заместители и заместители, усиливающие или ослабляющие их элскгронодо-норность и электроноакцепторность, а также комплексообразующие заместители и атомы металлов-комп-лексообразователей.
4.3.4. Классификация и номенклатура красителей
4.3.4.1. Химическая классификация
Первая химическая классификация красителей была основана на хромофорно-ауксохромной теории цветности, затем красители классифицировали по сходству химического строения. Принятая в настоящее время химическая классификация красителей основана на сходстве химического строения хромофорных систем красителей, их химических свойств и методов получения. По этим признакам все синтетические красители разделены на следующие классы.
674
Новый справочник химика и технолога
Полиметиновые красители. Хромофорная система полиметиновых красителей характеризуется наличием цепи сопряженных двойных связей, состоящей из свободных или замещенных метиновых групп с ЭД- и ЭА-заместителями по концам.
--С=Й-С=А
I I I R R' R" —in
Полициклохиноновые (антроновые) красители. Хромофорная система этих красителей характеризуется наличием замкнутой системы сопряженных двойных связей, состоящей из значительного числа конденсированных ароматических колец, с двумя ЭА-заместителями в виде карбонильных групп. Красители этого класса делятся на следующие группы.
1. Красители группы дибензопиренхинона.
2. Красители группы антантрона.
3. Красители группы пирантрона.
4. Красители группы дибензантрона.
4. Красители группы ацедиантрона.
Нитро- и нитрозокрасители. Хромофорная система этих красителей состоит из замкнутой (ароматической) цепи сопряженных двойных связей, к которой присоединены ЭД-заместитель и нитро- или нитрозогруппа в качестве ЭА-заместителя.
О i// —Ar-N —Ar—N=O
\ О
Арилметановые красители. Цепь сопряженных двойных связей, составляющая основу хромофорной системы арилметановых красителей, состоит из двух ароматических колец, способных существовать в хиноидной форме, ЭД- и ЭА-заместителей и соединяющего кольца центрального атома углерода.
ЭД- Аг— С- Аг — ЭА ЭА'= Аг~ С- Аг'— ЭД'
R R
Арилметановые красители делятся на следующие группы.
1. Собственно арилметановые красители.
2. Ксантеновые красители.
3. Акридиновые красители.
Антрахиноновые красители. Для хромофорной системы антрахиноновых красителей характерно наличие двух несущих ЭД-заместители ароматических колец, которые связаны двумя карбонильными группами — ЭА-заместителями, разобщающими их сопряженные системы. Красители делятся на следующие группы.
1. Гидроксиантрахиноновые (ализариновые) красители.
2. Аминоантрахиноновые красители.
3. Ациламиноантрахиноновые красители.
4. Антримиды.
5. Антрахинонилоксадиазоловые красители.
Ариламиновые красители. Цепь сопряженных двойных связей, составляющая основу хромофорной системы ариламиновых красителей, состоит из двух ароматических колец, способных существовать в хиноидной форме, ЭД- и ЭА-заместителей и соединяющего кольца центрального атома азота.
ЭД-Аг-К=Аг'=ЭА ~ ЭА'=Аг=Ы-Аг'-ЭД'
Ариламиновые красители делятся на следующие группы.
1. Собственно ариламиновыс (хинониминовые) красители.
2. Оксазиновые красители.
3. Тиазиновые красители.
4. Диазиновыс красители.
Азометиновые красители. Для хромофорной системы азометиновых красителей характерно наличие цепи сопряженных двойных связей, в которую в качестве одного или нескольких звеньев входят азометиновые группы.
R-CH=N-R',
где R и R' = Aik или Аг.
Азокрасители. Для хромофорной системы азокрасителей характерно наличие цепи сопряженных двойных связей, в которую входят одна или несколько азогрупп.
R-N=N-Ar'-N=N-Ar"-
где R = Aik или Аг.
По числу азогрупп в хромофорной системе азокрасители разделяют на моноазокрасители (одна азогруппа), дисазокраситсли (две азогруппы), трисазокрасители (три азогруппы) и т. д.
Формазановые красители. Хромофорная система этих красителей характеризуется наличием цепи сопряжения, состоящей из азо- и гидразонной групп и соединяющего их центрального атома углерода.
Ar-N=N-CH=N-NH-Ar' ~ Ar-NH-N=CH-N=N-Ar'
Формазановая группировка может существовать в двух таутомерных формах, причем наряду с линейной структурой возможна циклическая (хелатная) структура с внутримолекулярной водородной связью.
Индигоидные красители. Для хромофорной системы индигоидных красителей характерно наличие внут-риионизированной цепи сопряжения, часть звеньев
Ароматические соединения
675
которой входит в состав гетероциклических остатков; по концам цепи находятся ЭД- и ЭА-заместители.
дигидропиримидиндиона (28) или имидазодигидропи-ридона (29).
(29)
Здесь X — гетероатом (N, S, О, Se и др.), А — группа атомов, образующих вместе с атомами углерода пятичленный или шестичленный ароматический или гетероциклический цикл.
В зависимости от природы циклических систем, из которых построены молекулы индигоидных красителей, они делятся на следующие группы.
1. Бис(индол)индигоиды.
2. Бис(бензотиофен)индигоиды.
3. Индолбензотиофениндигоиды.
4. Индоларен- и бензотиофенарениндигоиды.
Тиазоловые красители. Хромофорная система тиазоловых красителей характеризуется наличием пятичленного гетероцикла с атомами азота и серы — тиазола (26), конденсированного с различными ароматическими кольцами, например с бензольным в случае бензо-Итиазола (27).
(26)
Антрахиноногетероциклические красители. Основой хромофорных систем этих красителей являются гетероциклические соединения, конденсированные с антрахиноновым ядром. В зависимости от природы гетероцикла красители делятся на следующие группы.
1. Антраазоловые (антрахиноназоловыс) красители.
2. Нафтоакридиновыс (антрахинонопиридоновые, фта-лоилакридоновыс) красители.
3. Нафтохиноксалиновые (антрахинонопиразиновые, фталоилхиноксалиновые) красители.
4. Динафтофеназиновыс (антрахинонодигидроазиновые) красители.
Антроногетероциклические красители. Для хромофорных систем этих красителей характерно наличие гетероциклических соединений, конденсированных с ядром антрона. В зависимости от природы гетероцикла красители делятся на следующие группы.
1. Нафтохинолиновые (антрапиридоновые) красители.
2. Бензоперимидиновые красители.
3. Нафтоиндазолоновые (пиразолантро новые) красители.
4. Диазапирантреновые красители.
Периноновые красители. Хромофорные системы периноновых красителей характеризуются наличием «фм-ариленового остатка, конденсированного с ядром
В зависимости от природы гетероцикла, конденсированного с /?ф«-ариленовым остатком, псриноновыс красители делятся на следующие группы.
1. Азафеналеновые (яерглдикарбоксимидные) красители.
2. Диазаинденофеналеновые (пе/ш-ароиленимидазо-ловые) красители.
Макрогетероциклические красители. Для хромофорной системы макрогетероциклических красителей характерно наличие макрогетероциклов, которые построены из ароматических или гетероароматических колец, связанных мостиками из атомов углерода или гстероатомов.
Макрогетсроциклами (макроциклами), лежащими в основе хромофорной системы, являются шестнадцатичленные циклы — «октаазациклогексадецин» (30; X = Z = N), «тетраазациклогексадецин» (30; X = СН, Z = N), «гексаазадитиациклогексадецин» (30; X = N, Z = S), четырнадцатичленный цикл — «гексаазацикло-тетрадецин» (31) и др.
(31)
В зависимости от химической структуры макроцикла красители делятся на следующие группы.
1. Фталоцианиновые красители.
2. Сопряженные и несопряженные аналоги фталоцианина.
3. Порфирины.
4. Гексаазациклотетрадециновые красители.
Химическая классификация красителей удобна при изучении химического строения соединений, способов синтеза красителей, изучения зависимости различных свойств красителей от их строения.
4.3.4.2. Техническая классификация
При практическом применении красителей их химическое строение имеет второстепенное значение, а наиболее важными являются растворимость и химические свойства. Поэтому наряду с химической классификацией существует техническая, основы которой
676
Новый справочник химика и технолога
были сформулированы в 1896 г. академиком В.Г. Шапошниковым.
Современная техническая классификация красителей учитывает факторы, определяющие способ и области применения красителей, в частности, она позволяет свободно ориентироваться в вопросах применения красителей для крашения волокнистых материалов.
По технической классификации красители делят на следующие классы:
1. Кислотные красители. Представляют собой растворимые в воде соли органических кислот, главным образом сульфо-, реже карбоновых кислот, иногда соли фенолов. В водных растворах диссоциируют с образованием цветных анионов. Компенсирующим катионом большей частью является катион натрия, реже — аммония. Обладают сродством к волокнам, имеющим амфотерный характер (белковые и полиамидные волокна), и окрашивают их из водного раствора в присутствии кислот, вступая в солеобразование с молекулами этих веществ за счет содержащихся в них основных групп (аминогрупп); удерживаются на волокне силами ионных связей. К целлюлозным волокнам сродством нс обладают.
По химическому строению и способам применения кислотные красители делят на фуппы: кислотные обычные красители, кислотные металлсодержащие красители, окрашивающие из сильнокислой ванны (комплексы состава 1:1), кислотные металлсодержащие красители, окрашивающие из слабокислой ванны (комплексы состава 1 : 2) и кислотные антрахиноновые красители.
-► Азокрасители
(от желтых до синих, коричневые, черные)
- ► Антрахиноновые
(фиолетовые, синие, зеленые)
- ► Антроногетероциклические
(красные, рубиновые, фиолетовые)
- ► Арилметановые
(красные, синие, зеленые)
- ► Диазиновые
(синие)
-► Нитрозокрасители (зеленые)
2. Основные красители. Представляют собой растворимые в воде соли органических оснований. В водных растворах диссоциируют с образованием цветных катионов. Компенсирующими анионами обычно являются хлорид-, бисульфат- и оксалат-анионы. Обладают сродством к волокнам, имеющим амфотерный (белковые и полиамидные) и кислотный (ацетатные, полиэфирные, полиакрилонитрильные и т. п.) характер, и окрашивают их из водного раствора, вступая в солеобразование с молекулами этих веществ за счет содержащихся в них кислотных групп (карбоксильные и др.); удерживаются на волокне силами ионных связей. К целлюлозным волокнам сродством не обладают, но
могут окрашивать их после предварительной обработки волокна веществами фенольного характера (таннины, синтетические фенольные олигомеры и т. п.), придающими целлюлозным волокнам слабокислый характер (крашение по танниновой и т. п. протравам).
Основные красители образуют на волокнах очень яркие и чистые окраски, однако устойчивость окрасок к свету и мокрым обработкам низка, поэтому эти красители почти не применяются в текстильной промышленности. Исключение составляют катионные красители — основные красители, специально выпускаемые для крашения полиакрилонитрильного волокна.
Основные красители
Катионные красители
Азокрасители (желтые, коричневые)
Ариламиновые (от красных до зеленых)
Арилметановые (от желтых до зеленых)
— >• Азокрасители (красные, синие)
— > Антрахиноновые (фиолетовые, синие)
— >• Ариламиновые (бирюзовые)
— >• Полиметиновые
(от желтых до красно-фиолетовых)
3. Протравные красители. Представляют собой растворимые в воде (или водно-щелочной среде) красители, содержащие заместители, обусловливающие способность к комплексообразованию с металлами (крашение по металлической протраве). Не обладают достаточным сродством к целлюлозе, но закрепляются на ней после предварительной обработки целлюлозы солями металлов вследствие образования нерастворимого внутрикомплексного соединения (протравные красители для хлопка). При наличии кислотных групп обладают сродством к белковым волокнам (кислотнопротравные красители). Поскольку в комплексообразовании с металлами участвуют не только молекулы красителя, но и молекулы белкового вещества, кислотно-протравные красители удерживаются на белковом волокне как силами ионных связей краситель— волокно, так и силами координационных связей краситель—металл—волокно.
— ► Азокрасители
(от желтых до синих, коричневые, черные)
— >• Антрахиноновые
(от оранжевых до зеленых, коричневые)
— >• Арилметановые
(красные, фиолетовые, голубые)
> Периноновые
(желтые)
—► Фталоцианиновые
(бирюзовые)
Ароматические соединения
677
4. Прямые красители. Представляют собой растворимые в воде соли органических сульфокислот. В водных растворах диссоциируют с образованием цветных анионов, обладающих большой склонностью к ассоциации. Компенсирующими катионами обычно являются катионы натрия, реже — аммония. Обладают сродством к целлюлозным волокнам (хлопок, лен, волокна из регенерированной целлюлозы: вискозное, медноаммиачное и др.) и окрашивают их непосредственно из водного раствора в присутствии электролитов. Переходят на целлюлозное волокно в виде солей и удерживаются на волокне силами водородных связей и силами Ван-дер-Ваальса. Обладают также сродством к волокнам амфотерного характера (шерсть, натуральный шелк, кожа и т. и.) и окрашивают их из водного раствора в присутствии кислот; на волокно переходят в виде анионов и удерживаются силами ионных связей.
По свойствам и способам применения прямые красители делят на группы: прямые обычные красители, прямые светопрочные красители, прямые упрочняемые красители и прямые диазотируемые красители.
стильной промышленности дитионит натрия называют гидросульфитом, что не соответствует формуле Na2S2O4; гидросульфит натрия — это NaHSO3.) в щелочной среде, поэтому кубовые красители применяются главным образом для крашения целлюлозных волокон. Некоторые красители, способные восстанавливаться в слабощелочной среде в мягких условиях, могут применяться для крашения белковых волокон.
—► Антрахиноногетероциклические
(красные,фиолетовые, синие, коричневые)
—► Антроногетероциклические (синие, серые)
Диазиновые
(желтые)
Индигоидные
(оранжевые, красные, 1дэасно-коричневые, синие, черные)
Периноновые
(оранжевые,красные, бордо, коричневые)
Прямые красители
—► Азокрасители
(вся цветовая гамма)
—► Фталоцианиновые
(бирюзовые, зеленые)
—► Полициклохиноновые
(желтые, оранжевые, фиолетовые, синие, зеленые, черные)
—► Фталоилкарбазолы
(желтые, зеленые, коричневые, серые)
5. Активные красители. Представляют собой растворимые в воде соли органических кислот или оснований, содержащих подвижные (активные) атомы или группы, которые в момент крашения отщепляются, или активные (легко раскрывающиеся) связи. Достаточным сродством к окрашиваемым веществам, как правило, не обладают, закрепляются на них силами ковалентных связей, которые образуются между окрашиваемым веществом и красителем за счет отщепления от последнего активных атомов или групп или раскрытия активных связей. Применяются для крашения целлюлозных, белковых и некоторых синтетических волокон.
—► Азокрасители
(от желтых до фиолетовых)
Активные красители
—► Антрахиноновые (синие, голубые)
—► Фталоцианиновые
(бирюзовые, зеленые)
6. Кубовые красители. Представляют собой нерастворимые в воде красители (пигменты), способные восстанавливаться с образованием производных, растворимых в щелочных средах и обладающих сродством к целлюлозным волокнам. После крашения восстановленные соединения окисляются на волокне кислородом воздуха в исходный нерастворимый краситель и удерживаются на волокне вследствие нерастворимости. Восстановление производится большей частью действием дитионита натрия (в анилинокрасочной и тек-
—► Фталоцианиновые (голубые)
7. Сернистые красители. Представляют собой нерастворимые в воде красители, по способу применения аналогичные кубовым, но отличающиеся от них тем, что восстановление в растворимые производные осуществляется действием растворов сульфида натрия. Так как восстановление ведется в сильнощелочной среде, применяются лишь для крашения целлюлозных волокон.
Сернистые красители
►Диазиновые
(бордо, фиолетовые, коричневые, черные)
► Тиазиновые
(синие, зеленые, черные)
► Тиазоловые
(желтые, оранжевые, коричневые)
8. Дисперсные красители. Представляют собой не растворимые или слабо растворимые в воде красители, окрашивающие гидрофобные волокна (ацетатные, синтетические) из водных дисперсий. Процесс крашения заключается в растворении красителя в волокне с образованием твердого раствора. По химическим свойствам и способам крашения дисперсные красители делятся на три группы: дисперсные обычные красители (в том числе для полиэфирных и полиамидных волокон), дисперсные диазотируемые красители, дисперсные металлсодержащие красители.
678
Новый справочник химика и технолога
—► Азокрасители
(от желтых до синих)
Дисперсные красители
—► Антрахиноновые (от оранжевых до синих)
—► Нитрокрасители (желтые)
—► Периноновые
(желтые)
—► Полиметиновые
(желтые)
9. Красители, растворимые в органических средах (жирорастворимые, спирторастворимые, ацетонорастворимые и т. п.). Представляют собой не растворимые в воде красители, применяемые для окрашивания соответствующих органических веществ (углеводородов, восков, жиров, спиртов и т. п.), синтетических волокон в массе, пластических масс, резины.
Азокрасители
(от желтых до красных, коричневые)
Антрахиноновые
(фиолетовые, синие, зеленые)
Ариламиновые
(синие, черные)
10. Пигменты и лаки. Представляют собой не растворимые в воде красители (пигменты) или нерастворимые производные растворимых красителей (лаки). Применяются для изготовления типографских красок и красок для пигментной печати на тканях, а также для окрашивания резины, пластических масс, бумажных и карандашных масс и других целей. Процесс крашения заключается в механическом распределении в связующих веществах, растворах связующих веществ или непосредственно в окрашиваемых материалах.
11. Растворимые производные нерастворимых красителей: кубозоли — растворимые производные кубовых красителей, тиозоли — растворимые производные сернистых красителей, цианалы — растворимые производные макрогетероциклических фталоцианиновых красителей. Выпускаются для упрощения процессов крашения нерастворимыми красителями, повышения качества окрасок и расширения областей применения. Обладают свойствами растворимых красителей (прямых, основных, кислотных) и окрашивают волокна соответствующим способом из водных растворов. После крашения превращаются на волокне в исходные нерастворимые красители или в нерастворимые производные, отличающиеся от исходных, и закрепляются на субстрате вследствие нерастворимости.
12. Нерастворимые красители, образуемые на окрашиваемых материалах — азогены, компоненты для окислительного крашения, кубогены, фталоцианогены. Представляют собой промежуточные продукты, из которых красители синтезируются в момент
крашения непосредственно на окрашиваемом материале. Закрепляются на окрашиваемом субстрате вследствие нерастворимости.
► Азопигменты
(от желтых до красных, розовые)
► Антрахиноновые
(красные, зеленые)
► Антроногетероциклические (желтые)
► Ариламиновые
(фиолетовые, черные)
Пигменты
► Ар илметановые
(розовые, фиолетовые, синие)
► Индигоидные
(красные)
► Нитрозокрасители
(зеленые)
► Периноновые
(оранжевые, красные, бордо)
► Полициклохиноновые
(желтые, оранжевые, фиолетовые, зеленые)
► Фталоцианиновые
(голубые, зеленые)
— ► Азолаки
(от оранжевого до бордо)
— ► Антрахиноновые
(красные)
— ► Арилметановые
(красные, фиолетовые, синие, зеленые)
► Фталоцианиновые
(бирюзовые)
13. Особую группу красителей составляют оптические отбеливатели — вещества, применяемые для усиления эффекта «белизны» неокрашенных материалов. Оптические отбеливатели для целлюлозных волокон представляют собой растворимые в воде соли органических кислот, обладающие сродством к целлюлозным волокнам; соединения ведут себя как прямые красители. Оптические отбеливатели для белковых волокон выпускают в виде растворимых в воде натриевых солей ароматических сульфокислот, которые закрепляются на волокнах подобно кислотным красителям. Для синтетических волокон производят отбеливатели в дисперсной форме.
В настоящее время органические красители применяются в различных областях: цветная фотография, лазерная техника, современная копировальная и множительная техника, производство органических полупроводников и жидкокристаллических материалов, в качестве катализаторов химических процессов и пр.
Ароматические соединения
679
Однако основным назначением красителей по-прежнему является крашение текстильных материалов.
В зависимости от области применения красителей к ним предъявляются определенные требования. Для крашения текстильных материалов значение имеют лишь те красители, которые образуют окраски, достаточно устойчивые к различным физико-химическим воздействиям в процессе эксплуатации окрашенных изделий (устойчивость к действию света, стирке, глажению, поту, трению, химической чистке, дымовым газам и т. п.), а также в процессе переработки окрашенных материалов (устойчивость к щелочной отварке, к активному хлору, т. с. к отбеливанию гипохлоритом, к валке, декатировке, плиссировке и другим обработкам, которым подвергаются текстильные изделия, к вулканизации, которой подвергаются резиновые изделия и т. п.). Светостойкость окрасок оценивают по восьмибалльной шкале:
8 — максимальная устойчивость,
7 — превосходная,
6 — очень хорошая,
5 — хорошая,
4 — удовлетворительная,
3 — умеренная,
2 — низкая,
1 — плохая.
Устойчивость окрасок ко всем остальным воздействиям оценивают по пятибалльной шкале:
5 — оттенок не изменяется,
4 — очень слабое изменение,
3 — значительное,
2 — видимое,
1 — большое.
Устойчивость окрасок к некоторым воздействиям (мокрые обработки и др.) оценивается также по способности противостоять переходу красителя на неокрашенный материал:
5 — не закрашивает,
4 — очень слабое закрашивание,
3 — заметное закрашивание,
2 — сильное закрашивание,
1 — глубокое закрашивание.
Следует иметь в виду, что устойчивость окрасок зависит не только от химической природы красителя, но и от концентрации красителя в красильной ванне, способа крашения и других факторов. Так, для одного и того же красителя устойчивость к стирке и трению тем ниже, чем концентрированнее окраска, а устойчивость к свету, наоборот, с увеличением концентрации окраски повышается. Зависит устойчивость окрасок и от окрашиваемого материала. Например, некоторые основные красители, образующие на хлопковом волокне окраски с низкой светостойкостью, на полиакрилонитрильном волокне обнаруживают исключительную светостойкость.
Современные текстильные волокна делятся на натуральные, искусственные и синтетические. Натуральные волокна бывают животного происхождения — белко
вые (шерсть, шелк, волосы и пр.), и растительного — целлюлозные (хлопок, лен, джут, пенька). Искусственные волокна — это модифицированные целлюлозные волокна (вискозное, ацетатные), придающие несминае-мость тканям. Синтетические волокна — волокна, полученные синтетическим путем (полиамидные, полиэфирные, полиакрилонитрильные и др.). Для каждого вида волокна используются определенные классы красителей.
Активные
-► Индигозоли
Красители для протеиновых Кислотно-протравные волокон (шерсть, шелк) -► Кислотные
Кубозоли
->- Протравные
Красители для целлюлозных волокон (хлопок, лен и др.)
—> Азогены
—► Активные
—► Индигозоли
—>- Кубовые
—► Ку бо гены
—> Кубозоли
—>- Прямые
—> Сернистые
—Тиозоли
—> Фталогены
—>- Азоацеты
(ацетатный шелк, полиэфирные волокна)
—► Дисперсные
(ацетатный шелк, полиамидные, полиэфирные волокна)
—► Катионные
(ПАН-волокно)
—► Пигменты
(для пигментной печати)
4.3.4.3. Номенклатура
Названия первых синтетических органических красителей производились от слов, указывающих на цвет образуемых ими окрасок. Так, название Мовеин указывало на сходство цвета окраски с цветом мальвы, Фуксин — фуксии, Родамин — розы (по-гречески «ро-дон» —- роза), Сафранин — шафрана. Названия желтых красителей — Аурамин, Хризофенин, Хризоидин, Хризамин, Хризанилин происходят от латинского и греческого названий золота — «аурум» и «хризос» соответственно; нежно-розовый краситель Эозин был назван в честь Эос — богини утренней зари в древнегреческой мифологии.
680
Новый справочник химика и технолога
Хотя эти названия ничего не говорят о химической природе и химических свойствах красителей, они удобны своей краткостью и определенностью и быстро стали интернациональными. Положение осложнилось, когда число синтетических красителей превысило многие сотни, а производством их стали заниматься многочисленные конкурирующие между собой фирмы. Стремление скрыть от конкурентов химическую природу красителей, попытки обойти патентные ограничения с помощью новых названий привели к полному хаосу. Нередко одни и те же красители выпускаются различными фирмами, а иногда и одной фирмой, под разными наименованиями (например, краситель Паракрасный имеет около 40 фирменных обозначений, Фуксин — более 100 и т. д.). Чтобы понять, о каком красителе идет речь, в учебной и научной литературе наряду с наиболее употребительными фирменными названиями стали указывать номера, под которыми красители обозначены в специальных справочниках (в немецком, ныне устаревшем справочнике Шульца «Farbstofftabel-1еп», англо-американском — «Colour Index»).
Принятая у нас в стране рациональная номенклатура основана на технической классификации красителей. Названия красителей составляют из двух или более слов и буквенных обозначений. Первое слово показывает принадлежность красителя к той или иной группе: Прямой, Дисперсный, Сернистый, Кубовый, Протравной, Кислотный, Активный, Катионный, Основный, Пигмент, Лак, Кубозоль, Тиозоль, Спирторастворимый, Жирорастворимый, Ацетонорастворимый. Дополнительно в качестве первого слова в названиях красителей применяются также групповые обозначения: Катионный — для специальных основных красителей для полиакрилонитрильного волокна; Тиоиндиго — для кубовых тиоиндигоидных красителей, отличающихся от прочих кубовых красителей способностью восстанавливаться в лейкосоединения не только дитионитом, но и сульфидом нагрия; Хромовый — для кислотнопротравных (хромирующихся) красителей для шерсти; Однохромовый — для хромовых красителей, крашение которыми можно производить одновременно с обработкой солями хрома; Лаковый — для кислотных красителей, специально предназначенных для производства лаков; Белофор — для оптических (флуоресцентных) отбеливателей.
Второе слово в названии красителя указывает на его цвет, буквенный индекс — на оттенок окраски, например: Кислотный синий К.
В некоторых случаях к наименованию красителя прибавляют слова или индексы, указывающие на устойчивость окраски, особенности химического строения красителя, рекомендуемый способ применения или упрочнения окраски, область применения красителя, выпускную форму.
Слово «прочный» в названии красителя указывает, что краситель обладает повышенной устойчивостью к мокрым обработкам; слово «светопрочный» пишется
в названиях красителей, имеющих высокую устойчивость к действию света, например Прямой желтый светопрочный.
На особенность химического строения указывают слова: антрахиноновый, фталоцианиновый и др., например Хромовый зеленый антрахиноновый, а также индексы: Ц — краситель выпущен в виде двойной соли с хлоридом цинка, Бс — в виде бисульфитного производного.
На область применения красителей указывают слова: для кожи, для шелка, полиэфирный, полиамидный и т. д., например Дисперсный синий полиэфирный.
После наименования красителей, выпускаемых в пасте, ставится буква «П», например Кубовый ярко-голубой ЗП.
Для обозначения цвета приняты следующие термины: желтый, золотисто-желтый, оранжевый, алый, красный, розовый, рубиновый, бордо, красно-фиолетовый, фиолетовый, синий, голубой, бирюзовый, сине-зеленый, зеленый, оливковый, желто-коричневый, красно-коричневый, коричневый, серый, сине-черный и черный. Иногда для более точной характеристики цвета через дефис даются обозначения: чисто-, светло-, ярко-, темно- и другие.
Для указания оттенка красителей ставятся буквенные обозначения:
Ж — желтоватый,
К — красноватый,
С — синеватый,
3 — зеленоватый,
О — основной оттенок данного цвета.
Более резко выраженные оттенки обозначают цифрами, которые ставят перед индексами, например: 2Ж, 4Ж, 2К, 4К, 5К и т. д.; не употребляется лишь цифра «3» (т. к. ее путают с буквой «3»).
Кроме перечисленных общих обозначений в каждом классе красителей имеются дополнительные специфические индексы.
Для прямых красителей'.
М — в молекуле красителя имеется комплексносвязанный атом металла;
У — окраска должна быть закреплена солями меди или закрепителем ДЦМ т. е. продуктом конденсации дициандиамида, формальдегида и ацетата меди;
X — окраска может быть закреплена солями хрома;
Ш — краситель предназначен только для крашения шубной овчины.
Для сернистых красителей'.
У — окраска должна быть упрочнена закрепителем ДЦМ или солями меди;
Бс — краситель является бисульфитным производным (для водорастворимых сернистых красителей).
Для кубовых красителей'.
В — краситель в тонкодисперсной форме, предназначен для крашения вискозы в массе;
Д —- краситель в тонкодисперсной форме, предназначен для суспензионного крашения;
Ароматические соединения
681
М — краситель предназначен для крашения меха;
П — паста для печати;
X — краситель окрашивает целлюлозные волокна по «холодному» способу (т. е. при низкой температуре и малой щелочности среды, что позволяет применять эти красители для окрашивания белковых волокон).
Для кислотных красителей:
М — в молекуле красителя имеется комплексносвязанный атом металла;
Н — краситель окрашивает из нейтральной и слабокислой ванн;
Ш — краситель предназначен для крашения шубной овчины.
Для активных красителей:
П — краситель, предназначен для крашения полиамидных волокон;
Т — краситель окрашивает целлюлозные волокна по «теплому» способу (средний между обычным и холодным);
X — краситель окрашивает целлюлозные волокна по «холодному» способу (при низкой температуре);
Ш — краситель предназначен для крашения шерсти.
Для дисперсных красителей:
МП — металлсодержащий краситель для полиамидных волокон.
Для основных красителей:
Ц — краситель выпущен в виде двойной соли с хлористым цинком.
Для пигментов:
У — пигмент (фталоцианиновый) выпущен в особой устойчивой модификации;
ТП — пигменты для текстильной пигментной печати и крашения (тонкодисперсные);
В — пигменты для крашения вискозы в массе;
А — пигменты для крашения ацетатного шелка в массе;
Р — пигменты для крашения резины
Для лаков:
Б, К, М и Н — лак является солью бария, кальция, марганца или натрия соответственно.
Названия красителей, образованные по правилам рациональной номенклатуры, дают исчерпывающие сведения о свойствах, способах и областях применения красителей, а также о свойствах получаемых окрасок. Так, название Кислотный оранжевый светопрочный Н4КМ означает, что это металлсодержащий краситель для шерсти, образующий оранжевые с заметным красноватым оттенком окраски, которые обладают высокой светостойкостью; краситель можно применять для крашения полушерстяных изделий, т. к. крашение им ведут из нейтральной ванны. Название Прямой диазо-бордо светопрочный С указывает на то, что это краситель, способный окрашивать целлюлозные волокна непосредственно из водного раствора в присутствии электролита в цвет бордо с синеватым оттенком; образуемые окраски устойчивы к свету, а устойчивость к стирке может быть повышена путем диазотирования на
волокне и сочетания с соответствующей азосоставляющей (для получения красных окрасок — с 2-гидрокси-нафталином). Название Однохромовый оливковый Ж означает, что это кислотно-протравной краситель для шерсти, окрашивающий ее в оливковый цвет с желтоватым оттенком, причем протравление (обработку солями хрома) можно проводить одновременно с крашением. Аналогично расшифровываются названия и других красителей.
Как исключение из указанных выше правил для некоторых красителей сохранились старые названия: Аурамин, Индиго, Родамин, Сафранин, Эозин и др.
4.3.5. Синтез, строение и свойства красителей
4.3.5.1. Азокрасители
—► Активные
(от желтых до зеленых)
Азокрасители
— ► Дисперсные
(от желтых до фиолетовых)
— ► Катионные
(от желтых до синих) Кислотные
(вся цветовая гамма)
— >• Основные
(оранжевые, коричневые)
— ► Пигменты
(от желтых до бордо)
— >► Протравные
(вся цветовая гамма)
— >• Прямые
(вся цветовая гамма)
Азокрасители являются самой многочисленной и наиболее важной группой органических красителей. На их долю приходится почти треть от всего производства красителей, а по числу представителей они стоят на первом месте среди всех остальных классов красителей. Более 50 % красителей, приведенных в Color Index, относятся к классу азокрасителей.
Азокрасители выгодно отличаются от красителей других групп простотой использования, разнообразием свойств и цветов: в группе азокрасителей представлена вся цветовая гамма — от желтого до черного. Азокрасителями можно окрашивать практически все виды природных, искусственных и синтетических волокон, пластических масс, кожи, бумаги, резиновых изделий и т. д. В настоящее время известно несколько тысяч технически важных азокрасителей самых разнообразных цветов и оттенков. Они представлены во всех классах красителей технической классификации (кроме сернистых и кубовых).
Азокрасители получают путем последовательного проведения двух химических реакций: диазотирования первичных ароматических аминов и азосочетания (сочетания) полученной диазониевой соли с ароматиче
682
Новый справочник химика и технолога
скими и гетероароматическими соединениями, содержащими ЭД-заместители (обычно амино- и гидроксигруппы), и другими реакционноспособными компонентами. В отдельных случаях при получении азокрасителей используют реакции окисления аминосоединений, восстановления нитро- и нитрозосоединений, взаимодействия нитро- и нитрозосоединений с аминами, реакции гидразинов с хинонами, совместного окисления гидразинов или гидразонов с ароматическими соединениями.
Диазотирование
Диазотированием называют взаимодействие первичных аминов с азотистой кислотой, приводящее к образованию соли диазония (уравнение (4.3.6)). Так как азотистая кислота нестойка, на практике применяют ее натриевую соль, поэтому в реакцию вводят дополнительное количество сильной минеральной кислоты для вытеснения азотистой кислоты из ее соли (уравнение (4.3.7)).
ArNH2 + HNO? + НХ — ArN2X + 2Н2О (4.3.6)
ArNH2 + NaNO2 + 2НХ ArN2X + 2Н2О + NaX (4.3.7)
При проведении процесса диазотирования необходимо постоянно контролировать некоторые параметры реакционной массы, а именно: кислотность, температуру и наличие азотистой кислоты. Для каждого амина разработаны определенные условия диазотирования, при нарушении которых могут образоваться побочные продукты. Так, многие диазосоединения могут реагировать с исходным амином, образуя диазоаминосоединения (уравнение (4.3.8)):
ArN2X + H2NAr Ar-N=N-NH-Ar + НХ (4.3.8)
Для предотвращения этой побочной реакции необходимо, чтобы в течение всего процесса диазотирования в реакционной массе был избыток сильной минеральной кислоты, смещающий указанное равновесие влево, и постоянно присутствовал диазотирующий агент, конкурирующий с диазосоединением в реакции с амином. Постоянное присутствие диазотирующего агента достигается введением в реакцию раствора NaNO2 со скоростью, соответствующей скорости диазотирования; например, при диазотировании и-нитро-анилина раствор нитрита приливают с максимальной скоростью, при диазотировании бензидина — в течение нескольких часов. Контроль за наличием в реакционной массе ионов NO2 осуществляют с помощью иодкрах-мальной бумаги (посинение), красителя Метанилового желтого (покраснение) или непрерывным измерением окислительно-восстановительного потенциала системы с помощью редоксметра.
Если образующееся диазосоединение отличается высокой реакционной способностью, а исходный амин способен вступать с ним в реакцию азосочетания, мо
жет образоваться нежелательный побочный азокраситель. Чтобы избежать этого, необходимо создать условия, делающие невозможным побочный процесс. Это достигается понижением температуры реакции, увеличением избытка минеральной кислоты, затрудняющей азосочетание, а иногда применением «обратного порядка» диазотирования, при котором амин все время находится в присутствии большого избытка минеральной кислоты, а диазосоединение — в таких условиях, когда отсутствует избыток непрореагировавшего амина.
Для каждого амина имеется оптимальное значение pH, при котором диазотирование протекает наилучшим образом. Чем меньше основность амина, тем более кислой должна быть среда при диазотировании. Высокоосновные амины диазотируют при pH = 1^3, слабоосновные — при pH < 1.
По окончании диазотирования необходимо избавиться от избытка азотистой кислоты, которая в дальнейшем в процессе азосочетания может вступать в нежелательные реакции с компонентами или продуктами реакции. Для этой цели обычно применяют сульфаминовую кислоту (уравнение (4.3.9)), реже — мочевину (уравнение (4.3.10)), которые быстро реагируют с азотистой кислотой.
HNO2 + H2NSO3H N2 + H2SO4 + H2O (4.3.9)
2HNO2 + (NH2)2CO — 2N2 + CO2 + 3H2O (4.3.10)
Особые случаи диазотирования. При диазотировании о- и и-аминофенолов и аминонафтолов образуются диазофенолы (32) и диазонафтолы (34) соответственно, гидрокси труп па которых сразу же теряет протон и диазосоединения превращаются в амфионы (цвиттерионы), выделяемые из реакции в более стабильном неполярном состоянии. Такие диазосоединения называются хинондиазидами (33) и (35).
Ароматические соединения
683
о-Аминонафтолы под действием азотистой кислоты в среде сильной минеральной кислоты легко окисляются в хиноны, поэтому их диазотирование ведут в присутствии солей: CuSO4, ZnSO4 или ZnCl2; эти соли, гид-ролизуясь, обеспечивают необходимое для диазотирования количество кислоты.
Диазотирование о- и яе/ш-диаминов в производстве азокрасителей не применяется, т. к. при этом образуются устойчивые, не способные к азосочетанию циклические диазоаминосоединения: триазолы (36) и триазины (37).
Диазотирование и-диаминов также практически не применяется: под действием азотистой кислоты они легко окисляются в хиноны или хинонимины. На схеме представлено диазотирование и-фенилендиамина.
Бисазокрасители на основе этих диаминов получают обходным путем, используя я-нитроамины или А-моно-ацил-и-диамин с восстановлением или омылением промежуточно образующихся моноазосоединений и последующим повторным диазотированием и сочетанием. Например:
л/-Фенилендиамины, активно вступающие в реакцию с диазосоединениями, уже в процессе диазотирования образуют азокрасители. Во избежание этого л/-диамины следует диазотировать в присутствии глицерина и других многоатомных спиртов.
Диамины, содержащие аминогруппы в разных не-конденсированных ароматических ядрах (4,4-диаминопроизводные бифенила, стильбена, дифенилметана, дифениламина и др.), а также 1,5-нафтилендиамин диазотируются легко, образуя бисдиазосоединения.
Строение и превращения диазосоединений. Конечным продуктом реакции диазотирования является диазокатион. Строение его описывается резонансными структурами (3<3а) и (3<3б) или формулой (3<3в).
Аг— N= N ► Аг—N= N:
(3<3а) (3<3б)
Аг—N=N
(35в)
Электронная плотность на крайнем атоме азота диа-зониевой группы понижена, и это обусловливает способность диазониевой группы вступать в различные реакции, особенно азосочетания, в качестве электрофильного агента.
Под влиянием среды и заместителей диазосоединения претерпевают ряд превращений, в результате которых изменяются их свойства. Для практического использования диазосоединений наибольшее значение имеет зависимость их строения от pH среды. В кислой, нейтральной, а для некоторых диазосоединений и в слабощелочной средах они имеют строение катиона диазония — единственной частицы, способной вступать в реакцию азосочетания. В щелочной среде катион диазония быстро присоединяет гидроксид-ион и превращается в диазогидроксид (39) — самую нестабильную форму диазосоединения, от концентрации которой зависит степень разложения диазосоединения, количество нежелательных побочных продуктов, смол и пр. Для большинства диазосоединений концентрация диазогидроксида в растворе ничтожно мала (зависит от соотношения константы кислотности диазогидроксида и константы основности диазония), т. к. диазогидроксид, теряя протон, сразу же переходит в емн-диазотат-анион (40a), не способный вступать в реакцию азосочетания. смн-Диазотат-анион неустойчив: при действии кислот он моментально превращается в диазокатион (38), а при нагревании с концентрированными щелочами — в яндим-диазотат-анион (406). awww-Диазотат-анион устойчив: обратный переход его в емн-диазотат-анион для большинства диазосоединений возможен лишь при облучении ультрафиолетовым светом.
+ ОН”
ArN2^± (38) Н +
Аг—N=N—ОН
(39)
684
Новый справочник химика и технолога
Примечание. Кислотно-основное равновесие с участием органического катиона предполагает присутствие в нем трех равновесных форм:
IV ROH RO
(кислота) (амфолит) (основание)
Концентрация каждой равновесной формы в зависимости от кислотности среды может быть определена с помощью следующих формул:
Азосоставляющей, т. е. объектом электрофильной атаки диазосоединения, может быть соединение с повышенной электронной плотностью у атома углерода. Поэтому все азосоставляющие, используемые для синтеза азокрасителей, являются соединениями с ЭД-за-местителями, практически — амино- и гидроксисоединениями.
Активной формой аминосоединений в реакции сочетания является свободный (неионизированный) амин.
А- + АА'
И [„-у
Ar—N2X' +
где [R ]o — исходная концентрация соли.
Максимальная равновесная концентрация амфолита [ROH]MaKC зависит от соотношения констант и Кк и определяется с помощью следующей формулы:
|~R+1
1 + 2—
Кислотность среды, при которой достигается максимальная концентрация амфолита, определяется простым соотношением:
Рп (рА+р^л)
Р 2
Азосочетание
Реакцией азосочетания (сочетания) называют взаимодействие диазосоединений с веществами, в которых замещается атом водорода или иной заместитель у атома углерода, при этом образуются азосоединения (уравнение (4.3.11)):
Ar-N2X + R-Y Ar-N=N-R + Y+ + X” (4.3.11)
Амин, из которого образуется активный компонент реакции — диазосоединение, называется диазосоставляющей, а вещество, с которым диазосоединение реагирует с образованием азосоединения (пассивный компонент), — азосоставляющей.
Сочетание с аминосоединениями можно было бы проводить в щелочной среде, т. к. амин в этих условиях сохраняет свою активную форму. Однако в большинстве случаев в щелочной среде образуются не азосоединения, а диазоаминосоединения (см. уравнение (4.3.8)). Поэтому реакцию азосочетания с аминосоединсниями проводят в кислой, иногда нейтральной среде (pH = 3,5^7,0). Выбор оптимального значения pH такой реакции зависит от основности аминосоединения: чем меньше основность азосоставляющей, тем при более высокой кислотности среды следует проводить сочетание.
Гидроксисоединения (фенолы, нафтолы) могут вступать в реакцию сочетания как в неионизированной, так и в ионизированной (фенолят-ионной) формах. Однако активность ионизированных форм в реакции сочетания приблизительно на 10-12 порядков выше, чем неионизированных, и практически всегда сочетание проводят с фенолят-ионами, для образования которых нужна щелочная среда.
ОН он
Ar—N2X~ +
Ar-N=N
+ н2о +х
Сочетание с большинством гидроксисоединений проводят при pH = 7-5-9. Выбор оптимального значения pH для проведения сочетания в щелочной среде в большей степени зависит от диазосоединения, чем от азосоставляющей, т. к. активность диазосоединения в реакции сочетания определяется содержанием диазокатиона, которое заметно снижается, если pH раствора больше pXR. диазокатиона (см. выше Примечание).
Только с очень активными диазосоединениями сочетание некоторых гидроксисоединений (например, 2-гидроксинафталина) проводят в слабокислой среде (pH = 5-5-7), чтобы уменьшить скорость реакции и избежать образования побочных продуктов из-за повышения температуры (вследствие экзотермичности реакции).
Ароматические соединения
685
Из других соединений практическое значение в качестве азосоставляющих имеют производные пиразо-лона (47) и ацетоуксусной кислоты (42). Они реагируют в виде енолятов, в которых повышенная электронная плотность создается на углеродном атоме метиновой группы.
CONHAr' CONHAr'
Ar-N;X“+ R J2^Ar-N=N^. r . x’+H2O 0H OH
(42)
Азосоставляющие по их реакционной способности в реакциях азосочетания можно расположить в следующий ряд:
ArO > ArN(Alk)2 > ArNHAlk > ArNH2 > ArOAlk
Существуют прямой и обратный порядки сочетания. Прямой порядок применяют, когда реакцию сочетания проводят в щелочной среде: кислый раствор диазосоединения добавляют к раствору азосоставляющей, содержащему щелочной агент; в этом случае обеспечивается необходимая щелочность среды в течение всего процесса. Обратный порядок сочетания часто применяют, если реакцию необходимо вести в слабокислой среде. В этом случае раствор азосоставляющей, содержащей щелочной агент, добавляют к кислому раствору диазосоединения; таким образом в течение всего процесса обеспечивается необходимая кислотность среды.
Важным фактором успешного проведения реакции азосочетания является температура. В щелочной среде диазосоединения неустойчивы, поэтому сочетание в щелочной среде проводят, как правило, при низких температурах: 0-10 °C, в кислой — при 15-20 °C. В случае устойчивых или малореакционноспособных диазосоединений (диазосоединения антрахинонового ряда) сочетание ведут и при более высоких температурах: 40-50 °C.
Весьма перспективным является сочетание в двухфазной системе, состоящей из воды и несмешивающих-ся с водой полярных апротонных растворителей в присутствии катализаторов межфазного переноса (КМП). Этот способ дает возможность успешно сочетать диазосоединения, содержащие в ароматическом ядре атомы галогена, группы -CN, -NO2, -CF3, -CH3SO2, и т. п., с такими не растворимыми в воде, трудно сочетающимися азосоставляющими, как дифениламин, А-бензил-А-этиланилин, карбазол, А-этилкарбазол и др. В качестве
полярных апротонных растворителей пригодны ди-хлорметан, хлороформ, нитробензол и др., а в качестве КМП — калиевые или натриевые соли карбоновых и сульфокислот, содержащих тяжелые алкильные или ароматические остатки, например, соли декановой С9Н!9СООН, 2-додецилтетрадекановой (C12H2s)2CHC;OOH, диизопро-пилнафталинсульфокислоты (mo-QH^CwHjSO^, и-доде-цилбензолсульфокислоты «-Ci2H25C6H4SO3, тетрафе-нилборат натрия (С6Н5)4В Na+ и др.
Частные случаи сочетания. Некоторые амины бензольного ряда (анилин, о- и ц-толуидины, о- и и-ани-зидины и др.) при взаимодействии с диазосоединениями образуют диазоаминосоединения (уравнение (4.3.8)) даже в кислой среде. Чтобы процесс сочетания проходил нормальным образом, т. е. с образованием азосоединений, амины предварительно обрабатывают формальдегидом и бисульфитом. Образующаяся при этом ариламинометансульфокислота (43) сочетается с диазосоединением обычным образом, после чего сульфоме-тильную группу удаляют гидролизом в щелочной среде.
ArNH2 + CH2O +NaHSO3 ArNllCH2SO3Na^
(43)
Ar'N^V xiur^u слл xi Н2О, NaOH
> ArN= N— Ar— N HCH2SO3Na ——----------►
г i X
---► Ar'N= N— Ar------NH2 + CH2O + Na2SO3
Производные анилина, содержащие ЭД-заместители в л/е/ия-положении, благодаря совпадающей ориентации заместителей реагируют с диазосоединениями, образуя обычные азосоединения; л/-фенилендиамин (44) активно сочетается даже до трех раз.
Фенол (45) сочетается в царя-положение по отношению к гидроксигруппе, частично сочетание может идти и в ор/ио-положение, причем увеличение щелочности среды усиливает побочный процесс. В сильнощелочной среде фенол может образовать 2,4-дис-и 2,4,6-трисазосоединения.
Нафтол-1 (46) сочетается дважды: первый раз — в положение 4, второй — в положение 2. Однако в среде уксусной кислоты сочетание идет только в положение 4, в нейтральной и слабощелочной среде образуются два изомера, а в сильнощелочной среде более активным становится положение 2, и при сочетании с диазосоединениями, которые существуют в форме хинондиазидов, реакция сочетания идет только в положение 2.
Нафталинамин-1 (47) сочетается в положение 4, но одновременно (до 15 %) и в положение 2. Сочетание в положение 2 уменьшается при понижении температуры и кислотности среды.
Нафтол-2 (48) и нафталинамин-2 (49) сочетаются энергично только в положение 1, причем, если это положение занято некоторыми заместителями (сульфо-, карбоксильная, арилметильная группы), сочетание происходит с вытеснением этих заместителей.
686
Новый справочник химика и технолога
Если в молекулах сульфозамешенных нафтола-1 и нафталинамина-1 сульфогруппы находятся в положениях 3, 4 или 5 [(50)-(55)], сочетание идет в положение 2. Однако соединения (50) и (52) частично сочетаются в положение 4, при этом образуются изомеры.
1-Аминонафталин-6- и -7-сульфокислоты [(56), (57)] сочетаются преимущественно в положение 4, однако частично сочетаются и в положение 2 (т. с. всегда обра
зуются изомеры). 1,8-Аминонафталинсульфокислота [(55); wepw-кислота] и ее А-фенил- и А-толил-произ-водные сочетаются только в положение 4.
2-Гидроксинафталинсульфокислоты с сульфогруппами в положениях 6; 8; 3,6 и 6,8 [(59)-(62)] сочетаются только в положение 1, хотя сульфогруппа в положении 8 [соединения (60) и (62)] создает пространственные затруднения и резко замедляет реакцию сочетания.
В формулах «*» означает место, по которому проходит первое сочетание, «(*)» — частичное сочетание, «**» — второе сочетание.
При сочетании с азосоставляющими, содержащими одновременно гидрокси- и аминогруппы, решающим для ориентации является то обстоятельство, что элек-тронодонорность аминогруппы выше, чем электроно-донорность неионизированной гидроксигруппы, но ниже, чем электронодонорность ионизированной гидроксигруппы. Соответственно сочетание в кислой и нейтральной средах преимущественно определяется ориентирующим влиянием аминогруппы, а в щелочной — гидроксигруппы. Особенно часто с этим приходится сталкиваться в случае аминонафтолов, у которых гидрокси- и аминогруппы находятся в разных кольцах. К таким соединениям относятся Аш-кислота [4-амино-5-гидроксинафталин-2,7-дисульфокислота (63)], С-кис-лота (4-амино-5-гидроксинафталин-1 -сульфокислота), И-кислота (7-амино-4-гидроксинафталин-2-сульфокислота), Гамма-кислота (6-амино-4-гидроксинафталин-2-сульфокислота), М-кислота (8-амино-4-гидроксинафта-лин-2-сульфокислота) и К-кислота (4-амино-5-гидро-ксинафталин-1,7-дисульфокислота).
Ароматические соединения
687
Если сочетание с этими соединениями необходимо проводить два раза, первое сочетание всегда проводят в кислой среде, т. е. в кольцо, содержащее аминогруппу (как правило, с более активным диазосоединением), а второе — в щелочной среде, т. е. в кольцо, содержащее гидроксигруппу. Если вести процесс в обратном порядке, то второе сочетание (в кислой среде) с образовавшимся в щелочной среде моноазокрасителем протекает настолько медленно, что практически осуществить его с удовлетворительными результатами не удается. Исключение составляет К-кислота, которая достаточно активно сочетается второй раз в кислой среде.
Строение и свойства азокрасителей
Для азокрасителей характерна азо-гидразонная таутомерия, влияющая на многие свойства соединений.
хиногидразонная форма
Отсутствие у хинонгидразонной формы способной к ионизации гидроксигруппы является одной из причин трудной растворимости о-гидроксиазокрасителей в щелочах. о-Аминоазокрасители не способны диазотироваться, т. к. присутствие хинонгидразонной формы превращает их в хинонимины. Так, из двух изомерных красителей (64) и (65), полученных сочетанием одного и того же диазосоединения с Аш-кислотой в кислой и щелочной средах, диазотироваься способен лишь (65).
Затруднения, возникающие при диазотировании некоторых и-аминоазокрасителей в производстве полиазокрасителей, также объясняются образованием неспособной диазотироваться хинонгидразонной формы (66а). Перевод красителя в способную диазотироваться
азоформу (666) осуществляют длительной обработкой его едкой щелочью с последующим высаливанием NaCl и быстрым подкислением в момент диазотирования.
Азо-гидразонная таутомерия лежит в основе индикаторных свойств некоторых красителей, например Метилового оранжевого [4-(4-А,А-диметиламинофени-лазо)бензолсульфокислота (67)] и Конго красного. Так, желтый цвет Метилового оранжевого (67) в кислой среде изменяется на красный [структура (67а)].
Химические свойства азокрасителей
Энергичные восстановители (цинк и чугунная стружка с соляной кислотой, дитионит натрия в щелочном растворе, полисульфиды Na2Sx, SnCl2 и TiCl3 с соляной кислотой и др.) расщепляют азогруппу в красителе, при этом получается исходный амин и азосоставляющая, содержащая дополнительно аминогруппу (уравнение (4.3.12)).
Ar-N = N-Ar'-N = N-Ar" [н]->
ГН1 (4-3J2)
[HJ > ArNH2 + H2NAr'NH2 + H2NAr"
Восстановительное расщепление азокрасителей широко используется при установлении строения и количественном анализе красителей, в текстильной промышленности для вытравной печати по тканям, окрашенным азокрасителями, а также для получения некоторых аминов, которые нельзя получить обычными методами.
Мягкие восстановители (Na2S, Fe2+ в растворе аммиака и др.) не восстанавливают азогруппу. Это свойство используется в производстве азокрасителей для восстановления нитрогруппы в присутствии азогруппы (уравнение (4.3.13)).
Na S
HO-Ar-N = N-Ar'-NO2--------*—>
(4.3.13)
HO-Ar-N = N-Ar'-NH2
688
Новый справочник химика и технолога
Длительное кипячение с водой постепенно разрушает молекулы многих азокрасителей. Процесс ускоряется при нагревании с разбавленными кислотами и щелочами. Концентрированная серная кислота при умеренной температуре сульфирует некоторые азокрасители, а при повышенной температуре разрушает их.
На холоду под действием концентрированной азотной кислоты или галогенов (хлор, бром) азокраситель расщепляется на исходное диазосоединение (68) или (70) и продукт нитрования (69) или галогенирования (71) азосоставляющей, что может использоваться для установления строения азокрасителей.
Для сокращенного изображения структуры азокрасителей принято писать названия компонентов, из которых они получены, и соединять их стрелками. Стрелки всегда направлены от диазосоставляющих к азосоставляющим, а на стрелке помещается цифра, указывающая порядок сочетания (при получении дис- и полиазокрасителей), и буква (к) или (щ), обозначающая, в какой среде — кислой или щелочной — проводится сочетание, например:
II (1;к) Л (2;1Ц) Л
и-Нитроанилин —-——> Аш-кислота <—*----------Анилин
(63) (69)
Такой записи соответствует структурная формула красителя (73):
Практическое значение для производства некоторых азосоставляющих имеет окисление о-аминоазосоеди-нений, приводящее к образованию триазолов (72). Окисление обычно проводят в щелочной среде действием гипохлорита, перманганата и других окислителей.
Присутствие в молекуле азокрасителей способной диазотироваться первичной аминогруппы часто используется для проведения диазотирования после крашения непосредственно на волокне с целью последующего сочетания с азосоставляющими. В результате такой операции обычно значительно возрастает устойчивость окрасок к мокрым обработкам. Соответствующие красители называются «диазотирующимися» и имеют в названии слово «диазо» (например, Прямой диазо-алый).
Мо но азо красители
Моноазокрасители являются простейшими представителями класса азокрасителей. На их примере легко проследить зависимость между химическим строением азокрасителей и их цветом, светостойкостью, сродством к окрашиваемым материалам и другими свойствами. Эти закономерности, присущие моноазокрасителям, а также основные приемы производства сохраняют значение и для более сложных красителей.
Цвет моноазокрасителей зависит от их хромофорной системы, которая определяется природой ароматических и гетероароматических ядер, связанных азо-фуппой, а также числом и положением ЭД- и ЭА-за-местителей. Природа связанных азогруппой остатков определяет границу наиболее высокой окраски азосоединений данного типа. Так, самый высокий (желтый) цвет имеют азокрасители, в которых азогруппа соединяет бензольное ядро и остаток арилида р-кетокислоты или пиразолона; эти красители имеют наиболее короткую цепь сопряжения (5 звеньев). Немного больше цепь сопряжения у красителей на основе азобензола (7 звеньев), и у этих красителей более глубокий (желтооранжевый) цвет. У красителей на основе 1-бензолазонафталина в основной цепи сопряжения 9 звеньев, и этому соответствует оранжевый цвет. Еще «богаче» л-электронами система сопряжения азонафталина; красители — производные азанафталина имеют красный и более глубокие цвета. Вводя различные заместители, можно изменять цвет красителя, но только в сторону углубления по сравнению с его основой.
Среди моноазокрасителей имеются представители большинства классов технической классификации красителей.
Ароматические соединения
689
Дис- и полиазокрасители
В молекулах дис- и полиазокрасителей содержатся две и более азогрупп, Вследствие этого к закономерностям, характерным для моноазокраситслей, прибавляются и специфические закономерности, присущие лишь этим более сложным азокрасителям.
Все дис- и полиазокрасители делятся на две группы: красители с сопряженными азогруппами и красители с разобщенными азогруппами.
Красители с сопряженными азогруппами характеризуются тем, что в их молекулах все ароматические и гетероциклические ядра связаны друг с другом азогруппами:
Ar-N=N--Ar'-N=N~-Ar'' (дисазокрасители)
АгЧЧ=1Ч-Аг'-К=Ь1-Аг"-№=1Ч--Аг"'"-(полиазокрасители)
Цвет красителей с сопряженными азогруппами более глубокий, чем цвет каждого из моноазокрасителей, которые могли бы образоваться из тех же диазо- и азосоставляющих, и чем цвет смеси этих красителей. Например, дисазокраситель (74) имеет алый цвет, тогда как соответствующие моноазокрасители (75) и (76) — желтый и оранжевый, а их смесь — желто-оранжевый.
НО
Красители с разобщенными азогруппами отличаются тем, что в их молекулах часть ароматических и гетероциклических ядер связана друг с другом не азогруппами:
Ar-N=N-Ar'-X-Ar"-N=N-Ar"'
(дисазокрасители)
Ar-N=N-Ar'-X-Ar"-N=N-Ar"'-N=N-Ar""- • • (полиазокрасители с одним разрывом сопряженной системы)
Ar-N=N-Ar'-X-Ar"-N=N-Ar"'-X'-Ar""-N=:N-Ar""'" (полиазокрасители с дважды разорванной сопряженной системой)
К числу важнейших разобщающих атомов, групп и связей (X, X') относятся: метиленовая группа, иминогруппа, атом кислорода, атом серы, амидная группа, карбамидная группа, триазиновое (циануровое) кольцо, этиленовая группа, биарильная связь.
Для красителей с разобщенными азогруппами характерен эффект внутримолекулярного смешения цветов, который выражается в том, что цвет их приблизительно соответствует цвету смеси красителей, которые могли бы образоваться в результате разрыва молекул по месту разобщающихся связей и групп. Например, зеленый цвет трисазокрасителя (77) с разобщающим триазиновым кольцом практически не отличается от цвета смеси голубого дисазокраситсля (78) и желтого моноазокрасителя (79), которые образуются при разрыве связей с разобщающей группой.
NaO3S
соон
(79)
690
Новый справочник химика и технолога
Среди азокрасителей немало таких, в которых нет полного сопряжения между азогруппами, хотя разобщающие группы формально отсутствуют. Это красители с перекрещивающимися сопряженными системами, в молекулах которых азогруппы (все или часть) не входят в единую цепь сопряженных двойных связей. При этом возникает несколько различных сопряженных цепей, отдельные звенья которых являются общими. В результате этого смещения электронов в одной сопряженной цепи накладываются на смещения электронов в другой и получаются размытые полосы поглощения и неяркие тусклые оттенки. К таким красителям относятся продукты сочетания диазосоединений с ^-диаминами и jw-дигидроксисоединениями бензольного ряда [Кислотный светло-коричневый для кожи (76)], 1-ами-но-8-гидроксинафталинсульфокислотами [темно-синий краситель (73)], продукты сочетания бисдиазотиро-ванных jw-диаминов бензольного ряда с азосоставляющими и др.
Все красители с перекрещивающимися сопряженными системами имеют более глубокий цвет, чем каждый из соответствующих моноазокрасителей или их смесь. Среди дис- и полиазокрасителей с перекрещивающимися сопряженными системами преобладают коричневые, серые, коричневато-зеленые, оливковые и черные цвета. Многие из них представляют не меньший практический интерес, чем красители чистых, ярких тонов.
По схемам синтеза дис- и полиазокрасители делятся на три группы: первичные, вторичные и производные диаминов.
При изображении схем приняты следующие обозначения: М — моноамин (диазосоставляющая, например 4-нитроанилин), Д — диамин (бисдиазосоставляющая, например бензидин или .w-фенилендиамин), К — конечная азосоставляющая (сочетается при синтезе данного красителя один раз, например салициловая кислота), С — центральная азосоставляющая (сочетается при синтезе данного красителя два раза, например Аш-кислота, или три раза, например резорцин), А — азосостав ляющая-ам ин (применяется сначала в качестве азосоставляющей, но после сочетания аминогруппа диазотируется и сочетается с новой азосоставляющей; например, 1-аминонафталин). Сложные азосоставляющие, которые представляют собой синтезируемые отдельно азокрасители, заключаются в квадратные скобки (например, краситель из анилина и Аш-кислоты).
Первичные дис- и полиазокрасители получают последовательным сочетанием двух или трех одинаковых или разных диазосоединений с одной азосоставляющей по схемам:
М----► С <---М' М—► С <— М'
(дисазокрасители)
М"
(трисазокрасители)
В качестве центральной азосоставляющей С для синтеза первичных дисазокрасителей с сопряженными азогруппами применяют главным образом резорцин и Аш-кислоту, реже л/-фенилендиамин и другие соединения, способные сочетаться дважды. В качестве центральной азосоставляющей для синтеза первичных трис азокрасителей практически применяют один резорцин.
В результате сочетания двух или трех диазосоединений с перечисленными азосоставляющими образуются красители с перекрещивающимися сопряженными системами. Поэтому в данной группе красителей преобладают цвета коричневые (С — резорцин, л/-фени-лендиамин), черные и темно-зеленые (С — аминогидроксинафталинсульфокислоты).
При синтезе первичных дисазокрасителей с разобщенными азогруппами в качестве центральной азосоставляющей С применяются главным образом производные динафтиламина и динафтилмочевины, чаще других ди-И-кислота [5,5'-дигидрокси-2,2'-динафтил-амин-7,7'-дисульфокислота (<ЭД)] и алая кислота [УУ'-бис(4-гидрокси-2-сульфонафтил-7)мочевина (<$/)]. У красителей, полученных на основе этих соединений, преобладают красные цвета.
Вторичные дисазокрасители получают сочетанием диазосоединения с азосоставляющей-амином, диазотированием образовавшегося аминомоноазокрасителя и сочетанием его с конечной азосоставляющей. При получении вторичных трисазокрасителей промежуточный аминомоноазокраситель после диазотирования сочетают вновь с азосоставляющей-амином (с такой же или другой), диазотируют полученный аминодисазокраси-тель и сочетают его с конечной азосоставляющей. При получении вторичных полиазокрасителей процесс продолжается по той же схеме. Указанная последовательность синтеза изображается так:
М —* А —К (дисазокрасители)
М —» А —» А' -* -* К (полиазокрасители)
В группе вторичных дисазокрасителей есть представители всех цветов от оранжевого до черного. Отсутствуют только желтые красители, т. к. у самого и-бис-(бензолазо)бензола (82) Хмакс = 450 нм и введение
Ароматические соединения
691
одного ЭД-заместителя уже сообщает соединению оранжевую окраску.
(82)
При синтезе красителей с сопряженными азогруппами, имеющих практическое значение, в качестве среднего компонента А обычно применяются соединения, сочетающиеся в «ора-положение к имеющейся аминогруппе. Это анилин, .и-толуидин, крезидин (5-ме-тил-2-метоксианилин), нафталинамин-1 и его замещенные (5-аминонафталин-2- и 8-аминонафталин-2-сульфо-кислоты), а также 5-амино-6-этоксинафталин-2-сульфо-кислота. По влиянию на цвет красителя крезидин занимает промежуточное положение между бензольными и нафталиновыми компонентами, а введение его в состав молекулы обычно повышает светостойкость красителей.
Вторичные дисазокрасители, у которых компоненты М, А, и К относятся к бензольному ряду, имеют оранжевые цвета. Эти красители не имеют большого значения, т. к. они не обладают заметными преимуществами перед более дешевыми оранжевыми моноазокрасителями. Красители, у которых компоненты М и А — производные бензола, а конечный (К) — нафталина, имеют цвета от красного до фиолетового. Если М относится к бензольному ряду, а А и К — к нафталиновому, то цвета дисазокрасителей синие и синевато-черные. Красители, построенные из трех нафталиновых компонентов, имеют глубокие цвета, большей частью черные.
При синтезе промежуточного моноазокрасителя М —» А, если А — амин бензольного ряда, велика вероятность получить вместо необходимого моноазокрасителя диазоаминосоединение. Во избежание этого аминогруппу компонента А временно защищают сульфометилированием, действуя формальдегидом и бисульфитом (см. 4.3.5.1).
При диазотировании промежуточного «-аминоазокрасителя М—>А, если А — амин нафталинового ряда, часто возникают затруднения, связанные со склонностью этих соединений переходить в таутомерную недиазотирующуюся хинонгидразонную форму. В этих случаях моноазокраситель переосаждают из щелочного раствора (см. 4.3.5.1).
Большинство вторичных дисазокрасителей являются кислотными. При введении заместителей, сообщающих повышенное сродство к целлюлозе (амидные группы и др.), получают прямые красители.
Увеличение числа азогрупп в молекулах вторичных азокрасителей с сопряженными азогруппами до трех и более приводит к образованию прямых красителей, обладающих достаточным сродством к целлюлозным волокнам независимо от наличия заместителей, повышающих это сродство. При этом наблюдается уг
лубление цвета красителя. Однако, если количество азогрупп в молекуле красителя больше четырех, цвет красителя повышается из-за нарушения плоского строения молекулы вследствие усиления тенденции к закручиванию вдоль продольной оси. По этой же причине уменьшается сродство красителей к целлюлозным волокнам, но заметно возрастает их светостойкость, поскольку нарушение плоскостности молекулы затрудняет ее таутомерную перегруппировку в хинонгидразонную форму.
Вторичные полиазокрасители с разобщенными азогруппами получают, используя в качестве одного из компонентов соединения типа м- и «-аминобензоил-И-кислоты. В большинстве случаев эти соединения используются в качестве конечного компонента К. При этом получается диазотирующийся краситель, а сложный полиазокраситель с разобщенными азогруппами образуется уже на волокне в результате сочетания с азосоставляющей-проявителем. Так как амидная группа из-за возможной таутомерной перегруппировки в енольную форму не полностью прерывает сопряженную систему, целесообразно в качестве азосоставляющих использовать не и-, а ж-аминобензольныс производные аминов. В этом случае новая азо1руппа образуется в .мета-положении к амидной группе, т. е. не будет с ней сопряжена (83).
Другой способ устранения или ослабления сопряжения заключается в применении соединений из нескольких амидных I’pyuu, например и-аминобензоил-«-ами-нобензоил-И-кислоты {7-[4-(4-аминобензоиламино)бен-зоиламино]-4-гидроксинафталин-2-сульфокислота}(^4).
Азокрасители — производные диаминов. Дисазокрасители этой группы получают по схеме: К «— Д —► К'. Практическое значение имеют красители, получаемые из ж-фенилен- и л/-толуилендиаминов (перекрещивающиеся сопряженные системы), а также красители на основе диаминодиарильных производных (разобщенные сопряженные системы), причем арильные остатки могут быть связаны друг с другом непосредственно (бензидин и его производные) или через различные атомы и группы (-S-; =N-; -СН2-; -СН=СН- и т. п.).
692
Новый справочник химика и технолога
Диазотирование обеих аминогрупп диаминов как в одном ядре, так и в разных ядрах происходит относительно легко, т. е. сразу образуются бис(диазо)сое-динения. Напротив, скорости реакций сочетания, в которые вступают образовавшиеся диазониевые группы, достаточно различны, и вторая диазониевая группа вступает в реакцию только после того, как первая прореагировала полностью. Это позволяет получать как симметричные дисазокрасители — продукты сочетания обеих диазогрупп с одной и той же азосоставляющей, так и несимметричные — продукты сочетания с разными азосоставляющими.
По применению в текстильной промышленности азокрасители можно разделить на группы: дисперсные, основные, катионные, кислотные, протравные, прямые, активные и пигменты.
Дисперсные азокрасители
Дисперсные красители предназначены для крашения ацетатных и синтетических волокон, имеющих гидрофобный характер, плотную упаковку макромолекул и небольшие размеры микропор. Красители с большими размерами молекул не могут проникнуть в плотную структуру этих волокон, поэтому не растворимые или мало растворимые в воде моноазокрасители, имеющие небольшие размеры молекул, являются хорошими дисперсными красителями. В молекулах этих красителей азогруппы соединяют обычно бензольные и нафталиновые кольца, но могут содержать и гетероциклы.
Простейшими (по структуре) дисперсными красителями являются производные и-аминоазобензола (85). Эти красители обладают наибольшим сродством к ацетатным волокнам.
(85)
R, R-Н, СН3, С2Н5, С2Н4ОН и др.
Изменяя характер азо- и диазосоставляющих путем введения ЭД- и ЭА-заместителей, получают дисперсные красители — производные азобензола от желтого до зеленовато-синего цвета.
Обширную группу дисперсных азокрасителей составляют красители, которые получают диазотированием 4-нитроанилина или его производных и сочетанием полученных диазосоединений с алкилированными аминами. В табл. 4.3.2 приведены дисперсные моноазокрасители из этой серии.
Наличие в молекулах красителей гидроксиалкиль-ных остатков облегчает образование высокодиспсрсных суспензий и повышает растворимость дисперсных красителей в горячей воде.
ЭА-Заместитсли (-NO2, -CN, -CHF2, -CF3, -Cl, -Br, -SO2CH3, -COCH3) в пара- или o^wo-положении к азогруппе повышают устойчивость окрасок, уменьшают сублимацию красителей при термических обработках изделий из синтетических волокон. Такое же влияние оказывают эти заместители при введении их в боковую алкильную цепочку замещенных аминогрупп, например:
c2h4cn
—N \ с2н4он
ch2chf2
—N
с2н5
Сублимационная устойчивость красителей возрастает также при увеличении молекулярной массы соединения. Если красители устойчивы к сублимации при 180-200 °C и хорошо диспергируются, то их можно применять для крашения полиэфирного волокна. Название таких красителей включает слово «полиэфирный» (ПЭ).
Применение в качестве диазосоставляющих гетероциклических соединений позволяет получать моноазокрасители более глубоких цветов. Например, краситель [(56); 2-амино-5-метил-3-нитротиофен —» 3-метил-А-(2,3-дигидроксипропил)-Аг-этиланилин] синего цвета, краситель [(57); 2-амино-5-нитротиазол 3-метил-А-(2,3-
дигидроксипропил)-А-этиланилин] — голубого цвета.
O2N
Ароматические соединения
693
Таблица 4.3.2
Дисперсные моноазокрасители
X Y Z R1 r2 Название красителя
н н н н н Дисперсный оранжевый Ж [4-(4-нитрофенилазоанилин]
н н н с2н5 c2h4cn Дисперсный оранжевый [4-(4-нитрофенилазо)-?/-(2-цианоэтил)-?/-этиланилин]
н н н с2н5 С2Н4ОН Дисперсный алый Ж [4-(4-нитрофснилазо)-?/-(2-гидроксиэтил)-?/-этиланилин]
н CN н c2h4cn С2Н4ОС(О)СН3 Дисперсный красный ПЭ [4-(4-нитро-2-цианофенилазо)-/У-(2-ацетоксиэтил)-?/-(2-цианоэтил)анилин]
н С1 н с2н5 С2Н4ОН Дисперсный бордо С [4-(4-нитро-2-хлорфенилазо)-<¥-(2-гидроксиэтил)-?/-этил-анилин]
н С1 СНз С2Н4ОН С2Н4ОН Дисперсный бордо 2С [4-(4-нитро-2-хлорфенилазо)-М^ди(2-гидроксиэтил)-3-метиланилин]
н н н с2н5 c2h4cn Дисперсный рубиновый [4-(4-нитрофенилазо)-?/-(2-цианоэтил)-?/-этиланилин]
н CN н с2н5 c2h4cn Дисперсный рубиновый ПЭ [4-(4-нитро-2- цианофснилазо)-Л^-(2-цианоэтил)-Л^-этил-анилин]
н ОН СНз С2Н4ОН С2Н4ОН Дисперсный рубиновый С [4-(2-гидрокси-4-нитрофенилазо)-/У,?/-ди(2-гидроксиэтил)-2-метиланилин]
С1 С1 н с2н5 c2h4cn Дисперсный желто-коричневый [4-(2,6-дихлор-4-нитрофенилазо)- Л^-(2-цианоэтил)-Л^-этил-анилин]
С1 С1 н с2н5 С2Н4ОН Дисперсный красно-коричневый [4-(2,6-дихлор-4-нитрофенилазо)-?/-(2-гидроксиэтил)-Л-этил анилин]
н no2 СНз С2Н4ОН С2Н4ОН Дисперсный фиолетовый 4К [4-(2,4-динитрофенилазо)-Л(Л\ди(2-гидроксиэтил)-3-мстил-анилин]
В качестве гетероциклических диазосоставляющих при получении моноазокрасителей чаще других используют 2-амино-6-метоксибензотиазол (88), 2-амино-6-нитробензотиазол (89) и 3-амино-1,2,4-триазол-5-карбоновую кислоту (90).
H3COx/^S °2N\^^S
U />~NH2 Ц ДГ NH2
(88) (89)
N-N
Л к
HOOC^n/^NH2 н (90)
Дисперсные азокрасители, молекулы которых содержат гетероциклы, образуют на волокнах яркие, но недостаточно устойчивые окраски; поэтому красители, имеющие в гетероциклах атомы азота, способные переходить в онисвое состояние, обычно применяют как промежуточные продукты для получения катионных красителей.
Дисперсные моноазокраситсли, содержащие свободную аминогруппу в wapa-положении к азогруппе, способны диазотироваться на волокне. Эти красители, как и прочие дисперсные красители, окрашивают химические волокна из водной суспензии, но затем краситель на волокне диазотируют и сочетают с различными азосоставляющими (фенол, нафтолы, производные пи-разолона и др.), в результате чего происходит значи
694
Новый справочник химика и технолога
тельное углубление цвета. Азосоставляющие, при взаимодействии с которыми изменяется окраска, называют проявителями. В названии такого красителя указывается цвет, возникающий после проявления на волокне, и добавляется слово «диазо». Наиболее часто на практике применяют два красителя из этой группы: Дисперсный диазо-синий 3 [5-метил-2-мстокси-4-(4-нитрофенилазо)анилин (9/); 4-нитроанилин -» 5-метил-2-метоксианилин] и Дисперсный диазо-черный С [4-(4-аминофенилазо)нафталинамин-1 (93)], полученный восстановлением нитрогруппы в красителе [4-(4-нитро-фенилазо)нафталинамин (92); 4-нитроанилин —> нафта-линамин-1].
(92) (93)
кулы азокрасителя связаны с одним атомом металла (кобальта или хрома); красители не растворимы в воде. При синтезе большинства красителей этой группы в качестве диазосоставляющих используют нитропроизводные о-аминофенолов, в качестве азосоставляющих— 3-метил-1-фенилпиразолон-5 (красители оранжевого и красного цвета) и 2-нафтол (красители фиолетового, бордового и серого цветов). Так, краситель Дисперсный оранжевый МП {натриевая соль бис[3-метил-4-(2-оксидо-5-нитрофенилазо)-5-оксидо-1-фенил-пиразол]кобальта(Ш) (94}} представляет собой кобальтовый комплекс состава 1 : 2 азокрасителя (2-амино-4-нитрофенол —* 3-метил-1-фенилпиразолон-5). При использовании в качестве азосоставляющей 2-нафтола происходит углубление окраски и получается краситель Дисперсный фиолетовый СМП {натриевая соль бис[2-оксидо-1-(2-оксидо-5-нитрофснилазо)нафталин]кобаль-та(Ш)(95)}.
Полученные на волокне красители по своему строению относятся к полиазокраситслям, т. к. содержат больше одной азогруппы. Так, после крашения красителем (93), диазотирования и сочетания, например, с 2-гидрокси-З-нафтойной кислотой внутри волокна образуется черный краситель следующего строения:
(95) М = Со; (96) М = Сг
Дисперсные металлсодержащие азокрасители. Окраски с высокой устойчивостью ко всем физико-химическим воздействиям на полиамидных волокнах можно получить с помощью дисперсных металлсодержащих красителей, которые выпускаются с маркой МП (металлсодержащие для полиамидов). Они представляют собой комплексы состава 1 : 2, в которых две моле-
На цвет красителя оказывает влияние природа ме-талла-комплексообразователя, т. к. он включен в сопряженную систему и влияет на нее своей электронной оболочкой и зарядом ядра. Так, хромовый комплекс того же азокрасителя (2-амино-4-нитрофенол -» 2-нафтол), из которого получают Дисперсный фиолетовый СМП, имеет серый цвет и выпускается под названием Дисперсный серый СМП {натриевая соль бис[2-
Ароматические соединения
695
оксидо-1-(2-оксидо-5-нитрофенилазо)нафталин]хро-ма(Ш) (96)}.
Основные и катионные азокрасители
Основные и катионные азокрасители растворимы в воде; они диссоциируют с образованием окрашенных катионов и окрашивают волокна, содержащие группы кислотного характера. Молекулы этих красителей содержат свободные или алкилированные аминогруппы и не содержат ни сульфо-, ни карбоксильных групп.
Основные красители выпускаются в виде солянокислых солей органических оснований с общей формулой ArNH3Cl. Наибольшее значение из основных азокрасителей имеют Хризоидин [4-фенилазобензолди-амин-1,3 (97); анилин -> jw-фенилендиамин] — краситель красновато-оранжевого («золотистого») цвета и Основной коричневый 2К [(95); 2,4-диаминотолуол -> 2,4-диаминотолуол], являющийся смесью дис-[2,4-бис-(2,4-диамино-5-метилфснилазо)толуол] и моноазокрасителя [4-(3-амино-4-метилфенилазо)-2-метилбснзолди-амин-1,5].
(95)
Основные красители отличаются исключительной яркостью и чистотой оттенков, однако они образуют окраски с очень низкой устойчивостью к свету и мокрым обработкам и поэтому почти не применяются в текстильной промышленности. Эти красители используются для окраски бумаги, в производстве цветных карандашей, для приготовления чернил и туши, в парфюмерной промышленности и медицине.
Большое значение для текстильной промышленности имеют катионные красители, с помощью которых окрашивают полиакрилонитрильные волокна. Катионные красители представляют собой алкилированные производные основных красителей общей формулы ArN+R3X“ (где R — Aik или Ar, X — С1 или CH3SO4), причем четвертичный атом азота может быть как в алифатической цепи, так и входить в состав гетероцикла.
Так, красители Катионный оранжевый 4К [4-(4-нитрофенилазо)-А-метил-А-(2-метилдиэтиламмоний)-этиланилин хлорид (99)], Катионный красный 4Ж [4-(4-
нитро-2-хлорфенилазо)-А-метил-А-(2-метилдиэтилам-моний)этиланилин хлорид (100)] и Катионный желтокоричневый [4-(2,6-дихлор-4-нитрофенилазо)-А-метил-Л7-(2-метилдиэтиламмоний)этиланилинхлорид (101)] получают алкилированием дисперсных азокрасителей, являющихся продуктами сочетания соответственно 4-нитробензолдиазония, 4-нитро-2-хлорбензолдиазония и 2,6-дихлор-4-нитробензолдиазония с Л7-метил-А-(2-ди-этиламиноэтил)анилином. Поскольку алкилируемый атом азота не входит в общую цепь сопряжения, цвет дисперсных азокрасителей при алкилировании не меняется.
(99) X Y H; (100) X = Н, Y = С1; (101)Х = Y = С1
Красители, у которых положительно заряженный четвертичный атом азота входит в цепь сопряженных двойных связей, являются производными ароматических гетероциклических соединений. Они являются продуктами алкилирования дисперсных моноазокрасителей, полученных на основе гетероциклических диазосоставляющих. Например, из красителя [3-(4-А,А-ди-этиламинофенилазо)-! ,2,4-триазол-5-карбоновая кислота (102)', 3-амино-1,2,4-триазол-5-карбоновая кислота-* А,А-диэтиланилин] декарбоксилированием соединения путем нагревания в кислой водной среде и последующим алкилированием диметилсульфатом получают Катионный красный 2 С [2,4-диметил-3-(4-АА-диэтил-аминофенилазо)-1,2,4-триазолийметилсульфат (/03)], а из красителя [2-(4-А-2-гидроксиэтил-А-этиламино-фенилазо)-6-метоксибензотиазол (104)', 2-амино-6-метоксибензтиазол -* А-этил-А-(2-гидроксиэтил)ани-лин] — Катионный синий О [2-(4-А-2-гидроксиэтил-А-этиламинофенилазо)-3-метил-6-метоксибензотиазолий метилсульфат (/05)]. При алкилировании происходит значительное углубление цвета красителя.
(ЮЗ)
696
Новый справочник химика и технолога
(105)
Поскольку катионные красители предназначены для крашения гидрофобных волокон с плотной структурой, они имеют относительно небольшие размеры молекул. Среди них нет красителей зеленого цвета, а все коричневые и черные красители — смесевые.
Кислотные азокрасители
Больше половины отечественного ассортимента кислотных красителей составляют кислотные азокрасители, главным образом моно- и дисазокрасители. В молекулах этих красителей содержатся сульфогруппы, которые сообщают красителю растворимость и кислотные свойства. С помощью кислотных азокрасителей можно окрашивать белковые волокна во все цвета, окраски отличаются яркостью и чистотой тона.
В простейших по структуре моноазокрасителях оранжевых, красных и бордовых цветов азогруппа связывает бензольное ядро с нафталиновым. Первый представитель этой группы — Кислотный оранжевый [натриевая соль 2-гидрокси-1 -(4-сульфонатофенилазо)наф-талина (106); сульфаниловая кислота —» 2-нафтол] — был получен в 1876 г. и сохранил свое значение до сих пор. В молекуле красителя между атомом водорода гидроксигруппы и а-атомом азота азогруппы образуется водородная связь, благодаря которой снижается подвижность атомов водорода и повышается устойчивость окрасок к мокрым обработкам. Это характерно для всех азокрасителей, имеющих в о/^тио-положении к азогруппе гидроксигруппу.
Введение в молекулу ЭД- и ЭА-заместителей приводит к углублению цвета красителя. Даже метильные группы, обладающие относительно слабым электронодонорным действием, углубляют цвет до алого, например, краситель Кислотный алый [3-гидрокси-1-(2,4-диметилфенилазо)нафталин-2,7-дисульфонат натрия (107); 2,4-ксилидин —> Р-кислота]; сульфогруппы незначительно влияют на цвет красителей.
Еще большее углубление цвета происходит при введении в азосоставляющую сильного ЭД-заместителя (-ОН, -NH2). Это видно на примере красителя Кислотного ярко-красного [4-ацетиламино-5-гидрокси-3-фенил-азонафталин-2,7-дисульфонат натрия (705)], полученного сочетанием диазотированного анилина с А-ацетил-Аш-кислотой.
Наличие ациламиногруппы в Кислотном ярко-красном повышает устойчивость окрасок к действию света, усиливает чистоту и яркость отгенка и препятствует образованию изомерного красителя (с азогруппой в о/7/ио-положснии к аминогруппе).
Красители красного цвета образуются в том случае, если азогруппа связывает два нафталиновых кольца; например, Кислотный красный 2С [4-гидрокси-3-(4-сульфонатонафтилазо)нафталин-1 -сульфонат динатрие-вая соль (109); нафтионовая кислота —> 4-гидрокси-нафталин-1-сульфокислота], Кислотный бордо [3-гидрокси-4-(нафтилазо)нафталин-2,7-дисульфонат натрия (110); нафталинамин-1 —> Р-кислота].
(Ю9)
Введение в систему азонафталина ЭД-заместителей, в частности ариламиногруппы, углубляет цвет до синего. Так, краситель Кислотный синий 2К [5-(8-гидрокси-3,6-дисульфонатонафтилазо)-8-фениламинонафталин-1-сульфонат тринатриевая соль (777)] получают сочетанием диазотированной Аш-кислоты с фенил-ие/ш-кислотой. Краситель образует на шерсти окраски глубокого синего цвета, устойчивые к свету, мокрым обработкам и трению.
Ароматические соединения
697
nhc6h5 осн3
Для получения красителей более высокого (желтого) цвета необходимо уменьшить общую цепь сопряжения в молекуле (см. 4.3.5.1). Это красители группы азобензола, например, Кислотный желтый метаниловый [4-(3-сульфонатофенилазо)дифениламин натриевая соль (/72); метаниловая кислота (3-аминобензолсульфокислота) —> дифениламин] и бензолазопиразолона, например, Кислотный желтый светопрочный [5-гидрокси-З-метил-1 -(4-сульфонатофенил)-4-фенилазопиразол натриевая соль (113); анилин —> 3-метил-1-(4-сульфофенил)пира-золон-5].
Для кислотных красителей большое значение имеет способность давать ровные окраски, или ровняющая способность. Она зависит главным образом от сродства красителей к волокну и их растворимости, а эти свойства красителей в значительной степени определяются числом сульфогрупп в молекуле красителя. Если доля молекулярной массы (ДММ) красителя, приходящаяся на одну сульфогруппу, не превышает 300, красители хорошо растворимы в воде и обладают хорошей ровняющей способностью. К таким красителям, например, относятся Кислотные красный 2С [(109); ДММ 229], бордо [(ПО); ДММ 229], синий 2К [(777); ДММ 210] и др.]. Если доля молекулярной массы красителя, приходящаяся на одну сульфогруппу, больше 400, красители хуже растворимы в воде и являются плохоровняющи-ми. К таким красителям относятся Кислотный черный 2С [4-гидрокси-5-(2-метокси-4-нитрофенилазо)-6-фе-ниламинонафталин-2-сульфонат натрия (114); 2-ме-токси-4-нитроанилин —* 4-гидрокси-6-фениламино-нафталин-2-сульфокислота; сочетание в кислой среде; ДММ 494], Кислотный коричневый К [4-гидрокси-3-(2-метокси-4-нитрофенилазо)-6-фениламинонафталин-2-сульфонат натрия (115); 2-метокси-4-нитроанилин —* 4-ги-дрокси-6-фениламинонафталин-2-сульфокислота; сочетание в щелочной среде; ДММ 494] и др. Красители с промежуточными значениями ДММ относятся к сред-неровняющим.
Для кислотных красителей, применяемых для окрашивания шерсти, большое значение имеет устойчивость к валке. Процессу валки (свойлачивания) подвергаются как шерстяные волокна, так и шерстяные ткани с целью повышения их механической прочности и снижения теплопроводности. Устойчивость к валке возрастает при увеличении сродства красителей к волокну и уменьшении их растворимости. Одним из реальных путей улучшения этих показателей является увеличение молекулярной массы красителей. Для этого используют диазосоставляющие, гидроксигруппы которых ацилированы остатками арилсульфокислот, или диазосоставляющие, содержащие арилсульфонамидные группы. Примерами таких красителей являются соответственно Кислотный желтый прочный Ж [5-гидрокси-3-метил-4-(4-толуолсульфонилоксифенилазо)-1 -(4-сульфонатофе-нил)пиразол натриевая соль (116); 4-(Отолуол-сульфониламинофенол —> 3-метил-1-(4-сульфофенил)-пиразолон-5] и Кислотный оранжевый прочный [(117); 5-У-(5-амино-2-метилфенилсульфонил)аминонафталин-1 -сульфокислота 6-гидроксинафталин-2-сульфокис-лота].
NaO3S
Другим способом увеличения молекулярной массы красителей является введение в их молекулы тяжелых алкильных или циклоалкильных остатков. Получаю
698
Новый справочник химика и технолога
щиеся красители близки по свойствам к карболановым красителям антрахинонового ряда; их часто и называют карболанами, например Карболан желтый ЗГС [5-гидрокси-4-(4-додецилфенилазо)-3-метил-1 -(4-сульфо-натофенил)пиразол натриевая соль (//5); 4-додецил-анилин 3-метил-1-(4-сульфофенил)пиразолон-5].
Среди дис- и нолиазокраситслей кислотных красителей немного. Из первичных дисазокрасителей практическое значение имеют красители, полученные при сочетании диазосоединений с резорцином и Аш-кис-лотой, например Кислотный светло-коричневый для кожи [4-(4-сульфонатофенилазо)-6-(4-сульфонатонаф-тилазо)бензол-1,2-диол (119); нафтионовая кислота (4-аминонафталинсульфокислота) —► резорцин (бензолдиол-1,2) «— сульфаниловая кислота (4-аминобензолсуль-фокислота)] применяется для крашения кожи и анодированного алюминия.
Краситель Кислотный сине-черный [5-амино-4-гидрокси-6-(4-нитрофенилазо)-3-фенил азонафталин-2,7-дисульфокислота (120); 4-нитроанилин —> Аш-кислота «— анилин] — один из наиболее широко применяемых красителей для шерсти. В смеси с Кислотным оранжевым (106) и Кислотным бордо (НО) Кислотный синечерный образует смесевой краситель Кислотный черный для валенок, образующий глубокие черные окраски. Устойчивость окрасок умеренная, но краситель дешев, доступен и поэтому производится в больших количествах. Восстановлением нитрогруппы в (120) сульфидом натрия в аминогруппу получают зеленый кислотный дисазокраситель Ацилан темно-зеленый Б [5-амино-6-(4-аминофенилазо)-4-гидрокси-3-фенилазо-нафталин-2,7-дисульфокис лота (121)], окрашивающий шерсть в умеренно устойчивый красивый темнозеленый цвет.
(120) X = NO2; (121) X = NH2
Кислотный коричневый К для кожи [4-(2-гидрокси-3,5-динитрофенилазо)-6-(8-гидрокси-3,6-дисульфонато-нафтилазо)-2-(4-нитрофенилазо)бензолдиол-1,2 динат-риевая соль (122)] — один из немногих первичных трисазокрасителей, имеющих практическое значение. Краситель получают последовательным сочетанием резорцина с диазосоединениями, полученными на основе Аш-кислоты, пикраминовой кислоты (2-амино-4,6-динитрофенол) и 4-нитроанилина. Он применяется для крашения кожи и шелка, образуя окраски удовлетворительной устойчивости.
NaO3S ||(2)
N
Все наиболее ценные кислотные дисазокрасители принадлежат к вторичным, их получают по схеме: М — * А —> А'. К таким красителям относится Кислотный синий К {5-[4-(3-сульфонатофенилазо)нафтил-1-азо]-8-толиламинонафталинсульфонат динатриевая соль (123); метаниловая кислота —> 1-аминонафталин N-to-лилперикислота}. Краситель образует на белковых волокнах красивые темно-синие окраски с хорошей устойчивостью к мокрым обработкам и валке.
(123)
Вторичные дисазокрасители, молекулы которых содержат три остатка нафталина, имеют еще более глубокие цвета, например краситель Кислотный черный С {5-[4-(5-сульфонатонафтил-1 -азо)нафтил-1 -азо-8-толил-аминонафталин-1-сульфонат динатриевая соль (124); 5-аминонафталин-1-сульфокислота нафталинамин-1^ —> А-фенилперикислота]. Это один из лучших черных красителей, он образует на белковых волокнах окраски, устойчивые к свету, мокрым обработкам, валке и к действию кислот.
Ароматические соединения
699
(/24)
Из дисазокрасителей — производных диаминов — в качестве кислотных используются красители, у которых нет полноценной цепи сопряжения между хромофорами, образованными на основе этих аминогрупп. К таким красителям относятся производные 2,2'-диза-мещенных бензидинов: заместители, находящиеся в непосредственной близости к бифенильной связи, нарушают плоское строение молекулы и выводят из взаимного сопряжения бензольные кольца и связанные с ними хромофорные системы. К таким красителям относится Кислотный желтый К [4,4'-бис(5-гидрокси-3-метил-1-фенилпиразолил-4-азо)-бифенил-2,2'-дисульфонат натрия (/25); бензидин-2,2'-дисульфокислота —> 3-метил-1-фенилпиразолон-5].
Краситель применяется для крашения шерсти и шелка, окраски имеют удовлетворительную светостойкость и хорошую устойчивость к стирке.
Практически ценным является краситель Кислотный желтый для валки [4,4'-бис(4-этоксифенилазо)дифенил-сульфид-2,2'-дисульфонат натрия (/26)], получаемый сочетанием бисдиазотированной 4,4'-диаминодифенил-сульфида-2,2'-дисульфокислоты с двумя молекулами фенола и последующим этилированием гидроксигрупп.
Несмотря на длинную цепь сопряженных двойных связей, краситель имеет неглубокий цвет. Это объясняется поворотом бензольных ядер вокруг сульфидной связи, вследствие чего плоское строение молекулы нарушается и сопряжение прерывается. Кислотный жел
тый для валки образует на белковых волокнах окраски с высокой устойчивостью к свету, мокрым обработкам, трению и валке.
Устойчивые к валке кислотные дисазокрасители получают также на основе производных дифенилциклогексана. К таким красителям относятся Кислотный алый 2Ж {1-[4-(2-гидрокси-6,8-дисульфонато)нафтил-1-азо]фенил-1-[4-(1-гидрокси-4-сульфонатонафтил-2-азо)фенил]-циклогексан динатриевая соль (/27); 4-гидроксинафталинсульфокислота «— 1,1-бис(4-аминофенил) циклогексан —* 7-гидроксинафталин-1,3-дисульфокислота}, Кислотный ярко-красный прочный Ж {1,1-бис[4-(1,7-дигидрокси-3-нафтил-2-азо)фенил]циклогексан динатриевая соль (/25); 1,1-бис(4-аминофенил)цикло-гексан —► 4,6-дигидроксинафталин-2-сульфокислота}, Кислотный красный 4С {1,1-бис[4-(1,7-дигидрокси-3-сульфонатонафтил-2-азо)-3-метилфенил]циклогексан динатриевая соль (/29); 1,1-бис(4-амино-3-метилфе-нил)циклогексан —> 4,6-дигидроксинафтал ин-2-сульфо-кислота}, Кислотный бордо 4С {1,1-бис[4-(1,7-дигид-рокси-3-сульфонатонафтил-2-азо)-3-метоксифенил]цик-логексан динатриевая соль (130У 1,1-бис(4-амино-3-метоксифенил)циклогексан —> 4,6-дигидроксинафта-лин-2-сульфокислота}.
(/25)R=H; (/29) R = CH3; (/30)R = OCH3
Протравные азокрасители
Протравные азокрасители окрашивают белковые волокна так же, как кислотные красители, но в отличие от последних закрепляются на волокнах с помощью металлической протравы. В качестве протравы используют соли хрома, чаще всего бихромат калия К.2Сг2О7, поэтому процесс протравления называют хромированием. Хромирование может проводиться перед крашением, одновременно с крашением и после крашения. Для
700
Новый справочник химика и технолога
крашения с одновременным хромированием можно применять лишь определенную небольшую группу красителей, которые получили название однохромовых. Красители, применяемые для крашения с предварительным или последующим хромированием, называют хромовыми.
По сравнению с кислотными красителями хромовые и однохромовые красители образуют на белковых волокнах окраски менее яркие и чистые, но значительно более устойчивые к различным физико-химическим воздействиям. Это объясняется способностью програв-ных азокрасителей образовывать комплексные соединения с металлами, что сопровождается уменьшением растворимости красителей и приводит к образованию дополнительной связи между красителем и волокном через атом металла.
Способность протравных красителей к образованию комплексных соединений с металлами связана с особенностями их химического строения: они содержат в молекулах так называемые комплексообразующие группировки. К ним относятся о,о -дигидрокси-, о-гид-рокси-о-амино- и о-гидрокси-о'-карбоксиазокрасители:
а также красители (131) — производные хромотроповой кислоты (4,5-дигидроксинафталин-2,7-дисульфокислота), (132) — производные 8-гидроксихинолина и (133) — производные салициловой кислоты (2-гидро-ксибензойная кислота).
Ar—N ОН ОН
(131)
Ar-N=N—ОН
СООН (133)
В комплексообразовании с данными группировками принимает участие атом хрома(Ш), который образуется в красильной ванне при восстановлении К2Сг2О7. В случае о,о'-дигидрокси-, о-гидрокси-о'-амино- и о-ги-дрокси-о'-карбоксиазокрасителей атом хрома замещает подвижные атомы водорода в группах -ОН, -NH2 или -СООН и образует координационную связь с одним из атомов азота в азогруппе. Атомы азота азогруппы участвуют в образовании внутрикомплексных соединений своими неподеленными электронами.
В зависимости от соотношения реагентов и условий хромирования один и тот же краситель может образовывать хромовые комплексы различного состава, отличающиеся соотношением числа атомов хрома и числа молекул красителя. Это могут быть катионные комплексы состава 1 : 1 (134), анионные комплексы состава 1 : 2 (135) и нейтральные комплексы состава 2 : 3 (136), в которых взаимно компенсируются заряды катионного (1 : 1) и анионного (1:2) комплексов.
(134)
(136)
Комплексы состава 1 : 2 и 2 : 3 имеют более глубокую окраску, чем комплексы состава 1:1. Координационно связанная вода удерживается прочно при нагревании до температуры 120 °C. Все комплексы неплоские, т. к. связи в атомах шестикоординационного хрома («р3^-гибридизация) направлены к углам октаэдра. Наибольшее практическое значение имеют комплексы состава 1 : 1 и 1 : 2.
Для получения красителей с комплексообразующими заместителями в о^/ио-положениях к азогруппе в качестве диазосоставляющих применяют о-аминофенолы (З-амино-4-гидроксибензолсульфокислота, пикрамино-вая кислота, 2-амино-4-хлорфенол), о-аминонафтолы (4-амино-З-гидроксинафталин-1 -сульфокислота), о-ами-нокарбоновые кислоты (антраниловая кислота), в качестве азосоставляющих — соединения, сочетающиеся
Ароматические соединения
701
в ортио-положение к гидрокси- или аминогруппе (3-метил-1-фенилпиразолон-5, 2-нафтол, 4-гидрокси-нафталин-1-сульфокислота, Аш-кислота, хромотроповая кислота, 2,4-диаминобензолсульфокислота).
Так как координационная связь с азогруппой возникает за счет неподеленных электронов атомов азота, входящих в общую цепь сопряжения молекулы, комплексообразование сопровождается углублением цвета. Поэтому для получения оранжевых окрасок применяют желтые красители (производные бензолазопиразолона), для получения красных окрасок — оранжевые красители (производные бензолазонафталина и нафталиназо-пиразолона), для фиолетовых — красные (производные бензолазонафталина), для синих — красные и фиолетовые (производные бензолазонафталина), для синечерных — фиолетовые (производные азонафталина), для получения черных — синие (производные азонафталина).
Хромовые азокрасители. Хромовые азокрасители относятся в основном к моноазокрасителям, т. к. при наличии одной азогруппы в молекуле они образуют устойчивые и глубокие окраски. Среди хромовых имеются красители всех цветов: желтые, оранжевые, красные, фиолетовые, синие, зеленые, коричневые, черные.
Самую обширную группу составляют о,о'-дигид-роксиазокрасители. Из этой группы красителей практически важными являются Хромовый синий 2К [5-аце-тиламино-4-гидрокси-3-(2-гидрокси-5-хлорфенилазо)наф-талин-2,7-дисульфонат натрия (/37); 2-амино-4-хлор-фенол —> N-ацетил-Аш-кислота], Хромовый темносиний [4,5-дигидрокси-3-(2-гидрокси-5-хлорфенилазо)-нафталин-2,7-дисульфонат натрия (/35); 2-амино-4-хлорфенол —* хромотроповая кислота], Хромовый темно-зеленый С [5-амино-4-гидрокси-3-(2-гидрокси-3,5-динитрофенилазо)нафталин-2,7-дисульфонат натрия (/39); пикраминовая кислота Аш-кислота; сочетание в щелочной среде], Хромовый сине-черный [3-гидрокси-4-(2-гидроксинафтил-1 -азо)нафталин-1 -сульфонат на-
трия (140)\ 4-амино-З-гидроксинафталин-1-сульфокислота —► 2-гидроксинафталин], Хромовый черный С [3-гидрокси-4-(2-гидроксинафтил-1 -азо)-7-нитронафталин-1-сульфонат натрия (14 Гу, 4-амино-3-гидрокси-7-нитронафталин-1-сульфокислота 2-нафтол].
В названиях красителей указан цвет окраски, образующийся после хромирования. До хромирования окраски имеют более высокие цвета, например краситель (137) окрашивает шерсть в красно-фиолетовый цвет, краситель (138) — в красный цвет, краситель (141) — в фиолетовый.
К числу практически важных о-амино-о '-гидроксиазокрасителей относится Хромовый коричневый К [2,4-диамино-5-(2-гидрокси-3,5-динитрофенилазо)бензол-сульфонат натрия (142)\ пикраминовая кислота 2,4-диаминобензолсульфокислота]. Краситель окрашивает шерсть в светло-коричневый цвет, углубляющийся в результате хромирования до темно-коричневого (каштанового). К о-гидрокси-о '-карбоксиазокрасителям от-
носится Хромовый бордо С [4-гидрокси-3-(2-карбоксифенилазо)нафталин-1-сульфонат натрия (143)\ антраниловая кислота 4-гидроксинафталин-1-
сульфокислота]. Краситель окрашивает шерсть в оранжевый цвет, который после хромирования становится бордовым.
(137) X = Н, Y = Cl, Z = NHCOCH3
(/35) X = Н, Y = Cl, Z =ОН
(139) X = Y = NO2, Z = NIL,
ОН но
(141) X = NO2
Моноазокрасители, комплексообразование которых не сопровождается изменением цвета, содержат остатки салициловой кислоты или 8-гидроксихинолина. В комплексообразовании здесь участвуют гидроксигруппы, электронная структура которых не изменяется, и атомы кислорода или азота соответственно, неподеленные электронные пары которых не участвуют в общей цепи сопряжения молекулы.
Азокрасители на основе салициловой кислоты отличаются от других протравных азокрасителей яркостью оттенков. Их хромовые комплексы (144) построены по анионному типу: в образовании комплексов принимают участие три молекулы красителя и два атома хрома, один из которых входит во внутреннюю координационную сферу, а второй является компенсирующим катионом.
702
Новый справочник химика и технолога
N=N—Аг (144)
К производным салициловой кислоты относится краситель Хромовый желтый К [2-гидрокси-5-(4-сульфонатофенилазо)бензойная кислота (145)', сульфаниловая кислота —> салициловая кислота], применяемый для крашения шерсти и шелка в желтый цвет; окраски отличаются чистотой тона и прочностью ко всем обработкам.
СООН
Так как салициловая кислота относится к числу трудно сочетающихся азосоставляющих, в ряде случаев удобнее вводить комплексообразующую группировку в состав диазосоставляющей. В качестве диазосоставляющей применяют 5-аминосалициловую кислоту (5-амино-2-гидроксибензойная кислота) или (лучше) продукты ацилирования ее аминогруппы остатками аминокарбоновых или аминосульфокислот, например, 5-[(2-аминотолуил-4)амино]салициловую кислоту {5-[2-аминотолуил-4)амино]-2-гидроксибензойная кислота (146)}. Диазопроизводные таких аминов сочетаются легко, а полученные красители обладают хорошим сродством к волокну и образуют ровные и прочные окраски. К таким красителям относится, например, Хромовый прочно-оранжевый РД (147), у которого азосоставляющей является Г-кислота.
Иногда салициловую кислоту вводят в состав другой азосоставляющей, сочетание с которой проходит легко, например, Аш-кислоту. Так, краситель Хромовый ярко-красный 2С (148) получают сочетанием диазотированной сульфаниловой кислоты с Аш-кислотой, в которой аминогруппа ацилирована сульфосалициловой кислотой.
Хромирование красителей, полученных сочетанием диазосоединений с 8-гидроксихинолином, происходит без изменения цвета. Красители окрашивают шерсть и шелк в цвета, устойчивые ко всем воздействиям. Примером такого красителя является Хромовый прочнооранжевый Г [8-гидрокси-5-(2-сульфонато-5-хлорфе-нилазо)хинолин натриевая соль (149)', 2-амино-4-хлор-бензолсульфокислота —> 8-гидроксихинолин].
Хромовые дисазокрасители составляют немногочисленную группу. Вторичный дисазокраситсль Хромовый оранжевый {2-гидрокси-5-[4-(4-сульфофенил-азо)фенилазо]бензойная кислота (150)} получают по схеме: М —* А —» К (сульфаниловая кислота —> анилин —> салициловая кислота). Анилин перед сочетанием с диазотированной сульфаниловой кислотой переводят в А-сульфометиланилин (А-метиланилин-со-сульфо-кислоту). После сочетания сульфометильную группу удаляют кипячением с раствором NaOH, диазотируют образовавшийся и-аминоазобензол и сочетают его с салициловой кислотой. Комплексообразование происходит без углубления окраски.
HO3S
(150) СООН
Вторичный дисазокраситель Хромовый ярко-красный {5-бензоиламино-4-гидрокси-3[5-(4-гидрокси-3-карбоксифенилазо)-2-сульфонатофенилазо]нафталин-2,7-дисульфонат тринатриевая соль (757)} получают
Ароматические соединения
703
следующим образом: диазотируют З-нитроанилин-4-сульфокислоту и сочетают с салициловой кислотой, в полученном моноазокрасителе восстанавливают нитрогруппу, диазотируют его и сочетают с бензоил-Аш-кислотой.
Первичный хромовый дисазокраситель Хромовый черный О [4-гидрокси-3-(2-гидрокси-5-нитрофенилазо)-8-(2-карбоксифенилазо)нафталин-2,7-дисульфонат натрия (/52)] получают по схеме: М —► С *— М' (антраниловая кислота —* И-кислота <— 2-амино-4-нитрофенол), причем первое сочетание проводят в кислой среде, второе — в щелочной.
Хромовый черный О — один их лучших черных красителей для шерсти. В его молекуле содержатся две комплексообразующие группировки: о, о'-дигидрокси- и о-амино-о-карбоксигруппировки, что объясняет высокую устойчивость окрасок к различным воздействиям.
Однохромовые азокрасители. Однохромовые азокрасители отличаются от хромовых тем, что имеют сравнительно небольшую молекулярную массу, содержат в молекуле не более одной сульфогруппы, а иногда вместо сульфогруппы содержат карбоксильную или сульфамидную группы. Однохромовые красители имеют слабокислые свойства, что позволяет применять их для крашения из слабокислых ванн. Для повышения сродства к волокну в молекулы однохромовых красителей вводят аминогруппы, ациламиногруппы, гетероциклические азотсодержащие ядра с алкильными группами и др., а для понижения реакционной способности по отношению к металлам — нитрогруппы и атомы галогена. Благодаря этому комплексообразование однохромовых красителей с металлом протекает медленнее, чем выбирание их волокном из ванны, поэтому крашение можно совмещать с хромированием.
Типичными представителями одно хромовых красителей являются Однохромовый оранжевый 4К [2-гидро-кси-5-(4-нитро-2-хлорфенилазо)бензойная кислота (/53); 4-нитро-2-хлоранилин —> салициловая кислота], Однохромовый синий 3 [4-ацетиламино-5-гидрокси-6-(2-гидрокси-3,5,6-трихлорфенилазо)нафталин-1 -сульфонат натрия] (154\, 2-амино-3,4,6-трихлорфенол -* А-аце-тил-С-кислота], Однохромовый бордо С [(/55); 3-ами-но-2-гидрокси-5-хлорбензол-1-сульфокислота N-бу-тил-4-гидроксихинолон-2] и Однохромовый оливковый Ж [4-ацетиламино-2-(2-гидрокси-3,5-динитрофенилазо) фенол (/56); пикраминовая кислота —> А-ацетил-и-ами-нофенол].
Кислотные металлсодержащие азокрасители
Кислотные металлсодержащие азокрасители представляют собой готовые комплексные соединения азокрасителей с металлами. По методам применения они аналогичны кислотным красителям, а по устойчивости образуемых окрасок — хромовым. Комплексообразующие группировки такие же, как у протравных красителей. В качестве металлов-комплексообразователей обычно применяют хром, иногда кобальт.
При хромировании в комплексообразовании с красителем участвует трехвалентный хром. При хромировании на волокне (в случае протравных красителей) используются соединения шестивалентного хрома (бихроматы и др.), которые восстанавливаются белковым веществом шерсти, что сопровождается довольно зна
704
Новый справочник химика и технолога
чительной потерей механической прочности волокна (до 25-30 %). Этот недостаток устраняется при использовании металлсодержащих красителей.
Металлизацию в производстве хромсодержащих красителей осуществляют солями Сг3+. Наиболее удобно для этой цели использовать формиат хрома или хлорид хрома в присутствии формиата натрия.
Взаимодействие красителей с солями хрома проводят обычно в водной среде (в растворе или суспензии красителя) при pH = 2-М и температуре кипения реакционной массы (103-105 °C). Для сокращения времени комплексообразования процесс можно осуществлять при более высокой температуре (105-135 °C) под давлением 120-400 кПа. Реакцию следует проводить в эмалированном аппарате во избежание образования внутрикомплексных соединений с железом, имеющих другой цвет и загрязняющих краситель.
Другой способ получения хромсодержащих азокрасителей заключается в сочетании соответствующих диазо- и азосоставляющих в присутствии солей хрома. Образующийся азокраситель сразу же вступает в комплексообразование с металлом.
В качестве поставляющих хром соединений используют также хромово-аммиачныс комплексы салициловой кислоты (/57). При взаимодействии красителя с таким комплексом при 90-100 °C образуется металлсодержащий азокраситель. Хромово-аммиачные комплексы применяют в том случае, когда образующийся металлсодержащий азокраситель неустойчив в сильнокислой среде, поэтому хромирование проводят в слабокислой, нейтральной или слабощелочной среде.
о,о '-Дигидрокси-, о-гидрокси-о '-амино- и о-гидрок-си-о'-карбоксиазосоединсния с солями трехвалентных металлов могут образовывать комплексы трех типов: 1 : 1 (одна молекула азокрасителя связана с одним атомом металла), 1 : 2 (две молекулы азокрасителя связаны с одним атомом металла) и 2 : 3 (три молекулы азокрасителя связаны с двумя атомами металла). По яркости и чистоте тона эти красители уступают обычным кислотным красителям, однако в ряде случаев они образуют значительно более яркие окраски, чем такие же красители, получаемые хромированием на волокне.
Все металлсодержащие красители имеют в названии букву «М». Если крашение шерсти производится из нейтральной ванны, в название красителя входит буква «Н», что означает «нейтральнокрасящий».
Комплексы состава 1:1. Для получения этих комплексов хромирование обычно осуществляют действием формиата хрома на водные растворы моноазокрасителей
при температуре несколько выше 100 °C и pH = 2^-4. Подбирая подходящие исходные азососдинения, можно получить металлсодержащие красители всех цветов.
Большое практическое значение имеет Кислотный зеленый ЖМ (/5/?), получаемый хромированием темнокрасного моноазокрасителя — продукта сочетания диазотированного 2-амино-5-нитрофенола и 6-амино-нафталин-1-сульфокислоты. Кислотный зеленый ЖМ применяется для крашения шерсти и кожи, окраски отличаются яркостью и устойчивостью. Это особенно ценно, т. к. хромирование на волокне красителей — производных 2-аминонафталина — дает лишь тусклые окраски зеленого цвета. Практически значимыми являются также Кислотный желтый 4КМ [(/59); хромовый комплекс светло-желтого азокрасителя (З-амино-2-гидрокси-5-нитробензолсульфокислота —* анилид ацетоуксусной кислоты)], Кислотный розовый М [(/60); хромовый комплекс оранжевого азокрасителя (4-амино-З-гидроксинафталин-1-сульфокислота -* 3-метил-1-(3-сульфофенил)пиразолон-5)], Кислотный синий ЗМ [(/6/); хромовый комплекс азокрасителя (/40)]. Интересно отметить, что сам азокраситель (/40) выпускается под названием Хромовый сине-черный, т. к. при образовании хромового комплекса на волокне он окрашивает шерсть в более тусклый синевато-черный цвет.
Ароматические соединения
705
Красители применяют для крашения шерстяных тканей, трикотажа, фетра, ковровой пряжи. Особый интерес представляют эти красители для крашения кар-бонизованной шерсти, т. к. в этом случае отпадает необходимость в нейтрализации волокна.
Хромовые комплексы состава 1 : 1 обладают большим сродством к белковому волокну и при крашении из слабокислых ванн выбираются волокном с такой высокой скоростью, что окраски получаются неровными. Для замедления процесса крашения и получения более ровных окрасок приходится повышать концентрацию кислоты в красильной ванне до 6-8 % от массы волокна, тогда как при использовании обычных кислотных красителей концентрация кислоты составляет 1-2 %. Применение специальных выравнивателей, поверхностно-активных веществ, позволяет снизить содержание кислоты в ванне, тем нс менее, такие комплексы нельзя применять для крашения полушерстяных тканей.
Комплексы состава 1 : 2. Если в моноазокраситс-лях, используемых для получения комплексов состава 1:1, заменить свободные сульфогруппы сульфонамидными или алкилсульфонильными, а карбоксильные — амидными или ацильными и комплексообразование вести при таком соотношении количеств красителя и соединения металла, чтобы образовался комплекс состава 1 :2, получаются своеобразные кислотные (анионные) красители, у которых отрицательный заряд обусловлен не наличием сульфо-, карбокси- или иной кислотой группы, а принадлежит всему комплексу (комплексы анионного типа). Примерами таких красителей являются Кислотный алый прочный НЖМ [(762); хромовый комплекс азокрасителя (4-амино-З-гидрокси-бензолсульфонамид -* 3-метил-1-(2-хлорфенил)пиразо-лон-5)], Кислотный алый прочный НМ [(763); хромовый комплекс азокрасителя (4-амино-З-гидроксибен-золсульфонамид -> 3-метил-1-(4-хлорфенил)пиразолон-5)], Кислотный оранжевый светопрочный Н4КМ [(764); хромовый комплекс азокрасителя (З-амино-4-гидрокси-бензолсульфонамид -> 3-метил-1-(2-хлорфенил)пира-золон-5], Кислотный оранжевый светопрочный Н2КМ [(765); хромовый комплекс азокрасителя (З-амино-4-гидроксибензолсульфонамид -> 3-метил-1-(4-хлорфенил) пиразолон-5].
(762) X = Cl, Y = Н; (763) X = Н, Y = С1
(764) X = Cl, Y = Н; (765) X = Н, Y = CI
Натриевые, калиевые и аммониевые соли этих комплексов растворимы в воде и равномерно окрашивают белковые волокна из нейтральных или слабокислых ванн. Они пригодны также для крашения полушерстяных тканей и синтетических волокон (капрона и др.). Поскольку атом металла в комплексах состава 1 : 2 координационно насыщен, при крашении не происходит комплексообразования с белковым веществом и краситель закрепляется на волокне силами межмолекулярного взаимодействия и ионными связями.
В отличие от комплексов состава 1 : 1 комплексы состава 1 : 2 неустойчивы в сильнокислой среде, поэтому хромирование проводят в слабокислой, нейтральной или щелочной среде обычно с помощью хромсалицилата аммония.
Комплексы состава 1 : 2 можно получать как обычным способом металлизации, так и взаимодействием комплекса состава 1:1с эквивалентным количеством свободного красителя. Этот способ особенно удобен для получения смешанных комплексов, в которых один атом металла связан с двумя разными красителями или одним красителем и одним бесцветным комплексообразующим соединением, например салициловой кислотой. Смешанные комплексы двух разных красителей позволяют варьировать цвета и оттенки исходных красителей. Смешанные комплексы с бесцветным компонентом дают возможность получить красители, образующие окраски такой же чистоты и яркости, как комплексы состава 1 : 1, но способные окрашивать волокна из нейтральных ванн.
Примером смешанного комплекса двух моноазокра-ситслсй является Кислотный красный НЖМ [(766); хромовый комплекс азокрасителей (4-амино-З-гидро-ксибензолсульфонамид -> 3-метил-1-(2-хлорфенил)-пиразолон-5) и (З-амино-4-гидроксибензолсульфона-мид —> 1-бутил-4-гидроксихинолон-2].
Примером комплекса состава 1:2с бесцветным компонентом является зеленый кислотный краситель [(767); хромовый комплекс азокрасителя (3-амино-2 -гидрокси-5-хлорбензолсульфокислота 2-аминонаф-
талин-1-сульфокислота) и 8-гидроксихинолина].
706
Новый справочник химика и технолога
(166)
Na+
(/67)
Наряду с хромом в качестве металлов-комплексо-образователей для получения комплексов, красящих из нейтральных ванн, используют кобальт, реже — никель, железо и другие металлы. Обычно цвет кобальтовых комплексов выше цвета соответствующих хромовых комплексов, а светостойкость окрасок несколько больше. Примером такого комплекса является Кислотный рубиновый Н2СМ {натриевая соль бис[6-оксидо-5-(2-оксидо-5-хлорфенилазо)нафталинсульфонамид-2]-кобальта (/65); кобальтовый комплекс азокрасителя
(2-амино-4-хлорфенол —> 6-гидроксинафталин-2-сульфо-намид}, образующий на шерсти и шелке окраски с высокой прочностью к различным обработкам.
H2NO2S (168)
Nab
Металлсодержащие азокрасители состава I : 2 применяют для крашения шерсти в виде волокна, ленты, пряжи и ткани. В смеси с прямыми светостойкими красителями их применяют для одновременного крашения полушерстяных и смешанных тканей. Эти красители используются также для крашения полиамидного волокна и для печати по шерстяным и полиамидным тканям.
Комплексы состава 2 :3. При хромировании солями хрома моноазокрасителя (141) образуется металлсодержащий азокраситель состава 2:3, который выпускается под названием Кислотный черный М (169). Краситель представляет собой соль катионного комплекса с анионным, он окрашивает шерсть в глубокий черный цвет значительно лучшего качества, чем цвет, образуемый при хромировании этого же моноазокрасителя на волокне (см. Хромовый черный С).
(/69)
Ароматические соединения
707
Прямые азокрасители
Прямые красители способны непосредственно из водных ванн в присутствии электролитов окрашивать целлюлозные волокна, за что они и получили название прямых, или субстантивных. С их помощью можно получить окраски широкой гаммы цветов — от желтого до черного. По яркости и насыщенности цветов прямые красители уступают кубовым, активным и кислотным. Из общего числа марок прямых красителей около 70 % составляют азокрасители.
По химическому строению и методам получения прямые азокрасители разделяются на следующие подгруппы: моноазокраситсли, дис- и полиазокрасители (фосгенированные, первичные, вторичные, производные диаминов и красители с триазиновым кольцом), металлсодержащие азокрасители.
Моноазокрасители. Среди моноазокрасителей, отличающихся в основном небольшими размерами молекул, прямых красителей мало: в основном это красители, содержащие в молекулах амидные группы или гетероциклические ядра.
Для получения азокрасителей с амидными группами в качестве азосоставляющих применяют ^ацилированные, чаще бензоилированные, аминогидроксинафталинсульфокислоты. Обычно применяют У-бензоил-И-кислоту, которая при сочетании в щелочной среде образует красители, отличающиеся чистотой оттенков. При этом во избежание сочетания в пара-положение к гидроксигруппе следует выбирать не очень активные диазосоединения и вести процесс в слабощелочных средах.
Образующиеся моноазокрасители обладают достаточным сродством для того, чтобы закрепиться на целлюлозе, но недостаточным для того, чтобы обеспечить высокую устойчивость к мокрым обработкам. Для повышения устойчивости окрасок в бензольное кольцо вводят аминогруппу, чтобы после крашения продиазо-тировать краситель на волокне и сочетать с новой азосоставляющей, так называемым проявителем окраски. В названии такого красителя есть слово «диазо», причем цвет, указанный в названии, соответствует конечной окраске после диазотирования и проявления на волокне. Краситель, образующийся на волокне, уже не является моноазокрасителем.
В качестве проявителей окраски, как правило, применяют азосоставляющие, не содержащие сульфогрупп
и других заместителей, повышающих растворимость образующихся на волокне красителей. Для получения конечных окрасок оранжевого, красного, бордо и синего цвета обычно используется 2-нафтол, желтого и зеленого — 3-метил-1-фенилпиразолон-5, коричневого, серого и черного — jw-фенилен- и л/-толуилендиамины.
Увеличение количества амидных групп в молекулах красителей усиливает их сродство к целлюлозе, поэтому в качестве азосоставляющих для получения прямых моноазокрасителей предпочитают использовать соединения типа У-[4-(4-аминобензоиламино) бензоил]-И-кислоты (84). Кроме того, наличие нескольких амидных групп более надежно разобщает сопряженные системы двух частей молекулы образующегося на волокне красителя, что имеет большое значение для чистоты оттенка.
Красителем такого типа является Прямой диазо-алый {7-[4-(4-аминобензоиламино)бензоиламино]-4-гид-рокси-3-(2-метоксифенилазо)нафталин-2-сульфонат натрия (770); диазосоставляющая — о-анизидин}. Ярко-алый цвет возникает после диазотирования красителя на волокне и сочетания с 2-гидроксинафталином, образующиеся окраски отличаются большой устойчивостью к мокрым обработкам.
Часто применяемый на практике краситель Прямой диазо-желтый светопрочный {172} принадлежит к немногим азокрасителям, получаемым без использования традиционных реакций диазотирования и сочетания. Краситель получают взаимодействием 4-нитробен-зоилхлорида с 2,5-диаминобензолсульфокислотой и последующим восстановлением образовавшейся 2,5-ди(4-нитробензоиламино)бензолсульфокислоты {171} избытком Na2S в щелочной среде. Восстановление происходит таким образом, что в каждых двух молекулах динитропроизводного только две нитрогруппы восстанавливаются до аминогрупп, а вторые две нитрогруппы этих молекул восстанавливаются до азогруппы.
708
Новый справочник химика и технолога
Наличие четырех амидных групп сообщает красителю (172) большое сродство к целлюлозному волокну, которое он окрашивает в желтый цвет. После диазотирования красителя на волокне и сочетания с З-метил-1-фенилпиразолоном окраски становятся яркими, интенсивно желтыми и отличаются высокой устойчивостью к свету и мокрым обработкам.
Прямые моноазокрасители, содержащие в своих молекулах гетероциклы, имеют меньшее значение. К их числу относится Прямой желтый светопрочный (174), который получают осторожным окислением 2-(4-ами-нофенил)-6-метилбензотиазол-5-сульфокислоты (173) гипохлоритом натрия в щелочной среде при 20 °C. Это еще один пример синтеза азокрасителя без применения реакций диазотирования и сочетания.
IX MX-n,,2 -s* IXМГУn=nXX</ ТТ
(173) (
Фосгенированные азокрасители. Красители этой группы получают, ацилируя аминогруппы азокрасителей дихлорангидридом угольной кислоты (фосгеном) (см. уравнение 4.3.14).
В результате этой реакции молекула «удваивается» и в ней появляется группа NHCONH (уравнение (4.3.14)), сродство к целлюлозе возрастает и краситель приобретает свойства прямого, т. е. фосгенирование — это удобный способ превращения кислотных азокрасителей в прямые. Взаимодействие с фосгеном обычно осуществляется в водно-содовых растворах или суспензиях.
Этим способом получают ряд красителей желтого, розового и красного цветов. Так, фосгенированием оранжевого кислотного моноазокрасителя (3-амино-нафталин-1,5-дисульфокислота —> л/-толуидин) получают Прямой желтый светопрочный К (175).
При наличии в молекуле фосгенируемого красителя свободной гидроксигруппы ее предварительно необходимо защитить легко удаляемой группой. Например, при получении Прямого красного светопрочного С (177) фосгенированием моноазокрасителя из Аш-кис-лоты и крезидина гидроксигруппу Аш-кислоты предварительно ацилируют бензолсульфонилхлоридом в присутствии NaOH. Образовавшуюся О-фенилсульфонил-Аш-кислоту диазотируют и сочетают с крезидином, получая моноазокраситель (176), после фосгенирования которого сульфоэфирные группы удаляют нагреванием дисазокрасителя с раствором NaOH.
Аналогичным образом получают практически важный краситель Прямой розовый светопрочный С (178).
2Ar-N = N-Ar'-NH2 C0C1 > Ar-N = N - Ar'-NHCONH - Ar'-N = N - Ar (4.3.14)
Ароматические соединения
709
Краситель применяется для крашения хлопка и вискозного волокна, окраски обладают высокой устойчивостью к свету и мокрым обработкам.
(/75)
Первичные дисазокрасители. Эти красители получают по схеме: М —* С *— М'. В качестве центральной азосоставляющей применяются главным образом производные динафтиламина и динафтилмочевины, так называемые ди-И-кислота (80) и алая кислота (81). Как группа -NH-, так и группа -NHCONH- являются хорошими разобщающими (изолирующими) группами, поэтому получаемые красители имеют неглубокие цвета. Примерами таких красителей являются Прямой красный 4С {бис[5-гидрокси-7-сульфонато-6-(фснил-азо)нафталин-2]-имин динатриевая соль (/79); анилин—* ди-И-кислота}, Прямой ярко-оранжевый [(180); анилин *— алая кислота], Прямой алый [(181); анилин -» алая кислота <— 4-аминоацетанилид].
(/79) R = NH; (180) R = NHCONH
Красители — производные алой кислоты — отличаются большим сродством к целлюлозному волокну и более высокой светостойкостью, чем аналогичные производные ди-И-кислоты, однако устойчивость окрасок к различным обработкам и у тех и у других красителей недостаточно высокая.
При замене бензольных диазосоставляющих нафталиновыми происходит углубление цвета, например в красителе Прямой красный 2С [(182); 5-амино-нафталин-1-сульфокислота —> алая кислота]. Краситель
образует окраски, недостаточно устойчивые к свету и мокрым обработкам, но очень устойчивые к трению,
поэтому применяется для крашения галошной байки.
HNCONH
Вторичные дис- и полиазокрасители получают по схеме: М —> А —> А' —* ” —> К. Увеличение числа азогрупп в молекулах вторичных азокрасителей с сопряженными азогруппами до трех и более приводит к образованию прямых азокрасителей, обладающих сродством к целлюлозным волокнам независимо от наличия заместителей, повышающих это сродство. Практическое значение имеют азокрасители, содержащие нс более четырех азогрупп, т. к. с дальнейшим увеличением их числа нарушается плоское строение молекулы вследствие усиления тенденции к закручиванию вдоль продольной оси.
При получении вторичных полиазокрасителей в качестве первого компонента (М) обычно используют диазосоставляющие бензольного или нафталинового ряда, в качестве промежуточных (А) — 1 -аминонафталин и его производные (кислоты Клеве, этоксикислота Клеве) и иногда крезидин, в качестве конечной азосоставляющей (К) — гидроксинафталин- и аминогидроксинафталинсульфокислоты и их производные.
В производстве полиазокрасителей возникают некоторые специфические трудности, заключающиеся в том, что скорости третьего и последующих сочетаний значительно уменьшаются, уменьшается и устойчивость соответствующих диазосоединений (особенно в щелочной среде). В результате скорость распада диазосоединений становится соизмеримой со скоростью сочетания, что приводит к потерям и загрязнению красителя продуктами распада, затрудняющими фильтрацию и ухудшающими качество красителя. Во избежание этого необходимо строго соблюдать температурный режим и кислотность среды, не допускать излишнего разбавления реакционной массы, т. к. снижение концентраций реагентов замедляет процесс азосочетания. В некоторых случаях необходимо вводить специальные добавки, ускоряющие сочетание (пиридин, многоатомные спирты и др.).
Представителями практически значимых вторичных полиазокрасителей являются Прямой красный светопрочный 2С {7-бензоиламино-4-гидрокси-3-[4-(4-суль-фонатофенилазо)фенилазо]нафталин-2-сульфонат динатриевая соль (183); сульфаниловая кислота —> анилин —> А-бензоил-И-кислота}, Прямой синий светоп
710
Новый справочник химика и технолога
рочный [7-амино-4-гидрокси-3-{4-[4-(4,8-дисульфонато-нафтил-2-азо)нафтил-1 -азо]-6(7)сульфонатонафтил-1 -азо} -нафталин-2-сульфонат тетранатриевая соль {184\, 3-ами-нонафталин-1,5-дисульфокислота —> нафталинам ин-1 —> —► (смесь 5-аминонафталин-2- и 8-аминонафталин-2-суль-фокислот —► И-кислота].
Красители в значительных количествах используются для крашения хлопка и вискозного волокна, окраски устойчивы к свету и стирке.
Прямой диазо-зеленый светопрочный [(755); метани-ловая кислота —► 8-аминонафталин-2-сульфокислота -* —► этоксикислота Клеве —► А'-(3-аминобснзоил)-И-кис-лота] — один из самых светостойких зеленых прямых красителей; его выпускают в виде трисазокрасителя. В процессе синтеза красителя для успешного проведения третьего сочетания требуется проведение реакции в среде пиридина.
Краситель {185) окрашивает хлопок и вискозное волокно в голубой цвет. После крашения краситель на волокне диазотируют и сочетают с 3-метил-1-фенил-пиразолоном. Получается тетракисазокраситель {186),
четвертая азогруппа которого разобщена с тремя первыми. А т. к. моноазокраситель, построенный из бензольного и пиразолонового ядер, является чистожелтым, то цвет красителя, образовавшегося на волокне, будет результатом смешения голубого и желтого, т. е. зеленым. Диазотирование и сочетание на волокне делают светостойкую окраску устойчивой и к мокрым обработкам.
Из других диазотируемых на волокне красителей практическое значение имеют Прямой диазо-бордо С [(757); метаниловая кислота —> л/-толуидин —> У-(4-аминобензоил)-И-кислота] и Прямой диазо-бордо Ж [(755); 4-аминоазобензол-4'-сульфокислота —> М-(4-ами-нобензоил-4'-аминобензоил)-И-кислота].
Оба красителя окрашивают целлюлозные волокна в фиолетово-красный цвет, который после диазотирования на волокне и сочетания с 2-гидроксинафталином переходит в цвет бордо. Повышение цвета объясняется тем, что после сочетания на волокне образуются трисазокрасители с разобщенными азогруппами, цвет кото
Ароматические соединения
711
рых является результатом внутримолекулярного смешения цветов фиолетово-красных дисазокрасителей и оранжевых моноазокрасителей.
Производные диаминов. Прямые дис- и полиазокрасители — производные ароматических диаминов — включают практически всю цветовую гамму: от желтых до черных красителей. Дисазокрасители получают по схеме:
К - Д - К'.
Для получения трисазокрасителей используют азо-составляющие, способные сочетаться дважды:
К <Д- С < или азосоставляющие, содержащие свободные аминогруппы, способные диазотироваться:
К — Д — А — К'.
Тетракис- и другие полиазокрасители получают по еще более сложным схемам, например:
К — А — Д А' К' К А > А' > К'.
В качестве диаминов для получения дисазокрасителей с разобщенными азогруппами чаще всего используют следующие соединения: бензидин (189), о-толи-дин (190), о-дианизидин (191), 4,4'-диаминостильбен-2,2'-дисульфокислоту (192), 4,4'-диаминодифениламин-2-сульфокислоту (193), 4,4'-диаминобензанилид (194).
Диазотирование обеих аминогрупп диаминов с аминогруппами в разных ядрах происходит практически одновременно, т. е. сразу образуются бис(диазо)сое-динения. Напротив, скорости реакций сочетания, в ко
торые вступают образовавшиеся диазониевые группы, достаточно различны, и вторая диазониевая ipynna вступает в реакцию только после того, как первая прореагировала полностью. Это позволяет получать как симметричные дисазокрасители — продукты сочетания обеих диазогрупп с одной и той же азосоставляющей, так и несимметричные — продукты сочетания с разными азосоставляющими.
Самой многочисленной группой красителей на основе диаминов являются красители ряда бифенила, в первую очередь — бензидина. Однако вследствие канцерогенности бензидина производство бензидиновых красителей постепенно сокращается.
Цвет бензидиновых красителей всегда глубже, чем цвет моноазокрасителей, которые образовались бы при разрыве молекулы по месту бифенильной связи. Так, краситель (195) из анилина и Аш-кислоты (сочетание в щелочной среде) имеет = 545,3 нм, а соответствующий краситель из бензидина — Прямой голубой К [4,4'-бис(8-амино-1-гидрокси-3,6-дисульфонафтил-2-азо)дифенил (196)] — = 580 нм.
К бензидиновым дисазокрасителям относятся Конго красный [(/97); бензидин —► нафтионовая кислота] и его производные Бснзопурпупин 4Б [(198)', о-толидин —► -^•нафтионовая кислота] и Бензопурпурин 10Б [(199)', о-дианизидин —> нафтионовая кислота].
Все три красителя применяются в качестве индикаторов в аналитической химии, т. к. при действии кислот резко изменяют окраску (с красной на синию).
Прямые дисазокрасители такие, как краситель (196) образуют окраски с низкой устойчивостью к мокрым обработкам. Для повышения устойчивости окрасок к мокрым обработкам при синтезе красителей используют азосоставляющие, способные образовывать комплексы с металлами. Так, из бензидина, салициловой кислоты и Гамма-кислоты получают несимметричный дисазокраситель Прямой коричневый КХ [4-(7-амино-1-гидрокси-3-сульфонафтил-2-азо)-4'-(4-гидрокси-3-карбокси-фенилазо)дифенил (200)], образующий окраски, упрочняемые солями хрома. Другой путь повышения устойчивости окрасок к мокрым обработкам — синтез красителей, диазотируемых на волокне; например, Прямой диазо-черный С [4-(8-амино-1-гидрокси-3,6-дисульфонафтил-2-азо)-4 '-(7-амино-1 -гидрокси-3-сульфо-нафтил-2-азо)дифенил (201)], получаемый из бензидина, Аш-кислоты и Гамма-кислоты (сочетание в щелочной среде). Краситель окрашивает целлюлозу в сине-черный цвет, переходящий в глубокий черный после диазотирования и сочетания на волокне с л/-фенилендиамином. Прямой диазо-черный С применяется в больших количествах для крашения хлопка и вискозного волокна.
712
Новый справочник химика и технолога
Для повышения устойчивости окрасок к свету бензидин заменяют дианизидином и в качестве азосоставляющих используют соединения, сочетающиеся в орто-положение к гидроксигруппе. Образующиеся о-гидро-кси-о'-метоксиазокрасители при обработке на волокне солями меди вступают в комплексообразование, значительно повышающее светостойкость окрасок. Так, имеющий большое практическое значение краситель Прямой чисто-голубой [4,4'-бис(8-амино-1-гидрокси-5,7-дисульфонафтил-2-азо)-3,3'-диметокси дифенил (202); дианизидин —► 4-амино-5-гидроксинафталин-1,3-дисульфокислота] окрашивает хлопок и вискозное волокно в красивый, яркий голубой цвет, однако совершенно неустойчивый к свету. Обработка солями меди делает окраски светостойкими, но ухудшает чистоту и яркость оттенка.
Несимметричный краситель Прямой синий светопрочный КУ [4-( 1 -гидрокси-4-сульфонафтил-2-азо)-4'-(1 -гидрокси-3,6-дисульфонафтил-2-азо)-3,3'-диметокси-дифенил (203); И-кислота «— дианизидин 4-гидрокси-нафталин-1-сульфокислота (оба сочетания в щелочной среде)] применяется в основном для крашения полушерстяных тканей. Образуемые окраски после обработки на волокне солями меди становятся достаточно устойчивыми и к свету, и к стирке.
Полиазокрасители на основе бензидина и его производных имеют более глубокие цвета: синие, зеленые, коричневые и черные. Краситель Прямой черный 3 (204) — один из самых распространенных полиазокрасителей, применяемый для крашения хлопка, полушерсти, кожи, бумаги и др. Краситель получают по схеме:
Ароматические соединения
713
М —* С Д —* К, где М — анилин, С — Аш-кислота, Д — бензидин, К — ж-фенилендиамин. Очередность и условия сочетания определяются тем, что с Аш-кислотой первое сочетание следует проводить в кислой среде, а ж-фенилендиамин — активная азосоставляющая — вводится в реакцию последним.
По этой же схеме получают Прямой черный К (205), но вместо ж-фенилендиамина применяют ж-толуилен-диамин.
Для обоих красителей черный цвет есть результат внутримолекулярного смешения цветов: желто-оранжевого и темно-синего, поскольку красители таких цветов образовались бы при разрыве молекулы по месту разобщающей бифенильной связи. При использовании в качестве конечной азосоставляющей фенола вместо ж-диамина образуется краситель Прямой темно-зеленый (206), т. к. в данном случае в смешении цветов с синим красителем участвует нс оранжевый, а желтый.
При использовании в качестве азосоставляющих аминов, способных далее диазотироваться и сочетаться с новыми азосоставляющими, красители получают по схеме: К *— Д -+ А -* К'. Очередность сочетания определяется в основном активностью азосоставляющей К.
По этой схеме получают Прямой коричневый светопрочный ЖХ [(207); Д — бензидин, А — смесь 5-амино- и 8-аминонафталин-2-сульфокислот, К и К' — салициловая кислота]. Краситель применяют для крашения хлопковых и вискозных тканей, трикотажа
и чулочно-носочных изделий. Устойчивость окрасок повышают обработкой солями хрома (к стирке) и солями меди (к свету).
Замена салициловой кислоты фенолом при третьем сочетании приводит к образованию красителя Прямого коричневого светопрочного 2ЖХ (208), отличающегося более чистым желтым оттенком.
Для получения красителя Прямого зеленого ЖХ (209) необходимо предварительно приготовить моноазокраситель (4-нитроанилин —* Аш-кислота; сочетание в кислой среде), и уже с моноазокраситслем проводить второе сочетание бис(диазо)соединения, т. е. краситель получают по схеме: К <— Д [С •*— М], где Д — бензидин, С — Аш-кислота, М — 4-нитроанилин, К — салициловая кислота. Если этот краситель получать по схеме получения красителей (204) и (205), то после сочетания с Аш-кислотой в щелочной среде второе сочетание в кислой среде осуществить с хорошим результатом практически не удается.
Прямой зеленый ЖХ применяется для крашения хлопка, иногда шерсти и шелка. Устойчивость окрасок увеличивается при обработке солями хрома и меди (от солей меди оттенок ухудшается — становится оливковым).
Если вместо салициловой кислоты применять фенол, то образуется Прямой зеленый (210). В этом случае сочетание с фенолом как с активной азосоставляющей проводят в последнюю очередь.
(205) R, V NH2, R3 = СН3;
(206) R, = R3 = 11, R2 ОН;
(210)
714
Новый справочник химика и технолога
По этой же схеме получают краситель Прямой коричневый ЖХ [(211); салициловая кислота «— бензидин —» сульфохризоидин (л/-фенилендиамин <— сульфаниловая кислота)]. Краситель применяется главным образом для крашения хлопчатобумажного трикотажа, т. к. светостойкость окрасок невысока, а устойчивость к стирке (важнейший показатель для красителей, применяемых для крашения нательного трикотажа) повышается обработкой солями хрома на волокне.
Применение 2,2'-дизамещенных бензидинов исключает возможность получения прямых красителей, т. к. пространственные затруднения, вызываемые заместителями в непосредственной близости к бифенильной связи, полностью нарушают плоскостность молекулы и лишают ее сродства к целлюлозе. Образующиеся красители могут применяться лишь в качестве кислотных или протравных, например, Кислотный желтый К (125}.
Большое практическое значение имеют прямые азокрасители — производные 4,4'-диаминостильбена (192}. Разобщающей группой здесь является виниленовая
группа -СН=СН-. Свободное вращение вокруг двух простых связей между виниленовой группой и бензольными ядрами обеспечивает более полное разобщение, чем в случае производных бензидина, поэтому окраски, образуемые стильбеновыми красителями, как правило, чище и ярче. Они отличаются также хорошей светостойкостью и устойчивостью к мокрым обработкам.
Наиболее простой из красителей этого ряда — Бриллиантовый желтый [4,4'-бис(4-гидроксифенилазо)-стильбен-2,2'-дисульфонат натрия (212}\ 4,4'-диамино-стильбен-2,2'-дисульфокислота —» фенол] — применяется в качестве индикатора: при ионизации в щелочной среде его цвет становится красным. Для устранения чувствительности к щелочам гидроксигруппы Бриллиантового желтого этилируют хлористым этилом, при этом образуется красивый яркий краситель золотистожелтого цвета — Хризофенин [4,4'-бис(4-этоксифенил-азо)стильбен-2,2'-дисульфонат натрия (2/3)], широко применяемый для крашения хлопка, вискозного волокна и бумаги.
СООН (27/)
(2/3)
Стильбеновые полиазокрасители имеют желтые, оранжевые, красные и коричневые цвета. Значительную часть этих красителей получают без использования реакций диазотирования и сочетания: для синтеза красителей данной группы применяют не 4,4'-диаминостиль-бен-2,2'-дисульфокислоту, а промежуточные продукты ее синтеза — 4,4'-динитростильбен-2,2'-дисульфокис-лоту (215} и 4-нитротолуол-2-сульфокислоту.
При взаимодействии 4,4'-динитростильбен-2,2'-ди-сульфокислоты с аминоазосоединениями (как правило, с и-аминоазокрасителями) образуются азоксипроизводные, которые легко восстанавливаются сульфидом натрия или глюкозой до азосоединений. Полученные красители отличаются устойчивостью к свету и мокрым обработкам.
Тетракисазокраситель Прямой алый светопрочный 2Ж (216} получают взаимодействием моноазокрасителя
[(2/4); 4-амино-анизол-2-сульфокислота —» крезидин] с 4,4'-динитростильбен-2,2'-дисульфокислотой (215} в растворе NaOH при кипении с последующим восстановлением сульфидом натрия. Краситель применяется для крашения хлопка и вискозного волокна.
Используя другие аминоазосоединения, аналогичным способом получают ряд ценных оранжевых, красных и коричневых красителей.
Из 4-нитротолуол-2-сульфокислоты стильбеновые красители получаются при нагревании этого соединения с водным раствором NaOH в результате окислительно-восстановительных процессов. По-видимому, первым продуктом этого процесса является 4,4'-ди-нитрозостильбен-2,2'-дисульфокислота (2/7), образующаяся в результате окисления метильных групп нитрогруппами; далее она превращается в трисазокраситель. Таким способом получают Прямой желтый К (218).
Ароматические соединения
715
Прямой желтый К применяют для крашения хлопка, шерсти, шелка и полушерстяных тканей в красивый золотисто-желтый цвет. Окраски не очень светостойки, но устойчивы к мокрым обработкам.
Если в процессе синтеза Прямого желтого К к реакционной массе добавить мягкие восстановители (сульфид натрия, сульфит натрия, глюкозу), образуется смесь Прямого желтого К (главный компонент) и продукта его восстановления (азоксигруппы восстанавливаются в азогруппы, нитрогруппы — в аминогруп
пы) — трисазокрасителя (279)), обладающего более глубоким цветом.
Смесь красителей (218) и (219) выпускается под названием Прямой оранжевый прочный и окрашивает хлопок, шерсть и шелк в оранжевый цвет.
4,4'-Диаминодифениламин-2-сульфокислота (193) применяется для синтеза ценных прямых красителей черного цвета. Иминогруппа является хорошим изолятором сопряжения, а в качестве ЭД-заместителя она углубляет цвет полиазокрасителей.
1. NaOH; Н2О
2. Na2S
HO3S н3со
HO3S
(218)
(219)
716
Новый справочник химика и технолога
Практически важные красители этой группы получают по схеме: К *— А «— Д —» А'—* К'.
Большое практическое значение имеет краситель Прямой черный 2С [(220); Д — 4,4'-диаминодифенил-амин-2-сульфокислота, А и А' — Гамма-кислота, К и К' — А-(2-гидроксиэтил)-л/-фенилендиамин, получаемый алкилированием л/-фенилендиамина этиленхлор-гидрином]. Сочетание бис(диазо)соединения с Гамма-кислотой (первое сочетание) необходимо проводить в щелочной среде, т. к. при сочетании в кислой среде образуется недиазотируемое о-аминоазосоединение. Краситель Прямой черный 2С применяют для крашения ниток, окраски имеют красивый иссиня-черный цвет и устойчивы к стирке.
Применяя вместо А-(2-гидроксиэтил)-л/-фенилен-диамина л/-фенилендиамин, получают краситель с зеленоватым оттенком — Прямой черный 23 (221), образующий менее светостойкие окраски.
Хорошим сродством к целлюлозе и высокой светостойкостью обладают дисазокрасители — производные 4,4'-диаминобензанилида (194). Разобщающей группой здесь служит амидная группа -NHCO-, которая вследствие способности к енолизации не может обеспечить надежного разрыва сопряженной системы дисазокрасителя. На основе 4,4'-диаминобензанилида могут быть получены как симметричные, так и несимметричные дисазокрасители. К числу несимметричных
относится Прямой коричневый светопрочный 2КХ (222), который получают сочетанием в щелочной среде бис(диазо)производного 4,4'-диаминобензанилида с салициловой кислотой и Гамма-кислотой последовательно.
Этот краситель — аналог бензидинового дисазокрасителя Прямого коричневого КХ (200), но превосходит его по свстопрочности.
Полиазокрасители — производные бис(фенил-амида) фумаровой кислоты. Яркие прямые полиазокрасители, образующие устойчивые к свету и мокрым обработкам окраски, могут быть получены ацилированием кислотных аминоазокрасителей дихлорангидри-дом фумаровой кислоты — фумароилдихлоридом. Этот способ получения прямых красителей аналогичен фос-генированию и также приводит к удвоению молекулы красителя, что и обусловливает необходимое сродство к целлюлозе.
Представителем этой группы красителей является Прямой оранжевый светопрочный 6Ж (224), получаемый взаимодействием оранжевого кислотного дисазокрасителя [(223); 4-аминоазобензол-3,4'-дисульфокис-лота —* jw-толуидин] с фумароилдихлоридом в присутствии соды. Благодаря хорошим изолирующим свойствам фумароилдиаминогруппы -NHCOCH=CHCONH-тстракисазокраситель (224) сохраняет чистоту оттенка дисазокрасителя (223).
Ароматические соединения
717
С помощью фумароилдихлорида можно связать остатки разных азокрасителей или остаток азокрасителя с остатком красителя другого класса, например, антрахинонового, и таким образом использовать эффект внутримолекулярного смешения цветов.
Полиазокрасители с триазиновым кольцом. Исключительно ценные полиазокрасители с чистыми и яркими оттенками образуются при разрыве сопряженной системы триазиновым кольцом (225). Триазиновое кольцо увеличивает сродство красителей к целлюлозе, повышает светостойкость окрасок и их устойчивость к мокрым обработкам.
Триазиновое кольцо вводится в молекулу красителя или его промежуточного продукта с помощью цианур-хлорида [2,4.6-трихлор-1,3,5-триазин (226)]. Атомы хлора в цианурхлориде легко обмениваются на -NH2, -ОН и другие группы, содержащиеся в молекулах красителя. Замещение атомов хлора происходит с различной скоростью: первый атом хлора замещается при 0-5 °C, второй — при 20-Л0 °C, третий — при 70-100 °C. Это позволяет проводить замещение ступенчато, вводя в реакцию последовательно различные красители. Комбинируя красители различных цветов, можно по правилу внутримолекулярного смешения цветов в азокрасителях с разобщенными азогруппами получать интересные колористические эффекты.
Так, краситель Прямой зеленый светопрочный (227) получают, последовательно вводя в реакцию с цианур-хлоридом синий дисазокраситель [(7&); Аш-кислота —> крезидин —* Аш-кислота (щел.)], желтый моноазокраситель [(79); 4-нитроанилин -» салициловая кислота; восстановление нитрогруппы] и анилин.
Цвет этого красителя является результатом сложения цветов синего и желтого красителей. Прямой зеленый светопрочный — один из лучших зеленых прямых красителей, он образует окраски более устойчивые по всем показателям, чем бензидиновые зеленые красители [(Прямой зеленый ЖХ (209) и Прямой зеленый (270)].
С помощью цианурхлорида можно соединять азокрасители с красителями других классов, например антрахиноновых, в этом случае также соблюдается эффект внутримолекулярного смешения цветов. Такое объединение целесообразно, если среди красителей одного класса трудно подобрать компоненты, обеспечивающие получение красителя нужного цвета, или когда трудно подобрать компоненты, равные по качеству (светостойкости и пр.). Например, среди азокрасителей есть желтые красители, обладающие очень высокой светостойкостью, тогда как красителей синего и голу
бого цветов с такой же высокой светостойкостью практически нет. Однако такие красители есть среди антрахиноновых, а желтые наоборот отсутствуют. Поэтому комбинация желтого азо- и голубого антрахинонового красителей может дать светостойкий зеленый краситель.
Примером такого красителя является Прямой ярко-зеленый светопрочный 4Ж (228), в молекуле которого светостойкий голубой антрахиноновый краситель соединен через триазиновое кольцо со светостойким желтым моноазокрасителем. Оба исходных красителя — кислотные, однако увеличение размеров молекулы, ее линейность, плоскостность и наличие триазинового кольца превращают гибридный краситель в прямой, обеспечивая ему высокое сродство к целлюлозе.
Прямые металлсодержащие азокрасители
Прямые красители, содержащие в ор^ио-положениях к азогруппе комплексообразующие группировки (гидрокси-, метокси-, амино-, карбокси- и др.), способны образовывать комплексы с металлами. Атомы хрома
718
Новый справочник химика и технолога
и кобальта для металлизации прямых красителей не применяют, т. к. шестикоординационные металлы образуют неплоские комплексы, в которых связи от атомов металла направлены к углам октаэдра. Для металлизации прямых красителей применяют соли двухвалентной меди (координационное число 4). Медь с азокрасителями образует достаточно устойчивые комплексы состава 1 : 1, в которых один атом меди приходится на одну азогруппу с комплексообразующими заместителями. В зависимости от характера комплексообразующих заместителей красители после омеднения образуют различные комплексы: о,о'-дигидроксиазокрасите-ли — (229), о-гидрокси-о'-метоксиазокрасители — (230), о-гидрокси-о'-аминоазокрасители — (231), о-гидрокси-о'-карбоксиазокраситсли — (232), о-гидрокси-о'-карбокси-метоксиазокрасители — (233).
Все комплексы плоские, т. к. связи от четырехкоординационного атома меди направлены к углам квадрата (5р2б7-гибридизация) и расположены в одной плоскости. Так как в молекулах большинства прямых красителей содержится не менее двух азогрупп, то при наличии комплексообразующих заместителей каждая из них может принять участие в комплексообразовании, в результате чего в молекулу вступит несколько атомов меди.
Образование медных комплексов (омеднение) возможно как до крашения, так и после. В первом случае краситель выпускается в виде готового комплекса, так называемые медьсодержащие красители (в названии такого красителя есть буква «М»); причем, как правило, это не ухудшает сродства прямых красителей к волокну, а иногда и повышает. Во втором случае омеднение производится непосредственно на волокне путем обработки окрашенного волокна солями меди или закрепителем ДЦМ (продукт конденсации дициандиамида, формальдегида и ацетата меди); в названии такого красителя есть буква «У».
Получение медьсодержащих азокрасителей осуществляют двумя способами:
1) при получении азокрасителей в щелочной среде соли меди можно добавлять в готовую реакционную массу. Здесь лучше применять растворимые в воде комплексные соли типа [Cu(NH3)4]SO4, чтобы избежать осаждения меди в виде гидроксида;
2) омеднение уже готовых красителей путем нагревания красителя с медным купоросом при 50-120 °C в слабощелочной среде, лучше в присутствии аммиака и органических оснований (пиридина, этаноламинов и др.).
Известны и другие способы омеднения, например сушка при 120 °C пасты красителя, содержащей медный купорос и аммиак.
В тех случаях, когда образующиеся медьсодержащие красители не растворимы или плохо растворимы в воде, в комплексы вводят органические основания, сообщающие им растворимость, например моноэтанол-амин. Такие красители содержат хелатную группировку (234). При крашении, в момент выбирания красителя
целлюлозным волокном, происходит отщепление органического основания и на волокне прочно закрепляется нерастворимый медьсодержащий краситель.
(230)
В большинстве случаев комплексы, образующиеся при омеднении на волокне, не отличаются от соответствующих медьсодержащих красителей. Исключение составляют красители с алкоксигруппами в орто-положении к азогруппе (например, производные о-ани-зидина или дианизидина), у которых при омеднении в процессе производства медьсодержащих красителей часто происходит дезалкилирование; при этом образуется комплекс, содержащий не алкокси-, а незамещенную гидроксигруппу. При омеднении на волокне, которое проводится в более мягких условиях, дезалкилирование обычно не происходит. Как правило, дезалкилирование увеличивает устойчивость комплексов.
Для синтеза полиазокрасителей, омедняемых на волокне, в качестве диазосоставляющих чаще всего используют 3,3'-дигидроксибензидин, дианизидин, бензидин-3,3'-дикарбоновую кислоту и 3,3'-ди(карбокси-метокси)бензидин, в качестве азосоставляющих — одинаковые или разные соединения, сочетающиеся в орто-положение к гидроксигруппе.
Так, краситель Прямой голубой СУ (235) получают бисдиазотированием 3,3'-дигидроксибензидина с последующим сочетанием диазосоединения с И-кислотой в щелочной среде. Краситель Прямой фиолетовый светопрочный СУ (236) получают аналогичным образом из бензидин-3,3'-дикарбоновой кислоты и jV-фенил-И-кислоты, Прямой чисто-синий светопрочный 2КУ (237)— из 3,3'-ди(карбоксиметокси)бензидина и 7V-(4-метоксифенил)-И-кислоты.
Ароматические соединения
719
(235) R= ОН; R' = Н;
(236) R = СООН; R' = С6Н5;
(237) R = ОСН2СООН; R' = и-СН3ОС6Н4;
Обработка солями меди волокон, окрашенных этими красителями, во всех случаях повышает устойчивость окрасок к действию света (в среднем на 3 балла) и к мокрым обработкам (в среднем на 1 балл).
Процесс крашения значительно упрощается при использовании готовых медьсодержащих красителей. Как правило, светостойкость образуемых ими окрасок выше, чем при омеднении на волокне. Многие медьсодержащие азокрасители по светостойкости не уступают лучшим кубовым красителям (6-7 и даже 7-8 баллов по восьмибалльной шкале).
Медьсодержащие азокрасители можно получить омеднением красителей (263), (235)-{237). Другой способ заключается в синтезе комплексообразующих азокрасителей более простого строения (например, о, о-дигидроксиазокрасителей), затем их превращают в полиазокрасители методами сочетания, фосгенирова-ния и др. Например, при синтезе красителя Прямого коричневого светопрочного М (239) сначала получают моноазокраситель (З-амино-4-гидроксибензолсульфо-кислота —» резорцин), который превращают в медный комплекс (238) действием щелочного раствора сульфата меди. Медный комплекс моноазокрасителя далее используют в качестве азосоставляющей для второго сочетания с бисдиазотированным бензидином.
Окраски, образуемые этим красителем на целлюлозном волокне, имеют светостойкость 6 баллов (по восьмибалльной шкале), устойчивость к стирке и другим воздействиям — 2-3 балла (по пятибалльной шкале). Устойчивость к стирке может быть повышена обработкой солями хрома (благодаря наличию остатка салициловой кислоты).
При синтезе красителя Прямого фиолетового светопрочного 2КМ (241) сначала получают моноазокраситель (5-амино-4-метокси-2-нитробензолсульфокисло-
та —» 6-гидроксинафталин-2-сульфокислота), затем восстанавливают нитрогруппу в моноазокрасителе сульфидом натрия, фосгснируют образовавшийся аминоазокраситель (240) и омедняют полученный дисазокра-ситель нагреванием с медноаммиачным раствором; омеднение сопровождается деметилированием метоксигрупп.
(247)
720
Новый справочник химика и технолога
Краситель образует окраски с устойчивостью к свету 7-8 баллов (по восьмибалльной шкале) и к стирке 3-4 балла (по пятибалльной шкале).
Активные азокрасители
При введении в молекулы азокрасителей заместителей с активными (подвижными) атомами, группами или связями, обусловливающими способность реагировать с окрашиваемым веществом с образованием ковалентных связей, получаются активные (реакционноспособные) красители. Окраски, образуемые активными красителями, исключительно устойчивы, особенно к мокрым обработкам, трению и химической чистке, т. к. связанный ковалентной связью краситель становится составной частью окрашенного волокна и практически с него не смывается. По яркости активные красители не уступают кислотным и близки к основным, они просты в применении и сравнительно недороги.
Активные красители различаются природой реакционноспособных заместителей и групп, содержащих эти заместители. В настоящее время важнейшими видами активных красителей являются триазиновыс, пиримидиновые и винилсульфоновыс.
Триазиновые красители. Эти красители содержат в качестве реакционноспособных заместителей чаще всего атомы хлора, иногда брома, а в качестве их носителя — триазиновое кольцо (225). В большинстве случаев триазиновые азокрасители получают взаимодействием красителей, содержащих первичные или вторичные амино-, гидрокси- или меркаптогруппы, с цианурхлоридом (226), при этом происходит замещение атомов галогена на основные группы красителя. Оставшиеся незамещенными атомы галогена способны замещаться гидроксигруппами целлюлозы или аминогруппами белковых и синтетических полиамидных волокон, например:
Целл—ОН + Кр—Т—Cl + Na2CO3
-> Целл—О—Т—Кр + NaCl + СО2 + Н2О (4.3.15)
где Целл — остаток целлюлозы, Кр — остаток красителя, Т — триазиновое (или пиримидиновое) кольцо.
На основе моноазокрасителей получают активные красители желтого, оранжевого, красного и коричневого цветов. В зависимости от числа оставшихя незамещенными атомов хлора в молекуле цианурхлорида (226) красители делятся на дихлортриазиновые и монохлортриазиновые. Дихлортриазиновые красители можно получить различными способами, например, взаимодействием моноазокрасителей, содержащих первичные или вторичные аминогруппы, с цианурхлоридом при 0-5 °C. Примером такого красителя является Активный золотисто-желтый КХ [(272); моноазокраситель 3-аминонафталин-1,5-дисульфокислота —> л/-толуидин].
По другому способу в диазо- или азосоставляющую сначала вводят активную группу, а затем проводят ди
азотирование и азосочетание. Так, взаимодействием Аш-кислоты с цианурхлоридом при 0-5 °C получают А-(2,4-дихлор-1,3,5-триазинил-6)-Аш-кислоту (243). Сочетанием ее с диазосоединениями получают дихлор
триазиновые красители, например, при сочетании с диазотированным анилином получают Активный ярко-красный 5СХ (244).
CI
Дихлортриазиновыс красители способны в мягких условиях взаимодействовать с окрашиваемым веществом (на что указывает буква X в их названиях — см. 4.3.4.3): при 20-30 °C в присутствии соды.
Монохлортриазиновые красители получают из дихлортриазиновых, замещая один атом хлора в триазиновом кольце алифатическим или ароматическим (чаще) амином. Так, краситель Активный ярко-красный 6С (245) получают действием цианурхлорида на моноазокраситель (4-аминотолуол-З-сульфокислота -» Аш-кис-лота; сочетание в щелочной среде) с последующим замещением второго атома хлора в цианурхлориде А-метил-
анилином.
Ароматические соединения
721
Исходными веществами для получения активных красителей могу!' быть комплексы моноазокрасителей с металлами. Так, металлсодержащий краситель Активный фиолетовый 4К (246) получают последовательным взаимодействием цианурхлорида сначала с медным комплексом моноазокрасителя (З-амино-4-гидрокси-бензолсульфокислота Аш-кислота; сочетание в щелочной среде), затем с аммиаком. Краситель образует окраски, обладающие высокой светостойкостью.
Монохлортриазиновые красители, не содержащие групп, придающих им растворимость в воде, применяются как дисперсные активные красители («процинай-лы») для крашения полиамидных волокон. К таким красителям относится, например, Процинайл желтый (247).
ОН
(247)
Молекулы красителей этого типа содержат группировки, характерные для дисперсных красителей, а присутствие триазинового кольца придает им активность в реакции с волокном.
Пиримидиновые красители. Носителем активного атома хлора в этих красителях является ядро пиримидина. Для получения активных красителей используются 2,4,6-трихлорпиримидин (248) и 2,4,5,6-тетрахлор-пиримидин (249).
дине — при 70 °C. Соответственно в более жестких условиях происходит и фиксирование красителя на окрашиваемом материале — при температурах выше 100 °C.
Активные красители, содержащие остаток пиримидина, получают аналогично триазиновым красителям. Так, активный красновато-желтый дихлорпиримидиновый краситель (250) получают взаимодействием моноазокрасителя (3-аминонафталин- 1,5-дисульфокислота .м-толуидин) с 2,4,6-трихлорпиримидином при 60 °C.
S°3Na (250)
Трихлорпиримидиновые красители более реакционноспособны по отношению к целлюлозе, чем дихлорпиримидиновые, и более устойчивы к щелочному гидролизу, чем триазиновые красители. Это свойство весьма ценно в технологии крашения и печатания, т. к. красильные растворы и печатные краски иногда приходится подвергать длительному хранению. Печатные краски на основе пиримидиновых красителей значительно устойчивее по сравнению с красками на основе триазиновых красителей.
Винилсульфоновые красители. Винилсульфоно-вые активные красители содержат 0-сульфатоэтил-сульфонильную группу: -8О2(СН2)2О8ОзЫа. В процессе крашения под действием щелочи от этой группы отщепляется остаток серной кислоты и образуется ви-нилсульфонильная группа, взаимодействующая с окрашиваемым веществом, например с целлюлозой (уравнение (4.3.16)). Процесс протекает при 60-70 °C.
Кр— SO2(CH2)2OSO3Na
NAOH
Кр— so2CH= сн2 (4 3л 6)
—► Кр—SO2(CH2)2—О—Целл
С1 (248)
С1 (249)
Активность атомов хлора в хлорпиримидинах значительно ниже по сравнению с цианурхлоридом: например, замещение первого атома хлора в цианурхло-риде происходит при 0-5 °C, а в 2,4,6-трихлорпирими-
Синтез активных винилсульфоновых азокрасителей практически не отличается от синтеза обычных азокрасителей, т. к. активная группа этих красителей уже присутствует в одном из исходных промежуточных продуктов. Например, Активный желтый 2КТ (251) получают сочетанием диазотированного (З-амино-4-метоксифенил)сульфонилэтилсульфата натрия с 3-ме-тил-1-(4-сульфофенил)пиразолоном-5. При сочетании этого же диазосоединения с 7-гидроксинафталин-1,3-дисульфокислотой получают Активный оранжевый ЖТ (252).
722
Новый справочник химика и технолога
Активные триазиновые и особенно винилсульфоно-вые азокрасители применяют и для крашения шерсти. Специальные активные красители для шерсти и натурального шелка содержат а-бромакрилоиламино-(-NHCOCBr=CH2) или хлорацетиламиногруппу (-NHCOCH2C1). Примером такого красителя является Ланазоль красный [(253); 4-а-бромакрилоиламино-анилин-2-сульфокислота —> Гамма кислота, сочетание в кислой среде].
Специальные активные красители для синтетических полиамидных волокон содержат активные 2-гидрокси-З-хлорпропиламиногруппу (-NHCH2CHOHCH2C1) или Р-хлорэтиламиносульфонильную группу (~SO2NHCH2CH2C1). Примером такого красителя является Процинайл оранжевый Г [(254); 4-(Р-хлорэтиламиносульфонил)ани-лин -> 4-Аг,А-ди(Р-гидроксиэтил)-3-метиланилин].
C1(H2C)2HNO2S
(254)
При крашении в кислой среде краситель ведет себя как дисперсный и равномерно окрашивает волокно. При последующем подщелачивании и нагревании до 100 °C атом галогена замещается аминогруппами полиамидного волокна, вследствие чего между красителем (Кр) и волокном (В) образуется ковалентная связь (уравнение (4.3.17)):
Kp—SO2NHCH2CH2C1 + H2N—В —
— Kp—SO2NHCH2CH2—NH—В (4.3.17)
Недостатком многих активных красителей является относительно малая фиксируемость на волокне в процессе крашения. Это объясняется тем, что скорость взаимодействия красителя с волокном (уравнения (4.3.16) и (4.3.17)) соизмерима со скоростью гидролиза красителя, приводящего к образованию неактивного производного (уравнения (4.3.18) и (4.3.19); Т — группа, содержащая активный галоген).
Kp—Т—С1 + "ОН — Kp—Т—ОН + СГ (4.3.18)
Kp—SO2CH2CH2OSO3Na + “ОН -*
— Kp—SO2CH2CH2OH + Na2SO4 (4.3.19)
В результате этих конкурирующих процессов степень фиксации, т. е. полезного использования красителя, часто составляет менее 70 %, остальное количество красителя теряется и загрязняет сточные воды красильных фабрик.
Эффективным способом повышения фиксируемости активных красителей является введение в их молекулы двух и более активных групп, причем иногда комбинируют хлортриазиновую активную группировку с суль-фатоэтилсульфонильной. Вводят эти группировки обычными способами: хлортриазиновую — с помощью цианурхлорида или его монозамещенных, сульфато-этилсульфонильную — в составе диазо- или азосоставляющих. Степень фиксации таких красителей составляет 95 % и выше.
Активный азокраситель (255) получен сочетанием диазо- и азокомпонентов, содержащих триазиновые кольца, а именно: в качестве диазосоставляющей используется 2-амино-4-[4-(3-сульфофениламино)-2-хлор-1,3,5-триазинил-6]аминобензолсульфокислота, в качестве азосоставляющей — Аг-[4-(3-сульфофениламино)-2-хлор-1,3,5-триазинил-6]Аш-кислота. Краситель окрашивает целлюлозные волокна в красный цвет, степень фиксации на волокне составляет около 97 %.
Содержащий хлортриазиновую и сульфатоэтил-сульфонильную группы активный краситель (256) получают взаимодействием азокрасителя (7-аминонафта-лин-1,3,6-трисульфокислота —> А-ацетил-л/-фениленди-амин) с цианурхлоридом и З-ф-сульфатоэтилсульфо-нил)анилином (или с продуктом взаимодействия двух последних). Краситель окрашивает целлюлозные волокна в желтый цвет, степень фиксации 95-97 %.
Активные красители с высокой степенью фиксации на волокне значительно дороже красителей с одной активной группировкой.
Ароматические соединения
723
(255)
Жирорастворимые азокрасители
Жирорастворимыми называют азокрасители, способные растворяться в жирах. В молекулах таких красителей отсутствуют кислотные группы (сульфо-, карбокси-), нитрогруппы и атомы галогенов. Применяют жирорастворимые красители для окрашивания жиров, воска, парафина, сапожных кремов, а также пластических масс, резиновых изделий и пр. Жирорастворимые азокрасители обычно имеют желтый, оранжевый и кра-ный цвета. Представителями практически значимых жирорастворимых азокрасителей являются Жирорастворимый желтый К [Д-фенилазо-Л^УУ-диэтиланилин (257); анилин —* М,УУ-диэтиланилин], Жирорастворимый желтый 3 [5-гидрокси-3-метил-1-фенил-4-фенил-азопиразол (255); анилин —> 3-метил-1-фенил-пиразо-лон-5], Жирорастворимый оранжевый [2-гидрокси-1-фенилазонафталин (259); анилин —> 2-нафтол], Жирорастворимый красный С [2-гидрокси-1-(2-метокси-фенилазо)нафталин (260); о-анизидин —> 2-нафтол].
Пигменты
Нерастворимые амино- и гидроксиазокрасители можно использовать в качестве пигментов. Пигменты в значительных количествах используются в лакокрасочной и полиграфической промышленности, их применяют также для крашения резины, пластических масс, изготовления цветных карандашей, обоев и т. п.
(260) R = ОСН3;
В текстильной промышленности азопигменты используются для печати по различным тканям. Они не имеют сродства к волокнам и не вступают с ними в химическое взаимодействие, поэтому их закрепляют на волокнах с помощью специальных связующих, образующих на ткани пленку, в которой распределяется краситель. Пигментные печатные краски готовят простым
724
Новый справочник химика и технолога
смешением компонентов. Смешивать пигменты и печатные краски на их основе можно в любых соотношениях, что дает возможность значительно расширить цветовую гамму, печать получается яркой и ровной. Пигментные способы печати и крашения пригодны для всех волокон (натуральных, искусственных, синтетических) и особенно рекомендуются для декоративных тканей, тентов, занавесей, штор, галантерейных изделий (галстуки, носовые платки и др.).
В зависимости от области применения к пигментам предъявляются различные требования, Однако независимо от специфических требований все они должны быть светостойкими, не растворяться в органических растворителях, выдерживать высокую температуру нагревания, обладать миграционной устойчивостью и т. д. Оптимальные размеры частиц пигмента 1-2 мкм.
Известны азопигменты различных цветов: от желтого до бордо. Пигменты желтого цвета получают с использованием арилидов ацетоуксусной кислоты. Из них наибольшее практическое значение имеет Пигмент желтый светопрочный [(26/); 4-амино-З-нитротолуол —> анилид ацетоуксусной кислоты], отличающийся чисто-желтым цветом и высокой устойчивостью к различным воздействиям.
Пигмент желтый светопрочный применяется в полиграфии, производстве цветных карандашей, в текстильной промышленности.
Пигменты оранжевого и красного цветов являются производными бензолазонафталина. Представителями этой группы практически значимых пигментов являются Пигмент оранжевый прочный [2-гидрокси-1-(2,4-динитрофенилазо)нафталин (262)], Пигмент красный Ж [2-гидрокси-1-(4-нитрофенилазо)нафталин (263)], Пигмент алый Ж [2-гидрокси-1-(4-нитро-2-хлорфенилазо)-нафталин (264)], Пигмент алый [2-гидрокси-1-(2-нитро-4-метилфенилазо)нафталин (265)]. Все эти пигменты получены на основе 2-нафтола (азосоставляющая), в качестве диазосоставляющей использовались различные производные анилина.
(262) R = R' = NO2; (263) R H, R' - NO2;
(264) R - Cl, R' = NO2; (265) R = NO2, R' = CH3.
Пигмент бордо [2-гидрокси-1-(нафтил-1-азо)наф-талин (266); нафталинамин-1 2-нафтол] является производным азонафталина.
(266)
Пигменты, применяемые в текстильной промышленности для печати по различным тканям, имеют маркировку ТП (для текстильной печати). Для синтеза азопигментов ТП обычно в качестве диазосоставляющих применяют производные анилина и толуидинов, в качестве азосоставляющих — арилиды 3-гидроксинафта-лин-2-карбоновой кислоты (азотолы) или ацетоуксусной кислоты. Примерами таких пигментов являются Пигмент алый 2СТП [(267); 2,5-дихлоранилин —> анилид З-гидроксинафталин-2-карбоновой кислоты], Пигмент ярко-красный 4ЖТП [(268); 2,5-дихлоранилин ->
2-метоксианилидид З-гидроксинафталин-2-карбоно-вой кислоты].
(267) R = Н; (268) R = ОСН3.
Пигменты выпускают нанесенными на различные минеральные субстраты (гидроксид алюминия, сульфат бария, мел), часто с добавкой минеральных наполнителей для понижения интенсивности окраски. Иногда необходимо переводить пигмент из одной кристаллической модификации в другую.
Лучшим способом нанесения (осаждения) пигментов на субстраты, обеспечивающим однородность продукта, высокую степень дисперсности и яркость оттенка, является синтез красителя в присутствии субстрата. ‘ Например, Пигмент алый (265) получают сочетанием < диазосоединения из 4-амино-З-нитротолуола с 2-наф-' толом в присутствии смешанного субстрата: BaSO4 и А1(ОН)3.
Иногда нерастворимый краситель смешивают с субстратом уже в готовом виде. В этих случаях субстрат по существу является наполнителем. Таким способом получают Пигмент оранжевый прочный (262). Краситель является продуктом сочетания диазосоединения из 2,4-динитроанилина (диазотирование нитрозилсерной кислотой при 15-25 °C) и 2-гидроксинафталина (сочетание в сильно кислой среде во избежание отщепления о-нитро-
Ароматические соединения
725
группы). Субстрат — смесь BaSO4 и А1(0Н)3 — добавляют перед сушкой промытого красителя.
Для увеличения молекулярной массы, повышающей стойкость пигментов к органическим растворителям, в их молекулы вводят арилсульфоновые, алкилсульфонамидные, ациламиногруппы, а также нитрогруппы и атомы галогенов. Так, Пигмент розовый Ж [(269); 2-аминоанизол-4-А,А-диэтилсульфонамид -+ 2,4-димс-токси-5-хлоранилид З-гидроксинафталин-2-карбоновой кислоты)] обладает высокой светостойкостью и устойчив к действию растворителей и щелочей.
(269)
Азолаки
Нерастворимые в воде соли (кальциевые, бариевые и марганцевые (реже)) кислотных азокрасителей называются лаками, а красители, используемые для получения лаков, — лаковыми. Поскольку лаки предназначены в основном для тех же целей, что и пигменты, их также выпускают нанесенными на различные минеральные субстраты часто с добавкой минеральных наполнителей.
Нанести лак на субстрат можно, осаждая нерастворимую соль красителя в присутствии субстрата или смешивая с субстратом готовую нерастворимую соль. При осаждении соли красителя в присутствии субстрата образующийся лак отличается большой однородностью и яркостью. Высокого качества лак получается также при одновременном проведении сочетания и ла-кообразования в присутствии субстрата. Так, в производстве Лака оранжевого [бариевая соль 2-гидрокси-1 -(4-сульфонатофенилазо)нафталина (270)] осаждение нерастворимой бариевой соли красителя Кислотного оранжевого (106) проводят в момент сочетания в присутствии смеси BaSO4 и А1(ОН)3.
В производстве Лака красного ЖБ [бариевая соль 2-гидрокси-1 -(5-метил-2-сульфонато-4-хлорфенилазо)-нафталина (277)] нерастворимая бариевая соль моно
азокрасителя Лакового красного Ж (5-амино-2-хлорто-луол-4-сульфокислота —> 2-гидроксинафталин) образуется при действии сухого ВаС12 на раствор натриевой соли красителя. Затем к суспензии бариевой соли красителя добавляют сухой сульфат бария, размешивают и отфильтровывают лак.
(271)
Азокрасители, получаемые на волокне
Синтез пигментов непосредственно на ткани явился новой вехой в крашении. Способ такого крашения заключается в последовательной обработке хлопчатобумажной ткани щелочным раствором азосоставляющей и диазосоставляющей. В результате такой обработки образование красителя и крашение происходит одновременно.
Широкое применение этот метод крашения получил после того, как было освоено производство так называемых азогенов — соединений, используемых для образования нерастворимых азокрасителей непосредственно на волокне. К азогенам относятся азотолы, стойкие диазопрепараты (активные и пассивные) и полные красочные составы.
Азотолы. Арилиды гидроксикарбоновых кислот, применяемые в качестве азосоставляющих при образовании красителей на волокне, получили название азо-толов. Наибольшее практическое применение нашли арилиды З-гидроксинафталин-2-карбоновой кислоты (272) (звездочкой отмечено место сочетания). Используя для ацилирования различные амины ароматического и гетероциклического рядов, получают азотолы, позволяющие образовать на волокне красители разнообразных оттенков. На природу ацилированного амина, как правило (есть исключения), указывают буквенные обозначения в названии азотола, взятые из названия амина, например: А — анилин, ОТ — о-толуи-дин, МНА — jw-нитроанилин и т. д.
Азотолы на основе З-гидроксинафталин-2-карбо-новой кислоты используются, главным образом, для получения оранжевых, красных, бордо и синих цветов. Желтые, зеленые, коричневые и черные цвета получают, используя азотолы на основе других гидроксикар-
726
Новый справочник химика и технолога
боновых кислот, а также р-кетокислот. Буквенные обозначения в названиях таких азотолов обычно (не всегда) указывают на цвет наиболее важных красителей, образующихся при сочетании с ними диазосоединений.
Таблица 4.3.3
Азотолы — производные
З-гидроксинафталин-2-карбоновой кислоты
R Название азотола
С6Н5 Азотол А
С6Н4СН3-о Азотол ОТ
С6Н4ОСН3-о Азотол ОА
С6Н4ОСН3-и Азотол ПА
C6H4NO2-.m Азотол МНА
5-С1С6Н3ОСН3-2 Азотол ХА
5-С1С6Н2(ОСН3)2-2,4 Азотол О
Нафтил-1 Азотол АНФ
В качестве азотолов для получения желтых окрасок используют производные р-кетокислот, главным образом, ацетоуксусной [Азотол 2Ж (275)] и бензоилуксусной [Азотол ЖН (274)]. С ними происходит сочетание по активным метиленовым группам, отмеченным звездочкам.
Для получения коричневых окрасок используют арилиды 2-гидроксикарбазол-З-карбоновой кислоты [Азотол К (275)] и З-гидроксидибензофуран-2-карбо-новой кислоты [Азотол КТ (276)], для получения черных окрасок — арилиды гидроксибензокарбазолкарбоновой кислоты [Азотол Ч (277)]. В качестве азотолов для получения зеленых окрасок применяют арилиды З-гидроксиантрацен-2-карбоновой кислоты [Азотол 3 (275)] или более сложные (комбинированные) азотолы (см. 4.3.5.13)
(275)
Звездочками отмечены места, по которым происходит сочетание.
Азоамины. Вторым компонентом (диазосоставляющей) для получения красителей на волокне является первичный амин, называемый азоамином. К названию азоамина обычно добавляются слова и буквы, указывающие цвет и оттенок наиболее важного красителя, образующегося с участием данного азоамина, например, Азоамин желтый О (2-хлоранилин), Азоамин красный Ж (4-нитроанилин), Азоамин красный С (2-амино-4-хлортолуол), Азоамин синий О (4-амино-4'-метоксидифениламин). Вследствие технических неудобств (в частности, из-за необходимости заниматься диазотированием) азоамины применяются крайне редко и в ограниченном количестве. Наиболее удобной формой аминов для получения красителей на волокне являются стойкие формы диазосоединений (диазопрепараты), разделяющиеся на активные и пассивные.
Активные стойкие диазопрепараты представляют собой соли диазония с различными компенсирующими анионами. Они выпускаются под названием диазоли', это слово заменяет слово «азоамин» в названии исходного аминосоединения. Например, Диазоль красный Ж — активный стойкий диазопрепарат, полученный из Азоамина красного Ж.
Диазоли выпускают в виде двойных солей хлоридов или сульфатов диазония с солями некоторых металлов: Zn (предпочтительно), Са, Mg и др. [Диазоль оранжевый О (279), Диазоль алый 2Ж (256)], в виде солей с ароматическими сульфокислотами [Диазоль розовый О (257)], в форме борфторидов (фторборатов) диазония [Диазоль красный 4С (252)] и иногда в виде хлоридов или сульфатов диазония [Диазоль синий О (255), выпускается в виде водной пасты].
(279)
(256)
Ароматические соединения
727
2. Амин-стабилизатор не должен образовывать диазоаминосоединения, легко подвергающиеся таутомерному превращению, в результате которого при расщеплении образуются вещества, отличные от исходных. Например, при взаимодействии 3-хлорбензолдиазония с сульфаниловой кислотой образуется диазоаминосоединение (284), легко переходящее в другую таутомерную форму. При расщеплении этого диазоаминосоединения кроме исходных соединений образуются и другие, в том числе диазопроизводное сульфаниловой кислоты, способное сочетаться с азотолами.
Независимо от различий в химическом составе диазолей способ применения их одинаков: для сочетания с азотолом на волокне диазоль достаточно растворить в воде.
Сухие соли диазония способны разлагаться со взрывом, и, несмотря на то, что у диазолей эта способность понижена, чтобы полностью устранить опасность взрыва, диазоли перед сушкой смешивают с наполнителями — сухим AI2(SO4)3 • 6Н2О, безводным Na2SO4 и т. п.
Пассивные стойкие диазопрепараты представляют собой диазосоединения, не имеющие ионных связей. Это продукты взаимодействия диазосоединений с первичными и вторичными аминами, со слабыми кислотами и др. Общим для всех пассивных форм диазосоединений является неспособность вступать в реакцию азосочетания без предварительной специальной обработки. К пассивным стойким диазопрепаратам относятся диазамины, триазоны, диазосульфонаты и нитрозамины.
Диазамины. При взаимодействии диазосоединений с первичными и вторичными жирными и ароматическими аминами в нейтральной или слабощелочной среде образуются диазоаминосоединения (уравнение (4.3.20)).
ArN*X + H2NR + NaOH
> Ar-N=N—NH—R + H2O + NaX (4.3.20)
Диазоаминосоединения неактивны к сочетанию и в отсутствие кислоты устойчивы, при подкислении расщепляются с образованием исходных продуктов: соли диазония и амина. Диазоаминосоединения выпускаются под названием диазамины.
Первичные и вторичные амины, применяемые для получения диазаминов, называют стабилизаторами. Амины, применяемые в качестве стабилизаторов, должны удовлетворять ряду требований.
1. Амин-стабилизатор при взаимодействии с диазосоединениями не должен сочетаться в ядро с образованием азосоединения. Например, анилин, который в нейтральной и щелочной средах образует с солями диазония диазоаминосоединения, после расщепления последних вступает в нормальное сочетание (уравнение (4.3.21)) и поэтому не применяется как стабилизатор.
ArNXl’ + СбН5\Н2 (ней|р) > Ar N-N-NHCJls -н<? >
--нс1-> Ar-N=N-C6H4NH2 (4.3.21)
Таутомерное равновесие сдвигается вправо (в сторону образования нежелательного продукта) тем сильнее, чем больше основность амина-стабилизатора превосходит основность исходного азоамина. Поэтому в качестве стабилизаторов могут применяться такие амины, основность которых понижена наличием ЭА-заместителей в ароматическом ядре.
3. Амин-стабилизатор должен образовывать такие диазоаминосоединения, которые достаточно устойчивы к действию СО2, но легко расщепляются под действием более сильных минеральных (соляная, серная) и органических (муравьиная, уксусная) кислот.
Этим гребованиям в наибольшей степени соответствуют 4- и 5-сульфоантраниловые кислоты [(285) и (286)', R = Н] и их моноалкильные производные (R = СНз, С2Н5), а также А-моноалкильные производные антраниловой кислоты [(257); R = (СН2)2ОН; СН2СООН]. Эти соединения и применяются в основном качестве аминов-стабилизаторов.
728
Новый справочник химика и технолога
Диазамины получают взаимодействием солей ди-азония с амином-стабилизатором в слабощелочной, нейтральной или в слабокислой среде с последующим подщелачиванием при 5-10 °C в течение нескольких часов. Так, при получении Диазамина красного С (288) из Азоамина красного С (2-амино-4-хлортолуола) и 5-сульфоантраниловой кислоты необходимую щелочность среды создают добавлением ацетата натрия.
Антраниловую кислоту (287; R = Н) и ее А-моно-алкильные замещенные применяют для получения диазаминов, расщепляющихся с образованием солей ди-азония, активных к сочетанию в нейтральной среде (при нагревании). К таким диазаминам относится Диазамин красный К (289), полученный из Азоамина красного К (2-амино-4-хлоранизола) и замещенной антраниловой кислоты.
Способность образовывать активные к сочетанию в нейтральной среде диазониевые соли является очень ценным свойством диазоаминосоединений типа (289) при использовании их для узорчатой расцветки тканей способом печатания. Чтобы перевести такие диазамины в активную форму, достаточно просто обработать их водяным паром.
Для перевода обычных диазаминов в активную форму необходимо обработать их смесью паров муравьиной или уксусной кислоты с водяным паром, т. е. провести так называемую «кислую запарку», что является большим недостатком, т. к. требует применения
коррозистойкой аппаратуры. Необходимость создания щелочной среды для взаимодействия с азотолами является вторым недостатком этих диазаминов, т. к. делает невозможным использование их вместе с красителями других классов, в частности с кубовыми, которые в щелочной среде восстанавливаются в лей-косоединения.
Для стабилизации диазосоединений с большим числом сильных ЭД-заместителей применяют вторичные амины жирного ряда, в частности саркозин [А-метил-глицин (290)], метилтаурин [метиламиноэтансульфокислота (29/)]. Так, взаимодействием Азоамина синего 2С (4-бензоиламино-2,5-диэтоксианилина) с метилтау-рином получают Диазамин синий 2С (292).
.NH /СООН нзс
SO3H
(290)
(297)
Гриазоны — это соединения ряда 3,4-дигидро-бензо[е]1,2,3-триазинона-4. Их получают фосгенирова-нием 4-сульфоантраниловой кислоты (285). При этом образуется сульфоизатовая кислота (293), которая при взаимодействии с азоаминами ArNH2 и последующем диазотировании полученных А-(2-амино-4-сульфобен-зоильных) производных (294) образует триазоны (295).
При взаимодействии со щелочами триазоны расщепляются с образованием диазоаминосоединений (296) — производных сульфоантраниловой кислоты, которые превращаются в активные к сочетанию соли диазония в нейтральной среде; при этом всегда образуется соль диазония исходного азоамина, т. к. для диазоаминосоединений на основе производных антраниловой кислоты (см. выше) таутомерное равновесие практически полностью сдвинуто в сторону (297).
Ароматические соединения
129
Диазосульфонаты. При взаимодействии солей диазония с Na2SO3 в нейтральной или слабощелочной среде образуются натриевые соли диазосульфокислот — диазосулъфонаты (уравнение (4.3.22)). Диазосульфонаты устойчивы в щелочной и нейтральной средах и неактивны к сочетанию. При нагревании в водном растворе или действии водяного пара диазосульфонаты гидролизуются с образованием бисульфита и диазогидроксида, легко переходящего при подкислении в активную диазониевую форму (уравнение (4.3.23)). Еще легче переход в активную форму происходит под действием окислителей, например, К2Сг2О7; диазосульфонат превращается при этом в сульфат или бисульфат диазония (уравнение (4.3.24)).
АгЫ2СГ + Na2SO3 — Ar-N=N-SO3Na + NaCl (4.3.22)
Ar-N=N-SO3Na—Ar-N=N-OH До >ArN2 (4.3.23)
Ar-N=N-SO3Na |0':”2H° >ArN2SO4H~ (4.3.24)
J -NaOH 2 4 \ /
В настоящее время в форме диазосульфоната (298) получают пассивный стойкий диазопрепарат Азоамина синего О, который не удается удобно переводить в форму диазамина. Другие диазосульфонаты не получили практического применения.
Нитрозамины. При нагревании солей диазония со щелочами образуются диазотаты — соли диазосоединений и щелочных металлов (уравнение (4.3.25)).
ArN2X~ + 2NaOH Ar-N=N -CTNa+ + NaX + H2O
(4.3.25)
Диазотаты не активны к сочетанию и значительно устойчивее солей диазония; при подкислении они превращаются вновь в диазониевые соли. Выпускные формы диазотатов называются нитрозаминами, например, Нитрозамин оранжевый О (299).
N=N-O~Na+
(299)
Устойчивые диазосоединения в форме нитрозами-нов получают из аминов, содержащих ЭА-заместители в орто- и «ара-положении к аминогруппе. Для перевода их в активную форму проводят обработку парами минеральных или органических кислот. Большим не
достатком нитрозаминов является их большая чувствительность к парам кислот, в том числе к диоксиду углерода: достаточно небольшого повреждения тары, чтобы под действием СО2 началось превращение диазотата в неустойчивую и легко разлагающуюся соль диазония. Поэтому в настоящее время нитрозамины применяют крайне редко.
Полные красочные составы — это составы, которые содержат оба компонента, необходимые для образования нерастворимого азокрасителя на волокне. Применение таких составов особенно удобно при печати цветных узоров на тканях. В этом случае отпадает необходимость в предварительной обработке ткани растворами азотола или диазосоединения, как это делается при раздельном применении азогенов. Полный красочный состав вводят в состав печатной краски, которую наносят на поверхность ткани в виде узора с помощью печатных машин. Затем ткань подвергают кратковременной обработке для перевода диазосоединения в активную к сочетанию форму (например, действию паров органической кислоты при 100 °C в течение нескольких секунд). При этом в местах узора происходит сочетание и образующийся нерастворимый краситель прочно закрепляется на волокне.
Для приготовления полных красочных составов пригодны лишь неактивные стойкие диазопрепараты, т. к. активные будут реагировать с азотолами уже в момент смешения. В зависимости от используемых диазопрепаратов полные красочные составы делятся на диа-заминолы, пологены, рапидозоли, диазотолы.
Диазаминолы. Смесь азотолов с диазаминами выпускают под названием диазаминолы с добавлением слов и буквенных обозначений, указывающих цвет и оттенок красителя, образующегося из данной комбинации азогенов после проявления. Например, Диазаминол красный 2Ж является смесью Диазамина красного С (288) с Азотолом ОА (272; R == С6Н4ОСН3-о). Под действием паров муравьиной или уксусной кислоты диазоаминосоединение расщепляется с образованием соли диазония, которая вступает в сочетание с азотолом, в результате на ткани образуется нерастворимый красный азокраситель (300). Регенерировавшийся растворимый амин-стабилизатор удаляется с ткани при промывке.
Особый интерес представляют диазаминолы, расщепляющиеся практически в нейтральной среде; в их состав входят диазамины на основе производных антраниловой кислоты. Полные красочные составы с их участием получили название диазаминолов Н (Н — от слова нейтральный), или нейтрогенов. Таков, например, Диазаминол желтый светопрочный НЗ — смесь Диазамина красного К (289) с Азотолом 2Ж (273). После проявления на ткани действием водяного пара в местах узора образуется нерастворимый желтый азокраситель (301); амин-стабилизатор удаляется с ткани при промывке.
Пологены. Смеси азотолов с триазонами называют пологенами (разработаны в Польше). При печати или гладком крашении их растворяют в щелочах, при этом
730
Новый справочник химика и технолога
триазоны гидролизуются с образованием диазоаминосоединений. При последующей обработке водяным паром пологены ведут себя как нейтрально проявляемые диазаминолы. Например, при проявлении на ткани узора, напечатанного смесью триазона (302) с Азотолом АНФ (272; R = нафтил-1), образуется нерастворимый азокраситель (303) цвета бордо; амин-стабилизатор удаляется с ткани при промывке.
Рапидозоли. Смеси азотолов с диазосульфонатами получили название рапидозолей. Ассортимент их ограничен, и применяются они значительно меньше диаза-минолов. Типичным представителем является Рапидо-золь синий ИБ — смесь диазосульфоната (298) из Азоамина синего О с Азотолом А (272; R = С6Н5). При проявлении этого рапидозоля на ткани с помощью окислителя образуется синий краситель (304).
(303)
Ароматические соединения
731
Смеси азотолов с нитрозаминами выпускали под названием диазотолы. Например, Диазотол оранжевый 2К представляет собой смесь Нитрозамина оранжевого О (299) и Азотола А (272; R = С6Н5). При обработке парами кислоты ткани с узором, напечатанным этим диазотолом, происходит образование красителя (305).
(305)
В настоящее время диазотолы практически не применяют, т. к. они чувствительны к действию СО2 и влаги воздуха, вследствие чего неустойчивы при хранении (нитрозамин переходит в активную форму и сочетается с азотолом).
Обычные полные красочные составы непригодны для крашения ацетатных и полиэфирных волокон, т. к. ни один из стойких диазопрепаратов не способен диффундировать в глубь этих волокон. В то же время амины, применяемые в качестве диазосоставляющих, обладают такой способностью, Это используется в специальных полных красочных составах для крашения ацетатных и полиэфирных волокон, которые выпускаются под названием азоацеты.
Азоацеты представляют собой смеси тонкодиспер-гированных азоаминов с азотолами. Например, Азоацет алый — это смесь Азоамина алого К (2-амино-4-нитро-анизола) с Азотолом О А (272; R = C6H4OCH3-o).
При крашении ацетатных волокон азоацеты наносят на волокно из слабощелочной ванны при 75 °C, затем волокно обрабатывают подкисленным раствором NaNO2, при этом происходит диазотирование амина, после чего вновь создают слабощелочную среду, в которой происходит сочетание диазосоединения с азотолом (проявление окраски).
На полиэфирное волокно азоацеты наносят либо под давлением при 120-130 °C, либо при 90-95 °C в присутствии так называемых переносчиков (о- и «-гидрокси-дифенилы, салициловая кислота и др.), вызывающих набухание волокна и облегчающих диффузию азоацета. После этого обрабатывают волокно подкисленным раствором NaNO2 при 80-85 °C; образовавшееся диазосое
динение сразу сочетается с азотолом и проявляется окраска. Так, при проявлении Азоацета алого на лавсане образуется краситель алого цвета (306).
(306)
Меры предосторожности в производстве азокрасителей и азогенов
Производство азокрасителей и азогенов связано с использованием и получением ряда токсичных, горючих и взрывоопасных веществ.
К числу токсичных веществ относятся, прежде всего, ароматические амины (анилин, толуидин и др.), а также нитрит натрия и оксиды азота, образующиеся в процессе диазотирования. Некоторые аминосоединения, применяемые для синтеза азокрасителей, являются канцерогенными веществами: бензидин и его производные (толидин, дихлор- и дигидроксибензидины), аминоазобензол и др. Работа с этими веществами должна быть организована таким образом, чтобы контакт с ними был минимальным и соединения не накапливались в атмосфере помещений.
Диазосоединения в сухом состоянии чрезвычайно взрывчаты, причем причиной взрыва могут быть нагревание, удар, сотрясение воздуха, электрическая искра и т. д. Поэтому растворы, суспензии, пасты диазосоединений не должны попадать в такие места, где они могут потерять влагу (стенки и крышки аппаратов, пол и стены помещений, вентиляционные системы и др.).
Стойкие формы диазосоединений: диазоли, нитроз-амины, диазоаминосоединения, — менее взрывчаты, но при повышенной температуре вероятность взрыва не исключается. Поэтому хранение этих соединений и работа с ними должны проводиться в условиях, исключающих значительное нагревание соединений.
Азокрасители, не содержащие сульфогрупп, горючи, а смеси их пыли с воздухом взрывчаты. Особенно опасны в этом отношении нерастворимые азокрасители, содержащие нитрогруппы. При работе с ними, в частности при сушке, надо исключить возможность перегрева, искрения, пылеобразования.
732
Новый справочник химика и технолога
Особую опасность представляет процесс фосгени-рования, используемый при синтезе некоторых прямых азокрасителей, т. к. фосген очень ядовит. Отличаясь большой относительной плотностью (в 3,5 раза тяжелее воздуха), фосген способен накапливаться в низких местах помещений, причем вследствие относительной устойчивости может сохраняться в течение длительного времени. Особое внимание надо обратить на улавливание фосгена в отходящих газах.
4.3.5.2. Полиметиновые красители
Поли метановые красители
—►Дисперсные
(желтые)
—МСатионные
(от желтых до красно-фиолетовых)
—>-Оптические сенсибилизаторы
Из полиметиновых красителей наибольшее практическое значение имеют соединения, у которых ЭД- и ЭА-заместители или один из них, а также часть метиновых групп входят в состав гетероциклических систем: пиридина, хинолина, индола, бензотиазола и др. Часть метиновых групп цепи сопряжения может входить также в состав ароматических систем: бензола, нафталина и др.
Цвет полиметиновых красителей зависит главным образом от длины цепи сопряжения между ЭД- и ЭА-за-местителями. При увеличении цепи сопряжения на одно звено (-СН=СН-) максимум поглощения смещается в длинноволновую область спектра на 90-140 нм, что хорошо видно на примере красителей (307) — производных бензотиазола (табл. 4.3.4).
Таблица. 4.3.4
Зависимость цвета красителей от длины цепи сопряжения
п ^-макс* НМ Цвет
0 422 Желтый
1 558 Пурпурный
2 650 Голубой
3 762 Зеленый
4 890 Бесцветный (ИК-часть спектра)
5 990 Бесцветный (ИК-часть спектра)
Заметное влияние на цвет красителей оказывает также гетероатом, входящий в состав цикла. Как видно из табл. 4.3.5, разница в положении А.макс составляет от 10 до 120 нм в зависимости от природы группы X.
Таблица. 4.3.5
Зависимость цвета красителей от природы группы X
X Гетероцикл ^-макс- НМ
-О- Бензоксазол 486
>N(C2H5) N- Эти лбе нз и м ид азол 496
-S- Бензотиазол 558
-Se- Бензоселеназол 572
>С(СН3)2 3,3-Диметилиндоленин 548
-СН=СН- Хинолин 605
Большая часть полиметиновых красителей представляет собой соли довольно сильных оснований и является основными (катионными) красителями. Некоторые полиметиновые красители являются нейтральными соединениями, не растворимыми в воде, и могут применяться в качестве дисперсных красителей и пигментов.
Как правило, полиметиновые красители характеризуются узкой полосой поглощения и образуют яркие и чистые окраски. На природных волокнах — белковых (шерсть, натуральный шелк) и целлюлозных (танниро-ванный хлопок) — светостойкость окрасок обычно низка, поэтому для крашения таких материалов полиметиновые красители практически не применяются. Однако на синтетических волокнах (особенно полиакрилонитрильных) многие полиметиновые красители образуют окраски очень высокой светостойкости (7 по восьмибалльной шкале), вследствие чего широко применяются для крашения этих волокон. Важной областью применения полиметиновых красителей является производство кинофотоматериалов. Некоторые полиметиновые красители нашли применение в качестве активных сред лазеров (основных компонентов лазерных устройств, генерирующих лазерное излучение), а также в качестве модуляторов добротности лазеров (компонентов лазерных устройств, улучшающих важнейшие характеристики лазерного излучения). Применение красителей в качестве активных сред дает возможность создавать лазеры с перестраиваемой частотой излучения, а их использование в качестве модуляторов добротности позволяет получать гигантские импульсы излучения сверхкороткой длительности.
Симметричные полиметиновые красители
Полиметиновые красители, содержащие одинаковые гетероциклы по концам полиметиновой цепи, называются симметричными. Если в состав гетероциклов входят атомы азота, красители называют цианиновыми.
Ароматические соединения
733
Симметричные цианиновые красители, например (307), отличаются высокой выравненностью связей в сопряженной полиметиновой цепи и равномерным распределением (делокализацией) положительного заряда между атомами азота. Такие красители нашли применение в производстве кинофотоматериалов в качестве оптических сенсибилизаторов* («очувствите-лей»), т. е. соединений, повышающих чувствительность фотоэмульсий к световым лучам определенной части спектра.
Симметричные цианиновые красители с одной метановой группой (п = 0) называются монометинциани-нами. Их получают взаимодействием двух гетероциклических соединений одного класса, из которых одно содержит активную метильную группу, а второе — подвижный заместитель (атом галогена, -ОН и др.). Реакцию ведут в присутствии оснований. Так, при взаимодействии иодидов 2-метил-1 -этилхинолиния (308) и 2-иод-1-этилхинолиния (309) в спирте в присутствии щелочи образуется краситель Псевдоцианин (310), сенсибилизирующий фотоэмульсии к голубовато-зеленым лучам.
(308) (309)
* Бромид серебра, входящий в состав светочувствительных эмульсий фотографических пластинок и пленок., обладает ограниченной чувствительностью к действию света. Фотохимический процесс с его участием способен вызвать только фиолетовые и синие лучи (длина волны до 500 нм, энергия фотонов не ниже 240 кДж/моль). Остальные лучи (зеленые, желтые, оранжевые, красные) не действуют на бромид серебра, и эти цвета на пластинках и пленках выходят черными. Кроме того, вследствие значительного поглощения фиолетовых и синих лучей атмосферой обычные фотоматериалы невозможно использовать для фотосъемок с больших расстояний (например, для аэрофотосъемок). Введение в фотоэмульсию ничтожно малых количеств некоторых полиметиновых красителей (несколько мг на 1 м2 пленки или пластинки) делает кинофотоматериалы чувствительными к световым лучам длинноволновой части спектра, в том числе и к инфракрасным лучам. Применение подобных сенсибилизаторов делает возможным фотографирование на больших расстояниях (например, из космоса), в темноте, сквозь туман и облака.
Красители с тремя метиновыми группами называются триметинцианинами (карбоцианинами). Их получают конденсацией гетероциклических соединений, содержащих активную метильную или метиленовую группу, с муравьиной кислотой или ее производными, обычно С ЭТИЛОВЫМ эфиром OjPWO-форМЫ муравьиной кислоты. Так, при нагревании иодида 2-метил-1-этилхинолиния (308) с этилортоформиатом в уксусном ангидриде образуется краситель Пина-цианол (311), сенсибилизирующий фотоэмульсии к оранжевым и красным лучам (Хмакс сенсибилизации 635 нм).
(3/7)
Аналогичным образом из иодида 4-метил-1-этилхинолиния (313) получают краситель Криптоцианин (312), сенсибилизирующий фотоэмульсии к лучам ближней ИК-области спектра — до 800 нм (Хмакс сенсибилизации 750 нм). Криптоцианин оказался хорошим модулятором добротности для рубинового лазера.
Симметричные цианиновые красители с более длинной цепочкой метиновых групп называются полиме-тинцианинами (поликарбоцианинами). Их получают взаимодействием гетероциклических соединений, содержащих активные метильные или метиленовые группы, с полиметиновыми соединениями, содержащими активные заместители на концах цепи. Например, краситель Хеноцианин (315), относящийся к ряду гепта-метинцианинов (трикарбоцианинов), получают конденсацией иодида 4-метил-1-этилхинолиния (313) с дианилом глутаконового альдегида (314) в спиртовой щелочи. Хеноцианин также является сенсибилизатором фотоэмульсий к лучам ближней ИК-области спектра G-макс сенсибилизации 850 нм).
734
Новый справочник химика и технолога
Несимметричные полиметиновые красители
Полиметиновые красители с различными гетероциклами по концам полиметиновой цени называются несимметричными. Если только один из азотсодержащих заместителей входит в состав гетероцикла, красители называются гемицианиновыми. Если один из заместителей содержит азот, а другой — кислород, красители называются мероцианиновыми.
Из несимметричных полимстиновых красителей наибольшее практическое значение имеют красители, полученные путем реакции конденсации гетероциклических соединений, содержащих активную метильную или метиленовую группу, с ароматическими альдегидами, содержащими ЭД-заместитсли. Эти красители в основном используются для окраски синтетических волокон. Большинство из них являются производными индола {316). Для индола характерна повышенная электронная плотность в положении 3, вследствие чего он способен участвовать в реакциях в таутомерной форме индоленина (317), не существующей в свободном состоянии.
Именно в форме индоленина реагирует 2-метил-индол с алкилирующими агентами, например с метиловым эфиром бензолсульфокислоты, образуя соль 1,2,3,3-тетраметилиндолиния, которая при действии щелочи превращается в 1,3,3-триметил-2-метилиденин-долин (318) — ценный полупродукт для получения катионных красителей. Так, Катионный розовый 2С {1,3,3-тримстил-2-[4-^-метил-Л^-(2-хлорэтил)аминости-рил]индолиний хлорид (320)} получают конденсацией 1,3,3-триметил-2-метилидениндолина (318) с 4-[М-ме-тил-Л^-(2-хлорэтил)амино]бензальдегидом (319) в ледяной уксусной кислоте при 100 °C.
Замена хлорэтильной группы 4-этоксифенильной усиливает электронодонорные свойства ЭД-замести-теля, и цвет красителя углубляется до красно-фиолетового. При конденсации соединения (318) с 4-[М-ме-тил-Л/-(4-этоксифенил)амипо]бензальдегидом получают краситель Катионный красно-фиолетовый (321).
Практически значимые полиметиновые красители желтого цвета получают конденсацией альдегида Фишера [1,3,3-триметил-2-формилметилидениндолин (322)] с первичными ароматическими и гетероциклическими аминами. Так, при взаимодействии соединения (322) с 6-амино-2-метилбензтиазолом (323) получают гемициа-ниновый краситель для полиакрилонитрильного волокна — Катионный желтый 23 (324), а при взаимодействии с 4-анизидином — Катионный желтый 43 (325).
Ароматические соединения
735
Полиметиновые катионные красители применяются для крашения полиакрилонитрильного волокна и других волокон, модифицированных основными группами. Окраски, особенно на полиакрилонитрильном волокне, отличаются яркостью, чистотой тона и высокой светостойкостью (6-7 по восьмибалльной шкале). На природных волокнах — белковых (шерсть, натуральный шелк) и целлюлозных (таннированный хлопок) — светостойкость окрасок обычно низкая, поэтому для кра-
шения таких материалов полиметиновые красители
практически не применяются.
Если красители гемицианинового ряда являются нейтральными соединениями, они нерастворимы в воде и могут быть использованы в качестве пигментов или дисперсных красителей. К таким соединениям относятся мероцианиновые красители. Так, мероцианиновый краситель Дисперсный желтый 43 (326) образуется при конденсации 4-диэтиламинобензальдегида с циануксусным эфиром в спиртовой среде в присутствии пиперидина. Краситель применяют для крашения ацетатного и синтетических волокон. Окраски на ацетатном волокне отличаются высокой светостойкостью.
CN
N(C2H5)2 (H5C2)2N
(326)
К мероцианинам относятся хинофталоновые красители, которые получают конденсацией 2-метилхино-лина и его замещенных с ангидридами орто- и пери-дикарбоновых кислот. Представителем этого класса красителей является практически важный желтый дисперсный краситель (329), который получают при взаимодействии 4-бром-3-гидрокси-2-метилхинолина (327) с фталевым ангидридом (328) (сплавление при 200-220 °C в присутствии ZnCl2).
Дисперсный краситель (329) используется для крашения полиэфирных волокон, т. к. он относится к не-сублимирующимся красителям, т. е. не возгоняется при температуре крашения волокна (180-200 °C). Устойчивость к сублимации — это особое требование, предъявляемое к дисперсным красителям, предназначенным для крашения полиэфирных волокон. Чтобы повысить устойчивость к сублимации, в молекулы красителей вводят заместители, увеличивающие полярность молекул, например -CN, -NO2, -CF3, -C(O)NH2, атомы галогенов и другие.
Меры предосторожности в производстве полиметиновых красителей
Производство полиметиновых красителей связано с использованием ядовитых, сильнодействующих, горючих, взрывоопасных веществ. Из них особо следует отметить чрезвычайно ядовитый метанол, который по запаху трудно отличим от этанола; работа с метанолом регламентирована специальными правилами.
К числу сильнодействующих относятся едкие щелочи, попадание которых (в твердом виде или в виде концентрированных растворов) на кожу вызывает тяжелые ожоги. Очень тяжелые травмы вызывает попадание на кожу концентрированной уксусной кислоты и уксусного ангидрида; это связано с тем, что они вызывают не поверхностные ожоги, а активно всасываются белковыми веществами кожной и мышечной тканей, вследствие чего поражение может быть глубоким и трудно заживающим.
Раздражающим действием на слизистые оболочки обладают альдегиды, хлориды фосфора (в том числе вследствие образования газообразного НС1 при действии влаги воздуха).
Многие гетероциклические соединения (пиридин, хинолин и др.) и их производные, применяемые в производстве полиметиновых красителей, обладают биологической активностью и служат основой лекарственных средств. Среди них есть ядовитые вещества и соединения, оказывающие мутагенное действие. Поэтому одной из важнейших задач при организации производства полиметиновых красителей является защита работающих от действия вредных веществ.
4.3.5.3. Нитро- и нитрозокрасители
Нитрокрасители
—► Дисперсные (желтые)
—►Кислотные
Нитрозокрасители
(коричневые)
—► Кислотные
(зеленые)
Пигменты (зеленые)
736
Новый справочник химика и технолога
Hump окра сит ели
В зависимости от природы ЭД-заместителя, входящего в состав молекулы, нитрокрасители подразделяются на нитрофенолы (нитронафтолы) и ароматические нитроамины.
Нитрофенолы обладают свойствами кислотных красителей и ранее использовались для крашения шерсти, шелка, кожи, а нерастворимые производные некоторых нитрофенолов (лаки) находили применение в полиграфии. Достоинством нитрофенолов является красивый, чистый желтый цвет, недостатком — малая светостойкость окрасок. Нитрофенолы в настоящее время как красители не используются.
Из нитронафтолов практическое значение имеет только Нафтоловый желтый [8-гидрокси-5,6-динитро-нафталин-2-сульфокислота (35/)], который получают при взаимодействии 4-гидроксинафталин-1,3,6-трисульфокислоты (330) с разбавленной азотной кислотой, при этом сульфогруппа вытесняется нитрогруппой.
Нафтоловый желтый — кислотный краситель, однако вследствие низкой устойчивости окрасок в текстильной промышленности не применяется. Его используют для подкрашивания пищевых продуктов, а в виде бариевой соли — для окраски бумажной массы и при изготовлении цветных карандашей.
Нитроаминокрасители содержат в качестве ЭД-заместителя аминогруппу. Аминогруппа — более сильный ЭД-заместитель по сравнению с гидроксигруппой, поэтому эти красители имеют более глубокую окраску, чем нитрофенолы. Они окрашены в желтые, желтокоричневые и коричневые цвета.
Общим методом получения красителей группы ароматических нитроаминов является реакция активированного нуклеофильного замещения. Замещают, как правило, атом галогена, находящийся в сопряжении с ЭА-заместителем (в частности, с нитрогруппой), заместителями являются производные ароматических аминов. Реакцию обычно проводят в водной среде при 70-150 °C (при необходимости в автоклаве) в присутствии веществ, связывающих образующийся хлористый водород (мел, сода и т. д.); иногда в качестве катализатора применяют медь и ее соединения.
Красители группы нитроаминов более светостойки по сравнению с красителями группы нитрофенолов, но обладают менее чистыми оттенками. Красители, не содержащие сульфо- и карбоксильных групп, применяются в качестве дисперсных красителей для окрашивания ацетатного и полиамидных волокон по суспензионному
способу и для крашения пластических масс. Красители с сульфо- или карбоксильными группами являются кислотными красителями.
Краситель Дисперсный желтый прочный 2К [4-гид-рокси-2',4'-динитродифениламин (334)] получают взаимодействием 4-аминофснола (332) с 2,4-динитрохлор-бензолом (333) в водной среде в присутствии NaHSO3 (для предохранения и-аминофенола от окисления) и мела при 80 °C.
ОН
(332)
С1 (334)
(333)
Краситель Дисперсный желтый ПЭ (336) относится к числу специальных дисперсных красителей для полиэфирных волокон, т. к. хорошо сорбируется и распределяется в волокне, несмотря на малые размеры микропор и плотную молекулярную упаковку волокна. Краситель получают взаимодействием З-нитро-4-хлор-бензол-1 -сульфонилхлорида (335) с анилином.
Практически важный кислотный краситель Антра-лан желтый РРТ (337), полученный взаимодействием 2,4-динитрохлорбензола (333) с фенилпараминовой кислотой [5-амино-2-фениламинобензол-1 -сульфокислотой (55с?)], применяется для крашения шерсти, шелка, синтетических полиамидов и кожи.
Накопление ариламиногрупп в молекулах нитрокрасителей приводит к расширению полосы поглощения и переходу окраски от желтой к желто-коричневой. Так, при взаимодействии фенилпараминовой кислоты (338) с 3,3'-динитро-4,4'-дихлордифенилсульфоном (339) образуется краситель Кислотный коричневый 13 (340). Краситель окрашивает шерсть в ровный коричневый цвет, устойчивый к мокрым обработкам и валке.
Ароматические соединения
737
Нитрозокрасители
Из нитрозокрасителей в настоящее время практическое значение имеют нитрозопроизводныс 2-нафтола и его замещенных. Нитрозопроизводные 2-нафтола получают при действии водного раствора NaNO2 на раствор 2-нафтола в присутствии кислоты.
(341a) (3416)
1-Нитрозо-2-нафтол (341), как и другие нитрозофенолы и нитрозонафтолы, существует в двух таутомерных формах: нитрозо- (341a) и хиноноксимной (3416), причем преобладающей для данного соединения является хиноноксимная форма (результаты спектрального исследования растворов нитрозосоединений).
Так как 1-нитрозо-2-нафтол (341) не растворим в воде, его применяют в виде растворимого бисульфит-ного производного (342), которое получают действием бисульфита натрия на нитрозопроизводное.
Бисульфитное производное 1 -нитрозо-2-нафтола выпускалось под названием Протравной зеленый Бс [(342)] и использовалось для крашения и печатания хлопка; в первом случае ткань предварительно обрабатывали солями Fe2 , во втором — такие соли вводили в печатную краску. Образующееся на волокне внутри-комплексное соединение 1-нитрозо-2-нафтола с железом имеет красивый темно-зеленый цвет; окраски отличаются высокой светопрочностью. В настоящее время Протравной зеленый Бс практически утратил свое значение в качестве красителя и применяется как промежуточный продукт в производстве очень ценного Пигмента зеленого (343) — готового внутрикомплексного соединения 1-нитрозо-2-нафтола с железом. Пигмент зеленый легко образуется при действии водного раствора гидроксида натрия и соды на смесь растворов Протравного зеленого Бс и FeSO4.
Пигмент зеленый (343) не растворим в воде и большинстве органических растворителей, он обладает высокой светостойкостью и выдерживает температуры до 200 °C. Благодаря этим качествам Пигмент зеленый находит широкое применение в лакокрасочной и полиграфической промышленности, в производстве цветных карандашей, в крашении обоев, резины, пластических масс и др.
В классе нитрозокрасителей находится один из лучших зеленых красителей для шерсти и шелка — Кислотный зеленый 4Ж (344). Он представляет собой внутрикомплексное соединение 1-нитрозо-2-гидрокси-нафталин-6-сульфокислоты с солью железа. Краситель получают действием нитрита натрия на 6-гидрокси-
738
Новый справочник химика и технолога
нафталин-2-сульфокислоту (59) в кислой среде с последующей обработкой нитрозопроизводного сульфатом железа в присутствии извести и соды.
Кислотный зеленый 4Ж (344) применяют для крашения шерсти и шелка; окраски устойчивы к свету, мокрым обработкам, валке, заварке, трению. Водные растворы этого красителя чрезвычайно интенсивно поглощают световые лучи видимой и инфракрасной частей спектра. Даже при разведении 1 : 300 000 эти растворы поглощают около 90 % падающих на них лучей. Поэтому добавление ничтожных количеств красителя к морской воде заметно ускоряет ее испарение под действием солнечных лучей, что используется при извлечении из морской воды содержащихся в ней солей. Кислотный зеленый 4Ж применяют также для подкрашивания мыла, а в виде нерастворимой бариевой соли (лака) — в лакокрасочной и полиграфической промышленности, в производстве обоев и т. п.
При замене сульфогруппы в Кислотном зеленом 4Ж сульфонамидной группой получают краситель Кислотный зеленый Н5ЖМ (345). Исходным веществом для его синтеза служит 6-гидроксинафталин-2-сульфон-амид, легко образующий с солями двухвалентного железа внутрикомплексное соединение (345).
Анионные свойства Кислотного зеленого Н5ЖМ (345) обусловлены только отрицательным зарядом комплекса в целом в отличие от обычных кислотных красителей, анионные свойства которым придают кислотные группы (сульфо-, карбоксильные, иногда фенольные). При крашении белковых веществ таким комплексом в красильную ванну не надо вводить большие количества кислоты, как в случае обычных кислотных красителей. Кислотный зеленый Н5ЖМ способен окрашивать шерсть из слабокислой, почти нейтральной ванны, что дает возможность применять его для крашения полушерстяных тканей.
Устойчивые и яркие зеленые окраски при взаимодействии с солями железа (Fe2+) образует нитрозопро
изводное анилида З-гидрокси-2-нафтойной кислоты (Азотола А), выпускаемое под названием Нитрозол А (346). Железный комплекс Нитрозола А применяют для окрашивания белого портландцемента в яркий, устойчивый к действию света и воды зеленый цвет.
Меры предосторожности в производстве нитро- и нитрозокрасителей
Нитросоединения весьма токсичны, а полинитросоединения взрывоопасны. При работе с этими веществами необходимо исключить возможность попадания их на тело и одежду работающих и накопления в виде пыли на полах и стенах помещений.
В процессе нитрования и нитрозирования возможно выделение оксидов азота, поражающих дыхательные пути и вредно действующих на центральную нервную систему. Аппаратура, в которой осуществляются эти процессы, должна быть оборудована локальной вытяжной вентиляцией.
При нитрозировании применяется чрезвычайно ядовитый нитрит натрия, а нитрозосоединения оказывают раздражающее действие на кожу человека, поэтому, как и в случае нитросоединений, следует принимать меры, исключающие попадание их на тело и одежду работающих. Транспортировка, загрузка и выгрузка нитрозосоединений должны быть механизированы.
4.3.5.4. Арилметановые красители
-► Кислотные
(от красных до зеленых)
Арилметановые красители
—► Лаки
(от красных до зеленых)
Основные
(от желтых до зеленых)
► Пигменты
(розовые, фиолетовые)
Арилметановые красители можно рассматривать как производные метана, у которых центральный («метановый») атом углерода входит в единую сопряженную цепь хромофорной системы. При восстановлении арилметановых красителей ЭА-заместитель (347) превращается в ЭД-заместитель, образующиеся при этом бесцветные лейкосоединения (348) представляют собой продукты замещения атомов водорода в молекуле метана остатками Аг, Аг' и R. Если заместитель R — атом водорода или неароматический остаток, краситель
Ароматические соединения
739
является диарилметановым, если R — ароматический остаток, т. е. R = Аг", — триарилмстановым.
(377а)
(3776)
(37S)
Арилметановые красители являются солями органических катионов (379), положительный заряд которых делокализован (рассредоточен) по всей хромофорной системе.
Делокализация положительного заряда по всей хромофорной системе молекул арилметановых красителей приводит к тому, что при химических и, особенно, фотохимических (т. е. активированных световой энергией) реакциях деструкция молекул начинается именно с хромофорной системы. Поэтому устойчивость окрасок на целлюлозных (хлопок) и белковых (шерсть, шелк)
волокнах к свету, как правило, низка. Это привело к тому, что в настоящее время арил метановые красители для крашения природных волокон почти не применяются, несмотря на то, что в большинстве случаев они дают чистые и яркие окраски.
Однако на гидрофобных волокнах, в частности полиакрилонитрильных (например, нитроне), у которых проникновение влаги, являющейся средой или активным участникам фотохимического процесса, в глубь микропор затруднено, устойчивость окрасок арилметановыми красителями к свету выше. Поэтому некоторые из них находят применение в крашении полиакрилонитрильных волокон, главным образом в составе смесевых композиций для получения окрасок черного и некоторых других цветов, являющихся результатам смешения нескольких дополнительных, которые не могут быть образованы с помощью индивидуальных красителей.
Основными областями применения арилметановых красителей в настоящее время являются крашение бумаги, дерева, изготовление чернил, цветных карандашей, лаков для полиграфии. Используются они также в гистологической практике для окрашивания тканей и клеток организмов.
Некоторые бесцветные производные арилметановых красителей (например, лейкосоединения) нашли широкое применение в современной копировальной и множительной технике в качестве цветообразующих компонентов благодаря способности легко превращаться в красители при действии электрофильных реагентов.
Примечание. На лицевую сторону листа бумаги, используемой в множительной технике, наносят тонкий слой твердого электрофильного реагента (кислые неорганические соединения — каолин, сульфат алюминия, цеолит и т. п.), а на обратную сторону — столь же тонкий слой желатиновых или агар-агаровых микрокапсул с раствором бесцветного цветообразующего компонента в гидрофобном растворителе (например, в хлорзамещенном бифениле). Микрокапсулы образуются при отверждении тонкой эмульсии раствора компонента в водном желатиновом растворе. При надавливании на пачку бумаги микрокапсулы на обратной стороне вышележащих листов разрушаются, бесцветное производное вступает в контакт с кислым агентом на лицевой стороне нижележащих листов и превраща
ется в краситель; в результате на лицевой стороне бумаги в точках соприкосновения (буквы, рисунки) получаются цветные отпечатки.
Собственно арилметановые красители
Собственно арилметановые красители делятся на диарилметановые и триарилметановые.
Диарилметановые красители. Из диарилметановых красителей наиболее известным является Аурамин (73), отличающийся очень чистой и красивой желтой окраской. Аурамин можно получить при сплавлении кетона Михлера (350) с хлоридом аммония в присутствии безводного хлористого цинка.
Недостатком Аурамина является легкая гидроли-зуемость: при температуре ~ 70 °C под действием воды он превращается в кетон Михлера. Поэтому крашение Аурамином следует проводить при температуре не выше 50-60 °C. В настоящее время производство Аурамина значительно сократилось из-за его канцерогенности.
740
Новый справочник химика и технолога
О
(13)
Бесцветные производные лсйкоаурамина (351), содержащие алкильные, арильные или ацильные остатки при аминогруппе у центрального атома углерода, применяются в качестве цветообразующих компонентов для множительной техники. Их получают взаимодействием гидрола Михлера (4) с соответствующими аминами или амидами. При контакте этих бесцветных соединений с электрофильными реагентами (каолин) образуются цветные отпечатки. Так, если R = —SO2C6H5, об
разуются отпечатки синего цвета.
(H3C)2N
R — алкил, арил или ацил
Триарилметановые красители содержат три арильных кольца у центрального атома углерода. Эти красители находят большое применение. В зависимости от числа и вида ауксохромов их делят на диаминотриарилметановые, триаминотриарилметановые, дигидрокситриарилметановые, тригидрокситриарилметановые. Основными методами получения этих красителей являются бензальдегидный и бензгидрольный.
По бензальдегидному способу центральный («метановый») углеродный атом красителя образуется из карбонильной группы бензальдегида. Метод состоит в конденсации вторичных или третичных ароматических аминов или фенолов со свободным пара-положением по отношению к заместителю с бензальдегидом (или его замещенными) в присутствии кислых конденсирующих агентов (безводный ZnCl2, соляная и серная кислоты, безводная щавелевая кислота и др.). В результате реакции конденсации образуется бесцветное лейкосоединение красителя, которое переводят в краситель с помощью окислителей (РЬО2, МпО2, бихроматы).
Бензальдегидным способом получают большое количество практически важных красителей. Ниже приведена схема синтеза красителя Основного ярко-зеленого [4,4'-бис(А( М-диэтиламино)трифенилкарбоний хлорид (353)]: МЛ-диэтиланилин конденсируют с бензальдегидом в присутствии серной кислоты, лейкосоединение (352) окисляют в краситель с помощью РЬО2.
По бензгидрольному способу центральный («метановый») углеродный атом красителя вводится с помощью формальдегида через дифенилметановое, а затем бензгидрольное производное. Метод состоит в конденсации ароматических аминов или фенолов (со свободным пара-положением по отношению к заместителю) с формальдегидом в водной среде в присутствии небольшого количества серной или сульфаниловой кислоты. Образующееся дифенилметановое производное окисляют в симметрично замещенный бензгидрол, который конденсируют с ароматическими соединениями, обладающими достаточно подвижным атомом водорода.
Бензгидрольный способ получения красителей значительно сложнее и дороже бензальдегидного и применяется в том случае, если невозможно или достаточно трудно получить необходимый альдегид. Этим способом, в частности, получают краситель Основной бирюзовый [4,4'-бис(Аг,2У-диметиламино)-2"-метил-5"-нитро-трифенилкарбоний хлорид (357)].
7У,7У-диметиланилин взаимодействует с формальдегидом в присутствии небольшого количества сульфаниловой кислоты, образуя 4,4'-бис(МАЧдиметиламино)-дифенилметан (354), который окисляют в бензгидрол (355) с помощью МпО2 в кислой среде. Затем бензгид
Ароматические соединения
741
рол конденсируют с 4-нитротолуолом в присутствии серной кислоты. При этом образуется лейкосоединение (556), которое переводят в краситель (557), вторично
окисляя МпО2. Окисление лейкосоединения в краситель в данном случае не отличается от соответствующей стадии бензальдегидного способа.
(556) (557)
Основные красители. При отсутствии сульфо- и карбоксильных групп диамино- и триаминотриарилметановые красители диссоциируют в водных средах с образованием цветного катиона и, следовательно, относятся к числу основных красителей. Выпускают их в виде солей с минеральными или органическим кислотами (хлориды, сульфаты, оксалаты) или в виде двойных солей хлоридов с хлоридом цинка.
Типичными представителями основных диаминотриарилметановых красителей являются Малахитовый зеленый (14) и Основной ярко-зеленый (555). Оба красителя образуют яркие, но мало устойчивые к свету и стирке окраски. Применяются главным образом для крашения бумаги, дерева, изготовления лаков. Малахитовый зеленый в смеси с Фуксином новым (565) применяется для крашения полиакрилонитрильных волокон в черный цвет, причем светостойкость окраски смесью красителей значительно выше, чем при крашении каждым из них в отдельности.
Красители, компенсирующие анионы которых содержат достаточно длинные алкильные цепочки (например, анион дибутилфосфорной кислоты), растворимы в маслах и углеводородах и пригодны для окрашивания полиолефиновых волокон. Так, при нагревании основания Малахитового зеленого с дибутилфосфорной кислотой в водном растворе образуется дибутилфосфат красителя (358), окрашивающий полиолефины в глубокий зеленый цвет.
(358)
Краситель Основной ярко-зеленый обладает бактерицидными свойствами и в виде спиртового раствора под
названием «Бриллиантовый зеленый» применяется для обеззараживания ран (в этом случае компенсирующим анионом красителя вместо хлорида является оксалат).
Красители, имеющие заместители в оршо-ноложе-нии к центральному атому углерода, образуют более устойчивые окраски. К таким красителям относится Основной бирюзовый (557). Пространственные затруднения, создаваемые метильной группой, нарушают плоское строение молекулы настолько, что происходит значительное повышение цвета (по сравнению с Основным ярко-зеленым). По этой же причине при действии щелочей затрудняется атака центрального атома углерода гидроксид-анионом, приводящая к переходу красителя в бесцветное карбинольное соединение (т. е. увеличивается устойчивость окрасок к стирке).
Практически значимым является также краситель Основной голубой 3 [4,4'-бис(7У-этиламино)-2"-хлор-трифенилкарбоний хлорид (359)], который получают бензальдегидным способом из Л^-этил-о-толуидина и о-хлорбензальдегида (конденсацию проводят в серной кислоте). Здесь плоскостность молекулы нарушается атомом хлора, также находящимся в оршо-положении к центральному атому углерода.
Введение свободной или замещенной аминогруппы в третий ароматический остаток диаминотриарилметановых красителей в ия/дз-положение к центральному атому углерода приводит к значительному повышению
742
Новый справочник химика и технолога
цвета. Простейшими триаминотриарилметановыми красителями являются красные красители Парарозанилин [4,4',4"-триаминотрифенилкарбоний хлорид (360)] и его производные (361)-(363), содержащие метильные группы. Накопление метильных групп приводит к незначительному углублению оттенка.
(360) R = R - R’- Н; (362) R = R’= СН3, R"H;
(361) R = СН3, R - R"= Н; (363) R = R' R"= СН3
Все четыре красителя отличаются яркостью, но невысокой устойчивостью окрасок; используются главным образом для крашения бумаги, кожи, приготовления чернил.
Смесь Парарозанилина (360) с его моно- (361) и ди-метил- (362) замещенными выпускают под названием «Фуксин». Ее получают окислением смеси анилина, о-толуидина и и-толуидина, в качестве окислителя используют нитробензол или нитротолуол в присутствии FeCl3. Процесс образования красителя идет по схеме, аналогичной схеме бензальдегидного метода. Из о-толуидина и формальдегида по бензгидрольному способу получают Фуксин новый [4,4',4"-триамино-3,3',3"-три-метилтрифенилкарбоний хлорид (363)].
Алкилирование аминогрупп триаминотриарилметановых красителей углубляет цвет от красного до фиолетового. Краситель Основной фиолетовый К [4,4'-бис-(А,А-диэтиламино)-4"-А-этиламинотрифенилкарбоний хлорид (364)] получают окислением А,А-диметилани-лина кислородом воздуха в присутствии медного купороса. Процесс протекает по схеме бензгидрольного метода, т. к. первой стадией является окисление А,А-ди-метиланилина с образованием А-метиланилина и формальдегида.
(H3O2N
Фактически Основной фиолетовый К (364) представляет собой смесь красителей с разным числом
А-моно- и А,А-диметиламиногрупп, т. к. формальдегид может вступать в конденсацию не только с диметила-нилином, но и с монометиланилином. В зависимости от соотношения монометил- и диметиламиногрупп оттенки красителя могут изменяться от красноватого (больше молекул с А-монометиламиногруппами) до синеватого (больше молекул с А,А-диметиламино-группами).
Основной фиолетовый К не используется в текстильной промышленности из-за низкой светостойкости окрасок. Краситель широко применяется для изготовления полиграфических лаков, чернил, «химических» карандашей, штемпельной краски, копировальной бумаги, лент для пишущих машин и т. п.
Для получения триаминотриарилметановых красителей более глубокого цвета необходимо либо заменить часть бензольных ядер нафталиновыми, либо ввести в аминогруппы арильные остатки вместо алкильных. Так, краситель Основной синий К [бис(4-А,А-диметилами-нофенил)-4-А-этиламинонафтил-1-карбоний хлорид (365)] получают по видоизмененному бензгидрольному способу конденсацией кетона Михлера (350) с А-этил-нафталинамином-1 в присутствии РОС13 в толуольном растворе. Полученное в результате конденсации карбинольное основание превращают в краситель подкислением соляной кислотой.
Лаки основных красителей. При взаимодействии основных триарилметановых красителей с гетерополикислотами: фосфорномолибденовой Н7[Р(МО207)6], фосфорновольфрамовой H7[P(W2O7)6], кремнемолибденовой Hs[Si(Mo2O7)6] и другими — образуются нерастворимые соли — лаки. Часто для лакообразования используют смешанные гетерополикислоты, в частности фосфорновольфрамовомолибденовую кислоту H7[P(W2O7)4(Mo2O7)2], получаемую из фосфорновольфрамовой и фосфорномолибденовой кислот, взятых в отношении 4 : 2.
Для образования лаков растворы гетерополикислот приливают к нагретым до 100 °C растворам основных красителей. Катионы красителей замещают часть протонов в молекуле кислоты с образованием кислой соли— лака основного красителя. Так, из Основного ярко-зеленого получают Лак основной зеленый (366).
Лаки основных красителей иногда называют «фана-левыми», т. к. под этим наименованием они были впер-
Ароматические соединения
743
вне выпущены. Эти лаки обладают очень высокой светостойкостью, несмотря на то, что являются производными красителей, отличающихся крайне низкой устойчивостью к свету. Кроме того, в лаках сохраняется главное достоинство триарилметановых красителей —
чистота и яркость оттенков, поэтому фаналевые лаки нашли широкое применение в полиграфии (для цветной печати), а также для изготовления художественных красок и цветных карандашей, окраски бумаги и обоев, росписи по стеклу и т. д.
H3[P(MojO7)2(W2O7)4f-
(366)
Кислотные красители. Для получения практически интересных кислотных триарилметановых красителей в их молекулы необходимо ввести не менее двух кислотных групп. Одна из них своим отрицательным зарядом компенсирует положительный заряд катиона красителя, а другая придает красителю кислотный характер и вступает в солеобразование с аминогруппами белковых и или полиамидных волокон. Выпускают кислотные красители обычно в виде натриевых солей.
Прямым сульфированием красителей типа Основного ярко-зеленого (353) или их лейкосоединений удается ввести только одну сульфогруппу, которая вступает в незамещенное бензольное кольцо (367).
Для введения второй и более сульфогрупп молекула красителя должна содержать арильные кольца, не связанные непосредственно с центральным углеродным атомом. Так, сульфированием лейкосоединения, образующегося при конденсации А'-бензил-А'-этиланилина с бензальдегидом, и последующим окислением трисульфокислоты диоксидом свинца получают Кислотный зеленый для кожи (368).
Наличие в красителях с относительно небольшой молекулярной массой более двух сульфогрупп нежелательно, т. к. сообщаемая ими повышенная растворимость красителей уменьшает устойчивость окрасок на текстильных материалах к мокрым обработкам. Триарилметановые красители с тремя сульфогруппами используют для крашения кожи или в качестве промежуточных продуктов для синтеза других красителей.
Так, краситель Кислотный ярко-синий (369) получают путем нуклеофильного замещения сульфогруппы красителя (368) молекулой «-фенетидина (4-этокси-анилина). Из трех сульфогрупп красителя замещается та, которая находится в «ара-положении к центральному атому углерода и обладает повышенной подвижностью вследствие активирующего действия положительного заряда, имеющегося на углеродном атоме.
Краситель (369) окрашивает шерсть в красивый яркосиний цвет; окраски обладают не очень высокой светостойкостью, но проявляют высокую устойчивость к стирке (щелочам) и солевым растворам (морской воде).
Замена сульфогруппы на ариламиногруппу превращает диаминотриарилметановый краситель в триаминотриарилметановый и приводит к значительному повышению цвета вследствие появления более интенсивной конкурирующей хромофорной системы. Чтобы сохранить зеленый цвет красителя с двумя сульфогруппами, для синтеза красителей используют компоненты, в молекулах которых уже имеются сульфогруппы.
К таким красителям относится Кислотный зеленый (370), который получают из ,У-(л/-сульфобензил)-У-этил-
744
Новый справочник химика и технолога
анилина и бензальдегида (конденсирующий агент — серная кислота); лейкосоединение окисляют бихроматом или диоксидом свинца. Краситель применяют для крашения шерсти и шелка в яркий зеленый цвет.
чечной соломки) и в производстве фотоматериалов. Вступление сульфогруппы в л/е/тш-положение к центральному атому углерода на цвете красителя практически не сказывается.
Краситель с нафталиновым ядром — Кислотный зеленый Ж (371) — получают из /V,/V-диэтил анилина, формальдегида и нафталин-2,7-дисульфокислоты бензгидрольным методом. Этот краситель используется для крашения шерсти, шелка, кожи, в лакокрасочной промышленности (для спиртовых лаков). Оба красителя (370) и (371) образуют окраски, не отличающиеся высокой устойчивостью к свету и стирке.
Значительно устойчивее к действию щелочей (стирке) окраски, образуемые красителями с сульфогруппами в о/7Аио-положении к центральному атому углерода. Пространственные затруднения, создаваемые таким заместителем, нарушают плоскостность молекулы настолько, что при действии щелочей затрудняется атака центрального атома углерода гидроксид-анионом, приводящая к переходу красителя в бесцветное карбинольное основание (т. е. увеличивается устойчивость окрасок). По этой же причине происходит значительное повышение цвета (по сравнению с аналогичным красителем без заместителя), одновременно возрастают светостойкость, чистота оттенка и способность давать ровные окраски. К таким красителям относится, например, Кислотный ярко-голубой 3 (372), получаемый из ЛСД- диэтил анилина и 4-формилбензол-1,3-дисульфокислоты (конденсирующий агент — серная кислота); окисляют лейкосоединение бихроматом.
Кислотные красители можно получить прямым сульфированием триаминотриарилметановых красителей. Так, при сульфировании Парарозанилина (360) олеумом могут быть получены ди- и трисульфопроизводные, например краситель Кислотный фуксин (373), применяемый для крашения шерсти, кожи, дерева (спи-
Гидрокситриарилметановые красители. Из гидрокситриарилметановых красителей практическое значение имеют лишь такие, для синтеза которых используют о-гидроксикарбоновые кислоты со свободным пара-положением к гидроксигруппе: салициловую (374), о-крезотиновую [2-гидрокси-З-метилбензойная кислота (375)], 1-гидроксинафтойную-2 (376).
(376)
Наличие в молекулах таких красителей карбоксильных групп сообщает красителям хорошую растворимость и кислотность, достаточную для высокого сродства к белковым волокнам. Присутствие гидроксигрупп в орио-положении к карбоксильной группе обусловливает способность к образованию внутрикомплексных соединений с металлами, что дает возможность применять их по кислотно-протравному способу крашения. Получаемые при этом окраски обладают очень высокой устойчивостью к мокрым обработкам и повышенной светостойкостью. Так как крашение производится практически по хромовой протраве, эти красители получили название хромоксановых.
Ароматические соединения
745
Хромоксановые красители получают главным образом бензальдегидным способом с использованием в качестве конденсирующего агента серной кислоты. Для окисления лейкосоединения в краситель необходимо применять мягкие окислители из-за легкой окисляемо-сти гидроксипроизводных. Подходящим окислителем оказалась азотистая кислота, которая образуется при внесении NaNO2 в реакционную массу после конденсации. Поскольку при этом возможно нитрозирование гидроксисоединений, во избежание его удобнее использовать такие о-гидроксикарбоновые кислоты, у которых занято и второе ор/ио-положение к гидроксигруппе и которые, следовательно, не могут нитрозироваться. Именно поэтому для синтеза хромоксановых красителей собственно триарилметанового ряда применяют преимущественно о-крезотиновую кислоту (375). Такие красители получили название хромоксановых из группы о-крезотиновой кислоты.
Характерной особенностью хромоксановых красителей из группы о-крезотиновой кислоты является углубление окраски при взаимодействии с солями хрома (хромирование). Так, краситель Хромовый чистоголубой для шелка (377), получаемый конденсацией кислоты (375) с 2,6-дихлорбензальдегидом в серной кислоте при 15-20 °C с последующим окислением лейкосоединения нитритом натрия, окрашен в цвет бордо. Такую же окраску он сообщает белковым волокнам. После обработки окрашенного волокна солями хрома цвет углубляется до чисто-голубого, т. к. при комплексообразовании связь кислорода карбонильной группы с атомом хрома образуется за счет одной из неподелен-ных пар электронов атома кислорода, входящего в сопряженную систему, ответственную за поглощение данным красителем света в видимой части спектра. Одновременно с углублением цвета при хромировании происходит повышение устойчивости окрасок ко всем воздействиям.
(377)
Хромоксановые красители обладают хорошей ровняющей способностью и применяются для крашения натурального шелка, шерсти и кожи. Окраски достаточно устойчивы к свету, мокрым обработкам и валке.
Для получения хромоксановых красителей из группы о-крезотиновой кислоты более высокого цвета, чем голубой, необходимо ввести в молекулу второй ЭД-заместитель. Удобнее всего это осуществить заменой подвижного заместителя в иоро-положении к центральному атому углерода. Таким способом получают краси
тель Хромовый фиолетовый 2С для шелка (379), имеющий большое практическое применение.
Краситель (378) получают бензальдегидным способом, конденсируя о-крсзоти новую кислоту с бензальдегидом в среде серной кислоты с последующим сульфированием образовавшегося лейкосоединения до моносульфокислоты и окислением сульфокислоты лейкосоединения нитритом натрия. В красителе (378) сульфогруппа достаточно подвижна, ее вытесняют и-толилами-ногруппой, нагревая сульфопроизводное (378) с избытком и-толуидина.
Отдельные представители гидрокситриарилметановых красителей обладают противотуберкулезной активностью, в частности Руброкол (380), получаемый по бензальдегидному методу из гваякола (2-метоксифенола) и ванилина (4-гидрокси-3-метоксибензальдегида).
СН3 СН3
(379)
Фталеиновые красители. Гидрокситриарилметано-вые красители, содержащие в o/wo-положении к центральному атому углерода карбоксильную или сульфогруппу, называются фталеиновыми.
Фталеиновые красители получают конденсацией фенолов с фталевым ангидридом (328) или ангидридом о-сульфобензойной кислоты при нагревании в присут
746
Новый справочник химика и технолога
ствии водоотнимающих веществ (ZnCh или H2SO4). Таким способом получают, например, известный индикатор Фенолфталеин (38 Г). В ходе реакции сначала образуется бесцветный лактон Фенолфталеина — 4,4'-дигидроксифталофенон (357а), устойчивый в нейтральной и кислой средах. При действии щелочи лактонное кольцо раскрывается, образующийся при этом бесцветный карбинол неустойчив и мгновенно с потерей воды
превращается в желтую мононатриевую соль Фенолфталеина (3576), гидроксигруппа которой при pH = = 8,2-Н0 диссоциирует с образованием красной динат-риевой соли Фенолфталеина (35 7 в).
При pH > 10 образуется бесцветная тринатриевая соль карбинольного основания (352), поэтому титровать концентрированные щелочи в присутствии Фенолфталеина нельзя.
При замене фталевого ангидрида ангидридом 2-суль-фобензойной кислоты образуются сульфофталеины, также являющиеся ценными индикаторами. Аналогом Фенолфталеина является Феноловый красный (353), получаемый по такой же схеме, как и Фенолфталеин. Переход окрасок Фенолового красного [от бесцветной (353а) к красной (3536)] наблюдается в интервале pH = = 6,8^-8,4. Высокая чувствительность Фенолфталеина и других фталеиновых красителей к изменениям pH среды исключает возможность использования их для крашения текстильных и прочих материалов, но делает ценными индикаторами для алкали- и ацидиметрии.
Бесцветные 4,4'-диаминофталофеноны (лактоны диаминотриарилметановых красителей), например соединение (354), применяют в качестве цветообразующих компонентов для множительной техники, При контакте с кислыми средами они превращаются в красители и образуют цветные отпечатки, например, голубой краситель (355).
Молеотпугивающие средства. Некоторые бесцветные триарилметановые соединения, например, 2-[бис(2-гидрокси-3,5-дихлорфенил)метил]-5-хлорбензолсульфо-
Ароматические соединения
747
кислота (386), рекомендованы в качестве средств против моли. Соединения этого типа наносят на шерстяные или шелковые ткани по способу кислотного крашения.
(1:40 000 000), поэтому краситель используют для изучения водных течений.
Ксантеновые красители
Ксантеновые красители являются производными гетероциклического соединения ксантена [9//-ксантен (387)] (соответствуют диарилметановым красителям) и 9-фенилксантена (388) (соответствуют триарилметановым красителям).
(387)
(388)
Все представляющие практический интерес красители этой группы являются производными 9-фенилксантена, имеющими в ор/ио-положении к центральному атому углерода карбоксильную или сульфогруппу. Являясь, таким образом, гетероциклическими аналогами соответствующих фталеиновых красителей, ксантеновые красители в отличие от них не изменяют окраску под действием щелочей. Атом кислорода, входящий в состав гетероцикла, повышает цвет ксантеновых красителей по сравнению с собственно арилметановыми.
Ксантеновые красители делятся на дигидроксиксантеновые и диаминоксантеновые.
Дигидроксиксантеновые красители. Дигидроксиксантеновые красители получают из .и-дигидрокси-производных ароматического ряда. Простейший представитель красителей этого ряда — Флуоресцеин (389) — получают конденсацией фталевого ангидрида (328) с резорцином в присутствии водоотнимающих веществ, например безводного ZnCl2. Продуктом конденсации является дигидроксифлуоран (389a), представляющий собой бесцветную лактонную форму Флуоресцеина, которая в результате таутомерного превращения переходит в желтую хиноидную форму (3896).
Флуоресцеин не растворим в воде, но легко растворяется в щелочах. Щелочной раствор Флуоресцеина имеет желтовато-красный цвет с сильной зеленой флуоресценцией в отраженном свете. Флуоресценция заметна даже при значительном разбавлении водой
Динатриевая соль Флуоресцеина — Уранин (390) — применялась раньше для крашения шерсти и шелка в ярко-желтый цвет. В настоящее время Уранин применяют для окрашивания морских опознавательных знаков, которые видны на большом расстоянии благодаря исключительно яркой флуоресценции при дневном свете.
(391) X = Вг; (392) X = 1
Флуоресцеин имеет малое сродство к волокнам, поэтому устойчивость окрасок к мокрым обработкам невелика. Введение в молекулу атомов галогена повышает сродство красителей к волокну, при этом происходит углубление света и тем больше, чем больше масса галогена. Так, бромированием Флуоресцеина получают яркий розовый краситель Эозин [тетрабромфлуоресцеин (391)], иодированием — яркий красный краситель Эритрозин [тетраиодфлуоресцеин (392)]. Недостаточно высокая устойчивость этих красителей к действию света и мокрым обработкам не позволяет применять их в текстильной промышленности. Эти красители исполь
748
Новый справочник химика и технолога
зуются в производстве чернил, цветных карандашей, художественных красок (в виде лаков — солей с металлами), губной помады, румян, для крашения бумаги и пищевых продуктов, а также в качестве сенсибилизаторов в фотографии.
Применение вместо фталевого ангидрида ангидрида гидрокситримеллитовой кислоты (393) позволяет получать хромоксановые красители, сочетающие яркость ксантеновых красителей с высокой устойчивостью окрасок. Применяют хромоксановые красители в виде комплексов с металлами, в частности, с хромом; причем комплексообразование, резко повышая устойчивость окрасок к стирке и свету, не отражается на цвете, т. к. не изменяет электронную структуру атомов основной хромофорной системы. Так, Хромоксановый ярко-красный ГД (394) отличается от Эозина (391) только наличием о////?//-расположенных гидрокси- и карбоксильной групп, благодаря которым краситель и образует комплексы с металлами. Получают его конденсацией резорцина с ангидридом гидрокситримеллитовой кислоты в присутствии концентрированной серной кислоты и с последующим бромированием образовавшегося продукта конденсации.
Диаминоксантеновые красители. Диаминоксантеновые красители получают из л/-аминогидроксипроиз-водных ароматического ряда. По яркости окрасок они не уступают дигидроксиксантеновым красителям, но несколько превосходят их по устойчивости окрасок.
Красный краситель Родамин С (397) получают из л/-диэтиламинофенола и фталевого ангидрида. При нагревании веществ в присутствии небольшого количества серной кислоты образуется лактонная форма красителя — диаминофлуоран (395). При действии щелочи лактонное кольцо раскрывается и образуется карбинольное соединение (396), которое превращается в краситель при обработке хлороводородной кислотой.
Родамин С — основной краситель, он окрашивает шелк и шерсть в яркий синевато-красный цвет с сильной флуоресценцией; хлопок окрашивает по таннино-вой протраве (окраска не флуоресцирует). Применяется для крашения кожи, бумаги, мыла, подкрашивания спиртовых лаков. С фосфорновольфрамовомолибдено-вой кислотой образует светостойкий Лак основной красный.
Наличие карбоксильной группы снижает основность Родамина С и уменьшает его сродство к белковым веществам, а следовательно, и устойчивость окрасок к стирке. Для повышения основности необходимо блокировать карбоксильную группу, например, превратить ее в сложноэфирную.
Краситель Родамин Ж (399) получают взаимодействием 4-гидрокси-2-этиламинотолуола с фталевым ангидридом по схеме получения Родамина С. Полученное карбинольное производное (398) алкилируют этилхло-ридом в спиртовом растворе.
Родамин Ж имеет красивый чистый и яркий красный цвет. Он применяется для крашения шелка (флуоресцирующая окраска) и для приготовления очень ценного светостойкого Лака основного розового для полиграфии. Большое значение Родамин Ж приобрел в лазерной технике: он оказался лучшей активной средой для лазеров на красителях.
Диаминоксантеновые красители в бесцветной лактонной форме (диаминофлуораны) применяют в каче-
Ароматические соединения
749
стве цветообразующих компонентов для множительной техники. Возникновение окраски при контакте с кислой средой обусловлено теми же причинами, что и в случае лактонов арилметановых красителей [см. переход (384) (385)].
Для получения аминоксантеновых красителей более глубокого цвета, чем родамины, вместо алкиламиногрупп необходимо вводить ариламиногруппы. Удобнее всего это осуществлять через галогенпроизводные ксантена, при нагревании которых с ароматическими аминами и происходит замещение атомов галогена на ариламинопроизводные. Таким путем получают практически важный краситель Кислотный фиолетовый 2К (401)', для араминирования применяют о-толуидин, бесцветную лактонную форму подкислением переводят в основной краситель (400), который затем сульфируют.
Кислотный фиолетовый 2К (401) применяют для крашения шерсти и шелка. Устойчивость окрасок к свету выше, чем у родаминов. Нерастворимое в воде основание красителя (400) образует спиртовые растворы крас
ного цвета и под названием Спирторастворимый красный применяется для подкрашивания спиртовых лаков.
Применяя вместо фталевого ангидрида 4-формил-бензол-1,3-дисульфокислоту, получают аналогичные родаминам кислотные красители — сульфородамины, которые образуют на шерсти более устойчивые к стирке окраски, чем родамины. Например, краситель Сульфородамин С (402) получают конденсацией jw-диэтил-аминофенола с 4-формилбензол-1,3-дисульфокислотой в присутствии серной кислоты с последующим окислением лейкосоединения бихроматом. Сульфородамин С окрашивает шерсть в чисто-красный цвет.
Исключительно ценные аминоксантеновые красители получают при использовании ангидрида гидрокситри-меллитовой кислоты (393) вместо фталевого ангидрида. Образующиеся при этом хромоксановые красители вступают в комплексообразование с металлами без изменения цвета красителя. На шерсти и шелке эти красители образуют устойчивые окраски, сохраняющие красоту и яркость родаминов. Так, краситель Хромовый ярко-красный 4С (403), получаемый из ;и-диэтиламинофенола и ангидрида (393) по технологии, близкой к технологии получения Родамина С, является кислотным и дает окраски, близкие по оттенку к Родамину С. После хромирования на волокне устойчивость окрасок к мокрым обработкам возрастает до высшего балла (5 по пятибалльной шкале), а к свету — до хорошего (5 по восьмибалльной шкале), в то время как у родаминов светостойкость не превышает 2 балла (по восьмибалльной шкале).
(403)
Акридиновые красители
Акридиновые красители являются производными гетероциклического соединения акридина (404) (соответствуют диарилметановым красителям) и 9-фенилакридина (405) (соответствуют триарилметановым красителям).
750
Новый справочник химика и технолога
(404)
Атом азота гетероцикла повышает цвет акридиновых красителей по сравнению с собственно триарилметановыми красителями, причем в большей степени, чем кислород в случае ксантеновых красителей.
Акридиновые красители получают конденсацией ароматических „п-диаминов, имеющих хотя бы одну незамещенную аминогруппу, с альдегидами. В зависимости от природы альдегида образуются ди- или триарилметановые производные. При нагревании их с кислотами (обычно с серной кислотой) под давлением отщепляется молекула аммиака и происходит замыкание акридинового кольца. Полученное лейкосоединение окисляют в краситель.
Так, Основной желтый К (407) получают конденсацией л/-толуилендиамина с формальдегидом в присутствии серной кислоты с последующим окислением лей-кососдинения (406) кислородом воздуха в кислой среде.
Основной желтый К по оттенку близок к Аурамину, но в отличие от него устойчив к нагреванию с водой; светостойкость красителя невысока. Он находит ограниченное применение для крашения хлопка (по танни-новой протраве), шелка, а также кожи.
Некоторые акридиновые красители нашли применение в медицине, например Акрихин (408) применяется в качестве противомалярийного препарата, Риванол [лактат этакридина (409)] является антисептическим средством.
Линейные хинакридоны. Важной подгруппой акридиновых красителей являются линейные хинакридоны [производные транс-хинакридиндиона-7,14 (413)], которые применяют как пигменты.
Хинакридон можно получить, исходя из w-ксилола: и-ксилол вначале хлорируют в ядро в присутствии FeCl3 и получают 2,5-дихлор-и-ксилол (410), который окисляют кислородом воздуха. Образовавшуюся 2,5-ди-хлортерефталевую кислоту (4/1) взаимодействием с анилином превращают в 2,5-ди(фениламино)терефтале-вую кислоту (412), дегидратацией которой получают хинакридон (413).
С12 _
ЬеСЦ*"
С1
сн3 соон
(410) (411)
Линейный /и/?<7нс-хинакридон (413) не растворим в воде и применяется в качестве пигмента. Однако продукт, образовавшийся в результате синтеза, непригоден к непосредственному использованию. Это объясняется тем, что в процессе синтеза хинакридон образуется в красной кристаллической a-модификации, отличающейся тусклым оттенком, неустойчивостью к органическим растворителям и плохими красящими свойствами. Для того чтобы получить пигмент с нужными свойствами, необходимо изменить кристаллическую структуру его частиц, т. е. придать ему необходимую выпускную форму. Диспергированием a-модификации хинак-ридона в вибромельнице в присутствии хлорида натрия и ксилола или о-дихлорбензола получают кристалличе-
(409)
Ароматические соединения
751
скую P-модификацию, имеющую красновато-фиолетовый цвет, которую выпускают под названием Пигмент фиолетовый хинакридоновый. Диспергированием a-модификации в присутствии NaCl и диметилформами-да или в присутствии резината калия получают у-моди-фикацию, имеющую розовый цвет с синеватым оттенком, — Пигмент розовый хинакридоновый С. Оба пигмента применяют для окрашивания поливинилхлорида и других пластмасс, в полиграфической и лакокрасочной промышленности, в частности для изготовления автомобильных эмалей горячей сушки, а также для пигментной печати на тканях. Окраски отличаются очень высокой устойчивостью ко всем видам воздействия.
Меры предосторожности в производстве арилметановых красителей
Производство арилметановых красителей связано с использованием ядовитых, горючих и взрывоопасных веществ, что требует соответствующей организации работы. Особое внимание следует уделять работе с ароматическими аминами (анилин и др.), которые чрезвычайно ядовиты, энергично всасываются через кожу, поражают центральную нервную систему и кровь.
Некоторые арилметановые красители ядовиты и оказывают раздражающее действие на кожу, а в виде пыли — на слизистые оболочки; здесь более опасны основные красители, т. к. они хуже растворимы. Однако опасны и кислотные красители: они могут вызывать отиты и ларингиты, заболевания пищеварительного тракта, сердечно-сосудистой системы.
4.3.5.5. Ариламиновые красители
Ариламиновые красители
—► Катионные (бирюзовые)
—► Кислотные
(голубые, синие, черные)
—> Кубовые (желтые)
—► Основные
(красные, голубые, зеленые)
—► Пигменты
(фиолетовые, черные)
Прямые (голубые)
ЭД-Аг-1Ч=Аг'=ЭА + [Н] -> ЭД-Аг-МН-Аг'-ЭД'
(4.3.26)
Центральный атом азота в молекулах ариламиновых красителей и их лейкосоединений может быть связан с третьим ароматическим кольцом; в этом случае красители являются триариламиновыми.
Ариламиновые красители делятся на следующие группы: собственно ариламиновые (хинониминовые), оксазиновые, тиазиновые и диазиновые.
Собственно ариламиновые (хинониминовые) красители
По своему строению хинониминовые красители аналогичны диарилметановым красителям, но отличаются от них тем, что место центрального атома углерода занимает более электроотрицательный атом азота. Поскольку хинониминовые красители представляют собой нечетные альтернантные системы, их цвет значительно глубже цвета соответствующих арилметановых красителей. Это видно из сравнения диарилметанового красителя гидрола Михлера [(7); = 603,5 нм] и ана-
логичного хинониминового красителя Зеленого Бинд-шедлера [(5); Хмакс = 726 нм].
Хинониминовые красители можно рассматривать как производные хинонмоноимина (415) или хинонди-имина (417), полученные замещением атомов водорода иминогруппы ароматическим остатком с ЭД-замести-телем. В зависимости от характера этого заместителя из соединений (415) и (417) могут быть получены индофенолы (414), индоанилины (416) и индамины (418).
В названиях этих соединений имеется частица «инд» — от названия синего красителя Индиго, который по цвету напоминает многие хинониминовые красители.
—► Сернистые
(от бордо до черных)
—► Тиозоли
(от бордо до черных)
Ариламиновые красители можно рассматривать как производные диариламина, у которых центральный атом азота входит в единую цепь сопряжения. При восстановлении ариламиновых красителей (уравнение (4.3.26)) образуются бесцветные лейкосоединения (ЭА-заместитель превращается в ЭД).
752
Новый справочник химика и технолога
Практическое значение имеют два способа получения хинониминовых красителей: окислительный и нит-розный.
Окислительный способ заключается в окислении смеси арилендиамина или аминофенола с ариламином или фенолом. В зависимости от комбинации указанных компонентов образуются индофенол [(777); аминофенол + фенол], индоанилин [(776); аминофенол + амин или диамин + фенол] или индамин [(775); диамин + + амин]. В качестве окислителей обычно применяют бихроматы калия или натрия в среде минеральной кислоты или гипохлорит в щелочной среде.
Так, при окислении смеси Д-амино-А^АЧдиметилани-лина и А^-диметиланилина бихроматом в кислой среде при 15-20 °C образуется индамин — основной краситель Зеленый Биндшедлера (5).
N(CH3)2
Нитрозный способ заключается во взаимодействии С-нитрозодиалкилариламина или нитрозофенола с ариламином или фенолом. В зависимости от комбинации указанных компонентов образуются индофенол [(777); нитрозофенол + фенол], индоанилин [(776); нитрозоамин + фенол или нитрозофенол + амин] или индамин [(775); нитрозоамин + амин]. Поскольку взаимодействие нитрозосоединений, реагирующих в таутомерной хиноноксимной форме, с аминами и фенолами происходит с выделением воды, его часто осуществляют в присутствии водоотнимающих средств, например концентрированной H2SO4, которая одновременно служит и растворителем. Реакцию проводят при 0-5 °C. Нитрозосоединения применяются свежеприготовленными.
Нитрозофенолы получают нитрозированием фенолов действием серной или соляной кислоты на смесь раствора феноксида и нитрита натрия при охлаждении. С-нитрозодиалкилариламины получают нитрозированием МА^-диалкилариламинов действием водного раствора нитрита натрия на раствор соли амина в присутствии избытка минеральной кислоты при охлаждении.
Так, индоанилин — основный краситель а-Нафто-ловый синий (420) — получают нитрозированием ди-метиланилина действием водного раствора NaNO2 на раствор гидрохлорида амина в присутствии соляной кислоты с последующим взаимодействием полученной соли 4-нитрозодиметиланилина (779а), реагирующей в таутомерной хиноноксимной форме (7796) с 1-гидроксинафталином при 0-5 °C.
(729)
Хинониминовые красители имеют глубокие цвета: от красновато-синего до зеленого. Они довольно светостойки, но чувствительны к действию химических реагентов. При действии восстановителей они восстанавливаются до бесцветных лейкосоединений — производных диариламина, окислителями окисляются до хинонов. При действии разбавленных кислот хинониминовые красители гидролизуются по двойной связи между центральным атомом азота и хиноидным ядром, образуя хинон или хинонимин и диамин или аминофенол.
Из-за неустойчивости к действию химических реагентов использование индофенолов, индоанилинов и инда
минов в качестве красителей стало нецелесообразным. Некоторые из них нашли применение в аналитической химии в качестве окислительно-восстановительных индикаторов и в цветной фотографии, где с их помощью воспроизводятся синие (голубые) тона.
В настоящее время хинониминовые красители применяются главным образом в качестве промежуточных продуктов при синтезе диазиновых, оксазиновых и тиазиновых красителей. При этом используется характерное свойство хинониминовых красителей как соединений с хиноидными ядрами — способность легко присоединять различные реагенты с превращением хиноидных ядер в ароматические.
Ароматические соединения
753
Оксазиновые красители
Оксазиновые красители являются производными гетероциклического соединения — феноксазина {421}. Их разделяют на монооксазиновые и диоксазиновые красители.
{421}
Монооксазиновые красители. Это красители с одним оксазиновым кольцом. Их получают из хинониминовых красителей, содержащих гидроксигруппу в ор-wo-положении к центральному атому азота (происходит внутримолекулярное присоединение гидроксигруппы с замыканием оксазинового цикла). Практически синтез исходного хинониминового красителя, замыкание гетероцикла и окисление образующегося при этом лейкосоединения осуществляют в одну технологическую операцию без выделения продуктов отдельных стадий.
В настоящее время монооксазиновые красители не применяются для крашения текстильных материалов из природных волокон вследствие недостаточной устойчивости окрасок к свету и стирке. Однако некоторые из них применяют для крашения синтетических волокон, в частности полиакрилонитрильных, на которых они образуют достаточно устойчивые окраски.
NH(C2H5)2C1~
{423}
tN(C2H5)2CT
{422}
(H5C2)2N
~C1(H5C2)2N
{424}
Наибольшее практическое значение из монооксазиновых красителей имеет Катионный бирюзовый 23 {424}. Краситель получают следующим способом: избыток гидрохлорида 4-нитрозо-Л'',Л'-диэтиланилина на
гревают в спирте с 3-(?/,ЛЧдиэтиламино)фенолом, при этом образуется индамин {422}, превращающийся в результате внутримолекулярного присоединения гидроксигруппы в лейкосоединение красителя {423}, которое окисляется избытком нитрозосоединения или специально вводимым окислителем.
Катионный бирюзовый 23 {424} окрашивает полиакрилонитрильное волокно в красивый бирюзовый цвет, окраски обладают хорошей устойчивостью к свету и мокрым обработкам. Раствор перхлората Катионного бирюзового 23 (анион С1О4 вместо СГ ) в метиловом спирте используется в качестве активного компонента жидкостного лазера с излучения 715 нм.
В жидкостных лазерных системах (растворитель — метанол) используются также дигидроксифеназиновый краситель {425}, получаемый из 4-нитрозофенола и резорцина по схеме, аналогичной схеме получения Катионного бирюзового 23, и /V-оксид этого красителя {426}', красители генерируют излучения с Лмакс = 608 и 656 нм соответственно.
Диоксазиновые красители. Красители с двумя оксазиновыми кольцами — производные трифенодиоксазина {427} имеют большое практическое значение.
{427}
Плоское строение значительных по размеру молекул и наличие четырех гетероатомов, способных участвовать в образовании водородных связей, сообщают диоксазиновым красителям большое сродство к целлюлозе, вследствие чего они могут окрашивать целлюлозные волокна без протрав, т. е. являются прямыми красителями. Цвета диоксазиновых красителей — глубокие (фиолетовые, синие, голубые); окраски отличаются высокой яркостью и светостойкостью.
Диоксазиновые красители получают взаимодействием первичных аминов ароматического и гетероциклического рядов, у которых свободно о/?то-положение по отношению к аминогруппе, с 2,3,5,6-тетрахлор-бензохиноном (хлоранилом) в присутствии оснований (оксид магния, ацетат натрия, пиридин) для связывания выделяющегося НС1 при температурах до 80 °C с последующим замыканием оксазиновых колец. При отсутствии в исходных веществах сульфогрупп образовавшиеся замещенные грифенодиоксазина сульфируют для придания им растворимости. Замыкание оксазиновых колец осуществляют взаимодействием с водоотни-
754
Новый справочник химика и технолога
мающими средствами или с помощью окислителей, например нагреванием с арилсульфонилхлоридами в высо-кокипящих растворителях при 180-260 °C, с безводными хлоридами металлов, нитробензолом или концентрированной H2SO4 при 95-100 °C, с олеумом при 50-55 °C.
Так, Прямой ярко-голубой светопрочный {431) получают взаимодействием 5-амино-2-фениламинобензол-
сульфокислоты (428) с хлоранилом [2,3,5,6-тетрахлор-циклогексадиен-2,5-дион-1,4 (429)] в водной среде в присутствии MgO с последующим окислением образовавшегося сульфопроизводного ди(ариламино)дихлор-бензохинона (430) 20%-м олеумом. Полученный сульфат красителя гидролизуют нагреванием с разбавленной серной кислотой.
Краситель Прямой ярко-голубой светопрочный (431) применяется для крашения хлопка, вискозного волокна и натурального шелка. Окраски отличаются высокой устойчивостью к действию света и к мокрым обработкам.
Нерастворимые в воде диоксазиновые красители используются в качестве пигментов. Пигменты на основе трифенодиоксазина имеют большое практическое значение. Например, из З-амино-А’-этил карбазол а и хлоранила получают очень ценный пигмент — Пигмент фиолетовый диоксазиновый (432). Он обладает высокой красящей способностью и применяется в полиграфии для цветной печати, в лакокрасочной промышленности, для крашения пластмасс и химических волокон в массе.
Тиазиновые красители
Тиазиновые красители являются производными гетероциклического соединения — фенотиазина (433).
Н
Эти красители имеют глубокие цвета: от фиолетового до зеленого. Окраски отличаются чистотой и яркостью оттенков, но не очень устойчивы к свету. Практическое применение находят основные тиазиновые красители, окрашивающие шерсть и шелк непосредственно, а хлопок — по танниновой протраве. Шелк также можно красить по танниновой протраве, и в этом случае светостойкость окрасок значительно повышается.
Тиазиновые красители получают из соответствующих хинониминовых, у которых в opwo-положении к центральному атому азота находится заместитель, содержащий серу и участвующий в замыкании тиазинового цикла. Таким заместителем обычно является остаток тиосерной кислоты -SSO3H, от которого в момент циклизации отщепляется группа -SO3H.
Остаток тиосерной кислоты вводят в молекулу действием тиосульфата натрия Na2S2O3 в кислой среде на соль и-хинондиимина при температуре около 0 °C. Получение и-хинондиимина окислением соответствующего диамина, взаимодействие с тиосульфатом и окисление тиосульфокислоты диамина совместно с амином для получения хинониминового красителя обычно осуществляют в ходе одной операции технологического процесса. Последняя стадия проходит при температуре около 20 °C. Замыкание тиазинового цикла требует повышения температуры до 90-100 °C. Нагревание до этой температуры необходимо проводить с максимальной скоростью, чтобы быстрее миновать температурный интервал 50-80 °C, в котором циклизация протекает медленнее гидролитического расщепления хинониминового красителя. Быстрый нагрев удобнее всего осуществлять действием острого пара. Замыкание тиазинового кольца легче идет в присутствии соли меди. Выпускают тиазино-
(433)
Ароматические соединения
755
вне красители в виде растворимых в воде хлоридов или в виде двойных солей с хлористым цинком.
По такой схеме получают важнейший представитель тиазиновых красителей — Метиленовый голубой (439). Исходным соединением является 4-амино-^Л^-диме-тиланилин, который готовят нитрозированием N,N-jpa-метиланилина с последующим восстановлением нитрозосоединения. При добавлении бихромата и тиосульфата натрия к раствору сульфата 4-амино-А^,А^-диметил-анилина (434) соединение окисляется в хинондиимин (435), который, присоединяя -SSO3H, превращается в 2-амино-5-диметиламинофенилтиосульфат (436). При добавлении новых порций МД-диметиланилина и Na2Cr2O7 происходит совместное окисление смеси аминов и образуется хинониминовый краситель (437) — производное Зеленого Биндшедлера. При быстром нагревании реакционной массы до кипения замыкается тиазиновый цикл и образовавшееся лейкосоединение (438) окисляется в краситель (439), который осаждают соляной кислотой.
Метиленовый голубой (439) окрашивает хлопок (по танниновой протраве) и шелк в очень чистый голубой цвет, светостойкость окрасок невысока.
Метиленовый голубой Ц (440) является двойной солью красителя (439) с хлористым цинком; его получают добавлением ZnCl2 при осаждении красителя из раствора соляной кислотой. Этот краситель применяется для изготовления цветных карандашей, окраски бумаги, в полиграфической и лакокрасочной промышленности, а также в качестве реактива в аналитической химии, в гистологии и в качестве лекарственного вещества — ([Кр]2 ZnCI42") (440).
Подобно оксазиновым красителям некоторые тиазиновые красители используются в лазерной технике.
Селеновый аналог Метиленового голубого — хлорид 3,7-бис(диметиламино)феноселеназиния с радиоактивным изотопом 75Se в молекуле предложен в качестве лекарственного препарата, воздействующего на эпителиальные клетки некоторых опухолей (аденомы).
Сернистые тиазиновые красители. Введение в хинониминовые красители серы (осернение) с помощью тиосульфата натрия, применяемое при синтезе основных тиазиновых красителей, — не единственный способ получения красителей с тиазиновым кольцом. Гораздо большее практическое значение имеет способ, основанный на осернении с помощью полисульфидов натрия (от Na2S2 до Ма2Б6).
Процесс осуществляется взаимодействием хинониминовых красителей с полисульфидом натрия в водном (иногда спиртовом) растворе при 100-120 °C и носит название мокрого сернистого плава, или сернистой «варки». В реакциях с хинониминовым красителем и продуктами его превращения во время сернистой «варки» могут участвовать как продукты распада полисульфида натрия (Na2S, Ma2S2, активная сера), так и H2S и Na2S2O3, образующиеся при взаимодействии серы и Na2S2 с водой
и реагирующими веществами. В зависимости от этого могуг протекать различные реакции: восстановление и окисление, осернение, циклизация с образованием тиазиновых колец и тиантреновых систем.
Направление процесса определяется температурой и продолжительностью реакции, составом полисульфида, характером заместителей в осерняемом соединении, наличием примесей и др.
Продукты сернистой варки представляют собой нерастворимые в воде вещества с относительно высокой молекулярной массой, т. к. при окислении происходит соединение отдельных молекул в результате образования дисульфидных мостиков. Такие продукты получили название сернистых красителей.
2RSH '°' > R— S— S— R
—ri2vJ
756
Новый справочник химика и технолога
Чтобы осуществить крашение, необходимо перевести нерастворимый краситель (441) в растворимое состояние (443). С этой целью его восстанавливают действием Na2S в щелочной среде, при этом дисульфидные связи разрываются и образуются соединения с меньшей молекулярной массой (442), а возникающие -SH-ipyn-пы ионизируются. После крашения лейкосоединение действием воздуха (О2 + СО2) превращается на волокне в краситель.
R-S-S-R 2R-SH 2R—S“Na+
(441) (442) (443)
Процесс крашения сернистыми красителями аналогичен процессу крашения кубовыми красителями. В отличие от последних сернистые красители восстанавливаются легче — действием сульфида натрия, который восстанавливает лишь некоторые кубовые красители (тиоиндигоидные).
При окислении лейкосоединений сернистых красителей (на волокне после крашения или при выделении красителя продувкой воздуха через раствор лейкосоеди-
нения) могут происходить процессы окисления, в которых участвуют атомы серы. В результате этого в молекулах сернистых красителей Moiyr присутствовать сульфоксидные —S(O)— и дисульфоксидные -S(O)-S(O)-группы. При восстановлении сернистых красителей эти группы переходят в исходные (сульфидные и дисульфидные соответственно).
Сернистый синий К (447) является продуктом осернения индоанилина (444), который получают нитроз-ным способом взаимодействием о-толуидина с и-нитро-зофенолом. Осернение проводят «варкой» с полисульфидом натрия состава Na2S48 (смесь Na2S4 и Na2S5) в течение 20-24 ч. Температуру при варке постепенно поднимают до 105-110 °C периодическим упариванием реакционной массы. В ходе осернения образуется фс-нотиазон (445) и лейкосоединение красителя (446). Краситель (461) выделяют продуванием воздуха через разбавленную реакционную массу.
В процессе окисления отдельные остатки лейкосое-динения связываются друг с другом дисульфоксидны-ми группами —SO—SO— в крупные молекулы нерастворимого красителя.
SH SH
121^
(446)
(447)
Химизм процесса осернения и строение красителя (447), как и других сернистых красителей, не доказаны. Возможно, феназиновые остатки связаны не сульфоксидными группами, а атомами серы, т. е. в процессе осернения образуется тиантреновая система. В этом случае Сернистый синий К будет иметь строение (448), а его лейкосоединение — (449).
Сернистый синий К производится в большом количестве и применяется для крашения хлопка. Окраски достаточно устойчивы к свету и стирке, но не устойчивы к хлору.
Если осернению подвергают индоанилины, содержащие не свободную аминогруппу, как в случае Серни
стого синего К, а диалкиламино- или ариламиногруппу, то образуются красители более глубокого цвета. Например, краситель Сернистый чисто-голубой К (450; одна из возможных структур) получают осернением индоанилина из Д-амино-А^/У-диметиланилина и фенола «варкой» с полисульфидом натрия состава Na2S3 в течение 24 ч при 110-115 °C.
Осернение индоанилинов, содержащих нафталиновое ядро, которое связано в a-положении с центральным атомом азота [например, из 5-амино- и 8-амино-нафталин-2-сульфокислот (кислот Клеве) и 4-амино-фенола] приводит к образованию красителей еще более глубокого цвета — зеленовато-голубых. Для получения
Ароматические соединения
757
зеленых сернистых красителей осернение проводят в присутствии солей меди. В результате комплексообразования красителя с медью, в котором участвуют своими неподеленными парами электронов атомы кислорода карбонильной группы, входящей в хромофорную систему красителя, цвет углубляется от синего или голубого до сине-зеленого или зеленого.
(448)
SH
SH
(449)
(HjC)2N (450)
п
Сернистый ярко-зеленый Ж (452) получают «варкой» индоанилина (451), приготовленного из фенилперикислоты и 4-аминофенола окислительным спосо
бом (окислитель NaClO), с полисульфидом натрия состава Na2S4<26 в присутствии CuSO4 в течение 50 ч при 102-103 °C. Молекулы этого красителя содержат сульфогруппы, однако количество их недостаточно для сообщения красителю растворимости. Сернистый ярко-зеленый Ж окрашивает хлопок и вискозное волокно из раствора лейкосоединения в водном растворе Na2S. Окраски достаточно устойчивы к стирке, но обладают малой устойчивостью к свету и мокрому трению.
При осернении индоанилинов, содержащих нафталиновое ядро, которое связано с центральным атомом азота в p-положении, образуются черные красители.
Исходный индоанилин (453) для Сернистого черного С (454) получают в виде лейкосоединения взаимодействием р-нафтола и 4-аминофенола с водным раствором NaHSO3. Осернение проводят «варкой» с полисульфидом натрия состава Na2S5 в течение 30 ч в кипящем бутиловом спирте в присутствии небольших количеств 4,4'-дигидроксидифениламина и фенола.
Сернистый черный С образует окраски, обладающие очень высокой устойчивостью к свету, стирке и хлору. Ценным качеством этого красителя, отличающим его от многих сернистых красителей, является то, что он не способствует разрушению окрашенного им волокна.
758
Новый справочник химика и технолога
{454}
или
либо путем присоединения первичного амина к хиноидному ядру хинониминового красителя. В первом случае в качестве одного из компонентов для синтеза исходного хинониминового красителя берут ароматический диамин, имеющий по крайней мере одну незамещенную аминогруппу.
Например, для синтеза Толуиленового красного {459} исходный индамин [хинониминовый краситель Толуиленовый голубой {457}] получают из N,N-an-метиланилина и л/-толуилендиамина нитрозным способом, добавляя Д-нитрозо-А^АЧдиметиланилин к раствору л/-толуилендиамина в соляной кислоте в присутствии небольшого количества FeCl2. Образующийся индамин {457} сразу же циклизуется, причем полученное при этом лейкосоединение азинового красителя {458} тут же окисляется в краситель {459} избыточным нитрозосоединением.
{457}
Диазиновые красители
Диазиновые красители являются производными гетероциклических соединений — феназина {455} (соответствуют диарилметановым красителям) и TV-фенил-феназония {456} (соответствуют триарилметановым красителям). Эти красители имеют наибольшее практическое значение среди всех ариламиновых красителей.
(CH3)2NC6H4NO^
{459}
{456}
Основные диазиновые красители. Диазиновые красители, не содержащие сульфо- и карбоксильных групп являются основными. Их получают из соответствующих хинониминовых красителей, которые содержат в о/>/ио-положении к центральному атому азота первичную или вторичную аминогруппу, участвующую далее в замыкании диазинового цикла в результате внутримолекулярного присоединения. Циклизация осуществляется легко, обычно сразу же после образования о-аминохинониминового красителя.
Необходимая для образования гетероцикла первичная или вторичная аминогруппа вводится в молекулу хинониминового красителя либо в составе одного из исходных компонентов при синтезе этого красителя,
Толуиленовый красный применялся раньше для крашения хлопка по танниновой протраве в красный цвет. В настоящее время не применяется в качестве красителя, т. к. очень чувствителен к щелочам. Следует отметить, что все диазиновые красители, соответствующие диариламиновым красителям (типа Толуиленового красного), чувствительны к щелочам и не применяются в качестве красителей. Их используют для получения сернистых красителей красного цвета.
Диазиновые красители, соответствующие триариламиновым, устойчивы к действию щелочей и применяются в качестве красителей. Представителем этого класса соединений является Сафранин — краситель ярко-красного цвета. Получают Сафранин совместным окислением w-толуилендиамина, о-толуидина и анилина бихроматом в среде соляной кислоты. При окислении смеси аминов в реакцию с w-толуилендиамином может вступать любой из двух оставшихся аминов, при этом образуются различные по строению индамины. Поэтому наряду с красителем {460}, являющимся
Ароматические соединения
759
основным продуктом, образуются его изомеры и гомологи (461)-{463), различающиеся числом и расположением метильных групп. Все они очень близки по цвету и по свойствам; смесь без разделения выпускается под названием Сафранин.
(460) R = СН3, R' = Н; (461) R = R' = Н;
(462) R = Н, R* = СН3; (463) R = R’ = СН3
Сафранин окрашивает шерсть и шелк непосредственно, а хлопок — по танниновой протраве в ярко-красный цвет (несколько желтее Фуксина). Окраски красивы, но неустойчивы к свету, поэтому Сафранин применяется в настоящее время только для крашения бумаги и кожи.
Диазиновые красители типа Сафранина, соответствующие триариламиновым, используют для получения
сернистых красителей фиолетового цвета.
Алкилирование аминогрупп в молекуле Сафранина (и других солей диаминофенилфеназония) углубляет цвет до фиолетового; образующиеся красители не имеют практического значения. Арилирование аминогрупп углубляет цвет до синего.
Кислотные красители. Для того чтобы диазиновые красители обладали свойствами кислотных красителей, в их молекулах должно присутствовать не менее двух кислотных групп: одна из них своим зарядом компенсирует положительный заряд катиона феназония, а вторая сообщает красителю растворимость и кислотные свойства.
Практически ценным красителем является Кислотный темно-голубой (468). Его получают из индамина (466), содержащего в opwo-положении к центральному атому азота ариламиногруппу. Индамин (466) образуется при окислении 6,8-бис(фениламино)нафталин-1-сульфокислоты (464) и фенилпараминовой кислоты (465) кислородом воздуха в водно-бутанольной среде в присутствии соды и медноаммиачной соли (получаемой растворением CuSO4 в водном МНз). Образующийся индамин сразу циклизуется, превращаясь в лейкосое-динение диазинового красителя (467), которое далее окисляется в краситель (468).
(467) (468)
Кислотный темно-голубой применяют для крашения шерсти. Окраски очень красивы, устойчивы к свету и к стирке.
Кислотный темно-голубой 3 (469) получают аналогичным путем из 6,8-бис(фениламино)нафталин-1-сульфо-кислоты и 5-амино-2-(2-метоксифениламино)бензолсульфо-кислоты. Он окрашивает шерсть в голубой цвет более зеленоватого оттенка и является более светостойким, чем Кислотный темно-голубой.
(469)
760
Новый справочник химика и технолога
Индулины. Это красители синего цвета, которые получают взаимодействием и-аминоазобензола с анилином и его гидрохлоридом при 150-200 °C («индули-новая плавка»). При этом сначала из и-аминоазо-бензола, который реагирует в хинонгидразонной форме, образуется индамин. Индамин, взаимодействуя с гидрохлоридом анилина, образует Феносафранин (470), отличающийся от Сафранина отсутствием метильных групп.
(V70)
Дальнейшая плавка с анилином приводит к арилиро-ванию Фсносафранина и к присоединению новых ариламиногрупп к продукту арилирования. В результате образуется сложная смесь красителей [например, фениламинофеносафранины (471)] с различным числом фениламиногрупп. В зависимости от условий индулиновой плавки (соотношение реагентов, температура, продолжительность реакции) получаются красители различной степени араминирования и, соответственно, различных оттенков: от красновато-синего до зеленовато-синего.
Фениламинофеносафранины находятся в плаве в форме хлоридов, не растворимых в воде, но растворимых в спирте. Их выпускают под названием Индулин спирторастворимый и применяют для изготовления спиртовых лаков.
При обработке индулинового плава разбавленным раствором NaOH при 100 °C образуются соответствующие основания, растворимые в спирте, восках, жирах, маслах, углеводородах (парафин, бензин и др.). Их выпускают под названием Индулин жирорастворимый и применяют для изготовления типографских красок, черного лака для резиновой обуви, а также для крашения пластических масс.
Сульфированием Индулина спирторастворимого или жирорастворимого 100% серной кислотой получают сульфокислоты, натриевые соли которых растворимы в воде и являются кислотными красителями. Под названием Индулин водорастворимый их применяют для крашения кожи, шелка, шерсти и для приготовления чернил.
Нигрозины. Это красители черного цвета, которые получают нагреванием анилина, его гидрохлорида и нитробензола с чугунной стружкой при 170-180 °C («нигрозиновая плавка»). Химизм нигрозиновой плавки сложен. На первой стадии процесса из анилина и нитробензола в результате окислительно-восстановительных реакций из анилина и нитробензола образуется индоанилин (416), который претерпевает обычные для хинониминовых красителей превращения (присоединение к хиноидному ядру, замыкание циклов и т. д.). В результате образуется сложная смесь красителей с диазиновыми и оксазиновыми кольцами. Красители имеют различные оттенки: от красновато-черных до синевато-черных в зависимости от условий проведения плавки. Главной составной частью нигрозинов являются соединения с одним диазиновым и одним оксазиновым кольцами \(472) и (473)] и соединения с двумя диазиновыми кольцами [(474) и (475)]. Красители (473) и (475), являющиеся главной составной частью синеваточерных нигрозинов, отличаются от красновато-черных нигрозинов (472) и (474) наличием еще одной фениламиногруппы.
Н
(474) R=H
(475) R = NHC6H5
Кроме этих красителей в нигрозинах содержится большое количество тетрафениламинопроизводного TV-фенилфеназония (476) — одного из компонентов ин-дулинов.
Подобно индулинам Нигрозины выпускают в виде Нигрозинов спирторастворимого, жирорастворимого
Ароматические соединения
761
и водорастворимого. Нигрозин спирторастворимый образуется в результате «плавки» и применяется для крашения пластмасс, дерева и изготовления спиртовых лаков. Нигрозин жирорастворимый получают обработкой Нигрозина спирторастворимого 40% NaOH при нагревании; его применяют для изготовления сапожных кремов, краски для лент пишущих машин, типографских красок и т. д. Сульфированием Нигрозина спирторастворимого 100% H2SO4 получают Нигрозин водорастворимый, применяемый в качестве кислотного красителя для кожи, шелка и шерсти, а также для изготовления чернил.
Полидиазиновые красители. Это красители, содержащие несколько диазиновых колец. К ним относятся черные красители — продукты окисления анилина.
Краситель Анилиновый черный (477) образуется при окислении анилина непосредственно на волокне (так называемое окислительное крашение). Окислительное крашение проводят на текстильных отделочных фабриках. Для получения черной окраски ткань пропитывают смесью гидрохлорида анилина, окислителей (хлорат натрия или бихромат калия) и катализаторов (соли меди, железа или ванадия) и обрабатывают при повышенной температуре (~ 100 °C) паром. Если окисление анилина произошло недостаточно, то образовавшаяся черная окраска зеленеет на воздухе, Для предотвращения этого ткань дополнительно обрабатывают раствором бихромата. Опасность образования зеленой окраски уменьшается при добавлении к анилину и-фенилендиамина, который облегчает процесс окисления.
Образование Анилинового черного (477) проходит через ряд стадий, представляющих собой чередующиеся реакции окисления и конденсации, при этом последовательно образуются глубоко окрашенные промежуточные продукты — индамины фиолетового, синего, темно-синего и черного цветов.
Окраски, образованные Анилиновым черным на целлюлозных волокнах, отличаются глубоким, «сочным», черным цветом, на фоне которого особенно ярко выглядят расцветки другими красителями. Ни один из черных красителей других классов не может сравниться с ним в этом отношении. Окраски отличаются высокой устойчивостью к действию кислот, окислителей, вос
становителей, света, погоды, горячим мыльно-содовым обработкам, но недостаточно устойчивы к глажению. Кроме того, в процессе окислительного крашения происходит ослабление волокна, и сам процесс крашения весьма неудобен из-за высокой токсичности анилина.
Рыболовные сети, окрашенные Анилиновым черным методом окислительного крашения, устойчивы к гниению.
На анилинокрасочных заводах Анилиновый черный получают под названием Пигмент глубоко-черный, окисляя разбавленный водный раствор гидрохлорида анилина бихроматом калия в присутствии H2SO4 и CuSO4 при 25-30 °C. Окисление можно проводить и кислородом воздуха, если процесс вести в присутствии и-фенилендиамина (до 15 % от массы анилина) и CuSO4 при температуре выше 70 °C и pH ~ 2. Пигмент глубокочерный устойчив к свету, действию кислот, щелочей и органических растворителей. Он применяется для крашения пластических масс, изготовления копировальной бумаги, краски для лент пишущих машин, лаков и т. п.
Красители для меха. Окислением анилина и других ароматических аминов можно окрашивать меха в различные цвета. Образующиеся при этом красители также относятся к классу диазиновых.
Окислительное крашение меха обычно проводят при низких температурах (20-30 °C) действием пероксида (перекиси) водорода в присутствии солей металлов (хрома, железа, меди), которые являются катализаторами окисления, а затем вступают в комплексообразование с образующимися красителями.
Амины и аминофенолы, применяемые для окислительного крашения меха, называют «красителями для меха», хотя они сами по себе бесцветны. Например, и-фенилендиамин — это краситель Черный для меха Д, 2-аминофенол — Желтый для меха А, 4-аминофенол — Коричневый для меха А, 1-аминодифениламин — Серый для меха Д и т. д.
Кубовые красители. В молекулы диазиновых красителей можно ввести группировки, сообщающие им способность восстанавливаться под действием дитионита натрия. Образующиеся при восстановлении лей-косоединения обладают сродством к целлюлозным волокнам и легко окисляются (например, кислородом воздуха) с образованием исходного красителя. Такие красители могут применяться в качестве кубовых. Подобные свойства азинам придает, в частности, остаток нафтохинона.
762
Новый справочник химика и технолога
Практически значимым является краситель Кубовый желтый ЗХ (481}. Исходным продуктом для синтеза красителя является 8-аминонафталин-1-сульфокислота, которая при взаимодействии с РОС13 в нитробензоле превращается в 1,8-нафталинсультам [«нафтсультам» (478)]. Действием NaNO2 в кислой среде на нафтсуль
там получают его нитрозопроизводное (479a), которое, реагируя в хиноноксимной форме (4796) с о-фенилен-диамином, образует так называемый нафтсультамфена-зин (480). При взаимодействии нафтсультамфеназина с 2,3-дихлор-1,4-нафтохиноном в нитробензоле в присутствии поташа образуется краситель (481).
(478)
NaNO2, H,SO<
Кубовый желтый ЗХ восстанавливается в лсйкосое-динение в аммиачно-щелочной среде и может применяться для крашения не только хлопка, но и шерсти. Окраски очень устойчивы к свету, стирке и другим воздействиям.
Сернистые красители. Осернением диазиновых красителей методом мокрого сернистого плава («сернистая варка») получают сернистые красители красного, коричневого и фиолетового цветов. Предполагают, что при этом сохраняется хромофорная система диазиновых красителей, но возникают дисульфидные и ди-сульфоксидные группы, соединяющие диазиновыс остатки в крупные молекулы нерастворимых красителей. В процессе крашения при восстановлении Na2S эти крупные молекулы распадаются из-за разрыва дисульфидных (дисульфоксидных) связей, при этом образуются -SH-группы. После крашения -SH-группы на волокне снова окисляются, образуя дисульфидные (ди-сульфоксидные) связи.
Осернение диазиновых красителей, соответствующих диариламиновым, приводит к получению сернистых красителей красного и коричневого цветов. Однако красители чисто-красного цвета при этом не образуются (и вообще отсутствуют среди сернистых красителей).
Осернением диазина (482), приготовленного окислительным способом из л/-толуилендиамина и п-амино-фенола, получают Сернистый коричневый К. Диазин осерняют варкой с полисульфидом состава Na2S4 (4,58 моль на 1 моль диазина) с добавкой CuSO4 в течение 10-12 ч при 115-118 °C. Сернистый коричневый К окрашивает хлопок и вискозное волокно в красновато-коричневый цвет.
При осернении того же диазина (482) варкой с полисульфидом состава Na2S5 5 (6,8 моль на 1 моль диазина) в течение 20 ч при 115-116 °C образуется краситель Сернистый бордо С, окрашивающий хлопок и вискозное волокно в темно-красный цвет с коричневым оттенком.
Н (482)
Осернение диазиновых красителей, соответствующих триариламиновым — производным А-фснилфена-зония, приводит к получению сернистых красителей фиолетового цвета. Например, при осернении основания Феносафранина (483) полисульфидом состава Na2S515 (с добавкой соли меди) получают Сернистый фиолетовый К.
Сернистые диазиновые красители черного цвета получают методом сернистой варки из 2,4-диамино-фенола. В результате процессов, происходящих во время варки, образуются вещества, молекулы которых содержат диазиновые, тиазиновые, а возможно, и иные
гетероциклы.
(483)
Ароматические соединения
763
Краситель Сернистый черный (484‘, одна из возможных структур) получается осернением 2,4-диамино-фенола. Однако на практике исходным соединением для получения красителя является 2,4-динитрохлор-бензол, который в расплавленном состоянии вносят в горячий раствор NaOH; при этом сразу же образуется 2,4-Динитрофеноксид. Раствор 2,4-динитрофеноксида натрия приливают к раствору полисульфида состава Na2S3 7, взятому в избытке, и постепенно упаривают до тех пор, пока реакционная масса не достигнет определенной плотности, а краситель — стандартной концентрации и нужного оттенка (~ 70 ч).
Химизм этого процесса изучен недостаточно; точно только установлено, что вначале происходит восстановление нитрогруппы и образование 2,4-диаминофе-ноксида, который и подвергается осернению.
(484)
Сернистый черный является самым дешевым и распространенным красителем. Он окрашивает хлопок, лен, вискозное волокно в черный и серый (в зависимости от количества красителя) цвет. Окраски устойчивы ко всем видам воздействия, за исключением мокрого трения и активного хлора. Недостатком Сернистого черного является ослабление окрашенного им волокна при хранении. Причиной ослабления волокна является действие сернистой или серной кислот, образующихся в результате окисления красителя на волокне кислородом воздуха. Ткани, периодически подвергающиеся стирке, ослабляются в значительно меньшей степени, т. к. кислоты при стирке вымываются.
Некоторые коричневые и красновато-коричневые сернистые красители получают не из самих диазинов, а из соединений, которые могут образовать диазины в процессе осернения. Осернение таких соединений требует более жестких условий, чем осернение хинониминовых и заранее приготовленных диазиновых красителей, и обычно осуществляется способом так называемого сухого сернистого плава («запекания»).
Способ заключается в нагревании смеси исходных продуктов с полисульфидом натрия или элементной серой при высокой температуре (обычно выше 200 °C, до 250-300 °C) в отсутствие растворителя. При этом либо сразу запекают смесь, в которой отсутствует растворитель (запекание с серой), либо предварительно удаляют растворитель (обычно воду) выпариванием (запекание с полисульфидом).
Так, краситель Сернистый темно-коричневый К получают при осернении 4-гидрокси-2',4'-динитродифе-ниламина, краситель Сернистый коричневый Ж — при осернении 2,4-динитротолуола. Предполагают, что в обоих случаях одной из первых стадий осернения этих соединений является образование диазинов. Оба красителя используются для крашения хлопка, окраски устойчивы к мокрым обработкам, но недостаточно устойчивы к действию света и трению.
Тиозоли. Растворимые производные сернистых красителей выпускаются под названием тиозоли. Из всех способов получения растворимых производных или препаратов сернистых красителей наиболее часто применяются взаимодействие с монохлоруксусной кислотой и обработка бисульфитом или сульфитом натрия. Цвет окрасок тиозолями часто отличается от цвета, полученного при обычном крашении исходным сернистым красителем, что свидетельствует о существенных изменениях в химическом строении красителя.
При взаимодействии с монохлоруксусной кислотой в молекуле появляются остатки тиогликолевой кислоты (—SCH2COOH), которые и обусловливают растворимость красителя. Таким способом получают Тиозоль бордо (из Сернистого бордо С), Тиозоль синий К (из Сернистого синего 3) и др.
При взаимодействии сернистых красителей или их лейкосоединений с бисульфитом или сульфитом натрия или их смесями при нагревании образуются растворимые соединения типа бисульфитных производных хинонов. Так, взаимодействием Сернистого черного с Na2SO3 и NaHSO3 получают Тиозоль черный Бс, взаимодействием Сернистого чисто-голубого К с Na2S03 — Тиозоль голубой Бс, Сернистого темно-синего с NaHSO3 — Тиозоль синий Бс, Сернистого темно-коричневого Ж с NaHSO3 — Тиозоль коричневый Бс и т. д.
Значительно реже в производстве тиозолей применяется сульфирование сернистых красителей серной кислотой, в результате которого в молекуле появляются сульфогруппы, придающие растворимость в воде. Красители при этом приобретают свойства прямых красителей, чему способствуют значительные размеры и плоскостность молекул сернистых красителей. Так, сульфированием Сернистого ярко-зеленого Ж получают Тиозоль ярко-зеленый Ж.
Меры предосторожности в производстве ариламиновых красителей
Производство ариламиновых красителей связано с использованием и получением ряда взрывоопасных (ди- и полинитросоединения), токсичных (нитросоединения, амины, сероводород, основные красители, не содержащие сульфогрупп), канцерогенных (аминоазотолуол) веществ.
При работе с полинитросоединениями необходимо предотвращать возможность ударов, попадания посторонних веществ, перегрева и накопления нитросоединений на полах и стенах рабочих помещений. При про-
764
Новый справочник химика и технолога
ведении реакций с ароматическими аминами и нитросоединениями при высоких температурах (сернистые, индулиновые и нигрозиновые плавки, проведение реакций в среде нитробензола и т. п.) должна быть исключена возможность попадания паров этих веществ в атмосферу помещений.
В производстве сернистых красителей особое внимание следует уделять контролю за содержанием в атмосфере помещений сероводорода, который не только чрезвычайно ядовит (причем человек быстро утрачивает способность чувствовать запах сероводорода вследствие паралича окончаний обонятельного нерва), но и образует с воздухом взрывчатые смеси. Все аппараты, в которых возможно образование сероводорода, должны быть подключены к вытяжной вентиляции, а вентиляционные трубопроводы подведены к скрубберам с раствором NaOH, чтобы исключить выбрасывание H2S в атмосферу.
Опасность представляет и продукт взаимодействия сероводорода с железом, так называемое пирофорное железо, которое при действии кислорода воздуха окисляется; вследствие экзотермичности этой реакции она может привести к пожару или взрыву.
4.3.5.6. Тиазоловые красители
Молекулы тиазоловых красителей содержат пятичленный гетероцикл — тиазол (26), конденсированный с различными ароматическими системами. Плоское тиазоловое кольцо с двумя гетероатомами, способное к участию в водородных связях, относится к числу структур, обусловливающих сродство к целлюлозным волокнам.
Простейшим техническим способом получения красителей — производных тиазола — является осернение смеси ароматических соединений, содержащих метильную группу, с первичными аминами, имеющими свободное ортио-положение по отношению к аминогруппе, или соединений, содержащих одновременно метильную и аминогруппы. Осернение проводят нагреванием соединений с серой при высоких температурах (осернение методом запекания или сухого сернистого плава).
Так, при нагревании с серой и-толуидина при 175-180 °C образуется 2-(4-аминофенил)-6-метилбензотиа-зол (485). Он имеет слабо-желтую окраску и применяется в качестве промежуточного продукта для синтеза азокрасителей.
Если осернение (запекание с серой) ароматических аминов, содержащих метильные группы, проводить при температурах порядка 200 °C в течение длительного времени (20 ч и больше) или при более высоких температурах (до 240-250 °C), образуются нерастворимые
соединения с несколькими тиазоловыми кольцами и меркаптогруппами; при окислении меркаптогрупп (воздухом) образуются дисульфидные или дисульфок-сидные группы, которые связывают друг с другом отдельные частицы, содержащие остатки бензотиазола. Получаются типичные сернистые красители с большой молекулярной массой, не растворимые в воде и переходящие в раствор при восстановлении сульфидом натрия.
В группе сернистых тиазоловых красителей имеются красители желтого, оранжевого, желто-коричневого и коричневого цветов.
Сернистый желтый (486) получают запеканием смеси и-толуидина и бензидина (в отношении 2 : 1) с большим избытком серы при 200 °C в течение 20 ч. В его молекуле бензотиазольные остатки образованы как за счет двух молекул и-толуидина, так и с участием молекул бензидина (189); образовавшиеся структурные группы связываются друг с другом дисульфидными связями. Сернистый желтый образует окраски, мало устойчивые к свету, вследствие чего находит ограниченное применение.
Несколько выше светостойкость окрасок у красителя Иммедиаль желтый Г, который получают запеканием с серой 2,4-динитроацетанилида и фталевого ангидрида при 130 °C в течение 11 ч. Структура этого красителя не установлена, лишь известно, что в молекуле его есть тиазоловые кольца.
Введение аминогрупп в остатки бензотиазола приводит к углублению цвета сернистых тиазоловых красителей. Так, Сернистый оранжевый получают запеканием л/-толуилендиамина с серой при 215-250 °C в течение 10-15 ч. При этом, по-видимому, образуются прямые (с линейным расположением) (487) или разветвленные (488) цепочки из шести-восьми остатков бензотиазола.
Сокращение времени плавки приводит к получению красителей более желтого оттенка, очевидно, вследствие уменьшения числа связанных друг с другом бензотиазольных остатков.
Сернистый оранжевый образует окраски, устойчивые к мокрым обработкам, но недостаточно светостойкие. Обработка на волокне солями хрома и меди увеличивает устойчивость окрасок к свету.
(486)
Ароматические соединения
765
По своему строению к Сернистому оранжевому близок краситель Сернистый коричневый Ж, который получают осернением (методом запекания) 2,4-динитротолуола полисульфидом натрия состава (Na2S7)6. Так как первой стадией является восстановление 2,4-динитротолуола в л/-толуилендиамин (исходный продукт для получения Сернистого оранжевого), то запекание его и приводит в дальнейшем к образованию желто-коричневого красителя, по цвету довольно близкого к Сернистому оранжевому.
При получении Сернистого коричневого Ж к раствору полисульфида натрия (приготовленному взаимодействием серы с водным раствором Na2S при ЮЗ-105 °C) прибавляют расплавленный 2,4-динитротолуол и ведут восстановление при 108-118 °C, после чего медленно (на 10 °C в час) повышают температуру до 240 °C. При этом происходит упаривание и загустевание плава. Запекание при 240 °C ведут до получения красителя нужного оттенка.
Сернистый коричневый Ж применяется для крашения хлопка. Окраски устойчивы к стирке, однако устойчивость к свету и мокрому трению невысокая.
Запеканием с серой других аминов, смесей аминов, нитросоединений, ацильных производных аминов, а также сложных полициклических соединений получают различные по оттенкам и свойствам желтые и оранжевые сернистые красители, строение которых мало исследовано.
Так, запеканием с серой о-толуидина и и-нитро-анилина в течение 8 ч при 180-250 °C получают Имме-диаль желтый ЗГТ, из .м-толуилендиамина, бензидина и
.м-нитроанилина (15 ч при 230-250 °C) — Иммедиаль желтый 4РТ, из .м-толуилендиамина и /У,Лг-дифталоил-и-фенилендиамина (489) (10 ч при 210-215 °C) — Иммедиаль оранжевый ФР и т. д.
Меры предосторожности в производстве тиазоловых красителей
Производство тиазоловых красителей связано с использованием и получением ряда токсичных («-толуидин, ,и-тол уилендиамин, сероводород и др.), горючих и взрывоопасных (нитробензол, сера, аммиак и др.) веществ. Свойства некоторых из них и сведения о мерах предосторожности приведены в предыдущих главах.
4.3.5.7. Индигоидные красители
Дисперсные (красные)
Индигоидные красители
-► Кубовые (оранжевые, красные, красно-коричневые, синие, черные)
-► Кубозоли
(оранжевые, красные, красно-коричневые, синие, черные)
-►Пигменты (красные)
766
Новый справочник химика и технолога
В зависимости от природы циклических систем, из которых построены молекулы индигоидных красителей, они делятся на следующие группы.
1. Бис(индол)индигоиды, например 2,2'-бис(индол)-индиго (490) и 2,3'-бис(индол)индиго (491).
2. Бис(бензотиофен)индигоиды, например 2,2'-бис-(бензотиофен)индиго (492).
(492)
3. Индолбензотиофениндигоиды, например 2-индол-2'-бензотиофениндиго (493) и 2-бензотиофен-3'-индол-индиго (494).
(494)
4. Индоларсн- и бензотиофенарениндигоиды, например 2-индол-2'-нафталининдиго (495) и 2-бензотио-фен-2'-аценафтениндиго (496).
(495)
(496)
5. Прочие индигоидные красители, например 2,2'-бис(кумарон)индиго (497) и 2,2'-бис(бензоселенафен)-индиго (498).
(497) (498)
Индигоидные красители могут существовать в двух стереоизомерных формах — цис (490a) и транс (4906). Электронные спектры этих стереоизомеров отличаются положением Хмакс, причем более длинноволновый максимум поглощения имеет щ/?анс-форма. В обычном (не
возбужденном) состоянии красители находятся в транс-форме, которая более устойчива.
При отсутствии в молекулах индигоидных красителей солеобразующих групп они нерастворимы в воде и обладают свойствами кубовых красителей, т. с. при восстановлении переходят в лейкосоединения, натриевые соли которых хорошо растворяются в воде и обладают сродством к целлюлозному волокну (растворы щелочных солей лейкосоединений называют «кубами», отсюда и название красителей). После крашения под действием диоксида углерода и кислорода воздуха соли лейкосоединений превращаются в нерастворимые красители, прочно закрепляющиеся на волокне.
Поскольку индигоидные красители нерастворимы в воде, а молекулы большинства из них невелики по размерам, то при введении в них заместителей, например -СООСН3, облегчающих проникновение в глубь гидрофобных волокон с образованием твердых растворов, они могут использоваться в качестве дисперсных красителей.
Бис(индол)индигоиды
Молекулы бис(индол)индигоидов содержат гетероциклические пиррольные остатки, конденсированные с бензольными (индол), нафталиновыми и др. В этой группе индигоидов практическое значение имеют симметричные красители, а именно 2,2’-бис(индол)индигоиды.
Важнейшим представителем бис(индол)индигоидов является синий краситель Индиго (490) — родоначальник всего класса индигоидных красителей. До установления его строения Индиго добывали из листьев индигоносных растений (индигофера, красильная вайда). В листьях этих растений содержится глюкозид индоксила — индикан (499). При ферментативном гидролизе он распадается на глюкозу и индоксил (500), который при окислении кислородом воздуха легко превращается в Индиго (490).
(490)
Ароматические соединения
767
Синтетическим путем Индиго впервые был получен в 1883 г. А.Байером, установившим строение этого красителя. Промышленное производство синтетического Индиго началось в 1897 г.
В настоящее время известно свыше 30 различных способов получения Индиго. Все они сводятся к получению индоксила (500) с его последующим окислением. Наиболее распространенный способ — это взаимо
действие анилина с монохлоруксусной кислотой в присутствии гидроксида железа, перевод образовавшейся железной соли фенилглицина (501) в калиевую соль (502), плавление калиевой соли в смеси NaOH, КОН и NaNH2 (Т ~ 200 °C и р ~ 0,3 МПа, при этих условиях происходит замыкание гетероцикла) и окисление щелочной соли индоксила (500) кислородом воздуха в Индиго (490).
NaOH, КОН, NaNH?, 200 °C
Причины глубокой (синей) окраски Индиго до сих пор вызывают интерес, т. к. молекулы других красителей с таким же количеством л-электронов в цепи сопряжения имеют значительно более высокий цвет (например, Катионный оранжевый К). Одной из причин является внутримолекулярная поляризация молекул (503), вследствие которой возникает единая сопряженная система и появляется сильный ЭД-заместитель. В молекуле дегидроиндиго (504), образующейся при осторожном окислении Индиго, внутримолекулярная ионизация невозможна и соединение имеет неглубокий цвет — коричневато-красный.
Н
Второй причиной глубокого цвета Индиго является ассоциация отдельных молекул в твердом (кристаллическом) состоянии за счет межмолекулярных водородных связей. В парообразном состоянии и в некоторых растворителях его цвет не синий, более высокий — пурпурный.
Индиго является кубовым красителем . При восстановлении дитионитом натрия в щелочной среде он об-
Так как все кубовые красители не растворимы в воде, в процессе приготовления красильной ванны их переводят в растворимое состояние. Для этого используют способность карбонильных групп красителей восстанавливаться в енольные группы, диссоциирующие в щелочной среде и обусловливающие растворимость соединения.
разует бесцветное лейкосоединение (505), натриевая соль (506) которого хорошо растворима в воде и в процессе крашения выбирается из ванны целлюлозным волокном. При дальнейшем гидролизе и окислении кислородом воздуха на волокне образуется не растворимый в воде краситель.
Продукты восстановления красителей получили название «лейкосоединений» (по-гречески «лаукос» — белый, неокрашенный) по аналогии с названием почти бесцветного продукта восстановления синего Индиго — древнейшего красителя, крашение которым производится таким же способом. Однако в случае других кубовых красителей лейкосоединения не только окрашены, но часто имеют более глубокую окраску, чем сами красители, т. к. при восстановлении сохраняется мощная сопряженная система двойных связей красителя.
Крашение проводят из раствора, после чего лейкосоединение окисляется на волокне кислородом воздуха в исходный краситель.
ONa+ + О2 + СО2---------► ^>=0 + М^СОз
Так как в древности восстановление Индиго в лейкосоединение осуществляли в больших чанах («кубах»), подобный процесс крашения получил название кубового, а сами красители — кубовых. Словом «куб» часто называют щелочной раствор лейкосоединения.
768
Новый справочник химика и технолога
Лейкосоединение индиго может быть выделено в твердом состоянии при действии диоксида углерода на его раствор. Под названием Индиго белый (505) такой препарат раньше применялся для крашения; при этом исключалась стадия восстановления красителя перед крашением.
Восстанавливать Индиго в лейкосоединение можно и в слабощелочной среде (например, дитионитом натрия в среде аммиака), поэтому его можно применять для крашения не только целлюлозных, но и белковых волокон.
Индиго образует довольно светостойкие, но не очень яркие окраски, умеренно устойчивые к стирке и мало устойчивые к трению и действию хлора. Вследствие этих недостатков применение Индиго частично сокращается, однако недостатки компенсируются сравнительно низкой стоимостью Индиго по сравнению со стоимостью других кубовых красителей синего цвета. Под названием Индиго М краситель в специальной выпускной форме применяется для крашения меха.
Из всех производных индиго наибольшее практическое применение находят его галогенпроизводные. По сравнению с Индиго они образуют не только более красивые и яркие окраски, но и обладают большим сродством к волокну; поэтому лейкосоединения этих красителей легче и прочнее адсорбируются волокном, а окраски устойчивее к мокрым обработкам, трению и хлору. Светостойкость окрасок также увеличивается при введении нескольких атомов галогена (1-3), однако при большом числе атомов галогена светостойкость резко падает: гексаброминдиго обесцвечивается под действием света через несколько часов.
Важнейшим галогенпроизводным Индиго является 5,5',7,7'-тетраброминдиго, выпускаемый под названием Ьроминдиго (507). Ьроминдиго получают бромированием Индиго в растворе серной кислоты. Для уменьше
ния расхода брома добавляют окислитель (NaNO2), регенерирующий бром из образующегося бромистого водорода.
(507)
Броминдиго окрашивает целлюлозные волокна в яркий и чистый синий цвет, окраски устойчивы к мокрым обработкам, хлору и трению.
Натриевая соль сернокислого эфира лейкосоединения Броминдиго выпускается под названием Кубозоль синий (508). Применение кубозолей не требует предварительного восстановления и не связано с использованием сильнощелочных ванн. Кубозоль синий применяется для крашения целлюлозных волокон из нейтральной ванны и белковых волокон из кислой ванны.
(508)
При сульфировании Индиго концентрированной серной кислотой образуется 5,5'-дисульфокислота Индиго — синий кислотный краситель Индигокармин (509). Индигокармин окрашивает шерсть в красивый синий цвет, но не применяется для этой цели из-за исключительно низкой светостойкости окрасок. Индигокармин используется даже в качестве эталона неустойчивости окрасок к свету: краситель, выцветающий с такой же скоростью, как Индигокармин, получает оценку 1 (по восьмибальной шкале устойчивости к свету). Применяется Индигокармин для изготовления синих чернил и подкрашивания пищевых продуктов.
Применяя производные дииндоксила, можно получить полимерные индигоидные красители. Так, при окислении кислородом воздуха 5,5'-дииндоксил-2,2'-дикарбоновой кислоты (510) образуется голубой Полииндиго (511).
Ароматические соединения
769
Полииндиго стабилен на воздухе до 350 °C и обладает полупроводниковыми свойствами.
Бис(бензотиофен)индигоиды
В отличие от бис(индол)индигоидов (собственно индигоидных красителей) бис(бензотиофен)индигоиды (тиоиндигоидные красители) содержат в пятичленном гетероцикле атом серы вместо атома азота. Основой этих красителей является 3-гидроксибензотиофен, существующий, как и индоксил, в таутомерных оксо-(572а) и гидрокси- (5726) формах.
(572а)
При окислении 3-гидроксибензотиофена образуется краситель Тиоиндиго красный С (492).
Замена атома азота в гетероцикле атомом серы приводит к повышению цвета — от синего (Хмакс = 591 нм) до красного с синеватым оттенком (Хмакс = 546 нм).
Тиоиндигоидные красители более устойчивы к химическим воздействиям (к действию окислителей, кислот, сильных щелочей и др.), по сравнению с индигоидными красителями. Например, окраска Тиоиндиго красным С (492) не изменяется при действии гипохлорита в условиях, когда окрашенное волокно полностью разрушается, не обесцвечивается под действием разбавленной азотной кислоты (в противоположность Индиго) и т. д. Тиоиндигоидные красители восстанавливаются в лейкосоединения не только дитионитом натрия, но и растворами сульфида натрия, что позволяет использовать их в крашении в смесях
с сернистыми красителями. Во многих случаях тиоиндигоидные красители могут восстанавливаться в лейкосоединения при небольшой щелочности и невысокой температуре, что позволяет применять их для крашения не только целлюлозных волокон, но также шерсти и шелка.
Из тиоиндигоидных красителей, как и из индигоидных, получают кубозоли.
Практическое значение в группе бис(бензотиофен)-индигоидов имеют симметричные красители — 2,2'-бис(бензотиофен)индигоиды. Синтез их сводится к синтезу 3-гидроксибензотиофена и его замещенных с последующим окислением серой или полисульфидами натрия в щелочной среде. Использование других окислителей может привести к окислению 3-гидроксибензо-тиофена по атому серы.
Способы получения тиоиндигоидных красителей отличаются друг от друга в основном способом введения в ароматическое кольцо меркаптогруппы, необходимой для синтеза 3-гидроксибензотиофена и его замещенных.
Синтез с использованием диазосоединений. Меркаптогруппа в ароматическое кольцо вводится путем нуклеофильного замещения диазониевой группы, полученной в результате диазотирования аминосоединения. Таким способом получают простейший тиоиндигоид-ный краситель — Тиоиндиго красный С (492).
Исходным соединением для синтеза красителя является антраниловая кислота, которую переводят в диазосоединение действием NaNO2 в кислой среде. Добавляя раствор диазосоединения к смеси растворов NaOH и Na2S2, постепенно переводят диазосоединение в соль ди(2-карбоксифенил)дисульфида (513), которая восстанавливается в тиосалициловую кислоту (514). Действуя на натриевую соль тиосалициловой кислоты монохлоруксусной кислотой, получают соответствующую соль (2-карбоксифенилтио)уксусной кислоты (575), которая при обработке концентрированной щелочью превращается в З-гидроксибензотиофен-2-карбоновую кислоту (516). При окислении соединения (516) серой в растворе NaOH образуется Тиоиндиго красный С (492).
770
Новый справочник химика и технолога
Тиоиндиго красный С применяется для крашения целлюлозных и белковых волокон. Окраски имеют хорошую светостойкость и удовлетворительную устойчивость к стирке. Под названием Пигмент красный тио-индигоидный С краситель в специальной пигментной форме применяется для окраски натуральной кожи и в полиграфии для цветной печати.
Алкоксикарбонилзамещенные Тиоиндиго красного С обладают свойствами дисперсных красителей и могут применяться для крашения полиэфирных и других гидрофобных волокон. Например, 6,6-диалкоксикарбонил-производные (517) являются красными дисперсными красителями. Кроме групп -C(O)OR соединения могут содержать атомы галогена, алкильные или алкоксигруппы.
Синтез с использованием хлорида серы (способ Герца). Этим способом получают краситель Тиоиндиго розовый 2С (526).
При действии на гидрохлорид анилина хлористой серы образуется соль соответствующего 1 ДЗ-дитиазолия [(518); хлорид 6-хлор-1,2,3-бензо[б/|дитиазолия], которая гидролизуется с образованием 6-хлор-ЗЯ-1,2,3-бензо[</]дитиазо-локсида-2 (519). Под действием щелочи дитиазоловое кольцо расщепляется и образуется натриевая соль 2-мер-капто-4-хлоранилина (520), которая при взаимодействии с монохлоруксусной кислотой превращается в соответствующую соль (2-амино-5-хлорфенилтио)уксусной кислоты (521). Эту соль действием NaNO2 в соляной кислоте переводят в диазосоединение (522), при взаимодействии которого с Na3Cu(CN)4 образуется натриевая соль (5-хлор-2-цианофенилтио)уксусной кислоты (523). При нагревании ее с водным раствором NaOH тиофеновое кольцо замыкается и образуется натриевая соль З-имино-6-хлорбензо-тиофен-2-карбоновой кислоты (524), которая при нагревании в разбавленной серной кислоте вначале гидролизуется с образованием 3-оксо-6-хлорбензотиофен-2-карбоновой кислоты, а затем декарбоксилируется. Образовавшийся З-оксо-6-хлорбензотиофен (525) окисляют в краситель действием серы в растворе NaOH.
R = СН3, С2Н5, С6Н5, СН2, СН3ОС2Н4, СН2=СН и др.
(524)
(525)
(526)
Ароматические соединения
771
Этим же методом получают Тиоиндиго ярко-розовый Ж (527) из гидрохлорида о-толуидина и Тиоиндиго оранжевый КХ (528) из гидрохлорида я-фенетидина.
Из обоих красителей получают соответствующие кубозол и: Кубозоль ярко-розовый Ж и Кубозоль оранжевый К.
Синтез из сульфокислот. Меркаптосоединения можно получить из сульфокислот, превращая их в суль-фонилхлориды и восстанавливая последние цинковой пылью и серной или концентрированной соляной кислотой (реже оловом и соляной кислотой). Процесс
идет через стадии образования сульфиновой кислоты ArSO2H, арилового эфира арилтиосульфокислоты ArSSO2Ar и дисульфида ArSSAr. По этому способу получают в основном тиоиндигоидные красители на основе производных нафтотиофена. Например, так получают Тиоиндиго красно-коричневый Ж (534).
Исходным продуктом для получения Тиоиндиго красно-коричневого Ж является нафталин-2-суль-фокислота, которую переводят в сульфонилхлорид (529) действием РС15 в среде хлорбензола. Восстанавливая сульфонилхлорид цинковой пылью в среде 20% H2SC>4, получают 2-меркаптонафталин (530). При взаимодействии последнего с монохлоруксусной кислотой в щелочной среде получают натриевую соль (нафтил-2)тиоуксусной кислоты (531), которую переводят в хлорангидрид соответствующей кислоты (532) действием РС13. Замыкание тиофенового кольца происходит под действием безводного А1С13 в среде хлорбензола. 3-Оксонафто[2,1-/?]тиофен (533) образуется в виде комплекса с алюминием, который разрушают действием раствора NaOH, после чего окисляют кислородом воздуха, предварительно добавив раствор CuSO4 (катализатор), и получают Тиоиндиго красно-коричневый Ж (534).
Тиоиндиго красно-коричневый Ж (534) широко применяется для крашения хлопка, вискозного волокна, льна и шелка. По устойчивости окрасок этот краситель превосходит все другие тиоиндигоидные красители и относится к числу лучших кубовых красителей. Под названием Кубовый красно-коричневый 4ЖМ применяется для крашения меха.
Тиоиндиго красно-коричневый Ж может быть получен другим более простым и дешевым способом — осернением 1-ацетилнафталина методом варки с полисульфидом натрия Na2S7 в бутаноле. Однако краситель, полученный методом осернения, имеет не желтый, а зеленоватый и более тусклый оттенок, поэтому пригоден только для крашения меха, где яркость и чистота оттенка не имеют такого значения, как для текстильных материалов.
Из Тиоиндиго красно-коричневого Ж получают Кубозоль красно-коричневый Ж.
Несимметричные индигоидные красители
Несимметричные индигоидные красители делятся на две группы: красители, построенные из двух одинаковых циклических систем, но связанных в разных положениях, например 2,3'-бис(индол)индиго (491), 2,3'-бис(бензотиофен)индиго, и красители, построенные из двух разных циклических систем, например, 2-индол-2'-бензотиофениндиго (493).
Как те, так и другие несимметричные индигоидные красители получают взаимодействием индоксила (500) или 3-гидроксибензотиофена (512) с карбонильными соединениями (хиноны, кетоны, тиокетоны), их производными (анилы, бисульфитные производные) и гало-гензамещенными с активным атомом галогена.
Если в качестве второго компонента применяют карбонильные соединения типа изатина [(535); продукт окисления индиго], содержащего две карбонильные
772
Новый справочник химика и технолога
группы, то реакция идет по атому углерода С-3, электрофильная активность которого выше, чем атома углерода С-2. Напротив, в молекуле изатинхлорида (536), образующегося при взаимодействии изатина с РС15, электрофильная активность выше у атома углерода С-2 (индукционное влияние атома хлора).
Следовательно, взаимодействие индоксила (537; X = NH) или 3-гидроксибензотиофена (537; X = S), реагирующих в оксоформе, с изатинхлоридом (536) приводит к образованию 2,2'-производных (533), а с изатином (535) — к образованию 2,3'-производных (539).
(533) (539)
Цвет несимметричных индигоидных красителей зависит от гетероциклов, входящих в состав молекулы, и от вклада предельных структур в возбужденном состоянии. Так, фиолетовый цвет 2-индол-2'-бензотио-фениндиго (493) соответствует цвету эквимольной смеси двух симметричных красителей, построенных из его гетероциклических фрагментов, т. е. Индиго (490)
и Тиоиндиго красного С (492). Следовательно, обе структуры (493a) и (4936), возникающие в возбужденном состоянии, вносят приблизительно равный вклад в образование цвета.
Индолбензотиофениндигоиды. Важнейшим представителем этой группы красителей является Тиоиндиго черный (549) — один из немногочисленных кубовых красителей черного цвета. Его получают взаимодействием 3-оксо-9-хлорнафто[1,2-6]тиофена (546) с 5-бром-изатинхлоридом (548).
Исходным продуктом для получения З-оксо-9-хлор-нафто[1,2-6]тиофена (546) является 8-аминонафталин-1-сульфокислота. Ее переводят в диазосоединение (540) действием NaNO2 в соляной кислоте и заменяют диазо-ниевую группу на хлор в присутствии CuCl. Полученную 8-хлорнафталин-1-сульфокислоту (541), обрабатывая РСЬ в хлорбензоле, переводят в соответствующий сульфонилхлорид (542), который восстанавливают цинковой пылью в среде серной кислоты; при этом образуется 1-меркапто-8-хлорнафталин (543). При взаимодействии меркаптосоединения с монохлоруксусной кислотой в присутствии NaOH образуется натриевая соль [(8-хлорнафтил-1)тио]уксусной кислоты (544), которую переводят в хлорангидрид (545) действием РС13. Добавляя к хлорбензольному раствору хлорангидрида А1С13, замыкают тиофеновое кольцо и получают З-оксо-9-хлорнафто[ 1,2-6]тиофен (546).
Для получения 5-бромизатинхлорида (548) изатин (535), полученный окислением Индиго (490) бихроматом калия в серной кислоте, бромируют в разбавленной
соляной кислоте, а образовавшийся 5-бромизатин (547) обрабатывают PCI5 в хлорбензоле.
Ароматические соединения
из
Заключительную стадию синтеза красителя (549) осуществляют, натровая до 50 °C объединенные хлорбензольные растворы 3-оксо-9-хлорнафто[1,2-£>]тиофе-на (546) и 5-бромизатинхлорида (548).
Тиоиндиго черный (549) применяется для печати по хлопку; окраски устойчивы к свету и мокрым обработкам. Поскольку краситель имеет заметный синий оттенок [по-видимому, превалирует вклад структуры типа (493a)}, для получения чистого черного цвета к нему добавляют некоторое количество желтого или оранжевого кубового красителя (например, Кубового золотисто-желтого КХ или Кубового золотисто-оранжевого 2Ж), чем достигается суммарное равномерное поглощение по всей видимой части спектра. Обычно краситель выпускается в виде готовой смеси.
Из Тиоиндиго черного получают Кубозоль серый С.
(512а) (535)
Из этой же группы красителей практическое значение имеет Тиоиндиго алый (550), получаемый конденсацией 3-гидроксибензотиофена [(5/2а); таутомерная
Индоларен- и бензотиофенарениндигоиды. Хромофорная система индигоидных красителей может быть образована без участия второго гетероциклического остатка. Красители этой группы по своему строению являются продуктами конденсации производных индоксила и 3-гидроксибензотиофена с хинонами. К ним относятся, например, Тиоиндиго алый Ж (496), Алголе-вый голубой 4Р (551), Алголевый синий Г (552).
Цвет таких красителей зависит как от гетероциклического, так и от ароматического фрагмента молекулы. Поэтому часто эти красители имеют более глубокую окраску, чем симметричные индигоиды, построенные из двух таких же гетероциклических остатков.
Наиболее значимым красителем данной группы является Тиоиндиго алый Ж (496) (из группы 2-бензо-тиофен-2'-аценафтениндиго) — продукт конденсации 3-гидроксибензотиофена (512) с бисульфитным производным аценафтенхинона (556).
Исходным продуктом для получения аценафтенхинона является аценафтен (553), который окисляют нитрозилхлоридом (образуется при взаимодействии NaNO2 с НС1) до аценафтенхинонмонооксима (554), образующего при взаимодействии с формальдегидом в разбавленной серной кислоте аценафтенхинон (555). Обрабатывая аценафтенхинон NaHSO3, получают его бисульфитное производное (556). При взаимодействии бисульфитного соединения с натриевой солью З-гидроксибензотиофен-2-карбоновой кислоты (511) образуется Тиоиндиго алый Ж (496).
774
Новый справочник химика и технолога
Тиоиндиго алый Ж (496) отличается красивым алым цветом. Он применяется для крашения хлопка, вискозного волокна, шерсти и шелка, а также для печа
ти по хлопчатобумажным и вискозным тканям. Окраски устойчивы к мокрым обработкам и довольно светостойки.
(553)
(554) (555)
Меры предосторожности в производстве индигоидных красителей
Производство индигоидных красителей связано с использованием ряда ядовитых и сильнодействующих веществ (цианид натрия, хлор, бром, монохлоруксусная кислота и др.), а также веществ, бурно реагирующих с водой и поэтому пожаро- и взрывоопасных (металлический натрий, амид натрия) .
Все операции с цианидом натрия (хранение, взвешивание, загрузка) должны осуществляться ограниченным числом специально обученных людей. Необходимо иметь в виду, что при подкислении растворов NaCN образуется легколетучий, чрезвычайно ядовитый и огнеопасный цианистый водород, предельно допустимая концентрация которого в рабочей зоне производственных помещений составляет 0,3 мг/м^; область воспламенения 5.6 40 об. %. Во время загрузки цианида натрия в аппарат из помещения должны быть удалены все, не имеющие отношения к проведению этой операции
При работе с А1С1з следует иметь в виду, что от следов влаги он разлагается с выделением НС1, раздражающего слизистые оболочки, а при действии большего количества воды разлагается со взрывом.
При работе с металлическим натрием и амидом натрия должна быть полностью исключена возможность попадания воды. При получении амида натрия, сопровождающемся выделением водорода, необходимо принимать меры для предотвращения образования взрывоопасной смеси с воздухом.
Хлорид серы раздражает слизистые оболочки, горюч, с водой реагирует со взрывом.
Применяемый в производстве нитрит натрия также чрезвычайно ядовит, что надо учитывать при организации работы с ним.
Вредным действием обладают некоторые промежуточные продукты, образующиеся в ходе производства индигоидных красителей. З-Гидрокси-6-этоксинафто-тиофен ядовит и угнетает кроветворение, 6-этокси-
1,2,3-бе нзодитиазолийхлорид раздражает слизистые оболочки и вызывает кожные заболевания. Следует учитывать, что далеко не все промежуточные продукты изучены с точки зрения их биологического действия, а поэтому работа с ними должна производиться как с потенциально опасными веществами.
Тщательного соблюдения всех мер предосторожности требует работа с едкими щелочами при высоких температурах, а также с бромом и монохлоруксусной кислотой, попадание которых на тело причиняет тяжелые ожоги и приводит к образованию трудно заживающих ран.
4.3.5.8. Антрахиноновые красители
-► Активные
(голубые, синие, зеленые) Дисперсные (от оранжевых до синих) -► Жирорасворимые (голубые, зеленые) -► Катионные
Антрахиноновые (фиолетовые, синие)
красители -► Кислотные (от фиолетовых до зеленых) -► Кубовые (желтые, оранжевые, бордо, синие, зеленые, сливковые, серые, коричневые) Протравные
(от оранжевых до синих, коричневые, черные)
Антрахиноновые красители являются производными 9,10-антрахинона [(557); антрацендион-9,10]. Молекула антрахинона состоит из двух бензольных колец, соединенных двумя карбонильными группами, которые в хромофорной системе антрахиноновых красителей являются ЭА-заместителями.
Ароматические соединения
775
О
О (557)
Введение ЭД-заместителя в любое положение молекулы антрахинона приводит к взаимодействию между ним и одной из карбонильных групп по более или менее длинной цепочке сопряженных двойных связей. Так как ЭД-заместитель в a-положении образует более длинную цепь сопряжения (четыре звена), чем в 0-положении (три звена), то при одинаковой электронодонорности заместителя а-замещенные антрахиноны (558) всегда имеют более глубокий цвет, чем 0-замещенные (559).
О
(^) каке = 480 НМ
Если заместитель X в a-положении антрахинонового ядра (560) содержит атом водорода, способный участвовать в образовании водородной связи, возникает внутримолекулярная водородная связь с атомом кислорода соседней карбонильной группы. В результате снижается подвижность атома водорода и увеличивается устойчивость молекулы к химическим и фотохимическим воздействиям, в частности к процессу фотодеструкции. В этом одна из причин высокой светостойкости многих антрахиноновых красителей.
(560) X = О, NH, NR
Гидроксиантрахиноновые (ализариновые) красители
Из гидроксиантрахиноновых красителей практическое значение приобрели лишь такие, в молекулах которых имеется не менее одной гидроксигруппы в а-поло-жении, т. е. в we/w-положении к атому кислорода карбонильной группы, что обусловливает возможность образования внутрикомплексных соединений с металлами и, следовательно, применения этих соединений в качестве протравных красителей.
Представителем гидроксиантрахиноновых красителей является Ализарин [(563); 1,2-дигидроксиантра-цендион-9,10] — один из старейших известных человеку органических красителей, давший название всей группе протравных антрахиноновых красителей.
Ализарин (563) в настоящее время получают щелочным плавлением 2-хлорантрахинона (561) или ан-трахинон-2-сульфокислоты (562); оба процесса ведут в присутствии окислителя (KNO3).
Процесс идет через промежуточное образование аниона 2-гидроксиантрахинона, который в одной из таутомерных форм подвергается нуклеофильной атаке и присоединяет второй гидроксид-ион.
Крашение Ализарином обычно проводят но алюми-нисво-кальциевой протраве. При этом с алюминием образуется внутрикомплексное соединение ярко-красного цвета с красивым синеватым оттенком («кумачовый цвет»), с кальцием за счет 0-гидроксигрупп происходит солеобразование. Алюминиево-кальциевое соединение Ализарина под названием Крапплак (564) применяется для изготовления художественных и полиграфических красок высокого качества.
С солями других металлов Ализарин образует соединения других цветов: с солями хрома — коричневое, с солями железа — фиолетовое и др.
Гидроксиантрахиноны не обладают достаточной кислотностью, необходимой для взаимодействия с белковыми волокнами, и поэтому их не окрашивают. Для крашения белковых волокон в красители необходимо ввести сульфогруппу.
При сульфировании Ализарина олеумом образуется краситель Хромовый красный ализариновый [(565); 1,2-дигидрокси-9,10-диоксоантрацен-3-сульфокислота]. Этот краситель окрашивает шерсть в алый цвет по алюминиевой протраве и в цвет бордо по хромовой. Окраски отличаются высокой устойчивостью к свету, стирке и валке.
116
Новый справочник химика и технолога
При нитровании Ализарина 62 % HNO3 в среде о-дихлорбензола образуется 3-нитроализарин — краситель Ализариновый оранжевый [(566); 1,2-дигидрокси-З-нитроантрацендион-9,10], образующий устойчивые окраски оранжевого цвета по алюминиевой протраве, фиолетового — по железной, красновато-оранжевого — по хромовой. При восстановлении 3-нитроализарина сульфидом натрия образуется 3-аминоализарин — краситель Ализариновый каштановый Б [567]; 3-амино-1,2-дигидроксиантрацендион-9,10], образующий красивые темно-коричневые («каштановые») окраски по хромовой протраве и цвета бордо — по алюминиевой. Нагревание 3-аминоализарина с глицерином в среде серной кислоты (в этих условиях из глицерина образуется акролеин) в присутствии 3-нитроализарина приводит к образованию нерастворимого в воде фталоилдигидроксихинолина (568). Это краситель Ализариновый синий, который применяется в виде растворимого бисульфитного производного под названием Ализариновый синий Бс [(569); бисульфитное производное образуется при взаимодействии красителя с водным раствором NaHSO3]. Краситель окрашивает хлопок, шерсть и шелк но хромовой протраве в синий цвет, устойчивый к свету, стирке, солевььм растворам (морской воде).
(566) (567)
(568) (569)
Из других гидроксипроизводных антрахинона имеют значение Хинизарин [(570); 1,4-дигидроксиантра-цендион-9,10] и Пурпурин [(577); 1,2,4-тригидро-ксиантрацендион-9,10]. Одно время оба соединения
применялись для крашения тканей (по алюминиевой протраве) в более глубокий красный цвет, чем Ализарин. В настоящее время и Хинизарин, и Пурпурин используются как исходные продукты в синтезе аминоантрахиноновых красителей.
Хинизарин (570) получают конденсацией фталевого ангидрида с 4-хлорфенолом в среде серной кислоты и в присутствии борной кислоты или конденсацией фталевого ангидрида с гидрохиноном в расплаве хлоридов алюминия и натрия. Пурпурин (571) получают окислением Ализарина диоксидом марганца в среде серной кислоты.
А мин о антрахиноновые красители
Аминоанграхиноны окрашены значительно глубже, чем соответствующие гидроксиантрахиноны, вследствие более сильного электронодонорного характера аминогрупп.
Аминоантрахиноны получают восстановлением соответствующих нитроантрахинонов или обменом имеющихся заместителей (главным образом атомов галогена, NO2, ОН” и SO3H групп) в ароматических ядрах. При обменных реакциях, имеющих гораздо большее практическое значение, используются более высокая подвижность заместителей в a-положениях, различия в подвижности заместителей в антрахиноновом ядре (обычно уменьшается в ряду: Вг > Cl > NO2 > ОН > > NH2) и последовательность вступления в реакции одинаковых заместителей, что позволяет получать несимметричные продукты.
Ассортимент аминоантрахиноновых красителей большой и разнообразный, имеются красители практически всех классов (по технической классификации).
Дисперсные аминоантрахиноновые красители. Не растворимые в воде амино- и аминогидроксиантрахиноны используются в качестве дисперсных красителей для крашения из водной суспензии гидрофобных волокон: ацетатных, полиэфирных, полиамидных, полиакрилонитрильных и др.
Цвет дисперсных красителей зависит от числа, характера и положения ЭД-заместителей, как это видно из табл. 4.3.6.
Ароматические соединения
777
Таблица 4.3.6
Дисперсные красители
X Y z Название красителя
nh2 CH3 H Дисперсный оранжевый
nh2 H OH Дисперсный красный 2С
nh2 OCH3 OH Дисперсный розовый Ж
nh2 OCH3 nh2 Дисперсный ярко-розовый
nh2 H nh2 Дисперсный фиолетовый К
nh2 conh2 HNCH3 Дисперсный синий 3
HNCH3 H hnc6h5 Дисперсный голубой
Краситель Дисперсный оранжевый (1-амино-2-метилантрацендион-9,10) получают нитрованием 2-ме-тилантрахинона с последующим восстановлением нитрогруппы сульфидом натрия.
Дисперсный красный 2С (1-амино-4-гидроксиантра-цендион-9,10) получают нитрованием 1 -гидроксиантрахинона в присутствии борной кислоты также с последующим восстановлением нитрогруппы.
Дисперсный розовый Ж (1-амино-4-гидрокси-2-метоксиантрацсндион-9,10) получают действием аммиака на Пурпурин (57/) с последующим метилированием 0-гидроксигруппы диметилсульфатом. Аналогичным образом получают Дисперсный ярко-розовый (1,4-диамино-2-метоксиантрацендион-9,10).
Дисперсный фиолетовый К [(572); 1,4-диамино-антрацендион-9,10)] получают аминированием хиниза-рина (570): хинизарин восстанавливают дитионитом натрия в лейкосоединение и нагревают с водным раствором аммиака; образовавшееся при этом лейкосоединение 1,4-диаминоантрахинона окисляют хлором в серной кислоте. При нитровании 1,4-диаминоантрахинона (572) получают краситель — Дисперсный фиолетовый 2С [(573); 1,4-диамино-5-нитроантрацендион-9,10)].
Особый интерес в качестве дисперсных красителей представляют соединения с гидроксиалкильными заместителями в аминогруппе, т. к. присутствие гидроксиал-кильных фрагментов облегчает диспергирование красителя и диффузию его в глубь волокна. К таким красителям относится Дисперсный синий К [(574); 1-(2-гидроксиэтил)амино-4-метиламиноантрацендион-9,10], имеющий важное практическое значение.
Дисперсный синий К получают при взаимодействии Хинизарина (570), предварительно переведенного в лейкосоединение действием дитионита натрия в щелочной среде, с метиламином и моноэтаноламином, при этом образуется смесь красителя и его лейкосоедине-ния, которое окисляют кислородом воздуха в краситель. В процессе реакции наряду с несимметричным красителем [(574); основной продукт] образуются два симметричных красителя (575) и (576).
Эту смесь без разделения выпускают под названием Дисперсный синий К. Подобные смеси близких по строению дисперсных красителей обычно образуют более ровные и интенсивные окраски, чем индивидуальные компоненты.
Для получения дисперсных красителей более глубокого цвета необходимо арилировать аминогруппы красителя. Так, краситель Дисперсный голубой [(577); 1 -метиламино-4-фениламиноантрацендион-9,10] образуется при взаимодействии 1-метиламино-4-бромантра-хинона с анилином.
Вышеназванные дисперсные красители не применяются для крашения ацетатных и полиэфирных волокон, поскольку они недостаточно устойчивы к выхлопным (дымовым) газам и не устойчивы к действию высоких температур. Это обусловлено тем, что ацетатное волокно активно адсорбирует из воздуха оксиды азота, содержащиеся в дымовых газах (особенно много их в атмосфере больших городов с интенсивным движением автотранспорта), которые вступают с молекулами красителей в реакции нитрозирования, диазотирования, окисления, в результате чего окраска на волокне обесцвечивается. Крашение полиэфирных
778
Новый справочник химика и технолога
волокон обычно проводят при высоких температурах (180-200 °C), и красители не должны возгоняться (сублимироваться) при таких температурах. Введение в молекулы красителей в o/w/о-положение к аминогруппе ЭА-заместителей: -SO2NH2, -CONH2, -CN, -CF3, -CHF2 и др. повышает и устойчивость красителей к действию дымовых газов, и температуру сублимации красителей. Такие красители, в основном синего и голубого цвета, имеют наибольшее практическое значение.
Представителем этой группы красителей является Дисперсный синий 3 [(579); 1-амино-9,10-диоксо-4-метиламиноантрацен-2-карбоксамид], образующий на ацетатном волокне устойчивые и красивые окраски. Краситель получают взаимодействием 1 -амино-4-бром-антрахинон-2-карбоновой кислоты (578) с метиламином (происходит замещение брома), затем карбоксильную группу последовательно переводят в хлоран-гидридную и карбамидную.
ствием 1-амино-2,4-дибром- или 1-амино-4-бром-2-хлорантрахинона с фенолом в щелочной среде; при этом вначале обменивается на гидроксигруппу атом брома в положении 4 (более подвижный), а затем атом брома в положении 2 или еще менее подвижный атом хлора — на фсноксигруппу.
Среди дисперсных антрахиноновых красителей есть ряд красителей, синтезированных специально для крашения полиэфирных волокон (в названиях таких красителей имеются буквы ПЭ). Они отличаются от прочих дисперсных красителей несколько более высокой молекулярной массой и наличием в молекулах таких групп, как -Br, -Cl, -NO2, -С6Н5, -ОН, -О-, -SO2N(Alk)2 и др.
Так, краситель Дисперсный темно-синий ПЭ [(581); 1,8-дигидрокси-4,5-диметиламиноантрацендион-9,10] получают нитрованием 1,8-дигидроксиантрахинона (580) с последующим восстановлением нитрогруппы сульфидом натрия и метилированием образующихся аминогрупп димсти л сульфатом.
(580)
(581)
Специальный краситель для полиэфирного волокна Дисперсный розовый 2С ПЭ [(582); 1-амино-4-гидрок-си-2-феноксиантрацендион-9,10)] получают взаимодей-
При бромировании красителя Дисперсного фиолетового 2С (573) образуется более глубоко окрашенный краситель — Дисперсный синий 4К ПЭ [(553); 1,4-ди-амино-2,3-дибром-5-нитроантрацендион-9,10].
Краситель Дисперсный синий ПЭ (585) получают нитрованием 1,5-дигидроксиантрахинона (584) с последующим восстановлением нитрогрупп сульфидом натрия и бромированием образовавшегося 4,8-диамино-1,5-дигидроксиантрахинона. Краситель представляет собой смесь моно- и дибромпроизводных с различным расположением атомов брома.
Для крашения полиэфирных волокон применяются также такие антрахиноновые красители, как Дисперсный синий светопрочный ПЭ (586) и Дисперсный голубой 3 ПЭ (557).
Ароматические соединения
779
ОН О он
Большие трудности возникают с получением дисперсных красителей черного цвета. Чтобы краситель интенсивно и достаточно равномерно поглощал световые лучи всей видимой части спектра, нужна сложная хромофорная система, как правило, перекрещивающаяся, что обычно затруднительно при малых размерах молекул. Красители с молекулами больших размеров для крашения полиэфирных и других синтетических волокон непригодны, т. к. они не могут проникать в чрезвычайно малые микропоры таких волокон. Поэтому для получения окрасок черного (и серого) цветов приходится применять смеси дисперсных красителей разного цвета, которые в сумме обеспечивают интенсивное поглощение по всей видимой части спектра. Обычно черные смесе-вые красители готовят смешением красителей желтого или оранжевого цвета (поглощение в коротковолновой части видимой области спектра), красного или розового
цвета (поглощение в средней части видимой области) и синего или сине-зеленого (голубого) цвета (поглощение в длинноволновой части видимой области).
Смеси могут составляться как из красителей одного класса (например, антрахиноновых), так и из красителей разных классов (антрахиноновых, азо- и др.). Необходимо только, чтобы компоненты смеси обладали приблизительно одинаковыми свойствами как в процессе крашения (одинаковая устойчивость к сублимации, одинаковая скорость диффузии в глубь волокна), так и в процессе использования окрашенного изделия (одинаковая устойчивость к свету, стирке, выхлопным газам и т. д.). Если последнее условие не соблюдается, в процессе эксплуатации изделия может произойти нежелательное изменение цвета. Например, если один из компонентов смеси (допустим, красный) обладает более низкой светостойкостью и «выцветает» раньше других, окраска станет зеленеть (смешение оставшихся желтого и синего цветов).
Катионные аминоантрахиноновые красители. Для получения катионных аминоантрахиноновых красителей применяют соединения, у которых в ониевое состояние переводят аминогруппы, связанные с алкильными остатками в боковых цепях, т. к. антрохино-ниламмониевые соли неустойчивы и не могут быть использованы в качестве катионных красителей.
Краситель Катионный фиолетовый 4С (589) получают взаимодействием 1-амино-2,4-дибромантрахинона с 1-амино-2-диэтиламиноэтаном и обработкой образующегося 1 -амино-2-бром-4-(2-диэтиламиноэтилами-но)антрахинона (588) диметилсульфатом. Аналогично из 4-бром-1-метиламиноантрахинона получают Катионный синий 4К (590).
О
NHCH3
О (590
CH3SO4
NH(CH2)2N(C2H5)2 сн3
Красители применяются для окрашивания полиакрилонитрильных волокон, окраски обладают хорошей устойчивостью к свету и мокрым обработкам.
Кислотные аминоантрахиноновые красители. Амино- и ариламиноантрахиноновые красители, содержащие сульфогруппу в антрахиноновом ядре или в арильном
заместителе, обладают кислотными свойствами и применяются для крашения шерсти во всех видах.
Для введения сульфогруппы в антрахиноновое ядро, дезактивированное карбонильными группами к реакциям электрофильного замещения, требуются жесткие условия (20% олеум, температура выше 100 °C), поэтому сульфирование проводят в качестве одной из первых стадий синтеза красителей. Если же сульфогруппу вводят в арильный фрагмент ариламиногруппы, то сульфирование протекает значительно легче (3-5% олеум, температура 15^40 °C) и является заключительной стадией получения красителей.
Из кислотных аминоантрахиноновых красителей, содержащих сульфогруппу в ядре антрахинона, следует
780
Новый справочник химика и технолога
назвать Кислотный синий антрахиноновый 3 (592), полученный М.А. Ильинским в 1891 г. и выпускавшийся в Германии под названием Ализарин сафирол Б, и Кислотный синий антрахиноновый (593). Оба красителя получают из 1,5-дигидроксиантрахинона.
1,5-Дигидроксиантрахинон (584) сульфируют 20% олеумом до 1,5-дигидроксиантрахинон-2,6-дисульфокислоты (591), затем нитруют, динитросоединсние восстанавливают и получают Кислотный синий антрахиноновый 3 [(592); 4,8-диамино-1,5-дигидрокси-9,10-диоксоантрацен-2,6-дисульфокислота]. Нагревая соединение (592) с 96% H2SO4 в присутствии борной кислоты, удаляют одну из сульфогрупп и получают краситель Кислотный синий антрахиноновый [(593); 4,8-диамино-1,5-дигидрокси-9,10-диоксоантрацен-2-сульфо-кислота].
Красители (592) и (593) окрашивают шерсть в яркосиний цвет с зеленоватым и красноватым оттенком соответственно. Окраски устойчивы к свету и к любым мокрым обработкам при крашении Кислотным синим антрахиноновым (593). Окраски, образованные Кислотным синим антрахиноновым 3 (592), неустойчивы к действию солевых растворов (в частности, к морской воде), т. к. две сульфогруппы при наличии большого числа гидрофильных заместителей сообщают красителю повышенную растворимость в таких растворах.
При арилировании одной из аминогрупп 1,4-диами-ноантрахинона цвет углубляется от фиолетового до голубого, при арилировании обеих аминогрупп — до зеленого. Краситель Кислотный чисто-голубой антрахиноновый 3 [(595); 1 -амино-9,10-диоксо-4-фенилами-ноантрацен-2-сульфокислота] получают взаимодействием бромаминовой кислоты [(594); 1-амино-4-бром-9,10-диоксоантрацен-2-сульфокислота] с водно-щелочным раствором анилина. Краситель образует на шерсти окраски, устойчивые к свету и стирке, но недостаточно устойчивые к валке.
(594) (595)
Более широкую цветовую гамму (от фиолетового до зеленого цвета) имеют ариламиноантрахиноновые красители, содержащие сульфогруппу в арильных остатках. Эти красители относятся к числу лучших красителей для шерсти, т. к. отличаются исключительной яркостью и чистотой оттенков, а также высокой устойчивостью окрасок к свету и мокрым обработкам. Некоторые из этих красителей окрашивают шерсть и шелк как обычные кислотные красители, другие красят из кислой ванны по хромовой протраве или с последующим хромированием. Их называют хромовыми красителями. Красители, содержащие длинные алкильные цепи (с числом атомов углерода от 4 до 20), окрашивают белковые волокна из нейтральной ванны и имеют в названии букву «Н».
Краситель Кислотный чисто-голубой антрахиноновый (597) получают конденсацией 1-амино-2,4-дибро-мантрахинона с 4-толуидином с последующим сульфированием образовавшегося 1 -амино-2-бром-4-(4-толи-ламино)антрахинона (596) 5% олеумом при 15-20 °C. Краситель находит широкое применение для крашения шерсти и шелка. Он образует окраски без зеленоватого оттенка, свойственного Кислотному чисто-голубому антрахиноновому 3, очень светостойкие и довольно устойчивые к стирке.
(596) (597)
Промежуточный продукт (596) выпускают под названием Жирорастворимый чисто-голубой антрахиноновый. Он применяется для окрашивания жиров, восков, резины, пластических масс и др.
Кислотный ярко-фиолетовый антрахиноновый 4К (599) получают взаимодействием 1,4-диамино-2,3-ди-хлорантрахинона (598) с фенолом в присутствии поташа с последующим сульфированием 2% олеумом образовавшегося дифеноксипроизводного антрахинона.
Ароматические соединения
781
(599)
Большое число ариламиноантрахиноновых красителей получают путем замещения гидроксигрупп в ядре антрахинона ариламиногруппами. Замещая одну гидроксигруппу, получают фиолетовые красители, две гидроксигруппы — зеленые красители.
Краситель Кислотный фиолетовый антрахиноновый (602) получают из Хинизарина (570), нагревая его с 4-толуидином в среде кипящего этанола (78-80 °C; при этой температуре замещается только одна гидроксильная группа Хинизарина) в присутствии небольшого количества цинковой пыли и соляной кислоты. Затем соединение (600) сульфируют 2% олеумом и получают краситель (602), образующий на шерсти и шелке окраски, устойчивые к свету; хромированием на волокне повышают устойчивость окрасок к стирке и валке.
Краситель Хромовый зеленый антрахиноновый (603) получают из тех же исходных продуктов, но реакцию замещения ведут в присутствии борной кислоты (с добавкой соляной кислоты и цинковой пыли) при 100 °C. В этих условиях происходит замещение двух гидроксигрупп в молекуле Хинизарина. Образовавшийся 1,4-бис(4-толиламино)антрахинон (601) сульфируют 3% олеумом.
Хромовый зеленый антрахиноновый (603) образует очень яркие зеленые окраски, устойчивые к свету, стирке и валке, применяется для крашения шерсти, шелка, кожи, а также для приготовления лаков. Не-сульфированный промежуточный продукт (601) под названием Жирорастворимый зеленый антрахиноновый применяется для крашения жиров, восков, пластических масс и т. п., а под названием Пигмент зеленый
782
Новый справочник химика и технолога
антрахиноновый А — для крашения ацетатного волокна в массе.
Взаимодействием Хинизарина с мезидином и последующим сульфированием получают краситель Кислотный ярко-синий антрахиноновый {604). Более высокий цвет этого красителя по сравнению с Хромовым зеленым антрахиноновым объясняется наличием в его молекуле метильных групп, создающих пространственные затруднения и выводящих ариламиногруппы из плоскости антрахинонового ядра, нарушая их взаимодействие с карбонильными группами. Эти же метильные группы повышает сродство красителя к белковым волокнам, что благоприятно сказывается на устойчивости окрасок к мокрым обработкам и валке.
(604)
Для крашения шерсти в цвета от серого до черного часто применяют краситель Хромовый сине-черный антрахиноновый С (605). Краситель получают взаимодействием Пурпурина (571) с анилином в присутствии борной кислоты с последующим сульфированием продукта замещения 100% Н28О4.Вместо анилина в реакцию можно вводить сульфаниловую кислоту 4-НОз8С6Н4МН2, в этом случае нс нужно сульфировать
продукт реакции.
Хромовый сине-черный антрахиноновый С окрашивает шерсть и шелк в красновато-фиолетовый цвет, углубляющийся в результате комплексообразования с хромом (крашение по хромовой протраве) до черного с синеватым оттенком.
Карболаны. Недостатком многих ярких и светостойких аминоантрахиноновых красителей является
относительно невысокая устойчивость к мокрым обработкам и валке. Оказалось, что введение в молекулы этих красителей длинных «тяжелых» алкильных остатков (С4-С20) заметно повышает их сродство к белковому волокну (около 1,7 кДж на каждую -СН2-группу), вследствие чего окраски становятся устойчивее к валке и мокрым обработкам. Особенно ценно то, что такие красители могут окрашивать белковые волокна из слабокислой, почти нейтральной ванны и, следовательно, пригодны для крашения полушерстяных тканей. Эти красители получили название карболанов, однако отечественной анилинокрасочной промышленностью они выпускаются под названием «Кислотные антрахиноновые Н». Под названием «карболаны» их выпускает английская фирма «1С1».
Алкильный остаток может быть связан с молекулой красителя любым способом: через атомы углерода антрахинонового ядра или ариламиногруппы, через атомы кислорода и т. д. Если алкильный остаток содержит небольшое число углеродных атомов (например, четыре), то вводят не менее двух таких остатков.
Существует ряд способов получения карболанов. Алкильную цепь можно ввести заменой атома галогена или сульфогруппы в молекуле соответствующего производного антрахинона взаимодействием с высшими спиртами или алкилзамещенными фенолами. Таким способом получают, например, Кислотный фиолетовый антрахиноновый НК (606), замещая в Кислотном чистоголубом антрахиноновом 3 (595) сульфогруппу смесью высших спиртов и вновь сульфируя продукт реакции.
Кислотный фиолетовый антрахиноновый Н4К (607) получают из 1,4-диамино-2,3-дихлорантрахинона (598) и 4-ти£>ети-бутилфенола (с последующим сульфированием) по такой же схеме, по которой получают краситель Кислотный ярко-фиолетовый антрахиноновый 4К (599).
Ароматические соединения
783
По другому способу замещенные антрахиноны ара-минируют алкиланилинами. Такие ценные красители, как Кислотный зеленый антрахиноновый Н2С (608) и Кислотный ярко-синий антрахиноновый Н4К (609) получают аналогично Хромовому зеленому антрахиноновому (603) из Хинизарина и 4-бутиланилина или 2-метил-4-бутил-6-броманилина соответственно с последующим сульфированием оснований красителей. Повышение цвета второго красителя является результатом пространственных затруднений, создаваемых оршо-распо-ложенными заместителями (СН3, Вг).
Аналогичные по свойствам красители, способные окрашивать белковые волокна из нейтральных ванн, образуются при увеличении молекулярной массы красителя. Примером такого красителя является голубой кислотный краситель (610), образующийся при взаимодействии 2 молей бромаминовой кислоты (594) с 1 молем 4,4-диаминодифенилметана.
Активные аминоантрахиноновые красители. Самыми распространенными активными антрахиноновыми красителями являются монохлортриазиновые, дихлортриазиновые и винилсульфоновые. Для их синтеза большое значение имеет бромаминовая кислота. На ее основе получают активные красители фиолетового, синего, голубого и зеленого цветов.
Дихлортриазиновый краситель Активный ярко-голубой КХ (612) получают взаимодействием бром
аминовой кислоты (594) с 2,4-диаминобензолсульфо-кислотой с последующим ацилированием образовавшейся 1 -амино-4-(3-амино-4-сульфофениламино)антра-хинон-2-сульфокислоты (611) цианурхлоридом (226) при 0-5 °C.
Активный ярко-голубой КХ, как и все дихлортриазиновые красители, обладает высокой активностью и взаимодействует с целлюлозой уже при 20 °C в слабощелочной среде. Окраски отличаются высокой устойчивостью к свету и мокрым обработкам.
Замещая второй активный атом хлора в реакционной группировке триазиновых красителей ариламино-фуппой, получают монохлортриазиновые красители. Так, при взаимодействии красителя (612) с метанило-вой кислотой при 40 °C образуется монохлортриазиновый краситель Активный ярко-голубой К (613).
Замещение второго атома хлора в триазиновом кольце протекает значительно медленнее замещения первого атома и при более высокой температуре.
Если при синтезе монохлортриазиновых красителей вместо бесцветного соединения типа метаниловой кислоты взять другой краситель, в молекуле которого имеются способные ацилироваться заместители, цвет образовавшегося монохлортриазинового красителя будет соответствовать цвету смеси обоих исходных красителей, т. к. триазиновое кольцо не позволяет создать единую хромофорную систему. Например, монохлортриазиновый краситель (614) имеет зеленый цвет, т. к. к триазиновому кольцу присоединены голубой антрахиноновый краситель (613) и желтый азокраситель.
Винилсульфоновые активные красители содержат Р-сульфатоэтилсульфонильную группу (-SO2(CH2)2OSO3Na), превращающуюся в процессе крашения под действием щелочи в винилсульфонильную группу ( SO2CH CH2). которая взаимодействует с окрашиваемым веществом (см. уравнение (4.3.16)).
Винилсульфоновый краситель Активный ярко-голубой 2КТ (616) получают взаимодействием бромаминовой кислоты (594) с гидрохлоридом 3-(2-гидрокси-этилсульфонил)анилина с последующей этерификацией гидроксигруппы соединения (615) 3-5% олеумом.
Активный ярко-голубой 2КТ, как и все винилсульфоновые красители, окрашивает волокнистые целлюлозные материалы при 60 °C (в названии такого красителя имеется буква Т). Винилсульфоновые красители менее активно взаимодействуют с волокном, чем дихлортриазиновые, но более активно, чем монохлортриазиновые.
Окраски, образованные активными антрахиноновыми красителями на целлюлозных волокнах, отличаются повышенной устойчивостью к действию света и к мокрым обработкам. В отличие от активных азокрасителей, они не вытравляются вытравными составами, содержащими восстановители; поэтому их нельзя использовать для крашения под вытравную печать. Не рекомендуется также применять эти красители для пестротканых изделий, подвергаемых отбеливанию из-за невысокой устойчивости окрасок к действию активного хлора.
784
Новый справочник химика и технолога
Многие активные триазиновые и винилсульфоновые красители могут окрашивать не только целлюлозные, но и белковые, и полиамидные волокна. Однако для крашения этих волокон удобнее приметать специальные активные красители.
Активные красители для шерсти и натурального шелка содержат такие активные группировки, как а-бром-акрилоиламино- (-NHCOCBr=CH2) или хлорацетиламино- (-NHCOCH2C1), а для полиамидных волокон — такие, как 2-гидрокси-З-хлорпропиламиногруппа (-NHCH2CHOHCH2C1). В процессе крашения подвижные атомы галогена активных группировок реагируют с аминогруппами белковых и полиамидных волокон. Примером активного красителя для шерсти является Цибалан ярко-голубой ГЛ (677), для полиамидных волокон — Процинайл синий Р (618), сочетающий свойства дисперсного и активного красителей.
О NHCHrCHCH2Cl (618)
Ароматические соединения
785
Прямые аминоантрахиноновые красители. Если краситель обладает достаточно высоким сродством к целлюлозе, он может непосредственно («прямо»), т. е. без участия протрав, окрашивать целлюлозные волокна. Увеличению сродства к целлюлозе способствуют плоская линейная форма молекул красителя, облегчающая проявление сил межмолекулярного взаимодействия с плоской линейной молекулой целлюлозы, и наличие заместителей, обусловливающих возможность образования межмолекулярных водородных связей с гидроксигруппами целлюлозы. Одним из лучших заместителей с такими свойствами является амидная группа NHCO. Межатомные расстояния в этой группе таковы, что атомы кислорода и водорода легко взаимодействуют с гидроксигруппами молекулы целлюлозы, образуя водородные связи.
Н- • -O=CR'
I I
Целл—О' ’' H-NR
Водородные связи — это главные силы, которые удерживают на целлюлозном волокне красители, не закрепляемые протравами. Прочность водородной связи (21-30 кДж/моль) значительно превосходит ван-дер-ваальсовские силы обычного межмолекулярного взаимодействия (2-5,5 кДж/моль).
При ацилировании 1 -амино-4-(4-аминофенилами-но)антрахинон-2-сульфокислоты [(6/9); получена взаимодействием бромаминовой кислоты {594) с А-ацетил-я-фснилендиамином с последующим омылением ацил-аминшруппы в щелочной среде] дихлорангидридом фумаровой кислоты в мольном соотношении 2 : 1 образуется краситель {620), молекулы которого имеют значительные линейные размеры и содержат две амидные группы и два плоских антрахиноновых кольца. Все это обеспечивает ему настолько высокое сродство к целлюлозе, что краситель может применяться в качестве прямого.
Прямые антрахиноновые красители образуют окраски высокого качества, но применяются мало, т. к. они значительно дороже прямых красителей других классов.
{620)
Ациламино антрахиноновые красители
Гидрокси- и аминопроизводные антрахинона способны восстанавливаться с образованием растворимых лейкосоединений. Однако сродство этих лейкосоедине-ний к волокнам столь мало, что они не выбираются волокном из раствора или выбираются очень слабо. Для использования аминоантрахинонов в качестве кубовых красителей в их молекулы необходимо ввести заместители, повышающие сродство к целлюлозе, в частности, амидные группы. Таким образом, наиболее простой путь к получению кубовых антрахиноновых красителей — это ацилирование аминоантрахинонов.
Практически ацилирование аминоантрахинонов осуществляют действием хлорангидридов кислот (бензойной, изофталевой, терефталевой дифенилдикарбо-новой-4,4' и др.) в среде высококипящих органических растворителей (нитробензол, о-дихлорбензол, трихлор
бензол). Например, кубовые красители {621)-{624) получают ацилированием производных 1-аминоантрахинона дихлорангидридом изофталевой кислоты.
Окраски, образуемые этими ациламиноантрахиноновыми красителями (табл. 4.3.7), имеют недостаточную устойчивость к свету (4-5 баллов по восьмибалльной шкале). Кроме того, красители желтого и оранжевого цветов ускоряют фотохимическое разрушение целлюлозного волокна.
Таблица 4.3.7
Ациламиноантрахиноновые красители
№ Название красителя X X' Y Y'
621 Кубовый желтый 23Х Н н н Н
622 Кубовый желтый Н н NHCOC6H5 NHCOC6H5
623 Кубовый красно-оранжевый NHCOC6H5 NHCOC6H5 н н
624 Индантреновый оранжевый ГГ nhcoc6h5 н н NHCOC6H5
786
Новый справочник химика и технолога
При использовании в качестве ацилирующего агента хлористого цианура получают кубовые антрахиноновые красители, образующие устойчивые окраски и не ускоряющие разрушение волокна под действием света. Так, при взаимодействии 1-аминоантрахинона с циа-нурхлоридом в среде кипящего фенола получают краситель Кубовый желтый 2КХ (627). Более удобным способом синтеза этого красителя (как и других кубовых красителей, содержащих триазиновое кольцо)
является взаимодействие галогенантрахинонов (625) с меламином [(626); 2,4,6-триамино-1,3,5-триазин] в присутствии меди или ее галогенидов. Данный способ позволяет избежать использования дорогого и токсичного цианурхлорида, заменив его дешевым и нетоксичным меламином. В частности, Кубовый желтый 2КХ (627) получают взаимодействием 1-хлорантрахи-нона с меламином в присутствии Cui в нитробензоле при 200 °C.
Антримиды
В молекулах антримидов два или более остатков антрахинона связаны иминогруппами. По числу связанных остатков антрахинона различают ди-, три- и тетра-антримиды.
Цвет антримидов зависит от того, какими положениями связаны остатки антрахинонов в молекуле красителя. Если антрахиноновые кольца связаны иминогруппой по положениям 1,1', то красители окрашены глубже, чем в том случае, когда кольца связаны по положениям 2,2'. Обычно антримиды имеют оранжевые, красные и бордовые цвета.
Антримиды не растворимы в воде, но продукты их восстановления (лейкосоединения) растворимы в щелочных средах. Лейкосоединения большинства антримидов обладают сродством к целлюлозному волокну, и эти соединения можно использовать в качестве кубовых красителей. Образуемые ими окраски обладают высокой устойчивостью к свету (6-8 по восьмибалльной шкале) и прочим воздействиям (4-5 по пятибалльной шкале), однако недостаточно яркие, и поэтому данные кубовые красители не имеют преимуществ перед кубовыми красителями других классов того же цвета. В связи с этим антримиды обычно используют как промежуточные продукты для получения более сложных кубовых красителей — производных карбазола (карба-золированных антримидов или фталоилкарбазолов).
Общий способ получения антримидов заключается во взаимодействии аминоантрахинонов с галогенантра-хинонами в среде высококипящих растворителей (нит
робензол) в присутствии щелочных агентов для связь вания выделяющегося галогенводорода (сода, ацет< натрия) и порошка меди или ее соединений (катализ; тор) при высокой температуре (обычно выше 200 °C Так, при взаимодействии 1,4-диаминоантрахиноь (572) с 1-хлорантрахиноном (625) получают триантрь мид (628), используемый для синтеза красителя Кубе вого коричневого СК (632).
(628)
Фталоилкарбазолы (карбазолированые антри миды). Эти красители (630) можно рассматривать Kai продукты конденсации карбазола (629) с двумя моле кулами фталевого ангидрида.
Исходными продуктами для получения фталоилкар базолов (630) являются антримиды (631), у которых ] процессе реакции происходит отщепление двух атомо] водорода в положениях 2,2' и образование гетероцикл; (пиррола). Так как процесс замыкания гетероцикла на зывается карбазолированием, фталоилкарбазолы пазы вают карбазолированными антримидами.
Ароматические соединения
787
коричневый СК (632), образующий на хлопке исключительно устойчивые окраски (устойчивость к свету — 7 по восьмибалльной шкале, к стирке и хлору — 5 по пятибалльной).
Аналогичным образом из триантримида (продукта взаимодействия 1,5-дихлорантрахинона с 1-аминоантрахиноном) получают краситель Кубовый желтый 4К (633), изомерный красителю (632). Более высокая окраска красителя (633) объясняется тем, что группы NH находятся в разных кольцах молекулы антрахинона.
При образовании новой связи между антрахиноновыми кольцами молекула красителя становится строго плоскостной, т. к. исчезает возможность свободного вращения антрахиноновых колец по связи ~=С— Это приводит к резкому возрастанию сродства лейко-соединений фталоилкарбазолов к целлюлозному волокну по сравнению с исходными антримидами. Так сродство лейкосоединения антримида (631) к целлюлозе настолько мало, что соединение не может применяться в качестве кубового красителя, тогда как фталоилкарба-зол (630) является типичным кубовым красителем и выпускается под названием Индантреновый желтый.
Существует несколько способов карбазолирования антримидов, в частности на условия синтеза большое значение оказывает наличие в молекуле антримида ацил аминогрупп.
Карбазолирование незамещенных (не содержащих ациламиногрупп) антримидов проводят чаще всего сплавлением с хлоридом алюминия обычно с добавкой NaCl. Поскольку выделяющийся при карбазолирова-нии водород восстанавливает краситель с образованием продуктов, не являющихся лейкосоединениями (восстановление по карбонильным группам затруднено комплексообразованием с хлоридом алюминия: ^С=О ... А1С13, полученный продукт реакции окисляют Na2Cr2O7 в кислой среде или NaOCl в щелочной среде. Именно так получают краситель (630).
В некоторых случаях карбазолирование с помощью хлорида алюминия проводят в среде органических растворителей, что позволяет снизить температуру реакции. Так, при нагревании триантримида (628) с хлоридом алюминия в среде пиридиновых оснований при 135 °C с последующим окислением образовавшегося продукта гипохлоритом получают краситель Кубовый
(633)
При взаимодействии 1,4,5-трихлорантрахинона (1 моль) с 1-аминоантрахиноном (3 моль) в присутствии соединений меди и карбазолированием образовавшегося тетраантримида — 1,4,5-три[(антрахинонил-1 )амино]антрахинона в расплаве А1С13 и NaCl с последующим окислением продукта реакции получают очень ценный краситель Кубовый коричневый 53 (634).
Карбазолирование антримидов, содержащих ациламиногруппу, происходит значительно легче — взаимодействием с концентрированной серной кислотой в течение нескольких часов при 30 °C с последующим окислением продукта реакции NaC103 или Na2Cr2O7 в разбавленной H2SO4. Этим способом получают ценные красители для хлопка Кубовый оливковый К (636), Кубовый золотисто-оранжевый 2Ж (637), Кубовый коричневый К (638). Все три красителя являются изомерами, отличающимися друг от друга только различным расположением бензоиламиногрупп; по этой же причине красители имеют различные цвета.
Кубовый оливковый К (636) является продуктом карбазолирования другого кубового красителя — Алго-левого серого К (635). Одним из способов получения Алголевого серого К является нитрование диантримида (631) с последующим восстановлением нитрогрупп сульфидом натрия и бензоилированием образовавшегося 4,4'-диаминоантримида (639).
788
Новый справочник химика и технолога
(634)
(635)
Для Кубового золотисто-оранжевого 2Ж (637) исходный антримид получают взаимодействием 1-амино-5-бензоиламиноантрахинона с 5-бензоиламино-1-хлор-антрахиноном.
(637)
Карбазолированые антримиды, содержащие ациламиногруппу, образуют на хлопке окраски, очень устойчивые к свету, мокрым обработкам, хлору и поту. Устойчивость окрасок возрастает с накоплением в молекуле красителей антрахиноновых ядер, поэтому в некоторых случаях в качестве ацилирующего агента применяют хлорангидрид антрахинонкарбоновой кислоты, получаемый действием на кислоту тионилхло-рида. Так, краситель Кубовый оливковый 2Ж (642),
образующий на хлопке исключительно устойчивые ко всем воздействиям окраски, получают ацилированием антримида (639) хлорангидридом антрахинон-2-карбо-новой кислоты (640) с последующим карбазолирова-нием диацильного производного (641) в серной кислоте и окислением образующегося при этом продукта КС1О3.
Кубовый коричневый К (638) получают при карба-золировании антримида из 1-амино-4-бензоиламино-антрахинона и 5-бензоиламино-1-хлорантрахинона.
При карбазолировании ациламиноантрахинонов, содержащих фениламиногруппы, в среде серной кислоты одновременно с замыканием гетероцикла возможно сульфирование бензольных ядер. В результате образуются кубовые красители, лейкосоединения которых значительно лучше растворяются и процесс получения красильного «куба» упрощается. Однако главная роль сульфогрупп заключается в том, что своим отрицательным зарядом они снижают сродство лейкосоединений красителей к целлюлозе, которая при кубовом крашении (т. е. в щелочной среде) приобретает отрицательный заряд. Вследствие этого выбирание лейкосоединения из «куба» замедляется и одновременно его облегчается диффузия в глубь волокна; окраски получаются более ровными и устойчивыми к трению.
Ценные свойства карбазолированных антримидов побудили распространить этот метод получения кубовых красителей на иные амины, также часто называемые антримидами. Так, при взаимодействии Кубового ярко-оранжевого КХ (643) с 1-амино-4-бензоиламино-антрахиноном (644) с последующим карбазолировани-ем образовавшегося антримида (645) действием H2SO4 при 30 °C получают краситель Кубовый серый С (646). Этот краситель образует окраски, устойчивые ко всем видам воздействия; он особенно пригоден для окрашивания плотных тканей, т. к. обладает способностью хорошо диффундировать в толщу материала.
При взаимодействии 1,Г-дихлорацедиантрона (647) с 1-амино-5-бензоиламиноантрахиноном (648) с последующим карбазолированием антримида получают краситель Кубовый коричневый 4Ж (649), образующий очень светостойкие окраски.
Ароматические соединения
789
790
Новый справочник химика и технолога
Если вместо 1-амино-5-бензоиламиноантрахинона использовать его изомер — 1 -амино-4-бензоилантрахи-нон (644), аналогичным способом можно получить другой краситель — Кубовый коричневый 3 (650), образующий окраски, устойчивые ко всем воздействиям.
Большое практическое значение имеет краситель Кубовый темно-зеленый Ж (653). Он образуется при взаимодействии 3-бромбензантрона (651) с 1-аминоантрахиноном. Вначале в присутствии соды и оксида меди происходит замещение брома на аминогруппу и образование антрахинонилбензантрониламина (652), затем замыкание гетероцикла. Гетероцикл замыкается при нагревании соединения (652) с КОН в кипящем изобутиловом спирте (так называемая «изобутанольная плавка»). Этот процесс аналогичен карбазолированию; на производстве он так и называется, хотя в данном случае образуется не пятичленный цикл, характерный для карбазола, а шестичленный.
Кубовый темно-зеленый Ж применяется для крашения хлопка, льна, вискозного волокна (в том числе для крашения вискозы в массе). Окраски, образованные этим красителем, характеризуются высшей устойчивостью к свету (8 по восьмибалльной шкале), хорошей устойчивостью к стирке и хлору (4-5 по пятибалльной шкале).
На практике часто используется краситель Кубовый серый 23 (654). Краситель образуется при изобутаноль-ной плавке антримида, полученного из 3,9-дибром-бензантрона и 1-аминоантрахинона. Краситель образует на целлюлозных волокнах окраски, высокоустойчивые к различным воздействиям.
Ароматические соединения
791
Антрахинонилоксадиазоловые красители
К этой группе красителей относятся производные антрахинона, связанные с системой 1,3,4-оксадиазола и находящиеся с ней в сопряжении, вследствие чего цвет антрахинонилоксадиазоловых красителей глубже, чем
цвет соответствующих антрахиноновых производных. Плоское кольцо оксадиазола с тремя гетероатомами, способными участвовать в образовании водородных связей, сообщает лейкосоединениям антрахинонилок-садиазолов сродство к целлюлозе. Поэтому антрахинонилоксадиазоловые красители могут использоваться в качестве кубовых.
Производные оксадиазола получают взаимодействием хлорангидридов соответствующих карбоновых кислот с гидразином и замыканием в образующихся гидразидах оксадиазолового цикла дегидратацией под действием водоотнимающих средств.
При получении Кубового бордо С (658) гидразин, взаимодействуя с хлорангидридом 1-нитроантрахинон-2-карбоновой кислоты (655), образует диацилгидразид (656), который в среде олеума превращается в 2,5-бис-(1-нитроантрахинонил-2)-1,3,4-оксадиазол (657). Затем в автоклаве при взаимодействии 2,5-дизамещенного оксадиазола с водным раствором аммиака нитрогруппы замещаются аминогруппами, и образуется краситель (658).
Кубовый бордо С окрашивает хлопок в яркий бордовый цвет, устойчивый к свету, мокрым обработкам, хлору и трению. Краситель применяют также для печатания по хлопку и для крашения вискозы в массе. Высокая светостойкость красителя и повышенное сродство к волокну объясняется тем, что аминогруппы красителя, находящиеся в о/?/ио-положениях к кольцу оксадиазола, образуют водородные связи с атомами азота гетероцикла, которые стабилизируют краситель к фотоокислительным процессам и препятствуют нарушению плоскостности молекулы.
Для получения красителей более глубокого цвета в положение 4 антрахинонового ядра вводят амино- или ациламиногруппы. Например, краситель Кубовый синий 3 (659) содержит бензоиламиногруппы. Такие красители, как Кубовый синий 3, образуют на целлюлозных волокнах окраски, обладающие высокой устойчивостью ко всем видам воздействия.
Меры предосторожности в производстве антрахиноновых красителей
Производство антрахиноновых красителей связано с использованием и получением ряда токсичных и огнеопасных веществ. Токсичны многие производные антрахинона, особенно аминоантрахиноны, поэтому необходимо исключить возможность попадания их на тело и одежду работающих. В виде пыли вместе с воздухом они могут попадать в легкие рабочих. Поэтому особое внимание следует обращать на нерастворимые (лишенные сульфогрупп) производные, которые не могут быстро выводиться из организма и поэтому особенно опасны.
(659)
792
Новый справочник химика и технолога
Ряд процессов синтеза антрахиноновых красителей протекает при высоких температурах с участием едких щелочей, а также ядовитых и огнеопасных (нитробензол и др.) веществ. Особенно тщательно надо соблюдать меры безопасности при работе с гидразином, который вызывает тяжелые отравления при попадании в организм и обладает кумулятивным действием. В производстве некоторых ациламиноантрахиноновых красителей в значительных количествах выделяется хлороводород — ядовитый газ, раздражающий слизистые оболочки. Соблюдение всех мер предосторожности, герметизация аппаратуры (в необходимых случаях), поддержание в должном порядке приточно-вытяжной вентиляции являются непременными условиями проведения таких процессов.
При работе с концентрированной уксусной кислотой должны быть созданы условия, исключающие возможность попадания ее на тело работающих. Концентрированная уксусная кислота быстро впитывается белковыми веществами кожи и мышечной ткани и вызывает болезненные и труднозаживающие ожоги и язвы.
Самые строгие меры предосторожности следует соблюдать при работе с активными красителями, исходными веществами для них и промежуточными продуктами, образующимися в процессе их синтеза. Соединения с активными группами (цианурхлорид, моно- и дихлортриазиновые красители и другие продукты взаимодействия цианурхлорида с различными соединениями, сохраняющие активные атомы галогенов; красители и промежуточные продукты с винилсульфоно-выми или сульфатоэтильными группами, а также другими активными группами) опасны своей способностью химически взаимодействовать с белковыми веществами. Результатом этого взаимодействия могут быть как простое раздражение кожи и слизистых оболочек, так и более серьезные заболевания. Поскольку биологическое действие активных красителей, компонентов для их производства и промежуточных продуктов изучено недостаточно, к ним следует относиться как к потенциально опасным веществам. При работе с ними должны быть созданы условия, исключающие возможность попадания веществ на тело и спецодежду работающих, а также накопления их в виде пыли и грязи в производственных помещениях.
4.3.5.9. Антрахиноногетероциклические красители
Антрахиноногетероциклические красители
► Кубовые (желтые, красные, фиолетовые, синие, бирюзовые, коричневые)
► Кубозоли (желтые, красные, фиолетовые, синие, бирюзовые, коричневые)
► Пигменты (синие)
Антрахиноногетероциклические красители можно рассматривать как продукты конденсации антрахинона с гетероциклическими системами. Антрахиноновый фрагмент в молекулах этих красителей обусловливает их способность восстанавливаться в лейкосоединения, что при плоскостном строении молекулы и наличии гетероатомов, способных участвовать в образовании межмолекулярных водородных связей, сообщает лейко-соединениям сродство к целлюлозе. Поэтому антрахиноногетероциклические красители могут применяться в качестве кубовых (фактически все практически важные антрахиноногетероциклические красители и являются кубовыми). Особенно велико сродство к целлюлозе у красителей, в молекулах которых гетероциклы конденсированы с антрахиноновым ядром в положениях 2,3 (т. е. линейно), т. к. в этом случае молекулы имеют большие линейные размеры. В случае ангулярно конденсированных систем (в положениях 1,2) для повышения сродства к целлюлозе обычно увеличивают размеры молекул путем введения двух гетероциклов, конденсированных с антрахиноновым ядром, или двух антрахиноновых ядер, конденсированных с гетероциклом.
В зависимости от природы гетероцикла, конденсированного с антрахиноном, красители делятся на ряд групп.
Антраазоловые {антрахиноназоловые} красители
В основе молекул анграазоловых красителей лежат гетероциклические системы, образованные пятичленными гетероциклами (660): оксазолом (X = О), тиазолом (X = S) или имидазолом (X = NH), конденсированными с ядром антрахинона в положениях 2,3 или 1,2. По современной номенклатуре соответствующие гетероциклические системы называются антра[2,3-</]азол-дионы-5,10 (661) и антра[1,2-</]азолдионы-6,11 (662), т. к. антрахинон рассматривается как производное антрацена. Отсюда название красителей — антраазоловые, однако на практике обычно используется второе (традиционное) название — антрахиноназоловые.
(66Г> (662)
Практическое значение в настоящее время имеют красители, содержащие кольца оксазола (X = О) и тиазола (X = S).
Антрахиноноксазоловые красители. В основе молекул этих красителей лежит гетероциклическая система антра[2,3-</]оксазолдиона-5,10 (66Г, Х—О). Исходными соединениями для получения антрахинонокса-золовых красителей являются производные 2-амино-З-гидроксиантрахинона (663).
Ароматические соединения
793
Наибольшее практическое значение имеет Кубовый красный С (666), который получают взаимодействием 2-амино-З-гидроксиантрахинона [(663); 2-амино-З-гид-роксиантрацендион-9,10] с хлорангидридом 1-нитро-антрахинон-2-карбоновой кислоты (655) с последующей циклизацией продукта ацилирования (664) в среде сер
ной кислоты и замещением нитрогруппы в 2-(1-нитро-антрахинонил-2)антраоксазолдионе-5,10 (665) аминогруппой.
Кубовый красный С применяется для крашения хлопка, льна и вискозного волокна. Окраски устойчивы ко всем видам воздействия.
(663)
Антрахинонотиазоловые красители. В основе молекул этих красителей лежат гетероциклические системы антра[2,3-б/]тиазолдиона-5,10 (661; X = S) и антра-[1,2-</]тиазолдиона-6,11 (662; X = S). Получают антрахинонотиазоловые красители дегидратацией 2-ацил-амино-3-меркаптозамещенных антрахинона в среде концентрированной серной кислоты, при этом происходит замыкание тиазолового цикла.
Большое практическое значение имеет краситель Кубовый красно-фиолетовый Ж (670). Его получают из 2-амино-З-хлорантрахинона (667) и хлорангидрида 1-нитроантрахинон-2-карбоновой кислоты (655). Нитрогруппу в ацильном производном (668) замещают ами
ногруппой действием 15% раствора NH3 в автоклаве, затем замещают хлор меркаптогруппой действием ИагБ и замыкают тиазоловое кольцо, нагревая соединение (669) в серной кислоте.
Кубовый красно-фиолетовый Ж образует на целлюлозных волокнах окраски, отличающиеся высокой светостойкостью (7 по восьмибалльной шкале). При введении в краситель второй аминогруппы в «^«-положение к имеющейся цвет углубляется. Из этих красителей практически значимым является Индантре-новый голубой ЦЛБ (671); его получают ацилированием аминогруппы в положении 4 л/-трифторметилбензоил-хлоридом.
(669)
(668)
794
Новый справочник химика и технолога
Представителем антрахинонотиазоловых красителей, в которых тетероцикл конденсирован с антрахиноновым ядром ангулярно (в положениях 1,2) является Цибанон желтый ГЦ (672). Краситель получают осернением продукта взаимодействия 2,6-диаминоантра-хинона с трихлорфенилметаном.
Нафтоакридиновые (антрахинонопиридоновые или фталоилакридоновые) красители
Основой молекул антрахинонопиридоновых красителей является гетероциклическая система (675), полученная в результате присоединения бензопиридона-4 (675; хинолона-4) к ядру антрахинона. Это соединение также можно рассматривать как продукт присоединения нафтохинона-1,4 или остатка фталевой кислоты к ядру акридона-9 (674); отсюда другие названия красителей данной группы. Название соединения (675) по современной номенклатуре — 14/7-нафто[2,3-с]акридин-трион-5,8,13, а современное название красителей данной группы — нафтоакридиновые. Два других названия, обычно используемые на практике, антрахи-нонопиридоновые и фталоилакридоновые являются традиционными.
В молекулах всех имеющих практическое значение нафтоакридиновых красителей ^NH-группа гетероцикла связана с антрахиноновым ядром в а-поло-жении, т. к. только в этом случае образуется водородная связь с карбонильной группой антрахинона, усиливающая устойчивость окрасок к свету и другим воздействиям. Цвет этих красителей практически не отличается от цвета соответствующих ариламиноантрахинонов.
Наличие в молекуле одного бензопиридонового остатка, ангулярно конденсированного с антрахиноновым ядром, недостаточно для того, чтобы соединение можно было применять в качестве кубового красителя. Сродство к волокну повышают введением атомов галогена, амидных групп или присоединением к антрахиноновому ядру двух бснзопиридоновых фрагментов.
Исходными продуктами для получения нафтоакридиновых красителей являются а-ариламиноантрахино-ны, имеющие в opwo-положении к -NH-группе карбоксильную или метильную группу. В первом случае замыкание пиридинового цикла осуществляется дегидратацией, во втором — хлорированием и последующим гидролизом в щелочной среде. При хлорировании атомы хлора вступают не только в метильную группу, но и в арильный остаток, а также в антрахиноновое ядро, связанное с ариламиногруппой. Это повышает сродство красителей к волокну и делает более яркими образуемые окраски.
Так, Кубовый бирюзовый ЗХ (678) получают на основе 1-(2-карбоксифениламино)антрахинона (676) — продукта взаимодействия 1-хлорантрахинона с антраниловой кислотой. При нагревании соединения (676) с РООз происходит замыкание пиридонового кольца и образование 1477-нафтоакридинтриона (675), который хлорируют в присутствии иода (катализатор) и соды, при этом образуется трихлорпроизводное (677). Атом хлора, находящийся в антрахиноновом кольце три-хлорпроизводного (677), при действии w-толуол- или бензолсульфонамида замещается арьлсульфонамидным остатком, Сульфонамидная группа гидролизуется при нагревании с концентрированной серной кислотой и образуется краситель Кубовый бирюзовый ЗХ (678).
Практически важный краситель Кубовый фиолетовый С (680) получают при взаимодействии 1,5-ди-хлорантрахинона с калиевой солью антраниловой кислоты в присутствии оснований с последующим замыканием двух пиридоновых колец в процессе обработки 1,5-ди(2-карбоксифениламино)антрахинона (679) хлорсульфоновой кислотой или концентрированной серной кислотой.
Ароматические соединения
795
(681) (682)
Красители Кубовый бирюзовый ЗХ (678) и Кубовый фиолетовый С (680) применяются для крашения льна, хлопка, вискозного волокна; окраски устойчивы к свету, хлору, стирке.
Большое практическое значение имеет краситель Кубовый красный КХ (682), содержащий нафталиновое ядро, конденсированное с пиридоновым. Краситель получают взаимодействием 1 -хлорантрахинон-2-карбо-новой кислоты с 2-аминонафталин-1 -сульфокислотой (вместо канцерогенного 2-аминонафталина). При нагревании соединений в нитробензоле в присутствии Na2B4O7 и Н3ВО3 происходит замещение хлора (681), затем отщепление сульфогруппы и замыкание пиридо-нового кольца.
Кубовый красный КХ применяется для крашения хлопка, вискозного волокна и вискозы в массе; окраски отличаются высокой устойчивостью к свету, хлору, трению и стирке.
Метод замыкания пиридонового кольца хлорированием используется при синтезе Кубового ярко-розового С. Исходным соединением для синтеза красителя является 2-метил-1-фениламиноантрахинон (683), получаемый при взаимодействии 2-метил-1-нитроантрахинона с анилином. При хлорировании соединения (683) в трихлорбензоле последовательно происходят образование трихлорметильного производного и циклизация, при этом образуется соединение (684), содержащее остаток 4-хлорпиридина. При нагревании последнего с водным раствором соды хлор замещается на гидроксигруппу и образуется краситель Индантреновый розовый Б (685). Краситель (685) неустойчив в условиях кубового крашения. При восстановлении его дитионитом натрия в щелочной среде отщепляется один из атомов хлора в антрахиноновом ядре и после окисления воздухом образуется смесь двух изомерных, очень близких по свойствам, пентахлорсодержащих красителей (686) и (687). Эта смесь выпускается под названием Кубовый ярко-розовый С.
Кубовый ярко-розовый С применяется для крашения хлопка, вискозного волокна и льна; окраски устойчивы к свету и мокрым обработкам.
Высокой устойчивостью окрасок отличаются карба-золированые производные нафтоакридиновых красителей. Большое практическое значение имеет краситель Кубовый коричневый Ж (689), получаемый нагреванием трихлорпроизводного фталоилакридона (677) — промежуточного продукта синтеза Кубового бирюзового ЗХ (678) — с 1-амино-5-бензоиламиноантрахиноном и карбазолированием образовавшегося антримида (688).
Кубовый коричневый Ж (689) образует окраски с устойчивостью к свету 7—8 баллов (по восьмибалльной шкале), хлору 5 (по пятибалльной шкале) и стирке 4-5 (по пятибалльной шкале).
Нафтоакридиновые красители способны образовывать бисульфитные соединения (690) за счет карбонильной группы пиридонового кольца. Их получают обработкой красителя РОС13, а затем бисульфитом натрия.
796
Новый справочник химика и технолога
В процессе крашения бисульфитное производное красителя наносится на волокно, затем окрашенное волокно обрабатывается раствором соды. В результате обработки бисульфит отщепляется и на волокне остается исходный краситель.
Нафтохиноксалиновые (антрахиноно пир азиновые, фталоилхиноксалиновые) красители
В основе молекул нафтохиноксалиновых красителей лежит гетероциклическая система (692), полученная в результате конденсации ядер антрахинона и пиразина. Это же соединение можно рассматривать как продукт конденсации 1,4-нафтохинона и хиноксалина (69Г, бензопиразина) или как продукт присоединения остатка фталевой кислоты к ядру хиноксалина. Название соединения (692) по современной номенклатуре — наф-то[2,3-/|хиноксалиндион-7,12; отсюда общее название красителей — нафтохиноксалиновые, два других названия (антрахинонопиразиновые и фталоилхиноксалиновые) являются традиционными.
(690)
(692)
Пиразиновое кольцо образует единую сопряженную систему с конденсированным антрахиноновым кольцом,
Ароматические соединения
191
поэтому заместители в пиразиновом кольце оказывают существенное влияние на цвет красителей.
Нафтохиноксалиновые красители получают взаимодействием о-диаминоантрахинонов с щавелевой кислотой и последующим замещением гидроксигрупп в образующемся дигидроксинафтохиноксалиндионе различными заместителями.
Исходным продуктом для синтеза Кубового ярко-алого ЖХ (694) является 1,2-диаминоантрахинон, который сплавляют с щавелевой кислотой при 150 °C. Образующийся при этом 2,3-дигидроксинафтохиноксалин-дион-7,12 (693) нагревают с ж-толуидином в нитробензоле в присутствии хлорида цинка.
Кубовый ярко-алый ЖХ применяется для крашения хлопка и вискозного волокна; окраски отличаются высокой устойчивостью к свету (7 по восьмибалльной шкале) и хлору (5 по пятибалльной шкале); устойчивость к стирке (действию горячей щелочи) несколько меньше (3—4 по пятибалльной шкале).
Динафтофеназиновые
(антрахиноноди гидр о азиновые) красители
В основе молекул динафтофеназиновых красителей лежит гетероциклическая система (696), построенная из двух молекул антрахинона и молекулы 1,4-дигидро-пиразина. Соединение (696) можно рассматривать также как продукт конденсации двух остатков нафтохинона-1,4 с ядром феназина (695); поэтому по современной номенклатуре оно называется 6,15//-динафто[2,3-с; 2',3'-у]феназинтетраон-5,9,14,18, а красители называются динафтофеназиновыми. Традиционное название красителей данной группы — антрахинонодигидроазиновые.
Соединение (696) является красителем, по цвету (синий) и свойствам (кубовый краситель) похожее на Индиго; поэтому оно было названо Индантроном («инд» — от Индиго, «антр» — от антрахинона). Лейкосоединение Индантрона обладает сродством к цел
люлозным волокнам. Водородные связи между >NH-группами дигидроазинового кольца и кислородными атомами карбонильных групп стабилизируют Индантрон к фотоокислительным процессам, что обеспечивает высокую светостойкость окрасок.
Индантрон (696) получают щелочным плавлением 2-аминоантрахинона при 210-230 °C в присутствии нитрата натрия (окислитель) и безводного ацетата натрия. В качестве красителя для текстильной промышленности Индантрон выпускают под названием Кубовый синий О.
При восстановлении Кубового синего О (696) дитионитом натрия в щелочной среде образуется динат-риевая соль дигидроиндантрона (697), раствор которой («куб») имеет синюю окраску. В более жестких условиях восстановления (например, цинковой пылью) образуется тетранатриевая соль (698), раствор которой («куб») имеет коричневый цвет. Чтобы окраски получались чистого тона, восстановление надо проводить до динатриевой соли (697) (т. е. красильный «куб» должен быть синего цвета).
Кубовый синий О образует на целлюлозных волокнах окраски красивого красновато-синего оттенка, обладающие высокой устойчивостью к свету и стирке, но мало устойчивые к хлору и зрению.
Краситель не разлагается при нагревании на воздухе до 500 °C, в концентрированной соляной кислоте — до 400 °C, в расплавленной едкой щелочи — до 300 °C, выделяясь своей химической устойчивостью среди многих органических соединений. Под названием Пигмент синий антрахиноновый применяется в полиграфии, для крашения пластических масс и резины, крашения вискозы в массе и для пигментной печати.
Дважды переосажденный растворением в слабом олеуме и выливанием в воду краситель выпускается под названием Кубовый чисто-синий О. В особой кристаллической модификации, которая образуется при переосаждении из олеума с одновременным сульфированием части молекул, краситель образует голубые с зеленоватым оттенком окраски и выпускается под названием Кубовый ярко-голубой 3.
798
Новый справочник химика и технолога
При введении в молекулу красителя Кубового синего О атомов хлора (методом хлорирования) увеличивается сродство лейкосоединения красителя к волокну и повышается устойчивость окрасок к действию хлора и трению. Выпускаются монохлорпроизводное красителя под названием Кубовый голубой О (699) и дихлорпро-изводное — под названием Кубовый голубой К (700). Оба красителя используются для крашения хлопка и вискозного волокна. Окраски обладают высокой устойчивостью к свету и стирке, а по устойчивости к хлору и трению значительно превосходят Кубовый синий О.
Меры предосторожности в производстве антрахиноногетероциклических красителей
Производство антрахиноногетероциклических красителей связано с применением сильнодействующих (концентрированные кислоты и едкие щелочи, хлор, бром), горючих и взрывоопасных веществ (нитробензол, хлорбензол, аммиак) при высоких температурах.
Необходимо тщательно соблюдать все меры техники безопасности при работе с такими веществами.
В ходе производства некоторых нафтоакридиновых красителей возможно образование в качестве побочного продукта канцерогенного 2-аминонафталина. Поэтому необходимо создать условия, исключающие возможность попадания веществ на одежду и тело работающих. В помещениях не должна накапливаться пыль, т. к. в ней могут находиться вредные вещества и они могут попадать в легкие работающих.
4.3.5.10. Полициклохиноновые (антроновые) красители
Кубовые
(желтые, оранжевые, красно-коричневые, фиолетовые, синие, зеленые, черные)
Кубозоли
(желтые, оранжевые, красно-коричневые, фиолетовые, синие, зеленые)
Пигменты
(желтые, оранжевые, фиолетовые, синие, зеленые)
Все практически важные полициклохиноновые красители можно рассматривать как производные антрона (701), поскольку они содержат в своих молекулах остатки антрона, конденсированные друг с другом непосредственно [дибензопиренхинон (704) и антантрон (705)] или при помощи других циклических систем; в последнем случае красители можно рассматривать как производные бензантрона (702) [пирантрон (706), дибензантрон (707), изодибензантрон (70#)] и ацеантрона (703) [ацедиантрон (709)].
Все полициклохиноновые красители являются кубовыми, они окрашивают целлюлозные волокна в цвета,
Ароматические соединения
799
отличающиеся высокой светостойкостью. В процессе крашения их необходимо перевести в растворимое состояние, т. е. получить лейкосоединения красителей.
Восстановление большинства кубовых красителей класса полициклических хинонов в лейкосоединения проходит в жестких условиях: при значительной щелочности среды и высокой температуре. Так как белковые вещества разрушаются (гидролизуются) в таких условиях, эти красители неприменимы для окрашивания шерсти и шелка. Лишь некоторые ку
бовые красители, способные восстанавливаться в более мягких условиях (при меньшей щелочности среды и низкой температуре), могут использоваться для крашения белковых волокон. Эти красители имеют в названии букву «X», указывающую на возможность крашения по так называемому холодному способу.
Восстановление кубовых красителей в лейкосоединения обычно осуществляют при помощи дитионита натрия Na2S2O4 (при простом крашении) и его производного — продукта взаимодействия с формальдегидом (гидроксиметансульфината натрия) HOCH2SO2Na, называемого ронгалитом (при печати). Оба восстановителя активны в щелочной среде.
Красители группы дибензопиренхинона
Основу молекул этих красителей составляют два ядра антрона, конденсированные друг с другом, однако соединения можно рассматривать и как производные пирена, содержащие два конденсированных бензольных кольца. Примером такого красителя является Кубовый золотисто-желтый ЖХ [(707); дибен-зо[/>,/]пиренхинон-7,14]. Общим методом получения красителей данной группы является ацилирование соответствующих ароматических соединений бензо-илхлоридом в присутствии хлорида алюминия с последующей циклизацией образовавшихся ароматических кетонов. Циклизацию проводят нагреванием ацильного производного с избытком хлорида алюминия или со смесью хлоридов алюминия и натрия (5 : 1). Применение смеси А1С13 и NaCl позволяет проводить циклизацию в расплаве при более низкой температуре, и при этом не происходит возгонки хлорида алюминия, летучесть которого резко снижается в присутствии NaCl (вследствие образования равновесной системы А1С13+NaCl —> Na+AlCl”).
Так, краситель Кубовый золотисто-желтый ЖХ (704) получается взаимодействием бензоил хлорида с нафталином в присутствии хлорида алюминия; образующийся 1,5-дибензоилнафталин (710) при нагревании в расплаве смеси А1С13 и NaCl в присутствии окислителя (кислорода или 2,4-динитрохлорбензола) образует краситель (704). При бензоилировании нафталина, кроме 1,5-дибензоилнафталина, образуется побочный продукт — изомерный 1,8-дибензоилнафталин; изомеры разделяют перекристаллизацией их смеси из хлорбензола.
Выделенный из реакционной массы краситель очищают, окисляя примеси NaClO (пропускают хлор через суспензию красителя в растворе щелочи), а затем переосаждая из «куба» (краситель восстанавливают дитионитом натрия в щелочной среде в лейкосоединение (711), а далее окисляют, продувая воздух через раствор). «Куб» красителя окрашен в вишневокрасный цвет.
Кубовый золотисто-желтый ЖХ является очень ценным красителем, дающим красивые желтые окраски,
800
Новый справочник химика и технолога
устойчивые к мокрым обработкам и довольно стойкие к свету и трению. Широко применяется для крашения хлопка и вискозного волокна, печати по хлопку, вискозному волокну и натуральному шелку. Недостатком этого красителя является участие в процессе фотохимического окисления окрашенного волокна, приводящее к уменьшению механической прочности материала.
При бромировании Кубового золотисто-желтого ЖХ бромом в среде 12,5% олеума в присутствии небольшого количества иода (катализатор) и NaNO2 (окислитель, снижающий расход брома за счет реакции 2НВг + [О] —> Вг2 + Н2О) образуется Кубовый золотисто-желтый КХ [(7/2); 2,9-дибромдибензо[6,/]пирсн-хинон-7,14]. Атомы галогена углубляют оттенок красителя до красноватого и повышают его сродство к волокну, вследствие чего возрастает устойчивость окрасок к мокрым обработкам и трению.
Красители Кубовый золотисто-желтый ЖХ и Кубовый золотисто-желтый КХ находят широкое применение в качестве пигментов; они выпускаются под названием Пигмент золотисто-желтый антрахиноновый Ж и Пигмент золотисто-желтый антрахиноновый К соответственно. Применяются в полиграфической промышленности и для крашения пластических масс.
Красители группы антантрона
Антантрон (705) — это соединение ярко-оранжевого цвета, но в качестве красителя он не применяется, т. к. его лейкосоединение обладает слишком слабым сродством к волокну. Для повышения сродства к волокну в молекулу антантрона вводят атомы галогенов, при этом оттенок становится несколько глубже (тем сильнее, чем выше атомная масса галогена) и увеличивается яркость окрасок.
Антантрон (705) образуется в результате реакции циклизации «дина-кислоты» [(7/3); 1,Г-динафтил-8,8'-дикарбоновая кислота]; циклизацию проводят в среде серной кислоты. При действии на антантрон газообразного хлора в среде серной кислоты получают краситель Кубовый ярко-оранжевый ЖХ (714), при действии брома в олеуме — Кубовый ярко-оранжевый КХ (643).
О
(7/4)Х = С1; (643)Х = Вг
Оба красителя образуют окраски, обладающие высокой устойчивостью к свету (7-8 по восьмибалльной шкале), хлору (5 по пятибалльной шкале) и стирке (4 по пятибалльной шкале). Применяются для крашения и печатания хлопчатобумажных, вискозных и льняных тканей, а также для окрашивания бумаги. Кубовый ярко-оранжевый КХ (643) под названием Пигмент ярко-оранжевый антрахиноновый КХ применяется для крашения пластических масс и в полиграфии.
Красители группы пирантрона
Исходным продуктом для синтеза красителей группы пирантрона является 2-метил-1-хлорантрахинон (715), который при взаимодействии с порошком меди в о-дихлорбензоле в присутствии пиридина образует 2,2'-диметил-1,Г-диантрахинонил (716). Последний при кипении в изобутиловом спирте с КОН образует циклическое соединение — пирантрон (706). Сам пиран-трон является кубовым красителем ярко-оранжевого цвета, однако из-за высокой фотохимической активности не применяется для крашения тканей, а используется как светостойкий ярко-оранжевый пигмент.
Ароматические соединения
801
Красители группы дибензантрона
Представителем красителей группы дибензантрона является Кубовый темно-синий О [дибензантрон, или виолантрон (707)]. Краситель получают сплавлением бензантрона (702) с эквимольной смесью КОН и NaOH в присутствии окислителя (NaNO2). Реакция идет через образование промежуточных соединений: дигидроди-бензантронил-аниона (717) и 4,4'-дибензантронила (721).
Кубовый темно-синий О окрашивает хлопок из красновато-фиолетового «куба» в сине-фиолетовый цвет, окраски устойчивы к действию света, к стирке, хлору.
При нитровании Кубового темно-синего О в уксусной кислоте или нитробензоле образуется 16,17-ди-нитродибензантрон (718), выпускаемый в качестве красителя под названием Кубовый черный. Черный цвет появляется в процессе крашения, т. к. само нитропро
изводное (718) синего цвета. Процессы, происходящие при крашении, можно представить следующим образом.
При восстановлении красителя (718) в лейкосоединение, кроме карбонильных, восстанавливаются и нитрогруппы; образуется «куб» синевато-фиолетового цвета. После крашения и окисления на волокне остается 16,17-диаминодибензантрон (719), который имеет зеленый цвет. При действии на окрашенное волокно окислителей (NaNO2 или NaClO) аминогруппы красителя окисляются, образуя гетероциклическое соединение (720), сообщающее волокну глубокую черную, исключительно устойчивую окраску.
К группе дибензантрона относится и краситель Кубовый ярко-зеленый С (723) — один из самых ярких и красивых красителей зеленого цвета. Краситель получают, нагревая бензантрон с КОН в изобутиловом спирте, затем окисляют гипохлоритом и выделяют 4,4'-
дибензантронил (721), который после окисления МпО2 превращается в 16,17-дигидроксидибензантрон (722). Соединение (722) алкилируют метиловым эфиром бензолсульфокислоты.
802
Новый справочник химика и технолога
Кубовый ярко-зеленый С (723) широко применяется для крашения хлопка, вискозного волокна, льна, натурального шелка, а также пластических масс (полистирол, аминопласты) и резины. Окраски отличаются высокой устойчивостью к свету (7-8 по восьмибалльной шкале), к стирке и хлору (4-5 по пятибалльной шкале).
Бромированием Кубового ярко-зеленого С в серной кислоте в присутствии борной кислоты при 25-30 °C получают дибромпроизводное (положение атомов брома точно не установлено), причем частично происходит деметилирование одной из мстоксигрупп. Дибромпроизводное выпускается под названием Кубовый ярко-зеленый Ж. Он образует окраски несколько более желтого оттенка и применяется для крашения хлопка, льна и вискозного волокна, а также для крашения вискозы в массе; устойчивость окрасок к различным воздействиям достаточно высокая, но ниже, чем у Кубового ярко-зеленого С.
Кубовые ярко-зеленые С и Ж под названиями соответственно Пигменты ярко-зеленые антрахиноновые С и Ж применяются для крашения пластических масс и в полиграфии.
При взаимодействии 16,17-дигидроксидибензантро-на (722) с этиленоксидом или Р-хлорэтиловым эфиром бензолсульфокислоты (C6H5SO3CH2CH2CI) образуется Кубовый темно-синий (724). Краситель применяется для крашения хлопка, льна, вискозного волокна; окраски обладают превосходной светостойкостью.
Ацилированием лейкосоединения дигидроксидибензантрона хлорангидридом стеариновой кислоты получают тетрастеароильный эфир — Дефектол (725; Флуорол HP). Дефектол растворяется в алифатических
углеводородах с образованием желтовато-красных растворов, отличающихся сильной желто-зеленой флуоресценцией, что используется в дефектоскопии металлов для обнаружения микротрещин. Он применяется для подкрашивания искусственных смазочных масел, сообщая им способность флуоресцировать, а также для крашения полистирола и некоторых других полимерных материалов.
OCOR
(725) R = С17Н35
Красители подгруппы изодибензантрона
Для синтеза изодибензантрона (708), называемого также изовиолантроном, в качестве исходного вещества применяют не сам бензантрон, а его 3-бромпроизвод-ное, которое получают бромированием бензантрона (702). При взаимодействии 3-бромбензантрона (651) с эквимольной смесью Na2S и Na2S2 образуется 3,3'-дибензантронилсульфид (726), который при нагревании с КОН в среде изобутилового спирта превращается в изодибензантрон (708).
Изодибензантрон окрашивает целлюлозные волокна из синего «куба» в красновато-фиолетовый цвет, но в качестве красителя не применяется, т. к. образует тусклые оттенки. Для повышения яркости оттенка в молекулу вводят атомы галогена; одновременно возрастает сродство красителя к волокну и увеличивается устойчивость окрасок к стирке.
При хлорировании изодибензантрона сульфурил-хлоридом (SO2C12) в присутствии пиридина получают дихлоризодибензантрон (положение атомов хлора не установлено), выпускаемый под названием Кубовый
Ароматические соединения
803
ярко-фиолетовый К. Этот краситель широко применяется для крашения хлопка, вискозного волокна и шелка. Окраски отличаются яркостью и высокой устойчивостью. Под названием Пигмент ярко-фиолетовый антрахиноновый К он используется для крашения пластических масс (аминопласты, полистирол), а также в лакокрасочной и полиграфической промышленности.
Бромированием изодибензантрона в серной или хлорсульфоновой кислоте в присутствии небольшого количества серы получают Кубовый ярко-фиолетовый 2С (монобромизодибензантрон). Краситель применяется для крашения хлопка, льна, вискозного волокна и шелка, а также резины. Окраски отличаются высокой устойчивостью к свету, к мокрым обработкам, хорошо выдерживают отбеливание гипохлоритом натрия.
Красители группы ацедиантрона
Красители этой группы получают взаимодействием соответствующих производных антрона, например, 2-хлорантрона-9 (727) с глиоксалем или глиоксальсульфатом с последующим окислением образовавшегося бис(антронилиден)этана (728) в бис(антронилиден) этилен (729), который в среде серной кислоты и олеума превращается в циклическое соединение — 2,2'-ди-хлорацедиантрон (730). Соединение (730) является кубовым красителем и выпускается под названием Ин-дантреновый красно-коричневый 2Р.
Кубозоли
Кубовые полициклохиноновые красители представляют большой интерес для текстильной промышленности. Многие из них относятся к числу лучших красителей среди всех известных. Однако они имеют ряд недостатков.
Во-первых, перед крашением их необходимо восстанавливать («переводить в куб»), т. е. осуществлять чисто химический процесс, не имеющий прямого отношения к текстильной технологии. Во-вторых, перевод красителей в «куб» часто весьма нелегок, т. к. многие кубовые красители образуют прочные кристалл-лические структуры, с трудом разрушающиеся при действии щелочного раствора восстановителя. В-третьих, восстановление кубовых красителей проводится в щелочной среде, что исключает возможность использования большинства из них для крашения белковых материалов. В-четвертых, лейкосоединения полициклохиноновых красителей обладают очень высоким сродством к целлюлозе, поэтому в момент крашения краситель закрепляется на наиболее доступных участках поверхности и с трудом проникает в глубь волокна; в результате окраска получается неровной.
Многие проблемы, возникающие при использовании кубовых красителей, удается преодолеть путем превращения кубовых красителей в кубозоли.
Кубозолями называют растворимые (обычно натриевые) соли кислых сернокислых эфиров (бисульфатов) лейкосоединений кубовых красителей общей формулы ROSO3Na. Они устойчивы к действию воздуха, не расщепляются в нейтральных, слабощелочных и слабокислых растворах при нагревании. Применение их не требует предварительного восстановления и не связано с использованием сильнощелочных ванн. Поэтому кубозолями можно окрашивать как целлюлозные, так и белковые волокна. Белковые волокна окрашивают кубозолями из кислых ванн, целлюлозные — из нейтральных или слабощелочных. Сродство кубозолей к целлюлозе меньше, чем
804
Новый справочник химика и технолога
у исходных лейкосоединений, поэтому они более равномерно распределяются по поверхности целлюлозного волокна и легче проникают в глубь его, что позволяет получать ровные окраски, более устойчивые к трению, чем при крашении исходным кубовым красителем.
После крашения кубозоль на волокне подвергают гидролизу в присутствии слабых окислителей. Сложный эфир расщепляется, и освободившееся лейкосоединение окисляется в краситель. Гидролиз осуществляют в слабокислой среде; в качестве окислителей обычно применяют NaNO2 или FeCl3 (уравнение (4.3.27)).
^С—OSO3Na + Н2О + FeCl3 ------►
------>^С—О +NaHSO4+ FeCI2+HCl (4.3.27)
В названиях кубозолей слово «кубозоль» заменяет слово «кубовый» в названии исходного красителя; например, Кубозоль золотисто-желтый ЖХ (731) — производное Кубового золотисто-желтого ЖХ, Кубозоль ярко-зеленый С (732) — производное Кубового ярко-зеленого С.
Меры предосторожности в производстве полициклохиноновых красителей
Производство полициклохиноновых красителей связано с использованием ряда токсичных (нитросоединения, хлорпроизяодные бензола, пиридин, бензантрон), потенциально канцерогенных (дибензопиренхинон и другие многоядерные соединения), огне- и взрывоопасных (спирты, нитросоединения) веществ, а также концентрированных кислот, щелочей, хлора, брома и др.
Необходимо тщательно следить за тем, чтобы эти вещества не попадали на тело и одежду работающих (использование спецодежды, защитных очков, шлемов-масок, перчаток), а также не допускать накопления этих веществ в атмосфере помещения, на полах, стенах и т. д. Везде, где это допускам технологический процесс, аппараты должны быть герметизированы, а в остальных
случаях снабжены эффективно действующей локальной вытяжной вентиляцией. Работа с летучими и пылящими веществами должна проводиться в противогазах соответствующих марок.
При работе с А1С13 следует иметь в виду, что от следов влаги он разлагается с выделением HCI, раздражающего слизистые оболочки, а при действии большего количества воды разлагается со взрывом.
Антроногетероциклические красители
4.3.5.11. Антроногетероциклические красители
Дисперсные
(от оранжево-красных до фиолетовых)
Капрозоли (рубиновые)
-► Кислотные
(красные, рубиновые)
► Кубовые
(желтые, красные, темно-синие, серые)
В основе молекул красителей этого класса лежат системы, построенные из конденсированных ядер антрона и различных гетероциклов. В зависимости от природы гетероцикла красители делятся на ряд групп.
Нафтохинолиновые {антрапиридоновые) красители
С точки зрения современной номенклатуры, основу молекул этих красителей составляет гетероциклическая система, представляющая собой продукт конденсации нафтохинона-1,4 и хинолона-2 (734) и называемая 2,3,7//-нафто[1,3-б/,е]хинолиндион-2,7 (735). Однако традиционное название красителей — антрапиридоновые, т. к. соединение (735) можно рассматривать как продукт присоединения остатка пиридона-2 (733) к ядру ангрона (701).
Н (733)
О
о
(735)
Нафтохинолиновые красители по свойствам близки антрахиноновым. Иногда в названиях этих красителей используется слово «антрахиноновый», что, конечно, неправильно, с точки зрения строения соединений, но оправдано близостью их колористических свойств.
Нафтохинолиновые красители получают дегидратацией А-ацильных производных 1-аминоантрахинона и его замещенных, сопровождающейся замыканием пи-ридонового цикла. Так, практически важный краситель Дисперсный рубиновый 2С (738) получают, нагревая
Ароматические соединения
805
1 -(/У-ацетил-тУ-метиламино)-4-бромантрахинон [(736); продукт взаимодействия 4-бром-1 -метиламиноантрахи-нона с уксусным ангидридом] с 3% NaOH при 120 °C (200-250 кПа) с последующим замещением брома фениламиногруппой. Краситель хорошо окрашивает синтетические гидрофобные волокна из водных дисперсий, образуя окраски, устойчивые к различным воздействиям.
При сульфировании Дисперсного рубинового 2С (738) 3% олеумом получают краситель Кислотный рубиновый антрахиноновый (739), окрашивающий шерсть и шелк в красивый красный цвет с синеватым оттенком, напоминающим окраску Фуксина. Окраски светостойки, устойчивы к мокрым обработкам и умеренно устойчивы к валке.
О
Очень ценный краситель Карболан красный ЗБ (741) получают на основе 1,4-бис(4-бутилфениламино)антра-хинона [основание красителя Кислотного зеленого антрахинонового Н2С (608)]. Действием 1 моля ацетил-хлорида на 1 моль этого соединения получают моно-ацетильное производное (740), которое вначале нагревают в щелочной среде для образования пиридонового цикла, а затем сульфируют. Карболан красный ЗБ (741) окрашивает шерсть из нейтральной ванны подобно другим карболановым красителям.
Нафтохинолиновые красители, не растворимые в воде, являются не только ценными дисперсными красителями: они применяются также для крашения полиамидных волокон в массе (например, капрона).
Найти красители, способные окрашивать полиамидные волокна в массе, — задача весьма непростая. Расплавы полиамидов обладают восстанавливающей способностью, а т. к. формование нитей из полиамидов производится из расплава при 220-250 °C, красители должны быть устойчивы к действию восстановителей при такой температуре. Этому требованию удовлетворяет сравнительно ограниченное число известных красителей, поэтому для крашения капрона из расплава (в массе) выпускаются специальные красители под названием «капрозоли».
806
Новый справочник химика и технолога
Способы получения капрозолей нафтохинолинового ряда аналогичны способам получения дисперсных красителей, в частности Дисперсного рубинового 2С (738).
Взаимодействием 6-бром-З-метил нафтохинолиндио-на (737) с 2-, 3- и 4-хлоранилинами получают соответственно Капрозоль рубиновый К (742), Капрозоль рубиновый С (743) и Капрозоль красно-фиолетовый (744), при взаимодействии с w-анизидином — Капрозоль фиолетовый 4К (745).
(742) Аг = С6Н4С1-о; (743) Аг = С6Н4С1-л<;
(744) Ar = С6Н4С1-«; (745) Аг = С6Н4ОСН3-и
На основе нафтохинолинов получают полимерные красители. Например, при взаимодействии 6-бром-4-метил-1-фенилнафтохинолиндион-2,7 (746) с поли(ами-ноэтиленом) в водном растворе NaOH в присутствии CuCl и пиридина образуется полимерный краситель (747; п = 180^-200; т - 260-^700; х = п + т).
Краситель (747) окрашивает лаки в ярко-красный цвет, устойчивый к действию кислот.
Бензоперимидиновые красители
В основе молекул бензоперимидиновых красителей лежат гетероциклические системы, построенные из ядер бензола и перимидинона-6 ( 748) или бензола
и перимидиндиона-2,6 (749). Эти системы соответственно называются бензо[е]перимидинон-7 (752) и бен-зо[е?]перимидиндион-2,7 (753).
Соединения (752) и (753) можно рассматривать как продукты присоединения к ядру антрона (701) остатков пиримидина (750) или пиримидона-2 (751); поэтому второе (традиционное) название красителей, обычно используемое на практике, — антрапиримидиновые и антрапиримидоновые.
В названиях многих бензоперимидиновых красителей имеется слово «антрахиноновый», указывающее на сходство свойств и способов применения этих красителей и антрахиноновых.
Бензоперимидиноновые (антрапиримидиновые) красители. Наибольшее практическое значение имеют бензоперимидиноны (антрапиримидины), содержащие в положении 2 арильную, а в положении 6 — ариламиногруппу. Удобным способом их синтеза является взаимодействие 1-амино-4-галогенантрахинонов с А-алкил-амидами ароматических карбоновых кислот и тионил-хлоридом в инертных растворителях с последующей заменой атома галогена в образовавшемся 2-арил-6-галогенбензоперимидиноне ариламиногруппой и сульфированием полученного продукта (если необходимо получить кислотный краситель).
Таким способом получают кислотные красители (755). Вначале из 1-амино-4-бромантрахинона и А-ме-тилбензамида получают 6-бром-2-фенилбензоперими-динон (754), который араминируют действием анилина или 4-толуидина и сульфируют. Образующиеся кислотные красители (755) окрашивают шерсть и полиамидные волокна из нейтральной ванны (подобно кар-боланам) в алый (R = Н) и красный (R = СН3) цвета; окраски устойчивы к свету и мокрым обработкам.
Соединения (756), не замещенные в положении 2 и не содержащие сульфогрупп, но имеющие в положениях 6,8,11 заместители (R-NH-C6H5, -NHC6H4SO2NH2, -ОН и др.), применяют в качестве дисперсных красителей для крашения полиэфирных и ацетатных волокон (цвета — от оранжево-красного до фиолетового).
Ароматические соединения
807
Бензоперимидиндионовые (антрапиримидоновые) красители. Эти красители имеют более глубокие цвета по сравнению с антрапиримидиновыми красителями. Их получают обычно взаимодействием 1-аминоантрахинонов с мочевиной в расплаве фенола в присутствии ZnCl2 или NH4C1. Например, из 1-амино-2-(4-/ире/и-бутилфенокси)-4-мезидиноантрахинона (757) таким способом получают 4-(4-гире/и-бутилфенокси)-6-
мезидинобензоперимидиндион-2,7, превращающийся после сульфирования в кислотный краситель (758). Краситель (758) окрашивает шерсть в очень яркий, рубиновый цвет; окраски устойчивы к свету и мокрым обработкам.
11афтойндазолоновые (пиразолантроновые) красители
Основой молекул нафтоиндазолоновых красителей является гетероциклическая система — 2,6//-нафто[1,3-с,б(]индазалон-6 (760a), существующая также в таутомерной 1,6//-форме (7606). Система построена из конденсированных ядер 1/7-индазолона (759) и 1,4-нафто-
хинона.
(760a) (7606)
Соединение (760) можно рассматривать как продукт присоединения пиразола к ядру антрона, поэтому традиционное название красителей данной группы — пи-разолантроновые.
808
Новый справочник химика и технолога
2,6//-Нафто[1,3-с,б/]индазолон-6 (760) получают циклизацией 1-антрахинонилгидразина (761) — продукта взаимодействия 1-хлорантрахинона с гидразином. Циклизацию проводят нагреванием соединения (761) в среде концентрированной серной кислоты при 90-95 °C. Этим же способом получают различные производные пиразолантрона (760).
На основе 3-бромпиразолантрона (762) по реакции Ульмана (нагревание галогенпроизводного с порошком меди) получают кубовый краситель (763), имеющий ограниченное практическое применение из-за невысокой устойчивости окрасок к стирке. Алкилированием NH-групп этого красителя диэтил- или диизопропилсульфа
том получают красители Цибанон красный 6Б (764; R = CH3) и Цибанон красный ЗБ [764; R - (СН3)2СН] соответственно. Красители образуют окраски, устойчивые ко всем видам воздействия, в том числе к щелочам.
Из пиразолантроновых красителей наибольшее практическое значение имеют сложные полициклические красители: Кубовый темно-синий К (766) и Кубовый серый С (769). Эти красители по своим свойствам близки дибензантроновым красителям, т. к. пиразолантрон (760) является изоэлектронным аналогом бензантрона (702) и имеет такую же хромофорную систему.
Кубовый темно-синий К (766) получают нагреванием пиразолантрона (760) с 3-бромбензантроном (651) в нитробензоле в присутствии безводного К2СО3 и СиСО3 с последующим щелочным плавлением образующегося 2-(бензантронил-3)-2,6/7-нафтоиндазолона (765). Процесс аналогичен карбазолированию антримидов, однако в данном случае образуется не пятичленный, а шестичленный гетероцикл.
Кубовый темно-синий К применяется для крашения хлопка и вискозного волокна; окраски очень устойчивы к свету (7-8 по восьмибалльной шкале), хлору (4-5 по пятибалльной шкале) и достаточно устойчивы к стирке (3-4 по пятибалльной шкале).
Кубовый серый С (769) получают последовательным взаимодействием 3,9-дибромбензантрона (767) с пиразолантроном (760) и 1-аминоантрахиноном (вначале замещается более подвижный атом брома в положении 3) и карбазолированием образовавшегося антрими-доподобного соединения (768).
Кубовый серый С (769) применяется для крашения хлопка, льна и вискозного волокна, устойчивость окрасок такая же, как у Кубового темно-синего К.
Диазапирантреновые красители
Единственный краситель данной группы, который нашел широкое практическое применение, — это желтый кубовый краситель Флавантрон (770) — 5,13-диазапирантрендион-8,16 (диазапирантрон).
(770)
Ароматические соединения
809
Флавантрон (770) является гетсроаналогом Пиран-трона (706). Он образуется при щелочном плавлении 2-аминоантрахинона, если реакцию проводить при температуре более высокой, чем при получении Индантрона (696), а именно: при температуре > 270 °C (лучше при 300-350 °C). Однако в промышленности этот способ не используется из-за низкого выхода Флавантрона (~ 30 %).
Обычно Флавантрон получают из 2-амино-1-хлор-антрахинона, аминогруппу которого сначала защищают взаимодействием с фталевым ангидридом в присутствии FeCI3, а затем при нагревании 2-фталимидо-1-хлор-антрахинона с порошком меди в трихлорбензоле получают 2,2'-ди(фталимидо)-1,Г-диантрахинонил (771). При нагревании соединения (771) в растворе NaOH происходит гидролиз и циклизация с образованием Флавантрона.
При восстановлении Флавантрона дитионитом натрия в щелочной среде образуется растворимая натриевая соль 5,16-дигидрофлавантрона (лейкосоединения Флавантрона) (772) — «куб» фиолетового цвета; более энергичное восстановление затрагивает и вторую половину молекулы, причем образующаяся коричневая динатриевая соль 5,8,13,16-тетрагидрофлавантрона (773)
очень устойчива и не окисляется до Флавантрона даже при действии бихромата. Это осложняет процесс крашения Флавантроном, т. к. при перевосстановлении соединения окраски чистого тона не получаются.
Флавантрон образует окраски чисто-желтого цвета с высокой светостойкостью. В отличие от многих желтых кубовых красителей он не участвует в процессе фото-
810
Новый справочник химика и технолога
химического окисления окрашенного волокна, а следовательно, не способствует ослаблению окрашенного волокна при действии света, что очень ценно. Однако Флавантрон дорог, и это препятствует его использованию в качестве красителя для текстильных изделий. Под названием Пигмент желтый антрахиноновый К он применяется в полиграфии для изготовления высококачественных красок для цветной печати.
Периноновые красители
—► Дисперсные (желтые)
—► Кубовые
(оранжевые, красные, бордо)
—► Кубогены
(красные, синие, фиолетовые)
—► Пигменты
(оранжевые, красные, бордо)
—► Протравные (желтые)
Азафеналевые {пери-дикар б оксимидные} красители
Основой молекул азафеналевых красителей является гетероциклическая система — 2-аза-2,3//-феналендион-1,3 (774).
(774)
Меры предосторожности в производстве антроногетероциклических красителей
Производство антроногетероциклических красителей связано с использованием концентрированной серной кислоты и олеума, растворов едких щелочей при высокой температуре, высококипящих горючих и взрывоопасных растворителей (нитробензол, три-хлорбензол), уксусного ангидрида, брома, хлора, нитрита натрия, ароматических аминов (анилин, 4-анизидин и др.). О мерах предосторожности при работе с этими веществами говорилось в предыдущих главах.
Особое внимание следует обратить на используемый в производстве некоторых красителей метиламин. В обычных условиях это газообразное вещество, горючее и взрывоопасное, хорошо растворимое в воде, раздражающее слизистые оболочки и кожу и являющееся ядом для центральной нервной системы. Работа с ним требует крайней осторожности. Весьма неприятный, вызывающий тошноту запах имеет тионилхлорид; кроме того, подобно многим галогенангидридам, при действии влаги он выделяет газообразный НС1, раздражающий слизистые оболочки. Соблюдение всех мер предосторожности, герметизация аппаратуры, поддержание в должном порядке приточно-вытяжной вентиляции являются обязательными условиями организации подобных производств.
4.3.5.12. Периноновые красители
Молекулы этих красителей содержат ие/ш-ари-леновый остаток, конденсированный с гетероциклом. В зависимости от природы гетероцикла красители делятся на группы.
Соединения этого типа являются имидами ароматических ие/?«-дикарбоновых кислот, поэтому второе (традиционное) название красителей данной группы — пери-дикарбоксимидные. Атом водорода имидной группы обычно замещен алкильным или арильным остатком. В молекулах красителей может быть одна или две «e^w-дикарбоксимидные группировки.
Азафеналеновые красители получают взаимодействием ангидридов ароматических «epw-дикарбоновых кислот с первичными аминами в органическом растворителе (например, в уксусной кислоте) или в водной среде. Так, при нагревании ангидрида 4-амино-З-сульфонафталин-1,8-дикарбоновой кислоты (775) с 5-ами-носалициловой кислотой получают кислотно-протравной краситель Хромовый желтый для шелка (776). Краситель образует по хромовой протраве окраски, обладающие высокой устойчивостью ко всем воздействиям.
А-Алкилзамещенные 4-аминонафталимиды обладают флуоресцентной способностью. Так например, 4-ацетиламино-А-бутилнафталин-1,8-дикарбоксимид (777) — желтый краситель, отличающийся сильной зеленой флуоресценцией. Его получают взаимодействием 4-нитронафталевого ангидрида [ангидрид 4-нит-ронафтал ин-1,8-дикарбоновой (4-нитронафталевой)
кислоты] с бутиламином в уксусной кислоте с последующим восстановлением нитрогруппы чугунной стружкой и ацетилированием аминогруппы уксусным ангидридом. Краситель применяется для подцветки органических растворителей.
При взаимодействии диангидрида перилентетракар-боновой-3,4,9,10 кислоты (775) с jw-ксилидином образуется Пигмент красный 1 (779), который применяют в лакокрасочной и полиграфической промышленности и для крашения пластических масс.
Ароматические соединения
811
Диазаинденофеналеновые (пери-ароиленимидазоловые) красители
В основе молекул диазаинденофеналеновых красителей лежит гетероциклическая система — 7а,12-диаза-индено[1,2-6]феналенон-7 (783). Традиционное название красителей данной группы — пери-ароиленимидазоловые, т. к. соединение (783) можно рассматривать как продукт последовательного ацилирования 1,3-диаза-индена (бензимидазола) аренкарбоновой кислотой (в данном случае нафталинкарбоновой-1) и дегидрирования образовавшегося I-(нафтоил-1 )бензимидазола (782).
(783)
Если в молекулах азафеналевых красителей имеется не менее двух сопряженных карбонильных групп, эти красители могут использоваться в качестве кубовых. Их лейкосоединения, благодаря плоскому линейному строению, наличию большой я-электронной системы и атомов, способных участвовать в образовании межмолекулярных водородных связей, обладают хорошим сродством к целлюлозе. Так, продукты взаимодействия диангидрида перилентетракарбоновой кислоты с метиламином и 4-анизидином являются кубовыми красителями и выпускаются под названиями Индантреновый красный ГГ (780) и Индан-треновый алый (781).
Красители окрашивают хлопок в яркие цвета; окраски обладают высокой устойчивостью к действию света, к стирке и хлору.
В молекулах таких красителей может быть одна или две диазаинденофеналеновые группировки.
Диазаинденофеналеновые красители получают взаимодействием ароматических о-диаминов с ангидридами ие/?м-дикарбоновых кислот. Так, соединение (783) — краситель Жирорастворимый желтый 43 — получают при нагревании ангидрида нафталин-1,8-дикарбоновой кислоты (784) с о-фенилсндиамином в среде уксусной кислоты.
Аналогично получают нерастворимые в воде красители для синтетических волокон. Например, Капрозоль желтый 43 (785) образуется при взаимодействии ангидрида нафталин-1,8-дикарбоновой кислоты (784) с 3,4-диаминохлорбензолом.
Краситель Дисперсный желтый 43 ПЭ (786) является продуктом взаимодействия ангидрида 4-бензо-илнафталин-1,8-дикарбоновой кислоты с о-фенилен-диамином.
812
Новый справочник химика и технолога
Некоторые замещенные нафтоиленбензимидазолы обладают флуоресцентными свойствами и применяются для приготовления дневных флуоресцентных красок.
Особую практическую ценность представляют кубовые диазаинденофеналеновые красители. Кубовые красители получают с использованием диангидридов пери-тетракарбоновых кислот: нафталинтетракарбоновой-1,4,5,8, перилентетракарбоновой-3,4,9,10 (778) и др.
Так, при взаимодействии нафталинтетракарбоновой кислоты или, лучше, ее диангидрида (787) с о-фени-лендиамином в ледяной уксусной кислоте образуется ММ-бис(о-аминофенил)нафталинтетракарбоксдиимид (788), который, отщепляя воду, образует смесь транс-(789) и цис- (790) нафтоиленбис(бензимидазолов). Эту смесь выпускают под названием Кубовый алый 2Ж и используют для крашения хлопка и вискозного волокна.
При разделении смеси (например, с помощью серной кислоты, в которой растворим шр<а//с-изомер) получают индивидуальные красители: шрш/с-изомер — Кубовый ярко-оранжевый (789) и z/wc-изомер — Кубовый бордо (790).
Кубовый ярко-оранжевый — это самый яркий среди всех оранжевых кубовых красителей. Окраски его обладают высокой устойчивостью к свету (7 по восьмибалльной шкале), хлору (5 по пятибалльной шкале) и достаточно устойчивы к стирке (3-4 по пятибалльной шкале). Окраски, образуемые Кубовым бордо, также отличаются яркостью и устойчивостью к свету, хлору и стирке.
При восстановлении красителей образуются щелочные растворы лейкосоединений («кубы») — (791) и (792); оба «куба» имеют оливковый цвет.
Под названиями Пигмент ярко-оранжевый антрахиноновый и Пигмент бордо антрахиноновый красители (789) и (790) соответственно применяются для окрашивания полимеров, в лакокрасочной промышленности и полиграфии.
Ароматические соединения
813
Большие возможности для синтеза кубовых диаза-инденофеналеновых красителей открывает использование других лера-тетракарбоновых кислот, например, перилентетракарбоновой кислоты, а также ле/?м-дикар-боновых кислот, которые содержат карбонильную группу, сопряженную с одной из карбоксильных групп, например бензантрон-ле/?г/-дикарбоновая кислота (793). При взаимодействии с о-диаминами эта кислота образует кубовые красители различных цветов и оттенков, например с диаминами бензольного ряда — оранжевые (794) и красные (795).
Большой интерес представляет синтез диазаиндено-феналеновых красителей в процессе крашения. Компонентами для такого крашения являются те же пери-ди-и лфм-тетракарбоновые кислоты и ароматические орто- и лера-диамины. На ткань наносят натриевую или аммониевую соль кислоты, диамин, хлорид или другую соль аммония, после чего ткань высушивают и подвергают термообработке при 130 °C в течение 3-5 мин. При этом на волокне образуются красители типа Жирорастворимого желтого 43 [(783) — при применении ифм-дикарбоновых кислот] и типа Кубового алого 2Ж [смесь (789) и (790) — при применении «фм-тетракар-боновых кислот]. Соответствующим подбором компонентов можно получить цвета от лимонно-желтого [краситель (796) — из 4-бромнафталиндикарбоновой-1,8 кислоты и о-фенилендиамина] до серо-черного [краситель (797) — из нафталинтетракарбоновой кислоты и 1,8-нафтиленд нами на].
Кубогены
Кубогенами называют соединения, применяемые для образования нерастворимых кубовых красителей (пигментов) непосредственно на волокне. Они представляют собой промежуточные продукты для синтеза периноновых красителей — производных перилентетракарбоновой кислоты. Это симметричные кубогены ряда диазафеналенила, например, (799; R = алкил, арил или гетерил); симметричные кубогены ряда бидиазаи-денофеналенила, например, (800); несимметричные комбинированные кубогены, например (801).
Симметричные кубогены типа (799) образуют окраски красного цвета разных оттенков. Получают кубогены с выходами, близкими к количественным, взаимодействием диангидрида 1,1'-динафтилгексакарбоновой-4,4',5,5',8,8' кислоты (798) с первичными алифатическими, ароматическими или гетероциклическими аминами в избытке амина, в воде или в органических растворителях при 100-150 °C. Они представляют исключительный интерес, т. к. среди кубовых красителей отсутствуют красители, окрашивающие в алый и чисто-красный цвета. Оттенки зависят от природы заместителей в арильном остатке, связанном с имидной группой, которые влияют на кристаллическую структуру агрегатов красителя, образующихся на волокне в процессе крашения. Например, при взаимодействии диангидрида (798) с 2,5-диметиланилином получается кубоген [799; R = 2,5-(СН3)2С6Н3], образующий окраски алого цвета, с .м-толуидином — кубоген [799; R = л/-СН3СбН4], образующий окраски красного цвета, с 3,5-диметиланилином — кубоген [799; R = 3,5-(СН3)2С6Н3], образующий окраски нейтральнокрасного цвета.
Симметричные кубогены типа (800) образуют окраски сине-фиолетовых и синих цветов. Получают кубогены взаимодействием диангидрида (798) с ароматическими орто- или ле/щ-диаминами в водной среде при 100-110 °C и pH = 6,3-^6,8. В отличие от многих синих кубовых красителей, образуемые ими синие окраски не изменяются при смачивании водой.
Несимметричные кубогены типа (801) образуют окраски фиолетового цвета. Получают кубогены взаимодействием диангидрида (798) последовательно с ароматическими орто- или ле/ш-диаминами и первичными алифатическими, ароматическими или гетероциклическими аминами. Синтез проводят следующим образом: сначала диангидрид (798) взаимодействует с орто-диамином [1,3 моль диамина на 1 моль (798)] в водной среде при 100-107 °C и pH = 6,3^-6,8, т. е. в условиях синтеза кубогенов типа (800). При этом образуется мо-нодиазаинденофеналеновое производное, содержащее до 25 % примеси соединения типа (800). Примесь легко отделяется, т. к. при pH = 9^-9,5 выпадает в осадок, и может без дополнительной очистки применяться в качестве кубогена синего цвета. Оставшееся же в водном растворе монодиазаинденофеналеновое производное обрабатывают первичными аминами в той же среде при
(797)
814
Новый справочник химика и технолога
100-110 °C. Так получают, в частности, на основе о-фенилендиамина и м-толуидина кубоген (802), образующий окраски фиолетового цвета. Фиолетовые окраски, полученные с помощью кубогенов, не изменяются при смачивании водой.
соединение перинонового красителя, которое далее окисляют кислородом воздуха, пероксидом водорода или другими окислителями, как при обычном кубовом крашении. В результате на волокне образуются периноновые красители, например, алый (803) из кубогена (799; R = 2,5-(СНз)2С6Н3), синий (804) — из кубогена (800), фиолетовый (805) — из кубогена (802).
Кубогены хорошо растворимы в воде и равномерно распределяются на ткани, что обеспечивает получение ровных окрасок. Они могут применяться сами по себе, а также с обычными кубовыми и активными красителями, что весьма ценно при узорчатой расцветке тканей методом печати. Применение кубогенов дает возможность снизить расход восстановителей и щелочных агентов при крашении, а следовательно, уменьшить загрязнение сточных вод текстильных предприятий. Все это выдвигает кубогены в число наиболее перспективных видов красителей.
Меры предосторожности в производстве периноновых красителей
Производство периноновых красителей связано с использованием и получением ряда токсичных (ароматические амины и др.), пожаро- и взрывоопасных (растворители) веществ. При работе с ними следует соблюдать необходимые меры безопасности, сведения о которых имеются в предыдущих главах.
Крашение кубогенами производится в щелочной среде (pH = 10,5-И 2,8) в присутствии восстановителя (дитионит натрия, ронгалит, диоксид тиомочевины); скорость превращения кубогена в краситель зависит от температуры: при 80 °C оно завершается за 30 мин, при 95-100 °C — за 5-7 мин. В процессе крашения от молекулы кубогена отщепляются две молекулы СО2 и образуется периленовое ядро. При этом получается лейко-
4.3.5.13. Макрогетероциклические красители
Фталоцианиновые красители
Основой молекул фталоцианиновых красителей является тетразапорфиновое (порфиразиновое) кольцо (806), построенное из четырех остатков пиррола, связанных атомами азота («внешние» атомы макроцикла). Тетразапорфин близок по строению к порфину (807) —
Ароматические соединения
815
соединению, входящему в состав молекул красящих веществ природного происхождения: гемина крови, хлорофилла, витамина В)2 и др.
—► Азогены (зеленые) Активные (бирюзовые, зеленые) Кубовые (голубые)
—► Пигменты
Фталоцианиновые (голубые, бирюзовые, зеленые) красители
—► Протравные (бирюзовые)
-► Прямые (бирюзовые)
—Цианалы (голубые)
(808)
Все практически интересные фталоцианиновые красители содержат остатки бензопиррола (изоиндола), связанные атомами азота в тетрабензотетразапорфиновое (тетрабензопорфиразиновое) кольцо фталоцианина (808).
Тетразапорфин (806) и его тетрабензопроизводное (фталоцианин) могут существовать в шести таутомерных формах. Каждая из таутомерных форм может быть описана двумя предельными структурами, т. е. распределение электронов в тетразапорфине описывается двенадцатью предельными структурами.
Атомы водорода -NH-групп в молекулах тетразапорфина и фталоцианина способны замещаться катионами металлов, например при нагревании с металлом или его солью в высококипящем органическом растворителе. Но поскольку атомы азота пиррольных колец в молекулах тетразапорфина и фталоцианина пространственно сближены, то возможно не только простое со-леобразование, но и комплексообразование. С катиона
ми К , Na+, Са2+, Ва2’ и Cd2* фталоцианин образует соли, не растворимые в органических растворителях; они не возгоняются, а при действии кислот распадаются с образованием свободного («безметалльного») фталоцианина. С катионами большинства остальных металлов образуются типичные внутрикомплексные соединения, возгоняющиеся в вакууме без разложения, устойчивые к действию кислот, слабо растворимые в высококипящих органических растворителях (например, в хинолине).
Поскольку в комплексообразовании с металлами участвуют своими неподеленными парами электронов два атома азота макроцикла, комплексообразование сопровождается изменением цвета. В случае фталоцианина цвет красителя изменяется от красновато-голубого до зеленого в зависимости от природы комплексообра-зователя (платина, железо, кобальт, свинец, серебро, никель, цинк, медь, алюминий, бериллий, хром, церий, стронций, магний). Вследствие сложности сопряженной системы и глубокого цвета самого фталоцианина резкого изменения цвета при комплексообразовании не происходит. Как тетразапорфин и фталоцианин, так и их комплексы имеют сложные кривые поглощения с несколькими максимумами в видимой части спектра.
Фталоцианины образуются при нагревании ароматических о-дикарбоновых кислот или их ангидридов с аммиаком или веществами, разлагающимися с выделением аммиака (например, с мочевиной), что удобнее, т. к. процесс можно вести при нормальном давлении. Реакцию можно вести как в среде растворителя, так и без него (методом запекания), а также с применением катализаторов. Растворителем обычно служит трихлорбензол. В качестве катализаторов применяют пентаоксид мышьяка, молибдат аммония, борную кислоту и др.
Практически можно применять любое из производных о-дикарбоновых кислот, причем реакция всегда протекает через стадию образования о-динитрила. Например, в случае фталевой кислоты последовательно образуются фталевый ангидрид, фталимид (809), фталамид (810) и фталодинитрил (81 /а), который далее реагирует в мезомерной форме биполярного иона ими-ноизоиндоленина (8116), образуя молекулу фталоцианина (808).
Заключительная стадия процесса образования фталоцианина облегчается присутствием металла, выполняющего роль координационного центра, вокруг которого группируются биполярные ионы иминоизоиндо-ленина (так называемая темплейтная, т. е. «по шаблону», циклизация)', при этом образуется комплекс фталоцианина с соответствующим металлом— металлфталоцианин (812).
Наиболее чистые продукты с высоким выходом образуются при использовании о-динитрила. Однако фталодинитрил (811) очень токсичен и дорог. Получают его продуванием аммиака через расплавленный фталевый ангидрид при 340 °C с последующим подогревом образующейся смеси паров ангидрида и аммиака до 400 430 °C.
816
Новый справочник химика и технолога
(808) (812^
Вместо фталевого ангидрида, подобрав соответствующий катализатор, можно применять о-ксилол, который, окисляясь во фталевый ангидрид, сразу реагирует с аммиаком с образованием фталодинитрила. Из-за токсичности и высокой стоимости фталодинитрила фталоцианины часто предпочитают получать непосредственно из фталевого ангидрида. При этом, несмотря на то, что при проведении реакции в среде растворителя (трихлорбензол) процесс протекает более гладко и продукт получается лучшего качества, нередко предпочитают обходиться без растворителя (методом запекания), т. к. при нагревании трихлорбензола в условиях реакции могут образовываться токсичные продукты.
Металлфталоцианины существуют в четырех кристаллических модификациях: двух а- (устойчивой и неустойчивой), 0- и у-, которые отличаются по оттенкам и свойствам. Практическое значение имеют главным образом а- и 0-модификации.
При синтезе металлфталоцианинов любым способом образуется 0-модификация, легко переходящая в неустойчивую a-модификацию при осаждении металлфталоцианина водой из раствора в концентрированной H2SO4 или при его возгонке в вакууме при температуре ниже 200 °C. При действии органических растворителей или при нагревании выше 200 °C неустойчивая a-модификация снова переходит в 0-модификацию. При наличии хотя бы в небольшой части молекул медьфталоцианина атома хлора в положении 4, что может быть достигнуто частичным хлорированием, или при добавлении к нехлорированному медьфталоцианину небольшого количества монохлорзамещенного, а-мо-дификация становится устойчивой к органическим растворителям. При размешивании металлфталоцианина в разбавленной серной кислоте (концентрации ниже 60 %) получается у-модификация.
Экономически наиболее выгодно использование 0-модификации металлфталоциаиинов, т. к. при этом отпадает необходимость в дополнительных операциях, в ходе которых к тому же образуется нежелательный отход — разбавленная серная кислота. Однако красящая способность 0-модификации хуже, и это часто вынуждает переводить ее в другие, главным образом, в одну из а-модификаций.
0-Модификация и устойчивая a-модификация применяются в красочных составах, содержащих органические растворители. Неустойчивая a-модификация обладает наибольшей красящей способностью (образует наиболее интенсивные окраски) и применяется в полиграфических красках и лакокрасочных составах, не содержащих органических растворителей.
Фталоцианиновые пигменты. Важнейшими фталоцианиновыми красителями являются пигменты на основе медьфталоцианина (812’, М = Си). Они не растворимы в воде, маслах, спиртах и большинстве других органических растворителей, исключительно устойчивы к действию света, высокой температуры, к действию кислот и щелочей. Медьфталоцианин на воздухе выдерживает без разложения нагревание до 500 °C, в вакууме возгоняется без разложения при 580 °C, не разрушается расплавленными едкими щелочами и кипящими кислотами. Высокая свето- и термостойкость, красивые и чистые оттенки делают пигменты на основе медьфталоцианина исключительно ценными для полиграфии (цветная печать), лакокрасочной промышленности (окраска автомобилей и т. п.), для крашения резины, пластических масс и т. д.
Для получения медьфталоцианина из фталодинитрила тщательно измельченную смесь последнего с CuCl нагревают (запекают) во вращающейся печи непрерывного действия до расплавления фталодинитрила (Тпл = 141 °C), после чего начинается экзотермический
Ароматические соединения
817
процесс образования медьфталоцианина. Температура при этом поднимается до 260-300 °C. Наряду с медьфталоцианином образуется некоторое количество его 4-хлорзамещенного в результате участия в реакции СиС12 (уравнения (4.3.28) и (4.3.29)). Образование примеси медьмонохлорфталоцианина дает возможность получать краситель в устойчивой a-модификации без дополнительной операции частичного хлорирования.
4(C6H4)(CN)2 + 2CuCl -> C32H16N8Cu + CuCl2 (4.3.28)
4(C6H4)(CN)2 + CuCl2 -> C32H15C1N8Cu + HCI (4.3.29)
Очистка красителя от примесей и превращение 0-модификации в устойчивую a-модификацию происходит в процессе переосаждения соединения из серной кислоты. Полученный таким образом краситель выпускается под названием Пигмент голубой фталоцианиновый У (У — устойчивый).
Для получения более яркого пигмента с зеленоватым оттенком технический медьфталоцианин, содержащий примесь монохлорзамещенного, переводят в сульфат, последний выделяют и гидролизуют. Полученный продукт выпускают под названием Пигмент голубой фталоцианиновый ЗУ.
Из-за примеси монохлорзамещенного таким способом невозможно получить пигмент в неустойчивой a-модификации, которая благодаря яркости и интенсивности окраски представляет большую ценность для производства полиграфических красок. Поэтому пигмент в неустойчивой a-модификации получают из фталевого ангидрида, мочевины и CuCl (мольное соотношение приблизительно 4:14:1) в трихлорбензоле в присутствии катализатора (As2O5) при 200 °C. Полученный технический продукт обрабатывают серной кислотой и касторовым маслом. В результате взаимодействия касторового масла с кислотой образуется поверхностно-активное вещество «ализариновое масло», в присутствии которого краситель выделяется в высокодисперсном состоянии. Таким способом получают самый яркий среди всех голубых фталоцианиновых пигментов — Пигмент ярко-голубой фталоцианиновый К.
При диспергировании этого пигмента в органических растворителях в присутствии NaCl вновь образуется 0-модификация — Пигмент голубой фталоцианиновый Б43У (Б — бета), обладающий чистым зеленоватым оттенком и применяющийся в полиграфии и лакокрасочной промышленности в составах, содержащих органические растворители.
Самый дешевый фталоцианиновый краситель — Пигмент голубой фталоцианиновый — получают из фталевого ангидрида, мочевины и CuCl методом запекания; в качестве катализатора при этом обычно используют борную кислоту.
Частичным хлорированием медьфталоцианина, полученного из фталевого ангидрида, или добавлением
к нему монохлорсодержащего медьфталоцианина можно получить исходные продукты для производства пигментов в устойчивой а-модификации.
Некоторые фталоцианиновые красители не содержат координационно-связанного атома металла; их называют «безметалльными» фталоцианинами. Безме-талльный фталоцианин (808) образуется в неустойчивой a-модификации; по оттенку он зеленее медьфталоцианина. Частичным хлорированием его переводят в устойчивую a-модификацию. В зависимости от степени хлорирования получают Пигмент зеленовато-голубой У (5 % хлора) или Пигмент бирюзовый 43 (20 % хлора). Оба пигмента применяются в полиграфии и лакокрасочной промышленности, но постепенно вытесняются более дешевыми пигментами на основе 0-модификации медьфталоцианина.
Исчерпывающим хлорированием медьфталоцианина в расплаве хлоридов алюминия и натрия или тионил-хлорида (SOC12) и хлорида алюминия, с последующим переосаждением продукта хлорирования из 100% серной кислоты, получают соответственно Пигмент зеленый фталоцианиновый и Пигмент ярко-зеленый фталоцианиновый. В обоих случаях в молекулу вступают от 14 до 16 атомов хлора.
Зеленые фталоцианиновые пигменты по химической устойчивости и устойчивости окрасок несколько уступают голубым (влияние большого числа атомов хлора), но, тем не менее, являются самыми ценными зелеными пигментами для полиграфии, лакокрасочной промышленности, крашения пластических масс и резиновых изделий.
Практический интерес в качестве пигментов представляют арилированные фталоцианины, т. к. в отличие от хлорсодержащих красителей, таких, как Пигмент зеленый фталоцианиновый, они устойчивы к действию щелочей при нагревании. Представителем арилирован-ных фталоцианинов является Гелиоген зеленый П (814), получаемый нагреванием 3,4-дицианодифснила (813) с CuCl. При этом образуется смесь изомеров Си-Ф(С6Н5)4, различающихся положением фенильных остатков.
с6н5
(814)
818
Новый справочник химика и технолога
Прямые красители. При сульфировании медьфталоцианина (Си-Ф) 25% олеумом образуется дисульфокислота (положение сульфогрупп не установлено), натриевая соль которой [Си-Ф(80з\а)2; Ф — остаток фталоцианина] выпускается под названием Прямой бирюзовый светопрочный. Краситель применяется для крашения хлопка, вискозного волокна, полушерсти и шелка, а также для изготовления Лака бирюзового (бариевая соль, осажденная на гидроксиде алюминия), который используется в производстве обоев, полиграфической и бумажной промышленности.
При взаимодействии медьфталоцианина с хлорсульфоновой кислотой в присутствии тионилхлорида образуется тетрасульфонилхлорид Си-Ф(8О2С1)4, который является исходным продуктом для получения ряда красителей. Например, обработка тетрасульфонилхло-рида аммиаком приводит к получению смеси моно- и дисульфонамидов; оставшиеся сульфонилхлоридные группы гидролизуют до сульфогрупп. При этом получается смесь красителей, выпускаемая под названием Прямой бирюзовый светопрочный К (575); краситель образует окраски более чистого оттенка и более светостойкие, чем Прямой бирюзовый светопрочный.
Си-Ф(8О2С1)4 + NH3 -► Си-Ф(8О2\Н2)1 2 (SO2C1)3 2
Си-Ф(8О2МН2)]_2 (SO2C1)3 2 + Н2О Си-Ф(8О2ЫН2)]_2 (SO3H)3_2 (815)
Взаимодействием тетрасульфонилхлорида с 3-ами-но-5-сульфосалициловой кислотой получают краситель Хромовый бирюзовый для шелка (816). Краситель содержит 1-2 сульфоанилидных остатка, содержащих орио-расположенные гидрокси- и карбоксильную группы, обусловливающие способность к комплексообразованию с металлами.
Особую ценность имеют прямые красители, полученные на основе арилированных фталоцианинов. Исключительно светостойкий прямой краситель Сириус ярко-зеленый ФФГЛ (818) получают нагреванием дифенилтрикарбоновой-2,4,5 кислоты (817) с мочевиной и СиС12.
НООС с6н5 {818)
Трудности, связанные с получением дифенилди- и трикарбоновых кислот, ограничивают возможности производства этих светостойких зеленых красителей.
Введение в бензольные кольца молекул фталоцианинов разветвленных алкильных остатков, в частности m/jew-бутильных групп: (СН3)3С, делает кристаллическую структуру красителей рыхлой, т. е. ослабляет силы межмолекулярного взаимодействия между отдельными молекулами в кристаллах. Такие красители растворимы в органических растворителях, что расширяет возможности их практического использования. В частности, они пригодны для изготовления высококачественных паст для шариковых ручек.
При сульфировании S-содержащего аналога фталоцианина меди, полученного из дигидродитиоциклоизо-
индоленина, jw-фенилендиамина и соли меди, образуется растворимый краситель (819), окрашивающий целлюлозное волокно в черный цвет.
Ароматические соединения
819
Кубовые фталоцианиновые красители. Фталоцианиновые красители могут использоваться в качестве кубовых. При восстановлении их дитионитом натрия в щелочной среде образуются лейкосоединения, обладающие хорошим сродством к целлюлозным волокнам (мощная л-электронная система, атомы азота, способные участвовать в образовании водородных связей). Чтобы лейкосоединение легче переходило в раствор, в молекулу фталоцианина часто вводят одну сульфогруппу.
Исключительный интерес представляет моносульфокислота кобальтфталоцианина (820). Она не растворима в воде, т. к. одной сульфогруппы недостаточно, чтобы сообщить растворимость соединению с такой большой молекулярной массой. Но сульфогруппа облегчает переход в раствор лейкосоединения (821). Не исключено, что в процессе восстановления красителя в лейкосоединение и в процессе крашения происходит десульфирование красителя, т. е. краситель, образующийся на волокне после окисления лейкосоединения, не содержит сульфофуппы.
(820) (821)
Моносульфокислота кобальтфталоцианина выпускается под названием Кубовый голубой фталоцианиновый (820). Краситель применяется для крашения хлопка и вискозного волокна; окраски обладают высокой устойчивостью к свету, устойчивы к стирке, но мало устойчивы к действию хлора.
Активные фталоцианиновые красители. Введение в молекулы фталоцианиновых красителей заместителей, способных взаимодействовать с окрашиваемыми материалами с образованием ковалентных связей, приводит к образованию активных фталоцианиновых красителей.
Активные фуппы в молекулы фталоцианинов обычно вводят, используя сульфонилхлориды. При этом в реакции с сульфон ил хлоридом применяют либо амин, уже содержащий активные фуппировки, либо сначала получают промежуточный продукт, содержащий способную ацилироваться аминофуппу, в которую и вводят активную фуппу.
Первым способом получают Ремазол бирюзовый Г (822). Краситель образуется при взаимодействии суль-фонилхлорида медьфталоцианина с натриевой солью 4-аминофенилсульфонилэтилсульфата при pH = 8-8,5.
По второму способу обычно сначала в реакцию с сульфонилхлоридом вводят соединения типа 2,4-ди-аминобензолсульфокислоты, а затем вторую аминофуппу остатка этой кислоты ацилируют цианурхлоридом с последующим или предварительным замещением в нем одного из атомов хлора аминофуппой (действием аммиака) или остатком аминобензолсульфокислоты (например, действием метаниловой кислоты). Таким путем получают активный краситель Цибакрон бирюзовый ГФП (823).
Си—Ф(8О2С1)4 +
SO2(CH2)2OSO3H
Си-Ф^О^а)^
(822)
Си-Ф(8О3№)3
Накопление сульфофупп в красителях такого типа очень выгодно, т. к. они понижают сродство к целлюлозе и увеличивают растворимость как самого красителя, так и продуктов его гидролиза, образующихся
820
Новый справочник химика и технолога
в процессе крашения, что облегчает удаление продуктов гидролиза с окрашенного материала и тем самым повышает качество окрасок.
Смешивая активные бирюзовые фталоцианиновые красители с активными азокрасителями ярко-желтого (лимонного) цвета, получают смесевые активные ярко
зеленые красители. Однако с помощью цианурхлорида остатки фталоцианиновых красителей и азокрасителей можно связать в единую молекулу гибридного азофталоцианинового красителя, в котором проявляется эффект внутримолекулярного смешения цветов. Таков, например, активный ярко-зеленый краситель (824).
Cu-<D(SO3Na)3_2
(824)
Азогены на основе фталоцианинов. Использование обычных азотолов (см. 4.3.5.1) не позволяет получать окраски ярко-зеленого цвета, равноценные по светостойкости окраскам желтого, красного и других цветов. Для этой цели применяют сложные (комбинированные) азотолы, с помощью которых
нужный цвет получается на основе эффекта внутримолекулярного смешения цветов. К числу таких азотолов относится Азотол зеленый (827), который получают взаимодействием тетрасульфонилхлорида никельфталоцианина (825) с 1-(4-аминофенил)-3-метилпиразо-лоном-5 (826).
НО
Ароматические соединения
821
При сочетании этого азотола на волокне с диазосоединениями бензольного ряда, например, с диазосоединением, полученным из Азоамина красного С (2-амино-4-хлортолуола), образуется сложный гибридный азофталоцианиновый краситель ярко-зеленого цвета [четыре азогруппы вступают в положения 4 пиразолонового кольца (отмечены звездочкой)]. Окраски отличаются высокой устойчивостью к свету и стирке.
Из Азотола зеленого (827) и диазамина [(828)', на основе Азоамина красного С] получают Диазаминол зеленый светопрочный Н; при проявлении его на волокне образуется тот же ярко-зеленый гибридный краситель.
Цианалы (алцианы). Цианалами называют фталоцианиновые красители, содержащие четвертичные аммониевые или третичные сульфониевые группы, благодаря которым красители способны растворяться в воде. В широком смысле слова цианалы — это один из видов растворимых производных любых нерастворимых красителей; например, кубовые красители, не являющиеся производными фталоцианина, могут быть превращены в растворимые производные типа циана-лов, способные окрашивать текстильные волокна из водных растворов.
Получение цианаловых красителей состоит из двух стадий.
1. Хлорметилирование нерастворимого красителя, например, действием формальдегида и хлористого водо
рода в присутствии хлорида алюминия и пиридина (уравнение (4.3.30)).
Cu-Ф + СН2О + НС1 Л1СЦ>- Си-ФСН2С1 (4.3.30)
(829)
В молекулу медьфталоцианина удается таким способом ввести до восьми хлорметильных групп. Обычно для получения цианаловых красителей бывает достаточно двух хлорметильных групп.
2. Взаимодействие хлорметильных производных медьфталоцианина (829) с третичным амином (в том числе с пиридином), алкантиолом (с последующим алкилированием диалкилсульфатом или алкиловым эфиром п-толуолсульфокислоты), или тетраалкилтиомочс-виной. В результате соответственно образуются четвертичные аммониевые (830), пиридиниевые (831), третичные сульфониевые (832) или тиурониевые (833) соли — цианалы.
Тиурониевая соль медьфталоцианина выпускается под названием Цианал голубой (833).
Цианаловые красители растворимы в воде и обладают сродством к целлюлозным волокнам. Применяются в гладком крашении и печати. После крашения волокно обрабатывают раствором соды, а после печати — запаривают (в состав для печати наряду с цианалом входят уксусная кислота и ацетат натрия). Четвертичные и третичные ониевые соли при этом распадаются и на волокне прочно закрепляется нерастворимый краситель (уравнения (4.3.31) и (4.3.32)).
В случае пиридиниевой и тиурониевой солей также образуется нерастворимый краситель или эти соли ведут себя как активные красители, образуя ковалентную связь с целлюлозой за счет отщепления пиридиниевой или тиурониевой групп (уравнения (4.3.31) и (4.3.32)).
N(C2H5).
Си-ФСН2С1 (829)
CH,SNa
N(CH3)2 (H3c')2N—Z
s
Си—ФСН2М(С2Н5)3СГ
(830)
Си-ФСН2МС5Н5СГ
c5h5n Л
/ Сц-ФСН28СН3 N(CH3)2
/ Си-ФСН?8—
N(CH3)2 (833)
(CH3)2SO.
(831) Си-ФСН28(СН3)2СН38О4
(832)
Си-ФСН2Ь1(С2Н5)3СГ
Сц-ФСН21Ч(С2Н5)3 + с2н5ои
(4.3.31)
Си-ФСН28(СН3)2СН38О4 -co^^NaSO^ Си“фсн25снз + СН3ОН
(4.3.32)
822
Новый справочник химика и технолога
Си-ФСН2ТЧС5Н5СГ + Целл—ОН ^аа-н2сЛ Целл-ОСН2Ф—Си + C5H5N (4.3.33)
+
N(CH3)2 COONa
Си-ФСН28-С + Целл-ОН _CH соон'"NaO Целл—ОСН2Ф—Си + (CH3)2NCS (4.3.34)
N(CH3)2
Фталоцианогены. Фталоцианогенами (или фталогенами) называют соединения, из которых получают нерастворимые фталоцианиновые красители непосредственно на волокне.
Большая часть фталогенов — это производные фта-лодинтрила. Наиболее распространенным из них является 1-амино-З-иминоизоиндоленин (834), который получают из фталевого ангидрида, мочевины и нитрата аммония при 165-190 °C. Образующийся в виде нитрата продукт при действии щелочи превращается в свободное основание, которое выпускается под названием Фталоцианоген голубой 43М (834).
Известны фталогены бирюзового и зеленого цветов, например, Фталоген ярко-зеленый ИФФБ, являющийся фенильным производным 1-амино-З-иминоизоиндоле-нина (835).
1-Амино-З-иминоизоиндоленин (834) хорошо растворяется в воде при нагревании; при этом он гидролизуется с образованием «неактивных» форм (1-оксо-З-иминоизоиндоленина и фталимида).
Для предупреждения гидролиза фталогенов их вводят в красильные растворы и печатные краски только после предварительного растворения в органических растворителях (реже в муравьиной или уксусной кислоте). Исключение составляют отечественные фталогены, которые выпускают в виде порошков, содержащих мо
чевину. При растворении этих порошков в воде мочевина предупреждает гидролиз и агрегацию молекул фталогена.
Фталоцианогены применяются в виде паст, в состав которых кроме них входят соли металлов-комплексо-образователей (обычно хлориды, бромиды или ацетаты меди или никеля), высококипящие растворители, обладающие свойствами восстановителей (этилен- и диэтиленгликоли, формамид, диметилформамид и др.), и различные добавки (поверхностно-активные вещества и др.). После нанесения пасты на ткань и высушивания в течение нескольких минут при 45-70 °C ткань подвергают действию перегретого водяного пара при 135— 140 °C. В этих условиях на волокне происходит образование тетразапорфинового кольца и комплексообразование с металлом; в результате образуются яркие и очень устойчивые окраски.
Полимерные фталоцианины. Если в качестве исходных продуктов для синтеза фталоцианинов взять тетракарбоновые кислоты или их производные (ангидриды, имиды, нитрилы и т. п.) с попарно о/это-распо-ложенными карбоксигруппами, например пиромеллитовую кислоту (836) или кислоту [837; X = СН2, (СН2)„, СО, О, SO2 и т. п.], то образуются полимерные фталоцианины, в макромолекулах которых внутренние макрокольца фталоцианинового остатка связаны друг с другом.
НООС./^.СООН НООС./^. ^<^,соон
ТУ ТУСГ
НООС^^^ТООН НООС'^^ ^^соон
(836)
(837)
Например, сплавлением пиромеллитовой кислоты (836) с мочевиной и солями металлов в присутствии катализаторов получают полимеры сетчатой структуры, в которых внутренние макрокольца связаны бензольными остатками. Если в реакцию ввести соли разных металлов, получаются полиметаллические полимерные хелаты, содержащие в одной макромолекуле различные металлы.
Полимерные фталоцианины представляют большой интерес в качестве органических полупроводников и катализаторов.
Применение фталоцианинов в электронной технике и в качестве катализаторов. Металлфталоцианины нашли применение в электронной технике в качестве органических полупроводников, а также в лазерной технике.
Ароматические соединения
823
В отличие от неорганических полупроводников металлфталоцианины сочетают высокое электрическое сопротивление и относительно безынерционную фотопроводимость с большой кратностью фототока к темновому току. Это позволило использовать слои медьфталоцианина в качестве фоточувствительной мишени для передающей телевизионной трубки. Прессованные таблетки магнийфталоцианина, покрытые тонкой пленкой тетраметил-«-фенилендиамина, используются в качестве фотопреобразователей. Тонкопленочные диоды из медьфталоцианина применяются в электронных цифровых вычислительных машинах. Диоды на основе медьфталоцианина с электродами из меди и из пленки алюминия или серебра работают как выпрямители с коэффициентом выпрямления 103.
Все эти области применения фталоцианинов основаны на уникальных особенностях их молекул — наличии макроциклической сопряженной системы, в которой степень делокализации л-электронов очень велика, уровни энергий верхней занятой МО и нижней свободной МО настолько сближены, что молекула способна одинаково легко отдавать и присоединять электрон, что характерно для полупроводников. В то же время сочетание высокой химической и термической устойчивости металлфталоцианинов со способностью легко возгоняться, позволяющей получать слои толщиной 10~5-10”4 см, которые обладают высокой механической и электрической устойчивостью и воспроизводимыми электрофизическими характеристиками, обусловливают простоту технологии соответствующих электронных устройств.
Некоторые металлфталоцианины используют в качестве катализаторов. Применение их для катализа реакций окисления позволяет очищать отходящие газы
промышленных предприятий от трудно удаляемых малых примесей органических соединений, а также осуществлять обессеривание нефтепродуктов.
Особый интерес в качестве катализаторов представляют полимерные фталоцианины. Некоторые из них обладают более высокой каталитической активностью, чем соответствующие мономеры. Полимерные фталоцианины с разными металлами в макромолекуле проявляют синергизм и избирательность в реакциях каталитического окисления.
Сопряженные и несопряженные аналоги фталоцианина
Все известные фталоцианиновые красители имеют глубокие цвета — голубые, бирюзовые, зеленые, т. к. их основу составляет тетрабензотетразапорфин, который сам имеет синий цвет.
Для получения подобных фталоцианину макрогс-тероциклических красителей более высокого цвета необходимо разорвать (разомкнуть) цепочку сопряжения макрокольца фталоцианина или уменьшить число л-элсктронов в хромофорной системе красителя. Получение такого типа соединений осуществляют ступенчатым синтезом: сначала получают нециклические фрагменты молекул и затем макрогетероциклические соединения (макрогетероциклы). Нециклические соединения получают, используя 3,3-диалкокси-1-иминоизоиндоленин (838) или 1-амино-З-иминоизо-индоленин (834), которые при взаимодействии с ароматическими диаминами образуют бис[(1-амино-изоиндоленилиден-3)амино]арилены (839). Полученные арилены легко взаимодействуют с диаминами (теми же или другими), образуя макрогетероциклические соединения (840).
Ar(NH2)2^
-ROH
N—Ar—N
(839)
Ar'(NH2)2
-NH3
N—Ar—N
N=Ar'=N
(840)
По этой схеме, применяя в качестве диаминов лг-фе-нилендиамин, 2,6-диаминопиридин, 2,5-диамино-1,3,4-тиадиазол и др., получены различные макрогетероциклические соединения (841)-(846).
В соединении (841) единая сопряженная система макрокольца сохраняется, но число л-электронов по сравнению с фталоцианином (тетрабензотетразапорфином) значительно меньше. Во всех остальных соединениях не только уменьшилось число л-электронов, но и сопряженная система макрокольца разомкнута остатками диаминов: в соединениях (842), (843) и (844) — один раз, а в соединениях (845) и (846) — дважды. Соответственно соединение (841) имеет красно-коричневый цвет, соединение (842) — пурпурный, (843)
и (844) — оранжевый, а (845) и (846) — желтый. Образование комплексных соединений с металлами приводит к незначительному углублению цвета: например, при комплексообразовании соединения (845) с солями меди цвет изменяется от желтого до оранжевого. Медный комплекс соединения (842) известен как высокоэффективный свето- и термостабилизатор полиамидной смолы под названием Стабилин-9.
Подобно фталоцианинам, комплексные соединения макрогетероциклических соединений существуют в различных кристаллических модификациях; например, желтый цвет кристаллов соединений (845) и (846) после возгонки в вакууме изменяется до оранжевого и красного соответственно.
824
Новый справочник химика и технолога
(841) (842>> ^45) (846)
(843) (844у
Несопряженные макрогетероциклические соединения (бесцветные) используются в качестве носителей хромофорной системы при получении пигментов, относящихся к другим классам красителей. Бесцветная мак-рогетероциклическая основа таких пигментов обусловливает их высокую температуру плавления, миграционную устойчивость и низкую растворимость в органических растворителях, а хромофорная система — чистоту и яркость окраски. В качестве примера можно привести ярко-желтый пигмент (847), полученный из цианурхлорида, 2,6-диаминопиридина и моноазокрасителя:
Пигменты такого типа отличаются высокой устойчивостью к действию органических растворителей и различных химических реагентов, высокой термостойкостью и миграционной устойчивостью в лакокрасочных покрытиях и резине.
Порфирины
Порфирины являются структурными аналогами фталоцианинов [простейшее соединение данной группы — порфин (807)]. Порфирины играют исключительно важную роль в природе: зеленый магниевый комплекс одного из порфиринов является основой структуры молекулы хлорофилла, красный железный комплекс— основой структуры гена (составной части гемоглобина крови).
Некоторые производные порфиринов применяются в качестве красителей. Из этих соединений большой
интерес представляют производные тетрабензопорфирина [(848)’, R = алкил, арил и др.] и их комплексы с металлами (849) — полные структурные аналоги фталоцианина.
Соединения (849) получают методом темплейтной циклизации фталимида или его калиевой соли с фенилуксусной кислотой и ее замещенными в присутствии солей металлов. Так, при взаимодействии фталимида калия с избытком фенилуксусной кислоты в присутствии ацетата цинка в течение 30 мин в токе азота при 350-360 °C получают цинковый комплекс мезо-тетра-фенилтетрабензопорфирина (850), представляющий собой зеленый жирорастворимый краситель, применяемый для крашения пластмасс. Аналогично получают кадмиевый комплекс, также являющийся зеленым жирорастворимым красителем.
Ароматические соединения
825
Гексаазациклотетрадециновые красители
Гексаазациклотетрадецин — это четырнадцатичленный макроцикл, обладающий способностью образовывать устойчивые комплексы с металлами. Красители данной группы получают темплейтной циклизацией о-амино-о'-галогеназосоединений или смесей о,о'-диа-мино- и о,о'-дигалогеназосоединений в присутствии солей металлов. Так, взаимодействием азокрасителя (857) с тетрагидратом ацетата никеля в диметилформа-миде в присутствии К2СО3 при кипении получают никелевый комплекс (852) — краситель темно-зеленого цвета.
(852)
Из о,о'-диаминоазобензола (853), азокрасителя (854) и Ni(OCOCH3)2 • 4Н2О в тех же условиях получают краситель (855) темно-зеленого цвета.
Гексаазациклотетрадециновые красители используются в качестве пигментов для крашения пластмасс, а в качестве дисперсных красителей — для крашения полиэфирных волокон и их смесей с целлюлозными волокнами в оливково-зеленые цвета разных оттенков; окраски устойчивы к свету и мокрым обработкам.
Меры предосторожности в производстве макро гетероциклических красителей
Производство макрогетероциклических красителей связано с использованием ядовитых, горючих, взрывоопасных, сильнодействующих веществ, таких как оксид
мышьяка, цианурхлорид, цианид натрия, концентрированная серная кислота, хлор, нитробензол и т. п., и таких процессов, как плавка при высокой температуре, хлорирование в расплаве хлоридов алюминия и натрия и т. п. О работе с такими веществами говорилось в предыдущих главах.
4.3.5.14. Флуоресцентные (оптические) отбеливатели
Флуоресцентные (оптические) отбеливатели представляют собой своеобразный класс белых красителей, применяемых для усиления эффекта «белизны» неокрашенных материалов (текстильных, бумаги, пластиче
826
Новый справочник химика и технолога
ских масс и др.), и являются частным случаем люминесцентных (флуоресцентных) красителей.
Люминесценцией называется выделение энергии в виде электромагнитного излучения (т. е. света) при переходе молекулы из возбужденного состояния в основное. Как правило, при люминесценции молекула излучает фотон меньшей энергии, чем поглощенный при возбуждении, т. к. часть поглощенной энергии расходуется на внутримолекулярные процессы и в конечном счете передастся окружающей среде в виде тепла (безызлучательные переходы). Но поскольку фотонам меньшей энергии соответствуют световые лучи больших длин волн, практически люминесценция заключается в преобразовании световых лучей в более длинноволновые.
Если этим свойством обладают соединения, поглощающие в видимой части спектра, т. е. обычные красители, то это приводит к значительному возрастанию яркости окраски. Такие красители называют флуоресцентными, люминесцентными, красителями-люминофорами. Они широко применяются в тех случаях, когда надо повысить яркость надписей или знаков, которые должны быть хорошо видны на больших расстояниях (например, в дневных флуоресцентных красках, используемых для нанесения опознавательных знаков на самолеты, морские суда, аэродромные устройства и т. п.), или для усиления декоративного эффекта (плакаты, театральные декорации, рекламные щиты и т. п.).
Если же флуоресцентными свойствами обладают бесцветные (т. е. не поглощающие в видимой области спектра) соединения, то их можно использовать в качестве флуоресцентных (оптических) отбеливателей.
Тела, поглощающие свет только в УФ-области спектра, кажутся нам белыми (или бесцветными). Однако многие «белые» тела (например, отбеленные ткани, бумага) в результате химических и физических воздействий (стирка, продолжительное действие солнечных лучей и т. п.) приобретают способность слабо поглощать и в коротковолновой видимой части спектра (400-480 нм). Именно поэтому белые ткани после стирки приобретают неприятный желтоватый оттенок (как и белая бумага, находящаяся длительное время на свету). Эффект подсинивания белья заключается в том, что механическое нанесение на поверхность выстиранных тканей ничтожного количества синего ультрамарина компенсирует убыль коротковолновых лучей видимой части спектра и искусственно дополняет спектр отраженных лучей до белого.
Такой же эффект вызывает нанесение на неокрашенные (белые) тела бесцветных соединений, способных поглощать лучи ближней УФ-части спектра и преобразовывать их в лучи коротковолновой видимой части (400-480 нм), т. е. именно в те лучи, которые поглощаются «пожелтевшими» белыми телами. Это приводит к компенсации поглощенной части видимых лучей и восполнению спектра отраженного света, вследствие чего тела кажутся часто даже значительно белее, чем сами по себе. Этот эффект называется эф
фектом оптического, или флуоресцентного, отбеливания, а соединения, обладающие такими свойствами, — оптическими (флуоресцентными) отбеливателями. Они широко используются при стирке, белении природных и синтетических текстильных материалов, бумаги, пластических масс, для повышения белизны при вытравной печати узоров на тканях и т. п.
Оптические отбеливатели входят в состав стиральных порошков, а также в состав веществ, используемых при химической чистке. В химической чистке для синтетических волокон обычно используются оптические отбеливатели, нс растворимые в воде, но растворимые в органических растворителях.
Как и красители, оптические отбеливатели должны обладать хорошей светостойкостью, устойчивостью к действию кислот и оснований, окислителей и восстановителей; они не должны образовывать комплексных соединений с металлами. Отбеливатели, используемые для отбеливания полимерных смол в массе, должны быть термостойкими.
Способ применения оптических отбеливателей аналогичен способу крашения прямыми и кислотными красителями: целлюлозные волокна обрабатывают соответствующими оптическими отбеливателями в нейтральной или слабощелочной ванне, полиамидное волокно, шелк, шерсть (весьма редко) — в слабокислой среде. Полиэфирное и ацетатное волокно отбеливаются дисперсными отбеливателями, а полиакрилонитрильные — катионными отбеливателями.
Отечественная промышленность выпускает оптические отбеливатели под названием «Белофоры» с добавлением буквенных обозначений. Первая буква означает сообщаемый отбеленному материалу оттенок, например, К — красный, О — оранжевый, С — синеватый. Вторая и третья буквы указывают на область применения: Ц — для целлюлозных волокон, Б — для бумаги, П — для полиамидного волокна, Д — для детергентов (моющих средств), Л — для полиэфирных волокон (лавсан), А — для ацетатных волокон, Н — для полиакрилонитрильного волокна (нитрон), Ш — для шерсти и шелка, В — для вискозы в массе, М — для других синтетических волокон в массе.
В качестве оптических отбеливателей применяются различные производные диаминостильбена, кумарина, пиразолина, нафталимида и т. д. Наиболее широкое распространение из них получили продукты ацилирования 4,4'-диаминостильбен-2,2'-дисульфокислоты (792) цианурхлоридом (226), имеющие общую формулу (856). Оставшиеся в цианурхлориде после взаимодействия с дисульфокислотой атомы хлора замещают одинаковыми или разными остатками, которые не оказывают значительного влияния на оптические свойства отбеливателей, но препятствуют химическому взаимодействию с отбеливаемым материалом и влияют на некоторые другие свойства соединений (растворимость и пр.). Эти отбеливатели обладают интенсивной фиолетово-голубой флуоресценцией и высоким сродством к целлюлозе.
Ароматические соединения
827
Примерами таких оптических отбеливателей являются:
Белофор КЦБ (557; R = Н, R' = R" - СН2СН2ОН) применяется для оптического отбеливания хлопка, льна, вискозного волокна и изделий из этих волокон, используется также для отбеливания бумаги и добавления в моющие средства. Растворимость препарата в воде небольшая, но увеличивается при добавлении соды.
Белофор ОЦД (557; R = Н, R' = С6Н4С1-о, R" = СН2СН2ОН) имеет более высокое сродство к целлюлозе, применяется для оптического отбеливания целлюлозных волокон и изделий из них. Рекомендуется для добавления в моющие средства, предназначенные для стирки изделий из шерсти, целлюлозных и полиамидных волокон. Растворимость в воде увеличивается при добавлении соды.
Белофор СБВ (557); R = R' = СН2СН2ОН, R" = С6Н4 SO3H-jk) применяется для отбеливания бумаги и вискозы в массе, хорошо растворяется в воде.
Очень ценный оптический отбеливающий препарат — Белофор КЦПБ (555) — получают из 4,4'-диами-ностильбен-2,2'-дисульфокислоты, цианурхлорида, метанола и анилина.
Белофор КЦПБ рекомендуется для отбеливания целлюлозных волокон и капрона, добавляется в моющие средства. Устойчив в растворах с pH = 5-Н2 и может применяться для оптического отбеливания в гидросуль-
фитной и перекисной ваннах, хорошо совместим с отделочными препаратами. Белофор КЦПБ обладает высокой субстантивностью и пригоден для совместного применения с пероксидом водорода и прямыми красителями при крашении трикотажных изделий в светлые тона.
Из других производных стильбена большое значение в качестве оптических отбеливателей имеют соединения с триазольными и оксазольными гетероциклическими остатками. Так, сочетанием бис(диазо)производ-ных 4,4'-диаминостильбен-2,2'-дисульфокислоты с 2-ами-нонафталин-1-сульфокислотой с последующим окислительным замыканием триазолового цикла получают 4,4'-бис(нафтотриазолил)стильбен-2,2'-дисульфокисло-ту (559).
При взаимодействии w-толилазолов, например 5-ме-тил-2-«-толилбензоксазола, с азобензолом и КОН в ди-метилформамидс в отсутствие воздуха образуется 4,4'-бис(5-метилбензоксазолил-2)стильбен (860).
Свойствами флуоресцентных отбеливателей обладают и более простые сопряженные азолы, например Белофор 2КМ (861), который получают взаимодействием З-амино-4-гидрокситолуола с малеиновым ангидридом.
828
Новый справочник химика и технолога
(861) СН3
могут быть получены, например, взаимодействием арилгидразинов с галогензамещенными жирноароматическими кетонами или с халконами.
Белофор 2КМ и другие производные бензоксазола нс растворимы в воде. Их применяют в виде тонкодисперсной суспензии для оптического отбеливания полиэфирных, ацетатных, полиамидных и полиакрилонитрильных волокон. Они обладают очень высокой светостойкостью, устойчивы к окислителям, в том числе к хлору, поэтому обработку ими можно совмещать с отбеливанием гипохлоритом натрия.
Хорошими оптическими отбеливателями являются производные кумарина, например Бланкофор АЦФ [этиловый эфир бензо[/]кумарин-3-карбоновой кислоты (863)], образующийся при конденсации 2-гидрокси-1-формилнафталина (862) с малоновым эфиром.
Бланкофор АЦФ (864) применяется для оптического отбеливания ацетатного шелка, капрона, лавсана, нитрона, он устойчив в растворах кислот, гипохлорита натрия, устойчив к дымовым газам.
Отбеливатель для ацетатных и полиамидных волокон 7-диэтиламино-4-метилкумарин (864) получают конденсацией jw-диэтиламинофенола с ацетоуксусным эфиром в присутствии безводного ZnCl2. Этот отбеливатель не растворим в воде и для оптического отбеливания химических волокон применяется в дисперсной форме. Его водорастворимая сернокислая соль применяется для отбеливания шерсти и натурального шелка. Арилированием 7-диэтиламино-4-метилкумарина солью бензолдиазония в среде органического растворителя в присутствии CuCl и CH3COONa получают ценный отбеливатель для ацетатных волокон — 7-диэтиламино-4-метил-З-фенилкумарин (865).
Большое практическое значение для оптического отбеливания ацетатных и синтетических (полиакрилонитрильных, полиамидных) волокон, а также моющих средств, применяемых для стирки изделий из таких волокон, имеют арилзамещенные пиразолины, которые
Так, при взаимодействии 4-хлорфенил-2-хлор-этилкетона с 4-сульфамоилфенилгидразином образуется гидразон (866), далее циклизующийся в 1 -(4-сульфамоилфенил)-3-(4-хлорфенил)пиразолин (867) — Белофор СНПА, который применяется для отбеливания полиакрилонитрильных, полиамидных и ацетатных волокон.
При взаимодействии халкона (868) с фенилгидрази-ном образуется гидразон (869), который циклизуется в 1,3,5-трифенилпиразолин (870), пригодный для оптического отбеливания природных и синтетических волокон и пленок.
При наличии в молекуле кислотных групп, например сульфогруппы, соединение проявляет свойства кислотного красителя и может быть использовано для отбеливания шерсти. К таким соединениям относится Тинопаль ВГ (871). Этот отбеливатель хорошо растворим в воде, имеет зеленовато-голубую флуоресценцию и применяется для оптического отбеливания белковых волокон из кислой ванны.
Ароматические соединения
829
На основе производных пиразолина получают также катионоактивные отбеливающие препараты (872), растворимые в воде и предназначенные специально для отбеливания полиакрилонитрильных соединений.
(872)
Практическое значение имеют отбеливатели на основе арилзамещенных имидазолов. Так, при взаимодействии бензоина с мочевиной и последующем сульфировании образовавшегося 4,5-дифенилимидазоли-нона-2 образуется отбеливатель Бланкофор ВТ (873), используемый для оптического отбеливания белковых волокон.
(873)
Производные имидазола общей формулы (874) используются для оптического отбеливания целлюлозных и полиамидных волокон.
(874) R = Н, СН3; R' = CH^ CH2SO3Na
Меры предосторожности в производстве оптических отбеливателей
Производство оптических отбеливателей по ассортименту используемых промежуточных продуктов мало отличается от производства других красителей, в частности активных хлортриазиновых красителей. Сведения о работе с ядовитыми, горючими и т. п. веществами содержатся в предыдущих главах.
4.3.6. Выпускные формы красителей
Технические красители не являются химически чистыми продуктами. Они содержат различное количество минеральных и органических примесей, которые могут быть как бесцветными, так и окрашенными. В техническом красителе также всегда имеется гигроскопически связанная вода, содержание которой может колебаться от 1 до 8 %. Поэтому для получения красителей со строго определенными колористическими свойствами: красящей способностью, оттенком и т. д. производится установка красителя на тип. За «тип» принимается образец стандартного красителя, с которым затем сравнивается качество красителя данной партии. Сначала производятся пробные выкраски испытуемым красителем и типовым образцом. Затем интенсивность окраски сравнивается визуально, или с помощью цветовых компараторов, или сопоставлением спектров поглощения растворов. Концентрация выпускаемого красителя, интенсивность окраски и оттенок должны совпадать с показаниями типового образца.
Расчет концентрации красителя обычно ведется не по содержанию химически чистого вещества в техническом препарате, а по способности такого препарата давать выкраску одинаковой интенсивности с той, которая получается при использовании такого же количества типового образца красителя. Поэтому концентрация красителя в техническом препарате может быть как ниже, так и выше типовой; например, концентрации 150 %, 200 % и т. д. означают, что для получения одинакового колористического эффекта следует брать в полтора, два и т. д. раза меньше красителя, чем типового.
Выпуск красителей с концентрацией ниже типовой не допускается. Выпуск красителей с концентрацией выше типовой допускается, однако нежелателен, т. к. потребителям удобнее иметь дело с красителями, концентрация которых точно соответствует «типу».
При установке на тип смешивают красители различных партий, отличающиеся по концентрации и оттенку
830
Новый справочник химика и технолога
от типового образца, подцвечивают небольшим количеством красителя другого цвета и добавляют разбавители (соли), если концентрация красителя выше концентрации типового образца. При этом необходимо учитывать влияние добавок на свойства красителей. Так, добавка солей (NaCl, Na2SO4) к кислотным красителям в дальнейшем замедляет процесс крашения, к прямым — ускоряет; добавка NaCl к сернистым красителям, как правило, ухудшает их красящие свойства и стабильность растворов, в то время как добавка тиосульфата улучшает эти свойства. Так как электролиты, особенно NaCl, ухудшают растворимость красителей в воде, то более предпочтительно применять в качестве разбавителей вещества типа декстрина или мочевины, которая иногда улучшает растворимость красителей.
Подцветка другими красителями с целью подгонки оттенка под типовой может производиться лишь с помощью таких красителей, которые не отличаются от подцвечиваемого по химическим свойствам (т. е. также являются кислотными или прямыми и т. д.) и близки по способности выбираться волокном из раствора, по светостойкости, сродству к волокну и др.
Основными выпускными формами красителей являются порошки и насты. Порошки удобнее для транспортировки и хранения, т. к. не содержат излишнего балласта (воды), не боятся низких температур (замерзания), но они образуют много пыли; в результате ухудшаются санитарные условия при их применении и часть красителя теряется. Пасты, как правило, удобнее для крашения, т. к. в этом случае красители не подвергают сушке, в процессе которой происходят дегидратация и агрегация частиц красителя, ухудшающие его смачиваемость, растворимость, устойчивость растворов и другие свойства, имеющие огромное значение для крашения. Поэтому предпочтительнее выпускать красители в виде непылящих порошков и гранул. Непылящие порошки содержат 1-2 % силиконовой жидкости или минерального масла, которые не ухудшают качества красителей. В этом случае пылеобразование снижается в 10-40 раз, что значительно улучшает условия при дозировке и приготовлении растворов красителей.
Гранулы красителей готовят путем подсушивания пасты красителя до содержания влаги 10-30 %, дробят крупные куски до размера 0,1-0,8 мм и окончательно высушивают. По другому способу суспензию красителя высушивают в распылительных сушилках со специальными распыляющими устройствами, сразу получая гранулы. Гранулы не слеживаются при хранении, легко смачиваются и суспензируются, удобны для дозировки.
Одним из важнейших показателей, характеризующих выпускные формы красителей, является степень дисперсности частиц. Требования к степени дисперсности красителя зависят от области применения и технологии крашения. Так, дисперсные и кубовые красители, предназначенные для крушения вискозы в массе (марка В), должны иметь наигысшую степень дисперсности (размер частиц менее Г мкм). Кубовые красители
в форме порошков для суспензионного крашения (марки Д) должны иметь высокую степень дисперсности (размер частиц не более 5 мкм). В то же время для кубовых красителей в форме паст для печати нежелательна высокая степень дисперсности (размер частиц ~ 15 мкм, не более), т. к. это может привести к браку при печатании узоров на тканях (пробивание гравюры). Нет необходимости в чрезмерно высокой степени дисперсности и в случае кубовых красителей в форме порошков для крашения, поскольку при крашении краситель переводят в раствор соли лейкосоединения («куб») или в тонкодисперсную суспензию свободного лейкосоединения («лсйкокислоту»).
Большое значение при выборе необходимой и достаточной степени дисперсности красителей имеет экономика производства, т. к. стоимость красителей значительно возрастает с увеличением степени их дисперсности.
Особое значение имеет добавка в порошки и пасты вспомогательных поверхностно-активных веществ. В случае порошков такие вещества облегчают смачивание и растворение красителя, для паст обеспечивают сохранение нужной степени дисперсности частиц красителя, устойчивость и однородность пасты.
Выпускают и жидкие формы красителей. Жидкие формы отличаются от обычных паст большей устойчивостью к осаждению и низкой вязкостью, хорошо размешиваются и дозируются; их доводят до нужной концентрации холодной водой. Они содержат меньше диспергаторов, смачивателей и других веществ, чем гранулы и порошки, что облегчает получение ровных окрасок.
Особое значение имеет выпуск красителей в виде стабильных концентрированных растворов (мелкодисперсных суспензий), в которых постоянство степени дисперсности обеспечивается добавкой поверхностноактивных веществ и защитных коллоидов. Такие растворы катионных красителей применяются для крашения полиакрилонитрильных и других волокон, растворы основных красителей применяются для крашения бумаги и др.
4.3.7. Очистка сточных вод в производстве красителей
Производство красителей связано с использованием огромного количества воды, значительная часть которой раньше сбрасывалась в загрязненном состоянии. В среднем на 1 т красителя расходуется около 225 т воды. Так как материальный индекс производства красителей составляет в среднем 10-20 т на 1 т готовой продукции, а по сложным красителям до 160-170 т, то при выпуске каждой тонны красителей вместе со сточными водами предприятия (при отсутствии очистных сооружений) сбрасывают в виде отходов десятки и сотни тонн различных минеральных и органических соединений, нарушающих кислородный режим водоемов, ядовитых для их флоры и фауны.
Ароматические соединения
831
Идеальным способом избавиться от загрязненных стоков является организация безотходных производств, при которых все соединения находят полезное применение. Это очень непростая задача, и в течение определенного периода времени производство красителей еще не станет безотходным. Поэтому неотложной проблемой является очистка сточных вод до такого состояния, когда они могут быть возвращены в производственный цикл, а при невозможности или экономической нецелесообразности этого — доведены до такой степени чистоты, когда сброс их в естественные водоемы не нанесет ущерба природе.
Действующие в нашей стране санитарно-гигиенические правила запрещают спуск загрязненных вод в естественные водоемы. Сбрасываемые сточные воды не должны изменять pH естественного водоема ниже 6,5 и выше 8,5, не должны снижать содержание растворенного кислорода ниже 4 мг/л, не должны изменять органолептические свойства воды и т. д. Поскольку сточных вод производства красителей, удовлетворяющих этим требованиям, практически не бывает, возникает проблема их очистки, которая нередко лимитирует не только расширение, но и нормальную эксплуатацию действующих заводов.
Из известных способов очистки сточных вод наибольший интерес представляют те, которые позволяют извлекать вещества, содержащиеся в сточных водах, для их дальнейшего использования. К ним относятся: экстракция, сорбция, ионный обмен, упаривание, флокуляция, обратный осмос и другие методы.
При очистке сточных вод методом экстракции подбором подходящих растворителей (углеводороды и их галогенпроизводные, простые и сложные эфиры и др.) удается извлечь значительную часть органических соединений (фенолы, нитро- и аминосоединения, ароматические карбоновые и гидроксикарбоновые кислоты и т. д.), которые затем легко поддаются отделению от растворителя и дальнейшей очистке. Однако метод экономически целесообразен лишь при некоторой минимальной концентрации органических веществ в сточных водах, т. к. в противном случае производительность установок будет слишком мала.
Адсорбция с помощью активированных углей различных марок и других сорбентов с последующей отгонкой поглощенных веществ перегретым водяным паром без разгрузки сорбционных фильтров в ряде случаев может заменить или дополнить методы экстракции. Большие перспективы открывает применение ионообменных смол. Однако и здесь производительность является лимитирующим фактором.
Упаривание особенно пригодно для извлечения из сточных вод минеральных солей. При достаточно концентрированных растворах солей удобно применять устройства типа распылительных сушилок.
Для извлечения из сточных вод органических катионов и анионов в ряде случаев полезно применение флокулянтов — водорастворимых ионитов противопо
ложного знака, вызывающих флокуляцию органических примесей. Образующиеся осадки отделяют затем декантацией или фильтрованием. Методом флокуляции, в частности, удается избавиться от фенолов, органических кислот, небольших количеств катионных и анионных красителей, содержащихся в фильтратах и промывных водах, и т. п. В случае необходимости эти вещества могут быть затем извлечены из полученных осадков экстракцией и другими способами.
Взаимная нейтрализация щелочных и кислых вод целесообразна тогда, когда она приводит к получению полезных продуктов (например, сульфата аммония из стоков, содержащих аммиак и серную кислоту) и не сопровождается образованием минеральных солей, таких как NaCl, Na2SO4 и др. В последнем случае целесообразнее извлекать содержащиеся в кислых и щелочных стоках кислоты и щелочи путем низковольтного электродиализа с использованием ионоактивных мембран. Это позволяет получить ценные вещества, возвратить воду в производственный цикл и избежать сбрасывания в водоемы образующихся при нейтрализации солей.
Перспективной является очистка сточных вод с помощью полупроницаемых мембран — методами ультрафильтрации и обратного осмоса. Первый основан на способности полупроницаемых мембран пропускать молекулы низкомолекулярных соединений и задерживать высокомолекулярные при действии на раствор давления, превышающего атмосферное. Второй метод основан на способности растворителя переходить из раствора через полупроницаемую мембрану при действии на раствор давления, превышающего осмотическое. В результате ультрафильтрации по одну сторону мембраны накапливается концентрат высокомолекулярного соединения, а по другую — раствор низкомолекулярных веществ, в результате обратного осмоса — соответственно концентрат растворенного вещества и более разбавленный раствор или чистый растворитель. Оба процесса отличаются от обычной фильтрации тем, что конечными продуктами здесь являются не твердое вещество и раствор или растворитель, а два раствора, один из которых обогащен растворенным веществом (при обратном осмосе) или высокомолекулярным веществом (при ультрафильтрации).
Для анилинокрасочной промышленности, имеющей дело главным образом с низкомолекулярными соединениями, наибольший интерес представляет обратный осмос. Соответствующим подбором мембран и условий проведения процесса удается достичь очень высоких показателей разделения жидких смесей.
Одним из эффективных методов обезвреживания сточных вод, достаточно распространенных на анилинокрасочных предприятиях, является биологическая очистка. Этот метод применяют для очистки стоков, содержащих органические примеси в малых концентрациях и для доочистки вод после удаления большей части органических веществ другими методами. В настоящее время имеются культуры микроорганизмов, способных потреблять органические вещества, в том
832
Новый справочник химика и технолога
числе анилин, нитро- и аминофенолы, нафтолы, салициловую кислоту и ряд других. Проводится работа по выведению микроорганизмов, способных потреблять и другие органические соединения. Разросшиеся колонии микроорганизмов могут в дальнейшем использоваться в качестве ценных удобрений. К сожалению, имеются органические вещества, трудно поддающиеся или не поддающиеся биоочистке, например хлорсодержащие соединения и некоторые другие.
Сточные воды, которые не могут быть эффективно очищены ни одним из известных методов, подвергаются термическому разложению (сжиганию) или (при наличии подходящих геологических условий) закачиванию в подземные горизонты. При сжигании хлорсодержащих продуктов образуются хлористый водород, диоксид углерода и водяной пар, которые могут быть утилизированы.
На многих предприятиях существует порочная практика смешения сточных вод от разных производств, что чрезвычайно затрудняет их последующую очистку и, как правило, делает нецелесообразным извлечение из стоков полезных веществ.
Так, в производстве красителей широко применяется высаливание конечных продуктов, в результате которого образуются сточные воды, содержащие NaCl, часто в значительных концентрациях, и органические примеси. Упариванием и дожиганием из таких вод можно извлечь NaCl, пригодный к повторному использованию. Точно так же из других сточных вод может быть извлечен сульфат натрия, который пригоден, например, для производства сульфида натрия. Смешение же стоков, содержащих NaCl и Na2SO4, делает практически невозможным использование этих отходов.
Литература
1. Гордон П., Грегори П. Органическая химия красителей / Пер. с англ, под ред. Г.Н. Ворожцова. М.: Мир, 1987.
2. Степанов Б.И. Введение в химию и технологию органических красителей. М.: Химия, 1984.
3. Бородкин В.Ф. Химия красителей. М.: Химия, 1981.
4. Чекалин М.А., Пассет Б.В., Иоффе Б.А. Технология органических красителей и промежуточных продуктов. Л.: Химия, 1980.
5. Химия синтетических красителей / Под ред. К. Венкатарамана / Пер. с англ, под ред. Л.С. Эфроса. Л.: Химия. 1974. Т. 3. 1975. Т. 4. 1977. Т. 5. 1977. Т. 6.
6. Органические синтетические красители. Кат. НИОПиК. М., 1977.
7. Введение в фотохимию органических соединений / Под ред. Г.О. Беккера / Пер. с нем. под ред. А.В. Ельцова. Л.: Химия, 1976.
8. Красители для текстильной промышленности. Колористический справочник / Под ред. Л.Л. Бяльско-го, В.В. Карпова. М.: Химия, 1971.
9. Лаптев Н.Г., Богословский Б.М. Химия красителей. М.: Химия, 1970.
10. Андросов В.Ф., Голомб М.М. Синтетические красители для текстильной промышленности. М.: Легкая индустрия, 1968.
11. Теренин А.Н. Фотоника молекул красителей и родственных органических соединений. М.: Наука, 1967.
12. Порай-Кошиц Б.А. Азокрасители. Л.: Химия, 1960.
13. Цоллингер Г. Химия азокрасителей / Пер с нем. под ред. Б.А. Порай-Кошица. Л.: Госхимиздат, 1960.
14. Коган И.М. Химия красителей. М.: Госхимиздат, 1956.
Приложение 4.3
Красители, выпускаемые зарубежными странами
Кислотные красители
Страна Фирма Красители
Англия ICI Дарамины, Карболаны, Кумасси, Лиссамины, Найломины
Германия BASF Ацидолы, Безоланы, Ортолы
Bayer Ациланы, Супрамины, Супранолы, Супрацены, Телон-прочные
Hochst Амидо прочные, Антраланы, Альфанолы, Ремаланы
Польша Кислотные, Металаны, Фоланы
США Du Pont Метанилы, Литосоли, Понтацилы
Франция Francolor Валкопрочные, Супрациды, Сульфациды
Чехия Chemapol Мидлоны, Рибациды, Эгациды
Швейцария CIBA Бензилы, Китоны, Ирганолы
Geigy Новазолы, Эрио, Эриозины, Эрионилы
Sandoz Сандоланы
Япония KKK Дайшики, Кайанол, Кайацил, Такаока
Ароматические соединения
833
Дисперсные красители
Страна Фирма Красители
Англия Германия Польша США Франция Чехия Швейцария ICI BASF Bayer Hochst CIECH Du Pont Francolor Chemapol CIBA Geigy Sandoz Дюранолы, Дисперсолы Виалоны, Паланилы, Пер литоны, Цилла, Целлитоны Виалоны прочные, Резолины Самароны Синтены Ацетамины, Латилы, Цслантрены Амихромы, Ацетохиноны, Нейлохиноны, Эстерофилы, Эстерохиноны Остацены Теразилы, Цибацеты Авилоны, Сетароны, Сетацилы Артизилы, Фороны
Прямые красители
Страна Фирма Обычные Светопрочные Упрочняемые солями меди Дисазокрасители
Англия Германия Польша США Франция Чехия Швейцария ICI BASF Bayer Hochst Volfen Chemicolor Du Pont Francolor Chemapol Geigy Sandoz Айсилы, Хлоразоли Бензокрасители Колумбия Прямые Понтамины Диазоли Прямые Дифенилы Хлорамины Дюразоли Лурантины Сириус-супра, Сириус светопрочный Рсмастрали Соламины, Соласины фау Гелионы Понтамины прочные, Резофиксы Диазоли светопрочные Сатурны Солифенилы Дифенилы прочные Люмикризы, Пиразолы, Соляры Дюразол-купро Бензокупроли, Бензокуппер Купроксоны Понтамины куппср Купродиазоли Купростаны Купрофенилы Купрофиксы, Резофиксы Хлоразоли Бензамины Дианилы Замбези, Нафтогены Диазо Понтамины диазо Диазоамины Азогены Диазофенилы Диазоамины
Катионные красители
Страна Фирма Красители
Англия Германия Польша США Франция Швейцария Япония ICI BASF Bayer Bitterfeld Boruta Du Pont Francolor CIBA Geigy Sandoz Hodogaye Mitsubishi Акролоны, Синакрилы Базакрилы Астразоны Крипуры Аниланы Севроны Лиркамины Деорлины Максилоны Сандокрилы Айзен-катилоны Диакрилы
834
Новый справочник химика и технолога
Хромовые и однохромовые красители
Страна Фирма Хромовые Однохромовые
Англия Г ермания Польша США Франция Чехия Швейцария ICI BASF Bayer Hochst Du Pont Francolor Chemapol CIBA Geigy Sandoz Омегахром Базоланы хромовые Диаманты, Хромовые Салицин хромовые Кислотные хромовые Пентахром ы Франколаны Ализарины хромовые Хромпрочные Эриохромы Ализаины, Омегахромы Солохромы Монохромы, Хромогены, Хромоксаны Метахром Ортохромовые Хроматы Криноланы Ализаринхром Синтохроматы Эриохромали Метамегахромы
Металлсодержащие красители (комплексы состава 1:1 и 1 : 2)
Страна Фирма Комплексы 1 : 1 Комплексы 1 : 2
Англия ICI Ионохромы, Ультраланы Вариланы
Германия BASF Палатины прочные Ацидолы М, Виалоны прочные, Ортоланы
Bayer Изоланы, Леваланы
Hochst Азарины, Ремаланы прочные
Vol fen Вофанилы Вофаланы
Польша Нейтраланы, Польфоланы
США Du Pont Хромацилы Капранилы
Франция Francolor Инохромы, Супрациды Нейтрихромы-С
Чехия Chemapol Хромоланы Осталаны
Швейцария CIBA Неоланы Ланакроны, Цибаланы
Geigy Гиколаны Иргаланы
Sandoz Витроланы Ланазины, Сандоланы, Супраланы
Япония KKK Кайякаланы
Активные красители
Страна Фирма Красители
Англия Германия Польша Чехия Швейцария ICI BASF Bayer Hochst CIECH Chemapol CIBA Geigy Sandoz Проциланы, Проционы M, Проционы Н, Примазины, Примазины Р Левафиксы, Левафиксы Е Ремазоли Гелактины, Гелактины D Остазины, Остазины Н Цибакроланы, Цибаланы Реактоны Дримарены
Кубовые красители и кубозоли
Страна Фирма Кубовые красители Кубозоли
Англия Германия ICI BASF Bayer Дюриндоны, Каледоны Индантрены Индантрены Дюриндоны, Соледоны
Ароматические соединения
835
Окончание
Страна Фирма Кубовые красители Кубозоли
Германия Италия Польша США Франция Чехия Швейцария Hochst ACNA CIECH Du Pont Francolor Chemapol CIBA Geigy Sandoz Антра, Индантрены Романтрены, Солиндены Гелантрены Понсоли, Сульфантрсны Гелианы, Солантрены Остантрены Циба, Цибаноны Тина, Тиноны Сандантрены Антразоли Солиндолы Гелазоли Понтозоли Гелиазоли, Солазоли Цибантины Тинозоли Сандозоли
Сернистые красители
Страна Фирма Красители
Англия Германия Италия Польша США Франция Чехия Швейцария ICI Cassella Hochst Volfcn ACNA CIECH Du Pont Francolor Chemapol CIBA Geigy Sandoz Тионолы Гидроны, Иммедиали Сульфуры Тиолоны (Сольфо) Сульфуры Сульфогены Сульфанолы Сульфогены Пирогенны, Циба Тиотиноны, Эклипсы Сандоны, Тионалы
Азогены
Страна Фирма Азотолы Азоамины и диазоли Диазотолы Диазаминолы Азоацеты
Англия ICI Брентолы Брентамины Брентогены Брентацеты
Германия Bayer Hochst Нафтолы AS Вариогены, Соли прочные Рапид-прочные Рапидогены Офнацеты
Италия ACNA Акнафтолы Основания прочные Цитазины Цитазолы
Польша Нафтоэланы Основания прочные Пологены
Франция Francolor Нафтазолы Основания прочные Нейтрогены, Нефтазогены
Чехия Chemapol Ультразолы Основания прочные
Швейцария CIBA Цибанафтолы Соли Циба, Основания Циба Цибагены Цибаногены
Geigy Ирганафтолы Соли Ирга, Основания Ирга Тиногены Иратрали
Sandoz Целькоты Деволи Моментогены Сандогены
836
Новый справочник химика и технолога
Оптические отбеливатели
Страна Фирма Отбеливатели
Англия Германия Германия Венгрия Польша Чехия Швейцария Япония ICI BASF Bayer Bitterfeld Hochst CIECH Chemapol CIBA Geigy Sandoz Флюолайты Паланилы, Ультрафоры Бланкофоры Вайсстонеры Хосталюксы Оптиноли Гелиофоры Рилюксы Увитексы Тинопали Лейкофоры Уайтексы
Раздел 5. ХИМИЯ ФОТОГРАФИЧЕСКИХ ПРОЦЕССОВ
Автор: д.т.н., проф. А.В. Редько
«... В истории развития науки еще никогда не было так, чтобы великое открытие или новый технический .метод зарождались на пустом месте. Этим событиям всегда предшествуют вековые наблюдения и многолетняя работа ученых. Так произошло и с изобретением фотографии. Благодаря значительным открытиям в области физики, химии, оптики и механики удалось разработать фотографический метод получения изображений ...»
5.1. История изобретения и этапы развития галогенсеребряной фотографии
Первое упоминание о светочувствительных веществах, обладающих свойством изменяться под действием света, относится к VIII в. н. э., когда арабский медик Ябир Ибн Хайям обнаружил, что «ляпис» (азотнокислое серебро) под действием света темнеет и теряет свои целебные свойства. В XVI в. геолог Г. Фабрициус заметил, что «роговое серебро» (хлорид серебра) темнеет на свету. В 1725 г. известный русский политический деятель А. Бестужев-Рюмин, занимавшийся прикладной химией, открыл светочувствительность солей железа. В 1727 г. немецкий врач И.Х. Шульце на солях серебра, освещая их солнечным светом, впервые получил изображение листьев деревьев и фигур, вырезанных из картона, используя для этого порошок из мела, пропитанный азотнокислым серебром. Это было практически первое в мире изображение, которое получили при помощи светочувствительного вещества.
В 1777 г. известный шведский химик К. Шееле, зная о светочувствительности солей серебра, обнаружил светочувствительность хлорида серебра к синефиолетовым лучам, проецируя на его поверхность изображение спектра, полученного разложением белого света с помощью призмы. Чуть позже И.В. Риттер в 1801 г., повторяя опыты К. Шееле, установил, что хлорид серебра темнеет за коротковолновой границей видимого спектра и открыл существование невидимых глазом ультрафиолетовых лучей. Таким образом, фотография еще не существовала как таковая, но тем не менее с ее помощью было сделано важное научное открытие.
Одновременно с изучением светочувствительных веществ и попытками с их помощью получить изображение различных предметов велись исследования по разработке методов получения оптического изображения. Еще в XVII в. такого рода работы были направлены на создание оптического устройства для облегчения труда художников. Первым прибором такого рода была так называемая камера-обскура (темная камера), изобретение которой приписывается итальянцу Леонардо да Винчи, гениальному ученому, мыслителю и художнику. Камера-обскура представляет собой закрытый ящик с небольшим отверстием в одной из стенок. Будучи направлена на какой-либо предмет, она позволяла получить на задней стенке камеры перевернутое изображение предмета. Однако яркость изображения, получаемого в камере-обскуры, была невелика. Увеличение же диаметра отверстия в камере повышало яркость изображения, но делало его нерезким. Существенное улучшение камеры-обскура было сделано в XVIII в. итальянцем Делла Порте, вставившем в отверстие камеры линзу из очков, что значительно повысило как яркость, так и резкость получаемого изображения. Эта камера явилась прообразом современного фотоаппарата. К этому же времени в связи с общим развитием науки, в том числе и химии, была открыта группа галогенов: хлора (1774 г.), иода (1811 г.), брома (1826 г.), что дало возможность создавать светочувствительные се-ребряно-галогенные системы. Все это в значительной мере ускорило изобретение фотографии.
Дагеротипия. Первая попытка получить изображение с помощью камеры-обскуры было предпринято
838
Новый справочник химика и технолога
в Англии в 1802 г. Гемфри Дэви и Томасом Веджвудом, которые экспонировали в камере-обскуре обычную бумагу, пропитанную сначала раствором азотнокислого серебра, а затем раствором поваренной соли. С помощью такой бумаги, между волокнами которой образовывался в результате пропитки хлорид серебра, можно было получить изображение различных фигур. Правда, вскоре эксперименты были прекращены, т. к. экспонирование длилось часами, а изображение получалось нечетким и при рассмотрении на свету полностью исчезало.
Несколько позже во Франции начал свои исследования по разработке методов получения изображения на светочувствительных веществах Жозеф Нисефор Ньепс. Изучая различные светочувствительные вещества, он обнаружил, что если чистый кристаллический иод подвергнуть возгонке, а затем пары его конденсировать на серебряную пластинку, то такая пластинка становится светочувствительной. Ж.Н. Ньепс в то время не мог понять, что в этом случае образуется светочувствительный иодид серебра. Учитывая то обстоятельство, что изображение получалось при экспонировании в камере-обскуре нечетким, он пришел к заключению, что иод непригоден для получения изображения окружающих нас предметов.
Это побудило Ж.Н. Ньепса направить свои усилия по другому пути — на исследование асфальта-смолы природного органического происхождения, который обладал хорошей растворимостью в некоторых растительных маслах, например в лавандовом масле. Светочувствительный асфальт в начале наносился тонким слоем на цинковую или оловянную пластину, которая затем экспонировалась в камере-обскуре. При действии света асфальт становился твердым, а в лавандовом масле происходило растворение асфальта только в участках, где не действовал свет. После обработки в лавандовом масле цинковая пластинка погружалась в раствор азотной кислоты и травилась на определенную глубину, а затем механическим путем остатки затвердевшей смолы удалялись с поверхности пластин. Полученные при травлении в кислоте углубления на пластине заполнялись типографской краской с помощью валика. Прикладывая сверху лист бумаги, можно было получить одноцветное позитивное изображение. Несмотря на очень низкую светочувствительность асфальта (выдержка на прямом солнечном свету достигала 6-8 ч), Ж.Н. Ньепс считал, что предложенный процесс может быть с успехом применен для изготовления типографских клише картин, рисунков, чеугежей. В 1825 г. он опубликовал свое открытие, назвав его гелиографией. Однако предложенный процесс широкого развития не получил. Итак, Ж.Н. Ньепс был первым, кто в 1826 г. получил фотографические изображение на светочувствительном веществе с помощью камеры-обскуры. Оригинал изображения на цинковой пластине с нанесенным на поверхность светочувствительным асфальтом, которую Ж.Н. Ньепс экспонировал в течение 8 ч, находится сегодня в музее Техасского университета США.
В то же самое время в Париже художник-декоратор Луи Жак Манде Дагер изобрел так называемую диораму. Диорама представляла собой ряд картин очень больших размеров на длинной ленте холста, закрепленного на двух вертикальных валах. Перематывая эту ленту с одного вала на другой, Л.Ж. Дагер демонстрировал свои пейзажи зрителям: «Дремучий лес в разные часы дня», «Извержение Везувия» и другие, применяя при этом разные приемы освещения. Это было любимым зрелищем парижан. За короткий период времени диорама несколько раз горела, и Л.Ж. Дагер тратит много усилий на восстановление диорамы и одновременно настойчиво искал способ, позволяющий быстрее рисовать большие полотна. Л. Ж. Дагер, однажды посетив в Париже оптическую мастерскую знаменитого оптика Винсента Шевалье, узнал от него об экспериментах Ж.Н. Ньепса по изысканию светочувствительных веществ, позволяющих регистрировать всякого рода изображения.
В 1827 г. Л.Ж. Дагер и Ж.Н. Ньепс заключили договор о совместном сотрудничестве. В 1833 г. Ж.Н. Ньепс умер и Л.Ж. Дагер по условиям договора получил оборудование и все дневники экспериментов.
Повторяя опыты Ж. Н. Ньепса по возгонке иода на серебряную полированную пластину, при случайных обстоятельствах Л.Ж. Дагер получил отчетливое и хорошо видимое позитивное изображение объекта съемки.
В августе 1839 г. способ был обнародован и назван дагеротипией. Это выдающееся изобретение легло в основу всего последующего развития фотографии.
Существо процесса заключалось в том, что медная пластина, покрытая тонким слоем серебра, тщательно отполированная до зеркального блеска, помещалась в специальный ящик полированной стороной вниз. Снизу ящика под пластиной помещали чашку с кристаллическим иодом. При подогреве иод начинал возгоняться, и пары его оседали на полированной пластине. Иод вступал в реакцию с серебром, и пластина покрывалась тонким слоем иодида серебра, становясь светочувствительной.
После экспонирования в камере-обскуре пластину помещали в тот же ящик, но теперь в чашку вместо иода наливали ртуть. При подогревании ртуть испарялась, и ее пары оседали на поверхности экспонированной пластины только в тех местах, где действовал свет, образуя при этом отчетливое позитивное изображение объекта съемки.
Заслуга Л.Ж. Дагера состояла в том, что он впервые нашел способ превращения скрытого изображения в видимое. Суть этого явления, которое сам Л.Ж. Дагер не смог объяснить, заключалось в том, что иодида серебра под действием света разлагалось с выделением мельчайших частиц металлического серебра, на которых конденсировались пары ртути. Проявленная в парах ртути пластинка затем обрабатывалась в течение нескольких часов в растворе поваренной соли для растворения иодида серебра, оставшегося в участках, где
Химия фотографических процессов
839
не действовал свет. Позже удалось существенно сократить процесс растворения неэкспонированного иодида серебра за счет применения тиосульфата натрия (гипосульфита). Способ был предложен в 1839 г. астрономом Д. Гершелем. Л.Ж. Дагер рекомендовал разработанный им процесс в основном для получения портретов. При портретной съемке выдержки достигали на ярком солнечном освещении 15 мин из-за низкой светочувствительности иодида серебра. Это было большим неудобством. Для преодоления этих трудностей интенсивно проводились работы по усовершенствованию процесса дагеротипии в двух направлениях, а именно: как по пути повышения яркости оптического изображения, даваемого камерой-обскурой, так и по пути увеличения светочувствительности пластинок.
Для увеличения светочувствительности пластин в несколько раз позже стали применять не чистый иод, а смесь иода с небольшим количеством брома. Все эти мероприятия привели к тому, что уже в 1841 г. выдержки сократились с 15 до 3 мин, а дагеротипия как дешевый и быстрый способ получения портретов получила повсеместное распространение несмотря на то, что ей были присущи следующие недостатки:
- изображение было видно только при рассмотрении под определенным углом;
- для получения изображения нужна была дорогостоящая серебряная пластина;
- невозможность моментальной съемки из-за малой светочувствительности;
- пары ртути, которая использовалась для визуализации изображения, очень ядовиты;
- изображение малоустойчиво, т. к. амальгама постепенно разлагалась с выделением ртути;
- изображение на пластинке получалось в одном экземпляре и было зеркально-обращенным.
Последующая замена дорогих серебряных пластинок на стеклянные с нанесенным на них тонким слоем из металлического серебра еще более удешевила этот процесс, и это способствовало тому, что он просуществовал до 1852-1853 гг.
Калотипия (тальботипия). Почти одновременно с Ж.Н. Ньепсом и совершенно независимо от него в Англии над методами получения фотоизображения работал видный ученый того времени Вильям Генри Фокс Тальбот. В своей работе он исходил из способа, предложенного в 1802 г. Г. Дэви и Т. Веджвудом, купавших бумагу в растворе азотнокислого серебра, а затем в растворе поваренной соли и сумевших получить видимое изображение предметов, положенных на очувствленную бумагу. Фокс Тальбот нашел, что изменение последовательности купания бумаги в указанных растворах существенно повышает светочувствительность. Если Г. Деви и Т. Веджвуд не смогли найти способа закрепления полученного на бумаге изображения, которое при рассмотрении под действием света исчезало, то Фокс Тальбот впервые предложил обработать про
питанную бумагу после длительного экспонирования сначала в растворе галловой кислоты, а затем в растворе поваренной соли, для удаления оставшегося хлорида серебра. Это позволило «закреплять» полученное изображение на светочувствительной бумаге и делать его устойчивым по отношению к дальнейшему воздействию света. Разработанный Фоксом Тальботом 20 августа 1835 г. процесс получил название «калотипия».
Сущность процесса, предложенного Фоксом Тальботом, заключалась в том, что обычная бумага купалась в растворе иодида калия, а затем в растворе азотнокислого серебра. Светочувствительность такой бумаги была много выше, чем пластинок Л.Ж. Дагера, а выдержка при съемке сокращалась до одной минуты. После экспонирования бумаги в камере-обскуре получалось слабое видимое изображение снимаемого объекта, которое существенно усиливалось обработкой в растворе галловой кислоты. Негатив (изображение, на котором распределение яркостей обратно распределению яркостей в объекте съемки) после полного цикла химикофотографической обработки погружался в расплавленный воск, что делало его почти прозрачным и давало возможность вести печать на светочувствительную бумагу (рис. 5.1.1). Таким образом, благодаря открытию Фокса Тальбота, впервые можно было осуществить несколько позитивных копий с одного негатива. Кроме того, Фокс Тальбот создал так называемый «волшебный фонарь» — прообраз современного фотоувеличителя — и применил его для получения увеличенного позитивного изображения. Тальботипия по сравнению с дагеротипией несомненно явилась более совершенным техническим методом, т. к. она обладала рядом прогрессивных черт, открывших перспективу дальнейшему развитию фотографии. Тем не менее впоследствии из-за широкого распространения дагеротипии процесс, предложенный Фоксом Тальботом, так и не смог ее вытеснить.
Рис. 5.1.1. Фотоснимок, получаемый с помощью тальботипии
Мокрый коллодионный процесс. В 1852 г. дагеротипия и тальботипия были полностью заменены новым методом, более совершенным, который стал следующим шагом в развитии фотографии. Предложенный в 1851 г. англичанином Фредериком Скоттом Арчером, он получил название «мокрый коллодионный процесс».
840
Новый справочник химика и технолога
Применение этого процесса существенно повысило светочувствительность и позволило получить изображение исключительно высокого качества, особенно по резкости. Это обстоятельство привело к тому, что мокрый коллодионный процесс применяется и по настоящее время в некоторых специальных областях (изготовление сеток, шкал и т. д.). Способ, предложенный Ф. С. Арчером, основан на применении раствора коллодия особого сорта нитроклетчатки (коллоксилина), растворенной в смеси спирта и эфира и представляющей собой густую и быстро сохнущую жидкость. На стеклянную пластинку наносят слой свежеприготовленного коллодия, который теряет текучесть только после испарения эфира. До тех пор, пока в слое сохраняется спирт, он остается влажным и проницаемым для воды и различных водных растворов. Такая пластинка с нанесенным слоем коллодия купается сначала в растворе иодида калия, а затем в растворе азотнокислого серебра. При этом в слое коллодия образуются мельчайшие кристаллы иодида серебра. В таком виде мокрая пластинка экспонируется и проявляется в проявителе, содержащем соли сернокислого закисного железа или пирогаллола.
Наряду с мокрым коллодионным процессом был предложен сухой коллодионный процесс, который отличался от первого тем, что в слой коллодия вводились гигроскопические вещества — слои лития, магния. Последние, в силу своей гигроскопичности, создавали возможность проникновения влаги в высохший слой коллодия. Сухой коллодионный процесс устранил некоторые недостатки мокрого способа, но несколько уменьшил светочувствительность слоя и резкость изображения. Мокрый коллодионный способ вытеснил все предшествующие ему методы получения фотографического изображения и просуществовал почти 20 лет (до 1871).
Сухие бромсеребряные желатиновые слои. В 1871 г. английский врач Ричард Лич Мэддокс впервые предложил для приготовления «светочувствительной жидкости» использовать желатин — белок животного происхождения, получаемый из костей и кожи крупного рогатого скота, который хорошо набухает в холодной воде и становится проницаемым для водных растворов. При нагревании он плавится, а при охлаждении опять студенится. При сушке в мягком режиме получается пленка, хорошо набухающая в воде.
Р. Мэддокс неожиданно обнаружил, что если в подогретый желатиновый раствор вначале ввести азотнокислое серебро, а затем добавить бромид и иодид калия, то приготовленная таким образом «светочувствительная жидкость», получившая название в фототехнологии не совсем правильное «фотографическая эмульсия», обладает светочувствительностью во много раз выше, чем известные до сих пор светочувствительные системы. Причем, если раствор желатина с образовавшимися в нем микрокристаллами галогенида серебра выдержать некоторое время при повышенной
температуре, то светочувствительность эмульсии возрастает в сотни и тысячи раз. Это случайно обнаруженное свойство желатина привело к тому, что с момента открытия до настоящего времени все фотографические эмульсии изготавливаются в основном на желатине.
Применение желатина стало крупным шагом в дальнейшем развитии фотографии и создало широкие предпосылки для промышленного изготовления фотоматериалов.
Еще одним важным шагом вперед, открывшим новые возможности в фотографии, было изобретение немецкого химика Германа Вильгельма Фогеля, который в 1873 г. обнаружил, что введение в галогенсеребряную эмульсию некоторых красителей вызвало расширение спектральной светочувствительности галогенидов серебра от сине-фиолетовой к длинноволновой части видимого излучения. Это явление получило название «оптическая» или «спектральная сенсибилизация» (процесс очувствления галогенида серебра к зеленым и красным лучам) и обеспечило прогресс в цветной фотографии и кинематографии.
Цветная фотография. На заре возникновения фотографии многие исследователи искали ответ на вопрос: как же передать с помощью фотографического метода краски окружающего мира?
Исаак Ньютон полагал, что многообразие цветных тонов, существующих в природе, можно получить за счет смешения семи цветов: красного, оранжевого, желтого, зеленого, голубого, синего, фиолетового. Великий русский ученый М.В. Ломоносов 1 июля 1756 г. в своем труде «Слово о происхождении света, новую теорию о цветах представляющее» показал, что число простых цветов, необходимых для получения цветного изображения, может быть сведено к трем — желтому, зеленому, голубому.
В 1802 г. английский физик Томас Юнг, создатель волновой теории света, выдвинул предположение, что в человеческом глазу имеются три вида нервных окончаний-рецепторов, чувствительных только к синей, зеленой, красной составляющим спектра, возбуждение которых вызывает ощущение цвета. Трехцветная теория Т. Юнга долгое время оставалась гипотезой и только в работах немецкого биолога и физика Германа Гельмгольца нашла свое подтверждение.
Противником этой теории был немецкий физиолог и физик Эвальд Геринг, который в 1870 г. предложил теорию четырех основных цветов (зеленый, синий, желтый, красный), а с учетом белого и черного — шести цветов. Э. Геринг считал, что использование четырех основных цветов дает больше возможностей, чем трех цветов, тем более, что четырехцветная печать с успехом применяется в полиграфии.
Противники четырехцветной теории считали, что пяти различных цветоприемников в человеческом глазу многовато и зачем желтый рецептор, если есть красный и зеленый, которые, возбуждаясь, дают желтый цвет.
Химия фотографических процессов
841
Кроме того, почему дополнительные цвета — желтый и синий — дают белый, а зеленый и красный — желтый?
Сегодня физиологи, благодаря исследованиям голландского ученого П. Уолварена, который связал четырех- и трехкомпонентную теории, считают что трехкомпонентная теория Г. Гельмгольца получила подтверждение и является общепринятой теорией цветового зрения. Но некоторые ученые все же полагают, что процесс цветового зрения соответствует комбинации обеих теорий.
В 1855 г. английский физик Д. Максвелл, опираясь на принципы трехкомпонентной теории цветного зрения Томаса Юнга и Германа Гельмгольца, сформулировал теорию образования цвета. Все цвета, окружающие нас, согласно этой теории, можно получить из трех основных цветов: синего, зеленого, красного. Первое в мире цветное изображение на основе фотографического метода Максвелл получил 17 мая 1861 г.
Галогенсеребряные эмульсионные фотослои в то время обладали чувсвительностью только к коротковолновой части видимого спектра (синим лучам), и развитие цветной фотографии, как мы понимаем сейчас, было бы невозможным без спектральной сенсибилизации, открытой при случайных обстоятельствах в 1873 г. профессором Берлинского университета Германом Фогелем. Благодаря научной оценке неожиданного эффекта, который имел место при добавлении в галогенсеребряную эмульсию, чувствительную к синим, фиолетовым и ультрафиолетовым лучам, некоторых красителей, Г. Фогель открыл новую и очень важную страницу в истории цветной фотографии.
Однако многим до сих пор не понятно, как же Д. Максвелл еще задолго до открытия спектральной сенсибилизации смог продемонстрировать большой I'pynne английских ученых в Лондоне способ получения цветного изображения, проводя съемку цветного объекта за синим, зеленым и красным светофильтрами на несенсибилизированную фотопластину, а затем проецируя на экран черно-белые цветоделенные позитивы за этими же светофильтрами. В технической литературе по этому вопросу высказываются различные мнения, порой даже неправильные. Сегодня, благодаря исследованиям в области цветной фотографии англичанина Джона Хеджкоу, стало известно, что Д. Максвеллу просто сопутствовала удача, т. к. красные цвета снимаемой клетчатой ленты отражали ультрафиолетовые лучи, которые и регистрировались фотопластиной в процессе съемки, а зеленый светофильтр не был строго зональным, пропуская не только зеленые, но и синие лучи.
Спустя два года после открытия спектральной сенсибилизации французский ученый Луи Хайрон получил за синим, зеленым, красным светофильтрами цветоделен-ное изображение, используя сенсибилизирующее действие хлорофилла. В 1869 г. он сообщил о хромоскопе — приборе, в котором три цветоделенных позитива объединялись с помощью систем зеркал, что позволяло довольно просто получать цветное изображение.
Луи Дюко дю Орон в книге «Цвета в фотографии», опубликованной в 1869 г. и посвященной проблемам цветной фотографии, впервые изложил принципы аддитивного и субтрактивного методов фотографии, включая и схему современной цветной фотографии на многослойных фотоматериалах. В фотографии существуют два метода получения цветного изображения: аддитивный (additio — сложение) и субтрактивный (subtrahere — вычитание). В первом случае складываются световые потоки, а в другом — цветное изображение получают, вычитая из белого основные цвета (синий, зеленый, красный). Первое в мире цветное изображение субтрактивным методом было изготовлено Луи Дюко дю Ороном (сегодня оно находится в музее Национальной Техники в Лондоне). Сначала он получил три цветоделенных черно-белых негатива, снимая цветной объект за зональными (пропускающими одну зону видимого спектра) светофильтрами: синим, зеленым, красным. Копируя с цветоделенных негативов на три желатиновые фолии, содержащие в слое красители (желтый, пурпурный, голубой), дополнительные к цветам светофильтров, за которыми велась съемка объекта, получал три рельефных цветоделенных окрашенных позитива. Затем, совмещая окрашенные позитивы и освещая их белым светом, он получил цветное изображение субтрактивным способом.
Заслуга Луи Дюко дю Орона заключалась в том, что он, используя на начальной стадии аддитивный метод Д. Максвелла, разработал принцип субтрактивного метода получения цветного изображения и увидел большую перспективу данного метода Но уровень техники и технологии того времени все же не позволил ему реализовать на практике свои идеи, обстоятельно рассмотренные во второй книге «Цветная фотография», которую он написал вместе с братом в 1878 г.
Растровая фотография. Созданию современных многослойных цветных фотоматериалов предшествовали растровые методы получения цветного изображения. Одним из первых, кто достиг больших успехов в области растровой фотографии, был Джон Джоули, который в 1893 г. сумел изготовить комбинированный трехцветный светофильтр, нанося на стекло на 1 см около 80 параллельных полосок синего, зеленого и красного цветов. Изопанхроматическая пластинка, обладающая светочувствительностью к лучам видимого спектра, экспонировалась в фотокамере за таким светофильтром, а затем черно-белый позитив, полученный с негатива, совмещался с растром и проецировался на экран.
Изготовление цветных растровых фотопластин было в свое время излюбленным занятием изобретателей, работающих в области цветной фотографии. Необходимо было решить задачу: какой должна быть структура растровых фильтров — регулярной или нерегулярной. Некоторые исследователи для того, чтобы получить лучшую цветопередачу, пытались использовать четыре цвета, в качестве четвертого брали обычно желтый.
842
Новый справочник химика и технолога
Но всякий раз возвращались все же к трехцветному принципу.
Сначала фотопластины и растр изготавливали раздельно, во время фотосъемки цветной растр накладывали на панхроматическую пластину. После химикофотографической обработки фотопластины получали негатив, а затем с негатива позитив. Полученный позитив и цветной растр, за которым велась съемка, перед рассмотрением совмещали. Это, естественно, вызывало большие трудности, и вскоре начали изготавливать фотопластины двухслойные, т. е. цветной мозаичный растр и изопанхроматическую эмульсию наносили на одну подложку. С помощью пишущей машины на пластину, покрытую желатиновым слоем, наносились три цветные линии, лежащие очень близко друг к другу. Ширина этих линий сначала составляла 0,12 мм, а затем 0,08 мм. Некоторые фирмы применяли для своих фотопластин нерегулярный цветной растр, который изготовлялся напылением на покрытую клеем подложку точно составленной смеси окрашенных мельчайших частиц смолы.
Особо хочется отметить большой вклад в развитие цветной растровой фотографии братьев Огюста и Луи Люмьеров, которые в Лионе в 1907 г. наладили производство растровых фотопластинок под названием «Автохром». Высокое качество и простота получения цветного изображения обеспечили большой спрос среди фотолюбителей на данный вид фотопродукции на период свыше 30 лет.
В то время как много средств и усилий вкладывалось в развитие и усовершенствование линзово-растровой фотографии (линзовый растр представляет собой множество сферических или цилиндрических линз очень малого размера 0,10-0,15 мм, расположенных на поверхности прозрачной пластины, которые, как правило, наносятся тиснением), немецкий ученый Рудольф Фишер положил первый камень в основу процесса цветной фотографии, превзошедшего вскоре все известные до сих пор. Заслуга Р. Фишера состояла в том, что он выполнил большую часть подготовительных работ, которые дали цветной фотографии через 20 лет неожиданный подъем. В первом патенте 1912 г. Р. Фишер предложил способ изготовления цветных изображений, отличающийся тем, что содержащиеся в эмульсионном слое фотоматериала бесцветные вещества (цветообразующие компоненты) в процессе окисления проявителем образовывали труднорастворимые субтрактивные красители: желтый, пурпурный, голубой. Низкий уровень эмульсионной технологии и техники того времени не позволил осуществить замыслы Фишера, и 17 октября 1936 г. сотрудники фирмы «AGFA» в г. Вольфен.
Вильгельм Шнайдер и Густав Вильманнс, опираясь на патенты Р. Фишера и применив бесцветные цветообразующие компоненты в эмульсионном слое, изготовили сначала цветную обращаемую (на данной пленке получают позитив, используя особую схему обработки)
многослойную пленку, а вскоре и негативную. Последняя едва ли представляла интерес для фотолюбителей, но зато она открывала дорогу для цветной кинематографии.
Однако первая в мире цветная обращаемая пленка «Кодахром» была изготовлена в 1935 г. в США двумя одаренными фотолюбителями, музыкантами по профессии: пианистом Леопольдом Маннесом и виолончелистом Лео Годовски. В июле 1931 г. они заключили договор с фирмой «Kodak», на основе которого могли проводить свои исследования в фотографической лаборатории г. Рочестер. Пять лет спустя они завершили свои исследования и опубликовали статью «Процесс кодахром для любительской кинематографии в натуральных цветах».
Первая цветная многослойная фотопленка «Кодахром» была 16-миллимстровой обращаемой и не содержала в эмульсионных слоях цветообразующих компонент. Л. Маннес и Л. Годовски предложили совершенно другой принцип получения цветного изображения, отличающийся от метода Р. Фишера. Основой этого метода являлось использование цветообразующих компонент, которые диффундировали из проявителя в эмульсионные слои и, взаимодействуя с окисленной формой проявляющего вещества, давали нерастворимые красители в эмульсионном слое фотоматериала.
В 1960 гг. нашего столетия появились цветные негативные пленки второго поколения с окрашенными маскирующими цветообразующими компонентами, а 1970 гг. ознаменовались появлением цветных негативных пленок третьего поколения, которые обеспечивали высокую чувствительность и хорошее качество изображения за счет применения так называемых DIR-kom-понент. В 1980 гг. ведущие фотографические фирмы начали производство цветных негативных пленок уже четвертого поколения с очень высокой светочувствительностью и с улучшенным качеством изображения за счет использования новых типов эмульсий и новых цветообразующих компонент.
Современные цветные негативные фотоматериалы по сравнению с пленками первого поколения претерпели существенные изменения. Их светочувствительность выросла в сотни раз и составляет 1600-3200 ед. ASA. Это было достигнуто за счет применения новой эмульсионной технологии. Синтез качественно новых цветообразующих компонент способствовал созданию принципиально нового поколения цветных фотопленок и процессов их обработки.
При изготовлении цветных негативных фотоматериалов некоторые фирмы применяют структурированные двойниковые кристаллы-близнецы, которые имеют меняющуюся химическую структуру от центра микрокристалла к его поверхности. Такие микрокристаллы, помимо достоинств Т-кристаллов, обладают повышенной реакционной способностью к DIR-веществам (Development Inhibitor Releasing), отщепляющим в ходе
Химия фотографических процессов
843
реакции цветного проявления ингибиторы проявления, что усиливает краевые эффекты и улучшает резкость цветного изображения.
Современные негативные фотоматериалы в эмульсионном слое содержат DIR-компоненту (приблизительно 10 % от общего количества цветного компонента в слое). Ингибитор, образующийся в процессе проявления, легко диффундирует из экспонированных участков в соседние области, понижая оптическую плотность и образуя «кайму» (эффект Эбергарда). Это увеличивает микроконтраст и резкость края изображения, причем ингибиторы проявления уменьшают гранулярность цветного изображения за счет частичного восстановления микрокристаллов галогенида серебра и уменьшения диаметра цветного облака красителя. Фирма «Fuji», совершенствуя свои цветные негативные фотоматериалы, применила микрокристаллы типа «ядро-оболочка с двойниковой структурой» (Double Structured Grains) (рис. 5.1.2). Ядро с такой структурой содержит большое количество иодида серебра, а бромид серебра, расположенный на наружной оболочке двойникового кристалла, обеспечивает при экспонировании большой квантовый выход. В процессе проявления ядро существенно влияет на размер серебряной частицы, что обусловливает в дальнейшем при очень высокой светочувствительности (до 1600 ед. ASA), низкий уровень гранулярности цветного изображения. Кроме того, для повышения светочувствительности и улучшения гранулярности изображения применяют новый класс цветообразующих компонент, так называемых FR-компонент (Fog Releasing), т. е. отщепляющих вуаленты (например, формилгидразин), которые за счет образования на них центров вуали способствуют восстановлению ма-лоэкспонированных микрокристаллов, соседствующих с проявляемыми элементами. Такие компоненты вводят как в зональные слои, так и в промежуточные.
В последнее время для повышения светочувствительности цветных негативных материалов и уменьшения зернистости изображения применяют DAR-kom-поненты (Development Accelerator Releasing), отщепляющие при образовании красителя вещества-ускорители процесса проявления.
Для значительного уменьшения рассеивания света в процессе экспонирования применяют совершенно новый тип цветообразующих компонент — L-компоненты, являющиеся синтетическими полимерами, в которых водород замещен на хромофорную группу. Применение L-компонент позволило существенно уменьшить толщину слоя негативных фотопленок (на 10-20 %), а также улучшить структурно-резкостные свойства цветного изображения за счет уменьшения рассеивания света в слое и более компактной формы красителя, образующегося в процессе цветного проявления.
Эмульсии современных цветных негативных материалов нового поколения более однородны по размеру микрокристаллов и уже не являются смесью крупных и очень мелких микрокристаллов галогенида серебра.
Почти все зональные эмульсионные слои негативных фотоматериалов наносят, как правило, двумя-тремя полуслоями, состоящими из эмульсии различной чувствительности (рис. 5.1.3). Верхний высокочувствительный слой, содержащий Т-кристаллы галогенида серебра, определяет максимальную светочувствительность материала, нижний среднечувствительный полуслой с мелкими микрокристаллами способствует лучшей передаче деталей в изображении. Применение принципа двойного-тройного полуслоя для негативных фотоматериалов при высокой светочувствительности обеспечивает малую зернистость цветного изображения и довольно широкий интервал экспозиций при съемке. Для улучшения цветоделения при изготовлении негативных фотоматериалов применяют активные разделительные слои с неокрашенными компонентами, которые предотвращают образование красителя в соседних зональных слоях за счет диффузии окисленной формы проявляющего вещества в процессе проявления из одного зонального слоя в другой. Отличительная особенность современных цветообразующих компонент — повышенная устойчивость красителя к выцветанию. Так, у современных фотоматериалов сохраняемость цветного изображения определяется желтым, а не голубым, как у большинства пленок, красителем, причем устойчивость голубого красителя к выцветанию сохраняется в течение примерно ста лет.
Существенные изменения за последние десятилетия произошли не только в технологии производства цветных фотоматериалов, но и в технологии их химикофотографической обработки. Так, в обработке цветных обращаемых фотоматериалов наблюдается тенденция к применению унифицированного высокотемпературного процесса («Kodak Е-6»). Вместо амидольного чернобелого проявления все фирмы отдают предпочтение активным фенедон-гидрохиноновым проявляющим системам, малочувствительным к накоплению бромидов. Для увеличения активности черно-белого проявляющего раствора применяют специальные вещества, которые вводят не только в проявляющий раствор, но и в эмульсионный слой фотоматериала при его изготовлении. В качестве цветного проявляющего вещества почти все ведущие фотографические фирмы рекомендуют применять CD-3, CD-4. Для уменьшения максимальных плотностей и контраста цветного изображения в цветной проявляющий раствор вводят цитразиновую кислоту, которая связывает избыток окисленной формы проявляющего вещества и уменьшает за счет этого образование красителя в слое. Соединения, которые при этом образуются, легко растворимы и в процессе промывания удаляются из слоя. С целью исключения второго экспонирования предложено вводить в высокоактивные проявляющие растворы соединения с сильным вуалирующим действием, например, этилендиамин (основания) или перед цветным проявлением применять ванну химического обращения с хлоридом олова. Что касается процесса отбеливания, то сегодня специа-
844
Новый справочник химика и технолога
листы отдают предпочтение экологически безвредным отбеливающим системам на основе Fe(III)EDTA.
Рис. 5.1.2. Микрокристаллы галогенида серебра ядро-оболочка:
а) двойниковая структура; б) многооболочная структура; в) плоский микрокристалл с латеральными оболочками;
I — ядро МК AgHal; 2 — оболочка микрокристалла
а
-2 -1 О
lg/7
Рис. 5.1.3. Формирование суммарной характеристической кривой цветного фотоматериала (5) при однослойном строении (а) зонального эмульсионного слоя и характеристических кривых элементарных слоев при расположении изображения в поверхностной зоне (7) и в глубине слоя (2), а также при нанесении на основу крупнозернистой (3) и мелкозернистой (4) эмульсий двумя полуслоями (б):
D -оптическая плотность; Н — экспозиция
Рис. 5.1.4. Треугольник (а) и пирамида (б) качества, иллюстрирующие взаимосвязь между светочувствительностью (5), функцией передачи модуляции (Tv), зернистостью (oD) и цветовоспроизведением (F) для цветных негативных пленок нового поколения фирмы «Agfa-Gevaert» (2) по сравнению с предшествующими пленками (7)
В настоящее время химико-фотографическая обработка цветных фотобумаг имеет четкую тенденцию к уменьшению продолжительности процесса. Это достигается повышением температуры обрабатывающих растворов до 33-38 °C, объединением двух-трех стадий в одну и полным исключением промежуточных и даже окончательных промываний. При высокотемпературной обработке фотоматериалов примерно 32 % затрат составляют расходы на промывную воду и ее подогрев и только 40 % общей стоимости обработки расходуется на химические реактивы. Это обстоятельство побудило специалистов разработать беспромывочные методы химико-фотографической обработки цветных негативных фотоматериалов. Недавно фирмой «Konica» было предложено для обработки цветной фотобумаги на заключительной стадии использовать вместо трех баков промывания проточной водой раствор суперстабилизатора (процесс RA-4), который подают в баки по принципу противотока. В растворе суперстабилизатора происходит связывание ионов железа, в результате чего блокируется и обесцвечивается Fc(lII)EDTA, что и предотвращает возникновение желтой вуали в процессе хранения. Для повышения стабильности цветного изображения при хранении в эмульсионный слой вводят вещества, которые в процессе сушки отпечатков разлагаются и автоматически снижают pH до значений, обеспечивающих наилучшую стабильность красителей. За 72 года цветной фотографии современные цветные негативные фотопленки претерпели существенные изменения нс только в плане повышения светочувствительности и улучшения качества изображения, но и в строении эмульсионных слоев. В этом большая заслуга фирмы «Kodak». Согласно представлениям, которыми долгое время руководствовались специалисты в области фотографии и кинематографии, высокие значения фотографической светочувствительности фотопленок могли быть достигнуты за счет применения эмульсий с более крупными микрокристаллами галогенида серебра, т. е. с большей зернистостью. Всякое увеличение светочувствительности фотоматериалов в этом случае должно было обязательно сопровождаться ухудшением резкости и увеличением гранулярности изображения. Однако, благодаря большим успехам в области эмульсионной технологии, а также другим достижениям, стало возможным преодолеть эти препятствия, существенно улучшив структурно-рсзкостные характеристики и цветовоспроизведение негативных фотопленок при очень высокой их светочувствительности (рис. 5.1.4). В новых современных цветных негативных фотопленках последнего поколения высокая насыщенность цвета и его бриллиантность достигаются за счет интеримидж эффекта (Inter Image Effect), для получения которого необходимо не только образование ингибиторов процесса проявления и их взаимодействие с микрокристаллами галогенида серебра, но и различие в кинетике проявления зональных эмульсионных слоев. С помощью Super DIR-компонент, применяемых в зональных эмульсионных слоях цветной негативной фото-
Химия фотографических процессов
845
пленки, можно уменьшать гранулярность и компенсировать вредное поглощение субтрактивных красителей, образующихся при цветном проявлении, а также улучшать цветоделение и изменять эффективную спектральную чувствительность зональных эмульсионных слоев. Ингибитор процесса проявления, образующийся при цветном проявлении в зеленочувствительном эмульсионном слое, может диффундировать в смежный синечувствительный слой, причем чем выше экспозиция и плотность зеленочувствительного слоя, тем больше будет образовываться ингибитора проявления, который приведет к дальнейшему существенному замедлению процессов восстановления микрокристаллов галогенида серебра светочувствительного слоя и уменьшению выхода красителя. Возникший при этом меж-слойный эффект по своему действию очень близок к цветоделительному процессу маскирования и приводит к компенсации вредного поглощения пурпурного красителя в синей части спектра, что и способствует существенному улучшению воспроизведения.
Сегодня галогенсеребряные фотографические системы, по сравнению с другими носителями информации, обладают самой высокой светочувствительностью (цветные негативные и обращаемые фотоматериалы 3200 ед. ASA, а черно-белые при форсированной обработке 12 500-25 000 ед. ASA); большим сроком хранения как неэкспонированных, так и экспонированных фотоматериалов (несколько лет без ухудшения фотографических параметров); довольно высокой плотностью записи информации (в десять раз больше, чем при магнитной записи), а также великолепным качеством изображения, включая цветопередачу. Если говорить о светочувствительности галогенсеребряных фотоматериалов, то, как считают эксперты, граница максимальной чувствительности пока еще не достигнута, несмотря на то, что она выросла за 168 лет существования фотографии более чем в 100 раз. Высказываются мнения, что чувствительность теоретически можно увеличить еще на несколько ступеней, т. е. к 2010 г. светочувствительность цветных негативных фотопленок может достигнуть индекса экспозиции 8000 при сохранении структурно-резкостных характеристик на уровне современных пленок. Такой процесс будет достигнут за счет того, что эмульсионный микрокристалл галогенида серебра будет проявляться при поглощении 2-4 фотонов, в то время как сегодня для этого необходимо более 10 фотонов. Такой эффект может быть достигнут за счет существенного повышения квантовой эффективности микрокристаллов галогенида серебра.
Некоторые специалисты предсказывают, что при незначительном ухудшении зернистости светочувствительность цветных негативных фотопленок в 2016 г. может достигнуть величины 100 000 ед. ASA, что позволит проводить фотосъемку в лунную ночь с выдержкой 1/60 при диафрагме 4, получая при этом хорошее качество изображения. В настоящее время можно констатировать, что современная фотография на галогенидах серебра представляет собой хорошо отработанный технический
метод, благодаря своему неисчерпаемому многообразию и высокому качеству изображения. На ближайшее время у фотографии на галогенидах серебра нет потенциальных конкурентов и, естественно, она имеет свое будущее, как научно-техническое так и экономическое. Однако в обозримом будущем ей предстоит принять вызов со стороны электронной фотографии, тем более, что уже сегодня отчетливо наблюдается в мире тенденция соединить передовую фотографическую технологию на галогенидах серебра с электроникой и оптоэлектроникой. Что касается качества изображения-разрешающей способности, получаемой с помощью электронной фотокамеры, то она ниже, чем на цветной фотопленке, но многие специалисты считают, что в ближайшее время появятся фотокамеры с разрешением 10”15 млн элементов при сохранении современного уровня светочувствительности. Но для того, чтобы достигнуть разрешения, получаемого сегодня на 35-миллиметровой галогенсеребряной фотопленке, необходимо иметь фотокамеру с 20 млн элементов изображения, однако решение этой проблемы потребует от специалистов в области электроники больших усилий.
Сегодня широкое применение электронных систем записи изображения сдерживается высокой стоимостью оборудования. Методы электронной фотографии пока не могут конкурировать с современным методам классической фотографии, они лишь дополняют ее. Но вскоре совершенствование технологии производства приведет к тому, что любительские фотокамеры станут дешевле, меньше по массе и габаритам, а качество изображения электронных цветных отпечатков будет соответствовать качеству обычных фотографий. Все это позволит рассматривать ближайшее будущее фотографии как сочетание электроники и фототехнологии, но, по мнению ведущих специалистов в области цветной фотографии, это не приведет к значительному сокращению классических методов галогенсеребряной фотографии, пожалуй, до 2050 г.
5.2. Фотоматериалы и механизм действия света
5.2.1. Схема фотографического процесса на галогенсеребряных слоях
В фотографии из огромного количества светочувствительных веществ, химических соединений, которые под действием света претерпевают какие-то изменения, широкое применение нашли лишь соли галогенидов серебра: хлорид серебра (AgCl), бромид серебра (AgBr) и иодид серебра (Agl), обладающие светочувствительностью только к сине-фиолетовой части видимого спектра. Отличительная особенность этих соединений — очень плохая растворимость в воде. Так, растворимость хлорида серебра равна 1,25 • 10 5 моль/л, а бромида серебра и иодида серебра соответственно 7,94- 10”7 моль/л и 1,22 • 10”8 моль/л. Фторид серебра (AgF) в фотографии не применяется из-за своей малой светочувствительности и очень высокой растворимости в воде (15,0 моль/л).
846
Новый справочник химика и технолога
Светочувствительные вещества должны обладать свойством не только изменяться под действием света, но и иметь способность в присутствии восстановителей усиливать те изменения, которые произошли в процессе экспонирования. Так, например, Agl и РЫ2 обладают светочувствительностью, причем соль свинца под действием света темнеет сильнее, чем соль серебра, но результат действия света усиливается в процессе химического восстановления только в случае иодида серебра. Эти и другие уникальные свойства галогенидов серебра по сравнению с другими светочувствительными веществами предопределили их широкое применение в фотографии не только в настоящее время, но и в обозримом будущем.
Схему фотографического процесса в приложении к галогенидам серебра можно представить следующим образом. Первой стадией являются установочные операции — установка света и фотокамеры, выбор фотоматериала, — с помощью которых получается оптическое изображение (ОИ). Во время второй стадии в процессе экспонирования фотоматериала образуется скрытое фотографическое изображение (СФИ). Далее следуют химико-фотографическая обработка, во время которой скрытое изображение превращается в видимое фотографическое изображение (ВФИ), и, наконец, отделочные операции, направленные на улучшение видимого изображения (ретушь и т. д.).
На заключительной стадии процесса на фотоматериале получается изображение объекта съемки, в котором распределение яркостей обратно распределению яркостей в объекте. Такое изображение называют негативным, или негативом. В позитивном изображении (позитиве) должно наблюдаться соответствие яркостей объекта съемки и изображения. Для этого необходимо проэкспонировать фотоматериал через негатив и повторить стадии обработки.
Двухступенчатость фотографического процесса, несмотря на трудоемкость, позволяет исправлять ошибки, полученные при съемке, и предоставляет возможность увеличивать изображение с негатива и безгранично его размножать.
Существует в практике фотографии и способ прямого получения позитивного изображения, так называемый процесс обращения, но одноступенчатость в этом случае — кажущаяся, т. к. она скрыта в самой схеме химико-фотографической обработки обращаемых фотоматериалов.
Фотоматериалы подразделяют на негативные (фотопленки, кинопленки, аэропленки, фотопластины), позитивные (кинопленки, фотобумага) и обращаемые. Никаких принципиальных различий между ними с точки зрения строения эмульсионного слоя почти нет, однако они различаются общей светочувствительностью, спектральной чувствительностью, контрастностью, фотографической широтой, зернистостью, разрешающей способностью и т. д.
5.2.2. Строение фотоматериала
Любой фотоматериал состоит из двух основных частей: подложки, или основы, и эмульсионного слоя (рис. 5.2.1, 5.2.2). На основу , которая может быть прозрачной, непрозрачной, жесткой или гибкой, при изготовлении фотоматериала наносят эмульсию. Чаще всего в качестве основы применяют прозрачную пленку толщиной 0,1-0,15 мм, стекло толщиной 1,2-2,0 мм, бумагу толщиной 0,2-0,3 и 0,7-0,8 мм, ткань, пластмассу, керамику или металл.
Рис. 5.2.1. Строение черно-белой фотопленки: / — защитный слой; 2 — эмульсионный слой; 3 — подслой; 4 — основа; 5 — противоореольный слой
Рис. 5.2.2. Строение черно-белых фотобумаг с баритовым слоем (а) и с полиэтиленовым покрытием (б): / — бумажная подложка; 2 — баритовый слой (BaSO^);
3 — эмульсионный слой; 4 — защитный слой;
5 - - белый полиэтиленовый слой (ТЮг);
6 — прозрачный полиэтиленовый слой
Эмульсионный слой гораздо тоньше, чем основа, имеет толщину 3-25 мкм и представляет собой тонкую взвесь микрокристаллов галогенида серебра в желатине. При высыхании эмульсии на основе микрокристаллы равномерно распределяются в желатиновой среде, причем они изолированы друг от друга и ориентированы силами желатина большей стороной параллельно основе. Средний размер микрокристаллов галогенида серебра в поперечнике колеблется (0,03-3 мкм).
Микрокристаллы могут иметь пластинчатое строение и форму правильных шестиугольников, треугольников,
Изготовление основы см.: Брагинский Г.И., Кудрна С.Н. Технология основы кинофотоматериалов и магнитных лент. Л.: Химия, 1980.
Химия фотографических процессов
847
усеченных треугольников, квадратов и т. д. (рис. 5.2.3). Кроме того, в современной технологии находят применение и микрокристаллы, имеющие кубическую, октаэдрическую, кубооктаэдрическую и более сложную, двойниковую форму (рис. 5.2.4, 5.2.5).
Рис. 5.2.3. Микрофотографии микрокристаллов галогенида серебра пластинчатого строения
Рис. 5.2.4. Идеальная форма кубического микрокристалла галогенида серебра (а) и кристаллов двойниковой структуры (б, в)
Светочувствительность микрокристаллов связана с их размерами, т. е. чем крупнее микрокристалл галогенида серебра, тем больше светочувствительность фотоматериала.
Однако существуют приемы, позволяющие синтезировать эмульсии, в которых микрокристаллы малых размеров имеют довольно высокую светочувствительность. По величине светочувствительности (5) галогениды серебра в порядке ее уменьшения можно расположить в ряд:
^AgBr/Agl > *S*AgBr > *^AgCl > *^Agl (5.2.1)
При изготовлении фотобумаг могут быть использованы и другие смеси галогенидов серебра, например AgBr/AgCl, AgCl/AgI, AgCl/AgBr.
Дисперсность микрокристаллов галогенида серебра в эмульсионном слое фотоматериала характеризуется кривой распределения по размерам, определяющей в эмульсии относительное содержание микрокристаллов данного размера (рис. 5.2.6).
Важную роль в эмульсионной технологии играет и желатин, который является смесью белков животного происхождения очень сложного состава.
Звено макромолекулы желатина состоит из большого числа остатков различных аминокислот, на концах и в боковых цепях ее содержатся функциональные группы —NH2 и —СООН:
NH2
RCH—СООН,
где R — полярные, неполярные, кислотные, и основные группы.
В щелочной среде молекула желатина приобретает отрицательный заряд в результате диссоциации функциональной группы —СООН:
а
Рис. 5.2.5. Идеальная форма октаэдрического микрокристалла галогенида серебра (а) и кристаллов двойниковой структуры (б, в)
О 0,1 0,2
0,3 0,4
2 X , МКМ
Рис. 5.2.6. Кривые распределения микрокристаллов по размерам низкочувствительного (7) и высокочувствительного (2) фотоматериалов: х — размер микрокристалла; Nx — число микрокристаллов данного размера на 1 000
848
Новый справочник химика и технолога
NH2
RCH—СОО“
В кислой среде за счет того, что аминогруппы (—NH2) желатина присоединяют ионы водорода, образуя группы —NH3, молекула приобретает положительный заряд:
NH3
RCH—СООН
Значение pH, при котором макромолекула желатина электронейтральна, т. е. суммарный заряд равен нулю, соответствует изоэлектрической точке желатина (для желатина изоэлектрическая точка соответствует pH = 4,7-5,2):
NH3 I RCH—COO
При изготовлении эмульсии желатин выполняет ряд важнейших функций:
а) является носителем светочувствительного вещества и удерживает галогенид серебра на основе;
б) обеспечивает роль защитного коллоида, обволакивая микрокристалл галогенида серебра при изготовлении эмульсии, изолирует кристаллы друг от друга и препятствует их слипанию;
в) способствует значительному увеличению собственной светочувствительности галогенидов серебра за счет фотографически активных примесей (ФАП).
Первые две функции могут выполнять любые синтетические полимеры, а третья присуща только желатину. Различают высокоактивный желатин, содержащий много активных примесей и применяемый при изготовлении высокочувствительных фотоматериалов, малоактивный желатин, содержащий мало активных примесей, и инертный желатин, который не содержит активных примесей.
Что касается подслоя и баритового слоя в случае фотобумаг, то они способствуют лучшему сцеплению (адгезии) эмульсионного слоя с основой. Баритовый же слой, кроме того, придает соответствующую белизну фотоотпечатку благодаря наличию BaSO4 и препятствует проникновению из фотоподложки в эмульсионный слой вредных примесей — ионов тяжелых металлов Fe2+, Cu2\ которые могут привести к понижению светочувствительности эмульсионного слоя (десенсибилизации) в процессе хранения фотоматериала и появлению белых точек на фотоотпечатке после обработки.
5.2.3. Схема изготовления фотоматериалов
Технология производства фотоматериалов очень сложна, т. к. при синтезе эмульсии и отливе основы протекает огромное количество различных физико
химических процессов. Схему изготовления фотоматериалов можно представить в виде двух стадий: синтеза фотографической эмульсии и нанесения эмульсии на подложку.
Синтез же фотографической эмульсии представляет собой следующие производственные стадии: эмульси-фикацию; физическое созревание; удаление побочных продуктов; химическое созревание.
В основе эмульсификации лежит реакция двойного обмена:
AgNO3 + KBr -» AgBr4< + KNO3 + KBr (5.2.2)
Эта операция осуществляется в определенной емкости (объемом 300-500 л), изготовленной из хромоникелевой стали, имеющей водяную рубашку и автоматические устройства для поддержания необходимой температуры в реакционном объеме. Исходными растворами при этом являются: раствор I (0,5% желатин, MeHal (KBr, КС1, К1), вода) и раствор II (азотнокислое серебро, вода). После полного растворения компонент раствор II вливают в раствор I, который находится в эмульсионноварочном аппарате и постоянно перемешивается с помощью мешалки.
Количество желатина во всем реакционном объеме невелико (~0,5 %), но его вполне достаточно, чтобы выполнять коллоиднозащитную функцию — обволакивать ультрамикроскопические частицы галогенида серебра, возникающие в процессе эмульсификации, препятствовать их слипанию и выпадению в осадок. После эмульсификации галогенид серебра практически не обладает светочувствительностью. В дальнейшем (на второй стадии) в процессе физического созревания эмульсию выдерживают при повышенной температуре (45-65 °C) в течение 0,5-1,0 ч.
Учитывая то обстоятельство, что растворимость частиц различна в зависимости от размеров, можно представить следующую картину. Ультрамикроскопические частицы галогенида серебра, обладающие хорошей растворимостью, через желатиновую оболочку, растворяясь, уходят в раствор и осаждаются на более крупных, плохо растворимых частицах. Это приводит к тому, что число частиц в реакционном объеме уменьшается, размер их увеличивается, а масса галогенида серебра при этом остается постоянной. В процессе укрупнения частиц происходит построение кубической электронейтральной кристаллической решетки галогенида серебра. Для увеличения растворимости плохо растворимого в воде галогенида серебра и ускорения процесса перекристаллизации в реакционный объем во время эмульсификации вводят избыток бромида калия (сверхэквивалентное количество), который хорошо растворяет бромид серебра. Для увеличения растворимости бромида серебра часто применяют и аммиак. Таким образом, в процессе физического созревания происходят перенос твердой фазы через жидкую и образование микрокристаллов галогенида серебра определенной формы и необходимой степени дисперсности.
Химия фотографических процессов
849
Светочувствительность эмульсии после физического созревания довольно низкая, примерно на уровне мокрого коллодионного процесса, т. к. еще не сказалась фотохимическая активность желатина. Поэтому после физического созревания в эмульсию добавляют желатин до 7-8 %, охлаждают ее в специальных кюветах студе-нения, измельчают и промывают водой от побочных продуктов (КМО3, избытка КВг или аммиака).
После этого проводят стадию химического созревания. Измельченную эмульсию -загружают в эмульсионноварочный аппарат второго созревания и включают мешалку. Затем эмульсию плавят, добавив небольшое количество желатина, содержащего фотографически активные примеси, и выдерживают ее в течение 30-50 мин при 40-50 °C. В процессе химического созревания на поверхности микрокристалла галогенида серебра протекают топохимические реакции между фотсирафически активными примесями (ФАП) и поверхностными ионами серебра, в процессе которых образуются термически неустойчивые серебряно-желатиновые комплексы, распадающиеся на металлическое серебро атомно-молекулярной дисперсности и сернистое серебро:
+ /о =rAg
Ag + ФАП—>. комплекс ^5 2 3) Ag2S
Инородные вкрапления, возникшие в микрокристалле в виде Ag и Ag2S, называемые центрами светочувствительности, нарушают электронейтральность решетки галогенида серебра и уменьшают ее устойчивость к действию света, т. е. в процессе химического созревания происходит увеличение светочувствительности микрокристалла. Чем больше продолжительность химического созревания, тем больше размер центра светочувствительности и выше светочувствительность микрокристалла. При большой продолжительности химического созревания центр светочувствительности перерастает в центр вуали, который может катализировать процесс восстановления микрокристалла галогенида серебра без действия на него света.
В процессе второго созревания дальнейший рост размеров микрокристаллов галогенида не наблюдается, т. к. при промывании эмульсии после физического созревания удаляется избыток бромида калия или аммиака, что приводит к полному прекращению перекристаллизации.
Таким образом, после химического созревания эмульсия готова к нанесению на подложку. Чтобы обеспечить определенные свойства готового фотомате-
Существуют и другие способы промывания эмульсии с выделением твердой фазы — коагуляцией и осаждением (подробно об этом см.: Шеберстов В.И. и др. Основы технологии светочувствительных слоив. М., «Химия», 1977).
риала, перед поливом в эмульсию вводят эмульсионные стабилизаторы, антисептики, дубители, смачиватели, спектральные сенсибилизаторы и другие вещества.
Эмульсионные стабилизаторы — это сложные органические соединения, которые препятствуют продолжению химического созревания в сухом эмульсионном слое в процессе его хранения, т. е. прерывают рост центров светочувствительности и превращение их в центры вуали. Кроме того, в эмульсию вводят антисептики — бактерицидные вещества, препятствующие размножению колоний бактерий, что может вызвать дефекты на поверхности желатинового эмульсионного слоя в виде серых пятен и привести к порче фотоматериала.
Для улучшения физико-механических свойств эмульсионного слоя перед поливом вводят вещества, называемые дубителями, например, формальдегид, соли хрома (III) и алюминия, глиоксаль и другие соединения. Реагируя с функциональными группами желатина, дубитель образует стабильные межмолекулярные поперечные мостичные связи, повышая тем самым его прочность и температуру плавления эмульсионного слоя.
Быстрое и равномерное растекание жидкой эмульсии на основе и высокая равномерность полива в процессе изготовления фотоматериалов обеспечивается смачивателями — веществами, снижающими поверхностное натяжение желатинового раствора. Спектральные сенсибилизаторы — сложные органические соединения, например красители цианинового ряда, —- при введении в эмульсию перед поливом расширяют спектральную чувствительность галогенидов серебфа.
Для повышения собственной светочувствительности во время химического созревания добавляют так называемые химические сенсибилизаторы: очень малые количества соединений серы (II) — тиосульфата натрия или комплексных солей золота (I) и других металлов (родия, иридия, ...).
После введения добавок в эмульсию ее фильтруют, проводят дезаэрацию и с помощью поливных машин при неактиничном освещении наносят на основу, смотанную в рулон. Готовый фотоматериал затем разрезают на соответствующий формат, перфорируют и упаковывают.
5.2.4. Основные представления о природе и механизме образования скрытого фотографического изображения
После экспонирования фотоматериала часть микрокристаллов галогенида серебра, на которые подействовал свет, приобретают новое качество, что и обусловливает их восстановление в проявляющем растворе до металлического серебра. Что же происходит с микрокристаллами в процессе экспонирования?
Давно было замечено, что на экспонированных микрокристаллах галогенида серебра по сравнению с неэкспонированными кристаллами увеличивается количество
850
Новый справочник химика и технолога
металлического серебра. Казалось, все понятно — в процессе фотолиза (photos — свет, lisis — разложение) молекула галогенида серебра разлагается на металлическое серебро и галоген:
AgHal + hv Ag + Hal, (5.2.4)
где hv — квант света.
На первом этапе такой взгляд многих устраивал. Однако с развитием спектрального и структурного анализа стало известно, что галогенид серебра имеет кубическую ионную решетку, в вершинах которой находятся разноименные ионы (рис. 5.2.7). Причем решетка галогенида серебра электронсйтральна — скомпенсирована по зарядам, т. е. каждый ион серебра (Ag ) со всех сторон окружен шестью ионами галогена (НаГ), а ион галоида — шестью ионами серебра, симметрично расположенными в пространстве.
Все это позволило реакцию (5.2.4) представить в следующем виде:
Hal ’ + hv —> Hal + ё
(5-2.5) Ag + е —> Ag
где ё — электрон; Hal — атом галоген; Ag — атом серебра.
В дальнейшем с развитием элекгронной микроскопии стало возможным наблюдать фотолиз иод микроскопом. Фотолитическое серебро, образующееся под действием света, имеет вид дискретных частиц и выделяется на поверхности в определенных местах микрокристалла.
С учетом многочисленных экспериментальных наблюдений английские ученые Р. Герни и Н. Мотт в 1938 г. предложили теорию, объясняющую механизм образования скрытого фотографического изображения. Они обратили внимание на то, что реальный эмульсионный микрокристалл отличается от идеального наличием:
- примесных центров (центров светочувствительности из металлического серебра [Ag]„);
- «дефектов» решетки по Френкелю, обусловленных подвижными ионами серебра (Ag(‘).
Под действием температуры ионы, составляющие решетку галогенида серебра, покидают свои места, и часть ионов серебра при этом не в состоянии вернуться обратно. Они перемещаются в межузельном пространстве и называются межузельными. Механизм перемещения ионов серебра в кристалле был объяснен советским ученым Френкелем.
Согласно теории Р. Герни и Н. Мотта, квант света поглощается ионом галогена, а выделившийся при этом электрон попадает в зону пониженной энергии (потенциальную яму), где нарушена взаимосвязь ионов за счет наличия примесного центра светочувствительности ([Ag]„). Фотоэлектрон захватывается центром и заряжает его отрицательно. Затем к отрицательно заряженному центру ([Ag]w) притягивается находящийся вблизи межузельный ион серебра (Ag^) и нейтрализуется здесь, превращаясь в атом серебра (рис. 5.2.8).
Атом брома, образующийся в процессе поглощения кванта света, эстафетно перемещается к поверхности микрокристалла как «положительная дырка» (неуравновешенные положительные ионы серебра, окружающие атом брома), получая эстафетно электрон от соседнего иона галогена. При этом атом брома становится ионом, а ион брома — атомом и т. д., т. е. атом брома и ион брома как бы обмениваются местами в решетке галогенида серебра. Процесс повторяется до тех пор, пока атом свободного брома не окажется на поверхности микрокристалла, где он связывается желатином эмульсионного слоя, что и препятствует возможному окислению центров скрытого изображения бромом.
Теория Р. Герни и Н. Мотта предусматривает вначале электронную, а затем ионную стадии, разобщенные во времени и в пространстве, в процессе которых центр светочувствительности при поглощении одного кванта света увеличивает свою массу и размер на один атом серебра:
Hal + hv —> Hal + е [Ag]n+e->[Ag];
(5.2.6)
[Ag]„+Ag0+ —>[Ag]n+1
Рис. 5.2.7. Строение кристаллической решетки бромида серебра
Рис. 5.2.8. Схематическое представление о фотографических элементарных процессах в микрокристалле галогенида серебра при его экспонировании
Химия фотографических процессов
851
Необходимо отметить, что только после нейтрализации отрицательного заряда первого электрона, закрепившегося на центре межузельным ионом серебра, и присоединения к центру светочувствительности первого атома серебра к центру сможет подойти следующий фотоэлектрон, который будет нейтрализован затем другим межузельным ионом серебра, и т. д.
Мельчайшую коллоидную частицу из металлического серебра, возникшую при этом, еще не способную катализировать восстановление микрокристалла галогенида серебра, но довольно стабильную (два-три атома серебра), т. е. не подвергавшуюся распаду длительное время, называют субцентром скрытого изображения. В свою очередь устойчивую коллоидную частицу, достигшую критических размеров (минимальный размер центра — четыре атома серебра) и способную катализировать восстановление экспонированного микрокристалла в проявляющем растворе, называют центром проявления.
От уровня освещенности микрокристалла зависят размер центров скрытого изображения и их топография. При больших освещенностях образуются как поверхностные, так и глубинные центры скрытого изображения. При средних освещенностях образуются поверхностные центры, а при низких освещенностях — субцентры.
Помимо теории Р. Герни и Н. Мотта существует и другая теория (Дж. Митчелла), объясняющая образование скрытого фотографического изображения. Согласно этой теории, начальной стадией является присоединение центром светочувствительности межузельного иона серебра, а затем его нейтрализация электроном, образовавшимся при поглощении кванта света. Отличительная особенность теории Митчелла состоит в том, что скрытое изображение может образоваться без участия центров светочувствительности, а им отводится лишь роль акцепторов «положительных дырок». В процессе экспонирования скрытое фотографическое изображение возникает по схеме:
Ag^ + ё + Ago <=^ Ag + Ago <=* Ag* (предцентр)
Ag;+e<=»Ag2 (субцентр)
Ag2 + Ago + ё <=> Ag; + ё -> Ag3
Ag3 + Ag0+ —> Ag; (центр проявления).
Вначале образуется неустойчивый центр, стабильность которого составляет десятые доли секунды; его называют предцентром.
Субцентры, состоящие из двух, трех атомов серебра, стабильны только в течение нескольких десятков часов; центры из четырех и более атомов серебра достаточно устойчивы и способны выполнять роль центров проявления.
Исследования последних лет показали, что первичные центры атомно-молекулярной дисперсности не способны локализовать электроны, в то же самое время
они хорошо присоединяют межузельные ионы серебра. Это позволяет предполагать, что рост центров на ранних стадиях экспонирования микрокристаллов осуществляется по механизму, предложенному Митчеллом. В свою очередь электронно-акцепторная способность более крупных предколлоидных центров, состоящих из большого числа атомов серебра, обнаруженная советским ученым Белоусом, позволяет считать, что рост таких центров на стадии фотолиза происходит по механизму Герни и Мотта.
Таким образом, различие в скорости восстановления экспонированных и неэкспонированных микрокристаллов галогенида серебра в эмульсионном слое обусловлено в основном наличием в экспонированном кристалле катализатора из металлического серебра — центра скрытого изображения, который ускоряет процесс восстановления. Неэкспонированные же микрокристаллы галогенида серебра, не имеющие центров скрытого изображения, не могут восстанавливаться до металлического серебра. Механизм восстановления экспонированных микрокристаллов галогенида серебра в присутствии серебряных центров скрытого изображения подробно рассмотрен в подразделе «Процессы химико-фотографической обработки светочувствительных материалов».
5.3. Процессы химико-фотографической обработки светочувствительных материалов
Химико-фотографическая обработка светочувствительных слоев на основе галогенидов серебра представляет собой совокупность сложных физико-химических процессов, которые проводят после экспонирования фотоматериала; целью их является получение устойчивого видимого изображения. Различают первичную и вторичную химико-фотографическую обработку.
Первичная обработка — это необходимый ряд операций, направленных на получение видимого фотографического изображения.- К этому виду обработки относят проявление, фиксирование, промывание, иногда отбеливание.
Вторичная обработка направлена, как правило, на улучшение качества изображения, полученного в процессе первичной химико-фотографической обработки, и включает следующие процессы: ослабление, усиление, вирирование (тонирование) и в некоторых случаях отбеливание.
5.3.1. Процесс проявления и проявляющие растворы
Проявление — избирательный процесс восстановления экспонированных микрокристаллов галогенида серебра в эмульсионном слое фотоматериала, способа ствующий превращению скрытого изображения в видимое. Специальные растворы, применяемые для этих целей, называются проявляющими, или проявителями. Они представляют собой сложную многокомпонентную систему, состоящую из одного проявляющего вещества или нескольких, щелочи, антиоксиданта, антивуалента и других веществ.
852
Новый справочник химика и технолога
5.3.1.1. Проявляющие вещества
Проявляющими веществами называют химические соединения, которые легко отдают электрон и восстанавливают ионы серебра до металлического серебра. Не всякий восстановитель можно применять в фотографии: не все они обладают свойствами избирательного восстановления, т. е. способностью восстанавливать только те микрокристаллы галогенида серебра, на которых имеется серебряный центр скрытого изображения — катализатор процесса проявления.
В химии существует довольно много энергичных восстановителей различных классов, которые очень легко передают электрон галогениду серебра, но многие из них при этом неизбирательно восстанавливают как экспонированные, так и неэкспонированные микрокристаллы галогенида серебра.
Проявляющее вещество должно восстанавливать экспонированные микрокристаллы галогенида серебра с гораздо большей скоростью, чем неэкспонированные кристаллы. Немаловажное значение имеют и другие свойства проявляющих веществ, такие, как хорошая растворимость в воде или щелочных растворах, экологическая безвредность, плохая окисляемость кислородом воды и воздуха, способность образовывать при окислении бесцветные и легкорастворимые соединения.
В качестве проявляющих веществ применяются как неорганические, так и органические соединения, к которым можно отнести:
- ионы металлов или комплексные ионы переменной валентности, меняющие свою валентность с низшей на высшую с последующей отдачей электрона (ионы Fe2+, Ti3+, V2+);
- соединения или ионы, которые содержат неметаллы с переменной валентностью (Na2S2O4 — дитионат натрия, NH2OH — гидроксиламин, NH2NH2 — гидразин);
- органические соединения — производные ароматических углеводородов, содержащие по крайней мере две активные группы —ОН и —NH2 или их сочетания:
H2N(—С=С)„-------NH?
НО(—С=С)„—оч, НО(—С=С)„---------------NH2
— органически»7 соединения — производные гетероциклов (фенидс! и др.).
Неорганические проявляющие вещества. Из неорганических проявляющих веществ практический интерес представляют соединения железа(П), которые применялись еще на раннем этапе развития фотографии. Процесс проявления соединениями железа можно записать уравнением:
Fe++—> Fe++++ё (5.3.1)
Ag*+e^Ag (532)
Эта реакция является обратимой, и для того чтобы она шла в нужном направлении, необходимо ионы высшей степени валентности удалять из проявляющего раствора за счет связывания их в комплексы или путем восстановления.
В последние годы особый интерес вызывают у специалистов ванадиевые проявляющие растворы на основе VBr2, которые по своим восстановительным свойствам существенно превосходят малоактивные неорганические проявители на основе соединений железа(П). Восстановление ионов серебра при этом происходит по следующей схеме:
V’'->V~"+? (5.3.3)
Ag++e->Ag (5 34)
Проявляющие растворы, содержащие соль Вг2 (-0,45 моль/л), в присутствии серной или бромистоводородной кислоты восстанавливают ионы серебра в 50-180 раз быстрее, чем обычные проявители. Так, например, позитивная мелкозернистая кинопленка при температуре проявителя 15 °C проявляется за 15-20 с практически без индукционного периода. Использование ванадиевых проявителей для обработки кинофотоматериалов представляет особый интерес в машинах непрерывного действия (телевидение, кинематография и т. д.), в которых концентрацию V + можно поддерживать на постоянном уровне путем электролитической регенерации проявителя:
V++*+e^V+4 (5.3.5)
Для неорганических неметаллических проявляющих веществ, таких, как дитионат натрия (Na2S2O4), гидразин (N2H4), гидроксиламин (NH2OH), восстановление ионов серебра происходит по следующей схеме:
Na2S2O4 + 2Н2О -> 2NaHSO3 + 2Н+ + 2ё (5.3.6) 2 Ag++ 2ё —> 2Ag (5.3.7)
N2H4 —> N2 + 4Н + 4е (5.3.8)
4Ag+ + 4ё —> 4Ag (5.3.9)
NH2OH + OH^H2NO +П2О (5.3.10) H2NO~ + Ag+—> Ag + H2NO (5.3.11)
2H2NO —> 2H2O +N2 (5.3.12)
При восстановлении ионов серебра гидразином, как считают многие ученые, имеет место не одна, а несколько стадий; не исключается при этом образование промежуточных продуктов. В случае восстановления гидроксиламином, по Т. Джеймсу, образуется N2
Химия фотографических процессов
853
(при каталитическом его окислении) и NO (при некаталитическом). В сочетании с другими проявляющими веществами гидроксиламин может быть активатором процесса восстановления галогенида серебра, особенно при цветном проявлении.
гидрохинон «-диоксибензол
1,4-диоксибензол
пирокатехин о-диоксибензол
1,2-диоксибензол
пирогаллол 1,2,3-триокси-бензол
Органические проявляющие вещества. В настоящее время почти все основные проявляющие вещества — органические: производные ароматических углеводородов (бензола). Для того чтобы производные бензола восстанавливали галогенид серебра, необходимо провести замещение в молекуле бензола не менее двух водородов на активные гидрокси —ОН или аминогруппы —NH2 и их сочетания. Можно провести реакцию так, что активные группы —ОН или —NH2 окажутся в орто-, мета- и няря-положениях:
2) аминофенолы: «-аминофенол, метол, глицин,
бензол а
амидол:
метол
4-метиламинофенол-сульфат
«-аминофснол
1,4-аминофснолгидрохлорид
глицин
«-гидроксифснилглицин
амидол
1 -гидроиси-2,4-ди-аминобензолхлорид
Почти все полученные соединения могут быть рекомендованы в качестве проявляющих веществ, за некоторым исключением. Рассматривая связь между строением органических соединений и проявляющей способностью, К. Ляликов указал, что восстановительная способность соединения связана с плотностью электронного облака в отдельных точках молекулы. Оказалось, что высокая электронная плотность наблюдается только для орто- и «аря-замещений, содержащих активные группы. Метазамещение не вызывает повышения плотности электронного облака, что не способствует отдаче электрона. Таким образом, органическое соединение (производное бензола), имеющее активные группы в орто- и «оро-положениях, обладает проявляющей способностью, а в л/е/и<7-положении практически не проявляет.
Если активные группы —ОН и —NH2 будут находиться в местах, отмеченных (X) на формуле (случай д), то данное соединение обладает проявляющей способностью за счет активных групп, расположенных в орто-положении.
Органические проявляющие вещества (производные бензола) можно разделить на три типа:
1) многоатомные фенолы: гидрохинон, пирокатехин, пирогаллол и их производные:
3) ароматические диамины (проявляющие вещества
данного класса применяют в цветной фотографии):
«-фенилендиамин
этилоксиэтил-«-фенилен-диаминсульфат
(ЦПВ-2, Т-32)
диэтил-«-фенилендиамин-сульфат (Ц11В-1, Т-22)
2-амино-5-диэтиламино-
толуолгидрохлорид (CD-2)
854
Новый справочник химика и технолога
<?Н3
NH2’3/2 H2SO
Н5С2
c^h4nhso2ch3
2-амино-5-[А-этил-Л/-(Р-метилсульфонамидоэтил)]-аминотолуолсульфат моногидрат (CD-3)
NH2’ h2so
с2н4он
4
2-амино-5-[А-этил-Л/-(|3-гидроксиэтил)]-амино-толуолсульфат (CD-4)
4-амино-Л/-этил-^(Р-метоксиэтил)-/и-толуидинди-и-толусульфонат (CD-6)
Н9С4 XC4H8SO3H-H2SO4
4-[А/-и-бутил-А/-р-сульфо-и-бутил-амино]-анилинсульфат (АС-60)
В последние десятилетия широкое применение в фотографии нашло синтезированное (1890 г.) проявляющее вещество — производное пиразолидона — l-фенил-З-пиразолидон (фенидон), проявляющая способность которого была обнаружена Кендаллом еще в 1940 г.:
Я n ..
* I 4 3 I
Н,СВ 1 2.NH
пиразолидон-3
н2?Т~а1?’0 * I W W |
н9с513ин
1 -фенил-З-пиразолидон (фенидон)
Сам фенидон проявляет слабо и только до оптической плотности —1,0, но при добавлении его в гидрохиноновый проявитель существенно возрастает скорость процесса проявления. Практически фенидон нечувствителен к накоплению ионов брома в проявляющем растворе. Этим объясняется его применение при машинной обработке кинофотоматсриалов, где он полностью вытеснил метол — более чувствительный к накоплению бромидов в проявителе.
Универсальной теории, объясняющей взаимосвязь между строением проявляющих веществ и их проявляющей способностью, пока еще нет. Правда, сегодня существует общая формула строения проявляющих веществ, предложенная Дж. Кендаллом и усовершенствованная В. Пельцем, которая охватывает проявляющие вещества, относящиеся как к ароматическим, так и к алифатическим соединениям:
I I
а (—С = А)„ — а'
где а и а'—активные группы—ОН,—NH2, —NHR,
—NRiR2; А — углерод (=С—) или азот (=N—), п = 0, 1,2,3.
Так, случай п = 0 в формуле соответствует неорганическим проявляющим веществам: пероксиду водорода (НООН), гидроксиламину (NH2—ОН), гидразину (H2N—NH2). При п = 2 формула соответствует гидрохинону, парааминофенолу и п-фенилендиамину.
Природа активных групп и их положение в молекуле влияют на скорость процесса проявления. Проявляющие вещества, функциональные группы которых находятся в «ара-положении, активнее чем вещества, имеющие заместители в opwo-положении. Замещение атомов водорода в фенольном ядре на группы —СООН и —SO3H снижает активность проявляющих веществ, а введение хлора и брома в бензольное ядро в свою очередь повышает их активность. Диоксибензолы активнее, чем аминофенолы, а последние активнее, чем фенилендиамины. Проявляющие вещества, имеющие две гидроксильные группы, требуют, как правило, использования в проявителе сильной щелочи, а вещества при двух аминогруппах или активных группах —ОН и — NH2 не требуют высокого значения pH при проявлении.
5.3.1.2. Роль щелочи в проявителе
Водные растворы большинства проявляющих веществ почти не обладают проявляющей способностью, и только при добавлении незначительного количества щелочи скорость процесса проявления начинает резко возрастать. Это объясняется тем, что в присутствии щелочи существенно увеличивается степень диссоциации проявляющих веществ, которые являются в основном слабыми кислотами, основаниями или амфолитами, что и приводит к увеличению концентрации активной (ионной) формы проявляющего вещества в проявителе и в дальнейшем обеспечивает повышение скорости про
Химия фотографических процессов
855
цесса восстановления галогенида серебра. Таким образом, щелочь в проявляющем растворе создает определенную концентрацию ионов гидроксила ОН” (повышает pH = —lg[H4]) и является регулятором этой концентрации в процессе проявления, способствуя при этом смещению равновесия системы: молекулярная форма ионная форма проявляющего вещества в сторону увеличения концентрации ионной (активной) формы. Диссоциация гидрохинона, я-аминофенола, метола, я-фенилендиамина происходит по следующей схеме:
константа диссоциации гидрохинона
[н-][с;н4оно]16 10 [С6Н4(ОН)2]
[НД[С6Н4О-] 12
2 [С6Н4ОНО]
(5.3.13)
диссоциация «-аминофенола по кислотному типу
(5.3.14)
диссоциация «-аминофенола по основному типу
(5.3.15)
диссоциация метола по кислотному типу
к _[H+][CH3NHC6H4Q-]_1 1О.„ (5>316)
кисл [CH3NHC6H4OH]
диссоциация «-фенилендиамина
К,= 10”8
К2 = 3,5 • 1О'10 (5.3.17)
Щелочь нейтрализует также бромистоводородную кислоту, образующуюся в процессе проявления и накапливающуюся в проявителе, количество которой пропорционально металлическому серебру, выделяющемуся в процессе восстановления галогенида серебра:
Кроме того, щелочь связывает кислоту, которая вводится с проявляющим веществом в проявитель, т. к. большинство проявляющих веществ плохо растворимы в воде и для повышения растворимости их обычно применяют в виде солянокислых или сернокислых солей. Определенное количество щелочи расходуется также и на титрование желатина фотографического слоя до значения pH, обеспечивающего начало процесса проявления галогенида серебра данным проявляющим веществом (пороговое значение pH) (табл. 5.3.1).
В фотографической практике находят применение различные щелочи:
«м-->.......... -...»..—.........t----- pH
13,0 Т2.0 Ю.5 8.3
—---------------------------------------- р
При одинаковых эквивалентных концентрациях щелочи pH проявляющего раствора возрастает в случае применения Na2B4O7 и КОН от 9,0 до 13,0, а буферная емкость проявителя 0, характеризующая его способность сохранять в процессе работы на постоянном уровне pH, наоборот, уменьшается. Выбор щелочи определяется
856
Новый справочник химика и технолога
многими факторами, которые учитывают природу проявляющего вещества и характер процесса проявления. В случае быстрой или скоростной обработки кинофотоматериалов проявитель готовят обычно на едкой щелочи (КОН, NaOH). Это обеспечивает высокую скорость процесса проявления, но в связи с тем, что едкая щелочь полностью диссоциирована в проявителе, по мере ее расходования через определенное время наступает понижение pH проявителя и замедление процесса проявления. В случае же применения углекислых щелочей (К2СО3, Na2CO3), тринатрийфосфата (Na3PO4) и буры (Na2B4O7) по мере расходования щелочи на титрование бромистоводородной кислоты и желатина эмульсионного слоя в процессе проявления все новые порции указанных щелочей подвергаются гидролизу, что и обусловливает поддержание pH проявляющего раствора на постоянном уровне за счет образования едкой щелочи:
Na2CO3 + Н2О = NaHCO3 + NaOH (5.3.19)
Na2B4O7 + Н2О = NaHB4O7 + NaOH (5.3.20)
Na3PO4 + H2O = Na2HPO4 + NaOH (5.3.21)
Таблица 5.3.1
Пороговое значение pH для органических проявляющих веществ
Проявляющее вещество Пороговое значение pH
Гидрохинон 9,5
Метол 7,25
Фенидон 6,0
и-Фенилендиамин 6,25
Глицин 9,0
Амидол 4,0
и-Аминофенол 9,35
Пирогаллол 8,0
Пирокатехин 9,5
Учитывая то обстоятельство, что проявители с едкой щелочью быстро истощаются, в фотографической практике иногда применяют смеси КОН и К2СОз или NaOH и Na2CO3, которые позволяют получать довольно хорошие результаты. В последнее время в качестве щелочи применяют тринатрийфосфат, который обеспечивает высокую буферную емкость проявителей в интервале pH от 11,0 до 12,0.
5.3.1.3. Роль сульфита натрия в проявителе
Сульфит натрия в проявляющем растворе выполняет несколько функций. Одна из них — защита органических проявляющих веществ от окисления кислородом, растворенным в воде. При высоком значении pH
в отсутствие сульфита натрия, например, гидрохинон окисляется с образованием хинона, что приводит к тому, что проявляющий раствор становится сначала светло-желтым, а затем темно-коричневым за счет оксихинона, теряя при этом способность восстанавливать галогенид серебра:
Сульфит нагрия, добавляемый в малых количествах в проявляющий раствор, существенно снижает скорость поглощения кислорода проявляющим веществом (рис. 5.3.1) за счет того, что он сам связывает кислород и превращается при этом в сульфат натрия:
(5.3.24)
В свою очередь метол и гидрохинон в малых количествах резко снижают окисляемость сульфита. Механизм этого явления до сих пор до конца не ясен. Правда, существует мнение, что сульфит связывает окисленную форму, которая значительно катализирует окисление самого проявляющего вещества.
В процессе проявления сульфит натрия играет очень важную роль — обеспечивает низкую концентрацию окисленной формы проявляющих веществ и переводит ее в растворимые в воде бесцветные соединения (сульфонаты):
(5.3.25)
Кроме того, сульфит натрия в процессе проявления связывает окисленную форму проявляющего вещества и сдвигает равновесие реакции проявления вправо,
Химия фотографических процессов
857
обеспечивая при этом постоянную скорость процесса за счет образования нового восстановителя (моносульфоната гидрохинона), который способен восстанавливать экспонированный галогенид серебра.
При высоких концентрациях сульфита натрия в проявителе (-125 г/л) происходит уменьшение зернистости фотографического изображения в результате частичного подрастворения микрокристаллов галогенида серебра, которое в свою очередь приводит к обнажению внутренних центров скрытого изображения кристалла и увеличению оптической плотности почернения (рис. 5.3.2). Причем чем медленнее работает проявитель, тем в большей степени сказывается растворяющее действие сульфита на микрокристалл галогенида серебра. Образующийся при этом растворимый серебряно-сульфитный комплекс [Ag/SO^]3 восстанавливается в проявляющем растворе (физическое проявление), и за счет более компактной формы восстановленного серебра наблюдается понижение зернистости, обусловливающее улучшение качества негативного фотографического изображения.
О 0,2 0,4 0,6 0,8 1
Метол Сульфит
Рис. 5.3.1. Взаимное влияние метола и сульфита натрия на их окисление в проявляющем растворе при pH = 6,6
CNa2SO,, МОЛЬ/Л
5.3.1.4. Антивуалирующие вещества
В процессе химико-фотографической обработки фотоматериала на участках эмульсионного слоя, не получивших экспозицию, возникает, как правило, почернение, которое называют плотностью вуали. Образование вуали, с одной стороны, может происходить в результате того, что центр светочувствительности на микрокристалле галогенида серебра в процессе второго химического созревания эмульсии или хранения фотоматериала увеличивает свой размер до критического и при этом превращается в так называемый центр вуали, который действует так же, как центр скрытого изображения, и способен вызывать самопроизвольное проявление, т. е. катализировать восстановление микрокристалла галогенида серебра без действия света. Такой вид вуали называют эмульсионной вуалью. Для ее уменьшения в эмульсию при изготовлении вводят вещества, называемые эмульсионными стабилизаторами (например, 7-гидрокси-5-метил-1,2,4-триазаиндолицин, 1-фенил-5-меркаптотетразол и др.), которые препятствуют дальнейшему росту центра светочувствительности в процессе хранения фотоматериала.
Кроме того, вуаль на фотоматериале может возникать также и в результате восстановления ионов серебра из проявляющего раствора и последующего осаждения образовавшихся вновь высокодисперсных частиц металлического серебра на неэкспонированных участках слоя. Это вуаль проявления. Для уменьшения вуали в проявляющий раствор вводят вещества, называемые антивуалентами. Чаще всего это бромид калия, который существенно увеличивает индукционный период проявления (промежуток времени от начала погружения фотоматериала в проявляющий раствор до появления первых следов почернения на эмульсионном слое) неэкспонированных участков слоя и практически не оказывает влияния на проявление экспонированных. Кроме бромида и иодида калия при проявлении фотоматериалов в качестве антивуалентов применяют и некоторые органические вещества, относящиеся к различным классам гетероциклических соединений: бензотриазол, 5-метилбензотриазол, бензимидазол, 5-нитро-бензимидазол, 6-нитробензимидазол, 2-меркаптобенз-имидазол, 5-нитроиндазол, 1-фенил-5-меркаптотетра-зол, дифенилтетразолдисульфид и др.:
бензимидазол 5*нитробензимидазол
Рис. 5.3.2. Влияние содержания сульфита натрия в гидрохиноновом проявителе на величину оптической плотности D при проявлении фотографического слоя в гидрохиноновом проявителе в течение 2 (/), 3 (2), 4 (3), 5 (4) и 6 (5) мин
6-нитробензимидазол 5-нитроиндазол
858
Новый справочник химика и технолога
2-меркаптобензимидазол 1-фенил-5-меркаптотетразол
c«Hz-N---CS—SC N—CftH
° & | н Ц | 6
дифенилтетразолдисульфид или бис-(1-Фенил -тетразолил-5) дисульфид
Большинство органических антивуалентов, применяемых в проявителях для понижения оптической плотности вуали, представляют собой слабые кислоты, которые диссоциируют по следующей схеме:
константа диссоциации
Ка = 7,94 • Ю’10
рКа =-lgKa = 9,1 (5.3.26)
Таблица 5.3.2
Константы диссоциации антивуалентов и произведения растворимости солей серебра (по В. Павловой)
Антивуалент Константа кислотной диссоциации антивуалента ка Произведение растворимости серебряной соли* ПР = [Ag+] - [А ]
Бензотриазол Бензимидазол 5-Нитробензимидазол 2-Меркаптобенз-им ид азо л 1 -Фенил-5-меркаптотетразол 5-Метил-7-окситри-азоиндолицин Бромид серебра Хлорид серебра 5 • 10 9 2,7 • 10’12 4,9 • 10“” 2,5 • Ю"10 4,6- 10 4 3,2 • 10’7 4 • 10“14 3 • 10 12 6 • 10“13 4- 10 16 1 • 10’14 3•10’” 5,3 • 10’13 1,78 • 10 10
*Произведение растворимости (ПР) труднорастворимого соединения (/СтЛ„) при данной температуре характеризуется произведением концентраций ионов в степени стехиометрических коэффициентов ПР = [K"+]w • [А"'”]", где К”" — катион, А"'“ — анион.
5-метилбензотриазол
константа (3.27) диссоциации Ка = 1,26 • 10’12
рКа- lgKa= 11,9 (5.3.27)
Растворимость солей серебра большинства органических антивуалентов существенно понижается с увеличением pH раствора (рис. 5.3.3), и она в этом случае становится гораздо меньше, чем растворимость хлорида серебра. При этом и концентрация свободных ионов серебра в растворе с увеличением значения pH также понижается (рис. 5.3.4). Ее величину в насыщенном растворе серебряной соли антивуалента для оценки эффективности различных органических антивуалентов в проявителе можно вычислить по формуле, которую предложил Б. Бирр:
Константы диссоциации некоторых органических антивуалентов и произведения растворимости их солей серебра приведены в табл. 5.3.2.
В проявляющем растворе анионы органических антивуалентов при pH = 9,5-ь 13,0 образуют с ионом серебра труднорастворимые соли серебра, произведение растворимости которых меньше, чем у бромида серебра (табл. 5.3.2):
Ag+ + А’ «=> AgA Н++А” <=^НА,
(5.3.28)
(5.3.29)
где А — анион органического антивуалента (кислотная форма); AgA — серебряная соль антивуалента.
(5.3.30)
где К5р — константа равновесия реакции (5.3.28), определяющая величину растворимости серебряной соли AgA; Ка — константа диссоциации антивуалента.
В отношении механизма тормозящего действия антивуалирующих веществ существуют различные точки зрения. Некоторые исследователи объясняют понижение эмульсионной вуали и вуали проявления химическим сродством антивуалентов к ионам серебра и уменьшением эффективной концентрации ионов серебра в проявителе, которое происходит за счет образования солей серебра и антивуалента, обладающих гораздо меньшей растворимостью, чем галогенид серебра
Химия фотографических процессов
859
(см. рис. 5.3.3), и труднее восстанавливаемых в проявителе (рис. 5.3.5). При этом адсорбция бромистым серебром антивуалента или его серебряной соли способствует созданию вокруг микрокристалла галогенида серебра защитного слоя, наличие которого считается одним из важных факторов антивуалирующего действия.
Рис. 5.3.3. Влияние pH раствора на растворимость серебряных солей — концентрацию ионов серебра в растворе (pAg = - 1g [Ag+]:
1 — хлористоводородной кислоты;
2 — 5-метил-7-окси-1,3, 4-триазоиндолицина; 3 — бензимидазола;
4 — бромистоводородной кислоты;
5-- 2-метилбензимидазола; 6 — нитробензимидазола;
7 — бензотриазола; 8 — 1 -фенил меркаптотетразола (по В. Павловой)
Рис. 5.3.4. Изменение потенциала, характеризующего концентрацию серебра в зависимости от pH раствора (по Е. Кляйну)
Существует, кроме того, точка зрения других ученых, согласно которой антивуаленты, селективно адсорбируясь на центрах светочувствительности микрокристалла галогенида серебра, значительно понижают каталитическую активность этих центров в процессе проявления. Данные X. Вуда подтверждают наличие адсорбции многих антивуалентов на Ag2S и Ag, причем обнаружено, что адсорбция на Ag2S гораздо больше, чем на Ag и AgBr (табл. 5.3.3). Это и приводит к изоляции потенциального центра вуали из Ag2S и понижению его каталитической активности в процессе восстановления неэкспонированного микрокристалла галогенида серебра. Кроме того, органические антивуаленты, например 1-фенил-5-меркаптотетразол, хорошо адсорбируемые металлическим серебром, по этой же причине заметно замедляют процесс физического проявления после фиксирования, даже при концентрациях антивуалента, существенно нс снижающих активность ионов серебра в проявителе.
Эффективность антивуалирующих веществ в процессе проявления, как и проявляющих веществ, можно оценить избирательной способностью (U), или селективностью, которая пропорциональна отношению скоростей проявления (v) изображения до оптической плотности D = 1,5 и вуали до плотности DQ = 0,3 как в отсутствие антивуалента, так и в его присутствии:
VDo=0,3
гдеЛ> 100; vD=15
1 1
/пр ДО £> = 1,5’ ^О'3”/прдо£> = 0,3’
Гпр до D - 1,5 — время проявления, за которое достигается оптическая плотность изображения, равная 1,5 на равномерно экспонированном участке фотоматериала; /пр до Do = 0,3 — время проявления, за которое достигается оптическая плотность вуали, равная 0,3.
/, с
Рис. 5.3.5. Восстановление золей серебряных солей органических антивуалентов в проявляющем растворе при pH = 10,6 (обозначения те же, что и на рис. 5.3.3): D — оптическая плотность
860
Новый справочник химика и технолога
В фотографии практический интерес представляют только те антивуаленты, которые повышают избирательность процесса проявления, т. е. оказывающие существенное тормозящее действие на процесс образования вуали и почти не влияющие при этом на величину оптической плотности изображения.
Наличие отрицательного электрического барьера из ионов брома вокруг микрокристалла галогенида серебра (рис. 5.3.6) препятствует в процессе проявления неэкспонированного кристалла подходу отрицательно заряженного иона проявляющего вещества к поверхности микрокристалла и его восстановлению. Отрицательный барьер обусловлен значительной адсорбцией избыточных ионов брома на поверхности галогенида серебра, которые присутствуют всегда в процессе образования твердой фазы (бромида серебра) при изготовлении эмульсии (эмульсификация, физическое созревание).
Таблица 5.3.3
Теплота адсорбции по X. Вуду (мкал/м2)
Антивуалент Адсорбент
AgBr Ag Ag2S
2-Тиоурацил — — 103
6-Метил-2-тиоурацил 44 15 80
5,6-Диметил-З -этил-2-тиоурацил 27 26 69
1,2-Диметил-5-меркапто- 1,3,4-триазол 14 12 52
5-Метил-7-гидрокси-л-триазоло-(2,3 я)-пиримидин 5 8 46
2,5-Димсркапто-1,3,4-тиадиазол — — 158
1 -Фенил-5-меркапто-1,2,3,4-тетразол 43 53 93
1 -Метил-5-меркапто- 1,2,3,4-тетразол 179 60 104
Бензотриазол 2 11 41
2-Меркаптобензимидазол 26 13 71
6-Нитробензимидазол 16 25 40
В процессе экспонирования микрокристалла галогенида серебра происходит увеличение центра светочувствительности и образование, как правило, на поверхности кристалла центра скрытого изображения из металлического серебра, который как бы разрывает двойной электрический слой в определенных местах на поверхности микрокристалла (см. рис. 5.3.6), куда беспрепятственно подходят в процессе проявления отрицательно заряженные ионы проявляющего вещества, восстанавливая микрокристалл галогенида серебра. В процессе проявления наблюдается разрушение двойного электрического слоя, т. к. восстановление кристалла, согласно данным Т. Джеймса, протекает в пределах толщины двойного электрического слоя или в его непосредственной близости.
Рис. 5.3.6. Схематическое изображение двойного отрицательного электрического слоя вокруг неэкспонированного (а) и экспонированного (б) микрокристалла бромида серебра
Таким образом, наличие центра скрытого изображения на микрокристалле галогенида серебра обусловливает снижение энергетического барьера на пути электронных переходов и понижение энергии активации проявления, что и повышает избирательность процесса проявления. Энергия активации проявления скрытого изображения равна -40 кДж/моль, причем она гораздо меньше, чем энергия активации проявления вуали, составляющая -80-85 кДж/моль. Добавление бромида калия в проявляющий раствор приводит к дополнительной адсорбции избыточных ионов брома на поверхности неэкспонированных микрокристаллов и способствует повышению избирательности процесса проявления за счет существенного снижения скорости образования вуали.
5.3.1.5. Специальные добавки и их роль в проявителе
Кроме проявляющего вещества (одного или нескольких), щелочи, сульфита натрия, антивуалента проявляющий раствор содержит водоумягчающее вещество, предназначенное для предотвращения образования известковых соединений (осадков), которые могут возникать в случае применения воды повышенной жесткости. Для этих целей в фотографии чаще всего применяют гексаметафосфат натрия (М-19) , динатриевую соль этилендиаминтетрауксусной кислоты (трилон Б) в концентрации 1-2 г/л. Эти вещества связывают ионы кальция и магния в растворимые устойчивые комплексные соединения, например Na2[Ca(PO3)6], и пре
Энергия активации — это дополнительная энергия, которую надо сообщить молекулам для перевода их в активное состояние. Аррениус предложил уравнение, характеризующее скорость протекания реакции, из которого можно вы-Е
числить энергию активации: v = Kze RT , где К — константа; z — число столкновений реагирующих частиц; R — газовая постоянная; Т— абсолютная температура; Е — энергия активации (кДж/моль).
**При высокотемпературной обработке вещество имеет склонность к гидролизу.
Химия фотографических процессов
861
пятствуют тем самым образованию нерастворимых осадков — кальциевых солей (СаСО3, Сах(ОН)Л(8О3)2), которые в отсутствие ингибиторов отложения солей жесткости оседают на эмульсионном слое фотоматериала и приводят к дефекту — так называемой кальциевой сетке. Кроме того, в присутствии ингибиторов в проявляющем растворе происходит связывание в устойчивые растворимые соединения ионов меди и других ионов тяжелых металлов, которые катализируют окисление цветного проявляющего вещества. Необходимо иметь в виду и то обстоятельство, что увеличение содержания этилендиаминтетрауксусной кислоты, или трилона Б, в проявителе может привести к понижению pH и замедлению процесса проявления.
Ряд зарубежных фирм в качестве эффективного ингибитора отложения солей жесткости применяют вещество, называемое калгон, представляющее собой смесь гексаметафосфата натрия (NaPO3)6 и пирофосфата натрия Na4P2O7.
В цветных проявляющих растворах предпочтение отдают гексаметафосфату калия, т. к. использование этилендиаминтетрауксусной кислоты или ее солей оказывает вредное воздействие на гидроксиламин, который разлагается в их присутствии с образованием N2 и NH3. Гидроксиламин теряет при этом роль вещества, защищающего производные п-фенилендиамлта. от окисления кислородом воды и воздуха, что в конечном счете приводит к нестабильной работе проявляющего раствора Кроме того, в литературе имеются указания, что этилен-диаминтетрауксусная кислота или ее соли образуют с катионами Fe3+, Cr3, Си2+ комплексные соединения, которые в значительной степени катализируют реакцию аутоокисления цветного проявляющего вещества.
В качестве ингибитора солеотложения в процессе обработки вместо трилона Б и М-19 совсем недавно было предложено использовать оксиэтилендифосфоновую кислоту (О=Р(ОН)2—С(ОН) — СН3—Р(ОН)2=О). Она полностью предотвращает солеобразование в цветном проявителе за счет возникновения на поверхности потенциальных зародышей из микрокристаллов карбонатов кальция малорастворимой адсорбционной пленки, которая препятствует росту зародышей солеотложения и их агломерации.
Применение в цветном проявителе оксиэтилендифосфоновой кислоты, которая является еще и консервантом, в концентрациях 10-20 мг/л вместо динатрие-вой соли этилендиаминтетрауксусной кислоты значительно понижает окисление цветного проявляющего вещества (более чем в 10 раз) и предотвращает разложение гидроксиламина, что в конечном счете существенно повышает стабильность цветного проявляющего раствора.
В последние годы в фотографии прослеживается четкая тенденция к использованию высококонцентрированных жидких проявляющих растворов (микрофильмирование, микроэлектроника, полиграфия и т. д.), которые обладают хорошей сохраняемостью в течение длительного периода времени (более 1 года). Для этих
целей в проявляющий раствор вводят органические растворители, являющиеся гораздо лучшими растворителями для компонент проявителя, чем вода, и, с другой стороны, они легко смешиваются с водой в любых соотношениях. К таким веществам необходимо отнести: диэтаноламин, триэтаноламин, эфиры этиленгликолей, которые, являясь прекрасными растворителями, одновременно выполняют роль антиоксидантов, обеспечивая довольно высокую сохраняемость жидких концентрированных проявляющих растворов.
В связи с интенсификацией процессов химикофотографической обработки сегодня особое внимание специалисты уделяют применению различного рода активаторов, которые вводят в эмульсионный слой не только при изготовлении фотоматериала, но и в процессе его обработки. В литературе сообщается о применении в качестве ускорителей проявления феносафранина, пинакриптола зеленого, мочевины, гидразина, аргинина и др. Большинство ускорителей проявления, адсорбируясь на поверхности бромида серебра, снижают большой отрицательный поверхностный заряд микрокристалла за счет десорбции избыточных ионов брома, что ускоряет диффузию в большинстве случаев отрицательно заряженных ионов проявляющего вещества.
Особый интерес в качестве ускорителей процесса проявления вызывают полиэтиленоксиды (полиэтиленгликоли) общей формулы НО(СН2—СН2—О)„Н, которые добавляют в эмульсию при поливе или вводят в проявляющий раствор в концентрации от 1,0 до 10 г/л. Наибольшее ускоряющее действие наблюдается для полиэти-леноксидов с молекулярной массой 1550-2000, причем только при наличии ионов иода в кристаллической решетке галогенида серебра или в проявляющем растворе.
Механизм ускоряющего действия проявления поли-этиленоксидами еще не совсем ясен. Некоторые исследователи считают, что полиэтиленоксид, проникая в эмульсионный слой, снижает отрицательный заряд соответствующих участков микрокристалла галогенида серебра, облегчая тем самым доступ к ним отрицательно заряженных ионов гидрохинона
Существуют и другие точки зрения. Согласно некоторым из них, полиэтиленоксид вытесняет желатин с поверхности микрокристалла галогенида серебра, в кристаллической решетке которого присутствуют ионы иода. Адсорбируясь на поверхности микрокристалла галогенида серебра, желатин замедляет процесс восстановления кристалла за счет того, что в щелочном проявляющем растворе он, являясь амфолитом, заряжается отрицательно и значительно повышает величину уже существующего отрицательного барьера вокруг микрокристалла, возникающего за счет адсорбции на поверхности избыточных ионов брома. Вытеснение желатина с поверхности микрокристалла приводит к снижению величины отрицательного заряда и исключает торможение процесса проявления галогенида серебра, обусловленное наличием желатина на поверхности микрокристалла.
862
Новый справочник химика и технолога
В некоторых случаях в проявитель добавляют и другие вещества, например смачиватели (поверхностно-активные вещества), обеспечивающие равномерность проявления эмульсионного слоя, особенно при быстрой обработке фотоматериалов. При обработке черно-белых и цветных кинофотоматериалов по методу обращения для более полного проявления эмульсионного слоя в первый, черно-белый проявитель вводят растворители галогенида серебра (тиоцианат калия, тиосульфат натрия и др.) в концентрации 1-10 г/л. При цветном проявлении в качестве антиоксиданта применяют совместно с сульфитом натрия гидроксиламин, концентрация которого в проявителе обычно не превышает 1,2 г/л.
5.3.1.6. Разновидности проявляющих растворов
Для химико-фотографической обработки экспонированных фотоматериалов широкое распространение получили различные виды проявляющих растворов: однорастворные, двухрастворные, концентрированные, таблеточные и пастовые, или вязкие. При составлении однорастворных проявителей обычно все компоненты растворяют в одном растворе в определенной последовательности. Вначале растворяют 1/5-1/6 часть сульфита натрия, вторым — проявляющее вещество, затем остаток сульфита натрия, далее щелочь и антивуалент. Такие проявляющие растворы имеют ограниченный срок хранения и использования (3^4 недели).
Для увеличения срока хранения проявителей применяют двухрастворные проявители. В одном растворе растворяют сульфит натрия и проявляющие вещества, а в другом — щелочь и антивуалент. Такие проявители хранят отдельно несколько месяцев в закрытом сосуде, а перед обработкой фотоматериала смешивают одинаковые объемы первого и второго растворов. Концентрации компонент проявителя при составлении исходных растворов необходимо в этом случае увеличивать в 2 раза, так при смешении происходит разбавление раствора в 2 раза. Применение двухрастворных проявителей позволяет получать всегда хорошие и постоянные результаты. Иногда обработку экспонированного фотоматериала ведут в двух растворах: сначала в растворе проявляющих веществ, а затем в растворе щелочи.
Большой популярностью не только у фотолюбителей, но и у профессионалов заслуженно пользуются концентрированные проявляющие растворы, в которых концентрация компонент в 10-15 раз выше, чем у обычных проявителей. Это существенно повышает их устойчивость к окислению кислородом и позволяет увеличить срок хранения (более чем 1 год). Для повышения растворимости компонент проявителя применяют органические растворители, которые, как правило, выполняют дополнительно функцию антиоксидантов и хорошо смешиваются при разбавлении водой в любых соотношениях.
Иногда фотолюбители отдают предпочтение таблеточным проявителям, которые содержат все компо
ненты в одной прессованной таблетке. Для более быстрого растворения ее в воде вводят дополнительно специальные вещества, нс оказывающие влияния на результаты процесса проявления.
В некоторых областях науки и техники для обработки фотоматериалов применяют пастовые проявители, которые кроме основных компонент содержат полимеры, например поливиниловый спирт или карбоксиметил-целлюлозу, обеспечивающие высокую вязкость проявляющего раствора. С помощью специальных устройств такой проявитель наносят тонким слоем (30-60 мкм) со стороны эмульсионного слоя фотоматериала, а затем (после завершения процесса проявления) смывают сильной струей воды или другими приемами. Этот вид проявления обеспечивает высокое постоянство результатов процесса обработки и малый (дозированный) расход химикатов.
В зависимости от характера работы проявителя и его назначения различают: выравнивающее, мелкозернистое, контрастное, быстрое проявление. Бурное развитие малоформатной фотографии привело к разработке выравнивающих и мелкозернистых проявляющих растворов. Отличительная особенность выравнивающих проявителей состоит в том, что они обладают низкой кислотно-основной или окислительно-восстановительной буферностью и быстро истощаются. Это достигается за счет использования гидроксида калия или натрия, а также путем значительного понижения концентрации проявляющих веществ в проявляющем растворе. В участках эмульсионного слоя, получивших большие уровни экспозиций в результате выделения в процессе проявления бромистоводородной кислоты (реакция (5.3.25)), происходит резкое понижение pH внутри слоя, что приводит к замедлению процесса проявления и понижению максимальной оптической плотности. Малоэкспонированные участки слоя при этом проявляются нормально. Такая кинетика проявления эмульсионного слоя в зависимости от экспозиции исключает перепроявление и приводит к хорошей проработке деталей в светах (темные участки на негативе), увеличивает фотографическую широту и снижает контраст негатива при съемке объекта с большим интервалом яркостей, обеспечивая при этом высокую светочувствительность.
Примером выравнивающего проявления может служить проявитель, разработанный С. Богдановым, состав и количественное содержание которого представлено ниже.
Фенидон, г 0,05
Гидрохинон, г 0,2
Сульфит натрия (безводный), г 100
Гидроксид натрия, г 0,66
Бромид калия, г 2,5
Вода, л, до 1,0
* Выравнивающие проявители как бы выравнивают скорости проявления участков фотоматериала, получивших различные уровни освещенности.
Химия фотографических процессов
863
Продолжительность проявления 18-25 мин при Т = 20 °C.
Выравнивающее действие данного проявляющего раствора обусловлено довольно низким значением кислотно-основной и окислительно-восстановительной буферности за счет того, что концентрации основных компонент (проявляющих веществ и щелочи) в 15-20 раз меньше, чем в обычных проявителях. Важным условием выравнивающего проявления является также применение проявляющих веществ (метола, фенидона), обладающих малым индукционным периодом проявления. Это приводит к тому, что малоэкспониро-ванные участки эмульсионного слоя начинают проявляться гораздо раньше и более полно, чем обычно, что обеспечивает повышение светочувствительности.
Мелкозернистые проявители, как правило, содержат большое количество сульфита натрия (до 125 г/л), который способствует подрастворению микрокристаллов галогенида серебра и уменьшению их размеров. Металлическое серебро изображения в этом случае за счет восстановления ионов серебра, перешедших в раствор при растворении галогенида серебра сульфитом, имеет более компактную форму. Как правило, мелкозернистые проявители являются одновременно и выравнивающими проявителями, т. е. работают медленно и проявляют до низких значений коэффициента контрастности, что в значительной степени обусловливает понижение зернистости, т. к. последняя растет с увеличением коэффициента контрастности и величины оптической плотности почернения.
Хорошие результаты можно получить в так называемых простых мелкозернистых проявителях, которые не содержат щелочи, а в качестве проявляющих веществ в них применяются производные п-фенилен-диамина или вещества, относящиеся к классу НО(—С=С)„—NH2.
При высокой концентрации сульфита натрия подобные проявители, например с п-фенилендиамином, дают очень мелкозернистое изображение (за счет проявления, близкого к физическому). При этом восстановленное серебро обладает высокой кроющей способностью , т. е. в негативе обеспечивает высокую копировальную плотность при печати на фотографическую бумагу.
Особое место в фотографии отводится контрастным, сверхконтрастным или инфекционным проявителям.
Контрастные проявители, как правило, содержат едкую щелочь, а в качестве проявляющего вещества применяется гидрохинон, обладающий большим индукционным периодом проявления. Иногда для повышения активности проявителя вводят небольшие коли-
*Кроющая способность (К) характеризует полезность использования серебра в фотослое и представляет собой
D 2
К =-----, где CAg — масса серебра, г/м .
CAg
чества фенидона и метола. При контрастном проявлении сильно экспонированные участки эмульсионного слоя проявляются с гораздо большей скоростью, чем мало экспонированные, что, в конечном счете, приводит к увеличению разности максимальной и минимальной плотностей на негативе. В качестве антивуалирующих веществ чаще всего рекомендуют бензотриазол и другие органические антивуаленты.
Сверхконтрастные проявители по сравнению с контрастным проявителем содержат мало сульфита натрия (1-2 г/л). Это обстоятельство приводит к тому, что хинон в процессе проявления почти не связывается сульфитом натрия, а, взаимодействуя с дианионом гидрохинона, образует и-бензосемихинон (ссмихинон), который является по сравнению с гидрохиноном очень активным восстановителем. В сильноэкспонированных участках слоя его концентрация очень высока, что приводит к возникновению в этих местах фотослоя большой оптической плотности (более 4,0) и значительному увеличению контраста. Данный тип проявления, называемый ЛИТ-проявлением, широко используют в репродукционной фотографии. Более подробно этот вопрос рассмотрен в подразделе 5.5.
Особой проблемой в фотографии является получение изображения за очень короткое время. Такой вид проявления называется быстрым или скоростным. Быстрые, или скоростные, проявители имеют очень короткий индукционный период проявления (0,2-0,4 с) за счет использования активаторов и нейтральных солей, понижающих отрицательный потенциальный барьер вокруг микрокристалла галогенида серебра. Для повышения скорости набухания эмульсионного слоя применяют едкие щелочи (гидроксид калия или натрия). Концентрацию проявляющих веществ в скоростных проявляющих растворах увеличивают в 5-10 раз по сравнению с обычными проявителями. Для уменьшения плотности вуали при быстрой (скоростной) обработке, которую проводят, как правило, при температуре 30-60 °C, применяют органические антивуалирующие вещества в довольно высокой концентрации. С основными принципами ускорения процесса проявления и рецептурой обрабатывающих растворов рассмотрены в подразделе 5.5.
Основные реакции при проявлении и явление су пер аддитивности
При восстановлении бромида серебра гидрохиноном имеют место три стадии:
1) диссоциация гидрохинона:
гидрохинон дианиом гидрохинона
864
Новый справочник химика и технолога
2) окисление дианиона гидрохинона на центре проявления:
ион семихинона хинон
(5.3.32)
ЛИТ-проявления, как установил И. Блюмберг, молекулярный выход серебра по гидрохинону, с уменьшением концентрации сульфита натрия, при высоком значении pH проявителя (бессульфатное проявление) возрастает до 9,0 за счет образования в отсутствие сульфита натрия гидроксигидрохинона, который обладает значительным вуалирующим действием.
При проявлении метолом в присутствии сульфита натрия образуется моносульфонат метола, который способен восстанавливать бромид серебра самостоятельно:
3) восстановление ионов серебра:
ОН +2ASBr+Na2SO3 --------►
2Ag*+2е” —> 2Ag (5.3.33)
Суммарное уравнение процесса проявления в этом случае можно записать так:
ОН
SOgNa 2Ад + ♦NaBr+HBr
NHCH3 ионосульфояат метола
(5.3.34)
В присутствии сульфита натрия в проявителе хинон реагирует с сульфитом, образуя моносульфонат гидрохинона, который восстанавливает экспонированный галогенид серебра, превращаясь в дисульфонат гидрохинона, практически не обладающий проявляющей способностью:
ОН
+2Na1SO<i+H1O^K)l +NaOH 4 4 4
SO з N a OH
(5.3.35)
моиосульфокат гидрохинона
OH
+2AgBr+Na28O3 —*• 2Ag + iCxl *Na8r*H8r
SO,Na
OH дисульфонат гидрохинона
(5.3.36)
Таким образом, одна молекула гидрохинона в присутствии сульфита натрия восстанавливает четыре молекулы бромида серебра, т. е. молекулярный выход серебра по гидрохинону равен ~4. В случае же
* Молекулярный выход серебра в процессе проявления характеризуется числом молекул бромида серебра, восстановленных одной молекулой проявляющего вещества.
(5.3.37)
Большинство проявляющих растворов содержит, как правило, два проявляющих вещества, чаще всего метол и гидрохинон или фенидон с гидрохиноном. Некоторые авторы в специальных случаях рекомендуют применять в проявителе совместно три проявляющих вещества: фенидон, метол и гидрохинон. Наиболее эффективными проявляющими растворами на практике являются метол-гидрохиноновые и фенидон-гидрохиноновые, которые обнаруживают так называемый супераддитивный эффект. Под супераддитивностью понимают способность проявляющего вещества, например фенидона и метола, в сочетании с другим проявляющим веществом (гидрохиноном) значительно увеличивать скорость проявления при определенных соотношениях их концентраций в проявителе. При супераддитивном эффекте общая скорость процесса как при химическом, так и физическом проявлении для смеси двух проявляющих веществ гораздо больше арифметической суммы частных скоростей каждого из проявляющих веществ, взятых отдельно (рис. 5.3.7).
При проявлении фенидоном в щелочной среде происходит вначале диссоциация фенидона с отщеплением иона Н+ от иминогруппы, затем образование равновесной таутомерией лактам-лактимной системы:
моленуяа анкон
фенидона (А) фенидона (В|
(5.3.38)
При этом ион фенидона обладает почти такой же активностью, как и недиссоциированная молекула фенидона. Ион фенидона легко отдает электрон при окисле-
Химия фотографических процессов
865
нии и образует положительный радикал (D) оранжевокрасного цвета:
радинал фенидона (О)
ион фенидона
При проявлении фенидоном продукты окисления фенидона не взаимодействуют с сульфитом натрия и накапливаются в проявителе, замедляя процесс восстановления галогенида серебра.
При добавлении гидрохинона оранжево-красная окраска раствора фенидона постепенно исчезает за счет восстановления положительного радикала фенидона (D) ионом гидрохинона и образования иона фенидона, т. е. реакция (5.3.39) протекает справа налево.
Е. Кляйн с сотрудниками предложил схему, которая характеризует возможные пути протекания реакций при окислении фенидона в супсраддитивной смеси с гидрохиноном (реакция (5.3.40)).
Как считают многие исследователи, окисление фенидона в проявляющем растворе с высоким значением pH, вероятнее всего, протекает по схеме I, в то время как схема III является определяющей при супераддитивном действии смеси фенидон-гидрохинон (реакция (5.3.40)).
Что касается механизма супераддитивного действия смеси проявляющих веществ (метол-гидрохинон, фенидон-гидрохинон и т. д.), то в первую очередь необходимо рассмотреть регенерационный механизм. Так,
например, при проявлении одним фенидоном наблюдаются образование радикала фенидона (реакция (5.3.39)) и замедление процесса проявления. При проявлении смесью фенидона и гидрохинона скорость процесса проявления резко возрастает (см. рис. 5.3.7) за счет того, что радикал фенидона тотчас же восстанавливается гидрохиноном в ион фенидона, который в свою очередь снова принимает участие в процессе проявления. Регенерация фенидона происходит только в присутствии гидрохинона и сульфита натрия, в то время как в отсутствие сульфита не может образоваться снова 1-фенил-З-пиразолидон, а образуется 1-фенил-З-гидроксипиразол.
(5.3.40)
V пр
1,6 7
% В 100
% В 100
Рис. 5.3.7. Влияние соотношения гидрохинона (А) и фенидона (В) в проявляющем растворе при общей их концентрации 0,01 моль/л на скорость химического (а) и физического (б) проявления: 1 — правило аддитивности скоростей (расчетные данные); 2 — эффект суперадцитивности; v — скорость проявления (экспериментальные данные Т. Джеймса)
866
Новый справочник химика и технолога
Существует и другая точка зрения в отношении механизма супераддитивности, согласно которой снижение величины отрицательного зарядного барьера вокруг микрокристалла (см. рис. 5.3.6), обусловленное образованием положительно заряженных продуктов окисления метола и фенидона, приводит к повышению адсорбции проявляющего вещества. Адсорбируясь на центре проявления или микрокристалле галогенида серебра, продукты окисления фенидона облегчают адсорбцию гидрохинона и служат как бы химическим мостиком, по которому передаются электроны от гидрохинона к центру проявления; при этом снижается индукционный период проявления и существенно активируется процесс восстановления галогенида серебра гидрохиноном. Концентрация фенидона в проявляющем растворе при супераддитивном действии остается почти неизменной.Считают, что при фотографическом проявлении наиболее вероятны оба механизма, объясняющие явление супераддитивности, т. е. регенерационный механизм: концепция снижения зарядного барьера и повышения адсорбции проявляющих веществ, хотя существуют и другие точки зрения по этому вопросу. Так, В. И. Шеберстов объясняет явление супераддитивности образованием комплекса с переносом заряда между окисленной формой фенидона и активной формой гидрохинона. При этом отмечается, что в некоторых случаях присутствие сульфита натрия является важным условием супераддитивности. Это объясняется тем, что в отсутствие сульфит-ионов первичный продукт окисления гидрохинона — семихинон (Q*), — будучи очень активным, окисляет фенидон, адсорбированный на центре проявления, и мешает его проявляющей способности. Супераддитивный эффект в этом случае возможен только при наличии сульфит-ионов, которые связывают семихинон.
Согласно гипотезе В.И. Шеберстова, фенидон (Фадс), адсорбируясь на центре проявления, передает электрон и окисляется до катион-радикала (Ф'+):
Ф + Ag+ —> Ф*+ + Ag аде с? ' аде о
Сульфит-ионы не восстанавливают окисленную форму фенидона, поэтому катион-радикал фенидона остается в адсорбированном состоянии на центре проявления и препятствует адсорбции новых порций фенидона. Анионы гидрохинона (Red ) в свою очередь образуют с катион-радикалом фенидона комплекс с переносом заряда (ORed ), который на центре проявления распадается с регенерацией фенидона (Ф) и образованием окисленной формы гидрохинона (Ох); это может быть и радикал семихинона Q»:
ФХ + Red- <=± ф+Red- —> Фялр + Ох
Регенерированный фенидон принимает участие в восстановлении серебра микрокристалла:
Ф + Ag+ —> Ф’+ + Ag аде Ь аде о
Комплекс с переносом заряда может образовываться и в растворе, где имеются нейтральные молекулы фенидона (Ф) и гидрохинона (Red):
Ф + Red ФRed <=> Ф+ Red-
Он распадается на поверхности центра проявления с образованием адсорбированного фенидона, который восстанавливает далее ионы серебра.
При эффекте супераддитивности решающее значение имеют следующие реакции:
Ф + Ag Br-->Ф’Л + Ag + Br-аде о аде о
°X+Red’ «=*Фадс+Ох
Ox + SOj- —> RedSO-
Введение в проявляющий раствор антивуалентов приводит к увеличению супераддитивного эффекта фенидон-гидрохиноновых смесей. Введение ионов брома в проявитель изменяет поверхностный потенциал и затрудняет подход ионов гидрохинона за счет создания отрицательного барьера. В случае фенидонгидрохинонового проявляющего раствора фенидон свободнее подходит к поверхности центра проявления и, адсорбируясь на нем, захватывает при этом гидрохинон. Кроме того, В.И. Шеберстов особое внимание обращает на тот факт, что совместная адсорбция смеси фенидон-гидрохинон гораздо больше, чем адсорбция этих веществ порознь.
5.3.1.7 Физическое и химическое проявление
В фотографической практике имеют место случаи, когда экспонированный фотоматериал вначале помещают в фиксирующий раствор, а после завершения процесса фиксирования и промежуточной промывки дальнейшую обработку проводят на свету в проявителе, содержащем восстановитель и растворимую соль серебра (AgNO3) в довольно высокой концентрации. В процессе проявления компоненты проявляющего раствора проникают в эмульсионный слой фотоматериала и оба партнера реакции — подвижный ион серебра Ag+ и молекула или ион проявляющего вещества (R(©)) — со всех сторон диффундируют из раствора к серебряному центру скрытого изображения, возникшему при экспонировании микрокристалла. Ионы серебра избирательно восстанавливаются на центрах скрытого изображения, которые остались в желатиновом слое фотоматериала нетронутыми в процессе фиксирования.
Металлическое серебро, восстановленное на центрах проявления, в этом случае имеет компактную сферическую форму. Такой вид проявления называют физическим (рис. 5.3.8 и 5.3.9). Свое название оно получило еще на раннем этапе развития фотографии, т. к. в то время считалось, что при данном типе прояв
Химия фотографических процессов
867
ления существенную роль играют физические процессы кристаллизации восстановленного серебра.
Различают несколько разновидностей физического проявления. Одна из них — физическое проявление с предварительным фиксированием. В этом случае экспонированный фотоматериал фиксируют не в кислом, а в щелочном, или нейтральном, фиксирующем растворе , т. к. кислый фиксаж оказывает растворяющее действие на центры скрытого изображения и может привести к их полному исчезновению. Поскольку проявляющие растворы для физического проявления содержат обычно не только проявляющее вещество (метол, глицин), кислоту (лимонная, серная), но и растворимую соль серебра (азотнокислое серебро), то их приготавливают не в щелочной , а в кислой среде непосредственно перед использованием. Но, несмотря на это, через несколько минут после приготовления может наступить спонтанное восстановление ионов серебра в растворе даже в отсутствие зародыша восстановления. Стабильность физических проявителей можно существенно повысить (например, добавлением в раствор желатина или 1-фснил-5-меркапто-тетразола в очень малой концентрации). Физическое проявление с предварительным фиксированием нашло применение для обработки ядерных слоев.
Другой вид физического проявления называют физическим проявлением до фиксирования. В этом случае серебряное изображение в слое образуется не только за счет прямого восстановления экспонированных микрокристаллов галогенида серебра, но и восстановления серебряных комплексных ионов. Комплексы серебра образуются в процессе проявления в результате частичного подрастворения галогенида серебра в слое не только сульфитом натрия, концентрация которого довольно велика, но и тиоцианатом калия, бромидом калия, тиосульфатом натрия и другими комплексообразо-вателями, являющимися составной частью проявляющих растворов (мелкозернистое проявление, проявляю-щефиксирующие растворы и т. д.). Проявление, при котором часть микрокристаллов галогенида серебра в эмульсионном слое растворяется, а ионы серебра, перешедшие в жидкую фазу, восстанавливаются на центре проявления, иногда называют физическим проявлением через раствор.
’Щелочной фиксирующий раствор для физического проявления: тиосульфат натрия — 300 г; гидроксид натрия — 6 г; вода — до 1 л (pH = 10,0).
’’физический проявитель: и-оксифенилглицин (глицин) — 1,67-3,34 г; азотнокислое серебро — 9,8 г; серная кислота (конц.) — 24,5 мл; 1-фенил-5-меркаптотетразол — 2,67 • 10“3 г; желатин — 0,5 %; вода — до 1 л. (Раствор А: параоксифенил-глицин, серная кислота. Раствор Б: азотнокислое серебро, желатин, 1-фенил-5-меркаптотетразол. Раствор Б вливают в раствор А при легком перемешивании.)
В щелочной среде азотнокислое серебро образует оксид серебра, который выпадает в осадок:
2AgNO3 + 2NaOH = Ag2c4 + 2NaNO3 + H2O
При полном отсутствии растворителей галогенида серебра в проявляющем растворе ионы серебра при проявлении поставляются к центру скрытого изображения непосредственно из твердой фазы микрокристалла галогенида серебра по поверхности или через его объем и восстанавливаются на границе раздела фаз серебро— галогенид серебра. Такой вид проявления, в результате которого происходит химическое взаимодействие с микрокристаллом галогенида серебра, называют прямым или химическим проявлением (см. рис. 5.3.8 и 5.3.9); при этом форма восстановленного серебра нитевидная.
При использовании проявляющих растворов, содержащих проявляющее вещество, сульфит натрия, щелочь, бромида калия, наряду с химическим проявлением протекает и физическое проявление через раствор, причем доля физического проявления в каждом конкретном случае может быть различной; она определяется составом проявителя. При этом за счет осаждения серебра из раствора происходит утолщение серебряных нитей, возникающих в процессе химического проявления. Вклад физического проявления в конечное изображение оценивается кроющей способностью серебра (чем она ниже, тем больше доля физического проявления).
Рис. 5.3.8. Схема и последовательность стадий процесса химико-фотографической обработки фотоматериала при физическом (/) и химическом (2) проявлении
а Экспонирование
в Фиксирование
Рис. 5.3.9. Электронные микрофотографии металлического серебра, восстановленного при физическом (а) и химическом (б) проявлении (по Е. Кляйну)
868
Новый справочник химика и технолога
5.3.1.8. Теория фотографического проявления
В основе фотографического проявления, открытого В.Ф. Тальботом, своеобразного способа химического усиления скрытого изображения (в 1О10 раз), возникающего при действии света на микрокристалл галогенида серебра, лежит окислительно-восстановительная реакция, в результате которой происходит восстановление ионов серебра до металлического серебра:
Ag+ +Red<=> Ag°+Ox (5.3.41)
где Red — исходная, а Ox — окисленная формы проявляющего вещества.
Возникает вопрос: почему микрокристаллы галогенида серебра, имеющие одинаковые свойства после химического созревания в случае их экспонирования, по-разному ведут себя в проявляющем растворе по сравнению с неэкспонированными? Почему проявитель восстанавливает только экспонированные микрокристаллы галогенида серебра, в то время как неэкспонированные микрокристаллы не восстанавливаются? На этот и другие вопросы многие ученые, работающие в области фотографии со времен В.Ф. Тальбота, долго не находили ответа.
Первая попытка создать теорию фотографического проявления принадлежит нашему соотечественнику — ассистенту Петербургского университета В. В. Лерман-тову, который высказал идею по поводу электрохимического механизма процесса проявления, рассматривая его как локальную гальваническую пару, образованную серебряной частицей, растворенной солью серебра, и проявителем. Эта гениальная идея заняла свое прочное место в фотографии только лишь благодаря работам советских ученых Г.П. Фаермана, С.И. Чербова, В.А. Вейденбаха, Н.Н. Шишкиной, С.Г. Богданова и других, а также зарубежных исследователей В. Енике, Р. Ма-теека, Р. Майера. Это можно объяснить тем, что в то время еще не были разработаны и сформулированы теория гальванических элементов, теория электролитической диссоциации, теория концентрационных и окислительных потенциалов и явлений перенапряжения. Кроме того, против признания идеи В.В. Лермантова выступал тогда и высокий научный авторитет — немецкий химик Вильгельм Оствальд, сформулировавший довольно наглядную и простую теорию проявления, которая получила название теории пересыщения. Суть ее заключалась в том, что реакция проявления рассматривалась как осаждение серебра из растворенной фазы, пересыщенной серебром. Согласно этой теории, серебряный зародыш не участвует в химической реакции проявления, а его действие сводится к чисто физическому влиянию на ход процесса проявления. Данная теория была несовершенна, т. к. не могла объяснить различия в селективности некоторых проявляющих веществ и неодинаковые значения температурных коэффициентов проявления вуали и изобра
жения, а также нитевидную структуру восстановленного серебра.
На смену теории пересыщения В. Оствальда пришла новая, каталитическая теория проявления, разработанная Максом Фольмером. Согласно этой теории, серебряный центр скрытого изображения в процессе проявления является частицей гетерогенного катализатора, который, участвуя в химической реакции проявления, ускоряет окисление проявляющего вещества, способствуя тем самым увеличению скорости процесса. Несмотря на то, что относительно механизма каталитического действия центров скрытого изображения не было высказано никаких предположений, все же эта концепция имела большое значение для теории фотографического проявления.
Дальнейшим совершенствованием каталитической теории фотографического проявления явилась теория, предложенная А.И. Рабиновичем, которая ставила на первый план процессы адсорбции. Адсорбционная теория проявления предполагала, что адсорбция проявляющего вещества на каталитическом серебряном центре скрытого изображения приводит к локальному повышению его концентрации по сравнению с проявляющим раствором, что и способствует резкому возрастанию скорости восстановления экспонированных микрокристаллов по сравнению с неэкспонированными. Кроме того, предполагалось, что адсорбированный на каталитическом центре ион серебра существует в форме Ag2+, который обладает более высокими реакционными возможностями, чем ион серебра в кристалле или растворе. Однако вскоре адсорбционная теория проявления была поставлена под сомнение, т. к. рядом известных ученых было экспериментально подтверждено, что на металлическом серебре не может наблюдаться адсорбция проявляющих веществ, в частности гидрохинона.
Несмотря на это, все же адсорбционный механизм процесса проявления некоторыми учеными поддерживается и до сих пор (например, Т. Джеймсом, который считает, что на центрах скрытого изображения происходит адсорбция только ионов серебра, проявляющее вещество при этом адсорбируется на поверхности галогенида серебра или границе раздела трех фаз Ag— AgHal—проявляющий раствор, передача электрона в этом случае происходит не через каталитический центр проявления, а непосредственно от проявляющего вещества к иону серебра).
Следующим этапом в обосновании механизма фотографического проявления явилось создание теории поверхностных зарядов. По этой теории, неэкспонированный микрокристалл галогенида серебра не проявляется, потому что он несет на себе значительный отрицательный поверхностный заряд (см. рис. 5.3.6), который препятствует контакту проявляющего вещества, последующей передаче электрона центру проявления и восстановлению микрокристалла. Теория поверхностных зарядов также не нашла своего применения в качестве
Химия фотографических процессов
869
основного принципа, раскрывающего механизм процесса проявления проявляющими веществами, молекулярная, а не ионная форма которых восстанавливает галогенид серебра. Сегодня эта теория, правда, в несколько измененном виде, объясняет природу индукционного периода процесса проявления проявляющими веществами, имеющими различный знак и величину заряда иона.
Р. Герни и Н. Мотт предложили теорию, которая предусматривала, что после хемосорбции проявляющего вещества на центре проявления происходит отдача электрона серебряному зародышу, который заряжается при этом отрицательно. Серебряный центр в процессе проявления увеличивает свои размеры по механизму, подобно тому, который они предложили, объясняя рост центра светочувствительности до центров скрытого изображения при экспонировании галогенида серебра, т. е. в процессе проявления электрон поступает от проявляющего вещества, а ион серебра — из среды, окружающей серебряный зародыш. Согласно этой теории, гетерогенная граница трех фаз — галогенид сереб-ра/серебро/раствор — должна обладать очень сильным электрическим полем, которое должно обеспечивать транспортирование в процессе проявления иона галогенида с поверхности микрокристалла в растворенную фазу.
Теорией, наиболее полно объясняющей механизм и особенности процесса проявления, сегодня является электродная теория, которая рассматривает его с позиций электрохимии как процесс, имеющий черты обратимой реакции.
Фотографическое проявление, согласно электродной теории, представляет собой электрохимический процесс, действующей силой которого является величина электрохимической разности потенциалов ХЕ между окислительно-восстановительным потенциалом ЕКей1(Ук проявляющего вещества и потенциалом £Л </Ag проявляющего раствора при данных условиях (pH, pAg, температуре и т. д.). Для того чтобы начался процесс восстановления ионов серебра, окислительно-восстановительный потенциал ERcd/Ox проявляющего вещества для данного проявляющего раствора должен быть более отрицательным, чем Е^. ,Ag; разность потенциалов при этом должна превышать некоторую критическую величину (ХЕ = Е -ERed ^50-г 90 мВ), но быть не более 300 мВ, иначе в присутствии активных проявляющих веществ может произойти самопроизвольное восстановление ионов серебра.
Центр скрытого изображения (металлический зародыш) в процессе проявления, по электродной теории, действует так же, как электрохимический центр реакции: молекулы или ионы проявляющего вещества, окисляясь, отдают электроны серебряному центру проявления, а ионы серебра, получая электрон, восстанавливаются. Восстановление ионов серебра рассматривается как катодный процесс, а окисление проявляющего вещества — как анодный.
Механизм физического проявления. При физическом проявлении, когда проявляющее вещество мигрирует к центру проявления, на его поверхности могут иметь место следующие реакции, характеризующие анодный процесс физического проявления (окисление проявляющего вещества):
- хемосорбция проявляющего вещества на поверхности серебряного зародыша;
- передача электрона серебряному зародышу проявления от адсорбированного проявляющего вещества в процессе его окисления; десорбция окисленной формы проявляющего вещества с поверхности зародыша.
Одновременно на серебряном зародыше при физическом проявлении будут протекать также и реакции, характеризующие катодный процесс (восстановление ионов Ag+ из раствора), такие, как:
- адсорбция ионов серебра или серебряных комплексов на поверхности зародыша проявления;
- диссоциация серебряного комплекса в адсорбированном состоянии или в растворе непосредственно у поверхности зародыша с образованием ионов серебра и свободного комплексообразующего лиганда;
- восстановление и введение иона серебра в решетку зародыша проявления.
В связи с тем что в процессе физического проявления принимают участие только две фазы (раствор и серебро), а при химическом проявлении — три фазы (раствор, серебро, галогенид серебра), электродная модель для физического проявления получается гораздо проще. В этом случае катодный процесс физического проявления можно представить следующим образом.
Если серебряный зародыш сначала находится в среде, которая содержит только подвижные ионы серебра (может быть, даже в форме серебряных комплексов) и не содержит молекул проявляющего вещества, то серебряный центр проявления приобретает равновесный электрохимический потенциал £Л ./Л , который зависит только от концентрации свободных ионов серебра , находящихся в растворенной фазе, и определяет-
ся известным уравнением Нернста:
, И-----111 Vz + , 1 I
Ag /Ag Ag /Ag p Ag
где EAg Ag — стандартный потенциал для пары Ag+/Ag (+0,799 В); R — газовая постоянная (8,313 Дж/моль- град); Т — абсолютная температура, К; F — число Фарадея (96 500 кулон/г-экв).
В этом случае между серебряным зародышем и его окружением не существует никакой электрохимической разности потенциалов, т. е. не будет потока ионов серебра из раствора к серебряному центру проявления.
Ионы серебра начнут перемещаться к центру проявления, если будет приложен электрохимический потен
870
Новый справочник химика и технолога
циал Еп, более отрицательный, чем упомянутый потенциал ^Ag’ /Ag • увеличением разности потенциалов Е^, /Ag - Еп поток серебряных ионов i будет возрастать.
Для случая, когда центры скрытого изображения находятся в контакте с раствором, который содержит только Red/Ox-форму проявителя и не содержит Ag+-ионов, зародыш серебра приобретает электрохимический потенциал ^RedOx, определяемый уравнением Петерса:
^Red/Ox = ^ed/Ox + ~1п-^ (5.3.43)
nF [Red]
где £^ed/Ox — нормальный окислительно-восстановительный потенциал проявляющего вещества при [Ох] .
------ = 1; п — число электронов, участвующих в реак-[Red]
ции; [Ox], [Red] — активная концентрация окисленной и восстановленной форм проявляющего вещества.
Поток электронов ie к серебряному зародышу начинает перемещаться, как только к нему приложен электрохимический потенциал Е„; при этом протекание тока в этом случае соответствует анодному окислению молекул проявляющего вещества на поверхности центра проявления. Потенциал Е„ при данных условиях более положителен, чем потенциал FRed/Ox, причем сила электронного тока 1е возрастает в основном с ростом разности потенциалов Еп - Е^ао*.
Если же оба партнера реакции — подвижные ионы серебра и ионы проявляющего вещества — присутствуют в среде, окружающей частицу металлического серебра, то поток ионов серебра и электронный ток будут течь одновременно по направлению к серебряному зародышу. Сначала серебряный зародыш может иметь электрохимический потенциал, значительно отличающийся от потенциала Е*, соответствующего точке пересечения Р* катодной и анодной вольт-амперной характеристики (рис. 5.3.10). В этом случае избыток ионов Ag' и молекул проявляющего вещества R 0 будет перемещаться к серебряному центру, электрохимический потенциал которого будет сдвигаться в направлении точки Р*, соответствующей пересечению кривых. Как только потенциал серебряного зародыша достигнет значения Е*, наступит состояние, при котором поток ионов серебра Ag+ будет равен потоку электронов R©, т. е. сила катодного тока i . станет равной
силе анодного ie: i . = i= i .
Ag e
n •» dn
При этом сила тока i = е— в точке пересечения анодной и катодной вольт-амперной характеристик Р* соответствует скорости роста серебряного зародыша.
Из рис. 5.3.10 видно, что ток проявления z, который обусловливает увеличение серебряной частицы, существует только тогда, когда потенциал £Red/ox проявляющего раствора более отрицателен, чем потенциал Е . .
Ag /Ag
R(e)
Рис. 5.3.10. Комбинация анодных и катодных вольт-амперных кривых при физическом проявлении после фиксирования (по Р. Матееку)
Механизм химического проявления. Если в процессе проявления серебряный зародыш находится в контакте с микрокристаллом галогенида серебра, а проявляющий раствор не содержит растворенных серебряных ионов, то анодные и катодные процессы в этом случае проходят на разных границах фаз. Передача электрона от проявляющего вещества R 0 к серебряному центру скрытого изображения происходит на границе фаз серебро—раствор. Ионы серебра (дефекты в микрокристаллах, по Френкелю) мигрируют через кристалл галогенида серебра к центру проявления и восстанавливаются на границе AgBr/Ag (см. рис. 5.3.8). В этом случае ионы серебра поставляются непосредственно из кристаллической решетки микрокристалла галогенида серебра, а металлическое серебро как бы выталкивается из микрокристалла и имеет при этом форму тонких нитей.
Перемещение ионов серебра к центру проявления в случае бромида и иодида серебра осуществляется в основном только через микрокристалл, причем из тех участков, где находятся структурные дефекты в кристалле. Е. Кляйн показал, что при химическом проявлении в тех местах микрокристалла, откуда переместились ионы серебра в виде дефектов, по Френкелю, образуются углубления (кратеры) — «ямки травления». Это подтверждается микрофотографиями, полученными с помощью электронного микроскопа. Так, на одной из них (рис. 5.3.11) при химическом проявлении кристалла бромида серебра отчетливо видны серебряная нить и три отделенных друг от друга симметричных относительно центра углубления на поверхности микрокристалла. При химическом проявлении кубических микрокристаллов из хлорида серебра, как правило, возникают плоские частицы металлического серебра, а серебряные нити образуются в редких случаях: только при использовании специальных проявляющих растворов. Плоская форма восстановленного серебра обусловлена тем, что в случае
Химия фотографических процессов
871
применения хлорида серебра перемещение ионов серебра к центру проявления происходит главным образом по поверхности микрокристалла, а не через его объем, т. к. объемная электропроводность хлорида серебра гораздо меньше, чем объемная электропроводность микрокристаллов бромида и иодида серебра.
Ответ на вопрос, как же происходит перемещение ионов серебра к центру проявления: через микрокристалл галогенида серебра или по его поверхности, дали Е. Кляйн и Р. Матеск, используя для этих целей эксперименты с большим плоским микрокристаллом бромида серебра толщиной 5-10 мкм. На наружную поверхность плавающего на воде плоского микрокристалла (рис. 5.3.12) они помещали каплю проявляющего раствора, по составу соответствующего химическому проявителю. После завершения процесса проявления на поверхности микрокристалла со стороны, имеющей контакт с водой, как раз напротив того места, где была капля проявителя, были обнаружены с помощью микроскопа видимые углубления — «ямки травления». Этот эксперимент наглядно показал, что ионы серебра при химическом проявлении микрокристалла бромида серебра перемещаются не по поверхности микрокристалла, а через его объем. В том случае, когда микрокристалл не имел контакта с водой, травление поверхности с нижней противоположной стороны кристалла не наблюдалось. Е. Кляйн и Р. Матеек сделали предположение, что при отсутствии контакта микрокристалла с водой ион галогенида не может покинуть своего места в кристаллической решетке галогенида серебра, и избыточный отрицательный заряд, обусловленный этим, препятствует перемещению большого количества положительных ионов серебра из этих участков кристалла к центру проявления. Необходимо также отметить, что «ямки травления» наблюдаются в процессе фиксирования на поверхности микрокристалла со стороны, имеющей контакт с водой, если вместо проявителя на наружную поверхность микрокристалла поместить каплю фиксирующего раствора.
При химическом проявлении серебряный центр поделен на анодную поверхность, погруженную в проявляющий раствор, и катодную, имеющую непосредственный контакт с микрокристаллом галогенида серебра.
Анодный процесс в этом случае протекает по такому же механизму, как и при физическом проявлении. Центр проявления при восстановлении микрокристалла все время находится на его поверхности, а за счет диффузии проявляющих веществ к границе фаз серебропроявляющий раствор и последующего их окисления на центре происходит выделение электронов.
Механизм катодного процесса при химическом проявлении существенно отличается от катодного процесса физического проявления. В начале процесса химического проявления поток ионов серебра перемещается через микрокристалл галогенида серебра к поверхности контакта между серебряным центром проявления и микрокристаллом, на которой они восстанавливаются. С развитием процесса проявления во времени (удлинением серебряной нити) анодная поверхность раздела фаз серебро—раствор увеличивается намного быстрее, чем катодная поверхность ссребро/галогенид серебра; при этом происходит возрастание скорости проявления (рис. 5.3.13). При химическом проявлении серебряные нити выталкиваются из микрокристалла с постоянной скоростью, а в случае восстановления крупных микрокристаллов на поверхности наблюдаются кратеры — «ямки травления» рядом с проявляемыми участками микрокристалла.
б
> мкм
Рис. 5.3.11. Электронная микрофотография кристалла бромида серебра при химическом проявлении (по Е. Кляйну)
Рис. 5.3.12. Проявление модельного микрокристалла бромида серебра, плавающего на поверхности воды:
1 микрокристалл; 2 - капля проявителя (а); электронная микрофотография «ямок травления» (кратеров) на поверхности микрокристалла бромида серебра (случай А\ по Е. Кляйну) (б)
872
Новый справочник химика и технолога
Рис. 5.3.13. Комбинация анодных и катодных вольт-амперных кривых при химическом проявлении AgCl, AgBr, AgJ в гидрохиноновом проявителе (по Р. Матееку и Р. Майеру): I
/ — длина серебряной нити; г — радиус нити: — : 0(7); 10° (2); 3-10° Г
(ЗУ, 10' (V); 3-10'(5); 102 (6); 3-102 (7); 103 (8); ЗЮ3 (9); 104 (/0); 3-104 п I dn
(1 /). Ордината: — —-----ток, отнесенный к радиусу центра
г г dt
проявления (г)
Роль основных компонент проявителя в процессе проявления. На основании анализа развернутых выражений электродной теории и допуская, что увеличение разности потенциалов ЛЕ = Е f - ERed/Ox сопровода-ется ускорением процесса проявления*, Г. П. Фаерман с сотрудниками пояснил роль и действие основных компонент проявителя в процессе проявления.
Для случая физического проявления основное выражение электродной теории ЛЕ = EAg - ERed можно записать так:
АЕ = Е — Е,,„ = Е° ч------------In С — Ер
Ag / Ag Red/Ох Ag /Ag p Ag Red/Ox
_«11п[Ох]_ет
nF Red nF
(5.3.44)
При химическом проявлении бромида серебра это выражение принимает вид:
Скорость проявления не может зависеть только от разности потенциалов, однако в случае химической кинетики процесса проявления для данного проявляющего раствора и фотоматериала может наблюдаться прямая зависимость между скоростью и ДЕ. В случае кинетики процесса проявления, близкой к диффузионной, величина ЛЕ перестает быть определяющей.
RT
~ ~ ^Red/Ох = AgBr ~ [ВГ ] - ERedyOx
Rt [Ox] ~nF П [Red]
Rt
-^/ln[H‘]
(5.3.45)
где EAgBr — нормальный потенциал бромосеребряного электрода: [Br~] — концентрация ионов брома в проявляющем растворе; /1п[Н+] — функция, определяющая зависимость EReci/ox от концентрации ионов водорода в проявляющем растворе.
С учетом того, что в рассмотренных выражениях Red-формой для большинства проявляющих веществ (гидрохинона, метола, глицина, пирогаллола и др.) является не молекула, а ион проявляющего вещества, можно сказать, что щелочь ускоряет процесс восстановления галогенида серебра за счет повышения степени диссоциации и увеличения концентрации активной ионной формы проявляющего вещества. При этом необходимо отметить, что скорость процесса проявления в большей степени зависит от величины pH, чем от природы щелочи, создающей данное значение pH проявляющего раствора. С увеличением pH наблюдается смещение окислительно-восстановительного потенциала проявляющего вещества в сторону отрицательных значений (рис. 5.3.14), что в конечном счете приводит к увеличению значения разности потенциалов ЛЕ и ускорению процесса проявления.
При использовании в проявителе едкой щелочи и низкой концентрации бромида калия в растворе в участках эмульсионного слоя, получивших большие уровни экспозиций, происходят резкое понижение величины pH, обусловленное малой буферной емкостью щелочи, и связанные с этим уменьшение разности потенциалов ЛЕ и замедление процесса проявления. Этот случай соответствует выравнивающему проявлению. В свою очередь в проявителе с углекислым калием замедление процесса проявления не наблюдается, т. к. образующаяся в эмульсионном слое бромистоводородная кислота в течение всего процесса проявления титруется щелочью, имеющей высокую буферную емкость; при этом величина pH, потенциалы ERed/Ox, EAg(/Ag, ЛЕ практически не изменяются.
Добавление в проявитель органических антивуалирующих веществ, таких, как бензотриазол, 1-фенил-5-меркаптотетразол, и других, образующих с ионами серебра труднорастворимые соединения, произведения растворимости которых меньше произведения растворимости бромида серебра, как и в случае бромида калия, приводит к понижению величины ЛЕ и замедлению процесса проявления за счет того, что ^Ag./Ag становится более отрицательным.
Присутствие в проявляющем растворе сульфита натрия приводит к образованию в процессе проявления сульфопроизводных проявляющих веществ, которые восстанавливают галогенид серебра с более положи-
Химия фотографических процессов
873
тельным окислительно-восстановительным потенциалом, чем у самого проявляющего вещества, и гораздо меньшей скоростью. Основная же роль сульфита натрия в процессе проявления сводится к поддержанию на очень низком уровне концентрации окисленной формы проявляющего вещества и постоянной величины окислительно-восстановительного потенциала проявляющей системы (рис. 5.3.16). При этом в случае химического проявления при постоянной концентрации окисленной формы для большинства проявляющих веществ окислительно-восстановительный потенциал и оптическая плотность почернения линейно зависят от логарифма концентрации проявляющего вещества в проявителе.
При физическом проявлении с предварительным фиксированием концентрация ионов серебра в проявляющем растворе всегда гораздо больше, чем в обычном проявителе, и это обстоятельство объясняет тот факт, что потенциал ^Ag+/Ag при физическом проявлении более положителен, чем при химическом. Чтобы не происходило самопроизвольного восстановления ионов серебра в растворе, в физический проявитель вводят кислоту, наличие которой обеспечивает сдвиг окислительно-восстановительного потенциала Е , в сторону положительных значений и уменьшение величины разности потенциалов ДЕ.
Объясняя роль бромида калия в проявителе, необходимо напомнить, что в процессе восстановления экспонированного гало-генида серебра в эмульсионном слое происходит образование больших количеств бромистоводородной кислоты, которая существенно понижает величину pH внутри фотослоя (рис. 5.3.15). Это обстоятельство приводит к замедлению проявления за счет уменьшения разности потенциалов ДЕ, т. к. с уменьшением pH окислительно-восстановительный потенциал ERed/Ox смещается в сторону более положительных значений, а потенциал ^Ag./Ag за счет увеличения концентрации ионов брома в слое становится более отрицательным:
RT
Е , =Е°--------1п[Вг ].
Ag / Ag AgBr р L J
Роль и действие основных компонент проявляющего раствора и соотношения потенциалов ERed/Ox и Е .
для различных случаев процесса проявления, рассмотренные здесь, наглядно иллюстрируются диаграммой потенциальных уровней, предложенной С. Чербовым и Г. Фаерманом (рис. 5.3.17).
Электродная теория сегодня довольно достоверно описывает процесс фотографического проявления, но она все же еще не может объяснить ряд фактов, касающихся, например, того, что структурные дефекты микрокристалла галогенида серебра в процессе химического проявления могут способствовать процессу его восстановления, как и центры скрытого изображения.
15
pH
Рис. 5.3.14. Влияние pH раствора на величину восстановительного потенциала Е„ органических проявляющих веществ: пирокатехина (7); парааминофеиола (2), метола (3), пирогаллола (4), гидрохинона (5), п-фенилендиамина (б) (по С. Богданову и X. Фризеру)
Рис. 5.3.15. Изменение pH внутри эмульсионного слоя в процессе проявления в метол-гидрохиноновом проявителе до экспонирования (а) и после экспонирования (б): /, 2, 3, 4 — соответствуют различной толщине эмульсионного слоя (по Дж. Эггерсу и К. Деттмару)
Рис. 5.3.16. Изменение восстановительного потенциала метола при титровании окислителем в присутствии сульфита натрия (7) и в его отсутствие (2) (по С. Богданову)
874
Новый справочник химика и технолога
+ 1 2
Е
Ох/Rec
Ад /Ад Ад+/Ад
"1 Г"
I Д|2
Д«Й I Ox /Red
3 ( 4 ( 5 6
Рис. 5.3.17. Схема потенциальных уровней проявляющей и серебряной систем при обычном химическом проявлении (7); при pH проявителя < 7,0 (2);
при проявлении в слабозабуферснном проявителе (3);
при отбеливании серебра (4); при добавлении в проявитель антивуалентов (5); при физическом проявлении после фиксирования (6) (по Г. Фаерману)
Рис. 5.3.18. Разновидности проявления микрокристаллов галогенида серебра в эмульсионном слое (по X. Эгеру и X. Фризеру): диффузное (а), регулярное (б), точечное (в), нерегулярное (г), взрывное (Э), инфекционное (е)
Кроме того, электродная теория проявления неприменима к начальной стадии химического проявления, когда частицы серебра, возникшие при экспонировании микрокристалла, очень маленькие по размеру, по мнению некоторых ученых, представляют собой нс металлическую, а промежуточную фазу со свойствами полупроводников и по этой причине не могут рассматриваться как серебряный электрод в электрохимическом процессе.
Проявление микрокристаллов галогенида серебра в эмульсионном слое. В фотографической практике в зависимости от состава проявляющего раствора, условий экспонирования, параметров эмульсионного слоя различают несколько видов проявления микрокристаллов галогенида серебра. X. Фризер и X. Эгер по внешним признакам условно выделили шесть разновидностей: диффузное, регулярное, точечное, нерегулярное, взрывное и инфекционное проявление.
Диффузное проявление. При наличии нескольких равноценных центров скрытого изображения на микрокристалле галогенида серебра в процессе его восстановления происходит образование множества очень коротких и тонких нитей из металлического серебра («моха»), которые растут из центра проявления (рис. 5.3.18, а). В начальной стадии проявления зерно кажется серым, а затем чернеет по всей поверхности. Появление «моха» происходит, как правило, при восстановлении микрокристаллов, получивших большие уровни экспозиций, когда образуется много серебряных центров проявления. Концентрация сульфита натрия в проявителе в этом случае должна быть довольно высокой, в противном случае с уменьшением содержания сульфита эффект появления «моха» исчезает полностью. Это говорит о том, что не все центры проявления находятся на поверхности микрокристалла, а сульфит натрия способствует «обнажению» внутренних центров скрытого изображения.
Возможность появления «моха» в активном проявителе с высоким значением pH всегда гораздо меньше, чем в малоактивном с малым значением pH, т. к. в последнем случае участвует большее число центров проявления, чем в первом.
Регулярное проявление. Проявление микрокристалла бромида серебра в этом случае начинается в одной точке, а затем постепенно распространяется по всей поверхности микрокристалла (рис. 5.3.18, б). Форма кристалла при этом практически не изменяется. Такой вид проявления характерен для гидрохиноновых проявителей с довольно большим индукционным периодом проявления микрокристаллов галогенида серебра, имеющих малое число центров проявления.
Точечное проявление. Проявление микрокристалла галогенида серебра при наличии большого числа центров проявления начинается в нескольких точках на его поверхности и протекает очень медленно (рис. 5.3.18, в). Такой вид проявления наблюдается в малоактивных проявителях, обладающих сильным растворяющим действием (большая концентрация сульфита натрия в проявителе). Форма восстановленного зерна соответствует физическому проявлению. Это обстоятельство дает основание точечное проявление рассматривать как физическое, т. к. в процессе проявления микрокристалл бромида серебра вокруг восстановленного металлического серебра растворяется, что и приводит к нарушению контакта между Ag и AgBr. Восстановление на центре проявления серебряносульфитных комплексов, образовавшихся в процессе растворения бромида серебра, высвобождает ион сульфита, концентрация которого вокруг восстановленного серебра растет, что и обеспечивает дальнейшее растворение микрокристалла бромида серебра в процессе проявления.
Нерегулярное проявление. При данном типе проявления микрокристалла серебро от центра проявления выталкивается в виде короткой нити, которая утолщается и медленно растет в длину
Химия фотографических процессов
875
(рис. 5.3.18, г). Форма микрокристалла в этом случае всегда изменяется, что в конечном счете может привести к увеличению зернистости изображения.
Взрывное проявление. При проявлении микрокристалла галогенида серебра имеют место случаи, когда от одного из центров проявления сначала медленно, а затем довольно быстро вырастает серебряная нить, которая может быть очень длинной (рис. 5.3.18, д). Форма микрокристалла в процессе проявления существенно изменяется за счет того, что восстановленное серебро распространяется в сторону. Такой вид проявления характерен для проявителей с высоким значением pH и имеющих низкую концентрацию сульфита натрия. При этом чем меньше на микрокристалле центров проявления, тем выраженнее протекает взрывное проявление. Как правило, оно начинается в одной точке микрокристалла галогенида серебра. За очень короткий промежуток времени после начала проявления возникают большие клубки серебряных нитей, являющихся, согласно электродной теории проявления, серебряными электродами, увеличение поверхности которых приводит к повышению скорости проявления за счет большой поверхности контакта проявляющего раствора с электродом.
Инфекционное проявление — вид проявления, при котором восстанавливаемый микрокристалл галогенида серебра вызывает проявление близлежащего соседнего неэкспонированного микрокристалла (рис. 5.3.18, в). При этом различают:
- «инфекцию», переходящую радиально от одного микрокристалла к соседнему близлежащему и распространяемую далее на другие микрокристаллы;
- «инфекцию», которая после полного восстановления одного микрокристалла тотчас же переходит на соседний микрокристалл;
- «инфекцию», при которой серебряная нить одного микрокристалла при соприкосновении с соседним микрокристаллом вызывает его самопроизвольное восстановление.
Такому виду проявления способствуют большая плотность упаковки микрокристаллов галогенида серебра в эмульсионном слое, образование длинных серебряных нитей при восстановлении микрокристалла и незначительное содержание сульфита натрия в проявляющем растворе.
5.3.1.9. Кинетика процесса проявления эмульсионного слоя
В начальной стадии процесса проявления при погружении экспонированного фотоматериала в щелочной проявляющий раствор происходит набухание эмульсионного слоя и проникновение компонент проявителя к микрокристаллам галогенида серебра. Концентрация проявляющих веществ, щелочи, сульфита натрия при этом непрерывно возрастает. После достижения опре
деленной величины значения pH внутри эмульсионного слоя начинается процесс восстановления микрокристаллов галогенида серебра.
Общая скорость проявления в этом случае может зависеть от продолжительности слагающих исходных стадий процесса: набухания эмульсионного слоя, диффузии компонент проявителя, адсорбции проявляющих веществ на поверхности микрокристаллов галогенида серебра, индукционного периода химической реакции восстановления ионов серебра, десорбции продуктов реакции и т. д. Самая медленная слагающая стадия определяет характер кинетики и общую скорость процесса проявления. Так, например, если скорость диффузии компонент проявителя в эмульсионный слой в 10 раз меньше, чем скорость других исходных стадий процесса проявления, то кинетика процесса является диффузионной. Кинетика проявления слоя будет химической, адсорбционной или набухания, если самой медленной стадией будет, соответственно, химическая реакция восстановления галогенида серебра, адсорбция или набухание. На практике имеют место случаи, когда не одна стадия процесса, а две или несколько исходных стадий определяют общую скорость проявления. В этом случае кинетика процесса будет смешанной, например, диффузионно-адсорбционной, адсорбционно-химической, диффузионно-химической и т. д.
С. Шеппард и К. Миз, рассматривая процесс проявления с физико-химической точки зрения и считая, что кинетика проявления химическая, вывели уравнение кинетики процесса проявления, которое впоследствии получило название уравнения Шеппарда и Миза:
D^DJX-e^),
где D, — оптическая плотность почернения за время проявления /пр; — предельная оптическая плотность, которая возникает на фотоматериале при /ир = оо; к — константа скорости проявления.
В дальнейшем с учетом индукционного периода проявления уравнение кинетики проявления принимает вид:
D,=D„0-e‘"’
где to — время индукционного периода проявления.
Характер кинетики проявления можно определить измерением скоростей слагающих исходных стадий процесса. Однако иногда это выполнить просто невозможно, и тогда прибегают к определению температурного (ат) и гидродинамического (ЛГг) коэффициентов процесса проявления, значения которых позволяют судить о характере кинетики (табл. 5.3.4). Для этого при-
* Кинетикой называют учение о скорости и механизме химических реакций.
* * Кг — отношение времен проявления без разрушения пограничного слоя и с разрушением, обеспечивающих получение одинаковых плотностей почернения или одинаковых коэффициентов контрастности.
876
Новый справочник химика и технолога
меняют простые уравнения, характеризующие изменение фотографических параметров при проявлении в диапазоне температур до 10 °C:
^пр., Г-Д 7
^пр., Т+ЛТ
D-const
Н -const
ИЛИ
а7
(t
пр , 7'-А7
k ^пр„ Т+ЛТ
'/-const
где Т — температура, °C; ДГ = 5 °C.
Обычно для распознавания вида кинетики процесса проявления или кинетики фиксирования рассматривают вместе значения температурного и гидродинамического коэффициентов, т. к. это позволяет более точно определять характер кинетики (табл. 5.3.4) и управлять этими процессами на практике.
Если значения температурного коэффициента суммарного процесса близки значениям температурных коэффициентов соответствующих исходных слагающих стадий процесса, то эти слагающие и определяют характер кинетики проявления эмульсионного слоя. Так, например, если температурный коэффициент проявления а,т~ 1,5, а гидродинамический коэффициент Кг- 3,0, то кинетика проявления эмульсионного слоя близка к диффузионной (табл. 5.3.4), т. е. самой медленной стадией является диффузия компонент проявителя в эмульсионный слой; для ускорения процесса в этом случае необходимо ускорить их доставку в глубь слоя.
Если же температурный коэффициент ат = 1,6, а гидродинамический коэффициент Кг = 1,0, то кинетика проявления будет близка к набуханию (табл. 5.3.4). Для ускорения процесса проявления необходимо экспонированный фотоматериал предварительно размочить в воде или щелочи.
Таблица 5.3.4
Значения температурных и гидродинамических коэффициентов в зависимости от вида кинетики процесса (по И. Б. Блюмбергу)
Вид кинетики процесса ат Е,
Набухания 1,2-1,6 1,0
Диффузионная 1,4-1,6 2,0-20,0
Химическая 2,0-4,0 1,0
Адсорбционная 0,9-1,4 1,0
Хемисорбционная 1,0-1000 1,0
Кинетика процесса проявления эмульсионного слоя, как установил И.Б. Блюмберг, неодинакова в участках слоя, получивших различные уровни экспозиций. В сильно экспонированных участках слоя кинетика близка к диффузионной, т. к. в набухшем слое недостаточно компонент проявителя для полного восстановления большого количества экспонированных микрокри
сталлов галогенида. Для завершения процесса проявления фотоматериала в этом случае необходим интенсивный диффузионный обмен с внешним раствором проявителя. Величину диффузионного обмена между эмульсионным слоем и внешним раствором проявителя характеризуют фотографической емкостью слоя, которая, согласно определению И.Б. Блюмберга, представляет собой отношение количества компонент проявителя (щелочи, гидрохинона) в набухшем эмульсионном слое к тому количеству указанных веществ, которое необходимо для завершения процесса проявления всех экспонированных микрокристаллов галогенида серебра в слое без диффузионного обмена. При диффузионной кинетике фотографическая емкость слоя, как правило, всегда меньше единицы.
В слабоэкспонированных участках эмульсионного слоя кинетика близка к химической, т. к. в набухшем слое компонент проявителя вполне достаточно, чтобы восстановить совсем небольшое количество экспонированных микрокристаллов галогенида серебра. Фотографическая емкость слоя в этом случае гораздо больше единицы, и скорость процесса проявления зависит в основном от fRed/ox, EAg,/Ag, Р^, и Т величин, кото-рые и определяют скорость химической реакции восстановления галогенида серебра.
Обычный процесс проявления фотоматериала осложняется не только протеканием сопряженных реакций, их кинетикой, но и их индукционным периодом, который в большей степени зависит от величины заряда ионов проявляющего вещества (табл. 5.3.5, рис. 5.3.19), чем от его химической природы.
Проявляющие вещества с нулевым зарядом, как установил Т. Джеймс, практически не обладают индукционным периодом проявления, в то время как отрицательно заряженные ионы проявляющих веществ имеют индукционный период; причем он тем больше, чем отрицательнее заряд иона проявляющего вещества. Это можно объяснить влиянием отрицательного зарядного барьера, который существует на поверхности микрокристалла галогенида серебра (см. рис. 5.3.6). Двухзарядному иону проявляющего вещества в этом случае гораздо труднее приблизиться к микрокристаллу, чем однозарядному. Силы электростатического отталкивания препятствуют адсорбции проявляющего вещества на поверхности кристалла, повышению концентрации восстановителя вблизи центра проявления и началу процесса проявления.
С увеличением концентрации бромида калия в проявляющем растворе индукционный период проявления возрастает, правда, только в том случае, когда проявляющее вещество имеет отрицательный заряд. Скорость процесса проявления при этом незначительно понижается за счет того, что величина разности потенциалов ДЕ между серебряной EAg и восстановительной ERed системами становится меньше. Индукционный период можно существенно сократить с помощью нейтральных солей или положительно заряженных ионов,
Химия фотографических процессов
877
добавляемых в проявитель, которые, адсорбируясь на поверхности микрокристалла галогенида серебра, вытесняют избыток бромида и уменьшают величину отрицательно заряженного барьера, что способствует более быстрому достижению ионами проявляющего вещества поверхности кристалла.
Необходимо отметить при этом, что почти все проявляющие вещества довольно хорошо адсорбируются на галогениде серебра, причем гидрохинон и хинон имеют более высокую степень адсорбции на экспонированном бромде серебра.
Рис. 5.3.19. Влияние заряда проявляющего вещества на величину ин аукционного периода проявления и оптическую плотность почернения на фотоматериале (по Т. Джеймсу)
Таблица 5.3.5
Классификация проявляющих веществ по заряду (по Т. Джеймсу)
Заряд Проявляющее вещество
0 П-фенилендиаымн и его производные
-1 Метол, «-аминофенол, гидроксиламин, ц-аминофенилглицин
-2 Гидрохинон, хлоргидрохинон, аскорбиновая кислота, пирогаллол
-3 Натрий моносульфонат гидрохинона, галловая кислота
-4 Калий дисульфонат гидрохинона
Таблица 5.3.6
Адсорбция проявляющих веществ на металлическом серебре (по Р. Понтиусу)
Проявляющее вещество Степень адсорбции, %
Гидрохинон 0
и-Фенилендиамин 30
Метол 23
Диэтил-и-фенилендиамин (ТСС) 100
4-Амино-3-метил-Аг-этил-Аг-(метилсульфонамидоэтил)-анилин (CD-3) 100
На общую скорость процесса проявления оказывает также большое влияние диффузия компонент проявителя в эмульсионный слой и продуктов реакции из слоя. Адсорбция и связывание компонент проявляющего раствора галогенидом серебра и желатином эмульсионного слоя существенно замедляют проникновение их через эмульсионный слой. Скорость диффузии и коэффициент диффузии компонент проявителя зависят не только от природы, строения, концентрации диффундирующих веществ (табл. 5.3.7), но и от структуры эмульсионного слоя, степени его задубленности, концентрации и размера микрокристаллов галогенида серебра (рис. 5.3.20).
Таблица 3.7
Коэффициент диффузии D основных компонент проявляющего раствора
(по X. Ивано)
Вещество D, см2/с
Сульфит натрия 2,01 • 10’5
Натрий углекислый 2,15- 10’5
Натрий сернокислый 0,98- 10’5
Фенидон 1Д7- 10’7
Гидрохинон 0,69 • 10 7
Пирогашюл 0,42 • 10’7
Амидол 1,42 • IO"7
Метол 1,58 • 10'7
и-Аминофенол 1,69 • 10’7
Диэтил-и-фснилендиамин (ТСС) 1,85 • 10'7
Этилоксиэтил-и-фенилендиамин (Т-32) 1,77- 10’7
CD-2 1,56- 10 7
CD-4 1,46- 10’7
Бромид калия 1,59- 10’5
Иодид калия 1,49- 10’5
Бензотриазол* 3,12- 10’8
1 -Фенил-5-меркаптотетразол* 0,79- 10’8
*Данные автора.
Для начала процесса проявления экспонированного фотоматериала концентрация не только проявляющих веществ, но и щелочи в эмульсионном слое должна достигнуть определенной величины. С этой точки зрения диффузия щелочи в эмульсионный слой часто становится определяющим фактором при проведении процесса проявления, т. к. создание в глубине эмульсионного слоя порогового значения pH, необходимого для начала проявления, имеет важное значение в практике фотографии.
Скорость проникновения щелочей через желатиновый слой уменьшается в ряду
КОН > NaOH > К3РО4 > К2СО3 > Na2CO3,
878
Новый справочник химика и технолога
а для производных п-фенилендиамина (ПФДА) уменьшается с увеличением молекулярной массы вещества, размера замещенных групп и возрастает в ряду
CD-3 < CD-4 < CD-2 < Т-32 < ТСС < ПФДА.
Рис. 5.3.20. Влияние размеров микрокристаллов галогенида серебра на продолжительность проникновения производных п-фенилендиашта (ПФДА) через воздушно-сухой эмульсионный слой (X = 10 мкм; CAg = 2,15 г/м2): / — ПФДА; 2 - ТСС; 3 — Т-32; 4 — CD-2; 5 — CD-3;
6 CD-4
Что касается антивуалирующих веществ, то бромид калия и иодид калия диффундируют в эмульсионный слой довольно быстро; скорость их диффузии определяется различной гидратируемостью аниона. Органические антивуалирующие вещества, такие, как бензотриазол и 1-фенил-5-меркаптотетразол, диффундируют в слой очень медленно. Они, как правило, обеспечивают уменьшение плотности вуали на различных уровнях эмульсионного слоя — на поверхности или в глубине его.
5.3.2. Процесс фиксирования
После завершения процесса проявления фотоматериала следует промежуточная промывка водой или кислая стоп-ванна, содержащая слабую кислоту. Во время этих операций происходит прерывание процесса проявления за счет удаления из фотографического слоя избытка компонент проявляющего раствора или нейтрализации проявителя кислотой, что и приводит к понижению pH эмульсионного слоя ниже «порогового» значения. Далее следует процесс, называемый фиксированием, задачей которого является перевод непроявлен-ных труднорастворимых соединений галогенида серебра (AgCl, AgBr, Agl) в неэкспонированных участках эмульсионного слоя в водорастворимые соединения, которые затем (в процессе окончательной водной промывки) легко и полностью удаляются из слоя, что обеспечивает стабильность и длительный срок хранения изображения на фотоматериале.
Для перевода практически нерастворимых в воде галогенидов серебра широкое распространение получил тиосульфат натрия (Na2S2O3 • 5Н2О), который образует
с серебром легкорастворимыс в воде стабильные комплексные соединения, не оказывая при этом вредного воздействия на восстановленное серебро и желатин фотослоя. Существуют и другие соединения, способные образовывать с галогенидами серебра комплексные соединения (такие, как тиоцианат калия, тиоцианат аммония, тиомочевина), которые находят ограниченное применение в фотографии в связи с тем, что они ядовиты и дороже, чем тиосульфат натрия, и, кроме того, существенно размягчают желатин эмульсионного слоя. Применяют такие соединения в основном при быстрой обработке высокозадубленных специальных фотоматериалов для стабилизации изображения — перевода неэкспонированного и непроявленного галогенида серебра в прозрачные и светостойкие комплексные соединения. После процесса стабилизации, как правило, исключается окончательная водная промывка фотоматериала, при этом срок хранения фотографического изображения значительно сокращается.
5.3.2.1. Химические основы процесса фиксирования и комплексные соединения серебра
Как известно, ионы серебра могут образовывать комплексы со многими соединениями. Лучшими ком-плексообразователями являются те вещества, которые имеют свободные электронные пары, необходимые для образования ковалентных координационных связей. Ионы серебра склонны образовывать тетраэдрическую форму комплексов. Это происходит путем последовательного добавления четырех лигандов, каждый из которых имеет свободную пару электронов. Примером служат тиоцианатные, тиомочевинные и другие серебряные комплексы. В случае же, например, S-сульфитных и S-тиосульфатных комплексов каждый из двух лигандов в состоянии насыщения добавляется в качестве хелатной группы к иону серебра с двумя электронными парами. Склонность ионов серебра к образованию комплексов с некоторыми комплексообразу-ющими веществами настолько велика, что в этих комплексах даже более высокие уровни окисления серебра (Ag2+, Ag3+) становятся очень устойчивыми.
Процесс комплексообразования галогенидов серебра в присутствии лиганда можно представить в общем виде следующей схемой:
Ag++L '’<=»[AgL] (5.3.46)
[AgLr+1 + 17” <=± [AgL2]-2”+1 (5.3.47)
[AgL(f)_1)]4”-l)”+l+L*” <=2 [AgLJ-””
(5.3.48)
Константа стабильности или устойчивости Кп (величина, обратная константе диссоциации) комплексного иона вида [AgL„]~"” + 1 выражается в этом случае
уравнением:
к [AgL„r-
" [Ag+][L-q«
(5.3.49)
Новый справочник химика и технолога
879
которое определяет соотношение между равновесной концентрацией комплексного иона [AgL„] концентрацией свободных ионов серебра и концентрацией свободных комплексообразующих лигандов [L ^].
Из большого числа комплексных соединений серебра рассмотрим лишь те, которые имеют наибольшее значение в практике.
Определенную роль при проведении фотографического процесса играют комплексы сульфита и серебра, которые образуются в присутствии сульфита натрия, при добавлении его в обрабатывающий раствор для предотвращения окисления проявляющих веществ. Константы устойчивости ионов приведены в табл. 5.3.8.
Таблица 5.3.8
Константы устойчивости сульфитно-серебряных комплексных ионов
Комплекс- Название 2 ® о о s X t; g X о
ный ион комплексного иона о х О s Ег О д у 3§ S
[Ag(SO3)]' Моносульфитарген- 2 2 • 105
тат
[Ag(SO3)2]3 Дисульфитаргентат 4 1,9- 108
[Ag(SO3)3]5 Трисульфитаргентат 6 109
В процессе стабилизации изображения тиоцианатом калия или аммония тиоцианат-ионы последовательно добавляются к иону серебра, образуя различные комплексные ионы вида [Ag(NCS)„]1-”, константы устойчивости которых приведены в табл. 5.3.9.
Таблица 5.3.9
Константа устойчивости тиоцианатсеребряных комплексных ионов
Комплексный ион Название комплексного иона Константа устойчивости при 25 °C
AgNCS [Ag(NCS)2]’-[Ag(NCS)3|2~ [Ag(NCS)4]3" Тиоцианат серебра Моноаргентодитиоциа-нат Моноаргентотритиоциа-нат 5,56 • 104 1,67 • 108 5,6- 109 3,7 • 1О10
На первой стадии процесса стабилизации образуется практически нерастворимый тиоцианат серебра:
AgBr + KNCS-» AgNCS + KBr (5.3.50)
Далее в избытке тиоцианат-ионов в результате их адсорбции на галогениде серебра образуются раство
* Название «тиоцианат-ион» соответствует номенклатуре, разработанной Международным союзом теоретической и прикладной химии (ИЮПАК), согласно которой написание формулы аниона в виде CNS” и использование названия «роданид-ион» не допускаются.
римые высшие серебряно-тиоцианатные комплексные соединения:
AgNCS+ KNCS <=» K[Ag(NCS)2]
К[ Ag(NCS)2 ] + KNCS <=> К2[Ag(NCS)3] (5.3.51)
K2[Ag(NCS)3] + KNCS «=> K3[Ag(NCS)4]
Однако необходимо иметь в виду, что при окончательной промывке фотоматериала после стабилизации растворимые комплексные соединения тиоцианата разлагаются с образованием нерастворимого тиоцианата серебра белого цвета:
[Ag(NCS)2]1- +Hz° >AgNCS+NCS'~ (5.3.52)
Наиболее важная роль при проведении фотографического процесса отводится фиксированию галогенсеребряных материалов тиосульфатом натрия, константы устойчивости серебряных комплексов которого представлены в табл. 5.3.10.
Наиболее устойчивым серебрянотиосульфатным ионом является [Ag^O^]3-, в котором каждый из двух лигандов в форме хелатной группы присоединяется к иону серебра, образуя, вероятно, тетраэдрическую конфигурацию следующей структуры:
(5.3.53)
Во многих случаях при реализации фотографического процесса важно знать концентрацию, до которой будет растворять галогенид серебра тот или иной ком-плексообразователь (L/?) при определенной его концентрации. Эти данные можно получить, используя значения констант устойчивости соответствующих комплексных ионов серебра (табл. 5.3.8-5.3.10), а также величину произведения растворимости (ПРАёХ) используемого галогенида серебра (AgX):
ПРАёХ = [Agb] [Х-] (5.3.54)
Соотношение между концентрацией комплексного иона [AgLJ "77'1 и концентрацией свободного комплексообразующего вещества в этом случае имеет вид:
([AgL„r'+1 = ПР^4(Ь’Р)^ (5-3.55)
5.3.2.2. Факторы, определяющие скорость процесса фиксирования
Известно, что твердый галогенид серебра эмульсионных микрокристаллов в воде находится в равновесии с растворенной частью, т. к. ионы серебра в сольватированной форме уходят из кристаллической решетки в раствор:
(AgHal)^ (AgHal)paCTB <=> Ag+ + НаГ (5.3.56)
880
Новый справочник химика и технолога
Таблица 5.3.10
Константы устойчивости серебрянотиосульфатных комплексных ионов
Комплексный ион Название комплексного нона Константа устойчивости при 20 °C Растворимость соли в воде
[Ag3(S2O3)2]1- Триаргентодитиосульфат Очень плохо растворима
[Ag(S2O3)]!- Моноаргентотритиосульфат 6,7 • 108 * * * * Умеренно растворима
[Ag3(S2O3)4]5 Триаргентотетратиосульфат Легко растворима
[Ag2(S2O3)3]4- Диаргентотритиосульфат
[AgfS'O,!,]' Моноаргентодитиосульфат 2,85 • 1013 Легко растворима
[Ag(S3O3)3]5- Моноаргентотритиосульфат 3,5 • 1013 Легко растворима
Если резко понижать концентрацию ионов серебра в растворе за счет образования комплексных ионов с высоким значением константы устойчивости, то равновесие реакции (5.3.56) будет нарушаться и смещаться вправо, что приведет к дальнейшему повышению скорости растворения микрокристаллов галогенида серебра.
При фиксировании тиосульфатом натрия (как считают многие ученые), ион тиосульфата диффундирует к поверхности микрокристалла галогенида серебра и, адсорбируясь на нем, образует на начальной стадии процесса соединение Ag2S2O3, довольно трудно растворимое. В дальнейшем во время реакции фиксирования при избытке тиосульфата натрия образуются отрицательно заряженные комплексные ионы [Ag(S2O3)2]3 , [Ag(S2O3)3]5’, которые за счет сил электростатического отталкивания легко покидают поверхность микрокристалла. При этом из кристаллической решетки микрокристалла высвобождаются и диффундируют в фиксирующий раствор ионы брома, концентрация которых будет пропорциональна количеству растворенного тиосульфатом галогенида серебра.
Процесс фиксирования бромида серебра тиосульфатом натрия протекает по следующей схеме:
2AgF + S2O3~ -> Ag2S2O3 (5.3.57)
Ag2S2O3 + Na2S2O3 <=> 2Na[Ag(S2O3)] (5.3.58)
Na[Ag(S2O3)] + Na2S2O3 ?=> Na3[Ag(S2O3)2] (5.3.59)
В процессе фиксирования происходят образование бесцветного комплексного соединения и полное исчезновение молочного помутнения эмульсионного слоя, обусловленного наличием галогенида серебра. В фотографической практике часто применяют термин «время осветления эмульсионного слоя», под которым понимают промежуток времени от начала погружения фотоматериала в фиксирующий раствор до полного исчезновения молочного помутнения слоя на
неэкспонированных его участках. Время полного ос-
ветления эмульсионного слоя соответствует образова-
нию растворимой комплексной соли серебра и тио-
сульфата. Продолжительность процесса фиксирования
определяется сроком хранения изображения. Так, при
обычном хранении продолжительность фиксирования негативных фотоматериалов равна или больше двух времен осветления Гфикс > 2госв, а для негативных фотоматериалов, которые предназначены для архивного хранения, Гфикс > 3/оев. В случае малой продолжительности процесса фиксирования образуются комплексные соединения, которые при окончательной промывке водой трудно удаляются из фотографического слоя, а затем (в процессе хранения) разлагаются и вызывают порчу изображения:
Ag2S2O3+H2O-> Ag,S+H2SO4 (5.3.60)
Серебряное изображение приобретает в этом случае грязно-коричневую окраску как правило, существенно снижается и оптическая плотность за счет образования сульфида серебра.
Природа галогенида серебра. Процесс фиксирования эмульсионного слоя фотоматериала можно описать уравнением:
x = a(\-kf), (5.3.61)
где х — количество галогенида серебра, оставшегося в эмульсионном слое в момент времени I; а — общее количество галогенида серебра в эмульсионном слое; к — константа скорости реакции.
Константа скорости реакции фиксирования зависит от природы галогенида серебра; для хлорида серебра ее величина гораздо больше, чем для бромида и иодида серебра:
^AgCl > ^AgBr> ^AgJ-
Фотоматериалы, эмульсионный слой которых изготовлен из хлорида серебра, фиксируются очень быстро, в то время как слои, содержащие иодистое серебро или примеси иодида серебра в растворе тиосульфата натрия, фиксируются гораздо медленнее. Это связано с тем, что количество растворенного галогенида серебра определяется его произведением растворимости (уравнение (5.3.54)). Чем меньше произведение растворимости галогенида серебра, тем меньшая концентрация ионов серебра отвечает допустимой концентрации ионов
Химия фотографических процессов
881
серебра в растворе. В связи с тем, что произведение растворимости иодида серебра ПРАё] = 10 !6 по сравнению с произведениями растворимости бромида серебра ПРАёВг = Ю’13 и хлорида серебра nPAgC1 = 10'10 гораздо меньше, иодид серебра существенно хуже растворяется в растворе тиосульфата натрия. Для более быстрого и полного растворения иодида серебра необходимо применить комплексообразователь, константа диссоциации серебряного комплексного иона которого должна быть гораздо меньше, чем произведение растворимости иодида серебра. Увеличение концентрации комплексообразователя в фиксирующем растворе приводит также к ускорению процесса фиксирования за счет понижения концентрации свободных ионов серебра в растворе, т. к. в этих условиях образуются комплексные соединения, серебряный комплексный ион которых очень плохо диссоциирован (табл. 5.3.10).
Существенное влияние на продолжительность процесса фиксирования оказывает размер микрокристаллов галогенида серебра в эмульсионном слое фотоматериала. При одинаковой толщине слоя крупнозернистые эмульсионные слои фиксируются гораздо дольше, чем эмульсионные слои, содержащие микрокристаллы галогенида серебра малых размеров. Это объясняется тем, что при одинаковой поверхностной концентрации серебра мелкие микрокристаллы имеют гораздо большую общую поверхность, что и способствует значительно большей адсорбции ионов тиосульфата на кристалле и приводит в конечном счете к более быстрому протеканию реакций комплексообразования (рис. 5.3.21). Различия в продолжительности осветления эмульсионных слоев, содержащих неодинаковые по степени дисперсности микрокристаллы галогенида серебра, становятся более ощутимыми при низких концентрациях тиосульфата натрия.
и температуры раствора. Максимальная скорость процесса наблюдается в интервале концентраций 200-400 г/л. Применение высококонцентрированных фиксирующих растворов на основе тиосульфата натрия приводит к замедлению процесса фиксирования (рис. 5.3.22), т. к. громадная солевая концентрация обусловливает существенное уменьшение набухания желатина эмульсионного слоя за счет его дегидратации тиосульфатом, молекулы которого в растворе довольно сильно гидратированы — окружены молекулами воды за счет водородных связей.
Особое внимание при проведении процесса фиксирования необходимо уделять поддержанию на высоком уровне концентрации тиосульфата натрия, т. к. в истощенном фиксирующем растворе не исключено образование труднорастворимого в воде комплексного соединения, бедного тиосульфатом [Aga^Ch^]1”, которое практически нерастворимо и не вымывается из фотослоя.
При воздействии света, температуры и влаги в процессе хранения происходит его разложение, что приводит к ухудшению качества изображения (коричневым пятнам и т. д.). Поэтому часто в практике фотографии применяют для фиксирования две фиксирующие ванны; причем последняя ванна должна быть свежей и иметь довольно высокую концентрацию тиосульфата. В этих условиях, как правило, образуется легкорастворимый серебрянотиосульфатный комплекс, который еще в процессе фиксирования полностью диффундирует из фотослоя в фиксирующий раствор. Это обстоятельство имеет важную практическую ценность, т. к. при окончательной промывке в этом случае из слоя необходимо удалить только ионы тиосульфата.
Рис. 5.3.21. Влияние размера микрокристалла галогенида серебра в эмульсионном слое на количество Q растворенного серебра:
1 — мелкозернистая эмульсия; 2 — крупнозернистая эмульсия
Влияние концентрации тиосульфата, вида катиона, температуры и перемешивания. Как и большинство химических реакций, процесс фиксирования ускоряется с увеличением концентрации тиосульфата натрия
0 100 200 300 400 500 600
С, г/л
Рис. 5.3.22. Влияние концентрации тиосульфата натрия на продолжительность осветления эмульсионного слоя
Если же комплексные соединения в процессе фиксирования не продиффундировали из слоя в фиксирующий раствор, то при окончательном промывании водой в первую очередь будут удаляться из слоя ионы тиосульфата (как более подвижные). Понижение концентрации тиосульфата в слое в процессе промывания при наличии серебрянотиосульфатных комплексов при
882
Новый справочник химика и технолога
ведет к смещению равновесия обратимых реакций (5.3.59), (5.3.58) влево, в сторону образования труднорастворимых соединений серебра и тиосульфата, таких, как Ag2S2O3, которые практически не вымываются из слоя.
На скорость процесса фиксирования можно воздействовать различными катионами, имеющими неодинаковую степень гидратации (рис. 5.3.23). Известно, что катионы NH*, Na+, К\ Li+ оказывают существенное влияние не только на продолжительность фиксирования, но и на скорость проникновения ионов 82Оз“ через желатиновые слои. Это обусловлено тем, что катионы NH^, Na+, К+, Li4 и желатин эмульсионного слоя, являясь конкурентами в отношении воды, вызывают различное набухание желатина. Большая степень гидратации катионов Li+, К4, Na+ по сравнению с NH^ приводит к меньшему набуханию желатинового слоя и замедлению диффузии комплексообразователя. Подтверждением того, что уменьшение степени набухания эмульсионного слоя замедляет процесс фиксирования (рис. 5.3.24) за счет понижения скорости проникновения тиосульфата в слой, служат данные табл. 5.3.11.
Для набухших желатиновых слоев скорость проникновения иона тиосульфата вырастает в ряду
Li2S2O3 < Na2S2O3 < K2S2O3 < (NH4)2S2O3,
а для иона тиоцианата в ряду
LiNCS < Mg(NCS)2< NaNCS < NH4NCS.
Увеличение скорости осветления эмульсионных слоев тиосульфатом находится в прямой зависимости от величины коэффициента диффузии иона тиосульфата, величина которого определяется степенью гидратации катиона (рис. 5.3.23). Возможной причиной увеличения скорости фиксирования и проникновения в случае тиосульфата аммония может быть меньшая степень гидратации катиона NH^ по сравнению с катионом Na+. Необходимо отметить, что отношения скоростной диффузии иона тиосульфата в набухшие слои в присутствии катионов Li+, К4, Na+, NH^ очень близки к отношениям коэффициентов диффузии соответствующих катионов в желатине (рис. 5.3.24, табл. 5.3.12, 5.3.13).
В последнее время в технологии обработки зарубежных кинофотоматериалов все большее предпочтение отдается применению в фиксирующих растворах тиосульфата аммония. Такие растворы позволяют существенно сократить продолжительность процесса фиксирования при обработке цветных кинофотоматериалов и фотобумаг.
Т. к. тиосульфат аммония в твердом виде менее устойчив, чем тиосульфат натрия, то его применяют в виде 58% раствора. Чаще всего, однако, в качестве комплексообразователя используют тиосульфат натрия, который гораздо дешевле, чем тиосульфат аммония, а для сокращения продолжительности фиксирования
в фиксаж добавляют хлорид аммония в концентрации 30-50 г/л. Такие фиксирующие растворы называют быстрыми. Наибольший эффект ускорения процесса фиксирования при этом наблюдается при концентрациях тиосульфата натрия в фиксирующем растворе ~ 200 г/л. При машинной обработке кинофотоматериалов предпочтение все же отдается тиосульфату аммония, т. к. хлорид аммония оказывает вредное воздействие на детали лентопротяжного тракта проявочной машины.
Повышение температуры фиксирующего раствора приводит к сокращению продолжительности процесса фиксирования эмульсионных слоев, причем величина эффекта существенно зависит от концентрации тиосульфата натрия (см. рис. 5.3.22).
Рис. 5.3.23. Влияние величины энергии гидратации катиона (-ДЯ гидрат.) на коэффициент диффузии иона тиосульфата(D)
0 0,5 1 1,5 2 2,5 3 3,5 4 4,5
Концентрация, моль/л
Рис. 5.3.24. Продолжительность осветления эмульсионного слоя тиосульфатом в зависимости от природы катиона
Таблица 5.3.11
Влияние концентрации Na2SO4 на продолжительность проникновения тиосульфата (с) через желатиновый слой при быстрой обработке
Толщина желатинового слоя, мкм Концентрация Na2SO4, г/л
0 25 50 75 100
5,0 0,9 1,2 1,4 1,9 2,2
13,0 3,7 4,8 6,2 8,1 9,9
28,0 11,2 14,7 20,6 27,0 36,0
Химия фотографических процессов
883
Таблица 5.3.12
Влияние природы катиона на величину коэффициента диффузии в желатине
Вид катиона Коэффициент диффузии, см7с Отношение коэффициентов диффузии
Li+ 0,49- 10’5 1,0
Na+ 0,84- 10’5 1,7
К 1,09- 10 5 2,2
nh; 1,17- 10’5 2,4
Таблица 5.3.13
Влияние природы катионов на скорость диффузии тиосульфата
Вещество Скорость диффузии, мм/с Отношение скоростей диффузии
Li2S2O3 1,18 • 103 1,0
Na2S2O3 2,11 • 10’3 1,8
K2S2O3 2,62- 10’3 2,2
(NH4)2S2O3 2,75 • 10’3 2,3
Перемешивание фиксирующего раствора в свою очередь также оказывает влияние на скорость фиксирования, и весьма существенное, в связи с тем, что кинетика процесса близка к диффузионной. За счет ускорения диффузии тиосульфата в эмульсионный слой время осветления его сокращается до 50 %, причем эффект ускорения в значительной степени происходит при использовании разбавленных фиксирующих растворов и тонкослойных эмульсионных слоев. Для концентрированных растворов тиосульфата натрия и фотоматериалов, имеющих большую толщину эмульсионного слоя, перемешивание раствора в меньшей мере оказывает влияние на скорость процесса. Особое внимание необходимо уделять перемешиванию раствора при фиксировании фотобумаг, т. к. это избавит от многих дефектов, обусловленных неправильным проведением этого ответственного процесса химико-фотографической обработки фотоматериалов.
Что касается предела использования фиксирующих растворов на практике, то он определяется не только концентрацией тиосульфата натрия, но и содержанием серебрянотиосульфатных комплексов и ионов галогенов (Г, Вт , СГ), которые накапливаются в процессе фиксирования и существенно его замедляют.
Процесс фиксирования замедляется, кроме того, и проявляющими веществами, например гидрохиноном, который при непродолжительной промежуточной промывке заносится с проявителем в фиксирующий раствор. Тормозящий эффект фиксирования наблюдается и в присутствии эмульсионных стабилизаторов и антивуалентов (1-фенил-5-меркаптотетразола, бензотриазола), которые вымываются из слоя или заносятся проявителем. Это обстоятельство необходимо учитывать особенно при фиксировании фотобумаг. Причем наи
больший эффект тормозящего действия и неполного фиксирования указанные вещества оказывают в кислой среде при pH, соответствующих значениям pH кислых фиксирующих растворов. Применение на практике фиксирования в двух ваннах со свежим фиксирующим раствором на заключительной стадии позволяет полностью избавиться от всех дефектов, которые могут возникать в процессе фиксирования фотоматериалов.
5.3.2.3. Состав и разновидности фиксирующих растворов
В черно-белой фотографии применяют различные виды фиксирующих растворов: нейтральные, кислые, дубящие и быстрые. Нейтральный фиксирующий раствор содержит один тиосульфат натрия в концентрации 200-300 г/л. При использовании этих растворов на фотоматериале могут возникать дихроическая вуаль и пятна за счет восстановления серебрянотиосульфатных комплексов проявителем, который заносится в фиксаж набухшим эмульсионным слоем фотоматериала. Кислые фиксирующие растворы содержат кроме тиосульфата натрия и некоторое количество слабой кислоты (уксусной, лимонной, борной и т. д.) или кислые соли (бисульфит натрия, метабисульфит калия), которые при этом не разрушают тиосульфат натрия.
В кислом фиксирующем растворе происходит нейтрализация избытков проявителя в эмульсионном слое фотоматериала, что приводит к резкому понижению pH слоя ниже порогового значения и прекращению процесса проявления. Кроме того, низкое значение pH фиксажа (pH = 4,04-5,5) позволяет вводить дополнительно вещества, называемые дубителями (алюмокалиевые и хромовые квасцы), которые способствуют улучшению физико-механических свойств желатина, обладая максимумом дубления в данной области pH. Такие фиксирующие растворы называют дубящими.
Однако чаще всего вместе дорогостоящих слабых кислот применяют сильные кислоты, например серную кислоту, которая гораздо дешевле. При этом обязательно в раствор вместе с кислотой вводят сульфит натрия, в противном случае подкисление фиксирующего раствора до pH = 3,5 в отсутствие сульфита натрия приводит к разложению тиосульфата и порче раствора:
Na2S2Q3 .H2SO-4- >Na2SQ3+Si (5.3.62)
S2O32’ + H+ HSO3 + S Ф (5.3.62, a)
HSO; + Н+ ё* H2SO3 -> SO2 T +H2O (5.3.62, 6)
В присутствии же сульфита натрия в кислом фиксаже с серной кислотой образуются в избытке ионы HSO3 , что резко сдвигает реакцию (5.3.62, а) влево и предотвращает разложение тиосульфата и выпадение серы:
884
Новый справочник химика и технолога
Na2SO3 2Na+ + S02'
23 3 (5.3.63)
SO2+H+ ^HSO,
Кислые соли, такие, как бисульфит натрия NaHSO3, метабисульфит калия K2S2O5, обеспечивая хорошую кислотно-основную буферность фиксирующего раствора, поддерживают также на высоком уровне концентрацию HSO3 в фиксаже и тем самым предотвращают разложение тиосульфата:
NaHSCK <=» Na' +HSO7
3 3 (5.3.64)
K2S2O5 +Н2О <=» 2KHSO3 2К/ +2HSO;
В кислых фиксирующих растворах, обогащенных кислородом, наблюдается уменьшение оптической плотности серебряного изображения, причем оно будет тем сильнее, чем больше продолжительность пребывания фотоматериала в фиксаже и чем выше дисперсность металлического серебра в изображении (фотобумаги). По этой причине при физическом проявлении с предварительным фиксированием применяют только нейтральные или щелочные фиксирующие растворы, т. к. в кислом фиксаже скрытое изображение, состоящее из высокодисперсного коллоидного серебра, полностью исчезает.
Что касается набухания фотослоя, то в кислых фиксирующих растворах оно меньше, чем в нейтральных или щелочных, за счет того, что pH фиксажа в первом случае близок к изоэлектрической точке желатина (pH = 4,84-5,0) (рис. 5.3.25).
Я 80 X X
£60 св
“ 40
20
0
0 1 2 3 4 5 6 7 8 9 10 11 12 13
pH
Рис 5.3.25. Величина набухания (увеличение веса на 1 кг желатина) и заряд желатина в зависимости от pH раствора
5.3.3. Процесс промывания
После фиксирования фотоматериала следует процесс окончательного промывания водой, в результате которого из фотослоя полностью удаляется избыток ионов тиосульфата и часть комплексных соединений серебра, не перешедших в фиксирующий раствор. При недостаточном промывании слоя в процессе хранения фотоматериала при высоких влажности и температуре может наблюдаться разложение указанных солей, что приводит к образованию пятен и к постепенному пожелтению изо
бражения за счет образования Ag2S, особенно в участках малых плотностей. У цветных фотоматериалов при недостаточном промывании наблюдается обесцвечивание красителей, чаще всего голубого. Как правило, окончательное промывание проводят в проточной воде, используя при этом различные способы (душ, противоток и т. д.). В некоторых случаях, когда отсутствует проточная вода, ограничиваются небольшим ее количеством; при этом многократно меняют воду в баке (обычно через 5 мин), где находится промываемый фотоматериал.
Процесс промывания фотоматериала от тиосульфата натрия можно описать уравнением, предложенным Т. Джеймсом и К. Мизом:
— = DF—, (5.3.65)
dt dt
где dM — количество тиосульфата, которое диффундирует из слоя за время dt', D — коэффициент диффузии тиосульфата (1,61-10 5 см2/с); F— поверхность промы-dc
ваемого слоя; — — градиент концентрации в желати-dt
новом слое.
На практике количество тиосульфата, вымытого из фотослоя М за момент времени t, можно определить по упрощенной формуле, которую предложили Д. Спенсер и Дж. Кребтри:
— = К(А-М), (5.3.66)
dt
„ 1 . л С при /, z ,
где К =------10-------L — константа (с ); А — ис-
t2~t] С при /2
ходное количество тиосульфата в слое; Спри , — концентрация тиосульфата в определенный момент времени t.
Удаление избытка тиосульфата из фотослоя в первые моменты процесса промывания водой протекает по уравнению (5.3.66); в дальнейшем (на второй стадии промывания) тиосульфат, адсорбированный желатином эмульсионного слоя, вступает в обмен с анионами раствора и уходит из слоя.
Промывание фотопленок и фотобумаг
Скорость удаления из фотослоя избытка ионов тиосульфата и серебрянотиосульфатных комплексных соединений зависит от состава фиксирующего раствора и степени его истощения, от pH и температуры промывной воды, наличия в ней солей, а также от величины оптической плотности изображения на фотографическом материале.
Состав фиксирующего раствора и условия проведения процесса в значительной степени определяют полноту удаления из слоя избытка тиосульфата и комплексных соединений. Так, например, в случае применения дубящих фиксирующих растворов с хромовыми или алюмокалиевыми квасцами ион тиосульфата при
Химия фотографических процессов
885
промывке удаляется из слоя гораздо медленнее, чем при использовании обычного кислого фиксирующего раствора без дубящих веществ. В то же самое время фиксирование проявленного фотоматериала в нейтральном фиксирующем растворе способствует более быстрому промыванию, но может произойти замедление процесса удаления иона тиосульфата за счет большого набухания желатина эмульсионного слоя при данном значении pH (см. рис. 5.3.25).
Большое влияние на скорость удаления тиосульфата из фотослоя оказывает pH фиксирующего раствора и промывной воды. При значениях pH ниже изоэлектрической точки желатина процесс промывания значительно замедляется в связи с тем, что положительно заряженный желатин хорошо удерживает отрицательно заряженные ионы тиосульфата и серебрянотиосульфат-ных комплексов. При pH выше изоэлектрической точки желатин заряжается отрицательно и наблюдается более быстрое удаление из фотослоя отрицательно заряженного иона тиосульфата и комплексов за счет сил электростатического отталкивания.
Практика показала, что значение pH фиксажа, близкое к изоэлектрической точке желатина (pH = 4,9^-5,2), является наиболее благоприятным для более быстрого удаления компонент фиксирующего раствора из слоя в процессе окончательной промывки. Особое внимание в процессе обработки фотоматериалов необходимо уделять в этой связи и значению pH промывной воды, особенно при промывке фотоотпечатков, т. к. баритованная бумажная подложка хорошо удерживает S2O2“ и [Ag(S2O3)2]3 . Для ускорения промывки отпечатков ряд фирм рекомендует после кислого фиксирующего раствора (перед окончательной промывкой) применить сульфитную ванну (2% раствор, pH - 7,0) в течение 2-3 мин. В процессе этой операции желатин изменяет свой заряд с положительного на отрицательный, что в конечном счете приведет к уменьшению электростатического притяжения ионов S2O2 и [Ag(S2O3)2]3“ и более быстрому удалению их из фотослоя и фотоподложки. Использование сульфитной ванны позволяет сократить продолжительность окончательного промывания фотобумаг на 70-80 % по сравнению с промыванием по обычной схеме. Необходимо помнить, что в случае цветных фотоматериалов при pH слоя более 7,0 наблюдается уменьшение стабильности красителей, поэтому после промывания следует стабилизирующая ванна с pH = 5,Олб,0.
Особое внимание необходимо уделять промыванию фотоотпечатков на плотной картонной подложке, т. к. она поглощает вдвое больше компонент фиксирующего раствора, чем тонкая подложка, что требует соответственно более продолжительной промывки (-30-45 мин).
Что касается температуры промывной воды, то необходимо отметить, что обычно с ростом температуры продолжительность процесса промывания существенно сокращается. Однако нужно помнить и о том, что при
увеличении температуры промывной воды происходит увеличение набухания желатина эмульсионного слоя, а это может привести к замедлению процесса промывания. Современные высокозадубленные тонкослойные фотоматериалы позволяют использовать высокую температуру промывной воды (от 27 до 38 °C), что существенно сокращает как окончательную, так и промежуточные промывки, целью которых является частичное удаление из эмульсионного слоя избытков компонент соответствующих обрабатывающих растворов, что препятствует их занесению в последующие ванны.
Продолжительность окончательного промывания определяется максимально допустимой концентрацией тиосульфата натрия Na2S2O3 • 5Н2О в фотослое. Дж. Кребтри с сотрудниками на основании своих исследований еще в 1943 г. определил допустимые концентрации остаточного тиосульфата в фотослое различной фотопродукции, предназначенной для массового хранения (-20 лет) и архивного хранения (-80 лег), которые за последние десятилетия были существенно уточнены и дополнены (табл. 5.3.14).
Таблица 5.3.14
Допустимые концентрации тиосульфата натрия в фотослое (мг/см2)
Вид фотопродукции Вид хранения
массовое архивное
Черно-белый любительский негатив 0,023-0,039 0,008
Рентгеновский негатив 0,023-0,039 0,008
Черно-белый кинонегатив 0,03 0,0008
Черно-белый кинопозитив 0,006 0,0015
Дубль-позитив 0,003 0,0008
Микрофильм 0,003 0,0007
Цветной позитив 0,003
Цветной негатив 0,0007
Черно-белый фотоотпечаток на тонкой подложке 0,015-0,02 0,0
Черно-белый фотоотпечаток на картонной подложке 0,030-0,039 0,0
Данные таблицы свидетельствуют о том, что на фотоотпечатках при архивном хранении не должно быть остаточного тиосульфата, причем чем меньше размер исходного микрокристалла галогенида серебра в эмульсионном слое фотоматериала, тем меньше должна быть допустимая остаточная концентрация тиосульфата. Это обусловлено тем, что изображение, состоящее из высокодисперсного металлического серебра, разрушается (выцветает) быстрее, чем изображение из крупных серебряных частиц. Причем чем больше плотность изображения, тем больше адсорбция тиосульфата и комплексов на серебре и тем больше эффект выцветания.
886
Новый справочник химика и технолога
Полностью удалить тиосульфат из подложки баритованных фотобумаг практически невозможно, поэтому для понижения его концентрации применяют специальные разрушители тиосульфата. Наиболее эффективным составом в настоящее время является разбавленный раствор смеси пероксида водорода и аммиака, в который помещают фотоотпечатки после окончательной промывки на 4-5 мин, а затем (перед сушкой) еще раз промывают в проточной воде 5-6 мин. В этом случае разрушение тиосульфата в фотослое протекает согласно уравнению:
Na2S2O3 + 4Н2О2 + 2NH4OH ->
-> Na2SO4 + (NH4)2SO4 + 5Н2О (5.3.67)
5.3.4. Процесс отбеливания
При химико-фотографической обработке фотоматериалов по методу черно-белого обращения, а также цветных кинофотопленок и цветных фотобумаг необходимо удалять из фотослоя металлическое серебро, которое возникает в процессе проявления и в дальнейшем маскирует цветное изображение. Для этих целей применяют процесс отбеливания, в результате которого металлическое серебро в фотослое переводится в соединения, растворимые в тиосульфате натрия.
Отбеливание можно представить как окислительно-восстановительную реакцию, обратную реакции проявления:
отбеливание(окисление)
Ag < ' 'е ...... > Ag"
_е проявление (восстановление)
В этой связи процесс отбеливания можно описать, применяя электродную теорию. В случае химической кинетики скорость процесса отбеливания будет определяться разностью потенциалов A£’ = £'Ox/Red-£' ,/Ag; при этом окислительно-восстановительный потенциал £Ox/Red Должен быть всегда более положительным, чем потенциал ^Ag./Ag (рис. 5.3.17, случай 4). С увеличением концентрации окислителя и понижением pH среды для некоторых окислителей (бихромата, хинона, перманганата) (табл. 5.3.15) потенциал окислительной системы становится более положительным.
Потенциал серебряной системы в свою очередь, согласно уравнению Нернста, становится более отрицательным с понижением концентрации ионов серебра в отбеливающем растворе:
£ =0,80 + 0,0581gC (5.3.69)
Учитывая эти обстоятельства, для ускорения процесса окисления металлического серебра в отбеливающий раствор вводят вещества KBr, КО, KI и другие, анионы
которых связывают ионы серебра в труднодиссоциируе-мые соединения. В этом случае происходит понижение концентрации свободного серебра в реакционном объеме, а потенциал серебряного электрода становится более отрицательным и определяется уравнением:
=°А0 + — (IgL-lgC^,,), (5.3.70)
где п — валентность аниона; L — произведение растворимости соединения; — концентрация аниона.
Часто в качестве активаторов процесса окисления металлического серебра в отбеливающий раствор вводят комплексообразователи, такие, как KNCS, Na2S2O3, Na2SO3 и т. д., которые резко понижают в растворе концентрацию свободных ионов серебра, что и способствует смещению потенциала серебра в сторону отрицательных значений и ускорению процесса отбеливания. При этом чем больше константа устойчивости серебряного комплекса, тем более отрицательным становится потенциал серебра (табл. 5.3.16), а соответственно больше разность потенциалов ДЕ = EOx/Red _^А • /Ag и тем активнее протекает процесс окисления металлического серебра.
Таблица 5.3.15
Потенциалы некоторых окислителей металлического серебра
Окислитель ^Ох/Red’ B
К2Сг2О7 1,33-0,138 pH
K3Fe(CN)6 +0,36
K2s2o8 +2,01
KMnO4 1,65- 0,079 pH
Хинон (Q) 0,70-0,059 pH
Fe(III)EDTA* + 0,117
CuBr2 + 0,159
Co(IlI) + 1,79
*Мононатриевожелезная соль этилендиаминтетрауксусной кислоты.
Таблица 5.3.16
Влияние природы комплексообразователей на потенциал серебра (по А. Рабиновичу)
c ^AgNO, ’ ММОЛЬ E Чк ’MB Ag /Ag’
Без KOM-плексооб-разователя 0,1 моль NH3 0,1 моль Na2SO3 0,1 моль Na2S2O3 0,1 моль KCN
0,2 +590 +280 +250 -68 -490
1,0 +630 +322 +294 -26 -467
2,0 +648 +340 +315 -8 -455
Химия фотографических процессов
887
Окисление серебра феррицианидом, бихроматом, персульфатом и комплексной солью Fe(III) • EDTA
В практике черно-белой фотографии для отбеливания металлического серебра широкое распространение получили бихромат калия К2Сг2О7 и бихромат аммония (NH4)2Cr2O7, которые хорошо окисляют серебро только в кислой среде (pH = 3,04-3,5), с довольно высокой скоростью, задубливая при этом желатин эмульсионного слоя:
6Ag + Cr2O;~+14H+ >6Ag+ + 2Сг3* +7Н2О
(5.3.71)
В цветной фотографии бихромат, как правило, не применяют, т. к. в кислой среде при pH < 4,0 наблюдается обесцвечивание красителей в фотослое цветной пленки. В связи с этим для окисления металлического серебра, которое образовалось при цветном проявлении, используют наиболее распространенный окислитель — феррицианид калия (красная кровяная соль), — обладающий довольно высокой скоростью отбеливания при pH, близких к нейтральным, что предотвращает обесцвечивание красителей в процессе отбеливания. Феррицианид, окисляя металлическое серебро, восстанавливается до ферроцианида (желтая кровяная соль)
4K3[Fe(CN)6] + 4Ag—Ag4[Fe(CN)6] + 3K4[Fe(CN)6]
(5.3.72)
Как правило, отбеливающий раствор для обработки цветных фотоматериалов на основе феррицианида калия содержит довольно высокую концентрацию бромида калия (от 10 до 25 г/л), который способствует ускорению процесса и образованию в фотослое наряду с Ag4[Fe(CN)6] и бромида серебра, хорошо растворимого в тиосульфате натрия:
Ag + K3[Fe(CN)6 ] + KBr —> AgBr + K4[Fe(CN)6 ]
(5.3.73)
Кроме бромида калия в отбеливающий раствор с феррицианидом калия вводят однозамещенный фосфат калия (КН2РО4) и двузамещенный фосфат натрия (Na2HPO4), которые выполняют роль буфера, поддерживая pH отбеливающей системы на постоянном уровне в течение длительного времени.
В последнее время у специалистов, работающих в области обработки цветных фотоматериалов, особый интерес вызывают отбеливающие системы, применение которых позволяет не только интенсифицировать процесс отбеливания, но и решить важную проблему снижения загрязнения сточных вод за счет феррицианида и бихромата. В этой связи особое предпочтение специалистами отдается соединениям персульфата, которые являются бесцветными, обладают высоким окислитель
ным потенциалом (+2,01 В) и экологически безвредны. Однако, несмотря на высокий окислительно-восстановительный потенциал, персульфат до недавнего времени применяли только лишь в ослабляющих растворах, т. к. наличие двойного отрицательного электрического слоя на поверхности металлического серебра существенно тормозит диффузию дианиона персульфата к металлическому серебру, что и обусловливает неполное окисление серебра и очень медленное протекание процесса.
Для ускорения процесса отбеливания персульфатом в конце 1970 гг. фирма «Kodak» применила при обработке цветных позитивных кинопленок дополнительную ванну с ускорителем процесса, предшествующую отбеливающей ванне и содержащую тиоловые соединения, которые, адсорбируясь на поверхности металлического серебра, облегчают перенос электрона при окислении серебра и способствуют тем самым увеличению скорости процесса отбеливания. Правда, плохая адсорбция тиоловых соединений на поверхности металлического серебра, покрытой другими веществами, например тиосульфатом, и неприятный запах этих веществ вызывают определенные технологические трудности.
Исходя из того, что негативное изображение, плохо промытое после черно-белого проявления в гидрохиноновом проявителе, ослабляется в персульфатном ослабителе гораздо быстрее, чем хорошо промытое Г. Пол-лаковски и И. Кайлер предложили в качестве активатора процесса отбеливания применять хинон. После достижения устойчивого равновесия в системе «хинон «=* гидрохинон» (24 ч) персульфатные ионы окисляют металлическое серебро в широком интервале pH:
2Ag + K7S7O„ + Н2О -» Ag7O + K7SO4 + Н7SO4
Z Z Л Z *»«’Z z *+ z ч 5 7 И
Ag2O +H2SO4-> Ag2SO4 + H2O ( ’
Механизм действия хинонового активатора, согласно Дж. Уиллемсу, характеризуется супераддитивным эффектом и основан на преодолении двойного отрицательного электрического слоя на металлическом серебре. Хинон Q, адсорбируясь на металлическом серебре и имея более положительный окислительно-восстановительный потенциал, чем система Ag/Ag+, начинает окислять серебро, образуя при этом стабильный радикал — семихинон Q :
Ag + Q-> Ag1 +Q (5.3.75)
Семихинон, проникая внутрь отрицательного барьерного слоя, повышает адсорбцию дианиона персульфата на металлическом серебре и облегчает перенос электрона при окислении серебра. При этом дианион персульфата окисляет семихинон до хинона:
S20g +2Q —>2Q + 2SO4- (5.3.76)
888
Новый справочник химика и технолога
COO
COO—.Fe
3H2O
(5.3.77)
Как показали исследования, однованные хинон-персульфатные отбеливающие растворы Г. Поллаков-ски с успехом могут быть применены для обработки не только цветных позитивных, но и негативных и обращаемых кинофотоматериалов.
С экологической точки зрения особый интерес вызывает у специалистов, работающих в области фотографии, применение в качестве окислителя металлического серебра железной комплексной соли этилен-диаминтетрауксусной кислоты (Fe(III) • EDTA):
СН2—
СН2— W
Х:н2—
СН2— । СН2—W ^СН2—(
Правда, низкий окислительно-восстановительный потенциал не позволяет проводить процесс отбеливания металлического серебра с высокой скоростью. Поэтому, как правило, комплексную соль Fe(III) • EDTA применяют в основном в комбинированных отбели-вающе-фиксирующих системах. Объединение отбеливания и фиксирования в одну операцию позволяет существенно упростить и ускорить процесс отбеливания Fe(IlI) • EDTA в присутствии специальных активаторов, таких как тиомочевина, тиосемикарбазид, тиоцианат, которые снижают концентрацию серебра в реакционном объеме за счет образования устойчивых комплексов, что и сдвигает потенциал £А >/А в сторону отрицательных значений.
Впервые отбеливающе-фиксирующие растворы на основе Fe(III) • EDTA для обработки цветных фотобумаг были предложены в Германии в 1944 г. В. Шнайдером.
В настоящее время почти все фотографические фирмы для обработки цветных фотобумаг применяют в основном отбеливающе-фиксирующие растворы на основе Fe(III) EDTA (табл. 5.3.17). Замена тиосульфата натрия в отбеливающе-фиксирующем растворе на тиосульфат аммония позволяет существенно повысить активность систем.
Процесс отбеливания металлического серебра и процесс фиксирования в отбеливающе-фиксирующем растворе протекают почти одновременно. Суммарное уравнение реакции можно представить следующим образом:
Ag + Na[Fe(III) • EDTA] + п Na2S2O3 -> феррикомплекс
(5.3.78)
-> Na2[Fe(II).EDTA] + Na2„_1[Ag(S2O3)„]
феррокомплекс
Персульфатный отбеливающий раствор: персульфат аммония — 8,5 г; бромид калия — 20,0 г; натрий уксуснокислый — 4,5 г; уксусная кислота — 15 мл; гидрохинон — 1,0 г; сульфат меди — 1,50 г; вода — до 1 л; pH = 3,7 ± 0,2.
Необходимо заметить, что феррокомплекс, который образуется в процессе отбеливания, спонтанно реагирует с кислородом воздуха и окисляется до ферриком-плекса:
2Na2[Fe(II)EDTA] + XO2 +Н2О ->
->2Na[Fe(III)EDTA] + 2NaOH ( '
Таким образом, перемешивая отбеливающе-фиксирующий раствор кислородом или воздухом, его можно очень просто регенерировать, то есть поддерживать на постоянном уровне концентрацию ферриком-плекса, которая и определяет в значительной мере скорость процесса отбеливания.
От величины pH раствора существенно зависят активность и стабильность отбеливающе-фиксирующей системы. Так, чем ниже значение pH, тем выше окислительно-восстановительный потенциал системы и тем меньше стабильность раствора в связи с тем, что в кислой среде происходит разложение тиосульфата натрия с образованием серы:
S2O3 + Н+ -> HSO3 + S Ф (5.3.80)
Добавление сульфита натрия в отбеливающе-фиксирующий раствор стабилизирует его и предотвращает образование серы. Увеличение же pH раствора (более 7,0) понижает оксилительно-восстановительный потенциал и скорость процесса отбеливания; при этом за счет окисления производных п-фенилендиамина в отбеливающем растворе при данном значении pH может происходить образование цветной вуали на фотоотпечатке.
Серьезной технической проблемой сегодня при использовании отбеливающе-фиксирующих растворов для обработки цветных фотобумаг, содержащих в качестве окислителя Fe(III) • EDTA, является извлечение серебра. Самым эффективным методом регенерации серебра в настоящее время является электролитический метод, который осуществляют при интенсивном перемешивании раствора и сверхвысоких плотностях тока (6,5-9,7 А/дм2), чтобы исключить влияние присутствующего в растворе окислителя металлического серебра, т. к. при низких и средних плотностях тока скорость осаждения металлического серебра на катоде не превышает скорости отбеливания. Схема установки электролитического извлечения серебра приведена на рис. 5.3.26.
В процессе электролиза отбеливающе-фиксирующего раствора на катоде протекают следующие реакции.
Диссоциация комплекса
AgS2O3“ —> Ag+ +S2O3’
Осаждение серебра
Ag+ +е—> Ag
Образование сульфита
S2O32" + 2ё -> SO32’ + S2- (5.3.81)
Химия фотографических прогрессов
889
Таблица 5.3.17
Рецептура отбеливающе-фиксирующих растворов для обработки цветных фотобумаг
Компоненты Фотобумага «Фотоцвет» (Ф-2, Ф-4, Ф-9) Фотобумага «FORMACOLOR» (FL-153) Фотобумага «ORWO-COLOR» (ORWO-168) Фотобумага фирм «Kodak» «Fuji» «AGFA-Г еверт» Фотобумага обращаемые фирм «Kodak», «Fuji», «AGFA-Gevert»
Трилон Б, г 25,0 15,0 5,0 55,0 15,0 6,0
Fe(III) • EDTA, г FcCl3, г 60,0 40,0 50,0 25,0 40,0 40,0
Калий иодистый, г Натрий углекислый, г Натрий тетраборно-кислый (бура), г 30,0 20,0 2,0 10,0 2,0
Калий углекислый, г Аммиак (33% р-р), г Калий фосфорнокислый однозамещенный, г 15,0 30,0 12-14 мл
Сульфит натрия, г Бромид натрия, г 2,0 10,0 15,0 20,0 10,0
Тиомочевина, г 3,0 2,5
Тиосульфат натрия, г 280,0 170,0 150,0 125,0 170,0 200,0
Калий метабисульфит, г 5,0
Вода, до 1 л 1,0 1,0 1,0 1,0 1,0 1,0
рн 6,0 ± 0,3 6,0 ±0,3 6,8 ±0,1 7,2 ± 0,2 6,8 ± 0,2 7,1 ±0,1
Температура обработки, °C 20,0 25,0 25,0 20,0 32,0 32,0
Время обработки, мин 7,0 3,0 3,0 5,0-10,0 1,5 3,5
Рис. 5.3.26. Схема установки SilvBAC-BF электролитического извлечения серебра и регенерации отбеливающе-фиксирующого раствора:
1 — баки проявочной машины; 2 — фильтр; 3 — бак-сборник; 4 — электролизер; 5 — устройство, контролирующее аэрацию; 6 — бак аэрации раствора; 7 — разбрызгиватель; 8-11 — насосы; 12 — бак регенерации; 13 — напорный бак;
14 — подача воздуха от компрессора
890
Новый справочник химика и технолога
Образование сульфида серебра
2AgS2O;- +S2’ -> Ag2S + 2S2O2”
Восстановление железа
Fe(III) • EDTA1- + ё -> Fe(II) • EDTA2-
Отбеливание серебра
Fe(III) • EDTA1' + Ag -> Ag+ + Fe(Il) • EDTA2-
B то время как на аноде протекают реакции:
Окисление железа
Fe(II)EDTA2- Fe(IIl)-EDTA1 +е
Образование тетратионата
2S2O2-—> S4O2-+ё (5.3.82)
Сверхвысокая плотность тока не только обеспечивает на катоде протекание реакции осаждения серебра, а на аноде окисление феррокомплекса в феррикомплекс, но и практически исключает образование сульфида серебра. Правда, часть тока расходуется на восстановление железа на катоде, что снижает эффективность выхода серебра по току. Концентрация серебра в растворе во время электролиза понижается с 2,5-4,6 г/л до 0,5-1,0 г/л. Ряд фирм при электролизе для более стабильного восстановления серебра на катоде рекомендуют поддерживать общую концентрацию железа в пределах 8-12 г/л, а концентрацию бисульфита натрия — 7 г/л и более при pH отбели-вающе-фиксирующего раствора > 7,2. Серебро, восстанавливаемое на катоде, имеет коричневый цвет и содержит ~96 % чистого продукта. Что касается конструкции электролизера, то наиболее удачной специалисты многих фирм считают установку, имеющую вращающийся цилиндрический катод.
5.4. Цветная фотография
5.4.1. Цветоделение и способы цветоделительной съемки
Любой цветофотографический процесс представляет собой три стадии: цветоделение, промежуточные (градационные) процессы и синтез цвета. В процессе цветоделительной съемки цветной объект с помощью зональных светофильтров (синего, зеленого и красного) или другими приемами можно разделить на три оптических изображения, содержащих синюю, зеленую
*В качестве зональных светофильтров можно рекомендовать комбинацию цветных стекол из каталога, выпускаемого промышленностью: синий (стекла СС-4 толщиной 5 мм и СЗС-18 толщиной 2 мм), зеленый (стекла ЖС-18 толщиной 3 мм и СЗС-18 толщиной 3 мм), красный (стекло КС-14 толщиной 2 мм).
и красную информацию. На первом этапе цветоделительную съемку проводили на черно-белую изопанхро-матическую пленку. После ее химико-фотографической обработки получали три черно-белых цветоделенных негатива.
Цветоделение осуществляли несколькими способами. Например, последовательной съемкой объекта одной фотокамерой за тремя зональными светофильтрами. При этом фотокамера и объект должны быть неподвижны. Такой метод цветоделительной съемки име-ег недостаток — временной параллакс — и применяется в основном в полиграфической промышленности. Цветоделительную съемку можно осуществить и другим способом: съемкой объекта тремя фотокамерами за зональными светофильтрами. В этом случае исключается временной параллакс, но имеет место другой недостаток — пространственный параллакс. Только съемка одной фотокамерой со светорасщепляющей системой (рис. 5.4.1) с помощью полупрозрачного зеркала позволяет одновременно экспонировать за светофильтрами три негативные кинопленки, что исключает полностью временной и пространственный параллаксы. Правда, этот способ цветоделительной съемки имеет ряд недостатков, таких, как значительное ослабление света и различные уровни экспозиции в кадровом окне фотокамеры, необходимость синхронного протягивания трех пленок в фильмовом канале, трудность совмещения изображений из-за различной усадки основы кинопленок.
Рис. 5.4.1. Схема фотокамеры фирмы «Техниколор» со светорасщепляющей системой для одновременного получения трех цветоделенных негативов: объектив (0); панхроматический (/), несенсибилизированный (2), ортохроматический (3) фотоматериалы; зеленый (4) и пурпурный (5) светофильтры; полупрозрачное зеркало (б)
Цветоделение можно осуществить также, используя гри фотоматериала, имеющих различную спектральную светочувствительность к синей, зеленой и красной областям видимого спектра.
Однако во всех рассмотренных случаях мы имеем дело с тремя цветоделенными негативными и позитивными изображениями, которые на какой-то определенной стадии процесса необходимо совмещать. Полностью избавиться от трудностей, которые возникают при
**Параллакс — изменение визуального положения объекта при съемке его с двух точек, расположенных на определенном расстоянии друг от друга.
Химия фотографических процессов
891
совмещении цветоделенных изображений на трех пленках, можно только за счет нанесения трех эмульсионных слоев различной спектральной чувствительности на одну прозрачную основу, т. е. провести цветоделение с помощью цветной многослойной пленки. Это явилось в свое время крупным шагом вперед, несмотря на технологические трудности, возникшие при изготовлении цветных фотоматериалов, эмульсионный слой которых должен иметь толщину, одинаковую с эмульсионным слоем черно-белых материалов.
5.4.2. Синтез цвета. Аддитивный и субтрактивный методы
В фотографии существуют два метода синтеза цвета: аддитивный (additio — сложение) и субтрактивный (subtrahere — вычитание). Аддитивный метод синтеза цвета предусматривает использование черно-белых цветоделенных позитивов. При этом совмещают не сами цве-тоделенные изображения, а их проекции на экране, причем световой поток в проекторах должен быть окрашен в цвет светофильтра, за которым велась съемка. Таким образом, при аддитивном синтезе используют черно-белые цветоделенные позитивные изображения, а функцию создания цвета в суммарном изображении несут те же съемочные зональные светофильтры, которые применяют при цветоделительной съемке.
В результате наложения друг на друга двух световых потоков, окрашенных в синий, зеленый или красный цвета, мы можем получить в зависимости от интенсивности световых потоков дополнительные цвета различных цветовых оттенков:
Желтый = Зеленый + Красный
Пурпурный = Синий + Красный
Голубой = Синий + Зеленый
При наложении друг на друга трех световых потоков, окрашенных в синий, зеленый, красный цвета, получим белый цвет. Белый цвет можно также получить смещением двух световых потоков, окрашенных в синий и желтый, в зеленый и пурпурный, в красный и голубой цвета.
Два цвета называют дополнительными друг к другу (синему — желтый, зеленому — пурпурный, красному — голубой), если они при аддитивном синтезе дают белый.
Аддитивный метод получил развитие в основном при разработке различных модификаций растровых методов цветной фотографии.
При субтрактивном синтезе для получения окончательного суммарного цветного изображения совмещают друг с другом цветоделенные позитивы; при этом они должны быть не черно-белыми, а окрашенными в цвет, дополнительный цвету светофильтра, за которым они были получены, т. е. цветоделенные позитивы окрашивают в желтый, пурпурный и голубой цвета.
Если при аддитивном синтезе желтый, пурпурный и голубой цвета образуются за счет сложения излучений
(световых потоков), окрашенных в основные цвета (синий, зеленый и красный), то при субтрактивном синтезе, например, желтый цвет получают за счет вычитания из белого светового потока синих лучей, а пурпурный и голубой цвета — за счет вычитания, соответственно, зеленых и красных лучей:
Желтый = Белый — Синий
Пурпурный = Белый — Зеленый
Голубой = Белый — Красный
Основные же цвета при субтрактивном синтезе получают в результате вычитания из белого потока двух основных цветов. Практически это можно осуществить с помощью наложения друг на друга двухзонных светофильтров (желтого, пурпурного и голубого), которые помещают в различных сочетаниях на пути белого светового потока.
Если на пути белого светового потока поставить пурпурный и голубой светофильтры, то получим синий цвет, т. к. пурпурный светофильтр задержит зеленую составляющую видимого спектра (500-600 нм), а голубой задержит красную составляющую (600-700 нм). В конечном счете, через эти два светофильтра пройдут только синие лучи. Другие основные цвета мы можем получить, используя следующие комбинации двухзонных светофильтров, которые необходимо поставить на пути белого светового потока:
Желтый + Голубой = Зеленый
Желтый + Пурпурный = Красный
Желтый + Пурпурный + Голубой = Черный
5.4.3. Технические методы цветной фотографии
Пожалуй, самым первым техническим методом получения цветного изображения можно назвать автохромный процесс с нерегулярным растром братьев Люмьер, который был реализован на практике в 1907 г. во Франции и просуществовал до 1935 г. При разработке этого метода авторы руководствовались принципом: технические сложности производству, а простоту — потребителю. На стеклянную основу, покрытую липким подслоем из каучука, наносили мозаичный растр из крахмальных зерен одинакового размера (0,015 мм), окрашенных в синий, зеленый и красный цвета. Просветы между нерегулярно расположенными в один слой окрашенными зернами крахмала заполняли сажей. Затем нерегулярный растр защищали прозрачным водонепроницаемым слоем, на который сверху наносили панхроматический эмульсионный слой. Экспонирование автохромных фотопластин проводили через основу и нерегулярный цветной растр, а химико-фотографическую обработку— по методу черно-белого обращения.
Существовали и другие растровые методы цветной фотографии, в которых вместо водорастворимых крахмальных зерен применяли водонерастворимые зерна из искусственной смолы, окрашенные в синий, зеленый
892
Новый справочник химика и технолога
и красный цвета (фирма «AGFA») и расположенные хаотически (как в автохромном процессе). На смену растровой фотографии с нерегулярным растром пришла цветная фотография с регулярным растром, которая и сегодня находит широкое применение, т. к. позволяет получать в короткие сроки цветные изображения, очень близкие по цвету к оригиналу.
В 1930-40 гг. зародилась идея использования фотокамеры со светорасщепляющей системой для получения сначала трех черно-белых цветоделенных негативов, а затем окрашенных цветоделенных позитивов, которые после последовательного переноса на особую пленку, называемую бланк-филъмом, позволяли получать хорошее цветное изображение. Этот метод тиражирования цветных кинофильмов получил название гидротипия.
В основе гидротипного метода получения цветного изображения лежат бессеребряныс процессы, так называемые пигментные процессы. После получения трех черно-белых цветоделенных негативов печать осуществляли вначале на слоях из хромированного желатина, содержащего хромовые соли (К2Сг2О7). Под действием ультрафиолетового излучения в желатиновом слое возникали соединения хрома(Ш), которые задубливали желатин. При погружении экспонированного слоя из хромированного желатина в горячую воду в тех местах, где не действовал свет, желатин плавился при 40 °C, а в участках слоя, где в процессе экспонирования образовывалась высокая концентрация соединений хрома(Ш), происходило дубление желатина, что приводило к повышению температуры плавления слоя. В результате возникал рельеф вымывания. Затем полученный рельеф окрашивали в цвет, дополнительный цвету светофильтра, за которым велась съемка соответствующего черно-белого цветоделенного негатива. После окраски рельефа в водорастворимых красителях желтого, пурпурного и голубого цветов получали три цветоделен-ные матрицы, которые последовательно переносили на бланк-фильм. В процессе совмещения и последовательного контакта окрашенных матриц и бланк-фильма за счет диффузии красителей из матриц на бланк-фильме возникало цветное позитивное изображение.
В дальнейшем рельеф вымывания стали получать, применяя вместо хромированного желатина специальные матричные галогенсеребряные пленки с незадуб-ленным эмульсионным слоем. Существует несколько методов получения рельефа. Один из них — проявление матричной пленки пирогаллоловым дубящим проявителем. В процессе проявления происходит образование в экспонированных участках слоя окисленной формы пирогаллола, которая задубливает желатин. При этом высота желатинового рельефа будет пропорциональна концентрации в слое окисленной формы пирогаллола.
Другой метод предусматривает проявление матричной пленки обычным проявителем, например фенидонгидрохиноновым, а отбеливание изображения осуществляют в отбеливающем растворе на основе хромовых солей аммония. В процессе отбеливания металли
ческого серебра возникают соединения хрома(Ш), которые задубливают желатин в тех местах, где идет окисление металлического серебра; высота рельфа в этом случае будет пропорциональна величине оптической плотности изображения и концентрации хрома(Ш).
Этот метод получения цветного изображения на первом этапе обеспечивал хорошие результаты, хотя при этом необходимо было преодолевать большие технические сложности, такие, как съемка специальной камерой со светорасщепляющей системой, исключительная точность совмещения трех изображений при переносе и т. д.
Наиболее перспективными техническими способами цветной фотографии сегодня являются все же негативно-позитивный и обращаемый цветофотографические процессы, которые имеют по сравнению с другими методами ряд существенных преимуществ, таких, как простота цветоделения, съемка обычной фотокамерой, автоматическое совмещение окрашенных цветоделенных изображений и т. д.
5.4.4. Цветное проявление. Особенности строения и обработки цветных фотоматериалов
Открытие реакции цветного проявления позволило Р. Фишеру заложить основы нового цветного фотографического процесса, который в дальнейшем превзошел все известные. В галогенсеребряные эмульсии, зонально чувствительные к синей, зеленой и красной частям спектра и нанесенные на общую основу, Р. Фишер предложил вводить различные по строению бесцветные недиффундирующие цветообразующие компоненты. В процессе проявления такого экспонированного фотоматериала производными и-фенилендиамина в эмульсионном слое происходит образование нерастворимых красителей, по цвету дополнительных максимуму спектральной чувствительности зональных эмульсионных слоев. В синечувствитсльном эмульсионном слое в этом случае образуется желтый краситель, в зеленочувствительном — пурпурный, а в красночувствительном — голубой. Для правильного цветоделения и значительного уменьшения светочувствительности к синим лучам среднего, ортохроматического эмульсионного слоя и нижнего, панхроматического было предложено наносить между верхним синечувствительным и двумя нижними зональными слоями желтый фильтровый слой из коллоидного серебра, который поглощает практически все синие лучи и становится прозрачным в процессе обработки фотоматериала. Для устранения диффузии цветообразующих компонент из слоя в слой между зональными светочувствительными эмульсионными слоями при изготовлении фотоматериала наносят очень тонкие прозрачные промежуточные желатиновые слои толщиной 1-2 мкм.
Перед поливом в галогенсеребряную эмульсию в зависимости от ее спектральной чувствительности вводят различные по природе бесцветные цветообразующие компоненты, представляющие собой сложные органические соединения, которые за счет наличия в молекуле
Химия фотографических процессов
893
длинных углеводородных цепей — от Си до С]8 — и адсорбции на желатине трудно диффундируют из одного слоя в другой. Компоненты, содержащие в своей молекуле гидрофильные группы —СООН и —SO3H, хорошо растворяются в водных растворах щелочей, что позволяет легко их вводить перед поливом в галогенсеребряную эмульсию. Такие цветообразующие компоненты называются гидрофильными.
В качестве компонент, образующих в процессе проявления и-фенилендиамином желтый краситель, чаще всего применяют органические соединения, содержащие метиленовую группу —СН2—, связанную с двумя карбонильными группами. Цветообразующис компоненты, образующие пурпурный краситель, имеют также метиленовую группу, правда, входящую в состав гетероциклического ядра. Что касается компонент, образующих голубой краситель, то это чаще всего соединения типа фенолов и 1-нафтолов, имеющих в молекуле метиновую группу =СН-
В качестве примера гидрофильных компонент могут служить:
желтая гидрофильнфя компонента Ж-2
СООН
СООН
(5.4.1)
пурпурная гидрофильная компонента П-6
О
с6н5
голубая гидрофильная компонента Г-1
ОН
(5-4.3)
* Термины «гидрофильный» и «гидрофобный» характеризуют наличие или отсутствие способности у веществ связывать воду или смачиваться водой.
Для исключения диффузии цветообразующих компонент из одного эмульсионного слоя в другой почти все фотографические фирмы начали недавно применять вместо гидрофильных так называемые гидрофобные защищенные компоненты, которые имеют алкильную цепь малой молекулярной массы и в молекуле которых отсутствуют гидрофильные группы —СООН и —SO3H, что и делает их практически нерастворимыми в растворах щелочей. Эти цветообразующие компоненты растворяют в высококипящих органических растворителях (например, смеси дибутилфталата и трифенилфосфата), не смешиваемых с водой, затем механически диспергируют в желатине в присутствии смачивателя на ультразвуковом диспергаторе до размера частиц 0,1-0,3 мкм и вводят в галогенсеребряную эмульсию. В этом случае цветообразующая компонента находится в специальной оболочке, что и предотвращает его взаимодействие с желатином эмульсионного слоя. Примером таких компонент являются:
пурпурная защищенная компонента ЗП-7
пурпурная защищенная компонента ЗП-7
*) сн3
С5Иц(трст): ---с—СН2—СН3
СН3
(5.4.4)
голубая защищенная компонента ЗГ-2
(5.4.5)
Гидрофобным компонентам по сравнению с гидрофильными отдается сегодня предпочтение, т. к. первые почти не взаимодействуют с желатином эмульсии и при введении их в эмульсию не увеличивают ее вязкость. В случае же гидрофильных компонент происходит увеличение вязкости эмульсии, что вызывает большие технологические трудности при изготовлении цветных многослойных кинофотоматериалов.
Сравнивая реакции черно-белого и цветного проявления, можно заметить, что первой стадией в обоих случаях является восстановление экспонированного серебра и образование металлического серебра. В процессе черно-белого проявления окисленная форма гидрохинона связывается сульфитом натрия, концентрация которого в проявителе колеблется обычно от 30 до 125 г/л. При цветном проявлении во время второй стадии процесса образуется краситель за счет взаимо
894
Новый справочник химика и технолога
действия окисленной формы производных и-фенилен-диамина и бесцветный цветообразующих компонент. Схему этих реакций можно представить следующим образом:
а) черно-белое проявление
AgBr + Red —> Ag + Ox + Br”
Ox + Na2SO3 -> Red SO3Na (5.4.6)
б) цветное проявление
AgBr + Red —> Ag + Ox + Br (5.4.7)
Ox + компонент —> краситель,
где Red — ион или молекула проявляющего вещества; Ох — окисленная форма проявляющего вещества; RedSO3Na — сульфопроизводное проявляющего вещества.
Краситель образуется в непосредственной близости от восстанавливаемого микрокристалла галогенида серебра, где очень высока концентрация окисленной формы производного w-фенилендиамина. Краситель обволакивает серебряную частицу и образует цветное облако (глобулу). Концентрация красителя будет пропорциональна количеству света, подействовавшего на фотоматериал. В связи с тем, что количество металлического серебра пропорционально экспозиции, а концентрация окисленной формы пропорциональна выделившемуся металлическому серебру, количество красителя будет пропорционально концентрации окисленной формы проявляющего вещества в эмульсионном слое.
Содержание сульфита натрия в цветном проявляющем растворе обычно не превышает 2,0-4,0 г/л, в противном случае увеличение концентрации сульфита резко понизит выход красителя в фотослое (за счет того, что сульфит активно связывает окисленную форму проявляющего вещества). Правда, в противоположность этому ряд зарубежных фирм предложил рецептуру цветного проявителя, содержащего сульфит натрия до 10 г/л, который обеспечивает получение хороших фотографических параметров без заметного снижения выхода красителя. Вероятно, выход красителя для новых классов цветообразующих компонент в меньшей мере определяется количеством присутствующего сульфита натрия, а зависит от соотношения скоростей образования красителя и сульфопроизводных проявляющего вещества. Применение новых высокоактивных цветообразующих компонент обеспечивает быстрое сочетание и образование красителя, подавляя при этом влияние сульфита.
Учитывая то обстоятельство, что после цветного проявления возникает и серебряное изображение, которое маскирует цветное перед фиксированием цветного фотоматериала применяют дополнительную операцию — отбеливание. В процессе отбеливания металлическое серебро переводится в галогенид серебра, который затем хорошо растворяется в растворе тиосульфата натрия; в фотографическом слое остается только красочное изображение.
Для увеличения сохраняемости и стабильной работы цветного проявителя кроме сульфита натрия дополнительно вводят еще и гидроксиламин (в концентрации не более 1,2 г/л), который является хорошим восстановителем. Повышение содержания гидроксиламина в проявителе приводит к восстановлению экспонированных микрокристаллов и уменьшению выхода красителя за счет того, что окисленная форма гидроксиламина не образует с компонентом красителя.
Образование красителя при цветном проявлении производными п-фенилендиаммнь происходит по следующей схеме:
проявляющее вещество
натиои-семихинона
ХИКОМДИИМЯЯ
аннон цветной лейкооокование
компоненты красителя
ХЯЯОНДИйМНН
нрасятвяь
Суммарную реакцию можно записать так:
ezx
C-Y —>
ЧН
(5.4.9)
Компоненты, образующие краситель по данной схеме, т. е. при отношении компонент : серебро, равном 1 : 4, называются четырехэквивалентными компонентами.
Химия фотографических процессов
895
В последнее время получили широкое распространение двухэквивалентные компоненты, которые образуют краситель при соотношении компонент : серебро, равном 1 : 2, т. е. для получения одной молекулы красителя необходимо восстановить не четыре, а два иона серебра. Суммарная реакция в этом случае имеет вид:
2 Ag* +HaN
+ C-Y
*2 4Z
Л’ nC
+ 2Н +
где Z«Cl, Вг, 8О3Н
(5.4.10)
Применение таких двухэквивалентных компонент позволяет резко снизить содержание галогенида серебра в эмульсионном слое цветных фотоматериалов.
При изготовлении современных негативных цветных кинофотоматериалов широкое распространение получили так называемые DIR-соединения (Development Inhibitor Releasing), отщепляющие при сочетании с хинондиимином ингибитор процесса проявления, что в конечном счете проводит к улучшению резкости негативного изображения и уменьшению его зернистости.
Когда DIR-соединения образуют в процессе реакции краситель, то его называют DIR-компонентой, а если бесцветное соединение — DIR-веществом. DIR-компо-нента отличается от обычного компонента тем, что она содержит в молекуле гетероциклическое соединение (1-фенил-5-меркаптотетразол или бензотриазол), которое в процессе сочетания отщепляется и замедляет процесс проявления как антивуалент:
(5.4.12)
Адсорбируясь на поверхности проявляемого микрокристалла, ингибитор проявления образует с галогенидом серебра соединения, которые восстанавливаются труднее, чем бромид серебра. Это приводит к неполному восстановлению микрокристаллов галогенида серебра, уменьшению диаметра зерен металлического серебра, что и обусловливает уменьшение размера цветного облака (глобулы) красителя вокруг серебряных зерен. Т. к. концентрация ингибитора в процессе проявления в участках слоя, получивших большие уровни экспозиций, будет довольно высока, то проявление замедляется не только в сильно экспонированных участках слоя, но и в смежных, слабо экспонированных за счет боковой диффузии в слое ингибитора процесса проявления. Это приводит к увеличению резкости края изображения на цветных фотоматериалах.
В некоторых случаях, например при изготовлении цветных обращаемых пленок, находят применение и DIR-вещества, синтезированные на основе гидрохинона, которые вводятся в эмульсионные и промежуточные слои фотоматериала и отщепляют ингибитор в процессе черно-белого проявления:
пурпурный краситель ингибитор проявления
(5.4.11)
Для существенного улучшения качества изображения ряд фирм применил DIR-компоненты с согласованием эффекта DIR во времени:
(5.4.13)
ОН
DIR-вещвсгво
896
Новый справочник химика и технолога
В настоящее время в технологии производства кинофотоматериалов широко применяют другой, очень эффективный способ уменьшения гранулярности (зернистости) цветного изображения, заключающийся в том, что зональные светочувствительные эмульсионные слои наносят на основу двумя или тремя полуслоями.
Верхний эмульсионный полуслой зонального эмульсионного слоя имеет более высокую светочувствительность по сравнению с нижним полуслоем (в 4-8 раз). При формировании зональных слоев цветного фотоматериала полуслоями наблюдают снижение гранулярности изображения и увеличение светочувствительности.
Так, негативный фотоматериал, изготовленный полуслоями и содержащий, кроме того, DIR-компоненту в полуслоях, обладает зернистостью, примерно в 2 раза меньшей, чем аналогичный материал, изготовленный традиционным способом.
Почти все современные негативные цветные фотоматериалы в ортохроматическом эмульсионном слое и панхроматическом содержат не бесцветные цветообразующие компоненты, а окрашенные в желтый или оранжевый цвет. В процессе проявления такие компоненты образуют соответствующий краситель, а оставшийся в слое непрореагировавшая компонента образует окрашенное в цвет компоненты позитивное изображение по отношению к пурпурному и голубому негативным изображениям. Этот прием направлен на улучшение цветопередачи изображения, и его называют внутренним маскированием. Окрашенные цвето-образующие компоненты, применяемые для этих целей, называют, соответственно, маскирующими компонентами. Образование красителя в случае маскирующей компоненты происходит по уравнению (5.4.14).
А,
маскирующая пурпурная компонента желтого цвета
(5.4.14)
Согласно патентным данным, эмульсионные слои современных цветных фотоматериалов, обладающие высокой светочувствительностью, содержат особый вид микрокристаллов галогенида серебра, так называемых плоских таблитчатых — Т-кристаллов (tabular, т. е. таблитчатый). Отличительная особенность Т-кристаллов состоит в том, что они гораздо меньше рассеивают свет, чем объемные кристаллы галогенида серебра, благодаря своему строению (рис. 5.4.2). Толщина Т-кристаллов составляет 0,01-0,03 мкм, а соотношение диаметра микрокристалла и его толщины колеблется в пределах от 100 : 1 до 500 : 1. По светочувствительности Т-крис-таллы не превосходят обычные кубические или другие объемные микрокристаллы галогенида серебра, но довольно большая поверхность Т-кристаллов делает их более эффективными при спектральной сенсибилизации, т. к. при одинаковой концентрации галогенида серебра они поглощают больше фотонов. Увеличение светочувствительности фотоматериала в случае Т-кристаллов не сопровождается утолщением эмульсионного слоя и ухудшением его структурно-резкостных свойств, как это имеет место при использовании обычных эмульсий, в связи с тем, что таблитчатые кристаллы в процессе проявления распадаются по линиям спайности на большое число мелких микрокристаллов.
В целях дальнейшего повышения светочувствительности цветных негативных фотоматериалов совсем недавно были предложены эпитаксиальные осаждения хлорида серебра на углах или вдоль ребер основных граней бромосеребряных Т-кристаллов (см. рис. 5.4.2),
что позволило увеличить число светочувствительности фотопленок до 1000 ISO*.
Фирма «AGFA-Gevert» при изготовлении своих цветных негативных фотоматериалов применяет структурированные кристаллы-близнецы (рис. 5.4.3), которые имеют меняющуюся химическую структуру от центра микрокристалла и его поверхности. Такие микрокристаллы галогенида серебра кроме достоинств, присущих Т-кристаллам, имеют еще повышенную реакционную способность к DIR-веществам, отщепляющимся в ходе реакции цветного проявления, что и приводит к усилению краевых эффектов и улучшению резкости цветного изображения.
Фирма «Fuji» при совершенствовании своих цветных негативных фотоматериалов применила микрокристаллы типа ядро-оболочка с двойниковой структурой DSG (Double Stuctured Grains). Ядро этих микрокристаллов содержит большое количество иодида серебра, а оболочка изготовлена чаще всего из бромида серебра (см. рис. 5.4.3). Галогенид серебра, расположенный на наружной оболочке двойникового микрокристалла, обеспечивает большой кван> овый выход при экспонировании, в то время как ядро микрокристалла в процессе проявления оказывает существенное влияние на размер серебряной частицы, что и обусловливает в дальнейшем низкий уровень зернистости цветного изображения при очень высокой светочувствительности фотоматериала — до 1600 ISO.
Определение светочувствительности цветных негативных фотопленок по ISO (International Standards Organisation).
Химия фотографических процессов
897
Рис. 5.4.2. Электронная микрофотография эмульсионных Т-кристаллов (а) и Т-кристалла из AgBr /1 с эпитаксами из AgCl (б). Светорассеяние (в) в случае обычного микрокристалла AgBr (/) и Т-кристалла (2)
Примером таких Super DIR-компонент может служить желтая компонента фирмы «Fuji»:
а
в
(5.4.15)
Отличительной особенностью современных цветообразующих компонент является повышенная устойчивость красителей к выцветанию. Так, у фотоматериалов фирмы «Fuji» сохраняемость цветного изображения определяется желтым красителем, а нс голубым, как у большинства негативных фотопленок, причем устойчивость голубого красителя к выцветанию примерно сто лет.
С целью увеличения светочувствительности цветных негативных фотоматериалов и улучшения гранулярности красочного изображения фирма «Fuji» предложила новый класс цветообразующих компонент, так называемых FR-компонент (Fog Releasing), т. с. отщепляющих вуаленты. В процессе реакции цветного проявления экспонированных кристаллов AgHal высвобождается FR-вещество (например, формилгидразин), которое способствует восстановлению соседних с проявляемыми кристаллами недостаточно экспонированных микрокристаллов галогенида серебра за счет образования на них центров вуали:
Рис. 5.4.3. Структурированные микрокристаллы-близнецы фирмы «AGFA-Геверт» (а) и микрокристаллы галогенида серебра с двойниковой структурой типа ядро — оболочка фирмы «Fuji» (б) и «Конисироку» (в): / -ядро: (AgBr/Agl); 2 оболочка (AgBr)
В последнее время ведущие фотсирафичсские фирмы применяют при изготовлении цветных негативных фотоматериалов так называемые Super D1R-компонеит, которые часто являются маскирующими. Введение Super DIR-компонент в эмульсионные слои негативных фотоматериалов приводит к понижению оптической плотности маски, что в дальнейшем облегчает процесс копирования на цветные позитивные фотоматериалы.
FR— вещество
нонен 2) 2-s- ch2-c-nh о
NH-NH-C^
Н
(5.4.16)
898
Новый справочник химика и технолога
Эффект вуалирования наблюдается в основном в участках фотослоя, получивших определенные уровни экспозиций. Зернистость цветного изображения при этом не возрастает, т. к. повышение оптической плотности изображения происходит за счет увеличения числа восстановленных кристаллов в фотослое. FR-kom-поненты вводят как в соседние зональные, так и в промежуточные желатиновые слои. К недостаткам такого вида компонент необходимо отнести неизбиратель-ность вуалирования микрокристаллов галогенида серебра FR-соединениями, отщепляющимися в процессе проявления.
Для существенного повышения светочувствительности цветных негативных фотоматериалов и уменьшения зернистости изображения ряд фирм в последнее время применяет так называемые DAR-компоненты {Development Accelerator Releasing) — отщепляющиеся при образовании красителя ускорители процесса проявления. В присутствии DAR-компонент достигается очень высокая светочувствительность — до 1600 ISO — за счет того, что в ходе реакции цветного проявления отщепляются соединения, например анионы тиоцианата (реакция (5.4.17)), которые подрастворяют микрокристаллы галогенида серебра, получившие экспозицию на уровне «пороговой»:
(5.4.17)
Отличительной особенностью цветных негативных фотопленок повышенной светочувствительности — до 1000 ISO (VR-1000) — является отсутствие традиционного желтого фильтрового слоя. Это стало возможным за счет того, что в процессе спектральной сенсибилизации эмульсии, состоящей из плоских Т-кристал-лов, чувствительность к зеленой и красной областям спектра возрастает во много раз по сравнению с пониженной собственной чувствительностью эмульсии к сине-фиолетовой части спектра. Кроме того, введение в эмульсионный слой соединений, поглощающих ультрафиолетовые лучи, способствует дальнейшему улучшению качества цветопередачи изображения.
При изготовлении цветных негативных фотоматериалов применяют так называемые активные промежу
точные слои — ICL {Image Controlling Layer), — которые располагаются между высокочувствительными и низкочувствительными элементарными эмульсионными полуслоями и предотвращают проникновение образующегося в процессе проявления цветового облака из верхнего, высокочувствительного слоя в нижний, низкочувствительный, что способствует дополнительному улучшению структурно-резкостных свойств цветного изображения. Зернистость изображения высокочувствительной цветной негативной фотопленки, изготовленной полуслоями, при данном строении соответствует зернистости низкочувствительной эмульсии. Применение на практике рассмотренных выше эффектов позволило ведущим фотографическим фирмам выпустить на мировой рынок серию высокоразрешающих и высокочувствительных (до 1600 ISO) фотопленок типа HR (фирма «Fuji»), XR (фирма «AGFA»), SR (фирма «Конисироку»), VR (фирма «Kodak») для фотолюбителей.
С целью значительного уменьшения рассеяния света при изготовлении цветных негативных фотоматериалов сегодня применяют совершенно новый тип цветообразующих компонент, так называемых L-компонент {латексных компонент), являющихся синтетическим полимером, в котором водород замещен на хромофорные ipynribi:
(5.4.18)
Применение латексных компонент позволило значительно уменьшить толщину эмульсионных слоев негативных фотопленок (10-20 %), а также улучшить структурно-резкостные свойства цветного изображения за счет уменьшения рассеяния света в слое и более компактной формы красителя, образующегося в процессе цветного проявления.
Хорошая цветопередача и насыщенность цвета в широком интервале экспозиций у современных цветных фотоматериалов обеспечиваются точно выверенным балансом трех технологических приемов: применением не только маскирующих, но и DIR-компонент и DIAR-компонент {Development Inhibitor Anchimeric Releasing) с согласованием эффекта DIR во времени. DIAR-компоненты аналогичны DIR-компонентам, за исключением того, что они содержат «химический выключатель» ингибирующего действия. Это обстоятельство позволяет образовавшемуся ингибитору проявления продиффундировать из слоя довольно далеко, прежде чем он начнет тормозить восстановление сереб
Химия фотографических процессов
899
ра, а следовательно, и образование красителя. В случае DIAR-компоненты при проявлении полностью экспонированной пленки ингибиторы, образовавшиеся в сине-и зеленочувствительных слоях, диффундируют в глубину и тормозят проявление красночувствительного слоя; в свою очередь ингибитор из красночувствительного слоя, диффундируя в два других зональных слоя, тормозит проявление. В случае же, когда экспонирован один из зональных слоев, например зеленочувствительный, ингибитор проявления возникает только в одном слое, в то время как в сине- и красночувствительных слоях ингибиторы отсутствуют, что приводит к восстановлению большого количества серебра в зелено-чувствительном слое и, естественно, к повышению цветового контраста (насыщенности).
Хинондиимин, образующийся в процессе реакции цветного проявления, как установили японские ученые, может окислять центры скрытого изображения на микрокристаллах галогенида серебра и, расходуясь при этом, не принимает в дальнейшем участия в образовании красителя. Учитывая это обстоятельство, фирма «Fuji» при создании новых цветных кинопленок серии «F» (F-64, F-64D, F-125, F-250, F-500) освоила новые цветообразующие компоненты — Image Amplifier Release Coupler (компонента усиления — ослабления изображения). Эти цветообразующие компоненты в процессе цветного проявления выделяют вещества (усилители), которые защищают от разрушения (окисления) центры скрытого изображения, обеспечивая тем самым восстановление экспонированных микрокристаллов галогенида серебра и образование красителя, что приводит к повышению светочувствительности без ухудшения гранулярности.
Кроме того, фирма «Fuji» при производстве цветных негативных кинопленок применяет цветообразующие компоненты, формирующие подвижный краситель (Movable Dye Forming Coupler), которые перемещаются на незначительное расстояние в эмульсионном слое, обусловливая при этом уменьшение плотности облака красителя и повышение оптической плотности между глобулами красителя, а это в конечном счете приводит к заметному уменьшению гранулярности цветного изображения.
5.5. Основные химические соединения, применяемые в фотографии
Алюминий сульфат октадекагидрат
Сернокислый алюминий 18-водный
A12(SO4)3 • 18Н2О (М.М.*: 666,43).
Белый порошок, легко растворимый в воде. Является составной частью дубящих растворов и по своему действию подобен алюмокалиевым квасцам. Уменьшает гидролитическое разложение красителей в фотографическом слое цветных кинофотоматериалов.
’ М.М. — молекулярная масса.
Алюминий хлорид гексагидрат
А1С13 • 6Н2О (М.М.: 241,43).
Белый порошок, растворимый в воде. Применяется как составная часть дубящих фиксирующих растворов.
Амидол
2,4-Диаминофенол дигидрохлорид
1 -Гидрокси-2,4-диаминобензол гидрохлорид
А-140 (ОРВО)
(М.М. 197,06).
Бесцветные, при длительном хранении коричневые игольчатые кристаллы, легко растворимые в воде (25 г в 100 мл). Применяется в качестве очень активного проявляющего вещества в черно-белой фотографии. Начинает проявлять в кислой среде при pH ® 4,0. При обработке фотобумаг амидоловый проявитель обеспечивает получение изображения сине-черных оттенков. Сохраняемость амидоловых проявителей на открытом воздухе очень мала. Для увеличения срока их службы добавляют метабисульфит калия в концентрации 5-7 г/л.
2-Метил-А^ 4^V 4-диэтил бензол-1,4-диамин гидрохлорид
4-Амино-А,У-диэтил-3-метиланилин
4-Амино-А,У-диэтил-л/-толуидин
3-Метил-А,У-диэтил-я-фенилендиамин
Activol N 2 («Johnson»)
CD-2 («Kodak»)
Colour Developer 2 («Merck»)
Tolochrome («May and Baker»)
(M.M. 214,73).
Светло-серые кристаллы, растворимые в воде. Применяется в качестве проявляющего вещества при обработке цветных позитивных материалов фирм «Kodak», «Fuji», «AGFA-Gevaert» (процесс ЕСР-2).
А-{2-[(4-Амино-3-метилфенил)(этил)амино]этил}-метансульфонамид сульфат моногидрат
А-Этил-3-метил-А-(|3-метилсульфонамидоэтил)-я-фенилендиамин
4-Ам и но-А-этил-3-метил-А-ф-метилсульфономи-доэтил)-анилин
4-Амино-А-этил-А-(|3-метилсульфонамидоэтил)-ш-толуидин
CD-3 («Kodak»)
900
Новый справочник химика и технолога
17D («Fuji»)
Activol № 3 («Johnson»)
Mydochrome («Мау and Baker»)
Colour Developer 3 («Merch»)
Светло-серые кристаллы, растворимые в воде. Применяется в качестве проявляющего вещества при обработке цветных негативных, обращаемых кинофотоматериалов и цветных фотобумаг фирм «Kodak», «Fuji», «AGFA-Gevaert» (процесс ECN-2; VNF-I; «Ektaprint-2»; «Agfacolor Proccss-92»).
2-[(4-Амино-3-метилфенил)(этил)амино]этанол сульфат
2-Амино-5-[А-этил-А-(Р-гидроксиэтил)амино]то-луолсульфат
4-Амино-3-метил-А-этил-А-(Р-гидроксиэтил)анилин
2-[(4-Амино-л/-толил)этиламино] этанол
CD-4 («Kodak»)
21D («Fuji»)
Colour Developer 4 («Merck»)
Применяется в качестве нового, более активного проявляющего вещества при высокотемпературной обработке цветных негативных кинофотопленок фирм «Kodak», «Fuji», «AGFA-Геверт» (процесс С-41).
2-[(4-Аминофенил)(этил)амино|этанол 2-(л-Амиинофенил-А-этиламино)этанол 4-Амино-А-этил-А-(Р-гидроксиэтил)анилин л-Амино-А-этил-А-2-гидроксиэтиланилин n-V идроксиэтилэтиламиноанилин
Г идроксиэтилэтил-л-фениледиамин А-Этил-А-гидроксиэтил-л-фенилендиамин Этилоксиэтил-л-фенилендиамин
ЦПВ-2 (СССР)
Activol N 8 («AGFA»)
Activol X («Johnson») Color Developer-32 Dioxychrome
S-41 («Ferrania ЗМ»)
S-5 («Ansco»)
T-32 (OPBO)
H2N---(Y ------N
CH2CH2OH (M M 180 25)
Мелкий светло-серый порошок, легко растворимый в воде. Применялся в качестве проявляющего вещества при проявлении цветных фотобумаг типа «Фотоцвет», а также некоторых цветных обращаемых фотоматериалов (фирма «Анско»). Оказывает вредное воздействие на кожу человека, как и А,А-диэтилбензол-1,4-диамин, хотя менее токсичен.
4-Аминофенол гидрохлорид
л-Аминофенол гидрохлорид
НО ( ( —NH2-HC1
>----' (М.М. 145,59).
Светло-коричневые кристаллы, хорошо растворимые в воде (33 г в 100 мл). Применяется в качестве проявляющего вещества при проявлении черно-белых кинофотоматериалов. Является составной частью высококонцентрированного щелочного проявителя фирмы ОРВО «Родинал».
Аммоний хлорид
Аммоний хлористый
NH4C1 (М.М. 53,49).
Белые кристаллы, хорошо растворимые в воде (37,5 г в 100 мл). Применяется как составная часть быстрых фиксирующих растворов на основе тиосульфата натрия.
Аммоний дихромат
Аммоний бихромат
(NH4)2Cr2O7 (М.М. 252,07).
Желто-красные кристаллы, легко растворимые в воде (~35 г в 100 мл). Применяется при отбеливании, ослаблении, усилении и сенсибилизации слоев в случае пигментных и подобных копировальных процессах. Ядовит!
Аммоний пероксидисульфат
Аммоний персульфат
(NH4)2S2O8 (М.М. 228,20).
Бесцветные кристаллы, легко растворимые в воде (60 г в 100 мл). Применяется при ослаблении чернобелых негативов. В последнее время рекомендован рядом фирм в качестве окислителя металлического серебра при отбеливании цветных позитивных кинопленок.
Аммоний тиосульфат
(NH4)2S2O3 (М.М. 148,21).
Химия фотографических процессов
901
Бесцветные, легко растворимые в воде кристаллы (85 г в 100 мл). Применяется в качестве комплексообразователя в быстрых фиксирующих растворах в концентрации 100-150 г/л. Чаще всего находит применение в фотографической практике 58% раствор тиосульфата аммония (150-200 мл/л). 1 мл 58% раствора соответствует 0,78 г безводной соли.
Аммоний тиоцианат
Аммоний роданид
NH4SCN (М.М. 76,12).
Бесцветные, легко растворимые в воде кристаллы (170 г в 100 мл). Применяется как энергичный комплек-сообразователь при быстрой химико-фотографической обработке черно-белых фотоматериалов для фиксирования и стабилизации высокозадубленных эмульсионных слоев в концентрации 5-8 моль/л.
Аскорбиновая кислота
Витамин С
НО
Н0 0Н (М.М. 176,12).
Бесцветные кристаллы, хорошо растворимые в воде. Применяется в качестве проявляющего вещества при химико-фотографической обработке черно-белых фотоматериалов. Высокой скоростью восстановления галогенида серебра обладает изоаскорбиновая кислота:
НО
НО ОН
Продукты окисления аскорбиновой кислоты не реагируют с сульфитом натрия и не тормозят процесс проявления. Чаще всего она используется в комбинации с пирогаллолом, гидрохиноном и метолом.
АС-60 («AGFA»)
4-[(4-Аминофенил)(бутил)амино]бутан-1 -сульфоновая кислота
^Бутил-Аг-(4-сульфобутил)-«-фенилендиамин
4-(Аг-(о-Сульфобутил-Аг-бутиламино)анилин
Colour Developer 60 («Merck»)
h2n
CH2CH2CH2CH2SO3H
СН2СН2СН2СН3
(М.М. 300,42).
Применялся в качестве проявляющего вещества при обработке цветных фотобумаг фирмы «AGFA-Gevaert». Обеспечивает хорошую насыщенность цветного отпечатка.
Бензиловый спирт
Фен и л метано л
С6Н5СН2ОН (М.М. 108,14).
Почти бесцветная маслянистая жидкость с характерным запахом. Применяется при цветном проявлении цветных фотобумаг, обращаемых многослойных кинофотоматериалов с защищенными цветообразующими компонентами фирм «Kodak», «Fuji». Обеспечивает не только набухание синтетической оболочки из смолы, окружающей цветной компонент, но и хорошую ее проницаемость для проявляющего вещества и других компонентов проявителя в процессе обработки. Вводится в цветной проявляющий раствор в концентрации 5-25 мл/л. В фотографической практике применяют обычно 35% раствор бензилового спирта, для приготовления 100 мл которого берут 35 мл бензилового спирта, 45 мл диэтиленгликоля и 20 мл воды.
Бензол-1,4-диамин
1,4-Диаминобензол
1,4-Фенилсндиамин и-Фенилендиамин
(М. М. 108,14).
Белый порошок, растворимый в воде. Применяется в черно-белой фотографии в качестве проявляющего вещества при мелкозернистом проявлении, чаще всего вместе с глицином. Пороговое значение pH для бензол-1,4-диамина равно 6,25. Ядовит!
1,2,3-Бензотриазол
(М.М. 119,12).
Белые или светло-желтые кристаллы, трудно растворимые в воде, легко растворимые в метаноле или растворах щелочи. Применяется в качестве антивуалирующего вещества (в концентрации 0,05-2,0 г/л) в основном при быстрой высокотемпературной химикофотографической обработке или проявлении фотоматериалов, срок использования которых давно истек. Повышает контраст изображения.
Бензо-1,4-хинон
Бензохинон «-Бензохинон
Хинон
О
(М.М. 108,09).
902
Новый справочник химика и технолога
Желтые кристаллы, плохо растворимые в воде. Применяется в процессе ослабления или как активатор отбеливания цветных позитивных кинопленок с помощью пероксидисульфата аммония.
Борная кислота
Ортоборная кислота
Н3ВО3 (М.М. 61,83).
Бесцветный порошок без запаха, растворимый в воде (4,8 гв 100 мл). Применяется в проявляющих и фиксирующих растворах для увеличения их кислотноосновной буферности.
Гидразин сульфат
Диамид сульфат
H2N—NH2 • H2SO4 (М.М. 130,12).
Белые, водорастворимые кристаллы. Энергичный восстановитель. Применяется в черно-белой фотографии как добавка в проявитель, обеспечивающая высокую скорость процесса проявления. При черно-белом процессе обращения использование гидразина позволяет исключить операцию второго экспонирования (засветки). Ядовит!
Гидроксиламин сульфат
Гидроксиламин сернокислый
S-55 (ОРВО)
(NH2OH)2 • H2SO4 (М.М. 164,14).
Белые кристаллы, легко растворимые в воде. Применяется как добавка в цветной проявитель. В малом количестве (~ 1,2 г/л) совместно с сульфитом натрия обеспечивает высокую сохраняемость проявляющего вещества от окисления. При высоких концентрациях гидроксиламин используется в черно-белой фотографии как энергичное проявляющее вещество.
7У-(4-Г идроксифенил)глицин
и-Г идроксифенилглицин
Глицин («AGFA»)
и-Оксифениламиноуксусная кислота
G-141 (ОРВО)
НО---(( ---NHCH2COOH
(М.М. 167,16).
Белый кристаллический порошок, очень трудно растворимый в воде. Легко растворим в растворах щелочи. Глициновые проявители хорошо сохраняются, работают практически без вуали и обеспечивают хорошую проработку деталей в тенях и светах негатива. Глицин применяется в качестве проявляющегося вещества при физическом проявлении после фиксирования. Чувствителен к накоплению ионов брома в проявителе.
Гидрохинон
1,4-Дигидроксибензол
1,4-Диоксибензол
и-Диоксибензол
Н-142 (ОРВО)
H2Q (США)
Белые блестящие игольчатые кристаллы, хорошо растворимые в воде (6,5 г в 100 мл). Применяется как контрастно работающее проявляющее вещество в черно-белой фотографии большей частью в комбинации с метолом или фенидоном. Чувствителен к накоплению бромидов в проявителе. Пороговое значение pH для гидрохинона равно ~9,5.
2,6-Дигидроксиизоникотиновая кислота
2,6-Дигидроксипиридин-4-карбоновая кислота
Цитразиновая кислота
Citrazinic Acid
СООН
Является составной частью цветных проявляющих растворов при обработке обращаемых фотоматериалов. Предотвращает сильный рост максимальных плотностей и предназначается для уменьшения контраста изображения. Связывает избыток окисленной формы цветного проявляющего вещества и образует растворимый краситель, который удаляется из фотослоя в процессе промывки.
Динатрий дигидроэтилендиаминтетраацетат дигидрат
Динатриеван соль этилендиаминтетрауксусной кислоты двуводная
Трилон Б
Chelaton 111
EDTA-2Na
М-23 (ОРВО)
Sequestrene Na2
Trilon BF
NaOOCCH2 CH2COOH
\ /
N-CH2-CH2-N • 2H2O
HOOCffl/ 'cH2OOONa
Белое кристаллическое вещество, легко растворимое в воде (~9 г в 100 мл). Применяется для уменьшения жесткости воды, добавляется в черно-белый проявитель в концентрации 1-2 г/л. EDTA-2Na в присутствии гид
Химия фотографических процессов
903
роксиламина существенно снижает сохраняемость цветного проявителя, поэтому вместо него используют в цветном проявителе гексаметафосфат натрия. Является составной частью отбеливающе-фиксирующих растворов при отбеливании цветных фотобумаг солями Fe(III)EDTA-2Na образует с солями кальция, меди, железа, магния и другими элементами, стойкие и хорошо растворимые комплексы.
Ряд зарубежных фирм использует для аналогичных целей тетранатриевую соль этилендиаминтетрауксус-ной кислоты (EDTA-4Na; Sequestrene-ЗОА; Syntron В; Celon Е; Sequestrene Na 4) или этилендиаминтетраук-сусную кислоту (EDTA, Sequestrene АА; Trilon BS; Che-laplex II).
3,5-Динитробензойная кислота
Kodak Anti-Fog N 9
Применяется как антивуалент при цветном проявлении кинопленок по режиму ECN-2.
А^У-Диэтилбензол-!, 4-диамин
4-Амино-TV,/V-диэтиланилин
п- Ам и нод иэти ланил ин
и-Ам и ho-TV,TV-д иэти л ани л и н
п-Диэтиламиноанилин
Диэтил-и-фенилендиамин ЛТ,А-Диэтил-и-фенилендиамин ЦПВ-1 (СССР)
2D («Fuji»)
Activol N 6
Activol Н (Англия)
CD-I («Kodak»)
Genochrome («Мау and Baker») Gevadiamin («Gevaert») S-28 («Ferrania ЗМ»)
T-22 (OPBO);
TSS («AGFA»)
(M.M. 164,25).
Кристаллы светло-желтого или розового цвета, растворимые в воде. Применяется в качестве проявляющего вещества при цветном проявлении многослойных кинофотоматериалов, чаще всего в виде сернокислой соли (Т-22; TSS; S-28 Activol S; ЦПВ-1), а иногда и солянокислой (CD-I, Activol Н.). Требует осторожного обращения в процессе приготовления проявителя и работы с ним. Вызывает сильное раздражение кожи и экзему.
Железо(Ш) сульфат
Сернокислое железо
Феррисульфат
Fe2(SO4)3 (М.М. 399,88).
Белый или светло-серый порошок, легко растворимый в воде. Применяется как составная часть ослабителей и отбеливающе-фиксирующих растворов при обработке цветных фотобумаг.
Железо(Ш) хлорид гексагидрат
Феррихлорид
Хлорное железо
Ас-107 («AGFA»)
FeCl3 • 6Н2О (М.М. 270,30).
Светло-коричневые кристаллы, которые на открытом воздухе интенсивно поглощают влагу. В 100 мл воды легко растворяется 92 г. Применяется в качестве окислителя металлического серебра в отбеливающе-фиксирующих растворах при обработке цветных фотобумаг.
Железо(Ш) натрий этилендиаминтетраацетат тригидрат
Железная соль трилона Б
Мононатриевожелезная соль этилендиаминтетраук-сусной кислоты
EDTA-NaFe
Fe(III)EDTA
Sequestrene NaFe
Trilon Fe
N(CH2COO)2
112^ i
| Fe Na • 3H2O
НэС^
2 ^N(CH2COO )2
L (M.M. 421,09).
Коричневый или желто-зеленый порошок, легко растворимый в воде. Применяется для окисления металлического серебра в отбеливающе-фиксирующих растворах с тиосульфатом натрия при обработке цветных фотобумаг. EDTA-NaFe можно приготовить из трилона Б и хлорида железа(Ш) или сульфата желе-за(Ш). Для составления отбеливающе-фиксирующего раствора в 1 л воды растворяют 25 г хлорида железа(Ш) или 18,5 г сульфата жслеза(Ш) и 55 г трилона Б.
Калгон
Гомогенная механическая смесь гексаметафосфата (NaPO3) и пирофосфата натрия (Na4P2O7) в соотношении 1:1. Рекомендуется фирмой «Kodak» как составная часть цветных проявляющих растворов для уменьшения жесткости воды в концентрации ~2 г/л.
Калий бромид
Калий бромистый
КВг (М.М. 119,00).
904
Новый справочник химика и технолога
Белые, хорошо растворимые в воде кристаллы (65,8 г в 100 мл). Применяется в качестве антивуалирующего вещества при проявлении кинофотоматериалов. Является составной частью отбеливающих растворов, обеспечивая перевод металлического серебра в бромид серебра.
Калий гекса циан ид оферрат(П) тригидрат
Желтая кровяная соль
Калий гексацианоферрат(П)
Калий железистосинеродистый
Калий ферроцианид
K4[Fe(CN)6 • ЗН2О (М.М. 422,39).
Желтые кристаллы, хорошо растворимые в воде (25 г в 100 мл). Ядовит! Применяется как индикатор на соединения трехвалентного железа.
Калий гексацианидоферрат(Ш)
Калий гексацианоферрат(Ш)
Калий железосинеродистый
Калий феррицианид
Красная кровяная соль
K3[Fe(CN)6] (М.М. 329,24).
Красно-рубиновые кристаллы, легко растворимые в воде (44 г в 100 мл). Применяется в качестве окислителя металлического серебра при отбеливании, тонировании, усилении и ослаблении. Ядовит!
Калий гидроксид
Гидроокись калия
Кали едкое
КОН (М.М. 56,11).
Легко растворяется в холодной воде, с большим выделением тепла (112 г в 100 мл). Применяется в качестве щелочи в проявителе для быстрых и скоростных проявителей. На открытом воздухе интенсивно поглощает влагу. Хранится в стеклянных банках с резиновой пробкой. Водный раствор имеет сильнощелочную реакцию. Ядовит! Работать с защитными очками.
Калий дигидрофосфат
Калий дигидрогенфосфат
Калий фосфорнокислый однозамещенный
КН2РО4(М.М. 136,09).
Белые кристаллы или порошок, легко растворимый в воде (25 г в 100 мл). Применяется в отбеливающих растворах при обработке цветных многослойных фотоматериалов для поддержания постоянного значения pH в процессе работы.
Калий дихромат
Двухромовокислый калий
Калиий бихромат
К2Сг2О7 (М.М. 294,19).
Ярко-красные кристаллы, легко растворимые в воде (~12 г в 100 мл). Сильный окислитель. Ядовит! Применяется как составная часть ослабляющих и отбеливающих растворов при обработке черно-белых кинопленок по методу обращения. В процессе отбеливания серебра дубит желатин. Используется для изготовления хромированных желатиновых слоев.
Калий иодид
Калий иодистый
К1(М.М. 166,00).
Белые кристаллы, хорошо растворимые в воде (144 г в 100 мл). Применяется в качестве антивуалирующего вещества в концентрации, в 10 раз меньшей, чем бромид калия. Хорошо уменьшает вуаль на поверхности фотографического слоя. Часто используется при проявлении черно-белых негативных фотоматериалов и фотобумаг, срок хранения которых давно истек.
Калий карбонат
Калий углекислый
Поташ
К2СО3(М.М. 138,21).
Белый порошок, очень легко растворимый в воде (111,7 гв 100 мл). Применяется в проявляющих растворах в качестве основания. Хранится в хорошо закрытой стеклянной банке с резиновой пробкой.
Калий метабисульфит
Калий дисульфит
Калий пентаоксидодисульфат(2~)
Калий пироссрнистокислый
Калий пиросульфит
K2S2O5 (М.М. 222,32).
Бесцветные кристаллы, хорошо растворимые в воде (44,5 г в 100 мл). Применяется в кислых фиксирующих и останавливающих проявление растворах, иногда в концентрированных пирогаллоловых проявителях (как антиоксидант).
Калий пероксидсульфат
Калий персульфат
K2S2O8 (М.М. 270,32).
Бесцветные, очень трудно растворимые в воде кристаллы (0,5 г в 100 мл). Применяется при тонировании и ослаблении, а также регенерации (окислении) калия гексацианидоферрата(П) в калий гексацианидо-феррат(Ш).
Химия фотографических процессов
905
Калий тиоцианат
Калий роданид
Калий сульфоцианат
KSCN (М.М. 97,18).
Бесцветные, легко растворимые в воде кристаллы (217 гв 100 мл). Применяется в качестве комплексооб-разователя при скоростном фиксировании высокоза-дубленных тонкослойных материалов в концентрации 2-5 моль/л. Является составной частью первого чернобелого проявляющего раствора при обработке фотоматериалов по методу черно-белого и цветного обращения (2,5-6,0 г/л).
Калий фосфат
Калий фосфорнокислый трехосновный
Трикалий фосфат
К3РО4(М.М. 212,27).
Белые кристаллы, легко растворимые в воде (100 г в 100 мл). Применяется в качестве сильного основания в черно-белых и цветных проявляющих растворах.
Калий фосфорнокислый однозамещенный
(см. Калий дигидрофосфат)
Калий цианид
Калий цианистый
KCN (М.М. 65,12).
Белая соль, хорошо растворимая в воде (70 г в 100 мл). Является очень сильным ядом! На воздухе разлагается. Применяется только в специальных целях для фиксирования или в репродукционной технике для фиксирования коллодионных слоев.
Карбоксиметилцеллюлоза
кмц
Целлин
S (ОРВО)
ch2or
OR J
n R = H, CH2COONa
(M.M. 40000-250000).
Применяется как загуститель вязких проявляющих и фиксирующих растворов, а также при глянцевании фотоотпечатков (0,5% раствор). Легко набухает в холодной воде. При повышении температуры до 30-35 °C хорошо растворяется. Чаще всего используется натриевая соль КМЦ (NaKMLl). В водных растворах хорошо гидролизуется и применяется как поверхностно-активное вещество.
Квасцы алюмокалиевые
Алюминий калий сульфат додекагидрат
A1K(SO4)2 • 12Н2О (М.М. 474,39).
Бесцветные кристаллы или белый порошок, растворимый в воде (11,4 г в 100 мл). Применяется для дубления фотографических желатиновых слоев при фиксировании (pH = 3,5^-4,0).
Квасцы хромокалиевые
Калий хром(Ш) сульфат додекагидрат
CrK(SO4)2 • 12Н2О (М.М. 499, 40).
Темно-фиолетовые кристаллы, легко растворимые в воде (9 г в 100 мл). Применяются в качестве дубителя при дублении фотобумаг, фотопленок и в процессе фиксирования.
Магний сульфат гептагидрат
Магний сернокислый семиводный
MgSO4 • 7Н2О (М.М. 246,47).
Белые кристаллы, хорошо растворимые в воде (35 г в 100 мл). Применяется 2% раствор при обработке цветных обращаемых фотоматериалов для уменьшения набухания эмульсионного слоя в случае промывания мягкой водой. Ванна с сернокислым магнием должна следовать сразу же после проявления. Ополаскивание водой и короткая промежуточная промывка при этом исключаются.
Медь(П) сульфат пентагидрат
Медный купорос
Медь сернокислая пятиводная
CuSO4 • 5Н2О (М.М. 249,69).
Темно-голубые крупные кристаллы, хорошо растворимые в воде (42 г в 100 мл). Применяется в процессах тонирования, усиления и отбеливания.
4-(Метиламино)фенол сульфат
Монометил-и-аминофенол сульфат 4-Монометиламинофенол сульфат Метол
Elon («Kodak»)
М-143 (ОРВО)
Monol («Fuji»)
(М.М. 344,38).
Бесцветные частицы, растворимые в воде (8 г в 100 мл). В растворах сульфита натрия метол очень мало растворим (~2 г в 100 мл). Применяется в качестве проявляющего вещества при проявлении черно-белых фотоматериалов (как один, так и вместе с гидрохиноном). Начинает проявлять при pH ® 7,2. Мало чувствителен к накоплению ионов брома в проявляющем растворе.
906
Новый справочник химика и технолога
Метоловые проявители хорошо сохраняются. Максимальная скорость проявления в метол-гидрохиноновом проявителе обеспечивается при концентрации метола -28 % от содержания гидрохинона в растворе.
2-Метил-7У 4-(2-метоксиэтил)-7У 4-этилбензол-1,4-
диамин бис(4-метилбензолсульфонат)
4-Амино-?/-этил-?/-(Р-метоксиэтил)-л/-толуидин ди-ц-толусульфонат
CD-6 («Kodak»)
QH5
(М.М. 552,70).
Новое проявляющее вещество фирмы «Kodak». Применяется при высокотемпературной обработке цветных фотоматериалов фирм «Kodak», «Fuji».
Натрий ацетат
Натрий уксуснокислый
CH3COONa (М.М. 82,03).
Бесцветные прозрачные кристаллы, хорошо растворимые в воде (50 г в 100 мл). Совместно с уксусной кислотой выполняет роль буфера для поддержания на постоянном уровне pH стабилизирующих и дубяще-фиксирующих растворов.
Натрий гексаметафосфат
М-19
(NaPO3)6 (М.М. 611,77).
Белое кристаллическое вещество. Применяется в черно-белых и цветных проявляющих растворах для уменьшения жесткости воды в концентрации 2-4 г/л. Хорошо связывает ионы кальция, меди, железа, магния и образует при этом стабильные растворимые комплексы.
Натрий гидрокарбонат
Натрий бикарбонат
Натрий двууглекислый
Натрий кислый углекислый Сода питьевая
NaHCO3 (М.М. 84,01).
Белый порошок, растворимый в воде (~ 10 г в 100 мл). Применяется как составная часть проявителей, способствует повышению их кислотно-основной буферности.
Натрий гидроксид
Гидроокись натрия Едкий натр
Сода каустическая
NaOH (М.М. 40,00).
Белые пластинки или кусочки, легко растворяющиеся в воде (80 г в 100 мл), с выделением большого количества тепла. Применяется в качестве щелочи в проявляющем растворе при быстрой обработке (в концентрации 5-40 г/л). Очень гигроскопичное вещество. Хранится в банках с герметичной упаковкой. Водный раствор имеет сильнощелочную реакцию. Ядовит! При работе необходимо надевать защитные очки.
Натрий гидрофосфат додекагидрат
Натрий фосфорнокислый двузамещенный двенадцативодный
Na2HPO4 • 12Н2О (М.М. 358,14).
Бесцветные кристаллы, растворимые в воде (8 г в 100 мл). Совместно с фосфорнокислым однозамещенным калием выполняет роль буферной системы для поддержания на постоянном уровне величины pH отбеливающих растворов при обработке цветных кинофотоматериалов.
Натрий бисульфит
NaHSO3 (М.М.: 104,1).
Белый порошок, легко растворимый в воде (39 г в 100 мл), с сильным запахом сернистого газа. Применяется как составная часть кислых фиксирующих растворов. Препятствует разложению тиосульфата натрия при низких значениях pH. Можно получить из сульфита натрия и серной кислоты, причем первый берется в избытке.
Натрий дитионит дигидрат
Na2S2O4-2H2O (М.М. 210,14).
Белый легко растворимый в воде порошок (25,4 г в 100 мл). Энергичный восстановитель. Применяется для чернения изображения в процессе обработки кинопленок по методу черно-белого обращения вместо второго проявителя.
Натрий карбонат
Натрий углекислый
Сода
Na2CO3 (М.М. 105,99).
Белый порошок, легко растворимый в воде (21,5 г в 100 мл). Применяется в качестве щелочи в проявителях. Проявители на карбонате натрия обладают высокой кислотно-основной буферностью.
Натрий метаборат
NaBO2 • 2Н2О (М.М.: 101,83).
Химия фотографических процессов
907
Белые, легко растворимые в воде кристаллы (7 г в 100 мл). Применяется как щелочь в проявляющих растворах. Получается при сплавлении эквивалентного количества гидроксида натрия и тетрабората натрия: Na2B4O7 + 2NaOH = 4NaBO2 + Н2О.
Натрий сульфат
Глауберова соль
Натрий сернокислый
Na2SO4 (М.М. 142,04).
Бесцветные кристаллы, легко растворимые в воде (19,4г в 100 мл). Существенно уменьшает набухание эмульсионного слоя при химико-фотографической обработке. Является составной частью проявляющих растворов, работающих при высокой температуре окружающего воздуха (тропическое проявление).
Натрий сульфид нонагидрат
Сернистый натрий девятиводный
Na2S • 9Н2О (М.М. 240,18).
Бесцветные кристаллы, легко растворимые в воде (20 г в 100 мл). Применяется при тонировании и для чернения изображения в процессе черно-белого обращения (второе экспонирование при этом исключается). Химический процесс протекает по следующему уравнению: 2AgBr + Na2S —> Ag2S + 2NaBr. Храниться в темной стеклянной посуде с резиновой пробкой. Имеет резкий запах сероводорода.
Натрий сульфит
Натрий сернистокислый
Na2SO3 (М.М. 126,04).
Белый порошок, легко растворимый в воде (26,9 г в 100 мл). Применяется в проявителе в качестве антиоксиданта проявляющих веществ. Ускоряет процесс проявления с метолом, н-аминофенолом, окисленная форма которых тормозит восстановление галогенида серебра. Входит в состав осветляющей ванны при обработке фотоматериалов по методу черно-белого обращения и предназначен для удаления желтой окраски желатина, которая возникает в отбеливающей ванне с дихроматом калия.
Натрий тетраборат декагидрат
Бура
Натрий тетраборнокислый десятивоный
Na2B4O7 • 10Н2О (М.М. 381,37).
Белый кристаллический порошок, растворимый в воде (5 г в 100 мл). Применяется как слабая щелочь в выравнивающих проявителях и составная часть дубящих фиксирующих растворов.
Натрий тиосульфат пентагидрат
Натрий серноватистокислый пятиводный
Гипосульфит
Na2S2O3 • 5Н2О (М.М. 248,18).
Бесцветные прозрачные кристаллы солоноватогорького вкуса, хорошо растворимые в воде, с поглощением тепла (79,4 г в 100 мл). Применяется как прекрасный комплексообразователь в процессе фиксирования кинофотоматериалов. Является составной частью тонирующих ванн и ослабителя по Фармеру. При низком значении pH тиосульфат натрия разрушается с образованием серы. Кислые фиксирующие растворы часто приготавливают с использованием кислых солей, таких, как гидросульфиты натрия или калия.
Натрий фосфат додекагидрат
Натрий фосфорнокислый тризамещенный двенадцативодный
Тринатрий фосфат додекагидрат
Na3PO4 • 12Н2О (М.М. 380,12).
Белые растворимые в воде кристаллы (25,8 г в 100 мл). Применяется в проявляющих растворах как сильная щелочь. Обеспечивает значение pH в проявителе выше, чем карбонаты калия или натрия (pH ® 12,0), за счет того, что в результате гидролиза соли образуется едкая щелочь:
Na3PO4 + Н2О -> Na2HPO4 + NaOH.
Хранят в плотно закрытой посуде в связи с тем, что вещество изменяется на воздухе.
Натрий хлорид
Натрий хлористый
Поваренная соль
NaCl (М.М. 58,44).
Бесцветные кристаллы, легко растворимые в воде (36 г в 100 мл). Применяется как составная часть отбеливающих растворов, усилителей, ослабителей.
Натрий цитрат 5,5-гидрат
Натрий лимоннокислый тризамещенный водный
Na3(C6H5O7) • 5,5Н2О (М. М. 357,1).
Белый порошок, хорошо растворимый в воде. Применяется как составная часть буферной системы в проявляющих растворах.
5-Нитробензимидазол
«Kodak Antifog N 2» (AF-71).
H (M. M. 163,14).
908
Новый справочник химика и технолога
Вещество желтого цвета, трудно растворимое в воде. Применяется в качестве антивуалирующего вещества в цветной и черно-белой фотографии вместо иодида и бромида калия (0,2% раствор от 20-60 мл/л).
Параформальдегид
Параформ
(НСНО)„
Бесцветные кристаллы с запахом формальдегида. Плохо растворяется в холодной воде. При увеличении температуры воды растворимость повышается. Получают упариванием водных растворов формальдегида в вакууме. Представляет собой смесь полиоксиметиленов (СН2О)„ с п = 8-10. Применение см. Формальдегид.
Пирогаллол
Бензол-1,2,3-триол
1,2,3-Тригидроксибензол
(М. М. 126,11).
Легко растворимые в воде игольчатые кристаллы (55 г в 100 мл). Применяется в качестве проявляющего вещества в черно-белой фотографии. Окисленная форма пирогаллола обладает дубящим действием на желатин эмульсионного слоя. Пирогаллоловые проявители в основном используются для получения рельефного изображения на матричных пленках при гидротипном производстве кинофильмов. Ядовит!
Пирокатехин
Бренцкатехин о-Дигидроксибензол 1,2-Диоксибензол
ОН
ОН (М.М. 110,11).
Белые кристаллы, легко растворимые в воде (45 г в 100 мл). Применяется в качестве проявляющего вещества при высококонтрастном проявлении черно-белых фотоматериалов.
Пиросульфит калия
(см. Калий метабисульфит).
Полиэтиленгликоль
«Полиокс» (СССР) Полиэтиленоксид РЕО (США)
НО(СН2СН2О)„Н (М.М. 600-6000).
Белое твердое вещество, растворимое в растворах щелочи. Применяется как активатор процесса проявления, фиксирования и отбеливания. Наибольшим ускоряющим действием обладает полиэтиленгликоль молекулярной массой 1550 («Полиокс-100») при концентрации 5-10 г/л.
Серебра нитрат
Серебро азотнокислое
AgNO3 (М.М. 169,87).
Бесцветные, хорошо растворимые в воде кристаллы (218 г в 100 мл). Применяется при усилении, физическом проявлении и изготовлении фотографических эмульсий. Хранится в хорошо закрытой посуде из темного стекла. Ядовит!
Серная кислота
H2SO4 (М.М. 98,08).
Бесцветная маслянистая жидкость, d = 1,84 (96 % H2SO4), гигроскопична, смешивается с водой в любых соотношениях с выделением тепла в связи с образованием гидратов. Кислоту приливают в воду маленькими порциями, а не наоборот, при этом постоянно перемешивая раствор. Применяется как составная часть кислых фиксирующих растворов для приготовления гидросульфита, а также в отбеливающих и ослабляющих растворах с дихроматом калия, сульфатом меди и перманганатом калия. Хранить в стеклянной посуде. Ядовита! При работе необходимо надевать защитные очки!
Соляная кислота
Хлороводородная кислота
НС1 (М.М. 36,46).
Бесцветная жидкость, дымит на воздухе, смешивается с водой в любых соотношениях. Применяется как составная часть усиливающих растворов. Растворяет большинство металлов. Ядовита!
Тиомочевина
Тиокарбамид
NH2 /
NH2 (М.М. 76,12).
Белые горькие кристаллы, растворимые в воде (11г в 100 мл). Применяется как составная часть тонирующих, ослабляющих растворов, а также отбеливающе-фиксирующих при обработке цветных фотоматериалов (как активатор отбеливания). Используется для стабилизации при скоростной обработке фотоматериалов; образует с серебром при низком значении pH светоустойчивые комплексы. Фотографический материал после стабилизации тиомочевиной не требует оконча
Химия фотографических процессов
909
тельной промывки водой; при этом изображение имеет ограниченный срок хранения.
Тиосемикарбазид
Аминотиомочевина
Амид гидразинтионкарбоновой кислоты
NHNH, / 2
S=C \
(М.М. 91,14).
Является составной частью отбеливающе-фикси-рующих растворов на основе железной соли трилона Б при обработке цветных фотобумаг.
Образует с серебром устойчивые комплексы и ускоряет процесс отбеливания за счет понижения концентрации ионов серебра в реакционном объеме. Предельная концентрация 1 г/л, дальнейшее увеличение приводит к выпадению осадка.
Трилон Б
(см. Динатрий дигидроэтилендиаминтетраацетат дигидрат).
Уксусная кислота
СНзСООН (М.М. 60,05).
Бесцветная жидкость с характерным запахом. Смешивается с водой в любых соотношениях. Совместно с ацетатом натрия выполняет роль буфера для поддержания на постоянном уровне величины pH отбеливающей и фиксирующей ванн при обработке как черно-белых, так и цветных фотоматериалов. Ядовита!
1-Фенил-1Я-тетразол-5-тиол
1-Фенил-5-меркаптотетразол (ФМТ)
HS zc6ii5
)--N
Г \
NX <N
N (М.М. 178,21).
Белый порошок, трудно растворимый в воде. Растворим в растворах щелочи. Применяется в качестве антивуалирующего вещества при быстрой и скоростной обработке фотоматериалов (50-60 °C) в концентрации 0,05-1,0 г/л. Очень сильно повышает контраст изображения. В малых концентрациях (~ 1,5-10”5 моль/л) добавляется в физический проявитель, содержащий нитрат серебра и восстановитель, для повышения стабильности и увеличения срока жизни рабочего раствора.
1-Фенилпиразолидин-З-он
Фенидон
1 -Фенил-З-пиразолидон
(М.М. 162,19).
Белый или светло-желтый порошок, трудно растворимый в холодной воде. Хорошо растворим в горячей воде (50-60 °C) или растворах щелочи. Применяется в качестве проявляющего вещества, чаще всего — совместно с гидрохиноном. Является активатором процесса проявления, способствует значительному увеличению скорости процесса (эффект супераддитивности). Пороговое значение pH для фенидона равно 6,0. Сам фенидон работает очень медленно и проявляет изображение до оптической плотности не более 1,0 в связи с тем, что его окисленная форма почти не связывается сульфитом натрия и тормозит процесс восстановления галогенида серебра. При высокотемпературной обработке целесообразно применять 4-метил-1-фенилпиразолидин-З-он (фенидон Б), который обеспечивает хорошую стабильность и сохраняемость проявителей при высокой температуре. Практически не чувствителен к накоплению ионов брома в проявляющем растворе, что объясняет его широкое применение при машинной обработке кинофотоматериалов. Повышает светочувствительность фотоматериалов. Фенидон-гидрохиноновые проявители работают быстрее, чем метол-гидрохиноновые при концентрации фенидона 7 % от содержания гидрохинона в растворе. Фенидон в 18 раз активнее, чем метол.
Формальдегид
Формалин (30-40% раствор)
Параформальдегид (продукт полимеризации формальдегида)
Н2С=О (М.М. 30,03).
Применяется как составная часть дубящих растворов для фотобумаг, фотопленок и фотопластин. Эффективно дубит в щелочной среде. В проявляющем растворе связывает сульфит натрия и обеспечивает получение на фотоматериалах очень высокого контраста (у > 10) за счет бессульфитного проявления семихиноном (ЛИТ-проявление).
Цитразиновая кислота
(см. 2,6-Дигидроксиизоникотиновая кислота).
Этан-1,2-диамин
1,2-Диаминоэтан
Этилендиамин
H2NCH2CH2NH2 (М.М.:60,10).
Бесцветная жидкость с запахом аммиака. Смешивается с водой в любых соотношениях. Токсичен, предельная концентрация паров в воздухе — 0,001 мг/л. Применяется при обработке цветных обращаемых фотоматериалов как химический активатор цветного проявления. Хорошо адсорбируясь на микрокристаллах галогенида серебра, повышает скорость его растворения. Освобожденные при этом ионы серебра, взаимодействуя с проявляющим веществом, образуют серебряные центры, инициирующие прямое восстановление
910
Новый справочник химика и технолога
неэкспонированного микрокристалла галогенида серебра. На 1 л цветного проявителя добавляют обычно 15-20 мл 50% раствора этан-1,2-диамина. Вторичное экспонирование (засветка) при обработке цветных обращаемых фотоматериалов в этом случае исключается.
Этиленгликоль
Этан-1,2-диол
НОСН2СН2ОН (М.М. 62,07).
Бесцветная жидкость без запаха, сладковатого вкуса. С водой смешивается в любых соотношениях. Применяется как растворитель при приготовлении жидких высококонцентрированных проявляющих растворов, которые хорошо сохраняются длительное время.
Этилендиаминтетрауксусная кислота
«Комплексон II»
ЭДТУ
EDTA
НООССН2 СН2СООН
\ /
n-ch2-ch2-n
нооссн/ ЧСН2СООН (М М. 292,24).
Белый кристаллический порошок, плохо растворим в воде, хорошо растворим в растворах щелочей. Применение см. Динатрий дигидроэтилендиаминтетра-ацетат дигидрат.
CD-I («Kodak»)
(см. Диэтилбензол-1,4-диамин).
CD-2 («Kodak»)
(см. 2-Метил-^,N4-диэтилбензол-1,4-диамин гидрохлорид).
CD-3 («Kodak»)
(см. N-{2-[(4-Амино-3-метилфенил)(этил)амино]-этил}метансульфонамид сульфат моногидрат).
CD-4 («Kodak»)
(см. 2-[(4-Амино-3-метилфенил)(этил)амино] этанол сульфат).
CD-6 («Kodak»)
(см. 2-Метил-^4-(2-метоксиэтил)-^4-этилбензол-
1,4-диамин бис(4-метилбензолсулъфонат)).
Т-32 (ЦПВ-2)
(см. 2-[(4-Аминофенил)(этил)амино] этанол).
TSS (ЦПВ-1)
(см. N,N-Диэтилбензол-1,4-диамин).
5.6. Галогенсеребряная и цифровая фотография
5.6.1. Галогенсеребряная фотография
Сравнивая светочувствительный материал на галогенидах серебра с другими носителями фотографической информации, можно убедиться в существенных преимуществах, выгодно отличающих фотоматериал от этих носителей. К отличительным особенностям, которые характеризуют галогенссрсбряный фотоматериал и фотографический метод, следует отнести: аккумулирующую способность, спектральную универсальность, обеспечивающую широкий диапазон спектральной чувствительности от 0,1 А до 1200 нм, высокую информационную емкость (~109 бит/см2) и достоверность, геометрическую точность и документальность фотографического снимка, возможность быстрого, безграничного размножения изображений и простое аппаратурное оформление.
Эти удивительные достоинства галогенсеребряных фотоматериалов способствовали не только ряду выдающихся открытий в физике, химии, биологии и медицине, но и оказали существенное влияние на бурное развитие таких областей науки и техники, как астрономия, кинематография, полиграфия, телевидение, микроэлектроника, голография, картография, космическая аэрофотография и др.
За более чем 166-летнюю историю своего существования и развития галогенсеребряная фотография достигла поразительного совершенства, особенно в последние десятилетия.
Достигнут значительный прогресс не только в эмульсионной технологии, но и в технологии химикофотографической обработки цветных фотоматериалов. Разработаны новые быстрые высокотемпературные (38-41 °C) унифицированные процессы обработки цветных кинопленок для кинематографии (процессы Kodak ECN-2, ЕСР-2), цветных негативных фотопленок для фотолюбителей и профессионалов (Kodak С-41), обработки обращаемых фотопленок (Kodak Е-6) и цветных фотобумаг (Kodak RA-4, Kodak RA-100, Kodak R-3). Это обстоятельство позволило соединить в единую систему фотоматериалы, приборы и химикофотографическую обработку, обеспечив при этом не только высокую производительность, но и качество изображения, особенно в случае цветной негативнопозитивного процесса.
Возможности галогенсеребряной фотографии не исчерпаны, например возможно увеличение светочувствительности до 5 • 106 ISO (рис. 5.6.1), что может быть достигнуто синтезом полифорных микрокристаллов галогенида серебра с различным числом лучей, исходящих из вершин зародышевых микрокристаллов (рис. 5.6.2). Такие микрокристаллы имеют высокоразвитую поверхность, благодаря которой поглощение света возрастет, по сравнению с обычными микрокристаллами галогенида серебра, что приведет к уменьшению в 2-3 раза числа квантов света, вызывающих обра
Химия фотографических процессов
911
зование скрытого изображения за счет лучшей организации электронно-донорных и ионных процессов. Предлагается в галогенсеребряной фотографии в будущем применять многокаскадное усиление, что должно привести к существенному увеличению светочувст-витвльности. Так, например, при коэффициенте усиления 103—104 на второй стадии при исходной светочувствительности 100 ASA применение двухкаскадного усиления позволит увеличить светочувствительность до 10-106 AS А.
Традиционная фотография остается своеобразной формой творчества и изначально ценится больше цифровой фотографии из-за трудности найти в природе изображение «по-настоящему», т. к. с помощью компьютерных технологий можно легко сделать любое изображение. В то же самое время многие специалисты считают, что цифровые камеры не обогатили фотографию никаким новым измерением, они могут только лишь дополнить традиционную фотографию, но не заменить ее.
^ISO
1839 1900 2000 2040
год
Рис. 5.6.1. Кривая роста светочувствительности галогенсеребряных фотоматериалов до 2040 г.
(по Б.И. Шапиро)
Рис. 5.6.2. Полифорные микрокристаллы бромида серебра: а) октафоры;
б) гексафоры;
в) дидодекафоры
(по Б.И. Шапиро)
5.6.2. Особенности классического фотографического процесса, обусловливающие его широкое применение в науке и технике
Бурное развитие фотохимической промышленности в начале XX в. породило возникновение мировых объединений (фирм), производящих фотографические материалы. Самым крупным изготовителем фотоматериалов сегодня является фирма «Kodak» (г. Рочестер, США), которую многие считают фотографическим гигантом, имеющая свои отделения в Англии, Франции, ФРГ и других странах. Среди других изготовителей фотографических материалов можно назвать такие фирмы, как «Fuji» (г. Токио, Япония), «AGFA-Геверт» (г. Антверпен, Бельгия, г. Леверкузен, ФРГ), «Konica» (г. Токио, Япония), «Перутц» (г. Мюнхен, ФРГ), «Форте» (Венгрия), «Фома» (Чехия), «Циба-Гейги» (Швейцария) и др., которые имеют не только предприятия по выпуску продукции, но и мощные научно-исследовательские центры.
В настоящее время фотографические материалы находят еще самое широкое распространение во многих областях науки и техники, а фотографический процесс является самым совершенным техническим методом исследований и контроля различных технологических процессов.
5.6.2.1. Аккумулирующая способность
Любой приемник лучистой энергии, (например, человеческий глаз, селеновый фотоэлемент) реагирует на мощность излучения, и до тех пор, пока действует свет, существует какая-то ответная реакция приемника. Фотоматериал же реагирует на общее количество суммарной световой энергии, он запоминает, аккумулирует то, что на него действует. Это свидетельствует о том, что у фотоматериала, по сравнению с глазом, гораздо выше пороговая чувствительность. Различия мощности световой энергии всегда можно скомпенсировать продолжительностью экспонирования фотоматериала. Так, при очень низком уровне освещенности объекта выдержка при съемке может быть очень длительной, в то время как при больших освещенностях она существенно сокращается.
5.6.2.2. Спектральная универсальность
Широкий спектр электромагнитных колебаний, который существует в природе, можно разделить на следующие диапазоны:
- гамма-излучение — <0,1 А;
- рентгеновские лучи —0,1-100 А;
- ультрафиолетовое излучение — 100-4000 А (400 нм);
- видимый свет — 400-700 нм;
- ближнее инфракрасное излучение — 700-1300 нм;
- дальнее инфракрасное излучение — 1300 нм-1,5 мм;
- радиоволны — >1,5 мм.
Из всего этого диапазона излучений человеческий глаз воспринимает лишь излучения очень узкой, только
912
Новый справочник химика и технолога
видимой зоны спектра в интервале длин волн от 400 до 700 нм, в то время как селеновый фотоэлемент чувствует еще более узкую зону видимого спектра. Фотоматериал выгодно отличается от других приемников тем, что он реагирует не только на электромагнитные колебания в довольно широком диапазоне длин волн от 0,1 А до 1200 нм (табл. 5.6.1), но и способен регистрировать еще и существующие в природе корпускулярные излучения.
Таблица 5.6.1
Спектральная, общая чувствительность и разрешающая способность носителей фотографической информации
Носитель или система Диапазон спектральной чувствительности, нм Светочувствительность, Джем'2 Разрешающая способность, мм'1
Галогенид серебра 0,1-1200 А Ю“5-1О“10 2000
Электрофотогра- 250-900 106-107 200
фия Диазотипные 350-420 10"' 3000
системы Фотополимери- 300-700 10“2-10 6 2000
зующиеся материалы Т елелвизионная 400-800 10’11 25
камера Человеческий 400-700 10-1° 10
глаз Матрица ПЗС 400-700 10’5-10”1() 10-30
5.6.2.3. Информационная емкость
Человеческий глаз дает высокое качество изображения объекта в пределах очень малого угла зрения, равного примерно 7 ° в то время как на фотоматериале можно получить хорошее качество изображения в пределах гораздо большего поля зрения, величина которого определяется типом съемочного объектива, применяемого при фотосъемке. Сравнивая изображения, полученные с помощью различных носителей фотографической информации, можно сказать, что фотографическое изображение на галогенсеребряном светочувствительном материале, благодаря своей разрешающей способности, имеет высокую информационную емкость и содержит больше достоверных сведений об объекте (табл. 5.6.2).
5.6.3. Цифровая фотография
Началом становления цифровой фотографии считают 1969 г., когда фирма «Bell Labs» создала новый тип полупроводниковых устройств, получивших название CCD (Charge Coupled Device — прибор с зарядовой свя
зью, ПЗС) и предназначенных для регистрации изображений.
Цифровая фотография обладает рядом присущих только ей достоинств, таких как полная интеграция процессов фотосъемки и обработки цветной изображения при помощи различных редакторов, что позволяет вносить исправления и управлять качеством изображения: изменять цветовую насыщенность, контраст, проводить ретушь изображения и т. д. Кроме удобства и оперативности, цифровая фотография позволяет применять не только большой набор периферийных устройств, но и размещать снимки во всемирной информационной сети Internet. Подключение к Internet особенно важно для редакторов и фотожурналистов, которые теперь могут передавать в любую точку планеты свои фотоснимки по глобальным компьютерным системам связи.
Сегодня в фотографии существуют три различных способа получения изображения: аналоговый (от греч. avdXoyoo — сходство, подобие), цифровой и комбинированный цифроаналоговый, совмещающий аналоговый и цифровой подходы.
В первом случае фотосъемку проводят на галогенсеребряную фотопленку, а печать осуществляется на обычную фотобумагу. Для фотолюбителя при реализации данного способа самым проблемным местом является печать фотоотпечатков в минифотолаборатории.
При цифровом способе фотосъемку проводят цифровой фотокамерой, а печать, при наличии компьютера, струйного принтера и определенных навыков, можно осуществить самостоятельно или отдать свои файлы с изображениями в цифровые минилаборатории для печати, где, правда, могут возникнуть проблемы с качеством изображения.
Таблица 5.6.2
Информационная емкость различных носителей информации
Максимаьнос значение
Носитель информации информационной емкости, бит • см2
Страница машинописно- > 10’
го текста
Термографические слои ®102
Электрографические слои:
с сухим проявлением «103
с жидким проявлением «ю5
Черно-белый галогенсеребряный фотоматериал «ю7
средней чувствительности Галогенсеребряный микрофильм «ю8
Галогенсеребряная микрофиша «ю9
Везикулярный слой > ю8
Фотохромный слой «ю9
Магнитная лента > 106
Матрица ПЗС «106
Химия фотографических процессов
913
Третий комбинированный способ получения изображения наиболее прост и удобен. После фотосъемки на галогенсеребряную фотопленку и ее химико-фотографической обработки печать позитивного изображения можно осуществить цифровым методом после сканирования традиционного слайда или негатива. При применении хорошего слайд-сканера можно получить изображение, по разрешению и динамическому диапазону не сравнимое с изображением, снятым с матрицы ПЗС цифровой фотокамеры. Дальнейшая обработка изображения, включающая этап автоматизированной коррекции цвета, контрастности, яркости и прочих параметров, и последующая печать с помощью трехлучевой лазерной оптической системы на цветную фотобумагу — практически единственный вариант качественной печати со слайда;
С уверенностью можно утверждать, что на сегодняшний день галогенсеребряная фотография — наиболее простой и качественный способ получения изображения. Гибридные же (комбинированные) методы фотографии позволяют реализовать на практике достоинства как галогенсерсбряной, так и цифровой технологии. Цифровые методы незаменимы при просмотре результатов съемок в компьютере, наполнении wed-страниц или в случае оперативное получения изображения.
На сегодня светочувствительность ПЗС матриц достигла величины 400-1600 ISO, что практически соответствует светочувствительности цветных негативных фотопленок. Что касается разрешающей способности, то у нового поколения матриц она почти соизмерима с величиной разрешения фотопленки и составляет 17,2 млн пикселей. Однако в настоящее время серьезной проблемой для цифровой фотографии является очень высокая стоимость хороших профессиональных фотокамер.
Цифровая фотография представляет собой в равной степени разновидность фотографического искусства и одну из периферийных компьютерных технологий и зависит не только от технических характеристик и стоимости цифровых фотокамер, но и от ряда других факторов. Во-первых, для широкого внедрения необходимо создание и развитие самой широкой и полноценной инфраструктуры цифровой фотографии (передача, хранение, обработка и печать изображений) аналогично той инфраструктуре, которую имеет сегодня традиционная галогенсеребряная фотография и без которой она просто невозможна. Другим серьезным моментом этой проблемы является квалификация «пользователей», т. к. цифровая фотография является все-таки фотографией, и поэтому для реализации всех возможностей цифровых фотокамер необходимы знания не только в области компьютерных технологий, но и знания основ фотографических процессов, а также хороший вкус и творческие способности.
В 1999 г. фирма «Fuji» разработала датчик Super CCD (Chargde Coupled Device), в котором вместо обычных прямоугольных фотодиодов применены восьми
угольные фотодиоды, собранные в сотовую модель. Чип, изготовленный по технологии Super CCD, имеет ряд преимуществ, включающих увеличенную светочувствительность, более широкий динамический диапазон, довольно высокое отношение сигнал/шум и улучшенную разрешающую способность до 4 млн пикселей.
Продолжая совершенствовать изготовление чипов типа Super CCD, фирма «Fuji» в 2004 г. создала для цифровых фотокамер матрицы четвертого поколения Super CCD HR (от англ, high resolution — высокое разрешение) и Super CCD SR. Матрица Super CCD HR позволяет получить фотоснимки с высоким разрешением до 12,3 млн пикселей, а матрица Super CCD SR, изготовленная с помощью тех же технологий, что и первая матрица HR, при высокой чувствительности и разрешении предлагает новое решение, расширяющее динамический диапазон в четыре раза по сравнению с существующей линейкой цифровых фотокамер, выпускаемых фирмой «Fuji».
Матрица Super CCD SR сочетает в себе как большие по размеру и площади поверхности высокочувствительные S-пикссли, так и более маленькие с малой площадью поверхности, соответственно менее чувствительные /^-пиксели, что и обеспечивает широкий и плавный динамический диапазон, без потерь деталей в темных и светлых участках объекта съемки. Объединяя информацию с обоих типов пикселей, при оптимальном их соотношении (50 % S-пикселей и 50 % /^-пикселей) в общую комбинацию кадра (рис. 5.6.4), матрица Super CCD SR позволяет получать при высоких значениях чувствительности и разрешения существенное расширение динамического диапазона. Этот подход сотрудниками фирмы «Fuji» заимствован из цветной галогенсеребряной фотографии, где зональные эмульсионные слои современных цветных негативных фотопленок изготавливаются как минимум из двух полуслоев — высокочувствительного и низкочувствительного. В высокочувствительном полуслое, определяющем чувствительность всего зонального слоя, микрокристаллы галогенида серебра крупные и высокочувствительные и реагируют на малый уровень освещенности, а в низкочувствительном полуслов, определяющем структурно-резкостные свойства зонального слоя, содержатся микрокристаллы галогенида серебра малого размера, которые обладают низкой светочувствительностью и реагируют на большие уровни освещенности.
Теперь в цифровой фотокамере с разрешением до 3,7 млн пикселей, благодаря применению нового поколения матриц типа Super CCD SR, как и в зональном эмульсионном слое современной цветной фотопленки, изготовленной из двух полуслоев, происходит объединение информации из низкочувствительных /^-пикселей и высокочувствительных S-пикселей (рис. 5.6.5), что в конечном счете и обеспечивает существенные улучшения цифрового изображения.
Однако следует заметить, что, несмотря на поразительные успехи, достигнутые в области микротехноло
914
Новый справочник химика и технолога
гий изготовления нового поколения матриц, они все же до сих пор не могут сравниться с фотопленкой на основе галогенидов серебра по главному параметру — динамическому диапазону передачи тонов (фотографической широте).
Рис. 5.6.4. Влияние количества света (Н) на величину накопленного заряда (Q) матрицы Super CCD SR:
1 — /?-пиксель; 2 — S’-пиксель;
3 — комбинация R- и S'-пикселей
Рис. 5.6.5. Соотношения размеров МК AgHal в высокочувствительном (а) и низкочувствительном (б) полуслоях цветной фотопленки и 5-пикселей и /^-пикселей в матрице Super CCD SR (в)
Фирма «Foveon» разработала светочувствительные матрицы ПЗС по технологии CMOS (Complementary metal-oxide semiconductor), которые способны создавать изображение с разрешением 16,8 млн пикселей. Чипы CMOS обеспечивают втрое более высокое разрешение и гораздо дешевле в производстве, чем высококачественные CCD-датчики.
Получение резких фотоснимков с правильной цветопередачей для цифровых фотокамер, разрешение которых достигает нескольких миллионов пикселей, является непростой задачей. Однако появление нового сенсора Foveon ХЗ обещает изменить такое положение. Фирма «Foveon» в данном сенсоре заложила новый для цифровой фотокамеры метод фиксации информации — каждый пиксел сенсора Foveon ХЗ имеет три слоя све
точувствительных фотодетектора, каждый из элементов которого воспринимает один из трех основных цветов — красный, зеленый и синий,в то время как традиционная матрица ПЗС или сенсор изготавливают по технологии CMOS имеют по одному слою фотодетекторов и для регистрации света на поверхности каждого пиксела располагают красный, зеленый или синий светофильтры. Такой метод приводит к потере деталей изображения или к появлению артефактов, в то время как применение сенсора Foveon ХЗ предполагает втрое больше информации о цвете.
Сопоставляя галогенсеребряную фотографию с цифровой, следует заметить, что 35-миллиметровая негативная фотопленка светочувствительностью 100 ISO имеет разрешение 20 млн пикселей на кадр 24 х 36 мм (для сравнения разрешение человеческого глаза равно 120 млн пикселей), в то время как самый совершенный чип Super CCD не может соответствовать галогенсеребряным пленкам по числу пикселей, чувствительности и ряду других аспектов — качеству изображения, соотношению цена/качество и удобной инфраструктуре для обработки. Однако не только фирма «Fuji», активно работающая в области цифровых изображений, но и ряд других крупных производителей фотографических материалов достигли такого качества, что цифровые отпечатки до размера 5x7 дюймов трудно отличить от фотоотпечатков, полученных с помощью галогенсеребряной технологии.
Ведущие ученые, работающие в области цифровых технологий, считают, что в ближайшее время фотопленка на основе галогенида серебра не будет заменена полностью цифровым изображением, несмотря на то что наблюдается очень быстрое совершенствование цифровых технологий. Соревнование между этими двумя технологиями будет продолжаться, т. к. совершенствование галогенсеребряных фотоматериалов далеко еще не завершено. Галогенсеребряная технология сегодня доведена до высочайшего совершенства, и это дает много преимуществ, например, по качеству изображения, по отношению цена/качество и по широко развитой и удобной инфраструктуре для химикофотографической обработки. Самое главное, чтобы фотопромышленность научилась адаптироваться к быстрому прогрессу, и скорость изменений здесь должна быть гораздо выше, чем прежде. В то же самое время цифровая технология допускает простую обработку изображения и его передачу, что может расширить мир изображения, создавая новые возможности.
В профессиональной области цифровое изображение получило более широкое распространение, чем в любительской, т. к. быстрая и эффективная обработка и передача изображения более важны для профессионалов.
Наибольший интерес представляет применение на практике так называемых гибридных систем, объединяющих возможности галогенсеребряной и цифровой фотографии. Комбинированные гибридные системы, объединяющие цифровые технологии с галогенсереб
Химия фотографических процессов
915
ряными фотоматериалами, позволяют существенно расширить рынок записи изображения.
Галогенсеребряная и цифровая фотография — превосходные технологии, которые будут совершенствоваться и расти вместе, чтобы расширить мир записи изображений, а в будущем не будет существовать границ между галогенсеребряной и цифровой фотографией.
Принцип и особенности цифровой фотографии
В 1981 г. японская электронная фирма «Sony», а затем и фирма «Konica» осуществили технологический прорыв, представив на рынок первую в мире электронную систему для фотосъемки неподвижных изображений, получившую широкое распространение на телевидении и в видеозаписи. В этом виде фотографию называют электронной, или видеофотографией.
В случае электронной фотографии регистрация изображения объекта съемки осуществляется твердотельным преобразователем «свет-сигнал», так называемым фоточувствительным прибором с зарядовой связью (ПЗС, CCD — Chardge Coupled Device). Это изделие электронной техники, преобразующее оптическое изображение в электрический сигнал, действие которого основано на формировании и быстром переносе по поверхности или внутри полупроводника регенерированных при действии света дискретных зарядовых пакетов. Зарядовые пакеты передаются к выходному устройству вследствие перемещения положения потенциальных ям.
В процессе экспонирования ПЗС преобразует сфокусированное на его поверхности оптическое изображение объекта в электрический видеосигнал. ПЗС является полупроводниковым прибором, представляющим собой структуру металл—оксид—полупроводник, который в одной твердотельной пластинке (матрице) содержит элементы изображения, называемые пикселями (pixel — сокр. от англ. Picture Elements), секции накопления и хранения зарядов, регистры сдвига и выходной усилитель.
ПЗС обладает рядом уникальных достоинств: готов к работе немедленно, не чувствителен к магнитным полям рассеяния, обеспечивает высокий контраст изображения при низких освещенностях, не нарушает баланс белого, исключает прожигание при очень больших освещенностях.
При изготовлении матрицы ПЗС на полупроводниковую кремниевую подложку, покрытую слоем диэлектрика из оксида кремния, наносится линейка (ряды) отдельных, регулярно расположенных тончайших и поэтому прозрачных металлических электродов очень маленького размера 5x5 мкм (рис. 5.6.6).
Металлические электроды вместе с оксидом кремния и полупроводниковой подложкой из кремния образуют элементарные светочувствительные ячейки (фотодатчики).
В электронных фотокамерах применяют матрицы, или чипы (от англ, chip — пластинка), ПЗС небольшого размера, например, 6,6 х 8,8; 7,8 х 14 или 18,5 х 27,5, 36,4 х 42,8 мм и др. Количество пикселей при этом мо
жет колебаться от 500 000 до 16 • 106, причем чем больше их количество по горизонтали и вертикали, тем выше разрешение фотокамеры, более резкое изображение и более мягкие цветовые переходы.
В процессе съемки электронной фотокамерой при действии света регенерируются, а затем под светочувствительной ячейкой накапливаются пакеты электрических зарядов, количество которых пропорционально интенсивности освещенности электрода.
При оптоэлектронном преобразовании считывание накопленных зарядов (потенциального рельефа) в ПЗС осуществляется тактовыми импульсами, подаваемыми на электроды. Особая форма импульсов и очередность их следования позволяют перемещать зарядовые пакеты от одного электрода к другому и один за другим переводить их в секцию хранения зарядов. На практике используют ПЗС с построчным и покадровым переносом зарядов. В дальнейшем с сопротивления, на которое подаются заряды, снимается видеосигнал.
Для регистрации сигнала, содержащего видеоинформацию об изображении, необходим магнитный или магнитооптический диск, на который происходит запись в цифровой форме. В канале записи полученный сигнал из аналоговой формы, который описывается только непрерывными функциями, преобразуется в цифровую форму (рис. 5.6.7) или перекодируется из одной цифровой формы в специальный цифровой код, удобный для передачи по каналу магнитной записи. Это преобразование и дало электронной фотографии название «цифровая фотография». В цифровой фотокамере происходит оптоэлектронное преобразование изображения объекта съемки в видеосигнал, который записывается на магнитный диск и вводится в память цифровой фотокамеры. В современных электронных камерах информация записывается также и на так называемые твердотельные карты памяти, имеющие форму кредитной карточки и представляющие собой многослойную интегральную микросхему, по своему устройству и действию аналогичную чипу ПЗС.
Для воспроизведения записи кассету с магнитным диском вынимают из цифровой фотокамеры и устанавливают в проигрыватель (MD-плейер), сигнал с которого подается на видеопринтер, являющийся составной частью системы электронной фотографии.
Рис. 5.6.6. Строение прибора с зарядовой связью (ПЗС):
1 — полупроводниковая подложка из кремния;
2 — слой диэлектрика;
3 — прозрачные металлические электроды;
4 — зарядовые пакеты;
5 — напрвление перемещения зарядовых пакетов
916
Новый справочник химика и технолога
' ООО !001'0101100'101'111 ' 111' 110'001'000'110'001
! ппп ni; ! : i; п :п: п
Рис. 5.6.7 Схема преобразования аналогового сигнала в цифровую форму:
а) график аналогового сигнала: по оси ординат отложены восемь уровней квантования (истинные значения дискретных отсчетов видеосигналов заменяются ближайшими к их величине разрешенными квантованными значениями): по оси абсцисс отложены номера уровней, соответствующие каждому отсчету. Tq — период дискретизации;
б) цифровая последовательность 3-битовых слов, представляющих данный аналоговый сигнал;
в) измерение намагниченности носителя, соответст вующей данной кодовой последовательности
Видеопринтер, совмещенный с видеомагнитофоном и телевизором, при воспроизведении видеозаписи позволяет остановить любой кадр изображения, отпечатать его как на обычной, так и на специально обработанной бумаге и получить цветную копию, часто называемую «твердой копией». Печать может проводиться также и на галогенсеребряную цветную фотобумагу или фотопленку. В практике цифровой фотографии применяются лазерный, струйный или термосублимационный способы печати. Лазерный способ характеризуется высокой разрешающей способностью и используется при печати как на обычную бумагу, так и на галогенсеребряный фотоматериал, при этом происходит сканирование лазерных лучей трех основных цветов [красного (X. = 633 нм), зеленого (X = 543 нм), синего (X = 458 нм)] по поверхности цветной фотоматериала.
В системах цифровой фотографии применяют предложенный еще в 1995 г. фирмой «Kodak» термосублимационный способ печати цветной открытки с использованием сублимационного цветного картриджа. При печати твердой копии бумага снизу плотно прилегает к термопечатающей головке принтера, которая управляется видеосигналом и построчно развертывает изображение. В термопечатающей головке наблюдается под действием тока видеосигнала выделение тепла, которое обусловливает сублимацию красителей и их перенос с красящих листов на бумагу. При этом перенос красителей происходит в последовательности: желтый, пурпурный, голубой, черный, что приводит к образованию цветного изображения субтрактивным методом. Продолжительность печати на принтере цветной твердой копии размером 80 х 100 мм составляет 20 с, при этом разрешающая способность равна 8 мм’1.
Запись информации в первой фотокамере «Мави-ка» осуществлялась на магнитный диск диаметром 47 мм и толщиной 45 мкм, который находился в прямоугольной полужесткой пластмассовой кассете размером 60 х 54 х 3,6 мм и массой около 8 г. Информацион
ная емкость таких дисков достигает 4,5 Мбайт (1 байт = 8 бит*; 1 Мбайт = 106 байт = 8 • 106 бит). На магнитном диске, который вместе с кассетой располагается с задней стороны цифровой фотокамеры, можно записать 25 полнокадровых или 50 полукадровых цветных изображений.
В профессиональных и любительских цифровых фотокамерах последнего поколения для записи информации применяется твердотельная карта памяти размером 85,6 х 54 х 3,3 мм, которая позволяет хранить 20, 32, 43, 84 цветных полнокадровых снимка, а камеры высокого класса имеют карту памяти с информационной емкостью, равной 131 Мбайт, что позволяет хранить до 114 цветных снимков. В технической литературе было сообщено, что уже освоены твердотельные карты, в которых ячейки памяти имеют размер менее 1 мкм, а в дальнейшем прогнозировалось уменьшить размер ячейки памяти твердотельных карт до 0,5 мкм, что уже привело к увеличению памяти до 512 Мбайт или 1^4 Гбайт.
Фотокамера для цифровой фотографии имеет не только внешнее, но и функциональное сходство с обычной фотокамерой, применяемой в галогенсеребряной фотографии, и представляет собой:
- светонепроницаемый корпус;
- фотообъектив с механизмом наводки на резкость; оптический видоискатель или встроенный видоискатель на жидких кристаллах;
- фотозатвор;
- автоспуск;
- матрицу или чип ПЗС;
- кассету с магнитным диском;
- электрический привод магнитного диска;
- источник питания (аккумулятор);
- переключатель рода работы (покадровая или непрерывная фотосъемка);
- электронные блоки камеры и видеоканала, зеркала.
Цифровые фотокамеры подразделяются на любительские и профессиональные для фотостудий.
Необходимо отметить, что первый в мире электронный фотоаппарат «Мавика» имел матрицу ПЗС около 280 000 пикселей, а цветное изображение при такой низкой разрешающей способности было невысокого качества.
В середине 1990-х гг. появились цифровые фотокамеры, у которых число пикселей стало соизмеримым с их числом у цветной негативного фотоматериала.
Рассматривая конструкцию цифровой фотокамеры, необходимо остановиться на вопросе формирования цветного изображения. Широко распространенным способом получения цветного изображения в любительской и профессиональной цифровой фотографии
* Бит (от англ, binary — двойной и digit — цифра). В цифровой технике слова и числа представляются в виде комбинации двух знаков 0 и 1. Знаки или единицы двоичного кода называются битами.
Химия фотографических процессов
917
является фотосъемка камерой с одним цветным чипом ПЗС и однократной выдержкой (рис. 5.6.8). Цветоделение в этом случае осуществляется мельчайшими аддитивными светофильтрами: красным, зеленым и синим, нанесенными на пиксели. Причем половина всех пикселей покрыта зелеными светофильтрами, а остальную часть поровну делят между собой красные и синие светофильтры, покрывая пиксели. Данным способом можно проводить фотосъемку движущихся объектов при дневном освещении и применяя лампу-вспышку. Для фотосъемки неподвижных объектов и получения высокого качества цветного конечного изображения чаще всего применяют другой способ цветоделения. Матрица ПЗС при этом экспонируется три раза за зональными аддитивными светофильтрами, закрепленными во вращающейся турели (рис. 5.6.9).
Рис. 5.6.8. Схема цветоделительной системы цифровой фотокамеры с одним чипом ПЗС, покрытым аддитивными светофильтрами:
1 — фотообъектив; 2 — диафрагма; 3 — затвор; 4 — чип ПЗС;
5 —аддитивные светофильтры; 6 — свой пикселей;
7 — подложка из кремния; 8 — аналогоцифровой преобразователь; 9 — твердотельная карта памяти;
10 — основное запоминающее устройство
Рис. 5.6.9. Схема цветоделитсльной системы цифровой фотокамеры с вращающейся турелью со светофильтрами: 1 —турель с красным, зелеными синим светофильтрами;
2 — фотообъектив; 3 — диафрагма; 4 — затвор; 5 — чип ПЗС
Кроме того, существуют цифровые фотокамеры, в которых с помощью призмы происходит разделение изображения на красную, зеленую и синюю составляющие, попадающие каждая на свою матрицу ПЗС. Такие цветоделящие системы обеспечивают высокое качество цветовоспроизведения и устраняют помехи, которые могут возникнуть между цветными составляющими.
Следующий вариант цветоделительной системы используется в цифровых фотокамерах с разверткой кадра
строчным ПЗС. Чип ПЗС в этом случае представляет собой три ряда пикселей, соответствующих одной строке изображения. Один ряд пикселей покрыт красным фильтром, другой — зеленым, третий — синим. При фотосъемке ПЗС перемещается и в каждый момент времени регистрирует только одну строку изображения, что в конечном счете обеспечивает высокое качество. В дорогих любительских и профессиональных цифровых фотокамерах применяются три чипа ПЗС и цветоделительная система с дихроическими полупрозрачными зеркалами (рис. 5.6.10). Каждый из трех чипов ПЗС при фотосъемке воспринимает только свою часть спектра — красную, зеленую или синюю, аналогично цветной многослойной фотопленке, состоящей из трех зональных слоев, сенсибилизированных к трем зонам спектра. Такие камеры позволяют проводить фотосъемку движущихся объектов, обеспечивая при этом высокое качество изображения, т. к. разрешающая способность сенсора цифровой фотокамеры, состоящего из трех чипов ПЗС утраивается по сравнению с разрешающей способностью одного чипа ПЗС.
ПЗС
Рис. 5.6.10. Схема цветоделительной системы цифровой фотокамеры:
/ — с полупрозрачными дихроичными зеркалами, отражающими синие и пропускающими красные и зеленые лучи;
2 — с полупрозрачными дихроичными зеркалами озражающими красные лучи и пропускающими зеленые лучи;
3 — обычные озражательные зеркала: Er, Ео, Ев — электрические сигналы красного, зеленого, синего цветов на выходе чипа II3C
Сопоставляя цифровую фотографию с галогенсеребряной, следует заметить, что при полутоновой записи информации для получения изображения высокого качества на цветной фотопленке необходимо, по крайней мере, передать не менее 64 градаций интенсивности света или цветовой насыщенности, что составляет 6 бит (64 = 26). Такую интенсивность света в галогенсеребряной фотографии, как считает И. Лохман, можно передать 250 микрокристаллами галогенида серебра, при этом данная группа микрокристаллов имеет размер «грани» ~13 мкм, что соответствует одному пикселю. Принимая во внимание, что 35-миллиметровую негативная фотопленка светочувствительностью 100 ASA имеет разрешающую способность 20 млн пикселей на фотокадр размером 24 х 36 мм, легко подсчитать максимальный объем информации на фотопленке, который составит (20 • 106) х 6 бит = 120 • 106 бит = 15 Мбайт. Что касается матрицы ПЗС, то у современных цифровых фотокамер высокого класса каждый пиксель различает
918
Новый справочник химика и технолога
больше градаций интенсивности света, чем фотопленка на основе галогенида серебра. Так, пиксели современной профессиональной цифровой фотокамеры различают 4096 градаций (12 бит). При различаемости каждым пикселем такого числа градаций (4096) и общем числе пикселей около 20 млн на кадр максимальный объем информации, передаваемой матрицей ПЗС в цифровой фотокамере, теоретически может составить (20 • 106) х 12 бит = 240 Мбит = 30 Мбайт.
Бяок управления
Сканер
для фотопленок
В ысо шскоросгной интерфейс
Блок жеггоиирования
фасный излучатель
(МШ-матрниа)
Зеленый i тучате-
(VFPI 1-магрина н снетофнлыр) Синий излучатель
(VI'PH-матрнца и светофильтр)
Рис. 5.6.11. Печатный блок мини-лаборатории на основе светодиодных матриц (Konica QD-21)
Наибольший интерес для специалистов сегодня представляет использование на практике так называемой гибридной технологии (рис. 5.6.11), в которой роль носителя изображения отводится фотографическим пленкам. При этом оптическое изображение с цветной фотонегатива высокого качества, полученного традиционным способом на галогенсеребряных слоях, преобразуется в цифровой электрический сигнал, и после коррекции печатается твердая копия.
Литература к 5.1-5.6
1. Редько А. В. Основы фотографического процесса: Уч. пособие. С.-Пб.: Лань, 1999. 512 с.
2. Шапиро Б. И. // Наука в России. 2000 № 1. С. 40-49.
3. Riedl М. // Fotowirtschafi. 1988. № 3. С. 10
4. Film mit ISO 100.000/61°- MPT. 1987. № 6. С. 256-259.
5. Современные тенденции развития кинопленки Fuji // Материалы симпозиума фирмы «Fuji». М.: НИК-ФИ, 1989.
6. Belloni J., Treguer М., Remita Н. И Nature. 1999. Vol. 402. N 23. С. 865-867.
7. Василевский Ю. А. Цифровая фотография. М., 1998. 31 с.
8. International Contact. 2000. N 1. С. 18-20.
9. ФОТО Сибирский успех. 1998. № 8-9. С. 51.
5.7. Фотолитография
(к.т.н. А.Г. Вавилов)
Фотолитография — блок технологических процессов фотохимической технологии, направленных на создание рельефа в диэлектрической пленке, а также пленке металла, нанесенного на подложку. Методы, основанные на применении фотолитографии широко
распространены при изготовлении печатных плат, пленочных микросхем, твердых схем, трафаретов (масок) для напыления и нанесения паст по толстопленочной технологии и т. д.
Технологические процессы фотолитографии включают в себя:
- получение фотошаблона;
- разработку состава фоторезиста;
- нанесение пленок фоторезиста на подложку;
- сушку нанесенного слоя;
- экспонирование;
- проявление;
- термообработку слоя фоторезиста;
- химическое травление, включая выбор травителя и режима травления, или электроосаждение металла на незащищенные фоторезистом участки;
- удаление пленок фоторезиста.
Фотолитография основана на применении технологических процессов, при которых изображение формируется в результате изменения физико-химического состояния системы (в первую очередь растворимости), содержащей светочувствительное вещество и некоторые высокомолекулярные соединения.
Впервые метод фотопечати был применен для изготовления печатных плат. Преимущества этого метода перед трафаретной и офсетной печатью заключаются в экономичности обработки малых серий изделий (т. к. не требуется создание сетчатых трафаретов или клише), а также в четком изображении элементов рисунка. Широкое применение печатных плат в радиоаппаратуре вызвало интенсивное развитие фотолитографических методов в радиотехнической промышленности. Дальнейшее развитие и усовершенствование техники фотолитографии напрямую связано с ее использованием в электронной промышленности. В производстве твердых и пленочных схем к фотолитографии предъявляются специфические требования, отличающиеся от требований, принятых в радиотехнической промышленности. Достаточно указать, что при изготовлении твердых схем на кремнии и германии методами фотолитографии уже к 1969 г. получали отдельные элементы с линейными размерами до 2,5 мкм и менее, а в качестве ближайшей перспективы уже тогда обсуждались требования воспроизведения элементов схем с субмикронными размерами. Применение фотолитографии в технологии полупроводниковых приборов позволяет добиться полной воспроизводимости линейных размеров, конфигурации и взаимного расположения различных элементов схем.
Использование фотолитографического метода при создании электронной аппаратуры основано на применении органических светочувствительных материалов, нанесенных на полупроводниковые материалы, металлические пленки, стекло и другие подложки, на переносе на них изображения и локальной защите поверхности от воздействия физических, электрохимических и других агрессивных факторов.
Химия фотографических процессов
919
Светочувствительные материалы (композиции), используемые в фотолитографических процессах и изменяющие свою растворимость при облучении называют фоторезистами [1].
В зависимости от длины волны облучения различают оптическую или собственно фотолитографию (X = 300^-400 нм), рентгеновскую (X = 0,1-4,0 нм), электронную (X < 0,1 нм) и ионно-лучевую (X = 0,054), 1 нм) литографии [22]. Материал, изменяющий свои свойства, прежде всего растворимость, под воздействием ускоренных свободных электронов называется электронорези-стом. Материал, изменяющий свои свойства и прежде всего растворимость, под действием рентгеновских лучей представляет собой рентгенорезист. Фоторезист, электронорезист, рентгенорезист, обладающий малой скоростью распьшения в ионном или плазмохимическом разряде по отношению к удаляемым этими способами материалам подложки называется ионорезист.
Сущность органических фотохимических реакций состоит в активации системы поглощенным квантом света [2-6].
5.7.1. Фоторезисты
Химическая природа фоторезистов весьма многообразна. Исторически первым и весьма удачным фоторезистом можно считать аравийский асфальт, который был применен Ньепсом около двух веков назад для работы на литографском камне. С точки зрения устойчивости к воздействию агрессивных сред он является практически идеальным, но вследствие весьма низкой светочувствительности давно потерял значение.
Различают негативные и позитивные, жидкие и твердые фоторезисты. Выбор того или иного фоторезиста определяется требованиями, предъявляемыми к технологическому процессу и изделию в целом.
Негативные фоторезисты — это синтетические высокомолекулярные соединения или композиции, молекулы которых под действием поглощающего излучения образуют разветвленные (поперечно-сшитые) структуры, вследствие чего становятся устойчивыми к воздействию растворителей.
Позитивные фоторезисты — при облучении разрушаются и при проявлении удаляются с освещенных (экспонированных) участков.
Жидкие фоторезисты представляют собой раствор светочувствительного полимера (полимера и светочувствительной компоненты) который различными методами (центрифугирование, окунание, вытягивание) наносится на подложку для получения защитной пленки после сушки.
Комбинированная пленка, у которой негативный или позитивный светочувствительный слой толщиной 10-40 мкм находятся между защитными пленками из полиэтилена и полиэфира (Riston, DuPont, Laminar, Dynachem, СПФ-ВЩ) называют твердым фоторезистом.
В настоящее время промышленность стран мира выпускает большей ассортимент фоторезистов, отличающихся по своим свойствам (светочувствительности, разрешающей способности, химической стойкости и др.) [1,7-11].
В табл. 5.7.1-5.7.6 приведены некоторые фоторезисты и их физические свойства.
Фоторезисты делятся на группы в зависимотсти от применяемых светочувствиетельных материалов в слоях фоторезиста, на которые воздействует поглощающее излучение:
- желатина и поливиниловый спирт, содержащие соли хромовой кислоты;
- поливинилциннамат;
- полимеры с двойными связями (в первую очередь каучуки и циклокаучуки), содержащие в качестве светочувствительной компоненты различные бисазиды;
- светочувствительные слои типа «Дайкрил».
Таблица 5.7.1
Негативные фоторезисты [9]
Фоторезист Раствори- тель Проявитель Фирма
KPR KPR KPR Eastman Kodak Co.,
KPR-2 KOR KOR Rochester, N. Y.
KPR-3 KOR KOR
KPL KPR KPR
KOR KOR KOR
KMER KMER KMER Dynachem Corp.,
KTFR KTFR KTFR Downey, Calif
DCR-3140 3140 Dynachem
DCR-3154 DCR-3118 DCR-3170 3154 Dynachem Dynachem DCR3170
Waycoat N 10 N 10 Waycoat Philip A. Hunt Chemical Co.,
Waycoat N20 N20 Waycoat Palisades Park. N. J.
Emuisitone Деионизи- Emuisitone Co.,
N 150 рованная вода (50 °C) Livingston, N. J.
Таблица 5.7.2
Состав фоторезистов KPR-2 и KTFR [9]
По данным Левина, Лезайна и Оффенбаха KPR-2 KTFR
Растворитель 86-87 % Хлорбензола; 13-14 % циклогексанона 82 % о-, м-, и-Ксилола; 12 % этилбензола; 6 % метилцел-лозольва
920
Новый справочник химика и технолога
Окончание табл. 5.7.2 Таблица 5.7.3
По данным Левина, Лезайна и Оффенбаха KPR-2 KTFR позитивные фоторезисты |У|
Фоторезист Разбавитель Проявитель Поставщик
AZ-1350 AZ-1350H AZ-340 AZ-111 AZ-119 AZ-345 AZ-165 KAR-3 AZ AZ AZ AZ AZ-119 AZ AZ KAR разбавитель AZ AZ AZ-300 AZ-330 AZ-303 AZ-303 AZ-303 KAR проявитель, КОНЦ. Shipley Eastman Kodak Со., Rochester, N.Y.
Полимер Средний молекулярный вес Сенсибилизатор Добавка Поливинилциннамат 315 000-350 000 1,4 г на 100 г полимера Производные нафтотиазола с 10 % серы Поливиниловый спирт, коричная кислота, гидрохинон, следы воды Частично цик-лизированный г/цс-полиизо-прен с одной двойной связью на 10 атомов углерода 120 000 Диазид ароматического ряда
Таблица 5.7.4 Физические свойства фоточувствительных резистов фирмы «Kodak»
Свойства KPR KPR-2 KPR-3 KPL KOR KMER KTFR
Вязкость при 25 °C, 10'3 Па • с Содержание твердого продукта, масс. % Плотность при 20 °C*, 103 кг/м3 Коэффициент отражения сухой неэкспонированной пленки Поверхностное натяжение, 103 Н/м Спектральная чувствительность, нм, (А) 11,7-18,1 6,4-7,6 1,010 1,610 30,1 22,6-27,6 8,4-9,2 1,090 1,611 33,2 34,0-38,5 9,1-9,9 1,070 31,7 620-800 23-27 1,2406 1,610 46-54 9,2-9,8 1,040 1,616 31,2 250-550 (2500-5500) 396-504 24,7-27,3 0,901 1,554 28,9 310-480 (3100-4800) 465-535 27,2-28,8 0,893 1,541 29,2 310-480 (3100-4800)
260-460 (2600-4600)
приведены типовые данные, которые могут колебаться от партии к партии.
Таблица 5.7.5
Характеристики отечественных фоторезистов для технологии микроэлектроники
Марка фоторезиста Тип фоторезиста Пик спектральной чувствительности, нм Разрешающая способность R при толщине d Концентрация, % Плотность, 103 кг/м3 при 20 °C Кинематическая вязкость, 10’6 м2/с Относительная летучесть (по ацетону) Поверхностное натяжение, 10'3 Н/м, при 20 °C
d, мкм R, мкм
ФП-383 ФП-307 ФП-ЗЗЗВ ФП-330 ПВЦ Позитивный То же » » Негативный 407 407 475 407 280-320 1 1 1 1 0,3 4 2,5 2,5 5,0 20 20 20 22 20 5-7 1,102 1,103 0,997 5,9 6,9 3,5 3,8 3,8 12 32,26 35,26 28,7
Таблица 5.7.6
Фоторезисты, применяемые в промышленном производстве полупроводниковых приборов и их свойства [11]
Фоторезист (тип) фирма- изготовитель Химический состав Свойства Формирование слоя Разрешающая способность
Полимер, (молярная масса) Светочувствительный компонент Растворитель Максимальное содержание твердого вещества, масс. % Уд. вес (плотность жидкости), 103 кг/м3 Вязкость, 10 3 Па • с Показатель преломления хност-24 °C), Проявитель Время проявления, с Раствор для промывки Время промывки, с Толщина пленки, нм Минимальная ширина линии, мкм
CU S
Коэффициент пов ного натяжения (щ 10“3Н/м
KPR-2 (негативный), «Kodak» Поливинил-циннамат (2 000 000) Органический сенсибилизатор 8,4-9,2 1,090 (25 °C) 27,5- 32,5 (25 °C) 1,611 (25 °C) 33,2 Трихлорэтилен 30 Смесь трихлорэтилена и изопропилового спирта (1 : 1) 30 900 2,5
KMER (негативный), «Kodak» Полиизопрен (60 000) Бифункциональный азид Ксилол 25,4-28,0 0,901 (25 °C) 396-504 (25 °C) 1,554 (25 °C) 28,9 Растворитель Стод-дарта 30 Смесь растворителя Стоддарта и изопропилового спирта (3 : 1) 30 1250 5,08
KTFR (негативный), «Kodak» г/мс-Полиизо-прен (60 000) То же То же 27,2-28,2 0,897 (25 °C) 485-555 (25 °C) 1,541 (25 °C) 28 Проявитель марки KTFR 40 Раствор KTFR 60 900 2,54
Waycoat (негативный), «Hunt» цис-Поли-изопрен » 15 (0,059 Па-с) 12,5 (0,036 Па-с) 9,7 (0,22 Па-с) 0,900 (25 °C) 56-62 (25 °C) 1,5465 «33,2 Специальный проявитель 30 /V-Бутил-ацетат 20 1200 2,54
Химия фотографических процессов
Q о 5 ° 5^ sc 8 । о s- So TL^SCu 8 s- § s (V 42s^ « s - | S. 7 g * 7 £ ^7 СЛ ~ r-h Фоторезист (тип) фирма- изготовитель
2 > 20 2^»од g £ g £ £ £ g £ § x 0 н oo q % e ° I §§ i s SC • О ' ~ £ P и о S3 1 1 Полимер, (молярная масса) Химический состав
Ja H Q ho s o © s Л p й g p X W g W s о p S S at. й § S = Светочувствительный компонент
w w л о s n 2 H e g *3 E h 1 s i g B g g SB' Растворитель
V « I L g *> OO H— Максимальное содержание твердого вещества, масс. % Свойства
'Ci о Cj — Cj o O 00 ^ o Ъ ° OO ° 4P О oo О о О о Г) ui Уд. вес (плотность жидкости), 103 кг/м3
CS — К)' Ю Cj L- » ° £ Cj £ О ;zy >—к О ( Л о "* о Г о ? о 00 f Вязкость, 10-3 Па • с
— Сэ — 'С — LZ1 ° Ъ1 ° LZ1 О\ о LZ1 о LZ1 К> -J 'О LZ1 Показатель преломления
Коэффициент поверхностного натяжения (при 24 °C), 10“3Н/м
й д ей и ^й а О й .. й .. й о Л. g w Р § О-РхИ ч-^^>ся и S Si S OS i L>* I LU i Проявитель Формирование слоя
1—‘ bJ U1 '•^1 о о Время проявления, с
ИЬИЮННИД - t35 bJ S S О Й — p PT p • 2EP^’ p •u ? о • ®s a^S^ffiSc^SJsgsc0^^ ® g ®S sE^S®§gs3^^S “£“§ Iwog^oSg-sc^ p 1 p g s ? £ p s S о I? 1 1 1 1 Раствор для промывки
10 1200 10 1200 120 Время промывки, с
700 1200 1000 Толщина пленки, нм Разрешающая способность
6J 6J 6J U1 LZl LZl 4^ 4^ 4a Минимальная ширина линии, мкм
Окончание табл 5.7.6
пгогюнхэш п nnnwnx ymuhodvduo тчноц
ZZ6
Химия фотографических процессов
923
В пленках различных типов светочувствительных систем протекают следующие реакции.
При применении поливинилциннамата протекают фотохимические реакции, приводящих к образованию «сшитой» (нерастворимой) структуры молекул полимера:
hv
При применении фоторезистов на основе нафтохинондиазидов под действием поглощающего излучения (участки слоя, подвергнувшиеся облучению, становятся растворимыми):
В случае фоторезистов на основе полимеров, содержащих двойные связи при введении бисазидов под действием УФ-облучения происходит образование продуктов фотолиза бисазидов, которые далее (темновая стадия процесса) взаимодействуют с молекулами полимера:
_ „ _ hv hv
N3— R— N3 ------► N3— R— N :---------►
- n2 - n2
В результате действия света на слои поливинилового спирта, содержащие соли хромовой кислоты:
2-
(Сг2О7) + hv
2
(Сг2О7)
- —। *
2- +3
(Сг2О7) + полимер ---------->• Сг + полимер ...,
где [(Сг2О7)2 ] показывает возбужденное состояние иона бихромата.
Предполагается, что [(Сг2О7)2^] легко разрушаются, обеспечивая свободные Сг3+ и О2”. Образующиеся ионы хрома(Ш) играют роль сшивающего агента в системе, содержащей желатину, поливиниловый спирт и другие полимеры.
Светочувствительные слои типа «Дайкрил» основаны на применении инициированной полимеризации под действием света. В состав таких светочувствительных композиций входят ненасыщенный мономер, сшивающий мономер, инициатор полимеризации и ряд других компонент. При действии поглощающего излучения инициатор фотополимеризации распадается на свободные радикалы, которые инициируют полимеризацию мономера. Введение «сшивающего» мономера приводит при совместной полимеризации с ненасыщенным мономером к образованию поперечных мостиковых связей, что увеличивает прочность получаемого рельефного изображения.
5.7.1.1. Светочувствительность фоторезистов
Все фоторезисты отличаются в первую очередь по своей чувствительности к излучению и спектральной чувствительности. В настоящее время в литературе
924
Новый справочник химика и технолога
известно множество методов определения интегральной светочувствительности полимеров и композиций, анализ которых приведен в работе [8].
Выбор метода определения светочувствительности проводят по следующим критериям:
- условия проведения испытаний должны быть близки к практическим условиям их применения;
- высокая воспроизводимость получаемых результатов;
- получение максимума информации для изучения фотографических свойств данных светочувствительных систем.
На основании проведенного анализа в наибольшей степени данным критериям отвечает методика, разработанная К.С. Ляликовым с сотрудниками [57].
Идея метода заключена в том, что слой произвольной толщины вносится на кварцевую подложку. Экспонирование слоя производится со стороны подложки, пропускающей УФ-излучение. В случае негативного фоторезиста с увеличением экспозиции Н возрастала толщина «сшитого» слоя, прилегающего к подложке. После проявления в растворителе получается ступенчатая сенситограмма. Экспонирование производится при постоянной освещенности слоя.
Между источником излучения (лампа ДРШ-250) и экспонируемым образцом помещается вращающийся диск с секторными вырезами (скорость вращения диска 2 мин”1). Толщина слоев полей сенситограммы измеряется с помощью микроскопа Линника МИИ-4.
По полученным результатам строятся характеристические кривые в координатах d (толщина слоя, мкм) и 1g//, по которым определяется светочувствительность фоторезиста по различным критериям:
с - 1 S_______________' -S - 1
k'nop j, ’ = 0,5 jj ’ = 1,0 jj '
"пор Hd 0,5 Hd = \,0
где Нпор — минимальная экспозиция, достаточная для образования первого сшитого слоя сенситограммы; Нс/ = 0 5 и Hd_ ] о — экспозиции, необходимые для «сшивания» слоев толщиной 0,5 мкм и 1,0 мкм, соответственно.
При исследовании светочувствительности позитивных фоторезистов данный метод несколько видоизме-нется. В этом случае экспонирование слоя производится со стороны слоя. После проявления на подложке получается рельеф вымывания. При этом необходимо строго контролировать толщину и равномерность политого слоя по всей подложке. В качестве критериев принимаются:
$ —!—s ' -s - 1
^пор г, ’ к'<7 = 0,5 jj ’ = 1,0 jj ’
П пор h d = 0,5 "j-1,0
где //nop — минимальная экспозиция, при которой обнаруживается рельеф вымывания; Hd = 0,5 и Hd = ] 0 — экспозиции, при которых толщина вымываемого рельефа равна 0,5 мкм и 1,0 мкм, соответственно.
В табл. 5.7.7 приведены значения светочувствительности различных слоев, определенных по данной методике.
Таблица 5.7.7
Значения светочувствительности различных полимеров [8]
Полимер, фоторезист, композиция, содержание Светочувствительность, см2/(Вт • с)
5 ‘-’пор S<J =- 0,5 $d= 1,0
KMER 12,0 7,0 0,4
KTFR 24,0 16,0 10,0
SCR-I 56,0 24,0 18,0
СЦК-1 12,0 5,0 1,2
ФН-11Т 7,0 5,0 3,5
Р7-1 5,0 4,5 4,0
РН7-2 7,0 5,0 4,5
Поливиниловый спирт (с солями хромовой кислоты) 7,0 6,0 4,0
Поливинилциннамат (ПВЦ) 47,0 5,0
ПВЦ-250 200,0 9,0 3,2
Циклокаучук (ГИПИ-4) + 4,4'-бис(азидо)дифенилметан (33 масс. %) 3,0 0,58 0,1
Циклокаучук (ГИПИ-4) + 2,6-бис(4'-азидобензаль)метилциклогексанон (11 масс. %) 12,0 5,0 1,2
Циклокаучук (ЛТИ) + 2,6-бис-(4'-азидобензаль)-метилциклогексанон (6 масс. %) 24,0 12,0 4,0
Полиизопреновый каучук + 4,4'-бис(азидо)дифенилметан (20 масс. %) 0,8 0,28 <0,1
СКС-30 + 4,4'-бис(азидо)дифенилметан (20 масс. %) 0,8 0,24 <0,1
Бутилкаучук + 4,4'-бис(азидо)дифенилметан (20 масс. %) 0,4 0,005
Химия фотографических процессов
925
Окончание табл. 5.7.7
Полимер, фоторезист, композиция, содержание Светочувствительность, см2/(Вт • с)
° пор $d = 0,5 $d-- 1,0
СКС-30 + 2,6- бис(4'-азидобензаль)метилциклогексанон (20 масс. %) 12,0 1,2 0,16
Циклокаучук (ГИПИ-4) + 4,4'-бис(азидо)дифенилметан (33 масс. %) + + 2,6-бис(4'-азидобензаль)метилциклогексанон (11 масс. %) 12,0 5,8 2,5
Сополимер поливинил-Р-бензоилакриловой кислоты с нафталином 6,0 0,51 0,16
Сополимер стирола с винилнафталином 0,8 0,31 0,1
Поливинилциннамальацетофенон 55,0 6,0
Поливинилфенилпропаргальацетофенон 55,0 4,6
Поливинил-л/-нитробензалацетофенон 30,0 3,5
ФП-383: 7,0 5,0 3,0
ФП-383 при введении эпоксида ЭД-5 28,0 6,0 1,4
Новолак смола + продукт 30 (в соотношении 5 : 3) 14,0 2,9
ФП-234: 13,0 2,0 0,8
Новолак + продукт 54 (в соотношении 5 : 3) 14,0 3,0
Новолак + продукт 83 (в соотношении 5:3) 14,0 3,0
Новолак + продукт 27 180,0 7,5 3,6
Новолак + продукт 7 (в соотношении 5 : 3) 14,0 2,75
Новолак + продукт 331 (в соотношении 5:3) 100,0 13,5
Новолак + продукт 331 и 7(в соотношении 2:1) 28,0 4,5
Новолак + продукт 331 и 7(в соотношении 1 : 2) 14,0 1,5
Слои типа «Дайкрил» «0,1
Как видно из приведенных в табл. 5.7.7 данных, наиболее светочувствительными являются слои на основе поливилциннамата и диазосоединений. Затем располагаются слои на основе циклокаучука с бисазидами, хромированный поливиниловый спирт. Наименьшую пороговую светочувствительность проявляют слои типа «Дайкрил».
В случае поливинилциннамата при действии УФ-излучения образуется бирадикал, который отщепляет водород от близлежащей молекулы светочувствительного полимера, в результате чего происходит сшивка молекул. В этом случае рекомбинация бирадикалов также приводит к образованию сшитой структуры молекул поливнилцин-намата. Светочувствительность этих слоев будет зависеть от молярной массы полимера, степени этерификации. Скорость реакции сшивания будет определяться скоростью образования бирадикалов. Квантовый выход реакции сшивания поливинилциннамата под действием УФ-излучения близок к 0,5 [12]. Число молекул, окружающих образовавшийся бирадикал, велико, что увеличивает вероятность взаимодействия бирадикала и молекулы полимера. Кроме того, светочувствительность может быть значительно увеличена введением оптических сенсибилизаторов типа кетона Михлера, 2-бензоилметилен-З -метил-[3-нафтотиазолина (примерно в два раза) и др. [13].
При использовании фоторезистов на основе нафтохинондиазидов (фоторезисты позитивного действия) фактором, определяющим светочувствительность, является скорость разложения диазогруппы. Квантовый выход фотолиза о-нафтохинондиазидов равен 0,3-0,5.
При применении фоторезистов на основе каучуков с бисазидами под действием УФ-излучения происходит образование продуктов фотохимической реакции бис-азида, которые взаимодействуют с окружающими их молекулами полимера. Эффективность световой стадии процесса довольно высока. Квантовый выход фотолиза различных бисазидов равен 0,26-0,70 [8]. Однако интегральная светочувствительность данных слоев довольно низка по сравнению со слоями поливинилциннамата и нафтохинондиазидов. Лимитирующей стадией, очевидно, является темновая стадия процесса, то есть химическая реакция взаимодействия продуктов фотолиза бисазидов с молекулами полимера. Кроме того, следует отметить, что продукты фотолиза бисазидов могут взаимодействовать между собой (реакция рекомбинации), что в отличие от слоев поливинилциннамата приводит к понижению интегральной светочувствительности, поскольку уменьшается вероятность образования поперечно-сшитой структуры молекул полимера продуктами фотолиза бисазидов. Вероятность рекомбинации
926
Новый справочник химика и технолога
продуктов фотолиза возрастает с увеличением содержания бисазида в слое выше оптимального. Светочувствительность системы зависит от молярной массы полимера, типа выбранного бисазида (квантового выхода его фотолиза), используемого растворителя и др.
При работе с фоторезистами, содержащими в качестве светочувствительной компоненты бисазиды, необходимо учитывать влияние кислородного эффекта, который особенно проявляется в тонких слоях (0,5 мкм и менее). Кислородный эффект заключается в том, что светочувствительная компонента под действием света разлагается, но продукты фотолиза взаимодействуют с кислородом воздуха и потому не участвует в образовании поперечных связей в молекулах полимера.
Введение азидной группы в молекулу светочувствительного полимера, например, поливинилциннамата, приведет к возрастанию светочувствительности слоя [14] (табл. 5.7.8).
Таблица 5.7.8
Значения светочувствительности полимеров [14]
Полимер S, отн. ед.
Поливинилциннамат (несенсиб.) 2,2
Поливинилацетат-З-азидофталат 50,0
Поливинилацетат-4-азидофталат 220,0
Поливинилацетат-н-азидобензоат 110,0
Сополимер стирола и малеинового ангидрида, этерифицированный Р-(4-азидофенокси)этанолом 120,0
При использовании слоев на основе поливинилового спирта, желатины, содержащих в качестве светочувствительной компоненты соли хромовой кислоты, образование сшитой нерастворимой структуры молекул полимера происходит также в несколько стадий. Под действием УФ-излучения (темновое дубление молекул полимера в присутствии солей хромовой кислоты не рассматривается) происходит образование ионов трехвалентного хрома, играющих роль сшивающего агента в данной светочувствительной системе. Светочувствительность слоев зависит от концентрации бихромата в слое (причем светочувствительность возрастает в широких пределах с увеличением содержания бихромата в слое) [15]. Лимитирующей стадией является реакция «сшивания» молекул полимера.
Реакция образования «сшитой» структуры в слоях типа «Дайкрил» также протекает в несколько стадий и порогов и светочувствительность данной системы довольно низка.
5.7.1.2. Спектральная чувствительность фоторезиста
Одной из важнейших характеристик фотографического материала является его спектральная чувствительность.
Один из основных фотохимических законов — закон Гротгуса — Дрепера: химическое изменение вызы
вают только те лучи, которые поглощаются веществом. Случай отступления от этого закона неизвестны. Следует помнить, что не все поглощаемые лучи приводят к химическим изменениям; некоторые из них хотя и поглощаются, но вызывают только нагревание системы. Не обязательно, чтобы свет, инициирующий химическую реакцию, поглощался реагирующим веществом; он может поглощаться и веществом, непосредственно не участвующим в реакции, но находящимся в тесном контакте с реагирующим веществом (сенсибилизированные фотохимические реакции). Световое излучение, воздействующее на фоторезист, вызывающее протекание фотохимических реакций и изменение растворимости облученных участков покрытия называется актиничным излучением.
Зная спектральную чувствительность фоторезиста, можно правильно выбрать эффективный источник облучения, определить возможность использования стеклянных фотошаблонов, сознательно подойти к выбору того или иного оптического сенсибилизатора, определить возможность использования фоторезиста в проекционной фотолитографии. В табл. 5.7.9 приведены данные по спектральной чувствительности вышеупомянутых светочувствительных систем.
Таблица 5.7.9
Спектральная чувствительность полимеров
Полимер А., мкм Хтах, мкм
Поливинилциннамат 240-365 280
Поливиниловый спирт 240-436 290-365
(хромированный)
Каучуки с бисазидами 248-436 265, 365
Нафтохинондиазиды 240-550 365, 404
Слои типа «Дайкрил» 240-340 300
Однако, если чувствительность поливинилциннамата к длинам волн в пределах 240-313 нм приблизительно одинакова, то она резко падает в более длинноволновой области и при Т = 365 нм в 350 раз ниже чувствительности в максимуме [13].
Введение оптических сенсибилизаторов позволяет расширить область спектральной чувствительности слоя до 436 нм (при введении 2-бензоилметилен-З-метил-р-нафтотиазолина). Новый максимум спектральной чувствительности появляется в этом случае при 404 нм. Введение таких сенсибилизаторов, как 1,2-бензантра-хинон и 9-метил-1,3-диазо-1,9-бензантрон, вызывает появление новых максимумов спектральной чувствительности слоя сенсибилизированного поливинилциннамата при 420 и 470 нм соответственно. При этом область спектральной чувствительности слоя расширяется до 470 и 490 нм соответственно [16].
Для позитивных фоторезистов на основе нафтохинондиазидов спад чувствительности начинается при длинах волн порядка 430-450 нм. Максимум чувствительности на кривых спектральной чувствительности выражен значительно слабее, чем в случае поливинилциннамата.
Химия фотографических процессов
927
Все это позволяет при работе с данными фоторезистами применять при экспонировании стеклянные фотошаблоны и использовать стеклянную оптику при проекционной фотолитографии и исключает острую необходимость введения оптических сенсибилизаторов с целью увеличения чувствительности данных фоторезистов к более длинноволновой части спектра.
Кривые спектральной чувствительности хромированного поливинилового спирта имеют резко выраженный максимум при 290 нм и слабо выраженный при 360 нм, и простирается до длин волн порядка 440 нм, что позволяет широко использовать стеклянные фотошаблоны в производстве точных печатных плат.
Спектральная чувствительность слоев каучуков с би-сазидами зависит от введения того или иного бисазида (рис. 5.7.1 и 5.7.2) и оптических сенсибилизаторов (табл. 5.7.10). Сенсибилизация происходит с триплетного уровня, т. е. оптический сенсибилизатор активен в триплетном возбужденном состоянии. Эффективность оптический сенсибилизации бисазидов зависит от температуры слоя в момент его облучения, особенно с уменьшением концентрации сенсибилизатора в слое. Это явление наблюдается уже при температуре облучения слоя 35 40 °C.
Рис. 5.7.1. Кривые спектральной чувствительности слоев фенольного циклокаучука, содержащего 4,4’(бисазидо)-дифенилметан, при введении оптических сенсибилизаторов: / — без введения сенсибилизатора; 2 — кетон Михлера;
3 — 2-бензоилметилен-З-метил-р-нафтотиазолин; 4 — бензатрон
Рис. 5.7.2. Кривые спектральной чувствительности слоев циклокаучука (ГИПИ-4), содержащих: -------4,4-бис(азидо)дифснилметан (33 масс. %); -------2,6-бис(4-азидобензаль)метилциклогексанон (И масс. %)
Далее приведены основные физико-химические факторы, определяющие эффективность оптического сенсибилизатора светочувствительных полимеров и бисазидов:
- интенсивность поглощения излучения сенсибилизатором;
- способность передавать поглощенную энергию молекулам светочувствительного полимера или бисазида: сенсибилизатор активен в триплетном состоянии;
- наличие «контакта» между взаимодействующими молекулами полимера или бисазида и оптического сенсибилизатора, т. е. такое распределение молекул сенсибилизатора в слое, при котором расстояние между центрами взаимодействующих молекул сенсибилизатора и акцептора (полимера или бисазида) равняется сумме их молекулярных радиусов;
- наличие следов растворителя в слое сенсибилизированного фоторезиста;
- температура слоя в момент экспонирования (повышение температуры приводит к увеличению эффективности действия сенсибилизатора).
5.7.1.3. Разрешающая способность фоторезистов
Разрешающая способность — одна из важнейших характеристик любого фотографического материала. Разрешающая способность фоторезиста равна максимальному числу линий на 1 мм поверхности, которое воспроизводится в слое фоторезиста. Для определения (7?сл) используют специальные штриховые миры. Мира состоит из 25 групп параллельных штрихов, разделенных промежутками той же ширины, что и штрихи. В каждой группе штрихов имеются четыре подгруппы, имеющие различное направление штрихов. Следует отметить, что, говоря о разрешающей способности применительно к фоторезистам, необходимо различать разрешающую способность фотолитографического слоя фоторезиста (7?сл) и разрешающую способность фотолитографического процесса (7?п). Первую определяют после проявления экспонированного слоя фоторезиста, вторую — после травления какого-либо материала, нанесенного на подложку. В последнем случае на разрешающую способность (7?сл) будут влиять тип и толщина стравливаемого покрытия, свойства травителя, адгезия фоторезиста к стравливаемому материалу, эффективность газообразования в процессе травления, температура травящего раствора и другие факторы. Разрешающая способность слоя фоторезиста, естественно, выше разрешающей способности фотолитографического процесса в целом, вследствие неизбежно имеющего место бокового подтравлива-ния стравливаемого материала под защитной маской фоторезиста.
На разрешающую способность слоя фоторезиста (7?сл) также влияют ряд факторов: тип фоторезиста (позитивный или негативный), толщина слоя фоторезиста, характеристика источника излучения (размеры светящегося тела, расположение источника излучения относительно штрихов изображения миры, расстояния его до слоя, спектральные характеристики); степень контакта между слоем фоторезиста с мирой в случае контактного экспонирования; чистота поверхности подложки.
928
Новый справочник химика и технолога
В табл. 5.7.11 приведены данные по разрешающей способности различных фоторезистов, выпускаемых промышленностью ряда стран. [16].
Можно видеть, что наибольшую разрешающую способность показывают позитивные фоторезисты на основе нафтохинондиазидов, поскольку в данных слоях не происходит укрупнения молекул под действием УФ-облучения. Ф.П. Прессом [16] показано, что в случае негативного фоторезиста дифракционное огибание света на краю непрозрачного элемента фотошаблона не играет существенной роли, а диффузионное рассеяние в слое сказывается больше, чем в случае позитивных фоторезистов. Существенное влияние на разрешающую способность негативных фоторезистов оказывает отражение света от подложки, которое приводит к образованию ореола вокруг защитных участков сшитого слоя (в результате чего и происходит понижение разрешающей способности слоя).
В табл. 5.7.12 приведены значения /?сл циклокаучука с бисазидом при различной толщине политого слоя. Экспонирование осуществляли контактным способом, используя вакуумный прижим миры к подложке со слоем фоторезиста. Минимальный размер штриха в используемом наборе мир составлял 1,25 мкм, что соответствует 400 лин./мм. Следует отметить, что при экспонировании слоев толщиной белее 6 мкм сшитый слой при проявлении снимался с подложки. Это можно объяснить тем, что излучение довольно полно поглощается в верхней части слоя как молекулами бисазида, так и продуктами их фотолиза, в результате чего излучение не проникает на глубину более 6 мкм при данной концентрации бисазида в слое (6 масс. % от веса циклокаучука). Поэтому слой, примыкающий к подложке, не сшивается и растворяется проявителем, в результате чего сшитый слой отделяется от подложки.
Таблица 5.7.10
Эффективность введения различных сенсибилизаторов [16]
Сенсибилизатор S, см2/(Вт • с) Эффективность по - 0,5 1 ^тах^ НМ
^лор = о,5
Амино-, нитросоединения
п-Нитроанилин 3,0 1,10 1,9 370
2-Нитрофлуорен 6,0 1,70 3,0 400
Кетоны
Бензофенон 6,0 1,80 3,1 280
N,N '-Тетраэтилдиаминобензофенон 6,0 1,90 3,3 365
МЛ'-Тетраметилдиаминобензофенон 6,0 1,90 3,3 365
Антроны
Бензантрон 3,0 1,70 3,0 320
Бромбензантрон 3,0 1,60 2,8
Дибромбензантрон 3,0 1,10 1,9
Тиазолы
2-Бензоилмегилен-3-метил-[3-нафтотиазолин 3,0 1,40 2,4 410
2-Бензоилметилен-З-метил-а-нафтотиазолин 3,0 1,00 1,7
Азины
Сафранин-Т 3,0 1,50 2,6 290
Хиноны
[З-Аминоантрахинон 3,0 1,00 1,7
Нафталины
Нафталин 3,0 0,70 1,2
Аценафтен 3,0 1,00 1,7
Оксазолы
3-Этил-5-фенил-оксазол-2 3,0 1,20 2,1 436
Пираны
1 -Бензоилантрапиридон 3,0 1,10 1,9
Химия фотографических процессов
929
Таблица 5.7.11
Характеристики фоторезисторов, используемых в полупроводниковой технологии
Фоторезист Тип Производство Граница спектральной чувствительности нм Разрешающая способность, лин./мм Кислото-стойкость2) Примечание
резиста травления оксида
Поливинилцинна-мат Негативный СССР 410 >500 200 15 ВТУ УПРПиК №871-65
Нафтохинондиазид с новолаком Позитивный 480 1000 300 60 РТУ № 13-64
«Kodak Photo Resist» (KPR) Негативный США, «Eastman 450 1000; 20 003) 250 20
«Kodak Ortho Resist» (KOR) Kodak Со.» >460 Чувствителен к зеленой линии ртутного спектра
«Kodak Thin Film Resist» (KTFR) 470 2000 Разработан специально для нужд микроэлектроники, характеризуется высокой разрешающей способностью
«Kodak Metal Etch Resist» (KMER) 450 50 Наиболее кислос-тоек (из резистов фирмы «Kodak»)
AZ-1350 Позитивный США, «Shipley Со.» 490 2000 770 Высокое разрешение достигается даже при толщине пленки 1,8 мкм
AZ-340 490 1000 Более стоек, чем AZ-1350, выдерживает действие растворов аммиака, электролитов, применяемых в гальванопластике
AZ-15, 17 500
«Kodak Resifax» Негативный Франция, «Kodak Pathe» 500 1000 250 15 Можно экспонировать под лампой накаливания
«Fuji Super Resist» Япония, «Fuji Со.» 450 25 Очевидно, аналогичен KMER
Указана примерно длинноволновая граница, нм.
2) Весьма приближенная оценка по глубине (мкм) рельефа, вытравленного в кремнии.
3) Данные электронно-лучевой фотолитографии.
930
Новый справочник химика и технолога
Таблица 5.7.12
Разрешающая способность слоев циклокаучука с бисазидом
Толщина политого слоя, мкм Разрешающая способность слоя R „, СЛ 5 лин./мм Разрешающая способность слоя /?ш, лин./мм
0,46 320 125
0,65 300 ПО
1,00 180 100
2,00 30 17
4,00 21 8
6,00 12 5
Можно видеть, что разрешающая способность слоев циклокаучука с бисазидом при толщине слоя 0,46 мкм равна 320 лин./мм и с увеличением его толщины значительно понижается и при 6 мкм равняется 12 лин./мм. При толщине слоя порядка 1 мкм она довольно высока и позволяет получать воспроизводимые штрихи шириной 5 мкм. Для получения более узких штрихов необходимо применять более тонкие слоя порядка 0,6 мкм и менее. Однако применение тонких слоев фоторезиста приводит к увеличению числа дефектов в слое, что усложняет проведение процессов фотолитографии [11].
Однако, говоря о разрешающей способности фоторезистов, на практике интересно знать, насколько точными по ширине получаются штрихи и промежутки проявленного изображения миры на слое фоторезиста по отношению к оптическому изображению миры. Другими словами, какой минимальный размер штриха может быть воспроизведен слоем фоторезиста. В связи с этим целесообразно определять значения /?“ . Величина показывает число штрихов и промежутков на 1 мм изображения миры в том случае, когда ширина штрихов отличается от ширины промежутков, передаваемых слоем фоторезиста не более чем на 5 %. Значение величины R™ дает возможность знать предельную наименьшую воспроизводимую ширину линии.
Разрешающая способность процесса, определяемая после травления, зависит от природы стравливаемого материала, его толщины и типа выбранного травителя, а также условий травления.
Следует отметить, что в процессе проявления и последующей сушки при комнатной температуре [18] экспонированного слоя уменьшается его толщина, что связано с переходом в раствор проявителя растворимых компонент слоя (например, рекомбинированные продукты фотолиза бисазида, несшитые молекулы полимера и др.). Уменьшение толщины слоя в процессе его обработки необходимо учитывать особенно в тех случаях, когда требуется получение контролируемой толщины слоя после проведения операций образования рельефа (например, в случае применения этих слоев в качестве ма
териала межслойной изоляции в многослойных пленочных схемах, т. к. величина усадки может достигать величин порядка 10-15 % от исходной толщины политого слоя при толщинах слоев 0,8-2,0 мкм).
5.7.1.4. Кислотостойкость фоторезиста
Под кислотостойкостью (одной из важнейших характеристик фоторезиста) понимают способность слоя фоторезиста противостоять действию кислот, в том числе таких, как азотная и плавиковая. Обычно [19] кислотостойкость характеризуется временем, в течение которого фоторезист выдерживает воздействие тех или иных растворов кислот. Окончание этого периода отмечают по появлению локальных, точечных растравливаний подложки в местах, покрытых фоторезистом (из-за микродефектов — посторонних включений, пустот, пылинок в слое фоторезиста); сильному растравливанию подложки по границам фоторезистивного рельефа или по краям окон в слое фоторезиста (из-за невысокой адгезии фоторезиста к подложке); разрушению или отслаиванию слоя фоторезиста (из-за нестойкости слоя фоторезиста, слабой адгезии к подложке).
Кислотостойкость фоторезиста на основе поливи-нилциннамата — удовлетворительная: он не выдерживает воздействия концентрированной плавиковой кислоты, однако устойчив к травителю, содержащему плавиковую кислоту в небольших концентрациях.
Повышенной кислотостойкостью обладают негативные фоторезисты на основе циклокаучуков с бис-азидами.
Кислотостойкость позитивных фоторезистов во многом определяется тем, какая полимерная основа этери-фицирована сульфохлоридом о-нафтохинондиазида. Как было показано М.С. Динабургом [15], кислотостойкость позитивного фоторезиста может быть увеличена путем хлорирования новолака. Положительные результаты дает введение в состав кислотостойких компонентов (например, лака марки 3-30-59, в состав которого входят эпоксиды).
Можно получить увеличение адгезии и кислотостойкое™ фоторезиста на основе продукта 383 введением в его состав эпоксида ЭД-5, предварительно сплавленного с новолаком К-18 в соотношении 1 : 5. После проявления слоя проводили его термообработку при 185-200 °C. Следует отметить, что без введения эпоксида термообработка слоя не приводила к уменьшению числа пор в защитном слое. Уменьшение числа проколов после травления указывает на то, что введение эпоксида улучшает смачивание подложки фоторезистом и адгезию слоя фоторезиста [16].
Щелочестойкость позитивных фоторезистов на основе нафтохинондиазидов крайне низка, слой разрушается даже в водном растворе аммиака. Введение 0,5-0,6 г поливинилбутираля на 100 мл фоторезиста позволяет выдерживать кратковременное воздействие 3—5% раствора едкого натра. Помимо этого поливинилбутираль улучшает пленкообразование и адгезию слоя.
Химия фотографических процессов
931
5.7.7.5. Диэлектрические свойства пленок фоторезистов
В некоторых случаях в качестве материала межслойной изоляции начинают применяться органические диэлектрики, такие как метилметакрилат, акролеин и др. Применение пленок из органических материалов имеет ряд преимуществ по сравнению с пленками из оксида кремния и оксидов металлов, а именно:
- возможность получения пленок из органических диэлектриков без создания больших температурных перепадов между осаждаемым материалом и подложкой, какие мы имеем при вакуумном осаждении неорганических материалов;
- органические пленки более стойки к гермоударам, чем пленки из оксида кремния и других неорганических материалов.
Применение пленок фоторезистов в качестве материала межслойной изоляции и защиты плат микросхем от внешнего воздействия дает еще ряд дополнительных преимуществ:
- уменьшение числа технологических операций, необходимых для создания пленочной микросхемы;
- легкость получения изоляционных пленок любой конфигурации и размера.
В работах Ф.П. Пресса [16] приведены данные о диэлектрических параметрах слоев поливинилциннамата: £ = 2-4, tg 8 = 0,064-0,082, ри = 101'-1012 Ом • м (измерения производились на частотах 1 и 5 кГц). Результаты проверки показали, что диэлектрические свойства слоев поливинилциннамата стабильны во времени.
В случае циклокаучука (ГИПИ-4) с бисазидами [21 ] получены следующие значения диэлектрических параметров изоляционных слоев, которые были определены при нормальных условиях и после воздействия ряда климатических факторов — (табл. 5.7.13).
Можно видеть, что диэлектрическая проницаемость испытуемых слоев довольно низка (1,7-2,1). Уменьшение значений £ и tg 8 при введении бисазидов и после действия УФ-облучения объясняется тем, что происходит образование сшитой структуры молекул циклокаучука продуктами фотолиза бисазида.
Характеристики промышленно выпускаемых фоторезистов строго определены рядом технических условий: ТУ-6-36-0206844-16-89; ТУ 6-36-0206844-15-89; ТУ 6-14-252-77; ТУ 6-14-632-86; ТУ 6-14-919-86; ТУ 6-14-19-4-0275-88; ТУ-6-14-09-05-83; ТУ 6-14-19-40504-87 и т. д. [22]; ТУ 6-17-369-77; ТУ 6-17-691-83 [23] (для пленочных фоторезистов).
В табл. 5.7.14 приведены [16] сводные требования к фоторезистам для полупроводниковой технологии. Трудно представить универсальный фоторезист, отвечающий всем перечисленным пунктам. Нужды планарной технологии производства полупроводниковых приборов более полно могут быть удовлетворены сочетанием негативного и позитивного фоторезистов.
Таблица 5.7.13
Значения диэлектрических параметров изоляционных слоев при нормальных условиях и после воздействия ряда климатических факторов
Условия испытания Определяемые параметры
tg8 £ pi-Ом • м
Циклокаучук + бисазид 1
Нормальные условия 0,0178 1,7-2,1 8,4 • 10й
После 5 термоциклов 0,0183 2,6 0,9- 10”
После воздействия температур (°C):
50 0,0184 2,45 0,9 • 10”
100 0,0180 2,50 0,3 • 10”
200 0,033 2,60 0,2 • 10”
После воздействия тропической влаги (сут):
10 0,0177 2,80 0,3 • 109
30 0,0174 2,70 0,2 • 108
Термостарение 720 ч 0,029 2,25 2 • 10”
Циклокаучук + бисазид 2
Нормальные условия 0,0185 1,7-2,1
Циклокаучук без введения бисазида
Нормальные условия 0,0632 2,54
Примечания:
1. Пробивное напряжение L/’np = 58 В/мкм (при нормальных условиях);
2. Бисазид 1 — 4, 4 -бис(азидо)дифенилметан (33 масс. %);
3. Бисазид 2 — 2.6-бис(4-азилобензаль)метилциклогек-санон (11 масс. %).
5.7.2. Технологический процесс фотолитографии
Основные понятия и определения процессов фотохимической технологии при создании фоторезиста.
Контактная маска — рельефное покрытие из пленки фоторезиста или другого материала, воспроизводящее заданные элементы рисунка и обеспечивающее защиту заданных участков подложки от последующего воздействия (травления, электроосаждения и т. д.).
Рельефное изображение, рельеф из фоторезиста — изображение элементов схем, сформированное пленкой фоторезиста после проявления [1].
Получение рельефного изображения из фоторезиста — на подложку наносят слой фоторезиста, который затем после предварительной сушки подвергают
932
Новый справочник химика и технолога
воздействию определенной дозы облучения, очень часто УФ-облучения. Между источником излучения и фоторезистом помещают фотошаблон с изображением элементов прибора, микросхемы.
Фотошаблон — стеклянная или иная пластинка, либо полимерная пленка со сформированным на ее поверхности рисунком элементов схем из материала, не пропускающего актиничное излучение.
Таблица 5.7.14
Сводные требования к фоторезистам для полупроводниковой технологии
Свойства Требования (наиболее жесткие) Применение (наиболее критическое)
Кислотостойкость Щелочестойкость Разрешающая способность Спектральная чувствительность Термостойкость Адгезионные свойства Пленкообразующие свойства Диэлектрические свойства Стабильность свойств Полнота удаления рельефа с подложки Смесь 48% плавиковой и 60% азотной кислот (1 :2) — 5 мин, 20 °C Плавиковая кислота (конц.) — 2 мин, 20 °C Азотная кислота (конц. и разб.) — 2 мин, 20 °C Соляная кислота (конц.) — 1 мин, 20 °C Царская водка — 5 мин, 20 °C Ортофосфорная кислота (конц.) — 65 °C Едкие кали и натр (10-30%), нагретые 2000 лин./мм при толщине пленки 0,3-0,5 мкм Около 500 нм (длинноволновая граница) Около 700 °C в вакууме, 5 мин К подложкам: полированному германию, кремнию, арсениду галлия; диоксиду кремния, при-месно-силикатным стеклам, пленкам металла Обеспечивать сплошные кроющие пленки без пор и дефектов при толщине от 0,2 до 5 мкм Проводимость 10 6 Ом“* • м"' при 5-50 В от -60 до +125 °C; диэлектрическая проницаемость: 3,5-4.5 Не менее 1 года Неизменность свойств подложки или характеристик приборов Кремниевые высоковольтные меза-диоды Пленки нитрида кремния Тонкопленочные приборы и схемы Хромовые фотошаблоны Пленки золота Пленки алюминия Кремний, алюминий Мощные высокочастотные транзисторы, интегральные схемы Проекционная фотолитография Контакты к кремниевым приборам Примесно-силикатные стекла Нанесение пульверизацией и центрифугированием Защита приборов от влияния внешней среды, межслойная изоляция Серийное производство Тонкопленочные приборы
5.7.2.1. Экологические требования
Вне зависимости от того, какой используется фоторезист существуют общие меры предосторожности для получения качественного результата. Прежде всего, это относится к окружающей среде, в которой выполняются технологические операции. Особо чувствительные к загрязнениям операции, а именно, очистка подложек, нанесение фоторезиста, совмещение фотошаблонов и экспонирование должны осуществляться в чистых комнатах, скафандрах с ламинарным потоком. Химические операции, в особенности проявление, промывание и разжижение фоторезистов, в которых используются органические растворители, могут привести к образованию
взрывоопасных и токсичных паров. Поэтому необходимо соответствующая вентиляция рабочего пространства.
Существует целый ряд нормативных документов, определяющих требования к рабочим помещениям фотолитографии, которые известны на каждом предприятии, где происходит изготовление изделий радиотехнической промышленности и электронной промышленности. Другим фактором, играющим весьма важную роль, является влажность воздуха в рабочем помещении. Адсорбция влаги поверхностью подложки перед нанесением фоторезиста может уменьшать адгезию пленки фоторезиста с подложкой. С другой стороны слишком сухая атмосфера приводит к образованию электростатического заряда
Химия фотографических процессов
933
и далее накоплению пылинок на поверхности подложек. Следовательно, относительная влажность в рабочем помещении должна поддерживаться в пределах 30-50 %.
5.7.2.2. Методы нанесения слоя на подложку фоторезиста
В случае жидких фоторезистов для нанесения слоя на подложку используют методы центрифугирования, пульверизации, окунания, вытягивания, полива. На малых скоростях центрифугирования слой фоторезиста неоднороден по толщине. Краевое утолщение занимает значительную часть площади пластины.
С увеличением скорости краевое утолщение уменьшается по ширине и смещается все ближе к периферии пластины. Слой становится более однородным по толщине. Толщина слоя уменьшается [16]. Для заданной концентрации резиста имеется определенная критическая скорость, превышение которой не вызывает дальнейшего уменьшения толщины слоя. Этот момент соответствует равновесию когезионных и центробежных сил. В табл. 5.7.15 представлены значения критической скорости и равновесной толщины резиста для трех значений концентрации [16].
Можно видеть, что второе нанесение увеличивает толщину слоев, хотя и не вдвое (за счет растворения). Согласно Ф.П. Прессу [16], скорость нанесения в целях увеличения воспроизводимости результатов всегда следует выбирать больше критической.
Таблица 7.15
Характеристика слоев фоторезиста (ПВЦ), нанесенных центрифугированием
Концентрация, масс. % 5,0 10,0 15,0
Критическая скорость, мин”' Равновесная толщина, мкм: одно покрытие два покрытия 600 0,30 0,35 800 0,40 0,50 1000 0,50 0,75
Плохая адгезия фоторезиста к подложке часто выявляется лишь на стадии избирательного травления (происходит растравливание, искажение рисунка) и причиной ее является некачественная подготовка подложки.
Локальные неоднородности рельефа слоя фоторезиста, имеющие вид вытянутых капелек размером около 0,1 мм и более, связаны с попаданием пылинок на подложку или присутствием посторонних частиц в фоторезисте. Нарушение рельефа получается из-за обтекания этих частиц фоторезистом во время его центрифугирования. Потому на практике рекомендуется фильтрация самого фоторезиста. Резисты фильтруют минимум 2-3 раза через стеклянные фильтры Шотта (№ 2, 3); в случае высокой вязкости применяют вакуумную фильтрацию. Метод пульверизации резистов характеризуется рядом достоинств [16]:
- хорошо контролируемая толщина пленки, широкие интервалы изменения толщины от 0,5 до 20 мкм;
- однородность по толщине, отсутствие утолщения на краях;
- отсутствие проколов и нарушений пленки, возникающих на дефектах подложки за счет центробежных сил при центрифугировании;
- возможность нанесения слоя резиста на профилированную подложку, в мельчайшие углубления и отверстия подложки;
- сравнительно малый расход фоторезиста;
- высокая производительность и широкие возможности для автоматизации;
- лучшая, по сравнения с центрифугированием, адгезия пленки к подложке.
Но в то же самое время данный метод требует специального подбора растворителей, т. к. слой должен стекать по подложке; тщательной очистки резиста и используемого для пульверизации воздуха или газа; наконец, разработки довольно сложного технологического оборудования.
Заимствованные из полиграфии простейшие методы нанесения слоя на подложку фоторезиста — купание в растворе и полив на нивелированную поверхность, не нашли широкого применения. Последний метод, правда, позволяет получать толстые слои фоторезиста (10-20 мкм) и обычно применяется при сенситометрии фоторезистов. Метод окунания (купания в растворе) позволяет наносить резист на обе стороны подложки, но практически всегда наблюдается клиновидность по толщине: в нижней части слой фоторезиста всегда значительно толще.
Метод вытягивания подложки из раствора фоторезиста позволяет получить более или менее равномерные по толщине пленки на подложках прямоугольной формы при резком различии между их шириной и длиной. Толщина пленки определяется вязкостью раствора и скоростью вытягивания подложки из кюветы. Для уменьшения испарения растворителей из кюветы зеркало делается соизмеримым с габаритами подложки.
В производстве печатных плат широкое применение нашли пленочные фоторезисты [23]. Они значительно технологичнее жидких фоторезистов, обеспечивают возможность нанесения рисунка схемы на заготовки с отверстиями. Наносятся на подготовленную поверхность плат посредством прокатывания их горячим валиком через защитную лавсановую пленку в установках— ламинаторах. Температура валков 100-120 °C. В том случае, когда СПФ наносится с целью защиты от вытравливания, используют фоторезист толщиной 20 мкм, для гальванических операций применяют пленку толщиной 40-60 мкм. В связи с тем, что при ламинировании выделяются газообразные продукты в виде хлорированных углеводородов — дихлорметан(мети-ленхлорид) и трихлорэтилен, в установках для ламинирования должна быть предусмотрена вытяжная вентиляционная система.
934
Новый справочник химика и технолога
Помещение, где производится накатка фоторезиста должно быть сухим (отн. влажн. 50 %) и обеспыленным.
После накатки СПФ платы выдерживают в течение 30 мин при комнатной температуре при неактиничном освещении для снятия внутренних напряжений в пленке, а также для образования химической связи с поверхностью подложки с целью повышения адгезии к подложке.
5.7.2.3. Сушка нанесенного слоя
В случае жидких фоторезистов завершающей стадией формирования слоя является операция сушки. Слишком быстрая сушка может провести к возникновению напряжений в пленке. В общем случае возникающие напряжения тем больше, чем больше растворителя удаляется из пленки и чем выше скорость испарения. Содержание оставшегося в слое растворителя в основном зависит от температуры сушки. Пределом повышения температуры сушки является термическое сшивание слоя. Поливи-нилциннамат сшивается при температуре 140-150 °C. Позитивные фоторезисты на основе нафтохинондиазидов нельзя сушить при температуре около 140 °C, так как слой перестает проявляться. В случае слоев на основе циклокаучуков с бисазидами нельзя повышать температуру сушки выше 125 °C, т. к. при этой температуре происходит термическое разложение бисазидов с образованием свободных радикалов, что приводит к сшиванию слоя фоторезиста.
В табл. 5.7.16 приведены режимы сушки слоев фоторезистов, предлагаемые Ф.П. Прессом [16].
Воможна инфракрасная сушка слоев, но по мнению Ф.П. Пресса [16] она эффективна лишь для формирования толстых слоев — порядка 3-5 мкм и выше; для обычных же толщин (0,3—0,4 мкм) различие в методах сушки мало заметно.
Обычно, роль первой сушки недооценивают, считая, что на этой операции достаточно удалить растворитель. Действительно, присутствие остатков растворителя может ослабить адгезию фоторезиста к подложке. Но, как показали исследования фирмы Кодак [9], при плохой сушке могут также изменяться требования к экспонированию, потому что растворитель препятствует образования поперечных связей и превращению функциональных групп. С другой стороны, если покрытие пересушено, то возможны нежелательные явления, например, «помутнения». Это обуславливается образованием в негативных фоторезистах термически активированных поперечных связей. В позитивных фоторезистах при этом может произойти плавление или разложение покрытия. В случае оптически сенсибилизированных негативных фоторезистов на основе каучуков с бисазидами полное удаление растворителя их слоя приводит к резкому снижению эффективности оптической сенсибилизации. Резкий уход растворителя из слоя приводит к образованию большого количества дефектов в пленке фоторезиста. Поэтому при разработке конкретных технологических процессов проведения фотолитографии следует уделять серьезное внимание операции первой сушки слоя фоторезиста, что одинаково важно, как для жидких, так и сухих фоторезистов.
Таблица 5.7.16
Режимы сушки фоторезистов [16]
Фоторезист Растворитель Толщина, мкм Выдержка Сушка
время, мин Г, °C время, мин Г, °C
Позитивный на основе нафтохинондиазидов Монометиловый эфир ацетатглико-ля (2 части) с диметилформами-дом (1 часть) и этилцеллозольвом (1 часть) 0,3-0,6 15±3 20±5 20±3 100±10
3,0-5,0 30±5 20±5 60±5 100±10
Негативный на основе поливинилцинна-матов Монометиловый эфир ацетатглико-ля (1 часть) с ксилолом (3 части) 0,3-0,6 15±3 20±5 20±3 100±10
5.7.2.4. Экспонирование
Экспонирование слоя производят УФ-источником излучения (А, = 300-М00 нм). Поскольку при экспонировании часть излучения отражается от подложки, то при передержках начинает полимеризоваться слой фоторезиста, прилегающий к поверхности, что приводит к ухудшению четкости рисунка. Следует отметить, что недопустим перегрев плат, так как он может привести
к прилипанию защитной пленки из лавсана к фоторезисту. После экспонирования заготовка плат выдерживается в темноте для завершения процесса полимеризации тех участков фоторезиста, которые подверглись воздействию света. Лавсановая пленка удаляется примерно через 30 мин после экспонирования. В табл. 5.7.17 приведены основные неполадки, встречающиеся при получении защитного рисунка с применением пленочных фоторезистов [23].
Химия фотографических процессов
935
Таблица 5.7.17
Основные неполадки, встречающиеся при получении защитного рисунка с помощью пленочных фоторезистов [23]
Вид дефекта Причина дефекта
Складки и вздутия в пленке Отслаивание пленки с заготовки Механические включения Плохое отделение лавсановой пленки при проявлении Набухание, приподнятые края, разрушение защитного рисунка Прилипание фотошаблона к пленке при экспонировании Вуаль, уменьшение ширины линий или зазоров Смещение рисунка схемы относительно отверстий Закатка фоторезиста в отверстия Фоторезист не удаляется Плохая намотка рулона. Не отрегулировано натяжение в пленке Плохая подготовка поверхности заготовок. Нарушение режимов нанесения Загрязненность фоторезиста или воздушной среды помещения Повышенная температура или увеличенное время при экспонировании Недостаточное экспонирование. Передержка при проявлении. Нарушение режимов нанесения Завышена температура в зоне экспонирования. Несоответствие времени выдержки характеристикам ламп Переэкспонирование, недостаточная оптическая плотность фотошаблона, nepeipeB при нанесении, экспонировании. Недостаточное время проявления и недостаточное давление проявителя Усадка фотошаблона. Неисправность оснастки для экспонирования. Ошибки при сверлении отверстий Неравномерная толщина СПФ. Дефекты валика в установке. Пыль и другие твердые частицы на валках Избыточная толщина гальванических покрытий. Загрязнен раствор для удаления. Недостаточно давление, под которым подается раствор
Выбор источника излучения для экспонирования того или иного фоторезиста определяется спектральным распределением светочувствительности данного резиста. Зная спектральные характеристики фоторезиста и источников, можно рассчитать, какой из них наиболее эффективен. Большие по площади источники света применяются редко и только в случае использования подложек больших размерах. Свет от таких источников — рассеянный и не позволяет выявить мелкие де
тали рисунка, поэтому он применим только для получения широких линий (от 50 мкм до 0,5 мм). Рисунки с тонкими линиями экспонируются точечным источником света, который создает поток почти коллимированного света, если он находится на достаточном удалении от подложки. Весьма эффективным источником излучения является ртутная лампа типа СВДШ [16]. Сдвиг кривой спектральной чувствительности в сторону длинных волн у позитивных фоторезистов на основе нафтохинондиазидов позволяет использовать источники меньшей мощности или сокращать время экспонирования. Известны фоторезисты (например, «Kodakresi-fax»), которые чувствительны к излучению ламп накаливания, что упрощает установку экспонирования, но зато налагает дополнительные требования по экранированию всех операций (нанесение фоторезиста, первая сушка и др.) от попадания света [16].
Правильность экспонирования зависит от типа и природы фотошаблона, толщины и технологических параметров фоторезиста. Основным условием качественного проведения операции экспонирования является определение оптимальной экспозиции, при которой обеспечиваются наилучшее качество и воспроизводимость результатов данного фотолитографического процесса. На практике для определения оптимальной экспозиции приготавливают серию контрольных слоев, экспонируемых с разными выдержками, проявляют их стандартным образом и контролируют полученное изображение с помощью МИИ-4 для определения толщины сшитого слоя (для негативного фоторезиста) и качество (полноту) проявления.
Для фоторезистов, содержащих белее двух светочувствительных компонент, закон взаимозаместимости не соблюдается [24]. Иными словами, удовлетворительное экспонирование при сравнительно низкой интенсивности излучения требует несоразмерно больших времен экспонирования по сравнению с экспонированием при высокой интенсивности излучения.
Следует учитывать, что спектральное распределение источника излучения со временем меняется, поэтому необходимо время от времени контролировать установленное время экспонирования.
5.7.2.5. Проявление и окончательная термообработка слоя
Процесс проявления для фоторезистов заключается в удалении (растворении) ненужных участков слоя, в результате на поверхности остается защитный рельеф требуемой конфигурации. В случае негативных фоторезистов процесс проявления заключается в удалении (растворении) несшитых участков слоя (иногда в том же растворителе, который использовался для приготовления резиста). В случае позитивных фоторезистов процесс проявления связан с химической реакцией превращения инденкарбоновых кислот в растворимые соли. Проявление позитивных слоев зависит от ряда факторов [16]:
936
Новый справочник химика и технолога
- тип проявителя (щелочное соединение, добавки и др.);
- время и температура проявления;
- дополнительное механическое удаление растворенных участков.
В качестве проявителя чаще всего используют сильно разбавленные водные растворы едкого натра или тринатрийфосфата. Наиболее оптимальным является проявление в 2% растворе гринатрийфосфата с глицерином при движении проявителя относительно слоя, поскольку в этом случае колебания во времени проявления сказывается меньше, а качество проявленного рельефа выше. Для негативных фоторезистов перепро-явление не является критичным при условии, что слой полностью сшит при экспонировании. Если слой недостаточно сшит, то при проявлении наблюдается его на
бухание, и после сушки слой морщится и теряет свои защитные свойства. В качестве проявителя слоев на основе ПВЦ, каучуков с бисазидами применяются трихлорэтилен, толуол, хлорбензол и другие проявители (см. табл. 5.7.1.-5.7.3). Наряду с окунанием в раствор проявителя, используют проявление в парах растворителей, а также пульверизацию.
Большое влияние на физико-химические свойства защитной пленки фоторезиста (адгезия, кислотостойкость, пористость и др.) оказывает термообработка слоя после проявления и сушки при комнатной температуре. Температура и время обработки пленки зависят от типа применяемого фоторезиста, его толщины и условий, в которых он будет использоваться в качестве защитной маски. Полученные результаты представлены в табл. 5.7.18.
Таблица 5.7.18
Зависимость температуры и времени обработки пленок от типа применяемого фоторезиста и условий, в которых он будет использоваться [47]
Фоторезист Стравливаемый материал Травитель Время травления, мин Г, °C т, мин
Фп-383 ФП-РН7 SiO2 HF + NH4F + H2O До 7 125-130 125-130 15 15
ФП-РН7 SiO2 hf + nh4f + h2o Свыше 7 В процессе травления до 150-175 По 15* между слоями
Фп-383 ФП-РН7 Al HNO3 + H3PO4 + H2O + CH3COOH 1 130 130 15 15
Фп-383 ФП-РН7 Au K3[Fe(CN)6] + H2NCSNH2 + + Na2S2O3 • 5H2O ДоЗ 130 130 15 15
ФП-РН7 Cr—Cu—SiCr HC1; HF + HC1; HNO3 + H2SO4 + + H3PO4 + CH3COOH + H2O До1 170 180 190 По 15* между слоями
ФП-РН7 Ni—Cu—Cr H3PO4 + H2SO4 + HNO3 + H2O + + CH3COOH; K3[Fe(CN)6] + KOH До1 150 15
ФП-РН7 V—Cu—SiCr H3PO4 + H2SO4 + HNO3 + H2O 4 + CH3COOH; HF + HC1 До1 170 180 По 15* между слоями
ФП-РН7 V—Cu—Cr HNO3 + H2SO4 + H3PO4 + H2O + + CH3COOH; HC1 До1 150 15
В случае последовательной фотолитографии через одну защитную маску фоторезиста.
Дополнительную последовательную термообработку пленки фоторезиста осуществляют при травлении (см. 5.7.2.6) остеклованного оксида на полупроводниковой подложке или при селективной фотолитографии при использовании одной защитной маски фоторезиста для стравливания 2-3 слоев металлов или сплавов, а также при травлении на большую глубину. Слой фоторезиста термообрабатывают при 170-180 °C, через окна в слое
вытравливают металл, затем проводят вторичную термообработку этого же слоя фоторезиста, но при более высокой температуре (порядка 200 °C) и дотравливают оставшийся слой металла. При вторичной термообработке зависающие над окном края фоторезиста (вследствие бокового подтравливания металла), размягчаясь, затекают на стенки окна, и при дальнейшем травлении исключается подтравливание этих участков.
Химия фотографических процессов
937
В случае использования негативного фоторезиста ФН-11 в качестве материала межслойной изоляции, защиты микросхем от внешнего воздействия или технологической защиты при УЗ-обработке подложек оптимальный режим термообработки слоя фоторезиста составляет 30 мин при 140 °C.
При использовании пленок ФН-11 в качестве защитной маски при получении элементов необходимой конфигурации (катушки индуктивности, шариковые выводы и др.) методом электрохимического наращивания меди в борфторидном электролите оптимальной температурой термообработки слоя является температура 125 °C.
Термообработка слоев фоторезистов при повышенных температурах оказывает существенное влияние на физико-химических свойства (механическую прочность, адгезию, усадку, спектральное поглощение) негативного фоторезиста ФН-11 (на основе циклокаучука с бисазидом) и позитивного ФП-РН2-7В. Механическую прочность определяли путем царапания иглой пленки фоторезиста, нанесенной на стеклянную подложку, при приложении определенной нагрузки; диаметр острия иглы 0,8 мкм. Усилие царапания (прорезания пленки фоторезиста) определяли с помощью прибора ПМТ-3, при этом образец с нанесенным слоем фоторезиста передвигался с постоянной скоростью по отношению к закрепленной игле, к которой прикладывалась определенная нагрузка. Данный метод позволяет определять минимальное значение нагрузки, оказывающее воздействие на пленку фоторезиста (появление видимого следа под микроскопом) и максимальную нагрузку, которую может выдержать пленка данного фоторезиста (повреждение пленки на 100 % его начальной толщины). В последнем случае величина нагрузки может характеризовать величину адгезии пленки фоторезиста к подложке. Толщину пленок фоторезиста определяли с помощью МИИ-4.
Термообработку пленок фоторезистов вели на воздухе в термостате с термостатированием ±5 °C и постепенным подъемом до заданной температуры со скоростью порядка 10°С/мин. Термообработку образцов проводили при температуре от 150 до 450 °C в течение 15 мин. После термообработки и выдержки образцов при комнатной температуре не менее часа определяли влияние приложения нагрузки на глубину процарапывания пленки фоторезиста (см. рис. 5.7.3 и 5.7.4). Можно видеть, что кривые имеют две характерные точки: появление видимого следа процарапывания и переход к удалению слоя фоторезиста с подложки. Последняя величина нагрузки характеризует адгезию слоя фоторезиста к подложке [25]. Первая точка характеризует механическую прочность термообработанной пленки фоторезиста (стойкость к истиранию).
Наличие точек перегиба на кривых рис. 5.7.3 и 5.7.4 показывает, что в этих точках прочность когезионной связи в пленках фоторезиста превышает адгезионную прочность слоя к подложке. Изменение температуры
термообработки для пленок сшитого фоторезиста ФН-11 в интервале 120-150 °C практически не влияет на их механическую прочность. Дальнейшее повышение температуры термообработки приводит к значительному повышению механической прочности слоя, очевидно, вследствие уплотнения структуры пленки фоторезиста и удаления низкомолекулярных продуктов. Влияние температуры термообработки на механическую прочность пленок позитивного фоторезиста проявляется уже при повышении температуры до 150 °C за счет термолиза нафтолизованных хинондиазидных групп, упрочнения рельефа с образованием неплавких и нерастворимых структур значительно большей молекулярной массы [6]. Повышение температуры свыше 300 °C для слоев позитивного фоторезиста и 450 °C для ФН-11, вплоть до выгорания, не приводит к повышению их механической прочности. Определение адгезии термообработанных пленок фоторезистов ФН-11 и ФП-РН2-7В проводили по методике, предложенной Г.А. Старожук [26].
Рис. 5.7.3. Зависимость глубины процарапывания 5 пленок фоторезиста ФН-11 от приложенной нагрузки Р при различных температурах термообоаботки:
/ — без термообработки; 2 — 150 °C; 3 — 200 °C; 4 — 250 °C; 5 — 300 °C; 6 — 350 °C; 7 — 400 °C; 8 — 450 °C
Рис. 5.7.4. Зависимость глубины процарапывания 5 пленок фоторезиста ФН-РН2-7В от приложенной нагрузки Р при различных температурах термообоаботки:
/ — без термообработки; 2 — 150 °C; 3 — 200 °C; 4 — 250 °C;
5 — 300 °C; б — 350 °C; 7 — 400 °C
На рис. 5.7.5 показаны зависимости нагрузки, необходимой для появления видимой линии процарапывания пленки, от температуры термообработки образца. Наибольшая механическая прочность пленок негативного и позитивного фоторезистов достигается при различных
938
Новый справочник химика и технолога
температурах термообработки: для ФН-11 она составляет 350—400 °C, а для ФП-РН2-7В значительно ниже — 250 °C. Механическая прочность пленок негативного фоторезиста ФН-11 несколько выше, чем пленок позитивного фоторезиста (при обработке при оптимальных температурах).
Рис. 5.7.5. Зависимость начала появления видимой линии процарапывания Р пленок фоторезистов от температуры термообработки:
1 — фоторезист (ФН-11); 2 — фоторезист (ФН-РН2-7В)
т, С
100 200 300 400 500
Рис. 5.7.6. Температурно-временные зависимости адгезионной способности образцов с пленками фоторезистов: 1 — негативного (ФН-11); 2 — позитивного (ФН-РН2-7В)
Рис. 5.7.7. Зависимости адгезионной способности пленок фоторезистов от времени термообработки:
/ — негативного (ФН-11) при постоянной температуре 350 °C;
2 — позитивного (ФН-РН2-7В) при постоянной температуре 200 °C
Кривые на рис. 5.7.6 показали, что для ФН-11 имеют место два явно выраженных максимума: при — 130 °C, предшествующий понижению адгезии, и резко выраженный при 350 °C. При температурах выше 450 °C происходит полное сгорание полимера. Повышение адгезии происходит, очевидно, вследствие
структурных изменений в молекулах полимера за счет взаимодействия с кислородом воздуха и разрыва связей в результате воздействия повышенных температур. В случае образцов позитивного фоторезиста наблюдалось постепенное увеличение адгезионной способности с возрастанием температуры термообработки (с максимумом при 250 °C), сопровождающееся возрастанием их механической и химической стойкости. Из кривых, приведенных на рис. 5.7.7 видно, что оптимальное время термообработки составляет 15 мин.
(«)
X, нм
(б)
Рис. 5.7.8. Зависимость коэффициента пропускания слоя негативного фоторезиста ФН-11 (а) и позитивного фоторезиста ФП-РН2-7В (б) действующего излучения при различных температурах термообработки слоя
Из кривых, приведенных на рис. 5.7.8 можно видеть, что наряду с изменением механических свойств, происходит и изменение оптических характеристик в области длин волн излучения 300-900 нм. Коэффициент отражения обоих фоторезистов в малой степени зависит от температуры термообработки. В случае ФН-11 пленки (при 350 °C) наряду с низким пропусканием в УФ-области спектра сохраняют достаточно высокую прозрачность в области видимых длин волн, поэтому данные слои могут быть использованы в качестве маскирующего покрытия для изготовления бессеребряных фотошаблонов. Одной из важнейших стадий получения требуемой конфигурации элементов является электрохимическое наращивание или химическое травление с целью получения топологии рельефного рисунка в технологическом слое с последующим удалением слоя
Химия фотографических процессов
939
фоторезиста. Как и все предыдущие технологические процессы фотолитографии: выбор фоторезиста, его нанесение на подложку, экспонирование и термообработка, качество получаемого рисунка методом травления в значительной степени определяется искусством оператора. Все операции фотолитографии связаны между собой и изменение режимов проведения той или иной операции ведет к изменению режимов проведения последующих операций.
5.7.2.6. Травление
Химическое жидкостное травление основано на растворении в химических реагентах незащищенных маской фоторезиста участков технологического слоя и состоит из ряда стадий: диффузии и адсорбции молекул травителя к поверхности подложки, химической реакции, десорбции продуктов реакции и удаления их из раствора.
Применяемые травители должны:
- обладать селективностью, т. е. способностью активно вступать в реакцию с основным технологическим слоем, не взаимодействуя с пленкой фоторезиста и нижележащими технологическими слоями;
- не образовывать продуктов реакции (сильное газо-выделение), способствующих отслаиванию пленки фоторезиста по контуру элементов рисунка и подтравливанию;
- допускать возможность подбора оптимальной для данных условий скорости травления, обеспечивающей минимальную плотность дефектов полученного рисунка.
К сожалению, процесс жидкостного травления изотропен, т. е. неизбежно приводит к боковому подтравливанию элементов рисунка.
Результат травления зависит от качества сформированного защитного рельефа фоторезиста, его адгезии, клина травления, типа травителя, температуры травления и толщины стравливаемого материала.
Почти все металлы, используемые для создания печатных токонесущих линий, травятся в системах, содержащих различные неорганические кислоты. При взаимодействии кислот с металлами происходит выделение газообразных продуктов, отрицательно влияющих на защитные свойства фоторезистов, что увеличивает степень бокового подтравливания металла. С увеличением концентрации неорганической кислоты в растворе и его температуры степень бокового подтравливания повышается. Учитывая это, необходимо подбирать такие травящие системы и условия травления, чтобы не происходило нарушения сцепления слоя фоторезиста с поверхностью стравливаемого материала по краю рисунка печатных элементов микросхемы. Последнее может быть достигнуто путем снижения температуры травителя, либо увеличением его вязкости.
Медь является основным материалом для создания токонесущей части микросхемы. Медь не вытесняет водород, поэтому ее травление можно вести только в тех системах, которые содержат окислитель меди и ве
щества, растворяющие образующийся оксид. Широкое распространение на практике получила система травления, содержащая в своем составе следующие компоненты:
HNO3 + Н3РО4 + СН3СООН + Н2О
Для изменения скорости травления в данной системе в зависимости от требуемого размера элементов и их компоновки можно предложить различные соотношения кислот Н3РО4 и СН3СООН. Эту травящую систему можно представить как слабый раствор азотной кислоты. Так как окисляющим агентом является азотная кислота, то, следовательно, скорость травления зависит от концентрации азотной кислоты, подведенной к поверхности стравливаемого металла. Уксусная и фосфорная кислоты растворяют оксид меди, но при этом фосфорная кислота образует слабо диссоциирующие продукты, что способствует замедлению скорости реакции. Кроме того, фосфорная кислота увеличивает вязкость системы, способствует более равномерному подводу азотной кислоты к поверхности меди, следовательно, более равномерному стравливанию материала и уменьшению бокового подтравливания. Наличие фосфорной кислоты в травящей системе позволяет использовать травитель многократно в течение длительного времени (10-15 дней), так как наличие слабо диссоциирующих продуктов не дает возможности для образования нерастворимого соединения Си(ОН)2 при насыщении травителя ионами меди.
Следовательно, регулирование скорости травления меди в данной системе травления возможно путем изменения соотношения уксусной и фосфорной кислот при постоянном содержании азотной кислоты и температуре гравящего раствора. Следует отметить, что содержание азотной кислоты в системе должно быть минимальным для того, чтобы ее роль заключалась лишь в окислении меди, а растворение СиО происходило бы благодаря наличию в системе фосфорной и уксусной кислот.
При травлении слоев меди толщиной порядка 3-5 мкм для получения линий шириной порядка 50-30 мкм при высокой плотности компоновки проводников хорошие результаты можно получить в травящем растворе с повышенным содержанием фосфорной кислоты, мл:
Уксусная кислота 15
Фосфорная кислота 70
Азотная кислота 3
Вода 59
Температура раствора 17-25 °C, скорость травления 1-1,5 мкм/мин.
При травлении слоев меди толщиной более 5 мкм можно рекомендовать травитель на основе этих же компонентов следующего состава, мл:
940
Новый справочник химика и технолога
Уксусная кислота 66
Фосфорная кислота 17
Азотная кислота 17
Вода 50
Такое изменение соотношения уксусной и фосфорной кислот в травящей системе приводит к значительному увеличению скорости травления меди при той же температуре травящего раствора. Однако из-за уменьшения вязкости среды происходит увеличение газообразования по краю пленки фоторезиста, что приводит к возрастанию степени бокового растравливания элементов по сравнению с результатами при использовании первого раствора.
При травлении меди в указанных системах степень подтравливания зависит от толщины пленки фоторезиста. Чем тоньше пленка фоторезиста, тем меньше величина усадки ее после термообработки, но уменьшение толщины пленки приводит к уменьшению ее механической прочности, при воздействии агрессивных сред пленка фоторезиста растрескивается. Введение эпоксида ЭД-5 в состав позитивного фоторезиста дает возможность получать хорошие защитные свойства пленки фоторезиста даже при ее толщине 0,4-0,6 мкм, стравливая слои меди до 10 мкм. При этом степень подтравливания определяется лишь толщиной стравливаемого слоя и составляет 5-6 мкм при толщине меди 4-6 мкм.
Следует отметить, в указанных травителях меди одновременно происходит стравливание никеля.
При травлении меди в системах, содержащих в своем составе вещества, образующие с Си+ стойкие комплексы, таких как NH4NO3, NH4C1, (NH4)2CO3, К4Р2О7, не происходит выделения газообразных продуктов, что уменьшает подгравливание проводников под слоем фоторезиста (не происходит нарушения сцепления пленки фоторезиста с поверхностью стравливаемого материала). Правда, скорость травления меди в таких растворах значительно ниже (в 1,5-2 раза) по сравнению с выше приведенными растворами меди. Но благодаря малой агрессивности среды даже при времени травления порядка 10 мин не происходит разрушения пленки фоторезиста. В качестве окисляющего агента в таких травящих системах [28] применяют медные соли: CuCl2, CuSO4, CuO3, Cu(NO3)2, (СН3СОО)2Си.
Один моль меди(И) окисляет один моль металлической меди (с нулевой степенью окисления) до двух молей меди(П):
Си°+ Си+-----► 2Си
2Си
+ °2 2+
-----► 2Си
Соотношение окислителя и комплексообразователя в данной системе 1 : 2. Скорость травления меди в этом случае является функцией pH раствора. Максимальная
скорость травления достигается при pH = 7,3-^7,5. Для поддержания постоянного значения pH раствора применяют НС1 и NH4OH.
В табл. 5.7.19 приведены примерные составы травителей (I-1V) меди.
Таблица 5.7.19
Состав травителей [28]
Пояснение. Температура травящих растворов 65-75 °C.
Травитель Концентрация, г/л
I II Ill IV
CuSO4 • 5Н2О СиС12 • 2Н2О К4Р2О7 50 50 50 50 100
NH4NO3 100 100 50
nh4ci 100 100 50
Монометанолам ин V2O5 200 25 200 150
При травлении меди в приведенных травящих растворах нет необходимости осуществлять зачистку схемы после травления, так как растворение металла по всей поверхности подложки происходит равномерно в отличие от травления пленок меди в травителях на основе уксусной и фосфорной кислот. Данными травителями можно пользоваться в течение длительного времени при условии своевременной корректировки pH раствора.
Состав травителей меди для производства печатных плат подробно описан в пособии В.А. Ильина [23], а также даны рекомендации по наиболее эффективным травителям, основные характеристики ряда применяемых в производстве растворов, рассмотрены требования, предъявляемые к травильным растворам.
В производстве печатных микросхем хром применяется в качестве адгезионного подслоя под медь, а также для создания резисторов. Обычно травление хрома осуществляют в разбавленных серной или соляной кислотах с применением металлического алюминия в качестве инициатора реакции. Травление весьма агрессивное (время травления — секунды), что затрудняет получение точных размеров резисторов.
В случае селективного травления при изготовлении микросхем с резисторами с точно заданными размерами наилучшие результаты достигаются при травлении хрома в растворе красной кровяной соли.
Травление «мягкое», без выделения газообразных продуктов. Данный травитель хрома содержит некоторое количество КОН. При взаимодействии КОН с красной кровяной солью происходит образование желтой кровяной соли по реакции:
2К3 [Fe(CN)6] + 2KOH----->
---->2К4 [Fe(CN)6] + H2O + 0,5О2
Химия фотографических процессов
941
и уже последняя, взаимодействуя с металлическим хромом, связывает его в комплекс [29].
Как и в случае травления меди, скорость травления хрома определяется pH среды. Максимальная скорость травления достигается при pH = 13,2^-13,5 (при дальнейшем увеличении pH раствора происходит разрушение фоторезиста ФП-383 даже с добавкой эпоксида ЭД-5). В состав травителя хрома входят:
K3[Fe(CN)6] 30 г
2% КОН 100 мл
Скорость травления в указанном составе значительно ниже, чем в неорганических кислотах НС1 и H2SO4. Например, слой хрома толщиной 0,06 мкм стравливается в составе с красной кровяной солью в течение минуты, тогда как в НС1 он стравливается мгновенно. Но, с другой стороны, при травлении в неорганических кислотах равномерность стравливания и качество получаемого рисунка зависят от режимов напыления хрома. Чем выше температура напыления, тем труднее добиться полного и равномерного стравливания хрома с подложки.
При травлении в составе с красной кровяной солью режимы напыления не влияют на полноту стравливания и качество получаемого рисунка. Кроме того, травление в данном составе дает возможность использовать хром и в качестве резистивного слоя, и в качестве защиты меди от атмосферного воздействия одновременно.
Алюминий часто используют для создания устройств на поверхностных активных волнах, для получения электродов с малыми размерами и промежутками между ними [30].
При защите позитивными резистами в основном при травлении алюминия [16] пользуются нагретой орто-фосфорной кислотой, либо «холодным» травителем, состоящим из смеси ортофосфорной, уксусной и азотной кислот и воды. Ортофосфорная кислота имеет большую вязкость, поэтому удаление пузырьков водорода, образующихся при травлении, затруднено; удалять же их необходимо для того, чтобы не оставались непротравленные участки — характерные круглые «пятачки» алюминия. Из-за повышенной вязкости скорость травления ограничена диффузией молекул травителя и, следовательно, зависит от толщины слоя алюминия.
Для тонких слоев алюминия (не толще 1,6 мкм) можно рекомендовать 45% раствор ортофосфорной кислоты при 60±1 °C.
Для толстых пленок (5-10 мкм) рекомендуется раствор:
Ортофосфорная кислота (оотн = 1,73) 60 мл
Изопропиловый спирт 15 мл
Деионизованная вода 10 мл
Количества указаны для одновременной обработки 10 пластин; скорость травления 0,33 мкм/мин, температура 60±1 °C.
Соотношения компонентов в «холодных» травителях могут быть следующими [16]:
Ортофосфорная кислота (оотн = 1,73) 12 ч.
Уксусная кислота 5 ч.
Азотная кислота 2 ч.
Вода 1 ч.
а также:
Ортофосфорная кислота (оотн = 1,73) 75 ч.
Уксусная кислота 15 ч.
Азотная кислота 3 ч.
Вода 5 ч.
При работе с этими травителями также с успехом применяется вибрация. Уменьшить вредное влияние вязкости травителя помогает вибрация с частотой 30-50 Гц и малой амплитудой; скорость травления при этом возрастает, а ее зависимость от толщины слоя ослабевает.
При работе с негативными фоторезистами появляется возможность использования щелочных травителей. Так, в случае применения фоторезиста на основе циклокаучука с бисазидами можно успешно использовать травитель состава [30]:
Едкий натрий 1 г
Желтая кровяная соль 88 г
Вода 800 мл
Температура раствора комнатная, скорость травления 0,5 мкм/мин.
В случае травления термостабильного сплава 44НХМТ, который используется при изготовлении ДУЛЗ с отражательными решетками [31] применяется травитель на основе хлорида железа.
Время травления на глубину 7-8 мкм в растворе хлорида железа в присутствии азотной кислоты составляет 8-10 мин, а в растворе хлорида железа (с относительной плотностью 1,30) без азотной кислоты 1,0-1,5 мин. Кроме того, введение кислоты увеличивает боковое подтравливание под пленку фоторезиста (пленочный фоторезист СПФВ), что ухудшает качество получаемых линий задержки. Поэтому предпочтительнее использовать травитель, содержащий хлорид железа с относительной плотностью 1,30 без кислоты. Травление производится при комнатной температуре.
Для создания конфигурации пленочных элементов в процессе фотолитографии используют селективное растворение многослойных структур, осажденных в едином технологическом цикле вакуумного напыления. На подложки последовательно напыляют резистивную пленку и структуру контактных площадок, состоящую обычно из двух-трех материалов. С целью получения тонкопленочных резисторов (ТПР) и проводников с контактными площадками применяют двойную фотолитографию. Первая фотолитография — для суммарного резистивного и проводящего слоев, вторая — для снятия
942
Новый справочник химика и технолога
проводящего слоя с резистивной пленки избирательным травлением [10]. При двойной фотолитографии производят тщательный выбор травителей, селективно воздействующих на материал или группу материалов в соответствии с конструкцией ТПР. Ряд травителей для проведения фотолитографических процессов с избирательным травлением структур «резистивная пленка— контактная площадка» приведены в табл. 5.7.20.
Таблица 5.7.20
Травители для избирательного травления структур ТПР [10]
Структура ТПР Травители
Хром—медь—никель С г—Cu—Ni Нихром—медь—никель NiCr—Cu—Ni РС-3710—хром— медь—никель РС-3710—С г—Cu—Ni Рений—хром—никель Re—С г—Ni РС-3710—нихром— медь—никель РС-3710—NiCr—Си— Ni МЛТ-ЗМ—ванадий— медь МЛТ-ЗМ—V—Си МЛТ-ЗМ—нихром— медь МЛТ-ЗМ—NiCr—Си Для Cu—Ni — 38% HNO3. Для Сг — раствор состава: NaOH — 20 г/л; K3Fe(CN)6 — 300 г/л; вода — 1 л Для Си—Ni — 38% HNO3 Для NiCr —НС1 Для Си—Ni — 38% HNO3 Для Cr раствор состава: NaOH — 20 г/л; K3Fe(CN)6 — 300 г/л; вода— 1 л. Для РС-3710 смесь состава: HNO3 — 30 г; HF— 10 г; НС1 —0,50 г Для Ni — 38% HNO3 Для Re раствор состава: NAOH — 20 г/л; K3Fe(CN)6 — 300 г/л; вода — 1 л Для Си—Ni — 38% HNO3 Для РС-3710 смесь состава: HNO3 — 30 г; HFe — Юг; НС1 — 0.50 г. Для NiCr — HCI Для Си раствор состава: Н3РО4 — 40 мл; HNO3 — 10 мл; СН3СООН — 10 мл; вода — 40 мл. Для МЛТ-ЗМ смесь состава: НС1 —45 мл; HF — 5 мл; вода — 50 мл, ИЛИ НС1 — 30 мл; HF — 10 мл. Для Си — любой из травителей Для Си (см. выше). Для NiCr — соляная кислота. Для МЛТ-ЗМ смесь состава: HNO3 — 35 мл; HF — 5 мл; вода — 60 мл
Окончание табл. 5.7.20
Структура ТПР Травители
МЛТ-ЗМ—ванадий— алюминий (Си) МЛТ-ЗМ—V—A1 (Си) МЛТ-ЗМ—ванадий— алюминий (Си) МЛТ-ЗМ—V—A1 (Си) Для V—А1 раствор состава: Н3РО4 — 40 мл; HNO3 — 10 мл; СН3СООН— 10 мл; вода — 40 мл. Для МЛТ-ЗМ смесь состава: HNO3 — 35 мл; HF — 5 мл; вода — 60 мл
Молибден химически менее активен, чем хром: хром травится в разбавленной соляной и серной кислотах, молибден не поддается травлению (растворяется в горячих кислотах).
Травление молибдена осуществляют в смеси кислот, например, азотной и соляной (3:1) или азотной и серной: 12 ч. азотной кислоты, 1 ч. серной кислоты, 7 ч. воды [16]. Скорость травления ~0,8 мкм/мин, окончание травления точно зафиксировать трудно, поэтому наблюдается значительная неоднородность результатов. Лучшее качество фотолитографии наблюдается при использовании более медленных травителей, состоящих из смеси азотной, ортофосфорной и уксусной кислот. В табл. 5.7.21 приведены рецептуры травителей. Скорость травления в них лежит в пределах от 0,2-0,25 мкм/мин (травители № 3 и 4) до 0,66 мкм/мин (травитель № 5).
Таблица 5.7.21
Составы травителей молибдена [16]
Вещество Соотношение компонентов, ч.
1 2 3 4 5
Ортофосфорная кислота 15 75 7 2 15
Азотная кислота 7 3 1 1 2
Уксусная кислота 3 15 1 2 3
Вода 1 5 1 2 1-3
Для электролитического травления с защитой фоторезистом применяют [32] электролит следующего состава: 40 % ортофосфорной кислоты, 16 % серной кислоты, 43,5 % воды, 0,5 % поверхностно-активного вещества. Плотность тока 1,16 А/см2 температура 60 °C. Можно также травить в 30% серной кислоте при плотности тока 0,1 А/см2 и комнатной температуре.
Вольфрам. Для травления вольфрама используют смесь аммиака с пероксидом водорода в соотношении 3 : 2 или 4 : 3 [33]. Скорость травления 40 нм/мин, причем рекомендуется нагревать травитель до 30 °C и применять ступенчатое травление с промежуточными стадиями промывки и сушки при 160 °C в течение 5 мин. Можно также применять травитель следующего состава [34]: 1 ч. NaOH, 3,5 ч. K3Fe(CN)6,75 мл воды. Однако у обоих травителей мала скорость травления и большие значения pH. Для снижения степени воздействия на пленку фоторезиста предложено [16] использовать травители, в которых гексацианоферрат(ферроцианид)
Химия фотографических процессов
943
калия сочетается со слабыми основаниями, такими, как этилендиамин или аммиак, например 0,5 М этилендиамина — 0,5 М НС1, 0,1 М K3Fe(CN)6 [35]. У такого травителя pH = 7,5^-9,5 и скорость травления велика (1 мкм/мин).
Вольфрам хорошо травится электролитически с защитой негативным фоторезистом в составе: 5 % КОН, 5 % K3Fe(CN)6, 1 % поверхностно-активного вещества, остальное вода. Скорость травления 5 нм/с при плотности тока 200 мА/см2 [36].
Тантал. Травят в смеси азотной и плавиковой кислот в соотношении 1 : 1 [34].
Золото. Можно травить в царской водке, но наиболее приемлемые результаты дает травитель, состоящий из иодида калия, иода и воды [37].
Кермет. Рекомендуется [16] применение «взрывной» фотолитографии, т. к. трудно подобрать травитель, обеспечивающий хорошее качество при обычном травлении.
На маску позитивного резиста толщиной более 1 мкм наносят при температуре подложки 300 °C подслой ванадия толщиной 0,5 мкм и затем слой кермета толщиной 0,2 мкм, после чего «взрывали» фоторезистив-ную маску в 54% азотной кислоте [38].
На 1 ч. этого правителя добавляли 5 ч. этиленгликоля и 4 ч. воды. Такой состав позволяет проводить фотолитографию по золоту в системе золото—молибден, не действуя на молибден; скорость травления 0,36 мкм/мин [39].
Платина. Применяют нагретые смеси азотной кислоты с фтористоводородной (1:5, 70 °C) [40], либо с соляной кислотой.
Арсенид галлия. Для изотропного травления используют составы:
- 1 ч. брома и 1000 ч. метанола;
- 1 ч. 30% перекиси водорода, 5 ч. серной кислоты и 1-2 ч. воды;
- 3% раствор гипохлорита натрия.
Обычно применяют дополнительную защиту оксидами кремния или алюминия. Растравливание даже с защитой оксида достаточно сильное — до 20 мкм при размерах окна 100 мкм и глубине травления 25 мкм. Такое большее растравливание и неровность дна лунок, вероятно, связаны [ 16] с адсорбцией молекул травителя на границах оксидной маски; это затрудняет диффузию молекул. Применение травителя 0,7 М Н2О2 + 1 М NaOH, для которого лимитирующим фактором является не диффузионный, а химический механизм, позволяет улучшить качество фотолитографии на негативном фоторезисте. Арсенид галлия, так же, как и другие интерметаллические соединения, можно травить в смесях азотной, фтористоводородной и уксусной кислот, аналогично кремнию.
Анизотропное травление арсенида галлия осуществляют в составе: Н2О2 — NH4OH [40]. Скорость травления составляет 0,1-0,2 мкм/мин при травлении пластины, ориентированной по плоскости (100).
Арсенид индия, фосфид галлия, антимонид индия. Для травления арсенида индия пригодны составы [41], из которых для фотолитографии чаще [16] применяют следующий: 3 ч. азотной кислоты, 1 ч. фтористоводородной кислоты и 2 ч. воды. Травление при комнатной температуре со скоростью около 40 мкм/мин для плоскости (111).
Фосфид галлия травят в смесях азотной кислоты с соляной или фтористоводородной 1 : 1 [41].
Антимонид индия можно травить в этих же смесях, добавляя, если нужно замедлить реакцию, 1 ч. воды.
Диоксид кремния. Для травления термически выращенного диоксида кремния используют составы на основе фтористоводородной кислоты и фторида аммония [16]. Рекомендуемый в зарубежной практике травитель имеет состав: 7 ч. фторида аммония в 40% водном растворе и 14 ч. фтористоводородной кислоты.
В работе [39] предложен тот же травитель с соотношением 32 : 2,5, скорость травления при температуре 22±3 °C составляет примерно 0,08 мкм/мин. При повышении температуры скорость возрастает и при 40 °C достигает 0,22 мкм/мин, т. е. необходимо тсрмостати-ровать процесс травления. Применяют также травители с другими соотношениями составляющих, например:
1) 10 ч. фторида аммония, 3 ч. фтористоводородной кислоты и 20 ч. воды; скорость травления 0,12 мкм/мин [42];
2) 3 ч. фторида аммония, 1 ч. фтористоводородной кислоты и 7 ч. воды; скорость травления 0,06 мкм/мин [43].
Травители при длительном хранении «стареют», скорость травления уменьшается (примерно на 20 %). В работе [43] предложен скоростной травитель (0,22 мкм/мин): 2 ч. серной кислоты (<70Т1, = 1,135), 1 ч. фторида аммония.
Монооксид кремния. Все травители содержат в тех или иных количествах фтористоводородную кислоту; введя различные компоненты можно регулировать скорость и качество травления [16]. Чаще всего травление монооксида кремния приходится выполнять в составе многослойной системы — разведки металлизации в интегральных схемах или пассивирующих покрытиях. В этих случаях важно, чтобы травитель не воздействовал на другие слои. Рекомендуются следующие составы:
1) монооксид кремния на слоях молибден— золото—молибден [44]: 1 ч. фтористоводородной кислоты, 5 ч. 2% раствора AgNO3, 5 ч. воды;
2) монооксид кремния на слоях хром—золото—хром [44]: 2 ч. фтористоводородной кислоты, 2 ч. фторида аммония, 5 ч. нитрата серебра, 20 ч. воды;
3) монооксид кремния на слое РЬО • SiO2 • В2О3 • МеО [45]: 13 ч. фтористоводородной кислоты, 100 ч. 2-ме-тилпропан-1-ола(изобутилового спирта), скорость травления 0,5-0,8 мкм/мин.
Оксиды металлов. Травление А12О3 осуществляют в нагретой ортофосфорной кислоте. Для травления Fe2O3 используют [46] водный раствор соляной кислоты (в равном соотношении), при комнатной температуре скорость травления составляет около 3 нм/с и сильно
944
Новый справочник химика и технолога
зависит от условий осаждения пленки оксида железа, в частности от температуры осаждения. Оксиды индия 1пО2 и олова SnO2 химически очень стойки к кислотам (за исключением фтористоводородной кислоты) и их солям. Травить эти оксиды можно в нагретых щелочах, но маски из фоторезиста не выдерживают подобной обработки. Поэтому для фотолитографии чуть ли не единственным выходом [16] является использование реакции замены олова или индия активным металлом, например, цинком:
2НС1 Zn - ZnCl2 + Н2
+ 2 НС1
SnO2 + Н2 SnCI2 + 2 Н2О
Практически цинк вводят в раствор соляной кислоты в виде цинковой пыли. Приготавливают водную суспензию цинковой пыли, наносят ее на пластину и опускают
пластину в кислоту [16]. Травление происходит только в момент выделения водорода, т. е. цинка должно хватить для образования водорода в течение всего времени травления. В случае неполного травления пластину можно извлечь, промыть, просушить, снова нанести эмульсию и продолжить травление.
Германий. Наиболее широко используется травитель состава [16]: 1 ч. фтористоводородной кислоты, 1 ч. азотной кислоты, 1 ч. пероксида водорода и 4 ч. воды. Скорость травления около 3 мкм/мин, степень растравливания не превышает 10 % при травлении на глубину не более 10 мкм. В табл. 5.7.22 приведены травители для германия и кремния, применяемые на практике [1]. Скорость травления кремния и германия зависит от химического состава и температуры травителей, кри-сталллографической ориентации поверхности, концентрации примесей в полупроводнике.
Травители* для германия и кремния [1]
Таблица 5.7.22
Название травителя Состав травителя Условия травления Скорость травления, мкм/мин Примечание
Германий
Иодный СР-4 СР-4А Ртутный ДЭША Ртутный Медный Серебряный Перекисный №2 (супер оксоль) Травитель фирмы RCA 10 мл HNO3 + 5 мл HF + 11 мл СН3СООН + + 30 мл 12 25 об. ч. HNO3+ 15 об. ч. HF+ + 15 об. ч. СНзСООН + 0,3 об. ч. Вг2 5 об. ч. HNO3 + 3 об. ч. HF + 3 об. ч. СН3СООН 4 об. ч. HNO3 + 2 об. ч. HF + 15 об. ч. СН3СООН 30 мл HNO3 + 30 мл HF + 40 мл Н2О с 1,33 г Hg(NO3)2 1 об. ч. HNO3 + 2 об. ч. HF + + 1 об. ч. 10%Cu(NO3)2 1 об. ч. HNO3 + 2 об. ч. HF + 2 об. ч. 5% AgNO3 2 об. ч. 30% Н2О2 + 1 об. ч. 48% HF 1 об. ч. Н2О2 + 1 об. ч. HF + 4 об. ч. Н2О 600 см3 HNO3; 300 см3 СН3СООН; 100 см3 HF; 25 мг KI Комнатная температура То же » » » » 25 °C Комнатная температура То же Комнатная температура 37 30-50 30 25 12 25 8,5 1,2 Применяется для травления плоскости (100) Применяется для травления плоскостей (100), (111) Применяется для травления плоскости (110) с осаждением на поверхности серебра
Химия фотографических процессов
945
Окончание табл. 5.7.22
Название травителя Состав травителя Условия травления Скорость травления, мкм/мин Примечание
Травитель фирмы RCA Гипохлорит натрия 10 мл HNO310 мл насыщенного раствора щавелевой кислоты СООН- СООН 7 мл НС1; 1 мл HNO3 в уксусной кислоте или глицерине 1 об. ч. 10% NaOCl + 10 об. ч. Н2О 35 °C 35 °C 40 °C 0,8 1,5
Кремний
Травитель Уайта СР-4А SD-1 Серебряно-гликолевый 3 об. ч. HNO3 + 1 об. ч. HF 5 об. ч. HNO3 + 3 об. ч. HF + 3 об. ч. СН3СООН 18 мл HNO3 + 25 мл HF + 5 мл СН3СООН + + 0,1 мл Вг2 + 10 мл Н2О + 1 г (Cu(NO3)2 7 об. ч. 0,6% Na2Cr2O7 + 20 об. ч. HF; 30 об. ч. HNO3 400 мл HNO3; 10 мл HF; 10 мл раствора AgNO3 (1 г AgNO3 в 300 мл Н2О); 200 мл пропиленгликоля Комнатная температура То же » » » 184,5 0,1 Полирующий травитель
Кислоты HNO3, HF. НС1, H2SO4, СН3СООН — концентрированные, Н2О2 — 30% раствор.
Реакции, имеющие место при химическом травлении, могут быть представлены в следующей упрощенной схемой:
Ge--------► GeO---------► GeO2;
2- +
GeO2 + 6HF -------► GeF + 2 H2O + 2H
Источником атомов кислорода служит азотная кислота или пероксид водорода. Наиболее распространенными травителями для кремния являются смеси на основе азотной и плавиковой кислот, реагирующие по реакции:
3Si + 4HNO3 + 18HF = 3H2(SiF6) + 4NO + 8Н2О
Пероксид водорода является плохим травителем для кремния из-за нерастворимости поверхностного оксида кремния в воде [1].
После получения требуемой конфигурации рисунка методом травления или наращивания необходимо удалить слой фоторезиста, прошедшего термообработку при повышенных температурах. В табл. 5.7.23 приведены составы для удаления пленок различных фоторезистов в зависимости от температуры их термообработки.
Таблица 5.7.23
Составы для удаления пленок фоторезистов в зависимости от температуры термообработки [48]
Фто-резист Г, °C Состав для удаления Примечание
ФП- 120-125 Ацетон, При нормальных
383 ФП- 120-125 диоксан Ацетон условиях То же
РН7 ФП- 135-150 Диметилформ- »
РН7 ФП-117 170-185 амид, мономе-таноламин H2SO4; NaOH; С подогревом
ФН-11 125 HNO3 Хлобензол, С механическим
ФИ-И 140 и выше ксилол, толуол воздействием Практически снимается только в плазме
946
Новый справочник химика и технолога
5.7.2.7. Удаление пленки фоторезиста
Химические способы удаления пленок фоторезистов не всегда удобны, т. к. требуют применения агрессивных кислотных и щелочных растворов при повышенных температурах или использования смеси токсичных растворителей с применением механического воздействия на удаляемый слой, что может привести к подтрав-ливанию токонесущих слоев или к их механическому повреждению. Кроме того, химические методы не гарантируют полного удаления органической пленки с поверхности металла [47].
Физико-химические способы обработки подложек имеют ряд преимуществ по сравнению с другими химическими способами, например, чистоту получаемых продуктов реакции, отсутствие высоких температур нагрева эле
ментов конструкции, возможность проведения низкотемпературных реакций в любой газовой среде, возможность проведения прецизионной локальной обработки отдельных участков подложки без термического воздействия на всю подложку, возможность автоматического управления процессом и т. д. [48]. Впервые такая обработка была проведена фирмой «Signetics», которая использовала вместо химических травителей плазму, возбужденную радиочастотой. Эксперименты показали, что низкотемпературное воздействие плазмы позволяет полностью очистить подложки от слоя фоторезиста, не ухудшая свойств полупроводникового материала [49]. Сведения об установках удаления фоторезиста в плазме, разработанных различными американскими фирмами приведены в табл. 5.7.24.
Таблица 5.7.24
Установки для удаления фоторезиста в плазме [48]
Модель Фирма, страна Основное назначение Параметры установок
1101 International Plasma Corp., США Удаление фоторезиста Мощность 1 кВт Частота 13, 56 МГц
2101 То же Удаление фоторезиста, очистка подложек перед диффузией, очистка стекла Длина камеры 90 см Диаметр 80 см
1003 » Удаление фоторезиста
Radio Frequency Со., Очистка кремниевых подложек в иони- Мощность 3 кВт
США зированнм кислороде; лабораторное обеззоливание карбо содержащих материалов; электродно-плазменное исследование ионизирумых газов Частота 40, 68 МГц Температура 100 °C
YPS 2003 Monte Toal Assaciates, США Удаление фоторезиста с пластин Мощность 0-300 Вт Расход газа 0-900 см3/мин Время 0-90 мин
PDS-302 PDS-504 Отделение Trapelo Division фирмы LEE, США То же Удаление фоторезиста с пластин
YPC-1013B International Plasma Corp., США Удаление фоторезиста, нанесение фотомасок, очищение подложек Мощность 300 Вт
YPC-1101B То же Удаление фоторезиста Мощность 1000 Вт
YPC-1201B » То же Мощность 2000 Вт
2003В » » Мощность 300 Вт
2103В » » Мощность 1000 Вт
2104 » » Мощность 300 Вт
2101В » » Мощность 2000 Вт
140В Radio Frequency Со., США Очистка подложек и удаление фоторезиста Мощность 1500 Вт
В [48] приведены результаты работы по созданию установки для удаления различных фоторезистов в плазме, определены оптимальные режимы обработки пластин и приведена оценка воздействия плазмы на металлические и диэлектрические пленки, нанесенные на ситалловые подложки. В качестве фоторезистов применяли негативные (на основе циклокаучука с бисазидом) и позитивные
(ФП-383 и СФ-200). В состав ряда образцов пленок фоторезиста ФП-383 вводился эпоксид ЭД-5, предварительно сплавленный с новолаком К-18 в соотношении 1 : 5. Величина колебательной мощности на выходе генератора изменялась в пределах от 300 до 1500 Вт, а разрежение в реакционной камере меняли от 66,6 Па до 1,3 кПа (от 0,5 до 10 мм рт. ст.).
Химия фотографических процессов
947
С увеличением мощности генератора при постоянном значении давления в реакционной камере продолжительность процесса полного удаления фоторезистов с подложек уменьшалась, после чего изменялась незначительно (рис. 5.7.9).
На рис. 5.7.10 приведена кривая зависимости времени удаления фоторезиста от давления в реакционной камере. Начальный участок кривой (до р = 533,2 Па = = 4 мм рт. ст.) показывает, что время удаления фоторезиста обратно пропорционально величине давления газа.
200 600 1000
Z, МИН
Рис. 5.7.9. Зависимость продолжительности удаления фоторезиста от мощности генератора на входе (р = 66,6 Па = 0,5 мм рт. ст.)
Рис. 5.7.10. Зависимость времени удаления фоторезиста от давления в реакционной камере
Было установлено, что в созданном устройстве плазма не возбуждалась при разрежении менее 66,6 Па (0,5 мм рт. ст.) и концентрировалась только в области индуктора при значении давления 1,3 кПа (10 мм рт. ст.) и более. При дальнейшем увеличении давления уменьшение времени очистки пластин от фоторезиста практически несущественно.
Между продолжительностью воздействия плазмы на пластину с нанесенным фоторезистом и типом фоторезиста существует определенная зависимость. Как видно из кривых, приведенных на рис. 5.7.11, наиболее быстро происходит удаление слоев фоторезиста на основе циклокаучука с бисазидом и фоторезиста ФП-383. Добавление в состав ФП-383 эпоксида ЭД-5 очень мало отражается на времени удаления фоторезиста с пластины. Следует отметить, что удаление таких слоев химическим способом представляет большую трудность и практически решается одновременным применением растворов и механическим воздействием.
Анализ подверженных плазменному воздействию пластин показал, что при значениях давления 399,9-799,8 Па (3-6 мм рт. ст.) и величинах мощности на выходе генератора порядка 1 кВт происходит окисление медных и никелевых слоев. Однако оксидная пленка легко удалялась в обычных слабых декапирующих растворах. После удаления оксидной пленки на поверхность, освобожденную от слоя фоторезиста, электрохимически осаждали медь или никель толщиной порядка 20-50 мкм. Электрохимически осадки металлов были сплошными, по всей поверхности, расслаивания между слоями вакуумного и электрохимически осажденного металлов не наблюдалось, что указывает на полное удаление следов фоторезиста с поверхности пластины в плазме.
Однако, следует отметить, применение плазмы для удаления пленок фоторезистов несовместимо со схемами, чувствительными к поверхностным зарядам, например, схемами на МОП-приборах и матрицами высоковольтных диодов [50].
Рис. 5.7.11. Зависимость продолжительности удаления фоторезиста от типа фоторезиста
(р = 1,3 кПа = 5 мм рт. ст.; U = 2250 В):
1 — СФ-200 (20 %); 2 — ФП-383; 3 — ФП-383 с добавлением ЭД-5;
4 — СФ-200 (10 %); 5 — циклокаучук (ГИПИ-4) с бисазидом
5.7.3. Другие виды литографии
Как видно из табл. 5.7.25, в которой сравниваются различные методы литографии, рентгеновская литография позволяет получать размеры элементов около 0,1 мкм [16, 54].
Рентгенолитография представляет собой метод контактной печати, аналогичный методу фотолитографической контактной печати с зазором и использующий актиничное излучение мягких рентгеновских лучей с X = 0,2-4,5 нм, что способствует устранению дифракционных ограничений, характерных для фотолитографии [55]. Ей присущи такие неоспоримые преимущества, как высокая разрешающая способность (примерно 500 нм), нечувствительность к пыли и загрязнениям, отсутствие проблем, связанных с рассеянием, возможность применения как позитивных, так и нега-
948
Новый справочник химика и технолога
тивных рентгенорезистов, возможность экспонирования всей пластины в отсутствие вакуума, простота и низкая стоимость [56]. Разрешающая способность реально ограничена величиной поглощения рентгеновского излучения металлическим рисунком шаблона. Шаблоны, применяемые в процессе рентгенолитографии, изготавливаются с помощью электронолитографии из пленок золота на кремниевой подложке толщиной 2—5 мкм. Кремний может быть заменен майларом, который обладает меньшим коэффициентом поглощения, что позволяет увеличить толщину подложки [56]. Рисунок шаблона выполняется на пленке золота, обладающего большим коэффициентом поглощения рентгеновских лучей. Дальнейшее повышение разрешающей способности обеспечивают электронно-лучевые методы (табл. 5.7.25).
Вышеуказанные методы литографии для получения требуемой конфигурации элементов с высоким разрешением, как и метод оптической литографии, требуют
специальной разработки новых резистов, технологического оборудования, технологических процессов и условий их проведения, а также отдельного и детального описания этих методов литографии (достоинств, недостатков, возможностей и технологических режимов и т. д.).
К основным достоинствам фотолитографии относятся:
- повышение разрешающей способности, проявляющееся в разработке методов проекционной фотолитографии и, особенно, в переходе от оптической фотолитографии к рентгеновской и электронно-лучевой литографии;
- улучшение реального качества процесса, в первую очередь снижение плотности локальных дефектов за счет повышения производственной гигиены, автоматизации процесса, сокращения числа операций (например, создание рисунка без шаблона, т. е. непосредственно на рабочей пластине).
Таблица 5.7.25
Сравнение различных методов литографии
Характеристика процесса Оптическая литография Рентгеновская литография Электронно-лучевая литография
контактная проекционная сканирующая полная проекция
Длина волны излучения, нм 300 300 0,4-1,4 0,01 0,01
Практическое разрешение, мкм 0,6-1,0 0,4-1,0 0,7 0,1-0,15 1,0-2,0
Шаблон Стекляный с хромовым покрытием Стекляный Кремниевый с золотым покрытием Не нужен Сложный фотокатод
Время экспонирования (стандартная пластина) Секунды Десятки секунд От нескольких секунд до нескольких минут От нескольких минут до нескольких часов (сложные рисунки) Десятки секунд
Совмещение Визуальное, фотоэлектрическое С помощью датчика рентгеновского излучения С помощью специального датчика электрического сигнала
Достоинства Простота, высокая производительность Отсутствие износа шаблонов, более чистые условия, отсутствие дифракции в зазоре между шаблоном и резистом Отсутствие контакта при обеспечении высокой разрешающей способности, высокая производительность, относительная простота (пластина не в вакууме) Отсутствие шаблона, высокая разрешающая способность Высокие производительность и разрешающая способность
Химия фотографических процессов
949
Окончание табл. 5.7.25
Характеристика процесса Оптическая фотолитофафия Рентгеновская фотолитография Электронно-лучевая фотолитофафия
контактная проекционная сканирующая полная проекция
Недостатки Износ шаблонов и повреждение слоя при контакте, дифракция в зазоре между шаблоном и резистом Сложная оптика, мощные УФ осветители, трудности фокусировки высокоразрешающих объективов Трудности фокусировки рентгеновских лучей, необходимость вакуумной системы для источника Сложное оборудование, помещение пластины в вакуум, фудности совмещения, низкая производительность Сложное оборудование, помещение пластины в вакуум, фудности совмещения, сложности изготовления шаблонов-фото катодов
5.7.4. Математическое моделирование фотолитографических процессов
Характерной особенностью научно-исследовательских и опытно-конструкторских работ в области разработки и промышленного производства современных интефальных схем (ИС) является широкое использование профаммных средств автоматизированного проектирования (САПР) и математического моделирования (СММ) технологических процессов и самих полупроводниковых усфойств [51]. Необходимость включения подобных инсфументов в арсенал инженера-исследователя определяется, в основном, сфемлением к уменьшению стоимости конечного продукта и времени его выхода на рынок. Процесс математического моделирования фотолитофафических процессе состоит из нескольких этапов.
1. Предварительный анализ возможностей технологического процесса.
Увеличение степени интефации ИС сопровождается уменьшением размеров сфуктурных элементов, размещаемых на кристалле. На рис. 5.7.12 показаны реальный професс и ближайшие перспективы промышленных методов литофафии [52]. Если считать, что темпы развития микроэлекфоники до 2010 г. не изменятся, то каждые фи года по-прежнему, минимальный размер элементов будет уменьшаться с коэффициентом 0,7. Для достижения таких разрешений, естественно, понадобятся и новые маскирующие материалы (резисты), новые производительные установки экспонирования и новые, интефированные технологические процессы, отличающиеся от современных повышенными экологическими фебованиями. Подобная тенденция, естественно, приводит к необходимости периодического обновления производственного оборудования, поскольку каждая фотолитофафическая установка, и каждый метод литофафии имеют свои офаничения относительно максимально достижимой разрешающей способности. В табл. 5.7.26 приведены технические возможности методов создания конфигурации элементов [10] на основании данных, приведенных Б.С. Данилиным и В.Ю. Киреевым. В то же время, с точки зрения возврата
инвестиций необходимо, чтобы приходящее на замену оборудование могло применяться для производства нескольких (обычно не менее фех) поколений ИС.
2. Выбор оптимальных парамефов технологического процесса.
Для обеспечения приемлемого выхода годных ИС используемый литографический процесс должен обеспечивать воспроизведение защитного рельефа с фе-буемыми геомефическими характеристиками и заданными допусками ухода этих характеристик [51]. Основными парамефами фотолитофафического процесса являются: толщина резиста и антиофажающего покрытия, расфокусировка и дозы экспозиции. Основная роль математического моделирования в этой области сводится к предварительному сужению диапазонов возможных изменений конфолируемых парамефов с целью минимизации всего времени, затрачиваемого на определение оптимальных значений парамефов процесса.
1983 1986 1989 1992 1995 1998 2001 2004 2007 2010
/, ГОДЫ
Рис. 5.7.12. Професс и перспективы промышленных методов литографии:
1 — оптическая литография с длиной волны 356 нм, 248 нм и 193 нм; П — рентгенолитография или прямое получение рисунка с помощью электронного луча; III — электронно-лучевая проекционная литография; N — количество логических элементов микропроцессора на 1 см2 кристалла БИС
Таблица 5.7.26
Разрешающая способность методов создания конфигурации пленочных элементов [53]
Теоретическое предельное разрешение метода, мкм Принципиальное ограничение, определяющее предельное разрешение метода Максимальное разрешение метода, мкм Рабочая площадь, на которой обеспечивается разрешение метода, мм2 Основные преимущества метода Основные недостатки метода Минимальный размер воспроизводимой микроэлектронной структуры, получаемой на площади 2000 мм2, (диаметр 50 мм), мкм Факторы, ограничивающие минимальный размер воспроизводимой микроэлектронной структуры Основная область применения метода
Трафаретное маскирование
Определяется разрешением маски Ограничения метода создания маски. Механическая прочность материала маски 12,5 2500 Простота изготовления долговечных масок, возможность быстрой смены масок Необходимость в комплекте масок 60 Разрешение метода, точность совмещения масок и рисунков на масках и пластине Простые тонкопленочные электронные структуры с малой степенью интеграции. Криоэлектроника
Контактная фотолитография, обычный вариант
0,25 для света с X = 0,4 мкм Дифракция света 1,25 2000 Высокое разрешение при сравнительно простой аппаратуре Трудность совмещения и быстрое изнашивание фотошаблонов. Необходимость в комижге фотошаблонов 2-3 Наличие зазора между фотошаблонами и между фотошаблоном и пластиной. Точность совмещения фотошаблонов и рисунков на фотошаблоне и пластине Получение конфигурации ИС и микроэлектронных приборов
Контактная фотолитография с зазором между фотошаблонами и пластинами
2,0 для света с X = 0,4 мкм при зазоре 20 мкм. Зависит от размера зазора Дифракция света 10 2000 Практически неограниченный срок службы фотошаблонов. Нет передачи мелких дефектов (до 4 мкм) с шаблона на пластину Ухудшение разрешения 15-20 Разрешение метода Стадия разработки
950 Новый справочник химика и технолога
Продолжение табл. 5.7.26
Теоретическое предельное разрешение метода, мкм Принципиальное ограничение, определяющее предельное разрешение метода Максимальное разрешение метода, мкм Рабочая площадь, на которой обеспечивается разрешение метода, мм2 Основные преимущества метода Основные недостатки метода Минимальный размер воспроизводимой микроэлектронной структуры, получаемой на площади 2000 мм2, (диаметр 50 мм), мкм Факторы, ограничивающие минимальный размер воспроизводимой микроэлектронной структуры Основная область применения метода
Проекционная фотолитография
0,25 для света с X = 0,4 мкм Дифракция света 0,4 3 1 0,04 2000 10 Высокое разрешение. Неограниченный срок службы шаблонов Сложность изготовления высокоразрешающих объектов и трудность наводки на резкостъ 1,25 Точность перемещения координатных столов Создание конфигурации элементов схем
Голография
0,25 для света с X -- 0,4 мкм Дифракция света 1 100 Не нужны объективы Жесткие требования к плоскостности фотошаблонов и их бездефектности Стадия лабораторных исследований
Последовательная электронолитография
с управлением от ЭВМ
Зависит от ускоряющего напряжения Дифракция электронов о,1 4 Субмикронное разрешение. Не нужны шаблоны Малая площадь сканирования. Низкая производительность 1 Точность перемещения координатных столов Получение элементов с субмикронной геометрией
с управлением от фотокапира
Зависит от разрешения электроннолучевой трубки Ограничения по созданию высокоразрешающих электро нно-лучевых трубок 5 2000 Дешевизна фотокапира Нужны шаблоны. Низкое разрешение 5-10 Разрешение метода Изготовление больших фотошаблонов
Химия фотографических процессов
Окончание табл. 5.7.26
Теоретическое предельное разрешение метода, мкм Принципиальное ограничение, определяющее предельное разрешение метода Максимальное разрешение метода, мкм Рабочая площадь, на которой обеспечивается разрешение метода, мм2 Основные преимущества метода Основные недостатки метода Минимальный размер воспроизводимой микроэлектронной структуры, получаемой на площади 2000 мм2, (диаметр 50 мм), мкм Факторы, ограничивающие минимальный размер воспроизводимой микроэлектронной структуры Основная область применения метода
Проекционная электронолитография
Зависит от напряжения поля и энергии эмитированных фотокадом электронов Дифракция электронов 0,2 2000 Высокая производительность Необходимость в комплекте преце-зионных шаблонов для фотокатодов 1 Точность совмещения рисунков на фотокатоде и пластине Создание конфигурации элементов схем
Термические электронные и лазерные пучки
Зависит от материала Наличие тепловой зоны плавления и нарушений 100 (для кремния) 30(для алюминия) 2000 Практически любая (с координатным столом) Не нужны шаблоны при управлении от ЭВМ и резист Большое число образующихся дефектов Резка, скрайбирование, пайка и сварка, сверление
Ионные пучки
Зависит от диаметра полного пучка с током не менее 10-4 А Малая яркость ионных источников 200 Практически любая (с координатным столом) Не нужны шаблоны и резист. Разрешение определяется только диаметром пучка. Нет дефектов материала Принципиальных технологических ограничений не имеет Ионное травление и ионное внедрение (стадия разработки)
952 Новый справочник химика и технолога
Химия фотографических процессов
953
3. Оптимальная коррекция фотошаблонов.
Как правило, в задачах исследования и оптимизации фотолитографических процессов [51] рассматриваются только простые элементы шаблона ИС, такие как изолированные или периодические проводящие линии, а также контактные площадки. Такие элементы обычно характеризуются одним размером, например, шириной поперечного сечения линии или контакта, воспроизведение какового размера и является основным критерием при выборе оптимальных значений технологических параметров. Однако при воспроизведении реальной топологии ИС в проявленном профиле фоторезиста могут наблюдаться искажения формы отдельных элементов, существенные с точки зрения конечных электрических характеристик, таких как сопротивление, емкость, индуктивность и т. д., создаваемых микроэлектронных устройств [51]. Основной причиной появления подобных искажений является как взаимное влияние соседних элементов шаблона (т. н. «эффект близости»), так и то обстоятельство, что размеры воспроизводимых элементов могут быть сравнимы с длиной волны излучения.
С помощью математического моделирования можно:
- предсказывать тенденции таких важнейших характеристик фотографического процесса как разрешающая способность, доступная глубина фокуса, допустимый разброс по дозе экспозиции;
- значения таких технологических параметров, как толщина резиста и антиотражающего покрытия, номинальные значения расфокусировки проекционной системы и дозы экспозиции, числовая аппертура объектива и степень когерентности источника излучения;
- проводить оптимальную коррекцию фотошаблона с целью достижения лучшего воспроизведения требуемой защитной формы рельефа.
При разумном использовании математического моделирования можно добиться многократного сокращения временных и материальных затрат [51].
Литература
1. Боков Ю.С., Корсаков В.С., Лаврищев В.П., Макаров Н.В. Фоторезисты И Обзоры по электронной технике. 1969. Вып. 56(125).
2. Введение в фотохимию органических соединений / Под ред. Г.О. Беккера и А.В. Ельцова; Пер. с нем. Л.: Химия, 1976.
3. Калверт Дж., Питтс Дж. Фотохимия. М.: Мир, 1968.
4. Туррс Н. Молекулярная фотохимия. М.: Мир, 1967.
5. Теренин А.Н. Фотоника молекул красителей. Л.: Наука, 1967.
6. Фотохимические процессы в слоях / Под ред. А.В. Ельцова. Л.: Химия, 1978.
7. Ханке Х.И., Фабиан X. Технология производства радиоэлектронной аппаратуры. М.: Энергия, 1980.
8. Вавилов А Г. И Вопросы радиоэлектроники. Сер. Общетехническая. 1977. Вып. 22. С. 91-103.
9. Майсел Л., Глэнг Р. Технология тонких пленок: Справ. / Пер. с англ, под ред. М.И. Елинсона и Г.Г. Смолко. Т. 1. М.: Советское Радио, 1977.
10. Готра З.Ю., Мушкарден Э.М., Смеркло Л.М. Технологические основы гибридных интегральных схем. Львов: Вища Школа, 1977.
11. Кларк. Свойства фоторезисторов и их применение в процессе фотолитографии И Зарубежная электронная техника. 1972. № 2.
12. Кирш Ю.Э. и др. И Журнал физической химии. 1965. №39. С. 1886.
13. Гаева Г.Л. Спектроскопические исследования светочувствительных полимеров И Международный конгресс по фотографической науке. Секция Е. М., 1970. С. 157-160.
14. Меррил, Апрух И Химия и технология полимеров. 1968. №9. С. 41-50.
15. Динабург М.С. Светочувствительные диазосоединения и их применение. М.; Л.: Химия, 1964.
16. Пресс Ф.П. Фотолитография в производстве полупроводниковых приборов. М.: Энергия, 1964.
17. Вавилов А.Г. И Журн. науч, и прикл. фотографии и кинематографии. 1969. Т. 14, № 2. С. 112-115; 1970. № 6. С. 421—424; 1971. № 1. С. 15-18; 1971. № 4. С. 277-282; 1973. № 6. С. 412-418.
18. Вавилов АГ., Бычева В.А., Митяева Л.А. И Журн. науч, и прикл. фотографии и кинематографии. 1972. №3. С. 185.
19. Мокеев О.К., Романов АС. Химическая обработка и фотография в производстве полупроводниковых приборов и микросхем. М.: Высш, шк., 1979.
20. Вавилов АГ., Водолазская С.К., Бычева В.А. И Журн. науч, и прикл. фотографии и кинематографии. 1973. № 1.С. 26.
21. Вавилов А.Г., Бычева В.А. // Тр. / ЛИКИ. 1972. С.134-140.
22. Севастьянов В.П., Решетников Б.К., Мраморное И.В., Каширский М.Л. Знакосинтезирующая электроника: фотолитография. Саратовский Университет, 1993.
23. Ильин В.А. Прогрессивные технологические процессы производства печатных плат. М., 1989. С. 91.
24. Гаева Г.Л., Ляликов К.С., Вавилов А.Г., Калинка И.Н. И Журн. науч, и прикл. фотографии и кинематографии. 1976. № 6. С. 456-458.
25. Сорокин Е.В., Вавилов АГ. И Обмен опытом в радиопромышленности. 1985. № 5. С. 37-38.
26. Сторожук Г.Л. и др. И Электронная техника. Сер. 2. Полпроводниковые приборы. 1973. Вып. 10(82).
27. Мартынов В.В., Базарова Т.Е. Литографические процессы. М.: Высш, шк., 1990.
28. Пат. США № 3650957; 3650958; 3650959.
29. Метод аналитической химии. Л.: Химия, 1959.
30. Водолазская С.К., Вавилов А.Г., Минаков В.И. // Обмен опытом в радиопромышленности. 1984. № 9. С. 1-3; 1985. №3. С. 13-16.
31. Бершадский Е.Я., Вавилов АГ., Кузнецова М.А. и др. И Обработка радиосигналов акустоэлектронными
954
Новый справочник химика и технолога
и акустооптическими устройствами. Л.: Наука, 1983. С. 4-8.
32. Курносов А.И., Климовицкая А.В. // Электронная техника. Сер. 2. 1969. Вып. 5. С. 8-13.
33. Качурина Е.Е., Немировский Л.Н., Анохин Б.Г. // Электронная техника. Сер. 2. 1970. Вып. 4(54). С. 91-97.
34. Гусев В.К., Никитин В.И., Никитина Т.А. // Электронная техника. Сер. 7. 1974. Вып. 6. С. 12-16.
35. Shankoff Т.А., Chandross Е.А. // J. Electrochem. Soc.
1975. V. 122, N 2. P. 294-298.
36. Пат. США № 355951, кл. 204-15, 1967.
37. Пат. США № 3388048, кл. 204-15,1965.
38. Лубашевская А.В. и др. // Вопросы электроники.
Сер. Общетехническая. 1968. Вып. 9. С. 29-34.
39. Штраусе Л.С., Ивченко А.Е. // Электронная техника. Сер. 7. 1974. Вып. 4. С. 44-48.
40. Gannon J.J., Nuese С.J. // J. Electrochem. Soc. 1974.
V. 121, N 9. P. 1215-1219.
41. Травление полупроводников / Пер. с англ, под ред. С.Н. Горина. М.: Мир, 1965.
42. Максимова М.И. и др. // Электронная техника. Сер. 7. 1974. Вып. 4. С. 39-43.
43. Раснецова Б.Е., Белевич Г.М., Колмакова Г.Л. И Электронная техника. Сер. 7. 1974. Вып. 3. С. 3-12.
44. Пат. Японии № 34214, кл. 99/5.
45. Маркова Т.П., Янсон В.Ю. // Электронная техника. Сер. 14. 1970. Вып. 4. С. 71-78.
46. Sullivan M.V. // J. Electrochem. Soc. 1972. V. 120, N 4. P. 545-550.
47. Вавилов А.Г., Водолазская С.К. // Обмен опытом в радиопромышленности. 1977. № 7. С. 28-31.
48. Мамаев Г.Н. и др. // Вопросы радиоэлектроники. Сер. Общетехническая. 1971. Вып. 22. С. 67-72.
49. Электроника. 1968. Т. 41. № 14. С. 37.
50. Грегор Л. Технология толстых и тонких пленок. М.: Мир, 1972. С. 9-26.
51. Ивин В.В., Махвиладзе Т.М. Использование математического моделирования в исследовании и оптимизации фотолитографических процессов. Препринт. М.: МАКСпресс, 2000. С. 30.
52. Степаненко И.П. Основы микроэлектроники. М: Лаборатория базовых знаний, 2000. С. 192.
53. Данилин Б.С., Киреев Ю.В. Методы получения конфигурации элементов ИС // Зарубежная электронная техника. М.: 1973. № 18(66).
54. Фрексон И. Развитие рентгено-лучевой литографии // Электроника. 1974. № 17. С. 77-80.
55. Боков Ю.С. Фото-электронно-рентгено-резисты // Радио и связь. 1982.
56. Данилин Б.С. Получение тонкопленочных элементов микросхем. М.: Энергия, 1977. С. 122-125.
57. Ляликов К.С. и др. // Журн. науч, и прикл. фотографии и кинематографии. 1965. Т. 10, № 3. С. 200-206.
58. Ляликов К.С. и др. И Тр. ЛИКИ. Л., 1967. Вып. XII. С. 147-152.
Раздел 6. СОВРЕМЕННАЯ НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Авторы-составители', д. х. н. А.Ф. Хлебников, к. х. н., доц. М.С. Новиков
Без знания номенклатуры органических соединений не может обойтись ни один химик, причем не только химик-органик, но и химики других специальностей, поскольку органические соединения давно стали объектами исследования различных отраслей химии, биологии и других наук. Химическая номенклатура — это язык, необходимый для общения исследователей органических соединений друг с другом. Хотя в настоящее время существует достаточно много компьютерных программ, позволяющих называть органические соединения и по названию соединения восстанавливать его структурную формулу, понятно, что читая литературу, невозможно «за каждым словом лезть в словарь». Кроме того, относительно доступные программы непригодны при работе с достаточно сложными соединениями, а главное — они оперируют только с названиями на английском языке.
Огромное число органических соединений, сложность и разнообразие их строения обусловливает сложность их номенклатуры. Материал данного раздела научит вас составлять правильные названия органических соединений данного строения и обратной операции восстановления структурной формулы по названию. Кроме того, вы сможете «ориентироваться» в разнообразии номенклатур, понять, почему одно и то же соединение может иметь несколько правильных названий и какое из них целесообразней использовать.
Переходя от простого к сложному, рассмотрены принципы составления названий органических соединений важнейших классов, включая ациклические и циклические углеводороды, гетероциклические соединения, их функциональные производные, азот-, фосфор- и серасодержащие соединения. Рассмотрена усовершенствованная номенклатура для сложных полициклических мостиковых соединений и новейшая номенклатура фанов. Разобраны способы наименования ионов и радикалов. Специальные главы посвящены номенклатуре важнейших природных соединений —
углеводов, стероидов, витаминов, аминокислот и пептидов, терпенов, нуклеиновых кислот, порфиринов и др., а также новых классов молекул, таких как фуллерены. Отдельная глава посвящена стереохимической номенклатуре.
При составлении пособия использованы последние рекомендации IUPAC, ссылки на которые приведены в списке литературы. Там же приведены страницы в Internet, которые могут быть использованы для более подробного ознакомления с правилами IUPAC.
Номенклатура органических соединений благодаря работе комиссий IUPAC постоянно совершенствуется. Понятно, что новые правила наименования тех или иных соединений не мгновенно повсеместно становятся руководством к действию, даже если они принимаются научным сообществом. Поэтому в литературе часто в течение достаточно продолжительного времени встречаются несколько вариантов названий. В книге в приведенных примерах по возможности указываются варианты устаревших названий, встречающиеся в старой литературе и, к сожалению, в современной. При этом используются следующие пометки: (устар.) — обозначает устаревшее название, которое больше не рекомендуется правилами IUPAC; (трад.) — обозначает незапрещенное название, для которого, однако, согласно новейшим правилам имеется более предпочтительный вариант; равноценные названия разделены союзом или. Пометка (зам.) обозначает название по заместительной номенклатуре в тех случаях, когда оно сравнивается с названием по радикало-функциональной номенклатуре (рад.-ф.)‘, пометка (трив.) использована там, где необходимо подчеркнуть, что данное название является тривиальным.
Название соединения на русском языке часто отличается от его английского эквивалента не только алфавитом. Поэтому в пособии практически для всех соединений приводятся оба варианта названий, иллюстрирующие различия между ними, что поможет правильно осуществлять перевод с одного языка на другой.
956
Новый справочник химика и технолога
6.1. Общие сведения о систематической номенклатуре
6.1.1. Типы номенклатур
Химическая номенклатура — это совокупность названий индивидуальных химических веществ, их групп и классов, а также правила составления этих названий. Химическое название — это слово или ряд слов, однозначно указывающих на определенное вещество. Любое органическое вещество может иметь несколько названий. Все названия органических соединений можно подразделить на три типа: тривиальные, полусистема-тические и систематические. Различие между тривиальными и систематическими названиями заключается в том, что тривиальные названия относятся к веществам, а систематические — к их структурам. В полусис-тематическом названии имеется только частичное указание на структуру вещества. До сих пор широко используемые тривиальные названия веществ, как правило, вообще никак не связаны с их строением; более того, часто они появлялись еще до установления строения соединения, и происхождение их носило случайный характер. Некоторые соединения, например, были названы по природному источнику, из которого они были выделены: муравьиная и лимонная кислоты, мочевина. Названия других веществ отражают какое-либо их свойство: глюкоза — сладкий вкус; азулен — голубую окраску; кубан, альбатроссидин — форму молекулы. И хотя тривиальные названия не отражают структуру вещества, многие из них часто используются и будут использоваться в дальнейшем, поскольку соответствующие систематические названия порой оказываются слишком громоздкими для написания и совершенно непригодными для устной речи.
Полусистематическая, или рациональная, номенклатура, частично отражающая строение вещества, рассматривает органическое вещество как производное наиболее простого представителя определенного ряда соединений, для которого используется тривиальное название. Для разветвленного алкана за основу берется метан, алкена — этилен, алкина — ацетилен, предельного спирта — карбинол, и т. д. Эта номенклатура оказалась удобной для простейших производных тех соединений, которые имеют общеупотребительные тривиальные названия, и в этих случаях она используется по-прежнему. Однако для более сложных производных она неприменима, т. к. выбор родоначального соединения часто становится произвольным.
Систематическая номенклатура, полностью отражающая строение веществ, берет свое начало со второй
половины XIX в., когда стала проводиться серьезная работа по классификации и систематизации названий органических соединений (Женевская конференция 1892 г.). Правила и принципы Женевской номенклатуры оказались достаточно удачными, и они широко применялись в ряде справочных изданий, например в Beilsteins Handbuch der organischen Chemie (Beilsteine).
В настоящее время в IUPAC (International Union of Pure and Applied Chemistry) и, параллельно, в реферативном журнале Chemical Abstracts ведется работа по усовершенствованию и стандартизации химической номенклатуры на английском языке. Комиссии IUPAC по номенклатуре в области неорганической, органической и биологической химии были организованы в 1922 г. и с тех пор регулярно публикуют свои рекомендации. Характерной особенностью номенклатуры IUPAC является то, что она создана с учетом сложившихся традиций и в ней допускаются альтернативные названия. Напротив, Chemical Abstracts придерживается более жестких правил, оставляя только одно название каждого соединения, пригодное для индексации и машинного использования. В настоящем пособии рассмотрены основные принципы построения названий органических соединений в соответствии с правилами IUPAC и особенности их адаптации к русскому языку.
6.1.2. Типы систематической номенклатуры
Номенклатура органических соединений формировалась в течение длительного времени, отвечая на потребности развивающейся науки. В результате к настоящему моменту сформулирован ряд принципов и положений, определяющих несколько типов номенклатур, допускаемых правилами IUPAC.
В радикало-функциональной номенклатуре, часто употребляемой в учебной и научной литературе, за основу берется название класса молекул с данной функциональной группой (определение функциональной группы см. подразд. 6.1.3.1). Основа является заключительным элементом сложного названия, перед которым ставятся слова, описывающие остальную часть молекулы, например см. рис. 6.1.1.
Принцип замещения атома водорода другим атомом или группой в названии-основе (родоначальном гидриде) используется в заместительной номенклатуре. Каждый заместитель характеризуется определенным префиксом или суффиксом, которые добавляются, соответственно, к началу (бензол хлорбензол) или к концу (метан метанол) названия родоначального гидрида, в котором произошло замещение атомов водорода.
Н3С—ОН
‘О'
метиловый спирт диэтиловый эфир метилэтилкетон англ.: methyl alcohol англ.: diethyl ether англ.: ethyl methyl ketone
Рис. 6.1.1
Современная номенклатура органических соединений
957
В соединительной (конъюнктивной) номенклатуре название молекулы образуется путем соединения названий составных частей, из которых данная молекула может быть (формально) собрана при удалении соответствующего числа атомов водорода. Этот подход наиболее часто используется для соединений, состоящих из двух компонентов, один из которых является циклом или циклической системой, а второй — цепью (или цепями) с главной функциональной группой. При этом в качестве цепи рассматривается отрезок, ограниченный с одной стороны циклом, а с другой — главной функциональной группой. Остальные фрагменты, присоединенные к цепи, описываются как заместители, место присоединения которых указывается буквами греческого алфавита, начиная от атома, ближайшего к главной функциональной группе, см. рис. 6.1.2.
Кроме того, данный подход используется для наименования соединений, состоящих из одинаковых фрагментов, путем объединения названия фрагмента с соответствующей умножающей приставкой (см. номенклатуру ансамблей, подразд. 6.6).
Для соединений, содержащих гетероатомы в середине цепи или в составе цикла, для упрощения названия иногда используют заменительную или «а»-но-менклатуру, в которой за основу берут соответствующий углеродный аналог молекулы, а гетероатомы, заменяющие определенные атомы углерода, указываются с помощью специальных префиксов (см. табл. 6.13, подразд. 6.3.5). Эта номенклатура широко используется в случае сложных полиэфиров и полиаминов,
но имеет строгие ограничения в случае гетероциклических соединений, например:
Пентан-1,5-диол
♦
2,4-Диоксапентан-1,5-диол
В основе присоединительной или аддитивной номенклатуры лежит процедура присоединения недостающих атомов к родоначальной структуре, например см. рис. 6.1.3.
Субтрактивная номенклатура, основанная на удалении атомов или групп, используется сравнительно редко. В частности, она применяется в названиях природных соединений, где удаление атомов водорода может быть обозначено с помощью префикса «дегидро», а удаление атома кислорода — префиксом «дезокси» (англ, «deoxy»). Другими префиксами, указывающими на отщепление, являются «ангидро», обозначающий отщепление воды, и «нор», свидетельствующий об удалении ациклического атома углерода или о сокращении размера кольца на метиленовую группу, см. рис. 6.1.4.
Ни одна из перечисленных номенклатур не может охватить все многообразие органических соединений; некоторые из них имеют строго ограниченное применение. Наиболее употребительной является заместительная номенклатура, которая подробно рассматривается в следующих разделах.
н3с.
2 ?Н'
ОН
Циклопентан Этанол
/ ОН
•С^
сн-сн2
н2с—он
Циклопентан-1,2-диэтанол
Бензол Уксусная Бензолуксусная
кислота кислота
СН3
+ сн2 I
а-Этилбензол уксусная
кислота
Рис. 6.1.2
1,2,3,4-тетрагидронафталин нафталин
стирол стиролоксид
Рис. 6.1.3
958
Новый справочник химика и технолога
6.1.3. Заместительная номенклатура
6.1.3.1. Основные понятия
Формат записи названия любого соединения по заместительной номенклатуре представлен на схеме 6.1
Схема 6.1
Те или иные элементы названия, за исключением родоначального гидрида, в названии конкретного соединения могут отсутствовать, например:
6-хлоргептан-2-ол
родоначальный
гидрид
главная функциональная
группа
Основа (родоначальная структура)
Основу названия, как правило, составляет родоначальный гидрид. Родоначальный гидрид представляет собой неразветвленную ациклическую или циклическую структуру, имеющую полусистематическое или триви
альное название, в которой лигандами у скелетных атомов являются только атомы водорода (например: метан, циклогексан). Хотя некоторые тривиальные названия для разветвленных ациклических углеводородов сохранены в правилах IUPAC (табл. 6.1), их названия не рекомендуется использовать для наименования замещенных производных. При составлении названия конкретного соединения сначала называют родоначальный гидрид и только потом к этому названию добавляют аффиксы (общее название префиксов и суффиксов в названии), обозначающие соответствующие заместители.
Названия моноядерных гидридов элементов, которые в заместительной номенклатуре используются как родоначальные, приведены в табл. 6.2. Систематические названия для гидридов с устоявшимися названиями, такие как азан для аммиака, оксидан для воды, хло-ран для гидрохлорида, броман для гидробромида и т. д., в настоящее время используются редко. Однако они необходимы для наименования некоторых производных и образования названий полиядерных гидридов.
Современная номенклатура органических соединений
959
Таблица 6.1
Тривиальные названия ациклических и моноциклических углеводородов, допускаемых IUPAC в качестве родоначальных
Допускается неограниченное замещение атомов водорода
СН4 — метан (methane), СН3СН3 — этан (ethane), СН3СН2СН3 — пропан (propane), СН3СН2СН2СН3 — бутан (butane), НС^СН — ацетилен (acetylene), Н2С=С=СН2 — аллен (allene), С6Н6 — бензол (benzene)
Допускается ограниченное замещение атомов водорода (только в кольце и только префиксными заместителями)
С6Н5-СН3 — толуол (toluene), С6Н5 -СН=СН2 — стирол (styrene), С6Н5-СН=СН-С6Н5 — стильбен (stilbene)
Замещение атомов водорода не допускается
(СН3)2СНСН3 — изобутан (isobutane), (СН3)2СНСН2СН3 — изопентан (isopentane),
(СН3)4С — неопентан (neopentane), Н2С=СН(СН3)-СН=СН2 — изопрен (isoprene),
С6Н4(СН3)2 — ксилол (о-, м~, и-изомеры) (xylene), С6Н5-СН(СН3)2 — кумол (cumene), СН3-С6Н4-СН(СН3)2 — цимол (о-, м-, и-изомеры) (cymene),
—— мезитилен (mesitylene) ==<С^ — фульвен (fulvene)
Таблица 6.2
Моноядерные гидриды
Гидрид Название Гидрид Название
вн3 Боран (borane) OH2 Оксидан/водаб) (oxidane/water)
сн4 Метана)/карбан (methanea)/carbane) SH2 Сульфан (sulfane)
SiH4 Силан (silane) SH4, Х4-Сульфан (X4-sulfane)B)
GeH4 Герман (germane) SH6 Х6-Сульфан (X6-sulfane)B)
SnH4 Станнан (stannane) SeH2 Селан (selane)
PbH4 Плюмбан (plumbane) TeH2 Теллан (tellane)
NH3 Азан/аммиакб) (azane/ammonia) PoH2 Полан (polane)
PH3 Фосфана)/фосфин (phosphanea)/phosphine) FH Фторан/гидрофторидб) (fluorane/hydrogen fluoride6))
PH5 Х5-Фосфана)/фосфоран (X5-phosphanea)/phosphorane)в) C1H Хл оран/ ги дрох л оридо) (chlorane/hydrogen chloride6))
AsH3 Арсана)/арсин (arsanea)/arsine) BrH Броман/гидробромидб) (bromane/hydrogen bromide6))
AsH5 Л5-Арсана)/арсоран (X5-arsanea)/arsorane)в) IH Иодан/гидроиодид б) (iodane/hydrogen iodide б))
SbH3 Стибана)/стибин (stibanea)/sti bi ne) IH3 Х3-Иодан (X3-iodane)в)
SbH5 Х5-Стибана)/стиборан (X5-stibanea)/stiborane)B) IH5 Х5-Иодан (X.5-iodane)в)
BiH3 Висмутана)/висмутин (bismuthanea)/bismuthine) AtH Астатан (astatane)
а) Предпочтительное название.
Общеупотребительное название. в) См. Х-обозначения, подразд. 6.4.
960
Новый справочник химика и технолога
Гомогенные гидриды (исключая углеводороды и гидриды бора), представляющие собой цепи нескольких идентичных гетероатомов, могут быть названы путем добавления соответствующего умножающего префикса к названию гидрида из табл. 6.2, например:
Н Н
H2N—NH2 HS—S—SH
H H
Диазан или 2Х6-Трисульфан
гидразин (трад.) .
англ.: Diazane или англ.-. 2Z. -Trisulfane
hydrazine
Гетерогенные гидриды, представляющие собой цепи из атомов углерода и гетероатомов (с атомами углерода на концах цепи), могут быть названы по заменительной номенклатуре (см. подразд. 6.3.5).
Ациклические углеводородные родоначальные гидриды, не включенные в табл. 6.1 и 6.2, имеют систематические названия. Их наименование, а также наименование углеводородных полициклических и гетероциклических родоначальных гидридов рассмотрено далее в соответствующих подразд. 6.2.1.1,6.2.5.1,6.3.1 и 6.3.2.
Локант
Для того чтобы указать положение заместителей или кратных связей в родоначальном гидриде, используются цифровые или буквенные локанты. Две или более цифры (буквы), отделенные запятыми и расположенные в возрастающем (алфавитном) порядке, обозначают положение двух или более одинаковых заместителей, например: 1,1,2-трихлорэтан. Если имеется несколько заместителей, каждый из которых присоединен к основе двумя связями, то пары локантов разделяются двоеточиями, как в названии 1,2:5,6-ди-(9-изо-пропилиденглюцит. После запятых или двоеточий пробела не делается. Локанты соединяются с последующими и предшествующими частями названия с помощью дефисов. Для отнесения заместителей к различным частям молекулы используют локанты со штрихами. При этом локант со штрихом следует сразу за соответствующим локантом без штриха (например, 1,2,2',2",3), а локант, состоящий из цифры и строчной буквы, следует за соответствующим цифровым локантом (например, 1,2,2а,3).
Важным понятием является «наименьший набор локантов», под которым понимают набор локантов, который при сравнении с другим набором (в каждом наборе для сравнения локанты расположены в порядке увеличения) имеет меньший локант при первом встретившемся различии. При этом считается, что
(а) немеченый штрихом локант меньше такого же меченого штрихом, который в свою очередь меньше меченого двумя штрихами (2 < 2' < 2"; но 2' < 3), (б) локант с буквой больше такого же цифрового локанта без буквы (3 < За, 8а < 8Ь, 4' < 4а, 4'а < 4а'), (в) буквенные локанты, выраженные заглавными курсивными буквами и строчными буквами латинского алфавита, меньше локантов, выраженных греческими буквами, которые в свою очередь меньше цифровых локантов (А,а, 1,2 < 1,2,4.6). Например, набор локантов 2,3,6,8 меньше, чем 3,4,6,8 или 2,4,5,7; набор 1,1,5,7 меньше, чем 1,2,3,4 (сумма цифр не имеет значения!).
Названия заместителей в цепи или цикле добавляются к основе названия в виде префиксов или суффиксов.
Суффикс
Особым типом заместителей являются функциональные группы. Функциональной группой называют гетероатом или группу атомов, содержащих гетероатом, которые определяют основные химические свойства соединения. В зависимости от того, может ли функциональная группа быть указана как суффикс или нет, все функциональные группы разде.)гяют соответственно на главные (табл. 6.3) и неглавные (табл. 6.4). Кроме того, суффиксами обозначаются кратные связи («ен» — двойная связь, «ин» — тройная связь); суффикс двойной связи указывается перед суффиксом тройной, а тот, в свою очередь — ггеред суффиксом главной функциональной группы. Только один тигг функциональных групп может обозначаться в названии суффиксом или определять функциональный класс. Это ограничение, однако, не относится к суффиксам, обозначающим ненасыщенность («ен», «ин»), а также к ионным и радикальным суффиксам (например, «ий», «ид», «ил», подразд. 6.12).
3 1
Главная группа: -ОН, суффикс "-ол" Родоначальный гидрид: СНзСН2СН2СНз—бутан Название = гидрид+одна группа: бутан-1-ол
НО.
1 2 3 4 0Н
Главная группа: -ОН, суффикс "-ол" Родоначальный гидрид: СН3СН2СН2СН3 — бутан Название = гидрид+две группы: бутан-1,4-диол
Остальные заместители отражаются в названии с помощью префиксов.
Современная номенклатура органических соединений
961
Таблица 6.3
Суффиксы и префиксы важнейших функциональных групп в заместительной номенклатуре
Класс Формулаа) Обозначение в префиксе Обозначение в суффиксе
Свободные (отщепление Н’) б) -ил (-yl)
радикалы
Катионы (отщепление Н") (присоединение Н+) б) -илий (-ylium) -ий (-ium)
Анионы (отщепление Н ) (присоединение Н”) б) -ид (-id), -ит (-ite), -ат (-ate) -уид (-uide)
Карбоновые -СООН карбокси- (carboxy-) -карбоновая кислота (-carboxylic acid)
кислоты -(С)ООН -овая кислота (-oic acid)
Сульфоновые -SO3H сульфо- (sulfo-) -сульфоновая кислота (-sulfonic acid)
кислоты
Карбоксилаты -COO карбоксилато- -карбоксилат
(соли) -(С)ОО“ (carboxylato-) (-carboxylate) -оат (-oate)
Сложные эфиры -COOR R-оксикарбонил- R ... карбоксилат
(карбоновых (R-oxycarbonyl) (R... carboxylate)
кислот) -(C)OOR R... оат (R...oate)
Ацилгалогениды -COHal -(C)OHal галогснкарбонил-[ранее: галоген-формил-] (halocarbonnyl-) -карбонилгалогенид (-carbonyl halide) -оилгалогенид (-oyl halide)
Амиды -CONH, -(C)ONH2 карбамоил-(carbamoyl-) -карбоксамид (-carboxamide) -амид (-amide)
Амидины -C(=NH)NH2 -(C)(=NH)NH2 карбамимидоил-[ранее: амидино-] (carbamimidoyl-) -карбоксимидамид [ранее: -карбоксамидин] (-carboximidamide) -имидамид [ранее: -амидин] (-imidamide)
Нитрилы -C=N -(C>N циано- (cyano-) -карбонитрил (-carbonitrile) -нитрил (-nitrile)
Альдегиды -CHO формил- (formyl-) -карбальдегид (-carbaldehyde)
-(C)HO оксо- (-охо) -аль (-al)
Кетоны >C)=O оксо- (-охо) -он (-one)
Спирты, фенолы -OH гидрокси-(hydroxy-) -ол (-01)
Тиолы -SH сульфанил-[ранее: меркапто-] (sulfanyl-) -тиол (-thiol)
Амины -nh2 амино- (amino-) -амин (-amine)
Имины -NH имино- (imino-) -имин (-imine)
а) Заключенный в скобки атом углерода входит в название родоначального соединения, но не в префикс или суффикс.
б) См. подразд. 6.12.
962
Новый справочник химика и технолога
Таблица 6.4
Функциональные группы, указываемые только в префиксах
Группа Префикс Группа Префикс
-Вг бром-(bromo-) -1Х2 X= галоген: дигало-ХЛиоданил-\ранее\ дигалоиод-] (dihalo-X?-iodanyl-)
-Cl хлор- (chloro-) =n2 диазо- (diazo-)
-СЮ хлорозил- (chlorosyl-) -N3 азидо- (azido-)
-сю2 хлорил- (chloryl-) -NO нитрозо- (nitroso-)
-С1О3 перхлорил-(регсЬ1огу1-) -no2 нитро- (nitro-)
-F фтор- (fluoro-) -OR R-окси- (R-oxy-)
-I иод-(iodo-) -SR R-сульфанил-\ранее‘. R-тио-] (R-sulfanyl-)
-ю иодозил-(iodosyl-) -SeR R-селанил- \ранее\ R-селено-] (R-selanyl-)
-ю2 иодил- \ранее\ иодокси-] (iodyl-) -TeR R-телланил- [ранее-. R-теллуро-] (R-tellanyl-)
-1(ОН)2 дигидрокси-ХЛиоданил-(dihydroxy-X?-iodanyl-) -SH3 ХЛсульфанил-(X.4-sulfanyl-)
Префикс
Префиксы разделяют на отделяемые и неотделяе-мые. Неотделяемые префиксы, обозначающие модификацию родоначального гидрида, являются составной частью основы названия (см. схему в подразд. 6.1.3.1). К ним относятся:
1) префиксы, указывающие на удаление («апо», «дез», «нор») скелетных атомов из родоначального гидрида или их добавление («гомо»);
2) префиксы, указывающие на изменение порядка соединения атомов в родоначальном гидриде («абео», «изо», «ретро», «секо», «спиро», «цикло»);
3) «а»-префиксы заменительной номенклатуры, обозначающие замену скелетных атомов углерода на гетероатомы: «аза», «окса», «тиа» и т. п.;
4) конденсирующие префиксы («бензо», «циклопента», «фуро» и т. п.);
5) мостиковые («метано», «бензоло», «эпициклопента» и т. п.).
«Гидро» префиксы обычно рассматривались и как отделяемые и как неотделяемые, однако последние рекомендации ШРАС (1993 г.) предлагают классифицировать их как неотделяемые.
При наименовании достаточно сложных структур, как правило, имеющих в основе тривиальное название, может появиться необходимость использовать несколько неотделяемых префиксов. Порядок их перечисления перед названием родоначального гидрида представлен на схеме 6.2.
Если в названии присутствуют несколько неотделяемых префиксов из одной группы, то они перечисляются в алфавитном порядке.
Префиксы заместителей (простых и сложных) являются отделяемыми и приводятся перед основой (т. е. перед родоначальным гидридом или неотделяемыми префиксами, если они присутствуют) в алфавитном порядке. Умножающие приставки для идентичных простых заместителей не учитываются при определении алфавитного порядка. То же правило применяется при определении порядка расположения простых заместителей в сложном заместителе. Сложный заместитель при определении его места перед основой рассматривается как единое целое. Применение алфавитного порядка приводит к тому, что часто в названиях на русском и английском языках порядок перечисления префиксов различен, например:
сложный заместитель простой заместитель q] '
основа (родоначальный гидрид)
1 -(1,4-Дибром-2,3-дихлорбутил)-3-хлорциклогексан англ.-. 1-Chloro-3-(1,4-dibromo-2,3-dichlorobutyl)cyclohexane
Префиксы для основных функциональных заместителей (замещающих групп) (В последних рекомендациях правил IUPAC употреблять термин «радикал» как эквивалент терминов «заместитель» и «замещающая группа» не рекомендуется.) приведены в табл. 6.3, 6.4. Префиксы заместителей, являющихся производными родоначальных гидридов, формируются по следующим
Современная номенклатура органических соединений
963
правилам. Свободные валентности, получающиеся при отщеплении одного или нескольких атомов водорода от родоначального гидрида, обозначаются суффиксами, приведенными в табл. 6.5.
Указанные суффиксы используются двумя способами. В первом, который рекомендуется использовать только для насыщенных ациклических и моноциклических углеводородных заместителей и моноядерных гидридов Si, Ge, Sn, Pb и В, суффиксы «-ил», «-илиден», «-илидин», заменяют окончание «ан» соответствующего гидрида. При этом в ациклических фрагментах атом со свободной валентностью находится на конце цепи и имеет локант «1», который не указывается в названии. По второму способу любой из приведенных суффиксов может быть добавлен к названию родоначального гидрида. При этом атомам со свободными валентностями присваиваются наименьшие возможные локанты, согласующиеся с нумерацией родоначального гидрида, см. рис. 6.1.5.
Сокращенные и тривиальные названия, допускаемые правилами IUPAC для углеводородных ациклических, циклических и гетероциклических заместителей, приведены в табл. 6.8.
Умножающие приставки (умножающие префиксы) (табл. 6.6) используются в названиях для обозначения числа одинаковых заместителей и помещаются перед соответствующим префиксом или суффиксом этого заместителя.
В англоязычной литературе локанты пишутся перед префиксами и перед суффиксами. Например, соединение 1 следует называть (£)-l-chloropent-2-ene (стереодескриптор (£-) указывает на конфигурацию двойной связи (см. подразд. 6.15)). Такой же порядок принят и в Beilsteine.
1
Замена скелетных атомов
<__________________/
Изменение порядка соединения атомов \_________________/
Удаление/добавление скелетных атомов
Родоначальный гидрид
аза, окса, абео, ретро,
апо, гомо, дез, нор
тиа и т.д. секо, спиро, цикло
Схема 6.2
Н3ССН2СН2СН2СН2СН2—
1) Гексил, англ.-. Hexyl;
2) Гексан-1-ил, англ.: Hexan-1-yl
Н3ССН2СН2СНСН3
1) 1-Метилбутил, англ.-. 1-Methylbutyl;
2) Пентан-2-ил, англ.-. Pentan-2-yl
Н3СССН3
1) 1 -Метилэтан-1,1 -ди ил, англ.-. 1-Methylethane-1,1-diyl;
2) Пропан-2,2-диил, англ.'. Propan-2,2-diyl
НзССН2СН2С=
2) Бутан-1-ил-1-илиден, англ.-. Butan-1-yl-1-yliden
Н3СССН3
1) 1-Метилэтилиден, англ.-. 1-Methylethylidene;
2) Пропан-2-илиден, англ;. Propan-2-ylidene; трив;. Изопропилиден, англ.: Isopropylidene
—СН2СН2СН2—
2) Пропан-1,3-диил, англ; Propan-1,3-diyl
Н ггн Г— 1 2) Пропан-1,1,1 -триил, H3GGN2G англ.: Ргорап-1,1,1 -triyl
1) Циклопентил, англ.: Cyclopentyl;
2) Циклопентан-1-ил, англ.: Cyclopentan-1-yl
Н3ССН2С=
1) Пропилидин, англ.: Propylidyne;
2) Пропанилидин, англ. :Propanylidyne
Рис. 6.1.5
964
Новый справочник химика и технолога
Суффиксы для обозначения свободных валентностей заместителей а)
Таблица 6.5
Одновалентные Двухвалентные Трехвалентные Четырехвалентные
-ил (-yl) (Е-) -диил (-diyl) (-Е-) -илиден (-ylidene) (Е=) -триил (-triyl) (-Е<) -илидин (-ylidyne) (Es) -илилиден (-ylylidene) (-Е=) -тетраил (-tetrayl) (>Е<) -илилидин (-ylylidyne) (-Е=) -диилиден (-diylidene) (=Е=) -диилилиден (-diylylidene) (>Е=)
а) Суффиксы «-илиден», «-илидин» рекомендуется применять для обозначения заместителей, которые присоединены к основе двойной или тройной связью соответственно. Буква Е в примере обозначает элемент.
Таблица 6.6
Умножающие приставкиа)
Умножающий фактор Префикс Умножающий фактор Префикс Умножающий фактор Префикс
1 моно б) 11 ундека 30 триаконта
2 ДИ 12 додека 31 гентриаконта
3 три 13 тридека 32 дотриаконта
4 тетра
5 пента 20 эйкоза 40 тетраконта
6 гекса 21 генэйкоза
7 гепта 22 докоза 100 гекта
8 окта 23 трикоза 200 дикта
9 нона 24 тетракоза
10 дека 243 тритетраконта-дикта
а) Для сложных заместителей (например, идентичных, одинаково замещенных групп) могут быть использованы иные умножающие префиксы: ди —> бис, три -> трис, тетра -> тетракис, пента -» пентакис и т. д.
б) В названии обычно не указывается.
Программы для автоматического наименования соединений, встроенные в современные химические программные комплексы ChemDraw, IsisDraw и др., также следуют этому правилу. В русскоязычной литературе соответствующие локанты часто записывают перед префиксами, но после суффиксов, т. е. соединение 1 называют как (Е)-1-хлорпентен-1. Такой порядок записи мотивируют тем, что в этом случае название меньше разбивается и его легче воспринимать на слух. Это довольно слабая аргументация, поскольку в устной речи сложными названиями, содержащими много локантов, вообще нельзя пользоваться эффективно. Поэтому при написании названий следует придерживаться рекомендаций ВИНИТИ (Всероссийского института научной и технической информации), которые в данном аспекте совпадают с англоязычной традицией, и в русскоязычном варианте название соединения 1 рекомендуется записывать как (£)-1 -хлорпент- 1-ен.
Иллюстрация основных принципов составления названия на простом примере
Как показывает практика, при составлении названия соединения во избежание ошибок и излишних потерь времени полезно придерживаться определенного порядка действий:
- написать развернутую структурную формулу соединения;
- идентифицировать все имеющиеся в соединении функциональные группы (табл. 6.3, 6.4);
- выбрать старшую из главных функциональных групп, которая будет обозначена в названии суффиксом (если таковая имеется) (табл. 6.7);
- исходя из природы соединения, выбрать наиболее подходящий тип номенклатуры;
- выбрать главную цепь или цикл (родоначальный гидрид, включая необходимые неотделяемые префиксы);
- пронумеровать структуру;
- определить все префиксные заместители (табл. 6.3, 6.4) в главной цепи или цикле с соответствующими умножающими приставками (см. табл. 6.6);
- определить сложные заместители;
- определить локанты заместителей и кратных связей;
- сформировать название, последовательно записывая префиксные заместители в алфавитном порядке (при определении алфавитного порядка умножающие приставки в простых заместителях не учитываются!), основу и суффикс старшей функциональной группы с соответствующими умножающими приставками и локантами.
Проиллюстрируем применение этого алгоритма на примере построения названия соединения 2.
Современная номенклатура органических соединений
965
Первое, что нужно сделать, это определить все имеющиеся в соединении функциональные группы. В данном случае это: -СООН, -СНО и -С1. Две первые из них в названии соединений могут быть главными (суффиксными), а гретья, —С1, — только префиксной. Затем, пользуясь табл. 6.7, следует выбрать из двух
главных групп старшую, причем это необходимо сделать в первую очередь независимо от того, каким типом номенклатуры вы решили воспользоваться. Эта и только эта функциональная группа указывается в суффиксе, а все остальные помещаются в виде префиксов (табл. 6.3, 6.4).
Рис. 6.1.6
Таблица 6.7
Классы соединений, расположенные в порядке падения старшинства главных групп
1 Свободные радикалы
2 Анионы
3 Катионы
4 Цвиттер-ионные соединения
5 Кислоты в следующем порядке: RCOOH, RC(O)O2H, затем последовательно их S- и Se-производные, далее сульфоновые, сульфиновые, селеноновые и т. д., фосфоновые и т. д., арсоновые и т. д. кислоты
4 Производные кислот в следующем порядке: ангидриды, эфиры, ацилгалогениды, амиды, гидразиды, имиды, амидины и т. д.
5 Нитрилы, изоцианиды и т. д.
6 Альдегиды, затем последовательно их S-, Se- и Те-аналоги, затем их производные
7 Кетоны, затем последовательно их S-, Se- и Те-аналоги
8 Спирты, затем фенолы, затем S-, Se- и Те-аналоги спиртов, затем сложные эфиры спиртов с неорганическими кислотами (за исключением галогеноводородных кислот), затем аналогичные производные фенолов в той же последовательности
9 Амины, затем имины, гидразины, фосфаны и др.
10 Эфиры, затем сульфиды, селениды, теллуриды
11 Пероксиды, затем дисульфиды, диселениды, дителлуриды
966
Новый справочник химика и технолога
Главная группа определяет порядок формирования названия и, как правило, нумерации соединения, и именно поэтому построение названия нужно начинать с нее, а не с выбора, например, главной цепи (родоначального гидрида). Так, если в рассматриваемом примере начинать построение названия с выбора главной цепи, а это — декан, то мы придем к неправильному названию — арил-замещенному декану. Из трех имеющихся функциональных групп в соединении 2 (рис. 6.1.6) две (-СООН, -СНО) могут быть суффиксными, а третья, -С1 — только префиксной. Руководствуясь табл. 6.7, определяем главную группу наибольшего старшинства — карбоксильная (формула 2а). Следующий шаг — определение родоначального гидрида; это название той цепи (цикла), к которой присоединена главная группа. Выбор главной цепи иногда может вызвать определенные затруднения. Если имеются варианты, предпочтение отдается более ненасыщенной цепи, хотя эта цепь может быть и не самой длинной. Если имеется возможность выбора между цепями с равной степенью гидрирования, то пользуются критериями, приведенными в разделе 6.2.1.1 (см. также подразд. 6.13).
Для соединения 2 родоначальным гидридом является бутан, поскольку именно в состав бутановой цепи входит карбоксильная группа (главная функциональная группа наибольшего старшинства) (формула 26). Главную цепь следует пронумеровать так, чтобы атом углерода, несущий главную группу, получил наименьший номер. Функциональные группы типа -С(=О)Х (где Х=Н, ОН, OR, элемент) однозначно определяют начало нумера
ции цепи, начиная с атома углерода функциональной группы, т. е. этому атому приписывается локант «1».
Таким образом, в основе названия соединения 2 получаем бутановую кислоту со сложным заместителем в положении 4 цепи, который весь следует записать в префикс. Заместитель представляет собой бензольное кольцо (соответствующий префикс — фенил, см. табл. 6.8) с четырьмя заместителями (префиксы см. в табл. 6.3 и 6.4): формил-, хлор-, метил- и сложный углеводородный заместитель (ранее такие заместители называли радикалами). Названия неразветвленных одновалентных заместителей (алкильных замещающих групп) производятся от названий алканов путем замены суффикса «ан» на «ил», например, метан —> метил (табл. 6.5). Для некоторых сложных заместителей правила 1UPAC допускают тривиальные названия (табл. 6.8). Поскольку для углеводородного заместителя у ароматического кольца соединения 2 не существует простого тривиального названия, допускаемого правилами 1UPAC, то его следует называть, как сложный заместитель. Порядок составления названия сложного заместителя следующий: выбрав основную цепь заместителя, перечисляют в алфавитном порядке все имеющиеся в нем заместители с соответствующими локантами, начиная нумерацию с места присоединения цепи к основному фрагменту (в данном случае к фенилу). Проделав эту операцию с углеводородным заместителем в ароматическом кольце соединения 2, получим — «1,5-диметил-7-этилнонил» (формула 2в). При формировании названий сложных префиксных заместителей используются круглые, а при необходимости и квадратные скобки.
Таблица 6.8
Тривиальные названия углеводородных заместителей, разрешенные правилами IUPAC в качестве префиксов
Допускается неограниченное замещение атомов водорода
-СН2-----метилен (methylene), -СН2СН2------ этилен (ethylene),
СН2=СН2------винил (vinyl), Н2С=СНСН2- — аллил (allyl),
С6Н5-----фенил (phenyl), -С6Н4- — о-, м-, или и-фенилен (phenylene)
Допускается ограниченное замещение атомов водорода (только в кольце)
С6Н5-СН2-----бензил (benzyl), С6Н5-СН2= — бензилиден (benzylidene),
С6Н5-СН=СН------стирил (styryl), С6Н5-СН2СН2-----фенэтил (phenethyl),
С6Н5-СН:=СН-СН2-----циннамил (cinnamyl),
(С6Н5)2СН----бензгидрил (benzhydryl), (С6Н5)3С---тритил (trityl)
Замещение атомов водорода не допускается
(СН3)2СН-----изопропил (isopropyl), (СН3)2С= - изопропилиден (isopropylidene),
СН2=С(СН3)------изопропенил (isopropenyl), (СН3)2СНСН2-----изобутил (isobutyl),
СН3СН2СН(СН3)-------вшрр-бутил (sec-butyl), (СН3)3С—— трет-бутил (ZerZ-butyl),
(СН3)2СНСН2СН2- — изопентил (isopentyl), СН3СН2С(СН3)2------- шре/и-пентил (ZerZ-pentyl),
(СН3)3ССН2------неопентил (neopentyl),
СН3-С6Н4-----толил (tolyl), 2,4,6-(СН3)3СбН2--мезитил (mesityl)
Современная номенклатура органических соединений
967
Следующий шаг — это определение локантов для заместителей в бензольном кольце. Нумерацию начинают от места присоединения кольца к главному фрагменту — бутановой кислоте и далее ведут в направлении, обеспечивающем наименьшую последовательность локантов: 2-хлор, 3-метил, 4-( 1,5-диметил-7-этилнонил), 5-формил (формула 2г). Если последовательность локантов в обоих направлениях одинакова, то наименьший локант присваивается заместителю, стоящему первым по алфавиту. Для завершения названия необходимо определить последовательность перечисления всех префиксных заместителей. Все префиксы расставляются в алфавитном порядке независимо от величины локанта, при этом умножающие приставки не учитываются, если только они не принадлежат сложному заместителю. В результате для соединения 2 получаем название:
4-[4-(1,5-диметил-7-этилнонил)-3-метил-5-формил-2-хлорфенил |бутановая кислота.
Следует помнить, что расстановка префиксов в алфавитном порядке приводит к тому, что в английском варианте порядок перечисления префиксов, как правило, отличается от русского; так, английское название соединения 2 будет выглядеть следующим образом:
4-|2-chloro-4-(7-ethyl-l,5-dimethylnonyl)-5-formyl-3-methylphenyl]butanoic acid.
6.2. Номенклатура углеводородов
6.2.1. Ациклические углеводороды
6.2.1.1. Алканы
Для построения названия алкана следует:
1. Найти главную цепь углеводорода, которой является самая длинная цепь, и назвать ее путем объединения умножающей приставки (табл. 6.6), соответствующей числу атомов углерода в цепи, с суффиксом «ан» («апе»). Исключение представляют названия первых четырех членов ряда: метан, этан, пропан, бутан (табл. 6.1).
З-Метил-4-пропилоктан англ:. 3-Methyl-4-propyloctane
З-Метил-4-бутилгептан
Перед названием неразветвленного углеводорода иногда приписывают курсивную букву «н-» (нормальный), подчеркивая этим линейный характер молекулы.
Если есть несколько цепей одинаковой длины, то предпочтение последовательно отдается цепи:
- в которой имеется наибольшее количество ответвлений, например см. рис. 6.2.1;
- в которой заместители имеют наименьший набор локантов, например см. рис. 6.2.2;
- которая имеет наибольшее количество атомов углерода в наиболее коротких ответвлениях, например см. рис. 6.2.3;
- которая имеет наименьшее количество разветвленных боковых цепей, например см. рис. 6.2.4.
, но не
2,3,5-Триметил-4-пропилгептан 4-(втор-Бутил)-2,3-диметилгептан англ:. 2,3,5-Trimethyl-4-propylheptane
Рис. 6.2.1
4-(втор-Бутил)-2,6-диметилгептан
4-Изобутил-2,5-диметилгептан англ:. 4-lsobutyl-2,5-dimethylheptane
Рис. 6.2.2
968
Новый справочник химика и технолога
7,7-Бис(2,4-диметилгексил)- 7-(2,4-Диметилгексил)-3,5,9,11-тетраметил-
5,9,11-триметил-З-этилтридекан 7-(2-метил-5-этилгексил)тридекан
англ.: 7,7-Bis(2,4-dimethylhexyl)-3-ethyl-
5,9,11 -trimethyltridecane
Рис. 6.2.3
6-(1-Изопропилпентил)-5-пропилдодекан
англ.: 6-(1-lsopropylpenthyl)-
5-propyldodecane
5-(Изопропил)-6-(1-пропилпентил)до-декан
Рис. 6.2.4
2. Последовательно пронумеровать атомы углерода главной цени, начиная с ближайшего к разветвлению конца. Если первые разветвления имеются на одинаковом расстоянии от обоих концов цепи, то нужно составить две возможных последовательности локантов и выбрать наименьшую (см. подразд. 6.1.3.1).
3. Назвать замещающие группы (боковые цепи) в соответствии с числом имеющихся в них атомов углерода, записать их в алфавитном порядке перед названием главной цепи и указать их положение, поставив перед каждой группой номер атома главной цепи (локант), с которым она связана. Если имеются две или несколько одинаковых алкильных групп, то перед соответствующим префиксом следует использовать умножающую приставку; одинаковые локанты в этом случае пишутся через запятую (см. примеры выше).
Алкены
Для некоторых алкенов правила IUPAC допускают использование тривиальных названий (см. табл. 6.1). Систематические названия алкенов образуются из соответствующих названий алканов путем замены суффикса «ан» на «ен» («епе») и указанием положения двойной связи в цепи с помощью локанта. В качестве главной цепи выбирается наиболее ненасыщенная (не обязательно самая длинная!). Нумерация начинается
с конца цепи, который ближе к двойной связи. В полиенах для указания количества двойных связей к суффиксу «ен» добавляют умножающие приставки, а цепь нумеруют так, чтобы двойные связи были обозначены наименьшими локантами, например см. рис. 6.2.5.
Алкины
Названия алкинов образуются из соответствующих названий алканов путем замены суффикса «ан» на «ин» и указания положения тройной связи в цепи с помощью локанта. Правила выбора главной цепи и начала нумерации такие же, как для алкенов. Все правила номенклатуры, представленные для алкенов, сохраняют силу и для алкинов, например см. рис. 6.2.6.
Енины
Углеводороды, в которых одновременно присутствуют двойные и тройные связи, получают названия, в которых суффикс «ан» в названии соответствующего алкана заменяется на «енин», «адиенин», «ендиин» и т. д., т. е. сначала всегда указывается суффикс двойной, а затем тройной связи. Нумерацию проводят так, чтобы кратным связям соответсвовал наименьший набор локантов, даже если при этом суффикс «ин» получает меньший номер, чем «ен». Если имеется несколько вариантов нумерации, то наименьшие номера получают двойные связи (рис. 6.2.7).
Современная номенклатура органических соединений
969
Свободные валентности в ациклических углеводородах
При использовании углеводородных цепей в качестве замещающих групп соответствующие свободные валентности обозначают с помощью суффиксов, приведенных в табл. 6.5. Атомам углерода, несущим свободную валентность, присваивается локант «1». Углерод
ный атом с номером «1» обязательно входит в главную цепь (рис. 6.2.8); если остается выбор, то используются принципы, приведенные выше. Для некоторых углеводородных замещающих групп правила IUPAC допускают применение тривиальных и полусистематических названий (табл. 6.8).
2,5,5-Т риметил гекс-2-ен англ.-. 2,5,5-Trimethylhex-2-ene
2-Метил-6-этилокта-2,5-диен
англ.-. 6-Ethyl-2-methylocta-2,5-diene
Рис. 6.2.5
4,5-Диметилгекс-2-ин
англ.-. 4,5-Dimethylhex-2-yne
Рис. 6.2.6
Гекса-1,5-диен-З-ин
англ.-. Hexa-1,5-dien-3-yne
4-Метилпент-3-ен-1 -ин
англ.-. 4-Methylpent-3-en-1-yne
Гекса-1,3-диен-5-ин
англ.-. Hexa-1,3-dien-5-yne
Рис. 6.2.7
1-Метиленпент-4-ен-2-ин-1-ил
англ.: 1-Methylenepent-4-en-2-yn-1 -yl
4-Метилпент-3-ен-1 -ин-1 -ил англ.: 4-Methylpent-3-en-1-yn-1-yl
1 -Винил-2-изобутилбут-3-ин-1 -илиден англ.: 2-lsobutyl-1-vinylbut-3-yn-1-ylidene
Рис. 6.2.8
970
Новый справочник химика и технолога
6.2.2. Моноциклические алифатические углеводороды
Названия алициклических углеводородов образуют из названий алифатических углеводородов с тем же числом атомов углерода путем добавления неотделяс-мого префикса «цикло» («cyclo»). Определенные сложности могут возникать при наличии в цикле боковой цепи. Основная проблема заключается в том, какой фрагмент взять в качестве родоначального названия: цепь или цикл. В этом случае рекомендуется руководствоваться двумя критериями: а) максимальная заме-щенность фрагмента и б) размер фрагмента (см. также подразд. 6.13). В соответствии с этими критериями основной фрагмент выбирают следующим образом:
- в углеводороде, содержащем несколько цепочек, присоединенных к циклу, за основу берется цикл, например см. рис. 6.2.9;
- в углеводороде, содержащем несколько циклов, присоединенных к цепи, за основу берется цепь, например см. рис. 6.2.10;
- если цикл по размеру больше цепи, за основу, как правило, берется цикл, например см. рис. 6.2.11;
- если цепь по размеру больше цикла, то за основу, как правило, берется цепь, например см. рис. 6.2.12.
Нумерация насыщенного цикла как основного фрагмента проводится таким образом, чтобы заместители получили наименьший набор локантов. При выполнении этого условия и при наличии выбора меньший локант приписывается тому заместителю, который стоит первым по алфавиту. Следует иметь
в виду, что нумерация цикла в русском названии может отличаться от его нумерации в английском названии, например:
русс:. 6-Метил-1-пропил-3-этилциклооктан
англ: 1 -Ethyl-6-methyl-3-propylcyclooctane
При построении названий циклоалкенов и циклоалкинов используется совокупность правил, перечисленных в предыдущих разделах, посвященным алкенам и алкинам. Нумерацию начинают с кратной связи в цикле (при приоритете двойной связи над тройной) и проводят таким образом, чтобы атом под номером 2 принадлежал той же кратной связи, а другие кратные связи получили наименьшие номера. При выполнении вышеупомянутых условий локанты заместителей должны получить наименьшие из возможных значений, например:
5-Метилциклогекса-1,3-диен англ:. 5-Methylcyclohexa-1,3-diene
1 -Бутил-2-метилциклопропан англ:. 1 -Butyl-2-methylcyclopropane
Рис. 6.2.9
1,2-Дициклопропилпропан англ: 1,2-Dicyclopropylpropane
Рис. 6.2.10
Изобутилциклопентан англ: Isobutylcyclopentane
Рис. 6.2.11
11 -Циклооктилдодец-1 -ен англ: 11-Cyclooctyldodec-1-ene
Рис. 6.2.12
Современная номенклатура органических соединений
971
6.2.3. Моно циклические ароматические углеводороды (производные бензола)
Правила IUPAC разрешают использовать тривиальные названия для некоторых моноциклических замещенных ароматических углеводородов (табл. 6.1). Для указания положения заместителей в бензольном кольце используют две системы. В одной из них в качестве локантов применяются цифры, в другой — буквы. В первой системе атому, несущему заместитель, присваивают локант «1» и ведут нумерацию так, чтобы получить наименьшую последовательность локантов. Если возможен выбор между одинаковым набором локантов, то нумерацию начинают с заместителя, стоящего первым по алфавиту, например см. рис. 6.2.13.
По второй системе для указания положения заместителей используются префиксы «.орто-» («ortho-»), «мета-» («meta-»), «пара-» («рага-»), обозначающие относительное расположения заместителей:
орто-мета-
R
6орто-мета-пара-
Префиксы «орто-», «мета-», «пара-» в несокращенном виде используются в устной речи, а записывают их чаще всего однобуквенными символами о-, м-, п- (курсив). Эту номенклатуру удобно использовать при наличии в кольце двух одинаковых заместителей либо при использовании разрешенных тривиальных названий в качестве основы, например см. рис. 6.2.14.
Если ароматическое кольцо не является основой названия, то оно записывается в виде префикса арильной замещающей группы, например, фенил, «-толил и т. п. (см. табл. 6.8), а при отсутствии тривиального названия для арильного заместителя — в виде префикса замещенного фенильного заместителя.
з
1 -Бутил-4-этилбензол англ.-. 1-Butyl-4-ethylbenzene
нумерация представлена для русского названия
1 -Метил-2-пропил-З-этилбензол
англ.: 1 -Ethyl-3-methyl-2-propylbenzene
Рис. 6.2.13
jw-Дивинилбензол я-Этилстирол о-Аллил-о-пропилтолуол
англ.-. m-Divinylbenzene англ.: p-Ethylstyrene англ.: o-Allyl-o-propyltoluene
Рис. 6.2.14
6.2.4. Полициклические углеводороды
(см. также номенклатуру ансамблей (подразд. 6.6))
6.2.4.1. Спираны
Спиранами называются соединения, в которых два (или три) кольца имеют только один общий атом и эти кольца не связаны мостиком. Общий атом называется спиро-атомом.
Моноспираны
Названия моноспиросоединений, состоящих из двух моноциклов, начинаются с префикса «спиро», за которым следуют квадратные скобки, в которых указывает
ся число атомов сначала меньшего цикла, а затем, после точки — большего (общий атом углерода при этом не учитывается). После скобок следует название углеводорода, содержащего суммарное число атомов углерода всей спиро-системы. Нумерация атомов молекулы начинается с атома в меньшем цикле ближайшего к спиро-атому и идет по периметру молекулы. Если циклы содержат кратные связи, то они должны иметь по возможности наименьшие локанты, например см. рис. 6.2.15.
Неразветвленные полиспираны
Неразветвленные полиспираны, состоящие только из моноциклов, называют, используя префиксы «дис-
972
Новый справочник химика и технолога
пиро-», «триспиро-» и т. д., указывающие общее число спироатомов, и название углеводорода с соответствующим числом атомов. Между ними в квадратных скобках указывается число атомов, присоединенных к спиро-атому и связывающих спиро-атомы. Числа перечисляются, начиная с меньшего крайнего кольца в направлении другого крайнего кольца и затем назад к первому по другим связывающим цепочкам. Для три-спиро-систем и спиро-систем большего размера, при перечислении цепочек, связывающих спиро-атомы, когда спиро-атом встречается второй раз, его локант приводится в виде надстрочного индекса к числу, показывающему количество атомов в соответствующей цепочке. Нумерация атомов в полиспиро-системах производится аналогично нумерации в моноспиро-соедине-ниях, начиная с наименьшего крайнего цикла, причем спиро-атомы должны получить, по возможности, наименьшие локанты. Если, по-прежнему, имеется выбор, то числа в скобках рассматривают в порядке перечисления в названии и выбирают вариант с наименьшим числом при первом различии, например см. рис. 6.2.16.
Разветвленные полиспираны
Названия разветвленных полиспиранов, состоящих только из моноциклов, составляются аналогично, например см. рис. 6.2.17.
Если существуют варианты при нумерации спиро-систем, содержащих гетероатомы (при использовании «а»-номенклатуры), функциональные группы или заместители, последовательно руководствуются следующими критериями, пока не будет достигнут однозначный выбор:
1) Низший набор локантов приписывается гетероатомам.
2) Низшие локанты приписываются гетероатомам в следующем порядке: 0>S>Se>Te>N>P>As>Sb > Bi > Si > Ge > Sn > Pb > В > Hg (рис. 6.2.18).
3) Низшие локанты приписываются гетероатомам в нестандартном валентном состоянии, выражаемом
с помощью ^.-символов (при этом X6 < X4 и т. д.) (рис. 6.2.19).
4) Низшие локанты приписываются радикальным центрам или, если система является заместителем, точке се присоединения (рис. 6.2.20).
5) Низшие локанты приписываются катионным центрам.
6) Низшие локанты приписываются суффиксным главным группам.
7) Низшие локанты приписываются двойным связям (рис. 6.2.21).
8) При определении локантов заместителей следуют обычным принципам заместительной номенклатуры.
Моноспираны с двумя идентичными полициклическими компонентами
Такие соединения называют, помещая префикс «спироби» перед названием компонента в квадратных скобках. Нумерация компонентов, определяемая соответствующими правилами, сохраняется, причем для одного из компонентов используются локанты со штрихом. Положение спиро-атома указывается с помощью соответствующих локантов (первым приводится нештрихованный). При наличии выбора низшие локанты приписываются спиро-атомам (меньший локант указывают без штрихов), а затем, при необходимости, — «обозначенному водороду» (см. подразд. 6.2.5.2). Локанты «обозначенного водорода» указываются перед локантами спиро-атома (рис. 6.2.22).
При использовании «а»-номенклатуры для мостиковых компонентов, локанты для гетероатомов, функциональных групп и заместителей присваиваются в соответствии с приведенными выше принципами. «Обозначенный водород» имеет преимущество перед главными группами в присвоении наименьшего локанта. По возможности используются нештрихованные локанты (рис. 6.2.23).
2-Метилспиро[3.4]октан
англ.-. 2-Methylspiro[3.4]octane
Спиро[4.5]дека-1,6-диен англ.-. Spiro[4.5]deca-1,6-diene
Диспиро[5.1.7.2]гептадекан англ.-. Dispiro[5.1,7.2]heptadecane
Рис. 6.2.15
Триспиро[2.2.2.29 26.33]гексадекан, а не триспиро[2.2.2.29.36.23]гексадекан
англ.: Trispiro[2.2.2.29.26.33]hexadecane
Рис. 6.2.16
Современная номенклатура органических соединений
973
12 13 14 1
Триспиро[2.1.25.2.210.23]тетрадекан англ.: Т rispi го[2.1.25.2.21 °.23]tetradecane
10 8
Нонаспиро[2.0.0.0.26.0.29.05.0.0.2130.216.012.04.0.219.03]генэйкозан англ.-. Nonaspiro[2.0.0.0.26.0.29.05.0.0.2130.216.012.04.0.219.03]henicosane
Рис. 6.2.17
9-Т иа-6-азаспиро[4.5]декан англ.-. 9-Thia-6-azaspiro[4.5]decane
6-Тиа-10-азаспиро[4.5]декан англ.-. 6-Thia-10-azaspiro[4.5]decane
Рис. 6.2.18
6k5,10-Дифосфаспиро[4.5]декан англ.: 6k5,10-Diphosphaspiro[4.5]decane
Рис. 6.2.19
Спиро[4.5]декан-2-ил
англ.-. Spiro[4.5]decan-2-yl
3,9-Диазаспиро[5.5]ундекан-9-ий-3-ил англ.-. 3,9-Diazaspiro[5.5]undecan-9-ium-3-yl
1-Оксаспиро[4.4]нонан-7-ил
англ.-. 1-Oxaspiro[4.4]nonan-7-yl
Рис. 6.2.20
Спиро[4.5]дека-1,9-диен-6-он англ.-. Spiro[4.5]deca-1,9-dien-6-one
Рис. 6.2.21
974
Новый справочник химика и технолога
8,8'-Спироби[бицикло[5.1.0]октан] англ: 8,8'-Spirobi[bicyclo[5.1.0]octane]
1Н, 1 'Н-2,2'-Спироби[нафталин] англ: 1Н, 1 'H-2,2'-Spirobi[naphthalenej
2'Н,ЗН-2,3'-Спироби[[1]бензотиофен] гл:. 2'H,3H-2,3'-Spirobi[[1]benzothiophene]
Рис. 6.2.22
Диспираны с идентичными полициклическими компонентами
Соединения такого типа называют, помещая префикс «диспиротер» перед названием компонента в квадратных скобках. Для нумерации среднего компонента используют штрихованные цифры, а оставшийся компонент помечают двойными штрихами. Положение спиро-атомов указывается перед названием двумя парами локантов, разделенных двоеточием. Если имеется выбор, то спиро-атомам приписываются наименьший набор локантов, при их рассмотрении в убывающем порядке, а если выбор остается, то в порядке перечисления в названии (рис. 6.2.24).
Моноспираны с различными компонентами
Моноспиросоединения с различными компонентами, по крайней мере один из которых является полициклом называют, помещая названия компонентов в алфавитном порядке в квадратные скобки, перед которыми расположен префикс «спиро». Положение спиро-атома обозначают соответствующими локантами, которые помещают между названиями компонентов. Локанты второго компонента помечаются штрихами, однако другие локанты, необходимые для наименования этого компонента, используются без штрихов, но помещаются в квадратные скобки. «Обозначенный водород» приводится перед полным названием (рис. 6.2.25).
7 1 1'
Неразветвленные полиспиросоединения с двумя и более различными компонентами
Неразветвленные полиспиросоединения с двумя и более различными компонентами, из которых по крайней мере один является полициклом, называют, последовательно помещая название каждого компонента, начиная с крайнего, первого но алфавиту компонента, в квадратные скобки, перед которыми расположен префикс «диспиро», «гриспиро» и т. д. (рис. 6.2.26).
Разветвленные полиспираны
с одним и более полициклическим компонентом
Название соединения, в котором центральный компонент спиро-сочленен с тремя и более идентичными компонентами, состоит из префикса «триспиро» и т. д., за которым в квадратных скобках последовательно помещают название центрального компонента, умножающую приставку (трис, тетракис и т. д.) и название терминального компонента. Положение спиро-атомов указывается с помощью пары локантов (для терминальных компонентов со штрихами, двойными штрихами и т. д.) (рис. 6.2.27).
Если два или более различных терминальных компонента спиро-сочленены с центральным компонентом, то сначала указывают компонент первый по алфавиту (если надо — с умножающими приставками), затем — центральный компонент и далее — остальные компоненты по алфавиту (рис. 6.2.28).
т
5,6'-Диокса-2,2'-спироби[бицикло[2.2.2]октан]-7,7|-диен англ: S^'-Dioxa^^'-spirobitbicyclo^^JoctaneJ^J'-diene
1/-/,1'Н-2,2'-Спироби[нафталин]-1-он англ: 1H,17-/-2,2'-Spirobi[naphthalen]-1-one
Рис. 6.2.23
Современная номенклатура органических соединений
975
1 "Н,2Н,ЗНАТНА ,6': 1 ',2"-Диспиротер[нафталин] англ.-. 1"/-/,2/-/,5,/-/,7'/-/-1,6':r,2"-Dispiroter[naphthalene]
Рис. 6.2.24
Спиро[инден-1,Г-циклогексан] англ.-. Spiro[cyclohexane-1,Г-indene]
Рис. 6.2.25
2"Н,4"Н-Триспиро[цикпогексан-1,Г-циклопентан-3',3"-циклопента[Ь]пиран-6", 1 '"-циклогексан],
но не
27-/,4'Н-триспиро[цикпогексан-1,6'-циклопента[Ь]пиран-3',Г-циклопентан-
3", 1"'-циклогексан]
(циклопентан раньше, чем циклопента[Ь]пиран)
англ.-. 2"Н,4"/-/-Тrispiro[cyclohexane-1 ,r-cyclopentane-3',3"-cyclopenta[b]pyran-
6", 1'"-cyciohexane]
Рис. 6.2.26
Триспиро[1,3,5-тритиан-2,2':4,2":6,2,"-трис(бицикло[2.2.1]гептан)] англ.-. Trispiro[1,3,5-trithiane-2,2,:4,2":6,2",-tris(bicyclo[2.2.1]heptane)]
Рис. 6.2.27
976
Новый справочник химика и технолога
Т риспиро[адамантан-2,3'-[1,2,4>5,7,8]гексоксонан-6', 1 ":9', 1 "'-бис(цикпогексан)] англ.-. Trispiro[adamantane-2,3'-[1-2,4,5,7,8]hexoxonane-6',1":9',r"-bis(cyclohexane)]
Рис. 6.2.28
6.2.4.2. Мостиковые углеводороды (система Байера)
Основные понятия
Системы, в которых для двух или большего числа циклов несколько атомов являются общими, называются мостиковыми. При построении названий мостиковых полициклов оперируют следующими понятиями.
Узловым атомом («головой мостика», bridgehead) называют атом циклической системы, который связан с тремя или более скелетными атомами. Мостиком называют неразветвленную цепь атомов, атом или связь, соединяющую два узловых атома. Два узловых атома выбирают в качестве главных. Эти узловые атомы должны быть связаны по крайней мере тремя мостиками. В качестве главного цикла выбирают кольцо полициклической системы, содержащее максимальное число атомов и, в том числе, два главных узловых атома. Главным мостиком называют мостик, соединяющий два главных узловых атома и не входящий в основное кольцо. Вторичным мостиком называют любой мостик, не входящий в главное кольцо и основной мостик. Независимые вторичные мостики связывают узловые атомы, входящие в состав главного кольца и главного мостика. Зависимые вторичные мостики связывают узловые атомы, по крайней мере один из которых входит в состав вторичного мостика.
Считается, что полициклическая система содержит число колец, равное минимальному числу связей, которые надо разорвать, чтобы превратить систему в ациклическую. Число колец указывается в названии с помощью неотделяемых префиксов «бицикло», «трицикло», «тетрацикло» и т. д.
Карбобициклические мостиковые соединения
Насыщенные мостиковые карбоциклические соединения, состоящие только из двух циклов, называются как алканы с тем же общим числом атомов углерода с добавлением префикса «бицикло». Число скелетных атомов в каждом из трех мостиков указывают в квадратных скобках между префиксом «бицикло» и названием углеводорода. Цифры располагают в порядке уменьшения и отделяют друг от друга точками. Для указания положения заместителей систему нумеруют,
начиная с одного из узловых атомов, и, ведя нумерацию по самому длинному пути ко второму узловому атому, далее идут также по самому длинному пути к первому узловому атому, затем последовательно нумеруют атомы мостика, начиная с ближнего к первому узловому атому, например см. рис. 6.2.29.
В приведенных примерах жирными линями выделено главное кольцо.
Карбополициклические мостиковые соединения
Для построения названия более сложной мостиковой системы, содержащей п циклов, например, соединения 3 (рис. 6.2.30), его структурную формулу целесообразно нарисовать так, чтобы все циклы были расположены в одной плоскости, избегая по возможности пересечений связей (формула За).
Число циклов, указываемое в начале названия, равно минимальному числу связей, которые необходимо разорвать для получения ациклического соединения (формула За). Далее выделяют главный (наибольший) цикл (формула 36). После идентификации главного цикла его удобно изобразить как кольцо, разметив на нем атомы точками и пронумеровав их (формула Зс). Затем следует соединить атомы главного кольца соответствующими мостиками. Такой рисунок позволяет легко идентифицировать главный мостик и вторичные мостики. После определения главного мостика как содержащего максимально возможное число атомов (формула Зс) может потребоваться изменение нумерации главного кольца, чтобы нумерация начиналась от основного узлового атома. Узловые атомы главного мостика делят главный цикл на два сегмента, больший и меньший, длина которых указывается первыми двумя цифрами в квадратных скобках названия соединения (для соединения 3 — это 5 и 3). Третья цифра в квадратных скобках обозначает длину главного мостика (для соединения 3 — это 2). Главный цикл и главный мостик составляют мостиковую бициклическую систему, правила нумерации которой описаны выше. Остальные мостики считаются вторичными; их положение (номера соответствующих узловых атомов, приведенные через запятую в возрастающем порядке) указывается с помощью надстрочных индексов к цифрам, обозначающим число атомов в мостике (для соединения 3 — это О4,9). Пере-
Современная номенклатура органических соединений
977
числение вторичных мостиков в квадратных скобках производят в убывающем порядке после главного (независимые мостики указываются перед зависимыми). Нумерация любого вторичного мостика, исходя из уже пронумерованной основной бициклической системы, проводится от узлового атома, имеющего наибольший номер. Завершается название указанием названия алкана с числом атомов углерода, равным числу скелетных атомов полициклической системы. Таким образом, соединение 3 получает название трицикло|5.3.2.04,9]додекан.
Общий формат записи названия мостикового углеводорода, содержащего п циклов, имеет следующий вид, представленный на схеме 6.3.
Сумма цифр в квадратных скобках, указывающих число атомов в мостиках плюс два, равна числу скелетных атомов, например, в нижеприведенном соединении (13 + 7 + 4 + 3 + 1) + 2 = 30 — триаконтан, см. рис. 6.2.31.
Выбор мостиков
Если возможны варианты при выборе мостиков для составления названия, последовательно руководствуются приведенными ниже критериями до тех пор, пока выбор нс будет сделан:
1) Главное кольцо должно разделяться главным мостиком как можно более симметрично, см. рис. 6.2.32.
2) Длина первого (затем второго и т. д.) независимого вторичного мостика должна быть максимально возможной, см. рис. 6.2.33.
3) Число зависимых вторичных мостиков должно быть минимальным.
4) Надстрочные локанты вторичных мостиков должны быть как можно меньше при рассмотрении мостиков в убывающем порядке, причем выбор следует делать при первом различии, см. рис. 6.2.34.
5) Надстрочные локанты должны быть как можно меньше, при рассмотрении их в порядке перечисления в названии, см. рис. 6.2.35.
Нумерация мостиков
После проведения нумерации главного кольца и главного мостика (начиная с узлового атома с локантом «1») нумеруют все независимые, а затем зависимые вторичные мостики. Нумерацию продолжают от атома главного кольца или главного мостика с наивысшим номером. Все вторичные мостики нумеруют по очереди, начиная с независимого вторичного мостика, связанного с узловым атомом, имеющим наивысший номер, затем нумеруют независимый вторичный мостик, связанный с узловым атомом, имеющим следующий по величине номер, и т. д. (см. приведенные выше примеры). Если имеется выбор, то более низкие локанты приписываются атомам в мостике, связанном с узловыми атомами с наивысшими номерами, например см. рис. 6.2.36.
Если по-прежнему имеется выбор, то более длинные мостики нумеруются перед короткими, например см. рис. 6.2.37.
1,2-Диметилбицикло[1.1.0]бутан англ.-. 1,2-Dimethylbicyclo[1.1,0]butane
3,6,6-Триметилбицикло[3.2.2]нонан англ.-. 3.6.6-Trimethylbicyclo[3.2.2]nonane
Рис. 6.2.29
За
Трицикло[5.3.2.04,9]додекан англ.: Tricyclo[5.3.2.04,9]dodecane
Рис. 6.2.30
978
Новый справочник химика и технолога
умножающая приставка, обозначающая число
циклов
надстрочные индексы, указывающие положение
п-цикло[А.В
число атомов в большом сегменте главного
цикла --------
вторичного мостика
Еху...]алкан
u,v
мостике
число ат главном
число атомов в зависимом вторичном мостике
число атомов в независимом вторичном
число атомов в малом
сегменте главного цикла
Схема 6.3
1
Пентацикло[13.7.4.33’8.018’20.113’28]триаконтан
англ.'. Pentacyclo[13.7.4.338.0182°. 113'28]triacontane
Рис. 6.2.31
Т рицикло[4.3.1.12,5]ундекан, а не трицикло[5.2.1.12,6]ундекан, т.к. 4.3 более симметрично, чем 5.2
англ.: Tricyclo[4.3.1,12,5]undecane
Рис. 6.2.32
Тетрацикло[8.6.6.52’9.123,26]октакозан, а не тетрацикло[8.6.6.42,9.222’25]октакозан (8.6.6.5.1 > 8.6.6.4.2)
англ.: Tetracyclo[8.6.6.52,9.123’26]octacosane
Рис. 6.2.33
Современная номенклатура органических соединений
979
Тетрацикло[5.3.2.12'4.03,6]тридекан Тетрацикло[5.3.2.14'6.02,5]тридекан англ.'. tetracyclo[5.3.2.12'4.03'6]tridecane 14 6 > 124 (критерий (4))
не Тетрацикло[5.3.2.12,4.06‘13]тридекан
О6,13 - зависимый вторичный мостик (критерий (3))
Тетрацикло[5.5.2.22,6.18,12]гептадекан англ.: Т etracyclo[5.5.2.22’6.18’12]heptadecane
Тетрацикло[5.5.2.28’12.12’6]-гептадекан (2,6,8,12 < 8,12,2,6)
Рис. 6.2.35
Тетрацикло[6.3.3.22’6.13’6]гептадекан англ.: Tetracyclo[6.3.3.22,6.13’6] heptadecane
Рис. 6.2.36
Тетрацикло[5.5.2.22,6.18’12]нонадекан англ.'. Tetracyclo[7.4.3.23’7.13’7]nonadecane
Рис. 6.2.37
980
Новый справочник химика и технолога
Мостиковые гетероциклы
Мостиковые гетероциклы могут быть названы с помощью «а»-номенклатуры (подразд. 6.3.5). При этом если при преобразовании названия соответствующего карбоцикла в гетероцикл возможны варианты, последовательно руководствуются следующими критериями, пока не будет сделан выбор:
1. По возможности низший набор локантов приписывается гетероатомам, см. рис. 6.2.38.
2. По возможности низшие локанты приписываются гетероатомам в следующем порядке:
0>S>Se>Te>N>P>As>Sb>
> Bi > Si > Ge > Sn > Pb > В > Hg.
3. По возможности низшие локанты приписываются гетероатомам в нестандартном валентном состоянии, выражаемом с помощью Х-символов (см. подразд. 6.4) (при этом X6 получает меньший локант, чем X4, и т. п.).
4. По возможности низшие локанты приписываются радикальным центрам или, если система является заместителем, точке ее присоединения к основе, см. рис. 6.2.39.
5. По возможности низшие локанты приписываются катионным центрам.
6. По возможности низшие локанты приписываются главным группам, см. рис. 6.2.40.
При указании ненасыщенности и заместителей следуют обычным принципам заместительной номенклатуры.
Для некоторых мостиковых соединений правилами IUPAC разрешены тривиальные названия, см. рис. 6.2.41.
неправильно: 3,6,8 < 3,7,9
неверная нумерация соответствующего карбоцикла: 2,6 < 3,5
3,6,8-Триоксабицикло[3.2.2]нонан англ.-. 3,6,8-Trioxabicyclo[3.2.2]nonane
3-Азатрицикло[2.2.1.02,6]гептан англ.'. 3-Azatricyclo[2.2.1.02,6]heptane
Рис. 6.2.38
2,6-Диоксабицикло[3.2.1]октан-7-ил англ.: 2,6-Dioxabicyclo[3.2.1]octan-7-yl
Бицикло[3.2.1]октан-2-ил
англ.-. Bicyclo[3.2.1]octan-2-yl
Рис. 6.2.39
Бицикло[2.2.1 ]гепт-5-ен-2-он англ.-. Bicyclo[2.2.1]hept-5-en-2-one
Рис. 6.2.40
Современная номенклатура органических соединений
981
1
Адамантан англ.-. Adamantane
7 6
3 2
з
1
Призман англ:. Prismane
Кубан англ.-. Cubane
Рис. 6.2.41
6.2.5. Конденсированные углеводороды
6.2.5.1. Родоначальные названия
Существует ряд названий полициклических углеводородов с максимальным числом некумулированных двойных связей (табл. 6.9), использование которых рекомендуется правилами IUPAC. Названия соединений, имеющих более сложные скелеты, строятся на основе названий этих структур методом конденсирования.
Таблица 6. 9
Циклические углеводороды с максимальным числом некумулированых двойных связей
Пояснение. Соединения расположены в порядке уменьшения предпочтительности их выбора в качестве компонента названия конденсированной полициклической системы. Обычным шрифтом приведено название конкретной полициклической системы, применяемое также при ее использовании в качестве основного компонента в методе конденсирования. Курсивом выделен префикс, обозначающий данную циклическую систему при ее использовании в качестве присоединенного компонента.
1. Полифенилен (polyphenylene)а) (C6)m *C2w, (w > 9), см. 32 2. Полинафтилен (polynaphthylene) 6) (Сб)2* *С2ь см. 24 {k > 4)
3. Полиацен (polyacene) в) (С6)„, см. 38 (и > 10) 4. Полиафен (polyaphene)г) (C6)„, см. 30 или 34 {п > 10)
5. Полигелицен (polyhelicene) д,е) (С6)„, см. 31 {п > 9) 6. Нонафенилен (nonaphenylene)а) (С6)9*С18, см. 32 {т = 9) Нонафенилено {nonaphenyleno)
7. Декацен (decacene)в) (С6)10, см. 38 (w = 10) Декацено {decaceno) 8. Декафен (decaphene)г) (С6)ю, см. 30 {п= 10) Декафено {decapheno)
9. Овален (ovalene) (С6)ю Овалено {ovalend) 13 14 1 Jq I l| bl l°n H I I < Tn T li л 8 7 6 10. Декагелицен (decahelicene)fl,e) (С6)10, см. 31 {п = 10) Декагелицено {decaheliceno)
11. Октафенилен (octaphenylene)a) (C6)8*C16, cm. 32 {m = 8) Октафенилено {octaphenyleno) 12. Тетранафтилен (tetranaphthylene)б) (С6)8*С8, см. 24 {к = 4) Тетранафтилено {tetranaphthyleno)
13. Нонацен (nonacene)B) (C6)9, cm. 38 (« = 9) Нонацено {nonaceno) 14. Нонафен (nonaphene)г) (С6)9, см. 34 {п = 9) Нонафено {nonapheno)
982
Новый справочник химика и технолога
Продолжение табл. 6.9
15. Нонагелицен (nonahelicene)д’а) (С6)9, см. 31 (п = 9) Нонагелицено (nonaheliceno)
17. Октацен (octacene)в) (С6)8, см. 38 (п = 8) Октацено (octaceno)
19. Пирантрен (pyranthrene) (С6)8 Пирантрено (pyranthreno)
16. Гептафенилен (heptaphenylene)а) (С6)7*С14, см. 32 (т - 7) Гептафенилено (heptaphenyleno)
18. Октафен (octaphene)г) (С6)8, см. 30 (п = 8) Октафено (octapheno)
20. Октагелицен (octahelicene)a e) (С6)8, см. 31 (п = 8) Октагелицено (octaheliceno)
21. Гексафенилен (hexaphenylene)а) (С6)б*С12, см. 32 (т = 6) Гексафенилено (hexaphenyleno)
23. Гептафен (heptaphene)г) (С6)7,см 34 (п-7) Гептафено (heptapheno)
22. Гептацен (heptacene)в) (С6)7, см. 38 (п = 7) Гептацено (heptaceno) 24. Тринафтилен (trinaphthylene)б) (С6)б*С6 (три нафталиновых системы, следовательно, k = 3) Тринафтилено (trinaphthyleno)
25. Коронен (coronene) (С6)7 Коронено (согопепо)
26. Гептагелицен (heptahelicene)д’е) (С6)7,см 31 (п = 7) Гептагелицено (heptaheliceno)
27. Рубицен (rubicene) (С5)2*(С6)5
Рубицено (rubiceno)
28. Пентафенилен (pentaphenylene)а) (С6)5*Сю, см. 32 (т = 5) Пентафенилено (pentaphenyleno)
Современная номенклатура органических соединений
983
Продолжение табл. 6.9
29. Гексацен (hexacene)в) (С6)б, см. 38 (я = 6) Гексацено {hexaceno)
30. Гексафен (hexaphene)г) Гексафено (hexapheno) (С6)6 (шесть колец, следовательно, п = 6)
9 8 7 6 5 4
31. Гексагелицен (hexahelicene) д’е) Гексагелицено (hexaheliceno) (С6)б (шесть колец, следовательно, п = 6)
32. Тетрафенилен (tetraphenylene)а) Тетрафенилено (tetraphenyleno) (С6)4*С8 (четыре бензольных кольца, следовательно, т = 4)
33. Пентацен (pentacene) в)(С6)5 Пентацено (pentaceno)
34. Пентафен (pentaphene)г) (С6)5 Пентафено (pentapheno) (пять колец, следовательно, п- 5)
35. Перилен (perylene) (С6)5
Перилено (peryleno)
36. Пицен (picene) (С6)5
Пицено (piceno)
37. Плеяден (pleiadene) (С6)3*С7
Плеядено (pleiadeno)
39. Тетрафен (tetraphene)г) (С6)4 Тетрафено (tetrapheno)
38. Тетрацен (tetracene)в,ж) (С6)4 Тетрацено (tetraceno) (четыре кольца, следовательно, п = 4)
10 11 12 1
40. Хризен (chrysene) (С6)4 Хризено (chryseno)
12 1
7 6
984
Новый справочник химика и технолога
Продолжение табл. 6.9
41. Пирен (pyrene) (С6)4 Пирено (ругепо) 10 1 ОТ’ 6 5 42. Трифенилен (triphenylene)а) (С6)4 Трифенилено (triphenyleno) 2 1|^13 "Ola 9 Т й 7
43. Ацеантрилен (aceanthrylene) Ацеантрилено (aceanthryleno) С5*(С6)з 1 2 10 1 1 э/^ОТ^ОТ/от з ECQ 7 6 5 44. Ацефенангрилен (acephenanthrylene) С5*(С6)3 А цефенантрилено (acephenanthryleno) 2 ю | II 9х^г\/'от/'ч\ 4 8от/от/ 5 7 6
45. Флуорантен (fluoranthene)3) Сз*(С6)з Флуорантена (fluorantheno) 2 w iPf ШТ 7 6 46. Антрацен (anthracene)е) (С6)з Антра (anthra) 8 о 9 г. 1 |р ®ь|
47. Фенантрен (phenanthrene)е) (С6)3 Фенантро (phenanthro) 9 10 8 &a/k 1 л\10а 1 7^1 J у-£-У. П 3^2 g i/4b 4^ с у 6 5 4 3 48. Фенален (phenalene) (С6)3 Феналено (phenalend) (показан 1/7-изомер) 2 1ОО3 9z??OT/OT4 См 7 6
49. Флуорен (fluorene) С5*(С6)2 Флуорена (fluorend) (показан 9/7-изомер) 9 7/~у_#Л2 50. Аценафтилен (acenaphthylene) С5*(С6)2 Аценафтилена (acenaphthylend) 1 2 sCO 7ОТ/'от/4 6 5
51. Бифенилен (biphenylene) и) С4*(С6)2 Бифенилено (biphenyleno) 8 1 'ОпО2 6 От/—ОТ/3 5 4 52. сгш-Индацен (s-indacene)и) (С5)2*С6 сим-Индацено (s-indaceno) Zl jZ /2
53. асим-Индацен (as-indacene)и) (С5)2*С6 асим-Индацено (as-indaceno) 1 2 7х I I xs^^OT/4 8 5 54. Полиален (polyalene) (С„)2 (п > 6), показан гептален, п = 7 Гепталено (heptaleno) 8 / jT 23 7^65 4
Современная номенклатура органических соединений
985
Окончание табл.6. 9
55. Азулен (azulene) С5*С7 Азулено (azuleno) 6\ I/2 ° 4 56. Нафталин (naphthalene) (С6)2 Нафто (naphtho) 8 1 7ПП2 5^ 4
57. Инден (indene) С5*С6 Индено (indeno) (показан 1//-изомер) ? 1 />2 4 3 58. Пентален (pentalene) (С5)2 Пенталено (pentaleno) 6 1 б/ jT /2 4^3
59. Полиален (polyalene) (Ср)2, см. 58 (р = 3 или 4) 60. [/?]Аннулен ([/?]annulene)к) Ср(р>6)
61. Бензол (benzene) С6 Бензо (benzo) 6Q 5\^3 4 62. [/?]Аннулен ((/?]annulene)л) Ср(р<6)
а) Полициклическая система [(C6)m*C2m], состоящая из монокарбоцикла с четным числом атомов углерода, к связям которой (через одну) ор/ио-конденсированы бензольные кольца. Название такой системы образуется из умножающей приставки, соответствующей числу бензольных колец, и окончания «фенилен». Пример — см. соединение № 32.
б) Полициклическая система Г(С6)2л*С2а], состоящая из монокарбоцикла с четным числом атомов углерода, к связям которой (через одну) o/wo-конденсированы по связи 2-3 нафталиновые системы. Название такого соединения образуется из умножающей приставки, соответствующей числу нафталиновых систем, и окончания «нафтилен». Пример — см. соединение № 24.
в> Полициклическая система [(С6)„], состоящая из линейно о/?то-конденсированных бензольных колец, название которой образуется из умножающей приставки, соответствующей числу колец, и окончания «ацен». Пример — см. соединение № 38.
^Полициклическая система [(C6)„J. построенная из п ор/ио-конденсированных бензольных колец (п > 3) в виде двух линейных фрагментов, состоящих из (и + 1 )/2 и (и + 1 )/2 (если п нечетное) или п/2 и (и/2) + 1 (если п четное) колец, соединенных через одно общее бензольное кольцо под углом 120°. Название такой системы образуется из умножающей приставки, соответствующей числу колец, и окончания «афен». Пример — см. соединения № 30, 34.
д) Полициклическая система [(С6)„], состоящая из шести или более бензольных колец, скелет которой формально образуется путем последовательного конденсирования бензольных колец в 3,4-положение фенантрена. Название такой системы образуется из умножающей приставки, соответствующей числу колец, и окончания «гелицен». Пример — см. соединение №31.
с) Нестандартная нумерация.
ж) Старое название нафтацен (naphthacene) до сих пор используется в Chemical Abstracts и Beilstein.
з) Между флуорантеном и антраценом Chemical Abstracts и Beilstein включают тринден (trindene) — циклопента[е]-асм.м-индацен.
и) В ранних версиях правил IUPAC индацен был старше бифенилена.
к) Это название может быть использовано только для основного компонента, а для наименования присоединенного компонента используется соответствующий префикс «циклоалка».
л) Нельзя использовать для наименования моноциклов. Только название [5]аннулен может быть использовано в качестве названия основного компонента, а для наименования присоединенного компонента используется соответствующий префикс «циклоалка».
6.2.5.2. Метод конденсирования
Конденсированные системы как карбоциклические, так и гетероциклические принято подразделять на ор-шо-конденсированные и орто-нерм-конденсированные. Два кольца называют орто-конденсированными, если
они имеют только два общих атома и одну общую
связь, например:
986
Новый справочник химика и технолога
Если один цикл в полициклическом соединении ор-тио-конденсирован за счет своих соседних связей с двумя другими циклами, которые в свою очередь орто-конденсированы друг с другом, то этот цикл называют орто-лери-конденсированным по отношению к двум другим, например:
При наименовании конденсированной полициклической системы ее формально разделяют на составные части и общее название формируют из названий полученных фрагментов, например см. рис. 6.2.42.
Компоненты, на которые может быть разделена конденсированная полициклическая система для правильного построения названия, представлены в табл. 6.9, где они расположены в порядке уменьшения предпочтительности их выбора в качестве компонента. Самый старший из возможных компонентов называется основным (родоначальным) и его название приводится самым последним в названии всей конденсированной системы. Остальные компоненты называются присоединенными и приводятся в названии в виде префиксов к основному. Префиксы, соответствующие компонентам, прямо связанным с основным, называются префиксами первого порядка, остальные называются префиксами второго, третьего и т. д. порядков, в зависимости от того, соответствуют ли они компонентам второго, третьего и т. д. порядков (при определении порядка компоненты рассматриваются последовательно, начиная от основного).
Согласно рекомендациям IUPAC 1993, 1998 гг., мо-ноциклические углеводородные основные компоненты конденсированных систем (кроме бензола) называются [п]аннуленами, где п — число звеньев в цикле. (Ранее, а в Chemical Abstracts и Beilstien и сейчас, в таких случаях использовалось название соответствующего циклоалкана с окончанием «ен».) Префиксы, соответствующие присоединенным моноциклическим углеводородным компонентам (кроме «бензо»), образуются из названия соответствующего циклоалкана с окончанием «а», см. рис. 6.2.43.
При составлении названия конденсированной полициклической системы рекомендуется придерживаться следующей последовательности действий:
1. Систему разъединяют на отдельные моно- и/или полициклические компоненты и выбирают самый старший компонент из табл. 6.9 в качестве основного. Например, в рассматриваемом ниже соединении в качестве основного компонента следует выбрать пентафен (а не перилен), а в качестве присоединенного компонента — бензол, см. рис. 6.2.44.
В сложных случаях, если возможно несколько мест локализации основного компонента, последовательно руководствуясь приведенными ниже критериями, положение основного компонента выбирают так, чтобы:
а) вся система могла быть названа с помощью метода конденсирования, а не другим способом, см. рис. 6.2.45;
б) вся система могла быть названа без использования присоединенных компонентов высоких порядков, см. рис. 6.2.46;
в) вся система могла быть названа с использованием максимального числа присоединенных компонентов первого порядка (второго и т. д.), см. рис. 6.2.47;
1 Н-Бензо[сУе]антрацен англ.: 1 H-Benzo[cte]anthracene
Антрацен Бензол
англ.: Anthracene англ.: Benzene
Рис. 6.2.42
1 Н-Циклопента[8]аннулен Бензо[22]аннулен
англ.: 1H-Cyclopenta[8]annulene англ.: Benzo[22]annulene
Camical Abstracts или Belstein: Benzocyclodocosene
Рис. 6.2.43
Современная номенклатура органических соединений
987
Рис. 6.2.44
Правильно
Пенталено[2,1,6-сс/е]циклопента[/)]азулен англ:. Cyclopenta[/j]pentaleno[2,1,6-ccfe]azulene
Неправильно
1,9-Метенопенталено[1,6-е/]азулен использование номенклатуры мостиковых соединений
Рис. 6.2.45
Индено[2,1-/]нафто[2,3-а]циклопента[/7]азулен
Неправильно-. бензоГа]бензо[5.61инденоГ2.1-#циклопента[Ъ]азулен или 6eH3of5,6lindenof1,2-е]индено[2,1-/?]азулен
англ:. Cyclopenta[/7]indeno[2,1-/]naphtho[2,3-a]azulene
Рис. 6.2.46
988
Новый справочник химика и технолога
Дибензо[с,д]фенантрен
Неправильно-. нафто[2,1 -с]фенантрен
(2 присоединенных компонента предпочтительнее, чем 1) англ.-. Dibenzo[c,g]phenanthrene
Рис. 6.2.47
г) чтобы вся система могла быть названа с использованием максимального числа идентичных присоединенных компонентов с умножающими приставками:
Динафто[1,2-с:2',Г-т]пицен
Неправильно-. бензо[с]фенантро[2,1-т]пицен англ.-. Dinaphthon^-c^'J'-mJpicene
Дополнительные критерии см. [9].
2. Если после выбора основного компонента остаются неопределенными два или более присоединенных компонента или имеется несколько вариантов их локализации, последовательно руководствуются следующими критериями, пока не будет сделан выбор:
а) положение присоединенного компонента выбирают так, чтобы набор локантов, показывающих порядок присоединения к основному компоненту, был минимальным;
б) положение присоединенного компонента выбирают так, чтобы локанты, показывающие порядок присоединения к основному компоненту, были минимальными в порядке их перечисления в названии;
в) при необходимости критерии (а, б) могут быть применены для выбора присоединенных компонентов второго порядка и т. д.
3. Руководствуясь табл. 6.9, формируют название конденсированной системы, добавляя к названию основного компонента префиксы присоединенных компонентов. Префиксы компонентов второго порядка помещаются перед префиксами компонентов первого порядка, к которым они присоединены, и т. д. до компонентов самого высокого порядка. Если имеется несколько разных компонентов, присоединенных к компоненту более низкого порядка, то они приводятся в алфавитном порядке. Два или более идентичных компонента, присоединенных к третьему компоненту, приводятся с использованием умножающих приставок «ди», «три» и т. д., или «бис», «трис» и т. д. Умножающие приставки не учитываются при определении алфавитного порядка для компонентов, находящихся на одном и том же уровне. Наконец, префиксы всех компонентов и/или групп, соединенных между собой
компонентов, которые «приконденсированы» к основному, помещаются в алфавитном порядке перед названием основного компонента.
Связи, по которым соединены в молекуле основной и присоединенные компоненты, указываются с помощью цифровых и буквенных локантов. Для определения локантов атомы циклической системы присоединенных компонентов нумеруются, как показано в табл. 6.9. Связи основного компонента последовательно обозначают курсивными латинскими буквами а, Ь, с и т. д., начиная со связи 1-2 согласно нумерации этого компонента (см., например, соединение № 9 в табл. 6.9). В случае нестандартной нумерации полициклической системы связи обозначаются буквами последовательно по периметру, начиная со связи 1-2 (см., например, соединение № 46 в табл. 6.9). Если в компоненте более 26 периферийных связей, дополнительно используются Ъ\ и т. д. <я2, ^2 и т. д. Буквенные локанты используются для обозначения связей основного компонента, по которым происходит «конденсирование». Соответствующие связи присоединенных компонентов обозначаются парой цифровых локантов, при этом локанты компонентов второго порядка отмечаются штрихами, третьего — двойными штрихами и т. д. В названии локанты записываются в квадратных скобках между названием основного компонента и префиксами (цифровые и буквенные локанты разделяются дефисом, например, [ 1,2-а], [3,2,1 -de\) или между префиксами соответствующих присоединенных компонентов (цифровые локанты присоединенных компонентов разного порядка разделяются двоеточием, например, [4',5':5,6], [Г,2":Г,2']). При этом номера атомов присоединенного компонента первого порядка приводятся в последовательности, которая по направлению соответствует увеличению номеров атомов в основном компоненте, а номера атомов присоединенного компонента второго порядка приводятся в последовательности, которая по направлению соответствует увеличению номеров атомов в компоненте первого порядка, и т. д.
Если возможны несколько вариантов цифровых и буквенных локантов, то последовательно руководствуясь следующими критериями, выбирают:
а) наименьший набор буквенных локантов основного компонента (например: «a,h» предпочтительнее, чем «/>,/»);
Современная номенклатура органических соединений
989
б) наименьшие буквенные локанты основного компонента в порядке их перечисления в названии (например: с...е предпочтительнее, чем е...с);
в) наименьший набор локантов присоединенных компонентов первого порядка, относящихся к «конденсации» с основным компонентом (например: «1,7-я» предпочтительнее, чем «3,4-а»);
г) наименьшие локанты присоединенных компонентов первого порядка, относящихся к «конденсации» с основным компонентом, в порядке перечисления в названии;
д) наименьший набор локантов присоединенных компонентов более низкого порядка, относящихся к «конденсации» с присоединенными компонентами более высокого порядка;
е) наименьшие локанты присоединенных компонентов более низкого порядка, относящихся к «конденсации» с присоединенными компонентами более высокого порядка, в порядке перечисления в названии;
ж) наименьший набор локантов присоединенных компонентов более высокого порядка, относящихся к «конденсации» с присоединенными компонентами более низкого порядка;
з) наименьшие локанты присоединенных компонентов более высокого порядка, относящихся к «конденсации» с присоединенными компонентами более низкого порядка, в порядке перечисления в названии.
В качестве примера составим название следующего соединения, см. рис. 6.2.48.
1Н-Дициклобута[5,,6,:7,,8,]циклоокта[Г,2,:6,7]нафто[2,3-д]циклопропа[а]азулен англл IH-CyclopropatajdicyclobutatS'.e'^'.S'Jcyclooctatr^'^JJnaphtho^.S-glazulene
Рис. 6.2.48
Основной компонент, азулен (соединение № 55 из табл. 6.9), сочленен с циклопропеном и нафталином, причем последний является компонентом первого порядка в группе присоединенных компонентов. Буквенная нумерация азулена может быть проведена двумя способами: при первом «конденсация» с циклопропеном происходит по стороне а, с нафталином — по стороне g, а при втором — соответственно по сторонам b и f (если эквивалентную нумерацию связей азулена проводить в противоположном направлении по сравнению с показанной на схеме). В соответствии с вышеприведенными правилами выбора локантов (пункт «а») следует использовать первый вариант, т. к. набор локантов ag предпочтительней, чем bf. Место сочленения азулена с нафталином должно быть указано локантами [2,3-g]. Нафталиновый фрагмент нумеруем, как показано на схеме, при этом направлению увеличения буквенных (азуленовых) локантов соответствует порядок 2,3 цифровых (нафталиновых) локантов, поэтому пишем 2,3, а не 3,2. Нумерацию нафталина в противоположном направлении, которая привела бы к локантам [3,2-g] (в этом случае направлению увеличения буквенных локантов азулена соответствовал бы порядок 3,2 цифровых локантов), следует отвергнуть, поскольку набор локантов 2,3 < 3,2. Место сочленения нафталина с 8-звенным циклом указывается с помощью группы локантов [l',2':6,7J, причем локанты 8-звенного цикла также следует приводить (согласно рекомендациям
IUPAC 1998 г.), т. к. он сочленен с другими кольцами. Место сочленения 8-звенного цикла с двумя 4-звенными, префикс которых приводится с умножающей приставкой «ди», указывается локантами [5',6':7',8'], при этом локанты 4-звенных циклов не указываются, т. к. они являются терминальными (см. ниже). Далее префиксы в группе присоединенных компонентов расставляются в порядке понижения уровня (на одном уровне — по алфавиту без учета умножающих приставок): дицикло-бута-циклоокта-нафто (dicyclobuta-cycloocta-naphtho). Наконец в полном названии по алфавиту расставляются префиксы компонентов и групп компонентов, присоединенных к основному: дициклобута-циклоокта-нафто-циклопропа-гаулен. (cvc/oprqpa-dicyclobuta-cycloocta-naphtho-azulene); в данном случае умножающая приставка учитывается и в результате порядок перечисления префиксов в русском и английском названиях различный. Вставив локанты, показывающие порядок сочленения колец и положение «обозначенного водорода» («1//-»), получаем полное название соединения, представленное на схеме.
Если не возникает неопределенность, то цифровые и/или буквенные локанты могут быть опущены в названиях систем с присоединенными компонентами только первого порядка и системах с терминальными присоединенными компонентами, например см. рис. 6.2.49.
В opwo-wepw-конденсированных системах цифровые локанты присоединенного компонента опускаются для атомов, которые в этом компоненте имеют буквенно-
990
Новый справочник химика и технолога
цифровой локант (см. пример 6.2.45 в и. 1а: циклопен-та[/у]пенталено[2,1,6-сг/е]азулен, а не циклопента[//]пен-талено[2,1,6а,6-сг/е]азулен).
4. Нумерация атомов в конденсированных системах проводится независимо от вышеперечисленных действий. Для нумерации полициклической системы се прежде всего определенным образом ориентируют. Кольца располагают так, чтобы последовательно выполнялись следующие условия:
а) как можно больше opwo-конденсированных циклов с вертикальными общими связями оказалось в горизонтальном ряду, см. рис. 6.2.50;
б) как можно больше циклов оказалось в правом верхнем квадранте, см. рис. 6.2.51;
в) при наличии выбора в нижнем левом квадранте должно быть минимально возможное количество циклов, см. рис. 6.2.52;
г) максимальное число колец должно располагаться выше горизонтального ряда, см. рис. 6.2.53.
Нумерацию правильно ориентированной системы начинают с самого правого кольца, находящегося в самом верхнем ряду. В качестве начала нумерации в этом кольце выбирают атом, самый удаленный в направлении против часовой стрелки и не участвующий в образовании конденсирующих связей. Если по-прежнему существует выбор, начинают с самого верхнего атома. Если выбранное кольцо не имеет неконденсированных атомов, тогда начало нумерации выбирают в следующем по часовой стрелке кольце системы. Нумерацию ведут по периметру молекулы по часовой стрелке. Узловые атомы углерода (в отличие от узловых гетероатомов, см. подразд. 6.3.3.1) не включают в нумерацию; они получают номер предыдущего атома с добавлением буквы латинского алфавита: а, Ь, с и т. д. (рис. 6.2.54).
Если по-прежнему нумерация неоднозначна, то выбор ограничивают, последовательно руководствуясь следующими критериями:
а) наименьшие номера должны получить узловые атомы;
б) наименьшие номера должны получить атомы с «обозначенным водородом».
Внутренние атомы нумеруются в последнюю очередь. Согласно рекомендациям IUPAC (1998 г.), нумерация проводится по кратчайшему пути (минимальное число связей), начиная с узлового атома (при наличии вариантов с узлового атома с наименьшим локантом). Внутреннему атому приписывается цифровой локант соответствующего узлового атома с надстрочным индексом, равным числу связей от узлового атома до внутреннего. Прежние правила IUPAC рекомендовали проводить нумерацию по кратчайшему пути, начиная с узлового атома с наибольшим номером, к цифровому локанту которого добавляют соответствующие буквы. Эта система по-прежнему используется в Chemical Abstracts и Beilstein (рис. 6.2.55).
В тех случаях, когда в названии необходимо отразить различие между изомерами, которые отличаются только локализацией двойных связей, это можно сделать, используя для указания локализации греческую букву «А» с надстрочным(и) локантом(ами), показывающим^) положение двойной связи у атома с низшим номером (рис. 6.2.56).
В тех случаях, когда название может соответствовать нескольким изомерным системам с максимальным числом некумулированных двойных связей, но может стать специфичным при указании положения одного или нескольких атомов водорода, определенный изомер называют добавляя к обычному названию соответствующий локант и букву II («обозначенный водород»). В ряде случаев, в частности для устоявшихся названий и при отсутствии неопределенности «обозначенный водород» может быть опущен. Например, флуорен = = 9/7-флуорен, инден = 1//-инден, фенален = 1//-фена-лен.
5Н-Бензо[7]аннулен англ.: 5//-benzo[7]annulene
Циклогепта[ссУ]-С1//и-индацен .: Cycloheptafccfl-s-indacene
Рис. 6.2.49
предпочтительнее, чем
Рис. 6.2.50
Современная номенклатура органических соединений
991
только 2 кольца в горизонтальном ряду орто-кондесированы
1+0.5+0.5 = 2 предпочтительнее, чем 0.5+0.5= 1
3+0.5 = 3.5 предпочтительнее, чем 2+0.5+0.5=3
Рис. 6.2.51
Рис. 6.2.52
1+1+0.5+0.5+0.5 = 3.5 предпочтительнее, чем 1 + 0.5+0.5+0.5 = 2.5
Циклопропа[с/е]антрацен англ.-. Cyclopropa[cfe]anthracene
5Н-Индено[1,2,3-/7/]циклодека[с/е]гексацен англ.-. 5H-Cyclodeca[cte]indeno[1,2,3-/?/]hexacene 6-звенный цикл индена находится во 2-м ряду, а 10-звенный - в 1-м
1НЪензо[6\73циклоокта[Г,2\4,5]бензо[1,2,3-с/е]тетрацен англ.: 1 H-Benzo[6', 7’]су cloocta [ 1' ,2' :4,5]benzo[ 1,2,3-cte]tetracene
Нумерацию не начинают с атома 15
Рис. 6.2.54
992
Новый справочник химика и технолога
новая система нумерации
внутренних атомов
старая система нумерации
внутренних атомов
Коронен англ.-. Coronene
Пирен англ.-. Pyrene
Рис. 6.2.55
1,6-Диметил-Д1 -гептален
англ.-. 1,6-Dimethyl-A1-heptalene
1,6-Диметил-Д1 (10а)-гептален англ.'. 1, 6-Dimethyl-A1 Oa>-heptalene
Рис. 6.2.56
Названия конденсированных систем с числом неку-мулированых двойных связей меньше максимального образуются добавлением префиксов «дигидро», «тетрагидро», и т. д. с соответствующими локантами (или добавлением префикса «пергидро» в случае предельных молекул) к названиям негидрированных соедине
ний. Для ряда частично гидрированных соединений ранними версиями правил IUPAC было разрешено использование тривиальных названий (табл. 6.10). Из этих соединений в рекомендациях 1998 г. оставлен только индан.
Таблица 6.10
Тривиальные названия частично гидрированных полициклических углеводородов
Современная номенклатура органических соединений
993
6.2.6. Мостиковые конденсированные системы
Соединения, одновременно содержащие конденсированные фрагменты и мостики, можно называть, добавляя к названию конденсированного соединения название соответствующего мостика с локантами, показывающими его положение. В конденсированной системе максимальное число некумулированых двойных связей размещается так, чтобы оставалась возможность образования связи с мостиком. Последовательно руководствуясь приведенными ниже критериями, мостик выбирают таким образом, чтобы остающаяся после выделения мостика конденсированная система:
а) содержала максимально возможное число колец;
б) содержала максимально возможное число скелетных атомов;
в) была наиболее предпочтительной согласно табл. 6.9;
г) позволяла использовать минимальное число сложных мостиков;
д) позволяла использовать минимальное число зависимых мостиков (см. подразд. 6.2.4.2);
е) позволяла использовать минимальное число атомов в зависимых мостиках;
ж) позволяла использовать минимальное число поливалентных мостиков («диил» предпочтительнее «илилиден», «триил», «диилиден» и т. д.)
з) обеспечивала положение мостиков, приводящее к наименьшим локантам присоединения сначала у независимых, а затем зависимых мостиков.
и) позволяла использовать низшие локанты для главных групп;
к) включала максимальное число некумулирован-ных двойных связей.
Названия мостиков в полном названии молекулы приводятся в виде префиксов. Префиксы ациклических
двухвалентных углеводородных мостиков образуются из названия соответствующего углеводорода путем добавления окончания «о». Для непредельных мостиков локант двойной связи указывается в квадратных скобках перед окончанием «ено». Например:
«метано» -СН2-, «этано» -СН2СН2-,
«пропано» -СН2СН2СН2-,
«этено» -СН=СН-
«проп[1]ено» -СН=СНСН2~,
«бут[ 1 ]сно» -СН=СНСН2СН2-, «бут[2]ено» -СН2СН=СНСН2-«бута[ 1,3]диено» СНСНСЛСН.
Названия мостиков, образованных моноцикличе-скими углеводородами (кроме бензола) формируют, добавляя приставку «эпи» («epi-») к префиксу, используемому в методе конденсирования для соответствующего моноцикла. Предполагается, что мостик имеет максимально возможное число некумулированых двойных связей. Положение свободных валентностей указывается в квадратных скобках прямо перед названием мостика (рис. 6.2.57).
Названия мостиков, образованных другими циклическими углеводородами, получают, добавляя окончание «о» к названию углеводорода из табл. 6.9. Если такое название совпадает с соответствующим префиксом, используемым в методе конденсирования, то к нему добавляют приставку «эпи» (рис. 6.2.58).
Одноатомные поливалентные мостики называют с помощью соответствующего префикса: метено -СН=, метантриил -СН<, метандиилилиден >С=, метантет-раил >С<
эпициклопропа [1,2]эпициклопента [1,5]эпициклоокта
англ.-, epicyclopropa англ.-. [1,2]epicyclopenta англ.-. [1,5]epicycloocta
[1,3]эпиндено
англ.-. [1,3]epindeno
Рис. 6.2.57
[1,3]бензоло [2,3]нафталино
англ.-. [1,3]benzeno англ.-. [2,3]naphthaleno
Рис. 6.2.58
Многоатомные поливалентные мостики называют как соответствующие поливалентные группы (см. табл. 6.5). Если необходимо, положение свободной валентности
указывают локантом прямо перед соответствующим окончанием. Использование окончания «илиден» ограничено случаями, где имеется двойная связь между
994
Новый справочник химика и технолога
мостиком и конденсированной системой. При наличии выбора низшие локанты присваиваются последовательно: «ил», «илиден», двойной связи. Например,
этанилилиден: -СН2СН=;
этан[ 1,1,2]триил: -СН2СН<;
этандиилиден: =СНСН=;
этан[1,1]диил[2]илиден: =СНСН<;
этан[1,1,2,2]тетраил: >СНСН<;
этен[ 1,1,2]триил: -СН=С<;
пропан[1,2,3]триил: -СН2СН(-)СН2-;
пропан[1]ил[3]илиден: -СН2СН2СН= и т. д.
Префиксы сложных мостиков описывают группу атомов, которая может представлять собой только последовательность простых смежных мостиков. Их называют, последовательно располагая префиксы соответствующих простых мостиков, начиная с простого терминального мостика, выбор которого осуществляют последовательно руководствуясь следующими критериями:
а) содержит «старшую» циклическую систему (см. табл. 6.9);
б) содержит более длинную ациклическую цепь;
в) первый по алфавиту, например, «-(-СбНдСН?-) ([ 1,4]бензолометано).
Если в системе имеется несколько независимых мостиков, в названии они перечисляются по алфавиту. Зависимые мостики помещаются перед всеми независимыми. Конденсированную систему нумеруют обыч
ным образом, и положение мостика указывается с помощью локантов, которые в случае симметричных мостиков перечисляются в порядке увеличения, а несимметричных — в порядке, подразумеваемом префиксом мостика. Далее выбор локантов, указывающих положение мостиков, осуществляют, последовательно руководствуясь следующими критериями:
а) наименьший набор локантов для всех мостиков, например см. рис. 6.2.59;
б) наименьшие локанты в порядке их перечисления в названии, например см. рис. 6.2.60.
Одинаковые мостики в названии указываются соответствующими префиксами с умножающими приставками «ди», «три» и т. д. или, если в случае сложных мостиков может возникнуть неопределенность, приставками «бис», «трис» и т. д. Локанты для идентичных мостиков разделяют двоеточием (рис. 6.2.61).
Атомы мостика нумеруются последовательно, продолжая нумерацию конденсированной системы. Нумерацию ведут от атома мостика, присоединенного к узловому атому с высшим локантом. В случае сложных мостиков каждый компонент полностью нумеруется прежде, чем переходят к следующему компоненту. Если при этом возможны варианты, то нумерацию мостика проводят таким образом, чтобы (последовательно): а) низшие локанты получили гетероатомы; б) низшие локанты получили узловые атомы в мостике. Остальные атомы мостика нумеруются непрерывно, например см. рис. 6.2.62 (см. также примеры выше).
9,10-Метано-5, 8-пропано-1,3-этаноантрацен англ:. 1,3-Ethano-9,10-methano-5, 8-propanoanthracene
набор 1,3,5,8,9,10 меньше, чем 1,4,5,7,9,10
Рис. 6.2.59
1,4-Метано-5,8-этаноантрацен англ:. 1,4-Ethano-5,8-methanoanthracene
Рис. 6.2.60
1,4:5,8-Диметанонафталин англ:. 1,4:5,8-Dimethanonaphthalene
6 5
5,12:6,11 -Ди[1,2]бензолодибензо[а, е][8]аннулен англ:. 5,12:6,11-Di[1,2]benzenodibenzo[a,e][8]annulene
Рис. 6.2.61
Современная номенклатура органических соединений
995
20
21 19
18
22
16
15
6
6,13-(Метано[1,2]бензолометано)пентацен англ.: 6,13-(Methano[1,2]benzenomethano)pentacene
Рис. 6.2.62
При наличии нескольких мостиков сначала нумеруются: а) независимые, а затем зависимые мостики; б) из мостиков одного порядка — мостик, присоединенный к узловому атому с высшим локантом; в) из мостиков, присоединенных к одному и тому же узловому атому, — первый по алфавиту.
6.2.7. Фуллерены
Фуллерены — это соединения, состоящие исключительно из атомов углерода, соединенных в конденсированную поликарбоциклическую систему каркасного типа, состоящую из 12 пятизвенных циклов и нескольких шестизвенных. Фуллеранами называют полностью гидрированные фуллерены: С60Н60, С70Н70. Гетерофуллерены, норфуллерены, гомофуллерены, а также секофуллерены называют фуллероидами. В настоящее время IUPAC предложены правила номенклатуры только для фуллеренов Сео и С70.
По систематической номенклатуре фуллерен С6о рекомендуется называть (С60-/ь)[5,6]фуллерен, а С7о — (С7о-Г>5Ь(б))[5,6]фуллерен. В круглых скобках указывается содержание атомов углерода и символ точечной группы для рассматриваемой молекулы, а цифры в квадратных скобках означают размеры циклов в фуллерене. Во втором соединении обозначение «6» в символе точечной группы поясняет, что пятизвенный цикл, расположенный вокруг оси симметрии пятого порядка, окружен шестизвенными циклами. Такая запись позволяет отличить это соединение от изомерного (С70-£)5Ь(5))[5,6]фуллерена, который содержит пятизвенные циклы вокруг пятизвенного кольца с осью симметрии пятого порядка. Для (С60-/ь)[5,6]фуллерена и (С7о-£>5Н(б))[5,6]фуллерена в литературе, кроме того, встречаются устаревшие неполные названия: [60-/ь]фуллерен и [70-7)5}1]фуллерен, которые в настоящее время рассматриваются как тривиальные.
6.2.7. /. Нумерация атомов в фуллеренах
Атомы в (Сбо-/ь)[5,6]фуллерене и (С70-Аь(6))[5,6]фулле-рене по систематической номенклатуре нумеруют руководствуясь правилами:
Правило 1.
Одна из осей симметрии (Сп) выбирается в качестве реперной, причем выбор производят, начиная с осей более высокого порядка. Для этой оси должен существовать по крайней мере один последовательный спира
левидный спуск, начинающийся либо в кольце, через центр которого эта ось проходит, либо на конце связи, которую она делит пополам, либо на атоме, через который она проходит. Нумерация начинается на конце этого спуска.
Правило 2.
а) если есть выбор между осями одного и того же порядка, то предпочтение отдается той, которая проходит через кольцо, затем той, которая — через связь, а затем той, которая — через атом;
б) если есть выбор между кольцами, то предпочтительней кольцо большего размера, т. е шестизвенное;
в) если есть выбор между связями, то предпочтительней та, которая лежит на сочленении больших по размеру колец: 6:6 > 6:5 > 5:5;
г) если есть выбор между атомами, то предпочтительней тот, который является общим для больших по размеру колец: 6:6:6 > 6:6:5 > 6:5:5 > 5:5:5.
Правило 3.
В тех случаях, где остается выбор спиралевидного спуска для нумерации, предпочтительным спуском является тот, который ближе (по числу связей) к оси спирали.
На схемах 6.4 и 6.5 представлены систематические нумерации атомов в (С60-/ь)[5,6]фуллерене и (С70-Г>5Ь(б))[5,6]фуллерене (двойные связи в структурах опущены).
В тривиальных названиях этих соединений: [60-/ь.]фуллерен и [70-£>5ь]фуллерен применяется другой порядок нумерации, который представлен на схемах 6.6 и 6.7. Он основан на принципе «начало нумерации на более активной связи».
Далее рассматривается исключительно систематическая номенклатура производных фуллеренов.
Выбор начала нумерации в производных (С60-/ь)[5,6]-и (С70-Г>5Ь(б))[5,6]фуллеренов из-за высокой симметрии часто представляет собой довольно непростую задачу. В соответствии с приведенными выше правилами нумерацию в (С60-/ь)[5,6]фуллерене можно начинать с любого атома одного из двенадцати пятизвенных циклов и вести по выбранному циклу и далее по спирали в любом направлении (направления по часовой стрелке и против часовой стрелки в данном случае равнозначны). Соответственно в его производных выбор атома пятизвенного цикла с локантом «1» и направления нумерации определяется принципом наименьшего набора
996
Новый справочник химика и технолога
локантов. В (С70-/)5Ь(б))[5,6]-фуллерене нумерация может начинаться только из четырех положений одного из пяти шестизвенных циклов, расположенных перпендикулярно оси С2, как показано на схеме (возможное начало нумерации обозначено точками) и может осуществляться только в одном направлении из каждого положения (в противоположную сторону от соседнего обозначенного точкой центра):
Наименьший набор локантов в производных (С70-/)5Ь(б))[5,6]фуллерена определяет, с какого из отмеченных на схеме атомов начнется нумерация.
6.2.7.2. Структурно-модифицированные фуллерены
Для наименования соединений с измененным углеродным скелетом для фуллеренов, также как и для природных соединений, используют модифицирующие префиксы (см. такжеподразд. 6.16.4.6 и 6.16.5.2.): «гомо», «нор» и «секо». Использование этих префиксов для фуллеренов имеет некоторые особенности.
Трехмерное изображение
Схема 6.4. Нумерация атомов в систематическом названиии (С60-4)[5,6]фуллерена в трехмерном изображении и проекции Шлегеля
Схема 6.5. Нумерация атомов в систематическом названии (С70-£)5Ь(б))[5,6]фуллерена в трехмерном изображении и проекции Шлегеля
Современная номенклатура органических соединений
997
Трехмерное изображение
Схема 6.6. Нумерация атомов в тривиальном названиии (С60-/ь)[5,6]фуллерена в трехмерном изображении и проекции Шлегеля
Схема 6.7. Нумерация атомов в тривиальном названии (С70-£)5Ь(б))[5,6]фуллерена в трехмерном изображении и проекции Шлегеля
6.2.7.3. Гомофуллерены
Добавление неотделяемого префикса «гомо» перед родоначальным названием означает внедрение в одну из связей фуллерена группы СН2 с сохранением прежней нумерации молекулы. Положение «нового» атома углерода фиксируется сложным локантом, состоящим из цифровых локантов атомов, между которыми внедрена метиленовая группа (больший из которых берется в круглые скобки) и буквы «а», если между атомами внедрена одна группа, «Ь» если две подряд и т. д. Если метиленовая группа внедрена между атомами с соседними номерами, то второй локант может опускаться. Поскольку двойные связи в гомофуллеренах могут менять свое положение, для фиксации дополнительного атома водорода у гомоатома в записи названия даже ди-, три- и т. д. гомофуллеренов добавляют локант «обозначенного водорода», например, «1а/7-», см. рис. 6.2.63.
6.2.7.4. Норфуллерены
Неотделяемый префикс «нор», стоящий перед основой названия, указывает на удаление атома углерода из родоначального соединения. Перед префиксом приводится локант того атома, который был удален, а общая нумерация атомов остается прежней. Однако в отличие от норстероидов (разд. 6.16.4.6), норкаротиноидов (подразд. 6.16.5.2) и др. соединений, в фуллеренах те атомы, с которыми был соединен удаленный атом, не соединяют связью, а добавляют к ним недостающие атомы водорода. Если в результате применения нор-процедуры получилось нечетное количество атомов углерода, соединенных с атомами водорода, то у одного из них неизбежно меняется гибридизация с sp2 на sp\ и в названии это положение должно быть отражено с помощью «обозначенного водорода», как это сделано в первом из двух приведенных ниже примерах, см. рис. 6.2.64.
998
Новый справочник химика и технолога
Если удалить достаточно большое количество атомов из структур С60 или С70, то может оказаться, что название, составленное в соответствии с рекомендациями номенклатуры для полициклов, будет проще для восприятия, чем «норфуллереновое» название. Вместе с тем, жестких ограничений на количество нор-операций нет, поскольку сложность полученного названия сильно зависит от того, какие именно структурные фрагменты удалены. Фуллереновую номенклатуру рекомендуется применять, если в результате удаления атомов у (Сб<г4)[5,6]- и (С7о-£>5ь(б))[5,6]фуллеренов остается либо не менее двух «поясов» колец, либо половина атомов исходного фуллерена.
6.2.7.5. Секофуллерены
Секофуллерен — это фуллерен с удаленной связью. Перед неотделяемым префиксом «секо» через запятую пишется пара локантов, которая соответствует удаленной связи. Нумерация атомов соответствует нумерации родоначального фуллерена. Освободившиеся валент
ности, как и в случае норфуллеренов, «заполняют» атомами водорода. Если имеется выбор, то секо-положениям приписывают по возможности меньшие локанты. При разрыве нескольких связей их локанты перечисляются попарно через двоеточие, см. рис. 6.2.65.
6.2.7.6. Гетерофуллерены
Фуллерены, в которых атом(ы) углерода заменен(ы) на гстероатом(ы), называют с использованием «aw-номенклатуры (разд. 6.3.5). Присутствие трехвалентного гетероатома в структуре может привести к необходимости указать в названии «обозначенный водород», как, например, во втором из приведенных ниже примерах, см. рис. 6.2.66.
Следующие несколько структур представляют собой примеры структурно модифицированных гетеро-фуллеренов, а также фуллеренов, содержащих заряженный гетероатом и гетероатом с нестандартным числом связей, см. рис. 6.2.67а и 6.2.676.
1 аН-1 (9)а-Гомо(С6о-/ь)[5-6]фуллерен англ.: 1 аН-1 (9)a-Homo(C60-/h)[5,6]fullerene
1 (2)аН, 1 (9)аН-1 (2)а, 1 (9)а-Дигомо(С6о-/ь)[5-6]фуллерен англ.: 1 (2)аН, 1 (9)аН-1 (2)а, 1 (9)a-Dihomo(C6o-/h)[5-6]fullerene
Рис. 6.2.63
1,2,3,4,5,6,61,64,65,66,69,70-Додеканор(С7о-£)5Ь(б))[5,6]фуллерен англ.\ 1,2,3,4,5,6,61,64,65,66,69,70-Dodecanor(C7o-.£>5h(6))[5.6]fullerene
Рис. 6.2.64
Современная номенклатура органических соединений
999
22,23:24,25-Дисеко(С7о-/)5ь(б))[5,6]фуллерен англ.: 22,23:24,25-Diseco(C70-Z)5h(6))[5,6]fullerene
Рис. 6.2.65
1-Аза-9-бора(С60-/ь)[5,6]фуллерен англ.: 1 -Aza-9-bora(C60-Zh)[5,6]fullerene
2/-/-1 -Аза(С60-/и)[5,6]фуллерен англ.: 2/-/-1 -Aza(C60-/h)[5,6]fullerene
Рис. 6.2.66
1 а-Метил-1 аН-1 а-аза-1,9-секо-1 (2)а-гомо(Сбо-Л>)[5,6]фуллерен англ.: 1 a-Methyl-1 аН-1 a-aza-1,9-seco-1 (2)a-homo(C6o-4i)[5,6]f ullerene
Рис. 6.2.67a
1000
Новый справочник химика и технолога
1 -Азониа(С6о-/ь)[5,6]фуллерен англ.: 1 -Azonia(C60-/h)[5,6]fullerene
1 Х4-Т иа(С60-/ь)[5,6]фуллерен англ.: 1 X4-Th ia (C6o-/h)[5,6]fu Here n e
Рис. 6.2.676
6.2.7.7. Продукты присоединения к фуллеренам, фуллереновые ионы, радикалы и ион-радикалы
Молекулы (С60-Л)[5,6]- и (С70-£>5Ь(б))[5,6]фуллеренов не содержат атомов водорода. Тем не менее, их производные, а также их радикалы и ионы называют по заместительной номенклатуре в соответствии с теми правилами, которые используются для узловых атомов конденсированных систем. Все префиксные атомы или группы рассматриваются как замещающие атомы водорода, предварительно добавленные к кратным связям. Процедура присоединения водорода обозначается не-отделяемым префиксом «гидро», например, 1,9-дихлор-1,9-дигидро(Сбо-4)[5,6]фуллерен. Наличие суффиксных групп при узловых атомах также требует предварительного добавления водорода, которое в названии помечается в виде «добавленных водородов» (в круглых скобках курсивная Н с локантом), например, (С60-4)[5,6]фуллерен-1(9//)-ол (рис. 6.2.68).
Ниже представлены варианты названий ионов, радикалов, ион-радикалов (С60-/ь)[5,6]фуллерена:
х - •, Y = Н (С60-/и)[5,6]фуллерен-1 (9/7)-ил fiW277.:(C60-/h)[5,6]fulleren-1 (9//)-у1
X = +, Y = Н (Сбо-4)[5,6]фуллерен-1 (9//)-илий англ.: (C60-/h)[5,6]fulleren-l(9//)-ylium
X = •, Y = + (С60-/ь)[5,6]фуллерен-9-илий-1 (9Н)-ил англ.: (C6o-/h)[5,6]fulleren-l-ylium-1 (9/7)-у1
X II II (Сбо-4)[5,6]фуллерен-1 (9/7)-ид англ.: (C60-/h)[5,6]fulleren-l(9A/)-ide
X = •, Y = - (С60-/ь)[5,6]фуллерен-9-ид-1 (9//)-ил англ.: (C6o-/h)[5,6]fulleren-1 (9/7>id-1 (9tf)-yl
X = •, Y = • (С60-/ь)[5,6]фуллерен-1,9-диил англ.: (C60-4)[5,6]fullerene-l,9-diyl
Если фуллереновый фрагмент является заместителем в родоначальном соединении с главной функциональной группой, название его свободного радикала используется в качестве префикса, см. рис. 6.2.69.
В последнем названии благодаря наличию двух одинаковых фенольных фрагментов используется более короткая и простая для восприятия номенклатура ансамблей (подразд. 6.6).
Современная номенклатура органических соединений
1001
1,9,52,60-Тетрбром-! ,9,52,60-тетрагидро-
(СбоЛ)[5,6]фуллерен
англ.-. 1,9,52,60-Tetrabromo-! ,9,52,60-tetrahydro-
(C6o-/h)[5.6]fullerene
Диэтил-1аН-1 (9)a-roMo(C6o-/h)-
[5,6]фуллерен-1 а, 1 а-дикарбоксилат англ.'. Diethyl 1aH-1(9)a-homo(C60-/h)-
[5,6]f u I lere ne-1 a, 1 a-dicarboxylate
Рис. 6.2.68
35
cyclopropane-1-carbonitrile _ „ .rc „
7 K r 2,4-[24аН-24(25)а-Гомо(С70-Р5Ь(б))[5,6]-
фуллерен-24а,24а-диил]дифеноп
англ.-. 2,4'-[24aH-24(25)a-Homo(C7Q-D5h(6))[5.6]-
fullerene-24a,24a-divlldiphenol
Рис. 6.2.69
1002
Новый справочник химика и технолога
6.2.7.8. эндо-Замещенные фуллерены
Фуллерены С60 и С70 имеют достаточно объемную внутреннюю полость для того, чтобы заместители могли располагаться не только снаружи сферы, но и внутри ее. Такие «внутренние» заместители в названии обозначаются дескриптором «эндо», который записывают в круглых скобках после соответствующего локанта:
1,7(эндо)-Дибром-1,7-дигидро(Сбо-/ь)[5.6]фуллерен англ.: 1,7(endo)-Dibromo-1,7-dthydro(C6o-/h)[5.6]fullerene
6.2.7.9. Конденсированные фуллерены
Фуллерены, «/^«-конденсированные с органическим циклом или циклической системой, называют по модифицированной номенклатуре конденсированных систем. В соответствии с общими принципами метода конденсирования атомы связи, по которой фуллерен сконденсирован с другой циклической системой, принадлежат обоим компонентам. Принципиальными от
личиями в построении названия фуллсренсодержащих систем в сравнении с обычными карбоциклическими (разд. 6.2.5.2) и гетероциклическими (разд. 6.3.3) конденсированными полициклами являются: а) сохранение собственной нумерации каждого из компонентов; б) выбор фуллеренового компонента как основного независимо от строения второго компонента за исключением спироциклических систем. Вследствие этого локанты фуллереновой системы всегда являются нештрихованными, а штрихами помечаются локанты второй циклической системы. В названии соединения место сочленения указывается после префикса нефуллеренового компонента перечислением в квадратных скобках штрихованных локантов узловых атомов в этом компоненте, а затем, через двоеточие — нештрихованные локанты этих атомов в фуллерене. Если одним из компонентов является моноциклический углеводород, то его локанты опускаются (рис. 6.2.70а и 6.2.716).
Если с фуллереном сконденсированы две (или более) одинаковые циклические системы, то меньшим количеством штрихов помечаются атомы того компонента, узловые атомы которого имеют меньшие локанты в фуллереновом компоненте, например см. рис. 6.2.71.
Если с фуллереном сконденсированы разные циклические системы, то меньшим количеством штрихов помечаются атомы того компонента, префикс которого идет раньше по алфавиту, например см. рис. 6.2.72.
Как видно из последнего примера, выбор начала нумерации определяется наименьшим набором локантов для всех узловых атомов. Штрихи к локантам нефуллереновых компонентов добавляются в порядке их перечисления в названии соединения.
3-carboxylic acid 9',10'-Дигидро[9,10]этаноантра-
[1112': 1,9](С60-^)[5,6]фуллерен
англ.: 9', 10'-D i hy d го[9,10]ethanoanthra-
[11,,12’:1,9](C60-/h)[5,6]fullerene
Рис. 6.2.70a
Современная номенклатура органических соединений
1003
[1 ^Оксазоло^'Д'И ,9]-(Сбо-41)[5,6]фуллерен англ.: П.ЗКЗхагоМб'ДЧ.Э]-
(C6o-/h)[5>6]fullerene
2'-Метил-[7]окса[2]азабицикло[2.2.1]гептано-[5',6':1,9](Сбо-/ь)[5>6]фуллерен
англ.: 2'-Methyl-[7]oxa[2]azabicyclo[2.2.1 ]heptano-[5',6':1,9](C6o-/h)[6,6]fullerene
Рис. 6.2.706
Триоксирено[2',3': 1,9; 2",3":2,12; 2",,3,":7,8](С60-/и)[5,6]фуллерен англ.: Trioxireno[2',3':1,9; 2",3":2,12; 2"',3,":7,8](C60-/h)[5,6]fullerene
Рис. 6.2.71
3"'Н,3""Н,3.Н-Дибензо[16,17:44,45]трициклопропа[1,9:21,40:30,31](С60-/и)[5,6]фуллерен
англ. : 3' "Н,3""Н,3.H-Dibenzo[16,17:44,45]tricyclopropa[1,9:21,40:30,31 ](C60-7h)[5,6]fullerene
Рис. 6.2.72
1004
Новый справочник химика и технолога
6.2.7.10. Мостиковые фуллерены
Фуллерены, содержащие мостики между несоседними атомами, называют в соответствии с общими принципами номенклатуры для мостиковых конденсированных систем (подразд. 6.2.6). Нумерация мостиковых атомов начинается с номера, следующего после наибольшего локанта фуллеренового остова (например, для С60 это номер 61) и начинается с атома, соседнего с фуллереновым атомом с наивысшим локантом, см. рис. 6.2.73.
6.2.7.11. Спирофуллерены
Сами по себе (C60-7h)[5,6]- и (С7о-7>5Ь(б))[5,6]фул-лерены не могут давать спиросоединения. Однако в спирановые структуры могут быть включены гомофуллерены и фуллерены, конденсированные с другими
циклами. Эти соединения называют в полном соответствии с правилами спирономенклатуры (разд. 6.2.4.1). Следует заметить, что в отличие от правил нумерации конденсированных фуллеренсодержащих соединений (см. подразд. 6.2.7.9), в спирофуллеренах атомы фуллеренового каркаса не обязательно всегда имеют нештрихованные локанты, поскольку штрихи добавляются компонентам в порядке их алфавитного перечисления в названии. Именно поэтому часто определение нештрихованного набора локантов зависит от языка, на котором пишется название. Так, например, в первом из ниже приведенных соединений фуллереновые атомы в русском названии нештрихованные, а в английском — помечены штрихами, во втором соединении — наоборот (на схеме представлена нумерация для русского названия), см. рис. 6.2.74.
1,4-Пропано(С70--О5И(б))[5,6]ФУллеРен англ.-. 1,4-Ргорапо(С7о-Л5Г|(6))[5,6]Ти11егепе
71 Н,75/-/-1,4-[3,4]Фурано(С7о-Л5И(6))[5,6]фуллерен-72,74-дион англ. -. TWIJSH-A ,4-[3,4]Furano(C7o-7)5h(6)X5,6]fullerene-72,74-dione
1 а,За-Этано-1 а,За-диаза-1 (2)а:3(4)а-дигомо(С60-/ь)[5,6]фуллерен
англ.: 1a,3a-Ethano-1a,3a-diaza-1(2)a:3(4)a-dihomo(C6o-/h)[5,6]fulleren
7,20:8,10:11,13:14,16:17,19-Пентаэтено-
1,2,3,4,5,6,9,12,15,18-деканор(Сбо-41)[5>6]фуллерен англ.: 7,20:8,10:11,13:14,16:17,19-Pentaetheno-
1,2,3,4,5,6,9,12,15,18-decanor(C6o-/h)[5,6]fulleren
Рис. 6.2.73
Современная номенклатура органических соединений
1005
Спиро[[1(9)а]гомо(С60-/и)[5,6]-фул-лерен1а,1'-циклопентан]
англ. . Spiro[cyclopentane-1,1'а-
[1(9)a]homo(C6o-/h)[5.6]fullerene]
Спиро[флуорен-9,3"-циклопропа[1,9](С6о-Л1)[5,6]-фуллерен] англ.-. Spiro[cyclopropa[1.9](C60-/h)[5.6]fullerene-3\9,,-fluorene]
Рис. 6.2.74
6.3. Номенклатура гетероциклических соединений
Необычайное разнообразие гетероциклических соединений, отличающихся друг от друга типом входящих в них гетероатомов, их количеством, расположением в молекуле, а также размером и числом циклов в молекуле, которые могут конденсироваться рядом различных способов, привело к появлению особой «гетероциклической» номенклатуры.
6.3.1. Тривиальные названия гетероциклических соединений
Для соединений гетероциклического ряда, даже если не считать гетероциклов природного происхождения, например алкалоидов, существует необычайно большое количество тривиальных и полусистематиче-
ских названий. Правилами ШРАС допускается использование строго ограниченного набора таких названий для относительно простых гетероциклов. Сложные полициклические гетероатомные системы называют с помощью метода конденсирования на основе разрешенных тривиальных или полусистематических названий. (Метод конденсирования для карбоциклических соединений см. подразд. 6.2.5.2). В табл. 6.11 приведены названия гетероциклических систем, разрешенные правилами IUPAC. Эти названия следует использовать при составлении названий сложных систем методом конденсирования. Кроме того, правила IUPAC допускают использование ряда тривиальных названий простейших гидрированных гетероциклических систем (табл. 6.12), однако их применение в методе конденсирования не рекомендуется.
Таблица 6.11
Гетероциклические системы и их тривиальные и полусистематические названия, разрешенные правилами IUPAC для построения сложных названий методом конденсирования (расположены в порядке уменьшения старшинства)
1. Феноксазин (phenoxazine) 9 мЮ 1 6 5 4 показан 10//-изомер 2. Фенотиазин (phenothiazine) Л йю 1 :ооа 6 5 4 показан 10//-изомер
3. Феноселеназин (phenoselenazine) ~ ОС 6 5 4 показан 10//-изомер 4. Фенотеллуразин (phenotellurazine) 9 мЮ 1 :OQO: 6 5 4 показан 10/7-изомер
1006
Новый справочник химика и технолога
Продолжение табл. 6.11
5. Фенофосфазинин (phenophosphazinine) 9 !? 1 :ССО: 6 5 4 6. Фснарсазинин (phenarsazinine) 9 1л° 1 хХс: 6 5 4
7. Феномеркуразин (phenomercurazine) 9 10 1 OXS 6 Н5 4 показан 5/7-изомер 8. Феназин (phenazine) 9 10 1 :сса 654
9. Фенантролин (phenanthroline)а) 2 10 1 и показан 1,7-изомер (по одному атому азота в терминальных кольцах) 10. Перимидин (perimidine) А з HN^N3 9||XZZJ4 7 6 показан 1/7-изомер
11. Акридин (acridine) б) 8 9 1 7 гХХХ"а5!2 ДХ ЛД 5 10 4 12. Фенантридин (phenanthridine) 2 7 6
13. Карбазол (carbazole) б) 8 Но 1 5 4 показан 9/7-изомер 14. Птеридин (pteridine) 8 1 ^N N 5 4
15. Циннолин (cinnoline) <N2 5 4 16. Хиназолин (quinazoline) 8 1 CO1. 5 4
17. Хиноксалин (quinoxaline) 8 М СО: 5 4 18. Нафтиридин (naphthyridine)B) 7| 11 г 5 4 показан 1,5-изомер (по одному атому азота в каждом кольце)
19. Фталазин (phthalazine)в) 8 1 1 5 4 20. Хинолин (quinoline) 8 1 7i iX А2 6 ЧАХ3 5 4
21. Изохинолин (isoquinoline) 8 1 5 4 22. Хинолизин (quinolizine) 9 1 8г??гчХ::гЧч12 7A-x-N-\As с 5 ; 6 4 показан 2/7-изомер
Современная номенклатура органических соединений
1007
Продолжение табл. 6.11
23. Пурин (purine) б) 6 Ну Nq N 4 У 3 показан 7/7-изомер 24. Индазол (indazole) 7 Н1 ✓ N.J бг^ N2 ААа 4 показан 1/7-изомер
25. Индол (indole) АГ Г 5^4/ 3 4 показан 1/7-изомер 26. Изоиндол (isoindole) 7 1 .А 2 1 з 4 показан 2/7-изомер
27. Индолизин (indolizine) 8 1 ‘А 3 28. Пирролизин (pyrrolizine) fcp.’ 5 4 показан 1/7-изомер
29. Пиридазин (pyridazine) 1 6r< ^N2 3 4 30. Пиримидин (pyrimidine) Т4)2 5<^N3 4
31. Пиразин (pyrazine) х52 5<n^3 4 32. Пиридин (pyridine) 1 ✓ N. 6fT 5X^3 4
33. Пиразол (pyrazole) н. .n 4 5fl N 2 у у2 4 'З показан I/7-изомер 34. Имидазол (imidazole) JJ- 5O2 4 N3 показан 1/7-изомер
35. Пиррол (pyrrole) н. .nJ 5Оз 4 'З показан 1/7-изомер 36. Феноксатиин (phenoxathiine) 9 10 1 :OCO: 6 5 4
37. Феноксаселенин (phenoxaselenine) 9 1° 1 :ОСО: 6 5 4 38. Феноксателлурин (phenoxatellurine) 9 1° 1 '.ООО! 6 5 4
39. Феноксафосфинин (phenoxaphosphinine)г) А 10р А :СОО: 6 5 4 40. Феноксарсинин (phenoxarsinine)д) 9 юУе 1 :сса 6 4
41. Феноксастибинин (phenoxastibinine)е) 9 юЬи 1 :ОСО: 6 5 4 42. Оксантрен (oxanthrene)ж) 9 п 1 “ООО2
1008
Новый справочник химика и технолога
Продолжение табл. 6.11
43. Ксантен (xanthene)б) 8 9 1 7 П МН 'А <1 2 5 Ю 4 показан 9//-изомер 44. Хромен (chromene) 8 1 7ОО2 5 4 показан 2/7-изомер
45. Изохромен (isochromene) 8 1 OQ2 5 4 показан I//-изомер 46. Пиран (pyran) 1 6П2 5 А^3 4 показан 2//-изомер
47. Фуран (furan)3) 1 .0. О 4 3 48. Фенотиарсинин (phenothiarsinine)и) 9 10л 1 ССО: 6 5 4
49. Тиантрен (thianthrene) 9 1° 1 :ССО: 654 50. Тиоксантен (thioxanthene) а) 8 9 1 К , я
51. Тиохромен (thiochromene) 7| Il 1 бА-АА3 5 4 показан 2//-изомер 52. Изотиохромен (isothiochromene) 8 1 7г<гг;>тХ^52 б^ЧхЧ^3 5 4 показан 1//-изомер
53. Тиониран (thiopyran) 1 6Q2 4 показан 2//-изомер 54. Тиофен (thiophene) 1 5Оз
55. Селенантрен (selenanthrene) 9 1° 1 :ОСО: 654 56. Селеноксантен (selenoxanthene)6) 8 9 1 О Ч^з Y Se 5 10 4
57. Селснохромен (selenochromene) 8 е /Se 7г V 5 4 показан 2//-изомер 58. Изоселенохромен (isoselenochromene) » А 2 7г II Se 6^ЧхЧ^*3 5 4 показан 1//-изомер
59. Теллурантрен (telluranthrene) 9 10 1 :ОСО 8 5 4 60. Теллуроксантен (telluroxanthene)б) 8 9 1 Те 5 10 4
Современная номенклатура органических соединений
1009
Продолжение табл. 6.11
61. Теллурохромен (tellurochromene) 8 т 7ПГет 64AA3 5 4 показан 277-изомер 62. Изотеллурохромен (isotellurochromene) ЛА 2 7г Iе 6 Хх^х^А3 5 4 показан 177-изомер
63. Фосфантрен (phosphanthrene) 9 Юр 1 :0Q0- 6 Н5 4 64. Акридофосфин (acridophosphine) 9 10 1 7хЛЛгХХгА3 6 Н5 4
65. Фосфантридин (phosphanthridine) 2 1хфХ.з ю Г Г 7 6 66. Фосфинолин (phosphinoline) XjO2 6 ХХхф3 5 4
67. Изофосфинолин (isophosphinoline) 8 1 rVr 6 x/x^3 5 4 68. Фосфинолизин (phosphinolizine) 9 1 вг^^Х^^Хг 7фМ3 6 5 4 показан 277-изомер
69. Фосфиндол (phosphindole) бПО 5Хчф 3 4 показан 177-изомер 70. Изофосфиндол (isophosphindole) 7 1 2 бг^Хг^ РН 5 Хф *3 4 показан 277-изомер
71. Фосфиндолизин (phosphindolizine) 8 1 7ГП2 3 72. Арсантрен (arsanthrene) Оф 6 Н 5 4
73. Акридарсин (acridarsine) 9 10 1 7Х/\Л/\О ;; As к 6 H ° 4 74. Арсантридин (arsanthridine) 2 10 I IJ 4 =\Аф 7 6 5
75. Арсинолин (arsinoline) 8 J 7i |И Л 6х/х^3 5 4 76. Изоарсинолин (isoarsinoline) Т II Is бхАхЛз 5 4
77. Арсинолизин (arsinolizine) 9 1 бФ^ХФО2 3 6 5 4 показан 277-изомер 78. Арсиндол (arsindole) ’По 5хЛ 3 4 показан 177-изомер
1010
Новый справочник химика и технолога
Окончание табл. 6.11
79. Изоарсиндол (isoarsindole) 7 1 2 3 4 показан 2/7-изомер 80. Арсиндолизин (arsindolizine) 8 1 6^4^As—^3 5 4
81. Силантрен (silanthrene) 6 Н2 4 82. Борантрен (boranthrene) 9 юУ 1 :а.» 6 Н5 4
83. Меркурантрен (mercuranthrene)K) 9 1° 1 :д:р ° 5 4
а) Последовательность уменьшения старшинства изомеров: 1.7-. 1,8-, 1,9-, 1,10-, 2,7-, 2,8-, 2,9-, 3,7-, 3,8-, 4,7-.
б) Нестандартная нумерация.
в) Последовательность уменьшения старшинства изомеров: 1,5-, 1,6-, 1.7-, 1,8-нафтиридины, фталазин, 2,6-нафтиридин, 2,7-нафтиридин.
г) Старое название — феноксафосфин (phenoxaphosphine).
д) Старое название — феноксарсин (phenoxarsine).
с) Старое название — феноксантимонин (phenoxantimonine).
ж) Старое название — дибензо[Де][1,4]диоксин (dibenzo[£»,e][l,4]dioxine).
з) Бензофуран и изобензофуран в методе конденсирования не используются.
и) Старое название — фенотиарсин (phenothiarsine).
к) Старое название — феномеркурин (phenomercurine).
Таблица 6.12
Тривиальные и полусистематические названия гидрированных гетероциклических систем, не применяемые для построения сложных названий методом конденсирования
1. Морфолин (morpholine)а) N Н 2. Хинуклидин (quinuclidine) 6/N\\ 2 5^3 4
3. Изоиндолин (isoindoline) ? А2 6ПСг 3 4 4. Индолин (indoline) 7 Н Сй 4
5. Пиперазин (piperazine) н Ж Т’1 н 6. Пиперидин (piperidine) н 6| 1 |2 5\^3 4
7. Пиразолин (pyrazoline)б) н 5<1 N2 I] 4 з показан 2-изомер 8. Пиразолидин (pyrazolidine) н 5<i NH I 2! 4 3
9. Имидазолин (imidazoline)б) н Ом 41 N показан 2-изомер 10. Имидазолидин (imidazolidine) н А2 4 NH
Современная номенклатура органических соединений
1011
Окончание табл. 6.12
11. Пирролин (pyrroline)б) 5Й2 4 ‘з показан 2-изомер 12. Пирролидин (pyrrolidine) н Г’'I2 4' '3
13. Хроман (chromane)а) и 1^2 5 4 14. Изохроман (isochromane)а) 8 1 7[И5::тх^'02 5 4
а) Халькогеновые аналоги называют, используя префиксы «тио» («thio»), «селено» («seleno»), «теллуро» («telluro»).
б) Правила IUPAC 1993 г. не рекомендуют использовать эти тривиальные названия.
6.3.2. Расширенная система Ганча — Видмана
Моноциклы с одним гетероатомом и числом звеньев не более 10 (кроме насыщенных азотсодержащих моноциклов с числом звеньев не более пяти) называют, объединяя префикс из табл. 6.13 и основу из табл. 6.14. Нумерацию гетероцикла начинают с гетероатома, при этом «обозначенный водород» получает наименьший из возможных локантов. Буква «а» в префиксе опускается перед последующей гласной (рис. 6.3.1).
Для обозначения двух или более одинаковых гетероатомов применяют умножающие приставки, добавляя их к префиксу элемента. Буква «а» в префиксе опускается перед последующей гласной. Нумерацию гетероцикла начинают с гетероатома и продолжают в направлении наименьшей последовательности локантов (рис. 6.3.2).
При наименовании гетероцикла, содержащего два или более различных гетероатома, префикс гетероатома (табл. 6.13) с соответствующей умножающей приставкой помещают перед основой (в порядке их расположения в табл. 6.13). Положение гетероатомов указывают с помощью цифровых локантов, которые помещаются перед префиксом первого гетероатома в том же порядке, в каком располагаются сами префиксы. Нумерацию гетероцикла начинают с гетероатома, чей префикс появляется в табл. 6.13 первым, и продолжают в направлении наименьшей последовательности локантов всех гетероатомов, а при одинаковых наборах локантов — в порядке расположения префиксов гетероатомов в табл. 6.13 (рис. 6.3.3).
Гетероциклы с числом некумулированных двойных связей меньшим, чем максимально возможное, называют: а) добавляя неотделяемые префиксы «дигидро», «тетрагидро» и т. д. к родоначальному названию соответствующего соединения с максимальным числом некумулированных двойных связей; б) неотделяемые префиксы «дидегидро», «тетрадегидро» и т. д. к родоначальному названию соответствующего полностью насыщенного соединения. Метод (а) является предпочтительным. При нумерации гетероатомы и «обозначенный водород» имеют преимущество перед «гидро»-и «дегидро»-префиксами (рис. 6.3.4).
Таблица 6.13
Префиксы для системы Ганча — Видмана а,б)
№ п/п Элемент (валентность) Префикс
1 фтор(1) фтора (fl нога)
2 хлор(1) хлора (chlora)
3 бром(1) брома (broma)
4 иод(1) иода (ioda)
5 кислород(П) окса(оха)
6 сера(П) тиа (thia)
7 селен(П) селена (selena)
8 теллур(П) теллура (tellura)
9 азот(Ш) аза (aza)
10 фосфор(Ш) фосфа (phospha)
11 мышьяк(Ш) арса (arsa)
12 сурьма(Ш) стиба (stiba)
13 висмут(Ш) висма (bisma)
14 кремний(1У) сила (sila)
15 германий(1У) герма (germa)
16 олово(1У) станна (stanna)
17 свинец(1У) плюмба (plumba)
18 бор(1П) бора (bora)
19 ртуть(П) меркура (mercura)
а) Гетероатомы расположены в порядке уменьшения старшинства.
б) Префиксы для галогенов введены для того, чтобы обеспечить возможность наименования гетероциклов, содержащих катионные атомы галогенов в нестандартном валентном состоянии, например, -К — Х3-иода, -Г----иодониа.
1012
Новый справочник химика и технолога
Таблица 6.14
Основы названий гетероциклов в расширенной системе Ганча — Видманаа)’б)’в)
Размер кольца Ненасыщенные д) Насыщенные
3 ирен (irene)е) иран (irane)ж)
4 ет (ete) етан (etane)ж)
5 ол (ole) олан (etane)ж)
6Аг) ин (ine) ан (апе)
6В г) ин (ine) инан (inane)
6С г) инин (inine) инан (inane)
7 епин (epine) епан (ерапе)
8 оцин (ocine) окан (осапе)
9 онин (onine) онан (опапе)
10 ецин (ecine) екан (есапе)
а) Окончание «е» в английском названии является необязательным.
б) Основы для 3, 4, 7, 8. 9, 10-звенных циклов могут рассматриваться как следующие из численных префиксов: «ir» из tri, «et» из te/ra, «ер» из hepta, «ос» из octa, «оп» из попа, «ес» из deca.
в) Основы «етин» («etine») и «один» («oline») использовать нельзя, т. к. они ранее использовались для наименования соответственно 4- и 5-звенных циклов содержащих азот и имеющих только одну из двух возможных двойных связей.
г) Для того, чтобы определить основу названия для шестизвенных циклов, прежде чем использовать табл. 6.14, из наборов [6А: О, S, Se, Те, Bi, Hg; 6В: N, Si, Ge, Sn, Pb; 6C: B, F, Cl, Br, 1, P, As, Sb] необходимо выбрать тот, который содержит гетероатом наименьшего старшинства (табл. 6.13) для называемого цикла (т. е. тот, который в названии будет прямо предшествовать основе). Например, правильную основу для диоксазинового цикла можно найти в наборе 6В, который содержит азот (кислород «старше» азота).
д) Используется, когда кольцо с гетероатомами, имеющими валентность, приведенную в табл. 6.13, содержит максимальное число некумулированых двойных связей (по крайней мере, одну двойную связь).
с) Традиционная основа «ирин» («irine») может быть использована для колец, содержащих только азот.
ж) Традиционные основы «иридин» («iridine»), «етидин» («etidine») и «олидин» («olidine») предпочтительны для колец, содержащих азот.
Насыщенные моноциклы с числом звеньев не более пяти и имеющие только один атом азота называют путем добавления префикса «аза-» («aza-») (см. табл. 6.13), опуская конечное «а» к основам «-иридии», «-етидин» или «-олидин» («-iridine», «-etidine» или «-olidine») в зависимости от того, имеет ли кольцо 3, 4 или 5 звеньев соответственно. Нумерация атомов в гетероцикле начи
нается с атома азота. Наличие двух и более атомов азота обозначают умножающими приставками. Другие гетероатомы, входящие в состав гетероцикла, указываются с помощью соответствующих префиксов из табл. 6.13. Префиксы гетероатомов с соответствующими умножающими приставкой помещают перед основой в порядке их расположения в табл. 6.13. Положение гетероатомов указывают с помощью цифровых локантов, которые помещаются перед префиксом первого гетероатома в том же порядке, в каком располагаются в названии префиксы, к которым они относятся. Нумерацию гетероцикла начинают с гетероатома, чей префикс появляется в табл. 6.13 первым и продолжают в направлении наименьшей последовательности локантов всех гетероатомов, а при одинаковых наборах локантов — в порядке расположения префиксов гетсроатомов в табл. 6.13 (рис. 6.3.5).
Если гетероциклический фрагмент молекулы не входит в основу названия, то его записывают в виде префикса, который получают из тривиального или систематического названия гетероцикла путем добавления соответствующего окончания из табл. 6.5 с соответствующим цифровым локантом. Помимо этого, некоторые гетероциклические замещающие группы, перечисленные ниже, записываются в сокращенном виде (локант, показывающий положение свободной валентности в сокращенных префиксах замещающих групп, помещается перед этим префиксом, а не перед окончанием «ил», например: 2-фурил, 1-нафтил, 2-антрил, 2-фенантрил):
показан 2-изомер
Фурил англ.'. Furyl
показан 2-изомер
Пиперидил англ.-. Piperidyl
показан 2-изомер
Пиридил англ.: Pyridyl
показан 2-изомер
Хинолил англ.: Quinolyl
Фурфурил англ.: Furfuryl
показан 3-изомер
Изохинолил англ.: Isoquinolyl
Тенил англ.: Thenyl
Следует иметь в виду, что при модификации последних двух префиксов замещение атомов водорода допустимо только в кольце.
Современная номенклатура органических соединений
1013
2
Оксиран англ:. Oxirane
2 lA HN-*3
1 Н-азирен* англ: 1H-Azirene
Традиционно используется название 1Н-азирин (1H-azirine), допускаемое правилами IUPAC
3.---.2
Дзет
англ:
1
Силолан англ: Silolane
2Н-Фосфол англ:. 2H-Phosphole
Фосфинин, фосфорин (устар.) англ:. Phosphinine
5
Тиепин
англ:. Thiepine
Боринан англ:. Borinane
Азокан, октагидроазоцин (устар.) англ: Azocane
Рис. 6.3.1
2
1,3-Дитиолан 1,3,5,7-Т етроксокан
англ: 1,3-Dithiolane англ: 1,3,5,7-Tetroxocane
2Н.4Н-1,3-Диоксин англ: 2Н,4Н-1,3-Dioxine
4
1,2,4-Триазин англ: 1,2,4-Triazine
4Н-1,3-Дифосфепин англ: 4Н-1,3-Diphosphepine
Рис. 6.3.2
HN-----SiH2
4 3
1,3-Оксатиолан англ: 1,3-Oxathiolane
1,2,4,3-Т риазасилолидин англ: 1,2,4,3-Triazasilolidine
6Н-1,2,5-Т иадиазин англ: 6Н-1,2,5-Thiadiazine
Рис. 6.3.3
1014
Новый справочник химика и технолога
1,2-Дигидроазет англ.-. 1,2-Dihydroazete ранее: 2-Азетин
2,3,4,7,8,9-Г ексагидрооксонин англ.-. 2,3,4,7,8,9-Hexahydrooxonine
3,6-Дигид ро-2/-/-фосфепин англ.-. 3,6-Dihydro-2/-/-phosphepine
Рис. 6.3.4
2
1Л
HN^3
Азиридин англ.-. Aziridine
1 4
HN—। HAs—N?l
1,3,2-Диазарсетидин англ.-. 1,3,2-Diazarsetidine
1,3-Диазетидин англ.-. 1,3-Diazetidine
1,4,2-Оксафосфолидин англ.-. 1,4,2-Oxazaphospholidine
Рис. 6.3.5
6.3.3. Метод конденсирования
6.3.3.1. Основные принципы метода конденсирования
Названия ор/ио-конденсированных и орто-пери-конденсированных гетероциклов строятся на основе тех же принципов, что и названия карбоциклических конденсированных систем (подразд. 6.2.5). При наименовании полициклической системы ее формально разделяют на составные части и общее название формируют из названий полученных фрагментов, например:
бензимидазол бензол имидазол
При составлении названия конденсированной полициклической системы рекомендуется придерживаться следующей последовательности действий:
1. Разъединить систему на отдельные моно- или полициклические компоненты, выбирая по возможности самые старшие компоненты из табл. 6.11, например, «индол», а не «пиррол» + «бензол». Пользуясь табл. 6.9 и 6.11, назвать полученные компоненты. В случае отсутствия тривиального названия следует использовать систематическое название по Ганчу — Видману.
2. Если система состоит из двух и более компонентов, для составления названия необходимо выбрать один в качестве основного. Например, в соединении
Если в месте сочленения находится гетероатом, то названия компонентов, которые конденсируются, выбираются так, чтобы они оба содержали этот гетероатом, например:
имидазо[1,2-а]пиридин пиридин имидазол
пирано[3,4-Ь]хинолизин
хинолизин (не пиран и не пиридин!) (см. табл. 6.11) выступает в качестве основного компонента, а пиран — в качестве второго компонента. В подразд. 6.3.3.2 представлена схема выбора основного компонента.
3. Второй компонент добавляется к основному в виде префикса. Этот префикс образуется добавлением к названию соответствующей циклической системы буквы «о». Так, пиридазиновый цикл обозначается в префиксе как «пиридазино», хиноксалиновая система — как «хиноксалино» и т. д. Имеется несколько исключений, которые перечислены в табл. 6.15.
Современная номенклатура органических соединений
1015
Таблица 6.15
Нестандартные префиксы в названиях конденсированных соединений
Гетероцикл Префикс
Изохинолин Изохино (isoquino)
Имидазол Имидазо (imidazo)
Пиридин Пиридо (pyrido)
Пиримидин Пиримидо (pyrimido)
Тиофен Тиено (thieno)
Фуран Фуро (furo)
Хинолин Хино (quino)
4. Атомы циклической системы второго (третьего и т. д.) компонента нумеруются, как показано в табл. 6.11, если для него есть тривиальное название, или в соответствии с системой Ганча — Видмана, если используется систематическое название. Связи основного компонента последовательно обозначают курсивными латинскими буквами а, Ь, с и т. д., начиная со связи 1-2 согласно нумерации этого компонента (см., например, соединение № 1 в табл. 6.11; в случае нестандартной нумерации связи обозначаются последовательно, соединения № 11, 13, 23, 43, 50, 56, 60). В названии гетероциклической системы место соединения двух циклов обозначается соответствующими цифрами и буквой, помещенными в квадратные скобки. При этом номера атомов второго компонента приводятся в последовательности, которая по направлению соответствует увеличению номеров атомов в основном компоненте. В качестве примера приведем название следующего соединения:
имидазол
1,3-тиазол
Основной компонент— 1,3-тиазол (подразд. 6.3.3.2, п. 6); циклы соединены по стороне b тиазола и стороне 1,2 имидазола. Направление нумерации в имидазоле противоположно направлению нумерации в основном компоненте — тиазоле. Поэтому «имидазольная» сторона в названии гетероциклической системы обозначается как 2,1, а не 1,2. Таким образом, соединение следует называть имидазо[2,1-/?][1,3]тиазол. Следует обратить внимание на то, что если для какого-либо компонента необходимо приводить цифровые локанты гетероатомов, например, при использовании для него названия по Ганчу — Видману (в последнем примере 1,3-тиазол), то в названии конденсированной гетероциклической системы они помещаются в квадратные скобки перед названием компонента ([1,3]-тиазол). При этом эти
цифры в скобках относятся только к нумерации данного компонента, а не всей конденсированной системы.
Когда в соединении сконденсировано более двух компонентов, то фрагменты, сочлененные с основным компонентом, указывают в алфавитном порядке, а остальные -— в том порядке, в котором они соединяются в структурной формуле, например:
2/-/-Пирано[3',2':4,5]циклопента
[<Уе]пиридо[4,3-Ь][1,8]нафтиридин англ.'. 2/-/-Pyrano[3',2':4,5]cyclopenta[de]
pyrido[4,3-Ь][1,8]naphthyridine
4 5
3' 2
Нумерация атомов в конденсированных системах проводится независимо от вышеперечисленных действий. Для нумерации полициклической системы се прежде всего ориентируют, как указано в подразд. 6.2.5.2. Нумерацию начинают от первого атома правого верхнего цикла, не участвующего в слиянии с другими циклами, и ведут по часовой стрелке по периметру молекулы, включая узловые гетероатомы. Узловые атомы углерода, в отличие от узловых гетероатомов, отдельно не нумеруют; они получают номер предыдущего атома с добавлением буквы латинского алфавита: а, Ь, с и т. д. (см. подразд. 6.2.5.2). Внутренние гетероатомы нумеруют в последнюю очередь, продолжая численную последовательность. Если имеется выбор, то определяют наиболее короткий путь от каждого гетероатома до периферийного атома и меньший локант приписывают гетероатому, ближайшему к периферийному с наименьшим номером. Гетероатомам по возможности присваивают номера тем меньше, чем раньше они расположены в табл. 6.13 (рис. 6.3.6).
Наибольшая сложность обычно заключается в определении начала нумерации. Если есть выбор между равноценными ориентациями молекулы, то атомы системы нумеруют так, чтобы последовательно были выполнены следующие условия:
- меньший номер получил гетсроатом, например:
1-Бензофуран
англ.-. 1-Benzofuran
Циклопента[Ь]пиран англ.: Cyclopenta[6]pyrane
- последовательность локантов гетероатомов должна быть наименьшей (рис. 6.3.7);
- меньший номер получил гетероатом, расположенный выше в табл. 6.13 (рис. 6.3.8);
- узловой атом углерода следовал по возможности за атомом с меньшим номером (рис. 6.3.9);
1016
Новый справочник химика и технолога
- «обозначенный водород» получил по возможности наименьший номер (рис. 6.3.10).
В тех случаях, когда требуется использование более чем одной пары квадратных скобок, места сочленения
указываются с использованием нештрихованных и штрихованных цифр, причем нештрихованные цифры приписываются циклу, непосредственно присоединенному к основному компоненту (рис. 6.3.11).
Пирроло[2,3-с]карбазол англ:. Pyrrolo[2,3-c]carbazole
Фосфинолизино^'.б'.б'ДД.бН! ,4]аза-фосфинино[2,1,6-с/е]хинолизин англ: Phosphinolizino[4’,5',6':3,4,5][1,4]aza-phosphinino[2,1,6-cte]quinolizine
Рис. 6.3.6
4H-[1,3]Оксатиоло[5,4-Ь]пиррол ------*------
англ: 4Н-[1,3]Oxathiolo[5,4-6]pyrrole неправильно: 1,3,6 или 1,4,6
последовательность локантов 1,3,4
Рис. 6.3.7
Т иено[2,3-Ь]фуран англ: Thieno[2,3-b]furan
Рис. 6.3.8
Имидазо[1,2-Ь][1,2,4]триазин англ: lmidazo[1,2-b][1,2,4]triazine
Рис. 6.3.9
4/7-[1,3]Диоксоло[4,5-сУ]имидазол англ: 4/7-[1,3]Dioxolo[4,5-c(]imidazole
Рис. 6.3.10
Современная номенклатура органических соединений
1017
Пиридо[1',2’:1,2]имидазо[4,5-Ь]хиноксалин англ.: Pyrido[1 ',2':1,2]imidazo[4,5-b]quinoxaline
Рис. 6.3.11
Гетеробициклическую систему (если она отсутствует в табл. 6.11), в которой к гетероциклу с числом атомов больше четырех примыкает бензольное кольцо, называют как «бенз(о)гетероцикл» с цифровыми локантами, указывающими положение гетероатомов (в соответствии с нумерацией полициклической системы в целом), например:
З-Бензоксепин англ:. 3-Benzoxepine
4/-/-3.1 - Бензоксазин
англ:. 4/-/-3.1-Benzoxazine
Если конденсированная система с тремя и более циклами, содержащая изолированный бензокомпонент (т. е. бензокомпонент, который не может быть включен в систему из табл. 6.11), о/?/ио-конденсированный с гетероциклом, то эти два цикла называют вместе как единый компонент («бенз(о)гетероцикл») (этот подход, однако, имеет ряд ограничений при использовании мультипликативных основ и префиксов (см. [9])), например:
Т иено[3,2-/][2,1 ]бензотиазол англ:. Thieno[3,2-/][2,1]benzothiazole
6.3.3.2. Схема определения основного компонента конденсированных гетероатомных систем
Для определения основного компонента конденсированной гетероатомной системы существует определен
ный набор правил, которые применяются в порядке понижения приоритетности. Если правило не позволяет определить основной компонент системы, то следует переходить последовательно к следующим до тех пор, пока выбор не будет сделан. Если в молекуле присутствует только один гетероциклический компонент, то он всегда выбирается в качестве основного, даже если оставшийся карбоцикл имеет больший размер (если гетероциклическая система имеет тривиальное название, то выбирается та, которая имеет меньший номер в табл. 6.11) (рис. 6.3.12).
Если молекула содержит несколько гетероциклических компонентов, то в качестве основного выбирается:
1. Компонент с гетероатомом, стоящим раньше в следующем ряду: N, F, Cl, Br, I, О, S, Se, Те, Р, As, Sb, Bi, Si, Ge, Sn, Pb, B, Hg (рис. 6.3.13a и 6.3.136).
2. Компонент, содержащий большее число циклов (рис. 6.3.14).
3. Компонент с большим по размеру циклом, даже если в меньшем цикле содержится большее количество гетероатомов (рис. 6.3.15).
4. Компонент, содержащий большее количество гетероатомов любого типа (рис. 6.3.16).
5. Компонент, отличающийся большим разнообразием гетероатомов (рис. 6.3.17).
6. Компонент с наибольшим числом гетероатомов, находящихся выше в табл. 6.13 (рис. 6.3.18).
7. Компонент, имеющий более предпочтительное расположение колец (линейное более предпочтительно, чем ангулярное) (рис. 6.3.19). В этом примере акридин более предпочтителен, т. к. содержит три кольца в горизонтальном ряду против двух колец у фенантридина.
8. Компонент, у которого гетероатомы имели наименьший набор локантов до объединения циклов (рис. 6.3.20).
1018
Новый справочник химика и технолога
основной компонент - тиет основной компонент - оксирен
2/-/-Нафто[2,3-Ь]тиет 8а/-/-Флуорено[1,2-Ь]оксирен
англ.'. 2H-Naphtho[2,3-b]thiete англ.: 8a/-/-Fluoreno[1,2-b]oxirene
Рис. 6.3.12
основной компонент - изохинолин 8/-/-Тиопирано[2,3-Ъ]изохинолин англ.: 8/-/-Thiopyrano[2,3-/7]isoquinoline
основной компонент - пиррол
1,4-Диоксепино[5,6-с]пиррол англ.: 1,4-Dioxepino[5,6-c]pyrrole
Рис. 6.3.13а
5
основной компонент - оксепин
Т иепино[2,3-сУ]оксепин
англ.: Thiepino[2,3-d]oxepine
основной компонент - оксирен
[1,2]Фосфаборинино[4,5-Ь]оксирен англ.: [1,2]Phosphaborinino[4,5-bjoxirene
Рис. 6.3.136
основной компонент - хинолин (хинолин - 2 цикла, пиримидин -1 цикл)
Пиримидо[5,4-Ь]хинолин
англ.: Pyrimido[5,4-b]quinoline
основной компонент - карбазол (карбазол - 3 цикла, хиноксалин- 2 цикла)
7/-/-Пиразино[2,3-с]карбазол
англ.: 7/-/-Pyrazino[2,3-c]carbazole
Рис. 6.3.14
основной компонент - пиран За/-/-Фуро[3,2-Ь]пиран
англ.: 3a/-/-Furo[3,2-b]pyran
основной компонент - азепин [1,3]оксазоло[3,2-а]азепин англ.: [1,3]oxazolo[3,2-a]azepine
основной компонент - пиран
4/-/-[1,3,2]диоксафосфоло[4,5-с]пиран англ.: 4Н-[1,3,2]dioxaphospholo[4,5-c]pyran
Рис. 6.3.15
Современная номенклатура органических соединений
1019
5 4
основной компонент - оксазин 5Н-Пиридо[2,3-с/][1,2]оксазин англ.: 5H-Pyrido[3,2-d][1,2]oxazine
основной компонент - диоксол 2Н-Фуро[2,3-сУ][1,3]диоксол англ.: 2H-Furo[2,3-d][1,3]dioxole
Рис. 6.3.16
5 4
8 1
основной компонент - оксатиин
[1,4]Диоксино[2,3-Ь]оксатиин англ.: [1,4]Dioxino[2,3-b]oxathiine
основной компонент - азасилин
Пиримидо[4,5-Ь][1,4]азасилин англ.: Pyrimido[4,5-b][1,4]azasiline
Рис. 6.3.17
основной компонент - оксазол основной компонент - бензотиазол
[1,3]Тиазоло[5,4-<7][1,3]оксазол [1,3]Селеназоло[5,4-Л[1,3]бензотиазол
англ.: [1,3]rhiazolo[5,4-dJ[1,3]oxazole англ.: [1,3]Selenazolo[5,4-f][1,3]benzothiazole
Рис. 6.3.18
основной компонент - акридин Хино[4,3-Ь]акридин
англ.: Quino[4,3-b]acridine
Рис. 6.3.19
основной компонент - пиридазин (1,2 предпочтительней чем 1,4) Пиразино[2,3-с1]пиридазин
англ.: Pyrazino[2,3-d]pyridazine
основной компонент - [1,2,3]-оксатиазол
(1,2,3 предпочтительней чем 1,3,2)
ЗН,5Н-[} ,3,2]Оксатиазоло[4,5-сО[1,2,3]оксатиазол англ.: ЗН,5Н-[1,3,2]Oxathiazolo[4,5-d][1,2,3]oxathiazole
Рис. 6.3.20
1020
Новый справочник химика и технолога
6.3.4. Гетеромостики
Как и в случае карбоциклических молекул (подразд. 6.2.6) гетероциклические соединения, одновременно содержащие конденсированные фрагменты и мостики, можно называть, добавляя к названию карбоциклического конденсированного соединения мостики с гетероатомами или добавляя к названию гетероциклического конденсированного соединения название соответствующего мостика с локантами, показывающими его положение. Префиксы простых гетеромостиков называют по эпи-системе:
- О---«эпокси» («ероху»),
-ОО------«эпидиокси» («epidioxy»),
— S---«эпитио» («epithio»),
- NH----«эпимино» («epimino»).
Префиксы сложных мостиков описывают группу атомов, которая может представлять собой только последовательность смежных простых мостиков. Их называют, как показано на примере следующего префикса: эпоксиметано = эпокси + метано = -О-СН2- Для некоторых мостиков правила IUPAC рекомендуют название без приставки «эпи»:
-NHNH- «диазано» («diazano»),
-N=N- «диазено» («diazeno»),
- N=NNH- «триаз[1]ено» («triazfl ]епо»),
- РН- «фосфано» («phosphano») и др.
Названия гетероциклических мостиков образуют из названий соответствующих гетероциклов, приведенных в табл. 6.11, путем добавления буквы «о». При необходимости перед названием мостика в квадратных скобках приводятся локанты свободных валентностей. В тех случаях, когда название мостика совпадает с названием компонента в методе конденсирования, к названию первого добавляют приставку «эпи».
о
эпоксирено англ:, epoxireno
[2,3]фурано англ: [2,3]furano
[2,3]эпипирано англ.. [2,3]epipyrano
[3,4]эпи[1,2,4]триазоло англ:. [3,4]epi[1,2,4]triazolo
Например:
6,9-Дигидро-6,9-[2,3]фуранопиримидо[5,4-Ь]хинолин англ: 6,9-Dihydro-6,9-[2,3]furanopyrimido[5,4-b]quinoline
6.3.5. «а»-Номенклатура
«а»-Номенклатура, или заменительная номенклатура, используется только для гетеромоноциклических систем с более чем десятью звеньями, простых (некон-денсированных) мостиковых систем и простых (некон-денсированных) спирогетероциклов (этот тип номенклатуры иногда удобен и при наименовании некоторых гетероатомных ациклических молекул (см. подразд. 6.1.2)). Для моногетероциклов с количеством звеньев менее десяти, даже в случае полностью насыщенных производных, используют систему Ганча — Видмана.
По «а»-номенклатуре название гетероциклической молекулы строится на основе родоначального названия карбоциклического аналога с добавлением префиксов («а»-обозначений) (название «а»-обозначение происходит от окончания «а» в префиксах гетероатомов (аза-, окса-, сила- и т. д.)) гетероатомов, перечисленных в табл. 6.13, и, если необходимо, цифровых локантов, указывающих их положение в цикле. Порядок перечисления префиксов и нумерация атомов в моногетероцик-лических системах проводится так же, как в системе Ганча — Видмана (разд. 6.3.2) (рис. 6.3.21).
В спирогетсроциклах сохраняется нумерация атомов карбоциклического аналога (рис. 6.3.22).
Если в конденсированном гетероцикле основным компонентом является моногетероцикл с более чем десятью звеньями, то этот компонент называют по «aw-номенклатуре, заменив в названии родоначального углеводорода суффикс «ан» на суффикс «ин» (рис. 6.3.23).
В приведенном ниже названии гетероциклического соединения использованы различные типы номенклатуры: «а» и спиро (7-фосфадиспиро[2.0.2.5|ундека-7,10-диен-9-илокси), Ганча — Видмана (3-фенил-оксазиридин-2-ил), метода конденсирования (пирроле! 1,2-с|хиназолин-2-карбоновая кислота метиловый эфир) (рис. 6.3.24).
1 -Т иа-7-аза-3,11 -дисилациклододекан англ.: 1-Thia-7-aza-3,11-disilacyclododecane
1 -Т иа-6-селена-8-аза-3,11 -дисилациклододекан англ.: 1-Thia-6-selena-8-aza-3,11-disilacyclododecane
Рис. 6.3.21
Современная номенклатура органических соединений
1021
14 15
3,11 -Диокса-7,14,15-тритиадиспиро[5.1.5.2]пентадекан англ.: 3,11 -Dioxa-7,14,15-trithiadispiro[5.1.5.2]pentadecane
Рис. 6.3.22
Оксепино[4,5-е][1,4,8,11]тетраазациклотетрадецин англ.: Oxepino[4,5-e][1,4,8,11]tetraazacyclotetradecine
Рис. 6.3.23
СО2Ме
Метиловый эфир 3-(3-фенилоксазиридин-2-ил)-9-(7-фосфадиспиро-[2.0.2.5]ундека-7,10-диен-9-илокси)пирроло[1,2-с]хиназолин-2-карбоновой кислоты
англ.: 3-(3-Phenyloxaziridin-2-yl)-9-(7-phosphadispiro[2.0.2.5]undeca-
7,10-dien-9-yloxy)pyrrolo[1,2-c]quinazoline-2-carboxylic acid methyl ester
Рис. 6.3.24
6.4. Элементы с переменной валентностью в органической номенклатуре (Х-обозначения)
Общий метод наименования органических родоначальных соединений, содержащих скелетные атомы, которые могут находиться в нескольких валентных состояниях, основан на Х-обозначении. При его использовании оперируют следующими понятиями.
Число связей (bonding number) «п» скелетного атома в родоначальном гидриде есть суммарное число валентных связей с соседними скелетными атомами и атомами водорода. Например,
SH2: n = 2; NH2-NH2: п = 3; PH4-NH-PH4 , для N: п = 3, для Р: п = 5; пиридин, для N: п = 3, для С: п = 4; SH6: п = 6 и т. д.
Число связей нейтрального скелетного атома в родоначальном гидриде считается стандартным, если оно равно следующим значениям: для В: п = 3; С, Si, Ge, Sn и Pb: n = 4; N, P, As, Sb и Bi: n = 3; O, S, Se, Те и Ро: n = 2; F, Cl, Вг, I и At: n = 1.
Нестандартное число связей нейтрального скелетного атома в родоначальном гидриде указывается с по
мощью символа Хп, где п — число связей. Если цифровой локант атома с нестандартным числом связей используется в названии стандартного родоначального гидрида, то символ Хп помещают сразу после этого локанта. В противном случае символ Хп с соответствующим локантом приводятся перед названием родоначального гидрида. Если в названии присутствует префикс «обозначенного водорода», то он предшествует Х-символу. При нумерации соединения с атомами в нестандартном валентном состоянии следуют обычным правилам, а если имеется выбор между атомами одного типа, атом в нестандартном валентном состоянии получает меньший локант (рис. 6.4.1).
Гидрированные системы с родоначальным названием, соответствующим максимально возможному числу некумулированных двойных связей, и содержащие атом(ы) с нестандартным числом связей, называют последовательно записывая перед основой названия префикс «дигидро» (или «тетрагидро» и т. д.) и символ(ы) Хп с соответствующими локантами (рис. 6.4.2).
1022
Новый справочник химика и технолога
SH4
Х4-Сульфан англ.'. X4-Sulphane
HS-SH4-SH Н4Р-РН3-РН4
2Х6-Трисульфан 1 Х5,2Х5,ЗХ5-Трифосфан англ.-. 2X6-Trisulfane англ.: 1X5,2X5,3X5-Triphosphane
2/7-5Х5-Фосфинино[3,2-Ь]пиран англ.: 2/7-5X5-phosphinino[3,2-b]pyran
1 Х4,5-Бензодитиепин англ.: 1 X4,5-Benzodithiepine
2/7-5Х4-Дибензотиофен англ.: 2H-5X4-dibenzothiophene
3/7-2Х4-Циклогепта[с]тиопиран англ.: 3/7-2X4-Cyclohepta[c]thiopyran
Рис. 6.4.1
3,4-Дигидро-1,ЗХ5-азафосфинин англ.: 3,4-Dihydro-1,3X5-azaphosphinine
Декагидро-1 Х4,4Х4-бензодитиин англ.: Decahydro-1 X4,4X4-benzodithiine
Рис. 6.4.2
6.5. Циклические соединения со смежными двойными связями (5-обозначения)
При описании смежных двойных связей в циклических родоначальных гидридах, названия которых обычно подразумевают наличие максимального числа некумулированных двойных связей, скелетный атом, который участвует в образовании более чем одной двойной связи, обозначается символом «п5с», где «п» -его цифровой локант, а «с» — арабская цифра, обозначающая число смежных двойных связей. Если этот скелетный атом имеет нестандартное число связей, то между его цифровым локантом и символом 5е помещают символ Хп (см. подразд. 6.4) (рис. 6.5.1).
После введения в родоначальную циклическую структуру смежных связей в остальной части структуры следует разметить максимально возможное число некумулированных двойных связей, принимая в расчет модифицированную валентность атомов с нестандартным числом связей. Атом кольца с числом связей 3 или более, связанный с соседними кольцевыми атомами только простыми связями и несущий один или несколько атомов водорода, указывается с помощью символа «обозначенный водород»:
а4 ц3 4/7-2Х452,1,3-Бензотиадиазин
1<-S англ.: 4Н-2Х452,1,3-Benzothiadiazine
N 2
852-Бензо[8]аннулен
англ.: 852-Benzo[8]annulene
1
2Х452,5Х452-Тиено[3,4-с]тиофен
англ.: 2X452,5X452-Thieno[3,4-c]thiophene
Рис. 6.5.1
Современная номенклатура органических соединений
1023
При наличии нескольких вариантов нумерации, после того как в соответствии с принципами, приведенными в подразд. 6.3.3.1, пронумерованы гетероатомы и учтена предпочтительность для нестандартных валентных состояний (в порядке уменьшения количества числа связей), наименьшие номера получают скелетные атомы с наибольшими значениями «с» в обозначении «8е», азатем положения с «обозначенным водородом»:
5/7-382-Тиофен, а не 2/7-452-тиофен англ:. 5/7-382-Th io phene
у меньший локант получает атом
6 z,SH серы X4, а не 7? и Х462, а не X4 S—N 3
5 4
6/7-1Х432, ЗХ4,5,7,2,4,6,8-Тегратиатетразоци н англ:. QH-Л Х462,ЗХ4,5,7,2,4,6,8-Tetrathiatetrazocine
6.6. Номенклатура ансамблей
Некоторым сложным молекулярным системам можно давать достаточно простые и короткие названия, используя так называемую номенклатуру ансамблей.
Если соединение состоит из двух или более идентичных циклических систем, соединенных друг с другом простыми или двойными связями (причем число таких связей на единицу меньше, чем число циклических систем, участвующих в объединении), то оно может быть названо с использованием номенклатуры ансамблей.
ансамбль
конденсированная система
Ансамбли двух идентичных циклических систем называют двумя способами:
а) добавляя префикс «би» к названию соответствующего циклического заместителя (при необходимости в круглых скобках);
б) добавляя префикс «би» к названию соответствующего родоначального гидрида (при необходимости в круглых скобках).
В настоящее время способ (б) не рекомендуется для наименования ансамблей, соединенных двойной связью. Для компонентов ансамбля сохраняется нумерация исходного углеводорода; места соединения получают
наименьшие возможные локанты, а набор локантов одного из компонентов помечается штрихами (рис. 6.6.1).
Неразветвленные ансамбли из трех или более идентичных циклических систем называют, добавляя префикс «тер», «кватер», «квинкве», «секси» и т. д. к названию родоначального гидрида, соответствующего повторяющейся единице. Как исключение неразветвленные ансамбли, состоящие из бензольных колец, называют, используя в качестве основы название соответствующего заместителя — «фенил» (рис. 6.6.2).
Номенклатура ансамблей применяется также для наименования соединений, состоящих из одинаковых циклических или ациклических компонентов, в которых заместителями являются только главные группы, и которые соединены между собой с помощью симметричных поливалентных замещающих групп. Такие молекулы можно назвать, последовательно перечисляя:
1) локанты, показывающие положение присоединения поливалентной замещающей группы к компонентам ансамбля;
2) название симметричной поливалентной грушгы [-СН2- «метилен», -О- «окси», -S- «сульфандиил»,
«имино», -N\ «нитрило» (см. также табл. 6.5,6.8)];
3) умножающую приставку «ди» или «три» и т. д.;
4) название основного компонента, включающее суффиксы главных групп.
При формировании названия ансамбля нумерация для основных компонентов и главных групп сохраняется. Если возможен выбор, то места присоединения поливалентной группы получают по возможности наименьшие локанты. Для того чтобы различать локанты идентичных компонентов, используются штрихи. При наличии выбора большее число штрихов добавляется к локантам компонента, имеющего наивысший локант в месте присоединения поливалентной группы. Название сложной симметричной поливалентной замещающей группы образуют, объединяя названия индивидуальных поливалентных групп, начиная с центральной, например,
—О—СН2—О— «метилендиокси»,
-СН2СН2-О-СН2СН2- «оксидиэтилен»,
O(CH2CH2-N ^)2 «оксибис(этиленнитрило)»
и т. д. (рис. 6.6.3).
Если наряду с главными функциональными группами компоненты содержат другие заместители, последние отражаются в названии с помощью соответствующих префиксов (рис. 6.6.4).
Номенклатура ансамблей не используется для соединений, в которых одинаковые фрагменты связаны несимметричными поливалентными группами, а также для соединений, в которых одинаковые фрагменты содержат различное число главных функциональных групп. В этих случаях используют заместительную номенклатуру.
1024
Новый справочник химика и технолога
1,1 ’-Би(циклопропилиден) англ.-. 1,1'-Bi(cylopropylidene)
(а) 1,Г-Би(циклобутил),
(б) 1,Г-би(циклобутан) англ.: (a) 1,r-Bi(cyclobutyl),
(б) 1,1'-bi(cyclobutane)
(а) 2,2'-Бипиридил,
(б) 2,2-бипиридин англ.: (a) 2,2'-Bipyridyl,
(б) 2,2'-bipyridine
Рис. 6.6.1
1,1':2', Г-Терциклопропан англ.: 1,1 ':2', 1 "-Т ercyclopropane
Бифенил англ.: Biphenyl
1,1':4',1 "-Терфенил англ.: 1 ,T:4',1"-Terphenyl
2,2':6',2":6",2"'-Кватерпиридин англ.: 2,2':6',2":6",2'"-Quaterpyridine
N(CH2COOH)3
Нитрилотриуксусная кислота англ.: Nitrilotriacetic acid
Рис. 6.6.2
4,4-Метилендибензальдегид англ.: 4,4-Methylenedibenzaldehyde
4,4'-Метилендиоксидипиридин-2-карбоновая кислота англ.: 4,4'-Methylenedioxydipyridine-2-carboxylic acid
Рис. 6.6.3
О 4-Хлор-2,4'-иминодибензойная кислота англ.: 4-Chloro-2,4'-inriinodibenzoic acid
Рис. 6.6.4
Современная номенклатура органических соединений
1025
6.7. Номенклатура фанов
Сложные полициклические соединения, состоящие из циклов и цепей, объединенных в линейные структуры, называют фанами, а объединенных в циклические структуры — циклофанами. В принципе, все эти структуры могут быть названы как мостиковые полициклические соединения. Однако при таком подходе (используется в Chemical Abstracts) даже близкородственные соединения часто имеют абсолютно непохожие названия, в которых без «расшифровки» не видны важные составные части молекулы. Поэтому для такого сорта соединений была разработана специальная номенклатура, лишенная указанных недостатков.
Номенклатура фанов представляет собой адаптацию заместительной номенклатуры к построению названий сложных органических соединений из названий составных частей молекулы.
Основные операции номенклатуры фанов, предложенной IUPAC, проиллюстрированы на схеме 6.8.
Операция, переводящая левую структуру в правую, называется упрощением (simplification) фана; обратная операция называется усложнением (amplification) или восстановлением фана. Операция упрощения представляет собой первый шаг к формированию родоначального названия фана, при которой важные с точки зрения номенклатуры сегменты сложной циклической структуры заменяются одним «атомом», называемым суператомом (в упрощенной структуре Б суператомы помечены жирными точками в положениях 1 и 4). Соответствующие локанты (в данном случае 1,4) называются локантами суператомов.
Структура Б называется упрощенным скелетом фана, который определяет упрощенное скелетное название; локанты в этом скелете, называемые скелетными локантами, являются первичными локантами для фанового родоначального гидрида.
Многоатомные структурные единицы, замещающие супсратом при процедуре усложнения, называют ам-плификантами (в структуре А амплификантами являются шестизвенные циклы). В родоначальном названии фана их выражают с помощью амплификационных префиксов. Каждый амплификант имеет нумерацию соответствующей циклической системы (амплифика-ционные локанты показаны в структуре А нежирными курсивными цифрами). Амплификационные локанты атомов, к которым присоединены помеченные стрелками связи, называются локантами присоединения.
6.7.1. Компоненты родоначальных названий фанов
6.7.1.1. Упрощенные скелетные названия
Упрощенное скелетное название состоит из слова «фан», которому предшествует название упрощенного родоначального скелета. Порядок всех связей, выраженных упрощенным скелетным названием, предполагается равным единице. Согласно конвенции атомы, не являющиеся суператомами, представляют собой четырехвалентные атомы углерода. Напротив, валентность суператомов не фиксирована; они никогда не имеют связей иных, чем их скелетные связи.
Суператому(ам) упрощенного скелетного названия присваивается наименьший из возможных локантов (наименьший набор локантов) для данного скелета.
6.7.1.2. Неразветвленные ациклические (моноциклические) упрощенные скелеты
Название неразветвленных ациклических (моноцик-лических) упрощенных скелетов состоит из умножающей приставки «три», «тетра» и т. д., указывающих число атомов в цепи (цикле), за которым следует слово «фан» («циклофан»). Атомы цепи (цикла) нумеруются последовательно так, чтобы суператомы получили наименьшие номера (рис. 6.7.1).
Исходная структура А
упрощение усложнение
Упрощенная структура Б (• - суператом)
Схема 6.8
нонафан
циклогептафан
• - суператом
Рис. 6.7.1
1026
Новый справочник химика и технолога
6.7.1.3. Полициклические упрощенные скелеты
Название упрощенных скелетов, которые содержат суператомы в узловых положениях (голове моста), но не содержат суператомов в спиро-положсниях, образуются в соответствии с принципами расширенной системы Байера для мостиковых соединений. Узлы нумеруются так, чтобы суператомы получили наименьшие возможные номера.
Бицикло[8.6.0]гексадекафан
англ.-. Bicyclo[8.6.0]hexadecaphane
6.7.1.4. Полициклические упрощенные скелеты с суператомами в спиро-положениях
Название упрощенных скелетов, содержащих суператомы в спиро-положениях, но без суператомов в узловых положениях мостиковых структур, образуются в соответствии с обычными правилами наименования спиро-углеводородов, включающих только моноцикли-ческие компоненты. Атомы нумеруются так, чтобы суператомы получили, по возможности, наименьшие номера (рис. 6.7.2).
Спиро[5.7]тридекафан англ.-. Spiro[5.7]tridecaphane
Триспиро[5.2.2.612.39.26]трикозафан англ.-. Т ri sp i го[5.2.2.612.39.26]tricosaphane
Рис. 6.7.2
6.7.1.5. Амплификационные префиксы
Амплификационные префиксы, соответствующие многоатомным циклическим фрагментам структуры (суператомам), помещают непосредственно перед названием упрощенного скелета. Название амплификаци-онного префикса образуют из названия соответствующего циклического родоначального гидрида путем добавления окончания «а» с сохранением нумерации, например, «бензола», «пиридина» и т. п.
Амплификанты, встречающиеся несколько раз в родоначальном скелете фана, отражаются в названии с помощью умножающих приставок («ди», «три», и т. д., «бис», «трис» и т. д.), добавляемых к амплификацион-ному префиксу. Причем необязательно, чтобы идентичные амплификанты имели одинаковые локанты присоединения.
Для образования названий амплификационных префиксов нельзя использовать:
1) названия с префиксами «гидро», такие как 9,10-дигидроантрацен, или с суффиксами типа «ен», как в циклогексене;
2) названия типа «спироби», как в «1,Г-спиро-би[индене]», названия спироциклических систем с по крайней мере одним конденсированным или полициклоалкановым компонентом, таким как «спиро[1,3-диоксан-2, Г-инден]»;
3) названия ансамблей, таких как «2,2'-бинафта-лин»;
4) названия колец с использованием «а»-номенкла-туры, например, 1 -азабицикло[2.2.2]октан;
5) названия с заместительными суффиксами, такими как «ол», «он», «илий» и т. п.;
6) названия с замещающими префиксами, такими как «этил», «дибром» и т. д.;
7) названия замещенных колец или циклических систем, таких как «толуол», «анизол», «анилин»;
8) названия частично гидрированных конденсированных циклов, таких как «индан».
6.7.1.6. Порядок цитирования амплификационных префиксов
Порядок цитирования двух или более амплификационных префиксов в родоначальном названии фана определяется следующим порядком старшинства циклов и циклических систем:
а) все гетроциклы старше карбоциклов (пиридин > > фенантрен);
б) старше гетероциклы с гетероатомами в следующем порядке:
N>O>S>Se>Te>P>As>Sb>
>Bi > Si > Ge > Sn > Pb > В (пирролидин > фуран > тиофен);
в) старшим является циклическая система с большим числом циклов
(хинолин > пиридин; фенантрен > нафталин > бензол);
г) старшим является цикл или циклическая система с большим числом атомов в наибольшем цикле
(нафталин > инден; пиридин > 1,2-оксазол):
д) старшим является цикл или циклическая система с большим числом гетероатомов любого сорта
(пиримидин > пиридин; 1,2,5-оксадиазол > пиррол);
е) старшим является менее гидрогенизированный цикл или циклическая система (пиридин > пиперидин; бензол > циклогексан).
Современная номенклатура органических соединений
1027
Следует иметь в виду, что выбор старшей циклической системы следует проводить последовательно, начиная с пункта а).
6.7.1.7. Локанты суператома и локанты присоединения
Локанты суператома и локанты присоединения помещаются перед амплификационным префиксом, причем первым располагается локант суператома, за которым следуют локанты присоединения в круглых скобках. Например, в названии «3(5,2)-пиридина-1(3,1)-пиперидина-6(3,1 )-нафталинациклононафан» локанты 3, 1,6 — локанты суператомов, а (5,2), (3,1), (3,1) — локанты присоединения для трех амплификантов (рис. 7.3).
Амплификационным префиксам с умножающими приставками должно предшествовать соответствующее число локантов суператомов, которые приводятся в возрастающем порядке (рис. 6.7.4).
В тех случаях, когда одинаковые амплификанты имеют одинаковые локанты присоединения, последние приводятся один раз у соответствующего набора суператомов в возрастающем порядке (рис. 6.7.5).
Первым в скобках приводится локант присоединения, который является соседним к меньшему локанту упрощенного скелета фана. По возможности амплифи-кант нумеруется таким образом, чтобы наименьший локант присоединения был соседним с наименьшим локантом упрощенного скелета. Положение заместителей в амплификантах указывается с помощью сложного локанта, состоящего из локанта суператома соответствующего амплификанта с надстрочным индексом, обозначающим его положение в амплификанте (амплифи-кационный локант) (рис. 6.7.6).
Упрощенный скелет ( • - суператом)
3(5,2)-Пиридина-1(3,1)-пиперидина-6(3,1)-нафталинацикпононафан-4-ен англ.-. 3(5,2)-Pyridina-1(3,1)-piperidina-6(3,1)-naphthalenacyclononaphan-4-ene
Рис. 6.7.3
1 (1,3).4(1,4)-Дибензолациклогепгафан Упрощенный скелет
англ:. 1(1,3), 4(1,4)-Dibenzenacycloheptaphane (• -суператом)
Рис. 6.7.4
2,4,6,8-Тетрааза-1,9(1),3,5,7(1,4)-пентабензоланонафан англ:. 2,4,6,8-Tetraaza-1,9(1),3,5,7(1,4)-pentabenzenanonaphane
Г2 I Ч 6 7 8 ^
Упрощенный скелет
( • - суператом, X - гетероатом)
Рис. 6.7.5
1028
Новый справочник химика и технолога
Упрощенный скелет
( • - суператом)
4,66-Дибром-12,34-дихлор-1(4)-пиримидина-3,6(5,2),9(3)-трипиридинанонафан
англ.: 4,66-Dibromo-12,34-dichloro-1(4)-pyrimidina-3,6(5,2),9(3)-
tripyridinanonaphane
Рис. 6.7.6
6.7.2. Примеры названий и нумерации фанов
13
Упрощенный скелет
( • - суперагом, X - гетероатом)
7-Окса-1 -аза-17(5,2)-пиридина-5(4,2)-фурана-13(4,2)-тиофенабицикло[8.5.3]октадекафан
англ.: 7-Оха-1-aza-17(5,2)-pyridina-5(4,2)-furana-13(4,2)-
thiophenabicyclo[8.5.3]octadecaphane
8 9
Упрощенный скелет
( • - суператом)
1(5,8)-Хинолина-4(2,5)-пиридина-7(4,1)-фенантренациклононафан англ.: 1 (5,8)-Quinolina-4(2,5)-pyridina-7(4,1)-phenanthrenacyclononaphane
Упрощенный скелет
( • - суператом)
1(4,2,6),10(2,4,6)-Дипиридина-12(1,3)-Ьензопабицикло[8.6.0]гексадекафан англ.: 1(4,2,6),10(2,4,6)-Dipyridina-12(1,3)-benzenabicyclo[8.6.0]hexadecaphane
Современная номенклатура органических соединений
1029
3,15(1Л).6(1Д2,5),9(1,2Л4)^2(1Л2/)-Пентабензолатриспиро-[5.2.2.612 З9. 26)грикозафан
англ:. 3,15(1,4),6(1,4,2,5),9(1,2,5,4),12(1,5,2,4)-Pentabenzenatrispiro-
[5.2.2.612.39.26]tricosaphane
(• - суператом)
Таким образом, при составлении названия фана рекомендуется придерживаться строгой последовательности действий:
1. Рассортировать гетероциклические амплификанты на два типа:
а) амплификанты, которые могут быть названы как гетероциклы (следуя пунктам 2-7) без использования «а»-номенклатуры;
б) амплификанты, называемые с помощью «а»-номенклатуры. Последние должны быть названы как углеводороды (следуя пунктам 2-7) и затем модифицированы в пункте 8 с помощью «а»-номенклатуры.
2. Упростить молекулу для получения упрощенного скелета фана.
3. Пронумеровать упрощенный скелет фана так, чтобы суператомы получили наименьшую последовательность локантов.
4. Назвать и пронумеровать амплификанты, учитывая пункт 1 и принципы наименьшей последовательности локантов (см. подразд. 6.1.3.1).
5. Назвать фановый родоначальный гидрид, если нет вариантов для нумерации упрощенного скелета или амплификантов.
6. Выбрать нумерацию для симметричного упрощенного скелета фана в соответствии со следующими критериями, применяя их последовательно до тех пор, пока не будет сделан однозначный выбор:
а) наименьшие локанты для старших амплификантов;
б) наименьшие локанты для амплификантов с меньшими локантами присоединения.
7. Пронумеровать родоначальный фановый гидрид как целое.
8. Применить принципы «а»-номенклатуры для получения гетероциклического фанового гидрида.
Если после нумерации родоначального гидрида фана имеется выбор, то наименьшие локанты последовательно присваиваются:
1) гетероатомам, которые модифицируют скелет с помощью «а»-номенклатуры;
2) «обозначенному водороду»;
3) неотделяемым префиксам «гидро» или «дегидро»;
4) «суффиксным» главным функциональным группам;
5) двойным и тройным связям (выраженным с помощью инфиксов «ен» и «ин» или префиксами «гидро» и «дегидро»;
6) заместителям, выраженным префиксами (в алфавитном порядке).
При записи названий замещенных фанов следует придерживаться следующего порядка размещения аффиксов относительно названия родоначального гидрида:
1) отделяемые префиксы в алфавитном порядке;
2) неотделяемые «гидро» или «дегидро» префиксы;
3) неотделяемые заменительные «а»-префиксы;
4) название родоночального гидрида;
5) «ен» и «ин» инфиксы;
6) суффиксы главных функциональных групп (рис. 6.7.7а и 6.7.76).
О
6-Метил-3-метокси-15,16,17,18-тетрагидро-2-аза-
1,4(2,7)-динафталинациклогексафан-5-ен-14(11/-/)-он англ: 3-Methoxy-6-methyl-15,16,17,18-tetrahydro-2-aza-
1,4(2,7)-dinaphthalenacyclohexaphan-5-en-14(11/-/)-one
Рис. 6.7.7а
1030
Новый справочник химика и технолога
6 5
42-Бром-1,4(1,4)-дибензолациклогексан-2-ен-12-карбоновая кислота англ.: 42-Bromo-1,4(1,4)-dibenzenacyclohexaphan-2-ene-12-carboxylic acid
Рис. 6.7.76
6.8. Номенклатура функциональных производных углеводородов
В данном разделе представлены сведения по заместительной номенклатуре основных классов органических соединений, дополняющие положения, изложенные в подразд. 6.2. Кроме того, обсуждаются особенности построения радикало-функциональных названий соединений, которыми иногда бывает удобно пользоваться для некоторых функциональных производных углеводородов.
6.8.1. Галогенпроизводные
Для наименования галогенпроизводных кроме заместительной номенклатуры (названия типа 1-бром-6-хлоргептан) также широко используется и радикалофункциональная (рис. 6.8.1).
Удобство этих названий состоит в том, что они ясно подчеркивают главную химическую особенность сое
динений. Для тригалогенметанов сохранены тривиальные названия СНХ3: фтороформ (fluoroform) X=F, хлороформ (chloroform) Х=С1, бромоформ (bromoform) Х=Вг, йодоформ (iodoform) Х=1.
Заместительная номенклатура галогенпроизводных, в которых все атомы водорода замещены каким-либо одним галогеном, допускает использование префикса «пер» вместо умножающей приставки, например, «пер-хлорэтан» вместо «гексахлорэтана».
6.8.2. Спирты
Спирты — соединения, в которых гидроксильная группа присоединена к предельному атому углерода. В заместительной номенклатуре присутствие в молекуле гидроксильных групп -ОН обозначается суффиксом «ол», «диол» и т. д., если «-ОН» является старшей главной группой, в противном случае — префиксом «гидрокси» (рис. 6.8.2).
Бензилхлорид (рад.-ф.), (хлорметил)бензол (зам.) англ.: Benzyl chloride,
(chloromethyl)benzene
Этилендихлорид (рад.-ф.), 1,2-дихлорэтан (зам.) англ.: Ethylene dichloride,
1,2-dichloroethane
Бензилидендихлорид (рад.-ф.), (дихлорметил)бензол (зам.) англ.: Benzylidene dichloride, (dichloromethyl)benzene
Рис. 6.8.1
Пент-З-ен-1,2-диол англ.: Pent-3-ene-1,2-diol
Бицикло[4.1,0]гептан-3,4-диол англ.: Bicyclo[4.1,0]heptane-3,4-diol
2-Гидроксипент-4-еновая кислота англ.: 2-Hydroxypent-4-enoic acid
Рис. 6.8.2
Современная номенклатура органических соединений
1031
Следует отметить, что названия типа трет-бу-танол, встречающиеся в литературе, некорректны, поскольку в них суффикс «ол» модифицирует неправильное название алкана трет-бутан.
Для спиртов несложного строения иногда удобно использовать радикало-функциональные названия, например:
Бензиловый спирт англ.: Benzyl alcohol
-----ОН
mpem-Бутиловый спирт англ.: tert-Butyl alcohol
Для некоторых спиртов правила ШРАС допускают использование тривиальных названий (табл. 6.16).
6.8.3. Фенолы
Ароматические углеводороды с гидроксильной группой (или группами), непосредственно присоединенной к кольцу, относятся к классу фенолов. Их названия так же, как и названия спиртов, строятся на основе родоначального ароматического соединения с добавлением суффикса «ол». Для ряда фенолов правилами сохранены тривиальные названия (табл. 6.16), и они могут использоваться как родоначальные для построения названия их производных (рис. 6.8.3 и 6.8.4).
Таблица 6.16
Тривиальные и полусистематические названия гидроксисоединений и эфиров, разрешенные правилами IUPAC в качестве родоначальных
Допускается неограниченное замещение атомов водорода С6Н5-ОН — фенол (phenol)а) Допускается ограниченное замещение атомов водорода (только в кольце и только префиксными заместителями) С6Н5-ОСН3 — анизол (anisole)
Замещение атомов водорода не допускается б’в)
НО-СН2СН2-ОН — этиленгликоль (ethylene glycol), НО-СН2СН(ОН)СН2-ОН — глицерин (glycerol), С(СН2ОН)4— пентаэритрит (pentaeiythritol), (СН3)2С(ОН)-С(ОНХСНз)2 — пинаколин (pinacol),
он
(показан орто-изомер) Крезол (o-cresol)
Карвакрол (carvacrol)
Тимол (thymol)
Резорцин (resorcinol)
Гидрохинон (hydroquinone)
Пирокатехин
Пикриновая кислота (picric acid)
а) Для нафталинолов, антраценолов и фенантренолов допускается использование сокращенных названий, соответственно, нафтол, антрол и фенантрол с соответствующим локантом, например, 2-нафтол.
б) Допускается замещение атома водорода гидроксильной группы, которое может быть рассмотрено как функционализация, например, образование сложного эфира.
в) Ранними версиями правил IUPAC допускалось также использование тривиальных названий ксиленол для моногидрокси производных изомерных ксилолов, пирогаллол — для бензол-1,2,3-триола, флороглюцин — для бензол-1,3.5-триола, стифнино-вая кислота — для 2,4,6-тринитробензол-1,3-диола.
НО
2-Фтор-4-хлорфенол англ.: 4-Chloro-2-fluorophenol
3,4,5-Тригидроксибензойная кислота англ.: 3,4,5-Trihydroxybenzoic acid
Рис. 6.8.3
1032
Новый справочник химика и технолога
Бифенил-2,4,6,3* 1,5'-пентаол англ.: Biphenyl^AS.S'.S'-pentaol
Рис. 6.8.4
Названия солей спиртов и фенолов образуют, объединяя название катиона металла с названием соответствующего аниона (см. подразд. 6.12.3).
6.8.4. Простые эфиры
Названия простых эфиров, а также их S-, Se- и Те-аналогов формируют, используя одну из трех номенклатур: радикало-функциональную, заместительную или заменительную (см. подразд. 6.1.2).
В несложных случаях для простых эфиров (ethers) (особенно в устной речи) удобно применять радикалофункциональные названия. Для симметричных эфиров в названии указывается углеводородная ipynna с мно
жительным префиксом «ди» с добавлением слова «эфир». В названии несимметричных эфиров замещающие группы, связанные с кислородом, перечисляются в алфавитном порядке (рис. 6.8.5).
Наиболее общим является заместительный подход, согласно которому к родоначальному гидриду добавляют префикс группы RO-. Такие префиксы образуют, добавляя окончание «окси» к заместительному префиксу группы R-, например, СН3(СН2)5-О---гексилокси,
СН3(СН2)5СН(СН3)-О----1-метилгептилокси. Для ряда
заместителей RO- правила IUPAC разрешают использование сокращенных префиксов (табл. 6.17).
Диизопропиловый эфир англ: Diisopropyl ether
Пропил этиловый эфир англ:. Ethyl propyl ether
Винилэтиловый эфир англ:. Ethyl vinyl ether
Рис. 6.8.5
Таблица 6.17
Сокращенные названия префиксов алкоксизаместителей RO-, разрешенные правилами IUPAC
Допускается неограниченное замещение атомов водорода
СН3О-----метокси (methoxy); СН3СН2О----этокси (ethoxy); СН3СН2СН2О----пропокси (propoxy);
СН3СН2СН2СН2-О-------бутокси (butoxy); С6Н5О--фенокси (phenoxy)
Замещение атомов водорода не допускается
(СН3)2СНО-----изопропокси (isopropoxy); (СН3)2СНСН2О---изобутокси (isobutoxy);
СН3СН2СН(СН3)О------вшор-бутокси (^ec-butoxy); (СН3)3СО--шреш-бутокси (ZerZ-butoxy)
Вг
5-Фе нокси п и р и д и н-2-ол англ: 5-Phenoxypyridin-2-ol
О
1 -(2-Бромэтокси)пропан англ: 1-(2-Bromoethoxy)propane
Cl
1-(вл?ор-Бутоксиметил)-2-хлорциклопропан англ: 1 -(sec-Butoxymethyl)-2-chlorocyclopropane
Современная номенклатура органических соединений
1033
6.8.5. Гидропероксиды и пероксиды
Соединения, содержащие гидропероксигруппу R-O-ОН, называют, помещая префикс «гидроперокси» перед названием родоначального гидрида, соответствующего группе R, или по радикало-функциональной номеклатуре, помещая префикс группы R перед названием класса «гидропероксид» (рис. 6.8.6).
Пероксиды R-O-O-R' называют, помещая префикс «R-перокси» перед названием родоначального гидрида, соответствующего группе R', или по радикало-функциональной номеклатуре, помещая префикс группы R и R' в алфавитном порядке перед названием класса «пероксид» (рис. 6.8.7).
6.8.6. Альдегиды
Альдегидами называют соединения, содержащие группу -СНО, присоединенную к атому углерода. Названия альдегидов составляются по одному из следующих правил:
1. К названию ациклического углеводорода добавляют суффикс «аль» (или «диаль» для диальдегидов). В этом случае карбонильный атом углерода, с которого начинается нумерация, входит в состав родоначального углеводорода (рис. 6.8.8).
2. К названию ациклического или циклического углеводорода или гетероцикла для обозначения присое
динения формильной группы -СНО добавляется суффикс «карбальдегид» (рис. 6.8.9а и 6.8.96).
3. В тривиальных названиях кислот (табл. 6.19-6.21) окончание «овая кислота» (или «ойная кислота») изменяют на окончание «овый (ойный) альдегид» (рис. 6.8.10).
Уксусный и бензойный альдегиды имеют альтернативные названия — «ацетальдегид» («acetaldehyde») и «бензальдегид» («benzaldehyde»).
Тривиальное название альдегида ОНС-СНО соответствующего щавелевой кислоте, — «глиоксаль» («glyoxal»), акрилового альдегида, — «акролеин» («acrolein»), а альдегида, соответствующего пирослизевой кислоте (2-фуранкарбоновой кислоте), — «фурфурол» («furfural»). Ранее, кроме того, для некоторых альдегидов широко использовались тривиальные и по-лусистематические названия, например:
Ванилин Пиперональ
англ:. Vanillin англ: Piperonal
ООН
1-Гидроперокси-1Н-инден или 1/7-инден гидропероксид англ: 1-Hydroperoxy-1H-indene или 1 H-inden-1 -yl hydroperoxide
Рис. 6.8.6
2-Метилпероксинафталин или метил-2-нафтилпероксид англ: 2-Methylperoxynaphthalene или methyl 2-naphthyl peroxide
Рис. 6.8.7
Бутан англ: Butane
Бутаналь англ: Butanal
2-(Формилметил)гептандиаль англ: 2-(Formylmethyl)heptanedial
Рис. 6.8.8
1034
Новый справочник химика и технолога
Бутан-1,2,4-трикарбальдегид Циклопропанкарбальдегид
англ:. Butane-1,2,4-tricarbaldehyde англ: Cyclopropanecarbaldehyde
Т иофен-2-карба льдегид англ: Thiophene-2-carbaldehyde
Циклопента-3,5-диен-1,3-дикарбальдегид англ: Cyclopenta-3,5-diene-1,3-dicarbaldehyde
Рис. 6.8.9
Глутаровый альдегид англ: Glutaraldehyde
транс-Коричный альдегид англ: frans-Cinnamaldehyde
Рис. 6.8.10
6.8.7. Кетоны
Кетонами называют соединения, содержащие карбонильную группу, соединенную с двумя атомами углерода. В заместительной номенклатуре кетонов группа (=0) обозначается суффиксом «он» или префиксом «оксо», в зависимости от того, является ли эта группа старшей среди остальных суффиксных групп соединения или нет. При наименовании соединений, содержащих несколько кетонных карбонильных групп, используют соответствующие умножающие приставки. При использовании радикало-функциональной номенклатуры названия соединений этого класса составляют путем добавления к слову «кетон» названий заместителей у >00 функции в алфавитном порядке.
1-Фенилбутан-2-он (зам.), бензилэтилкетон (рад.-ф.) англ: 1-Phenylbutan-2-one или benzyl ethyl ketone
4-Оксопентаналь англ: 4-Oxopentanal
Циклогексан-1,3-дион англ: Cyclohexane-1,3-dione
При формировании названий циклических кетонов иногда необходимо показать атомы водорода, которые добавляются к структуре при использовании суффикса «он». Это можно сделать двумя способами:
1) с помощью особого типа «обозначенного водорода», называемого «добавленный водород», который обычно указывается в круглых скобках после локанта, показывающего положение суффикса «он»;
2) с помощью неотделяемого префикса «дигидро», «тетрагидро» и т. д. (рис. 6.8.11).
Для ряда кетонов допускается использование тривиальных и полусистематических названий (табл. 6.18).
Дикетоны, получающиеся из циклических родоначальных гидридов с максимальным числом некумулированых двойных связей путем замены -СН= групп на группы >С=0 с перегруппировкой двойных связей до хиноидной структуры, могут быть названы путем добавления суффикса «хинон» («quinone») с соответствующими локантами к имени родоначального гидрида (рис. 6.8.12).
Нафталин-1 (2/-/)-он англ: Naphthalen-1 (2Н)-опе
3,7-Дигидро[1,6]нафтиридин-4,8-дион англ: 3,7-Dihydro[1,6]naphthyridine-4,8-dione
Рис. 6.8.11
Современная номенклатура органических соединений
1035
2
Хризен-5,6-дион или хризен-5,6-хинон
О англ:. Chrysene-5,6-dione или chrysene-5,6-quinone
Рис. 6.8.12
Таблица 6.18
Тривиальные и пол у систематические названия карбонильных производных, разрешенные правилами IUPAC
Допускается неограниченное замещение атомов водорода
Ацетон* а) (acetone)
н2С=С=о
Кетен (ketene)
(показан п-изомер)
Бензохинон (benzoquinone)
(только \,2-изомер)
о
(показан 1,4-изомер)
о
(показан 9,10-изомер)
Аценафтехинон (acenaphthoquinone)
Нафтохинон (naphthoquinone)
Антрахинон (anthraquinone)
Замещение атомов водорода не допускается
С6Н5-СО-СН3 — ацетофенон (acetophenone)6);
С6Н5-СО-СО-С6Н5 — бензил (benzil); C6H5-CO-C6H5 — бензофенон (benzophenone);
СН3-СО-СО-СН3 — биацетил (biacetyl); С6Н5-СН=СН-СО-С6Н5 — халкон (chaicone); С6Н5-СО-С2Н5 — пропиофенон (propiophenone)
а) Соответствующая замещающая группа СН3С(О)СН2- называется «ацетонил» («acetonyl»).
^Соответствующая замещающая группа С6Н5С(О)СН2- называется «фенацил» («phenacyl»).
6.8.8. Карбоновые кислоты
Заместительная номенклатура предусматривает два различных варианта построения названий карбоновых кислот. Выбор между ними определяется тем, включен ли углеродный атом карбоксильной группы в родоначальное название или нет. В первом случае в качестве суффикса в названии используется «овая кислота», во втором — «карбоновая кислота». Для ациклических карбоновых кислот, как правило, используется суффикс «овая кислота» (рис. 6.8.13).
Однако в некоторых случаях, например, для многоосновных кислот, где все карбоксильные группы в молекуле связаны одной цепочкой, рекомендуется употреблять суффикс «карбоновая кислота», не включая углеродные атомы карбоксильных групп в состав родоначального углеводорода. Это позволяет существенно упростить название, т. к. для всех карбоксильных групп используется только один суффикс (рис. 6.8.14).
Названия соединений, в которых карбоксильная группа непосредственно присоедина к циклу, образуют из названия родоначального гидрида и суффикса «карбоновая кислота», добавляя при необходимости соответствующие локанты и умножающую приставку (рис. 6.8.15).
В последнем примере (рис. 6.8.15) одна из карбоксильных групп включена в состав сложного заместителя в виде префикса «карбокси». При наличии в молекуле функциональной группы старшей, чем карбоксильная (см. табл. 6.7), последняя рассматривается как заместитель и также записывается в названии в виде префикса «карбокси». Необходимость в употреблении этого префикса может возникнуть при построении названий трех- и более основных карбоновых кислот с разветвленной углеводородной цепью (рис. 6.8.16).
Наряду с систематическими названиями карбоновых кислот для всех низших членов рядов моно- и дикарбоновых кислот используют тривиальные названия (табл. 6.19-6.22) (рис. 6.8.17).
1036
Новый справочник химика и технолога
В табл. 6.19 приведены тривиальные названия карбоновых кислот, рекомендуемые правилами IUPAC, в том числе и для использования в качестве родоначальных структур при образовании замещенных соединений и/или производных, таких как альдегиды, ацильные замещающие группы, галогенангидриды, гидразиды, амиды, имиды, нитрилы. Тривиальные названия остальных алифатических карбоновых и дикарбоновых кислот (табл. 6.20-6.22) не рекомендуется использовать для наименования их производных.
Тривиальные названия существуют также для многих непредельных, ароматических и гетероциклических кислот, например, кротоновая кислота (СН3-СН=СН-СООН). За исключением структур, представленных в табл. 6.19, в них не допускается замещение атомов водорода.
Многие непредельные карбоновые кислоты с количеством углеродных атомов 18, 20, 22 и 24 являются природными соединениями и поэтому также имеют тривиальные названия (табл. 6.22). В научной литературе наряду с систематическими и тривиальными названиями иногда используются две сокращенные системы обозначений этих соединений, не нашедшие официального признания. Первый тип обозначений, представленный в табл. 6.22, включает набор цифр и латинских курсивных букв. Например, запись «18:4 9с1П13Л5с» обозначает кислоту состава С18, содержащую четыре двойных связей, две из которых, при С9 и С15, имеют i/wc-конфигурацию, а другие две, при С11 и С13 — транс. Тройная связь обозначается буквой «а», а двойная связь неизвестной конфигурации — буквой «е».
5-Метил-3-оксогекс-4-еновая кислота англ.'. 5-Methyl-3-oxohex-4-enoic acid
ОН
2-Нитро-4-этилпентандиовая кислота англ.'. 2-Ethyl-4-nitropentanedioic acid
2-Карбоксиметилциклопропанкарбоновая кислота англ.: 2-Carboxymethylcyclopropanecarboxylic acid
СО2Н
НО2С
Рис. 6.8.15
1-Бензил-2-карбоксипиридинийхлорид англ.: 1-Benzyl-2-carboxypyridinium chloride
Рис. 6.8.16
Современная номенклатура органических соединений
1037
CI
Br
Cl
2| Г ОН
З1--4
Бром(2-хлорциклобутил)уксусная кислота Q 0
англ.: Bromo(2-chlorocyclobutyl)acetic acid
2-Хлормалоновая кислота
англ.: 2-Chloromalonic acid
Рис. 6.8.17
Таблица 6.19
Тривиальные названия карбоновых кислот, разрешенные правилами IUPAC для использования в качестве родоначальных структур
Допускается неограниченное замещение атомов водорода
Алифатические
СНзСООН Уксусная кислота (acetic acid* *) ^^.соон Акриловая кислота (acrylic acid) ноос^^соон Малоновая кислота (malonic acid*)
Алифатические
-XX. -СООН ноос Янтарная кислота (succinic acid*) ноос/Ч/соон Фумаровая кислота (fumaric acid) ноос^ /С°он Малеиновая кислота (maleic acid)
Ароматические
;оон
соон
Бензойная кислота (benzoic acid)
ноос соон
6
3
5
5
(показан \-изомер)
Нафтойная кислота (naphthoic acid) Jk -СООН
ноос соон 2
ноос'д5^ 2 з
Фталевая кислота (phthalic acid)
Изофталевая кислота (isophthalic acid)
Терефталевая кислота (terephthalic acid)
Замещение атомов водорода не допускается а)
Монокарбоновые кислоты
Н-СООН — муравьиная кислота (formic acid*);
СН3СН2-СООН — пропионовая кислота (propionic acid*); НСЬС СООН — пропиоловая кислота (propiolic acid*); СН3СН2СН2-СООН — масляная кислота
(butyric acid*); (СН3)2СНСН2-СООН — изомасляная кислота (isobutyric acid*); СН2=С(СН3)-СООН — метакриловая кислота (methacrylic acid); CH3(CH2)i4-COOH — пальмитиновая кислота (palmitic acid); CH3(CH2)i6-COOH — стеариновая кислота (stearic acid);
C6H5-CH=CH-COOH — коричная кислота (cinnamic acid)
Дикарбоновые кислоты
НООС-СООН — щавелевая кислота (oxalic acid*);
НООС-(СН2)з-СООН — глутаровая кислота (glutaric acid*);
НООС-(СН2)4-СООН — адипиновая кислота (adipic acid);
НООС^СН2)7-СН=СН-(СН2)7-СООН — олеиновая кислота (oleic acid)
* См. текст в подразд. 6.8.8.2.
а) Допускается замещение атома водорода карбоксильной группы, которое может быть рассмотрено как функционализация, например, образование сложного эфира и т. д.
1038
Новый справочник химика и технолога
Таблица 6.20
Тривиальные названия монокарбоновых кислот R-CO2H (с неразветвленным заместителем R), включая нерекомендуемые правилами IUPAC
Число С-атомов Название кислоты Число С-атомов Название кислоты Число С-атомов Название кислоты
1 Муравьиная 8 Каприловая # 18 Стеариновая #
2 Уксусная 2) 9 Пеларгоновая # 20 Арахидоновая #
3 Пропионовая 3) 10 Каприновая # 22 Бегеновая #
4 Масляная 4) 12 Лауриновая # 24 Лигноцериновая #
5 Валериановая 14 Миристиновая # 26 Церотиновая #
6 Капроновая # 16 Пальмитиновая # 28 Монтановая #
7 Энантовая # 17 Маргариновая # 30 Мелиссовая #
#Не рекомендуются правилами IUPAC 1993 г.
’’ Название карбоксилата — формиат.
2) Название карбоксилата — ацетат.
3) Название карбоксилата — пропионат.
4) Название карбоксилата — бутират.
Таблица 6.21
Тривиальные названия дикарбоновых кислот НО2С-(СН2)И-СО2Н и их карбоксилатов, включая нерекомендуемые правилами IUPAC
Число С-атомов Название кислоты Название карбоксилата Число С-атомов Название кислоты
2 Щавелевая Оксалат 7 Пимелиновая #
3 Малоновая Малонат 8 Субериновая #
4 Янтарная Сукцинат 9 Азелаиновая #
5 Глутаровая Глутарат 10 Себациновая #
6 Адипиновая Адипинат
#Не рекомендуются правилами IUPAC 1993 г.
Тривиальные названия непредельных карбоновых кислот
Таблица 6.22
Тривиальное название кислоты Сокращенное обозначение Формула
Элаидиновая 18:1 9/ 9 1
Вакценовая 18:1 ИГ и 1 ^/Х^^/Х^^^хг^Х^хХх^^Х/Х^хХ^^СОгН
Олеиновая 18:1 9с 18 9 1со н
Тарировая 18:1 6а 18 6 и —==—XZ\>°2H
Крепениновая 18:2 9с12а 18X4ZX 12
Линолевая 18:2 9с12с 12 Q 18
Линэлаидиновая 18:2 9/12/ 9 18/X/\/4/X4XzXzX/X/C02H 12
Календовая 18:3 8/10/12с 12 10 8
Современная номенклатура органических соединений
1039
Окончание табл. 6.22
Тривиальное название кислоты Сокращенное обозначение Формула
Катал повая 18:3 9/1П13С 18 13 11 . Л. 1СО2Н
а-Линоленовая 18:3 9с12с15с 18 15 12 9 х 1СО2Н
у-Линоленовая 18:3 6с9с12с 18 12 9 6 ^СО2Н
Элеостеариновая 18:3 9 с 11/13/ 18 13 11 9 1СОэН
Паринаровая 18:4 9cl 1/13/15с 18/ 15 13 11 9 1СОэН
Арахидоновая 20:4 5с8с11с14с 2CI/-X. 14 11 8 5 ^^СО2Н
Эруковая 22:1 13с 22 13 .. 1СОоН
Нервоновая 24:1 15с 24 15 1
Вторая система обозначений касается природных полиеновых кислот с метиленразделенными цис-двойными связями. Для их обозначения достаточно указать цифрами только положение первой двойной связи, их число и общее количество атомов углерода в молекуле. Отсчет положения первой двойной связи производится в отличие от предыдущей системы обозначений не от карбоксильной группы, а от со-ме-тильного атома углерода. Например, запись «20:4 соб» обозначает арахидоновую кислоту (табл. 6.22), которая содержит цепочку из 24 атомов углерода с четырьмя метиленразделенными г/цс-двойными связями, начинающимися с шестого атома от концевой метильной группы. Подчеркнем, что такой подход не рекомендуется правилами IUPAC.
6.8.8.1. Замещенные карбоновые кислоты (Аминокислоты см. подразд. 6.16.3.1)
Гидрокси-, алкокси- и оксокислоты
Систематические названия гидрокси-, алкокси- и оксокислот образуют в соответствии с общими правилами заместительной номенклатуры, используя префиксы «гидрокси», «алкокси», «оксо» и «формил». Тривиальные названия гидрокси- и оксокарбоновых кислот, разрешенные правилами IUPAC приведены в табл. 6.23.
Более ранние версии правил 1UPAC допускали использование и других тривиальных названий замещенных кислот (табл. 6.24), которые до сих пор встречаются в литературе.
Таблица 6.23
Тривиальные названия гидрокси- и оксокарбоновых кислот, разрешенные правилами IUPAC (замещение атомов водорода не допускается)а)
но^^соон Гликолевая кислота (glycolic acid) \—СООН но Молочная кислота (lactic acid) Dh ОН Ph\l У—СООН Рп Бензиловая кислота (benzilic acid)
ОН .СООН ноос ОН Винная кислота (tartaric acid) НООС ОН НООС^У*^СООН Лимонная кислота (citric acid) СООН НО—< '—ОН Глицериновая кислота (glyceric acid)
о^^соон Глиоксиловая кислота (glyoxylic acid) \^СООН О Пировиноградная кислота (pyruvic acid) О ^JL^COOH Ацетоуксусная кислота (acetoacetic acid)
а) Допускается формальное замещение атома водорода карбоксильной группы, которое может быть рассмотрено как функционализация, например, образование сложного эфира и т. п.
1040
Новый справочник химика и технолога
Таблиц 6.24
Тривиальные названия некоторых гидрокси-, алкокси- и оксозамещенных карбоновых кислот
Систематическое название кислоты Тривиальное название кислоты Формула
он
Г идроксипропандиовая тартароновая (tartaronic) но2с ^Х''СО2Н
О
Оксопропандиовая мезоксалевая (mesoxalic) но2с ^ТО2Н
он
Г идроксибутандиовая яблочная (malic) но2сх 'Х^ЧСО2Н
ДЭН
З-Гидрокси-2-фснилпропановая троповая (tropic) Phx т:о2н
s.CO2H
2-Г идроксибензойная салициловая (salicylic) || 'дэн
Х^/С°2Н
4-Метоксибензойная анисовая (anisic) Н3ССГ ^^со2н
4-Гидрокси-З-метоксибензойная ванилиновая (vanillic) нет" ОСН3
х^/С°2Н
3,4-Диметоксибензойная вератровая (veratric) Н3ССГ ОСНз
^.СО2Н
3,4-Метилендиоксибензойная пиперониловая (piperonylic) с> 7 V— о ^,СО2Н
3,4-Д игидроксибензойная протокатеховая (protocatechuic) но^4 он
2,5-Дигидроксибензойная гентизиновая (gentisic) НО^. <^/СО2Н
^тэн
^.СО2Н
3,4,5-Тригидроксибензойная галловая (gallic) НО'^''"
он
Н3СО ^,СО2Н
4-Гидрокси-3,5-диметоксибензойная сиреневая (syringic) но-^ ОСНз
/^^С02Н
(Е)-3-(4-Гидроксифенил)проп-2-еновая н-кумаровая (/7-coumaric) С:
Современная номенклатура органических соединений
1041
Окончание табл. 6.24
Систематическое название кислоты Тривиальное название кислоты Формула
ХСО2Н
(£)-3-(3,4-Дигидроксифенил)проп-2-еновая кофейная (caffeic) нох ОН ХСО2Н
(£)-3 -(4-Гидрокси-3 -метоксифенил)проп-2-еновая феруловая (ferrulic) но^ ОСН3
6.8.8.2. Производные карбоновых кислот
Соли карбоновых кислот
Название солей карбоновых кислот образуют на основе названия соответствующей кислоты, заменяя суффикс «овая кислота» на суффикс «оат» или суффикс «-карбоновая кислота» — на суффикс «карбоксилат» и добавляя название катиона; при необходимости используются умножающие префиксы (рис. 6.8.18).
Кислые соли полиосновных кислот называют аналогично нейтральным солям, обозначая оставшиеся атомы водорода словом «водород», «диводород» и т. д., помещаемым между названием катиона и аниона (рис. 6.8.19).
В тех случаях, когда карбоксилатные функции нельзя отразить в названии одним суффиксом с умножающей приставкой, а также в тех случаях когда в соединении присутствует функциональная группа более высокого старшинства, используется префикс «карбоксилате» (рис. 6.8.20).
В качестве альтернативных названий солей карбоновых кислот в русском языке используют выражения со словом «соль», например: «калиевая соль бензойной кислоты» или «калиевонатриевая соль пентандиовой кислоты».
О’ Na
О
О’ nh4
Натрия 3-метилпентаноат англ.-. Sodium 3-methylpentanoate
Аммония циклобутанкарбоксилат англ.: Ammonium cyclobutanecarboxylate
О
К+ О2с'
Калия натрия бутандиоат англ.-. Potassium sodium butanedioate
О’ РЬ2+ О
Свинца диацетат англ.-. Lead diacetate
НО'
Калия водород гександиоат Na 0 англ.-. Potassium hydrogen hexanedioate
О. ЮН
ОН
О
Натрия диводород цитрат англ.-. Sodium dihydrogen citrate
Рис. 6.8.19
СО2 К+
Дикалия 2-карбоксилаггоциклогексанацетат
OQ- к+ англ:. Dipotassium 2-carboxylatocyclohexane acetate
О
Рис. 6.8.20
1042
Новый справочник химика и технолога
Эфиры карбоновых кислот
Названия сложных эфиров (esters) образуют, записывая название замещающей группы в «спиртовой» части молекулы перед названием кислоты, в котором суффикс «овая кислота» заменяют на суффикс «оат» или суффикс «карбоновая кислота» — на суффикс «карбоксилат», например, СН3СН2О-С(О)СНз этилацетат. Следует обратить внимание на то, что в русском языке название эфиров пишутся слитно, в то время как в английском языке — раздельно. При написании русского названия эфира замещенной карбоновой кислоты, включающего локанты, название «спиртовой» части молекулы пишется в начале названия через дефис (рис. 6.8.21). Однако если в «спиртовой» части молекулы содержатся заместители, то подобная форма записи русского названия приводит к путанице: название «спиртового» фрагмента «сливается» с префиксами заместителей в «кислотной» части молекулы (в английском варианте этого удается избежать в силу раздельного написания названия). В этих случаях название эфира рекомендуется записывать в виде «... эфир ... кислоты» (рис. 6.8.22).
При наличии в молекуле функциональной группы (см. табл. 6.7) старшей, чем сложноэфирная, последняя рассматривается как заместитель, указываемый в названии с помощью префикса. В зависимости от того, каким концом сложноэфирная группа присоединена к основной части молекулы, «кислотным» или «спиртовым», употребляют либо префикс «R-оксикарбонил», где R — название «спиртового» заместителя, либо
«ацилокси = ацил + окси». Префиксы для ацильных замещающих групп R(C=O)~ образуют из систематического названия соответствующей кислоты RCOOH путем замены суффикса «овая кислота» («oic acid») на «оил» («оу1») или окончания «карбоновая кислота» («carboxylic acid») на суффикс «карбонил» («carbonyl»), например: гексановая кислота — гексаноил, циклопропанкарбоновая кислота — циклопропанкарбонил. В случае образования ацильных префиксов из тривиального названия кислоты (табл. 6.19) ситуация сложнее, т. к. за основу берутся не русские тривиальные названия, а гранслитерированные англоязычные названия. При этом окончание «oic acid» или «ic acid» заменяется на «оу1», за исключением названий помеченных «звездочкой» (*) в табл. 6.19; в этом случае окончание «ic acid» заменяется на «у1» («ил»), например:
уксусная кислота (acetic acid*) — ацетил (acetyl); акриловая кислота (acrylic acid) — акрилоил (acryloyl); малоновая кислота (malonic acid*) — малонил
(malonyl);
бензойная — бензоил;
пропионовая кислота (propionic acid*) — пропионил (propionyl);
масляная кислота (butyric acid*) — бутирил (butyryl);
коричная кислота (cinnamic acid) — циннамоил (cinnamoyl) и т. д. (рис. 6.8.23а и 6.8.236).
CI
Этил-4-фенил-2-хлорбут-3-иноат англ.: Ethyl 2-chloro-4-phenylbut-2-ynoate
Рис. 6.8.21
2-Хлорэтиловый эфир 4-гидрокси-З-метоксибензойной кислоты англ.: 4-Hydroxy-3-methoxybenzoic acid 2-chloroethyl ester или
2-chloroethyl 4-hydroxy-3-methoxybenzoate
Рис. 6.8.22
О Y^o-r R-оксикарбонил
Натрия (2-метоксикарбонилциклолролил)ацетат англ.: Sodium (2-methoxycarbonylcyclopropyl)acetate
Рис. 6.8.23а
Современная номенклатура органических соединений
1043
ацилокси
например:
4-Пропионилоксибензойная кислота англ.: 4-Propionyloxybenzoic acid
Рис. 6.8.236
Лактоны
Циклические эфиры гидроксизамещенных карбоновых кислот называются лактонами. Эти соединения являются кислородсодержащими гетероциклами и могут быть названы с использованием номенклатуры гетероциклов (подразд. 6.3). Кроме того, лактоны, получаемые из моногидроксикислот, можно называть, заменяя окончание «овая кислота» («oic acid») в систематическом названии негидроксилированной кислоты на окончание «о-локант-лактон», где локант указывает положение гидроксильной группы. При использовании в качестве основы тривиального названия гидроксикислоты окончание «овая кислота» («ic acid») заменяется на «олактон» (в этом случае часто используются не русские, а транслитерированные англоязычные названия). Использование допускаемых ранними версиями правил IUPAC названий, образованных добавлением к названию соответствующего углеводорода суффикса «олид», в настоящее время не рекомендуется (рис. 6.8.24).
Некоторые гетерополициклические соединения, которые формально представляют собой лактоны, могут быть названы путем добавления суффикса «карболактон» к основе, представляющей собой название соответствующего полицикла, в котором группировка -С(О)О- заменена на два атома водорода. Перед суффиксом помещают два локанта: первый показывает положение карбонильной группы, а второй — гидроксильного атома кислорода (рис. 6.8.25).
Ангидриды
Ангидриды карбоновых кислот — это продукты (формального) отщепления одной молекулы воды от двух карбоксильных функций. Из двух одинаковых молекул кислоты образуются симметричные ангидриды. Их называют, заменяя слово «кислота» в систематическом или тривиальном названии соответствующей карбоновой кислоты на слово «ангидрид» (рис. 6.8.26).
Если ангидрид состоит из остатков двух различных кислот, то его называют смешанным ангидридом. В названии таких соединений перечислятся в алфавитном порядке названия кислот с добавлением слова «ангидрид»; в русском варианте названия обеих кислот пишутся одним словом с соединительной гласной «о» (рис. 6.8.27).
Циклические ангидриды поликарбоновых кислот, получающиеся из кислотных функций, присоединенных к одному и тому же родоначальному гидриду, могут быть названы аналогично ангидридам одноосновных кислот или как соответствующие гетероциклы (рис. 6.8.28).
Галогенангидриды
Галогенангидриды карбоновых кислот или ацилга-логениды — это соединения, у которых гидроксил карбоксильной группы заменен на галоген. Для этого класса соединений широко распространены радикало-функциональные названия, в которых перед названием галогенида указывается название соответствующего ацильного заместителя R-C(O)- (см. подразд. 6.8.8.2) (рис. 6.8.29).
Если в соединении имеются функциональные группы более высокого старшинства, чем галогенангидрид-ные (см. табл. 6.7), то последние приводятся в названии как префиксы: «фторкарбонил» («fluorocarbonyl»), «хлор карбонил» («chlorocarbonyl»), «бромкарбонил» («bromocarbonyl») или «иодкарбонил» («iodocarbonyl»). В более ранних версиях номенклатурных правил 1UPAC использовался префикс «галогенформил» (рис. 6.8.30).
Для хлорангидридов угольной и тиоугольной кислот широко используются тривиальные названия «фосген» («phosgene») (СОС12) и «тиофосген» («thiophosgene») (CSC12).
Амиды, лактамы, имиды и гидразиды карбоновых кислот
Соединения, в которых гидроксил карбоксильной группы заменен на аминогруппу (общая формула RC(O)NH2), называются амидами карбоновых кислот. Систематические названия этих соединений образуют, заменяя в названии соответствующей кислоты суффикс «овая кислота» («oic acid», «ic acid») или «карбоновая кислота» («carboxylic acid») на суффикс «амид» («amide») или «карбоксамид» («carboxamide») соответственно в зависимости от того входит ли углерод функциональной группы в состав родоначального названия или нет. В качестве родоначальных названий часто используются тривиальные названия кислот, при этом в качестве основы для названий амидов на русском языке используется транслитерированное название соответствующей кислоты на английском (рис. 6.8.31).
Замещенные у атома азота амиды называют, добавляя к названию незамещенного соединения префикс заместителя с локантом в виде курсивной буквы А (рис. 6.8.32).
В том случае, когда заместителем у атома азота является фенильная группа, можно использовать названия типа ацетанилид, бензанилид и т. п. (от названия соответствующего амина: C6H5NH2 — анилин) («aniline»).
Когда в молекуле дополнительно содержится функциональная группа большего старшинства (см. табл. 6.7), чем амидная, последняя указывается в названии как
1044
Новый справочник химика и технолога
префикс. Если амидная группа присоединена к основной части молекулы со стороны карбонильной группы, то используют префикс «карбамоил» для H2NC(O)- или «R-карбамоил» для RHNC(O)-, где R — название заместителя при азоте, если присоединение со стороны азота, то применяется префикс «R-карбоксамидо». В последнем случае альтернативно может быть использован соответствующий префикс «ациламино» (рис. 6.8.33).
Соединения, содержащие группу -CO-NH- или -CO-NR-, включенные в состав цикла, рекомендуется
называть как гетероциклические соединения (см. подразд. 6.3), хотя они могут рассматриваться как циклические амиды карбоновых кислот, называемые лактамами. Название в этом случае строится по аналогии с лактонами (см. подразд. 6.8.8.2), с использованием суффикса «лактам» вместо «лактон» (рис. 6.8.34).
Для некоторых циклических амидов правилами IUPAC разрешено использование тривиальных названий (рис. 6.8.35).
Бутано-4-лактон, тетрагидрофуран-2-он, у-бутиролактон (трад.), бутанолид-4 (устар.)
англ:. Butano-4-lactone, tetrahydrofuran-2-one, y-butyrolactone (трад.) butanolide-4 (устар.)
Рис. 6.8.24
Пирен-4,3-карболактон англ:. Pyrene-4,3-carbolactone
Рис. 6.8.25
Пропионовый ангидрид англ:. Propionic anhydride
Циклопропанкарбоновый ангидрид англ:. Cyclopropanecarboxylic anhydride
Рис. 6.8.26
Бромуксусноуксусный ангидрид Бензойнопропионовый ангидрид англ.: Acetic bromoacetic anhydride англ.: Benzoic propionic anhydride
Рис. 6.8.27
Глутаровый ангидрид англ:. Glutaric anhydride
Циклогептан-1,2-дикарбоновый ангидрид англ: Cycloheptane-1,2-dicarboxylic anhydride
Рис. 6.8.28
Современная номенклатура органических соединений
1045
Г ександиоилбромидхлорид англ.-. Hexanedioyl bromide chloride
Циклопентанкарбонилхлорид англ.: Cyclopentanecarbonyl chloride
Ацетилхлорид англ.-. Acetyl chloride
Циннамоилхлорид англ.-. Cinnamoyl chloride
Фталоилдифторид англ.-. Phthaloyl difluoride
Рис. 6.8.29
(Бромкарбонил)уксусная кислота
англ.: (Bromocarbonyl)acetic acid
Этиловый эфир 2-(фторкарбонил)бензойной кислоты
англ.: Ethyl 2-(fluorocarbonyl)benzoate
2,4-Диметилгексанамид
англ.-. 2,4-Dimethylhexanamide
Рис. 6.8.30
Ацетамид англ.: Acetamide
Нафталин-2-карбоксамид англ.: Naphthalene-2-carboxamide
О
i| nh2 Бензамид
J англ.: Benzamide
Рис. 6.8.31
Л/-(2-Хлорэтил)фенилацетамид англ.: /V-(2-Chloroethyl)phenylacetamide
Л/-Бензил-Л/-этилбутанамид англ.: /V-Benzyl-/V-ethylbutanamide
N, Л/-Диэтилциклогексанкарбоксамид англ.: /V,/V-Diethylcyclohexanecarboxamide
Рис. 6.8.32
1046
Новый справочник химика и технолога
О \X^NH2 карбамоил
Пропил-3-карбамоилциклогексанкарбоксилат англ:. Propyl 3-carbamoylcyclohexanecarboxylate
4-(Л/-Метилкарбамоилметил)бензойная кислота англ:. 4-(/V-Methylcarbamoylmethyl)benzoic acid
Метил-6-этилкарбоксамидо-2-нафтоат или метил-6-(пропиониламино)-2-нафтоат англ: Methyl 6-ethylcarboxamido-2-naphthoate или methyl 6-(propionylamino)-2-naphthoate
Рис. 6.8.33
Азепан-2-он или гексано-6-лактам, е-капролактам (трад.)
англ:. Azepan-2-one или hexano-6-lactam, e-caprolactam (трад.)
Рис. 6.8.34
(показан 1 -изомер)
Изохинолон (трив.), 2/-/-ИЗОХИНОЛИН-1-ОН (сист.) англ:. Isoquinolone
{показан 2-изомер)
Пирролидон (трив.), пирролидин-2-он (сист.) англ: Pyrrolidone
Хинолон (трив.),
1 /-/-хинолин-2-он (сист.) англ: Quinolone
(показан 2-изомер)
Рис. 6.8.35
Современная номенклатура органических соединений
1047
Имидами называют соединения, которые содержат группировку -C(O)-NR-C(O)-. Они являются диациль-ными производными аммиака или ацильными производными амидов и могут быть соответствующим образом названы (рис. 6.8.36).
Циклические имиды дикарбоновых кислот называют, заменяя суффиксы «диовая кислота» и «дикарбоновая кислота» соответственно на «имид» и «дикарбок-симид» или модифицируя соответствующее тривиальное название (рис. 6.8.37).
Эти соединения также принято называть по гетероциклической номенклатуре (см. подразд. 6.3) (рис. 6.8.38).
Гидразиды карбоновых кислот — соединения общей формулы RC(O)NHNH2 — называют, заменяя в систематических или тривиальных названиях кислот
окончание «овая кислота» на «огидразид» или окончание «карбоновая кислота» на «карбогидразид», например октаногидразид. Если атомы азота содержат заместители, то необходимо указать их положение, пронумеровав атомы азота, начиная от карбонильной группы. Можно использовать два типа локантов: буквенные (/V и N’) и цифровые (Г и 2') (нештрихованный набор цифровых локантов относится к «кислотной» части молекулы) (рис. 6.8.39).
В тех случаях, когда заместитель у атома азота имеет приоритет при определении родоначального названия, то соединение называется как «ацилгидразино» или «ацилдиазанил» производное; атом азота, присоединенный к родоначальному фрагменту, имеет локант W или 1, а другой — W' или 2 (рис. 6.8.40).
Ацетил(бензоил)амин или
Л/-ацетилбензамид
аигл. \ Acetyl(benzoyl)amine или
/V-acetylbenzamide
Рис. 6.8.36
М-Фенэтилмалеимид англ.: /V-Phenethylmaleimide
Циклогептан-1,2-дикарбоксимид англ.-. Cycloheptane-1,2-dicarboximide
Рис. 6.8.37
Изохинолин-1,3(2Н,4Н)-дион англ.: Isoquinoline-1,3(2H,4H)-dione
Рис. 6.8.38
N ‘-Мети Л-Л/-ЭТИЛ гептаноги дразид или 2'-метил-1 '-этилгептаногидразид
англ.: W-Ethyl-Л/ '-methylheptanohydrazide или
r-ethyl-2'-methylheptanohydrazide
'"N
н
Л/-(2-Метоксиэтил)-Л/ '-этил (фенил ацетогидразид) или 1'-(2-метоксиэтил)-2'-этил(фенилацетогидразид)
англ.: N '-Ethyl-/V-(2-methoxyethyl)phenylacetohydrazide или 2'-ethyl-r-(2-methoxyethyl)phenylacetohydrazide
Рис. 6.8.39
1048
Новый справочник химика и технолога
Метил-5-(Л/ '-ацетил-Л/-метил-Л/ '-этилгидразино)фуран-2-карбоксилат или
метил-5-(2-ацетил-1-метил-2-этилдиазанил)фуран-2-карбоксилат англ.-. Methyl 5-(Л/ '-acetyl-Л/ '-ethyl-A/-methylhydrazino)furan-2-carboxylate или
methyl 5-(2-acetyl-2-ethyl-1 -methyldiazanyl)furan-2-carboxylate
6-(Л/-Ацетил-Л/ '-метилдиазанил)-2-нафтойная кислота или 6-( 1 -ацетил-2-метилгидразино)-2-нафтойная кислота
англ.-. 6-(/V-Acetyl-/V '-methyldiazanyl)-2-naphthoic acid или
6-(1-acetyl-2-methylhydrazino)-2-naphthoic acid
Рис. 6.8.40
Пероксикислоты
Кислоты, содержащие группу -С(О)ООН, относятся к классу пероксикислот. Эти соединения называют, помещая префикс «перокси» перед тривиальным или систематическим (с суффиксом «овая кислота») названием соответствующей карбоновой кислоты. Если в систематическом названии кислоты используется суффикс «карбоновая кислота», то префикс «перокси» помещают перед этим суффиксом. Для полиосновных кислот употребляются префиксы «моноперокси», «диперокси» и т. д. Если в молекуле наряду с гидроперокси-карбонильной присутствует суффиксная группа большего старшинства, то первая указывается в названии с помощью префикса «гидропероксикарбонил» (рис. 6.8.41).
Исключениями являются:
НСО3Н — пермуравьиная кислота, СН3СО3Н — перуксусная кислота, С6Н5СО3Н — пербензойная кислота.
Амовые кислоты
Дикарбоновые кислоты с разрешенными тривиальными названиями (табл. 6.19), у которых одна из карбоксильных групп заменена на карбамоильную группу -C(O)NH2, называют, модифицируя тривиальное название дикарбоксилата заменой суффикса «ат» («ate») на суффикс «амовая кислота» («amic acid») (рис. 6.8.42).
Для первых членов ряда H2N-COOH и H2N-C(O)-COOH сохранены тривиальные названия соответственно карбаминовая кислота («carbamic acid») и ок-саминовая кислота («oxamic acid»). В том случае, если в амовой кислоте атом азота содержит фенильный (С6Н5) заместитель, то в названии используется суффикс «ани-ловая кислота» («anilic acid») (рис. 6.8.43).
В Chemical Abstracts для таких соединений используются систематические названия, например, для последнего соединения: 3-(фениламинокарбонил)пропановая кислота.
англ.-. Peroxypentanoic acid
Пероксипентановая кислота
Дипероксималеиновая кислота О
англ.-. Diperoxymaleic acid
Монопероксифталевая кислота
англ.: Monoperoxyphthalic acid
СОООН .г с 4
4-Г идропероксикарбонил-1 -метилп иридии иихлорид англ.: 4-Hydroperoxycarbonyl-1 -methylpyridinium chloride
Рис. 6.8.41
Современная номенклатура органических соединений
1049
Сукцинамовая кислота Фталамовая кислота
англ.-. Succinamic acid англ.: Phthalamic acid
Рис. 6.8.42
Карбамиловая кислота англ.-. Carbanilic acid
Сукцинаниловая кислота англ.: Succinanilic acid
Рис. 6.8.43
Имидовые, гидразоновые, гидроксимовые и гидроксамовые кислоты
Производные карбоновых кислот, полученные заменой карбоксильного карбонила на группы >C=NH, >C NNH2 или >C=NOH, называют, используя систематическое или тривиальное название кислоты с заменой суффикса «овая» (или «карбоновая») на суффиксы, представленные в табл. 6.25. Название кислоты, в которой гидроксил карбоксильной группы заменен на группу -NH-OH, может быть образовано с использованием суффикса из табл. 6.25, однако по правилам IUPAC 1993 г. гидроксамовые кислоты предпочтительнее называть как А-гидроксиамиды (рис. 6.8.44).
При формировании названий имидовых, гидразоновых и гидроксимовых кислот следует быть внимательным при употреблении в качестве родоначальных тех тривиальных названий карбоновых кислот, у которых названия кислоты и соответствующего карбоксилата в русском варианте имеют разные корни (уксусная кислота — ацетат, щавелевая кислота — оксалат). В английском языке корни в названии кислоты и карбоксилата всегда совпадают (acetic acid — acetate, oxalic acid — oxalate). В русских названиях этих производных используются транслитерированные английские названия карбоксилатов (см. подразд. 6.8.8.2), например:
ОН
Л0Н Ацетогидроксимовая кислота
Nx англ.: Acetohydroximic acid
Пентанимидовая англ.: Pentanimidic acid
кислота Циклопропанкарбогидразоновая кислота англ.: Cyclopropanecarbohydrazonic acid
З-Хлорбензогидроксимовая кислота англ.: 3-Chlorobenzohydroximic acid
Л/-Г идроксиацетамид,
ацетогидроксамовая кислота (трад.)
англ.: /V-Hydroxyacetamide, acetohydroxamic acid (трад.)
Рис. 6.8.44
1050
Новый справочник химика и технолога
Таблиц 6.25
Суффиксы в названиях имидовых, гидразоновых, гидроксимовых и гидроксамовых кислот
Функциональная группаа) Суффикс Префикс
NH // -(C) 'он имидовая кислота (imidic acid)
NH -г Ън карбоксимидовая кислота (carboximidic acid) имидокарбокси (imidocarboxy)
N—NH2 —(C)Z ОН огидразоновая кислота (ohydrazonic acid)
N—NH2 —cz ОН карбогидразоновая кислота (carbohy-drazonic acid) гидразонокарбокси (hydrazonocar-boxy)
N-OH // -(C) он огидроксимовая кислота (ohydroximic acid)
N-OH -с" хон карбогидроксимовая кислота (carbo-hydroximic acid) гидроксимидокарбокси (hy-droxyimidocarboxy)
/z° -(C) N-OH / H огидроксамовая кислота (ohydroxamic acid)
_/ N-OH / H карбогидроксамовая кислота (carbohydroxamic acid) гидроксикарбамоил (hydroxycarbamoyl)
а) Заключенный в скобки атом углерода входит в название родоначального гидрида.
Тиокарбоновые кислоты и их производные
Названия сернистых аналогов карбоновых кислот образуют из названий карбоновых кислот, модифицируя их как показано в табл. 6.26.
Принципы построения названий основных производных тио- и дитиокарбоновых кислот суммированы в табл. 6.27.
Построение названий тио- и дитиокарбоновых кислота)
Таблица 6.26
Модификация суффикса или префикса карбоновой кислоты Формула функциональной группыб) Пример1*)
-овая кислота тиовая кислота о со' о Г Бутантиовая кислота или тиомасляная кислота англ.: Butanethioic acid или thiobutyric acid
Современная номенклатура органических соединений
1051
Продолжение табл. 6.26
Модификация суффикса или префикса карбоновой кислоты Формула функциональной группыб) Пример”)
-овая кислота карбоновая кислота карбокси —> тиовая 5-кислота —> тиовая О- кислота —> дитиовая кислота —> карботиовая кислота —> карботиовая 5-кислота —>карботиовая (9-кислота —>карбодитиовая кислота —>тиокарбокси -(C) SH //S -(C) он //S -(C) SH —с|°|н Sj J \ SH S -с" он _/ \ SH н1°)с-SJ Ph О З-Фенилпропантиовая S-кислота ши 3-фенилтиопропионовая S-кислота англ:. 3-Phenylpropanethioic S-acid или 3-phenylthiopropionic S-acid S 2-Метилпропантиовая О-кислота или тиоизомасляная О-кислота англ: 2-Methylpropanethioic O-acid или thioisobutyric O-acid S JL /SH HS S Бутанбисдитиовая кислота англ: Butanebisdithioic acid Циклопропанкарботиовая кислота англ: Cyclopropanecarbothioic acid 0 0^ [1 O^sh Фуран-2-карботиовая S-кислота англ:. Furan-2-carbothioic S-acid 0 S 6-Оксоциклогекс-1 -ен карботиовая О-кислота англ: 6-Oxocyclohex-1-encarbothioic O-acid S s Бензол-1,2-д и карбодитиовая кислота или тетратиофталевая кислота англ: Benzene-1,2-dicarbodithioic acid или tetrathiophthalic acid 0 IsJ у OH 2-T иокарбоксипропановая кислота англ:. 2-Thiocarboxypropanoic acid
1052
Новый справочник химика и технолога
Окончание табл. 6.26
Модификация суффикса или префикса карбоновой кислоты Формула функциональной группыб) Примерв)
карбокси —> гидрокситиокарбонил —> сульфанилкарбонил (ранее: меркаптокарбонил) —> дитиокарбокси S V но7 %-/ HS S HS7 S НО О (Е)-3-Гидрокситиокарбонилпропеновая кислота англ:. (E)-3-Hydroxythiocarbonylpropenoic acid S о 4-Сульфанилкарбонилбензолкарботиовая О-кислота 4-меркаптокарбонилбензолкарботиовая О-кислота (устар.) англ.: 4-Sulfanylcarbonylbenzenecarbothioic O-acid 4-mercaptocarbonylbenzenecarbothioic O-acid s 4-Дитиокарбоксифенилуксусная кислота англ 4-Dithiocarboxyphenylacetic acid
а) Соответствующие Se-содержащие кислоты называют аналогично, заменяя «ти» («thi») на «селен» («selen») и «сульфанил» («sulfanyl») на «селанил» («selanyl»).
б) Заключенный в скобки атом углерода входит в название родоначального соединения.
в) Дополнительно приведено полусистематическое название.
Построение названий производных тио- и дитиокарбоновых кислот
Таблица 6.27
Современная номенклатура органических соединений
1053
Продолжение табл. 6.27
Модификация суффикса или префикса производного карбоновой кислоты Пример
Эфиры
карбоксилат R-оксикарбонил —> карбодитиоат —> Я-окси(тиокарбонил) —> Я-тио(карбонил) или R-сульфанилкарбонил б) —> R-тиo(тиoкapбoнил) или R-сульфанилтиокарбонил S Ni \ Этил-пиридин-З-карбодитиоат или дитионикотиновой кислоты этиловый эфир англ.. Methyl pyridine-3-carbodithioate или dithionicotinic acid ethyl ester О 1 SH s 3-[Метокси(тиокарбонил)]тиопропановая S-кислота англ.: 3-[Methoxy(thiocarbonyl)]thiopropanoic S-acid CK o 'y 1,2-Бис(метилсульфанилкарбонил)-бутановая кислота англ.: 1,2-Bis(methylsulfanylcarbonyl)butanoic acid S 1 0 Калия 5-(изопропилсульфанил-тиокарбонил)фуран-2-карбоксилат англ.: Potassium 5-(isopropylsulphanyl-thiocarbonyl)fu ran-2-carboxyl ate
Галогенангидриды
оил галогенид карбонил галогенид —> тиоилгалогенид —> карботиоилгалогенид S S p^X/^/^p Пентандитиоилдифторид англ.: Pentanedithioyl difluoride 5\\ Ij2 Cl 4'—3 5-Цианотиофен-2-карботиоилхлорид англ:. 5-Cyanothiophene-2-carbothioyl chloride
Амиды
амид —>тиоамид ^xxA4VNH2 IT II II4 s З-Этилбут-3-ентиоамид англ: 3-Ethylbut-3-enethioamide
1054
Новый справочник химика и технолога
Окончание табл. 6.27
Модификация суффикса или префикса производного карбоновой кислоты Пример
Амиды
карбоксамид -> карботиоамид / \ /S ' ' nh2 Би цикл о[2.2,2]октан-1 -карботиоамид англ.: Bicyclo[2.2.2]octane-1 -carbothioamide
а) Альтернативная замена «...эфир ...овой кислоты» на «...эфир ...тиовой кислоты».
б) Название префикса «алкилсульфанилкарбонил» для группы RSC(O)- является более предпочтительным чем алкил-тио(карбонил), поскольку последний легко перепутать (особенно на слух) с группой RC(S)-, например, фенилтио(карбонил) соответствует ipynne PhSC(O)-, а фенил(тиокарбонил) — группе PhC(S)-.
Названия ангидридов тиокислот строятся аналогично ангидридам карбоновых кислот с использованием инфикса «тио» в случае присутствия тиокарбонильных(ой) групп(ы) или завершающего слова «тиоангидрид», если ацильные или тиоацильные заместители соединены через атом серы (Ac-S-Ac). Некотрые примеры названий смешанных ангидридов представлены в табл. 6.28.
В названиях сернистых производных угольной кислоты используются инфиксы тио-, дитио-, тритиокарбонат, тиокарбамат, тиосеми карбазид и т. д. (рис. 6.8.45а и 6.8.456).
Таблица 6.28
Построение названий смешанных ангидридов карбоновых, тио- и дитиокарбоновых кислот
Смешанный ангидрид Формула
Пропионовоуксусный тиоангидрид (acetic propionic thioanhydride) 0 4SX 0
Тиопропионовоуксусный ангидрид (acetic thiopropionic anhydride) 0 s
Пропионовотиоуксусный ангидрид (propionic thioacetic anhydride) s 0
Тиопропионовоуксусный тиоангидрид (acetic thiopropionic thioanhydride) 0 s
Тиопропионовотиоуксусный ангидрид (thioacetic thiopropionic anhydride) s s
Tиопропионовотиоуксусны й тиоангидрид (thioacetic thiopropionic thioanhydride) s 'S" s
/С
' S
°] Sj
S-Этилгидротиокарбонат англ.: S-Ethyl hydrogen thiocarbonate
Калия S-этилдитиокарбонат англ.: Potassium S-ethyl dithiocarbonate
S
Диэтилтритиокарбонат англ.: Diethyl trithiocarbonate
Натрия О-мети л дитиокарбон ат англ.: Sodium O-methyl dithiocarbonate
Рис. 6.8.45а
Современная номенклатура органических соединений
1055
1-Метил-4,4-диэтилтиосемикарбазид англ.-. 4,4-Diethyl-1 -methyl thiosemicarbazide
О-Изопропил-/\/-фенилтиокарбамат англ.-. O-lsopropyl-/V-phenyl thiocarbamate
Рис. 6.8.456
Нитрилы и родственные соединения
Нитрилы (цианиды) представляют собой производные карбоновых кислот, у которых группа -СООН заменена на группу -ON. Нитрилы называют, добавляя к родоначальному названию суффикс «нитрил», если атом углерода группы -ON входит в состав родоначального гидрида, или суффикс «карбонитрил», если не входит (рис. 6.8.46).
Нитрилы, образованные из карбоновых кислот, имеющих тривиальные названия (табл. 6.19), могут быть названы на их основе с добавлением суффикса «нитрил» (рис. 6.8.47).
Радикало-функциональные названия соединений R-CN образуют путем добавления названия группы R
к названию функционального класса — цианид (рис. 6.8.48).
При наличии в молекуле нитрила функциональной группы более высокого старшинства, группу -ON отражают в названии с помощью префикса «циано» (рис. 6.8.49).
Нитрилоксиды — соединения общей формулы RONO — называют, добавляя к названию нитрила слово «оксид» (при этом нельзя использовать радикалофункциональную форму названия с основой «цианид»).
Согласно правилам IUPAC, если соединение содержит в качестве главной группы одну из тех, которые приведены в табл. 6.29, то название составляется но радикало-функциональной номенклатуре (рис. 6.8.50).
З-Метилгексаннитрил англ.-. 3-Methylhexanenitrile
О
2-Оксопентандинитрил англ.-. 2-Oxopentanedinitrile
2-Формилциклопропанкарбонитрил англ.: 2-Formylcyclopropanecarbonitrile
Рис. 6.8.46
Н3С-CN
Ацетонитрил англ.-. Acetonitrile
CN
NC
NO2
3-Н итробензонитрил англ.-. 3-Nitrobenzonitrile
Фумародинитрил англ.: Fumarodinitrile
Рис. 6.8.47
mpem-Бутилцианид Бензилцианид Бензоилцианид
англ.: tert-Butyl cyanide англ.: Benzyl cyanide англ.: Benzoyl cyanide
Рис. 6.8.48
1056
Новый справочник химика и технолога
СООН
а СООН
CN
5-Цианопентановая кислота 2-Цианобензойная кислота англ.-. 5-Cyanopentanoic acid англ.-. 2-Cyanobenzoic acid
Рис. 6.8.49
Фенилизоцианат англ.-. Phenyl isocyanate
Бензилтиоцианат англ.-. Benzyl thiocyanate
Рис. 6.8.50
Таблица 6.29
Некоторые азотсодержащие функциональные группы, применяемые в радикало-функциональной номенклатуре (приведены в порядке убывания старшинства)
Функциональная группа Суффикс Префикс
-N=C изоцианид (isocyanide) изоциано (isocyano)
-OON цианат (cyanate) цианато (cyanato)
-N=C=O изоцианат (isocyanate) изоцианато (isocyanato)
-O-N=C фульминат (fulminate)
-SON тиоцианат (thiocyanate) тиоцианато (thiocyanato)
-NOS изотиоцианат (isothiocyanate) изотиоцианате (isothiocyanato)
-SeON селеноцианат (selenocyanate) селеноцианато (selenocyanato)
-N=C=Se изоселеноцианат (isose-lenocyanate) изоселеноцианато (isoselenocyanato)
Амидины
Амидинами называются соединения формулы R-C(=NH)NH2. Названия этих соединений образуют из названий соответствующих карбоновых кислот путем замены суффиксов «овая кислота» на «имидамид» (в ранних версиях правил IUPAC «амидин») и «карбоновая кислота» на «карбоксимидамид» (в ранних версиях правил IUPAC «карбоксамидин») (рис. 6.8.51).
Заместители у атомов азота указывают с помощью локантов A(-NH2 группа) и A'(=NH группа) (рис. 6.8.52).
При наличии в молекуле функциональной группы более высокого старшинства (амидная и выше) амидиновая группа записывается в префикс, вид которого зависит от характера его присоединения к основному фрагменту (рис. 6.8.53).
NH
NH2
Бутанимидамид, бутанамидин (устар.) англ.: Butanimidamide, butanamidine
Циклопентанкарбоксимидамид, циклопентанкарбоксамидин (устар.) англ.-. Cyclopentanecarboximidamide, cyclopentanecarboxamidine
Рис. 6.8.51
Современная номенклатура органических соединений
1057
CI
Л/'-Метил-4-хлор-Л/-этилбензолкарбоксимидамид, Л/'-метил-4-хлор-Л/-этилбензамидин (устар.)
англ.-. 4-Chloro-/V-ethyl-/V'-methylbenzenecarboximidamide, 4-chloro-/V-ethyl-/V’-methylbenzamidine
например:
Карбамимидоил, амидино (устар.) англ.-. Carbamimidoyl, amidino (устар.)
Рис. 6.8.52
Иминометиламино Аминометиленамино
англ.: Iminomethylamino англ.: Aminomethyleneamino
О
h2n
NH2 4-Карбамимидоилбензамид, 4-амидинобензамид (устар.) англ.: 4-Carbamimidoylbenzamide, 4-amidinobenzamide
(Иминометиламино)ацетонитрил англ.: (Iminomethylamino)acetonitrile
3-(Аминометиленамино)циклопентансульфоновая кислота англ.: 3-(Aminomethyleneamino)cyclopentanesulfonic acid
Рис. 6.8.53
6.9. Азотсодержащие соединения
В настоящем разделе рассматривается номенклатура соединений, содержащих следующие азотсодержащие функциональные группы: -NHOH, -NH2,
-nhnh2, -n=nh, =n=n , -n(O)=nh, -n+h2-o ;
>C=N- -N3, -NO, -NO2.
6.9.1. Амины, имины, гидроксиламины и оксиды аминов
Номенклатура аминов в настоящее время переживает период становления, что находит отражение в большом числе допускаемых вариантов названия одного и того же соединения. Первичные амины RNH2 могут быть названы одним из следующих способов:
1) путем добавления названия замещающей группы R к названию родоначального гидрида NH3 — «азан» («azane») (новые рекомендации);
2) путем добавления суффикса «амин» («amine») к названию родоначального гидрида R.H (традиционные названия);
3) путем добавления слова «амин» к названию замещающей группы R (традиционные названия, радикало-функциональный вариант) (рис. 6.9.1).
Симметричные вторичные и третичные амины R2NH и R3N называют одним из следующих способов:
1) путем добавления названия замещающей группы R с соответствующей умножающей приставкой к названию родоначального гидрида NH3 — «азан»;
2) путем добавления слова «амин» к названию замещающей группы R с соответствующей умножающей приставкой.
Несимметричные вторичные RR'NH и третичные амины (R2NR' и RR'R"N) называют аналогично, располагая названия замещающих групп по алфавиту. При необходимости используется локант N (рис. 6.9.2).
1058
Новый справочник химика и технолога
Первичные диамины и полиамины удобно называть в соответствии с принципами заместительной номенклатуры (рис. 6.9.3).
При наличии в молекуле функциональной группы более высокого старшинства аминогруппа указывается в названии в виде префикса «амино» (рис. 6.9.4).
Иминами альдегидов, или альдиминамии, называют соединения общей формулы R’-CH=N-R1 2, а иминами кетонов, или кетиминамии, — соединения формулы R'R2CH=N-R3. Эти соединения можно назвать несколькими способами. Наиболее распространеными являются радикало-функциональные названия, записываемые как «алкилиденамин», где «алкилиден-» соответствует названию двухвалентной группы R'-CH- (см. табл. 6.5). Подобное название получается на основе азана (NH3) как родоначального азотистого гидрида — «алкилиденазан». Кроме того, можно построить название имина, взяв за основу алкан R*-CH3 в качестве родоначального углеродного гидрида и добавив окончание «имин» с соответствующим локантом, указывающим положение иминной функции в углеводородной цепи (рис. 6.9.5).
При наличии в молекуле функциональной группы более высокого старшинства иминная группа указывается в названии в виде префикса, вид которого зависит от характера ее соединения с основой (рис. 6.9.6).
Соединения общей формулы R-NH-OH называются гидроксиламинами по названию простейшего представителя этого ряда— гидроксиламина (NH2OH). Ра-
дикало-функциональные названия, которые, как правило, используются для соединений R-NH-OR', состоят из названия замещающей группы R (R') с окончанием «гидроксиламин» и буквенным локантом N- или/и О-, обозначающим, у какого гетероатома находится заместитель (рис. 6.9.7).
При наличии в молекуле функциональной группы более высокого старшинства гидроксиламинная группа указывается в названии в виде префиксов «гидроксиамино» (HONH-) и «R-оксиамино» (RONH-), если она присоединена к основной части молекулы атомом азота, или в виде префикса «аминоокси» (H2NO-) — если атомом кислорода (рис. 6.9.8).
А'-Ацилпроизводныс гидроксиламина RC(O)NH-OH можно называть либо как А-гидроксипроизводные амидов карбоновых кислот, либо как гидроксамовые кислоты (см. подразд. 6.8.8.2). Однако номенклатурные правила IUPAC 1993 г. уже не рекомендуют использовать последний вариант (рис. 6.9.9).
(9-Ацилпроизводные гидроксиламина NH2-OC(O)R называют как (9-ацилгидроксиламины:
О
xNH2
О О-Бензоилгидроксиламин
англ.-. O-Benzoylhydroxylamine
1) Пропилазан (нов., зам.), англ.-. 1) Propylazane,
2) пропанамин (трад.,зам.), 2) propanamine,
3) пропиламин (трад., рад.-ф.) 3) propylamine
NH2
1) Антрацен-9-илазан (нов., зам.),
2) антрацен-9-амин (трад.,зам.),
3) антрацен-9-иламин (трад., рад.-ф.)
англ.-. 1) Anthracene-9-ylazane,
2) anthracene-9-amine,
3) anthracene-9-ylamine
Рис. 6.9.1
1) Триэтилазан,
2) триэтила мин ангп.-. 1) Triethylazane,
2) triethylamine
1) Л/-Бензил-/\/-этилазан,
2) /\/-бензил-/\/-этиламин англ.-. 1) /V-Benzyl-/V-ethylazane,
2) /V-benzyl-/V-ethylamine
1) /\/-Метил-/\/-(2-метоксиэтил)-/\/-этилазан)
2) /\/-метил-/\/-(2-метоксиэтил)-/\/-этиламин англ.-. 1) /V-Ethyl-/V-(2-methoxyethyl)-/V-methylazane,
2) /V-ethyl-/V-(2-methoxyethyl)-/V-methylamine
Рис. 6.9.2
Современная номенклатура органических соединений
1059
2-Метилпропан-1,3-диамин англ.-. 2-Methylpropane-1,3-diamine
Нафталин-1,8-диамин англ.-. Naphthalene-1,8-diamine
Рис. 6.9.3
5-Аминопентаннитрил англ.-. 5-Aminopentanenitrile
Метил-4-диметиламинобензоат
англ.-. Methyl 4-dimethylaminobenzoate
Рис. 6.9.4
Гексилиденамин или гексилиденазан или гексан-1-имин англ.-. Hexylideneamine или hexylideneazane или hexane-1 -imine
Л/-Бензилиден-Л/-метиламин или Л/-бензилиден-Л/-метилазан англ.: A/-Benzylidene-A/-methylamine или A/-benzylidene-A/-methylazane
Рис. 6.9.5
например:
Алкилиденамино англ.-. Alkylideneamino
Алкилимино англ.: Alkylimino
4-(1-Фенилэтилиденамино)бензонитрил англ.: 4-(1 -Phenylethylideneamino)benzonitrile
Рис. 6.9.6
Н
h2n
Л/-(4-Аминофенил)гидроксиламин англ.: A/-(4-Aminophenyl)hydroxylamine
6-Метилиминогексан-З-он
англ.: 6-Methyliminohexan-3-one
Л/,Л/-Диметил-О-фенилгидроксиламин англ.: A/,A/-Dimethyl-O-phenylhydroxylamine
Рис. 6.9.7
1060
Новый справочник химика и технолога
О. N
НО' З-Метоксиаминобензойная кислота англ.: 3-Methoxyaminobenzoic acid
4-(Л/-Метил-Л/-этиламиноокси)бутан-1-ол
англ.: 4-(/V-Ethyl-/V-methylaminooxy)butan-1-ol
Рис. 6.9.8
О ^ОН Л/-Гидроксициклогексанкарбоксамид, Г Т Н циклогексанкарбогидроксамовая кислота (устар.) L J англ.: /V-Hydroxycyclohexanecarboxamide,
cyclohexanecarbohydroxamic acid
Рис. 6.9.9
I Триметиламиноксид или
—N— О триметилазаноксид
| англ.: Trimethylamine oxide или trimethylazane oxide
Пиперидин-1 -оксид англ.: Piperidine 1-oxide
Рис. 6.9.10
Оксиды аминов формулы R3NO, где R — одинаковые или различные замещающие группы, называют, добавляя к названию соответствующего амина (см. выше) окончание «оксид». Названия циклических аналогов образуют подобным образом, при этом положение атома кислорода лучше указывать с помощью цифровых локантов (рис. 6.9.10).
При наличии в молекуле функциональной группы более высокого старшинства группа H2N(O)- указывается в названии в виде префикса «азиноил»:
ч (| 4-(Диметилазиноил)бензонитрил
англ.: 4-(Dimethylazinoyl)benzonitrile s' \ О
6.9.2. Нитро- и нитрозосоединения
Нитросоединения (R-NO2) и нитрозосоединения (R-NO) называют только по заместительной номенклатуре с помощью префиксов «нитро» и «нитрозо» (рис. 6.9.11).
Соединения, содержащие «аг/м-нитрогруппу» =N(O)OH, могут быть названы либо как производные азиновой кислоты H2N(O)OH, либо добавлением префикса «гид-роксинитрорил» (рис. 6.9.12).
Органические производные кислот азота, в том числе содержащие другие главные группы могут быть названы с использованием префиксов, представленных в табл. 6.30.
Н3СХ 'О
N Нитрометан
англ.. Nitromethane
° 1-Нитро-4-нитрозобензол англ.: 1-Nitro-4-nitrozobenzene
Рис. 6.9.11
Современная номенклатура органических соединений
1061
О
2-(Гидроксинитрорил)циклопентан-1-сульфоновая кислота англ.-. 2-(Hydroxynitroryl)cyclopentane-1 -sulfonic acid
Рис. 6.9.12
Таблица 6.30
Префиксы заместителей для построения названий органических производных азоновой и азиновой кислот
Кислота Замещающая ipynna Префикс
NH(O)(OH)2 Азоновая кислота (azonic acid) -N(O)(OH)2 >NH(O) aзoнoдигидpoкcинитpopил-(azonodihydroxynitroryl-) азонои л-/гидронитрорил-(агопоу 1 -/hydron itrory 1 -)
NH2(O)(OH) Азиновая кислота (azinic acid) -NH(O)(OH) >NH2(O) >N(O)(OH) =N(O) гидрогидроксинитрорил- (hydrohydroxynitrory 1-) азиноил-/дигидронитрорил-(агтоу1-4Ш^гопйгогу1-) гидроксинитрорил-(1^гохупйгогу1-) нитрорил- (nitroryl-)
6.9.3. Гидразин и его производные
Гидразином называют соединение NH2-NH2. С другой стороны, это соединение представляет собой родоначальный гидрид, который называется диазаном (димер азана NH3). Поэтому, аналогично аминам, замещенные гидразины (ацилзамещенные гидразины см. в подразд. 6.8.8.2) могут быть названы двумя способами: либо как замещенные гидразины, либо как замещенные диазаны. Положение заместителей указывают с помощью локантов 1 и 2 или У и N' (рис. 6.9.13).
Если приоритет имеет другая функциональная группа в молекуле, то фрагмент NH2NH- записывается в виде префикса «гидразино». При этом атом азота, который соединен с основной частью молекулы, независимо от характера остальных заместителей получает локант 1 или У (рис. 6.9.14).
Ранее по правилам IUPAC 1979 г. гидразины, содержащие одинаковый заместитель у обоих атомов
азота или заместители, у которых одинаковые функциональные родоначальные названия, назывались по аналогии с азосоединениями (R-N=N-R) (см. подразд. 6.9.4), используя вместо префикса «азо» префикс «гидразо» (рис. 6.9.15).
Обратите внимание на то, что во избежание путаницы с нумерацией атомов азота и атомов бензольных колец в последнем примере для атомов азота используются только буквенные локанты N и N'. Бензольное кольцо, присоединенное к N '-атому азота, имеет штрихованный набор локантов. Приведенные названия этого соединения еще раз иллюстрируют то обстоятельство, что различия в алфавитном порядке заместителей в русском и английском языках приводят не только к различному порядку перечисления в названии этих заместителей, но и к различной нумерации атомов.
1(ло/
H2N—N
Л/,Л/- или 1,1-Диметил гидразин, Л/,Л/- или 1,1-диметилдиазан англ.: N,N- или 1,1-Dimethylhydrazine,
Л/,Л/- или 1,1-dimethyldiazane
Л/-Метил-Л/'-фенил-Л/-этилгидразин или 1 -метил-2-фенил-1 -этилгидразин англ.: A/-Ethyl-/\/-methyl-/\/ -phenylhydrazine или 1 -ethyl-1 -methyl-2-phenylhydrazine
Рис. 6.9.13
1062
Новый справочник химика и технолога
3-Г идразинопропионитрил англ.-. 3-Hydrazinopropionitrile
Г идразобензол англ:. Hydrazobenzene
4-(Л/’-Бензил-Л/-метилгидразино)фенол или 4-(2-бензил-1-метил гидразино)фенол англ:. 4-(/V'-Benzyl-/\/-methylhydrazino)phenol или
4-(2-benzyl-1-methylhydrazino)phenol
Рис. 6.9.14
Л/-Метил-Л/'-этилгидразобензол-2,4'-дикарбоновая кислота англ:. A-Ethyl-A/'-methylhydrazobenzene^'A-dicarboxylic acid
Рис. 6.9.15
6.9.4. Азо- и азоксисоединения
Соединения общей формулы R-N=N-R' традиционно называют как «азосоединения». Однако для этого класса соединений «более систематической» и более универсальной является система названий на основе родоначального гидрида HN=NH: диазена. Его производные называют как замещенные диазены в соответствии с правилами заместительной номенклатуры (рис. 6.9.16).
Для рассмотренных соединений приведены широко употребляемые в настоящее время и допускаемые правилами IUPAC традиционные названия с использованием префикса «азо». По этой номенклатуре в зависимости от строения азосоединения его называют одним из двух способов. Если азогруппа -N=N- соединяет структурные фрагменты с одним и тем же родоначальным названием, то оно и используется в качестве основы названия с добавлением префикса «азо»; заместители в обоих фрагментах указываются в начале названия с соответствующими локантами, причем для одного фрагмента используется нештрихованный набор локантов, а для второго — штрихованный, например, 2,4'-дихлоразобензол. Второй способ применяется, когда фрагменты при азогруппе имеют разные родоначальные названия. В этом случае они перечисляются, начиная с более сложного*, а между ними помещают префикс «азо». Если необходимо указать положение присоединения азогруппы, то соответствующий локант
* Выбор более сложного заместителя из двух возможных часто неочевиден. Поэтому систематическое диазеновое название более предпочтительно.
помещают между префиксом «азо» и названием соответствующего фрагмента, например, нафталин-2-азо-бензол.
Моноазосоединения (соединения с одной азогруппой) R-N N R', у которых заместитель R содержит старшую функциональную группу, удобнее называть на основе углеродного гидрида RH, замещенного R'-диазенильной группой R'-N=N- (рис. 6.9.17).
В тех случаях, когда главные функциональные группы с обеих сторон азогруппы удается обозначить одним суффиксом, можно использовать номенклатуру ансамблей, применяя префикс «диазендиил» для -N=N- группы (рис. 6.9.18).
Азосоединения общей формулы R-N=N-X, где X — главная функциональная группа (см. табл. 6.3), предпочтительней называть на основе родоначального диазена HN=NH с добавлением суффикса группы (рис. 6.9.19).
Бисазосоединения и более сложные аналоги называют аналогично, руководствуясь приведенными выше правилами. Традиционные «азо»-названия таких соединений при условии отсутствия главных функциональных групп строят, перечисляя все компоненты, начиная с более сложного из терминальных (рис. 6.9.20).
A-Оксиды азосоединений общей формулы R-N(O)=N-R' известны как азоксисоединения. Если молекула соответствующего азосоединения симметрична или положение атома кислорода азоксигруппы неизвестно, то такие соединения называют, добавляя слово «оксид» к названию азосоединения (рис. 6.9.21).
В остальных случаях необходимо указать, у какого атома азота находится атом кислорода. В названиях, построенных на основе родоначального гидрида диазена,
Современная номенклатура органических соединений
1063
атомам азота приписываются локанты 1 и 2, и локант атома, который связан с кислородом, указывается перед словом «оксид», например, «дифенилдиазен-1-оксид». Аналогично азосоединениям азоксисоединения можно называть, употребляя префикс «азокси». В этих названиях для указания положения кислорода используют трехбуквенные локанты ONN и NNO. Обозначение ONN указывает на то, что первый из перечисляемых заместителей при азоксигруппе присоединен непосредственно к NO; локант NNO обозначает, что второй из пере
числяемых заместителей присоединен к NO. Правила перечисления заместителей в названии такие же, что и для азосоединений (рис. 6.9.22).
Нередки случаи, когда азосоединение содержит главную функциональную группу, которую следует помещать в суффикс названия. Для таких соединений используется только второй из перечисленных выше способов, «азокси»-названия, причем общее название строится на основе гидрида RH, замещенного R-азокси-группой (рис. 6.9.23).
Диэтилдиазен, азоэтан (трад.) англ.: Diethyldiazene, azoethane
(1-Нафтил)(2-нафтил)диазен, 1,2'-азонафталин (трад.) англ.-. (1 -Naphthyl)(2-naphthyl)diazene, 1,2'-azonaphthalene
Рис. 6.9.16
2-(2-Метил-4-хлорфенилдиазенил)анилин
2-(2-метил-4-хлорфенилазо)анилин (трад.) англ.-. 2-(4-Chloro-2-methylphenyldiazenyl)aniline
2-(4-chloro-2-methylphenylazo)aniline
1-(1-Гидрокси-2-нафтилдиазенил)нафталин-2-сульфоновая кислота
1 -(1 -Гидрокси-2-нафтилазо)нафталин-2-сульфоновая кислота (трад.) англ:. 1-(1-Hydroxy-2-naphthyldiazenyl)naphthalene-2-sulfonic acid
1-(1-Hydroxy-2-naphthylazo)naphthalene-2-sulfonic acid
Рис. 6.9.17
CN
2,4'-Диазендиилдибензонитрил,
2,4'-азодибензонитрил (трад.) англ:. 2,4'-Diazenediyldibenzonitrile,
2,4'-azodibenzonitrile
Рис. 6.9.18
1064
Новый справочник химика и технолога
4-Хлорфенилдиазенол англ.: 4-Chlorophenyldiazenol
МеО2С—N=N—СО2Ме
Диметилдиазендикарбоксилат, диметилазодикарбоксилат (трад.) англ.: Dimethyl diazenedicarboxylate, dimethyl azodicarboxylate
. /к Л/,Л/-Диэтилфуран-2-илдиазенкарбоксамид,
N 1У А/,А/-диэтилфуран-2-илазокарбоксамид (трад.)
I англ.: A/,A/-Diethylfuran-2-yldiazenecarboxamide, A/,A/-diethylfuran-2-ylazocarboxamide
Рис. 6.9.19
2-Фенантрил[7-(фенилдиазенил)-2-нафгил]диазен, фенантрен-2-азо-2'-нафталин-7'-азобензол (трад.) англ.: 2-Phenanthryl[7-(phenyldiazenyl)-2-naphthyl]diazene, phenanthrene-2-azo-2-naphthalene-7'-azobenzene
Рис. 6.9.20
Ди(«-толил)диазеноксид, азокси-п-толуол (трад.) англ.: Di(p-tolyl)diazene oxide, azoxy-p-toluene
(2-Нафтил)(4-хлорфенил)диазеноксид, нафталин-2-азокси-4-хлорбензол (трад.) англ.: (4-Chlorophenyl)(2-naphthyl)diazene oxide, naphthalene-2-azoxy-4-chlorobenzene
Рис. 6.9.21
2-(1 -Бром-2-нафтил)-1 -фенилдиазен-1 -оксид,
1 -бромнафталин-А/А/О-азоксибензол (трад.) 2-(1 -Bromo-2-naphthyl)-1 -phenyldiazene 1 -oxide, 1-bromonaphthalene-A/A/O-azoxybenzene
Рис. 6.9.22
2-(Фенил-ОА/А/-азокси)-1 -нафтойная кислота
О англ.: 2-(Phenyl-OA/A/-azoxy)-1 -naphthoic acid
Рис. 6.9.23
Современная номенклатура органических соединений
1065
6.9.5. Диазосоединения и диазониевые соли
В диазосоединениях группа N2 присоединена к углеродной части молекулы только одним атомом азота. Эти соединения называют, добавляя префикс «диазо» к названию родоначального гидрида RH (рис. 6.9.24).
Соединения общей формулы R-N=N+X~ относят к классу диазониевых солей. Названия подобных веществ состоят из названия родоначального гидрида RH с суффиксом «диазоний» и добавлением названия аниона X (рис. 6.9.25).
+ h2c=n=n
Диазометан англ.-. Diazomethane
Метил-2-диазо-2 -фенилацетат англ.-. Methyl 2-diazo-2-phenylacetate
n2 ci
Рис. 6.9.24
Пропандиазонийхлорид англ.: Propanediazonium chloride
4-Гидроксибензолдиазонийтетрафторборат англ.: 4-Hydroxybenzenediazonium tetrafluoroborate
Рис. 6.9.25
6.9.6. Соединения с цепочкой из трех и более атомов азота
Азидами называются соединения, содержащие функциональную группу -N3. Наиболее употребительной номенклатурой для этих соединений в настоящее время является радикало-функциональная номенклатура (при условии отсутствия в молекуле функциональной группы более высокого старшинства), согласно которой соединение RN3 называется как «R-азид». При
использовании заместительной номенклатуры название соединения состоит из названия гидрида RH с префиксом «азидо» (рис. 6.9.26).
Другие соединения, содержащие цепочку из трех и более атомов азота, рассматривают как полиазаны, полиазены, полиазадиены и т. д. (рис. 6.9.27).
Триазены формулы R-NH-N=N-R с одинаковыми заместителями у триазеновой группы могут быть названы как «диазоамино...» соединения.
1-Нафтилазид (рад.-ф.), ___у
1-азидонафталин (зам.)
англ.: 1-Naphthyl azide, 4-Азидобензолсульфокислота
1-azidonaphthalene англ:. 4-Azidobenzenesulfonic acid
Рис. 6.9.26
Н 3 1
1 -Фенил-6,6-диэтилгексааза-1,3-диен англ.: 6,6-Diethyl-1-phenylhexaaza-1,3-diene
4-(Триаз-2-енил)бензойная кислота англ.: 4-(Triaz-2-enyl)benzoic acid
Рис. 6.9.27
1066
Новый справочник химика и технолога
6.9.7. Другие полиазотистыеродоначальные системы
Существует целый ряд полиазотистых соединений, тривиальные названия которых рекомендуются правилами IUPAC к использованию в качестве родоначальных для построения названий более сложных произ-
водных. В табл. 6.31 приведен перечень этих соединений, а также структуры и названия соответствующих им замещающих групп, которые можно использовать в качестве префиксов.
Таблица 6.31
Тривиальные названия полиазотистых родоначальных соединений
Родоначальное соединение Префикс замещающей группы
Аллофановая кислота (allophanic acid) О II 1 4 А? СО2Н H2N 3 N Аллофан(о)ил (allophan(o)yl) О О 4 1г JG H2N 3N 1Л Н
Гидантоиновая кислота (hydantoic acid) О JJ 3 /х. 1 H2N4 N 2xC02h 5 Н Гидантоил (hydantoyl) О JL 3 /\ H2N 4 N 5 Н II1 О
Гуанидин (guanidine) 2 NH з JL 1 h2n nh2 Гуанидино (guanidino) 2 NH зЖ1Х h2n h
Бигуанидa) (biguanide) 4 2 NH NH JL 3 JL h2n n nh2 5 H 1
Биурет 6) (Biuret) 0 0 JI 3 JL H2N 4 N 2 NH2 5 H 1
Карбазон (carbazone) 5 H HNk JI 2 NH2 N 3 N 1 4 H Карбазоно (carbazono) 0 HN< A2 Jb 5 N 3 N 1?' 4 H
Карбодиазон (carbodiazone) 0 HNx JI /NH 5 N 3 N^1 4 2
Карбодиимид (carbodiimide) HN=C=NH
Карбоногидразид (carbonohydrazide) 0 5 II 1 H2N^4 2NH2 N 3N Н Н
Современная номенклатура органических соединений
1067
Окончание табл. 6.31
Родоначальное соединение Префикс замещающей группы
Мочевина (urea) О з 1 H2N 2 NH2 Уреидо (ureido) О 3 1 V H2N 2N^ Н
Изомочевина (isourea) ОН НГ2 NH2
Семикарбазид (semicarbazide) О II 1 4 2 ЫН2 H2N 3 N Н О II н 4J<2 H2N 3 N 1 О 4>L 2 H2N 3 N H r Семикарбазидо (semicarbazido) Семикарбазоно (semicarbazono)
Формазан (formazan) HN<4/^2x'NH2 5 N 1
а) Аналогично: тригуанид и т. д.
0) Аналогично: триурет и т. д.
6.10. Серасодержащие соединения
Построение названий многих серасодержащих соединений часто заключается в модификации названий соответствующих кислородсодержащих соединений путем добавления префикса «тио» («thio»). Расположенный непосредственно перед префиксом или суффиксом кислородсодержащей группы префикс «тио» означает замену атома кислорода на серу. Не следует путать префиксы «тио» и «тиа»; последний используется в «а»-номенклатуре и наименовании гетероциклов по системе Ганча — Видмана.
6.10.1. Тиолы
Соединения, содержащие группу -SH, называются тиолами. Это название, которое буквально расшифровывается как сернистый спирт («тио» — сера, «ол» — спирт), происходит от суффикса «тиол»; по заместительной номенклатуре он добавляется к систематическому названию родоначального углеводорода. Фактически название тиола отличается от названия соответствующего спирта добавленным слогом «ти»* (рис. 6.10.1).
Согласно ранним версиям правил IUPAC (1979 г.), название тиола, соответствующего спирту или фенолу
с разрешенным тривиальным названием, получали, добавляя к последнему приставку «тио», например, «тиофенол» или «тио-9-антрол». Правилами IUPAC 1993 г. такой подход не рекомендуется.
В тех случаях, когда группа -SH не является самой старшей суффиксной группой в соединении, в названии соединения она обозначается префиксом «сульфанил» («sulfanyl») . Ранее в этих ситуациях использовался префикс «меркапто» (рис. 6.10.2).
Тиолы ранее часто называли меркаптанами. Например, метантиол — это метилмеркаптан; по радикалофункциональной номенклатуре его следует называть метилгидросульфид (methyl hydrosulfide). Эта номенклатура широко используется для наименования гидрополисульфидов RS„H, например, метилгидродисульфид, метилгидротрисульфид и т. д. Альтернативное название гидрополисульфидов можно построить на основе сернистых гидридов H2S„, например, метилди-сульфан, метилгрисульфан, метилполисульфан. Эти названия рекомендуется использовать в тех случаях, когда необходимо подчеркнуть неразветвленный характер цепи атомов серы.
Названия солей тиолов получают из названий солей соответствующих спиртов простой заменой суффикса «олят» («olate») на «тиолят» («thiolate»). Если алкоголят
Для Se- и Те-аналогов используются суффиксы «селе-нол» («selenol») и «теллурол» («tellurol»).
’’ Для Se- и Те-аналогов используются префиксы «селанил» («selanyl») и «телланил» («tellanyl»).
1068
Новый справочник химика и технолога
называют с использованием окончания «оксид», например, метоксид натрия, то его заменяют суффиксом «сульфид», получая альтернативное название — ме-тилсульфид натрия (рис. 6.10.3).
При наличии в молекуле функциональной группы более высокого старшинства может возникнуть необходимость указать группу -S в виде префикса «сульфиде» (рис. 6.10.4).
Пропантиол англ.-. Propanethiol
2-Аминоэтан-1 -тиол англ.: 2-Aminoethane-1 -thiol
Цикогексан-1,2-дитиол англ.: Cyclohexane-1,2-dithiol
Рис. 6.10.1
2-Сульфанилбензонитрил,
2-меркаптобензонитрил. (устар.) англ.: 2-Sulfanylbenzonitrile,
2-mercaptobenzonitrile
Л/-(2-Сульфанилметилциклопентил)ацетамид,
Л/-(2-меркаптометилциклопентил)ацетамид (устар.) англ.: /\/-(2-Sulfanylmethylcyclopentyl)acetamide,
/\/-(2-mercaptomethylcyclopentyl)acetamide
Рис. 6.10.2
Пропантиолят калия или пропилсульфид калия Potassium propanethiolate или potassium propyl sulfide
я-Толуолтиолят натрия или я-толилсульфид натрия, тио-я-крезолят натрия (устар.) англ.: Sodium p-toluenethiolate,
sodium p-tolyl sulfide, sodium thio-p-cresolate
Рис. 6.10.3
5-Сул ьфидонафталин-1 -сульфонат дикалия англ.: Dipotassium 5-sulfidonaphthalene-1 -sulfonate
Рис. 6.10.4
Современная номенклатура органических соединений
1069
6.10.2. Сульфиды и полисульфиды
Соединения общей формулы R-S-R', где R и R' — углеводородные заместители, называют сульфидами. В соответствии с заместительной номенклатурой их следует называть по аналогии с простыми эфирами, используя префиксы «алкилсульфанил» или «арил-сульфанил» [ранее использовались префиксы «алкилтио» или «арилтио» (правила IUPAC 1979 г.)] вместо «алкокси» или «арилокси». Для относительно простых производных часто используются радикало-функциональные названия, в которых префиксы заместителей перечисляются в алфавитном порядке перед окончанием «сульфид» (для Se- и Те-аналогов используются
окончания «селенид» («selenide») и «теллурид» («telluride»)) (рис. 6.10.5). В названии последнего соединения использована номенклатура ансамблей (см. подразд. 6).
Номенклатура циклических сульфидов принципиально отличается от номенклатуры, описанной выше для ациклических аналогов. Циклические сульфиды называют, используя номенклатуру гетероциклических соединений (рис. 6.10.6).
Дисульфиды, трисульфиды и т. д., а также полисульфиды называют аналогично моносульфидам (см. выше), добавляя к суффиксу или префиксу серасодержащей группы соответствующую умножающую приставку «ди», «три» и т. д., «поли» (рис. 6.10.7).
Дифенилсульфид англ:. Diphenyl sulfide
Метилэтилсульфид англ.: Ethyl methyl sulfide
1,2-Бис(метилсульфанил)бензол,
1,2-бис(метилтио)бензол (устар.) англ: 1,2-Bis(methylsulfanyl)benzene,
1,2-bis(methylthio)benzene
4,4‘-Т иодибензонитрил англ: 4,4-Thiodibenzonitrile
Рис. 6.10.5
1
4
З-Эти лтетрагидротиоп и ра н англ: 3-Ethyltetrahydrothiopyrane Тривиальное название гетероцикла -тиопиран
2-Метилтиетан англ: 2-methylthietane Название гетероцикла по системе Ганча-Видмана
8-Тиабицикло[3.2.1]октан англ: 8-Thiabicyclo[3.2.1]octane Название по номенклатуре Байера и "а "-номенклатуре
1,7-Дитиациклододекан англ: 1,7-Dithiacyclododecane Название по "а"-номенклатуре
9,10-Дигидро-9,10-эпитиоантрацен англ: 9,10-Dihydro-9,10-epithioanthracene Название по "мостиковой" номенклатуре
Рис. 6.10.6
1070
Новый справочник химика и технолога
S—S \
S—
Дициклопропилдисульфид или дициклопропилдисульфан англ.-. Dicyclopropyl disulfide или dicyclopropyl disulfane
Метилэтилтрисульфид или метилэтилтрисульфан или метилтрисульфанилэтан (зам.) метилтритиоэтан (зам., трад.) англ.-. Ethyl methyl trisulfide или ethyl methyl trisulfane или methyltrisulfanylethane (зам.) methyltrithioethane (зам., трад.)
НзС^
(S)n
'СН3
Диметилполисульфид или диметилполисульфан англ.-. Dimethyl polysulfide или dimethyl polysulfane
s
1,3,5-Трис(метилдисульфанил)бензол,
1,3,5-трис(метилдитио)бензол (трад.) англ.-. 1,3,5-Tris(methyldisulfanyl)benzene,
1,3,5-tris(methyldithio)benzene
9-Антрил(изопропил)трисульфид или
9-антрил(изопропил)трисульфан или
9-(изопропилтрисульфанил)антрацен (зам.) или
9-(изопропилтритио)антрацен (зам., трад.)
англ.-. 9-Anthryl isopropyl trisulfide или
9-anthryl isopropyl trisulfane или
9-(isopropyltrisulfanyl)anthracene (зам.) или
9-(isopropyltrithio)anthracene (зам., трад.),
4-(Фенилдисульфанил)бензонитрил или 4-(фенилдитио)бензонитрил (трад.) англ.-. 4-(Phenyldisulfanyl)benzonitrile или
4-(phenyldithio)benzonitrile (трад.)
2-Нафтилдисульфанилкарбоновая кислота англ.: 2-Naphthyldisulfanylcarboxylic acid
/SO3K s s
Калия З-этилтрисульфан-1 -сульфонат англ.: Potassium 3-ethyltrisulfane-1-sulfonate
О
о
4,4-Дитиодибутанамид или
NH2 4,4'-ДИ сул офанди и иди бута нам ид
«H2fl.:4,4'-Dithiodibutanamide или
4,4'-disulfandiyldibutanamide
Рис. 6.10.7
Современная номенклатура органических соединений
1071
6.10.3. Тиоальдегиды, тиокетоны и родственные соединения (тиоацетали)
Названия тиоальдегидов (RHC=S) и тиокетонов (RR'OS) формируют путем модификации суффикса или префикса (табл. 6.32) в соответствующем альдегиде или кетоне.
В ранних версиях правил IUPAC тривиальные названия альдегидов и кетонов можно было использовать для формирования названия соответствующего тиопроизводного с помощью приставки «тио», например, тиобензальдегид, тиоацетон и т. п. Версия правил IUPAC 1993 г. не рекомендует такой подход.
Сернистые аналоги ацеталей — дитиоацетали R’R^CSR^SR4 и монотиоацетали R'r2C(OR3)SR4,
Построение названий ти
принято называть по заместительной номенклатуре с использованием префиксов «алкилсульфанил» (ранее «алкилтио») и «алкокси», «арилсульфанил» (ранее «арилтио») и «арилокси» и т. д. (названия типа «дитиоацеталь ...альдегида» и т.п. в систематической номенклатуре обычно не используют за исключением особых разделов, например углеводов; при необходимости указывают S- и (9-локанты) (рис. 6.10.8).
Монотиополуацетали типа R'R2C(SRj)OH рассматривают как спирты, замещенные -SR3 группой, а монотиополуацетали типа R*R2C(OR3)SH — как тиолы, замещенные OR3 группой (рис. 6.10.9).
Таблица 6.32
льдегидов и тиокетонов
Модификация суффикса или префикса альдегида или кетона
Пример
Заместительная номенклатура
а) аль —> тиаль
карбальдегид —> карботиальдегид* а)
Бутантиаль англ Butanethia!
Циклопропанкарботиальдегид англ.: Cyclopropanecarbothialdehyde
формил тиоформил
4-Т иоформилбензальдегид англ.-. 4-Thioformylbenzaldhyde
он —> тион
Циклопентан-1,3-дитион англ.: Cyclopentane-1,3-dithione
оксо —> тиоксо
О
nh2
4-(2-Т иоксопропил)бензамид англ.: 4-(2-Thioxopropyl)benzamide
Радикало-функциональная номенклатура
кетон —> тиокетон
а) Для Se-аналогов используются суффиксы «селеналь» («selenal») и «карбоселенальдегид» («carboselenaldehyde»).
З-Метил-1 -метил сульфанил-1 -этоксипентан, 3-метил-1-метилтио-1-этоксипентан (устар.) англ.: 1-Ethoxy-3-methyl-1-methylsulfanylpenthane, 1 -ethoxy-3-methyl-1 -methylthiopenthane
2-(Бензгидрилсульфанил)-2-(метилсульфанил)пропан,
2-(бензгидрилтио)-2-(метилтио)пропан (устар.)
англ.-. 2-(Benzhydrylsulfanyl)-2-(methylsulfanyl)propane,
2-(benzhydrylthio)-2-(methylthio)propane
Рис. 6.10.8
1072
Новый справочник химика и технолога
1 -(Фенэтилсульфанил)бутан-1 -ол, 1 -(Фенэтилокси)бутан-1 -тиол
1-(фенэтилтио)бутан-1-ол (устар.) англ.-. 1-(Phenethyloxy)butane-1 -thiol англ.-. 1-(Phenethylsulfanyl)butan-1-ol
1 -(phenethylthio)butan-l-ol
Рис. 6.10.9
6.10.4. Сульфоксиды, сульфоны и их производные
Соединения общей формулы R*S(O)R2 и R'S(O2)R2 называются соответственно сульфоксидами и сульфонами. Широко употребляемые в литературе радикалофункциональные названия включают в себя слова «сульфоксид» или «сульфон» с перечисленными перед ними в алфавитном порядке названиями заместителей R1 и R2, например, метилэтилсульфон, диметилсульфоксид ит. п. В заместительной номенклатуре группы R'S(O)— и R’S(O2)- рассматриваются как заместители с префиксами соответственно «алкилсульфинил» и «алкилсуль-фонил» (в случае ароматических заместителей «арилсульфинил» и «арилсульфонил») в родоначальном углеводороде R2H, где R2 старше R1 (для Se-аналогов используют префиксы «R-селенинил» («R-seleninyl»), «R-селенонил» («R-selenonyl»)) (рис. 6.10.10).
Кроме того сульфоксиды и сульфоны можно называть как оксопроизводные сульфана с использованием ^-обозначений (см. подразд. 6.4), например: Ph2SO — оксодифенил-Х,4-сульфан.
Префиксы «сульфинил» и «сульфонил-» используются в номенклатуре ансамблей (см. подразд. 6.6) для обозначения двухвалентных групп -S(O)— и -S(O2)—, соединяющих идентичные фрагменты (рис. 6.10.11).
Циклические сульфоксиды и сульфоны называют по гетероциклической номенклатуре как оксиды и диоксиды соответствующих 5-гетероциклов, например, Z,6-тиофен-1,1 -диоксид.
Соединения, содержащие последовательно соединенные группы -S(O)- или -S(O2)~, называют дисульфоксидами, трисульфоксидами..., дисульфонами, трисульфонами и т. д. (рис. 6.10.12).
В номенклатуре азотистых производных сульфоксидов и сульфонов используются родоначальныс названия гипотетических соединений H2S=NH: «сульфимид» и H2S(O)=NH: «сульфоксимид» (рис. 6.10.13).
Соединения RHC=SO и RHC=SO2 следует рассматривать как оксиды и диоксиды соответствующих тиоальдегидов, а соединения R'R2C=SO и R’r2OS02 — как оксиды и диоксиды тиокетонов. Помимо этого, до сих пор используются устаревшие названия этих соединений, образуемые из родоначальных соединений «сульфин» (H2C=SO) и «сульфсн» (H2C=SO2). Более однозначная современная номенклатура этих соединений основана на использовании родоначального названия сульфан с атомом серы соответствующей валентности (рис. 6.10.14).
Пропилэтилсульфоксид (рад.-ф.) или 1-(этилсульфинил)пропан (зам.) англ.-. Ethyl propyl sulfoxide (рад.-ф.) или 1-(ethylsulfinyl)propane (зам.)
1,6-Бис(метилсульфинил)нафталин
англ.-. 1,6-Bis(methylsulfinyl)naphthalene
2-Пиридилфенилсульфон (рад.-ф.) или
2-(фенилсульфонил)пиридин (зам.) англ.-. Phenyl 2-pyridyl sulfone (рад.-ф.) или
2-(phenylsulfonyl)pyridine (зам.)
Метил-4-метилсульфинилфенилсульфон (рад.-ф.) или 1-метилсульфинил-4-метилсульфонилбензол (зам.) англ.-. Methyl 4-(methylsulfinyl)phenyl sulfone (рад.-ф.) или
1 -methylsulfinyl-4-methylsulfonylbenzene (зам.)
Рис. 6.10.10
Современная номенклатура органических соединений
1073
НО'
II
он
3,3-Сульфинилдипропанол англ.-. 3,3-Sulfinyldipropanol
2,4'-Сульфонилдибензамид англ.: 2,4'-Sulfonyldibenzamide
Рис. 6.10.11
Рис. 6.10.12
S
о
/V-Бензил сульфонил-5,5-диметил сульфимид англ.: /V-Benzylsulfonyl-S, S-dimethylsulfimide
5-Метил-Л/-хлор-5-этилсульфоксимид англ.: /V-Chloro-S-ethyl-S-methylsulfoximide
Рис. 6.10.13
Н
англ.
Бензил и де н (о ксо)-Х4-су л ьфа н, тиобензальдегидоксид (трад.), фенилсульфин (устар.) Benzylidene(oxo)-X4-sulfane thiobenzaldehyde oxide, phenyl sulfine
Д ио ксо (ц и кл о гекси л и де н )-Х6-су л ьфа н циклогексантиондиоксид (трад.) англ.: Cyclohexylidene(dioxo)-X6-sulfane cyclohexanethione dioxide
(1-Метилпропилиден)(диоксо)-Х6-сульфан, бутан-2-тиондиоксид (трад.), метилэтилсульфен (устар.)
англ.: (1-Methylpropylidene)(dioxo)-X6-sulfane, butane-2-thione dioxide, ethyl methyl sulfene
Рис. 6.10.14
1074
Новый справочник химика и технолога
6.10.5. Сульфеновые, сульфиновые, сульфоновые кислоты и их производные
Органические оксикислоты серы, в которых органическая часть непосредственно соединена с серой, называются сульфеновыми (не включены в правила IUPAC 1993 г.) (R-S-OH), сульфиновыми (R-S(O)OH) и сульфоновыми кислотами (R-S(O2)OH) (перечислены в порядке увеличения старшинства); их названия сгроят в соответствии с правилами заместительной номенклатуры, употребляя суффикс «сульфеновая, сульфиновая или сульфоновая кислота» (рис. 6.10.15).
Функциональные группы -SOH, -SO2H и -SO3H указываются в названии в виде префиксов соответственно «гидроксисульфанил», «сульфино» и «сульфо», если в молекуле присутствует функциональная группа более высокого старшинства (табл. 6.7) (рис. 6.10.16). В названиях кислот серы, а также их эфиров и солей, в которых один, два или три атома кислорода заменены атомами серы, непосредственно перед суффиксом добавляют инфикс «тио», «дитио» или «тритио» (рис. 6.10.17).
Производные серасодержащих кислот, у которых гидроксильная группа замещена такими функциональными группами, как галогены, -N3, -NC и т. п. (см. табл. 6.29), называют по радикало-функциональной номенклатуре, используя названия для замещающих групп RS-, RSO- и RSO2- соответственно «R-суль-фанил», «R-сульфинил» и «R-сульфонил». Для некоторых сульфонильных замещающих групп существуют тривиальные названия (рис. 6.10.18).
Ниже представлены примеры систематических и полусистематических названий некоторых соединений (рис. 6.10.19).
Если вышепредставленные функциональные группы присутствуют в молекуле наряду с функцией более высокого старшинства и их необходимо указать в названии в качестве заместителей, то используют префиксы типа «хлорсульфанил», «азидосульфинил», «хлорсуль-фонил» и т. д.
Для таких производных серасодержащих кислот как амиды и гидразиды используется заместительная номенклатура, в соответствии с которой, например, названия соединений RSNH2, RSONH2, RSO2NH2 записы-ватся соответственно «...сульфенамид», «...сульфи-намид» и «...сульфонамид» (в русском языке в названиях сульфонамидов слог «он» часто опускается, например «бензолсульфамид»). В случае А-фенилзаме-щенных амидов можно использовать суффикс «анилид» (рис. 6.10.20).
Разрешено использовать следующие тривиальные названия:
Тиураммоносульфид (thiuram monosulfide)
Тиурамдисульфид (thiuram disulfide)
Сульфаниловая кислота (только п-изомер) (sulfanilic acid)
S-ОН
1 -(Г и дро кси суп ьфа н и л )-4-мети л бе нзол, 4-метилбензолсульфеновая кислота (трад.)
англ.: 1-(Hydroxysulfanyl)methylbenzene, 4-methylbenzenesulfenic acid
Бутан-2-сульфиновая кислота
англ.: Butane-2-sulfinic acid
2-Карбамоилэтенсульфоновая кислота англ.: 2-Carbamoylethenesulfonic acid
4-Метил-1,3-бензолдисульфоновая кислота, англ.: 4-Methyl-1,3-benzenedisulfonic acid
Рис. 6.10.15
Современная номенклатура органических соединений
1075
2-[(3-Нитрозо-4-сульфофенил)диазенил]нафталин-1-карбоновая кислота англ.-. 2-[(3-Nitroso-4-sulfophenyl)diazenyl]naphthalene-1 -carboxylic acid
5-Сульфинофуран-2-карбоксимидовая кислота англ.-. 5-Sulfinofuran-2-carboximidic acid
4 5
2-Гидроксисульфанилциклопент-2-енсульфиновая кислота англ.-. 2-Hydroxysulfanylcyclopent-2-enesulfinic acid
Рис. 6.10.16
Бутантиосульфиновая S-кислота англ.-. Butanethiosulfinic S-acid
5-(4-Диметиламинофенил)метандитиосульфонат англ:. S-(4-Dimethylaminophenyl) methanedithiosulfonate
Натрия бензолсульфонотиоат англ:. Sodium benzenesulfonothioate
3,4-Диметилбензолдитиосульфоновая S-кислота
англ:. 3,4-Dimethylbenzenedithiosulfonic S-acid
Рис. 6.10.17
Тозил
(только п-изомер) англ:. Tosyl
О
И 5>
Н3С-S-Мезил
Ц англ:. Mesyl
Рис. 6.10.18
1076
Новый справочник химика и технолога
F
F—г-S \
F CI
Трифторметансульфанилхлорид англ:. Trifluoromethanesulfanyl chloride
Бензолсульфинилазид англ:. Benzenesulfinyl azide
О. ,0
X
Н3С NCS
Тозилхлорид или
4-метилбензолсульфонилхлорид англ:. Tosyl chloride или
4-methylbenzenesulfonyl chloride
Мезилизотиоцианат или метансульфонилизотиоцианат англ:. Mesyl isothiocyanate или methanesulfonyl isothiocyanate
Рис. 6.10.19
Циклогексансульфенамид англ: Cyclohexanesulfenamide
Л/,Л/-Диметилпропан-2-сульфинамид англ.: A/,A/-Dimethylpropane-2-sulfinamide
Нафталин-2-сульфонамид англ: Naphthalene-2-sulfonamide
Метансульфинанилид англ.: Methanesulfinanilide
Рис. 6.10.20
Группы H2NS(O)~, H2NS(O2)- в качестве префиксных заместителей записывают в названия как «сульфинамоил» и «сульфамоил» (рис. 6.10.21). Эти же функциональные группы могут быть присоединены к основному фрагменту молекулы и атомом азота. В этом случае группы RSONH- и RSO2NH- указываются в префиксе как «...сульфинамидо» и «...сульфонамидо» соответственно (рис. 6.10.22).
Ниже представлены примеры названий других азотсодержащих производных (рис. 6.10.23).
В табл. 6.33 представлены суффиксные окончания серасодержащих кислот, у которых кислород заменен на азотсодержащую группу.
В названиях солей и эфиров этих кислот суффикс «овая кислота» заменяется соответственно на окончание «...ат» («...имидат», «...гидразонат», и т.п.). Для построения названий галогенангидридов, а также соединений, в которых эти группы выступают в качестве префиксных заместителей, исходное название кислоты трансформируют в название соответствующей замещающей группы с окончанием «ил» («...имидоил», «...гидразоноил» и т. п.) (рис. 6.10.24).
О
МН2 4-(Л/-Метил-Л/-этилсульфамоил)бензамид или 4-(Л/-метил-Л/-этиламиносульфонил)бензамид англ:. 4-(A/-Ethyl-A/-methylsulfamoyl)benzamide или 4-(A/-ethyl-A/-methylaminosulfonyl)benzamide
Рис. 6.10.21
Современная номенклатура органических соединений
1077
4-(Фенилсульфонамидо)циклопент-1 -ен-1 -карбоновая кислота англ.-. 4-(Phenylsulfonamido)cyclopent-1-ene-1 -carboxylic acid
Рис. 6.10.22
оч ,о
\х//
.NH2
Н3С N
NH II
н3с nh2
Метансульфоногидразид англ.-. Methanesulfonohydrazide
Метансульфинимидамид, метансульфинамидин (устар.) англ.-. Methanesulfinimidamide, methanesulfinamidine
С) NH
X н3с nh2
Метансульфонимидамид англ.-. Methanesulfonimidamide
HN NH
X н3с nh2
Метансул ьфоноди и м идам ид англ.-. Methanesulfonodiimidamide
Рис. 6.10.23
Суффиксные окончания серасодержащих кислот
Таблица 6.33
Группа Кислота Группа Кислота
NH -s'-' он сульфинимидовая (sulfinimidic) ЮН N II —S—ОН II О сульфоногидроксимовая (sulfonohydroximic)
N—NH2 -s" он сульфиногидразоновая (sulfmohydrazonic) NH II —S—ОН II NH сульфонодиимидовая (sulfonodiimidic)
N—ОН -s" он сульфиногидроксимовая (sulfinohydroximic) NH II —S—ОН II S тиосульфонимидовая О-кислота (thiosulfonimidic O-acid)
NH II —S—ОН II О сульфонимидовая (sulfonimidic) NH II —S—SH II О тиосульфонимидовая S'-кислота (thiosulfonimidic S-)
^.NH2 N И —S—ОН II О сульфоногидразоновая (sulfonohydrazonic) ^.nh2 N II —s-он II NH сульфоногидрзонимидовая (sulfonohydrazonoimidic acid)
1078
Новый справочник химика и технолога
N.
ОН
Этил-М-гидроксиметансульфонимидоат англ.-. Ethyl /V-hydroxymethanesulfonimidoate
,NH2 N II н3с—s—Cl II N.
OH
/V-Гидроксиметансульфоногидразонимидоилхлорид англ.-. /V-Hydroxymethanesulfonohydrazonimidoyl chloride
4-(Этилсульфонимидоил)бензойная кислота англ.: 4-(Ethylsulfonimidoyl)benzoic acid
A O NH
OH
Б-Этил-М-метилэтансульфонимидотиоат англ.: S-Ethyl /V-methyl-1-ethanesulfonimidothioate
Рис. 6.10.24
6.10.6. Сультоны и сультамы
Соединения, содержащие группы -S(O2)O- и S(O2)N\ как фрагменты цикла, называются соответственно сультонами и сультамами. Названия этих соединений образуют из названий лактонов (см. подразд. 6.8.8.2), заменяя окончание «карболактон» соответственно на «сультон» или «сультам». При нумерации цикла меньший локант получает атом, соединенный с атомом серы, а не кислорода (рис. 6.10.25).
Сультамы и сультоны могут быть названы альтернативным способом по гетероциклической номенклатуре (см. подразд. 6.3):
1,5-Пентансультон или
1,2Х6-оксатиепан-2,2-диоксид англ.: 1,5-Pentanesultone или
1,2X6-oxathiepane 2,2-dioxide
1,8-Нафталинсультон англ.: 1,8-Naphthalenesultone
8-Бром-1/-/-1,9-феналенсультам
англ.: 8-Вгото-1/-/-1,9-phenalenesultam
Рис. 6.10.25
6.11. Фосфорсодержащие соединения
Номенклатура ШРАС 1979 г. использовала в качестве названий родоначальных гидридов РН3 — термин фосфин (phosphine) и РН5 — термин фосфоран (phosphorane). В настоящее время для тех же гидридов более предпочтительными названиями являются фосфан (phosphane) и Х5-фосфан (X5-phosphane) (см. подразд. 6.4). С использованием этих названий по обычным правилам заместительной номенклатуры
образуются названия фосфорорганических соединений (рис. 6.11.1).
Номенклатура фосфорсодержащих гетероциклов представлена в подразд. 6.3.
Важным разделом номенклатуры соединений фосфора является номенклатура кислот фосфора и их производных, основные принципы которой обсуждаются ниже.
Современная номенклатура органических соединений
1079
Ph
Метил (фенил)этилфосфан, метил(фенил)этилфосфин (трад.) англ.-. Ethylmethylphenylphosphane, ethylmethylphenylphosphine
Метил (4-хлорфенил)циклопропил(этил)-Х5-фосфан, метил(4-хлорфенил)циклопропил(этил)фосфоран (трад.)
a^7/.;(4-Chlorophenyl)cyclopropyl(ethyl)methyl-X5-phosphane,
(4-chlorophenyl)cyclopropyl(ethyl)methylphosphorane
(Пропилэтилфосфанил)уксусная кислота, (пропилэтилфосфино)уксусная кислота (трад.) англ.-. (Ethylpropylphosphanyl)acetic acid,
(ethylpropylphosphino)acetic acid
5-[Фенил(циклогексил)этил-Х5-фосфанил]-1Н-пиррол-3-карбоновая кислота
5-[фенил(циклогексил)этилфосфоранил]-1/7-пиррол-3-карбоновая кислота (трад.)
англ.-. 5-[Cyclohexyl(ethyl)phenyl-Z.5-phosphanyl]-1 /7-руrrole-3-carboxylic acid,
5-[cyclohexyl(ethyl)phenylphosphoranyl]-1/7-pyrrole-3-carboxylic acid
___ (Е)-(Фенилфосфанилиден)ацетонитрил,
=N (Е)-(фенилфосфиниден)ацетонитрил (трад.) англ.-. (E)-(Phenylphosphanylidene)acetonitrile,
(E)-(phenylphosphinidene)acetonitrile
4-(Диэтилфенил-Х5-фосфанилиден)бутановая кислота,
4-(диэтилфенилфосфоранилиден)бутановая кислота (трад.) англ.-. 4-(Diethylphenyl-Z5-phosphanylidene)butanoic acid,
4-(diethylphenylphosphoranylidene)butanoic acid
Рис. 6.11.1
1080
Новый справочник химика и технолога
6,11.1. Кислоты фосфора
Оксокислоты фосфора и производные, содержащие пятивалентный фосфор прямо присоединенный к органической группе, могут быть названы по заместительной номенклатуре как производные соответствующего родоначального соединения (табл. 6.34).
Другие производные могут быть образованы с использованием аффиксов, приведенных в табл. 6.35.
Органические производные кислот фосфора, в том числе содержащие другие главные группы, могут быть названы с использованием префиксов, представленных в табл. 6.36.
Таблица 6.34
Родоначальные кислоты фосфора и их S- и Л-производные
Родоначальное соединение Замещение —ОН на —SH и/или =0 на =S Замещение =0 на =NH
О II Н—Р—ОН 1 Н Фосфиновая кислота (phosphinic acid) s\ /он X Н Н Фосфинотиовая О-кислота (phosphinothioic O-acid) NH II H—P—OH 1 H Фосфинимидовая кислота (phosphinimidic acid)
О. SH < и' хн Фосфинотиовая S-кислота (phosphinothioic S-acid)
% zSH z\ H H Фосфинодитиовая кислота (phosphinodithioic acid)
О II Н—Р-ОН 1 ОН Фосфоновая кислота (phosphonic acid) z0H z\ н OH Фосфонотиовая О, О -кислота (phosphonothioic 0,0 -acid) NH II H—P—OH 1 SH Фосфонимидотиовая кислота (phosphonimidothioic acid)
Оч ZSH z\ н OH Фосфонотиовая О,S -кислота (phosphonothioic О,S-acid)
% zSH z\ H SH Фосфонодитиовая S,S-кислота (phosphonodithioic S,S-acid)
S\\ zSH P4 H SH Фосфонотритиовая кислота (phosphonotrithioic acid)
Рассматриваются кислоты фосфора, в которых атом фосфора прямо соединен с органической группой.
Современная номенклатура органических соединений
1081
Таблица 6.35
Аффиксы заместителей
Префикс Инфикса) Замещаемая группа Замещающая группа
Амидо- / Amido- -амидо- / -amido- -ОН -nh2
Азидо- / Azido- -азидо- / -azido- -ОН -N3
Бром- / Bromo- -бромидо- / -bromido- -он -Вг
Хлор- / Chloro- -хлоридо- / -chlorido- -он -Cl
Цианато- / Cyanato- -цианатидо- / -cyanatido- -он -OCN
Циано- / Cyano- -цианидо- / -cyanido- -он -CN
Дитиоперокси- / Dithioperoxy- -(дитиопероксо)- / -(dithioperoxo)- -О- -S-S-
Фтор- / Fluoro- -фторидо- / -fluorido- -он -F
Иод- / Iodo- -иодидо- / -iodido- -он -I
Изоцианато- / Isocyanato- изоцианатидо- / -isocyanatido- -он -NCO
Изоциано- / Isocyano- -изоцианидо- / -isocyanido- -он -NC
Нитридо- / Nitrido- -нитридо- / -nitrido- -о-, -он sN, =N-, >N-
Тиоцианато- / Thiocyanato- -(тиоцианатидо)- / -(thiocyanatido)- -он -SCN
Изотиоцианате- / Isothiocyanato- -(изотиоцианатидо)- / -(isothiocyanatido)- -он -NCS
Имидо- / Imido- -имидо- / -imido- =0 =NH
Гидразидо- / Hydrazido- -гидразидо- / -hydrazido- -он -NH-NH2
Перокси- / Peroxy- -пероксо-/-peroxo- -0- -0-0-
Селено- / Seleno- -селено- / -seleno- =0,-0- =Se, -Se-
Теллуро- / Telluro- -теллуро- / -telluro- =0, -0- =Te, -Те-
Тио- / Thio- -тио- / -thio- =0,-0- =s, -s-
Тиоперокси- / Thioperoxy- -(тиопероксо)- / -(thioperoxo)- -0- -OS-, -SO-
а) Инфиксами называют приставки, модифицирующие суффиксы, т. е. это «префиксы для суффиксов». Например, в названии «пропантиосульфиновая кислота» модифицирующий префикс «тио», обозначающий замену атома кислорода в суффиксе «сульфиновая кислота» на серу, стоит после основы названия (в данном случае родоначального гидрида «пропан»), и поэтому его корректней называть инфиксом, а не префиксом (инфиксы в скобках в названиях также берутся в скобки).
Таблица 6.36
Префиксы заместителей для построения названий органических производных кислот фосфора
Кислота Замещающая группа Префикс
PH(OH)2 -P(OH)2 дигидроксифосфанил- / dihydroxyphosphanyl-
Фосфонистая кислота / Phosphonous acid -P(OH)O’ гидроксиоксидофосфанил- / hydroxyoxidophosphanyl-
PH2(OH) -РН(ОН) гидроксифосфанил- / hydroxyphosphanyl-
Фосфинистая кислота / Phosphinous acid >Р(ОН) гидроксифосфандиил- / hydroxyphosphanediyl-
=Р(ОН) гидроксифосфанилиден- / hydroxyphosphanylidene-
-Р(ОСН3)2 диметоксифосфанил- / dimethoxyphosphanyl-
>Р(0)(0) фосфинате- / phosphinato-
1082
Новый справочник химика и технолога
Окончание табл. 6.36
Кислота Замещающая группа Префикс
РН(О)(ОН)2 Фосфоновая кислота / Phosphonic acid РН2(О)(ОН) Фосфиновая кислота / Phosphinic acid -Р(О)(ОН)2 >Н(О) -Р(О)(О)2 -Р(О)(ОН)(О) -РН(О)(ОН) -РН2(О) >(О)(ОН) -Р(О)(ОН)(ОСН3) =Р(О) фосфоно- / phosphono-дигидроксифосфорил- / dihydroxyphosphoryl- фосфоноил- / phosphonoyl-гидрофосфорил- / hydropho sphoryl- фосфонато- / phosphonato-гидроксиоксидофосфорил- / hydroxyoxidophosphoryl-гидрогидроксифосфорил- / hydrohydroxyphosphoryl-фосфиноил- / phosphinoyl-дигидрофосфорил- / dihydrophosphoryl-гидроксифосфорил- / hydroxyphosphoryl-гидроксиметоксифосфорил- / hydroxymethoxyphos-phoryl- фосфорил- / phosphoryl-
О
II Ph—Р-ОН
I
Ph
Дифенилфосфиновая кислота
англ:. Diphenylphosphinic acid
ОН
ОН
Этилфосфоновая кислота
англ:. Ethylphosphonic acid
НО
ОН
он
Фосфоноуксусная кислота
англ:. Phosphonoacetic acid
6.12. Радикалы и ионы
6.12.1. Радикалы
Согласно органической номенклатуре родоначальным радикалом называют соединение, получающееся при формальном удалении одного или нескольких атомов водорода от одного или нескольких атомов родоначального гидрида, родоначального соединения или их гидропроизводных. Атом, при котором остается неспаренный электрон, называют радикальным центром. Атом с одним свободным (несвязывающим) электроном называют моновалентным радикальным центром. Атом с двумя (тремя) свободными (несвязывающими) электронами, которые могут быть спаренными, т. е. иметь антипараллельные спины (синглет), или неспаренными, т. е. иметь параллельные спины (триплет), но которые не могут быть несвязывающими электронными парами (неподеленные пары) атома в исходной молекулярной структуре, называется двухвалентным (трехвалентным) радикальным центром. Радикал с двумя или более моновалентными радикальными центрами называется бирадикалом, трирадикалом и т. д.
6.12.1.1. Радикальные центры в родоначальных гидридах
Название молекулы с моновалентным радикальным центром, полученным путем формального отщепления атома водорода от терминального атома насыщенного неразветвленного ациклического углеводорода, насыщенного моноциклического углеводорода, моноядерного родоначального гидрида метана (СН4), силана (SiH4), германа (GeH4), станнана (SnH4) или плюмбана (РЬН4), образуют из названия углеводорода или гидрида, заменяя суффикс «ан» на «ил».
В случае удаления атома водорода из любого положения исходного гидрида название образуют, добавляя суффикс «ил» к названию исходного гидрида. Можно использовать тривиальные названия (например, фенил), а также сокращенные названия: нафтил, антрил, фенантрил, фурил, пиридил, пиперидил, хинолил, изохинолил, тиенил, гидразил. Другие устоявшиеся тривиальные и сокращенные названия, которые используются для наименования замещающих групп в качестве префиксов, а также радикалов, приведены в табл. 6.8. Локанты, показывающие положение радикального центра, помещают перед таким сокращенным названием. Для незамещенных радикалов НО’, НОО’ используются традиционные названия «гидроксил», «гидропероксил» (рис. 6.12.1).
Современная номенклатура органических соединений
1083
6.12.1.2. Двух- и трехвалентные радикальные центры (карбены, карбины, нитрены и силилены)
Двухвалентные радикальные центры, получающиеся при формальном удалении двух атомов водорода от СН4, NH3, SiH4, т. е. :СН2, :NH, :SiH2, могут быть названы (независимо от мультиплетности) как карбен (метилен), нитрен (аминилен) и силилен соответственно. Их производные могут называться в соответствии с обыч
ными принципами заместительной номенклатуры (рис. 6.12.2).
Другие двухвалентные и трехвалентные радикальные центры, получающиеся при формальном удалении атомов водорода от одного и того же скелетного атома, могут быть названы, используя суффиксы «илиден» и «илидин», аналогично тому, как это описано для применения суффикса «ил» для одновалентных радикальных центров (рис. 6.12.3).
Метил
НзС англ.'. Methyl
Гермил
НзСе англ.-. Germyl
СНз-СН2-СН2
Пропил англ.'. Propyl
gh Циклобутил
Н2с—СН2 англ.'. Cyclobutyl
Азанил или аминил, h2n амино (трад.) англ.', azanyl или aminyl, amino
Hg- Сульфанил меркапто (устар.) англ.'. Sulfanyl mercapto
SiH3-SiH-SiH3 Трисилан-2-ил англ.: Trisilan-2-yl
СН3-СН-СН3 CH3-S-S(CH3)2
1-Метил эти л или пропан-2-ил, 1,1,2-Триметил-1А.4-дисульфан-1-ил изопропил (трад.) англ.: 1,1,2-Trimethyl-1X4-disulfan-1-yl
англ.: 1-Methylethyl, propan-2-yl, isopropyl
Бицикло[2.2.1]гептан-2-ил, бицикло[2.2.1]гепт-2-ил (устар.) англ.: Bicyclo[2.2.1 ]heptan-2-yl
2/-/-Пиран-6-ил англ.: 2/-/-Pyran-6-yl
2-Метилциклопента-2,4-диен-1 -ил англ.: 2-Methylcyclopenta-2,4-dien-1-yl
CI3C
С13С
4,5-Бис(трихлорметил)-1,3,2-дитиазол-2-ил англ.: 4,5-Bis(trichloromethyl)-1,3,2-dithiazol-2-yl
Ph2c:
Дифенил карбен или дифенил метилен англ.: Diphenylcarbene или diphenylmethylene
Рис. 6.12.1
Цикло пропили итрен или циклопропиламинилен
англ.: CycloprpyInitrene или cycloprpylaminylene
PhCH2-Si-H
Бензилоилилен англ.: Benzylsilylene
4-Хл орфен ил ка рбин англ.: 4-Chlorophenylcarbyne
Рис. 6.12.2
1084
Новый справочник химика и технолога
H2N—N:
Диазанилиден или гидраз ин ил идеи, аминонитрен (устар.)
англ.-. Diazanylidene или hydrazinylidene
PhCH2—С—Cl
Н2Р—р:
Дифосфанил идеи англ.-. Diphosphanylidene
СН2=СН—С—Н
П ро п-2-ен-1 - ил и де н англ.-. Prop-2-en-1-ylidene
2-Фенил-1-хлорэтилиден, бензилхлоркарбен (устар.) англ.: 1 -С hlo ro-2-phe ny lethy I ide ne
4Н-Т иопиран-4-илиден англ.-. 4H-Thiopyran-4-ylidene
Рис. 6.12.3
6.12.1.3. Радикальные центры на функциональных группах
Для радикальных центров, локализованных на функциональных группах, предпочтительнее строить названия на основе структур, включающих родоначальный гидрид вместе с функциональной группой.
Ряд традиционных названий образуется путем добавления к названию группы (табл. 6.3, 6.4) окончания «л» или «ил» (если они отсутствуют в названии) вместо «о». Например:
НО2С* — «карбоксил»,
НО* — «гидроксил»,
НОО’ — «гидропероксил»,
ОС: — «карбонил»,
OS: — «сульфинил»,
O2S: — «сульфонил»,
О2СГ — «хлорил»,
О3СГ — «перхлорил»;
NC* — «цианил»,
CN’ — «изоцианил»,
ON’ — «нитрозил»,
O2N* — «нитрил»,
*N3 — «азидил» и т. д.
Ацильные радикалы
Радикал, в котором атом халькогена или азота присоединен (формальной) двойной связью к радикальному центру и который может быть рассмотрен как образованный путем удаления гидроксильной группы от любой кислотной функциональной группы, называют, заменяя в названии соответствующей кислоты окончание «овая кислота» или «карбоновая кислота» на «ил», «оил» или «-карбонил» в соответствии с методом образования названия соответствующей ацильной группы (см. подразд. 6.8.8.2) (рис. 6.12.4).
Гексантиоил англ.: Hexanethioyl
Ацетил англ.: Acetyl
Циклопропанкарбонил англ.: Cyclopropanecarbonyl
Терефталоил Бензол-1,4-дисульфинил Диметилфосфиноил
англ.: Terephthaloyl англ.: Benzene-1,4-disulfinyl англ.: Dimethylphosphinoyl
Рис. 6.12.4
Современная номенклатура органических соединений
1085
Радикальные центры на атоме азота аминной, иминной, амидной или имидной функциональных групп
Одновалентные радикальные центры, формально получающиеся при удалении одного атома водорода от аминной, иминной, амидной или имидной функциональных фупп, называют, заменяя в названии суффикс соответствующей функциональной группы на суффикс «ами-нил», «иминил», «амидил», «карбоксамидил», «сульфон-амидил» и т. д. Двухвалентные радикалы, образующиеся при формальном удалении обоих атомов водорода от аминной или амидной фупп, называются как производные нитрена, аминилена или X1-азана.
Ацетилнитрен или ацетиламинилен или ацетил-Х1-азан
англ.: Acetylnitrene или acetylaminylene или acetyl-X1-azane
Радикальные центры на атоме кислорода кислотной, надкислотной,гидроксильной или гидропероксильной функциональных групп
Радикалы, формально получающиеся при удалении атома водорода от атома кислорода кислотной, надкислотной, гидроксильной или гидропероксильной функциональных фупп, называют, добавляя к названию родоначального гидрида или кислотного остатка, присоединенного к атому кислорода, суффикс «оксил» или «пероксид». Для ряда радикалов используются сокращенные названия: метоксил, этоксил, пропоксил, бутоксил, феноксил, ацетоксил, аминоксид. В сложных названиях, построенных по заместительной номенклатуре, название исходного незамещенного радикала (за исключением приведенных сокращенных названий) заключается в скобки (рис. 6.12.5).
Этоксил англ.'. Ethoxyl
О
Н5С2-о’
Бромацетоксил англ;. Bromoacetoxyl
Пентаноилпероксил англ; Pentanoylperoxyl
Метокси[(тиоацетил)оксил] англ.: Methoxy[(thioacetyl)oxyl]
2,2,6,6-Тетраметил(пиперидин-1-илоксил) англ;. 2,2,6,6-Tetramethyl(piperidin-1-yloxyl)
N 0 (1-трет-Бутил-2,2-диметилпропилиден)аминоксил англ.: (1 -tert-Butyl-2,2-dimethylpropylidene)aminoxyl
Рис. 6.12.5
Радикальные центры на атоме серы тиокислотной, тиольной или дитиогидропероксильной функциональных групп
Хотя радикалы, формально получающиеся при удалении атома водорода от атома серы тиокислотной, тиольной или дитиогидропероксильной функциональных фупп, могут быть называны аналогично соответствующим кислородным радикалам путем использова
ния суффиксов «тиил» или «пертиил», более предпочтительными являются названия, построенные на основе родоначальных названий соответствующих радикалов «сульфанил», «дисульфанил» и т. д., см. рис. 6.12.6.
Соединения с радикальными центрами на других функциональных фуппах обычно называют на основе правил, изложенных для радикальных центров в родоначальных гидридах (подразд. 6.12.1.1), см. рис. 6.12.7.
1086
Новый справочник химика и технолога
Н5С6—S'
Фенилсульфанил или фенилтиил англ:. Phenylsulfanyl или phenylthiyl
А цетил сульфанил или ацетилтиил англ: Acetylsulfanyl или acetylthiyl
Этокси[(тиоацетил)сульфанил] или этокси[(тиоацетил)тиил] англ: Ethoxy[(thioacetyl)sulfanyl] или
ethoxy[(thioacetyl)thiyl]
Рис. 6.12.6
H5c6-o-s
Феноксисульфанил англ:. Phenoxysulfanyl
Ph
—s—О-О о
(Бензоилсульфанил)диоксиданил бензоил(сульфанилпероксил)
англ:. (Benzoylsulfanyl)dioxidanyl benzoyl(sulfanylperoxyl)
(1 -Гидроксипропилиден)азанил или (1-гидроксипропилиден)аминил или 1-гидроксипропан-1-иминил англ:. (I-Hydroxypropylidene)azanyl или
(l-hydroxypropylidene)aminyl или
1 -hydroxypropan-1 -iminyl
Рис. 6.12.7
6.12.1.4. Полирадикалъные центры
Полирадикалы с радикальными центрами на разных скелетных атомах родоначальных гидридов или их гидропроизводных, получающиеся при формальном удалении одного или нескольких атомов водорода от каждого из двух или более скелетных атомов, называют, используя суффиксы «ил», «илиден», «илидин» с соответствующими локантами и умножающими префиксами, см. рис. 6.12.8а и 6.12.86.
Для наименовании полирадикалов с радикальными центрами, находящимися в родоначальных гидридах или на функциональных ipynnax идентичных структурных единиц, которые расположены в различных частях молекулы (исключая полиацильные или поли-имидные радикалы), может использоваться номенклатура ансамблей, например см. рис. 6.12.9.
Префикс заместителя с радикальным центром, образуют, добавляя префикс «ило» к названию замещающей группы (рис. 6.12.10).
HN—NH
Диазан-1,2-диил, гидразо (трад.) англ.: Diazane-1,2-diyl, hydrazo
Н2С-СН2
Этан-1,2-диил, этилен (трад.) англ.: Ethane-1,2-diyl, ethylene
Бензол-1,4-диил, и-фенилен (трад.), 1,4-фенилен (трад.) англ.: Benzene-1,4-diyl, p-phenylene, 1,4-phenylene
Рис. 6.12.8a
Современная номенклатура органических соединений
1087
1-Оксо-4-циклопропилбутан-1,4-диил англ.-. 4-Cyclopropyl-1-oxobutane-1,4-diyl
Циклогексан-1 -ил-3-ил идеи англ.-. Cyclohexan-1-yl-3-ylidene
Рис. 6.12.86
Циклопропан-1,2-диилдиметил англ.-. Cyclopropane-1,2-diyldimethyl
Этиленбис(азанил) или этиленбис(аминил) англ.-. Ethylenebis(azanyl) или ethylenebis(aminyl)
Нафталин-2,б-диилбис(дисульфанил) англ.-. Naphthalene-2,6-diylbis(disulfanyl)
Рис. 6.12.9
н2с-|-
Илометил англ.-, ylomethyl
HN-|-
Илоамино англ.: yloamino
6-1-
Илоокси, неправильно: илогидрокси англ.: Ylooxy
4-Илофенил англ.: 4-ylophenyl
2,5-Диило-2,5-диметилгептил
англ.: 2,5- Di methyl-2,5-diyloheptyl
Рис. 6.12.10
6.12.2. Катионы
Согласно органической номенклатуре катион представляет собой молекулу с по крайней мере единичным положительным зарядом, получающуюся при формальном присоединении одного или нескольких протонов, при формальном удалении одного или нескольких гид-рид-ионов или при комбинации этих операций. Атом, несущий положительный заряд, называется катионным центром. Катионы с двумя или более катионными центрами называются дикатионами, трикатионами и т. д.
6.12.2.1. Катионы с катионными центрами, получающимися в результате присоединении протонов
Катионные центры в родоначальных гидридах
Родоначальные катионы, получающиеся при формальном присоединении одного протона к родоначаль
ным одноядерным гидридам азота, халькогенов или галогенов в их стандартном валентном состоянии, называют, добавляя суффикс «оний» к основе для данного элемента, как показано в табл. 6.37.
Катионные центры, получающиеся при формальном присоединении одного или нескольких протонов к любому положению нейтрального родоначального гидрида, исключая приведенные в табл. 6.37, называют, добавляя к названию гидрида суффикс «ий», «диий», «триий» и т. д. (рис. 6.12.11).
Катионные центры на функциональных группах
Катионные центры, получающиеся при формальном присоединении одного протона к функциональной группе, называют путем добавления катионного суффикса из табл. 6.38 к названию соответствующего родоначального гидрида.
1088
Новый справочник химика и технолога
Когда один из вышеуказанных суффиксов в названии подразумевает наличие в молекуле двух (или более) одинаковых функциональных I'pynn, как например,
в названии «малонамид», соответствующий катионный суффикс обозначает присоединение по протону к каждой функциональной группе (рис. 6.12.12).
Таблица 6.37
Названия одноядерных родоначальных катионов в систематической заместительной номенклатуре 1UPAC
h4n+ аммоний (ammonium) H3Se+ селеноний (selenonium)
Н4Р+ фосфоний (phosphonium) H3Te+ теллуроний (telluronium)
H4As+ арсоний (arsonium) h2f+ фтороний (fluoronium)
H4Sb+ стибоний (stibonium) H2CI+ хлороний (chloronium)
H4Bi+ висмутоний (bismuthonium) H2Br+ бромоний (bromonium)
н3о+ оксоний (oxonium) H2I+ иодоний (iodonium)
H3S+ сульфоний (sulfonium)
(CH3)4N+
Тетраметиламмоний англ.-. Tetramethylammonium
С1(С2Н5)3Р+
Хлортриэтилфосфоний англ.: Chlorotriethylphosphonium
(CH3)2S+H
Диметилсульфоний англ.: Dimethylsulfonium
Ph2l+
Дифенилиодоний англ.: Diphenyliodonium
Н5С+ Метаний англ.: Methanium
СН3—S+F4
Метил (тетрафтор)-Х4-сульфаний англ.: Tetrafluoro(methyl)-X4-sulfanium
(H3C)2N-N+(CH3)3
Пентаметилдиазаний, пентаметилгидразиний (трад.) англ.: Pentamethyldiazanium, pentamethylhydrazinium
(Н3О0-0+(СН3)г
Вг2Р-Р+(СН3)3
Т риметилдиоксиданий 2,2-Дибром-1,1,1 -триметилфосфан-1 -ий
англ.: trimethyldioxidanium англ.: 2,2-Dibromo-1,1,1-trimethyldiphosphan-1-ium
Бензолий англ.: Benzenium
н-о о—н
1,4-Диоксан-1,4-диий англ.: 1,4-Dioxane-1,4-diium
1,1 '-Диметил[4,4'-бипиридин]-1,1 '-диий англ.: 1,T-Dimethyl[4,4'-bipyridine]-1 ,T-diium
Рис. 6.12.11
Современная номенклатура органических соединений
1089
Таблица 6.38
Катионные суффиксы
Суффикс функциональной группы Катионный суффикс
овая кислота, только для оксокислот (-ic acid) амид (-amide) имид (-imide) нитрил (-nitrile) амин (-amine) имин (-imine) овый ацидий (-ic acidium) амидий (-amidium) имидий (-imidium) нитрилий (-nitrilium) аминий (-aminium) иминий (-iminium)
Л/,Л/-Диметилацетимидовый ацидий или (1-гидроксиэтил иден)диметиламмоний англ.-. Л/, /V-Dimethylacetimidic acidium или
(l-hydroxyethylidene)dimethylammonium
CI2N N
Л/,Л/-Дихлор-3-(дихлорамино)проп-2-ен-1-иминий или дихлор[3-(дихлорамино)проп-2-ен-1-илиден]аминий англ.-. /V,/V-Dichloro-3-(dichloroamino)prop-2-en-1-iminium или
dichloro[3-(dichloroamino)prop-2-en-1-ylidene]aminium
Л/,Л/,А/-Триметилбензамидий англ.-. A/,A/,/V-Trimethylbenzamidium
Глутаронитрилий англ.-. Glutaronitrilium
2-Карбокси-Л/'Л/'-диметил-Л/,Л/-диэтилциклопентан-1-карбоксимидамидий анг-i.: 2-Carboxy-A/,A/-diethyl-W,W-dimethylcyclopentane-1-carboximidamidium
Рис. 6.12.12
Уронивые ионы и их халькогеновые аналоги
Катионные центры, получающиеся при формальном присоединении одного протона к мочевине (или тиомочевине), называют, используя в качестве основы катион «уроний», который может быть представлен следующими таутомерными структурами:
О ОН
+А — +Д
H3N NH2 H2N—'NH2
При необходимости используют локанты, принятые для соответствующих соединений. Халькогеновые аналоги называют, используя в качестве основы катионы
«тиоуроний» и т. д. Когда невозможно сделать выбор между несколькими формами, используют локанты N, N’ и О, S и т. п. (рис. 6.12.13).
Катионные центры на других функциональных группах
Катионные центры, получающиеся при формальном присоединении одного или нескольких протонов к другим функциональным группам, называют, добавляя к названию соответствующего соединения суффикс «ий», «диий» и т. д., или используют в качестве основы катионные родоначальные гидриды, название которых сформировано в соответствии с вышеизложенными правилами (рис. 6.12.14).
1090
Новый справочник химика и технолога
1,3-Диметил-2-фенилуроний англ.-. 1,3-Dimethyl-2-phenyluronium
/V-Метил-А/', S-дифенилтиоуроний англ.-. /V-Methyl-/V',S-diphenylthiouronium
Рис. 6.12.13
Пролиний англ.-. Prolinium
О
2,2-Диметилгуанидиний англ.-. 2,2-Dimethylguanidinium
Этилиденоксоний англ.: Ethylideneoxonium
Бензоилдиметил сульфоний англ.: Benzoyldimethylsulfonium
Рис. 6.12.14
6.12.2.2. Катионы с катионными центрами, получающимися при отщеплении гидрид-ионов
Радикало-функциональные названия
Катионы, которые получаются при формальном удалении электронов от радикала, могут быть названы по радикало-функциональной номенклатуре путем добавления слова «-катион» («-дикатион», «-трикатион» и т. д.) (рис. 6.12.15). Правила заместительной номенклатуры такого рода катионов обсуждаются ниже.
Катионные центры в родоначальных гидридах
Название молекулы с катионным центром, полученным путем формального отщепления одного гидрид-иона от терминального атома насыщенного неразветв-ленного ациклического углеводорода, насыщенного моноциклического углеводорода, моноядерного родоначального гидрида (метана (СН4), силана (SiH4), германа (GeH4), станнана (SnH4) или плюмбана (РЬН4)), образуют, заменяя в соответствующем названии суффикс «ан» на «илий», см. рис. 6.12.16.
chJ
Метил-катион англ.: Methyl cation
CIHNH
Другие катионные центры, полученные путем формального отщепления одного или нескольких гидрид-ионов из любого положения исходного гидрида или гидропроизводного, называют, добавляя к соответствующему названию суффикс «илий», «бис(илий)», «трис(илий)» и т. д. Можно использовать тривиальные названия фени-лий для [С6Н5] . а также сокращенные названия нафти-лий, антрилий, фенантрилий; локанты, показывающие положение радикального центра, помещают перед сокращенным названием. Для образования названий катионов производных моноядерных родоначальных гидридов РН3 и AsH3 в качестве основы следует использовать систематические названия фосфан и арсан, а не фосфин и арсин. Для незамещенных катионов НО4, НОО+ используются традиционные названия — «гидроксилий», «гидропероксилий» (рис. 6.12.17).
Ионы диазония содержат группу -N2+, присоединенную к родоначальному гидриду; их традиционно называют, добавляя суффикс «диазоний» к названию гидрида. Можно также использовать названия на основе катиона диазенилия, HN=N+ (рис. 6.12.18).
Ацетил-катион
w англ.: Acetyl cation
Хлоразанил-катион
или хлораминил-катион англ.: Chloroazanyl cation
или chloroaminyl cation
+ + н2с-сн2
Этан-1,2-диил-дикатион англ.: Ethane-1,2-diyl dication
Циклогексилиден-дикатион англ.: Cyclohexylidene dication
Рис. 6.12.15
Современная номенклатура органических соединений
1091
Н3С+
Метилий или карбений англ.-. Methylium или carbenium
+ н2с-сн н2с-сн2
Циклобутилий англ.-. Cyclobutylium
+ (CH3)2HGe
Диметилгермилий англ.-. Dimethylgermylium
+
СН3-СН3-СН2
Пропилий англ.-. Propylium
Рис. 6.12.16
H2N+
Азанилий или аминилий или нитрений
англ.-. Azanylium или aminylium или nitrenium
(СН3)4Р+
PhS+
Фенилсульфанилий англ.-. Phenylsulfanylium
SiH3-SiH-SiH3
Трисилан-2-илий
англ.-. Trisilan-2-ylium
Тетраметил-^5-фосфанилий или тетраметилфосфоранилий или тетраметилфосфоний
Tetramethyl-^5-phosphanylium или tetramethylphosphoranylium или tetramethylphosphonium
+ сн3-сн-сн3
1-Метилэтилий или пропан-2-илий, изопропилий (трад.)
англ.: 1-Methylethylium или prop-2-ylium
Фуран-2-илий англ.-. Furan-2-ylium
Спиро[4.5]декан-8-илий англ.: Spiro[4.5]decan-8-ylium
3,5-Диметил-1,4-ди гидропиридин-1 -илий или 3,5-диметилпиридин-1(4Н)-илий англ.: 3,5-Dimethyl-1,4-dihydropyridin-1-ylium или 3,5-dimethylpyridin-1 (4/-/)-ylium
+ H2 +
H2C-C-CH2
Пропан-1.З-бис(илий)
пропан-1,3-диилий (устар.) англ.: Propane-1,3-bis(ylium)
2+ н3с-с-сн3
Пропан-2,2-бис(илий) англ.: Propane-2,2-bis(ylium)
Рис. 6.12.17
h3c-n2
N2
n2
Метандиазоний или метилдиазенилий англ.: Methanediazonium или methyldiazenylium
Бензол-1,4-бис(диазоний) или
1,4-фениленбис(диазенилий) англ.: Benzene-1,4-bis(diazonium) или
1,4-phenylenebis(diazenylium)
Рис. 6.12.18
1092
Новый справочник химика и технолога
Ряд устоявшихся тривиальных и сокращенных названий радикалов (табл. 6.8) может быть использован для образования названий монокатионов путем замены радикального суффикса «ил» на суффикс «илий», например: винилий, тритилий и т. д.
6.12.2.3. Катионные центры на функциональных группах
Ациливые ионы
Катионы, в которых атом халькогена или азота присоединен (формальной) двойной связью к катионному центру и образование которых может быть представлено как формальное удаление гидроксид-иона (ОН ) от любой кислотной функциональной группы (кроме пе-роксикислотной), называют, заменяя в названии соответствующей кислоты окончание «овая кислота» на «илий» или иногда на «оилий», а «карбоновая кислота» — на «карбонилий»:
Ацетилий англ.-. Acetylium
Циклопропанкарбонилий англ.-. Cyclopropanecarbonylium
Диметилфосфиноилий англ.: Dimethylphosphinoylium
Глутарилий или пентандиоилий англ.: Glutarylium или pentanedioylium
Гексантиоилий англ.: Hexanethioylium
Монокатионные центры на атоме азота аминной, иминной, амидной или имидной функциональных групп
Одновалентные катионные центры, формально получающиеся при удалении гидрид-иона от аминной, имин
ной, амидной или имидной функциональных групп, называют, добавляя к суффиксу соответствующей функциональной группы суффикс «илий», см. рис. 6.12.19.
Катионные центры на атоме кислорода кислотной, надкислотной,гидроксильной
или гидропероксильной функциональных групп
Катионные центры, формально получающиеся при удалении гидрид-иона от атома кислорода кислотной, надкислотной, гидроксильной или гидропероксильной функциональных групп, называют, добавляя к названию родоначального гидрида или кислотного остатка, присоединенного к атому кислорода, суффикс «окси-лий» или «пероксилий». Для ряда катионов используются сокращенные названия: метоксилий, этоксилий, пропоксилий, бутоксилий, фсноксилий, ацетоксилий, аминоксилий. В сложных названиях, построенных по заместительной номенклатуре, название основы (за исключением приведенных сокращенных названий) заключается в скобки, см. рис. 6.12.20.
Катионные центры на атоме серы тиокислотной, тиольной или дитиогидропероксильной функциональных групп
Хотя катионы, формально получающиеся при удалении гидрид-иона от атома серы тиокислотной, тиольной или дитиогидропероксильной функциональных групп, могут быть названы аналогично соответствующим кислородным радикалам путем использования суффиксов «тиилий» или «пертиилий», более предпочтительными являются названия, построенные на основе родоначальных названий соответствующих радикалов «сульфанилий» или «дисульфанилий», см. рис. 6.12.21.
Катионные центры на других функциональных группах, формально получающиеся при удалении гидрид-иона, называют на основе правил, изложенных выше для катионных центров в родоначальных гидридах.
H3CHN+
Метанаминилий англ.: Methanaminylium
h5c6-hn+ Анилинилий или бензоламинилий англ.: Anilinylium или benzenaminylium
Циклопентаниминилий или циклопентилиденаминилий англ.: Cyclopentaniminylium или cyclopentylideneaminylium
Ацетамидилий англ.: Acetamidylium
Сукцинимидилий или
2,5-диоксопирролидин-1-илий англ.: Succinimidylium или
2,5-dioxopyrrolidin-1-ylium
Рис. 6.12.19
Современная номенклатура органических соединений
1093
Н5С2-О+
Зтоксилий \|-О+ Диметиламиноксилий
англ.-. Ethoxylium / Dimethylaminoxylium
Бромацетоксилий англ.-. Bromoacetoxylium
трет-Бутилпероксилий англ.-. tert-Butylperoxylium
Метокси[(тиоацетил)оксилий] англ.-. Methoxy[(thioacetyl)oxylium]
Рис. 6.12.20
PhS+
Фенилсульфанилий или фенилтиилий англ.-. Phenylsulfanylium или phenylthiylium
Ацетилсульфанилий или ацетилтиилий
англ.-. Acetylsulfanylium или acetylthiylium
Этокси[(тиоацетил)сульфанилий] или этокси[(тиоацетил)тиилий]
англ.-. Methoxy[(thioacetyl)sulfanylium] или methoxy[(thioacetyl)thiylium]
PhS-S+
Фенилдисульфанилий или фенилпертиилий англ.-. Phenyldisulfanylium или phenylperthiylium
(2,2-Дихлорэтил)сульфанилий или
2,2-дихлор(этилтиилий)
англ.-. (2,2-Dichloroethyl)sulfanylium или
2,2-dichloro(ethylthiylium)
Рис. 6.12.21
6.12.2.4. Гетероциклические катионы, получающиеся в результате образования дополнительной связи с гетероатомом
Гетероциклические катионы с катионным центром на гетероатоме, который имеет на одну связь больше, чем в нейтральном гетероцикле, называют, добавляя суффикс «илий» к названию нейтрального гетероцикла, в котором данный гетероатом связан по крайней мере с одним атомом водорода. При этом для описания нестандартного валентного состояния гетероатома используется ^.-обозначение.
Для описания катионных гетероциклических систем также удобно использовать заменительную «а»-номен-
клатуру (см. подразд. 6.3.5). Катионные замещающие префиксы получают, заменяя окончание «а» в соответствующих префиксах из табл. 6.13 на окончание «ониа» для катионных центров, имеющих число связей на единицу больше, и «илиа» — для катионных центров, имеющих число связей на единицу меньше (исключение: висмут — висмутониа) (рис. 6.12.21).
Используя те же принципы, можно называть и ациклические катионные гетероатомные системы (рис. 6.12.22).
Следующие устоявшиеся тривиальные и сокращенные названия можно применять для наименования халькогеновых производных (включая Se и др.), см. рис. 6.12.23.
1094
Новый справочник химика и технолога
Азониа Тиониа
англ.-. Azonia англ.-. Thionia
L I 1 +
Иодониа Боранилиа Азанилиа англ.-, lodonia англ.; Boranylia англ.: Azanylia
3/-/-А.4-Тиофен-1-илий 5А.5-Фосфаспиро[4.4]нонан-5-илий-1-ил или
англ.; 3/-/-A.4-Thiophen-1-ylium 5-фосфониаспиро[4.4]нонан-1-ил
англ.; 5A.5-Phosphaspiro[4.4]nonan-5-ylium-1-yl или
5-phosphoniaspiro[4.4]nonan-1-yl
1 /-/-4А.5-Индолизин-4-илий англ.; 1/-/-4A.5-lndolizin-4-ylium
5А.5,11А.5-Дипиридо[1,2-а:Г,2'-с0пиразин-5,11-бис(илий) англ.: 5А.5,11 A.5-Dipyrido[1,2-а: r,2'-d]pyrazine-5,11 -bis(ylium)
СйО
5/-/-5А.3-Дибензоиодол-5-илий или 9/-/-9А.3-иодафлуорен-9-илий
Н I англ.; 5/-/-5A.3-Dibenzoiodol-5-ylium или
9/-/-9A3-iodafluoren-9-ylium
4/-/-7А.5-Пиримидо[1,2,3-сс0пурин-7-илий
англ.; 4/-/-7A.5-Pyrimido[1,2,3-ccflpiirin-7-ylium
Рис. 6.12.21
6,9,9-Триметил-3,12-диокса-6-тиониа-9-азониатетрадекан или 6,9,9-триметил-3,12-диокса-6-тиа-9-азатетрадекан-6,9-диий
англ.; 6,9,9-Trimethyl-3,12-dioxa-6-thionia-9-azoniatetradecane или
6,9,9-trimethyl-3,12-dioxa-6-thia-9-azatetradecane-6,9-diium
Рис. 6.12.22
Современная номенклатура органических соединений
1095
Е=О:Пирилий
E=S: Тиопирилий англ.: Е=О: Pyrylium
E=S: Thiopyrylium
Е=О: Изохроменилий
E=S: Изотиохроменилий англ.: Е=О: Isochromenylium
л w E=S: Isothiochromenylium
E=O: Хроменилии
E=S: Тиохроменилий англ.: E=O: Chromenylium
E=S: Thiochromenylium
E=O: Флавилий
E=S: Тиофлавилий англ.: E=O: Flavylium
E=S: Thioflavylium
Рис. 6.12.23
E=O: Ксантилий
E=S: Тиоксантилий англ.: E=O: Xanthylium
E=S: Thioxanthylium
6.12.2.5. Поликатионные центры
Поликатионы с однотипными катионными центрами в нескольких положениях родоначального гидрида называют, используя описанные выше суффиксы «ий» или «илий» с умножающими приставками (см. также приведенные выше примеры) (рис. 6.12.24).
Кроме того, название таких поликатионов может быть образовано на основе номенклатуры ансамблей идентичных единиц (рис. 6.12.25).
Соединения с несколькими катионными центрами в родоначальном гидриде, по крайней мере один из которых образован присоединением протона к скелету, а другой (по крайней мере один) — отщеплением гидрид-иона, называют, добавляя суффикс «ий» к названию родоначального гидрида, за которым следует суффикс «илий» с соответствующими умножающими приставками и локантами. При наличии выбора низшие локанты относят к катионным центрам не «илисвого» типа (рис. 6.12.26).
Названия поликатионов, состоящих из катионных функциональных групп, присоединенных к родоначальным катионным гидридам, могут быть образованы путем добавления катионного суффикса функциональной группы к названию катионного гидрида. При нали
чии выбора меньший локант получает скелетный катионный центр, например см. рис. 6.12.27.
Соединения с катионными центрами и в основе и в заместителях могут быть названы путем добавления к названию той части структуры, которая содержит наибольшее число катионных центров, префиксов остальных катионных фрагментов. Префиксы для моноядер-ных родоначальных катионов образуются путем замены окончания «оний» в родоначальном катионе на «онио». Префиксы для монокатионных полиядерных родоначальных гидридов со свободной валентностью у гете-роатомного катионного центра образуют путем замены окончания «ий» в родоначальном катионе на «ио», см. рис. 6.12.28.
Префиксы для других катионных заместителей могут быть образованы путем добавления суффиксов «ил», «илиден», «диил» и т. д. (с соответствующими локантами) к названию родоначального катиона. (рис.6.12.29). (Примеры использования катионных префиксов см. в подразд. 6.12.2.4).
Традиционное название «диазонио» относится как к структуре -N’WN, так и -N=N+, тогда как систематическое название диазин-1-ий-1-ил относится к первой, а диазен-2-илий-1 -ил — ко второй.
I + N, N, N', N -Тетраметил пропан-1.З-бис(аминий)
англ.: N,N,N',N'-Tetramethylpropane-1,3-bis(aminium)
Рис. 6.12.24
Н3Р
1,4-Фениленбис(фосфоний) англ.: 1,4-Phenylenebis(phosphonium)
1,1 '-Оксидициклогепта-2,4,6-триен-1 -илий англ.: 1 ,T-Oxydicyclohepta-2,4,6-trien-1-ylium
Рис. 6.12.25
1096
Новый справочник химика и технолога
1-Метил-5Н-циклогепта[Ь]пиридин-1-ий-5-илий или 1-метил-5/-/-1-азониабензоциклогептен-5-илий англ.-. 1-Methyl-5/-/-cyclohepta[b]pyridin-1-ium-5-ylium или
1 -methyl-5H-1 -azoniabenzocyclohepten-5-ylium
Рис. 6.12.26
—N—
Л/,Л/,Л/,2-Тетраметил-2,6-нафтиридин-2-ий-5-аминий, а не Л/,Л/,Л/,6-тетраметил-2,6-нафтиридин-6-ий-1-аминий англ.-. A/,A/,A/,2-Tetramethyl-2,6-naphthyridin-2-ium-5-aminium, а не A/,A/,A/,6-tetramethyl-2,6-napthyridin-6-ium-1-aminium
Рис. 6.12.27
4-nh3
Аммонио англ.-. Ammon io
-^-SeH2
Селенонио
англ.-. Selenonio
-|-|ph
Фенилиодонио англ.-. Phenyliodonio
Пиридинио
англ.-. Pyridinio
-pci3
Т рихлорфосфонио англ.: Trichlorophosphonio
HN~N=NH
Триаз-2-ен-1-ио англ:. Triaz-2-en-1-io
Рис. 6.12.28
Ннсн3-сн3
Этан-1-ий-1-ил
=сн
Метанилийилиден англ: Ethan-1-iuт-1-уI англ: Methanyliumylidene
=N(CH3)2
Диметилазанийилиден англ: Dimethylazaniumylidene
1-Метилпиридин-1-ий-4-ил англ: 1-Methylpyridin-1-ium-4-yl
4-Метилпиразин-1,4-диий-1-ил англ.: 4-Methylpyrazine-1,4-diium-1 -у!
1 -Метил-1 -азониабицикло[2.2.1 ]гептан-2-ил или
1 -метил-1 -азабицикло[2.2.1 ]гептан-1 -ий-2-ил англ:. 1-Methyl-1-azoniabicyclo[2.2.1]heptan-2-yl или
1 -methyl-1 -azabicyclo[2.2.1 ]heptan-1 -ium-2-yl
Рис. 6.12.29
6.12.3. Анионы
Согласно органической номенклатуре анион — это молекула с но крайней мере единичным отрицательным зарядом, которая получается либо при формальном присоединении одного или нескольких гидрид-ионов, либо при формальном удалении одного или нескольких протонов или при комбинации этих операций. Атом, несущий отрицательный заряд, называется анионным центром. Анионы с двумя или более анионными центрами называются дианионами, трианионами и т. д.
6.12.3.1. Анионы с анионными центрами, получающимися при отщеплении протонов
Радикало-функциональные названия
Анионы, которые получаются в результате формального присоединения электронов к соответствующим радикалам, могут быть названы по радикалофункциональной номенклатуре путем добавления слова «-анион» после названия радикала. По этой схеме полианионы называют, добавляя умножающие приставки «ди», «три» и т. д. к слову «анион», см. рис. 6.12.30.
Современная номенклатура органических соединений
1097
Правила заместительной номенклатуры анионов такого типа обсуждаются ниже.
Анионные центры в родоначальных гидридах
Анионные центры, получающиеся при формальном отщеплении одного или нескольких протонов от нейтрального родоначального гидрида, называют, добавляя к названию этого гидрида суффикс «ид» или «диид» и т. д. Можно использовать тривиальные названия «амид» и «имид» для анионов HN” и HN2 , «ацетилид» (acetylide) — для fC2]2 . Традиционные названия анионов НО , НОО и HS“, HSS соответственно «гидро
ксид», «гидропероксид» и «гидросульфид», «гидродисульфид» не используются в качестве основы в заместительной номенклатуре (рис. 6.12.31).
В тех случаях, когда в нейтральной циклической системе (с максимальным числом некумулированных двойных связей) недостаточно атомов водорода для формирования названия аниона с использованием суффикса «ид», название образуют из названия соответствующего дигидропроизводного. При этом для «гидрирования» могут быть использованы как «обозначенный» водород, так и неотделяемые префиксы «гидро», как проиллюстрировано на приведенных ниже примерах (рис. 6.12.32).
О
Фенил-анион англ.-. Phenyl anion
Ацетил-анион Этанаминил-анион или
англ.-. Acetyl anion этилазанил-анион
англ.-. Ethanaminyl anion или ethylazanyl anion
1,4-Дигидронафталин-1,4-Диил-дианион англ.-. 1,4-Dihydronaphthalene-1,4-diyl dianion
Н3С.-,СН3 н
Пропан-2-ид англ.-. Propan-2-ide
Рис. 6.12.30
2,4-Дихлорбензол-1 -ид
англ.: 2,4-Dichlorobenzen-1-ide
(NC)3C'
Т рицианометанид англ.: Tricyanomethanide
0-0“
H3C-NH"
3-Метилбут-1-ин-1-ид Метиламид или метилазанид
англ.: 3-Methylbut-1-yn-1-ide англ.: Methylamide или methylazanide
Дифенилметандиид англ.: Diphenylmethanedi ide
Ph-N2-
Фенилимид
англ.: Phenylimide Диметилфосфанид диметилфосфинид (трад.) англ.: dimethylphosphanide,
Dimethylphosphinide
N 7 II
1 Н-Бензотриазол-1 -ид англ.: 1 /-/-Benzotriazol-1-ide
7Ь/-/-Индено[1,2,3-)к]флуорен-7Ь-ид англ.: 7bH-lndeno[1,2,3-jk]fluoren-7b-ide
1,4,6,9-Тетрагидролирен-1 ,4,6,9-тетраид англ.: 1 Ae.g-Tetrahydropyrene-l^.e^-tetraide
Рис. 6.12.31
1098
Новый справочник химика и технолога
1,10Ь-Дигидроциклопента[е(]гептален-2а1-ид или циклопента[е/]гептален-2а1 (1 Н)-ид англ.: 1,10b-Dihydrocyclopenta[ef]heptalen-2a1-ide или cyclopenta[ef]heptalen-2a1 (1 H)-ide
1 -Метил-1,2-дигидробенз[Ь]азоцин-2,2-диид или 1 -метил-1 -бензазоцин-2,2(1 Н)-Диид англ.: 1 -Methyl-1,2-dihydrobenzo[b]azocine-2,2-diide или 1 -methyl-1 -benzoazocine-2,2(1 /-Л-diide
Рис. 6.12.32
Анионные центры на атомах кислотных функциональных групп
Анионы, получающиеся при отщеплении протона от атома халькогена кислотной функциональной группы соединения, название которого построено с использованием суффикса «овая кислота» (исключая смешанные пероксикислоты типа R-CS-O-OH или R-CO-S-SH), или имеющего полусистематическое или тривиальное название с окончанием «овая кислота», называют, заменяя это окончание на суффикс «ат», см. рис. 6.12.33.
Анионы, получающиеся при отщеплении протона нс ото всех гидроксильных групп многоосновной кислоты, могут быть названы путем указания оставшихся атомов водорода с помощью слова «водород», которое помещается с соответствующими локантами перед названием аниона, образованным по вышеуказанным правилам. Неиони-зованные кислотные, а также сложноэфирные группы могут быть названы как заместители (рис. 6.12.34).
Анионные центры на гидроксильных группах и их халькогенных аналогах
Для анионов, получающихся при отщеплении протона от гидроксильных групп ациклических спиртов С1-С4, фенолов или гидроксиламинов, используются сокращенные радикало-функциональные названия, такие как метоксид, аминоксид и т. д. Названия таких неразветвленных ациклических анионов, в отличие от разветвленных (например, изопропоксид), могут ис
пользоваться в качестве основы в заместительной номенклатуре.
Названия остальных анионов, получающихся при отщеплении протона от гидроксильных групп или их халкогенных аналогов (обозначаемых суффиксами «ол», «тиол» и др.), образуют, добавляя к соответствующему названию суффикс «ят», например «олят», «тиолят». Если суффикс «ол» в родоначальном соединении подразумевает наличие нескольких гидроксильных групп, то соответствующий анионный суффикс «олят» обозначает удаление протонов от всех гидроксильных групп. Чтобы избежать неопределенности для полиолов и их аналогов, используют множительные префиксы «бис», «трис» и т. д., т. к. суффикс «диолят» обозначает моноанион из диола. Как исключение, названия пикрат и стифнат используются для аниона пикриновой (2,4,6-тринитрофенол) и дианиона стифнино-вой (2,4,6-тринитробензол-1,3-диол) кислот соответственно (рис. 6.12.35).
Моноанионные центры на атомах азота аминогрупп, получающиеся при отщеплении протона от атома азота, называют, добавляя к названию родоначального соединения суффикс «ид» или используя заместительную номенклатуру с основами «амид» или «азанид» (рис. 6.12.36).
Анионные центры на других функциональных группах, получающиеся при отщеплении протона, называют на основе анионных родоначальных гидридов (рис. 6.12.37).
О
^О"
Ацетат англ.: Acetate
О Ph-S-O"
6
Бензолсульфонат англ.: Benzenesulfonate
Пероксибензоат или пербензоат англ.: Peroxy benzoate или perbenzoate
Фталат англ.: Phthalate
Ph2PO~
Дифенилфосфинат англ.: Diphenylphosphinate
П ирид ин-2,6-ди карбоксил ат англ: Pyridine-2,6-dicarboxylate
Рис. 6.12.33
Современная номенклатура органических соединений
1099
НО
Водород гептандиоат или 6-карбоксигексаноат англ.: Hydrogen heptanedioate или 6-carboxyhexanoate
Рис. 6.12.34
°'^С1
2-Хлорэтоксид англ:. 2-Chloroethoxide
Пентан-1-олят англ:. Pentan-1-date
Диметиламиноксид англ:. Dimethylaminoxide
Cl
“р
1 -Метил-1 -хлорэтоксид или 2-хлорпропан-2-олят
англ: 1-Chloro-1 -methylethoxide или 2-ch I о горго ра п-2-о late
Циклогексанселенолят англ:. Cyclohexaneselenolate
"О 0“
Бензол-1,2,3-трис(олят) или пирогалл олят (трив.) англ: Pyrogallolate
или benzene-1,2,3-tris(olate)
Рис. 6.12.35
NH-
Этанами нид или этиламид или этилазанид англ: Ethanaminide или ethylamide или ethylazanide
Анилинид или бензоламинид или фениламид или фенилазанид
англ: Anilinide или benzenaminide или phenylamide или phenylazanide
Рис. 6.12.36
1-Оксоэтанид англ: 1-Oxoethanide
Этилдиоксанид англ.: Ethyldioxidanide
Диметилоксо-Х5-фосфанид или диметилоксофосфоранид англ.: Dimethyloxo-X5-phosphanide или dimethyloxophosphoranide
N“ (1-Гидроксипропилиден)амид или
НО-д (1-гидроксипропилиден)азанид у англ: (l-Hydroxypropylidene)amide или ' (l-hydroxypropylidene)azanide
Cl
(2-Хлорфенилсульфанил)оксиданид англ: (2-Chlorophenylsulfanyl)oxidanide
О Ph^ HN-N2'
2-Бензоилдиазан-1,1-диид или
2-бензоилгидразин-1,1 -ди ид англ: 2-Benzoyldiazane-1,1 -diide или
2-benzoylhydrazine-1,1 -di ide
1,3-Диоксо-2,3-дигидро-1 /-/-бенз[с/е]изохинолин-2-ид или
1,3-диоксо-1 Н-бенз[с/е]изохинолин-2(3/-/)-ид
англ: 1,3-Dioxo-2,3-dihydro-1/-/-benzo[cfe]isoqiJinolin-2-ide или
1,3-dioxo-1/-/-benzo[de]isoquinolin-2(3/-/)-ide
Рис. 6.12.37
1100
Новый справочник химика и технолога
6.12.3.2. Анионы с анионными центрами, получающимися при формальном присоединении гидрид-ионов
Название для таких анионов может быть образовано двумя способами:
а) добавлением суффикса «уид» («uide»), «диуид» и т. д. к названию родоначальното гидрида;
б) добавлением суффикса «ид», «диид» и т. д. к названию родоначального гидрида, в котором имеется по крайней мере на два атома водорода больше (с учетом ^-обозначений), чем в стандартном валентном состоянии нейтрального гидрида, см. рис. 6.12.38.
6.12.3.3. Заменительная номенклатура для анионов
Анионные центры в родоначальных гидридах могут быть названы с помощью принципов заменительной «а»-номенклатуры. Анионные заместительные префиксы образуют, добавляя к названию моноядерного гидрида суффиксы «и да» или «у и да» для анионных центров с числом связей на единицу меньше или больше соответственно, чем в нейтральном гидриде (рис. 6.12.39).
Эти префиксы являются неотделяемыми, т. е. они помещаются непосредственно перед названием родоначального гидрида. Согласно рекомендациям 1UPAC, где возможно, предпочтительнее использовать суффиксы «ид» или «уид», чем префиксы «ида» или «уида», см. рис. 6.12.40.
6.12.3.4. Многозарядные анионные цетры
Полианионы, образованные идентичным образом в разных положениях одного и того же родоначального гидрида, называют, используя соответствующие суффиксы с умножающими приставками (см. примеры выше).
Анионы с несколькими анионными центрами, по крайней мере один из которых формально образован отщеплением протона от скелета и один — присоединением гидрид-иона, называют, добавляя суффикс «ид», за которым следует суффикс «уид» с соответствующими локантами и умножающими приставками.
При наличии выбора более низкие локанты присваивают «уид»-центрам, например см. рис. 6.12.41.
Полианионы, образованные путем отщепления протона от нескольких гидроксильных групп (или их халькогенных аналогов), называют используя суффиксы «бис(олят)», «трис(тиолят)» и т. п.
Полианионы с анионными центрами как в родоначальном гидриде, так и в суффиксных функциональных группах называют, добавляя анионный суффикс фуппы к названию родоначального аниона. При наличии выбора низший локант относят к анионному скелетному атому, см. рис. 6.12.42.
Анионы с анионными центрами, образованными из одного и того же гидрида, но расположенными в различных частях молекулы, можно называть с помощью номенклатуры ансамблей, используя множительные приставки «бис», «трис» и т. д. (рис. 6.12.43).
Полианионы с анионными центрами как в родоначальном соединении, так и в заместителях, называют, выбирая часть структуры, содержащую наибольшее число анионных центров, в качестве основы, к которой добавляют соответствующие анионные префиксы.
Префиксы для анионных центров из кислотных характеристических групп, полученных отщеплением протона от гидроксильных, тиольных и т. п. групп, образуют, заменяя окончание «овая кислота» на суффикс «ато» (рис. 6.12.44).
Префиксы анионов халькогенидов могут быть образованы путем добавления буквы «о» к названию соответствующего моноатомного аниона, например: -О' «оксидо».
Систематически анионные префиксы для замещающих групп образуют, добавляя к названию родоначального аниона суффиксы «ил», «илиден», «диил». При наличии выбора низший локант приписывают атому анионного заместителя, который присоединен к родоначальной структуре, см. рис. 6.12.45а и 6.12.456.
(СН3)4Р
CH3-S1H4 / \ т . .
4 (а) Тетраметилфосфануид или
(а) Метилсилануид (б) тетраметил-А.5-фосфанид,
англ., (a) Methylsilanuide тетраметилфосфоранид (трад.)
Ph2r англ.', (a) Tetramethylphosphanuide или
(б) Дифенил-А.3-иоданид (б) tetramethyl-Z5-phosphanide,
англ.-, (б) Diphenyl-Z3-iodanide (б) tetramethylphosphoranide
Рис. 6.12.38
Фосфанида англ.-. Phosphanida
Борануида англ.'. Boranuida
Сульфануида или тАсульфанида
I англ.-. Sulfanuida или
/Asulfanida
Рис. 6.12.39
Современная номенклатура органических соединений
1101
2,2-Диметил-2Н-2-борануидаинден или
2,2-диметил-2Н-2-бораинден-2-уид англ.-. 2,2-Dimethyl-2H-2-boranuidaindene или
2,2-dimethyl-2H-2-borainden-2-uide
5А,5-Фосфануидаспиро[4.4]нонан или
5А,5-фосфаспиро[4.4]нонан-5-уид англ.: 5A,5-Phosphanuidaspiro[4.4]nonane или
5X5-phosphaspiro[4.4]nonan-5-uide
Рис. 6.12.40
2,4-Дигид ро-2,2-диметилциклопента[с]борол-4-ид-2-уид англ.: 2,4-Dihydro-2,2-dimethylcyclopenta[c]borol-4-id-2-uide
Рис. 6.12.41
-.z-х О
1 / \4 II
НС~ H-S-0
\ / II
'— о
Циклогексан-1 -ид-4-сульфонат
англ.: Cyclohexan-1 -ide-4-sulfonate
Пент-1 -ин-1 -ид-5-олят англ.: Pent-1 -yn-1-id-5-oate
Рис. 6.12.42
1,4-Фениленбис(фосфанид) англ.: 1,4-Phenylenebis(phosphanide)
Пропан-1,3-диилбис(амид) или
_ пропан-1,3-диилбис(азанид)
англ.: Propane-1,34liylbis(amide) или
propane-1,3-diylbis(azanide)
| Этиленбис(диоксиданид)
англ.: Ethylenebis(dioxidanide)
Рис. 6.12.43
J_Cq_q- Карбоксилато
5 англ.: Carboxylato
-l-SOo-O" Сульфонато
англ.: SulfonatO
ро(СГ )г Фосфонато англ.: Phosphonato
-UasH(O)(O“ ) АРСИ нат0
англ.: Arsinato
Рис. 6.12.44
-^-СН2
Метанидил англ.: Methanidyl
4-РН
Фосфанидил англ.: Phosphanidyl
4-SS'
Дисульфанидил англ.: Disulfanidyl
-^-NH
Ам ид ил или азанидил англ.: Amidyl или azanidyl
+вн3
Борануидил англ.: Boranuidyl
\\ СН Циклогекса-2,5-диен-4-ид-1-илиден
’ \=/ англ.: Cyclohexa-2,5-dien-4-id-1-ylidene
Рис. 6.12.45а
1102
Новый справочник химика и технолога
Имидил или азандиидил англ.-. Imidyl или azanediidyl
Амидилилиден или азанидилиден или азаниддиил англ.: Amidylidene или azanidylidene или azanidediyl
Циклопента-1,4-диен-3-ид-1,2-диил англ.: Cyclopenta-1,4-dien-3-ide-1,2-diyl
Рис. 6.12.456
6.12.4. Катионные и анионные центры в одной структуре
6.12.4.1. Цвиттер-ионные соединения с равным числом катионных и анионных центров в одном и том же родоначальном соединении
Цвиттер-ионные родоначальные гидриды называют, добавляя к названию нейтрального гидрида соответствующие суффиксы в следующем порядке «-ий», «-илий», «-ид», «-уид» или соответствующие префиксы. В любом случае анионные аффиксы помещаются после катионных. Для указания количества ионных центров каждого типа используются умножающие приставки. При наличии выбора низшие локанты присваиваются ионным центрам в следующем порядке: «-уид» («-уида»), «-ид» («-ида»), «-илий» («-илиа»), «-ий» («-ониа») (рис. 6.12.46).
6.12.4.2. Цвиттер-ионные соединения с ионным центром на функциональной группе
Цвиттер-ионные соединения с ионным центром на функциональной группе, который может быть выражен с помощью суффикса, называют путем добавления этого суффикса к названию ионного родоначального гид
рида. При выборе локантов ионные центры на скелетных атомах имеют приоритет (рис. 6.12.47).
Префиксы для цвиттер-ионных родоначальных гидридов образуют, добавляя к названию цвиттер-ионного гидрида суффиксы «ил», «илиден» или «диил». При выборе локантов свободная валентность имеет приоритет.
\
3-Метил-1/-/-имидазол-3-ий-1-ид-4-ил
? англ.: 3-Methyl-1H-imidazol-3-ium-1-id-4-yl
6.12.4.3. Соединения с ионными центрами, находящимися в более чем одной родоначалъной структуре
Ионные соединения с ионными центрами, не находящимися в одной и той же родоначальной структуре (или в тех случаях, когда нежелательно включать все эти центры в одну родоначальную структуру), называют, выражая катионные структуры через заместительные префиксы к названию анионного родоначального соединения, см. рис. 6.12.48.
1,2,2-Т риметилдиазан-2-ий-1 -ид или
I + 1,2,2-триметилгидразин-2-ий-1-ид ''4Ny"N\ ан2Л-- 1,2,2-Trimethyldiazan-2-ium-1-ide или 1,2,2-trimethylhydrazin-2-ium-1-ide
2-Этанилидиндиазан-2-ий-1-ид или
_ +_ 2-этанилидингидразин-2-ий-1-ид
HN-N=C-CH3 англ.: 2-Ethanylidynediazan-2-ium-1-ide или 2-ethanylidynehydrazin-2-ium-1-ide
+N=N /
2,2-Диметилдиазен-2-ий-1-ид или 2,2-диметилдиазан-1-илиден или 2,2-диметил-1 V-диазан
англ.: 2,2-Dimethyldiazen-2-ium-1-ide или 2,2-dimethyldiazan-1-ylidene или 2,2-dimethyl-1 A.-diazane
5
7 6
11 А5-5/-/-Индоло[2,3-Ь]хинолизин-1 1-илий-5-ид
4
англ.: 11 A5-5/-/-lndolo[2,3-b]quinolizin-11-ylium-5-ide
Рис. 6.12.46
Современная номенклатура органических соединений
1103
н о 1.1.1 -Т риметилдиазан-1 -ий-2-сульфонат или
1 -1 >1-триметилгидразин-1-ий-2-сульфонат
\ qz англ.-. 1,1,1-Trimethyldiazan-1-ium-2-sulfonate или
1,1,1-trimethylhydrazin-1-ium-2-sulfonate
Ph
О
1-Метил-4,6-дифенилпиридин-1-ий-2-карбоксилат англ:. 1-Methyl-4,6-diphenylpyridin-1-ium-2 -carboxylate
’О
НО
\ /7 О 4-Карбокси-3-метил-1,2,3-оксадиазол-3-ий-5-олят
Д англ.: 4-Carboxy-3-methyl-1,2,3-oxadiazol-3-ium-5-olate
+/
О 3-Метил-5-оксо-2,5-дигидро-1,2,3-оксадиазол-3-ий-2-ид-
НО 4-карбоновая кислота или
\। _ 3-метил-5-оксо-1,2,3-оксадиазол-3-ий-2(5/-/)-ид-4-карбоновая
о' + N"N кислота
/ англ:. 3-Methyl-5-oxo-2,5-dihydro-1,2,3-oxadiazol-3-ium-2-ide-4-carboxylic acid или
3-methyl-5-oxo-1,2,3-oxadiazol-3-ium-2(5/-/)-ide-4-carboxylic acid
Рис. 6.12.47
Ph3P4+
>-
Ph3P+
Бис(трифенилфосфонио)метандиид англ: Bis(triphenylphosphonio)methanediide или bis(triphenylphosphoniumyl) methanediide
Пирролидин-1 -ий-1-илиденамид или пирролидин-1-ий-1-илиденазанид англ: Pyrrolidin-1-ium-1-ylideneamide или pyrrol idin-1-iu m-1-ylideneazanide
2-(Диметилсульфонио)циклопропан-1-ид англ: 2-(Dimethylsulfonio)cyclopropan-1-ide или 2-(dimethylsulfoniumyl)cyclopropan-1-ide
7-(1 A.4,2-Дитиол-1 -илий-4-ил)-2-нафтолят англ: 7-(1 A4,2-Dithiol-1-ylium-4-yl)-2-naphtholate
(1-Метилпиридин-1-ий-4-ил)ацетат англ: (1 -Methylpyridin-1 -ium-4-yl)acetate
4-(Диоксидан-2-илий)феноксид англ: 4-(Mioxidan-2-ylium-1-yl)phenoxide
Рис. 6.12.48
1104
Новый справочник химика и технолога
6.12.5. Радикал-ионы (ион-радикалы)
Согласно органической номенклатуре радикал-ион представляет собой молекулу, имеющую по крайней мере один радикальный центр и один катионный, анионный или оба центра, которые могут быть локализованы либо на одном, либо на различных атомах.
Радикал-ионы, получающиеся при формальном присоединении или удалении одного или нескольких электронов от родоначального соединения, могут быть названы путем добавления фразы «радикал-катион» или «радикал-анион» к названию родоначального гидрида или соединения. Умножающие приставки «ди», «три» и т. д. используются в названиях соединений с полиради-кальными и многозарядными центрами. Альтернативно знак и величина заряда могут быть указаны в скобках, например: радикал-ион (2-).
Названия такого типа наиболее полезны в тех случаях, когда положение ионных и радикальных центров неизвестно или его не желательно указывать. В литературе используется также название «ион-радикал», что
является приемлемой альтернативой (относительное положение радикальной точки и знака заряда в формулах также может быть противоположным, например, в масс-спектрометричсской литературе) (рис. 6.12.49).
6.12.5.1. Радикал-ионы — производные родоначальных гидридов
Радикал-ионы, получающиеся при формальном отщеплении одного или более атомов водорода от одного или нескольких скелетных атомов ионного или цвиттер-ионного родоначального гидрида, называют, добавляя к их названию суффиксы «ил», «илиден», «диил» и т. д. Скелетный радикальный центр имеет преимущество перед скелетным ионным центром при определении наименьшей последовательности локантов.
Радикал-катионы представлены на рис. 6.12.50а и 6.12.506.
Радикал-анионы, см. рис. 6.12.51.
Цвиттер-ионные радикал-ионы приведены на рис. 6.12.52.
[С2Н6]*+
Этан радикал-катион или этан радикал-ион(1+) англ.-. Ethane radical cation или ethane radical ion(1+)
[C4H6]'+
Бутадиен радикал-катион или бутадиен радикал-ион(1+) англ.-. Butadiene radical cation или butadiene radical ion(1+)
\ Бицикло[5.3.1]ундека-1,3,5,7,9-пентаен радикал-анион или
' бицикло[5.3.1 ]ундека-1,3,5,7,9-пентаен радикал-ион(1-)
англ.-. Bicyclo[5.3.1]undeca-1,3,5,7,9-pentaene radical anion или bicyclo[5.3.1]undeca-1,3,5,7,9-pentaene radical ion(1-)
[CH3-SF5]”
Метил(пентафтор)-Х6-сульфан радикал-анион или метил(пентафтор)-Х6-сульфан радикал-ион(1-) англ.-. Pentafluoro(methyl)-X6-sulfane radical anion или
pentafluoro(methyl)-X6-sulfane radical ion(1-)
[C6H5-C6H5]*2-H2-)
Бифенил дирадикал-дианион или бифенил дирадикал-ион(2-) англ.: Biphenyl diradical dianion или biphenyl diradical ion(2-)
Рис. 6.12.49
H2C*+
Метилийил англ.: Methyliumyl
НС+ СН
Циклогекса-2,5-диен-4-илий-1-ил англ.: Cyclohexa-2,5-dien-4-ylium-1-yl
[СН3-СН2]( ^2+) Этанийилийил англ.: Ethaniumyliumyl
Бензолийил
англ.: Benzeniumyl
Рис. 6.12.50а
Современная номенклатура органических соединений
1105
Этен-2-илий-1 -ил идеи ?~2Н или '1^2-этен"2-илий англ.: Ethen-2-ylium-1-ylidene или 1X2-ethen-2-ylium
/ Триметиламмонийил
—N*+ триметилазанийил
\ англ.-. Trimethylammoniumyl trimethylazaniumyl
2-Оксо-1-этил-1,2-дигидропиридин-1 -ий-1 -ил англ.: 1 -Ethy l-2-охо-1,2-dihydropy rid in-1 -ium-1 -у I
Рис. 6.12.506
Амидил или азанидил j ,4-Дигидронафталин-4-ид-1 -ил англ.: Amidyl или azanidyl англ.: 1,4-Dihydronaphthalen-4-id-1-yl
Н Ph^c;-xPh С С Н Н
Г ексацианобут-2-ен-4-ид-1-ил 1,3-Дифенилпропан-1,3-диид-2-ил
англ.-. Hexacyanobut-2-en-4-id-1-yl англ.: 1,3-Diphenylpropane-1,3-diid-2-yl
Рис. 6.12.51
1 Н-Бензо[с][1,2]тиазин-2-ий-1 -ид-2-ил или 1Н-2,1 -бензотиазин-2-ий-1-ид-2-ил англ.: 1 H-Benzo[c][1,2]thiazin-2-ium-1-id-2-yl или 1 Н-2,1 -benzothiazin-2-ium-1 -id-2-yl
3-Метил-1-(триметилсилил)триаз-2-ен-2-ий-1-ид-2-ил англ.: 3-Methyl-1-(trimethylsilyl)triaz-2-en-2-ium-1 -id-2-yl
Рис. 6.12.52
6.12.5.2. Радикал-ионы с центрами на функциональных группах
Радикал-ионы с центрами на ионных «суффиксных» функциональных группах
Радикал-ионы, получающиеся при формальном отщеплении одного или более атомов водорода от катионных функциональных групп (табл. 6.38) или анионных функциональных групп (типа «-аминид»), называют, добавляя суффиксы «ил», «илиден», «диил» к ионным суффиксам, см. рис. 6.12.53.
Другие радикал-ионы с центрами на функциональных группах называют, используя в качестве основы родоначальные радикал-ионы, см. рис. 6.12.54.
Ионные и радикальные центры в разных родоначальных структурах
Радикал-ионы, получающиеся при формальном отщеплении одного или более атомов водорода от ионных или цвиттер-ионных соединений, в которых ионные и радикальные центры не могут быть включены в одну и ту же основу, называют, выражая ионные структуры через заместительные префиксы к названию радикальной части структуры, см. рис. 6.12.55.
1106
Новый справочник химика и технолога
Анилинийил англ.-. Aniiiniumyl или benzenaminiumyl
Бензонитрилийил англ.-. Benzonitriliumyl
Метанаминидил или метиламидил или
H3C-N метилазанидил
англ.-. Methanaminidyl или methylamidyl methylazanidyl
Сукцинимидийилиден англ.-. Succinimidiumylidene
\ Ацетамидилийил
х/ N'+ англ.: Acetam idyl iu my I
О
Рис. 6.12.53
Ацетил(метил)оксонийил англ.: Acetyl(methyl)oxoniumyl
Н2С=С=О'+
Винилденоксонийил англ.: Vinylideneoxoniumyl
Н3С
о
Ацетиламидил или ацетилазанидил англ.: Acetylamidyl или acetylazanidyl
c6h5-so2-nh-n’
2-(Бензолсульфонил)диазан-1 -ид-1 -ил англ.: 2-(Benzenesulfonyl)diazan-1-id-1 -yl
Рис. 6.12.54
[4-(Дифенилметилийил)фенил]дифенилметил англ.: [4-(Diphenylmethyliumyl)phenyl]diphenylmethyl
сн2+
2-Метилийил-1,2,3,4-тетрагидро-1,4-метанонафталин-2,6-диил англ: 2-Methyliumyl-1,2,3,4-tetrahydro-1,4-methanonaphthalene-2,6-diyl
5-Бензил-3,7,8,10-тетраметил-4-оксидо-2-оксо-2,3,5,10-тетрагидробензо[д]птеридин-5-ий-5-ил
англ.: 5-Benzyl-3,7,8,10-tetramethyl-4-oxido-2-oxo-2,3,5,10-
tetrahydrobenzo[g]pteridin-5-ium-5-yl
Рис. 6.12.55
6.13. Построение названий сложных систем (резюме)
В данном подразделе суммированы рассмотренные ранее в различных разделах важные положения, касающиеся выбора основы названия и нумерации сложного соединения.
При выборе основы названия (родоначальной структуры) сложного соединения, содержащего цепные и циклические компоненты, основным критерием является присутствие в цепи или цикле главной группы, от
ражаемой в названии суффиксом. Если одна и та же главная группа присутствует и в цепи и в цикле, то в качестве основы выбирают компонент, содержащий большее число таких групп. Если и этот критерий не позволяет сделать выбор, то руководствуются «химической» интуицией (большее число заместителей, атомов, и т. п.). К сожалению, правила IUPAC не позволяют сделать однозначный выбор. Chemical Abstracts в такой ситуации отдает предпочтение циклу.
Современная номенклатура органических соединений
1107
6.13.1. Выбор главной цепи
Главную цепь как основу названия выбирают, последовательно руководствуясь приведенными ниже критериями. Рассмотрение прекращают на той стадии, которая позволила сделать выбор. Главная цепь должна иметь:
1) максимальное число главных функциональных групп;
2) максимальное число гетероатомов (для цепей с гетероатомами, названных с помощью «а»-номенклагуры);
3) максимальное число кратных связей;
4) максимальное число атомов;
5) максимальное число старших гетероатомов (табл. 6.13) (в случае применения «а»-номенклатуры для наименования цепей, содержащих гетероатомы);
6) максимальное число двойных связей;
7) наименьший набор локантов для всех гетероатомов (в случае применения «а»-номенклатуры для наименования цепей, содержащих гетероатомы);
8) низшие локанты для гетероатомов, имеющих более высокое старшинство согласно табл. 6.13 (в случае применения «а»-номенклатуры для наименования цепей, содержащих гетероатомы);
9) низшие локанты для главных функциональных групп, отражаемых в названии суффиксами (табл. 6.7);
10) низшие локанты для кратных связей;
11) низшие локанты для двойных связей;
12) максимальное число заместителей, отражаемых в названии префиксами;
13) низшие локанты для всех префиксных заместителей;
14) низшие локанты для префиксных заместителей в порядке их расположения в названии.
6.13.2. Выбор главного цикла
Главный цикл как основу названия выбирают, последовательно руководствуясь приведенными ниже критериями. Рассмотрение прекращают на той стадии, которая позволила сделать выбор. Большее старшинство имеют:
1) цикл с максимальным числом главных функциональных групп;
2) гетероцикл по сравнению с карбоциклом;
3) гетероциклы расположены в порядке уменьшения старшинства в табл. 6.11 (дополнительно для определения старшинства гетероциклов могут быть использованы критерии, рассмотренные в подразд. 6.3.3.2);
4) циклическая система с максимальным числом колец;
5) циклическая система с кольцом максимального размера;
6) циклическая система с максимальным числом атомов, общих для двух или более колец;
7) конденсированный цикл с наименьшим буквенным локантом, показывающим место сочленения;
8) конденсированный цикл с наименьшими цифровыми локантами, показывающими место сочленения;
9) наименее гидрогенизированный цикл;
10) цикл с низшими локантами для «обозначенного водорода»;
И) цикл с низшими локантами для свободных валентностей;
12) цикл с низшими локантами для главных групп, отражаемых в названии суффиксами;
13) цикл с максимальным числом заместителей, отражаемых в названии префиксами;
14) цикл с низшими локантами для префиксных заместителей и кратных связей;
15) цикл с низшими локантами для префиксных заместителей в порядке их расположения в названии.
6.13.3. Нумерация сложного соединения
Если правила, используемые при нумерации родоначальных структур, описанные в соответствующих разделах, не приводят к однозначному варианту, соединение нумеруют так, чтобы:
1) наименьшие локанты были присвоены скелетным атомам с «обозначенным водородом» (но не с «добавленным водородом»)*;
2) наименьшие локанты были присвоены свободным валентностям;
3) наименьшие локанты были присвоены главным группам, отражаемым в названии суффиксами;
4) кратные (двойные и тройные связи) связи имели наименьший набор локантов;
5) двойные связи имели наименьший набор локантов;
6) префиксные заместители имели наименьший набор локантов;
7) наименьшие локанты получили заместители, идущие первыми по алфавиту.
6.13.4. Порядок размещения составных частей названия
При записи полного названия соединения следует придерживаться следующего порядка размещения составных частей:
* Особый тип «обозначенного водорода» — «добавленный водород», показывающий атомы водорода, которые добавляются к структуре при использовании некоторых суффиксов или префиксов, описывающих модификацию структуры (например, суффикса «он» в циклических кетонах или суффикса «илиден» при образовании названия замещающей группы из ненасыщенного цикла), обычно указывается в круглых скобках после локанта, показывающего положение данного аффикса.
1108
Новый справочник химика и технолога
1) отделяемые префиксы в алфавитном порядке (умножающие приставки для простых заместителей при определении алфавитного порядка не учитываются);
2) неотделяемые «гидро» или «дегидро» префиксы;
3) «обозначенный водород»;
4) неотделяемые заменительные «а»-префиксы (при использовании «а»-номенклатуры: «окса», «тиа», «аза» и т. п. в порядке, описанном в подразд. 6.3.2, табл. 6.13);
5) неотделяемые префиксы, показывающие изменение порядка соединения атомов в родоначальном гидриде («абео», «ретро», «секо» в алфавитном порядке);
6) неотделяемые префиксы, показывающие удале-ние/добавление скелетных атомов в родоначальном
О CI
гидриде («апо», «гомо», «дез», «нор» в алфавитном порядке);
7) название основы (родоначального гидрида);
8) суффиксы «ен», а затем «ин», показывающие ненасыщенность;
9) суффиксы главных функциональных групп (порядок размещения ионных и радикальных суффиксов обсуждается в подразд. 6.12.4.1).
Те же принципы используются при построении названия сложного заместителя.
Следующие примеры иллюстрируют приведенные обобщающие положения (рис. 6.13.1 и 6.13.2).
5,7-Дибром-2-(5-оксо-4-хлор-4а,5-дигидронафталин-2(1 Й)-илиден)[1,3]дитиокан-6-он
англ:. 5,7-Dibromo-2-(4-chloro-5-oxo-4a,5-dihydronaphthalen-
2(1 /-/)-ylidene)[1,3]dithiocan-6-one
2-(5-Тиоксо-4-фтор-5,6-дигидрохинолин-2-ил)циклопропанкарбоновой кислоты 2-(9,10-дииодантрацен-2(ЗЛ/)-илиденметил)циклопентиловый эфир
англ: 2-(4-Fluoro-5-thioxo-5,6-dihydro-quinolin-2-yl)cyclopropanecarboxylic acid 2-(9,10-diiodoanthracen-2(3H)-ylidenemethyl)cyclopentyl ester
2-{2-[6-Ацетил-4-(нафталин-2-илимино)-4,5-дигидропиридин-2-ил]-1 -метилэтил}-5-метил-3-(1 -тиа-8-азациклотетрадец-12-ен-10-ин-6-ил)бензонитрил
англ.: 2-{2-[6-Acetyl-4-(naphthalen-2-ylimino)-4,5-dihydropyridin-2-yl]-1 -methylethyl}-5-methyl-3-(1 -thia-8-azacyclotetradec-12-en-10-yn-6-yl)-benzonitrile
Рис. 6.13.1
Современная номенклатура органических соединений
1109
2-{3-{3-[2-(Фторметил)проп-2-енил]-1-оксаспиро[4.4]нон-7-ил}пропил}-А/-(3-тиоксо-ЗЙ-пиррол-4-ил)бут-3-енамид
англ:. 2-{3-{3-[2-(Fluoromethyl)prop-2-enyl]-1-oxaspiro[4.4]non-7-yl}propyl}-
A/-(3-thioxo-3H-pyrrol-4-yl)but-3-enamide
Рис. 6.13.2
6.14. Изотопно-модифицированные соединения
Соединения, в которых часть или все элементы имеют нуклидый состав, отличающийся от природного, называют изотопно-модифицированными.
Для обозначения нуклида в формуле или названии соединения используют символ элемента с левым надстрочным индексом, указывающим массовое число нуклида. Например, для «неприродных» нуклидов наиболее часто используемых в органической химии: 13С, l4C, 15N, i7O, 18О, 34S, j2P. Обозначения и названия изотопов водорода (атомов и ионов) представлены в табл. 6.39.
Изотопно-модифицированные соединения разделяются на изотопно-замещенные и изотопно-меченые. Последние, в свою очередь, подразделяются на специфически меченые, селективно меченые, неселективно меченые и изотопно-дефицитные.
Изотопно-замещенные соединения имеют такой состав, что по существу все молекулы соединения имеют только указанные нуклиды в каждом обозначенном положении. При этом для всех других положений изотопный состав соответствует природному. Формулы изотопно-замещенных соединений изображаются обычными способами с использованием символа соответствующего нуклида. При наличии изотопов одного и того же элемента в одном и том же положении их записывают в порядке увеличения массового числа. Так, например, (1-2Н])этанол записывается как СН3-СН2Н-ОН, а не СН3-С2НН-ОН. Названия таких соединений образуют, добавляя в круглых скобках перед названием соединения или, что предпочтительнее, перед названием той части молекулы, которая является изотопно-модифицированнной, символ нуклида с соответствующим локантом и подстрочным умножающим префиксом.
Таблица 6.39
Обозначения и названия изотопов атомов и ионов водорода
Обозначения 'Н 2Н а) 3На) Нб)
Атом н- протий (protium) дейтерий (deuterium) тритий (tritium) водород (hydrogen)
Катион Н+ протон (proton) дейтрон (deuteron) тритон (triton) гидрон (hydron)
Анион Н" протид (protide) дейтерид (deuteride) тритид (tritide) гидрид (hydride)
а) Символы D (для 2Н) и Т (для 3Н) можно использовать в тех случаях, когда в соединении отсутствуют другие нуклиды, модифицирующие природный изотопный состав.
б) Используется в случае природного или неопределенного изотопного состава.
С3Н212 или CT2I2 С62Н6 “ C6D6
Дииодо(3Н2)метан Дииодо(Т2)метан (2Н6)Бензол (О6)Бензол
НО
1-(15М)Аминоциклопропанкарбоновая кислота
Изотопно-меченые соединения представляют собой смесь изотопно-немодифицированного соединения с одним или несколькими изотопно-замещенными соединениями. Изотопно-меченое соединение называется специфически меченым, когда одно изотопнозамещенное соединение формально добавлено к соответствующему изотопно-немодифицированному соеди
нению. В структурных формулах таких соединений символ нуклида и подстрочные умножающие индексы приводятся в квадратных скобках. Названия таких соединений образуют, добавляя в квадратных скобках перед названием немеченого соединения или, что предпочтительнее, перед названием той части молекулы, которая является изотопно-модифицированнной, символ
1110
Новый справочник химика и технолога
нуклида с соответствующим локантом и подстрочным умножающим индексом. Умножающий индекс «1» приводится для тех монозамещенных положений в молекуле, в которых возможно полизамещение (например, [2Н]]метан) (рис. 6.14.1).
Изотопно-меченое соединение называется селективно меченым, когда смесь изотопно-замещенных соединений формально добавлена к соответствующему изотопно-немодифицированному соединению таким образом, что известно положение меток, но необязательно известно их число. Селективно меченые соединения можно рассматривать как смесь специфически меченых соединений. Названия таких соединений образуют, добавляя в квадратных скобках перед названием немеченого соединения или соответствующего фрагмента молекулы символ нуклида с соответствующим локантом, но без подстрочного умножающего индекса. При наличии различных нуклидов их символы записываются в алфавитном порядке, а в тех случаях, когда соответствующие атомные символы одинаковы, — в порядке увеличения массового числа (рис. 6.14.2).
Если селективно меченое соединение получено путем формального смешивания нескольких известным образом изотопно-замещенных соединений, то число или возможное число меченых ядер для каждого положения может быть указано с помощью подстрочных индексов у символа нуклида. В этом случае подстроч
ные индексы, относящиеся к символу данного нуклида, разделяются точкой с запятой. Ноль используется для того, чтобы показать, что одно из изотопно-замещенных соединений не модифицировано в рассматриваемом положении (рис. 6.14.3).
Изотопно-меченое соединение называется неселективно меченым, когда и число и положение меток являются неопределенными. К формуле соответствующего соединения добавляют символ соответствующего нуклида в квадратных скобках, например: [13С]СН3-СН2-СН2-СООН. Названия таких соединений образуют так же, как и селективно меченых соединений, но без локантов и подстрочных умножающих префиксов у символа нуклида, например: хлор[3Н]бензол, [,4С]глицерин.
Изотопно-меченое соединение называется изотопно-дефицитным, когда содержание одного или нескольких нуклидов меньше природного. Названия таких соединений образуют, добавляя перед названием немеченого соединения группу символов [^/«символ нуклида»]. Например, формула: [<7е/3С]СНС13, название: [б/е/13С]хлороформ. С другой точки зрения последнее соединение является «обогащенным» по сравнению с природным нуклидным составом, т. е. [12С]СНС13, название: [12С]хлороформ.
В обобщенном виде примеры формул и названий изотопно-модифицированных соединений приведены в табл. 6.40.
14СН22Н2 + сн4
(14С,2Н2)Метан Метан
г-----> [14С]Н2[2Н2]
[14С,2Н2]Метан
изотопно-замещенное соединение
изотопно-немодифицированное соединение
специфически меченое соединение
[1 -13С,2,6,6-3Н3]Циклогекса-2,4-диен-1 -он
[2H]S-CH2-CH(N[2H2])-COO[2H]
(RS)-[/V, N, О,5-2Н4]Цистеин
Рис. 6.14.1
13сн32н, 13сн22н2 СН2Н3 + СН4 I--------------------------------------------------------------------------------------------->
Изотопно-немодифицированное соединение
[13С,2Н]СН4
[13С,2Н]Метан
Селективно меченое соединение
Смесь изотопнозамещенных соединений
[4-3Н]Циклогексанол
L -..или [4-Т]циклогексанол,
но не [4,4-3Н2]циклогексанол
Рис. 6.14.2
Современная номенклатура органических соединений
1111
13СН2Н2-СН2-СН2-1 8он сн2н2-сн2-сн2-он
• + сн3-сн2-сн2-он
1-----> [3-13С0;1,3-2Н2;2,18О0.1]СН3СН2СН2ОН
[3-13С0 j ,3-2Н212>180о; 1 ]Пропан-1 -ол
Рис. 6.14.3
Таблица 6.40
Примеры формул и названий изотопно-модифицированных соединений
Тип соединения Формула Название
Немодифицированное Изотопно-замещенное Специфически меченое Селективно меченое Неселективно меченое Изотопно-дефицитное СН3-СН2-ОН С2Н3-СН2-О2Н С[2Нз]-СН2-О[2Н] [<9,2-2Н]СНз-СН2-ОН [2-2Н2;2,|8О0;]]СНз-СН2-ОН [2Н]СН3-СН2-ОН [def 13С]СНз-СН2-ОН Этанол (2,2,2-2Н3)Этан(2Н)ол (<9,2,2,2-2Н4)Этанол [2,2,2-2Н3]Этан [2Н]ол [<9,2,2,2-2Н4]Этанол [<9,2-2Н]Этанол [2-2Н22,18О0;1]Этанол [2Н]Этанол [<&/3С]Этанол
6.15. Стереохимическая номенклатура
Изомерами называют соединения, имеющие одинаковый элементный состав и отличающиеся либо последовательностью связывания атомов, либо расположением атомов молекулы в пространстве. Изомеры, имеющие различный порядок связывания атомов в молекуле, называют структурными изомерами. Изомеры, в которых порядок связывания атомов одинаковый, а молекулы отличаются только формой, называются стереоизомерами (рис. 6.15.1).
При изображении формул стереоизомеров принято использовать следующие линии: простые линии изображают связи, находящиеся в плоскости чертежа; с помощью жирных линий или закрашенных клиньев (обращенных узким концом к атому в плоскости) изображают связи, направленные к атомам, находящимся над плоскостью чертежа; с помощью пунктирных линий или линий из коротких параллельных штрихов изображают связи к атомам, находящимся под плоскостью чертежа. («Рубленый» клин не рекомендуется использовать из-за неопределенности.) Неизвестная конфигурация стереоцентра может быть обозначена с помощью волнистой линии. Для обозначения конфигурации узлового атома в конденсированных циклических системах иногда используется жирная точка, показывающая, что атом водорода расположен над плоскостью чертежа. В настоящее время такой способ изображения конфигурации не рекомендуется IUPAC (рис. 6.15.2).
В ряде областей химии (химия углеводов, белков), особенно в старой литературе, используются специальные способы изображения стереоизомеров — проекционные формулы Фишера. В этих формулах главная цепь располагается вертикально, причем атом, имеющий наименьший локант, помещают наверху. Атомы и группы, расположенные слева и справа от атомов вертикальной цепи, рассматриваются как направленные к наблюдателю, а атомы и группы вертикальной цепи — от наблюдателя, например см. рис. 6.15.3.
Стереоизомеры, которые являются зеркальными отображениями друг друга и не могут быть совмещены, называют энантиомерами. Стереоизомеры, не являющиеся зеркальными отображениями друг друга, называют диастереомерами. Структура является хиральной (от греческого %£ир — рука), если она не совместима со своим зеркальным отображением. В противном случае она является ахиральной. (Примером хиральных немолекулярных структур являются правые и левые перчатки, носки же, как правило, являются ахиральными.) Любая структура, не имеющая плоскости симметрии, является хиральной и может существовать в виде пары энантиомеров (зеркальной пары). Любая структура с плоскостью симметрии является ахиральной и не может существовать в виде пары энантиомеров (рис. 6.15.4).
Стереогенным элементом молекулярного объекта называется группа атомов, определяющая наличие стереоизомерии. Различают три основных типа стереогенных элементов для молекулярных объектов, состоящих из атомов с количеством лигандов у каждого не более четырех:
1112
Новый справочник химика и технолога
1. Группировка атомов, состоящая из центрального атома с различными лигандами такая, что взаимозамена двух из них приводит к стереоизомеру. В частности, если молекула содержит атом, связанный с четырьмя
неидентичными группами, она не будет иметь плоскости симметрии и, следовательно, будет хиральной; соответствующий атом называется асимметрическим атомом или хиральным центром, например см. рис. 6.15.5.
Рис. 6.15.2
сно но-с-н н-с-он н-с-он н-с-он
СН2ОН
сно I но—с—н I н—с-он I н—с-он
I н—с-он I СН2ОН
сно но---н
н----он
н----он
н----он
СН2ОН
формула Фишера
Рис. 6.15.3
о
энантиомеры
диастереомеры
О энантиомеры
Ph, />РО2Ме О
сСО2Ме
Рис. 6.15.4
о-
СН3
Т со2н
^N—С—Н
(асимметрический атом)
Рис. 6.15.5
Современная номенклатура органических соединений
1113
2. Цепь из четырех некомпланарных атомов (или жестких групп) в стабильной конформации такой, что воображаемое или реальное (ограниченное) вращение (с изменением знака торсионного угла) относительно центральной связи приводит к стереоизомеру (см., например, приведенные ниже соединения с аксиальной хиральностью).
3. Группировка атомов, состоящая из двойной связи с заместителями, ведущими к возникновению цис-, транс-изомерии (см. примеры, приведенные ниже).
Для отражения пространственного строения соединения к его названию добавляют специальные стереохимические префиксы (стереодескрипторы). Обозначение конфигурации стереогенного элемента (в частности, описание пространственной ориентации связей у хирального центра) проводят на основе правил Канна — Ингольда — Прелога, которые включают:
- определение старшинства лигандов (атомов или групп) при хиральном центре;
- определение направления уменьшения старшинства трех лигандов, располагаемых в плоскости, при условии, что лиганд с наименьшим старшинством находится под этой плоскостью.
Для определения старшинства лигандов используются пять правил, которые применяются последовательно до нахождения первого различия по одному из следующих признаков:
1. Предпочтение по старшинству отдается атомам с более высокими атомными номерами.
2. Если атомные номера одинаковы, то предпочтение отдается изотопу с большей атомной массой.
3. Олефиновый лиганд, в котором заместитель более высокого старшинства находится на той же стороне двойной связи, что и хиральный центр, старше лиганда, в котором реализуется противоположная ситуация.
4. Равнозначная пара стереодескрипторов предшествует разнозначной паре.
5. R предшествует S, М предшествует Р.
Более подробно правила старшинства описаны в работах [18-22].
Порядок старшинства в первую очередь устанавливается для атомов лигандов, непосредственно связанных с центральным атомом. Лиганды в порядке падения старшинства обозначают буквами а > b > с > d; лиганды а, Ь, с располагают в плоскости, а младший лиганд d располагают за плоскостью бумаги. Если при такой ориентации молекулы падение старшинства лигандов а —> b —> с происходит по ходу часовой стрелки, то хиральному центру приписывают конфигурацию R (от латинского слова rectus — правый), если против — S (от латинского слова sinister — левый). Соответствие между направлением убывания старшинства и обозначением конфигурации стереоцентра легко запомнить, нарисовав буквы R и S, как показано ниже на рис. 6.15.6.
Иногда младший лиганд удобнее расположить над плоскостью листа. В этом случае при падении старшинства лигандов а —> b —> с по часовой стрелке хирально
му центру надо приписать противоположную конфигурацию S (заменить R на 5) (рис. 6.15.7).
Если при установлении порядка старшинства лигандов оказывается, что некоторые атомы ближайшего окружения хирального центра одинаковы, то процедуру оценки следует провести для атомов следующей «сферы». Если в молекулярной цепи лиганда встречается разветвление, то анализ производится в направлении цепи наибольшего старшинства. Первое предпочтение, полученное лигандом, рассматривается как окончательное и не подлежит дальнейшей переоценке. В качестве примера приведем последовательность определения конфигурации стереоцентра в соединении 4. Для удобства рассмотрения рядом с символом рассматриваемого атома в скобках в порядке уменьшения старшинства записывают атомы, с которыми он связан (рис. 6.15.8).
Если атомы связаны кратными связями, то для определения старшинства двойная связь заменяется двумя, а тройная связь — тремя простыми связями с фиктивными атомами того же типа. Фиктивный атом заключается в скобки и рассматривается как атом с одним лигандом (рис. 6.15.9).
В тех случаях, когда заместители у хирального центра являются циклами, для определения старшинства циклическая структура разрывается по связям у точки разветвления, а затем к концу каждой полученной таким образом цепи добавляют фиктивный атом такой же, как находящийся в точке разветвления. Например, в соединении 5 пирролидиновый цикл разрывают по связям (/) и (2). Таким образом получают четыре цепи, две из которых, содержащие в [3-положении атом азота, имеют более высокое старшинство по сравнению с цепями, в которых атом азота находится в у-положении. В свою очередь цепь -CH2-NH-CH2-CH2-(C) старше, чем -СН2—NH СН2-СН3, из-за наличия фиктивного атома С. Напротив, цепь -CH2-CH2-NH-CH2-CH3 старше, чем -CH2-CH2-NH-CH2-C), т. к. в первой концевой атом углерода связан с тремя атомами водорода, а фиктивный атом углерода во второй по определению не связан с другими атомами (рис. 6.15.10).
Во многих случаях, когда порядок старшинства заместителей у хиральных центров в циклических молекулах очевиден уже при рассмотрении ближайшего окружения, операцию «расчленения кольца» проводить не обязательно, см. рис. 6.15.11.
Описание стереохимии спиросоединений с хираль-ным спиро-атомом в большинстве случаев может быть произведено по описанным выше правилам (рис. 6.15.12).
Примеры, приведенные ниже, иллюстрируют применение правила 3 определения старшинства заместителей, см. рис. 6.15.13.
При определении стереодескриптора для названий молекул с хиральными трех- или четырехкоординированными гетероатомами принимается, что неподелен-ная электронная пара у хирального центра имеет наименьшее старшинство (рис. 6.15.14).
1114
Новый справочник химика и технолога
Рис. 6.15.6
(Я)-1 -Бром-1 -иодэтан англ.-. (/?)-1-Bromo-1 -iodoethane
(S)-1 -Дейтериопропан-1 -ол англ.: (S)-1 -Deuteriopropan-1 -ol
Рис. 6.15.7
nh2
C4(N,C,H) I
1 сфера
С3(С,Н,Н)
с1(о,н,н) а
он
C1(O,H,H) > C1(N,H,H) = C1(N,H,H) > H
a I ♦ d
N2(C,C) = N2(C,C)
C3(C,H,H) = C3(C,H,H) = C3(C,H,H) = C3(C,H,H)
t ♦ ♦ t
C4(N,C,H) < C4(O,H,H) = C4(O,C,H) > C4(C,H,H)
♦ I
C5(F,C,H) < C5(CI,C,H)
c b
Br F
C^F.C.H)
OH , Ol
YC,w,w^CH3 faa.c.H)
(o3(C, H, H) c’H)
N-------^^OH
N2(C,C)
'(O.C.H)
2 сфера
3 сфера
с
C1(N,H,H)
N2(C,C) N
4
C(N,H,H)
4 сфера
5 сфера
направление наибольшего
старшинства [CfQ, С,Н)>С4(С,Н,Н)}
[направление наибольшего
[старшинства [с4(О,с,Н)>с4(ы,с,Н)\
Рис. 6.15.8
p P-(C)
—C = — C-(O) OH_____________OH
1 сфера C(O,О,О)
2 сфера
,P p-(C)
> —C = — C-(O)
_____H_________H
C1(O,O,H)
*
O2(C)
OH OH
> — с-он > — cx
H H H I
C1(O,O,H) C(O,H,H)
opH)
(C) (C) (C)(0)(C)
CH-C-C-C-C-(C) j H H H H
\ H H H H ен-c-c-d-c-(C)
(C) (C) (C)(0)(C)
(C)(C)
> — CECH = — C-CH
(C)(C)
pHj
> -C-CHj CH3
u
H3CxC"N'XH2
H2 (1) \
1 сфера C4(C,C,C)
i
2 сфера C2(C C,H)
3 сфера C3(C,C,H)
C1(C,C,C) c4 (0,0,0)
+ . i
C2(C,C,H) c2(H,H,H)
H
Рис. 6.15.9
•(2) ZCH2
HN
)^H2
H3C
b
CH2-NH-CH2—CH3 d (C)-H2C-HN-H2C-H2C—CH2—CH2—NH—CH2—CH3 c
CH2-NH-CH2-CH2-(C)
a (1)
H
5
(5)-3-(Этиламинометил)-3-[2-(этиламино)этил]пирролидин англ: (S)-3-[2-(Ethylamino)ethyl]-3-(ethylam!nomethyl)pyrrolidine
(S)
Рис. 6.15.10
Современная номенклатура органических соединений
1115
(4а8,58,8аЯ)-5-Фторгексагидро-1/-/-тиопирано[3,4-с]пиридин-4(ЗН)-он англ.-. (4aS,5S,8aR)-5-Fluorohexahyclro-1/-/-thiopyrano[3,4-c]pyridin-4(3H)-one
с b
Рис. 6.15.11
(Я)-2'Н-Спиро[инден-1,2'-[1,3]оксазин] англ.-. (f?)-2'H-Spiro[indene-1,2’-[1,3]oxazine]
Рис. 6.15.12
а
(8,2Е,57)-Гепта-2,5-диен-4-ол f англ.: (S,2E,5Z)-Hepta-2,5-dien-4-ol
с
(8,2Е,77)-5-Метил-2,3,7,8-тетрафторнона-2,7-диен
англ.: (S,2E,7Z)-2,3,7,8-Tetrafluoro-5-methylnona-2,7-diene
Рис. 6.15.13
(Я)-Метилэтилсульфоксид англ.: (R)-Ethylmethylsulfoxide
(25)-3-Метил-2-[(8)-метилфенилфосфиноил]бутановая кислота англ.: (2S)-3-Methyl-2-[(S)-methylphenylphosphinoyl]bytanoic acid
Рис. 6.15.14
В простых случаях можно использовать следующий ряд старшинства наиболее распространенных лигандов в органических соединениях: -I > -Br > -Cl > -SO3H > > -SO2R > -SOR > -SR > -SH > > -PR, > -SiR3 > -F > >-OTs > -OAc > -OPh > -OMe > -OH > -NO2 > > -N’Me3 > -NEt2 > -NMe2 > -NHCOPh > -NHR > -NH2> > -CO2R > > -CO2H > -COPh > -COMe > -CHO > > -CH2OR > -CH2OH > -CN > -CH2NH2 > -Ph > -C=CH > > wpew-бутил > циклогексил > ewop-бутил > -CH-CH2 > > изоггропил > -CH2Ph > -CH2CH=CH2 > изобутил > -Et > > -Me >Li>T>D>H> электронная пара.
Энантиомеры не отличаются по скалярным физическим свойствам. В то же время они вращают плоско-поляризованный свет в противоположные стороны, например (8)-аланин вращает плоскость поляризации вправо [(+)-энантиомер], а (Я)-аланин — влево [(-)-энантиомер]*. Это обстоятельство может отражать-
‘ Использование дескрипторов d, I, dl, как альтернативы дескрипторам (+), (-) и (±) не рекомендовано в настоящее время IUPAC.
ся в названии соединения, особенно когда абсолютная конфигурация хирального центра неизвестна, а известен только знак оптического вращения. Например, (8)-аланин — это (+)-аланин, (Я)-миндальная кислота PhCH(OH)COOH — это (-)-миндальная кислота, (Я)-глицериновый альдегид НОСН2СН(ОН)СНО — это (+)-глицериновый альдегид. Приведенные примеры иллюстрируют тот факт, что между знаком оптического вращения и конфигурацией стереоцентров соединения нет прямой связи.
В названиях рацематов, смесей равных количеств энантиомеров, используются стереодескрипторы (RS) и (SR) (без запятой). При этом хиральному центру с наименьшим локантом присваивается дескриптор (RS). Для того чтобы отличать индивидуальные энантиомеры от рацематов, с названиями и формулами последних могут использоваться дескрипторы «(±)» или «рац» («гас») (рис. 6.15.15).
Не следует путать префиксы, написанные прописными и заглавными буквами: d и D, I и L. Последние до сих пор часто используются для обозначения абсолютной
1116
Новый справочник химика и технолога
конфигурации аминокислот и сахаров. Если в проекции Фишера с атомом С1 наверху функциональная группа у определяющего стереоцентра находится справа, то это абсолютная конфигурация D, если слева — L. Для аминокислот определяющим стереоцентром является атом С2, а для сахаров — стереоцентр с наивысшим локантом (рис. 6.15.16).
Если в диастереомере известна только относительная конфигурация стереоцентров, то перед названием ставится префикс «ге1» и далее указывают конфигурацию хиральных центров, при этом атому с наименьшим локантом приписывают (^-конфигурацию.
Для обозначения относительной конфигурации могут также использоваться дескрипторы R* или S*. При наличии в молекуле центров с известной абсолютной конфигурацией и центров, для которых известна только относительная конфигурация, последние обозначаются как R* или S* (рис. 6.15.17).
Для обозначения относительной конфигурации стереоцентров в названиях циклических систем, которые можно изобразить как плоские, в случаях, не допускающих двойного толкования, для одинаковых заместителей (или атомов водорода) можно использовать префикс «цис» («cis»), если они расположенны по одну сторону плоскости цикла, и префикс «транс» («trans») — если по разные. Кроме того, согласно правилам IUPAC можно применять префиксы «cis» и «trans», сокращенные до «с», «/», по отношению к заместителю с наименьшим локантом, который отмечают префиксом «г» (от слова reference), например см. рис. 6.15.18.
В некоторых спиросоединениях может присутствовать хиральный центр и одновременно цис-, транс-изомерия. В таких случаях можно использовать комбинации стереодескрипторов, например см. рис. 6.15.19.
ио
(S) (2RS)-1 -[(1 /?8,28ЯЗЯ8)-2-Метил-3-этилциклопропил]пропан-2-ол
англ.'. (2/?S)-1-[(1/?S,2/?S,3S/?)-2-Ethyl-3-methylcyclopropyl]propan-2-ol
рац-(2Я,68)-2-Бензил-6-метилциклогексанон англ.-. rac-(2/?,6S)-2-Benzyl-6-methylcyclohexanone
со2н н—он но—н
со2н
СО2Н но—н н—он
СО2Н
но СО2Н
НО2С он
(R, /?)-винная кислота или (+) или (d)- или (!_)-винная кислота
(8,8)-винная кислота или (-) или (/)- или (О)-винная кислота
рацемат - эквимолярная смесь: рац- или (Я8,Я8)-винная кислота или (±) или (di)- или (О!_)-винная кислота
Рис. 6.15.15
СНО
н
но
н
н
он
н
он
ОН
СН2ОН
СНО
но
н
но
но
н
он
н
н
СН2ОН
н
D-глюкоза
L-глюкоза
СО2Н
NH2
СН2ОН
D-серин
СО2Н
h2n
н
СН2ОН
L-серин
* определяющий стереоцентр
Рис. 6.15.16
Современная номенклатура органических соединений
1117
[относительная конфигурация^
CI
rel-(2R,5R,8S)- или (2К*,5К*,8$*)-2-Гидрокси-5,8-
дихлорнонаналь
англ.-. rel-(2R,5R,8S)- или
(2K*,5K*,8S*)-5,8-Dichloro-2-
hydroxynonanal
(1 /?,2$,5/?)-2-Изопропил-5-метилциклогексиловый эфир (2/?*,3S*)-1,3-дифенилазиридин-2-карбоновой кислоты англ.'. (1/?,2S,5/?)-2-lsopropyl-5-methylcyclohexyl (2R*,3S*)-1,3-
diphenylaziridine-2-carboxylate
Рис. 6.15.17
Cl
соон
н
цис-2-Хлорциклопентанкарбоновая кислота англ.-. c/s-2-Chlorocyclopentanecarboxylic acid
Cl
сно
£-3-Метил-с-5-хлорциклогептан-г-1-карбальдегид англ.-. c-5-Chlorocycloheptane-f-3-methyl-r-1-carbaldehyde
г-1,с-5,с-8,М1-Тетраоксатетраспиро[2.0.24.0.27.0.21°.03]додекан англ.: г-1,с-5,с-8,М 1-Tetraoxatetraspiro[2.0.24 0.27.0.21°.03]dodecane
Рис. 6.15.18
Н xCN
С и 7-CN находятся в транс-положении
I I относительно циклогексанового кольца (S\/^
NO'"'< >з (1S, г-1)-Спиро[3.5]нонан-1Л7-дикарбонитрил
2 англ.: (1S, r-1)-Spiro[3.5]nonane-1 J-7-dicarbonitrile
Рис. 6.15.19
Хотя стереодескрипторы «эндо», «экзо», «син» и «анти» не рекомендованы IUPAC, они довольно широко используются в химической литературе для обозначения стереохимии в бицикло[Х.У.7]алканах (X > Y > Z). Дескрипторы «син» и «анти» описывают положение заместителей у атомов мостика Z по отношению к мостику X, а дескрипторы «экзо», «эндо» — положение заместителей у атомов мостиков X и Y относительно
мостика Z. Их применение можно проиллюстрировать следующей схемой:
Х> Y>Z
1118
Новый справочник химика и технолога
В названиях стереоизомеров, связанных с присутствием в молекуле двойной связи (геометрических изомеров), в случаях, исключающих двойное толкование, для обозначения одинаковых заместителей (либо атомов водорода), расположенных по одну сторону кратной связи, может использоваться префикс «цис», и префикс «транс» — для заместителей, расположенных по разные стороны (рис. 6.15.20).
Однако если у двойной связи имеются разные заместители, применение стереодескрипторов «цис» и «транс» приводит к неопределенности. Поэтому для замены этих стереодескрипторов было предложено использовать стереодескриптор «Z» для заместителей, имеющих набольшее старшинство (по правилам Канна — Ингольда — Прелога) в случае их расположения по одну сторону двойной связи, и стереодескриптор «Е» — для тех же заместителей, расположенных по разные стороны (от немецких слов ^usammen — вместе и entgegen — напротив). Дескрипторы «Z», «Е» с указанными в случае необходимости локантами располагают перед названием в скобках. Следует подчеркнуть, что нет никакого соответствия между «цис» и «Z», а также «транс» и «Е». Например, для первой из изображенных ниже молекул правильными будут названия: (Z)-2-хлорбут-2-ен и щранс-2-хлорбут-2-ен (рис. 6.15.21). Те же стереодескрипторы можно использовать и для кумуленов, содержащих нечетное число двойных связей, и некоторых других соединений, в которых все четыре заместителя находятся в одной плоскости (рис. 6.15.22).
Для отражения в названии стереохимии относительно связи >C=N- также рекомендуется использовать Z, Е префиксы (рис. 6.15.23).
В названиях хиральных соединений с осью хиральности (которые альтернативно могут быть рассмотрены как спирали) используются дескрипторы R. S (или /?а, Еа, если надо подчеркнуть, что данный дескриптор описывает спиральную хиральность), хотя предпочтительнее использовать дескрипторы Р (плюс) и М (минус). Для отнесения дескрипторов Р или М идентифицируют ось спирали и на каждом конце выделяют лиганды наивысшего старшинства по Кану — Ингольду — Прелогу.
Если для наименьшего угла между этими лигандами (т. с. < 180° в проекции) движение от старшего к младшему происходит по часовой стрелке, то используют префикс Р или «+», если против, то М или «-». При этом согласно дополнительному правилу, действующему в этих случаях, принимается, что лиганды, ближе расположенные к «наблюдателю», старше удаленных. Следует отметить, что независимо от того, с какого конца рассматривается спиральная молекула, будут получены одни и те же дескрипторы.
Дескрипторы Р, М могут быть использованы для обозначения энантиомерных конформеров, например, гош-бутана, и абсолютных конфигураций стереогенных осей и плоскостей, см. рис. 6.15.24.
Если молекула может быть представлена в виде вытянутого тетраэдра, то для существования оси хиральности второго порядка достаточно, чтобы лиганды с каждого конца были различными (L1 Ф L2, L1' * L2'). При определении старшинства лигандов в таких молекулах по Кану — Ингольду — Прелогу для отнесения R, S дескрипторов действует дополнительное правило: считается, что два лиганда на конце, с которого рассматривается молекула (выбор произволен), старше, чем лиганды на противоположном конце. Для стереогенных осей имеет место соответствие дескрипторов: /?а <-> М Еа <-> Р.
Типичными представителями молекул с осью хиральности являются аллены, 2,2',6,6'-тетразамещенные бифенилы, алкилиденциклоалканы типа А и спираны типа Б, см. рис. 6.15.25.
В некоторых случаях для определенности указывают положение оси, относительно которой определяется дескриптор, см. рис. 6.15.26.
Для определения стереодескриптора в спиросоедине-ниях типа В произвольно выбирают одно из колец в качестве «старшего» и приписывают более замещенной цепи (или гетероатому) в этом кольце приоритет а, а менее замещенной — с, тогда как в «младшем» кольце соответственно b и d. Далее определяют стерео дескриптор в соответствии с обычными правилами, а спироатом рассматривают как хиральный центр, см. рис. 6.15.27.
_______/СООН ноос/
НООС СООН
транс-Бутендиовая кислота (фумаровая кислота)
англ.-. frans-Butenedioic acid
(fumaric acid)
цис-Бутендиовая кислота (малеиновая кислота)
англ.-. c/s-Butenedioic acid
(maleic acid)
цис-З-Фтор-1 -хлорпроп-1 -ен англ.-, cis-l-Chloro-3-fluoroprop-1 -ene
Рис. 6.15.20
Современная номенклатура органических соединений
1119
(Е) СООН
(Z)
(2)-2-Хлорбут-2-ен англ.: (Z)-2-Chlorobut-2-ene
(2Е, 4Z)-Pекса-2,4-Диеновая кислота англ.: (2Е, 4Z)-Hexa-2,4-dienoic acid
(2Е,52)-[(2)-2-Хлорвинил]окта-2,5-диеновая кислота англ.: (2E,5Z)-[(Z)-2-Chlorovinyl]octa-2,5-dienoic acid
Рис. 6.15.21
\ /н
Н
(Е)-Гепта-2,3,4-триен или транс-гепта-2,3,4-три ен англ.: (E)-Hepta-2,3,4-triene или frans-hepta-2,3,4-triene
(2)-1,4-Бис(1-бромэтилиден)циклогексан англ.: (Z)-1,4-Bis(1-bromoethylidene)cyclohexane
цис-1,9-Диоксадиспиро[4.2.4.2]тетрадекан
англ.: cis-1,9-Dioxadispiro[4.2.4.2]tetradecane
Рис. 6.15.22
(Е)-Семикарбазон (2)-бут-2-еналя англ.: (Z)-But-2-enal (E)-semicarbazone
(Е)-оксим бензальдегида англ.: Benzaldehyde (E)-oxime
Рис. 6.15.23
Р - гош конформация бутана
Рис. 6.15.24
1120
Новый справочник химика и технолога
(М)- или (Р)-Пента-2,3-диен англ.'. (М)- или (R)-Penta-2,3-diene
ь со2н
(Р)- или (8)-6,6'-Дииодбифенил-2,2'-дикарбоновая кислота англ.-. (Р)- или (S)-6,6'-Diiodobiphenyl-2,2'-dicarboxylic acid
К /СООН
X =
II h Н /<^-СООН
II I е а
(S)<CH3 н гсоон
Н3с ''Н
(8а)-(4-Метилциклогексилиден)уксусная кислота /
англ.-. (Sa)-(4-Methylcyclohexylidene)acetic acid
НХ СООН
(S) Н
(8а)-Спиро[3.3]гептан-2,6-дикарбоновая кислота
англ.-. (Sa)-Spiro[3.3]heptane-2,6-dicarboxylic acid
Рис. 6.15.25
(5(11)Ра)-1,12-Диоксатриспиро[4.2.2.411.28.25]нонадекан англ.'. (5(11 )Ra)-1,12-Dioxatrispiro[4.2.2.411.28.25]nonadecane
Рис. 6.15.26
Современная номенклатура органических соединений
1121
(/?)-Триспиро[2.0.0.25.14.13]нонан англ.'. (R)-T rispi го [2.0.0.25.14.13]попапе
(S)-1,6-Диоксаспиро[4.4]нонан
англ.: (S)-1,6-Dioxaspiro[4.4]nonane
Рис. 6.15.27
В названиях хиральных соединений с плоскостью хиральности используются префиксы /?, S (или Р, М, или /ф, Sp, если надо подчеркнуть, что данный дескриптор описывает планарную хиральность). Плоскостью хиральности (если она имеется) является плоскость, содержащая максимально возможное количество атомов молекулы (но не все!). Для определения стерео дескриптора плоскость хиральности рассматривают со стороны атома, ближайшего к плоскости (реперный атом), но находящегося вне нее. При наличии нескольких вариантов выбирают атом, ближайший к атому наибольшего старшинства. Если при этом для соседних
трех атомов, последовательно обозначенных а, Ь, с, движение в направлении а -> b -> с в хиральной плоскости происходит по часовой стрелке, то конфигурация обозначается R (или Р, или /ф), в противном случае 5 (или Л/, или Sp). Если имеются варианты, «соседние атомы» выбирают в соответствии со старшинством (рис. 6.15.28).
Как видно, для стереогенных плоскостей имеет место соответствие дескрипторов: R <-»• Р, S <-»• М, противоположное тому, что имеет место для стереогенных осей.
стрелкой указан реперный атом
(Sp) или (Л4)-Циклооктен
англ.: (Sp) или (M)-Cyclooctene
(Кр) или (Р)-2,11-Диоксабицикло[10.2.2]гексадека-1 (14),12,15-триен-13-карбонитрил
англ.: или (Р)-2,11 -Dioxabicyclo[10.2.2]hexadeca-1 (14), 12,15-triene-
13-carbonitrile
в соответствии с правилом старшинства выбран атом с, а не с1
(Sp) или (М)-Трицикло[8.2.2.24,7]гексадека-
1 (13),4,6,10(14), 11,15-гексаен-5-ол
англ.: (Sp) или (М)-Т ricyclo[8.2.2.24'7]hexadeca-
1 (13),4,6,10(14), 11,15-hexaen-5-ol
Рис. 6.15.28
6.16. Номенклатура природных соединений
6.16.1. Углеводы
Класс углеводов включает моносахариды, олигосахариды и полисахариды, а также вещества, получающиеся из моносахаридов при удалении карбонильной группы, при окислении одной или более терминальных
групп в карбоновые кислоты или при замене одной или более гидроксильных групп атомом водорода, аминогруппой, тиольной группой или подобными гетеро-атомными группами.
Родоначальные моносахариды являются полигидроксиальдегидами Н(СНОН)ПСНО или полигидроксикетонами H(CHOH)nCO(CHOH)mH с тремя или более
1122
Новый справочник химика и технолога
атомами углерода. Название моносахариды (в противоположность олигосахаридам и полисахаридам) относится к молекулам без гликозидной связи с другими подобными молекулами и включает альдозы, кетозы, диальдозы, альдокетозы, дикетозы, а также дезокси-и аминосахара и их производные при условии, что исходные соединения имеют (потенциальную) карбонильную группу. Термин «потенциальная альдегидная/ке-тонная карбонильная группа» относится к полуацеталь-ной/полукетальной группе, возникающей при замыкании кольца.
6.16.1.1. Альдозы
Моносахариды с одной альдегидной карбонильной группой или потенциальной альдегидной карбонильной группой называются альдозами. Тривиальные названия альдоз с числом атомов углерода 3-6, которые образуют основу конфигурационных префиксов в систематических названиях углеводов, приведены в табл. 6.41.
Систематические названия моносахаридов образуются из основы и конфигурационных префиксов. Для альдоз с 3-10 атомами углерода основами названия яв
ляются соответственно: триоза, тетроза, пентоза, гексоза, гептоза, октоза, ноноза и декоза. Цепь нумеруется таким образом, чтобы карбонильная группа находилась в положении «1». Конфигурация СНОН групп обозначается с помощью конфигурационных префиксов (табл. 6.41). Например, D-рмбо-пентоза для D-рибозы. Для родоначальных сахаров и их производных с неизмененными стереоцентрами предпочтительнее использовать тривиальные названия (табл. 6.41-6.43).
Альдозы, содержащие более четырех хиральных центров, называют, добавляя к основе два или более конфигурационных префикса. Префиксы сначала выбирают для групп из 4 стереоцентров, ближайших к С1, опираясь при этом на конфигурацию для соединений из табл. 6.41. Конфигурационные префиксы для групп атомов углерода, наиболее удаленных от С1 (которые могут содержать менее четырех стереоцентров), приводятся в названии первыми. Пример приведен на рис. 6.16.1. При определении конфигурационного префикса ахиральные центры, разделяющие последовательность хиральных центров, игнорируются (см. примеры в разделах «кетозы» и «дезоксисахара»).
Таблица 6.41
Тривиальные названия альдоз, символы для их обозначения, конфигурационные префиксы и формулы в проекции Фишера (показаны только D-формы, L-формы являются зеркальными отображениями)
сно н-с-он СН2ОН D-Глицериновый альдегид Хд-глицеро D-Glyceraldehyde D-g/ycero сно н-с-он н-с-он СН2ОН D-Эритроза Хд-эритро D-Erythrose Xd-erythro сно но-с-н н-с-он СН2ОН D-Треоза Хд-трео D-Threose Xd-threo
сно н-с-он н-с-он н-с-он СН2ОН D-Рибоза Хд-рибо D-Ribose Xd-ribo (D-Rib) сно но-с-н н-с-он н-с-он н-с-он СН2ОН D-Арабиноза Хд-арабино D-Arabinose Xd-arabino (D-Ara) сно н-с-он но-с-н н-с-он СН2ОН D-Ксилоза Хд-ксило D-Xylose V)-xylo (D-Xyl) сно но-с-н но-с-н н-с-он СН2ОН D-Ликсоза Хд-ликсо D-Lixose Хд-lixo (D-Lix)
сно н-с-он н-с-он н-с-он н-с-он СН2ОН D-Аллоза Хд-алло D-Allose D-allo (D-All) сно но-с-н н-с-он н-с-он н-с-он СН2ОН D-Альтроза Хд-альтро D-Altrose Xd-altro (D-Alt) сно н-с-он но-с-н н-с-он н-с-он СН2ОН D-Глюкоза Хд-глюко D-Glucose Xd-gluco (D-Glc) сно но-с-н но-с-н н-с-он н-с-он СН2ОН D-Манноза Хд-манно D-Mannose Хд-таппо (D-Man)
Современная номенклатура органических соединений
1123
Окончание табл. 6.41
СНО СНО СНО СНО
н-с-он но-с-н н-с-он но-с-н
н-с-он н-с-он но-с-н но-с-н
но-с-н но-с-н но-с-н но-с-н
н-с-он н-с-он н-с-он н-с-он
СН2ОН СН2ОН СН2ОН СН2ОН
D-Гулоза D-Идоза D-Галактоза D-Талоза
D-гуло D-udo D-галакто D-тало
D-Gulose D-Idose D-Galactose D-Talose
D-gu/o D-ido D-galacto D-talo
(D-Gul) (D-Ido) (D-Gal) (D-Tal)
СНО
Н-С-ОН'
НО-С-Н п
। D-глюко
н-с-он Н-С-ОН> Н-С-ОН D-глицеро
СН2ОН
Правильно: О-глицеро-О-глюко-Гептоза
Неправильно: О-глюко-О-глицеро-Гептоза
СНО
Н-С-ОН ) Н-С-ОН I
Н-С-ОН j н-с-он J н—j—ОН 1 но-с-н J
СН2ОН
D-алло
L-mpeo
Правильно: L-mpeo-D-алло-Октоза
Неправильно: О-алло-Стрео-Октоза
Рис. 6.16.1
Циклические формы
Большинство моносахаридов существует в виде циклических полуацеталей и полукеталей. Циклические формы, имеющие 3 атома в цикле, называются оксирозами, 4 — оксетозами, 5 — фуранозами, 6 — пиранозами, 7 — септанозами, 8 — октанозами и т. д. Для того, чтобы избежать неопределенности, положение замыкания цикла может быть указано с помощью локантов, при этом локант карбонильной группы указывается первым, а гидроксильной группы — вторым (см. пример в разделе «кетоальдозы»).
При изображении циклической формы сахара в проекции Фишера длинную связь обычно рисуют между кислородом, входящим в гетероцикл, и атомом углерода полуацетальной группы. Новый хиральный центр, возникающий при замыкании полуацетального кольца, называется аномерным центром. Два возможных стереоизомера (аномера), обозначают с помощью греческих букв а и Р в соответствии с конфигурационными отношениями между аномерным центром и аномерным реперным (reference) атомом. Аномерный реперный атом совпадает с конфигурационным атомом (т. е. нижним хиральным атомом в проекции Фишера) родоначального сахарида при условии, что в названии не используются несколько конфигурационных префиксов. В противном случае аномерным реперным атомом яв
ляется атом, имеющий наивысший номер в ближайшей к аномерному центру группе хиральных центров, при условии, что эта группа обозначена одним конфигурационным префиксом и участвует в образовании гетероцикла. В а-аномере экзоциклический атом кислорода при аномерном центре (в простейшем случае — полуацетальный гидроксил) в проекции Фишера находится по одну сторону от вертикальной оси с атомом кислорода, присоединенным к аномерному реперному атому, в Р-аномере эти атомы кислорода расположены с разных сторон, см. рис. 6.16.2. В выше приведенных примерах наряду с проекционными формулами Фишера показаны соответствующие формулы Хеуорса. Ниже показана схема замыкания пиранозного кольца D-глюкозы (рис. 6.16.3).
В формуле Хеуорса а-аномера сахара D-ряда (циклическая форма ориентирована таким образом, что при рассмотрении кольца сверху номера кольцевых атомов возрастают по часовой стрелке) ОН-группа при С1 располагается снизу, а в Р-аномере — сверху. Для сахаров L-ряда ситуация противоположная.
6.16.1.2. Диальдозы
Моносахариды с двумя (потенциальными) альдегидными группами называются диальдозами. Название диальдозы образуется из названия соответствующего
1124
Новый справочник химика и технолога
названия альдозы путем замены окончания «оза» на «одиальдоза». При выборе основы предпочтение отдается альдозе, первой по алфавиту (включая конфигурационный префикс). В названиях циклических форм
указывается локант аномерного атома, а вслед за ним локант второго атома углерода, присоединенного к эн-доциклическому атому кислорода (рис. 6.16.4).
н-бчэн но—н
н—он н-^о-
н
*—аномерный центр
с разных сторон - 0 \
♦ — аномерный реперный атом
0 — конфигурационный атом
н—^-он' .НО-С—Н ' I ч Н—С-0-7 = 'нр-с—Н
\ Jo но-с—н I сн2он
0-L-Глюкооксетоза англ.: 0-L-Glucooxetose
сн2он н----он
н----он
^он
СН2ОН
a-D-Альтрофураноза англ.: a-D-Altrofuranose
\ н—с-он н—I—он
но—н н—он н— -о-7
сн2он
a-D-Глюкопираноза англ.: a-D-Glucopyranose
Н-С-ОМе
НО----H
НО---H
но——H
СН2ОН
сн2он н—с—он
Метил 1_-глицеро-а-О-манно-гептопиранозид англ.: Methyl L-g/ycero-a-D-manno-heptopyranoside
Рис. 6.16.2
Рис. 6.16.3
Современная номенклатура органических соединений
1125
СНО
Н---ОН
НО---Н
СНО
L-mpeo-T етродиальдоза (QR)-D-gluco-V ексодиальдо-6,2-пираноза
англ.-. L-fftreo-Tetrodialdose англ.: (6R)-D-g/wco-Hexodialdo-6,2-pyranose
Рис. 6.16.4
6.16.1.3. Кетозы
Моносахариды с кетонной или потенциальной ке-тонной карбонильной труппой называются кетозами. Тривиальные и систематические названия кетоз с числом атомов углерода 3-6 приведены в табл. 6.42. Положение карбонильной труппы указывается в названии с помощью локанта. В случае 2-кетоз локант может быть опущен, если это не приведет к неопределенности. В систематическом названии кетозы за основу берется соответствующее название альдозы, а окончание «оза» заменяется на «улоза», с предшествующим локантом, показывающим положение кетогруппы, например, гекс-3-улоза. Если карбонильная группа находится в середине цепи с нечетным числом атомов углерода, то из двух возможных вариантов названия предпочтение отдается первому по алфавиту. Для кетоз используются те же конфигурационные префиксы, что и для альдоз. При определении этого префикса в случае 3-, 4- и т. д. кетоз карбонильная группа игнорируется, и набор хиральных центров называется согласно табл. 6.41 (рис. 6.16.5). Систематические названия дикетоз формируют аналогично, игнорируя при определении конфигурационного префикса ахиральные центры (рис. 6.16.6).
6.16.1.4. Кетоальдозы (альдокетозы)
Названия кетоальдоз формируют подобно названиям дикетоз, заменяя в названии соответствующей альдозы окончание «а» на «улоза». Нумерацию начинают с (потенциальной) альдегидной группы, однако локант 1 не указывают в названии; локант (потенциальной) кетонной карбонильной группы помещают в названии перед окончанием «улоза»; в том случае, когда этот локант 2, он может быть опущен. Для циклических форм в тех случаях, где возможна неопределенность, положение кольца может быть указано с помощью локантов, при этом локант (потенциальной) карбонильной группы указывается первым. В биохимической литературе для кетоальдоз часто используют соответствующие «дегидро» названия (рис. 6.16.7).
6.16.1.5. Дезоксисахара
Систематическое название дезоксисахаров состоит из префикса «дезокси» («deoxy») с предшествующим локантом, за которым следует основа с конфигураци
онными префиксами (последние приводятся, начиная с конца молекулы, наиболее удаленного от С1). Префикс «дезокси» является отделяемым и, следовательно, наряду с другими префиксами (кроме конфигурационных) перечисляется в алфавитном порядке и используется как с систематическими, так и тривиальными названиями сахаров. При определении конфигурационного префикса группа ^СН2 (также как и ^С=О) игнорируется (рис. 6.16.8).
6.16.1.6. Аминосахара
Систематическое название аминосахаров состоит из комбинации «дезокси» и «амино» префиксов, располагаемых в алфавитном порядке наряду с другими отделяемыми префиксами перед основой, в которой аминогруппа замещает гидроксильную (при определении конфигурационных префиксов аминогруппа рассматривается как эквивалент гидроксильной группы) (рис. 6.16.9). В случае замещения гидроксильной группы в положении 2 на аминогруппу обычно используют тривиальные названия с окончанием «озамин»: D-галактозамин для 2-амино-2-дезокси-О-галактозы; D-глюкозамин для 2-амино-2-дезокси-О-глюкозы; D-маннозамин для 2-амино-2-дезокси-О-маннозы; D-фукозамин для 2-амино-2,6-дидезокси-О-галактозы и т. д. (см. табл. 6.43).
6.16.1.7. Другие замещенные моносахариды
Моносахариды, в которых замещен атом водорода при нетерминальных атомах углерода, называют как С-замещенные соединения. При отнесении конфигурации старшая группа (согласно правил Канна— Ин-гольда — Прелога) рассматривается как эквивалент ОН-группы. Соединения, в которых замещена ОН-группа при нетерминальном, неаномерном атоме углерода, называют как дезоксисахара. Группа, замещающая ОН-группу, определяет конфигурационное описание. Соединения, в которых замещена ОН-группа и атом водорода при нетерминальном атоме углерода, называют как дизамещенные дезоксисахара. Конфигурацию определяют, рассматривая старший заместитель как эквивалент ОН-группы. Для описания модифицированного стереоцентра, чтобы избежать неопределенности, можно использовать /?,5-стереодескрипторы (рис. 6.16.10).
1126
Новый справочник химика и технолога
Таблица 6.42
Тривиальные и систематические названия кетоз, символы для их обозначения и формулы в проекции Фишера (показаны только D-формы, L-формы являются зеркальными отображениями)
СН2ОН с=о СН2ОН 1,3-Дигидроксиацетон (1,3-Dihydroxyacerone) CH2OH c=o Н-С-ОН CH2OH D-Эритрулоза, D-глмг/еро-тетрулоза (D-Erythrulose, D-g/ycero-tetrulose)
СН2ОН с=о н-с-он н-с-он СН2ОН D-Рибулоза, О-эрмлтро-пент-2-улоза [D-Ribulose (D-Rul), D-eryr/zro-pent-2-ulose] CH2OH C=O но-с-н н-с-он CH2OH D-Ксилулоза, О-лтрео-пент-2-улоза [D-Xylulose (D-Xul), D-r/zreo-pent-2-ulose]
СН2ОН с=о н-с-он н-с-он н-с-он сн2он D-Псикоза, О-рибо-гекс-2-улоза [D-Psicose (D-Psi), D-r/Z?o-hex-2-ulose] CH2OH c=o но-с-н H-C-OH H-C-OH CH2OH D-Фруктоза, О-арабш/о-гекс-2-улоза [D-Fructose (D-Fru), D-ara/?z«o-hex-2-ulose]
СН2ОН с=о н-с-он но-с-н н-с-он СН2ОН D-Сорбоза, О-ксшю-гекс-2-улоза [D-Sorbose (D-Sor), D-xy/o-hex-2-ulose] CH2OH c=o но-с-н но-с-н н-с-он CH2OH D-Тагатоза, О-лглссо-гекс-2-улоза [D-Tagatose (D-Tag), D-Zyxo-hex-2-ulose]
сн2он с=о
но-с-н н-с-он н-с-он н-с-он
сн2он
О-альтро-Г епт-2-улоза
англ.: D-a/fro-Hept-2-ulose
L-Седогептулоза (трив.)
СН2ОН н-с-он "I I
с=о н-с-он
I
> D-алло
СН2ОН но-с-н н-с-он 6=0 но-с-н но-с-н
СН2ОН
н-с-он н-с-он>
н-с-он] но-с-н J I
L-mpeo
СН2ОН
L-mpeo-D-алло-Нон-З-улоза англ.: L-fbreo-D-a//o-Non-3-ulose
L-глюко-Г епт-4-улоза, а не О-гуло-гепт-4-улоза англ.: D-g/uco-Hept-4-ulose
Рис. 6.16.5
C }H2OH
CH2OH h— —OH
=O но— —H
HO— —H =O о о Illi
H— —OH HO- —H
( :h2oh ho— c —H }H2OH
D-mpeo-Г ексо-2,4-Диулоза 1_-альтро-Окто-4,5-диулоза,
англ.: D-tf?reo-Hexo-2,4-diulose а не 1_-тало-окто-4,5-диулоза
англ.: L-a/fro-Octo-4,5-diulose
Рис. 6.16.6
Современная номенклатура органических соединений
1127
сно
н-с-он1 о=с
Н-С-ОН >- D-алло н-с-он н-с-он.
СН2ОН
D-алло-Гептоз-3-улоза англ.: D-a//o-Heptos-3-ulose
► D-глюко
СНО н-с-он^ но-с-н о=с н-с-он Н-С-ОНJ н-с-он но-с-н
СН2ОН
1-трео-О-глюко-Ноноз-4-улоза
англ.: L-t/)reo-D-g/uco-Nonos-4-ulose
Стрео
МеО-С-Н
Н---ОН
но—н =0 н—о-^
СН2ОН
ОН
ОН
ОН
Метил-0-О-ксш7О-гексопиранозид-4-улоза англ.: Methyl p-D-xy/o-hexopyranosid-4-ulose
МеО-С-СНО
НО---Н
Н---ОН
о оме
НОН2С
ОН Н
H ОН
СНО
СН2ОН
Метил-а-1-кс1/ло-гексоз-2-уло-2,5-фуранозид англ.: Methyl a-L-xy/o-hexos-2-ulo-2,5-furanoside
Рис. 6.16.7
н-(5-он Н-С-Н н-с-он н-с-он
н-с-он
сн2он
сн2он но-с-н
ОН
2-Дезокси-а-О-алло-гептопираноза англ.: 2-Deoxy-a-D-a//o-heptopyranose
СНз с=о но-с-н н-с-он н-с-он н-с-он но-с-н
сн2он
1-Дезокси-Ь-глацеро-О-альтро-окт-2-улоза англ.: 1 -Deoxy-L-g/ycero-D-a/tro-oct-2-ulose
Рис. 6.16.8
нон2С'Т^о-уг°Н
HO-L-^x/NHMe но
2-Дезокси-2-метиламино-1_-глюкопираноза англ.: 2-Deoxy-2-methylamino-L-glucopyranose
он
4,6-Дидезокси-2,3-ди-0-метил-4-формамидо-0-маннопираноза англ.: 4,6-Dideoxy-4-formamido-2,3-di-O-methyl-D-mannopyranose
Рис. 6.16.9
1128
Новый справочник химика и технолога
2-С-Фенил-а-0-глюкопираноза англ.-. 2-C-Phenyl-a-D-glucopyranose
2-Дезокси-2-фенил-а-О-глюкопираноза или
2-Дезокси-2-С-фенил-а-О-глюкопираноза или
(2/?)-2-Дезокси-2-фенил-а-0-арабино-гексопираноза
англ.-. 2-Deoxy-2-phenyl-a-D-glucopyranose
0N02
2,З-Диазидо-4- О-бензои л-6-бром-2,3,6-тридезокси-а-О-маннопиранозилнитрат англ.-. 2,3-Diazido-4-O-benzoyl-6-bromo-2,3,6-
trideoxy-a-D-mannopyranosyl nitrate
(2/?)-2-Бром-2-дезокси-2-хлор-а-О-арабино-
гексопираноза (Br старше Cl) или
2-бром-2-дезокси-2-хлор-а-О-глюкопираноза
англ.-. (2R)-2-Bromo-2-chloro-2-deoxy-a-D-arab/no-hexopyranose
Рис. 6.16.10
Если замещение при терминальном атоме углерода приводит к образованию нового центра хиральности, для указания стереохимии применяют /?, S'-стерео дескрипторы. Моносахариды с терминальной метильной группой называют как дезоксисахара, а не как С-метил-производные. Замещение альдегидного водорода циклической системой обозначают с помощью соответствующего С-префикса, например см. рис. 6.16.11.
Производные сахаров, образующиеся путем замещения карбонильного кислорода азотсодержащей группировкой (оксимы, гидразоны, озазоны и т. д.), называют традиционными способами. Производные сахаров, получающиеся в реакциях карбонильной группы со спиртами, получают традиционные названия как соответствующие (полу)ацетали и т. д. (рис. 6.16.12).
6.16.1.8. Альдиты
Альдиты (alditols) или алканполиолы, получающиеся при восстановлении сахаров, называют, заменяя суффикс «оза» в названии соответствующей альдозы на суффикс «ит» («itol»). Если альдит может быть производным двух различных альдоз либо альдозы и кетозы, выбор основы осуществляют в соответствии с критериями, приведенными в подразд. 6.16.1.14 (рис. 6.16.13).
6.16.1.9. Кислоты — производные сахаров
При окислении терминальных альдегидных и гид-роксиметильных групп моносахаридов может быть получено четыре типа кислот. Их систематические названия легко получить, заменив суффикс «оза» или «улоза» в названии моносахарида на соответствующие окончания, которые приведены ниже. Кроме того, многие из этих соединений имеют широко употребимые тривиальные названия. Производные кислот называют, используя обычные способы наименования производных органических кислот.
1. Альдоновые кислоты — окисление альдегидной группы моносахарида; суффикс «оновая кислота» («-onic acid») (рис. 6.16.14).
2. Уроновые кислоты — окисление гидроксиме-тильной группы моносахарида; суффикс «уроновая кислота» («-uronic acid») (рис. 6.16.15).
3. Аль даровые кислоты — окисление обеих терминальных групп моносахарида до карбоксильных; суффикс «аровая кислота» («-aric acid») (рис. 6.16.16).
4. Кетоальдоновые кислоты — окисление терминальной карбонильной группы кетозы; суффикс «уло-зоновая кислота» («-ulosonic acid») (рис. 6.16.17).
Современная номенклатура органических соединений
1129
СНО
(5/?)-5-С-Фенил-5-С-циклогексил-О-ксилоза англ.: (5/?)-5-C-Cyclohexyl-5-C-phenyl-D-xylose
Ph =0 Н---ОН
НО---Н
Н---ОН
н—он
СН2ОН
1-С-Фенил-О-глюкоза,
а не 1-С-фенил-0-алюко-гекс-1-улоза англ.: 1-C-Phenyl-D-glucose
Рис. 6.16.11
Н—f=N-NH2
Н---ОН
НО---Н
Н---ОН
Н---ОН
СН2ОН
Н—f=N—NHPh
SMe
Н—I— SMe
Н---ОН
НО---Н
Н---ОН
Н---ОН
Гидразон D-глюкозы англ.: D-Glucose hydrazone
=N—NHPh
НО---H
Н---ОН
Н---ОН
СН2ОН
СН2ОН
S.S-Диметилдитиоацеталь D-глюкозы
англ.: D-Glucose S,S-dimethyl dithioacetal
Бис(фенилгидразон) О-арабаяо-гексоз-2-улозы или фенилозазон D-фруктозы
англ.: D-arab/no-Hexos-2-ulose bis(phenyhydrazone) или D-Fructose phenylosazone
Рис. 6.16.12
СН2ОН н—он но—н но—н н—он н—он
СН2ОН
СН2ОН н—он н—он но—н но—н
СНз
В-глицеро-Сгалакто-Г ептит, а не О-аляцеро-1_-маяяо-гептит англ.: D-g/ycero-L-ga/acto-Heptitol
L-Рамнит или
1 -дезокси-Ь-маннит англ.: L-Rhamnitol или
1-Deoxy-L-mannitol
СН2ОН
Н---ОН
НО---Н
Н---ОН
Н---ОН
СН2ОН
СН2ОН н—он но—н н—он но—н н—он
СН2ОН
D-Глюцит, а не L-гулит англ.: D-Glucitol
Сорбит (трив.) не рекомендуется
мезо-0-глицеро-\_-идо-Гептит, а не 1_-гляцеро-О-ядо-гептит англ.: meso-D-glycero-L-ido-Hepbto\
Рис. 6.16.13
изо
Новый справочник химика и технолога
СООН
Н---ОН
НО---Н
Н---ОН
Н---ОН
СН2ОН
СООМе
НО---Н
Н---Н
Н---ОН
СН2ОН
D-Глюконовая кислота Метил-З-дезокси-О-тлрео-пентонат англ.-. D-Gluconic acid англ.-. Methyl 3-deoxy-D-tfjreo-pentonate
С=О н—он н—н н—он
сн2он
3-Дезокси-0-рибо-гексоно-1,5-лактон англ.: 3-Deoxy-D-r/bo-hexono-1,5-lactone
Рис. 6.16.14
СНО н—он но—н н—он н—он
СООН
D-Глюкуроновая кислота англ.: D-Glucuronic acid
COOEt
н-с-он^
BzO----ОН
BzO----Н
COOEt
Этил-2,3,5-три-О-бензоил-а-О-маннофурануронат англ.: Ethyl 2,3,5-tri-O-benzoyl-a-D-mannofuranuronat
Рис. 6.16.15
СООН СООН н—1—он СООН н—1—он
н—он но- —н но- —н
но—н но- —н = н— -он
н—он н— -он н— -он
н—он но- —н но- —н
СООН ( :оон ( :оон
D-Глюкаровая кислота L-глицеро-О-галакто-Гептаровая кислота
англ.: D-Glucaric acid англ.: L-g/ycero-D-ga/acto-Heptaric acid
Рис. 6.16.16
Современная номенклатура органических соединений
1131
СООН =0
Н---ОН
Н---ОН
СН2ОН
О-эрил?ро-Пент-2-улозоновая кислота англ.-. D-efyttwo-Pent-2-ulosonic acid
EtO2C—С-ОМе НО—I— Н
Н---ОН
Н---ОН
Н2С-0--'
Этил-(метил-а-0-арабино-гекс-2-улопиранозид)онат англ.-. Ethyl (methyl a-D-arab/no-hex-2-ulopyranosid)onate
L-Аскорбиновая кислота - равновесная смесь трех изомеров
Спиксо-Г екс-2-
улозоно-1,4-лакгон англ.: Ыухо-Нех-2-
ulosono-1,4-lactone
L-ксило-Г екс-2-улозоно-1,4-лакгон англ.-. L-xy/o-Hex-2-
ulosono-1,4-lactone
L-mpeo-Г екс-2-еноно-1,4-лакгон
англ.-. L-//)reo-Hex-2-enono-
1,4-lactone
Рис. 6.16.17
6.16.1.10. О-Замещенные производные
Заместители, заменяющие атом водорода гидроксильной группы сахаридов, в названиях обозначаются как D-заместители. Локант «(9-» не повторяется при множественном замещении одним и тем же заместителем. При полном замещении цифровые локанты не указываются. Для (9-ацилпроизводных можно использовать традиционные названия для эфиров. Ацильное замещение при аномерном гидроксиле обозначают префиксом (9-ацил-, однако соответствующие (9-алкил-производные называют как гликозиды. Сложные эфиры сахаридов и фосфорной кислоты называют фосфатами. В биохимии термин «фосфат» используют независимо от противоиона и степени ионизации. Префиксами, используемыми в органической номенклатуре для сложных эфиров фосфорной кислоты, являются «(9-фос-фоно» и «(9-фосфонато» соответственно для групп (НО)2Р(О)~ и (О )2Р(0)~, присоединенных к кислороду. Если сахар этерифицирован двумя или более фосфатными группами, соединения называют бисфосфатами, трисфосфатами и т. д. Термин «дифосфат» обозначает эфир дифосфорной кислоты. Эфиры серной кислоты называют, используя префиксы «(9-сульфо» и «(9-суль-
фонато» соответственно для групп (HO)S(O)2- и (ОЭ8(О)2-, присоединенных к кислороду (рис. 6.16.18).
Циклические ацетали, получающиеся из сахаридов при взаимодействии с альдегидами и кетонами, называют как и,ли-(9-алкилиденпроизводные, где п, т — локанты гидроксильных групп, принимающих участие в образовании гетероцикла, а алкилиден — префикс соответствующего двухвалентного радикала. При обозначении двух и более идентичных ацетальных фрагментов локанты разделяются двоеточием (рис. 6.16.19).
6.16.1.11. Разветвленные сахара
Разветвленные сахара называют в соответствии с вышеизложенными правилами. Если разветвленный моносахарид образует циклический полуацеталь (полукеталь), то цепь, которая образует цикл, берется в качестве основы названия. В противном случае основу выбирают в соответствии с критериями, приведенными в подразд. 6.16.1.14. Некоторые разветвленные сахара имеют устоявшиеся тривиальные названия (рис. 6.16.20а и 6.16.206).
6.16.1.12. Моносахариды как замещающие группы
В тех случаях, когда основой для названия является неуглеводная структура, а моносахарид выступает в роли
1132
Новый справочник химика и технолога
замещающего радикала, для обозначения последнего используются следующие префиксы.
1. Для обозначения моносахаридного радикала, образующегося при удалении аномерной гидроксильной труппы, используется суффикс «озил» без локанта см. рис. 6.16.21.
2. Для обозначения моносахаридного радикала, образующегося при удалении атома водорода от С1 при сохранении гидроксильной группы, используется суффикс «озил» без локанта с добавлением префикса «1-гидрокси». В этом случае аномерный дескриптор а или Р относится к свободной валентности, см. рис. 6.16.22.
3. Для обозначения в моносахариде свободной валентности при любом, кроме аномерного, атоме углерода с гидроксильной труппой используется суффикс «оз-л-С-ил», где п — соответствующий локант, см. рис. 6.16.23.
4. Для обозначения в моносахариде свободной валентности при любом атоме кислорода, кроме аномерного, используется суффикс «оз-л-(?-ил», где п — соответствующий локант, см. рис. 6.16.24.
5. Для обозначения в моносахариде свободной валентности при восстановленном атоме углерода используется суффикс «оз-л-ил» и префикс «и-дезокси», где п — соответствующий локант, см. рис. 6.16.25.
СНО
Н---ОАс
АсО---Н
Н----ОАс Пента-О-ацетил-альдегидо-О-глюкоза
Н----ОАс или альдегидо-О-глюкоза пентаацетат
СН2ОАс аугл ' Penta-O-acetyl-a/debydo-D-glucose
ОН
2,4-Д и- О-a цетил-6- О-б ен зил-D-гл ю коп ира ноза англ: 2,4-Di-O-acetyl-6-O-benzyl-D-glucopyranose
D-Глюкопираноза 6-фосфат
или 6-О-фосфонато-Ь-глюкопираноза англ.: D-Glucopyranose 6-phosphate
Рис. 6.16.18
Ме2С
1,2-0-Бензилиден-0-глюкофураноза англ.: 1,2-0-Benzylidene-D-glucofuranose
/О-СН2
-----Н НО---Н
Н----ОН
Н----О-
СН2О'
СМе2
1,2:5,6-Ди-О-изопропилиден-О-маннит англ.-. 1,2:5,6-Di-O-isopropylidene-D-mannitol
Рис. 6.16.19
СНО
н—j- он
НОН2С~|~ОН
СН2ОН
З-С-Гид рокси метил-D-глицеро-тетроза, D-Апиоза (трив.)
англ.: 3-C-Hydroxymethyl-D-g/ycero-tetrose
НО,
Н3С
сно
У н-^он
у----он
н—н
н—он
4,6-Дидезокси-3-С-(1-глицеро-
1 -гидроксиэтил)-0-рнбо-гексоза англ.-. 4,6-Dideoxy-3-C-(L-g/ycero-
1 -hydroxyethyl)-D-ribo-hexose
СН3
Рис. 6.16.20а
Современная номенклатура органических соединений
1133
СНО
Н---ОН
Н----ОН
Н-------
НО----Н
С=О
I
СН2ОН
4-Дезокси-4-[(1 R,2S)- или (L-opumpo)-! ,2,3-тригидроксипропил]-1-п7ало-гептоз-6-улоза
англ.'. 4-Deoxy-4-[(1 R,2S)- или (L-erythro)-
1,2,3-trihydroxy]-L-fa/o-heptos-6-ulose
СН2ОН НО—I—Н
X---°\
\ ОЮ Н, ОН 3-Дезокси-3-[(1/?,28)-1,2-дигидрокси-3-оксопропил]-
I \ |Х О-глацеро-О-альтро-гептопираноза
он англ.-. 3-Deoxy-3-[(1/?,2S)-1,2-dihydroxy-3-oxopropyl]-
НО-----Н D-g/ycero-D-a/fro-heptopyranose
Н----ОН
СНО
Рис. 6.16.206
4-(2,3,4,6-Тетра-О-ацетил-а-О-альтропиранозил)бензойная кислота англ.-. 4-(2,3,4,6-Tetra-O-acetyl-a-D-altropyranosyl)benzoic acid
ОМё NHAc
2-С-Ацетамидо-2,3,4,6-тетра-О-метил-а-О-маннопиранозилфторид англ.-. 2-C-Acetamido-2,3,4,6-tetra-O-methyl-a-D-mannopyranosyl fluoride
Рис. 6.16.21
ОН
1-Г идрокси-а-О-аллопиранозил англ.: 1 -Hydroxy-a-D-allopyranosyl
Рис. 6.16.22
h2noc
сно
—он но—н
но—н н—он
СН2ОН
3-(О-Галактоз-2-С-ил)циклобутанкарбоксамид англ.: 3-(D-Galactos-2-C-yl)cyclobutanecarboxamide
Рис. 6.16.23
1134
Новый справочник химика и технолога
ОН
(P-D-Глюкопиранозил-2-О-ил)уксусная кислота англ.-. (P-D-Glucopyranos-2-O-yl)acetic acid
ОСН2СООН
Рис. 6.16.24
jh3
N аЗООН Л/-(1-Дезокси-О-фруктопираноз-1-ил)-1_-аланин
н англ.: /V-(1-Deoxy-D-fructopyranos-1-yl)-L-alanine
Рис. 6.16.25
6.16.1.13. Гликозиды и гликозильные соединения
Смешанные ацетали (кетали), образованные из циклических форм моносахаридов путем замены аномерного гидроксила на группы -OR/-SR/-SeR, называют гликозидами/тиогликозидами/селеногликозидами. Используют три варианта наименования гликозидов.
1. В названии соответствующего моносахарида заменяют суффикс «оза» на суффикс «озид», а перед названием помещают название соответствующей замещающей группы R, см. рис. 6.16.26.
2. Префикс «...озилокси» («...озилтио») в соответствующей форме помещают перед основой названия
(эти префиксы включают О/S атомы гликозидной связи), см. рис. 6.16.27.
3. Используются префиксы «O/S/Se-гликозил» к названию гидрокси/тио/селено соединения, см. рис. 6.16.28.
Соединения, в которых аномерный гидроксил замещен на атом галогена или псевдогалогена (азид, тиоцианат и т. д.), называют как гликозильные производные соответствующих классов соединений. ^Гликозильные производные называют гликозиламинами (включая случай сложных гетероциклических аминов, таких как нуклеозиды) (рис. 6.16.29).
ОН ОН
Н—ОН
СН2ОН
Мети л-а-D-гул офуранозид англ.: Methyl a-D-gulofuranoside
Этил-1-тио-р-О-глюкопиранозид англ.: Ethyl 1-thio-p-D-glucopyranoside
СНО
он Метил-(6Я)-О-глюко-гексодиальдо-6,2-пиранозид англ.: Methyl (6R)-D-g/uco-hexodialdo-6,2-pyranoside
Рис. 6.16.26
ОН
(205)-За-(Р-0-глюкопиранозилокси)-5р-прегнан-20-ол англ.: (20S)-3a-(3-D-glucopyranosyloxy)-5p-pregnan-20-ol
Рис. 6.16.27
Современная номенклатура органических соединений
1135
$е-р-О-Рибопиранозил-О-селеноцистеин
или 3-(р-О-Рибопиранозилселено)-О-аланин англ.: Se-p-D-Ribopyranosyl-D-selenocysteine
или 3-(p-D-ribopyranosylseleno)-D-alanine
Рис. 6.16.28
Тетра-О-ацетил-а-О-маннопиранозилбромид англ.: Tetra-O-acetyl-a-D-mannopyranosyl bromide
9-(5-5-Метил-5-тио-р-О-рибофуранозил)аденин англ.: 9-(5-S-Methyl-5-thio-p-D-ribofuranosyl)adenine
Л/-Фенил-а-О-фруктопиранозиламин англ.: /V-Phenyl-a-D-fructopyranosylamine
Рис. 6.16.29
6.16.1.14. Олигосахариды
Выбор родоначальной структуры
В тех случаях, когда молекула углевода составлена из более чем одной моносахаридной структуры, в качестве основы названия выбирают название моносахарида в соответствии с приведенными ниже критериями, которые применяют последовательно до тех пор, пока не будет сделан выбор:
1) основа названия должна включать старшую функциональную группу в соответствии с общими принципами органической номенклатуры (см. подразд. 6.6.1.3). Таким образом, старшинство падает в ряду: альдаровая кислота > уроновая кислота / кетоальдоновая кислота / альдоновая кислота > диальдоза > кетоальдоза/альдоза > > дикетоза > кетоза;
2) предпочтение отдается молекуле с более длинной цепочкой атомов углерода, например, гептоза старше гексозы;
3) предпочтение отдается следующему первым по алфавиту тривиальному названию или конфигурационному префиксу систематического названия, например, аллоза старше глюкозы, глюко старше гуло производного;
4) конфигурационный символ D старше L;
5) аномерный символ а старше Р;
6) предпочтение отдается системе, содержащей максимальное число заместителей, обозначенных префиксами (мостиковый заместитель, типа 2,3-О-метилен, в этом случае рассматривается как множественный);
7) предпочтение отдается системе с наименьшим набором локантов для префиксов;
8) предпочтение отдается системе с наименьшим локантом для первого префикса.
Олигосахариды без свободных полуацетальных групп
Дисахариды, которые могут быть рассмотрены как результат взаимодействия друг с другом двух гликозидных (аномерных) ОН-групп (невосстанавливающие дихариды), систематически называют как гликозил-гликозиды. Основу (гликозид) выбирают в соответствии с критериями, приведенными в подразд. 6.16.1.14. Оба аномерных дескриптора, как гликозид-основы, так и гликозил-заместителя, должны быть включены в название (рис. 6.16.30).
Олигосахариды, связанные через аномерную гидроксильную группу, можно называть «последовательным» способом как гликозил-(гликозил)„-гликозиды. Локанты, показывающие порядок связывания моносахаридов, помещаются в круглых скобках между названиями индивидуальных моносахаридных единиц в формате «(локант аномерного атома -» локант атома кислорода следующего моносахарида)». Тот же формат используется для короткой записи. Трисахариды могут быть названы также как гликозил-дисахариды. Выбор названия основы в этом случае осуществляется в соответствии с критериями, приведенными в подразделе 6.16.1.14 (рис. 6.16.31).
1136
Новый справочник химика и технолога
Олигосахариды со свободными полуацетальными группами
Данные соединения называют как гликозил-(гликозил)„-гликозы. Локанты, показывающие порядок связывания моносахаридов, помещаются в круглых скобках между названиями индивидуальных моносахаридных единиц (рис. 6.16.32).
6.16.1.15. Полисахариды
Названия полисахаридов (гликанов), состоящих из моносахаридных остатков одного типа, получают путем замены окончания «оза» в названии сахара окончанием «ан» (например, «ксилан» для полимеров ксилозы, «маннан» для полимеров маннозы и т. д.).
(2->1)-Р-0-Фруктофуранан англ: (2^1)-P-D-Fructofuranan
Наряду с систематическими названиями углеводов и их производных в литературе широко используются тривиальные названия, наиболее часто встречающиеся из которых приведены в табл. 6.43.
а-О-Глюкопиранозил-а-О-глюкопиранозид англ.: a-D-Glucopyranosyl a-D-glucopyranoside
р-О-Фруктофуранозил-а-О-глюкопиранозид, сахароза (трив.)
англ.: p-D-Fructofuranosyl a-D-glucopyranoside
Рис. 6.16.30
a-D-галактоза <
a-D-глюколираноза -
ft-D-фруктофураноза«
ОН
Р-0-Фруктофуранозил-(а-0-галактопиранозил-(1->6)-а-0-глюкопиранозид) (глюкоза предпочтительнее, чем фруктоза в качестве гликозида), или (последовательный метод)
а-О-галактопиранозил-(1->6)-а-О-глюкопиранозил-р-О-фруктофуранозид
[a-D-Galp-(1 —>6)-a-D-Glcp-(1 —>2)-p-D-Fruf ] (трив: раффиноза)
англ.: p-D-Fructofuranosyl a-D-galactopyranosyl-(1 ->6)-a-D-glucopyranoside или a-D-galactopyranosyl-(1 ->6)-a-D-glucopyranosyl p-D-fructofuranoside
Рис. 6.16.31
Современная номенклатура органических соединений
1137
ОН
ОН
а-0-Глюкопиранозил-(1н>4)-р-0-глюкопираноза
[a-D-Glcp-(1 ->4)-p-D-Glcp]
или 4-0-а-0-глюкопиранозил-р-0-глюкопираноза
(трив.: р-мальтоза, а не p-D-мальтоза)
англ.-. a-D-Glucopyranosyl-(1 -^4)-p-D-glucopyranose
w^w4-O-a-D-glucopyranosyl-p-D-glucopyranose
ОН
а-0-Глкжопиранозил-(1н>4)-[а-0-глюкопиранозил-(1->6)]-0-глюкопираноза или 4,6-с1|-0-(а-0-глюкопиранозил)-0-глюкопираноза
англ.-. a-D-Glucopyranosyl-(1 ->4)-[a-D-glucopyranosyl-(1 -7>6)]-D-glucopyranose
или 4,6-di-O-(a-D-glucopyranosyl)-D-glucopyranose
Рис. 6.16.32
Таблица 6.43
Тривиальные и систематические названия углеводов и их производных
Тривиальное название (символ) Систематическое название
Аллоза Allose (АП) twzo-Гексоза «//o-Hexose
Альтроза Altrose (Alt) альгаро-Гексоза tf7/ro-Hexose
Арабиноза Arabinose (Ara) ярябш/о-Пентоза агабшо-Pentose
Галактоза Galactose (Gal) галякгао-Гексоза galacto-Hexose
Галактозамин Galactosamine (GalN) 2-Амино-2-дезоксигалактоза 2-Am ino-2-deoxygalactose
D-Г алактозаминит D-Galactosaminitol (GalN-ol) 2-Амино-2-дезокси-О-галактит 2-Amino-2-deoxy-D-galactitol
Глицерин Glycerol (Gro) Пропан-1,2,3-триол Propane-1,2,3-triol
Глицериновый альдегид Glyceraldehyde 2,3-Дигидроксипропаналь 2,3-Dihydroxypropanal
1138
Новый справочник химика и технолога
Продолжение табл. 6.43
Тривиальное название (символ) Систематическое название
Глицерон Glycerone (1,3-dihydroxyacetone) 1,3- Дигидроксипропан-2-он 1,3-Dihydroxypropan-2-one
Глюкозамин Glucosamine (GlcN) 2-Амино-2-дезоксиглюкоза 2-Amino-2-deoxyglucose
Глюкозаминит Glucosaminitol (GlcN-ol) 2-Амино-2-дезоксиглюцит 2-Amino-2-deoxyglucitol
Глюкоза Glucose (Glc) глюко-Гексоза g/wco-Hexose
Гулоза Gulose (Gul) гуло-Гексоза gw/o-Hexose
Идоза Idose (Ido) wdo-Гексоза zcfo-Hexose
Ликсоза Lyxose(Lyx) лмксо-Пентоза /yxo-Pentose
Манноза Mannose (Man) лшнно-Гексоза manno-Hexose
Маннозамин Mannosamine (ManN) 2-Амино-2-дезоксиманноза 2-Amino-2-deoxymannose
Псикоза Psicose (Psi) /?мбо-Гекс-2-улоза rzZzo-Hex-2-ulose
Рамнит Rhamnitol (Rha-ol) 1 -Дезоксиманнит 1 -Deoxymannitol
Рамноза Rhamnose (Rha) 6-Дезоксиманноза 6-Deoxymannose
Рамнозамин Rhamnosamine (RhaN) 2-Амино-2,6-дидезоксиманноза 2-Amino-2,6-dideoxymannose
Рибоза Ribose (Rib) /?мбо-Пентоза rz’Zw-Pentose
Рибулоза Ribulose (Rul) эрмя?/2о-Пент-2-улоза erythro-? ent-2-ulose
Сорбоза Sorbose (Sor) ксг^ло-Гекс-2-улоза xy/o-Hex-2-ulose
Тагатоза Tagatose (Tag) лмксо-Гекс-2-улоза /yro-Hex-2-ulose
Талоза Talose (Tai) wa/zo-Гексоза /л/o-Hexose
Фруктоза Fructose (Fru) арабмно-Гекс-2-улоза araZwo-Hex-2-ulose
Фукоза Fucose (Fuc) 6-Дезоксигалактоза 6-Deoxygalactose
Современная номенклатура органических соединений
1139
Окончание табл. 6.43
1 — Тривиальное название (символ) Систематическое название
Фукозамин Fucosamine (FucN) 2-Амино-2,6-дидезоксигалактоза 2-Amino-2,6-dideoxygalactose
D-Фуцит D-Fucitol (D-Fuc-ol) б-Дезокси-Э-галактит 6-Deoxy-D-galactitol
L-Фуцит L-Fucitol (L-Fuc-ol) 1 -Дезокси-Э-галактит 1 - Deoxy-D-galactitol
Хиновоза Quinovose (Qui) 6-Дезоксиглюкоза 6-Deoxyglucose
Хиновозамин Quinovosamine 2-Амино-2,6-дидезоксиглюкоза 2-Amino-2,6-dideoxyglucose
Эритроза Erythrose эритро-Ч етроза erylhro-Tetrose
Эритрулоза Erythrulose глицеро-Тетрулоза g/vcero-Tetrulose
6.16.2. Циклиты
Циклитами называют циклоалканы, содержащие по одной гидроксильной хруппе у грех и более углеродных атомов. Для таких соединений предложена номенклатура со специальной нумерацией циклогексанового кольца и особым описанием стереохимии. Эта номенклатура пригодна главным образом для самих циклитов, их простых и сложных эфиров, а также для производных, у которых замещены одна или более гидроксильных групп.
Проекционные формулы циклитов изображают подобно проекционным формулам Хеуорса для пираноз, в которых вертикальные линии обозначают связи С-О:
При нумерации кольца заместители получают по возможности наименьший набор локантов. Далее расположенные над и под плоскостью кольца гидроксильные группы рассматривают отдельно как две серии заместителей. Заместители серии с наименьшим набором локантов обычно рисуют над кольцом, что иногда требует переориентации молекулы. Положение НО- и RO-заместителей указывается перед названием соединения
путем перечисления локантов одной серии, а затем, через косую черту — локантов второй серии, например «1,2,4/3,5,6-». Чтобы сделать правильный выбор начала нумерации, последовательно руководствуются приведенными ниже критериями. Наименьшие локанты должны получить:
- все заместители, как набор независимо от конфигурации, например см. рис. 6.16.33.
- заместители более протяженной серии, например см. рис. 6.16.34.
- заместители серии, для которой возможен меньший набор локантов (1,2/3,5 < 1,5/2,3) , например см. рис. 6.16.35.
- заместители с модифицированными гидроксильными группами, например см. рис. 6.16.36.
- заместитель, стоящий первый по алфавиту, например см. рис. 6.16.37.
- серия, которая приводит к L, а не D стередескрипто-рам (только для .мезо-форм), например см. рис. 6.16.38.
6.16.2.1. Относительная конфигурация стереоцентров в циклитах
Относительная конфигурация стереоцентров указывается перед названием соединения путем перечисления локантов первой серии, а затем, через косую черту, — локантов оставшихся заместителей, например «1,2,4/3,5,6-». Для циклитов с гидроксильными или О-замещенными гидроксильными группами конфигурационные локанты одновременно служат локантами, показывающими положение заместителей (при наличии других заместителей конфигурационные локанты указывают в круглых скобках), например см. рис. 6.16.39.
1140
Новый справочник химика и технолога
1L-1,2/3,4-Циклогексантетрол англ.: 1 L-1,2/3,4-Cyclohexanetetrol
1Е-(1/2,3,4,5)-5-Сульфанил-1,2,3,4-циклогексантетрол англ.: 1L-(1/2,3,4,5)-5-Sulfanyl-1,2,3,4-cyclohexanetetrol
Рис. 6.16.33
1D-1,2,5/3,4-Циклогексанпентол англ.: 1 D-1,2,5/3,4-Cyclohexanepentol
Рис. 6.16.34
1L-1,2/3,5-Циклогексантетрол англ.: 1 L-1,2/3,5-Cyclohexanetetrol
Рис. 6.16.35
1D-1 -О-Этил-1,2/3,4-Циклопентантетрол англ.: 1 D-1 -O-Ethyl-1,2/3,4-Cyclopentanetetrol
1 L-1,2-Ди-О-метил-5-О-этил-нео-инозит англ.: 1L-5-O-Ethyl-1,2-di-O-methyl-neo-inositol
Рис. 6.16.36
русс.: 1 L-1 -О-Метил-4-О-этил-муко-инозит
англ.: 1L-1 -O-Ethyl-4-O-methyl-mi/co-inositol
Рис. 6.16.37
5
1,2,3,4,5/0-Циклогептанпентол англ.: 1,2,3,4,5/0-Cycloheptanepentol
2-О-Метил-мио-инозит англ.: 2-O-Methyl-myo-inositol
Рис. 6.16.38
Современная номенклатура органических соединений
1141
1L-1,2,3,4,5/6-Цикпогептангексол англ.: 1 L-1,2,3,4,5/6-Cycloheptanehexol
11_-(1 /2,3,4,5)-5-Амино-1,2,3,4-цикпогексантетрол англ.: 1L-(1/2,3,4,5)-5-Amino-1,2,3,4-cyclohexanetetrol
Рис. 6.16.39
6.16.2.2. Абсолютная конфигурация стереоцентров в циклитах
При описании абсолютной конфигурации формулу циклита изображают в виде вертикальной проекции Фишера — Толленса с атомом С1 в вершине и атомами С2 и С3, расположенными перед плоскостью листа. Если гидроксильная группа или заменяющая ее группа (алкокси, амино и др.) при атоме углерода с наименьшим локантом направлена вправо, то применяют стереодескриптор D, а если влево, то дескриптор L:
6.16.2.3. Циклиты с гидроксильными
или О-замещенными гидроксильными группами
Существуют девять циклогексан-1,2,3,4,5,6-гексо-лов, для которых используется название «инозит» (inositol). В названиях изомеров перед словом «инозит» пишут курсивом соответствующий конфигурационный префикс, показывающий относительное расположение гидроксильных групп (табл. 6.44).
Циклиты, отличные по структуре от инозитов, называют как замещенные циклоалканполиолы, даже если некоторые или все гидроксильные группы являются О-замещенными. Названия простых и сложных эфиров циклитов записываются по аналогии с соответствующими производными углеводов с использованием таких префиксов как «1 -О-метил-», «2-О-ацетил-» и т. д. или же добавляя окончания «1-метиловый эфир», «2-ацетат» после названия полиола.
Для 1 Е-1,3,4/2,5-циклогексанпентола сохранено тривиальное название (+)-кверцит:
Перед стереодескриптором указывают локант атома, определяющего абсолютную конфигурацию (в изображенной формуле, как и в большинстве случаев, это локант 1). Для рацемических соединений используют обозначение DL. Отсутствие стереодескриптора D, L или DL указывает на л/ело-форму.
Дескриптор абсолютной конфигурации циклита можно определять, пользуясь не вертикальной, а горизонтальной проекцией, в которой основная серия гидроксизаместителей расположена над кольцом: последовательность нумерации против часовой стрелки будет у D-изомера и по часовой стрелке — у L-изомера:
(+)-Кверцит англ.: (+)-Quercitol
1 D-xupo-Инозит англ.: 1 D-chiro-\nositol
1 L-xupo-Инозит англ.: 1 L-c/?/ro-lnositol
Таблица 6.44
Названия и проекционные формулы инозитов
Название Формула
г/мс-инозит (czs-inositol) (1,2,3,4,5,6/0-) энм-инозит (epz-inositol) (1,2,3,4,5/6-) алло-инозит (a//o-inositol) (1,2,3,4/5,6-) 5 4 5 4
1142
Новый справочник химика и технолога
Окончание табл. 6.44
Название Формула
лшо-инозит |i [2 1
(/wyo-inositol) 6 Ixl / 3
(1,2,3,5/4,6-) 5 И
л/уко-инозит Il |2
(wwco-inositol) 6lxl l/l3
(1,2,4,5/3,6-) 5 4 1
/zeo-инозит Il [2 ।
(weo-inositol) 6 lx /3
(1,2,3/4,5,6-) |5 Г4
cz/iwzo-инозит Jj—t?l
(scz/Zo-inositol) 6<J73
(1,3,5/2,4,6-) ' 5 |4
1 D-xwpo-инозит 11 |2
(1 D-c/wro-inositol) 6 M И3
(1,2,5/3,4,6-) 5 И ।
1 L-xwpo-инозит Il [2
(1 L-c/zzra-inositol) 6 lx l>3
(1,2,4/3,5,6-) । |5 1 '
6.16.2.4. Производные инозитов
Инозиты, содержащие вместо одного, двух или трех гидроксилов другие функциональные группы, которые могут быть записаны в префикс (-SH, -NH2 (х-амино-х-дезоксиинозиты объединяют под общим названием
«инозамины»), галогены и т. п.), называют по «дезокси» номенклатуре с сохранением конфигурационного префикса и нумерации кольца родоначального соединения, например см. рис. 6.16.40. Заместитель в кольце инозита может замещать не только гидроксильную группу, но и атом водорода. В таком случае его называют как замещенный инозит при условии, что этот заместитель или функциональная группа не превосходит по старшинству гидроксильную, см. рис. 6.16.41. Если в молекуле присутствует функциональная группа старше гидроксильной (^С=О, -СО2Н и т. д.), то родоначальное название «инозит» не используется; соединение в этом случае называют как производное соответствующего циклита с употреблением суффикса функциональной группы (см. подразд. 6.16.2.5).
6.16.2.5. Производные циклитов
Циклиты, содержащие заместители, иные чем гидроксильные или (9-замещенные гидроксильные группы (за исключением некоторых производных инозитов, см. подразд. 6.16.2.4), называют согласно общим правилам 1UPAC с той оговоркой, что заместители RO записываются не префиксами алкокси-, ацилокси- и т. д., а (9-алкил-, (9-ацил и т. д., например см. рис. 6.16.42. Следует помнить, что наличие главных функциональных групп старших, чем гидроксильная (триалкиламмонийная, карбоксильная, циано, ацильная, оксо- и т. д., см. табл. 6.7) меняет упомянутые ранее правила нумерации кольца, фиксируя за атомом углерода, соединенным с этой группой, локант «1» , например см. рис. 6.16.43.
В соответствии с рекомендациями 1UPAC в некоторых случаях более предпочтительными являются не систематические, а тривиальные названия, например см. рис. 6.16.44.
1D-1 -Амино-1 -дезокси-мс/о-инозит англ.: 1 D-1 -Amino-1 -deoxy-myo-inositol
1L-1 -Дезокси-6-О-метил-1 -сульфанил-хс/ро-инозит англ.-. 1 L-1-Deoxy-6-O-methyl-1-sulfanyl-c/wro-inositol
NH2
11 2 nh2
6 S^H2 'x3 1.3,5-Tриамино-1,3,5-тридезокси-сцилло-инозит
। 5 4| англ.: 1,3,5-Triamino-1,3,5-trideoxy-scy//o-inositol
Рис. 6.16.40
З-С-Метил-мс/о-инозит англ.: 3-C-Methyl-/7?yo-inositol
Рис. 6.16.41
Современная номенклатура органических соединений
1143
(1 ,4/2,3,5,б)-2,3,5,б-Тетрамино-1 ,4-Циклогександиол англ.: (1,4/2,3,5,6)-2,3,5,6-Tetramino-1,4-cyclohexanediol
11_-(1/2,3,4,5)-5-Амино-1,2,3,4-Циклогексантетрол англ.: 1 L-(1/2,3,4,5)-5-Amino-1,2,3,4-cyclohexanetetrol
NH2 SH
1 D-(1,2/4,5)-4-Амино-1-О-метил-5-сульфанил-1,2-циклогександиол англ.: 1 D-(1,2/4,5)-4-Amino-1 -O-methyl-5-sulfanyl-1,2-cyclohexanediol
Рис. 6.16.42
21-(2,3,5/4,6)-Пентагидроксициклогексанон англ.: 2L-(2,3,5/4,6)-Pentahydroxycyclohexanone
1 L-(1,5/2,3,4)-2,3,4,5-Тетрагидроксициклопентанкарбоновая кислота англ.: 1 L-(1,5/2,3,4)-2,3,4,5-Tetrahydroxycyclopentanecarboxylic acid
Рис. 6.16.43
6
L-Хинная кислота (mpue.) или
з 1 L-1 (ОН),3,4/5-тетрагидроксициклогексанкарбоновая кислота (сист.)
англ: L-Quinic acid или
1 L-1 (OH),3,4/5-tetrahydroxycyclohexanecarboxylic acid
Рис. 6.16.44
6.16.3. Аминокислоты и пептиды
6.16.3.1. Аминокислоты
Природные аминокислоты имеют общепринятые тривиальные названия (табл. 6.45). Систематические названия производных аминокислот строятся на основе общих принципов номенклатуры IUPAC/IUB путем добавления к тривиальному названию аминокислоты соответствующих префиксов. Положение заместителей указывается с помощью цифровых (что более предпочтительно) или буквенных локантов (а, Рит. д.). Для производных ациклических аминокислот атому углерода карбоксильной группы, находящемуся рядом с аминогруппой, приписывается локант «1». При использо-
вании буквенных обозначений положения заместителей локант «а» получает атом С2:
NH2
I 5>1з h 1 Лизин
англ.: Lysine
Особый случай представляет нумерация атомов аминокислот с разветвленными углеводородными радикалами, такими как валин, лейцин и изолейцин, представленная в табл. 6.45.
Положение заместителей при атоме азота в ациклических аминокислотах указывается буквой N с надстрочным индексом, равным номеру атома углерода,
1144
Новый справочник химика и технолога
к которому присоединен данный атом азота, например М-ацетиллизин. В аргинине при обозначении атомов азота используют буквенные локанты:
а
Аргинин англ.-. Arginine
В циклической аминокислоте, пролине, нумерация цикла проводится как в пирролидине, начиная с атома азота (табл. 6.45). При нумерации атомов углерода в аминокислотах, содержащих арильные заместители, таких как фенилаланин, дофа, тирозин, тиронин и тироксин, используют смешанную нумерацию: для атомов бензольных колец применяют цифровые локанты, а для атомов цепи — буквенные (табл. 6.45). Более сложная нумерация атомов используется для гистидина, что обусловлено тем, что долгое время для этой аминокислоты применялись две различные системы нумерации имидазольного кольца (биохимики приписывали ближайшему к основной цепи атому азота локант «1», а химики-органики — локант «3»), Чтобы избежать двусмысленности, в настоящее время рекомендуется атомы гистидина нумеровать следующим образом:
Г истидин англ.-. Histidine
где буквой л (от слова pros) обозначают ближний к боковой цепи азот, а буквой т (от слова tele) — дальний.
Стереохимические обозначения аминокислот
Абсолютные конфигурации а-углеродных атомов а-аминокислот обозначаются капительными буквами (в английском языке small caps) D или L, которые ставятся сразу перед тривиальным названием аминокислоты, которые указывают на формальное соответствие конфигурациям D- или L-серина и, следовательно, — конфигурациям D- или L-глицеринового альдегида. Таким образом, даже при наличии нескольких хираль-ных атомов, конфигурация аминокислоты (D или L) определяется по конфигурации хирального атома, имеющего наименьший локант, в отличие от углеводов, у которых стереодескриптор относится к хиральному атому с наибольшим локантом. а-Аминокислоты, являю-
щиеся аминопроизводными углеводов и содержащие больше пяти атомов углерода, называют по номенклатуре углеводов (подразд. 6.16.1.5). Использование стереодескрипторов «DL», «рац», или «±» указывает на рацемическую форму аминокислоты.
Более общей системой стереообозначений конфигурации хиральных центров является 7?,S-система. Почти все природные L-аминокислоты, встречающиеся в белках, имеют S-конфигурацию. Наиболее важными исключениями из этого правила являются L-цистин и L-цистеин, хиральный центр которых имеет ^-конфигурацию. Для обозначения конфигурации атомов иных, чем а-углеродные, рекомендуется пользоваться 7?,S-системой. Во избежание использования сразу двух систем стерсообозначений 7?, S-номенклатура часто употребляется и для обозначения а-углеродного атома, например, (25,45)-4-гидроксипролин вместо (4S)-4-гидрокси-Ь-пролин. Для аминокислот с несколькими хиральными центрами использование углеводных стереопрефиксов, таких, например, как «D-эритро», нежелательно.
В случае замещенных пролинов допустимо использование префиксов «цис» и «транс» для указания расположения дополнительного заместителя в пирролидиновом кольце относительно карбоксильной группы, например г/мс-4-гидрокси-Е-пролин.
Строение аминокислот с учетом конфигурации стереоцентров может быть изображено либо с помощью проекции Фишера, либо направленными связями, см. рис. 6.16.45.
Функциональные производные аминокислот
Правила IUPAC/1UB в отличие от правил Chemical Abstracts для названий функциональных производных аминокислот, т. е. аминокислот, содержащих дополнительные функциональные группы или модифицированные карбоксильную или аминогруппу, рекомендуют использовать тривиальные названия в качестве родоначальных с добавлением обычных суффиксов функциональных групп. В качестве примера в табл. 6.46 приведены названия функциональных производных лизина.
Для основных природных аминокислот в систематической номенклатуре приняты трехбуквенные обозначения (табл. 6.45). Эти обозначения, которые, как правило, не используются для обозначения свободных аминокислот, удобны для описания пептидов. Кроме того, для компактного изображения длинных пептидных последовательностей (особенно при трехмерном изображении молекул протеинов) используется однобуквенная система обозначений (табл. 6.45).
со2н СО2Н
H2N----Н или H2N—Ь-Н
R Й
или
СО2Н
NH2
или
Рис. 6.16.45
Современная номенклатура органических соединений
1145
Таблица 6.45
Тривиальные названия аминокислот
Тривиальное название Обозначение Формула
трехбуквенное однобуквенное
Аланин (alanine) Ala A nh2 н3сх'^хсо2н
Аллизин (allysine) 0 nh2 H‘z^x/^/‘SsCO2H
Аргинин (arginine) Arg R nh2 H H2N. /hk Y CO2H NH
Аспарагин (asparagine) Asn а) N 0 nh2 H2N'z^X^XCO2H
Аспарагиновая кислота (aspartic acid) Asp а) D 0 nh2 HO^^^COzH
Валин (valine) Vai V nh2 H3C. J<1 Y CO2H 4CH3
Гистидин (histidine) His H ZXJ? Y°CO2H
Глицин (glycine) Gly G H2N''XX'CO2H
Глутамин (glutamine) Gin 6) Q nh2 H2N. /s. zl Y TO2H 0
Глутаминовая кислота (glutamic acid) Glu 6) E nh2 HO. „ Y XO2H 0
Дофа (dopa) но. J. T2 НО'3^’^“'С°2Н
Изолейцин (isoleucine) He I nh2 5^. 3 J.2 1 H3C'X^YXCO2H 31l Спз
Лантионин (lanthionine) Ala Cys nh2 nh2 zL zS. X. HO2C TO2H
Лейцин (leucine) Leu L 5’ CH3 nh2 5 Js. 3 zL 1 H3C4\^ 2XO2H
Лизин (lysine) Lys К nh2 НгЫ'''”’''4^
Метионин (methionine) Met M nh2 H3C. /s. zl 3 TO2H
1146
Новый справочник химика и технолога
Окончание табл. 6.45
Тривиальное название Обозначение Формула
Трехбуквенное Однобуквенное
5-Оксопролин (5-oxoproline) Glp б) H1 Oc==^N\^CO2H \4 3/^
Орнитин (ornithine) От nh2 H2N. TO2H
Пролин (proline) Pro P H1 /N\^CO2H 5 \4
Саркозин (sarcosine) Sar НзСхы^чсо2н H
Селеноцистеин (selenocysteine) Sec в) nh2 HSe. Js. XO2H
Серин (serine) Ser S nh2 HO. J. XO2H
Тирозин (tyrosine) Туг Y HO. JL n2 ?H2 Y ^oCOjH
Тироксин (thyroxine) Thx 1 ijH2 HO'y^ 1'Х^^ХХ^'СО2Н I
Тиронин (thyronine) 2' л 3 'XTi^X|l2 nh2 Да sL JL JL HO ° ТГ a CO2H 5' 6 P г
Треонин (threonine) Thr T nh2 H3C. Y TO2H OH
Триптофан (tryptophan) Trp W Й1 „ОЛТ2 \=/ bA?o2h
Фенилаланин (phenylalanine) Phe F Г2 ^/A'-/\o2h
Цистеин (cysteine) Cys C nh2 HS. TO2H
Цистин (cystine) Cys Cys nh2 HO2C. /S. J. S ьО2Н nh2
Цитруллин (citrulline) Cit h H2N. /N. Y \^\^>ю2н 0
Неу стано в л е н ная аминокислота Xaa X
Современная номенклатура органических соединений
1147
а' Символ Asx обозначает Asp (аспарагиновая кислота) или Asn (аспарагин).
б) Символ Glx обозначает Glu (глутаминовая кислота) или Gin (глутамин) или Gia (4-карбоксиглутаминовая кислота) или Glp (оксопролин), который превращается в глутаминовую кислоту при гидролизе пептидов.
в) Название селеноцистеин более предпочтительно, чем альтернативное селеносерин.
Названия функциональных производных лизина
Таблица 6.46
Класс соединений Производное лизина
Название Формула
Соли Лизинат натрия (sodium lysinate) h2n'x*' nh2 XxZ~x/t:O2 Na+
Сложные эфиры Метиллизинат (methyl lysinate) h2n^ nh2 Чч/Чх/\о2сн-.
Амиды Лизинамид (lysinamide) Лизинанилид (lysinanilide) h2nx K2N^ nh2 nh2
Кетоны Лизинилметан (lysinylmethane) H2Nx nh2 0
Альдегиды Лизиналь (lysinal) h2n' nh2 0
Спирты Лизинол (lysinol) H2Nx nh2
A-Замещенные производные А6-Ацетиллизин (A^’-acetyllysine) 0 H3(T nh2 H
С-Замещенные производные 3-(Метоксиметил)лизин (3-(methoxymethyl)lysine) . h2n" nh2
6.16.3.2. Пептиды
Пептиды — продукты формальной конденсации аминокислот, получающиеся при образовании амидной связи между карбоксильной группой одной аминокислоты и а-аминогруппой другой. Такая амидная связь в пептидах называется пептидной связью. Другие амидные связи в пептидах называют изопептидными связями. Пептиды, содержащие 10-20 аминокислотных остатков, называют олигопептидами, а цепи из аминокислот в количестве, превышающем 20, — полипептидами. Природные полипептиды, состоящие из более чем 50 аминокислотных остатков, называются протеинами или белками. В состав белков, кроме того, могут входить и непептидные компоненты.
Пептид, состоящий из двух аминокислотных остатков, называется дипептидом, из трех — трипептидом и т. д. Аминокислотный фрагмент пептида, который содержит свободную аминогруппу, называется А-конце-вым, а фрагмент, содержащий свободную карбоксильную группу, называется С-концевым.
Название пептида строится на основе названия С-аминокислоты, перед тривиальным названием которой пишутся по порядку, начиная с А-аминокислоты, названия остальных аминокислот в виде замещающих групп с использованием суффикса «ил». В структурной формуле аминокислотные фрагменты записываются в том же порядке, начиная с А-аминокислоты и заканчивая С-аминокислотой, например см. рис. 6.16.46.
1148
Новый справочник химика и технолога
Система трехбуквенных обозначений и способы изображения аминокислотных остатков в пептидах
Природные высшие олигопептиды и полипептиды, как правило, имеют тривиальные названия. Для краткости структура низкомолекулярных пептидов чаще изображается с помощью трехбуквенных обозначений; однобуквенные обозначения в этом случае не используются, поскольку они в меньшей степени ассоциируются с названиями соответствующих аминокислот. Вышеупомянутый трипептид в трехбуквенных обозначениях выглядит следующим образом: Leu-Ala-His. Отсутствие стереодескриптора перед аминокислотными остатками однозначно указывает на природную L-конфигурацию; для D-аминокислот в пептидной последовательности их конфигурация должна быть указана. Замещенные амино- или карбоксильная группа концевых аминокислот пептидной последовательности обозначают добавлением символа соответствующего заместителя, например, Ac-Lys-Gly (А 2-цетиллизилгли-цин) или Gly-Ser-OMe (метиловый эфир глицилсерина). Обозначения защитных ipynn концевых функций указаны в табл. 6.47-6.49.
В приведенных примерах дефис, разделяющий трехбуквенные символы аминокислот, обозначает пептидную связь, образованную карбоксильной группой аминокислоты, расположенной справа, и аминогруппой
аминокислоты, расположенной слева. Однако в пептидах связь между отдельными аминокислотами не всегда бывает пептидной, т. с. образованной за счет а-функ-циональных групп. Для обозначения таких связей используют ломаные или вертикальные линии как показано на схеме 6.9.
При записи пептида с помощью трехбуквенных обозначений для №,А2-дизамещенного аминокислотного остатка допустим следующий способ изображения, см. рис. 6.16.47.
Для циклических гомодетных пептидов, т. е. пептидов с циклами, сформированными при помощи обычных пептидных связей, используют три различных способа изображения, см. рис. 6.16.48.
Символика представления гетеродетных пептидов, т. е. пептидов, в образовании циклических связей которых участвуют не только пептидные, но и изопептидные, дисульфидные, эфирные или другие связи, обычно логически вытекает из природы аминокислот, участвующих в образовании этих связей, например см. рис. 6.16.49.
Кроме аминокислот, представленных в табл. 6.45, номенклатурой IUPAC/IUB разрешено использовать трехбуквенные обозначения и для некоторых производных природных а-аминокислот, а также для ряда других, более редко встречающихся аминокислот. Их названия, обозначения и структурные формулы представлены в табл. 6.50.
1_-Лейцил-1_-аланил-1_-гистидин англ.: L-Leucyl-L-alanyl-L-histidine
Рис. 6.16.46
ONx^
Ala—Gly
NO
Ala-'-Giy
Gly Gly-I- Ala
1-Аланил-Л/-нитрозоглицин англ.-. L-Alanyl-/V-nitrosoglycine
Л/,Л/-Диглицил-1_-аланин англ.-. A/./V-Diglycyl-L-alanine
Рис. 6.16.47
1. cyclo(-Gly-Orn-Leu-D-Phe-Pro-Gly-Orn-Leu-D-Phe-Pro-)
2.
3.
L Gly-Orn-Leu-D-Phe-Pro-Gly-Om-Leu-D-Phe-Pro—I или
Gly-Orn-Leu-D-Phe-Pro-Gly-Orn-Leu-D-Phe-Pro —।
Gly—►Orn—►l_eu-»-D-Phe—► Pro-Pro-*- D-Phe-*-Leu Orn Gly
Рис. 6.16.48
Современная номенклатура органических соединений
1149
I I
Cys-Tyr-lle-Gln-Asn-Cys-Pro-Leu-Gly-NH2
Thr-Gly-Gly-Ala
Окситоцин L-Т реонилглицилглицил-Ьаланин
англ: Oxytocin англ: L-Threonylglycylglycyl-L-alanine
Рис. 6.16.49
1150
Новый справочник химика и технолога
Таблица 6.47
Защитные группы уретанового типа
Название Обозначение
Адамантилоксикарбонил (adamanthyloxycarbonyl) Adoc-
/и/»вАМ-Амилоксикарбонил(гег/-ату1охусагЬопу1) Аос-
5-Бензизоксазолилметоксикарбонил (5-benzoisoxazolylmethoxycarbonyl) Bic-
Бензилоксикарбонил (benzyloxycarbonyl) Z- или Cbz-
1 -(Бифенил-4-ил)-1 -метилэтоксикарбонил (1 -(biphenyl-4-y 1)-1 -methylethoxycarbonyl) Врос-
4-Бромбснзилоксикарбонил (4-bromobenzyloxycarbonyl) Z(Br)-
ти/эети-Бутоксикарбонил (/erZ-butoxycarbonyl) Вос-
а.а-Диметил-3,5-диметоксибензилоксикарбонил (a,a-dimethyl-3,5- Ddz-
dimethoxybenzyloxycarbonyl)
3,5-Диметоксибензилоксикарбонил (3,5-dimethoxybenzyloxycarbonyl) Z(OMe)2-
Изоборнилоксикарбонил (isobomyloxycarbonyl) Bomoc-
Изоникотинилоксикарбонил (isonicotinyloxycarbonyl) Noc-
Р-Метилсульфонилэтоксикарбонил (2-methylsulfonylethoxycarbonyl) Nsc-
4-Метоксибензилоксикарбонил (4-methoxybenzyloxycarbonyl) Z(OMe)-
4-Нитробензилоксикарбонил (4-nitrobenzyloxycarbonyl) Z(NO2)-
4-Фенилазобензилоксикарбонил (4-phenylazobenzyloxycarbonyl) Pz-
9-Флуоренилметоксикарбонил (9-fluorenylmethoxycarbonyl) Fmoc-
4-Хлорбензилоксикарбонил (4-chlorobenzyloxycarbonyl) Z(C1)-
Таблица 6.48
Защитные группы азота, кислорода и серы неуретанового типа
Название Обозначение
Ацетамидометил (acetamidomethyl) Ацетил (acetyl) 5-(Диметиламино)нафт-1 -илсульфонил, дансил (5-(dimethylamino)naphth-l-ylsulfonyl, dansyl) 2,4-Динитрофен ил (2,4-dinitrophenyl) (3-Карбокси-4-нитрофенил)тио ((3-carboxy-4-nitrophenyl)thio) З-Карбоксипропаноил (3-carboxypropanoyl) Малеоил (maleoyl) (-ОС-СН=СН-СО-) Малеил (maleyl) (НО2С-СН=СН-СО-) 2-Нитрофенилтио (2-nitrophenylthio) 4-Иодфенилсульфонил, пипсил (4-iodophenylsulfonyl, pipsyl) Сукцинил (succinyl) (-ОС-СН2СН2-СО-) Тозил (tosyl) Аст- Ас- Dns- Dnp- или N2ph-Nbs- Suc- -Mal- или Mal< Mal- NpS- или Nps Ips--Suc- или Suc< Tos-
Современная номенклатура органических соединений
1151
Окончание табл. 6.48
Название Обозначение
Трифенилметил, тритил (triphenylmethyl, trityl) Фенилтиокарбамоил (phenylthiocarbamoyl) Формил (formyl) Фталил, о-карбоксибензоил (phthalyl, o-carboxybenzoyl) Фталоил (phthaloyl) Trt- Ptc- For- Pht- -Pht- или Pht<
Таблица 6.49
Защитные группы карбоксильной функции
Название Обозначение
Бензилокси (benzyloxy) -OBzla)
Бензотриазол-1 -илокси (benzotriazol-1 -уloxy) -OBt6)
wpew-Бутокси (ter/-butoxy) -OBu'
Дифенилметокси (diphenylmethoxy) -OBzh
Метокси (methoxy) OMe
4-Нитробензилокси (4-nitrobenzyloxy) -ONb
4-Нитрофенилтио (4-nitrophenylthio) -OSNp B)
4-Нитрофенокси (4-nitrophenoxy) -ONp
Сукцинимидокси (succinimidoxy) -Onsu или -Osu
2,4,5-Трихлорфенокси (2,4,5-trichlorophenyloxy) -OTcp
Хинолин-8-илокси (quinolin-8-yloxy) -Oqur)
Этокси (ethoxy) -OEt
а) Например, название глицинового производного: бензиловый эфир глицина.
б) Например, название глицинового производного: (1-глицилокси)бензотриазол.
в) Например, название глицинового производного: 5'-(4-нитрофениловый эфир) тиоглицина.
г) Например, название глицинового производного: хинолин-8-иловый эфир глицина.
Трехбуквенные обозначения других аминокислот
Таблица 6.50
Тип аминокислоты Трехбуквенное обозначение Название Формула
Гидроксиамино- 5Ну1 5-Гидроксилизин nh2
кислоты
он
ЗНур 3-Гидроксипролин н /NyCO2H
«Гомо» амино- Hse Гомосерин nh2
кислоты НО^^^^СОгН
Неу Гомоцистеин nh2
HS/^X''^XCO2H
1152
Новый справочник химика и технолога
Окончание табл. 6.50
Тип аминокислоты Трехбуквенное обозначение Название Формула
Высшие неразветвленные аминокислоты Карбоксилирован-ные аминокислоты Окисленные аминокислоты рА1а Abu Аре Ahx sAhx Aad PAad Apm A2pr или Dpr A2bu или Dab A2pm или Dpm Gia Cya P-Аланин 2-Аминобутановая кислота 2-Аминопентановая кислота 2-Аминогексановая кислота 6-Аминогексановая кислота 2-Аминогександиовая кислота З-Аминогександиовая кислота 2-Аминогептандиовая кислота 2,3-Диаминопропановая кислота 2,4-Диам инобутано вая кислота 2,6-Диаминогептановая кислота 4-Карбоксиглутаминовая кислота Цистеиновая кислота nh2 Н3С. 3 ХО2Н nh2 Н3Сх^х^Х'СО2Н nh2 Н3С. А. — ТО2Н H2N^X^'X'-/''xCO2H nh2 но2с. ТО2Н НО2С. ХО2Н nh2 nh2 nh2 h2n. XO2H nh2 H2N'/X''/^CO2H nh2 nh2 н3с^х''-хХХх^х^о2н CO2H nh2 НОгС^^^^СОгН nh2 HO3S.
Стереообозначения в пептидах
Стереодескриптор, обозначающий конфигурацию стереоцентра, указывается непосредственно перед соответствующей аминокислотой. Отсутствие стереодескриптора указывает на природную L-конфигурацию аминокислоты. Рацемическая смесь L-Leu-L-Ala-L-His и D-Leu-D-Ala-D-His записывается как rac-L-Leu-L-Ala-L-His. Для записи смесей рацематов неопределенного состава используется префикс «амбо», например, смесь rac-L-Leu-L-Ala, состоящая из равных количеств L-Leu-L-Ala и D-Leu-D-Ala, с rac-L-Leu-D-Ala, состоящая из равных количеств L-Leu-D-Ala и D-Leu-L-Ala, удобно записывать как амбо-Ьеи-амбо-А1а. Смесь L-Leu-L-Ala-L-His и L-Leu-D-Ala-L-His также можно записывать как L-Leu-owdo-Ala-L-His.
Простые пептидные полимеры, состоящие из остатков только одной аминокислоты, называют, употребляя
умножающие префиксы, например, «пентаглицин», «по-ли(Ь-аланин)» и т. п.
Нумерация атомов пептидной цепи
Если в пептидной цепи присутствуют заместители, то ее атомы нумеруют. В простых случаях для относительно низкомолекулярных пептидов, чтобы указать положение заместителя, можно ограничиться нумерацией только той аминокислоты (см. подразд. 6.16.3.1), которая его содержит (рис. 6.16.50).
Однако во многих случаях бывает необходимо указать положение заместителя в общей пептидной цепи. В этом случае перед префиксом или суффиксом (если это главная функциональная группа) заместителя указывается номер замещенного атома (по внутренней нумерации аминокислоты) и порядковый номер этого аминокислотного остатка (начиная с А-конца),
Современная номенклатура органических соединений
1153
разделенные точкой. По этой номенклатуре предыдущее соединение называется «3,2-бром(глицил-Ь-ала-нил-Ь-серин»). Пример пептида с суффиксным заместителем представлен ниже на рис. 6.16.51.
Особенно удобным этот способ нумерации оказался в случае замещенных пептидов, имеющих тривиальные названия. Так, из названия «А 5,4-метилокситоцин» следует, что при азоте № глутаминового остатка, который имеет порядковый номер 4 в пептиде с тривиальным названием «окситоцин», содержится метильный заместитель.
Модификация тривиальных названий пептидов
Часто для пептидов, особенно имеющих значительную молекулярную массу, удобно использовать в качестве основы названия уже имеющееся тривиальное название ближайшего пептидного аналога с добавлением модифицирующих обозначений. В табл. 6.51 на примере пентапептида Ala-Lys-Glu-Tyr-Leu, которому дано произвольное название «номенклатурин», представлены различные модификации его структуры с соответствующими модифицирующими обозначениями.
Гл ицил-3-бром-1_-аланил-1_-серин англ.: Glycyl-3-bromo-L-alanyl-L-serine
Рис. 6.16.50
Глицил-1_-серил-1_-аланил-1_-аспартил-глицин-4.4-3.2-лактон
англ.: Glycyl-L-threonyl-L-alanyl-L-aspartyl-glycine-4.4-3.2-lactone
Рис. 6.16.51
Таблица 6.51
Названия производных пептида Ala-Lys-Glu-Tyr-Leu с гипотетическим тривиальным названием «номенклатурин» а)
Модификация Модифицированное тривиальное название Структура
Замена фрагментова) [Рйе4]номенклатурин 4 Ala-Lys-Glu-Phe-Leu
Расширение пептидной цепи с А-конца Arg-номенклатурин 1 5 Arg-Ala-Lys-Glu-T yr-Leu
Расширение пептидной цепи с С-конца номенклатурин-Gly 1 5 Ala-Lys-Glu-Tyr-Leu-Gly
Вставка фрагментов б) эндо-Т11Г2а-номенклатурин 2 2a 3 Ala-Lys-Thr-Glu-Tyr-Leu
1154
Новый справочник химика и технолога
Окончание табл. 6.51
Модификация Модифицированное тривиальное название Структура
Удаление фрагментов в) дез-G 1и3-номенклатурин 2 4 Ala-L.ys-Tyr-L.eu
Ацилирование аминогруппы боковой цепи г) №2-Уа1-номснклатурин Vai—। Arg-Lys-Glu-Tyr-Leu
Ацилирование карбоксильной группой боковой цепи д) С^-номенклатурин-Уа! ।—Vai Arg-Lys-Glu-Tyr-Leu
Фрагменты последовательнос-теи ’ номенклатурин-(2-4)-пептид Lys-Glu-Tyr
Пептиды с обращенной последовательностью ж) ретро-номенклатурин Leu-Tyr-Glu-Lys-Ala
Энантиомеры 3) эши-номенклатурин D-Ala-D-Lys-D-Glu-D-Tyr-D-Leu
Замена фрагмента -CO-NH-на другой фрагмент и) [3\|/4,СН2-8]номенклатурин Ala-Lys-Glu-v|/(CH2-S)-Tyr-Leu
а) Замену q-ro аминокислотного остатка (начиная с A-терминальной аминокислоты) на аминокислоту Хаа обозначают путем добавления [Хаа4] перед тривиальным названием исходного пептида; при замене Gin на Glu или Asn на Asp допустимо использование префикса «дезамидо», например, дезамидо30-кортикотропин; аналогично при замене Gia на Glu используют префикс «декарбокси».
Вставку аминокислотного остатка Хаа между q-м и (q+l)-M звеньями (начиная с Л'-терминальной аминокислоты) обозначают путем добавления префикса «эндоча» перед тривиальным названием исходного пептида.
в) Формальное удаление аминокислотного остатка Хаа из положения q (начиная с А-терминальной аминокислоты) обозначают путем добавления префикса «дез4» перед тривиальным названием исходного пептида.
г) Ацилирование аминокислотой аминокислоты пептида обозначают путем добавления названия радикала ацилирующей кислоты перед тривиальным названием исходного пептида с указанием положения ацилирования с помощью буквенных локантов. Например, №2-Val означает, что второй по счету аминокислотный остаток (начиная с А-терминальной аминокислоты) про-ацилирован валином по £-аминогруппе; аналогичным образом могут быть указаны и другие заместители в аминокислотных остатках пептида, например, А62-метилноменклатурин.
л) Наличие дополнительного аминокислотного остатка, соединяющегося своей а-аминогруппой с боковой карбоксильной группой пептидной цепи, обозначают путем добавления названия этой аминокислоты к тривиальному названию исходного пептида.
с) Пептид, образованный из другого пептида удалением всех аминокислотных остатков до р-го и всех после q-ro, называют путем добавления к исходному названию -(р-д)-пептид.
ж) Пептид с обратной последовательностью аминокислотных остатков называют путем добавления перед тривиальным названием исходного пептида префикса «ретро».
з) Пептидные энантиомеры называют путем добавления перед тривиальным названием исходного пептида префикса «энт».
и) Пептидные аналоги, у которых структурный фрагмент -СО-NH- заменен на структурный фрагмент Z, называют путем добавления [PV|/4,Z], где р и q — это порядковые номера (начиная с А-терминальной аминокислоты) модифицированных аминокислотных остатков.
6.16.4. Стероиды
6.16.4.1. Родоначалъные названия
Стероидами называют соединения с углеводородным скелетом циклопента[а] фенантрена, а также их производные, образующиеся либо при разрыве одной и более связей, либо расширении или сужении циклов. Кольца в стероидах обозначают заглавными латинскими буквами, а атомы нумеруют в соответствии со схемой 6.10.
Если одна из метильных групп при С25 содержит заместитель, то ей приписывают наименьший номер, т. е. 26. Если же заместители содержатся в обеих метильных группах, наименьший номер дается атому углерода
с заместителем, идущим первым по алфавиту. Углеродным атомам боковой цепи при С17, например, атомам этильной группы при С24, номера 28, 29 и 30 не присваивают, а оставляют их для обозначения дополнительных метильных групп: двух при С4 и одной при С14. Эти триметильные производные стероидов также могут рассматриваться как тетрациклические терпеноиды, и проведенная нумерация в этом случае будет полностью соответствовать нумерации атомов, принятой для тритерпеноидов. Дополнительные атомы углерода в боковой цепи нумеруют, используя цифры с надстрочными индексами.
Современная номенклатура органических соединений
1155
вой цепи при С17. Следующие восемь соединений, прегнан, холан, холестан, эргостан, кампестан, порифера-стан, стигмастан и горгостан, отличаются друг от друга строением боковой цепи при С17 и конфигурацией содержащихся в ней стереоцентров (атом С20 везде имеет ^-конфигурацию). Последние два соединения в табл. 6.52 являются триметилзамещенными стероидами. В табл. 6.53 представлены четыре родоначальных стероида, содержащие гетероциклические фрагменты.
Схема 6.10
Таблица 6.52
Тривиальные названия родоначальных стероидов
При написании структурных формул стероидов молекулу, как правило, ориентируют указанным выше способом (схема 6.10), кроме особых случаев, например, димеров стероидов. Кроме того, могут использоваться перспективные изображения молекул, часто удобные для изображения стереоизомеров:
Название стероидов строят на основе тривиального родоначального названия, указывая заместители, функциональные группы и кратные связи с помощью префиксов или суффиксов с соответствующими цифровыми локантами. Абсолютная конфигурация хиральных центров молекулы задается родоначальным стероидом (абсолютная конфигурация, указанная в формуле на схеме 6.10, является наиболее характерной для природных стероидов), а конфигурация дополнительных стереоцентров, например, при С5, определяющая характер сочленения колец А и В, обозначается стереодескрипторами а (Н под плоскостью чертежа) и 0 (Н над плоскостью чертежа). Большинство стероидов содержат боковые алифатические цепи или дополнительные кольца, в том числе и спиросочлсненные, которые уже не лежат в одной плоскости с основной циклической системой. Для обозначения конфигурации хиральных центров в этих цепях и циклах используют R, S-стерео дескрипторы. Если конфигурация стереоцентра неизвестна, то после цифрового локанта, соответствующего этому атому углерода, ставится греческая буква S, (кси).
В табл. 6.52, 6.53 представлены тривиальные названия родоначальных соединений, которые применяются для построения систематических названий стероидов. Гонан (соединение № 1, табл. 6.52) используется в качестве родоначального соединения для стероидов, у которых отсутствуют боковые цепи при С17 и метильные группы С18 и С19. В производных эстрана (соединение № 2, табл. 6.52) имеется только одна метильная группа С18, андростана (соединение № 3, табл. 6.52) — две метильные группы, С18 и С19, при отсутствии боко-
1. Гонан (gonane) н
3. Андростан (androstane)
СНз
6. Холестан (cholestane)
7. Эргостан (ergostane)
8. Кампестан (campestane)
9. Пориферастан (porifera-stane)
11. Горгостан (gorgostane)
НзС21 У
10. Стигмастан (stigma-stane)
12. Ланостан (lanostane)
1156
Новый справочник химика и технолога
Тривиальные названия родоначальных стероидов с гетероциклическими заместителями
а) Название «спиростан» определяет конфигурацию всех стереоцентров, кроме С5 и С25 (изображен (255)-спиростан).
б) Название «фуростан» определяет конфигурацию всех стереоцентров, кроме С5 и С22.
^9 /~х!0 13 14 z~x20
рацию атомов С, С , С , С и С , а именно, 9а,10р,13[3,14а,17а,20/?. Этим условиям удовлетворяет холестан (соединение № 6, табл. 6.52). Кроме упомянутых заместителей циклопентано[а]фенантреновая система 5 содержит пять гидроксильных групп при С2, С3, С14, С22 и С25, двойную связь между атомами С7 и С8 и оксогруппу при С6. Записывая двойную связь и кетогруппу (главная группа) в суффикс, а гидроксильные группы в префикс с соответствующими локантами и стереодескрипторами для гидроксильных групп, находящихся у хиральных атомов углерода (23,30,14а,22/?), получаем название (22/?)-2р,Зр,14а,22,25-пентагидро-кс и-5 Р-олест-7-ен-6-он.
Построение названия стероида имеет ряд особенностей, которые описаны ниже.
6.16.4.2. Двойные связи в стероидах
При наличии двойной связи между атомами, имеющими несоседние номера, в названии приводят оба номера в виде соединенного локанта, например:
Г она-1,3,5(10)-триен англ.: Gona-1,3,5(10)-triene
Если есть выбор между набором простых локантов двойной связи и набором, содержащим объединенный локант, предпочтение отдают первому, например:
В качестве иллюстрации ниже приведен пример построения систематического названия стероида 5:
Гона-5,7,9-триен а не гона-5(10),6,8-триен англ. -. Gona-5,7,9-triene
При наличии двойной связи между атомами С24-С25 метильной группе, находящейся в транс- положении по отношению к С23, дается номер 26, а оставшейся — 27, например:
Прежде всего молекулу следует расположить указанным на рисунке способом. Далее для определения родоначального углеводорода обратимся к табл. 6.52 и выберем стероид, во-первых, содержащий метильные группы С18 и С19, а также 1,6-диметилгексильный заместитель при С17 и, во-вторых, имеющий аналогичную конфигу-
6.16.4.3. Алкильные заместители в стероидах
Если соединение имеет два алкильных заместителя при С17 и один из них включен в состав родоначального стероида (табл. 6.52, 6.53), то соединение называют
Современная номенклатура органических соединений
1157
как алкильное производное этого стероида, например см. рис. 6.16.52.
Если соединение имеет два алкильных заместителя при С17 и ни один из них не включен в состав родоначального стероида, то его называют как 17,17-дизаме-щеннос производное этого стероида. Атомы более короткой цепи получают штрихованные цифровые локанты (171, 172 и т. д.). Если боковые цепи одинаковой длины, то штрихованными локантами обозначают атомы цепи, находящиеся на a-стороне, например см. рис. 6.16.53.
Цифровые локанты со штрихом используются для идентификации атома, например, в спектре 13С ЯМР, а не как локанты для указания положения заместителей.
6.16.4.4. Дополнительные кольца внутри стероидного скелета
Если в стероиде путем образования связи между несоседними углеродными атомами циклопента[<я]фенан-
тре нового скелета или углеродным атомом скелета и атомом боковой цепи образуется дополнительный цикл, то такое соединение называют обычным способом с добавлением префикса «цикло», перед которым ставятся цифровые локанты, указывающие на положение связанных в цикл атомов; при появлении нового хирального центра к соответствующему локанту добавляют стереодескриптор (а, Р или Q, например см. рис. 6.16.54.
3,5-Циклопроизводные стероидов часто называют /-стероидами, например, первое из вышеприведенных соединений иногда называют /-холестерином.
6.16.4.5. Гетероатомы в циклопента[а]фенантреновом скелете
Если в циклопента[я]фенантреновом скелете один или более атомов углерода заменены на гетероатомы, то для названия соединения используют «а»-обозначения (подразд. 6.3.5) с использованием стероидного родоначального названия и нумерации, например см. рис. 6.16.55.
НзО.21
А
17-Метил-5а-холан англ.-. 17-Methyl-5a-cholane
17-(2-Хлорэтил)-5а,17а-кампестан
англ.: 17-(2-Chloroethyl)-5a, 17a-campestane
Рис. 6.16.52
171
н
17р-Метил-17а-пропил-5а-андростан англ.: 170-Methyl-l 7a-propyl-5a-androstane
Н
17,17-Диметил-5а-андростан англ.: 17,17-Dimethyl-5a-androstane
За, 5-Цикл о-5а-холестан-6р-ол англ.: 3a,5-Cyclo-5a-cholestan-6p-ol
(20/?)-18,21-Цикло-5а-холан англ.: (20/?)-18,21 -Cyclo-5a-cholane
Рис. 6.16.54
1158
Новый справочник химика и технолога
он
170-Г идрокси-4-оксаандрост-5-ен-3-он англ.: 170-Hydroxy-4-oxaandrost-5-en-3-one
Рис. 6.16.55
6.16.4.6. Изменение длины боковых цепей и размера циклов
С целью избежать появления большого количества дополнительных тривиальных родоначальных названий для построения производных стероидов, содержащих отличный от приведенных в табл. 6.52, 6.53 углеводородный скелет, были введены специальные структурные префиксы, которые также используются в номенклатуре других природных соединений.
Префикс «дез» в стероидах
Префикс «дез» («des») обозначает удаление терминального кольца с добавлением атомов водорода к каждому из бывших узловых атомов. При записи названия после префикса «дез» ставится курсивная заглавная буква, обозначающая удаленное кольцо, например:
Нумерация атомов в полученном углеводороде остается той же, что и в родоначальном стероиде.
Префикс «нор» в стероидах
Префикс «нор» указывает на укорочение боковой цепи или сужение цикла на одну метиленовую группу. Если боковая цепь или цикл в молекуле уменьшены на две метиленовые группы по сравнению с родоначальным стероидом, то используют префикс «динор». Если возможна альтернатива, то из боковой цепи или в рассматриваемом цикле «удаляют» незамещенную метиленовую группу с наибольшим локантом, который указывается перед префиксом «нор». У оставшихся атомов остается первоначальная нумерация, например см. рис. 6.16.56.
Следует иметь в виду, что использование префикса «нор» неправомерно в том случае, если в результате удаления одной или нескольких метиленовых групп получается скелет другого родоначального стероида, например, вместо 19-норандростана следует использовать эстран, а вместо 18,19-динорандростана — гонан. Соединение, полученное укорочением боковой цепи прегнана на метиленовую группу, следует называть 17|3-метиландростан, а не 21-норпрегнан.
Префикс «гомо» в стероидах
Удлинение боковой цепи или расширение цикла на одну (или более) метиленовую группу обозначается префиксом «гомо» («дигомо» и т. д.); перед префиксом ставится локант, форма записи которого зависит от того структурного фрагмента, в который введена новая метиленовая группа. Если метиленовая грушга внедрена между неузловыми атомами колец или боковой цепи, то локант представляет собой номер атома углерода (если возможна альтернатива, то берется атом с наибольшим номером), к которому добавлена метиленовая группа, с добавлением буквы «а» («Ь» и т. д.), например см. рис. 6.16.57а и 6.16.576.
Если метиленовая группа введена между двумя точками разветвления боковой цепи или узловыми атомами колец или между атомами С13 и С17, то перед буквой «а» («Ь» и т. д.) пишутся номера обоих атомов, между которыми расположена новая метиленовая группа, причем больший номер берется в круглые скобки, например см. рис. 6.16.58.
Префикс «абео» в стероидах
Для удаления и добавления метиленовых групп в различных кольцах одной и той же молекулы допускается одновременное использование префиксов «нор» и «гомо». При этом рекомендуется использовать комбинации этих префиксов для модификации не более чем двух колец. Для модификации размера соседних колец в качестве альтернативы может использоваться префикс «абео» (курсив), который указывает на миграцию связи, общей для двух колец. Эта процедура записывается в названии соединения в следующей форме: х(у -> —> z)a6eo-, где х — это номер неподвижного конца мигрирующей связи, у — первоначальный номер подвижного конца мигрирующей связи, z — номер нового положения подвижного конца мигрирующей связи, см. рис. 6.16.59.
В полученном после миграции связи соединении сохраняется первоначальная нумерация атомов. Пространственное положение водородных атомов у новых хиральных атомов указывается в названии с помощью стереодескрипторов (а, |3 или %) и заглавной курсивной буквы Н, например см. рис. 6.16.60.
Префикс «секо» в стероидах
Разъединение связи кольца в родоначальном стероиде с добавлением атомов водорода к образовавшимся концевым группам обозначается префиксом «секо». Перед префиксом указываются номера атомов, между которыми разорвана связь. Нумерация всей системы остается прежней, например см. рис. 6.16.61.
Современная номенклатура органических соединений
1159
Следует иметь в виду, что если для получения углеродного остова молекулы приходится разрывать более одной связи родоначального стероида, то обычная систематическая номенклатура может оказаться более предпочтительной.
Кроме систематических названий в химии стероидов допускается использование и тривиальных названий, в основном для производных с особой биологической активностью. Некоторые из них приведены в табл. 6.54.
17-Г идрокси-19-нор-17а-прегн-4-ен-20-ин-3-он англ.: 17-Hydroxy-19-пог-17a-pregn-4-en-20-yn-3-one ~19
атом С отсутствует
4-Нор-5а-андростан
англ.: 4-Nor-5a-androstane
атом С4 в кольце А отсутствует
24-Нор-50-холан
англ.: 24-Nor-5p-cholane
18,19-Динор-5а-прегнан англ.-. 18,19-Dinor-5a-pregnane атомы С18 и С19 отсутствуют
Рис. 6.16.56
24а,24Ь,24с-Тригомохолест-5-ен-Зр,7а-диол англ.: 24a,24b,24c-Trihomocholest-5-ene-3p,7a-diol
Рис. 6.16.57а
1160
Новый справочник химика и технолога
З-Гидрокси-17а, 17Ь-дигомоэстра-1,3,5(10)-триен-17Ь-он англ.: 3-Hydroxy-17а, 17b-dihomoestra-1,3,5(10)-trien-17b-one
Рис. 6.16.576
17(20)а-Гомо-5а-холестан-3-он англ.: 17(20)a-Homo-5a-cholestan-3-one
13(17)а-Г омо-5а-прегнан англ.: 13(17)a-Homo-5a-pregnane
8(9)а-Г омо-5а-андростан
англ.: 8(9)a-Homo-5a-androstane
8(14)а-Г омо-5а-андростан англ.: 8(14)a-Homo-5a-androstane
Рис. 6.16.58
10(5-*6)абео-
Рис. 6.16.59
5а-Холестан 14(13->12)абео-5а, 12а(Н), 13а(Н)-Холестан
англ.: 5a-Cholestane англl4(13->12)abeo-5a,12a(^,13a(H)-Cholestane
Рис. 6.16.60
Современная номенклатура органических соединений
1161
2,3-Секо-5а-холестан З-Гидрокси-16,17-секоэстра-1,3,5(10)-триен-
англ.: 2,3-Seco-5a-cholestane 16,17-диовая кислота
англ.: 3-Hydroxy-16,17-secoestra-1,3,5(10)-triene-
16,17-dioic acid
(5Z,7E)-(1 S,3S)-9,10-Секохолеста-5,7,10(19)-триен-1,3-диол англ.: (5Z,7E)-(1S,3S)-9,10-Secocholesta-5,7,10(19)-triene-1,3-diol
Рис. 6.16.61
Таблица 6.54
Тривиальные названия некоторых производных стероидов, разрешенные правилами IUPAC
Тривиальное название Систематическое название
Альдостерон (aldosterone) Андростерон (androsterone) Брассинолид (brassinolide) Дезоксикортикостерон (deoxycorticosterone) Кортизол (cortisol) Кортизон (cortisone) Кортикостерон (corticosterone) Ланостерин (lanosterol) Литохолевая кислота (lithocholic acid) Прогестерон (progesterone) Псевдотигогенин (pseudotigogenin) Сарсасапогенин (sarsasapogenin) Смилагенин (smilagenin) Тестостерон (testosterone) Тигогенин (tigogenin) Холевая кислота (cholic acid) Холестерин (cholesterol) Экдизон (ecdysone) 18%-гидрокси-11Р, 18-эпоксипрегн-4-ен-3,20-дион За-гидрокси-5а-андростан-17-он (22/?,23/?)-2а,За,22,23-тетрагидрокси-6,7-секо-5а-кампестано-6,7-лактон 21 -гидроксипрегн-4-ен-3,20-дион 11Р, 17,21 -тригидроксипрегн-4-ен-3,20-дион 17,21 -дигидроксипрегн-4-ен-3,11,20-трион 11 Р,21 -дигидроксипрегн-4-ен-3,20-дион ланоста-8,24-диен-3 Р-ол 3а-гидрокси-5Р-холан-24-овая кислота прегн-4-ен-3,20-дион (25/?)-5а-фурост-20(22)-ен-Зр,26-диол (255)-5р-спиростан-Зр-ол (25/?)-5 Р-спиростан-3 Р-ол 17р-гидроксиандрост-4-ен-3-он (25/?)-5а-спиростан-Зр-ол За,7а, 12а-тригидрокси-5р-холан-24-овая кислота холест-5-ен-Зр-ол (22И)-2р,ЗР,14а,22,25-пентагидрокси-5р-холест-7-ен-6-он
1162
Новый справочник химика и технолога
Таблица 6.54
Тривиальное название Систематическое название
Эргостерин (ergosterol) Эстрадиол (17a-estradiol) Эстриол (estriol) Эстрон (estrone) (22£)-эргоста-5,7,22-триен-3 0-ол эстра-1,3,5( 10)-триен-3,17а-диол эстра-1,3,5( 10)-триен-3,16а, 170-триол 3-гидроксиэстра-1,3,5( 10)-триен-17-он
6.16.4.7. Витамины группы D
Термин «витамин D» объединяет все стероиды, которые проявляют биологическую активность кальциола (холекальциферола), а термин «витамин D3» является его синонимом, см. рис. 6.16.62.
В принципе, все соединения этой группы можно назвать по стероидной номенклатуре (табл. 6.55). Здесь, однако, следует отметить, что написание систематических названий секостероидов, коими являются витамины группы D, иногда сопряжено с определенными проблемами. Так, например, для изображения витамина D3 используются обе представленные выше структурные формулы, и применение стереодескрипторов а или 0 к атому С3 кольца А в стероидном названиии «(5Z,7£)-9,10-секохолеста-5,7,10(19)-трисн-3-ол» приводит к неопределенности: в первом случае для обозначения конфигурации атома С3 нужно добавлять дескриптор а, а во втором — 0. По этой причине эти дескрипторы не
следует употреблять для обозначения конфигурации атомов кольца А, а также атомов С6 и С7. Вместо них используются R,S обозначения.
Тривиальные названия этой группы соединений существенно короче систематических и более удобны в употреблении. Так, например, витамин D3 имеет тривиальное название «холекальциферол», которое использовалось для наименования его метаболитов по полу-систематической номенклатуре. В настоящее время рекомендованы еще более короткие названия основных витаминов группы D, представленные в табл. 6.55. Например, для витамина D3 «новым» тривиальным названием, является «кальциол». Именно его следует использовать как родоначальное в написании нолусисте-матических названий производных, а «холекальциферол» остается как альтернативное тривиальное название витамина D3.
Таблица 6.55
Тривиальные названия витаминов группы D
Рекомендованное тривиальное название Устаревшее тривиальное название Систематическое стероидное название
Кальциол или холекальциферол (calciol или cholecalciferol) холекальциферол (5Z,7£)-(3S)-9,10-секохолеста-5,7,10( 19)-триен-3-ол
Кальцидиол (calcidiol) 25-гидроксихолекальциферол (5Z,7£)-(3S)-9,10-секохолеста-5,7,10( 19)-триен-3,25-диол
Кальцитриол 1 а,25-дигидроксихолекальци- (5Z,7£)-( 1£,3/?)-9,10-секохолеста-
(calcitriol) ферол 5,7,10( 19)-гриен-1,3,25-триол
Эркальциол или эргокальциферол (ercalciol или ergocalciferol) эргокальциферол (5Z,7£,22£)-(3/?)-9,10-ceKO3procTa- 5,7,10( 19)22-тетраен-3-ол
Эркальцитриол (ercalcitriol) 1 а,25-дигидроксиэркальци-ферол- (5Z,7£, 22£)-( 15,3 £)-9,10-секоэргоста-5,7,10( 19)22-тетраен-1,3,25-триол
(245)-Метилкальциол или 22,23-дигидроэркальциол ((245)-methylcalciol или 22,23-dihydroercalciol) 22,23-дигидроэркальциферол- (5Z,7£)-(35)-9,10-секоэргоста-5,7,10( 19)-триен-3-ол
Кальцитетрол (calcitetrol) 1 а,24£,25-тригидро-ксихолекальциферол (5Z,7£)-( 1 £,3/?,24/?)-9,10-секохолеста-5,7,10( 19)-триен-1,3,24,25-тетрол
(67)-Такальциол ((6Z)-tacalciol) провитамин D3 (6Z)-(3/?)-9,10-секохолеста-5( 10),6,8-триен-3-ол
Такальциол (tacalciol) тахистерин3 англ'. tachysterol3 (6£)-(3/?)-9,10-секохолеста-5( 10),6,8-триен-3-ол
(5£)-Изокальциол ((5£)- isocalciol) изовитамин D3 (5Z,7£)-(35)-9,10-секохолеста-1 (10),5,7-триен-3-ол
Современная номенклатура органических соединений
1163
Кальциол или холекальциферол англ: Calciol или cholecalciferol
Рис. 6.16.62
6.16.5. Терпены и терпеноиды
6.16.5.1. Общие сведения
Терпенами называют природные ненасыщенные углеводороды состава (С5Н8)„, где п = 2, 3, 4, 6 и т. д.: C10H]6 — терпены, С]5Н24— сесквитерпены, С20Н32 — дитерпены, Сз0Н48 — тритерпены и политерпены. Терпены удобно рассматривать как продукты формальной ди-, три- и более высокой полимеризации изопрена С5Н8. Природные производные терпенов (спирты, альдегиды, кетоны и др.) называются терпеноидами. Для ациклических терпенов и терпеноидов помимо триви
альных названий, которые имеют большинство природных соединений, используется систематическая заместительная номенклатура, см. рис. 6.16.63.
В отличие от ациклических терпенов, циклические монотерпены (СюН16) по правилам IUPAC рекомендуется называть по полусистематической номенклатуре, которая содержит девять родоначальных соединений, охватывающих основные структурные типы этого класса веществ. В табл. 6.56 представлены родоначальные названия циклических монотерпенов с указанием нумерации атомов.
Мирцен (трив.) или 7-метил-3-метиленокта-1,6-диен (сист.) англ-. Myrcene или 7-methyl-3-methyleneocta-1,6-diene
Рис. 6.16.63
Таблица 6.56
Родоначальные названия циклических монотерпенов
Ментан а) (menthane) показан и-изомер
Туйан (thujane)
Каран Ь) (сагапе)
Пинан Ь) (pinane)
Борнан Ь) (bomane)
Норкаран (norcarane)
Норпинан (norpinane)
Норборнан (norbomane)
Камфен а) (camphene)
а) При наличии дополнительных алкильных групп следует использовать систематическое название.
С) Если в молекуле присутствуют боковые цепи, отличные от метильной или метиленовой групп, то в качестве родоначальных названий используются «норкаран», «норпинан» или «норборнан».
1164
Новый справочник химика и технолога
6.16.5.2. Каротиноиды
К каротиноидам относят каротины и их кислородсодержащие производные (ксантофиллы и др.), состоящие из восьми изопреновых фрагментов, соединенных таким образом, что две центральные метильные группы связаны цепочкой из шести, а остальные — пяти атомов углерода (кроме терминальных метильных групп). Все каротиноиды можно рассматривать как производные углеводорода 5, получающиеся в результате его гидрирования, дегидрирования, циклизации, окисления или комбинации этих процессов. Кроме того, к каротиноидам относят соединения, образованные путем некоторых перегруппировок углеродного скелета 6 и удаления фрагментов молекулы. Волнистыми линиями в формуле 6 (рис. 6.16.64) показано разъединение молекулы на изопреновые фрагменты.
В качестве основы названий всех каротиноидов служит родоначальное название «каротин» («carotene»). Терминальные С9-фрагменты молекулы могут быть ациклическими или пяти-, шестизвенными циклическими структурами. Для их обозначения к основе «каротин» добавляют два префикса в виде букв греческого алфавита (перечисляются через занятую в алфавитном порядке*), каждая из которых соответствует определенной структуре одного из терминальных С9-фрагмснтов молекулы (см. табл. 6.57), например см. рис. 6.16.65.
В тех случаях, когда модифицированная концевая группа каротиноида может быть представлена как производная двух или даже трех базовых структур из табл. 6.57, название строится на основе той структуры, которая расположена раньше по алфавиту.
Нумерация атомов каротиноидов производится так, как показано в вышеприведенных примерах и табл. 6.57. Она начинается сразу с обоих концов молекулы и заканчивается на центральной двойной связи, причем один из полученных наборов локантов помечается штрихами. Если молекула несимметрична, то нештрихованные локанты получает фрагмент, чей префикс расположен раньше по алфавиту. Структуры рекомендуется рисовать так, чтобы «штрихованные» атомы оказались справа.
В \|/-каротиноидах концевая метильная группа при двойной связи, тиранс-расположенная относительно основной цепи, имеет локант 16 (16'), а г/мс-метильная группа —локант 17 (17').
Иногда необходимо провести дифференциацию метильных групп при С1 или С1 в концевых С9-фрагментах Р-, у-, к- или s-типа. При стандартном изображении молекулы (соединение 6) метил, расположенный за цлоско-
Греческие буквы (в алфавитном порядке), используемые в качестве префиксов: р (бета), у (гамма), с (эпсилон), к (каппа), ф (фи), х (хи), \|/ (пси). Происхождение префиксов: р и е — от тривиальных названий симметричных каротиноидов, «р-каротина» и «е-каротина»; к — от названия симметричного «капсорубина»; у — от «у-ионона», ф — от названия радикала «фенил».
стью листа, получает номер 16 (16'), а тот, который расположен перед плоскостью листа, — номер 17(17'):
В названиях каротиноидов сначала перечисляются по порядку все нештрихованные локанты, после чего — штрихованные, например, 1,2,3,1 ',2',3'. Следует обратить внимание на то, что этот порядок локантов отличается от того, который принят в заместительной номенклатуре (см. подразд. 6.1.3.1), где локанты записывают так: «х,х',у,у'...», например, 1, Г,2, 2',3, 3'.
Для наименования гидрированных производных каротина используют неотделяемые префиксы «дигидро» «тетрагидро» и т. д.; для обозначения наличия тройных связей или алленовых группировок применяют неотделяемые префиксы «дидегидро» и т. д. Следует помнить, что неотделяемые префиксы помещают непосредственно перед основой названия, в данном случае перед греческими буквами терминальных фрагментов каротина; если в названии присутствуют несколько неотделяемых префиксов такого типа, то их располагают по алфавиту, причем умножающие приставки не учитываются при определении алфавитного порядка, например, «7,8-дидегидро-7',8'-дигидро-» например, см. рис. 6.16.66.
Префиксы «нор» и «секо» в каротиноидах
В номенклатуре каротиноидов широко используются модифицирующие префиксы «нор» и «секо». Неот-деляемый префикс «нор» означает удаление группы СНз, СН2 или СН из родоначального каротина с сохранением первоначальной нумерации атомов. При наличии выбора префикс «нор» получает по возможности наименьший локант например, см. рис. 6.16.67.
Структуры, полученные в результате разрыва связи между атомами терминальных колец (за исключением связи 1-6), также могут быть названы на основе родоначального названия «каротин» с добавлением префикса «секо» и цифровых локантов, указывающих, между какими атомами разорвана связь. Здесь атомы секока-ротина, как и в предыдущем случае, сохраняют нумерацию исходного каротина, например, см. рис. 6.16.68.
Префикс «ретро» в каротиноидах
В номенклатуре каротиноидов часто используется модифицирующий префикс «ретро» (курсив) {«retro»), обозначающий сдвиг на одну позицию системы двойных и одинарных связей в сопряженной системе, размер которой описывается двумя локантами (перед префиксом «ретро»)', первый локант — это номер атома, который потерял атом водорода, а второй — который его приобрел. Префикс «ретро» является неотделяе-мым, и поэтому помещается непосредственно перед основой названия, например, см. рис. 6.16.69.
Современная номенклатура органических соединений
1165
Рис. 6.16.64
Рис. 6.16.65
англ. -. 7,8-Didehydro-5,6,r,2,,3,,4,,5',6',7',8'-decahydro-E,x-carotene
Рис. 6.16.66
4'
англ.: 12,13,20-Т rinor-p,p-carotene атомы 12, 13 и 20 отсутствуют
Рис. 6.16.67
1166
Новый справочник химика и технолога
Префиксы терминальных фрагментов каротиноидов
Таблица 6.57
Тип Префикс Формула
Ациклический Циклогексен Метилен циклогексан Циклопентан Арил V ₽ £ Y к Ф X 17 18 2 4 6 16 17 [Хл И . 5 И 16 17 16 17 17| бр< # 16] 'МчЛ' |рв[ 1’3 и 5-1 Ч^ХДб 16| Т|21 Ik Л 5.1
Рис. 6.16.68
Рис. 6.16.69
Современная номенклатура органических соединений
1167
Префикс «апо» в каротиноидах
Присутствие в названии каротиноида префикса «апо» с предшествующим ему локантом указывает на то, что молекула укорочена на все атомы углерода, имеющие номера до указанного локанта (включая метильные группы с более высокими номерами, присоединенные к удаленным атомам). Префикс «апо» записывается непосредственно перед греческими буквами концевых групп. Если указанный локант больше 5, то греческие буквы удаленного фрагмента опускаются. При значении локанта 5 и менее считается, что «удаленный» фрагмент был ациклического \|/-типа. Если молекула укорочена с обоих концов, то применяют префикс «диапо», см. рис. 6.16.70.
Кислородсодержащие каротиноиды
Кислородсодержащие и другие производные каротиноидных углеводородов называют в соответствии с общими правилами органической номенклатуры с использованием соответствующих суффиксов и префиксов с той лишь разницей, что нумерация главной цепи определяется не характером или положением функциональной группы, а исключительно природой терминальных С9-фрагментов, о чем говорилось выше,
например см. рис. 6.16.71. Если терминальные углеводородные С9-фрагменты идентичны, т. е. обозначаются одной и той же греческой буквой, то нештрихованный (старший) набор локантов получает та половина молекулы, которая содержит суффиксную функциональную группу (табл. 6.3). Не следует забывать, что у каротиноидов все нештрихованные локанты старше, чем штрихованные, и перечисляются в первую очередь, см. рис. 6.16.72. В последнем примере второе название неверно, поскольку набор локантов «1,2,5',6'-» при неот-деляемом префиксе «тетрагидро» предпочтительнее, чем «5,6, Г,2'-».
Природные каротиноиды кроме систематических названий, как правило, имеют тривиальные названия, некоторые из которых представлены в табл. 6.58.
Ретиноиды — это класс соединений, состоящий из четырех изопреновых фрагментов, соединенных по типу «голова к хвосту». Ретиноиды по своей структуре (но не по названию) можно рассматривать как производные моноциклического родоначального дитерпена (первое соединение в табл. 6.59), у которого терминальный метил боковой цепи заменен на функциональную группу. Некоторые примеры этих соединений с их названиями представлены в табл. 6.59.
6,6'-Диапокаротин-6,6'-диовой кислоты монометиловый эфир англ.-. Methyl hydrogen 6,6'-diapocarotene-6,6'-dioate
Рис. 6.16.70
Рис. 6.16.71
1168
Новый справочник химика и технолога
англ.: 2'-Methoxy-E,E-carotene-2,3'-clione
3,2'-Диметокси-1,2,5',6'-тетрагидро-к|/,к|/-каротин, а не
2,3,-Диметокси-5,6,1',2'-тетрагидро-ч/,ч/-каротин
англ.: 3,2'-Dimethoxy-1 ^^'.e’-tetrahydro-vi/.v-carotene
Рис. 6.16.72
Таблица 6.58
Тривиальные названия некоторых природных каротиноидов
Тривиальное название Систематическое название
Углеводороды
Ликоперсен (lycopersene) Фитофлуен (phytofluene) гсксагидроликопин (hexahydrolycopene) Торулин (torulene) а-Зеакаротин (a-zeacarotene) 7,8,11,12,15,7',8', 1 Г, 12', 15'-декагидро-\|/,\|/-каротин 15-г/мс-7,8,11,12,7',8'-гексагидро-у,\|/-каротин 3',4'-дидегидро-£,\|/-каротин 7',8'-дигидро-£,\|/-каротин
Спирты
Аллоксантин (alloxanthin) криптомонаксантин (cryptomonaxanthin) псктеноксантин (pectenoxanthin) цинтиаксантин (cynthiaxanthin) Крустаксантин (crustaxanthin) Газаниаксантин (gazaniaxanthin) ОН-Хлоробактен (OH-chlorobactene) Лороксантин (loroxanthin) Ликоксантин (lycoxanthin) Родоп ин (rhodopin) Родопинол (rhodopinol) Сапроксантин (saproxanthin) (3/?,3'/?)-7,8,7',8'-тетрагидро-р,р-каротин Р,Р-каротин-3,4,3 ',4'-тетрол (3/?)-5'-г/мс-р,\|/- каротин-3-ол 1 ',2'-дигидро-ф,\|/-каротин-1 '-ол Р,£-каротин-3,19,3 '-триол \|/,\|/-каротин-16-ол 1,2-дигидро-\|/,\|/-каротин-1 -ол 13-цис-1,2-дигидро-\|/,\|/-каротин-1,20-диол 3',4'-дидегидро-1',2'-дигидро-р,\|/- каротин-3,Г-диол
Гликозиды
Осциллаксантин (oscillaxanthin) Плейксантофилл (phleixanthophyll) 2,2'-бис(р-Ь-рамнопиранозилокси)-3,4,3',4'-тетрадегидро- 1,2,1 ',2'-тетрагидро-\|/,\|/- каротин-1,1 '-диол 1 '-(Р-О-глюкопиранозилокси)-З ',4'-дидегидро-1 ',2'-дигидро-Р,\|/-каротин-2'-ол
Современная номенклатура органических соединений
1169
Продолжение табл. 6.58
Тривиальное название Систематическое название
Эфиры
Родовибрин (rhodovibrin) Сфероиден (spheroidene) 1 '-метокси-3',4'-дидегидро-1,2,1 ',2'-тетрагидро-\|/,\|/- каротин-1 -ол 1 -метокси-3,4-дидегидро-1,2,7',8'-тетрагидро-\|/,\|/- каротин
Эпоксиды
Лютеоксантин (luteoxanthin) Мутатоксантин (mutatoxanthin) цитроксантин (citroxanthin) зеаксантина фураноксид (zeaxanthin furanoxide) Неохром (neochrome) фолиахром (foliachrome) троллихром (trollichrome) Ваучериаксантин (vaucheriaxanthin) 5,6:5',8'-диэпокси-5,6,5',8'-тетрагидро-р,р-каротин-3,3'-диол 5',8'-эпокси-5,6,5',8'-тетрагидро-р,р-каротин-3,3'-диол 5',8'-эпокси-6,7-дидегидро-5,6,5',8'-тетрагидро-р,р-каротин-3,5,3'-триол 5',6'-эпокси-6,7-дидегидро-5,6,5',6'-тетрагидро-р,р-каротин-3,5,19,3'-тетрол
Альдегиды
Родопиналь (rhodopinal) Торулародинальдегид (torularhodinaldehyde) 13-цис-1 -гидрокси-1,2-дигидро-\|/,\|>- каротин-20-аль 3',4'-дидегидро-р,\|/-каротин-1 б'-аль
Кислоты
Торулародин (torularhodin) 3',4'-дидегидро-р,\|/-каротин-16'-овая кислота
Кетоны
Кантаксантин (canthaxanthin) афаницин (aphanicin) хлореллаксантин (chlorellaxanthin) Капсантин (capsanthin) Капсорубин (capsorubin) Криптокапсин (cryptocapsin) 2,2'-Дикетоспириллоксантин (2,2-diketospirilloxanthin) Флексиксантин (flexixanthin) 3-ОН-Кантаксантин (3-OH-canthaxanthin) адонирубин (adonirubin) фоеникоксантин (phoenicoxanthin) Гидроксисфероиденон (hydroxyspheroidenone) Окенон (okenone) Пектенолон (pectenolone) Фоениконон (phoeniconone) Дегидроадонирубин (dehydroadonirubin) Фоеникоптерон (phoenicopterone) Рубиксантон (rubixanthone) Сифонаксантин (siphonaxanthin) Р,р-каротин-4,4'-дион (3/?,3'5,5'/?)-3,3'-дигидрокси-р,к-каротин-6'-он (3/?,5К,3'5,5'/?)-3,3'-дигидрокси-к,к-каротин-6,6'-дион (3'/?,5'/?)-3'-гидрокси-р,к-каротин-6'-он 1,1 '-диметокси-3,4,3',4'-тетрадегидро-1,2,1 ',2'-тетрагидро-\|/,\|/-каротин-2,2'-дион 3,Г-дигидрокси-3',4'-дидегидро-1 ',2'-дигидро-р,\|/-каротин-4-он 3-гидрокси-р,р-каротин-4,4'-дион 1 '-гидрокси-1 -метокси-3,4-дидегидро-1,2,1 ',2',7',8'-гексагидро-\|/,\|/-каротин-2-он 1 '-метокси-1 ',2'-дигидро-х,\|/-каротин-4'-он 3,3'-дигидрокси-7',8'-дидегидро-р,р-каротин-4-он 3-гидрокси-2,3-дидегидро-р,р-каротин-4,4'-дион Р,е-каротин-4-он 3-гидрокси-р,\|/-каротин-4'-он 3,19,3 '-тригидрокси-7,8-дигидро-0 ,е-каротин-8-он
1170
Новый справочник химика и технолога
Окончание табл. 6.58
Тривиальное название Систематическое название
Сложные эфиры
Астацеин (astacein) Фукоксантин (fucoxanthin) Изофукоксантин (isofucoxanthin) Физалиен (physalien) зеаксантина дипальмитат (zeaxanthin dipalmitate) Сифонеин (siphonein) 3,3'-биспальмитаилокси-2,3,2',3'-тетрадегидро-р,р-каротин-4,4'-дион 3'-ацетокси-3,5'-дигидрокси-5,6-эпокси-6',7'-дидегидро-5,6,7,8,5',6'-гексагидро-р,р-каротин-8-он 3'-ацетокси-3,5,5'-тригидрокси-6',7'-дидегидро-5,8,5',6'-тетрагидро-р,р-каротин-8-он (3/?,3'/?)-3,3'-биспальмитоилокси-р,р-каротин 3,3'-дигидрокси- 19-лауроилокси-7,8-дигидро -р,£-каротин-8-он
Апо-каротиноиды
Р-Апо-2'-каротиналь (p-apo-2-carotenal) Апо-2-ликопиналь (apo-2-lycopenal) Апо-б'-ликопиналь (apo-6'-lycopenal) Азафринальдегид (azafrinaldehyde) Биксин (bixin) Кроцетин (crocetin) Кроцетинсемиальдегид (crocetinsemialdehyde) Кроцин (crocin) Метил-апо-б'-ликопиноат (methyl apo-6'-lycopenoate) 3',4'-дидегидро-2'-апо-р-каротин-2'-аль 6'-апо-\|/-каротин-6'-аль 5,6-дигидрокси-5,6-дигидро-10'-апо-р-каротин-10'-аль 9'-г/ис-6,6'-диапокаротин-6,6'-диовой кислоты монометиловый эфир 8,8'-диапо-8,8'-каротиндиовая кислота 8'-оксо-8,8'-диапо-8-каротиновая кислота 8,8'-диапокаротин-8,8'-диовой кислоты дигентиобиосиловый эфир б'-апо-\|/-каротин-6'-овой кислоты метиловый эфир
Нор- и секо-каротиноиды
Актиниоэритрин (actinioerythrin) p-Каротинон (p-carotenone) Перидинин (peridinin) Пирроксантининол (pyrrhoxanthininol) Семи-а-каротинон (semi-a-carotenone) Семи-р-каротинон (semi-p-carotenone) Трифазиаксантин (triphasiaxanthin) 3,3'-бисацилокси-2,2'-динор-Р,р-каротин-4,4'-дион 5,6:5',6'-дисеко-р,р-каротин-5,6:5',6'-тетрон 3'-ацетокси-3,5'-дигидрокси-5,6-эпокси-6',7'-дидегидро-5,6,5',6'-тетрагидро-12', 13 ',20'-тринор-р,р-каротин-19,11 -олид 3,3'-дигидрокси-5,6-эпокси-7',8'-дидсгидро-5,6-дигидро-12', 13 ',20'-тринор-р,р-каротин-19,11 -олид 5,6-секо-р,£-каротин-5,6-дион 5,6-секо-р,р-каротин-5,6-дион 3'-гидрокси-5,6-секо-р,р-каротин-5,6-дион
pewpo-Каротиноиды
Эшшолтзксантин (eschscholtzxanthin) Эшшолтзксантон (eschscholtzxanthone) Родоксантин (rhodoxanthin) 4',5 '-ди дегидро-4,5 '-ре>иро-р,р-каротин-3,3 '-диол 3'-гидрокси-4',5'-дидегидро-4,5'-ре>иро-р,р-каротин-3-он i 4',5 '-дидегидро-4,5 '-ре/иро-р,р-каротин-3,3 '-дион
Высшие каротиноиды
Нонапреноксантин (nonaprenoxanthin) Бактериоруберин (bacterioruberin) 2-(4-гидрокси-3-метилбут-2-енил)-7',8', 11', 12'-тетрагидро-8,у-каротин 2,2'-бис(3-гидрокси-3-метилбутил)-3,4,3',4'-тетрадегидро-1,2,1 ',2'-тетрагидро-\|/,\|/-каротин-1,1 '-диол
Современная номенклатура органических соединений
1171
6.16.5.3. Ретиноиды
Строение и названия ретиноидов
16^-/17 Г I20 15
Таблица 6.59
R Название (синонимы)
СН3а) СН2ОН СН2ОСОСН3 ch2nh2 сно CH=NOH CH=N(CH2)4CH(N Н2)СО2Н СО2Н СО2С2Н5 НО2С о \ он О Дезоксиретинол б) (аксерофтен) англ:. Deoxyretinol (axerophthene) Ретинол (витамин А спирт, аксерофтол, аксерол) англ:. Retinol (vitamin A alcohol, axerophthol, axerol) Ретинилацетат англ:. Retinyl acetate Рстиниламин англ:. Retinylamine Ретиналь (витамин А альдегид, ретинен) англ:. Retinal (vitamin A aldehyde, retinene) Ретиналя оксим англ:. Retinal oxime Л^-Ретинилиден-Ь-лизин англ:. V’-Retinylidene-L-lysine Ретиноевая кислота (витамин А кислота, третиноин) англ:. Retinoic acid (vitamin A acid, tretinoin) Этилретиноат англ:. Ethyl retinoate 1 -ОРетиноил-Р-О-глюкопирануроновая кислота англ\ 1-O-Retinoyl-P-D-glucopyranuronic acid
а) Названия радикалов (R: СН2-) и (R: СН=) «ретинил» и «ретинилиден» соответственно,
б) В названии «дезоксиретинол» суффикс «дезокси» является неотделяемым и пишется без локанта непосредственно перед основой.
Кроме того, к классу ретиноидов следует относить соединения, формально образующиеся при изменении степени гидрирования вышеприведенных структур, продукты замещения атомов водорода, продукты раскрытия цикла (секоретиноиды) и удаления атомов углерода (норретиноиды), а также структуры со смещенной системой кратных связей (ретроретиноиды). Названия этих соединений строятся аналогично названиям каротиноидов (подразд. 6.16.5.2), и ниже представлены без комментариев лишь примеры этих производных с названиями:
Изменение степени гидрирования
3,4-Дидегидроретинол (витамин А2) англ:. 3,4-Didehydroretinol (vitamin А2)
1172
Новый справочник химика и технолога
4
4,5-Дидегидро-5,6-дигидроретинол (a-витамин А) англ:. 4,5-Didehydro-5,6-dihydroretinol (a-vitamin А)
Замещенные ретиноиды
5,6-Эпокси-5,6-дигидроретинол (гепаксантин) англ.: 5,6-Epoxy-5,6-dihydroretinol (hepaxanthin)
Секо-ретиноиды
1,6-Секо-1,2-дидегидроретинол (у-витамин А) англ:. 1,6-Seco-1,2-didehydroretinol (y-vitamin А)
Нор-ретиноиды
отсутстуют атомы С4 и С1 &
Ре/иро-ретиноиды (рис. 16.73)
Заметим, что в последнем примере предложенное название более предпочтительно, чем «14,15-дидегид-ро-4,14-ре/иро-дезоксиретинол», поскольку набор локантов «4,5-» старше, чем «14,15-».
6.16.6. Нуклеозиды, нуклеотиды и нуклеиновые кислоты
Нуклеиновые кислоты, являющиеся основной органической частью ядер клеток, играют главную роль в хранении и передаче генетической информации. Полимерные цепочки нуклеиновых кислот построены из нуклеотидов, которые состоят из азотистого основания, пентозы и фосфатной группы. Углеводным фрагментом обычно является D-рибоза (в рибонуклеиновых кислотах, сокращенно РНК) или 2-дезокси-В-рибоза (в дезоксирибонуклеиновых кислотах, сокращенно ДНК). Азотистыми основаниями нуклеотидов могут быть производные пурина (соединение № 23 в табл. 6.11) — аденин, гуанин, ксантин и гипоксантин — и производные пиримидина (соединение № 30 в табл. 6.11) -— урацил, тимин и цитозин. В табл. 6.60 представлены
структурные формулы и нумерация атомов наиболее распространенных пуриновых и пиримидиновых оснований, входящих в состав нуклеотидов. Для краткого обозначения азотистого основания принята система трехбуквенных символов (табл. 6.60). Эти обозначения, представляющие собой первые три буквы названия соединения, следует употреблять исключительно для обозначения свободных оснований (например, Ura — урацил) или их замещенных производных (например, FUra — фторурацил).
Гликозилированные азотистые основания, т. е. нуклеотиды без фосфатной группы, называются нуклеозидами. Большинство нуклеозидов называют, используя название входящего в него основания с окончанием «-озин» или «-идин» (табл. 6.60). Локанты углеродных атомов углеводного остатка помечаются штрихами. Названия нуклеотидов, фосфорных эфиров нуклеозидов, строятся из названий нуклеозидов с добавлением окончания «фосфат» и цифрового локанта, соответствующего месту присоединения фосфатной группы к рибозе или дезоксирибозе (это, как правило, 2'-, 3'- или 5'-гидроксильная группа), например тимидин-5'-фосфат.
Для написания названий нуклеотидных цепей используются две системы буквенных обозначений нуклеозидных остатков: трехбуквенная и однобуквенная. Первая из них применяется для сравнительно небольших олигонуклеотидов, в то время как вторая, предназначена для олиго- и полинуклеотидов, а также их фрагментов и нековалентных ассоциатов. Ее не рекомендуется употреблять для мононуклеотидов и нуклеозидов. Если в названии соединения, записанном с использованием любой из этих систем, отсутствуют какие-либо уточняющие символы, то подразумевается, что
- все нуклеозиды, за исключением псевдоуридина, являются 1-гликозилпиримидинами или 9-гликозил-пуринами;
- все аномерные центры имеют Р-конфигурацию;
- все моносахариды имеют D конфигурацию;
- пентозные остатки везде рибозильные*;
- все дезоксирибозильные остатки являются 2'-де-зоксирибозильными;
- присоединение нуклеозидов к фосфатным группам только 3'—>5' (при прочтении названия слева направо).
6 .16.6.1. Трехбуквенная система обозначений
Трехбуквенные обозначения нуклеозидов представлены в табл. 6.60. Перед обозначениями дезоксирибо-зильных производных добавляется буква «d» (dAdo). Если перед символом нуклеозида стоит буква «х» или «1», то это указывает на замену сахарного остатка соответственно на ксилозу или ликсозу.
* Иногда во избежание путаницы для производных рибозы добавляют префикс «г», который может стоять как перед отдельным остатком, так и перед целой серией нуклеотидов.
Современная номенклатура органических соединений
1173
Нуклеотиды по этой системе обозначений записываются либо в виде «нуклеозид-локант-Р», либо «Р-локант-нуклеозид», где курсивной заглавной буквой «Р» обозначается фосфатная группа, например, Guo-3'-/’ или Р-З'-Guo для гуанозин-3'-фосфата. Названия циклических фосфодиэфиров содержат локанты обоих атомов, к которым присоединена фосфатная ipynna,
например, Ado-3':5'-/’ или /’-3':5'-Ado (соответсвующий дифосфат имеет вид Ado-3':5'-/’?).
Если в олигонуклеотиде некоторые нуклеозиды присоединены к фосфатным группам не по типу 3'-»5', то места соединения должны быть указаны дополнительными локантами, располагающимися перед фосфатной группой и после нее, например Xao-2'/’5'-rThd-2'P.
4
4,5-Дидегидро-15,5-ретро-дезоксиретинол (ангидровитамин А) англ.: 4,5-Didehydro-15,5-retro-deoxyretinol (anhydro vitamin А)
Рис. 6.16.73
Таблица 6.60
Пурины, пиримидины, нуклеозиды и их буквенные обозначения а)
Азотистое основание Нуклеозид
Формула Название и трех- и однобуквенные обозначения
Аденин (adenine) nh2 1 ЛА Ji NH N 4 9 3 Ade nh2 7N HO. c. 9 3 4 lv J/1 HV"HH OH R R = OH Аденозин (adenosine) Ado (А)
R = H Дезоксиаденозин (deoxyadenosine) dAdo (dA)
Гуанин (guanine) о II 7 1 J4. о hn Г Js Р- NH H*N2N3 4 9 Gua 0 7 1 N NH |i II JZ H%5 .o^n^n^nh2 4kj HJF^TH OH R R OH Гуанозин (guanosine) Guo (G)
R= H Дезоксигуанозин (deoxy guanosine) dGuo (dG)
Ксантин (xanthine) о II 7 1 Js. ✓N. Q HN Y Us Ji NH n;4 9 H3 Xan 0 7 sA 1 N if NH II II [2 H0Y 4Kj OH R R = OH Ксантозин (xanthosine) Хао (X)
R = H Дезоксиксантозин (deoxyxanthosine) dXao (dX)
Гипоксантин (hypoxanthine) 0 1 JU^N. HN Y 2^ U NH N3 4 9 Hyp 0 7 5 UL1 N T| NH НО 8\ /A -^2 W “ н]Г"Ян OH R R = OH Инозин (inosine) Ino (I)
R = H Дезоксиинозин (deoxyinosine) dlno (di)
1174
Новый справочник химика и технолога
Окончание табл. 6.60
Азотистое основание Нуклеозид
Формула Название и трех- и однобуквенные обозначения
Урацил (uracil) О зА HN |15 6 Н1 U га О 3 JU HN J]5 R = OH Уридин (uridine) Urd (U)
HO. 0 2 ^l5 ✓Ox. H H |3’ 2^ OH R H R = H Дезоксиуридин (deoxyuridine) dUrd (dU)
Тимин (thymine) о 3 ✓СНз НУ |Т^ oH>n:; 6 н1 Thy 0 3 HN HO. ,, 0<2^N hTF"2TH OH R t/СНз It Д R OH Рибозилтимин (ribosylthymine) Thd (T)
R = H Тимидин (thymidine) dThd (dT)
Цитозин (cytosine) nh2 3 ✓-U. ||5 6 н1 Cyt nh2 R = OH Цитидин (cytidine) Cyd (C)
но. 0 2 OH R ✓^6 Nl J1' R = H Дезоксицитидин (deoxycytidine) dCyd (dC)
Оротат (orotate) о 3 .JU HN >5 .1 o'x2'n; co2 H1 Oro О 3 HN HO. O^'N ^l5 ✓Ox. 4Kj l/ 1 hV/h OH R * H ^со2 R = OH Оротидин (orotidine) Ord (0)
R = H Дезоксиоротидин (deoxyorotidine) dOrd (dO)
а) Неизвестное пуриновое основание обозначается «Риг», а пиримидиновое основание — «Руг»; неизвестный пуриновый нуклеозид обозначается «Рио», а пиримидиновый нуклеозид — «Pyd»; рибозил никотинамид обозначается «Nir».
6 .16.6.2. Однобуквенная система обозначений
Однобуквенные символы рибонуклеозидов, представленные в табл. 6.60, представляют собой первую заглавную букву названия соединения*. В 2'-дезокси-производных впереди добавляется буква «d». Если перед символом нуклеозида уже стоят какие-либо буквенные префиксы, например защитных групп, и добаление «дезокси»-префикса может внести путаницу, то букву «d» пишут подстрочным индексом, например, -bzAd- для N 6-бензоиладенозильного фрагмента полинуклеотида.
* А — аденозин, В — 5-бромуридин, С — цитидин, D — 5,6-дигидроуридин, G — гуанозин, I — инозин, О — ороти-дин, S — тиоуридин, U — уридин, X — ксантозин, Т — псевдоуридин, R — неустановленный пуриновый нуклеозид, Y — неустановленный пиримидиновый нуклеозид.
Однобуквенные символы рибонуклеозидов используются в сокращенных обозначениях монорибонуклеотидов, например 2'-UMP для уридин-2'-фосфата. Первая буква обозначает нуклеозид, вторая — количество фосфатных групп (М — моно, D — ди, Т — три), а третья буква «Р» означает фосфат (phosphate). Дезоксирибонуклеотиды записываются аналогичным способом с добавлением впереди буквы «d», например см. рис. 6.16.74.
Форма записи олиго- и полинуклеотидов включает в себя перечисление через дефис однобуквенных символов нуклеозидов, последовательно связанных между собой посредством фосфатных групп. Моноэтерифици-рованная фосфатная группа, находящаяся на конце цепи, обозначается буквой «р». «Внутренние» диэтери-фицированные фосфатные группы обозначаются дефисом, если соотвегсвующие нуклеозиды соединены по типу 3'—>5'. Другими словами, дефис в нуклеотидном
Современная номенклатура органических соединений
1175
фрагменте A-dG обозначает фосфатную группу, присоединенную к атому углерода С-3' аденозина (слева) и к атому углерода С-5' дезоксигуанозина (справа). Если последовательность соединения нуклеозидов неизвестна, то соединительные фосфатные группы обозначаются запятой. Неизвестные последовательности, примыкающие к известным, выделяются круглыми скобками. Для других способов соединения дефисы заменяются на цифровые обозначения, например, 2'-5' (или 2'р5'). В качестве примера приведем запись декануклеотида pG-C-A(C2U)T-A2'p5'C-C, согласно которой он начинается с 5'-фосфорилированного гуанозина, заканчивается нефосфорилированным цитидином и содержит между аденозином и тимидином тринуклеотид C2U с неизвестной последовательностью соединения. Все нуклеозиды цепи соединены по типу 3'-5', кроме восьмого и девятого нуклеозидов, между которыми связь 2'-5'.
Кодоновые триплеты нуклеотидов с определенной последовательностью соединения и подразумеваемым 3'-5'-фосфатным связыванием нуклеозидов могут записываться без дополнительной пунктуации, как, например, триплет CAT, кодирующий гистидин.
6.16.7. Порфирины
6.16.7.1. Систематические названия порфиринов
Систематические названия циклических тетрапирролов, их производных и гетероатомных аналогов в принципе могут быть построены на основе единого родоначального названия «порфирин»*, которому соответствует первая структура в табл. 6.61.
Однако правилами IUPAC сохранены еще несколько родоначальных структур (табл. 6.61) для наименования ряда гидрированных (хлорин, бактериохлорин, порфириноген), бензоконденсированных (фталоцианин), норпроизводных* (коррин, коррол) порфиринов, а также ациклических пентапирролов (сапфирин). В табл. 6.61, кроме того, перечислены родоначальные названия ациклических тетра-, три- и дипирролов.
Сами порфирины являются соединениями, содержащими циклическую тетрапиррольную систему (в табл. 6.61 также представлена принятая IUPAC нумерация порфиринового кольца). Эти соединения представляют собой «дигидросистемы», содержащие на одну двойную связь меньше, чем максимально ненасыщенный аналог. Вследствие таутомерии атомы водорода могут быть присоединены к любым двум из четырех атомов азота порфириновой системы. Если нет особого указания на существование определенной таутомерной формы, то с позиции номенклатуры подразумевается, что spy гибри-дизованные атомы азота имеют локанты 21 и 23. Положения 1,4, 6, 9, 11, 14, 16 и 19 часто называют «а-поло-
* Наряду с названием «порфирин» также широко используется термин «порфин», являющийся его синонимом.
* Префикс «нор» в данном случае означает удаление =СН-фрагмента.
жениями» (по a-положению пиррольного кольца). Аналогично положения 2, 3, 7, 8, 12, 13, 17 и 18 называют «^-положениями», а 5, 10, 15 и 20 — «л/езо-положе-ниями». Однако во избежание двусмысленности (буквы а и Р используются также как стереодескрипторы) употребление данных терминов в этом контексте не рекомендуется.
6.16.7.2. Замещенные порфирины
Порфирины, содержащие заместители в кольце, называют в соответствии с общими правилами заместительной номенклатуры. Если есть выбор начала и направления нумерации в порфириновом ядре, то его нумеруют так, чтобы наименьшие локанты последовательно получили:
1) «обозначенный водород»;
2) старшая функциональная суффиксная группа;
3) префиксные заместители и «гидро»-префиксы, рассматриваемые вместе в рамках единого наименьшего набора локантов (см. подразд. 6.1.3.1);
4) префиксные заместители, идущие первыми по алфавиту (рис. 6.16.75).
В последнем примере главной функциональной группой, записываемой в суффикс, является карбоксильная, т. к. она стоит раньше в табл. 6.7, чем сложноэфирная.
6.16.7.3. Конденсированные порфирины
Среди природных порфиринов довольно часто встречаются соединения с дополнительными циклами, конденсированными с порфириновым ядром. Если в соединении с порфириновым ядром сконденсированы карбоциклы, то его название образуют по правилам, рассмотренным в подразд. 6.2.5.2 с учетом того, что главным циклом является порфириновый с нумерацией, указанной в табл. 6.61. Атомы карбоциклов получают локанты с надстрочными индексами, начиная с атома, ближайшего к узловому порфириновому атому с наименьшим локантом. Тетрабензо[6,£,/,<7]порфирин, который разрешается записывать просто как тетрабензопорфирин, имеет нумерацию атомов, представленную ниже на схеме 6.11.
Дигидропроизводное циклопента[дД порфирина, изображенного последним на вышеприведенной схеме, имеет тривиальное название «форбин» («phorbine»), нумерация и принятая ориентация молекулы которого отличается от систематической, см. рис. 6.16.76.
Форбин англ.: Phorbine
Рис. 6.16.76
1176
Новый справочник химика и технолога
О
Гуанозин-З'-фосфат (З'-GMP) англ.: Guanosine-3-phosphate
Аденозин-5-фосфат (5'-АМР) англ.: Adenosine-5'-phosphate
Аденозин-3',5'-циклофосфат (сАМР) Тимидин-5'-дифосфат (5'-dTDP) англ.: Adenosine-3',5’-cyclophosphate англ.: Thymidine-5-diphosphate
Рис. 6.16.74
3,8,13,18-Тетраметил-2,7,12,17-тетраэтил порфир ин
англ.'. 2,7,1 2,17-Tetraethyl-3,8,13,18-tetramethylporphyrin
8,18-Ди метил-2,12,17-триэтил-7,13-бис(этоксикарбонил)-3-[2-(этоксикарбонил)этил]-порфирин-5-уксусная кислота
англ.: 2,12,17-Triethyl-7,13-bis(ethoxycarbonyl)-3-[2-
(ethoxycartoony l)ethy l]-8,18-dimethylporphyrin-5-acetic acid
Рис. 6.16.75
Современная номенклатура органических соединений
1177
Таблица 6.61
Родоначальные названия порфиринов и их аналогов
2 d f /8 аХ—NH №=Z/7 / 21 22 А 20<\s i//10 V? 24 23 i/J HN/\ 18 px° Mm ^12 4 17 15 13 Порфирин (porphyrin) 3 5 7 2\ 1 n /8 X—NH N—Л Л' 21 22 W 20 V у Ю \ 24 23 Z. 1v==:N HN-Xy1 18X k. >12 17 15 13 Хлорин (chlorin) 2< / л /8 iV NH N=/9 /21 22 \ 20 \\ //10 V 24 23 П HN-^V1 18 X Jk zZ12 \Zi6X^l4\Z 17 15 13 Бактериохлорин (bacteriochlorin)
3 5 7 2€ / \ #8 X—-NH HN—У9 /21 22 \ 20 < /Ю \ 24 23 / 1y-NH HN-"W1 18< >k 712 XZi6\/l4^< 17 15 13 Порфириноген (porphyrinogen) 24 25 1^ 23 h \ 27 II)3 Л /k^N^^y Jj 22 \ 2X=n hn-У5 /30 29 \ 20 Nv ,N6 31 32 f/. 1^T-NH N-"y 18 Z J/ П \r<4^N<2^Z A 17\ J 13 V=^z9 1Г15 11 Ю Фталоцианин (phthalocyanine) A-nh n=/9 24/ 25 26 X гэг^Хгэ Д10 I NH 27 >(11 24 7?/ HN />12 21 \ 28 \ IJ 2ок*/к _Z14 13 19V—X^5 18 17 Сапфирин (sapphyrin)
3 5 7 /X'-zAZA 2\l \ /8 X—NH N=Z 21 22 \ />10 24 23 1y-—NH N^y1 «к JL >12 xz'ie'b^14 ' 17 15 13 Коррин (corrin) 3 5 7 2< / л 78 X--NH HN—(9 21 22 yio 24 23 / 1y=N HN-^J1 ю4 L. >k >12 17 15 13 Коррол (corrole)
2 3 7 8 12 13 17 18 .ГМ111Д. N 6 n'’’9'4x114N H21 5 N22 10 {-|23 15 P)24 Билан (bilane) 2 3 7 8 12 13 17 18 -СХХккХЛ- Билин (bilin)
2 3 7 8 12 13 Трипиррин (tripyrrin) 2 3 7 8 iCk >0 10 H11 Дипиррин (dipyrrin)
Т етрабензопорфирин англ.: Tetrabenzoporphyrin
Циклопента[а(]порфирин англ.: Cyclopenta[af]porphyrin
Схема 6.11
1178
Новый справочник химика и технолога
6.16.7.4. Порфирины с гетероатомами
Порфирины, у которых атомы углерода или азота заменены на гетероатом, называют с использованием «а»-номенклатуры. Замена одной >1ЧН-группы двухвалентным гстероатомом приводит к структуре только с одним насыщенным атомом азота. Такая структура более не рассматривается как дигидросистема с соответствующей нумерацией с закрепленными наименьшими локантами на насыщенных атомах азота, а называется с использованием «обозначенного водорода» с учетом старшинства гетероатомов по системе Ганча — Видмана (2-й из нижеприведенных примеров) (рис. 6.16.77).
6.16.7.5. Восстановленные порфирины
Наиболее часто встречаются гидрированные порфирины, в которых атомы водорода присоединены к неузловым атомам углерода. 2,3-Дигидропорфирин, являющийся родоначальным соединением для дигидропорфиринов, имеет название «хлорин» («chlorin») (табл. 6.61). Тетрагидропорфирины с насыщенными атомами углерода в диагональных пиррольных кольцах являются производными бактериохлорина; если эти атомы углерода находятся в соседних кольцах, то родоначальный порфирин называется «изобактериохлорин». Названия гексагидропорфиринов, в которых все атомы азота и четыре .мезо-углсрода являются насыщенными, записывают, используя родоначальное название «порфириноген». Более гидрированные производные, а также иные, чем вышеперечисленные гидрированные незамещенные порфириновые системы рекомендуется называть как гидропорфирины, например см. рис. 6.16.78.
Замещенные производные с частично гидрированными порфирированными кольцами хлорина, бактериохлорина, изобактериохлорина и порфириногена называют по заместительной номенклатуре, используя эти родоначальные названия с указанием заместителей с помощью соответствующих префиксов и/или суффиксов, см. рис. 6.16.79.
6.16.7.6. Тривиальные и полусистематические названия порфиринов
Помимо систематических названий замещенных порфиринов, хлоринов и других аналогов широко используются устоявшиеся тривиальные названия некоторых замещенных производных этих соединений. Тривиальные названия замещенных порфиринов и замещенных хлоринов (соответствуют 17,18-дигидропроизводным порфиринов, названным по тривиальной номенклатуре) перечислены в табл. 6.62. В качестве примеров ниже изображены структуры и тривиальная нумерация атомов пирропорфирина и родохлорина (рис. 6.16.80).
Следует иметь в виду, что нумерация атомов в тривиальном и систематическом названиях не совпадает. Ниже для сравнения приведена систематическая нумерация атомов этих же соединений (рис. 6.16.81).
Три соединения в табл. 6.62, а именно, копропорфи-рин, этиопорфирин и уропорфирин имеют дополнительные обозначения в виде римских цифр. Каждое из этих производных имеет четыре одинаковые пары заместителей, которые расположены в порфириновом кольце так, что каждое пиррольное кольцо содержит заместители обоих типов. Такому замещению порфиринового ядра соответствуют еще три позиционных изомера упомянутых соединений, которые имеют такие же тривиальные названия, но отличаются римской нумерацией. Ниже изображен порядок замещения порфиринового ядра в изомерах I, II, III и IV, с учетом того, что заместитель R1 меньше, чем К2(табл. 6.62), см. рис. 6.16.82.
Соединения, имеющие такой же характер замещения порфиринового ядра, как и порфирины из табл. 6.61, но отличающиеся от них заменой одного или нескольких атомов водорода на другие атомы или функциональные группы, можно называть по полусистематичс-ской номенклатуре, используя тривиальные названия замещенных производных и соответствующие префиксы и/или суффиксы дополнительно введенных заместителей. Если появляется выбор между несколькими тривиальными названиями, то за основу полусистематического названия берут порфирин, стоящий раньше в табл. 6.61 (аналогично и для хлоринов), см. рис. 6.16.83а и 6.16.836.
2Н-5-Т иа-15-азапорфирин
англ.-. 2/-/-5-Thia-15-azaporphyrin
23/-/-21-Оксапорфирин англ.'. 23Н-21 -Oxaporphyrin
Рис. 6.16.77
Современная номенклатура органических соединений
1179
5,22-Дигидропорфирин, флорин (устар.)
англ.: 5,22-Dihydroporphyrin, phlorin
5,15-Дигидропорфирин, порфодиметен (устар.) англ.: 5,15-Dihydroporphyrin, porphodimethene
Рис. 6.16.78
(25,35)-8-Винил-18-карбокси-3,7,12,17,20-пента-метил-13-этилхлорин-2-пропионовая кислота
англ.: (2S,3S)-18-Carboxy-13-ethyl-3,7,12,17,20-
pentamethyl-8-vinylchlorin-2-propionic acid
Рис. 6.16.79
Пирропорфирин англ.: Pyrroporphyrin
Родохлорин англ.: Rhodochlorin
Рис. 6.16.80
1180
Новый справочник химика и технолога
(28,38)-3,7,12,17-Тетраметил-8,13-
диэтилхлорин-2-пропионовая
кислота (родохлорин)
англ.: (2S,3S)-8,13-Diethy 1-3,7,12,17-
tetramethylchlorin-
2-propionic acid
3,7,12,17-T етра метил-8,13-д иэти л порфи ринг-пропионовая кислота (пирропорфирин) англ.: 8,13-DiethyI-3,7,12,17-tetramethylporphyrin-
2-propionic acid
Рис. 6.16.81
но2с
6
NH
22
16
со2н
23
HN
24
N
15-Метилродопорфирин (полусист.), 18-карбо кси-3,7,12,17,20-пентаметил-8,13-диэтилпорфирин-2-пропионовая кислота (сист.)
англ.-. 15-Methylrhodoporphyrin,
18-carboxy-8,13-diethyl-3,7,12,17,20-pentamethylporphyrin-2-propionic acid
Рис. 6.16.83a
Современная номенклатура органических соединений
1181
19
НО2С
22
18
16
NH
2
23
HN
24
N
со2н
151
Филлопорфирин-151-овая кислота (полусист.), 20-карбокси-3,7,12,17-тетраметил-8,13-диэтилпорфирин-2-пропионовая кислота (сист.) англ.-. Phylloporphyrin-15'l-oic acid, 20-carboxy-8,13-diethy l-3,7,12,17-tetramethylporphyrin-2-propionic acid
Рис. 6.16.836
Таблица 6.62
Тривиальные названия замещенных порфиринов и хлоринов
Название Заместители и локанты
2 3 7 8 12 13 15 17 18
Порфирины
Дейтеропорфирин Me H Me И Me (CH2)2CO2H H (CH2)2CO2H Me
Пирронорфирин Me Et Me Et Me H H (CH2)2CO2H Me
Этиопорфирин I Me Et Me Et Me Et H Me Et
Филлопорфирин Me Et Me Et Me H Me (CH2)2CO2H Me
Родопорфирин Me Et Me Et Me CO2H H (CH2)2CO2H Me
Протопорфирин Me CH=CH2 Me CH=CH2 Me (CH2)2CO2H H (CH2)2CO2H Me
Мезопорфирин Me Et Me Et Me (CH2)2CO2H H (CH2)2CO2H Me
Гематопорфирин Me CH(OH)CH3 Me CH(OH)CH3 Me (CH2)2CO2H H (CH2)2CO2H Me
Копропорфирин I Me CH2)2CO2H Me (CH2)2CO2H Me (CH2)2CO2H H Me (CH2)2CO2H
Уропорфирин I CH2CO2H (CH2)2CO2H CH2CO2H (CH2)2CO2H CH2CO2H (CH2)2CO2H H CH2CO2H (CH2)2CO2H
Цитопорфирин Me R* Me CH=CH2 Me (CH2)2CO2H H (CH2)2CO2H CHO
Фитопорфирин Me Et Me Et Me —C(O>—CE •2 (CH2)2CO2H Me
Хлорины
Пиррохлорин Me Et Me Et Me H H (снжсадн Me, H
Филлохлорин Me Et Me Et Me H Me (Сн^садн Me, H
Родохлорин Me Et Me Et Me CO2H H (ОШВДН Me, H
Фитохлорин Me Et Me Et Me -C(O)-CE 2 (CH2)2CO2H. н Me, H
6.17. Металлорганические соединения
Металлорганическими (элементорганическими) соединениями называют соединения, в которых имеется по крайней мере одна связь между атомом органической молекулы, иона или радикала и атомом металла. При составлении названий таких соединений используются комбинации номенклатуры органических со
единений, рассматриваемой в данном разделе, и номенклатуры неорганической химии, включая бинарную, заместительную и координационную.
6.17.1. Заместительная номенклатура
металлорганических соединений
Заместительная номенклатура используется при наименовании металлорганических соединений элементов
1182
Новый справочник химика и технолога
III A, IVA, VA и VIA групп. Эти соединения называют по обычным правилам заместительной номенклатуры, используя название соответствующего родоначального гидрида (табл. 6.2) в качестве основы (рис. 6.17.1).
Металлорганические соединения с двойной связью между элементами основных групп могут быть названы подобно алкенам.
Ч V Т етраизопропилдисилен
__^|—англ.-. Tetraisopropyldisilene
Металлорганические соединения элементов других групп, в которых металл соединен только с атомом углерода органического заместителя и водородом, называют, перечисляя в алфавитном порядке перед названием металла префиксы заместителей и префикс «гидридо» («hydrido»), при необходимости с умножающими приставками (согласно правилам IUPAC 1993 г. для Sb, Bi, Се. Sn, Pb названия на основе соответствующих гидридов являются более предпочтительными).
Металлорганические соединения, содержащие анионные лиганды, могут быть названы путем перечисления: 1) названий замещающих органических групп (в алфавитном порядке); 2) названия металла; 3) названий анионных лигандов (в алфавитном порядке). В английских названиях следуют порядку «1, 2, 3», в названиях на русском языке используют порядок «1, 2, 3» или «3, 2, 1». Водород может быть включен как в число замещающих групп, так и в число анионных лигандов. Другой вариант наименования таких соединений, принятый в номенклатуре неорганических соединений, заключается в перечислении всех анионных лигандов перед названием металла (рис. 6.17.2) (согласно правилам IUPAC 1993 г. для Sb, Bi, Ge, Sn, Pb названия на основе соответствующих гидридов являются более предпочтительными).
6.17.2. Координационная номенклатура металлорга-нических соединений переходных металлов*
В линейных формулах координационных соединений сначала указывается центральный атом**, за которым в алфавитном порядке перечисляются анионные лиганды, а затем нейтральные. Полиатомные лиганды и сокращения, используемые для обозначения лигандов, приводятся в круглых скобках, а вся формула заключается в квадратные скобки, например: [1гС1Н2(СО){Р(СН3)3}2].***
* В данном разделе не рассматриваются детали номенклатуры неорганических координационных соединений [32], которая лежит в основе координационной номенклатуры ме-таллорганических соединений.
Центральным атомом является атом металла, к которому присоединены другие атомы и группы, называемые лигандами.
В сложных группах, если внешние скобки используются для всего комплекса, руководствуются следующим порядком «старшинства» скобок: [{()}].
В названии координационного соединения лиганды перечисляются в алфавитном порядке (независимо от их заряда) перед названием центрального атома. Умножающие приставки не учитываются при определении алфавитного порядка. В ионных соединениях катионы приводятся перед анионами. При необходимости можно указать заряд молекулы с помощью арабской цифры (с соответствующим знаком) в круглых скобках, которые помещаются сразу после названия центрального атома, например: [IrBrH2(CO)(PPh3)2] бромдигидридо-карбонилбис(трифенилфосфан)иридий / bromocarbonyl-dihydridobis(triphenylphosphane)iridium.
Бутиллитий англ.-. Butyllithium
Аллилнатрий англ.: Allylsodium
Дигидридоциклогексилалюминий англ.: Cyclohexyldihydridoaluminium
6.17.2.1. Названия органических лигандов
Лиганды, координированные одной простой связью металл—углерод
В координационной номенклатуре органические лиганды, соединенные с центральным атомом одной простой связью, при формировании названий могут рассматриваться как анионные (аддитивные названия) или радикальные (заместительные названия).
Названия анионных лигандов образуют, заменяя суффиксы «-ид» («-ide»), «-ит» («-ite») или «-ат» («-ate») в названиях анионов, формально получающихся при отщеплении протона от нейтральной молекулы (см. подразд. 6.12.3.1) на соответственно «-идо» («-ido»), «-ито» («-ito») или «-ато» («-ato»). Подобным образом образуют названия органических анионных лигандов, которые координированы с центральным атомом через гетероатом, например: СН3СОО — «ацетато» («acetato»), (CH3)2N — «диметиламидо» («dimethylamido»). Названия нейтральных и катионных лигандов используются без модификации. В табл. 6.63 приведены систематические и традиционные названия часто встречающихся в металлорганических соединениях органических и «неорганических» лигандов с элементами IVA-VIIA групп.
При наименовании лигандов как радикальных заместителей для них используются названия соответствующих радикалов, полученных при формальном отщеплении атома водорода от соответствующего родоначального гидрида (подразд. 6.12.1.1) или названия соответствующих замещающих групп (табл. 6.5) (рис. 6.17.3).
Современная номенклатура органических соединений
1183
Дициклопропилборан Метил(фенил)(циклопропил)этилгерман
англ.-. Dicyclopropylborane англ.: Cyclopropyl(ethyl)(methyl)phenylgermane
Тетра(и-толил)плюмбан или тетра(4-метилфенил)плюмбан англ.-. Tetra(p-tolyl)plumbane или
tetra(4-methylphenyl)plumbane
Дихлортриэтил-Х5-стибан, дихлортриэтилстиборан (трад.) англ.: Dichlorotriethyl-A.5-stibane, dichlorotriethylstiborane (трад.)
Рис. 6.17.1
Этилмагния хлорид, хлор(этил)магний англ. : Ethylmagnesium chloride, chloro(ethyl)magnesium
Хлорид гидридо(фенил)сурьмы, (фенил)сурьмы гидрид-хлорид, гидридо(фенил)хлорсурьма, фенилхлорстибан
англ.: Hydrido(phenyl)antimony chloride, phenylantimony chloride hydride, chloro(hydrido)phenylantimony, chloro(phenyl)stibane
Хлор(этил)станнан, этилолова дигидрид-хлорид, дигидридо(этил)олова хлорид, дигидридохлор(этил)олово
англ.: Chloro(ethyl)stannane ethyltin chloride dihydride ethyldihydridotin chloride Chloro(ethyl)dihydridotin
Рис. 6.17.2
Таблица 6.63
Названия лигандов элементов групп IVA-VIIA
Формула Систематическое название Альтернативное название
СГ Хлоридо (chlorido) Хлоро (chloro)
Вг Бромидо (bromido) Бромо (bromo)
Г Иодидо (iodido) Иодо (iodo)
О2’ Оксидо (oxido) Оксо (охо)
s2~ Сульфиде (sulfido) Тио (thio)
Н2О Оксидан (oxidane) Аква (aqua)
1184
Новый справочник химика и технолога
Окончание табл. 6.63
Формула Систематическое название Альтернативное название
ОН" Гидроксидо (hydroxide) Гидроксо (hydroxo)
(СН3О)- Метанолято (methanolato) Метоксиде (methoxide)
(С2Н5О)- Этанолято (ethanolato) Этоксидо (ethoxide)
(С6Н5О)- Фенолято (phenolato) Феноксидо (phenoxido)
(C6H5S)- Бензолтиолято (benzenethiolato) Фенилсульфидо (phenylsulfido)
(нсо2) Метаноато (methanoato) Формате (formato)
(СН3СО2)- Этаноато (ethanoato) Ацетате (acetato)
n2 Диазот (dinitrogen)
N3" Нитридо (nitrido)
Рз Фосфидо (phosphide)
NH3 Азан (azane) Аммин (ammine)
РН3 Фосфан (phosphane) Фосфин (phosphine)
(NH2) Азанидо (azanido) Амидо (amido)
(NH)2 Азандиидо (azanediido) Имидо (imido)
ch3nh2 Метанамин (methanamine) Метиламин (methylamine)
(CH3)2NH А-Метилметанамин (A-methylmethanamine) Диметиламин (dimethylamine)
(CH3)3N N, А-Диметилметанамин (AA-dimethylmethanamine) Триметиламин (trimethylamine)
CH3PH2 Метилфосфан (methylphosphane) Метилфосфин (methylphosphine)
(CH3)2PH Диметилфосфан (dimethylphosphane) Диметилфосфин (dimethylphosphine)
(CH3)3P Триметилфосфан (trimethylphosphane) Триметилфосфин (trimethylphosphine)
(CH3N)2- Метанаминато(2-) [methanaminato(2-)] Метилимидо (methylimido)
[(CH3)2N] А-Метилметанаминато (A-methylmethanaminato) Диметиламидо (dimethylamido)
[(CH3)2P]- Диметилфосфанидо (dimethylphosphanido) Диметилфосфанил (dimethylphosphanyl)
(CH3P)2' Метилфосфандиидо (methylphosphanediido) Метилфосфандиил (methylphosphanediyl)
(CH3PH) Метилфосфанидо (methylphosphanido) Метилфосфино (methylphosphino)
(NO2)- Диоксонитрато(1-)-кО [dioxonitrato( 1-)-кО] или диоксонитрато (1-)-кА [dioxonitrato(l-)-KA] Нитрито-0 (nitrito-O), нитрито-А (nitrito-A), нитро (nitro)
(NO3)- Триоксонитрато( 1 -) [trioxonitrato( 1 -)] Нитрате (nitrate)
NO Азота монооксид (nitrogen monoxide) Нигрозил (nitrosyl)
CO Углерода монооксид (carbon monoxide) Карбонил (carbonyl)
CO2 Углерода диоксид (carbon dioxide)
CS Углерода моносульфид (carbon monosulfide) Тиокарбонил (thiocarbonyl)
CN" Цианиде (cyanide) Циано (cyano)
Современная номенклатура органических соединений
1185
Бромид тетрааммин(диметил)осмия(1 +) англ.: Tetraammine(dimethyl)osmium(1+) bromide
[Os(CH3)2(NH3)4]Br
Бицикло[2.1.1]гексан-5-ил(трициклопропил)хром англ.: Вicyclo[2.1.1 ]hexan-5-yl(tricyclopropyl)chromium
rpt/r н vru rnwpph \ 1 Ацетилбис(трифенилфосфан)этилплатина
LHT(G2M5)(GM3GU)iHHn3)2J ямгл.: Acetyl(ethyl)bis(triphenylphosphane)platinum
Li[Cu(C2H5)2]
Диэтилкупрат(1-) лития англ.: Litium diethylcuprate(l-)
Рис. 6.17.3
Лиганды, координированные несколькими простыми связями металл—углерод
Заместительные названия таких органических лигандов представляют собой названия соответствующих замещающих групп с несколькими свободными валентностями, образованные по правилам, описанным в табл. 6.5, или названия соответствующих поливалентных радикалов (подразд. 6.12.1.2). Аддитивные названия органических лигандов образуют, используя суффиксы «-диидо» («-diido») и «-гриидо» («-triido»).
Для того, чтобы отличать лиганды, образующие мостики между атомами металлов, от «хелатирующих»* лигандов, соединенных с центральным атомом несколькими простыми связями, используются ц- и г|-обоз-начения.
Мостиковые лиганды обозначают греческой буквой ц, которую помещают перед названием лиганда. Если возникает необходимость указать число центров, связываемых мостиковым лигандом, используют подстрочный индекс Цп (п > 2); индекс 2 обычно не указывают. Мостиковые лиганды перечисляют в названии в алфавитном порядке вместе с другими, при этом мостиковые лиганды (в убывающем порядке) помещаются перед таким же немостиковым лигандом, например: ц3-оксо-ц-оксо-триоксо.... Название «метилен» для СН2 используется для мостикового лиганда М-СН2-М, тогда как «метилиден» — для лиганда, связанного с одним атомом металла СН2=М. Для лиганда -^СН имеется три названия: «ц3-метантриил» — для мостикового лиганда, связанного с тремя атомами металла
’ Хелатированием называют координацию более чем одной о-электронной пары донорной группы одного и того же лиганда с одним и тем же центральным атомом. Число донорных групп лиганда, присоединенных к одному и тому же центральному атому, называется дентатностью (бидентатный, тридентатный и т. д.).
(М(М)=СН-М), «ц-метанилилиден» — для мостикового лиганда, связанного с двумя атомами металла (М=СН-М), «метилидин» — для мостикового лиганда, связанного с одним атомом металла (СН^М). Лиганд СН2СН2 как мостиковый называют «ц-этан-1,2-диил», а в том случае, когда оба атома углерода присоединены к одному и тому же атому металла — «г|2-этен». Лиганд >СНСН< как мостиковый называют «ц-этен-1,2-диил» (М-СН=СН-М) или «ц-этандиилиден» (М=СН-СН=М), а в том случае, когда оба атома углерода присоединены к одному и тому же атому металла, — «т|2-этин».
Атомы лиганда, участвующие в образовании хелата, могут быть указаны в названии с помощью локантов свободных валентностей, например бутан-1,4-диил. Второй вариант заключается в использовании сложного локанта «к'\¥т» с греческой буквой «к», например, бу-тандиил-к2С',С 4.* Для лигандов, координированных с центральным атомом только атомами углерода, предпочтительным является первый способ (рис. 6.17.4).
Можно использовать комбинацию упомянутых способов обозначения мест хелатирования (рис. 6.17.5).
Связь металл—металл в названии комплекса указывают с помощью группы символов (М-Мг), где Ми М’ — символы соответствующих элементов, которая помеща-
’ При использовании к-обозначений локант лиганда в виде кпХт помещается после той части названия лиганда, которая обозначает функцию, кольцо, цепь или радикал и в которой находится атом, участвующий в образовании хелата. Положение этого атома в лиганде указывается с помощью надстрочного индекса «т» у символа элемента X. В случае полидентатных лигандов с идентичными атомами, участвующими в образовании связи с центральным атомом, к к-сим-волу добавляют правый надстрочный индекс «п», показывающий число таких атомов. Если в образовании хелата участвуют неэквивалентные атомы полидентатного лиганда, то каждый из них указывается с помощью к-символа, за которым следует курсивный символ элемента.
1186
Новый справочник химика и технолога
ется после названий центральных атомов, но перед зарядом иона. При этом с позиций номенклатуры порядок связи металл—металл не имеет значения (рис. 6.17.6).
При нумерации атомов металлов гетеробиядерных комплексов номер «1» присваивается атому, имеющему более высокий приоритет, при этом нумерация может не соответствовать порядку перечисления металлов в названии. Для указания места координации атома лиганда с определенным центральным атомом используют символ 1кп% т, где 1 — локант центрального атома, к которому присоединен лиганд, п — число эквивалентных атомов лигандов, связанных с данным центральным атомом, X — курсивный символ элемента центрального атома, m — локант атома лиганда, участвующего в координации. В том случае, когда различные атомы одного лиганда связаны с различными центральными атомами, соответствующие символы 1кг\¥'п разделяются двоеточием, например: ц-пропандил-1 кС'^кС2 (образование мостика указывается буквой ц) (рис. 6.17.7).
Лиганды, координированные кратной связью углерод—металл
Названия лигандов, координированных кратной связью углерод — металл, образуют так же, как названия соответствующих замещающих групп с двумя и тремя свободными валентностями (см. табл. 6.5, а также разделы, посвященные соответствующим родоначальным гидридам), используя суффиксы «-илиден» для двойной связи С=М и «-илидин» для тройной связи С=М (рис. 6.17.8).
Если хелатирующий лиганд соединен с центральным атомом простой и кратной связями, то суффиксы перечисляются в порядке «-ил», «-илиден», «-илидин». Наименьший набор локантов относят к свободным валентностям, а если остается выбор, то наименьшие локанты по возможности приписывают последовательно суффиксу «-ил», суффиксу «-илиден», боковым заместителям (рис. 6.17.9).
6.17.2.2. Комплексы с ненасыщенными молекулами или группами (п-комплексы)
Соединения, в которых ненасыщенные лиганды координируются с центральным атомом за счет л-электронов кратных связей, называют с помощью «гапто»-номенклатуры. Топологическое описание связывания между ненасыщенным лигандом и центральным атомом осуществляют, используя символ «г|» (эта). Если все ненасыщенные атомы углерода координированы с металлом, то перед названием соответствующего лиганда через дефис помещают букву «г|». Число координированных атомов углерода можно указать правым надстрочным индексом, например: г|3 = «эта три» или «тригапто», г|4 = «эта четыре» или «тетрагапто» и т. д.
Подобным образом могут быть названы также л-комп-лексы с кратными связями углерод—гетероатом, гетероатом—гетероатом. Названия распространенных органических лигандов в л-комплексах приведены в табл. 6.64.
НгС QH2 р(СН3)3
Н2С Pt
H2W2W)3
(Пентан-1,5-диил)бис(триметилфосфан)платина англ.-. (Pentane-1,5-diyl)bis(trimethylphosphane)platinum
z—(ц-2-Циклопропилэтан-1,1 -диил)бис(пентакарбонилрений) । 2 англ.: (ц-2-Cyclopropylethane-l ,1-diyl)bis(pentacarbonylrhenium)
(OC)5RexCH'Re(CO)5
[2-(Дифенилфосфанил-кР)фенил-кС1]гидридо(триметилфосфан)никель англ.: [2-(Diphenylphosphanyl-KP)phenyl-KC1]hydrido(trimethylphosphane)nikel
Мп (СО)4
[Тетракарбонил[2-(фенилдиазенил-кЛ/2)нафтил-кС1]марганец англ.: Tetracarbonyl[2-(phenyldiazenyl-K/V2)naphtyl-KC1]manganese
Рис. 6.17.4
Современная номенклатура органических соединений
1187
PPh3
Бромогидридо(3-оксо-кО-2-этилпент-1-ен-1-ил)бис(трифенилфосфан)родий англ.: Bromohydrido(2-ethyl-3-oxo-KO-pent-1-en-1-yl)bis(triphenylphosphane)rhodium
Рис. 6.17.5
Н2
Н2С сн2
I I
(0C)40s-----Os(CO)4
(ц-Пропан-1,3-диил)бис(тетракарбонилосмий)(О8-Оз) англ.: (ц-Ргорапе-1,3-diyl)bis(tetracarbonylosmium)(Os-Os)
(СО)з
(цз-З-Метилбутан-1,1,1 -триил)-Л7реуаольно-трис(трикарбонилкобальт)(3 Со-Со)
англ.: (цз-3-Methylbutane-l ,1,1-triy\)-triangulo-
tris(tricarbonylcobalt)(3 Co-Co)
Рис. 6.17.6
4
Н3С. 3 3 хсн2
2 а I
(0С)5Мп>1 СНХ 1
ХС 2 Re(CO)5 н2
Декакарбонил-1 к5С, 2к5С-(ц-бутанди ил-1 кС2:2кС1)марганецрений
англ.: Decacarbonyl-lK5C,2K5C-(p-butanediyl-lKC2:2KC1)manganeserhenium
Рис. 6.17.7
СО
Cl—Cr=C—N^j
ОС (Lq транс-(Азиридин-1-илметилидин)тетракарбонилхлорохром
англ.-. frans-(Aziridin-1-ylmethylidine)tetracarbonylchlorochromium
ON ?РЬз /
,^=с=\
PPh3
Иодо(2-метилпроп-1-ен-1-илиден)нитрозилбис(трифенилфосфан)осмий
англ.: Iodo(2-methylprop-1-en-1-ylidene)nitrosylbis(triphenylphosphane)osmium
Рис. 6.17.8
lr(PEt3)3
(2,5-Диметилпента-1,3-диен-1-ил-5-илиден)трис(триэтилфосфан)иридий англ.: (2,5-Dimethylpenta-1,3-dien-1-yl-5-ylidene)tris(triethylphosphane)iridium
Рис. 6.17.9
1188
Новый справочник химика и технолога
Таблица 6.64
Названия некоторых распространенных органических лигандов в тс-комплексах
Лиганда) Систематическое аддитивное название Систематическое заместительное название Традиционное название
г|3-пропенидо (r|3-propenido) г|3-пропенил Cq3-propenyl) Л3-аллил б) (л3-ally 1)
г|3-(2)-бутенидо (T]3-(2)-butenido) г|3-(2)-бутенил б) r|3-(2)-butenyl)
Л -2-метилпропенидо (•q3-2-methylpropenido) Л -2-метилпропенил (r|3-2-methylpropenyl) Л3-2-метил аллил Cn3-2-methylallyl)
г|4-2-метилиденпропан-1,3-диидо (r|4-2-methylidenepropane-1,3-diido) Л4-2-метилиденпропан-1,3-диил б) (r|4-2-methylidenepropane-1,3 -diyl)
н Л 6-2,3-диметил иденпропан-1,3-ДИИДО (r|6-2,3-dimethylidenepropane-1,3-diido) Л6-2,3-диметилиденпропан-1,3-диил б) (p6-2,3-dimethylidenepropane-l,3-diyl)
г|5-(2,7)-пентадиенидо (r|5-(Z,Z)-pentadienido) Л5-(2,7)-пентадиенил б) (^5-(Z,Z)-pentadienyl)
г|5-циклопентадиенидо (r|5-cyclopentadienido) Л5-циклопентадиенил б) Cn5-cyclopentadienyl)
пентаметил-г|5-цик-лопентадиенидо (pentamethyl-T]5-cyclopentadienido) пентаметил-л 5-цикл опентад иен ил б) (pentamethyl^5-cyclopentadienyl)
г|5-циклогексадиенидо (r|5-cyclohexadienido) Л5-циклогексадиенил б) (r|5-cyclohexadienyl)
7 Л -циклогептатриенидо (г|7-су с loheptatrien ido) Л7-циклогептатриенил б) (r|7-cycloheptatrienyl) Л7-тропилв) (p7-tropyl)
Л 7-циклооктатриенидо (r|7-cyclooctatrienido) Л7-циклооктатриенил ® 0]7-cyclooctatrienyl) Л7-гомотропилв) (r|7-homotropyl)
1 -метил-г| 5-борол б) (1 -methyl-r|5-borol)
г|5-азациклопентадиенидо (ri5-azacyclopentadienido) Л5-пирролил б) (л5-ругго1у1) Л5-азацикло-пентадиенил (r|5-azacyclopentadienyl)
г|5-фосфациклопентадиенидо Cq5-phosphacyclopentadienido) Л5-фосфолилб) Cq5-phospholyl) Л5-фосфаци-клопентадиенил Cq5-ph°spha-cyclopentadienyl)
е Л5-арсациклопентадиенидо (r|5-arsacyclopentadienido) Л5-арсолил б) (r|5-arsolyl) Л5-арсацикло-пентадиенил (Л5-агзасус1о-pentadienyl)
От А г|6-боринин-1 -идо (r|6-borinine-1 -ido) Л6-боратабензол б) (jr|6-boratabenzcnc)
а) Дуга в формулах показывает делокализацию по аналогии с кружком в бензольном кольце.
б) Предпочтительное название.
в) При рассмотрении этого лиганда как катиона добавляется окончание «ий» («ium»).
Современная номенклатура органических соединений
1189
Символ «г|» предшествует названию лиганда или той части лиганда, которая участвует в образовании л-комплекса (рис. 6.17.10).
При необходимости перед символом г| указывают локанты атомов, участвующих в образовании комплекса, например, (1 -4т|) (рис. 6.17.11).
При необходимости символы г| могут комбинироваться в названии с символами «ц» и «к», применение которых описано выше (рис. 6.17.12).
6.17.2.3. Металлоценовая номенклатура
Металлоценовая номенклатура применяется для наименования соединений, имеющих строение «бис(г|5-циклопентадиенил)металл», в которых металл относится к ^-элементам, а циклопентадиенильные кольца являются почти копланарными. Название таких соединений образуют из названия соответствующего металла путем использования окончания «-оцен» («-ocene»): Fe — ферроцен (ferrocene), Ru — рутено-цен (ruthenocene), Os — осмоцен (osmocene), V — ва-надоцен (vanadocene), Cr — хромоцен (chromocene), Со — кобальтоцен (cobaltocene) и Ni — никелоцен (nickelocene).
Металлоценовая номенклатура неприменима в тех случаях, когда не выполнены вышеприведенные условия, например, в случае s- и /2-элементов — Ва(С5Н5)2, Sn(C5H5)2; название титаноцен может привести к неправильной интерпретации, т. к. имеется несколько изомеров TiC|OHio, не имеющих «правильной» сэндвичевой структуры, и т. д.
Производные металлоценов могут быть названы с использованием стандартной заместительной номенклатуры. Для первого кольца используются локанты 1-5, для второго — Г-5'. При рассмотрении металлоценового фрагмента как замещающей группы используют суффиксы из табл. 6.5 (рис. 6.17.13).
Хотя соли металлоценов традиционно называют метал лоцениевыми(и+) [metal 1осепшт(и+)] солями, суффикс «-ий» («-ium») имеет иной смысл, чем в заместительной номенклатуре органических катионов, где он обозначает присоединение протона к нейтральной молекуле. Поэтому металлоценисвые катионы, получающиеся при формальном окислении, чтобы избежать неопределенности, лучше называть бис(г|5-циклопента-диенил)металл(и+) вместо металлоцсний(и+) (рис. 6.17.14).
Циклопента-2,4-Диен-1-ил-г|2-этен англ.-. Cyclopenta-2,4-dien-1 -yl-r|2-ethene
М
Винил-г|5-циклопентадиенил
англ.-. Vinyl-r|5-cyclopentadienyl
Рис. 6.17.10
Трис(г|3-алл ил)хром англ.-. Tris(r|3-allyl)chromium
f?PH3
о Leo
""OSv. о
н^\н I СО Дикарбонилбис(трифенилфосфан)(г| -формальдегид)осмий ррНз англ.: Dicarbonyl(r|2-formaldehyde)bis(triphenylphosphane)osmium
[(1,2,5,6г|)-Циклооктатетраен](г|5-циклопентадиенил)кобальт англ.: [(1,2,5,6r|)-Cyclooctatetraene](r|5-cyclopentadienyl)cobalt
1 2
[(1-Зг|)-Бут-2-ен-1-ил-4-илиден]карбонил(г|5-циклопентадиенил)хром англ.: [(1-3r|)-But-2-en-1-yl-4-ylidene]carbonyl(r|5-cyclopentadienyl)chromium
Рис. 6.17.11
1190
Новый справочник химика и технолога
[ц-{2(1-3,3а,8ат]): 1 (4-6т))}Азулен](пентакарбонил-1 к3С,2к2С)дижелезо(Яе-Яе) англ.-. [p-{2(1-3,3a,8ar]):1(4-6T])}Azulene](pentacarbonyl-lK3C,2K2C)cliiron(Fe-Fe)
Рз-Карбонил-1 кС:2кС, О:ЗкС, О-треугольно-трис[дикарбонил-(т]5-циклопентадиенил)ниобий](3 Nb-Nb)
англ.: p3-Carbonyl-lKC:2KC,O:3KC,O-tnangu/o-tris[dicarbonyl(r|5-cyclopentadienyl)-niobium](3 Nb-Nb)
Рис. 6.17.12
[Fe(n5-C5H4CH3)2]
1,1'-Диметилферроцен или бис(метил-д5-циклопентадиенил)-железо
англ.: 1,1'-Dimethylferrocene или bis(methyl-r]5-cyclopentadienyl)iron
[Ni{n5-C5(CK3)4C2H5}2]
1,1 '-Диметил(октаэтил)никелоцен или
бис(1-метил-2,3,4,5-тетраэтил-г]5-циклопентадиенил)никель англ.: 1,T-Dimethyl(octaethyl)nickelocene или
bis(1-methyl-2,3,4,5-tetraethyl-T]5-cyclopentaclienyl)nickel
[1 -(Диэтиламино)пропил]хромоцен или
1-хромоценил-Л/,Л/-диэтилпропан-1-амин англ.: [1-(Diethylamino)propyl]chromocene или
1-chromocenyl-A/,A/-diethylpropan-1 -amine
Рис. 6.17.13
[Fe(n5-C5H5)2] [BF4] Ферроцений тетрафторборат или
бис(д5- циклопентадиенил)железо(1+) тетрафторборат англ.: Ferrocenium tetrafluoroborate или
bis(r]5-cyclopentadienyl)iron(1 +) tetrafluoroborate
Рис. 6.17.14
Современная номенклатура органических соединений
1191
Литература
Общая литература
1. Номенклатурные правила ИЮПАК по химии. Т. 2, полутом 1, 2. Органическая химия. М., 1979. 886 с.
2. Номенклатурные правила ИЮПАК по химии. Т. 3. полутом 1, 2. Органическая химия. Высокомолекулярные соединения. М., 1983. 343 с.
3. Кан Р., Дермер О. Введение в химическую номенклатуру. М.: Химия, 1983. 224 с.
4. Бенке Дж. Названия органических соединений. М.: Химия, 1980. 304 с.
5. International Union of Pure and Applied Chemistry. Organic Chemistry Division. Commission on Nomenclature of Organic Chemistry, Nomenclature of Organic Chemistry, Sections А, В, C, D, E, F and H. 1979 Edition, J. Rigaudy and S. P. Klesney eds., Per-gamon Press, Oxford. 1979. 559 p.
6. International Union of Pure and Applied Chemistry. Organic Chemistry Division. Commission on Nomenclature of Organic Chemistry, A Guide to IUPAC Nomenclature of Organic Compounds, Recommendations 1993. R. Panico, W.H. Powell and J.-C. Richer (Senior Editor). Blackwell Scientific Publications, Oxford. 1993.190 p.
Номенклатура спиранов
7. Extension and Revision of the Nomenclature for Spiro Compounds (Recommendations 1999) / G.P. Moss // Pure Appl. Chem. 1999. V. 71. P. 531-558.
http://www.chem.qmul.ac.uk/iupac/spiro/
Номенклатура полициклических соединений
8. Extension and Revision of the von Baeyer System for Naming Polycyclic Compounds (Including Bicyclic Compounds) (Recommendations 1999) / G.P. Moss // Pure Appl. Chem. 1999. V. 71, P. 513-529.
http://www.chem.qmul.ac.uk/iupac/vonBaeyer/
Номенклатура конденсированных углеводородов
и гетероциклов
9. Nomenclature of Fused and Bridged Fused Ring Systems (Recommendations 1998) / G.P. Moss П Pure Appl. Chem. 1998. V. 70. P. 143-216.
http://www.chem.qmul.ac.uk/iupac/fusedring/
Номенклатура фанов
10. Part I: Phane Nomenclature (IUPAC Recommendations 1998) / W.H. Powell // Pure Appl. Chem. 1998. V. 70. P. 1513-1545.
http://www.chem.qmul.ac.uk/iupac/phane/
11. Part II: Modification of the Degree of Hydrogenation and Substitution Derivatives of Phane Parent Hydrides (IUPAC Recommendations 2002) I H.A. Favrel, D. Hell-winkel, W.H. Powell, H.A. Smith and S.S.-C. Tsay // Pure Appl. Chem. 2002. Vol. 74. P. 809-834.
http://www.chem.qmul.ac.uk/iupac/phane2/
Номенклатура фуллеренов
12. Nomenclature for the C60-Ih and C7o-D5h(6) Fullerenes. (IUPAC Recommendations 2002) / W.H. Powell 1, F. Cozzi, G.P. Moss, C. Thilgen, R.J.-R. Hwu and A. Yerin // Pure Appl. Chem. 2002. V. 74. P. 629-695.
http://www.chem.qmul.ac.uk/iupac/fullerene/
Номенклатура гетеромоноциклов
13. Revision of the extended Hantzsch—Widman system of Nomenclature for Heteromonocycles (Recommendations 1982) I W.H. Powell // Pure Appl. Chem. 1983. V. 55. P. 409-416.
http://www.chem.qmul.ac.uk/iupac/hetero/HW.html
Номенклатура соединений с элементами в нестандартном валентном состоянии (^-обозначения)
14. Treatment of variable valence in organic Nomenclature (7. convention) (Recommendations 1983) I W.H. Powell // Pure Appl. Chem. 1984. V. 56. P. 769-778.
http://www.chem.qmul.ac.uk/iupac/hetero/Lm.html
Номенклатура соединений co смежными двойными связями (^-обозначения)
15. Nomenclature for cyclic organic compounds with contiguous formal double bonds (the 8-convention) // Pure Appl. Chem. 1988. V. 60. P. 1395-1401.
http://www.chem.qmul.ac.uk/iupac/hetero/De.html
Номенклатура радикалов, ионов и радикал-ионов
16. Revised Nomenclature for Radicals, Ions, Radical Ions and Related Species (IUPAC Recommendations 1993) / W.H. Powell // Pure Appl. Chem. 1993. V. 65. P. 1357-1455.
http://www.chem.qmul.ac.uk/iupac/ions/
Номенклатура изотопно-модифицированных соединений
17. Isotopically Modified Compounds (Recommendations 1978)// Pure Appl. Chem. 1979. V. 51. P. 353-380. http://www.chem.qmul.ac.uk/iupac/sectionH/
Стереохимическая номенклатура
18. Basic Terminology of Stereochemistry (IUPAC Recommendations 1996) / G.P. Moss // Pure Appl. Chem. 1996. V. 68. P. 2193-2222.
http://www.chem.qmul.ac.uk/iupac/stereo/
19. Cahn R. S., Ingold С. K., Prelog V. Specification of Molecular Chirality’s // Angew. Chem., Int. Ed. Engl. 1966. V. 5. P. 385-414 (errata: 1966. V. 5. P. 511); Angew. Chem. 1966. V. 78. P. 413-447.
20. Prelog V., Helmchen G. Basic Principals of the CIP-System and Proposals for a Revision // Angew. Chem. 1982. V. 94. P. 614-631; Angew. Chem. Int. Ed. Engl., 1982. V. 21. P. 567-583.
1192
Новый справочник химика и технолога
21. Mata Р., Lobo А.М., Marshall С., Johnson А.Р. The CIP Sequence Rules: Analysis and Proposal for a Revision I I Tetrahedron: Asymmetry. 1993. V. 4. P. 657-668.
22. Eliel E.L., Wilen S.H. Stereochemistry of organic compounds. Wiley-Interscience. 1994.
Номенклатура углеводов
23. Nomenclature of Carbohydrates (Recommendations 1996) // Adv. Carbohydr. Chem. Biochem. 1997. V. 52. P. 43-177; McNaught A.D. Nomenclature of Carbohydrates // Carbohydr. Res. 1997. V. 297. P. 1-90; J. Carbohydr. Chem. 1997. V. 16. P. 1191-1280; Pure Appl. Chem. 1996. V. 68. P. 1919-2008.
http://www.chem.qmul.ac.uk/iupac/2carb/
Номенклатура циклитов
24. Nomenclature of Cyclitols (Recommendations, 1973) // Biochem. J. 1976. V. 153. P. 23-31; Eur. J. Biochem. 1975. V. 57. P. 1-7; Pure Appl. Chem. 1974. V. 37. P. 283-297; Biochemical Nomenclature and Related Documents. 2nd ed. Portland Press, 1992. P. 149-155.
http://www.chem.qmul.ac.uk/iupac/cyclitol/
Номенклатура аминокислот и пептидов
25. Nomenclature and Symbolism for Amino Acids and Peptides (Recommendations 1983). IUPAC-IUB Joint Commission on Biochemical Nomenclature (JCBN) // Biochem. J. 1984. V.219. P. 345-373; Eur. J. Biochem. 1984. V. 138. P. 9-37; 1985. V. 152. P. 1; 1993. V. 213. P. 2; Intemat. J. Pept. Prot. Res. 1984. V. 24. following p. 84; J. Biol. Chem. 1985. V. 260. P. 14-42; Pure Appl. Chem. 1984. V. 56. P. 595-624; Amino Acids and Peptides. 1985. V. 16. P. 387-410; Biochemical Nomenclature and Related Documents, 2nd ed. Portland Press, 1992. P. 39-69.
http://www.chem.qmul.ac.uk/iupac/AminoAcid/
Номенклатура стероидов
26. The Nomenclature of Steroids (Recommendations 1989) П Eur. J. Biochem. 1989. V. 186. P. 429 458; 1993. V.213. P. 2; Pure Appl. Chem. 1989. V. 61. P. 1783-1822; Dictionary of Steroids edited R.A. Hill, D.N. Kirk, H.L.J. Makin and G.M. Murphy. Chapman and Hall. London: 1991; Biochemical Nomenclature and Related Documents. 2nd ed. Portland Press, 1992. P. 192-221.
http://www.chem.qmul.ac.uk/iupac/steroid/
Номенклатура витаминов D
27. Nomenclature of Vitamin D (Recommendations 1981) // Arch. Biochem. Biophys. 1982. V. 218. P. 342-346; Endocrinol. Inform. 1982. V. 2. P. 53-62; Eur. J. Biochem. 1982. V. 124. P. 223-227; Mol. Cell. Biochem. 1982. V.49. P. 177-181; Pure Appl. Chem. 1982. V. 54. P. 1511-1516; Biochemical Nomenclature and Related Documents, 2nd ed. Portland Press, 1992. P. 242-246. http://www.chem.qmul.ac.Uk/iupac/misc/D.html
Номенклатура каротиноидов и ретиноидов
28. Nomenclature of Carotenoids (Rules Approved 1974) 11 Pure Appl. Chem. 1974. V. 41. P. 407 431; Biochem. J. 1972. V. 127. P. 741-752; Biochem. 1971. V. 10. P. 4827-4837; Eur. J. Biochem. 1972. V.25. P.397-408; J. Biol. Chem. 1972. V. 247. P. 2633-2643; IUPAC Information Bulletin Appendix № 19 (February 1972); Biochemical Nomenclature and Related Documents. 2nd ed. Portland Press, 1992. P. 226-236; Biochem. J. 1975. V. 151. P. 5-7; Biochem. 1975. V. 14. P. 1803; Eur. J. Biochem. 1975. V. 57. P. 317-318; Biochemical Nomenclature and Related Documents. 2nd ed. Portland Press, 1992. P. 237-238.
http://www.chem.qmul.ac.uk/iupac/carot/
29. Nomenclature of Retinoids (Recommendations 1981) // Arch. Biochem. Biophys. 1983. V. 224. P. 728-731; Eur. J. Biochem. 1982. V. 129. P. 1-5; J. Biol. Chem. 1983. V.258. P. 5329-5333; Pure Appl. Chem. 1983. V. 55. P. 721-726; Biochemical Nomenclature and Related Documents. 2nd ed. Portland Press, 1992. P. 247-251. http://www.chem.qmul.ac.uk/iupac/misc/ret.html
Номенклатура тетрапирролов
30. Nomenclature of Tetrapyrroles (Recommendations 1986) 11 Eur. J. Biochem. 1988. V. 178. P. 277-328; Pure Appl. Chem. 1987. V. 59. P. 779-832; Biochemical Nomenclature and Related Documents. 2nd ed. Portland Press, 1992. P. 278-329.
http://www.chem.qmul.ac.uk/iupac/tetrapyrrole/
Номенклатура металлорганических соединений
31. Nomenclature of organometallic compounds of the transition elements (IUPAC recommendations 1999)// A. Salzer. Pure Appl. Chem. 1999. V. 71. P. 1557-1585.
32. Leigh G.J. Nomenclature of Inorganic Chemistry, Recommendations 1990 (The Red Book). Blackwell Scientific Publications. Oxford. UK. 1990.
Раздел 7. КРАТКИЕ СВЕДЕНИЯ О ТЕХНИКЕ ЛАБОРАТОРНЫХ РАБОТ
Автор-составитель: О.А. Пинчук
7Л. Лабораторная посуда
7.1.1 Материалы
При выполнении различных аналитических операций необходимо правильно выбирать материал, из которого изготавливается посуда. Например, для отбора и хранения проб воды выбор материала для сосудов и емкостей зависит от определяемого показателя (см. ГОСТ Р 51592-2000).
7.1.1.1. Химико-лабораторное стекло
Химико-лабораторное стекло обладает высокой устойчивостью к воздействию большинства органических растворителей, растворов минеральных кислот, за исключением фтороводородной (плавиковой) и фос
форной. Концентрированные щелочи разрушают поверхность стекла, особенно при повышенных температурах. Показатели стойкости стекла к воздействию дистиллированной воды, кислот и щелочей приведены в ГОСТ 21400-75 и в [5].
По ГОСТ 21400-75, стекло в зависимости от химической и термической стойкости подразделяется на шесть групп: ХС1, ХС2, ХСЗ — химически стойкое 1, 2 и 3-го классов соответственно; ТХС1, ТХС2 — термически и химически стойкое стекло 1-го и 2-го классов соответственно; ТС — термически стойкое стекло (боросиликатное).
В табл. 7.1.1 представлен состав основных марок выпускаемого в России химико-лабораторного стекла.
Таблица 7.1.1
Состав (масс. %) основных марок химико-лабораторного стекла
Группа стекла Марка стекла SiO2 В2О3 А12О3 СаО MgO ВаО Na2O к2о Fe2O3 ZrO2
ХСЗ №29 68,8 3,7 7,5 3,5 3,5 10 3,0 0,2
ХСЗ Л-80 71,5 2,0 2,5 6,5 2,5 14,5 0,5
ХСЗ AM 72,0 1,5 10,0 2,5 14,0
ТХС1 ТХС1 72,4 8,4 3,6 2,0 4,5 5,1 1,8 1,9
ТХС2 Л-50 74,5 6,6 5,5 0,7 4,5 4,2 4,0
тс Пирекс 80,64 12,0 2,0 0,36 4,0 1,0
Медицинское 7,30 4,0 4,5 7,0 1,0 8,5 2,0
7.1.1.2. Кварцевое стекло
Кварцевое стекло получают из диоксида кремния [12]. Посуда из кварцевого стекла обладает высокой термической устойчивостью (ее можно нагревать до 1000 °C) и химической инертностью к кислотам, за исключением плавиковой и ортофосфорной кислот. Посуду из кварцевого стекла нельзя употреблять при работе со щелочами.
7.1.1.3. Фарфор
Фарфоровые изделия изготавливают из тонких смесей каолина, кварца, полевого шпата и алюмосиликатов [12]. В зависимости от состава, массы и температуры обжига различают твердый фарфор, обжигаемый при 1380-1420 °C и выше, и мягкий, температура обжига которого ниже 1350 °C. Мягкий фарфор — белый, просвечивается лучше, чем твердый фарфор, но менее термостойкий
1194
Новый справочник химика и технолога
и прочный. По сравнению с мягким твердый фарфор содержит больше каолина и меньше полевого шпата. Фарфоровые изделия покрывают тонким слоем глазури специального состава, которая обеспечивает высокую абразивную прочность и стойкость к воздействию кислот и щелочей. В зависимости от типа изделий и их назначения используют глазури разного состава: прозрачные, непрозрачные (глухие), цветные, матовые и др.
7.1.1.4. Фторопласты
Фторопласты — техническое название фторсодержащих полимеров, к которым относятся политетрафторэтилен, политрифторхлорэтилен, полифторэтилен, поли-1,1-дифторэтилен и др. [11]. Фторопласт (р = 2170 кг/м3) обладает гибкостью и высокой химической устойчивостью ко многим типам химических соединений (кислотам, щелочам, алифатическим спиртам, простым и сложным эфирам и всевозможным углеводородам). Температурный диапазон эксплуатации от -260 до +260 °C. Химическая лабораторная посуда из фторопласта Ф-4 и Ф-4МБ по химическим и физико-химическим свойствам имеет преимущества перед посудой из стекла, кварца, фарфора и других материалов, поэтому она широко применяется для препаративных и химико-аналитических работ.
7.1.1.5. Полипропилен
Полипропилен — термопластичный полимер [6]. Плотность от 905 до 920 кг/м3, температура плавления от 160 до 176 °C. Устойчив в воде и агрессивных неорганических средах (кроме сильных окислителей), ниже 80 °C — в органических растворителях. Лабораторная посуда из полипропилена обладает высокой химической устойчивостью и может использоваться при температурах ниже 135 °C.
Посуду из полипропилена рекомендуется применять при определении металлов (см. ГОСТ Р 51592-2000).
7.1.2. Химическая посуда
В соответствии с ГОСТ 23932-90 посуда и оборудование (лабораторное стеклянное) выпускается из химико-лабораторного, медицинского (ГОСТ 19808-90) или другого стекла, по физико-химическим свойствам соответствующего требованиям ГОСТ 21400-75.
По назначению посуду можно разделить на посуду общего назначения и мерную. По материалу — из химико-лабораторного стекла, фарфора, кварца.
Посуда может изготавливаться с взаимозаменяемыми конусами и без них.
Конус
Конусы изготавливаются по ГОСТ 8682-70 двух исполнений:
КШ — со шлифованной поверхностью;
КН — с нешлифованной поверхностью.
Пример условного обозначения
Конус КШ диаметром 19 мм и высотой 9 мм:
Конус КШ 19/9 ГОСТ 8682-70.
Более полная информация о взаимозаменяемых конусах (например, о форме и номинальных размерах) содержится в ГОСТ 8682-70.
Выпускаемая посуда регламентируется Государственными стандартами.
7.1.2.1. Посуда общего назначения
ГОСТ 25336-82 распространяется на стеклянную лабораторную посуду (стаканы, стаканчики для взвешивания, колбы, колбы Фаворского, колбы с тубусом, пробирки, чашки, сосуды) и оборудование (соединительные элементы и грубки, воронки, фильтры, капельницы, спиртовки, склянки с тубусом, насос водоструйный, эксикаторы, насадки, холодильники, дефлегматоры, каплеуловители, склянки для промывки газов, приборы для поглощения газов и паров воды, аппараты для получения газов), изготавливаемые из химико-лабораторного стекла, и регламентирует их типы, основные параметры и размеры.
Маркировка
На каждом изделии (см. ГОСТ 23932-90) должны быть нанесены:
- товарный знак предприятия-изготовителя;
- номинальная вместимость, мл (см3), на круглодонных, плоскодонных, конических колбах и стаканах;
- размеры взаимозаменяемых конусов;
- класс фильтра (на изделиях с фильтрами);
- матовая поверхность для нанесения лабораторных надписей (если требует характер изделия).
Стаканы
Лабораторные стаканы представляют собой тонкостенные цилиндры различной вместимости. Стаканы предназначены для фильтрования, выпаривания и приготовления растворов в лабораторных условиях. Стаканы изготавливаются в соответствии с ГОСТ 25336-82 двух типов (В — высокие; Н — низкие) и двух исполнений (1 — с носиком; 2 — без носика). Края стаканов имеют воронкообразную развертку.
Номинальная вместимость в обозначении и наименовании стаканов является условной. Стаканы номинальной вместимости 100 см3 и более могуг быть изготовлены со шкалой, обозначающей ориентировочную вместимость.
Пример условного обозначения
Стакан типа В исполнения 1, номинальной вместимости 250 см3, из термически стойкого стекла группы ТС:
Стакан В-1—250 ТС ГОСТ 25336-82.
Основные размеры стаканов представлены в табл. 7.1.2.
Краткие сведения о технике лабораторных работ
1195
Таблица 7.1.2
Основные размеры стаканов типа В и Н
Номинальная вместимость, см3 Диаметр (до расши рения по краю), мм Высота, мм
Тип В Тип Н Тип В Тип Н
Номинальный Предельное отклонение Номинальный Предельное отклонение Номинальная Предельное отклонение Номинальная Предельное отклонение
5 ±1,0 22 ±1,0 ±2,0 30 ±2,0
10 26 35
25 34 50
50 38 42 70 60
100 48 50 80 70
150 54 60 ±1,5 95 80
250 60 ±1,5 70 120 ±3,0 95
400 70 80 ±2,0 130 110 ±3,0
600 80 ±2,0 90 150 125
800 90 100 175 135
1000 95 105 180 145
2000 120 130 ±3,0 240 ±4,0 185
3000 135 ±3,0 150 280 210 ±4,0
5000 170 270
Стаканчики для взвешивания (бюксы)
Стаканчики предназначены для взвешивания и хранения веществ при лабораторных работах. В соответствии с ГОСТ 25336-82 выпускаются стаканчики двух типов: СВ — высокие, СН — низкие.
Пример условного обозначения
Стаканчик типа СВ с взаимозаменяемым конусом 14/8:
Стаканчик СВ—14/8 ГОСТ 25336-82.
Основные размеры стаканчиков приведены в табл. 7.1.3.
Таблица 7.1.3
Основные размеры стаканчиков типов СВ и СН
Тип Диаметр (до шлифа, предельное отклонение ± 1,0), мм Высота, мм, не более Обозначение конусов горловин стаканчиков по ГОСТ 8682-70
СВ 20 30 14/8
25 40 19/9
30 50 24/10
40 65 34/12
СН 32 34/12
43 45/13
50
58 60/14
82 85/15
Колбы
Колбы предназначены для проведения различных препаративных и аналитических работ (фильтрования, выпаривания, перегонки, разгонки, дистилляции, синтеза) в лабораторных условиях. ГОСТ 25336-82 предусматривает изготовление колб следующих типов:
К — круглодонные с взаимозаменяемыми конусами (исполнение 1), без взаимозаменяемых конусов и с цилиндрической горловиной (исполнение 2);
П — плоскодонные с взаимозаменяемыми конусами (исполнение 1), без взаимозаменяемых конусов и с цилиндрической горловиной (исполнение 2);
КГУ-2 — круглодонные с двумя горловинами, расположенными под углом, с взаимозаменяемыми конусами (исполнение 1), без взаимозаменяемых конусов (исполнение 2);
КГУ-3 — круглодонные с тремя горловинами, расположенными под углом, с взаимозаменяемыми конусами (исполнение 1), без взаимозаменяемых конусов (исполнение 2);
КГП-3 — круглодонные с тремя горловинами, расположенными параллельно, с взаимозаменяемыми конусами (исполнение 1), без взаимозаменяемых конусов (исполнение 2);
КГП-4 — круглодонные с четырьмя горловинами, расположенными параллельно, с взаимозаменяемыми конусами;
Кн — конические с взаимозаменяемыми конусами (исполнение 1), без взаимозаменяемых конусов и с цилиндрической горловиной (исполнение 2);
Гр — грушевидные с взаимозаменяемыми конусами;
Кьельдаля — грушевидные с взаимозаменяемыми конусами (исполнение 1) и с цилиндрическими горловинами (исполнение 2);
О — остродонные с взаимозаменяемыми конусами;
ОГ-2 — остро донные с двумя горловинами и с взаимозаменяемыми конусами;
ОГ-3 — остродонные с тремя горловинами с взаимозаменяемыми конусами (исполнение 1), без взаимозаменяемых конусов (исполнение 2);
КП — круглодонные для перегонки с взаимозаменяемыми конусами (исполнение 1), без взаимозаменяемых конусов (исполнение 2);
ОП — остродонные для перегонки с взаимозаменяемыми конусами;
1196
Новый справочник химика и технолога
КРН — круглодонные для разгонки нефти и нефтепродуктов.
Колбы Фаворского — остродонные колбы с двумя горловинами с взаимозаменяемыми конусами по ГОСТ 8682-70, прямая горловина которых выполнена в виде дефлегматора, предназначены для перегонки при атмосферном давлении и при остаточном давлении 13,3 Па (10 мм рт. ст.). Колбы Фаворского выпускаются в соответствии с ГОСТ 25336-82. Дефлегматор должен иметь по окружности чередующиеся в шахматном порядке наколы по 4 шт. в ряду, расположенные наклонно к оси под углом не менее 30°.
Колбы с тубусом предназначены для фильтрования в вакууме. Выпускаются двух исполнений: 1 — без взаимозаменяемого конуса, 2 — с взаимозаменяемым конусом.
Номинальная вместимость в обозначении и наименовании колб является условной.
В табл. 7.1.4 приведены основные характеристики наиболее широко применяемых колб. Полная информация о выпускаемых колбах (например, размеры, коды ОКП, примеры условных обозначений) представлены в ГОСТ 25336-82, некоторые из них показаны в табл. 7.1.4: полужирным шрифтом колбы исполнения 1, курсивом — исполнения 2.
Таблица 7.1.4
Характеристики колб разных типов
Тип колб Номинальная вместимость, см3 Номинальный диаметр горловины (для колб исполнения 2). мм Обозначение конусов по ГОСТ 8682-70 (для колб исполнения 1) Примеры условного обозначения (ТС — термически стойкое стекло, ТХС — термически и химически стойкое стекло)
К 10 18 14/23
25 22
50, 100 18, 22,34 14/23, 19/26, 29/32
250, 500 34, 40, 50 29/32, 34/35, 45/40 Колба К-1—250—29/32 ТС ГОСТ 25336-82 Колба К-2—250—34 ТХС ГОСТ 25336-82
1000 42 29/32, 34/35, 45/40
2000 50, 76 29/32, 45/40
4000 50, 76 45/40
6000, 10000 65, 89 45/40, 60/46
П 50, 100 18, 22, 34 14/23, 19/26, 29/32
250, 500, 750 34, 40, 50 29/32, 34/35, 45/40 Колба П-1—250—29/32 ТС ГОСТ 25336-82 Колба П-2—250—34 ТХС ГОСТ 25336-82
1000 42 29/32, 45/40
2000 50, 76 29/32, 45/40
4000 50, 76 45/40
6000, 10000 65, 89 45/40, 60/46
КГУ-2, КГУ-3 50 18, 22 14/23
(конус боко- 100 18, 22 14/23, 19/26 Колба КГУ-2-1—100—14/23
вых горловин ТС ГОСТ 25336-82
14/23) 250, 500, 1000 34 29/32 Колба КГУ-3-2—250—34 ТХС ГОСТ 25336-82
2000,4000 50 45/40
6000,10000 65 60/46
кгп-з 250, 500, 1000 34 29/32
(конус боковых горловин 2000,4000 50 45/40
14/23)
Кн 10 18, 22 14/23
25 18, 22 14/23, 19/26
50 18, 22, 34 14/23, 19/26, 24/29,
29/32
Краткие сведения о технике лабораторных работ
1197
Окончание табл. 7.1.4
Тип колб Номинальная вместимость, см3 Номинальный диаметр горловины (для колб исполнения 2), мм Обозначение конусов по ГОСТ 8682-70 (для колб исполнения 1) Примеры условного обозначения (ТС — термически стойкое стекло, ТХС — термически и химически стойкое стекло)
Кн Гр Кьельдаля О ОГ-2 Колбы Фаворского Колбы с тубусом 100 250 500 750 1000, 2000 3000, 5000 10, 25, 50, 100 250 50 100 250 500, 1000 10, 25, 50, 100 250, 500 50 100, 250 500 25 50, 100,250, 500 100 250, 500 1000, 2000, 5000 22, 34 34, 40, 50 34, 40, 50 42 50 50 29 19*2 29*2 45 *2 14/23, 19/26, 24/29, 29/32 19/26, 24/29, 29/32, 34/35, 45/40 24/29, 29/32, 34/35, 45/40 24/29, 29/32, 34/35, 45/40 24/29, 29/32, 34/35, 45/40 34/35,45/40 14/23 29/32 14/23 14/23,29/32 19/26, 29/32 19/32 14/23 29/32 14/23, 10/19*' 14/23, 14/23*' 29/32, 14/23*' 10/19 14/23 19/26*3 29/32*3 45/40*3 Колба Гр—50—14/23 ТС ГОСТ 25336-82 Колба Кьельдаля 1—250— 29/32 ТС ГОСТ 25336-82 Колба Кьельдаля 2—250—29 ТХС ГОСТ 25336-82 Колба ОГ-2—100—14/23 ТС ГОСТ 25336-82 Колба Фаворского 250 ГОСТ 25336-82 Колба 1—250 ГОСТ 25336-82 Колба 2—500—29/32 ГОСТ 25336-82
*’ Обозначение конусов по ГОСТ 8682-70 для боковой горловины.
*2 Колбы исполнения 1.
*3 Колбы исполнения 2.
Пробирки
Пробирки предназначены для проведения различных лабораторных работ и, согласно ГОСТ 25336-82, изготавливаются следующих типов:
П1 — цилиндрические с развернутым краем;
П2 — цилиндрические;
П2Т — цилиндрические толстостенные;
ПЗ — остродонные;
П4 — с взаимозаменяемым конусом;
П40 — с взаимозаменяемым конусом и отводом.
Номинальная вместимость в обозначении и наименовании пробирок является условной.
В табл. 7.1.5 и 7.1.6 представлены размеры наиболее широко применяемых пробирок и примеры их условных обозначений, где ХС — химически стойкое стекло и ТС — термически стойкое стекло.
1198
Новый справочник химика и технолога
Таблица 7.1.5
Основные характеристики пробирок типов П1, П2 и П2Т
Тип пробирок Номинальная вместимость, см3 Номинальный диаметр, мм Номинальная высота, мм Примеры условного обозначения
П1 7 40
12 60
14 120
16 150 Пробирка П1—16—150 ХС ГОСТ 25336-82
21,25 200
30 250, 270
П2 7 60
10 90
14 100 Пробирка П2—14—100 ХС ГОСТ 25336-82
16 150, 180
19 150, 180
21 200
П2Т 5 15 55
10 21 60 Пробирка П2Т—10 ТС ГОСТ 25336-82
25 31 70
50 31 115
100 44 100
250 60 155
Таблица 7.1.6
Основные характеристики пробирок типа П4
Номинальная вместимость. см3 Номинальная высота, мм Обозначение конусов по ГОСТ 8682-70
1 40 10/19
2 90 14/23
5 НО 10/19
10 150 14/23
15 180
20 190
25 210
50 130 29/32
Пример условного обозначения
Пробирка типа П4 номинальной вместимостью 10 см3 с взаимозаменяемым конусом 14/23 из химически стойкого стекла группы ХС:
Пробирка П4—10—14/23 ХС ГОСТ 25336-82.
Чашки
Чашки предназначены для проведения химических и биологических работ. По ГОСТ 25336-82 чашки изготавливаются следующих типов:
ЧКЦ — кристаллизационные цилиндрические (исполнение 1 — с носиком; исполнение 2 — без носика);
ЧВП — выпарные плоскодонные сферические (исполнение 1 — с носиком; исполнение 2 — без носика);
ЧВК — выпарные круглодонные сферические (исполнение 1 — с носиком; исполнение 2 — без носика);
ЧБВ — биологические (Коха), с крышками высокие;
ЧБН — биологические (Петри), с крышками низкие.
Номинальная вместимость в обозначении и наименовании чашек является условной. Основные параметры
для чашек различных типов приведены в табл. 7.1.7 и 7.1.8.
Основные параметры чашек типов ЧКЦ, ЧВП и ЧВК
Таблица 7.1.7
Номинальная вместимость, см3 Номинальный диаметр, мм Номинальная высота, мм
ЧКЦ ЧВП ЧВК ЧКЦ ЧВП ЧВК
1 22 15
5 36 32 14 17
10 38 42 42 20 16 23
50 58 64 64 30 24 33
100 72 85 85 40 32 43
250 82 105 105 65 40 53
400 131 50
500 120 136 65 68
1000 150 166 166 75 63 85
2500 200 236 236 100 90 118
5000 250 125
Краткие сведения о технике лабораторных работ
1199
Таблица 7.1.8
Основные параметры чашек типов ЧБВ и ЧБН
Тип чашки Номинальный диаметр чашки, мм Номинальный диаметр крышки, мм Номинальная высота чашки, мм Номинальная высота крышки, мм
ЧБВ 100 106 30 20
150 156 35 25
200 206 45 35
ЧБН 40 46 20 16
(исполнение 1) 100 106
150 156
ЧБН 100 НО 20 18
(исполнение 2)
Примеры условного обозначения
Чашка типа ЧКЦ, исполнения 1, номинальной вместимостью 1000 см3:
Чашка ЧКЦ-1— 1 000 ГОСТ 25336-82.
Чашка ЧБВ номинальным диаметром 100 мм:
Чашка ЧБВ— 100 ГОСТ 25336- 82.
Чашка ЧБН, исполнения 1, номинальным диаметром 100 мм:
Чашка ЧБН-1— 100 ГОСТ 25336-82.
Чашка ЧБН, исполнения 2:
Чашка ЧБН-2 ГОСТ 25336-82.
Сосуды, ванны, кюветы
При проведении лабораторных и исследовательских работ применяют сосуды, ванны, кюветы различных форм и размеров. По ГОСТ 25336-82 сосуды, ванны, кюветы изготавливаются следующих типов:
СЦ — сосуды цилиндрические;
СП — сосуды прямоугольные;
ВП — ванны прямоугольные;
КП — кюветы прямоугольные.
Номинальная вместимость сосудов и ванн является условной.
В табл. 7.1.9 и 7.1.10 приведены основные характеристики изделий. Более полная информация представлена в ГОСТ 25336-82 и [12].
Таблица 7.1.9
Основные параметры сосудов типа СЦ
Номинальная вместимость, дм3 Диаметр, мм, не менее Высота, мм, не менее
0,1* 38 83
0,5 78 125
1,0 102 160
2,0 122 195
3,0 147
5,0 175 245
10,0 245
20,0 300 305
*Сосуд вместимостью 0,1 дм3 должен выпускаться с пластиной диаметром (42 ± 2) мм.
Таблица 7.1.10
Основные параметры сосудов различных типов
Тип сосудов Номинальная вместимость, дм3 Дтина, мм, не менее Ширина, мм, не менее Высота, мм, не менее
СП 0,1 40 30 95
1,5 98 98 195
4,0 147 205
147
6,0 245
195
9,0 265
195
20,0 295 опг
35,0 395 245 J7J
ВП 0,5 98 98 65
1,0 147 148
2,0 295 195
3,0 147 125
195
5,0 155
195
10,0 295 195
15,0 395 245 175
Примеры условного обозначения
Сосуд типа СЦ номинальной вместимостью 0,5 дм3: Сосуд СЦ—0,5 ГОСТ 25336-82.
Ванна типа ВП номинальной вместимостью 10 дм3: Ванна ВП—10,0 ГОСТ 25336-82.
Воронки
Воронки предназначены для выполнения лабораторных работ. По ГОСТ 25336-82, воронки изготавливаются следующих типов:
В — лабораторные;
ВД — делительные;
ВР — с ребрами;
ВК — капельные;
ВП — для порошков;
ВПр — предохранительные;
ВС — для сахарного производства;
ВСП — для собирания паров;
ВФ — для фильтрования.
Основные размеры воронок приведены в табл. 7.1.11.
1200
Новый справочник химика и технолога
Таблица 7.1.11
Основные размеры воронок различных типов
Тип воронок Номинальная вместимость, см3 Номинальный диаметр, мм Номинальная высота, мм Обозначение конусов по ГОСТ 25336-82
горловины стебля
В 25 38
36 50, 80
56 80
75 110, 140, 170
100 150, 200
150 230
250 345
ВР 56 80
75 НО
100 115
вд 10 18 200 14/23 14/23
(без взаимозаменяемых 25 24 225
конусов на стебле — 50 30 245
исполнение 1, с взаимозаменяемыми конусами на стебле — 100 250 40 50 290 340 19/26 29/32 19/26
исполнение 2) 500 65 390
100 83 470
Примеры условного обозначения
Воронка типа В диаметром 36 мм, высотой 80 мм из химически стойкого стекла ХС:
Воронка В—36—80 ХС ГОСТ 25336-82.
Воронка типа ВД исполнения 1, номинальной вместимости 100 см3 из химически стойкого стекла группы ХС:
Воронка ВД-1—100 ХС ГОСТ 25336-82.
Выпускаются делительные воронки исполнения 3 номинальной вместимости от 50 до 2000 см3 (см. ГОСТ 25336-82 и [11]).
Фильтры стеклянные и изделия с фильтрами
Стеклянные фильтры — это пластинки из измельченного и сплавленного стекла. Пластинки впаивают в трубки, стаканы, воронки, тигли и другую посуду из стекла того же состава. Изделия с фильтрами предназначены для фильтрования растворов (например, горячих растворов, концентрированных кислот, разбавленных щелочей) и очистки газов.
В зависимости от формы фильтры изготавливаются следующих типов:
ФКП — круглые плоские;
ФКВ — круглые выпуклые;
ФК — квадратные;
ФП — прямоугольные;
ФПЦ — патронные цилиндрические;
ФПК — патронные конические;
ФКБ — конические бактериологические.
Стеклянные изделия с фильтрами изготавливаются типов:
ВФ — воронки фильтрующие с взаимозаменяемыми конусами (исполнение 2) и без взаимозаменяемых конусов (исполнения 1,3);
ВФО — воронки фильтрующие с отводом и взаимозаменяемым конусом;
ВФОТ — воронки фильтрующие обратные;
ТФ — тигли фильтрующие;
ГФП — газопромыватели с прямым отводом;
ГФИ — газопромыватели с изогнутым отводом;
ФГ — газовые фильтры.
По ГОСТ 2533-6-82 фильтры изготавливаются следующих классов:
Класс фильтров
ПОР 500
ПОР 250
ПОР 160
ПОР 100
ПОР 40
ПОР 16
ПОР 10
ПОР 3,0
ПОР 1,6
ПОР 1,0
Размеры пор, мкм свыше 250 до 500 свыше 160 до 250 свыше 100 до 160 свыше 40 до 100 свыше 16 до 40 свыше 10 до 16 свыше 3 до 10 свыше 1,6 до 3 свыше 1,0 до 1,6 до 1,0
Основные размеры фильтров и изделий с фильтрами приведены в ГОСТ 25336-82 и [12].
Краткие сведения о технике лабораторных работ
1201
Соединительные элементы
Соединительные элементы — переходы, изгибы, керны, муфты, алонжи, затворы, насадки — применяют при сборке различных лабораторных приборов, аппаратов и установок. Они изготавливаются в соответствии с ГОСТ 25336-82.
Соединительные элементы изготавливаются с взаимозаменяемыми конусами различных типов: элементы прямые с двумя муфтами; элементы прямые с двумя кернами; элементы прямые с муфтой и керном; переходы с одной горловиной и отводом; переходы с одной горловиной изогнутые; переходы с несколькими горловинами, параллельными и под углом; изгибы под углом 75° с двумя кернами или с керном и муфтой; изгибы под углами 90° и 105° с керном и муфтой; керны с прямым и изогнутым отводами; муфты с прямым и изогнутым отводами; алонжи прямые; алонжи прямые и изогнутые с отводом; алонжи «паук»; затворы высокие и низкие; насадки с одной и двумя горловинами; насадки с двумя горловинами и отводом.
Информация по этому вопросу представлена также В [12].
Трубки соединительные
Соединительные и хлоркальциевые трубки предназначены для сборки различных установок.
В соответствии с ГОСТ 25336-82 соединительные и хлоркальциевые трубки изготавливаются следующих типов:
ТС-Т — Т-образная;
ТС-У — У-образная;
ТС-В — вилкообразная;
ТС-П — прямая с разными диаметрами;
ТХ-П — прямая с одним шаром под пробку (исполнение 1) и с взаимозаменяемым конусом (исполнение 2);
TXZ450 — изогнутая под углом 45° с взаимозаменяемым конусом;
TX-U — U-образная без отводов под резиновые пробки (исполнение 1), с отводами под резиновые пробки (исполнение 2) и с отводами и пришлифованными пробками (исполнение 3).
Трубки ТС-Т, ТС-У и ТС-В выпускаются следующих номинальных диаметров, мм: 6, 10, 15. Трубка ТС-П имеет диаметры, мм: 6, 10, 14, 17.
Примеры условного обозначения
Соединительная трубка ТС-Т диаметром 10 мм: Трубка ТС-Т—10 ГОСТ25336-82.
Трубка ТС-П:
Трубка ТС-П ГОСТ 25336-82.
Хлоркальцевая трубка типа ТХ-П исполнения 1 диаметром 17 мм:
Трубка ТХ-П-1—17 ГОСТ 25336-82.
Информация по этому вопросу представлена также в [12].
Эксикаторы
В лабораторной практике эксикаторы применяются для высушивания и хранения веществ, легко поглощающих влагу из воздуха. Некоторые зарубежные фирмы выпускают вакуум-эксикаторы с электрическим обогревом. Отечественная промышленность выпускает эксикаторы в соответствии с ГОСТ 25336-82 двух исполнений: 1 — с краном; 2 — без крана. Выпускаются эксикаторы следующих номинальных диаметров корпуса, мм: 100, 140, 190, 250.
Пример условного обозначения
Эксикатор исполнения 1 диаметром корпуса 100 мм:
Эксикатор 1—100 ГОСТ 25336-82.
Сведения о лабораторной посуде общего назначения, не рассмотренной выше (капельницы, спиртовки, склянки с тубусом, водоструйные насосы, насадки для экстрагирования, холодильники, каплеуловители, склянки для промывания газов, приборы для поглощения газов, аппараты для получения газов) содержатся в ГОСТ 25336-82 и [10, 12].
7.1.2.2. Посуда мерная лабораторная
К мерной посуде (меры вместимости стеклянные) относятся цилиндры, мензурки, колбы, бюретки, пипетки и др. Мерная посуда изготавливается из химиколабораторного стекла групп ХС2 и ХСЗ. Пробирки допускается изготавливать из медицинского стекла по ГОСТ 19908-90. Общие требования к мерной посуде приведены в ГОСТ 29227-91. Мерная посуда проходит первичную поверку на предприятии-изготовителе. Импортная мерная посуда должна быть поверена в установленном порядке (см. ГОСТ 8.234—77) в центрах стандартизации и метрологии.
За единицу вместимости принимается кубический сантиметр (см3). Допускается использование термина «миллилитр» (мл).
Номинальный объем мерной посуды определяется при 20 °C. Для правильного отсчитывания устанавливают отметку шкалы на уровне глаза так, чтобы видеть ее как касательную к кривизне мениска. Отсчитывание показаний производят по нижнему краю мениска, в точке касания его верхней части отметки. Мерная посуда градуируется по нижнему краю мениска.
Для мерной посуды устанавливается два класса точности:
1 -й — для более высокой точности измерений;
2-й — для менее точных измерений.
На мерной посуде наносятся:
- товарный знак предприятия изготовителя;
- номинальная вместимость в мл (см3) на колбах, пипетках, бюретках;
- надписи мл (см3);
- обозначение класса;
- «20 °C»;
- буква О (отлив), буква Н (налив);
- обозначение стандарта.
1202
Новый справочник химика и технолога
Цилиндры
Мерные цилиндры — это сосуды цилиндрической формы с нанесенными на их наружной стенке делениями, указывающими объем. Мерные цилиндры изготавливают вместимостью от 5 до 2000 см3.
В соответствии с ГОСТ 1770-74 цилиндры изготавливают 1 и 2 классов точности следующих исполнений: исполнение 1 — с носиком;
исполнение 2 — с пришлифованной пробкой;
исполнение 3 — с носиком и пластмассовым основанием;
исполнение 4 — с пришлифованной пробкой и пластмассовым основанием.
Пример условного обозначения
Цилиндр исполнения 1 вместимостью 250 см3, 2 класса точности:
Цилиндр 1—250—2 ГОСТ 1770-74.
Мензурки
Мензурки — это сосуды конической формы, на наружной стороне которых нанесены деления. Мензурки изготавливают в соответствии с ГОСТ 1770-74 вместимостью от 50 до 100 см3. Их вымеряют на отливной объем.
Пример условного обозначения
Мензурка вместимостью 100 см3:
Мензурка 100 ГОСТ 1770-74.
Колбы
Мерные колбы используются для проведения большого числа аналитических работ: приготовления растворов, разбавления растворов и др. Мерные колбы изготавливают с одной кольцевой отметкой на цилиндрической части и двумя. Первые предназначены для отмеривания
определенного объема жидкости, а вторые — для отбора определенного объема жидкости. Мерные колбы изготавливают вместимостью от 5 до 2000 см3.
В соответствии с ГОСТ 1770-74 мерные колбы выпускают 1 и 2 классов точности следующих исполнений: исполнение 1 — с одной отметкой;
исполнение 2 — с одной отметкой и пришлифованной пробкой;
исполнение 3 — с двумя отметками;
исполнение 4 — с двумя отметками и пришлифованной пробкой.
Пример условного обозначения
Колба исполнения 2 вместимостью 100 см3 2 класса
точности:
Колба 2—100—2 ГОСТ 1770-74.
Пробирки
В соответствии с ГОСТ 1770-74 пробирки выпускают без пришлифованной пробки (исполнение 1) и с пришлифованной пробкой (исполнение 2).
Примеры условного обозначения
Пробирка исполнения 1 вместимостью 10 см3 с ценой деления 0,1 см3 из химически стойкого стекла:
П-1—10—0,1 ХС ГОСТ 1770-74.
Пробирка исполнения 2 вместимостью 15 см3 с взаимозаменяемыми конусами 14/23 из химически стойкого стекла:
П-2—15—14/23 ХС ГОСТ 1770- 74.
Допускаемые отклонения от номинальной вместимости посуды при 20 °C не должны превышать указанных в табл. 7.1.12.
Предельные отклонения от номинальной вместимости пробирок при 20 °C составляют ±0,2 см3 для исполнений 1 и 2 и для исполнения П-2—10/19.
Таблица 7.1.12
Предельные отклонения от номинальной вместимости мерной посуды при 20 °C, см3
Номинальная вместимость, см3 Цилиндры Мензурки Колбы
1 класса 2 класса 1 класса 2 класса
5 ±0,10 ±0,10 ±0,025 ±0,05
10 ±0,10 ±0,20 ±0,025 ±0,05
25 ±0,25 ±0,50 ±0,04 ±0,08
50 ±0,25 ±1,00 ±2,5 ±0,06 ±0,12
100 ±0,50 ±1,00 ±5,00 ±0,10 ±0,20
200 ±0,15 ±0,30
250 ±1,25 ±2,00 ±5,00 ±0,15 ±0,30
300 ±0,20 ±0,40
500 ±2,50 ±5,00 ±12,50 ±0,25 ±0,50
1000 ±5,00 ±10,00 ±25,00 ±0,40 ±0,80
2000 ±10,00 ±20,00 ±0,60 ±1,20
Пипетки
Пипетки с одной меткой изготавливаются по ГОСТ 29169-91 1 и 2 классов точности номинальной вместимостью: 0,5; 1; 2; 5; 10; 20; 50; 100; и 200 см3.
Допускается изготовление пипеток номинальной вместимостью 10,77 см3.
Пипетки номинальной вместимостью 0,5 см" изготавливают без резервуара, 1 см3 — с резервуаром и без
Краткие сведения о технике лабораторных работ
1203
него, 2 см3 — с резервуарам для 1 класса и с резервуаром и без него — для 2 класса. Пипетки остальных вместимостей изготавливаются с резервуаром. Иногда пипетки изготавливаются с предохранительным резервуаром над градуировочной отметкой.
Пипетки выпускаются следующих исполнений: 1 — прямые; 1а — прямые с запасным резервуаром; 2 — с расширением; 2а — с расширением и запасным резервуаром.
Допускаемые отклонения от номинальной вместимости пипеток с одной отметкой при 20 °C не должны превышать указанных в табл. 7.1.13.
Таблица 7.1.13
Предельные отклонения от номинальной вместимости пипеток с одной отметкой при 20 °C
Номинальная вместимость, см3 Предельные отклонения, см3
1 класс 2 класс
0,5 ±0,005 ±0,01
1 ±0,008 ±0,015
2 ±0,01 ±0,02
5 ±0,015 ±0,03
10 ±0,02 ±0,04
10,77 ±0,02 ±0,04
20 ±0,03 ±0,06
25 ±0,03 ±0,06
50 ±0,05 ±0,01
100 ±0,08 ±0,15
200 ±0,1 ±0,2
Пример условного обозначения
Пипетка исполнения 1, 2 класса точности, номинальной вместимостью 50 см3:
Пипетка 1-2—50 ГОСТ 29169-91.
Пипетки градуированные общего назначения выпускаются в соответствии с ГОСТ 29227-91.
Конкретные требования для каждого типа градуированных пипеток установлены в следующих стандартах:
- пипетки градуированные без установления времени ожидания (первый и второй классы) — по ГОСТ 29228-91;
- пипетки градуированные со временем ожидания 15 с (первый класс) — по ГОСТ 29229-91;
- пипетки выдувные (второй класс) — по ГОСТ 29230-91.
Пипетки подразделяются на пять типов.
1. Градуированные пипетки, вымеряемые на слив жидкости от верхней нулевой отметки до любой отметки. Нижняя отметка соответствует номинальной вместимости. Такие пипетки выпускаются 1 и 2 классов точности. Время ожидания нс устанавливается (пипетки типа 1 по ГОСТ 29228-91).
2. Градуированные пипетки, вымеряемые на слив жидкости от любой отметки до сливного кончика. Верхняя отметка соответствует номинальной вмести
мости. Такие пипетки выпускаются 1 и 2 классов точности. Время ожидания не устанавливается (пипетки типа 2 по ГОСТ 29228-91).
3. Градуированные пипетки, вымеряемые на слив жидкости от верхней нулевой отметки до любой отметки. Нижняя часть сливного кончика соответствует номинальному объему. Такие пипетки выпускаются 2 класса точности. Время ожидания не устанавливается (пипетки типа 3 по ГОСТ 29228-91).
4. Градуированные пипетки, вымеряемые на слив жидкости от верхней нулевой отметки до любой отметки. Нижняя часть сливного кончика соответствует номинальному объему. Пипетки 1 класса точности. Время ожидания 15 с (пипетки типа 4 по ГОСТ 29229-91).
5. Градуированные пипетки, вымеряемые на слив жидкости от любой отметки до сливного кончика. Верхняя отметка соответствует номинальной вместимости. Пипетки 2 класса. Последняя капля в пипетке выдувается (выдувные пипетки — пипетки типа 5 по ГОСТ 29230-91).
Градуированные пипетки изготавливаются следующих исполнений:
1 — с делениями прямые;
1а — с делениями прямые с запасным резервуаром;
2 — с делениями и расширением;
2а — с делениями и запасным резервуором.
Допускаемые отклонения по сливному объему градуированных пипеток при 20 °C не должны превышать указанных в табл. 7.1.14.
Таблица 7.1.14
Предельные отклонения сливного объема в зависимости от номинальной вместимости градуированных пипеток при 20 °C
Номинальная вместимость, см3 Цена наименьшего деления шкалы, см3 Предельные отклонения, см’
1 класс 2 класс
0,5 0,01 ±0,005
1 0,01 ±0,006 ±0,01
2 0,02 ±0,01 ±0,02
5 0,05 ±0,03 ±0,05
10 0,1 ±0,05 ±0,1
25 0,1 ±0,1
0,2 ±0,1 ±0,2
Пример условного обозначения
Пипетка типа 1, исполнения 2, 2 класса точности вместимостью 10 см3:
Пипетка 1-2-2-10 ГОСТ 29228-91.
Бюретки
Бюретки изготавливаются в соответствии с ГОСТ 29251-91 двух типов:
тип I — без установленного времени ожидания 1 и 2 классов точности (см. ГОСТ 29252-91);
тип II — с установленным временем ожидания, только 1 класса точности (см. ГОСТ 29253-91).
1204
Новый справочник химика и технолога
Бюретки изготавливаются 5 исполнений (см. ГОСТ 29251-91):
1 — с одноходовым краном;
2 — с боковым краном;
3 — без крана 2 класса точности;
4 — с двухходовым краном;
5 — с двухходовым краном и автоматическим нулем.
Таблица 7.1.15
Предельные отклонения сливного объема в зависимости от номинальной вместимости бюреток при 20 °C
Номинальная вместимость, см3 Цена наименьшего деления шкалы, см3 Предельные отклонения, см3
1 класс 2 класс
1 0,01 ±0,01 ±0,02
2 0,01 ±0,01 ±0,02
5 0,02 ±0,01 ±0,02
10 0,02 ±0,02 ±0,05
0,05 ±0,02 ±0,05
25 0,05 ±0,03 ±0,05
0,1 ±0,05 ±0,10
50 0,1 ±0,05 ±0,15
100 0,2 ±0,1 ±0,2
Допускаемые отклонения измерения объема сливаемой жидкости между двумя любыми точками
шкалы при 20 °C не должны превышать указанных в табл. 7.1.15.
Пример условного обозначения
Бюретка типа 1, исполнения 2, 2 класса точности вместимостью 25 см3, цена деления 0,1 см3;
Бюретка 1-2—2—25—0,1 ГОСТ 29251-91.
7.1.2.3. Посуда из фарфора
Ассортимент фарфоровой посуды, применяемой в обычных лабораториях, не так многочислен, как стеклянной. Фарфоровая посуда имеет ряд преимуществ перед стеклянной: она более прочная, не боится сильного нагревания, в нее можно наливать горячие жидкости, не опасаясь за целостность посуды, и т. д. Недостатком изделий из фарфора является то, что они тяжелы, непрозрачны и значительно дороже стеклянных.
В соответствии с ГОСТ 9147-80 выпускается следующая фарфоровая посуда: стаканы, выпаривательные чашки, кастрюли, низкие тигли, высокие тигли, крышки к тиглям, тигли Гуча, тигли Розе, кружки, воронки Бюхнера, ступки и пестики, ложки, шпатели, вставки для эксикаторов.
Основные характеристики наиболее часто используемой посуды представлены в табл. 7.1.16 и 7.1.17. Более полная информация по данному вопросу представлена в ГОСТ 9147-80 и [12].
Таблица 7.1.16
Основные характеристики фарфоровой посуды (стаканы, выпаривательные чашки, кастрюли, кружки)
Номер изделия Стакан Выпарительная чашка Кастрюля Кружка
Номинальная вместимость, см3 D Н Номинальная вместимость, см3 D Н Номинальная вместимость, см3 D Н Номинальная вместимость, см3 D Н
1 25 35 40 25 62 25 100 75 40 250 65 115
2 50 35 70 50 77 30 250 100 55 500 85 135
3 150 50 90 100 97 35 500 120 70 1000 105 170
4 250 60 ПО 150 107 40 1000 150 85 1500 120 195
5 400 75 120 250 123 50 2000 190 100 2000 135 205
6 600 85 135 450 163 55
7 1000 100 170 850 205 60
8 2000 125 205 1500 265 75
9 4000 175 220 4000 335 100
Примечание. D — наибольший наружный диаметр (номинальное значение, для стакана и кружки — средней и нижней частей), мм; Н— номинальная высота, мм.
Примеры условного обозначения
Стакан № 3 номинальной вместимостью 150 см3:
Стакан 3 ГОСТ 9147-80.
Выпаривательная чашка № 4 номинальной вместимостью 150 см3:
Чашка выпаривательная 4 ГОСТ 9147-80.
Краткие сведения о технике лабораторных работ
1205
Таблица 7.1.17
Основные характеристики фарфоровой посуды (низкие тигли, высокие тигли, воронки Бюхнера, ступки)
Номер изделия Низкий тигель Высокий тигель Воронка Бюхнера Ступка
D Н D Н D Число отверстий, не менее D Н
1 20 15 20 25 65 60 50 35
2 25 19 25 32 80 61 70 40
3 35 26 35 43 100 91 90 45
4 45 35 45 55 130 169 110 50
5 55 42 55 70 175 169 140 70
6 75 57 215 169 180 90
7 240 110
Примечание. D — наибольший наружный диаметр (номинальное значение), мм; Н — номинальная высота, мм.
Пример условного обозначения.
Низкий тигель № 3 с наибольшим диаметром 35 мм: Тигель низкий 3 ГОСТ 9147-80.
7.1.2.4. Посуда из кварцевого стекла
Посуда из прозрачного кварцевого стекла применяется для работы с кислотами и нейтральными веществами при температуре до 1000 °C. Недостатком изделий из кварцевого стекла является их высокая стоимость (значительно дороже стеклянных).
В соответствии с ГОСТ 19908-90 выпускается следующая посуда: тигли, чаши, стаканы, различные колбы, воронки, пробирки и др.
Тигли изготавливаются двух типов: В — высокие; Н — низкие.
Основные характеристики тиглей и чаш представлены в табл. 7.1.18.
Таблица 7.1.18
Основные характеристики посуды из кварцевого стекла (тигли, чаши)
Номинальная вместимость, см3 Тигли типа В Тигли типа Н Чаши
D Н D Н D Н
10 30 30 36 21
20 36 40 45 26 53 25
40 45 50 56 32 60 28
50 48 53 60 36 67 32
80 56 63 71 40 75 36
100 60 67 75 45 85 40
160 95 45
200 105 50
Примечание. D — наибольший наружный диаметр (номинальное значение), мм; Н— номинальная высота, мм.
Примеры условного обозначения Тигель высокий вместимостью 40 см3:
Тигель В—40 ГОСТ 19908-80.
Чаша вместимостью 80 cmj:
Чаша—80 ГОСТ 19908-80.
Стаканы изготавливают четырех типов: ВН — высокие с носиком; ВБН — высокие без носика; НН — низкие с носиком; НБН — низкие без носика, следующей вместимостью, см3: 50, 100, 200, 400, 800, 1000, 1600.
Пример условного обозначения
Стакан высокий с носиком вместимостью 800 см3:
Стакан ВН—800 ГОСТ 19908-80.
Колбы изготавливаются вместимостью 50, 100, 200, 400, 800, 1000 и 1600 см3 восьми типов:
КД — круглодонные длинногорлые;
КК — круглодонные короткогорлые (наружный диаметр горловины, номинальное значение, мм: 21, 26, 31,48, 62);
Гр----грушевидные;
П — плоскодонные (наружный диаметр горловины, номинальное значение, мм: 26, 31, 37, 48);
Кн — конические;
Колбы
Примеры условного обозначения
Колба круглодонная длинногорлая вместимостью 100 см3:
Колба КД— /00 ГОСТ 19908-90.
Колба круглодонная короткогорлая вместимостью 100 см3 с наружным диаметром горловины 26 мм:
Колба КК—100—26 ГОСТ 19908-90.
Колба грушевидная вместимость 200 см3:
Колба Гр—200 ГОСТ 19908-90.
Колба плоскодонная вместимостью 100 см3 с наружным диаметром горловины 31 мм:
Колба П—100—31 ГОСТ 19908-90.
Колба коническая вместимостью 400 см3:
Колба Кн—400 ГОСТ 19908-90.
Более полная информация о посуде из кварцевого стекла содержится в ГОСТ 19908-90.
1206
Новый справочник химика и технолога
7.2. Измерение объема
Для измерения объема следует пользоваться мерной посудой по ГОСТ 1770-74.
Номинальный объем мерной посуды определяется при температуре 20 °C. Для правильного отсчитывания устанавливают отметку шкалы на уровне глаза так, чтобы видеть ее как касательную к кривизне мениска. Мерная посуда градуируется по нижнему краю мениска.
7.2.1. Измерение объема жидкости с помощью пипеток
Чистую пипетку, находящуюся в вертикальном положении, заполняют раствором или дистиллированной водой на несколько миллиметров выше нулевой отметки, затем при движении мениска сверху вниз его устанавливают на нулевой отметке.
Капли, оставшиеся на сливном кончике пипетки, удаляют касанием сливного кончика стенки стеклянного сосуда.
Затем проводят слив в чистый стеклянный сосуд, который должен быть наклонен так, чтобы сливной кончик соприкасался с внутренней стенкой сосуда. Движение сливного кончика относительно стенки сосуда не допускается. Слив должен происходить свободно до установки мениска на требуемой отметке. Затем пипетку извлекают из стеклянного сосуда.
Для пипеток градуированных типа 1 слив производят от нулевой до требуемой отметки. Время ожидания слива жидкости со стенок до окончательной установки мениска не устанавливают.
Для пипеток типа 2 слив осуществляют от любой отметки до сливного кончика. Для обеспечения полного слива жидкости из пипетки устанавливают время ожидания 3 с. Это предельное время ожидания, которое не обязательно выдерживать. Достаточно убедиться, что мениск установился в сливном кончике.
Для пипеток типа 3 слив осуществляют от нулевой до требуемой отметки или, в случае слива полного объема, до сливного кончика. При сливе жидкости от нулевой до требуемой отметки время ожидания слива жидкости со стенок до окончательной установки мениска не устанавливают. При сливе жидкости до сливного кончика устанавливают предельное время ожидания 3 с, которое не обязательно выдерживать. Достаточно убедиться, что мениск установился в сливном кончике.
Для пипеток типа 4 слив осуществляют от нулевой до требуемой отметки или, в случае слива полного объема, до сливного кончика. Слив должен происходить свободно до установки мениска на несколько миллиметров выше требуемой отметки. Окончательно устанавливают мениск по отметке после времени ожидания 15 с. В случае полного слива время ожидания 15 с необходимо обязательно выдерживать.
Для пипеток типа 5 слив осуществляют от требуемой отметки до сливного кончика. Слив должен происходить свободно, пока мениск не установится в сливном кончике. Для обеспечения полного слива жидкости
время ожидания должно составлять 3 с, затем последнюю каплю выдувают из пипетки, а пипетку извлекают из приемной склянки.
7.2.2. Установка мениска
Мениск устанавливают одним из приведенных ниже способов:
- мениск устанавливают таким образом, чтобы плоскость верхнего края отметки находилась горизонтально по касательной к нижней точке мениска; взгляд наблюдателя при этом находится в той же плоскости.
- мениск устанавливают таким образом, чтобы плоскость середины отметки находилась горизонтально по касательной к нижней точке мениска. Взгляд наблюдателя направлен вверх к этой плоскости, при этом одновременно наблюдаются передняя и задняя части отметки, сходящиеся в нижней точке мениска.
Для уменьшения возможных погрешностей мениск следует одним и тем же способом устанавливать на нулевой и последней отметках.
Для измерения объема удобно использовать пипеточные дозаторы. В последние годы выпускаются пипеточные дозаторы различных типов. Метрологические характеристики указанных средств измерения приводятся в описании типа и паспорте. Межповерочный интервал, обычно, составляет один год.
7.3. Измерение массы
Измерение массы осуществляется с помощью весов. Лабораторные весы общего назначения и образцовые выпускаются по ГОСТ 24104-88. Весы зарубежного производства можно использовать в лабораторной практике только в том случае, если они внесены в государственный реестр средств измерений.
По назначению весы разделяются на образцовые и общего назначения, которые в основном используются в лабораторной практике.
В зависимости от принципа действия весы изготавливаются механические или электронные, с автоматическим, полуавтоматическим или неавтоматическим уравновешиванием.
В зависимости от конструктивных признаков механические весы изготавливают равноплечные, двухпризменные, квадрантные.
Весы общего назначения делятся на аналитические, технические и специальные.
Аналитические весы используются для взвешиваний высокой точности (при выполнении химических анализов, в научных исследованиях).
Аналитические весы общего назначения выпускаются 1-4 классов. Пределы допускаемой погрешности весов общего назначения приведены в табл. 7.3.1.
Гири, используемые при взвешивании должны соответствовать ГОСТ 7328-82 и поверены в установленном порядке.
Краткие сведения о технике лабораторных работ
1207
Таблица 7.3.1
Пределы допускаемой погрешности весов общего назначения
Пределы взвешивания Пределы допускаемой погрешности весов общего назначения, ±мг, для классов
1 2 3 4
До 200 мг 0,0050 0,015
200 мг-1 г 0,0075 0,025
1-2 г 0,015 0,030
2-20 г’ 0,030 0,10 0,25
20-50 г 0,075 0,30 0,50
50-200 г 0,15 0,75 2,0 15
200-500 г 0,30 1,5 5,0 38
500 г-1 кг 0,75 3,0 10 75
1-2 кг 1,5 7,0 20 150
2-5 кг 3,0 15,0 50 375
Правила взвешивания
В настоящее время на рынке представлено большое количество различных модификаций весов. Правила работы с весами описаны в прилагающейся к ним технической документации, при этом особое внимание необходимо обращать на правила установки весов. Общие правила работы с аналитическими весами заключаются в следующем:
- перед каждым взвешиванием необходимо проверить, а в случае необходимости установить нулевую точку;
- не допускается никаких прикосновений к неарре-тированнным весам. Взвешиваемый предмет или разновески кладутся на чашки весов или снимаются с них после предварительного арретирования весов;
- не следует нагружать весы сверх установленной предельной нагрузки;
- нельзя ставить на весы влажные и грязные предметы;
- гигроскопичные вещества, а также летучие жидкости взвешивают в герметически закрытых сосудах;
- нельзя взвешивать горячие или холодные предметы;
- при взвешивании необходимо закрывать боковые дверки шкафа весов;
- разновески следует класть или снимать специальным пинцетом с роговыми кончиками;
- нельзя облокачиваться на полку, на которой установлены весы;
Подробную информацию по данному вопросу см. в [7].
7.4. Подготовка посуды для выполнения аналитических работ
Подготовка химической посуды для аналитических работ включает в себя выполнение следующих операций [1,5, 9, 13]:
- механическая очистка посуды с помощью щеток и ершей;
- физическое мытье при помощи воды, моющих средств, органических растворителей (спирт, гексан и т. п.);
- химические методы очистки посуды, мытье окислителями — кислотами, растворами солей (серная кислота, азотная кислота, растворы солей и т. п.);
- сушка.
Мытье посуды необходимо начинать с удаления со стенок загрязнений способом физического или химического мытья.
Для этого посуду сначала ополаскивают водой, затем загрязнения удаляют ершами различных размеров и диаметров при ггомощи горячей воды с применением моющих средств (как правило, применяют 20% раствор синтетического моющего средства (СМС), 5-10% раствор соды, хозяйственное мыло).
Использовать органические растворители следует для удаления нерастворимых в воде органических веществ. Посуду моют путем трехкратного ополаскивания ее небольшими порциями растворителя, причем для первого раза допускается брать использованный растворитель. Мытье посуды органическими растворителями следует проводить в вытяжном шкафу вдали от нагревательных приборов.
Химические методы очистки посуды
Мытье хромовой смесью. Мытье стеклянной посуды хромовой смесью производится только в случае ее сильного загрязнения или необходимости обезжиривания. В остальных случаях производят мытье посуды окисляющей смесью или ггериодическое мытье хромовой смесью с интервалом 7-10 дней. Сначала стеклянную посуду ополаскивают водой, а затем вливают небольшими порциями хромовую смесь в таком количестве, чтобы она занимала примерно одну четвертую часть ее объема, и осторожно обмывают смесью стенки сосуда, наклоняя и поворачивая его во все стороны. Затем смеси дают стечь на дно и сливают обратно в склянку для хранения. Обработанную смесью посуду тщательно, не менее пяти раз, обмывают водопроводной водой, набирая полные емкости. После этого посуду необходимо трижды ополоснуть дистиллированной водой и поставить сушиться.
Сильно загрязненную посуду моют хромовой смесью несколько раз.
Хромовую смесь не применяют, если посуда загрязнена продуктами перегонки нефти (парафином, воском, керосином, минеральными маслами и т. д.). Ее нельзя также применять, для мытья посуды, загрязненной солями бария, т. к. сульфат бария образует на стенках трудноудаляемый осадок.
Приготовление хромовой смеси. Приготовление хромовой смеси описано в [5, 14]. Хромовую смесь приготавливают несколькими способами.
1. Смешивают 300 см3 концентрированной серной кислоты, находящейся в фарфоровом стакане, с 15г измельченного в фарфоровой чашке дихромата калия (или натрия). После тщательного перемешивания и отстаивания темно-бурую жидкость сливают с осадка и хранят в толстостенной стеклянной посуде или в фарфоровом стакане, снабженных крышками.
* Хромовая смесь состоит из равных объемов насыщенного водного раствора К2Сг2О7 и концентрированной H2SO4.
1208
Новый справочник химика и технолога
2. В фарфоровом стакане готовят насыщенный раствор дихромата калия (натрия) в небольшом количестве воды (на холоду) и осторожно добавляют равный объем концентрированной серной кислоты. Хранят в толстостенной стеклянной посуде или в фарфоровом стакане, снабженных крышками.
Сосуды с хромовой смесью следует устанавливать (для хранения и работы) на эмалированные или керамические поддоны. После длительного употребления цвет хромовой смеси из темно-оранжевого переходит в темно-зеленый, что служит признаком ее непригодности для мытья посуды.
Мытье окисляющей смесью. Для выполнения аналитических работ посуда может быть подготовлена с помощью окисляющей смеси. Мытье посуды выполняют так же, как и хромовой смесью. Окисляющую смесь приготавливают смешением раствора разбавленной азотной кислоты (1:1) с 3% раствором пероксида водорода. Хранят в толстостенной стеклянной посуде.
Мытье серной кислотой и растворами щелочей. Когда посуда загрязнена смолистыми веществами или в лаборатории нет окисляющей или хромовой смеси, посуду можно мыть концентрированной серной кислотой или концентрированным раствором щелочи (NaOH, КОН). Мытье выполняют так же, как и хромовой смесью.
Подготовка посуды для анализа проб на металлы. В предварительно вымытую стеклянную или пластиковую посуду вливают небольшими порциями разбавленную азотную кислоту (1:1) квалификации «ос. ч.» в таком количестве, чтобы она занимала примерно половину ее объема, и осторожно обмывают стенки сосуда, наклоняя и поворачивая его во все стороны. Затем кислоту сливают обратно в склянку для хранения. Обработанную посуду не менее 5 раз обмывают водопроводной водой, набирая полные емкости. Затем в емкости добавляют разбавленную соляную кислоту (1:1) квалификации «ос. ч.» в таком количестве, чтобы она занимала примерно половину ее объема, и осторожно обмывают стенки сосуда. Кислоту сливают в склянку для хранения. Обработанную кислотами посуду не менее 5 раз моют водопроводной водой, набирая полные емкости. После этого посуду не менее трех раз ополаскивают дистиллированной водой.
При мытье посуды необходимо выполнять следующие правила:
1. Нельзя использовать синтетические моющие средства для мытья посуды, в которой в дальнейшем будут определять содержание различных форм фосфора.
2. Хромовую смесь нельзя использовать для мытья посуды, в которой в дальнейшем будут определять содержание сульфатов и металлов.
3. Стеклянная посуда, предназначенная для отбора проб воды для определения в ней бензо[а]пирена и нефтепродуктов, должна быть дополнительно промыта чистым гексаном, после чего высушена.
4. Работать с концентрированными кислотами, щелочами, хромовой и окисляющей смесями необходимо в тяге, соблюдая правила техники безопасности.
7.4.2. Мытье паром
Этот способ мытья посуды является достаточно эффективным, но он редко применяется, т. к. требует длительного времени. Различные способы мытья посуды паром изложены в [1, 5].
7.4.2.1. Контроль чистоты посуды
После мытья проверяют чистоту посуды по стеканию воды. С чистых сосудов вода стекает пленкой, равномерно смачивая изнутри стенки. Если на стенках остаются висячие капли или образуются подтеки, то посуду следует вымыть еще раз.
7.1.2.2. Сушка посуды
Сушить посуду можно на колышках, на специальном столе, в сушильном шкафу (термостате), теплым воздухом, спиртом. Сушка на колышках и на сушильном столе (метод холодной сушки) — наиболее простой, но довольно медленный способ. При сушке при нагревании посуду помещают в холодный сушильный шкаф (не переворачивая) и постепенно повышают температуру до 105-110 °C. Выдерживают 1-1,5 ч, затем шкаф постепенно охлаждают до комнатной температуры. Мерную посуду нельзя сушить при высоких температурах! Сушку посуды из полимерных материалов допускается производить в сушильном шкафу при температуре 50 °C.
7.5. Работа со шлифами
При хранении соединений на шлифах в собранном виде между шлифами помещают небольшие кусочки тонкой (папиросной) бумаги, чтобы предупредить возможное «заедание» шлифов. В таком виде хранят стеклянные краны и сосуды со шлифами.
Перед началом работы шлифы рекомендуется смазать. Смазка предохраняет шлиф от разъедания и «заедания», повышает герметичность соединения и облегчает вращение притертых поверхностей. Если сама конструкция предусматривает вращение притертых поверхностей, например в случае кранов, то смазка шлифов абсолютно необходима. Особенно это относится к шлифам, являющимся частью аппаратуры, работающей в вакууме. Однако в тех случаях, когда смазка может загрязнить вещества, соприкасающиеся со шлифами, или вымывается растворителем, смазывания проводить не следует.
Шлифы обычно смазывают вазелином такой вязкости, чтобы при нормальной температуре его легко можно было нанести в виде тонкого равномерного слоя. Если шлифы сферические или конические, то их одновременно проворачивают. При этом между притертыми поверхностями возникает тонкая пленка и поверхности шлифов становятся совершенно прозрачными. Пра
Краткие сведения о технике лабораторных работ
1209
вильно смазанное и притертое соединение на шлифах выглядит оптически гомогенным. Неплотное прилегание шлифов проявляется в образовании заметных простым глазом каналов. В особых случаях применяют специальные смазки. Так, работа в высоком вакууме требует применения более вязкой смазки. Хорошие результаты дает смазка, приготовляемая растворением каучука в вазелине (смазка Рамзая для шлифов). Исключительно хорошей смазкой является силиконовый вазелин, который в отличие от обычного вазелина лишь незначительно растворяется в органических растворителях. При работе с углеводородами, растворяющими обычные смазки типа вазелина, хорошо себя зарекомендовали вязкие вещества гидрофильного характера типа этиленгликоля, глицерина, различных полигликолей или мыла. Хорошо уплотняет шлифы мелкодисперсный политетрафторэтилен.
При работе со шлифами иногда происходит их «заедание». Причины этого разнообразны. Иногда «заедание» шлифов происходит вследствие механического вдавливания внутреннего шлифа во внешний. Это случается при энергичном соединении шлифов вращательным движением или же в вакуумированных аппаратах, когда шлифы вдавливаются друг в друга давлением воздуха. Чаще всего «заедают» шлифы, длительное время работающие при повышенной температуре, особенно под вакумом. Наиболее прочно «заедают» шлифы под действием некоторых химических веществ, приставших к стеклу или химически разрушающих его поверхность. К числу таких веществ относятся жидкости щелочного характера, соединения, гидролизующиеся с образованием оксида кремния (водорастворимое стекло, SiCl4 и др.)
Извлечение плотно сидящих пришлифованных стеклянных пробок
Для того чтобы извлечь из стеклянного сосуда плотно сидящую пришлифованную пробку, применяют различные приемы.
Если пробку трудно вынуть из-за образовавшихся в горлышке кристаллов растворенного вещества, то на нее наливают несколько капель воды (или ПАВ), которые постепенно проникают в горлышко склянки.
Можно погрузить горлышко сосуда в воду или разбавленную соляную кислоту. Если в сосуде находится раствор щелочи или карбонатов щелочных металлов, то почти всегда, спустя некоторое время (иногда несколько дней), пробку удается извлечь.
У склянок с другими веществами рекомендуется нагреть горлышко небольшим коптящим пламенем горелки, после чего пробку довольно легко извлечь, постукивая по ней деревянной колотушкой. Разумеется, нагревать открытым пламенем можно лишь в случае, когда вещество, находящееся в сосуде, не огнеопасно. В противном случае горлышко сосуда закутывают тряпкой и на нее осторожно льют горячую воду. Можно прибегнуть и к такому приему: верхнюю часть стеклянной пробки закутывают в мягкую тряпку, осторожно
зажимают в тиски и пробуют с небольшим усилием вращать пробку.
7.6. Смазки и замазки
7. 6.1. Смазки
Для смазывания вращающихся металлических и стеклянных деталей в химической лаборатории используют обычные смазки — минеральное масло, вазелин и т. п. Особое внимание следует уделять осям стеклянных мешалок, кранам, шлифам, эксикаторам и т. д.
Смазка для эксикатора. В теплое время года употребляется смесь, состоящая из 3 масс. ч. безводного ланолина и 1 масс. ч. желтого вазелина. В холодное время года или для холодных помещений рекомендуется смесь 2,5 масс. ч. ланолина и 1,5 масс. ч. вазелина.
Вакуумная смазка готовится сплавлением каучука, вазелина и парафина. На водяной бане сплавляют 50 г белого вазелина с 20 г парафина и добавляют 40-50 г натурального каучука. Однородную массу, образующуюся после набухания, фильтруют и помещают в баночку с притертой пробкой.
Для смазывания кранов и стеклянных пробок употребляют вазелиновую мазь, которую готовят сплавлением равных частей парафина (или церезина) и вазелина.
Смазки для шлифов. 1. Маленькие краны обычных установок обрабатывают смазкой из фосфорного ангидрида. На чистую сухую пробку насыпают порошок Р2О5 и оставляют на несколько минут . Когда фосфорный ангидрид начнет расплываться, пробку вставляют во втулку и несколько раз поворачивают.
2. Маленькие краны установок, находящихся в вытяжных шкафах, можно смазывать чистым графитом.
3. Густые, устойчивые по отношению к хлору смазки можно получить хлорированием расплавленного парафина. Но они со временем твердеют и, кроме того, выделяют хлороводород.
7. 6.2. Замазки
Менделеевская замазка. Применяется для скрепления стеклянных, металлических и пластмассовых деталей, для создания герметичности. Готовят по одному из рецептов, смешивая (масс, ч.):
1. Канифоль...............................100
Воск желтый............................25
Мумия (или пемза)......................40
Льняная олифа.......................0,1-1
2. Канифоль................................30
Воск желтый............................5
Мумия (или пемза).....................10
Льняное масло..........................1
* При работе с Р2О5 соблюдать осторожность, с учетом его токсичности. Помнить, что Р2О5 вызывает ожоги кожи и раздражает слизистые оболчки.
1210
Новый справочник химика и технолога
К расплавленному в металлической чашке воску, помешивая, добавляют мелкорастертую канифоль и смесь нагревают при 150-200 °C. Затем добавляют просеянную и прокаленную мумию (или пемзу) и нагревают ее до полного смешения. Приготовлению более мягкой замазки поможет небольшой избыток льняной олифы или масла. Расплавленную замазку переливают в форму и дают остыть. Перед употреблением замазку расплавляют на медленном огне.
Кислотно-щелочеупорная замазка. Смешивают (масс, ч.): сульфат бария — 1, асбестовую муку — 2, растворимое стекло — 2.
Замазка, выдерживающая действие воды, кислот, щелочей и нерастворимая в большинстве органических растворителей. Смешивают 1 масс. ч. безводного глицерина и 10 масс. ч. свинцового глета (предварительно прокаленного при 300 °C) в однородную густую массу. Перед применением места, на которые будет наноситься замазка, предварительно смазывают глицерином.
7.7. Трубки и пробки
7.7.1. Резиновые трубки и пробки
В табл. 7.7.1-7.7.3 приведены стандартные размеры каучуковых пробок, технических и вакуумных резиновых трубок.
Таблица 7.7.1
Стандартные размеры каучуковых пробок
№ пробки Диаметр горла сосуда, мм Диаметр концов пробки, мм Высота пробки, мм
узкого широкого
8 9 8 11 16
10 11 10 13 20
12 13 12 15 20
14 15 14 17 20
16 17 16 19 22
18 19 18 21 23
22 23 22 26 27
27 28 27 31 32
29 30 29 34 35
36 38 36 41 42
38 40 38 43 44
45 47 45 51 52
Таблица 7.7.2
Стандартные размеры технических резиновых трубок
Внутренний диаметр, мм Толщина стенки, мм*
размер допуск
2,0 ±0,5 1,25
3,0 ±0,5 1,25 2,0
4,5 ±0,5 1,25 2,0
6,0 ±0,5 1,25 2,0 3,0
8,0 ±1,0 1,25 2,0 3,0
10,0 ±1,0 1,25 2,0 3,0
12,0 ±1,0 2,0 3,0 4,0 5,0
16,0 ±1,0 2,0 3,0 4,0 5,0
20,0 ±1,5 2,0 3,0 4,0 5,0 6,0 8,0
24,0 ±1,5 2,0 3,0 4,0 5,0 6,0 8,0
28,0 ±1,5 3,0 4,0 5,0 6,0 8,0
32,0 ±1,5 3,0 4,0 5,0 6,0 8,0
36,0 ±1,5 3,0 4,0 5,0 6,0 8,0
40,0 ±1,5 3,0 4,0 5,0 6,0 8,0
* При толщине стенок до 2 мм допуск ±20 %, при 3-4 мм допуск ±15 %, при толщине стенок свыше 4 мм допуск ±10 %.
Стандартные размеры вакуумных резиновых трубок
Таблица 7.7.3
Внутренний размер, мм Толщина стенки, мм Внутренний размер, мм Толщина стенки, мм
размер допуск размер допуск размер допуск размер допуск
2,0-6,0 ±0,5 2,0-5,0 ±0,3 21,0-25,0 ±2,0
7,0-19,0 ±0,75 6,0-8,0 ±0,5 Свыше 30 ±2,0 26,0-35,0 ±2,5
20-25 26-30 ±1,0 ±1,5 9,0-15,0 16,0-20,0 ±1,0 ±1,5 Свыше 35,0 ±3,0
Краткие сведения о технике лабораторных работ
1211
Гибкие полихлорвиниловые трубки применяются для изоляции проводов, работающих при температуре от -10 до +60 °C, а также для подачи воды, масел, воздуха и газов.
Внутренний диаметр трубок от 4 до 50 мм, толщина стенок от 1 до 6 мм.
Хранение резиновых трубок и пробок. Хороший способ хранения резиновых трубок и пробок заключается в том, что их помещают в дистиллированную воду. При другом способе хранения резиновые изделия слегка натирают вазелином или посыпают тальком. Если резиновые предметы затвердели из-за длительного кипячения, то их можно снова сделать пригодными для работы, поместив в 1% раствор пентатионата калия. При этом трубки не следует сгибать.
7.7.2. Корковые пробки
Вместо резиновых пробок (например, для склянок с аммиаком) можно применять корковые пробки, покрытые двойным слоем фольги. Применяются также корковые пробки с резиновым колпачком.
Очистка пробок, бывших в употреблении.
1-й способ. В горячей воде растворяют перманганат калия, в раствор помещают пробки и оставляют их там примерно на сутки, время от времени переворачивая. Затем жидкость сливают, а грязь удаляют, споласкивая пробки чистой водой. Наконец, вновь наполняют сосуд водой и для обесцвечивания добавляют раствор тиосульфата натрия или технической соляной кислоты.
2-й способ. Засаленные жирные пробки отделяют от других пробок и обрабатывают раствором соды. Затем все пробки помещают в воду с 3% пероксидом водорода, разбавленным горячей водой приблизительно в 8-10 раз. При добавлении около 5 мл крепкого раствора аммиака на каждый литр жидкости образуется активный кислород, благодаря действию которого пробки полностью очищаются в течение одного часа.
Слишком долгое пребывание пробок в растворе пероксида водорода вредно, т. к. они становятся ломкими. После того как пробки вынуты из раствора, их надо тщательно промыть теплой водой и обсушить.
Приготовление непромокаемых пробок. Самый надежный и дешевый способ заключается в пропитывании пробок расплавленным парафином, который устойчив по отношению к едким щелочам, соляной и азотной кислотам.
Сосуды с едкими щелочами рекомендуется закрывать только парафинированными корковыми пробками, т. к. стеклянные пробки обычно трудно извлечь из горлышка.
7.8. Охлаждающие смеси
Для получения низкой температуры можно воспользоваться поглощением тепла при растворении некоторых солей в воде. Если взять не воду, а лед или снег, то поглощение тепла при их плавлении дает возможность получить еще более низкую температуру. Целесообразно соль и лед перемешивать в мелкоизмельченном виде для создания большей поверхности соприкосновения. В табл. 7.8.1-7.8.6 приведены составы охлаждающих смесей и их эффективность, о которой судят по криогидратной точке, А Г и Г смеси.
Таблица 7.8.1
Охлаждающие смеси из воды (или снега) и соли
Пояснение. Если А г соли смешать со 100 г воды при 10-15 °C, то температура понизится на А Т, °C. При смешении В г соли со 100 г льда или снега температура понижается до криогидратной точки, т. е. до температуры затвердевания водных растворов эвтектического состава.
Соль А, г A T, °C В, г Криогидратная точка, °C
СаС12 126,9 23,2 42,2 -55
CH3COONa 51,1 15,4
FeCl3 49,7 -55
КС1 30 12,6 30 -H,l
KNO3 13 -2,9
K2SO4 6,5 -1,6
MgCl2 27,5 -33,6
MgSO4 41,5 8,0 23,4 -3,9
NaCl 36 2,5 30,4 -21,2
Na2CO3 14,8 9,1 6,3 -2,1
NaNO3 75 18,5 59 -18,5
Na2S2O3 70 18,7 42,8 -11
NH4C1 30 18,4 25 -15,8
nh4 60 27,2 45 -17,3
(nh4)2S04 75 6,4 62 -19
Таблица 7.8.2
Охлаждающие смеси из воды и двух солей
Пояснение. Если в 100 г воды при 15 °C растворять указанные количества солей, то наступает охлаждение на А Т, °C.
Смесь солей A T, °C
29rNH4Cl+ 18rKNO3 10,6
38 г KNO3 + 13rNH4Cl 9,8
52 г NH4C1 + 40 г NaCl 17
13 rNH4Cl + 37,5 rNaNO3 20,4
2 г KNO3 + 112rKSCN 27
41,6 г NH4NO3 + 41,6 г NaCl 35
1212
Новый справочник химика и технолога
Таблица 7.8.3.
Охлаждающие смеси из кислот и снега
1. При смешении 1 масс. ч. 66% H2SO4 со снегом при температуре -1 °C получают следующие температуры смеси.
Количество снега, масс. ч. Температура смеси, °C
1,097 -37,0
2,52 -30,0
4,32 -25,0
7,92 -20,0
13,08 -16,0
2. При смешении А г 66% H2SO4 с (100 - А) г снега при 0 °C температура понижается на АГ, °C.
А г H2SO4 АТ, °C
47,8 37
42,0 35
35,7 33
31,0 31
25,8 29
22,1 27
18,8 25
15,6 23
12,6 21
9,9 19
3. При смешении указанных ниже кислот со снегом получают смеси с минусовой температурой.
Кислота Количество снега, масс. ч. Температура смеси, °C
формула количество, масс. ч.
НС1 (конц.) 50 100 -18
НС1 (конц.) 100 100 -37,5
HNO3 (разб.) 100 100 -40
H2SO4 (конц.) 25 100 -20
Таблица 7.8.5
Охлаждающие смеси с твердой углекислотой
Твердая углекислота, взятая в избытке, дает с некоторыми жидкостями при атмосферном давлении следующие температуры.
Вещество Т, °C
(С2Н5)2О -77
СН3С1 -82
РС13 -76
С2Н5ОН -72
С2Н5С1 -60
СНС13 -77
Таблица 7.8.4
Охлаждающие смеси из солей с кислотами
1. При смешении кислот с солями температура понижается на АТ, °C.
Кислота Соль A T, °C
фор- количест- форму- количест-
мула во, вес. ч. ла во, вес. ч.
НС1 4 Na2SO4 6 35
(2:1) nh4ci 4
KNO3 2
НС1 (конц.) 5 Na2SO4 8 32
HNO3 2 Na2SO4 3 30
(2:1)
HNO3 4 Na3PO4 6 30
(2:1)
HNO3 Na2SO4 6 38
(2:1) □ NH4NO3 5
H2SO4 (1:1) 4 Na2SO4 5 28
2. При смешении А г Na2SO4 • 10 Н2О с (100 - А) г НС1 (24,5% раствор) при 20 °C температура понижается на АТ, °C.
А г Na2SO4 • 10H2O AT, °C
38,1 28,1
50,4 29,8
63,9 32,5
75,4 32,8
Таблица 7.8.6
Антифризные растворы
Наиболее распространены антифризы на основе водных растворов одно-, двух- и трехатомных спиртов.
Этанол—вода
Содержание этанола, масс. % Относительная >20 плотность а4 Температура замерзания, °C
2,5 0,9936 -1,о
4,8 0,9897 -2,0
6,8 0,9866 -3,0
11,3 0,9801 -5,0
13,8 0,9767 -6,1
16,4 0,9733 -7,5
17,5 0,9719 -8,7
18,8 0,9702 -9,4
20,3 0,9682 -10,6
22,1 0,9658 -12,2
24,2 0,9628 -14,0
26,7 0,9591 -16,0
29,9 0,9540 -18,9
33,8 0,9472 -23,6
Краткие сведения о технике лабораторных работ
1213
Окончание
Содержание этанола, масс. % Относительная >20 плотность а4 Температура замерзания, °C
39,0 0,9372 -28,7
46,3 0,9219 -33,9
56,1 0,9001 -41,0
71,9 0,8631 -51,3
Этиленгликоль—вода
Содержание этиленгликоля, об. % Относительная >15,6 плотность а4 Температура замерзания, °C
12,5 1,019 -3,9
17,0 1,026 -6,7
25,0 1,038 -12,2
32,5 1,048 -17,8
38,5 1,056 -23,3
44,0 1,063 -28,9
49,0 1,069 -34,4
52,5 1,073 -40,0
Г лицерин—вода
Содержание глицерина, масс. % Относительная >15 плотность а15 Температура замерзания, °C
10 1,0242 -1,6
20 1,0494 -4,8
30 1,0756 -9,5
40 1,1026 -15,4
50 1,1299 -23,0
60 1,1577 -34,7
70 1,1854 -38,9
80 1,2129 -20,3
90 1,2395 -1,6
100 1,2656 +17,0
7.9. Поддержание постоянной влажности
Для поддержания постоянной влажности в замкнутом объеме (например, в эксикаторе) готовят насыщенные водные растворы, у которых давление пара находится в равновесии с твердой фазой (табл. 7.9.1).
Таблица 7.9.1
Растворы для поддержания постоянной влажности
Твердая фаза Температура, °C Относительная влажность, %
Н3РО4 • 0,5Н2О 24 9
КСН3СОО 168 13
LiCl • Н2О 20 15
КСН3СОО 20 20
Продолжение табл. 7.9.1
Твердая фаза Температура, °C Относительная влажность, %
KF 100 22,9
NaBr 100 22,9
NaCl, KNO3 и NaNO3 16,39 30,49
СаС12 • 6Н2О 24,5 31
СаС12 6Н2О 20 32,3
СаС12 • 6Н2О 18,5 35
СгОз 20 35
СаС12 • 6Н2О 10 38
СаС12 • 6Н2О 5 39,8
Zn(NO3)2 • 6Н2О 20 42
К2СО3 • 2Н2О 24,5 43
К2СО3 • 2Н2О 18,5 44
kno2 20 45
KSCN 20 47
Nal 100 50,4
Ca(NO3)2 • 4Н2О 24,5 51
NaHSO4 • Н2О 20 52
Na2Cr2O7 • 2Н2О 20 52
Mg(NO3)2 • 6Н2О 24,5 52
NaClO3 100 54
Ca(NO3)2 • 4H2O 18,5 56
Mg(NO3)2 • 6H2O 18,5 56
KI 100 56,2
NaBr • 2H2O 20 58
Mg(CH3COO)2 • 4H2O 20 65
NaNO2 20 66
NH4C1 и KNO3 30 68,6
KBr 100 69,2
NH4CI и KNO3 25 71,2
NH4CI и KNO3 20 72,6
NaClO3 20 75
(NH4)2SO4 108 75
NaCH3COO • 3H2O 20 76
H2C2O4 • 2H2O 20 76
Na2S2O3 5H2O 20 78
NH4CI 20 79,5
NH4CI 25 79,3
NH4CI 30 77,5
(NH4)2SO4 20 81
(NH4)2SO4 25 81,1
(NH4)2SO4 30 81,1
KBr 20 84
T12SO4 104,7 84,8
KHSO4 20 86
H2CO3 • 10H2O 24,5 87
BaCl2 • 2H2O 24,5 88
K2CrO4 20 88
Pb(NO3)2 103,8 88,4
ZnSO4 • 7H2O 20 90
Na2CO3 • 10H2O 18,5 92
NaBrO3 20 92
K2HPO4 20 92
1214
Новый справочник химика и технолога
Окончание табл. 7.9.1
Твердая фаза Температура, °C Относительная влажность, %
nh4h2po4 30 92,9
nh4h2po4 25 93
Na2SO4 • 10Н2О 20 93
NH4H2PO4 20 93,1
ZnSO4 • 7H2O 5 94,7
Na2SO3 • 7H2O 20 95
Na2HPO3 • 12H2O 20 95
NaF 100 96,6
CuSO4 • 5H2O 20 98
Pb(NO3)2 20 98
CaSO4 • 2H2O 20 98
T1NO3 100,3 98,7
T1C1 100,1 99,7
7.10. Осушители
Жидкие растворы, а также газы высушивают с помощью твердых неорганических веществ, способных поглощать воду и образовывать при этом кристаллогидраты (табл. 7.10.1) [4].
Таблица 7.10.1
Эффективность осушающих средств при сушке воздуха
Осушающее средство Содержание водяного пара, г/м3*
Охлаждение воздуха до -194°С 1,6 • 10’23
р2о5 2 • 10’5
ВаО 0,00065
Mg(C104)2 0,0005
Mg(C104)2 • ЗН2О 0,002
КОН (плавленый) 0,002
H2SO4 (100%) 0,003
А12О3 0,003
CaSO4 0,004
MgO 0,008
Охлаждение воздуха до -72 °C 0,106
Силикагель 0,03
Охлаждение воздуха до - 21 °C 0,045
СаВг2 0,14
NaOH (плавленый) 0,16
СаО 0,2
H2SO4 (95,1 %) 0,3
СаС12 0,36
ZnCl2 0,85
ZnBr2 1,16
CuSO4 1,4
* Приведены значения влажности, остающейся при сушке воздуха указанными в таблице средствами. Влажность выражена в граммах водяного пара на 1 м3 воздуха.
Для обезвоживания веществ воздухом, осушаемым химическими реагентами, употребляют эксикаторы. Осушающий реагент помещают на дно эксикатора. Чашку или часовое стекло с осушаемым веществом устанавливают над осушающим реагентом на сетке или на фарфоровой пластинке с отверстиями.
Эксикаторы, заполненные свежепрокаленным СаС12, широко используются для хранения гигроскопичных веществ.
7.11. Газовые баллоны
Для хранения газов применяют специальные баллоны, имеющие определенную окраску (табл. 7.11.1).
По конструкции баллоны бывают двух типов — для газов сжатых и сжиженных; последние обычно имеют внутри сифонную трубку.
Таблица 7.11.1
Окраска и маркировка баллонов для хранения сжатых сжиженных газов
Газ Окраска баллона Цвет надписи с названием газа Цвет полосы под надписью
Азот Черная Желтый Коричне-
Аммиак Желтая Черный вый
Аргон: чистый Серая Зеленый Зеленый
технический Черная Синий Синий
сырой Черная Черный Белый
Ацетилен Белая Красный
Бутилен (смесь Красная Желтый Черный
изомеров С4Н8) Водород Темно- Красный
Воздух зеленая Черная Белый
(сжатый) Гелий Коричневая Белый
Оксид азота(1) Серая Черный
Кислород Голубая Черный
Метан Красная Белый
Сероводород Белая Красный Красный
Диоксид серы Черная Белый Желтый
Углекислота Черная Желтый
Фосген Защитная Красный
Фреон-12 Алюминие- Черный
Фреон-11 вая Алюминие- Черный Синий
Фреон-13 вая Алюминие- Черный (одна) Красный
Фреон-22 вая Алюминие- Черный (три) Желтый
Хлор вая Защитная (две) Зеленый
Циклопропан Оранжевая Черный
Краткие сведения о технике лабораторных работ
1215
Окончание табл. 7.11.1
Газ Окраска баллона Цвет надписи с названием газа Цвет полосы под надписью
Этилен Другие горючие газы Другие негорючие газы Фиолетовая Красная Черная Красный Белый Желтый
Основные правила работы с газовыми баллонами:
- на баллон в нерабочем состоянии должен быть всегда навинчен колпак;
- передвигать баллон следует осторожно, т. к. толчки или падение могут привести к взрыву; обычно баллоны помещают в специальные стойки или крепят к стене с помощью ремней;
- нельзя помещать баллоны в местах, где они могут надеваться; от нагревательных приборов баллоны должны быть удалены не менее чем на 1 м;
- при работе с баллонами сначала открывают редукционный вентиль (редуктор), а затем осторожно — регулировочный (рис. 7.11.1); для каждого баллона должен быть свой редуктор;
- выпускной (регулировочный) вентиль редуктора должен быть чистым; категорически запрещается смазывание вентилей любым жиром или маслом (это чрезвычайно опасно для кислородных баллонов);
- расходуя газ, никогда не следует снижать его давление в баллоне до атмосферного;
- баллоны необходимо периодически испытывать на давление (на заводе);
- нельзя работать с неисправными баллонами или баллонами, которые не проверялись в течение длительного времени;
- нельзя исправлять вентиль баллона собственными силами;
- отбирая сжатый или жидкий газ в реакционный сосуд, следует предварительно пропустить этот газ через предохранительную склянку;
- баллоны со сжиженными газами, имеющие сифонные трубки, при работе следует переворачивать; это предохраняет от выбрасывания из баллона струи сжиженного газа.
Рис. 7.11.1. Редуктор и его крепление к газовому баллону:
/ — баллон; 2 — горловина баллона; 3 — накидная гайка редуктора;
4 — корпус вентиля баллона; 5 — маховичок; 6 — маномегр высокого давления; 7 — манометр низкого давления;
8 — редукционный вентиль (редуктор);
9 — регулировочный винт; 10 — штуцер
7.12. Индивидуальные средства защиты
Для защиты органов дыхания, глаз и кожи лица от воздействия вредных веществ, содержащихся в воздухе в виде паров и аэрозолей (пыли, дыма, тумана), предназначены промышленные фильтрующие противогазы, которые являются средством индивидуального пользования. В комплект такого противогаза входят фильтрующая коробка цилиндрической формы, резиновая маска-шлем с гофрированной грубкой и сумка (для ношения противогаза). Маска-шлем выпускается пяти размеров (0, 1, 2, 3, 4).
Противогазы марок А, В, Г, Е, КД, на коробке которых имеется белая вертикальная полоса, защищают одновременно от пыли, дыма, тумана (табл. 7.12.1).
Таблица 7.12.1
Фильтрующие противогазы и вещества, от которых они защищают
Марка коробки противогаза Окраска фильтрующей коробки к противогазам Вредные вещества, от которых защищает противогаз
А Коричневая Пары органических веществ: бензина, керосина, ацетона, бензола, ксилола, сероуглерода, толуола, спиртов, эфиров, анилина, нитросоединений бензола и его гомологов, галогенорганических соединений, тетраэтилсвинца
В Желтая Кислые газы: сернистый газ, хлор, сероводород, циановодород, оксиды азота, хлороводород, фосген
Г Желтая с черной полосой Пары ртути
Е Черная Мышьяковистый и фосфористый водород
кд Серая Аммиак и его смесь с сероводородом
СО Белая Оксид углерода(П)
1216
Новый справочник химика и технолога
Окончание табл. 7.12.1
Марка коробки противогаза Окраска фильтрующей коробки к противогазам Вредные вещества, от которых защищает противогаз
М* Красная Кислые газы, мышьяковистый водород, аммиак, смесь сероводорода с аммиаком, оксид углерода(П) (меньшее время защитного действия, чем у коробок марок В, Е, КД, СО)
БКФ Защитная с белой вертикальной полосой Кислые газы и пары органических веществ (с меньшим временем защитного действия, чем у коробок марок В и А), мышьяковистый и фосфористый водород, циановодород
* При наличии в воздухе органических веществ пользование коробками марки М запрещается.
Фильтрующие респираторы — небольшие фильтры, расположенные на полумаске, отделяющей от загрязненной атмосферы только органы дыхания.
Респираторы бывают противопылевые, противогазовые, универсальные. При больших концентрациях пыли наиболее часто используют респираторы типа Ф-62Ш, при средних концентрациях — У-2К, при одноразовом использовании — респиратор типа «Лепесток».
Респиратор Ф-62Ш — резиновая полумаска со съемной пластмассовой коробкой, в которой находятся съемные фильтры. В нижней части полумаски смонтирован выдыхательный клапан.
Респиратор У-2К изготовлен из мягкого фильтрующего материала, покрытого поролоном. Внутренняя часть полумаски изготовлена из полиэтиленовой пленки. Респиратор имеет два вдыхательных и один выдыхательный клапаны.
Респиратор «Лепесток» — кусок мягкого фильтрующего материала с небольшим каркасом из пластмассы (или без него).
Противогазовые респираторы предназначены для защиты органов дыхания от не действующих на глаза паро- и газообразных веществ (при небольшой концентрации в воздухе). Противогазовый респиратор типа РПГ-67 представляет собой резиновую полумаску с двумя резиновыми муфтами по бокам. В муфты вставлены сменные цилиндрические патроны из картона или пластмассы, содержащие сорбенты.
Универсальные респираторы применяют при небольшом содержании вредных газов, паров и пыли в воздухе. Универсальный респиратор РУ-60М представляет собой резиновую полумаску со сменными противогазовыми патронами, содержащими сорбент и аэрозольный фильтр.
Противогазовые и универсальные респираторы снабжены патронами различных марок: А, В, Г, КД и Г. Каждый патрон используется строго по назначению (табл. 7.13.2).
Респираторы запрещается применять для защиты органов дыхания от высокотоксичных веществ (циановодород, арсин и фтороводород), а также веществ, которые в паро- и газообразном состоянии могут проникать в организм через кожу.
Таблица 7.13.2
Фильтрующие патроны респиратора РУ-60М и вещества, от которых они защищают
Марка патрона Надпись в центре крышки патрона Перечень вредных веществ, от которых защищает респиратор
А РУ-60М-А Аэрозоли и пары бензина, хлорэтана, ацетона, бензола и др.
В РУ-60М-В Аэрозоли и кислые газы (ангидриды)
КД РУ-60М-КД Аэрозоли, аммиак, сероводород
Г РУ-60М-Г Аэрозоли и пары ртути
7.13. Средства пожаротушения
Существует несколько типов огнетушителей: пенные (химически пенный ОХП-10, углекислотные ОУ-1, ОУ-2, ОУ-3, ОУ-5, ОУ-8, порошковые ОП-16, ОПУ-2-02, ОП-5, ОП-10).
Универсальное средство гашения — песок. Он должен быть чистым, сухим, сыпучим и находиться в специально отведенных ящиках.
Для ликвидации небольших очагов пожара (особенно при загорании жидкостей в открытых сосудах) можно пользоваться асбестом, огнестойкими накидками из войлока или толстой шерстяной тканью (одеялом), пропитанными специальным составом.
Литература
1. Алексеев В.Н. Количественный анализ. М.: Химия, 1972. 504 с.
2. Аналитический контроль производства искусственных волокон / Под ред. А.К. Дибровой, В.С. Матвеевой. М.: Химия, 1986. 336 с.
3. Аппен А.А. Химия стекла. Л.: Химия, 1974. 351 с.
4. Артеменко А.И., Тикунова И.В., Малеванный В.А. Справочное руководство по химии. М.: Высш, шк., 2003. 367 с.
5. Воскресенский П.И. Техника лабораторных работ. М.: Химия, 1973. 717 с.
Краткие сведения о технике лабораторных работ
Y2A1
6. Иванюков Д.В., Фридман М.Л. Полипропилен. М.: 1974. 270 с.
7. Измерения массы, плотности и вязкости / Под ред. Ю.В. Тарбеева. М.: Изд-во стандартов, 1988. 176 с.
8. Коростылев П.П. Техника лабораторных работ в металлургическом анализе. М.: Металлургия, 1978. 200 с.
9. Лабораторная техника органической химии / Под ред. Б. Кейла. М.: Мир, 1966. 751 с.
10. Мусакин А.П., Рачинский Ф.Ю., Суглобова К.Д. Оборудование химических лабораторий. Л.: Химия, 1978.480 с.
11. Паншин Ю.А., Малкевич С.Г., Дунаевская Ц.С. Фторпласты. М.: Химия, 1978. 230 с.
12. Правдин П.В. Лабораторные приборы и оборудование из стекла и фарфора.: Справ, изд. М.: Химия, 1988. 336 с.
13. Спектроскопические методы определения следов элементов. М.: Мир, 1979. 495 с.
14. Сусленникова В.М., Киселева Е.К. Руководство по приготовлению титрованных растворов. Л.: Химия, 1978. 184 с.
ГОСТ 8682-70 Посуда и оборудование лабораторные стеклянные. Конусы взаимозаменяемые. Основные размеры и технические требования, методы испытаний и маркировка.
ГОСТ 1770-74 Посуда мерная лабораторная стеклянная. Цилиндры, мензурки, колбы, пробирки. Технические условия.
ГОСТ 21400-75 Химико-лабораторное стекло.
ГОСТ 8.234-77 Государственная система обеспечения единства измерений. Меры вместимости стеклянные. Методы и средства поверки.
ГОСТ 9147-80 Посуда и оборудование лабораторные фарфоровые. Технические условия
ГОСТ 7328-82 Меры массы общего назначения и образцовые. Технические условия.
ГОСТ 25336-82 Посуда и оборудование лабораторные стеклянные. Типы, основные параметры и размеры.
ГОСТ 24104-88 Весы лабораторные общего назначения и образцовые. Общие технические условия.
ГОСТ 23932-90 Посуда и оборудование лабораторные стеклянные. Общие технические условия.
ГОСТ 19908-90 Тигли, чаши, стаканы, колбы, воронки, пробирки и наконечники из прозрачного кварцевого стекла. Общие технические условия.
ГОСТ 29251-91 Посуда лабораторная стеклянная.
Бюретки. Часть 1. Общие требования.
ГОСТ 29252-91 Посуда лабораторная стеклянная. Бюретки. Часть 2. Бюретки без установленного времени ожидания.
ГОСТ 29253-91 Посуда лабораторная стеклянная. Бюретки. Часть 3. Бюретки с временем ожидания 30 с.
ГОСТ 29227-91 Посуда лабораторная стеклянная.
Пипетки градуированные. Часть 1. Общие требования.
ГОСТ 29228-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 2. Пипетки градуированные без установленного времени ожидания.
ГОСТ 29229-91 Посуда лабораторная стеклянная. Пипетки градуированные. Часть 3. Пипетки градуированные с временем ожидания 15 с.
ГОСТ 29230-91 Посуда лабораторная стеклянная.
Пипетки градуированные. Часть 4. Пипетки выдувные.
ГОСТ 29169-91 Посуда лабораторная стеклянная. Пипетки с одной отметкой.
ГОСТ 29044-91 Посуда лабораторная стеклянная. Принципы устройства и конструирования мерной посуды.
ГОСТ Р 51592-2000 Вода. Общие требования к отбору проб.
Раздел 8. ОСНОВЫ ТЕХНОЛОГИИ
Автор: д. т. н., проф. Б.П. Саушкин
Список используемых сокращений и обозначений
БИС — большая интегральная схема
ВП — возвратно-поступательное движение
ВПК — вектор показателей качества
ГАЗ — гибкий автоматизированный завод
ГАУ — гибкая автоматизированная линия или участок
ГАЦ — гибкий автоматизированный цех
ГП — гибкое производство
ГПМ — гибкий производственный модуль
ГПС — гибкая производственная система
ЗУ — запоминающее устройство
ИВЦ — информационно-вычислительный центр
ИО — исполнительные органы
ИР — информационные ресурсы
ИС — интегральная схема
ИТ — информационная технология
КИМ — коэффициент использования материалов
ЛПР — лицо, принимающее решение
ЛЭП — линия электропередачи
М — возмущающие воздействия
МАК — машинно-аппаратурный комплекс
МО — метод обработки
МР — материальные ресурсы
МЭИ — межэлектродный промежуток
НТР — новое техническое решение
ОУ — объект управления
ПП — производственный процесс
ППД — поверхностно-пластическое деформирование
ПРР — погрузочно-разгрузочные работы
ИТО — парк технологического оборудования предприятия
САПР ТП — система автоматизированного проектирования технологических процессов
СБИС — сверхбольшие интегральные схемы
СО — способ обработки
СПУ — система программного управления
СУ — система управления
ТМ — технологический модуль
ТО — технологическая операция
ТП — технологический процесс
ТР — трудовые ресурсы
ТС — технологическая система
ТЭР — транспортно-экспедиционные работы
УУ — устройство управления
ФРС — фоторезистивный слой
ФТЭ — физико-технический эффект
ХТЭ — химико-технический эффект
ЧПУ — числовое программное управление
ЭИ — электрод-инструмент
ЭП — эвристический прием
ЭР — энергетические ресурсы
ЭХРО — электрохимическая размерная обработка
8.1. Технология как особая форма движения материи
8.1.1. Зарождение и развитие технологической деятельности человека
В практической деятельности человек ставит перед собой конкретные цели, направленные на удовлетворение различных нужд и обеспечение жизнедеятельности путем создания искусственных предметов утилитарного назначения. Для достижения этих целей необходимы определенные методы и средства.
Совокупность методов, способов, приемов предметной деятельности называют технологией, а совокупность средств достижения цели — техникой. Существует ряд других эмпирических определений технологии.
Технология — совокупность приемов и способов получения, обработки или переработки сырья, материалов, полуфабрикатов или изделий в различных отраслях промышленности.
Технология — наука, которая разрабатывает способы переработки природных тел в целесообразные формы (В.И. Северин).
Технология — это организация естественных процессов, направленная на создание искусственных объектов.
Несмотря на внешнее различие процитированных определений, в них есть общее: технология представля
Основы технологии
1219
ется как процесс целенаправленного изменения свойств материальных объектов. Следовательно, для ее определения необходимо знать элементы такого процесса (методы, способы, приемы) и характер изменения свойств материальных объектов в результате технологического взаимодействия.
Технологические навыки, эмпирическая технология сопутствовали человеку с ранних стадий формирования человеческих сообществ. Однако считается, что технологическая наука (теория) возникла в 1-м тысячелетии до н. э., и связано это с появлением орудий труда из железа. При обосновании этого предположения выдвигаются два основных аргумента:
- в это время знание (наука) приобретает статус особого вида духовной (умственной) деятельности людей;
- происходит интеграция рационально-практических знаний в некоторую теорию.
Дальнейшее развитие технологической науки происходило путем накопления опытных данных вплоть до XVIII в., когда промышленная революция в Англии резко повысила социальный интерес к технологии и промышленному оборудованию. Многие ученые обстоятельно занялись изучением ремесел. В это же время появился термин «технология». В 1772 г. профессор Геттингенского университета И. Бекман определил технологию как ремесленное искусство, включающее соответствующие навыки человека, эмпирические представления об орудиях и трудовых операциях. Именно в этот период выделяется научно-профессиональная деятельность, которая начинает генерировать технологические знания.
Создателем технологической науки в России считается М.В. Ломоносов, написавший целый ряд трудов, в том числе «Курс истинной физической химии» (1752) и «Первые основания металлургии или рудных дел» (1763). В последней книге им разработаны научные основы металлургии.
Начала химической технологии были обобщены, по-видимому впервые, немецким ученым И. Гмелиным в книге «Руководство по технической химии» (1795). В начале XIX в. химическую технологию уже читают как дисциплину в ведущих технических учебных заведениях Европы.
Возникновение научной технологии машиностроения (обработка металлов резанием) относят к концу XIX в. Значительный вклад в создание теории этой технологической дисциплины внес И.А. Тиме. Он провел ряд технологических исследований, результаты которых отражены в трудах: «Сопротивление металлов и дерева резанию. Теория резания и приложение ее к машинам-орудиям» (1870), «Мемуар о строгании металлов» (1877), «Основы машиностроения» (1885).
Для XX в. характер но бурное развитие техники и технологии, что позволяет говорить о научно-технической революции в общественном производстве. Заметно продвинулись вперед традиционные технологические науки, выделились и развились новые области техноло
гии (производство электронных приборов, средств управления, в том числе ЭВМ, аэрокосмической техники и технологии), произошло глубокое проникновение технологической методологии в такие сферы, как медицина, биология, социология.
Особенностью современной технологии является все более широкое привлечение фундаментальных знаний и соответствующих наук для решения технологических задач. Технология стала наукоемкой. Все в большей степени используются новейшие физические, химические эффекты для получения технологического результата, сокращается время между получением нового результата в фундаментальных науках и его технологическим применением. Так, например, завершение основополагающих работ в квантовой электронике, посвященных эффекту усиления света, датируют 1960 г. (в этом году создан первый лазер на рубине). В настоящее время лазерная индустрия, включающая в себя как производство, так и разнообразное прикладное применение лазеров, может рассматриваться как отдельная отрасль технологии с развитой инфраструктурой.
Если темпы развития технологических наук не замедлятся в результате ограничений, обсуждаемых ниже, то можно прогнозировать следующее. К концу XXI в. появятся самовоспроизводящие технологии как следствие полной расшифровки миссии генов, разовьется генная инженерия, будет освоен синтез белка. Предполагается, что в 2180-2230 гг. произойдет передача интеллектуальных способностей человека технике, основанной на биотропных технологиях (этап биоин-теллектуальной революции).
Динамику развития технологии можно представить в виде упрощенной математической модели. Если допустить, что основные научные результаты (в том числе технологические) адекватно отражаются в научных публикациях (книги, статьи, патенты) и существует корреляция между степенью прогресса в данной научной области и скоростью нарастания числа публикаций по этому направлению, то можно использовать модель, предложенную В.В. Налимовым.
Эта модель основана на гипотезе, согласно которой скорость изменения числа научных результатов (публикаций об этих результатах) пропорциональна их мгновенному значению^:
= (*>0). (8.1.1)
dt
Действительно, каждый научный результат вызывает отклики (результаты-следствия), развивающие данное направление и увеличивающие общий объем научных знаний. Решив это уравнение, получим закон экспоненциального роста научных знаний:
у = A exp(kt),
где к, А — некоторые постоянные величины.
1220
Новый справочник химика и технолога
Справедливость данного закона подтверждается анализом ряда научных направлений в начальный период их развития. При действии этого закона удвоение научных знаний происходит очень быстро — в течение 5-10 лет. Очевидно, это требует привлечения в данную область деятельности все новых и новых материальных и трудовых ресурсов. В качестве иллюстрации на рис. 8.1.1 представлена динамика суммарных затрат на НИОКР в США в 1920-х—1960-х гг., отражающая прогресс научных знаний. Однако ресурсы, которые общество в состоянии выделить на развитие данного научного направления, ограниченны. В результате рано или поздно экспоненциальный закон развития нарушается. В простейшем случае, если потенциальные возможности прогресса в какой-то области исчерпываются, экспонента заменяется линейной функцией dy/dt = const.
В общем случае может происходить замедление прогресса в данной области науки. Этот процесс описывается уравнением
0<y<b, к>0. (8.1.2)
dt
Его решение описывается логистической зависимостью вида:
Ь
У~ \ + Ae~khl ’
На рис. 8.1.2 приведено графическое изображение трех рассмотренных вариантов развития научного направления. Анализ показывает, что развитие технологических знаний также подчиняется описанным закономерностям. Как правило, новое технологическое направление быстро развивается в течение некоторого времени после своего зарождения. Затем темп развития этой области знаний начинает снижаться.
В заключение сделаем несколько общих замечаний. Экспонента (кривая 7) дает хорошее объяснение прогресса науки на микроуровне при изучении развития отдельных узких научных направлений и дисциплин за небольшой промежуток времени. Для описания развития крупных направлений за длительный период времени используют выражения вида
У„=24ехр[Л,(/-(,)], /=о (0.1.3)
к, < 0, (/-/,)> О,
где (J - tt) задает смещение начала отсчета экспонент роста в различных странах и в разных узких областях, формирующих данное укрупненное направление.
Скорость нарастания научных результатов (знаний) по отдельным направлениям или дисциплинам может служить мерой их актуальности, общественной потребности в них в данное время.
Анализ динамики развития научных направлений, отраслей позволяет прогнозировать общий уровень научных результатов, общественную потребность в них, необходимые затраты на их развитие.
Конечно, рассмотренная выше модель справедлива лишь при нормальных условиях развития общества и предполагает отсутствие в рассматриваемом интервале времени социально-экономических катаклизмов, при которых из-за резкого снижения материальных, энергетических и трудовых ресурсов, направляемых в данную сферу общественного производства, прирост новых знаний может вообще прекратиться. Более того, возможна частичная потеря ранее полученных знаний (dyldt < 0) в результате, например, массовой миграции специалистов, оттока способной молодежи, снижения уровня специальной подготовки, исключения из сферы производства уникального оборудования. Такого рода тенденция проявилась, по всей видимости, в последнем
Рис. 8.1.1. Динамика суммарных расходов на НИОКР в США
Рис. 8.1.2. Варианты развития научного направления:
экспонента (7); экспонента, переходящая в линейную
функцию (2); логистическая кривая (3)
Основы технологии
1221
десятилетии XX в. в государствах СНГ. Так, известно, что уже к концу 1996 г. оборонная промышленность России безвозвратно потеряла около 300 уникальных технологий.
8.1.2. Техника и технология — две стороны производственной деятельности людей
С философской точки зрения противоречия, постоянно возникающие между социальной сферой (обществом) и природой, разрешаются через промежуточную фазу, где специфически сливаются природное и социальное, посредством технической формы материи и технологической формы ее движения. Таким образом, технику рассматривают как специфическую (техническую) форму материи, а технологию — как форму ее движения. Техника как совокупность средств деятельности не имеет значения, она приобретает социальную значимость тогда, когда движение всей ее структуры подчинено технологическим функциям. Следовательно, в диалектике развития техники и технологии последняя всегда остается главной, доминирующей стороной.
Развитие технических средств в конечном счете всегда подчинено технологическим задачам. Необходимо подчеркнуть единство, взаимосвязь техники и технологии: нет технологии без технического объекта, так же как нет технического объекта без технологии, поскольку технический объект создается с целью проявить себя в движении.
Технология как особая форма движения материи (технологическая) — это прогрессирующая и управляемая человеком природно-социальная совокупность процессов целенаправленного изменения различных форм (механических, физических, химических, биологических) вещества, энергии, информации, протекающая в системах техники в соответствии с их специфическими законами строения и функционирования. По-видимому, это наиболее обобщенное определение технологии, сформулированное на философском уровне.
Заметим, что в качестве объектов деятельности, включенных в технологическое движение, в технологии выступают вещество, энергия и информация.
Как правило, в технических системах преобразования этих компонентов происходят одновременно, причем одно из таких преобразований отражает технологическую функцию технической систеы, а другие являются сопутствующими, в ряде случаев негативными с точки зрения эффективного достижения технологической цели.
В настоящее время считается, что предметом изучения инженерно-технологических дисциплин являются теоретико-технологические, общенаучные и инженерно-методические знания, на основе которых разрабатываются технологические методы, способы и теории расчета, проектирования, организации и управления технологическими процессами с целью их постоянной социально-экономической оптимизации. Следовательно, в любой технологии можно выделить ее теоретическую (научную) и инженерную стороны. Предмет
теоретической технологии — это анализ соотношений между исходным набором физических (химических, биологических) явлений, исходным набором веществ (энергических или информационных потоков) и базовыми принципами организации процессов. Объектом исследований при этом является теоретическая модель технологического процесса.
Инженерная технология представляет собой реализацию теоретических знаний, трансформирование их в эффективные методы, способы и методики расчета, проектирования, организации и управления производственным процессом.
8.1.3. Классификация технологий и основные технологические законы
Из сказанного выше следует, что технология как научная дисциплина включает в себя комплекс знаний, воплощенных в методах, способах, приемах труда, наборах материально-вещественных факторов производства, способах их соединения для создания какого-либо продукта или услуги. Авторы работы выделяют следующие наиболее существенные аспекты такого определения технологии:
• технология неразрывно связана с некоторым процессом как совокупностью взаимосвязанных действий, осуществляемых во времени;
• технология реализуется в искусственных системах, созданных человеком для удовлетворения каких-то потребностей ;
• новые технологии появляются тогда, когда возникают новые общественные потребности.
Следовательно, понятие «технология» применимо к любым процессам, имеющим искусственное происхождение (см. 8.5).
Анализируя различные определения понятия «технология», можно выделить основные компоненты, формирующие его. Это объекты, состояние которых целенаправленно искусственно изменяется; процессы и вытекающие из них методы и способы воздействия на эти объекты; средства реализации технологических воздействий; правила и процедуры сочетания, упорядочивания, согласования технологических воздействий на объект производства. Выделение указанных компонентов позволяет сформулировать классификационные признаки и построить классификацию технологий.
А. По характеру объекта технологического воздействия можно, следуя Н. Винеру, представить три основные группы технологий:
* Встречаются и исключения из этого правила. Например,
электрохимическая размерная обработка токопроводящих
материалов была предложена В.Н. Гусевым и Л.А. Рожковым
в 1928 г., но соответствующая технология получила практи-
ческое применение лишь в 1960-е гг., когда возникла потреб-
ность в производстве нового поколения авиадвигателей
и изделий космической техники.
1222
Новый справочник химика и технолога
• технологии перерабатывающие (изменение состояние вещества);
• технологии энергетические (превращение энергии);
• технологии информационные (накопление, преобразование, передача, хранение информации).
Как уже отмечалось, «чистые» виды технологического движения почти не встречаются — основному, функциональному виду движения всегда сопутствуют один или два других.
Очевидно, конкретизируя объекты технологического воздействия на разных уровнях обобщения, можно получить развернутый классификатор для каждой из основных групп технологий. Например, общественное разделение труда в области обрабатывающих технологий позволяет естественно классифицировать эти технологии по признаку вида человеческой деятельности (обработка группы функционально близких объектов). Одна из первых классификаций такого рода имела следующий вид:
• металлургические технологии;
• машиностроительные технологии;
• горно-добывающие технологии;
• технологии топлив;
• деревообрабатывающие технологии;
• технологии переработки пищевого сырья;
• химические технологии;
• переработка продуктов животноводства;
• текстильное и обувное производство;
• производство бумаги и изделий из нее.
По мере развития цивилизации такой классификатор постоянно пополняется в связи с появлением новых объектов производства. Дальнейшую детализацию технологий произведем на примере машиностроительного производства:
• станкостроительные технологии;
• энергомашиностроение;
• тракторостроение и производство сельскохозяйственной техники;
• авиа- и ракетостроение;
• судостроительные технологии;
• оружейное производство;
• химическое и пищевое машиностроение;
• автомобилестроение.
Далее в области авиастроения, например, можно выделить производство самолетов, авиадвигателе- и агрегатостроение, авиационное приборостроение. Ясно, что, продолжая сужение предметной области, мы в конечном счете придем к технологиям производства конкретных изделий.
Б. По характеру изменения состояния предмета деятельности (цель воздействия) в результате его участия в технологическом движении выделяют технологии с такими специфическими формами технологического движения, как получение, преобразование, хранение, транспортировка, накопление вещества, энергии, информации. Перечисленные формы движения
выражают качественные, количественные или пространственно-временные изменения состояния объекта производства.
В. По характеру процессов, ответственных за результат технологического воздействия, выделяют технологии механические, физические, химические, биологические, комбинированные.
Для обрабатывающих технологий часто рассматривают в качестве классификационного признака степень проникновения в структуру вещества при технологическом воздействии:
• макротехнологический уровень с механическим воздействием на предмет труда;
• микротехнологии с более глубоким воздействием на структуру материала;
• нанотехнологии, т. е. технологии молекулярного уровня (химические, биологические);
• технологии атомного уровня;
• технологии уровня атомного ядра.
Процессы технологического воздействия на объект производства могут по-разному протекать во времени. Можно выделить две группы технологий:
• технологии непрерывного воздействия на объект;
• технологии дискретного воздействия.
Предполагается, что изменение первоначальных свойств объекта производства при реализации технологии второй группы имеет несколько последовательных стадий с паузами между ними.
Г. По признаку, отражающему уровень качества управления технологическим процессом, выделяют технологии частично и полностью механизированные, частично и полностью автоматизированные. Такая классификация отражает естественный исторический процесс изменения характера участия человека в производстве: человек не только постепенно освободился от непосредственного воздействия на объект труда, но и оставляет за собой все менее конкретные (но более содержательные) функции управления.
Для достаточно узких предметных областей технологического движения разработаны конкретные классификаторы технологических процессов.
При представлении технологии в качестве научной дисциплины выделяются специфические законы:
• закон стоимостной переменной, устанавливающий максимально допустимые затраты на производство, определяемые рыночной стоимостью продукта. Никакие технологии или технологические разработки не имеют право на реализацию, если стоимость производимого продукта выше некоторого допустимого уровня;
• закон экономии рабочего времени и повышения производительности труда, отражающий тенденцию к экономии прошлого и настоящего труда в технологических системах как за счет снижения ресурсоемкое™ производства, так и за счет повышения качества производимого продукта. Таким образом, его можно трактовать как закон повышения производительности труда — обобщенной меры его качества;
Основы технологии
1223
• закон спиралевидного развития качества технологий, выступающий как специфическое проявление всеобщего закона развития в технологических системах;
• закон большого числа переменных, устанавливающий возможность учета ограниченного числа доминирующих переменных при анализе технологических объектов;
• закон шкального эффекта, рассматривающийся как проявление более общего закона перехода количества в качество на определенной стадии количественных изменений в технологических системах;
• закон автоматизации, устанавливающий, что изменчивость может удерживаться в заданных пределах только в автоматизированных процессах. Следовательно, развитие технологии неразрывно связано с повышением уровня автоматизации технологических систем.
Представленные законы отражают наиболее общие, существенные связи и отношения, проявляющиеся при движении технической формы материи. Они позволяют сформулировать следующие закономерности развития технологических и технических объектов, приобретающие существенное значение при анализе эволюции технологий и их прогнозировании:
• закономерность перехода от эмпирических к научным методам производства, которая предполагает все большее привлечение фундаментальных наук к решению прикладных, производственных задач и развитие на их основе собственной научной базы отдельных технологических дисциплин. Вместе с тем чрезвычайная сложность многих технологических объектов затрудняет их аналитическое описание или делает его весьма дорогостоящим. Этим объясняется относительно высокий уровень применения эмпирических знаний в современных технологиях;
• закономерность внедрения непрерывных процессов производства вместо дискретных, которая представляет собой проявление закона ресурсосбережения, рассмотренного выше, поскольку непрерывные (поточные) процессы обеспечивают предпочтительные экономические показатели;
• закономерность увеличения объема использования низкокачественного исходного сырья, которая отражает противоречие между стремлением к росту потребления и конечным, ограниченным характером материальных ресурсов;
• закономерность перехода к малоотходным и безотходным технологиям, котрая связана с глубокой переработкой сырья, полуфабрикатов, готовых продуктов производства;
• закономерность внедрения экологически чистых технологий, которая представляет собой проявление закона шкального эффекта и отражает тот факт, что количественная мера используемых человеком технологических, технических объектов (результаты их функционирования) породила новое качество — необратимые негативные изменения свойств окружающей среды, угрожающие существованию человеческого общества.
Конечно, рассмотренные выше законы и закономерности не отражают все многообразие явлений, присущих технологической форме движения материи. Систематизация и дальнейшее обобщение этих явлений — актуальная область истории и философии естествознания.
8.1.4. Понятийный аппарат технологии
Выше обсуждались общие представления о технологии, позволившие сформулировать это понятие, выявить взаимосвязь технологии и техники, описать основные закономерности, присущие этой специфической форме движения материи. Дальнейшее, более конкретное описание технологии требует введения основных понятий, определений, терминов, необходимых для рассмотрения различных аспектов технологического движения. Ограничим обсуждение этого вопроса обрабатывающими технологиями, понятийный аппарат которых наиболее полон и используется в качестве базы для всех других описанных видов технологий.
Воспользовавшись представлениями об основных компонентах, формирующих понятие «технология», выделим три взаимосвязанные группы понятий, описывающих соответственно содержательную, материальную и специфическую стороны технологии.
Содержательная сторона технологии включает в себя такие понятия, как «процесс», «метод», «способ», «прием».
Основным исходным понятием является процесс, под которым понимают ход какого-либо явления, последовательную смену состояний, стадий развития. Более строгое определение «процесса» представляет его как пространство состояний, функцию действия в этом пространстве и некоторые особые элементы пространства состояний, называемые начальными состояниями . Содержание любого процесса рассматривают во времени и пространстве, получая соответственно динамическую и статическую модели (описание) процесса. Именно процесс служит основой и выражением любого технологического движения. Однако сами по себе элементарные физические, химические, биологические процессы не имеют технологического содержания до тех пор, пока их протекание не будет связано с целенаправленным изменением свойств некоторого технологического объекта. В связи с этим введем понятия «метод обработки» и «способ обработки». Четкого разделения или общепринятого определения их в технологической литературе нет, они часто используются как синонимы.
Метод обработки (МО) — совокупность взаимосвязанных процессов физической, химической, биологической природы, совместное протекание которых приводит к заданному изменению состояния объекта производства. Следовательно, для метода обработки
* Под «процессом» понимают также совокупность после-
довательных действий, необходимых для достижения какого-
нибудь результата. В этом смысле говорят о производствен-
ном, технологическом процессе.
1224
Новый справочник химика и технолога
характерны три признака: перечень процессов той или иной природы, ответственных за заданное изменение состояния объекта; пространственно-временное взаимодействие этих процессов и. характер воздействия (изменения состояния объекта). МО дает широкое, общее представление о взаимодействии потоков энергии, генерируемых при протекании базовых процессов с веществом, преобразовании энергии в работу по изменению состояния вещества. Поэтому определение МО не включает в себя какие-либо ограничения или требования, конкретизирующие объект обработки , степень изменения его состояния, средства реализации или правила, регламентирующие их функционирование. Конкретизация перечисленных факторов порождает множество способов обработки. Можно сказать, что МО в известной степени инвариантен относительно свойств объекта.
Способ обработки (СО) — упорядоченная совокупность приемов воздействия на объект с целью заданного изменения его свойств, выполняемая с соблюдением определенных правил, условий, ограничений. Отличительными признаками СО являются перечень приемов воздействия, последовательность их выполнения, правила (условия, ограничения) выполнения и характер изменения свойств объекта.
Таким образом, МО отражает искусственный (технологический) характер протекания того или иного процесса, его целенаправленность. Следовательно, МО определяет целостный признак технологии, раскрывает ее природу, отражает общее, устойчивое в ней. Метод характеризует технологию на самом высоком абстрактном ее уровне. Способ есть форма выражения, конкретного проявления, специфическая разновидность метода. Каждый метод реализуется через множество способов. В способе можно выделить относительно устойчивые, повторяющиеся элементы с соответственной целевой функцией — приемы. Составную часть СО, описывающую протекание отдельной законченной стадии процесса преобразования свойств объекта, назовем приемом обработки. Иллюстрируем сказанное конкретным примером.
Процесс: электрический разряд в жидкой или газообразной диэлектрической среде. Естественно протекает в природе (молния). Имеет достаточно строгую физическую интерпретацию (рис. 8.1.3, а).
Метод обработки: электрический разряд в жидкой или газообразной диэлектрической среде, осуществляемый между двумя электропроводящими электродами с целью изменения конфигурации (электро-эрозионная обработка) или состояния поверхности (электроискровое легирование) одного из электродов. Несмотря на использование физически однотипных
Заметим, что такие ограничения могут вытекать из условий протекания базовых процессов данного МО. Например, электрические процессы предполагают использование электропроводных объектов.
процессов, указанные методы разделяют из-за различия в характере воздействия на обрабатываемый объект (рис. 8.1.3, б).
Способ обработки: электроэрозионная обработка непрофилированным электродом-проволокой. Способ заключается в том, что электрод-инструмент в виде бесконечной гибкой проволоки 1 перематывается между бобинами 2 и 3 со скоростью V) и перемещается относительно обрабатываемого электрода по заданной программе со скоростью V2. Рабочая часть электрода-проволоки перпендикулярна поверхности обрабатываемой детали-электрода 4. Электрическое напряжение, регулируемое в пределах 120-250 В, подается на электрод 4 и инструмент 1 через подвижный контакт 5. Обработка осуществляется в рабочей среде — смеси керосина и индустриального масла, подаваемой в зону обработки через сопло 6 (рис. 8.1.3, в).
Земля
Электрод 2
в
Электрод 1
Рис. 8.1.3. Естественный процесс разряда в газе (а), метод
электроэрозионной обработки (б), способ обработки
электродом-проволокой (в)
Основы технологии
1225
Приемы обработки: перемотка проволоки, подача напряжения на нее через подвижный контакт, перемещение проволоки по заданной траектории, подача рабочей среды в зону обработки, регулирование рабочего напряжения. Каждый из перечисленных приемов является законченной частью и вместе с тем необходимым элементом СО. Последний реализуется через последовательность приемов, выполняемых в определенном порядке, по определенным правилам, с учетом конкретных условий и ограничений. Каждый из выделенных приемов может быть описан с помощью элементарных действий — процедур.
Материальная сторона технологии выражается через технические объекты, реализующие разнообразные технологические функции посредством материальной структуры. Эти объекты (технологическое оборудование, средства технологического оснащения) называют технологическими машинами или аппаратами.
Машина — устройство, выполняющее механическое движение для преобразования вещества, энергии или информации.
Аппарат — устройство, в котором для преобразования вещества, энергии или информации используются физические, химические, биологические или комбинированные процессы.
Машинно-аппаратурный комплекс (линия) — совокупность машин, аппаратов, установленных в определенном порядке, связанных транспортной и управляющей системами и предназначенных для поэтапной реализации некоторой технологии.
Машинно-аппаратурные комплексы вместе со вспомогательным оборудованием и производственными площадями представляют организационно-структурные единицы современного предприятия — цехи, участки, заводы. Машины и аппараты, используемые в конкретных технологиях, часто называют в соответствии с их функциональным названием: станки, реакторы, печи, смесители и т. д.
Содержательная и материальная стороны технологии взаимосвязаны. Действительно, любой метод, способ обработки представляет собой, по сути дела, некий алгоритм, систему действий, выполняемых по определенным правилам, условиям и приводящих к заданному результату. Однако для реализации этого алгоритма необходима материальная структура. С другой стороны, любое средство технологического оснащения создается тогда и постольку, когда и поскольку требуется осуществить определенную систему действий над объектом производства. Указанные взаимосвязи выражают специфическую сторону (собственно технологическую) технологии.
Основным понятием этого аспекта технологии является технологическая система (ТС) — совокупность функционально взаимосвязанных процессов (методов, способов), материальных средств для их осуществления и предметов производства, предназначенная для получения законченного технологического результата. Данное определение дополняется или уточняется в отдельных
предметных областях технологии, но неизменным является его суть — это завершенный, содержащий все необходимые компоненты элемент технологии, способный осуществлять конкретные, заданные изменения свойств объекта производства, т. е. технологический процесс. Очевидно, ТС должна включать в себя людей (исполнителей, операторов), если она не является автоматизированной. Для описания ТС используют систему терминов и понятий — «производственный процесс», «технологический процесс», «технологическая операция», «модуль».
Производственный процесс (ПП) — совокупность действий людей и орудий труда, необходимых на данном предприятии для выпуска заданной продукции.
Технологический процесс (ТП) — часть производственного процесса, непосредственно связанная с изменением и контролем свойств предмета производства.
Технологической операцией (ТО) называют законченную часть технологического процесса, выполняемую на данном рабочем месте . Это понятие наиболее широко применяется в машиностроении, где используется более подробная редакция: технологическая операция — это часть технологического процесса, выполняемая непрерывно на одном рабочем месте, над одним или несколькими одновременно обрабатываемыми изделиями рабочим или группой рабочих. ТО является основной единицей производственного планирования и учета. На ее основе определяется трудоемкость изделия, устанавливаются нормы времени и расценки, требующееся количество рабочих, единиц оборудования, вспомогательных технологических средств и материалов, рассчитывается себестоимость обработки, осуществляется оперативное планирование производства, контроль качества и устанавливаются сроки выполнения работ.
Очевидно, элементами структуры операции являются один или несколько СО (алгоритм проведения работ), одна или несколько единиц оборудования (материальные средства реализации алгоритма). Содержательная сторона технологической операции отражается в специальном документе (карте, регламенте, инструкции).
Декомпозиция СО на приемы дает возможность выделить технологические элементы низшего уровня иерархии, составляющие в совокупности технологическую операцию. В машиностроении такие элементы называют переходами и широко используют в технологическом проектировании. В более широком смысле элементарную технологическую составляющую ТО, не подлежащую дальнейшей декомпозиции, называют технологическим модулем.
Технологический модуль (ТМ) — первичная технологическая составляющая операции, неразделимая во временном и аппаратном (по отношению к оборудованию) смысле, вызывающая идентифицируемый конкретный технологический результат.
* Рабочим местом называют часть производственной пло-
щади (или объема) с находящимся на ней основным и вспо-
могательным оборудованием.
1226
Новый справочник химика и технолога
Для пояснения сказанного представим себе, что изготавливается некоторая деталь, состоящая из нескольких взаимосвязанных поверхностей, путем последовательного удаления «лишнего» материала с исходной цилиндрической заготовки (рис. 8.1.4). Получение каждой из пронумерованных поверхностей дает идентифицируемый результат (изменилась конфигурация или свойства материала, что можно измерить и количественно оценить) и представляет собой ТМ. Совокупность модулей, выполняемых на одном и том же оборудовании (рабочем месте), составляет технологическую операцию.
Рис. 8.1.4. Деталь, заготовка и отдельные поверхности (1-8), обработка которых дает идентифицированный технологический результат
Используя сделанные выше определения, сформулируем понятие ТС в соответствии с имеющимся стандартом.
Технологическая система — это совокупность функционально взаимосвязанных средств технологического оснащения, предметов производства и исполнителей, предназначенная для выполнения в регламентированных условиях производства заданных ТП или ТО в соответствии с требованиями нормативно-технической документации. Таким образом, ТС — это обобщенное понятие, включающее в себя содержательную, материальную и специфическую стороны технологии. Более подробно многоаспектность понятия ТС рассматривается ниже.
Завершая определение основных понятий, уточним сущность объекта (предмета) производства. В процессе реализации любой перерабатывающей технологии происходит преобразование материальных структур. Физические процессы вызывают, как правило, изменение формы тела и его физических свойств, химические— приводят к изменению химического состава и внутреннего строения вещества, биохимические процессы реализуются на уровне
живой клетки. Объект производства до технологического воздействия на него будем называть исходным продуктом, сырьем. В большинстве случаев в качестве сырья выступают предметы минерального, растительного или животного происхождения. Сырьевые ресурсы чрезвычайно разнообразны по физическим, химическим, биологическим свойствам. Некоторые виды сырья породили целые отрасли промышленности и соответствующие технологии (нефть, каменный уголь, газ, древесина). Объект производства, находящийся в промежуточном состоянии между двумя следующими друг за другом воздействиями, часто называют полуфабрикатом. Наконец, объект производства, обладающий после завершения технологических воздействий конкретными потребительскими свойствами, называют конечным продуктом. Последний, как правило, непосредственно используется для удовлетворения нужд человека. Заметим, что в ряде случаев технологическая цепочка по преобразованию сырья в конечный продукт достаточно длинна и реализуется на нескольких предприятиях. Следовательно, исходным и (или) конечным продуктом соответствующих технологий будет являться полуфабрикат. Например, на заводах первичного виноделия производят переработку растительного сырья в виноматериал (полуфабрикат), который служит исходным продуктом для заводов розлива вин. После переработки виноматериала получают и расфасовывают вина различных марок, которые передают в торговую сеть для реализации в виде конечной продукции.
В заключение отметим, что все приведенные выше понятия, описывающие различные стороны технологии, иерархичны, т. е. соответствующие множества элементов упорядочены отношениями включения:
ТМ < ТО < ТП < ПП; П < СО < МО < ПР; М(А) < МАК < ПТО,
где МАК — машинно-аппаратурный комплекс; ПТО — парк технологического оборудования предприятия.
Указанная иерархия и взаимосвязи между иерархическими структурами иллюстрируются рис. 8.1.5. Так, на низшем уровне иерархии ТМ воплощает отдельные приемы, присущие СО, и реализуется функциональными составными частями технологического оборудования.
Процессы <=> ПП <=> Общезаводской парк оборудования
U U U
Методы <=> ТП <=> МАК
U U U
Способы о то <=> Машины, аппараты
U U U
Приемы и процедуры <=> ТМ <=> Составная часть машины
Рис. 8.1.5. Иерархия и взаимосвязь элементов различных аспектов технологии
Основы технологии
1227
8.1.5. Системное представление технологий
Из предыдущего обсуждения следует, что технологическая система представляет собой сложный организационно-технический объект искусственного происхождения, имеющий собственную структуру, реализующий достижение некоторой цели и обладающий рядом свойств. Рассмотрим наиболее общие свойства таких объектов, представляющие интерес с точки зрения их изучения, описания и развития.
1 . Целостность — это свойство ТС, отражающее обособленность от окружающей среды, относительную самостоятельность, автономность, возможность ее отдельного рассмотрения и описания. Предполагается, что ТС может быть отделена от среды некоторой гипотетической оболочкой, как нечто целое, а взаимодействие ее с этой средой осуществляется через внешние связи — входы и выходы ТС. Так, на рис. 8.1.6 представлена простейшая модель ТС, которая взаимодействует со своим окружением посредством входных и выходных материальных, энергетических, информационных потоков. Потребляя из среды перечисленные ресурсы, ТС воздействует на нее, выделяя конечный продукт (используемый вне ТС) и отходы производства.
2 . Многомерность отражает наличие в системе достаточно сложных составных частей, называемых подсистемами, которые взаимодействуют между собой за счет внутренних связей. Описывая выше ТС, мы, по сути дела, выделили содержательную, материально-техническую и собственно технологическую подсистемы в ней. Именно совокупность этих подсистем, взаимосвязь, взаимодействие между ними обеспечивают целенаправленное функционирование ТС.
Некоторыми учеными предложено более полное разделение ТС на отдельные подсистемы:
• технологическая подсистема включает в себя процессы, методы, способы, технологические воздействия, регламенты, режимы — так называемую технологическую среду;
• материально-техническая подсистема — это технологическое оборудование, оснастка, инструменты, исходные материалы, реагенты, полуфабрикаты, изделия;
• эргономическая включает в себя операторов, психофизиологические требования к ним, эргономические характеристики оборудования, т. е. эта подсистема отражает человеческий фактор в функционировании ТС;
• информационная подсистема — это базы данных, базы знаний, исходная информация, данные и модели, необходимые для контроля и управления ТП;
• организационная подсистема включает формы и методы организации ТП, нормирование количества и качества труда, социальные факторы;
• экономическая подсистема охватывает экономические цели, критерии, ограничения, накладываемые на ТП, его ресурсообеспечение, оценки эффективности функционирования ТС.
Очевидно, степень детализации и характер разделения ТС на подсистемы зависят от ее специфики и задач анализа. Например, для автоматизированных систем нет необходимости выделять эргономическую подсистему.
3. Иерархичность подразумевает возможность выделить подсистемы разного уровня в рамках данной системы или включить ее в более сложные структуры. Выше (рис. 8.1.5) рассмотрена иерархия отдельных подсистем ТС и показано, что элементарная ТС младшего ранга представляет собой технологический модуль. Дальнейшее деление нецелесообразно из-за отсутствия идентифицируемого технологического результата.
4. Эмерджентность отражает тот факт, что система в целом обладает качественно новыми свойствами, которых нет ни у одной из ее частей, взятых в отдельности.
5. Динамичность ТС проявляется прежде всего в том, что изменение свойств объекта производства протекает во времени. Другая сторона вопроса связана с изменением во времени свойств самих ТС, например в результате физического износа материальных средств производства.
Рис. 8.1.6. Модель технологической системы в виде «черного ящика»
1228
Новый справочник химика и технолога
6. Управляемость — это свойство ТС, отражающее возможность поддерживания высокой эффективности ее функционирования и адаптации к изменению внешней среды. Управление ТС реализуется за счет управляющих воздействий и наличия обратных связей между объектом и органом управления, связанных между собой информационными потоками. Подробнее эти вопросы обсуждаются в 8.2.5.
Сформулированные свойства технологических систем позволяют выявить в них общее, дать описание их функционирования. Основной функцией ТС будем считать преобразования входов в выходы, т. е. процесс функционирования ТС — это преобразование ресурсов на входе ТС в целевые конечные результаты на выходе из нее. Конкретизируем сказанное применительно к обрабатывающим технологиям, объектами производства в которых являются материальные тела.
Выделим наиболее значимые, существенные свойства объекта производства, изменяемые в результате функционирования ТС. Наборы таких свойств, соответствующие начальному и конечному состояниям обрабатываемого объекта, назовем векторами соответственно его исходных (Ло) и конечных (Ак) свойств. Тогда функция ТС может быть формально представлена в следующем виде:
ЛоТ^Л, (8.1.4)
где Т — технологический оператор, описывающий это преобразование.
Действительно, преобразование «вход => выход» в ТС, показанной на рис. 8.1.6, сводится к указанному изменению свойств объекта производства. Вообще говоря, состав и размерность векторов Ао и Ак могут не совпадать. В химических, пищевых и некоторых других технологиях в ТП участвуют несколько видов исходного сырья и (или) образуются различные конечные продукты. Это несколько усложняет выражения, описывающие функцию ТС, не изменяя сущности приводимых рассуждений.
Как уже говорилось, описанная выше трансформация состояния объекта производства в большинстве случаев осуществляется путем последовательных приближений в несколько стадий (например, операций):
Ло’Т]—Л1-Т2—>Л2; ...,
ЛМ-Т^Л. (8.1.5)
В таком случае технологический оператор Т выражается в виде совокупности операторов меньшего ранга ТА , описывающих изменения состояния объекта на отдельных стадиях:
Т = Т1лТ2лТз,...,лТ, (8.1.6)
Достижение заданного конечного результата является необходимым условием функционирования ТС, но не является достаточным. В связи с этим возникает вопрос
об эффективности функционирования ТС. В общем случае эффективность технологических систем рассматривают как отношение целевых конечных результатов к затратам ресурсов на их достижение (с учетом устранения негативных последствий функционирования системы). Таким образом, высокий уровень эффективности функционирования является определяющим фактором при выборе однопредметных ТС, а повышение этого уровня — целью развития, совершенствования ТС.
В заключение уточним понятие «структуры технологической системы». В общем виде структура любой системы представляется выражением
S - {3, С, О}, (8.1.7)
где Э = {эь э2, ..., э„} — множество элементов, составляющих систему; С = {с(э, )} — множество свойств этих элементов; О = {о(э„ э,)} — множество отношений между элементами; i = 1,2,..., n',j = 1, 2,..., и; &j.
Для того чтобы выделить элементы ТС, вернемся к ее определению, данному ранее. Очевидно, в качестве таких элементов можно принять составляющие отдельных подсистем ТС, как это показано на рис. 8.1.7:
Э] — подмножество элементов — объектов производства;
Э2 — подмножество средств технологического оснащения;
Э3 — подмножество элементов: процессов, методов, способов;
Э4 — подмножество элементов: регламенты, карты, инструкции, правила, ограничения.
Отношения оч между указанными подмножествами являются, как правило, двусторонними и выражают внутренние связи в системе.
Выбор конкретных элементов, входящих в указанные подмножества, определяется уровнем рассмотрения структуры ТС. Так, на уровне операции целесообразно за элементы структуры принять способы обработки, технологические машины или аппараты, операционные карты, регламенты, инструкции. Действительно, запись вида
Г Э*, э', эп‘, э", с(э^), с(э2), с(э3"), с(э; )? о —
^12’^21 ’^13’^31 ^14’^41 ’^23’^32 >
означает конкретную структуру технологической операции, в которой преобразуются свойства с(э*) объекта э* посредством способа э”, реализуемого аппаратом э2 по технологическому регламенту э", причем указанные элементы связаны отношениями оу. При этом
Э[ еЭ,,э2 еЭ2, ..., э4 еЭ4, i,j= 1; 2; 3; 4.
Приведенная запись структуры громоздка и неудоб-
на для оперативного использования. Поэтому для ана-
лиза структур технологических систем часто использу-
ют упрощенную запись, основанную на общепринятой
Основы технологии
1229
иерархии таких систем (рис. 8.1.5) и понятиях ТМ и ТО. Для этого за элементы ТС яг-го уровня принимают множество ТС (w l)-ro уровня. Структуру ТС w-ro уровня записывают в виде:
S„={TCW ь С, О}, (8.1.7а)
где ТСт 1 — множество технологических систем предыдущего иерархического уровня; СиО — соответственно множества свойств этих систем и отношений между ними.
Таким образом, структура технологической операции выражается через технологические модули, структура ТП — через ТО, высшие технологические структуры — через ТП. Такую структуру удобно представлять в виде ориентированного графа, вершинами которого являются элементы множества TCW i , а дуги, соединяющие эти вершины, — отношения, связи между элементами (например, отношения упорядочивания). Такой граф представлен на рис. 8.1.8. Как видно, возможный порядок следования отдельных операций регламентирован соответствующими дугами. Здесь / и 9 — начальная и конечная операции, 2-8 — возможные промежуточные операции. Из рис. 8.1.8 следует, что из вершины 7 в вершину 9 можно попасть различными путями. Это означает, что для многих технологий возможны несколько альтернативных структур. Следовательно, возникает проблема выбора наилучшей из них. Этот вопрос подробно обсуждается в 8.3.
Системное представление технологий позволяет использовать развитый методологический аппарат системного анализа для их изучения и проектирования, выявить наиболее общие закономерности их функционирования, обобщить с единых позиций богатый и многообразный эмпирический материал, накопленный в различных отраслях современного производства.
ЭЛ. Процессы, методы,способы
Оу
Эр Объекты производства
о
о-
Э4. Карты, регламенты, инструкции
Э2. Средства оснащения
о42
Рис. 8.1.7. Структурная схема технологической системы
Рис. 8.1.8. Структурный граф технологических альтернатив
Центральным, основополагающим звеном в системном представлении технологий является процесс, порождающий физико- или химико-технологический эффект, основанный на нем метод обработки с заданным технологическим результатом и совокупность способов реализации, проявления данного метода. Поиск или разработка новых физико(химико)-технологических эффектов — это один из магистральных путей развития современных технологий.
8.2. Анализ технологий
8.2.1. Основные процессы и методы обработки
В промышленном производстве используется множество разнообразных процессов. Напомним, что банк физико-технических эффектов, основанный на протекании процессов физической природы, содержит по различным данным от 3 до 5 тысяч описаний; информационный объем банка химико-технических эффектов примерно такой же. Выделим наиболее общие классификационные признаки, характеризующие множество процессов.
1. По характеру основных свойств входного потока веществ (исходного сырья) выделяют процессы переработки минерального, растительного и животного сырья, а также процессы переработки газообразных, жидких, твердых и комбинированных сред.
2. По характеру и утилитарному назначению выходного потока веществ различают процессы химических, пищевых, машиностроительных и других производств.
3. В зависимости от характера основных законов, определяющих скорость протекания процессов и их теоретическое описание, выделяют физические, химические, биологические, механические, тепловые, массообменные, комбинированные и прочие процессы.
4. По характеру протекания в пространстве и во времени процессы подразделяют на локальные и глобальные, стационарные и нестационарные, периодические и непрерывные, протекающие в объеме или на поверхности.
Обсуждая вопрос технологического применения процессов различной природы, необходимо помнить, что один и тот же технологический результат может быть следствием протекания различных процессов. Например, удалить слой металла с поверхности исходной заготовки можно путем силового воздействия со стороны более твердого тела-инструмента (процесс резания металлов), химическим или электрохимическим травлением поверхности, эрозионным воздействием электрического разряда или воздушных пузырьков (элек-троэрозионная и гидрокавитационная обработка).
С другой стороны, одни и те же процессы могут
дать различные технологические результаты. Напри-
мер, электрохимический процесс можно использовать
для изменения массы электродов (растворение или
осаждение металла на электродах) или для получения
1230
Новый справочник химика и технолога
газов: водорода, кислорода, хлора. Из сказанного следует, что каждый физико-химический процесс может входить в структуру нескольких методов обработки.
Воспользуемся вторым классификационным признаком для описания основных процессов различных производств. Для облегчения понимания сущности отдельных процессов и методов обработки будем использовать простейшие схемы, поясняющие их реализацию. Наиболее разнообразная группа процессов используется в химической технологии. Существует даже гипотеза, что жизнь на земле зародилась в результате протекания химических процессов. Так, экспериментально доказано, что в среде, содержащей воду, метан, водород, углекислый газ (первоначальная атмосфера Земли), под действием электрических разрядов (аналог молнии) образуются аминокислоты — основные элементы живой природы.
8.2.1. /. Процессы и методы химической технологии
Основой химической технологии являются химические процессы (превращения) различного типа, приводящие к получению некоторых конечных продуктов из исходных веществ. В общем виде химическую реакцию можно представить уравнением:
WjAi + /И2А2 + ... + w^A*
—*+ л2В2 + ... + «/В7, (8.2.1)
где тк, п} — стехиометрические коэффициенты; Ак, В7 — исходные и конечные вещества.
В химической кинетике все реакции делят на две группы: обратимые и необратимые. Реакции первого типа протекают одновременно и независимо как в прямом, так и в обратном направлении, что приводит в конечном счете к установлению динамического химического равновесия. При определенных условиях реакции протекают практически только в одном направлении. Как правило, это случается тогда, когда хотя бы один продукт выводится из сферы реакции, например выпадает в осадок или выделяется в газообразном состоянии. Такие реакции называются необратимыми и широко используются в технологии.
Скоростью химической реакции v называется количество молекул Аа данного вида, реагирующих в единицу времени в единице объема реакционного пространства. При расходовании исходного вещества Ак:
При постоянном объеме И реакционного пространства скорость реакции выражают через концентрации реагирующих веществ. Скорость химической реакции зависит от многих факторов: природы и концентрации реагентов, температуры, давления, присутствия и природы катализаторов и пр.
Основной постулат химической кинетики гласит, что скорость химической реакции пропорциональна концентрации реагирующих веществ, т. е.
v = kC%C%...C%, (8.2.3)
где к — константа скорости химической реакции, численно равная скорости реакции при условии, что концентрации реагирующих веществ равны единице; mt — числовые коэффициенты.
Влияние температуры на скорость химической реакции описывается известным уравнением Аррениуса:
< £ Л к = сехр---— ,
I RT
(8.2.4)
где с — предэкспоненциальный множитель; Еа — постоянная, называемая энергией активации; R — универсальная газовая постоянная; Т — температура, К.
Как видно, изменение температуры сильно влияет на скорость химической реакции: изменение температуры в арифметической прогрессии приводит к изменению величины к в геометрической прогрессии.
Влияние различных факторов на скорость химических реакций позволяет управлять процессом превращения веществ, находить оптимальные условия его проведения. Этот факт лежит в основе классификации химических процессов по условиям их проведения. Согласно этому признаку, химические процессы разделяют следующим образом: высокотемпературные, проводимые при повышенных или пониженных давлениях, электрохимические, плазмохимические, каталитические, радиационно-химические, фотохимические.
Наряду с химическими реакциями непосредственного превращения веществ, химические технологии включают в себя различные физические и физико-химические процессы, используемые, как правило, на стадиях подготовки сырья и выделения конечного продукта.
Механические процессы связаны с непосредственным (контактным) воздействием твердых тел (инструменты или рабочие органы машины) на обрабатываемый объект. В зависимости от требуемого изменения свойств этого объекта механические процессы делят на три группы: измельчение, перемешивание, классификация. Измельчение твердых тел осуществляют с целью увеличения поверхности контакта материала с технологической средой, т. к. от величины этой поверхности зависит производительность многих процессов (химических, диффузионных, тепловых). Для этого при воздействии инструмента в измельчаемом материале создаются напряжения того или иного вида, приводящие к разрушению этого материала. Результат воздействия характеризуется степенью измельчения Си, равной отношению среднего характерного размера кусков материала до измельчения D к соответствующему размеру d после измельчения. Работа внешних сил, затрачиваемая на измельчение, расходуется на объемную деформацию разрушаемых кусков и на образование новых поверхностей:
Основы технологии
1231
А = Адеф + А„,п. (8.2.5)
В зависимости от требований к геометрической форме измельченных кусков используют два способа измельчения: резание и дробление. Резание применяют при необходимости получения кусков регулярной геометрической формы (кубики, бруски, диски). Этот способ широко используют в пищевых технологиях, например для измельчения корнеплодов. Дробление применяют в случаях, когда регулярная геометрическая форма измельченных кусков не требуется. В связи с широким диапазоном изменения характерных размеров исходного и измельченного материала дробление условно делят на несколько видов (табл. 8.2.1).
Таблица 8.2.1
Виды дробления твердых материалов
Наименование вида дробления Размер, мм
до измельчения после измельчения
Крупное дробление Среднее дробление Мелкое дробление Тонкое измельчение Сверхтонкое измельчение 300-1500 100-300 10-50 2-10 (2-75)- 10’3 100-300 10-50 2-10 (2-75)- 10’3 Менее 10“3
Для пояснения некоторых способов дробления рассмотрим схемы двух распространенных дробилок. Валковая дробилка (рис. 8.2.1, а) состоит из пары встречно вращающихся цилиндрических или профилированных валков 7 и 2 с рабочим зазором а между ними. Исходный материал поступает из бункера 3, затягивается в зазор и измельчается в основном из-за сжимающих напряжений. Такие дробилки используют для измельчения материалов средней твердости при Си = 5-И5.
Шаровая мельница (рис. 8.2.1, б) представляет собой вращающийся барабан 7, заполненный мелющими телами 2 — стальными шарами диаметром 25-150 мм — примерно наполовину своего объема. При вращении барабана шары под действием центробежных сил увлекаются на высоту Л, падая с которой измельчают материал. Помимо этого происходит истирание материала о поверхность барабана и мелющих тел. Исходный материал поступает через загрузочное устройство в один из открытых торцов барабана, перемещается вдоль его оси за счет перепада уровней загрузки и выгрузки и выводится из машины под действием собственного веса или воздушным потоком. Такие мельницы применяют для тонкого измельчения.
Перемешивание твердых, сыпучих материалов выполняют для получения однородной смеси нескольких компонентов в смесителях различной конструкции. Смесители с вращающимися лопастными рабочими органами применяют также для приготовления густых и вязких тестообразных масс и паст.
Рис. 8.2.1. Схемы валковой дробилки (а), шаровой мельницы (б), установки для классификации (в)
Классификацией называют разделение твердых зернистых материалов на группы с различным размером зерен. Этот процесс используется, например, в технологии получения абразивных материалов различной зернистости. Для этого сыпучие материалы просеивают через набор сит 1-3 с различными размерами ячеек (рис. 8.2.1, в). Отбор фракций различной степени измельчения осуществляют в секциях 1-IV.
Тепловые процессы используют для изменения температуры обрабатываемого объекта (нагрев, охлаждение) и для осуществления фазовых превращений (выпаривание, конденсация). Перенос энергии в форме тепла, происходящий между телами, имеющими различную температуру, называют теплообменом. Существуют три принципиально разных вида теплообмена: теплопроводность, конвекция и тепловое излучение.
Теплопроводность — перенос тепла за счет движе-
ния микрочастиц (молекул, атомов, электронов), не-
посредственно соприкасающихся друг с другом. Это
1232
Новый справочник химика и технолога
основной вид теплопереноса в твердых телах. Процесс теплопроводности описывается законом Фурье, который гласит, что количество тепла q, передаваемого через единицу поверхности в единицу времени, т. е. плотность теплового потока, пропорционально температурному градиенту поверхности:
9 = (8.2.6)
ап
где А, — характерная для данного материала величина, называемая коэффициентом теплопроводности. При обычных температурах и давлении лучше всего проводят тепло металлы, а хуже всего — газы.
Конвекция — перенос тепла вследствие движения и перемешивания макроскопических объемов жидкости или газа. Конвекция бывает естественной и вынужденной.
Тепловое излучение — процесс распространения электромагнитных колебаний с различной длиной волны, обусловленный тепловым движением атомов или молекул излучающего тела. Все тела способны излучать и поглощать энергию, за счет чего и осуществляется лучистый теплообмен. В большинстве практически важных случаев перенос тепла происходит комбинированным путем с участием всех перечисленных видов теплообмена.
Если два жидких или газообразных тела (теплоносители) разделены твердым телом в виде плоской перегородки, то процесс переноса тепла в такой системе описывается уравнением теплопередачи, выражающим связь между тепловым потоком Q и поверхностью теплообмена F\
Q = kF&TcpT, (8.2.7)
где к — коэффициент теплопередачи; ДГср — средняя разность температур между теплоносителями или температурный напор; т — время.
Процессы теплопередачи широко распространены в химической технологии. Тепловые процессы осуществляются в специальных аппаратах — теплообменниках. Первичными источниками тепла в химической технологии служат продукты сгорания различных топлив или электроэнергия. Вещества, получающие тепло от первичных источников и передающие его нагреваемой среде через стенку теплообменника, называют промежуточными теплоносителями. В качестве последних при нагревании используют водяной пар, горячую воду, минеральные масла, органические жидкости, расплавы солей и металлов. При охлаждении применяют воду и воздух, лед, а для более глубокого охлаждения — пары низкокипящих жидкостей (аммиак), сжиженные газы (СО2) или холодильные рассолы. Наибольшее распространение в качестве промежуточного теплоносителя получил насыщенный водяной пар, обладающий рядом преимуществ: дешевизна, неток-сичность, возможность транспортировки на значительные расстояния и распределения по потребителям, простота регулировки температуры за счет изменения
давления, небольшой расход пара. Некоторые теплообменные аппараты представлены на рис. 8.2.2.
Кожухотрубчатый теплообменник (рис. 8.2.2, а) состоит из корпуса 7 с установленными в нем верхней и нижней трубными решетками 2 и 4, в которых закреплены трубы 3. Среды, обменивающиеся теплом, движутся противотоком: одна (I) — по системе труб, а другая (II) — по межтрубному пространству.
Двухтрубный теплообменник состоит из внутренних 1 и наружных 2 труб (рис. 8.2.2, б). Теплоноситель движется по внутренним трубам, а продукт — по межтрубному пространству.
В погружном змеевиковом теплообменнике (рис. 8.2.2, в) теплоноситель I движется по спиральному змеевику 7, изготовленному из трубы диаметром 20-75 мм и noipy-женному в жидкость II, находящуюся в корпусе 2.
Выпариванием называют процесс концентрирования малолетучих веществ в жидких летучих растворителях за счет частичного удаления растворителя из объема раствора при кипении последнего. Получение концентрированных растворов, практически сухих и кристаллических продуктов облегчает и удешевляет их транспортировку и хранение. Если начальная и конечная концентрации сухих веществ в растворе равны соответственно 60 и (масс. %) (под концентрацией сухих веществ понимают отношения их массы к общей массе раствора), в аппарат поступает GQ (кг/с) исходного раствора, а выводится 6* (кг/с) концентрата, то, учитывая неизменность массы сухих веществ, получим:
А.
СД = G.b.;G. = G()—;
ь (8.2.8)
w^G0-Gk =ед1--ч
где IV — масса выпаренного растворителя.Процесс выпаривания осуществляют под вакуумом, при атмосферном и повышенном давлениях. В последнем случае раствор кипит при более низких температурах, что позволяет использовать нагревающие агенты более низких параметров (температура, давление). На этом основано применение многокорпусных вакуум-выпарных установок (рис. 8.2.3), в которых достигается значительное снижение расхода греющего пара на единицу массы выпаренного растворителя за счет использования для обогрева каждого корпуса (кроме первого) вторичного пара предыдущего корпуса.
Греющий пар поступает в теплообменник корпуса 7 и доводит до кипения исходный раствор, предварительно подогретый в подогревателе 4. Вторичные пары первого корпуса направляются в нагреватель корпуса 2 и т. д.
Очевидно, это возможно лишь при соответствую-
щем снижении давления в рабочем пространстве кор-
пусов 2 и 3. Вторичный пар из последнего корпуса от-
водится в конденсатор 5, где создается требуемое
разрежение. Конденсат отводится в бассейн, а воздух
через ловушку-каплеуловитель 6 отсасывается вакуум-
насосом 7.
Основы технологии
1233
Рис. 8.2.2. Схемы теплообменников: кожухотрубчатого (а), типа «труба в трубе» (б) и змеевикового (в)
Рис. 8.2.3. Схема трехкорпусной вакуум-выпарной установки
Массообменные процессы характеризуются переходом одного или нескольких веществ из одной фазы в другую. Они сопровождаются переносом вещества в пределах одной фазы к границе раздела фаз, переносом его через эту границу и переносом вещества в пределах другой фазы. Перенос вещества в пределах одной фазы происходит по механизму молекулярной или конвективной диффузии. Молекулярная диффузия описывается первым законом Фика, который по аналогии с законом Фурье, приведенным выше, выражается линейным уравнением:
de
4m=-D — ’ (8-2-9)
dn
где qm — скорость молекулярной диффузии; D — коэффициент диффузии, м2/с; dc/dn — градиент концентраций переносимого вещества.
Скорость конвективного переноса вещества вместе с движущейся со скоростью wc средой в направлении потока среды:
<7К=«, (8.2.10)
где ск — коэффициент пропорциональности.
Суммарный перенос вещества за счет диффузии и конвекции описывается достаточно сложной системой уравнений, не имеющей аналитического решения.
В промышленности применяются семь основных процессов массопереноса.
1. Абсорбция — объемное поглощение газа жидкостью, т. с. процесс разделения, характеризуемый переходом вещества из газовой фазы в жидкую. Обратный процесс выделения газа из жидкости называется десорбцией. Указанные процессы осуществляются в аппаратах — абсорберах различной конструкции, обеспечивающих развитую поверхность соприкосновения между жидкостью и газом. Так, трубчатый абсорбер сходен по устройству с кожухотручатным теплообменником (рис. 8.2.2, а). Абсорбент поступает на верхнюю трубную решетку 2, распределяется по трубам 3 и стекает по ним в виде тонкой пленки. Газ движется по трубам снизу вверх. Для отвода тепла, выделяющегося при абсорбции, по межтрубному пространству циркулирует охлаждающий агент. Для увеличения поверхности соприкосновения фаз рабочее пространство абсорбера заполняют насадкой — твердыми инертными телами различной формы из металла, керамики, стекловолокна.
1234
Новый справочник химика и технолога
2. Перегонка — разделение жидких гомогенных смесей путем одно- или многократного взаимного обмена компонентами между жидкой и паровой фазами, движущимися обычно противотоком. Разделение перегонкой основано на различной летучести компонентов смеси при одной и той же температуре. Если исходная смесь состоит только из двух компонентов, то при ее перегонке паровая фаза обогащается низкокипящим компонентом, а жидкая — обедняется этим компонентом.
Существуют два вида перегонки. Дистилляция — процесс однократного частичного испарения жидкой смеси и конденсации образующихся паров. Его используют для грубого разделения смесей.
Ректификация — процесс многократного частичного испарения жидкости и конденсации паров, осуществляемый путем контакта потоков пара и жидкости, имеющих различную температуру. При каждом контакте из жидкости испаряется низкокипящий компонент, которым обогащаются пары. Многократное проведение такого контакта приводит к тому, что получаемые в конечном счете пары представляют собой почти чистый низкокипящий компонент. Эти пары после конденсации дают ректификат. Ректификация широко применяется при переработке нефти, получении спирта, в процессах органического синтеза. Схема ректификационной установки приведена на рис. 8.2.4.
Исходную смесь загружают в куб I со змеевиковым встроенным обогревателем. После подогрева до кипения пары поступают в ректификационную колонну 2 со встроенными контактными устройствами в виде тарелок 3. Пары, поднимаясь вверх, контактируют с жидкостью в тарелках, нагревая эту жидкость. При этом высо-кокипящий компонент паров, конденсируясь, переходит в жидкую фазу, а низкокипящий компонент жидкости — в паровую фазу. В верхней части колонны пар почти полностью состоит из низкокипящего компонента. Этот пар направляется в дефлегматор 4, где и конденсируется. Часть конденсата направляется в колонну и создает поток жидкости сверху вниз, а часть охлаждается в холодильнике 5 и направляется в сборник 6.
3. Экстракция в системе «жидкость—жидкость» — извлечение вещества, растворенного в жидкости другой жидкостью, практически не смешивающейся с первой. Извлекаемый компонент переходит из одной жидкой фазы в другую. Экстракция — диффузионный процесс, протекающий с участием двух жидких фаз, между которыми распределяется экстрагируемое вещество. Для увеличения скорости процесса исходный раствор и экстрагент перемешивают в смесителях различного типа, после чего разделяют на два слоя: экстракт — раствор извлеченных веществ в экстрагенте и рафинат — остаточный исходный раствор с пониженным содержанием исходного вещества. Экстракт и рафинат отделяют друг от друга отстаиванием или центрифугированием, после чего производят извлечение целевых конечных продуктов из экстракта, например путем ректификации. Принципиальная схема процесса приведена на рис. 8.2.5 а.
Исходный раствор и свежий экстрагент поступают в экстракционную колонну 7, где перемещаются противотоком. Осуществляется перенос вещества из одной жидкости в другую. Выделение вещества из экстракта происходит в ректификационной колонне 2, а в колонне 3 путем ректификации извлекают экстрагент из рафината.
Экстракционные колонны и аппараты различных типов используются в промышленности, например, в виде полочной (рис. 8.2.5, б) или распылительной (рис. 8.2.5, в) колонн. В последней легкая жидкость диспергируется распылительным устройством и в виде капель движется вверх сквозь тяжелую фазу, заполняющую колонну. В верхней отстойной зоне капли сливаются и образуется слой легкой жидкости — экстракта, отводимого из колонны. Тяжелая жидкость выводится из колонны через гидравлический затвор. Основным достоинством процесса экстракции по сравнению с другими процессами разделения жидких смесей является низкая, как правило, комнатная рабочая температура. Этот процесс незаменим при разделении веществ, чувствительных к высоким температурам.
Рис. 8.2.4. Схема ректификационной установки
4. Экстракция в системе «твердое тело— жидкость» представляет собой процесс диффузионного извлечения растворителем некоторого компонента из пористого твердого материала. Жидкость проникает в поры твердого тела, растворяет извлекаемый компонент или вступает с ним в реакцию. Вещество, перешедшее в раствор (или продукт реакции), диффундирует к поверхности твердого тела и переходит в объем раствора. В отличие от простого растворения в этом процессе извлекаемый компонент перемещается
Основы технологии
1235
в глубину пор инертного материала. Из-за этого скорость процесса значительно зависит от скорости переноса вещества в порах. Поэтому для интенсификации процесса стремятся измельчить твердый материал перед экстрагированием. Процесс применяют при переработке минерального сырья для отделения ценных компонентов от пустой породы.
Регенерированный экстрагент
Рис. 8.2.5. Схемы экстракционной установки (а), полочной (б) и распылительной (в) экстракционных колонн
5. Адсорбцией называют процесс поглощения одного или нескольких компонентов из газовой смеси или раствора поверхностью твердого вещества — адсорбента. Поглощаемое вещество называется в этом процессе адсорбатом. Процесс выделения поглощенных веществ из адсорбента носит название десорбции. Процесс адсорбции применяют при очистке и сушке газов, очистке и осветлении растворов, разделении смесей газов или паров. Различают химическую и физическую адсорбцию. Последняя вызвана взаимным притяжением молекул адсорбата и адсорбента под действием сил Ван-дер-Ваальса. При химической адсорбции между молекулами поглощаемого вещества и поверхностными молекулами поглотителя возникает химическая связь. В качестве поглотителей применяют активированные угли с удельной поверхностью 600-1600 м2/г, минеральные адсорбенты (400-800 м2/г), смолы, способные обмениваться содержащимися в их составе свободными ионами с эквивалентным количеством ионов раствора, например по реакциям:
2RC1 + Na2SO4 <-» R2SO4 + 2NaCl;
2NaR + СаС12 <-» CaR2 + 2NaCl,
где R — молекула ионообменного вещества, связанная с подвижным ионом.
Десорбцию проводят в основном двумя путями: адсорбционным вытеснением из адсорбента поглощенных компонентов реагентами с более высокой адсорбционной способностью и испарением поглощенных компонентов при нагреве слоя адсорбента.
6. Сушка — это процесс удаления влаги из твердых материалов, главным образом путем испарения. Влага переходит из твердой фазы в газовую или паровую. Сушка является сочетанием связанных между собой процессов тепло- и массопереноса. По способу подвода тепла к высушиваемому материалу выделяются следующие виды сушки:
• конвективная (осуществляется при непосредственном контакте высушиваемого материала с сушильным агентом — нагретым воздухом, топочными газами);
• контактная (проводится путем передачи тепла от теплоносителя к материалу через разделительную стенку);
• диэлектрическая (путем нагревания материала в электрическом поле высокой частоты);
• радиационная (путем передачи тепла материалу инфракрасным излучением);
• сублимационная (замороженный материал сушат в условиях глубокого вакуума).
Если в материале массой G содержится влаги и
Gc сухого вещества, то величина со - GJGC называется
влажностью. Учитывая тот факт, что при сушке на-
чальная Go и конечная GK массы высушиваемого веще-
ства связаны с количеством удаляемой при сушке влаги
И7 соотношением Go = GK + W, выведем следующие рас-
четные выражения:
1236
Новый справочник химика и технолога
Gq(I-COq).
1-4 уу _ °о(юо ~
!-со.
(8.2.11)
Поясним процесс сушки на конкретных примерах. Распылительная конвективная сушилка (рис. 8.2.6, а) используется для получения твердого порошкового материала, например сухого молока. За счет тонкого распыления высушиваемого материала поверхность испарения очень велика и процесс завершается за 15-30 с. Материал подается в сушильную камеру / через распылительное устройство 2. Сушильный агент вентилятором 3 через калорифер 4 подается параллельным потоком или противотоком, очищается в циклоне 5 и фильтре 6 и выбрасывается в атмосферу. Порошкообразный продукт отводится из сушилки транспортером.
Процесс сушки на аппарате, представленном на рис. 8.2.6, б, происходит в две стадии. Материал из бункера 1 подается на сушильный барабан 2 и распределяется по его поверхности. В полость сушильного барабана подается греющий пар. По мере движения вместе с барабаном происходит подсушка материала, который удаляется с поверхности барабана ножом 3, попадает на ленточный транспортер 4 и перемещается в сушильную камеру 5 для окончательной сушки горячим воздухом или топочным газом в смеси с воздухом. Готовый продукт отводится в сборник 6.
7. Кристаллизация — это процесс выделения твердой фазы из растворов и расплавов в виде кристаллов, осуществляемый с целью получения различных веществ в чистом виде. Кристаллизацию из растворов производят, уменьшая растворимость кристаллизуемого вещества за счет снижения температуры раствора или удаления из него части растворителя. Кристаллизацию из расплавов осуществляют охлаждением последних. Кинетика кристаллизации определяется скоростями двух стадий этого процесса: стадии образования центров кристаллизации в пересыщенных или переохлажденных растворах и стадии роста кристаллов за счет адсорбции частиц растворенного вещества на центрах кристаллизации.
Гидромеханические процессы основаны на законах гидростатики и гидродинамики и включают в себя перемещение жидких сред насосами, перемещение и сжатие газов компрессорами, разделение жидких и газообразных неоднородных систем, перемешивание жидких сред. Ниже приведено описание основных процессов разделения неоднородных, состоящих из двух или более фаз, систем, которые в зависимости от физического состояния фаз подразделяются на суспензии, эмульсии, пены, пыли, дымы и туманы.
Суспензии состоят из жидкости и взвешенных в ней твердых частиц размерами от 0,1 до 100 мкм. При меньших размерах частиц образуются коллоидные растворы. Эмульсии состоят из двух несмешивающихся
жидкостей, одна из которых распределена в другой в капельной форме. Пеной называют двухфазную систему, состоящую из жидкости и распределенных в ней газовых пузырьков. По своим свойствам пены близки к эмульсиям. Пыли и дымы представляют собой газы с распределенными в них частицами твердого вещества с размерами 3-70 мкм (пыли) и 0,3-5 мкм (дымы). При образовании дисперсной фазы из частиц жидкости (0,3-5 мкм) в газе образуются системы, называемые туманами. Пыли, дымы и туманы носят общее название аэрозоли.
Разделение неоднородных систем осуществляют обычно одним из следующих методов: осаждением, фильтрованием, центрифугированием и мокрым разделением.
Осаждение основано на процессе отделения дисперсной фазы в поле сил тяжести, инерции или электростатических сил. Осаждение твердых частиц в поле гравитационных сил часто называют отстаиванием.
Фильтрование основано на процессе разделения суспензий с использованием пористых перегородок, задерживающих твердую фазу. Пористая перегородка является основным элементом фильтра—аппарата для фильтрования (рис. 8.2.7, а). Суспензию 6 подают в приемную зону / фильтра.
Рис. 8.2.6. Схемы распылительной (а)
и барабанно-ленточной (б) сушилок
Основы технологии
1237
Между приемной и выходной 2 зонами создается перепад давлений \р, под действием которого жидкая фаза проходит через поры перегородки 3. образуя чистый фильтрат 4. Твердая фаза образует осадок 5. Фильтровальные перегородки изготавливаются из материи, бумаги (картон), металла, керамики и других материалов. Часто используют намывные фильтры, в которых перед фильтрованием на жесткую пористую перегородку намывают пористый слой вспомогательного вещества, препятствующего проникновению твердых частиц. В качестве такого вещества используют асбест, целлюлозу, активированный уголь.
Основное уравнение, описывающее процесс фильтрования, имеет вид:
dV _ кр
Й“ц(Яос + Яфг,)’
(8.2.12)
щийся на стенках ротора, перемещается к отверстиям 5 в роторе и удаляется через патрубок 6. Очищенная жидкая фаза отводится через отверстия 7 в торце ротора и далее через патрубок 8.
где Уф — скорость фильтрования, м/с; V — объем фильтра, м3; F — поверхность фильтрования, м2; ц — вязкость жидкой фазы суспензии, Па • с (Н • с/м2); Roc и /?фп — соответственно сопротивление слоя осадка и жесткой фильтрующей перегородки, м '.
На практике используют два основных режима фильтрования: при постоянной разности давлений (Д/7 = const) и при постоянной скорости процесса (у = const).
На рис. 8.2.7, б представлено устройство для очистки газов от пыли, называемое электрофильтром. Он обеспечивает степень улавливания 95-99 %. Запыленный газ через сетку / поступает в неоднородное электрическое поле, образованное коаксикальными электродами 2 и 3, смонтированными в корпусе 4. Напряжение 35-70 кВ и расстояние между электродами 100-200 мм обеспечивают высокую напряженность электрического поля. Получая заряд, частицы пыли перемещаются в пространстве между электродами и оседают преимущественно на аноде.
Очистка газов от аэрозолей имеет большое значение с точки зрения экологической безопасности крупнотоннажных производств.
Разделение неоднородных систем в поле центробежных сил называют центрифугированием, а соответствующее оборудование — центрифугой, или циклоном. В центрифуге поле центробежных сил создается быстровращающимся ротором, а в гидроциклоне — за счет искривления потока жидкости стенками аппарата, в который жидкость поступает аксиально. Процесс разделения неоднородной системы центрифугой непрерывного действия представлен схемой на рис. 8.2.7, в. Суспензия подается через отверстие в неподвижной трубе 1 и поступает в зону между коническим ротором 2 со сплошными стенками и цилиндрическим основанием 3 шнека 4. Ротор и шнек вращаются в подшипниковых опорах, но с частотами, несколько отличающимися друг от друга. За счет этого слой осадка, образую-
Рис. 8.2.7. Схемы механического (а), электрического (6)
фильтров и центрифуги (в) непрерывного действия
1238
Новый справочник химика и технолога
8.2.1.2. Процессы и методы, связанные с переработкой пищевого сырья
Перечисленные выше основные процессы химических производств применяются практически во всех отраслевых технологиях, например при производстве пищевых продуктов. Вместе с тем пищевые технологии содержат ряд специфических процессов.
Обжаривание — тепловой процесс, осуществляемый в горячем растительном масле, в результате чего поры обрабатываемого материала, например картофеля, освобождаются от влаги и пропитываются высокоценным в пищевом отношении растительным маслом. Образуется корочка с оригинальными вкусовыми свойствами. Обжаривание осуществляется в специальных печах.
Стерилизация — тепловой процесс, направленный на подавление жизнедеятельности микроорганизмов с целью увеличения длительности хранения пищевых продуктов. Процесс заключается в нагреве предварительно расфасованного в стеклянную или металлическую тару продукта до температур, обеспечивающих бактерицидное действие, выдержке при этой температуре и охлаждении до комнатной температуры. Процесс осуществляется в аппаратах периодического действия — автоклавах (производство мясных и овощных консервов), аппаратах непрерывного действия различной конструкции (производство консервированного зеленого горошка). В производстве фруктовых соков используют так называемое асептическое консервирование: продукт стерилизуют в потоке, используя теплообменники различного типа, затем разливают в предварительно обработанную по специальной технологии крупнотоннажную тару, в которой осуществляют длительное хранение перед расфасовкой продукта в потребительскую тару.
Мойка — комбинированный процесс гидромеханического и бактерицидного воздействия на поверхность сырья или тары с целью удаления загрязнений и подавления жизнедеятельности микроорганизмов. Мойка является начальной операцией технологического процесса, которая в зависимости от механических свойств сырья осуществляется на моечных машинах различной конструкции. Мойку оборотной стеклотары производят на высокопроизводительных многорядных моечных машинах, обеспечивающих последовательную отмочку загрязнений в ваннах холодной, горячей воды, горячего щелочного раствора, а затем шприцевание внутренней и ополаскивание наружной поверхности стеклотары щелочным раствором, горячей и холодной водой.
Механическая обработка пищевого сырья включает, наряду с рассмотренными выше, специфические процессы и операции на их основе. К таким процессам относится, например, отделение малоценных в пищевом отношении компонентов плодоовощного сырья: плодоножек, косточек, семян, кожуры. На рис. 8.2.8, а представлена схема процесса отделения плодоножки вишни, сливы и других плодов. Валики / и 2 вращают
ся навстречу друг другу, затягивая плодоножку в зазор между ними. В результате действия сил трения и реакций валиков возникает растягивающее усилие, приводящее к отрыву плодоножки 4 от ягоды 3. Диаметр валиков выбирают в соответствии с расчетом из условия предотвращения затягивания ягоды в рабочий зазор. Продольное перемещение плодов вдоль оси валиков обеспечивается в таких машинах наклоном их оси или специальными скребками.
Протиркой называют процесс отделения семян и кожицы, например при производстве томатной пасты или сока. Этот процесс заключается в продавливании дробленой томатной массы через отверстия в специальном сите под действием центробежных сил. Принцип действия протирочной машины показан на рис. 8.2.8, б. Она состоит из цилиндрического перфорированного барабана (сита) / с размерами отверстий 0,4-1,5 мм. Внутри барабана вращается вал 2, на котором установлены специальные бичи 3. Плоскость планки бича наклонена к осевой плоскости барабана под углом опережения 0. Дробленая масса поступает в машину через приемный бункер 4 и перемещается вдоль ее оси за счет наклона бичей под углом 0. Одновременно центробежные силы отбрасывают томатную массу на стенки перфорированного барабана. Квазижидкая фракция продавливается через отверстия и скапливается в приемной емкости 5, а отходы отводятся в бункер 6.
Рис. 8.2.8. Схемы процессов отделения плодоножки (а)
и протирки (б)
Основы технологии
1239
Важную роль в технологических процессах пищевой и химической промышленности играют заключительные операции, включающие в себя дозирование готового продукта, перемещение дозы в потребительскую тару, укупоривание и герметизацию тары, нанесение на нее информации. Рассмотрим соответствующие процессы на примере производства жидких пищевых продуктов.
Дозирование жидких сред осуществляют в большинстве случаев двумя способами: по объему и по уровню. В первом случае доза формируется в специальном мерном стакане строго определенного объема и лишь затем перемещается в тару. Для этого мерный стакан опускают ниже уровня жидкости в продуктовом баке, а после заполнения извлекают его из бака и по гидравлическому тракту транспортируют дозу самотеком или за счет разности давлений в предварительно подготовленную тару. Во втором случае дозировочное устройство обеспечивает заполнение тары до заданного уровня. Очевидно, дозирование но объему имеет то преимущество, что исключает влияние неточности изготовления тары на товарную массу продукта.
Укупоривание стеклотары осуществляют одним из трех способов: 1) напрессовкой (запрессовкой), 2) пластическим деформированием укупорочного элемента (пробка, крышка, колпачок), 3) навинчиванием. Первый способ наиболее прост и легко осуществим. На рис. 8.2.9, а показана схема укупорки бутылки капсульной пробкой 1, которая запрессовывается в отверстие горлышка 2 осевым усилием Р. Герметизация достигается за счет деформации кольцевых выступов на пробке.
На рис. 8.2.9, б приведена схема герметизации по второму способу. Металлическая пробка-колпачок / обжимается вокруг буртика на горлышке 2 путем обкатывания роликами специальной обкатной головки.
Рис. 8.2.9. Герметизация стеклотары запрессовкой (а), закаткой (б), навинчиванием (в) и жестяной тары путем образования двойного закаточного шва (г)
Герметизация достигается по торцу горлышка за счет деформации нанесенного на пробку герметика 3. При укупоривании этим способом стеклянной консервной тары деформируется специальное резиновое кольцо, вмонтированное в металлическую крышку.
Третий способ реализуется при навинчивании укупорочного элемента на горлышко бутылки или банки. Для этого на горлышке тары и на укупорочном элементе предусмотрены элементы резьбы (рис. 8.2.9, в). Для повышения надежности укупоривания часто используют комбинацию описанных способов.
Укупоривание жестяной тары в консервной промышленности осуществляется по второму способу путем образования двойного закаточного шва (рис. 8.2.9, г). Крышка / с нанесенным на нее пастообразным герметиком 2 накладывается на корпус банки 3 с продуктом, поджимается некоторым усилием Р и обкатывается роликами специального профиля. Первый ролик 4 осуществляет предварительную деформацию (подвивку), а второй 5 — окончательное формирование шва. Ролики совершают планетарное движение, вращаясь вокруг оси банки, собственной оси и совершая поступательное движение подачи по радиусу банки. Для реализации описанных способов укупоривания разработаны и применяются специальные высокопроизводительные роторные автоматы.
Нанесение информации на тару с продуктом осуществляют, используя краску или специальный элемент-этикетку. Схема процесса нанесения этикетки показана на рис. 8.2.10. Банки 1 поступают на транспортер 2 машины для нанесения этикеток и перемещаются этим транспортером в рабочую зону. Специальный делитель 3 обеспечивает заданный шаг между осями банок. Вакуумный барабан-этикеткопереносчик 4 с рабочими накладками 5 вращается вокруг собственной оси. При настройке машины обеспечивается синхронное поступление банки и рабочей накладки в точку А рабочей зоны. При вращении барабана накладкой в точке Б осуществляется вакуумный захват этикетки из магазина этикеток 6, совершающего сложное движение по заданной программе. При дальнейшем вращении барабана на отобранную этикетку наносится последовательно информация (дата выпуска, смена и пр.) накатным роликом 7 и полоска клея роликом 9. В точке А при контакте покрытой клеем этикетки с поверхностью банки вакуум отключается, и этикетка переносится на тару. За счет разглаживающего ременного устройства 10 достигается плотное прилегание этикетки к таре, которая обкатывается на этом участке по направляющей / /. В настоящее время разработаны и используются высокопроизводительные роторные этикетировочные машины. На жестяных крышках и бумажной таре информацию иногда выдавливают.
Структура и содержание технологических процес-
сов пищевых производств определяются видом исход-
ного сырья, свойствами готового продукта. Конкретные
технологии описаны в специальной литературе.
1240
Новый справочник химика и технолога
Рис. 8.2.10. Схема процесса нанесения этикетки на тару
8.2.1.3. Машиностроительные процессы и методы
Технология машиностроения — это наука об изготовлении машин требуемого качества в установленном производственной программой количестве и в заданные сроки при наименьших затратах живого и овеществленного труда. Технология машиностроения связана с процессами (методами) преобразования свойств твердых тел: металлов, сплавов, пластических и композиционных материалов. В результате такого преобразования появляется связное твердое тело, имеющее заданную совокупность свойств, полученное из однородного по наименованию и марке материала, называемое деталью. Исходное вещество, также представляющее собой в большинстве случаев твердое тело, называют заготовкой. Таким образом, технологическую функцию можно представить как преобразование некоторого вектора свойств заготовки в соответствующий вектор свойств детали. С позиции технологии машиностроения состояние твердого тела описывается тремя группами характеристик:
1) геометрической — одним или несколькими уравнениями поверхности вида F(xv, yr, zr) = 0 в некоторой системе координат, жестко связанной с самим телом. Индекс «г» относится к граничным точкам твердого тела (детали или заготовки);
2) совокупностью физико-химических параметров тонкого поверхностного слоя, определяющих эксплуатационные характеристики детали и в первом приближении являющихся функциями точки ее поверхности:
А = Д(хг’ Уг’ zr)>
где i — условный номер параметра. К таким параметрам относят показатели оценки микрогеометрии поверхности, микротвердость, остаточное напряжение и пр.
3) группой объемных параметров, характеризующих состояние точек сердцевины детали (локальная плотность, проводимость, структурно-фазовый состав и пр.):
Y, = Y,(*>b^).
Требуемые свойства детали определяются ее функциональным назначением и формируют некоторую модель, задаваемую, например, в виде чертежа. Характеристики модели можно представить в виде:
LM=LM(x",y",z^ (8.2.13)
ум =yM(xM,yM,zM).
Очевидно, степень приближения некоторого параметра дегали к соответствующему параметру модели можно оценить, сравнивая его реальное значение с величиной, вычисленной по соответствующему уравнению, и получая количественную меру отклонения. Эта мера характеризует точность обработки по заданному параметру.
Процессы (методы), формирующие первую группу характеристик детали и ответственные за ее геометрическую конфигурацию, называют формообразующими, а вторую группу — отделочными и (или) упрочняющими.
Изготовление отдельных деталей не является, как правило, конечной целью машиностроительного производства — последнее выпускает машины, аппараты и их комплексы, состоящие из элементов-деталей, соединенных между собой заданным образом. Такой интегративный процесс целесообразной пространственно-временной организации некоторой совокупности деталей, приобретающей при этом новое свойство по отношению к каждой составляющей детали, называется сборкой, а соответствующие процессы, методы или операции —
Основы технологии
1241
сборочными. Как правило, технология сборки машины включает в себя также испытание изделия — оценку соответствия его параметров заданным.
В машиностроительной практике укрупненные стадии технологического процесса изготовления изделия носят название передела.
Заготовительный передел включает в себя процессы, методы и технологии, обеспечивающие получение конфигурации изделия в первом приближении (заготовку) из исходного вещества (исходной заготовки). В большинстве случаев используют следующие виды заготовок: отливки, поковки, штамповки, заготовки из сортового проката и комбинированные заготовки, например штампосварные.
Отливки получают в процессе литья, основанном на фазовом переходе «жидкость—твердое тело» при температурах затвердевания расплава. Для получения требуемой конфигурации расплавленный металл заливают в специальную форму, где и происходят затвердевание и последующее охлаждение отливки. Затем отливку подвергают обрубке (удаляют литники и прибыль) и очистке. Литейные формы изготавливают как из неметаллических материалов (песчаные формы, оболочковые формы), так и из металлов (кокили, пресс-формы для литья под давлением и др.).
Некоторые способы литья приведены на рис. 8.2.11. Литье под давлением (рис. 8.2.11, а.) обычно используют для получения точных заготовок из цветных сплавов. Камера прессования расположена в обогреваемом тигле 1 с расплавом. При верхнем положении плунжера 2 расплав через отверстие заполняет камеру, а при движении плунжера вниз расплав под давлением 10-30 МПа перемещается в полость 3. После затвердевания отливки плунжер возвращается в исходное положение, остатки металла сливаются в камеру прессования, отливка удаляется из пресс-формы выталкивателями 4. Для получения отливок — тел вращения — используется поле центробежных сил. На рис. 8.2.11, б приведена схема центробежного литья с вертикальной осью вращения формы 2. Расплавленный металл из ковша 1 заливают в форму, частота вращения которой составляет 160-500 мин-1. После затвердевания металла форму охлаждают и извлекают из нее отливку кольцевого сечения 3.
Поковки и штамповки получают путем пластического деформирования предварительно нагретого (горячая штамповка) или холодного (холодная штамповка) материала силовым воздействием инструмента. Для пластического деформирования материалов используют два основных вида оборудования: молоты и прессы. Горячей объемной штамповкой называют процесс получения заготовки заданной формы за счет перераспределения объема металла нагретой исходной заготовки в специальном инструменте-штампе. Для нагрева исходной заготовки используются газовые печи, электро-контактные и индукционные нагревательные устройства. Такую штамповку производят в открытых или закрытых штампах. В первом случае излишек материала исходной заготовки перетекает в кольцевую канавку, образуя так называемый облой (рис. 8.2.12, а). На последующих операциях производят обрезку облоя (рис. 8.2.12, б) и пробивку перемычек с образованием центрального отверстия (рис. 8.2.12, в). При обрезке штамповку устанавливают на матрицу 1. При движении пуансона 2 вниз происходит отделение облоя 3 в виде кольца. Штамповку в закрытых штампах (рис. 8.2.12, г) производят при изготовлении точных заготовок относительно простой формы.
Холодная листовая штамповка служит для получения тонкостенных деталей заданной формы и основана на использовании процессов двух типов: разделительных и формоизменяющих. Разделительные процессы базируются на направленном механическом разрушении материала при силовом воздействии инструмента, в результате которого одна часть материала отделяется от другой по замкнутому или незамкнутому контуру (отрезка, вырубка, пробивка). Формоизменяющие процессы реализуются в результате пластического деформирования части материала (гибка, вытяжка, отбортовка, раздача, обжим).
На рис. 8.2.13 схематически представлены отдельные процессы листовой штамповки и холодной объемной штамповки, в частности процесс выдавливания — формообразование заготовки путем всестороннего сжатия с истечением металла в полость штампа.
Рис. 8.2.11. Схемы процессов литья под давлением (а) и центробежного литья (б)
1242
Новый справочник химика и технолога
Рис. 8.2.12. Схемы получения штамповки (а), обрезки облоя (б), пробивки перемычки (в)
и штамповки в закрытых штампах (г)
Рис. 8.2.13. Схема процессов листовой штамповки: пробивка (а), гибка (б), вытяжка (в), отбортовка (г) и холодной объемной штамповки — выдавливание (б)
Заготовки из порошковых материалов получают методом порошковой металлургии', готовят смесь порошков требуемых компонентов (металлов или неметаллов с металлами), засыпают смесь в пресс-форму, прессуют, а затем спекают при температурах ниже температур плавления основного компонента.
Заготовки из проката получают путем отрезки от стержня с заданным поперечным сечением (круг, квадрат, полоса, шестигранник, труба и пр.). Такую отрезку производят в специальных разделительных штампах или на металлорежущих станках.
Таким образом, на первой стадии машиностроительного производства получают заготовку — промежуточное изделие, геометрическая форма которого является первым приближением к требованиям чертежа конечной детали. Дальнейшая обработка заключается в удалении с поверхности заготовки или нанесении на нее отдельных слоев металла для получения конфигурации готового изделия.
Передел механообработки объединяет те процессы, которые предназначены для получения окончательной геометрической формы изделия. В большинстве случаев это достигается последовательным удалением слоев металла с поверхности заготовки в результате реализации процесса резания металлов. Так называют управляемое разрушение материала вследствие силового механического взаимодействия двух тел с различными значениями поверхностной энергии с последующим отделением части материала, называемой стружкой. Твердое тело определенной геометрической формы и высокой твердости и прочности, воздействующее на заготовку при резании, является режущим инструментом (рис. 8.2.14, а). Инструмент 7, поперечное сечение которого имеет форму клина и характеризуется углом заострения 0, перемещается относительно заготовки со скоростью v, воздействует на заготовку 2 силой Р, сосредоточенной вблизи вершины А, и отделяет стружку 3. В результате обрабатываемая поверхность размером D преобразуется в обработанную поверхность размером d.
Основы технологии
1243
Рис. 8.2.14. Схема процесса стружкообразования при резании металлов (а), классическая кривая растяжения (б) и схема микрорезания при обработке абразивом (в)
Отделению стружки предшествует деформация материала заготовки, которая в наибольшей степени проявляется в объеме, ограниченном углом ZBAC. Поясним это, используя зависимость деформации (удлинение образца А/) от приложенной силы Р при растяжении образца (рис. 8.2.14, б). Видно, что вплоть до точки 1 на кривой растяжения наблюдается прямо пропорциональная зависимость вида Р = ЛА/, где к — некоторый коэффициент, характеризующий материал образца. Это область упругой деформации: после прекращения действия силы первоначальная длина образца восстанавливается, остаточная деформация отсутствует.
При большем нагружении указанная зависимость становится нелинейной, развиваются пластические деформации, после снятия нагрузки наблюдается остаточное удлинение образца. Дальнейшее нагружение приведет к разрушению образца. Очевидно, при внедрении режущего клина инструмента в поверхность заготовки в области, ограниченной углом ZBAC, развиваются упругие и пластические деформации с последующим разрушением материала и отделением стружки.
Процесс резания имеет место не только при силовом контакте заготовки с лезвийным инструментом (рис. 8.2.14, а), но и при обработке абразивным инструментом. Такой инструмент представляет собой совокупность абразивных зерен, находящихся в матрице-связке, изготовленной из керамики, полимерных или эластичных материалов. Абразивному инструменту придают в большинстве случаев форму тела вращения и называют абразивным кругом (рис. 8.2.14, в). Круг 2 вращается с некоторой частотой пК, а абразивные зерна /, соприкасаясь с поверхностью, удаляют микрообъемы материала. При перемещении заготовки 3 относительно оси круга со скоростью S интегральный эффект от воздействия абразивных зерен выразится в снятии с поверхности тонкого слоя металла.
Как ясно из вышесказанного, удаление стружки при резании металлов, или их пластическая деформация, лежат в основе всех способов механической обработки
деталей машин. Однако разрушение материала и удаление слоя материала с обрабатываемой поверхности может происходить в результате протекания процессов иной природы. Так, тепловое воздействие на элемент поверхности, приводящее к расплавлению и/или испарению микрообъемов материала, лежит в основе методов электроэрозионной, лазерной, электронно-лучевой, плазменной обработки и некоторых других.
В качестве примера на рис. 8.2.15, а приведена схема лазерной прошивки отверстия в материале. Поток излучения (плотность 105—108 Вт/см2), генерируемый оптическим квантовым генератором (лазером), посредством устройства / фокусируется на поверхности заготовки 2, вызывая быстрый разогрев небольшого объема приповерхностного слоя материала вплоть до температур плавления или кипения. Образуется микрованна расплавленного металла, который выбрасывается в виде мельчайших капель 3 или паров. В результате воздействия серии импульсов лазерного излучения можно получить, например, отверстие в сплошном материале диаметром 10-100 мкм. Лазерное излучение используют также для реализации процессов сварки, резки металлов и сплавов, упрочнения поверхности деталей машин.
Аналогичное воздействие на поверхность материала оказывает сфокусированный пучок электронов, разогнанный до больших скоростей в электронной пушке. Торможение электронов в тонком поверхностном слое материала сопровождается выделением тепловой энергии, которая приводит к разрушению материала в результате его плавления и испарения. Этот эффект используется в технологиях электронно-лучевой обработки (сварка, резка, прошивка отверстий).
К процессам, в основе которых лежат фазовые пе-
реходы, связанные с нагревом (плавление, испарение),
относится и эрозия материала под действием электри-
ческого разряда в жидкой или газовой среде. Элек-
троэрозионная обработка материалов широко ис-
пользуется в технологиях размерного формообразо-
вания.
1244
Новый справочник химика и технолога
Рис. 8.2.15. Схемы процессов лазерной (а), электрохимической (б) и химической (в) обработки
Плазменная обработка также относится к методам, основанным на нагреве материала до температур плавления и испарения. Плазмообразующий газ прокачивается через мощное температурное поле, образующееся при протекании дугового разряда в специальном устройстве, называемом плазмотроном. В результате молекулы газа частично разрушаются, атомы ионизируются и образуется струя горячей плазмы, воздействующая на поверхность материала.
При электрохимическом механизме удаления материала поверхностные атомы металла под действием сил электрического поля ионизируются и переходят в раствор, образуя продукты электродных реакций (рис. 8.2.15, б). Метод реализуется следующим образом. Инструмент 7 требуемой формы устанавливают относительно заготовки 3 с небольшим рабочим зазором (0,2-0,5 мм). Через зазор прокачивают рабочую жидкость-электролит 2. Придавая инструменту поступательное перемещение относительно заготовки и пропуская по цепи «инструмент—электролит—заготовка» электрический ток от источника питания, получают на заготовке отпечаток, идентичный конфигурации рабочей части электрода-инструмента. Такой метод получения полостей сложной формы называют методом прямого копирования. Очевидно, его реализация возможна в том случае, когда инструмент практически не изнашивается при обработке и сохраняет свою конфигурацию, что характерно для технологий электрохимического формообразования.
Химическое разрушение материала заготовки осуществляется при обработке изделий в растворах сильных кислот (иногда щелочей). На рис. 8.2.15, в показана схема химического фрезерования заготовки 2, которая со скоростью v3 опускается в ванну 7 с химически агрессивной по отношению к материалу заготовки средой. Можно показать, что при постоянной величине v3 слой металла 3, снимаемый с заготовки, будет иметь форму клина. Химическое травление часто применяют для равномерного удаления дефектных слоев, например окалины с поверхности заготовки.
Интересным примером нетрадиционных видов обработки материалов является гидроабразивная резка.
Использование водяной струи большой мощности (давление около 1000 МПа) для разрушения материалов (водоструйная обработка) привлекло внимание инженеров во второй половине XX в. Физическая сущность водоструйной обработки заключается во взаимодействии высокоскоростной струи жидкости с твердотельной преградой, что приводит к эрозионному разрушению последней. Эффективность разрушения материала высокоскоростной водяной струей значительно повышается при добавлении в нее частиц абразива, т. е. при использовании абразивных суспензий. Поэтому для резки машиностроительных материалов используют преимущественно гидроабразив-ную обработку. На рис. 8.2.16 показан принцип гидроабразивной резки. С помощью насоса высокого давления (250-500 МПа) вода подается через приемное отверстие 7 в смесительную камеру 2. В нее же потоком воздуха производится дозированная подача абразивного порошка через патрубок 3. Смесь воды, абразива и воздуха 4 выходит из сопла металлокерамической смесительной трубки и режет материал. Ширина реза обычно составляет 0,7-1,5 мм. Осуществляя относительное перемещение струи и обрабатываемой заготовки по заданной программе, вырезают из листа толщиной до 400 мм сложноконтурные детали с высокой точностью (± 0,1 мм).
В последние десятилетия интенсивно развиваются технологии комбинированной обработки материалов, которые основаны на единовременном протекании в зоне обработки процессов различной природы. В современном машиностроении нашли применение технологии электроэрозионно-электрохимической обработки, ультразвуковой электрохимической обработки, электрохимического шлифования и мн. др. Так, при электрохимическом шлифовании удаление материала осуществляется в результате микрорезания и анодного растворения.
Основы технологии
1245
Рис. 8.2.16. Схема рабочей головки гидроабразивной установки (а) и рабочая зона операции резки (б)
Наряду с технологиями, в основе которых лежат процессы разрушения материала с последующим удалением стружки с поверхности заготовки, в последние годы интенсивно развиваются технологии, в которых пространственная форма детали получается в результате последовательного нанесения слоев материала на исходную заготовку или специальный субстрат (подложку) (аддитивные технологии). Особый интерес представляют те из них, которые позволяют
быстро получать твердые тела различной формы из жидкой или паровой фазы, порошка или иных материалов (технологии быстрого прототипирования).
Рассмотрим в этой связи технологию получения твердых форм методом лазерной стереолитографии. Этот метод запатентован в 1986 г. и получил быстрое распространение. Он основан на послойном затвердевании жидкого фотополимеризующегося материала под действием сканирующего по заданной программе лазерного луча. Толщина каждого из последовательно накладываемых слоев 0,05—0,2 мм. Таким образом, цифровая модель трехмерного объекта материализуется в виде твердого тела заданной конфигурации путем выделения твердой фазы из жидкой рабочей среды со специальными свойствами. Для этой цели используется излучение с длиной волны 320-370 нм (ультрафиолетовый диапазон) и мощностью 20-200 мВт.
Методом лазерной стереолитографии получают пространственно сложные объекты высокой точности, например мастер-модели для различных видов литья.
Схема технологической установки представлена на рис. 8.2.17. Установка состоит из ванны 7, заполненной жидким фотополимером, в которой расположен стол 2, совершающий точные вертикальные перемещения с помощью механизма 4. Твердотельная модель 3 выращивается на поверхности стола следующим образом. Область фокусировки луча лазера 5 и оптической системы 6 перемещается по заданной программой траектории с помощью поворотных отражающих зеркал 7. В этой области осуществляются полимеризация рабочей жидкости и затвердевание узкого слоя в некотором сечении физической модели. После получения z-го слоя стол опускается на один шаг, нивелир 10, перемещаясь, выравнивает поверхность вязкой жидкости и начинается формирование (/ + 1)-го слоя. Уровень рабочей жидкости над моделью и его равномерность контролируются лазерной системой 8 с датчиком 9, по сигналу которого начинается процесс фотополимеризации. Коррекция уровня жидкости в ванне осуществляется погружением или подъемом специального устройства 11.
В нашей стране разработана установка для лазерной стереолитографии ЛС-250, позволяющая получать физические объекты с максимальными габаритами 250x250x250 мм с точностью ±0,1 мм. Использование этой установки позволяет за короткое время (от нескольких часов до нескольких дней) пройти путь от проектной идеи до готового изделия.
Метод селективного лазерного спекания (Selective Laser Fritting) отличается тем, что сканирующий по заданной программе лазерный луч осуществляет послойное спекание порошкового материала заданного состава (рис. 8.2.18). Порошок поступает из картриджа 1, раскатывается роликом 2 на поверхности рабочей камеры 4. Область фокусировки лазерного луча, излучаемого лазером 3, перемещается по заданной программе с помощью системы зеркал 5 и формирует слой спеченного порошкового материала заданной толщины
1246
Новый справочник химика и технолога
(в диапазоне 70-500 мкм). Указанный цикл периодически повторяется, обеспечивая формирование пространственно-сложной модели 6. Применяются мелкодисперсные термопластичные быстротвердсющие порошки на основе полимеров, металлов, керамик. К настоящему времени предложено несколько разновидностей описанного выше процесса.
Другой метод быстрого изготовления твердых форм заданной конфигурации основан на формировании объектов слоистой структуры. Сущность данного технологического процесса (Laminated Object Manufacturing) заключается в последовательном наклеивании тонких листов специальной бумаги (0,01-0,05 мм) или пластика с вырезанием контура соответствующего сечения лазером (рис. 8.2.19). Система управления установки по цифровой модели детали, подлежащей изготовлению, рассчитывает необходимое количество сечений (слоев) и геометрию каждого слоя. Лента 7, покрытая связующим веществом, дискретно перематывается между бобинами 2 и 3 по поверхности стола-платформы 4. В рабочей зоне лазер 5 с использованием системы зеркал 6 и оптической головки 7 вырезает контур /-го слоя, разрезает на квадраты излишки материала для создания поддерживающей структуры и вырезает общий прямоугольный контур обоймы, одинаковый для всех слоев. Надежное приклеивание слоя осуществляется термоваликом 8. После этого платформа опускается на величину шага, равного толщине наносимого слоя, и наносится следующий слой по вышеописанному циклу. Повторение этих циклов требуемое число раз приводит к построению всей детали слоистой структуры. Изделие, снимаемое с установки, имеет вид прямоугольного блока. Излишки материала легко удаляются вручную. Материалы для данного процесса недорогие, изготовление идет быстро, детали не требуют дальнейшей обработки и внешне похожи на древесину. Технологические установки фирмы «HEL1SYS» обеспечивают изготовление деталей из листового рулонного материала толщиной 0,05-0,5 мм с точностью ±0,25 мм и скоростью разрезания 400-600 мм/с.
Рис. 8.2.17. Схема установки для лазерной стереолитографии
По прогнозам ученых, XXI в. станет веком бурного развития и применения подобных (аддитивных) технологий в машино- и приборостроении.
Любой из рассмотренных выше процессов направленного разрушения реализуется посредством различных способов обработки, имеющих кинематические, геометрические и прочие особенности, но единый механизм удаления материала с поверхности заготовки. Так, на рис. 8.2.20 показаны различные способы обработки металлов резанием, отличающиеся кинематикой движения и формой применяемого инструмента.
При токарной обработке (рис. 8.2.20, а) заготовка 7 совершает вращательное движение вокруг собственной оси с частотой п1Ц, а инструмент, называемый в данном случае резцом, движется поступательно вдоль (5^) или поперек (SIIon) оси заготовки. В результате такого перемещения резцов 2 и 3 происходит формообразование соответственно цилиндрических или торцевых поверхностей.
Рис. 8.2.18. Схема установки для селективного лазерного спекания
5
Рис. 8.2.19. Схема изготовления объектов слоистой структуры
Основы технологии
1247
Для обработки плоскостей и пазов применяют фрезерование (рис. 8.2.20, б). В этом случае инструмент 2, называемый фрезой, совершает вращательное движение вокруг собственной оси, а заготовка 1 перемещается со скоростью При этом зубья последовательно снимают стружку, в результате удаляется слой материала толщиной H-h.
Для обработки отверстий применяют специальные многолезвийные инструменты (сверло 2, зенкер 3), вращающиеся вокруг собственной оси и перемещающиеся поступательно вдоль этой оси со скоростью (рис. 8.2.20, в). Таким образом, обрабатывают отверстия в сплошном материале (сверло) или увеличивают диаметр существующего отверстия (зенкер, развертка).
Более подробные сведения о способах обработки резанием, инструменте и применяемом оборудовании приведены в специальной литературе.
Процессы, направленные на изменение механических и физико-химических свойств материала изделия путем теплового воздействия на него, но не изменяющие при этом геометрическую конфигурацию материала, также объединены в один передел. Термическая обработка приводит при определенных условиях к изменению структурно-фазового и химического состава материала, от чего, в свою очередь, зависят такие его характеристики, как твердость, прочность, пластичность. Наибольшее распространение получили процессы отжига, закалки и отпуска. Каждый из них включает в себя три основных этапа: нагрев заготовки до определенной, зависящей от наименования и марки материала температуры Тр в течение времени нагрева выдержку при этой температуре определенное время (в и охлаждение до комнатной температуры в течение времени /0 с заданной скоростью охлаждения (рис. 8.2.21).
Отжиг выполняется с целью устранения неоднородности химических и физических свойств заготовки, созданной предшествующей обработкой (литье, ковка, штамповка). Например, в крупногабаритных отливках и штамповках возникают внутренние напряжения, перераспределение которых в объеме заготовки может привести в дальнейшем к короблению изделия и потере его точностных характеристик. Поэтому такие заготовки отжигают перед механической обработкой, а иногда и после частичной (черновой) механообработки.
Закалку производят с целью повышения твердости, прочности, износостойкости сталей и некоторых сплавов. Особенностью этого процесса являются высокие скорости охлаждения (до 500 °С/с). В качестве охлаждающих сред используют воду, масло минеральное. Закалка ухудшает обрабатываемость металлов резанием, вызывает хрупкость и напряжения в металле. Поэтому после закалки обычно производят отпуск. Отпуск устраняет внутренние напряжения, повышает пластичность материала, облегчает снятие стружки.
Часто термообработку совмещают с пластическим деформированием материала. Такие процессы носят название термомеханических.
Рис. 8.2.20. Способы обработки резанием: точение (а), фрезерование (б), сверление и зенкерование отверстий (в)
Четвертый передел объединяет процессы модификации свойств поверхностного слоя деталей машин. Именно этот слой определяет эксплуатационные свойства детали машины, такие как износостойкость и коррозионная стойкость, усталостная прочность при действии знакопеременных нагрузок, декоративные свойства изделия. По характеру воздействия эти процессы можно разделить на несколько групп.
1248
Новый справочник химика и технолога
Поверхностно-пластическое деформирование (ППД) применяют для упрочнения деталей за счет структурных изменений в поверхностном слое и образования в нем остаточных напряжений сжатия в результате силового, механического контакта с инструментом без разрушения материала детали. Обработку производят путем обкатки поверхности закаленными шариками или роликами, выглаживанием ее алмазным инструментом, обдувкой поверхности дробью. На рис. 8.2.22, а показана схема обработки, которую используют для повышения точности и упрочнения поверхности отверстия, так называемое калибрование. Заготовку / устанавливают на упорную плиту 2 и под действием силы Р протягивают через предварительно подготовленное отверстие инструмент (шарик или бочкообразный дорн), диаметр которого несколько больше диаметра отверстия.
На рис. 8.2.22, б приведена схема процесса виброобкатывания цилиндрической поверхности. Заготовка / совершает вращательное движение, а инструмент 3 перемещается вдоль нее с подачей 5пр и одновременно совершает колебания с некоторой частотой и амплитудой. Рабочим телом является шарик 2, контактирующий под некоторым усилием с поверхностью заготовки. В результате на последней образуется сетка канавок заданного рисунка, которые не только упрочняют поверхностный слой, но и удерживают смазку в процессе эксплуатации детали.
Алмазное выглаживание осуществляют обычно на токарных станках по схеме точения поверхности вращения (рис. 8.2.23) с использованием инструмента из природных или синтетических алмазов со сферической рабочей поверхностью радиусом 0,5-5 мм. Инструмент прижимается к обрабатываемой поверхности с некоторым усилием и перемещается вдоль нее. При этом микронеровности поверхности, образовавшиеся при механической обработке, сглаживаются, увеличивается твердость поверхностного слоя, формируются сжимающие остаточные напряжения.
Обработка микрошариками является одним из современных методов ППД, который широко используется, например, для упрочнения деталей авиационной техники. В качестве рабочей среды используются стальные или стеклянные шарики диаметром 30-300 мкм, которые с помощью транспортера подаются к вращающимся соплам, ускоряются под действием центробежных сил и бомбардируют поверхности упрочняемых деталей. Для обеспечения равномерности упрочнения сопла совершают возвратно-поступательное движение (ВП) (рис. 8.2.24).
Достоинством обработки микрошариками является возможность упрочнения деталей с острыми кромками, канавками, проточками, резьбами, а также нежестких тонкостенных деталей. Сохранение геометрии деталей достигается за счет малых размеров частиц среды.
Легирование поверхностных слоев металлическими или неметаллическими элементами позволяет существенно повысить эксплуатационные свойства изделий и осуществляется различными методами и способами.
Рис. 8.2.22. Схемы упрочнения калиброванием (а) и виброобкатыванием (б)
Рис. 8.2.23. Алмазное выглаживание цилиндрической
поверхности на токарном станке
Основы технологии
1249
Ионная имплантация основана на прямом облучении поверхности потоком ионов, генерируемых специальной ионной пушкой. Электроискровое легирование заключается в переносе материала электрода-инструмента в поверхностный слой детали при возникновении между ними искрового электрического разряда. Диффузионное насыщение поверхностного слоя углеродом, азотом, бором при повышенных температурах позволяет получать твердые и прочные поверхностные слои толщиной до нескольких миллиметров.
Рис. 8.2.24. Схема установки для упрочнения изделий микрошариками:
1 — упрочняемая деталь; 2 — вращающиеся сопла;
3 — рабочая среда; 4 — конвейер
Нанесение на поверхность функциональных покрытий производят химическим или электрохимическим осаждением металлов из растворов, термическим напылением поверхностных слоев. Широкое распространение в машино- и приборостроении получили процессы электрохимического осаждения на поверхность деталей машин тонких, сплошных и прочно сцепленных с основой слоев железа, никеля, хрома, других металлов и сплавов.
Плазменное напыление является одним из широко применяемых способов термического напыления. В зоне плазменной струи достигаются температуры, достаточные для плавления любых материалов. Плазмотрон (рис. 8.2.25) включает в себя катод (электрод) и анод (охлаждаемое сопло), отделенные друг от друга небольшой камерой. При подаче напряжения между анодом и катодом образуется электрическая дуга. В результате ионизации газовой среды, прокачиваемой через камеру, формируется струя плазмы. Когда нестабильная плазма снова переходит в газовое состояние, выделяется тепловая энергия. Вводимый в виде порошка или проволоки материал покрытия плавится и переносится струей на субстрат (подложку). Типичными плазмообразующими газами являются водород, азот,
аргон и гелий. Достоинствами данного процесса являются универсальность, высокая гибкость, большое количество наносимых материалов, неограниченная толщина покрытий, простота автоматизации, высокая производительность.
На рис. 8.2.26 показана рабочая зона термического нанесения защитного жаростойкого покрытия на лопатку турбины.
К настоящему времени известно большое число различных методов и способов модификации свойств поверхностного слоя, разработаны и используются соответствующие технологии.
Пятый передел машиностроительного производства составляют технологические процессы сборки изделий, предназначенные для взаимной ориентации и закрепления отдельных деталей машин относительно друг друга путем создания различных видов соединений. Эти соединения подразделяют на неподвижные и подвижные, разъемные и неразъемные.
Последовательность выполненных соединений создает геометрическую и кинематическую структуру изделия в целом, а качество соединений определяет качественные показатели изделия.
Рис. 8.2.25. Схема плазменного напыления покрытий: 1 — катод; 2 — плазмообразующий газ; 3 — анод;
4 — ввод порошка
Рис. 8.2.26. Плазменное нанесение жаростойкого покрытия
на лопатку турбины
1250
Новый справочник химика и технолога
Для получения неподвижных неразъемных соединений в большинстве случаев используются механические (вальцовка, заклепывание) и физико-химические (сварка, пайка, склеивание) процессы. Получение заклепочного шва см. на рис. 8.2.27, а. Заклепка 2 с предварительно сформированной головкой вставляется специальным устройством 3 снизу в отверстия соединяемых деталей 7. При ударе бойка 4 верхняя часть заклепки деформируется, замыкая стык.
Сварные соединения наиболее распространены и выполняются с использованием различных методов сварки, отличающихся главным образом процессами тепловыделения. К ним относятся: ручная электродуговая, или газовая, сварка', автоматическая сварка под слоем специального вещества — флюса', электроконтактная сварка', сварка трением. Особо ответственные сварные швы получают с использованием технологии электронно-лучевой, или лазерной, сварки; в них требуемое для плавления материала температурное поле формируется при взаимодействии электронного пучка или лазерного луча с тонким поверхностным слоем материала.
На рис. 8.2.27, б представлена схема ручной элек-тродуговой сварки. Соединяемые детали 7 с предварительно подготовленными кромками выставляются друг относительно друга с помощью специальной оснастки и присоединяются к источнику питания (ИП). Электрод 2, представляющий собой металлический стержень в рубашке из специальной обмазки, подсоединенный к другому выводу источника питания, подводится к стыку. Возбуждается электрическая дуга, развиваются высокие температуры, металл оплавляется, образуется ванночка расплава. После застывания металла формируется сварочный шов (при перемещении электрода по заданному контуру).
Паяные соединения отличаются от сварных тем, что материал соединяемых деталей не доводится до температуры плавления. Плавится специальный материал (припой), подаваемый в виде проволоки или порошка в рабочую зону пайки. Подогрев соединяемых деталей осуществляют в печах, газовыми горелками или электропаяльниками.
Клеевые соединения получают, используя специальные самотвердеющие клеи различного состава. Склеивание позволяет получать изделия из однородных или неоднородных материалов путем нанесения слоя клея соответствующего состава на предварительно подготовленные, очищенные и обезжиренные поверхности склеиваемых изделий. Толщина слоя клея на поверхности в пределах 10-150 мкм. Через определенное время соединяемые детали приводят в соприкосновение, сжимают некоторым усилием и выдерживают при обычной или повышенной температуре.
К неподвижным разъемным соединениям относятся прежде всего соединения резьбовые и прессовые. Основную роль в таких соединениях играют силы трения, возникающие при силовом контакте сопрягаемых деталей. Пример прессового соединения показан на рис. 8.2.27, в.
Запрессовываемая деталь 7 усилием Р вводится в охватывающую деталь 2. За счет упругих свойств материала диаметры деталей 7 и 2 изменяются соответственно на 2С] и 2е2, а в месте сопряжения возникают нормальные давления ру, обеспечивающие прочность и плотность образованного соединения. Усилие запрессовки Р и максимальный передаваемый соединением крутящий момент Мрассчитывают по формулам:
P = TuUfp,', M = ^d2lfpy, (8.2.14)
где d—диаметр сопряжения; f— коэффициент трения; / — длина сопряжения.
Пример резьбового соединения показан на рис. 8.2.27, г. Крышка 7 и корпус 2 некоторого аппарата, работающего под давлением р, прочно соединены между собой резьбовыми соединениями, каждое из которых состоит из болта 3, гайки 4. Затягивая гайку специальным ключом, создают усилие затяжки Р3. Для предотвращения самоотвинчивания гайки под действием вибраций в процессе эксплуатации применяют специальные детали: шайбы различной конструкции (5), шплинты. Резьбовые соединения получили большое распространение в технике: их удельная доля в общем объеме сборочных работ достигает 25 %.
Важной операцией на стадии сборки изделия является балансировка, которую осуществляют после сборки вращающихся узлов и которая призвана устранить неуравновешенность масс — дисбаланс путем удаления или добавления небольших масс материала изделия в специально предусмотренных местах.
После сборки изделия машиностроения подвергаются испытаниям, которые должны подтвердить соответствие фактических технических характеристик изделия их проектным значениям. Кроме того, испытания позволяют выявить возможные погрешности сборки или изготовления отдельных элементов изделия. Для испытаний сложных образцов техники используются специальные стенды. В зависимости от степени ответственности данного изделия, степени его сложности, типа производства испытанию подлежат все изделия данного наименования, типоразмера и исполнения или некоторая часть из них (выборка). В ряде случаев стендовые испытания предусматривают и для отдельных составных частей изделия в процессе их изготовления.
Таким образом, процессы и методы машиностроительных производств многочисленны и разнообразны. Главной, определяющей чертой этих производств является их функциональная направленность — получение заданной пространственной конфигурации твердого тела или системы таких тел с высокой точностью. Достаточно сказать, что в прецизионном машино- и приборостроении точность изготовления изделий достигает 107м.
Основы технологии
1251
Рис. 8.2.27. Соединение деталей машин с помощью заклепок (а), сваркой (б), прессованием (в) и резьбовыми элементами (г)
8.2.2. Средства технологического оснащения
Выше отмечалось, что материальная сторона технологий выражается через технические средства: машины, аппараты, их комплексы или составные части. Совокупность орудий производства, необходимых для осуществления технологического процесса, называется средствами технологического оснащения. Их основой является технологическое оборудование — такие орудия труда, в которых размещаются сырье, полуфабрикаты или материалы, средства заданного воздействия на них, а также технологическая оснастка. В последнюю включают те средства технологического оснащения, которые дополняют технологическое оборудование для выполнения конкретных работ: инструменты, устройства для ориентации, закрепления, контроля и измерения предметов труда.
В любой технологической машине можно выделить четыре основных структурных элемента: двигатель, передаточный механизм, исполнительное устройство и устройство управления.
Двигатель является преобразующим элементом, в котором первичная, подводимая извне энергия (электрическая, пневматическая, гидравлическая, тепловая) преобразуется в энергию механического движения. В современном технологическом оборудовании наибольшее применение нашли электрические двигатели переменного и постоянного тока. Последние дают возможность легко регулировать частоту вращения выходного вала двигателя.
Передаточный механизм машины может выполнять целый ряд функций:
• распределение энергии двигателя между несколькими рабочими органами;
• передачу движения между пространственно разнесенными объектами, расположенными на различных расстояниях друг от друга;
• изменение направления движения рабочего органа (реверсирование);
• повышение (мультипликация) или понижение (редукция) частоты вращения вала исполнительного устройства по отношению к валу двигателя с соответствующим изменением крутящего момента на валу;
• ступенчатое или плавное изменение степени редуцирования или мультипликации.
Передаточный механизм представляет собой совокупность элементов — механических передач различного назначения.
Исполнительные устройства непосредственно реализуют заданные воздействия на объект производства. Так, например, этикетировочная машина, схема которой представлена на рис. 8.2.10, включает в себя следующие исполнительные устройства: транспортные (пластинчатый транспортер подачи тары 2, барабан-этикеткопереносчик 4), дозировочно-разделительные (магазин поштучной выдачи этикеток 6, шнек-распределитель подачи тары 3), устройства подготовки этикеток 7 и 8, рабочую накладку 5 с вакуум-системой
1252
Новый справочник химика и технолога
закрепления этикетки на барабане, накатной ремень. Все перечисленные исполнительные устройства с соответствующими рабочими органами действуют синхронно за счет соответствующей конструкции передаточного механизма.
Устройство управления обеспечивает заданную последовательность срабатывания отдельных исполнительных механизмов, контроль и корректировку скоростей и траекторий движения рабочих органов, ввод и вывод технологической информации в форме, удобной для считывания, взаимодействие с управляющими системами того же или более высокого иерархического уровня.
В отличие от машины, в которой для проведения работы по преобразованию свойств обрабатываемого объекта совершаются механические движения, в аппарате технологическая цель достигается при протекании тех или иных физико-химических процессов. Типичным аппаратом является, например, корпус вакуум-выпарной установки, рассмотренной нами ранее. В этом аппарате снижение влагосодержания томатной пульпы достигается ее тепловой обработкой при температуре кипения.
Из сказанного следует, что технологические машины и аппараты перерабатывают исходные материальные потоки (сырье, полуфабрикаты), потребляя при этом соответствующие энергетические и информационные потоки. Таким образом, триединая технологическая функция, описанная ранее, находит выражение в соответствующих элементах технологического оборудования.
Рассмотрим классификацию технологических машин и аппаратов по некоторым основным признакам:
• по степени универсальности оборудование подразделяют на универсальное, специализированное и специальное. Первый вид предназначен для обработки объектов широкой номенклатуры с большим диапазоном изменения физико-химических свойств, габаритных и массовых параметров. Специализированное оборудование используют для обработки объектов узкой номенклатуры с достаточно близкими свойствами, а специальное оборудование проектируется и используется для обработки, как правило, одного объекта с конкретными свойствами;
• по уровню автоматизации различают оборудование с ручным управлением, полуавтоматы и автоматы. Автоматы функционируют в автоматическом цикле без участия человека-оператора. В полуавтоматах функции оператора сводятся к загрузке объектов производства в рабочую зону, выгрузке из нее, пуске и выключении оборудования;
• по отраслевому признаку оборудование делят на оборудование химических, пищевых, лесоперерабатывающих производств, машиностроительное, сельскохозяйственное, швейное, обувное и т. д. в соответствии с приведенной ранее классификацией технологических процессов по указанному признаку;
• по функциональному признаку оборудование подразделяют на группы в зависимости от вида реализуемых на нем процессов. Так, тепловое оборудование химических производств можно разделить на нагреватели, охладители, выпарные аппараты, ректификационные аппараты, сушилки. Машиностроительное оборудование по этому признаку подразделяют на литейное, кузнечно-прессовое, сварочное, металлорежущее (станки), сборочное, вспомогательное. Очевидно, в зависимости от степени детализации технологических процессов можно построить развитую, иерархическую классификацию оборудования по функциональному признаку. Такая классификация используется, например, для металлорежущих станков и служит основой системы их обозначений. Следует отметить, что оборудование одного и того же функционального назначения может использоваться в различных отраслях промышленности. Это замечание относится к дробилкам, фильтрам, нагревательным устройствам и многим другим функциональным группам оборудования;
• по конструктивному признаку подразделяют, как правило, оборудование одного и того же функционального назначения. Так, выделяют дробилки валковые, центробежные, молотковые, щелевые и пр.;
• по пространственно-временным характеристикам объекта обработки в процессе технологического воздействия на него выделяют оборудование периодического и непрерывного действия. В первом из них обрабатываемый объект загружается в рабочую зону, находится в ней в течение обработки и затем выгружается из нее. В оборудовании непрерывного действия обрабатываемый объект перемещается через рабочую зону по тому или иному закону. Исполнительные устройства с рабочими органами либо закреплены за определенными рабочими позициями, либо перемещаются вместе с объектом, сопровождая его на некотором участке траектории движения.
В некоторых отраслях промышленности получила распространение классификация оборудования по массо-габаритному признаку или по признаку качества исполнения (обычное, экспортное, тропическое, прецизионное).
Металлорежущие станки делят на пять классов в зависимости от степени точности: нормальной (Н), повышенной (П), высокой (В), особо высокой (А) точности и станки особо точные (С). За счет повышения качества исполнения станков в указанном ряду возрастает точность изготавливаемых на них деталей, но соответственно повышается трудоемкость изготовления станков и, следовательно, их стоимость (табл. 8.2.2).
В литературе описаны и другие, более общие подходы к классификации технических объектов.
При разработке технологических процессов важной
задачей является выбор требуемого оборудования. Эту
процедуру выполняют в следующем порядке после
представления технологии в виде последовательности
операций:
Основы технологии
1253
• выбирают требуемую функциональную группу оборудования для каждой операции с учетом отраслевой принадлежности рассматриваемой технологии;
• в выбранной группе находят подгруппу (тип) оборудования, обеспечивающую требования к качеству технологии. В большинстве случаев на данном этапе принимают в расчет требуемую производительность, мощность, степень универсальности и уровень автоматизации оборудования;
• выбирают конкретную модель оборудования, исходя из физико-химических свойств объекта, его массо-габаритных показателей. Практически выбор оборудования осуществляют с помощью каталогов, справочников, проспектов.
Таблица 8.2.2 Влияние степени точности металлорежущего станка на погрешность изготавливаемой детали
и трудоемкость изготовления станка
Класс точности станка Погрешность обработки, % Трудоемкость, %
Н 100 100
П 60 140
В 40 200
А 25 280
С 16 450
По сути, изложенная процедура заключается в последовательном уменьшении мощности множества существующего оборудования путем наложения все более жестких ограничений на свойства элементов этого множества. Таким образом, каждая единица оборудования характеризуется некоторым набором свойств, выражающих, с одной стороны, ее принадлежность к некоторому классу, типу, а с другой — ее индивидуальность. Такая совокупность свойств, имеющих количественную меру, называется вектором показателей качества (ВПК) оборудования и используется при решении ряда задач, связанных с его проектированием, изготовлением и эксплуатацией.
При осуществлении вышеприведенной процедуры выбора требуемого оборудования часто складывается ситуация, при которой на последнем этапе оказываются несколько альтернативных вариантов, пригодных для решения технологической задачи, но отличающихся одним или несколькими показателями качества. Например, имеется возможность выбора оборудования, производимого несколькими различными фирмами. В этом случае возникает задача выбора лучшего в некотором смысле варианта, решение которой возможно лишь путем сравнения векторов показателей качества вариантов-альтернатив.
Рассмотрим подробнее содержательную сторону ВПК. Обычно выделяют три вида показателей качества, объединенных однородностью характеризуемых ими свойств.
1. Функциональные показатели качества выражают потребительские свойства оборудования, его соответствие выполняемой технологической функции.
• Показатели технического эффекта характеризуют способность оборудования выполнять свои функции в заданных условиях использования по назначению. Применительно к технологическому оборудованию основным показателем такого рода является производительность — величина, оценивающая количество кондиционной продукции, производимой данным оборудованием в единицу времени.
• Показатели надежности характеризуют одно или несколько свойств, составляющих надежность технического объекта. Надежность — это свойство объекта сохранять во времени способность к выполнению требуемых функций при условии соблюдения правил эксплуатации, предусмотренных нормативно-технической документацией (ГОСТ 27.002-89). Надежность — комплексное свойство оборудования, включающее в себя безотказность, долговечность, ремонтопригодность, сохраняемость.
Безотказность — свойство технического объекта непрерывно сохранять работоспособность в течение некоторого времени или некоторой наработки.
Долговечность — свойство технического объекта сохранять работоспособность до наступления предельного состояния при установленной системе технического обслуживания и ремонта.
Ремонтопригодность характеризует приспособленность технического объекта к предупреждению и обнаружению причин отказов, повреждений и устранению их последствий путем проведения ремонтов и технического обслуживания. Отказом называют событие, заключающееся в нарушении работоспособности технического объекта.
Сохраняемость — свойство объекта находиться в исправном и работоспособное состояние в течение и после хранения и (или) транспортировки.
Все перечисленные показатели надежности оцениваются совокупностью соответствующих количественных характеристик, которые получают, используя аппарат теории вероятности. Это связанно с тем, что отказ является следствием большого числа трудноучи-тываемых внешних и внутренних возмущений и по своей сути имеет статистическую природу. Рассмотрим в качестве примера некоторые из таких характеристик.
Вероятность безотказной работы — это вероятность того, что в пределах заданной наработки изделия отказ не возникает:
Р(/) = Р*{т>/},
где t — время или суммарная наработка объекта; Р* —
вероятность события, заключенного в скобках. Возник-
новение первого отказа — случайное событие, а соот-
ветствующая наработка т до этого события — случай-
ная величина. Часто используют понятие вероятности
1254
Новый справочник химика и технолога
отказа — вероятности того, что объект откажет хотя бы один раз в течение заданной наработки, будучи работоспособным в начальный момент времени. Очевидно, вероятность наступления отказа Q(t) на отрезке [0, ?] связана с вероятностью безотказной работы простым соотношением
2(0=1-Р(0. (8.2.15)
Средняя наработка до отказа — математическое ожидание соответствующей случайной величины наработки объекта до отказа:
TH = pWf. (8.2.16)
о
При оценке долговечности технического объекта используют такую характеристику, как у — процентный ресурс. Это суммарная наработка, в течение которой при заданных режимах и условиях применения объект не достигает предельного состояния с вероятностью у, %.
Средний ресурс и средний срок службы — это показатели долговечности, равные математическому ожиданию соответственно суммарной наработки и календарной продолжительности до наступления предельного состояния.
Комплексные показатели надежности характеризуют два (или более) свойства, входящие в определение надежности, например безотказность и ремонтопригодность. Примером комплексного показателя надежности может служить коэффициент готовности А',. Это вероятность того, что объект окажется в работоспособном состоянии в произвольный момент времени, кроме планируемых периодов, в течение которых применение объекта не предусматривается.
(8.2.17)
где Тв — среднее время восстановления работоспособности.
Показатели надежности, по сути, дополняют характеристику свойств изделия, оцениваемых показателями технического эффекта, т. к. предопределяют длительность и полноту проявления этого эффекта у потребителя. Так, суммарный полезный эффект Э за весь период функционирования объекта с учетом степени его безотказности составляет:
Э = Э0Т(ЛФ> (8.2.18)
где Эо — годовой полезный эффект функционирования объекта при безотказной работе; Тс — срок службы объекта, годы; Кэ$ — коэффициент сохранения эффективности, учитывающий степень безотказности изделия при его эксплуатации.
• Показатели эргономичности характеризуют систему «человек—машина» и учитывают комплекс гигиенических, антропометрических, физио- и психологических свойств человека, проявляющихся в производственных и бытовых процессах. При оценке эргономичности изделия в нем выделяют элементы, оказывающие влияние на работоспособность, производительность, утомленность оператора.
• Показатели эстетичности характеризуют эстетические свойства технического объекта: информационную выразительность, целостность композиции, соответствие окружающей среде, рациональность формы, оригинальность и гармоничность. Состав показателей эстетичности определяется спецификой технического объекта.
2. Ресурсосберегающие показатели качества характеризуют затраты различного вида ресурсов на разработку и изготовление изделия, а также на поддержание качества изделия в сфере потребления (эксплуатации).
• Показатели технологичности технического объекта характеризуют его конструктивные особенности, изменение которых влияет на уровень затрат ресурсов и позволяет оптимизировать эти затраты. Основными видами ресурсов, потребляемых в сфере производства и эксплуатации изделия, являются затраты материалов, энергии, труда и времени. Выделяют следующие показатели технологичности: материале-, энерго- и трудоемкость.
• Показатели унификации и транспортабельности относят к показателям технологичности конструкции технического объекта. Первый из них характеризует главным образом относительную долю в конструкции изделия оригинальных, разработанных только для данного изделия, составных частей, а второй — приспособленность данного изделия к перемещению в пространстве (транспортировке).
• Показатели ресурсоемкости рабочего процесса отражают способность объекта потреблять различные виды ресурсов в процессе функционирования по назначению. Например, для транспортных машин — это расход горюче-смазочных материалов на 100 км пробега, для технологического оборудования — расход электроэнергии на выпуск единицы продукции.
3. Природоохранные показатели качества технического объекта характеризуют те его свойства, которые оказывают вредное влияние на окружающую среду или представляют опасность для человека при функционировании системы «человек—машина—окружающая среда».
• Экологические показатели выбирают с учетом требований рационального взаимодействия между человеком и окружающей средой, прямого и косвенного влияния результатов эксплуатации технического объекта на природу. К экологическим показателям, например, относятся:
- содержание вредных примесей, выбрасываемых
в окружающую среду (твердых, жидких, газообразных);
Основы технологии
1255
- вероятность выброса вредных частиц, газов, излучений при хранении, транспортировке, эксплуатации объекта.
Оценка качества технических объектов по показателям экологичности производится путем сопоставления фактических значений этих показателей с установленными нормативными величинами по охране природной среды.
• Выбор показателей безопасности обусловлен необходимостью обеспечения безопасности человека при изготовлении, обслуживании, ремонте, хранении, транспортировке технических объектов. К таким показателям относятся, например, вероятность безопасной работы человека в течение определенного времени, вероятность травматизма, время срабатывания защитных устройств.
Для определения показателей качества технических объектов разработаны специальные методы и методики.
В заключение отметим взаимосвязь между стадиями жизненного цикла изделия и вектором показателей качества. Как видно на рис. 8.2.28, каждой стадии жизненного цикла соответствует свой ВПК. Первые требования к качеству изделия формулируют уже на этапе социального заказа на объект данного функционального назначения, аккумулирующего общественную потребность в нем. Следовательно, ВПК является динамичной, развивающейся характеристикой изделия.
Таким образом, качество технологических машин оценивается ВПК:
ВПК = (а„ Ь/, ck),
где a,, bj, ск — показатели соответственно функциональные, ресурсосберегающие и ограничительные, / = 1, ..., п’, j = 1, ..., nr, k = 1, ..., /. Номенклатура показателей качества определяется функциональным назначением технического объекта и устанавливается по отношению к группе родственного по назначению и свойствам оборудования.
В альтернативной ситуации выбор наилучшего оборудования осуществляют в два этапа:
- исключают из рассмотрения те виды оборудования, у которых хотя бы один показатель качества ниже некоторого установленного приемлемого уровня;
- из оставшихся вариантов выбирают тот, для которого наибольшие значения принимают коэффициенты К или К':
„К у R~Z
К = — или К =--
Z Z
где R — результат использования данного оборудования в стоимостном выражении; Z — суммарные затраты на приобретение и эксплуатацию данного оборудования.
К настоящему времени широкое распространение в отраслях промышленности получили роботы и манипуляторы. Промышленный робот — это машина-автомат, предназначенная для воспроизведения определенных функций человека при выполнении производственных операций и наделенная для этого некоторыми способностями человека, такими как сила, память, способность к обучению, адаптация в производственной среде.
Рис. 8.2.28. Схема взаимосвязи вектора показателей качества и жизненного цикла изделия
1256
Новый справочник химика и технолога
Робот состоит из манипулятора, информационной системы и системы программного управления. Манипулятор предназначен для выполнения двигательных функций, аналогичных функциям руки человека при перемещении предмета в пространстве. Он управляется оператором или автоматически.
Система программного управления представляет собой совокупность средств, предназначенных для формирования и выдачи управляющих сигналов манипулятору в соответствии с заданной программой. Ее назначение — формирование логической последовательности действия всех механизмов робота в автоматическом режиме. По способу управления движением эти системы делятся на программные и адаптивные. Информационная система включает в себя технические средства, обеспечивающие получение, переработку и передачу информации о состоянии робота и внешней среды.
Следует особо отметить, что помимо техникоэкономических преимуществ, таких как повышение производительности труда и качествГ продукции, снижение трудоемкости, применение промышленных роботов имеет социальное значение (освобождение человека от тяжелого, опасного или монотонного труда).
К настоящему времени промышленность выпускает роботы различного назначения с диапазоном грузоподъемности 10-1—104 кг, быстродействия 0,1-1 м/с, точностью позиционирования до 0,05 мм, с одним или несколькими манипуляторами, с рабочей зоной различной формы и размеров.
В промышленности используются роботы трех поколений, отличающиеся способом управления манипулятором.
Роботы первого поколения работают по заранее заданной жесткой программе, воспроизводят программные циклы и не реагируют на изменение окружающей обстановки.
Роботы второго поколения с адаптивным управлением работают по заранее заданному алгоритму управления. За счет наличия у них технического зрения, устройств ориентации, датчиков усилий и других средств восприятия внешней среды они реагируют на изменения этой среды и способны вырабатывать программы управления по обходу препятствий, выбору нужных объектов и решению других оперативных задач.
Роботы третьего поколения с искусственным интеллектом обладают способностью к самообучению, выбору и запоминанию наиболее эффективных приемов выполнения действий.
На рис. 8.2.29 представлены структурная схема робота и характеристика обслуживаемой им рабочей зоны. Устройство программного управления 1 и силовой агрегат 2 размещены на подвижной платформе 3 манипулятора. Колонна 4 расположена на поворотном столе 5 и поворачивается в пределах угла ср. Траверса 6 способна совершать прямолинейное возвратно-поступательное движение вдоль колонны, а смонтированный на ней шток 7 с захватным устройством 8 совершает ана
логичные движения в горизонтальной плоскости. Захват способен дополнительно перемещаться. Все отмеченные движения дают возможность роботу обслуживать рабочую зону в виде кольцевого цилиндрического сектора.
Рис. 8.2.29. Схема промышленного робота (а) и его рабочая зона (б)
Роботы относятся к оборудованию межотраслевого применения и широко используются в промышленности развитых стран.
8.2.3. Технологические операции и модули
Выше отмечалось, что структура технологической операции (ТО) может быть представлена упорядоченной последовательностью технологических модулей (ТМ) — далее неделимых в содержательном отношении элементов технологии. Каждый такой модуль осуществляет элементарное технологическое воздействие на обрабатываемый объект, а упорядочивание модулей во времени производят путем их последовательной, параллельной или последовательно-параллельной реализации. Если модули следуют один за другим, то при определении операционного времени их длительности суммируются. При параллельном выполнении ТМ операционное время равно длительности наиболее продолжительного ТМ. Отсюда следует, что последовательность выполнения отдельных ТМ существенно сказывается на длительности операции /0-
Рис. 8.2.30. Структурные схемы и формулы двух вариантов ТО
Основы технологии
1257
Действительно, выделим два варианта структуры ТО, включающие в себя 8 различных ТМ (рис. 8.2.30). Стрелки условно изображают длительности соответствующих модулей т,. Очевидно, операционное время зависит от временной структуры операции:
a) t0 = Т] + т2 + тах(т3,т4,т5) + тах(т6,т7) + т8;
б) t0 = тах(Т], т2) + т3 + тах(т4, х5) + х6 + т7 + т8.
Рассмотрим числовой пример. Зададим произвольные числовые значения ТМ и примем, что длительность модуля не зависит от его расположения во временной структуре ТО. Пусть Т] = т8 = 3 мин; т2 = т7 = 1 мин; т3 = т6 = 2 мин; т4 = т5 = 4 мин. Тогда, подставляя эти значения в расчетные выражения, получаем: a) to = 13 мин; б) to = 15 мин.
Легко посчитать, что при последовательном выполнении всех модулей операционное время равно 20 мин, а при параллельном — 4 мин. Этот пример показывает влияние временной структуры ТО на ее длительность и акцентирует внимание на важности этой характеристики ТО. Конечно, далеко не всегда ТМ независимы друг от друга и могут располагаться произвольным образом в структуре операции. Например, ТМ, определяющий нагрев объекта до заданной температуры, должен предшествовать тем модулям, которые содержат технологические воздействия на уже нагретый объект. Несмотря на то, что каждой технологии соответствуют свои правила упорядочивания технологических модулей, во многих случаях существуют несколько приемлемых структур организации ТО во времени. К вопросу выбора наилучшей из возможных структур мы вернемся в следующей главе.
Правила выполнения отдельных технологических воздействий регламентируются параметрами режима обработки. Сформулируем основные требования к этим параметрам, общие для большинства технологий:
• параметры режима должны представлять собой физические величины, которые могут быть быстро и точно измерены для текущего контроля за ходом ТП. Часто измерения некоторых параметров не производят, т. к. их величина и точность ее поддерживания обеспечиваются предварительной настройкой технологического оборудования;
• параметры режима должны гарантировать получение заданного технологического результата с требуемой точностью;
• число параметров режима должно быть достаточным для эффективного управления процессом;
• число параметров режима должно быть минимально необходимым для эффективного управления процессом. Отсюда следует, что параметры режима должны быть независимыми величинами (так, давление и температура конденсации насыщенных водяных паров не могут одновременно выступать как параметры режима в тепловых процессах, поскольку они взаимосвязаны);
• параметры режима обработки предусматривают работу технологического оборудования в нормальных условиях эксплуатации.
Рассмотрим некоторые примеры. На рис. 8.2.21 графически представлен весьма распространенный технологический процесс (стерилизация пищевой продукции, химические превращения при высоких температурах, закалка деталей машин). Очевидно, идентифицируемыми технологическими результатами являются нагрев объекта до рабочей температуры Тр за время т„, функциональное воздействие при этой температуре в течение тв и охлаждение до исходной температуры То за время т0- Вообще говоря, как при нагреве, так и при охлаждении характер зависимости температуры от времени требует специального обоснования и служит параметром режима. В большинстве практически важных случаев эта зависимость близка к линейной и параметром режима является скорость нагрева или охлаждения. Параметрами режима являются начальная и рабочая температуры. Значения времени нагрева или охлаждения к ним не относятся, т. к. определяются расчетом. Время тв является параметром режима, потому что определяет степень и полноту температурного воздействия. Это время назначают эмпирически или определяют инженерным расчетом. Например, при стерилизации пользуются зависимостями остаточного количества жизнеспособных микроорганизмов данного типа от времени при различных температурах, при закалке сталей — зависимостями степени превращения «аустенит—мартенсит» от времени и т. д.
На рис. 8.2.20, а представлена схема токарной обработки цилиндрической поверхности. Параметрами режима являются величины, определяющие скорость относительного перемещения рабочей кромки резца и обрабатываемой заготовки диаметром D: скорость перемещения кромки резца по касательной к окружности поперечного сечения заготовки (скорость резания v) и скорость поступательного перемещения вдоль оси заготовки Snp. Однако кинематических параметров недостаточно для достижения технологического результата — получения детали диаметром D и длиной /. Следовательно, необходимо регламентировать траекторию движения вершины резца относительно оси заготовки по требуемой цилиндрической поверхности, параметры которой, таким образом, являются параметрами режима. Обычно в технологической практике в документации приводится так называемая глубина резания, равная полуразности диаметров заготовки и обработанной детали, а также зависимый параметр — частота вращения заготовки пш, необходимый для настройки станка и рассчитываемый по выражению:
где k — коэффициент, определяемый размерностью
входящих в формулу величин.
1258
Новый справочник химика и технолога
В общем виде для операций, в которых исполнительный орган (инструмент) перемещается в пространстве относительно обрабатываемого объекта, задаются кинематические параметры такого перемещения и параметры, описывающе траекторию движения в виде линии или поверхности.
Выше отмечалось, что любой ТП связан с преобразованием материала, энергии или информации и протекает во времени. Поэтому важными характеристиками ТО являются нормы ресурсозатрат', материальных, энергетических, информационных и трудовых. Последние отражают участие человека (оператора) в производственном процессе. Установление технически обоснованных норм расхода производственных ресурсов называют техническим нормированием (ГОСТ 3.1109-82). При этом технически обоснованной нормой расхода каждого вида ресурсов называют такую его величину, которая необходима для выполнения работы при рациональной ее организации в данных условиях производства и требуемом качестве ее результата.
Нормы расхода материалов устанавливаются на основе уравнений материального баланса, связывающих массу конечного продукта, исходного сырья и отходов производства. Например, норму расхода сырья на выпуск единицы массы продукции на операциях выпаривания или сушки можно определить по уравнениям (8.2.8) и (8.2.11). Норму расхода материала на изготовление детали машины находят, определив по чертежу массу готовой детали (рассчитывают или определяют по специальным таблицам объем элементарных геометрических элементов, определяющих конфигурацию детали, суммируют эти элементы и находят массу с учетом плотности материала) и прибавив к ней массу металла, удаляемого при технологическом воздействии (стружка, облой, литники). Ясно, что чем современнее технология, тем меньше отходов. Поэтому коэффициент использования материалов (КИМ) служит одним из показателей качества технологии:
т
КИМ тс
где /ип, тс — массы соответственно конечного продукта и исходного сырья для рассматриваемой технологии или отдельной операции. Учитывая последовательный характер выполнения операций, можно показать, что КИМ для технологии в целом равен произведению соответствующих величин для каждой операции.
Расчетные нормы расхода материалов корректируют с учетом опытно-производственных данных. Последние часто используют также для определения норм расхода вспомогательных материалов (технологические среды, ветошь).
Нормы энергозатрат характеризуют требуемый расход электроэнергии, тепла, сжатого воздуха, прочих энергоносителей. Так, расчет затрат электрической энергии на проведение ТО производится по выражению:
N t
Это=—(8-2.19) Л
где 7VT в, /т в — соответственно мощность и время технологического воздействия; т| — коэффициент полезного действия оборудования. Если операция состоит из нескольких модулей, то норма энергозатрат находится суммированием.
Норма информационных затрат оценивает количество информации, необходимой для реализации данного технологического воздействия. Очевидно, что для ТП в целом информационные затраты на отдельные операции суммируются. Полученная величина отражает норму информационных затрат на единицу продукции. В технологиях обработки материалов эта величина в настоящее время практически не учитывается. Дальнейшая автоматизация этих процессов, насыщение их управляющей техникой, появление новых поколений оборудования сделают такое нормирование актуальным.
Нормирование труда предполагает установление нормы как количества, так и качества труда для каждой операции ТП, что необходимо, в первую очередь, для оплаты труда производственных рабочих. Нормирование труда позволяет выявить резервы рабочего времени, оценить рациональность и эффективность его использования, обосновать целесообразность и необходимую степень автоматизации производства. К настоящему времени развиты и широко используются два основных метода нормирования: аналитический и опытно-статистический. Первый метод предполагает применение расчетных формул и нормативов для получения технически обоснованной нормы времени. В его основе лежит расчленение трудового процесса по элементам, изучение и формализация описания этих элементов вплоть до получения простых рабочих формул. Второй метод основан на сравнении нормируемого трудового процесса с ранее осуществленным (по прецеденту) с привлечением опытно-статистических данных о фактических затратах времени на аналогичные работы в прошлом.
Для количественной оценки качества труда разработана тарифно-квалификационная система. В соответствии с этой системой сначала устанавливают профессию рабочего-оператора, участвующего в данной операции (обычно профессию связывают с используемым технологическим оборудованием и типовыми работами), затем определяют степень сложности работы (по перечню предназначенных к выполнению операций или модулей) и по соответствующей таблице — разряд работы. Этот разряд является мерой качества труда и определяет уровень его оплаты.
Мерой количества труда служит норма времени, определяемая на каждую операцию /0- Ее структура в общем виде представляется выражением вида
'» =—+*прХ4.+Е'.7’ <8-2-20)
и , ,
Основы технологии
1259
где Тп.3 — подготовительно-заключительное время, необходимое для подготовки и завершения обработки партии изделий на данной операции; п — число изделий в этой партии; /'в — время технологического воздействия при выполнении z-ro модуля; Апр — коэффициент перекрытия, учитывающий параллельное выполнение отдельных ТМ; /н' — время, непосредственно не связанное с технологическим воздействием, но необходимое для его осуществления; К, L — соответственно число технологических воздействий и элементов непроизводительных затрат времени по нормируемому элементу технологии.
При анализе представленного выражения следует иметь в виду следующее:
• норма времени тесно связана со структурой операции, рассмотренной в начале настоящего раздела, и, по сути, выражает эту структуру. Так, суммирование отдельных элементов /'в и Л, производится по правилам, изложенным выше, с учетом порядка следования отдельных воздействий;
• при достаточно большом размере партии изделий первый член выражения пренебрежимо мал и может не учитываться;
• второй член выражения, связанный с протеканием некоторого физико-химического процесса, как правило, поддается расчету;
• суммированию по L подлежат значения или те части , которые не перекрываются временем технологического воздействия.
Анализируя представленное выражение, можно наметить пути уменьшения ty.
• снижение количества технологических воздействий К и элементов непроизводительного времени L в структуре операции (при сохранении, конечно, технологического результата);
• снижение величины t'TB для каждого воздействия. Это достигается интенсификацией параметров режима, изменением способа или метода обработки при одинаковом технологическом результате;
• увеличение степени перекрытия элементов t\ в и tJH нормы времени;
• снижение подготовительно-заключительного времени при обработке партии изделий.
Подробнее вопросы технического нормирования технологических операций изложены в отраслевой технологической литературе.
Выше говорилось о том, что один и тот же технологический результат может быть достигнут путем реализации различных по составу и структуре операций. Важное значение в связи с этим приобретает вопрос оценки уровня качества ТО. Для такой оценки используют группу организационно-технических показателей, которые в совокупности образуют вектор показателей качества ТО. Рассмотрим основные единичные показатели, составляющие этот вектор.
• Показатель быстродействия характеризует скорость достижения технологического результата при осуществлении данной технологической операции. В общем случае для его определения можно использовать кинетическую модель, основанную на следующих рассуждениях. Если при реализации ТО происходит преобразование материальных, энергетических, информационных потоков, то такое преобразование описывается кинетической моделью вида
«подвод (vn) => преобразование (упр) => отвод (v0T)»,
которая справедлива для любого из перечисленных потоков.
Можно показать, что скорость v суммарного процесса изменения состояния обрабатываемого объекта лимитируется скоростью наиболее медленной из выделенных стадий переноса или преобразования вещества, энергии или информации, а время технологического воздействия на объект определяется наибольшим временем, затраченным на реализацию лимитирующей стадии:
t , t\tK ,t", ] (8.2.21)
где верхние индексы определяют вид потока, а нижние — соответствующую стадию. В большинстве обрабатывающих технологий лимитирующими являются стадии, описывающие поток вещества (материала), хотя это условие не является обязательным. Естественной мерой быстродействия в этом случае является производительность процесса — количество обрабатываемой продукции в единицу времени. В зависимости от вида выпускаемой продукции этот показатель измеряется количеством массы или объема готовой продукции в единицу времени (жидкие, сыпучие, газообразные продукты) или количеством единиц продукции, выпущенной в единицу времени (штучная производительность). Легко заметить, что в последнем случае при длительности операции /0 производительность есть величина обратная этой длительности. Отсюда следует, что задание нормы времени, по сути, регламентирует производительность ТО, а все рассмотренные выше пути снижения операционного времени направлены на повышение производительности.
• Показатели надежности ТО численно отличаются от соответствующих показателей технологического оборудования хотя бы потому, что технологический результат зависит от действий людей (операторов), управляющих программ и других факторов, обусловливающих отказы. Последние с технологической точки зрения вызывают не только задержки в выполнении работ, но и появление некондиционной продукции — брака. Для некоторых технологий, например используемых в производстве микроэлектроники, выпуск некондиционной продукции составляет десятки процентов.
1260
Новый справочник химика и технолога
• Показатели энергоемкости характеризуют удельные энергозатраты при производстве данной продукции. Поскольку в большинстве технологических систем используются электродвигатели, в качестве такого показателя выступает количество электроэнергии, затрачиваемое на выпуск единицы продукции. Для его расчета используют выражение:
п
м
(8.2.22)
где NyB, ттв — соответственно мощность, реализуемая при технологическом воздействии, и длительность последнего; т] — коэффициент полезного действия оборудования, учитывающий потери при передаче энергии от двигателя к исполнительному органу машины.
Обсудим пример, иллюстрирующий возможность получения одного и того же технологического результата при различных удельных энергозатратах. При обработке изделий путем удаления части материала с поверхности заготовки в машиностроении используются различные методы и способы. В табл. 8.2.3 сравниваются затраты энергии, необходимой для съема одного килограмма материала при различных методах обработки.
Видно, что при одном и том же технологическом результате в приведенном примере удельные энергозатраты могут отличаться на два порядка величины. Это подчеркивает значение данного показателя при оценке качества технологии.
Таблица 8.2.3
Значения показателей энергопотребления при различных методах обработки
Метод обработки Мощность оборудования, кВт Л Удельный расход энергии, кВт • ч/кг
1. Электро-эрозионная 1-100 0,1-0,6 7-50
2. Электрохимическая 1-120 0,6-0,9 8-30
3. Ультразвуковая 0,1-25 0,2-0,4 25-250
4. Светолучевая 0,5-5 0,02-0,2 250-2000
• Показатели качества обрабатываемой продукции включаются в вектор показателей качества соответствующей технологии, г. к. отражают эффективность ее функционирования. Более того, в ряде случаев показатель качества продукции выступает как основной критерий, определяющий выбор варианта технологии (операции). Номенклатура показателей качества продукции зависит от вида обрабатываемого объекта. Так, в машиностроении при изготовлении деталей машин широко используются показатели точности и качества поверхностного слоя изделий.
• К экономическим показателям технологической операции относятся прежде всего трудоемкость и себестоимость обработки. Под трудоемкостью операции понимают время, необходимое для ее выполнения, измеряемое в нормо- или человекочасах. Трудоемкость отражает затраты живого труда на проведение операции. Трудоемкость ТП складывается из трудоемкостей отдельных составляющих операций, а трудоемкость операций — из трудоемкостей входящих в нее модулей. Например, трудоемкость изготовления легкового автомобиля одинакового класса на различных предприятиях и в различных странах колеблется от 15 до 35 нормочасов. Это, несомненно, отражает уровень применяемых технологий.
Себестоимость операции является комплексным показателем, оценивающим суммарные затраты живого и овеществленного труда, необходимые на ее осуществление и выраженные в денежной форме. Понятие «себестоимость» используется на всех этапах и уровнях производственного процесса и является иерархичным. Различают технологическую (на отдельную операцию или ТП), цеховую, производственную и полную себестоимость продукции. Полная себестоимость определяет оптовую цену продукта и в связи с этим характеризует ее конкурентоспособность, возможности сбыта. Следовательно, это важный показатель эффективности производства в целом. Технологическая себестоимость является основой при формировании себестоимости продукции и отражает эффективность ТО или ТП.
Себестоимость изготовления данного продукта по данному технологическому процессу можно представить следующим выражением:
с« +XI3C, +СО, +э, +(1 + ^)3,), (8.2.23) J т
где Му — расходы на основные и вспомогательные материалы на единицу продукции за вычетом стоимости отходов; ЗС, — расходы на амортизацию той части зданий и сооружений, которая относится к z-му рабочему месту (операции); СО, — расходы на содержание и амортизацию средств технологического оснащения /-й операции; Э, — расходы на энергопотребление на /-й операции; 3, — расходы на заработную плату основных производственных рабочих; Кс — коэффициент, учитывающий начисления на зарплату. Первое суммирование производится по числу д различных материалов, расходуемых на единицу продукции, а второе — по числу операций т в ТП. Отсюда следует, что выражение в квадратных скобках представляет собой себестоимость ТО. В различных отраслях производства относительная доля отдельных элементов себестоимости различна, а их расчет производится по соответствующим методикам.
Таким образом, каждая операция ТП характеризует-
ся перечнем технологических модулей, структурой их
реализации во времени, параметрами режима каждого
модуля, средствами технологического оснащения. Уро-
вень качества каждой операции оценивается вектором
показателей качества. Рассмотрим технологические
Основы технологии
1261
элементы более высокого уровня — технологические процессы, элементами которых являются технологические операции.
8.2.4. Технологические процессы
В современном многономенклатурном производстве решаются две основные задачи:
- обеспечение выпуска заданной номенклатуры продукции путем реализации комплекса соответствующих рабочих технологий;
- подготовка выпуска перспективной продукции, коррекция действующих технологий в связи с изменением объема выпуска изделий, их конструктивным совершенствованием, изменением номенклатуры наименований или другими факторами.
Очевидно, вторая из перечисленных задач, называемая технологической подготовкой производства, всегда предшествует началу производства новой продукции. При ее решении ориентируются на современные достижения науки и техники, направленные на повышение эффективности производства, анализируют опыт передовых предприятий родственного профиля, учитываются долгосрочные тенденции развития данной отрасли и соответствующих технологий. Совместное решение указанных задач предопределяет тот факт, что технологические процессы постоянно развиваются, совершенствуются.
Выше отмечалось, что структура и содержание технологического процесса определяются перечнем и последовательностью выполнения отдельных технологических операций, каждая из которых обеспечивает конкретное изменение свойств объекта производства, а совокупность таких изменений и приводит к заданному преобразованию сырья (полуфабриката) в конечный продукт. В связи с этим удобно использовать маршрутное описание ТП, содержащее упорядоченный перечень операций (маршрут) с необходимыми пояснениями. Рассмотрим в качестве примера маршрутное описание технологии производства томатной пасты в пищевой промышленности (табл. 8.2.4).
Как видно, маршрутное описание дает представление о технологии в целом, однако параметры режима на каждой операции и прочие сведения, касающиеся организационно-технической стороны проведения операций, в маршруте не указываются. Подробное операционное описание технологии приводится в операционных картах и содержит наименование операции, перечень всех входящих в нее технологических модулей с указанием параметров режима обработки и последовательности выполнения этих модулей, технически обоснованные нормы расхода ресурсов, сведения о средствах технологического оснащения и др.
В ряде случаев экономически выгодно применять маршрутно-операционное описание технологии, которое содержит маршрут обработки (маршрутную карту) и операционные карты на наиболее сложные и ответственные операции.
Таблица 8.2.4
Технологический маршрут изготовления томатной пасты
№ п/п Наименование операции Т ехнологическое оборудование
1 Мойка томатов. Отделение кусочков почвы, грязи и пыли путем отмочки в ванне и последующего ополаскивания томатов Моечная машина для мойки растительного сырья
2 Инспекция. Отбраковка некондиционных томатов, удаление посторонних предметов Инспекционный транспортер
3 Подогрев и дробление томатов. Дробление и подогрев дробленой массы для облегчения последующей обработки Дробилка-подогреватель
4 Протирка. Отделение малоценной в пищевом отношении фракции (кожица, семена) Протирочная машина
5 Выпаривание. Концентрирование сухих веществ от 5-6 до 25-30 масс. % Вакуум-выпарная установка
6 Расфасовка. Дозирование по объему и расфасовка в потребительскую тару Расфасовочный автомат
7 Герметизация тары Закаточная машина
8 Стерилизация. Тепловая обработка продукта с целью бактерицидного воздействия на микроорганизмы Стерилизационный аппарат
9 Нанесение информации на тару Этикетировочная машина
10 Контроль продукции Контрольный стол
11 Пакетирование Пакетоформующая машина
На наиболее ответственные операции часто разрабатывают также технологические инструкции или регламенты работ.
Основным фактором, определяющим структуру и содержание ТП, форму его описания, является тип производства.
Многочисленные исследования показали, что про-
изводство является наиболее экономичным, эффектив-
ным, если структура и содержание ТП соответствуют
определенному типу. Так, в соответствии с ГОСТ
14.004-83, в зависимости от широты номенклатуры вы-
пускаемых изделий, регулярности, стабильности и объема
1262
Новый справочник химика и технолога
выпуска изделий современное машиностроительное производство подразделяется на три типа: единичное, массовое и серийное.
Единичное производство характеризуется широкой номенклатурой изготавливаемых или ремонтируемых изделий и малым объемом их выпуска.
Массовое производство характеризуется узкой номенклатурой и большим объемом выпуска изделий, непрерывно изготавливаемых или ремонтируемых в течение длительного времени.
Серийное производство характеризуется ограниченной номенклатурой изделий, изготавливаемых или ремонтируемых периодически повторяющимися партиями и сравнительно большим годовым объемом выпуска. Этот тип производства занимает промежуточное положение и по своим характеристикам может приближаться к единичному (мелкосерийное) или массовому (крупносерийное) типам производств. Характерным признаком серийного производства является выполнение на большинстве рабочих мест от 2 до 40 периодически повторяющихся операций. Серийное производство представляет особый интерес как наиболее распространенный тип. Так, в машиностроении распределение выпускаемой продукции по типам соответствующих производств имеет следующий вид: единичное — 5-10 %, массовое — 10-20 %, серийное — 75-80 %. Основной тенденцией развития технологий серийного производства, как будет показано далее, яв
ляется поиск разумного компромисса между высокой производительностью массового производства и исключительной мобильностью, гибкостью единичного.
Несмотря на то что деление производств на типы, приведенное выше, является достаточно условным, понятие «тип производства» нашло широкое распространение в машиностроении и может быть полезным при анализе технологий других отраслей. Это связано с существенными отличиями отдельных элементов и принципов проектирования технологий для различных типов производства. Для пояснения сказанного рассмотрим сравнительные характеристики единичного и массового производств, принимая во внимание тот факт, что характеристики серийного производства носят промежуточный характер (табл. 8.2.5).
Из приведенных данных видно, что отнесение данного производства к тому или иному типу автоматически регламентирует целый ряд его характеристик, что облегчает проектирование технологий.
Для определения типа конкретного производства используют обобщенные опытно-статистические данные. В машиностроении для определения типа производства задаются годовым объемом выпуска изделий, степенью сложности и массогабаритными показателями изделия. Кроме того, существуют расчетные критерии для определения типа производства, основанные на определении числа операций, выполняемых на большинстве рабочих мест в течение планируемого промежутка времени.
Таблица 8.2.5
Сравнительная характеристика различных типов производств
Технологические характеристики Тип производства
единичное массовое
Применяемые средства технологического оснащения Квалификация основных производственных рабочих Описание технологий Повторяемость выпуска изделий одного наименования, типоразмера и исполнения Форма организации производства Нормирование ресурсов Уровень автоматизации Характерный признак Область применения Универсальные Высокая и универсальная Маршрутное Не повторяется или повторяется через неопределенное время Расположение оборудования по функциональному признаку Укрупненные, опытно-статистические нормы Низкий, большая доля ручного труда Выполнение на рабочих местах разнообразных операций без их периодического повторения Продукция тяжелого машиностроения: крупные гидротурбины, прокатные станы, металлургическое оборудование Специализированные и специальные Низкая, ориентированная на выполнение ограниченного числа операций Маршрутное и операционное Повторяется в течение длительного времени Поточные формы организации, автоматические и роторно-конвейерные линии Расчет и тщательное обоснование норм ресурсозатрат Высокий, вплоть до комплексноавтоматизированного Выполнение на большинстве рабочих мест одной повторяющейся операции Однородные изделия стандартного типа, имеющие широкое применение
Основы технологии
1263
Важной характеристикой ТП в целом является длительность технологического цикла Т1(, т. е. промежуток времени от начала до конца периодически повторяющегося ТП. На рис. 8.2.31 представлена технологическая линия, состоящая из N рабочих мест. На z-м рабочем месте обрабатываемый объект находится в течение времени (время выполнения z-й операции); время t‘m соответствует перемещению объекта с z-й на (z + 1)-ю операцию, а время — выдержке объекта производства перед (z + 1)-й операцией, например на промежуточном складе, в накопителе, отстойнике. Тогда в общем случае время цикла определяется выражением:
t„=E';+Z'-+Z<- <8-2-24)
/V tf-l ЛМ
Представляется очевидным, что уменьшение времени цикла упрощает и удешевляет производство. Проанализируем приведенную формулу с этой точки зрения и выделим возможные пути сокращения времени цикла:
• уменьшение числа операций N, переход к малооперационным технологиям;
• сокращение операционного времени на отдельных операциях;
• уменьшение времени транспортирования. Это достигается за счет перекрытия (частично одновременного выполнения) основных и транспортных операций;
• сокращение времени задержки полуфабриката в промежутках между операциями.
Организация и управление технологическим процессом существенно упрощаются, если последний организован по поточному принципу, в основе которого лежат непрерывность движения объектов производства и равномерность их выпуска. Этот принцип наиболее зримо проявляется при обработке в потоке жидких или сыпучих сред, например при тепловой обработке пищевых жидкостей (пастеризация вин, асептическое консервирование соков). При обработке штучных изделий движение последних по ходу ТП организуется двумя различными методами. Первый из них предусматривает дискретное перемещение объекта обработки по схеме «движение—выстой» от одной операции к другой, подвергаемого на каждом рабочем месте технологическому воздействию в соответствии с содержанием операции в течение времени t[. Непрерывность процесса достигается расположением рабочих мест в последовательности операций, сокращением времени межоперационной транспортировки и хранения. Равномерность выпуска
изделий достигается такой организацией технологических операций, при которой время их выполнения примерно одинаково:
= т = const.
Величина т называется тактом выпуска изделий. Ясно, что при выполнении сформулированного условия межоперационные заделы не потребуются, а время межоперационной транспортировки минимально. В этом случае время цикла рассчитывают по выражению:
Тц=/т,
где z — число рабочих мест (операций). Производительность такой линии есть величина, обратная такту выпуска.
Если указанное условие не выполняется, то перед лимитирующей операцией с максимальным временем проведения образуется задел обрабатываемых изделий, а оборудование более производительных операций оказывается незагруженным. Это снижает экономические показатели ТП. Производительность линии определяется производительностью лимитирующей операции. Для увеличения производительности линии в таких случаях оборудование лимитирующей операции часто дублируют.
Второй метод предусматривает организацию ТП по схеме параллельного движения исполнительных устройств технологического оборудования и обрабатываемого объекта с выполнением операций обработки и транспортировки одновременно. На рис. 8.2.32 показана роторно-конвейерная линия, обеспечивающая последовательную реализацию трех операций, закрепленных за соответствующими роторными автоматами. Исходные штучные заготовки поступают с заданным шагом по транспортеру и на позиции 3А загружаются на рабочий стол ротора А, вращающегося с частотой z?A. Перемещаясь вместе со столом в пределах рабочего угла (pi, объект обрабатывается на первой операции исполнительными устройствами ротора А. По завершении первой операции в позиции Зв объект перегружается на автомат В (рабочий угол <р2), а после завершения второй операции — на автомат С. Конечная операция (угол <р3) завершается выгрузкой обработанного объекта на отводящий транспортер.
Вход
Выход
Рис. 8.2.31. Схема прямоточной линии с промежуточными складами (С), накопителями (Н), распределителями потоков (Р)
1264
Новый справочник химика и технолога
Таким образом, обрабатываемый объект, непрерывно перемещаясь, на отдельных участках траектории своего перемещения подвергается технологическим воздействиям. Такая линия применяется, например, при расфасовке вин. На первой операции осуществляется расфасовка, на второй — укупоривание бутылки и на третьей — оформление бутылки (этикетка, колпачок). Безусловно, работа всех машин, входящих в рассматриваемую линию, должна быть синхронизирована, что обеспечивается их конструкцией. В основе такой синхронизации лежит условие одинаковой пропускной способности П (производительности) всех автоматов:
П = mn - const,
где т — число рабочих позиций ротора; п — частота его вращения.
Время цикла для рассмотренной линии определяется выражением:
тц +to +to
где tm — неперекрываемое время транспортировки объекта. Последнее слагаемое обусловлено конструктивными причинами и невелико по отношению к операционному времени. Поэтому такого рода линии обеспечивают максимальную производительность и минимальное время цикла. Однако они рассчитаны на выпуск узкой номенклатуры однородной продукции, и их целесообразно использовать в массовом и крупносерийном производстве. Роторные машины и роторно-конвейерные линии нашли широкое применение в производстве боеприпасов, при розливе больших объемов жидких продуктов в розничную тару (линии розлива).
Рис. 8.2.32. Схема трехоперационной роторно-конвейерной линии
Таким образом, анализируя ТП в целом, можно рассматривать его как динамичный системный объект и выделять его технологическую и организационную функции. Отсюда вытекает необходимость оценки уровня качества такого объекта. Заметим, что приведенные выше показатели качества отдельных операций применимы и к ТП в целом. Подробнее показатели качества технологии будут рассмотрены ниже.
8.2.5. Управление технологическими процессами
К числу наиболее общих и значимых свойств ТС, как уже говорилось, относится управляемость, т. е. приспособленность к поддерживанию высокой эффективности функционирования и адаптации к изменению внешней среды. Это свойство реализуется через управляющие воздействия на техническую систему. Для любой ТС существует некоторый набор управляющих воздействий Уь Y2, ..., Ym, формирующих т — мерное пространство воздействий. Поскольку каждое из таких воздействий физически или технически ограничено некоторыми предельными условиями вида
Y'<Y,<Y^, /=1,2,...,щ,
постольку в указанном т выделяется область, называемая областью возможных управляющих воздействий. Таким образом, выбирая точку или траекторию в этой области, целенаправленно изменяют состояние ТС, т. е. управляют ею.
Управление — это воздействие на объект, выбранное из множества возможных воздействий на основании имеющейся для этого информации, улучшающее функционирование или развитие данного объекта.
Такое определение вытекает из опыта решения управленческих задач, положивших начало бурному развитию промышленности XX в.
Рассмотрим некоторые определения и положения, относящиеся к теории управления — научной дисциплине, которая дает возможность создавать системы управления для объектов различной природы по единым принципам, учитывая конкретные особенности этих объектов только при разработке способов получения информации о состоянии объекта и вводе управляющих воздействий в него.
Для того чтобы управлять каким-либо объектом, необходимо определенным образом изменять во времени управляющие воздействия на него. Это осуществляется с помощью сигналов управления, несущих сообщения о требуемых значениях управляющих воздействий. Совокупность элементов, предназначенная для вырабатывания таких сигналов, называется устройством управления (УУ). Управляемый объект и присоединенное к нему управляющее устройство образуют систему управления (СУ). Совокупность правил, по которым информация, поступающая в УУ, перерабатывается в сигналы управления, носит название алгоритм управления. Элементы СУ, преобразующие сигналы управления в требуемые изменения управляющих воздействий,
Основы технологии
1265
являются исполнительными органами (ИО). На рис. 8.2.33, а представлена схема, иллюстрирующая систему управления. На основании обработки информации Z УУ вырабатывается сигнал управления U, который преобразуется ИО в управляющее воздействие Y объек
та управления (ОУ), обеспечивающее требуемое значение или закон изменения выходной величины X. Заметим, что наряду с управляющими воздействиями на вход реального ОУ подаются воздействия, не контролируемые УУ, называемые возмущающими (М).
К
Рис. 8.2.33. Схемы систем управления
Свойства СУ существенно зависят от характера источника информации, используемой для формирования сигнала управления. В связи с этим выделяют два типа систем управления.
Системы, в которых для формирования управляющих воздействий не используется информация о значениях управляемых выходных величин, называются разомкнутыми. Структура одной из таких систем представлена на рис. 8.2.33, б. Алгоритм управления, реализуемый УУ, основан на идее компенсации возмущений: для каждого возмущения М подбирается такое значение У, которое компенсирует искажающее влияние М на управляемую величину X.
Системы, в которых для формирования управляющих воздействий используется информация о значениях управляемых величин, получили название замкнутых. Структура такой системы показана на рис. 8.2.33, в. Как видно, между выходом и входом ОУ в такой СУ имеется связь.
Связь между выходными величинами X, z-го элемента системы и входными воздействиями какого-либо иного элемента этой системы называется прямой связью, а связь между X, и входными воздействиями на тот же z-й элемент системы Y, — обратной.
Обратная связь, увеличивающая влияние входного воздействия на выходную величину элемента системы, называется положительной, а уменьшающая это влияние — отрицательной. В общем случае отрицательная обратная связь способствует восстановлению равнове
сия в системе, если оно нарушается внешним воздействием, а положительная — усиливает это отклонение от равновесия. Понятие «обратная связь» является одним из основных в теории управления техническими системами.
Замкнутые СУ позволяют обеспечить достижение цели функционирования ОУ, если возмущающих воздействий много и не все из них могут быть измерены, а также в тех случаях, когда заранее неизвестно влияние возмущений на управляемые величины. Преимущество разомкнутых СУ состоит в том, что возмущения не успевают существенно изменить значение управляемой величины. Совмещение приведенных преимуществ достигается в комбинированной СУ (рис. 8.2.33, г). Видно, что в формировании сигнала управления участвуют как информация об основных возмущающих воздействиях, так и информация о значении управляемой величины.
В связи со сказанным ясно, какую роль приобретает первичная информация о состоянии управляемой величины. Для ее получения используют разнообразные датчики, конструкция и точность функционирования которых постоянно совершенствуются. Например, для точного измерения линейных координат все в большей степени применяют лазерные датчики.
Несмотря на упрощенный характер, приведенные
выше схемы лежат в основе практически всех СУ тех-
ническими объектами. Такие СУ призваны решать сле-
дующие основные типы задач управления:
1266
Новый справочник химика и технолога
1. Задача стабилизации заключается в поддержании некоторых выходных величин ОУ вблизи неизменных заданных значений Хо, несмотря на действие возмущений М. Так, например, в системах энергоснабжения должны быть стабилизированы напряжение и частота тока в сети независимо от изменения энергопотребления. В технологических процессах необходимо получать стабильные показатели качества готового продукта, несмотря на изменение свойств исходного сырья, температуры воздуха в цехе и прочих возмущений.
2. Задача выполнения заданной программы состоит в том, чтобы состояние ОУ удерживалось вблизи изменяющегося во времени по заранее заданному закону состояния XQ(t). Информация о законе изменения состояния ОУ может фиксироваться и храниться в каком-либо запоминающем устройстве (ЗУ), присоединяемом к СУ с образованием системы программного управления (СПУ). Реализация программы в этом случае может достигаться в условиях применения как разомкнутых, так и замкнутых СПУ (рис. 8.2.33, а, б). Принцип программного управления широко используется в современных ТС. Так, технологии и оборудование с числовым программным управлением (ЧПУ) составляют основу многономенклатурного машиностроительного производства, обеспечивая обработку изделий по заданному контуру и на заданных параметрах режима. Программное управление лежит в основе развития живых организмов.
3. Задача слежения решается в тех случаях, когда закон изменения во времени заданного состояния ОУ заранее не известен, а определяется в ходе самого процесса функционирования ОУ в соответствии с некоторым внешним сигналом. СУ, предназначенная для изменения состояния X(i) ОУ по закону XQ(i), задаваемому внешним, не известным заранее сигналом, называется следящей системой.
4. Задача оптимального управления заключается в нахождении и реализации такого варианта управления, при котором некоторая величина J, называемая критерием эффективности функционирования ОУ, принимает наивыгоднейшее значение. Под оптимальным управлением понимают такую совокупность управляющих воздействий, совместимую с наложенными на систему ограничениями, которая обеспечивает наилучшее в каком-то смысле значение J. Очевидно, в качестве таких критериев можно использовать показатели качества технологий, описанные ранее, или их совокупности. Часто в практически важных случаях наилучшим значением критерия является его экстремальная величина.
5. Задача адаптивного управления состоит в таком изменении свойств ОУ, которое обеспечивает приемлемое (или наилучшее в каком-то смысле) его функционирование в изменяющихся внешних условиях. Схема, приведенная на рис. 8.2.33, Э, иллюстрирует сказанное. Стоящий в цепи обратной связи идентификатор И в процессе работы ОУ по информации о воз
мущениях М, сигналах управления U, управляемой величине X непрерывно уточняет параметры К объекта управления. Адаптация (приспосабливаемость) характерна для многих объектов живой природы. Адаптивные СУ нашли применение в машиностроении (металлорежущие станки), химической и биотехнологии, в технологиях военного назначения и других областях.
Следует отметить, что в реальных системах управления ТП, как правило, приходится решать несколько различных типов задач управления.
Выше при рассмотрении системного характера технологий были отмечены такие свойства ТС, как целостность, многомерность, иерархичность. Очевидно, при построении СУ ТП необходимо учитывать перечисленные свойства. Это достигается за счет соблюдения нескольких общих принципов.
Централизация управления предполагает наличие единого органа, отвечающего за достижение глобальных целей ТС и принимающего соответствующие решения. В этом выражается целостность сложной ТС, направленность ее на решение единой задачи.
Специализация управления предполагает разбиение СУ на отдельные подсистемы с «горизонтальными» взаимосвязями, каждая из которых решает задачи управления соответствующими подсистемами ТС (управление технологической средой, материально-техническими ресурсами, организацией трудового процесса и др.).
Иерархичность СУ ТП выражается в многоступенчатом, пирамидальном принципе ее построения, разбиении на уровни с «вертикальными» связями и подчинением низших ступеней высшим. Устанавливается приоритет управляющих сигналов высших уровней.
Такое построение управления большими системами позволяет согласовать локальные цели отдельных элементов ТС с ее глобальными целями, обеспечивает повышенную устойчивость ОУ к внешним возмущениям, позволяет локализовать внутренние конфликты в системе. Схематично иерархическая система управления показана на рис. 8.2.34, а ее функционирование подчиняется следующим требованиям:
• каждая управляющая подсистема контролирует и управляет объектами в пределах выделенной ей зоны ответственности;
• каждая управляющая подсистема рассматривает подчиненную ей систему низшего уровня как самостоятельную и не вмешивается в ее работу;
• каждая управляющая подсистема обобщает информацию о результатах своей работы и передает ее в систему более высокого уровня.
Из сказанного следует, что работа развитой СУ ос-
новывается на обмене различных ее элементов потока-
ми информации, обработке этой информации и приня-
тии решений. При этом сведения о состоянии управляе-
мых объектов передаются от систем низшего ранга
к высшим во все более обобщенном и систематизиро-
ванном виде. Команды управления (приказы, распоря-
Основы технологии
1267
жения, директивы) вырабатываются УУ высшего ранга в наиболее общей форме и все более детализируются и конкретизируются по мере продвижения к УУ низших
рангов. Системы одного уровня обмениваются необходимой для принятия решений информацией, которая, как правило, не носит директивного характера.
Рис. 8.2.34. Схема четырехуровневой системы управления
В качестве примера разбиения СУ на уровни рассмотрим автоматизированную систему управления многономенклатурным машиностроительным производством, в которой выделяют три уровня управления. На оперативно-организационном уровне осуществляют оперативно-производственное планирование, учет и контроль за ходом производства, технологической подготовкой производства, включая подготовку управляющих программ для станков с ЧПУ; на оперативнодиспетчерском уровне — координацию выполнения работ на отдельных позициях, управление материальными потоками; на оперативно-технологическом уровне — программное управление отдельными единицами оборудования, исполнительными устройствами, средствами автоматизации и их взаимодействием. Очевидно, в качестве подсистем СУ одного уровня можно выделить функциональные подсистемы управления технологическим оборудованием, транспортной и складской системами, системой обеспечения инструментом и оснасткой, техническим обслуживанием и ремонтом и др.
Каждую из описанных подсистем СУ можно формализовать, используя в первом приближении одну из представленных на рис. 8.2.33 схем, описать математически и автоматизировать с привлечением технических и программных средств вычислительной техники.
С технологической точки зрения наибольший интерес представляют СУ низшего уровня иерархии (управление ТО и ТМ), оперирующие с наиболее подробной и конкретной технологической информацией. Обсудим некоторые особенности этого уровня управления.
Прежде всего, отметим все более широкое применение вычислительной техники на самом нижнем уровне иерархии СУ ТП. Это стало возможным в связи с появлением дешевых и надежных микроэлектронных устройств — микропроцессоров, представляющих собой, по сути, небольшой компьютер, который совместно с датчиком состояния образует измерительный преоб
разователь. Последний способен передавать или выводить на устройство считывания скорректированную и масштабированную информацию о состоянии ОУ по заданному параметру в цифровой, удобной для дальнейшего использования форме. Появление измерительных преобразователей существенно повысило быстродействие и надежность СУ, обеспечило компьютеризацию всех уровней управления ТП.
Все большее развитие получает технологическое оборудование, в систему управления которым встроена микроЭВМ. Вычислительно-логические возможности современной микроЭВМ обеспечивают решение всех задач управления данной единицей оборудования и контроля ТП. На микроЭВМ управление ТП реализуется с помощью программ, которые записывают в постоянное запоминающее устройство с использованием универсальных языков программирования, имеющихся в составе программного обеспечения. Многие микроЭВМ содержат блоки сопряжения с универсальными устройствами ввода-вывода информации, например стандартными телевизорами и магнитофонами. Это дает возможность производить отладку программ управления непосредственно на оборудовании.
Применение микропроцессоров, перерабатывающих информацию преимущественно в цифровой форме, измерительных преобразователей и микроЭВМ, использование систем числового программного управления оборудованием указывает на тенденцию развития цифровых систем управления ТП. Такие СУ отличаются высокой гибкостью, эффективным взаимодействием применяемых технических средств, возможностью их самоконтроля и самонастройки.
Из сказанного выше следует, что существует боль-
шое многообразие вариантов функциональных, органи-
зационных, аппаратурных и программных решений при
выборе или проектировании СУ ТП. Следовательно,
возникает вопрос о сравнении их эффективности.
1268
Новый справочник химика и технолога
В связи с этим разработана группа показателей качества и эффективности СУ.
Так, например, стоимость С некоторой операции (или группы операций) управления длительностью т, осуществляемой некоторой СУ, рассчитывается по выражению
-+Г
С = ^— т, (8.2.25)
где К — капитальные затраты, необходимые для создания СУ; Д — срок службы СУ; Г — годовые эксплуатационные расходы; F — годовой фактический фонд времени работы СУ. Очевидно, этот стоимостный показатель можно успешно использовать при сравнении систем управления ТП.
8.2.6. Моделирование технологий
При решении ряда задач, связанных с проектированием, подготовкой и функционированием технологических процессов прибегают к их моделированию, т. е. к изучению отдельных сторон, характеристик, свойств ТП не на реальном объекте, а на его модели. Под моделью понимают такую мысленно представленную или материально реализованную систему, которая, отображая объект исследования, способна воспроизводить с той или иной точностью его функции и замещать его на определенном этапе исследования. Таким образом, модель — это некоторая система, сохраняющая существенные свойства оригинала и допускающая исследование определенных свойств последнего физическими или математическими методами. Иными словами, модель — это отображение, описание технологического объекта (процесса или оборудования) с помощью некоторого языка, разработанное для достижения определенной цели. К настоящему времени разработана общая теория моделирования сложных систем, которая указывает на возможность использования различных видов моделей для описания технических и технологических объектов.
Модель играет активную роль в исследовании ТП: с ее помощью можно с минимальными затратами и в сжатые сроки определять различные характеристики ТП, такие как расход сырья и выход готового продукта, показатели качества этого продукта, количество отходов, бракованных изделий, конструктивные параметры элементов оборудования. Можно наметить и апробировать эффективную стратегию управления технологией, произвести процедуру оптимизации и т. д.
Из сказанного следует, что целесообразность моделирования ТП определяется двумя основными условиями:
- исследование на модели дешевле, проще, безопаснее, быстрее, чем на объекте-оригинале;
- известно правило пересчета характеристик и параметров модели в соответствующие величины ориги
нала, т. к. в противном случае моделирование теряет смысл.
Цель, поставленная при разработке модели, определяет ее вид, информативность и степень соответствия реальному объекгу, т. е. при формулировке цели необходимо тщательно отобрать те существенные свойства, которые в полной мере характеризуют рассматриваемый объект, определить требуемую степень соответствия модели реальному объекту (точность модели). Это позволяет в ряде случаев упростить модель, устранить из рассмотрения малозначимые, несущественные взаимосвязи между величинами, снизить затраты на моделирование.
При описании технологических процессов чаще используются натурное, физическое и математическое моделирование.
Натурное моделирование предполагает проведение экспериментального исследования реального технологического объекта и последующую обработку результатов с применением теории подобия, регрессионного анализа, таблиц соответствия. Это позволяет получить качественные или количественные зависимости, описывающие с той или иной точностью функционирование объекта. Однако эмпирические зависимости, основанные на представлении процесса в виде «черного ящика», хотя и позволяют решить частные технологические задачи, обладают существенными недостатками:
- эмпирические зависимости, строго говоря, нельзя распространять на весь возможный диапазон изменения параметров режима — они справедливы лишь при тех условиях и ограничениях, при которых проводился натурный эксперимент;
- такие зависимости отображают прошлый опыт, поэтому на их основе не всегда возможно выявить и обосновать пути повышения эффективности соответствующих технологий.
В ряде случаев эмпирические зависимости носят качественный характер, т. е. устанавливают лишь характер влияния одних величин на другие, без установления количественных закономерностей.
Физическое моделирование также предполагает проведение экспериментальных исследований с последующей обработкой результатов. Однако такие исследования проводятся не на реальном технологическом объекте, а на специальных лабораторных установках, которые сохраняют природу явлений и обладают физическим подобием. Таким образом, физическое моделирование основано на подобии процессов одной природы, протекающих в объекте-оригинале и в физической модели, и заключается в следующем:
- устанавливают основные, подлежащие численно-
му определению параметры технологического процесса,
характеризующие его качество;
- рассчитывают и изготавливают одну или несколь-
ко физических моделей в виде лабораторных или полу-
производственных (опытных, пилотных) установок.
Расчет этих установок производят на основе теории
Основы технологии
1269
подобия, что гарантирует возможность переноса результатов на реальный объект;
- в результате эксперимента на модели получают численные значения и взаимосвязи выделенных параметров и пересчитывают их для оригинала.
При физическом моделировании удается получить обширную информацию об отдельных процессах, определяющих структуру данной технологии.
Аналоговое моделирование связано с подобием процессов различной природы и основано на том факте, что для различных физических явлений существуют одинаковые закономерности их описания. Аналогичными считаются объекты или процессы, описываемые одинаковыми по форме уравнениями. В качестве примера сравним приведенные в данной книге уравнения Фурье (8.2.6) и Фика (8.2.9). Несмотря на различие входящих в них физических величин, все операторы совпадают и следуют в одной и той же последовательности. Следовательно, изучая один процесс, мы получим зависимости, справедливые (с точностью до обозначений) для другого. Для аналогового моделирования используют как экспериментальные методы, так и аналоговые вычислительные машины.
Аналитическое моделирование дает наиболее мощный инструмент для их исследования и предполагает получение и исследование различных математических моделей. Так, структурные модели используются для общего или предварительного описания объекта и позволяют выявить и определить его элементы, их свойства и взаимосвязи между элементами и свойствами элементов. Обычно для построения структурной модели используют аппарат теории множеств. Классификационные модели позволяют упорядочить исследуемые объекты, выделить в них общие признаки и ранжировать по этим признакам. Такие модели необходимы при построении систем автоматизации управления, создании банков данных и разработке систем автоматизированного проектирования, информационно-поисковых систем и в ряде других случаев. Познавательные модели используются для количественного описания закономерностей протекания различных процессов или функционирования оборудования. Они устанавливают взаимосвязи, соотношения между величинами, характеризующими процесс или оборудование.
Познавательная модель описывает, как правило, физико-химический механизм процесса и может не содержать технологические параметры или характеристики объекта.
Между частными моделями, описывающими отдельные процессы или иные структурные составляющие изучаемого объекта, существуют взаимосвязи. Учет таких взаимосвязей, т. е. совместное решение уравнений, описывающих отдельные единичные процессы, приводит к построению обобщенной модели метода или способа обработки.
Технологические модели отличаются от познавательных тем, что целью их построения является нахож
дение количественных взаимосвязей между параметрами режима, условиями функционирования — входами технологической системы и показателями ее технического уровня, т. е. выходами системы. Построение технологических моделей всегда связано с оценкой уровня качества и повышением эффективности функционирования технологических систем. Обычно технологические модели строятся на основе математических моделей отдельных процессов или на основе обобщенной модели объекта. Однако в ряде случаев полное аналитическое описание объекта невозможно, и при построении технологических моделей используют некоторые эмпирические зависимости. Как правило, технологические модели строят для изучения отдельных сторон функционирования технологической системы, т. е. они носят частный характер.
Отметим, что для большинства технологических процессов в связи с их сложностью построение единой обобщенной модели, адекватно описывающей все стороны и особенности их протекания, затруднено или невозможно. Поэтому при моделировании ТП используют принцип декомпозиции и решения локальных задач, позволяющий выделять и моделировать отдельные стороны, свойства ТП. В результате такого подхода ТП представляется совокупностью моделей, описывающих отдельные закономерности его функционирования и предназначенных для решения определенного круга задач. Такое представление естественно вытекает из системного характера технологий, описанного в 8.1. Иерархичность технологии порождает иерархичность моделей (модели ТП, ТО, ТМ), многомерность технологий — разнообразие моделей (модели физико-химических процессов, технологий, оборудования).
В качестве примера многообразия моделей рассмотрим технологию электрохимической размерной обработки (ЭХРО) (рис. 8.2.15, б). Модели, используемые при исследовании и описании такой технологии, показаны на рис. 8.2.35.
К числу частных познавательных моделей в данном случае относятся следующие:
• кинематическая (описание кинематики взаимного перемещения электродов);
• гидравлическая (описание движения жидкости в узком межэлектродном канале);
• электрическая (описание электрического поля в меж-электродном промежутке);
• тепловая (описание поля температур);
• электрохимическая (описание электродных процессов и процессов переноса в электрохимической системе);
• химическая (описание химических стадий сум-
марного электродного процесса, химических превра-
щений вещества в растворе).
К технологическим моделям относятся модель фор-
мообразования (описание движения границы анода при
электрохимическом растворении его поверхности), мо-
дель электрода-инструмента и ряд других.
1270
Новый справочник химика и технолога
Частные модели формообразования
Частные модели проектиро-вания инструмента
Модель наводороживания поверхностного слоя
Модель оптимизации параметров режима
Модель системы регенерации электролита и утилизации отходов
Классификационные модели
МОДЕЛИ ПРОЦЕССОВ ЭХРО
Структурные модели
Электрические процессы
Электрохимические процессы
Гидродинамическиё процессы
Модели единичных физических или химических процессов
Кинематические процессы
Тепловые процессы
Взаимосвязь между моделями
Химические процессы
ОБОБЩЕННАЯ МОДЕЛЬ ПРОЦЕССА ЭХРО
ТЕХНОЛОГИЧЕСКИЕ МОДЕЛИ
Решение технологических
параметров режима, оптимизации, управления, проектирования средств технологического оснащения, оценки параметров уровня качества, нормирования
Модель оценки производительности и энергоемкости
Модель оценки точности работы
Модель формирования микрогеометрии
Модель станочной системы
Модель оценки технологической надежности
Рис. 8.2.35. Виды моделей для описания процессов электрохимической обработки материалов
Основы технологии
\Z1\
В основе моделирования лежат основные представления теории подобия, в соответствии с которой явления, процессы называются подобными, если данные, полученные при изучении одного из них, можно распространить на другие. Для подобных явлений необходимо постоянство отношений некоторых величин, характеризующих процесс, или сочетаний таких величин, называемых критериями подобия. Так, например, при изучении течения жидких сред широко используется критерий Рейнольдса:
где v — скорость потока жидкости, м/с; d — гидравлический диаметр потока, м; v — кинематическая вязкость среды, м2/с. Число Рейнольдса — безразмерная величина, от значения которой зависит характер движения жидкости, распределение скоростей течения по сечению канала и другие параметры потока.
Основная (третья) теорема подобия гласит, что для подобия явлений необходимо и достаточно, чтобы их условия однозначности были подобны. Это означает, что должны соблюдаться геометрическое подобие, подобие физических констант, начальных и граничных условий, а критерии подобия, составленные из величин, входящих в условия однозначности, были бы одинаковы. Следовательно, все подобные явления отличаются друг от друга только масштабами характерных величин. Таким образом, если явления или процессы подобны, то закономерности, полученные при изучении одних из них, можно переносить на другие, а модельные результаты пересчитать с учетом масштабных факторов.
Суммируя сказанное, можно заключить, что основное требование к модели состоит в ее соответствии моделируемому объекту. Степень соответствия модели тому реальному явлению, которое она описывает, называют адекватностью модели. Доказательство адекватности — один из основных этапов построения любой модели. Для количественной оценки адекватности используют понятие «точность модели». Каждая модель должна сопровождаться информацией о ее точности для надежного использования результатов моделирования.
Точность детерминированных величин определяется *
отклонением результата моделирования х от соответствующей ему реальной величины х, а точность стохастических моделей оценивают вероятностными характеристиками.
Для обеспечения адекватности модели на этапе ее построения рекомендованы следующие правила:
• выбирают рациональную последовательность построения модели;
• используют итеративный процесс построения модели, т. е. многоэтапную процедуру ее разработки с оценкой промежуточных результатов, анализом их точности и коррекцией модели предыдущего этапа;
• уточняют модели на основе имеющихся экспериментальных данных;
• уточняют модели на основе получения экспертных оценок, результатов функционирования объекта и прочих дополнительных данных.
В настоящее время при анализе технологий используют различные виды моделирования.
Усложнение технологических процессов, увеличение числа параметров, значимых при построении моделей, ужесточение сроков моделирования, ограничение материальных средств, выделяемых на эти цели, — все эти факторы затрудняют, а в некоторых случаях исключают предметное моделирование. Поэтому на первый план выдвигается математическое моделирование ТП, получившее развитие во второй половине XX в. в связи с появлением и доступностью мощных и быстродействующих вычислительных машин.
Математическим моделированием ТП называют исследование, осуществляемое путем решения системы математических соотношений, описывающих ТП, и имеющее три этапа:
• составление математического описания процесса или его элемента;
• выбор метода решения системы уравнений математического описания и реализация его в виде алгоритма, программы для получения количественных величин или соотношений;
• установление адекватности модели оригиналу.
При построении математических моделей реальный процесс упрощается, схематизируется, и полученная схема в зависимости от ее сложности описывается гем или иным математическим аппаратом. В конкретном случае математическое описание представляется в виде системы алгебраических, дифференциальных, интегральных уравнений или их совокупности.
С точки зрения анализа математической модели целесообразно выделить три ее стороны:
• смысловой аспект отражает физическое описание моделируемого объекта;
• аналитический аспект представляет соьой систему уравнений, описывающих происходящие процессы и взаимосвязи между ними;
• вычислительный — метод и алгоритм решения, реализованные в виде программы на одном из языков программирования.
В последнее время для исследования сложных систем, в том числе технологических процессов, все большее применение находит имитационное моделирование, в основе которого лежит машинный эксперимент. Для реализации математической модели на ЭВМ строится моделирующий алгоритм, воспроизводящий процесс функционирования системы во времени. Путем изменения входных данных получают сведения о состояниях процесса в заданные моменты времени, по которым оценивают характеристики объекта. Таким образом, при имитационном моделировании имеют дело с моделями, по которым нельзя заранее рассчитать или предсказать результат.
1272
Новый справочник химика и технолога
Рассмотрим в качестве примера моделирование процесса электрохимической анодной обработки материала, описанного ранее (рис. 8.2.15, б). Эта технология получила распространение при изготовлении пространственно сложных изделий машиностроения, таких как лопатки турбин и компрессоров. С технологической точки зрения необходимо уметь рассчитывать время t, необходимое для снятия слоя металла толщиной z (машинное время обработки), или же величину слоя металла (припуска) zn, снятого за время t. Для получения расчетных зависимостей воспользуемся частной моделью плоскопараллельного межэлектродного промежутка (МЭП), смысловой аспект которой ясен из рис. 8.2.36, а. Как видно, электрод-инструмент (ЭИ) движется поступательно со скоростью ги, а на поверхности анода (А) формируется эпюр локальных скоростей электрохимического растворения межэлектродный промежуток заполнен электролитом, а между электродами приложено напряжение U.
Сделаем некоторые допущения, упрощающие модель. Пусть скорость электрохимического растворения одинакова для всех точек анодной поверхности и свойства электролита также одинаковы для всех точек МЭП. Тогда для описания процесса можно воспользоваться законами Ома и Фарадея:
la cr]i
U = — и у, =---,
X Р
где U — напряжение на электродах; i — плотность тока; а — текущий межэлектродный зазор; % — удельная электропроводность электролита; с — электрохимический эквивалент металла; р — выход по току реакции растворения металла; р — плотность обрабатываемого металла.
Из расчетной схемы следует, что da/dt = уэ - уи, поскольку растворение поверхности компенсируется смещением ЭИ в сторону заготовки. Отсюда получаем дифференциальное уравнение, описывающее изменение МЭП во времени:
^=Ж0±у(Г) (8.2.26)
dt а
при начальном условии t = 0; а = а0
Анализ модели значительно упрощается, если принять А = const. Такое допущение корректно для многих практически важных задач. Рассмотрим два случая, реализуемые в большинстве схем электрохимического формообразования: уи = 0 (случай неподвижного ЭИ) и уи = const (движение ЭИ с постоянной скоростью). Интегрируя приведенное выше дифференциальное уравнение, получаем для первого случая:
а = (^+2Л/)2, (8.2.27)
а для второго:
(^-1)ехрф = (^-1)ехр(^)ехр(-^). (8.2.28) A A A A Z
Преобразуя полученные выражения, можно получить зависимости времени от величины МЭП.
Несмотря на упрощенный характер предложенной модели, она успешно используется в технологических расчетах и во многих случаях хорошо описывает экспериментальные данные.
Однако в тех случаях, когда отношение длины меж-, / электродного зазора к его ширине к = — достаточно а
велико (в реальных процессах к достигает значений 200-1000), свойства электролита по длине МЭП сильно изменяются из-за сопутствующего выделения тепла и газа, и сделанные выше допущения неприемлемы.
Необходимо строить модели, в которых учитываются зависимости параметров процесса от координаты гидравлического тракта и времени.
Рис. 8.2.36. Схема к построению математической модели (а)
и установка для физического моделирования
процесса ЭХРО в узком длинномерном зазоре (б)
Основы технологии
1273
Для получения подобных зависимостей широко используется физическое моделирование. На рис. 8.2.36, б приведена физическая модель длинномерного МЭИ, позволяющая получать распределения плотности тока, температуры электролита, газосодержания, эффективной электропроводности межэлектродной среды, локальной скорости съема металла и других параметров по длине МЭИ прямым экспериментом. Насос / прокачивает электролит через гидравлический тракт, образованный плоскопараллельными электродами 2 и 3, встроенными в диэлектрические плиты 4. Величина межэлектродного зазора определяется толщиной сменной прокладки 5 и изменяется в пределах 0,2-2 мм. Варьируемыми параметрами режима электролиза являются: величина зазора, напряжение на электродах, входное давление электролита, его состав, начальная температура, скорость подачи катода на анод, длина МЭП, материал электродов. Газовыделение, профиль скоростей течения электролита изучались с помощью скоростной киносъемки процесса, для получения распределения локальных плотностей тока по длине МЭП использовался секционный анод, распределения давления и температуры фиксировались тензодатчиками давления и термопарами, специальными зондами измерялись электродные потенциалы в различных сечениях МЭП. Изменение съема металла по длине канала фиксировалось прямыми измерениями.
Анализ показывает наличие соответствия между представленной физической моделью и оригиналом: соблюдается геометрическое, гидравлическое, электрическое подобие, подобие физических констант, начальных и граничных условий. Поэтому полученные экспериментальные данные позволили не только уточнить математическую модель, но и получить технологические результаты, пригодные для непосредственного использования в производственных условиях. Отметим, что аналоговое моделирование электрических полей в МЭП на электропроводной бумаге также позволило получить важные практические результаты.
Таким образом, приведенный пример показывает, что различные виды моделей дополняют и уточняют друг друга, давая в совокупности надежные данные для практического использования. К настоящему времени трудно найти такие области технологии, в которых отсутствовал бы развитый аппарат математического моделирования основных процессов. Особый интерес представляют модели, описывающие процессы проектирования технологий. Такие модели позволяют генерировать новые технологические объекты с помощью машинных методов и являются базой при переходе к автоматизированному проектированию технологий.
8.3. Проектирование технологий
Выше показано, что технологические процессы, представляющие собой сложные системы, характеризуются большим разнообразием элементов различного уровня, свойствами этих элементов и связями между
ними. В отраслевых технологиях накоплены значительные теоретические и эмпирические знания, позволяющие успешно решать задачи анализа технологий, в первую очередь устанавливать функциональные взаимосвязи между входными параметрами процесса и единичными показателями качества технологий и их элементов. Такие взаимосвязи дают возможность не только оценить достигаемые значения единичных показателей данного ТП, но и управлять ими. Однако рассмотренный выше аппарат анализа технологий не позволяет создавать новые технологические объекты.
Создание новых ТС основано на использовании аппарата синтеза технологий, который содержит семантические, логические и аналитические правила, процедуры, модели, алгоритмы, предназначенные для получения новых вариантов технологий и их элементов, обеспечивающих заданный результат воздействия на объект производства. Две основные трудности выступают на первый план при решении задач синтеза:
• создание новых технических объектов — это область инженерного творчества, отличающаяся привлечением нетрадиционных, порой парадоксальных или интуитивных подходов к решению проблем, трансформацией известных решений из других областей науки и техники, применением эвристических методов;
• задачи синтеза слабо формализованы, что затрудняет применение ЭВМ и существенно увеличивает трудоемкость проектных работ. Формализация технологических знаний, т. е. переход от содержательных моделей к аналитическим, служит необходимым условием автоматизации проектирования и является предметом многих исследований, выполненных в последнее время.
Для дальнейшего обсуждения данного вопроса важно определить следующие обстоятельства. Синтезируя новые технологии или их элементы, мы формируем множество возможных вариантов решения задач проектирования. Однако предстоит решать задачу выбора элемента этого множества, лучшего в каком-то смысле, т. е. оптимизировать проектное решение. Таким образом, синтез технологий, являясь сердцевиной, ключевым звеном, не охватывает весь процесс проектирования технологий.
8.3.1 Основные принципы и общая методика проект ирован ия
Проектирование технологии можно рассматривать как некоторую научно-техническую проблему, определенную на множестве технологических систем, а результат проектирования — как решение этой проблемы. Для большинства сложных систем решение проблем характеризуется существованием множества путей, направлений достижения цели (подпроблем) и возможностью нескольких вариантов решения для каждой подпроблемы и проблемы в целом. Отсюда следует, что проектирование технологий можно представить как процесс проработки, анализа проблемы с выявлением
1274
Новый справочник химика и технолога
возможных путей ее решения, определением вариантов решения, обоснованием выбора тех вариантов, которые в данных условиях обеспечивают наилучшее решение проблемы. Если к сказанному добавить, что объектом проектирования является сложная технологическая система, то становится очевидной необходимость обсуждения процесса проектирования с системных позиций.
Следовательно, процесс технологического проектирования — это система, обладающая перечнем свойств, рассмотренных в 8.1.5, имеющая собственные структуру и функцию и состоящая из элементов-подсистем, объединенных принципом единства цели. Связь подсистем проявляется также через непосредственное взаимодействие многих из них, вызванное условием следования: результаты проектирования одних подсистем служат исходными данными для других.
Иерархичность и многомерность ТС порождают иерархичность и многомерность процесса проектирования. Это означает, что последний представляется в виде вертикальных уровней — этапов проектирования, упорядоченных условием соподчиненности, а на каждом из таких уровней выделяются взаимосвязанные подсистемы, описывающие различные стороны процесса проектирования. Многоуровневый процесс проектирования можно иллюстрировать следующей схемой:
Уровень 1. Принципиальная схема технологии
Ф
Уровень 2. Проектирование маршрута
Ф
Уровень 3. Проектирование операции
Ф
Уровень 4. Проектирование модуля
Очевидно, каждый уровень проектирования будет отличаться степенью детализации проектных решений. На каждом уровне можно выделить взаимосвязанные проектные задачи, описывающие собственно технологическую, материально-техническую, информационную, организационную, эргономическую, экономическую и другие стороны процесса проектирования.
Функция технологического проектирования может быть сформулирована в достаточно общем виде следующим образом: спроектировать технологию, обеспечивающую требуемый целевой результат воздействия на объект производства при выполнении заданных условий и ограничений.
Если представить процесс проектирования в виде «черного» ящика, то можно описать его входы и выходы, основываясь на сделанном определении.
Входы, вектор X:
а) объект производства и его свойства. Как уже отмечалось, свойства, определяющие качество производимой продукции, включаются в вектор показателей
качества соответствующей технологии. Поэтому полная и достоверная информация о конечном продукте является необходимым условием процесса проектирования. Так, для проектирования технологии изготовления некоторой детали машины должны быть представлены чертеж и технические условия на изготовление изделия или иная информация, полностью характеризующая готовую, годную деталь.
Полная или частичная информация об исходном продукте (сырье) также предоставляется проектировщику перед началом проектирования. Так, например, при проектировании технологий механообработки изделий машиностроения указывается, как правило, лишь материал детали, а вид заготовки и способ ее получения устанавливают в процессе проектирования. В технологиях переработки сельхозпродуктов, в химических и пищевых технологиях приводится полная информация об используемом сырье;
б) объект проектирования и его свойства. Набор свойств проектируемой технологии или ее элементов необходим для последующего сравнения вариантов проектных решений. Поэтому такой набор должен быть задан или выбран проектировщиком перед началом проектирования. Обычно в качестве таких свойств используют единичные показатели качества технологии, перечень которых выбирают в зависимости от решаемых задач и условий производства;
в) целевой технологический результат характеризуется конкретными приемлемыми значениями единичных показателей качества технологии или некоторой их совокупности, удовлетворяющими пользователя технологий;
г) условия и ограничения, накладываемые на процесс проектирования, можно разделить на две группы.
Элементы первой группы относятся к объекту проектирования и отражают условия его функционирования. Они могут относиться к целевым конечным результатам, регламентируют какие-либо показатели качества технологии или оговаривают производственные условия применения данной технологии.
Элементы второй группы относятся к процессу проектирования и отражают правила (условия) выполнения отдельных этапов или их согласования, а также ограничивают ресурсозатраты на проектирование. Так, для того чтобы выбрать наилучший вариант из множества альтернатив, необходимо сформулировать некоторые условия предпочтения. На процесс могут быть наложены ограничения по срокам проектирования, стоимости проектных работ, трудоемкости, затратам машинного времени при автоматизированном проектировании.
Условия выражают некоторую взаимосвязь между элементами, обязательную для выполнения и сформулированную словесно или аналитически. Ограничения выступают, как правило, в виде одно- или двухсторонних строгих или нестрогих неравенств вида:
Основы технологии
1275
где х} — параметр, подвергаемый ограничению; [2f]^ax, IXJmin — соответствующие предельные значения этого параметра.
По обязательности выполнения ограничения подразделяют на жесткие и корректируемые. Первые подлежат безусловному выполнению, а вторые могут уточняться в ходе проектирования.
Выбор условий и численных значений ограничений подлежит тщательному обоснованию перед началом проектирования.
Выходы, вектор Y:
а) полный набор документов (объем информации), необходимый и достаточный для реализации данной технологии или последующего ее проектирования на другом уровне.
Необходимо отметить, что в информационном отношении результаты проектирования значительно превосходят исходные данные, т. е. в процессе проектирования генерируется новая информация.
Таким образом, функция проектирования может быть формально представлена как X х В —> У, т. е. выражать преобразование входов в выходы с помощью оператора проектирования В. Очевидно, процесс проектирования может быть разбит на отдельные последовательные этапы, каждому из которых соответствует свой оператор, описывающий функцию этапа. Пример разбиения процесса проектирования на этапы будет рассмотрен ниже.
Для описания структуры процесса проектирования технологий (ПТ) необходимо определить состав ее элементов и связи (отношения) между ними. Ясно, что совокупность таких элементов должна обеспечивать достижение цели, т. е. представлять собой один из путей решения проблемы. Выделим и обсудим пять основных элементов такой структуры, представив ее в виде
ПТ = (И, А, С, О, Р). (8.3.1)
Множество И элементов структуры ПТ содержит информационно-поисковые работы и процедуры, основанные на использовании справочников, каталогов, методик, банков данных. Заметим, что объем информации, необходимой для проектирования достаточно сложных объектов, настолько велик, что даже опытный проектировщик, изолированный от информационной среды, сможет решать лишь простейшие задачи проектирования.
Множество А элементов включает в себя решение задач анализа технологий и тесно взаимодействует с И. Задачи анализа приходится решать не только при постановке и конкретизации проектного задания и обсуждении проекта технологии, принятого к реализации,
но и в процессе нахождения вариантов решения совместно с задачами синтеза.
Множество С элементов включает проектные действия, охватывающие решение задач синтеза технологий. На этом этапе генерируется, как правило, наибольшее количество новой информации об объекте проектирования. Полнота множества альтернативных вариантов технологий, полученных на этапе синтеза, во многом определяет качество проектного решения, степень риска при выборе наилучшего варианта. Формирование множества вариантов-альтернатив требует мощного информационного обеспечения и в наибольшей степени нуждается в автоматизации работ с помощью ЭВМ.
Множество О элементов структуры ПТ формирует проектные действия, ответственные за выбор наилучшего варианта среди множества альтернатив. Задачи, решаемые при этом, носят название оптимизационных. Такого рода задачи возникают на различных этапах проектирования, в том числе на конечном этапе при принятии проектного решения.
Множество Р элементов объединяет работы и процедуры, связанные с реализацией проектного решения. Строго говоря, реализация спроектированной технологии не входит в задачу проектировщиков. Однако практически в ходе реализации возникают и требуют решения вопросы, относящиеся к компетенции и требующие привлечения проектировщиков. Эти вопросы связаны с изменением внешней среды, условий функционирования технологии, изменением свойств объекта производства, социальными и другими факторами. Их решение может потребовать изменения отдельных элементов технологии: пересчета параметров, корректировки системы управления, замены отдельных единиц и перепланировки оборудования.
Таким образом, структура процесса проектирования, его подсистем, вплоть до решения конкретных проектных задач, может быть представлена совокупностью элементов описанных выше множеств И, А, С, О, Р, обладающих определенными свойствами и связанных отношениями. Так, некоторая частная задача пт проектирования записывается в виде:
пт = ( и,,а7, с,,оър2>,
и, с: И, i = 1,..., b;
а, с А,у= 1,..., с;
с1 с:С, / = 1,...,
Ok g О, к = 1,..., е;
#cP,z=l,..., f
Поскольку каждый элемент перечисленных мно-
жеств представляет собой некоторое проектное дейст-
вие, процедуру, необходимо определить правила выбо-
ра и сочетания этих элементов. Совокупность таких
правил, определяющих последовательность проектных
действий, называют стратегией проектирования. Та-
кую стратегию предлагается разрабатывать в два этапа:
1276
Новый справочник химика и технолога
• разбиение задачи проектирования на части предполагает построение многоуровневой структуры объекта проектирования с последующим выявлением и формулированием на основе такой структуры частных задач проектирования. Разбиение задачи проектирования на части, по сути, есть выявление подсистем проектирования на каждом уровне вплоть до формулировки конкретных проектных задач;
• выбор стратегии проектирования. Прежде всего, выявим стратегию взаимодействия уровней проектирования. Возвращаясь к описанному выше представлению процесса проектирования четырехуровневой иерархической моделью, выделим и обсудим два возможных подхода к ее реализации. Первый из них основывается на проектном движении «сверху вниз» — от высших иерархических уровней к нижним. Этот подход получил широкое распространение в технологическом проектировании и назван В.Д. Цветковым итерационным многоуровневым процессом последовательной детализации и оптимизации проектных решений. Схематически такой подход приведен на рис. 8.3.1. Так как в процессе формирования варианта решения появляется новая информация, может случиться, что прорабатываемый вариант не удовлетворяет проектировщика. Это вызывает необходимость возвратиться на один из предыдущих уровней и повторить проектные действия.
Второй подход основывается на проектном движении «снизу вверх» и предполагает в качестве первоначального этапа проектирование ТП на уровне модулей. Далее по специальным правилам модули упорядочивают, формируя операции. Упорядочивание операций приводит к генерированию маршрутов, а последние формируют схему процесса. Такой вариант проектирования используют, например, в машиностроении при проектировании ТП обработки детали, которая имеет поверхности с повышенными требованиями к качеству изготовления. Нет оснований отрицать целесообразность комбинирования рассмотренных вариантов при проектировании сложных многоэтапных технологий.
Анализ показывает, что при решении любой проектной задачи последовательность действий проектировщика определяется одной из следующих стратегий:
• линейная стратегия представляет собой цепочку последовательных действий, каждое из которых зависит от исхода предыдущего, но не зависит от результатов последующих действий (рис. 8.3.2, <а);
• циклическая стратегия применяется тогда, когда на некоторой стадии проектирования приходится возвращаться к одному из предыдущих этапов. В этом случае в линейной цепи проектных действий появляется петля или несколько охватывающих друг друга петель (рис. 8.3.2, б). Такая петля отражает так называемую итерационную процедуру. Подобная стратегия выражает процесс последовательного приближения к цели проектирования путем улучшения разрабатываемых вариантов;
• разветвленная стратегия используется в тех случаях, когда имеется возможность одновременного решения нескольких задач проектирования (рис. 8.3.2, в). Параллельное выполнение проектных действий позволяет сократить сроки проектирования. Кроме того, такая схема обеспечивает одновременное выполнение альтернативных этапов с принятием промежуточных решений и возможным изменением последующих действий;
• адаптивные стратегии (рис. 8.3.2, г) отличаются тем, что в них выбор каждого действия зависит от исхода предыдущего. Отсюда вытекает, что при такой стратегии можно задавать только первое действие. Подобная схема поиска решения приводит к тому, что каждый этап проектирования имеет наиболее полную исходную информацию. Поэтому такая стратегия считается одной из самых разумных и используется при попытках создания машинного интеллекта. Недостатком адаптивных стратегий является невозможность априорной оценки затрат на проектирование и сроков его выполнения;
• стратегия случайного поиска основывается на отсутствии каких-либо планов поиска решения (рис. 8.3.2, д). Каждый этап проектирования выполняют без использования информации о результатах предыдущих этапов. Считается, что это придает поиску решения непредубежденный характер. Такую стратегию часто используют при поиске новых идей, новаторских решений, когда разумно не пренебрегать ни одним из внесенных предложений до появления дополнительной информации.
С1...С4 — синтез вариантов решения на каждом уровне проектирования;
ОЦ1...ОЦ4 — оценка и отбор наиболее рациональных вариантов решения на каждом уровне;
ТЗ — техническое задание на проектирование (исходные данные); ПР — проектное решение (результат проектирования)
Основы технологии
1277
Выбрать наугад любую
Определить решение
точку в поле поиска
в этой точке
Рис. 8.3.2. Схематическое изображение стратегий:
Э, — проектное действие; ПВР — решение типа «продолжить или вернуться?»
• стратегия случайного поиска основывается на отсутствии каких-либо планов поиска решения (рис. 8.3.2, Э). Каждый этап проектирования выполняют без использования информации о результатах предыдущих этапов. Считается, что это придает поиску решения непредубежденный характер. Такую стратегию часто используют при поиске новых идей, новаторских решений, когда разумно не пренебрегать ни одним из внесенных предложений до появления дополнительной информации.
Все рассмотренные стратегии проектирования могут быть реализованы на ЭВМ. Выбор конкретной стратегии определяется характером и условиями решения проектной задачи.
Завершая обсуждение стратегий проектирования, подчеркнем тот факт, что процесс проектирования сам по себе выступает в качестве технологии и поэтому обладает собственным вектором показателей качества. Этот вектор включает в себя показатели
качества объекта проектирования и единичные показатели, аналогичные рассмотренным нами ранее. Так, показатель быстродействия определяет сроки проектирования, показатель надежности — степень риска получить не самый лучший результат, показатель себестоимости — затраты живого и овеществленного труда на проектирование и т. д. Отсюда следует, что если определяющими факторами процесса являются сроки проектирования и затраты на его проведение, то целесообразно, по крайней мере на верхних уровнях проектирования, использовать линейные и разветвленные стратегии с максимально возможным выполнением параллельных этапов.
Из сказанного понятно, что стратегия проектирова-
ния определяет только общий план проектного движе-
ния. Для выявления методов и средств решения про-
ектных задач разработаны методики проектирования.
Прежде чем их обсуждать, заметим, что представление
процесса проектирования в виде некоторой технологии
1278
Новый справочник химика и технолога
дает возможность привлечения для его описания понятийного аппарата, в частности понятий «проектный модуль», «операция», «маршрут». Однако в практике проектирования эти термины четко не определены и не нашли широкого применения. Вместе с тем любая методика проектирования основана на последовательном выполнении законченных этапов, включающих определенный перечень упорядоченных действий и процедур. Анализ таких методик указывает на неоднозначность в выборе конкретных этапов, их содержании и последовательности выполнения. Применительно к технологическому проектированию рассмотрим следующую методику, включающую наиболее общие этапы проектных действий. Каждый этап этой методики имеет законченный характер и обладает собственной структурой и функцией.
Этап 1. Исходная постановка и формулирование проектной задачи
Как правило, задачу проектирования представляют в виде технического задания на проектирование, которое содержит следующие данные:
1.1. Информация об объекте производства и его свойствах.
1.2. Информация об объекте проектирования и его свойствах.
1.3. Информация о целях проектирования.
1.4. Информация об условиях и ограничениях, накладываемых на проектируемый объект и на процесс проектирования.
Постановка проектной задачи обычно включает в себя также формирование информационной среды проектирования: методики, руководящие материалы, справочники, каталоги, инструкции, базы данных.
Этап 2. Анализ проектной задачи. Конкретизация целей, условий, ограничений
2.1. На основе анализа объектов производства и проектирования уточняются, обосновываются и (или) принимаются условия и ограничения. Выясняются их полнота, однозначность и непротиворечивость.
2.2. Анализируются свойства объекта производства, выделяются те из них, которые усложняют поиск проектного решения, т. е. производят анализ технологичности этого объекта.
2.3. Конкретизируются цели, обосновываются их количественные и качественные характеристики, устанавливается возможность их достижения при выполнении условий и ограничений. Если цель можно формализовать, то получают ее математическое выражение через входные параметры, называемое целевой функцией.
2.4. Анализируя векторы X и У, пытаются сузить область возможных проектных решений, используя опытные данные или укрупненные количественные оценки .
Этап 3. Анализ проектной ситуации
3.1. Разбиение проблемы на уровни, этапы, частные задачи.
3.2. Моделирование проблемы, отдельных подпроблем и задач.
3.3. Обоснование путей решения проблемы и подпроблем, обоснование и выбор методов и средств проектирования.
Этап 4. Формирование множества вариантов решения (разработка альтернатив)
4.1. Выбор или синтез вариантов решения.
4.2. Оценка эффективности каждого варианта.
Этап 5. Выбор варианта, наилучшего по принятому критерию эффективности.
5.1. Выбор оптимального варианта: структурная оптимизация, параметрическая оптимизация.
Этап 6. Реализация решения
6.1. Проверка непротиворечивости результатов и соответствия их техническому заданию.
6.2. Оформление результатов в виде информационной модели технологии и представление ее в нужной форме.
6.3. Контроль, авторский надзор за реализацией.
Не претендуя на полноту отражения отдельных этапов в приведенной методике, сделаем некоторые выводы, важные для дальнейшего рассмотрения и вытекающие из ее содержания:
• любая проектная задача на каждом уровне проектирования может быть представлена последовательностью описанных выше этапов;
• каждый этап носит завершенный в логическом смысле характер, а его результаты необходимы для дальнейшего проектного движения;
• каждый этап проектирования можно представить последовательностью взаимосвязанных проектных действий и процедур;
• при выполнении отдельных этапов и проектных действий в них возможны итерационные петли, улучшающие результат.
Описанные этапы проектирования формируют его структуру в соответствии с выражением (8.3.1). Этапы 1 и 2, по сути, охватывают предпроектные действия, хотя их влияние на процесс проектирования трудно переоценить. Именно на этих этапах реализуется смысл известного высказывания, принадлежащего математику Хемингу: «Прежде чем решать задачу — подумай, что будешь делать с ее решением». Проектные действия, касающиеся анализа объекта проектирования, обсуждались выше. Рассмотрим подробнее четвертый этап представленной методики, предназначенный для выработки проектных вариантов-альтернатив.
8.3.2. Формирование множества вариантов проектных решений
Укажем на три основных направления решения про-
ектной задачи на данном этапе, в той или иной степени
используемые в отраслевых технологиях. Первое из них
*В машиностроении существенного сужения области возможных проектных решений достигают за счет отнесения проектируемой технологии к определенному типу производства.
Основы технологии
1279
предполагает применение существующих решений на всех уровнях и этапах проектирования. Сущность его заключается в том, что для данного объекта производства находят объект-аналог, для которого имеется готовое, как правило, апробированное проектное решение. Это решение корректируется с учетом незначительных отличий свойств объекта-оригинала и найденного аналога. Очевидно, технологический процесс, полученный в результате вышеописанных действий, не является оптимальным. Однако этот недостаток решения проблемы компенсируется выигрышем, получаемым за счет снижения затрат на проектирование и реализацию технологии. Такой подход целесообразен при проектировании технологий обработки достаточно простых объектов ограниченной номенклатуры.
Стремление расширить номенклатуру объектов, технология изготовления которых может быть получена в результате поиска готовых решений, привело к разработке концепции унифицированных ТП. В основе этого направления проектирования технологий лежит классификация объектов производства по признакам, определяющим структуру и содержание технологии. Так, например, объекты машиностроительного производства классифицируют по схеме: «класс—подкласс— группа—подгруппа—тип», основываясь на общности конструктивно-технологических признаков деталей машин. Для каждого типа объектов разрабатывается прогрессивный унифицированный ТП.
Методика проектирования выражается следующей схемой:
Объект производства
1
Классификационный тип
I
Унифицированный технологический процесс
I
Корректировка ТП
I
Разработка проектной документации
В данном случае корректировка ТП может оказаться достаточно существенной и затрагивать структуру (маршрут): исключаются отдельные операции, изменяется их состав, подлежат замене отдельные элементы средств технологического оснащения. Такая методика наиболее эффективна при использовании человеко-машинных проектирующих систем в режиме диалога. Заметим, что данный путь проектирования также не содержит в явном виде этапы синтеза новых решений и их оптимизации и базируется на развитой информационно-поисковой системе.
При отсутствии готовых проектных решений используется третье направление проектирования — синтез технологий. Как отмечалось ранее, это наименее формализованный элемент процесса проектирования, трудно поддающийся автоматизации с помощью ЭВМ.
Основная доля проектных работ выполняется проектировщиком и существенно зависит от его опыта, уровня теоретической подготовки, профессионального кругозора, владения эвристическими методиками и приемами.
Рассмотрим подробнее это направление проектирования технологических объектов, связанное с генерированием новых (не имеющих аналогов) технических решений и выделим присущие ему свойства, важные для дальнейшего обсуждения.
Примем, что новое техническое решение (НТР) должно обеспечивать заданное функциональное преобразование объекта производства безотносительно к эффективности этого преобразования, т. е. на данном этапе формируется множество принципиально возможных технологий, а задача выбора наилучшего в каком-то смысле варианта оставляется для рассмотрения на последующем этапе проектирования
НТР отражает достигнутый на момент проектирования уровень знаний в данной предметной области, в том числе фундаментальных знаний.
НТР наряду с эволюционным совершенствованием существующих технологий может привести к скачкообразному повышению уровня их качества. Например, применение излучения оптического квантового генератора резко продвинуло вперед медицинские технологии. Заметим, что рутинный выбор существующих технологий подобным свойством не обладает.
Поскольку технологические объекты обладают структурой (элементы, их свойства и отношения), процесс проектирования во многих случаях целесообразно разделять на два этапа:
• этап создания структуры технологического объекта, называемый структурным синтезом, структурным проектированием',
• нахождение параметров элементов структуры, т. е. внутренних параметров ТС, называемых параметрическим проектированием.
Так, при поиске технологического маршрута определяют перечень операций и правила их упорядочивания, отношения между ними, при проектировании операций находят перечень и взаимосвязи технологических модулей. Это задачи структурного проектирования. Определение параметров операций в первом случае и переходов во втором — задачи параметрического проектирования. Выделение перечисленных этапов упрощает синтез технологий и облегчает решение задач оптимизации проектных решений, рассматриваемых ниже.
Иерархичность технологических объектов обусловливает иерархичность задач синтеза. Отметим следующую закономерность: чем выше уровень проектирования, тем меньше вариантов решения и тем выше влияние качества решения на конечный результат.
Многомерность описания технологии выражается в
разработке методик и относительно независимом под-
ходе к решению перечисленных ниже задач синтеза:
• синтез методов обработки (МО) заключается
в нахождении такой совокупности процессов физической,
1280
Новый справочник химика и технолога
химической или иной природы, совместное протекание которых обеспечивает заданное изменение состояния объекта технологического воздействия. В основе МО лежит некоторый физико- или химико-технический эффект (ФТЭ или ХТЭ), описывающий результат протекания соответствующих процессов; понятия «метод обработки» и «физико-технический эффект» часто выступают в качестве синонимов, хотя первое из них, как правило, в большей степени объектно ориентировано. При разработке методов обработки пользуются банком ФТЭ и ХТЭ, реализуя тем самым процедуру выбора готового решения. Для синтеза МО предложены методики и алгоритмы, базирующиеся на комбинировании физически и химически совместимых между собой процессов;
• синтез способов обработки (СО), основанных на данном МО, заключается в нахождении такой совокупности приемов, правил, ограничений, которая делает возможным достижение технологического результата или повышает эффективность этого результата. Для идентификации СО как отдельного элемента соответствующего множества, часто используют понятие «отличительный признак», характеризующее индивидуальность структуры СО: перечень приемов, отношений, свойств. Синтез МО и СО тесно связан с патентноправовой защитой новых инженерных решений, являющейся важным аспектом технической политики государства. Изобретательская деятельность играла и играет важную роль в разработке эффективных методик и алгоритмов поиска НТР;
• синтез технологий',
• синтез средств технологического оснащения представляет собой, строго говоря, проектную задачу создания технических объектов (конструкций), которая несколько отличается от задач технологического проектирования. Однако исходные данные формирует технолог, он же использует результаты проектирования для решения разнообразных технологических задач.
Поиск НТР во всех рассмотренных задачах синтеза и их модификациях подчиняется следующей общей методике:
• выделяются элементы структуры объекта, их свойства и отношения;
• строится математическая модель объекта с использованием аппарата теории множеств или математической логики. Модель на ранних стадиях разработки может носить также описательный характер из-за трудностей формализации проектной задачи;
• формируется множество возможных вариантов объектов проектирования, т. е. таких сочетаний элементов, их свойств и отношений, которые обеспечивают функцию объекта и удовлетворяют наложенным условиям и ограничениям. Это достигается за счет перебора всех возможных сочетаний.
На первый взгляд описанная методика не вызывает особых затруднений, может быть формализована и выполнена с помощью ЭВМ. Однако при достаточно
большом числе элементов количество возможных комбинаций столь велико, что путь перебора окажется бесперспективным даже при использовании ЭВМ. Так, в микроэлектронных технологиях при производстве интегральных схем число возможных вариантов ТП имеет порядок 106. Кроме того, до сих пор не решены или решены не полностью задачи формализации комплекса условий, правил и ограничений, регламентирующих технологию. Из сказанного следует необходимость привлечения более рациональных стратегий поиска новых решений. Такие стратегии, как правило, основываются на эвристических приемах (ЭП).
Метод эвристических приемов заключается в обобщении и представлении пользователю в методически доступной форме опытных правил, рекомендаций по решению творческих инженерных задач и инструкций по их применению. Создано уже около десяти модификаций этого метода, разработан универсальный фонд ЭП, содержащий до 500 отдельных приемов. Этот фонд для удобства пользования разбивают на отдельные функционально связанные группы, содержащие кратко сформулированные приемы, требующие конкретизации для применения в задачах предметного проектирования и позволяющие находить новые эффективные решения. Чтобы подтвердить целесообразность применения метода эвристических приемов, обсудим основные приемы одной из групп указанного фонда, иллюстрируя обсуждение примерами из области технологического проектирования. Заметим попутно, что выполнение действий, обратных ЭП (инверсия ЭП), также является эвристическим приемом.
Эвристические приемы преобразования элементов объекта проектирования во времени
ЭП 1. Перенести выполнение действия на другое время. Выполнить требуемое действие до или после окончания работы.
В 8.2.4 обращалось внимание на тот факт, что ряд действий выносится в начало и конец работы, выполняемой на данном рабочем месте, а на их выполнение выделяется подготовительно-заключительное время. Это позволило упростить и уточнить нормирование ТО.
При использовании в ТП технологических операций с высоким уровнем надежности целесообразно перенести действия по контролю состояния объекта производства (контрольные операции) на завершающий этап технологии.
При формировании структуры операции следует оценить целесообразность выполнения отдельных ТМ на предыдущих или последующих операциях.
ЭП 2. Перейти от непрерывного процесса к периодическому или импульсному.
Этот прием — дискретизация объекта во времени — весьма распространен в технологических нововведениях хотя бы потому, что любая технология как совокупность последовательных действий дискретна по своей сути.
Основы технологии
1281
2.1. Часто эффективность технологии повышается за счет «разукрупнения» операций вплоть до разработки операций, состоящих из одного ТМ. Такой подход к проектированию называется принципом дифференциации операций и часто используется в технологиях массового производства (конвейерные, поточные формы организации производства).
2.2. Инверсия этого приема выражается в принципе концентрации операций. Очевидно, первый подход приводит к проектированию технологических процессов, состоящих из большого числа относительно простых по структуре ТО, а второй — к разработке малооперационных ТП со сложной многомодульной структурой отдельных ТО. Эффективность применения описанных принципов зависит от условий производства. Из сказанного следует, что рассмотренный ЭП целесообразно применять при синтезе структур технологических объектов.
2.3. Обсуждаемый ЭП использован во многих новых методах и способах обработки материалов. Так, на рис. 8.2.15 приведена схема процесса электрохимической обработки. Основное технологическое воздействие — растворение поверхности анода — сопровождается побочными явлениями: тепловыделением в слое электролита (джоулево тепло) и газонасыщением последнего за счет электродного газовыделения. Эти явления осложняют основной процесс. Действительно, за счет конвективного переноса газа и тепла формируется анизотропия электропроводности электролита вдоль гидравлического тракта, эпюр локальных плотностей тока становится неравномерным, образуется погрешность формы обработанной поверхности (в рассматриваемом случае — непрямолинейность). Как результат — снижение точности обработки изделия. Переход к импульсному электролизу позволил существенно повысить точность данного метода обработки деталей машин. Время паузы между импульсами тока выбирают таким, чтобы электропроводные свойства электролита в зазоре полностью восстановились, а длительность импульса была достаточно мала (10 4—10 3с), чтобы пренебречь конвективным сносом газа и тепла. Различные модификации импульсной электрохимической обработки приведены в специальной литературе.
ЭП 3. Перейти от стационарного во времени режима к изменяющемуся.
3.1. Возвращаясь к предыдущему примеру, заметим, что при постоянной скорости перемещения электрода-инструмента устанавливается некоторый стационарный межэлектродный зазор. При достаточно большой скорости электрохимического растворения его величина близка к 0,1 мм, что затрудняет эвакуацию продуктов электролиза и тепла из МЭП. Для разрешения этого противоречия от стационарного процесса отказались — ЭИ стали подвергать механическим колебаниям заданной частоты и амплитуды. Величина межэлектродного зазора изменялась во времени, и при больших ее значениях рабочая среда интенсивно прокачивалась, а продукты электролиза удалялись.
3.2. Данный ЭП отражает один из путей развития средств технологического оснащения: наблюдается тенденция перехода от оборудования с жестко зафиксированными параметрами режима к оборудованию с функционально изменяющимися по заданной программе параметрами и далее — к оборудованию с адаптивной системой изменения параметров.
ЭП 4. Исключить бесполезные (вредные) интервалы времени. Использовать паузу между импульсами (периодическими действиями) для осуществления другого действия.
4.1. Этот прием чрезвычайно эффективен при проектировании новых и совершенствовании существующих технологий. Он объединяет действия, направленные на сокращение длительности технологического цикла Тц. При проектировании ТО этот прием реализуется путем параллельного осуществления различных ТМ, совмещения во времени технологического воздействия на объект и вспомогательных действий.
4.2. Способ комбинированной электрохимической обработки предполагает импульсную обработку изделий в таких средах, которые химически активны по отношению к материалу изделия или продуктам электролиза. Таким образом, во время паузы между импульсами тока происходит химическое воздействие на обрабатываемую поверхность, что при соответствующем выборе длительностей импульса и паузы позволяет достичь лучшего технологического результата.
4.3. В ряде случаев пауза между технологическими воздействиями на объект используется для контроля его состояния, например при импульсной электрохимической обработке — для измерения тем или иным способом величины межэлектродного зазора.
ЭП 5. Осуществлять работу объекта непрерывно, без холостых ходов. Все элементы проектируемого объекта должны работать с полной нагрузкой.
5.1. При использовании в ТП отдельных операций, быстродействие которых существенно больше, чем остальных, соответствующее оборудование остается незагруженным, что снижает технико-экономические показатели технологии. Целесообразность использования данного ЭП для совершенствования технологии можно оценить по коэффициенту загрузки оборудования, равному отношению фактического времени работы данной единицы оборудования к плановому времени работы производственного подразделения. Усредняя коэффициенты загрузки по всем операциям, получают величину, характеризующую ТП в целом. Чем ближе ее значение к 1, тем совершеннее ТП.
ЭП 6. Изменить последовательность выполне-
ния действий.
6.1. Как будет показано далее, последовательность
операций регламентируется некоторыми правилами
упорядочивания. Поэтому применение этого приема
при проектировании вариантов структуры ТП ограни-
ченно. При проектировании операций этот прием поз-
1282
Новый справочник химика и технолога
воляет достигнуть цели и получить различные структуры операции.
Представленные данные указывают на то, что ЭП универсального фонда широко используются при проектировании новых технологических объектов, находя свое выражение в правилах, рекомендациях, алгоритмах. Безусловно, ЭП указывает лишь возможный путь приближения к цели — реальные результаты достигаются методом проб и ошибок при переборе различных ЭП. Однако количество ЭП ограниченно (для конкретных проектных задач используются фонды, состоящие из нескольких десятков ЭП), что существенно упрощает достижение результата по сравнению с простым перебором вариантов структур. Опытные проектировщики имеют индивидуальные наборы ЭП, отражающие предметную область проектирования, техническую оснащенность и психофизиологические качества проектировщика.
Наряду с универсальными ЭП при проектировании новых технологических объектов пользуются некоторыми общими правилами, учитывающими специфику технологического движения. Рассмотрим в связи с этим основные правила, регламентирующие проектирование маршрутной технологии.
Правило 1. На каждом последующем этапе технологии должно улучшаться хотя бы одно свойство объекта технологического воздействия без ухудшения остальных его свойств.
Используя выражение (8.1.5), описывающее технологическое движение путем последовательного приближения свойств объекта к заданным, представим это правило неравенством типа
i= 1,2, ..., m; j = 1,2, ..., п, где а' — компонент вектора Ау свойств объекта, сформированных на j-й операции; т — число таких компонентов; п — число операций ТП. Для определенности принята эквивалентность понятий «больше» и «лучше».
В различных технологиях это правило выполняется в явном виде или опосредствованно. Так, в формообразующих технологиях обработки твердых тел каждая последующая операция должна уточнять конфигурацию исходного тела, приближая ее к конечной, заданной. Поэтому в машиностроении часто выделяют этапы черновой, чистовой и финишной обработки, подчеркивая тем самым целевую направленность технологического воздействия. В технологиях, связанных с превращениями веществ, выделяют подготовительный этап, ответственный за придание объекту таких свойств, которые облегчают и повышают качество основного технологического воздействия. Например, измельчение многих видов сырья выполняют для увеличения его
поверхности перед проведением тепловых, диффузионных и прочих процессов.
Отметим тот факт, что встречаются и исключения из этого правила. Так, при изготовлении изделий сложной формы, например зубчатых колес, в машиностроении для упрочнения зубьев используют термическую обработку, которая приводит к ухудшению точности зубьев. Приходится вводить в ТП дополнительные операции, удорожая тем самым производство этих изделий. Это исключение подтверждает правило, нарушение которого снижает экономические показатели ТП.
Правило 2. Свойства объекта, достигнутые на предыдущей операции, должны обеспечить успешное проведение последующей.
Под успешным проведением операции здесь понимается достижение ее локальной цели при рациональных ресурсозатратах. Возвращаясь к выражению (8.1.5), отметим, что подобная запись функции ТП предполагает, что каждый технологический оператор способен выполнить требуемое преобразование свойств объекта обработки. Однако при проектировании технологии такую способность надо обеспечить. Если представить технологический оператор в виде черного ящика (рис. 8.1.6), то правило 2 можно сформулировать как требование соответствия (состыковки) выходов z-й операции входам (/ +1)-й. Из сказанного можно заключить, что для каждой операции существует множество операций, которые могут ей предшествовать, и другое множество — это операции, которые не могут предшествовать данной.
Правило 3. При наличии технологического риска (получение брака) дорогостоящие операции выполняют на конечном этапе ТП. Если при воздействии на объект образуются отходы, то большая часть из них отделяется на начальных этапах технологии.
Данное правило направлено на снижение ресурсозатрат и основано преимущественно на экономических соображениях. Так, при производстве виноградных вин на первых операциях отделяются отходы (гребни, косточки, кожица), а сусло подвергается дальнейшей обработке. Обогащение руды (отделение породы) является начальным этапом многих технологий. Этап черновой обработки при изготовлении деталей машин связан с удалением основной массы отходов.
Правило 4. На первом этапе технологии формируются те свойства объекта обработки, которые необходимы для получения остальных его свойств.
Так, отбор жидкой фазы является необходимым условием дальнейшего изменения ее свойств, придание металлу некоторой исходной формы нужно для дальнейшей обработки его на металлорежущих станках, получение тестовой массы — начальный этап технологий хлебопекарного производства. Это правило является одним из основных при проектировании процессов металле-
Основы технологии
1283
обработки. Оно выражается в том, что вначале обрабатывается комплекс конструктивных элементов (базы), необходимых для ориентации и фиксирования обрабатываемого объекта в координатной системе станка на последующих операциях.
Как видно, сформулированные правила описывают некоторые условия упорядочивания операций в маршруте (порядок следования и условия согласования). С другой стороны, они выступают в роли ограничений и позволяют уменьшить число возможных вариантов структур, полученных простым перебором операций. Используя эти правила, можно синтезировать маршрут обработки по тому или иному алгоритму. Приведем один из наиболее простых алгоритмов синтезирования маршрутов.
7. Формулировка задачи проектирования до-
создается система условий и ограничений
2. Из множества технологических операций, характеризуемых индивидуальными входами и выходами, выбирают такие, для которых выполняется условие:
ajk=a'k.
Получается множество однооперационных маршрутов.
3. Из множества технологических операций формируют два подмножества:
А) = А)} (подмножество первых операций),
А'к = А*к (подмножество конечных операций).
Выбирают такие пары элементов этих подмножеств, для которых выполняется условие совместимости (согласования):
А}к = А^ i =1, ..., т; j =1, ..., к.
Образуется множество двухоперационных маршрутов.
4. Формируют множество вторых операций:
А^=А),, А'к - А^: t =],..., тк.
Образуется множество трехоперационных маршрутов.
5. Продолжая данную процедуру, получают все более длинные операционные цепочки.
6. На каждом этапе выделяют и оставляют для дальнейшего рассмотрения допустимые варианты маршрутов, проверяя соответствие каждого из возможных вариантов, удовлетворяющих правилу совместимости, всей совокупности условий и ограничений.
К их числу относится вытекающее из существа задачи ограничение числа операций в маршруте, предпочтения или запреты на использование отдельных операций и т. д. В результате формируется множество допустимых вариантов маршрута.
7. Производят оценку качества решения, т. е. каждому варианту маршрута ставят в соответствие некоторую величину, определяющую его эффективность.
Для такой оценки обычно используют ВПК технологии, описанный в 8.2.2, или его отдельные компоненты. Количество компонентов ВПК можно в данном случае сократить, исключив показатели качества объекта обработки, одинаковые (в допустимых пределах) для всех вариантов маршрута в связи с выполнением функционального условия 5.
8. Нахождение наилучшего варианта маршрута (структурная оптимизация) из множества допустимых вариантов.
Из описанного алгоритма следует, что синтез маршрутов в данном случае основан на использовании банка технологических операций. Такие банки носят предметно ориентированный характер и создаются в отраслевых технологиях. Каждая операция такого банка имеет свой код или идентификационный номер, набор функциональных и оценочных характеристик. Отметим попутно, что в реальных технологиях входы и выходы операций задаются в виде диапазонов изменения соответствующих параметров. Это создает неопределенность в оценке эффективности маршрута и придает приближенный характер такой оценке. Лишь после уточнения параметров каждой операции можно будет обоснованно судить об эффективности варианта маршрута.
На качество проектного решения, полученного с помощью описанного алгоритма, значительно влияет степень полноты используемого банка операций. Действительно, отсутствие в таком банке прогрессивных операций, основанных на современных научных достижениях, ставит вопрос о правомерности выбора наилучшего варианта в процедуре 8 вышеприведенного алгоритма. Кроме того, может оказаться, что информационные ресурсы банка вообще не позволяют получить приемлемый маршрут. Это выражается в невыполнимости условия согласования операций (разрыв операционной цепочки) или неэффективности маршрута из-за наличия в нем неэффективных операций. В том и другом случае необходим синтез новых операций.
Синтез выполняется по схеме:
«процесс метод способ —> операция —> модуль»
или по фрагменту этой схемы.
Такая ситуация сложилась в машиностроении в 1940-1950-х гг. Суть проблемы заключалась в том, что существовавшие операции механообработки, основанные на различных способах резания металлов, не обеспечивали формирование приемлемых маршрутов обработки изделий из вновь появившихся конструкционных материалов с высокими механическими свойствами. Потребовалась разработка принципиально новых операций, эффективность которых не зависела бы от механических свойств обрабатываемого материала. Такие операции были созданы на основе электрохимического, электроэрозионного, ультразвукового, а позднее лазерного и других методов обработки. Рис. 8.1.3 иллюстрирует логику разработки операций электроэрозионной обработки.
1284
Новый справочник химика и технолога
Заметим, что появление новых методов и способов обработки и соответствующее расширение банка за счет включения в него прогрессивных высокоэффективных операций вызывает необходимость периодической ревизии и коррекции существующих технологий, в том числе унифицированных.
Если маршрут сформирован, приступают к технологическому проектированию на уровне операций. В первую очередь формируют структуру отдельных операций, т. е. выбирают и упорядочивают соответствующие модули.
Казалось бы, использование предложенного выше алгоритма решает задачу синтеза операции. Это действительно так в том случае, когда отдельные модули выполняются последовательно. Параллельное выполнение модулей возможно, если результаты и условия их выполнения не противоречат друг другу (условие непротиворечивости или независимости модулей). Такая ситуация возможна, поскольку каждый модуль позволяет получить единичный идентифицируемый технологический результат, т. е. связан с получением какого-то определенного параметра состояния объекта производства. Тогда множество модулей, принадлежащих данной операции, можно разбить на подмножества, относящиеся к формированию отдельных параметров состояния и соответственно поименованные. Для элементов каждого подмножества справедливо условие согласования входов и выходов, а элементы-модули, принадлежащие разным подмножествам, относительно независимы и могут выполняться параллельно с учетом имеющихся ограничений, в первую очередь связанных с конструктивными особенностями оборудования.
Очевидно, такой подход усложнит проектирование, увеличит число возможных вариантов структуры операции, но обеспечит условия для выбора действительно лучшей структуры для данного производства.
Далее для каждого модуля тем или иным способом подбирают параметры режима, средства технологического оснащения или их элементы и рассчитывают показатели качества операции.
Таким образом, в процессе технологического проектирования формируют варианты технологических решений на уровне принципиальных схем, маршрутов, операций. Следующим важным шагом, завершающим творческую сторону процесса проектирования, является принятие технического решения — выбор наилучшего варианта.
8.3.3. Выбор наилучшего проектного решения
В основе этого этапа проектирования лежат идеи и методы исследования операций — раздела прикладной математики, охватывающего принципы построения и анализа моделей операций, а также приемы исследования таких моделей в условиях неопределенностей. Под операцией в этой научной дисциплине понимают совокупность взаимосвязанных действий, направленных на достижение определенной цели. Нетрудно видеть, что любая технология может служить объектом исследования операций, чем и объясняется весьма широкий круг решаемых этой дисциплиной прикладных
задач. Выбор некоторой операции рассматривается здесь как процесс принятия решения, а поиск наилучшего решения в условиях неопределенности является основной задачей исследования операций. Прежде чем перейти к интересующей нас проблеме выбора наилучшего варианта технологии, обсудим некоторые общие положения исследования операций, на которых будем основывать дальнейшие рассуждения.
Методологический подход к проблеме принятия решения заключается в комбинировании формализованных и неформализованных процедур: формальными приемами получают информацию, позволяющую некоторому лицу (или коллективному органу) принимать обоснованное решение. Таким образом, постулируется принципиальная неформализуемость некоторых проектных действий, выполняемых на данном этапе , и вводится в рассмотрение субъективный фактор в виде лица, принимающего решение (ЛПР), и лиц, ему помогающих (эксперты, консультанты). Назначение последних — структуризация тех или иных аспектов проектного решения, создание качественных и количественных оценок, предпочтений в условиях недостаточной исходной информации. Экспертным методом получают прогнозы развития различных ситуаций, оценивают перспективность новых образцов техники и новых технологий.
Уточним понятие неопределенности при принятии решения. Заметим, что в задачах технологического проектирования встречаются неопределенности двух типов: неопределенности целей и условий.
Пусть сформировано множество вариантов решения Е и каждому варианту Е(, принадлежащему Е, соответствует некоторый результат et. Этот результат характеризует полезность, эффективность решения. Если существует функциональная зависимость вида е, = f (х), где х — вектор, определяющий способ действий, идентифицирующий решение, то функция ft (х) называется функцией полезности или целевой функцией.
Неопределенность условий заставляет принимать решения, когда целевые функции содержат неопределенный параметр а, т. е. они заданы не совсем точно. В зависимости от конкретных значений этого параметра для каждого варианта решения можно получить соответствующие результаты etJ = f (х, ау), представленные в виде матрицы решения:
а\ а2 а3 .. а} ап
£i бц 6 12 613 . еХ] .. • £ 1и
б21 6 22 6 23 • •• 6 2п
Ет 6W1 6 m2 6 m3 6 mj & mnj
Неопределенность условий связана либо со случайным характером тех или иных событий, характеризую-
*По мнению академика Н. Моисеева, процесс проектиро-
вания сложных технических систем никогда не сможет быть
до конца формализован.
Основы технологии
1285
щих проведение операций, и тогда а можно интерпретировать как вероятность наступления этих событий. Часто трудно предугадать характер влияния внешних условий на конечный результат и приходится просчитывать результаты решений при нескольких фиксированных значениях этих условий.
Неопределенность целей в технологическом проектировании связана с неоднозначностью результата решения. Это выражается в том, что каждому решению ставится в соответствие не один et, а несколько результатов etk, влияющих на выбор решения и выражающих оценку локальных целей Zk {к = 1,2, ..., К). Выше было показано, что эффективность технологии оценивается набором единичных показателей, формирующих соответствующий вектор показателей качества. Естественно представить результат проектирования таким вектором.
В общем случае матрица решений имеет вид ||eyJt||, где elJk — эффективность z-ro варианта при условиях а, применительно к цели Zk.
Неопределенность целей описанного типа существенно усложняет выбор наилучшего решения и приводит к целому классу задач многокритериальной оценки альтернатив. Подробный анализ методов решения задач данного класса приводится в специальной литературе. Наиболее употребительные способы решения подобных задач будут рассмотрены ниже.
Для выбора решения необходимо сформулировать некоторое правило предпочтения. В простейшем случае однозначного результата правило предпочтения выражается чаще всего в зависимости от того, соответствует ли большая оценка более эффективному результату (производительность, надежность) или наоборот (ресурсозатраты, себестоимость, трудоемкость) в виде
войтах, е, или е0= min, е,; z = 1,2,..., т. (8.3.2)
Если результат неоднозначен, то используют более сложные правила предпочтения, позволяющие свести матрицу решений к одному столбцу ||е,г||, т. е. каждому варианту решения поставить в соответствие некоторый единственный результат е1Г, получаемый по этому правилу. Конкретный вид этого правила (часто называемого оценочной функцией) зависит от позиции ЛПР. Применительно к представленной выше матрице решений можно указать следующие наиболее употребительные правила предпочтения.
Оптимистическая позиция’.
е0 = max, eir = max, (max, e,7). (8.3.3)
Нейтральная позиция:
(1 "
~Xeи
(8.3.4)
Пессимистическая позиция:
е0 = max, etr = max, (min7 e,7). (8.3.5)
Относительно пессимистическая позиция:
e0 = min, etr = min, max, (max, e,7 - e,,), (8.3.6) z=l,..., w; y = l,..., n.
Представленные правила хорошо иллюстрируют роль ЛПР в процессе принятия решения и возможность получения различных решений в зависимости от занятой при оценке альтернатив позиции. В связи с этим возникает вопрос о риске получить не самый лучший результат. Проблема риска при принятии решений связана также с тем, что все или некоторые параметры, определяющие данную технологию, а также показатели эффективности могут быть недетерминированными, случайными величинами. Так, выше обсуждались такие показатели эффективности, как вероятность безотказной работы, вероятность травматизма и др. При обработке партии деталей машин показатели точности формообразования имеют статистический характер. Таким образом, выбор варианта решения так или иначе связан с риском, отражающим вероятность наступления некоторого неблагоприятного события и оценку его последствий.
Величину риска R можно количественно определить как произведение величины П, оценивающей последствия события, на вероятность р наступления этого события:
R = П/z. (8.3.7)
Последствия нежелательного события или состояния при принятии технических решений выражаются в виде материальных, ценностных потерь или как ущерб здоровью или угроза жизни людей. Обычно материальные потери можно количественно оценить в денежном выражении; оценка потерь второго вида гребует тщательного анализа и привлечения статистических справочных материалов. В качестве примера в табл. 8.3.1 приведены статистические данные, отражающие степень опасности для жизни людей, живущих в различных условиях и занимающихся разными видами деятельности.
Итак, можно сказать, что риск присутствует при принятии любых технических решений и в ряде случаев может выступать как один из основных критериев выбора решения. Необходимость принимать решения в условиях имеющего место и оправданного риска привела к разработке приемов формального описания и оценки риска.
Ранее отмечалось, что наличие векторного показателя эффективности технологии относит задачу выбора технологического проектного решения к классу задач многокритериальной оценки альтернатив. Рассмотрим в связи с этим некоторые наиболее употребительные способы решения таких задач.
1286
Новый справочник химика и технолога
Таблица 8.3.1
Вероятность летального исхода при различных видах деятельности
Условия или вид деятельности Вероятность, 10’7 чел./ год
Аварии автомашин 2700
Пожары и взрывы 400
Водоемы 280
Работа с механизмами 100
Воздушное сообщение 75
Работа с электрическими устройствами 51
Радиоактивное излучение 0,05
1. Прямой метод основан на скалярной свертке векторного показателя эффективности, т. е. на задании функциональной зависимости между некоторым обобщенным критерием эффективности и единичными показателями с учетом важности (весомости) этих показателей. Такая зависимость директивно задается ЛПР или экспертом без какого-либо теоретического обоснования и отражает их прошлый опыт в принятии подобных решений. Отсюда следует возможность разработки большого числа способов подобным образом. Действительно, для этого необходимо однозначно определить вид описанной выше функциональной зависимости, ее параметры и вероятностные оценки ее составляющих при принятии решения в условиях неопределенности. При технологическом проектировании используют следующие разновидности обсуждаемого метода:
Аддитивная свертка векторного показателя основана на замене К единичных показателей одним критерием вида
<=Ew Хс7=1’ (8-3-8)
j 1 /=1
где с} — весомость /-го показателя эффективности. Ранжирование показателей по значимости и назначение весовых коэффициентов производят эксперты.
Выполняя скалярную свертку, необходимо помнить о том, что эти показатели могут оцениваться величинами разного порядка и иметь различную размерность. Это затруднение устраняют путем использования в формуле (8.2.27) относительных частных показателей (по отношению к базовым значениям, устанавливаемым для каждого показателя экспертами).
Выделение главного критерия является простейшим приемом скалярной свертки для преодоления неопределенности целей. Он заключается в ранжировании К единичных показателей по значимости и выделении главного показателя eg, который вносит наибольший вклад в достижение цели. Остальные показатели представляют в виде ограничений. Задача выбора формулируется, например, так:
e0=max, е,*; е„>[е,];
i=l,...,m; j=\,...,n\ j*g,
(8.3.9)
где [e7] — допустимые значения /-го показателя эффективности.
Введение нормативов и оценка отклонений от них. Пусть имеется система нормативных значений показателей е”, заданных ЛПР. Свертку производят по формуле
(8.3.10)
Таким образом, получают скалярный критерий для каждого варианта решения. Дальнейший выбор наилучшего варианта по этому критерию не представляет затруднений. Несмотря на внешнюю простоту, все модификации прямого метода оценки альтернатив страдают общими недостатками, вытекающими из доминирующего характера субъективного фактора.
2. Метод порогов несравнимости основан на идее сужения множества альтернатив и базируется на отношениях предпочтения, эквивалентности и несравнимости при оценке альтернатив. Все показатели эффективности разбивают на группы. Внутри группы ухудшение одного показателя можно компенсировать улучшением другого. Но показатели, относящиеся к разным группам, сравнению не подлежат.
Сужение множества возможных решений осуществляется попарным сравнением альтернатив. Если альтернатива А по каждой группе показателей имеет оценки не хуже, чем В, а хотя бы по одной группе эти оценки лучше, то говорят, что А предпочтительнее В или А доминирует над В. Если оценки этих альтернатив по всем группам показателей совпадают, то альтернативы эквивалентны. Если же А превосходит В по одним группам критериев, но уступает В по другим, то альтернативы признаются несравнимыми. Используя условие предпочтения, можно выделить в множестве Е всех альтернатив подмножество Яц, состоящее из эквивалентных и несравнимых альтернатив, называемое ядром множества Е, или множеством Парето (по имени итальянского экономиста, предложившего в 1904 г. принцип отбора решений, описанный выше).
Принцип Парето не выделяет единственное решение: он позволяет лишь сузить круг альтернатив, из которых надлежит сделать выбор. Однако его использование дает возможность в ряде случаев многократно облегчить задачу. Известен пример использования описанной процедуры для выбора рациональной схемы угольных шахт. Несколько тысяч альтернатив оценивались по 25 показателям эффективности. В итоге всего за три итерации для окончательного выбора осталось лишь полтора десятка решений.
Для иллюстрации принципа Парето дадим его графи-
ческое представление. Пусть для каждого из допустимых
Основы технологии
1287
решений некоторого множества Е известны значения двух показателей эффективности ех и е2. Это ограничение не нарушает общности дальнейших рассуждений, но делает их наглядными. Введем прямоугольную систему координат, откладывая по оси абсцисс значения e/b а по оси ординат — значения е,2. В этой системе координат каждому варианту решения соответствует некоторая точка, а всему множеству Е — область с границей d (рис. 8.3.3). По Парето, вариант Е, лучше, чем £), если хотя бы одно из неравенств > е71 и е/2 > е/2 строгое.
Выясним геометрический смысл множества Парето. Для этого возьмем произвольную точку Ро € Е и проведем через нее прямые, параллельные осям. Видно, что все точки, лежащие в первом квадранте, лучше, чем Pq, а в гретьем — хуже по введенному выше отношению. Варианты, соответствующие квадрантам III и IV, несравнимы. Переместившись произвольным образом из Pq в Рх, получим лучшее решение. Продолжая такое движение, сформируем траекторию, проходящую через точки Ро, Рх, Р2, ..., Pd, каждая из которых находится в первом квадранте по отношению к предыдущей. Ясно, что такое движение можно продолжать до тех пор, пока для точки Pd соответствующий квадрант не окажется пустым. Это означает, что получена точка множества Парето. Очевидно, такая точка должна лежать на границе области Е. Сравнивая траектории 1 и 2, видим, что точки Парето располагаются на участке МХМ2 кривой d границы области Е (если неравенства, определяющие отношение предпочтения, заменить на противоположные, то множеству Парето соответствовал бы участок Мх М2 ). Произвольный выбор точки Ро и тра-ектории движения позволяет получить лишь одну точку ядра. Однако существуют способы построения множества Парето наиболее рациональным образом.
Как уже говорилось, дальнейшее сужение множества Парето в рамках сформулированных выше отношений частичного упорядочивания невозможно. Поэтому рассмотренный принцип используют для предварительного отбора вариантов. Следующий шаг должен основываться на некоторой новой гипотезе предпочтения, устраняющей неопределенность выбора, например на принятии обобщенного критерия эффективности.
3. Метод компенсаций основан на следующем компромиссе: допуская ухудшение решения по одному показателю, стремятся компенсировать потерю изменением другого. Так, например, показатели ех, е2, ..., ек ранжируют по значимости и находят вариант решения, соответствующий экстремальному значению показателя ех при произвольных значениях других показателей. Если такое решение найдено (ех = е*), то ищут решение, доставляющее экстремум показателю е2 при произвольных значениях е3, е4, ..., ек и ех = е* - Лех, где Дв1 — допустимое ухудшение первого показателя.
Далее ситуация повторяется (назначая Ле2, необходимо помнить об ограничении Ав]). Продолжая такие шаги, получают компромиссный вариант, выявляя по
путно взаимосвязи показателей и иную информацию, необходимую ЛПР.
Обсудим применение описанных выше идей в технологическом проектировании. Сначала уточним представления о показателях эффективности технологий, часть из которых уже рассматривалась в 8.2. Вектор показателей эффективности технологии е = (ех, е2, ... , ек) представим в виде суммы двух векторов:
е = еА + ев, еА = (еь е2,..., е,) и ев = (е/. ь ..., ек}, где ел — вектор собственно технологических показателей, ев — вектор показателей качества объекта технологического воздействия. Такое представление удобно с той точки зрения, что позволяет сократить размерность вектора е при сравнении вариантов, обеспечивающих требуемый уровень качества производимой продукции.
Подчеркнем тот факт, что единичные показатели е„ описывающие технологию, как правило, сами являются векторами, т. е. включают в себя набор однородных частных показателей, характеризующих один и тот же качественный признак. Однако в большинстве случаев такие частные показатели связаны между собой некоторыми отношениями, и для оценки признака достаточно привести один или несколько наиболее значимых из них. Это позволяет сократить размерность вектора е, и облегчает задачу выбора решения. Рассмотрим это важное положение на примере из области технологии машиностроения.
Точность изготовления детали машины оценивается набором частных показателей: точность размера тр, точность взаимного расположения поверхностей тп, точность формы m§, волнистость тв, шероховатость поверхности тш, описывающих соответствие конфигурации изделия некоторому эталону. Таким образом, показатель точности т представляется набором частных показателей т = (тр, т§, тв, тш).
1288
Новый справочник химика и технолога
Между перечисленными частными показателями существуют сложные взаимосвязи, которые обычно трудно выявить и учесть. Тем не менее во многих практически важных случаях можно ограничиться одним показателем (обычно это показатель точности размера), полагая, что выполнение условия соответствия по этому показателю автоматически обеспечит соответствие по всем другим. Основанием для этого служит правило вхождения 8р > 8П > Зф > 8В > 8[Ц, описывающее взаимосвязь допустимых отклонений (допусков) по соответствующим частным показателям. В связи с этим в характеристике операции обычно указывают значение обеспечиваемого ею квалитета точности, однозначно связанного с допуском на размер и характеризующего функциональные возможности операции.
Показатели эффективности могут находиться друг с другом в следующих отношениях:
• показатели взаимно нейтральны, т. е. изменение одного из них никак не отражается на величине другого. Очевидно, по таким показателям можно производить независимое сравнение или описание технологических объектов;
• показатели кооперируются. В этом случае удается осуществить выбор решения по одному показателю, а остальные улучшаются автоматически. Такая ситуация может быть в описанном выше примере с векторным показателем точности;
• показатели конкурируют, т. е. улучшение одного из них может достигаться лишь за счет ухудшения другого. Так, для ряда технологий повышение производительности (быстродействия) сопровождается снижением качества продукции, возрастанием энергоемкости. Повышение показателя надежности сопряжено, как правило, с увеличением затратных показателей и т. д.
Вектор показателей эффективности технологий содержит обычно компоненты со связями всех перечисленных типов. Рассмотрение нейтральных и кооперативных показателей не представляет сложности. Поэтому задачу принятия решения сводят к оценке вектора конкурирующих показателей эффективности.
Уточним перечень наиболее распространенных и применяемых в различных отраслевых технологиях показателей эффективности'.
et — показатель быстродействия, используется при оценке качества любых технологий;
е2 — показатель надежности. Это векторный показатель, содержащий достаточно широкую номенклатуру частных показателей, которые в большинстве своем носят вероятностный характер. В конкретных технологиях используют наиболее подходящие частные показатели;
е3 — показатель материалоемкости, характеризует выход готовой продукции по отношению к сырью или относительное удельное количество отходов при реализации данной технологии. Общее правило гласит, что чем меньше отходов, тем совершеннее технология;
е4 — показатель энергопотребления, характеризует удельные энергозатраты на производство единицы про
дукции. Этот показатель следует рассматривать не только с точки зрения стоимости энергозатрат, но и с учетом фактора дефицитности и возможных ограничений энергопотребления;
е5 — показатель затрат информационных ресурсов, позволяет оценить количество информации, требуемое на производство единицы продукции. В существующих обрабатывающих технологиях оценки такого рода производятся редко. Однако значимость этого показателя постоянно повышается в связи с возрастанием уровня технического интеллекта производственных систем, усилением роли информационных процессов в них;
е6 — показатель хронопотребления, отражает длительность технологического движения и может оцениваться временем технологического цикла;
е-] — показатель удельных трудозатрат, характеризует участие человека в технологическом процессе. В качестве такого показателя используют трудоемкость единицы продукции;
е8 — показатель суммарных удельных ресурсозатрат. В качестве такового используют себестоимость единицы продукции. По своей сути этот показатель является комплексным и основан на применении линейной свертки к набору ресурсозатратных показателей, выраженных в универсальной денежной форме. Заметим, что не всегда комплексный показатель и его компоненты кооперируются. Так, возрастание доли овеществленного труда в стоимостном выражении в балансе себестоимости может привести к снижению величины последней за счет уменьшения других составляющих (это одна из причин, стимулирующих внедрение прогрессивного оборудования).
Кроме того, показатели удельных ресурсозатрат, наряду с оценкой экономической стороны технологии, отражают также присущую каждому из них специфическую сторону. Это показано выше на примере показателя е4. Поэтому себестоимость и удельные ресурсозатраты часто выступают как конкурирующие показатели;
е9 — природоохранный показатель, отражает характер и степень прямого или косвенного воздействия технологии на среду обитания человека. Это векторный показатель, представляемый одним-тремя частными показателями в конкретных технологиях.
В связи с принятием в 1995 г. в России Федерального закона «Об экологической экспертизе», декларирующего принцип: «...исходить из потенциальной опасности любой намечаемой хозяйственной или иной деятельности», проектирование технологий должно обязательно сопровождаться экологическим прогнозированием и анализом последствий их реализации. Часто приходится вместе с основной технологией проектировать специальные природозащитные технологии;
е)0 — показатель безопасности жизнедеятельности,
отражает возможное влияние технологии или сопутст-
вующих факторов на жизнь, здоровье, работоспособ-
ность человека — участника технологической деятель-
ности. При проектировании технологии необходимо
Основы технологии
1289
выявить и оценить опасные и вредные производственные факторы, учитывать эти оценки при выборе лучшего решения;
£п — эргономический показатель, характеризует условия, ограничения, требования к человеку-оператору. Целесообразность выделения такого показателя эффективности технологий можно пояснить следующим примером. Известно, что ряд технологий требует профессионального отбора операторов (ряд военных специальностей, испытание новой техники, творческая деятельность, высокоточная сборка миниатюрных изделий). Появляется сопутствующая задача тестирования и отбора обслуживающего персонала, требующая для своего решения соответствующих затрат. Очевидно, из двух эквивалентных по прочим показателям технологий предпочтительнее та, которая не требует дополнительных затрат. Обсуждаемый показатель по своей природе векторный и может содержать гигиенические, антропометрические, физиологические, психологические частные показатели.
Завершая формирование вектора £Л, сделаем несколько общих замечаний. Во-первых, отметим, что приведенный перечень не является завершенным и может расширяться в случае необходимости. Во-вторых, при проектировании конкретных технологий каждый значимый показатель уточняют и вводят шкалу его оценки. Наконец, подчеркнем социальную направленность показателей e-j, £8, £9, непосредственно отражающих взаимосвязи в системе «человек— машина—окружающая среда». Внимание, которое обращается на эту группу показателей при технологическом проектировании, определяет, по сути, уровень цивилизованности общества. Замечено, что чем выше интеллектуальный потенциал проектировщиков, тем в большей степени и на более ранних этапах проектирования прорабатываются вопросы, связанные с обеспечением требуемых значений соответствующих показателей.
Формирование вектора ев не может носить безотносительный характер в связи с чрезвычайно широкой номенклатурой объектов технологического проектирования. Поэтому в качестве примера рассмотрим соответствующий вектор применительно к технологии машиностроения. В 8.2.1.3 при описании функции этой технологии выделены три группы свойств изделия, подвергаемые целенаправленному изменению с последующей оценкой степени соответствия заданным эталонным значениям. Такие группы свойств естественным образом формируют вектор показателей качества изделия:
^12 — показатель точности изготовления. Векторный характер этого показателя и его компоненты обсуждались выше;
£]3 — показатель качества поверхностного слоя изделия, является вектором и включает такие частные показатели качества, как параметры микрогеометрии поверхности, параметры, характеризующие механиче
ские свойства тонкого поверхностного слоя и структурно-фазовый состав этого слоя;
£и -— показатель качества объемных свойств изделия (твердость, вязкость, пористость и др).
Подобным образом для любой технологии формируется вектор показателей эффективности, отражающий ее специфику и необходимый для выбора наилучшего варианта технологического решения. При формировании этого вектора придерживаются следующего правила: число принятых единичных показателей должно быть необходимым и достаточным для всесторонней оценки уровня качества технологии — увеличение их числа усложняет и удорожает процедуру выбора наилучшего решения.
Нахождение вектора показателей эффективности технологии связано с построением целевых функций и выполняется в два этапа. На первом этапе рассчитывают, принимают по нормативам или оценивают экспертным методом значения соответствующих показателей на каждой операции. Затем определяют показатель е, для всей технологии с учетом ее пооперационной структуры.
Ресурсозатратные показатели, в том числе себестоимость, суммируют по числу операций с учетом возможных межоперационных потерь:
е = k^et, I = 1,2, ..., b,
где к — коэффициент, учитывающий межоперационные затраты ресурсов; b — общее число операций в ТП.
Показатель быстродействия определяют по лимитирующей операции:
£i = minz (£/).
Вероятностные показатели рассчитывают с учетом последовательности случайных событий. Например, при последовательном выполнении операций вероятность безотказной работы P(t) технологии и вероятность отказа Q(t) связаны со значениями этих величин для отдельных операций соотношениями вида:
Р(О = П/’(О/ и 0(/) = 1-Р(/).
/
Вредные выбросы в окружающую среду генерируются в большинстве случаев на какой-то конкретной операции. Поэтому, если не происходит их накопление по операциям, принимают:
е9 по выбросу G = max/ (e9z по выбросу G).
Для оценки эргономических показателей технологии
используются, как правило, экспертные методы.
Показатели качества продукции £в обеспечиваются
данной технологией и включаются в техническое зада-
ние на проектирование. В тех случаях, когда целью
проектирования является улучшение такого показателя,
1290
Новый справочник химика и технолога
строят целевую функцию, анализируют ее и находят пути решения задачи. Такая ситуация часто складывается в машиностроении при решении задачи повышения точности изготовления деталей машин.
Применение вероятностных показателей, экспертных методов оценки и приближенный характер расчетов показателей эффективности технологий приводят, как уже говорилось, к неопределенности при выборе решения. Рассмотрим этот вопрос несколько подробнее. Пусть сформировано множество X допустимых вариантов маршрута при структурном проектировании. Неопределенность задачи выбора можно представить как не совсем точное задание целевой функции: она содержит неопределенный параметр а. Следовательно, единичные показатели качества будут зависеть от этого параметра. Если правило предпочтения имеет, например, вид: е, а) —> max, j = 1,2, ..., К, то, решая задачу выбора, мы сможем определить наилучший маршрут х G X лишь как функцию параметра а, т. е. х = х (а). Степень уверенности в том, что найдено действительно лучшее решение, зависит от позиции ЛПР при выборе правила предпочтения.
Используем эти рассуждения для уточнения взаимосвязи между структурным и параметрическим проектированием. Поясним возникающие при этом затруднения следующим примером. Пусть в результате структурного проектирования выбран некоторый маршрут х . Входы и выходы составляющих его операций изменяются в зависимости от параметров режима. Это означает, что выбранный маршрут является функцией параметров отдельных операций. Есть ли гарантия того, что соотношение х > где Х] — некоторый другой маршрут из того же множества, не изменится на противоположное при соответствующем выборе параметров операций, т. е. при устранении неопределенности данного вида?
Выход из этого затруднения находят различными способами. Можно на стадии структурного проектирования оставить для дальнейшего рассмотрения несколько сопоставимых маршрутов (в этом случае говорят об отсутствии доминирующего предпочтения), провести параметрическое проектирование и окончательно сравнить детально проработанные варианты. Это, безусловно, трудоемкий путь, однако современные средства автоматизированного проектирования делают его возможным и в ряде случаев целесообразным. Можно также установить некоторые средние значения входов и выходов отдельных операций, что соответствует позиции нейтралитета при задании оценочной функции по формуле (8.3.4). Поясним последний прием примером из области технологии машиностроения.
Для каждого способа обработки деталей машин и соответствующей ему операции можно указать достижимую точность обработки. Однако экспериментально доказано, что использование достижимой точности экономически невыгодно (между себестоимостью и погрешностью обработки существует ги
перболическая зависимость). Поэтому для характеристики операций приводят значения экономической точности обработки, под которой понимают точность, обеспечиваемую в нормальных условиях работы, при использовании исправного оборудования, инструментов стандартного качества, персонала средней квалификации и при затрате времени и средств, не более, чем для других, сопоставимых по результату, способов обработки.
Выше рассматривались проектные действия, связанные с выбором лучшего варианта технологического решения. В литературе подобные действия часто сводят к задачам оптимизации: структурной и параметрической. Необходимо помнить, что оптимизационные задачи связаны с поиском экстремумов функции, и в этом смысле оптимальное решение является наилучшим. Обратное утверждение неверно.
В заключение обратим внимание на проектные задачи, направленные на улучшение (модернизацию) технологий. Эти задачи связаны с постоянным обновлением методов и способов технологического воздействия, средств технологического оснащения. Для них характерны наличие исходного (базового) варианта ТП и замена лишь некоторых элементов его структуры. Очевидно, оценка эффективности модернизации связана со сравнением некоторого базового и нескольких модернизированных вариантов технологии по изменяемым показателям эффективности. Обычно используют скалярную свертку показателей по главному критерию, получившую развитие в методе «затраты — эффективность». Чаще всего этим методом решаются две распространенные практические задачи. Первая из них формулируется как достижение максимальной технической эффективности по главному показателю (обычно это производительность процесса) при ограниченных затратах, а вторая — как достижение минимальных затрат при заданном уровне технической эффективности. Нетрудно осуществить формальную запись этих задач, пользуясь выражением (8.3.9).
8,3,4. Принципы автоматизированного проектирования технологий
Необходимость автоматизации проектирования технических объектов и технологий стала очевидной в 1950-1960-х гг. по следующим основным причинам.
Во-первых, увеличение числа и степени сложности вновь разрабатываемых технических систем привело к резкому возрастанию объемов проектных работ и требований к квалификации исполнителей. Так, например, во второй половине XX в. каждые десять лет объем проектных работ увеличивался примерно на порядок, а число специалистов-проектировщиков — не более чем в 3 раза. Учитывая тот факт, что лишь 20 % проектировщиков способны решать творческие, высокоинтеллектуальные задачи, можно отметить явное несоответствие между наблюдаемым ростом объемов проектирования и количеством квалифицированных исполнителей при традиционном «ручном» проектировании. Дефицит кадров
Основы технологии
1291
оказывал и до сих пор оказывает негативное влияние на качество многих новых изделий.
Во-вторых, острая конкуренция за рынки сбыта привела к расширению и быстрому обновлению номенклатуры производимых изделий (число различных классов технических объектов удваивается примерно каждые десять лет). Это потребовало разработки методов и средств «быстрого» проектирования при условии сохранения высокого качества проектных работ.
В-третьих, появление мощных и доступных средств вычислительной техники позволило не только освободить человека от рутинных, монотонных, низкоквалифицированных работ, но и значительно увеличить число одновременно прорабатываемых вариантов, повысить тем самым качество проектных решений.
Наконец, появление новых видов высокопроизводительного и гибкого оборудования с высоким уровнем автоматизации стало приводить к тому, что традиционный процесс проектирования превратился в лимитирующий этап создания новых изделий.
Все вышесказанное вызвало потребность в технических системах, предназначенных для переработки буквенно-цифровой и графической информации, необходимой в процессе проектирования технологий. Такие системы были созданы и получили название систем автоматизированного проектирования технологических процессов (САПР ТП). Аббревиатура САПР, широко используемая в технической литературе, является смысловым эквивалентом английского CAD (Computer Aided Design), что означает проектирование с помощью ЭВМ. Применение САПР, как показывает опыт, позволяет на 10-25 % повысить технико-экономические показатели проектируемых объектов, на 10-30 % снизить ресурсозатраты, в несколько раз сократить сроки проектирования.
Разработке и эксплуатации САПР в различных областях техники и технологии посвящено большое количество работ, созданы соответствующие стандарты. Рассмотрим наиболее общие принципы функционирования систем автоматизированного проектирования технологических объектов.
Материальной основой любой САПР является программно-технический комплекс, включающий в себя технические и программно-методические средства. Технические средства САПР содержат следующие согласованные между собой элементы:
• устройства ввода информации в виде различного периферийного оборудования ЭВМ (дисплеи, считыватели графической информации, ввод с различных носителей информации);
• устройства хранения информации (внешние запоминающие устройства ЭВМ);
• устройства переработки информации (программное обеспечение и центральные процессоры ЭВМ);
• устройства отображения и вывода информации в удобной для проектировщика форме (чертежный автомат, дисплей, печатающие устройства);
• устройства управления процессами обработки информации при проектировании.
Программно-методические средства включают в себя пакеты программ, базы данных и документацию по эксплуатации САПР.
Функциональными составляющими САПР являются проектирующие и обслуживающие подсистемы. К первым из них относятся подсистемы, предназначенные для выполнения операций проектирования отдельных частей объекта или определенных стадий проектирования (например, подсистема выполнения расчетов). Обслуживающими называют подсистемы, обеспечивающие функционирование проектирующих подсистем. Это информационно-поисковая, подсистема графического отображения объектов, формирования документов и др.
Проектирующие подсистемы САПР в большинстве случаев являются объектно-ориентированными, т. е. применимыми только для данного вида проектируемых объектов. Обслуживающие подсистемы чаще всего выполняют инвариантными, объектно-независимыми.
Перечисленные подсистемы САПР обладают всеми свойствами систем, т. е. могут функционировать самостоятельно и подвергаться декомпозиции на составляющие элементы, которые принято называть компонентами САПР. В отечественной литературе обычно выделяют следующие обязательные компоненты САПР:
• методическое обеспечение, содержащее комплекс документов описания САПР, данные о составе, правила обслуживания и использования;
• лингвистическое обеспечение — совокупность специальных проблемно-ориентированных языков проектирования;
• математическое обеспечение — совокупность математических методов, моделей, алгоритмов, необходимых для выполнения проектных процедур;
• программное обеспечение — комплекс всех программ и эксплуатационной документации к ним;
• техническое обеспечение — совокупность всех технических средств, используемых при автоматизированном проектировании, диагностике и ремонте вычислительной техники;
• информационное обеспечение — совокупность информации, используемой проектировщиком непосредственно для получения проектных решений и содержащейся в машинных банках данных или в иных документах;
• организационное обеспечение — комплект документов, устанавливающих правила выполнения проектирования, в том числе: правила выпуска, корректирования и использования выходных документов, правила доступа к базам данных, приоритеты использования средств САПР, порядок взаимодействия всех проектирующих и обслуживающих подразделений.
При разработке САПР, их подсистем и компонентов
учитывают несколько основополагающих прин-
ципов:
1292
Новый справочник химика и технолога
• принцип системного единства и совместимости, предполагающий взаимосвязь и взаимодействие подсистем в процессе функционирования САПР, стремление к достижению единой цели системы;
• принцип развития, предусматривающий возможность пополнения и обновления подсистем и компонентов САПР;
• принцип оптимального распределения процессов преобразования информации (задач проектирования) между человеком и ЭВМ с учетом возможностей их взаимодействия;
• принцип унификации компонентов и инвариантности их по отношению к широкому кругу проектируемых объектов;
• принцип смежности этапов проектирования, согласно которому выходная информация одного этапа проектирования является исходной для последующего (конвейерная обработка информации);
• блочно-иерархический принцип построения подсистем САПР, естественно вытекающий из иерархического характера процесса проектирования.
Перечисленные принципы позволили создать и успешно эксплуатировать системы автоматизированного проектирования, их подсистемы и элементы в различных областях проектной деятельности.
Говоря о разработке и внедрении САПР, необходимо подчеркнуть динамичный, развивающийся характер автоматизации проектных работ. На ранних стадиях осуществляется привлечение машинных методов и средств к выполнению рутинных, повторяющихся операций. Далее разрабатываются модели и программы для решения с помощью ЭВМ частных проектных задач, создается некая взаимосвязанная система. Эта система расширяется и постепенно охватывает задачи все более высокого уровня формализации вплоть до задач, связанных с творческой стороной процесса проектирования.
Наиболее сложным этапом создания САПР, определяющим при прочих равных условиях эффективность системы в целом, является разработка математического обеспечения. Несмотря на то что в явном виде этот компонент в автоматизированном проектировании не используется (используют производный компонент — программное обеспечение), его роль и значение трудно переоценить. В зависимости от назначения и способа реализации в математическом обеспечении выделяют две взаимосвязанные части. К первой относят математические методы и модели, описывающие объекты проектирования или их элементы и отражающие их специфику. Вторая часть включает в себя формализованное описание технологии автоматизированного проектирования и носит инвариантный или достаточно обобщенный характер по отношению к конкретному объекту. Разработка вопросов, относящихся ко второй части математического обеспечения, представляет собой сложную задачу в связи с необходимостью отражения в них всей логики технологии проектирования, включая
творческие, слабо формализованные ее элементы. Развитие математического обеспечения САПР происходит по двум базовым направлениям:
• разработка и совершенствование методов получения оптимальных проектных решений в условиях автоматизированного проектирования;
• совершенствование и типизация процессов и элементов автоматизированного проектирования, инвариантных по отношению к объекту проектирования.
Точные математические методы поиска оптимальных проектных решений малодоступны. Поэтому, как уже говорилось, эту задачу часто решают на основе использования банков (фондов) знаний и типовых эвристических методов.
При оценке эффективности автоматизированного проектирования необходимо учитывать не только экономическую сторону вопроса, связанную с оценкой затрат, но и такие аспекты проблемы, как повышение качества проектного решения, большая глубина проработки проектной ситуации, более высокая вероятность получения принципиально новых решений, социальная сторона автоматизации умственной деятельности. К настоящему времени САПР и ее подсистемы широко используются при решении различных проектных задач.
8.4. Перспективные направления развития технологий
8.4.1. Ресурсосберегающее направление
Для реализации любой технологии необходимо привлечение ресурсов: материальных (МР), трудовых (ТР), энергетических (ЭР) и информационных (ИР). Количественная сторона использованных ресурсов находит непосредственное отражение в экономическом показателе качества технологии. Действительно, себестоимость продукции включает в себя в качестве слагаемых стоимость материалов, энергии, живого и овеществленного груда.
Материалосберегающее направление реализуется различными путями.
1. Снижение отходов исходных материалов при производстве изделий. Так, в машиностроении при переработке черных металлов отходы составляют примерно 27-28 %, около 13 % переработанных металлов превращаются в стружку при механообработке. В нашей стране есть значительные резервы сокращения отходов. Это видно, например, из сравнения усредненных коэффициентов использования материалов (КИМ) в машиностроении России и США за 1989 г., которые равны соответственно 0,78 и 0,83. Повышение КИМ достигается приближением конфигурации заготовки к конфигурации готовой детали за счет совершенствования заготовительных процессов и операций.
2. Снижение расхода материалов на ремонт и вос-
становление машин в процессе эксплуатации. На изго-
товление запасных частей и ремонт машин ежегодно
расходуется около 25 млн т металла. Задача решается за
счет повышения надежности и долговечности изделий.
Основы технологии
1293
3. Рациональное использование отходов основного производства существенно повышает эффективность применения исходных материалов.
Например, после отделения жидкой фракции (сусла) в технологии производства виноградных вин отходы основного производства (мезга) используются для производства вторичных продуктов: виннокислой извести, пищевого красителя, спирта, белковой муки, косточкового масла.
При сверлении отверстий большого диаметра в машиностроении используются кольцевые сверла. Получаемые отходы в виде дисков или цилиндров являются заготовками для изготовления деталей другого наименования.
4. Замена дорогостоящих материалов более дешевыми, с близкими физико-механическими свойствами. Так, в ряде случаев возможна эквивалентная замена деревянных деталей изделиями из прессованной стружки или опилок, металлических — пластмассовыми или композиционными.
5. Применение современных технологий получения заготовок дает существенную экономию материалов в легкой промышленности, при изготовлении мебели, в машиностроении. Так, применение плазменной, гид-роабразивной и лазерной резки позволяет экономить до 40 % металла при одновременном уменьшении потребности в металлорежущем оборудовании для последующей обработки изделий.
Несмотря на постоянное расширение номенклатуры и повышение качества промышленных источников энергии, проблема снижения энергопотребления определяет характер развития многих производств. Дело нс только в том, что энергозатраты непосредственно влияют на себестоимость продукции. По ряду причин многие предприятия вынуждены работать в условиях лимитированного энергопотребления, что заставляет их уделять значительное внимание экономии энергоресурсов. Так, в целом ряде случаев удельные энергозатраты являются главным критерием выбора наилучшего технологического процесса. В табл. 8.2.3 приведены данные, иллюстрирующие удельные энергозатраты для различных методов обработки материалов, применяемых в машиностроении. Как видно, лазерная обработка материалов характеризуется повышенным энергопотреблением, что ограничивает сферу применения технологических лазеров. Из приведенных в таблице данных следует также, что одним из основных показателей энергетической эффективности технологического процесса является КПД преобразователя энергии.
Наряду с повышением энергетической эффективности отдельных процессов и оборудования, используют ряд общезаводских мероприятий по экономии энергоресурсов: снижение потерь тепла в тепломагистралях, сжатого воздуха в воздуховодах, использование обратного тепла. Интересным примером рационального использования теплоресурсов является многокорпусная вакуум-выпарная установка, применяемая в пищевой
промышленности для получения концентрированных соков, томат-пасты, производстве сахара и описанная выше. В ней каждый последующий корпус обогревается паром, образовавшимся при уваривании продукта в предыдущем корпусе, а конденсат из нагревательных элементов может использоваться для обогрева помещений.
8.4.2. Экология и технология
Любая технологическая форма движения вещества, энергии, информации неизбежно связана с генерированием побочных продуктов, как на отдельных технологических стадиях, так и при реализации технологии в целом (промежуточные и конечные побочные продукты). Например, в деревообрабатывающей промышленности побочным продуктом являются отходы: стружка и опилки; при производстве электроэнергии на ТЭС — это газы, образующиеся при сгорании топлива, и тепло, отдаваемое в окружающую среду; при передаче и переработке информации — это помехи, шумы. Побочные продукты технологий являются результатом жизнедеятельности человека, поэтому они оказывают влияние на естественные природные процессы, в том числе на те из них, которые формируют и определяют среду существования человека. В этом проявляется действие обратных связей в системе «технология— техника—человек—окружающая среда». Если технологическая деятельность человека не согласована с возможностями самовосстановления природной среды, то легко перешагнуть ту грань, с которой начинается экологическая катастрофа.
Уже сейчас мы являемся свидетелями развития глобальных экологических процессов, порожденных технологической деятельностью человека, которые могут вылиться в экологические катаклизмы и вызвать существенные генетические изменения в живой природе.
Парниковый эффект проявляется в повышении средней температуры воздуха вблизи поверхности Земли. Причиной наблюдаемого изменения температуры является возрастание содержания углекислого газа в атмосфере, главным образом из-за работы энергетических установок на химическом топливе, и, как следствие, нарушение теплового баланса Земли. Если в 1985 г. эта температура составляла 14°С, то к 2025 г. ожидается потепление на 2-3 °C, к 2050 г. — на 3-5 °C. Это может привести к таянию антарктических и арктических льдов и повышению уровня Мирового океана (при полном таянии льдов этот уровень повысился бы на 70-80 м).
Разрушение озонового слоя (появление озоновых дыр) приводит к снижению защитных свойств атмосферы по отношению к ультрафиолетовому излучению Солнца. В соответствии с химической гипотезой этого явления разрушение озонового слоя связано с химическим взаимодействием его с продуктами антропогенного происхождения, попадающими в верхние слои атмосферы (концентрация озона максимальна на высоте 20-25 км). К таким продуктам технологической
1294
Новый справочник химика и технолога
деятельности относятся, например, галогеноуглеводо-роды (фреоны), оксиды азота, метан и пр.
Кислотные дожди — это атмосферные осадки с повышенной кислотностью, оказывающие сильнейшее воздействие на флору и фауну. Причина их появления — выброс в атмосферу огромных количеств оксидов углерода, азота, серы (СО2, NO2, SO2) в результате промышленного сжигания твердых топлив, работы двигателей внутреннего сгорания и других причин. Соединяясь с водой, эти оксиды образуют соответствующие кислоты, растворы которых при избытке воды и выпадают в виде кислотных дождей:
2NO2 + Н2О = HNO3 + НЫО2;
3HNO2 = HNO3 + 2NO + Н2О;
SO2 + Н2О = H2SO3;
2H2SO3 +О2 = 2H2SO4
Кислотные дожди особенно характерны для регионов с развитым металлургическим производством и для мегаполисов, перенасыщенных автотранспортом.
Отходы крупнотоннажных химических производств в ряде случаев пытаются утилизировать, производя из них вторичные продукты. Так появились печально известные препараты на основе диоксина — сильнейшего токсина и канцерогена, синтезированного в начале 1930-х гг. Это гербициды — вещества для химической прополки сорняков в сельскохозяйственном производстве, некоторые технологические среды. Ежегодно в мире вводятся в употребление примерно 200 тыс. новых веществ, часть из которых является вторичными продуктами отходов тех или иных производств. Опасность их непредсказуемого или трудно прогнозируемого негативного влияния на окружающую среду очевидна, а жесткие требования к технологиям их изготовления и применения вполне оправданны.
Радиоактивное заражение планеты является прямым следствием развития соответствующих технологий. Так, на рис. 8.4.1 представлена схема получения чистого урана (первый этап) из руды. Урановая руда —
уранит (UO2, UO3) с содержанием урана менее 2 % — измельчается в порошок, который пропускают через сильное магнитное поле, отделяя магнитную фракцию Fe3O4. Далее методом флотации отделяется легкая порода, после чего концентрат обрабатывают последовательно серной кислотой, растворами соды и щелочи.
Конечным продуктом этого этапа является натриевая соль урановой кислоты. Стрелками на схеме показаны возможные пути загрязнения ураном окружающей среды с промежуточными побочными продуктами данной технологии. Последующие этапы производства металлического урана еще более сложны в техническом отношении, поэтому полностью предотвратить миграцию урана в окружающую среду при реализации существующих технологий невозможно.
Еще более сложные проблемы возникли при разработке технологий регенерации ядерного горючего, а многие из них не решены до сих пор.
В результате рассмотренных выше явлений происходит интенсивное загрязнение воздушного бассейна. Общий выброс вредных веществ в атмосферу нашей страны превышает 65 млн т/год, в том числе вследствие эксплуатации автомобильного транспорта 40 млн т/год (конец 1980-х гг.). Суммарный выброс диоксида серы превысил 20 млн т/год. В результате к концу 1980-х гг. более чем в 100 городах бывшего СССР концентрация вредных веществ в 10 раз и более превышала допустимые нормы. Лидерами в этом печальном списке являлись (и являются) города с развитым металлургическим производством: Магнитогорск, Днепропетровск, Липецк, Череповец, Челябинск и др.
Вторым важным следствием безответственной технологической деятельности людей явилось сильнейшее загрязнение подземных вод и водоемов. Процессы естественной фильтрации уже не справляются с антропогенной нагрузкой.
Описанные выше глобальные экологические ката-лизмы порождаются совместным действием множества различных технологий, число которых постоянно увеличивается. Следовательно, можно говорить о двух путях
Рис. 8.4.1. Первый этап получения чистого урана
Основы технологии
1295
решения экологических проблем. Первый из них связан с разработкой и широким использованием специальных экологически активных технологий, направленных на снижение уровня уже накопленных негативных последствий антропогенного воздействия (очистка воздуха, воды, рекультивация земель и пр.).
Второй путь связан с введением ограничений на новые технологии: разработке и внедрению подлежат только те технологии, в которых отсутствуют или сведены до допустимого уровня вредные выбросы в окружающую среду — экологически чистые технологии. Такой подход предполагает обязательную экологиче
скую экспертизу каждой новой технологии и постепенную замену неблагополучных в экологическом отношении существующих технологий в условиях жесткой правозащитной деятельности органов государственного экологического контроля.
Выше уже говорилось о неизбежности получения побочных продуктов в процессе реализации технологий. Поэтому второй путь экологозащитного направления в современных технологиях реализуется следующим образом. Наряду с проектированием основного технологического процесса параллельно разрабатывают технологии регенерации и утилизации побочных продуктов.
Рис. 8.4.2. Технологическая схема регенерации электролитов и утилизации шламов
1296
Новый справочник химика и технолога
Регенерация — это технология, направленная на повторное использование части побочных продуктов в основном технологическом процессе. Например, побочным продуктом технологии преобразования энергии сгорания жидкого топлива в механическую энергию, реализуемой в двигателях внутреннего сгорания, является отработанное масло. После очистки последнего от загрязнений и добавления израсходованных компонентов (регенерации) масло можно вновь заливать в двигатель и использовать повторно.
Важной проблемой во многих отраслевых технологиях с большим объемом водопотребления является регенерация свойств воды. С этой целью разработаны и широко используются технологии и оборудование для водоподготовки.
Утилизация — это технология получения вторичных продуктов утилитарного назначения из отходов или побочных продуктов основного производства. Например, получение соков или джемов из косточковых плодов сопровождается накоплением отходов — косточек. По соответствующей технологии из этих отходов можно получить ценное косточковое масло, порошок для тонкой полировки изделий машиностроения и другие вторичные продукты.
В машиностроительном производстве стремятся получить такие отходы, которые можно использовать в качестве заготовок при изготовлении других деталей. Вместе с тем задача утилизации стружки была и остается одной из побочных задач любого машиностроительного предприятия.
Во многих отраслевых технологиях важное значение придается операции раскроя исходной заготовки, на которой формируются отходы производства.
Обсуждаемое направление в развитии современных технологий известно как проектирование безотходных и малоотходных технологий. Рассмотрим пример реализации такой технологии, относящийся к области химических, точнее электрохимических, производств, который иллюстрируется схемой, представленной на рис. 8.4.2.
Основной функциональный технологический процесс заключается в электрохимическом растворении материала с целью получения заданной геометрической конфигурации детали. В качестве рабочей среды используется электропроводящая жидкость-электролит, например 15% раствор NaCl в воде, которая в процессе электролиза загрязняется продуктами растворения металла (соли, оксиды, оксихлориды, гидроксиды), нагревается и теряет в определенной степени свои технологические свойства. Возникает задача регенерации электролита и утилизации вторичных продуктов электролиза.
Как следует из представленной схемы, после разделения фаз (отстаивание, фильтрация, центрифугирование) реализуются технологии регенерации электролита с возвращением последнего в основной процесс и утилизации твердофазных отходов (шлама) с получением из него целой гаммы вторичных продуктов. Очевидно,
представленная технология регенерации и утилизации требует соответствующего оборудования. Поэтому при проектировании современных цехов и участков электрохимической обработки деталей машин предусматривают соответствующий участок подготовки и регенерации электролита.
8.4.3. Гибкие производственные процессы и роботизированные производства
Важным направлением развития ряда отраслей промышленности является создание и совершенствование гибких производственных систем (ГПС). Концепция гибких систем порождена двумя противоречивыми тенденциями развития современного производства: с одной стороны, сокращаются сроки подготовки и выпуска новых изделий, расширяется их номенклатура, снижается количество изделий, выпускаемых по неизменной технологической документации, а с другой, проявляется стремление снизить трудоемкость и себестоимость продукции при сохранении высокого качества. Первая тенденция предусматривает возрастание степени универсальности оборудования и систем управления, возможность реализовать любые заранее не спланированные производственные ситуации, быстро переходить на выпуск новой продукции, т. е. увеличение мобильности производства.
Вторая тенденция связана с использованием специального или специализированного оборудования, высоким уровнем автоматизации производственного процесса, стремлением к высокопроизводительному выпуску продукции ограниченной номенклатуры в течение длительного времени.
Легко заметить противоречивость требований, регламентирующих перечисленные направления развития производства. Концепция гибкого производства как раз и направлена на объединение, совместное использование позитивных сторон рассмотренных направлений, создание мобильного высокопроизводительного производства.
Гибкость — это свойство производственной системы быстро перестраиваться на выпуск новой продукции, т. е. переходить в пределах установленных технологических возможностей из одного работоспособного функционального состояния в другое для выполнения очередного производственного задания или новой функции. Рассмотрим подробнее основные характеристики гибкого производства (ГП):
• ГП — это многономенклатурное производство, в котором переналадка оборудования на выпуск нового изделия осуществляется параллельно с выпуском изделия старого наименования или при минимальных затратах времени на переналадку;
• ГП — комплексно автоматизированное производ-
ство, управляемое центральной ЭВМ;
• свойство гибкости многоаспектно. Различаются:
гибкость состояния (способность системы функциони-
ровать при различных внешних и внутренних измене-
Основы технологии
1297
ниях); гибкость действия (способность расширять свои возможности за счет включения нового оборудования); гибкость технологии (оценивается числом операций, реализуемых в данной производственной системе); организационная гибкость (оценивается сложностью перехода на обработку любого изделия данной номенклатуры);
• понятие гибкости иерархично: от отдельных единиц оборудования и операционных технологий до заводского производственного процесса в целом;
• ГП основывается на безлюдной (малолюдной) технологии и позволяет отказаться от традиционной технической и сопроводительной документации (безбумажные технологии);
• ГП способны обрабатывать изделия заданной номенклатуры в любом порядке их следования;
• ГП функционирует на основе принципа централизации обработки — объект производства не требует дополнительной доработки на другом оборудовании;
• ГП функционирует, как правило, на основе унифицированных технологий.
Как свойство производственной системы гибкость имеет четыре основных признака:
1) повторяемость — способность системы многократно возвращаться к выполнению ранее освоенных работ после завершения данной работы;
2) универсальность — способность системы обрабатывать различные изделия и в различных количествах без какой-либо модификации;
3) приспособляемость — способность системы к переналадке на новое изделие путем воздействия извне или самонастройки;
4) адаптивность — способность системы приспосабливаться к изменению внешних или внутренних факторов в определенных пределах без нарушения собственного функционирования или потери качества продукции.
Для количественной оценки степени гибкости ГПС используют интегральный показатель гибкости'.
где п — число различных функциональных состояний производственной системы в пределах ее технологических возможностей; т,7 — время перехода из f-го в у-е функциональное состояние; Т — некоторый плановый базовый период работы оборудования.
Очевидно, наибольшее значение этого показателя при предельном переходе п -> оо и т,у- —> 0 равно единице.
Между производительностью ПС и ее гибкостью существует взаимосвязь, качественно характеризуемая кривой, представленной на рис. 8.4.3. Видно, что чем шире номенклатура выпускаемых изделий, тем ниже производительность, и каждому сочетанию этих параметров соответствует определенная группа оборудования.
Рис. 8.4.3. Область применения оборудования с различным показателем гибкости
Введем несколько общепринятых определений. В соответствии с ГОСТ 26228-84 ГПС — это совокупность технологического оборудования и системы обеспечения ее функционирования в автоматическом режиме, обладающая свойством автоматизированной переналадки при производстве изделий заданной номенклатуры в установленных пределах значений их характеристик.
По организационной структуре ГПС формируются в виде гибкого производственного модуля (ГПМ), гибкой автоматизированной линии или участка (ГАУ), гибкого автоматизированного цеха (ГАЦ) и гибкого автоматизированного завода (ГАЗ). Очевидно, перечисленные формы ГПС отражают ее иерархическую структуру.
Исходной единицей ГПС является ГПМ — автономно функционирующая единица технологического оборудования с программным управлением, автоматически осуществляющая все функции изготовления изделий заданной номенклатуры, имеющая возможность встраиваться в ГПС более высокого уровня. Последние включают в себя 2-25 единиц технологического оборудования, объединенных общей функциональной задачей. Количество изделий, обрабатываемых на современных ГПС, колеблется от 2 до 140 (чаще всего 10-12).
Типовой ГПМ для механической обработки деталей, используемый в машино- и приборостроении, представлен на рис. 8.4.4.
Как видно, важным элементом в рассматриваемой схеме автоматизированного производства является робот-манипулятор, который обеспечивает загрузку-рагрузку основного технологического оборудования. В ряде случаев робот выполняет основные технологические функции (сварку, сборку, пайку и пр.). Масштабы роботизации современного производства весьма велики. Динамика промышленного освоения роботов хорошо видна на примере промышленности США: в 1979 г. в этой стране использовалось 3 тыс. промышленных роботов, в 1984 г. — 13 тыс., в 1990 г. — 150 тыс.
1298
Новый справочник химика и технолога
Рис. 8.4.4. Структурная схема ГПМ механообработки:
/ — робот-манипулятор; 2 — система управления; 3 — накопитель инструмента; 4 — накопитель заготовок;
5 — станок с 411У; 6 — устройство для удаления стружки
Рассматривая эффективность внедрения ГПС, следует иметь в виду, что потенциально ГПС могут обрабатывать изделия 5-5,5 тыс. ч в год, если обеспечить их трехсменную работу в течение 250 дней. В то же время металлорежущий станок, например, обрабатывает изделия в среднем 600-700 ч в год (при односменной 8-часовой работе в течение 250 рабочих дней с коэффициентом использования 0,3-0,4). Обеспечение работы ГПС в безлюдном режиме в течение 24-48 ч позволит организовать работу в выходные и праздничные дни, что в общем составит почти 7800 ч продуктивной работы оборудования, оставляя лишь несколько дней на профилактические работы и ремонтное обслуживание. Таким образом, фондоотдача при использовании ГПС возрастает более чем в 10 раз, что следует учитывать при оценке целесообразности их внедрения.
8.4.4. Повышение эффективности существующих технологических процессов
Выше рассмотрены наиболее важные направления развития современных технологий, которые необходимо учитывать при их проектировании. Вместе с тем на значительной части промышленных предприятий используются технологии и эксплуатируется оборудование, спроектированные 10-20 лет тому назад. Закрывать такие производства не всегда выгодно. Как правило, их реконструируют, модернизируют, совершенствуют.
Техническое перевооружение действующих производств выполняется как на уровне единичного оборудования, так и на уровне участков, линий, цехов. Все чаще причиной замены технологического оборудования становится не физический, а моральный износ. В связи с этим актуальной становится задача вторичного использования списанного оборудования, которая в ряде случаев находит успешное решение (применение газотурбинных двигателей, отработавших свой летный ресурс, для перекачки газов в газопроводах, очистки
взлетных полос от обледенения; восстановление и вторичное использование металлорежущих станков на производствах более низкого технологического уровня и т. д.). Интересным примером вторичного использования оборудования служит разработка роторного полуавтомата для электрохимической обработки изделий на базе элементов конструкции морально и физически устаревшего автомата для расфасовки жидкостей. Такое решение существенно снизило стоимость и длительность проектирования и изготовления изделия.
Эффективность технического перевооружения связана не только с заменой технологического оборудования, но и с внедрением новых типов вспомогательной и управленческой техники. Так, использование автоматизированных складов позволяет снизить затраты малоквалифицированного ручного труда, сократить потребные производственные площади. Современная управленческая техника интенсифицирует процесс принятия и реализации решений, обеспечивает надежный оперативный контроль производства.
Снижение относительной величины бракованной продукции достигается путем возрастания технологической надежности производства. Например, на предприятиях, производящих элементы электронной техники (большие интегральные схемы, многослойные платы, изделия из микропровода), любые организационно-технические мероприятия, позволяющие снизить процент брака, весьма эффективны.
Особенно высокие требования по технологической надежности предъявляются к конечным, финишным операциям в связи с тем, что возможный брак на этой стадии производства приводит к убыткам не только за счет стоимости использованных материалов, но и за счет потерь живого и овеществленного труда на предыдущих стадиях.
На многих производствах часть бракованной про-
дукции может быть исправлена путем доработки (с со-
ответствующими дополнительными затратами), а часть
Основы технологии
1299
приводит к невосполнимым потерям. Такая ситуация характерна, например, для машиностроительного производства.
Организация производства существенным образом влияет на его эффективность. Так, предложенная Г. Фордом конвейерная сборка автомобилей (непрерывно-поточное производство) на многие годы определила стратегию автомобилестроения. Однако современные требования к автомобилю заставили изменить эту стратегию. Например, шведская фирма «Вольво», используя концепцию гибкого автоматизированного производства, перешла на бесконвейерную сборку и резко сократила серийность выпуска одной модели. Это одна из причин высокой конкурентоспособности продукции фирмы.
Возрастание степени сложности и стоимости промышленной продукции значительно удорожает незавершенное производство, приводит к увеличению оборотных средств. В связи с этим перспективной является организация производства по принципу «все только тогда, когда нужно». Этот принцип предопределяет снижение производственных заделов, сокращение складов. Он основан на централизации, интеграции, высоком уровне качества управления производством. Применительно к машиностроению этот принцип заключается в изготовлении отдельных деталей и получении комплектующих изделий только тогда, когда они необходимы на сборке. Очевидно, реализация принципа требует высокой степени организации производства.
Эффективная организация производственного процесса предусматривает также улучшение социальных факторов, направленных на поддерживание высокой работоспособности и надежности действий оператора и другого производственного персонала. Одним из таких факторов является безопасность жизнедеятельности при осуществлении производственного процесса. Современные достижения в области инженерной психологии позволяют сформулировать требования к условиям труда на каждом рабочем месте, подобрать оператора с соответствующими физическими и психологическими качествами.
8.4.5. Технологическое применение новых физико-технических эффектов
Заметное, как правило, скачкообразное повышение качества любой технологии достигается при использовании новых технических эффектов, основанных на физическом, химическом, биологическом или комбинированном воздействии на объект производства. Выше отмечалось, что в научной литературе описано более 3000 физико-технических эффектов (ФТЭ), лишь незначительная часть которых используется в отраслевых технологиях. Вместе с тем бурное развитие технологий XX в. оказалось возможным именно на основе технологического применения ультразвука, электрохимии, достижений в области физики пучков заряженных частиц, нелинейной оптики, физики электрического разряда в различных средах, плазмохимии, катализа и др. При
менение новых технических эффектов в отраслевых технологиях описано в специальной литературе.
Рассмотрим в качестве примера применение эффектов, сопровождающих электрический пробой диэлектрических сред. Если диэлектриком является жидкость, то после пробоя возникают вторичные физические явления: распространение ударной волны в жидкой среде, тепловой эффект разряда при прохождении тока значительной силы через канал разряда, излучение электромагнитных волн видимого диапазона и др. Электрический разряд в жидком диэлектрике и сопутствующие явления используют для решения различных технологических задач.
Применение ФТЭ в пищевой технологии. При получении фруктовых соков исходное сырье подвергают дроблению, а затем отбирают жидкую фракцию-сусло самотеком с последующим прессованием. При этом отбирается механически связанная влага, клетки растительного сырья практически не разрушаются, их протоплазма в жидкую фракцию не переходит. Для разрушения клеток дробленую массу пропускают через рабочую камеру, и в ней инициируется электрический разряд. Такой процесс называют электроплазмолизом, а соответствующее оборудование — плазмолизатором растительного сырья. Этот процесс успешно используется в производстве соков, при отделении жидкой фракции в процессе переработки сахарной свеклы и других видов сырья. При этом достигается увеличение выхода жидкой фракции на 5-15 % по отношению к традиционному процессу механического отделения сусла.
Применение ФТЭ в машиностроении. На тепловом эффекте электрического разряда в жидком диэлектрике основан метод электроэрозионной обработки деталей машин (рис. 8.1.3), описанный в 8.1. Метод позволяет обработать любые электропроводные материалы независимо от их механических свойств и в ряде случаев является единственным методом, обеспечивающим решение технологической задачи.
Применение ФТЭ в других областях. При определенных значениях параметров электроразрядного импульса в жидкой диэлектрической среде развиваются очень высокие давления. Это явление носит название электрогидравлического эффекта. В замкнутом пространстве это приводит к силовому воздействию на стенки рабочей камеры, деформации или разрушению конструктивно слабых элементов. Этот эффект нашел применение при производстве габаритных листовых изделий (электрогидравлическая штамповка), разрушении твердых горных пород и в других областях.
Как видно, один и тот же процесс позволяет эффективно решить разнохарактерные технологические задачи в различных отраслях промышленности.
Многие ФТЭ еще более универсальны. Например, звукокапиллярный эффект, заключающийся в увеличении (в десятки и сотни раз) высоты подъема жидкости в капилляре под действием ультразвука, используют в технологии пропитки капиллярно-пористых тел лака-
1300
Новый справочник химика и технолога
ми, смолами и другими жидкими средами. Этот эффект облегчает подачу смазочно-охлаждающих жидкостей в зону резания при обработке материалов резанием, влияет на процессы, протекающие в живой природе: озвучивание растений волнами ультразвукового диапазона интенсифицирует их рост.
8.5. Технологические процессы в окружающем мире
В 8.1 показано, что краеугольным камнем любого определения технологии является процесс изменения свойств некоторого объекта в искусственных технологических системах. Многообразие объектов, подвергаемых такому воздействию, привело к широкому распространению технологических принципов, понятий и подходов практически во всех сферах деятельности человека.
8.5.1. Информационные технологии
Информацией называют некоторую совокупность сведений, определяющих меру наших знаний о событиях, фактах, явлениях и их взаимосвязи. Это динамичный объект, подвергаемый различным преобразованиям при протекании процессов сбора и регистрации данных (получение первичной информации), передаче данных по тем или иным коммуникационным каналам, переработке данных, их хранении, подготовке данных для оценки и интерпретации, поиске данных, соответствующих запросу, и др. Упорядоченная совокупность воздействий на информационный объект для целенаправленной переработки информации представляет собой информационную технологию (ИТ). Конкретизируем наиболее употребительные общетехнологические понятия применительно к процессам переработки информации.
Технологическая операция ИТ — это программноаппаратурный комплекс, предназначенный для выполнения функций обработки данных путем реализации соответствующих методик, правил, инструкций, процедур.
Технологическим модулем является законченный элемент ТО, неразделимый во времени и пространстве и вызывающий конкретный идентифицируемый результат обработки данных. Используя сделанные определения, можно сформулировать понятие ИТ.
Технологический информационный процесс — это совокупность технологических операций переработки информации, структурированных в соответствии с требованиями эффективного достижения какой-либо цели в данной предметной области.
Объектом обработки в ИТ являются данные (информация), целью ИТ служит получение или преобразование некоторой информации, а средством достижения цели — программные, аппаратные и программновычислительные комплексы (средства технологического оснащения). Разделение технологического процесса на ТО осуществляют в соответствии с данной предметной областью. Показателями уровня качества ИТ являются время, затраченное на преобразование информа
ции, надежность получаемой информации, ее полнота, доступность. Эти показатели имеют количественную меру и используются для оптимизации ИТ.
Исследованием общих характеристик информационных технологий занимается информатика. На основе этой науки разрабатываются ТП в конкретных предметных областях. Так, создание любой автоматизированной системы обработки данных рассматривают как реализацию конкретной ИТ.
Функциональная сторона ИТ заключается в полном и своевременном удовлетворении информационных потребностей конечных пользователей: обеспечение лица, принимающего решение, полной информацией, предоставление этой информации с требуемой скоростью и в форме, удобной для принятия решения, обеспечение контроля за информационным взаимодействием и согласованностью принимаемых решений.
Под технологической системой ИТ понимают часть производственного процесса предприятия, реализующую сбор, обработку, хранение, передачу данных, созданную для эффективной реализации информационных функций в данной предметной области и состоящую из взаимодействующих функциональных подсистем:
• технологической, объединяющей лингвистические средства, методическое обеспечение, создающей технологическую среду в виде сценариев, регламентов, описаний, инструкций, включающей методы, способы и режимы обработки данных, модели предметной области;
• материально-технической, представляющей собой комплексы вычислительных средств, программ;
• эргономической (исполнители, психофизиологические требования к ним и к пользователям);
• информационной (базы данных, базы знаний, исходная информация, модели информационных потоков в данной предметной области и пр.);
• организационной, охватывающей формы и методы организации ТП, описывающей структуру сети рабочих мест;
• экономической, содержащей экономические цели функционирования ИТ, критерии, ограничения, ресурсы.
Центральными элементами информационной технологии являются предметная область, пользователь, вычислительный и программный комплексы.
Рассмотрим обобщенный маршрут обработки данных на информационно-вычислительном центре, представленный на рис. 8.5.1:
Ф<2НЗ>Ч4}<5Н6)-----------------
_______i____________
---------Библиотека программ
(ZHlHlMMiHg)
Рис. 8.5.1. Маршрутная схема обработки данных на ИВЦ
1. Разработка методики решения (постановка задачи).
2. Разработка технического задания на программи-
рование.
Основы технологии
1301
3. Написание программы.
4. Отладка программы.
5. Оформление программной документации.
6. Передача документации в библиотеку программ.
7. Прием и первичная обработка данных.
8. Подготовка данных на машинных носителях.
9. Ввод и формирование информационного массива.
10. Проведение расчетов.
11. Анализ и оформление результатов.
12. Представление результатов лицу, принимающему решение.
Добавим к сказанному, что системы автоматизированного управления производством основаны на предметно-ориентированных информационных технологиях. Более того, информационные технологии, по сути, лежат в основе многих социальных явлений, процессов, связанных с мыслительной деятельностью человека. Технологии проектирования, обсуждаемые в 8.3, являются информационными, а информационные технологии являются основой и определяют качество любого процесса обучения.
8.5.2. Социальные технологии
Объект воздействия в социальных технологиях — общественное сознание; цель, функциональная сторона — выработка установки, решения или действия, направленных на достижение социально значимой цели. В качестве средств воздействия используются различные каналы массовой информации.
Хорошим примером реализации подобной технологии являются выборы в органы исполнительной или законодательной власти, выборы административного руководителя предприятия или региона. Такие мероприятия протекают по следующему примерному маршруту.
1. Формируется группа людей, объединенных общими политическими, экономическими или иными целями.
2. Выделяется лидер группы — лицо, обладающее высокими личностными качествами и аккумулирующее групповую целевую установку.
3. Строится информационная модель лидера и группы в целом.
4. Модель внедряется в массовое сознание через СМИ, личные встречи с электоратом, с использованием экономических и иных рычагов воздействия.
5. Формулируются и активно пропагандируются правила предпочтения данной модели.
6. Проводятся выборы.
7. Анализируются результаты, корректируются модели.
Конечно, эффективность реализации такой технологии будет непосредственно зависеть от возможности привлечения средств массовой информации, т. е. от финансовых возможностей группы. Подобные технологии получили широкое распространение в конце XX и начале XXI в., в настоящее временя сформирован развитый рынок технологических услуг в этой области.
8.5.3. Транспортные технологии
Если к числу значимых свойств объекта, определяющих его состояние, относится расположение в некоторой системе координат, то изменение этого состояния, вызванное перемещением объекта, следует рассматривать как результат технологического воздействия. Такого рода технологии называются транспортными, а их роль и значение в жизнедеятельности человека трудно переоценить.
Рассмотрим некоторые особенности технологий транспортировки материальных тел. Прежде всего, обратим внимание на многообразие последних. Перемещаются люди (пассажирские перевозки), грузы различного агрегатного состояния, химического состава, массогабаритных показателей (грузовые перевозки). Функциональная сторона таких технологий заключается в перемещении объекта в географическом отношении и характеризуется траекторией перемещения, временем и пройденным при этом расстоянием. Она включает также ограничения, накладываемые на показатели качества груза: эти показатели нс должны ухудшаться в процессе транспортировки или же их изменения должны быть нормированы.
Выполнение транспортной функции сопряжено с преобразованиями энергии и информации. Энергия затрачивается на выполнение работы по пространственному перемещению физических тел и зависит в первую очередь от массы груза и скорости его перемещения. Информационные сопутствующие потоки отражаются в товарораспорядительных и перевозочных документах, служат для учета и контроля состояния транспортируемого объекта, финансирования перевозок, таможенного оформления грузов.
В качестве средств технологического оснащения выступают транспортные средства, которые в зависимости от вида ггеревозок подразделяют на железнодорожные, автомобильные, морские, для внутренних водных путей, воздушные, трубопроводные. Каждый вид транспортных средств включает в себя совокупность изделий одного наименования, но разного типоразмера и исполнения. Это позволяет в зависимости от характера и количества груза, предназначенного к транспортировке, подобрать наиболее выгодное в экономическом отношении транспортное средство. Так, например, наиболее универсальным и эффективным средством доставки больших масс грузов на дальние расстояния, обеспечивающим перевозки более 80 % объема международной торговли, является морской транспорт. Морской торговый флот включает суда, отличающиеся по характеру перевозимых грузов (наливные, навалочные, насыпные, тарно-штучные грузы), грузоподъемности, ограничениям по районам плавания и т. д.
К средствам технологического оснащения транспорт-
ных операций относится также оборудование для по-
грузочно-разгрузочных и транспортно-складских работ.
В ряде случаев технология перевозки предусматривает
операции по доработке грузов, требующие специально-
1302
Новый справочник химика и технолога
го оборудования (упаковка, маркировка, комплектация, пакетирование). В общем случае перевозка груза может осуществляться несколькими видами транспортных средств с промежуточной перевалкой, например по схеме, представленной на рис. 8.5.2. При этом ТП наряду с собственно транспортными операциями (перевозкой) включает еще два вида работ: транспортно-экспедиционные (ТЭР) и погрузочно-разгрузочные (ПРР). Первый из этих видов работ объединяет операции по организации и оформлению перевозки, передаче груза от одного транспортного предприятия другому, складские операции, операции по приведению груза в транспортабельное состояние. ПРР включают в себя операции по перемещению, укладке, закреплению (раскрепле
нию) груза на грузовых площадках транспортных средств.
К настоящему времени около 75 % всех мировых перевозок грузов выполняется с помощью транспортноэкспедиторских компаний и предприятий, которые обеспечивают перевозки, сами не являясь перевозчиками. На них лежит основная доля организации перевозок.
Качество транспортных технологий оценивается соответствующей системой показателей. Себестоимость перевозок калькулируется с учетом затрат на все виды работ. Часто используют удельный показатель оценки качества транспортной технологии, представляющий собой суммарные затраты, грсбуемые на перемещение единицы массы груза на единицу расстояния.
Грузоотправитель
I
Морская перевозка
Грузополучатель
T3Pt
I
ПРР, —►
Железнодорожная перевозка
ПРР3 t
—>ТЭР2
ТЭР3 ТЭР4
; ------------------------ t
ПРР2 —► Автомобильная —► ПРР4
перевозка
Рис. 8.5.2. Маршрутная схема многоэтапной перевозки груза от грузоотправителя к грузополучателю
Развитие транспортных технологий идет по пути создания специализированных средств транспорта, обеспечивающих высокую эффективность перевозок (нефтеналивные суда нового поколения, лихтеровозы), повышения уровня механизации и автоматизации погрузочно-разгрузочных и транспортно-складских работ, организационного совершенствования технологий, исключающего или резко сокращающего непроизводительные перемещения транспортных средств.
8.5.4. Технологии военного назначения
В докладе «Единое видение 2010 г.» председатель Комитета начальников штабов ВС США генерал Д. Шаликошвили высказал мысль о том, что только новые технологии способны значительно увеличить поражающую способность войск. Основой военной технологии будущего, по его мнению, является ее информационная составляющая — методы и средства сбора, анализа, хранения и передачи информации о противнике. Ожидается, что в 2010 г. скорость обмена информацией в системах военных коммуникаций примерно на шесть порядков превысит уровень 1990 г. Это позволит использовать мощное, высокоточное и быстродействующее оружие: лазерные пушки, беспилотные высокоскоростные летательные аппараты, многофункциональные аппараты и устройства.
Анализируя высказанный прогноз, выделим несколько его аспектов, важных для дальнейшего обсуждения.
Во-первых, проведение боевых действий рассматривается сточки зрения технологии. Действительно, можно определить объект воздействия, обладающий набором входных характеристик (противник), цель воздействия, например вытеснение противника с определенной территории. Для достижения поставленной цели разрабатывается и осуществляется последовательность взаимосвязанных операций, в том числе определяется их содержание, регламентируются правила выполнения, выявляются соответствующие ресурсные ограничения, т. е., по сути, проектируется технология. Такое проектирование многостадийно: от предварительного укрупненного описания основных этапов (маршрут) до детальной проработки всех операций с синхронизацией их во времени и определением ресурсозатрат.
Очевидна многовариантность таких технологий, наличие вектора показателей оценки их качества, возможность их оптимизации по выбранному критерию. Военная техника выступает в качестве средств технологического оснащения.
Во-вторых, военная область человеческой деятельности наиболее восприимчива к новым техническим и технологическим идеям. Как правило, такие идеи первоначально реализуются в военном деле и лишь затем конверсируются в иные области. Это связано, по-видимому, с высоким уровнем конкуренции военных технологий, исключительной общественной значимостью конечных результатов.
Основы технологии
1303
В-третьих, на первый план при оценке эффективности рассматриваемых технологических систем выдвигается функция переработки информации. Именно эта функция определяет быстродействие военных технологий, надежность достижения результата. Поэтому в развитие системы военных коммуникаций, совершенствование систем управления войсками вкладываются значительные средства.
Безусловно, военная область во многом специфична. Однако применение общетехнологических методов, подходов к решению конкретных задач может оказаться полезным и в этой сфере человеческой деятельности.
8.5.5. Микроэлектронные технологии
Пожалуй, ни одна отрасль обрабатывающих технологий не развивалась во второй половине XX в. такими высокими темпами и не оказывала такое влияние на наше общество, как производство микроэлектронных приборов. Это связано с революционным достижением в электронике — созданием к началу 1960-х гг. монолитных интегральных схем (ИС) — миниатюрных устройств, отличающихся огромными функциональными возможностями и низким энергопотреблением. Этот технический объект появился благодаря разработке специальных технологий, развитие которых привело к тому, что за период с 1965 по 1990 г. плотность упаковки элементов-транзисторов в одной интегральной схеме площадью 5 мм2 возросла на пять порядков, а удельная площадь одного элемента снизилась на шесть порядков! Сейчас линейный размер такого дискретного элемента в ИС составляет 0,8-2 мкм, а плотность их в одной ИС равна 105-106 единиц. Такие устройства, последние поколения которых называют большими (БИС) и сверхбольшими (СБИС) интегральными схемами, составляют сегодня примерно половину всех применяемых элементов электронной техники. Однако наиболее важным достижением микроэлектронных технологий стало создание микропроцессора, представляющего собой миниатюрный компьютер с вычислительной логикой и цифровой памятью, выполненный на одном кристалле БИС. Массовое производство дешевых микропроцессоров позволило резко повысить уровень качества управления техническими системами, существенно расширить потребление компьютерной техники.
Приведенные выше характеристики ИС указывают на специфический характер применяемых при их производстве процессов, методов и технологий. Главная особенность таких технологий — это высокая разрешающая способность, избирательность воздействия, обеспечивающая столь высокий уровень миниатюризации. С другой стороны, высокую избирательность процесса трудно контролировать, поэтому основной проблемой развития микроэлектронных технологий является повышение надежности. Выше уже отмечалось, что выход годной продукции в производстве сложных БИС составляет лишь несколько процентов. Вторая особенность — массовый, автоматизированный
характер технологий, обеспечивающий низкую стоимость единицы продукции
Исходным сырьем для изготовления ИС в большинстве случаев является специально очищенный полупроводниковый материал — кремний, важной особенностью которого является относительная простота получения на нем изоляционных оксидных слоев диоксида кремния. Монокристаллический слиток рафинированного кремния диаметром 50-200 мм и длиной до 2 м разрезают на отдельные пластины, на каждой из них размещают сотни ИС. После завершения изготовления ИС пластину разрезают на отдельные микросхемы, которые устанавливают в защитные корпуса, а затем тонкими золотыми проводниками присоединяют к ним выводы. За один технологический цикл обрабатывают до сотни кремниевых пластин, что позволяет получить одновременно примерно 20 000 микросхем.
Основой технологии производства ИС является формирование на поверхности кристалла транзисторных структур путем многократных итераций, каждая из которых включает стадии нанесения слоев вещества на поверхность кремния (оксид, нитрид, их модификации), фотолитографии и травления незащищенных участков поверхности (удаление слоев вещества). Упрощенные схемы такой технологии представлены на рис. 8.5.3 и 8.5.4. Главной технологической стадией, лимитирующей возможности обсуждаемой технологии, является фотолитография, которая обеспечивает заданное разрешение и позволяет получить на поверхности требуемый «рисунок».
Эта стадия состоит из следующих операций: формирование на поверхности фоторезистивного слоя (ФРС) вещества, передача требуемого изображения с фотошаблона на этот слой (экспонирование), формирование конфигурации элементов схемы с помощью маски из фоторезиста.
После получения на первой стадии «слоеной» структуры типа «субстрат (подложка)—оксид—нитрид— оксид» с помощью химических или термохимических реакций на поверхность наносится слой жидкого фоторезистивного вещества толщиной около 1 мкм и высушивается. Далее на слой фоторезиста накладывают фотошаблон с заданным рисунком и производят экспонирование с помощью источника ультрафиолетового излучения (рис. 8.5.4, «). При экспонировании необратимо изменяется растворимость фоторезистивного вещества вещества в определенных средах — проявителях. После проявления образуется рельефное изображение, соответствующее использованному фотошаблону (рис. 8.5.4, б).
Таким образом, на поверхности сформирована фо-торезистивная маска, позволяющая на дальнейших операциях избирательно травить или подвергать ионной имплантации незащищенные участки. На рис. 8.5.4, в показаны результаты травления слоя нитрида кремния после удаления фоторезиста с поверхности. В результате повторения данного технологического цикла (итерации) с использованием различных фотошаблонов
1304
Новый справочник химика и технолога
образуются многослойные интегративные структуры, формирующие микросхему.
Специфика используемых в данных технологиях физико-химических процессов накладывает свои ограничения на организацию соответствующего производства. Специальные меры предпринимаются для исключения или снижения вероятности попадания твердых микрочастиц (пыли) из атмосферы в рабочую зону. Ряд процессов производят в вакууме, для контроля и тестирования используют современные физические приборы и методики.
В заключение обратим внимание на взаимосвязь развития рассматриваемых технологий с информационными. Появление микропроцессоров породило новые поколения вычислительной техники, что инициировало развитие информационных, в частности программных технологий. Это, в свою очередь, позволило автоматизировать весьма трудоемкий процесс проектирования новых сверхсложных микропроцессоров для будущих поколений техники.
8.5.6. Энергетические технологии
Существование человечества немыслимо без получения, распределения и потребления энергии в различных ее формах: механической, тепловой, электрической, ядерной и др. Энергетика является одним из столпов экономики развитых стран. Удельное потребление энергоресурсов служит одним из показателей уровня жизни в стране. Например, в США на долю каждого гражданина приходится около 2500 кг потребляемого в год бензина, в то время как в некоторых странах Африки этот показатель равен всего нескольким десяткам килограммов.
Выше отмечалось, что те или иные процессы преобразования энергии свойственны всем технологиям. Однако в технологиях переработки вещества, информации эти процессы являются обеспечивающими, т. е. их протекание является лишь достаточным условием получения требуемого технологического результата. В энергетике используются технологии, в которых преобразо-ваниеэнергии является основной функциональной задачей, т. е. энергия выступает в качестве объекта производства.
Сформулируем функциональное содержание энергетической технологии как представление потребителю, находящемуся в заданной географической точке, требуемого количества энергии в требуемой форме, с требуемыми параметрами, в заданное время (или в соответствии с утвержденным графиком поставки во времени) и с минимально возможными удельными затратами живого и овеществленного труда.
Обобщенную маршрутную схему такой технологии можно представить следующим образом:
1. Получение первичной энергии.
2. Преобразование энергии в требуемую форму и (или) получение требуемых параметров.
3. Аккумулирование энергии.
1. Получение монокристалла кремния
I
2. Получение кремниевой пластины.
3. Наложение одного или нескольких слоев вещества (оксиды, нитриды и пр.)
I
4. Фотолитография
I
5. Травление, имплантация
I
6. Контроль (тестирование)
I
7. Разрезание пластины на отдельные микросхемы
I
8. Монтаж микросхемы в корпус.
Рис. 8.5.3. Технологический маршрут изготовления ИС
Рис. 8.5.4. Схема процесса фотолитографии
(а , б, в см. по тексту)
Основы технологии
1305
4. Передача энергии на расстояние.
5. Распределение энергии по потребителям.
Эта схема включает ряд основных стадий преобразования энергии. Энергия производится, как правило, в больших количествах, и каждая из выделенных выше стадий или их сочетание выполняется на отдельных крупномасштабных производствах (ТЭС, ГЭС, АЭС и пр.).
Энергетические технологии характеризуются набором показателей качества, к числу которых относятся:
• количество энергии, производимой в единицу времени;
• временной график производства (или потребления) энергии (суточный, декадный, месячный, сезонный);
• коэффициент, учитывающий потери энергии на отдельных стадиях или технологии в целом;
• количество одновременно обслуживаемых потребителей;
• показатели технологической надежности (вероятность прекращения подачи энергии, частота отказов, среднее время восстановления работоспособности и др.);
• показатели экологической безопасности.
Рассмотрим подробнее отдельные стадии приведенной выше схемы. Источники первичной энергии подразделяют на тепловые, гидравлические, ядерные и нетрадиционные.
Тепловые источники основаны на превращении химической энергии в тепловую при протекании экзотермических химических реакций горения органических топлив. Так, например, термохимическая реакция горения метана имеет вид:
СН4 + 2О2 = СО2 + 2Н2О + 890,5 кДж.
По оценкам, запасы органического топлива (уголь, горючие сланцы, торф, нефть, природные газы) составляют 1013 т условного топлива (топлива с теплотворной способностью 29 290 кДж/кг (7000 ккал/кг)), причем на долю твердого топлива приходится 80 %. Расчеты показали, что запасы органического топлива обеспечат жизнедеятельность всего человечества на ближайшие 250 лет.
В ядерных источниках энергии используют процесс деления ядер тяжелых элементов (уран, плутоний, торий) в результате попадания в них нейтронов и развития цепной реакции деления. Заметим, что ядерная энергия подобна химической в том смысле, что оба вида энергии проявляются в процессах превращения частиц: атомных ядер или молекул. Однако эти превращения принципиально отличны по масштабам энерговыделения: энергия ядерных превращений на шесть порядков выше, чем молекулярных. Так, 1 кг 235U энергетически эквивалентен 2,7 • 106 кг условного топлива. В настоящее время не прекращаются попытки использовать в энергетике ядерные реакции синтеза легких элементов (термоядерный управляемый синтез), хотя на сегодняшний день обозримые перспективы использования этого вида энергии проблематичны.
Гидравлические источники основаны на превращении потенциальной энергии больших масс воды
в механическую и связаны с сооружением специфических инженерных объектов — гидроэлектростанций.
Нетрадиционные, или возобновляемые, источники энергии связаны с использованием природных эффектов. Так, энергию солнца, передаваемую лучеиспусканием, можно использовать, преобразовав в тепловую, электрическую, механическую или иные формы на гелиоустановках различной конструкции. Подсчитано, что на 1 м2 поверхности Земли приходится около 0,16 кВт солнечной радиации, следовательно, для всей поверхности величина радиационного потока составляет около 1014 кВт. Установлено, что эффективное использование этой энергии могло бы удовлетворить потребности человечества в обозримом будущем.
Геотермальная энергия связана с утилизацией тепловой энергии Земли. Известно, что температура нашей планеты повышается от поверхности к центру. Если ограничить рассмотрение глубинами до 5 км, то условный расчетный запас геотермальной энергии будет эквивалентен 1014 т условного топлива, что не меньше, чем запас всех видов органических топлив. Однако технические трудности по созданию и реализации соответствующих технологий крупномасштабного использования геотермальной энергии указывают на то, что это технологии будущего.
Энергия ветра использовалась человечеством давно (ветряные мельницы), но лишь во второй половине XX в. оно всерьез приступило к решению задачи развития крупномасштабной ветроэнергетики с использованием установок мощностью до 10’ кВт. Одним из развивающихся направлений ветроэнергетики является использование энергии морских волн.
Целесообразность применения тех или иных источников энергии обосновывается технико-экономическими расчетами. Так, очевидно, что ГЭС «привязаны» к рекам, ТЭС — к источникам органического топлива, АЭС должны располагаться в малонаселенных местах в связи с экологической безопасностью, гелиоэнергетика выгодна в широтах, близких к экватору.
Стадия преобразования энергии в требуемую форму обычно организационно и технически связана с получением первичной энергии. Так, преобразование тепловой энергии в механическую осуществляется, как правило, по одной из следующих схем:
1. А. Процесс с использованием паровой турбины
2. Получение тепла за счет сжигания органического топлива в топке котла.
3. Нагрев подаваемой в котел воды для получения насыщенного пара.
4. Перегрев пара для получения требуемых его параметров (температура, давление).
5. Преобразование тепловой энергии пара в механическую энергию ротора турбины.
Б. Процесс с использованием газовой турбины
1. Получение первичного тепла за счет сгорания
топлива в рабочей камере.
1306
Новый справочник химика и технолога
2. Нагрев продуктов сгорания до температур порядка 1000 °C.
3. Преобразование тепловой энергии продуктов сгорания в кинетическую энергию потока газа.
4. Преобразование последней в механическую энергию ротора турбины.
В процессе преобразования энергии часто приходится использовать различные энергоносители для тех или иных целей. На рис. 8.5.5 представлена схема ядсрно-го реактора на быстрых нейтронах. Тепло, выделяющееся в реакторе А в результате цепной управляемой реакции деления, передается жидкому натрию, циркулирующему в контуре I, затем жидкому натрию в контуре II.
Рис. 8.5.5. Устройство АЭС с реактором на быстрых нейтронах
В контуре 111 циркулирует другой теплоноситель — вода, превращающаяся в результате фазового перехода в пар требуемых параметров. В паровой турбине Т происходит преобразование тепловой энергии в механическую, а в генераторе Г — преобразование механической энергии в электрическую. Отработанный пар конденсируется и откачивается насосом Н из конденсатора К в контур теплообмена III. Жидкий натрий слабо поглощает быстрые нейтроны, а трехконтурная схема передачи тепла предотвращает вынос продуктов радиационного распада из реактора.
Слабым звеном рассмотренной выше и большинства других схем превращения тепловой энергии в электрическую является наличие промежуточной стадии получения механической энергии. Это удорожает произ
водство энергии на ТЭС и АЭС, поэтому интенсивно проводятся работы по изысканию и применению процессов прямого преобразования тепловой энергии в электрическую.
Аккумулирование энергии является важной стадией энергетических технологий, потому что потребление энергии в течение суток подвержено резким колебаниям, а производство энергии целесообразно осуществлять на неизменном, наиболее выгодном режиме. Следовательно, необходимо промежуточное, компенсирующее звено технологической цепи.
Наиболее универсальным средством передачи энергии на большие расстояния являются линии электропередачи (ЛЭП). Их использование позволяет не только решить задачи транспортирования и распределения энергии, но и организационно-технически объединить отдельных производителей энергии в энергетические системы. Для передачи по ЛЭП электрическая энергия подвергается различным преобразованиям: повышению (понижению) напряжения, превращению переменного тока в постоянный, и наоборот. К настоящему времени разработаны перспективные проекты ЛЭП воздушного и кабельного типа, криогенных и сверхпроводящих.
Для передачи на расстояние тепла используют теплопроводы, а в качестве теплоносителей — пар и воду.
Таким образом, энергетические технологии лежат в основе жизнедеятельности человека, определяют возможность и результативность его технологической, преобразовательной деятельности в других сферах. Разработка новых энергетических технологий, новых источников энергии — глобальная задача, в значительной степени определяющая будущее человеческого общества.
По мере развития человеческого общества роль и значение технологий, технологического движения постоянно возрастает. Существует прогноз, согласно которому к концу XXI в. страны мира разделятся на четыре группы:
1) страны, производящие и поставляющие на рынок идеи, проекты, высокие технологии;
2) страны, способные производить образцы сложной техники и обладающие соответствующими технологиями;
3) страны, производящие технические объекты невысокого уровня сложности и поставляющие сырьевые ресурсы;
4) страны, поставляющие на рынок лишь дешевую рабочую силу.
Очевидно, уровень жизни в странах отдельных групп будет существенно отличаться. Вот почему в настоящее время развернулась борьба за обладание наукоемкими технологиями, контроль технологического рынка. США, Япония, Германия ушли далеко вперед в области электроники и процессов управления. Наша страна должна приложить максимум усилий для сохранения и упрочнения технологического суверенитета. В первую очередь необходимо существенно повысить
Основы технологии
1307
социальную роль технологической науки, сделать доступными и понятными накопленные общетехнологические знания.
Представления о технологии, технологическом движении пронизывают все сферы деятельности человека, лежат в основе его мировоззрения и определяют в конечном счете развитие общества. Все достижения человеческого разума рано или поздно находят концентрированное выражение в технологии, преобразовательной деятельности людей.
В наше время отраслевые технологии получили значительное теоретическое развитие, для их описания используется развитый математический аппарат, накоплены обширные базы данных и опыт проектирования и использования конкретных технологических процессов. На этом основании можно ставить вопрос о целесообразности разработки основных принципов общей (междисциплинарной) технологии, обобщенном изложении технико-технологического материала.
Обобщенная технологическая теория может стать фундаментальной частью инженерного образования. Она призвана интегрировать знания, описывающие технологические объекты, дать единое описание технологического движения, его объяснение и оценку.
Литература
1. Novikov Yu. Environmental Protection. M.: Mir Publishers, 1990. 221 p.
2. Амиров Ю.Д. Основы конструирования: творчество—стандартизация—экономика. М.: Изд-во стандартов, 1991. 392 с.
3. Андрианов Ю.М., Субетто А.И. Квалиметрия в приборостроении и машиностроении. Л.: Машиностроение, 1990. 216 с.
4. Ансеров Ю.М., Салтыков В.А., Семин В.Г. Машины и оборудование машиностроительных предприятий. М.: Политехника, 1991. 365 с.
5. Базров Б.М. Основы технологии машиностроения. М.: Машиностроение, 2005. 736 с.
6. Бондаренко А.Д. Современная технология: теория и практика. Киев: Выща шк., 1985. 171 с.
7. Волкова В.И., Денисов А.А. Основы теории систем и системного анализа. СПб.: Изд-во СПбГТУ, 1997. 510 с.
8. Джонс Дж. Методы проектирования / Пер. с англ. М.: Мир, 1986. 326 с.
9. Дорфман В.Ф. О научных основах развития технологии//Вопр. филос. 1985. № 1. С. 116-124.
10. Информатика: данные, технология, маркетинг / Под ред. А.Н. Романова. М.: Финансы и статистика, 1991. 222 с.
11. Информационные технологии в испытаниях сложных объектов: методы и средства / В.И. Скурихин, В.Г. Квачев, Ю.Р. Валькман и др. Киев: Наукова думка, 1990. 320 с.
12. Информационные технологии в университетском образовании: Сб. статей / Под ред. В.А. Садовничего. М.: Изд-во МГУ, 1991. 201 с.
13. Кардашев Г.А. Физические методы интенсификации процессов химических производств. М: Химия, 1990. 208 с.
14. Кафаров В.В., Глебов М.Б. Математическое моделирование основных процессов химических производств: Учеб, пособ. для вузов. М.: Высш, шк., 1981.400 с.
15. Каширин В.П. Философские вопросы технологии. Томск: Изд-во ТГУ, 1988. 284 с.
16. Кузичкин Н.В., Саутин С.Н., Пунин А.Е. Методы и средства автоматизированного расчета химикотехнологических систем. Л.: Химия, 1988. 150 с.
17. Моисеев Н.Н. Математические задачи системного анализа. М.: Наука, 1981.488 с.
18. Мушик Э., Мюллер П. Методы принятия технических решений / Пер. с нем. М.: Мир, 1990. 208 с.
19. Основы технологии производства летательных аппаратов /А.С. Чумадин, В.И. Ершов, В.А. Барвинок и др. М.: Наука и технологии, 2005. 912 с.
20. Основы химической технологии / Под ред. И.П. Мухленова. М.: Высш, шк., 1991. 462 с.
21. Остапчук Н.В. Основы машинного моделирования процессов пищевых производств. Киев: Вища шк., 1991. 367 с.
22. Панфилов В.А., Ураков О.А. Технологические линии пищевых производств: создание технологического потока. М.: Пищевая пром-сть, 1996. 472 с.
23. Половинкин А.И. Основы инженерного творчества: Учеб, пособ. для вузов. М.: Машиностроение, 1988. 368 с.
24. Прангишвили И.В., Пащенко Ф.Ф., Бусыгин Б.П. Системные законы и закономерности в электродинамике, природе и обществе. М.: Наука, 2001. 525 с.
25. Проектирование технологических процессов сборки машин / А.А. Жолобов, В.А. Лукашенко, И.С. Сазонов, А.Н. Рязанцев. Минск: Новое знание, 2005.410 с.
26. Процессы и аппараты химической технологии (Основы инженерной химии): Учеб, для вузов / Под ред. Н.Н. Смирнова. СПб.: Химия, 1996. 408 с.
27. Процессы механической и физико-химической обработки в производстве авиационных двигателей / А.Г. Бойцов, А.П. Ковалев, А.С. Новиков и др. М.: Изд-во МАИ, 2007. 768 с.
28. Робертсон Б. Современная физика в прикладных науках / Пер. с англ. М.: Мир, 1985. 272 с.
29. Саушкин Б.П. Проектирование технологий электрохимической обработки деталей авиационных двигателей. М.: Машиностроение, 2007. 402 с.
30. Саушкин Б.П., Лупашко А.С. Новые методы и оборудование для обработки пищевого сырья. Кишинев: Изд-во КГТУ, 1988. 90 с.
31. Саушкин Б.П., Масликов С.В., Кузенков С.Е.
Физико-химические методы модификации свойств по-
верхностного слоя деталей машин. Липецк: Изд-во
ЛГТУ, 1998. 120 с.
32. Силин С.С. Теория подобия в приложении к тех-
нологии машиностроения. Ярославль: Изд-во ЯПИ,
1989. 108 с.
1308
Новый справочник химика и технолога
33. Симоненко В.Д., Матяш Н.В. Основы технологической культуры. М.: Вентана-Графф, 2003. 176 с.
34. Сысоев В.В. Структурные и алгоритмические модели автоматизированного проектирования изделий электронной техники. Воронеж: Изд-во ВТИ, 1993. 207 с.
35. Тамм Б.Г., Пуусепп М.Э., Таваст Р.Р. Анализ и моделирование производственных систем. М.: Финансы и статистика, 1987. 191с.
36. Технологическое оборудование пищевых производств / Под ред. Б.М. Азарова. М.: Агропромиздат, 1988.462 с.
37. Технология пищевых производств / Под ред. Л.П. Ковальской. М.: Агропромиздат, 1988. 286 с.
38. Токарев В.Е. Основы технологии интеллектуальной деятельности. М.: Изд-во МАИ, 2004. 172 с.
39. Транспорт, экономика, техника: Сб. статей. М.: Знание, 1990. 63 с.
40. Транспортное обеспечение внешнеторговых операций: Коммерч, справ. СПб.: ЦНИИМФ, 1995. 430 с.
41. Управление — это наука и искусство: А. Файоль, Г. Эмерсон, Ф. Тэйлор, Г. Форд. М.: Республика, 1992. 351 с.
42. Физико-химические методы обработки в производстве газотурбинных двигателей: Учеб, пособ. / Под ред. Б.П. Саушкина. М.: Дрофа, 2002. 656 с.
43. Холодное В.В. Математическое моделирование и оптимизация химико-технологических процессов. СПб.: Профессионал, 2005. 478 с.
44. Челищев Б. Е., Боброва И.В. Автоматизация проектирования технологии в машиностроении. М.: Машиностроение, 1987. 264 с.
45. Шпур Г., Краузе Ф. Автоматизированное проектирование в машиностроении / Пер. с нем. М.: Машиностроение, 1988. 648 с.
46. Ягодин Г.А., Раков Э.Г., Третьякова Л.Г. Химия и химическая технология в решении глобальных проблем. М.: Химия, 1988. 176 с.
Раздел 9. ИНТЕЛЛЕКТУАЛЬНАЯ СОБСТВЕННОСТЬ
В конце 2006 г. Государственная дума рассмотрела и приняла во втором чтении четвертую часть Гражданского кодекса Российской Федерации. Данная часть кодекса посвящена правам на результаты интеллектуальной деятельное™ и средствам индивидуализации. Законодатель считает необходимым объединить в одном законодательном акте все действующие в настоящее время отдельные законы, относящиеся к интеллектуальной собственности. Предположительно, четвертая часть Гражданского кодекса вступит в действие в 2008 г. Несмотря на достаточно кардинальное изменение законодательства, раздел Справочника, посвященный интеллектуальной собственности, и после принятия четвертой части Гражданского кодекса полностью не потеряет своей актуальности, законодатель не предусматривает коренной ломки законодательства в данной области, а стремится к приведению его в соответствие с требованиями времени и международного законодательства.
9.1. Что такое интеллектуальная собственность
9.1.1. Основные понятия
Конституция Российской Федерации (ст. 44) [ 1 ] гарантирует каждому гражданину свободу литературного, художественного, научного, технического и других видов творчества. Созданная интеллектуальная собственность охраняется законом.
Не только в России, но и во всем мире считается, что интеллектуальная собственность является результатом творческой деятельности. Конвенция об учреждении Всемирной организации интеллектуальной собственности (ВОИС), принятая в 1967 г., предусматривает следующие объекты интеллектуальной собственности [2]:
- литературные, художественные произведения и научные труды;
- исполнительская деятельность артистов, фонограммы и передачи радио и телевидения;
- изобретения;
- научные открытия;
- промышленные образцы;
- товарные знаки, знаки обслуживания, фирменные наименования и обозначения;
— пресечение недобросовестной конкуренции.
Автор-составитель: к. т. н А.М. Марков
Гражданский кодекс Российской Федерации (ст. 138) дает такое определение интеллектуальной собственности:
«В случаях и в порядке, установленных настоящим Кодексом и другими законами1, признается исключительное право (интеллектуальная собственность) гражданина или юридического лица на результаты интеллектуальной деятельности и приравненные к ним средства индивидуализации юридического лица, индивидуализации продукции, выполняемых работ или услуг (фирменное наименование, товарный знак, знак обслуживания и т. п.).
Использование результатов интеллектуальной деятельности и средств индивидуализации, которые являются объектом исключительных прав, может осуществляться третьими лицами только с согласия правообладателя ».
Данное определение является более узким, чем определение, принятое вышеупомянутой Конвенцией, т. к. в нем говорится только об исключительных правах на результаты интеллектуальной (творческой) деятельности. Поэтому в России считается неправомерным относить к интеллектуальной собственности научные открытия, фирменные наименования, а также пресечение недобросовестной конкуренции. Впрочем, научные открытия не охраняются практически нигде в мире. В России недобросовестная конкуренция регулируется законом «О конкуренции и ограничении монополистической деятельности на товарных рынках».
Обратим внимание на то, что понятие «интеллектуальная собственность» является обобщающим и его роль сводится к обозначению объектов, которые не относятся к сфере материальных. Поэтому, когда речь идет об интеллектуальной собственности, то имеются в виду права на результаты творческой деятельности, в том числе права на использование этих результатов,
1 С законами, определяющими права на отдельные объек-
ты интеллектуальной собственности, мы познакомимся ниже.
1310
Новый справочник химика и технолога
в частности на выпуск в свет литературного произведения, а не права на материальные вещи: книги, аудио-и видеодиски, оборудование, созданное на основе изобретений и других объектов интеллектуальной собственности.
Достаточно часто встречаестя термин «промышленная собственность», к которой обычно относят:
- изобретения;
- полезные модели;
- промышленные образцы;
- товарные знаки, знаки обслуживания;
- фирменные наименования;
- наименования мест происхождения товаров;
- пресечение недобросовестной конкуренции.
9.1.2. Законы Российской Федерации, определяющие правоотношения в области интеллектуальной собственности, и международные соглашения
Основные законы, касающиеся интеллектуальной собственности, действующие в Российской Федерации:
1. Патентный закон № 3518-1 от 23 сентября 1992 г. (в ред. от 7 февраля 2003 г., № 22-ФЗ).
2. «Об авторском праве и смежных правах» № 5351-1 от 9 июля 1993 г. (в ред. от 20 июля 2004 г., № 72-ФЗ).
3. «О правовой охране программ для электронных вычислительных машин и баз данных» № 3523-1 от 23 сентября 1992 г. (в ред. от 24 декабря 2002, № 177-ФЗ).
4. «О товарных знаках, знаках обслуживания и наименованиях мест происхождения товаров» № 3520-1 от 23 сентября 1992 г. (в ред. от 24 декабря 2002 г., № 176-ФЗ).
5. «О правовой охране топологий интегральных микросхем» № 3526-1 от 23 сентября 1992 г. (в ред. от 9 июля 2002 г., № 82-ФЗ).
6. «О селекционных достижениях» № 5605-1 от 6 августа 1993 г.
7. «О коммерческой тайне» № 98-ФЗ от 29 июля 2004 г.
8. «О конкуренции и О1раничении монополисгиче-ской деятельности на товарных рынках» № 948-1 от 22 марта 1991 г. (в ред. от 7 марта 2005 г., № 13-ФЗ).
9. Гражданский кодекс РФ, Ч. 1, 30 ноября 1994 г., № 51-ФЗ (в ред. от 30 декабря 2004 г., № 217-ФЗ).
10. Гражданский кодекс РФ, Ч. 2, 26 января 1996 г., № 14-ФЗ (в ред. от 8 июля 2005 г., № 89-ФЗ).
Основные международные соглашения, в которых участвует Российская Федерация:
1. Парижская конвенция об охране промышленной собственности от 20 марта 1883 г. (изменена 2 октября 1979 г.).
2. Бернская конвенция об охране литературных и художественных произведений от 9 сентября 1886 г. (изменена 2 октября 1979 г.).
3. Всемирная конвенция об авторском праве, подписаная в Женеве 6 сентября 1952 г.
4. Конвенция «Об охране интересов производителей фонограмм от незаконного воспроизводства их фонограмм» от 29 октября 1971 г.
5. Конвенция об учреждении Всемирной организации интеллектуальной собственности, подписаная в Стокгольме 14 июля 1967 г. (изменена 2 октября 1979 г.).
6. Ниццкое соглашение о международной классификации товаров и услуг для регистрации знаков от 15 июня 1957 г. (изменено 28 сентября 1979 г.).
7. Договор о патентной кооперации (РСТ).
8. Евразийская патентная конвенция.
9.1.3. Интеллектуальная собственность как фактор научно-технического прогресса
Интеллектуальная собственность охватывает все стороны человеческой деятельности и играет значительную роль в развитии человеческого общества. Приведем характерное высказывание президента отделения полупроводников фирмы «Texas Instruments» Уильяма Пата Уэбера: «По существу защита интеллектуальной собственности является императивом для выживания как крупных, так и мелких компаний, а также для разработки следующего поколения технологий.
Защита интеллектуальной собственности стоит как часовой у входа в здание научно-технического прогресса. Без нее ни у одной из компаний не будет уверенности в том, что она сможет защитить свои изобретения от нарушителей. Обладая ею, компании получают возможности добиваться справедливого и адекватного дохода на свои дорогостоящие капиталовложения либо путем устранения с рынка конкурентов, либо путем получения отчислений от тех из них, которые пользуются их запатентованными технологиями. Ключевым фактором в этой схеме является то, что доходы по обеим этим статьям генерируют доллары, которые можно реинвестировать в завтрашние НИОКР».
Важнейшими объектами интеллектуальной собственности традиционно считаются изобретения. Патентование изобретений в области химии и фармацевтической промышленности позволяет вести дальнейшие дорогостоящие научные исследования, получать новые вещества, материалы, фармацевтические препараты.
В настоящее время все большее значение приобретают новые объекты интеллектуальной собственности: биотехнологии, разработки в области информационных цифровых технологий, программ для ЭВМ.
Дерево интеллектуальной собственности зеленое, оно растет и развивается в различных областях творчества. Ключевой фигурой в творческом процессе является ученый, инженер, изобретатель. Защита интеллектуальной собственности — это защита интересов не только юридических лиц, но и людей, вносящих свой вклад в развитие научно-технического прогресса.
Интеллектуальная собственность
1311
9.1.4. Основные системы защиты результатов творческой деятельности
Авторское и патентное право образуют две основные системы охраны результатов творческой деятельности. Термин «авторское право» не следует путать с термином «права автора». Объектами авторского права являются произведения литературы, искусства, науки, а к объектам патентного права относятся прежде всего изобретения, полезные модели, промышленные образцы, товарные знаки. Права же автора существуют как в патентном, так и в авторском праве.
Рассмотрим главные отличительные черты этих двух систем.
Патентное право для обестечения охраны предусматривает:
- подачу заявки на получение охранного документа в Государственное патентное ведомство;
- проведение экспертизы по критериям, установленным законодательством;
- выдачу охранного документа — патента от имени государства.
Патент охраняет суть решения. Например, в качестве изобретений и полезных моделей охраняются конструктивные решения, т. е. сама суть технического решения.
Патентная охрана действует только на территории государства, которое выдало патент, или на территории, где действует региональный патент2, и имеет достаточно жесткие ограничения по срокам действия. Например, патент на изобретение действует максимум двадцать лет.
Авторское право для обеспечения охраны, как правило, не предусматривает подачи заявки на регистрацию объекта, его регистрации и выдачи охранного документа.
Авторское право охраняет только форму произведения, суть же его (идеи, методы, способы и факты) не охраняется. Срок охраны авторского права (при жизни автора и в течение 50 лет после его смерти) более длительный по сравнению с патентным правом, а территория, где произведение получает охрану, шире в силу действия международных соглашений.
Чтобы суть различий стала понятнее, рассмотрим следующий пример.
Изобретатель создал новый состав вещества и описал это вещество и способ его получения в научной статье. Научная статья относится к объектам, охраняемым авторским правом (как произведение науки и одновременно произведение литературы). Если кто-то возьмет текст этой статьи и опубликует
2 Региональные патенты — патенты, которые выдаются на основании соглашений между несколькими странами о выдаче одного патента, как правило, действующего в странах-участницах соглашения как национальный патент. О выдаче региональных патентов, например Европейского и Евразийского патентов, речь пойдет ниже.
его в другом издании без разрешения или под своим именем, он нарушит авторское право.
Но предприниматель, прочитавший статью, может, использовав эту информацию, начать выпуск данного вещества на своем предприятии, причем тем же способом, не испрашивая разрешения изобретателя. И он не нарушит авторского права, потому что оно защищает только форму, в данном случае письменную форму, в которой изложены сведения о данном изобретении, а не суть технического решения.
Для защиты от использования другими лицами состава нового вещества и способа его получения изобретателю необходимо получить патент на эти изобретения, тогда никто без его разрешения будет не вправе выпускать это вещество.
Авторское право обеспечивает защиту объектов, для которых форма имеет определяющее значение. Например, для произведений художественной литературы, музыки, программ для ЭВМ. Ведь если в программе для ЭВМ заменить один оператор другим или поменять их местами, программа работать не будет. Именно поэтому предоставляемая авторским правом защита для таких объектов чаще всего достаточна. Произведениям, для которых содержание важнее их формы, авторское право не может предоставить достаточную защиту. В этом случае, если это возможно с точки зрения законодательства, следует обратиться к патентной охране.
При определении нарушения прав на объект, охраняемый авторским правом, например на литературное произведение, эксперты проводят исследование текстуальных совпадений в контрафактном произведении и источнике, не обращая внимания на сюжет и идею произведения. При нарушении патентного права исследуется вопрос использования самого решения.
Как патентное, так и авторское право предусматривают исключительные права на объекты охраны. Суть исключительных прав состоит в том, что никто не может использовать объект без разрешения правообладателя. В ходе дальнейшего изложения будут рассмотрены конкретные механизмы действия авторского и патентного права.
Наряду с авторским и патентным правом для охраны результатов творческой деятельности используются и другие правовые механизмы. Например, защита с помощью коммерческой и служебной тайны (ноу-хау), пресечение недобросовестной конкуренции.
9.1.5. История возникновения и развития права на товарный знак, изобретение и произведения авторского права
Охрана объектов интеллектуальной собственности возникла очень давно, и ее развитие и совершенствование продолжаются непрерывно.
Товарные знаки имеют наиболее долгую историю. Они появились еще в древности у скотоводческих племен и служили для клеймения животных, чтобы владельцы могли легко отличать их даже в общем стаде. Изготовители гончарных изделий отмечали их знаками, иногда это был просто отпечаток пальца. В Средние
1312
Новый справочник химика и технолога
века появились знаки гильдии, которыми помечали товары, выпущенные тем или иным сообществом мастеровых людей. Закон о регистрации торговых знаков был принят в Британии 13 августа 1875 г. Интересно, что первый зарегистрированный здесь товарный знак — красный треугольник, который компания «Басс & К0» собиралась ставить на бутылки с элем, — действует до сих пор [3]. Законодательство об охране товарных знаков в его современной форме возникло также в XIX в.
Русский правительственный указ об обязательном клеймении товаров особыми фабричными знаками вышел в 1774 г. Законом 1830 г. были введены достаточно точные правила и способы клеймения. По закону 1896 г. свидетельство на товарный знак выдавалось отделом торговли Министерства финансов, что предоставляло правообладателю возможность защиты от подделки.
Изобретения, как правило, охраняются с помощью патентов. Термин «патент» применялся, в частности, королевской (и царской) властью с целью выдачи различных привилегий, в том числе в области торговли и промышленности.
Начиная с времен правления английской королевы Елизаветы I, в XVI в. королевской властью предоставлялись особые привилегии лицам, создававшим новые отрасли промышленности, которые были основаны на импортных технологиях, путем пожалования исключительного права. Такие временные права назывались Letters Patent [4]. Следует отметить, что предусматривалось публичное объявление о пожалованных правах. Раскрытие сущности патента для широкой общественности и сейчас составляет один из главных и важнейших принципов патентной системы.
Постепенно количество привилегий, связанных с введением новых технологий, росло, но выдача их королем по его усмотрению тормозила развитие промышленности. Одним из важных шагов в становлении патентной системы стал переход в выдаче патентов не от имени короля, а от имени государства. Если изобретение отвечало требованиям, предъявляемым к изобретению, то выдавался патент. В Великобритании в 1628 г. был введен статус о монополиях: все монополии не имели юридической силы, кроме патентных грамот, выдаваемых на определенный срок первому изобретателю. В дальнейшем патентная система прошла большой путь от системы первого изобретателя к системе первого заявителя. Первоначально патенты выдавались тому, кто изобрел что-либо и мог доказать это. Сейчас практически в любой стране мира патент выдается тому, кто первый подал заявку на изобретение.
В дальнейшем появились другие объекты, на которые стали выдаваться патенты: полезные модели, промышленные образцы.
История правовой охраны изобретений в России началась с Манифеста «О привилегиях на разные изобретения и открытия в художествах и ремеслах» Алексан
дра I, вышедшего 17 июня 1812 г., практически во время вторжения войск Наполеона в Россию.
В дальнейшем патентное право развивалось достаточно динамично. В 1896 г. с принятием «Положения о привилегиях на изобретения и усовершенствования» сформировались основы патентной системы в России, при этом патент на изобретение действовал 15 лет.
В советское время патентная система была практически разрушена, изобретения были объявлены достоянием государства. После Великой Отечественной войны, в 1959 г., вышло «Положение об открытиях, изобретениях и рационализаторских предложениях», согласно которому изобретения охранялись в основном авторскими свидетельствами, причем исключительное право на изобретения принадлежало государству. Несмотря на отчуждение прав на изобретения от предприятий и организаций, Положение оказало большое влияние на развитие изобретательства и подготовку патентных кадров в нашей стране.
С принятием в 1991 г. законов «Об изобретениях в СССР» и «О промышленных образцах», а в 1992 г. Патентного закона Российской Федерации в России возродилась патентная система в ее современном понимании. В настоящее время действует вторая редакция Патентного закона РФ, принятая в 2003 г.
Копирайт — это транслитерация английского слова «copyright», что в переводе означает «авторское право». Идея охраны авторского права зародилась только с изобретением книгопечатания. До этого переписка книг была трудным и дорогим делом, а печатный станок резко удешевил процесс копирования произведений литературы. Защита от продавцов незаконных копий также пошла по пути выдачи королевских привилегий. К концу XVII в. все громче стали раздававаться голоса авторов, требовавших предоставления им прав распоряжаться своими произведениями. В Англии был принят первый закон об авторском праве, известный как Статут королевы Анны. Суть закона ясна из его названия — «О поощрении образования путем закрепления за авторами или приобретателями копий печатных книг прав на последние на время, устанавливаемое отныне».
Первоначально авторское право во всех странах действовало сравнительно короткий срок и распространялось только на произведения литературы. В дальнейшем срок действия авторского права увеличился, и оно стало распространяться на все большее число произведений. В настоящее время идут жаркие дискуссии по вопросам совершенствования механизмов действия авторского права в связи с возникновением новых способов хранения, копирования и передачи произведений.
История развития авторского права в России нераз-
рывно связана с личностью А.С. Пушкина, т. к. именно
он содействовал появлению на свет проекта закона,
который разработал его друг В.Ф. Одоевский [5]. Нель-
зя сказать, что этот закон отводил первое
место автору. «Положение о правах сочинителей» было
помещено в виде приложения к новому цензурному
Интеллектуальная собственность
1313
уставу и устанавливало довольно куцые права, которые через два года пришлось уточнять и развивать. Но это Положение оказало достаточно большое влияние на жизнь литературного и книгоиздательского общества.
Советское время характеризовалось достаточно жесткой регламентацией отношений между авторами и издателями со стороны государства, ведь издательства были государственными учреждениями. С принятием в 1993 г. закона Российской Федерации «Об авторском праве и смежных правах» авторское право в нашей стране находится на вполне современном уровене, охватывает новые объекты, например программы для ЭВМ и современные средства распространения произведений.
Развитие международных отношений способствовало, с одной стороны, унификации национальных законов в области интеллектуальной собственности, а с другой — созданию механизмов, позволяющих произведениям получать охрану в других странах.
9.2. Промышленная собственность
9.2.1. Патент
Термин «патент» имеет два значения: первое — собственно охранный документ и второе — защита, предоставляемая охранным документом. Главное — это те права, которые дает патент3 и которые содержаться в исключительном праве на изобретение, полезную модель или промышленный образец4. Приведем примеры титульных листов патента Российской Федерации (рис. 9.1) и патента СССР (рис. 9.2), которые продолжают действовать в нашей стране.
Полезно сравнить права, которые предоставляются патентом Российской Федерации, с правами, которые предоставлялись по авторскому свидетельству СССР5. По авторскому свидетельству, исключительное право на использование изобретения принадлежало государству, и государственные предприятия могли использовать изобретение бесплатно. Не обладая исключительным правом, предприятия не были заинтересованы в использовании изобретений, к этому их понуждали с помощью административных мер. Авторам от имени государства предоставлялось право на вознаграждение при использовании изобретений, а авторам служебных изобретений также право на поощрительное вознаграждение.
3 Здесь и в дальнейшем речь идет о законодательстве Российской Федерации.
4 Далее термины «изобретение», «полезная модель» и «промышленный образец» иногда будут заменены термином «объект».
Авторские свидетельства СССР, у которых не истек 20-летний срок с даты подачи заявки, могут быть преобразованы в патент РФ на оставшийся срок согласно Правилам подачи и рассмотрения ходатайств о прекращении действия на территории РФ авторских свидетельств СССР на изобретения, свидетельств СССР на промышленные образцы, патентов СССР и выдачи патентов РФ на оставшийся срок (в ред. Приказа Роспатента от 30 октября 1996 г., № 125).
ж »л о lie гпзлй г
X» 2146029
f'Xvx > . г < ->х к к-л>.лм !<•> fJd-x.x
1 <. > *4 х х г » sxtKrws '•« ц>>*.
< В< ШИЛ MW»» i tlBKWOFA ВАГА (ЙАПШИМ)
xxtfvxcft'xvx Р-х-<as:
Рис. 9.1. Пример патента на изобретение, принятого в Российской Федерации
ОШ ««МЙЛ» ЖЖЖ
sew® s« «жшивйю » «лкй
< t"
S
BitSjXKS Si
Рис. 9.2. Пример патента на изобретение, принятого
в Союзе Советских Социалистических Республик
1314
Новый справочник химика и технолога
9.2.1.1. Исключительное право
По законодательству Российской Федерации [6], никто не вправе без разрешения патентообладателя использовать запатентованное изобретение, полезную модель или промышленный образец, в том числе совершать следующие действия: ввозить на территорию РФ, изготовлять, применять, делать предложение о продаже, продавать, иначе вводить в гражданский оборот или хранить для этих целей продукт, в котором использован запатентованный объект, и осуществлять способ, в котором используется запатентованное изобретение.
Нарушением исключительного права патентообладателя считается также осуществление всех действий, перечисленных ранее, в отношении продукта, полученного запатентованным способом. Это положение особенно важно для новых химических веществ, полученных каким-либо новым способом. Владельцу патента на способ не нужно доказывать, что вещество получено его способом, бремя доказательства обратного лежит на ответчике6.
Патентообладатель имеет монополию, которая действует только на территории страны, где выдан патент, и действует сравнительно короткое время7.
Герой Марка Твена в романе «Янки при дворе короля Артура» говорил: «Страна, не имеющая патентной системы, подобна раку, который может двигаться только вбок или назад». Не слишком ли сильно сказано? Если какая-то фирма, небольшая или крупная, создала новый, привлекательный для потребителя продукт, вложив в его создание талант своих изобретателей и затратив немалые средства, что мешает конкурентам повторить его, скопировав и при этом не затратив средств на его разработку? Только патентная система. Без патентов не было бы возможности создавать новое, выводить новый продукт на рынок, возвращать затраченные средства.
Система патентования в современном мире стимулирует создание новых технологий, обеспечивает условия для их успешного промышленного применения, служит инструментом технического планирования и стратегии, поощряет инвестиции.
Наличие патентной охраны способствует процессам передачи технологий и обмена ими, что обеспечивает развитие промышленности в мире.
Исключительное право — достаточно серьезный рычаг, действующий в предпринимательской сфере. Чтобы у патентообладателя не возникало соблазна использовать это право только для запрещения выпуска изобретенной им и нужной обществу продукции дру
6 Часто это положение закона называют косвенной охраной вещества через способ его получения.
7 В большинстве стран патент на изобретение действует максимум 20 лет, с некоторыми оговорками в отношении лекарственных средств, пестицидов и агрохимикатов.
гим лицам, а самому не предпринимать усилий по ее выпуску, патентная система имеет различные механизмы, чтобы сгладить негативные последствия монополии. О некоторых механизмах, в частности о принудительной лицензии, речь пойдет ниже, здесь же обратим внимание на следующее. Выдача патента всегда предусматривает публикацию материалов о сущности патентных прав, причем эти материалы раскрывают суть объекта настолько, чтобы средний специалист мог использовать его. Благодаря этому конкуренты патентообладателя и весь мир изобретателей могут делать следующие шаги в творчестве, учитывая новую информацию. Необходимо отметить, что патентное законодательство ведущих стран мира предусматривает публикацию материалов о содержании не только выданных патентов, но и поданных патентных заявок на изобретения через 18 месяцев после их подачи.
Патент также удостоверяет приоритет и авторство.
Патент может продаваться, и в этом случае говорят об уступке патента, о переходе патента от одного патентообладателя к другому. Может выдаваться разрешение на использование прав, связанных с запатентованными изобретениями, промышленными образцами, полезными моделями, тогда речь идет о лицензии. Чаще всего в практике встречаются простые и исключительные лицензии. Простая лицензия предусматривает, что владелец патента может выдать столько лицензий, сколько посчитает нужным. Исключительная лицензия предусматривает предоставление прав на использование одному лицу. Далее более подробно будет рассмотрен вопрос о передаче прав.
9.2.1.2. Приоритет
Понятие «приоритет» — одно из самых сложных в патентном праве. В простейшем случае это дата подачи первой заявки в стране происхождения8 объекта на данное изобретение9. Как мы уже знаем, первоначально в патентном праве использовалась система не первого заявителя, а первого изобретателя. В настоящее время во всех развитых странах применяется система первого заявителя. Она состоит в том, что изобретатель (или лицо, имеющее право на подачу заявки10), подавший заявку первым, получит патент вне зависимости от того, является ли он автором этого изобретения или нет. При этом учитывается день подачи заявки, а в некоторых странах и время ее подачи.
8 Сложность понятия «приоритет» заключается в том, что приоритет может быть установлен по дате подачи заявки, поданной в другой стране (так называемый «конвенционный приоритет») или по дате подачи дополнительных материалов, других, более ранних заявок и т. д.
9 Полезную модель, промышленный образец.
10 тт
На подачу заявки имеет право лицо, которому автор передал право на получение патента, или, в случае служебных изобретений, что будет рассмотрено ниже, работодатель, с которым автор состоит в трудовых отношениях.
Интеллектуальная собственность
1315
9.2.1.3. Автор
Автором изобретения11 12 признается физическое лицо, чьим творческим трудом создан объект. Если в его создании принимали участие несколько лиц, они считаются соавторами, а права между ними распределяются по соглашению между участниками. Не признаются авторами лица, не внесшие личного творческого вклада в создание объекта, оказавшие автору только техническую, организационную или материальную помощь либо только способствовавшие оформлению прав на него и его использованию. Определение авторов изобретения является их, авторов, гражданским делом. Никто посторонний, в том числе и в случае служебных изобретений, не может вмешиваться в определение состава авторов. Принуждение к соавторству является уголовно наказуемым преступлением. Право авторства относится к личным правам, является неотчуждаемым и охраняется бессрочно.
Автор является ключевой фигурой в создании объектов, на которые далее получаются патенты. Именно из права авторства вытекает главное право — право на получение патента, право быть патентообладателем.
9.2.1.4. Патентообладатель
В Российской Федерации право на получение патента имеют:
- автор изобретения, полезной модели или промышленного образца;
- работодатель, когда речь идет о служебном изобретении, полезной модели или промышленном образце;
- правопреемники указанных лиц.
Рассмотрим последовательно все указанные случаи.
Автор может получить патент на свое имя или передать это право любому физическому или юридическому лицу.
Т. к. закон под термином «автор» имеет в виду всех авторов созданного объекта, патент может быть выдан 12 на имя всех авторов или на имя одного . Следует сразу заметить, что в любом случае уступки своих прав автор должен заключить соглашение с той стороной, которой уступаются права. Иногда задают вопрос, а как лучше: самому получить патент или передать это право другому лицу? Естественно, готового рецепта в этом деле не существует. Есть один совет — поступать так, как лучше для судьбы самого изобретения. Авторы сами должны принять решение.
Патент на изобретение, полезную модель, промышленный образец и право на его получение переходят по наследству.
Служебные изобретения, полезные модели, промышленные образцы
В Патентном законе [6] сказано:
«Право на получение патента на изобретение, полезную модель или промышленный образец, созданные
работником (автором) в связи с выполнением своих трудовых обязанностей или конкретного задания работодателя (служебное изобретение, служебная полезная модель, служебный промышленный образец), принадлежит работодателю, если договором между ним и работником (автором) не предусмотрено иное».
Данная формулировка нуждается в пояснениях.
Первое условие, необходимое для признания объекта служебным, заключается в том, что отношения между автором и работодателем должны быть трудовыми. Автор должен работать по трудовому контракту в организации (фирме), т. е. выполнять у работодателя трудовые обязанности13. Не следует путать с трудовым контрактом договор подряда, который относится к гражданско-правовым договорам и регулируется совсем другим документом — Гражданским кодексом РФ. При выполнении работ по договору подряда право на получение патента переходит к заказчику14 только в том случае, если это прямо указано в договоре. Если прямого указания нет, право на получение патента сохраняется за автором15.
Второе условие заключается в том, что объект должен быть создан в результате выполнения работником своих трудовых обязанностей или конкретного задания работодателя. Если в трудовые обязанности работника не входило создание объекта, который может быть защищен патентом, или он создал его вне конкретного служебного задания, не выполняя служебных обязанностей, связанных с его созданием, то право на получение патента принадлежит ему как автору.
Процитируем следующую норму закона, относящуюся к служебным объектам.
«В случае если работодатель в течение четырех месяцев с даты уведомления его работником (автором) о полученном им результате, способном к правовой охране в качестве изобретения, полезной модели или промышленного образца, не подаст заявку на выдачу патента на эти изобретение, полезную модель или промышленный образец в федеральный орган исполнительной власти по интеллектуальной собственности, не передаст право на получение патента на служебное изобретение, служебную полезную модель или служебный промышленный образец другому лицу и не сообщит работнику (автору) о сохранении информации о соответствующем результате в тайне, право на получение патента на такие изобретение, полезную модель или промышленный образец принадлежит работнику (автору)».
В обязанности работника входит уведомить работодателя о созданном объекте, на который может быть
13 Перечень признаков трудовых отношений между работ-
ником и работодателем приведен в Трудовом кодексе РФ.
14 Заказчик — тот, кто заказывает работы по договору
подряда.
15 Следует отметить, что практически такое же положение
существует в авторском праве.
11 Полезной модели, промышленного образца.
12 Выдается одна патентная грамота независимо от числа
патентообладателей.
1316
Новый справочник химика и технолога
получен патент. Такое уведомление, с общепринятой точки зрения, должно быть подано работником в письменном виде. Если работодатель в течение четырех месяцев не выполнит действия, предусмотренные законом, в частности не подаст заявку или не предупредит работника о сохранении информации о результате в тайне, не совершит других действий, предусмотренных законом, то право на получение патента будет иметь автор.
Патентный закон [6] предусматривает право автора служебного произведения на вознаграждение. Размер вознаграждения и порядок его выплаты определяются договором между работником (автором) и работодателем.
Если патент на служебное изобретение, полезную модель или промышленный образец получит автор, работодатель в течение срока действия патента имеет право на их использование в собственном производстве с выплатой патентообладателю компенсации, определяемой на основе договора.
Объекты, созданные при выполнении работ по государственному контракту
Новыми в нашем патентном законодательстве являются положения закона, связанные с правами на изобретение, полезную модель и промышленный образец, созданные при выполнении работ по государственному контракту.
Право на получение патента принадлежит исполнителю, если государственным контрактом не установлено, что это право принадлежит Российской Федерации или субъекту Российской Федерации, от имени которых выступает государственный заказчик.
Государственный заказчик может подать заявку на выдачу патента в течение шести месяцев с момента его уведомления в письменной форме исполнителем о получении результата, способного к правовой охране в качестве изобретения, полезной модели или промышленного образца. Если в течение указанного срока государственный заказчик не подаст заявку, право на получение патента будет иметь исполнитель.
Если патент получен исполнителем, по требованию государственного заказчика он обязан предоставлять указанному им лицу (лицам) неисключительную безвозмездную лицензию на использование в целях выполнения работ или осуществления поставок продукции для федеральных государственных нужд или нужд субъекта Российской Федерации.
9.2.1.5. Секретные изобретения
На секретные изобретения с 1 января 2004 г. может быть получен патент. Как известно, сведения, составляющие государственную тайну, относятся к секретным, и отношения, возникающие в связи с отнесением сведений к государственной тайне, их засекречиванием или рассекречиванием, регулируются законом «О госу
дарственной тайне»16. Патентный закон устанавливает, что заявки на секретные изобретения подаются в уполномоченные государством органы исполнительной власти или в Роспатент.
Рассмотрение заявок на секретные изобретения производится по тем же правилам и критериям, что и на несекретные изобретения. Использование запатентованного секретного изобретения, уступка патента секретного изобретения и предоставление права на его использование другим лицам осуществляются с соблюдением закона «О государственной тайне».
Если изобретение, на которое выдан патент, будет рассекречено, в дальнейшем этот патент будет участвовать в гражданском обороте наравне с обычными патентами.
9.2.1.6. Ограничения исключительного права патентообладателя
По Патентному закону РФ [6], не признаются нарушением исключительного права патентообладателя:
- применение продукта или изделия, в котором использованы патенты, в конструкции, во вспомогательном оборудовании или при эксплуатации 'гранспортных средств иностранных государств (водного, воздушного, автомобильного и железнодорожного транспорта и космической техники), если они временно или случайно находятся на территории РФ;
- проведение научного исследования или эксперимента над продуктом, способом или изделием;
- использование запатентованного изобретения, полезной модели или промышленного образца при чрезвычайных обстоятельствах;
- использование изобретения, полезной модели или промышленного образца для удовлетворения личных, семейных, домашних нужд;
- разовое изготовление в аптеках по рецептам врачей лекарственных средств с использованием запатентованного изобретения;
- если продукт или изделие ранее были введены в гражданский оборот на территории РФ патентообладателем или иным лицом с разрешения патентообладателя17.
Рассмотрим, в частности, вопрос о проведении научного исследования и эксперимента. Это ограничение патентных прав введено прежде всего для удовлетворения потребности общества в новых разработках, товарах.
Последний пункт перечня также следует пояснить. Если патентообладатель произвел продукцию, в которой
16 Закон «О государственной тайне» (в редакции феде-
ральных законов от 06 октября 1997 г., № 131—ФЗ, от 30 июня 2003 г., № 86-ФЗ).
17 Данный перечень не является полностью идентичным
перечню, приведенному в законе. Здесь и далее не ставится
задача текстуального повторения закона, иначе, с точки зре-
ния автора, снизится уровень понимания главных его поло-
жений. При применении Патентного закона на практике сле-
дует обращаться к его тексту.
Интеллектуальная собственность
1317
используется запатентованный объект, и ввел его в гражданский оборот, например продал произведенную партию продукта, то далее этот продукт может продаваться, перепродаваться уже без согласия патентообладателя, т. к. его патентные права исчерпаны в момент введения продукта в оборот. Наступает так называемое исчерпание прав.
Принудительная лицензия
Механизм принудительной лицензии предназначен для ограничения прав обладателя патента в тех случаях, когда изобретение, полезная модель, промышленный образец не используются или недостаточно используются, что приводит к недостаточному предложению соответствующих товаров или услуг на товарном рынке или рынке услуг. Тогда у лица, желающего использовать это изобретение, при отказе патентообладателя от заключения с этим лицом лицензионного договора на условиях, соответствующих установившейся практике, возникает право обратиться в суд с иском к патентообладателю о предоставлении принудительной неисключительной лицензии на его использование.
В случае если патентообладатель не может доказать, что неиспользование или недостаточное использование патента обусловлено уважительными причинами, суд принимает решение о предоставлении указанной лицензии и об условиях ее предоставления. Суммарный размер платежей должен быть установлен не ниже, чем цена лицензии, обычно определяемая при сравнимых обстоятельствах. Действие принудительной лицензии может быть прекращено в судебном порядке, если причины, обусловившие се предоставление, перестанут существовать.
Принудительная лицензия может быть предоставлена и в случае, если обладатель патента не может его использовать, не нарушая при этом прав обладателя другого патента, отказавшегося от заключения лицензионного договора на условиях, соответствующих установившейся практике.
Принудительная лицензия широко используется в мире, особенно там, где существует жесткая конкуренция на рынке.
Право преждепользования
Любое лицо, которое до даты приоритета добросовестно использовало созданное независимо от автора запатентованного изобретения, полезной модели, промышленного образца тождественное решение или сделало необходимые к этому приготовления, сохраняет право на дальнейшее его безвозмездное использование без расширения объема такого использования.
Право преждепользования может быть передано другому лицу только совместно с производством, на котором имело место использование тождественного решения или были сделаны необходимые к этому приготовления.
Право преждепользования защищает права тех лиц, которые самостоятельно создали объект, на который
другое лицо позже получило патент, но сами по каким-то причинам не захотели его патентовать или подали заявку позже, но при этом стали выпускать продукцию или готовить ее производство. В интересах общества разрешить им дальнейшее производство, т. к. важно поддерживать добросовестного производителя, даже в ущерб монополии патентообладателя. Право преждепользования не распространяется на тех лиц, которые, создав изобретение раньше патентообладателя, не начали производить продукцию до даты приоритета.
Право послепользования
Действие патента на изобретение, полезную модель или промышленный образец, которое было прекращено в связи с тем, что ежегодная патентная пошлина за поддержание патента в силе не была уплачена в установленный срок, может быть восстановлено. Ходатайство должно быть подано в течение трех лет с даты истечения срока уплаты указанной патентной пошлины, но до истечения установленного срока действия патента.
Любое лицо, которое в период между датой прекращения действия патента на изобретение, полезную модель или промышленный образец и датой публикации в официальном бюллетене сведений о восстановлении действия патента начало использовать запатентованный объект либо сделало в указанный период необходимые приготовления к этому, сохраняет право на дальнейшее безвозмездное использование его без расширения объема такого использования.
9.2.1.7. Передача прав, связанных с изобретением, полезной моделью или промышленным образцом
Начиная с момента создания объекта промышленной собственности, охраняемого патентом, у автора (для служебных объектов — у работодателя) возникает право на подачу заявки. В период с даты приоритета до даты получения патента у заявителя есть право на получение патента. С даты выдачи патента появляется ряд имущественных исключительных прав. Все эти права могут участвовать в гражданском обороте [7].
Передача прав до подачи заявки
До подачи заявки на изобретение, полезную модель или промышленный образец достаточно часто авторы сталкиваются с такой проблемой, как принятие решения — кто будет патентообладателем. Им могут быть автор, все авторы, один из них или любое физическое или юридическое лицо, которому автор (авторы) передаст право на получение патента.
Рассмотрим случай, когда все авторы хотят быть патентообладателями изобретения18. Тогда они должны быть готовы к тому, что распоряжаться правами им придется совместно, и чтобы подписать в дальнейшем, например, лицензионный договор потребуется согласие
18 Если автор изобретения один, таких проблем не возни-
кает.
1318
Новый справочник химика и технолога
каждого патентообладателя. А если один из них уедет работать за границу? Вопрос можно решить путем выдачи этим автором или всеми авторами доверенности тому автору, который в дальнейшем будет вести дела, связанные с данным изобретением.
Авторы вправе выбрать в качестве патентообладателя, например, одного автора из своего коллектива. Тогда другие должны заключить с этим автором договор о передаче ему своего права на получение патента и оговорить условия, на которых эта передача должна произойти.
Следует заметить, что в любом случае полезно заключить между соавторами соглашение о разделе доходов, которые могут появиться от использования патентных прав. Чаще всего доля каждого из соавторов определяется в виде процента от будущих доходов.
Другой случай: авторы решают передать права на получение патента третьему лицу. Такое соглашение обязательно должно быть составлено в письменной форме и содержать условия, на которых авторы передают эти права.
При заключении указанных соглашений у авторов часто возникает такая проблема: партнер по соглашению не хочет покупать «кота в мешке» и требует раскрыть суть изобретения до подписания соглашения. Как справедливо полагают авторы, со стороны партнера по переговорам возможны недобросовестные действия. Узнав суть изобретения и отказавшись подписать соглашение, партнер может сам подать заявку на это предложение. Где выход?
Во-первых, подбирать надежных партнеров, а не бросаться в объятия первого попавшегося. Во-вторых, стараться убедить партнера, объясняя ему результат, который дает изобретение, а не суть его. И третье. Международная практика, сталкиваясь с этой проблемой и ей подобными, выработала форму соглашения о конфиденциальности, в котором сторона, получающая конфиденциальную информацию, берет на себя обязательство не разглашать ее третьим лицам и не использовать ее в своей деятельности. Это соглашение не является панацеей, но серьезные фирмы не хотят портить свою репутацию, нарушая его. Кроме того, если партнер по переговорам все же нарушит это соглашение и подаст заявку на изобретение от своего лица, то имеется возможность доказать свое право в суде.
Передача прав во время рассмотрения заявки в патентном ведомстве
В период с момента подачи заявителем заявки в патентное ведомство и до момента выдачи патента возможна уступка права на получение патента. Это соглашение, по сути, отличается от рассмотренного только тем, что лицо, которое уступает право, должно сообщить в ведомство о новом заявителе.
При подаче заявки заявитель может сделать заявление, что готов предоставить любому лицу права на использование изобретения, полезной модели или промышленного образца (так называемая открытая
лицензия). В этом случае размер государственных пошлин уменьшается на 50 %.
Заявитель освобождается от уплаты пошлин, если к документам заявки приложит заявление о том, что в случае выдачи патента он обязуется передать исключительное право на изобретение (уступить патент) на условиях, соответствующих установившейся практике, лицу, первым изъявившему желание принять такое право и уведомившему об этом патентообладателя и патентное ведомство, — гражданину Российской Федерации или российскому юридическому лицу.
Передача прав после получения патента
Любое лицо, не являющееся патентообладателем, вправе использовать запатентованные изобретение, полезную модель, промышленный образец лишь с разрешения патентообладателя, на основе лицензионного договора. По лицензионному договору патентообладатель (лицензиар) обязуется предоставить право на использование охраняемого объекта в объеме, предусмотренном договором, другому лицу (лицензиату), а последний принимает на себя обязанность вносить лицензиару обусловленные договором платежи и (или) осуществлять другие действия, предусмотренные договором.
Различают лицензии исключительные и неисключительные (простые). При исключительной лицензии лицензиату передается право на использование изобретения, полезной модели, промышленного образца в пределах, оговоренных договором, с сохранением за лицензиаром права на его использование в части, не передаваемой лицензиату. При неисключительной лицензии лицензиар, предоставляя лицензиату право на использование изобретения, полезной модели или промышленного образца, сохраняет за собой все права, подтверждаемые патентом, в том числе и на предоставление лицензий третьим лицам.
Лицензионный договор действителен только в том случае, если он зарегистрирован в патентном ведомстве.
Передача прав может происходить и путем уступки патентообладателем патента другому лицу. Такой договор также необходимо зарегистрировать в патентном ведомстве.
9.2.2. Изобретение
В качестве изобретения охраняется техническое решение в любой области, относящееся к продукту, в частности устройству, веществу, штамму микроорганизма, культуре клеток растений или животных, или к способу — процессу осуществления действий над материальным объектом с помощью материальных средств.
9.2.2.1. Условия патентоспособности
Изобретению предоставляется правовая охрана, ес-
ли оно отвечает следующим критериям: является но-
вым, имеет изобретательский уровень и промышленно
применимо.
Интеллектуальная собственность
1319
Новизна
Изобретение является новым, если оно не известно из уровня техники. При установлении новизны в понятие «уровень техники» включаются любые сведения, ставшие общедоступными в мире до даты приоритета, и поданные в России другими лицами заявки на изобретения и полезные модели (кроме отозванных), а также запатентованные изобретения и полезные модели при условии их более раннего приоритета.
Как отмечалось ранее, одним из важнейших юридически значимых фактов является дата подачи первой заявки (дата приоритета). С даты приоритета отсчитываются все сроки, которые, как мы увидим далее, имеют важное значение. В настоящий момент при определении новизны изобретения дата приоритета является тем рубежом, по которому определяется, может ли быть противопоставлен какой-либо источник информации поданной заявке. По закону, такие источники информации разделены на две группы:
- любые сведения, ставшие общедоступными до даты приоритета;
- поданные в России другими лицами заявки на изобретения и полезные модели с более ранней датой при-19 оритста .
Что понимается в законе под «любыми сведениями, ставшими общедоступными»? Любой источник информации: книга или научная статья; автореферат диссертации; рекламный проспект; представление экспоната, раскрывающего суть изобретения, на выставке; устное сообщение на международной конференции и т. д. при условии, что доступ к этим источникам открыт или был открыт для любого лица. При этом не важно, в каком уголке мира произошло это раскрытие информации, в России или любой другой стране. Также не важно, кто автор этих сведений. Вам могут противопоставить вашу же статью, в которой вы раскрыли собственное изобретение и которая была опубликована до даты приоритета. Поэтому существует важное правило — никаких публикаций, раскрывающих суть вашего изобретения, полезной модели или промышленного образца до подачи заявки.
Критерий «новизна» понимается как «мировая новизна». Следует отметить, что в патентных законах большинства стран мира также используется критерий «мировой новизны».
В уровень техники также включаются еще не опубликованные (а также опубликованные) заявки, которые находятся на рассмотрении в Патентном ведомстве России, с более ранней датой приоритета других заявителей.
1 9 Мы не включаем в этот перечень «запатентованные изобретения и полезные модели при условии их более раннего приоритета» в связи с тем, что практически сведения об изобретениях и полезных моделях становятся общедоступными с даты выдачи патента, т. к. при выдаче патента обязательно производится публикация.
Не признается обстоятельством, препятствующим признанию патентоспособности изобретения, такое раскрытие информации, относящейся к изобретению, автором, заявителем или любым лицом, получившим от них прямо или косвенно эту информацию, при котором сведения о сути изобретения стали общедоступными, если заявка на изобретение подана не позднее чем через 6 месяцев с даты раскрытия информации. При этом обязанность доказывания данного факта лежит на заявителе.
Несмотря на существующую в России льготу по новизне, о которой речь шла выше, не следует до подачи заявки раскрывать сущность изобретения. Этой льготой придется воспользоваться только в том случае, если произошло раскрытие информации вопреки вашим намерениям, но сознательно раскрывать информацию, а затем пользоваться льготой не следует. Дело в том, что в большинстве стран такая льгота не предоставляется, и получить патент за рубежом на это изобретение уже не будет возможности.
Изобретательский уровень
Изобретение имеет изобретательский уровень, если оно для специалиста явным образом не следует из уровня техники.
При определении изобретательского уровня в понятие «уровень техники» включаются любые сведения, ставшие общедоступными в мире до даты приоритета; сведения о рассматриваемых в ведомстве и неопубли-20 кованных заявках не включаются .
Не признаются соответствующими условию изобретательского уровня изобретения, основанные, в частности [8]:
- на дополнении известного средства какой-либо известной частью, присоединяемой к нему по известным правилам, для достижения технического результата, в отношении которого установлено влияние именно таких дополнений;
- замене какой-либо части известного средства другой известной частью для достижения технического результата, в отношении которого установлено влияние именно такой замены;
- исключении какой-либо части средства (элемента, действия) с одновременным исключением обусловленной ее наличием функции и достижением при этом обычного для такого исключения результата (упрощение конструкции, уменьшение массы, габаритов, материалоемкости, повышение надежности, сокращение продолжительности процесса и пр.);
- увеличении количества однотипных элементов, действий для усиления технического результата, обусловленного наличием в средстве именно таких элементов, действий;
20 Как мы узнаем далее, поданные заявки, по российскому
Патентному закону, через 18 месяцев с даты приоритета
публикуются. Опубликованная заявка уже содержит сведения,
ставшие общедоступными, несмотря на то что патент по та-
кой заявке не выдан.
1320
Новый справочник химика и технолога
- выполнении известного средства или его части из известного материала для достижения технического результата, обусловленного известными свойствами этого материала;
- создании средства, состоящего из известных частей, выбор которых и связь между которыми осуществлены на основании известных правил, рекомендаций; достигаемый при этом технический результат обусловлен только известными свойствами частей этого средства и связями между ними;
- применении известного продукта или способа по определенному назначению, если возможность реализации этого назначения обусловлена его известными свойствами, структурой, выполнением и известно, что именно такие свойства, структура, выполнение необходимы для реализации этого назначения.
Не могут быть признаны соответствующими изобретательскому уровню изобретения, основанные на изменении количественного признака (признаков), представлении таких признаков во взаимосвязи либо изменении ее вида, если известен факт влияния каждого из них на технический результат и новые значения этих признаков или их взаимосвязь могли быть получены исходя из известных зависимостей, закономерностей.
Условию изобретательского уровня соответствуют, в частности'.
- способы получения новых химических соединений (класса, группы) с установленной структурой;
- способы получения известных химических соединений (класса, группы) с установленной структурой, если они основаны на новой для данного класса или группы соединений реакции или на известной для данного класса или группы соединений реакции, условия проведения которой неизвестны;
- композиция, состоящая, по крайней мере, из двух известных ингредиентов, обеспечивающая синергический эффект, возможность достижения которого не вытекает из уровня техники (т. е. проявляющая свойства обоих ингредиентов, но количественные показатели хотя бы одного из этих свойств выше показателей свойств отдельного ингредиента);
- химическое соединение, подпадающее под общую структурную формулу группы известных соединений, но не описанное как специально полученное и исследованное и при этом проявляющее новые, неизвестные для этой группы свойства в качественном или количественном отношении (селективное изобретение).
Изобретение не рассматривается как не соответствующее изобретательскому уровню из-за его кажущейся простоты и раскрытия в материалах заявки механизма достижения технического результата, если такое раскрытие стало известно не из уровня техники, а только из материалов заявки.
Критерий изобретательского уровеня устанавливает, что изобретение должно быть новым и отличаться творческим элементом. Результат творчества изобретателя должен привести к созданию технического решения, результат которого является неожиданным.
Этот результат возникает не как сумма свойств известных элементов, из которых состоит изобретение, а как новый, неожиданный, неочевидный для специалиста сверхсуммарный результат, составляющий суть данного изобретения.
Другими словами, изобретение должно обладать новыми свойствами, которые не сводятся к сумме свойств отдельных элементов. В частности, решение, созданное обычным конструированием с заранее прогнозируемым специалистом результатом, полученное по известным методикам, не будет признано изобретением.
Критерий изобретательского уровня отвечает за творческую составляющую защищаемых патентом изобретений и является наиболее трудным для преодоления «планки», устанавливаемой экспертизой патентного ведомства.
Промышленная применимость
Изобретение является промышленно применимым, если оно может быть использовано в промышленности, здравоохранении и других отраслях деятельности [6]. Неважно, где изобретение может быть использовано, в какой отрасли деятельности, — важно, что его можно использовать.
Данный критерий препятствует выдаче патентов на решения, которые нельзя использовать.
Во-первых, патент не будет выдан на идею, он будет выдан только на реализуемое решение по указанному заявителем назначению.
Например, в Патентное ведомство России была подана и опубликована заявка с формулой следующего содержания.
Гравилет, отличающийся тем, что состоит из устройства жизнеобеспечения или транспортного отсека, оснащенного кинемагнитным преобразователем гравитационного потенциала или генератором нулъ-поля, причем их может быть несколько и они могут иметь магнитную линзу-отражатель, устройство привода или генератор бегущего поля, магнитный двигатель или генератор разомкнутого поля, рулевое устройство, причем гравилет может быть оснащен также телепортационным двигателем или генератором Абсолюта, устройством для прохождения космического Абсолюта или телетрансфером, а также те-- 21
лепортационным устройством .
Как видно любому лицу, знающему физику в объеме школьной программы, использовать подобное предложение невозможно, т. к. в нем нет сведений о том, как создать преобразователь гравитационного потенциала, генератор нуль-поля и т. д. Патент по данной заявке выдан не был.
Во-вторых, и это очень важно, в материалах заявки должны быть приведены средства и методы, с помощью которых возможно осуществление изобретения.
21 Заявка, номер которой мы здесь не приводим, офици-
ально опубликована и общедоступна.
Интеллектуальная собственность
1321
При отсутствии таких сведений в материалах заявки допустимо, чтобы упомянутые средства и методы были описаны в источнике, ставшем общедоступным до даты приоритета изобретения.
Иногда при пояснениях критерия промышленной применимости говорят, что материалы заявки должны содержать все необходимые сведения, чтобы средний специалист в данной отрасли мог осуществить изобретение, не прикладывая каких-либо новых изобретательских усилий.
Готовя описание заявки на изобретение, не следует скрывать каких-либо сведений, позволяющих его осуществить. Существует мнение, что не следует включать в описание некоторые ноу-хау, относящиеся к изобретению. К таким рекомендациям следует относиться осторожно. По патентному законодательству некоторых стран, в частности США, заявитель должен в описании раскрыть лучший из известных ему вариантов реализации изобретения. Если он скроет такую информацию, то данный факт может служить основанием для аннулирования патента. Важно другое. Не следует помещать в материалы заявки информацию, которая является лишней, не относящейся к данному изобретению, не нужной для его осуществления в объеме признаков, которые приведены в формуле22 изобретения.
Объекты, не считающиеся патентоспособными
В частности [6]:
- открытия, а также научные теории и математические методы;
- решения, касающиеся только внешнего вида изделий и направленные на удовлетворение эстетических потребностей;
- правила и методы игр, интеллектуальной или хозяйственной деятельности;
- программы для электронных вычислительных машин;
- решения, заключающиеся только в представлении информации.
Приведенный перечень содержит объекты, относящиеся к интеллектуальной собственности и охраняемые другими законами, например программы для ЭВМ, которые охраняются авторским правом, и объекты, на которые выдаются патенты, например промышленные образцы — решения, касающиеся только внешнего вида изделий и направленные на удовлетворение эстетических потребностей.
Но в перечне содержатся и другие объекты: открытия, правила и методы игр, интеллектуальной или хозяйственной деятельности, решения, заключающиеся только в представлении информации, — они не охраняются патентным правом, а описание этих объектов охраняется авторским правом, но, как мы знаем, оно охраняет только форму произведения и не охраняет его суть.
22 Формула — словесное описание изобретения или полезной модели, по которой определяется объем правовой охраны патентообладателя.
Простого ответа на вопрос, почему эти объекты исключены из сферы патентного права, нет. Существовали многочисленные попытки создать систему охраны открытий, но такие системы не были системами, охраняющими право на открытие23, или предложения не были осуществлены на практике24. Можно предположить, что такие объекты не охраняются потому, что, во-первых, открытия — это явления материального мира, которые существуют независимо от нас, и ученые только объясняют их. Вот изобретения, которые основываются на новых открытиях, естественно, патентоспособны.
С другой стороны, можете ли вы проконтролировать, применяют ли на предприятиях правила и методы интеллектуальной или хозяйственной деятельности, на которые вам, предположим, выдадут патент? Скорее всего, нет, т. к. материальных следов их применения, в частности на выпускаемой предприятием продукции, не остается. Вероятно, эти объекты исключены из охраны потому, что патентование их бесполезно, прежде всего для самого создателя.
Важно отметить, что исключается возможность отнесения указанных в перечне объектов к изобретениям только в случае, если заявка на выдачу патента на изобретение касается указанных объектов как таковых, т. е. они могут быть элементами патентоспособного технического решения.
Не признаются патентоспособными в смысле положений настоящего Закона:
- сорта растений, породы животных;
- топологии интегральных микросхем;
- решения, противоречащие общественным интересам, принципам гуманности и морали.
Сорта растений, породы животных, топологии интегральных микросхем охраняются специальным законодательством.
Срок действия патента на изобретение
Патент на изобретение действует с даты его выдачи в течение 20 лет, отсчитываемых с даты подачи заявки при условии уплаты ежегодных патентных пошлин, начиная с третьего года после даты приоритета.
Срок действия патента на изобретение, относящееся к лекарственному средству, пестициду или агрохимикату, для применения которых требуется разрешение, полученое в установленном законом порядке, продлевается на срок, исчисляемый с даты подачи заявки
23 В СССР открытия регистрировались на основании Положения об открытиях, изобретениях и рационализаторских предложениях с выплатой вознаграждения авторам. Другого значения, кроме регистрационного, положение не предусматривало. С принятием Патентного законодательства регистрация открытий была прекращена в силу ее бесполезности, хотя специальных актов, ее отменяющих, принято не было.
24 Существовал проект закона об охране открытий, разработанный Всемирной организацией интеллектуальной собственности, но он не был принят ни одной страной.
1322
Новый справочник химика и технолога
на изобретение до даты получения первого такого разрешения на применение, за вычетом 5 лет. При этом срок, на который продлевается действие патента на изобретение, не может превышать 5 лет.
Если действие патента прерывается по причине неуплаты ежегодной патентной пошлины, то оно может быть восстановлено по ходатайству патентообладателя в течение 3 лет с даты истечения срока уплаты указанной патентной пошлины, но до истечения срока действия патента. При этом у лиц, которые в период, когда нс действовал патент, начали использовать изобретение или сделали для этого необходимые приготовления, возникает право послепользования.
9.2.2.2. Процесс получения патента на изобретение
В процессе получения патента на изобретение можно выделить две стадии: первая — подготовка заявки на получение патента и ее подача, вторая — прохождение заявки в патентном ведомстве.
Подача заявки
Подготовка заявки на получение патента является одним из самых ответственных этапов приобретения патентных прав. Ведь заявку на одно и то же изобретение можно оформить так, что в одном случае патент будет получен, а в другом — нет. Кроме того, даже если патент получен, в одном случае объем прав патентообладателя будет максимально возможным, в другом — ничтожно малым, практически не защищающим созданное изобретение. Заявка может быть подана непосредственно в патентное ведомство25, точнее в его орган — Федеральный институт промышленной собственности (ФИПС), находящийся в Москве, или отправлена по почте. В Санкт-Петербурге, Казани, Новосибирске и Уфе расположены сектора приема заявок ФИПС, поэтому заявки из этих регионов не обязательно везти в Москву. В обозримом будущем начнется прием заявок в электронном виде, их экспериментальная подача осуществляется уже сегодня26. Прохождение заявки в патентном ведомстве сопровождается уплатой патентных пошлин за юридически значимые действия, связанные с получением патента, с обязательным уведомлением заявителем ведомства об их уплате. За подачу заявки уплачивается соответствующая пошлина.
Процесс рассмотрения заявки
Процесс рассмотрения заявки начинается с подготовки подачи заявки на получение патента, т. е. с даты приоритета (/).
25 Федеральный орган исполнительной власти по интеллектуальной собственности — так названо патентное ведомство в Законе [6]. В настоящее время официальное название патентного ведомства — Федеральная служба по интеллектуальной собственности, патентам и товарным знакам.
26 Ответы на многие практические вопросы, связанные с подачей заявок, авторы и заявители могут получить, обратившись на сайт ФИПС: www.fips.ru.
На рис. 9.3 показаны основные этапы процесса прохождения заявки в патентном ведомстве.
Рис. 9.3. Основные этапы процесса получения патента
В период (А), который называется формальной экспертизой, в основном проверяются наличие всех документов, которые необходимы для рассмотрения заявки, соблюдение установленных требований к документам заявки, а также правильность уплаты патентной пошлины. Если у экспертизы возникли вопросы к заявителю, она посылает запрос. По окончании формальной экспертизы заявки заявителю высылается уведомление о ее положительном результате.
Чтобы патентное ведомство провело экспертизу по существу (3), необходимо подать соответствующее ходатайство и уплатить пошлину. Такое ходатайство может быть подано одновременно с заявкой, тогда экспертиза по существу начнется после получения положительного результата формальной экспертизы или в любой момент в течение 3 лет. Заявитель сам выбирает, когда необходимо начать экспертизу по существу (эта процедура называется «отсроченной экспертизой»). Такой порядок позволяет не тратить лишние усилия и средства на уплату пошлин в тех случаях, когда заявитель не уверен, нужен ли ему патент на данное изобретение или нужна проверка различных вариантов воплощения идеи, и решение о выборе варианта будет сделано позднее, а в данный момент важно получить приоритет; может быть, нужна проверка, будет ли спрос на это изобретение? В этих и других случаях процедура отсроченной на три года экспертизы позволяет вернуться к решению о получении патента позже. Поэтому на рис. 9.3 показаны варианты, когда экспертиза по существу начинается сразу или в конце трехлетнего срока.
Экспертиза по существу
Во время проведения экспертизы по существу (В) в основном осуществляются:
- установление приоритета изобретения;
- проверка наличия в формуле изобретения сущест-
венных признаков и единства изобретения;
- информационный поиск в отношении изобрете-
ния, охарактеризованного в формуле, для определения
уровня техники и проверки соответствия изобретения
установленным условиям патентоспособности.
Интеллектуальная собственность
1323
По окончании экспертизы по существу (4) принимается решение о выдаче патента или об отказе в выдаче патента и направляется соответствующее уведомление заявителю.
Выдача патента
Выдача патента (5) (буквой С на рис. 9.3. обозначено время до его выдачи) производится в том случае, если заявитель уплатил соответствующую пошлину и уведомил об этом ведомство. Она осуществляется вместе с официальной публикацией сути выданных патентных прав, т. е. с публикацией библиографических данных патента, формулы, описания и чертежей. Именно с даты выдачи патента у патентообладателя появляются исключительные права и возможность их использовать.
Публикация заявки
Чрезвычайно важным моментом является публикация заявки через 18 месяцев (6) с даты приоритета (/). Публикация заявки служит нескольким целям.
Во-первых, выдача патента может затронуть интересы других лиц, выпускающих или собирающихся выпускать аналогичную продукцию. Публикация заявки позволит им узнать о предстоящей выдаче патентных прав и скорректировать свои планы.
Во-вторых, суть изобретения становится достоянием общественности раньше, всего через полтора года после подачи заявки, что позволяет другим изобретателям создавать новые решения с учетом недавно созданных, что также в интересах общества. Публикация заявки способствует ускорению технического прогресса.
В-третьих, с даты публикации заявки до даты публикации сведений о выдаче патента предоставляется временная правовая охрана заявленного изобретения в объеме опубликованной формулы, но не в большем, чем объем, определяемый формулой, содержащейся в решении о выдаче патента на изобретение. Физическое или юридическое лицо, использующее заявленное изобретение в этот период, выплачивает патентообладателю после получения им патента денежную компенсацию. Размер компенсации определяется соглашением сторон.
9.2.2.3. Составление заявки на изобретение
Собственно оформление заявки на изобретение определяется Правилами составления, подачи и рассмотрения заявки на выдачу патента на изобретение [8].
Правила содержат перечень документов, необходимых при подаче заявки:
- заявление о выдаче патента с указанием автора изобретения и лица, на имя которого испрашивается патент (заявителя), а также их местожительства или местонахождения;
- описание изобретения, раскрывающее его с полнотой, достаточной для осуществления;
- формулу изобретения, выражающую его суть и полностью основанную на описании;
- чертежи и иные материалы, если они необходимы для понимания сущности изобретения;
- реферат.
К заявке прилагаются следующие документы:
- документ, подтверждающий уплату патентной пошлины в установленном размере, или документ, подтверждающий основания для освобождения от уплаты патентной пошлины, либо уменьшения ее размера, либо отсрочки ее уплаты;
- документ о депонировании — к заявке на изобретение, относящееся к штамму микроорганизма, линии клеток растений или животных либо к средству с использованием неизвестных штамма микроорганизма или линии клеток, содержащей указание на их депонирование в уполномоченной на это коллекции микроорганизмов;
- перечень последовательностей нуклеотидов и/или аминокислот вместе с машиночитаемым носителем информации (дискетой) с записью копии того же перечня последовательностей и подписанное заявителем заявление относительно того, что информация, представляемая в машиночитаемой форме, идентична перечню последовательностей, представляемому в печатной форме;
- ходатайство о проведении экспертизы по существу с уплатой соответствующей пошлины — в том случае, если заявитель ходатайствует, чтобы проведение экспертизы по существу началось сразу по окончании формальной экспертизы.
Составление заявки на изобретение является одним из важнейших этапов, определяющих качество и объем прав, которые будет иметь патентообладатель. Еще раз отметим, что на одно и то же изобретение могут быть получены патенты с различным объемом прав, и все это определяется тем, как составлена заявка. Мы убеждены, что составление заявки следует поручать профессионалам, опытным патентоведам, патентным поверенным27, а точнее — процесс ее оформления должен проходить в совместной работе патентоведа и изобретателя. Составление заявки, в свою очередь, имеет несколько этапов. Рассмотрим их в той последовательности, которая, с нашей точки зрения, является правильной.
27 Патентовед — специалист, имеющий специальную подготовку в области интеллектуальной собственности, в частности промышленной собственности. Патентным поверенным является гражданин Российской Федерации, постоянно проживающий на ее территории и зарегистрированный в патентном ведомстве в этом качестве. Требования к патентному поверенному, порядок его аттестации и регистрации, а также правомочия на ведение дел, связанных с правовой охраной изобретений, полезных моделей и промышленных образцов, определяются Положением о патентных поверенных, утвержденным Постановлением Правительства № 122 от 12 февраля 1993 г.
1324
Новый справочник химика и технолога
Выявление объекта изобретения
Патентование для объектов промышленной собственности в фирмах или организациях может быть систематическим или однократным. Процесс выявления объекта изобретения в обоих случаях имеет общие черты.
1. Сбор информации об аналогах
Если этот этап выявления объекта изобретения не выполняется, то гарантировать, что заявитель получит надежный патент, практически невозможно. Существует общее правило: чем больше вы знаете об уровне техники в той узкой области, где располагается объект, на который оформляется заявка, тем больше вероятность, что патент будет надежным. Уровень техники, определяемый прежде всего патентной документацией ведущих в данной конкретной области стран мира, выявляется в результате патентных исследований. Вопросы регламента и методики проведения различных видов патентных исследований будут рассмотрены отдельно.
Патентные исследования на патентоспособность должны выявить ближайшие аналоги созданного изобретения и дать ответ на вопрос: является ли изобретение новым и соответствует ли оно критерию изобретательского уровеня. Естественно, что подобные выводы являются вероятностными, т. к. практически невозможно утверждать, что просмотрены все патентные и научно-технические источники информации, относящиеся к данной области. В настоящее время сбор патентной информации чаще всего производится с использованием электронных баз данных патентной информации28. В фирмах, которые обновляют свою продукцию, ведут поиск новых товаров для выпуска, процесс сбора научно-технической и патентной информации является непрерывным.
2. Определение объекта
Как мы уже знаем, объектами изобретений могут быть устройство, вещество, способ29. Например: создан способ получения нового керамического материала. В данном случае новым является и материал, и способ его получения. Кроме того, новыми и патентоспособными могут являться конструкции устройств для прессования, спекания этого материала. Что следует выбрать в качестве объекта патентования?
Решить эту задачу непросто.
Первое. Нужно определить, какие решения в данной технологии являются ключевыми, главными, без чего данная технология не может работать, что отличает ее от известных технологий.
Второе. Если патент на выбранный объект будет получен, возможно ли проконтролировать нарушения третьими лицами прав, предоставляемых патентом? Если
28 Сведения об электронных базах данных приведены в разделе о патентных исследованиях.
29 Кроме того, штамм микроорганизма и культура клеток
растений и животных.
проконтролировать нарушения этих прав, прежде всего, на основании анализа выпускаемой продукции невозможно, то необходимо решить, следует ли получать патент даже на патентоспособный объект, ведь конкуренты могут использовать его без особого риска, т. к. невозможно или весьма трудно доказать, что конкретное предприятие, фирма нарушает ваши патентные права.
Для химических веществ следует учитывать, что существует косвенная охрана веществ через способ их получения (см. 9.2.2.1).
Третье. Следует оценить вероятность получения патента и выбрать вид охраны. Решение вопроса о возможности получения патента базируется на анализе известных источников информации, полученных в результате патентных исследований. Изобретение должно отвечать критериям новизны и изобретательского уровня30. Анализ найденных аналогов изобретения также позволяет оценить вероятность получения патента перед подачей заявки.
3. Определение объектов, которые относятся к группе изобретений, связанных между собой настолько, что образуют единый изобретательский замысел
К группе изобретений, связанных единым изобретательским замыслом и отвечающих требованию единства изобретения [8], относятся изобретения:
- одно из которых предназначено для получения (изготовления) другого (например, устройство или вещество и способ получения или изготовления устройства или вещества в целом или их части);
- одно из которых предназначено для осуществления другого (например, способ и устройство для осуществления способа в целом или одного из его действий);
- одно из которых предназначено для использования другого (в другом) (например, способ и вещество, предназначенное для использования в способе; способ или устройство и его часть; применение устройства или вещества по определенному назначению и способ с их использованием в соответствии с этим назначением; применение устройства или вещества по определенному назначению и устройство или композиция, в которых они используются в соответствии с этим назначением как составная часть);
- относящиеся к объектам одного вида (несколько устройств, несколько веществ и т. д.), одинакового назначения, обеспечивающим получение одного и того же технического результата (варианты).
Выявление групп изобретений и подача одной заявки, содержащей группу изобретений, делает охрану более комплексной и снижает расходы на патентование.
Формула изобретения
Процесс составления заявки начинается с составления формулы изобретения.
30 Если часть технологии, которая относится к устройству,
отвечает только критерию новизны, возможна охрана такого
устройства как полезной модели.
Интеллектуальная собственность
1325
Формула изобретения — это формулировка изобретения, выражающая его суть и содержащая совокупность существенных признаков изобретения, достаточную для достижения технического результата. Объем правовой охраны, предоставляемой патентом, определяется формулой, поэтому ее составление является ответственной задачей, в дальнейшем определяющей качество полученных патентных прав.
Формула составляется по определенным, достаточно жестким правилам, изложенным в [8]31.
Приведем примеры формул изобретения на устройство, способ, вещество.
Пример 1
Патент РФ № 2118035.
1. Ротор электрической машины, выполненный в виде вала с постоянным магнитом и содержащий, по меньшей мере, одно посадочное место подшипника, отличающийся тем, что магнитоактивная часть ротора выполнена из постоянного магнита в виде вала, по меньшей мере одна торцевая часть вала снабжена центровочным элементом для соосного изготовления посадочного места подшипника и центра масс ротора, расположенного по оси вала.
2. Ротор, по п.1, отличающийся тем, что торцевая часть вала имеет наружную проточку, являющуюся центровочным элементом, на которой непосредственно или через промежуточный элемент выполнено посадочное место подшипника.
3. Ротор, по п. 1, отличающийся тем, что торцевая часть вала имеет выточку, являющуюся центровочным элементом, на которой непосредственно или через промежуточный элемент выполнено посадочное место подшипника.
4. Ротор, по п. 1, отличающийся тем, что торцевая часть вала имеет проточку, на которой закреплен промежуточный элемент с центровочным элементом в виде отверстия, в которое жестко установлена полуось, содержащая посадочное место подшипника.
5. Ротор, по любому из пп. 2-4, отличающийся тем, что промежуточные элементы выполнены из материалов, близких по плотности к материалу постоянного магнита.
Пример 2
Патент РФ № 2195469.
1. Способ формирования эластомерного покрытия на устройстве для штампования или обработки бруска детергента, при котором обрабатывают поверхность устройства химическими и/или механическими средствами для образования поверхности сцепления для эластомерного покрытия, формируют на поверхности
31 При написании подразделов «Формула изобретения» и «Описание изобретения» достаточно полно цитируются Правила [8], которые доступны любому лицу на сайте патентного ведомства (www.fips.ru).
сцепления первое отвержденное эластомерное покрытие, имеющее первый состав, формируют на первом отвержденном эластомерном покрытии, по меньшей мере, одно отвержденное эластомерное покрытие, имеющее второй состав, отличающийся от первого состава, при этом первое и второе эластомерные покрытия отверждаются при различных давлениях и/или каталитических системах, а модуль упругости эластомерного покрытия находится в диапазоне 0,1-50,0 МПа.
2. Устройство для обработки бруска детергента, содержащее контактную поверхность для контактирования с бруском детергента, имеющую эластомерное покрытие, состоящее, по меньшей мере, из двух покрытий, при этом первое отвержденное покрытие имеет первый состав, и второе эластомерное покрытие имеет второй состав, отличающийся от первого состава, причем первое отвержденное эластомерное покрытие имеет свойства, отличающиеся от свойств второго отвержденного эластомерного покрытия, а модуль упругости эластомерного покрытия находится в диапазоне 0,1-50,0 МПа.
Пример 3
Патент РФ № 2137791.
Заливочная эпоксидная композиция, включающая эпоксидную смолу, блоколигомер, отвердитель, вспениватель, отличающаяся тем, что в качестве эпоксидной смолы она содержит эпоксилапрол марки ЛЭК-50, в качестве блоколигомера — блоколигомер диглициди-лового эфира параоксибензойной кислоты и диэтилен-гликольсебацината марки VI1-680, в качестве отвердителя — имидазолин и дополнительно — мелкодисперсный наполнитель при следующем соотношении компонентов, масс, ч.:
Эпоксилапрол марки ЛЭК-50 — 100
Блоколигомер марки VII—680 — 10-25
Имидазолин — 38-48
Вспениватель — 0,2-0,4
Мелкодисперсный наполнитель — 0,3-0,5
Как видно из приведенных примеров, формула изобретения может состоять из одного пункта, как в примере 3 (однозвенная), или из нескольких пунктов, как в примерах 1 и 2 (многозвенная).
Однозвенная формула применяется для характеристики одного изобретения, а многозвенная — для характеристики группы изобретений (пример 2) или одного изобретения с развитием и/или уточнением совокупности его признаков применительно к частным случаям выполнения или использования изобретения (пример 1).
Многозвенная формула, характеризующая одно
изобретение, имеет один независимый пункт и сле-
дующие за ним зависимые пункты (пример 1), а такая
же формула, характеризующая группу изобретений
(см. 9.2.2.3), имеет несколько независимых пунктов,
каждый из которых характеризует одно из изобретений
1326
Новый справочник химика и технолога
группы (пример 2). При этом каждое изобретение группы может быть охарактеризовано с привлечением зависимых пунктов, подчиненных соответствующему независимому пункту (см. далее пример 6).
Юридическое значение для определения объема охраны изобретения имеют только независимые пункты формулы.
Зависимые пункты формулы применяются для того, чтобы построить многоступенчатую архитектурную конструкцию раскрытия изобретения: от общего к частному. При этом решается несколько задач:
- отражение вариантов выполнения признаков, охарактеризованных родовыми понятиями в независимом пункте формулы;
- возможность точного толкования признаков независимых пунктов формулы;
- отражение частных признаков решения изобретательской задачи, не включенных в независимый пункт, чтобы не сужать объем охраны изобретения.
Требования к формуле
Пункт формулы излагается в виде одного предложения.
Независимый пункт формулы включает признаки изобретения, в том числе родовое понятие, отражающее назначение, с которого начинается изложение формулы, и состоит, как правило, из ограничительной части, включающей признаки изобретения, совпадающие с признаками наиболее близкого аналога, и отличительной части, включающей признаки, которые отличают изобретение от него. Формула, разделенная на ограничительную и отличительную части, после изложения ограничительной части включает словосочетание «отличающийся тем, что».
Правила разрешают изложение формулы и без разделения на ограничительную и отличительную части, в частности, если она характеризует:
- индивидуальное химическое соединение;
- штамм микроорганизма, линию клеток растений или животных;
- применение по определенному назначению;
- изобретение, не имеющее аналогов.
Особенности формулы изобретения, относящейся к устройству
Признаки устройства излагаются в формуле так, чтобы характеризовать его в статическом состоянии (пример 1). При характеристике выполнения конструктивного элемента устройства допускается указание на его подвижность, на возможность реализации им определенной функции (например, на возможность торможения, на возможность фиксации) и т. п.
Признаки, используемые для характеристики устройств:
- наличие конструктивного (конструктивных) элемента (элементов);
- наличие связи между элементами;
- взаимное расположение элементов;
- форма выполнения элемента (элементов) или устройства в целом, в частности геометрическая форма;
- форма выполнения связи между элементами;
— параметры и другие характеристики элемента (элементов) и их взаимосвязь;
- материал, из которого выполнен элемент (элементы) или устройство в целом;
- среда, выполняющая функцию элемента.
Особенности формулы изобретения, относящейся к способу
При характеристике способа (пример 2) глаголы для описания действия (приема, операции) применяются в действительном залоге в изъявительном наклонении в третьем лице во множественном числе (нагревают, увлажняют, прокаливают и т. п.).
Признаки, используемые для характеристики способов:
- наличие действия или совокупности действий;
- порядок выполнения действий во времени (последовательно, одновременно, в различных сочетаниях и т. п.);
- условия осуществления действий; режим; использование веществ (исходного сырья, реагентов, катализаторов и т. д.), устройств (приспособлений, инструментов, оборудования и т. д.), штаммов микроорганизмов, линий клеток растений или животных.
Особенности формулы изобретения, относящейся к веществу [8]
Химические соединения могут характеризоваться в формуле с указанием назначения соединения (пример 3) или без такого указания. Указание назначения нового соединения сужает объем охраны изобретения, в то время как «абсолютная защита» соединения, без указания назначения, расширяет права патентообладателя не только на те области применения соединения, которые известны в момент подачи заявки, но и на другие области, где это соединение может применяться в дальнейшем.
В формулу изобретения, характеризующую химическое соединение с установленной структурой, включаются наименование соединения по одной из принятых в химии номенклатур или обозначение соединения и его структурная формула (см. далее пример 4).
Для химического соединения с неустановленной структурой в формуле изобретения приводятся наименование, содержащее характеристику назначения соединения, физико-химические и иные характеристики, позволяющие отличить данное соединение от других, в частности признаки способа его получения.
Для характеристики химических соединений используются, в частности, следующие признаки:
- для низкомолекулярных соединений с установленной структурой — качественный состав (атомы определенных элементов), количественный состав (число атомов каждого элемента), связь между атомами и взаимное их расположение в молекуле, выраженное химической структурной формулой;
- для высокомолекулярных соединений с установ-
ленной структурой — структурная формула элементар-
Интеллектуальная собственность
1327
ного звена макромолекулы, структура макромолекулы в целом (линейная, разветвленная), количество элементарных звеньев или молекулярная масса, молекулярномассовое распределение, геометрия и стереометрия макромолекулы, ее концевые и боковые группы;
- для сополимеров — дополнительно соотношение сомономерных звеньев и их периодичность;
- для нуклеиновых кислот — последовательность нуклеотидов или эквивалентный ей признак (последовательность, комплементарная известной по всей длине; последовательность, связанная с известной вырожденностью генетического кода);
- для белков — последовательность аминокислот или эквивалентный ей признак (кодирующая последовательность нуклеотидов);
- для соединений с неустановленной структурой — физико-химические и иные характеристики (в том числе признаки способа получения), позволяющие отличить данное соединение от других.
Пример 4
Патент РФ № 2194803.
Электролит блестящего никелирования, содержащий сернокислый и хлористый никель, борную кислоту, блескообразующую добавку и воду, отличающийся тем, что он дополнительно содержит ингибитор наводороживания — дигидрохлорид-2-аллилокси-1,3-диморфолинопропан, имеющий структурную формулу
а в качестве блескообразующей добавки — 2,4-ди-нитрофенилгидразин, имеющий структурную формулу
O2N--------------NH— NH2,
no2
при следующем соотношении компонентов:
никель сернокислый, г — 220-260;
никель хлористый, г — 30-50;
кислота борная, г — 30-50;
дигидрохлорид-2-аллилокси-1,3-диморфолинопро-пан, ммоль/л — 1-3;
2,4- динитрофенилгидразин, ммоль/л— 1-3;
вода, л — до 1.
В случае нуклеиновых кислот и белков в формулу изобретения включаются их наименование с указанием назначения, номер последовательности (нуклеотидов — в перечне последовательностей для нуклеиновых
кислот, аминокислот — в перечне последовательностей для белков), а также физико-химические и иные характеристики, позволяющие отличить данный продукт от других. Если последовательность нуклеотидов кодирует аминокислотную последовательность белка, дополнительно приводится функция этого белка.
В формуле, относящейся к композиции, приводятся ее наименование с указанием назначения, входящие в композицию ингредиенты и, при необходимости, количественное содержание ингредиентов. Если в формуле изобретения, относящегося к композиции, приводится количественное содержание ингредиентов, они выражаются в любых однозначных единицах, как правило, двумя значениями, характеризующими минимальный и максимальный пределы содержания. Допускается указание содержания одного из ингредиентов композиции одним значением, а содержания остальных ингредиентов — в виде интервала значений по отношению к этому единичному значению (например, содержание ингредиентов приводится на 100 масс. ч. основного ингредиента композиции или на 1 л раствора). Допускается указание количественного содержания антибиотиков, ферментов, анатоксинов и т. п. в составе композиции в иных единицах, чем единицы остальных ингредиентов композиции (например, тыс. ед. гго отношению к массовому количеству остальных ингредиентов композиции).
Для композиций, назначение которых определяется только активным началом, а другие компоненты являются нейтральными носителями из круга традиционно применяющихся в композициях этого назначения, допускается указание в формуле только этого активного начала и его количественного содержания в составе композиции, в том числе в форме «эффективное количество».
Другим вариантом характеристики такой композиции может быть указание в ней, кроме активного начала, других компонентов (нейтральных носителей) в форме обобщенного понятия «целевая добавка». В этом случае указывается количественное содержание активного начала и целевой добавки.
Если в качестве признака изобретения указано известное вещество сложного состава, допускается использование его специального названия с указанием функции или свойства этого вещества и его основы. В этом случае в описании изобретения приводится источник информации, в котором это вещество описано.
Для характеристики композиций используются следующие признаки:
- качественный состав (ингредиенты);
- количественный состав (содержание ингредиентов);
- структура композиции;
- структура ингредиентов.
Для характеристики веществ, полученных путем
ядерного превращения, используются следующие
признаки:
- качественный состав (изотоп/изотопы элемента);
1328
Новый справочник химика и технолога
- количественный состав (число протонов и нейтронов);
- основные ядсрные характеристики: период полураспада, тип и энергия излучения (для радиоактивных изотопов).
Для характеристики штаммов микроорганизмов (пример 5) используются, в частности, следующие признаки:
- родовое и видовое названия штамма (на латинском языке);
- происхождение (источник выделения, родословная);
- гено- и хемотаксономическая характеристики;
- морфологическая, физиологическая (в том числе культуральная) характеристики;
- биотехнологическая характеристика (условия культивирования; название и свойства полезного вещества, продуцируемого штаммом; уровень активности/ироду к-тивности);
- вирулентность, антигенная структура, серологические свойства (для штаммов микроорганизмов медицинского и ветеринарного назначения);
- принцип гибридизации (для штаммов гибридных микроорганизмов).
Пример 5
Патент РФ № 2195490.
Штамм мицелиального гриба Trichoderma longibrachiatum В КМ F-3634 D (Всероссийская коллекция микроорганизмов при ИБФМ им. Г.К. Скрябина РАН) — продуцент комплекса карбогидраз, содержащего целлюлазы, бета-глюканазы, ксиланазы, пектиназы и маннаназы.
Для характеристики линий клеток растений или животных дополнительно используются, в частности, следующие признаки:
- число пассажей;
- кариологическая характеристика;
- ростовые (кинетические) характеристики;
- характеристика культивирования в организме животного (для гибридов);
- способность к морфогенезу (для клеток растений).
Для характеристики консорциумов микроорганизмов, клеток растений или животных дополнительно к перечисленным выше признакам используются, в частности, следующие признаки: фактор и условия адаптации и селекции, таксономический состав, число и доминирующие компоненты, заменяемость, тип и физиологические особенности консорциума в целом.
Для характеристики генетических конструкций соответствующим образом используются признаки, предусмотренные для характеристики устройств, при этом конструктивными элементами могут являться энхансер, промотор, терминатор, инициирующий кодон, линкер, фрагмент чужеродного гена, маркер, фланкирующие области.
Для характеристики трансформированной клетки используются следующие признаки:
- трансформирующий элемент;
- приобретаемые клеткой признаки (свойства);
- указание происхождения клетки (для прокариотической клетки — род, семейство и/или вид);
- таксономические признаки;
- мутация природного генома;
- условия культивирования клетки и иные характеристики, достаточные для того, чтобы отличить данную клетку от другой.
Для трансгенного растения используются, в частности, следующие признаки:
- наличие модифицированного элемента в геноме;
- приобретаемые растением признаки (свойства);
- происхождение растения;
- таксономическая принадлежность и иные характеристики, достаточные для того, чтобы отличить данное растение от другого.
Для трансгенного животного используются, в частности, следующие признаки:
- ген и/или ДНК, трансформированный в геном животного и кодирующий или экспрессирующий целевой продукт;
- приобретаемые животным признаки (свойства);
- продуцируемый животным модифицированный продукт;
- принадлежность животного (тип, порода и т. д.) и иные характеристики, достаточные для того, чтобы отличить данное животное от другого.
Пример 6
Патент РФ № 2195463.
1. Рекомбинантный полипептид, который способен к индукции защитного иммунитета против инфекции Helicobacter pylori у млекопитающего, причем данный полипептид включает в себя аминокислотную последовательность, которая идентична или имеет, по меньшей мере, 90 % гомологии с аминокислотной последовательностью с положения 1 по положение 260 SEQ ID NO: 2; с положения 28 по положение 260 SEQ ID NO: 2; с положения 1 по положение 260 SEQ ID NO: 4 или с положения 28 по положение 260 SEQ ID NO: 4.
2. Полипептид, по п. 1, отличающийся тем, что данный полипептид включает в себя аминокислотную последовательность, которая имеет, по меньшей мере, 95 % гомологии с аминокислотной последовательностью с положения 1 по положение 260 SEQ ID NO: 2; с положения 28 по положение 260 SEQ ID NO: 2; с положения I по положение 260 SEQ ID NO: 4 или с положения 28 по положение 260 SEQ ID NO: 4.
3. Полипептид, по пп. 1 или 2, отличающийся тем, что данный полипептид липидизирован.
4. Полипептид, по пп. 1, 2 или 3, для лечения или
профилактики инфекции Helicobacter pylori у млекопи-
тающего.
5. Полипептид, по пп. 1, 2 или 3, для изготовления
вакцины для использования в элисировании защитного
иммунного ответа против Helicobacter pylori.
Интеллектуальная собственность
1329
6. Полипептид, по пп. 1, 2 или 3, для изготовления вакцины для терапевтического лечения млекопитающего, инфицированного Helicobacter pylori, с целью уничтожить или подавить указанную инфекцию.
7. Полипептид, по пп. 1, 2 или 3, для изготовления вакцины для профилактического лечения млекопитающего при риске инфекции Helicobacter pylori.
8. Фрагмент ДНК, содержащий нуклеотидную последовательность, кодирующую полипептид, по пп. 1 или 2.
9. Фрагмент ДНК, содержащий нуклеотидную последовательность, кодирующую полипептид, по пп. 1 или 2, выбранный из группы (а) фрагмента ДНК, который идентичен или существенно подобен положениям 796-1572 SEQ ID NO: 1; положениям 874-1572 SEQ ID NO: 1; положениям 796-1572 SEQ ID NO: 3 или положениям 874-1572 SEQ ID NO: 3; и (б) фрагмента ДНК, который является вырожденным как результат генетического кода по отношению к фрагменту ДНК, определенному в (а), и который кодирует полипептид, по пп. 1 или 2.
10. Вакцинная композиция для индукции защитного иммунного ответа на инфекцию Helicobacter pylori, содержащая иммуногенно эффективное количество полипептида, по пп. 1,2 или 3, возможно, вместе с фармацевтически приемлемым носителем или разбавителем.
Описание изобретения
В законе [6] сказано, что формула изобретения должна быть полностью основана на описании изобретения. Т. к. реально описание составляется после составления формулы, следует внимательно следить, чтобы в описании и формуле не было расхождений, в частности по терминологии.
Описание начинается с названия изобретения. Если заявитель установил рубрику Международной патентной классификации (далее — МПК), к которой относится заявляемое изобретение, индекс этой рубрики приводится перед названием 32.
Описание содержит следующие разделы:
- «область техники, к которой относится изобретение»;
- «уровень техники»;
- «раскрытие изобретения»;
- «краткое описание чертежей» (если они содержатся в заявке);
- «осуществление изобретения»;
- «перечень последовательностей» (если последовательности нуклеотидов и/или аминокислот использованы для характеристики изобретения).
В описании должны присутствовать все перечисленные разделы. Нельзя заменять разделы описания отсылкой к другим документам.
32 Международная патентная классификация (МПК) широко применяется для классификации изобретений. Она указывается в качестве библиографических данных во всех публикациях, связанных с изобретениями и полезными моделями.
Название изобретения
Название изобретения должно быть кратким и точным. Как правило, название изобретения характеризует его назначение. Название, как мы видели выше, входит в формулу изобретения и в этом смысле очерчивает объем прав патентообладателя.
В названии группы изобретений приводится полное название лишь одного изобретения и сокращенно названия других; для вариантов изобретения приводится слово «Варианты».
В название изобретения, относящегося к химическому соединению, включается его наименование по одной из принятых в химии номенклатур или наименование группы (класса), к которой оно относится; может быть включено также конкретное назначение соединения, а для биологически активных соединений — вид биологической активности.
Для изобретения, относящегося к нуклеиновым кислотам или белкам, включаются наименование вещества и его назначение.
В название изобретения, относящегося к химическому соединению с неустановленной структурой, смеси неустановленного состава, в том числе полученной биотехнологическим путем, или к способу их получения, включается назначение или вид биологической активности вещества.
Для штамма микроорганизма включаются родовое и видовое (в соответствии с требованиями международной номенклатуры) названия биологического объекта на латинском языке и назначение штамма.
В название изобретения, относящегося к линии клеток растений или животных, включаются название линии клеток и назначение.
В разделе «Область техники, к которой относится изобретение» указывается область применения изобретения. Если таких областей несколько, указываются преимущественные.
Уровень техники
В данном подразделе описания изобретения приводятся сведения об известных заявителю аналогах изобретения с выделением из них аналога, наиболее близкого к изобретению (прототипа). В качестве аналога изобретения указывается средство того же назначения, известное из сведений, ставших общедоступными до даты приоритета изобретения. Непосредственно в тексте приводятся библиографические данные источника информации, в котором раскрыт аналог, его признаки с указанием тех из них, которые совпадают с существенными признаками заявляемого изобретения. Указываются известные заявителю причины, препятствующие получению технического результата, который обеспечивается изобретением.
Если описывается группа изобретений, сведения об аналогах приводятся для каждого изобретения.
Раскрытие изобретения
В этом разделе описания подробно раскрывается за-
дача, на решение которой направлено заявляемое
1330
Новый справочник химика и технолога
изобретение, с указанием обеспечиваемого им технического результата.
Приводятся все существенные признаки, характеризующие изобретение. Указываются совокупность признаков, обеспечивающая получение технического результата во всех случаях, на которые распространяется испрашиваемый объем правовой охраны, и признаки, характеризующие изобретение лишь в частных случаях, в конкретных формах выполнения или при особых условиях его использования.
Не допускается замена характеристики признака отсылкой к источнику информации, в котором раскрыт этот признак.
Для изобретений, относящихся к штамму микроорганизма, линии клеток растений или животных, если данные объекты депонированы и на это имеется указание в заявке, кроме их признаков дополнительно приводятся название или аббревиатура коллекции-депозитария, уполномоченной на депонирование таких объектов, и регистрационный номер, присвоенный им коллекцией. Если указанные объекты не депонированы, приводится обозначение, присвоенное им автором.
Последовательность нуклеотидов или аминокислот в случае использования ее для характеристики изобретения представляется путем указания номера последовательности в перечне последовательностей в виде «SEQ ID NO...» с приведением соответствующего свободного текста, если характеристика последовательности в перечне последовательностей дана с использованием такого текста.
Для группы изобретений сведения, раскрывающие суть изобретения, в том числе и технический результат, приводятся для каждого изобретения.
В разделе «Краткое описание чертежей» дается перечень фигур с краткими пояснениями к тому, что изображено на каждой из них. Если используются другие иллюстративные материалы, приводится описание и их.
Осуществление изобретения
В этом разделе приводятся сведения, необходимые для осуществления изобретения, при этом подробность описания должна быть ориентирована на среднего специалиста в данной области техники.
Осуществление изобретения показывается предпочтительно путем приведения примеров, со ссылками на чертежи или иные графические материалы, если они имеются.
Для признака, выраженного общим понятием, в частности представленного на уровне функционального обобщения, описываются средство для реализации такого признака или методы его получения либо указывается на его известность.
Кроме того, приводятся сведения, подтверждающие возможность получения технического результата, который указан в разделе описания «Раскрытие изобретения». При использовании в формуле количественных признаков, выраженных в виде интервала значений,
показывается возможность получения технического результата во всем этом интервале.
Для изобретения, относящегося к устройству, приводится описание его конструкции (в статическом состоянии) и действия устройства (работа) или способа использования со ссылками на фигуры чертежей, а при необходимости — на иные поясняющие материалы (эпюры, временные диаграммы и т. д.).
Для изобретения, относящегося к способу, в примерах его реализации указываются последовательность действий (приемов, операций) над материальным объектом, а также условия проведения действий, конкретные режимы (температура, давление и т. п.), используемые при этом материальные средства (устройства, вещества, штаммы и т. п.), если это необходимо. Если способ характеризуется использованием средств, известных до даты приоритета изобретения, достаточно эти средства раскрыть таким образом, чтобы можно было осуществить изобретение. При использовании неизвестных средств приводится их характеристика и, в случае необходимости, прилагается графическое изображение.
В способе получения группы (ряда) химических соединений, описываемых общей структурной формулой, приводится пример получения этим способом соединения группы (ряда), а если группа (ряд) включает соединения с разными по химической природе радикалами, дается такое количество примеров, которое достаточно для подтверждения возможности получения соединений с этими разными радикалами. Для полученных соединений, входящих в группу (ряд), приводятся структурные формулы, подтвержденные известными методами, и физико-химические характеристики, а для неизвестных соединений и для известных соединений, назначение которых ранее не было установлено, — также сведения о назначении или биологической активности.
В способе получения химических соединений с неустановленной структурой или смесей неустановленного состава приводятся: характеристики, позволяющие отличить данные соединения от других; сведения об исходных реагентах для получения соединений или смесей, а также данные, подтверждающие возможность реализации указанного заявителем назначения этих соединений или смесей, в частности сведения о свойствах, обусловливающих такое назначение.
Для изобретения, относящегося к способу лечения, диагностики, профилактики состояния или заболевания людей или животных, приводятся сведения о выявленных факторах, объясняющих влияние его использования на этиопатогенез заболевания, или другие достоверные данные, подтверждающие его пригодность для лечения, диагностики или профилактики указанного состояния или заболевания (полученные, в частности, в эксперименте на адекватных моделях или иным путем).
Для изобретения, относящегося к веществу — хими-
ческому соединению с установленной структурой, при-
водятся структурная формула, доказанная известными
методами, физико-химические константы, описывается
Интеллектуальная собственность
1331
способ, которым соединение получено, и показывается возможность использования изобретения по указанному назначению. Если химическое соединение получено с использованием штамма микроорганизма, линии клеток растений или животных, описывается способ его получения с участием этого штамма, линии, данные о них, а при необходимости даются и сведения о депонировании.
Для биологически активного соединения приводятся количественная характеристика активности и сведения о токсичности, а в случае необходимости — об избирательности действия и другие показатели.
Если изобретение относится к группе (ряду) химических соединений с установленной структурой, описываемых общей структурной формулой, подтверждается возможность получения всех соединений группы (ряда) путем приведения общей схемы способа получения, а также примера получения конкретного соединения группы (ряда), а если группа (ряд) включает соединения с разными по химической природе радикалами— примеров, достаточных для подтверждения возможности получения соединений с этими разными радикалами.
Для полученных соединений приводятся также их структурные формулы, подтвержденные известными методами, физико-химические константы, доказательства возможности реализации указанного назначения с подтверждением такой возможности в отношении некоторых соединений с разными по химической природе радикалами. Если соединения являются биологически активными, даются показатели активности и токсичности для этих соединений, а в случае необходимости — показатели избирательности действия и др. Для промежуточных соединений показывается также возможность их переработки в известный конечный продукт либо возможность получения из них нового конечного продукта с конкретным назначением или биологической активностью.
Если изобретение относится к нуклеиновым кислотам или белкам, приводится указание номера последовательности в перечне последовательностей (нуклеотидов — в случае нуклеиновых кислот, аминокислот — в случае белков), а также физико-химические и иные характеристики, позволяющие отличить данный продукт от других. Описывается способ, которым продукт получен, и показывается возможность использования этого продукта по определенному назначению. Последовательность нуклеотидов или аминокислот представляется путем указания ее номера в перечне последовательностей в виде «SEQ ID NO...» с приведением соответствующего свободного текста, если характеристика последовательности в перечне последовательностей дана с использованием такого текста.
Для композиции (смеси, растворы, сплавы, стекло и т. п.) приводятся примеры, в которых указываются ингредиенты, входящие в состав композиции, их характеристика и количественное содержание. Описывается способ получения композиции, а если она содержит
в качестве ингредиента новое вещество, описывается способ его получения. В приводимых примерах содержание каждого ингредиента указывается в таком единичном значении, которое находится в пределах указанного в формуле изобретения интервала значений; при выражении количественного содержания ингредиентов в формуле изобретения в процентах (по массе или объему) суммарное содержание всех ингредиентов, указанных в примере, равняется 100 %.
Для изобретения, относящегося к штамму микроорганизма, линии клеток растений или животных либо к консорциумам штаммов или клеток, приводится описание способа получения штамма, линии клеток, консорциума. Если его описание недостаточно для осуществления изобретения, представляются сведения о депонировании штамма, линии клеток, консорциума или штаммов, входящих в консорциум (название или аббревиатура коллекции-депозитария, ее адрес, регистрационный номер, присвоенный коллекцией депонированному объекту), дата которого не должна быть более поздней, чем дата подачи заявки или дата приоритета, если он испрашивался.
Для изобретения, относящегося к генетической конструкции, приводятся сведения о его конструктивном выполнении, способе получения и данные, подтверждающие возможность реализации указанного назначения. Если признак генетической конструкции в формуле изобретения охарактеризован с использованием общего понятия, подтверждается возможность получения ряда генетических конструкций с реализацией указанного назначения.
Перечень последовательностей нуклеотидов и/или аминокислот
Этот раздел приводится только при патентовании последовательностей.
Дается детальное раскрытие последовательностей нуклеотидов и/или аминокислот, если они являются неразветвленными последовательностями из четырех и более аминокислот или неразветвленными последовательностями из десяти или более нуклеотидов.
Каждой последовательности должен быть присвоен отдельный номер. Номера последовательностей должны начинаться с единицы и увеличиваться последовательно на целое число.
Номер каждой последовательности в перечне должен соответствовать ее номеру, указанному в описании, формуле изобретения или на графических изображениях. Последовательности нуклеотидов и аминокислот должны представляться, по крайней мере, с помощью одной из следующих возможностей:
- только последовательностью нуклеотидов;
- только последовательностью аминокислот;
- последовательностью нуклеотидов совместно с соот-
ветствующей последовательностью аминокислот.
В последнем случае последовательность аминокис-
лот должна быть представлена как отдельная последо-
вательность аминокислот, имеющая отдельный номер.
1332
Новый справочник химика и технолога
Составление других материалов заявки
Материалы, поясняющие сущность изобретения
Материалы, поясняющие сущность изобретения, могут быть оформлены в виде графических изображений (чертежей, схем, рисунков, графиков, эпюр, осциллограмм и т. д.), фотографий и таблиц. Рисунки представляются в том случае, когда невозможно проиллюстрировать изобретение чертежами или схемами.
Фотографии представляются как дополнение к графическим изображениям. В исключительных случаях, например для иллюстрации этапов выполнения хирургической операции, фотографии могут быть представлены как основной вид поясняющих материалов.
Чертежи, схемы и рисунки представляются на отдельном листе, в правом верхнем углу которого рекомендуется приводить название изобретения.
Реферат
Реферат служит для целей информирования об изобретении и представляет собой сокращенное изложение содержания описания изобретения, включающее название изобретения, характеристику области техники, к которой относится изобретение, характеристику сущности изобретения с указанием достигаемого технического результата. Суть изобретения излагается в свободной форме с указанием всех существенных признаков изобретения, нашедших отражение в независимом пункте формулы изобретения.
Реферат может содержать дополнительные сведения, в частности указание на наличие и количество зависимых пунктов формулы, графических изображений, таблиц.
Рекомендуемый объем текста реферата — до 1000 печатных знаков.
Заявление о выдаче патента
Заявление является важнейшим документом заявки и составляется на типовом бланке, содержащем три листа33.
Требования к оформлению материалов заявки
Материалы заявки подаются в трех экземплярах на русском языке. Если заявка (описание изобретения, формула) подается не на русском языке, то представляется их перевод на русский язык. К заявке прилагается документ, подтверждающий уплату патентной пошлины в установленном размере, или документ, подтверждающий основания для освобождения (уменьшения размера, отсрочки) от уплаты патентной пошлины.
Для штамма микроорганизма предоставляется документ о депонировании, а для последовательности нуклеотидов и/или аминокислот прилагается машиночитаемый носитель информации с записью копии того же перечня последовательностей.
Заявка выполняется на листах белой бумаги форматом А4 (210 х 297 мм) только на одной стороне листа текстом, напечатанным через 1,5 интервала, с высотой заглавных букв не менее 2,1 мм. Графические символы, латинские наименования, латинские и греческие буквы, математические и химические формулы или символы выполняются, как правило, в графических редакторах, но могут быть вписаны чернилами, пастой или тушью черного цвета. Не допускается смешанное написание формул — в печатном виде и от руки.
Структурные формулы химических соединений, как правило, представляются на отдельном листе (как и графические материалы) с нумерацией каждой как отдельной фигуры и приведением ссылочных обозначений. Для структурных химических формул следует применять общеупотребительные символы элементов и четко указывать связи между элементами и радикалами.
Графические изображения (чертежи, схемы, графики, рисунки и т. п.) выполняются черными нестираемыми четкими линиями одинаковой толщины по всей длине.
Нумерация листов [8] осуществляется арабскими цифрами, последовательно, начиная с единицы, с использованием отдельных серий нумерации. К первой серии нумерации относится заявление, ко второй — описание, формула изобретения и реферат. Если заявка содержит чертежи или иные материалы, они нумеруются в виде отдельной серии. Так же нумеруется и перечень последовательностей нуклеотидов и/или аминокислот.
Подача заявки и ведение переписки с экспертизой
Оформленная заявка на изобретение подается в орган патентного ведомства РФ — Федеральный институт промышленной собственности (ФИПС), находящийся в Москве (см. также 9.2.2.2). Заявка может быть подана непосредственно в ФИПС или направлена по почте (ФИПС, Бережковская наб., д. 30, корп. 1, Москва, Г-59, ГСП-5, 123995). В настоящее время начат эксперимент с подачей заявок в электронной форме.
Федеральный институт промышленной собственности сообщает заявителю по почте о всех юридически значимых действиях и решениях, которые выносит экспертиза. Важно помнить, что сроки ответа на запросы и решения экспертизы установлены законодательно и важнейшие действия заявителя — подача заявки, ходатайство о проведении экспертизы, выдача патента — « 34
сопровождаются уплатой соответствующих пошлин .
33 Заявление подписывает заявитель (будущий патентообладатель или его представитель — патентный поверенный). Автор подписывает заявление только в случае, если он является будущим патентообладателем.
34 Размеры пошлин для различных категорий заявителей
указаны в Положении «О пошлинах за патентование изобре-
тений, полезных моделей, промышленных образцов, регист-
рацию товарных знаков, знаков обслуживания, наименований
мест происхождения товаров, предоставление права пользо-
вания наименованиями мест происхождения товаров». Так же
как и другие документы ФИПС, Положение доступно на сай-
Интеллектуальная собственность
1333
Следует отвечать на запросы и решения ФИПС в установленные сроки. При пропуске этих сроков ответы могут быть направлены и позднее, но с уплатой соответствующих пошлин за просрочку.
Преобразование заявок
Заявка на получение патента на изобретение может быть преобразована в заявку на получение патента на полезную модель. Преобразование должно быть осуществлено не позднее даты принятия решения о выдаче патента на изобретение, а в случае принятия решения об отказе в выдаче патента — до того, как будет исчерпана возможность подачи возражения против этого решения. Такое преобразование можно рекомендовать в тех случаях, когда в процессе экспертизы выяснится, что изобретение не отвечает критерию изобретательского уровеня.
При преобразовании заявок сохраняются приоритет изобретения или полезной модели и дата подачи заявки.
9.2.3. Полезная модель
В качестве полезной модели охраняется техническое решение, относящееся к устройству.
Таким образом, в качестве полезных моделей, в отличие от изобретений, может охраняться только ограниченный класс объектов — устройства.
9.2.3.1. Условия патентоспособности
Полезная модель признается соответствующей условиям патентоспособности, если она является новой и промышленно применимой. В отличие от изобретений к полезным моделям не применяется критерий изобретательского уровеня.
Новизна
Полезная модель является новой, если совокупность ее существенных признаков не известна из уровня техники. Уровень техники включает ставшие общедоступными до даты приоритета полезной модели опубликованные в мире сведения о средствах того же назначения, что и заявленная полезная модель, а также сведения об их применении в РФ. В уровень техники также включаются при условии их более раннего приоритета все поданные в РФ другими лицами заявки на изобретения и полезные модели (кроме отозванных) и запатентованные в РФ изобретения и полезные модели* 35.
Промышленная применимость
Полезная модель является промышленно применимой, если она может быть использована в промышленности, сельском хозяйстве, здравоохранении и других
те ведомства www.fips.ru. Следует помнить, что некоторым категориям граждан и организаций предоставляются льготы по уплате пошлин.
35 В отличие от изобретения, для критерия «новизна» полезной модели специально подчеркнуто, что в уровень техники включены сведения о применении средств того же назначения в Российской Федерации.
отраслях деятельности (толкование термина «промышленная применимость» см. в 9.2.2 «Изобретение»),
Правовая охрана не предоставляется'.
- решениям, касающимся только внешнего вида изделий и направленным на удовлетворение эстетических потребностей;
- топологиям интегральных микросхем;
- решениям, противоречащим общественным интересам, принципам гуманности и морали.
Срок действия патента на полезную модель
Патент на полезную модель действует до истечения 5 лет с даты подачи заявки при условии уплаты ежегодных патентных пошлин. Срок действия патента на полезную модель может быть продлен по ходатайству патентообладателя, но не более чем на 3 года.
Действие патента при неуплате ежегодных патентных пошлин может быть восстановлено в течение 3 лет с даты истечения срока уплаты указанной патентной пошлины, но до истечения срока действия патента. При этом у лиц, которые в период, когда не действовал патент, начали использовать полезную модель или сделали для этого необходимые приготовления, возникает право послепользования.
9.2.3.2. Процесс получения патента на полезную модель
Процесс получения патента на полезную модель отличается от процесса получения патента на изобретение только процедурой прохождения заявки в патентном ведомстве. Само же оформление заявки на получение патента на полезную модель аналогично составлению такой же заявки на изобретение, когда она составляется на устройство. Отличие в оформлении этой заявки состоит лишь в том, что нс надо доказывать, что предложение отвечает критерию изобретательского уровня, т. к. этот критерий не применяется к полезным моделям. Незначительно отличаются и бланки заявления.
На рис. 9.4 графически представлены основные этапы процесса получения патента на полезную модель.
Рис. 9.4. Процесс получения патента на полезную модель
Подача заявки
Процесс начинается с подачи заявки, даты приори--тета (7) в патентное ведомство. Заявка может быть подана непосредственно в патентное ведомство, в ФИПС или отправлена по почте. Процесс прохождения заявки в патентном ведомстве сопровождается уплатой патентных пошлин за юридически значимые действия, связанные с получением патента, с обязательным уведомлением заявителем ведомства об их уплате. За подачу заявки уплачивается соответствующая пошлина.
1334
Новый справочник химика и технолога
Экспертиза заявки на полезную модель
В течение времени (А), которое, по сути, является формальной экспертизой, но отличается от формальной экспертизы изобретения, проверяется:
- наличие документов, которые должны содержаться в заявке или прилагаться к ней;
- правильность уплаты патентной пошлины;
- отсутствие явного нарушения требования единства полезной модели;
- подана ли заявка на техническое решение, охраняемое в качестве полезной модели;
- правильность классифицирования полезной модели по МПК, осуществленного заявителем.
Если в процессе экспертизы заявки установлено, что заявка оформлена с нарушением требований или подана на объект, которому не предоставляется охрана как полезной модели, заявителю направляется запрос с указанием обнаруженных недостатков, приведением необходимых аргументов правового характера и предложением представить исправленные или недостающие документы в течение 2 месяцев с даты его получения.
Заметим, что в процессе экспертизы не проверяется новизна полезной модели и промышленная применимость.
При положительном исходе экспертизы полезной модели заявителю высылается решение о выдаче патента на полезную модель (2). После уплаты заявителем соответствующей пошлины за выдачу патента (процесс В) публикуются сведения о патенте на полезную модель и выдается патент.
9.2.3.3. Особенности патента на полезную модель
Патент на полезную модель выдается по регистрационному принципу. Если заявка оформлена правильно и объект относится к объектам, которые защищаются как полезные модели, то патент выдается без проверки на новизну. Такой порядок предусмотрен для того, чтобы патенты на полезные модели выдавались быстрее, т. к. срок их действия сравнительно невелик — не более 8 лет.
Значит ли это, что могут быть выданы патенты на те устройства, которые известны из уровня техники? Да, такие патенты могут быть выданы и выдаются. Если они кому-нибудь мешают или патентообладатель предъявляет производителям необоснованные претензии в нарушении патента, патент на полезную модель (как, впрочем, и патенты на изобретение и промышленный образец) в течение всего срока его действия может быть признан недействительным полностью или частично в случае несоответствия условиям патентоспособности, установленным Патентным законом.
Возражение против выдачи патента подается в Палату по патентным спорам Патентного ведомства Российской Федерации.
Следует заметить, что заявка на получение патента на изобретение в процессе экспертизы может быть преобразована в такую же заявку на полезную модель, как
и наоборот, заявка на получение патента на полезную модель до даты принятия решения о выдаче патента может быть преобразована в такую же заявку на изобретение.
Охрана новых устройств с помощью полезных моделей пока применяется не очень широко, т. к. в СССР такого объекта охраны не существовало.
9.2.4. Промышленный образец
В качестве промышленного образца охраняется художественно-конструкторское решение изделия промышленного или кустарно-ремесленного производства, определяющее его внешний вид [6]. Внешний вид изделия составляют, в частности, форма, контуры, линии, сочетания цветов, текстура или фактура материала, декор, в том числе орнаментация.
Промышленные образцы могут быть объемными и плоскостными.
Правовая охрана предоставляется промышленному образцу, если он является новым и оригинальным.
Промышленный образец признается новым, если совокупность его существенных признаков, нашедших отражение на изображениях изделия и приведенных в перечне существенных признаков промышленного образца, не известна из сведений, ставших общедоступными в мире до даты приоритета.
При установлении новизны также учитываются при условии их более раннего приоритета все поданные в России другими лицами заявки на промышленные образцы (кроме отозванных) и запатентованные промышленные образцы.
Промышленный образец признается оригинальным, если его существенные признаки обусловливают творческий характер особенностей изделия.
К существенным признакам промышленного образца относятся признаки, определяющие эстетические и (или) эргономические особенности внешнего вида изделия, в частности форма, конфигурация, орнамент и сочетание цветов [6]. На рис. 9.5 приведены примеры промышленных образцов из официального бюллетеня патентного ведомства.
На рисунке видно, что при официальной публикации приводятся библиографические данные о патенте, рисунок (фотография) изделия и перечень существенных признаков промышленного образца.
Объекты, не считающиеся патентоспособными
Не считаются патентоспособными:
- объекты, обусловленные исключительно технической функцией изделия;
- объекты архитектуры (кроме малых архитектурных форм), промышленных, гидротехнических и других стационарных сооружений;
- объекты неустойчивой формы из жидких, газообразных, сыпучих или им подобных веществ;
- изделия, противоречащие общественным интересам, принципам гуманности и морали.
Интеллектуальная собственность
1335
1ШБПО№10 16.10.2003
Промышленные образцы
(51) 14-02
(11) 53425 (13) S
(21)2002500600 (22)09.04.2002
(15) 16.10.2003 (24)09.04.2002
(31)2001-28837 (33) KR (32) 16.10.2001
(72) ПАРК CeaJla(KR)
(71) ЭЛ ДЖИ ЭЛЕКТРОНИКС ИНК. (KR)
(73) ЭЛ ДЖИ ЭЛЕКТРОНИКС ИНК. (KR)
(54) РАДИОТЕЛЕФОН
(55)
(98) 129010, Москва, ул. Б. Спасская, 25, стр.З, ООО "Юридическая фирма Городисский и Партнеры", начальнику отдела промышленных образцов пат. пов. А.К. Васильцу, per. № 390
(54) МОНИТОР
(55)
(57) Монитор, характеризующийся:
- составом композиционных элементов: прямоугольная лицевая панель с плоским прямоугольным экраном, задний кожух и подставка;
- наличием органов управления в нижней части лицевой панели;
- формообразованием заднего кожуха на основе четырехугольной горизонтально ориентированной усеченной пирамиды с S-образно изогнутой верхней стороной;
- выполнением боковых и заднего периферийных участков верхней стороны заднего кожуха скошенными;
- наличием вентиляционных прорезей на верхней стороне заднего кожуха;
отличающ ийся:
- наличием панели управления в нижней части лицевой панели;
- расположением органов управления на панели управления;
- выполнением панели управления горизонтально вытянутой и ограниченной сверху и снизу выгнутыми вниз линиями;
- выполнением вентиляционных прорезей на верхней стороне заднего кожуха U-образными.
(11)53426 (13) S (22) 19.10.2001 (24) 19.10.2001 (32) 30.04.2001
(51) 14-03
(21)2001502008
(15) 16.10.2003
(31)2001-11391 (33) KR
(72) ПАРК Хиун Cook (KR)
(73) ЛГ Электронике Инк. (KR)
(98) 129010, Москва, ул. Б. Спасская, 25, стр.З, ООО "Юридическая фирма Городисский и Партнеры", начальнику отдела промышленных образцов пат. пов. А.К. Васильцу, per. № 390
(57) Радиотелефон, характеризующийся:
- наличием корпуса, в основу формообразования которого положен удлиненный прямоугольный параллелепипед с S-об-разно изогнутой передней поверхностью со сходящимися верхними и нижними участками боковых сторон;
- наличием в верхней части передней стороны корпуса панели, ограниченной снизу выпуклой кромкой, по бокам - кромками, сходящимися в верхнем направлении;
- композиционным решением панели - сверху вниз расположены: средство для вывода звуковой информации, прямоугольный дисплей и фигурная функциональная кнопка;
- наличием клавиатуры набора номера под панелью;
- выполнением кнопок клавиатуры набора номера эллипсообразной формы;
отличающийся:
- выполнением средства для вывода звуковой информации в виде эллипсообразного углубления с прорезями;
- выполнением фигурной функциональной кнопки, состоящей из наружной эллипсообразной части и из внутренней кольцевой части;
- наличием в нижней части передней поверхности корпуса выступа в форме сегмента эллипсоида с прорезью для ввода звуковой информации;
- наличием Т-образного зажима на задней поверхности корпуса.
Рис. 9.5. Примеры промышленных образцов
1336
Новый справочник химика и технолога
Срок действия патента на промышленный образец
Патент на промышленный образец действует до истечения 10 лет с даты подачи заявки при условии уплаты ежегодных патентных пошлин. Срок действия патента на полезную модель может быть продлен по ходатайству патентообладателя, но не более чем на 5 лет.
Действие патента на промышленный образец, так же как и патентов на изобретение и полезную модель, может быть восстановлено, и при этом возникает право послепользования.
9.2.4.1. Процесс получения патента на промышленный образец
Процесс получения патента на промышленный образец приведен на рис. 9.6.
Рис. 9.6. Процесс получения патента на промышленный образец
Заявка на промышленный образец подается в патентное ведомство, дата подачи заявки (/) является датой приоритета. При подаче заявки уплачивается патентная пошлина за подачу заявки и проведение экспертизы.
Заявка на выдачу патента должна содержать:
- заявление о выдаче патента с указанием автора промышленного образца и лица, на имя которого испрашивается патент, а также их местожительства или местонахождения;
- комплект изображений изделия, дающих полное детальное представление о внешнем виде изделия (фотографии, рисунки или иные репродукции, в том числе выполненные средствами компьютерной графики);
- чертеж общего вида изделия, эргономическую схему, конфекционную карту, если они необходимы для раскрытия сущности промышленного образца;
- описание промышленного образца;
- перечень существенных признаков промышленного образца.
В течение времени (А), которое называется формальной экспертизой, в основном проверяется наличие всех документов, которые необходимы для рассмотрения заявки, соблюдение установленных требований к документам заявки, правильность уплаты патентной пошлины. Если у экспертизы возникли вопросы к заявителю, она посылает запрос. По окончании формальной экспертизы заявителю высылается уведомление о положительном результате формальной экспертизы заявки.
Сразу по окончании формальной экспертизы начинается экспертиза по существу (3). В процессе проведения экспертизы по существу, в течение времени (В), в основном проводится проверка соответствия промышленного образца установленным условиям патентоспособности.
По окончании экспертизы по существу (4) принимается рещение о выдаче патента или об отказе в его выдаче и заявителю направляется соответствующее уведомление.
Выдача патента (5) — время до выдачи (С) — производится после уплаты соответствующей пошлины. Выдача патента производится вместе с официальной публикацией библиографических данных патента, рисунков и перечня существенных признаков промышленного образца.
9.2.5. Товарный знак, знак обслуживания
Товарный знак позволяет потребителю выделить ваши товары и услуги среди массы других однородных товаров. В юридическом смысле товарными знаками и знакалт обслуживания6 называют обозначения, на которые распространяются исключительные права, однако товарный знак может использоваться его владельцем и без регистрации36 37, но в этом случае он нс имеет исключительных прав на этот знак, что означает, что другие лица также могут его применять.
Исключительные права на товарный знак возникают после регистрации знака в патентном ведомстве и позволяют избежать риска несанкционированного и бесплатного его использования. Это особенно важно в случаях, когда ваши товары или услуги становятся привлекательными для потребителя за счет своих потребительских свойств среди массы товаров других производителей. С другой стороны, мы знаем множество случаев, когда привлекательность товара или услуги создается самим товарным знаком, который потребители знают и которому доверяют.
В обыденной жизни и бизнесе применяется достаточно много терминов, которые, но расхожему мнению, относятся к товарному знаку: товарная марка, бренд, логотип, слоган и т. д. Все эти термины не отражают точного юридического понятия «товарный знак».
Создание привлекательного для потребителя товарного знака — непростой процесс. Учитываются вид и характер маркируемых товаров, профиль предприятия, культурные традиции. Однако следует помнить, что главным для судьбы знака является деятельность его владельца: если успешно и все более широко распространяется деятельность, все более известным и привлекательным становится знак.
Регистрация товарных знаков в Российской Федерации регулируется законом «О товарных знаках, знаках обслуживания и наименованиях мест происхождения товаров» [9]. В соответствии с этим законом
36 Знак обслуживания и товарный знак — это обозначения, которые используются для различения: однородных услуг — знак обслуживания, товаров — товарный знак.
37 Существуют товарные знаки, на которые распространяются исключительные права и без регистрации знаков — это общеизвестные знаки, о которых речь пойдет ниже.
Интеллектуальная собственность
1337
продолжает действовать регистрация знаков, которая велась в СССР с 1962 г.
Юридический статус товарного знака значительно отличается от статуса изобретений, полезных моделей и промышленных образцов.
9.2.5.1. Основные положения
С точки зрения закона [9] товарный знак и знак обслуживания — обозначения, служащие для индивидуализации товаров, выполняемых работ или оказываемых услуг юридических или физических лиц.
Таким образом, понятия «товарный знак» и «знак обслуживания» различаются только тем, что товарный знак применяется для индивидуализации товаров, а знак обслуживания — для индивидуализации услуг и выполняемых работ.
Товарный знак и знак обслуживания (далее — товарный знак) регистрируются на юридическое лицо, но могут быть зарегистрированы и на физическое лицо, осуществляющее предпринимательскую деятельность без образования юридического лица.
Товарные знаки регистрируются в отношении определенных товаров или услуг по выбору правообладателя, и исключительные права на знак действуют в отношении товаров и/или услуг, для индивидуализации которых он зарегистрирован, или однородных товаров.
При регистрации знака выдается свидетельство на товарный знак. Правовая охрана товарного знака действует в течение 10 лет с возможным продлением каждый раз еще на 10 лет.
9.2.5.2. Использование товарного знака
Товарные знаки можно использовать и без регистрации, однако значимые для бизнеса следует регистрировать. В качестве товарного могут применяться самые разнообразные обозначения, служащие для индивидуализации товаров. Это могут быть названия фирм, новых продуктов, лекарств, программных продуктов, разнообразные этикетки, девизы, доменные имена и др. Если не регистрировать свои знаки, то другое лицо может это сделать и получит на эти знаки исключительные права, ведь для знаков нет понятия «новизна», как для изобретений. Существует достаточно много ограничений для регистрации, с которыми мы познакомимся ниже. Среди них есть ограничения, препятствующие конкурентам регистрировать обозначения, уже используемые в бизнесе. Но уповать на эти ограничения нельзя. Известны многочисленные случаи, когда используемые одними фирмами без регистрации товарные знаки регистрировались другими лицами, в том числе и с недобросовестными, с точки зрения бизнеса, целями, и первые были вынуждены переходить на использование других знаков, выкупать права на использование своих же знаков или сворачивать какие-то направления бизнеса.
Следует помнить, что регистрация неиспользуемых товарных знаков может быть аннулирована в связи
с неиспользованием товарного знака непрерывно в течение любых 3 лет после его регистрации. Использованием товарного знака считается применение его на товарах, для которых товарный знак зарегистрирован, их упаковке, а также в рекламе, печатных изданиях, на официальных бланках, на вывесках, при демонстрации экспонатов на выставках и ярмарках.
Правообладатель может проставлять рядом с товарным знаком предупредительную маркировку в виде латинской буквы R или ® либо словесного обозначения «товарный знак» или «зарегистрированный товарный знак».
Правообладатель может использовать зарегистрированный знак сам, передать право на его использование другому лицу путем уступки знака или выдачи лицензии.
9.2.5.3. Исключительные права на товарный знак
Правообладатель вправе использовать товарный знак и запрещать использование его другими лицами [9]. Нарушением исключительного права правообладателя признается использование без его разрешения в гражданском обороте на территории РФ товарного знака или сходного с ним до степени смешения обозначения, в том числе размещение:
- на товарах, этикетках, упаковках этих товаров, которые производятся, предлагаются к продаже, продаются, демонстрируются на выставках и ярмарках или иным образом вводятся в гражданский оборот на территории РФ, либо хранятся и (или) перевозятся с этой целью, либо ввозятся на территорию РФ;
- при выполнении работ, оказании услуг;
- на документации, связанной с введением товаров в тражданский оборот;
- в предложениях к продаже товаров;
- в сети Интернет, в частности в доменном имени и при других способах адресации.
Товары, этикетки, упаковки этих товаров, на которых незаконно используется товарный знак или сходное с ним до степени смешения обозначение, являются контрафактными.
При нарушении исключительных прав на товарный знак нарушитель возмещает владельцу убытки, и за счет нарушителя удаляется с контрафактных товаров незаконно используемый товарный знак, за исключением случаев когда они передаются правообладателю в счет возмещения убытков или конфискуются в доход государства.
9.2.5.4. Виды знаков
В качестве товарных знаков могут быть зарегистрированы словесные, изобразительные, объемные и другие обозначения или их комбинации.
Словесные: сочетания букв, имеющие словесный характер, словосочетания, предложения, другие единицы языка, а также их сочетания.
Изобразительные: изображения живых существ, предметов, природных и иных объектов, а также фигуры любых форм, композиции линий, пятен, фигур на плоскости.
1338
Новый справочник химика и технолога
Объемные: трехмерные объекты, фигуры и комбинации линий, фигур.
К комбинированным обозначениям относятся комбинации элементов разного вида: изобразительных, словесных, объемных и т. д.
В качестве товарных знаков могут быть зарегистрированы звуковые, световые и иные обозначения.
Товарный знак может быть зарегистрирован в любом цвете или цветовом сочетании.
Приведем примеры объемного (рис. 9.7), изобразительного (рис. 9.8) и словесного (рис. 9.9) товарных знаков из Официального бюллетеня российского агентства по патентам и товарным знакам «Товарные знаки, знаки обслуживания и наименования мест происхождения товаров».
Как видно из приведенных примеров, товарные знаки регистрируются для определенных классов товаров или услуг38 39, и, как было сказано выше, исключительные права на знак действуют только в отношении этих товаров и/или услуг.
9.2.5.5. Нерегистрируемые обозначения
Далеко не все обозначения могут быть зарегистрированы в качестве товарных знаков. Одним из главных требований, предъявляемых к товарному знаку при регистрации, является наличие различительной способности. Различительная способность — очень емкое и многогранное понятие, являющееся одним из основных свойств товарного знака. Если знак не будет обладать различительной способностью, то как он будет выполнять свою функцию: индивидуализировать для потребителя товары, выполняемые работы или оказываемые услуги среди однородных товаров, работ или услуг?
Например, известна регистрация в США запахового товарного знака. В ответ на вопрос: для какого товара используется этот знак, чаще всего называют парфюмерию, духи или другие товары, обладающие запахом. Но разве может служить для индивидуализации товара его свойство, ведь один и тот же товар может производится разными производителями с практически одинаковыми свойствами. Таким образом, товар, который обозначается этим знаком, не должен изначально обладать выраженным запахом. В данном случае запаховый товар-„ 39
ныи знак зарегистрирован для пряжи .
38 В публикации товарных знаков перечень товаров и услуг располагается за международным цифровым кодом (57), служащим для идентификации библиографических данных, относящихся к товарным знакам, согласно Стандарту ВОИС. Другие цифровые коды означают, в частности, следующее: (11) — номер свидетельства на товарный знак; (22) — дата поступления заявки в патентное ведомство; (15) — дата регистрации; (18) — дата окончания срока действия зарегистрированного знака; (73) — владелец товарного знака.
39 Запаховые товарные знаки практически не регистрируются патентными ведомствами. Это связано с тем, что запах трудно хранить и идентифицировать, поэтому регистрация таких знаков в дальнейшем, вероятно, будет единичной.
К обозначениям, не обладающим различительной способностью, могут относиться, в частности [10]:
- обозначения, представляющие собой отдельные буквы, цифры, не имеющие характерного графического исполнения; сочетания букв, не имеющие словесного характера; линии, простые геометрические фигуры, а также их сочетания;
- реалистические или схематические изображения товаров;
- трехмерные объекты, форма которых обусловлена исключительно функциональным назначением;
- общепринятые наименования, представляющие собой, как правило, простые указания товаров, заявляемые для обозначения этих товаров; общепринятые сокращенные наименования организаций, предприятий, ограслей и их аббревиатуры.
Различительная способность знака не есть постоянная величина. Некоторые простые знаки, например сочетания цифр, в процессе их использования для обозначения товаров приобрели в глазах потребителя различительную способность и могут быть зарегистрированы в качестве товарных знаков. Другие товарные знаки в процессе их употребления теряют свою различительную способность и становятся названием товара, например: целлофан, новокаин, рубероид, аспирин, линолеум, термос. Эти процессы происходят и в настоящее время. Например, фирма «Xerox» очень много сделала для того, чтобы восстановить различительную способность своего знака, а ведь одно время термин «ксерокс» для потребителя означал просто копировальный аппарат.
Не допускается регистрация обозначений, которые состоят из элементов, являющихся общепринятыми символами и терминами для обозначения товаров определенного вида. Также нс регистрируются обозначения, характеризующие товары, в том числе указывающие на их вид, качество, количество, свойство, назначение, ценность, а также время, место, способ производства или сбыта.
Например, не будут зарегистрированы следующие изображения по отраслям хозяйства:
- машиностроение — шестерня;
- лесная и деревообрабатывающая промышленность — ель;
4-
- химическая и фармацевтическая промышленность — колба, реторта;
(22) 16.04.96 (И) 163893
(21) 96704849 (15) 15.05.98
(18) 16.04.06
(73) Открытое акционерное общество "Ультра-Т", Санкт-Петербург
(54)
(220) 18.02.1999 (111) 190353
(210)99702516 (151)28.06.2000
(181) 18.02.2009
(732) Общество с ограниченной ответственностью "МИАКОМ", Санкт-Петербург
(540)
(220)05.10.1999 (Ш) 206375
(210) 99715998 (151) 15.11.2001
(181)05.10.2009
(732) Общество с ограниченной ответственностью "Корк-Интерьер", Санкт-Петербург
(540)
КОРК-ИНТЕРЬЕР
(59) Товарный знак охраняется в синем цветовом сочетании.
(51) (57) 33 - водка;
42 - реализация водки.
(511) 09 - приборы и инструменты для научных целей, телефоны и радиотелефоны, телефонные и радиотелефонные станции, факсимильные аппараты, аппараты для внутренней связи, аппаратура для дистанционного управления, вычислительные машины и информационно-вычислительные комплексы, программы, записанные для вычислительных машин, информация, записанная на магнитных носителях.
(526) Интерьер.
(511)35- организация выставок для коммерческих целей, управление торговой деятельностью.
39 - доставка товаров, посредничество в перевозках, хранение товаров, хранение товаров на складах.
42 - дизайн в области оформления интерьера, консультативные и информационные услуги, включенные в 42 класс.
Рис. 9.7. Пример объемного товарного знака
Рис. 9.8. Пример изобразительного товарного знака
Рис. 9.9. Пример словесного товарного знака
Интеллектуальная собственность 1339
1340
Новый справочник химика и технолога
- медицина — змея и чаша
и т. д.
Однако эти элементы могут быть включены в товарный знак, если они не занимают в нем доминирующего положения.
Не допускается регистрация обозначений [10], состоящих только из элементов, представляющих собой государственные гербы, флаги и другие государственные эмблемы, сокращенные или полные наименования международных межправительственных организаций, их гербы, флаги и другие эмблемы, официальные контрольные, гарантийные и пробирные клейма, печати, награды и т. д. Такие элементы могут быть включены как неохраняемые элементы в товарный знак, если на это имеется согласие соответствующего компетентного органа.
Например, в товарный знак (рис. 9.10) включены элементы герба Российской Федерации, и это сделано, несомненно, с согласия компетентного органа.
(22) 07.10.97 (11) 163380
(21) 97714092 (15) 30.04.98
(18) 07.10.07
(73) Медицинский центр Управления делами Президента Российской Федерации, Москва
(54)
Рис. 9.10. Пример товарного знака, в который включена государственная символика Российской Федерации
Кроме того, не регистрируются знаки являющиеся ложными или способными ввести в заблуждение потребителя относительно товара или его изготовителя, а также противоречащие общественным интересам, принципам гуманности и морали.
Основной принцип закона состоит в том, чтобы в процессе регистрации не предоставлять владельцу зарегистрированного знака преимуществ перед другими владельцами зарегистрированных знаков за счет самого факта регистрации. Преимущества, в том числе и в отношении знака, должны возникать за счет добросовестной и эффективной работы на рынке и завоевания внимания потребителя.
Поэтому также не регистрируются знаки, в которые входят официальные наименования и изображения особо ценных объектов культурного или природного наследия.
Не могут быть зарегистрированы [9] в качестве товарных знаков обозначения, тождественные или сходные до степени смешения:
- с товарными знаками других лиц, заявленными на регистрацию или охраняемыми в РФ40 в отношении однородных товаров и имеющими более раннюю дату приоритета;
- товарными знаками других лиц, признанными общеизвестными41 в РФ в отношении однородных товаров.
Сходные до смешения товарные знаки могут быть зарегистрированы с согласия правообладателя.
Кроме того, не регистрируются обозначения, тождественные;
- охраняемому в РФ фирменному наименованию или его части в отношении однородных товаров, промышленному образцу, знаку соответствия;
- названию известного произведения науки, литературы или искусства, персонажу или цитате из такого произведения, произведению искусства или его фрагменту, без согласия обладателя авторского права или его правопреемника;
- фамилии, имени, псевдониму или производному от них обозначению, портрету и факсимиле известного лица, без согласия этого лица или его наследника.
Следует отметить, что общедоступного общероссийского классификатора фирменных наименований не ведется, и, соответственно, патентное ведомство не проверяет, нарушает ли регистрируемый знак права на чье-то фирменное наименование. А процедура аннулирования регистрации знака по этому основанию потребует времени и средств. Отсюда следует рекомендация: регистрируйте оригинальные фирменные наименования.
9.2.5.6. Коллективный товарный знак
В России еще не принято добиваться общих целей сообществом предприятий и фирм, выпускающих однородные товары, а значит, пока не популярно применение коллективных товарных знаков.
Коллективные товарные знаки предназначены для обозначения товаров, обладающих едиными качественными или иными общими характеристиками и производимых или реализуемых входящими в объединение использующих этот знак лицами.
При регистрации такого знака прилагается устав коллективного знака, который содержит наименование объединения, уполномоченного зарегистрировать коллективный знак на свое имя, перечень лиц, имеющих право пользования этим знаком, цель его регистрации, перечень и единые качественные или иные общие характеристики товаров, которые будут обозначаться
40 Охраняются в РФ знаки, которые зарегистрированы
в Российском патентном ведомстве, а также в соответствии с
международным договором — Мадридским соглашением
о международной регистрации знаков.
41 Особый вид охраны — охрана общеизвестных знаков,
о которой речь пойдет ниже.
Интеллектуальная собственность
1341
коллективным знаком, условия его использования, порядок контроля за его использованием, ответственность за нарушение устава коллективного знака.
Следующим шагом в направлении развития идеи коллективного знака являются так называемые сертификационные знаки. По законодательству многих развитых стран наряду с коллективными знаками регистрируются и сертификационные знаки, однако в РФ они пока не регистрируются.
9.2.5.7. Общеизвестные товарные знаки
В соответствии с законом [9], общеизвестные в РФ товарные знаки охраняются в силу своей общеизвестности. Такая особая охрана была закреплена Парижской конвенцией по охране промышленной собственности, и РФ как страна — участница Конвенции охраняет общеизвестные знаки. Чтобы знак был признан общеизвестным, он должен быть прежде всего широко известен потребителям. В качестве общеизвестных могут быть зарегистрированы как знаки, уже охраняющиеся как товарные знаки, так и знаки, нс охраняющиеся в РФ. Правовая охрана общеизвестного товарного знака действует бессрочно.
Правовая охрана общеизвестному товарному знаку предоставляется на основании решения патентного ведомства по заявлению его владельца.
На рис. 9.11 приведены примеры знаков, которые зарегистрированы в качестве общеизвестных в РФ.
9.2.5.8. Регистрация товарного знака
Заявка на регистрацию обозначения в качестве товарного знака подается в Патентное ведомство РФ — Федеральный институт промышленной собственности (ФИПС).
Заявка подается на каждый товарный знак отдельно, даже если это варианты одного и того же знака. Заявка содержит:
- заявление с указанием заявителя, его местонахождения;
- заявляемое обозначение;
- перечень товаров, в отношении которых испрашивается регистрация товарного знака и которые сгруппированы по классам Международной классификации товаров и услуг для регистрации знаков;
- описание заявляемого обозначения.
К заявке должны быть приложены: документ, подтверждающий уплату пошлины за подачу заявки; устав коллективного знака, если регистрируется коллективный знак.
Экспертиза заявки включает формальную экспертизу, которая проводится в течение месяца, и экспертизу заявленного обозначения. В случае решения о выдаче свидетельства производится официальная публикация знака и выдается свидетельство.
Регистрация товарного знака прекращается в связи с истечением срока регистрации, а в других случаях, например при ликвидации юридического лица, на которое
зарегистрирован знак, — при принятии решения о прекращении действия регистрации знака в связи с его неиспользованием, на основании решения о досрочном прекращении правовой охраны товарного знака в случае превращения зарегистрированного товарного знака в обозначение, вошедшее во всеобщее употребление как обозначение товаров определенного вида.
9.2.6. Наименование места происхождения товара
Наименование места происхождения товара [9] — это обозначение, представляющее собой либо содержащее современное или историческое наименование страны, населенного пункта, местности или другого географического объекта или производное от такого наименования и ставшее известным в результате его использования в отношении товара, особые свойства которого исключительно или главным образом определяются характерными для данного географического объекта природными условиями и (или) людскими факторами.
Приведем примеры обозначений —- наименований мест происхождения товаров:
зарубежные — коньяк, шампанское;
российские — Палех, Полюстрово, каслинское литье, боржоми, вологодское масло, гжель, Абрау-Дюрсо. В перечне соседствуют товары, особые свойства которых определяются природными ресурсами местностей, мастерством и традициями производителей.
Наименования места происхождения товара для многих стран является важнейшим ресурсом, к охране которого, в том числе к охране качества и репутации товара, страна и производители прилагают все усилия. Наиболее характерный пример — Франция, в области виноделия.
На рис. 9.12 приведены примеры регистрации наименований мест происхождения товаров.
Правовая охрана наименования места происхождения товара в Российской Федерации возникает на основании его регистрации или в силу международных договоров. Например, между РФ и Францией заключено соглашение, по которому в России можно использовать название «шампанское», хотя собственно шампанским, т. е. производящимся на территории провинции Шам-~ 42
пань, этот популярный напиток не является .
Заявка на регистрацию и предоставление права пользования наименованием места происхождения товара или на предоставление права пользования уже зарегистрированным наименованием места происхождения товара подается в ФИПС.
42 СССР никогда не экспортировал за границу «Советское шампанское» — только «Советское игристое» или «Армянское бренди». Интересен и тот факт, что «Советское шампанское» имело и, видимо, имеет до сих пор своих почитателей за рубежом, и даже известен случай, когда была пресечена попытка фальсификации крупной партии шампанского, якобы экспортированного из СССР.
1342
Новый справочник химика и технолога
ИЗВЕСТИЯ
Общеизвестный товарный знак
Решением Высшей патентной палаты Роспатента обозначение "ИЗВЕСТИЯ” признано общеизвестным товарным знаком на территории Российской Федерации.
Владелец общеизвестного знака
Открытое акционерное общество "Редакция газеты "Известия", ул.Тверская 18, корп.1, Москва, 103791
Дата вступления в силу решения Высшей патентной палаты о признании товарного знака общеизвестным
07.04.2000 г.
Дата, с которой товарный знак признан общеизвестным
31.12.1992 г.
Перечень товаров, в отношении которых товарный знак признан общеизвестным
16 класс МКТУ: общероссийская газета "ИЗВЕСТИЯ".
2.
УРАЛМАШ
Общеизвестный товарный знак
Решением Высшей патентной палаты Роспатента обозначение "УРАЛМАШ" признано общеизвестным товарным знаком на территории Российской Федерации.
Владелец общеизвестного знака
Открытое акционерное общество "Уральский завод тяжелого машиностроения", пл.
Первой пятилетки, ОАО "Уралмаш", г.Екатеринбург, 620012
Дата вступления в силу решения Высшей патентной палаты о признании товарного знака общеизвестным
10.07.2000 г.
Дата, с которой товарный знак признан общеизвестным
31.12.1977 г.
Общеизвестный товарный знак
Решением Высшей патентной палаты Роспатента обозначение "Coca-Cola" признано общеизвестным товарным знаком на территории Российской Федерации.
Владелец общеизвестного знака
The Coca-Cola Company, a Delaware corporation, One Coca-Cola Plaza, Atlanta, Georgia 30313 (US)
Дата вступления в силу решения Высшей патентной палаты о признании товарного знака общеизвестным
18.12.2001
Дата, с которой товарный знак признан общеизвестным
01.01.1996
Перечень товаров, в отношении которых товарный знак признан общеизвестным
32 класс МКТУ: безалкогольные напитки.
Рис. 9.11. Примеры общеизвестных в РФ товарных знаков
Интеллектуальная собственность
1343
Заявка содержит:
- заявление с указанием заявителя (заявителей), его (их) местонахождения или местожительства;
- заявляемое обозначение;
- указание товара, в отношении которого испрашивается регистрация;
- указание места происхождения (производства) товара (границ географического объекта);
- описание особых свойств товара.
Следует отметить, что в отличие от товарного знака регистрация наименования места происхождения товара не предоставляет исключительных прав какому-то одному пользователю. Наименование места происхождения не утрачивает своей охраны с прекращением действия свидетельства, а лишь с исчезновением характерных для данного географического объекта условий и невозможностью производства товара, обладающего указанными свойствами.
Экспертиза включает в себя формальную экспертизу и экспертизу по существу. При положительном исходе производится публикация в официальном бюллетене патентного ведомства и выдача свидетельства. Срок действия свидетельства на наименование места происхождения товара 10 лет с возможностью продления каждый раз еще на 10 лет.
Нарушитель права на наименование места происхождения товара по требованию обладателя свидетельства, государственного органа, прокурора или общественной организации обязан прекратить нарушение и возместить убытки. За его счет публикуется судебное решение и с контрафактного товара удаляются незаконно использованные наименования.
9.2.7. Охрана промышленной собственности за рубежом
Охрана объектов промышленной собственности, изобретений, полезных моделей, промышленных образцов и товарных знаков, на которые получены охранные документы в России, ограничивается только территорией РФ, т. к. патент и свидетельство на товарный знак действуют лишь на территории той страны, где они выданы.
Получение охраны в других странах в случае изобре-
- 43
тении чаще всего связано со следующими причинами:
- осуществление (планирование) экспорта продукции за рубеж;
- передача технологий, новых материалов, фармацевтических средств за рубеж (применяется термин «лицензирование», т. е. передача прав на использование технологии по лицензии, планирование лицензирования);
- подготовка (планирование) производства продукции в данной стране;
44
- инвестиции в развитие промышленности .
43 Термин «изобретение» в данном случае применяется как обобщающий (в том числе промышленные образцы и полезные модели).
Регистрация российских товарных знаков за рубежом или знаков российских предприятий, специально созданных для использования за рубежом43 44 45 *, производится (будет производиться) в следующих случаях:
- экспорт продукции за рубеж;
- оказание услуг за рубежом;
- распространение торговых и иных предприятий под единым товарным знаком в других странах;
- предоставление услуг и товаров по электронным сетям (через Интернет);
- экспорт технологий, новых фармацевтических
46 средств и материалов .
Перечисляя причины патентования изобретений и регистрации знаков за рубежом, приходится иметь в виду планы и предположения, т. к. начало патентования чаще всего по времени значительно опережает экспорт продукции или начало работы с партнерами по передаче технологии. В связи с тем, что защита промышленной собственности за рубежом связана со значительными расходами, следует приступать к конкретным действиям осознанно.
Международное сотрудничество в области охраны промышленной собственности привело к созданию достаточно удобной системы, которая создана с помощью ряда международных соглашений.
9.2.7.1. Парижская конвенция по охране промышленной собственности
Парижская конвенция [11], которая была заключена между одиннадцатью странами 20 марта 1883 г., в настоящее время47 ратифицирована 164 странами-участницами, в число которых входят все промышленно развитые страны мира. Конвенция содержит достаточно много положений, касающихся материального права, права приоритета, предписаний о правах и обязанностях юридических и физических лиц и т. д.
Основные положения, являющиеся определяющими в сфере международной охраны промышленной собственности, сводятся к следующему.
44 Эта причина защиты российской промышленной собственности за рубежом не является часто встречающейся, однако зарубежные инвесторы, вкладывающие средства и новые технологии в развитие промышленности в России, получают патенты в нашей стране, имея в виду и эту цель.
45 Далеко не всегда в другой стране для маркировки той же продукции применяется тот же знак. Необходимо учиты-
вать культурные, языковые, религиозные и тому подобные особенности страны, где будет использоваться знак. Напри-
мер, автомобиль «Жигули» экспортировался в Европу под другим названием, т. к. для людей, не говорящих на русском языке, буква «ж» достаточно трудна для произношения.
46 Как отмечалось ранее, новые, оригинальные названия
фармацевтических средств, новых материалов могут быть
зарегистрированы как товарные знаки.
47 На 1 января 2004 г.
1344
Новый справочник химика и технолога
(190) RU 2/3
ФЕДЕРАЛЬНАЯ СЛУЖБА
ПО ИНТЕЛЛЕКТУАЛЬНОЙ
СОБСТВЕННОСТИ,
ПАТЕНТАМ И ТОВАРНЫМ
ЗНАКАМ
(РОСПАТЕНТ)
Наименования мест происхождения товаров
Статус: поданным на 18.11.2005 - действует
Дата подачи заявки: 1998.12.22 Дата публикации: 2000.12.12
Дата регистрации: 2000.09.19 Обладатель свидетельства: Открытое акционерное
Номер заявки: 98720491 общество "Гжельский завод "Электроизолятор",
г, . ~ Ново-Харитоново Московской обл. (RU)
Дата истечения срока действия к '
свидетельства: 2010.09.19
Наименование места происхождения товара: ГЖЕЛЬ
Вид товара и описание его особых свойств:
Изделия народного художественного промысла бытового и художественно-прикладного назначения из фарфора (посуда, сервизы, самовары, соковыжималки, шкатулки, светильники, часы, подсвечники, канделябры, пепельницы, ароматницы, ладанницы, сувениры, скульптура малых форм). Отличительными чертами гжельских изделий являются декоративность, нарядность, эстетическая и функциональная выразительность, а также разнообразие форм. Роспись изделий отличается яркостью и контрастом кобальтовой краски с белым фоном благодаря использованию ручной подглазурной росписи кобальтом по утилю. В результате обжига черный, как сажа, кобальт становится ярким и синим. Изделие расписывается одной кистью, где каждый последующий мазок отличается от предыдущего и обладает широким тональным диапазоном: от глубоких и темных тонов до легких и светлых (так называемый "мазок с тенями"). Наряду с традиционными элементами росписи (растительным, сюжетным орнаментом) не менее важны и закручивающиеся усики, спиралевидные завитки, точечные и штриховые заполнения, полоски простого геометрического орнамента. Масштаб орнамента соответствует размерам изделий, а характер расположения рисунка подчеркивает красоту формы. Специфическая технология обеспечивает долгосохраняющуюся яркость и свежесть красок.
Рис. 9.12. Примеры регистрации наименований мест происхождения товаров
Интеллектуальная собственность
1345
(190) RU 17/2
ФЕДЕРАЛЬНАЯ СЛУЖБА
ПО ИНТЕЛЛЕКТУАЛЬНОЙ
СОБСТВЕННОСТИ,
ПАТЕНТАМ И ТОВАРНЫМ ЗНАКАМ
(РОСПАТЕНТ)
Наименования мест происхождения товаров
Статус: поданным на 18.11.2005 - действует
Дата подачи заявки: 2002.03.01
Дата регистрации: 2003.02.19
Номер заявки: 2002705326
Дата истечения срока действия свидетельства: 2012.03.01
Дата публикации: 2003.04.12
Обладатель свидетельства: Закрытое акционерное общество "Абрау-Дюрсо", г. Новороссийск (RU)
Наименование места происхождения товара: АБРАУ-ДЮРСО
Вид товара и описание его особых свойств: Вина.
(190) RU 68/1
ФЕДЕРАЛЬНАЯ СЛУЖБА
ПО ИНТЕЛЛЕКТУАЛЬНОЙ
СОБСТВЕННОСТИ,
ПАТЕНТАМ И ТОВАРНЫМ ЗНАКАМ
(РОСПАТЕНТ)
Наименования мест происхождения товаров
Статус: по данным на 18.11.2005 - действует
Дата подачи заявки: 2002.07.30 Дата регистрации: 2003.09.08 Номер заявки: 2002714587 Дата истечения срока действия свидетельства: 2012.07.30 Дата публикации: 2003.10.25 Обладатель свидетельства: Открытое акционерное общество "ОРЕНШАЛЬ", 460036, г. Оренбург, ул. Расковой, 10а (RU) Место происхождения (производства) товара (границы географического объекта): Территория Оренбургской области Российской Федерации.
Наименование места пр оисх оледени я товара: ОРЕНБУРГСКИЙ ПУХОВЫЙ ПЛАТОК
Вид товара и описание его особых свойств:
Пуховый платок.
Рис. 9.12. Примеры регистрации наименований мест происхождения товаров (продолжение)
1346
Новый справочник химика и технолога
Принцип национального режима
Каждая страна, участвующая в Конвенции, обеспечивает представителям других стран — участниц Конвенции такую же охрану промышленной собственности, какую она предоставляет своим собственным гражданам.
Принцип национального режима позволяет российским юридическим и физическим лицам получать охрану своей промышленной собственности наряду с гражданами любой страны — участницы Конвенции и, что также важно, защиту своих прав с помощью суда и иных государственных органов на условиях национального законодательства.
Принцип национального режима при этом не исключает удовлетворение требований о предоставлении лицу больших правомочий, которые вытекают из содержания собственно Парижской конвенции48. С другой стороны, при осуществлении своих прав иностранцы (нерезиденты) процессуально могут быть поставлены в особые условия при осуществлении судопроизводства.
Право приоритета
Право приоритета означает, что на основании подачи заявки на получение охраны объекта промышленной собственности, поданной в стране — участнице Конвенции, лицо, подавшее заявку, может ходатайствовать об охране этого объекта во всех других странах в течение определенного срока (12 или 6 месяцев в зависимости от вида объекта). Это положение означает, что если должным образом оформленное ходатайство будет подано в течение указанного срока, то приоритет в других странах будет установлен по дате подачи первоначальной заявки. Приоритет 12 месяцев установлен для изобретений и полезных моделей, 6 месяцев — для товарных знаков и промышленных образцов.
Поясним право приоритета на временных диаграммах.
На рис. 9.13 приьедена диаграмма, которая поясняет правило приоритета для изобретений и полезных моделей. Первоначальная заявка подана в России (RU), например, 10 января 2004 г. Для заявок, относящихся к тому же изобретению, поданных в США (US), Великобритании (GB49), Франции (FR) в течение 12 месяцев с даты подачи российской заявки и содержащих ходатайство о предоставлении приоритета на основании Парижской конвенции, будет установлен приоритет по дате подачи российской заявки, т. е. 10 января 2004 г.
48 Например, охрана общеизвестных товарных знаков. До 2002 г. законодательство Российской Федерации не содержало развернутых норм относительно охраны общеизвестных знаков, однако охрана общеизвестным знакам в РФ предоставлялась на основе Парижской конвенции.
49 Здесь и далее применяются коды стран, установленные Стандартами ВОИС для патентной документации.
Рис. 9.13. Диаграмма правила приоритета для изобретений и полезных моделей
На рис. 9.14 представлена поясняющая диаграмма для товарных знаков и промышленных образцов. Первоначальная заявка, поданная в России, устанавливает дату приоритета. Заявкам на тот же объект, поданным в Канаде (СА), Германии (DE) в течение 6 месяцев с даты приоритета, будет установлена та же дата приоритета, что и первичной заявке.
Рис. 9.14. Диаграмма правила приоритета для товарных знаков и промышленных образцов
Вопросы, касающиеся значимости даты приоритета при рассмотрении заявок и получении патентов и свидетельств на товарный знак, уже были рассмотрены выше.
Принцип национального режима и принцип приоритета открывают широкие возможности для получения охраны объектов промышленной собственности в других странах.
Парижская конвенция содержит и другие положения, относящиеся к промышленной собственности. Она содержит статьи, касающиеся права преждепользования, принудительной лицензии устанавливает принцип независимости патентов, полученных на один и тот же объект в разных странах.
9.2.7.2. Патентование изобретений за рубежом
Патентным законом РФ предписано, что при намерении патентовать изобретение или полезную модель за рубежом сначала должна быть подана заявка в патентное ведомство России. В течение 6 месяцев ведомство проверяет, не относится ли объект к секретным, и только после этого можно подавать соответствующую заявку за рубежом. В случае необходимости такая проверка по ходатайству заявителя может быть проведена и быстрее. Нарушение установленного порядка карается административным штрафом.
Интеллектуальная собственность
1347
Такое положение практически не дискриминирует российских заявителей. При подаче российской заявки возникает право приоритета, установленное Парижской конвенцией, и, таким образом, подача заявки за рубежом в оставшиеся 6 месяцев может быть произведена с сохранением приоритета по российской заявке.
Процедура патентования изобретений за рубежом может происходить одним из двух путей.
Подача национальных заявок в каждой стране патентования
Первый путь — подача в каждой стране, где необходимо получить патент, национальной заявки с испрашиванием приоритета, установленного Парижской конвенцией. Далее мы будем использовать термин «конвенционный приоритет».
Заявка на изобретение должна быть подана в течение 12 месяцев с даты подачи первой, российской заявки. При этом подать заявку в зарубежное патентное ведомство российский заявитель (физическое или юридическое лицо) напрямую не может, он должен действовать через представителя, патентного поверенного, гражданина той страны, где подается заявка.
Поэтому процедура выглядит так. Российская заявка направляется патентным поверенным, которые представляют иностранного заявителя перед патентным ведомством своей страны, те готовят заявку по правилам, существующим в данной стране, и подают ее в национальное патентное ведомство.
Такой путь патентования связан с достаточно большими расходами за короткий период времени, т. к. необходимо уплачивать пошлины в национальных ведомствах и оплачивать услуги патентных поверенных.
Абсолютным препятствием для получения патента за рубежом является любое раскрытие сути изобретения, которое произошло после подачи заявки, если пропущен срок 12 месяцев, установленный конвенционным приоритетом. Запаздывание подачи зарубежных заявок, т. е. после 12 месяцев (подчеркиваем, если не произошло раскрытие информации неопределенному кругу лиц тем или иным способом50, что вообще делает невозможным получение патента) после подачи российской заявки, приводит к следующим негативным последствиям:
- утере приоритета российской заявки (по каждой такой заявке, поданной в зарубежное ведомство, будет установлен приоритет по дате ее подачи в национальное ведомство);
- утере возможности получить зарубежный патент, например в США.
Возможность получения патента по истечении срока конвенционного приоритета существует очень короткое время, практически 6 месяцев, т. к. через 18 месяцев после подачи заявки в российское ведомство происходит публикация заявки и раскрытие сути изобретения.
50 См. разд. 9.2.2.1.
Таким образом, очень важно иметь в виду, что практически все необходимые действия по получению зарубежных патентов, т. е. подача заявок, должны быть произведены в течение 12 месяцев после подачи российской заявки.
Договор о патентной кооперации (РСТ)
Практически 90 % российских заявок патентуется за рубежом с использованием процедуры Договора о патентной кооперации (Patent Cooperation Treaty) (PCT) [12].
Договор о патентной кооперации был подписан в Вашингтоне 19 июня 1970 г. В настоящее время51 к нему присоединились 123 страны, в том числе все промышленно развитые страны. Договор не связан, как иногда неправильно думают, с выдачей какого-то общего, мирового патента. Процедура, предусматриваемая договором, — это промежуточная процедура, которая является мостиком между подачей национальной заявки и началом рассмотрения заявки на изобретение или полезную модель в национальных патентных ведомствах. Как мы увидим далее, эта процедура обладает для заявителя рядом весьма привлекательных черт.
Рассмотрим схему последовательности действий по процедуре РСТ.
После подачи российской заявки подается одна международная заявка (международная заявка при подаче обозначается РСТ/RU, а при публикации — аббревиатурой «WO») в так называемое получающее патентное ведомство (для российских заявителей это российское патентное ведомство52). В заявке указываются страны, где заявитель хочет получить патент. С 1 января 2004 г. в связи с изменениями, внесенными в Договор [12], заявителю не требуется указывать страну — априори считается, что указаны вес страны, входящие в процедуру РСТ. Если заявка подается с испрашиванием конвенционного приоритета, то для нее устанавливается приоритет по дате подачи российской заявки. Допускается подача сразу международной заявки в получающее патентное ведомство — Российское патентное ведомство, без предварительной подачи российской заявки, однако Россия в ней должна быть указана как страна, где заявитель намерен получить патент.
При подаче заявки уплачиваются пошлины, размер которых составляет примерно 1 000 швейцарских франков для российских юридических лиц. Размер пошлин уменьшается на 75 % в случае международных заявок, поданных физическими лицами из стран с годовым доходом менее 3000 USD, к которым пока относится и Россия.
Подать международную заявку в получающее ведомство заявитель может самостоятельно или через представителя, например российского патентного поверенного.
Российское патентное ведомство по материалам международной заявки проводит международный поиск
51 На 1 января 2004 г.
52 Договором РСТ установлено десять получающих ве-
домств.
1348
Новый справочник химика и технолога
с целью выявления соответствующего уровня техники и сообщает о результатах заявителю.
Получающее ведомство пересылает экземпляр заявки в Международное бюро в г. Женева (Швейцария) вместе с результатами международного поиска. Международное бюро публикует заявку через 18 месяцев с даты приоритета.
Следующий этап — перевод международной заявки в национальную фазу.
Перевод заявки в национальную фазу производится путем подачи заявления в соответствии с требованиями национального ведомства, уплаты необходимых пошлин за подачу заявки и представления перевода заявки с русского языка на язык национального ведомства.
Перевод заявки в национальную фазу должен быть произведен до истечения 20 месяцев с даты приоритета для следующих государств: Бразилии, Венгрии, Дании, Замбии, Китая, Люксембурга, Норвегии, Республики Корея, Сингапура, Танзании, Уганды, Финляндии, Швейцарии, Швеции, Эстонии, ЮАР.
Для остальных государств Договора перевод в национальную фазу должен быть произведен до истечения 30 месяцев с даты приоритета.
По требованию заявителя по его международной заявке может проводиться международная предварительная экспертиза. Проведение международной экспертизы не является обязательным, ее результат не предрешает выводов национальных патентных ведомств, и необходимо заявителю в следующих случаях:
- когда заявитель хочет получить дополнительные сведения, подтверждающие или не подтверждающие возможность получения патента;
- когда заявитель хочет перевести заявку в национальную фазу для вышеуказанных государств (Бразилии, Китая, Швейцарии и др.) до истечения 30 месяцев, а не 20 месяцев, как без международной предварительной экспертизы.
Подача перечисленных документов в национальные патентные ведомства производится через патентных поверенных, граждан той страны, где будет выдаваться патент.
Патентование за рубежом с использованием Договора о патентной кооперации (РСТ) имеет следующие преимущества для российского заявителя:
- подается одна — международная заявка в одно ведомство на русском языке;
- уплачиваются сравнительно небольшие пошлины, которые для физических лиц снижаются на 75 %;
- оплата основных расходов по уплате национальных патентных пошлин и услуг национальных патентных поверенных откладывается до истечения 30 месяцев с даты приоритета, т. е. почти на два с половиной года;
- за время прохождения процедуры по РСТ заявитель может уточнить свои коммерческие планы, в частности в выборе стран патентования, и тем самым избежать излишних расходов;
- перевод на национальную фазу обходится дешевле, т. к. необходимо представить только заявление и перевод международной заявки на язык ведомства, а не полностью оформленную заявку по требованиям ведомства.
Процедура, связанная с патентованием по РСТ, схематически представлена на рис. 9.15.
Рис. 9.15. Схема процедуры патентования по РСТ
Например, заявка на получение патента России подана 5 января 2003 г. В этом случае до 5 января 2004 г. должна быть подана одна международная заявка РСТ в российское патентное ведомство как получающее ведомство. Через 18 месяцев с даты приоритета, т. е. в июне 2004 г., российская и международная заявки будут опубликованы: одна — российским патентным ведомством, другая — Международным бюро в Женеве. Заявитель должен поручить патентным поверенным в соответствующих странах, где он хочет получить патенты, совершить необходимые действия по переводу международной заявки в стадию ее рассмотрения как национальной заявки в соответствии с национальным законодательством. На схеме показаны два ведомства: США (US) и Европейское патентное ведомство (ЕР)53. Следует отметить, что по всем национальным заявкам, которые поданы через процедуру РСТ, если международная заявка подана с использованием конвенционного приоритета, устанавливается дата приоритета по первоначальной заявке, в нашем случае — российской заявки. Заявитель может подать требование о проведении международной экспертизы, но на схеме это не отражено.
53 О Европейском патенте см. в подразделе «Региональные
патентные системы».
Интеллектуальная собственность
1349
Содержание международной заявки:
- заявление на типовых бланках с указанием заявителя, изобретателя, агента или представителя. В комплект заявления могут входить: декларации для национальных ведомств; описание с формулой и рефератом;
- необходимые иллюстративные материалы, например чертежи.
Необходимые сведения об оформлении заявки и процедуре ее прохождения содержатся в Инструкции к Договору о патентной кооперации [ 13]54.
Как показывают расчеты, патентование по процедуре РСТ экономически выгоднее в том случае, если число стран патентования превышает четыре-пять. Однако прямые расчеты не всегда отражают действительную экономию, выражающуюся в том, что решение о выборе стран патентования, принятое позднее, способствует более ясному пониманию, где нужен патент. Число стран патентования может быть сокращено, что приведет к экономии средств. При подаче заявок сразу в национальные ведомства решение необходимо принимать в течение 12 месяцев с даты приоритета, когда, возможно, еще не сформировался бизнес-план.
Однако если по каким-то причинам национальные патенты необходимо получить как можно быстрее, процедура РСТ становится излишней.
Региональные патентные системы
Кроме национальных патентов заявитель может получить также один из следующих региональных патентов.
Европейский патент
Европейское патентное ведомство (ЕПВ) учреждено Европейской патентной конвенцией в 1977 г. с целью создания единообразной процедуры выдачи Европейского патента (ЕР), который действует в каждой стране Европейской конвенции как национальный патент. Т. е. европейским странам удалось договориться о единообразной процедуре выдачи ЕП, однако единого патентного закона, действующего в странах ЕП, пока нет55.
В системе ЕР предусмотрены подача заявки на одном из языков ЕПВ и выдача патента, который будет действовать в странах по выбору заявителя, входящих в 25 стран, которые присоединились к Европейской патентной конвенции: Австрия, Бельгия, Болгария, Великобритания, Венгрия, Германия, Греция, Дания, Ирландия, Испания, Италия, Кипр, Лихтенштейн, Люксембург, Монако, Нидерланды, Португалия, Румыния, Словакия, Словения, Чехия, Швейцария, Финляндия, Франция, Эстония, и в число стран, присоединяющихся к ЕПВ: Албания, Латвия, Литва, Македония56.
Срок действия ЕП 20 лет.
54 Все необходимые сведения и тексты Договора и Инструкции можно получить на сайтах ФИПС — www.fips.ru и ВОИС — http://www.wipo.int/ru/index.html.
55 Европейские страны разрабатывают единый патентный закон, но его принятие — дело будущего.
56 Данные по региональным патентам на 1 января 2004 г.
Заявка на выдачу ЕП может быть подана и российским заявителем через европейского патентного поверенного в штаб-квартиру ЕПВ в Мюнхене или через процедуру РСТ.
Евразийский патент
Часть стран СНГ: Российская Федерация, Азербайджанская Республика, Республика Армения, Республика Беларусь, Республика Казахстан, Кыргызская Республика, Республика Молдова, Республика Таджикистан, Республика Туркменистан — ратифицировали Евразийскую патентную конвенцию, которая предусматривает выдачу Евразийского патента (ЕА), который действует как национальный на территории указанных выше стран.
Заявка на русском языке подается в Евразийское патентное ведомство: 101999, Москва, Малый Черкасский пер., 2/6.
Членство в Конвенции открыто для любого заинтересованного государства.
Российский заявитель может подать заявку на получение ЕА непосредственно, через 6 месяцев после подачи российской заявки или через процедуру РСТ.
Африканские региональные патенты
Англоязычные страны Африки договорились о патенте ARIPO (AR), в котором участвуют следующие страны: Гана, Гамбия, Зимбабве, Кения, Лесото, Малави, Мозамбик, Свазиленд, Судан, Сьерра-Леоне, Объединенная Республика Танзания, Уганда.
Франкоязычные страны объединены в систему OAPI (ОА): Бенин, Буркина-Фасо, Габон, Гвинея, Гвинея-Бисау, Камерун, Конго, Кот д'Ивуар, Мавритания, Мали, Нигер, Сенегал, Того, Чад, Центрально-Африканская Республика.
Система региональных патентов позволяет упростить получение патента в большем числе стран путем подачи одной заявки и получение одного патента.
9.2.7.3. Охрана промышленных образцов за рубежом
Для российских заявителей единственный путь получения охраны промышленного образца за рубежом —• подача в каждой стране, где необходимо получить патент, национальной заявки с испрашиванием приоритета, установленного Парижской конвенцией. Конвенционный приоритет для промышленных образцов составляет 6 месяцев с даты подачи первой заявки на данный промышленный образец.
Если бы Россия участвовала в Гаагском соглашении о международном депонировании промышленных образцов (в соглашении участвуют 36 стран57), то получить охрану промышленного образца в странах Соглашения было бы можно путем подачи одной заявки в Международное бюро ВОИС в Женеве.
57 На октябрь 2003 г. Следует отметить, что в данном Со-
глашении участвует сравнительно малое число ведущих в
промышленном отношении стран мира: Бельгия, Франция,
Германия, Греция, Италия, Испания, Нидерланды, Швейцария.
1350
Новый справочник химика и технолога
9.2.7.4. Охрана товарных знаков за рубежом
Охрана российских товарных знаков за рубежом может быть получена путем непосредственной подачи заявки на регистрацию товарного знака в стране, где это необходимо. Если заявка за рубежом подается до истечения 6 месяцев с даты подачи российской заявки на регистрацию знака, то заявитель вправе ходатайствовать о предоставлении приоритета по дате подачи заявки в России согласно Парижской конвенции.
Заявка на регистрацию товарного знака за рубежом может быть подана в любое время независимо от регистрации в стране происхождения. Для товарных знаков не применяется такой критерий, который применяется, в частности, для изобретений, — новизна. Не регистрируются уже зарегистрированные (или сходные с ними) в данной стране знаки, а также знаки, получившие в данной стране охрану путем регистрации по Мадридскому соглашению о международной регистрации знаков, и общеизвестные знаки.
Российская Федерация участвует в Мадридском соглашении о международной регистрации знаков от 14 апреля 1891 г. с июля 1976 г. как правопреемница СССР. В Соглашении участвуют 74 страны58, в том числе ведущие страны мира.
Регистрация товарного знака в странах Мадридского соглашения происходит путем подачи заявки в Международное бюро ВОИС в Женеве. Заявка на регистрацию знака может быть подана только после регистрации знака в стране происхождения. Срок охраны знака 20 лет, с возможным продлением каждый раз еще на 20 лет.
Заявка подается на французском языке непосредственно или через представителя.
Особый международный товарный знак — олимпийский символ в виде пяти переплетенных колец разного цвета, который охраняется в соответствии с Най-робским договором об охране олимпийского символа, заключенным 26 сентября 1981 г.
9.2.8. Патентная информация и патентные исследования
Патентная информация играет особую роль как при получении патентов, так и вообще в развитии техники и создании новых технологий. Об этом будет отдельный разговор в подразделах, посвященных осуществлению проектов и охране результатов. В настоящем подразделе пойдет разговор о технической стороне дела — поиске и обработке патентной информации.
Патенты могут быть выданы в промышленности, сельском хозяйстве, здравоохранении и т. д. Поэтому патентная информация является уникальным источником информации, т. к. обладает следующими свойствами59.
58 На октябрь 2003 г. Со 2 ноября 2003 г. к Мадридскому соглашению присоединились США.
59 Количество патентов в той или иной области техники и
науки не имеет прямой зависимости от ее значимости или массовости производства товаров. Поэтому в некоторых об-
Полнота. Патентные источники наиболее полно раскрывают весь спектр решений, которые имеются в той или иной области техники и хозяйства. Кроме того, именно в описаниях патентов техническая информация отражена наиболее подробно.
Оперативность. Публикация о том или ином решении, как правило, становится общедоступной через 18 месяцев с даты подачи заявки на получение патента. Непатентные источники информации, например журнал или книга, как правило, сообщают о решении позже патентной публикации.
Достоверность. Патентная информация чаще всего содержит достоверную информацию. Это не значит, что изобретатель или заявитель не могут заблуждаться относительно качеств и свойств своего решения — такое возможно. Речь о другом — в описаниях, как правило, нет сведений, которые сознательно вводили бы общественность в заблуждение, что более возможно во всех других видах публикаций, особенно рекламного характера.
Кроме того, следует отметить следующие характерные черты патентной информации:
- это правовая информация, сообщающая не только о сути решения, но и об объеме прав патентообладателя, дате приоритета, авторах и т. д.;
- структура описания единообразна не только в рамках патентов одной страны, но и практически во всем объеме патентной информации, относящейся к конкретному объекту промышленной собственности.
Для проверки патентной чистоты объектов техники это единственный вид информации.
9.2.8.1. Источники патентной информации
Источники патентной информации можно разделить на следующие группы.
Официальные источники — официальные публикации патентных ведомств. Это публикации в официальных бюллетенях патентных ведомств и описания заявок и патентов изобретений, полезных моделей, промышленных образцов и официальные публикации о товарных знаках.
Реферативная информация. Служит для облегчения поиска необходимой пользователям патентной информации. Реферативную информацию, подготовленную в процессе рассмотрения заявок в патентном ведомстве, в том числе с помощью заявителей, делают доступной сами патентные ведомства, как путем публикации, так и путем доступа к электронным базам данных патентных ведомств. Существуют также и специальные издания, например в России «Изобретения стран мира»60, где вместе с иллюстрациями публикуются на русском языке рефераты патентных документов ведущих стран мира.
ластях патентная информация не будет играть определяющей
роли. Однако таких областей техники сравнительно немного.
60 Данное издание теряет свое значение с появлением
электронных баз данных.
Интеллектуальная собственность
1351
Фирма «Derwent» готовит специальную единообразную реферативную информацию на основе официальных публикаций рефератов и полных описаний, которая полнее отражает суть и облегчает поиск информации.
Электронные базы данных. Строго говоря, электронные базы данных могут вбирать в себя все ранее отмеченные виды информации — официальную информацию, полные описания и реферативную информацию. Эта информация предоставляется пользователям в электронном виде путем бесплатного или платного доступа. Роль электронных баз данных в поиске патентной информации нельзя переоценить. Во многих случаях они становятся основным инструментом поиска.
9.2.8.2. Международная патентная классификация (МПК) (International Patent Classification — «Int.Cl.»)
Обработка огромных массивов патентной документации невозможна без использования Международной патентной классификации (МПК)61, которая используется на основе многостороннего международного договора [15]. Поиск без использования МПК практически невозможен, т. к. в мире, по статистике ВОИС, публикуется примерно миллион патентных документов. Национальные патентные классификации62, которые использовались некоторыми странами, постепенно теряют свое значение.
Наряду с МПК появилась новая патентная классификация, которая используется Европейским патентным ведомством для классификации патентных документов этого ведомства наряду с МПК.
Для промышленных образцов существует Международная классификация промышленных образцов (МКПО).
Товарные знаки классифицируются с помощью международной классификации товарных знаков (МКТУ).
Структура патентной классификации
МПК имеет восемь разделов, которые далее делятся на классы, подклассы, группы и подгруппы.
Разделы:
А — Удовлетворение жизненных потребностей человека;
В — Различные технологические процессы; транспортирование;
С — Химия; металлургия;
D — Текстиль; бумага;
Е — Строительство; горное дело;
61 Ранее, в СССР, использовалось другое название классификации — Международная классификация изобретений (МКИ).
62 Наиболее характерный пример — Национальная классификация Патентного ведомства США, которая используется до настоящего времени. Национальные классификации
патентных ведомств Великобритании и Германии сейчас не используются.
F — Механика; освещение; отопление; двигатели и насосы; оружие и боеприпасы; взрывные работы;
G — Физика;
Н — Электричество.
В качестве примера приведем обозначение для «Очистки горючих газов» (С).
Подгруппа
Приведем фрагмент МПК для группы С10К 1/00.
С10К 1/00 — Очистка горючих газов, содержащих оксид углерода (выделение водорода из смесей, содержащих водород и оксид углерода, С01В 3/50)63
1/02 удалением пыли
1/04 охлаждением с целью конденсации негазообразных материалов
1/06 в сочетании с водяным орошением
1/08 промыванием жидкостями; регенерация использованных промывных жидкостей (мокрые газоочистители BOID)
1/10 водными растворами
1/12 щелочного характера
1/14 • органическими
1/16 с неводными жидкостями
1/18 углеводородными маслами
1/20 обработкой твердыми веществами
1/22 устройства, например сухие очистители
1/24 носители для очистных масс
1/26 регенерация очистных масс
1/28 регулирование потока газа, проходящего через очистители
1/30 с движущимися очистными массами
1/32 с избирательно поглощающими твердыми веществами, например активированным углем
1/34 с каталитической конверсией загрязнений в более легко удаляемые вещества
Каждые 5 лет МПК пересматривается экспертами ВОИС. С 1 января 2000 г. действует 7-я редакция МПК.
С МПК можно ознакомиться на сервере Российского патентного ведомства http://www.fips.ru. Текст МПК на английском языке доступен на сайте ВОИС http://www.wipo.int.
63 Подчиненность подгрупп в МПК указывается числом
точек перед описанием подгруппы.
1352
Новый справочник химика и технолога
Определение классификационных рубрик
Первичное определение классификационных рубрик МПК начинается с Алфавитно-предметного указателя, издаваемого патентным ведомством, или с помощью оглавления МПК. Необходимо отметить, что классификация имеет одновременно отраслевое и функциональное деление, поэтому возможно, что объект поиска классифицируется сразу по двум и более разделам.
Необходимо иметь в виду, что МПК вводилась в первую очередь для целей патентного ведомства, и очень часто в ней применяется терминология, удобная для патентного эксперта, но непривычная для инженера. Поэтому результаты поиска рубрик не всегда будут сразу удачными.
Первоначально определенные рубрики очень часто корректируются в процессе поиска, поэтому всегда необходимо обращать внимание на классификацию найденных релевантных документов, как на основные, так и на дополнительные рубрики МПК, указанные в документе.
9.2.8.3. Проведение патентных исследований
Патентные исследования (ПИ) регламентируются действующим ГОСТ Р 15.011—96.
Различают следующие основные виды исследований:
- с целью определения уровня техники и тенденций развития;
- определения патентоспособности решений;
- определения патентной чистоты выпускаемых изделий и применяемых технологий.
Первый вид исследований проводится в тех случаях, когда возникает необходимость в исследовании патентной ситуации для нового объекта техники, например когда принято решение о разработке нового изделия. В этом случае ПИ позволяют собрать сведения о патентах в данной, конкретной области техники и на основании этой, как правило, обширной информации выявить не только достигнутый уровень техники, но и получить данные о ведущих фирмах в данной области, изобретателях, ведущих тенденциях и т. д.
Патентные исследования по проверке патентоспособности технического решения требуют выявления аналогов изобретения, что позволило бы определить, является ли решение новым и обладает ли оно изобретательским уровнем. Такие исследования обязательно должны проводиться до принятия решения по оформлению заявки на получение патента.
Исследования в целях определения патентной чистоты выпускаемой техники и применяемых технологий направлены на выявление патентов, которые могли бы быть нарушены выпуском изделия и применением какой-либо технологии64.
Патентные исследования включают следующие этапы:
- разработка задания на проведение ПИ и регламента поиска;
- поиск и отбор патентной и научно-технической документации;
- анализ отобранной документации;
- составление отчета о ПИ.
Эффективность поиска патентной информации зависит не только от точного следования методике его проведения, но также от запаса терпения, т. к. приходится просматривать массу информации. Естественно, она зависит также и от квалификации поисковика, его умения.
Успех исследований также в большой степени зависит от правильно составленного задания и выбранного регламента поиска.
Разработка задания
Задание является обязательным документом при проведении патентных исследований.
Прежде всего, необходимо определить и подробно описать объект патентных исследований, указать назначение поиска. Объектами патентных исследований могут быть:
• устройство (машина, прибор):
- устройство в целом (общая компоновка, принципиальная схема);
- способ (принцип) работы устройства;
- материалы (вещества), используемые для изготовления отдельных элементов устройства;
- технология изготовления устройства;
- области возможного применения;
• технологический процесс:
- технологический процесс в целом;
- этапы технологического процесса, если они имеют самостоятельное значение;
- исходные продукты;
- промежуточные продукты и способы их получения;
- конечные продукты и области их применения;
- оборудование, на базе которого реализуется данный способ;
• вещество:
- само вещество (качественный и количественный состав);
- способ получения вещества;
- исходные материалы.
Исходя из задачи исследований составляется регламент поиска.
Разработка регламента поиска
В зависимости от задачи исследований регламент
поиска будет разным. Например, при исследовании
патентной чистоты подготовленного к промышлен-
ному выпуску объекта техники необходимо прове-
рить, не подпадает ли этот объект под действующие
патентные документы. Поэтому для каждой страны,
64 Известен случай, когда пришлось снести построенный завод, т. к. в этой стране до начала строительства действовал патент, защищающий технологию переработки, которая была использована в технологическом цикле завода и права на которую принадлежали по патенту другому лицу.
Интеллектуальная собственность
1353
где проверяется патентная чистота, проверяются все действующие патентные документы, как в отношении объекта в целом, так и в отношении его составных частей.
Другие виды исследований носят более вероятностный характер, не ставится задача выявить все когда-либо опубликованные патентные документы по данному объекту техники, т. к. это чрезвычайно трудоемко и требует больших временных и финансовых затрат.
При разработке регламента поиска для проведения большинства видов патентных исследований кроме патентной чистоты устанавливается компромисс между полнотой поиска и трудовыми, временными и финансовыми затратами на его проведение. Но тем большее значение имеют опыт и искусство проводящего поиск, чтобы при наименьших затратах получить наилучший результат исследований, большую полноту и релевантность.
Некоторые отработанные временем нормы, закладываемые в регламент патентных исследований, будут приведены для соответствующих разделов регламента.
Далее выбор параметров регламента поиска обсуждается для исследований на уровень техники и патентоспособность.
Страны поиска
Обычно поиск ведут по патентным документам шести ведущих стран мира: США (US), Великобритании (GB), Франции (FR), Германии (DE), России (RU) и Японии (JP), а также по патентным документам Европейского патентного ведомства (ЕР) и заявкам РСТ (WO)65.
В иных случаях к данному обязательному перечню добавляется патентная документация стран, о которых известно, что они являются ведущими в данной области техники, например Швейцария (СН) в области создания часов.
Приведем расшифровку буквенных обозначений стран мира, которые применяется на патентных документах.
АР Патент AR1PO (Африканская региональная организация промышленной собственности): КЕ Кения (Kenya), LS Лесото (Lesotho), MW Малави (Malawi), SD Судан (Sudan), SZ Свазиленд (Swaziland), UG Уганда (Uganda).
BX Бюро Бенилюкса по товарным знакам и промышленным образцам.
ЕА Евразийский патент: АМ Армения (Armenia), AZ Азербайджан (Azerbaijan), BY Беларусь (Belarus), KZ Киргизстан (Kyrgyzstan), KZ Казахстан (Kazakstan), RM Республика Молдова (Republic of Moldova), RU Российская Федерация (Russian Federation), TJ Таджикистан (Tajikistan), ТМ Туркменистан (Turkmenistan).
EF Союз стран — участниц Патентной конвенции Европейского сообщества.
ЕР Европейский патент: АТ Австрия (Austria), BE Бельгия (Belgium), CH & LI Швейцария и Лихтенштейн (Switzerland and Liechtenstein) DE Германия (Germany), DK Дания (Denmark), ES Испания (Spain), FI Финляндия (Finland), FR Франция (France), GB Великобритания (United Kingdom), GR Греция (Greece), IE Ирландия (Ireland), IT Италия (Italy), LU Люксембург (Luxembourg), MC Монако (Monaco), NI Нидерланды (Netherlands), PT Португалия (Portugal), SE Швеция (Sweden).
OA Патент OAPI (Африканская организация интеллектуальной собственности): BJ Бенин (Benin), BF Буркина-Фасо (Burkina Faso), CF Центрально-Африканская Республика (Central African Republic), CG Конго (Congo), CI Кот д'Ивуар (Cote d'Ivoire), CM Камерун (Cameroon), GA Габон (Gabon), GN Гвинея (Guinea), ML Мали (Mali), MR Мавритания (Mauritania), NE Нигер (Niger), SN Сенегал (Senegal), TD Чад (Chad), TG Toro (Togo).
WO Всемирная организация интеллектуальной собственности (ВОИС).
Источники информации
Основными источниками информации при проведении большинства исследований являются бесплатные электронные базы данных, доступные через Интернет.
Российское патентное ведомство
Реферативная информация по заявкам и патентам РФ с 1994 г.
http://www.fips.ru/russite/index.htm
Доступ к МПК
http://www.fips.ru/russite/classificators/ipc7.htm
Доступ к МПК на английском
http://classifications.wipo.int/fulltext/newjpc/index.htm
Кроме того, на сайте ФИПС имеется доступ к «Открытым реестрам» (http://www.fips.ru/cdfi/index.htm) по изобретениям (с 1924 г.), полезным моделям (с 1994 г.), промышленным образцам (с 1986 г.), товарным знакам (с 1926 г.). Поиск в открытых реестрах производится по номеру документа.
Патентное ведомство США
Доступ к полнотекстовой БД патентов с 1976 г., реферативной БД патентов с 1976 г. Доступны факсимильные копии патентов США с 1836 г.
http://www.uspto.gov/patft/index.html
Европейское патентное ведомство http://ep.espacenet.com/
Поиск патентных документов всего мира.
Патентное ведомство Японии
Реферативная БД (PAJ) с 1993 г. (PN 05000001-11299300) на английском языке.
Имеется возможность получения полных текстов документов последних лет на английском языке.
База данных WIPO (РСТ)
http://www.wipo.int/ipdl/en/
65 Стандартами ВОИС (Всемирной организации интеллектуальной собственности) регламентировано единообразное применение сокращений, форматов патентной документации для патентных документов патентных ведомств всех стран мира.
1354
Новый справочник химика и технолога
Двухбуквенные коды государств и региональных организаций
АЕ Объединенные Арабские Эмираты CL Чили GW Г винея-Биссау LU Люксембург
AF Афганистан СМ Камерун GY Гайана LV Латвия
АО Антигуа и Барбуда CN Китай НК Гонконг LY Ливия
AI Антилья СО Колумбия HN Гондурас МА Марокко
AL Албания CR Коста-Рика НТ Гаити мс Монако
AM Армения CS Чехословакия ни Венгрия MD Республика Молдова
AN Антильские острова си Куба ID Индонезия MG Мадагаскар
АО Ангола CV Зеленого Мыса Острова IE Ирландия МК Бывшая югославская республика Македония
AR Аргентина CY Кипр IL Израиль ML Мали
AT Австрия CZ Чешская Республика IN Индия MN Монголия
AU Австралия DD ГДР IQ Ирак MR Мавритания
AZ Азербайджан DE Германия IR Иран (Исламская Республика) MS Монтсеррат
BA Босния и Герцеговина DJ Джибути IS Исландия мт Мальта
BB Барбадос DM Доминика IT Италия ми Маврикий
BD Бангладеш DO Доминиканская Республика JM Ямайка MV Мальдивы
BE Бельгия DZ Алжир JO Иордания MW Малави
BF Буркина-Фасо ЕС Эквадор JP Япония MX Мексика
BG Болгария ЕЕ Эстония KE Кения MY Малайзия
BH Бахрейн EG Египет KG Киргизстан MZ Мозамбик
BI Бурунди ES Испания KH Кампучия (Демократическая Республика) NE Нигер
BJ Бенин ET Эфиопия KI Кирибати NG Нигерия
BM Бермудские острова FI Финляндия KM Коморские острова NI Никарагуа
BN Бруней FJ Фиджи KN Сент-Кристофер и Невис NL Нидерланды
BO Боливия FK Фолклендские (Мальвинские) острова KP Корея (Народная Демократическая Республика) NO Норвегия
BR Бразилия FR Франция KR Корея, Южная NP Непал
BS Багамские острова GA Габон KW Кувейт NR Науру
ВТ Бутан GB Великобритания KY Каймановы острова NZ Новая Зеландия
BU Бирма GD Гренада KZ Казахстан OM Оман
BW Ботсвана GE Грузия LA Лаос PA Панама
BY Беларусь (Belarus) GH Гана LB Ливан PE Перу
BZ Белиз GI Гибралтар LC Сент-Люсия PG Папуа — Новая Гвинея
CA Канада GM Гамбия LI Лихтенштейн PH Филиппины
CF Центрально-Африканская Республика GN Гвинея LK Шри-Ланка PK Пакистан
CG Конго GQ Экваториальная Гвинея LR Либерия PL Польша
CH Швейцария и Лихтенштейн GR Греция LS Лесото PT Португалия
CI Кот д'Ивуар GT Гватемала LT Литва PY Парагвай
Интеллектуальная собственность
1355
Продолжение
QA Катар SL Сьерра-Леоне ТМ Туркменистан VC Сан-Винсент и Гренадины
RO Румыния SM Сан-Марино TN Тунис VE Венесуэла
RU Российская Федерация SN Сенегал ТО Тонга VG Виргинские Британские острова
RW Руанда SO Сомали TR Турция VN СРВ (Социалистическая Республика Вьетнам)
SA Саудовская Аравия SR Суринам ТТ Тринидад и Тобаго VU Вануату
SB Соломоновы острова ST Сан-Томе и Принсипи TV Тувалу WS Самоа
sc Сейшельские острова SU СССР TW Тайвань YD Йемен (Демократический)
SD Судан SV Эль-Сальвадор TZ Танзания YE Йемен
SE Швеция SY Сирия UA Украина YU Югославия
SG Сингапур SZ Свазиленд UG Уганда ZA Южно-Африканская Республика
SH Остров Святой Елены TD Чад US США ZM Замбия
SI Словения TG Того UY Уругвай ZR Заир
SK Словакия TH Таиланд UZ Узбекистан ZW Зимбабве
TJ Таджикистан VA Ватикан
Классы МПК
Классы Международной патентной классификации определяются для каждого объекта поиска до подгруппы. Чем точнее определен класс МПК, тем легче проходит поиск информации и тем более релевантны заданию его результаты.
Определение ключевых слов и других поисковых признаков
Определение ключевых слов является очень важным элементом поиска в электронных базах данных, облегчающим и ускоряющим его. Ключевые слова при поиске могут использоваться как совместно с рубриками МПК, так и отдельно. Могут применяться также усеченные слова (если база данных разрешает их применение).
В разных странах в одной и той же области техники может применяться различная терминология. Опыт показывает, что ключевые слова очень часто корректируются в процессе поиска.
Кроме ключевых слов в каждом конкретном случае могут использоваться дополнительные поисковые признаки: названия фирм-заявителей, имена изобретателей, номера патентных документов и т. д.
Применение ключевых слов и иных поисковых признаков может значительно улучшить результаты поиска, но может и привести к неверному результату. Нигде так не проявляется опыт и уменее поисковика, как в выборе дополнительных поисковых признаков.
Поиск только с помощью ключевых слов может дать неверные результаты. Поэтому, по нашему мнению, надо следовать такому правилу: первична МПК, ключевые слова — подсобный инструмент.
9.2.8.4. Поиск и отбор патентной и научно-технической информации
Поиск информации в электронных базах данных производится с помощью поисковых признаков, которые обсуждались в предыдущих подразделах.
Важно правильно классифицировать объект. Это не всегда удается сразу. Поэтому следует внимательно отслеживать классификацию найденных релевантных документов и корректировать регламент поиска.
На рис. 9.16-9.23 приведены примеры титульных листов патентных документов в области химических технологий.
Патентные документы содержат информацию о правовом статусе документа, авторах и заявителях, приоритетных данных... которая расшифровывается с помощью системы цифровой идентификации полей патентной документации (ИНИД), используемой на каждом патентом документе. Коды проставляются в виде цифр, заключенных в скобки Приведем коды ИНИД, позволяющие определить каждую библиографическую информацию патентного документа, изданного в любой стране.
Коды ИНИД и минимум библиографических данных, необходимых для идентификации
(10) Идентификация документа
(11) Номер документа
(12) Словесное обозначение вида документа
(13) Код вида документа в соответствии со Стан-
дартом ВОИС ST. 16
1356
Новый справочник химика и технолога
**( 19) Код в соответствии со Стандартом ВОИС ST.3 или другие средства идентификации ведомства, осуществившего публикацию документа
*В случае, когда библиографические элементы (И) и (13) или (19), (11) и (13) используются вместе и располагаются в одной строке, при желании может быть использована категория (10).
’’Минимум элементов библиографических данных только для патентных документов.
(20) Данные о национальной регистрации
(21) Номер(а), присвоенный(ые) заявке(ам), например «Numero d'enrigestrement national», «Aktenzeichen»
(22) Дата(ы) подачи заявки(ок)
(23) Прочая(ие) дата(ы), включая дату подачи полного описания после подачи предварительного описания и дату выставочного приоритета
(24) Дата, с которой начинается действие прав промышленной собственности
(25) Язык, на котором была первоначально подана библиографическая заявка
(26) Язык публикации заявки
(30) Приоритетные данные
(31) Номер(а), присвоенный(ые) приоритетной заявке
(32) Дата(ы) подачи приоритетной заявки
(33) Код в соответствии со Стандартом ВОИС ST.3, идентифицирующий национальное ведомство промышленной собственности, присвоившее номер приоритетной заявке, или организацию, присвоившую номер региональной приоритетной заявке; для международной заявки, поданной в соответствии с РСТ, следует использовать код «WO»
(34) Для приоритетных заявок, поданных в соответствии с региональными или международными соглашениями, код в соответствии со Стандартом ВОИС ST.3, идентифицирующий, по крайней мере, одну страну — участницу Парижской конвенции, в которую была подана региональная или международная заявка
*В случае, если данные, идентифицируемые кодами (31), (32) и (33), используются вместе и располагаются на одной строке, при желании можно использовать категорию (30). В случае публикации кода в соответствии со SТ.З, идентифицирующего страну, в которую была подана региональная или международная заявка, он должен быть идентифицирован посредством использования кода ИНИД (34) и должен располагаться на строке, отличной от той, на которой располагаются библиографические элементы, идентифицируемые кодами (31), (32) и (33) или (30);
Примечание:
Расположение номеров приоритетной заявки должно соответствовать положениям Стандартов ВОИС ST.10/C и ST.34.
(40) Дата(ы) предоставления документа для всеобщего ознакомления
**(41) Дата предоставления для всеобщего ознакомления посредством выкладки или предоставления копий по заказу не прошедшего экспертизу документа, по которому на эту или более раннюю дату не был выдан патентный документ
**(42) Дата предоставления для всеобщего ознакомления посредством выкладки или предоставления копий документа, прошедшего экспертизу, по которому на эту или более раннюю дату не был выдан патентный документ
(43) Дата публикации типографским или иным аналогичным способом документа, не прошедшего экспертизу, по которому на эту или более раннюю дату не был выдан патентный документ
(44) Дата публикации типографским или иным аналогичным способом документа, прошедшего экспертизу, по которому на эту или более раннюю дату не был выдан патентный документ
(45) Дата публикации типографским или иным аналогичным способом документа, по которому на эту или более раннюю дату был выдан патентный документ
(46) Дата публикации типографским или иным аналогичным способом только пунктов формулы документа
(47) Дата предоставления для всеобщего ознакомления посредством выкладки или предоставления по заказу копий документа, по которому на эту или более раннюю дату был выдан патентный документ
’’Минимум элементов библиографических данных только для патентных документов: для выполнения требования о минимуме библиографических данных достаточно указания даты предоставления для всеобщего ознакомления соответствующего документа.
(50) Техническая информация
(51) Международная патентная классификация
(52) Национальная классификация
(53) Универсальная десятичная классификация
(54) Название изобретения
(55) Ключевые слова
(56) Список документов-прототипов, если он не включен непосредственно в текст описания изобретения
(57) Реферат или формула изобретения
(58) Область поиска
(60) Ссылки на другие юридически связанные национальные патентные документы, включая неопубликованные заявки на них
(61) Номер и, если возможно, дата подачи более ранней заявки или номер более ранней публикации, или номер ранее выданного патента, авторского свидетельства, полезной модели или подобного документа, по отношению к которым настоящий документ является дополнительным
(62) Номер и, если это возможно, дата подачи более ранней заявки, из которой выделен настоящий документ
(63) Номер и дата подачи более ранней заявки, по
отношению к которой данный документ является про-
должением
(64) Номер переизданной более ранней публикации
(65) Номер ранее опубликованного патентного
документа, касающегося той же заявки
(iS)RU^2218381 (13/C1
(51 > 7 С10ИДИ), СЮМ15Ш2, C10N30:20
РОССИЙСКОЕ АГЕНТСТВО по ПАТЕНТАМ И ТОВАРНЫМ ЗНАКАМ
^ОПИСАНИЕ ИЗОБРЕТЕНИЯ
к патенту Российской Федерации
(14) Дате публикации. 2w3.12.1e
(21) Регистрационный номер заявки: 2902119912/84
(22) Дата подами заявлю 2ОД2.07.22
(24) Дата начала действия патента 2082,0742
(46) Дата пубяиедзии формулы изобретения.
годзлгло
(56) Аналоги изобретения: RU 2169266 С1.20.11.2000. US 5158653 А, 20.10.199Х WO 96/00272 А1,
(71) Мая заявителя Гссудеретвеиное унитарнее предприятие Научно, производственное объединение "Нефтвпромжим"
{72) Имя изобретателя . Герейшима А.З.;
Петухова Е.8.; Юсупова Д.8.; Лебедев Н.А.; Чертили*» Т.Н.; Пономарева А.З.
(73) Имя латеитосбпадетелА: Государственное унитарное
”|4ффТф{|рОМХ1И*1’*
(98) Адрес для переписки: 420046. г.Казеиь, уп. И. Ершова, 29, ОАО "ИИМиефтвлромхнм”, Патентно.
лицензионный сектор
04,01.1996.
(54) КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ НЕФТЕПРОДУКТ И МАРКЕР, СПОСОБ И РАСТВОР ДЛЯ МАРКИРОВАНИЯ НЕФТЕПРОДУКТА, СПОСОБ ИДЕНТИФИКАЦИИ НЕФТЕПРОДУКТА И СПОСОБ ПОЛУЧЕНИЯ МАРКЕРА
Изобретение отводится к области марзировзмия нефтепродуктов, а имение х совяивеииям для маркирования нефтепродуктов. способам идентификации нефтепродуктов в способам подучития маркеров. Композиция включает нефтепродукт и ебкаруедвавмое количестве мйргера, а занес гее которого иододъау ют биологический пигментный препарат - лродигиозин. причем маркер а указанном нефтепродукте содврмсттея в количестве (1.2-9.3). 10^ тФ. Содеав маркирования нефтепродукта включает добавление в нефтепродукт ебнаруамваемего количества маркера с вятальззввиием в «тчестве маркера биодстичодиото пигментного преодрвта в количестве {1^-9.ЭХ1&'в тф При добаддеиии е указанны» нефтепродукт маркер доджей находиться в растворенном содтсянзи Способ идентификации нефтепродукта содержит обмвружиеевмею едвичестод мэдеддо с добавлением прододяющегодя реактива в указанную пробу, причем а качестве маркера иоподьзуют вышеуказанный препарат, а а качестве яродвпякхцвтч реактиве • водный раствор соляной кмодсты 36%-ной кодцвитрвции. Раствор сод®»» кислоты добавляют а указанную пробу в «апвчестве 0,33'0.35% в зависимоотв от объема пробы, в яоличесгеоднод оодержаиве маркера в нефтепродукте определит методом абсорбционной агектрофстометрии. Раствор для маряфодзния одфяэдодутза содержит маркаер в растворитель, который смешиеевгеи с иефгелродуктом. в качестве маркера берут вышеуказанный биологический пигментный преаодзт - ододагиоаии а «одичаете® 0. 3-2.20%. В качестве растворителя иеподьзуют зтияовый спирт, пвтрспейный зфир. этетеодтат. Способ одпучения маодеод включает еыращиаание бактерии бсттатв marcesew. «в ж-арааодай.но» овсяной среде и проведение зестракоди «типовым спиртом $8%-иой коицвнтОДции при остодходании. Экотраиодю бактерий зтододыы одиртом проводят многократно де обедодечиввння бактериален»» модем, в после каждой обработки проводят содждеиие бактериальной модем о одслодуюстим од отделением от нядлсйдочной «едкости Изобретений одзводяст создать выижоаффехгиаиод средство с одподьзоводиим экедст югести чистого лриоддмсто «иг«лента, расширите ассортимент мод»вр<>а.
Рис. 9.16. Титульный лист патента Российской Федерации
(12) United States Patent Bradley et al.
IHNIIIIIIIIIIIHIII
US006672077B1
(io) Patent No.: US 6,672,077 Bl
(45) Date of Patent: Jan. 6,2004
(54) HYDROGEN STORAGE IN NANOSTRUCTURE WITH PHYSISORPTION
(75) Inventors Keith Bradley, El Cerrito, CA (US), Philip G. Collins, Oakland, CA (US), Jean-Christophe P. Gabriel, Pinole, CA (US), Young-Kyun Kwon, Albany, CA (US). Seung-Hoon Jhi, Albany, CA (US). George Gruner, Angeles. CA (US)
(73) Assignee Nanomlx, Inc., Emeryville, ('A (US)
(* ) Notice Subject to any disclaimer, the term of this patent is extended or adjusted under 35 US.C 154(h) by 82 days
(21) Appl No • 10/020392
(22) Filed. Dec. 11, 2001
(51) Int. Cl?
(52) U.S. Cl. . .
(58) Field of Search
.. .. F17C 1V00
......... 62/46.1
... 62/45.1, 46.1.
62/46 2,440, 451
(56) References Cited
U S PATEN Г DOCUMENTS
OTHER PUBLICATIONS
Ralph T Yang, "Hydrogen Storage By Alkali-doped Carbon Nanotubes-revisited”, Carbon vol 38 (2000), pp 623-626 P Chen et al. “High H? Uptake By Alkali-doped Carbon Nanolubcs Under Ambient Pressure And Moderate Temperatures”, 'Science vol 28.5 (Jul 2, 1999), pp. 91-93.
К Murata et al, "Pore Structure Of Single-wall Carbon Nanohorn Aggregates”, Chemical Phvsics letters vol 331, (Nov. 24, 2000), pp 14-20
Y Ye et al,‘‘Hydrogen Adsorption And Phase Transitions In Fullenlc”. Applied Phvsics Letters vol 77, No 14, (Oct. 2, 2000), pp 2171-2173
Chambers et al, “Hydrogen Storage in Graphite Nanofi-hers,” ITic Journal of Phvsical Chemistry В . vol 102, No 22. May 28, 19^8, pp 4253-1256
Dillon et al, “Storage of hydrogen in single-walled carbon nanotubes,” letters to Nature, vol 386, Mar 27, 1997, pp 377-379
Poiner et al, "Hydrogen adsorption in cartxm nanostructures,” International Journal of Hydrogen Energy 26, 2001, pp 831-835.
(List continued on next page.)
Primary Examiner—Denise L. Esquivel
Assistant Examiner—Malik N. Drake
(57) ABSTRACT
A hydrogen containing nanostructure is provided, where the hydrogen is adsorbed to the nanostructure by physisorption TTie nanostructure includes light elements, selected from the second and third rows of the periodic table The nanostructure is formed as a layered network of light elements coupled with covalent sp2 bonds. The chemical composition of the nanostructure can be such that the desorption temperature of hydrogen is greater than the liquefaction temperature of nitrogen, 77 K. Further, a hydrogen storage system is provided, including a container and a nanostructured storage matenal within the container, wherein the nanostructured storage materia) includes light elements, and the □anoslruc-tured storage material is capable of adsorbing hydrogen by physisorption The hydrogen storage system can include a liquid nitrogen based cooling system, capable of cooling the nanostructured storage material below the desorption temperature of hydrogen Some embodiments contain a heater to control the temperature of the nanostructured storage material
30 Claims 10 Drawing Sheets
126
Интеллектуальная собственность
Рис. 9.17. Титульный лист патента США
LU
L/l
Саю* С оцямису ачасмия Рвепувнни
ГосуОДрстмквы# ««aim; СССР
«О BMStt вэобрсми»* ' Я «ПфиОД* ;
О П1Й№«НЙИ Е ИЗОБРЕТЕНИЯ
<>., 740807
(72) Авторы . мэебдогеям»
(71) Заадитедд
К ЛВТООСКОМУ С8ЯД£ТШ%СТаУ
(«П ДоПОЛИИГВЯЬЯОв К Д»Т. с«ид»ву — (22)3»адюна 170257(211 24 73«05/23-84
г арисввдикододвм мявии HS ~
(23) Прыериодг -
Олувликедлно 15Л6.80 бюллетень N9 22 ДатвопуЙянедваиияопнеаыия 1ЗД&ЗД
(5Т)М. Кл?
С 18 G 5/02
(53) УДК $47.183.
.0$ <080.87
М.А.Веряив, Э.В.Кхеяый, Л>М.!Эяаулеиский. Б.А.Меркулов, И.М.Яоло'Чхиков, в.а.Лопатинский, 8.В.&в«впо» и й.Т.МеиайИко
рсесяаознма научно-иаадедавателведна и проектный институт по переработке гайв. ж Инс та тут г<мн» дк Укрсинокой ССР
(34) СНОСОВ ПОДГОТСРКИ ЙРИРвДМНХ и втавь» БАЗОЙ A УРАЙСЯОБТУ
1
' Иаов£и»т«жв<з отжоедтси к способу аодготовки природяых и нафтятод га-зо» И Транспорту я мажет «ВТ» иримй-аеио «а а&фтвйобыиатях предприятиях , и гвуедврврабаодгвааедих ваводвк.- 5 Прдредиме и нефтяные газы содержат до 100 г/м4, а ц оеделыодх случаях до <50 г/м* угвевоаорсйо» Су,»,
Й связи е этим газы вез соответ- ,_ стяуюавй подготояки не могут траяспвр-'У тяредать иа далвдие расстояние, так к«к »с время транспорте может праве-ходить коадедедцав углеводород»», которая приводит к обрезоаамию жнд-коетвых пробок, что снижает пропуск- “ иуй своеобвоета гааопроводоз, а- в стаедаанх слуха»к и «го полному перекрытию,
8 каетояазае время вря падготепка rase к транспорту из него выделяют «• вмеаоде гомедотк метая» (пропан, Сутаны, йевтавы и высшие!, которые «и-я «ютея еырвем для «ефод химической яромиедвввоств, а так же могут рыта .. иепслваовали » виде деиженнсг» газа *4 для патовых цеяед,
Известен способ подготовки природ» иык и иефтяиых газов х транспорту путей адсорбции нз газа углеводороде» С^,в(Н. ' 30
2
Согваеда этому спосоеу омред «е-псдгртожлвквыА газ педедт в едсйреер, ««ходящийся » режиме адсорбции; «а адсорбера стаодят отбеизииеивмй газ, который моадас транспортировать по ма-гиегредьиш* газаарояедам;» это - время второй адсорбер находится я режиме регенерация, мотору» осумвствля»т ксхадчин газом, вагрввдеыым а ракупе-ративиом теплообменнике и печи, ягеле чего газ вродуодедт а качестве десорбмрутаго агента через явей-щеияый уедеаодорадами С^^адсорденти затем газ, насыхеиный яардод выедим углеводородов, редаедают а тепяоов-иадвмке н хаяодильнвке с цела» конденсации углеводородов к направляют з седаратор, оде оодеяякт жидкие угле-водороды газа, а гвз после сепаратора подают на вход адсорбера, явиодямегодя в режиме адсорбции.
йаяако, способ подготовив газа к трвмсяорту путем адсорбция из «его C^.ieимеет недостягох, закяючдкемйся » бол майк кяпмтаповвошениях, требуемых для ere есуеествлаямя. Зто с»я-ваио с тем, что гады регенерации, еоставлпкяше от 10 до 25% ст исходного иодичестза газа, после регеяещаиви адсорбента напрадяают снова » виня
FR 2 820 754 - А1
(Э ЯёРУвиОУЕ RW4pAJSE iNSTtrUT NATIONAL DE LA РЙ0РЙ1ЁТЙ (NDVSTRIELLE
адз
® № de puMcwion:
11 л'ийЗад яке ₽e«f Ю» !«wfW< се едяххетеа;
^H^d’etws&trwnent дайопв!:
2820 754
01 01840
CWG»,83' &53/14,001 S®//B01S 18S:lO
OEMANDE DE BREVET D’INVENTION Д1
Oatotfecepfr: 1£й2.'3>.
Prtcdie.-
® Sate <fe rniae 41# Яихвйоа <fc рчШ de ig
aatnance; 1S,5S.O2 айййл <sm
Ц«1в аа» 4осв«ввтв еШ беле »гаррод sto recPWie ргейлйпяйе: Servp&wa peii^^&txiSs
fWtencBs A (Tentm Pocuroenis <Wofw* aswanaje;
@hwantea»(e): MAWKURW,WATRHWTLW-RENT et COW£F®C£ 3 WNO.
©ТИн&ЙШ};
{§}ssan®rtaifpi»i:
\§P ЕШаавва joncsHna ti" sspos® cenpwnsin a-j rnostis us adestsauf, a« motna un waiatew ti«d dent ast едтзиа «па prase jaswise од еододв t'sftmnw. за одйз «в >'e<ycag» ven- йей sSpaiatearWS -Уав mesns иле parte «a taSyent «одре еди од tasscuiw ел одод-од одес its Одзгра, ей ,одп5 «л од>уе« од :ОДодОДод роде йододод ?р «win® «п пкуал од гйа^аййл Одпе од> ОДп Зрийв еяОДОД »з 1ОДч!одЬуге5 !ева, з ОД«в ОДОД ОД-parateur (»од et ей nwiws да одуда I weww Оде од? ОД ййадОДи’; Оподподл ссоде-ч» 4од!модл« «в ОДОДОД jfpn одг «сод ап 1^ОД>§бод од да ршОДОД Од Одирйязйод 5да ёодод епод!» вп ОДУод&гродод даОДш «ОД <!йрод«!>
Новый справочник химика и технолога
IIIIWIIMillillllilMII
Рис. 9.18. Титульный лист авторского свидетельства СССР
Рис. 9.19. Титульный лист патента Франции
iJST Ewapttache* Patentamt
(19) EwogaanPetentcufiee
Office «tttoptat ttea btevete
ММШММ
(«5 EP 1 375 583 A1
EUROPEAN PATENT APPLICATION
published h accotdanse with Aft iS8{3} EPC
{43) Os» c* omcatton:
даш ашшвшдок
(2 J) App&stem «cSTtMsr 02788487.3
(22) Dates! <ifcg ЙМЙЖ1
(S1> tot».?; соек SMM. CORK 50575, C08L 23/00
{88} WsmtoonsiapplicaKoantenttor: pcwpaxea»»»
(87} Intctnwton» puSItoation naaeber
WO ЗДМПТДО (03 ЛОАХВ {gazette 20Q2M0)
(84) Dasigtotwa Gaat»«Stig State*
AT HE CH CY 08 OK 88 Я FR 88 OR IE ГГ U LU
MCNLPTSETR
Oewgnated g*ten»ton State*.
ALWLVMKSOS4
{Ш 7743.2001 UP ОДМ08Ю
ITT) Appfcawu ffiEW JAPAN CHSSttCAL CO. LTD
KyotoeM Kyoto «384924 (JP)
(72} tovwttor*.
» HOMOTQ. Hetutemn, taste gfatiahen В4Й Kyeto^tol. Кум» 81Э4Я01 (Jty
• ISHIKAWA ЙНЛЛ
UJMM, Kyoto «1 f-COKt (JP)
* KOSATASHl, Tnahtakl totfrSM, Hate C314S0S (4P)
{74} Hajxwentat.va Rant, Rater, Or, FlflflintlinWttft
KaiawpiateS
80«Ю«Ю1кШ(ОЕ)
{54} DtACETAL COMPOSWOH, NUCLEATING AGENT CONTAINING W COMPOSmON ЯЖ POLYOLEFIN, POLYOLEFIN RESOi COMPOSWON CONTAINING THE LHACETAL COMPOStrm PROCESS FOR PROQUCiNG THE RESIN COtePOSmON. ANO «OL0EO OBJECT
^7) Oisetoseestaa ^taawter or ptswdwy t^aaetel oaffigoa^o» wwwwhj (A) a dtesMte such а* 2,44)^i»riryitoene-C-wta^, (Bj a «utettte ««« *«3
ВП(1 (С) АЛ ffitWQcei'ftrtMfffig ftG^v
(S| a*d{C) betna ttoiiOTwy «te₽«ffc»e и«»ай®«ш m ttwgrwawar w «««tel «mpsMm. ase co»-«nenl (9j Mngf№M«nt to » pfwsrtlan gt 2Л to 3 wffi, «WcswwteRt (C) bstog present in a pwpa’feso «03
» 8 amt й» total amount of cemttoaeto |8} and cteoponem {C) aatoe net mote than 7 wOL. baaed t» too diacctei «траайоп; в ptWyatefin rasto дарийи cotopttetog th® <й««Ш compostoon and a potyotoln msin; a pn»isa*BtWMapsrte9to«nteinct»wa^ atw8«ns}wwoaiw«*i^t^ watoctan-Itea2ton.
EF»1 375 583А1
a*w«»«wx. naw aersr-st
Рис. 9.20. Титульный листЕвропейского патента
<n> SACK PKM VKRTRAO »S »i£ тВЖВАТЮВЛЖ ZtiSAM MKNAKBKft ABF ИЙИ GEftl'T BBS
WExrwmastFcn уижОтлшситк |хтш.4пошс лммшлт
(19) WdltorgM&ttieft f4r gefetigts EJgrMam 1актэвйв;&8 88m
(43) 1м*гиа«к>ааи* VrrttffeiliBefcttagMsiaffi
14 Oeaembtr ЖЗ (24.1 1.1003)
»ШИм№1И1ж&Я«тяВ1
(IS) interaetioeale Vertffeeftcl)»»gsnui9»taer
PCT WO 03/106552 Al
(51) lBtwurt9»at«p»t««rt<fc»riei<»»i0«': СМИ*. 13/80, Ж 23Л6
WO 03/106552 Al «miiuiHiiMamii
(11) («^«tioaatetAkamrdKbwi: KMtSVSMWXi
(H) tBtere«&»i*lat АшжМЫМша:
10 A»120O;S(lO0S.3s»3}
(25) CiiMeirfcee^sspraeShr: Deassch
(28) Dttotwh
(30) ЛярЬм mt PstorttM;
1B2 20 W0 S5. Ш 3002 (!5.»W> Ofi
US): RRHAl.l AG + CO (fWft RheMotobws, «5Ш Rsha»(tMt).
(72) ЕИЬийг; «пм!
(75) ЕгМ^ЛмиМи (met j& (/$t OftOW, Merlin (ГОЖ); Wsastodkwwae Ж. 9ЖВ11Ы<Ш>.
(SI) B«ttt>»»»»(Staat»e fyM&eijt AIL AO. AU AM, AT,
AC, AZ. BA. BS,BO, BR.BY.BZ. CA,CH,CN,CO.<X
cu, cat, ok, km, &zt-ii. (ft, he, oh. он.
Oft HR. HO, ft, U, ft, «,))>, KB. KO. Kft KR.KZ.tC, IX, 1.Й. LS. IT, W. tv, MA, MO. MO, MR, MN, MW. MX. MZ.Ni.mM CM. ft(, Pl. ft RO, R0,SC,80. ft, SO. SK, Sl„ TL TM, TN, TR, ГГ, TZ, UA, VO. I.!S, Ж VC, VN, YV. ZA, ZM. ZW.
(84) ОДНмвмдоашш» (Wgftteejli ARW-Pswtt «HL СЯМ. K& LS, MW, MZ, SO. St. SZ. TZ. Ш. ZM. ZSft waswto fttvM 1AM. AZ, RY. RO, KZ, MO, №. ft IM). wepSsshsa fttwst (АГ, Ж НО, СИЛЛ'; <X 4Ж BK. Ж 88. ft ftt, OS. OR. ftt, ft ft LU. ИС, NL. PT. RO, SF, ft SK. Т». ОЛИ Jtstew Ж ft CF< «5. et, m, ол. еж. oq. ow. ml hr. nb, skib, rot
£гкйгай**е*4в fteHWt
АЖМЙаЯйМ'
— »я?«еггш>'<глаАгт AtrAc^AaaAeHeAt
Zxr Лг XmsieelttMiUfCwii» uixt dfer ааЛочк .44»
iUnxtigtti vsti cuf dir я« Ctt-
FCf-CamsIff terwAtB
($< № COMWlftHTY iMFRWKMKNr ACJiftViai BY S YNOtOTACTlC POLYMra®
(S4) StawklmiMg: VtlR^OUCHKSfmWESSRRllSO fftRCH SVNtSOTAKTISCHBS РЙЗУЖЖПЖ
(57) Abstract; fte MveNtais «Sales S> (Мто^вс cfttetttsra base) oe e РРД:Р1Ж Ыеи) «Н» » erosMwtod JIFDM ptaee. Its MskA $уп&<!1ж1я: p<jiyrr<>pylw.c acts M &<t МеммЬ)' pramxcr. The Mdt&sn syndiytautic p^iypn^pyieyc wapwvc* the oar. f&abjgyjuxi tftetle^tagaalMhgs^stM&eMeft This ieata to sarahtnebly naprowsl sto&ecs of artieSes ihstsm ркМжМЬу e*tmiw> sx injoetlcn tawkdmg,
(57) KtMMtchMlKwviiap: &ts RtRreltsag hstsiffi taBHipJtto&sIto йю»яая« mf Bas» eSaw РРЖРЙМТЙктВ, <Mt wtseswter EfBM PItose. «wT«i syn^tsHfoMdxs iMypeofyfeit «St VistaaRtoswmltS'sif feftglert. &sr Zusscs vea «yteBohilrfecfW!»» Poiyfaspytos wrtsMSw) Aatiel dto MeejStotagto end ths fbesfeglsste VhSmSsm dra BfertSs Oles tstai an nhdltBels t»s*«W! ГЯяййкЪга dw rash d«a SSmsmt-, РвКвзихВя» SftStejtostwstailx*© txsjeasttai ArRtel,
Интеллектуальная собственность 1359
Рис. 9.21. Титульный лист международной заявки по процедуре РСТ
(jp) oa & $£ (А) (юшаягдят
^2003 -261369
(F2003—2G1369A)
_____ овжжй Wmjmiтш
F •
С04В W38 С0 4В W38 S> 4F2 0?
В2ЙС 4?/00 В2ЙС 47/«Э 4G 0 13
СС4В 28/Ж С04В Ж®
мшк иоо В29К 1:00
С04В Ш:30 С04В Ш:30
«ЖИЖ »гт®«2 OL 5 Ю
ДОйЯИИ »тв“®й23(ржг~вейгз) (
сггнжв уййшзянвож^ш ।
! !
(Шйяка шйвгйвв
^ж^хятлзж ЖЗЙЖТШЖЛЖХТЙ 6« i Чг
№&Ш* * Ж0
(хм№» dim » маджтшж-)
£Wfls«A »м м* фл »«з <М1«)
ЙМЖ«<
(м) йййй««й
а> (smi
ЖГй) (А) 1М^Ж», 50 0m )>* - «ш.й. зм.-П'&ййте Krm-x-fjix A<a~X&tX/.XJ^<>«i*Sttt EP=V>Xf>u Xf)WtAO~Xk. (В) t , 500fftPa • вШ.Г$>«ч 4сЖ&*>Р»~ЛХ~7-Л/£: t
I») ^^«т^яжвйййжййм^ш «, ^аж^я^-сМ' «охт
«шамло.
Рис. 9.22. Титульный лист заявки Японии
„UK Patent Application ,«>GB ... 2 380201 <«A
Applleettarr № SZHSSt.S
Й1)
aMsefRHne зтлэдйвг
(22)
(38)
PdorftyfWta i?u tameso m} ашлом иг® us
ЙЙ
(SS)
f?1)
ifrdl
SssoiTachnofoariPTys Umtree №««Ф<И«М4 й> Seuft АЙШ 1 Юм)» (tw«w Пока, 1947 Ssw&ure. Saud» АЫея
Арр&сагШ
Омтню IL&A. tae.
&M»«pwsfesd hr USA - tMamwel 2ДО C*Mtn« itomm. $*n Amon* СЫ№>гп1аЭ488МЖ< UhftMt StMOA 4» AwtMiw
(«) awe of а «еимлй»
OTi
titetard Ow*a Мест* -Л ДОДкЭДПФЙ
««
ИГ Г Cl?
СИЮЗЖ
b*CL (EdStoftVJ CBBSCA
Ос*;<кпв»Ч^ Cted oamswA укивтвл
и$впмг» a USASMMSA
FWsffia»«li ика.ЯЕЛЙгап VJCBF )Nt C?COTC.C«G W OMUNSE - EFOOOC. Wi.WM
(?4) Agent «ГкРоГ AdtfreeS fer S®W» Uk* * Co fatpsdei Home, 1S.19 tG»pxw*y, МЯвХЖк WCM «U&. t№red tUapdem
(54) Abstract ЗД»
fisntete RsthenTropsch syrrtiwtis «nd proewsina «f tautf site
tfi?) A psec»ss for ptepAting a finished feel producs (fpm a stabHiwai product тяШго, pc&duced Jrom the atfiuant et FiSEhec Tropjeh eyr<8wsit, Л F)sch»n rrojweft ayrthoaia pn>«v»s te conducted at в si» which is tamoie froch the nisttet sits whew the pKtducta from tha process ere rnart»»d. The НясЬег-ТгорквЬ product is hydroprocestsad, sad th« hydroprocassad cdfiuewt separstep ro remove a C^-lfraation end te yieid л stahilfted product roifitw)» whkii cert be exported to the market site. At ths msrtet sffit ths stabilised product mixture ш ftaetiortated into et least one fiaietad hwt product, A heavy fraction may Also be reeovnrad et the market ей» for •reparation Into at (seat one Mefcatinp oil bese eteek end then cemversicfl st fiydroteonwrthatwn ecmdhions to fcrro a lubricating base ci!.
Q Ш
N> GO CO
360 Новый справочник химика и технолога
M
Рис. 9.23. Титульный лист патента Великобритании
Интеллектуальная собственность
1361
Приоритетные данные должны быть отнесены к категории (30).
Примечание:
Код (65) предназначен главным образом для использования теми странами, законодательства которых предусматривают повторные публикации на различных процедурных стадиях под разными номерами, причем эти номера отличаются от основных номеров заявки.
(70) Идентификация лиц, имеющих отношение к документу
(71) Фамилия(и) заявителя(ей)
(72) Фамилия(и) изобретателя(ей), если он (они) из-вестен(тны)
(73) Фамилия(и) владельца(ев) охранного документа
(74) Фамилия(и) патентного(ных) поверенного(ых) или представителя(ей)
(75) Фамилия(и) изобретателя(ей), являю щего-ся(ихся) также заявителем(ями)
(76) Фамилия(и) изобретателя(ей), являющего-ся(ихся) также заявителем(ями) и владельцем(ами) охранного документа *♦ ' -
Для документов, по которым был выдан патент на дату предоставления для всеобщего ознакомления или на более раннюю дату, а также была осуществлена публикация в официальном бюллетене, требование о минимуме библиографических данных соблюдается посредством указания имени владельца охранного документа, а для остальных документов — посредством указания заявителя;
Примечание:
Коды (75) и (76) предназначены главным образом для использования в странах, национальные законодательства которых содержат требование о том, чтобы изобретатель и заявитель были одним лицом. В других случаях следует использовать коды (71) или (72) или (71), (72) и (73).
(80) Идентификация данных, относящихся к международным конвенциям, помимо Парижской конвенции
(81) Указанное(ые) государство(а) в соответствии с РСТ
(82) Указанные государства в региональном патенте (ЕР, ОАР)
(83) Информация о депонировании микроорганизмов, например в соответствии с Будапештским договором
(84) Указанные договаривающиеся государства в соответствии с региональными патентными конвенциями
(85) Дата выполнения требований ст. 22 и/или 39 РСТ о переходе к национальной процедуре в соответствии с РСТ
(86) Заявочные данные региональной заявки или заявки РСТ, т. е. дата подачи заявки, номер заявки и, факультативно, язык, на котором была первоначально подана опубликованная заявка
(87) Данные относительно публикации региональной заявки или заявки РСТ, т. е. дата публикации, номер публикации и, факультативно, язык публикации заявки
(88) Дата отсроченной публикации отчета о поиске
(89) Номер, дата подачи и страна происхождения первоначального документа в соответствии с Договором стран — членов СЭВ о взаимном признании авторских свидетельств и иных охранных документов
Примечания:
1. Коды (86) и (87) предназначены для использования:
- в национальных документах при идентификации одного или более элементов заявочных данных или данных о публикации в отношении региональных заявок или заявок РСТ или
- в региональных документах при идентификации одного или более элементов заявочных данных или данных о публикации в отношении другой заявки, поданной в соответствии с региональным соглашением или РСТ.
2. Все данные, идентифицируемые кодом (86), следует помещать вместе, желательно на одной строке;
3. Все данные, идентифицируемые кодом (87), следует также помещать вместе, желательно на одной строке.
Поиск в электронных базах данных
Поиск патентной документации в каждой электронной базе данных, адреса которых приведены выше в 9.2.8.3, имеет свои особенности. Рассмотрение методологии поиска в электронных базах данных выходит за рамки данного издания. В качестве пособия по поиску в электронных базах данных патентных ведомств и международных организаций можно рекомендовать издание [17].
Следует заметить, что кроме бесплатных электронных патентных баз данных большое значение имеют платные патентные базы данных, такие как DELPHION и DERWENT. Существуют также электронные системы автоматизированного поиска научно-технической (в том числе и патентной) информации. Наиболее известные из них STN INTERNATIONAL, QUESTEL-ORBIT и LEXIS-NEXIS.
Отбор релевантных документов
Отбор патентных документов, релевантных объекту и задаче исследований, проводится путем изучения чертежей и описания.
Патентные исследования проводятся не только по массивам патентной информации. При исследованиях на уровень техники и тенденции развития, а также при определении патентоспособности привлекаются и различные виды научно-технической информации: книги, статьи, обзоры, рекламные материалы. Вид и объем источников научно-технической информации зависят от объекта и задачи исследований. Особенно большое значение научно-техническая информация имеет в тех областях, которые по разным причинам непривлекательны для патентной охраны.
Анализ патентной информации
Анализ найденной документации позволяет решить задачи, которые были поставлены перед проведением патентных исследований. Укажем на те особенности патентной документации и информации, которые следует учесть при их обработке, а также приведем приемы, помогающие извлечь максимум информации из найденных документов.
Анализ технического содержания патентных доку-
ментов
При анализе технического содержания патентной
документации следует учесть, что патентные описания
1362
Новый справочник химика и технолога
(изобретений и полезных моделей) практически всегда имеют одну и ту же структуру.
Описание патентного документа состоит из формулы и собственно описания.
Объем прав66 определяется независимым пунктом формулы. Независимых пунктов в формуле изобретения может быть несколько, т. к. защищаться одним патентом могут, например, способ и устройство или несколько вариантов выполнения способа, устройства, вещества и другие варианты комбинаций объектов.
Зависимые пункты формулы уточняют и развивают конкретные случаи выполнения изобретений.
Описание изобретения имеет, как правило, следующую структуру:
- название;
- область техники, к которой относится изобретение;
- предшествующий уровень техники;
- задача, которая решена данным изобретением;
- суть изобретения;
- описание чертежей;
- примеры конкретного выполнения изобретения.
Первый раздел описания «Предшествующий уровень техники» содержит важные сведения об аналогах, их недостатках по отношению к изобретению.
В следующих разделах описания подробно раскрывается техническая сущность изобретения и приводятся примеры его конкретного выполнения. Однако описание, как правило, не содержит маркетинговой информации, сведений о применении изобретения, а также некоторых технических параметров, например конкретных размеров устройства.
При выполнении исследований на уровень техники и тенденции развития отобранные документы исследуются для определения конкретных направлений развития данного вида техники. Документы могут сортироваться по следующим признакам:
- цель изобретения;
- технико-экономический параметр, который улучшается;
- технический прием, с помощью которого решается задача.
Статистическая обработка патентной документации
Статистическая обработка патентных документов может дать дополнительную информацию исследователю. Результаты статистической обработки используются при определении тенденций развития уровня техники, а также при сборе конъюнктурной информации.
66 Исключительные права, которые предоставляются владельцу патента на срок действия патента и на территории, где он действует, предусматривают, что никто без его разрешения не может использовать (выпускать, продавать и т. д.) данное техническое решение.
Для промышленных образцов исключительные права означают, что никто не имеет права использовать изделие,
внешний вид которого защищен.
Динамика патентования
Динамические ряды количества патентных документов по годам могут быть построены следующим образом67:
- общее количество документов исследуемого объекта техники;
- количество документов по каждой стране исследования;
- количество документов по каждой фирме-заявителю;
- количество документов по целям изобретений;
- количество документов по технико-экономическим параметрам;
- количество документов по техническому приему, с помощью которого решается задача.
Возможны и другие параметры, по которым строятся динамические ряды. Динамические ряды особенно удобны для анализа в графической форме.
Построение динамических рядов патентных документов, несмотря на всю простоту приема, наталкивается на определенные трудности. Несколько патентов на одно и то же решение могут быть выданы в разных странах — учитывать один или учитывать каждый? Учитывать международные заявки или нет? Учитывать только опубликованные заявки или также выданные патенты?68 И так далее.
Существует простой выход из этой ситуации. Необходимо согласиться, что статистический анализ обладает определенными погрешностями, которые при достаточном количестве документов могут быть оценены математическими методами. А при выводах, следующих за статистическим анализом, следует учитывать вероятностный характер данных.
Однако при всех погрешностях статистического анализа наглядное представление об изобретательской активности в той или иной стране по любому из выбранных параметров может дать дополнительную информацию исследователю.
Рекомендация общего характера такова: если количество документов растет — возрастает интерес к данной области техники, если падает — данная область техники не считается перспективной. Данные выводы необходимо считать условными, т. к. в каждом конкретном случае возможно множество причин, влияющих на изобретательскую активность. Поэтому выводы делаются на основе всего комплекса имеющейся информации и требуют глубоких знаний в области техники и рынка данных изделий.
Семейство патентов
Это те патенты, которые выдаются на одно и то же техническое решение патентными ведомствами разных
67 Сортировка патентных документов по годам должна
опираться на один из двух параметров: дату приоритета или
дату публикации. Предпочтительнее дата приоритета.
68 В США до недавнего времени (до 15 марта 2001 г.)
осуществлялась публикация только о выданных патентах.
Интеллектуальная собственность
1363
стран или региональными организациями. Выявить такие патенты не всегда просто, т. к. в них могут быть указаны разные патентообладатели. Поиск таких документов в бесплатных базах данных, если это возможно, может вестись по номерам первичных заявок, фамилии изобретателя.
Поиск патентов-аналогов более прост в коммерческих базах данных, которые, как правило, предоставляют такую услугу.
Анализ таких патентов позволяет лучше оценить техническую и конъюнктурную значимость объекта и взаимодействие различных фирм на данном рынке.
9.3. Авторское право и смежные права
Авторское право представляет собой систему охраны результатов интеллектуальной деятельности, которая построена по принципам, отличающимся от принципов построения охраны патентного права.
Прежде всего это система, которая не охраняет суть произведения, а лишь его форму, т. е. форму, в которую создатель произведения облек свои мысли, идеи, открытия, факты.
Охрана произведений авторским правом возникает в силу создания произведения. Для получения охраны не требуется осуществления каких-либо специальных действий: регистрации произведения, его специального оформления, например оформления заявок и получения 69 охранных документов .
Авторское право не ограничивает перечень произведений, которые оно охраняет. Более того, система авторского права, например в период жизни нашего поколения, осуществляет защиту произведений, которые выражаются в новой, цифровой форме, характерной для произведений компьютерного творчества и программ для ЭВМ.
Система законодательства по авторскому праву опирается на два закона: «Об авторском праве и смежных правах» от 9 июля 1993 г., № 5351-1, редакция от 20 июля 2004 г., № 72-ФЗ, и «О правовой охране программ для электронных вычислительных машин и баз данных» от 23 сентября 1992 г., № 3523-1, редакция от 24 декабря 2002, № 177-ФЗ.
9.3. /. Основные положения авторского права
К объектам авторского права69 70 в соответствии с законом [18] относятся произведения науки, литературы,
69 Это не значит, что обладатель права на произведение не может предпринять какие-то специальные действия, чтобы юридически или каким-нибудь другим способом закрепить важные факты, например: кем создано произведение, когда, кому и в каком объеме принадлежат права на произведение и т. д.
70 Мы вынуждены давать понятие об охране всех объектов авторского права, но далее постараемся более подробно разобрать ситуации с теми произведениями, с которыми, по нашему мнению, может столкнуться в своей деятельности химик-технолог.
искусства, которые являются результатом творческой деятельности независимо от назначения и достоинств, а также от способа его выражения.
Результат творческой деятельности
В законе [18] не приводится расшифровка критерия творческого характера произведения, однако юридическая практика как в нашей стране, так и за рубежом, выработала практические критерии, которые позволяют разделять произведения, охраняемые авторским правом, и произведения неохраняемые, не принадлежащие к разряду результатов творческой деятельности.
Излишне доказывать, что не могут быть результатом творческой деятельности произведения, которые похищены у автора или скопированы и использованы. Такой вид «творчества» в цифровую эпоху, сознательно или бессознательно, становится достаточно частым явлением.
К практическим критериям определения результата творческой деятельности относится критерий объективной новизны творческого результата [20] — «неизвестность полученного творческого результата не только для лица, получившего этот результат, но и для остальных лиц». Важно также, чтобы этот результат был оригинальным, не повторяющимся при параллельном творчестве.
Приведем пример. Студентам вуза преподаватель дал задание написать учебную программу для ЭВМ для выражения: с = а2 + Ь2 на одном и том же языке программирования. Как будет сказано ниже, программы для ЭВМ относятся к объектам авторского права. Почти наверняка несколько студентов создадут одинаковые по форме программы. Кого считать автором произведения — всех вместе, того, кто первый написал, или того, кто первый сдал преподавателю? С точки зрения закона об авторском праве студенты создали произведения, которые не охраняются авторским правом, т. к. они неоригинальны, повторяющиеся при параллельном творчестве. Если студент написал оригинальную, никем не повторяемую программу, пусть даже и не самую лучшую с точки зрения программирования, он получит охрану своего произведения (ведь охраняются произведения независимо от назначения и достоинств).
Кто же определяет, относится произведение к результатам творческой деятельности или нет? Как это ни парадоксально, никто не определяет, априори считается, что все произведения, формально подпадающие под перечень, приведенный в законе, охраняются авторским правом. Только в процессе судебного разбирательства, если возникнет спор между сторонами конфликта, суд установит — охраняется это произведение авторским правом как результат творческой деятельности или нет.
На первый взгляд рассуждения о результате творче-
ской деятельности имеют теоретический характер. Од-
нако это не так. В настоящее время все большее число
объектов авторского права, в частности программы для
ЭВМ, являются экономически значимым результатом
деятельности. Поэтому следует до возникновения
1364
Новый справочник химика и технолога
нарушений права ясно представлять, охраняет авторское право это произведение или нет.
Часть произведения, например название, если она является оригинальной, также охраняется авторским правом.
Сфера деятельности авторского права
Авторское право распространяется на произведения, обнародованные или не обнародованные, но находящиеся в какой-либо объективной форме на территории России. Произведения авторов — граждан России и их правопреемников охраняются в России, если они обнародованы за рубежом или не обнародованы, но находятся там в объективной форме.
Закон [ 18] охраняет также находящиеся в объективной форме за пределами России, обнародованные и необнародованные произведения граждан других государств в силу международных договоров.
Обнародование произведения — осуществление с согласия автора действия, которое делает произведение доступным для всеобщего сведения путем его опубликования, публичного показа, публичного исполнения, передачи в эфир или иным способом.
Форма произведения
Произведение должно быть выражено в объективной форме [18]:
- письменной (рукопись, машинопись, нотная запись и т. д.);
- устной (публичное произнесение, публичное исполнение и т. д.);
- звуко- или видеозаписи (механической, магнитной, цифровой, оптической и т.д.);
- изображения (рисунок, эскиз, картина, план, чертеж, кино-, теле-, видео- или фотокадр и т. д.);
- объемно-пространственной (скульптура, модель, макет, сооружение и т. д.);
- в других формах.
Как видно из этого перечисления, закон не ограничивает форму произведения, этот перечень открытый. Иногда задается вопрос: разве устная форма может быть отнесена к объективной форме, слово произнесено и пропало?.. Устная форма произведения напрямую связана с публичным исполнением, во время которого это объективная форма, и при этом предполагается, что оно может быть зафиксировано. Если не зафиксировано и не существует далее в объективной форме, например в виде записи, то и не будет охраняться в дальнейшем.
Охраняются как обнародованные, так и необнародованные произведения, важно, чтобы они существовали в объективной форме. Например, стихи, сложенные поэтом по пути домой, не охраняются до тех пор, пока он не переведет их в объективную форму: запишет на бумаге, внесет в память ЭВМ, надиктует на магнитофон.
Авторское право не распространяется на идеи, методы, процессы, системы, способы, концепции, принципы, открытия, факты [18]. По сути в законе сказано: не охраняется суть произведения, охраняется только форма, в которой существует произведение.
Важным обстоятельством является тот факт, что авторское право не связано с правом на материальный объект, передача материального объекта не влечет за собой передачу авторских прав. Например, покупка коллекционером рукописи какого-либо автора не дает ему авторских прав, прав распоряжаться правами на произведение. При этом никто не оспариваег у него права на рукопись как материальный объект, если он, коллекционер, является добросовестным приобретателем.
Объекты авторского права
В законе приведен достаточно подробный перечень объектов авторского права:
- литературные произведения (включая программы для ЭВМ);
- драматические и музыкально-драматические произведения, сценарные произведения;
- хореографические произведения и пантомимы;
- музыкальные произведения с текстом или без текста;
- аудиовизуальные произведения (кино-, теле- и видеофильмы, слайдфильмы, диафильмы и другие кино-и телепроизведения);
- произведения живописи, скульптуры, графики, дизайна, графические рассказы, комиксы и другие произведения изобразительного искусства;
- произведения декоративно-прикладного и сценографического искусства;
- произведения архитектуры, градостроительства и садово-паркового искусства;
- фотографические произведения и произведения, полученные способами, аналогичными фотографии;
- географические, геологические и другие карты, планы, эскизы и пластические произведения, относящиеся к географии, топографии и к другим наукам;
- другие произведения.
В приведенном перечне указано, что программы для ЭВМ отнесены к литературным произведениям. Как мы знаем, авторским правом не охраняются методы и способы, факты, поэтому безразлично, какими значками написано литературное произведение, ведь его содержание для охраны не имеет значения. Даже программа в машинных кодах, записанная алфавитом, состоящим из «О» и «1», является, с точки зрения закона об авторском праве, произведением литературы.
К объектам авторского права также относятся:
- производные произведения (переводы, обработки, аннотации, рефераты, резюме, обзоры, инсценировки, аранжировки и другие переработки произведений науки, литературы и искусства);
- сборники (энциклопедии, антологии, базы данных) и другие составные произведения, представляющие собой по подбору или расположению материалов результат творческого труда.
Производные произведения и составные произведе-
ния охраняются авторским правом независимо от того,
являются ли объектами авторского права произведения,
на которых они основаны или которые они включают.
Интеллектуальная собственность
1365
Не являются объектами авторского права:
- официальные документы (законы, судебные решения, иные тексты законодательного, административного и судебного характера), а также их официальные переводы;
- государственные символы и знаки (флаги, гербы, ордена, денежные знаки и иные государственные символы и знаки);
- произведения народного творчества;
- сообщения о событиях и фактах, имеющие информационный характер.
Исключены из объектов охраны те произведения, которые являются официальными и информационными и ограничение на распространение которых нанесет обществу серьезный ущерб. С другой стороны, не охраняются произведения народного творчества, автор которых неизвестен.
Авторы и соавторы
Автором признается физическое лицо, творческим грудом которого создано произведение. Авторское право на произведение, созданное группой авторов (соавторами), принадлежит соавторам совместно независимо от того, образует ли такое произведение одно неразрывное целое или состоит из частей, каждая из которых имеет самостоятельное значение.
Если часть произведения может использоваться независимо от его других частей, то автор этой части может ее использовать по своему усмотрению, если иное не предусмотрено соглашением между соавторами.
Автору (составителю) составного произведения, например сборника, принадлежит авторское право на осуществленные им подбор или расположение материалов, представляющие результат творческого труда. Составитель пользуется авторским правом при условии соблюдения им прав авторов каждого из произведений, включенных в составное произведение.
Издателю энциклопедий, энциклопедических словарей, периодических и продолжающихся сборников научных трудов, газет, журналов и других периодических изданий принадлежат исключительные права на использование таких изданий. Авторы произведений, включенных в такие издания, сохраняют исключительные права на использование своих произведений независимо от издания в целом.
Переводчикам и авторам других производных произведений принадлежит право на осуществленные ими перевод, переделку или другую переработку. Переводчик пользуется авторским правом на созданное им произведение при условии соблюдения им прав автора произведения, подвергшегося переработке.
9.3.2. Имущественные и неимущественные права
9.3.2.1. Авторское право на служебные произведения
В законе об авторском праве сказано:
«Авторское право на произведение, созданное в порядке выполнения служебных обязанностей или служебного задания работодателя (служебное произведение), принадлежит автору служебного произведения.
Исключительные права на использование служебного произведения принадлежат лицу, с которым автор состоит в трудовых отношениях (работодателю), если в договоре между ним и автором не предусмотрено иное.
Размер авторского вознаграждения за каждый вид использования служебного произведения и порядок его выплаты устанавливаются договором между автором и работодателем».
Поясним данную формулировку.
Пункт первый данного определения закрепляет авторские права на служебное произведение за автором. Далее говорится, что имущественные права на такое произведение принадлежат работодателю. Здесь нет противоречия. Речь идет о том, что и у служебного произведения есть автор — конкретное физическое лицо (или ряд лиц — соавторы), и работодателю принадлежат только имущественные права на это произведение, а личные права остаются за автором. Доктрина российского законодательства отличается тем самым от законодательства других стран, например США, где автором служебного произведения может считаться работодатель.
Для признания произведения служебным необходимо, чтобы отношения между автором и работодателем были трудовыми. Автор должен работать по трудовому контракту в организации (фирме), т. е. выполнять у работодателя трудовые обязанности71. Не следует путать трудовые отношения с договором подряда, который относится к гражданско-правовым договорам и регулируется Гражданским кодексом РФ. При выполнении работ по договору подряда право на произведения пе-72
реходит к заказчику только в том случае, если это прямо указано в договоре. Если прямого указания нет, право на произведение сохраняется за автором.
Второе условие заключается в том, что произведение должно быть создано в результате выполнения работником своих служебных обязанностей или служебного задания работодателя. Если в служебные обязанности работника не входило создание произведения или оно создано вне служебного задания, то исключительные права на использование произведения принадлежат автору.
При создании в порядке выполнения служебных обязанностей или служебного задания работодателя энциклопедий, энциклопедических словарей, периодических и продолжающихся сборников научных трудов, газет, журналов и других периодических изданий положения вышепроцитированной статьи на отношения работодателя и работника не распространяются.
9.3.2.2. Личные неимущественные права
Автору принадлежат следующие личные неимущественные права:
- право признаваться автором произведения (право авторства);
71 Перечень признаков трудовых отношений между работ-
ником и работодателем содержится в Трудовом кодексе РФ.
72 Тому, кто заказывает работы по договору подряда.
1366
Новый справочник химика и технолога
- право использовать или разрешать использовать произведение под подлинным именем автора, псевдонимом либо без обозначения имени, т. е. анонимно (право на имя);
- право обнародовать или разрешать обнародовать произведение в любой форме (право на обнародование), включая право на отзыв;
- право на защиту произведения, включая его название, от всякого искажения или иного посягательства, способного нанести ущерб чести и достоинству автора (право на защиту репутации автора).
У автора существует также право на отзыв — право отказаться от обнародования произведения при условии возмещения тому, кто использует произведение, причиненных таким решением убытков, включая упущенную выгоду. Право на отзыв не может быть применено автором, если речь идет о служебных произведениях.
Личные права остаются у автора независимо от уступки им имущественных прав. Право авторства, право на имя и право на защиту репутации автора охраняются бессрочно.
9.3.2.3. Имущественные права
Автору принадлежат исключительные права использовать произведение любым способом и в любой форме. Исключительные права могут при условиях, рассмотренных выше, принадлежать работодателю. Исключительные права, как будет сказано далее, могут уступаться автором другим лицам.
Исключительные права, связанные с использованием произведения, называются имущественными правами и означают право осуществлять или разрешать следующие действия [18]:
- воспроизводить произведение (право на воспроизведение);
- распространять экземпляры произведения любым способом: продавать, сдавать в прокат и т. д. (право на распространение);
- импортировать экземпляры произведения в целях распространения, включая экземпляры, изготовленные с разрешения обладателя исключительных авторских прав (право на импорт);
- публично показывать произведение (право на публичный показ);
- публично исполнять произведение (право на публичное исполнение);
- сообщать произведение (включая показ, исполнение или передачу в эфир) для всеобщего сведения;
- сообщать произведение (включая показ, исполнение или передачу в эфир) для всеобщего сведения по кабелю, проводам или с помощью иных аналогичных средств (право на сообщение для всеобщего сведения по кабелю);
- переводить произведение (право на перевод);
- переделывать, аранжировать или другим образом перерабатывать произведение (право на переработку);
- сообщать произведение таким образом, чтобы любое лицо могло иметь к нему доступ в интерактивном
режиме из любого места в любое время (право на доведение до всеобщего сведения).
Кроме перечисленных имущественных прав в авторском праве существуют специальные правомочия, связанные с произведениями изобразительного искусства, дизайнерскими произведениями, которые мы не рассматриваем в данной работе, а отсылаем интересующихся ими к тексту закона [18].
В законе перечислены имущественные права, которые возникают в связи с созданием произведения авторского права. Такое перечисление помогает прежде всего авторам при передаче своих прав лицам, использующим произведение, т. к. чаще всего автор не сам использует имущественные права, а передает эти права другим лицам: издателям, продавцам, исполнителям и т. д.
Рассмотрим детальнее, что означают некоторые, самые важные имущественные права.
Воспроизведение произведения — изготовление одного или более экземпляров произведения или его части в любой материальной форме. Запись произведения в память ЭВМ также является воспроизведением, а тем более изготовление копий программы на материальных носителях.
Импортировать произведение — ввозить на территорию РФ из-за рубежа. Право на импорт произведения принадлежит обладателю имущественных прав. Например, за рубежом изготавливается аудиовизуальное произведение, охраняемое в России, — наглядный курс химии для школьников. Такое действие может производить или сам автор, или лицо, которому автор передал право на импорт.
Право на сообщение для всеобщего сведения по кабелю распространяется также на случай распространения сведений в сетях Интернет.
Имущественные права перестают действовать в отношении экземпляров произведений, которые введены в оборот правообладателем или с его согласия посредством продажи. Наступает так называемое исчерпание прав, т.е. авторское право не действует, например в отношении экземпляров книг, которые проданы; в дальнейшем эти экземпляры могут участвовать в обороте без согласия автора и без выплаты авторского вознаграждения.
Оповещение об исключительных правах
Обладатель исключительных авторских прав для оповещения о своих правах вправе использовать знак охраны авторского права, который помещается на каждом экземпляре произведения и состоит из трех элементов:
- латинской буквы С в окружности: ©;
- имени (наименования) обладателя исключительных авторских прав;
— года первого опубликования произведения.
В качестве примера приведем два варианта опове-
щения об исключительных правах: в первом случае
исключительные права принадлежат автору, во вто-
ром — юридическому лицу (издателю).
© А.М. Марков, 2004
© АНО НПО «Профессионал», 2004
Интеллектуальная собственность
1367
9.3.2.4. Воспроизведение произведения в личных целях
Без согласия автора и без выплаты авторского вознаграждения допускается воспроизведение правомерно обнародованного произведения исключительно в личных целях, кроме:
- программ для ЭВМ73, баз данных и их существенных частей;
- произведений архитектуры в форме зданий и аналогичных сооружений;
- репродуцирования книг полностью и нотных текстов.
Таким образом, в личных целях возможно воспроизведение и дальнейшее использование произведений. С этим мы сталкиваемся, в частности, при использовании информации из сети Интернет, когда часто при осуществлении копирования произведения подчеркивается — только для использования в личных целях.
9.3.2.5. Ограничения исключительных прав
Допускается без согласия автора и без выплаты авторского вознаграждения, но с обязательным указанием имени автора, произведение которого используется, и источника заимствования [ 18]74:
1) цитирование в оригинале и в переводе в научных, исследовательских, полемических, критических и информационных целях в объеме, оправданном целью цитирования;
2) использование обнародованных произведений и отрывков из них в качестве иллюстраций в изданиях, в радио- и телепередачах, звуко- и видеозаписях учебного характера в объеме, оправданном поставленной целью;
3) воспроизведение в газетах, передача в эфир или сообщение по кабелю для всеобщего сведения опубликованных в газетах или журналах статей по текущим экономическим, политическим, социальным и религиозным вопросам;
4) воспроизведение в газетах, передача в эфир или сообщение по кабелю для всеобщего сведения публично произнесенных политических речей, обращений, докладов и других аналогичных произведений в объеме, оправданном информационной целью;
5) воспроизведение или сообщение для всеобщего сведения в обзорах текущих событий средствами фотографии, путем передачи в эфир или сообщения для всеобщего сведения по кабелю произведений, которые становятся увиденными или услышанными в ходе таких событий, в объеме, оправданном информационной целью;
6) воспроизведение обнародованных произведений без извлечения прибыли рельефно-точечным шрифтом или другими специальными способами для слепых,
73 У этого ограничения есть исключения, которые будут рассмотрены в 1.3.4.
В данном издании не ставится задача полностью отразить
положения закона, а только разьяснить суть авторского права, поэтому нормы закона цитируются не полностью. При практическом применении рекомендуется обращаться к тексту закона.
кроме произведений, специально созданных для таких способов воспроизведения.
Допускаются другие случаи свободного использования произведений без согласия автора и выплаты ему вознаграждения библиотеками, архивами для исследовательских и учебных целей, в судебном делопроизводстве, а также для официальных церемоний.
9.3.2.6. Срок действия авторского права и наследование прав
Авторское право действует в течение жизни автора (последнего из соавторов) и 70 лет после его смерти75. Некоторые личные права (право авторства, право на имя и право на защиту репутации автора) охраняются бессрочно. После окончания действия авторского права произведение становится общественным достоянием.
Авторское право на произведение, обнародованное анонимно или под псевдонимом, действует в течение 70 лет после даты его правомерного обнародования. Авторское право на произведение, впервые выпущенное в свет после смерти автора, действует в течение 70 лет после его выпуска.
Авторское право для произведений репрессированных авторов и авторов — участников Великой Отечественной войны продлевается на сроки, связанные со сроком реабилитации автора и длительностью военных действий (4 года).
Произведения, которым на территории РФ никогда не предоставлялась охрана, также считаются перешедшими в общественное достояние.
Произведения, перешедшие в общественное достояние, могут свободно использоваться любым лицом без выплаты авторского вознаграждения.
Авторское право, прежде всего имущественные права, переходит по наследству.
Не переходят по наследству право авторства, право на имя и право на защиту репутации автора произведения. Наследники автора вправе осуществлять защиту указанных прав. Эти правомочия наследников сроком действия авторского права не ограничиваются.
9.3.2.7. Передача имущественных прав
Достаточно часто возникает необходимость в передаче имущественных прав на какое-либо произведение авторского права. Такая передача в соответствии с законом [18] может происходить только в форме авторского договора. Сторонами в договоре выступают автор и пользователь, но т. к. данный договор может быть заключен между лицом, которому от автора перешли имущественные права, то можно использовать термины «правообладатель» и «правоприобретатель». Не будет ошибкой называть вторую сторону в договоре по его фактической деятельности: издатель, изготовитель, продавец, исполнитель.
75 До революции в России авторское право действовало
25 лет после смерти автора.
1368
Новый справочник химика и технолога
Закон предусматривает передачу исключительных и неисключительных прав. В первом случае правопри-обретатель становится единственным владельцем тех прав, которые передаются ему по договору. При передаче неисключительных прав правообладатель оставляет за собой право передавать эти права и другим лицам.
Авторский договор подчиняется нормам Гражданского кодекса РФ [7], поэтому договор может и не называться авторским договором, но если в нем есть условия о передаче авторских прав, он должен соответствовать положению закона об авторском праве и смежных правах.
Авторский договор должен предусматривать следующие условия [18]:
— способы использования произведения (конкретные права, передаваемые по данному договору);
- срок и территорию, на которые передается право;
- размер вознаграждения и (или) порядок определения размера вознаграждения за каждый способ использования произведения, порядок и сроки его выплаты,
- другие условия, которые стороны сочтут существенными для данного договора.
В договоре должны быть указаны конкретные права, которые передаются по авторскому договору. По российскому законодательству может быть признан недействительным договор, в котором указана формулировка о передаче всех исключительных прав. Кроме того, данная формулировка чаще всего неоправданно расширяет права другой стороны. (Известен случай, когда писатель Владимир Войнович передал права на произведение «Жизнь и необычайные приключения солдата Ивана Чонкина» в данной общей формулировке немецкой фирме, что не способствовало выходу фильма, который хотел снимать по этому произведению Э.А. Рязанов, хотя этого же хотел В. Войнович.)
Все права на использование произведения, прямо не переданные по авторскому договору, считаются непе-реданными.
При отсутствии в авторском договоре условия о сроке, на который передается право, договор может быть расторгнут автором по истечении 5 лет с даты его заключения, если пользователь будет письменно уведомлен об этом за 6 месяцев до расторжения договора. При отсутствии в авторском договоре условия о территории, на которую передается право, действие передаваемого по договору права ограничивается территорией Российской Федерации.
Размер вознаграждения или порядок определения размера вознаграждения зависят от вида произведения, способа его использования и той прибыли, которую получит правоприобретатель.
Вознаграждение автору может быть предусмотрено в виде фиксированной суммы, которая может выплачиваться по частям, и сроки выплаты могут быть приурочены к таким датам, как дата подписания договора (аванс), дата сдачи произведения издателю, дата выхода книги. Вознаграждение может быть предусмотрено
в виде роялти, в частности процента от выручки издателя. Может быть и комбинированный платеж, предусматривающий фиксированную сумму, например аванс и роялти.
Предметом авторского договора не могут быть права на использование произведения, неизвестные на момент заключения договора. Эта формулировка закона не препятствует заключению авторского договора заказа. Такой договор должен быть заключен на конкретное произведение или серию произведений, которые в договоре должны быть охарактеризованы достаточно точно и конкретно: объем, вид, название и т. д. Недопустимы договоры, например, с такой формулировкой: «все произведения, которые будут созданы автором в течение ... лет».
Авторский договор должен быть заключен в письменной форме, кроме договора в периодической печати.
Сторона, нс исполнившая или ненадлежащим образом исполнившая обязательства по авторскому договору, обязана возместить убытки, причиненные другой стороне, включая упущенную выгоду. Если автор не представил заказное произведение в соответствии с условиями договора заказа, он обязан возместить реальный ущерб, причиненный заказчику
9.3.3. Авторское право на произведения науки и техники
Тематика данного издания требует особо рассмотреть вопрос действия авторского права в связи с произведениями науки и техники. В законе [18] сказано, что авторское право защищает произведения науки, литературы и искусства, но о каких конкретно произведениях науки идет речь — не указано.
Во-первых, можно предположить, что речь идет о произведениях, в которых отражены результаты научной деятельности: научные отчеты, статьи, книги. Эти произведения, по сути, имеют двойственную природу — они являются произведениями науки, но их также без всякого ущерба для их охраны можно отнести к произведениям литературы. Дело в том, что авторское право, как неоднократно подчеркивалось, не распространяется на идеи, методы, процессы, системы, способы, концепции, принципы, открытия, факты — все то, что составляет суть научных достижений. Формы, в которых эти достижения выражены, выражения, в которых записано научное достижение, не так важны, важно только, чтобы эта форма позволяла понять суть этого достижения.
Вот почему авторское право достаточно плохо работает в отношении произведений науки, для которых форма выражения не так важна, как суть этих результатов.
Вот почему не следует, описывая результаты в научной статье, рассчитывать, что охрана авторским правом позволяет защитить эти результаты. До той поры, пока эти результаты не перейдут в конкретные разработки, которые можно защитить с помощью патентного права, сохранять результаты в режиме «ноу-хау» — коммерческой и служебной тайны, о которых речь пойдет в 9.4.
Интеллектуальная собственность
1369
Конечно, такое положение вступает в противоречие с естественным желанием ученого публиковать свои результаты. Можно только посоветовать всегда соизмерять выгоду от публикаций с тем проигрышем, к которому может привести раскрытие ваших результатов, сразу делающихся достоянием всей мировой общественности, представители которой могут использовать эти результаты в своей деятельности, в том числе и сведения о ваших технологиях, не нарушая ваших авторских прав.
Что касается произведений техники, то здесь вопрос стоит не так остро. Действительно, авторское право защищает такие произведения, как, например, эскиз, план, чертеж. Но эта защита распространяется только на форму выражения. Т. е. любое лицо может воспользоваться вашим опубликованным чертежом для постройки машины, которую вы разработали, без вашего разрешения, и в лучшем случае оно (это лицо) сошлется на вас как на автора. Но претендовать на какие-то права в связи с использованием этой машины вы не можете, т. к. авторское право, по сути, препятствует только публикации вашего чертежа без вашего разрешения и помогает защитить свои права, если кто-то выдает ваш чертеж за свой.
9.3.4. Охрана программ для ЭВМ, баз данных и компьютерных произведений авторским правом
Правовая охрана программ для ЭВМ и баз данных (имеются в виду электронные базы данных) регулируется двумя законами: «Об авторском праве и смежных правах» [18] и «О правовой охране программ для ЭВМ и баз данных» [19]. Закон «О правовой охране программ для ЭВМ и баз данных» был принят раньше закона об авторском праве и в основной своей части повторяется в последнем. Поэтому, по мнению Э.П. Гаврилова [20], при наличии расхождений между ними должны применяться положения закона «Об авторском праве и смежных правах».
9.3.4.1. Особенности охраны программ для ЭВМ и баз данных
Как уже говорилось выше, программы для ЭВМ в смысле правовой охраны авторским правом принадлежат к литературным произведениям, а базы данных — к сборникам.
Определения
Программа для ЭВМ — это объективная форма представления совокупности данных и команд, предназначенных для функционирования электронных вычислительных машин (ЭВМ) и других компьютерных устройств с целью получения определенного результата. Под программой для ЭВМ подразумеваются также подготовительные материалы, полученные в ходе ее разработки, и порождаемые ею аудиовизуальные отображения [19].
Из определения следует, что под программой для ЭВМ понимается не только собственно программа,
как к этому привыкли программисты, но и «порождаемые ею аудиовизуальные отображения». В законе [18] отмечается, что охрана распространяется на все виды программ для ЭВМ (в том числе на операционные системы), которые могут быть выражены на любом языке и в любой форме, включая исходный текст и объектный код76.
Законодатель не поясняет, что следует понимать под подготовительными материалами, полученными в ходе разработки программ для ЭВМ. Однако можно точно сказать, что к ним не относятся идеи и принципы, лежащие в основе программы для ЭВМ, в том числе идеи и принципы организации интерфейса и алгоритма, а также языки программирования. С нашей точки зрения, к подготовительным материалам можно отнести описание блок-схемы алгоритма, тексты программы, являющиеся промежуточными, эскизы аудиовизуальных произведений и т. д.
База данных — это объективная форма представления и организации совокупности данных (например, статей, расчетов), систематизированных таким образом, чтобы эти данные могли быть найдены и обработаны с помощью ЭВМ [19].
В понятие базы данных, как следует из определения, не входит программа для ЭВМ, управляющая базой данных. Кроме того, необходимо различать понятие базы данных и информации, составляющей содержание этой базы данных. Содержание базы данных, в свою очередь, в зависимости от вида может охраняться или не охраняться авторским правом.
Следует помнить о том, что программа для ЭВМ и база данных должны быть результатом творческой деятельности и что только в этом случае программа или база данных подлежит правовой охране.
В разных странах предпринимались попытки использовать патентное право для охраны программ, но в силу объективных причин охрана патентом не получила широкого распространения.
В Патентном законе РФ [6] имеется специальная оговорка, что не признаются патентоспособными «алгоритмы и программы для вычислительных машин». Последнее, правда, не означает, что патентное право никак не применимо к охране программ для ЭВМ.
Во-первых, возможно включение алгоритмов обработки информации (т. е. программ в широком смысле) в способы, на которые возможно получение патента на изобретение.
Во-вторых, при охране программ для ЭВМ и баз данных должен обязательно применяться такой объект патентного права, как товарный знак.
76 Исходный текст — текст программы, составляемый программистами, на каком-либо языке программирования (Алгол, СИ, Паскаль и т. д.). Объектный код — машинный язык, которым программа записана в памяти компьютера или другого вычислительного устройства. Для перевода программы с исходного текста в объектный код (машинный язык) применяют специальные программы — трансляторы.
1370
Новый справочник химика и технолога
В-третьих, в некоторых случаях может использоваться охрана, предусмотренная для промышленных образцов (например, охрана шрифта, с которым работает программа).
Виды программ. Адаптация и декомпиляция
Для использования программы вполне достаточно объектного кода, и исходный текст обычному пользователю не нужен. Исходный же текст, в отличие от объектного кода, непосредственно позволяет полностью оценить все идеи, заложенные в программе, легко понять алгоритм. А идеи и принципы, заложенные в программе, авторским правом не защищаются. Поэтому необходимо до минимума сократить доступ посторонних лиц к исходному тексту.
Все же у пользователя программы может возникнуть необходимость иметь доступ к исходному тексту. У него имеются две возможности: обратиться к правообладателю программы или использовать процедуру декомпиляции. Декомпиляция, т. е. преобразование объектного кода в исходный текст, без разрешения владельца исключительных прав и без выплаты дополнительного вознаграждения разрешена законом только при следующих условиях:
- эти действия необходимы для достижения способности к взаимодействию независимо разработанной этим лицом программы с другими программами;
- информация, необходимая для достижения способности к взаимодействию, ранее не была доступна этому лицу из других источников;
- указанные действия осуществляются в отношении только тех частей декомпилируемой программы, которые необходимы для достижения способности к взаимодействию.
Информация, полученная в результате декомпилирования, не может использоваться для разработки про-граммы, существенно схожей по своему виду с декомпилируемой программой, или для любого другого действия, нарушающего авторское право.
Другое действие, которое приходится производить пользователю, — адаптация.
Адаптация программы или базы данных — это внесение изменений, осуществляемых исключительно в целях функционирования программы или базы данных на конкретных технических средствах пользователя или под управлением конкретных программ пользователя. Пользователю адаптация разрешена без дополнительного разрешения правообладателя.
Грань между адаптацией и модификацией достаточно условна. Также весьма неопределенна грань допустимости и недопустимости декомпиляции. В законе [18] по этому случаю приведена специальная оговорка, что применение адаптации и декомпиляции не должно наносить неоправданного ущерба нормальному использованию программы, но с другой стороны, не должно ущемлять необоснованным образом законные интересы автора или иного обладателя исключительных прав.
9.3.4.2. Программы и базы данных в процессе их создания и использования
Важно с самого начала работы установить правильные правовые отношения между авторами (разработчиками) и организацией, в которой создается программа, и принимать все меры, чтобы не было причин для споров о правах на разрабатываемую программу. Кроме того, программа для ЭВМ (база данных) может создаваться по заказу, за счет привлеченных средств, и в этом случае права на созданный продукт могут пониматься неодинаково сторонами, участвующими в проекте.
Автором программы признается физическое лицо, в результате творческой деятельности которого она создана. В этом случае имущественные права принадлежат автору.
Часто возникает вопрос: если программа создана на оборудовании организации, какие права на программу в этом случае она имеет? Работник использовал имущество организации для своих нужд и должен согласовать этот вопрос с администрацией. Но сам факт использования оборудования не дает никаких прав этой организации претендовать на авторские права в отношении созданного произведения.
Любая организация, в том числе и организация, где работает автор, имеет право приобрести имущественные права на использование произведения. Такая передача может быть осуществлена в виде полной уступки или путем выдачи лицензии на использование части этих прав. Для объектов авторского права, к которым, как мы знаем, принадлежат программы для ЭВМ и базы данных, такая передача производится путем заключения авторского договора.
Достаточно часто программа создается коллективом. Соавторы имеют равные права на созданное произведение, если только они путем заключения соглашения между собой не установили другие взаимоотношения. Заключение такого соглашения весьма желательно, чтобы в будущем у них не возникало споров по правовым или экономическим проблемам. Если соглашения нет, то все вопросы об использовании произведения должны решаться ими совместно.
В практике (прежде всего за рубежом, в нашей стране такая классификация только входит в практику) различают три типа программ с точки зрения их распространения: свободные, условно свободные и лицензионные.
Свободные программы могут использоваться любым заинтересованным лицом свободно, без разрешения автора и без выплаты ему вознаграждения.
Условно свободные программы могут использоваться свободно, но если пользователь регистрируется у разработчика программы и заплатит достаточно скромную сумму, в этом случае разработчик будет оповещать его о новых версиях, будет консультировать пользователя и т. д.
Лицензированные программы могут использоваться только после приобретения лицензии, на определенных условиях, с обязательной выплатой вознаграждения.
Интеллектуальная собственность
1371
Важно предпринять все меры, чтобы ваша программа, особенно за рубежом, не была принята за свободную или условно свободную.
В отличие от других объектов авторского права владелец имущественных прав на программу для ЭВМ и базу данных в России по закону [19] имеет право на регистрацию.
Такая регистрация является официальным уведомлением общественности о наличии у правообладателя прав, способствует защите прав в случае возникновения конфликтных ситуаций и является для судебных органов источником получения официальных сведений об авторах, правообладателях и собственно о программе или базе данных.
Напомним еще раз, что охрана произведений, защищаемых авторским правом, возникает в силу создания произведения. Регистрация программы не влияет на возникновение охраны.
Регистрация проводится по достаточно жесткому регламенту в отделе Регистрации программ для ЭВМ и баз данных Патентного ведомства Российской Федерации. Заявка на регистрацию должна содержать:
- заявление на официальную регистрацию с указанием правообладателя и автора;
- депонируемые материалы, идентифицирующие программу для ЭВМ или базу данных.
9.3.4.3. Компьютерные произведения
Цифровая эпоха, которая стремительно захватывает все большую часть человечества, порождает проблемы, которые вызваны возможностью легко передавать и копировать самые разнообразные произведения, записанные в цифровой форме.
Именно цифровая форма произведений породила массовые нарушений прав в отношении произведений, которые охраняются авторским правом. Наиболее остро эта проблема выражена в отношении аудио- и аудиовизуальных произведений, программ для ЭВМ, литературных и музыкальных произведений.
Условно виды нарушений можно разделить на две группы:
- незаконное копирование и распространение произведений;
- создание произведений путем использования частей других произведений, в том числе переработка произведений с помощью компьютерных средств.
Борьба с незаконным копированием идет не только путем совершенствования законодательства, в частности ужесточения наказания за распространение контрафактной продукции, но и путем усовершенствования технических приемов, которые позволяют легко отслеживать нарушения, в том числе и в сети Интернет, иметь бесспорные доказательства принадлежности прав правообладателю.
Речь идет о присвоении произведению в цифровой форме77 различного вида идентифицирующих цифровых
77 Договор Всемирной организации интеллектуальной
собственности по авторскому праву — WIPO Copyright
меток, цифровых подписей и т. д. Применение таких идентификаторов позволяет легко устанавливать правообладателя, отслеживать возможные нарушения и иметь доказательства нарушений для случая судебного разбирательства. Законом [18] запрещено без разрешения правообладателя удалять информацию об авторском праве и смежных правах, а также снимать ограничения, устанавливаемые техническими средствами защиты авторского права и смежных прав.
Второй вид нарушений, который выявить порой труднее, порожден соблазном легкого копирования произведений в цифровой форме и создания произведения путем его переработки.
Когда в компьютер пользователя из Интернета переписывается произведение, охраняемое авторским правом, например рисунок, осуществляется воспроизведение произведения, которое в личных целях не запрещено. Однако этот рисунок может быть легко перекомпонован, изменен, т. е. создано производное произведение, которое далее используется в коммерческих целях. А ведь право на переработку произведения принадлежит автору. Большинство пользователей компьютерных технологий не задумывается об этом, но это не значит, что проблемы не возникают.
Такое же положение существует в отношении произведений науки. Проблема здесь не столь остра, как для музыкальных, литературных и художественных произведений, но она также существует.
9.3.5. Смежные права
Смежные права являются правами, примыкающими к авторскому праву, также относятся к нематериальным объектам и охватывают:
- права исполнителей;
- права производителей фонограмм;
- права организаций эфирного и кабельного вещания78.
Смежное право исполнителя возникает с момента первого исполнения (исполнитель), записи фонограммы (производитель фонограммы), первой передачи в эфир (организация эфирного и кабельного вещания) и заканчивается через 50 лет, считая с начала календарного года, следующего за годом возникновения права.
Для возникновения и осуществления смежных прав не требуется соблюдения каких-либо формальностей. Производитель фонограммы и исполнитель для оповещения о своих правах вправе использовать знак охраны смежных прав, который помещается на каждом экземпляре фонограммы и (или) на каждом содержащем ее футляре и состоит из трех элементов:
Treaty— WCT и Договор ВОИС по исполнениям и фонограммам, известный как WIPO Performances and Phonograms Treaty. Эти договоры, подписанные, но не ратифицированные на настоящий момент, устанавливают механизмы цифровых идентифицирующих систем и цифровых кодов.
78 Ввиду того, что для темы данного Справочника смеж-
ные права не играют определяющей роли, дается только об-
щее понятие об этих правах.
1372
Новый справочник химика и технолога
- латинской буквы R в окружности — ®;
- имени (наименования) обладателя исключительных смежных прав;
- года первого опубликования фонограммы.
Исполнителю принадлежат личные права: право на имя; право на защиту от искажения, наносящего ущерб чести и достоинству автора; имущественные права, включающие права, связанные с передачей в эфир и записями исполнения.
Производители фонограмм имеют исключительные права на использование фонограммы в любой форме, включая право на получение вознаграждения за каждый вид использования фонограммы.
Организации эфирного и кабельного вещания получают исключительные права на использование своих передач.
Закон предусматривает случаи свободного использования объектов смежных прав, схожие с теми, которые предусмотрены для объектов авторских прав.
9.3.5.1. Коллективное управление имущественными авторскими и смежными правами
Авторы и владельцы авторских и смежных прав индивидуально часто не могут отслеживать использование своих прав, например при использовании прав исполнителей на радио и телевидении, репродуцировании произведений и т. д. С такими же трудностями могут столкнуться авторы, например, литературных произведений.
Для таких случаев закон предусматривает создание организаций-посредников, которые управляют имущественными правами на коллективной основе. Такие организации создаются непосредственно обладателями авторских и смежных прав и действуют в пределах полученных от них полномочий на основе устава, утверждаемого в порядке, установленном законодательством.
Организации заключают с авторами и исполнителями договоры на управление имущественными правами, а затем лицензионные договоры с конкретными организациями, в том числе и с иностранными, использующими эти права. Условия таких лицензий должны быть одинаковыми для всех пользователей одной категории. Указанные организации не вправе отказать в выдаче лицензии пользователю без достаточных на то оснований. Такая организация должна согласовывать с авторами размер вознаграждения, собирать и распределять его, а также совершать любые юридические действия для защиты прав автора и исполнителя.
Наиболее крупной организацией, управляющей имущественными правами авторов и исполнителей, является Российское авторское общество (РАО).
9.3.6. Защита авторских и смежных прав
За нарушение предусмотренных законом авторских и смежных прав наступает гражданская, уголовная и административная ответственность.
Экземпляры произведений, изготовленные, экспортируемые или распространяемые с нарушением авторского права, называются контрафактными.
За защитой своего права обладатели исключительных авторских и смежных прав вправе обратиться в установленном порядке в суд, арбитражный суд, третейский суд, орган дознания, органы предварительного следствия в соответствии с их компетенцией.
Прежде чем добиваться возмещения ущерба, понесенного владельцем прав, следует добиться прекращения нарушения. Этой цели отвечают нормы закона, посвященные запрету на использование контрафактных экземпляров в судебном порядке. Судья единолично, при наличии достаточных оснований, может вынести определение о наложении ареста и изъятии всех экземпляров произведений и фонограмм, в отношении которых предполагается, что они являются контрафактными, а также материалов и оборудования, предназначенных для их изготовления и воспроизведения.
Обладатель исключительных прав может защищать свои права способами, предусмотренными Гражданским кодексом Российской Федерации [7].
При установлении факта нарушения правообладатель может требовать возмещения убытков, включая упущенную выгоду. Однако порой сложно доказать сам факт наличия убытков или их размер. Поэтому, вместо возмещения убытков, по своему выбору правообладатель вправе требовать компенсации:
- в размере от 10 тысяч рублей до 5 миллионов рублей, определяемых по усмотрению суда, арбитражного суда или третейского суда, исходя из характера нарушения;
- в двукратном размере стоимости экземпляров произведения либо в двукратном размере стоимости прав, обычно определяемом при правомерном использовании произведений.
Обладатели исключительных прав вправе требовать выплаты компенсации за каждый случай неправомерного использования произведения либо за допущенные правонарушения в целом.
Автор или правообладатель также может требовать возмещения морального вреда.
Компенсация может быть взыскана в любом случае, даже если автор не понес убытков и нарушитель не имеет доходов от своей противоправной деятельности.
Контрафактные экземпляры произведений или фонограмм, а также материалы и оборудование, используемые для воспроизведения контрафактных экземпляров, подлежат обязательной конфискации. Эти экземпляры подлежат уничтожению, за исключением случаев их передачи обладателю авторских или смежных прав по его просьбе.
9.3.7. Охрана авторских и смежных прав за рубежом
Действие авторского права ограничивается территорией государства, где это произведение было создано. Произведения, созданные на территории одного государства, получают охрану в других государствах только в силу многосторонних и двусторонних договоров.
Россия участвует в следующих многосторонних договорах, связанных с авторским правом и смежными
Интеллектуальная собственность
1373
правами: Бернской конвенции об охране литературных и художественных произведений 1886 г. [22], Всемирной конвенции об авторском праве 1952 г. [23], Конвенции об охране интересов изготовителей фонограмм [24] и Конвенции о распространении несущих программы сигналов, передаваемых через спутники, 1974 г. [25].
В перечисленных конвенциях содержится положение о национальном режиме. Оно состоит в том, что опубликованные произведения граждан стран — участниц конвенции получают в каждой конкретной стране такую же охрану, как и произведения граждан данной страны. Таким образом, права российских авторов и исполнителей охраняются за границей в странах Всемирной и Бернской конвенций не по российскому закону, а по законам каждой конкретной страны. Автору в одиночку практически невозможно отстаивать свои права за границей, он прибегает к услугам зарубежного агента или Российского авторского общества, имеющего агентов в большинстве развитых стран.
К Всемирной конвенции об авторском праве СССР присоединился в 1973 г. Бернскую конвенцию Россия подписала в 1994 г. после того, как стал действовать закон об авторском праве. Требования, которые необходимо выполнять национальному законодательству по Бернской конвенции, в России обеспечиваются.
Наличие международных соглашений не отменяет важность каждого конкретного авторского договора, который заключается при переуступке прав с зарубежным партнером. Следует также помнить о необходимости проставления знаков © и ® для обозначения авторских прав или прав на фонограмму.
9.4. Служебная и коммерческая тайна (ноу-хау)
Ноу-хау как объект гражданских прав играет чрезвычайно важную роль в гражданских отношениях и гражданском обороте. Можно сказать, что правовая охрана ноу-хау является еще одной системой защиты, в частности, результатов творческой деятельности.
Термин «ноу-хау» (от англ, know-how, букв. — знаю как) широко применяется в международной практике. Это информация, которая в силу ее неизвестности третьим лицам дает ее владельцу преимущества в его деятельности. Это может быть информация различного характера, широко используемая в деловой практике: научно-техническая, экономическая, управленческая, правовая [27]. Общей чертой такой информации являются коммерческая ценность и желание владельца сохранить ее в тайне. Ведь такая информация и ее несанкционированное разглашение или хищение могут причинить законному владельцу серьезный ущерб. Большинство стран мира предоставляет обладателю такой информации правовую охрану.
Российская Федерация также предоставляет охрану такой информации (ст. 139 Гражданского кодекса
РФ) [7]79, хотя в законодательных документах России термин «ноу-хау» не применяется.
Информация составляет служебную или коммерческую тайну [7]80 в том случае, если выполняются следующие условия:
- информация имеет действительную или потенциальную коммерческую ценность в силу неизвестности ее третьим лицам;
- к этой информации нет свободного доступа на законном основании;
- обладатель информации принимает меры к охране ее конфиденциальности.
Лица, незаконными методами получившие информацию, которая составляет служебную или коммерческую тайну, обязаны возместить причиненные убытки. Такая же обязанность возлагается на работников, разгласивших служебную или коммерческую тайну вопреки трудовому договору, в том числе контракту, и на контрагентов, сделавших это вопреки гражданско-правовому договору.
Принятый в 2004 г. закон «О коммерческой тайне» [42] регулирует отношения, связанные с передачей информации о коммерческой тайне, охраной ее конфиденциальности в целях обеспечения баланса интересов обладателей информации и других участников отношений, в том числе государства, и определяет сведения, которые не могут составлять коммерческую тайну.
Чтобы иметь правовые возможности защищаться от лиц, незаконно копирующих, похищающих или разглашающих ваши ноу-хау81 (служебную или коммерческую тайну), необходимо принимать меры к охране ее конфиденциальности. Эти меры заключаются прежде всего в создании системы защиты ноу-хау, которая включает в себя организационную, правовою и техническую составляющие. В договора с персоналом включают соответствующие условия и принимают меры к перекрытию возможных каналов утечки информации.
9.4.1. Служебная и коммерческая тайна и интеллектуальная собственность
Патентное и авторское право предоставляют исключительные права, которые заключаются в праве владельца этих прав самому использовать произведение и запрещать это делать другим. Право на коммерческую и служебную тайну, связанное с конфиденциальной информацией, не относится к исключительным правам. Другие лица, самостоятельно и добросовестно создавшие такую же информацию, также могут ее
79 Близким понятием к служебной тайне является понятие
«банковская тайна». Федеральный закон «О банках и банков-
ской деятельности» от 2 декабря 1990 г., № 395-1.
80 Коммерческая тайна может быть у юридического и фи-
зического лица, термин «служебная тайна» относится к юри-
дическому лицу.
81 В данном разделе термины «ноу-хау» и «служебная
и коммерческая тайна» понимаются как синонимы.
1374
Новый справочник химика и технолога
использовать. Таким образом, право на коммерческую и служебную тайну не является монопольным правом.
Право на служебную и коммерческую тайну часто применяется для результатов творческой деятельности. Можно сказать, что все объекты патентного права после их создания проходят эту стадию до подачи заявки в патентное ведомство.
С другой стороны, как отмечалось выше, далеко не все потенциально патентоспособные объекты патентуются, многие из них охраняются владельцами в режиме «ноу-хау». Конфиденциальная информация, относящаяся к служебной и коммерческой тайне, достаточно часто дополняет патентные права. Например, вы получили патент на новое химическое вещество. А способ получения этого вещества содержит ноу-хау, без применения которого невозможно получение вещества экономически выгодным способом и которое владелец не посчитал целесообразным патентовать.
Конфиденциальная информация наряду с патентными правами достаточно часто становится объектом купли-продажи. Ноу-хау могут становиться объектом лицензии, вкладом в уставной капитал предприятия, предметом залога.
Во всех перечисленных операциях следует помнить, что информация, являющаяся служебной и коммерческой тайной (ноу-хау), не является объектом исключительных прав.
9.5. Топология интегральных микросхем
Топология интегральной микросхемы [28] (далее — топология) представляет собой зафиксированное на материальном носителе пространственно-геометрическое расположение совокупности элементов интегральной микросхемы и связей между ними.
Правовая охрана распространяется только на оригинальную топологию, т. е. топологию, созданную в результате творческой деятельности автора и являющуюся неизвестной в области разработки топологий на дату ее создания. Топология признается оригинальной до тех пор, пока не доказано обратное. Правовая охрана, предоставляемая законом, не распространяется на идеи, способы, системы, технологию или закодированную информацию, которые могут быть воплощены в топологии.
Нарушением исключительного права на охраняемую топологию признается:
- воспроизведение охраняемой топологии в целом или ее части путем включения ее в интегральную микросхему или иным образом;
- ввоз на территорию Российской Федерации, продажа и иное введение в оборот охраняемой топологии, интегральной микросхемы с этой топологией или включающего в себя такую интегральную микросхему изделия.
Начало срока действия исключительного права на охраняемую топологию82 определяется по наиболее
82 В настоящее время федеральным органом исполнитель-
ной власти по регистрации топологий интегральных микросхем
ранней из следующих дат: по дате первого использования топологии, по дате ее регистрации. Регистрация производится в федеральном органе исполнительной власти и не является обязательной. Срок действия охраны топологии интегральной микросхемы 10 лет.
Личные и имущественные права на топологию интегральных микросхем во многом схожи с авторскими правами. Исключительное право на охраняемую топологию, созданную работником (автором) в связи с выполнением служебных обязанностей или по заданию работодателя, принадлежит работодателю, если договором между ним и работником не предусмотрено иное.
Исключительные права на топологию могут быть переданы по договору другому лицу с обязательной регистрацией этого договора в федеральном органе исполнительной власти.
Охрана топологии интегральной микросхемы сходна с охраной объектов авторским правом, но имеет особенности, связанные с природой данного объекта интеллектуальной собственности.
9.6. Селекционные достижения
Селекционное достижение — сорт растений, порода животных. Право на селекционное достижение охраняется законом и подтверждается патентом, который удостоверяет исключительное право патентообладателя на его использование.
Критериями охраноспособности селекционного достижения являются: новизна, отличимость, однородность, стабильность. Право на подачу заявки на выдачу патента принадлежит селекционеру или его правопреемнику. Заявка подается в Государственную комиссию РФ83 по испытанию и охране селекционных достижений. Приоритет селекционного достижения устанавливается по дате поступления в Госкомиссию заявки на выдачу патента или заявки на допуск к использованию.
Оценка охраноспособности селекционного достижения осуществляется путем проведения предварительной экспертизы, в процессе которой происходит проверка документов, затем производится публикация сведений о достижении в официальном бюллетене. Любое заинтересованное лицо в течение 6 месяцев с даты опубликования сведений о заявке может направить в Госкомиссию претензию в отношении новизны заявленного селекционного достижения.
Выдача патента производится после положительного результата испытаний селекционного достижения на отличимость, однородность и стабильность.
Каждому автору, не являющемуся патентообладателем, Госкомиссией выдается авторское свидетельство.
является Патентное ведомство РФ. Сведения о порядке регист-
рации можно получить на сайте ведомства: www.fips.ru.
83 Государственная комиссия РФ по испытанию и охране
селекционных достижений создана при Министерстве сель-
ского хозяйства и продовольствия РФ (адрес: 107139, Москва,
Орликов пер., За).
Интеллектуальная собственность
1375
Исключительное право патентообладателя состоит в том, что любое лицо должно получить от обладателя патента лицензию на осуществление каких-либо действий с семенами, племенным материалом охраняемого селекционного достижения.
Срок действия патента на селекционное достижение составляет 30 лет (для некоторых сортов растений — 35 лет) с даты регистрации указанного достижения в Государственном реестре.
9.7. Недобросовестная конкуренция
Парижская конвенция по охране промышленной собственности [И] относит пресечение недобросовестной конкуренции к промышленной собственности. По сути, пресечение недобросовестной конкуренции является дополнением к институту интеллектуальной собственности. В России недобросовестная конкуренция регулируется Законом «О конкуренции и ограничении монополистической деятельности на товарных рынках» [26].
Недобросовестная конкуренция [26] — это любые направленные на приобретение преимуществ в предпринимательской деятельности действия хозяйствующих субъектов, которые противоречат положениям действующего законодательства, обычаям делового оборота, требованиям добропорядочности, разумности и справедливости и могут причинить (или причинили) убытки другим хозяйствующим субъектам — конкурентам либо нанести ущерб их деловой репутации.
Наиболее точное и развернутое определение недобросовестной конкуренции содержится в Парижской конвенции по охране промышленной собственности (ст. 10-bis) [11].
В частности, подлежат запрету:
- все действия, способные каким бы то ни было способом вызвать смешение в отношении предприятия, продуктов, промышленной или торговой деятельности конкурента;
- ложные утверждения при осуществлении коммерческой деятельности, способные дискредитировать предприятие, продукты, промышленную или торговую деятельность конкурента;
- указания или утверждения, использование которых при осуществлении коммерческой деятельности может ввести общественность в заблуждение относительно характера, способа изготовления, свойств, при-84 годности к применению или количества товаров .
Данное определение конкуренции актуально и для преследования лиц, осуществляющих акты недобросовестной конкуренции, т. к. положения конвенции на-
8 4 Действия, подпадающие под запрет недобросовестной конкуренции по российскому законодательству, см. в Законе РФ «О конкуренции и ограничении монополистической деятельности на товарных рынках» [26]. Выдержка из текста Парижской конвенции приведена потому, что наиболее сжато отражает действия недобросовестной конкуренции, в том числе и связанные с интеллектуальной собственностью.
ряду с законом [26] могут применяться при привлечении нарушителей к ответственности.
Политику государства в области недобросовестной конкуренции проводит Министерство РФ по антимонопольной политике и поддержке предпринимательства. Министерство осуществляет также предупреждение и пресечение недобросовестной конкуренции путем возбуждения дел, по результатам рассмотрения которых принимает решения и выдает предписания.
9.8. Интеллектуальная собственность в деятельности предприятия
9.8.1. Политика в области интеллектуальной собственност и
Существует политика ВОИС в области интеллектуальной собственности, политика отдельных государств, например Японии, опубликованная в 2002 г. и весьма подробно раскрывающая шаги, которые будут предприняты, чтобы преодолеть отставание Японии в области инноваций, но существует политика и отдельных фирм, организаций в области интеллектуальной собственности, которая далеко не всегда широко известна, но осуществляется последовательно и эффективно. В силу публичности деятельности широко декларируется и раскрывается политика университетов, в частности 85 американских .
На первый взгляд кажется, что раз существует общее законодательство в данной области, то достаточно выполнять его и никакой политики не нужно. Это не так. Простой пример. Права на объект промышленной собственности будут принадлежать работодателю только в том случае, если он создан при выполнении трудовых обязанностей или конкретного задания; при этом работник должен уведомить работодателя о создании такого объекта. Если работник этого не сделает, то работодатель может и не узнать, что создано изобретение, и, в свою очередь, не принять необходимых мер, чтобы защитить, может быть, важнейший ресурс фирмы, отсутствие правовой охраны которого принесет фирме убытки.
Из данного частного примера следует, что любая фирма, особенно фирма, занимающаяся промышленным производством, должна иметь систему, которая приводит в порядок отношения между персоналом и работодателем при создании и использовании результатов творческой деятельности, стимулирует процесс их создания и осуществляет процедуру правовой защиты и защиты интересов фирмы.
Политика фирмы в области интеллектуальной собственности может осуществляться на основании отдельного документа, а может существовать в виде системы мер, которые руководство осознанно применяет в своей деятельности, не выпуская специальных распоряжений.
85 С политикой университетов в области интеллектуаль-
ной собственности просто познакомиться, войдя на сайт уни-
верситета или набрав в поисковой системе соответствующий
поисковый образ.
1376
Новый справочник химика и технолога
К составляющим политики можно отнести:
- стратегические цели предприятия в области охраны результатов творческой деятельности на предприятии;
- разработку мер по созданию творческой атмосферы на предприятии и поощрению работников на создание интеллектуальной собственности работодателя при соблюдении баланса интересов между работником и работодателем;
- создание системы по закреплению и поддержанию права собственности за предприятием, включая заключение необходимых соглашений с персоналом, контрагентами и партнерами, получение охранных документов, деятельности патентных служб;
- правовая охрана средств индивидуализации юридического лица, индивидуализации продукции, выполняемых работ или услуг (товарные знаки, знаки обслуживания, наименования мест происхождения товаров);
- создание системы охраны служебной и коммерческой тайны предприятия;
- выделение финансовых и людских ресурсов для осуществления мероприятий по охране интеллектуальной собственности.
9.8.2. Стимулирование творческой деятельности
Развитие инновационной деятельности в странах, добившихся экономического и научно-технического успеха, является следствием государственной политики стимулирования научно-технического прогресса. Различают три направления в методах воздействия государства: финансовое, включая прямые бюджетные инвестиции, организационное — создание различных структур, поддерживающих инновационную деятельность, и законодательное, включая налоговое регулирование.
В данном подразделе мы рассмотрим два аспекта этой большой темы: методы государственного стимулирования инновационной деятельности по законодательству РФ и методы стимулирования инновационной деятельности, применяемые в деятельности фирм.
Государственное стимулирование декларируется, в частности, ст. 34 Патентного закона [6]:
«Государство стимулирует создание и использование изобретений, полезных моделей, промышленных образцов, устанавливает авторам и хозяйствующим субъектам, их использующим, льготные условия налогообложения и кредитования, предоставляет им иные
льготы в соответствии с законодательством Российской Федерации».
На практике меры государственного стимулирования сводятся только к установлению льгот для некоторых категорий изобретателей в части снижения патентных пошлин, а также льгот в налогообложении авторов объектов промышленной собственности и авторского права при получении дохода за счет их использования.
Налоговое стимулирование юридических лиц, направляющих свою прибыль на создание нововведений, в настоящее время отсутствует.
Стимулирование творческой деятельности на предприятии дает наибольший эффект при сочетании материальных и моральных методов.
К материальным методам стимулирования можно отнести следующие нормы, предусмотренные законодательством РФ.
Если работодатель получит патент на служебное изобретение, служебную полезную модель или служебный промышленный образец либо примет решение о сохранении информации о таких изобретениях, полезной модели или промышленном образце в тайне, либо передаст право на получение патента другому лицу, либо не получит патент по поданной им заявке по зависящим от него причинам, работник (автор), который создал этот служебный объект, имеет право на вознаграждение. Размер вознаграждения и порядок его выплаты определяются договором между автором и работодателем [6].
В авторском праве размер авторского вознаграждения за каждый вид использования служебного произведения и порядок его выплаты устанавливаются договором между автором и работодателем [18].
Материальные методы стимулирования творческой деятельности играют чрезвычайно важную роль в стимулировании авторов. Пренебрежение правами авторов на вознаграждение, как правило, приводит к их неудовлетворенности своим положением.
Наряду с материальными методами стимулирования большую роль играют так называемые «моральные» методы, которые не предусматривают прямого денежного вознаграждения авторам, но имеют большое значение в создании творческой, соревновательной атмосферы. Методы морального стимулирования, которые применялись в советское время, сейчас, может быть, незаслуженно забыты.
В табл. 9.1 приведены меры морального стимулирования, применяемые за рубежом.
Меры морального стимулирования, применяемые за рубежом
Таблица 9.1
Формы морального стимулирования творчества изобретателей, ученых, служащих Страны, фирмы
1. Повышение в должности, продвижение по службе США: осуществление принципа параллельной карьеры («двойной лестницы») — фирмы «Мобил», «Американ Сайнэмид», «ИКИ», «Юниор Карбайд», «Эйр продакте энд кемикалс», «Эмоко»
Интеллектуальная собственность
1377
Продолжение табл. 9.1
Формы морального стимулирования творчества изобретателей, ученых, служащих Страны, фирмы
2. Насаждение грамотами, значками, призами, учреждение почетных титулов 3. Поздравительные письма от руководства компании 4. Помещение благодарственных статей и сообщений (иногда с фотографиями ученых) в специальные пресс-бюллетенях, местной печати или научных журналах 5. Вывешивание портретов с поздравлениями в помещении лаборатории 6. Предоставление права лучшим специалистам выступить с речью на ежегодном торжественном обеде 7. Улучшение условий работы (кабинет, обстановка, канцелярское оборудование и т. п.) 8. Установление более удобного распорядка рабочего дня (время начала, окончания работы и т. и.) 9. Предоставление возможности проводить исследования по своему усмотрению в рабочее время 10. Предоставление возможности участвовать в разработке перспективных направлений работ лаборатории 11. Приглашение высшим руководством на совместные совещания по административным проблемам 12. Предоставление возможности общаться с высшим руководством 13. Право подписи некоторых официальных писем, счетов и т. д. 14. Отведение персональной стоянки для личного автомобиля 15. Выделение автомобиля компании в распоряжение сотрудника с оплатой стоимости бензина 16. Предоставление более длительных отпусков 17. Предоставление времени для написания статей в периодические издания и самообразования: - в университетах: освобождение ученого от чтения лекций для проведения индивидуальных исследований; - в лабораториях промышленных корпораций 18. Оплата отпускных поездок изобретателей 19. Выделение средств на совершенствование образования и повышение квалификации, посещение научных центров, поездки на конференции, симпозиумы 20. Оказание организационной и финансовой помощи: - в чтении лекций в других организациях; - при вступлении в профессиональные общества и членстве в них; - в получении патента на изобретение; - в коммерциализации патента США, «1ВМ», «Дженерал электрик»; Япония: призы министерства науки и техники, генерального директора патентного ведомства, президента института изобретательства и новаторства; «Приз императора», «Приз премьер-министра» — победителям конкурсов на лучшее изобретение среди преподавателей высшей школы, среди изобретателей Японии США: «Бэлл телефон лабораториз» США США США США США США, «1ВМ» США США США США США США, «Перкин-Элмерл» США США США США США, КНР
1378
Новый справочник химика и технолога
Окончание табл. 9.1
Формы морального стимулирования творчества изобретателей, ученых, служащих Страны, фирмы
21. Поддержка руководством исследователей, принимающих рискованные решения, в случае неудачи 22. Привлечение исследователей к консультативной деятельности 23. Оплата части расходов специалистов на медицинское обслуживание 24. Оплата аренды или приобретение частных домов 25. Выставки патентных документов компании США США США США США, «Бэлл телефон лабораториз»
9.8.3. Договорные отношения в области интеллектуальной собственности
Любые отношения, которые возникают в процессе создания интеллектуальной собственности, сопровождаются изложением условий этих отношений в договорах, соглашениях и других документах, главная цель которых — закрепить в юридической форме права и обязанности сторон процесса создания и использования интеллектуальной собственности.
Интеллектуальная собственность, как правило, проходит долгий путь, пока она в виде новой промышленной продукции, программ для ЭВМ, книг и т. д. станет доступна потребителю. На пути превращения идеи в конечный продукт может возникнуть множество препятствий, среди которых существенную роль может сыграть неотрегулированность отношений или непра-86 вильныс отношения между участниками инновационного процесса.
Установление баланса интересов — трудный процесс, требующий компромисса сторон, в том числе авторов интеллектуальной собственности.
9.8.3.1. Договорное регулирование, связанное с созданием интеллектуальной собственности
Создание объектов интеллектуальной собственности может происходить в порядке личной инициативы автора или при выполнении им служебных обязанностей или служебного задания, а также при выполнении заказных работ.
86 Термин «неправильные отношения» не юридический, а, можно сказать, эмоциональный. Мы применили его для того, чтобы подчеркнуть, что конечная цель любых усилий в инновационном процессе — установить между создателями интеллектуальной собственности, работодателями, теми, кто
будет осваивать и выпускать продукцию на основе изобретений, таких отношений, чтобы судьба инновации (изобрете-
ния) была наиболее успешной. Такие отношения можно назвать правильными, т. к. они учитывают интересы всех сторон этого процесса.
Договорные отношения при создании интеллектуальной собственности в порядке личной инициативы
В этом случае необходимость установления договорных отношений возникает у автора при следующих обстоятельствах:
- если у него есть соавторы;
- если ему оказывают финансовую, техническую, организационную и иную помощь.
Напомним, что автором по законодательству [6, 18] признается лицо, творческим трудом которого создано 87 произведение .
Таким образом, прежде всего необходимо определить состав авторов. Авторами являются те, кто внес творческий, а не технический, финансовый или организационный вклад в создание произведения. Определение состава авторов — гражданское дело их самих. Другие лица, в том числе руководители (при создании служебных произведений), не имеют права на определение авторского коллектива. Важно не забыть или не исключить волевым решением действительного автора (соавтора) произведения. Действительный автор (соавтор), исключенный из состава авторов, может в судебном порядке восстанавливать свои права, что, как правило, негативно сказывается на судьбе произведения. Это связано с тем, что никто не хочет затрачивать средства на введение в хозяйственный оборот произведения, права на которое оспариваются.
Между соавторами, как правило, заключается соглашение о распределении будущих доходов от использования произведения. Это соглашение в дальнейшем может быть пересмотрено, если один из авторов (или группа соавторов), например, вложит больший вклад в доведение произведения до стадии использования86 * 88.
87 В данном случае под произведением понимается любой
объект патентного или авторского права.
88 В данной работе не приводятся формы договоров и
иных соглашений, сопровождающих процесс создания и ис-
пользования интеллектуальной собственности. Формы дого-
воров можно найти в юридической литературе, на сайтах па-
тентного ведомства и юридических фирм. С другой стороны,
Интеллектуальная собственность
1379
Что касается лиц, которые оказали автору техническую, организационную помощь, то может производиться оплата этой помощи или составляться соглашение, предусматривающее оплату этой помощи в будущем, из доходов, которые будут получены от использования имущественных прав.
Лица, оказавшие финансовую помощь автору, например, финансирующие изготовление опытных образцов изобретения, как правило, участвуют в распределении будущих доходов.
В любых случаях автору придется передавать свое право на использование объекта промышленной собственности (имущественных прав для объектов авторского права) другим лицам, если это произведение будет использовано промышленным способом89. Важно понимать, что передача права на использование произведения должна происходить даже в том случае, если автор — владелец предприятия, которое будет выпускать продукцию. В этом случае также передается право на использование от физического лица юридическому лицу. О формах передачи прав мы поговорим ниже.
Договорные отношения при создании интеллектуальной собственности в деятельности предприятия
Трудовые отношения
Вопросы, связанные с тем, кому принадлежат права при создании служебных объектов промышленной собственности, рассмотрены в 9.2.1.4, а при создании служебных произведений авторского права — в 9.3.2.1.
Работодатель, осуществляющий деятельность в области, где создаются или могут быть созданы объекты интеллектуальной собственности, должен включить в трудовые договора (контракты) специальные разделы, предусматривающие следующие положения:
- все права на интеллектуальную собственность, созданную при выполнении служебных обязанностей или служебного задания, принадлежат работодателю;
- работник обязан незамедлительно информировать работодателя о созданных им объектах промышленной собственности (изобретениях, полезных моделях, промышленных образцах);
-работник обязан сохранять конфиденциальность сведений, отнесенных работодателем к служебной или коммерческой тайне, в том числе сведений, связанных с
заключение большинства соглашений требует квалифицированной работы специалиста в области передачи прав на интеллектуальную собственность.
89 Под использованием произведения промышленным способом здесь понимается любое использование, требующее производства продукции в количествах, которые выходят за рамки деятельности физического лица, например выпуск носителей программ для ЭВМ, издание книг и т. д. Отдельного рассмотрения требует деятельность индивидуального пред-
принимателя без образования юридического лица.
созданными объектами промышленной собственности и ноу-хау;
- работник обязуется оказывать работодателю содействие в патентовании созданных им объектов промышленной собственности.
Кроме заключения трудовых контрактов с перечисленными выше положениями работодателю следует создать систему фиксации служебных заданий работникам и систему охраны служебной и коммерческой тайны.
Договора подряда
Договора подряда относятся к гражданско-правовым. а не трудовым договорам. При выполнении работ физическими лицами по договору подряда права на объекты патентного и авторского права переходят к заказчику только на основании договора, а не автоматически при трудовых отношениях [6, 18].
В договорах подряда должно быть записано, что все исключительные права на конкретные объекты, создаваемые по договору подряда, — изобретения (полезные модели, промышленные образцы), если создаются разработки, которые могут защищаться патентным законом, или программы для ЭВМ, базы данных и т. д., если создаются объекты, права на которые защищаются авторским правом, принадлежат заказчику.
Договора на выполнение НИР, ОКРи технологических работ
В гл. 38 Гражданского кодекса РФ [7] «Выполнение научно-исследовательских, опытно-конструкторских и технологических работ» права на результаты работ распределяются следующим образом:
1. Стороны в договорах на выполнение научно-исследовательских, опытно-конструкторских и технологических работ имеют право использовать результаты работ, в том числе способные к правовой охране, в пределах и на условиях, предусмотренных договором.
2. Если иное не предусмотрено договором, заказчик имеет право использовать переданные ему исполнителем результаты работ, в том числе способные к правовой охране, а исполнитель вправе использовать полученные им результаты работ для собственных нужд.
При выполнении научно-исследовательских, опытно-конструкторских и технологических работ права на интеллектуальную собственность распределяются так, как указано в договоре. Чаще всего права на интеллектуальную собственность принадлежат заказчику, но может быть принято и другое распределение прав.
Исполнитель обязан90:
-согласовать с заказчиком необходимость использования охраняемых результатов интеллектуальной
90 Приводятся только те положения статей Гражданского
кодекса [7], которые имеют отношение к вопросам интеллек-
туальной собственности.
1380
Новый справочник химика и технолога
деятельности, принадлежащих третьим лицам, и приобретения прав на их использование;
- гарантировать заказчику передачу полученных по договору результатов, не нарушающих исключительных прав других лиц.
Перечисленные выше положения означают следующее. Исполнитель обязан передать заказчику результаты работ, которые не нарушают прав третьих лиц. Если необходимые результаты не могут быть достигнуты без использования интеллектуальной собственности, права на которую принадлежат третьим лицам, исполнитель обязан согласовать с третьим лицом ее использование и получить согласие заказчика.
Стороны обязаны обеспечить конфиденциальность сведений, касающихся предмета договора, хода его исполнения и полученных результатов. Объем сведений, признаваемых конфиденциальными, определяется в договоре.
При выполнении данных работ исполнитель должен установить такие отношения со своими сотрудниками, чтобы права на результаты принадлежали исполнителю, чтобы он мог выполнить положения договора, касающиеся прав на результаты работ (см. подразд. «Трудовые отношения»).
При выполнении госбюджетных работ необходимо выполнять положения законодательства относительно результатов, полученных при выполнении работ по государственному контракту (см. 9.2.14.2).
9.8.3.2. Договорное регулирование, связанное с реализацией прав
Договора, связанные с уступкой прав
В 9.2.1.7 рассмотрены варианты передачи прав на изобретения, полезные модели и промышленные образцы до подачи заявки, в процессе проведения экспертизы и во время действия патентных прав.
Договор о полной уступке прав на патент91 заключается в том случае, если патентообладатель (автор или другое лицо, которому принадлежит патент) полностью уступает свои права. Следует помнить, что уступается конкретный патент, действующий в данной стране. Если уступаются несколько патентов, то может быть заключен один договор или отдельные договора, связанные с данным патентом. Закон [6] не устанавливает особую форму договора. С примерной формой договора можно ознакомится на сайте Патентного ведомства РФ (www.fips.ru).
О передаче имущественных прав на объекты авторского права, в том числе о формах договоров, см в 9.3.2.7.
Лицензионные договора
Патентообладатель может предоставить право использовать изобретение, полезную модель или промышленный образец другому лицу на основе лицензи
91 До получения патента также может быть осуществлена полная передача патентных прав.
онного договора. По этому договору лицензиар обязуется предоставить право на использование запатентованного объекта лицензиату. В практике существуют разные виды лицензий:
а) по виду объекта, на который передаются права:
- патентная;
- беспатентная (лицензия на ноу-хау);
б) по объему передаваемых прав:
- исключительная;
- простая (см. 9.2.1.7);
- полная.
Имеются и другие виды лицензионных договоров, например перекрестная лицензия, при которой партнеры передают друг другу права на использование объектов интеллектуальной собственности.
Лицензионный договор всегда индивидуален, т. к. различны объекты интеллектуальной собственности, на которые передаются права, и различны ситуации, при которых эти права передаются.
Однако существуют примерные виды договоров, в частности договора на патентные исключительную и неисключительную лицензии, разработанные Патентным ведомством РФ (сайт www.fips.ru). Следует помнить, что любой договор об уступке патентных прав недействителен без регистрации в патентном ведомстве. К существенным положениям лицензионного договора, без которых он нс будет зарегистрирован, относятся:
- определение сторон;
- предмет договора;
- вид лицензии, объем передаваемых прав;
- территория действия договора;
- срок действия договора;
- размер вознаграждения.
Приведем примерную форму договора об исключительной лицензии с упомянутого сайта ФИПС.
Примерный договор об исключительной лицензии на использование объекта промышленной собственности (изобретения, полезной модели, промышленного образца), охраняемого патентами
РФ на территории РФ
(Фамилия, имя, отчество гражданина, его адрес или полное наименование юридического лица), именуем___в дальнейшем «Лицензиар», с одной стороны, и
(Фамилия, имя, отчество гражданина, его адрес или полное наименование юридического лица), именуем___в дальнейшем «Лицензиат», с другой стороны,
принимая во внимание, что:
1. Лицензиар является владельцем патента(ов) РФ №
2. Лицензиат желает приобрести на условиях настоящего Договора лицензию на использование изобретения(ий), на кото-рое(ые) получен(ы) патент(ы) РФ №№, в целях изготовления, применения, ввоза, предложения к продаже, продажи и иного введения в хозяйственный оборот продукта, изготовленного на основе указанного(ых) изобретения(ий), а также применения способа, охраняемого патентом, Договорились о нижеследующем:
Интеллектуальная собственность
1381
1. Определение терминов
Следующие термины, которые используются в настоящем Договоре, означают:
1.1. «Патенты» — полученные Лицензиаром патенты РФ, а также патенты, которые будут получены по уже поданным в Роспатент заявкам на изобретения (Приложение 1).
1.2. «Продукция по лицензии» — продукция, которая будет изготавливаться на основе лицензии.
1.3. «Специальная продукция» — продукция, не подпадающая под определение, данное в п. 1.2 настоящего Договора, дополнительно разработанная Лицензиатом с использованием изобретений, охраняемых патентами.
1.4. «Специальное оборудование» — оборудование, необходимое для изготовления продукции по лицензии (Приложение 2).
1.5. «Конфиденциальность» — соблюдение мер по предотвращению случайного или преднамеренного разглашения конфиденциальных сведений (ноу-хау), касающихся патентов, третьим лицам.
1.6. «Отчетный период» — период деятельности Лицензиата по выполнению условий настоящего Договора в течение каждых месяцев, начиная с вступления настоящего Дого-
вора в силу.
1.7. «Территория» — регионы в соответствии с политикоадминистративным делением РФ либо отрасль промышленности.
1.8. «Платежи» — платежи, при которых все возможные налоги и сборы уплачиваются в порядке, не противоречащем действующему законодательству.
2. Предмет договора
2.1. Лицензиар предоставляет Лицензиату на срок действия настоящего Договора и за вознаграждение, уплачиваемое Лицензиатом, исключительную лицензию на использование изобретений, охраняемых патентами.
При этом Лицензиату предоставляется право: на изготовление, применение, ввоз, предложение к продаже, продажу и иное введение в хозяйственный оборот продукции по лицензии и/или специальной продукции (в частности, с использованием при необходимости специального оборудования, комплектующих узлов, деталей и сырья, применяемых Лицензиаром на территории). При этом Лицензиар сохраняет за собой право самому использовать вышеуказанные изобретения в части, не передаваемой Лицензиату по настоящему Договору.
2.2. Лицензиар передает Лицензиату необходимую и достаточную для использования изобретений по п. 2.1 техническую и иную документацию, осуществляет оказание технической и другой помощи и, при необходимости, поставку образцов и материалов, а также специального оборудования.
3. Специальное оборудование
3.1. Вся техническая документация, необходимая и достаточная для изготовления продукции по лицензии (Приложение 3), передается Лицензиаром уполномоченному представителю Лицензиата в (адрес места передачи) на языке в______________________экземплярах в
течение со дня вступления в силу настоящего Договора.
3.2. При передаче технической документации составляется приемо-сдаточный акт за подписями уполномоченных представителей обеих сторон. Если Лицензиат или его уполномоченный представитель не явится в срок, установленный для передачи, то Лицензиар может переслать документацию заказной почтой в адрес и за счет Лицензиата.
Датой передачи документации будет соответственно дата подписания приемо-сдаточного акта или дата почтового штемпеля на накладной.
3.3. Если Лицензиат при передаче или в течение 3 (трех) месяцев после получения им документации установит неполноту или неправильность полученной им от Лицензиара документации, то Лицензиар обязан в течение 3 (трех) недель после поступления письменной рекламации передать недостающую документацию или исправить частичные недостатки и передать откорректированную документацию Лицензиату. В этом случае датой передачи документации будет считаться дата передачи недостающей или откорректированной документации, в соответствии с положениями абз. 2 п. 3.2.
3.4. Лицензиат может размножить документацию для своих нужд, но при соблюдении обязательств по обеспечению конфиденциальности.
4. Усовершенствования и улучшения
4.1. В течение срока действия настоящего Договора стороны обязуются незамедлительно информировать друг друга о всех произведенных ими усовершенствованиях и улучшениях, касающихся патентов, продукции по лицензии и специальной продукции.
4.2. Стороны обязуются в первую очередь предлагать друг другу все вышеуказанные усовершенствования и улучшения. Условия передачи этих усовершенствований и улучшений будут согласовываться сторонами дополнительно.
Усовершенствования и улучшения, которые защищены патентами РФ или в отношении которых поданы заявки в Роспатент на получение патентов и которые создаются одной из сторон, считаются принадлежащими ей.
В случае отказа любой из сторон или неполучения ответа на предложение, касающееся использования усовершенствований и улучшений в течение месяцев, стороны вправе
предлагать усовершенствования и улучшения третьим лицам.
5. Обязательства и ответственность
5.1. Лицензиар заявляет, что на момент подписания настоящего Договора ему ничего не известно о правах третьих лиц, которые могли быть нарушены предоставлением данной лицензии.
5.2. Лицензиар заявляет о технической осуществимости производства продукции по лицензии на предприятии(ях) Лицензиата и о возможности достижения показателей, предусмотренных настоящим Договором, при условии полного соблюдения Лицензиатом технических условий и инструкций Лицензиара. (Стороны могут не включать этот пункт в текст Договора.)
Механические, технологические, технико-экономические и
другие показатели продукции по лицензии приводятся в При-
ложении 4 к настоящему Договору.
1382
Новый справочник химика и технолога
5.3. Лицензиар заявляет, что техническая документация и другие материалы, передаваемые Лицензиату, будут комплектны и качественно изготовлены в соответствии с действующими ГОСТами и другими нормалями. (Стороны могут оговорить и другие требования к документации и другой информации.)
5.4. Лицензиат обязуется изготавливать продукцию по лицензии в полном соответствии с полученной технической документацией и инструкциями Лицензиара в части, касающейся изобретения.
5.5. Сторона, не выполнившая указанных условий, обязана возместить другой стороне понесенные ею в связи с этим невыполнением убытки в пределах .
5.6. За нарушение сроков передачи технической документации и другой необходимой информации, в соответствии со ст. 3 настоящего Договора, Лицензиар уплачивает Лицензиату штраф, исчисляемый в размерах, но не свыше.
5.7. Размер возмещения убытков и договорных штрафов, о которых одна сторона может заявить из-за различных нарушений условий настоящего Договора, не может в общей сложности превышать полученных или выплаченных по ст. 7 Договора сумм, если стороны не договорились об ином.
6. Техническая помощь в освоении производства продукции по лицензии
6.1. Для оказания технической помощи Лицензиату в освоении продукции по лицензии, а также для обучения персонала Лицензиата методам и приемам работы, относящимся к изготовлению и применению продукции по лицензии, Лицензиар командирует, по просьбе Лицензиата, на предприятие Лицензиата необходимое количество специалистов. Лицензиат сообщит Лицензиару о своей просьбе за месяцев
до даты предполагаемого выезда специалистов.
6.2. Лицензиат обеспечит специалистов Лицензиара на время их пребывания на предприятии Лицензиата помещениями в гостинице, транспортными средствами для проезда до места работы и обратно, телефонно-телеграфной связью и другими согласованными видами обслуживания.
6.3. Все расходы, связанные с командированием специалистов в целях оказания необходимой технической помощи, включая оплату стоимости ж/д или авиабилетов из до
места их назначения и обратно, провоза кг багажа
сверх полагающихся по авиабилету, а также вознаграждение в зависимости от квалификации специалистов, несет Лицензиат по следующим ставкам:.
6.4. В случае обращения Лицензиата к Лицензиару с просьбой о посещении предприятий, производящих продукцию по лицензии, в целях ознакомления с ее производством и оборудованием на месте Лицензиар удовлетворит такую просьбу*1. Все расходы, связанные с посещением и пребыванием специалистов на предприятиях Лицензиара, несет Лицензиат.
6.5. По просьбе Лицензиата и за его счет Лицензиар поставит ему образцы продукции по лицензии и материалов, а также специальное оборудование, необходимое для производства *2 продукции по лицензии .
7. Платежи
7.1. За предоставление прав, предусмотренных настоящим Договором, и за техническую документацию и другую информацию, указанную в Приложении 4, Лицензиат уплачивает Лицензиару вознаграждение согласно следующему.
Вариант 1
(предусматривает единовременные или поэтапные платежи заранее оговоренной сторонами суммы)
а) сумма в размере(цифрой и прописью) рублей уплачивается по предъявлению счета в трех экземплярах (Банк Лицензиара) в течение дней с даты_____;
б) сумма в размере(цифрой и прописью) рублей уплачивается по предъявлению счета в трех экземплярах (Банк Лицензиара) в течение дней
с даты вступления Договора в силу:
в) сумма в размере(цифрой и прописью) рублей уплачивается по предъявлению счета в трех экземплярах (Банк Лицензиара) и копии приемо-сдаточного акта или копии накладной, предусмотренных п. 3.2 настоящего Договора, в течение дней с даты приемки техниче-
ской документации;
г) сумма в размере(цифрой и прописью) рублей уплачивается в течение дней с даты начала серийного
производства*3.
Вариант 2
(предусматривает единовременные или поэтапные платежи и дальнейшие текущие отчисления в течение срока действия Договора)
а) первоначальный платеж в размере(цифрой и прописью) рублей уплачивается(Банк Лицензиара) в течение дней с даты вступления в силу
настоящего Договора;
- текущие отчисления (роялти) уплачиваются Лицензиару в размере__% от продажной цены продукции по лицензии
и% от продажной цены специальной продукции, изготовленной и реализованной Лицензиатом.
Либо:
- текущие отчисления (роялти) уплачиваются Лицензиару в размере (цифрой и прописью) рублей за единицу (штуку, килограмм и т. п.) продукции по лицензии и (цифрой и прописью) рублей за единицу специальной продукции, изготовленной и реализованной Лицензиатом*4;
б) первоначальный платеж в размере (цифрой и прописью) рублей, из которых:
- сумма в размере(цифрой и прописью) рублей уплачивается по предъявлению счета в трех экземплярах (Банк Лицензиара) в течение дней
с даты вступления настоящего Договора в силу (инкассо с немедленной оплатой, с последующим акцептом и т. д.);
- сумма в размере(цифрой и прописью) рублей
уплачивается в течение __ дней после передачи технической
документации, указанной в ст. 3 настоящего Договора. Опла-
та производится в этом же порядке, с приложением к счету
копии приемо-сдаточного акта или копии отправленной поч-
товой накладной, как это предусмотрено в п. 3.2 настоящего
Договора;
Интеллектуальная собственность
1383
- текущие отчисления (роялти) в % или в рублях, как это предусмотрено в поди, «а» варианта 2.
7.2. Текущие отчисления (роялти) производятся Лицензиатом в течение дней, следующих за отчетным периодом.
7.3. После прекращения срока действия настоящего Договора положения его будут применяться до тех пор, пока не будут окончательно урегулированы платежи, обязательства по которым возникли в период его действия.
8. Информация и отчетность*5
8.1. Лицензиат в течение дней, следующих за отчетным
периодом, предоставляет Лицензиару сводные бухгалтерские данные по объему производства и реализации продукции по лицензии и специальной продукции в течение отчетного периода, а также сведения о продажных ценах продукции по лицензии и специальной продукции.
8.2. Лицензиар имеет право производить проверку данных, относящихся к объему производства и реализации продукции по лицензии и специальной продукции на предприятиях Лицензиата по сводным бухгалтерским данным в соответствии сп. 1.6 настоящего Договора. Лицензиат обязуется обеспечить возможность такой проверки.
9. Обеспечение конфиденциальности
9.1. Стороны берут на себя обязательства по соблюдению конфиденциальности полученных от Лицензиара технической документации и информации, относящихся к производству продукции по лицензии и специальной продукции. Стороны предпримут все необходимые меры для того, чтобы предотвратить полное или частичное разглашение указанных сведений или ознакомление с ними третьих лиц без взаимной договоренности.
9.2. С переданной конфиденциальной документацией, информацией будут ознакомлены только те лица из персонала предприятий Лицензиата и его партнеров по кооперации, которые непосредственно связаны с производством продукции по лицензии.
9.3. В случае разглашения Лицензиатом или его партнерами по кооперации сведений, содержащихся в указанной документации и информации, Лицензиат возместит Лицензиару нанесенные в связи с этим убытки. Такую же ответственность несет Лицензиар.
10. Защита передаваемых прав
10.1. В течение всего срока действия настоящего Договора Лицензиат не будет оспаривать патенты Лицензиара.
10.2. Лицензиар обязуется поддерживать в силе патенты в течение всего срока действия настоящего Договора. Если Лицензиар намерен прекратить поддержание патентов в силе или уступить патенты третьему лицу, он заблаговременно информирует об этом Лицензиата, и в этом случае стороны урегулируют свои отношения, вытекающие из настоящего Договора, следующим образом.
10.3. О случаях противоправного использования третьими лицами изобретений, защищенных патентами Лицензиара на территории, ставших известными Лицензиату, он незамедлительно уведомит Лицензиара.
В случае, если к Лицензиату будут предъявлены претензии или иски по поводу нарушения им прав третьих лиц в связи с
использованием лицензии по настоящему Договору, Лицензиат известит об этом Лицензиара.
В обоих случаях Лицензиар обязуется урегулировать такие претензии или предпринять иные действия, исключающие возникновение расходов и убытков для Лицензиата.
10.4. В случае, если Лицензиат придет к заключению о целесообразности патентования за границей изобретений Лицензиара, по которым еще не получены патенты в РФ, он доводит свое мнение до сведения Лицензиара. Последний принимает решение о целесообразности правовой охраны своих изобретений за границей с учетом обоснованных интересов Лицензиата.
Все расходы, связанные с таким патентованием, распределяются между сторонами по дополнительному соглашению.
10.5. В случае, если Лицензиат придет к заключению о возможности и целесообразности продажи за границу лицензии на продукцию по лицензии и специальную продукцию, он информирует об этом Лицензиара, и стороны совместно предпринимают соответствующие действия и договариваются о распределении валютной выручки.
10.6. В случае, если Лицензиат придет к заключению о целесообразности экспорта продукции по лицензии и/или специальной продукции, он сообщает об этом Лицензиару. Порядок и валюта платежей в пользу Лицензиара в этом случае будут согласованы сторонами дополнительно.
11. Реклама
Лицензиат вправе/обязуется указывать в соответствующих рекламных материалах, а также на продукции по лицензии и специальной продукции, выпускаемой на его предприятиях, что эта продукция производится по лицензии Лицензиара.
Вопрос об использовании Лицензиатом товарного знака Лицензиара стороны урегулируют отдельным соглашением.
12. Разрешение споров
12.1. В случае возникновения споров между Лицензиаром и Лицензиатом по вопросам, предусмотренным настоящим Договором, стороны примут все меры к разрешению их путем переговоров между собой.
12.2. В случае невозможности разрешения указанных споров путем переговоров они должны решаться в
порядке (в случае, если одной из сторон Договора является гражданин — в судебном порядке; в случае, если обеими сторонами являются юридические лица и/или предприниматели — в арбитражном порядке).
13. Срок действия Договора
13.1. Настоящий договор заключен на лет и вступает
в силу с даты его регистрации в установленном порядке в Роспатенте.
13.2. Каждая из сторон письменно уведомит другую сторону о намерении досрочно расторгнуть настоящий Договор, если другая сторона не выполнит какое-либо условие по пп. настоящего Договора. Стороне, не выполнившей свои обязательства, будет предоставлено меся-
цев для устранения нарушения. В случае, если нарушение не
будет устранено, Договор подлежит досрочному расторже-
нию в порядке, установленном действующим законода-
тельством.
1384
Новый справочник химика и технолога
13.3. Если настоящий Договор будет досрочно расторгнут из-за невыполнения Лицензиатом своих обязательств, то он лишается права использовать изобретения по п. 2.1 в любой форме и обязан возвратить Лицензиару всю техническую документацию.
13.4. В случае признания патентов недействительными полностью или частично или при досрочном прекращении действия патентов до истечения срока действия настоящего Договора либо из-за невыполнения Лицензиаром своих обязательств по пп. настоящего Договора стороны урегулируют свои отношения следующим образом (с учетом ст. 5 и пп. 10.1 и 10.2 настоящего Договора).
14. Прочие условия
14.1. Права и обязанности каждой из сторон по настоящему Договору не могут быть переуступлены другому гражданину или юридическому лицу без письменного на то разрешения другой стороны, за исключением случаев, предусмотренных настоящим Договором.
14.2. Все изменения и дополнения к настоящему Договору должны быть совершены в письменной форме, подписаны уполномоченными на это лицами и зарегистрированы в Роспатенте, если такая регистрация необходима.
14.3. Во всем остальном, что не предусмотрено настоящим Договором, будут применяться нормы гражданского и гражданско-процессуального права РФ.
14.4. Упомянутые в настоящем Договоре Приложения 1-4 на
листах составляют его неотъемлемую часть.
14.5. Настоящий договор совершен в г.«_____»____20___г.
в двух экземплярах.
Юридические адреса сторон
Лицензиар____________________________________________
Лицензиат___________________________________________
Приложения
Приложение 1. Перечень патентов.
Приложение 2. Перечень специального оборудования.
Приложение 3. Перечень ноу-хау.
Приложение 4. Техническая документация.
Приложение 5. Механические, технологические, техникоэкономические и другие показатели продукции по лицензии
От имени Лицензиара От имени Лицензиата
М. п. М. п.
*’ Если Лицензиаром является гражданин, пп. 6.4 и 6.5 не применяются.
*2 Если Лицензиаром является гражданин, пп. 6.4 и 6.5, как правило, не применяются.
*3 Стороны определяют, что считается началом производства (серийного производства).
*4 С учетом специфики предмета Договора стороны могут договориться о платежах только в виде роялти, без первоначального платежа.
*5 Ст. 3 применяется в случаях, когда платежи осуществляются в соответствии со ст. 7 (вариант 2).
Уступка прав на объекты авторского права
Как известно, права на объекты авторского права разделяются на две группы: неимущественные (личные) права и имущественные права. Первая группа прав является неотчуждаемой, поэтому может рассматриваться только передача имущественных прав. В законе [18] сказано, что передача имущественных прав может производиться только по авторскому договору.
Авторские договора разделяются на договора о передаче исключительных прав и на договора о передаче неисключительных прав, по аналогии с лицензионными договорами. Закон об авторском праве [18] устанавливает также содержание авторского договора:
- способы использования произведения (конкретные права, передаваемые по данному договору);
- срок и территория, на которые передается право;
- размер вознаграждения и (или) порядок определения размера вознаграждения за каждый способ использования произведения;
- порядок и сроки его выплаты;
- другие условия, которые стороны сочтут существенными для данного договора.
Вознаграждение в авторском договоре определяется в виде процента от дохода за соответствующий способ использования произведения или фиксированной суммы.
При отсутствии в авторском договоре условия о сроке, на который передается право, договор может быть расторгнут автором через 5 лет с даты его заключения. При этом пользователя прав необходимо уведомить об этом за 6 месяцев. Если в договоре отсутствуют условия о территории, на которую передается право, считается, что право ограничивается территорией России.
Для создания произведений авторского права применяется авторский договор заказа. Договора заказа запрещено заключать на произведения, которые не определены в договоре. Например, недействителен договор с таким условием: «передается право на все произведения, созданные автором в течение__лет».
Когда передаются права на использование некоторых объектов авторского права, например программ для ЭВМ или баз данных, речь идет, по сути, о лицензионном соглашении92. Однако наше законодательство не называет договора о передаче прав на объекты авторского права [28] лицензионными договорами, что, по сути, не влияет на их содержание.
9.8.4. Осуществление проектов, правовая охрана результатов
Интеллектуальная собственность не возникает сама по себе, требуются квалификация, время и затраты для
92 Такой вывод подтверждается, в частности, тем, что в
зарубежной практике такие договора часто называются ли-
цензионными.
Интеллектуальная собственность
1385
ее создания. Ключевой фигурой в процессе создания интеллектуальной собственности является автор, но для использования изобретений, товарных знаков, программ для ЭВМ, селекционных достижений и других объектов интеллектуальной собственности для удовлетворения нужд промышленности, общества требуются усилия многих людей. Монополия, которая предоставляется патентным и авторским правом, ограничивает возможности конкурентов использовать то или иное нововведение без разрешения правообладателя, предоставляет ему возможность окупить затраты на создание и получить дополнительную прибыль. С другой стороны, патентная монополия, как и авторское право, не создана для того, чтобы задерживать технический прогресс, наоборот, в законодательстве предусмотрены механизмы, которые заставляют быстрее вводить нововведение в оборот. В частности, к этим механизмам относится публикация сути объекта, на который выдается патент, а во многих странах и публикация заявки до выдачи патента, механизм принудительной лицензии, право преждепользования.
Интеллектуальная собственность требует бережного отношения к ней автора и правообладателя на всех этапах ее жизненного цикла, начиная от возникновения идеи. Конкуренция на рынке интеллектуальной собственности не менее жесткая, чем на других рынках. Правообладатель должен быть предусмотрителен, точен во всех своих действиях по правовой охране, передаче прав на объекты интеллектуальной собственности другим лицам и защите своих прав и интересов.
Охрана результатов творческой деятельности как объектов интеллектуальной собственности должна носить комплексный характер, рассматриваться как процесс, протекающий во времени, и учитывать природу нововведения.
Эффективная охрана результатов интеллектуальной деятельности предусматривает:
- сбор научно-технической, конъюнктурной и патентной информации, информации об аналогах;
- выбор формы охраны, адекватной созданному объекту;
- своевременную подачу заявок на изобретения, полезные модели и промышленные образцы;
- соответствующее оповещение об авторских правах, особенно в отношении программ для ЭВМ и баз данных;
- использование товарных знаков на выпускаемой продукции и знаков обслуживания при оказании услуг;
- грамотное оформление договоров с авторами, разработчиками, заказчиками, контрагентами;
- отслеживание нарушений прав на интеллектуальную собственность на протяжении всего срока охраны и жизненного цикла изделия.
Кратко рассмотрим особенности каждого этапа по созданию объекта интеллектуальной собственности и приведем перечень действий, которые должны предприниматься для его охраны.
Этап разработки научно-исследовательских, конструкторских и технологических работ
Современная наука и техника развиваются все более ускоряющимися темпами. Поэтому ключевым моментом при создании нововведений в химии, материаловедении, других областях техники является владение информацией о новейших достижениях в этой области. Этой цели служат патентно-информационные исследования на уровень техники, о методике проведения которых говорилось в 9.2.8.
На стадии научных исследований и разработок большое значение имеет охрана результатов в качестве ноу-хау, коммерческой и служебной тайны. Разработчикам необходимо принимать все меры против преждевременного разглашения информации, которая может иметь чрезвычайно высокую коммерческую ценность.
Перед ученым очень часто возникает необходимость поделиться результатами своих исследований перед научным сообществом для проверки и признания результатов. Эта цель вступает в противоречие с необходимостью сохранения конфиденциальности информации и даже может служить препятствием дальнейшей охраны, например путем патентования. Поэтому в договорах с разработчиками должны быть также отрегулированы вопросы публикаций.
Серьезной проблемой для каждого полученного результата является выбор формы его охраны. В каких случаях достаточно охраны авторским правом, на какие объекты необходимо подать заявки на получение патента, какую информацию необходимо хранить как конфиденциальную — все эти действия должны продумываться с учетом всего жизненного цикла нововведения.
Достаточно часто для охраны разработки, которая включает в себя ноу-хау, программы для ЭВМ, патентоспособные объекты, приходится оценивать не только весомость результата, но и коммерческие последствия их реализации. В этом случае собирается и анализируется различная конъюнктурная информация. При оценке новизны технических решений, патентно-лицензионной ситуации проводятся различные виды патентных исследований.
Для эффективной охраны интеллектуальной собственности организации необходимы создание режима охраны служебной и коммерческой тайны93, своевременное заключение соответствующих договоров с персоналом. Следует уделять внимание договорам между заказчиками и исполнителями по созданию научно-технической продукции для разграничения прав на полученные результаты.
93 Зарубежные фирмы принимают самые серьезные меры
безопасности по охране научно-исследовательских центров.
Недаром говорят, что мы больше знаем о деятельности ЦРУ,
чем о деятельности исследовательских центров крупных кор-
пораций.
1386
Новый справочник химика и технолога
Этап подготовки к выпуску промышленной продукции
Следует проверить патентную чистоту подготавливаемой к выпуску промышленной продукции, не нарушите ли вы выпуском продукции патентные права третьих лиц. Проверку лучше поручать профессионалам. Пренебрежение этим правилом может обернуться запрещением выпуска изделия, использования технологии и крупными убытками. К сожалению, проверка на патентную чистоту нс стала правилом. Наилучшей стратегией наряду с такой проверкой является приобретение собственных патентных прав.
В предыдущих подразделах рассмотрены вопросы правовой защиты новых изделий, веществ и технологий. Здесь мы хотим подчеркнуть необходимость их комплексной защиты.
Например, подготовлен к выпуску новый товар, который включает новое химическое вещество. Для защиты этого товара могут быть привлечены следующие объекты интеллектуальной собственности.
На состав химического вещества, а также технологию его производства могут быть получены патенты на изобретения. Новое оборудование, которое необходимо для производства этого вещества, может быть защищено патентом на изобретение или полезную модель, новая упаковка вещества, в которой оно поступает в продажу, — патентом на промышленный образец.
Оригинальное название вещества может быть зарегистрировано в качестве товарного знака. Товарный знак предприятия должен проставляться на упаковке, инструкциях применения товара и давать еще одну степень защиты.
Технология производства может сохраняться как ноу-хау, в режиме служебной, коммерческой тайны.
Для объектов авторского права, программ для ЭВМ, баз данных следует применять знак оповещения об авторских правах (©). Производитель фонограмм также должен оповещать о своих правах.
Общее правило можно выразить в виде девиза:
«Не нарушаю чужие права и максимально защищаю свои».
Этап выпуска продукции
На этапе выпуска продукции на первый план выходит проблема отслеживания нарушителей ваших прав и пресечения этих нарушений. Правовые вопросы защиты прав на интеллектуальную собственность мы рассмотрим ниже.
Использование товарных знаков в деятельности предприятия должно подчиняться единому плану, в разработке которого, как правило, принимают участие отделы маркетинга и высшее руководство. У крупных зарубежных предприятий зарегистрированы десятки знаков, которые применяются для маркировки отдельных видов продукции. На различных рынках для одной и той же продукции могут применяться различные знаки. В качестве знаков регистрируются названия новых фармацевтических веществ, химических продуктов,
новых материалов. Распространение получила защита в качестве товарных знаков этикеток выпускаемых на рынок продуктов.
Таким образом в маркировке одного изделия может использоваться несколько товарных знаков. Однако важно не количество. Товарный знак, так же как и знак обслуживания, применяемый при оказании услуг и производстве работ, по своей изначальной сути, служит для того, чтобы потребитель отличал ваши товары, работы и услуги от товаров и услуг других производителей, и здесь потребителя нельзя запутать. Иначе знак начнет терять различительную способность и не будет работать на своего владельца.
Применение отдельных товарных знаков пошло по пути создания на их основе фирменного стиля предприятия. Правового понятия «фирменный стиль» не существует. Можно сказать, что фирменный стиль — это общность образной системы, которая пронизывает всю деятельность предприятия и направлена как на потребителя, партнеров по бизнесу, так и на персонал собственного предприятия. В фирменный стиль может входить все: от цветовой гаммы, применяемой в окраске продуктов и стен предприятия, архитектурных деталей зданий, до элементов оформления корреспонденции и вариантов общения персонала с клиентами.
Назначение фирменного стиля то же, что у товарного знака, — выделять предприятие из ряда других предприятий, поэтому, как правило, товарный знак предприятия и фирменный стиль связаны между собой.
9.9. Защита прав на интеллектуальную собственность
Использование результатов интеллектуальной деятельности и средств индивидуализации (товарных знаков, знаков обслуживания), которые являются объектом исключительных прав, может осуществляться третьими лицами только с согласия правообладателя [7].
Как Патентный закон, так и закон об авторском праве [6, 18] предусматривают тражданскую, уголовную и административную ответственность. В процессе защиты прав используется также законодательство о недобросовестной конкуренции и таможенное законодательство.
Можно следующим образом классифицировать виды нарушений прав на интеллектуальную собственность:
а) по субъектам прав:
- нарушения прав авторов;
- нарушения прав правообладателей (в том числе патентообладателей);
б) по нарушениям, связанным с объектами интеллектуальной собственности:
- патентные права;
- права на товарный знак, наименование места происхождения товаров;
- права на объекты авторского права;
- права на служебную и коммерческую тайну (ноу-хау).
Отдельно следует рассмотреть споры, связанные с
правомерностью регистрации объектов патентного
Интеллектуальная собственность
1387
права (изобретений, полезных моделей, промышленных образцов), а также товарных знаков и наименований мест происхождения товаров, которые рассматриваются в административном порядке в Палате по патентным спорам, являющейся структурой Патентного ведомства РФ.
В качестве резюме можно сказать следующее:
Правомерность выдачи или невыдачи охранных документов на изобретения, полезные модели, промышленные образцы, товарные знаки, наименования мест происхождения товаров оспаривается в Палате по патентным спорам Роспатента.
Остальные споры и нарушения связаны с гражданским или уголовным судопроизводством. Некоторые нарушения могут преследоваться в административном порядке.
9.9.1. Рассмотрение протестов и споров в Палате по патентным спорам
В Палате по патентным спорам Роспатента в административном порядке рассматриваются следующие основные дела.
Возражения заявителя на решения:
- об отказе в выдаче патента;
- об отказе в принятии заявки на регистрацию товарного знака, наименования места происхождения товара;
- о непредоставлении правовой охраны товарному знаку, наименованию места происхождения товара;
- о признании товарного знака общеизвестным.
Возражения третьих лиц:
- против выдачи патента, действия патента СССР, евразийского патента, против предоставления правовой охраны товарному знаку, наименованию места происхождения товара;
- против предоставления правовой охраны общеизвестному в Российской Федерации товарному знаку;
- заявление о досрочном прекращении правовой охраны товарного знака в случае превращения зарегистрированного товарного знака в обозначение, вошедшее во всеобщее употребление как обозначение товаров определенного вида.
Рассмотрение дел в зависимости от сути дела проводится с участием представителей заявителя, третьей стороны и представителей ФИПС.
Решение Палаты по патентным спорам может быть оспорено в судебных инстанциях.
9.9.2. Гражданское право
Осуществлять свои гражданские правомочия — право и обязанность обладателя этих прав. Если владелец прав на интеллектуальную собственность не принимает меры по ее охране, то практически не следует ожидать, что его права будут соблюдаться. Вопреки ложному убеждению, к сожалению, достаточно широко распространенному, заключающемуся в том, что закон не защищает права автора и правообладателя, как мы увидим далее, положения законодательства предоставляют все средства для защиты прав.
9.9.2.1. Патентное право
Как гражданские дела рассматриваются следующие виды споров [6]:
- об авторстве изобретения, полезной модели, промышленного образца;
- об установлении патентообладателя;
- о нарушении исключительного права;
- о заключении и об исполнении договоров о передаче исключительного права (уступке патента) и лицензионных договоров;
- о праве преждепользования;
- о праве послепользования;
- о размере, сроке и порядке выплаты вознаграждения автору;
„94
- о размере, сроке и порядке выплаты компенсации ;
- другие споры, связанные с охраной прав, удостоверяемых патентом.
В данном перечне приведены споры, касающиеся нарушений прав как авторов, так и патентообладателей.
Патентообладатель может требовать от нарушителя его исключительных прав:
- прекращения нарушения патента;
- возмещения причиненных убытков в соответствии с гражданским законодательством.
Такие же правомочия предоставляются владельцу исключительной лицензии, если в лицензионном договоре между ним и патентообладателем не сказано иное.
При защите своих имущественных прав патентообладатель может использовать все способы, предусмотренные законодательством Российской Федерации. Защищая свою деловую репутацию, он может требовать публикации решения суда.
9.9.2.2. Товарные знаки и наименования мест происхождения товаров
В порядке гражданского судопроизводства рассматриваются следующие споры:
- о нарушении исключительного права на товарный знак;
- о досрочном прекращении правовой охраны коллективного знака вследствие его использования на товарах, не обладающих едиными качественными или иными едиными характеристиками;
- о заключении и об исполнении лицензионного договора и договора об уступке товарного знака;
94 Патентный закон, в частности, предусматривает следующие виды компенсаций:
- компенсация при использовании изобретения в период временной правовой охраны, наступающей с даты публикации заявки (или предупреждения заявителя об имеющейся заявке на изобретение) и действующей до даты выдачи патента;
- компенсация за использование защищенного патентом
объекта при чрезвычайных обстоятельствах;
- компенсация за использование защищенного патентом
объекта в интересах национальной безопасности.
1388
Новый справочник химика и технолога
- о незаконном использовании наименования места происхождения товара.
При незаконном использовании товарного знака выдвигаются требования о прекращении нарушения и взыскании причиненных убытков.
Помимо этого закон [9] предусматривает:
- публикацию судебного решения в целях восстановления деловой репутации потерпевшего;
- удаление за счет нарушителя с контрафактных товаров, этикеток, упаковок незаконно используемого товарного знака или сходного с ним до степени смешения обозначения либо уничтожения за счет нарушителя контрафактных товаров, этикеток, упаковок в случае невозможности удаления знака.
Контрафактные товары, этикетки, упаковки могут быть обращены в доход государства либо переданы правообладателю по его заявлению в счет возмещения убытков.
Лицо, незаконно использующее наименование места происхождения товара, по требованию обладателя свидетельства, государственного органа, прокурора или общественной организации обязано:
- прекратить его использование, а также возместить причиненные убытки;
- опубликовать судебное решение в целях восстановления деловой репутации потерпевшего;
- удалить с контрафактных товаров, этикеток, упаковок незаконно используемое наименование места происхождения товара либо уничтожить контрафактные товары, этикетки, упаковки.
Владелец товарного знака и обладатель свидетельства на право пользования наименованием места происхождения товара вместо требования о взыскании причиненных убытков вправе требовать от лица, незаконно использующего товарный знак или наименование места происхождения товара, выплаты определяемой судом денежной компенсации в размере от 1 тысячи до 50 тысяч МРОТ95.
9.9.2.3. Авторское право
В законе об авторском праве лицо, не выполняющее требований закона [18], называется нарушителем авторских и смежных прав. Экземпляры произведений, изготовленные и распространенные с нарушением закона [18, 19], — контрафактные экземпляры.
1. Автор, обладатель смежных прав или иной обладатель исключительных прав вправе защищать свои права способами, предусмотренными Гражданским кодексом Российской Федерации.
2. Обладатели исключительных прав вправе требовать по своему выбору от нарушителя вместо возмещения убытков выплаты компенсации:
— в размере от 10 тыс. руб. до 5 млн руб., определяемом по усмотрению суда, арбитражного суда или третейского суда исходя из характера нарушения;
- в двукратном размере стоимости экземпляров произведений или объектов смежных прав либо в двукратном размере стоимости прав на использование произведений или объектов смежных прав, определяемой исходя из цены, которая при сравнимых обстоятельствах обычно взимается за правомерное использование произведений или объектов смежных прав.
Обладатели исключительных прав вправе требовать от нарушителя выплаты компенсации за каждый случай неправомерного использования произведений или объектов смежных прав либо за допущенные правонарушения в целом.
Компенсация подлежит взысканию при доказанности факта правонарушения независимо от наличия или отсутствия убытков.
3. Авторы и исполнители в случае нарушения их личных неимущественных или имущественных прав также вправе требовать от нарушителя возмещения морального вреда.
4. Автор, обладатель смежных прав или иной обладатель исключительных прав в установленном законом порядке вправе обратиться для защиты своих прав в суд, арбитражный суд, третейский суд, органы прокуратуры, органы дознания, органы предварительного следствия в соответствии с их компетенцией.
Возможность выбора путей получения материального возмещения при нарушении прав — возмещение убытков, взыскание дохода или выплата компенсации — дает возможность реально получить это возмещение. Практика показывает, что наиболее часто правообладатели требуют компенсации, т. к. убытки рассчитывать и доказывать гораздо сложнее.
Обладатель авторских и смежных прав также может потребовать принятия иных мер, связанных с защитой его прав.
Контрафактные экземпляры произведений подлежат обязательной конфискации и уничтожению, кроме случаев передачи их обладателю авторских или смежных прав по его просьбе. По решению суда могут также быть уничтожены материалы и оборудование, используемые для изготовления и воспроизведения контрафактных экземпляров.
При наличии достаточных оснований судебные органы, а также органы дознания, следователь могут принять меры досудебного характера по розыску и аресту контрафактных экземпляров произведений.
9.9.2.4. Служебная и коммерческая тайна
Гражданская ответственность за нарушение прав на
служебную и коммерческую тайну предусматривает
возмещение убытков, понесенных владельцем инфор-
мации [7].
Обязанность возмещения убытков возлагается и на
работников, разгласивших служебную или коммерче-
95 МРОТ — минимальный размер оплаты труда, устанавливаемый законодательством, в данном случае для оплаты штрафов.
Интеллектуальная собственность
1389
скую тайну вопреки трудовому договору, в том числе контракту, и на контрагентов, сделавших это вопреки гражданско-правовому договору.
Получение, использование, разглашение информации, составляющей коммерческую, служебную тайну, законом [26] относятся к недобросовестной конкуренции.
Необходимо отметить, что доказать нарушение прав на служебную или коммерческую тайну не очень просто, поэтому следует принимать все меры, чтобы избежать похищения или разглашения этой информации.
9.9.2.5. Топология интегральных микросхем
Автор охраняемой топологии и иной правообладатель вправе требовать [28]:
- признания прав;
- восстановления положения, существовавшего до нарушения права, и прекращения действий, нарушающих право или создающих угрозу его нарушению;
- возмещения лицом, виновным в нарушении прав, причиненных убытков.
9.9.2.6. Селекционные достижения
По требованию патентообладателя или Государственной комиссии РФ по испытанию и охране селекционных достижений нарушение должно быть прекращено с возмещением патентообладателю лицом, допустившим нарушение, причиненных убытков [29].
Требования к нарушителю патента могут быть заявлены также обладателем исключительной или неисключительной лицензии, если иное не предусмотрено лицензионным договором.
9.9.3. Уголовное право
Уголовный кодекс Российской Федерации [30] содержит несколько статей, связанных с интеллектуальной собственностью.
Статья 146 «Нарушение авторских и смежных прав» в части первой предусматривает наказание за присвоение авторства (плагиат), если это деяние причинило крупный ущерб автору или иному правообладателю. В части второй этой же статьи устанавливается уголовное наказание за «незаконное использование объектов авторского права или смежных прав, а равно приобретение, хранение, перевозку контрафактных экземпляров произведений или фонограмм в целях сбыта, совершенные в крупном размере».
Деяния признаются совершенными в крупном размере, если стоимость экземпляров произведений или фонограмм либо стоимость прав на использование объектов авторского права и смежных прав превышают 100 МРОТ, а в особо крупном размере — 500 МРОТ.
Статья 147 «Нарушение изобретательских и патентных прав» предусматривает наказание за незаконное использование изобретения, полезной модели или промышленного образца, разглашение без согласия автора или заявителя сущности изобретения, полезной
модели или промышленного образца до официальной публикации сведений о них, присвоение авторства или принуждение к соавторству, если эти деяния причинили крупный ущерб.
Статья 180 предусматривает наказание за незаконное использование чужого товарного знака, знака обслуживания, наименования места происхождения товара или сходных с ними обозначений для однородных товаров, если это деяние совершено неоднократно или причинило крупный ущерб.
Статья 183 «Незаконные получение и разглашение сведений, составляющих коммерческую, налоговую или банковскую тайну» предусматривает наказание за сбор сведений, составляющих коммерческую, налоговую или банковскую тайну, путем похищения документов, подкупа или угроз, а равно иным незаконным способом, а также незаконное разглашение или использование сведений, составляющих коммерческую, налоговую или банковскую тайну, без согласия их владельца лицом, которому она была доверена или стала известна по службе или работе.
Отдельно следует упомянуть преступления в сфере компьютерной информации (гл. 28, ст. 272-274) [30]: неправомерный доступ к компьютерной информации, создание, использование и распространение вредоносных программ для ЭВМ, нарушение правил эксплуатации ЭВМ, системы ЭВМ или их сети, в том числе свя-заных с охраной прав, предусмотренных правовой охраной программ для ЭВМ и баз данных [19].
Нарушения по вышеперечисленным статьям предусматривают наказание от штрафа до лишения свободы.
Право возбуждения уголовного дела [31] принадлежит, прежде всего, прокуратуре, а также в предусмотренных законом случаях следователю и дознавателю. В рамках уголовного процесса могут выдвигаться гражданским истцом и требования о возмещении имущественного ущерба. В этом случае гражданский истец освобождается от уплаты государственной пошлины.
9.9.4. Административное право
Выше, в 9.9.1, описан административный порядок рассмотрения некоторых видов дел в Палате по патентным спорам Патентного ведомства РФ.
Кодекс РФ об административных правонарушениях [32] также предусматривает ответственность за нарушения, связанные с интеллектуальной собственностью.
Ст. 7.12 предусматривает административную ответственность за нарушение авторских и смежных прав, а также изобретательских и патентных прав.
К нарушениям относятся:
- ввоз, продажа, сдача в прокат или иное незаконное
использование контрафактных экземпляров произведе-
ний или фонограмм в целях извлечения дохода;
- указание на экземплярах произведений или фоно-
грамм ложной информации об обладателях авторских
и смежных прав, об изготовителях и местах их произ-
водства;
1390
Новый справочник химика и технолога
- незаконное использование изобретения, полезной модели либо промышленного образца;
- разглашение без согласия автора или заявителя сущности изобретения, полезной модели либо промышленного образца до официального опубликования сведений о них;
- присвоение авторства или принуждение к соавторству.
За данные административные нарушения предусмотрены штрафные санкции, а также конфискация контрафактных экземпляров, материалов и оборудования, на котором они изготовлены.
В ст. 7.28 предусмотрено наказание в виде штрафа на граждан в размере от 10 до 20 МРОТ, на юридических лиц — от 500 до 800 МРОТ за нарушение порядка патентования объектов промышленной собственности в иностранных государствах. Патентный закон предусматривает следующий порядок патентования: сначала должна быть подана заявка на изобретение или полезную модель в РФ, и только затем, по истечении 6 месяцев с даты подачи заявки, можно подавать заявки за рубежом. Заявка может быть подана и раньше, но после проведения, по просьбе заявителя, проверки содержания в заявке сведений, составляющих государственную тайну. В соответствии с Договором о патентной кооперации (РСТ) или Евразийской патентной конвенцией заявки могут быть поданы и без подачи российской заявки, если они поданы в Роспатент как получающее ведомство.
9.9.5. Практика защиты прав на интеллектуальную собственност ь
Практика защиты патентных и авторских прав в Российской Федерации достаточно разнообразна. В данном издании не ставится задача рассмотрения конкретных случаев из судебной и арбитражной практики, т. к. конкретные дела составляют мозаику, знакомство с которой мало что дает для систематических знаний. Однако можно заметить, что суды все увереннее берутся за разрешение достаточно сложных дел, связанных с интеллектуальной собственностью.
Рассмотрим некоторые общие рекомендации, вытекающие из практики.
Надежность позиции правообладателя по отношению к нарушителям его прав обеспечивается условиями, которые сопровождают правообладателя на протяжении всего жизненного цикла объекта интеллектуальной собственности.
Рассмотрим самые важные из этих условий.
До возникновения спора
Правильное оформление договорных отношений на всех этапах создания и жизни объекта интеллектуальной собственности
Прежде всего, должны быть отрегулированы отношения между авторами и правообладателем. Отсутствие соответствующих договоров приводит к спорам
между авторами, особенно в тех случаях, когда объект интеллектуальной собственности имеет счастливую судьбу в экономическом смысле.
Отсутствие соответствующих договорных отношений между авторами и работодателем также приводит к ослаблению позиций той или иной стороны.
Следует внимательно относиться к договорам о передаче прав третьим лицам. Достаточно часто эти договора составляются формально, в расчете на то, что, как и в момент заключения договора, отношения между партнерами будут безоблачными. Но время идет, и отношения изменяются. В этом случае и выплывают все огрехи, допущенные на этапе фиксации соглашения, и иногда уже ничего нельзя исправить.
Общая рекомендация: относиться к договору как к жизненно важному документу и составлять его с помощью профессионалов. Однако необходимо помнить, что профессионал только оформляет отношения и страхует от грубых и типичных ошибок. Поэтому каждая из сторон должна внимательно и тщательно оценивать ситуацию и доводить всю информацию о содержании сделки и существа отношений до специалиста, оформляющего договор.
И последнее — вся история договорных соглашений должна сохраняться, т. к. при возникновении спора может потребоваться любой документ.
Ответственный подход к оформлению заявочных документов на объекты промышленной собственности
Нет ничего более обидного, чем убедиться в том, что ваш патент практически не защищает ваши права на изобретение или полезную модель. Например, формула изобретения или полезной модели составлена так, что ее легко обойти, сделав незначительные изменения, нс влияющие на сущность изобретения. Профессионалы знают, что на судьбу патента также может повлиять и неправильно составленное описание.
Составлять заявку должен профессионал. Изобретатель и заявитель должны внимательно контролировать материалы заявки.
В 9.2.2 уже говорилось о надежных и ненадежных патентах. Если в процессе подготовки заявки не проводилось патентных исследований (особенно это важно для полезных моделей, т. к. экспертиза по ним нс проводится) или заявитель и изобретатель знали о публикациях, которые порочат новизну изобретения, но скрыли этот факт от экспертизы, то эту информацию могут найти конкуренты и аннулировать патент как не отвечающий условиям патентоспособности.
Передача прав тому лицу, кто выпускает продукцию
Преследовать нарушителя имеет право правообладатель (патентообладатель для объектов промышленной собственности). Однако нередки случаи, когда патент принадлежит одному лицу, а выпускает продукцию другое лицо.
Например. Патент принадлежит физическому лицу,
а продукцию выпускает предприятие, которым он вла-
деет. Убытки возникают у производителя, юридического
Интеллектуальная собственность
1391
лица. Наличие убытков у физического лица практически трудно доказать. Дело должно рассматриваться в гражданском суде, а не в арбитражном. Передача нрав юридическому лицу перед подачей иска требует времени и мало помогает в доказательстве суммы ущерба. А вся причина в том, что права своевременно не были переданы путем заключения лицензионного соглашения или уступки патента.
Бывают и другие случаи, когда патент принадлежит предприятию, которое уже прекратило существование, а права не переданы вновь зарегистрированному.
Поддержание патента или свидетельства в силе
Патент на изобретение, полезную модель или промышленный образец действует только в том случае, если своевременно уплачиваются ежегодные пошлины за его поддержание.
Если патент не действует, любое лицо может использовать объект промышленной собственности, не испрашивая разрешения. Действие патента на изобретение, полезную модель или промышленный образец, которое было прекращено в связи с неуплатой ежегодной пошлины за поддержание патента в силе, может быть восстановлено. Однако любое лицо, которое начало использование запатентованного изобретения, полезной модели или промышленного образца либо сделало в указанный период необходимые к этому приготовления, пользуется правом послепользования.
Хранение информации, относящейся к объекту интеллектуальной собственности
Особенно важно это положение для объектов, которые охраняются авторским правом. Если в дальнейшем возникнут споры о том, кто создал, например, программу для ЭВМ, то подготовительные материалы будут служить документами, подтверждающими право автора и правообладателя.
Нарушение прав владельца произошло.
Период подготовки к преследованию нарушителя
Проверка и сбор документации
В предыдущем подразделе мы говорили о правильном оформлении договорных отношений, своевременной уплате пошлин и т. д. Пришло время проверить всю документацию и убедиться, что юридически ваши права подтверждаются необходимыми документами. На практике иногда приходится производить какие-то действия, чтобы исправить огрехи, допущенные ранее.
Разработка стратегии и тактики защиты
Достаточно часто людей, даже руководителей высокого ранга, в случае нарушения прав охватывает гнев. А любой спор проходит в борьбе с противником, и эмоции здесь помеха.
Первое. Кому же поручить борьбу? Вести ее автору самому или пригласить адвоката? Для юридического лица тоже существует выбор: поручить дело собственной юридической службе или нанять адвокатскую контору. Следует ли приглашать специалиста в области интеллектуальной собственности, патентного поверенного, патентоведа?
На все эти вопросы нет однозначного ответа. С точки зрения процессуального законодательства в гражданском суде физическое лицо может защищать свои права само или через представителя. В нашем случае это может быть адвокат, работающий в области интеллектуальной собственности, или патентный поверенный, патентовед. В любом случае в интересах дела это должен быть специалист.
В арбитражном суде представителем юридического лица должен быть или работник предприятия, или адвокат. С нашей точки зрения, для патентных дел лучше всего сочетание: адвокат, хорошо знающий процессуальные нормы, и специалист в области интеллектуальной собственности — патентный поверенный или опытный патентовед.
Для ведения спора потребуются финансовые ресурсы. И далеко не всегда расходы, понесенные в судебном деле, возмещаются выигравшей стороной.
Второе. Необходима реальная оценка своей позиции. Один из сложных вопросов — сбор доказательств нарушения. Доказательства с точки зрения суда делятся на прямые и косвенные. Если нет прямых доказательств, выиграть любое дело весьма проблематично. Необходимо собрать подробные сведения о нарушителе и прямые доказательства нарушения ваших прав.
Невозможно дать какие-то общие рекомендации в выработке стратегии и тактики ведения дела. В предыдущих разделах достаточно подробно рассматривались возможности, которые предоставляет закон. Все эти варианты должны быть рассмотрены при выработке тактики защиты.
С нашей точки зрения, правообладатель должен быть психологически готов к долгой процедуре, ведь существует несколько инстанций при рассмотрении судебных дел, а нарушители тоже борются до конца — им есть что терять. Любое дело, связанное с интеллектуальной собственностью, может затянуться и порой реально затягивается на годы.
Процедура судебного спора
Прежде чем подавать иск в суд, следует решить, смогут ли стороны прийти к соглашению при рассмотрении претензии в досудебном порядке. Достаточно много претензий решается вне суда. Может быть, нарушитель не знал о ваших правах, выпуская продукцию, нарушающую ваш патент, и будет согласен заключить с вами лицензионное соглашение, или просто прекратит нарушение.
Возможно, рассмотрение спора следует провести в третейском суде, который, как правило, действует быстрее и квалифицированнее, да и стоить это будет дешевле.
Мы не будем здесь рассматривать процедуру подго-
товки искового заявления и порядок предъявления ис-
ка. Для этого существует достаточно пособий.
Следует заметить, что от уплаты государственной
пошлины по делам, рассматриваемым в судах, освобо-
ждаются истцы — по спорам об авторстве; авторы —
по искам, вытекающим из авторского права, из права на
1392
Новый справочник химика и технолога
изобретение, полезную модель, промышленный образец, а также из других прав на интеллектуальную собственность [33].
Достаточно часто стороны в процессе судебного спора, поняв свою позицию и позицию другой стороны, заключают мировое соглашение.
Если сторона нарушителя непреклонна, то следует ожидать следующего хода. Ответчик в патентных делах или делах, связанных с нарушением прав на товарный знак, попробует аннулировать патент или свидетельство о регистрации знака. Эта процедура, проходящая в Патентном ведомстве — Высшей патентной палате может привести к аннулированию патента полностью или частично или является основанием для затягивания судебного процесса.
В заключение следует сказать, что патентные права и права, связанные с авторским правом, дают правообладателю серьезные преимущества, и за них стоит бороться.
9.10. Стоимость интеллектуальной собственности
Когда мы говорим об интеллектуальной собственности, мы говорим об объектах, которые не относятся к материальной сфере. Речь идет о результатах творческой деятельности, а еще точнее — о правах на использование этих результатов. Прибыль, ради которой в большинстве случаев и используются объекты интеллектуальной собственности, является мерилом деятельности в другой сфере — сфере материального производства. Переход от прав на нематериальные объекты к материальным результатам, которые получаются за счет этих прав, порождает заметные трудности в определении стоимости объектов интеллектуальной собственности.
Следующее замечание относится к ситуации, в которой проводится оценка стоимости. Ситуации и цели оценки могут быть различны. Исходя из этого, и применяемая методика оценки стоимости может быть разной, да и результаты также будут различаться.
Приведем пример, относящийся к материальным объектам. Бухгалтерская оценка любых материальных средств но годам производится исходя из стоимости актива в момент приобретения за вычетом амортизации96. Таким образом, стоимость актива снижается, и к концу срока амортизации актив с бухгалтерской точки зрения ничего не стоит. В реальной жизни этого не бывает практически никогда. Достаточно часто цена того или иного материального актива с течением времени растет. При продаже на рынке этого актива возникает существенная разница между ценой продажи и бухгалтерской оценкой его у продавца97. Данный
96 Амортизация в упрощенном понимании — начисление, ежегодно производящееся на актив и снижающее его стоимость, чтобы обеспечить соответствие затрат на приобретение актива с доходами, которые он создает за срок своей полезной службы. С точки зрения бухгалтерии стоимость актива со временем снижается.
97 Такое положение не должно смущать инженеров. Бух-
галтеры не могут ежегодно оценивать рыночную цену акти-
пример показывает, что рыночная цена объекта интеллектуальной собственности и его бухгалтерская оценка, например при постановке на баланс, будут разительно отличаться98.
Оценка объектов интеллектуальной собственности требуется в определенных случаях, в частности:
- уступка прав на объект интеллектуальной собственности другому лицу;
- заключение лицензионного договора;
- определение размера ущерба при незаконном использовании объектов интеллектуальной собственности;
- разработка инновационных проектов;
- получение кредита под залог прав на объекты интеллектуальной собственности;
- формирование уставного фонда при создании новых и реорганизации старых предприятий, если в уставной капитал вкладываются нематериальные активы99 в виде объектов интеллектуальной собственности;
- приватизация государственного имущества;
- постановка на баланс объекта интеллектуальной собственности в качестве нематериального актива.
Мы не ставили перед собой задачу подробно рассмотреть все методы оценки. Сделана попытка дать сравнительно простое понятие проблемы для инженера, бизнесмена, руководителя, чтобы он понимал сущность методов оценки и мог самостоятельно или вместе со специалистами, экономистами, оценщиками получить необходимые данные по стоимости того или иного объекта интеллектуальной собственности.
9.10.1. Процесс оценки
Кто может производить оценку? По закону «Об оценочной деятельности в Российской Федерации» [34] только при вовлечении в сделку объектов оценки, принадлежащих полностью или частично Российской Федерации, субъектам Российской Федерации либо муниципальным образованиям, оценку должен производить сертифицированный оценщик. Во всех других случаях оценку может производить сам владелец интеллектуальной собственности или можно привлекать специалистов, в том числе и сертифицированных оценщиков.
Сертифицированные оценщики должны действовать в рамках стандартов оценочной деятельности [35].
Стандарты оценки материальных средств и имущественных прав [35] устанавливают следующие виды стоимости:
- рыночная стоимость;
вов. Если бы они это делали, то результаты были бы непредсказуемы, открылось бы дополнительное поле для злоупотреблений. Кроме того, на цели оценки ежегодно уходили бы существенные суммы из бюджета предприятий.
98 Порой во внутренних бухгалтерских отчетах зарубеж-
ных компаний нематериальный актив (например, изобрете-
ние) ставится на баланс по символической цене в 1 доллар,
чтобы только этот актив не выпал из поля зрения.
99 О нематериальных активах см. в 9.10.5.
Интеллектуальная собственность
1393
- стоимость объекта оценки с ограниченным рынком — стоимость объекта оценки, продажа которого на открытом рынке невозможна или требует дополнительных затрат по сравнению с затратами, необходимыми для продажи свободно обращающихся на рынке товаров;
- стоимость замещения объекта оценки — сумма затрат на создание объекта, аналогичного объекту оценки, в рыночных ценах, существующих на дату проведения оценки, с учетом износа объекта оценки;
- стоимость воспроизводства объекта оценки — сумма затрат в рыночных ценах, существующих на дату проведения оценки, на создание объекта, идентичного объекту оценки, с применением идентичных материалов и технологий, с учетом износа объекта оценки;
- стоимость объекта оценки при существующем использовании — стоимость объекта оценки, определяемая исходя из существующих условий и цели его использования;
- инвестиционная стоимость объекта оценки — стоимость объекта оценки, определяемая исходя из его доходности для конкретного лица при заданных инвестиционных целях;
- стоимость объекта оценки для целей налогообложения — стоимость объекта оценки, определяемая для исчисления налоговой базы и рассчитываемая в соответствии с положениями нормативных правовых актов;
- ликвидационная стоимость объекта оценки — стоимость объекта оценки в случае, если объект оценки должен быть отчужден в срок меньше обычного срока экспозиции аналогичных объектов;
- утилизационная стоимость объекта оценки — стоимость объекта оценки, равная рыночной стоимости материалов, которые он в себя включает, с учетом затрат на утилизацию объекта оценки.
Далеко не все перечисленные виды стоимости применяются для оценки объектов интеллектуальной собственности. Например, трудно представить утилизационную стоимость.
Стандарты оценки предписывают следующие подходы к оценке [35]:
- доходный — совокупность методов оценки стоимости объекта оценки, основанных на определении ожидаемых доходов от объекта оценки;
- сравнительный — совокупность методов оценки стоимости объекта оценки, основанных на сравнении объекта оценки с аналогичными объектами, в отношении которых имеется информация о ценах сделок с ними;
- затратный — совокупность методов оценки стоимости объекта оценки, основанных на определении затрат, необходимых для восстановления либо замещения объекта оценки, с учетом его износа100.
100 Терминология в области методов оценки интеллектуальной собственности еще далека от единообразия. Кроме того, существуют различные взгляды на применение перечисленных и других методов. Однако далее автор постарается придерживаться терминологии, введенной стандартами оцен-
В помощь оценщику выпущены Методические рекомендации по определению рыночной стоимости интеллектуальной собственности [35], которые применяются при оценке:
- исключительных прав на результаты интеллектуальной деятельности и средства индивидуализации юридического лица, индивидуализации продукции, выполняемых работ или услуг, в том числе исключительных прав на изобретения, полезные модели, промышленные образцы, товарные знаки и знаки обслуживания, программы для ЭВМ и базы данных, топологии интегральных микросхем, селекционные достижения, произведения науки, литературы или искусства и др.;
- прав на секреты производства (ноу-хау);
- прав на результаты интеллектуальной деятельности и средства индивидуализации, передаваемых по договору, в том числе по лицензионному договору, авторскому договору, договору о передаче прав на использование топологии интегральных микросхем, программы для ЭВМ или базы данных, иному договору.
Данный документ содержит много полезных сведений, относящихся к процедуре оценки, однако не содержит конкретных методик расчета.
9.10.2. Рыночная стоимость интеллектуальной собственности
Под рыночной стоимостью понимается [35] «наиболее вероятная цена, по которой данный объект оценки может быть отчужден на открытом рынке в условиях конкуренции, когда стороны сделки действуют разумно, располагая всей необходимой информацией, а на величине цены сделки не отражаются какие-либо чрезвычайные обстоятельства».
Определяя максимально возможную цену объекта интеллектуальной собственности, можно руководствоваться достаточно простым соображением. Представим себе, что покупатель решил не приобретать у вас права на использование объекта интеллектуальной собственности, а создать сам (или с помощью других лиц) изобретение, решающее эту проблему, или подобную программу для ЭВМ. Можно определить затраты, которые на это необходимы, и учесть фактор времени, необходимый на создание. Такой расчет дает возможность определить максимальную стоимость. Этот прием весьма полезен и часто применяется, оценщики называют его принципом замещения.
На стоимость объекта влияют также следующие факторы.
Нематериальный характер объекта. Интеллектуальная собственность — это не материальный объект, а права, связанные с изобретением, программой для ЭВМ, литературным произведением, селекционным достижением. Объем прав зависит от характера объекта.
Стадия освоения объекта интеллектуальной собственности. Необходимость оценки стоимости возни-
ки и Методическими рекомендациями по определению ры-
ночной стоимости интеллектуальной собственности [35].
1394
Новый справочник химика и технолога
кает на различных стадиях освоения объекта, а от этого сильно зависит не только стоимость, но и выбор методики оценки.
Необходимость понимания сущности прав, которые существуют для данного объекта. В зависимости от сущности объекта, качества защиты, что особенно важно для объектов промышленной собственности, действительная стоимость может быть совершенно различной.
Вероятностный характер оценки, что обусловливается как причинами, приведенными выше, так и тем обстоятельством, что оценка, как правило, проводится в одно время, а доходы от использования объекта интеллектуальной собственности будут позже, в некоторых случаях спустя годы, и зависят от эффективности его использования.
Наличие различных методов оценки, в том числе и достаточно сложных, а также различное понимание авторами источников, где излагаются эти методы, сущности проблемы.
Факторы, влияющие на стоимость объекта в наибольшей степени
Существенное влияние на стоимость оказывает стадия разработки объекта.
Общий принцип можно сформулировать следующим образом. Чем дальше от настоящего времени начало использования объекта, тем ниже рыночная стоимость разработки.
Это положение можно пояснить на графике затрат и прибылей, связанных с новой технологией или объектом интеллектуальной собственности.
Как видно из графика, для того чтобы осуществить нововведение, сначала требуется понести значительные расходы на проведение НИР, ОКР, маркетинг, подготовку производства и выпуск продукции. Только после начала выпуска новая технология начинает приносить прибыль, компенсируя первоначальные затраты. В случае реализации успешного инновационного проекта (кривая 7) прибыль превышает затраты. Однако возможны и другие варианты (кривые 2 и 5), когда прибыль по инновационному проекту недостаточна или затраты вообще не окупаются.
Рис. 9.24. График затрат и прибылей, связанных с новой технологией
Инновационный проект всегда имеет вероятность быть убыточным. Предсказать успех, особенно на этапе НИР, достаточно сложно. Это обстоятельство влияет на цену объекта интеллектуальной собственности и на выбор методики расчета. Снижают стоимость объекта интеллектуальной собственности различные виды рисков, которым подвергается проект использования объекта интеллектуальной собственности в процессе его выхода на рынок.
Следует заметить, что у многих изобретателей присутствует ощущение, что главное дело сделано после того, как получен патент. Это не так. Предстоит приложить много усилий большому числу людей, производственникам, маркетологам, рекламистам и т. д., прежде чем продукт завоюет свою позицию на рынке. Изобретатели должны учитывать то обстоятельство, что без прибыли ни один предприниматель не будет производить продукт и что основные риски несет именно он.
Важно понять и другое обстоятельство. Некоторые объекты интеллектуальной собственности, например программы для ЭВМ, произведения литературы, музыки, сразу после их создания готовы к использованию в материальном мире. Например, программа для ЭВМ может устанавливаться на персональные компьютеры и использоваться конечным пользователем. Стоимость этой программы оценивается практически так же, как стоимость новых товаров — есть спрос, известна стоимость подобных программ. Умножай стоимость программы для ЭВМ на объем предполагаемых продаж и получишь доход, который является основой для определения, например, уступки прав на программу.
Другое дело изобретение. Патент на изобретение уже получен, а производство продукции еще не началось. Да и продукция по изобретению имеет связь с патентными правами не прямую, а более опосредованную.
Сущность объекта интеллектуальной собственности
Объекты интеллектуальной собственности можно условно разделить на две группы. К первой группе относятся объекты, в которых «материальная» сущность достаточно велика, т.е. они достаточно близки к объектам материального права: программы для ЭВМ, базы данных, литературные произведения, произведения живописи, музыки и т. д. Вторая группа объектов имеет меньшее «материальное» содержание. Это, скорее, информация, которая позволяет создавать новые материальные объекты: изобретения, полезные модели, технические ноу-хау, товарные знаки. В патенте на изобретение чаще всего описан общий принцип. Требуется разработка технической документации, технологии изготовления или использования и собственно изготовление какого-либо устройства, вещества (или применение способа) на основе изобретения, прежде чем объект на основе изобретения можно будет при
менять.
Интеллектуальная собственность
1395
Объем прав на объект интеллектуальной собственности
Для разных объектов интеллектуальной собственности даже в силу различий законодательства объем прав владельца этой собственности будет различным. Например, при получении патента на изобретение приобретаются исключительные права, в том числе и право запрещать кому бы то ни было использование этого изобретения, даже если оно другим лицом создано независимо и добросовестно. Другое дело — право на служебную и коммерческую тайну, о котором мы говорим, когда имеем в виду права на ноу-хау (новую беспатентную технологию, новое вещество и т. д.) Согласно законодательству, никаких исключительных прав при этом не возникает, любое другое лицо, добросовестно создавшее это же ноу-хау, имеет право его использовать.
Отдельная проблема при расчете стоимости заключается в определении доли дохода, которая приходится собственно на использование прав, связанных с объектом интеллектуальной собственности.
9.10.3. Методы оценки рыночной стоимости
Существует достаточно много методик по расчету стоимости тех или иных объектов интеллектуальной собственности. Однако следует принимать во внимание, что никто не может предложить математический точный метод оценки. Применение известных методов следует отнести не столько к науке, сколько к искусству их применения в конкретной ситуации.
Практика применения этих методов в рыночных условиях позволила выделить следующие основные методы.
9.10.3.1. Доходный подход
Доходный подход используется при наличии достаточно полной исходной информации. Доходом является разница между денежными поступлениями и денежными выплатами, рассчитанная за определенный период времени. Доход возникает у того лица, которое будет использовать объект интеллектуальной собственности, например у производителя.
Однако в некоторых случаях, например при уступке объекта интеллектуальной собственности, продаже лицензии, доход будет делиться между покупателем и продавцом, лицензиатом и лицензиаром. О проблемах раздела дохода и лицензионных платежах мы поговорим в 9.10.4 («Цена лицензии»).
Денежные поступления и затраты будут в будущем, да еще в разные годы. А стоимость средств, которые будут получены в будущем, с точки зрения настоящего времени, ниже, чем получаемая сейчас. Поэтому в расчетах применяется общепринятый прием, который позволяет привести денежные поступления и затраты к единому временному сроку, чаще всего настоящему времени. Этот прием называется дисконтированием, а приведение осуществляется с помощью коэффициента дисконтирования.
Инвестиции в производство и другие расходы предполагают не отдельные или единовременные платежи, а некоторую их последовательность во времени. Такие последовательности чаще всего называют потоками платежей.
Определение дохода от применения объекта интеллектуальной собственности тесно связано со стандартной процедурой технико-экономического обоснования инвестиционного проекта. Рассчитываются потоки платежей и затраты, которые приводятся с помощью процедуры дисконтирования к настоящему времени.
В принципе, на этом можно было бы остановиться. Доход определен. Однако, как правило, далее решаются следующие задачи: найти наиболее выгодный вариант использования интеллектуальной собственности или рассчитать платежи лицензиару.
Для решения этих задач могут использоваться следующие показатели:
- дисконтированный период окупаемости (Discounted Payback Period — DPP);
- чистая настоящая (приведенная) стоимость (Net Present Value — NRV);
- индекс прибыльности (Profitability Index — PI);
- внутренняя норма рентабельности (Internal Rate of Return — IRR).
Для расчета этих показателей существуют специальные методики, которых мы не будем касаться, но которые известны экономистам101.
9.10.3.2. Сравнительный подход
Сравнительный подход применяется при наличии достоверной и доступной информации о ценах аналогов объекта оценки и действительных условиях сделок с ними. При этом может использоваться информация о ценах сделок, предложениях и спросе [36]. Сравнительный подход можно рекомендовать для тех объектов интеллектуальной собственности, в которых степень «материальности» достаточно высока, в частности для программ для ЭВМ, произведений литературы, живописи и т. д. Определение рыночной стоимости производится путем введения поправок, учитывающих различие в аналогах, а также учета средней цены, полученной из значений некоторого числа аналогов.
В [37] раскрывается еще один метод, получивший распространение в мире в последнее время.
Он основан на стремлении доверять общим представлениям, интуиции и знаниям бизнесменов. При таком подходе ориентируются на свои ожидания относительно серии продуктов и бизнеса в целом, а не только на влияние отдельной лицензии на сбыт конкретного продукта.
Главная идея — покрыть затраты на исследования и развитие в целом за счет продажи патентов и лицензий.
101 Чтобы более подробно узнать об этих методах, см.
[37-39].
1396
Новый справочник химика и технолога
9.10.3.3. Затратный подход
Очевидно, что понесенные расходы на исследования и разработки неадекватны рыночной цене технологии, но в ряде случаев могут служить отправной точкой для ее определения. Рыночная цена может быть больше стоимости разработки, равна ей и даже меньше ее. Не будем забывать, что разработка продается на рынке, и продажа состоится, если применение разработки будет выгодно, прибыльно для покупателя.
Почему же затратный метод расчета цены лицензии имеет право на существование? Прежде всего потому, что понесенные затраты на создание необходимой обществу технологии в какой-то степени отражают ее стоимость.
Представим себе, что потенциальный покупатель технологии решил не приобретать ее, а создать технологию сам или заказать ее разработку другому лицу. В любом из этих случаев он понесет какие-то затраты и проиграет время. Если эти финансовые затраты (временные затраты также можно пересчитать в финансовые потери) будут больше, чем цена лицензии, рассчитанная лицензиаром на основе своих затрат, т. е. вероятность, что он согласится на предлагаемые условия. Затраты теоретически могут выступать минимальной ценой, допустимой при проведении переговоров о представлении результатов научно-технической деятельности и прав.
Затраты разных разработчиков на одну и ту же технологию могут серьезно различаться в зависимости от условий работы, квалификации, накладных расходов и т. д. Поэтому оценка будущих затрат имеет долю неопределенности.
При затратном методе расчета цена технологии может определяться величиной затрат на проведенные научно-исследовательские и опытно-конструкторские работы, а также на получение патентных прав.
Наиболее приемлем этот метод расчета для случаев, когда речь идет о технологии, нс приносящей прибыли или не дающей экономию. Это может быть, в частности, технология, касающаяся охраны окружающей среды.
Методология расчета с помощью затратного подхода изложена в [36, 38].
9.10.4. Цена лицензии
Выше рассмотрены подходы к определению стоимости интеллектуальной собственности. Рассмотрим некоторые особенности определения собственно цены лицензии как процедуры, в которой участвуют две стороны: продавец — лицензиар и покупатель — лицензиат.
При определении цены лицензии кроме проблем собственно оценки стоимости объекта интеллектуальной собственности существуют следующие специфические проблемы:
- виды платежей, которые выбираются при оплате лицензии;
- раздел прибыли, полученной лицензиатом, между лицензиаром и лицензиатом (если цена лицензии рассчитывается как часть прибыли или дохода).
9.10.4.1. Платежи по лицензионным сделкам
Приняты следующие виды платежей по лицензионным сделкам102:
- фиксированные по размеру (в международной практике их называют паушальные);
- роялти;
- комбинированные платежи — фиксированная часть и роялти.
Фиксированное вознаграждение — фиксированная сумма, не зависящая от прибыли, получаемой лицензиатом при реальном использовании объекта интеллектуальной собственности. Оно может выплачиваться в виде разового платежа, например при заключении договора, вступлении его в силу, передаче ноу-хау и т. д., а также в виде регулярных фиксированных выплат в течение определенного срока.
Роялти (Royalty) — установленная договором доля лицензиара в доходе (прибыли) лицензиата в процентах. Роялти широко применяются при расчетах за приобретение интеллектуальной собственности.
Комбинированные платежи — сочетание фиксированной части платежа и роялти. Какая часть цены лицензии выплачивается в виде фиксированного платежа, а какая — в виде роялти, решается в ходе переговоров.
Особый вид платежей может быть связан с процессом ознакомления будущего лицензиата с сущностью технологии, которую ему необходимо знать для того, чтобы принять решение о покупке. Продаваемая технология достаточно часто включает в себя ноу-хау, которое продавец (лицензиар) опасается раскрыть до заключения соглашения, а покупатель не хочет принимать решение, не ознакомившись с его сущностью. Кроме того, переговоры могут вестись с несколькими покупателями, и один из них хочет иметь приоритетное право на принятие решения, а также время на раздумье. В таких случаях и применяются опционные (предварительные) платежи.
По существу, опционный платеж является платой за риск, т. к. сделка может быть и не заключена, а также оплатой за невступление в переговоры с другими лицами в течение определенного времени.
9.10.4.2. Раздел прибыли между лицензиатом и лицензиаром
В международной практике принято, что доля лицензиара в прибыли лицензиата в зависимости от условий лицензионного соглашения колеблется в пределах 10-30 %. Такое распределение прибыли часто встречается в зарубежных и российских источниках. Нередко называют и более узкие пределы: 25-30 %.
102 Перечисленные виды платежей являются достаточно
универсальными и применяются для сделок со всеми объек-
тами интеллектуальной собственности. Отличие между объ-
ектами патентного права и, в частности, литературными про-
изведениями заключается в нюансах, которые в данной
работе не рассматриваются.
Интеллектуальная собственность
1397
Следует заметить, что в лицензионных договорах чаще всего речь идет о распределении дохода, а не прибыли.
Вышеприведенному диапазону распределения прибыли соответствует диапазон распределения дохода — роялти 1,0-10,0 %.
Роялти могут рассчитываться с помощью методов, основанных на доходном подходе; могут использоваться данные о так называемых средних роялти.
Идея средних роялти основывается на анализе условий лицензионных сделок для различных отраслей промышленности. Известны различные таблицы средних значений роялти, опубликованные в различных источниках и приведенные в [38, 37]. В качестве примера приведем таблицу средних значений, опубликованную еще в советское время Лицензионторгом.
Отрасли Роялти, %
Станкостроительная промышленность 4,5-7,5
Подъемно-транспортное оборудование 4,0-6,0
Автомобильная промышленность 1,0-3,0
Химическое машиностроение 4,0-7,0
Самолетостроение и авиационная техника 6,0-18,0
Оборудование металлургической промышленности 5,0-8,0
Приборостроение и радиоэлектроника промышленного типа 1,5-5,0
Бытовая радиоэлектроника 0,5-3,0
Сварочное оборудование 3,5-5,0
Химическая промышленность 1,0-3,5
Фармацевтическая промышленность 4,0-7,0
Оборудование для текстильной промышленности 3,0-6,0
Производство насосов 2,0-5,0
Нагревательное и холодильное оборудование промышленного типа 4,0-6,0
Конвейеры, строительное оборудование, горнорудное и другое, близкое по назначению оборудование 3,5-6,0
Данная таблица, при всей ограниченности и достаточной давности приведенных в ней сведений, может служить некоторым ориентиром в понимании границ диапазона роялти от дохода в различных отраслях промышленности.
В соответствии с международной практикой размер роялти при беспатентной лицензии уменьшается на 20-30 %.
9.10.5. Нематериальные активы
Понятие нематериальных активов связано с бухгалтерским учетом, который ведется по определенным правилам, прежде всего для правильной уплаты налогов. Бухгалтерскому учету подлежат только те нематериальные активы, которые используются в деятельности предприятия.
Порядок расчета и уплаты налогов определяется Налоговым кодексом [40], а порядок ведения бухгалтерского учета для нематериальных активов — Положением по бухгалтерскому учету «Учет нематериальных активов» [41].
К нематериальным активам в соответствии с Налоговым кодексом [40] относятся приобретенные и (или) созданные налогоплательщиком результаты интеллектуальной деятельности и иные объекты интеллектуальной собственности (исключительные права на них), используемые в производстве продукции (выполнении работ, оказании услуг) или для управленческих нужд организации в течение длительного времени (свыше 12 месяцев). Для признания нематериального актива необходимо наличие способности приносить налогоплательщику экономические выгоды (доход), а также наличие надлежаще оформленных документов, подтверждающих существование самого нематериального актива и (или) исключительного права у налогоплательщика на результаты интеллектуальной деятельности, в том числе патенты, свидетельства, другие охранные документы, договор уступки (приобретения) патента, товарного знака.
В [40] уточняется, какие объекты, в частности, относятся к нематериальным активам:
- исключительное право патентообладателя на изобретение, промышленный образец, полезную модель;
- исключительное право автора или иного правообладателя на использование программы для ЭВМ, базы данных;
- исключительное право автора или иного правообладателя на использование топологии интегральных микросхем;
- исключительное право на товарный знак, знак обслуживания, наименование места происхождения товаров и фирменное наименование;
- исключительное право патентообладателя на селекционные достижения;
- владение «ноу-хау», секретной формулой или процессом, информацией в отношении промышленного, коммерческого или научного опыта.
В соответствии с [40, 41 ] к нематериальным активам не относятся:
- нс давшие положительного результата научно-
исследовательские, опытно-конструкторские и техно-
логические работы;
- незаконченные и не оформленные в установленном
законодательством порядке научно-исследовательские,
опытно-конструкторские и технологические работы;
1398
Новый справочник химика и технолога
- материальные объекты (материальные носители), в которых выражены произведения науки, литературы, искусства, программы для ЭВМ и базы данных;
- интеллектуальные и деловые качества работников организации, их квалификация и способность к труду.
При принятии к бухгалтерскому учету активов в качестве нематериальных необходимо единовременное выполнение следующих условий [41]:
- отсутствие материально-вещественной (физической) структуры (имеется в виду, что речь идет о правах на результаты, а не о материальных носителях);
- возможность идентификации (выделения, отделения) организацией от другого имущества;
- использование в производстве продукции, при выполнении работ или оказании услуг либо для управленческих нужд организации;
- использование в течение длительного времени, т. е. срока полезного использования, продолжительностью свыше 12 месяцев или обычного операционного цикла, если он превышает 12 месяцев;
- организацией не предполагается последующая перепродажа данного имущества;
- способность приносить организации экономические выгоды (доход) в будущем;
- наличие надлежаще оформленных документов, подтверждающих существование самого актива и исключительного права у организации на результаты интеллектуальной деятельности (патенты, свидетельства, другие охранные документы, договор уступки (приобретения) патента, товарного знака и т. п.).
Между списком объектов, отнесенных к нематериальным активам, приведенным в Положении [41], и списком из Налогового кодекса [40] есть существенная разница. В частности, Налоговый кодекс относит ноу-хау к нематериальным активам, а в Положении о бухгалтерском учете упоминаний о ноу-хау нет.
Стоимость оценки нематериальных активов
Нематериальные активы принимаются к бухгалтерскому учету по первоначальной стоимости [41].
Первоначальная стоимость нематериальных активов, приобретенных за плату, определяется как сумма фактических расходов на приобретение.
Первоначальная стоимость нематериальных активов, созданных самой организацией, определяется как сумма фактических расходов на создание, изготовление (израсходованные материальные ресурсы, оплата труда, услуги сторонних организаций по контрагентским (соисполнительским) договорам, патентные пошлины, связанные с получением патентов, свидетельств, и т. п.).
Нематериальные активы считаются созданными при следующих условиях:
- исключительное право на результаты интеллектуальной деятельности, полученные в порядке выполнения служебных обязанностей или по конкретному заданию работодателя, принадлежит организации — работодателю;
- исключительное право на результаты интеллектуальной деятельности, полученные автором (авторами) по договору с заказчиком, не являющимся работодателем, принадлежит организации — заказчику;
- свидетельство на товарный знак или на право пользования наименованием места происхождения товара выдано на имя организации.
Первоначальная стоимость нематериальных активов, внесенных в счет вклада в уставный (складочный) капитал организации, определяется исходя из их денежной оценки, согласованной учредителями (участниками) организации.
Первоначальная стоимость нематериальных активов, полученных организацией по договору дарения (безвозмездно), определяется исходя из их рыночной стоимости на дату принятия к бухгалтерскому учету.
В некоторых случаях, например в бюджетных организациях, нематериальные активы проходят переоценку путем индексации балансовой стоимости объектов с использованием коэффициентов, применяемых для переоценки основных средств и нематериальных активов.
Литература
1. Конституция Российской Федерации.
2. Конвенция об учреждении Всемирной организации интеллектуальной собственности.
3. Фоли Дж. Энциклопедия символов и знаков. М.: Всче*Аст, 1997.
4. Интеллектуальная собственность. Основные материалы. В 2 частях. Новосибирск: Наука, 1993.
5. Ваксберг А.И. Не продается вдохновенье. М.: Книга, 1990.
6. Патентный закон Российской Федерации № 3518-1 (в ред. от 7 февраля 2003 г., № 22-ФЗ).
7. Гражданский кодекс Российской Федерации, Ч. 1 и 2.
8. Правила составления, подачи и рассмотрения заявки на выдачу патента на изобретение. Приказ Роспатента от 6 июня 2003 г., № 82.
9. «О товарных знаках, знаках обслуживания и наименованиях мест происхождения товаров». Закон Российской Федерации № 3520-1.
10. Правила составления, подачи и рассмотрения заявки на регистрацию товарного знака и знака обслуживания. Приказ Роспатента от 5 марта 2003 г., № 32.
11. Парижская конвенция по охране промышленной собственности (в ред. 1979 г.).
12. Договор о патентной кооперации (в ред. 1984 г.).
13. Инструкция к Договору о патентной кооперации.
14. Мадридское соглашение о международной регистрации знаков.
15. Страсбургское соглашение о Международной патентной классификации (МПК).
16. Патентная документация США. М.: ВНИИПИ, 1984.
17. Ненахов Г.С. и др. Патентная документация,
представленная патентными ведомствами и ВОИС
в Интернет. М.: ФИПС, 2000.
Интеллектуальная собственность
1399
18. «Об авторском праве и смежных правах». Закон Российской Федерации № 5351—1(в ред. от 20 июля 2004 г., № 72-ФЗ).
19. «О правовой охране программ для электронных вычислительных машин и баз данных». Закон Российской Федерации №3523-1 от 23 сентября 1992 г. (в ред. от 24 декабря 2002 г., № 177-ФЗ).
20. Гаврилов Э.П. Комментарий к Закону «Об авторском праве и смежных правах». М.: Фонд «Правовая культура», 1996.
21. Сергеев А.П. Право интеллектуальной собственности в Российской Федерации. Учебник. М.: ТК «Вел-би», 2004.
22. Бернская конвенция по охране литературных и художественных произведений.
23. Всемирная конвенция об авторском праве.
24. Конвенция об охране интересов производителей фонограмм от незаконного воспроизведения их фонограмм (Конвенция по фонограммам).
25. Брюссельская конвенция о распространении несущих программы сигналов, передаваемых через спутники (Конвенция по спутникам).
26. «О конкуренции и ограничении монополистической деятельности на товарных рынках». Закон Российской Федерации № 13-1 в ред. от 7 марта 2005 г.
27. Буч Ю.И., Колесникова М.А. Ноу-хау (справочно-методические материалы). Государственный комитет по высшему образованию (Серия «Инновационная деятельность»; Вып. 7). СПб., 1995.
28. «О правовой охране топологий интегральных микросхем». Закон Российской Федерации № 3526 от 23 сентября 1992 г. (в ред. от 09 июля 2002 г., № 82-ФЗ).
29. «О селекционных достижениях». Закон Российской Федерации № 5605-1 от 6 августа 1993 г.
30. Уголовный кодекс Российской Федерации, № 63-ФЗ, от 13 июня 1996 г. (в ред. от 28 декабря 2004 г., № 187-ФЗ).
31. Уголовно-процессуальный кодекс Российской Федерации, № 174-ФЗ, от 18 декабря 2001 г. (в ред. от 28 октября 2004 г., № 187-ФЗ).
32. Кодекс Российской Федерации об административных правонарушениях, № 195-ФЗ, от 30 декабря 2001 г. (в ред. от 28 декабря 2004 г., № 187-ФЗ).
33. Гражданский процессуальный кодекс Российской Федерации, № 138-ФЗ, от 14 ноября 2002 г.
34. «Об оценочной деятельности в Российской Федерации». Закон РФ N 135-ФЗ, от 29 июля 1998 г. (в ред. от 27 февраля 2003 г., № 29-ФЗ).
35. Постановление правительства РФ № 519 от 6 июля 2001 г. «Об утверждении стандартов оценки».
36. Методические рекомендации по определению рыночной стоимости интеллектуальной собственности. Минимущество, 26 ноября 2002 г., № СК-4/21297.
37. Козырев А.Н. Оценка интеллектуальной собственности. М.: Экспертное бюро, 1997.
38. Марков А.М. и др. Определение цены лицензии при реализации прав на объекты интеллектуальной собственности: Информационно-аналитический обзор. Ярославль: Изд-во ЯГТУ, 1999.
39. Козырев А.Н., Макаров В.Л. Оценка стоимости нематериальных активов и интеллектуальной собственности. М.: РИЦ ГШ ВС РФ, 2003.
40. Налоговый кодекс Российской Федерации, Глава 25. 5 августа 2000 года, № 117-ФЗ (в ред. от 24 июля 2002 г., № 110-ФЗ).
41. Положение по бухгалтерскому учету «Учет нематериальных активов». Приказ Минфина от 16 октября 2000 г., № 91 н ПБУ 14/2000.
42. «О коммерческой тайне». Закон Российской Федерации № 98-ФЗ от 29 июля 2004 г.
СОДЕРЖАНИЕ
Раздел 1. Общие сведения......................5
Относительные атомные массы элементов.........5
Таблица 1.2. Фундаментальные физические постоянные....................................8
Международная система единиц СИ.......10
Таблица 1.3. Физические величины и единицы СИ.11
Таблица 1.4. Внесистемные единицы, допускаемые к применению наряду с единицами СИ......18
Таблица 1.5. Соотношения между единицами физических величин....................19
Таблица 1.6. Множители и префиксы, используемые для образования наименований десятичных кратных и дольных единиц измерения физических величин...........................27
Раздел 2. Строение вещества..................28
2.1. Строение элементарных частиц..........28
2.2. Свойства изотопов.....................28
Таблица 2.1. Свойства элементарных частиц....29
Таблица 2.2. Свойства изотопов...............31
2.3. Цепочки распада, периоды полураспада и выходы продуктов деления урана-235 на тепловых нейтронах........................66
2.4. Ядерный магнитный резонанс и некоторые свойства ядер................................80
2.5. Электронные конфигурации атомов.......81
2.6. Энергия ионизации атомов и ионов......81
Таблица 2.3. ЯМР и некоторые свойства ядер...82
Таблица 2.4. Электронные конфигурации атомов..87
Таблица 2.5. Энергии ионизации атомов и ионов.91
2.7. Энергия сродства к электрону..........94
Таблица 2.6. Энергия сродства к электрону атомов и некоторых одноатомных ионов................94
2.8. Рентгено-спектральные свойства элементов....................................95
Таблица 2.7. Энергии связи электрон—ядро.....95
Таблица 2.8. Энергии фотонов для главных К-, L- и Л/-ЛИНИЙ рентгеновского излучения........98
Раздел 3. Физические свойства важнейших веществ.....................................100
3.1. Плотность и сжимаемость жидкостей и газов.....................................100
Таблица 3.1.1. Плотность воды, свободной от воздуха, при 0-30 °C.....................102
Таблица 3.1.2. Плотность воды, свободной от воздуха, при 30-250 °C...................103
Таблица 3.1.3. Плотность, удельный и молярный объемы воды и оксида дейтерия (тяжелой воды) при 0-34 °C...........................103
Таблица 3.1.4. Плотность и удельный объем ртути в зависимости от температуры.................104
Таблица 3.1.5. Плотность абсолютного этанола при 0-39 °C..................................105
Плотность чистых веществ в состоянии жидкости и пара, находящихся в равновесии.............106
Простые вещества и неорганические соединения..106
Органические соединения.......................108
3.2. Термическое расширение твердых тел, жидкостей и газов............................120
Таблица 3.2.1. Линейное расширение металлов и сплавов....................................120
Таблица 3.2.2. Средний коэффициент линейного расширения некоторых материалов..............121
Таблица 3.2.3. Объемное расширение жидкостей.121
3.3. Равновесные температуры и давления (гетерогенные равновесия)....................133
Таблица 3.3.1. Зависимость между давлением, температурой плавления и изменением объема некоторых веществ.....................133
Таблица 3.3.2. Зависимость между давлением, температурой плавления и изменением объема воды..................................136
Температуры кипения или возгонки индивидуальных веществ при различных давлениях....................................137
Простые вещества.............................137
Неорганические соединения....................142
Органические соединения.......................154
Давление пара в зависимости от температуры...227
Таблица 3.3.11. Давление пара простых веществ и неорганических соединений..................228
Таблица 3.3.12. Давление пара органических соединений...................................238
Давление насыщенного пара ртути..............259
Таблица 3.3.13. Давление насыщенного пара
ртути при температуре от 100 до 358 °C.259
Таблица 3.3.14. Давление насыщенного пара
ртути при температуре от 350 до 675 °C.260
Давление насыщенного пара диоксида углерода...260
Таблица 3.3.15. Давление насыщенного пара твердого диоксида углерода...................261
Таблица 3.3.16. Давление насыщенного пара жидкого диоксида углерода.............261
Таблица 3.3.17. Давление насыщенного пара
аммиака.................................... 261
Таблица 3.3.18. Давление насыщенного пара
серы и ее модификаций........................262
Таблица 3.3.19. Давление насыщенного водяного
пара в равновесии с водой....................262
Содержание
1401
Таблица 3.3.20. Давление насыщенного водяного пара в равновесии с переохлажденной водой.................................263
Таблица 3.3.21. Давление насыщенного водяного пара в равновесии со льдом............263
Таблица 3.3.2. Температура кипения воды при высоких давлениях.................263
3.4. Критические величины и константы
Ван-дер-Ваальса.......................264
Таблица 3.4.1. Критические температуры, давления, плотности простых веществ и неорганических соединений..................264
Таблица 3.4.2. Критические температуры, давления, плотности органических соединений............265
Таблица 3.4.3. Константы Ван-дер-Ваальса.....269
3.5. Теплоемкость.........................271
Таблица 3.5.1. Удельная теплоемкость простых веществ и неорганических соединений при температуре 10-298,15 К..................272
Таблица 3.5.2. Удельная теплоемкость простых веществ и неорганических соединений при температуре выше 0 °C....................275
Удельная теплоемкость воды и водяного пара....279
Таблица 3.5.3. Удельная теплоемкость воды и водяного пара при температуре кипения......................................279
Таблица 3.5.4. Удельная теплоемкость воды и водяного пара при температуре 0 500 °C......280
Таблица 3.5.5. Удельная теплоемкость водяного пара при давлении до 20,3 МПа................281
Таблица 3.5.6. Удельная теплоемкость водяного пара при давлении выше 20,3 МПа..............282
Удельная теплоемкость органических соединений.283
Таблица 3.5.7. Удельная теплоемкость органических соединений в твердом состоянии........283
Таблица 3.5.8. Удельная теплоемкость органических соединений в жидком состоянии.........285
Удельная теплоемкость веществ в газообразном состоянии.............................289
Таблица 3.5.9. Удельная теплоемкость веществ в газообразном состоянии..............289
Удельная теплоемкость газов в зависимости от температуры и давления.............291
Таблица 3.5.10. Удельная теплоемкость азота при давлении до 10,1 МПа..............291
Таблица 3.5.11. Удельная теплоемкость азота при давлении выше 20,3 МПа...................291
Таблица 3.5.12. Удельная теплоемкость аммиака при давлении до 2,03 МПа.....................292
Таблица 3.5.13. Удельная теплоемкость аммиака при давлении выше 2,03 МПа...................292
Таблица 3.5.14. Удельная теплоемкость водорода при давлении до 1,01 МПа.....................293
Таблица 3.5.15. Удельная теплоемкость водорода при давлении выше 2,53 МПа............293
Таблица 3.5.16. Удельная теплоемкость диоксида углерода..............................293
Таблица 3.5.17. Удельная теплоемкость кислорода .... 294
Таблица 3.5.18. Удельная теплоемкость метана.294
Таблица 3.5.19. Удельная теплоемкость монооксида углерода при давлении до 1,01 МПа....295
Таблица 3.5.20. Удельная теплоемкость монооксида углерода при давлении выше 2,58 МПа...............................295
Таблица 3.5.21. Удельная теплоемкость хлорметана.... 295
Таблица 3.5.22. Удельная теплоемкость хлорэтана....295
Таблица 3.5.23. Удельная и молярная теплоемкости ртути при постоянном давлении...............295
3.6. Термодинамические свойства...........296
Таблица 3.6.1. Термодинамические показатели.297
Таблица 3.6.2. Термодинамические показатели воды и перегретого водяного пара............338
3.6.1. Термодинамические показатели
органических соединений..............350
Таблица 3.6.3. Термохимические характеристики органических соединений.....................350
3.6.2. Расчет и экспериментальное определение
термохимических характеристик органических соединений..............365
Таблица 3.6.4. Экспериментальные и расчетные термохимические характеристики.......366
Таблица 3.6.5. Экспериментальные и расчетные значения теплотворной способности (теплоты сгорания)..........................405
3.6.3. Термодинамические свойства насыщенных паров чистых веществ.........................424
Таблица 3.6.6. Термодинамические свойства насыщенного пара аммиака.............424
Таблица 3.6.7. Термодинамические свойства насыщенного пара воды................425
Таблица 3.6.8. Термодинамические свойства насыщенного пара диоксида серы.......432
Таблица 3.6.9. Термодинамические свойства насыщенного пара диоксида углерода....432
Таблица 3.6.10. Термодинамические свойства насыщенного пара ртути...............433
Таблица 3.6.11. Термодинамические свойства насыщенного пара дисульфида углерода.........434
Таблица 3.6.12. Термодинамические свойства насыщенного пара метана..............434
Таблица 3.6.13. Термодинамические свойства насыщенного пара пропана.............434
Таблица 3.6.14. Термодинамические свойства насыщенного пара бутана..............435
Таблица 3.6.15. Термодинамические свойства насыщенного пара изобутана...........435
Таблица 3.6.16. Термодинамические свойства насыщенного пара дифтордихлорметана (фреона-12).................................436
Таблица 3.6.17. Термодинамические свойства
насыщенного пара дифторхлорметана
(фреона-22)..................................436
Таблица 3.6.18. Термодинамические свойства
насыщенного пара дихлорметана................437
1402
Содержание
Таблица 3.6.19. Термодинамические свойства насыщенного пара диэтилового эфира....437
Таблица 3.6.20. Термодинамические свойства насыщенного пара 1,1,2-трифтор-1,2,2-трихлорэтана (фреона-113)...................437
Таблица 3.6.21. Термодинамические свойства насыщенного пара грифторхлорметана (фреона-13).................................438
Таблица 3.6.22. Термодинамические свойства насыщенного пара фтортрихлорметана (фреона-11)..........................438
Таблица 3.6.23. Термодинамические свойства насыщенного пара хлорметана..........438
Таблица 3.6.24. Термодинамические свойства насыщенного пара тетрахлорметана.....439
Таблица 3.6.25. Термодинамические свойства насыщенного пара этана...............439
Таблица 3.6.26. Термодинамические свойства насыщенного пара хлорэтана...........440
Таблица 3.6.27. Термодинамические свойства насыщенного пара этилена.............440
3.6.4. Термодинамические функции Дебая для кристаллических веществ.................440
Таблица 3.6.28. Термодинамические функции Дебая................................441
Таблица 3.6.29. Характеристические температуры по Дебаю 0 некоторых простых веществ в кристаллическом состоянии.................442
3.6.5. Термодинамические функции Эйнштейна для линейного гармонического осциллятора.................................442
3.6.6. Эмпирические данные и зависимости для вычисления термодинамических параметров..................................443
3.7. Теплопроводность.....................455
Таблица 3.7.1. Коэффициенты теплопроводности металлов и сплавов...................456
Таблица 3.7.2. Коэффициенты теплопроводности некоторых сталей.....................458
Таблица 3.7.3. Коэффициенты теплопроводности некоторых чистых веществ в твердом состоянии...................................458
Таблица 3.7.4. Коэффициенты теплопроводности термоизоляционных, строительных и некоторых других материалов...............459
Таблица 3.7.5. Коэффициенты теплопроводности некоторых жидкометаллических теплоносителей.......................460
Таблица 3.7.6. Коэффициенты теплопроводности чистых органических жидкостей........461
Таблица 3.7.7. Коэффициенты теплопроводности некоторых хладагентов в жидком состоянии............................463
Таблица 3.7.8. Коэффициенты теплопроводности газов и паров........................463
Таблица 3.7.9. Коэффициенты теплопроводности некоторых газов при различных температурах.... 464
Таблица 3.7.10. Коэффициенты теплопроводности воды и водяного пара...................465
3.8. Электрическая проводимость и числа переноса.......................................466
Таблица 3.8.1. Удельное сопротивление р и температурный коэффициент сопротивления а простых веществ........467
Таблица 3.8.2. Удельное сопротивление р и температурный коэффициент сопротивления а сплавов.......................467
Таблица 3.8.3. Отношение удельных сопротивлений чистых металлов при различных значениях температуры...................................469
Таблица 3.8.4. Удельное сопротивление металлов и сплавов, применяемых в нагревательных устройствах............................471
Таблица 3.8.5. Удельная электрическая проводимость воды......................472
Таблица 3.8.6. Удельная электрическая проводимость жидкостей.................472
Таблица 3.8.7. Удельная электрическая проводимость твердых и расплавленных солей..........474
Таблица 3.8.8. Числа переноса катиона и аниона в твердых солях при различных температурах..................................477
3.9. Диэлектрическая проницаемость........478
Таблица 3.9.1. Диэлектрическая проницаемость газов и паров.................................479
Таблица 3.9.2. Диэлектрическая проницаемость жидкостей..............................481
Таблица 3.9.3. Диэлектрическая проницаемость твердых веществ........................489
3.10. Дипольные моменты некоторых веществ .... 492
Таблица 3.10.1. Дипольные моменты молекул простых веществ и неорганических соединений....................................492
Таблица 3.10.2. Дипольные моменты молекул органических соединений.......................495
Таблица 3.10.3. Дипольные моменты элементоорганических соединений...............503
3.11. Вязкость веществ и растворов.........506
Общие понятия................................506
Теоретические положения......................509
Таблица 3.11.1. Текучесть, вязкость и относительная вязкость воды в интервале температур 0-100 °C...............513
Таблица 3.11.2. Вязкость воды при температуре
выше 100 °C и давлении насыщенного пара при указанной температуре........514
Таблица 3.11.3. Вязкость и кинематическая вязкость воды при различных значениях температуры и давления........................514
Таблица 3.11.4. Относительная вязкость воды
при различных значениях температуры
и давления....................................514
Таблица 3.11.5. Вязкость переохлажденной воды
и окида дейтерия (тяжелой воды)...............515
Содержание
1403
Таблица 3.11.6. Вязкость простых веществ при различных значениях температуры....515
Таблица 3.11.7. Вязкость неорганических соединений при различных значениях температуры..................................516
Таблица 3.11.8. Вязкость некоторых твердых веществ при различных значениях температуры...........................517
Таблица 3.11.9. Вязкость углеводородов при различных значениях температуры....518
Таблица 3.11.10. Вязкость органических соединений...................................521
Таблица 3.11.11. Вязкость некоторых газов при низкой температуре.......................530
Таблица 3.11.12. Вязкость сжиженных газов при различных значениях температуры..........530
Таблица 3.11.13. Вязкость некоторых хладонов.531
Таблица 3.11.14. Вязкость водяного пара в зависимости от давления и температуры......533
Таблица 3.11.15. Вязкость газов и паров при давлении 0,1 МПа и константы Сазерленда для них...........................534
3.12. Поверхностное и межфазное натяжение...536
Таблица 3.12.1. Поверхностное натяжение воды на границе с воздухом........................538
Таблица 3.12.2. Поверхностное натяжение смесей воды и оксида дейтерия (тяжелой воды) на границе с собственным паром при 20 °C ....538
Таблица 3.12.3. Поверхностное натяжение простых веществ..............................538
Таблица 3.12.4. Поверхностное натяжение неорганических соединений.............539
Таблица 3.12.5. Поверхностное натяжение органических соединений...............540
Таблица 3.12.6. Поверхностное натяжение сжиженных газов на границе с собственным паром...................546
Таблица 3.12.7. Межфазное натяжение ртути на границе с водными растворами.......547
Таблица 3.12.8. Межфазное натяжение ртути на границе с органическими жидкостями.........548
Таблица 3.12.9. Межфазное натяжение воды на границе с органическими жидкостями.........548
3.13. Показатели преломления................550
Таблица 3.13.1. Длина волн и обозначения соответствующих линий спектров излучения некоторых стандартных источников...................................550
Таблица 3.13.2. Показатели преломления дистиллированной воды для желтой линии натрия в зависимости от температуры...551
Таблица 3.13.3. Абсолютные показатели преломления газов при нормальных условиях для зеленой линии ртути......551
Таблица 3.13.4. Показатели преломления дистиллированной воды для спектральных линий водорода, гелия и ртути................551
Таблица 3.13.5. Показатели преломления, их температурные коэффициенты и дисперсии органических жидкостей....552
Раздел 4. Ароматические соединения...........557
4.1. Бензол...............................557
4.1.1. Мировой рынок бензола................557
4.1.2. История бензола......................559
4.1.3. Строение бензола.....................561
4.1.4. Получение бензола....................563
4.1.4.1. Источники бензола....................563
4.1.4.2. Деалкилирование гомологов бензола....568
4.1.4.3. Синтез бензола из ацетилена..........569
4.1.4.4. Получение бензола из природного газа.569
4.1.4.5. Лабораторные методы получения
бензола................................569
4.1.5. Физические и химические свойства
бензола................................570
4.1.5.1. Физические свойства бензола..........570
4.1.5.2. Химические свойства бензола..........572
4.1.6. Применение бензола...................579
4.1.6.1. Алкилбензолы.........................580
4.1.6.2. Циклогексан..........................581
4.1.6.3. Малеиновый ангидрид..................582
4.1.6.4. Галогенбензолы.......................582
4.1.6.5. Сульфопроизводные бензола............583
4.1.6.6. Нитропроизводные бензола.............584
4.1.6.7. Ацилпроизводные бензола..............585
4.1.6.8. Продукты пиролиза бензола............585
4.1.7. Промышленные способы получения
основных производных бензола...........587
4.1.7.1. Получение алкилпроизводных бензола...587
4.1.7.2. Гидрирование бензола.................589
4.1.7.3. Окисление бензола....................590
4.1.7.4. Получение хлорпроизводных бензола....591
4.1.7.5. Получение нитропроизводных бензола...592
4.1.7.6. Получение сульфопроизводных бензола.594
4.1.7.7. Хлорметилирование бензола............596
4.1.7.8. Ацилирование бензола.................596
4.1.8. Методы определения бензола...........596
4.1.9. Техника безопасности при работе
с бензолом.............................597
4.1.9.1. Токсические свойства бензола и защита
от отравления..........................597
4.1.9.2. Охрана труда при работе с бензолом...599
4.1.10. Проблемы экологии....................600
Приложение 4.1. О защите от опасности отравления бензолом. Конвенция..............602
4.2. Анилин...............................605
4.2.1. Мировой рынок анилина................605
4.2.2. История анилина....................605
4.2.3. Методы получения анилина............607
4.2.3.1. Восстановление нитробензола........607
4.2.3.2. Аммонолиз фенола...................614
4.2.3.3. Получение анилина из толуола.......616
4.2.3.4. Получение анилина из хлорбензола...617
4.2.3.5. Замещение сульфогруппы аминогруппой....617
1404
Содержание
4.2.4. Физические и химические свойства
анилина..............................617
4.2.4.1. Физические свойства анилина.........617
4.2.4.2. Химические свойства анилина.........620
4.2.5. Применение анилина...................630
4.2.5.1. Полиизоцианаты......................630
4.2.5.2. Химические добавки к полимерам......630
4.2.5.3. Красители на основе анилина.........635
4.2.5.4. Пестициды...........................648
4.2.5.5. Лекарственные вещества..............650
4.2.6. Методы анализа анилина...............654
4.2.7. Техника безопасности и охрана труда
в производстве анилина...............654
4.2.7.1. Токсические свойства анилина и защита
от отравления........................654
4.2.7.2. Охрана труда в производстве анилина.655
4.2.8. Перспективы развития производства
анилина..............................656
Приложение 4.2. Торговые названия некоторых производных анилина, используемых в качестве химических добавок к полимерам.................................657
4.3. Органические красители...............660
4.3.1. Основные понятия.....................660
4.3.2. История красителей...................661
4.3.2.1. Красители растительного и животного происхождения...............................661
4.3.2.2. Первые синтетические красители......661
4.3.3. Теория цветности.....................662
4.3.3.1. Физические основы...................662
4.3.3.2. Энергия возбуждения молекул и цвет..664
4.3.3.3. Ранние химические теории цветности..664
4.3.3.4. Энергетические уровни молекул.......666
4.3.3.5. Основные положения современной теории цветности............................667
Электронные переходы в молекулах углеводородов...............................667
Электронные переходы в молекулах с гетероатомами.............................667
Поляризующие заместители.......................668
Ионизация молекул..............................669
Конкурирующие и перекрещивающиеся сопряженные системы.........................670
Влияние пространственных факторов............672
Комплексообразование с металлами.............673
4.3.4. Классификация и номенклатура
красителей...........................673
4.3.4.1. Химическая классификация............673
4.3.4.2. Техническая классификация...........675
4.3.4.3. Номенклатура........................679
4.3.5. Синтез, строение и свойства красителей.681
4.3.5.1. Азокрасители........................681
Диазотирование...............................682
Азосочетание.................................684
Строение и свойства азокрасителей............687
Химические свойства азокрасителей............687
Моноазокрасители.............................688
Дис- и полиазокрасители.....................689
Дисперсные азокрасители.....................692
Основные и катионные азокрасители...........695
Кислотные азокрасители......................696
Протравные азокрасители.....................699
Кислотные металлсодержащие азокрасители.....703
Прямые азокрасители.........................707
Прямые металлсодержащие азокрасители........717
Активные азокрасители.......................720
Жирорастворимые азокрасители................723
Пигменты....................................723
Азолаки.....................................725
Азокрасители, получаемые на волокне.........725
Меры предосторожности в производстве азокрасителей и азогенов....................731
4.3.5.2. Полиметиновые красители............732
Симметричные полиметиновые красители........732
Несимметричные полиметиновые красители......734
Меры предосторожности в производстве полиметиновых красителей....................735
4.3.5.3. Нитро- и нитрозокрасители..........735
Нитрокрасители..............................736
Нитрозокрасители............................737
Меры предосторожности в производстве нитро- и нитрозокрасителей..................738
4.3.5.4. Арилметановые красители............738
Собственно арилметановые красители..........739
Ксантеновые красители.......................747
Акридиновые красители.......................749
Меры предосторожности в производстве арилметановых красителей....................751
4.3.5.5. Ариламиновые красители.............751
Собственно ариламиновые (хинониминовые) красители...................................751
Оксазиновые красители.......................753
Тиазиновые красители........................754
Диазиновые красители........................758
Меры предосторожности в производстве ариламиновых красителей.....................763
4.3.5.6. Тиазоловые красители...............764
Меры предосторожности в производстве тиазоловых красителей.......................765
4.3.5.7. Индигоидные красители..............765
Бис(индол)индигоиды.........................766
Бис(бензотиофен)индигоиды...................769
Несимметричные индигоидные красители........771
Меры предосторожности в производстве индигоидных красителей......................774
4.3.5.8. Антрахиноновые красители...........774
Г идроксиантрахиноновые (ализариновые) красители...................................775
Аминоантрахиноновые красители...............776
Ациламиноантрахиноновые красители...........785
Антримиды...................................786
Антрахинонилоксадиазоловые красители........791
Меры предосторожности в производстве антрахиноновых красителей...................791
Содержание
1405
4.3.5.9. Антрахиноногетероциклические красители...................................792
Антраазоловые (антрахиноназоловые) красители.792
Нафтоакридиновые (антрахинонопиридоновые или фталоилакридоновые) красители....794
Нафтохиноксалиновые (антрахинонопиразиновые, фталоилхиноксалиновые) красители.....796
Динафтофеназиновые (антрахинонодигидроазиновые) красители............................797
Меры предосторожности в производстве антрахиноногетероциклических красителей...........................798
4.3.5.10. Полициклохиноновые (антроновые) красители....................................798
Красители группы дибензопиренхинона..........799
Красители группы антантрона..................800
Красители группы пирантрона..................800
Красители группы дибензантрона...............801
Красители подгруппы изодибензантрона.........802
Красители группы ацедиантрона................803
Кубозол и....................................803
Меры предосторожности в производстве полициклохиноновых красителей...............804
4.3.5.11. Антроногетероциклические красители.804
Нафтохинолиновые (антрапиридоновые) красители...................................804
Бензоперимидиновые красители.................806
Нафтоиндазолоновые (пиразолантроновые) красители...................................807
Диазапирантреновые красители.................808
Меры предосторожности в производстве антроногетероциклических красителей..........810
4.3.5.12. Периноновые красители..............810
Азафеналевые («фи-дикарбоксимидные) красители...................................810
Диазаинденофеналеновые («фи-ароиленимидазоловые) красители..........811
Кубогены.....................................813
Меры предосторожности в производстве периноновых красителей......................814
4.3.5.13. Макрогетероциклические красители...814
Фталоцианиновые красители....................814
Сопряженные и несопряженные аналоги фталоцианина................................823
Порфирины....................................824
Меры предосторожности в производстве макрогетероциклических красителей...........825
Гексаазациклотетрадециновые красители........825
4.3.5.14. Флуоресцентные (оптические) отбеливатели................................825
Меры предосторожности в производстве оптических отбеливателей....................829
4.3.6. Выпускные формы красителей............829
4.3.7. Очистка сточных вод в производстве
красителей...........................830
Приложение 4.3. Красители, выпускаемые зарубежными странами........................832
Раздел 5. Химия фотографических процессов....837
5.1. История изобретения и этапы развития
галогенсеребряной фотографии.........837
5.2. Фотоматериалы и механизм
действия света.......................845
5.2.1. Схема фотографического процесса
на галогенсеребряных слоях...........845
5.2.2. Строение фотоматериала................846
5.2.3. Схема изготовления фотоматериалов.....848
5.2.4. Основные представления о природе
и механизме образования скрытого фотографического изображения.........849
5.3. Процессы химико-фотографической
обработки светочувствительных материалов...........................851
5.3.1. Процесс проявления и проявляющие
растворы.............................851
5.3.1.1. Проявляющие вещества................852
5.3.1.2. Роль щелочи в проявителе............854
5.3.1.3. Роль сульфита натрия в проявителе...856
5.3.1.4. Антивуалирующие вещества............857
5.3.1.5. Специальные добавки и их роль в проявителе............................... 860
5.3.1.6. Разновидности проявляющих растворов.862
5.3.1.7. Физическое и химическое проявление..866
5.3.1.8. Теория фотографического проявления..868
5.3.1.9. Кинетика процесса проявления эмульсионного слоя..........................875
5.3.2. Процесс фиксирования..................878
5.3.2.1. Химические основы процесса фиксирования и комплексные соединения серебра..........................878
5.3.2.2. Факторы, определяющие скорость процесса фиксирования.......................879
5.3.2.3. Состав и разновидности фиксирующих растворов...................................883
5.3.3. Процесс промывания....................884
5.3.4. Процесс отбеливания...................886
5.4. Цветная фотография....................890
5.4.1. Цветоделение и способы
цветоделительной съемки..............890
5.4.2. Синтез цвета. Аддитивный
и субтрактивный методы...............891
5.4.3. Технические методы цветной
фотографии...........................891
5.4.4. Цветное проявление. Особенности
строения и обработки цветных фотоматериалов.......................892
5.5. Основные химические соединения,
применяемые в фотографии.............899
5.6. Галогенсеребряная и цифровая
фотография...........................910
5.6.1. Галогенсеребряная фотография.........910
5.6.2. Особенности классического
фотографического процесса,
обусловливающие его широкое
применение в науке и технике.........911
1406
Содержание
5.6.2.1. Аккумулирующая способность..........911
5.6.2.2. Спектральная универсальность........911
5.6.2.3. Информационная емкость..............912
5.6.3. Цифровая фотография..................912
5.7. Фотолитография.......................918
5.7.1. Фоторезисты..........................919
5.7.1.1. Светочувствительность фоторезистов..923
5.7.1.2. Спектральная чувствительность
фоторезиста...........................926
5.7.1.3. Разрешающая способность фоторезистов ... 927
5.7.1.4. Кислотостойкость фоторезиста........930
5.7.1.5. Диэлектрические свойства пленок
фоторезистов..........................931
5.7.2. Технологический процесс
фотолитографии........................931
5.7.2.1. Экологические гребования............932
5.7.2.2. Методы нанесения слоя на подложку
фоторезиста...........................933
5.7.2.3. Сушка нанесенного слоя..............934
5.7.2.4. Экспонирование......................934
5.7.2.5. Проявление и окончательная
термообработка слоя...................935
5.7.2.6. Травление...........................939
5.7.2.7. Удаление пленки фоторезиста.........946
5.7.3. Другие виды литографии...............947
5.7.4. Математическое моделирование
фотолитографических процессов.........949
Раздел 6. Современная номенклатура органических
соединений............................955
6.1. Общие сведения о систематической
номенклатуре..........................956
6.1.1. Типы номенклатур.....................956
6.1.2. Типы систематической номенклатуры....956
6.1.3. Заместительная номенклатура..........958
6.1.3.1. Основные понятия....................958
Основа (родоначальная структура).............958
Локант.......................................960
Суффикс......................................960
Префикс......................................962
Иллюстрация основных принципов составления названия на простом примере..................964
6.2. Номенклатура углеводородов...........967
6.2.1. Ациклические углеводороды............967
6.2.1.1. Алканы..............................967
Алкены ......................................968
Алкины ......................................968
Енины .....................................968
Свободные валентности в ациклических углеводородах................................969
6.2.2. Моноциклические алифатические углеводороды.................................970
6.2.3. Моноциклические ароматические углеводороды (производные бензола)........971
6.2.4. Полициклические углеводороды.........971
6.2.4.1. Спираны.............................971
Моноспираны..................................971
Неразветвленные полиспираны..................971
Разветвленные полиспираны....................972
Моноспираны с двумя идентичными полициклическими компонентами................972
Диспираны с идентичными полициклическими компонентами.................................974
Моноспираны с различными компонентами.......974
Неразветвленные полиспиросоединенияс с двумя и более различными компонентами...... 974
Разветвленные полиспираны с одним и более полициклическим компонентом...........974
6.2.4.2. Мостиковые углеводороды (система Байера).............................976
Основные понятия............................976
Карбобициклические мостиковые соединения....976
Карбополициклические мостиковые соединения...................................976
Выбор мостиков..............................977
Нумерация мостиков..........................977
Мостиковые гетероциклы......................980
6.2.5. Конденсированные углеводороды.......981
6.2.5.1. Родоначальные названия.............981
6.2.5.2. Метод конденсирования..............985
6.2.6. Мостиковые конденсированные системы .... 993
6.2.7. Фуллерены...........................995
6.2.7.1. Нумерация атомов в фуллеренах......995
6.2.7.2. Структурно-модифицированные фуллерены....................................996
6.2.7.3. Гомофуллерены......................997
6.2.7.4. Норфуллерены.......................997
6.2.7.5. Секофуллерены......................998
6.2.7.6. Гетерофуллерены....................998
6.2.7.7. Продукты присоединения к фуллеренам, фуллереновые ионы, радикалы и ион-радикалы..............................1000
6.2.7.8. эндо-Замещенные фуллерены.........1002
6.2.7.9. Конденсированные фуллерены........1002
6.2.7.10. Мостиковые фуллерены.............1004
6.2.7.11. Спирофуллерены...................1004
6.3. Номенклатура гетероциклических
соединений..........................1005
6.3.1. Тривиальные названия
гетероциклических соединений........1005
6.3.2. Расширенная система Ганча —Видмана... 1011
6.3.3. Метод конденсирования..............1014
6.3.3.1. Основные принципы метода
конденсирования.....................1014
6.3.3.2. Схема определения основного
компонента конденсированных гетероатомных систем................1017
6.3.4. Гетеромостики.......................1020
6.3.5. «а»-Номенклатура....................1020
6.4. Элементы с переменной валентностью
в органической номенклатуре (Х-обозначения).....................1021
6.5. Циклические соединения со смежными
двойными связями (5-обозначения)....1022
Содержание
1407
6.6. Номенклатура ансамблей...............1023
6.7. Номенклатура фанов...................1025
6.7.1. Компоненты родоначальных
названий фанов.......................1025
6.7.1.1. Упрощенные скелетные названия......1025
6.7.1.2. Неразветвленные ациклические
(моноциклические) упрощенные скелеты.... 1025
6.7.1.3. Полициклические упрощенные скелеты.1026
6.7.1.4. Полициклические упрощенные скелеты
с суператомами в спиро-положениях....1026
6.7.1.5. Амплификационные префиксы..........1026
6.7.1.6. Порядок цитирования амплификационных
префиксов...........................1026
6.7.1.7. Локанты суператома и локанты
присоединения........................1027
6.7.2. Примеры названий и нумерации фанов...1028
6.8. Номенклатура функциональных
производных углеводородов............1030
6.8.1. Галогенпроизводные...................1030
6.8.2. Спирты...............................1030
6.8.3. Фенолы...............................1031
6.8.4. Простые эфиры........................1032
6.8.5. Гидропероксиды и пероксиды...........1033
6.8.6. Альдегиды............................1033
6.8.7. Кетоны...............................1034
6.8.8. Карбоновые кислоты...................1035
6.8.8.1. Замещенные карбоновые кислоты......1039
Гидрокси-, алкокси- и оксокислоты...........1039
6.8.8.2. Производные карбоновых кислот......1041
Соли карбоновых кислот......................1041
Эфиры карбоновых кислот.....................1042
Лактоны.....................................1043
Ангидриды...................................1043
Г алогенангидриды...........................1043
Амиды, лактамы, имиды и гидразиды карбоновых кислот..........................1043
Пероксикислоты..............................1048
Амовые кислоты..............................1048
Имидовые, гидразоновые, гидроксимовые и гидроксамовые кислоты....................1049
Тиокарбоновые кислоты и их производные......1050
Нитрилы и родственные соединения............1055
Амидины.....................................1056
6.9. Азотсодержащие соединения............1057
6.9.1. Амины, имины, гидроксиламины
и оксиды аминов......................1057
6.9.2. Нитро- и нитрозосоединения...........1060
6.9.3. Гидразин и его производные...........1061
6.9.4. Азо- и азоксисоединения..............1062
6.9.5. Диазосоединения и диазониевые соли...1065
6.9.6. Соединения с цепочкой из трех
и более атомов азота.................1065
6.9.7. Другие полиазотистые родоначальные
системы..............................1066
6.10. Серасодержащие соединения............1067
6.10.1. Тиолы...............................1067
6.10.2. Сульфиды и полисульфиды.............1069
6.10.3. Тиоальдегиды, тиокетоны и родственные
соединения (тиоацетали).............1071
6.10.4. Сульфоксиды, сульфоны
и их производные....................1072
6.10.5. Сульфеновые, сульфиновые,
сульфоновые кислоты и их производные... 1074
6.10.6. Сультоны и сультамы................1078
6.11. Фосфорсодержащие соединения........1078
6.11.1. Кислоты фосфора....................1080
6.12. Радикалы и ионы....................1082
6.12.1. Радикалы...........................1082
6.12.1.1. Радикальные центры в родоначальных гидридах....................................1082
6.12.1.2. Двух- и трехвалентные радикальные центры (карбены, карбины, нитрены и силилены).................................1083
6.12.1.3. Радикальные центры на функциональных группах...................1084
Ацильные радикалы..........................1084
Радикальные центры на атоме азота аминной, иминной, амидной или имидной функциональных групп........................1085
Радикальные центры на атоме кислорода кислотной, надкислотной,гидроксильной или гидропероксильной функциональных групп.......................................1085
Радикальные центры на атоме серы тиокислотной, тиольной или дитиогидропероксильной функциональных групп........................1085
6.12.1.4. Полирадикальные центры...........1086
6.12.2. Катионы............................1087
6.12.2.1. Катионы с катионными центрами, получающимися в результате присоединении протонов......................1087
Катионные центры в родоначальных гидридах...1087
Катионные центры на функциональных группах .... 1087
Уронивые ионы и их халькогеновые аналоги....1089
Катионные центры на других функциональных группах..............................1089
6.12.2.2. Катионы с катионными центрами, получающимися при отщеплении гидрид-ионов................................1090
Радикало-функциональные названия............1090
Катионные центры в родоначальных гидридах...1090
6.12.2.3. Катионные центры на функциональных группах.....................................1092
Ациливые ионы...............................1092
Монокатионные центры на атоме азота аминной, иминной, амидной или имидной функциональных групп........................1092
Катионные центры на атоме кислорода кислотной,
надкислотной, гидроксильной или
гидропероксильной функциональных групп ... 1092
Катионные центры на атоме серы тиокислотной,
тиольной или дитиогидропероксильной
функциональных групп........................1092
1408
Содержание
6.12.2.4. Гетероциклические катионы, получающиеся в результате образования дополнительной связи с гетероатомом..........1093
6.12.2.5. Поликатионные центры...............1095
6.12.3. Анионы...............................1096
6.12.3.1. Анионы с анионными центрами, получающимися при отщеплении протонов....................................1096
Радикало-функциональные названия............1096
Анионные центры в родоначальных гидридах....1097
Анионные центры на атомах кислотных
функциональных групп..................1098
Анионные центры на гидроксильных группах и их халькогенных аналогах...........1098
6.12.3.2. Анионы с анионными центрами, получающимися при формальном присоединении гидрид-ионов...................1100
6.12.3.3. Заменительная номенклатура для анионов.................................1100
6.12.3.4. Многозарядные анионные цетры......1100
6.12.4. Катионные и анионные центры в одной структуре...........................1102
6.12.4.1. Цвиттер-ионные соединения с равным числом катионных и анионных центров в одном и том же родоначальном соединении...................................1102
6.12.4.2. Цвиттер-ионные соединения с ионным центром на функциональной группе.............1102
6.12.4.3. Соединения с ионными центрами, находящимися в более чем одной родоначальной структуре......................1102
6.12.5. Радикал-ионы (ион-радикалы)..........1104
6.12.5.1. Радикал-ионы — производные родоначальных гидридов.......................1104
6.12.5.2. Радикал-ионы с центрами на функциональных группах....................1105
Радикал-ионы с центрами на ионных «суффиксных» функциональных группах......................1105
Ионные и радикальные центры в разных родоначальных структурах....................1105
6.13. Построение названий сложных систем (резюме)....................................1106
6.13.1. Выбор главной цепи..................1107
6.13.2. Выбор главного цикла................1107
6.13.3. Нумерация сложного соединения.......1107
6.13.4. Порядок размещения составных частей названия.............................1107
6.14. Изотопно-модифицированные соединения..................................1109
6.15. Стереохимическая номенклатура.......1111
6.16. Номенклатура природных соединений....1121
6.16.1. Углеводы............................1121
6.16.1.1. Альдозы...........................1122
6.16.1.2. Диальдозы.........................1123
6.16.1.3. Кетозы............................1125
6.16.1.4. Кетоальдозы (альдокетозы).........1125
6.16.1.5. Дезоксисахара.....................1125
6.16.1.6. Аминосахара.......................1125
6.16.1.7. Другие замещенные моносахариды.......1125
6.16.1.8. Альдиты..............................1128
6.16.1.9. Кислоты — производные сахаров........1128
6.16.1.10. О-Замещенные производные.........1131
6.16.1.11. Разветвленные сахара.............1131
6.16.1.12. Моносахариды как замещающие [руппы ... 1131
6.16.1.13. Гликозиды и гликозильные соединения.1134
6.16.1.14. Олигосахариды....................1135
Выбор родоначальной структуры..................1135
Олигосахариды без свободных полуацетальных групп.................1135
Олигосахариды со свободными полуацетальными группами.............................1136
6.16.1.15. Полисахариды.....................1136
6.16.2. Циклиты................................1139
6.16.2.1. Относительная конфигурация стереоцентров в циклитах....................1139
6.16.2.2. Абсолютная конфигурация стереоцентров в циклитах....................1141
6.16.2.3. Циклиты с гидроксильными или О-замещенными гидроксильными группами....................................1141
6.16.2.4. Производные инозитов..............1142
6.16.2.5. Производные циклитов..............1142
6.16.3. Аминокислоты и пептиды..............1143
6.16.3.1. Аминокислоты......................1143
Стереохимические обозначения аминокислот....1144
Функциональные производные аминокислот......1144
6.16.3.2. Пептиды...........................1147
Система трехбуквенных обозначений и способы изображения аминокислотных остатков в пептидах.........................1148
Стереообозначения в пептидах................1152
Нумерация атомов пептидной цепи.............1152
Модификация тривиальных названий пептидов...1153
6.16.4. Стероиды............................1154
6.16.4.1. Родоначальные названия............1154
6.16.4.2. Двойные связи в стероидах............1156
6.16.4.3. Алкильные заместители в стероидах....1156
6.16.4.4. Дополнительные кольца внутри стероидного скелета.........................1157
6.16.4.5. Гетероатомы в циклопента[а]фенантреновом скелете.....................................1157
6.16.4.6. Изменение длины боковых цепей и размера циклов............................1158
Префикс «дез» в стероидах...................1158
Префикс «нор» в стероидах...................1158
Префикс «гомо» в стероидах..................1158
Префикс «абео» в стероидах..................1158
Префикс «секо» в стероидах..................1158
6.16.4.7. Витамины группы D.................1162
6.16.5. Терпены и терпеноиды................1163
6.16.5.1. Общие сведения....................1163
6.16.5.2. Каротиноиды.......................1164
Префиксы «нор» и «секо» в каротиноидах.........1164
Префикс «ретро» в каротиноидах.................1164
Содержание
1409
Префикс «апо» в каротиноидах..................1167
Кислородсодержащие каротиноиды................1167
6.16.5.3. Ретиноиды...........................1171
6.16.6. Нуклеозиды, нуклеотиды и нуклеиновые кислоты....................................1172
6.16.6.1. Трехбуквенная система обозначений...1172
6.16.6.2. Однобуквенная система обозначений...1174
6.16.7. Порфирины.............................1175
6.16.7.1. Систематические названия порфиринов.1175
6.16.7.2. Замещенные порфирины................1175
6.16.7.3. Конденсированные порфирины..........1175
6.16.7.4. Порфирины с гетероатомами...........1178
6.16.7.5. Восстановленные порфирины...........1178
6.16.7.6. Тривиальные и полусистематические названия порфиринов........................1178
6.17. Металлорганические соединения.........1181
6.17.1. Заместительная номенклатура металлорганических соединений..............1181
6.17.2. Координационная номенклатура металлорганических соединений переходных металлов........................1182
6.17.2.1. Названия органических лигандов......1182
Лиганды, координированные одной простой
связью металл—углерод.................1182
Лиганды, координированные несколькими простыми связями металл—углерод.....1185
Лиганды, координированные кратной связью углерод—металл......................1186
6.17.2.2. Комплексы с ненасыщенными молекулами или группами (л-комплексы) .... 1186
6.17.2.3. Металлоценовая номенклатура.......1189
Раздел 7. Краткие сведения о технике лабораторных работ.........................1193
7.1. Лабораторная посуда...................1193
7.1.1. Материалы.............................1193
7.1.1.1. Химико-лабораторное стекло...........1193
7.1.1.2. Кварцевое стекло.....................1193
7.1.1.3. Фарфор...............................1193
7.1.1.4. Фторопласты..........................1194
7.1.1.5. Полипропилен.........................1194
7.1.2. Химическая посуда.....................1194
7.1.2.1. Посуда общего назначения.............1194
7.1.2.2. Посуда мерная лабораторная...........1201
7.1.2.3. Посуда из фарфора....................1204
7.1.2.4. Посуда из кварцевого стекла..........1205
7.2. Измерение объема.......................1206
7.2.1. Измерение объема жидкости
с помощью пипеток.....................1206
7.2.2. Установка мениска......................1206
7.3. Измерение массы........................1206
Правила взвешивания...........................1207
7.4. Подготовка посуды для выполнения
аналитических работ...................1207
7.4.1. Химические методы очистки посуды....1207
7.4.2. Мытье паром...........................1208
7.4.2.1. Контроль чистоты посуды..............1208
7.4.2.2. Сушка посуды......................1208
7.5. Работа со шлифами...................1208
Извлечение плотно сидящих пришлифованных стеклянных пробок..........................1209
7.6. Смазки и замазки....................1209
7.6.1. Смазки..............................1209
7.6.2. Замазки.............................1209
7.7. Трубки и пробки.....................1210
7.7.1. Резиновые трубки и пробки...........1210
7.7.2. Корковые пробки.....................1211
7.8. Охлаждающие смеси...................1211
7.9. Поддержание постоянной влажности....1213
7.10. Осушители...........................1214
7.11. Газовые баллоны.....................1214
7.12. Индивидуальные средства защиты......1215
Раздел 8. Основы технологии.................1218
8.1. Технология как особая форма
движения материи.....................1218
8.1.1. Зарождение и развитие технологической
деятельности человека................1218
8.1.2. Техника и технология — две стороны
производственной деятельности людей..1221
8.1.3. Классификация технологий и основные
технологические законы...............1221
8.1.4. Понятийный аппарат технологии........1223
8.1.5. Системное представление технологий...1227
8.2. Анализ технологий....................1229
8.2.1. Основные процессы и методы обработки.1229
8.2.1.1. Процессы и методы химической
технологии...........................1230
8.2.1.2. Процессы и методы, связанные
с переработкой пищевого сырья........1238
8.2.1.3. Машиностроительные процессы
и методы.............................1240
8.2.2. Средства технологического оснащения..1251
8.2.3. Технологические операции и модули....1256
8.2.4. Технологические процессы.............1261
8.2.5. Управление технологическими
процессами...........................1264
8.2.6. Моделирование технологий.............1268
8.3. Проектирование технологий............1273
8.3.1. Основные принципы и общая методика
проектирования.......................1273
8.3.2. Формирование множества вариантов
проектных решений....................1278
8.3.3. Выбор наилучшего проектного решения ... 1284
8.3.4. Принципы автоматизированного
проектирования технологий............1290
8.4. Перспективные направления развития
технологий..........................1292
8.4.1. Ресурсосберегающее направление.......1292
8.4.2. Экология и технология...............1293
8.4.3. Гибкие производственные процессы
и роботизированные производства.....1296
8.4.4. Повышение эффективности существующих
технологических процессов...........1298
1410
Содержание
8.4.5. Технологическое применение новых
физико-технических эффектов..........1299
8.5. Технологические процессы
в окружающем мире....................1300
8.5.1. Информационные технологии............1300
8.5.2. Социальные технологии................1301
8.5.3. Транспортные технологии..............1301
8.5.4. Технологии военного назначения.......1302
8.5.5. Микроэлектронные технологии..........1303
8.5.6. Энергетические технологии............1304
Раздел 9. Интеллектуальная собственность.......1309
9.1. Что такое интеллектуальная
собственность........................1309
9.1.1. Основные понятия.....................1309
9.1.2. Законы Российской Федерации,
определяющие правоотношения в области интеллектуальной собственности, и международные соглашения...........1310
9.1.3. Интеллектуальная собственность как фактор научно-технического прогресса....................................1310
9.1.4. Основные системы защиты результатов творческой деятельности..........1311
9.1.5. История возникновения и развития права на товарный знак, изобретение и произведения авторского права.............1311
9.2. Промышленная собственность...........1313
9.2.1. Патент...............................1313
9.2.1.1. Исключительное право...............1314
9.2.1.2. Приоритет..........................1314
9.2.1.3. Автор..............................1315
9.2.1.4. Патентообладатель..................1315
9.2.1.5. Секретные изобретения..............1316
9.2.1.6. Ограничения исключительного права патентообладателя.....................1316
9.2.1.7. Передача прав, связанных
с изобретением, полезной моделью или промышленным образцом............1317
9.2.2. Изобретение..........................1318
9.2.2.1. Условия патентоспособности.........1318
9.2.2.2. Процесс получения патента на изобретение..............................1322
9.2.2.3. Составление заявки на изобретение..1323
9.2.3. Полезная модель......................1333
9.2.3.1. Условия патентоспособности.........1333
9.2.3.2. Процесс получения патента на полезную модель......................................1333
9.2.3.3. Особенности патента на полезную модель.... 1334
9.2.4. Промышленный образец.................1334
9.2.4.1. Процесс получения патента на промышленный образец.....................1336
9.2.5. Товарный знак, знак обслуживания.....1336
9.2.5.1. Основные положения.................1337
9.2.5.2. Использование товарного знака......1337
9.2.5.3. Исключительные права на товарный знак.1337
9.2.5.4. Виды знаков........................1337
9.2.5.5. Нерегистрируемые обозначения........1338
9.2.5.6. Коллективный товарный знак..........1340
9.2.5.7. Общеизвестные товарные знаки........1341
9.2.5.8. Регистрация товарного знака.........1341
9.2.6. Наименование места происхождения
товара................................1341
9.2.7. Охрана промышленной собственности
за рубежом............................1343
9.2.7.1. Парижская конвенция по охране
промышленной собственности............1343
9.2.7.2. Патентование изобретений за рубежом.1346
9.2.7.3. Охрана промышленных образцов
за рубежом............................1349
9.2.7.4. Охрана товарных знаков за рубежом...1350
9.2.8. Патентная информация и патентные
исследования..........................1350
9.2.8.1. Источники патентной информации......1350
9.2.8.2. Международная патентная
классификация (МПК) (International Patent Classification — «Int.Cl.»)...........1351
9.2.8.3. Проведение патентных исследований...1352
9.2.8.4. Поиск и отбор патентной и научно-
технической информации................1355
9.3. Авторское право и смежные права......1363
9.3.1. Основные положения авторского права..1363
9.3.2. Имущественные и неимущественные
права.................................1365
9.3.2.1. Авторское право на служебные
произведения..........................1365
9.3.2.2. Личные неимущественные права........1365
9.3.2.3. Имущественные права.................1366
9.3.2.4. Воспроизведение произведения
в личных целях........................1367
9.3.2.5. Ограничения исключительных прав.....1367
9.3.2.6. Срок действия авторского права
и наследование прав...................1367
9.3.2.7. Передача имущественных прав.........1367
9.3.3. Авторское право на произведения
науки и техники.......................1368
9.3.4. Охрана программ для ЭВМ, баз данных
и компьютерных произведений авторским правом......................1369
9.3.4.1. Особенности охраны программ
для ЭВМ и баз данных..................1369
9.3.4.2. Программы и базы данных в процессе
их создания и использования...........1370
9.3.4.3. Компьютерные произведения...........1371
9.3.5. Смежные права........................1371
9.3.5.1. Коллективное управление имущественными
вторскими и смежными правами..........1372
9.3.6. Защита авторских и смежных прав......1372
9.3.7. Охрана авторских и смежных прав
за рубежом............................1372
9.4. Служебная и коммерческая тайна (ноу-хау).... 1373
9.4.1. Служебная и коммерческая тайна
и интеллектуальная собственность......1373
9.5. Топология интегральных микросхем.....1374
Содержание
1411
9.6. Селекционные достижения..............1374
9.7. Недобросовестная конкуренция.........1375
9.8. Интеллектуальная собственность
в деятельности предприятия..........1375
9.8.1. Политика в области интеллектуальной
собственности........................1375
9.8.2. Стимулирование творческой
деятельности.........................1376
9.8.3. Договорные отношения в области
интеллектуальной собственности.......1378
9.8.3.1. Договорное регулирование, связанное
с созданием интеллектуальной собственности........................1378
9.8.3.2. Договорное регулирование, связанное
с реализацией прав...................1380
9.8.4. Осуществление проектов, правовая
охрана результатов...................1384
9.9. Защита прав на интеллектуальную
собственность........................1386
9.9.1. Рассмотрение протестов и споров
в Палате по патентным спорам.........1387
9.9.2. Гражданское право....................1387
9.9.2.1. Патентное право....................1387
9.9.2.2. Товарные знаки и наименования
мест происхождения товаров...........1387
9.9.2.3. Авторское право....................1388
9.9.2.4. Служебная и коммерческая тайна.....1388
9.9.2.5. Топология интегральных микросхем...1389
9.9.2.6. Селекционные достижения............1389
9.9.3. Уголовное право......................1389
9.9.4. Административное право...............1389
9.9.5. Практика защиты прав на интеллектуальную собственность...........1390
9.10. Стоимость интеллектуальной собственности...............................1392
9.10.1. Процесс оценки......................1392
9.10.2. Рыночная стоимость интеллектуальной собственности...............................1393
Факторы, влияющие на стоимость объекта в наибольшей степени........................1394
9.10.3. Методы оценки рыночной стоимости....1395
9.10.3.1. Доходный подход...................1395
9.10.3.2. Сравнительный подход..............1395
9.10.3.3. Затратный подход..................1396
9.10.4. Цена лицензии.......................1396
9.10.4.1. Платежи по лицензионным сделкам...1396
9.10.4.2. Раздел прибыли между лицензиатом и лицензиаром...............................1396
9.10.5. Нематериальные активы...............1397
ОГЛАВЛЕНИЕ «НОВОГО СПРАВОЧНИКА ХИМИКА И ТЕХНОЛОГА» В 11 ТОМАХ
ОСНОВНЫЕ СВОЙСТВА НЕОРГАНИЧЕСКИХ, ОРГАНИЧЕСКИХ И ЭЛЕМЕНТООРГАНИЧЕСКИХ СОЕДИНЕНИЙ (Красный)
Раздел 1. Неорганические соединения
1. Основы номенклатуры неорганических и в том числе координационных соединений...5
1.1. Номенклатурные правила построения
формул и названий неорганических соединений.............................5
1.1.1. Химические элементы....................5
1.1.2. Простые вещества.......................6
1.1.3. Ионы...................................6
1.1.4. Формулы и названия сложных веществ.....7
1.1.5. Бинарные соединения....................9
1.1.6. Гидроксиды............................12
1.1.7. Кислоты...............................12
1.1.8. Соли..................................15
1.1.9. Наиболее распространенные
ретро- и вненоменклатурные названия некоторых неорганических соединений...17
1.2. Номенклатурные правила построения
формул и названий комплексных (координационных) соединений..........19
1.2.1. Названия лигандов координационных соединений...................................19
1.2.2. Формулы комплексных (координационных) соединений.................20
1.2.3. Одноядерные комплексные соединения....21
1.2.4. Многоядерные комплексные (координационные) соединения.................21
1.3. Аддукты, бертоллиды и полиморфные
модификации сложных веществ...........22
1.3.1. Аддукты...............................22
1.3.2. Бертоллиды............................22
1.3.3. Полиморфные модификации сложных веществ..............................23
2. Свойства неорганических и координационных
соединений. Пояснения к таблице.......23
Свойства неорганических и координационных соединений. Принятые сокращения..............25
Таблица неорганических и координационных соединений...................................25
Раздел 2. Органические соединения
1. Классификация и номенклатура
органических соединений..............361
1.1. Классификация........................361
1.2. Номенклатура.........................362
1.2.1. Общие положения систематической
номенклатуры.........................363
1.3. Заместительная номенклатура..........364
1.3.1. Построение названий
органических соединений..............367
1.4. Радикало-функциональная номенклатура.369
1.5. Аддитивная номенклатура..............369
1.6. Субтрактивная номенклатура...........369
1.7. Конъюнктивная (объединительная)
номенклатура.........................369
1.8. Заменительная номенклатура...........370
2. Номенклатура наиболее распространенных
классов и рядов органических соединений... 370
2.1. Углеводороды.........................370
2.1.1. Ациклические углеводороды............370
2.1.2. Моноциклические углеводороды.........375
2.1.3. Конденсированные полициклические
углеводороды.........................378
2.1.4. Мостиковые углеводороды..............386
2.1.5. Спироуглеводороды....................390
2.1.6. Ансамбли углеводородных колец........392
2.1.7. Циклические углеводороды
с боковыми цепями....................394
2.1.8. Терпеновые углеводороды..............395
2.2. Гетероциклы..........................398
2.2.1. Тривиальные и полутривиальные
названия.............................400
2.2.2. Конденсированные гетероциклические
системы..............................404
2.2.3. Гетероциклические спиросоединення....408
2.3. Галогенпроизводные...................409
2.4. Спирты и фенолы......................409
2.5. Простые эфиры........................409
2.6. Кислоты и их производные.............410
2.7. Нитрилы и их производные.............411
2.8. Альдегиды............................412
2.9. Кетоны...............................412
2.10. Амины................................413
2.11. Соединения, содержащие серу..........413
3. Номенклатура стереоизомеров..........414
3.1. Правило последовательности...........414
3.2. Энантиомеры..........................416
3.3. Диастереомеры........................417
3.4. Конформеры...........................417
4. Свойства органических соединений.
Пояснения к таблице..................418
Свойства органических соединений. Принятые сокращения..........................420
Таблица органических соединений.............420
Раздел 3. Элементоорганические соединения
1. Основы номенклатуры
элементоорганических соединений......1135
1.1. Номенклатура основных классов
кремнийорганических соединений.......1135
Оглавление
1413
1.2. Номенклатура основных органических
соединений фосфора...................1136
2. Свойства элементоорганических соединений.
Пояснения к таблице..................1137
Принятые сокращения.........................1138
Таблица элементоорганических соединений.......1139
Фосфорорганические соединения.................1139
Мышьяк-, сурьма- и висмуторганические соединения..................................1178
Кремнийорганические соединения................1182
Гсрманийорганические соединения.............1216
Олово- и свинецорганические соединения........1225
Бор- и алюминийорганические соединения........1228
Формульный указатель к таблице «Свойства органических соединений».............1232
Формульный указатель к таблице «Свойства элементоорганических соединений».....1245
Указатель синонимов к таблице «Свойства органических соединений»....1250
Указатель синонимов к таблице «Свойства элсментоорганических соединений».....1268
ХИМИЧЕСКОЕ РАВНОВЕСИЕ. СВОЙСТВА РАСТВОРОВ (Сиреневый)
Раздел 1. Гомогенное химическое равновесие
1.1. Химическое равновесие в газовой фазе......5
1.1.1. Константы диссоциации двухатомных
молекул...................................9
Таблица 1.1.1. Диссоциация водорода, кислорода и азота .....................................9
Таблица 1.1.2. Диссоциация водорода при Р > 1 атм... 10
Таблица 1.1.3. Диссоциация водорода при Р < 1 атм... 10
Таблица 1.1.4. Диссоциация D2, HD, Т2, НТ и DT.11
Таблица 1.1.5. Диссоциация кислорода при Р > 1 атм 11
Таблица 1.1.6. Диссоциация фтора, хлора, брома и иода................................12
Таблица 1.1.7. Диссоциация C1F, BrF, FI, BrCl, СП
и BrI ...................................13
Таблица 1.1.8. Диссоциация галогенов©дородов
по схеме HHal Н + Hal....................13
Таблица 1.1.9. Диссоциация галогеноводородов
по схеме HHal 0,5Н2 + 0,5На12............14
Таблица 1.1.10. Диссоциация галогенидов дейтерия.16
Таблица 1.1.11. Диссоциация галогенидов трития .16
Таблица 1.1.12. Диссоциация серы...............17
Таблица 1.1.13. Диссоциация монооксида серы....17
Таблица 1.1.14. Диссоциация монооксида азота...17
Таблица 1.1.15. Диссоциация фосфора.............18
Таблица 1.1.16. Диссоциация монооксида
углерода................................18
Таблица 1.1.17. Диссоциация фторидов лития, натрия и калия........................18
Таблица 1.1.18. Диссоциация хлоридов лития, натрия и калия ............................ 19
Таблица 1.1.19. Диссоциация ВеО, MgO, CaO, SrO и ВаО ................................19
Таблица 1.1.20. Диссоциация BeN, MgN, BN и AIN...20
Таблица 1.1.21. Диссоциация радикалов ОН, OD
и ОТ.....................................21
1.1.2. Константы равновесия реакций между неорганическими соединениями............21
Таблица 1.1.22. Диссоциация водяного пара.......21
Таблица 1.1.23. Диссоциация водяного пара при Р > 1....22
Таблица 1.1.24. Диссоциация воды, оксида дейтерия и оксида трития...............................22
Таблица 1.1.25. Диссоциация пероксида водорода и пероксида дейтерия..........................23
Таблица 1.1.26. Диссоциация диоксида углерода...23
Таблица 1.1.27. Образование монооксида углерода.24
Таблица 1.1.28. Синтез аммиака..................24
Таблица 1.1.29. Влияние избытка реагентов и присутствия в газовой смеси инертных газов на выход аммиака при Р = 200 атм и Т = 500 °C .................................25
Таблица 1.1.30. Реальные значения Кр для реакции синтеза аммиака...............................25
Таблица 1.1.31. Окисление аммиака...............26
Таблица 1.1.32. Диссоциация аммиака и гидразина.26
Таблица 1.1.33. Образование оксида азота(П).....26
Таблица 1.1.34. Образование и диссоциация оксида азота(1)...............................27
Таблица 1.1.35. Диссоциация оксида азота(1У)....27
Таблица 1.1.36. Диссоциация озона...............28
Таблица 1.1.37. Диссоциация моносульфана........28
Таблица 1.1.38. Диссоциация диоксида серы.......28
Таблица 1.1.39. Диссоциация триоксида серы......28
Таблица 1.1.40. Диссоциация фторидов серы.......29
Таблица 1.1.41. Диссоциация дисульфида углерода.... 29
Таблица 1.1.42. Диссоциация галогенидов фосфора.... 30
Таблица 1.1.43. Диссоциация CF4, СС14 и СВг4....30
Таблица 1.1.44. Диссоциация оксидов лития, бора и циркония........................31
Таблица 1.1.45. Диссоциация фторидов и хлоридов бериллия и магния......................31
Таблица 1.1.46. Диссоциация галогенидов бора и алюминия.............................32
1.1.3. Константы равновесия реакций с участием органических соединений.......................32
Таблица 1.1.47. Образование метана из оксида углерода и водорода....................32
Таблица 1.1.48. Расщепление предельных углеводородов на соответствующий олефин и водород..............................33
Таблица 1.1.49. Расщепление предельных углеводородов на низший предельный углеводород и олефин..........................34
Таблица 1.1.50. Расщепление предельных углеводородов на две молекулы олефина и водород..............................34
Таблица 1.1.51. Образование ацетилена и водорода из метана или этана....................35
Таблица 1.1.52. Образование высшего предельного
углеводорода и водорода из двух молекул
низшего предельного углеводорода.............35
Таблица 1.1.53. Образование высшего и низшего
предельных углеводородов из двух молекул
«промежуточного» предельного
углеводорода.................................36
1414
Новый справочник химика и технолога
Таблица 1.1.54. Отщепление водорода от этилена, пропена, бут-1-ена и пент-1-ена................
Таблица 1.1.55. Образование и разложение циклогексана и бут-1,3-диена...................
Таблица 1.1.56. Расщепление бутенов и изобутилена на две молекулы этилена........................
Таблица 1.1.57. Расщепление олефина на две молекулы низшего олефина.......................
Таблица 1.1.58. Изомеризация бутанов и пентанов.
Таблица 1.1.59. Образование ароматических углеводородов из нормальных предельных углеводородов..................................
Таблица 1.1.60. Образование ароматических углеводородов из ацетилена или пропина.........
Таблица 1.1.61. Образование бензола из изомеров гексана........................................
Таблица 1.1.62. Образование алкилбензолов из бензола и олефинов..........................
Таблица 1.1.63. Изомеризация этилбензола........
Таблица 1.1.64. Образование метанола через формальдегид...................................
Таблица 1.1.65. Образование метанола и метилформиата................................
Таблица 1.1.66. Диссоциация этилового спирта на уксусный альдегид и водород.................
Таблица 1.1.67. Кето-енольное равновесие в газовой фазе этилацетоацетата(1), этил-3-оксо-2-хлорбутаноата(П) и этил-2-бром-З-оксобутаноата(Ш) ..............................
1.1.4. о/77ио-иа/?а-Равновесия..................
Таблица 1.1.68. орто-пара-Равновесия Н2, D2, Т2.
1.1.5. Константы равновесия реакций изотопного обмена..............................
Таблица 1.1.69. Обменные реакции изотопов водорода.......................................
Таблица 1.1.70. Реакции обмена между изотопно модифицированными водой и водородом....................................
Таблица 1.1.71. Реакции обмена между галогенидами водорода и трития.................
Таблица 1.1.72. Реакции обмена между водородом и галогенидами трития .........................
Таблица 1.1.73. Реакции обмена между водой и галогенидами трития..........................
1.1.6. Ионные равновесия в газовой фазе.................................
Таблица 1.1.74. Ионы водорода, кислорода и азота........................................
Таблица 1.1.75. Ионы лития, натрия, калия, рубидия и цезия................................
Таблица 1.1.76. Ионы магния, кальция, стронция и бария .......................................
Таблица 1.1.77. Фторид-, хлорид-, бромид-и иодид-ионы...................................
Таблица 1.1.78. Ион ОН-.........................
Таблица 1.1.79. Ионы ОН+, NO+, СО+..............
1.2. Химическое равновесие в жидкой фазе......
1.2.1. Константы диссоциации кислот
и оснований..............................
36
37
39
39
40
40
41
41
41
42
42
43
43
43
44
44
44
.44
.45
46
47
48
49
.49
.49
.50
.50 .51
.51
.51
.51
Таблица 1.2.1. Константы диссоциации неорганических кислот и оснований в водных растворах.....................52
Таблица 1.2.2. Константы диссоциации органических кислот и оснований в водных растворах..........57
Таблица 1.2.3. Зависимость констант кислотности некоторых кислот в водных растворах от температуры...................................87
Таблица 1.2.4. Интервалы значений рКа для органических соединений различных классов в водных растворах....................88
Таблица 1.2.5. Константа диссоциации воды при различных температурах.............89
Таблица 1.2.6. Влияние давления на диссоциацию воды...................................89
Таблица 1.2.7. Константы диссоциации кислот в смешанных растворителях..............89
Таблица 1.2.8. Константы диссоциации кислот в неводных растворителях ..............93
Таблица 1.2.9. Константы диссоциации оснований в неводных растворителях...............95
Таблица 1.2.10. Величины рК для солей в неводных растворителях..........................96
Таблица 1.2.11. Функции кислотности для растворов кислот........................................97
1.2.2. Константы устойчивости комплексных
ионов..................................98
Таблица 1.2.12. Константы устойчивости комплексных ионов в водных растворах..........98
1.2.3. Буферные растворы......................165
Таблица 1.2.13. Величины pH стандартных буферных растворов, рекомендованных ИЮПАК в 1980 г........................165
Таблица 1.2.14. pH образцовых буферных растворов при температурах 0-95 °C..............166
Таблица 1.2.15. Буферные растворы с pH 1,10-3,50 .. 167
Таблица 1.2.16. Буферные растворы с pH 1,10—4,96 .. 168
Таблица 1.2.17. Буферные растворы с pH 2,20-3,80 .. 169
Таблица 1.2.18. Буферные растворы с pH 4,00-6,20 .. 169
Таблица 1.2.19. Буферные растворы с pH 4,96-6,69 .. 170
Таблица 1.2.20. Буферные растворы с pH 4,80-8,00 .. 170
Таблица 1.2.21. Буферные растворы с pH 7,71-9,23 .. 171
Таблица 1.2.22. Буферные растворы с pH 9,23-11,02...............................171
Таблица 1.2.23. Буферные растворы с pH 8,53-12,90...............................172
Таблица 1.2.24. Уксусно-ацетатные буферные растворы......................................173
Таблица 1.2.25. Универсальная буферная смесь..173
Таблица 1.2.26. Буферные растворы из индивидуальных веществ.....................173
Раздел 2. Гетерогенное химическое равновесие
2.1. Равновесие
«жидкость—твердое вещество»...........175
2.1.1. Растворимость неорганических веществ
в воде................................176
2.1.1.1. Двойные системы......................176
Таблица 2.1.1. Двойные системы................177
2.1.1.2. Произведение растворимости...........278
Оглавление
1415
Таблица 2.1.2. Произведения растворимости.....279
2.1.1.3. Термодинамические (истинные) произведения растворимости....................343
Таблица 2.1.3. Термодинамические произведения растворимости.........................343
2.1.1.4. Понижение температуры замерзания водных растворов неорганических и некоторых органических соединений......................382
Таблица 2.1.4. Понижение температуры замерзания водных растворов неорганических соединений...................................383
Таблица 2.1.5. Максимальное понижение температуры замерзания водных растворов неорганических веществ.......................393
Таблица 2.1.6. Понижение температуры замерзания водных растворов органических соединений...................................395
2.1.2. Растворимость неорганических соединений в смешанных и неводных растворителях..........396
Таблица 2.1.7. Растворимость неорганических соединений в тяжелой воде при различных температурах..........................397
Таблица 2.1.8. Растворимость неорганических соединений в тяжелой воде при 5,0 °C...398
Таблица 2.1.9. Растворимость неорганических соединений в тяжелой воде при 25,0 °C.........399
Таблица 2.1.10. Растворимость неорганических соединений в пероксиде водорода.......399
Таблица 2.1.11. Растворимость щелочных и щелочноземельных металлов в аммиаке ...400
Таблица 2.1.12. Растворимость неорганических соединений в аммиаке..................400
Таблица 2.1.13. Растворимость неорганических соединений в аммиаке (доп. данные)....402
Таблица 2.1.14. Растворимость иодида калия в диоксиде серы при различных температурах..........................403
Таблица 2.1.15. Растворимость неорганических соединений в диоксиде серы при 0 °C...403
Таблица 2.1.16. Растворимость неорганических соединений в диоксиде серы при 25 °C...404
Таблица 2.1.17. Растворимость неорганических соединений в метаноле........................404
Таблица 2.1.18. Растворимость неорганических соединений в смесях метанол—вода......409
Таблица 2.1.19. Растворимость неорганических соединений в этаноле..................410
Таблица 2.1.20. Растворимость неорганических соединений в смесях этанол—вода.......415
Таблица 2.1.21. Растворимость неорганических соединений в ацетоне..................419
Таблица 2.1.22. Растворимость неорганических соединений в глицерине................420
Таблица 2.1.23. Растворимость неорганических соединений в диэтиловом эфире.........421
Таблица 2.1.24. Растворимость неорганических соединений в пиридине.................421
Таблица 2.1.25. Растворимость неорганических соединений в бензоле..................422
Таблица 2.1.26. Растворимость дииода в неводных и смешанных растворителях.....................422
Таблица 2.1.27. Растворимость дииода в водных растворах кислот и солей при 25,0 °C...423
Таблица 2.1.28. Растворимость ромбической серы в органических растворителях..................424
Таблица 2.1.29. Растворимость ромбической серы в водных растворах гидроксидов при 18-20 °C..................................425
Таблица 2.1.30. Растворимость ромбической серы в водном растворе сульфида натрия......425
Таблица 2.1.31. Растворимость белого фосфора в различных растворителях..............425
Таблица 2.1.32. Растворимость низших фуллеренов
Сбо и С70 в различных растворителях при 25,0 °C............................426
Таблица 2.1.33. Ориентировочная растворимость некоторых металлов в ртути при 18-20 °C..................................426
Таблица 2.1.34. Растворимость воды в галогензамещенных углеводородах.............426
2.1.3. Растворимость органических соединений.427
Таблица 2.1.35. Растворимость органических соединений в воде......................427
Таблица 2.1.36. Растворимость органических жидкостей и солей......................430
Таблица 2.1.37. Растворимость органических соединений в глицерине.................431
Таблица 2.1.38. Растворимость сахарозы в водных растворах различных солей..............432
Таблица 2.1.39. Растворимость сахарозы в водных растворах этанола.............................432
2.1.4. Равновесия в расплавах................433
Таблица 2.1.40. Равновесие в расплавах........433
2.2. Равновесие «газ—жидкость».............436
2.2.1. Растворимость газов в воде............437
Таблица 2.2.1. Растворимость газов в воде при различных температурах........................437
Таблица 2.2.2. Растворимость диазота в воде...438
Таблица 2.2.3. Растворимость диоксида углерода в воде.................................438
Таблица 2.2.4. Растворимость диводорода в воде.438
Таблица 2.2.5. Растворимость аммиака в воде....439
2.2.2. Растворимость газов в различных жидкостях.....................................439
Таблица 2.2.6. Растворимость газов в водных растворах неорганических веществ.......439
Таблица 2.2.7. Растворимость газов в концентрированных растворах хлорида натрия........................................441
Таблица 2.2.8. Растворимость газообразного диоксида серы в растворах серной кислоты и в олеуме....................................441
Таблица 2.2.9. Растворимость хлороводорода
в концентрированных растворах серной
кислоты......................................442
Таблица 2.2.10. Растворимость газов в органических
жидкостях....................................442
2.2.3. Растворимость газов в сжиженных газах..444
1416
Новый справочник химика и технолога
Таблица 2.2.11. Взаимная растворимость сжиженных газов и состав равновесных фаз..............444
Таблица 2.2.12. Растворимость твердых веществ, являющихся при нормальных условиях газами, в жидком кислороде и азоте..........454
2.2.4. Давление пара над растворами.........455
Таблица 2.2.13. Давление пара над растворами неорганических кислот.......................455
Таблица 2.2.14. Давление пара над водными растворами щелочей..........................462
Таблица 2.2.15.. Давление пара над водными растворами солей............................465
Таблица 2.2.16. Понижение давления пара над водными растворами неорганических соединений...........................467
Таблица 2.2.17. Давление пара над водными растворами органических соединений....470
2.2.5. Состав пара и температуры кипения растворов....................................472
Таблица 2.2.18. Температуры кипения растворов серной кислоты.......................472
Таблица 2.2.19. Состав пара водных растворов бромоводорода...............................472
Таблица 2.2.20. Температура кипения олеума..472
Таблица 2.2.21. Температуры кипения водных растворов НС1, НВг и HNO3...................473
Таблица 2.2.22. Температуры кипения и состав пара водных растворов фтороводорода.......473
Таблица 2.2.23. Температуры кипения и состав пара водных растворов азотной кислоты.....473
Таблица 2.2.24. Температуры кипения двойной системы H2SO4—HNO3...................473
Таблица 2.2.25. Состав пара водных растворов аммиака..............................473
Таблица 2.2.26. Температуры кипения водных растворов солей заданных концентраций........474
Таблица 2.2.27. Повышение температуры кипения водных растворов неорганических и некоторых органических соединений....475
Таблица 2.2.28. Температуры кипения и состав пара некоторых двойных систем.............480
Таблица 2.2.29. Концентрации водных растворов электролитов, отвечающие заданным температурам кипения.................486
2.2.6. Азеотропные растворы..................487
Таблица 2.2.30. Двухкомпонентные азеотропные растворы, содержащие воду............487
Таблица 2.2.31. Двухкомпонентные азеотропные растворы, не содержащие воды.........496
Таблица 2.2.32. Трехкомпонентные азеотропные растворы.............................593
Таблица 2.2.33. Четырехкомпонентные азеотропные растворы.............................603
2.3. Равновесие «твердое вещество—газ».....604
Таблица 2.3.1. Давление диссоциации оксидов металлов....................................604
Таблица 2.3.2. Давление диссоциации сульфидов металлов.............................605
Таблица 2.3.3. Давление диссоциации фосфидов металлов.............................605
Таблица 2.3.4. Давление диссоциации гидридов металлов.................................. 606
Таблица 2.3.5.. Давление диссоциации некоторых солей.......................................607
Таблица 2.3.6. Давление диссоциации карбонатов.607
2.4. Равновесие «жидкость—жидкость».........608
2.4.1. Взаимная растворимость двух жидкостей..............................608
Таблица 2.4.1. Взаимная растворимость двух жидкостей...................................609
2.4.2. Распределение веществ между двумя жидкими фазами..............................621
Таблица 2.4.2. Распределение веществ между двумя жидкими фазами при указанных температурах................................624
2.5. Криоскопические и эбулиоскопические постоянные..................................629
2.5.1. Криоскопические постоянные.............629
Таблица 2.5.1. Неорганические соединения.......630
Таблица 2.5.2. Органические соединения.........631
2.5.2. Эбулиоскопические постоянные...........635
Таблица 2.5.3. Неорганические соединения.......635
Таблица 2.5.4. Органические соединения.........635
Раздел 3. Свойства гомогенных жидких растворов
3.1. Плотность растворов....................639
3.1.1. Плотность водных растворов неорганических соединений и солей органических кислот.... 640
Таблица 3.1. Плотность водных растворов неорганических соединений и солей органических кислот (Таблицы 3.1.1-3.1.319)......................640
3.1.2. Плотность водных растворов органических соединений (Таблицы 3.1.320-3.1.338).........723
3.1.3. Практические шкалы плотности жидкостей (ареометрические шкалы) (Таблица 3.1.339)...........................752
3.1.4. Расчет плотностей при использовании полукубических аппроксимационных уравнений...................................753
3.2. Коэффициенты активности растворов электролитов.................................755
3.2.1. Коэффициенты активности отдельных ионов..............................756
Таблица 3.2.1. Коэффициенты активности отдельных ионов при 25 °C в соответствии с теорией Дебая — Хюккеля......................757
3.2.2. Таблицы коэффициентов активности растворов электролитов.......................757
Таблица 3.2.2. Коэффициенты активности, осмотические коэффициенты и активность воды для солей карбоновых кислот ...........758
Таблица 3.2.3. Коэффициенты активности, осмотические коэффициенты и активность воды для 1:1 электролитов...................763
Таблица 3.2.4. Коэффициенты активности,
осмотические коэффициенты и активность
воды для 1:2 электролитов...................781
Таблица 3.2.5. Коэффициенты активности,
осмотические коэффициенты и активность
воды для 2:1 электролитов...................787
Оглавление
1417
Таблица 3.2.6. Коэффициенты активности, осмотические коэффициенты и активность воды для 2:2 электролитов...................795
Таблица 3.2.7. Коэффициенты активности, осмотические коэффициенты и активность воды в растворах электролитов высших валентных типов (1:3, 3:1, 1:4 и 4:1).......797
3.2.3. Коэффициенты активности электролитов в неводных растворителях....................798
Таблица 3.2.8. Коэффициенты активности хлороводорода в спиртах.....................799
Таблица 3.2.9. Коэффициенты активности некоторых солей в метаноле............................799
Таблица 3.2.10. Коэффициенты активности бромида и иодида натрия в этаноле...................800
Таблица 3.2.11. Коэффициенты активности иодида натрия в н-бутаноле.........................800
3.3. Энергетические свойства растворов.....800
3.3.1. Изменение энтальпии при образовании водных растворов.............800
Таблица 3.3.1. Изменение энтальпии при образовании водных растворов неорганических веществ и солей органических кислот.........................800
Таблица 3.3.2. Изменение энтальпии при образовании водных растворов аммиака.........824
Таблица 3.3.3. Изменение энтальпии при образовании водных растворов хлороводорода...............................824
Таблица 3.3.4. Изменение энтальпии при образовании водных растворов органических веществ.................824
3.3.2. Теплоемкость водных растворов.........826
Таблица 3.3.5. Теплоемкость водных растворов некоторых неорганических и органических веществ..............................826
Таблица 3.3.6. Теплоемкость водных растворов азотной кислоты......................827
Таблица 3.3.7. Теплоемкость и температурное изменение энтальпии растворов серной кислоты и олеума.....................828
Таблица 3.3.8. Теплоемкость водных растворов некоторых органических веществ.......829
3.4. Термодинамические свойства веществ в состоянии стандартного водного раствора....................................830
Таблица 3.4.1. Термодинамические свойства веществ в состоянии стандартного водного раствора....................................830
3.5. Теплопроводность растворов...........855
Таблица 3.5.1. Коэффициенты теплопроводности водных растворов солей при 293 К.....855
Таблица 3.5.2. Коэффициенты теплопроводности водных растворов кислот..............857
Таблица 3.5.3. Коэффициенты теплопроводности водных растворов оснований...........858
Таблица 3.5.4. Коэффициенты теплопроводности водных растворов органических жидкостей...................................858
Таблица 3.5.5. Коэффициенты теплопроводности растворов в метаноле..........................859
Таблица 3.5.6. Коэффициенты теплопроводности растворов в этаноле...................860
Таблица 3.5.7. Коэффициенты теплопроводности растворов в изопентиловом спирте......861
Таблица 3.5.8. Коэффициенты теплопроводности растворов в ацетоне...................861
Таблица 3.5.9. Коэффициенты теплопроводности растворов в бензоле...................861
Таблица 3.5.10. Коэффициенты теплопроводности растворов, образованных двумя органическими компонентами............862
3.6. Электрическая проводимость растворов и числа переноса..............................863
3.6.1. Электрическая проводимость водных растворов.....................................866
Таблица 3.6.1. Удельная электрическая проводимость стандартных растворов.................866
Таблица 3.6.2. Электрическая проводимость концентрированных растворов электролитов при 18 °C.....................................867
Таблица 3.6.3. Эквивалентная электрическая проводимость разбавленных растворов солей при 18 °C.............................. 876
Таблица 3.6.4. Эквивалентная электрическая проводимость разбавленных растворов солей и неорганических кислот при 25 °C ... 877
Таблица 3.6.5.1. Эквивалентная электрическая проводимость кислот и оснований при 18 °C....................................878
Таблица 3.6.5.2. Эквивалентная электрическая проводимость кислот и оснований при 25 °C....................................879
Таблица 3.6.6. Эквивалентная электрическая проводимость растворов солей редкоземельных элементов при 25 °C....880
Таблица 3.6.7. Удельная электрическая проводимость насыщенных растворов труднорастворимых электролитов при 18 °C....................................882
Таблица 3.6.8. Удельная электрическая проводимость растворов органических кислот при 18 °C.............................882
Таблица 3.6.9. Молярная электрическая проводимость растворов органических оснований при 25 °C..........................883
Таблица 3.6.10. Предельная электрическая проводимость растворов электролитов при 25 °C....................................884
3.6.2. Электрическая проводимость неводных
растворов............................884
3.6.2.1. Неорганические растворители..........884
Таблица 3.6.11. Молярная электрическая
проводимость растворов электролитов
во фтороводороде при 15 °C...................885
Таблица 3.6.12. Молярная электрическая
проводимость растворов электролитов
во фтороводороде при 20 °C...................886
1418
Новый справочник химика и технолога
Таблица 3.6.13. Молярная электрическая проводимость растворов электролитов в хлороводороде при -93 °C....................886
Таблица 3.6.14. Молярная электрическая проводимость растворов электролитов в бромоводороде при -80 °C....................887
Таблица 3.6.15. Эквивалентная электрическая проводимость растворов электролитов в циановодороде при 18 °C.....................889
Таблица 3.6.16. Удельная и эквивалентная электрическая проводимость растворов электролитов в серной кислоте при 25 °C.....................................891
Таблица 3.6.17. Молярная электрическая проводимость растворов электролитов в диоксиде серы при 0 °C......................893
Таблица 3.6.18. Эквивалентная электрическая проводимость растворов электролитов в аммиаке при -40 °C..........................894
Таблица 3.6.19. Эквивалентная электрическая проводимость растворов электролитов в аммиаке при -33 °C..........................897
Таблица 3.6.20. Молярная электрическая проводимость растворов Li А1С14 в тионилхлориде при 25 °C..............898
3.6.2.2. Органические растворители.............898
Таблица 3.6.21. Эквивалентная и удельная электрическая проводимость растворов солей в метаноле..............................899
Таблица 3.6.22. Молярная электрическая проводимость растворов кислот в метаноле....................................902
Таблица 3.6.23. Предельная эквивалентная электрическая проводимость растворов электролитов в метаноле при 25 °C......902
Таблица 3.6.24. Эквивалентная и удельная электрическая проводимость растворов электролитов в метаноле при различных температурах..................................903
Таблица 3.6.25. Предельная эквивалентная электрическая проводимость растворов электролитов в метаноле при различных температурах..................................904
Таблица 3.6.26. Эквивалентная и удельная электрическая проводимость растворов солей в этаноле...............................905
Таблица 3.6.27. Молярная электрическая проводимость растворов кислот в этаноле ...907
Таблица 3.6.28. Предельная эквивалентная электрическая проводимость растворов в этаноле.....................................907
Таблица 3.6.29. Удельная электрическая проводимость растворов SbCI3 в этаноле.........908
Таблица 3.6.30. Предельная эквивалентная электрическая проводимость растворов электролитов в этаноле........................909
Таблица 3.6.31. Молярная и удельная электрическая проводимость растворов солей в пропан-1-оле................................909
Таблица 3.6.32. Молярная электрическая проводимость растворов кислот в пропан-1 -оле.........................910
Таблица 3.6.33. Предельная молярная электрическая проводимость растворов электролитов в пропан-1-оле при 25 °C...........910
Таблица 3.6.34. Удельная электрическая проводимость растворов SbCl3 в пропан-1-оле..........................910
Таблица 3.6.35. Предельная молярная электрическая проводимость растворов электролитов в пропан-1-оле при различных температурах....................................910
Таблица 3.6.36. Молярная и удельная электрическая проводимость растворов электролитов в пропан-2-оле при 25 °C........................911
Таблица 3.6.37. Предельная молярная электрическая
проводимость растворов электролитов в пропан-2-оле при 25 °C ..............911
Таблица 3.6.38. Удельная электрическая проводимость растворов SbCh в пропан-2-оле.........................911
Таблица 3.6.39. Предельная молярная электрическая проводимость растворов электролитов в пропан-2-оле при различных температурах...................................911
Таблица 3.6.40. Эквивалентная и удельная электрическая проводимость растворов солей в бутан-1 -оле при 25 °C.................912
Таблица 3.6.41. Молярная электрическая проводимость растворов хлороводорода в бутан-1 -оле при 25 °C...............913
Таблица 3.6.42. Предельная эквивалентная электрическая проводимость растворов электролитов в бутан-1 -оле при 25 °C..913
Таблица 3.6.43. Удельная электрическая проводимость растворов электролитов в бутан-1 -оле при различных температурах.....................914
Таблица 3.6.44. Предельная молярная электрическая проводимость растворов электролитов в бутан-1-оле при различных температурах...................................915
Таблица 3.6.45. Молярная и удельная электрическая проводимость растворов электролитов в 2-метилпропан-1-оле при 25 °C........915
Таблица 3.6.46. Предельная молярная электрическая проводимость растворов электролитов в 2-метилпропан-1 -оле при 25 °C...............915
Таблица 3.6.47. Молярная и удельная электрическая проводимость растворов электролитов в пент-1 -оле при 25 °C........................915
Таблица 3.6.48. Удельная электрическая проводимость растворов SbCl3 в 2-метилпропан-1 -оле.................916
Таблица 3.6.49. Предельная молярная электрическая
проводимость растворов иодида натрия
в 2-метилпропан-!-оле и бутан-2-оле............916
Таблица 3.6.50. Предельная молярная электрическая
проводимость растворов электролитов
в пент-1 -оле при 25 °C........................916
Оглавление
1419
Таблица 3.6.51. Удельная электрическая проводимость растворов SbCl3 в пент-1-оле..................................916
Таблица 3.6.52. Предельная молярная электрическая проводимость растворов электролитов в пент-1 -оле.................................916
Таблица 3.6.53. Молярая и удельная электрическая проводимость растворов электролитов в З-метилбутан-1-оле при 25 °C................917
Таблица 3.6.54. Удельная электрическая проводимость растворов SbCl3 в 3-метилбутан-1 -оле..................917
Таблица 3.6.55. Предельная молярная электрическая проводимость растворов электролитов в высших спиртах при 25 °C....................917
Таблица 3.6.56. Предельная молярная электрическая проводимость растворов электролитов в высших спиртах при различных температурах..................................918
Таблица 3.6.57. Молярная электрическая проводимость растворов электролитов в бензоле при 25 °C...........................918
Таблица 3.6.58. Удельная и молярная электрическая проводимость растворов электролитов в бензоле.....................................919
Таблица 3.6.59. Молярная электрическая проводимость растворов (C5H1i)4NSCN в w-ксилоле...................................919
Таблица 3.6.60. Эквивалентная электрическая проводимость растворов электролитов в ацетоне при 25 °C...........................920
Таблица 3.6.61. Эквивалентная электрическая проводимость растворов электролитов в ацетоне при 18 °C...........................920
Таблица 3.6.62. Удельная электрическая проводимость растворов электролитов в ацетоне при 22 °C...........................921
Таблица 3.6.63. Эквивалентная электрическая проводимость растворов электролитов в ацетофеноне.................................921
Таблица 3.6.64. Эквивалентная электрическая проводимость растворов электролитов в метилэтилкетоне.............................921
Таблица 3.6.65.. Удельная и эквивалентная электрическая проводимость растворов электролитов в муравьиной кислоте при 25 °C.....................................922
Таблица 3.6.66. Эквивалентная электрическая проводимость растворов электролитов в муравьиной кислоте при 8,5 °C...............924
Таблица 3.6.67. Удельная и эквивалентная электрическая проводимость растворов электролитов в уксусной кислоте при 25 °C.....................................924
Таблица 3.6.68. Эквивалентная электрическая проводимость растворов электролитов в хлоруксусной кислоте при 65 °C.......927
Таблица 3.6.69. Молярная и удельная электрическая проводимость растворов электролитов в формамиде при 25 °C.........................928
Таблица 3.6.70. Молярная электрическая
проводимость растворов электролитов в формамиде..........................929
Таблица 3.6.71. Удельная электрическая проводимость растворов Nal в У-метилформамиде при 25 °C................929
Таблица 3.6.72. Удельная и молярная электрическая проводимость растворов электролитов в У,У-диметилформамиде при 25 °C.....929
Таблица 3.6.73. Удельная и молярная электрическая проводимость растворов электролитов в У,У-диметилформамиде при различных температурах................................930
Таблица 3.6.74. Предельная эквивалентная электрическая проводимость растворов электролитов в У,У-диметилформамиде при 25 °C...................................932
Таблица 3.6.75. Предельная эквивалентная электрическая проводимость растворов электролитов в У,У-диметилформамиде при различных температурах..................932
Таблица 3.6.76. Удельная электрическая проводимость растворов электролитов в ацетамиде.................................932
Таблица 3.6.77. Удельная электрическая проводимость растворов электролитов в У-метилацетамиде при 25 °C................933
Таблица 3.6.78. Удельная электрическая проводимость растворов электролитов в У-метилацетамиде при различных температурах................................933
Таблица 3.6.79. Удельная электрическая проводимость растворов электролитов в У,У-диметилацетамиде при 25 °C.............934
Таблица 3.6.80. Удельная электрическая проводимость растворов в У,У-диметилацетамиде при различных температурах................................935
Таблица 3.6.81. Предельная эквивалентная электрическая проводимость растворов электролитов в У,У-диметилацетамиде при 25 °C...................................936
Таблица 3.6.82. Удельная и молярная электрическая проводимость растворов электролитов в У-метилпропионамиде при 25 °C..............936
Таблица 3.6.83. Удельная и молярная электрическая проводимость растворов электролитов в У-мстилпропионамиде при различных температурах................................936
Таблица 3.6.84. Эквивалентная и удельная электрическая проводимость растворов электролитов в пиридине при 25 °C............937
Таблица 3.6.85. Удельная электрическая проводимость растворов электролитов в пиридине..................................939
Таблица 3.6.86. Эквивалентная электрическая
проводимость растворов электролитов
в нитрометане...............................939
1420
Новый справочник химика и технолога
Таблица 3.6.87. Удельная электрическая проводимость растворов электролитов в нитрометане.................................940
Таблица 3.6.88. Эквивалентная и удельная электрическая проводимость растворов электролитов в нитробензоле при 25 °C..........941
Таблица 3.6.89. Удельная и молярная электрическая проводимость растворов электролитов в нитробензоле при различных температурах..................................942
Таблица 3.6.90. Удельная и молярная электрическая проводимость растворов электролитов в ацетонитриле при 25 °C......................942
Таблица 3.6.91. Удельная электрическая проводимость растворов электролитов в ацетонитриле при различных температурах..................................943
Таблица 3.6.92. Молярная электрическая проводимость растворов AgNO3 в бензонитриле при 25 °C......................944
Таблица 3.6.93. Удельная и молярная электрическая проводимость растворов электролитов в диметилсульфоксиде при 25 °C................944
Таблица 3.6.94. Удельная и молярная электрическая проводимость растворов электролитов в диметилсульфоксиде при различных температурах .................................946
Таблица 3.6.95. Удельная электрическая проводимость насыщенных растворов солей в диметилсульфоксиде при 25 °C...........949
Таблица 3.6.96. Удельная электрическая проводимость растворов LiC104 в сульфонах...................................949
Таблица 3.6.97. Предельная эквивалентная электрическая проводимость растворов LiC104 в сульфонах при 30 °C..................950
Таблица 3.6.98. Предельная эквивалентная электрическая проводимость растворов электролитов в этиленгликоле при 25 °C.........950
Таблица 3.6.99. Удельная электрическая проводимость растворов электролитов в метиленхлориде..............................950
Таблица 3.6.100. Удельная электрическая проводимость растворов электролитов в дихлорэтане.................................951
Таблица 3.6.101. Удельная электрическая проводимость растворов (C4H9)4NBr в хлороформе..................................951
Таблица 3.6.102. Удельная электрическая проводимость растворов H2SO4 в диэтиловом эфире............................951
Таблица 3.6.103. Удельная электрическая проводимость растворов SbCl3 в дибутиловом эфире...........................952
Таблица 3.6.104. Удельная и молярная электрическая проводимость растворов электролитов в 1,2-диметоксиэтане......952
Таблица 3.6.105. Удельная электрическая проводимость растворов LiC104 в трибутилфосфате.............................953
Таблица 3.6.106. Удельная электрическая проводимость растворов LiC104 в метилацетате................................953
Таблица 3.6.107. Удельная электрическая проводимость растворов электролитов в эти л ацетате.......................954
Таблица 3.6.108. Удельная электрическая проводимость растворов SbCl3 в пентилацетате...............................954
Таблица 3.6.109. Удельная электрическая проводимость растворов электролитов в тетрагидрофуране ...........................954
Таблица 3.6.110. Удельная электрическая проводимость растворов электролитов в бутиролактоне...............................954
Таблица 3.6.111. Молярная электрическая проводимость растворов электролитов в этиленкарбонате при 36,8 °C.................955
Таблица 3.6.112. Молярная электрическая проводимость растворов (C4H9)4N OC6H2(NO2)3 в этиленкарбонате при 91 °C.....................................956
Таблица 3.6.113. Удельная электрическая проводимость растворов электролитов в пропиленкарбонате...........................956
Таблица 3.6.114. Удельная и эквивалентная электрическая проводимость растворов электролитов в пропиленкарбонате......958
3.6.3. Удельная электрическая проводимость двойных твердых или расплавленных солевых систем................................962
3.6.4. Эквивалентная электрическая проводимость ионов в растворах.............................966
Таблица 3.6.115. Эквивалентная электрическая проводимость ионов в водных растворах при 18 °C.....................................966
Таблица 3.6.116. Предельная эквивалентная электрическая проводимость ионов в водных растворах при 25 °C..................967
Таблица 3.6.117. Предельная эквивалентная электрическая проводимость ионов в водных растворах при различных температурах..................................969
Таблица 3.6.118. Предельная эквивалентная электрическая проводимость ионов в органических растворителях при 25 °C.....................................971
Таблица 3.6.119. Предельная эквивалентная электрическая проводимость ионов в МА-диметилформамиде.........................972
3.6.5. Числа переноса........................972
Таблица 3.6.120. Числа переноса анионов t в водных растворах электролитов...............972
Таблица 3.6.121. Числа переноса катионов t+ в разбавленных водных растворах электролитов..................................973
Таблица 3.6.122. Числа переноса катионов /+
в концентрированных водных растворах
электролитов................................. 975
Оглавление
1421
Таблица 3.6.123. Числа переноса катионов /+ в разбавленных водных растворах электролитов при различных температурах..............................976
Таблица 3.6.124. Числа переноса катионов /+ в концентрированных водных растворах электролитов при различных температурах..............................978
Таблица 3.6.125. Числа переноса катионов в неводных растворах электролитов при 25 °C.................................979
Таблица 3.6.126. Числа переноса катионов в неводных растворах электролитов при различных температурах................979
ЭЛЕКТРОДНЫЕ ПРОЦЕССЫ. ХИМИЧЕСКАЯ КИНЕТИКА И ДИФФУЗИЯ. КОРРОЗИЯ.
КОЛЛОИДНАЯ ХИМИЯ (Синий)
Раздел 1. Электродные процессы..............5
1.1. Электродные процессы в растворах.....6
Таблица 1.1. Стандартные электродные потенциалы в водной среде..............................6
1.2. Дополнительные сведения ............34
1.2.1. Стандартные электродные потенциалы
в неводных средах...................34
Таблица 1.2.1. Стандартный электродный потенциал..................................34
1.2.2. Вспомогательные электроды и электроды
для измерения pH....................34
Таблица 1.2.2. Поправка для разбавленных водных растворов при различных давлениях..........35
Таблица 1.2.3. Стандартный потенциал хингидронного электрода....................35
Таблица 1.2.4. Потенциал каломельного электрода при различных температурах.................36
Таблица 1.2.5. Стандартный потенциал электрода ртуть—сульфат ртути(1)...............36
Таблица 1.2.6. Стандартный потенциал хлорсеребряного электрода............37
Таблица 1.2.7. Стандартный потенциал бромсеребряного электрода в водной среде.......................38
Таблица 1.2.8. Стандартный потенциал иодсеребряного электрода.............38
Таблица 1.2.9. Стандартный потенциал электрода с диоксидом свинца.........................38
1.2.3. Нормальные элементы.................38
1.2.4. Перенапряжение выделения водорода...38
Таблица 1.2.10. Константа для уравнения Тафеля.38
1.2.5. Потенциалы нулевого заряда металлов
и амальгам..........................39
Таблица 1.2.11. Потенциалы нулевого заряда металлов...................................39
Таблица 1.2.12. Потенциалы нулевого заряда металлов восьмой группы периодической системы элементов............................39
Таблица 1.2.13. Потенциалы нулевого заряда амальгам металлов.............................40
1.2.6. Стандартные токи обмена металлов........40
Таблица 1.2.14. Стандартные токи обмена металлов... 40
1.2.7. Дифференциальная емкость двойного электрического слоя на ртути.................40
1.3. Электродные процессы в расплавах........41
Таблица 1.3.1. Равновесные напряжения электрохимических систем с твердыми или расплавленными хлоридами металлов ....41
Таблица 1.3.2. Электродные потенциалы металлов в расплаве КС1—NaCl...................47
Таблица 1.3.3. Электродные потенциалы металлов в эвтектическом расплаве LiCl—КС1.....47
Таблица 1.3.4. Электродные потенциалы металлов в расплавах индивидуальных галогенидов металлов.....................................47
1.4. Коррозия. Виды коррозии, методы испытаний и способы предотвращения коррозионных повреждений.....................48
1.4.1. Понятие коррозии, основные виды
коррозионных повреждений металлов и сплавов............................48
1.4.1.1. Способы классификации коррозии......48
1.4.1.2. Химическая коррозия.................50
1.4.1.3. Электрохимическая коррозия..........52
1.4.1.4. Основные виды общей электрохимической
коррозии металлов и сплавов..........55
Атмосферная коррозия металлов и сплавов......55
Подземная коррозия металлов и сплавов........58
Морская коррозия металлов и сплавов..........60
1.4.2. Питтинговая коррозия..................61
1.4.3. Коррозионное растрескивание металлов
и сплавов............................64
1.4.3.1. Механизм коррозионного растрескивания.64
1.4.3.2. Основные теории, описывающие природу возникновения склонности материалов к коррозионному растрескиванию...............65
Адсорбционная теория.........................65
Водородная теория............................65
Дислокационная теория........................65
Механохимическая теория......................66
Пленочная теория.............................66
Электрохимическая теория.....................66
1.4.3.3. Коррозионное растрескивание углеродистых и низколегированных сталей...................67
Влияние химического состава стали на склонность к коррозионному растрескиванию........67
Влияние термической обработки на склонность сталей к коррозионному растрескиванию........69
1.4.3.4. Коррозионное растрескивание в аустенитных сталях.........................70
Влияние растягивающих напряжений на стойкость аустенитных сталей....................70
Влияние способа задания пластической деформации на скорость анодного процесса в аустенитных сталях.........................71
Влияние скорости нагружения на стойкость
к коррозионному растрескиванию
хромоникелевых аустенитных сталей ............74
1.4.3.5. Коррозионное растрескивание
в высокопрочных сталях........................77
1422
Новый справочник химика и технолога
1.4.3.6. Коррозионное растрескивание цветных сплавов........................................78
Коррозионное растрескивание титановых сплавов 78
Коррозионное растрескивание магниевых сплавов 79
Коррозионное растрескивание алюминиевых сплавов.................................79
1.4.4. Межкристаллитная коррозия в металлах и сплавах......................................80
1.4.4.1. Влияние основных легирующих и примесных элементов на стойкость
к межкристаллитной коррозии аустенитных
хромоникелевых сталей.................80
1.4.4.2. Влияние пластической деформации на стойкость стали к МКК......................84
1.4.4.3. Пути повышения стойкости хромоникелевых сталей к межкристаллитной коррозии............86
1.4.4.4. Контроль качества оборудования из аустенитных коррозионностойких сталей после расчетного срока службы с целью
обнаружения поврежденных или потенциально
склонных к межкристаллитной коррозии зон...........................89
1.4.4.5. Межкристаллитная коррозия хромистых
нержавеющих сталей.....................94
1.4.4.6. Межкристаллитная коррозия алюминиевых
сплавов................................94
1.4.5. Коррозионностойкие стали и сплавы......94
1.4.5.1. Стали ферритного, мартенситно-ферритного
и мартенситного классов................95
1.4.5.2. Высокопрочные хромоникелевые стали
аустенитно-мартенситного класса........96
1.4.5.3. Стали аустенитного и аустенитно-ферритного
классов................................97
1.4.5.4. Кислотоупорные сплавы................99
1.4.6. Коррозия и коррозионная стойкость
неметаллических материалов............102
1.4.6.1. Коррозионная стойкость горных пород.102
1.4.6.2. Коррозионная стойкость керамических
и других неметаллических материалов...103
1.4.6.3. Коррозионная стойкость бетонов......104
1.4.6.4. Коррозионная стойкость древесных
материалов............................106
1.4.6.5. Коррозионная стойкость синтетических
изоляционных покрытий.................106
1.4.6.6. Коррозионная стойкость полимерных материалов...................................107
Термическая деструкция полимеров.............108
Термоокислительная деструкция полимеров......109
Озонное разрушение каучуков, резин и пластиков.... 109
Фотодеструкция, радиационная деструкция и светостабилизация полимеров................109
Гидролитическая деструкция, механодеструкция
и биологическая деструкция полимеров..109
Эксплуатационная надежность оборудования, отработавшего расчетный срок службы в условиях агрессивного воздействия внешних и рабочих сред......................110
Особенности разрушения крупногабаритных конструкций.................................112
1.4.7.2. Способы испытаний коррозионной стойкости сталей и сплавов..................114
1.4.7.3. Испытания на общую коррозию........114
1.4.7.4. Определение склонности сталей и сплавов к питтинговой коррозии............115
Химические методы исследования..............116
Способы измерения глубины при анализе питтинговой коррозии........................116
Электрохимические методы исследования.......117
1.4.7.5. Испытания на межкристаллитную коррозию.....................................117
1.4.7.6. Испытания на стойкость сталей и сплавов к коррозионному растрескиванию...............118
1.4.7.7. Методы неразрушающего контроля крупногабаритного оборудования, отработавшего расчетный срок службы, с целью обнаружения зон, поврежденных различными видами коррозии..................121
1.4.8. Способы защиты металлических и неметаллических материалов от коррозии..................................126
1.4.8.1. Электрохимическая защита...........127
Катодная и протекторная защиты..............127
Некоторые виды катодной защиты..............128
Анодная защита..............................132
1.4.8.2. Ингибиторы коррозии................134
1.4.8.3. Антикоррозионные защитные покрытия..135
Металлические покрытия......................135
Неметаллические покрытия.....................136
1.4.8.4. Защита неметаллических конструкций.139
1.4.9. Коррозионная стойкость материалов..141
Таблица 1.4.62. Коррозионная стойкость
материалов...........................142
Таблица 1.4.63. Растворимость водорода в металлах..................................323
Таблица 1.4.64. Коррозия при контактах между металлами и сплавами........................325
Раздел 2. Химическая кинетика и диффузия....329
2.1. Кинетика...........................329
2.1.1. Основные понятия в химической кинетике гомогенных химических реакций...............329
Классификация кинетических кривых...........329
Кинетическая классификация химических реакций.....................................330
Кинетические и термодинамические параметры химических реакций...................331
Расчет константы скорости по частоте соударений
и энергии активации..........................334
2.1.1.1. Формальная кинетика химических реакций,
протекающих в реакторах периодического
и непрерывного действия.......................336
Кинетика гомогенных химических реакций
в статических условиях.......................336
1.4.7. Промышленная безопасность оборудования. Способы контроля качества деталей с целью
выявления коррозионных дефектов различных типов...................110
1.4.7.1. Проблемы промышленной безопасности оборудования на современном этапе.........110
Оглавление
1423
Кинетика гомогенных химических реакций в реакторах идеального перемешивания........336
Кинетика гомогенных химических реакций в непрерывных процессах..............341
Кинетика гомогенных химических реакций в режиме идеального вытеснения.......342
Кинетика гомогенных химических реакций в потоке в режиме идеального перемешивания...............................344
Мономолекулярные реакции в газовой фазе.....345
Таблица 2.1.15. Константы равновесия химических реакций, протекающих в жидкой фазе..........349
Таблица 2.1.16. Кинетические параметры химических реакций, протекающих в жидкой фазе...............................356
Таблица 2.1.17. Константы скорости гомолитических химических реакций, протекающих в газовой фазе..............................402
2.1.2. Гетерогенные реакции...............430
2.1.2.1. Топохимические реакции.............430
Формально-кинетический анализ топохимических реакций.....................................430
Влияние температуры и давления на кинетику топохимических реакций......................437
Кинетика окисления металлов.................446
2.1.2.2. Диффузионная кинетика..............449
2.1.3. Реакции изотопного обмена..........453
Таблица 2.1.36. Кинетика реакций изотопного обмена в гомогенной среде...................453
Таблица 2.1.37. Кинетика реакций изотопного обмена в гетерогенной среде.................468
2.2. Диффузия...........................475
2.2.1. Молекулярная диффузия................475
2.2.1.1. Диффузия в газах...................475
Таблица 2.2.1. Коэффициенты само диффузии газов при различных температурах и давлении /7 = 0,1 МПа................................477
Таблица 2.2.2. Коэффициенты взаимной диффузии в газах и парах D, полученные различными исследователями при давлении /7 = 0,1 МПа................................481
Таблица 2.2.3. Атомные и молекулярные диффузионные объемы для определения АВ..........................496
Таблица 2.2.4. Сводная таблица значений коэффициентов (при 293 К)............497
Таблица 2.2.5. Зависимость коэффициентов диффузии газов от давления...........497
2.2.1.2. Термическая диффузия в газах.......498
Таблица 2.2.7. Данные по термодиффузии в газовых смесях.....................498
2.2.1.3. Диффузия в жидкостях...............513
Таблица 2.2.8. Значения коэффициентов для некоторых веществ, растворенных в воде......................................514
Таблица 2.2.9. Коэффициенты диффузии веществ в водных растворах...................514
Таблица 2.2.10. Коэффициенты диффузии в неводных растворителях.............516
Таблица 2.2.11. Коэффициенты взаимной диффузии в жидких двухкомпонентных органических
системах.............................517
Таблица 2.2.12. Диффузия в расплавленных металлах....................................517
Таблица 2.2.13. Диффузия в амальгамах.......517
Таблица 2.2.14. Диффузия в расплавленных солях.... 517
Таблица 2.2.15. Экспериментальные значения коэффициентов диффузии различных газов и неэлектролитов в сильноразбавленных водных растворах............................518
Таблица 2.2.16. Коэффициенты взаимной диффузии для Н2, СН4 и СО2 в водных растворах солей.......................................518
Таблица 2.2.17. Экспериментальные значения коэффициентов диффузии в неводных растворителях при бесконечном разбавлении.................................519
Таблица 2.2.18. Аддитивные приращения объемов для расчета молярных объемов растворенных веществ при нормальной температуре кипения.....................................519
2.2.1.4. Диффузия в растворах электролитов..520
Таблица 2.2.19. Предельные ионные проводимости в воде при 25 °C............................520
Таблица 2.2.20. Коэффициенты взаимной диффузии неорганических соединений в водных растворах...................................521
Таблица 2.2.21. Коэффициенты взаимной диффузии для водорода и метана в водных растворах солей.......................................521
2.2.2. Диффузия в твердой фазе............522
2.2.2.1. Общие понятия......................522
2.2.2.2. Диффузия в непористых материалах...522
Таблица 2.2.22. Параметры для коэффициента взаимной диффузии металлов и сплавов.........525
Таблица 2.2.23. Параметры для коэффициента самодиффузии металлов.......................527
Таблица 2.2.24. Концентрационная зависимость констант £>о и Еа для диффузии металлов в меди при 800 °C...........................527
Таблица 2.2.25. Константы для диффузии металлов в солях.....................................528
Таблица 2.2.26. Коэффициент диффузии ионов в кристаллах при различных температурах................................528
Таблица 2.2.27. Параметры для коэффициента диффузии иона Ag+ в кристаллах.......528
Таблица 2.2.28. Коэффициент взаимной диффузии твердых солей........................528
Таблица 2.2.29. Самодиффузия в твердом водороде.. 529
Таблица 2.2.30. Параметры для коэффициента диффузии газов в твердых телах..............529
Таблица 2.2.31. Параметры для коэффициента
диффузии малой примеси в серебре.............529
Таблица 2.2.32. Параметры для коэффициента
диффузии малой примеси в меди...............529
Таблица 2.2.33. Параметры для коэффициента
диффузии малой примеси в золоте..............529
1424
Новый справочник химика и технолога
Таблица 2.2.34. Параметры для коэффициента диффузии малой примеси в никеле.....529
Таблица 2.2.35. Параметры для коэффициента диффузии различных примесей в металлах III и IV групп..................530
Таблица 2.2.36. Параметры для коэффициента диффузии атомов примесей в щелочных металлах...................................530
Таблица 2.2.37. Параметры для коэффициента диффузии атомов примеси в лантанидах и актинидах................................530
Таблица 2.2.38. Параметры температурной зависимости коэффициента диффузии малой примеси в 0-Ti................531
Таблица 2.2.39. Параметры для коэффициента диффузии ионов в кристаллах солей...531
Таблица 2.2.40. Параметры для коэффициента диффузии примесей в кристаллах солей........531
Таблица 2.2.41. Параметры для коэффициента диффузии атомов водорода и его изотопов в металлах..................532
Таблица 2.2.42. Параметры для коэффициента диффузии атомов инертных газов в кристаллах солей.........................532
Таблица 2.2.43. Параметры для коэффициента диффузии атомов примеси в полупроводниках..........................532
Таблица 2.2.44. Параметры для коэффициента самодиффузии в некоторых кристаллах.........534
Таблица 2.2.45. Коэффициенты диффузии атомов металлов в амальгамах......................534
Таблица 2.2.46. Коэффициент диффузии в расплавленных металлах...................534
2.2.2.3. Диффузия в капиллярно-пористых
материалах..........................534
2.2.2.4. Диффузия в коллоидных
капиллярно-пористых материалах......537
2.2.3. Диффузионная проницаемость через
мембраны............................538
2.2.4. Диффузия в ионообменных смолах......538
Таблица 2.2.47. Значение коэффициентов самодиффузии ионитов.......................539
Раздел 3. Физика, химия и технология дисперсных систем (Коллоидная химия)..................547
3.1. Поверхность. Фундаментальные свойства... 547
3.1.1. Геометрия дисперсной системы........547
3.1.2. Поверхностный слой..................549
3.1.3. Поверхностное натяжение.............551
3.1.4. Адсорбция газов на поверхности
твердых тел.........................554
3.2. Капиллярные явления.................559
3.2.1. Основные понятия....................559
3.2.2. Равновесие поверхности твердого вещества
с летучей жидкостью.................563
3.2.3. Равновесие поверхности твердой фазы
с двумя жидкими.....................565
3.3. Термодинамика поверхности...........569
3.3.1. Фундаментальное уравнение
и термодинамические потенциалы......569
3.3.2. Уравнения термодинамики гетерогенных
систем................................571
3.3.3. Работа образования поверхности........573
3.3.4. Термодинамика тонких пленок...........575
3.4. Поверхностное натяжение и адсорбция...577
3.4.1. Механизм адсорбции из растворов.......577
3.4.2. Поверхностно-активные вещества (ПАВ).... 578
3.4.3. Пленки нерастворимых ПАВ..............582
3.4.4. Мицеллярные растворы ПАВ..............584
3.4.5. Градиент поверхностного натяжения.....586
3.4.6. Адсорбция из раствора на поверхности
твердого вещества.....................588
3.4.7. Адсорбция на внутренней поверхности
поликристаллических веществ...........590
3.4.8. Электрокапиллярность..................591
3.4.9. Измерение поверхностного натяжения....592
3.5. Двойной электрический слой............594
3.5.1. Понятие двойного электрического слоя..594
3.5.2. Плотная и диффузная части ДЭС.........599
3.5.3. Специфическая адсорбция и емкость ДЭС.602
3.5.4. Двухслойная модель плотного слоя......604
3.5.5. Уравнение Нернста и адсорбция ионов...607
3.5.6. Электрокинетический и мембранный
потенциал.............................610
3.6. Расклинивающее давление в тонких
пленках...............................617
3.6.1. Молекулярное притяжение...............617
3.6.2. Электростатическое отталкивание ДЭС...619
3.6.3. Отталкивание адсорбционных слоев......621
3.6.4. Структурный и стерический эффекты.....621
3.6.5. Вытеснительное отталкивание
и притяжение..........................623
3.7. Устойчивость дисперсных систем........624
3.7.1. Вводные понятия.......................624
3.7.2. Взаимодействие сферических частиц.....625
3.7.3. Устойчивость против коагуляции........628
3.7.4. Критическая концентрация электролита..628
3.7.5. Силовая коагуляция и экстремумы
функций взаимодействия частиц.........630
3.7.6. Эффекты смещения плоскости
адсорбции ионов.......................631
3.7.7. Устойчивость многокомпонентных
суспензий.............................634
3.8. Молекулярно-кинетические явления......636
3.8.1. Регулярное и хаотичное движение частиц... 636
3.8.2. Диффузия..............................638
3.8.3. Равновесное распределение дисперсной
фазы..................................639
3.8.4. Оседание устойчивых концентрированных
суспензий.............................641
3.8.5. Седиментационный анализ...............644
3.9. Электромагнетизм коллоидов............645
3.9.1. Основы электростатики.................645
3.9.2. Поляризуемость частиц................651
3.9.3. Магнитное поле и магнетизм веществ...653
3.9.4. Дисперсные ферромагнетики............658
3.9.5. Суперпарамагнетизм Броуна и Нееля....667
3.10. Основы механики деформируемых сред...669
3.10.1. Предмет реологии....................669
Оглавление
1425
3.10.2 . Основные понятия и законы реологии.....669
3.10.3 . Вязкость и классификация текучих
материалов..............................673
3.11. Структура и реология дисперсных систем.676
3.11.1. Структурная классификация дисперсных
систем..................................676
3.11.2. Неструктурированные системы............680
3.11.3. Ориентационное структурирование........682
3.11.4. Вращательная вязкость..................688
3.12. Периодическая коллоидная структура.....689
3.12.1. Концентрационное структурирование......689
3.12.2. Уравнение структурного состояния ИКС...691
3.12.3. Уравнение напряжений и уравнение
реологии ПКС............................693
3.12.4. Время релаксации и потенциальный
барьер..................................695
3.13. Кинетика коагуляции
и структурирования......................695
3.13.1. Введение...............................695
3.13.2. Элементы кинетики коагуляции...........696
3.13.3. Фрактальная размерность и структура
флокул..................................697
3.13.4. Параметры состояния коагулирующей
взвеси и условие структурирования.......699
3.13.5. Скорость оседания флокул...............700
3.13.6. Альтернатива: расслоение или
структурирование........................701
3.13.7. Уравнения кинетики коагуляции..........703
3.13.8. Динамика и кинетика уплотнения осадка..704
3.14. Реология тиксотропных систем...........707
3.14.1. Прочность структурной сетки и флокул...707
3.14.2. Уравнение структурного состояния
и тиксотропия...........................708
3.14.3. Реологическое уравнение тиксотропных
систем................................ 709
3.14.4. Течение в тонких каналах...............710
3.14.5. Цепочечная структура...................712
3.14.6. Уравнение состояния и реологический
закон цепочечной структуры..............713
3.14.7. Послойное скольжение...................717
3.15. Основы вискозиметрии...................720
3.16. Полимеры и растворы полимеров..........726
3.16.1. Введение...............................726
3.16.2. Гибкость и форма макромолекул..........727
3.16.3. Модуль упругости и персистентная
длина макромолекулы.....................734
3.16.4. Гибкость молекул полиэлектролита.......735
3.16.5. Модуль упругости полимерных
материалов..............................736
3.16.6. Особенности растворения полимеров......737
3.16.7. Качество растворителя..................738
3.16.8. Вязкость растворов полимеров...........741
3.17. Оптические свойства дисперсных систем ....745
3.18. Получение дисперсных систем............748
3.18.1. Дробление..............................748
3.18.2. Физическая и химическая конденсация....751
3.18.3. Пептизация.............................752
3.19. Феррожидкости. Получение и свойства....753
3.19.1. Введение...............................753
3.19.2. Приготовление магнитных жидкостей.....754
3.19.2.1. Выбор метода и магнитного материала.754
3.19.2.2. Приготовление магнетитовых феррожидкостей...............................755
3.19.3. Свойства феррожидкостей...............757
3.19.3.1. Намагниченность.....................757
3.19.3.2. Эффекты коагуляции и структурирования феррожидкостей...............................758
3.19.4. Феррогидродинамика....................761
3.19.4.1. Магнитостатическое давление.........761
3.19.4.2. Неустойчивость свободной границы феррожидкости................................762
3.19.4.3. Применение феррожидкостей...........763
3.19.4.4. Применение эффектов взаимодействия частиц в магнитных суспензиях................766
Приложение 1. Поверхностное натяжение и поверхностно-активные вещества.............767
1.1. Поверхностное натяжение веществ.......767
1.1.1. Поверхностное натяжение веществ на границе с газовой фазой...................767
Таблица 1П1.1. Простые вещества...............767
Таблица 2П1.1. Неорганические соединения......768
Таблица ЗП 1.1. Вода на границе с воздухом....769
Таблица 4П1.1. Смеси Н2О и D2O при 20 °C......769
Таблица 5П1.1. Органические вещества..........770
Таблица 5аП1.1. Алифатические углеводороды....770
Таблица 56П1.1. Циклические углеводороды......770
Таблица 5вП1.1. Галогензамещенные углеводороды.................................771
Таблица 5гП1.1. Спирты, тиоспирты, фенолы.....772
Таблица 5дП1.1. Простые эфиры, альдегиды, кетоны.......................................772
Таблица 5еП1.1. Кислоты и их производные......772
Таблица 5жП1.1. Сложные эфиры.................773
Таблица 5зП1.1. Амины.........................774
Таблица 5иП1.1. Другие азотсодержащие соединения...................................774
Таблица 5кП1.1. Прочие органические вещества и масла......................................775
Таблица 6П1.1. Сводные данные для ряда распространенных органических растворителей................................775
Таблица 7П1.1. Межфазное натяжение воды на границе с другими веществами..............775
Таблица 8П1.1. Межфазное натяжение ртути на границе с водными растворами..............777
Таблица 9П1.1. Межфазное натяжение ртути на границе с органическими жидкостями...................................777
1.2. Поверхностное натяжение растворов....778
Таблица 1П1.2. Изотермы поверхностного натяжения водных растворов полярных веществ......................................778
Таблица 2П1.2. Изотермы поверхностного
натяжения водных растворов солей
жирных кислот...............................779
Таблица ЗП1.2. Изотермы поверхностного
натяжения водных растворов
катионоактивных ПАВ.........................781
1426
Новый справочник химика и технолога
Таблица 4П1.2. Изотермы поверхностного
натяжения водных растворов неионогенных ПАВ.....................783
Таблица 5П1.2. Поверхностное натяжение растворов неорганических веществ на границе с влажным воздухом..........................789
1.3. ГЛБиККМ..............................790
1.3.1. Гидрофильно-липофильный баланс
веществ..............................790
Таблица 1П1.3. Зависимость состояния ПАВ в воде от величины ГЛБ......................790
Таблица 2П1.3. Групповые числа А различных фрагментов молекул ПАВ......................790
Таблица ЗП1.3. ГЛБ поверхностно-активных веществ.....................................790
1.3.2. Критические концентрации
мицеллообразования (ККМ).............791
Таблица 4П1.3. Критические концентрации мицеллообразования типичных представителей поверхностно-активных веществ разного типа.........................791
1.3.3. Расчет количества ПАВ в дисперсной системе......................................792
Таблица 5П1.3. Площадь, занимаемая одной молекулой в насыщенном адсорбционном слое..........................792
1.4. ПАВ в неводных средах................792
1.4.1. Припои и флюсы.......................792
1.4.2. Легкоплавкие припои..................793
Таблица 1П1.4. Состав и свойства оловянно-свинцовых припоев..................793
Таблица 2П1.4. Припои на основе олова, цинка и кадмия....................................793
Таблица ЗП1.4. Состав и температура плавления сплавов ИНГАС...............................794
1.4.3. Флюсы для пайки легкоплавкими припоями....................................794
Таблица 4П1.4. Типовые составы флюсов на основе канифоли..........................794
Таблица 5П1.4. Флюсы для пайки алюминия.....794
1.5. Поверхностно-активные вещества,
растворимые в углеводородах..........795
1.5.1. Поверхностная активность в неполярной
среде................................795
Таблица 1П1.5. Основные функции присадок к маслам и топливам.........................796
Таблица 2П1.5. Перечень показателей, характеризующих свойства и эффективность ПАВ в смазочных маслах и жидких
топливах..............................796
1.6. Маслорастворимые ПАВ основных химических классов и области их применения................................797
1.6.1. Сульфонаты............................797
Таблица 1П1.6. Характеристика нефтяных и синтетических сульфонатов..................797
1.6.2. Амины, амиды, имиды...................798
Таблица 2П1.6. Свойства и функциональное назначение присадок к маслам.................798
Таблица ЗП1.6. Обобщенная характеристика действия маслорастворимых азотсодержащих ПАВ...................799
1.6.3. Кислородсодержащие ПАВ................799
Таблица 4П1.6. Свойства некоторых кислородсодержащих маслорастворимых ПАВ........................800
1.6.4. Хлор и серасодержащие соединения......800
1.6.5. Сополимеры, содержащие полярные и неполярные звенья.........................800
Приложение 2. Дисперсные системы.............803
2.1. Точки нулевого заряда.................803
Таблица 1П2.1. Точки нулевого заряда.........803
2.2. Константы молекулярного
взаимодействия........................803
Таблица 1П2.2. Пороги коагуляции отрицательно заряженных золей............................804
Таблица 2П2.2. Пороги коагуляции положительно заряженных золей............................804
Таблица ЗП2.2. Константы молекулярного притяжения частиц в водной среде............805
Таблица 4П2.2. Показатели преломления при длине волны X = 589,3 нм и плотности твердых веществ при 20 °C...........................805
Таблица 5П2.2. Показатели преломления жидкостей при 20 °C и длине волны 589,3 нм.....808
Таблица 6П2.2. Плотность жидкостей при различных температурах...............809
Таблица 7П2.2. Вязкость жидкостей при различных температурах.........................810
Таблица 8П2.2. Предельная эквивалентная электрическая проводимость ионов в водных растворах..........................812
2.3. Приготовление и свойства некоторых
коллоидных систем.....................813
2.3.1. Гель кремниевой кислоты H2SiO3........813
2.3.2. Феррожидкости.........................813
Таблица 1П2.3. Характеристики ферромагнитных
жидкостей фирмы «Ferrofluidics Corp.».813
Таблица 2П2.3. Характеристика феррожидкостей СПбГТИ(ТУ)...........................813
Приложение 3. Полимеры.......................815
3.1. Гибкость макромолекул.................815
Таблица 1ПЗ. 1. Потенциальные барьеры вращения мономеров...................................815
Таблица 2ПЗ. 1. Параметры гибкости полимеров.816
Таблица ЗПЗ. 1. Температура стеклования полимеров...................................816
3.2. Вязкость..............................818
Таблица 1П3.2. Критические величины молярных масс........................................820
Таблица 2П3.2. Значения констант формулы Фокса.......................................820
3.3. Вязкость разбавленных растворов......821
Таблица 1ПЗ. 3. Константы формулы Куна......821
3.4. Состояние системы
полимер—растворитель.................821
Таблица 1П3.4. Критические температуры
некоторых систем
полимер—растворитель.........................822
Оглавление
1427
Таблица 2П3.4. Параметры растворимости растворителей и полимеров...................823
Таблица 2П3.4а. Параметры растворимости растворителей...............................823
Таблица ЗПЗ.4. Донорные числа к SbCl5, относительная диэлектрическая проницаемость, параметры растворимости растворителей...............................823
Таблица 4ПЗ. 4. Параметр растворимости, температуры кипения и плавления растворителей с различной силой водородных связей...........................824
Таблица 5П3.4. Интервалы параметров растворимости полимеров в растворителях с разной силой водородной связи.............825
Таблица 6ПЗ. 4. Системы полимер—растворитель—осадитель........826
Приложение 4. Основные физико-химические константы.............................829
АНАЛИТИЧЕСКАЯ ХИМИЯ. Ч. 1 (Зеленый) Раздел 1. Информационные базы и общие вопросы аналитической химии
1.1. Основные печатные и электронные справочные источники по аналитической химии.........................................7
1.1.1. Рекомендации Международного союза теоретической и прикладной химии (ИЮПАК) по вопросам номенклатуры аналитической химии и их перевод в России...................7
1.1.2. Журналы по аналитической химии.........11
1.1.3. Справочники и руководства общего
характера..............................12
1.1.4. Серии монографий и обзорная информация
по аналитической химии.................13
1.1.5. Основная учебная литература
по аналитической химии.................21
1.1.6. Интернет: обзор основных сайтов
по аналитической химии.................22
1.2. Структура и методы аналитической
химии (АХ).............................33
1.3. Общая схема количественного анализа....35
1.4. Выбор метода анализа...................36
1.5. Отбор и подготовка проб к анализу......39
1.5.1. Отбор пробы............................39
1.5.2. Потери и загрязнения при отборе пробы.
Хранение пробы.........................43
1.5.3. Подготовка пробы к анализу.............44
Раздел 2. Метрологические основы методов количественного анализа
2.1. Количество вещества, эквивалентность, способы выражения концентраций...............53
2.2. Аналитический сигнал. Методы измерения ....59
2.3. Погрешности количественного химического анализа. Представление результатов химического анализа..........................61
2.3.1. Общие термины..........................62
2.3.2. Классификация погрешностей.............63
2.3.3. Систематические погрешности. Способы их выявления ................................64
2.3.4. Статистическая обработка результатов прямых равноточных наблюдений (определений).................................66
2.3.4.1. Термины, относящиеся к параллельным измерениям. Оценка воспроизводимости..........67
2.3.4.2. Оценка правильности результата
измерения (анализа)....................68
2.3.5. Оценка грубых погрешностей (промахов)..69
2.3.6. Сравнение двух средних.................70
2.4. Расчет уравнения линейного
градуировочного графика, его метрологических характеристик и метрологических характеристик результата анализа.....................71
2.5. Термины по представлению результатов химического анализа ..........................75
2.6. Предел обнаружения. Диапазон определяемых содержаний. Нижняя граница определяемых содержаний...............76
2.7. Значащие цифры и правила округления. Точные и приближенные вычисления..............89
Раздел 3. Методы разделения и концентрирования
3.1. Методы разделения, основанные на образовании выделяемым веществом новой фазы, в зависимости от агрегатного состояния исходной смеси и выделяемых веществ.......................................95
3.1.1. Осаждение..............................95
3.1.2. Отгонка из раствора...................103
3.1.3. Отгонка в парах реагента..............104
3.1.4. Упаривание, дистилляция, ректификация...107
3.2. Методы разделения, основанные
на различиях в распределении веществ между фазами..........................108
3.2.1. Общие характеристики методов,
основанных на различиях в межфазном распределении.........................109
3.2.2. Сорбционные методы....................110
3.2.2.1. Молекулярная адсорбция..............110
3.2.2.2. Ионный обмен........................113
3.2.2.3. Комплексообразующая сорбция.........133
3.2.2.4. Твердофазная экстракция.............138
3.2.3. Динамическая сорбция..................138
3.2.4. Кристаллизационные методы
концентрирования......................139
3.2.4.1. Соосаждение.........................139
3.2.4.2. Зонная плавка и направленная кристаллизация...............................155
3.2.5. Жидкостная экстракция.................156
3.2.5.1. Экстракция по механизму физического распределения................................156
3.2.5.2. Реакционная экстракция в органические экстрагенты..................................157
3.2.5.3. Реакционная экстракция в расплаве
металлов (пробирная плавка)..................168
3.2.6. Сверхкритическая флюидная
экстракция...................................169
3.2.7. Газовая экстракция....................170
3.2.8. Жидкостная абсорбция..................174
1428
Новый справочник химика и технолога
3.2.9. Хроматография и хроматографические методы разделения веществ...................176
3.2.9.1. Классификация хроматографических методов разделения веществ. Основные термины.....................................176
3.2.9.2. Теоретические основы хроматографии...181
3.2.9.3. Практические следствия теоретических представлений о хроматографическом процессе....................................184
3.2.9.4. Хроматографические методы, являющиеся вариациями хроматографического способа осуществления процесса межфазного распределения................................187
3.2.9.5. Варианты хроматографических методов разделения в зависимости от агрегатного состояния фаз и механизма удерживания разделяемых веществ стационарной фазой ... 191
3.2.9.6. Хроматографические методы анализа..214
3.3. Мембранные методы разделения веществ.214
3.3.1. Внутригрупповая классификация методов....214
3.3.2. Диффузионные мембранные методы.......215
3.3.3. Электромембранные методы.............218
3.3.4. Баромембранные методы (мембранная
фильтрация)..........................219
3.3.4.1. Мембранная фильтрация жидких сред..220
3.3.4.2. Мембранная фильтрация воздуха......226
3.4. Методы внутрифазного разделения......241
3.4.1. Электрофорез в растворе..............242
3.4.2. Проточное фракционирование
в поперечном поле....................244
3.5. Комбинированные и прочие методы
разделения...........................246
3.5.1. Фотохимические методы................246
3.5.2. Хроматомембранный массообменный
процесс и хроматомембранные методы...247
Раздел 4. Аналитическая хроматография и капиллярный электрофорез
4.1. Аналитическая хроматография..........254
4.1.1. Газовая хроматография................254
4.1.1.1. Параметры удерживания в газовой хроматографии...............................254
4.1.1.2. Параметры хроматографического пика...255
4.1.1.3. Основные виды размывания полос
в колонке..............................255
4.1.1.4. Основные уравнения в газовой хроматографии................................257
4.1.1.5. Влияние экспериментальных параметров на хроматографическое разделение............258
4.1.1.6. Аппаратура для газовой хроматографии.259
4.1.2. Газо-жидкостная хроматография........270
4.1.2.1. Преимущества и недостатки газо-жидкостной хроматографии...............270
4.1.2.2. Твердые носители...................275
4.1.2.3. Процесс приготовления сорбента.....277
4.1.3. Газоадсорбционная хроматография......279
4.1.3.1. Особенности газоадсорбционной хроматографии...............................279
4.1.3.2. Классификация адсорбентов по химической природе поверхности.........................280
4.1.3.3. Классификация адсорбентов по геометрической структуре..................280
4.1.3.4. Методы модифицирования адсорбентов в газовой хроматографии......................281
4.1.3.5. Основные типы адсорбентов...........281
4.1.4. Капиллярная газовая хроматография.....284
4.1.4.1. Особенности капиллярной хроматографии................................284
4.1.5. Основные рекомендации по выбору
сорбентов и условий хроматографического разделения смесей конкретных веществ..286
4.1.6. Качественный анализ в газовой
хроматографии.........................288
4.1.7. Основные методы количественного
анализа в газовой хроматографии.......290
4.1.8. Высокоэффективная жидкостная
хроматография (ВЭЖХ)..................300
4.1.8.1. Основные особенности метода и аппаратуры.................................300
4.1.8.2. Классификация хроматографических систем: сорбент—элюент—сорбат по типам
межмолекулярных взаимодействий.........301
4.1.8.3. Общие требования к элюентам в ВЭЖХ...306
4.1.8.4. Адсорбенты для ВЭЖХ..................308
4.1.8.5. Динамическое модифицирование адсорбентов..................................314
4.1.8.6. Общая схема жидкостного хроматографа.315
4.1.9. Ионная хроматография..................326
4.1.10. Метод тонкослойной
хроматографии (ТСХ)...................338
4.1.11. Особенности хроматографии с подвижной
фазой в сверхкритическом состоянии....340
4.2. Капиллярный электрофорез..............343
4.2.1. Основы метода КЭ......................343
4.2.2. Способы ввода пробы. Зона пробы
в капилляре...........................345
4.2.3. Ведущий электролит....................346
4.2.3.1. Добавки к ведущему электролиту......346
4.2.4. Основные варианты капиллярного
электрофореза.........................349
4.2.4.1. Капиллярный зонный электрофорез.....350
4.2.4.2. Мицеллярная электрокинетическая хроматография................................350
4.2.5. Детектирование в КЭ...................351
4.2.5.1. Зарубежные коммерческие системы капиллярного электрофореза...................353
4.2.5.2. Отечественные системы капиллярного электрофореза................................356
4.2.6. Характеристики удерживания............356
4.2.7. Количественный и качественный
анализ в КЭ...........................358
4.2.8. Эффективность, разрешение
и селективность метода КЭ.............358
4.2.9. Чувствительность метода КЭ............359
4.2.9.1. Селективность.......................362
4.2.10. Объекты для анализа методом
капиллярного электрофореза....................364
4.2.11. Подготовка пробы к анализу методом
капиллярного электрофореза....................368
Оглавление
1429
Раздел 5. Химические методы количественного анализа
5.1. Гравиметрические методы...............389
5.1.1. Методы гравиметрического определения неорганических ионов.........................427
5.1.2. Важные для гравиметрии свойства отдельных элементов.........................540
5.2. Титриметрический анализ (ТА)...........573
5.2.1. Общие положения........................574
5.2.1.1. Сущность ТА. Точка эквивалентности или точка стехиометричности.................574
5.2.1.2. Кривые титрования. Конечная точка титрования и способы ее регистрации.........577
5.2.2. Классификация титриметрических
методов анализа........................579
5.2.2.1. Классификация по способам титрования.579
5.2.2.2. Классификация титриметрических методов по типам реакций титрования.................585
5.2.3. Посуда мерная лабораторная: бюретки,
пипетки, колбы, цилиндры, мензурки.....586
5.2.4. Способы приготовления стандартных
растворов..............................589
5.2.4.1. Приготовление первичных стандартных растворов....................................589
5.2.4.2. Приготовление вторичных стандартных растворов (вторичный стандарт)...............591
5.2.4.3. Стандартизация растворов по точным навескам первичных стандартных (установочных) веществ: способ отдельных навесок, способ пипетирования...............591
5.2.4.4. Стандартизация по другому стандартному раствору........................592
5.2.4.5. Стандартизация растворов по стандартным образцам......................593
5.2.4.6. Расчет концентрации титрованных растворов с помощью поправочного коэффициента................................593
5.2.5. Общие правила выполнения титриметрических определений.................596
5.2.6. Практическое применение титриметрических методов анализа.............597
5.2.6.1. Кислотно-основное титрование. Общая характеристика и возможность метода.........597
5.2.6.2. Комплексонометрическое титрование....626
5.2.6.3. Техника и применение комплексонометрического титрования............................653
5.2.6.4. Косвенные комплексонометрические методы определения анионов неорганических кислот и катионов..................................683
5.2.6.5. Окислительно-восстановительное титрование..................................687
5.2.6.6. Осадительное титрование..............699
Раздел 6. Электрохимические методы анализа
6.1. Химические сенсоры. Потенциометрия.....710
6.1.1. Типы сенсоров и физические принципы их функционирования.........................710
6.1.2. Интеллектуальные сенсорные системы ....712
6.1.3. Основные характеристики потенциометрических сенсоров...............................713
6.1.3.1 Уравнение Никольского................713
6.1.3.2. Крутизна электродной функции........713
6.1.3.3. Предел обнаружения..................713
6.1.3.4. Селективность.......................714
6.1.3.5. Рабочая область pH..................716
6.1.3.6. Время отклика.......................717
6.1.4. Таблицы потенциометрических сенсоров.....................................718
6.1.5. Методы аналитического определения.....724
6.1.5.1. Прямая потенциометрия...............724
6.1.5.2. Потенциометрическое титрование......729
6.1.5.3. Другие методы («электронный язык»)..732
6.1.6. Список фирм, изготавливающих
оборудование для потенциометрического анализа...............................733
6.2. Кулонометрия..........................737
6.3. Вольтамперометрия.....................740
6.3.1. Классические методы...................740
6.3.2. Хронопотенциометрия...................747
6.3.3. Потенциалы полярографических полуволн в различных фоновых электролитах.............748
6.3.3.1. Потенциалы полярографических полуволн неорганических веществ.......................748
6.3.3.2. Потенциалы полярографических полуволн органических соединений......................761
6.4. Амперометрическое титрование..........764
6.5. Инверсионная вольтамперометрия........773
6.5.1. Сущность метода инверсионной вольтамперометрии (ИВ).......................773
6.5.2. Аналитический сигнал в методе ИВ......774
6.5.3. Инверсионная хронопотенциометрия......775
6.5.4. Факторы, влияющие на величину и форму аналитического сигнала.......................775
6.5.4.1. Тип индикаторного электрода.........775
6.5.4.2. Состав фонового раствора............775
6.5.4.3. Потенциал электролиза и его длительность.. 775
6.5.4.4. Обратимый и необратимый электродный процессы в ИВ................................775
6.5.4.5. Растворенные окислители.............776
6.5.4.6. Наложение пиков элементов. Образование интерметаллических соединений................776
6.5.4.7. Поверхностно-активные вещества......777
6.5.4.8. Катодная инверсионная вольтамперометрия. Адсорбционная ИВ.............................778
6.5.4.9. Техника работы в методе ИВ..........778
6.5.5. Электрохимические характеристики процесса разряда-ионизации элементов и условия анализа некоторых материалов методом инверсионной вольтамперометрии...............778
6.5.6. Свойства индикаторных электродов......800
6.5.7. Физико-химические свойства материалов
индикаторных электродов...............802
6.5.8. Способы изготовления и примеры
использования электродов в ИВ.........805
6.6. Кондуктометрия и кондуктометрическое
титрование............................817
Приложение 1.................................826
Приложение 2.................................832
Приложение 3.................................838
1430
Новый справочник химика и технолога
Раздел 7. Масс-спектрометрический метод анализа
7.1. Источники ионов.......................842
7.1.1. Источники с электронным ударом........842
7.1.2. Источники с поверхностной ионизацией
или термоионные источники.............847
7.1.3. Химическая ионизация..................847
7.1.4. Полевая ионизация.....................849
7.1.5. Эмиссия вторичных ионов...............849
7.1.6. Искровые ионные источники.............850
7.1.7. Источник с тлеющим разрядом...........850
7.1.8. Источники ионов с лазерной
десорбцией............................851
7.1.9. Источники с экстракцией ионов
электрическим полем...................851
7.1.10. Источник ионов с ионизацией
индуктивно-связанной плазмой..........852
7.2. Масс-анализаторы......................855
7.2.1. Магнитные секторные анализаторы.......855
7.2.2. Приборы с двойной фокусировкой
(тандемные)...........................855
7.2.3. Времяпролетный масс-анализатор........856
7.2.4. Квадрупольные масс-анализаторы........856
7.2.5. Омегатронный масс-спектрометр.........857
7.2.6. Масс-анализатор на основе
ионно-циклотронного резонанса.........858
7.3. Детектирование ионов..................859
7.4. Анализ изотопного и элементного состава
вещества..............................859
7.4.1. Идентификация органических соединений
и установление их структуры...........863
7.4.2. Определение индивидуального состава
смеси веществ.........................865
7.4.3. Метод изотопного разбавления..........884
7.4.4. Хромато-масс-спектрометр..............885
7.4.5. Жидкостной хромато-масс-спектрометр...886
Раздел 8. Газовый анализ
8.1. Определение газового анализа..........891
8.2. Анализируемые объекты и определяемые
компоненты в газовом анализе..........891
8.3. Задачи, решаемые с помощью газового
анализа...............................891
8.4. Основные направления развития газового
анализа...............................891
8.5. Величины, характеризующие химический
состав газов..........................891
8.6. Физические и физико-химические свойства
чистых газов..........................900
8.7. Методы получения и очистки газов......904
8.7.1. Очистка водорода......................910
8.7.2. Очистка оксида углерода...............911
8.7.3. Очистка диоксида углерода.............911
8.7.4. Очистка метана........................912
8.7.5. Очистка оксида азота..................912
8.7.6. Очистка кислорода.....................912
8.7.7. Очистка азота.........................914
8.7.8. Очистка аргона........................914
8.7.9. Очистка неона.........................915
8.7.10. Очистка гелия........................916
8.8. Производство газовых смесей (ПГС).....916
8.8.1. Основные типы ПГС и требования к ним..916
8.8.2. Условия и особенности приготовления ПГС...........................917
8.8.3. Способы приготовления ПГС.............917
8.8.4. Способы перемешивания компонентов в процессе приготовления смесей.............918
8.8.5. Источники загрязнения газов и методы его предупреждения..........................918
8.8.6. Вспомогательные вещества.............918
8.9. Методы газового анализа..............919
8.9.1. Химические методы....................919
8.9.1.1. Волюмометрический и манометрический методы......................................919
8.9.1.2. Титриметрический метод.............919
8.9.1.3. Термохимический метод..............920
8.9.1.4. Гравиметрический метод.............920
8.9.2. Оптические эмиссионные методы........920
8.9.2.1. Газоразрядный метод................920
8.9.2.2. Флуоресцентный метод...............921
8.9.2.3. Хемилюминесцентный метод...........921
8.9.2.4. Метод рэлеевского рассеяния........921
8.9.2.5. Метод комбинационного рассеяния....922
8.9.3. Оптические абсорбционные методы......922
8.9.3.1. Метод прямого линейного поглощения..922
8.9.3.2. Метод внутрирезонаторного лазерного поглощения..................................923
8.9.3.3. Оптико-акустический метод..........932
8.9.3.4. Термолинзовый метод................924
8.9.3.5. Колориметрический и спектрофотометрический методы..........................924
8.9.4. Масс-спектрометрический метод........925
8.9.5. Хроматографический метод.............925
8.9.6. Электрохимические методы.............926
8.9.7. Методы, основанные на зависимости интегральных свойств газов от содержания определяемого компонента....................926
8.9.7.1. Термокондуктометрический метод.....926
8.9.7.2. Магнитный метод....................927
8.9.7.3. Механический метод.................927
8.9.7.4. Акустический метод.................928
8.9.7.5. Рефрактометрический и интерферометрический методы...............928
8.9.8. Ионизационные методы.................928
8.9.9. Радиоспектроскопический метод........928
8.9.10. Метод изотопного разбавления........929
8.9.11. Методы изотопного анализа газов и газообразующих элементов..................929
8.9.12. Методы определения газовых включений и газообразующих элементов в веществах конденсированной фазы.......................930
8.9.13. Методы определения дисперсной фазы в газах.....................................932
8.9.13.1. Методы определения примесей масла в газах.....................................933
8.9.13.2. Методы измерения содержания влаги
в газах.....................................933
8.9.13.3. Методы измерения содержания твердой
дисперсной фазы (пыли)......................934
8.9.13.4. Методы определения радиоактивных
веществ в газах.............................936
Оглавление
1431
8.9.14. Дистанционные методы газового анализа.936
8.10. Метрологические аспекты газового анализа.....................................936
8.10.1. Понятие «метрологическое обеспечение газового анализа» и его структура...........936
8.10.2. Метрологический подход в газовом анализе, его основные направления и формы............937
8.10.3. Метрологические характеристики анализаторов газов..........................939
8.10.4. Чистые газы как средства обеспечения единства газоаналитических измерений.........940
8.10.5. Поверочные газовые смеси............941
8.10.6. Генераторы газовых смесей...........942
8.10.7. Использование стандартных образцов чистых газов и газовых смесей для построения градуировочных характеристик анализаторов..................943
8.10.8. Государственная поверочная схема для средств измерений содержания компонентов в газовых средах................945
АНАЛИТИЧЕСКАЯ ХИМИЯ. Ч. 2 (ЗЕЛЕНЫЙ) Раздел 9. Ядерно-физические и радиохимические методы анализа
9.1. Активационный анализ...................3
9.1.1. Теоретические основы активационного
анализа................................3
9.1.2. Инструментальный анализ. Другие варианты
активационного анализа.................4
9.1.3. Нейтронный активационного анализа......6
9.2. Фотоядерный активационного анализа..59
Раздел 10. Химические методы обнаружения ионов
(качественный химический метод анализа)
10.1. Основные понятия и терминология.......71
10.2. Приемы и техника выполнения реакций...73
10.3. Аналитические реакции ионов...........74
10.3.1. Индивидуальные реакции ионов.........74
10.3.2. Групповые реактивы..................106
10.4. Аналитические группы ионов и схемы
анализа..............................120
10.4.1. Катионы.............................120
10.4.2. Анионы..............................147
10.4.3. Реактивы для отдельных групп ионов..154
10.4.4. pH осаждения гидроксидов............157
10.4.5. Некоторые частные методы разделения ионов.......................................160
Раздел 11. Химические тест-методы анализа
11.1. Общая характеристика тест-систем.....209
11.1.1. Дефиниции...........................209
11.1.2. Цели использования и достоинства....209
11.1.3. Классификация.......................211
11.2. Химические основы тестов: реагенты и реакции...................................212
11.2.1. Общие сведения .....................212
11.2.2. Кислотно-основные реакции...........212
11.2.3. Реакции окисления—восстановления ...212
11.2.4. Реакции комплексообразования........213
11.2.5. Реакции синтеза органических соединений ...214
11.3. Способы использования реагентов......214
11.3.1. Тест-системы.........................214
11.3.2. Химическая иммобилизация.............216
11.3.3. Каталитические реакции...............217
11.4. Средства и приемы анализа жидких сред.218
11.4.1. Бумажные полоски и их аналоги .......218
11.4.2. Индикаторные бумаги для погружения в жидкость..................................218
11.4.3. Концентрирование продуктов реакции...219
11.4.4. Тест-титрование с бумагами...........219
11.4.5. Индикаторные порошки.................220
11.4.6. Индикаторные грубки..................220
11.4.7. Таблетки и подобные им формы.........222
11.4.8. Обычные ампулы и капельницы..........224
11.4.9. Самонаполняющиеся ампулы.............224
11.4.10. Наборы для титрования..................
11.5. Методология и области применения тест-систем.................................225
11.5.1. Анализ воды и почвы (как объектов окружающей среды) на неорганические компоненты...................................225
11.5.2. Обобщающие тесты. Определение суммарных показателей........................225
11.5.3. Анализ воды и почвы на органические компоненты..................................242
11.5.4. Анализ воздуха.......................243
11.5.5. Обнаружение паров алкоголя, наркотиков,
отравляющих и взрывчатых веществ......244
11.6. Области применения тест-систем........245
11.6.1. Использование в медицине.............245
11.6.2. Использование в учебных целях........245
Раздел 12. Проточно-инжекционный анализ (ПИА)
12.1. Теория ПИ А...........................252
12.2. Схемы осуществления ПИА...............255
12.2.1. ПИА с непрерывным потоком носителя...255
12.2.2. Последовательный инжекционный анализ
(Sequential Injection Analysis — SIA).261
12.2.3. Bead Injection (BI) инжекция в гидравлические линии с бусинками, зернами, шариками наполнителями......................264
12.2.4. Микропроточно-инжекционный анализ....264
Раздел 13. Кинетические методы анализа
13.1. Индикаторные реакции в кинетических методах анализа..............................278
13.2. Каталиметрическое титрование..........318
13.3. Кинетические методы анализа, основанные на гетерогенных каталитических электродных реакциях (каталитических полярографических волнах)....................320
13.4. Использование некаталитических реакций в кинетических методах анализа...............323
13.5. Методики определения некоторых элементов кинетическим методом в реальных
образцах.............................324
Раздел 14. Методы спектроскопического анализа
14.1. Общие положения.......................331
14.2. Методы атомной спектроскопии..........343
Основные положения..........................343
База опорных спектроскопических данных......354
14.2.1. Методы атомно-эмиссионной спектроскопии.... 359
1432
Новый справочник химика и технолога
Краткие теоретические сведения...............359
Источники возбуждения спектров...............363
Спектральные приборы.........................381
Регистрация спектров.........................391
Спектрографические методы анализа............398
Визуальный анализ............................409
Спектрометрический анализ....................413
Отбор и подготовка проб к анализу............416
Метрологические характеристики...............419
Приложение I. Справочные таблицы к 14.2.1....435
Таблица 1П1. Чувствительные линии, их вероятности переходов и силы осцилляторов (по элементам)...............................435
Таблица 2П1. Чувствительные линии (по длинам волн).............................452
Таблица ЗШ. Стандарты длин волн..............459
Таблица 4П1. Поправка ДХ для перехода от длины волны в воздухе (Хвозд) к длине волны в вакууме (Хвак): Хвак = Хвозд + ДХ..........465
Таблица 5П1. Аналитические линии атомов и канты молекулярных полос, возбуждаемые в пламени....................................465
Таблица 6Ш. Длины волн спектральных линий и кантов молекулярных полос, возбуждаемых в пламени (в порядке возрастания).....478
Таблица 7П1. Совпадения спектральных линий элементов.............................482
Таблица 8П1. Наиболее надежные табличные данные по длинам волн, энергетическим уровням, вероятностям переходов, полуширинам спектральных линий и их смещениям.............598
Таблица 9Ш. Энергии ионизации атомов и ионов.600
Таблица 10Ш. Температуры плавления и кипения элементов и их оксидов.......................601
Таблица 11П1. Степень ионизации и продолжительность пребывания атомов элементов в плазме «медной дуги».............603
Таблица 12П1. Таблицы для визуальных методов анализа...............................605
Таблица 13П1. Таблицы для качественного спектрографического анализа...........637
Таблица 14П1. Таблицы гомологических пар линий для полуколичественного спектрографического анализа..................647
Таблица 15Ш. Вспомогательные таблицы для количественного спектрографического анализа......................................651
Таблица 16Ш. Рекомендации по методам количественного спектрографического анализа различных материалов.................665
Таблица 17Ш. Применение химического обогащения при спектральном анализе чистых металлов.......................683
Таблица 18П1. Количественный анализ руд и минералов...........................686
Таблица 19П1. Методики спектрометрического анализа некоторых металлов и сплавов...725
Таблица 20Ш. Таблицы для работы с источником индуктивно-связанной плазмы...........730
Таблица 21П1. Справочные данные по аппаратуре для атомно-эмиссионного спектрального анализа.....................................775
Таблица 22П1. Российские и другие стандарты на методы атомно-эмиссионного спектрального анализа различных веществ и материалов................................821
14.2.2 . Методы атомно-абсорбционной и атомно-флуоресцентной спектроскопии ... 824
Физические основы атомно-абсорбционного метода.824
Источники резонансного излучения...............827
Принципиальные схемы атомно-абсорбционных спектрофотометров...........................828
Атомизация в пламенах..........................831
Формирование поглощающего слоя в электротермических атомизаторах...........837
Атомизаторы на основе тлеющего разряда.........843
Способы атомизации с образованием летучих соединений..................................844
Регистрация аналитических сигналов и способы градуировки атомно-абсорбционных спектрофотометров ..........................847
Метрологические характеристики ААС.............849
Метод атомно-флуоресцентной спектроскопии......850
Атомно-ионизационный спектральный анализ.......854
Подготовка проб к анализу......................858
Литература.....................................872
Приложение 11. Справочные таблицы к 14.2...... 879
Таблица 1ПП. Некоторые резонансные линии элементов, наиболее чувствительные при поглощении, и значения их сил осцилляторов.................................879
Таблица 2Ш1. Параметры ударного уширения спектральных линий....................880
Таблица ЗПП. Сверхтонкая структура некоторых спектральных линий....................880
Таблица 4ПП. Зависимость линейчатого поглощения от koi для нерасщепленной линии.......881
Таблица 5Ш1. Зависимость полного поглощения Aw от koi для изолированной нерасщепленной линии при различных значениях а.......883
Таблица 6ПП. Характеристики источников резонансного излучения................883
Таблица 7ПП. Характеристики некоторых пламен горения с предварительным смешением газов.......................................898
Таблица 8ПП. Ионизация некоторых элементов в пламенах «воздух—ацетилен» и «оксид азота(1)—азот—ацетилен»...............898
Таблица 9ПП. Совпадения линий элементов в атомно-абсорбционной спектрометрии.........899
Таблица ЮПП. Потенциальные спектральные помехи, обусловленные свойствами дейтериевого корректора фона................899
Таблица НПП. Коэффициенты диффузии атомов
элементна в аргоне при давлении
/> = 0,101 МПа.......................900
Таблица 12ПП. Максимальные температуры
пиролиза с палладий-магниевым
Оглавление
1433
модификатором и без него, а также оптимальные температуры атомизации некоторых элементов..................901
Таблица 13ПП. Факторы Зеемана, измеренные в режиме интегральной абсорбции в переменном магнитном поле 0,9 Тс на атомизаторе..............................902
Таблица 14ПП. Условия и некоторые особенности определения отдельных элементов атомно-абсорбционным методом в пламени...................................902
Таблица 15ПП. Условия и некоторые особенности определения отдельных элементов с применением электротермических
атомизаторов...........................917
Таблица 16ПП. Основные параметры определения элементов в графитовых печах в условиях квазиизотермической атомизации................922
Таблица 17ПП. Условия концентрирования гидридообразующих элементов в графитовых печах с модифицированной поверхностью...............................925
Таблица 18ПП. Основные технические характеристики атомно-абсорбционных спектрофотометров универсального
назначения............................925
Таблица 19ПП. Специализированные АА-спектрофотометры..........................933
ица 20ПП. Характеристики некоторых типов фотоэлектронных умножителей, применяемых для измерений сигналов абсорбции......936
Таблица 21ПП. Пределы обнаружения ряда элементов в твердых образцах с атомизатором на основе тлеющего разряда......................................937
Таблица 22ПП. Сравнительные данные по пределам обнаружения элементов с применением разных типов атомизаторов....................937
Таблица 23ПП. Характеристические массы элементов для разных видов электротермических атомизаторов.......938
Таблица 24ПП. Аналитические линии для метода атомной флуоресценции ................940
Таблица 25ПП. Пределы обнаружения элементов методами пламенной атомно-эмиссионной спектрометрии................................944
Таблица 26ПП. Пределы обнаружения элементов методами атомно-флуоресцентного анализа....944
Таблица 27ПП. Пределы обнаружения элементов для метода атомно-флуоресцентной спектрометрии при распылении анализируемых растворов в источник ИСП и применении ламп с полым катодом в качестве источника возбуждающего излучения......................945
Таблица 28ПП. Пределы обнаружения элементов для метода атомно-флуоресцентной спектрометрии при распылении анализируемых растворов в источник ИСП и применении лазеров для возбуждения флуоресценции....................946
Таблица 29ПП. Сводка аналитических результатов по применению пламенного и печного атомизаторов в методе АФС с лазерным возбуждением.................................947
Таблица ЗОПП. Аналитические характеристики основных оптических атомно-спектральных методов элементного анализа твердых и жидких чистых веществ......................948
Таблица 31ПП. Методики атомно-абсорбционного анализа воды и стоков, одобренные Агентством охраны окружающей среды США....................................949
Таблица 32ПП. Воды природные, питьевые, очищенные сточные, сточные и морские. Стандартизованные методики атомно-абсорбционного анализа................951
Таблица ЗЗПП. Почва и донные отложения. Стандартизованные методики атомно-абсорбционного анализа................954
Таблица 34ПП. Перечень стандартизованных методик атомно-абсорбционного анализа, применяемых в региональных лабораториях Госсанэпиднадзора М3 РФ......................956
Таблица 35ПП. Аттестованные методики анализа для АА-спсктрофотометров серии «КВАНТ»................................957
Таблица 35аП11. Аттестованные методики анализа для использования в комплекте с атомно-абсорбционным спектрофотометром МГА-915....................958
Таблица ЗбПП. Стандартные образцы состава водных растворов.............................959
Таблица 37ПП. Некоторые примеры практического применения метода атомно-флуоресцентной спектрометрии с возбуждением спектров в источнике индуктивно-связанной плазмы.......................................964
Таблица 38ПП. Спектроскопические методы многоэлементного анализа воды после предварительного концентрирования примесей.....................................965
Таблица 39ПП. Спектроскопические методы многоэлементного анализа материалов для электронной техники......................968
Таблица 40ПП. Спектроскопические методы многоэлементного анализа керамических материалов...................................969
Таблица 41 ПП. Спектроскопические методы определения алюминия в водах и диализных жидкостях....................................970
Таблица 42ПП. Спектроскопические методы определения кадмия в воде.............971
Таблица 43ПП. Спектроскопические методы определения мышьяка в воде............972
Таблица 44ПП. Спектроскопические методы
определения мышьяка в геохимических
материалах...................................972
Таблица 45ПП. Спектроскопические методы
определения кадмия в клинических
образцах.....................................973
1434
Новый справочник химика и технолога
Таблица 46ПП. Спектроскопические методы определения ртути в воде....................974
Таблица 47ПП. Спектроскопические методы определения ртути в геологических материалах..................................975
Таблица 48ПП. Спектроскопические методы определения ртути в биологических материалах...........................975
Таблица 49ПП. Спектроскопические методы определения селена в воде............976
Таблица 50ПП. Комбинированные процедуры определения селена в клинических образцах спектроскопическими методами................977
Таблица 51ПП. Спектроскопические методы определения селена в неклинических биологических материалах.............978
Таблица 52ПП. Спектроскопические методы определения урана в природных водах...979
АНАЛИТИЧЕСКАЯ ХИМИЯ. Ч. 3 (Зеленый)
Раздел 14. Методы спектроскопического анализа
14.3. Методы рентгеновской спектроскопии.....3
14.3.1. Физические основы......................4
14.3.2. Аппаратура............................11
14.3.3. Способы рентгенофлуоресцентного
анализа................................33
14.3.4. Подготовка проб к анализу.............36
14.3.5. Метрологические характеристики метода.39
14.3.6. Практическое применение
рентгенофлуоресцентного анализа........41
14.3.7. Электронно-зондовый микроанализ.......43
14.3.8. Рентгеновский дифракционный анализ....46
14.3.9. Метод Оже-электронный спектроскопии...50
Приложение III. Справочные таблицы к 14.3.....56
Таблица 1П1П. Длины волн и энергии линий характеристического излучения (по элементам)........................56
Таблица 2П1П. Длины волн основных аналитических линий...................92
Таблица ЗПП1. Длины волн и энергии краев поглощения...................................93
Таблица 3.1ПШ. Длины волн и соответствующие им энергии К- и L-краев поглощения...........93
Таблица 3.2ПШ. Длины волн и соответствующие им энергии М-краев поглощения................95
Таблица З.ЗПП1. Длины волн и соответствующие им энергии Nj-краев поглощения........98
Таблица 4ПП1. Относительные интенсивности линий.................................98
Таблица 4.1ПШ. К-серия........................98
Таблица 4.2ПШ. L-серия.......................100
Таблица 4.3П1П. М-серия......................102
Таблица 5ПШ. Скачки поглощения для К-, L- и М-краев................................102
Таблиц 6ПШ. Массовые коэффициенты ослабления рентгеновского излучения.........103
Таблица 6.1ПШ. Коэффициенты С, а, 0 и v для вычисления массового коэффициента ослабления излучения с длиной волны Х<ХМ, ......................................104
Таблица 6.2П111. Коэффициенты С„............105
Таблица 6.3П1П. Коэффициенты С, а и 0 для вычисления массового коэффициента ослабления излучения с длиной волны X>XMj ......................................106
Таблица 6.4П1П. Массовые коэффициенты фотоэлектрического поглощения для области длин волн от 4 до 44 А...107
Таблица 6.5ПШ. Массовые коэффициенты ослабления для линии КО] в интервале длин волн 0,1-10 А (по элементам)....110
Таблица 6.6П1П. Массовые коэффициенты ослабления для линии Кр в интервале длин волн 0,1-10 А (по элементам)....124
Таблица 6.7ПШ. Массовые коэффициенты ослабления для линии La) в интервале длин волн 0,1-10 А (по элементам)....138
Таблица 6.8ПШ. Массовые коэффициенты ослабления для линии Lp в интервале длин волн 0,1-10 А (по элементам)....149
Таблица 6.9П1П. Массовые коэффициенты ослабления для линии Ма) в интервале длин волн 0,1-10 А (по элементам)....159
Таблица 6.10П1П. Массовые коэффициенты ослабления для линии Мр в интервале длин волн 0,1-10 А (по элементам)....162
Таблица 7ПШ. Выход флуоресценции............166
Таблица 7.1ПШ. Экспериментальные и расчетные значения выхода флуоресценции К-оболочек..................................166
Таблица 7.2П1П. Выходы флуоресценции L-подоболочек........................167
Таблица 7.3П1П. Выход флуоресценции М-оболочек...........................168
Таблица 8ПШ. Характеристики кристаллов-анализаторов..............168
Таблица 8.1П1П. Монокристаллы для рентгеноспектральных исследований............170
Таблица 8.2П1П. Многослойные синтетические структуры для рентгеноспектральных исследований................................170
Таблица 8.3П1П. Кристалл-дифракционные диспергирующие элементы..............171
Таблица 9ПШ. Новые детекторы рентгеновского излучения............................171
Таблица 9.1ПШ. Газоразрядные пропорциональные и сцинтилляционные детекторы.........171
Таблица 9.2ПШ. Позиционно-чувствительные детекторы............................172
Таблица 9.3П111. Блок детектирования газовый
электролюминесцентный Б ДЭЛ Г-3 ДМ..........173
Таблица 10ПШ. Приборы для
рентгенофлуоресцентного анализа.............173
Таблица 10.1ПШ. Портативные рентгенофлуорес-
центные спектрометры серии
«Спектроскан»...................;...........173
Оглавление
1435
Таблица 10.2ПП1. Другие портативные и переносные рентгенофлуоресцентные анализаторы.................................175
Таблица 10.3П111. Зарубежные стационарные рентгенофлуоресцентные спектрометры..........181
Таблица 10.4П1П. Зарубежные рентгенофлуоресцентные анализаторы для контроля технологических процессов...................185
Таблица 11ПШ. Радиоизотопы, используемые в качестве источников возбуждения рентгеновской флуоресценции...........186
Таблица 12ПШ. Малоинформативные рентгенодифракционные спектры.................189
Таблица 13П111. Приборы для рентгенофазового анализа...............................195
Таблица 14П1П. Энергии KLL-переходов Оже-электронов........................195
Таблица 15TU1I. Эмпирические факторы элементной чувствительности для метода РФЭС......198
Таблица 16П111. Энергии связи электронов для различных оболочек атомов.........201
Таблица 17П1П. Таблицы для расчетов в методе рентгеноспектрального микроанализа....204
Таблица 17.1ПШ. Наиболее распространенные методы расчета ZAF-поправок...........204
Таблица 17.2П1Н. Длины волн, энергии фотонов и критические энергии возбуждения К-линий.....................................204
Таблица 17.3ПШ. Длины волн, энергии
Laj- и Lpj-линий и критические энергии возбуждения Ь1П-уровней..............205
Таблица 17.4ПШ. Длины волн и энергии фотонов Ма-линий......................206
Таблица 17.5ПП1. Формулы для расчета энергий эмиссионных линий и критических энергий возбужде ния..........................207
Таблица 17.6П111. Исходные данные для расчета поправочных факторов..................207
Таблица 17.7ПШ. Коэффициенты обратного рассеяния электронов..................209
Таблица 17.8ПШ. Значения фактора обратного рассеяния электронов..................209
Таблица 17.9Ш11. Коэффициенты полиномов Шпрингера для расчета фактора обратного рассеяния электронов........................210
Таблица 17.10ПШ. Значения массовых коэффициентов поглощения элементов-поглотителей с высокоэнергетической стороны от К-края поглощения элементов-излучателей, используемые при расчете поправки на флуоресцен-
цию, возбуждаемую непрерывным спектром...........................211
Таблица 17.11 ТИП. Формулы для расчетов массовых коэффициентов поглощения...212
Таблица 17.12П111. Коэффициенты q и гц для элементов с малыми z...........212
Таблица 17.13ПШ. Наименьшие атомные числа элементов, флуоресцентно возбуждающих Ка-линии..................................212
Таблица 17.14П111. Наименьшие атомные числа элементов, флуоресцентно возбуждающих
Ьа-линии................................213
Таблица 17.15ПП1. Данные для расчета поправки на К-К- и L-K-флуоресценцию..........213
Таблица 17.16ПП1. Данные для расчета поправки на L-L- и K-L-флуоресценцию..........214
Таблица 17.17ПШ. Отношение интенсивностей
Кр- и Ка-линий ряда элементов...........216
Таблица 17.18П111. Перекрывание Кр- и Ка-пиков.216
Таблица 17.19ПП1. Эмпирические коэффициенты перекрывания Ка-пиков в спектрах, регистрируемых ЭД-спектрометрами............216
Таблица 17.20ПШ. Сравнительная характеристика рентгеновских спектрометров.................217
14.4. Методы молекулярной спектроскопии....218
14.4.1. Электронные спектры поглощения.
Основные положения теории............221
14.4.2. Фотометрические методы анализа......223
Общие положения......................223
Спектрофотометрия в УФ- и в видимой области..............................224
Классификация фотометрических методов по типу используемых реакций.227
Оптические свойства окрашенных соединений в растворах...............228
Выбор спектральной области для фотометрических измерений........232
Светофильтры.........................234
Органические фотометрические реагенты.............................235
Органические растворители............267
Чувствительность фотометрических определений следов элементов.........268
Коэффициент чувствительности.........269
Условные характеристики чувствительности фотометрического определения...270
Выбор оптимальных условий фотометрического определения.........288
Воспроизводимость фотометрических методов анализа......................290
Спектрофотометрические методы в анализе природных, производственных объектов и объектов окружающей среды................................291
УФ- и видимая спектрофотометрия в анализе органических соединений....312
14.4.3. Фотометрические методы количественного анализа................................312
Фотометрические методы определения веществ в отсутствие мешающих компонентов..........................312
Методы определения одного вещества......312
Фотометрические методы анализа в присутствии мешающих компонентов...318
Дифференциальный фотометрический анализ...............................327
Экстракционно-фотометрический метод.....330
Спектрофотометрическое титрование.....331
1436
Новый справочник химика и технолога
Твердофазная спектрофотометрия........334
14.4.4. Аппаратура; общие замечания при работе на фотоколориметрах и спектрофотометрах..........................341
Растворы сравнения (нулевые растворы).341
Поправка на холостой опыт.............341
Чувствительность; правильность результата анализа....................342
Фотоэлектроколориметры................342
Спектрофотометры......................345
Краткие характеристики отечественных УВИ-спектрофотометров и некоторые области их применения.................345
Некоторые модели зарубежных спектрофотометров и аксессуары к ним.........350
Приложение IV. Справочные таблицы к 14.4.....362
Таблица 14.4.1. Обзор некоторых основных атласов по УФ- и видимой спектроскопии...............362
Таблица 14.4.5. Абсорбционные характеристики некоторых полициклических ароматических соединений...................................362
Таблица 14.4.8. Абсорбционные характеристики
А-гетероциклических соединений; некоторых производных бензола, нафталина и антрацена...........................363
Таблица 14.4.30. Методы определения алюминия в органических материалах.............365
Таблица 14.4.42. Методы определение олова в металлах и сплавах..................365
Таблица 14.4.43. Методы определения сурьмы в металлургических материалах.........367
Таблица 14.4.44. Определение сурьмы в цветных металлах и сплавах....................368
Таблица 14.4.45. Методы определения ниобия и тантала в минералах и рудах.........369
Таблица 14.4.46. Методы определения ниобия и тантала в железе и сталях..................371
Таблица 14.4.47. Методы определения титана в железе и сталях.....................373
Таблица 14.4.48. Методы определения тория в силикатных породах..................376
Таблица 14.4.49. Методы определения урана в силикатных породах..................377
Таблица 14.4.50. Методы определения циркония в железе и в сталях...................378
Таблица 14.4.51. Важнейшие органические реактивы для определения органических веществ .....................................381
Таблица 14.4.52. Типичные применения спектрофотометрии в органическом анализе, рассмотренные White..........................387
Таблица 14.4.53. Перечень групп органических соединений, для которых рассмотрены фотометрические методы определения.....387
Таблица 14.4.54. Химические реакции, использованные И.М. Коренманом для определения органических соединений ....387
Таблица 14.4.55. Перечень 18 важнейших функциональных групп, определение которых
в различных органических соединениях рассмотрены Siggia....................387
Таблица 14.4.56. Важнейшие реакции для фотометрических и флуориметрических определений альдегидов, кетонов и стероидов..................................388
Таблица 14.4.57. Спектральные характеристики растворов азосоединений, образующихся при взаимодействии 4-нитрофенилдиазония с фенолами в среде разных растворителей... 389
Таблица 14.4.58. Спектральные характеристики азосоединений, образующихся при фотометрическом определении первичных ароматических аминов.........................389
Таблица 14.4.59. Определение первичных ароматических аминов (диазосоставляющих) в виде азососдинений.........................390
Таблица 14.4.60. Определение фенолов в виде азосоединений................................393
Таблица 14.4.61. Спектральные характеристики продуктов, образующихся при определении фенолов с применением 4-аминоантипиринаи феррицианида калия...........................395
Таблица 14.4.62. Окраска растворов при реакциях
1,3- динитробензола с кетонами и альдегидами в щелочной среде........396
Таблица 14.4.63. Определение альдегидов, основанное на реакции с 4-диметиламиноанилиновом...................396
Таблица 14.4.64. Спектральные характеристики продуктов, полученных из ароматических нитросоединений в среде диметилформамида и ацетона....................................396
Таблица 14.4.65. Спектральные характеристики продуктов, полученных из динитросоединений в среде диметилсульфоксида...................397
Таблица 14.4.66. Спектральные характеристики продуктов, полученных из карбонильных соединений при реакции с 1,3-динитробензолом.....................................398
Таблица 14.4.67. Спектральные характеристики продуктов, полученных из карбонильных соединений при реакции с 4-нитрофенил-гидразином...................................398
Таблица 14.4.68. Окраска растворов и Хмакс при реакциях первичных ароматических аминов с 4-диметиламинобензальдегидом...............398
Таблица 14.4.69. Окраска растворов при реакциях альдегидов и кетонов с фенолом в сернокислой среде...................400
Таблица 14.4.70. Определение ароматических углеводородов.........................402
Таблица 14.4.71. Общие приемы, позволяющие устранить или минимизировать ошибки в фотометрических методах анализа, обусловленные посторонними веществами........403
Таблица 14.4.74. УВ-видимая спектрофотометрия:
минералы и другие неорганические твердые
вещества.....................................405
Оглавление
1437
Таблица 14.4.75. УФ-видимая спектрофотометрия: неорганические газы и пары.............406
Таблица 14.4.78. УФ-видимая производная спектрофотометрия: алкалоиды...........406
Таблица 14.4.79. УФ-видимая производная спектрофотометрия: антибиотики.........406
Таблица 14.4.80. Методы для анализа аминокислот и протеинов............................407
Таблица 14.4.81. УФ-видимая производная спектрофотометрия: аминокислоты........407
Таблица 14.4.82. УФ-видимая производная спектрофотометрия: протеины............408
Таблица 14.4.83. УФ-видимая производная спектрофотометрия: энзимы..............409
Таблица 14.4.84. УФ-видимая производная спектрофотометрия: гемоглобин..........409
Таблица 14.4.85. УФ-видимая производная спектрофотометрия: хлорофил и другие растительные пингменты.................409
Таблица 14.4.86. УФ-видимая производная спектрофотометрия: красители...........410
Таблица 14.4.87. Клинические и судебные анализы................................410
Таблица 14.4.90. УФ-видимая производная спектрофотометрия: напитки ............411
Таблица 14.4.91. Сопоставление некоторых экстракционно-фотометрических методов определения элементов с основными красителями..................................412
Таблица!4.4.92. Экстракционно-спектрофотометрическое определение с кислотными красителями; металлы закомплексованы 1.10-фенантролином............................413
Таблица 14.4.93. Флотационно-спектрофотометрические методы определения элементов..........413
14.4.5. Инфракрасные спектры поглощения......429
14.4.5.1. Основные положения теории колебательных спектров.......................429
14.4.5.2. Особенности техники и методики измерения инфракрасных спектров поглощения.........432
14.4.5.3. Качественный и количественный анализ по инфракрасным спектрам.....................435
Качественный анализ органических соединений по ИК-спектрам поглощения.......435
Алкильные радикалы....................435
Ароматические соединения..............452
Гетероциклические соединения..........453
Органические соединения азота.........453
Качественный анализ неорганических соединений по ИК-спектрам поглощения..454
Количественный анализ по ИК-спектрам поглощения............................474
14.4.6. Спектры нарушенного полного внутреннего отражения........................479
14.4.6.1. Основные положения теории..........479
14.4.6.2. Особенности жидкостной и твердотельной методики НПВО................................481
14.4.6.3. Качественный и количественный анализ по спектрам оптических постоянных............484
Оптические постоянные.....................485
14.4.7. Люминесценция и люминесцентные методы анализа............................498
14.4.7.1. Виды люминесценции..............498
14.4.7.2. Основные характеристики люминесценции.............................500
14.4.7.3. Интенсивность люминесценции и концентрации люминофора.................500
14.4.7.4. Атомная флуоресценция...........501
14.4.7.5. Молекулярная фотолюминесценция..502
14.4.7.6. Основные закономерности молекулярной люминесценции.............................503
14.4.7.7. Тушение люминесценции...........505
14.4.7.8. Рекомбинационная люминесценция кристаллофосфоров.........................508
14.4.7.9. Люминесцентные спектральные приборы... 512
14.4.7.10. Люминесцентный анализ..........513
Библиография..............................521
Русско-английский словарь терминов........592
Англо-русский словарь терминов............627
Приложение V. Приготовление стандартных растворов.................................667
Приготовление разбавленных растворов кислот и щелочей...................675
Правило креста.....................676
Плотность воды при различных температурах.......................676
Буферные растворы..................677
Маскирующие реагенты для металлов и некоторых анионов................684
СЫРЬЕ И ПРОДУКТЫ ПРОМЫШЛЕННОСТИ ОРГАНИЧЕСКИХ И НЕОРГАНИЧЕСКИХ
ВЕЩЕСТВ. Ч. 1. (Оранжевый)
Раздел 1. Вода и воздух 1.1. Вода................................5
1.2. Воздух.............................40
Раздел 2. Минеральное сырье
2.1. Характеристика важнейших видов
минерального сырья..................59
2.2. Требования к качеству минерального
сырья...............................79
2.3. Химический состав важнейших видов
сырья...............................97
2.4. Свойства важнейших минералов, входящих
в состав природного сырья..........116
Раздел 3. Характеристика важнейших продуктов промышленности неорганических веществ
Таблица «Характеристика важнейших продуктов промышленности неорганических веществ»..................................205
Дополнительные материалы к таблице «Характеристика важнейших продуктов промышленности неорганических веществ»...................278
Раздел 4. Неорганические вяжущие вещества
4.1. Воздушные вяжущие вещества.........287
4.1.1. Гипсовые вяжущие вещества..........287
4.1.2. Воздушная известь..................287
4.1.3. Магнезиальные вяжущие вещества.....288
1438
Новый справочник химика и технолога
4.2 Гидравлические вяжущие вещества.......288
4.2.1. Известь гидравлическая................288
4.2.2. Портландцемент........................288
4.2.3. Шлакопортландцемент...................289
4.2.4. Глиноземистые цементы.................289
4.2.5. Многокомпонентные цементы.............289
4.3 . Специальные цементы...............289
4.3.1. Декоративные цементы..................289
4.3.2. Расширяющиеся и напрягающие цементы ...289
4.3.3. Тампонажные цементы...................290
4.3.4. Свойства сульфатостойких цементов.....291
4.3.5. Кислотоупорные цементы................291
4.3.6. Шлакощелочные вяжущие вещества........291
4.3.7. Фосфатные вяжущие системы.............293
4.3.8. Щелочные силикатные связки............294
4.3.9. Полимерцементныс вяжущие..............295
4.3.10. Классификация цементов, общие
технические требования................296
4.3.11. Добавки..............................297
4.3.12. Перечень стандартов на материалы
и методы испытания вяжущих веществ....301
Раздел 5. Огнеупоры
5.1. Классификация огнеупоров..............323
5.2. Огнеупоры для черной металлургии......325
5.3. Огнеупоры для стекловарения...........326
5.4. Огнеупоры для цементных печей.........328
5.5. Теплоизоляционные огнеупоры...........329
5.6. Перечень стандартов на методы испытаний
и маркировку огнеупорных изделий и материалов..........................330
Раздел 6. Химически стойкая керамика
6.1. Посуда и оборудование лабораторные
фарфоровые (ГОСТ 9147-80).............333
6.2. Плитки кислотоупорные и
термокислотоупорные керамические (ГОСТ 961-89).........................335
6.3. Насадки кислотоупорные керамические
(ГОСТ 17612-89).......................338
6.4. Кирпич кислотоупорный (ГОСТ 474-90)...340
6.5. Трубы керамические канализационные
(ГОСТ 286-82).........................343
Раздел 7. Стекло
7.1. Важнейшие физико-химические свойства
стекла................................345
7.1.1. Пределы изменения физических свойств
стекла................................345
7.1.2. Вязкость стекол.......................345
7.1.3. Электрические свойства стекла.........346
7.1.4. Механические свойства стекла..........349
7.1.5. Химическая устойчивость стекол........349
7.2. Промышленные стекла, их состав
и свойства............................352
7.2.1. Кварцевое стекло......................352
7.2.2. Химико-лабораторное стекло............354
7.2.3. Электродное стекло....................355
7.2.4. Электровакуумное стекло...............356
7.2.5. Состав стекол для окон рентгеновских трубок
и пропускание ими рентгеновских лучей.358
7.2.6. Состав и свойства некоторых припоечных
стекол................................358
7.2.7. Стекла для квантовых генераторов света
(лазерные стекла).......................358
7.2.8. Стеклокристалличсские материалы
(ситаллы)...............................359
7.2.9. Оптическое стекло......................359
7.3. Состав промышленных стекол различного
назначения..............................360
7.3.1. Состав стекол, применяемых в атомной
технике.................................361
7.3.2. Пористые стекла........................361
Раздел 8. Неорганические сорбенты
8.1. Оксидные сорбенты......................363
8.1.1. Цеолиты................................363
8.1.1.1. Природные цеолиты.....................363
8.1.1.2. Синтетические цеолиты.................365
8.1.1.3. Молекулярно-ситовые свойства цеолитов ... 366
8.1.1.4. Кислотостойкие цеолиты................368
8.1.2. Силикагели.............................370
8.1.2.1. Типы промышленных силикагелей.........371
8.1.2.2. Химически модифицированные силикагели
(кремнеземы)............................372
8.1.3. Активный оксид алюминия................374
8.1.4. Глины..................................377
8.2. Технология получения сорбентов.........378
8.2.1. Получение синтетических цеолитов.......378
8.2.1.1. Гранулированные цеолиты...............379
8.2.1.2. Гранулирование цеолитов без связующих
веществ.................................381
8.2.1.3. Получение кислотостойких цеолитов.....381
8.3. Добыча природных цеолитов..............382
8.4. Технология получения силикагелей и
активного оксида алюминия, основные параметры процесса......................382
8.4.1. Получение силикагелей..................382
8.4.2. Получение активного оксида алюминия....384
8.5. Добыча глинистых материалов............385
8.6. Основные области применения
адсорбентов.............................368
8.6.1. Очистка газовых сред. Осушка газов.....386
8.6.2. Технология осушки газов на силикагелях.... 386
8.6.2.1. Принципиальные схемы осушающих
установок...............................386
8.6.2.2. Установки одновременной осушки
и отбензинивания газов..................388
8.6.2.3. Осушка газа под высоким давлением.....390
8.6.3. Технология осушки газов на цеолитах....391
8.6.3.1. Осушка в газовой промышленности.......391
8.6.3.2. Осушка природного газа на промыслах...391
8.6.3.3. Осушка газа на газобензиновых заводах.392
8.6.3.4. Осушка природного газа, закачиваемого
в пласт.................................392
8.6.3.5. Осушка природного газа на криогенных
установках...........................393
8.6.3.6. Осушка в нефтеперерабатывающей
промышленности.......................394
8.6.3.7. Осушка непредельных углеводородов..394
8.6.3.8. Осушка изопропилена с одновременной
очисткой от изопропилового спирта....395
8.6.3.9. Осушка газов риформинга............396
Оглавление
1439
8.6.3.10. Осушка сырья на установках алкилирования.................................396
8.6.4. Технология очистки от паров летучих соединений....................................397
8.6.4.1. Очистка от сероводорода.............397
8.6.4.2. Очистка от S-органических соединений.398
8.6.4.3. Очистка от диоксида углерода........398
8.6.4.4. Очистка газов от аммиака............400
8.6.5. Адсорбционное разделение газов и паров....401
8.6.5.1. Разделение веществ на основе молекулярно-ситовых свойств цеолитов..........401
8.6.5.2. Короткоцикловая безнагревная адсорбция...402
8.6.6. Осушка жидких сред....................403
8.6.6.1. Осушка фреоновых холодильных масел...403
8.6.6.2. Осушка трансформаторного масла.......405
8.6.7. Адсорбционный метод внесения удобрений и микроэлементов в почву......................405
Раздел 9. Твердые горючие ископаемые
9.1. Общие сведения........................409
9.2. Классификация горючих ископаемых......409
9.3. Физические и технические характеристики
углей.................................412
9.4. Формулы для пересчета результатов анализа
твердых горючих ископаемых............414
9.4.1. Формулы для вычисления теплоты сгорания
твердого топлива......................414
9.4.2. Теплота сгорания, определенная сжиганием
твердого топлива в калориметрической бомбе.................................415
9.4.3. Теплота сгорания, рассчитанная по данным
элементного анализа...................415
9.4.4. Теплота сгорания, определенная по данным
технического анализа..................415
9.5. Угли..................................416
9.5.1. Классификация.........................416
9.5.2. Кодификация...........................422
9.5.3. Разделение углей на классы............422
9.5.4. Угли важнейших месторождений СНГ......423
9.5.5. Теплофизические свойства некоторых углей
и сланцев.............................428
9.5.6. Буроугольный битум и воск.............428
9.5.7. Краткие сведения о зарубежных угольных
бассейнах.............................431
9.6. Горючие сланцы........................432
9.6.1. Общие сведения........................432
9.6.2. Свойства горючих сланцев..............433
9.7. Торф..................................434
9.7.1. Общие сведения........................434
9.7.2. Классификация.........................436
9.7.3. Гуминовые вещества торфа..............438
9.7.4. Битумы торфа..........................438
9.7.5. Торфяной воск.........................438
9.7.6. Обессмоленный торфяной воск...........441
9.7.7. Рафинированный торфяной воск..........441
9.7.8. Углеводороды торфа....................442
9.7.9. Комплексное использование торфа.......442
9.8. Структурные характеристики твердых
горючих ископаемых....................445
9.8.1. Структура угля........................445
9.8.2. Структура керогена сланца..............448
9.9. Переработка горючих ископаемых в товарные продукты и органические вещества............449
9.9.1. Полукоксование углей и сланцев.........449
9.9.2. Переработка сланцевой смолы............459
9.9.3. Переработка горючих сланцев за рубежом.461
9.9.3.1. Процессы переработки сланца в Китае...461
9.9.3.2. Процессы переработки сланца в США.....462
9.9.3.3. Процесс переработки сланца в Бразилии.466
9.9.3.4. Процессы переработки сланца в Германии.... 466
9.10. Технология переработки углей...........467
9.10.1. Основные критерии выбора углей для получения кокса, отвечающего международным стандартам....................467
9.10.2. Современное состояние проблемы
подготовки угольных шихт для коксования.........................468
9.10.3. Высокотемпературное коксование углей...470
9.10.4. Расчет материального баланса процесса
коксования.............................472
9.10.5. Характеристика каменноугольной смолы ....475
9.10.6. Переработка каменноугольной смолы......476
9.10.7. Переработка сырого бензола.............480
9.10.8. Технология процесса «Аммосульф»
(очистка коксового газа)...............481
9.10.9. Товарные продукты переработки углей....482
9.11. Производство искусственного жидкого
топлива................................494
9.11.1. Теоретические основы процесса..........494
9.11.2. Технология получения ИЖТ...............497
9.11.3. Производство ИЖТ за рубежом............498
Приложение.....................................501
Раздел 10. Углеродные адсорбенты (активные угли)
10.1. Физико-химические основы процесса......503
10.1.1. Сорбция из газовых сред................503
10.1.1.1. Теория мономолекулярной адсорбции....504
10.1.1.2. Теория полимолекулярной адсорбции....504
10.1.1.3. Теория объемного заполнения микропор.505
10.1.1.4. Определение параметров переходных пор... 509
10.1.2. Сорбция из водных растворов............512
10.2. Структурная химия активного углерода...516
10.3. Технология получения углеродных адсорбентов (активных углей)................520
10.3.1. Получение углеродных адсорбентов (активных углей) методом парогазовой активации...................................521
10.3.1.1. Механизм парогазовой активации.......521
10.3.2. Технология производства гранулированных активных углей методом парогазовой активации...................................524
10.3.3. Технология производства дробленых углеродных адсорбентов методом парогазовой активации.......................529
10.3.4. Технология получения углеродных
молекулярных сит.............................531
10.3.5. Производство дробленых активированных
углей из ископаемого сырья фирмой «Калгон
Карбон Корпорейшн» (США)..............533
10.3.6. Получение активных углей путем активирова-
ния неорганическими веществами...............536
1440
Новый справочник химика и технолога
10.3.6.1. Теоретические основы метода активирования неорганическими веществами...................536
10.3.6.2. Технология производства адсорбентов из торфа методом сернисто-калиевой активации....................................539
10.3.6.3. Технологическая схема производства углеродных адсорбентов из бурых углей, модифицированных гидроокисью калия............541
10.3.6.4. Технология получения углеродных адсорбентов из отходов древесного сырья, модифицированного ортофосфорной кислотой.....................................544
10.4. Применение углеродных адсорбентов........545
10.4.1. Очистка газов на активных углях.........545
10.4.1.1. Поглощение паров бензина на автотранспорте...............................546
10.4.1.2. Очистка газов от паров ртути..........547
10.4.1.3. Очистка газов от S-содержащих компонентов..................................547
10.4.1.4. Общие закономерности адсорбции смесей.549
10.4.1.5. Приближенный метод расчета равновесия бинарных смесей на основе изотерм адсорбции компонентов........................551
10.4.2. Очистка жидких сред.....................551
10.4.2.1. Очистка сточных вод от нефтепродуктов.552
10.4.2.2. Очистка от поверхностно-активных веществ и красителей..................................552
10.4.2.3. Доочистка сточных вод производства синтетического каучука........................552
10.4.2.4. Очистка сточных вод гидролизных заводов.......................................553
10.4.3. Использование в качестве пористых носителей.....................................553
10.4.3.1. Осушители.............................553
10.4.3.2. Химические поглотители................554
10.4.3.3 Катализаторы на пористой основе........556
10.4.3.4. Носители микроорганизмов..............556
10.4.4. Очистка и стабилизация почв.............559
10.4.4.1. Очистка почв от гербицидов и пестицидов.................................559
10.4.4.2. Разложение высокотоксичных компонентов в почвах.....................................563
10.4.5. Применение адсорбентов в медицине.......564
10.4.5.1. Хемосорбция...........................564
10.4.5.2. Энтеросорбция.........................566
10.4.5.3. Аппликационные материалы..............570
10.4.6. Эластичные адсорбенты...................570
10.5. Регенерация сорбирующих материалов......571
10.5.1. Термическая десорбция...................572
10.5.2. Химическая регенерация..................574
10.5.3. Десорбция, осуществляемая перепадом давлений.....................................576
10.5.4. Вытеснительная десорбция................578
10.5.5. Экстракционная регенерация..............580
10.5.6. Экономические аспекты регенерации.......580
10.6. Углеродные адсорбенты из сланце-и нефтепродуктов.............................583
10.6.1. Сланцепродукты как сырье для получения углеродных адсорбентов.......................583
10.6.1.1. Гранулированные адсорбенты из сланцевой смолы............................583
10.6.1.2. Гранулированные адсорбенты из сланцевых фенолов.......................................585
10.6.2. Сланцевая смола и фенолы в качестве связующих при получении углеродных адсорбентов...................................589
10.6.2.1. Свойства углеродных адсорбентов, сформованных сланцевой смолой.................591
10.6.2.2. Свойства углеродных адсорбентов, сформованных сланцевыми фенолами..............592
10.6.3. Импрегнаторы углеродных адсорбентов на основе сланцевых фенолов...................594
10.6.4. Углеродные адсорбенты с использованием нефтепродуктов................................594
10.6.4.1. Нефтяные остатки в качестве компонента шихты.........................................596
10.6.4.2. Использование нефтяных остатков в составе сополикондснсатов для получения гранулированных адсорбентов...................602
10.6.4.3. Использование остатков для формования углеродных адсорбентов........................607
10.6.5. Высокоэффективные углеродные адсорбенты при совместном использовании нефте- и сланцепродуктов......................611
10.6.5.1. Гранулированные углеродные адсорбенты из сополикондснсатов нсфтс-и сланцепродуктов.............................611
Каталог углеродных отечественных и зарубежных адсорбентов: основные физико-химические свойства и назначение.........................616
Активные угли России.........................616
Активные угли США............................633
Активные угли ФРГ............................642
Активные угли Японии.........................648
Активные угли Нидерландов....................652
Активные угли Франции........................655
Активные угли Великобритании.................657
Раздел 11. Углеводородные газы
11.1. Характеристика и состав природных углеводородных газов..........................661
11.1.1. Переработка природных газов..........664
11.1.2. Очистка газов от сернистых соединений и СО2.........................................664
11.1.2.1. Абсорбционные способы..............666
11.1.2.2. Адсорбционные способы..............668
11.1.2.3. Окислительные методы очистки газа от сероводорода...............................670
11.1.2.4. Очистка газов на мембранах.........673
11.1.3. Осушка газов.........................673
11.1.3.1. Метод абсорбции....................674
11.1.3.2. Метод адсорбции....................675
11.1.3.3. Осушка с помощью мембран...........676
11.1.4. Отбензинивание газов.................676
11.1.5. Разделение природных газов...........678
11.2. Состав и характеристика нефтезаводских
газов........................................678
11.3. Состав и характеристика газов термической
переработки твердых горючих ископаемых
и газификации................................680
Оглавление
1441
Раздел 12. Нефть и нефтепродукты
12.1. Общие сведения о нефти и углеводородных
газах..................................681
12.2. Подготовка нефти к переработке
и первичная переработка................694
12.2.1. Обезвоживание и обессоливание нефти...694
12.2.2. Установки АВТ.........................699
12.2.2.1. Атмосферная перегонка нефти.........699
12.2.2.2. Вакуумная перегонка мазута..........701
12.3. Производство нефтяных масел...........705
12.3.1. Химический состав масляных фракций
и базовых масел........................705
12.3.2. Деасфальтизация гудрона...............706
12.3.2.1 Установка одноступенчатой деасфальтизации гудронов жидким пропаном.....................................706
12.3.2.2. Установка двухступенчатой деасфальтизации гудронов жидким пропаном.....................................708
12.3.3. Процессы очистки масляного сырья избирательными растворителями................712
12.3.3.1. Селективная очистка масляного сырья.713
12.3.3.2. Установка очистки масляного сырья У-метилпирролидоном..........................714
12.3.3.3. Установка очистки масляного сырья фенолом......................................718
12.3.3.4. Установка очистки масляного сырья фурфуролом...................................720
12.3.4. Депарафинизация.......................723
12.3.4.1. Установка депарафинизации с двухступенчатым фильтрованием......723
12.3.4.2. Установка глубокой депарафинизации масляных рафинатов...........................725
12.3.4.3. Депарафинизация с применением кристаллизатора смешения.....................726
12.3.4.4. Депарафинизация с применением кристаллизатора пульсационного смешения.....................................728
12.3.4.5. Установка совмещенного процесса депарафинизации и обезмасливания.............730
12.3.4.6. Отделение регенерации растворителей из растворов депарафинированного масла, гача и петролатума...........................733
12.3.5. Гидродоочистка........................735
12.3.6. Гидрогенизационные процессы...........737
12.3.6.1. Гидрокрекинг........................737
12.3.6.2. Гидроизомеризация...................738
12.3.6.3. Каталитическая гидродепарафинизация.738
13.3.6.4. Гидроочистка........................739
12.3.7. Производство товарных масел...........739
12.4. Выделение, свойства и применение гетероатомных соединений нефтей и нефтепродуктов.............................740
12.4.1. Сернистые соединения..................741
12.4.1.1. Получение и применение нефтяных сернистых соединений.........................743
12.4.1.2. Применение концентратов нефтяных сульфидов и сульфоксидов.....................748
12.4.2. Азотсодержащие соединения.............749
12.4.3. Кислородсодержащие соединения........750
12.4.4. Смолисто-асфальтеновые вещества......751
12.5. Научные основы, техника и технология производства битумов из нефтяных остатков.....................................752
12.5.1. Состояние нефтеперерабатывающей промышленности России........................752
12.5.2. Сырье для производств битумов.......753
12.5.2.1. Нефти России, используемые для производства битумов.........................753
12.5.2.2. Получение и свойства нефтяных остатков... 754
12.5.2.3. Деасфальтизация нефтяных остатков.755
12.5.3. Исследование нефтяных остатков и битумов....................................757
12.5.3.1. Методы определения группового состава нефтяных остатков и битумов..................757
12.5.3.2. Физико-химические методы исследования нефтяных остатков и битумов..................758
12.5.4. Технические характеристики, ассортимент и область применения битумов.................760
12.5.4.1. Показатели свойств битумов........760
12.5.4.2. Физические характеристики битумов.764
12.5.4.3. Ассортимент и область применения битумов......................................767
12.5.5. Технология производства битумов.....768
12.5.5.1. Производство остаточных битумов...768
12.5.5.2. Производство окисленных битумов...771
12.5.5.3. Кинетика реакций и гидродинамический режим в барботажных реакторах колонного типа.........................................775
12.5.5.4. Интенсификация производства и управление качеством битумов............................779
12.5.5.5. Охрана окружающей среды при производстве битумов......................................783
12.5.5.6. Превращение компонентов сырья при производстве битумов.........................783
12.5.5.7. Межмолекулярные взаимодействия в битумах....................................785
12.5.5.8. Взаимодействие между компонентами в битумах....................................789
12.5.5.9. Особенности формирования битумов, определяемые межмолекулярными взаимодействиями их компонентов..............793
12.6. Термические процессы переработки
нефти................................800
12.6.1. Висбрекинг — процесс получения
котельного топлива из гудрона........800
12.6.2. Коксование..........................801
12.6.2.1. Полунепрерывное коксование тяжелых нефтяных остатков в необогреваемых реакторах....................................801
12.6.3. Производство низших олефинов. Пиролиз......................................802
12.6.3.1. Подготовка и разделение газов пиролиза 811
12.6.3.2. Получение и переработка жидких продуктов
пиролиза углеводородного сырья..............815
12.7. Термокаталитические процессы
переработки..........................823
12.7.1. Гидроочистка нефтяных фракций........823
1442
Новый справочник химика и технолога
12.7.1.1 . Термодинамика и химизм гидрогенолиза сернистых соединений.........................823
12.7.1.2 . Катализаторы гидроочистки.........828
12.7.1.3 . Влияние сырья и условий процесса на гидрообессеривание........................831
12.7.1.4 . Технология гидрообессеривания.....832
12.7.2. Каталитический крекинг...............836
12.7.2.1. Термодинамика крекинга.............836
12.7.2.2. Механизм каталитического крекинга..836
12.7.2.3. Кинетика каталитического крекинга..838
12.7.2.4. Катализаторы крекинга..............839
12.7.2.5. Влияние технологических факторов...843
12.7.2.6. Основные реакционные аппараты......844
12.7.3. Г идрокрекинг........................850
12.7.3.1. Катализаторы.......................852
12.7.3.2. Сырье..............................852
12.7.3.3. Технологические параметры процесса.853
12.7.3.4. Промышленные процессы гидрокрекинга....855
12.7.4. Риформинг углеводородов..............861
12.7.4.1. Превращение углеводородов в условиях процесса риформинга..........................861
12.7.4.2. Катализаторы риформинга............863
12.7.4.3. Сырье и условия процесса риформинга.865
12.7.4.4. Основы технологии процесса риформинга...................................869
12.7.5. Алкилирование углеводородов..........873
12.7.5.1. Реакции алкилирования..............873
12.7.5.2. Алкилирование алканов алкенами.....873
12.7.5.3. Алкилирование аренов...............875
12.7.5.4. Катализаторы алкилирования.........876
12.7.5.5. Технологические процессы алкилирования................................880
12.7.5.6. Процессы получения алкилароматических углеводородов для нефтехимии.................883
12.7.5.7. Получение кумола...................886
12.7.6. Изомеризация углеводородов...........890
12.7.6.1. Изомеризация углеродов различных классов......................................890
12.7.6.2. Катализаторы изомеризации..........893
12.7.6.3. Процессы изомеризации..............897
12.7.7. Олигомеризация углеводородов.........911
12.7.7.1. Олигомеризация как разновидность полимеризации................................911
12.7.7.2. Катализаторы олигомеризации........913
12.8. Присадки к нефтепродуктам..............929
12.8.1. Присадки к топливам..................929
12.8.1.1. Классификация присадок к топливам..929
12.8.1.2. Присадки, предназначенные для улучшения процесса сгорания топлива в двигателе.........930
12.8.1.3. Присадки, сохраняющие свойства топлив при хранении и транспортировке...............940
12.8.1.4. Депрессорные присадки..............943
12.8.1.5. Моющие присадки к автомобильным бензинам.....................................945
12.8.2. Присадки к смазочным маслам..........949
12.8.2.1. Классификация присадок к смазочным маслам.......................................949
12.8.2.2. Антиокислительные присадки (ингибиторы окисления).......................950
12.8.2.3. Антикоррозионные и защитные присадки (ингибиторы коррозии)........................953
12.8.2.4. Моюще-диспергирующие присадки (детергентно-диспергирующие).................956
12.8.2.5. Присадки, улучшающие смазочные свойства масел...............................962
12.8.2.6. Вязкостные присадки................966
12.8.2.7. Депрессорные присадки..............968
12.8.2.8. Антипенные присадки................969
12.8.2.9. Пакеты присадок....................969
СЫРЬЕ И ПРОДУКТЫ ПРОМЫШЛЕННОСТИ НЕОРГАНИЧЕСКИХ И ОРГАНИЧЕСКИХ ВЕЩЕСТВ. Ч. 2 (Оранжевый)
Раздел 13. Продукты органического синтеза......5
13.1. Процессы окисления.....................5
13.1.1. Общая характеристика процессов
окисления.............................7
13.1.2. Гомогенное окисление по насыщенному
атому углерода........................9
13.1.2.1. Механизм образования продуктов
окисления.............................9
13.1.2.2. Кинетика и катализ гомогенного
окисления............................11
13.1.2.3. Реакторы для процессов жидкофазного
окисления............................14
13.1.2.4. Окисление углеводородов
в гидропероксиды.....................14
13.1.2.5. Окисление алканов...................19
13.1.2.6. Окисление нафтенов и их производных.22
13.1.2.7. Окисление метилбензолов в ароматические
кислоты..............................27
13.1.2.8. Окисление насыщенных альдегидов
и спиртов............................32
13.1.3. Гетерогенно-каталитическое окисление
углеводородов и их производных.......35
13.1.3.1. Гетерогенные катализаторы окисления
и механизм реакций...................35
13.1.3.2. Кинетика и селективность реакций....36
13.1.3.3. Реакторы для гетерогенно-каталитического
окисления............................37
13.1.3.4. Окисление алкенов по насыщенному
атому углерода.......................38
13.1.3.5. Окислительный аммонолиз
углеводородов........................39
13.1.4. Окисление алкенов в присутствии
металлокомплексных катализаторов.....47
13.1.4.1. Эпоксидирование ненасыщенных
соединений...........................47
13.1.4.2. Окислительное сочетание алкенов
при катализе комплексами металлов....51
13.2. Продукты, полученные на основе оксида
углерода.............................57
13.2.1. Получение синтез-газа..............57
13.2.2. Процесс Фишера — Тропша............58
13.2.3. Синтез метанола....................60
13.2.4. Процесс оксосинтеза
(гидроформилирования)................62
13.2.4.1. Катализаторы реакции
гидроформилирования..................63
Оглавление
1443
13.2.4.2 . Влияние примесей на процесс
гидроформилирования......................65
13.2.4.3 . Механизм реакции
гидроформилирования......................65
13.2.4.4 . Реакционные устройства
для гидроформилирования олефинов.........66
13.2.4.5 . Технология процесса оксосинтеза.......67
13.2.5 . Производство бутиловых спиртов.........69
13.2.5.1 . Получение бутиловых спиртов
по нафтенатно-испарительной схеме........69
13.2.5.2 . Кобальтфосфиновые катализаторы
оксопроцесса.............................73
13.2.5.3 . Оксосинтез с использованием
карбонилов родия.........................74
13.2.6 . Гидрокарбоксилирование олефинов........78
13.2.7 . Гидрокарбалкоксилирование олефинов.....82
13.2.8 . Синтез спиртов на основе олефинов
Сц— Cj4 и С15—С|8........................84
13.2.9 . Синтез высших индивидуальных
разветвленных ненасыщенных монокарбоновых кислот....................85
13.2.10 . Получение пропионовой кислоты..........87
13.2.11 . Конденсационные процессы с участием
карбонильной группы......................88
13.2.11.1 . Синтез 2-этилгексанола из масляного альдегида.....................................89
13.2.11.2 . Синтез многоатомных спиртов..........91
13.2.12 . Карбонилирование спиртов...............96
13.3. Гидрирование...........................99
13.3.1. Классификация реакций гидрирования.....99
13.3.2. Факторы, влияющие на скорость
гидрирования.............................99
13.3.3. Катализаторы гидрирования.............101
13.3.4. Гидрирование углеводородов............102
13.3.4.1. Гидрирование бензола до циклогексана.102
13.3.4.2. Частичное гидрирование бензола
до циклогексена.........................106
13.3.4.3. Гидрирование нафталина...............107
13.3.4.4. Гидрирование циклододекатриена.......108
13.3.4.5. Гидрирование как способ очистки
углеводородного сырья и некоторых нефтепродуктов..........................109
13.3.5. Гидрирование кислородсодержащих
соединений..............................114
13.3.5.1. Производство алифатических
спиртов-флотореагентов C^-Cs и пластификаторов С6-С9.................114
13.3.5.2. Гидрирование карбоксильной
и сложноэфирных групп...................115
13.3.5.3. Гидрирование полифункциональных
кислородсодержащих соединений...........123
13.3.5.4. Гидрирование ароматических
кислородсодержащих соединений...........128
13.4. Дегидрирование углеводородов..........133
13.4.1. Основные реакции......................133
13.4.2. Равновесие реакций дегидрирования
углеводородов...........................133
13.4.3. Катализаторы дегидрирования...........137
13.4.3.1. Катализаторы дегидрирования
парафинов...............................137
13.4.3.2. Катализаторы дегидрирования
олефиновых и алкилароматических углеводородов.......................139
13.4.4. Технологические процессы
дегидрирования углеводородов........141
13.4.4.1. Дегидрирование легких парафинов...141
13.4.4.2. Дегидрирование высших парафинов...144
13.4.4.3. Дегидрирование олефинов...........145
13.4.4.4. Дегидрирование алкилароматических
углеводородов.......................146
13.5. Производство галогенпроизводных
углеводородов.......................148
13.5.1. Галогенпроизводные метана...........149
13.5.2. Галогенпроизводные ряда ............150
13.5.3. Производство винилхлорида...........153
13.5.4. Производство алкилхлоридов..........154
13.5.5. Производство хлоропрена.............155
13.5.6. Производство хлорбензола............156
13.5.7. Производство хладонов (фреонов).....156
13.5.8. Производство гексахлор циклогексана..157
13.5.9. Производство броморганических
продуктов...........................159
13.6. Производство алифатических аминов....160
13.6.1. Низкомолекулярные амины С2-С4.......160
13.6.2. Высокомолекулярные амины............163
13.6.2.1. Производство высших аминов
из кислот...........................163
13.6.2.2. Производство высших аминов
из алканов..........................165
13.6.2.3. Другие методы производства
высших аминов.......................167
Раздел 14. Полимерные соединения и материалы на их основе.....................169
14.1. Общие понятия о полимерах...........169
14.2. Классы полимеров и их химическое
строение............................171
14.3. Молекулярная масса полимеров
и олигомеров........................174
14.4. Пространственное строение
макромолекул........................175
14.4.1. Конфигурация макромолекул............175
14.4.2. Конформация, форма и размеры
макромолекул........................176
14.4.3. Надмолекулярная структура полимеров.... 176
14.4.4. Упругая и высокоэластическая
деформации полимеров................177
14.5. Производство полимеров..............177
14.5.1. Полимеризация.......................178
14.5.2. Поликонденсация.....................184
14.6. Каучуки.............................187
14.6.1. Каучук натуральный..................187
14.6.1.1. Состав, структура и физико-химические
свойства натурального каучука.......193
14.6.1.2. Химические свойства и модификаты
натурального каучука................194
14.6.1.3. Получение и области применения
натурального каучука................194
14.6.2. Каучуки синтетические.............195
14.6.2.1. Классификация.....................195
14.6.2.2. Способы синтеза...................196
1444
Новый справочник химика и технолога
14.6.2.3. Марки, области применения и физические
свойства некоторых типов каучуков синтетических.........................197
14.6.3 . Каучуки жидкие........................203
14.6.3.1 . Особенности технологии
производства КЖ.......................213
14.6.3.2 . Модификация КЖ на стадиях синтеза
и в условиях применения...............213
14.6.3.3 . КЖ как основа эластополимерных
материалов и каучуковых композитов....214
14.6.3.4 . КЖ в производстве лакокрасочных
материалов............................214
14.7. Латексы...............................215
14.7.1. Латекс на основе натурального каучука.215
14.7.2. Латексы на основе синтетических
каучуков..............................216
14.8. Каучуковые композиты..................219
14.9. Ионообменные материалы................230
14.9.1. Классификация. Типы ионитов, редокс-
полимеров, комплексообразователей, мембран, волокон, тканей..............231
14.9.2. Иониты................................239
14.9.2.1. Катиониты............................239
14.9.2.2. Анионообменные материалы
(аниониты)............................245
14.9.3. Полиамфолиты..........................249
14.9.4. Редокс-полимеры.......................250
14.9.5. Комплексообразующие ионообменные
полимеры..............................251
14.9.6. Растворимые полиэлектролиты...........252
14.9.7. Ионитовые мембраны....................253
14.9.8. Физико-химические свойства ионитов....255
14.9.8.1. Кислотно-основные свойства...........255
14.9.8.2. Селективность........................255
14.9.8.3. Основные свойства....................256
14.9.9. Характеристика, области применения
и зарубежные аналоги ионитов..........260
14.9.9.1. Сильнокислотные катиониты............260
14.9.9.2. Среднекислотные катиониты...........261
14.9.9.3. Слабокислотные катиониты............261
14.9.9.4. Высокоосновные аниониты.............262
14.9.9.5. . Низкоосновные аниониты............263
14.9.10. Порошковые иониты.....................265
14.9.11. Ионообменные мембраны.................266
14.9.11.1. Гетерогенные мембраны...............266
4.9.11.2. Гомогенные мембраны..................269
14.9.11. 3. Биполярные мембраны................270
14.9.12. Жидкие иониты.........................270
14.9.13. Ионообменные волокна..................271
14.9.14. Устойчивость ионообменных материалов . 272
14.9.14.1. Критерии оценки.....................272
14.9.14.2. Термогидролиз фосфорнокислых и карбоксильных катионитов..................275
14.9.14.3. Термогидролиз анионитов.............277
14.9.14.4. Термостойкость ионитов в газообразных средах.......................279
14.9.14.5. Химическая стойкость ионитов........279
14.9.14.6. Действие ионизирующих излучений на катиониты................................280
14.9.15. Иониты из нефтяных остатков........283
14.9.15.1. Свойства ионитов из смолистоасфальтеновых соединений нефти..............284
14.9.16. Методы исследования ионитов........292
14.9.16.1. Определение содержания твердого вещества....................................292
14.9.16.2. Характеристика ионогенных групп..293
14.9.16.3. Определение технологических свойств.298
14.9.17. Ионообменные реакторы..............300
14.9.17.1. Классификация....................300
14.9.17.2. Основные типы ионообменных аппаратов...................................301
14.10. Лакокрасочные материалы и покрытия......309
14.10.1. Общие сведения.....................309
14.10.2. Состав.............................309
14.10.3. Классификация......................311
14.10.4. Пленкообразователи (ПО)............319
14.10.4.1. Поликонденсационные ПО...........319
14.10.4.2. Полимеризационные ПО.............326
14.10.5. Сшивающие агенты...................327
14.10.5.1. Отвердители эпоксиолигомеров.....327
14.10.5.2. Сиккативы (катализаторы окислительной полимеризации масел)........................328
14.10.6. Растворители ЛКМ...................329
14.10.7. Целевые добавки....................333
14.10.7.1. Тиксотропные добавки.............333
14.10.7.2. Добавки для водно-дисперсионных красок......................................334
14.10.8. Пигменты и наполнители.............337
14.10.8.1. Минеральные пигменты и наполнители ....339
Таблица 14.87. Белые пигменты...............339
Таблица 14.88. Наполнители..................340
Таблица 14.89. Синтетические хроматические пигменты....................................342
Таблица 14.90. Зависимость свойств жслезооксидных пигментов от размера частиц...................349
Таблица 14.91. Цветные пигменты на основе циркона...................350
Таблица 14.92. Природные пигменты на основе оксидов железа..............................351
Таблица 14.93. Природные пигменты с другой красящей основой...................352
Таблица 14.94. Антикоррозионные пигменты....354
Таблица 14.95. Новые перспективные антикоррозионные пигменты фосфатного типа и области их применения...............................357
Таблица 14.96. Возможность применения антикоррозионных пигментов в грунтах разной природы....................357
Таблица 14.97. Металлические пигменты.......358
Таблица 14.98. Перламутровые пигменты.......358
Таблица 14.99. Характеристика
термочувствительных пигментов...............360
Таблица 14.100. Пигменты-светосоставы.......361
Таблица 14.101. Магнитные пигменты..........361
Таблица 14.102. Пигменты для антифрикционных
покрытий — твердые смазки...................361
Оглавление
1445
Таблица 14.103. Области применения белых пигментов и наполнителей.......362
Таблица 14.104. Области применения природных пигментов..................363
Таблица 14.105. Области применения синтетических пигментов......................363
14.10.8.2. Органические красители и пигменты..365
14.10.9. Водные дисперсии....................367
14.10.9.1. Водно-дисперсионные краски на основе поливинилацетата...................367
14.10.9.2. Полиакриловые дисперсии...........367
14.10.10. Технология получения лакокрасочных материалов...................................369
14.10.11. Характеристика лакокрасочных материалов...................................371
14.10.11.1. Грунты...........................371
14.10.11.2. Лаки, эмали, шпатлевки...........379
14.10.11.3. Порошковые краски................412
14.10.12. Подготовка поверхности под окраску..415
14.10.13. Выбор ЛКМ и методов их нанесения....420
14.10.14. Лакокрасочные материалы для покрытия пористых субстратов..........................423
14.10.14.1. Окраска древесины................423
14.10.14.2. Окраска строительных материалов..427
14.10.15. Лакокрасочные материалы для разметки дорог...........................429
Приложение. Методы испытаний лакокрасочных материалов и покрытий (перечень основных ГОСТов и стандартов ИСО)............431
Раздел 15. Растительное сырье................437
15.1. Общие представления о строении
и свойствах растительного сырья....438
15.1.1. Классификация растительного сырья...438
15.1.2. Строение и свойства органических
соединений..........................440
15.1.2.1. Низкомолекулярные соединения.......440
15.1.2.2. Высокомолекулярные соединения......453
15.1.3. Характеристика отдельных видов
растительного сырья.................469
15.1.3.1. Древесное сырье....................469
15.1.3.2. Волокносодержащее сырье............492
15.1.3.3. Крахмалсодержащее сырье............494
15.1.3.4. Пектинсодержащее сырье.............501
15.1.3.5. Сахаросодержащее сырье.............501
15.1.3.6. Масличное сырье....................502
15.1.3.7. Эфиромасличное сырье...............509
15.2. Производство и переработка
волокносодержащих материалов........515
15.2.1. Волокна.............................516
15.2.2. Характеристика древесного сырья
и волокнистых полуфабрикатов........516
15.2.2.1. Подготовка древесного сырья........517
15.2.2.2. Виды волокнистых полуфабрикатов....517
15.2.2.3. Показатели, характеризующие свойства
полуфабрикатов......................517
15.2.3. Производство сульфитной целлюлозы...518
15.2.3.1. Общая схема производства
сульфитной целлюлозы................518
15.2.3.2. Химические превращения компонентов
древесины...........................518
15.2.3.3. Приготовление сульфитных варочных
растворов............................522
15.2.3.4. Получение сульфитной целлюлозы......525
15.2.3.5. Переработка сульфитных щелоков......533
15.2.3.6. Регенерация химикатов и тепла
из отработанных сульфитных и бисульфитных щелоков...............535
15.2.4. Производство сульфатной целлюлозы....536
15.2.4.1. Общие сведения......................536
15.2.4.2. Химические реакции компонентов
древесины............................536
15.2.4.3. Варка натронной и сульфатной
целлюлозы............................541
15.2.4.4. Щелочные варки с использованием
антрахинона..........................548
15.2.4.5. Полисульфидный способ варки.........549
15.2.4.6. Получение целлюлозы для химической
переработки сульфатным способом с предварительным гидролизом.........549
15.2.4.7. Промывка целлюлозы..................552
15.2.4.8. Регенерация химикатов...............554
15.2.5. Производство полуцеллюлозы (ПЦ)......561
15.2.5.1. Способы производства полуцеллюлозы..561
15.2.5.2. Оборудование для получения ПЦ.......563
15.2.5.3. Области использования ПЦ............563
15.2.6. Производство древесной массы.........563
15.2.6.1. Дсфибрерная древесная масса.........563
15.2.6.2. Производство древесной массы из щепы... 566
15.2.7. Очистка волокнистых полуфабрикатов...568
15.2.7.1. Основные стадии очистки.............568
15.2.7.2. Переработка макулатурной массы......569
15.2.8. Производство волокнистых
полуфабрикатов из недревесных растений.............................570
15.2.8.1. Характеристика недревесного
растительного сырья..................570
15.2.8.2. Получение целлюлозы из соломы
и тростника..........................570
15.2.8.3. Регенерация химикатов...............572
15.2.8.4. Варка целлюлозы из других недревесных
растений.............................573
15.2.9. Отбелка целлюлозы....................573
15.2.9.1. Общие сведения......................573
15.2.9.2. Природа и свойства реагентов........574
15.2.9.3. Основные ступени отбелки............575
15.2.9.4. Отбелка сульфатной целлюлозы........581
15.2.9.5. Отбелка сульфитной целлюлозы........583
15.2.9.6. Отбелка целлюлозы для химической
переработки..........................583
15.2.9.7. Оборудование для отбелки целлюлозы...583
15.2.9.8. Назначение и показатели качества
беленых целлюлоз.....................584
15.2.9.9. Отбелка древесной массы.............589
15.2.10. Производство бумаги и картона........590
15.2.10.1. Основные стадии процесса...........590
15.2.10.2. Приготовление бумажной массы.......591
15.2.10.3. Изготовление бумаги на
бумагоделательной машине......................593
15.2.10.4. Основные виды и свойства бумаги
и картона.....................................594
1446
Новый справочник химика и технолога
15.2.11. Получение и переработка искусственных полимеров из целлюлозы.......................596
15.2.11.1. Эфиры целлюлозы....................596
15.2.11.2. Нитраты целлюлозы..................598
15.2.11.3. Фосфаты целлюлозы..................603
15.2.11.4. Ацетаты целлюлозы..................603
15.2.11.5. Эфиры целлюлозы и других алифатических кислот.........................605
15.2.11.6. Простые эфиры целлюлозы............606
15.2.11.7. Представители простых эфиров целлюлозы....................................608
15.2.11.8. Продукты избирательного окисления целлюлозы....................................610
15.2.11.9. Эфироцеллюлозные пластмассы........611
15.2.11.10. Пленки на основе производных целлюлозы....................................613
15.2.11.11. Использование эфиров целлюлозы для производства лакокрасочных материалов...................................614
15.2.11.12. Применение производных целлюлозы в медицине...................................614
15.2.11.13. Производство целлюлозы в форме порошка......................................616
15.2.12. Производство текстильных волокон.....617
15.2.12.1. Основные виды текстильных материалов....................................617
15.2.12.2. Основные стадии производства текстильных материалов........................617
15.2.12.3. Характеристика природных волокон......................................618
15.2.12.4. Производство химических волокон и нитей..............................618
15.2.12.5. Вискозные волокна..................619
15.2.12.6. Медноаммиачные волокна.............620
15.2.12.7. Другие способы получения гидратцеллюлозных волокон....................620
15.2.12.8. Модифицированные целлюлозные волокна......................................621
15.2.12.9. Углеродные волокна.................621
15.2.12.10. Ацетил цел лю лозные волокна......622
15.3. Древесные композиционные
материалы............................629
15.3.1. Определение и классификация..........629
15.3.2. Древесноволокнистые плиты............630
15.3.2.1. Классификация, свойства и применение
древесноволокнистых плит.............630
15.3.2.2. Характеристика сырья, связующих
и модифицирующих добавок.............632
15.3.2.3. Технологический процесс и способы
производства древесноволокнистых плит.................................632
15.3.3. Древесностружечные плиты.............633
15.3.3.1. Классификация, свойства и применение
древесностружечных плит..............633
15.3.3.2. Характеристика сырья, связующих
и модифицирующих добавок.............635
15.3.3.3. Технологический процесс и способы
производства плит....................636
15.3.4. Древеснослоистые пластики............637
15.3.4.1. Классификация, состав, свойства
древеснослоистых пластиков...........637
15.3.4.2. Технологический процесс производства
древеснослоистых пластиков...........638
15.3.4.3. Применение древеснослоистых
пластиков............................639
15.3.5. Декоративные бумажнослоистые
пластики.............................639
15.3.5.1. Определение и состав декоративных
бумажнослоистых пластиков............639
15.3.5.2. Характеристика бумаг и синтетических
связующих веществ....................640
15.3.5.3. Технологический процесс производства
декоративных бумажнослоистых пластиков............................640
15.3.5.4. Свойства и применение декоративных
бумажнослоистых пластиков............641
15.3.6. Модифицированная древесина..........642
15.3.6.1. Способы модифицирования............642
15.3.6.2. Модифицирование древесины
синтетическими полимерами............642
15.3.6.3. Технологический процесс
модифицирования древесины............643
15.3.6.4. Свойства и применение
модифицированной древесины...........644
15.3.7. Другие виды древесных композиционных
материалов...........................644
15.3.7.1. Древесные пресс-массы..............644
15.3.7.2. Пьезотермопластики.................646
15.3.7.3. Материалы на основе минеральных
вяжущих веществ......................646
15.4. Термическая переработка древесного
сырья................................649
15.4.1. Основные виды производств термической
переработки древесного сырья.........649
15.4.2. Химические превращения компонентов
древесины............................650
15.4.2.1. Полисахариды.......................650
15.4.2.2. Лигнин.............................659
15.4.3. Пиролиз древесины...................665
15.4.3.1. Характеристика сырья...............665
15.4.3.2. Основные стадии пиролиза...........666
15.4.3.3. Аппараты для термического разложения
древесины............................670
15.4.4. Древесный уголь.....................677
15.4.4.1. Свойства древесного угля...........678
15.4.4.2. Основные направления использования
древесного угля......................679
15.4.4.3. Использование углеродсодержащих
материалов в качестве топлива........683
15.4.4.4. Активные угли......................686
15.4.5. Переработка пироконденсата..........692
15.4.5.1. Технология обработки парогазовой
смеси................................692
15.4.5.2. Характеристика конденсата..........692
15.4.5.3. Получение продуктов из водного
раствора.............................693
15.4.5.4. Получение продуктов из отстойной
смолы................................693
15.4.6. Смолоскипидарное производство.......694
Оглавление
1447
15.4.6.1 . Технология процесса................694
15.4.6.2 . Характеристика продуктов...........695
15.4.7 . Дегтекурение.........................695
15.4.7.1 . Характеристика сырья...............695
15.4.7.2 . Технология дегте курения...........695
15.4.7.3 . Свойства дегтя.....................696
15.4.8 . Газификация древесины................697
15.4.8.1 . Теоретические основы процесса......697
15.4.8.2 . Технология процесса................698
15.4.8.3 . Синтезы на основе оксида углерода..700
15.5. Экстракционные производства..........703
15.5.1. Экстрактивные вещества древесного
сырья................................703
15.5.2. Продукты, получаемые из древесины....703
15.5.2.1. Канифольно-терпентинное
производство.........................703
15.5.2.2. Канифольно-экстракционное
производство.........................706
15.5.2.3. Производство талловых продуктов
и сульфатного скипидара..............707
15.5.2.4. Продукты на основе канифоли.........715
15.5.2.5. Продукты на основе скипидара.......718
15.5.3. Продукты переработки древесной
зелени...............................722
15.5.3.1. Запасы и химический состав древесной
зелени...............................722
15.5.3.2. Заготовка и хранение древесной зелени.....723
15.5.3.3. Основные направления переработки
древесной зелени.....................724
15.5.3.4. Производство витаминной муки........724
15.5.3.5. Производство эфирных масел..........725
15.5.3.6. Переработка древесной зелени
экстрагированием водой...............726
15.5.3.7. Экстрагирование древесной зелени
органическими растворителями.........726
15.5.3.8. Развитие технологий производства
продуктов из древесной зелени........732
15.5.4. Переработка древесной коры...........734
15.5.4.1. Основные направления утилизации
отходов окорки.......................734
15.5.4.2. Производство танинов................734
15.5.4.3. Перспективные направления
химической переработки коры..........735
15.5.5. Производство растительных масел......736
15.5.5.1. Основные методы выделения
растительных масел...................736
15.5.5.2. Хранение и первичная переработка
масличных семян......................736
15.5.5.3. Подготовка семян к экстракции.......738
15.5.5.4. Извлечение масла прессованием.......740
15.5.5.5. Получение растительных масел
методом экстракции...................741
15.5.5.6. Обработка и хранение жмыха и шрота...743
15.5.5.7. Переработка мисцеллы................744
15.5.5.8. Первичная очистка растительных
масел................................745
15.5.6. Рафинация растительных масел........746
15.5.6.1. Нежировые примеси и сопутствующие
вещества.............................746
15.5.6.2. Основные стадии рафинации...........746
15.5.6.3. Гидратация фосфолипидов из масел.....747
15.5.6.4. Щелочная нейтрализация жиров.........748
15.5.6.5. Адсорбционная рафинация масел........750
15.5.6.6. Дезодорирование жиров................750
15.5.6.7. Извлечение из масел восковых веществ.751
15.5.7. Химическая переработка растительных
масел.................................751
15.5.7.1. Гидрогенизация растительных масел....751
15.5.7.2. Переэтерификация триацилглицеринов
растительных масел....................755
15.5.7.3. Производство глицерина и жирных
кислот................................755
15.5.7.4. Производство мыла....................759
15.5.7.5. Производство пищевых
поверхностно-активных веществ.........761
15.5.7.6. Получение пленкообразующих веществ....762
15.5.7.7. Производство и свойства
нитроглицерина........................763
15.5.7.8. Основные направления использования
растительных масел....................763
15.5.8. Производство эфирных масел............763
15.5.8.1. Классификация эфиромасличного сырья .... 763
15.5.8.2. Способы получения эфирного масла.....764
15.5.8.3. Переработка зернового эфиромасличного
сырья.................................765
15.5.8.4. Переработка цветочно-травянистого
эфиромасличного сырья.................765
15.5.8.5. Переработка цветочного
эфиромасличного сырья.................766
15.5.8.6. Безотходная технология...............766
15.5.8.7. Свойства и области применения
эфирных масел.........................766
15.5.8.8. Краткая характеристика некоторых
эфирных масел.........................768
15.6. Химическая переработка
углеводсодержащего сырья..............774
15.6.1. Производство сахара...................775
15.6.1.1. Свойства сахарозы ...................775
15.6.1.2. Характеристика сырья ................775
15.6.1.3. Основные стадии переработки сахарной
свеклы................................776
15.6.1.4. Очистка диффузионного сока...........781
15.6.1.5. Получение сахара-песка...............790
15.6.1.6. Переработка тростникового
сахара-сырца..........................796
15.6.1.7. Характеристика сахара-песка..........798
15.6.1.8. Производство сахара-рафинада.........799
15.6.1.9. Химическая переработка сахарозы......802
15.6.1.10. Заменители сахара...................805
15.6.2. Производство и переработка крахмала..815
15.6.2.1. Технологические свойства
крахмалсодержащего сырья .............815
15.6.2.2. Получение сырого картофельного
крахмала.............................816
15.6.2.3. Получение сырого кукурузного
крахмала.............................819
15.6.2.4. Получение крахмала из пшеницы.......824
15.6.2.5. Получение крахмала из других видов
растительного сырья..................824
15.6.2.6. Производство сухого крахмала........827
1448
Новый справочник химика и технолога
15.6.2.7. Свойства крахмалов.................828
15.6.2.8. Производство модифицированных
крахмалов...........................829
15.6.2.9. Производства сахаристых веществ
из крахмала.........................843
15.6.2.10. Производство крахмальной патоки...848
15.6.2.11. Производство глюкозы..............853
15.6.2.12. Производство фруктозосодержащих веществ......................................857
15.6.2.13. Производство и применение сорбита.860
15.6.2.14. Производство и применение аскорбиновой кислоты.........................862
15.6.3. Производство пектиновых веществ.....864
15.6.3.1. Характеристика сырья...............864
15.6.3.2. Технология производства пектиновых
веществ.............................865
15.6.3.3. Свойства пектиносодержащих
продуктов...........................869
15.6.3.4. Применение пектиновых веществ......873
15.6.4. Переработка пентозансодержащего
сырья...............................874
15.6.4.1. Характеристика пентозансодержащего
сырья...............................875
15.6.4.2. Производство фурфурола.............876
15.6.4.3. Основные направления использования
фурфурола...........................882
15.6.4.4. Производство ксилита...............891
15.6.4.5. Получение пищевого ксилита.........894
15.7. Микробиологические производства.....904
15.7.1. Общая характеристика
микробиологических производств и биологических агентов.............905
15.7.1.1. Основные сведения
о микроорганизмах...................905
15.7.1.2. Строение и свойства бактерий.......907
15.7.1.3. Строение и свойства грибов.........908
15.7.2. Характеристика сырья................909
15.7.2.1. Вещества, необходимые для развития
микроорганизмов.....................909
15.7.2.2. Отходы производства сахара.........914
15.7.2.3. Отходы переработки крахмала........915
15.7.2.4. Целлюлозосодержащее сырье..........917
15.7.3. Основные стадии микробиологических
производств.........................927
15.7.3.1. Подготовка питательной среды.......928
15.7.3.2. Получение и поддержание чистой
культуры............................930
15.7.3.3. Основная ферментация...............933
15.7.3.4. Выделение и очистка продуктов......941
15.7.4. Производство микробной биомассы.....941
15.7.4.1. Белок одноклеточных организмов.....941
15.7.4.2. Производство кормового белка.......943
15.7.4.3. Получение белковых препаратов
для пищевых целей...................951
15.7.4.4. Производство хлебопекарных дрожжей.953
15.7.4.5. Получение пивных дрожжей...........957
15.7.4.6. Средства защиты растений...........958
15.7.4.7. Производство бактериальных удобрений ..962
15.7.5. Производство ферментных препаратов..964
15.7.5.1. Общая характеристика ферментов.....964
15.7.5.2. Основные стадии получения ферментов.... 966
15.7.5.3. Амилолитические ферменты...........970
15.7.5.4. Ферменты, воздействующие
на пектиновые вещества..............975
15.7.5.5. Целлюлолитические ферменты.........978
15.7.5.6. Гемицеллюлазные ферменты...........980
15.7.5.7. Липолитические ферменты............982
15.7.5.8. Протеолитические ферменты..........984
15.7.5.9. Ферментные препараты, содержащие
глюкозооксидазу и каталазу..........987
15.7.5.10. Препараты глюкоизомеразы..........989
15.7.5.11. Препараты 0-галактозидазы.........991
15.7.5.12. Препараты 0-фруктофуранозидазы....993
15.7.6. Производство аминокислот............994
15.7.6.1. Свойства и основные направления
использования а-аминокислот.........994
15.7.6.2. Способы получения аминокислот......995
15.7.6.3. Производство L-глутаминовой кислоты .... 998
15.7.6.4. Производство лизина...............1002
15.7.6.5. Производство ароматических
аминокислот........................1005
15.7.6.6. Получение других а-аминокислот.....1007
15.7.7. Производство витаминов и родственных
соединений.........................1010
15.7.7.1. Основные области применения
и способы получения витаминов.......1010
15.7.7.2. Производство 0-каротина...........1011
15.7.7.3. Производство рибофлавина..........1013
15.7.7.4. Производство витамина В]2.........1014
15.7.7.5. Получение витамина B]3............1019
15.7.7.6. Получение витамина D2.............1019
15.7.7.7. Получение витаминов группы F.......1020
15.7.7.8. Получение убихинонов..............1020
15.7.7.9. Производство гиббереллинов.........1022
15.7.8. Производство антибиотиков.........1023
15.7.8.1. Общие сведения об антибиотиках.....1024
15.7.8.2. Основные этапы промышленного получения антибиотиков......................1026
15.7.8.3. Антибиотики, образуемые бактериями.... 1031
15.7.8.4. Антибиотики, образуемые актиномицетами..............................1034
15.7.8.5. Антибиотики, образуемые грибами и лишайниками...............................1044
15.7.8.6. Применение антибиотиков в сельском хозяйстве и пищевой промышленности... 1051
15.7.9. Производство микробных полисахаридов...............................1053
15.7.9.1. Основные промышленные микробные полисахариды................................1053
15.7.9.2. Декстраны.........................1053
15.7.9.3. Ксантан...........................1054
15.7.9.4. Другие полисахариды................1058
15.7.10. Производство органических кислот....1061
15.7.10.1. Физико-химические свойства и производные кислот........................1061
15.7.10.2. Производство лимонной кислоты.....1064
15.7.10.3. Производство глюконовой кислоты...1071
15.7.10.4. Получение 2-кетоглюконовой
и изоаскорбиновой кислот....................1072
Оглавление
1449
15.7.10.5. Производство молочной кислоты....1072
15.7.10.6. Получение полигидроксиалканоатов.1077
15.7.10.7. Производство пищевого уксуса.....1080
15.7.10.8. Производство итаконовой кислоты..1086
15.7.11. Свойства и применение итаконовой кислоты....................................1086
15.7.12. Производство этанола...............1088
15.7.12.1. Подготовка мелассы...............1088
15.7.12.2. Подготовка крахмалсодержащего сырья......................................1089
15.7.12.3. Подготовка винограда.............1099
15.7.12.4. Подготовка целлюлозосодержащего сырья......................................1100
15.7.12.5. Технологический процесс спиртового брожения...................................1101
15.7.12.6. Выделение и очистка этанола......1109
15.7.12.7. Свойства и использование этанола.1117
15.7.12.8. Производство диоксида углерода...1121
15.7.12.9. Побочные продукты спиртового производства...............................1125
ПРОЦЕССЫ И АППАРАТЫ ХИМИЧЕСКИХ ТЕХНОЛОГИЙ. Ч. 1 (Голубой)
Раздел 1. Описание основных процессов и аппаратов
1.1. Образование дисперсной фазы.............7
1.1.1. Полезная и затраченная работа
диспергирования.........................7
1.1.2. Механизмы диспергирования капель
и пузырей ..............................9
1.1.3. Основные принципы механического
разрушения твердых тел..................9
1.2. Классификация дисперсных частиц........11
1.2.1. Классификация с помощью сит............11
1.2.2. Классификация в потоках жидкости ......13
1.2.3. Классификация в потоках газа...........13
1.3. Выделение дисперсной фазы из жидкостей
и газов................................19
1.3.1. Осаждение..............................19
1.3.2. Фильтрование ..........................21
1.3.3. Коагуляция.............................21
1.3.4. Выпаривание............................23
1.3.5. Вымораживание .........................23
1.4. Выделение компонентов из растворов.....24
1.4.1. Выделение газа из жидкости.............24
1.4.2. Выделение жидкого компонента из смеси
жидкостей испарением ..................28
1.4.3. Выделение солей из расплавов и растворов
кристаллизацией........................29
1.4.4. Мембранное разделение жидкостей........32
1.4.5. Мембранное выделение солей из растворов....33
1.4.6. Выделение растворенных компонентов
путем поглощения твердым телом.........34
1.4.7. Выделение компонентов раствора
экстракцией............................34
1.5. Разделение газовых смесей..............38
1.5.1. Разделение газов путем растворения
в жидкости............................38
1.5.2. Разделение путем поглощения
твердым телом .........................42
1.5.3. Мембранное разделение....................44
1.5.4. Разделение путем конденсации ............46
1.6. Растворение различных фаз
и их компонентов в жидкости..............47
1.6.1. Растворение газов .......................47
1.6.2. Растворение жидкостей....................48
1.6.3. Растворение твердых веществ .............49
1.7. Смешение различных фаз
и их компонентов.........................51
1.7.1. Основные принципы смешения...............51
1.7.2. Перемешивание жидкофазных сред...........52
1.7.3. Смешение зернистых материалов............54
1.7.4. Приготовление полимерных композиций......55
1.8. Реакционные процессы ....................56
1.8.1. Основные понятия химической кинетики.....56
1.8.2. Простые и сложные реакции. Теория
переходного состояния....................56
1.8.3. Моделирование химических реакторов.
Основные понятия.........................57
1.8.4. Гидродинамическая модель химического
реактора.................................57
1.8.5. Лимитирующая стадия
химико-технологического процесса.........58
1.8.6. Моделирование реакторов для проведения
гомогенных процессов.....................58
1.8.7. Моделирование реакторов для проведения
реакций в гетерогенных системах..........58
1.8.8. Устойчивость химических реакторов........59
1.8.9. Высокотемпературные химические
реакторы (печи и плазмохимические реакторы)................................59
Раздел 2. Прикладная механика сплошных сред
2.1. Основы механики сплошных сред ...........64
2.1.1. Основные понятия и определения...........64
2.1.2. Силы, действующие в сплошных средах......65
2.1.3. Классификация жидкостей..................66
2.1.4. Основные уравнения механики сплошных
сред.....................................67
2.2. Несжимаемые ньютоновские жидкости .......67
2.2.1. Основные уравнения механики
несжимаемых ньютоновских жидкостей.......67
2.2.2. Уравнение Рейнольдса.....................68
2.2.3. О подобии гидромеханических процессов....69
2.2.4. Плоские задачи гидромеханики ............70
2.2.5. Уравнения пограничного слоя..............71
2.2.6. Течение жидкости в трубах и каналах......72
2.2.7. Безнапорное течение жидкости.............78
2.2.8. Обтекание тел............................80
2.2.9. Течение затопленных струй................84
2.2.10. Пленочное течение.......................85
2.2.11. Гидростатика............................87
2.2.12. Одномерная гидромеханика (гидравлика)...89
2.2.13. Фильтрация в недеформируемой
пористой среде .........................102
2.3. Полуэмпирическая теория турбулентности .106
2.3.1. Введение................................106
2.3.2. Уравнения Рейнольдса и способы
их замыкания.........................107
2.3.3. Модели турбулентной вязкости.........108
1450
Новый справочник химика и технолога
2.3.4. Модели, не использующие гипотезу Ж.В. Буссинеска.............................113
2.3.5. Формулировка некоторых наиболее распространенных моделей турбулентности.............................116
2.3.5.1. Алгебраические и полудифференциальные модели......................................116
2.3.5.2. Модели с одним дифференциальным уравнением..................................116
2.3.5.3. Модели с двумя дифференциальными уравнениями................................117
2.3.5.4. Модели с тремя дифференциальными уравнениями................................119
2.3.5.5. Явные алгебраические модели
рейнольдсовых напряжений (EARSM).....119
2.4. Современные подходы к численному
моделированию турбулентности ........121
2.4.1. Прямое численное моделирование
турбулентности.......................121
2.4.2. Метод моделирования крупных вихрей...121
2.4.3. Метод моделирования отсоединенных
вихрей и другие гибридные подходы....122
2.5. Сжимаемые жидкости...................123
2.5.1. Одномерное движение идеального газа..123
2.5.2. Фильтрация газа в недеформируемой
пористой среде ......................125
2.5.3. Скорость звука в газосодержащих средах.
Истечение газосодержащих сред........127
2.5.4. Стоячие волны в газосодержащих
средах ..............................128
2.6. Неньютоновские жидкости..............130
2.6.1. Законы переноса в неньютоновских
жидкостях ...........................130
2.6.2. Сопротивление при течении в трубах
и каналах............................133
2.6.3. Общий случай течения неньютоновских
жидкостей............................135
2.7. Зернистые среды .....................137
2.7.1. Физико-механические свойства
зернистых сред.......................137
2.7.2. Предельное напряженное состояние
зернистой среды......................140
2.7.3. Статика зернистой среды..............141
2.7.4. Приближенные уравнения статики
зернистой среды......................143
Раздел 3. Прикладная механика неоднородных сред
3.1. Морфологические и дисперсионные
свойст ва неоднородных сред..........152
3.1.1. Пространственное соотношение долей
компонентов и его следствия..........152
3.1.2. Форма и размеры дисперсных частиц....152
3.1.3. Математическое представление
распределения частиц по размерам.....154
3.1.4. Капиллярно-пористые среды............156
3.2. Движение одиночных частиц............158
3.2.1. Влияние градиента давления в потоке
на движение частиц...................158
3.2.2. Несимметричное обтекание частиц......159
3.2.3. Обтекание частицы у стенки...........161
3.2.4. Моделирование движения частиц
в координатах Лагранжа...............162
3.2.5. Моделирование движения частиц
в координатах Эйлера.................167
3.2.6. Движение капель и пузырей............170
3.3. Взаимопроникающие континуальные
среды................................177
3.3.1. Законы сохранения массы и импульса...177
3.3.2. Одномерные вертикальные
дисперсные потоки....................178
3.3.3. Моделирование одномерных двухфазных
многокомпонентных потоков............195
3.3.4. Фильтрация в деформируемой пористой
среде................................197
3.3.5. Одномерное моделирование
двухфазных потоков...................200
3.3.6. Моделирование движения частиц
в координатах Эйлера — Лагранжа......203
3.4. Взаимопроникающие структурные среды..207
3.4.1. Структуры и режимы течения
газо-жидкостных потоков..............208
3.4.2. Одномерные модели газо-жидкостных
потоков..............................209
3.4.3. Газосодержание вертикальных
газо-жидкостных потоков..............211
3.4.4. Структуры неоднородного
псевдоожиженного слоя................213
3.4.5. Моделирование неоднородного
псевдоожиженного слоя................214
3.4.6. Структуры и режимы течения потоков
с частицами..........................215
3.4.7. Моделирование потоков с частицами
при пневмо- и гидротранспорте........217
3.4.8. У с ловия равновесия слоев частиц у стенки... 221
3.4.9. Эффект волны разрушения
в зернистой среде....................222
Раздел 4. Теплообменные процессы
4.1. Основы теплообменных процессов.......227
4.1.1. Основные виды переноса теплоты.......228
4.1.2. Уравнение распространения теплоты.
Условия однозначности................228
4.1.3. Стационарная теплопроводность
твердых тел..........................229
4.1.4. Нестационарная теплопроводность
твердых тел..........................231
4.1.5. Основы конвективного теплообмена
между теплоносителем и поверхностью..237
4.1.6. Основы лучистого теплообмена.........245
4.2. Теплообмен в технологической аппаратуре.. 246
4.2.1. Теплообмен при механическом
перемешивании жидкости...............246
4.2.2. Теплообмен в газо-жидкостных средах..248
4.2.3. Полуэмпирическая теория турбулентного
переноса теплоты.....................250
4.2.4. Теплообмен при ламинарном течении
неньютоновских жидкостей в трубах и каналах.......................;....252
4.2.5. Теплообмен в системах с дисперсной
твердой фазой...............................256
Оглавление
1451
4.2.6. Аналогия процессов конвективного переноса импульса и теплоты (аналогия Рейнольдса)......................260
Раздел 5. Массоперенос
5.1. Концентрационное равновесие...........265
5.2. Кинетика массопереноса................266
5.2.1. Элементарные виды переноса массы......266
5.2.2. Уравнение конвективно-диффузионного
переноса вещества в однофазном потоке.268
5.2.3. Модели массоотдачи....................269
5.2.4. Уравнение массоотдачи.................271
5.2.5. Критерии массообменного подобия.......271
5.2.6. Уравнение массопередачи...............273
5.3. Массоперенос при движении частиц......273
5.3.1. Общие замечания.......................273
5.3.2. Масссоперенос в сплошной фазе.........275
5.3.3. Массоперенос в частице................280
5.3.4. Массоперенос при соизмеримых
сопротивлениях фаз....................286
5.3.5. О применимости уравнения аддитивности
фазовых сопротивлений.................288
5.4. Массообмен при пленочном течении
жидкости .............................290
5.4.1. Массоперенос в жидкой пленке..........290
5.4.2. Массообмен в газовой фазе.............292
5.5. Продольная диффузия...................294
5.5.1. Тейлоровская диффузия.................294
5.5.2. Модели продольного перемешивания......295
5.6. Особенности массопереноса в твердых
телах. Волновая диффузия..............296
5.6.1. Гиперболическое уравнение диффузии....296
5.6.2. Использование волновой модели диффузии
для обработки экспериментальных данных...300
Раздел 6. Вспомогательные, типовые и многофункциональные процессы и аппараты
6.1. Аппараты с перемешивающими
устройствами .........................305
6.1.1. Конструкции аппаратов с перемешивающими устройствами............................306
6.1.2. Гидродинамические характеристики
аппарата с мешалкой...................312
6.1.3. Гидродинамические характеристики
аппарата с прецессирующей мешалкой...319
6.1.4. Гидродинамические характеристики
аппаратов с мешалками при перемешивании гетерогенных систем.....321
6.1.5. Тепло- и массообмен в аппаратах
с мешалками...........................325
6.1.6. Гомогенизация.........................327
6.1.7. Перемешивание жидких сред при больших
диссипациях мощности..................333
6.2. Теплообменная аппаратура..............337
6.2.1. Классификация теплообменных
аппаратов ............................338
6.2.2. Расчет теплообменных аппаратов
по уравнению теплопередачи............339
6.2.3. Итерационный и поинтервальный
методы расчета........................342
6.2.4. Об оптимизации теплообменных аппаратов...................................345
6.2.5. Конструкции и выбор теплообменных аппаратов...................................346
6.3. Машины и аппараты для перемещения жидкостей и газов...........................361
6.3.1. Общие сведения о машинах для подачи жидкостей и газов...........................362
Основные определения и классификация устройств для подачи жидкостей и газов.362
Основные параметры гидравлических машин для подачи жидкостей и газов.....364
Подача и напор объемных и динамических машин. Области применения насосов и компрессоров......366
Работа насоса, подключенного к сети....367
6.3.2. Насосы.................................367
Центробежные насосы....................367
Грязевые, фекальные насосы и насосы для сточных вод........................379
Вихревые насосы........................388
Центробежно-вихревые насосы............389
Поршневые и роторные насосы............389
Шестеренные насосы.....................390
Способы регулирования производительности насосов объемного типа.........................391
6.3.3. Компрессорные машины...................392
Основные понятия. Назначение и области применения компрессорных машин.........392
Устройство компрессорных машин.........394
Конструкции вентиляторов...............398
Элементы теории компрессорных машин..................................403
Регулирование производительности компрессорных машин....................404
6.3.4. Общие сведения о струйных аппаратах....405
6.3.5. Струйные аппараты для пневмотранспорта
зернистых материалов и жидкости........407
6.3.6. Струйные однофазные насосы.............418
6.3.7. Струйные аппараты для гидротранспорта
зернистых материалов ..................424
6.3.8. Жидкостно-газовые струйные аппараты ...425
6.4. Хранение и перевозка зернистых
материалов.............................429
6.4.1. Давление материала на стенки сосудов
и элементы аппаратов...................429
6.4.2. Явления сводо- и трубообразования......430
6.4.3. Истечение из отверстий сосудов.........433
6.4.4. Перевозка зернистых материалов
в транспортных емкостях................435
6.5. Конвейерный транспорт..................439
6.5.1. Классификация и область применения.....439
6.5.2. Ленточные конвейеры..................442
6.5.3. Пластинчатые конвейеры...............450
6.5.4. Скребковые конвейеры.................452
6.5.5. Грузоведущие и подвесные конвейеры...454
6.5.6. Ковшовые элеваторы...................456
6.5.7. Вертикальные конвейеры...............457
6.5.8. Конвейеры без тягового элемента......464
1452
Новый справочник химика и технолога
6.5.9. Рекомендации к проектированию
и расчету..............................467
6.5.10. Питатели..............................469
6.6. Пневматический и гидравлический
транспорт зернистых материалов.........472
6.6.1. Способы организации пневмотранспортных
процессов и их аппаратурное оформление.472
6.6.2. Устройства для забора материала
из насыпи..............................475
6.6.3. Питатели и затворы с запирающим слоем
материала..............................478
6.6.4. Шлюзовые и винтовые питатели ..........479
6.6.5. Камерные питатели......................484
6.6.6. Минимальная скорость транспортирования.
Максимальная концентрация материала. Завал..................................489
6.6.7. Аэрожелобы.............................494
6.6.8. Реализация и компоновка
пневмотранспортных установок...........495
6.6.9. Реализация и компоновка установок
гидротранспорта........................504
6.7. Барботажные аппараты...................511
6.7.1. Барботажные колонны....................512
6.7.2. Барботажные газлифтные аппараты........519
6.7.3. Барботажные аппараты с механическими
перемешивающими устройствами...........523
6.7.4. Барботажные аппараты с инжектированием
и диспергированием газа струями жидкости...............................529
6.8. Пленочные аппараты.....................534
6.8.1. Аппараты со стекающей пленкой..........535
6.8.2. Аппараты с восходящей пленкой..........541
6.8.3. Аппараты с закрученным газо-жидкостным
потоком................................545
6.8.4. Роторные пленочные аппараты............549
6.9. Контактные аппараты с неподвижным
и взвешенным зернистым слоем...........554
6.9.1. Общая характеристика зернистых слоев...555
6.9.2. Конструкции аппаратов с неподвижным
зернистым слоем........................559
6.9.3. Особенности аппаратов с насадками......562
6.9.4. Неоднородности в аппаратах с плотным
зернистым слоем........................566
6.9.5. Движение газо-жидкостных потоков
через слой насадки.....................568
6.9.6. Режимы работы аппаратов с взвешенным
зернистым слоем .......................578
6.9.7. Псевдоожижение под воздействием
колебаний..............................583
6.9.8. Конструкции аппаратов взвешенного слоя.... 585
6.10. Перспективы применения резонансных пульсационных воздействий
в процессах и аппаратах...............590
6.10.1. Введение.............................591
6.10.2. Нестационарная гидродинамика.........592
6.10.3. Капиллярная нестационарная гидродинамика................................595
6.10.4. Колебания поверхности капель и пузырей ....598
6.10.5. Гидродинамика стоячих волн в газосодержащих многофазных средах..........599
6.10.6. Принципы создания пульсационных резонансных аппаратов ......................601
Раздел 7. Методы математического
моделирования
7.1. Формальные математические модели.....605
7.1.1. Основные понятия и характеристики....605
7.1.2. Полный факторный эксперимент.........607
7.1.3. Дробный факторный эксперимент........611
7.1.4. Планы второго порядка................611
7.1.5. Составление формальных математических моделей в нестационарных условиях...........615
7.1.6. Анализ и исследование статистических
моделей в области высокой кривизны поверхности отклика..................618
7.1.7. Формальные математические модели множественной регрессии.....................621
7.2. Математические модели структуры
потоков..............................622
7.2.1. Исследование структуры потоков.......622
7.2.2. Основные характеристики распределения
элементов потока по времени пребывания в аппарате...........................625
7.2.3. Влияние структуры потоков на степень
завершенности физико-химических процессов............................626
7.2.4. Модели идеального смешения и идеального
вытеснения...........................628
7.2.5. Диффузионная модель..................630
7.2.6. Ячеечная модель .....................633
7.2.7. Комбинированные модели ..............638
7.2.8. Волновая модель продольного
перемешивания .......................640
7.3. Моделирование на основе марковских
процессов............................645
7.3.1. Стохастические модели................645
7.3.2. Цепи Маркова.........................649
7.3.3. Процессы Маркова с непрерывным
временем.............................652
7.3.4. Моделирование структур потоков
с использованием цепей Маркова.......655
7.4. Метод Монте-Карло в инженерном
приложении...........................661
7.4.1. Общие представления о методе.........661
7.4.2. Получение и преобразование случайных
величин на ЭВМ.......................661
7.4.3. Применение метода Монте-Карло
при проектировании технологического оборудования.........................662
7.4.4. Исследование волновой модели
продольного перемешивания методом
Монте-Карло..........................665
7.5. Стохастическое моделирование
дисперсных систем ...................671
7.5.1. Дисперсные системы...................671
7.5.2. Фрактальная размерность дисперсной
системы..............................673
7.5.3. Кинетическое уравнение ансамбля
дисперсных частиц....................682
7.5.4. Модель динамики ансамбля дисперсных
частиц как неоднородная цепь Маркова..685
Оглавление
1453
7.5.5. Примеры построения стохастических моделей.....................................689
7.6. Моделирование кинетики сложной газо-жидкостной реакции.....................699
Раздел 8. Процессы диспергирования
8.1. Образование капель и пузырей в объеме сплошной среды..............................705
8.1.1. Образование капель и пузырей при истечении диспергируемой среды из одиночных отверстий и сопел .............706
8.1.2. Капиллярная неустойчивость жидкой струи.......................................712
8.1.3. Диспергирование капель и пузырей в сдвиговом поле............................714
8.1.4. Образование капель и пузырей при гидродинамической неустойчивости границы раздела фаз ........................714
8.1.5. Диспергирование капель и пузырей
под действием турбулентных пульсаций..716
8.1.6. Дробление капель и пузырей при
совместном действии нескольких механизмов диспергирования............718
8.1.7. Дробление пузырей и капель в аппаратах
с мешалками ..........................720
8.2. Введение в процессы диспергирования
твердых тел ..........................721
8.2.1. Назначение операций диспергирования
твердых тел...........................721
8.2.2. Степень сокращения крупности..........722
8.2.3. Стадии и схемы дробления и измельчения....722
8.2.4. Механические свойства горных пород....723
8.2.5. Законы дробления......................726
8.2.6. Принципы селективного раскрытия
минералов.............................727
8.3. Дробление твердых материалов..........729
8.3.1. Эволюционное развитие приемов
дробления.............................729
8.3.2. Валковые дробилки и прессы............734
8.3.3. Щековые дробилки......................739
8.3.4. Конусные дробилки.....................742
8.3.5. Сравнительная характеристика
эксцентриковых и вибрационных дробилок..............................750
8.3.6. Дробилки ударного действия............751
8.4. Измельчение твердых материалов........759
8.4.1. Эволюционное развитие приемов
измельчения...........................759
8.4.2. Измельчители раздавливающего
и истирающего действия................763
8.4.3. Вибрационные и планетарные мельницы...768
8.4.4. Мельницы ударного действия............771
8.4.5. Барабанные мельницы (конструкции
и основные характеристики)............775
8.4.6. Технология измельчения в барабанных
мельницах.............................788
8.4.7. Производительность барабанных мельниц....799
8.5. Механическая активация
при диспергировании твердых материалов ...803
8.5.1. Сущность механической активации
материалов и области ее использования.803
8.5.2. Характеристика физико-химических эффектов на поверхности твердого тела..............................805
8.5.3. Изменение внутренней энергии при диспергировании.........................807
8.5.4. Реакционная способность активированных твердых материалов..........................808
8.5.5. Физические процессы, инициированные измельчением................................809
8.5.6. Механохимические реакции, инициированные измельчением.................810
8.5.7. Основные направления интенсификации технологических процессов с использованием механохимии...............811
8.5.8. Технические средства процессов
активации.............................813
8.6. Измельчение в процессах переработки
полимеров.............................814
8.6.1. Общие положения.......................814
8.6.2. Основное оборудование для измельчения.815
8.6.3. Экструзионные агрегаты
для гранулирования....................818
8.6.4. Агломерация термопластичных отходов...820
8.6.5. Технологические линии для измельчения
отходов пластмасс.....................821
8.6.6. Оборудование для измельчения в
технологических линиях переработки отходов резины........................823
8.7. Образование дисперсной фазы
конденсацией и коагуляцией............825
8.7.1. Фазовый переход жидкость—пар..........825
8.7.2. Гомогенное зародышеобразование........826
8.7.3. Коагуляция монодисперсных сферических
частиц. Приближение Смолуховского.....829
8.7.4. Особенности коагуляции в движущейся
среде.................................831
ПРОЦЕССЫ И АППАРАТЫ ХИМИЧЕСКИХ
ТЕХНОЛОГИЙ. Ч. 2 (Голубой)
Раздел 9. Классификация дисперсных частиц
9.1. Грохочение..............................5
9.1.1. Общие сведения. Просеивающая
поверхность............................5
9.1.2. Способы определения гранулометрического
состава. Ситовый анализ................9
9.1.3. Факторы, влияющие на процесс
грохочения............................12
9.1.4. Кинетика процесса грохочения...........14
9.1.5. Классификация грохотов.................15
9.1.6. Вибрационные грохоты,
их классификация......................17
9.1.7. Горизонтальные качающиеся грохоты......20
9.1.8. Расчет производительности вибрационных
грохотов с круговыми вибрациями
короба..............................20
9.1.9. Гидравлические грохоты тонкого
грохочения..........................25
9.1.10. Влияние конструкции ситовых тканей
на показатели гидравлического
грохочения..........................32
1454
Новый справочник химика и технолога
9.1.11. Вероятностные грохоты................34
9.2. Фракционирование дисперсных частиц
в потоках жидкости...................34
9.2.1. Седиментационный анализ..............35
9.2.2. Моделирование процессов осаждения
в емкостных аппаратах................36
9.2.3. Основные принципы классификации......39
9.2.4. Аппараты для гравитационного
разделения...........................40
9.2.5. Аппараты для разделения в инерционном
поле.................................45
9.2.6. Рекомендации по выбору и расчету
гидравлических классификаторов.......49
9.2.7. Рекомендации по выбору технологических
схем измельчения и классификации.....55
Раздел 10. Осаждение дисперсной фазы из жидкостей и газов
10.1. Осаждение дисперсной фазы
из жидкостных потоков................61
10.1.1. Сгущение.............................61
10.1.2. Математическое моделирование
гравитационного осаждения в гидросгустителе....................68
10.1.3. Принципы осаждения в тонкослойных
отстойниках..........................71
10.1.4. Конструкции тонкослойных отстойников.76
10.1.5. Коагуляция...........................80
10.2. Процессы фильтрационной
консолидации.........................83
10.2.1. Фильтрационная консолидация осадков..83
10.2.2. Истечение жидкости из пен............98
10.2.3. Уплотнение порошкообразных
материалов..........................103
10.3. Выделение дисперсной фазы
из газовых потоков..................105
10.3.1. Выделение дисперсной фазы
в осадительных камерах..............107
10.3.2. Инерционные пылеуловители...........111
10.3.3. Выделение дисперсной фазы
в центробежном поле.................112
10.3.3.1. Циклоны............................112
10.3.3.2. Вихревые пылеуловители.............120
10.3.3.3. Ротационные (динамические)
пылеуловители.......................122
10.3.4. Выделение дисперсной фазы из газовых
потоков в фильтрах..................123
10.3.4.1. Тканевые фильтры...................124
10.3.4.2. Волокнистые фильтры................127
10.3.4.3. Зернистые фильтры..................129
10.3.5. Выделение дисперсной фазы
в аппаратах «мокрого» типа..........130
10.3.5.1. Полые газопромыватели..............131
10.3.5.2. Насадочные газопромыватели.........132
10.3.5.3. Тарельчатые газопромыватели
(барботажные, пенные)...............133
10.3.5.4. Газопромыватели с подвижной
насадкой............................134
10.3.5.5. Газопромыватели ударно-инерционного
действия............................136
10.3.5.6. Газопромыватели центробежного действия.....................................137
10.3.5.7. Скоростные газопромыватели (скрубберы Вентури)..........................139
10.4. Осаждение частиц в электрофильтрах...141
10.4.1. Коронный разряд и зарядка аэрозольных
частиц в электрическом поле..........142
10.4.2. Факторы, влияющие на движение
частиц в электрофильтре..............145
10.4.2.1. Сопротивление среды.................145
10.4.2.2. Влияние силы тяжести................145
10.4.2.3. Электрический ветер.................145
10.4.2.4. Турбулентная диффузия...............146
10.4.2.5. Миграционная сила...................146
10.4.3. Эффективность пылеулавливания
в электрофильтре.....................146
10.4.3.1. Влияние неравномерности поля скоростей
газового потока на эффективность пылеулавливания......................147
10.4.3.2. Влияние неоднородности электрического
поля на эффективность пылеулавливания......................147
10.4.3.3. Факторы, определяющие унос пыли
из электрофильтра....................149
10.4.4. Пути снижения выбросов пыли
из электрофильтров...................150
10.4.4.1. Распределение газовых потоков
в системе коронирующих и осадительных электродов, устройства ввода и вывода газа........................151
10.4.4.2. Оптимизация режима встряхивания
осадительных электродов..............152
10.4.4.3. Импульсное питание электрофильтра...152
10.4.4.4. Типы осадительных и коронирующих
электродов...........................153
10.4.5. Практические конструкции
электрофильтров......................154
10.5. Флотация.............................154
10.5.1. Общие сведения.......................154
10.5.2. Теоретические основы флотации........156
10.5.2.1. Термодинамический анализ возможности
прилипания частицы к пузырьку газа...156
10.5.2.2. Физические основы минерализации
пузырьков............................157
10.5.2.3. Столкновение частиц с пузырьками....157
10.5.2.4. Закрепление частиц на пузырьках.....160
10.5.2.5. Удержание частиц на пузырьках
до выноса в пенный слой..............160
10.5.2.6. Удержание частиц в слое пены........161
10.5.2.7. Кинетика флотации в машинах
периодического действия..............161
10.5.2.8. Флотация не влияющих друг на друга
частиц различной флотируемости.......161
10.5.2.9. Кинетика флотации в машинах
непрерывного действия................162
10.5.2.10. Кинетика флотации в пневматической
машине.......................................163
10.5.2.11. Кинетика флотации в п-камерной
импеллерной машине, состоящей
Оглавление
1455
из полностью изолированных камер с идеальным перемешиванием.........163
10.5.3. Механические флотаторы..............163
10.5.4. Пневматические флотаторы............166
10.5.5. Флотаторы с выделением газа
из раствора........................169
10.5.6. Электрофлотаторы....................175
Раздел 11. Выпаривание
11.1. Теория выпарных аппаратов...........179
11.1.1. Классификация выпарных аппаратов....179
11.1.2. Материальный баланс выпарных
аппаратов..........................181
11.1.3. Тепловой баланс выпарных аппаратов..181
11.1.4. Гидродинамика выпарных аппаратов....182
11.1.5. Теплопередача в выпарных аппаратах..184
11.2. Расчет выпарных аппаратов...........186
11.2.1. Выпарные аппараты с естественной
циркуляцией........................186
11.2.2. Выпарные аппараты с принудительной
циркуляцией........................192
11.2.3. Выпарные аппараты пленочного типа...193
11.2.4. Выпарные аппараты прочих конструкций
и общие особенности расчета выпарных аппаратов..........................198
11.3. Многокорпусные выпарные
установки (МВУ)....................198
11.3.1. Формирование технологических
схем МВУ...........................198
11.3.2. Расчет МВУ..........................201
11.3.3. Оптимизация, проектирование
и особенности эксплуатации МВУ.....203
11.3.4. МВУ с термокомпрессией..............205
Раздел 12. Сушка
12.1. Статика процессов сушки.............210
12.1.1. Параметры и диаграмма состояния
влажного воздуха...................210
12.1.2. Материальные и тепловые балансы
конвективной сушки.................212
12.1.3. Основные варианты использования
сушильного агента..................213
12.1.4. О равновесном влагосодержании
материалов.........................214
12.1.5. Об экспериментальном определении
параметров влажного материала и сушильного агента................215
12.2. Кинетика процессов сушки............215
12.2.1. Внутренний перенос влаги и теплоты..215
12.2.2. Внешний тепломассообмен.............216
12.2.3. Экспериментальная кинетика сушки....218
12.3. Расчеты кинетики процессов в сушильных
аппаратах..........................221
12.3.1. Неподвижный фильтруемый слой
дисперсного материала. Перекрестное движение...........................221
12.3.2. Движущийся слой дисперсного
материала..........................223
12.3.3. Пневматическая сушка................225
12.3.4. Сушка в закрученных потоках.........226
12.3.5. Сушка в псевдоожиженном слое........229
12.3.6. Фонтанирующий слой..................234
12.3.7. Сушка жидкостей и паст в условиях псевдоожижения..............................236
12.3.8. Распылительная сушка................238
12.4. Конструкции сушильных аппаратов.....240
12.4.1. Конвективные сушилки................240
12.4.2. Контактные сушилки..................244
12.4.3. Специальные методы сушки............245
12.4.4. Вспомогательное оборудование........246
Раздел 13. Адсорбция
13.1. Материалы для адсорбционных
процессов..........................249
13.1.1. Физико-химические основы
адсорбционных процессов............249
13.1.2. Виды промышленных адсорбентов,
их основные характеристики и классификация....................251
13.1.3. Адсорбенты с модиф ицированной
поверхностью.......................254
13.1.4. Методы получения и области
применения адсорбентов.............257
13.2. Аппаратурное оформление
адсорбционных процессов............282
13.2.1. Адсорберы периодического действия
(вертикальный, горизонтальный, кольцевой, с теплообменными элементами, с прижимными устройствами).........282
13.2.2. Адсорберы непрерывного действия с движущимся слоем адсорбента...............286
13.3. Типовые схемы использования адсорбционных процессов.....................286
13.3.1. Осушка газов и органических жидкостей...................................286
13.3.2. Очистка промышленных газов..........294
13.3.3. Очистка воды........................296
Раздел 14. Кристаллизация
14.1. Кристаллизация из расплавов.........300
14.1.1. Процесс фракционной кристаллизации из расплавов.................300
14.1.1.1. Различные способы и особенности процесса массовой кристаллизации............302
14.1.1.2. Подходы к математическому описанию процесса массовой кристаллизации............303
14.1.1.3. Аппаратурное оформление процесса массовой кристаллизации.....................305
14.1.1.4. Процесс противоточной фракционной кристаллизации из расплавов.................310
14.1.1.5. Математические модели процесса противоточной кристаллизации................311
14.1.1.6. Аппаратурное оформление процесса
противоточной фракционной кристаллизации из расплавов........313
14.1.1.7. Особенности процесса фракционной
кристаллизации из расплавов
на охлаждаемых поверхностях........316
14.1.1.8. Математическое описание основных
параметров процесса фракционной
кристаллизации на охлаждаемых
поверхностях (с образованием
поверхности раздела фаз)............316
1456
Новый справочник химика и технолога
14.1.1.9. Аппаратурное оформление процесса кристаллизации на охлаждаемых поверхностях................................319
14.1.2. Фракционное выплавление.............321
14.1.2.1. Различные варианты процесса
фракционного выплавления............321
14.1.2.2. Математическая модель фракционного
выплавления.........................322
14.1.2.3. Аппаратурное оформление процесса
фракционного выплавления............324
14.2. Кристаллизация из растворов.........330
14.2.1. Обобщенная постановка задачи.
Основные характеристики массовой кристаллизации......................331
14.2.2. Зарождение и рост кристаллической
фазы................................331
14.2.3. Математическое описание процесса
массовой кристаллизации.............334
14.2.4. Периодическая массовая
кристаллизация......................337
14.2.5. Непрерывная кристаллизация
из растворов........................345
14.2.6. Аппаратурное оформление процессов
выделения твердой фазы из растворов (емкостные аппараты, вакуум-кристаллизаторы, колонные аппараты)........351
14.3. Вымораживание.......................355
14.3.1. Области применения и конструкции барабанных морозильных
аппаратов...........................355
14.3.2. Физические и математические основы описания процесса затвердевания материала....................................363
14.3.3. Особенности процесса тонкослойного замораживай ия...............................364
14.3.4. Расчет теплообмена при тонкослойном замораживании на вымораживающем барабане....................................365
14.3.5. Методика расчета вымораживающего барабана для процесса непрерывного замораживания в тонком слое.................367
Раздел 15. Мембранные процессы разделения
15.1. Мембраны............................374
15.1.1. Основные свойства мембран...........374
15.1.2. Факторы, влияющие на мембранные
процессы............................378
15.1.3. Концентрационная поляризация........381
15.2. Механизмы мембранного
массопереноса.......................383
15.2.1. Взаимодействие разделяемой системы
с мембраной.........................383
15.2.2. Разделение полимерными мембранами
жидких сред.........................385
15.3. Аппараты для мембранного разделения
жидких сред.........................388
15.3.1. Аппараты с плоскими мембранными
элементами..........................389
15.3.2. Аппараты с трубчатыми мембранными
элементами..........................390
15.3.3. Аппараты с рулонными мембранными элементами..................................394
15.3.4. Разделительные аппараты на основе полых волокон...............................395
15.3.5. Расчет аппаратов мембранного разделения жидких сред......................397
15.4. Установки мембранного разделения
жидких сред.........................402
15.4.1. Установки обратного осмоса...........402
15.4.2. Установки ультрафильтрации...........407
15.4.3. Установки микрофильтрационные........413
15.5. Мембранное разделение газов..........417
15.5.1. Мембраны для разделения газовых смесей.
Транспорт через пористые и непористые мембраны............................417
15.5.2. Приближенный метод расчета
мембранного модуля
для разделения газов................420
15.5.3. Одноступенчатые и многоступенчатые
мембранные газоразделитсльныс
установки...........................422
15.5.4. Практическое применение мембранного
разделения газовых смесей...........426
15.6. Испарение через мембрану
и мембранная дистилляция............430
15.6.1. Испарение через мембрану чистых
жидкостей и смесей жидкостей. Мембраны, используемые для осуществления процесса испарения через мембрану............430
15.6.2. Расчет процесса испарения
через мембран.......................433
15.6.3. Практическое применение процесса
испарения через мембрану............434
15.6.4. Мембранная дистилляция...............435
15.7. Диализ и электродиализ...............438
15.7.1. Диализ...............................438
15.7.2. Электродиализ........................439
Раздел 16. Растворение и экстрагирование в системе твердое тело—жидкость
16.1. Растворение твердых частиц в жидкости.... 444
16.1.1. Кинетика растворения.................444
16.1.2. Материальный и тепловой балансы
процессов растворения...............446
16.1.3. Методы расчета, основанные на кинетике
растворения индивидуальных частиц...446
16.1.4. Метод расчета, основанный
на экспериментальных данных по кинетике растворения представительных проб полидисперсного материала (применение инвариантных кинетических функций)..451
16.1.5. Аппараты для растворения твердых
веществ в жидкостях.................453
16.2. Экстрагирование......................456
16.2.1. Диффузионные модели экстрагирования
растворенных и твердых веществ......456
16.2.1.1. Извлечение вещества из капилляров.456
16.2.1.2. Извлечение вещества
из капиллярно-пористых тел..........460
16.2.1.3. Извлечение вещества из слоя
капиллярно-пористых тел.............466
Оглавление
1457
16.2.2. Диффузионно-конвективные режимы экстрагирования.............................470
16.2.2.1. Модели экстрагирования из пористых частиц в диффузионноконвективном режиме.........................470
16.2.2.2. Моделирование процесса экстрагирования из капиллярнопористой частицы с бидисперсной структурой..................................479
16.2.3. Инженерные методы расчета процесса
экстрагирования....................485
16.2.3.1. Расчет теоретических ступеней
экстрагирования....................485
16.2.3.2. Интервальные методы расчета.......489
16.2.3.3. Применение инвариантных
кинетических функций...............490
16.2.3.4. Энергетический подход к описанию
экспериментальных данных по кинетике экстрагирования........493
16.2.4. Аппаратурно-технологическое
оформление процесса................493
16.2.4.1. Методы интенсификации процесса
экстрагирования....................493
16.2.4.2. Аппараты для экстрагирования......502
Раздел 17. Химическая кинетика
17.1. Основные понятия и определения......524
17.1.1. Классификация и терминология........524
17.1.2. Скорость химической реакции.........525
17.1.3. Кинетическое уравнение химического
процесса...........................526
17.1.4. Закон Аррениуса. Энергия активации..526
17.2. Расчет скоростей элементарных реакций.
Теория переходного состояния.......526
17.2.1. Элементарные химические реакции.....526
17.2.2. Теория переходного состояния........528
17.2.3. Границы применимости теории
переходного состояния..............530
17.2.4. Схема мономолекулярной реакции......531
17.2.5. Химические реакции сталкивающихся
частиц.............................532
17.3. Кинетика сложных реакций............533
17.3.1. Обратимые реакции...................534
17.3.2. Параллельные реакции................535
17.3.3. Конкурирующие реакции...............536
17.3.4. Последовательные реакции............536
17.3.5. Последовательно-параллельные реакции...538
17.3.6. Последовательные реакции
с равновесными стадиями............540
17.4. Кинетика гетерогенно-каталитических
реакций............................540
17.4.1. Основные понятия ...................540
17.4.2. Дефекты структуры кристаллов........541
17.4.3. Адсорбция...........................541
17.4.4. Изотерма адсорбции..................542
17.4.5. Кинетика реакций на однородных
поверхностях. Ленгмюровская кинетика...........................543
17.4.6. Катализ металлами...................545
17.4.7. Особенности химической реакции
в системе газ—жидкость.............545
Раздел 18. Химические реакторы
18.1. Классификация реакторов.
Терминология.......................548
18.2. Структура потоков и распределение
времени пребывания в аппаратах.....549
18.2.1. Функция распределения частиц
по времени пребывания..............549
18.2.2. Модель идеального вытеснения........549
18.2.3. Модель идеального смешения..........549
18.2.4. Диффузионная модель.................549
18.2.5. Распределения времени пребывания
в трубчатых аппаратах..............550
18.3. Моделирование реакторов для проведения
гомогенных процессов...............550
18.3.1. Понятие лимитирующей стадии процесса.... 550
18.3.2. Материальный баланс реактора........552
18.3.3. Тепловой баланс реактора............552
18.3.4. Преобразование уравнений
к безразмерным переменным..........553
18.4. Моделирование реакторов для проведения
гетерогенных процессов.............557
18.4.1. Типы газожидкостных реакторов.......557
18.4.2. Реакторы барботажные................557
18.4.3. Реакторы с механическим
диспергированием газа..............558
18.4.4. Реакторы пленочные..................559
18.4.5. Реакционные процессы в системах
газ—твердое........................561
18.4.5.1. Феноменологическая теория
топохимических реакций.............561
18.4.5.2. Кинетика образования ядер фаз
твердого продукта..................562
18.4.5.3. Закономерности реакции в целом....564
18.4.6. Гетерогенно-каталитические реакторы.566
18.4.6.1. Общие сведения. Моделирование
реакторов для проведения гетерогеннокаталитических процессов...........566
18.4.6.2. Основные закономерности
массотеплопереноса.................566
18.4.6.3. Диффузия в пористых катализаторах.567
18.4.6.4. Диффузия в цеолитах...............569
18.4.6.5. Теплопроводность пористого
катализатора.......................569
18.4.6.6. Основные уравнения макрокинетики..570
18.5. Устойчивость химических реакторов...573
18.5.1. Основные понятия, используемые
при исследовании устойчивости химических реакторов...............573
18.5.2. Исследование реактора на устойчивость
к малым возмущениям................574
18.5.3. Классификация положений равновесия
динамических систем................574
18.5.4. Устойчивость к малым возмущениям
стационарных состояний реакторов....577
18.5.5. Исследование устойчивости реакторов
вторым методом Ляпунова.............579
18.6. Основные конструктивные типы
реакторов...........................580
18.6.1. Обоснование выбора реакционного
аппарата............................580
1458
Новый справочник химика и технолога
18.6.2. Примеры конструктивного исполнения для химических реакторов различных типов..............................581
18.6.2.1. Реакторы для проведения гомогенных реакций в газовой фазе.......................581
18.6.2.2. Реакторы для проведения гомогенных реакций в жидкой фазе........................583
18.6.2.3. Реакторы для проведения гетерогенных реакций в системе газ—жидкость...............583
18.6.2.4. Реакторы для проведения гетерогенных реакций в системе газ—твердое тело...........584
18.6.2.5. Реакторы для проведения гетерогенных реакций в жидкой фазе.......................585
Раздел 19. Высокотемпературные реакторы (печи)
19.1. Камерные и проходные печи............589
19.1.1. Тепловой расчет электрических печей
сопротивления.......................589
19.1.2. Расчет и конструирование нагревательных
элементов...........................600
19.1.3. Типовые конструкции камерных
и проходных печей...................611
19.1.3.1. Камерные печи......................611
19.1.3.2. Проходные печи.....................612
19.1.3.3. Топливосжигающис устройства........617
19.1.4. Особенности тепловой работы печей,
основы их расчета...................622
19.2. Руднотермические печи................636
19.2.1. Печи для производства карбида
кальция.............................636
19.2.2. Печи для производства желтого
фосфора.............................638
19.2.3. Печи для выплавки электрокорунда.....645
19.2.4. Выбор рабочих токов, напряжений
и геометрических размеров ванн руднотермических печей..............646
19.2.5. Печи для производства карбида
кремния.............................649
19.2.6. Печи графитации......................651
19.2.7. О режимах работы руднотермических
печей...............................652
19.3. Вращающиеся печи для производства
строительных материалов.............653
19.3.1. Вращающиеся печи для производства
цементного клинкера.................653
19.3.2. Типовые конструкции вращающихся
печей...............................655
19.3.2.1. Теплообменные устройства печей
мокрого способа производства........655
19.3.2.2. Встроенные теплообменники..........656
19.3.2.3. Теплообменники печей сухого способа
производства........................656
19.3.3. Теплообменники и вращающиеся печи
для огнеупоров......................657
19.3.4. Холодильники вращающихся печей.......659
19.3.5. Холодильниики печей для производства
огнеупоров..........................660
19.3.6. Печи кипящего слоя и циклонные
печи................................660
19.3.7. Принципы расчета при проектировании
вращающихся печей...................661
19.4. Общие принципы работы и классификация плазмохимических реакторов...................................665
19.4.1. Струйные реакторы с электродуговыми
плазмотронами.......................668
19.4.2. Струйные реакторы
с ВЧ-плазмотронами..................671
19.4.3. Объемные реакторы...................671
19.4.4. Расчет исходных данных
для проектирования плазмохимического реактора............................672
Раздел 20. Надежность технологических процессов и установок
20.1. Теория надежности...................675
20.1.1. Общие понятия надежности............675
20.1.2. Классификация отказов...............679
20.1.3. Классификация случайных величин
и функций (законов) распределения...682
20.1.4. Показатели надежности объектов......690
20.1.5. Расчет показателей надежности химикотехнологических объектов....................702
20.2. Обеспечение и поддержание надежности
объекта.............................717
20.2.1. Обеспечение надежности объекта
на стадии проектирования............717
20.2.2. Обеспечения надежности объекта
на стадии изготовления..............730
20.2.3. Поддержание надежности объекта
на стадии эксплуатации..............733
20.2.4. Восстановление, стратегия и тактика
технического обслуживания (ремонта).737
20.3. Анализ надежности химикотехнологических объектов (систем)...........751
20.3.1. Структурно-логический анализ систем.752
20.3.2. Методы расчета структурной надежности
систем..............................754
20.3.3. Методы повышения надежности
систем..............................759
Приложение П20..............................778
Приложение. Справочник по молекулярной диффузии в системах газ—жидкость и жидкость—жидкость.................785
1. Диффузия газов в жидкостях..........788
1.1. Основные уравнения для расчета коэффициента молекулярной диффузии газов в жидкостях...........................788
1.2. Экспериментальные методы определения коэффициентов молекулярной диффузии растворенных газов в жидкостях..............797
1.3. Экспериментальные значения коэффициентов молекулярной диффузии растворенных газов в жидкостях..............814
2. Диффузия жидкостей в жидких средах...824
2.1. Основные уравнения для расчетов
коэффициента молекулярной диффузии
в системе жидкость—жидкость.................824
2.2. Экспериментальные методы определения
коэффициентов молекулярной диффузии
в системе жидкость—жидкость..................837
Оглавление
1459
2.3. Экспериментальные значения коэффициентов молекулярной диффузии в системе жидкость—жидкость................848
Дополнение 1................................896
Дополнение 2................................901
РАДИОАКТИВНЫЕ ВЕЩЕСТВА. ВРЕДНЫЕ
ВЕЩЕСТЫВА. ГИГИЕНИЧЕСКИЕ
НОРМАТИВЫ (Черный)
Раздел 1. Радиоактивные вещества
1.1. Радиоактивность........................5
1.2. Законы радиоактивного распада..........5
1.3. Виды распада радиоактивных ядер........7
1.4. Накопление радиоактивных изотопов при
облучении ядер различными частицами...10
Раздел 2. Взаимодействие различных видов излучения с веществом
2.1. Взаимодействие альфа-частиц
с веществом...........................13
2.2. Взаимодействие электронов с веществом.15
2.3. Взаимодействие гамма-излучения
с веществом...........................16
2.4. Взаимодействие нейтронов с веществом ....17
Раздел 3. Дозы облучения
3.1. Система дозиметрических величин.......19
3.1.1. Физические величины...................19
3.1.2. Нормируемые величины..................20
3.1.3. Операционные величины.................22
3.2. Предельно допустимые уровни облучения.24
3.2.1. Основные пределы доз..................25
3.2.2. Годовое поступление радионуклидов через
органы дыхания........................25
3.2.3. Значения допустимых уровней
радиационного воздействия ............26
3.3. Расчет доз, создаваемых внешними
источн иками ионизирующих излучений...26
3.3.1. Доза, создаваемая параллельным потоком
моноэнергетических гамма-квантов......27
3.3.2. Доза от точечного источника со сложным
составом гамма-излучения..............27
3.3.3. Доза от внешнего источника
бета-излучения........................28
3.4. Свойства радионуклидов, поступивших
в организм человека...................30
Раздел 4. Биологическое действие излучения на организм
4.1. Радиочувствительность..................35
4.2. Прямое и косвенное действия ионизирующих
излучений............................36
4.3. Соматические и генетические
повреждения...........................36
4.4. Детерминированные и стохастические
эффекты...............................37
4.5. Реакции клеток на облучение.............38
4.6. Внешнее, контактное и внутреннее
облучение.............................41
4.7. Биологическая противолучевая защита
организма.............................41
4.8. Лечебное применение ионизирующих
излучений.............................42
4.9. Стерилизация и сохранение пищевых продуктов....................................43
Раздел 5. Защита от излучения
5.1. Защита временем и расстоянием.........45
5.2. Защитное экранирование................45
5.3. Расчет защиты от гамма-излучения......45
5.4. Защита от альфа- и бета-излучений.....53
5.5. Защита от тормозного излучения........54
5.6. Защита от нейтронного излучения.......55
Раздел 6. Детектирование, радиометрия и спектрометрия ядерных излучений
6.1. Детектирование ядерных излучений......63
6.1.1. Потери энергии........................63
6.1.2. Пробеги заряженных частиц в веществе..64
6.1.3. Взаимодействие у-квантов с веществом..66
6.2. Детекторы излучений...................67
6.2.1. Сцинтилляционные детекторы............69
6.2.2. Ионизационные детекторы...............75
6.2.3. Полупроводниковые детекторы...........85
6.2.4. Система наименований и нормируемые параметры ионизационных детекторов...........91
6.2.5. Трековые детекторы заряженных частиц..92
6.3. Спектрометрия ядерных излучений.......95
6.3.1. Основные параметры спектрометров......96
6.3.2. Спектрометры с ионизационными
детекторами (с газовым и жидким наполнением)..........................99
6.3.3. Сцинтилляционные спектрометры........101
6.3.4. Полупроводниковый спектрометр........103
Раздел 7. Радионуклиды в природе
7.1. Источники радиации на Земле..........127
7.2. Радионуклиды земного происхождения...127
7.3. Естественный радиационный фон
окружающей среды.....................134
7.4. Земные источники внутреннего
облучения человека...................143
7.4.1. Объемная активность радона в воздухе
помещений............................143
7.4.2. Объемная активность дочерних продуктов
распада радона в воздухе помещений...148
7.4.3. Оценка дозы от дочерних продуктов
распада изотонов радона..............150
7.4.4. Дозы облучения отдельных органов человека
радионуклидами земного происхождения.... 151
7.5. Космические лучи.....................151
Раздел 8. Техногенные радиоактивные источники
8.1. Искусственные радионуклиды техногенного
происхождения........................157
8.2. Естественные радионуклиды техногенного
происхождения........................158
8.2.1. Радиоактивность, связанная
с добычей нефти и газа...............158
8.2.2. Выделение радиоактивности
при сжигании угля....................159
Раздел 9. Техногенные естественные
и искусственные радиоактивные
источники ядерного топливного цикла
9.1. Добыча и переработка руды..............161
9.2. Извлечение и обогащение урана..........163
1460
Новый справочник химика и технолога
9.3. Накопление радионуклидов при
работе реактора........................164
9.4. Хранение и переработка топлива,
упаковка и захоронение отходов.........168
9.5. Оценка дозы излучения для ядерного топливного цикла..............................170
Раздел 10. Аварии на ядерных реакторах и ядерных объектах
10.1. Причины возникновения аварий и оценка утечки радиоактивности ......................173
10.2. Примеры инцидентов на ядерных объектах, приведших к значительным выбросам радиоактивных веществ. Мониторинг объектов захоронения радиоактивных отходов......................................175
10.2.1. Авария на военном объекте в Кыштыме...175
10.2.2. Авария в У индекс йлс.................176
10.2.3. Тримайл-Айленд........................177
10.2.4. Селлафилд.............................177
10.2.5. Кап-дс-ла-Аг..........................178
10.2.6. Чернобыль.............................178
10.2.7. Падение с космической орбиты советского
атомного реактора......................179
10.2.8. Падение установки спутника SNAP-9A....179
Раздел 11. Радиоактивные загрязнения и дезактивация
11.1. Источники радиоактивных загрязнений....181
11.1.1. Характеристика радиоактивных загрязнений..................................182
11.1.2. Физико-химические процессы элементарных актов радиоактивного загрязнения поверхности......................184
11.1.2.1. Общая характеристика взаимодействия радиоактивных веществ с поверхностью..........184
11.1.2.2. Адсорбционные процессы при радиоактивных загрязнениях...................185
11.1.2.3. Глубинные радиоактивные загрязнения.185
11.2. Дезактивация ..........................186
11.2.1. Количественная оценка эффективности дезактивации.................................186
11.2.2. Классификация способов дезактивации...187
11.2.3. Физико-химические основы способов
дезактивации...........................188
11.2.4. Кинетика процесса дезактивации........189
11.3. Безжидкостные способы дезактивации.....191
11.3.1. Дезактивация струей газа..............191
11.3.2. Абразивный обдув......................192
11.3.3. Дезактивация механическим воздействием
с пылеотсасыванием.....................193
11.3.4. Дезактивация путем снятия загрязненного
слоя и изоляции загрязненной
поверхности............................193
11.4. Дезактивация струей воды...............195
11.4.1. Механизм процесса дезактивации
струей воды ...........................195
11.4.2. Пути повышения эффективности
дезактивации струей воды...............196
11.5. Дезактивация растворами...............198
11.5.1. Растворы на основе ПАВ и
комплексообразующих добавок............198
11.5.2. Обработка растворами, содержащими окислители и восстановители ..................200
11.5.3. Применение растворов, содержащих сорбенты ......................................202
11.6. Интенсификация процесса дезактивации электрическим полем и ультразвуком.............203
11.6.1. Обработка загрязненных поверхностей растворами при наложении электрического поля ..........................203
11.6.2. Повышение эффективности дезактивации
с помощью ультразвуковых колебаний в растворе.............................205
11.7. Применение пленок и покрытий
различного состава.....................206
11.7.1. Назначение и состав пленок и покрытий.206
11.7.2. Изолирующие покрытия..................207
11.7.3. Дезактивация методом нанесения
и удаления пленок......................207
11.7.4. Локализация радиоактивных загрязнений
эмульсиями и твердеющими составами.....208
11.8. Дезактивация воды......................209
11.8.1. Радиоактивные загрязнения воды
и оценка методов очистки...............209
11.8.2. Методы дезактивации воды..............209
11.9. Очистка воздуха........................212
11.10. Дезактивация одежды....................214
11.10.1. Загрязнение и дезактивация одежды из хлопчатобумажной ткани........................214
11.10.2. Дезактивация одежды из шерстяных и искусственных тканей .......................217
11.10.3. Повышение эффективности дезактивации одежды........................................218
11.11. Дезактивация кожных покровов...........219
11.12. Дезактивация продовольствия............220
Раздел 12. Ядерно-физические свойства актиноидов
12.1. Общая характеристика актиноидов........225
12.1.1. Деление ядер. Цепная реакция деления..226
12.1.1.1. Делимость и барьер деления..........226
12.1.1.2. Энергия деления ....................228
12.1.1.3. Продукты деления ...................228
12.1.2. Размножение нейтронов.................229
12.1.2.1 .Коэффициент размножения для бесконечной среды.............................229
12.1.2.2.Утечка нейтронов.....................230
12.1.3. Получение трансурановых элементов.....231
12.2. Ядерная безопасность...................232
12.2.1. Допустимые и безопасные параметры ....234
12.2.2. Коэффициенты запаса...................234
12.2.3. Эффекты гетерогенности................234
12.2.4. Способы обеспечения ядерной
безопасности...........................235
12.2.5. Влияние замедлителей на критические
параметры нуклидов ....................236
12.2.6. Критические параметры смесей
нуклидов...............................236
12.3. Ядерные свойства элементов с Z
от 89 до 103 ..........................237
12.3.1. Актиний...............................238
12.3.2. Торий.................................240
12.3.3. Протактиний...........................242
Оглавление
1461
12.3.4. Уран.................................243
12.3.5. Нептуний.............................248
12.3.6. Плутоний.............................249
12.3.6.1 .Критические параметры..............251
12.3.6.2.Критические параметры смеси изотопов ....................................251
12.3.7. Америций.............................252
12.3.8. Кюрий................................254
12.3.9. Берклий..............................255
12.3.10. Калифорний..........................256
12.3.11. Эйнштейний .........................257
12.3.12. Трансэйнштейниевые элементы.........258
Раздел 13. Свойства, радиобиологическое воздействие и методы определения некоторых радионуклидов
13.1. Тритий, 3Н ..........................263
13.1.1. Образование трития в окружающей среде. Распределение в организме и радиационное воздействие на человека и животных............263
13.1.2. Методы определения и допустимые концентрации трития в воздухе рабочих помещений и в окружающей среде................264
13.2. Углерод 14С .........................265
13.2.1. Образование ,4С в окружающей среде, применение, распределение в организме и радиационное воздействие на человека и животных ..................................265
13.2.2. Методы измерения активности и допустимые концентрации 14С в воздухе рабочих помещений и в окружающей среде........................................266
13.3. Аргон 41 Аг. Образование, методы измерения активности и допустимые концентрации 41 Аг в воздухе рабочих помещений в зависимости от их объема..........267
13.4. Хром 51Сг. Образование, применение, распределение в организме человека и допустимые концентрации 51Сг в воздухе рабочих помещений и в окружающей среде.........................................268
13.5. Железо 59Fe...........................270
13.5.1. Образование, применение, распределение в организме человека и радиационное воздействие на человека и животных............270
13.5.2. Методы измерения радиоактивности 59г? и допустимые концентрации г е в воздухе рабочих помещений и в окружающей среде..........................271
13.6. Кобальт 60Со..........................271
13.6.1. Образование, применение, распределение в организме человека, радиационное воздействие на человека и животных............271
13.6.2. Методы измерения активности и допустимые концентрации Со в воздухе рабочих помещений и в окружающей среде.........................272
13.7. Криптон 85Кг.........................273
13.7.1. Образование, распределение 85Кг
в организме человека и животных.......273
13.7.2. Методы измерения активности и оцененные мощности дозы в различных органах для полубесконечного пространства, содержащего 85Кг...............274
13.8. Стронций 89Sr и 90Sr.................274
13.8.1. Образование и пути поступления 89Sr
и 90Sr в окружающую среду.............274
13.8.2. Распределение в организме
и радиационное воздействие радионуклидов стронция на человека и животных............................275
13.8.3. Методы определения 89Sr и 90Sr в организме и объектах окружающей среды и допустимые концентрации этих радионуклидов в воздухе рабочих помещений и в окружающей среде...............276
13.9. Радиоактивные изотопы иода i23I, 125I, ,291,13,1........................277
13.9.1. Образование, миграция в природной среде, применение, распределение в организме человека и радиационное воздействие радионуклидов иода...........................277
13.9.2. Измерение радиоактивности и допустимые концентрации изотопов иода в воздухе рабочих помещений и в окружающей среде.........................280
13.10. Цезий 134Cs, 137Cs...................281
13.10.1. Образование, применение, распределение в организме и радиационное воздействие цезия на человека и животных.................281
13.10.2. Методы определения и допустимые концентрации 134Cs и l37Cs в воздухе рабочих помещений и в окружающей среде........................................283
13.11. Торий................................283
13.11.1. Свойства, применение, распределение в организме человека и животных, радиационное воздействие, токсичность........283
13.11.2 Методы определения тория.............285
13.12. Уран 234U, 235U, 238U................286
13.12.1. Свойства, применение, распределение в организме человека и животных, радиационное воздействие, токсичность........286
13.12.2. Методы определения урана............287
13.13. Нептуний 237Np, 239Np ...............289
13.13.1. Получение и свойства нептуния.......289
13.13.2. Радиационное и токсическое воздействие нептуния на человека и животных .............290
13.13.3. Методы определения нептуния.........291
13.14. Плутоний 238Pu, 239Ри................292
13.14.1. Получение, свойства, применение, поступление в окружающую среду ..............292
13.14.2. Поступление и распределение в организме человека и животных, радиационное воздействие..................................293
13.14.3. Методы определения плутония.........294
13.15. Америций 241 Ат, 243Ат................296
13.15.1. Образование, свойства, применение
и поступление в окружающую среду.............296
1462
Новый справочник химика и технолога
13.15.2. Распределение америция в организме человека и животных и радиационное воздействие................................296
13.15.3. Методы определения и допустимые 241 а 243 а концентрации Ат и Ат в воздухе рабочих помещений, атмосферном воздухе, воде и пище........................297
Приложение I. Ядерно-физические и дозиметрические характеристики радионуклидов..............................301
Приложение II. Средства измерения ионизирующих излучений......................330
Приложение III. Организация работ с радиоактивными веществами.........339
ВРЕДНЫЕ ВЕЩЕСТВА Раздел 1. Неорганические соединения.........415
Раздел 2. Органические соединения
2.1. Алифатические углеводороды............536
Предельные алифатические углеводороды....536
Непредельные углеводороды этиленового ряда ...539
Непредельные углеводороды с двумя двойными связям..........................539
Непредельные углеводороды ацетиленового ряда.....................................540
Предельные алициклические углеводороды...541
Непредельные алициклические углеводороды.541
Ароматические углеводороды — производные бензола..................................542
Ароматические углеводороды с двумя и более неконденсированными кольцами.......547
Ароматические углеводороды с конденсированными кольцами...............548
2.2. Галогенпроизводные ароматических углеводородов..............................550
Алифатические галогеноуглеводороды.......550
Хлорпроизводные непредельных алифатических углеводородов..............560
Хлорпроизводные алициклических углеводородов............................565
Бромпроизводные предельных алифатических углеводородов..............567
Бромпроизводные непредельных алифатических углеводородов..............570
Иодпроизводные алифатических углеводородов............................570
Смешанные галогенпроизводные алканов ....571
Смешанные галогенпроизводные алкенов.....573
Галогенпроизводные ряда бензола..........574
Хлорпроизводные дифенилметана............577
Галогенпроизводные других ароматических углеводородов..............579
2.3. Кислородсодержащие соединения.........581
Спирты...................................581
Фенолы...................................592
Простые эфиры ...........................598
Пероксиды................................603
Альдегиды................................607
Кетоны...................................611
Хиноны .................................618
Карбоновые кислоты......................620
Галогенангидриды карбоновых кислот......634
Ангидриды карбоновых кислот.............639
Сложные эфиры ..........................643
Азотсодержащие производные карбоновых кислот .................................666
2.4. Азотсодержащие соединения.............680
Амины...................................680
Производные гидразина...................696
Изонитрилы..............................698
Цианаты и изоцианаты....................699
Тиоцианаты .............................701
Изотиоцианаты...........................702
Нитросоединения.........................703
А-Нитрозосоединения ....................709
Алкилнитриты............................711
Алкилнитраты ...........................711
2.5. Серасодержащие органические
соединения..........................713
Тиолы...................................713
Тиоэфиры................................714
Сульфоксиды ............................715
Сульфеновые и сульфоновые кислоты и их производные........................715
Раздел 3. Природные вещества Горючие газы............................718
Эфирные масла...........................721
Терпены ................................722
Яды.....................................725
Антибиотики ............................747
Ферменты................................760
Гормональные препараты .................763
Алкалоиды...............................766
Раздел 4. Гетероциклические соединения
Трехчленные гетероциклические соединения.774
Четырех- и пятичленные гетероциклические соединения с одним гетероатомом.........777
Пятичленные гетероциклические соединения с двумя гетероатомами...................781
Шести- и семичленные гетероциклические соединения с одним гетероатомом.........783
Шестичленные гетероциклические соединения с двумя гетероатомами........788
Гетероциклические соединения с тремя и более гетероатомами...................792
Раздел 5. Органические красители и пигменты
Индигоидные красители...................796
Антрахиноновые красители................797
Азокрасители............................798
Азиновые красители......................798
Ди- и трифенилметановые красители ......799
Ксантеновые красители...................801
Раздел 6. Полимеры и их композиции.........802
Раздел 7. Отравляющие вещества.............807
Отравляющие вещества
нервно-паралитического действия.........809
Отравляющие вещества кожно-нарывного
действия................................812
Оглавление
1463
Отравляющие вещества общеядовитого действия.............................815
Отравляющие вещества удушающего действия.............................816
Психотропные вещества................816
Раздражающие вещества................818
Раздел 8. Средства индивидуальной защиты.822
Приложение. Некоторые медицинские термины, встречающиеся в справочнике.............850
ГИГИЕНИЧЕСКИЕ НОРМАТИВЫ.................857
Общие принципы гигиенического нормирования химических веществ......858
Гигиеническое нормирование химических веществ в воздухе рабочей зоны.......860
Гигиеническое нормирование химических веществ в атмосферном воздухе
населенных мест............................863
Гигиеническое нормирование химических веществ в воде водоемов...................864
Таблица. 9. Гигиенические нормативы (ПДК, ОБУВ, ОДУ) химических веществ в воздухе рабочей зоны, атмосферном воздухе населенных мест,
воде водоемов.........................871
Литература...................................1099
Указатель названия веществ по номенклатуре ИЮПАК........................................1101
Указатель синонимов.........................1117
I !И 1И 8 iCHihM a rt.l-Bl.TiMUt ЙН| ГМПЯЯПРГ
яоШЕсеионал.
МУВЬГЙ СПРАВОЧНИК ХИМИКА И ТЕХНОЛОГА
Общие сведения Строение вещества Физические свойства важнейших веществ Ароматические соединения Химия фотографических процессов Номенклатура органических соединений Техника лабораторных работ Основы технологии Интеллектуальная собственность
Научное издание
Ответственный за издание А. А. Полуда Ответственный за выпуск Н.В. Емельянова Ответственный за подготовку Л.В. Белканова Научный редактор В.А. Столярова Редактор Л.Д. Чернухо Корректор С.Е. Парфенова Компьютерная верстка Н.В. Коробова, О.С. Фадеева Оператор компьютерной графики О.А. Круглова Техническое сопровождение Т.П. Жадобина Цифровая печать М.А. Бухтарова
Сдано в набор 16.09.2006. Подписано в печать 25.12.2006 Формат 60x90/8. Бумага офсетная, плотность 80 г/м2. Объем 183 печ. л.
Издание подготовлено НПО «Профессионал» 197341, Санкт-Петербург, ул. Горная, д. 1, корп. 1, оф. 22-Н Тел./факс: (812) 601-30-70, 601-32-49 mail@naukaspb.ru http://www.naukaspb.ru
Отпечатано в центре цифровой печати НПО «Профессионал»
яоо^ЕссионосхД
нстый СПРАВОЧНИК ХИМИКА И ТЕХНОЛОГА
Общие сведения Строение вещества Физические свойства важнейших веществ Ароматические соединения Химия фотографических процессов Номенклатура органических соединений Техника лабораторных работ Основы технологии Интеллектуальная собственность
НПО “Профессионал” Санкт-Петербург 2006
www.naukaspb.ru, mail@naukaspb.ru. (812) 6013248,6013249
о-савым:
СПРАВОЧНИК
ХИМИКА и ТЕХНОЛОГА
Общие сведения Строение вещества Физические свойства важнейших веществ Ароматические соединения Химия фотопроцессов Номенклатура органических соединений Техника лабораторных работ Основы технологии Интеллектуальная собственность Руководители проекта
А.А. Полуда, Н.В. Емельянова
Авторы
д. х. н., проф. А.В. Москвин к.х.н., доц. Л.М. Быкова к. х. н., доц. М.Ю. Скрипкин О.А. Пинчук
д.х.н., А.Ф. Хлебников д.т.н., проф. А.В. Редько к.х.н., доц. М.С. Новиков к.т.н. В.Г. Вавилов
А.А. Четвериков д.т.н., проф. Б.П. Саушкин к.х.н. С.Г. Изотова к.т.н. А.М. Марков
д.х.н., проф. Е.Е. Бибик
MMVI
Санкт-Петербург 2006