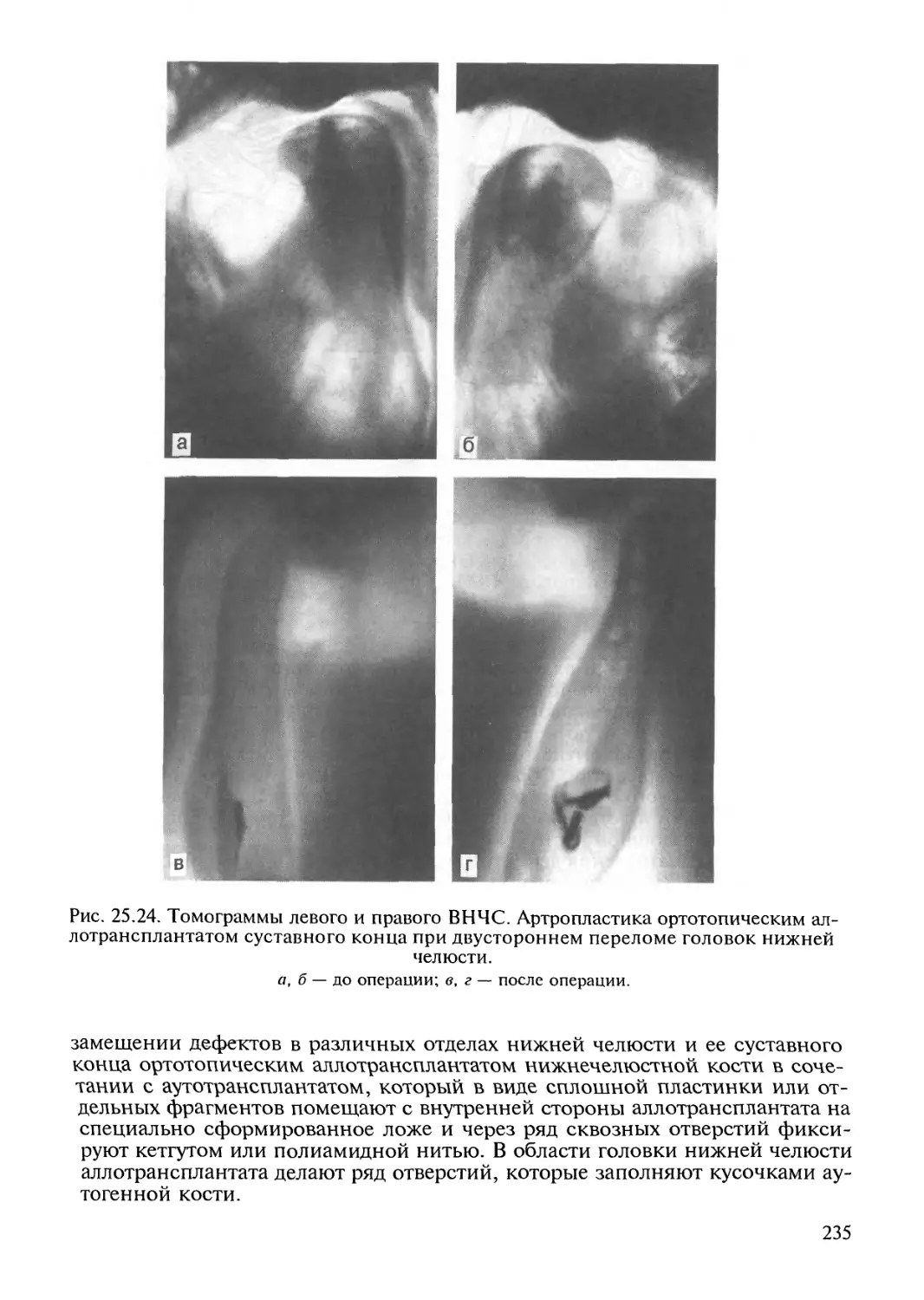
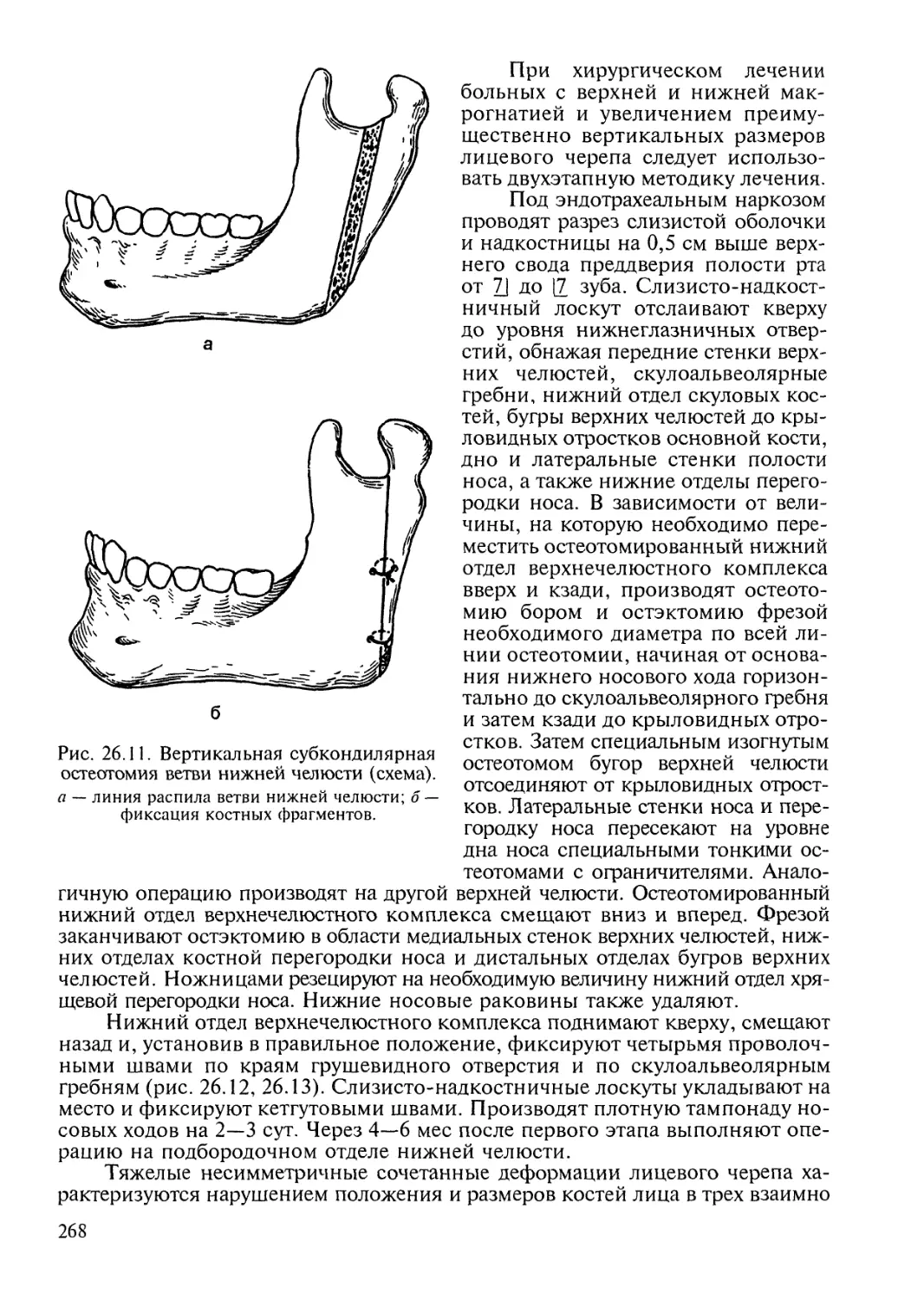
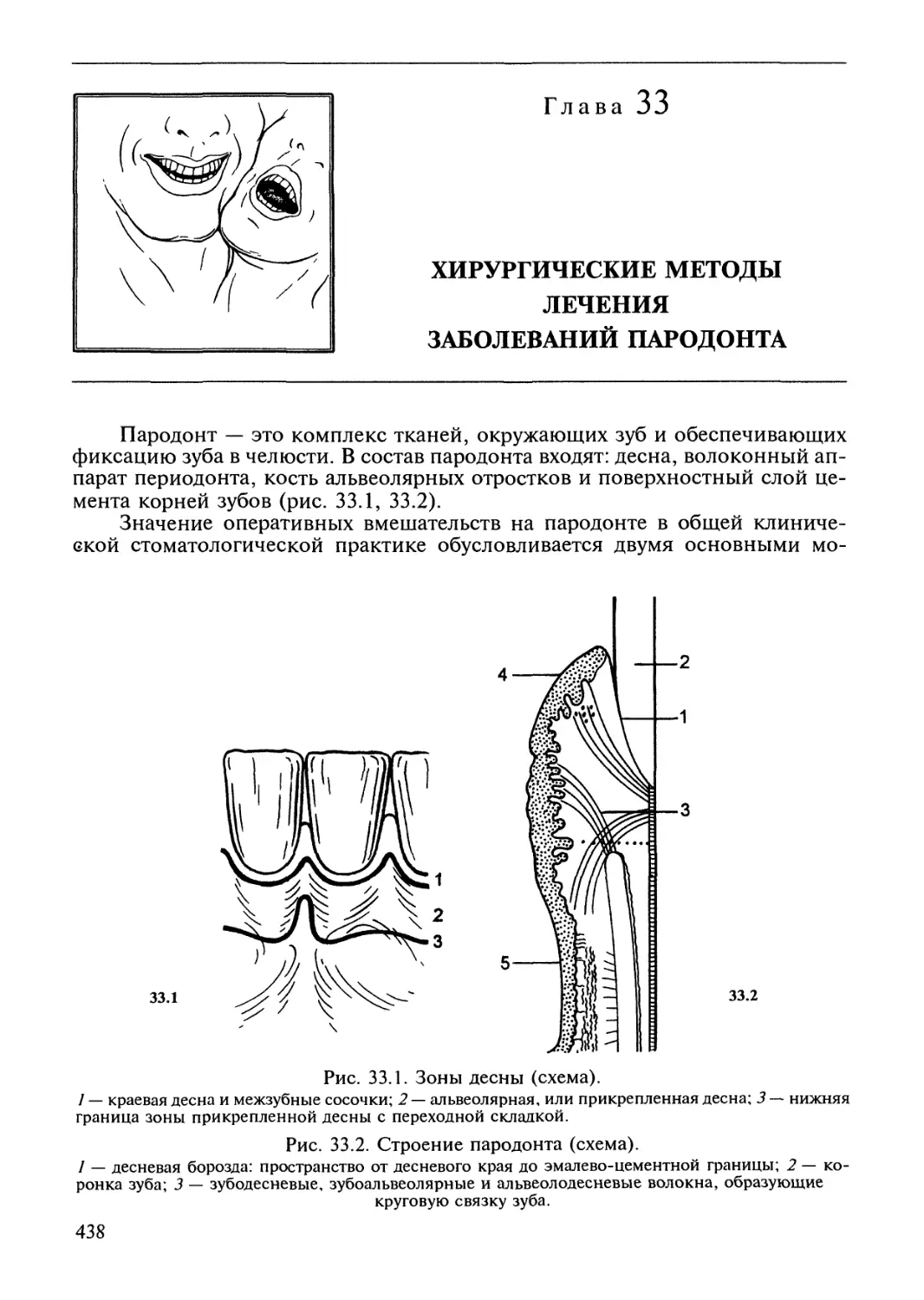
Автор: Робустова Т.Г.
Теги: полость рта рот стоматология хирургия ортопедия офтальмология медицина практическая медицина издательство медицина
ISBN: 5-225-04396-8
Год: 2000
РУКОВОДСТВО
по
ХИРУРГИЧЕСКОЙ
СТОМАТОЛОГИИ
И ЧЕЛЮСТНО-ЛИЦЕВОИ
ХИРУРГИИ
РУКОВОДСТВО
по
ХИРУРГИЧЕСКОЙ
СТОМАТОЛОГИИ
И ЧЕЛЮСТНО-ЛИЦЕВОЙ
ХИРУРГИИ
в 2 томах
Под редакцией
члена-корреспондента РАМН В.М. Безрукова,
профессора Т.Г. Робустовой
РУКОВОДСТВО
по
ХИРУРГИЧЕСКОЙ
СТОМАТОЛОГИИ
И ЧЕЛЮСТНО-ЛИЦЕВОЙ
ХИРУРГИИ
Под редакцией
члена-корреспондента РАМН В.М. Безрукова,
профессора Т.Г. Робустовой
I том I
2
Издание второе, переработанное
и дополненное
Москва
"Медицина"
2000
УДК 616.31-089+617.52-089
ББК 56.6
Р85
Федеральная программа книгоиздания России
Рецензент акад. РАМН, проф. Н. Н. Бажанов
зав. кафедрой хирургической стоматологии
и челюстно-лицевой хирургии ММА
им. И. М. Сеченова
Руководство по хирургической стоматологии и челюстно-лице-
Р85 вой хирургии: в 2-х томах. Т.2/Под ред. В. М. Безрукова, Т. Г. Ро-
бустовой. — Изд. 2-е, перераб. и доп. — М.: Медицина, 2000. —
488 с: ил.
ISBN 5-225-04396-8
Второй том переработанного и дополненного руководства посвящен
вопросам восстановительной хирургии челюстно-лицевой области —
лечению врожденных пороков, дефектов, деформаций. Описаны
современные методы хирургического лечения на основе разработок отечественных
и зарубежных авторов, получивших приоритет в последние годы. Многие
методики операций являются оригинальными.
Для практических врачей, научных работников по профилю
хирургической стоматологии и челюстно-лицевой хирургии, а также для
других специалистов.
Manual of Oral and Maxillofacial Surgery. In 2 vol. Vol. 2. Ed. by
V. M. Bezrukov and T. G. Robustova. — Second edition, revised and
supplemented. —- Moscow: Meditsina Publishers, 2000. — 488 pp.: ill.
The second volume of this revised and supplemented manual deals with
problems in repair maxillofacial surgery: treatment of congenital diseases,
defects, and deformations. Modern methods of surgical treatment based on the
research results of Russian and foreign scientists, introduced in recent years, are
presented Many of the methods presented in this book are original.
Addressed to practitioners, specialists engaged in oral and maxillofacial
surgery research, and physicians of other profile. tltlk 56 6
© Издательство "Медицина",
Москва, 1972
ISBN 5-225-04396-8 © Коллектив авторов, 2000
Все права авторов защищены. Ни одна часть этого издания не моэ/сет быть
занесена в память компьютера либо воспроизведена любым способом без
предварительного письменного разрешения издателя.
ОГЛАВЛЕНИЕ
Глава 22. Врожденные пороки черепно-лицевой области и
шеи. В. В. Рогинский, В. М. Безруков, В. П.
Ипполитов 7
Глава 23. Восстановительные операции на мягких тканях
лица и шеи. А. И. Неробеев, В. И. Малаховская,
Ц. М. Шургая 94
Глава 24. Костная пластика нижней челюсти. В. М.
Безруков, В. А. Сукачев, А. X. Шамсутдинов 175
Глава 25. Аллопластика височно-нижнечелюстного сустава.
A. А. Никитин 189
Глава 26. Хирургическое лечение аномалий и деформаций
челюстей. В. М. Безруков, В. И. Гунько 246
Глава 27. Хирургическое лечение посттравматических
деформаций лицевого черепа. В. М. Безруков, В. Я.
Ипполитов 277
Глава 28. Компрессионно-дистракционные методы лечения
при реконструкции верхней и нижней челюстей.
B. М. Безруков, А. X. Шамсутдинов 307
Глава 29. Основы эстетической хирургии лица и шеи.
В. А. Виссарионов, И. А. Фришберг 317
Глава 30. Основы эндопротезирования и эктопротезирова-
ния лица. В. М. Безруков, JI. А. Брусова 356
Глава 31. Предпротезная хирургия полости рта. Т. Г. Робу-
стова 388
Глава 32. Зубная и челюстно-лицевая имплантация.
Т. Г. Робустова, В. М. Безруков 406
Глава 33. Хирургические методы лечения заболеваний паро-
донта. А. И. Грудянов 438
Предметный указатель 473
CONTENTS
Chapter 22. Congenital defects of the craniofacial area and neck.
V. V. Roginsky, V. M. Bezrukov, V. P. Ippolitov... 7
Chapter 23. Repair surgery on the soft tissues of the face and neck.
A. I. Nerobeev, W. L Malakhovskaya, Z. M. Shurgaya 94
Chapter 24. Mandibular osteoplasty. V. M. Bezrukov, V. A. Su-
kachev, A. Kh. Shamsutdinov 175
Chapter 25. Alloplasty of the temporomandibular joint. A. A. Ni-
kitin 189
Chapter 26. Surgical treatment of abnormalities and
deformations of the jaws. V. M. Bezrukov, V. I. Gunko . . . 246
Chapter 27. Surgical treatment of posttraumatic deformations of
the facial skull. V. M. Bezrukov, V. P. ippolitov. . . 277
Chapter 28. Compression-distraction method in repair of the
maxilla and mandible. V. M. Bezrukov, A. Kh.
Shamsutdinov 307
Chapter 29. Fundamentals of esthetic surgery on the face.
V. A. Vissarionov, I. A. Frishberg 317
Chapter 30. Fundamentals of facial endoprostheses and ectopros-
theses. V. M. Bezrukov, L. A. Brusova 356
Chapter 31. Oral surgery preceding fitting with dentures.
T. G. Robustova 388
Chapter 32. Dental and maxillofacial implantation. T. G.
Robustova, V. M. Bezrukov 406
Chapter 33. Surgical methods for treating periodontal diseases.
A. I. Grudyanov 438
Глава 22
ВРОЖДЕННЫЕ ПОРОКИ
ЧЕРЕПНО-ЛИЦЕВОЙ ОБЛАСТИ
И ШЕИ
Врожденные пороки челюстно-лицевой и черепно-лицевой областей в связи
с их частотой, тяжестью анатомических и функциональных ьа эушений,
трудностью социальной адаптации пациентов, экономическими і.спектами
являются одной из важнейших проблем медицины. Интерес к этой проблеме
возрос после того, как была показана возможность реконструкций любых пороков
в этой области и полной социальной адаптации больных.
При решении проблемы реабилитации данного контингента больных
наиболее актуальным вопросом является создание концепции помощи этим
больным. Оказание ее требует проведения специфических организационных,
медико-технических и социальных мероприятий. Необходимо обоснование
сроков оперативных вмешательств, места их проведения последовательности и
комплексности, ранней медицинской реабилитации и социальной адаптации.
Комплексная реабилитация детей с врожденной патологией включает
медико-генетическое консультирование. Этот процесс делится на три
основных этапа: диагностику, оценку степени генетического риска, установление
соответствующего прогноза.
Различают проспективное и ретроспективное консультирование.
Проспективное консультирование — наиболее эффективный путь профилактики
наследственной патологии, когда риск рождения больного ребенка в семье
определен еще до наступления беременности или в ее ргнние сроки. Гакие
консультации проводятся при неблагоприятном семейном анамнезе, в случаях
кровного родства между супругами, а также при воздействии на организм
матери и плода неблагоприятных факторов внешней среды в период, когда
происходят закладка и активное формирование тканей челюстно-лицевой области.
Ретроспективное консультирование — это консульгирование после рождения
больного ребенка в семь^ относительно здоровья будущего потомства. При
этом определяют, является ли данное заболевание следствием новой мутации
или оно возникло как результат скрытого носительства и передачи ранее
возникшего патологического изменения генетического материала.
22.1. Статистические данные
Частота врожденных пороков развития в популяции является важной
характеристикой состояния здоровья населения. В 1991 г. в России пороки
зарегистрированы у 18,7 на 1000 родившихся. Смертность, связанная с этими по-
7
роками, занимает второе — пятое место в структуре детской смертности.
Среди прочих пороков одними из самых частых являются поражения челю-
стно-лицевой и краниофациальной областей.
Лицевые расщелины — это деформации, встречающиеся редко по
сравнению с расщелиной губы и неба. Они часто сочетаются с другими лицевыми
пороками, такими, как колобома века, дефект ноздри и носочелюстная
гипоплазия. Действительная заболеваемость не изучена, так как случаи черепно-
лицевых расщелин редки, методы, по данным литературы, не
стандартизованы. Возможная заболеваемость составляет от 1,9 до 6,8 на 100 000
рождений. Внутриматочная заболеваемость больных с редкими лицевыми
расщелинами является более высокой, чем отмеченная при родах [Salyer К., 1992].
По данным С. И. Блохиной и В. П. Козловой A995), челюстно-лицевые
поражения выявляются в среднем у одного из 500 новорожденных, причем в
последние 15 лет наблюдается тенденция к увеличению числа таких детей.
Наиболее часто встречаются расщелины верхней губы и неба. В
различных регионах их популяционная частота у новорожденных составляет от
1:1000 до 1:700 в год. В структуре поражений краниофациальной и челюстно-
лицевой областей расщелины губы и неба составляют до 90 %.
Ежегодно в республиках СНГ рождается около 30 000 детей с черепно-
челюстно-лицевыми деформациями. За небольшим исключением, такие дети
являются психически нормальными. Задержка психического развития их во
многом объясняется социальной дизадаптацией за счет отличного от
окружающих внешнего вида и может быть успешно корригирована путем
оперативного вмешательства.
22.2. Патогенез
Клинико-генеалогический анализ семейного материала позволил обосновать
гипотезу генетической гетерогенности несиндромальных форм врожденных
расщелин верхней губы и неба, где около 38 % случаев относятся к
категории "семейных", а 62 % — к "спорадическим" [Лильин Е. Т., Татуева Т. Α.,
1996].
Причины возникновения пороков черепно-челюстно-лицевой области
до настоящего времени остаются недостаточно выясненными. Некоторые из
них могут представлять собой одни и те же нарушения, степень различия
между которыми зависит от времени воздействия тератогенного фактора.
Наследственная природа челюстно-лицевых аномалий — наиболее частое
явление и рецессивно связано с хромосомой X, но также может быть вызвано
аутосомально-доминантной наследственностью.
Р. Д. Новоселов A988) так суммировал сведения о патогенезе врожденной
патологии челюстно-лицевой области: «Существуют две теории, объясняющие
патогенез врожденных расщелин лица. Теория В. Гиса A892) рассматривает их
как "несращение лицевых отростков", разделенных "сквозными щелями" в
любой неблагоприятный момент эмбриогенеза. В последние годы эта теория
признана несостоятельной. Зарубежные авторы [Fleischmann J., 1909; Veau V.,
1938; Stark R., 1958, 1971, и др.] установили, что "лицевые отростки"
являются лишь мнимыми отростками, а "сквозные щели" — не что иное, как глубоко
врезавшиеся эпителиальные складки. Была создана теория мезодермального
проникновения Флейшмана—Во. По этой теории формирование среднего
отдела лица происходит на 4—6-й неделе эмбрионального периода в
результате неравномерного дифференцированного роста мезенхимы под эпителием
эктодермальной закладки лица.
8
На поверхности лица скопления мезенхимы выявляются в виде
выпячиваний "эктодермальных валиков", разграниченных не щелями, а
эпителиальными складками — "бороздками". По мере пролиферации мезенхимы
"бороздки" сглаживаются, валики сливаются, образовавшиеся массы мезенхимы
дифференцируются в структуры соответствующих областей лица.
Согласно этой теории формирование среднего отдела лица, тесно
связано с первичным небом — участком тканей, расположенным между
первичной носовой полостью и первичной полостью рта. Этот участок формируется
путем слияния (фактически склеивания) верхнечелюстного и
медиально-носового валиков, при этом эктодермальный слой ("эпителиальная стенка") на
месте слияния (склеивания) должен прорасти мезенхимой. Мезенхима его
прорастает на 6-й неделе эмбриогенеза. Если этого не произойдет или
прорастание будет неполным, то эктодермальный слой в дальнейшем
разрушается как любая эмбриональная мембрана, образуется полная или частичная
расщелина верхней губы и альвеолярного отростка».
Проведя исследование на эмбрионах 4,5—7 нед, Р. Д. Новоселов
подтвердил теорию мезодермального проникновения и обосновал термин
"расщелина" верхней губы. Было установлено, что развитие первичного неба тесно
связано с формированием не только верхней губы и альвеолярного отростка,
но также носа и резцовой части верхней челюсти. Кроме расщелин губы,
возникают деформации носа, дефекты альвеолярного отростка, происходят
недоразвитие верхней челюсти, дисфункция мышц приротовой области.
Отмечено, что уже в антенатальный период порок развития средней части лица и
сопутствующие ему деформации полностью сформированы.
Органо- и морфогенез челюстей у плода может нарушиться под влиянием
наследственного воздействия на эмбрион перенесенных родителями
заболеваний (эндокринные и обменные нарушения в организме матери, инфекционные
болезни, радиоактивное облучение, отравление лекарственными препаратами
при беременности, заболевания крови), а также вследствие физиологических
и анатомических нарушений половых органов матери и неправильного
положения плода. В раннем детском возрасте деформация челюстей может
возникнуть под влиянием эндогенных (эндокринные нарушения, инфекционные
заболевания, нарушение обмена веществ, наследственность) или экзогенных
(воспаление в зоне роста челюстей, остеомиелит, анкилоз, нома и др.)
факторов, травмы, в том числе родовой, дисфункции жевательного аппарата,
нарушения акта глотания, дыхания, вредных привычек. Следует подчеркнуть,
что наиболее сложные черепно-лицевые деформации обычно наблюдаются
при генных синдромах и хромосомных болезнях. Среди проявлений этих
аномалий доминируют гипоплазия средней зоны лица, а также другие
внутричерепные и зубочелюстные изменения.
Тяжесть порока развития лица обусловливается не только внешней обез-
ображенностью, выраженными функциональными нарушениями,
социальной ущербностью ребенка в дошкольном и школьном коллективах,
конфликтной напряженностью и негативным психологическим фоном в семье,
но и тем, что деформация вызывает соматические расстройства, приводящие
к торможению роста и недоразвитию детского организма в целом. Возникшие
деформации челюстей у синдромальных больных являются одним из
неблагоприятных факторов, воздействующих на неокрепший организм, и вызывают в
нем грубые функциональные и морфологические изменения: отставание в
росте и увеличении массы тела наблюдается в возрасте до 10 мес. Б. А. Котов и
соавт. A984), изучая изменения иммунологической реактивности у больных
с синдромом первой и второй жаберных дуг, показали, что снижается также
иммунная защита ребенка. Особенности нервно-психического состояния де-
9
тей резко отличаются от нормы, т. к. изменения органического характера ведут
к непредсказуемым невротическим реакциям, связанным с астеническим
синдромом и вегетососудистой дистонией организма в целом. В возникновении
психогенных нарушений важную роль играют также неблагоприятные условия
воспитания и психическая травматизация детей в раннем школьном возрасте.
22.3. Основные типы пороков развития черепно-лицевой области и шеи
Различают следующие пороки развития черепно-лицевой области и шеи:
1. Расщелины верхней губы, неба, поперечная и косая расщелины лица.
2. Орбитальный гипертелоризм. Статистика частоты орбитального ги-
пертелоризма в популяции отсутствует, так как он сопровождает
разнородные в этиологическом и патогенетическом плане процессы.
3. Черепно-лицевые дизостозы. Средняя популяционная частота
входящих в эту группу простых (несиндромных) краниостенозов — один
случай на 1000 новорожденных. Синдром Крузона встречается в
одном случае на 10 000—25 000 в популяции, синдром Аперта — у
одного из 100 000—160 000 новорожденных.
4. Черепно-лицевые расщелины, являющиеся редкими состояниями по
сравнению с изолированными расщелинами губы и/или неба,
встречаются в 1,43—4,85 случаях на 100 000 новорожденных. Достаточно
часто наблюдаются и синципитальные мозговые грыжи (как
первичные, так и являющиеся компонентом черепно-лицевых расщелин),
сопровождающиеся выраженными деформациями лицевого скелета.
5. Синдром Тричера — Коллинза со среднепопуляционной частотой
один случай на 10 000.
6. Асимметрия лица (в том числе плагиоцефалия, гемифациальная мик-
росомия и некоторые типы посттравматических деформаций и
деформаций, развивающихся после удаления опухолей).
По данным мировой литературы, каждый мультидисциплинарный центр
черепно-лицевой хирургии должен охватывать регион с населением 20—30 млн
человек. В структуре центра работают хирурги (челюстно-лицевые,
нейрохирурги), отоларингологи, окулисты, ортодонты, невропатологи, логопеды,
психологи, педиатры, анестезиологи, методисты. Штат центра должен обеспечивать
полную медицинскую и социальную реабилитацию пациентов, т. е.
обеспечивать все виды необходимой помощи на протяжении лечения. Для этого
необходимы хорошо оснащенная клиническая база, поликлиническая служба,
интернат или гостиница.
Основными задачами центра являются консультирование, поэтапное
лечение, диспансеризация, психолого-педагогическая помощь и речевая
реабилитация детей и подростков в возрасте от 0 до 15 лет с врожденной челюстно-
лицевой и краниофациальной патологией и тяжелыми нарушениями речи.
После рождения ребенка с патологическими изменениями в данных
областях необходимо комплексное обследование специалистами (хирург,
педиатр, ортопед, отоларинголог, психоневролог) для выявления отклонений
соматического характера и сопутствующих пороков развития и проведения
необходимой коррекции отклонений в предоперационном периоде.
После осмотра ребенка составляют план непосредственных и
перспективных лечебных мероприятий в зависимости от степени деформации.
Нарушение социальной адаптации ребенка в раннем возрасте в связи с
дефектом не всегда удается исправить в старшем возрасте: во взрослую жизнь
вступает не только физически, но и психологически деформированная личность.
10
Сохраняющиеся анатомические нарушения вызывают нарушение
функций непосредственно пораженных и сопряженных с ними органов.
Нарушается гармония развития нескольких областей, возникают так называемые со-
четанные вторичные деформации.
Разброс мнений по вопросу о сроках оперативного вмешательства крайне
широк даже для таких хорошо изученных поражений, как расщелина верхней
губы и неба: в период новорожденное™ [Фролова Л. Е., 1976; Jackson J., 1988],
в 3—6 мес [Новоселов Р. Д., 1972; Jolleys S., 1980], в 9—12 мес [Бердюк И. В.,
1985]. Для более тяжелых врожденных синдромов и краниофациальных
поражений этот разброс еще более широк — от раннего возраста A—3 года) до
совершеннолетия.
Установлено, что раннее (в возрасте до 1,5—3 лет) хирургическое
лечение детей с врожденными расщелинами губы и неба приводит к раннему
восстановлению коммуникативных функций, предупреждает
психоэмоциональные нарушения. В то же время позднее (в возрасте старше 5—10 лет) лечение
больных с расщелиной неба даже при хороших анатомических и
функциональных результатах не позволяет достичь необходимого уровня функций
коммуникабельности, восстановить нормальный психологический статус
[Булатовская Б. Я., 1974; Виссарионов В. Α., 1989; Блохина С. И., 1995; Ма-
медов Α. Α., 1997].
Опыт многих клиник СНГ позволил обосновать сроки хирургических
вмешательств и разработать методы и приемы помощи больным данного
контингента (табл. 22.1).
Таблица 22.1. Программа реабилитации детей с врожденными пороками развития
черепно-челюстно-лицевой области
Группа детей
Новорожденные
@-1 мес)
Грудные дети
(до 1 года)
Ясельная группа
A—3 года)
Дошкольная группа
C—6 лет)
Любой возраст
Характер консультаций и лечебной помощи
Осмотр специалистами (педиатр, челюстно-ли-
цевой хирург, нейрохирург, ортодонт, ортопед),
составление комплексной предоперационной
программы, позволяющей произвести оперативное
вмешательство
Ортопедическое лечение, хейлоринопериостео-
пластика, пластика расщелин лица (поперечной,
косой, расщелины носа), физиотерапевтическое
лечение с повторением курса через 2 мес, лечение
сопутствующих заболеваний специалистами,
реконструктивные операции при краниостенозе
Велопластика, ортодонтическое лечение,
санация ЛОР-органов и полости рта, уранопластика,
краниопластика, все виды реконструкций назоорби-
тальной области, устранение дефектов нижней
челюсти при синдромах первой — второй жаберных
дуг, дистракция, физиотерапевтическое лечение,
занятия с логопедом
Уранопластика, ортодонтическое лечение,
занятия с логопедом, реконструктивная ринохейлопласти-
ка, реконструкции при синдромах Крузона, Аперта,
физиотерапевтическое лечение
Устранение анатомических дефектов
11
Вопрос о сроках проведения первичной операции у детей с расщелиной
верхней губы остается дискуссионным. Авторы находят обоснование как для
раннего хирургического устранения расщелины верхней губы (в первые дни и
недели жизни) [Фролова Л. Е., 1962, 1974; Колесов Α. Α., Каспарова Η. Η., 1978;
Jackson J., 1988; Jolleys S., 1990], так и для выполнения его во втором
полугодии жизни [Новоселов Р. Д., 1972; Бердюк И. В., 1985]. В настоящее время
большинство зарубежных авторов первичные операции производят в сроки
от 0 до 8 нед жизни [Jackson J., 1988; Salyer К., 1992]. J. Jackson предлагает
следующим образом определять время для операции при расщелинах верхней
губы: неполная расщелина — 24 ч — 3 мес, полная расщелина — 24 ч — 3 мес,
с предоперационным ортодонтическим лечением в течение 3—4 мес.
Заслуживает внимания подход к этой проблеме D. Millard A976, 1982),
который сформулировал общие предпосылки для проведения операции в виде
"правила более 10": масса тела более 4 кг, возраст старше 10 нед, содержание
гемоглобина в крови более 10 г/л, лейкоцитов — не более 10,0· 109/л.
Таким образом, акцент делается на соматический статус ребенка, его
способность перенести оперативное вмешательство, которое при
современном подходе к решению является хотя и более обширным, включает и
пластику носа и пластику расщелины альвеолярного отростка, но выполненное
в специализированном учреждении, позволит обеспечить более правильный
рост репонированных структур и предупредить вторичную деформацию.
На современном этапе проблема первичной хирургической помощи
детям с расщелиной верхней губы является важной и актуальной. Заметна
тенденция к более широкому применению первичной ринохейлопластики.
Однако, по мнению различных авторов, объем оперативного вмешательства
неодинаков и на основании данных литературы трудно отдать предпочтение
какому-либо методу. Процесс совершенствования должен идти по пути
разработки щадящих физиологических методов ринохейлопластики с учетом
анатомических изменений в расщепленной губе, носовых структурах,
верхней челюсти.
В настоящее время основная задача хирургов заключается в снижении
возрастного ценза для операций у больных данного контингента. Это
позволит наиболее эффективно восстановить утраченные функции и провести
раннюю медицинскую и социальную реабилитацию больного.
Положительными сторонами ранних реконструктивных операций
являются: восстановление анатомической формы и правильного
пространственного положения тканей, нормализация функций, в том числе жизненно
важной функции дыхания, гармоничное развитие всех отделов лицевого скелета,
возможность протезирования (в связи с этим облегчение приема пищи, речи
и эстетическая реабилитация). Более широкий репарационно-регенератор-
ный потенциал больного ребенка в большем проценте случаев обеспечивает
положительный исход. Предупреждаются грубые деформации мягких тканей
и лицевого скелета, атрофия на стороне поражения, вторичные деформации
челюстей, зубоальвеолярное удлинение верхней челюсти, нормализуется
прорезывание зубов-антагонистов и формируется правильная окклюзия,
значительно меньше объем хирургических и прочих мероприятий в процессе
реабилитации.
Социальная адаптация ребенка и формирование полноценной личности
находятся в прямой зависимости от косметического и функционального
результата операции. Удовлетворительный функциональный результат
возможен только при полной анатомической реконструкции пораженной области.
Первичную операцию следует проводить с учетом антропометрических
изменений костного скелета, мимической мускулатуры, хрящевого отдела носа
12
с целью ликвидировать разобщение, дистопию, натяжение всех элементов
лицевого скелета.
Полная реабилитация больного возможна только усилиями многих
специалистов, применяющих многочисленные вспомогательные методы.
Один из основных вопросов, который решает хирург, — время и объем
оперативных вмешательств при различных видах патологии. Оба эти вопроса
в лучших специализированных мировых центрах по лечению больных с че-
люстно-лицевой и краниофациальиой патологией решаются однозначно в
пользу снижения возрастного ценза и увеличения объема вмешательства. Это
становится возможным главным образом в связи с развитием
анестезиологического и реанимационного обеспечения, совершенствования техники и
методики самих вмешательств.
При дальнейшем изложении материала основное внимание будет
уделено тем разделам патологии, где может быть проведена хирургическая
коррекция. С этой точки зрения будут рассмотрены как локальные
анатомические нарушения, так и сложные синдромы.
Наиболее разработаны классификации врожденных пороков развития
губы и неба. Разнообразие данной патологии отражено в Международной
классификации болезней (Женева, 1995).
I. Расщелина губы: двусторонняя, срединная, односторонняя.
II. Расщелина неба.
1. Расщелина твердого неба двусторонняя.
2. Расщелина твердого неба односторонняя.
3. Расщелина мягкого неба двусторонняя.
4. Расщелина мягкого неба односторонняя.
5. Расщелина твердого неба с расщелиной мягкого неба двусторонняя.
6. Расщелина твердого неба с расщелиной мягкого неба односторонняя.
7. Расщелина неба срединная.
8. Расщелина язычка.
9. Расщелина неба нетипичная двусторонняя.
10. Расщелина неба нетипичная односторонняя.
III. Расщелина неба с расщелиной губы.
1. Расщелина твердого неба с расщелиной губы двусторонняя.
2. Расщелина твердого неба с расщелиной губы односторонняя.
3. Расщелина мягкого неба с расщелиной губы двусторонняя.
4. Расщелина мягкого неба с расщелиной губы односторонняя.
5. Расщелина твердого и мягкого неба с расщелиной губы двусторонняя.
6. Расщелина твердого и мягкого неба с расщелиной губы односторонняя.
7. Нетипичная расщелина неба с расщелиной губы двусторонняя.
8. Нетипичная расщелина неба с расщелиной губы односторонняя.
Другие, более редкие пороки и синдромы представлены в
Международной классификации болезней A995) в различных подрубриках раздела
"Врожденные изменения, деформации и хромосомные изменения". В руководстве
приведены только те рубрики, которые могут интересовать хирурга, хотя в
больших рубриках указаны единичные пороки (макро- и микростомия,
бронхиальные свищи и др.). Для учета этих поражений мы отсылаем читателя к
самой Международной классификации.
Приводим полностью следующие рубрики раздела XVII классификации.
I. Врожденные мышечно-скелетные деформации головы, лица, груди и
позвоночника.
1. Лицевая асимметрия.
2. Компрессия лица.
3. Долихоцефалия.
4. Плагиоцефалия.
13
5. Другие врожденные деформации черепа, лица и костей: атрофия
половины лица, гипертрофия половины лица, другие специфические
врожденные деформации черепа, лица и челюстей, атипичные врожденные
деформации черепа, лица или челюстей.
II. Другие врожденные изменения черепа и костей лица.
1. Краниостенозы: акроцефалия, первичный череп, оксицефалия, тригано-
цефалия.
2. Краниофациальные дизостозы: болезнь Крузона.
3. Гипертелоризм.
4. Макроцефалия.
5. Челюсти о-лицевые дизостозы.
6. Орбиточелюстные дизостозы.
7. Другие специфические врожденные изменения черепа и лицевых костей.
8. Врожденные изменения черепа и костей лица атипичные.
22.4. Предоперационная подготовка
Проблемы предоперационного периода могут состоять в нарушении
дыхания, питания, речи. Иногда их необходимо решать экстренно, в частности
при нарушении дыхания, связанном с глоссоптозом и западением языка у
больных с синдромом Пьера-Робена. Первичные мероприятия заключаются
в придании больному положения на животе. Обеспечивают максимальную
проходимость дыхательных путей с вытяжением за головную шапочку
(фиксированную клеолом или пластырем). Язык прошивают, вытягивают и
фиксируют к одежде или частям тела (губа, щека). Попытки интубации трахеи у
больных этой категории в родильных домах необоснованы в связи с
большими техническими трудностями этой процедуры.
Затрудненный прием пищи не должен побуждать к скорейшему
налаживанию искусственного питания. Обычно ребенок приспосабливается к
питанию грудью. Если этого добиться не удается, то используют различные
приспособления с целью обтурации расщелины: бутылочки со
специальными сосками, палец медицинской перчатки (или последнюю целиком),
обтураторы, мягкую (старую) соску с увеличенным отверстием, ложку, шприц с
катетером и т. д. При необходимости проводят парентеральную поддержку.
Я. П. Нагирный A990) выявил, что особенностью резистентности у 44,7 %
детей с врожденной расщелиной губы и неба всех возрастов является
депрессия клеточного звена иммунитета при напряжении гуморального и
повышение уровня перекисного окисления липидов (ПОЛ). Это является одним из
факторов более частого развития послеоперационных осложнений. Среди
этих нарушений чаще всего встречается снижение функциональной
активности Т-клеток, повышение уровня В-клеток, повышенная концентрация
иммуноглобулинов А, М в крови, повышение уровня малонового диальдеги-
да (МДА) в крови и снижение уровня SH-rpynn в эритроцитах. Дети с этими
нарушениями резистентности составляют группу риска повышенной частоты
возникновения послеоперационных осложнений. Необходим
дифференцированный подход при подготовке к оперативному вмешательству, который
заключается в следующих мероприятиях: проведение оперативного
вмешательства в условиях центра лечения детей с врожденной патологией с
привлечением наиболее опытных хирургов, сокращение времени оперативного
вмешательства, применение наиболее прочных шовных материалов, снятие
швов в более поздние сроки, применение пластиночных швов и средств,
ускоряющих заживление ран, предоперационная подготовка с применением
средств, повышающих устойчивость организма и др.
14
Бактериологическое исследование полостей рта и носа, горла,
кишечника, выявление патогенной флоры и лечение в значительной степени
снижают число послеоперационных осложнений. Инфекция верхних
дыхательных путей является противопоказанием к операции. Ребенка передают
педиатрам и выполняют операцию спустя 1 — 1,5 мес после излечения.
При тяжелых, особенно двусторонних, расщелинах, сопровождающихся
выраженной протрузией межчелюстной кости, с целью выравнивания
верхнечелюстных сегментов и создания более благоприятных условий для
операции проводят ортодонтическое лечение. Первичные лицевые признаки,
состояние окклюзии фиксируют в документах и на фотографиях.
Большинство авторов считают, что выполнять операцию следует в
возрасте 0—6 мес, и используют в основном вращательно-поступательный
принцип Милларда или треугольные лоскуты Теннисона—Обуховой.
Хирургия расщелин верхней губы прошла длинный путь
видоизменений, дополнений, усовершенствований от простого ушивания до сложной
пластической операции хейлоринопластики. "Хейлопластика из простого
закрытия дефекта верхней губы превратилась в сложное оперативное
вмешательство" [Новоселов Р. Д., 1989].
В основе каждого метода лежит представление автора о нарушениях
анатомических взаимоотношений, степени недоразвития и топографии дефекта
тканей. В соответствии с этим первичную пластику верхней губы подразделяют на
губную адгезию, хейлопластику, ринохейлопластику и ринохейлогнатопластику.
Первичная хейлопластика показана при скрытых и неполных
расщелинах в ранние сроки, когда деформация носа незначительна. Операция может
быть произведена на 2—12-й день жизни (в условиях родильного дома или
специализированного отделения).
При первичной хейлопластике, которая, по мнению Б. Н. Давыдова
A997), показана в основном при чрезвычайных обстоятельствах, закрывают
дефект и создают полноценную верхнюю губу. В то же время не исправляют
деформацию хрящей носа, не устраняют дисфункцию мышц приротовой
области и носа, сохраняют дефект альвеолярного отростка, не формируют дно
преддверия носа (рис. 22.1).
22.5. Хейлопластика
Методы линейной пластики. Данные методы основаны на представлении о
том, что расщепленная губа содержит все анатомические элементы, и задачей
хирургического лечения является их перемещение в правильное положение.
Одинаковая высота губы достигается путем освежения краев расщелины
овальным, дугообразным или прямолинейным разрезом. Основным
недостатком метода является утрата большого количества тканей верхней губы с
последующим развитием деформации верхней губы и челюсти, что побудило
хирургов разработать методы с использованием перекидных лоскутов с
красной каймы. Методы чисто линейной хейлопластики в настоящее время не
применяют.
Результаты линейной хейлопластики были значительно улучшены А. А. Лим-
бергом A938) благодаря новым приемам: 1) сближение фрагментов губы через
разрез в форме кочерги по переходной складке способствовало мобилизации
латерального фрагмента и отделение от верхней челюсти основания крыла
носа; 2) передний отдел дна преддверия носа создается треугольным
лоскутом, перемещенным на границу перегородки; 3) для устранения деформации
носа расслаивают ткани между арками крыльного хряща.
15
Нанесение ориентировочных точек на части пограничных линий
красной каймы позволяет с математической точностью раскроить ткани и
симметрично сформировать красную кайму. Дальнейшим совершенствованием
операции Миро является способ Во A938). Основание уплощенного крыла
носа мобилизуют, участок лука Купидона на центральном фрагменте
иссекают, но сохраняют круговую мышцу. На боковом фрагменте красной каймы
выкраивают лоскут с уступом на границе с кожно-слизистой линией,
который вшивают в соответствующий участок после иссечения красной каймы на
медиальном фрагменте. Точного сопоставления краев раны достигают при
использовании близнецовых игл.
В дальнейшем были выявлены существенные недостатки этого способа,
приводящие к выраженным анатомическим и функциональным нарушениям
[Губская А. Н., 1964; Новоселов Р. Д., Давыдов Б. Н., 1968, 1997; Козин И. Α.,
1996|. У больных, оперированных линейными методами, сужение верхней
губы по горизонтали, уплощенное тесное преддверие, основание уплощенного
крыла подтянуто с гиперкоррекцией и атрофировано. Нередко встречается
сужение носового отверстия, красная кайма на больной стороне подтянута
кверху, фильтрум укорочен, на нижнем крае губы втянутый рубец.
Губная адгезия. За рубежом довольно широко применяют так называемую
губную адгезию — предварительную операцию, заключающуюся в
непосредственном сближении краев расщелины губы без изменения границ губы и
повреждения тканей, необходимых для окончательной пластики [Seibert S.,
1993; Jackson J., 1988]. Операцию производят в первые (чаще на 4-й) недели
жизни. Обычно выполняют верхнюю адгезию, с целью частично закрыть
расщелину альвеолярного отростка и передний участок дна полости носа
местными слизисто-надкостничными лоскутами. К предположительным
достоинствам губной адгезии относят улучшение способности младенца питаться,
ортодонтическое влияние на расщепленные сегменты альвеолярного отростка,
уменьшение носовой расщелины и др. Эта операция показана небольшому
числу пациентов с односторонней расщелиной верхней губы и пациентам с
двусторонней расщелиной для достижения симметрии перед выполнением
окончательной операции. В случаях односторонней расщелины адгезию
выполняют при широких расщелинах со значительно выступающим вперед
участком челюсти (более 1 см перед окклюзионной плоскостью). Цель
заключается в создании более благоприятных условий (меньшее напряжение) при
окончательной операции, которую выполняют через 3—4 мес.
Неудовлетворенность хирургов результатами линейных пластик
побудила их к поискам, в результате которых были разработаны методы лоскутной
пластики (рис. 22.2—22.5).
Методы лоскутной пластики. После метода Миро A844) наиболее
прогрессивной была операция Хагедорна. Для увеличения высоты медиального
фрагмента губы автор использовал четырехугольный лоскут, выкроенный на
наружном фрагменте в нижней части края расщелины, состоящей из красной
каймы и кожи. В дальнейшем способ получил признание в различных странах.
После ряда модификаций [Любарский В. В., Фрыгина В. Α., 1965; Бердюк И. В.,
1985; Wang Μ., 1960; Thompson Η., 1971] наиболее удачными лоскутными ме-
~<
Рис. 22.1. Варианты хейлопластики (схема).
а — линейная; б — лоскутная с использованием треугольника в нижней трети губы; в — лоскутная
с использованием треугольника в верхней трети губы; г — лоскутная с использованием
прямоугольного лоскута.
17
2-1263
Рис. 22.2. Расположение волокон круговой мышцы рта {а) и направление при
оперативном перемещении волокон при оперативном вмешательстве (б) (схема).
тодами являются операции Теннисона и Обуховой A957), когда удлинение
медиального фрагмента достигается использованием кожно-мышечного
лоскута, но уже в пределах фильтрума. При этих способах сохраняется
значительное количество слизистой оболочки красной каймы, что позволяет
избежать уплощения в нижней трети губы и при соблюдении техники операции
сформировать правильную дугу Купидона.
Сравнительная оценка всех методов показывает следующее.
Недостатками методики Милларда считаются тенденция к сужению носового хода и
вертикальное сокращение по ходу рубца. Недостатки геометрических способов:
необходимость иссечения здоровых тканей, заметный рубец, нарушение
нормального строения фильтрума на непораженной стороне с образованием шва,
который пересекает анатомические структуры, сложность расчетов.
Преимуществами поступательно-вращательных методик являются возможность
использования их при любых формах расщелин, линия разреза (новый столбик
фильтрума), которая служит зеркальным отображением столба на
непораженной стороне, возможность полной мобилизации хряща крыла носа.
Варианты этих способов описаны в работах А. Randell A959), Л. Е.
Фроловой A962), В. И. Знаменского A963), Н. Н. Каспаровой, А. А. Колесова A970),
Рис. 22.3. Расположение мышечных пучков до и после применения различных
методов хейлопластики.
а — линейный метод Во; б — лоскутный метод с использованием треугольника в нижней трети
(Обухова—Теннисон); в — лоскутный метод с использованием треугольника в верхней трети
[Mollard D., 1957]; г — лоскутный метод с использованием прямоугольного лоскута (Хагедорн,
Лс Мезюрье).
18
Рис. 22.4. Операция с использованием ротационно-продвигаемых лоскутов (схема)
[Millard D., 1957].
а — обозначены линии разрезов; б, в — раскрой тканей и направление их перемещения; г — по-
. ложение лоскутов после ушивания раны.
Рис. 22.5. Операция с использованием треугольных лоскутов в нижней трети губы
(схема).
а — обозначены линии разрезов; б, в — раскрой тканей и направление их перемещения; г —
положение лоскутов после ушивания раны.
L. Barinka A976). По мнению И. А. Козина A996), иссечение большого
участка тканей в верхней трети губы значительно затрудняет проведение
завершающей ринохейлопластики.
Дальнейшее развитие метод лоскутной пластики получил в работах с
использованием перекидных лоскутов в нижней трети губы и у основания
перегородки носа. Второй лоскут улучшает положение крыла носа. В. И. Ильин
A963) предложил производить обмен треугольных лоскутов на границе кожи
и слизистой оболочки, а треугольный лоскут Лимберга подшивать к боковой
поверхности перегородки носа. Т. Skoog A958, 1965) и J. Delaire A975)
сочетают хейлопластику по методу Теннисона с образованием треугольного
лоскута пораженного крыла носа, который вшивают в разрез под кожной частью
перегородки носа. J. Bardach A967), L. Standi A987) предложили вариант
выполнения хейлопластики двумя малыми перекидными лоскутами в нижней
и верхней трети фильтрума.
Значительный прогресс в хирургии расщелин достигнут благодаря
работам Т. Millard A957, 1959), В. Cosman и G. Crikelair A965), которые показали,
что при односторонней расщелине верхней губы имеется абсолютный дефект
тканей трапециевидной формы с максимальной стороной на дне преддверия
носа, а максимальный фокус дефекта локализуется в области дна преддверия
носа и альвеолярной дуги. Это обстоятельство послужило причиной
совершенствования методов, предусматривающих взаимное перемещение
треугольных лоскутов в верхней трети губы и на дне носа.
Наибольшее распространение получили способы радикального поворота
и выдвижения по Милларду A976, 1977, 1990), которые автор постоянно
совершенствовал. D. Millard A990) предлагает на медиальном фрагменте через
все слои выкраивать дугообразный лоскут, который включает в себя красную
кайму и кожную часть от середины основания кожной части перегородки носа.
Если этого недостаточно, то проводят обратный разрез, позволяющий
сместить центр вращения укороченного фильтрума ближе к средней линии. В
результате удается получить косметический послеоперационный рубец в виде
выпуклой линии, симметричный противоположному столбику фильтрума.
Благодаря ротационному и обратному разрезам исправляют направление
волокон круговой мышцы рта (из косого оно становится горизонтальным) и
сшивают их с мышцей латерального фрагмента в более физиологическом
положении. Для одностороннего удлинения кожной части перегородки носа у
ее основания выкраивают малый лоскут С, который мобилизуют вместе с
медиальной ножкой уплощенного крыльного хряща от мембранозной части
перегородки, и перемещают его кверху с помощью послабляющего разреза на
боковой поверхности перегородки (см. рис. 22.2).
В образующуюся углообразную рану на медиальном фрагменте
перемещают лоскут с малого фрагмента губы. Поскольку успех устранения дефекта
на медиальном сегменте во многом зависит от массы лоскута латерального
фрагмента, D. Millard использует всю кожу в области порога ноздри от
основания завитка недоразвитого крыла. Важным моментом операции он
считает отсечение аномального прикрепления круговой мышцы рта к верхней
челюсти и мобилизацию аномального прикрепления пораженного крыла с
восполнением дефицита выстилки с использованием лоскута-"тореадора" с
красной каймы по L. Mir и А. Mir A957). Придавая большое значение
полноценному восстановлению круговой мышцы рта, автор использует
различные варианты лоскутов при дефиците мышечной ткани как на латеральном,
так и на медиальном мышечных фрагментах.
По мнению сторонников данного метода, применение его позволит
придать воссоздаваемой верхней губе форму, близкую к нормальной, значитель-
22
но исправить сопутствующую деформацию носа, получить хорошие
функциональные результаты. Реконструктивные операции легко выполнить, так
как сохранен максимум тканей губы и в случае необходимости повторение
хейлопластики может быть произведено по направлению тех же разрезов
[Козин И. Α., 1996; Кипянина И. Д., Шатуновская Е. Т., 1971; Koch J., 1969J.
В то же время при полных широких расщелинах, сопровождающихся
значительным недостатком тканей и укорочением высоты губы, нельзя
добиться хороших результатов. D. Millard при широких расщелинах
предварительно производит адгезию губы.
В нашей стране метод Милларда получил распространение и признание
благодаря работам И. А. Козина A996), который предложил свою
модификацию. Для профилактики сужения носового отверстия и восполнения
недостатка ткани на дне носа автор удлинил лоскут С за счет участка красной
каймы. Удлиненный лоскут вшивают в разрез перед завитком основания
уплощенного крыла, восполняя дефект выстилки, образованный при
выкраивании верхушки бокового лоскута латерального фрагмента.
Для увеличеня высоты медиального фрагмента ряд авторов используют
метод Z-пластики верхнего отдела губы и основания носового хода [Spina V.,
Lodovici О., 1960; Borde J., 1963; Wynn S., 1965]. При этом в верхней трети
перемещают кожные треугольные лоскуты, а удлинения мышцы достигают
перемещением треугольников в нижней трети губы. Эти методы разработаны
с учетом представлений об эпицентре дефекта в верхней трети губы и
основании дна носового хода. После операций, проведенных указанными
методами, зигзагообразный рубец располагается под основанием перегородки
носа и менее заметен, что повышает косметическую результативность.
P.Petit и соавт. A961, 1972) предлагают два варианта Z-пластики
односторонней сквозной расщелины. В первом варианте удлинение достигается
взаимным перемещением равнобедренного треугольника с основанием у ко-
лумеллы на медиальном фрагменте с треугольником, основание которого
направлено к красной кайме. Во втором варианте улучшение положения крыла
достигается взаимным перемещением треугольника медиального фагмента,
основание которого направлено в сторону красной каймы, с треугольником
латерального фрагмента, основание которого направлено к основанию
крыла. Подобную методику предложил и Р. Д. Новоселов A989).
По мнению И. А. Козина A996), наиболее рациональным методом при
лечении расщелин, особенно широких, является метод Z-пластики малыми
перекидными лоскутами в нижней и верхней трети [Skoog Т., 1965; Bardach J.,
1967, 1987; Petit P., 1972; Stanoli J., 1987] и метод сочетания применения
дугообразного разреза в верхней тети с Z-пластикой малым треугольным
лоскутом в нижней части фильтрума [Новоселов Р. Д., 1972; Delaire J., 1975].
Указанные способы позволяют получать хорошие эстетические и
функциональные результаты, наиболее полно восстанавливают
функциональную анатомию с учетом патоморфологических изменений, но ни
одним из методов нельзя полностью исправить сопутствующие и предупредить
послеоперационные деформации носа. По данным различных авторов,
деформации носа определяют от 85 до 100 % [Дмитриева В. С, 1956; Лимберг Α. Α.,
1952; Новоселов Р. Д., 1972; Виссарионов В. Α., 1982; Козин И. Α., 1968,
1969].
Сопутствующая деформация носа побуждала хирургов искать
оперативные приемы, позволяющие устранить эту деформацию при первичной
пластике губы.
Первоначально действия хирургов были направлены на изменение
положения основания уплощенного крыла, для чего использовали различные
23
варианты перекидного треугольного лоскута в области дна преддверия носа
[Лимберг Α. Α., 1938; Axhausen G., 1941], мобилизацию основания крыла от
челюсти и подшивание его погружным швом к перегородке [Маслов И. Д.,
1927]. В. И. Знаменский A971) и Б. А. Котов A984) устранение деформации
носа видят в устранении гребневидной складки путем перемещения
треугольных лоскутов и через разрез "птичкой" мобилизуют от кожи
уплощенный крыльный хрящ, подшивают его к арке здорового хряща. Однако
разрезы слизистой оболочки при выполнении Z-пластики могут повредить
ростковые зоны большого крыльного хряща.
При первичной ринохейлопластике задачи оперативного вмешательства
усложняются, а объем вмешательства увеличивается. Помимо
восстановления нормальной анатомии верхней губы, необходимы восстановление
правильного положения хрящей носа и нормализация положения и
прикрепления мышц приротовой области и носа.
В нашей стране развитию первичной ринопластики в значительной
степени способствовал Р. Д. Новоселов A972), который детально описал
изменение хрящей носа при расщеплении верхней губы, связанное с
дезориентирующим влиянием мимической мускулатуры, и предложил свой вариант
первичной ринопластики.
Поданным Б. Н. Давыдова и Р. Д. Новоселова A997), при
односторонних расщелинах расщепление круговой мышцы рта приводит к тому, что на
целом сегменте верхний пучок прикрепляется к внутренней ножке
крыльного хряща со стороны расщелины, а на пораженном — к основанию крыла
носа. Возникает дисфункция верхних пучков круговой мышцы, что и приводит
к смещению перегородки носа в сторону, противоположную расщелине,
уплощению наружной ножки крыльного хряща и смещению основания крыла
носа кзади и книзу.
Р. Д. Новоселов A972) первым из отечественных хирургов предложил
основанную на изучении механизмов деформации хрящей носа и
дисфункции мышц приротовой области методику первичной ринохейлопластики.
Помимо восстановления анатомической целости верхней губы, эта операция
включает коррекцию порочного расположения мышц носовых отверстий,
исправление формы хрящей носа с щадящим отношением к зонам их
активного роста. Не рекомендуется отслаивать и выделять хрящи по внутренней
поверхности, надсекать, рассекать и иссекать внутренние или наружные
ножки большого хряща крыла носа. Оптимальный возраст больных 6—8 мес.
По данным Р. Д. Новоселова A978), основные морфологические
изменения при врожденных односторонних полных расщелинах обусловлены
изменением направления волокон круговой мышцы рта: верхний пучок
глубокого мышечного слоя круговой мышцы рта на стороне расщелины
прикреплен к основанию деформированного крыла носа, а верхний пучок,
идущий со здоровой стороны, — к медиальной ножке крыльного хряща со
стороны расщелины. Сохранение такого порочного расположения после хей-
лопластики играет важную роль в развитии остаточных деформаций носа и
верхней губы после хейлопластики. Для достижения оптимального
результата при пластике врожденной расщелины необходимо соединить мышечные
пучки конец в конец. Наилучший результат достигается при использовании
методик, предусматривающих отсечение мышечных волокон от основания
крыла носа и колумеллы, а также ротацию мышечных компонентов.
Методика операции заключается в разметке операционного поля с
нанесением точек изгиба линии Купидона (рис. 22.6). Затем рисуют линию от
точки 3 до точки 5 — вершины расщелины. Далее по стенке перегородки носа
наносят контур угловой линии разреза внутрь ноздри длиной 6—8 мм. От точ-
24
Рис. 22.6. Первичная ринохейлопластика по Новоселову (схема).
а, б — этапы операции. Объяснения в тексте.
ки 3 проводят прямую линию длиной около 4 мм, равную разнице
расстояния между колонками губного желобка. Для формирования правильного
положения перегородки носа очерчивают лоскут у его основания (линия 7—8).
Намечают разрез по красной кайме от точки 3 под углом 45°. На пораженном
сегменте верхней губы намечают треугольный лоскут D—10—9), который
должен быть совмещен с линией 3—6. От точки 9 рисуют линию, равную
высоте колонки губного желобка на пораженной стороне, и контур лоскута
A1 — 12). Лоскут 13—14—15 выкраивают для формирования овала
уплощенного крыла носа и устранения складки слизистой оболочки в области свода
крыла носа.
После инфильтрации тканей производят разрезы с иссечением
патологических (избыточных) тканей (на рисунке заштрихованы). Рассепаровывают
ткани, уделяя основное внимание выделению культей круговой мышцы
верхней губы, сначала в нижней трети, затем в верхней. Верхний пучок глубокого
слоя круговой мышцы рта отсекают от внутренней ножки хряща крыла носа
на стороне расщелины, предупреждая вторичное смещение внутренней
ножки крыльного хряща на стороне расщелины. Перегородку носа тщательно
мобилизуют в области основания и передненижнего края хряща перегородки
носа. Тупым путем внутреннюю ножку большого крыльного хряща крыла носа
на стороне расщелины отслаивают от внутренней ножки на целом сегменте.
Через разрез в форме галочки на кончике носа по Рауэру расслаивают
внутренние ножки хряща крыла носа. Полностью отслаивают наружную ножку
крыльного хряща, после чего отсепарованные ткани крыла и перегородки
носа перемещают в правильное анатомическое положение и сшивают.
Выкраивают треугольный лоскут на альвеолярном отростке большого сегмента,
после чего этот лоскут и треугольные лоскуты мобилизуют. Выделяют культю
круговой мышцы, затем окончательно отделяют основание крыла носа от
грушевидного отверстия. При полных расщелинах дополнительно рассекают
ткани слизистой оболочки на стороне расщелины в форме кочерги.
Последовательность наложения швов: вершины треугольных лоскутов
слизистой оболочки, края слизистой оболочки в области преддверия и края
треугольника. Сшивают перемещенные ткани в зоне разреза "кочерга" и по
25
краю дефекта слизистой оболочки свода крыла носа. Сопоставляют и
сшивают пучки круговой мышцы, начиная снизу. Под основанием перегородки
носа и основанием крыла носа через верхний пучок круговой мышцы
проводят шов, окончательно регулирующий ширину носового отверстия. При
необходимости ширину красной каймы формируют путем обмена встречных
лоскутов на слизистой оболочке преддверия полости рта. Накладывают швы
по границе красной каймы, на перемещенный лоскут В, затем швы на
перемещенные лоскуты С и А. Перегородку носа перемещают вверх и фиксируют
вместе с внутренней ножкой крыльного хряща. Выравнивают ширину
носового отверстия и формируют овал крыла носа, для чего используют Π-образные
швы. В сформированный носовой ход вводят резиновую трубку, обернутую
марлей, смоченной йодоформной жидкостью. Формирующие П-образные
швы снимают на 12-й день, остальные — на 7-й день.
При изучении отдаленных результатов операций, выполненных поданной
методике, через 10— 15 лет не выявлено случаев недоразвития хрящей носа. Все
структуры средней зоны лица развиваются правильно.
В предложенной Л. Е. Фроловой A976) модификации операции Обуховой
также используется лоскут соответственно гребневидной складке. Способ
нельзя назвать физиологическим, так как И. А. Козин A969, 1983), В. А.
Виссарионов A982), М. Spiva A970) и D. Millard A976) убедительно доказали, что,
поскольку наблюдается не избыток, а дефицит слизистой оболочки выстилки
носа, вместо сферической поверхности образуется стягивающий рубец. Из
косметических соображений нецелесообразно и использование наружного
разреза "птичкой".
Зависимость форм носа от рельефа лицевого черепа установлена Μ. Μ.
Герасимовым A955). В связи с недоразвитием костной ткани по краю
грушевидного отверстия многие авторы дефицит костной ткани по краю грушевидной
апертуры восполняют костным или хрящевидным трансплантатом. Г. И. Се-
менченко A964), А. Н. Губская A963), Б. Н. Давыдов A967), Б. Я. Баркас
A966), Л. Е. Фролова и Г. Г. Мамедов A979) применяли эмбриональную
ткань. И. В. Бердюк A963) предлагает использовать гипертрофированную
нижнюю носовую раковину в качестве опоры под основание уплощенного
крыла. Операцию производят в два этапа с повторением рассечения верхней
губы, что значительно уменьшает достоинства операции, а введенные
хрящевые и костные трансплантаты рассасываются.
Ряд авторов, считаятіричиной деформации концевого отдела носа
неправильное положение большого крыльного хряща и его гипоплазию, производят
мобилизацию хряща и сшивание в правильном положении [Бутикова Н. И., 1955; Бу-
латовская Б. Я., 1958; Сорокин В. И., 1962]. Velasgiier и Ortis Monaskrio A974),
используя средний разрез на колумелле, производят резекцию серповидного
участка кожи симметрично здоровой ноздре. Разрезом по мембранной перегородке
с переходом на верхнюю губу выкраивают "скользящий" лоскут вместе с
медиальной ножкой и аркой большого крыльного хряща и после его перестановки
фиксируют его. Все эти способы предполагают разрезы на слизистой оболочке
носа, что чревато повреждением ростковых зон [Новоселов Р. Д., 1978]. Еще
большим радикализмом отличалась методика, при которой крыльный хрящ
отслаивают не только от кожи, но и от выстилки латерального фрагмента
(SkoogT., 1969]. При ушивании краев раны мобилизованный крыльный хрящ
вместе с выстилкой смещают медиально, а его латеральную ножку помещают
на треугольный хрящ. Одновременно производят пластику дефекта
альвеолярного отростка верхней челюсти слизисто-надкостничными лоскутами.
Н. McComb A985) при первичной хейлопластике предлагает отслаивать
кожу носа до переносицы и подшивать арку большого крыловидного хряща
26
швами, концы которых выводить на область переносицы. К. Salyer A992)
рекомендует отсепаровывать уплощенный крыльный хрящ от кожи и слизистой
оболочки через разрез у основания кожной части перегородки носа.
Перемещенный кверху крыльный хрящ фиксируют сквозными матрацными швами.
И. А. Козин A996) считает нецелесообразным такую субтотальную
мобилизацию у детей в первый год жизни. A. Fara A987) настоятельно рекомендовал
первичную репозицию перегородки путем не только отделения от челюсти,
но и выравнивания до совершенно выпрямленного положения и отделения
от крыльных хрящей. Однако технику фиксации в правильном положении
автор не описывает. К. Matsuo A989) первичную ринопластику производит
в раннем неонатальном периоде. В ходе операции мобилизуют переднюю
часть перегородки и основания больного крыла с восполнимой выстилкой
дефекта лоскутом на ножке из красной каймы латерального фрагмента.
J. Talmant A993), объясняя неудачи первичной ринохейлопластики
неправильно проведенной миопластикой, рекомендует отсекать от латеральной культи
круговой мышцы мышцу, поднимающую верхнюю губу, и носовую мышцу.
Культю носовой мышцы подшивают к надкостнице межчелюстной кости.
Затем глубокую часть круговой мышцы сшивают с культей на здоровой стороне,
а поверхностный слой подшивают внахлест, чтобы мышечная ткань
имитировала гребень. Освобожденную от кожи латеральную ножку фиксируют к
треугольному хрящу матрацным швом. После операции отмечается хорошее
положение завитка крыла по отношению к уровню дна носового хода.
Уплощение кончика носа и свода носового хода можно объяснить отсутствием
репозиции медиальной ножки, арки, перегородочного хряща.
И. А. Козин A996), обобщая опыт реконструктивных операций,
рекомендует при первичной пластике исправлять форму уплощенного крыла и
перегородочного хряща, создавать глубокое преддверие полости рта, дупли-
катуру дна преддверия носа, производить полноценную миопластику.
Коррекцию уплощенного крыла носа производят по его краю через
полуциркулярный разрез. Мобилизованный хрящ с перихондрием перемещают до
нормального уровня здорового крыльного хряща.
На протяжении десятилетий хирурги сосредоточивали усилия на
пластическом восстановлении мягких тканей верхней губы, а необходимость
пластики разобщенных сегментов верхней челюсти игнорировали. В 1955 г.
одновременно Е. Scfimid в Германии, К. Nordin и В. Johansson в Швеции
опубликовали сообщения о пластике расщелин альвеолярного отростка
костным трансплантатом. Положительные моменты этой операции
(нормализация формы верхней челюсти, перемещение зубных зачатков с краев
расщелин и их рост в костном трансплантате, стабилизация положения носа)
способствовали ее широкому распространению.
В начале 60-х годов остеопластика стала почти рутинной во всех
медицинских центрах мира, где занимаются проблемами расщелин неба [Семен-
ченко Г. И., 1964; Крыкляс Г. Т., 1966; Вакуленко В. И., 1982; Давыдов Б. Н.,
1984; Petit Μ., Pgaume Μ., 1962; Muir J., 1966; Koch J., 1969; Jackson J., 1972].
К сожалению, надежды, возлагаемые на эту операцию, не оправдались;
костный трансплантат не увеличивается по мере роста ребенка [Stenstrom S.,
1967; Friede Η., Johanson В., 1977J. Отмечается неблагоприятное влияние
костного трансплантата на рост верхней челюсти [Rehrmann Α. et аЦ 1970].
Отдельные отрицательные результаты полностью подтверждены F. Harle A971).
В настоящее время, по мнению многих авторов, единственной оправданной
формой применения костной трансплантации остается поздняя вторичная
остеопластика [Schmid Ε., 1966; Регко М., 1967; Epstein Μ. etal., 1970; Koberg W.,
1973].
27
В то же время имеются сообщения, в которых рекомендуется
осуществлять костную пластику при первичной хейлоринопластике. J. Jackson A988)
предлагает при значительном костном дефиците возмещать его
костномозговой смесью губчатой кости, пересаженной с гребешка подвздошной кости
путем кюретажа. Наряду с другими авторами (Т. Skoog, S. Silber) при
небольшом дефиците он рекомендует помещать под надкостницу небольшое
количество остеостимулирующих веществ (гели, пленки). Б. Н. Давыдов и Р. Д.
Новоселов A997) выполняют ринохейлогнатопластику с применением лио-
филизированных костных аллотрансплантатов "враспорку". Мягкотканное
ложе формируют из ротоносовой слизистой оболочки краев расщелины.
Надкостничную выстилку создают из аутотрансплантатов надкостницы боль-
шеберцовой кости. Образуется активно перестраивающийся с возрастом
костный регенерат, но непрерывность челюсти восстанавливается только на
уровне апикального базиса верхней челюсти в области наибольшей ширины
дефекта. Остальные элементы операции в основном соответствуют
приведенной методике хейлоринопластики тех же авторов.
J. Ames и соавт. A984), A. Eskeland и соавт. A985) описали костную
пластику расщелины у больных в возрасте от 8 до 10 лет. Время проведения
пластики зависит от расположения постоянных клыков. Перед прорезыванием
последних трансплантатом восстанавливают непрерывность альвеолярного
гребня, что позволяет зубам прорезаться в полноценной, цельной кости.
Однако костную пластику целесообразно осуществлять и в возрасте 13—19 лет
[Jackson J., 1988]. Хорошие результаты получили S. Rosenstain и соавт. A982),
которые использовали ребро, J. Jackson A988) и др., применившие массу из
губчатой и подвздошной кости. Они считают разработанный ими метод
оптимальным, так как, по их мнению, ринохейлогнатопластика создает условия,
необходимые для правильного роста и развития верхней губы, носа и верхней
челюсти.
В настоящее время в зарубежной литературе с целью профилактики
смещения и сдавливания сегментов верхней челюсти и, следовательно,
стабилизации положения основания носа большое внимание придается
использованию периостальных лоскутов. Основоположником этого метода можно
считать Т. Skoog A965). Он доказал, что на той стороне, откуда перемещали
лоскут, не развивается гипоплазия верхней челюсти.
Т. Skoog A971), J. Delaire A975), J. Hrivnakova A981, 1983) сообщают о
новообразовании кости в области вшитой надкостницы. Периостальный
трансплантат способствует улучшению соотношений расщепленных
сегментов верхней челюсти.
Первичную операцию проводят с учетом патоморфологических
изменений костного скелета, мимической мускулатуры, хрящевого отдела носа.
Ликвидируется разобщение, дистопия, натяжение не только элементов верхней
губы, но и хрящевой капсулы носа, носовых мышц. Первичная ринохейло-
периостеопластика позволяет уменьшить вторичную деформацию носа и
сократить объем последующих корригирующих операций [Савицкая Г. М.,
Агеева Л. В., 1998].
При выполнении операции ринохейлопериостеопластики по методике
авторов восстанавливают целость верхней губы, ликвидируют мышечную
дистопию и формируют полноценный сфинктер, осуществляют репозицию
перегородочного хряща и больших крыльных хрящей. Учитывая
естественный процесс сближения челюстных сегментов после операции, пластику
костного дефекта не производят.
Выполненное с учетом патоморфологических изменений оперативное
вмешательство на поврежденных ростковых зонах не только способствует ли-
28
квидации анатомического дефекта, но и создает условия для дозревания ги-
поплазированных тканей, а неустранение нарушений анатомических
взаимоотношений может быть причиной вторичной деформации, которая с
возрастом превращается в трудно устранимую. Дальнейшее изучение
нарушений анатомических взаимоотношений и стремление к максимальному их
устранению в ходе операции при врожденных уродствах, в частности
односторонних расщелин верхней губы, будет способствовать улучшению
функциональных и эстетических результатов лечения.
Объем оперативного вмешательства по Савицкой и Агеевой зависит от
степени анатомического дефекта.
У детей с неполной расщелиной верхней губы и сопутствующей
деформацией носа, у которых последняя выражается в более низком расположении
дна преддверия носа, асимметрии ноздрей, смещении хрящевой части
перегородки, ринопластику выполняют в следующем объеме. Перегородочный хрящ
освобождают от слизистой оболочки арки большого крыльного хряща на
больной стороне. Поднятие дна носового хода происходит в результате создания
субназальной мышечной поддержки. После рассепаровки круговой мышцы
рта и крыловидной части носовой мышцы последнюю подшивают к
надкостнице большого фрагмента. Затем глубокую часть круговой мышцы сшивают
с перемещенной вниз культей мышцей большого фрагмента, а
поверхностный слой — внахлест. Мышечную поддержку основания крыла усиливают
субпериостальным введением биогенного материала по краю грушевидного
отверстия. Поднятия опущенного носового свода и перемещения крыльного
хряща достигают мобилизацией тканей через разрез по краю ноздри.
У больных в возрасте от 5 до 9 мес с полной односторонней расщелиной
верхней губы и альвеолярного отростка верхней челюсти объем оперативного
вмешательства увеличивается по сравнению с описанным выше. В связи с
тем, что у них отсутствует выстилка носового хода, важнейшими моментами
являются формирование ее с помощью слизисто-надкостничных лоскутов с
перегородки и межчелюстной кости и сшивание этого лоскута со слизисто-
надкостничным лоскутрм малого фрагмента.
Поддержку крыла носа и предупреждение рубцевания по линии
расщелины альвеолярного отростка, помимо мышечной пластики, осуществляют пе-
риостальными лоскутами с краев расщелины альвеолярного отростка.
Мобилизация перегородки и крыльного хряща не отличается от описанной выше.
В связи с большей степенью опущения свода и кончика носа мобилизацию кожи
проводят более широко. Мобилизация перегородки не отличается от этого
этапа при неполной расщелине верхней губы. При сравнении больных этой
группы и больных с полной расщелиной верхней губы, у которых не
производилась ринопластика, отмечается симметричное расположение крыльев и
ската носа, выраженный кончик, повышение носового свода. В течение 3—
6 мес после операции все больные этой группы должны носить внутриносо-
вые вкладыши.
У ряда детей в возрасте от 6 мес до 1 года со сквозной расщелиной верхней
губы, альвеолярного отростка и неба выражена ротация большого фрагмента
альвеолярного отростка, малый фрагмент (а вместе с ним основание
недоразвитого крыла) смещен кзади и наружу. При этом отмечается также диастаз
альвеолярных отростков более 10 мм, гипоплазия малого фрагмента, что в
значительной степени затрудняет сшивание периостальных лоскутов. В таких
случаях необходимо предоперационное ортодонтическое лечение,
направленное на нормализацию положения альвеолярных отростков. В связи с
поздним обращением (в возрасте старше 6 мес) и невозможностью
проведения периостеопластики лоскутами с расщелины альвеолярного отростка
29
Рис. 22.7. Первичная двусторонняя ринохейлопластика (а, б) (схема) [Давыдов Б.Н.,
Новоселов Р.Д., 1997].
применяют периостальный лоскут, сформированный параллельно краю
расщелины твердого неба. Отмечены хорошее приживление лоскута, отсутствие
носоротовых соустий. Наблюдается интенсивное сближение альвеолярных
отростков. Функциональный и эстетический результат операции
превосходит аналогичные показатели у больных после хейлопластики.
Ортодонтическое лечение позволяет провести первый этап пластики —
хейлоринопериостеопладтику в оптимальные сроки (в возрасте 4—6 мес).
При этом риск повреждения так называемых ростковых зон при плановых
вмешательствах, проводимых профессионалами, является преувеличенным.
Оперативное вмешательство выполняют с учетом современных
представлений о патогенезе порока. Оно должно быть направлено на ликвидацию
элементов разобщения, дистопии, устранение нефизиологического давления
и натяжения элементов верхней губы и носа, стимуляцию костного роста в
гипоплазированных зонах.
В послеоперационном периоде в возрасте до 1 года продолжают
ортодонтическое лечение, периодически проводят курсы физиотерапии. В
возрасте 1 года осуществляют второй этап — велопластику, ортодонтическое
наблюдение и при необходимости лечение. В ясельном возрасте проводят
санацию ЛОР-органов, продолжают ортодонтическое лечение, позволяющее
в возрасте 3,5—4 лет провести третий этап — уранопластику, затем
физиотерапевтическое и ортодонтическое лечение, занятия с логопедом. В возрасте
4—6 лет при показаниях производят корригирующую рехейлоринопластику,
продолжают физиотерапевтическое, логопедическое и ортодонтическое
лечение. Таким образом, к 7 годам возможны окончание хирургического
лечения и социальная адаптация ребенка к занятиям в школе.
Двусторонняя хейлопластика. Анатомические нарушения при полной
двусторонней расщелине верхней губы складываются из нарушения ее
целости и разделения на три фрагмента: центральный (межчелюстная кость) и два
боковых. Межчелюстная кость может быть резко выдвинута вперед от зубной
дуги или недоразвита в той или иной степени вплоть до полной аплазии.
Боковые фрагменты могут занимать различное положение: сдвигаться вперед,
вниз, в стороны, к центру. Круговая мышца рта претерпевает значительные
изменения, аномально прикрепляется к фрагментам и отсутствует в области
межчелюстной кости.
30
Рис. 22.8. Первичная хейлопластика в два этапа при двусторонней сквозной расщелине
верхней губы с гипоплазированной межчелюстной костью (схема) [Millard D., 1977].
а — точки изгибов линии Купидона и линии раскроя тканей; б— ткани раскроены; в — положение
тканей после первого этапа операции; г — положение тканей после второго этапа операции.
При двусторонних расщелинах верхней губы пластику производят
одномоментно или в два этапа с интервалом 1,5—3 мес. Это связано с
величиной расщелины, положением и выраженностью гипоплазии межчелюстной
кости. Чем сложнее комплекс анатомических нарушений в зоне расщелины,
тем больше оснований для двухэтапного подхода к оперативному лечению.
Операцию выполняют по типу хейлопластики с использованием методик
Лимберга, Обуховой, Мезюрье, Милларда, а в последние два десятилетия —
чаще по типу хейлоринопластики (рис. 22.7—22.9).
Б. Н. Давыдов и Р. Д. Новоселов A997) предложили методику пластики
двусторонних симметричных неполных и полных расщелин верхней губы,
которую они рекомендуют выполнять в возрасте 6—8 мес. На боковых частях
губы одномоментно выкраивают два перекидных, с частью красной каймы
трапециевидных лоскута. Расслаивают внутренние ножки большого крыль-
ного хряща. Операция состоит из следующих этапов.
31
Рис. 22.9. Первичная хейлопластика при врожденной двусторонней симметричной
полной расщелине верхней губы с одновременным углублением преддверия рта (схема)
[Millard D., 1977].
а — линии раскроя тканей; δ — формирование преддверия; в — ушивание слизистой оболочки
и линии под междучелюстной костью; г — окончательная фиксация тканей; д — раны после
ушивания тканей; е — то же, пунктиром показано направление перемещения тканей в области
основных крыльев носа.
Рис. 22.10. Первичная ринохейлопластика
при двусторонней неполной расщелине
верхней губы [Давыдов Б.Н., Бессонов С.Н.,
1994].
а — намечены линии разрезов (схема); б— ткани
раскроены (схема); в — сопоставление тканей
(схема); г — больной 6 мес с неполной
расщелиной верхней губы; д — тот же больной через 1 год
после ринохейлопериостеопластики; е —
больная 5 мес с полной левосторонней расщелиной
верхней губы; ж — та же больная через I год
после ринохейлопериостеопластики; з — больная
7 мес с двусторонней полной расщелиной
верхней губы и неба; и — та же больная через 4 мес
после одномоментной хейлопластики; к —
больной 6 мес с поперечной расщелиной лица; л —
тот же больной после снятия швов.
После нанесения
опознавательных точек и линий разрезов последние
проводят по боковым частям, отступя
от границы красной каймы и кожи.
Одновременно выкраивают небольшие
треугольные лоскуты под основанием
крыльев Носа со сторонами 3—4 мм и
лоскуты в нижней трети боковых
частей губы трапециевидной формы
размером 1,5x4x3 мм.
На среднем фрагменте в пределах
кожной границы проводят
вертикальные разрезы, которые заканчиваются
небольшим разрезом по внутреннему
краю основания перегородки носа с
обеих сторон. В нижнем отделе
среднего фрагмента делают два разреза под
тупым углом длиной, равной длине
трапециевидного лоскута. Выделяют
слизистую оболочку, рассепаровывают
ткани с полным отделением их только
в области перегородки носа и с
выделением мышечных волокон.
Расслаивают внутренние ножки
до кончика носа и одновременно
отслаивают наружные ножки большого в
хряща крыла носа от кожных
покровов. Отсепаровывают ткани боковых частей губы, выделяют культи круговой
мышцы. Верхние пучки круговой мышцы рта отсекают от крыльных хрящей
мышц носа. Основание крыльных хрящей отслаивают по краям
грушевидного отверстия и в области Клыковых ямок. При необходимости делают
послабляющие разрезы в форме кочерги по сводам преддверия полости рта.
Ушивание начинают со слизистой оболочки преддверия рта. Затем между
тканью средней части губы и поверхностью межчелюстной кости накладывают
3-1263
33
Рис. 22.10. Продолжение.
ν
•^T4·
і
• '
У
Рис. 22.10. Продолжение.
П-образные швы на культю круговой мышцы. Накладывают узловые швы на
края мышечных культей и среднюю часть губы. Красную кайму формируют из
боковых участков после их пересечения под углом 45°. Накладывают швы на
границе красной каймы и кожи по коротким сторонам трапециевидных
лоскутов и на кожу выше последних. В основание перегородки носа вшивают тре-
35
з*
Рис. 22.11. Реконструктивная хейлопластика с перемещением "скользящего лоскута"
(схема) [Козин И.А., Виссарионов В.А., 1981].
а — намечены линии разрезов; б — направление движения "скользящего лоскута"; в — окончательное
сопоставление тканей.
угольные кожные лоскуты и формируют дно преддверия носа. На
мобилизованные крылья носа накладывают матрацные швы. В носовые отверстия
вводят резиновые трубочки, обернутые марлей, смоченной йодоформной
жидкостью. Узловые швы снимают на 5—6-й день, матрацные — на 12—14-й день.
Б. Н. Давыдов и Р. Д. Новоселов A997) предлагают также при
двусторонних расщелинах выполнять ринохейлогнатопластику. Костная пластика
принципиально не отличается от описанной выше для односторонних
расщелин (рис. 22.10).
а б в
Рис. 22.12. Операция перемещения "скользящего лоскута" с включением в его состав
кожи уплощенного крыла носа (схема) [Виссарионов В.Α., 19891.
а — намечены линии разрезов; б — направление перемещения скользящего лоскута.
Заштрихованный участок внутренней поверхности крыла носа иссечен; в — окончательное сопоставление
тканей.
36
Рис. 22.13. Этапы универсальной реконструктивной ринохейлопластики при
врожденной односторонней расщелине верхней губы (схема) [Козин И.А., 1996].
а — линии разрезов; б — выкраивание и иммобилизация тканей; в — носовая слизистая оболочка
ушита, мышечные волокна отсечены от небной пластины и мобилизованы; г — окончательное
перемещение и ушивание тканей.
В последние годы в мировой практике получила признание операция
первичной ринохейлопластики. Однако при первичной операции не всегда удается
добиться желаемых результатов. Большое значение приобретают хорошо
разработанные методы завершающей ринохейлопластики (рис. 22.11—22.13)
[Виссарионов В. Α., Козин И. Α., 1981; Виссарионов В. Α., 1987; Козин И. Α., 1996].
22.6. Уранопластика
Существуют различные методы оперативных вмешательств при врожденных
расщелинах неба: Бильрота, Розенталя, Львова, Лимберга, Хитрова,
Евдокимова, Новоселова, Давыдова, Вернадского, Фроловой, Милларда, Манчестера.
По данным литературы, эти методики имеют следующие недостатки.
Наблюдаются значительное укорочение неба, малая его подвижность, рубцы
в окологлоточном пространстве, рубец в центре неба, соединяющий края
бывшей расщелины, дефекты в переднем отделе твердого неба. Мягкое небо
подтягивается рубцами вверх с одной стороны, создается неравномерность
закрытия носоглотки. При резекции задневнутреннего края небного
отверстия, когда сосудисто-нервный пучок освобождается из костного кольца и
опускается, особенно выражено рубцевание. Рубцы мягких тканей, спаянные
с костью, искажают форму кости, особенно в период ее роста. Следует от-
37
метить грубые и мощные рубцы на обращенной в носовую часть глотки
слизистой оболочке неба, а также возрастные ограничения (выполнение
операции в 5—10 лет), травматичность операций. При операции по Швикендик
ширина расщелины не должна превышать 1 см.
В последние годы развитие методов уранопластики шло по пути наиболее
рационального использования элементов оригинальных методик
применительно к конкретному случаю и часто зависело от подготовки, возможностей и
квалификации хирурга. Второй тенденцией было усиление внимания к
восстановлению и формированию при первичной уранопластике небно-глоточного
кольца, что имеет определяющее значение для формирования правильной
речи в дальнейшем. Третьей тенденцией является повышенный интерес к
ликвидации недостаточности смыкания небно-глоточного кольца [Ананян С. Г.,
Безруков В. М., 1988; Ананян С. Г., 1993; Герасимова Л. П., 1997; Мамедов
Α. Α., 1997]. Установлено, что объективная функциональная оценка с
использованием соответствующих методик позволяет с высокой степенью
достоверности решить вопрос о показаниях к хирургическому устранению небно-гло-
точной недостаточности. В то же время высокие положительные результаты
достигаются и при использовании функциональных методов лечения.
Видимые анатомические нарушения при расщелине неба (сама
расщелина, патологическое сообщение полости рта с полостью носа, недоразвитие
малого фрагмента, укорочение мягкого неба, расширение глоточного кольца)
сопровождаются и невидимыми — костным дефектом твердого неба при так
называемой скрытой (подслизистой) расщелине, недоразвитием мышц
мягкого неба, изменением мест их прикрепления, вертикальным расположением
и т. д. Все эти патологические изменения должны быть оценены в каждом
случае при планировании операции.
Продолжается обсуждение вопроса о сроке операции на небе. Все
участники дискуссии находят необходимые аргументы в защиту своей позиции.
Однако социальные аспекты этой проблемы диктуют необходимость возможно
ранней реабилитации больных данного контингента. В большинстве
крупных отечественных и зарубежных центров, занимающихся данной
проблемой, операции производят в возрасте 1—3 года [Фролова Л. Е., 1975;
Мамедов Α. Α., 1997]. J. Jackson A988) считает, что при расщелине неба всех типов
операцию следует выполнять в возрасте 6 мес, а при тяжелых двусторонних
расщелинах — в два этапа: первый — в 3—4 мес, второй — через 1 мес.
Главным аргументом для обоснования этого срока является
нормализация анатомического аппарата, участвующего в речеобразовании, до
формирования порочных речевых навыков с вытекающими отсюда социальными,
логопедическими и другими проблемами. Объективные данные,
свидетельствующие о том, что осложнения возникают не чаще, чем при операциях в
более старшем возрасте, позволяют рекомендовать проведение операций при
расщелинах неба в эти сроки.
Раннее восстановление функциональной нагрузки мышц мягкого неба
и верхних отделов глотки при расщелинах способствует своевременному
развитию речи, а также оказывает стимулирующее влияние на рост верхней
челюсти. Ранняя операция предупреждает не только развитие осложнений в
полости рта, но и ухудшение общего состояния, которые свойственны детям
со сквозными расщелинами верхней губы и неба при лечении в более
поздние сроки (деформация челюстей, воспалительно-дистрофические и
склеротические изменения в тканях мягкого неба, гипотрофия и др.).
В отдаленном послеоперационном периоде отмечается правильное
формирование альвеолярной дуги, на всем протяжении челюсти ширина
расщелины значительно уменьшается за счет доразвития небных фрагментов под
38
а б в
Рис. 22.14. Уранопластика при врожденной расщелине неба (схема) [Фролова Л.Е.,
1977].
а — разрезы от вершины расщелины до границы твердого и мягкого неба, по носовой поверхности
мягкого неба косо вниз по боковой стенке глотки; б — образование слизисто-мышечного жома;
в — состояние тканей после наложения швов.
воздействием восстановленных мышц мягкого неба. Раннее речевое развитие
способствует ранней адаптации и социальной реабилитации детей с данной
патологией.
Разработанные Л. Е. Фроловой A977) методы операций позволяют
предупредить небно-глоточную недостаточность. Она предложила способ
пластики неба с сужением небно-глоточного кольца (рис. 22.14). Эта методика
предполагает продление разрезов по краям расщелины, далее по задней поверхности
фрагментов расщепленного язычка и вниз по боковым стенкам глотки.
Полученный после разреза слизисто-мышечный слой сшивают по средней линии.
Язычки рассекают вертикальными разрезами. При этом образуется единое
целое с ротовым слизисто-мышечным слоем, а фрагменты язычков сшивают друг
с другом. Этим достигается сужение небно-глоточного кольца. Слизистую
оболочку носа в области твердого неба мобилизуют и ушивают вместе со
слизисто-мышечным слоем области мягкого неба. Слизисто-надкостничные
лоскуты на обоих фрагментах неба отслаивают, смещают к центру и сшивают над
тканями, ушитыми ранее. Данный метод в различных модификациях может
быть использован при различных формах расщелин.
В дальнейшем появились модификации этого способа, разработанные
Э. У. Махкамовым A979—1997), А. А. Мамедовым A988—1989). Известны
модификации, позволяющие закрывать расщелины, которые имеют ширину
на границе твердого и мягкого неба до 2,5—3 см (рис. 22.15—22.19). А. А. Ма-
медов предложил A986) также оригинальный способ операции со сшиванием
дистальных концов группы мышц (мышца, поднимающая небную занавеску,
мышца, напрягающая ее, и небно-глоточная мышца) конец в конец или стык
в стык (см. рис. 22.15). По данным автора, этот способ наряду с другими
известными щадящими элементами первичной уранопластики можно
использовать при любой форме врожденной расщелины.
При широких расщелинах (на границе мягкого и твердого неба ширина
более 2—3 см) может быть применена методика двухэтапной уранопластики.
Первым этапом выполняют велопластику. Это дает возможность в возрасте до
3 лет создать условия для правильного развития небно-глоточного кольца, что
обеспечивает правильное звукообразование, не нарушая роста верхней челю-
39
Рис. 22.15. Первичная уранопластика при односторонней сквозной расщелине
верхней губы и неба (схема) [Мамедов A.A., 1995].
а — линии разрезов; б — выкраивание и иммобилизация тканей; в — выделение мышц в пределах
мягкого неба и направление их сшивания; г — окончательное ушивание тканей.
сти. После велопластики расщелина в области твердого неба уменьшается.
Последующая операция невелика по объему; ее выполняют в возрасте 5—6 лет.
В клинике, руководимой Л. Е. Фроловой (Москва), с 1972 г. применяли
двухэтапную хейловелопластику при одно- и двусторонней сквозной
расщелине губы и неба (цит. по А. А. Мамедову, 1978). В возрасте до 1 года
проводят одномоментно хейлопластику и в пределах мягкого неба велопластику
с сужением глоточного кольца. Второй этап (в 2—3 года) заключается в
закрытии врожденного дефекта, остающегося в переднем отделе. При
двусторонней расщелине верхней губы и неба предлагается соблюдать такую
последовательность: сначала производят хейлопластику с одной стороны и
одномоментно велопластику, через 2—3 мес — хейлопластику с другой
стороны, в возрасте 2—3 лет — пластику расщелины твердого неба.
40
Рис. 22.16. Двухэтапная пластика неба с сужением глоточного кольца при
врожденной сквозной (полной) расщелине верхней губы и неба. Первый этап — пластика в
пределах мягкого неба (велопластика) (схема) [Фролова Л.Е., 1972].
а — пунктиром намечены линии разрезов; б— ткани рассечены и отслоены; в — носовая слизистая
оболочка ушита; г — окончательное перемещение и ушивание тканей.
А. Э. Гуцан A982) предложил при первичной пластике расщелины неба
использовать взаимоперекидные слизисто-надкостничные лоскуты.
Для восстановления непрерывности костных структур неба и
альвеолярного отростка рядом авторов [Семенченко Г. И., 1964; Сысолятин П. Г., 1975;
Плотников Η. Α., 1980; Вакуленко В. И., 1982; Давыдов Б. Н., 1983]
разработаны методы уранопластики с использованием костных трансплантатов.
Большинство зарубежных авторов предлагают выполнять
костнопластическое восстановление альвеолярного отростка в возрасте не ранее 11 лет
(перед прорезыванием клыков).
41
Рис. 22.17. Двухэтапная пластика неба с сужением глоточного кольца при
врожденной изолированной (полной) расщелине неба. Второй этап — пластика в пределах
твердого неба с использованием одного ел изисто-надкостничного лоскута,
опрокинутого на области расщелины твердого неба (схема) [Фролова Л.Е., 1972].
а — линии разреза; б— слизисто-надкостничный лоскут, носовой слизисто-мышечный слой
отделены; в — слизисто-надкостничный лоскут опрокинут, ушит с тканями носового слизисто-
мышечного слоя; г — опрокинутый слизисто-надкостничный лоскут ушит с тканями ротового
слизисто-мышечного слоя.
Пластику переднего отдела расщелины при всех современных методиках
осуществляют одним из приемов, предложенных В. И. Заусаевым A953),
Б. Д. Кабаковым A964), Ю. И. Вернадским A964). Передний отдел
расщелины закрывают опрокидывающимся ел изисто-надкостничным лоскутом с
большого фрагмента челюсти или двумя лоскутами, опрокинутыми в сторону
носовой полости. Пластику переднего отдела при сквозных двусторонних
42
Рис. 22.18. Двухэтапная пластика неба с сужением глоточного кольца при
врожденной изолированной (полной) расщелине неба [Фролова Л.Е., 1977]. Второй этап —
пластика в пределах твердого неба с использованием двух перемещенных по
плоскости и одного опрокинутого на область расщелины твердого неба слизисто-надкост-
ничных лоскутов (схема) [Мамедов A.A., 1988].
а — линии разреза; б — отслоены три слизисто-надкостничных лоскута; в —
слизисто-надкостничныи лоскут опрокинут, ушит с тканями носового слизисто-мышечного слоя; г — опрокинутый
слизисто-надкостничныи лоскут закрыт двумя перемещенными по плоскости слизисто-надкост-
ничными лоскутами.
Рис. 22.19. Двухэтапная пластика неба с сужением глоточного кольца при
врожденной изолированной (полной) расщелине неба [Фролова Л.Е., 1977]. Второй этап —
пластика в пределах твердого неба с использованием одного опрокинутого и одного
перемещенного по плоскости и на область расщелины переднего отдела твердого
неба слизисто-надкостничных лоскутов (схема) [Мамедов A.A., 1988].
а — линии разрезов; б— отслоены два слизисто-надкостничных лоскута; в — опрокинутый слизисто-
надкостничный лоскут ушит с тканями носового слизисто-мышечного слоя; г — перемешенный по
плоскости слизисто-надкостничный лоскут ушит с тканями ротового слизисто-мышечного слоя.
расщелинах производят слизисто-надкостничными лоскутами с
межчелюстной кости, которые отслаивают, опрокидывают и сшивают с лоскутами,
отслоенными с краев расщелины. По методике Дубова слизисто-надкостнич-
ный лоскут с межчелюстной кости опрокидывают в сторону расщелины и
перекрывают перемещенными слизисто-надкостничными лоскутами с
боковых фрагментов.
Несмотря на большое число критических замечаний, радикальная
уранопластика продолжает использоваться в клинической практике, а ее
активные сторонники находят аргументы в ее защиту.
Б. Н. Давыдов и Р. Д. Новоселов A997) отмечают недостатки этой
методики в классическом варианте, предложенном А. А. Лимбергом в 1927 г.
Основным недостатком является послеоперационное укорочение неба,
которое происходит вследствие вторичного заживления и рубцового сморщивания
носовой поверхности небных лоскутов. Эта же причина приводит к задержке
развития верхней челюсти, в частности к сужению зубной дуги. Результаты
сужения среднего отдела глотки нестабильны, так как рубцевание в области
рассеченных крыловидных складок и рассепарованных крылочелюстных
пространств приводит к смещению боковой стенки глотки и пластинки
крыловидного отростка в прежнее положение. По мнению авторов,
предложенные в ряде клиник приемы и методика радикальной уранопластики
[Давыдов Б. Н., 1984J дают возможность предупредить эти осложнения. Одним
из необходимых элементов радикальной уранопластики, позволяющим
избежать рубцевания и смещения небных лоскутов, они считают отслойку и
ушивание слизисто-надкостничных лоскутов носовой поверхности небных
отростков. Улучшает результаты и предложенная автором свободная костная
пластика расщелины. Благоприятные результаты достигаются также за счет
исключения мезофарингоконстрикции. По данным Б. Н. Давыдова и Р. Д.
Новоселова, усовершенствованные методы радикальной уранопластики
обеспечивают полноценные анатомические результаты у 92—98 %, а полное небно-
глоточное замыкание в ближайшем послеоперационном периоде — у 71,6—
84,2 % больных. Удовлетворительное восстановление речи после пластики
неба наблюдается в 70—90 % случаев.
Необходимо отметить, что в достижении функциональных результатов
наряду с хирургическими и анатомическими аспектами существенную роль
играет качество до- и послеоперационного логопедического обучения.
Обсуждая приоритеты тех или других методов, следует обратить внимание
на такие аспекты, как возраст, в котором проводится операция, и возможности
формирования речи у начинающего говорить пациента или пациента с
патологическими стереотипами, а также на объем и сложность выполнения
различных методик, что не может не приводить к осложнениям.
На основании анализа 20-летнего опыта лечения врожденных расщелин
губы и неба А. А. Мамедов A996) сделал следующие выводы. Расщелина неба,
не оперированная в возрасте до 5 лет, приводит к компенсаторной гипертрофии
небных миндалин, носовых раковин, корня языка в сторону дефекта неба.
Происходит искривление носовой перегородки, сошника, что компенсирует
дефект, но значительно затрудняет ортодонтическую подготовку к
хирургическому лечению, ухудшает условия логопедического обучения, вследствие
чего увеличиваются сроки медико-социальной реабилитации,
восстановления нормального соматического статуса (дыхание, прием пищи,
профилактика поражения ЛОР-органов и др.), т. е. отсутствуют условия для
правильного всестороннего развития ребенка. Социальные аспекты формирования
личности следует учитывать в раннем ясельном возрасте.
45
Послеоперационный уход. В конце операции тщательно очищают
воздушные пути от крови и секрета. В первые 24 ч ребенок находится в
послеоперационной палате. Его укладывают в положении полулежа, что облегчает
дыхание и выделение секрета из полости рта. При широких полных
расщелинах верхней губы накладывают асептическую защитно-давящую повязку,
которая играет и определенную формирующую роль, различные варианты
валиков. Рекомендуется также наложение пластырных полосок, полосок с
асептическими мазями и ведение раны открытым способом. После операции
на небе на верхнюю челюсть целесообразно надевать защитную пластинку,
которую заранее изготавливает ортодонт. Под нее подкладывают марлевые
салфетки, пропитанные йодоформной жидкостью, на 5—7 дней. Затем для
формирования купола неба наслаивают термопластическую массу.
В носовые ходы на стороне расщелины вставляют индивидуальные
пластмассовые вкладыши, которые изготавливает ортодонт, или резиновые
трубки, обернутые марлей. Вкладыши предупреждают рубцевание и сужение
носовых ходов. Ребенок пользуется ими постоянно в течение 3—6 мес. При
необходимости вкладыши фиксируют через отверстие, проделанное в них
бором, и нитку, которую крепят к коже пластырем.
Перевязки делают ежедневно. Для профилактики осложнений
целесообразно облучение зоны швов лазером в течение нескольких дней. С 1-х суток
применяют магнитолазеротерапию. При открытом ведении раны на
следующие сутки образуются корочки по линии шва, удаление которых при перевязке
болезненно для ребенка и вызывает травму послеоперационной области.
Улучшает результаты применение пленки "Диплен", под которой не образуются
корочки и происходит более нежное рубцевание. Беспокойным пациентам
фиксируют кисти рук или локтевые суставы ("шинирование"). Кормление производят
через шприц с катетером.
Основными осложнениями операций на небе являются остаточные
дефекты, возникающие вследствие нарушения техники операции (натяжение
тканей, грубые манипуляции) или присоединения высокопатогенной флоры
и развития инфекционного процесса, что может закончиться расхождением
швов, некрозом.
По данным ряда авторов, послеоперационные дефекты наблюдаются в 3—
78 % случаев [Заусаев В. И., 1951; Дмитриева В. С, 1964; Лимберг Α. Α., 1967;
ГуцанА. Э., 1982; Самар Э. Н., 1986; Герасимова Л. П., 1997; Мамедов Α. Α.,
1997; Assungar J., 1993; Karling J. et al., 1993].
Небно-глоточная недостаточность может быть обусловлена
объективными анатомическими причинами или неправильным выбором метода, грубым
рубцеванием и т. д. Первичное вмешательство не всегда приводит к
восстановлению функции небно-глоточного кольца. Формирующуюся недостаточность
небно-глоточного затвора классифицируют с учетом анатомических и
функциональных нарушений, чтобы определить причины, которые привели к
формированию небно-глоточной недостаточности, пути реабилитации [Ананян С. Г.,
1985; Герасимова Л. П., 1997; Мамедов Α. Α., 1997].
Выявление и расшифровку небно-глоточной недостаточности следует
проводить с применением эндоскопического обследования пациента,
назальной аэроманометрии, изучением биоэлектрической активности мышц языка и
мягкого неба методом электромиографии, контрастной рентгенографии, а в
ряде случаев и с использованием цефалометрических параметров
небно-глоточного затвора методом компьютерной томографии. Только после
полноценного обследования можно ставить показания к оперативному вмешательству,
которое не всегда эффективно, а нередко и не нужно, так как восстановления
функций можно добиться другими методами.
46
Α. Α. Мамедов A997) отмечает, что причинами небно-глоточной
недостаточности или проявлениями, симулирующими ее, могут быть центральные,
в том числе приобретенные, нарушения на почве ограничений социальной
сферы, упущенное время проведения первичной уранопластики (операция в
возрасте старше 5 лет и как следствие патологические стереотипы речи).
Одним из проявлений небно-глоточной недостаточности служит рино-
лалия, для которой характерен комплекс нарушений артикуляции звуков,
речи и тембра голоса. Неполноценное смыкание небно-глоточного кольца
вследствие утечки воздуха через нос обусловливает патологическое
формирование звуков в носоглотке и глотке. Утечка воздуха из резонаторной зоны
носоротоглотки способствует формированию качественно измененной
воздушной струи, что придает голосу гнусавый оттенок (назальность речи). Дис-
координация функций носо- и ротоглотки делает речь малопонятной.
С. Г. Ананян A989) описал различные формы функциональной и
анатомической компенсации небно-глоточной недостаточности: небно-глоточ-
ную, языкоглоточную, носоглотку малой глубины, гиперплазию лимфоид-
ной ткани носоглотки, гиперплазию небных миндалин и носовых раковин,
искривление перегородки носа. Он выдвинул принципиально важное
предположение о том, что степень выраженности функциональных нарушений у
больных с послеоперационными дефектами неба зависит в первую очередь
от состояния небно-глоточного затвора, компенсаторных возможностей
артикуляционного аппарата и в значительно меньшей мере — от величины и
локализации дефектов неба.
Перед хирургическим вмешательством пациенту в обязательном порядке
проводят курс логопедического обследования и обучения. Это облегчает
последующее восстановление речи и дает возможность прогнозировать результаты.
Операции при небно-глоточной недостаточности. Различные способы
хирургического устранения небно-глоточной недостаточности разработаны
Л. Е. Фроловой A977), Ф. М. Хитровым A984), Г. И. Семенченко A986),
С. Г. Ананяном A993, 1995), А. А. Мамедовым A997).
Хирургические методы устранения небно-глоточной недостаточности
основаны главным образом на создании соединения (перемычки) задней стенки
глотки и мягкого неба (велофарингопластика). Разработано большое
количество модификаций этой операции, предложенной D. Schoenborn A976), с
целью профилактики Рубцовых перерождений перемычки, исключения такого
элемента операции, как отсечение ножки велофарингеального лоскута и др.
[Безруков В. М., 1981; Гунько В. И., 1984, 1986; Оразвалиев А. И., Ермакова И. И.,
1986]. А. А. Мамедов A976, 1977) установил, что подшивание слизисто-мы-
шечного лоскута только к небной занавеске способствует нарушению
анатомической формы и функции небно-глоточного кольца. Этот лоскут является
как бы "преградой в воротах", а боковые стенки глотки не принимают участия
в смыкании. Наличие неестественной преграды приводит к следующим
осложнениям: 1) нарушается проходимость устьев слуховых труб, вследствие чего
возникают воспалительные заболевания среднего и внутреннего уха; 2)
развиваются воспалительные процессы в ЛОР-органах и патологические
изменения в верхних дыхательных путях; 3) снижается острота слуха; 4) слизисто-
мышечный лоскут с задней стенки глотки влияет на проходимость, отток
воспалительного экссудата, слизистого отделяемого из носоглотки, так как
боковые отверстия справа и слева часто слишком узкие.
J. Jackson A988) сообщает о частом развитии апноэ во сне после фарин-
гопластики. Это проявляется ротовым дыханием, храпением, пробуждением
с интервалами ночью, вялостью, отставанием в учебе. В этом случае
необходимо провести тщательное исследование велофарингеальной зоны.
47
Рис. 22.20. Устранение небно-глоточной недостаточности, возникшей при
нарушении подвижности небной занавески (сужение глоточного кольца без отслойки сли-
зисто-надкостничных лоскутов) (схема) [Фролова Л.Е., 1972].
а — расширенное глоточное кольцо; б — пунктиром намечена линия разрезов; в — ткани рас-
сепарованы с образованием двух слизисто-мышечных лоскутов; г — ткани перемещены и ушиты.
А. А. Мамедов A997) отметил, что причиной патологии речи, помимо ана-
томо-функциональной недостаточности небно-глоточного кольца, могут быть
деформации носа, губы, преддверия полости рта, зубочелюстной дуги, неба,
гипертрофия миндалин, языка, патология со стороны ЛОР-органов
(понижение остроты слуха, постоянные воспалительные процессы).
48
Рис. 22.21. Устранение небно-глоточной недостаточности, возникшей при
нарушении подвижности небной занавески (сужение глоточного кольца с отслойкой слизи-
сто-надкостничных лоскутов) (схема) [Фролова Л.Е., 1972].
а — расширенное глоточное кольцо; б — намечены линии разрезов; в — мобилизованы ткани;
г — перемешенные ткани ушиты.
Дефекты речи, обусловленные недостаточностью небно-глоточного
кольца, возникают вследствие нарушения подвижности одной или нескольких его
структур. Это является определяющим при выборе тактики хирургического
вмешательства. В настоящее время разработаны оригинальные методы и
схемы операции для устранения различных видов небно-глоточной
недостаточности (рис. 22.20—22.24).
4-1263
49
Рис. 22.22. Устранение небно-глоточной недостаточности, возникшей при нарушении
подвижности боковой стенки глотки с одной стороны (схема) [Мамедов A.A., 1986].
а — расширенное глоточное кольцо с одной стороны; б — пунктиром намечена линия разреза;
в — мягкие ткани рассепарованы с выкраиванием фарингеального лоскута; г — выкроенный лоскут
подшит к боковой стенке глотки и небной занавеске.
Рис. 22.23. Устранение небно-глоточной недостаточности, возникшей при
нарушении подвижности обоих боковых стенок глотки, способом кисетной фар и нгоп
ластики (схема) [Мамедов A.A., 1996].
а — намечены линии разрезов; б — выкроены фарингеальные лоскуты; в — лоскуты подшиты
к носовому слизисто-мышечному слою тканей небной занавески и боковой стенки глотки; г —
раневые поверхности закрыты ротовым слизисто-мышечным слоем тканей боковой стенки глотки
и небной занавески.
Рис. 22.24. Устранение небно-глоточной недостаточности, возникшей вследствие
рубцовой деформации мягкого неба и крыловидно-челюстных складок.
а — намечены линии разрезов; б — ткани отсепарованы; в — фарингеальные лоскуты подшиты к
тканям боковой стенки глотки и небной занавески; г — ткани перемещены и ушиты.
22.7. Врожденные кисты и свищи мягких тканей
челюстно-лицевой области
К врожденным кистам и свищам лица и шеи относятся образования,
возникающие в результате аномалий развития жаберного аппарата эмбрионального
периода, его производных и щитовидной железы, которые проявляются сразу
же после рождения или в последующие годы. Дермоидные кисты образуются
в тех местах, где в стадии эмбрионального развития находятся щели и
борозды или складки энтодермы.
Для диагностики и разработки хирургической тактики необходимо четко
представлять себе происхождение врожденных кист и свищей.
Согласно данным исследований по эмбриологии, проведенных В. М.
Безруковым A965), в ранних стадиях развития эмбриона человека в головном и
шейном отделах его заключается жаберный аппарат — жаберные дуги, щели и
глоточные карманы. У эмбриона 6,5 нед жаберные щели и глоточные карманы
почти полностью редуцируются или дают начало своим производным (первый
глоточный карман — слуховой трубе, второй — тонзиллярной бухте, третий —
зобной и паращитовидной железам, грушевидным карманам глотки; из первой
жаберной щели образуется наружный слуховой проход). В основном из
второй жаберной дуги формируется наружное ухо, из первой — лишь козелок.
Предушные свищи постоянно обнаруживаются с момента рождения.
Наружное устье их располагается всегда у основания большого завитка ушной
раковины. Свищевой ход направляется между хрящами завитка и козелка,
доходя до наружного слухового прохода. Такое постоянство хирургической
анатомии этих свищей указывает на то, что они являются аномалиями
развития краниального отдела первой жаберной щели.
Кисты и свищи позадичелюстной области располагаются всегда лате-
рально от кивательной мышцы, латерально и близко от общего ствола
лицевого нерва и, как правило, связаны с наружным слуховым проходом. Кисты
и свищи данной локализации выстланы эпителием эктодермального типа —
многослойным плоским ороговевающим.
Указанные топографоанатомические и морфологические особенности
кист и свищей позадичелюстной области дают основание отнести их к
аномалиям развития первой жаберной щели.
Для сопоставления топографии глоточных карманов и жаберных щелей
с хирургической анатомией боковых кист и свищей шеи удобно брать за
основу их отношения к сонным артериям. Эти отношения постоянны, и их
легко проследить как у эмбрионов, так и во время операции. Эмбриологические
исследования показали, что отношения второго и третьего глоточных
карманов с артериями второй и третьей дуг (будущих сонных артерий)
неодинаковы. Второй глоточный карман располагается между этими артериями, а
третий вместе с зачатком зобной железы — дорсально от артерии третьей дуги
(будущей общей сонной артерии).
Боковые свищи шеи, как и второй глоточный карман, локализуются
между внутренней и наружной сонными артериями и открываются внутренним
устьем в области небной миндалины. Эти топографические особенности
боковых свищей шеи, а также их наличие с рождения позволяют считать их
аномалиями развития второго глоточного кармана и второй жаберной щели с
участием шейного синуса. Боковые кисты располагаются непосредственно на
сосудисто-нервном пучке шеи на уровне бифуркации общей сонной артерии.
Эмбриологические исследования показывают, что эти образования
связаны с аномалиями развития второго глоточного кармана и второй жаберной
щели. По происхождению боковые кисты и свищи лица и шеи могут быть на-
53
Рис. 22.25. Больная с воспалительными изменениями кожи в окружности врожденного
предушного свища.
званы бранхиогенными. Однако в связи с различными источниками
возникновения их (первая жаберная щель в одних случаях, вторая жаберная щель с
глоточным карманом — в других) в клинической практике следует различать
кисты и свищи околоушной области и боковые кисты и свищи шеи.
Постоянство хирургической анатомии срединных кист и свищей шеи
(связь их с подъязычной костью и слепым отверстием языка, соответствие
хода полного срединного свища с топографией зачатка щитовидной железы),
а также значительное количество полных срединных свищей
свидетельствуют о том, что источником развития этих образований может быть только
щитовидно-язычный проток. Он выявляется только в ранних стадиях развития
эмбриона и при нормальном развитии в дальнейшем превращается в тяж,
который также полностью редуцируется. Энтодермальный характер
эпителиальной выстилки срединных кист и свищей шеи, обнаружение в их стенке
железистой ткани типа щитовидной железы также подтверждают указанный
источник происхождения. Таким образом, срединные кисты и свищи шеи
являются аномалией развития щитовидно-язычного протока.
Кисты и свищи околоушной области проявляются в основном в детстве
или в первые 2—3 десятилетия жизни.
Предушные свищи. Устье их располагается впереди основания завитка
ушной раковины и малозаметно. Диаметр его около 1 мм. При надавливании
на козелок из свища выделяется салоподобная масса. В области предушных
свищей часто развивается воспаление с образованием абсцессов впереди
козелка. Диагностика не представляет трудностей.
Свищи часто бывают двусторонними. При длительно протекающем
воспалении кожа в окружности свищей мацерируется, краснеет и в дальнейшем
могут возникать грубые деформирующие кожу рубцы (рис. 22.25).
Кисты позадичелюстной области (околоушно-зачелюстные). Локализуются
под задним полюсом или основной массой околоушной слюнной железы.
Для уточнения диагноза большое значение имеют дополнительные методы —
цитологическое исследование пунктата и сиалография. Для цитологической
картины пунктата этих кист типично наличие клеток плоского ороговевшего
эпителия.
54
Кисты располагаются над кивательной мышцей и общим стволом
лицевого нерва и связаны с хрящевым отделом наружного слухового прохода. Эти
топографические отношения постоянны, что имеет значение при
планировании оперативного вмешательства и указывает на источник их происхождения.
Свищи позадичелюстной области образуются при нагноении кист этой
локализации. Наружное устье этих свищей, как правило, располагается между
углом нижней челюсти и передним краем кивательной мышцы. Хирургическая
анатомия свищевого хода сходна с таковой кист позадичелюстной области.
Данные клинического обследования и контрастная рентгенография
позволяют поставить правильный диагноз.
Кисты корня языка. Несмотря на общность происхождения с
остальными срединными кистами шеи, они должны быть выделены в отдельную
группу в связи с особенностями их локализации и клинической картины. Кисты
корня языка, так же как кисты других локализаций, наблюдаются чаще у
больных молодого возраста. Для них характерны воспалительные процессы,
что приводит к нарушению функций дыхания и глотания. Целесообразно
различать три типа кист корня языка: кисты, развивающиеся в сторону дна
полости рта, кисты, локализующиеся впереди надгортанника, и кисты в виде
ампуловидного расширения, находящиеся между слепым отверстием языка
и подъязычной костью. Каждая из этих групп имеет клинические
особенности, обусловливающие характер оперативного доступа. Остальные
срединные кисты шеи, как правило, локализуются вблизи подъязычной кости по
линии шеи и связаны с последней. Наблюдаются также кисты в
подчелюстной области, но связанные с серединой тела подъязычной кости.
При диагностике срединных кист в области корня языка и вблизи
подъязычной кости основываются на данных анамнеза, наличии типичных
клинических симптомов для этих образований. Ценным дополнением к
этому являются цитологическое исследование пунктата и контрастная
рентгенография.
Срединные свищи шеи. Образуются вторично при нагноении кист или
после неполного удаления кист. Лишь неполные внутренние свищи могут
возникать первично (рис. 22.26). Свищевой ход от наружного устья
направляется к середине подъязычной кости и располагается впереди нее, лишь в
редких случаях прободая ее. Огибая верхний край тела подъязычной кости,
свищевой ход по средней линии шеи и кзади под углом 40—45° направляется
к слепому отверстию языка. Нередко обнаруживают ответвления основного
хода свища, в основном выше подъязычной кости.
Боковые кисты шеи. Локализация типична. Они располагаются впереди
средней трети кивательной мышцы (рис. 22.27). Хирургическая анатомия их
также постоянна: верхний полюс кисты находится под задним брюшком
двубрюшной мышцы и шилоподъязычной мышцей, латеральная стенка кист
непосредственно прилежит к внутренней яремной вене на уровне бифуркации
общей сонной артерии.
Кисты обладают всеми признаками доброкачественных опухолей. В связи
с многообразием патологии области шеи диагностика представляет
значительные трудности. Однако на основании типичной локализации и характерных
признаков, свойственных кистозным образованиям, как правило, можно
предположить наличие боковой кисты шеи. Цитологическое исследование
пунктата позволяет уточнить диагноз и является ценным диагностическим
методом. Для цитологической картины боковых кист характерно наличие
зрелых клеток эпителия со слабыми признаками ороговения или без них, а
также значительное количество лимфоцитов. Наличие кристаллов
холестерина непостоянно.
55
Рис. 22.26. Удаление полного
срединного свища шеи (схема).
а — расположение свита (схема); б —
рассечены челюстно-подъязычные B), подбо-
родочно-подъязычные (J), грудиноподъ-
язычные D) мышцы. Резекция участка
подъязычной кости E) вместе с оболочкой
свища (/) (схема); в — больной со
срединным свищом шеи.
Боковые свищи шеи. Могут
образовываться первично или вторично
при нагноении кист. Локализация
наружного устья обычно по среднему
краю грудино-ключично-сосцевид-
ной мышцы. Локализация же
внутреннего устья постоянна — область
верхнего полюса небной
миндалины. Топография свищевого хода
сходна с расположением кист. Над
большим рогом подъязычной кости
свищевой ход направляется
медиально и вверх, проходит между
внутренней и наружной сонными
артериями и оканчивается у
внутреннего устья в области верхнего
полюса небной миндалины.
При диагностике боковых
свищей шеи следует учитывать данные
анамнеза и типичные клинические
проявления. В трудных случаях
можно использовать контрастную
рентгенографию.
Дифференциальную
диагностику врожденных кист и свищей
необходимо проводить со
специфическими процессами и
доброкачественными опухолями, солитарными
метастазами. У детей чаще всего
боковые свищи шеи необходимо
отличать от хронического лимфаденита.
Решающую роль играет пункция с последующим цитологическим
исследованием. Выявляются зрелые клетки эпителия со слабыми признаками
ороговения, а также значительное количество лимфоцитов. Нередко
обнаруживаются кристаллы холестерина. Получение при пункции кисты светлого
опалесцирующего или мутного с примесью гноя содержимого при
воспалении дает право поставить диагноз.
Абсолютными показаниями к операции в любом возрасте являются
функциональные нарушения, систематическое обострение хронического
воспаления в области кисты или свища, быстрый рост кисты, нарушение
формирования лицевого скелета, обусловленное кистой. В остальных случаях
показания к операции относительные.
При кистах корня языка операцию следует производить как можно
раньше, поскольку наличие их влияет на развитие лицевого скелета, а при
нагноении состояние больного ухудшается.
Выбор оперативного доступа зависит от локализации и хирургической
анатомии кист и свищей. Знание указанных выше постоянных
топографических особенностей каждой из выделенных групп позволяет четко
представлять себе объект операции и планировать ее характер.
При срединных кистах и свищах шеи наиболее удобен оперативный
доступ через горизонтальный кожный разрез. Этот разрез обеспечивает хороший
доступ вплоть до корня языка и не оставляет заметных деформирующих
рубцов после операции, что наблюдается при сагиттальных разрезах. При боко-
Рис. 22.27. Ребенок с врожденной кистой
шеи.
57
вых кистах шеи достаточный оперативный доступ дает кожный разрез по ходу
шейных складок. Однако при кистах больших размеров и свищах
предпочтителен разрез по переднему краю грудино-ключично-сосцевидной мышцы,
хотя менее эстетичный, но способствующий наилучшему доступу к
сосудисто-нервному пучку шеи, от которого приходится тщательно отделять
оболочку кисты или свища на большом протяжении.
Основной причиной рецидивов является неполное удаление всего
свищевого хода или первичного свищевого хода и кисты. В связи с
невозможностью в ряде случаев клинически обнаружить полный срединный свищ и
наличие свищевых ходов от кист до слепого отверстия языка возникает
необходимость резекции части тела подъязычной кости с ревизией
вышележащего отдела раны при всех операциях по поводу срединных кист и свищей
шеи. Только при этом условии операция может быть радикальной.
Радикальность операции удаления боковых свищей обеспечивается
иссечением свищевого хода на всем протяжении с удалением участка слизистой
оболочки на боковой стенке глотки. Значительное количество рецидивов можно
объяснить прежде всего отсутствием четкого представления об эмбриогенезе и,
следовательно, хирургической анатомии этих образований, в меньшей
степени — относительной сложностью оперативной техники.
Самым частым осложнением врожденных кист и свищей околоушной
области и шеи является воспалительный процесс. В литературе описаны редкие
случаи развития туберкулезного и актиномикотического процессов в боковых
кистах и свищах шеи. Несмотря на редкость таких наблюдений, их следует
учитывать при диагностике и лечении врожденных кист и свищей. Возможно
возникновение брахиогенного рака на фоне кист этой локализации.
Дермоидные кисты и свищи дна полости рта и носа. Локализуются в
области корня носа, надбровий, по средней линии дна полости рта и шеи, реже
в других отделах (рис. 22.28). Проявляются чаще в детском возрасте. Имеют
овальную форму, мягкую тестоватую консистенцию, располагаются под
кожей или слизистой оболочкой, хорошо подвижны, безболезненны. Растут
медленно. Кисты дна полости рта могут достигать больших размеров,
смещать язык, вызывать расстройство речи. Содержимое кист представляет
собой творожистую салоподобную массу, после воспаления — только гной.
Первичные проявления нередко определяются лишь при воспалении,
поэтому в таких случаях вначале диагностируют флегмону. Последняя
действительно может развиваться на фоне кисты, и тогда требуется соответствующее
лечение.
Дифференциальную диагностику проводят с воспалительными процессами,
опухолями. Дермоидные кисты носа необходимо отличать от врожденных
опухолей, связанных с эндокраниальными структурами, такими как глиомы
и менингоэнцефалоцеле. Такие кисты происходят из эктопированных
остатков эктодермы, которые могут находиться как под кожей, так и в более
глубоких тканях, что и обусловливает их клинические проявления.
Сложностью комплексного развития и отсутствием синхронизации
слияния лицевых отростков объясняется относительная частота
патологических процессов в области носа. Их диагностируют чаще в детстве, но иногда
они не имеют никаких клинических проявлений, пока не увеличатся в
размерах или не инфицируются. Дермоидные свищи являются первичными с
эндодермальной выстилкой. Вначале существуют как узкие отверстия, вокруг
которых кожа вдавлена в средней и нижней трети носа по средней линии.
Иногда в окружности отмечается рост волос. При надавливании или
самопроизвольно выделяется маслянистая жидкость. В случаях обструкции свища
отделяемое может стать гнойным. После воспалительных осложнений могут
58
Рис. 22.28. Свищ носа.
а — расположение врожденного свища в
тканях носа (схема); б — пунктиром
намечен блок удаляемых тканей (схема); в —
больной со свищом носа.
появиться вторичные отверстия,
соединенные с первичным свищом.
Свищ всегда идет вверх и внутрь,
обычно заканчиваясь в
грушевидной полости под костями носа.
Кости носа могут быть деформированы,
отдавлены. Иногда свищ мешает
полному срастанию костей носа.
Свищи могут заканчиваться слепо в
виде тяжа, распространяясь в
глубину до 2 см, и достигать решетчатого
лабиринта.
Лечение хирургическое. Его
необходимо начинать рано, поскольку это
помогает избежать костных
деформаций и воспалительных осложнений.
Проводят разрез в виде эллипса,
окружающий свищ. Предварительно
последний с помощью тупой иглы
наполняют метиленовым синим. Свищ
удаляют полностью с окружающими
перихондральными тканями и
надкостницей. Необходимо удалять не
только сам эпителиальный тракт, но
и всю рубцовую ткань, так как в ней
могут находиться порции
изолированного эпителия.
Удаление дермоидных кист не
представляет сложности, так как
они имеют толстую кожистую
оболочку и обычно не спаяны с окружающими тканями. При удалении кист носа
иногда обнаруживаются ^диагностированные дополнительные кисты, т. е.
первично-множественные (рис. 22.29).
Рис. 22.29. Больной с врожденной кистой
носа.
22.8. Краниофациальные деформации
Анализ результатов реконструктивного хирургического лечения краниофа-
циальных деформаций у детей и взрослых показал, что у большей части
больных анатомо-эстетические изменения сопровождались функциональными
нарушениями (диплопия, высокое внутричерепное давление, затрудненное
дыхание, нарушение акта жевания и др.).
При оценке состояния больного, возрастных показаний к операции,
хирургической тактики, медицинской и социальной реабилитации мы
руководствуемся следующими положениями. Наличие грубых анатомических и
функциональных нарушений является показанием к их хирургической
коррекции. Ранняя коррекция обезображенного внешнего вида положительно
влияет на формирование психики, личности, что создает для больного
равные со сверстниками социальные возможности. Такая коррекция нарушений
позволяет предупредить их усиление и вторичные деформации, а также в
результате восстановления функций создает предпосылки для гармоничного,
полноценного развития организма. Операции в раннем возрасте технически
легче выполнимы вследствие меньшей величины деформации и плотности
60
кости, что сокращает приблизительно в 2 раза время самой операции [Ро-
гинский В. В. и др., 1994].
Воздействие хирургической коррекции на рост лица является спорным
вопросом. Ряд авторов отмечают, что коррекция гипертелоризма не
оказывает вредного влияния на рост челюсти [Tessier Р., 1973; Tulasni Α., 1985; Маг-
chae D., 1989; Salyer К., 1989, и др.]. По их мнению, вмешательства,
совершаемые над уровнем зубов или вне зоны развивающихся зубов, безвредны
для роста и репозиция способствует перестройке аномальных сегментов че-
репно-лицевого скелета в ранний период, что дает преимущество при
дальнейшем росте и развитии. Остеотомия верхней и нижней челюсти в зубо-
содержащих зонах должна быть отсрочена до прорезывания постоянных
зубов. С этой целью в возрасте 5—10 лет при синдромах лицевых расщелин
проводят ортодонтическое лечение для стимуляции роста. Однако есть
мнение, что оперативное вмешательство может препятствовать росту лица,
поэтому его следует отложить до позднего пубертатного периода [Mulliken Α. et
al, 1986].
К л иническая картина, диагностика. При диагностике че-
репно-лицевых аномалий и планировании оперативного вмешательства
необходим мультидисциплинарный бригадный подход с обязательным
привлечением к оценке состояния пациента, помимо челюстно-лицевого хирурга,
радиолога, невропатолога, психоневролога, офтальмолога, отоларинголога,
анестезиолога, нейрохирурга. Важнейшим принципом бригадного подхода
являются сбор всеобъемлющей информации о пациенте, выявление
аномалий.
В лучших мировых черепно-лицевых центрах формируются команды из
15—20 различных специалистов по медицине, стоматологии и
вспомогательного медико-стоматологического персонала. Объединенные усилия по
лечению, уходу за пациентами с комплексными поражениями дают
наилучший эффект.
Существуют стандартизованные многопространственные
рентгенологические измерения, которые характеризуют пропорции и положение челюстей
и основания черепа. Эти исследования могут быть проведены в любом
возрасте и отражают особенности деформации и лечения. На основании
созданной модели составляют план операции.
Развитие компьютерной томографии повысило диагностические
возможности рентгенологии, в том числе при черепно-лицевых деформациях.
Она позволяет диагностировать объемные процессы головного мозга и сочетан-
ные пороки развития ЦНС, определять содержимое мозговой грыжи.
Возможность сделать фронтальные и аксиальные срезы, чтобы выявить соотношение
мозгового и лицевого скелета, способствует диагностике и планированию
хирургического лечения. Более поздние компьютерные программы
разработаны для создания трехмерных пространственных изображений из
сканированных пространственных данных, полученных при компьютерной томографии.
Трехпространственный визуальный эффект этих изображений оказал
большое влияние на диагностику и лечение таких комплексных черепно-лицевых
деформаций, как лицевые расщелины. Диагностика с помощью ядерного
магнитного резонанса позволяет получать дополнительную информацию о
взаимоотношениях мягких тканей при синдромах лицевых расщелин.
В настоящее время разрабатываются новые программы компьютерного
обеспечения, которые помогут улучшить результаты реконструирования че-
репно-лицевого скелета. Эти системы будут производить точный объемный
геометрический анализ с целью предоперационного планирования лечения
и послеоперационной оценки состояния пациентов со сложными деформа-
61
циями. Создается база цефалометрических данных, полученных из трехпро-
странственных компьютеризированных реконструкций. Прогрессу в
реконструкции черепно-лицевого скелета способствует развитие аллопластических
материалов. Уже выполнены имплантаты с помощью компьютера, точно
совпадающие с размерами дефекта черепа, определенного при трехпространст-
венной компьютерной реконструкции. Однако реконструкция мягких тканей
остается важнейшей проблемой, которую предстоит разрешить. Культура
тканей больших объемов кожи и методы тканевого растяжения являются
многообещающими в этой области [Salyer К., 1989].
Проводимое по полной схеме неврологическое обследование включает
исследование общемозговых и менингеальных симптомов, высших корковых
функций и функций черепных нервов, двигательной активности
конечностей и туловища, поверхностных и глубоких рефлексов, чувствительности и
состояния вегетативной нервной системы. Помимо основных методов
исследования, применяют дополнительные: электроэнцефалографию,
позволяющую оценивать функциональное состояние головного мозга, и эхоэнце-
фалографию, выявляющую структурно-дислокационную внутричерепную
патологию.
Основная задача психоневролога в качестве члена черепно-лицевой
бригады заключается в определении задержки психического развития,
выявлении олигофрении или другого психического заболевания.
Обязательными являются изучение функций зрительного анализатора
(острота и поле зрения, цвето- и светоощущение), определение клинической
рефракции и бинокулярного зрения, исследование подвижности глазных яблок
и их положения в глазнице, а также органов слезоотведения. Контакт пациента
с черепно-лицевой патологией, сопровождающейся орбитальным гипертело-
ризмом (ОГ), и офтальмолога не заканчивается на дооперационном этапе.
Следует осуществлять контроль в динамике послеоперационного периода.
Коррекцию часто встречающегося у пациентов с ОГ косоглазия следует
проводить после основной операции.
Нередко отмечаемые у пациентов с врожденной черепно-лицевой
патологией аномалии наружного слухового прохода, атрезии носовых ходов,
искривление носовой перегородки, инфицирование придаточных пазух носа
являются показанием к тщательному отоларингологическому
обследованию.
Хотя деформации зубочелюстной системы не имеют прямой связи с
коррекцией ОГ, ортодонт осматривает всех пациентов с нарушениями прикуса
и совместно с черепно-лицевым хирургом определяет порядок и характер ор-
тодонтического лечения.
Анестезиолог является одним из важнейших членов бригады, так как
непосредственно участвует в операции. С анестезиологической точки зрения,
к недостаткам коррекции ОГ внутричерепным доступом следует отнести: 1)
повышение внутричерепного давления (наиболее часто при краниосиностозах);
2) значительную кровопотерю; 3) большую продолжительность и травматич-
ность вмешательства; 4) опасность воздушной эмболии.
Проводимое накануне операции объективное обследование органов и
систем, изучение ЭКГ, результатов общих анализов крови и мочи,
биохимических исследований позволяют судить о состоянии пациента и определить
степень анестезиологического риска.
Нейрохирург проводит осмотр совместно с челюстно-лицевым хирургом
на заключительном этапе обследования пациента. Выявленные аномалии
(мозговые грыжи, краниосиностозы) тщательным образом оцениваются и
избирается оптимальный вариант проведения вмешательства.
62
22.9. Хирургическое лечение черепно-лицевых деформаций
Самые сложные случаи деформации требуют комплексной хирургической
коррекции, которая является наиболее эффективной при использовании
комплексного интра- и экстракраниального подхода квалифицированным
нейрохирургом и челюстно-лицевым хирургом. Лечение должно быть
тщательно спланировано для каждого пациента в индивидуальном порядке и
проведено в крупном центре специалистами широкого профиля, имеющими
опыт лечения сложных нарушений.
При внутричерепных вмешательствах кости черепа служат лучшим
пластическим материалом. Резорбция пересаженных костей черепа меньше, чем
тканей, взятых с донорских участков длинных костей. Кости черепа могут
быть использованы для трансплантации на дно глазницы и при синдромах
лицевой, глазничной и носовой расщелины [Бельченко В. В., 1988; Salyer К.,
1989].
В случае необходимости получения больших участков для
трансплантации используют подвздошную кость. Для замещения больших дефектов
требуются подвздошная, реберная и(или) черепные кости.
Остеотомия по Ле Фор I, II, III и сегментарные перемещения,
выполняемые одновременно как различные новейшие модификации, могут быть
необходимы при хирургической коррекции лицевых деформаций. В этих
случаях часто производят пересадку кости или других материалов (титан,
углепластики) для достижения фиксации и придания формы остеотомированным
областям. Методы фиксации включают формирование костной опоры,
межкостное шинирование, плоскостную и винтовую фиксацию, внутричелюст-
ную фиксацию и черепное подвешивание.
Результаты, полученные при лечении больных с синдромами расщелин,
не так хороши, как при синдромах черепных сращений [Salyer К., 1989].
Выраженное отсутствие мягких и твердых тканей, комбинированное с
различными асимметричными диспропорциями, ставят эту группу деформаций в
ряд наиболее сложных групп для достижения совершенства.
У детей младшего возраста степень осложнений ниже, чем у детей
старшего возраста.
В понятие "лицевые расщелины", которые захватывают верхнюю челюсть,
скуловую кость и нижнюю челюсть, включаются синдром Тричера —
Коллинза, гемифациальная микросомия и многие другие родственные синдромы.
Синдром Тричера — Коллинза наследуется по аутосомно-доминантному типу.
Он характеризуется гипоплазией скуловой кости с расщелиной скуловерхне-
челюстного шва. Латеральные углы глаз смещены вниз, в результате чего
развивается антимонголоидный наклон фиссуры век. Имеют место колобомы или
дефицит нижних век. Возможны ушные деформации, гипоплазия нижней
челюсти, высокая арка неба.
Гемифациальная микросомия — это синдром, появляющийся в
результате расщелины или дефекта в развитии первой и второй жаберных дуг.
Тяжесть деформации различна, но первично в процесс вовлекаются ухо и нижняя
челюсть. Могут наблюдаться также врожденный паралич лицевого нерва и
гипоплазия мягких тканей и жевательных мышц. Тяжесть деформации
наружного уха не связана с функцией слуха. Однако существует прямое соотношение
между тяжестью ушных и нижнечелюстных деформаций. Асимметрия
скелета характеризуется отклонением подбородка в пораженную сторону и, кроме
того, высоким окклюзионным наклоном также на стороне поражения.
Одной из актуальных и сложных проблем пластической хирургии
является устранение полных и частичных дефектов ушной раковины. Врожден-
63
Рис. 22.30. Микроотия II степени, атрезия слухового прохода.
а — больной 8 лет до операции; б — тот же больной после первого этапа пластики уха
(формирование ушной раковины аллохрящом и перемещение мочки уха); в — после второго этапа
пластики ушной раковины расщепленным кожным лоскутом с бедра (вид спереди); г — вид сзади.
ная деформация ушной раковины имеет различные анатомические
варианты, коррекция которых представляет определенные трудности.
Наиболее интенсивный рост ушной раковины наблюдается в первые
5 лет жизни. Уже на 2-м году можно производить оперативные
вмешательства по перемещению атипично расположенной мочки уха и рудимента
ушной раковины. Это дает детям возможность уже в раннем возрасте начать
адаптироваться в обществе. В 5 лет можно приступать ко второму этапу
пластики ушной раковины — моделированию каркаса из алло- или аутогенного
хряща и имплантации его под кожу сосцевидной области. В 6 лет формируют
заднюю поверхность ушной раковины свободным расщепленным кожным
лоскутом с плеча или бедра (рис. 22.30, 22.31).
Метод реконструкции ушной раковины с использованием височно-те-
менного артериализированного фасциального лоскута дает возможность
сократить число этапов и сроки лечения. Лоскут представляет собой
полноценное пластическое и биологическое покрытие для хрящевого каркаса и
благоприятной основой для приживления свободного кожного
трансплантата. Необходимым условием является наличие пульсации поверхностной
височной артерии, отчего зависит жизнеспособность лоскута. Лоскут, впервые
описанный Ohmori A978), — это фасциальный листок с тонкой прослойкой
жировой клетчатки, располагающийся под подкожной жировой клетчаткой
височной области. Питание осуществляется за счет поверхностных височных
артерий и вены, которые проходят в межфасциальной клетчатке лоскута. При
тяжелых формах синдрома 1—2-й жаберной дуги выявляются изменения
анатомического расположения или отсутствие поверхностных височных
сосудов. В этой ситуации нецелесообразно использовать фасциальный лоскут.
Необходимо отметить, что при всех способах пластики ушной раковины
с использованием собственных тканей, их комбинации с аллогенными
материалами дают большой процент осложнений. Основные из них:
рассасывание аллохрящей, некроз кожи вследствие ее натяжения над
сформированным каркасом ушной раковины, нагноение трансплантата. В последнее
время, как в нашей стране, так и за рубежом все больше хирургов при аплазии
ушной раковины используют эндопротезы.
В одних случаях лицевых расщелин показана контурная пластика, а в
других — устранение дефекта, в том числе срединных расщелин, связанных
с энцефалоцеле, где отмечается дефицит тканей (рис. 22.32). К. Salyer
рекомендует костную пластику верхнечелюстной альвеолярной расщелины
осуществлять после прорезывания клыков. Предпочтительнее губчатая кость. По его
мнению, она не препятствует движению и прорезыванию зубов и
стимулирует продукцию кости в соответствии с движением зубов.
Остеотомию производят после прорезывания постоянных зубов. Часто
коррекция синдромов расщелин требует ортодонтического лечения.
При краниостенозе операции выполняют в возрасте от 1 мес до 7 лет по
методике реконструкции лобной кости [Ананов М. В., 1995]. При сочетании
краниостеноза с другими видами патологии применяют расширенные
реконструктивные операции. Анализ результатов лечения больных с краниостено-
зами позволяет сделать вывод, что реконструктивные операции следует
производить в течение 1-го года жизни ребенка, оптимально в 3 мес, когда
происходит наиболее бурное увеличение объема мозга. При ранней
хирургической коррекции можно избежать развития в дальнейшем более грубой кра-
ниофациальной деформации.
Для лечения больных с различными формами краниостеноза
предложены модификации классических методик (рис. 22.33—22.35) [Ананов М. В.,
19951.
5-1263
65
Рис. 22.31. Дермоидная киста ушной раковины, аплазия ушной раковины, предуш-
ный свищ: открывающийся в глотку, правосторонняя аплазия мягкого неба,
недоразвитие нижней челюсти справа, синдром 1—2-й жаберных дуг.
а — больная 4 лет до операции; б — та же больная после удаления дермоидной кисты со свищом;
в — после первого этапа пластики ушной раковины аллохрящом; г — после второго этапа пластики
ушной раковины расщепленным кожным лоскутом с бедра.
При лобной плагиоцефалии (односторонний коронарный синостоз) на
первом этапе производят трепанацию в лобной области на стороне
поражения.
Второй этап — выпиливание супраорбитального блока на стороне
поражения. Нижний распил проходит через лобно-носовой и лобно-скуловой
швы, а также основание черепа. Супраорбитальный блок выпиливают с
заходом в височную область (по типу "костного замка") для последующей более
надежной фиксации. При помощи внутренних насечек и специальных щип-
66
i -
. :ь
ЯМ
Рис. 22.32. Врожденная срединная расщелина нижней губы, нижней челюсти,
эмбриональный рубцовый тяж шеи, дермоидная киста дна полости рта.
а — больная 4 лет до операции; б — та же больная после двух этапов операции (первый —
пластика расщелины нижней губы, удаление дермоидной кисты и рубцового тяжа; второй —
пластика расщелины нижней челюсти аутотрансплантатом); в — рентгенограмма нижней челюсти
до костной пластики; г — рентгенограмма нижней челюсти через 3 года после костной пластики.
5*
Рис. 22.33. Фронтомаксилоорбитальная остеотомия и выдвижение при синдроме
Крузона (схема).
а — пунктиром намечены линии остеотомии; б — перемещение фрагментов.
цов с изогнутыми браншами формируют необходимый изгиб
супраорбитального блока в соответствии с противоположной стороной (рис. 22.36, а).
После этого смоделированный фрагмент супраорбитального блока выдвигают
до достижения симметрии с непораженной стороной и фиксируют
проволочными швами в этом положении (рис, 2236, б). Необходимо отметить, что
в течение 1-го года жизни, когда рост мозгового скелета происходит наиболее
бурно, не следует производить жесткую фиксацию супраорбитального блока.
В этом случае формируют так называемый плавающий лоб с фиксацией лишь
в области лобно-носового и лобно-скулового швов.
Третий этап — реконструкция лобной кости. Существующие методики
не дают возможности максимально смоделировать кривизну лобной кости и
сформировать лобный бугор на пораженной стороне. Предлагаемая методика
реконструкции лобной кости позволяет смоделировать наиболее
приближенную к физиологической кривизну лобной кости и сформировать лобный бугор
на стороне поражения. Преимущество методики заключается в ее простоте.
Нет необходимости заниматься сложной реконструкцией уплощенного
участка лобной кости. Путем лишь одного распила можно достигнуть
удовлетворительного косметического результата, что значительно сокращает время
операции.
Уплощенный участок лобной кости распиливают на фрагменты 1 и 2.
Линию распила устанавливают путем сопоставления уплощенной лобной
кости с уже смоделированным и зафиксированным супраорбитальным
блоком. С целью формирования лобного бугра на стороне поражения
фрагменты 1 и 2 фиксируют друг к другу внакладку (рис. 22.36, в). После этого
оба фрагмента фиксируют к супраорбитальному блоку (рис. 22.36, г). За
счет фронтоорбитального выдвижения на стороне синостоза формируют
коронарный шов.
68
Рис. 22.34. Фронтосупраорбитапьная остеотомия и выдвижение при краниофациаль-
ном дизостозе (схема) [Marchac D., 1989].
а — намечены линии остеотомии; б, в — произведено выдвижение лобно-орбитального блока.
Хирургическое лечение больных
с синдромом Крузона проводят в два
этапа: первый — фронтоорбиталь-
ное выдвижение, второй —
остеотомия верхней челюсти с
выдвижением по Ле Фор III. Операции
выполняют в возрасте с 4—5 лет
(рис. 22.37) [Kaban L., 1986].
Проведенная в ЦНИИС работа
свидетельствует о возможности
ранних краниофациальных операций, а
отдаленные (до 8 лет) как анатомо-
эстетические, так и функциональные
результаты дают основание считать
часть больных полностью
реабилитированными.
В последние несколько лет
бурное развитие получили дистрак-
Рис. 22.35. Фронтосупраорбитальная остео- ционные методы лечения больных с
томия с образованием костного замка деформациями лицевого скелета.
(схема). Конгресс Европейской
ассоциации краниофациальных хирургов
(EACMFS), проходивший в Париже в 1997 г., был полностью посвящен этой
проблеме. Этот вопрос обсуждался также на XIV конгрессе EACMFS
(Хельсинки, 1998). Предложены десятки дистракционных и дистракционно-компрес-
сионных аппаратов для перемещения практически всех отделов лицевого и
мозгового черепа. Многими хирургами [Рогинский В. В. и др., 1999; Polley J.,
1995; Cohen S., 1995; Chin Μ., Toth В., 1997; Yamamoto Η. et al., 1997;
Monaster^ F. et al., 1997; Puelacher W. et al., 1998; Liou E., 1998; Karakasis D., 1998]
получены хорошие результаты. Реальностью становится возможность более
щадящими методами добиваться необходимых результатов.
Наибольшей сложностью отличаются оперативные вмешательства при
синдромах Крузона и Аперта. Первый, как правило, сочетается с двусторонним
коронарным синостозом. За счет компенсаторного роста черепа в области
сагиттального и метопического швов развивается характерная "башенная" форма
черепа с резко выраженным двусторонним экзофтальмом. Помимо этого, для
синдрома Крузона характерна гипоплазия верхней челюсти с грубым
нарушением прикуса.
Хирургическое лечение детей как с синдромом Крузона, так и с
синдромом Аперта осуществляют в два этапа, последовательность которых
определяет хирург. Один из этапов — фронтоорбитальное выдвижение с двух сторон,
другой — остеотомия верхней челюсти с выдвижением по Ле Фор III. Впервые
операция была описана P. Tessier A967). Ее производят с целью устранения
гипоплазии верхней челюсти и восстановления прикуса, а также для
устранения экзофтальма за счет выдвижения нижнего края глазниц и увеличения
их объема. Наиболее благоприятный возраст для операции 4—5 лет.
Специальная пластина, изготовленная ортодонтом перед операцией, позволяет
фиксировать верхнюю челюсть к нижней в положении правильного прикуса после
остеотомии и выдвижения. Для остеотомии используют осцилирующую
электропилу. Линия остеотомии проходит по линии лобно-носового шва, затем
кзади, к слезному гребешку, и вниз вдоль нижнего края глазницы. Распил
продолжают вверх, вдоль латерального края орбиты и заканчивают на уровне
лобно-скулового шва. При помощи долота через вертикальную пластинку ре-
70
Рис. 22.36. Выпиливание супраорбитального блока с перемещением (схема).
а — формирование изгиба; б — выдвижение супраорбитального блока; в — реконструкция лобной
кости; г — фиксация реконструированной лобной кости.
шетчатой кости и сошник в сторону ротовой полости, кзади от твердого неба
осуществляют остеотомию. После распилов при помощи щипцов Рове
производят "надламывание" задней стенки верхней челюсти, ее выдвижение и
фиксацию в положении правильного прикуса к нижней челюсти через ранее
описанную пластину. Затем при помощи микропластин и микрошурупов
верхнюю челюсть уклепляют в области переносицы и латеральных стенок
обеих глазниц. Как правило, жесткая фиксация верхней челюсти к нижней
длится от 4 до 6 нед, после чего пластину удаляют. В последнее время для
выдвижения верхней челюсти применяют дистракцию.
Среди детей, страдающих краниостенозом, немалую группу составляют
больные с тригоноцефалией или метопическим синостозом (рис. 22.38).
Реконструкцию производят по методике, предложенной D. Marchak A989).
71
Рис. 22.37. Второй этап реконструкции — остеотомия по Ле Фор III и выдвижение
верхней челюсти (схема).
а — отрыв и перемещение верхней челюсти; б — фиксация верхней челюсти в новой позиции.
При диагностике данной формы частичного краниостеноза необходима
компьютерная томография.
К опасным осложнениям после краниофациальных операций следует
отнести ликворею, воздушную эмболию, нагноение ран. Ликворею у всех
больных ликвидируют обычными мероприятиями (наружное люмбальное
дренирование, дегидратационная терапия).
Краниофациальные операции у детей еще не получили должного
развития. Накопленный опыт позволяет рекомендовать шире производить их у
детей раннего возраста. В нашей стране единственным показанием к
оперативному вмешательству при краниостенозе являлось наличие внутричерепной
гипертензии. Хирургическое лечение ограничивалось лишь двусторонней
лоскутной краниотомией. Операция позволяла сохранить больному зрение,
Рис. 22.38. Преждевременно стенозиро-
ванный коронарный шов (отмечен
пунктиром) (схема).
а — вид сверху; стрелками указано
направление компенсаторного роста в области
сохранных швов (сагиттального, ламбдовидного); б —
башенный череп (вид спереди).
Рис. 22:39. Односторонняя пла-
гиоцефалия.
а — больной 5 мес до операции; б —
тот же больной после операции.
?*
t %
Рис. 22.40. Плагиоцефалия.
а — больной 5 лет до операции; б —
тот же больной после операции.
Рис. 22.41. Тригоноцефалия.
а — ребенок 11 мес до операции. Характерная килевидная деформация лобной кости; б — тот
же больной после реконструктивной операции; в — компьютерная томограмма до операции; г —
после фронтоорбитальной реконструкции.
Рис. 22.42. Фронтоорбитальная
реконструкция при тригоноцефалии (схема).
а — линии предполагаемых распилов; б —
деформированная крыша черепа до
реконструкции (вид сверху); в — внутренние насечки суп-
раорбитального блока и его реконструкция с
восстановлением физиологической кривизны;
г — фиксация реконструктивных блоков.
однако не избавляла от грубых кра-
ниофациальных уродств, которые,
как правило, наблюдаются при
различных формах частичного кранио-
стеноза, в основном не
сопровождающихся внутричерепной гипертензией.
В настоящее время показания к
хирургическому лечению краниосте-
ноза расширены. Абсолютным
показанием является наличие признаков внутричерепной гипертензии.
Реконструктивная операция, произведенная в первые месяцы жизни,
позволяет избежать дальнейшего усиления деформации, особенно в течение
1-го года жизни, когда происходит максимальное увеличение объема мозга.
Кроме того, выполнение реконструктивной операции в раннем возрасте
избавляет ребенка от психологической травмы и обеспечивает нормальную
социальную адаптацию детей в окружающем их обществе (рис. 22.39 — 22.42).
22.10. Орбитальный гипертелоризм
Орбитальный гипертелоризм (ОГ) является нередким проявлением
врожденных пороков развития черепно-лицевой области, однако статистика
встречаемости ОГ в популяции отсутствует, так как он сопровождает разнородные
в этиологическом и патогенетическом отношении процессы, которые в свою
очередь не всегда характеризуются ОГ.
ОГ выраженной степени встречается реже такового слабой или умеренной
степени, но именно у пациентов с выраженным ОГ наблюдаются
манифестные клинические проявления, осложняющиеся неблагоприятными
психосоциальными факторами. Таким пациентам необходимо проводить коррекцию
фенотипа с использованием внутричерепных методик, что является мощным
фактором операционной агрессии и может повлечь за собой тяжелейшие
осложнения вплоть до летального исхода.
История коррекции ОГ внутричерепным доступом насчитывает около
трех десятилетий (впервые операция была произведена выдающимся
французским хирургом P. Tessier в 1963 г.), но внимание мировой медицинской
общественности к этой проблеме не ослабевает, что связано со сложностью полной
реабилитации пациентов, а также с совершенствованием хирургических
методик. В отечественной хирургии основной вклад в изучение данной патологии
и совершенствование оперативных методик внесли В. М. Безруков, В. П.
Ипполитов, В. В. Рогинский, М. В. Ананов, Г. В. Мешков, В. В. Бельченко,
Н. М. Хелминская, С. М. Кочанов.
ОГ — врожденное состояние и всегда остается вторичным по отношению
к основной патологии (срединные черепно-лицевые расщелины, синципи-
тальные мозговые грыжи, краниостенозы, фронтоназальная дисплазия, ос-
теохондродисплазия). Описано формирование ОГ вследствие опухолей интер-
75
Рис. 22.43. Пространственное изображение на муляже круговой остеотомии глазниц
с перемещением [Salyer К., 1989].
орбитального пространства, фиброзной дисплазии и в качестве казуистики в
результате травмы.
Под ОГ понимают увеличенное расстояние между глазницами и
следовательно между глазными яблоками, за счет увеличения элементов решетчатого
лабиринта. В большинстве случаев расстояние между каналами зрительных
нервов остается в пределах нормы. Частой аномалией является положение
решетчатой кости на 15—20 мм ниже уровня передней черепной ямки. ОГ
можно характеризовать по:
1) виду основной патологии (краниосиностозы, черепно-лицевые
расщелины, мозговые грыжи);
2) величине интерорбитального расстояния (ИОР). Tessier A972)
классифицирует ОГ в зависимости от интерорбитального расстояния: I степень —
30—34 мм, II степень — 34—40 мм, III степень — > 40 мм. Это расстояние
может быть точно измерено. У взрослых оно в среднем равно 24—32 мм. Эта
дистанция увеличивается у женщин до 13 лет, у мужчин — до 21 года;
3) стороне (или сторонам) поражения;
4) форме интерорбитального пространства: прямоугольной,
клиновидной с сужением в заднем отделе, овальной, клиновидной с сужением в
переднем отделе.
При исследовании краниограмм в разных проекциях наиболее точно
определяют величину интерорбитального расстояния, состояние основания
черепа и швов свода черепа, положение пластинки решетчатой кости, состояние
околоносовых пазух, наличие дефектов костей черепа, а также
рентгенологические признаки повышенного внутричерепного давления (рис. 22.43).
Оперативные способы коррекции орбитального гипертелоризма
внутричерепным доступом [Мешков Г. В., 1993]. Общие хирургические
принципы. Операция состоит из двух этапов: 1) нейрохирургического,
обеспечивающего оперативный доступ к структурам основания черепа и
костям лицевого скелета со стороны передней черепной ямки и включающего ряд
самостоятельных оперативных приемов; 2) черепно-лицевого (основного),
включающего как непосредственно костно-реконструктивную операцию, так
76
и дополнительные вмешательства на мягких тканях, которые представляются
весьма важными, если учесть существенную роль состояния мягкотканных
структур в достижении адекватного эстетического результата.
В целом операция заключается в: 1) костно-пластической трепанации
черепа в лобной области; 2) субтотальной резекции лобно-носорешетчатого
комплекса; 3) круговой остеотомии и перемещения глазниц с костной пластикой
дефектов в области боковых стенок глазниц; 4) двусторонней трансназальной
медиальной кантопексии. Наряду с этим по показаниям производят: 1) ремо-
дулирующую краниопластику лобной кости при фронтальной плагиоцефалии;
2) иссечение грыжевого выпячивания вещества мозга, реконструкцию твердой
мозговой оболочки и костных структур при мозговых грыжах и черепно-ли-
цевых расщелинах; 3) коррекцию вертикальной дистопии глазницы при
асимметричном орбитокраниальном дизморфизме; 4) реконструкцию кост-
но-хрящевого отдела носа при деформации последнего.
Операцию выполняют под эндотрахеальным наркозом с интубацией через
рот. На операционном столе пациент находится в положении на спине; голова
и спина на одном уровне. Накануне операции волосы на голове сбривают
полностью или частично в виде полосы шириной 2—2,5 см. В конъюнктивальные
ложа вводят 1 % синтомициновую эмульсию, линию кожного разреза намечают
раствором бриллиантового зеленого. Операционное поле двукратно
обрабатывают 1 % раствором йодоната и обкладывают стерильным операционным бельем.
Остеотомию черепно-лицевого скелета производят с помощью
хирургической пилы с электроприводом (при непрерывном орошении зоны
вмешательства изотоническим раствором натрия хлорида во избежание некроза кости),
а также остеотомов. При остеотомии структур передней черепной ямки
особое внимание обращают на ретракцию лобных долей головного мозга,
которую следует проводить как можно менее травматично, исключая давление на
ткани мозга (рис. 22.44—22.47).
Врожденные и операционные дефекты костных структур замещают с
применением костной пластики. В качестве костно-пластического материала
применяют аутотрансплантаты из фрагмента лобной кости, взятого при
краниотомии. С помощью хирургической пилы с электроприводом и остеотомов
фрагмент лобной кости через губчатое вещество расщепляют на наружную и
внутреннюю кортикальные пластинки по всей площади или частично, после
чего из внутренней пластинки формируют трансплантаты требуемых формы
и размера, а наружную возвращают на место по завершении
реконструктивного этапа. Другим источником костно-пластического материала являются
аутотрансплантаты из костных структур интерорбитального пространства,
резецируемых при этмоидэктомии. Остеотомированные фрагменты глазниц и
костных трансплантатов фиксируют с помощью проволочных швов или
мини-пластин с закреплением последних шурупами.
Оперативные приемы при коррекции ОГ внутричерепным доступом
различны. Целесообразнее скелетировать подлежащие остеотомии структуры
лицевого скелета непосредственно после отделения кожно-апоневротиче-
ского и надкостничного лоскутов лобно-теменных областей, т. е. до
краниотомии. В этом случае сокращается время, в течение которого головной мозг
остается "открытым", в результате чего снижается вероятность травматизации
(при надкостничном обнажении структур лицевого скелета) и
инфицирования мозговых оболочек.
Оперативный доступ к основанию черепа является сложным, так как
проникновение к его структурам возможно лишь после вмешательства на
своде черепа. При коррекции ОГ внутричерепным доступом применяют
классический нейрохирургический трансвенечный разрез кожи, проводимый
77
Рис. 22.44. Скелетирование свода чере- Рис. 22.45. Коррекция орбитального гипер-
па, верхней и средней зон лица транс- телоризма внутричерепным доступом. По-
венечным доступом (схема). казаны линии остеотомии черепно-
лицевого скелета (схема).
Рис. 22.46. Коррекция орбитального ги- Рис. 22.47. Коррекция орбитального гиперте-
пертелоризма внутричерепным доступом, лоризма внутричерепным доступом. Состояние
Состояние после субтотальной резекции после аппозиции глазниц, фиксации остеото-
лобно-носорешетчатого комплекса и мированных фрагментов и введения костных
круговой остеотомии глазниц. Ретракция аутотрансплантатов между боковыми стенка-
лобных долей головного мозга (схема), ми глазниц и большими крыльями основных
костей (схема).
между лобными и теменными ветвями поверхностных височных артерий.
Рассечение тканей продолжают в плоскости между надкостницей и
сухожильным "шлемом" после предварительной гидросепаровки изотоническим
раствором натрия хлорида, который вводят в рыхлую клетчатку,
расположенную между указанными образованиями. После остановки кровотечения
формируют скальпированный лоскут с основанием у надглазничных краев,
состоящий из кожи, подкожной жировой клетчатки и сухожильного "шлема".
Надкостницу лобно-теменных областей рассекают по форме раны, отделяют
от костей свода черепа и укладывают вместе со скальпированным лоскутом.
Выделение изолированного надкостничного лоскута имеет принципиальное
значение, так как впоследствии он может быть использован для пластики
твердой мозговой оболочки и при реконструкции костных образований.
Следующим этапом является костно-пластическая трепанация черепа,
производимая по канонам нейрохирургии. При краниосиностозах вследствие
повышенного внутричерепного давления изменяется внутренний рельеф
костей свода черепа, что проявляется чередованием вдавлений и выбуханий
костной ткани, а также образованием шипов, в области которых наблюдаются
сращения внутренней пластинки с твердой мозговой оболочкой. При отделении
костного лоскута возможно травмирование твердой мозговой оболочки в
указанных местах с образованием дефектов последней, в том числе в области
верхнего сагиттального синуса, чему сопутствует значительное кровотечение.
При черепно-лицевых расщелинах, не сопровождающихся пролабиро-
ванием вещества мозга, отмечаются рубцовые спаяния между твердой
мозговой оболочкой и надкостницей в области дефекта. При краниотомии
надкостницу и твердую мозговую оболочку необходимо отделить от костной ткани
по краям дефекта во избежание осложнений, описанных выше. При наличии
грыжевого выпячивания вещества мозга в области черепно-лицевой
расщелины или первичной мозговой грыжи методика операции не отличается от
таковой интракраниального вмешательства (экстра- или интрадурального),
производимого по поводу менингоэнцефалоцеле.
Нижняя граница краниотомии может изменяться в зависимости от
способа коррекции ОГ (см. раздел "Оперативные приемы").
Выделение структур основания черепа в области передней черепной ямки
достигается посредством ретракции лобных долей головного мозга. При
краниосиностозах костные шипы могут локализоваться не только в области свода
черепа, но и в области его основания, что необходимо учитывать при
отделении твердой мозговой оболочки от глазничной поверхности лобной кости,
пластинки решетчатой кости и больших крыльев основной кости. При
наличии назоэтмоидальных и назоорбитальных мозговых грыж ретракция
лобных долей сопровождается отделением твердой мозговой оболочки от костной
ткани по краям дефектов. По показаниям производят пластику твердой мозговой
оболочки. На этом нейрохирургический этап операции заканчивается.
Оперативные доступы к лицевому скелету при коррекции ОГ делятся на
доступы к лобно-носорешетчатому комплексу и к подглазничным краям и
нижним стенкам глазниц.
Надкостничное обнажение структур интерорбитального пространства,
верхних и наружных стенок глазниц производят трансвенечным доступом,
позволяющим подходить не только к своду черепа, но и к определенным
структурам лицевого скелета.
При скелетировании верхней стенки глазницы необходимо выделить
образования, непосредственно связанные с ней: надглазничный нерв и сухожилие
верхней косой мышцы глаза. На границе между средней и внутренней третями
надглазничного края лобной кости находится надглазничная вырезка (иногда
79
превращающаяся в надглазничное отверстие) — место прохождения одно-^
именных артерий и нерва. При прохождении сосудисто-нервного пучка
через вырезку, первый выводится из нее и укладывается на периорбитальные
ткани. При наличии отверстия его превращают в вырезку посредством ос-
теотома.
Медиальнее надглазничной вырезки у места перехода верхней стенки
глазницы во внутреннюю располагается блоковая ямка (иногда
превращающаяся в костный выступ — блоковую ость), где прикрепляется волокнисто-
хрящевое кольцо, через которое проходит сухожилие верхней косой мышцы
глаза. При скелетировании верхней стенки глазницы кольцо отделяют от
костной ткани, а проходящее через него сухожилие берут на лигатуру.
При скелетировании структур интерорбитального пространства
медиальные связки век отделяют от лобных отростков верхних челюстей и
слезных костей и берут на лигатуры. При наличии носовых костей от них
отделяют не только надкостницу, но и слизистую оболочку.
При скелетировании внутренней стенки глазницы обращают внимание
на слезный мешок и перепончатый слезно-носовой канал, целость которых
может быть нарушена при грубом манипулировании.
Проходящий в переднем решетчатом отверстии сосудисто-нервный
пучок (передние решетчатые артерия и нерв) в области лобно-решетчатого шва
при скелетировании внутренней стенки глазницы пересекают.
Незначительное кровотечение останавливают с помощью электрокоагуляции.
При поднадкостничном обнажении наружной поверхности латеральной
стенки глазницы височную мышцу тупым путем отделяют от височной
поверхности большого крыла основной кости и передних отделов чешуи
височной кости. Хотя указанная процедура приводится нами при описании
оперативных доступов к лицевому скелету, ее выполняют как
подготовительный этап при лобной краниотомии. Участки височной мышцы могут быть
использованы нейрохирургом для тампонады верхнего сагиттального синуса
твердой мозговой оболочки. Скелетирование височной поверхности
скуловой кости заканчивают на уровне нижних отделов скуловой дуги.
При отделении от периорбитальных тканей внутренней поверхности
латеральной стенки глазницы от последней в области лобно-скулового шва
отделяют и в ряде случаев идентифицируют латеральную связку век.
К подглазничным краям и нижним стенкам глазниц существуют
следующие оперативные доступы: инфраорбитальный, субцилиарный,
срединный инфрапальпебральный, трансконъюнктивальный, трансвестибулярный,
трансвенечный. Последний чаще используют при операциях у детей. Каждый
из указанных доступов имеет как преимущества, так и недостатки.
При инфраорбитальном доступе разрез кожи и глазничной части круговой
мышцы глаза проводят соответственно подглазничному краю, что является
самым коротким путем к последнему и позволяет получать широкий обзор. При
необходимости разрез может быть продолжен кнаружи. Недостатком
указанного доступа являются рубцы на лице и выраженный отек век в
послеоперационном периоде.
Субцилиарный и инфрапальпебральный доступы обеспечивают
достижение оптимального эстетического результата в виде отсутствия заметных
рубцов на лице. Недостатками рассматриваемых доступов являются: 1)
возможное развитие деформации нижнего века (вплоть до эктропиона) при
рассечении кожи и круговой мышцы глаза на разных уровнях, что объясняется
не всегда достижимым точным сопоставлением мышечных волокон; 2)
возможная неудовлетворительная адаптация кожи и мышечного слоя при
выделении изолированного тонкого кожного лоскута.
80
При трансконъюнктивальном доступе не остается наружных рубцов,
однако ему присущи следующие недостатки: 1) повреждение мышечных
оболочек; 2) значительное кровотечение из сосудов экстраокулярных мышц;
3) возможное развитие послеоперационной рубцовой контрактуры глазного
яблока; 4) неадекватный обзор при ретросептальном варианте.
В случаях комбинации внутриротовых разрезов и внутричерепного
доступа отмечен наибольший процент воспалительных осложнений.
Чаще применяют инфраорбитальный доступ с проведением разреза
соответственно орбитопальпебральной борозде. Объясняется это тем, что в
указанном случае операционные рубцы относительно незаметны и глазничная
перегородка не повреждается.
Подглазничный край скелетируется до уровня подглазничного
сосудисто-нервного пучка, дно глазницы освобождается от периорбитальных
тканей до уровня наружного края нижней глазничной щели.
Таким образом, внутренняя поверхность орбитального кольца
представляется освобожденной от периорбитальных тканей в следующих границах:
медиальная стенка — до уровня заднего решетчатого отверстия, латеральная и
нижняя стенки — до уровня наружного края верхней глазничной щели,
верхняя стенка — до уровня наружного края верхней глазничной щели.
Помимо этого, скелетируют структуры интерорбитального пространства,
над- и подглазничные края лобной кости, наружные поверхности латеральных
стенок глазниц, проводят ретракцию лобных долей головного мозга в области
глазничной поверхности лобной кости и образований основания черепа.
Как указывалось выше, универсальными оперативными приемами при
коррекции ОГ внутричерепным доступом, помимо костно-пластической
трепанации черепа, являются: субтотальная резекция лобно-носорешетчатого
комплекса, круговая остеотомия и перемещение глазниц, двусторонняя
медиальная кантопексия. Независимо от способов выполнения указанных
вмешательств существуют два основных метода коррекции ОГ внутричерепным
доступом: с созданием лобного обода и без такового.
Формирование лобного обода впервые предложено P. Tessier в 1969 г. Он
играет роль ориентира при аппозиции и фиксации остеотомированных
фрагментов глазниц, предупреждая их смещение от исходного уровня в передне-
заднем направлении и исключая тем самым образование энофтальма в
послеоперационном периоде. Лобный обод создают в виде полосы костной
ткани лобной области шириной 1 — 1,5 см и располагают на 1 — 1,5 см выше
надглазничных краев. Однако формирование такого обода возможно лишь в
отсутствие дефектов костной ткани лобной области, обусловленных черепно-
лицевыми расщелинами или назофронтальными мозговыми грыжами.
При оперативном вмешательстве с созданием лобного обода нижнюю
границу краниотомии необходимо формировать с таким расчетом, чтобы она
превышала уровень надглазничных краев на 2—3 см. При проведении
вмешательства без формирования лобного обода нижняя граница трепанации
черепа располагается на 0,7—1 см выше надглазничных краев.
При выполнении субтотальной резекции лобно-носорешетчатого
комплекса возможны два варианта: резекция центрального фрагмента единым
блоком и парамедиальная резекция с оставлением центрального фрагмента
интактным. Ширина резецируемого фрагмента (фрагментов) зависит от
исходного значения интерорбитального расстояния, возраста пациента и
является тем расстоянием, на которое в дальнейшем будут сближены глазницы.
Резекцию лобно-носорешетчатого комплекса начинают от лобного
обода или непосредственно от корня носа и продолжают на области
интерорбитального пространства и передней черепной ямки с включением в сегмент
81
6-1263
резецируемых тканей решетчатой пластинки после предварительной
электрокоагуляции обонятельных нервов. Резецированный фрагмент костной
ткани помещают в изотонический раствор натрия хлорида, так как он может
быть использован в качестве костнопластического материала. Наблюдаемое
обычно значительное кровотечение из клеток решетчатого лабиринта,
располагающихся латеральнее линий остеотомии, временно останавливают с
помощью тампонады. Окончательная остановка кровотечения происходит
самостоятельно по завершении аппозиции глазниц.
Большое значение необходимо придавать состоянию слизистой оболочки
носа. Разрывы ее, образующиеся при проведении этмоидэктомии,
ушиваются наглухо кетгутом. Наличие дефектов слизистой оболочки обусловливает
повышенный риск воспалительных осложнений в результате
инфицирования мозговых оболочек микроорганизмами носовой полости.
Кроме того, в большинстве случаев необходимо иссекать полуовальные
участки слизистой оболочки носа с обеих сторон с последующим ушиванием
ран наглухо кетгутовыми швами. В противном случае образующийся после
сближения глазниц избыток слизистой оболочки нарушает носовое дыхание
и благоприятствует воспалительным процессам в полости носа и околоносо-
вых пазухах.
Остеотомию глазниц начинают с их внутренних стенок и производят в
области решетчатых пластинок костей книзу до дна глазницы и вверх до
верхней ее стенки. От уровня последнего пропила начинают остеотомию
крыши глазницы со стороны передней ямки. Она сопровождается ретракцией как
лобных долей головного мозга, так и периорбитальных тканей под визуальным
контролем. Линию остеотомии верхней стенки глазницы продолжают на
область боковой ее стенки, которую необходимо остеотомировать как с
наружной, так и с внутренней стороны.
Если толщина латеральной стенки значительная, то возможно
непосредственное ее рассечение в саггитальной плоскости. При тонкой боковой
стенке линию остеотомии проводят с наружной ее стороны вниз до тела скуловой
кости, а внутреннюю поверхность рассекают до дна глазницы.
Линию остеотомии подглазничного края проводят сразу же ниже уровня
выхода из черепа сосудисто-нервного пучка и продолжают латерально до
соединения с пропилом в области наружной поверхности латеральной стенки
и медиально до края грушевидного отверстия. Нижнюю стенку глазницы ос-
теотомируют между пропилами в области внутренней и наружной стенок.
Необходимо отметить два существенных момента.
1. Остеотомию внутренних поверхностей орбитального кольца следует
проводить за экватором глазного яблока на расстоянии, которое
определяют индивидуально в каждом конкретном случае.
2. Остеотомию подглазничного края у детей следует проводить как
можно выше во избежание повреждения зачатков постоянных зубов.
Важным этапом при завершении остеотомии глазниц является
необходимая во многих случаях резекция треугольных участков костной ткани в
области нижневнутренних углов остеотомированных фрагментов глазниц.
Указанную манипуляцию производят, чтобы предупредить нарушение носового
дыхания после перемещения глазниц.
Заключительный этап остеотомии глазниц состоит в контроле пропилов
ударами тонким B—3 мм) остеотомом для их ревизии и рассечения костной
ткани в местах оставшихся соединений линий остеотомии.
Последующую аппозицию глазниц при технически правильном
выполнении подготовительных этапов осуществляют без значительных усилий и
82
заканчивают медиальной дислокацией остеотомированных фрагментов к
средней линии. Аппонированные глазницы фиксируют в области
интерорбитального пространства 2—3 проволочными швами или мини-пластиной,
которую закрепляют шурупами.
Образующиеся дефекты костной ткани между боковыми стенками
глазниц и большими крыльями основных костей замещают расщепленными ау-
тотрансплантатами краниотомированного фрагмента лобной кости, которые
скрепляют с окружающими структурами проволочными швами или мини-
пластинами. Выполнение указанной процедуры способствует более
стабильной фиксации остеотомированных фрагментов глазниц, а также
предупреждает развитие деформации лица в виде "песочных часов".
Идентифицированные при скелетировании внутренних стенок глазниц
медиальные связки век с помощью прикрепленных к ним лигатур проводят
через создаваемый канал в области интерорбитального пространства и
фиксируют друг к другу. В качестве шовного материала предпочтительнее
использовать титановую проволоку диаметром 0,15—0,2 мм.
Сухожилия верхних косых мышц глаза с помощью лигатур
прикрепляют к создаваемому каналу в области блоковой ости. Вновь создаваемое
прикрепление верхней косой мышцы головы нужно для того, чтобы
избежать нарушения функции мышцы (поворот глазного яблока вниз и
кнаружи).
Перед завершающим этапом операции осуществляют тщательную
ревизию твердой мозговой оболочки с целью выявления дефектов. При
обнаружении таковых их ушивают наглухо.
Краниотомированный фрагмент лобной кости укладывают на место и
фиксируют к окружающим костям свода черепа проволочными швами или
мини-пластинами. Надкостницу лобно-теменных областей ушивают. Височные
мышцы прикрепляют швами к перемещенным боковым стенкам глазниц.
Рану в области свода черепа, в подглазничных областях послойно ушивают.
Накладываются швы на кожу. В височных и подглазничных областях на 24—
48 ч оставляют резиновые дренажи, накладывают асептическую марлевую
повязку. Производят переднюю тампонаду полости носа турундами,
пропитанными йодоформной жидкостью.
Оперативные приемы коррекции ОГ внутричерепным доступом
описаны без учета основной аномалии, обусловившей развитие ОГ. В
определенных случаях оперативное вмешательство может заключаться в выполнении
только этих пособий.
Планирование оперативного вмешательства. Принцип бригадного
подхода играет ведущую роль не только в диагностике аномалий, но и в
планировании оперативного вмешательства, являющегося тем не менее
прерогативой черепно-лицевого хирурга. К ведущим составляющим этого процесса
относятся: установление возрастных показаний к операции, определение
показаний к внутричерепному доступу, установление величины предстоящей
медиальной дислокации глазниц.
Возраст, в котором проведение коррекции ОГ оптимально, зависит как
от медицинских, так и от социальных показаний. В возрасте моложе 2 лет
осуществить коррекцию ОГ внутричерепным доступом технически сложнее,
учитывая небольшую толщину и хрупкость костей лицевого скелета, что
может приводить к непредсказуемому повреждению костных структур.
Ориентируясь· на социальные показания, операцию желательно
производить до того, как ребенок пойдет в школу. К 3—5 годам кости лицевого и
мозгового черепа приобретают размеры, необходимые для безопасного
вмешательства и получения костнопластического материала.
б:і
83
Следует учитывать и то, что по мере роста ребенка увеличиваются не
только нормально развитые структуры, но и аномальные, что приводит к
дальнейшему развитию деформации и затрудняет достижение адекватного
эстетического результата в ходе хирургического лечения.
Для детского организма характерны следующие топографоанатомические
особенности, имеющие значение при коррекции ОГ внутричерепным доступом.
1. Отсутствие соединительных перемычек подкожной жировой клетчатки
лобно-теменно-затылочной области, благодаря чему кровеносные
сосуды указанной области спадаются, обусловливая менее выраженное
кровотечение, чем у взрослых пациентов, при проведении
трансвенечного разреза.
2. Прочное соединение твердой мозговой оболочки с костями свода
черепа, что важно при проведении костно-пластической трепанации
черепа и ретракции лобных долей головного мозга.
3. Наличие зачатков постоянных зубов верхней челюсти, что
обусловливает необходимость проведения остеотомии подглазничных краев
как можно выше во избежание повреждения указанных образований.
4. Более тонкие кости лицевого скелета облегчают остеотомию, что
выражается в уменьшении длительности вмешательства.
5. Остеотомию верхней челюсти в области нижнеглазничного края у
детей удается осуществить из трансвенечного доступа, не прибегая к
внутриротовым или наружным разрезам.
Абсолютным показанием к коррекции О Г внутричерепным доступом
является III степень его (ИОР > 40 мм). Двусторонняя U-образная
остеотомия глазниц с последующей аппозицией остеотомированных фрагментов
наружно-черепным доступом позволяет уменьшить ИОР не более чем на 1 см, что при
выраженном ОГ недостаточно для достижения адекватного эстетического
результата. Остеотомия внутренних стенок глазниц с последующей их
медиальной дислокацией в еще меньшей степени влияет на изменение ИОР и по
существу является средством реконструкции спинки носа.
В некоторых случаях показанием к использованию внутричерепного
доступа является также ОГ II степени, что связано со следующими
аномалиями: 1) положением носо-лобного сочленения выше уровня решетчатой
пластинки решетчатой кости. При экстракраниальном вмешательстве в этом
случае неизбежны проникновение в переднюю черепную ямку и
травмирование головного мозга; 2) мозговыми грыжами, фронтальной плагиоцефалией,
вертикальной дистопией одной из глазниц. Коррекция указанных аномалий
возможна лишь внутричерепным доступом; 3) овальной или клиновидной с
сужением в переднем отделе формой интерорбитального пространства. В этих
случаях выполнение частичной этмоидэктомии во фронтальном отделе при
U-образной остеотомии глазниц и последующей аппозиции
остеотомированных фрагментов не приводит к уменьшению истинного ИОР,
достигающего наибольшей величины за экваторами глазных яблок.
При удовлетворительном профиле носа и выраженности его спинки (что
является редким исключением при ОГ III степени) целесообразно
производить парамедиальную резекцию лобно-носорешетчатого комплекса с
оставлением центрального сегмента интактным.
У пациентов с краниостенозами в стадии декомпенсации и выраженным
повышением внутричерепного давления трепанация черепа служит средством
декомпрессии головного мозга. В этих случаях рекомендуется коррекция ОГ II
степени внутричерепным доступом.
Противопоказаниями к оперативному вмешательству следует считать
олигофрению и выраженную задержку психического развития.
84
Рис. 22.48. Фронтоназальная дисплазия, гипертелоризм III степени, полная
расщелина верхней губы и неба слева.
а — ребенок 1 года до хирургического лечения. В возрасте 1 года произведена ринохейлопластика,
в 1,5 года — велопластика, в 3 года — круговая остеотомия глазниц с репозицией интракраниальным
доступом, пластика носа, в 5 лет — пластика твердого неба; б — больная после операции.
Ширину резецируемого фрагмента лобно-носорешетчатого комплекса
определяют как разность ИОР и среднего его значения в популяции B5 мм у
женщин и 28 мм у мужчин). Помимо этого, производят гиперкоррекцию на 10 %,
необходимость которой обусловлена следующими факторами:
1. По мере роста ребенка в норме среднее значение ИОР за период с 3—
5 до 12 лет (когда оно достигает среднего значения у взрослых)
увеличивается на 4—5 мм. Следовательно, при резекции
лобно-носорешетчатого комплекса гиперкоррекция на указанную величину
компенсирует дальнейший рост аномального интерорбитального пространства.
2. У взрослых пациентов с краниосиностозами оперативное
вмешательство компенсирует воздействие повышенного внутричерепного
давления на увеличение ИОР.
3. При использовании в качестве фиксирующих приспособлений
проволочных швов гиперкоррекция также компенсирует некоторое
расхождение остеотомированных фрагментов глазниц в
послеоперационном периоде (рис. 22.48, 22.49).
Устранение ОГ I—II степени возможно экстракраниальным доступом
[Хелминская Н. М., 1993J. Подход к лицевому скелету осуществляют с двух
сторон (наружной и внутриротовой) для облегчения скелетирования и
проведения остеотомии в верхних и нижних полюсах нососкулоорбитального
комплекса. Применяют различные варианты наружного оперативного
подхода в зависимости от эстетической недостаточности. Утех больных, которые
нуждаются в сближении бровей, при избытке кожи в области надпереносья
и носа проводят разрез от нижнего отдела лобной области по спинке носа до
его концевого отдела. У остальных пациентов делают трансвенечный разрез,
85
Рис. 22.49. Мозговая грыжа,
орбитальный несимметричный гипертелоризм.
а — больная 6 лет после нерадикальной
операции по поводу грыжи; б, в — больная в фас
и профиль через 6 лет после операции. Ин-
тракраниальным доступом произведены
удаление остатков грыжевого мешка, круговая
остеотомия глазниц с перемещением,
пластика носа с использованием костного ауто-
трансплантата из костей черепа.
а в
Рис. 22.50. Экстракраниальная остеотомия и перемещение фрагментов носоглаз-
ничного комплекса (схема).
а — резекция носового комплекса во фронтальном отделе, остеотомия; б — медиальная
дислокация остеотомированных фрагментов; в — фиксация остеотомированных фрагментов (схема).
позволяющий подходить к структурам средней зоны лица и в случае
необходимости брать костный аутотрансплантант для пластики.
Для устранения деформации носоорбитальной области, сочетающейся с ОГI и
незначительно выраженной II степени применяют остеотомию
носоорбитальной области, вютючаюшую следующие этапы оперативного вмешательства:
1) резекцию носового комплекса во фронтальном отделе (рис. 22.50, а); 2)
остеотомию носо-глазничного комплекса с проведением линии остеотомии в
области медиальных стенок глазниц кзади от носо-слезных каналов; 3)
медиальную дислокацию и фиксацию остеотомированных фрагментов; 4)
двустороннюю медиальную кантопексию (рис. 22.50, б, в).
При первом варианте вмешательства, который применяют в отсутствие
носовых костей, хрящ, замещающий кость, отслаивают от слизистой
оболочки носа и надкостницы, а затем удаляют его. Второй вариант осуществляют
при грубой деформации костей носа. Производят назофронтотомию с
удалением всего костного сегмента.
Третий вариант, используемый при хорошо выраженной спинке носа,
но деформированных лобных отростках верхних челюстей, заключается в па-
расагиттальной остеотомии (рис. 22.51).
Операцию выполняют следующим образом. В конъюнктивальные ложа
вводят 1 % синтомициновую эмульсию. После предварительной гидросепаровки изо-
87
Рис. 22.51. Экстракраниальная остеотомия с сохранением части носолобного
комплекса (схема).
а — парасагитгальная остеотомия при хорошо выраженной спинке носа; б— медиальная дислокация
и фиксация остеотомированных фрагментов.
тоническим раствором натрия хлорида делают разрез от нижнего отдела лобной
кости по спинке носа до концевого отдела носа. Острым и тупым путем отсепа-
ровывают мягкие ткани. При скелетировании носовых костей от них отделяют
надкостницу и слизистую оболочку носа. При скелетировании медиальной стенки
глазниц соблюдают особую осторожность ввиду ее тонкости, поскольку легко
возникают трещины и надломы. В переднем отделе медиальной стенки глазниц
на слезной кости и на лобном отростке верхней челюсти имеется углубление,
где находятся слезный мешок и носослезный канал, которые могут быть
повреждены при травматичном вмешательстве, что также требует внимания.
При скелетировании структур интерорбитального пространства кантальные
связки отделяют от лобных отростков верхних челюстей и слезных костей и
фиксируются на лигатурах.
Проводят дополнительный разрез по переходной складке
соответственно первым моляром. Острым и тупым путем отслаивают мягкие ткани.
Скелетируют всю переднюю поверхность верхних челюстей до нижнего края
скуловой кости и до грушевидной апертуры. Подглазничный край скелетируют
до уровня подглазничного сосудисто-нервного пучка, дно глазниц — до
уровня нижней глазничной щели, которая расположена между наружной и
нижней стенками глазницы.
Линию остеотомии начинают в области корня носа, где в зависимости
от деформации производят назофронтальную или парасагиттальную
остеотомию. После удаления деформированного фрагмента образуется дефект
88
различной величины, который устраняют путем перемещения лобных
отростков верхних челюстей вместе со слезными костями. Для перемещения этих
фрагментов осуществляют остеотомию лобных отростков верхних челюстей,
слезных костей через линию, идущую от лобной кости по шву между слезной
и этмоидальной костью с переходом на дно глазницы и нижний глазничный
край, отступя 2 мм кзади от носослезного канала.
Затем линию остеотомии под углом 30° проводят по нижнему
глазничному краю до сочленения верхних челюстей и под таким же углом
продолжают на передней поверхности верхних челюстей до края грушевидной
апертуры. При помощи остеотома выполняют остеотомию лобных отростков
верхних челюстей в переднезаднем направлении. Для устранения
возможного нарушения носового дыхания после перемещения костных фрагментов в
завершение остеотомии носо-глазничного комплекса резецируют
треугольные участки костной ткани в области нижневнутренних углов остеотомиро-
ванных фрагментов. Остеотомированные костные фрагменты сближают и
жестко фиксируются друг к другу при помощи проволочных швов или мини-
пластин, закрепленных шурупами. Образовавшиеся костные дефекты при
необходимости устраняют костной пластикой с использованием алло- или
аутотрансплантата расщепленной черепной кости.
Кантальные связки с помощью прикрепляемых к ним лигатур проводят
через создаваемый в области интерорбитального пространства канал и
фиксируют друг к другу. Жесткую фиксацию костных фрагментов осуществляют
к лобной кости в верхнем отделе, в области нижнего края глазниц, а также к
верхней челюсти в нижнем отделе лицевого скелета. При наличии дефектов
слизистой оболочки носа последние ушивают наглухо кетгутом.
Полуовальными разрезами иссекают избыток кожи лобно-носовой области. Рану послойно
ушивают. В области корня носа оставляют резиновый дренаж на 24—48 ч. По
переходной складке накладывают кетгутовые швы. Затем проводят переднюю
тампонаду полости носа турундами, смоченными йодоформной смесью, и
накладывают асептическую повязку, которая выполняет моделирующую роль.
Применение данного метода устранения грубой врожденной
деформации носоорбитальной области, сочетающейся с орбитальным гипертелориз-
мом I—II степени, экстракраниальным доступом позволяет уменьшить
интерорбитальное расстояние от 6 до 10 мм (рис. 22.52).
Особенности ведения послеоперационного периода. Послеоперационный
период, начинающийся непосредственно после завершения оперативного
вмешательства, требует непрерывного наблюдения за пациентом в течение
всего периода времени до выписки из стационара, особенно в первые
несколько суток. Пробуждение пациента необходимо осуществлять на
операционном столе непосредственно после завершения операции с целью
контроля за функцией органа зрения.
Учитывая значительную продолжительность вмешательства (в среднем 8 ч
у детей и Ючу подростков и взрослых), а также выраженную кровопотерю
(в среднем 900 мл у детей и 1500 мл у подростков и взрослых), необходимо
проводить в полном объеме весь комплекс реанимационных мероприятий, а
также противовоспалительную, инфузионную и трансфузионную терапию.
Перевязки делают ежедневно, обращая особое внимание на характер
отделяемого по дренажам из раны в области свода черепа и из полости носа с
целью выявления ликвореи.
Послеоперационный отек, нарастающий в течение 1-х суток после
вмешательства, максимально выражен на 3—4-е сутки. Наиболее выраженный
отек отмечается в области век, в результате чего открывание глаз
становится невозможным. В этот период необходимо ежедневно тщательно прово-
89
Рис. 22.52. Срединная лицевая расщелина, орбитальный гипертелоризм II степени.
а — больная 17 лет до операции; б — та же больная после операции перемещения медиальных
стенок глазниц и пластики носа экстракраниальным доступом.
дить туалет конъюнктивы с введением в конъюнктивальные ложа глазной
гидрокортизоновой мази с целью профилактики офтальмогенных
осложнений.
Поскольку у пациентов с выраженным ОГ часто наблюдаются
сопутствующие аномалии, в большинстве случаев оперативное вмешательство
заключается не только в выполнении универсальных оперативных приемов по
коррекции О Г, но и в проведении комплексной черепно-лицевой
реконструкции, которую следует производить в специализированных центрах
ввиду технической сложности вмешательства и возможного развития
осложнений.
СПИСОК ЛИТЕРАТУРЫ
Агеева Л. В., Савицкая Г. М. Хирургическая реабилитация детей с односторонней
расщелиной верхней губы и неба в младшем возрасте//Актуальные проблемы
комплексного лечения и реабилитации детей с врожденной краниофациальной и
нейропатологией. — М., 1996.
Агеева Л. В., Савицкая Г. М., Рогинский В. В. Метод одномоментного устранения
дефекта верхней губы, альвеолярного отростка верхней челюсти с воссозданием
симметрии носа у детей с односторонней расщелиной верхней губы и неба:
Метод, рекомендации. — М., 1998.
Ананян С Г. Клиника, диагностика и лечение больных с нарушениями функции неб-
но-глоточного затвора после уранопластики: Автореф. дис. ... канд. мед. наук. —
М., 1985. - 22 с.
90
Лнанян С. Г., Безруков В. М. Классификация и сравнительная характеристика
нарушений функции небно-глоточного затвора после уранопластики//Стоматология. —
1988. -№ 2. -С. 35-37.
Лнанян С. Г. Клиника, диагностика и хирургическое лечение больных с
послеоперационными дефектами неба: Автореф. дис. ... д-ра мед. наук. — М., 1989. — 42 с.
Атлас пластической хирургии лица и шеи/Под ред. Ф. М. Хитрова. — М.: Медицина,
1984. - С. 116-117.
Безруков В. М., Хитрое Ф. М., Жибицкая Э. И. Клинико-рентгенологическая картина
орбитального гипертелоризма//Экспериментальная и клиническая
стоматология: Труды ЦНИИС. - Т.2. - М., 1975. - С 93-96.
Безруков В. М. Клиника, диагностика и лечение врожденных деформаций челюстно-
лицевого скелета: Автореф. дис. ... д-ра мед. наук. — М., 1981. — 42 с.
Блохина С. И. Диспансеризация детей с врожденными расщелинами лица и неба и
врожденными пороками сердца: Автореф. дис.... канд. мед. наук. — М., 1983. — 21 с.
Блохина С. И., Булатовская Б. Я., Павлов В. П., Уракова А. И. Социальная
реабилитация детей с врожденными расщелинами лица и неба в Свердловской области//
Медицинская реабилитация при заболеваниях и повреждениях челюстно-лице-
вой области. — Свердловск, 1985. — С. 109—113.
Блохина С. И., Козлова В. П. Детские реабилитационные центры нового типа в России
сегодня и завтра//Очерки медико-социальной реабилитации семей, имеющих
детей с проблемами здоровья. — Ч.ІІІ. — Екатеринбург, 1995. — С. 3—9.
Виссарионов В. А. Классификация и принципы хирургического лечения деформаций
верхней губы и носа после пластики врожденных расщелин//Вестн. хир., 1986. —
Т. 137, № 10. -С. 91-94.
Виссарионов В. А. Классификация деформаций носа и верхней губы после пластики
врожденных расщелин/Стоматология. — 1988. — № 2. — С. 37—39.
Герасимова Л. П. Применение программного многоканального биоэлектрического
управления в реабилитации детей с врожденными и приобретенными пороками
челюстно-лицевой области: Дис. ... д-ра мед. наук. — М., 1997.
Гуцан А. Э. Уранопластика взаимоперекидными лоскутами. — Кишинев: Штиинца,
1982. - 94 с.
Гунъко В. И. Клиника, диагностика и лечение больных с сочетанными деформациями
челюстей: Автореф. дис. ... д-ра мед. наук. — М., 1986. — 40 с.
Дмитриева В. С, Ландо Р. Л. Хирургическое лечение врожденных и
послеоперационных дефектов неба. — М., 1968.
Давыдов Б. И., Бессонов С. И. Первичная ринохейлопластика при двусторонних
неполных расщелинах верхней губы//Стоматология. — № 4. — 1994. — С. 54—57.
Давыдов Б. Н., Новоселов Р. Д. Восстановительная хирургия мягких тканей челюстно-
лицевой области/Под ред. А. И. Неробеева, Н. А. Плотникова. — М.: Медицина,
1997. - С. 287.
Дубов М. Д. Врожденные расщелины неба. — Л.: Медгиз, 1960. — 145 с.
Ипполитов В. П., Гунько В. И. Клиника, диагностика и лечение орбитального гипер-
телоризма//Вестн. хир. — 1978. — № 10. — С. 151.
Заусаев В. И. Модификация операции закрытия врожденных расщелин неба//Стома-
тология. — 1953. — № 1. — С. 59—61.
Козин И. А. Эстетическая хирургия врожденных расщелин лица. — М.: Мартис, 1996. — 568 с.
Лилыт Е. Т., Тутуева Т. А. Принципы медико-генетического консультирования
врожденных и наследственных заболеваний челюстно-лицевой области: Метод,
рекомендации. — М., 1996.
Мамедов А. А. Комплексная реабилитация больных с небно-глоточной
недостаточностью и нарушением речи после уранопластики: Дис. ... д-ра мед. наук. —
Екатеринбург, 1997.
Мамедов А. А. Врожденная расщелина неба и пути ее устранения. — Екатеринбург, 1998.
Макхамов Э. X. Раннее лечение детей с врожденной расщелиной верхней губы и неба. —
Дис. ... д-ра мед. наук. — М., 1981. — 293 с.
Макхамов Э. Х.} Убайдуллаев М. Б., Мамедов Т. Г. Оценка состояния небно-глоточной
области у детей с врожденной сквозной расщелиной неба//Стоматология. —
1989. - № 5. - С. 83-85.
91
Нагирный Я. П. Значение факторов резистентности организма в прогнозировании
послеоперационных осложнений при хирургическом лечении детей с врожденными
расщелинами губы и неба. — Дис. ... канд. мед. наук. — М., 1990.
Новоселов Р. Д. Основы теории и практики коррекции хрящевого и костного остова
носа в хирургии врожденных расщелин лица. — Калинин, 1989. — 11 с.
Рогинекий В. В. Ранняя реабилитация детей с врожденной патологией черепно-челю-
стно-лицевой области // Современные технологии лечения и реабилитации детей
с врожденными, наследственными заболеваниями челюстно-лицевой области и
сопутствующей патологией. — Екатеринбург — Москва, 1999. — С. 16—18.
Самар Э. И. Особенности хирургического лечения больных с врожденными
расщелинами неба в различном возрасте: Автореф. дис.... д-ра мед. наук. — М., 1987. — 45 с.
Семенченко F. И., Вакуленко В. И.} Лукьяненко В. Α., Крыкляс F. Г. Хирургические
способы восстановления небно-глоточного смыкания после неудачных исходов ура-
нопластики//Стоматология. — 1986. — № 3. — С. 51—52.
Фролова Л. Е. Костная пластика эмбриональным и лиофилизированным аллотранс-
плантатом при лечении тяжелых форм врожденных расщелин губы и неба:
Метод, рекомендации. — М., 1979.
Фролова Л. Е. Методика оперативного лечения расщелины неба//Стоматология. —
1977. - № 3. - С. 63-65.
Хитрое Ф. М., Козырев В. Α., Ипполитов В. П.у Гунько В. И. Диагностика и лечение
орбитального гипертелоризма//Экспериментальная и клиническая стоматология:
Труды ЦНИИС. - Т.8, 4.2. - М., 1978. - С. 59-65.
Billroth Т. Veber Vranoplastik//Wien klin. Wschr., 1889. - Bd 2. - S. 241.
Chin M.f Toch B. A. Le Fort III advancement with gradual distration using internal devices/
/Plast, reconstr. Surg. - 1997. - Vol. 100, N 4. - P. 819-830.
Cohen S. R. Distraction Osteogenesis of the Human Craniofacial Skeleton: Initial Experience
with a New Distration System//J. Craniofacial Surg. — 1995. — September. — P. 368.
Eskeland Α., Bergland 0.y Borchgrevink H. et al. Management of the cleft alveolar arch//Rec.
advances plast. Surg. — 1985. — Vol.3. — P. 13—32.
Fara M., Chlumska Α., Hrivnakova У. Musculus orbicularis oris in incomplete harelip//Acta
chir. plast. - 1965. — Vol.7, N 2. - P. 93-100.
Jackson J. T. Closure of secondary palatal fistulae with intra-oral tissue a: bone grafting//Brit.
J. plast. Surg. - 1972. - Vol. 25. - P. 93-105.
Jackson J. T. Cleft lip a. palate//Plastic surgery in infancy & childhood. — 3 ed./Ed. J. L. Mus-
tarde, J. T. Jackson. — Edinburg. — London. — Melbourne. — New York, 1988. — P. 1—41.
Jackson J. T. et al. Atlas of craniomaxillofacial surgery. — St. Louis, 1982.
Karakasis D., Dimitrakopoulos I., Lasaridis N. Distraction Techniques Applied in the Lowe!
and Middle third the Face//J. Craniomaxillofacal Surg. — 1998. — Vol. 26, Supplement
I. - P. 89.
Liou E. J. W., Hund К.-F., Chand S. et al. Create Real Hard Palate in Clift Palate Cases by
Using Distraction Osteogenesis//J. Craniomaxillofacial Surg. — 1998. — Vol. 26,
Supplement 1. — P. 105.
Manchester W. M. A method of primary double cleft lip repair//Transactions of the 5th
International Congress of Plastic a. Reconstructive Surgery. — Butterworths. —
Melbourne. — Chatswood, 1971.
Marchac D., Renter D. Craniosynostosis//World J. Surg. — 1989. — Vol. 13, N 4. — P. 358—365.
McComb H. Primary correction of unilateral cleft lip nasal deformity: a 10-year review//Plas-
tic reconstr. Surg. — 1985. — Vol. 75. — P. 791—797.
Millard D. R. A primary camouflage of the unilateral harelook//Transactions of the
International Society of Plastic Surgery: First Congress, Stochholm — Uppsalo. Ed. T. Skoog.
Baltimore: Williams a. Wilkins, 1957. - P. 160-165.
Monasterio F, Molina F., Andrade L. et al. Simultaneous mandibular and maxillary distraction
in hemifatial microsomia in adults: avoiding occlussal disasters/Plast. reconstr. Surg. —
1997. - Vol. 100, N 4. - P. 852-861.
Munro J. R. Craniofacial surgery//Plastic surgery/Ed. W. С Grabb, J. W. Smith. — 1979. —
P. 131-160.
Munro J. R. Craniofacial surgery: technique and philosophy//PJast. reconstr. Surg. — 1988. —
Vol. 81, N 6. - P. 970-974.
92 -
Nordin Κ Ε., Johanson В. Frei Knochen-Transplantation bei Defekten in alveolarkam nach
Kieferortopadischer Enstelluling der Maxilla bei Lippen-Kiefer-Gaumenspalton. —
Vol. 1. - Stuttgart: Thiere, 1955.
PolleyJ. W. Monobloc Craniomaxillofacial Distraction Osteogenesis in a Newborn with Sew-
ere Craniofacial Synostosis: A. Preliminary Report//J. Craniofacial Surg. — 1995. —
September. — P. 421.
Puelacher W. C, Waldhart Ε., Eder R., Zur Nedden D. Computer-Assisted-Planning of Dis-
tration-Osteo-Genesis//J. Craniomaxillofacial Surg. — 1998. — Vol. 26, Supplement 1. —
P. 148.
Randall P. A triangular flap operation for the primary repair of unilateral clefts of the lip//
Plast, reconstr. Surg. — 1959. - Vol. 23. - P. 331-347.
RehrmannA. H.} Koberg W. R., Koch H. Longterm postoperative results of priтагу & secondary
bone grafting in complete clefts of lip a. palate//Cleft Palate J. — 1970. — Vol. 7. —
P. 206-221.
Rosenstein S. W.y Monroe C. W.t Kemahan D. A. et al. The case of early bone grafting in cleft
lip a. cleft palate//Plast. reconstr. Surg. - 1982. - Vol. 70. - P. 297-309.
Salyer К. Е. Techniques in aestnetic craniofacial surgery. — New York — London, 1989.
Schoenborn D. Veber eine new Methode der Staphylorraphie//Arch. kiln. Chir. — 1976. —
Bd 19. - S. 527.
Skoog T. The use of periosteal flaps in the repair of clefts of the primary palate//Cleft Palate
J. - 1965. - Vol. 2. - P. 332-339.
Tennison C. W. The repair of the unilateral cleft lip by the stencil method//Plast. Reconstr.
Surg. - 1952. - Vol. 9. - P. 115-120.
TessierP. Chirurgie orbito-cranienne//Minerva chir. — 1971. — Vol. 26, N 16. — P. 878—904.
Tessier P. Anatomical classification of facial, craniofacial and laterofacial clefts//J. Maxillo-
fac. Surg. - 1976. - Vol. 4, N 2. - P. 69-92.
Veau V. Bec-de-lievre. — Paris, 1938.
Yamamoto #., Sawaki Y., Veda M. Maxillary advancement by distraction osteogenesis using
osseointegrated implants//J. Craniomaxillofacial. Surg. — 1997. — Vol. 25, N 4. —
P. 186-191.
Глава 23
ВОССТАНОВИТЕЛЬНЫЕ ОПЕРАЦИИ
НА МЯГКИХ ТКАНЯХ
ЛИЦА И ШЕИ
23Л. Анатомия и физиология лица и шеи
Лицо представляет собой комплекс анатомических образований, каждое из
которых самостоятельно несет на себе отдельные функциональные нагрузки
и в свою очередь является неотъемлемой частью в обеспечении общих
функций. Понимание этих взаимосвязей лежит в основе планирования и
успешной реконструкции утраченных структур.
Существуют два подхода к определению дефектов тканей на лице — то-
пографоанатомический и анатомо-функциональный. Согласно первому, в
соответствии с предложениями А. Э. Рауэра и Н. М. Михельсона лицо делят
на три зоны — верхнюю, среднюю и нижнюю.
Многочисленными антропометрическими измерениями, в частности
измерениями лица, проведенными Ф. М. Хитровым A954), было доказано
примерное соответствие по высоте лба, носа и верхней и нижней губ, что
предопределило деление лица на верхнюю, среднюю и нижнюю трети. После
измерения лиц у 100 человек Ф. М. Хитров установил следующие размеры:
высота лба (от корня носа до края волосистых покровов головы) — от 50 до
70 мм, расстояние от корня до основания кожной перегородки носа,
соответствующее средней зоне лица, — от 47 до 67 мм, расстояние между
основанием кожной перегородки и нижним краем подбородка, соответствующие
нижней трети лица, — от 65 до 75 мм.
В соответствии с этим подходом при оценке дефекта, а главное, способа
восстановительной операции рассматривают каждую зону по отдельности.
При втором варианте за основу берут отдельные части лица — нос, веки, щеки,
губы, подбородок и т. д. и описывают конкретные методы их
восстановления. Очевидно, что тот и другой подход имеют преимущества и недостатки,
но именно для целей пластического замещения утраченных тканей топогра-
фоанатомическая характеристика зоны кажется нам более ценной. Главное
при выборе восстановительной операции — возможность смещения местных
тканей на дефект. Не подлежит сомнению, что во всех случаях формировать
наружные покровы из близлежащих тканей предпочтительно за счет цвета и
толщины кожных покровов. Следовательно, главное при оценке варианта
реконструкции — возможность перемещения тканей к участку дефекта.
Детальный разбор каждой из топографоанатомических зон лица помогает хирургу
определить закономерности смещения тканей в этих зонах. Кроме того,
очень редко возникают изолированные дефекты отдельных органов, часто
94
повреждаются соседние структуры, так что правильнее выбирать участки
более широкие, чем кажущийся дефект. Разумеется, деление лица на зоны
достаточно условно, поскольку утрата тканей может происходить сразу в нескольких
зонах. Однако в связи с выраженным отличием (в анатомо-топографическом
смысле) одной зоны лица от другой имеет смысл детально рассмотреть их с
точки зрения клинико-функциональной анатомии.
Наиболее сложной для хирурга является средняя зона лица.
Особенности остальных зон описаны в соответствующих разделах.
Две верхнечелюстные кости образуют верхнюю челюсть, переднюю часть
верхнего неба, боковые стенки носовой полости и часть дна орбитальных
полостей. Эти кости соединены по средней линии межчелюстным швом.
Верхнечелюстная кость состоит из тела и четырех отростков: лобного, небного, скулового
и альвеолярного. Внутри тела верхней челюсти имеются парные
верхнечелюстные синусы. Эти синусы рудиментарны у младенцев, но в период взросления
расширяются с формированием костных полостей, выстланных дыхательным
эпителием. Тонкую кость верхнечелюстных синусов окружают более толстые
костные ткани, являющиеся опорами средней зоны лица и ее высоты [Manson P.,
Hoopes J., 1980]. Небо может быть разделено на три анатомические области:
твердое небо, мягкое небо и язычок. Твердое небо состоит из двух парных
небных отростков верхней челюсти, соединенных посередине небным швом.
Спереди резцовая кость отделена от парных небных пластин резцовым отверстием.
Сзади небные отростки соединены с горизонтальными пластинами
небных костей. Твердое небо разделяет ротовую и носовую полости и является
устойчивым противовесом языку при речи, формировании пищевого комка в
ротовой стадии глотания. У людей с узким и высоким лицом свод неба обычно
высокий, у людей с широким и низким лицом — уплощенный [Куприянов В. В.,
Стовичек Г. В., 1988].
Мягкое небо, являясь продолжением твердого, представляет собой
подвижную мышечную структуру, образованную четырьмя парами мышц,
покрытых слизистой оболочкой, которая участвует в речи и глотании. Одно из
главных условий его нормального функционирования — подвижность,
которая необходима для закрывания и отделения гортани от полости носа.
Глазницы являются парными пирамидальными полостями с крышей,
дном, медиальной и латеральной стенками, разделенными между собой
межорбитальным пространством. Внутри этого пространства находятся носовая
полость, клетки решетчатого лабиринта и основные синусы.
Межорбитальное пространство ограничено сверху передней черепной ямкой, и снизу —
твердым небом. Костные стенки глазницы образуются частями лобной,
клиновидной, основной, верхнечелюстной, скуловой, слезной и небной костей.
Скуловые кости и верхняя челюсть поддерживают глазное яблоко, а
медиальная стенка глазницы отделяет его от дыхательных путей.
Соответствующая глубина D—5,5 см) и расположение костей глазницы
обязательны для нормальной функции глаза и дыхания через нос [Золотко Ю. Α.,
1964]. Околоносовые пазухи моделируют прохождение воздуха через нос, а
также служат иммунологическими резервами и частично поглощают энергию
ударов по лицевому скелету, уменьшая их амплитуду при травме. Они влияют
также на дыхание и отделяют основание черепа и глазницы от полости рта и
носоглотки. Верхнечелюстные пазухи и верхняя челюсть являются основной
вертикальной опорой лица, поддерживающей глаза снизу, зубы — сверху и
являющейся промежуточной областью между нижней зоной лица, полостью
рта и основанием черепа.
Средняя зона лица характеризуется как структура, поддерживающая
основание черепа с индивидуальным количеством разделяющихся колонн и
95
опор, обеспечивающих вертикальные размеры, проекцию и стабильность
черепа [Manson Р. Ν., Hoopes J. Ε., 1980]. Ветви нижней челюсти через височ-
но-нижнечелюстной сустав являются самыми задними вертикальными
опорами, а нарушения, которые видны при односторонней нижнечелюстной
гипоплазии после лучевой терапии в раннем детском возрасте или при
анкилозе височно-нижнечелюстного сустава, подтверждают их
функциональную необходимость. Неправильный прикус, вызывающий наклон окклюзи-
онной плоскости, и переросшие в противоположную сторону кость и
мягкотканные структуры являются хорошо известными последствиями
дефицита задней опоры. Медиальная крылонебная опора обеспечивает задний
вертикальный размер и стабильность посредством пирамидальной проекции
небной кости и крыловидного отростка основной кости. Диспропорция этих
опор отрицательно влияет на окклюзию и функцию нижней челюсти,
нарушая взаимосвязи между расположением зубов.
Квадратные скуловые кости связывают среднюю зону с основанием
черепа через височный отросток, с костями свода черепа — через фронтальный
отросток к средней зоне лица через его инфраорбитальную позицию, с
нижней челюстью — своим широким основным отростком к верхнечелюстной
кости. Вертикальная недостаточность скуловой кости укорачивает лицо и
увеличивает глубину орбит. Носолобная опора обеспечивает переднюю
высоту средней зоны лица, поддерживая соответствующие взаимосвязи между
зубной дугой, носовой полостью, глазницами и лобным основанием черепа.
Верхняя челюсть, носовые, слезные и основная кости предопределяют
высоту лица и являются решающими в сохранении нормального внешнего вида
и функции лица. Помимо вертикальных опор лица, функциональную
нагрузку несут его горизонтальные составляющие.
Небо и альвеолярный отросток, грушевидное отверстие и
подглазничные щели являются основными детерминантами ширины лица и пропорций.
Горизонтальные опоры поддерживают функциональную связь между верхней и
нижней челюстями, орбитами и воздухопроводящими путями. Правильное
расположение квадратной скуловой кости и скуловой дуги является решающим в
поддержании соответствующих связей средней зоны лица в горизонтальном и
вертикальном измерениях. Более того, проекция средней зоны лица зависит от
взаимоотношения скуловой кости с височной и лобной [Coleman J. J., 1994].
Среднюю зону лица можно представить как непосредственное
соприкосновение трех полостей в виде костно-слизистых блоков: ротовой полости,
носоверхнечелюстного комплекса и полости глазницы с их содержимым.
Глаза являются одним из наиболее важных средств познания
окружающего мира. Это ворота, через которые световые сигналы извне поступают в
центральную нервную систему. Глазами называют глазные яблоки с окружающими
их мягкими тканями в орбите. Но на практике к глазу относят все, что заполняет
глазницу и окружает ее, например веки и ресницы. Нормальное
функционирование глазного яблока обеспечивает вспомогательный аппарат глаза,
представленный мышцами глазного яблока, фасциями глазницы, верхним и нижним
веками, соединительной оболочкой, слезным аппаратом, бровями.
Глазное яблоко окружено фасциальной пластинкой — влагалищем,
поверх которого располагается жировое тело глазницы. Оно заполняет
пространство между глазным яблоком и костными стенками глазницы, обеспечивает
легкость движений глазного яблока как шарообразного сустава. Жировая
соединительная ткань глазницы обладает высокой гидрофильностью и отекает
в условиях задержки воды в организме. Особенности лица зависят также от
состояния век и клетчатки глазницы. Обеднение последней жировыми
отложениями приводит к западению глазного яблока.
96
Атрофия эластичных элементов век ведет к изменению тургора кожи и
появлению складок на веках. В частности, при набухании клетчатки век
возникают "мешки" под глазами, лицо становится одутловатым. Веки являются
сложными анатомическими структурами. Основная функция последних
обеспечивается подвижным взаимодействием составляющих их компонентов.
Представленные в виде парных складок, покрытые снаружи тонкой кожей, а
изнутри гладкой слизистой оболочкой конъюнктивы, они повторяют форму
глазного яблока за счет плотно прикрепленных к конъюктиве хрящевых
пластин. Фиброзные продолжения верхней и нижней хрящевых пластин образуют
связки, которые медиально прикрепляются к слезной кости и латерально — к
наружной стенке глазницы. Отрыв этих связок в результате травмы или
удаления новообразования, разрушение костных структур, к которым она
прикреплена, проявляются изменением формы и направления глазной щели в
области повреждения.
Подвижность век обеспечивается действием двух мышц — круговой
мышцы глаза, иннервируемой ветвями лицевого нерва, и мышцы,
поднимающей верхнее веко, иннервируемой ветвями глазодвигательного нерва (II пара
черепных нервов) [Золотко Ю. Α., 1964]. Некоторые специалисты выделяют
мышцу Мюллера, расположенную между апоневрозом мышцы, поднимающей
верхнее веко, и конъюнктивой, идущей от верхнего края хряща к своду,
который в свою очередь является частью мышцы, поднимающей верхнее веко в ее
•нижнем отделе [Holmström Η. et al., 1986; Caraway J. E., 1987]. Иннервация
мышцы Мюллера осуществляется симпатической нервной системой. В
состоянии напряжения последняя обеспечивает подъем века на 2—3 мм, в
отсутствие тонуса — опущение его. Двигательные мышцы, помимо обеспечения
движений век при мигании и во время сна, поддерживают их на
определенном уровне. Эта функция связана с большинством анатомических структур
век. Выворот нижнего века может быть обусловлен дефицитом кожи при ее
Рубцовых изменениях или избыточной резекции, потерей тонуса круговой
мышцы глаза при параличе, перерастяжением хрящевой пластины или
отрывом кантальной связки. В свою очередь птоз верхнего века может быть
вызван изменениями мышц (при врожденных нарушениях или травме) или
апоневроза (при возрастных изменениях).
Экспрессия лица обеспечивается иннервируемыми лицевым нервом, 20
парными мимическими мышцами, 12 из которых расположены в области
средней зоны лица [Freilinger G. и др., 1987]. Согласно данным названных
авторов, наиболее важная группа мышц — подниматели верхней губы, которые
находятся на четырех уровнях соответственно местам их прикрепления и
глубины залегания.
Основные подниматели верхней губы — это большая скуловая мышца и
мышцы, поднимающие верхнюю губу и угол рта. Первая из них начинается
от скуловой кости кпереди от скуловисочного шва на втором уровне
залегания. В верхнем и боковых отделах она покрыта круговой мышцей глаза и
поверхностной порцией малой скуловой мышцы, относящимися к первому
уровню. Далее большая скуловая мышца направляется к углу рта, где ее
поверхностные фибриллы переплетаются с мышцей, опускающей угол рта,
щечной и мышцей, поднимающей угол рта. Второй по важности является мышца,
поднимающая верхнюю губу. Она прикрепляется у орбитального края выше
подглазничного отверстия. Ее верхнемедиальные отделы в области
прикрепления формируют носогубную складку, а латеральные идут к круговой мышце
рта, лежащей поверхностно по отношению к ней (третий уровень). Только
самые глубокие волокна мышцы сплетаются с другими поднимателями угла рта.
Мышца, поднимающая угол рта, прикрепляется в области тела верхней че-
7-1263
97
люсти ниже подглазничного отверстия, наполняет клыковую ямку и
направляется вниз, входя в сплетение поднимателей верхней губы. Частичная или
полная утрата этих мышц в результате травмы или резекции приводит к
выпадению движений различных областей лица. Кроме того, отсутствие точек
прикрепления мышц, например после резекции верхней челюсти, выключает
их из работы (опущение век, сглаженность носогубной складки).
Не менее важной функцией, выполняемой мимической мускулатурой,
является сфинктерная. Работу ротового сфинктера обеспечивает круговая мышца
рта и поддерживающие ее подниматели верхней губы. Ротовой сфинктер
участвует в речи, жевании и глотании. Он обеспечивает водонепроницаемость при
формировании пищевого комка, способствует эвакуации слюны из ротовой
полости как офаничитель. Кроме того, одной из составных частей сфинктерной
системы является щечная мышца, расположенная глубоко в щеке. Сзади она
прикрепляется к крылочелюстному шву и вплетается в волокна круговой
мышцы рта, сверху офаничивается верхней, а снизу — нижней челюстью. Покрытая
изнутри слизистой оболочкой, она участвует в функции сосания, свиста,
продвижении пищи при жевании и эвакуации ее из полости рта. Слизистая
оболочка щеки в свою очередь должна быть достаточно подвижной, чтобы
перемещать пищу при жевании, и достаточно тонкой для неограниченного
смыкания зубов. Натяжение тканей при глотании предотвращает застревание
пищи в щечных бороздах.
В анатомическом аспекте наружный нос как функциональный орган
может быть разделен на три отдела: костный, верхний хрящевой и нижний
хрящевой своды. Они имеют поддерживающую (костную и хрящевую)
перегородку, которая делит полость носа на две самостоятельно функционирующие
половины.
Костный свод сформирован выступами фронтальных отростков верхних
челюстей, которые соединяются с носовыми костями. Парные носовые кости
соединены корнем носа: вверху — с лобной костью, внизу — с верхним
хрящевым сводом, представленным латеральными хрящами. Хрящ перегородки
по центру разделяет верхний хрящевой свод и поддерживает кончик носа и
крылья, сформированные крыльными хрящами и фиброаденоидной тканью
(в заднебоковых отделах). Гибкие крылья носа могут растягиваться
мимическими мышцами при дыхании или мимике.
По мнению J. Sheen A992), костный свод носа с его свободно лежащим
верхним хрящевым сводом, соединенный с перегородкой, может быть
представлен в виде строительной "балки", распространяющейся от корня до
основания носа.
Носовые ходы открываются в носовые полости, которые расположены над
твердым небом и отделены одна от другой носовой перегородкой. Каждая
носовая полость имеет переднее и заднее отверстие, дно, крышу, боковую и среднюю
стенки, представленные носовой перегородкой. Дно каждой носовой полости
сформировано горизонтальной пластинкой небной кости. Крыша носовой
полости состоит из трех частей: передней, чей скат представлен нижней
поверхностью носовых костей, средней, сформированной решетчатой пластинкой
решетчатой кости, которая обеспечивает проникновение обонятельного нерва в
носовую полость, и задней частью крыши, образованной передней и задней
поверхностями тела основной кости, которая сзади соединяется с крышей
носоглотки. Носовые полости выстланы очень тонкой плотно прилегающей
слизистой оболочкой.
Слизистая оболочка на поверхности средней и верхней носовых раковин
общей площадью 240—500 мм2 содержит специальные обонятельные клетки.
Обоняние зависит от влажности обонятельной области слизистой оболочки
98
носа, которая должна быть оптимальной. Сухость слизистой оболочки, ее
чрезмерное набухание или увлажнение при воспалительных процессах
(насморк) приводят к утрате способности ощущать запахи.
Нос выполняет важную респираторную функцию. Эффективное дыхание
может быть достигнуто только через нос, который обеспечивает
контролируемое равновесие в фазах вдыхания и выдыхания. Так, при глубоком вдохе
работа мышц крыльев носа и внутренних клапанов продуцирует
контролируемое увеличение сопротивлению вдыхаемого воздуха.
За доставку воздуха через нос ответственны следующие компоненты: но-
согубной угол, мышцы крыльев, внутренние клапаны и раковины. Носогуб-
ной угол эстетически и функционально должен составлять от 90 до 115°.
В этих пределах преддверие находится в наилучшей позиции для
кондиционирования воздуха, доставляемого во внутренние части. Неправильно
ориентированный поток воздуха вызывает сильный порыв в носовых полостях,
повреждающий слизистую оболочку, результатом чего являются сухость и
метаплазия [Sheen J., 1992].
Форма основания носа оказывает прямое влияние на дыхательную
функцию. Последняя зависит от опорных структур — перегородки и латеральных
хрящей и мягких тканей. При уменьшении проекции кончика носа ноздри
меняют свою позицию, в результате чего меняется направление и объем тока
воздуха и возникают нарушения. Уменьшение преддверия носа в той или иной
степени вызывает функциональные изменения от легкого дискомфорта и
затруднения очищения носовой полости до полного отсутствия дыхания через нос.
Индивидуальные различия формы наружного носа зависят от
особенностей его костной и хрящевой основы. Профиль носа обусловлен формой
носовых костей и величиной угла, под которым они отходят от лобных костей,
а также глубиной переносья. Корень носа может иметь глубокое,
поверхностное, высокое или низкое положение относительно лба. Спинка носа,
сформированная боковыми хрящами и отчасти хрящом перегородки носа, бывает
в той или иной мере выпуклой, прямой или вогнутой. Контур и профиль носа
зависят от взаиморасположения носовых костей и указанных хрящей.
От угла, под которым сходятся боковые хрящи, нос может быть более
или менее плоским; хрящ перегородки носа при этом имеет большую или
меньшую длину. Если этот хрящ разрушается (при травме, особенно
характерной для боксеров, а также в результате патологического процесса), то
спинка носа западает. Хрящи крыльев формируют нижнюю часть носа. В
зависимости от вертикального размера крылья носа могут быть более или менее
высокими или низкими. При длинных массивных хрящах кончик носа
выступает кпереди. "Курносый" нос образуется при значительном отклонении
хрящей крыльев кверху. "Висячий" нос, который иногда полностью прикрывает
верхнюю губу, наблюдается в тех случаях, когда хрящи крыльев резко
наклонены книзу. Таким образом, форма наружного носа зависит от
взаиморасположения составляющих его костных и хрящевых элементов [Куприянов В. В.,
Стовичек Г. В., 1988].
Кожа наряду с другими анатомическими образованиями придает лицу
неповторимость. Ее состояние оценивают по окраске, степени эластичности
и упругости. Строение кожи на лице принципиально не отличается от
такового на других участках тела. В коже различают поверхностный слой —
эпидермис и глубокий слой — собственно кожу, связанные между собой
соединительнотканными сосочками различной величины. Высота сосочков на
лице и шее незначительна, что обусловливает тонкость и гладкость кожи на
этих участках в отличие от более плотной и шероховатой кожи на других
участках тела. Толщина эпидермиса на щеке составляет 0,08—0,3 мм, на веках —
7*
99
0,05—0,15 мм, на губах — до 0,3 мм, на ладони — 0,7 мм, на внутренней части
пальцев — 0,9 мм, на подошве — 1 мм. Степень развития эпидермиса,
выраженная числом слоев формирующих его клеток, несомненно, зависит от
локальных механических воздействий на кожу: чем сильнее и систематичнее
физическое воздействие, тем более толстым становится эпидермис.
Систематическое влияние на кожу лица оказывают мимические мышцы,
волокна которых прикрепляются в области ее сетчатого слоя. На тех
участках, где под действием мышц наиболее часто возникают складки, образуются
морщины, имеющие индивидуальный рисунок в зависимости от
особенностей психики человека и типа его высшей нервной деятельности. Однако при
всем многообразии индивидуального рисунка морщин есть общие
закономерности их формирования под влиянием систематического сокращения тех
мышц, которые работают чаще. Варианты строения мышц также играют
существенную роль. Лучистые морщины вокруг глаз образуются в основном
глазничной частью круговой мышцы глаза. Морщины вокруг рта в первую
очередь являются следствием действия его круговой мышцы, а также мышц
верхней и нижней губ и щечной мышцы.
Подкожная основа образована рыхлой соединительной тканью с более
или менее значительным жировым скоплением. Под кожей век такая основа
отсутствует, в области лба, спинки и крыльев носа выражена слабо (толщина
не более 2 мм), а на губах и щеках более толстая. Подкожная соединительная
ткань (клетчатка) является резервуаром питательных веществ (жир),
участвует в терморегуляции и играет защитную роль. Степень развития этой
клетчатки на лице, как, впрочем, и на других участках тела, зависит от половых
и возрастных особенностей, а главное, от качества питания.
Кожа лица исключительно подвижна, легко смещается, что
обусловливает возможность пластических операций с косметической целью и при
устранении дефектов.
23.2. Принципы планирования пластических операций на лице и шее.
Особенности операций на мягких тканях
Деформации и дефекты открытых частей лица тяжело отражаются на
психическом состоянии пациента. Люди, вынужденные носить защитные повязки,
испытывающие затруднения при контакте с окружающими и во время приема
пищи, становятся раздражительными, часто замыкаются в себе. Особенно
травмирует больных невозможность членораздельной речи, необходимость
письменно объяснять свои желания. Находясь в состоянии постоянного
напряжения, они легко выходят из равновесия, активно демонстрируя свое
недовольство непонятливостью окружающих.
Поскольку пластическую операцию врач производит для больного,
причем процесс восстановления утраченной ткани иногда продолжается
длительное время, растягиваясь на несколько этапов, то прежде всего должно
быть налажено взаимное сотрудничество между врачом и пациентом.
Искусство хирурга оценивается по объективно регистрируемым критериям —
краткости восстановительного периода, функциональным и косметическим
результатам. Степень участия пациента не поддается точному определению, во
многом субъективна, но нередко приобретает решающее значение. У любого
хирурга, длительное время занимающегося восстановительными операциями,
имеется печальный опыт послеоперационных осложнений, возникших по
вине больного (отрыв филатовского стебля, вторичный некроз пересаженных
тканей из-за передавливания их при неправильном положении тела во сне,
100
инфицирование из-за несоблюдения осторожности в период между
перевязками и т. д.).
Всего этого можно избежать, если поставить пациента в известность о
характере операций, их количестве и продолжительности, а также результатах
промежуточного лечения. Если пациент знает, что перемещенная на область
дефекта ткань вначале будет избыточна, выступать над поверхностью кожных
покровов, но в дальнейшем это различие удастся нивелировать
хирургическим путем, он с большим пониманием воспримет промежуточный результат
операции. Больной должен представлять себе, какая деформация может
возникнуть на донорском участке и согласиться на выбор зоны формирования
пластического материала с учетом эстетических и функциональных
нарушений. Многие люди, особенно молодого возраста и женщины, легче
соглашаются на функциональные потери, чем на появление рубцов на открытых
участках лица и тела.
Практически всегда имеется несколько возможностей проведения
пластической операции. Пациента следует в общих чертах ознакомить с их
особенностями. Например, мягкотканный дефект, образующийся после
иссечения кожи с подлежащими структурами, может быть устранен за счет
свободной пересадки кожи, аутотрансплантации ткани с реваскуляризацией,
применения филатовского стебля. Первый способ самый простой и
надежный, но не позволяет восстановить контуры поверхности (останется
углубление); возможна пигментация или восстановление прежней окраски при
обширных невусах и гемангиомах.
Аутотрансплантация многослойной ткани с микрососудистой техникой
не имеет указанных недостатков и может быть выполнена в один этап, но при
этом возможны неэстетичные рубцы в донорской зоне, всегда имеется риск
неудачи и возникает необходимость в проведении новых операций.
Устранение дефекта с помощью филатовского стебля можно провести с наименьшими
потерями — сформировать стебель в косметически закрытых зонах (паховая
область, внутренняя поверхность плеча), но лечение длительное, сопряжено
с вынужденным положением больного.
Окончательное решение остается за хирургом, так как он учитывает
соматическое состояние больного, возможность его перенести сложную
операцию, определяет характер повреждения окружающих дефект тканей и т. д.,
однако при обсуждении с пациентом способа пластики он должен побудить его,
соответственно расставляя акценты, согласиться с его планом, т. е. сделаться
соучастником лечения. Иногда при категоричной приверженности больного
какому-то не самому эффективному, но достаточно удовлетворительному
способу улучшения эстетического или функционального результата, следует
не переубеждать его, а выполнить операцию ограниченного объема.
Важно помнить, что имеется три категории людей, оценивающих
результаты восстановительного лечения. Наименее строгий судья, как правило,
хирург, который знает объективные возможности методов реконструкции и
бывает удовлетворен, если удалось воссоздать форму и функцию утраченного
участка. Как ни странно, но больной зачастую недостаточно придирчиво
оценивает результаты лечения, так как за время пребывания в стационаре он
наблюдал аналогичные деформации у других пациентов и прямо или косвенно
осознал реальность конечного результата лечения. Наиболее предвзятые и
жестокие судьи — здоровые лица, не имеющие никакого отношения к
медицине и лично не знакомые с пациентом. Недостаточно выдержанные люди,
особенно дети с их непосредственностью, могут высказывать негативное
отношение к остаточной деформации, которая причиняет больному
неприятные ощущения, формируя комплекс неполноценности, несмотря на опти-
101
мистичные заверения хирурга о блестящих результатах лечения. Каждый раз,
разрабатывая стратегию восстановительного периода, следует по
возможности ориентироваться на заключение людей третьей категории.
Основное правило реконструктивной хирургии — восстановление
отсутствующих тканей подобными им. Для достижения наилучших
функциональных и анатомических результатов каждый участок дефекта необходимо
детально изучить для оценки не только наступивших качественных изменений,
но и количественного измерения дефекта каждой ткани. Кожа со следами
лучевого повреждения, несмотря на видимую жизнеспособность, является
сомнительным пластическим материалом и во многих случаях должна быть
иссечена. В. С. Дмитриева и А. Н. Алексеева A985), изучавшие состояние
кровообращения поверхностных тканей у облученных пациентов методом
нанесения жидких кристаллов, установили, что фактические границы
дегенеративных изменений превышают определяемые визуально. Они
указывают, что бедная васкуляризация этих областей служит препятствием к
прорастанию сосудов в пересаженные стебельчатые лоскуты.
Однако к данной проблеме можно подходить по-другому, если
планировать перемещение в эти зоны тканей с независимым от них кровоснабжением.
Если атравматично подготовить воспринимающую поверхность, то можно
сохранить практически все мягкие ткани, а через некоторое время
констатировать заметное улучшение их цвета и тургора в результате прорастания
сосудов из хорошо васкуляризованного пластического материала.
Особенно сложно планировать восстановительную операцию у больных
со злокачественной опухолью. В настоящее время четко прослеживается
тенденция одномоментного пластического возмещения удаленной опухолевой
ткани. Хирург должен решать одновременно две задачи — полноценно удалить
опухоль и максимально полно закрыть дефект. Лучше, если операции
производят разные специалисты. Онколог, не думая о возможном дефиците
пластического материала, спокойно удаляет опухоль в надлежащих пределах, затем
хирург, широко владеющий приемами пластики, устраняет дефект. В
действительности операцию чаще всего выполняет один врач, от которого тем не менее
следует требовать высокой квалификации в обоих разделах хирургии.
Основная задача пластических операций состоит в передвижении тканей
к дефекту. Наилучшие результаты получаются при использовании местной
пластики, пересадка поверхностных тканей из отдаленных областей, включая
свободную пересадку кожи, часто требует последующей коррекции. Основным
фактором, влияющим на приживление тканей, является степень их
кровоснабжения. Наиболее понятной зависимость тканей от кровотока становится при
сравнении круглого стебля и лоскутов с осевым сосудистым рисунком.
Круглый стебель, предложенный В. П. Филатовым в 1916 г., произвел
качественный переворот в восстановительной хирургии. Формируемый без учета
зон кровоснабжения кожи при традиционном соотношении длины и ширины
1:1 или 1,5:1, но на двух питающих ножках (что в совокупности дает
коэффициент 2:1 и 3:1) за время созревания стебель фактически превращается в
самостоятельный кожный орган с осевым строением сосудов. Е. В. Груздковой A969)
и Ε. Φ. Черновым A969) доказано, что в стебле, подготовленном для
миграции, сосуды располагаются параллельно его оси, т. е. образуется замкнутая
система кровообращения. Развитие собственной сосудистой системы в
стебле происходит неравномерно: повышение притока крови в области ножек по
сравнению с окружающей кожей начинается уже на 2-е сутки, выравнивание
сниженного кровотока в центральном участке отмечается на 15—20-е сутки.
Артериальная система концевых отделов сохраняет афферентную
иннервацию, перестройка здесь незначительна. Максимальная дилатация, "вы-
102
прямление" сосудов наблюдаются в центре, в денервированной зоне. Эти
сосуды расширены, атоничны и не способны к местным изменениям. Условия
в них оптимальны для распространения крови: они шире нормальных, но не
настолько, чтобы вызвать тромбоз. По мере созревания стебля
метаболические процессы во всех отделах приближаются к норме, но после отсечения
одной из ножек сбалансированное состояние вновь нарушается и на этот раз
концевой участок попадает в условия сниженного питания. Повторная
стабилизация кровообращения происходит через 3—6 нед. Снижение кровотока
в отсеченном конце стебля сопровождается тканевой гипоксией, что
способствует более быстрому прорастанию сосудов в стебель из зоны миграции,
начинающемуся уже на 3—4-й день. О влиянии этого явления на скорость
развития новой сосудистой сети сообщали многие авторы. Реорганизация
сплетения состоит в уменьшении числа, но в увеличении диаметра сосудов.
Стимулом является изменение степени тканевой ишемии в течение
короткого периода.
Для ускорения созревания сосудистой сети в стебельчатом лоскуте
предложены методы механической, биологической и медикаментозной тренировки.
Тренировать стебель во всех случаях рекомендует и Ф. М. Хитров A984). Ряд
авторов возражают против механической тренировки стебля. "Слишком
высокий уровень гипоксии оказывает тормозящее влияние на развитие стебля, так
как при этом преобладают анаэробные обменные процессы, менее
эффективные в энергетическом отношении, чем аэробные" [Неупокоев Н. И., 1972].
В настоящее время считается доказанным, что биологическая
тренировка, т. е. предварительное подсечение с боков стебельчатого лоскута,
выкраиваемого на одной сосудистой ножке, позволяет формировать лоскут
большей длины при той же ширине. Фактически основу выкраивания
лоскута составляют предварительное подсечение кожной ленты и этапная
миграция.
R. Smith A973), изучая кровоснабжение стебля в зависимости от места
его формирования, доказал, что при включении поверхностных сосудов в
одну из его ножек удается создать полноценный стебель при соотношении
длины и ширины даже 8:1. Кожные лоскуты, поднятые без учета артериального
питания кожи, выживали только в соотношении 3:1 при двух ножках и 1:1
при одной ножке. Автор предложил изменить тактику выкраивания стеблей
по естественным складкам кожи и формировать их вдоль подкожных сосудов
осевого строения, назвав их "осевыми", или "регионарными".
Кровоснабжение кожи осуществляется за счет сосудистого сплетения из
подкожной жировой клетчатки, плотность которого неравномерна. Вблизи
от поверхностной артерии давление в сосудах выше и кровь течет в ту
сторону, где давление меньше, до тех пор, пока сопротивление крови на
соседних участках не выравнивает эту разницу. Равновесие между давлением двух
сетей сосудов обозначается как граница кровоснабжения, однако она
условна, поскольку уменьшение периферического сопротивления в одной области
позволяет крови из другой распространиться на большее расстояние. В
результате предварительного подсечения дистальной ножки лоскута
прекращается встречное давление со стороны пересеченных сосудов, а оставшееся
количество сосудов увеличивается и кровоснабжение из центрального отдела
улучшается. Фактические границы зоны с осевым кровообращением выше
определяемых при контрастировании сосудов, поэтому при подъеме лоскута
с сохранением питающей ножки допустимо включать в периферическую
часть дополнительный участок подкожной жировой ткани из расчета 1:1.
Добавочный фрагмент кожи рассматривается как стебельчатый лоскут,
выкроенный без учета кровоснабжения.
103
J. M. Gregor A976) установил, что соотношения длины и ширины
неприемлемы для кожных или "островных" лоскутов: основное значение имеет
не ширина ножки, а величина кровотока.
Согласно закону Пуаселья, перепад давления на концах трубки прямо
пропорционален расходу жидкости, ее вязкости, длине трубки и обратно
пропорционален четвертой степени внутреннего радиуса трубки. По этому закону
сосуд диаметром 1,6 мм пропускает в 256 раз больше крови, чем сосуд
диаметром 0,4 мм, а при увеличении его просвета еще на 0,4 мм, т. е. до 2 мм,
кровоток будет в 625 раз выше, чем через сосуд диаметром 0,4 мм.
Таким образом, кровоснабжение лоскута, обладающего единственным
большим сосудом, в несколько раз лучше, чем лоскута с большим числом
мелких, хаотично расположенных сосудов. В связи с этим известный ранее
факт формирования подкожного сплетения из мелких перфоративных
сосудов, поднимающихся вертикально от глубжележащих тканей, в сочетании с
самостоятельными подкожными сосудами приобрел новое значение для
пластической хирургии, так как при локализации ножки даже над одним из них
его кровоснабжение значительно увеличивается (схема 23.1).
Схема 23.1. Классификация лоскутов [Tolhurst D., 1987]
Ножка лоскута
кожная без кожи:
сосудистая,
подкожные ткани1
одна две фасциальная,
мышечная
Кровоснабжение лоскутов
аксиальных
свободно
ориентированных
Кожа, жир, фасция,
мышцы, хрящи, кости,
составные кожно-фасциальные t
и кожно-мышечные
Специальная подготовка
лоскутов
подсечение тканевое
растяжение
Предназначение
лоскутов
Формирование
лоскутов
местные
ротационных
отдаленные
транспозиционных
специальных
на ножке свободные
двухлопастных ромбовидных
104
Наряду с оценкой кровоснабжения перемещаемых тканей не меньшее
значение имеет геометрическое планирование их передвижения. Одной из
первых работ по геометрическому планированию пластических операций
считается работа Ю. К. Шимановского A865). Автор применил систематизацию
известных в то время пластических операций по принципу формы изъянов
соответственно фигурам треугольника, четырехугольника, круга и эллипса.
Геометрический принцип выбора способа оперативного вмешательства
значительно расширил кругозор хирургов и оказался ценным для того времени.
Более глубокое изучение основных закономерностей пластических
операций показывает, что их систематизация в зависимости от форм изъянов
является тем не менее односторонней и поэтому в настоящее время не может
быть принята за основу построения системы пластических операций на
поверхности тела человека вообще.
Век спустя принципы планирования местнопластических операций
нашли отражение в известной работе А. А. Лимберга, вышедшей в 1946 г. под
названием "Математические основы местной пластики на поверхности
человеческого тела". Автор внес в пластическую хирургию точные математические
расчеты. Применение математического анализа дает возможность предвидеть
и четко описывать все изменения положения тканей, которые происходят в
процессе пластической операции.
В развитие своих идей А. А. Лимберг в 1963 г. опубликовал следующую
монографию, посвященную этой же теме. Он критически оценил
имеющийся опыт и пришел к заключению, что внедрение математики в эту область
хирургии способствует созданию математически обоснованных построений и
показателей как для пластического формообразования, так и для оценки
результатов пластических операций.
Впервые в области пластической хирургии были широко использованы
принципы стереометрического разбора операций на жестких бумажных
моделях. Графическое построение фигур пластических операций и определение
внешних границ моделей были выполнены по единому геометрическому
алгоритму. Подбор материалов и построение моделей проводили таким образом,
чтобы процессы перемещения, растяжения и сокращения тканей были
видны отдельно друг от друга в четких математических определениях. Автор
подчеркивал, что отсутствие полного совпадения форм геометрических фигур с
таковыми на участках поверхности тела до и после операции не мешает
применению этого метода учета и планирования изменений формы, так как
благодаря эластическим свойствам кожи можно сглаживать все угловатости фигур,
создаваемых при пластической операции.
В дальнейшем идеи математического анализа при планировании
операции нашли отражение в работах других авторов. Алла А.Лимберг A994)
установила возможность математического моделирования исходов контурной
пластики хрящом в зависимости от состояния реципиента, донора и
способов воздействия на хрящевую ткань до ее пересадки. Построена
математическая модель, определяющая границы трех областей возможных исходов
лечения: сохранения хряща, его рассасывания, неопределенных результатов, когда
равновероятны исходы как с сохранением, так и с рассасыванием хряща.
Надежность построенной математической модели отвечает 95 % уровню.
Алгоритм оптимального планирования контурной пластики
определяется правилом L2 = L" — L\, где L2 — характеристика используемого
пластического материала, L" — граница области положительных исходов
пластики, L| — исходное состояние реципиента.
Для практической работы рассчитаны специальные кодировочные
таблицы, с помощью которых для каждого конкретного реципиента можно по-
105
добрать пластический материал, с наибольшей вероятностью ведущий к
положительному исходу пластики.
При выборе метода восстановления ушной раковины и определения
показаний к нему, а также для точного определения площади необходимого
покровного пластического материала мы считаем наиболее информативным
метод расчета площади дефекта и площади пластического материала с помощью
предложенного коэффициента отношения площадей. Использование арте-
риализированного пластического материала при правильном планировании
оперативного вмешательства, предварительном математическом обосновании
достаточности площади лоскута для повторения объемной формы опорно-
удерживающего каркаса по сравнению с общепринятыми методами аурикуло-
пластики позволяет значительно расширить показания к их применению.
В течение многих десятилетий планирование восстановительных операций
основывалось на эмпирических началах, опыте предшественников и личном
опыте каждого хирурга. При планировании восстановительной операции
необходимо решить ряд задач: какой тип ткани будет использоваться, в каком
объеме требуется идентифицировать донорскую зону и как лучше подготовить
реципиентную зону. Для упорядочения этих задач Е. A.Luce A995) предлагает
проводить планирование по следующей схеме: 1) оценить дефект и
дисфункцию; 2) определить силы, влияющие на образование дефекта; 3) определить
достигаемый идеал; 4) составить последовательный план достижения идеала;
5) согласовать требования плана с возможностями и желаниями пациента.
Одним из наиболее и широко распространенных средств планирования
восстановительных операций является применение выкроек и восковых
шаблонов. Двухмерные выкройки из бумаги или ткани для определения формы и
размеров кожных трансплантатов использовали П. И. Емиленко A980) и А. Г.
Мамонов A985), лоскутов на лице — В. М. Мессина A968), регионарных и
отдаленных артериализированных лоскутов — А. И. Неробеев A988). Л. А. Бру-
сова A996) для определения формы и размеров силиконовых имплантатов
применяла восковые шаблоны, изготовленные на масках лиц пациентов. А. И.
Неробеев и соавт. для этих же целей у пациентов с гемиатрофией лица использовали
восковые шаблоны, соответственно которым формировали артериализирован-
ные лоскуты. По ним подготавливали восковые шаблоны для создания модели
утраченных тканей носа, по которым выкраивали лоскуты на лбу.
J. Pribaz и соавт. описали методику измерения трехмерных дефектов с
целью определения необходимого количества тканей и ориентации эпители-
зированных поверхностей свободных лоскутов при выполнении
реконструктивных операций. Используя слепочную массу, авторы интраоперационно
устанавливали размеры и форму дефекта. После этого, обернув полученную
модель тканью, переводили ее из объемной в плоскостную ориентацию.
Получив выкройку, соответственно ей формировали лоскуты.
Выкраивание артериализированных лоскутов проводят соответственно
анатомическим ориентирам, установленным многими авторами.
G. Taylor и J. Palmer A987) исследовали кровоснабжение кожи и
подлежащих тканей на свежих человеческих трупах и изолированных конечностях.
В сосуды вводили красители, затем трупы препарировали и выполняли
рентгенографические исследования. По данным этих авторов, кровоснабжение
кожи и подкожных тканей осуществляется трехступенчатой системой
артериальных сосудов. В большинстве случаев кровоснабжение участка кожи и
соответствующего участка подкожных тканей происходит из одного
источника. На основании этого факта предложена концепция ангиосомов.
Артериальные сосуды находятся в соединительнотканных футлярах.
Первичная артерия сопровождается множеством мелких коллатеральных сосудов,
106
идущих от терминальных ветвей артерий, кровоснабжающих глубокие ткани.
В среднем в каждом опыте было выявлено по 374 крупные "перфорантные"
артерии, кровоснабжающие отдельные ангиосомы. Полученные данные, а также
разработанная карта артериального кровоснабжения позволяют выбрать
оптимальные разрезы для выкраивания кожных лоскутов.
Другие авторы применили зонд Допплера типа "Huhtleigh Niiii Dopplex"
(8 МГц) со способностью "прослушивать" ткани на глубине 2—3 см для
определения топографии подкожных артерий-перфорантов (ПАП) у 10 больных.
Целью исследования было определение основания оси, размера лоскута для
местной, отдаленной или свободной пересадки кожи. Расположение ПАП
диаметром более 0,5 мм на туловище и конечностях у больных помечали краской:
оно соответствовало тому, которое отмечали на коже свежих трупов при
введении в их сосуды окиси свинца и последующей рентгенографии.
Определив у больного с помощью зонда Допплера три ближайших ПАП
на предполагаемом участке, соединяли эти точки линией-осью и намечали
границы лоскута. Обычно брали кожно-подкожный лоскут, а на конечностях
и на голове еще и глубокую фасцию. Применение зонда Допплера требует
навыка. Звуковой сигнал его следует сравнивать с сигналом от парастернальных
ПАП, которые обычно имеют диаметр более 0,5 см. Интенсивность звука
регулируют, чтобы она была невысока. В ряде случаев трансплантат выгодно
брать по ходу нервно-сосудистых пучков, а также на участках, где кожа
подвижна. Применение зонда Допплера может оказать надежную помощь при
выборе участка для взятия лоскута.
J. Pribaz и соавт. A992) использовали ультразвуковой допплер-прибор для
определения хода лицевой артерии при подъеме предложенного
одноименного мышечно-слизистого лоскута для устранения дефектов полости рта.
В последнее десятилетие при планировании челюстно-лицевых
операций получил развитие метод компьютерного моделирования.
23.3. Методы компьютерного моделирования
Компьютерное двухмерное моделирование развивалось и использовалось в
теоретических разработках с 1974 г., прогрессируя в трехмерное с 1975 г. Вначале
применение компьютеров носило чисто теоретический академический характер,
но это был шаг к практическому использованию компьютерной техники. Начало
клиническому применению этой техники для трехмерного моделирования
изображения положила работа J. Marsh и M.Vaiiider A983). Исследование было
посвящено разработке и реализации компьютерной томографии (KT) для получения
трехмерных изображений при рентгеновском сканировании тканей. Оценив
перспективы диагностического и клинического использования усовершенствованной
KT, основанной на трехмерном моделировании, J. Marsh продолжал изучать
возможности использования микропроцессорной техники при трехмерном
моделировании, что дало толчок к развитию повседневной клинической диагностики и
черепно-лицевой хирургии с целью планирования операций.
Авторы применяют сканированные срезы, произведенные на аппарате Soma-
ton-2 (фирма "Siemens", Германия) с разрешающей способностью 256 х 256 пиксел,
используя от 30 до 64 двухмиллиметровых срезов в зависимости от объема
тканей. Сканограммьі были представлены на эвалускопе. Программа,
написанная на языке Fortran IV, реализована в алгоритме построения образов на
основании данных KT, что позволило отображать ткани с разных сторон,
показывать кости и рассчитывать конфигурацию мягких тканей. Изображение
можно было развертывать и поворачивать под разными углами.
107
В дальнейшем J. Marsh и соавт. A986) продолжили работу по
использованию компьютера для построения трехмерных изображений. При
использовании усовершенствованной компьютерной системы удавалось получить
одновременное изображение всех слоев тканей и более детализированное
представление о костных структурах и линиях переломов костей. Авторы
представили революционную программу, "оживляющую" изображение для показа
движений нижней челюсти. Для этого они использовали около 100
двухмиллиметровых KT с разрешением 512 х 512 пиксел. Работа была выполнена на
мини-компьютере ѴАХ-11/730 с использованием языка программирования
Fortran 77 и связана с современным процессором получения изображения и
системой программного обеспечения "International Imaging System". Анимация
образа с помощью специального программного обеспечения Movie byu
позволила изучать артикуляцию нижней челюсти, моделировать
корригирующие операции и прогнозировать результаты.
С.Cutting и соавт. A986) описали результаты, полученные при
разработке трехмерного компьютерного моделирования черепно-лицевых
операций, дающего возможность комбинировать цефалометрические и
томографические модели. С использованием своей системы авторы стали
проектировать оптимальные расстояния для движения костей и
планировать разрезы, костные реконструкции, достигая тем самым наилучшей
имитации нормальной формы.
K.Fukutura и соавт. A990) представили детальный отчет о работе по
созданию зеркальных образов в трехмерном изображении в черепно-лицевой
хирургии. Применяя сканирование на аппарате GЕСТ/Т 9900, авторы создавали
зеркальные образы контралатеральных, неповрежденных тканей при
реконструкции односторонних дефектов. Они использовали цифровое
воспроизведение зеркальных образов посредством программного обеспечения "Oblique",
которое позволяло, базируясь на данных асимметричной KT, планировать
нужную симметрию.
Трехмерное моделирование с использованием данных КТ-сканирования
выполняли способом зеркальных изображений, используя теоретические
модели и коммерческие системы моделей с помощью компьютера для
преобразования результатов сканирования в изображения.
Развитие методов сканирующей рентгеновской или
магнитно-резонансной томографии отчасти зависело от прогресса в создании недорогих, но
мощных компьютеров и программного обеспечения.
M.Matoyoshi и соавт. A994) разработали систему трехмерных измерений
лица человека для комплексного использования, обеспечивающую высокую
точность и простой ввод информации в персональные компьютеры.
Применяя эту систему, можно автоматически измерять двухмерные координаты
сотен точек сетки на фотографии лица человека. В качестве считывающего
устройства использовали зеркальный сканер, а расчет трехмерных координат
осуществляли с помощью компьютера. Информацию о лице человека
вводили до и после операции с помощью катодных лучей, в результате чего
получали данные измерения трехмерных координат.
В настоящее время средствами получения данных для компьютерного
моделирования являются KT, ядерно-магнитная резонансная томография (МРТ)
иУЗИ.
Компьютерное трехмерное моделирование — прогрессивный метод
диагностики и планирования хирургического лечения. Преимуществом этого
метода является возможность воспроизводить дооперационное состояние
пациента, планировать операции и прогнозировать результаты, получать естественных
размеров пространственную модель поврежденных тканей и изготавливать им-
108
плантаты или шаблон точных размеров для подготовки имплантата,
использовать для обучения студентов и начинающих хирургов.
Недостатками этой технологии являются необходимость иметь
дорогостоящее оборудование, а также проблемы, связанные с его эксплуатацией,
необходимость привлечения к работе на постоянной основе
высококвалифицированных специалистов по созданию нового программного обеспечения и
обслуживания техники, продолжительность процедуры, быстрое моральное
старение систем в результате развития диагностических и компьютерных
технологий.
Несмотря на то что KT как метод диагностики нашла широкое
применение в черепно-лицевой хирургии, сообщений об использовании
компьютерного моделирования в этой области хирургии в отечественной литературе
мы не встретили.
Компьютерное моделирование пластических операций. Мы использовали
двухмерное компьютерное моделирование с целью определения его
возможностей и роли в планировании операций. Технологический комплекс для
планирования изменений в зубочелюстно-лицевой системе в результате
стоматологических и оперативных вмешательств был разработан в 1992 г. фирмой
"Стоик" (Объединение "Стоматология"). В состав комплекса входят
высокоразрешающая видеокамера (стандарт Ні8 или SVHS), компьютерная станция на
базе РС-486, оснащенная устройствами ввода-вывода видеосигнала, комплект
взаимосвязанных программ, в том числе специализированная программа
Picture Man, цветной термопринтер Primera с набором расходных материалов.
Процесс компьютерного моделирования с использованием программы
Picture Man можно разделить на следующие этапы: получение данных, анализ
данных, обработка изображения, сравнение первичных и отредактированных
изображений, вывод данных на принтер и печать. Полученные данные
.образуют первое звено в цепи преобразований между пациентом и компьютером.
В идеальном варианте обследование должно быть непродолжительным, чтобы
не представлять неудобства для пациента, достаточно точным для получения
оптического изображения и не давать существенных побочных эффектов.
В наших наблюдениях исходную информацию получали при помощи
видеокамеры, подсоединенной к компьютеру. При планировании челюстно-
лицевых операций производили съемку лица пациента анфас, в профиль с
двух сторон и при необходимости — в прикусе.
Ввод изображения в память компьютера не занимал много времени.
Просмотр нескольких проекций изображения одновременно расширял
возможности при проведении анализа и решении вопроса о том, какие
изменения следует внести в облик пациента для достижения положительного
результата. Возможности программы позволяли нанести на изображение сетку,
делящую лицо на квадраты, что способствовало выявлению скрытой
асимметрии при сравнении относительно срединной оси.
С целью объективизации данных проводили измерения между
фиксированной точкой на срединной оси и заданными точками на
противоположных сторонах лица, выраженной в пикселах. Полученные данные являлись
относительными величинами, однако определяли степень различия при
сравнении. Осуществив определенные расчеты, с учетом масштаба
изображения и количества единиц изображения (пиксел) в 1 см определяли
абсолютную величину. При необходимости аналогичные измерения можно
провести на боковых снимках, сравнивая обе стороны.
Процесс моделирования изображения зависит от возможностей
программы, которая позволяет провести следующие основные виды обработки:
зеркальное отображение, смещение и вставку различных фрагментов, дорисовку
109
или удаление, сжатие или растяжение, изменение текстуры, цвета и четкости
границ, сглаженности цветового перехода.
Первоначально мы выделяли область, которую предполагалось как-либо
изменить, после чего вносили желаемые коррективы. Они могли быть
выполнены в одной области или включать несколько областей на изображении
лица пациента, что зависело от вида дефекта или деформации и объема
хирургического лечения, которое предполагалось провести для получения
планируемого результата.
Процесс моделирования можно осуществлять по двум направлениям: 1)
создать идеальный образ, исходя из своих эстетических представлений и желания
пациента; 2) внести только те изменения, которые можно реально получить,
выполняя планируемые оперативные вмешательства. По нашему мнению,
первый вариант целесообразен только в тех случаях, когда хирургу нужно
понять желание пациента. Внести изменения в изображение в этом случае может
любой человек, имеющий опыт работы на компьютере и уяснивший задачу.
Второй вариант, которому мы следовали, предполагает непосредственное
участие в моделировании хирурга, который создает модель, результирующую
оперативное вмешательство. Профессиональный уровень хирурга предполагает
достаточный опыт, знания и ментальное видение результата, который можно
достигнуть при выполнении планируемой операции. Можно моделировать
несколько изображений соответственно планированию различных операций.
Обрабатывая изображение, мы вносили необходимые коррективы,
создавая новое изображение, которое наиболее реально отражало те изменения,
которые могли возникнуть в результате операции. При изучении изображения
на экране можно было более точно оценить изменения и, составив ментальный
план операции, визуализировать его результат на экране. Возможности
программы позволяют увеличить корригируемый фрагмент изображения в 2, 4 или
8 раз для достижения большей точности в передаче формы и цвета, а затем
соответственно уменьшить масштаб. Новую моделированную копию
изображения можно ввести в память компьютера и продолжить работу, создавая
другие варианты.
Выводя на экране монитора оригинал и смоделированный результат или
несколько их вариантов одновременно, мы проводили сравнение, оценку и
выбор оптимального из них. Документирование полученных данных позволяло
ознакомить пациента с возможными результатами операции или ряда
операций и привести его ожидания в соответствие с реальными возможностями.
Однако при сложных дефектах лицо человека меняется в трех размерах и
невозможно понять объемные изменения полностью, применяя только этот метод.
Таким образом, компьютерное моделирование на основе программы
Picture Man является прогрессивным шагом в планировании операций.
Метод позволяет воспроизводить дооперационное состояние пациента,
помогает совершенствовать анализ нарушений и составление плана операции,
моделировать послеоперационные результаты.
Преимуществами используемого технологического комплекса являются
доступное и относительно недорогое оборудование, возможность
непосредственного участия хирурга в процессе моделирования.
Естественно, что, пользуясь простой компьютерной техникой, трудно
выявить все индивидуальные нюансы объемной анатомии объекта для
пластической коррекции. Тем не менее моделирующие системы имеют высокую
консультативную ценность. Воображение хирурга может помочь представить
непосредственный и отдаленный результаты вместе с изменениями мягких и
твердых тканей, что способствует формированию оперативного плана, а
пациенту позволяет понять то, что его ожидает. Простой персональный ком-
110
пьютер неспособен воспроизвести трехмерные модели, но может облегчить
выбор стратегического плана лечения для хирурга, представить
последовательность и результаты лечения пациенту.
23.4. Основные принципы пластической хирургии
Атравматичная техника. Главное внимание хирурга должно быть уделено
бережному отношению к тканям, так как большинство пластических операций >
сопровождается нарушением кровоснабжения тканей, их деваскуляризацией
в процессе перемещения на новое место. Ткани с редуцированным
кровообращением легко подвергаются воздействию микроорганизмов, которые
способны усилить процессы девитализации. Поскольку ткани имеют различную
структуру с характерным распределением основных волокон, оперативное
вмешательство следует выбирать по принципу максимально осторожного их
разъединения.
Используя так называемую атравматичную технику, следует помнить об
условности данного термина, так как во время операции всегда повреждаются
клетки. Многовековой опыт хирургии, подкрепленный последними
экспериментальными исследованиями, свидетельствует о том, что лучше заживают
раны, вызванные острыми инструментами. Разрозненные ткани легче
инфицируются и подвергаются некрозу. Очищение раны от некротического
компонента, нередко находящегося в глубоких слоях, сопровождается усилением
воспалительных процессов, вызывающих за счет сдавления дополнительную
гибель клеток. Начавшееся сравнительно недавно широкое изучение
микрохирургической техники позволило убедиться в преимуществе щадящих
методик выполнения операций под увеличением.
Основные инструменты хирурга при формировании пластического
материала — скальпель и ножницы. Если отсутствует навык определения точки
скальпеля вручную, то лучше пользоваться съемными лезвиями. Используют
лезвие бритвы, которое обламывают с одной стороны и вставляют в
иглодержатель. Для разъединения тканей удобны и сосудистые ножницы. Тонкие, но
тупые кончики их в сочетании с узкими изогнутыми щечками облегчают
поэтапное рассечение тканей. Так называемое тупое разъединение тканей
кровоостанавливающими зажимами, возможно, оправданное при вскрытии
флегмон, неприемлемо в пластической хирургии. Во время насильственного
разрыва тканей за счет перерастяжения, происходящего при тупой отсепа-
ровке, клеточные элементы и кровеносные сосуды повреждаются на большем
протяжении и зона ишемии увеличивается.
Целью операции формирования пластического материала является изъятие
определенного участка ткани, которое в любом случае должно сопровождаться
нарушением структурных взаимоотношений. Все сосуды и нервы,
препятствующие освобождению лоскута, все равно должны быть пересечены, но лучше
сделать это аккуратно и последовательно. Разведение краев раны,
необходимое для улучшения обзора операционного поля и перемещения тканей,
выполняют с помощью небольших острых крючков, которые последовательно
передвигают по мере углубления раны, или при помощи швов-держалок по ее
краям. Фиксация кожи хирургическими пинцетами вызывает кровоизлияния
и размозжение тканей в точках приложения кончиков пинцетов. Это особенно
заметно на следующий день после формирования филатовского стебля.
Гемостаз, гематома — одно из наиболее частых осложнений после
операции. Необходимость лигирования кровоточащих сосудов (диаметром 1,5 мм
и более) очевидна. Отношение к способу остановки кровотечения из мелких
111
источников различно. Наиболее часто используют два метода —
электрокоагуляцию кровоточащего участка биполярным пинцетом и прошивание или
перевязывание его после наложения кровоостанавливающего зажима. С точки
зрения атравматичности предпочтение надо отдать первому способу при
условии аккуратного выполнения манипуляции. Пинцетом следует захватывать
только стенки сосуда. Грубая коагуляция окружающих тканей,
сопровождающаяся их некрозом, может привести к поздней кровоточивости.
Прошиванием и перевязкой тканей удается уменьшить эту опасность, но, во-первых,
эти действия удлиняют операцию, во-вторых, наличие в ране большого
количества инородного материала, особенно кетгута, благоприятствует
развитию воспаления.
Определенные сложности возникают во время проверки нижней
поверхности сформированного лоскута на кровоточивость. Для осмотра раны
лоскут обычно отводят в сторону или переворачивают на 180°. В результате
пережатия ножки кровотечение может временно прекратиться и после
возвращения тканей на место возобновиться. Целесообразно проводить осмотр
лоскута в положении физиологического покоя. Если это невозможно и
сохраняется опасность последующего кровотечения, то в ране оставляют выпускники.
Отношение к дренированию чистой послеоперационной раны также
неоднозначно. В условиях хорошего гемостаза всегда лучше полностью закрыть
рану. Резиновые выпускники связывают дно раны с внешней средой и при
случайном загрязнении их во время перевязки из-за недостаточного
соблюдения асептики могут служить проводниками инфекции в глубину раны.
Для осушения раны можно использовать отрицательное давление.
Активное дренирование проводят, как правило, при ушивании (^бширных
раневых поверхностей и вероятном накоплении крови в глубине раны после
операции, а также при образовании пустот в подкожных тканях, в частности
после изъятия крупной мышцы, удаления обширной опухоли. Активное
выведение жидкости из раны целесообразно и во время небольших операций,
а также в тех случаях, когда необходимо добиться плотного слипания всех
слоев раны для получения точных контуров воссоздаваемого органа — ушной
раковины, носа и т. д. Основное условие, которое необходимо выполнять
при создании отрицательного давления, — герметичное ушивание раны.
Дренажную трубку выводят через специальное отверстие, наложенное вне
линии швов, и плотно фиксируют шелковой нитью. Для дренирования
обширных ран используют перфорированную резиновую или полиэтиленовую
трубку диаметром до 0,4—0,5 см, прикрепленную к резиновой груше.
Отсасывание содержимого из небольших ран осуществляют тонкими
хлорвиниловыми катетерами, соединенными с емкостью из полиэтилена. Полиэтиленовые
бутылки различного размера широко распространены в быту, легко
стерилизуются, стенки их прозрачны, что облегчает контроль их наполнения. По мере
заполнения емкостей их опорожняют, предварительно пережимая катетер у
выхода из раны. Слишком большое отрицательное давление может вызвать
повреждение стенок ушитой раны с появлением вторичного кровотечения,
поэтому после выполнения пластических операций принудительное
отведение содержимого с помощью водяных или электроотсосов не производят.
Ушивание раны — самая длительная часть большинства пластических
операций. Качество выполнения этого этапа в значительной мере
обусловливает конечный результат лечения. Тонкий, малозаметный рубец
получается не только при использовании оптимального для данных структур шовного
материала, но во многом зависит от знания хирургом структуры тканей и
условий их натяжения. Линии естественного образования кожных складок на
лице детально описаны еще Леонардо да Винчи. Они формируются в основ-
112
ном под влиянием специфического расположения мимических мышц.
Фиброзные и коллагеновые элементы кожных структур распределяются вдоль
этих линий, в связи с чем ушивание вдоль их слоев сопровождается меньшим
рубцеванием.
Натяжение тканей имеет большое значение для заживления раны. Так
называемые разгрузочные швы не должны применяться во время
пластических операций. Использование их доказывает ошибочность концепции
хирурга при планировании пластической операции. Исключение составляют
способы ушивания донорской раны в случае необходимости формирования
пластического материала в большом объеме. Натяжение тканей неизбежно
приводит к образованию гипертрофического рубца, который может появиться
через несколько недель после операции. Во время операции трудно оценить
точно степень натяжения тканей. Она зависит от толщины кожи, ее
эластичности, направления кожных линий. Основной критерий чрезмерного
натяжения — побледнение кожи вдоль линии шва. Если оно не исчезает в течение
15 мин, то необходимо распустить швы и применить другой способ закрытия
раны — провести перемещение ее краев пластикой или ротационными
лоскутами или использовать пересадку свободной кожи.
Во время послойного ушивания раны обращают внимание на аккуратное
сопоставление в одном слое глубоких участков раны. Так, соединение
мышечных структур облегчает сближение подкожной жировой клетчатки, а
ушивание ее на уровне поверхностной фасции позволяет свободно наложить швы
на кожу. Глубокол ежащие ткани соединяют Π-образными или узловыми
швами. Я. Золтан A984) рекомендует применять двухслойный шов из
полиамидной нити в тех случаях, когда края раны удается свести без видимых усилий.
Швы на кожу накладывают в различной последовательности. Длинные
линейные раны на открытых участках тела лучше зашивать внутрикожным
швом, но возможно и прямое наложение швов из тонкого материала на
атравматичной игле или рыболовной лески. Многие хирурги используют
правило дихотомического деления прямой линии: вначале накладывают шов
в центре, затем в центре оказавшихся боковыми участков, последние снова
делят швами пополам и т. д. Постепенное соединение кожи в разных местах
препятствует образованию "собачьего уха" по краям конуса. Если в результате
последовательного ушивания раны сформировался кожно-жировой конус, то
его иссекают в виде треугольника с основанием, обращенным к ране.
В послеоперационном периоде широко используют давящие повязки и
местную гипотермию. Сдавление раны одновременно с охлаждением
предотвращает развитие гематомы, однако наложение повязок на лице не всегда
эффективно. С этой целью применяют сетчатые бинты с прорезями для глаз, рта.
23.5. Устранение дефектов и рубцовых деформаций средней зоны лица
Средняя зона лица человека представляет собой область головы, которая в
большей степени, чем другие, характеризует внешний вид личности. Глаза,
нос, рельеф средней зоны являются основными носителями красоты лица и
выражения эмоций. Повреждения в этой зоне, кроме обезображивания,
мешают нормальному выполнению основных функций организма: зрения, дыхания,
пищеварения. Средняя зона поддерживает основание черепа, обеспечивая его
стабильность. Скуловые кости и верхняя челюсть служат опорой для глаз и ме-
Раздел написан совместно с В. И. Малаховской.
8-1263
113
Рис. 23.1. Гемиатрофия лица (схема).
а, б — деформация контуров лица; в — деформация лицевого черепа.
а ^j^^ б ч^— в
Рис. 23.2. Виды несквозных дефектов с повреждением опорных структур {а—в) (схема).
диально отделяют глаза от дыхательных путей. Околоносовые пазухи
регулируют прохождение воздуха, а также служат иммунологическими резервами и
компенсируют силу ударов в область лицевого скелета, уменьшая амплитуду
вызванных колебаний. Верхняя челюсть особенно важна как вертикальная
опора лица, поддерживающая глаза снизу, а зубы — сверху и являющаяся
промежуточной областью между нижней зоной лица, полостью рта и черепом.
Средняя зона лица — это анатомическое и функциональное объединение трех
комплексов: носоверхнечелюстного, ротовой полости и глазничной области.
Цель реабилитации пациентов с дефектами средней зоны лица
заключается в восстановлении нормальных анатомических и функциональных
взаимосвязей между этими тремя комплексами в различных комбинациях.
Основополагающими факторами успешной реабилитации являются
планирование последовательных хирургических мероприятий и выбор оптимального
метода оперативного вмешательства на каждом этапе и в каждом конкретном
случае с учетом клинико-функциональных, эстетических, социальных и
экономических предпосылок. Тщательный анализ дефекта, полное понимание
функциональных и анатомических взаимосвязей являются решающими при
планировании реконструктивных операций.
Дефекты средней зоны лица образуются в результате опухолей,
огнестрельных ранений, травм, ожогов, врожденных нарушений с
изолированным или сочетанным повреждением тканей на различных уровнях.
Преобладание последствий хирургического лечения опухолей в мирное время и
огнестрельных ранений в годы войны нашло отражение в многочисленных
классификациях. Тем не менее нам неизвестно ни одной классификации,
позволяющей идентифицировать многообразные проявления дефектов средней
зоны лица на основе ведущих клинических характеристик.
Независимо от причины дефекты характеризуются значительной
потерей тканей на различных уровнях и разнородных по структуре. Проблемы,
возникающие при их устранении, связаны со сложным рельефом средней
зоны лица, ограниченными возможностями использования пластического
материала из близлежащих областей и многочисленными реконструктивными
вмешател ьствами.
Методы реконструкции средней зоны лица отражают развитие
пластической хирургии в целом. Рассматривая многочисленные классификации
дефектов на лице и анализируя собственный значительный материал (более 150
наблюдений), мы пришли к выводу о целесообразности унификации и
упрощения подхода к восстановительным операциям. С этой целью нами
разработана схема дефектов, в соответствии с которой мы рекомендуем
планировать восстановительное лечение: 1) поверхностные несквозные дефекты,
ограничивающиеся мягкими тканями (рис. 23.1); 2) несквозные дефекты с
преимущественным повреждением опорных структур (рис. 23.2); 3)
несквозные дефекты, включающие мягкие ткани и опорные структуры; 4) сквозные
дефекты мягких тканей (рис. 23.3); 5) сквозные дефекты, включающие
опорные структуры (рис. 23.4); 6) комбинированные дефекты, в том числе
повреждения всех тканей на разном протяжении (рис. 23.5); 7) дефекты в
результате огнестрельных ранений (рис. 23.6).
Основной задачей при устранении поверхностных дефектов лица является
создание непрерывного кожного покрова из тканей, близких по цвету и
текстуре, соответствующей толщины и объема. При планировании операций мы
учитываем локализацию, размеры и глубину дефекта и состояние
окружающих тканей.
Известно, что наилучшим пластическим материалом для закрытия
дефекта по своим характеристикам (текстура, цвет) являются ткани соседних
115
8*
Рис. 23.3. Виды сквозных дефектов с потерей костной основы (а—в) (схема).
Рис. 23.4. Виды сквозных дефектов мягких тканей средней зоны лица (а— в) (схема).
Рис. 23.5. Виды комбинированных дефектов лица (а—в) (схема).
Рис. 23.6. Дефекты в результате огнестрельных ранений (схема).
Рис. 23.7. Замещение дефекта центральных отделов щеки ротационным лоскутом (схема).
а — смещение обширного кожно-фасциального лоскута со щеки и шеи без вертикального разреза
на шее; б — смещение лоскута с вертикальным разрезом на шее; в — смещение маленького лоскута;
г — смещение длинного лоскута. Указаны участки треугольного иссечения кожи по внешнему краю
для предотвращения образования конусовидных выпячиваний;
областей лица. В соответствии с классификацией D. Е. Tolhurst и соавт. A991)
их использование в виде транспозиционных, ротационных и продвинутых
лоскутов ограничено размерами дефекта и состоянием окружающих тканей.
Так называемые random flap — лоскуты, выкроенные наугад, моделируют без
учета кровообращения, что сопряжено с риском возникновения застойных
явлений и краевого некроза. Кроме того, использование местных тканей
связано с образованием дополнительных рубцов.
С этой точки зрения выгодно отличается описанный в 1917 г. Эссером
шейно-лицевой ротационный лоскут (рис. 23.7), модифицированный други-
118
Рис. 23.7. Продолжение.
д — больной с рубцовой деформацией подглазничной области справа до и после операции.
ми хирургами [Juri J., Juri С, 1979; Cholucky Т., 1995; Stark R., Kaplan J., 1972].
Он позволяет устранить как ограниченные, так и обширные поверхностные
дефекты, включающие одну—две анатомические области, расположенные
преимущественно в центральных отделах лица. В результате применения
такого лоскута большая часть рубцов может быть скрыта в естественных
складках кожи. Артериализированные лоскуты со лба сочетают в себе
преимущества независимого кровообращения и идентичность цвета и
текстуры кожи.
Свободные кожные трансплантаты позволяют восстановить кожный
покров значительных размеров, но существует проблема сокращения их
размеров в послеоперационном периоде и несоответствия цвета. Кроме того,
использование кожных трансплантатов при глубоких дефектах не позволяет
восполнить дефицит объема тканей. В связи с этим свободные кожные
трансплантаты мы применяли только при дефектах, ограниченных кожей.
Кожный трансплантат ретроаурикулярной области по цвету и толщине
соответствует коже век, однако он также подвержен сокращению размеров в
послеоперационном периоде. По этой причине для пластики век при пол-
нослойных дефектах мы применяем многослойные лоскуты. Используемые
нами для этих целей транспозиционные лоскуты лба — надбровный, васку-
ляризованный через надбровные сосуды, и лоскуты, артериализированные
ветвями поверхностной височной артерии, удовлетворяют требованиям
пластики (рис. 23.8). Кроме того, варианты лобных лоскутов на скрытой
сосудистой ножке, васкуляризованных через поверхностные височные сосуды,
позволяют произвести пластику век в один этап без последующего
сокращения перемещенных тканей и при необходимости восстановить ресничный
край, избежать деформаций донорской области.
119
Рис. 23.8. Пластика верхнего века лоскутом височной области.
а — дефект века. В височной области швы после пересадки свободной кожи: б — дублированный
кожный лоскут поднят на сосудах; β — раны после ушивания.
Дефекты большей глубины, образующиеся при иссечении кожи и
подкожной жировой клетчатки, необходимо закрывать послойно для
исключения западения тканей. Перенос свободных лоскутов из отдаленных областей
с последующей их реваскуляризацией дает возможность устранить дефекты
различной площади и глубины. Лоскут выбирают соответственно задачам
реконструкции.
Кожно-фасциальные лоскуты по своим характеристикам лучше
соответствуют поверхностным дефектам. Один из наиболее тонких лоскутов —
лучевой подходит для устранения дефектов глубиной 0,5—0,7 см в пределах
кожи и подкожной жировой клетчатки. Более глубоким дефектам соответствует
лопаточный лоскут, толщина клетчатки которого колеблется от 1 до 2 см.
Для пациентов, которым необходимо восстановить утраченные мышцы,
единственно приемлем кожно-мышечный лоскут. Имеется широкий выбор
кожно-мышечных лоскутов: из прямой мышцы живота, широчайшей мышцы
спины, нежной мышцы и др. Мы отдаем предпочтение торакодорсальному
лоскуту, учитывая его преимущества: надежность, длинный
сосудисто-нервный пучок, расположение донорской зоны в косметически малозначимой
области, радиальную ориентацию мышечных волокон. Длина сосудистой ножки
торакодорсального лоскута является важным фактором при пластике арте-
риализованными лоскутами. Это объясняется отдаленностью средней зоны
лица от наиболее часто используемых реципиентных сосудов — лицевых,
язычных, наружной яремной вены. Надежность анастомозов играет
решающую роль при выборе аутотрансплантата, а перенесенный лоскут можно
истончить при последующей коррекции.
Аутотрансплантацию свободных лоскутов для устранения
поверхностных дефектов мы применяем в тех случаях, когда пластика местными
тканями не представляется возможной, а использование свободного кожного
лоскута не позволяет достигнуть хороших эстетических результатов. К таким
случаям мы относим: 1) обширные дефекты, включающие несколько
областей или всю среднюю зону лица; 2) обширные дефекты, расположенные в
боковых отделах средней зоны лица; 3) необходимость восстановления
мимической мускулатуры; 4) рубцовые*изменения окружающих тканей.
При устранении несквозных дефектов покровных тканей и опорных
структур возникает необходимость в восстановлении кожных покровов, контуров и
опоры. Однако при дефектах костей и хрящей опора нарушена не всегда. У
некоторых пациентов в результате повреждения или недоразвития костей и
хрящей изменены контуры лица. Примерами таких дефектов являются
прогрессирующая гемиатрофия лица и недоразвитие облученных в детстве структур.
Мы считаем, что в отсутствие дефекта кости на протяжении преобладают
нарушения контуров лица. Детальное рассмотрение вопроса о нарушениях опоры
или контуров лица является принципиальным, так как хирургическая тактика
в таких случаях может быть различной. При восстановлении опоры для
пластики используют ткани или материалы, способные выдерживать нагрузку без
изменения своих контуров (кости, хрящи, металлические конструкции).
Традиционный подход к устранению комплексных дефектов мягких и
костных тканей предусматривает первоначально восстановление мягких
тканей для создания ложа, а затем — проведение опорно-контурной пластики.
Использование сложных кожно-костных лоскутов позволяет
одномоментно восстановить как покровные ткани, так и опору, а кожно-мышечных
и кожно-фасциальных лоскутов — устранить дефект кожи и создать
необходимые контуры лица. Для этого мы используем кожно-мышечные и кожно-
фасциальные лоскуты, выкраивая их таким образом, чтобы их мышечно-
жировая часть восполняла утраченный объем тканей, создавая контуры, а
121
кожная часть устраняла дефект кожи. Подобную тактику мы применяем при
дефектах с многослойной утратой тканей.
Выбор лоскута и его дизайн мы осуществляем, исходя из характеристик
дефекта, объема отсутствующих покровных тканей и подлежащих структур,
состояния реципиентных сосудов. При полнослойном дефекте на всей площади
моделирование в один этап невозможно провести из-за опасности нарушения
кровообращения и потери лоскута. В связи с этим в начале восстановительного
лечения мы переносим определенный объем тканей, коррекцию которых
проводим при повторной операции. Повторное вмешательство заключается в
перераспределении подкожной жировой клетчатки в виде жировых лоскутов на
ножке из областей избытка тканей в области дефицита. В случае отсутствия
дефицита тканей избытки жировой клетчатки иссекаем или аспирируем.
Вопрос о необходимости создания опоры окончательно не решен. На наш
взгляд, при дефектах средней зоны лица показанием к проведению пластики
опорных структур являются вызванные их отсутствием функциональные
и(или) грубые эстетические нарушения. Чаще всего такие нарушения
возникают после тотальной резекции верхней челюсти, в том числе дна глазницы и
при дефектах костно-хрящевой опоры носа. В первом случае возникает
смещение глазного яблока с деформацией и нарушением зрения, во втором —
деформация и затруднение дыхания. На необходимость создания опоры для
глазного яблока указывают многие авторы. Что касается устранения дефекта
передней стенки и альвеолярного отростка верхней челюсти при тотальном
поражении, то к решению этого вопроса подходят дифференцированно.
Большинство авторов [Brown К., 1968; Bartkowski S. et al., 1986; Fisher J.,
1986] считают, что резекционный протез верхней челюсти удовлетворительно
компенсирует все функциональные нарушения и является опорой для мягких
тканей средней зоны лица. Учитывая это, мы проводим опорную пластику
нижнего края, дна, верхней и боковых стенок глазницы и костно-хрящевого
отдела носа с использованием в большинстве случаев титановых
перфорированных пластинок. Выбор титана для замещения утраченных структур
обусловлен следующими его характеристиками: биоинертностью, коррозионной
устойчивостью, легкостью моделирования, устойчивостью к
инфицированию. Моделирование титановых конструкций мы проводим до операции на
маске лица пациента с последующей коррекцией во время операции.
Другим важным фактором, влияющим на выбор метода операции,
является причина образования дефекта. В условиях послелучевой дистрофии
тканей, выраженных рубцовых изменений, при дефектах значительной
длины без сохранения надкостницы успех костной пластики неваскуляризиро-
ванными трансплантатами может быть проблематичным [Coleman J., 1989;
Yaremchuk Μ., 1989; Gruss J. et al., 1991].
Артериализированные костные трансплантаты не зависят от этих
факторов, однако моделировать их сложно. Иногда им невозможно придать
необходимую форму из-за опасности отрыва от надкостницы и сосудистой
ножки. Титановые имплантаты легко моделировать, по толщине они вполне
соответствуют костям средней зоны лица. Их установку можно проводить
одновременно с пластикой мягких тканей (рис. 23.9).
Повреждения орбитальной области, как правило, сочетаются с
дефектами век и бровей. Комплексный подход предусматривает осуществление
операции одномоментно в максимальном объеме (рис. 23.10). Так, при
дефектах скулоорбитальной и подглазничной областей выполняют весь объем
тканей, осуществляя свободный перенос кожно-мышечного торако-дорсаль-
ного и кожно-фасциального височного лоскутов для восстановления брови
или век или одномоментно формируют мягкие ткани и опорные структуры,
122
Рис. 23.9. Устранение дефекта носа аутотрансплантатом с предплечья (схема).
а — дефект носа. Видны лицевые артерия и вена, пунктиром указана локализация сосудистого
пучка; б —^шаблон из воска, имитирующий отсутствующий нос; в — на предплечье уложен
развернутый шаблон; расположение сосудов; г — формирование внутренней выстилки в верхнем отделе
дефекта носа; д — дефект устранен, пунктиром указаны сосуды.
Рис. 23.9. Продолжение.
е, ж — больной с дефектом носа и глазницы до и после операции; з, и — больной с дефектом носа
до и после операции.
Рис. 23.10. Замещение дефекта щеки реваскуляризованным кожно-мышечным лоскутом
(схема).
а — сквозной дефект щеки; б — лоскут уложен на дефект, пунктиром указана его толщина; в — рана
ушита, видны микрососудистые анастомозы.
Рис. 23.11. Устранение сквозных дефектов частично деэпителизированным реваску-
ляризованным кожно-фасциальным лоскутом (схема).
а — внешние проявления дефекта; пунктиром указаны воспринимающие сосуды и путь
сосудистой ножки лоскута; б — истинные размеры дефекта лицевых костей; в — планирование
пластической операции; внутренняя выстилка образована из ткани кожно-фасциального лоскута;
г — деэпителизация и складывание лоскута; д — пациент после операции; е — дно и передний край
глазницы замещены титановой сеткой.
Рис. 23.11. Продолжение.
ж; з ~- больная со сквозным дефектом подглазничной области до и после операции.
используя преимущества артериализированных лоскутов и металлических
титановых конструкций. Объективная оценка дефекта и использование
преимуществ различных лоскутов позволяют в процессе одной операции осуществить
пластику разнородных тканей (рис. 23.11). При дефектах век, бровей и костей
области глазницы мы одномоментно восстанавливаем эти структуры,
применяя для устранения костного дефекта титановые конструкции, для
устранения дефекта мягких тканей орбитальной области и век — фасцию, а для
пластики брови — кожный фрагмент волосистой части головы.
Сквозные дефекты без потери опорных структур локализуются в области
щеки или губы и характеризуются полным или частичным их отсутствием.
Для удовлетворительного восстановления утраченных тканей щеки
необходимо воспроизвести форму, объем, текстуру и цвет утраченных наружных
тканей, внутреннюю выстилку достаточной площади, хорошей эластичности
и небольшой толщины с тем, чтобы создать верхний и нижний своды
преддверия полости рта, обеспечить свободное открытие рта и избежать
излишнего выбухания тканей в сторону зубных рядов. Кроме того, утрата
мимических мышц, обеспечивающих движения рта и сфинктерную функцию при
дефекте губ, требует замещения, а завершающей в реконструкции является
пластика красной каймы.
Факторами, обусловливающими выбор метода пластики, являются также
размеры дефекта и состояние окружающих тканей. Учитывая среднюю
площадь щечной области (по нашим данным, она составляет 23 см ), в случае
полного ее отсутствия или включения в дефект губ единственным способом
доставки пластического материала для внутренней выстилки и наружного
127
Рис. 23.12. Больной со сквозным дефектом подглазничной области.
а — до лечения; б — взятие трансплантата; а — в раннем послеоперационном периоде; г — через I год
после восстановительного лечения.
покрытия тканей является привлечение его из отдаленных областей (рис.
23.12). Для восстановления движений необходимы ткани, включающие
мышцу. Кроме того, функция утраченных мышц этой области может быть
воспроизведена только при фиксации мышечного трансплантата
соответственно их анатомической ориентации: при циркулярном, параллельном
линии смыкания зубов в области губ или косом (снизу вверх) на уровне
нижнего края щеки расположении. Последнее условие не позволяет использовать
кожно-мышечные лоскуты на ножке из большой грудной, трапециевидной и
широчайшей мышц спины, так как ограниченные дугой ротации, они не могут
быть ориентированы в нужном направлении.
Исходя из этого, одним из лучших методов восстановления утраченных
тканей и их реанимации мы считаем свободный перенос торакодорсального
кожно-мышечного лоскута. Его надежность, обусловленная сосудистой
анатомией, длина нерва, размеры, место расположения и многоплановость
использования позволяют оценивать этот лоскут как наилучший источник
пластического материала (рис. 23.13, 23.14).
Известны различные методы замещения утраченной мимической
мускулатуры лица при параличах лоскутом широчайшей мышцы спины.
Помещенный под отсепарованную кожу лица мышечный трансплантат после
регенерации нерва становится способным производить видимые сокращения.
При использовании кожно-мышечного лоскута и его реиннервации толстый
слой жировой клетчатки может ограничивать видимые движения и,
следовательно, нарушает симметричность двигательных функций по сравнению с
неповрежденной стороной лица. В таких ситуациях мы видим два пути
решения проблемы: 1) опрокидывание лоскута кожной поверхностью в сторону
полости рта и использование свободного кожного трансплантата или, по
возможности, ротационного лоскута из соседних неповрежденных областей для
восстановления покровных тканей; 2) обезжиривание лоскута путем прямого
иссечения подкожной жировой клетчатки или вакуумной ее аспирации.
Второй способ не является идеальным, так как приводит к образованию рубцов,
которые ухудшают экскурсии мышцы.
Мы считаем использование ротационных шейно-лицевых лоскутов
одним из лучших способов достижения текстурного и цветового соответствия
восстановленных тканей, хотя в межрегиональных эстетических
объединениях остаются рубцы. Однако формирование внутренней выстилки щечной
области кожной поверхностью торакодорсального лоскута приводит к
избыточному ее выбуханию в полость рта за счет значительной толщины
подкожной жировой клетчатки, в дальнейшем необходимо истончение лоскута.
При устранении сквозных дефектов средней зоны лица с потерей
костных структур наряду с пластикой мягких тканей возникает необходимость в
восстановлении опоры. В такой ситуации вопрос о методе вмешательства
решается по-разному. На наш взгляд, это обусловлено значимостью
функциональных нарушений, связанных с их отсутствием, и альтернативными вариантами их
устранения, а также соответствием объема и тяжести оперативного
вмешательства полученным результатам. Кроме того, на возможность реконструкции
верхней челюсти влияет этиологический фактор. Необходимость в наблюдении
за пациентами после резекции верхней челюсти исключает ее проведение.
При использовании свободных костных трансплантатов для пластики
верхней челюсти при сквозных дефектах проводят двухэтапное лечение: на
первом этапе создают хорошо васкуляризованное ложе, на втором —
выполняют костную пластику. Риск резорбции неваскуляризованной кости высок в
отсутствие надкостницы, при значительной протяженности дефекта и
двухточечной фиксации. Применение аутотрансплантата васкуляризованной кости
9-1263
129
Рис. 23.13. Варианты формирования кож-
но-мышечных лоскутов для контурной
пластики (схема).
а — кожно-мышечный лоскут заданной формы;
по краю лоскута оставлена кожно-фасциальная
площадка; б — две кожно-фасциальные
площадки: по краю и в центре по проекции перед
углом рта; в — подъем лоскута; г —
кожно-фасциальная площадка, расположенная
горизонтально по проекции скуловой области; д — две
кожно-фасциальные площадки: на месте угла рта
или верхней губы и по краю нижней челюсти
дает больше шансов для успеха.
Однако риск потери лоскута, сложность
метода и связанные с этим экономические
проблемы ограничивают возможность
более широкого его применения. По
мнению большинства авторов [Ваг-
tkowski S. et al., 1986; Wells M., Luce Ε.
1995], традиционно используемое зу-
бочелюстное протезирование верхней
челюсти дает хорошие результаты
благодаря обтурации дефекта и
восстановлению функций речи и жевания.
Целесообразность костной
пластики оправдана в случаях проведения последующей остеоинтеграции зубных
имплантатов и протезирования. Однако в нашей стране этот метод при
костной реконструкции еще не разработан и применение его ограничено в связи
с высокой стоимостью. Реконструкция верхней челюсти без последующей
зубной имплантации направлена главным образом на формирование проекции
средней зоны лица.
Правильный выбор наиболее подходящих тканей при устранении сквозных
дефектов и использовании соответствующих методов в большинстве случаев
позволяет создать контуры лица, симметричные с неповрежденной стороной.
Потеря нижнеорбитальной опоры при сохранившемся глазном яблоке,
бесспорно, вызывает необходимость восстановления ее в связи со смещением
глаза и следующими за этим эстетическими и функциональными
нарушениями. В отсутствие глазного яблока восстановление дна глазницы в большинстве
случаев утрачивает смысл. При таких дефектах цель операции заключается
преимущественно в исправлении эстетических недостатков и обеспечении эк-
топротезирования глазного яблока или полностью области глазницы, если
повреждено большинство структур придаточного аппарата глаза. Восстановление
утраченных мышечных структур подглазничной области, в основном подни-
мателя верхней губы, также нецелесообразно, поскольку связанные с этим
нарушения проявляются главным образом в опущении верхней губы и
сглаженности носогубной складки. Коррекцию последних проводят более
простыми статическими методами.
Качество восстановленной внутренней выстилки при устранении
дефектов подглазничной и глазничной областей и целесообразность ее создания не
имеют такой значимости, как при устранении сквозных дефектов щечной
области. Это связано с отсутствием той функциональной нагрузки, которую
выполняет слизистая оболочка щеки. Безусловно, использование многослойных
130
Г- t$y
tii
и
Рис. 23.14. Больная с пигментным волосатым невусом правой половины лица до (д, б)
и после (в, г) удаления и пластики.
тканей для образования внутренней выстилки гарантирует более высокую
степень ее надежности в заведомо инфицированной области. В то же время
эпителизация лоскутов расщепленным кожным трансплантатом дает вполне
удовлетворительные результаты.
По нашему мнению, подход к созданию внутренней выстилки, не
несущей динамической нагрузки, зависит только от локализации и величины
дефекта. При значительной толщине наружных тканей, восстановленных в
результате применения кожно-мышечных лоскутов, оправдано использование
расщепленных кожных трансплантатов, поскольку даже в случаях их
парциального некроза вторичная эпителизация не вызывает образования рубцовой
деформации покровных тканей.
При небольших сквозных дефектах также можно не формировать
полноценную внутреннюю выстилку многослойными хорошо васкуляризованными
тканями, превосходящими по площади размеры дефекта, в расчете на эпите-
лизацию по оппозиционному типу. В то же время пренебрежение качеством
внутренней выстилки при использовании для пластики кожно-жировых или
кожно-фасциальных тканей небольшой толщины, особенно в условиях
лучевой дистрофии, может привести к их частичной потере с рецидивом дефекта
или в лучшем случае к рубцеванию.
При восстановлении носа необходимость создания полноценной
внутренней выстилки, как и опорных структур, не вызывает обсуждения. Это
обусловлено его эстетической и функциональной значимостью для обеспечения
свободного прохождения потоков воздуха при дыхании. Преимущества применения для
пластики носа лоскутов со лба, в частности по методу Конверса, при тотальных и
субтотальных дефектах общеизвестны. Они объясняются идентичностью тканей
донорской и реципиентной зон и их кровоснабжения. В данной области
восстановление опорных структур при дополнительных оперативных вмешательствах
производят с использованием хрящевых аллотрансплантатов или силиконовых
имплантатов (Брусова Л. Α., 1996]. Применение с этой целью титановых
конструкций позволяет производить их фиксацию одновременно с восстановлением
мягких тканей, что предотвращает образование типичных складок на первом
этапе ринопластики и улучшает проекцию костно-хрящевого отдела носа.
Однако образование рубцов в области лба на участке гиперпигментиро-
ванной кожи после взятия лоскута приемлемо не для всех пациентов. Нами
разработан способ замещения тотальных и субтотальных дефектов носа,
который в отличие от метода Конверса позволяет осуществить одномоментную
реконструкцию мягких тканей и опорных структур носа без нанесения
дополнительных повреждений на лице. Используют аутотрансплантацию кож-
но-фасциального лоскута с предплечья для восстановления мягкотканного
компонента носа и металлическую сетку из титана в качестве опоры.
Внутреннюю выстилку создают за счет опрокидывания на 180° местных тканей с
краев дефекта. На нее помещают перфорированный титановый имплантат,
смоделированный по форме носа, а сверху его укрывают кожно-фасциаль-
ным лоскутом с предплечья, также моделируемым по форме носа. Реваску-
ляризацию осуществляют с сосудами верхних отделов шеи.
Предложенный способ дает возможность восстановить мягкие ткани и
опору носа одномоментно и избежать дополнительных повреждений на лице.
Это способ сочетает в себе преимущества как Т-образного стебля, так и ар-
териализированных тканей, что позволяет значительно сократить период
реабилитации и избежать дополнительных повреждений на лице.
Относительным недостатком способа можно считать неполное соответствие окраски
восстановленных тканей по отношению к коже лица. Повреждения в
донорской зоне минимальны и не вызывают чувства дискомфорта у пациентов.
132
Мы считаем целесообразным развитие принципов и методов устранения
комбинированных дефектов средней зоны лица с помощью филатовского стебля,
описанных в работах А. Э.Рауэра и Н. М. Михельоона A954), Ф. М. Хитрова
A954, 1984). Особенностью применяемых нами методов пластики является
использование артериализированных лоскутов с возможностью одноэтапного
устранения дефекта при широком выборе донорских тканей с различными
текстурными характеристиками.
При комбинированных дефектах, включающих боковые отделы лица,
сохраняется традиционный поэтапный подход: сначала восстанавливают отделы,
формирующие края грушевидного отверстия, а затем выполняют ринопластику.
Использование с этой целью микрохирургического переноса
артериализированных тканей сокращает период реабилитации за счет одномоментного
переноса блока тканей (см. рис. 23.10). Кроме того, включение в одну
операцию нескольких хирургических процедур и использование двух или трех
хирургических бригад также позволяют выполнить вмешательство в
максимально возможном объеме. Так, у пациентов с дефектами средней и нижней
зон лица восстановительные операции мы проводим в обеих зонах
одновременно. Например, одна бригада оперирует на лице, другая проводит подъем
лоскута, третья — забор гребешка подвздошной кости.
Перенос необходимого количества пластического материала к дефекту и
его устранение не являются завершающим этапом реабилитации пациента.
Сохраняется ряд проблем, требующих решения: несоответствие окраски и
контура восстановленных тканей по отношению к окружающим областям
лица, деформации, сопутствующие и возникающие при выполнении
операции дефекты, трудности проведения глазного и зубного протезирования,
обусловленные несоответствием протезного ложа.
Все лоскуты из отдаленных областей отличаются окраской от кожи лица.
Мы не выявили определенной закономерности в преобладании или снижении
пигментации в зависимости от вида лоскута. В связи с этим в наших
наблюдениях методом снижения текстурного и цветового несоответствия
восстановленных тканей была пластика ротационным шейно-лицевым лоскутом, что дало
хороший эстетический результат у всех пациентов (см. рис. 23.7, д).
Другим вариантом достижения цветового соответствия является дермо-
абразия лоскута, которая эффективна только при повышенной пигментации
восстановленных тканей.
Перемещение подкожно-жировых лоскутов из областей с избыточной
толщиной клетчатки в области, где ее мало, позволяет получить необходимые
контуры лица.
При устранении дефектов артериализированными лоскутами объем
восстановленных тканей зависит от анатомической толщины пересаживаемого
лоскута. В большинстве случаев при выборе метода доминируют и такие важные
характеристики, как надежность и функциональное соответствие.
Липосакция донорской зоны улучшает косметические результаты, но
включение ее в программу лечения приводит к отсрочке основной операции
и неприемлемо для некоторых пациентов.
Прямое иссечение жировой клетчатки, сопровождающее коррекцию
рубцов, и закрытая липосакция позволяют достичь полной симметрии при
избытке клетчатки лоскута. Кроме того, для создания необходимого рельефа
средней зоны лица мы перемещаем жировые лоскуты из областей с
избыточной толщиной клетчатки в области, где ее недостаточно.
В процессе устранения дефектов орбитальной области лоскутами из
отдаленных областей тела мы пришли к выводу, что формирование таких тонких
структур, как веки, из этих тканей не дает приемлемых эстетических резуль-
133
татов и что в случае полного отсутствия век при последующем эктопротезиро-
вании глазного яблока и век можно лучше имитировать утраченные структуры.
Пластика нижнего века и конъюнктивальной полости целесообразна только
при сохранности верхнего века. Применение артериализированного лоскута
для пластики брови у пациентов дало хороший результат во всех наблюдениях.
Даже в случаях эктопротезирования области глазницы бровь целесообразно
восстанавливать, так как это позволяет скрыть протез за оправой очков.
Взятие лоскутов из неповрежденных областей лица для пластики часто
вызывает их деформацию. Даже в случаях образования незаметных
послеоперационных рубцов возникает асимметрия по сравнению с
неповрежденной стороной лица (подъем брови, сглаженность носогубной складки,
выраженность морщин).
Реконструкция одной половины лица у людей среднего и пожилого
возраста сопряжена с некоторым несоответствием восстановленных отделов по
отношению к противоположной стороне в связи с такими возрастными
изменениями, как птоз и морщины. Эта разница особенно заметна в состоянии
век. Проведение эстетических коррекций — блефаропластики и(или)
иссечения избытка кожи на лице — несколько нивелирует эти отличия, улучшая
конечный эстетический результат. Перед зубным протезированием после
реконструктивных операций часто требуются различные коррекции с целью
формирования сводов полости рта, устранения микростомы и иссечения
избытков клетчатки в восстановленных тканях. Все эти вмешательства
удлиняют период реабилитации, но количество оперативных вмешательств можно
сократить за счет объединения нескольких коррекций в одну.
Таким образом, реабилитация пациентов с дефектами средней зоны
лица в большинстве случаев является многоэтапным процессом, направленным
на создание мягких тканей, опорных структур, восстановление функций и
эстетического соответствия. Рациональный подход к планированию и
проведению восстановительного лечения, сочетающий современные
достижения реконструктивной хирургии и традиционные методы пластики, а также
протетическое лечение, является залогом успеха.
23.6. Устранение дефектов областей лба, виска и глазницы
Деформации и дефекты мягких тканей верхнебоковых отделов лица
воспринимаются больными по-разному. Изолированные рубцовые изменения
наружных участков лба у молодых людей и женщин могут легко скрываться
волосами и не доставлять видимых огорчений. Отсутствие бровей, рубцовые
вывороты век, скальпированные раны лобно-височных областей вынуждают
пациентов носить защитные повязки, темные очки.
Возможности перемещения полнослойной безволосой ткани из
окружающих участков на лоб ограничены: сверху и с боков — волосяной покров,
снизу — скуловая область и веки. Формирование обширных лоскутов на ножке
в этой области может вызвать дополнительную рубцовую деформацию
открытой части лица.
Большинство дефектов мягких тканей лба при сохраненной
надкостнице закрывают путем свободной пересадки расщепленного или полнослойно-
го кожного лоскута. Ровная раневая поверхность в сочетании с малой, а при
повреждении лобных мышц полной неподвижностью реципиентной зоны
обеспечивают хорошее приживление трансплантата. Последующие дермоаб-
разии позволяют добиться идентичности цвета пересаженной и окружающих
тканей. При сохраненных лобных мышцах восстанавливается мимика лба и
134
образуются симметричные морщины, которые придают восстановленному
покрову естественный вид.
Подобным образом закрывают раны после удаления обширных
пигментных или волосатых невусов, сосудистых пятен, поверхностно расположенных
базалиом. О возможности перемещения тканей со здоровой половины лба
путем проведения послабляющих горизонтальных разрезов и небольшой
ротации лоскута сообщает J. Convers A977). Однако подобная методика не нашла
широкого распространения по причине образования дополнительных рубцов
и двухэтапности вмешательства, вызванной необходимостью иссечения
выпуклого конуса у нижней точки ротации лоскута.
Отсутствие надкостницы на дне раны существенно осложняет проблему
закрытия дефекта. Поскольку кортикальная пластинка покровных костей
черепа кровоснабжается из системы артерий, расположенных в мягких тканях,
немедленное ее укрытие предотвращает неизбежный остеомиелит и
отторжение. Прямая пересадка кожи на обнаженную поверхность кости
невозможна. Кость удаляют с помощью фрезы или долота до губчатого слоя либо
используют вторичную кожную пластику на грануляциях, для скорейшего
появления которых в кортикальной части кости создают множество
отверстий, через которые и появляется грануляционная ткань.
По нашему мнению, опасность отторжения поверхностного слоя кости
в значительной степени преувеличена. Мы неоднократно наблюдали
пациентов с отрывом обширных участков скальпа вместе с надкостницей, у
которых постепенно происходило гранулирование раны по концентрическому
типу со стороны сохранившихся мягких тканей без образования клинически
и рентгенологически определяемых секвестров. Однако перфорационные
отверстия ускоряют создание сплошного грануляционного поля. Добиться
уменьшения размеров дефекта можно за счет смещения вниз и к центру
границ волосяного покрова, т. е. уменьшения высоты и ширины лба.
Существуют почти неограниченные возможности формирования кожно-фасциаль-
ных лоскутов из скальпа. Чаще ткани перемещают по краям раны.
Известен способ ускоренного создания грануляций на дне раны за счет
временной миграции на нее полнослойного (вместе с надкостницей) лоскута
на ножке из скальпа. Через 2—3 нед прижившую часть скальпа отсекают ото
лба сразу же ниже уровня фиксации волосяных луковиц, т. е. расщепляют
лоскут в поперечной плоскости и возвращают на место. Образовавшуюся
раневую поверхность лба, представленную в глубоких отделах уже
надкостницей, а в поверхностных теменно-височным апоневрозом, укрывают
расщепленной кожей. Подобным образом в два этапа удается заместить дефекты
мягких тканей лба любых размеров. Раны в донорских областях временно
оставляют под мазевыми повязками. Мы использовали подобную методику для
устранения обширных дефектов мягких тканей и костных тканей лба, а также
прилегающего участка мозговой оболочки. Непрерывность мозговой
оболочки восстанавливали путем аутотрансплантации широкой фасции бедра.
Учитывая отсутствие кости, обратного смещения скальпированного лоскута не
проводили. Такие дефекты рекомендуется замещать аутотрансплантацией
реваскуляризованных тонких кожно-фасциальных лоскутов с тыла стопы,
дельтовидной и лопаточной областей. В качестве воспринимающих сосудов
используют поверхностные височные артерии и вены, а также лобные и над-
блоковые артерии и вены.
Сквозные дефекты лобно-височной области нуждаются в немедленном
закрытии для изоляции содержимого полости черепа от внешней среды.
Необходимо обеспечить многослойное тканевое покрытие, в которое в дальнейшем
можно будет пересадить костную ткань или поместить пластмассу. Наиболее
135
простой метод состоит в формировании и миграции на лоб филатовского
стебля, однако он требует нескольких подготовительных этапов и связан с
вынужденным наложением руки, фиксированной возле головы.
Дефекты лба можно замещать и многослойным кожно-фасциальным
лоскутом из заушной области. Рассекают до надхрящницы кожу по середине
задней поверхности ушной раковины, проводят разрез вниз, минуя
сосцевидный отросток, через 3—4 см поворачивают в сторону затылка, доходят до
границы волосяного покрова и направляют разрез параллельно первому,
сформируют языкообразный лоскут, включающий кожу ушной раковины и
сосцевидной области вместе с подлежащими тканями. Параллельные разрезы
продолжают по направлению к переднему краю ушной раковины
противоположной стороны, ориентируясь на проекцию теменной ветви
поверхностной височной артерии. Лоскут поднимают вместе с апоневрозом до тех пор,
пока дистальную его часть можно будет свободно расположить в нужном
отделе лба. Ширина кожной поверхности заушной области около 5—7 см, а
длина до 10—12 см, т. е. если эту часть лоскута положить горизонтально, то
можно полностью заместить всю поверхность лба. Раневую поверхность
ножки лоскута укрывают мазевой повязкой. Через 3—5 нед избыточную его часть
отсекают и возвращают на место.
D. Colemann A987) за счет имплантации тканевых экспандеров в
неповрежденные боковые отделы лба растягивает их до 250 см3 с одной стороны
и 100 см3 — с другой. После удаления экспандеров избыточной кожей
закрывают всю поверхность лба. Кровоснабжение кожно-жировых лоскутов на
ножке, несмотря на значительное увеличение в размерах, остается хорошим.
Обширные проникающие дефекты боковых отделов лба, сочетающиеся с
дефектами височной области и глазницы, удается заместить сложным кожным
лоскутом с включением большой грудной мышцы на ножке [Неробеев А. И.,
1988]. Границу кожной площадки лоскута определяют на 6—7 см ниже края
большой грудной мышцы, и поднимают лоскут вместе с поверхностным
листком фасции прямой мышцы живота. Кожно-фасциальную площадку
переносят над тканями шеи и нижних отделов лица прямо к дефекту, укрывая
ножку лоскута расщепленной кожей. В зависимости от размеров
повреждения и поставленных задач в дальнейшем эпителизированную ножку лоскута
используют для дополнительной пластики или иссекают.
Достоинство метода состоит в возможности одномоментного прикрытия
мозга хорошо кровоснабжаемым лоскутом. К отрицательным моментам
следует отнести двухэтапность вмешательства. Переносить на лобно-теменную
область можно и сложный кожный лоскут с включением широчайшей мышцы
спины, если ножку лоскута также укрыть расщепленной кожей, а предплечье
соответствующей руки привести к голове для сокращения расстояния между
передним краем подмышечной ямки и лбом. Руку фиксируют гипсовой
повязкой. За счет широчайшей мышцы спины можно укрыть дефект значительных
размеров, однако вынужденное положение руки больные переносят тяжело.
Ножку лоскута отсекают через 3—5 нед.
Этих недостатков лишены операции аутотрансплантации реваскуляри-
зованных кожно-фасциальных тканей. Для того чтобы полностью исключить
вероятность некроза аутотрансплантата, мы предложили метод его
промежуточной реваскуляризации через сосуды предплечья; при этом в качестве
пластического материала используют широчайшую мышцу спины вместе с
прикрывающим ее кожно-жировым слоем.
На первом этапе выделяют сосудистый пучок мышцы, низводят его вниз
вместе с подлежащим участком мышцы, формируют овальный кожно-жиро-
вой лоскут на предплечье, обнажают лучевую артерию и поверхностную вену
136
и под операционным микроскопом накладывают микрохирургические
анастомозы между грудоспинной и лучевой артериями конец в бок и на вены и
мышцы предплечья конец в конец. Кожно-жировой лоскут с предплечья
сшивают с кожной частью лоскута со спины.
Спустя 2—4 нед, убедившись в хорошем кровоснабжении
поверхностных тканей спины из сосудов предплечья, для чего целесообразно широко
подсечь их, выполняют операцию перемещения широчайшей мышцы спины
на голову. Артериальное кровоснабжение лоскута через ножку гарантирует
его приживление. В отличие от способа прямого перемещения с сохранением
непрерывности сосудов этого лоскута не происходит потеря пластического
материала и удается закрыть еще более протяженные дефекты. Кроме того,
ножка, фиксированная на предплечье, увеличивает подвижность руки в
плечевом суставе. Такая фиксация легче воспринимается пациентом.
Дефекты мягких тканей височно-теменной области сопровождаются
утратой волос, поэтому с целью достижения наилучшего косметического
результата их закрывают перемещением лоскутов с неповрежденных отделов скальпа.
М. Orticochea A971) предлагает использовать мостовидные лоскуты с ножками
у верхнего отдела лба и на затылке. Раневую поверхность, оставшуюся после
смещения лоскута вниз, закрывают свободной кожей. Участок кожи в центре
волосяного покрова легче закрыть, начесывая на него волосы. Операция
двухэтапна; на втором этапе иссекают стоячие кожные конусы у ножек.
Создать новую границу роста волос можно и за счет передвижения на
висок лоскута, выкроенного на горизонтальной ветви затылочной артерии.
После выхода из-под заднего края сосцевидного отростка основной
артериальный ствол направляется вверх параллельно средней линии. В нижних
отделах от него отходит горизонтальная ветвь, идущая в поперечном
направлении к противоположной стороне. Поскольку ее видимые границы
заканчиваются у средней линии, для получении лоскута больших размеров
вначале подсекают его периферическую часть — над сосцевидным отростком
противоположной стороны, доводя параллельные разрезы до середины
затылка. Через 7—10 дней, достаточных для переориентирования сосудистой
сети в подсеченной части, поднимают весь лоскут, поворачивая его на 180°,
и перемещают на висок. Истончение питающей ножки с тщательным
разъединением тканей вокруг затылочных сосудов облегчает подвижность
лоскута, уменьшает размеры кожного конуса. Рану в донорском участке закрывают
после широкой рассепаровки краев и продольных многочисленных насечек
на апоневрозе. Согласно J. Convers A977), каждая продольная насечка на
апоневрозе дает прирост ткани в 1 мм.
Г. И. Прохватилов A986), К. Ohmori A983) сообщают о возможности
восстановления волосяного покрова на виске за счет аутотрансплантации
части скальпа из противоположной височной или затылочной областей.
Учитывая специфику сосудистой архитектоники затылочного региона, частое
отсутствие затылочной вены, Г. И. Прохватилов предлагает в качестве дренирующей
системы в этих случаях использовать затылочную артерию противоположной
стороны, т. е. одна затылочная артерия подводит кровь к аутотрансплантату, а
другая служит для оттока крови. Это парадоксальное, на первый взгляд,
положение, анатомически и клинически наглядно продемонстрированное
автором, по-видимому, возможно только при использовании трансплантатов
из скальпа, в которых существует множество взаимно перекрывающих
территорию друг друга источников кровоснабжения.
На собственном опыте мы убедились в сложности этих операций, так
как при скальпированных ранах височно-теменной области повреждаются
височные артерия и вена. Облитерация вены вызывается длительным воспа-
137
лительным процессом с неизбежными явлениями флебита либо
предшествующим облучением, если причиной образования дефекта является
комбинированное лечение базально-клеточного рака. Поиск сосудов, пригодных к
наложению микрохирургических анастомозов, лучше всего проводить под
углом нижней челюсти, а реваскуляризацию трансплантата выполнять через
длинные аутовенозные вставки.
Деформации лба, вызванные отсутствием части или всей толщи лобной
кости, втяжения на месте лобных пазух с сохраненной кожей, традиционно
устраняют имплантатами из быстротвердеющей пластмассы или оргстекла,
металлической сетки. Рекомендуется использовать различные варианты
костной пластики расщепленным ауторебром, гребешком или частью тела
подвздошной кости, а также их комбинацией с ауторебрами, аллотрансплантацией
черепных костей. J. Convers A977), I. Baroiidi A986) ликвидируют втяжение
тканей в центре лба деэпителизированным островным лоскутом со лба, взятым
на сосудистой ножке вместе с подлежащими тканями. По их мнению, этот
метод более физиологичен, чем трансплантация кости без сосудистых связей
или имплантация контурных материалов, которые всегда подвержены
опасности инфицирования из элементов лобной пазухи.
J. Psilakis и соавт. A986) рекомендуют перемещать васкуляризованную
наружную пластинку височной и теменной кости вместе с покрывающей
надкостницей и безымянной фасцией, являющейся продолжением височного
апоневроза. Густая сеть анастомозов, проникающая в кортикальную часть кости
из систем наружной и глубокой височных артерий, позволяет при сохранении
височного апоневроза обеспечить кровоснабжение смещенной части кости.
Авторами выполнено 37 операций; резорбции кости не отмечено ни разу.
Л. А. Брусова A996) добивается хороших косметических результатов,
устраняя западение индивидуально изготовленными имплантатами из силикона.
Приготовленный в лабораторных условиях имплантат по величине и форме
точно соответствует тканевому дефекту. Введение его осуществляют через
разрез кожи в волосистой части головы.
Различают частичные и полные, сочетанные с окружающими тканями и
изолированные дефекты бровей. Наиболее часто причиной отсутствия
бровей является ожог лица, вызывающий рубцовую деформацию кожи лба, век.
Изолированные и частичные изъяны возникают после механической травмы.
Восстановление бровей проводят только по косметическим соображениям,
поэтому операцию выполняют после создания нормальных век,
обеспечивающих плотное смыкание глазной щели и кожи лба. Деформации бровей,
проявляющиеся поднятием одного из концов, устраняют перемещением
треугольных лоскутов. Первый треугольный лоскут очерчивают вдоль
изменившей форму частью брови, второй же в зависимости от требуемого места
перемещения формируют выше или ниже. Ломаную линию, возникающую в
середине брови, также исправляют, используя методы Z-пластики.
Частичные дефекты медиального края брови можно заместить за счет
другой брови. Благодаря сильно разветвленной артериальной сети в области
переносицы удается, расщепив горизонтально здоровую бровь,
сформировать из нее узкий кожно-жировой лоскут с медиальным основанием, в
котором при повороте на 180° сохраняется устойчивое кровообращение.
Небольшой кожный конус впоследствии иссекают. Внутренние части брови всегда
более широкие, и некоторое их истончение мало заметно. С возрастом брови
становятся гуще и шире и проведение операции облегчается. Полные дефекты
бровей лучше всего устранять артериализованными лоскутами на ножке из
височно-теменной области. В западноевропейской литературе операция
называется по именам авторов — J. Monks A895) и J. Esser A917). Следует от-
138
метить, что J. Monks впервые применил артериализированный лоскут со лба
для восстановления нижнего века.
Имеются два пути миграции лоскутов из височно-теменной области на
бровь. В первом варианте кожную ленту формируют непрерывной и затем
переносят над окологлазничными тканями к надбровной дуге. В этом случае
возможно выкраивание более широкой (до 2 см) ножки, в которую включают
поверхностные височные сосуды. Достаточно по пульсации определить место
расположения артерии, отступить в стороны на 1 см, после чего можно
проводить параллельные разрезы от середины теменной области до скуловой дуги.
Дистальный конец лоскута, приходящийся на бровь, суживают. Раневую
поверхность ножки лоскута закрывают мазевой повязкой. Впоследствии эту часть
возвращают на место или иссекают. Операция технически проста, всегда
гарантирован хороший результат, однако в связи с необходимостью второго
этапа увеличивается время излечения пациента.
По нашему мнению, предпочтительнее одномоментное восстановление
брови на скрытой сосудистой ножке. Вначале определяют размеры будущей
брови, затем отмечают их в теменной области по прямой линии,
соответствующей проекции поверхностной височной артерии. Для точного
обозначения кожно-жировой площадки лучше использовать циркуль, центральную
ножку которого ставят впереди ушной раковины. Затем очерчивают две
окружности; малая идет по латеральному краю брови, большая — по
медиальному. Расстояние между этими окружностями, отложенное на вертикальной
линии теменно-височной области, соответствует длине брови.
Согласно намеченному рисунку, рассекают кожу до фасции в верхнем
и боковых отделах. От нижнего края кожной части будущего лоскута проводят
вертикальный разрез кожи до скуловой дуги. Глубина разреза не должна
превышать 2 мм из-за поверхностной локализации сосудистого пучка. Сразу же
под волосяными луковицами рассепаровывают кожу в стороны на 1 см.
Определяют точное расположение сосудистого пучка и вдоль него рассекают
височную фасцию до глубокого листка. Кожный фрагмент вместе с
прикрепленными сосудами освобождают попеременно сверху и с боков, отделяя
сосудистый пучок от фасциального листка, покрывающего височную мышцу.
Между нижним отделом раны у скуловой дуги и наружной частью
надбровной дуги создают подкожный туннель, через который выводят кожную часть
лоскута и подшивают ее к окружающим тканям, стараясь повторить форму
сохранившейся брови. Рану в височно-теменной области ушивают наглухо.
Некоторая техническая сложность выделения сосудов компенсируется
скоростью реабилитации. Через 2—3 сут пациент может быть выписан под
амбулаторное наблюдение. Восстанавливая бровь на скрытой сосудистой ножке,
важно помнить о необходимости тщательного удаления из тканей,
окружающих ножку, волосяных фолликулов. В противном случае под кожей
развиваются кисты, подобные дермоидным.
Данный метод формирования брови следует признать наилучшим,
обеспечивающим устойчивый рост волос, но при обширных ожогах лица,
захватывающих височные и теменные регионы головы, применение его невозможно.
В этих случаях бровь восстанавливают путем свободной трансплантации кожи
с волосяными луковицами из сохранившихся участков скальпа. В отличие от
обычных кожных аутотрансплантатов, не превышающих по толщине 1 мм и
поэтому быстро реваскуляризующихся из реципиентного лоскута, кожно-
жировые лоскуты толщиной 2—4 мм, содержащие волосяные луковицы,
приживают значительно труднее. Простая пересадка многослойного лоскута из
затылочной области редко бывает успешной. Даже при сохранении
жизнеспособности пересаженной ткани волосяные луковицы, длительно находив-
139
шиеся в условиях аноксии и гипоксии, постепенно погибают и рост волос
прекращается. Для улучшения результатов предложены различные методы
трансплантации.
В. Brent A975) пересаживает несколько узких кожных полосок в
отдельные разрезы, которые в последующем объединяет, иссекая промежуточные
фрагменты кожи. Автор вполне резонно считает, что множество мелких
трансплантатов имеет большую площадь контакта с воспринимающей раневой
поверхностью. Это обстоятельство должно благоприятно отразиться на скорости
их прорастания новообразованными сосудами. Согласно J. Convers A977),
большую поверхность контакта между трансплантатом и ложем можно
обеспечить путем осторожного продольного расщепления пересаживаемой ткани
с внутренней стороны. Подготавливая ложе, рану по краям углубляют, а в
центре создают небольшое возвышение по типу гребня. Растягивая в стороны
края трансплантата, благодаря продольному разрезу разворачивают его
внутреннюю поверхность и насаживают на выступ в центре раны. Площадь
соприкосновения трансплантата с ложем существенно увеличивается, что
облегчает его реваскуляризацию.
В. Г. Чантладзе A976) рекомендует восстанавливать бровь за счет
погруженных трансплантатов. Рассекают кожу по центру надбровной дуги, рассепаровы-
вают, укладывают в рану трансплантат и кожу над ним зашивают наглухо. Через
10—14 сут снимают швы, раздвигают края раны, дно которой представлено
пересаженной кожей. Хорошее приживление погружных кожных
трансплантатов доказано в работах С. Ф. Хомича A987), О. П. Чудакова A998). Впрочем,
приживление кожи еще не гарантирует сохранение волосяных луковиц.
Отдельные сообщения о трансплантации волос с лобка не подтверждены
убедительными клиническими примерами. Мы несколько раз пытались
использовать этот метод пластики, но роста волос не наблюдали ни разу.
Волосяные луковицы лобка находятся в слое рыхлой клетчатки, редкие, легко
выпадают из трансплантата.
Г. И. Прохватилов A985) пытался в одном случае воссоздать бровь ау-
тотрансплантацией участка скальпа длиной 6 см и шириной 1,5 см с наложением
микрососудистых анастомозов, однако развился некроз лоскута. Обсуждая
проблемы применения с этой целью реваскуляризованных аутотрансплантатов,
следует отметить ряд отягощающих обстоятельств. Узкий и длинный лоскут можно
выкроить только из височной области противоположной стороны.
Затылочная артерия сильно извита, вена идет на расстоянии 1,5—2 см, часто
отсутствует. Воспринимающие сосуды на пораженной стороне либо резко сужены,
либо отсутствуют. Можно осуществить кровоснабжение трансплантата путем
удлинения сосудов аутовенозными вставками или наложить
микрохирургические анастомозы с сосудами у медиального края надбровной дуги — над-
блоковой и лобной артериями и венами при условии их сохранности.
Оба варианта не лишены отрицательных сторон: длинные сосудистые
шунты увеличивают вероятность тромбоза, воспалительно-некротические процессы
в трансплантате при условии оттока через надглазничную вену могут вызвать
тромбоз или флебит нисходящих сосудов. Главная сложность заключается в
значительном нарушении артериовенозного равновесия в небольшом
трансплантате, формируемом у основания магистральной артерии. В маленьких
трансплантатах, взятых из зон конечного разветвления осевых сосудов (фаланги пальцев,
ножка межпальцевых промежутков), характер распределения крови не
меняется: поступив через конечную ветвь артерии, она проходит через
сохранившуюся систему капилляров и оттекает через вену. Пытаясь создать маленький
и узкий (не шире 1 см) лоскут вдоль крупных сосудов — височной артерии и
вены, мы прерываем зону естественного их разветвления. Кровь, поступающая
140
в артерию под большим давлением, не успевает уйти в вену через резко
ограниченную зону капиллярного разветвления. Здесь действует одно из основных
правил аутотрансплантации тканей с микрососудистой техникой: чем полнее
сформирован трансплантат в пределах данного ангиотома, тем больше шансов
на успех операции, т. е. большие лоскуты пересаживать легче, чем маленькие.
Мы производим пересадку реваскуляризуемых тканей из теменно-височной
области по тем же принципам, что и их перемещение на скрытой сосудистой
ножке. Кожную площадку иссекаем на 8—10 см выше скуловой дуги, а затем
выделяем сосудистую ножку вместе с окружающими тканями, обнажая
сосуды только у ушной раковины непосредственно перед пересечением.
Смещение лоскута к периферии и сохранение тканей вдоль ножки благоприятно
отражаются на восстановлении кровообращения в трансплантате.
С. Lim A986) описал случай успешного восстановления брови височным
лоскутом, пересаженным на одной артерии. Венозный отток осуществляли за
счет непрерывного прикладывания к трансплантату повязок. Определенная
сложность и рискованность этого метода очевидны.
Строение век идеально приспособлено к их функции — защите глазного
яблока. Форма соответствует кривизне глазного яблока, пластичность кожи
обеспечивает высокую степень сократимости и растяжимости при
открывании глаз, а плотные образования (хрящи) создают опору векам. Хрящи
расположены у ресничных краев, ширина их в среднем 7 мм, толщина 1 мм.
Границей верхнего служит пальпебральная складка под верхним глазничным
краем, нижнего — горизонтальная складка нижнего века. Эластичная кожа
век и подкожная жировая клетчатка подвижны, легко собираются в складку,
могут значительно растягиваться, что наблюдается при гематомах,
воспалительных процессах в области глазницы.
Круговая мышца глаза состоит из наружного (орбитального) и внугреннего
(пальпебрального) слоев, волокна внутреннего растянуты вдоль медиальной
и латеральной кантальных связок, которые связывают хрящи с краями
глазницы. Мышца прикрепляется к костным краям глазницы.
Во время ожога повреждаются наружные слои век, причем круговая
мышца глаза чаще всего сохраняется, но функция ее снижается в результате
вторичного вовлечения в процесс рубцевания [Емиленко Г. И. 1980]. Деформации
век. возникающие под влиянием концентрического рубцевания,
сопровождаются образованием внутренних и внешних контрактур, что обусловливает их
многообразие. Вторичным изменениям подвергаются не только поврежденные
слои, но практически все отделы век и окружающих тканей: сниженная
эластичность и сократимость круговой мышцы глаза приводят к зиянию глазной щели,
деформируется хрящевая пластинка, приобретая вогнутую форму. Г. И.
Емиленко разработала следующую классификацию послеожоговых деформаций век.
I. Односторонняя рубцовая деформация
А. Рубцовая деформация одного из век.
1. Кожа век не поражена, выворот обусловлен Рубцовыми тяжами в
прилежащих областях.
2. Кожа века поражена, замещение ее рубцами приводит к вывороту века.
Б. Деформация обоих век одного глаза в сочетании с эпикантусами.
1. Частичная деформация.
2. Полная деформация.
II. Двусторонняя рубцовая деформация век.
А. Рубцовая деформация одного из век обоих глаз.
Б. Рубцовая деформация обоих век обоих глаз в сочетании с эпикантусом.
1. Частичная деформация.
2. Полная деформация.
141
Данная классификация позволяет определить локализацию деформации
и помогает выбрать метод хирургического лечения.
Восстановительные операции на веках целесообразно начинать в наиболее
ранние сроки после повреждения для предотвращения развития
воспалительных и деструктивных процессов в роговице и конъюнктиве. Небольшие эпикан-
тусы и рубцовые тяжи рассредоточивают, используя рекомендуемые А. А. Лим-
бергом A963) методы перемещения треугольных лоскутов.
При сочетании эпикантуса и рубцовой контрактуры за счет близлежащих
тканей не удается восполнить кожный дефицит, поэтому предложены
многочисленные способы перемещения кожи из других регионов. Наиболее
простым вариантом решения этой проблемы можно считать перемещение лоскутов
на питающей ножке, выкроенных в височной, лобной, скуловой,
нижнеглазничной областях, тем более что в каждой из них расположены подкожные
кровеносные сосуды, обеспечивающие хороший кровоток при относительно узкой
ножке [Зайкова М. В., 1969; Hatt Μ., Ι984]. Однако возможности применения
этих методов при рубцовой деформации окружающей кожи, возникающей после
ожога, ограничены. Восстановление поверхностного покрова век филатовским
стеблем [Зайкова М. В., 1969; Бондарь В. В., 1962] находит все меньше
приверженцев прежде всего из-за многоэтапности операций, а также малой
эластичности новообразованных век.
Самым распространенным и эффективным способом устранения
рубцовой послеожоговой деформации век следует признать трансплантацию
свободной кожи. Преимущество отдают полнослойным трансплантатам,
которые меньше сморщиваются, слабо подвержены пигментации, рано
приобретают подвижность за счет развития под ними жировой клетчатки [Киня-
пина И. Д., 1977; Falvey Μ., Brody J., 1978].
Φ. Μ. Хитров и соавт. A980) рекомендуют выполнять двухэтапную
операцию устранения рубцовых деформаций обоих век вместе с эпикантусом. Вначале
рассекают кольцевидный рубец, окружающий вывернутые веки, и эпикантус на
всю толщу. Разрезы по эпикантусам под углом 90° проводят у внутреннего и
наружного краев глазной щели, затем вдоль ресничных краев обоих век, отступя
2—3 мм до соединения с угловыми разрезами. После полного рассечения руб-
цового массива ткани выпячиваются через разрезы. Рассепаровку рубцов
заканчивают, выделяя волокна круговой мышцы глаза, добиваясь свободного и
естественного смыкания век, сшивают ресничные края друг с другом и на
образующуюся раневую поверхность подшивают кожный трансплантат, средний
участок которого продольно рассекают по проекции глазной щели. Трансплантат
подшивают под туннелеобразно отпрепарованные рубцовые края раны и
укрывают Рубцовыми тканями, а в центральных отделах марлевой повязкой. Через
14—16 сут иссекают рубцы по периферии прижившего лоскута, обнажают
трансплантат. Согласно многочисленным наблюдениям Ф. М. Хитрова и соавт., метод
дает хорошие косметические и функциональные результаты в 90 % случаев.
Дефекты век, образующиеся после удаления опухолей, в отличие от после-
ожоговых характеризуются более существенными различиями. Большинство
восстановительных операций целесообразно выполнить тотчас после
удаления опухоли, до появления отягощающей лечение рубцовой деформации.
Результаты пластики оценивают на основании анализа сохранившейся ткани.
В возрасте моложе 35 лет излишки кожи на веках отсутствуют, позднее
появляется небольшой избыток тканей в верхних отделах. При замещении
любого дефекта важно помнить, что простая рассепаровка краев раны и их
сведение под умеренным натяжением (обычный хирургический прием
ушивания ран во всех отделах туловища) неминуемо вызовут вторичную
деформацию век и изменение глазной щели.
142
Поверхностные дефекты замещают свободными кожными
трансплантатами, ротационными лоскутами и лоскутами на ножке из окружающих
областей. Пересадку свободной кожи производят по тем же правилам, что и при
устранении рубцовых выворотов. Несмотря на подбор донорского участка
(задняя поверхность ушной раковины, нижние отделы щек), цвет кожного
трансплантата все же отличается от естественного.
Можно восстанавливать не только поверхностные отделы нижнего века,
но и реснитчатый край путем свободной пересадки кожного лоскута из
надбровной области противоположной стороны. В трансплантат включают
участок брови с волосяными луковицами. В дальнейшем требуются коррекция
для выравнивания линии роста волос на ресницах и дермоабразия. Смещение
на дефект близлежащей кожи позволяет устранить несоответствие окраски,
но сопряжено с большими техническими трудностями. Для предотвращения
вторичной деформации, которая может возникнуть вследствие натяжения
краев раны, J. Convers A977) рекомендует формировать ротационный лоскут,
по размерам в 5—6 раз превышающий кожный дефект. Замещая
поверхностные слои нижнего века, дугообразный разрез кожи (выпуклой частью
вверх) проводят от наружного угла глаза до предушной области, перед
козелком поворачивают вниз и продолжают до мочки уха. Отсепаровывают кожно-
жировой слой всей скуловой области и смещают его медиально,
одновременно иссекая конус в передненижнем углу раны. Такое массивное перемещение
кожи помогает добиться равномерного ее натяжения по линии швов,
предотвращает сморщивание. Однако у людей с тонкой кожей остается длинный
различимый рубец на открытой части лица.
Лоскуты на узкой питающей ножке вызывают менее выраженные
вторичные повреждения, но большинство операций выполняют в два этапа.
Наиболее типичными местами формирования лоскутов являются нижние
отделы лба (параллельно брови), скуловисочная область (ось лоскута проходит
в вертикальном направлении, ножка — у скуловой кости), складка верхнего
века (при наличии избыточной кожи).
Устраняя сквозные дефекты век, в первую очередь заботятся о
восстановлении конъюнктивы. Небольшие сквозные изъяны века успешно закрывают
после рассечения наружного края глазной щели, освобождения конъюнктивы
от наружного кантального сухожилия и его пересечения. Веко становится легко
подвижным. Рану в наружном углу глаза ушивают в продольном направлении.
Изъяны большего размера устраняют свободной пересадкой слизисто-
хрящевого трансплантата, взятого из перегородки носа, который помещают
на внутреннюю часть века. Наружные ткани создают за счет перемещения
какого-либо из перечисленных выше лоскутов. С этой целью вместо
перегородочного лоскута иссекают крыльный хрящ носа вместе со слизистой. Однако
может возникнуть сужение носового хода. Наилучшие результаты получают,
пересаживая полнослойный лоскут из твердого неба, который отличается
плотностью, устойчивостью к инфицированию, простотой иссечения.
Донорская рана эпителизируется самостоятельно.
В. Smitli A977) в отсутствие центрального отдела верхнего века
восстанавливает его перемещением части нижнего века. Под реснитчатым краем
сквозным горизонтальным разрезом рассекают нижнее веко. Длина разреза
должна быть равна ширине изъяна верхнего века. По концам горизонтального
проводят вертикальные разрезы вниз, мобилизуют прямоугольный лоскут,
пропускают его под реснитчатым краем и подшивают к ране верхнего века.
Таким образом, конъюнктиву нижнего века сшивают с остатками
конъюнктивы верхнего века; соприкасаются также хрящи и кожа. Через 6 нед
отсекают ножку лоскута на уровне глазной щели и возвращают на место. Вто-
143
ричной деформации нижнего века В. Smitli не отмечал. По-видимому, при
6-недельной фиксации в вынужденном положении ткани растягиваются и
приобретают избыточную длину, достаточную для свободного ушивания раны.
Н. Holmström и соавт. A975) после иссечения злокачественных опухолей
век у 193 больных пришли к выводу, что наилучшим способом
восстановления является использование опрокидываемого конъюнктивально-хрящевого
лоскута из другого века на ножке. Нижнюю часть хряща оставляют на месте,
чтобы воспрепятствовать деформации донорского века.
Свободная пересадка сложных лоскутов, иссеченных во всю толщу из
века противоположной стороны, в настоящее время применяется редко из-
за высокой вероятности некроза и деформации здорового века.
Сквозные обширные дефекты век можно устранить аутотрансплантаци-
ей реваскуляризованных тонких кожно-фасциальных лоскутов. К
внутренней поверхности лоскута, соприкасающейся с глазным яблоком, подшивают
слизистую оболочку полости рта.
Ранее дефекты обоих век после экзентерации глазницы замещали фи-
латовским стеблем, лоскутом на ножке со лба [Thomson Η., 1970]. В
настоящее время наиболее простым и надежным следует признать метод смещения
височной мышцы в глазницу, предложенный J. Webster A957). В наружной
стенке глазницы создают отверстие, через которое проводят мышцу,
отсеченную по линии ее прикрепления от височной кости. Периферическая часть
мышцы шире ножки и полностью выполняет глазницу. Передний край
мышечной поверхности укрывают расщепленной кожей.
В. Jugurson A985) закрывает дефекты орбиты островным кожно-жиро-
вым лоскутом из заушной области, который формируют на затылочной ветви
височной артерии. Лоскут поднимают вместе с височной фасцией,
освобождая ее на всем протяжении от окружающих тканей и суживая ножку над
ушной раковиной. Передний отдел фасции укладывают на раневую поверхность
глазницы, кожную часть помещают сверху.
Препятствием к выполнению этих операций служит предварительная
перевязка наружной сонной артерии, которую нередко проводят при удалении
обширных опухолей данной локализации.
Немедленное замещение дефекта можно осуществить за счет сложных
лоскутов с включением большой грудной и трапециевидной мышц [Неро-
беев А. И., 1988].
23.7. Устранение дефектов и деформаций нижней зоны лица
Понятие "нижняя зона лица" достаточно условно. Оно включает различные
анатомические образования — губы, щеки, мягкие и костные ткани подбородка,
преддверие и дно полости рта, а также язык. Комплекс мягкотканных
образований кпереди от челюстной кости объединяют понятием "приротовая
область" [Сукачев В. Α., 1965; Сергеев Ю. Н., 1981].
Анатомическое строение мягких тканей соответствует главным функциям —
пережевыванию пищи и речеобразованию. Благодаря эластичности, высокой
растяжимости и мышечным футлярам все окружающие полость рта мягко-
тканные структуры активно участвуют в пережевывании пищи. Эластичная
стенка из губ спереди в сочетании со щеками с боков и языком изнутри
помогает пищевому комку возвращаться на жевательные поверхности зубов.
Процесс пережевывания пищи происходит при замкнутой полости рта и
повышенном давлении. Нарушение герметичности за счет изъяна губы или
щеки приводит к выпадению пищевой массы в образовавшийся дефект.
144
Глубина преддверия полости рта, особенно нижнего отдела, также имеет
значение для акта жевания. В глубоком преддверии, лишенном эластичных
стенок, может скапливаться пища. Подобные явления усугубляются в
случаях недостаточной подвижности кончика языка. При мелком преддверии
полости рта, сочетающемся с укорочением высоты подбородка и нижней губы,
пища и слюна легко выделяются из полости рта, так как исчезает
естественное препятствие в виде гребня альвеолярного отростка и фронтальных зубов.
Еще более затруднена эвакуации пищевой массы при нарушении
эластичности и высоты расположения дна полости рта.
Дефекты и деформации этой области, как правило, связаны с
ограничением движений языка. Если хирург сформирует слишком глубокое дно
полости рта, оно будет напоминать мзоб пеликана", в котором начнет
скапливаться пища. Следует также учесть отсутствие тактильной чувствительности
во вновь образованных тканях, в результате чего пациент не может постоянно
контролировать скопление пищи в полости рта.
Выделяя приротовую область в самостоятельное анатомофункциональ-
ное образование, Ю. Н. Сергеев A981) изучил топографическое строение
мягких тканей, взаимоотношение слоев и их толщину в норме. Красная
кайма характеризуется отсутствием зернистого слоя, а роговой слой истончен. Ее
цвет объясняется просвечиванием густой широкопетлистой сосудистой сети.
Толщина кожи губ колеблется в пределах 1,8—2.6 мм. Жировой слой
представлен неравномерно, в области фильтрума и углов рта часто отсутствует.
Под кожей губ толщина его не превышает 3,2 мм, т. е. толщины кожи.
Клетчатку пронизывают связанные с кожей многочисленные мышечные пучки,
прободающие слабо развитую фасциальную пластинку.
Круговая мышца рта, несущая основную функциональную нагрузку,
состоит из двух частей — краевой и губной. Волокна губной части расположены
вертикально, сплетаясь с другими мышцами приротовой области (опускающие
и поднимающие губы и углы рта, мышцы смеха, резцовые большая и малая
скуловые). Краевая часть круговой мышцы рта состоит из волокон,
расположенных концентрически и нависающих под углом 30—45° над губной частью.
От этой части мышцы зависит форма губ. В боковых отделах круговая мышца
связана со щечной, обеспечивающей напряжение щек. Толщина мышечного
слоя колеблется от 7 мм в центральном участке нижней губы до 11 мм в углах рта.
Слизистая оболочка вместе с подслизистым слоем достигает толщины 3 мм.
Между мышцами и слизистой оболочкой находятся жировая и рыхлая
соединительные ткани, небольшое количество слюнных желез. В этом слое нет
мышечных волокон, поэтому слизистую оболочку легко отделить от остальных
тканей и переместить на новое место. Таким образом, точные анатомические
расчеты, выполненные Ю. Н. Сергеевым, подтверждают положение о том,
что основную массу ткани губ составляют мышцы.
Дно полости рта состоит из нескольких слоев. Анатомия этого отдела
изучена в основном применительно к характеру распространения воспалительных
процессов. Наиболее важный в функциональном отношении передний отдел
представлен четырьмя слоями мышц (подбородочно-язычная, подбородоч-
но-подъязычная, челюстно-подъязычная, переднее брюшко двубрюшной),
расположенными под слизистой оболочкой. За счет подвижности подборо-
дочно-язычной мышцы глубина дна полости рта постоянно меняется.
Дефекты и деформации губ делятся на врожденные и приобретенные.
Среди врожденных деформаций губ чаще других встречается двойная губа —
увеличение в размерах слизисто-подслизистого слоя, преимущественно на
верхней губе, сразу же за красной каймой. В спокойном состоянии, при
сомкнутых губах деформация не видна. При разговоре и особенно при смехе,
10-1263
145
сопровождающемся напряжением и растяжением круговой мышцы рта, под-
слизистый слой, разделенный уздечкой на две половины, выступает под
красной каймой, создавая впечатление укороченной губы.
Излишки тканей убирают двумя параллельными разрезами вдоль губы,
не затрагивая круговую мышцу рта. Во избежание подворачивания красной
каймы внутрь и истончения линии губы гипертрофированные ткани подсли-
зистого слоя, включающие слюнные железы, иссекают более широко, чем
слизистую оболочку. Небольшой оставшийся избыток последней быстро
подтягивается рубцами. Определяя истинную причину возникновения
двойной губы, следует исключить наличие лимфангиомы, нейрофибромы, а
также врожденное укорочение верхней губы. Констатировав опухоль, выбирают
адекватный метод хирургического лечения — иссечение, эмболиэацию;
укороченную губу удлиняют.
В зависимости от вида повреждения приобретенные дефекты тканей
приротовой области существенно различаются. Отдельную группу составляют
рубцовые деформации после ожогов, травм и онкологических операций. Каждая
из групп имеет свои анатомо-топографические особенности,
предопределяющие специфику восстановительных операций.
Послеожоговые рубцы встречаются в виде тяжей, перепонок, рубцового
массива. Ю. Н. Сергеев A981) разработал классификацию рубцовых
деформаций приротовой области. По локализации и размерам поражения рубцовые
деформации делятся на: 1) изолированные (губы, углов рта, щек, подбородка),
частичные или полные; 2) сочетанные одной или обеих губ с повреждениями
прилегающих участков щек, носа, верхних отделов шеи. По глубине
поражения рубцами различают деформации кожи, кожи и подкожной жировой
клетчатки, промежуточных слоев в сочетании с поражением кожи или слизистой
оболочки, всей толщи мягких тканей.
Клинические проявления рубцов связаны со сроками, прошедшими после
ожога. В стадии набухания рубцы гиперемированные, болезненные,
выступают под окружающей кожей. Пальпаторно трудно установить глубину
повреждения из-за вовлечения мышечных структур в реактивный воспалительный
процесс. Сроки окончательного созревания рубцов оценивают по-разному, но
наиболее принятыми считают 12—18 мес [Александров Н. М., Аржанцев П. 3.,
1986J. За это время может полностью измениться первоначальная клиническая
картина: рубцы уплощаются, приобретают эластичность, бледнеют, исчезает
болезненность. Планируя пластическую операцию, следует по возможности
прогнозировать исход рубцевания. Электроожоги, прямое воздействие огня
вызывают глубокий некроз ткани. Вторичная рубцовая деформация остается
стойкой весь период наблюдения. После других видов термических
поражений возможно обратное развитие процесса. В связи с этим обычно операцию
начинают по окончании периода рубцевания, за исключением тех случаев,
когда нарастающая деформация вызывает страдания.
Характерной особенностью заживления ран приротовой области является
формирование концентрических рубцов, которые суживают ротовое отверстие и
сокращают площадь поражения. Вывороты губ и углов рта сопровождаются
слюнотечением из-за нарушения герметизма полости рта. Уменьшается высота губ,
обнажаются зубы. В углах рта образуются эпикантусы, открывание рта
ограничивается. Рубцовые поражения приротовой области, переходящие на щеки и
верхние отделы носогубных складок, вызывают появление рубцовых продольных
тяжей, идущих от подбородка до верхней границы ожога вплоть до века. Они
становятся видны только при смещении челюсти вниз, т. е. перерастяжении.
Келоидные рубцы характеризуются неравномерной толщиной, наличием
кратерообразных углублений наряду с выступавшей в виде валиков тканью.
146
В этих углублениях часто сокращается нормальная кожа или ее
поверхностные структуры — сальные железы, волосяные фолликулы, которые после
неполного иссечения и укрытия пластическим материалом могут привести к
развитию дермоидных и эпителиальных кист.
J. Convers A977) разделяет дефекты губ на поверхностные, дефекты всех
слоев и полное отсутствие одной или обеих губ, дополнительно выделяя
поражения бокового и срединного отделов. Если исходить из этой
классификации, то отнести большинство послеожоговых деформаций следует к первой
группе. Операция заключается в иссечении рубцовой ткани на всю глубину,
освобождении круговой мышцы рта, низведении красной каймы в
нормальное положение (на 2—3 мм перекрывая края резцов) и замещении раневой
поверхности полнослойным кожным трансплантатом.
Вместо поэтапного устранения сочетанных деформаций Ю. Н. Сергеев A981)
использует единый для обеих губ дермотрансплантат, который, по его
мнению, благодаря полноценным функциональным и косметическим свойствам
наиболее пригоден для пластики приротовой области. С целью улучшения
условий приживления дермотрансплантата автор использовал погружной
метод свободной кожной пластики. Четырьмя симметричными разрезами,
проведенными от углов рта в стороны под прямым углом друг к другу и 45° к линии
смыкания зубов, рассекают концентрические рубцы и эпикантусы углов рта.
Освобожденные от стяжения нормальные ткани губы устанавливают в
правильном положении. Для создания неподвижности губ в предоперационном
периоде изготавливают назубную каппу с выступающим изо рта козырьком, к
которому фиксируют губы. Рану укрывают кожным трансплантатом, края
которого заводят под отсепарованную рубцовую ткань, укладывая ее сверху на
кожу и фиксируя кетгутом. Ю. Н. Сергеев отмечает, что в условиях частичного
погружения дерматотрансплантат лучше срастается с дном раны. Через 16 сут
под местной анестезией иссекают ткани над лоскутом, тщательно адаптируют
края, на 7—10-е сутки закрывают повязкой с рыбьим жиром или каратолином.
23.7.1. Пластика дефекта переднего отдела дна полости рта
в сочетании с дефектом подбородочного отдела
нижней челюсти и слизистой оболочки нижней губы
В зависимости от состояния тканей в данной области можно использовать
два типа пластики. При поступлении больного с обширной опухолью,
занимающей передний отдел слизистой оболочки дна полости рта,
прорастающую в нижнюю челюсть и слизистую оболочку переходной складки,
операцию планируют с учетом быстрейшего закрытия дефекта.
Первый этап подготовки к восстановлению дна полости рта проводят
одновременно с удалением опухоли. Вместо традиционного разреза под краем
нижней челюсти вначале на передней поверхности шеи формируют языко-
образный кожный лоскут размером 6 х 6 см с основанием в области
подбородка. Если предполагается футлярно-фасциальное иссечение клетчатки шеи,
то целесообразно выкраивать лоскут без включения в него подкожной мышцы,
чтобы не нарушать анатомическое соотношение фасций шеи. После того как
лоскут отсепарован до уровня нижнего края подбородка, его откидывают
кверху и укрывают салфеткой, смоченной раствором фурацилина.
Затем электрохирургическим путем производят резекцию единым
блоком подбородочного отдела нижней челюсти, дна полости рта и при
необходимости удаление футлярно-фасциальной клетчатки шеи. В этом случае от
нижнего края кожного дефекта на шее проводят два горизонтальных разреза
10*
147
параллельно ключице. Для профилактики асфиксии вследствие западения
корня языка накладывают нижнюю трахеостому. После удаления опухоли
кожный лоскут вворачивают внутрь и подшивают к оставшейся слизистой
оболочке переходной складки или нижней губы. Подбородочный участок
покрывают кожей с наружной и внутренней сторон. Рану на шее ушивают,
формируя обширную переднюю оростому. Концы оставшихся костных
фрагментов нижней челюсти укрывают окружающими мягкими тканями. Больного
кормят через зонд.
Заживление раны после электрорезекции на фоне ранее проведенной
лучевой терапии, как правило, сопровождается выраженными
воспалительными явлениями с некротическим компонентом, после стихания которых
(через 24—30 дней) проводят второй этап восстановительной операции.
Дублированный кожный лоскут на подбородке рассекают с внутренней
поверхности на 1,5—2 см выше предполагаемого нижнего края подбородка. Границу
нижнего края подбородка можно установить по принципу деления лица на
три равные части. Внутреннюю часть кожного лоскута рассепаровывают
кверху и подшивают к оставшейся ткани нижней поверхности языка и
слизистой оболочки, формируя внутреннюю выстилку полости рта. Рану
ушивают наглухо, накладывая выворотные швы хромированным кетгутом или
полиамидной нитью. На передней поверхности грудной клетки выкраивают
дельтопекторальныи лоскут и латеральный конец его переносят к раневой
поверхности в подподбородочной области, образуя наружную выстилку дна
полости рта. Оставшуюся часть лоскута сворачивают в трубку и ушивают.
Рану на груди закрывают по описанной методике. Через 4—5 нед ножку лоскута
отсекают от подбородка и распластывают на грудной клетке.
Если после первого этапа операции возникли рубцы в верхнем отделе
шеи, иссекают их и нижнюю часть лоскута используют для закрытия дефекта.
Отсутствие соприкосновения тканей лоскута с содержимым полости рта
благоприятствует заживлению.
Однако данный способ несвободен от недостатков. Обильная саливация
при наличии обширной оростомы приводит к мацерации линии швов на шее,
требует частой смены повязки; возможно затекание слюны в трахеостому.
Наши наблюдения показывают, что при резекции челюсти необходимо шире
удалять костную ткань (на 2,5—3 см в стороны от краев шейного лоскута),
чтобы укрыть фрагменты местными тканями уже на первом этапе операции.
В процессе приживления периферического конца лоскута к слизистой
оболочке нижней губы обычно отмечается некоторое рубцовое сокращение его,
поэтому при выпрямлении на втором этапе ширины лоскута может не
хватить для изоляции выступающих участков кости от полости рта.
Пластика обширных дефектов губ и мягких тканей подбородка дельто-
пекторальным лоскутом отличается от замещения этих дефектов филатовским
стеблем тем. что кожно-жировую ленту подшивают перпендикулярно ране.
Измеряя ширину раны и устанавливая истинные размеры дефекта слизистой
оболочки и кожи, можно сформировать лоскут достаточной величины. Часто
во время разрушающей операции слизистую оболочку убирают в большем
объеме, чем поверхностные ткани. К тому же кожу окружающих областей легче
отсепаровать и сместить на рану, что приводит к уменьшению полости рта.
В связи с этим при выкраивании лоскута на грудной клетке его
периферическую часть на плече формируют на 3—4 см шире, чем стебельчатый
отрезок. Подшивая эту часть лоскута к слизистой оболочке полости рта в
перпендикулярном направлении, можно восполнить дефект шириной 12—14 см.
т. е. "лопасти" или "крылья" лоскута могут быть заведены в преддверие
полости рта до ST6 зубов.
148
Операцию удаления опухоли выполняют обычным способом, формируя
края дефекта. Через 3 нед после стихания воспалительного процесса и
заживления раны выкраивают дельтопекторальныи лоскут, который вшивают
поперек нижнего края дефекта, предварительно удалив эпидермис с
конечного участка лоскута на протяжении 2—2,5 см.
Через 3—5 нед после приживления ножку лоскута отсекают от грудной
клетки, продольно распластывают после удаления рубца и складывают
пополам в поперечном направлении, определяя количество ткани, необходимое
для воссоздания дна полости рта и подбородка. На уровне, соответствующем
красной кайме нижней губы, одновременно деэпидермизируют лоскут до
сетчатого слоя кожи в поперечном направлении, создавая раневую
поверхность шириной I —1,5 см, в которую вшивают красную кайму или ее
фрагменты. Оставшуюся часть лоскута используют для восстановления контуров
нижней губы и подбородка.
23.7.2. Пластика тотальных дефектов подбородка и дна полости рта
К образованию такого дефекта, когда отсутствуют нижняя губа, кожа и
подлежащие ткани подбородка и подподбородочной области, нижняя челюсть
(чаще от 6-го до 6-го зуба), ткани дна полости рта, язык лежит на передней
поверхности шеи, могут привести только два вида повреждений:
огнестрельный отрыв подбородка или удаление в блоке всех тканей при лечении
распространенного рака нижней губы. Возможен также некроз всех
перечисленных тканей в результате электроожога. Тяжесть повреждения усугубляется
психической травмой пациента, лишенного возможности общаться с
окружающими. Постоянное истечение слюны, зондовое питание или прием
пищи через поильник приводят к дефициту белка в организме, истощению.
Предшествующее облучение и интоксикация у онкологических больных
усложняют местные и общие условия, влияющие на заживление раны. После
огнестрельных ранений по краям дефекта образуются грубые, набухшие рубцы.
Кожа передних отделов шеи всегда красного цвета с явлениями резкого
раздражения из-за постоянной мацерации слюной. Один из наших пациентов
поступил в клинику со слюноприемником, сделанным из полиэтиленового
мешочка и привязанным к нижним отделам лица, в котором собиралось большое
количество слюны. Однако это не предотвращало ее попадания на кожу шеи.
В боковых отделах дефекта, как правило, выступают обнаженные
костные фрагменты нижней челюсти, окруженные гипертрофическими
грануляциями. Если не проведена ранняя фиксация остатков нижней челюсти (у
поступивших к нам пациентов со сформированным дефектом этого не было
сделано ни разу), то наступает вторичная деформация челюстей. Фрагменты
нижней челюсти жевательными мышцами подтягиваются кверху и при
наличии зубов упираются в ткани щечной области кнаружи от альвеолярного
отростка верхней челюсти, вызывая пролежни. Если зубы на нижней челюсти
отсутствуют, то альвеолярные концы фрагментов определяются под краем
скуловых костей, ветви челюстей выворачиваются. Верхняя челюсть
вследствие нарушения мышечного равновесия в лицевом скелете, потери зубов-
антагонистов и рубцового давления с боков быстро суживается. Небо
становится глубоким, альвеолярный отросток приобретает треугольную форму.
Сохранившаяся слизистая оболочка полости рта на 1,5—2 см по краям
дефекта истончена, со следами воспаления. Язык отечен. Совокупность
перечисленных факторов позволяет отнести эти дефекты лица к числу наиболее
тяжелых.
149
Для преодоления неблагоприятных местных условий необходимо
удалить все резко измененные мягкие ткани, инфицированные участки
нижнечелюстной кости и надежно укрыть их. Восстановительное лечение состоит
не только в реконструкции утраченных анатомических образований и
воссоздании физиологического смыкания полости рта. Не менее важны контуры
нового подбородка, упругость его, соответствие по форме и цвету остальным
отделам лица. Поскольку возможность последующей костной пластики
особенно у онкологических больных, достаточно проблематична, мы стремимся
уже на первом этапе сформировать упругий подбородок, не подверженный
рубцовому сморщиванию, даже если по каким-либо причинам невозможно
восстановить непрерывность нижней челюсти.
Должна быть создана прочная двойная эпителиальная выстилка и по
проекции самого подбородка, между эпителиальными слоями из избытка
мягких тканей сформирован каркас, который приобретает твердость при их
рубцевании.
В настоящее время эти дефекты закрывают с помощью двух филатов-
ских стеблей по способу Хитрова, предложенному в 1954 г. После сложных
многоэтапных операций удается создать полноценный подбородок, но
длительность восстановительного периода, многочисленность промежуточных
операций и необходимость пересаживать стебли в края раны, т. е. в условия
пониженного кровоснабжения, существенно сдерживают широкое
применение метода. Хорошие результаты получают только самые опытные
хирурги.
Пытаясь облегчить и по возможности стандартизировать пластические
операции, мы разработали способы ускоренного восстановления этой зоны
лица отдельно для женщин и мужчин. У женщин, а также у мужчин с редкими
волосами на голове и лице, дно полости рта, нижнюю губу и подбородок
восстанавливают путем формирования сложного лоскута с большой
грудной мышцы и дельтопекторального лоскута. Кожно-мышечным лоскутом
восстанавливаем ткани дна полости рта и за счет мышцы получаем избыток
ткани в области подбородка. Дельтопекторальным лоскутом создаем
кожную часть нижней губы, наружные отделы подбородка и подподбородочной
области.
По стандартной методике на грудной клетке от середины дельтовидной
мышцы до наружного края грудины выкраиваем кожно-жировую ленту и
отводим ее к центру. Обнажаем переднюю поверхность большой грудной
мышцы. Нижний край кожно-жировой раны, образовавшейся в результате
формирования дельтопекторального лоскута, является одновременно верхней
границей кожно-жировой площадки лоскута, включающего большую
грудную мышцу. Способ иссечения и подъема второго сложного лоскута
размером 10 х 14 см из мышцы стандартен, но в данном случае дополнительно
упрощен за счет широкого обнажения ее передней поверхности. Лоскуты
имеют разные источники кровоснабжения, которые сохраняются при
одновременном их формировании.
Вначале к остаткам слизистой оболочки дна полости рта подшиваем
верхний участок кожно-мышечного лоскута, ориентируя его вдоль сагиттальной
оси. Предварительно общепринятым способом создаем воспринимающую
раневую поверхность вокруг дефекта, удаляем измененные участки
нижнечелюстной кости. В нижний отдел раны на лице через туннель под кожей шеи
выводим кожно-мышечную площадку. Швы между кожей и слизистой
оболочкой дна полости рта накладываем с трех сторон — под языком и в боковых
отделах. Во время подшивания лоскута последовательно отгибаем его
периферический отдел кверху, стараясь повторить естественные формы дна полости
150
рта и переход их в нижнюю губу. Выстоящие костные фрагменты челюсти
укрываем мышечным слоем лоскута. К оставшемуся свободным переднему
краю грудного лоскута подшиваем дельтопекторальный лоскут, который
укладываем также вдоль сагиттальной оси на нижнюю раневую поверхность
грудного лоскута. Остальную часть кожно-жировой ленты сворачиваем в
трубку. Рану на грудной клетке удается ушить без дополнительных
трудностей, которые, на первый взгляд, может вызвать формирование сразу двух
лоскутов на одной стороне грудной клетки. У женщин раневая поверхность
хорошо закрывается после перемещения кнутри и кверху молочной железы,
у мужчин — после широкой отсепаровки нижнего края раны и приведения
предплечья к передней стенке живота. В дальнейшем отсекаем ножку дель-
топекторального лоскута и формируем из нее ткани подподбородочной
области. Красную кайму нижней губы моделируем из сохранившихся ее
остатков или за счет перемещения лоскута из верхней губы.
Описанный способ имеет следующие преимущества:
1. Оба лоскута при подшивании ориентируют вдоль сагиттальной оси,
что обеспечивает максимальный прирост ткани в переднезаднем
направлении.
2. Избыток ткани, образующийся при перенесении к дефекту двух кож-
но-жировых лоскутов в сочетании с массивной мышечной
подкладкой у одного из них, позволяет создать подбородок любых размеров
даже с учетом последующего рубцевания.
3. Состояние тканей, окружающих дефект, влияет на конечный результат
операции. Наложенные друг на друга сложные кожные лоскуты с
независимым от местных условий кровообращением всегда легко
срастаются. Расхождение швов возможно лишь по периферии раны у
места соприкосновения перемещаемых и окружающих тканей. Наличие
широких раневых поверхностей благоприятствует прорастанию сосудов
из богато васкуляризованной ткани в ишимизированную. Даже после
первоначального расхождения швов по краям постепенно происходит
сращение.
4. После операции остаются только два продольных рубца от углов рта
к подподбородочной области, которые более благоприятны в
косметическом отношении.
5. Дополнительные повреждения в донорской зоне незначительны.
При восстановлении нижней зоны лица наибольший эффект получают,
используя кожно-костный трансплантат из паховой области, перемещаемый
к дефекту с помощью микрососудистых анастомозов.
23.7.3. Выделение кожно-костного трансплантата
паховой области
Кожу с подлежащими тканями рассекают до наружной косой мышцы живота
по верхней границе планируемого лоскута выше паховой складки. Клетчатку
и тонкую соединительнотканную пластинку, прилегающую к мышце,
включают в лоскут и аккуратно отделяют от поверхности мышцы. Коагулируя
мелкие перфорантные сосуды, смещают поверхностные ткани вниз
равномерно по всей длине разреза. За 3—4 см до паховой складки отслойку
прекращают и на этом уровне рассекают наружную косую мышцу живота. Разрез
мышцы проводят также параллельно гребню подвздошной кости вдоль фиб-
151
рилл, на всю длину планируемого костного трансплантата, а у латерального
края поворачивают в сторону кости. Медиальный конец разреза закругляют
вниз до пахового канала. Затем выделяют семенной канатик и смещают его
вверх и внутрь, определяют пульсацию наружной подвздошной артерии под
поперечной фасцией и рассекают ее вдоль раны, в глубине которой
становятся видны артерия и вена. Сосудистый пучок прослеживают до периферии,
рассекая под ним поперечную фасцию и отделяя место прикрепления
внутренней косой и поперечной мышц живота от паховой складки. На уровне
передней ости подвздошной кости артерия делится на несколько ветвей,
включая восходящий сосуд и анастомотическую ветвь, поднимающуюся из
глубины на поверхность. На этом уровне рекомендуется прекратить
препаровку, поскольку несколько мелких ветвей прободают поперечную мышцу в
виде густого сплетения. Возникшее кровотечение сложно остановить без
нарушения кровообращения в этом регионе.
Сосудистый пучок освобождают от тканей сверху и со стороны живота,
тщательно сохраняя нижневнутреннее соединение с отсеченным мышечным
фрагментом, прикрепляющимся к подвздошной кости. Во время препаровки
сосудов можно заметить многочисленные ответвления, отходящие в сторону
кости. Рассечение мышц продолжают на протяжении 8—10 см за гребнем,
отодвигают базовую клетчатку и выделяют линию слияния поперечной и
подвздошной фасций, на 1 см кнутри от которой пересекают фасцию и
достигают надкостницы подвздошной кости. Низводят все ткани, обнажая
внутреннюю поверхность кости на 2—4 см и по линии будущей остеотомии
рассекают надкостницу. Затем скальпелем очерчивают нижний край кожной
части лоскута, обнажают мышцу, напрягающую широкую фасцию бедра, и
пересекают ее в направлении подвздошной кости вместе с прикрепленной к
ней большой ягодичной мышцей. Толщина мышечной массы достигает 3—
4 см. Кровотечение останавливают прошиванием или коагуляцией.
Медиальнее верхней передней ости подвздошной кости пересекают
сухожилие портняжной мышцы и отсекают паховую связку. Обнажают
наружную поверхность тазовой кости, следя за тем, чтобы линия остеотомии
находилась глубже сосудистого пучка. Пересечение кости производят
бором или широким долотом, защищая мягкие ткани лопаточкой Буяльского
или шпателем. Тонкая пластинка подвздошной кости отделяется очень
легко в отличие от гребешка. Во избежание натяжения сосудистого пучка при
отламывании костного сегмента необходимо вначале максимально
освободить его со всех сторон и затем, вставляя в линию распила долото или
распатор, колебательными движениями надламывать оставшиеся костные
перемычки.
Отдельные авторы предлагают оставлять освобожденный
комбинированный трансплантат в течение 30 мин на сосудистом пучке. За это время
визуально оценивают кровообращение в лоскуте по цвету кожи и капиллярной
реакции, кровоточивости костного саженца, пульсации артерии и наполнению
вены. Флоуметрическое измерение кровотока позволяет документировать
состояние сосудов. Ушивая рану, восстанавливают поврежденные анатомические
структуры, обращая особое внимание на сопоставление фасциальных и
мышечных слоев во избежание образования грыжи в послеоперационном
периоде. Вначале сшивают подвздошные фасцию и мышцу с поперечными
фасцией и мышцей, затем внутреннюю и наружную косые мышцы — с
ягодичной и мышцей, напрягающей широкую фасцию бедра. В конце
восстанавливают паховый канал и фиксируют паховую связку к кости.
G. Taylor и соавт. A979) следующим образом оценивают преимущества
данного лоскута:
152
1) сосуды идеально подходят для микрохирургических анастомозов.
Диаметр их B—3) мм достаточно велик, практически такой же, как
крупных сосудов, используемых в качестве реципиентных.
Оптимальный кровоток в них позволяет не опасаться артериальной
перегрузки при сшивании конец в конец;
2) сосудистая ножка достаточно длинная и может быть расположена под
углом к оси трансплантата, что облегчает его фиксацию к фрагментам
кости и технику выполнения микроэтапа;
3) удается переносить большой блок кости (средние размеры 10,6 х 3,6 см),
которым можно восстановить нижнюю челюсть. Предпочтение следует
отдавать той же стороне;
4) продолжительность образования костной мозоли между
трансплантатом и реципиентной костью равна времени консолидации обычной
кости после перелома, т. е. для нижней челюсти составляет 4—5 нед.
Мы отмечали полное сращение трансплантата через 3--4 нед;
5) одновременно с костью пересаживают крупный кожно-жировой
лоскут (возможные размеры 18x7 см);
6) хорошо кровоснабжаемые мягкие ткани, окружающие со всех сторон
костный трансплантат, помогают изолировать его от внешней среды,
предотвращая развитие воспаления;
7) повреждение донорской зоны минимальное, почти не отличается от
травмы, наносимой при заборе ткани из бессосудистого гребня
подвздошной кости. Натяжение мягких тканей у паховой складки
незначительно.
К отрицательным сторонам метода относят длительность оперативного
вмешательства (от 9 до 13 ч). При работе двух бригад хирургов нам удалось
сократить время операции до 5—6 ч. Выделение лоскута (наиболее
трудоемкий этап операции) начинаем одновременно с подготовкой реципиентной
зоны. К моменту переноса трансплантата все манипуляции у дефекта должны
быть закончены и в костные отверстия проведена фиксирующая проволока.
Мы убедились в необходимости первоначальной фиксации, следом за
которой наступает микрохирургический этап. Выполняя первые подобные
операции и стараясь сократить время ишемии трансплантата, вначале после
предварительной примерки накладывали сосудистые анастомозы. Однако
фиксация кости — достаточно грубая процедура. К тому же иногда для
наилучшей адаптации необходимо видоизменить положение костного саженца.
Вероятность повреждения или -чрезмерного натяжения сосудистого пучка в
этих условиях достаточно высока.
Укрепив трансплантат в правильном положении, определяем условия
сшивания сосудов и при необходимости удлиняем их за счет аутовенозных
вставок. Из реваскуляризованной кости возможно обильное кровотечение,
которое нельзя остановить прижатием или прошиванием. С целью
предотвращения или опорожнения гематомы дренируем рану. При длительной
кровоточивости переливаем кровь.
Кожный сегмент лоскута в крайних медиальных и латеральных участках
находится в условиях критического кровообращения из-за повреждения
мелких перфорантных сосудов. Частичную потерю кожи вследствие ишемии
описывают многие авторы. Из 16 операций, выполненных по этой методике,
в 3 случаях мы констатировали частичный и в одном — полный некроз
кожно-жировой ткани с сохранением жизнеспособности кости. У 2 пациентов
гипоксия кожи проявлялась изменением окраски с полным восстановлением
цвета через 10 сут.
153
23.8. Устранение дефектов глотки и шейного отдела пищевода
Сложность пластических операций у больных данной категории усугубляется
следующими обстоятельствами.
1. Кожа передних участков шеи с выраженными лучевыми изменениями
мацерирована в результате раздражающего влияния обильной слюны,
истончена.
2. У 85 % больных высеивается патогенный золотистый плазмокоагули-
рующий стафилококк, нечувствительный к большинству используемых
антибиотиков.
3. У больных, перенесших с одной или двух сторон операцию Крайля,
непосредственно под кожей и по краю дефекта определяется
пульсация общей сонной артерии. Освежение краев фарингоэзофагостомы
опасно из-за вероятности аррозивного кровотечения в
послеоперационном периоде.
4. Выраженный кашлевой рефлекс мешает добиться полного покоя в
ране уже в ближайшие часы после операции.
5. Длительное зондовое питание не может адекватно восполнять ресурсы
организма; большинство больных истощены, с низкими цифрами
гемоглобина и белков.
6. У большинства больных после многократных операций, проведенных
в других лечебных учреждениях, кожа переднебоковой поверхности
шеи покрыта рубцами.
Способ замещения дефекта зависит от состояния краев фарингостомы
и кожи боковых отделов шеи. Если есть возможность использовать ее для
внутренней выстилки (незначительная мацерация, достаточная
подвижность), то внутреннюю стенку глотки формируют в соответствии с
общепринятыми положениями путем отсепаровки и опрокидывания на 180° участка
кожи у края дефекта. Особое внимание уделяют тщательному ушиванию раны.
Мы накладываем двухрядный плотный шов хромированным кетгутом 3/0—
4/0. Наружную рану закрывают дельтопекторальным лоскутом, который
перемещают на всю раневую поверхность. Следует отметить, что ширина этого
лоскута обычно превышает ширину сформированной раневой поверхности
на шее, поэтому мы дополнительно удаляем кожу до сетчатого слоя по краям
дефекта глотки.
Данная манипуляция значительно расширяет воспринимающую раневую
поверхность и позволяет существенно перекрыть не только внутренний ряд
швов, но и края дефекта. Для облегчения снятия поверхностного слоя кожу
инфильтрируют 0,25 % раствором новокаина или изотоническим раствором
натрия хлорида. При подшивании дельтопекторального лоскута
первоначально накладывают швы между его фасцией и раневой поверхностью на шее.
От центра лоскута швы постепенно смещают к периферии в обе стороны,
стараясь добиться равномерного прилегания лоскута по всей поверхности.
Наибольшие трудности возникают при ушивании нижнего отдела раны в случае
дефекта шейного отдела пищевода. Внутреннюю выстилку, чаще при
расположении дефекта ниже яремной вырезки и низкой перемычке между трахеей
и пищеводом, удается создать без особого труда, используя рекомендованное
Ф. М. Хитровым низведение трахеи вперед с продольным рассечением
передних колец. Наружную же поверхность этого участка сразу укрыть
дельтопекторальным лоскутом невозможно из-за перегиба лоскута над трахеостомой.
Происходит смещение оси лоскута в ту сторону грудной клетки, на которой
он сформирован. При низкой локализации дефекта кожно-жировую площадку
154
подшивают только до границы средней и нижней трети шеи, отсрочивая
окончательное закрытие эзофагостомы до второго этапа.
Если кожа боковых отделов шеи непригодна для пластики и ширина
оставшейся части слизистой глотки недостаточна для сворачивания ее в трубку
диаметром 2—2,5 см, то внутреннюю выстилку нужно формировать из ткани
дельтопекторального лоскута [Вакаггуіап, 1965].
В таких случаях лоскут подшивают к одному из краев дефекта. По краю
фарингостомы иссекают полоску кожи шириной 2,5 см. Раневую
поверхность обязательно создают вдоль верхнего края дефекта. К узкой раневой
поверхности, окаймляющей !/2 или 2/з дефекта, подшивают сложенный вдоль
оси дельтопекторальный лоскут. Швы накладывают сразу на кожу. Объем
операционной травмы на этом этапе минимальный. Выраженных местных
воспалительных реакций мы не наблюдали.
Окончательно фарингоэзофагостому закрывают на следующем этапе.
Продольно рассекают свободный край прижившего лоскута и послойно
сшивают его с краями дефекта. За неделю до операции отсекают питающую ножку
от грудной клетки.
В 3 случаях мы пытались создать внутреннюю выстилку дублированием
периферического отдела дельтопекторального лоскута согласно рекомендациям
Т. Krizek и М. Robson A974). Первоначально на плече и грудной стенке
выкраивали кожно-жировую ленту, продольно рассекали концевой отдел на
расстоянии, равном длине фарингостомы, складывали раневыми
поверхностями рассеченные концы, формируя кожную дупликатуру, и подшивали
лоскут на место. У 2 больных пластика дефекта этим лоскутом была
проведена на 8-е и 12-е сутки, у третьего — на 30-е сутки (выписан по семейным
обстоятельствам).
Мы не смогли отметить преимуществ предварительного дублирования
лоскута. Одноэтапно операцию закрытия фарингостомы выполнить не удается,
так как эпителизированный участок внутренней поверхности лоскута
препятствует ушиванию нижнего края дефекта, а условия для накладывания швов
при дублированном лоскуте более сложные. К тому же воспалительная
реакция сильнее вследствие большей травмы. У одного пациента при
длительном сроке дублирования кожи для одномоментного закрытия дефекта было
произведено подсечение нижней части внутренней выстилки.
Дублированный участок кожи остался связанным с лоскутом только за счет сращения
раневых поверхностей и представлял собой кожный "островок" на внутренней
раневой поверхности лоскута. Однако после пластики наблюдалось нагноение
раны, расхождение швов и полный некроз внутреннего фрагмента лоскута.
Очевидно, даже 30 сут при осевом кровоснабжении недостаточно для
истинного срастания раневых поверхностей лоскута между собой. Кровоснабжение
обеих половинок обеспечивается из центральной ножки, и перерыв его в
одной из них не компенсируется сосудами из раневой поверхности другой.
Вероятно, и на этом участке нужна предварительная биологическая тренировка.
При полных дефектах глотки и шейной части пищевода, образовавшихся
после круговой резекции глотки, весь просвет пищепроводного пути лучше
сформировать из однородной ткани. Кожа шеи, которой укрывают
переднюю стенку позвоночника после удаления гортани и глотки, либо снабжена
волосами, которые в дальнейшем могут препятствовать прохождению пищи,
либо настолько атрофична, что не может быть использована для пластики.
Внутренние сонные артерии при таких дефектах располагаются сразу же под
кожей, поэтому при отсепаровке кожи возникают определенные технические
сложности. Следует учесть, что для всех больных этой группы доза при
лучевой терапии составляет 60 Гр и больше. Кроме того, если все же удается
155
подшить лоскут по обеим сторонам от средней линии, то образуется два ряда
швов, наложенных в неблагоприятных условиях.
Существуют три варианта восстановления пищепроводного пути.
Первый, описанный Ф. М. Хитровым, за счет формирования двух филатовских
стеблей, слишком длительный и предусматривает много этапов. К тому же в
условиях массивного предоперационного облучения надежда на хорошее
приживление стебля к мацерированному, инфицированному участку мала.
Второй вариант — использование двух дельтопекторальных лоскутов.
Замещая такие дефекты, сворачивают в трубку кожей внутрь один дельто-
пекторальный лоскут, предварительно удалив кожу над позвоночником для
образования воспринимающей раневой поверхности. Ткани лоскута,
находясь в условиях автономного питания, хорошо срастаются между собой,
образуется одна продольная линия швов. Другим дельтопекторальным
лоскутом укрывают раневую поверхность первого лоскута. Операцию проводят в
два этапа. Вначале формируют верхние 2/з дефекта, через 1,5—2 мес ножки
отсекают и закрывают дефект пищевода.
Наилучшие и более надежные результаты удается получить, используя
кожно-жировой лоскут с включением широчайшей мышцы спины. Он
отличается хорошим кровоснабжением и легкостью мобилизации.
При малейшем сомнении в жизнеспособности кожи по краям
глоточного дефекта мы полностью удаляем ее. Нередко после подобного иссечения
остается только задняя стенка глотки шириной до 2 см. В этой ситуации
одномоментное восстановление просвета глотки можно выполнить следующим
способом. Широко иссекают кожу по краям дефекта на 4—5 см в каждую
сторону либо деэпидермизируют ее на том же протяжении. Выделяют переднюю
стенку пищевода по нижнему краю раны, мобилизуют ее и подтягивают
вверх, а внизу вплоть до заднего края трахеостомического отверстия создают
раневую поверхность, также иссекая или деэпидермизируя кожу. Таким же
образом формируют раневую поверхность в верхнем углу раны. В результате
сохранившуюся слизистую оболочку глотки со всех сторон окружает
широкая раневая поверхность.
Кожный лоскут с включением большой грудной мышцы, выкроенный
в соответствии с размерами раны на шее, прикладывают к передней
поверхности шеи. К внутренней поверхности мышечной части лоскута,
соответствующей недостающей передней стенке глотки, пришивают полоску
расщепленной кожи, взятую с помощью дерматома с бедра. Ранее вводят
носопищеводный зонд. Ширина и длина кожного трансплантата зависят от
величины сохранившейся слизистой оболочки глотки. Для свободного
прохождения пищи достаточно, чтобы диаметр глотки был в пределах 2 см.
Следовательно, внутренняя окружность глотки может составлять 6 см. Из этой
величины вычитают ширину сохранившихся стенок глотки и получают
размеры подшиваемого кожного трансплантата, верхний и нижний концы
которого должны располагаться по контурам дефекта передней стенки глотки.
Мышечную часть лоскута подшивают вдоль краев кожного трансплантата
над зондом, постепенно смещая швы к периферии. Вокруг кожного мостика
по периметру раны накладывают в среднем два — три ряда швов. В
последнюю очередь ушивают кожу.
Заживление внутренней выстилки происходит вторичным натяжением
вдоль боковых стенок глотки. Свободный кожный трансплантат, аккуратно
подшитый к внутренней поверхности мышцы, как правило, хорошо срастается
с ней. В первые дни после операции возможно выделение слюны из боковых
отделов раны, но постепенно происходит слипание ткани лоскута с раневой
поверхностью на шее. Фактически наружную и внутреннюю стенку глотки
156
формируют без использования местных тканей, что увеличивает надежность
операции.
Если на коже переднебоковых поверхностей шеи отмечаются видимые
воспалительные и постлучевые изменения, но она легко смещается и
подвижна, то можно видоизменить пластическую операцию. После рассечения
боковых краев глоточного дефекта отсепаровывают кожу от центра в стороны
вместе с сохранившейся подкожной мышцей, создавая вокруг оставшихся
стенок глотки широкую раневую поверхность, как при использовании
описанного выше способа. Кожно-мышечный лоскут с передней стенки грудной
клетки опрокидывают на шею кожей внутрь и после примерки удаляют с
боков часть кожи, сохраняя ее в виде полоски лишь в центре, по проекции
передней глоточной стенки. Тщательно сшивают края глотки с кожей лоскута
на всем протяжении, затем подшивают мышечную часть лоскута к раневой
поверхности, образовавшейся после отсепаровки кожи шеи в стороны. Затем
смещают к центру отсепарованные ранее кожные лоскуты с шеи. Если не
удается соединить их между собой над оказавшейся снаружи внутренней
поверхностью фрагмента большой грудной мышцы, то оставшуюся рану
закрывают расщепленным кожным трансплантатом. При выполнении операции
данным способом внутреннюю выстилку формируют из интактной кожи
передней стенки грудной клетки. Сразу же можно добиться хорошей
герметизации глотки путем тщательного ушивания ее стенок с толстой кожей частью
лоскута. Однако если на передней стенке грудной клетки имеются волосы,
то они продолжают расти в просвет глотки, препятствуя прохождению
пищевого комка.
23.9. Устранение лицевых параличей
Лицевой паралич, или прозоплегия, встречается как результат аплазии либо
повреждения лицевого нерва или мимических мышц. Врожденные лицевые
параличи являются признаком внутриутробного или наследственного
поражения лицевого нерва или мимических мышц, формирующихся из II
жаберной дуги. Изолированное врожденное нарушение мимики лица встречается
крайне редко. В большинстве случаев данный симптом является частью
различных полинейропатий, иногда в сочетании с другими пороками развития
частей тела (ушные раковины, язык, пальцы и др.).
Причинами приобретенных лицевых параличей могут быть травма,
воспаление, опухоли, сосудистые заболевания, токсические и неврологические
факторы и др. В связи с тем что лицевой нерв имеет около 20 коммуникаций
с другими периферическими нервами (тройничный, языкоглоточный,
блуждающий, шейное сплетение), его повреждение может сопровождаться
нарушением речи, дыхания, глотания, слуха, вкусовой чувствительности языка,
продукции или дренажа слезы и слюны. Присоединение перечисленных
симптомов к основным дисфункциям, характерным для изолированного
повреждения лицевого нерва (неподвижность одной или обеих половин лица,
асимметрия лица разных степеней, лагофтальм, симптом Белла,
патологическое слезотечение, отсутствие естественных складок на пораженной стороне
лица и др.), создает тяжелую клиническую картину, сильно влияющую на
психику больных. По мнению E.J. Aviv и М. Urken A992), лицевой паралич
является катастрофой для больного.
Раздел написан совместно сЦ. М. Шургая.
157
У пациентов, которые в силу своей профессии нуждаются в хорошей речи
и нормальной внешности (учителя, актеры, тележурналисты и др.),
указанная патология может быть причиной потери работы.
Впервые клиническая картина периферических и центральных лицевых
параличей была описана Ch.Bell в 1936 г. В связи с этим для обозначения
процессов, вызванных поражениями лицевого нерва, в классификации ВОЗ
(Периферические нейропатии. — Женева: ВОЗ, 1982) принят термин
"Паралич Белла". В практической медицине указанным термином обозначают
типичный туннельный синдром, вызванный компрессией нерва в узком
лицевом канале после его воспалительного отека.
По данным ВОЗ, на 100 000 населения встречается 13—14 случаев
лицевого паралича (одинаково часто у мужчин и женщин), по данным П. М. Аль-
перовича A978), М. Podvinek A984), 17—18 случаев. Среди заболеваний
периферической нервной системы лицевой паралич занимает второе место после
пояснично-крестцового радикулита [Фарбер М. А. и др., 1976; Пщук Я. И.,
1979; Альперович П. М. и др., 1981; Гречко В. Е. и др., 1990].
Восстановление перечисленных функций является настолько сложной
проблемой, что, по мнению большинства авторов, любую удачную
операцию, нацеленную на динамическую коррекцию парализованного лица,
можно считать счастливой случайностью.
Методы исследования больных с лицевыми параличами. Из существующих
субъективных и объективных методов обследования больных с различными
нейропатиями в современной неврологии предпочтение отдают первым.
И. Н. Горбач в 1995 г. в книге "Критерии диагностики в невропатологии"
отметил: "...несмотря на то, что сегодня в медицинскую практику широко
внедряются сложнейшие технические исследования, клиническая
диагностика (топика, синдромология, нозология и др.), не только не утратила своей
значимости, но и стала еще более необходимой в решающей постановке
диагноза, отражающего индивидуальные особенности каждого конкретного
случая заболевания как нарушения адаптационного, энергетического и
репродуктивного гомеостаза".
При обследовании больных используют традиционные клинические методы
(изучение местного и общего статуса), а также оценку психоэмоционального
состояния больного, состояния других черепных нервов и ЦНС, возможных
донорских нервов, зон донорских мышц и реципиентных сосудов,
фотографирование, записи на видеопленках, рентгенологические исследования,
функциональную диагностику, электромиографию, электронейронографию.
В зависимости от этиологического фактора и давности заболевания,
используют разные клинические подходы и методы диагностики.
Сбор анамнеза. Начинают с выяснения основных жалоб и
этиологического фактора заболевания. Затем у больных каждой группы обращают
внимание на определенные моменты.
У больных с травматическими лицевыми параличами выясняют
характер начала заболевания (острое или через некоторое время после травмы). В
первом случае это признак повреждения нерва, а во втором — его
компрессии внутри- или паранервной гематомой или отечными тканями. Определяют
также характер течения болезни: прогрессирующий обратимый,
рецидивирующий или стойкий.
У больных с параличами Белла выясняют наличие вирусного продрома,
характер болей, начало и течение заболевания, состояние вкуса и слуха,
продукции слюны.
У больных с врожденными параличами обращают внимание на семейный
анамнез, характер родов, интеллект и психоэмоциональное состояние.
158
Объективные методы исследования применяют для объективной оценки
степени уровня повреждения лицевого нерва и послеоперационных результатов.
С этой целью используют следующие электрические тесты.
Электромиографический тест возбудимости нерва.
Данный метод с записью вызванных потенциалов позволяет определить
уровень денервации мышц лишь через 10—14 дней после начала паралича (время
начала дегенеративных изменений периферического отрезка нерва).
Суммарную электроактивность мышц изучают в трех состояниях: в покое, при
тонических реакциях и активном сокращении. Запись электрической активности
проводят с обеих сторон. Уровень патологических изменений определяют
по разнице формы, амплитуды и длительности потенциалов действия
одноименных мышц на здоровой и парализованной стороне. Снижение
амплитуды интерференционной ЭМГ свидетельствует об аксональном
поражении нерва. При центральных поражениях лицевого нерва наблюдаются
редкие колебания и резкое снижение амплитуды, что указывает на
уменьшение числа функционирующих мышечных волокон. При полных
параличах мышц наблюдается "электрическое молчание", что свидетельствует о
функциональной блокаде передачи нервных импульсов (до 1 года после
начала паралича) или полной атрофии мимических мышц (при параличах
давности более 1 года).
Тест максимальной стимуляции нерва проводят с
помощью накожных электродов, которые располагают в двигательных точках —
на уровне основного ствола и передней границы околоушной железы
(наиболее поверхностное расположение конечных ветвей нерва). Чтобы
определить максимальную стимуляцию, силу тока постепенно увеличивают до 5 мА
или до тех пор, пока больные не отметят дискомфорт. При данной методике
количество мышечных сокращений при реакции на максимальную стимуляцию
является конечной точкой. Реакцию на пораженной стороне сравнивают с
таковой на другой стороне. При минимальном снижении реакции считают, что на
стороне паралича подергивание мышц снижено на 50 % по сравнению с
нормальной стороной. Значительное снижение реакции означает, что
подергивание на стороне паралича на 25 % меньше, чем на непораженной стороне.
Электронейронография позволяет получить количественную
информацию о поврежденных аксонах. Для ее проведения используют
электромиограф с прямой записью. Измеряют скорость проводимости нервных
импульсов и амплитуду вызванных суммированных потенциалов обеих сторон
лица от пика до пика.
Количество дегенерированных нервных волокон определяют путем
сравнения скорости проводимости нервных импульсов (СПИ) на
парализованной и здоровой стороне, а также с учетом различия амплитуд измеряемых
суммарных потенциалов. Данную методику используют как при обследовании
больных с острыми травматическими параличами или параличами Белла, так
и при оценке количества регенерированных нервных волокон через длинные
нервные трансплантаты (икроножного нерва).
23.9.1. Травматические лицевые параличи
Несмотря на то что травматическим повреждениям периферических нервов
мирного времени посвящено огромное число работ, нет единого мнения об их
частоте [Лобзин В. С. и др., 1989].
По нашим данным, больные с травматическими лицевыми параличами
составляют 65—70 % общего числа больных с этой патологией.
159
По материалам ВОЗ, наиболее частыми формами травматических
повреждений нервов являются размозжение, ушиб, растяжение, а также сдав-
ление с наличием или отсутствием разрыва нервного ствола
(Периферические нейропатии. — Женева: ВОЗ, 1982).
Микроскопические изменения при повреждении нерва (по
классификации ВОЗ) сведены в три основные группы: невротмезис, невропраксия и
аксонотмезис. Эта патоморфологическая характеристика повреждений нервных
стволов дополняется двумя возможными функционально-морфологическими
формами: 1) аксонопатией — повреждением нервов, которое, как
предполагают, заключается в нарушении выработки энергии окисления в аксональных
митохондриях, что и приводит к угнетению аксонального переноса ацетил-
холина; 2) миелинопатией — утратой миелина (чаще сегментарная с нервной
локализацией около перехватов Ранвье) с явлениями миелинофагии,
осуществляемой макрофагами. Могут определяться также непропорционально
тонкие миелиновые оболочки, что свидетельствует о частичной демиелини-
зации или ремиелинизации.
В 1972 г. S. Sunderland предложил систему клинико-патологической
классификации повреждений лицевого нерва, в которой выделил пять
степеней повреждения и четыре вида восстановления нерва. В 1986 г. М. May
внес коррективы в эту классификацию (рис. 23.15).
I степень — компрессия нерва гематомой или анестетическими
веществами. Анатомическая структура нерва сохранена и блокада нервной
проводимости купируется без лечения. Восстановление начинается на 1—3-й
неделе и обычно заканчивается к началу 2-го месяца. Такой вид повреждения
нерва клинически выражается в ограничении движений лица в небольшой
степени или протекает без клинических проявлений. Повреждения нерва I
степени обозначают термином "нейропраксия".
II степень наблюдается в случаях, если компрессия не снимается.
Выявляется ишемия нерва (сеит-фактор), обструкция венозного дренажа
(увеличение интраневрального давления, надавливание проксимального и дис-
тального отека на аксоплазму, иногда прерывание тока питательных веществ
через сужение артериолы). В результате возможна потеря аксонов. Если
процесс обратим, то восстановление может быть полным, хотя выздоровление
займет намного больше времени, чем при повреждении I степени. После
подобного повреждения восстановление происходит спонтанно или на фоне
консервативного лечения, проводимого с целью устранения компрессионного
фактора. В случаях выздоровления паралич исчезает бесследно.
Повреждения нерва II степени обозначают термином "аксонотмезис".
III степень — интраневральное давление не снимается и происходит
потеря миелиновых трубок. Спонтанное восстановление после такого
повреждения не наступает в течение 2—4 мес. При регенерации аксонов возможно их
соединение с эндоневральными трубками чужих аксонов. Такой вид
восстановления называют ложным, или перекрестным. Клинически это проявляется
отдельными синкинезиями (синергичные движения некоторых частей лица).
Лечение проводят с целью спасения как можно большего количества
миелиновых трубок, чтобы поддержать ложную регенерацию.
IV степень повреждения наблюдается при разрыве нерва с сохранением
эпиневральной оболочки при различных операциях. В случаях регенерации
нерва ложное восстановление аксонов неизбежно. Клинически это проявляется
полным рефлекторным гемиспазмом (синергичное движение всей половины лица).
V степень — повреждения наступают при полном пересечении нервного
ствола. Восстановление возможно лишь хирургическим путем. Повреждение
нерва III, IV и V степени обозначают термином "нейротмезис".
160
Рис. 23.15. Клинико-патологическая классификация степени повреждения и видов
регенерации лицевого нерва.
/— степени повреждения; //— виды регенерации нерва: / — компрессия нерва с сохранением
анатомических структур (спонтанное восстановление); 2 — ишемия нерва (сеит-фактор) с
потерей периферических аксонов — восстановление на фоне консервативного лечения; 3— потеря всех
аксонов и миелиновых трубок — частичное восстановление; 4 — разрыв нерва с сохранением эпи-
невральной оболочки — перекрестное восстановление; 5 — полное пересечение нервного ствола —
восстановление хирургическим путем.
Установление степени повреждения нерва является очень важным
фактором при выборе вида лечения (консервативное или хирургическое).
В мировой практике параличи, возникшие в результате различных
операций, рассматриваются как ятрогенные или развившиеся по вине врача, так
как, по мнению многих авторов, все операции, сопровождающиеся
намеренными или случайными повреждениями нерва, должны завершаться его не-
1! - 1263
161
медленной первичной пластикой [Nicolai J., 1985; Medinaceli L., Seaber Α.,
1989; Clasby Μ. et al., 1992].
Послеоперационные лицевые параличи неизбежно возникают в тех
случаях, когда по поводу злокачественных образований околоушной железы,
самого нерва или других примыкающих структур (мукоэпидермоидная
опухоль, цилиндрома, рак, саркома и др.) приходится иссекать опухоль вместе
с фрагментом лицевого нерва. Во всех остальных случаях это является
результатом отсутствия интраоперационного мониторинга за лицевым нервом.
В 1983 г. С. Baker на основе анализа причин послеоперационных
параличей у больных после устранения морщин (собственный материал и данные
еще 21 автора — всего 9969 наблюдений) предложил возможные варианты
механизма интраоперационного повреждения лицевого нерва. В 1986 г.
М. May и R. Wiet модифицировали схему С. Baker и предложили свой
вариант данных механизмов при различных операциях.
Основными механизмами операционной травмы лицевого нерва
являются: коагуляция, рассечение, локальная анестезия, растяжение, компрессия
зажимом, повреждение иглой при накладывании подкожных швов, внутри-
или околонервная гематома. В результате перечисленных причин могут
развиться как обратимые — подлежащие консервативному лечению, так и
необратимые, стойкие лицевые параличи, требующие коррекции с
использованием хирургического лечения.
Лицевые параличи, вызванные механическими травмами, могут
сопровождаться грубыми Рубцовыми изменениями окружающих тканей нерва и
мышц, иногда потерями их фрагментов, наличием инородных тел,
нарушениями функции других нервов, в связи с чем при выборе плана оперативного
вмешательства необходим особый подход.
23.9.2. Общие принципы хирургии лицевого нерва
История хирургии лицевого нерва началась в 30-х годах. В 1927 г. S. Bunnel
выполнил первую успешную операцию сшивания концов нерва.
Сначала хирургические методы были нацелены исключительно на
динамические аспекты — восстановление движений лица путем перекрещивания
лицевого нерва с другими нервами и транспозицию мышц. Статические методы
коррекции парализованного лица были разработаны позже [Nicolai J., 1985].
В настоящее время существует множество методов хирургического
лечения больных с необратимыми лицевыми параличами. Несмотря на это,
интерес к данной проблеме не снижается. Об этом свидетельствует большое
количество работ, посвященных изучению как анатомии, так и хирургии нерва.
В 1985 г. J. Nicolai предложил схему существующих хирургических
методов лечения, в которой он разделил их на статические и динамические
классы. Подобное разделение методов относительно, так как в очень редких
случаях полная реабилитация больных возможна при использовании лишь
одного метода. В большинстве случаев этого можно достигнуть применением
сразу нескольких методов разных классов, а также при дополнении их
корригирующими методами.
Некоторые методы, рассмотренные в данной схеме, в настоящее время
имеют лишь историческое значение (например, перекрещивание лицевого нерва с
добавочным, диафрагмальным, языкоглоточным, язычным нервами,
транспозиция грудиноключично-сосцевидной, двубрюшной, ушной, скуловой мышц).
Свободная аутотрансплантация фрагментов скелетных мышц с немедленной
реиннервацией и реваскуляризацией практически ограничила их применение.
162
Рис. 23.16. Разрез Мак-Индоу,
выполняемый для идентификации лицевого
нерва.
Рис. 23.17. Этап операции:
идентификация основного ствола лицевого нерва.
/ — уровень сосцевидного отростка,
определенный пальпаторно, и место выхода
основного ствола лицевого нерва; 2 — заднее брюшко
двубрюшной мышцы.
Конечной целью хирургического лечения больных с лицевыми
параличами является восстановление утраченной двигательной функции лица и
симметрии в состоянии покоя. Тактика хирурга зависит главным образом от
давности поражения нерва. При сроках паралича до 1 года целью лечения
должна быть реиннервация парализованных мышц. По истечении
указанного срока мимические мышцы атрофируются и становится необходимым их
восстановление другими функционирующими мышечными единицами.
В зависимости от уровня повреждения нерва (интра- или
экстракраниальный) используют различные методы реиннервации. В случаях повреждения
нерва после выхода из черепа его целостность можно восстановить, используя
медиальный отрезок ипсилатерального нерва. В случаях повреждения на
внутричерепном уровне используют лицевой нерв с контралатеральной стороны
или другой интактный моторный черепной нерв (в основном подъязычный).
Окончательно план нейропластики разрабатывают на основании результатов
ревизии лицевого нерва при его повреждениях на экстракраниальном уровне.
Доступ к основному стволу нерва осуществляют через разрез по
Мак-Индоу (рис. 23.16, 23.17), после чего откидывают кожно-фасциальный лоскут,
включая поверхностную мышечно-апоневротическую систему лица. В случае
необходимости ревизии целого экстракраниального сегмента нерва
приходится рассекать околоушную железу по ходу нервных веточек и, таким
образом, разрушать ее собственную капсулу. Это может привести к развитию
слюнного свища, ретенционной кисты или синдрома Фрей (аурикулотемпо-
163
11*
Рис. 23.18. Хирургическая анатомия основного ствола и интрапаротидного сегмента
лицевого нерва.
/ — шиловидный отросток; 2 — основной ствол лицевого нерва; 3 — заднее брюшко двубрюшной
мышцы; 4— задняя лицевая вена; 5— фудиноключично-сосцевидная мышца; 6— наружная яремная
вена; 7 — большой ушной нерв.
ральный синдром). При сохранении поверхностной мышечно-апоневроти-
ческой системы лица риск подобных осложнений снижается.
Затем освобождают задний полюс околоушной железы, передний край
грудиноключично-сосцевидной мышцы и заднее брюшко двубрюшной
мышцы. Пальпаторно определяют шиловидный отросток височной кости, у
верхушки которого должен располагаться основной ствол нерва (рис. 23.18).
Для полноценного доступа к нерву зачелюстную и наружную яремные
вены перевязывают, а большой ушной нерв отодвигают в сторону (рис. 23.19).
Отдельные ветви нерва выделяют в тканях околоушной железы после
рассечения последней по их ходу. При обнаружении поврежденного участка нерва
макроскопический этап ревизии завершают и продолжают операцию под
оптическим увеличением.
23.9.3. Основные методы реиннервации парализованных мышц
при повреждении лицевого нерва на экстракраниальном уровне
Все методы, которые применяются в подобных случаях, нацелены на
восстановление целостности лицевого нерва с использованием медиального
отрезка на ипсилатеральной стороне.
Окончательно метод реиннервации выбирают после ревизии нерва, при
которой можно обнаружить несколько вариантов повреждения нейромышеч-
164
Рис. 23.19. Невромы на разных участках лицевого нерва.
а — иссечение травматической невромы на уровне основного ствола лицевого нерва; б — иссечение
эпиневральной оболочки на уровне бифуркации нерва; в — определение границы здоровых пучков;
г — иссечение невромы в пределах здоровой нервной ткани.
ной системы: компрессию лицевого нерва и блокаду нервной проводимости
за счет эндо- или параневральных рубцов при сохранении целости нерва,
нарушение целости лицевого нерва без дефекта нервной и мышечных тканей,
потерю сегментов нерва с сохранением медиальных и дистальных отрезков и
мышечных тканей, потерю дистальных отрезков нерва с Рубцовыми
изменениями мимических мышц, потерю медиального отрезка нерва с сохранением
или нарушением интактности мимических мышц, потерю целого
экстракраниального сегмента нерва с рубцовой контрактурой мимических мышц,
потерю сегментов нерва вместе с мимическими мышцами, наличие множества
инородных тел в зоне нерва и мышц (при огнестрельных ранениях из охотничьего
оружия). Каждый из перечисленных видов патологии требует особого подхода.
Можно использовать сразу несколько методов реиннервации.
Основным методом реиннервации при сохранении медиальных и
дистальных отрезков нерва является восстановление его целости.
Существуют четыре основных способа восстановления целости нерва на
ипсилатеральной стороне: невролиз (освобождение нерва от пери- или эн-
доневральных рубцов), прямая нейрорафия (сшивание концов нерва спосо-
165
бом конец в конец), замещение дефектов нервными аутовставками (с
использованием нервных аутотрансплантатов в качестве проводника нервных
импульсов) и транспозиция веточек нерва (переключение частей интактных
ветвей нерва на пораженные).
Невролиз — это восстановление проводимости нервных импульсов
путем их декомпрессии в мягких тканях (на экстракраниальном уровне).
Аналогичную операцию на уровне височной кости называют декомпрессией.
Существуют два возможных варианта блокирования нервной
проводимости: компрессионный (грубыми эндо- или периневральными рубцами) и
в результате нарушения целости экстракраниального отдела нерва. В первом
случае поврежденный участок нерва освобождают от рубцов, пальпаторно и
визуально оценивают данный участок. В отсутствие признаков, присущих
эндоневральным рубцам, проводят интраоперационную стимуляционную
диагностику без нагрузки больного миорелаксантами. Ответная реакция
мышц, находившихся в зоне иннервации дистального от поражения участка
нерва, свидетельствует о сохранности его анатомических структур.
Компрессионный паралич возможен и в результате рубцевания эпинев-
ральной оболочки, что определяют пальпаторно и инъекцией
изотонического раствора натрия хлорида под наружную оболочку нерва. Под нормальную
эпиневральную оболочку раствор проникает свободно, а при наличии эпи-
невральных рубцов введение его затруднено или невозможно. В последнем
случае невролиз проводят следующим образом.
Начиная от здоровых участков, по направлению к пораженному
рассекают эпиневральную оболочку, ретрагируя ее над рубцовым участком. Путем
внутреннего невролиза прослеживают каждый отдельный пучок.
Избыточную интрафасцикулярную ткань иссекают до тех пор, пока над всем
пораженным сегментом не будут прослежены отдельные фасцикулярные группы
и они не будут освобождены от сдавления. Затем проводят
интраоперационную стимуляцию. В случае отрицательного ответа иссекают поврежденный
участок и выполняют прямую нейрорафию, используя нейлоновый шовный
материал. Наличие травматической невромы является показанием к нейро-
пластике. Операционная тактика в отношении невромы зависит от
локализации повреждения нерва. Если неврома расположена на уровне основного
ствола, то ее иссекают в пределах здоровых тканей (см. рис. 23.19, а). В
случаях расположения невромы на более периферическом уровне сначала
производят иссечение эпиневральной оболочки (см. рис. 23.19, б), затем
определяют границу здоровых пучков (см. рис. 23.19, в) и пересекают их вместе
с невромой (см. рис. 23.19, г).
Прямая нейрорафия. Восстановление целости нерва путем прямой
или непосредственной нейрорафии дает лучшие результаты, чем любая другая
методика реиннервации [Millesi Η., 1979; Miehlke Α. et al., 1979; Griimley R., 1980].
Основными требованиями являются: сближение дистальных и медиальных
концов нервов без какого-либо натяжения, выполнение операции в наиболее
оптимальные сроки после травмы, правильное сопоставление нервных концов.
Последний фактор более важен, чем сшивание как можно большего
количества нервных аксонов с целью предупреждения перекрестной или ложной
регенерации, которая приводит к формированию синкинезии [Grumley R.,
1980; Lee К., Terzis J., 1984].
Техника нейрорафии в процессе своего развития претерпела
значительную эволюцию от первоначальных макросближений и анастомозирования
шовными материалами 5/0 — 7/0 до современного, утонченного метода с
использованием хирургического микроскопа (с увеличением до 40 раз) и
материала 9/0 - 12/0 [МсКіппоп S., 1989; Clasby M., 1992].
166
В мировой практике нейрорафию выполняют исключительно способом
конец в конец, хотя в отечественной литературе имеются сообщения об
использовании способа конец в бок [Кливолуцкая Е. Г. и др., 1991]. Результаты
подобной нейрорафии являются весьма сомнительными даже с чисто
теоретической точки зрения, так как трудно представить, какой из существующих
четырех способов (рис. 23.20) при этом используется и какие условия
создаются для повторного роста нервных аксонов.
Нейрорафию начинают с обнаружения травматической невромы в конце
медиального отрезка нерва, которая образуется через 2—3 нед после полного
анатомического перерыва нерва и без рубцового объединения концов его
отрезков. Неврома представляет собой булавовидное или шарообразное
утолщение конца центрального отрезка, диаметр которого в 1,5—3 раза
превышает диаметр нервного ствола. Подобное образование, которое формируется
на уровне медиального конца дистального отрезка нерва, называют глиомой
[Mario S., 1993]. Перед сшиванием нерва глиому иссекают в пределах
здоровой нервной ткани. Затем концы нерва сближают и выполняют прямую
нейрорафию. Основным требованием нейрорафии является ее выполнение без
какого-либо натяжения концов нерва. В зависимости от локализации
процесса в хирургии лицевого нерва используют различные методы нейрорафии:
на уровне основного ствола — эпиневральные швы (см. рис. 23.20, а), на
средних участках нерва — периневральные или комбинированные (пери- и
эпиневральные швы по методике Миллези) (см. рис. 23.20, б, в) [Millesi Η., 1979].
В 1980 г. А. Gary-Bobo и соавт. предложили оригинальный метод
нейрорафии, основанный на принципе "циферблата часов" или по четырем
точкам компаса (см. рис. 23.20, г), главным" образом для соединения с лицевым
нервом нервных трансплантатов. С этой же целью, а также для сшивания
концов экстрапаротидного сегмента нерва используют интрафасцикулярные
швы (см. рис. 23.20, д, е).
Наложение эпиневрального шва является традиционным методом
восстановления целостности нерва, но в большинстве случаев приводит к так
называемой ложной регенерации (некоторые аксоны могут прирасти к чу-
жым миелиновым оболочкам), что клинически выражается в синкинезиях. В
1972 г. Н. Millesi и соавт. впервые высказали предположение, что
периневральные швы имеют некоторые теоретические преимущества по сравнению
с эпиневральными из-за точного сопоставления нервных фасцикулов, что
обеспечивает меньшую потерю регенерирующих нервных аксонов и сводит
к минимуму ложную регенерацию. Данный факт имеет место и при
использовании межфасцикулярных швов. На каждую фасцикулу накладывают 1—2
простых шва. Остальные виды нейрорафии выполняют с возможным
минимальным количеством швов, так как вокруг даже самых тонких нейлоновых
швов наблюдается ответная воспалительная реакция. Большое число швов,
наложенных на нервы, может привести к повторному образованию рубцовой
ткани и блокаде нервной проводимости.
Если не выполняется первичная пластика нерва (после травматического
повреждения), то оптимальным сроком его вторичной пластики являются 21-е
сутки после повреждения [Tucker Η, Μ., 1978]. В это время нервные клетки
способны максимально синтезировать белок. Пролиферация леммоцитов и
образование фиброзной ткани происходят быстрее, что приводит к
образованию проксимальных невром, выбуханию фиброзной ткани в дистальных
нейроканальцах и последующей потере нейрофибрильных элементов, которые
не могут проникнуть внутрь дистальных нервных сегментов. Если на 21-е
сутки после травмы производят резекцию невромы и нейрорафию, то
регенерирующие нейроэлементы находятся в равных условиях скорости роста с
167
Рис. 23.20. Виды швов, используемых в хирургии лицевого нерва.
а — эпиневральные; б — пери неврал ьные; в — комбинированные (эпипериневральные); г— полярные;
д, е — фасцикулярные.
фиброзными клетками и леммоцитами. Таким образом, имеется
материальная основа для повышения вероятности того, что дистальный отрезок нерва
будет доступным для тех нервных волокон, которые могут успешно пересечь
участок анастомоза [Tucker Η. Μ., 1978]. В более поздние сроки дистальные
нейроканальцы начинают атрофироваться, эпимизион денервированной
мышцы становится тоньше. Оба этих фактора уменьшают вероятность
успешной реиннервации [Best J. et al., 1993].
Замещение дефектов нерва нервными аутовставками.
Данную методику используют в основном после преднамеренного иссечения
интрапаротидного сегмента лицевого нерва вместе с околоушной железой по
поводу злокачественных опухолей и тогда, когда при иссечении невром и
глиом в пределах здоровых тканей образуются дефекты нервов длиной более
2 см. В первом случае замещение дефектов нерва называют первичной, а во
втором — отсроченной пластикой.
В отличие от описания хирургической техники операции, в литературе
имеются единичные работы, в которых сообщается о хирургической тактике
при образованиях околоушной железы по отношению к лицевому нерву. В
1978 г. Н. Tucker на основе 30-летнего опыта определил показания к резекции
и удалению лицевого нерва.
В число относительных показаний к резекции лицевого нерва входят:
злокачественные опухоли с высокой степенью малигнизации, крупные
злокачественные опухоли, занимающие большую часть каротидной железы,
злокачественные опухоли глубокой доли железы, злокачественные опухоли,
приводящие к лицевому параличу, рецидивирующие злокачественные
опухоли. Относительными показаниями к сохранению лицевого нерва являются:
все доброкачественные опухоли и кисты, ранняя стадия злокачественных
опухолей мостомозжечкового угла и околоушной слюнной железы с низкой
степенью малигнизации; рецидивирующие опухоли смешанной природы. По
мнению автора, в двух последних случаях возможны сегментарная резекция
нерва, тотальная паротидэктомия и послеоперационная лучевая терапия.
Основным моментом первичной пластики лицевого нерва после
удаления его интракаротидного сегмента является предварительная маркировка
одноименных ветвей.
Вторичную, или отсроченную, пластику нерва начинают с обнаружения
и удаления невромы и глиомы концов нерва. Дефекты длиной менее 2 см
устраняют путем выделения концов нерва и прокладывания их более коротким
путем. При более обширных дефектах используют нервные вставки.
В качестве донорских используют в основном большой ушной и
икроножный нервы. Множество авторов предпочтение отдают последнему в связи
с соответствием его диаметра и количества аксонов таким же показателям
лицевого нерва, а также с возможностью забора нужной длины нерва (до 40 см)
при минимальной итоговой функциональной потере донорского участка.
Забор трансплантата большого ушного нерва проводят путем продления
разреза Мак-Индоу книзу на 1,5—2 см. Нерв находят под кожей на уровне
верхней трети грудинокпючично-сосцевидной мышцы. В случаях потери указанного
нерва в результате травмы (доказательством является потеря чувствительности
нижней половины ушной раковины), а также при сложных дефектах общей
длиной больше 7 см используют икроножный нерв. Кроме того, при методике
замещения дефектов нервными аутовставками икроножный нерв используют в
70 % операций, выполняемых на лицевом нерве. В связи с этим мы считаем
целесообразным детальный разбор его хирургической анатомии и техники забора.
Трансплантат икроножного нерва берут следующим образом. Нога больного
находится в полусогнутом положении (рис. 23.21, а). Первый разрез длиной
169
Рис. 23.21. Этапы операций забора икроножного нерва с помощью инструмента
"стриппер".
а — положение ноги больного и уровень первого разреза; 6 — выделение икроножного нерва;
в, г — уровни последующих разрезов; д — завершающий этап — забор трансплантата.
DD
Рис. 23.22. Варианты дефектов лицевого нерва
и форм нервных аутовставок (а—г).
2,5—3 см делают на уровне
задней части латеральной лодыжки.
Идентифицируют икроножный
нерв, малую подкожную вену;
последнюю отодвигают в
сторону. Нерв пересекают выше
бифуркации и берут на держалку
(рис. 23.21, б). Затем, пользуясь
специальным инструментом
стриппером ("обдиратель" нерва),
выделяют нерв вслепую до тех
пор, пока не почувствуют
препятствие. Этот уровень соответствует
бифуркации нерва (рис. 23.21, в).
Над концом стриппера
выполняют следующий разрез.
Бифуркацию пересекают, стриппер
вынимают и вводят его в новую рану
(рис. 23.21, г). Следующий разрез
делают в месте присоединения к
нерву латерального подкожного
нерва икры. Последний
пересекают и вновь продолжают
выделение нерва с помощью
стриппера; дальше он выделяется более
свободно. Последний разрез проводят с учетом нужной длины нерва. Таким
образом, через небольшие разрезы можно получить нервный трансплантат
длиной до 40 см.
В зависимости от характера дефекта лицевого нерва нервные
трансплантаты забирают или с их терминальными ветвями или без них. При
необходимости нервный трансплантат расщепляют на отдельные фасцикулы,
помещают в дефект и выполняют нейрорафию, используя методику Миллези. На
рис 23.22 показаны возможные варианты дефектов лицевого нерва и формы
нервных трансплантатов.
Методика замещения дефектов нервными аутовставками и ее
функциональные результаты при различных вариантах изучена многими авторами:
Н. М. Tucker A978), Η. Millesi A979), К. К. Lee и J. Terzis A984), Μ. Fujii и
N. Goto A989), L. Medinacelli и V. Seaber A989), J. Best и соавт. A993), J. D. Terzis
и Ε. W. Fee A993), U. McCorbick A994). По их мнению, эти результаты
зависят от точности соединения нервных волокон, длины дефекта нерва,
расстояния между участком повреждения и телом нервной клетки, длительности
времени между моментом травмы и операции, степени сопутствующих
травм, психоэмоционального состояния больного (степени стресса во время
травмы), возраста больного.
Транспозиция веточек лицевого нерва. При потерях
отдельных сегментов нерва методом выбора является транспозиция его веточек,
хотя показания к ней крайне ограничены и ее выполняют в случаях
изолированного повреждения скуловой или маргинальной ветви лицевого нерва.
Суть методики заключается в перекрещивании интактных ветвей нерва,
имеющих меньшее значение для мимики лица, с поврежденными, являющимися
более важными (рис. 23.23). По данным А. Miehlke A979), U. Fisch A979),
пожертвование частью веточек лобной и шейной ветви не вызывает опасных
функциональных нарушений на донорских участках и в целом результаты
171
удовлетворительные. Если имеют
место изолированные
повреждения именно перечисленных
ветвей, то методике транспозиции
ветвей отдают преимущество перед
замещением дефектов нервными
аутовставками. Это объясняется
тем, что при транспозиции ветвей
нервным аксонам приходится
прорасти через один нервный
анастомоз, а при замещении дефектов
аутовставками — через два. Тем
самым их число уменьшается на
15—20 %. Примерно такое
количество аксонов теряется при
пересечении каждого нервного шва [Lee
К., Terzis J., 1984].
Невротизация. В тех
случаях, когда имеются потери дис-
тального отрезка или целого
экстракраниального сегмента нерва,
реиннервацию производят с
использованием метода невротизации.
Невротизация — это реиннер-
вация мышц с помощью новых
моторных пластинок, что
достигается за счет аксонов рассеченного
нерва (нервная невротизация), или прорастанием аксонов от соседней иннер-
вированной мышцы (мышечная невротизация).
Реиннервация мышц после сшивания нерва не называется невротиза-
цией, поскольку в таком случае восстанавливаются первоначальные,
собственные конечные моторные пластины моторных нервов.
Эффективность метода мышечной невротизации (мионевротизация)
сомнительна. По мнению многих авторов, такой вид невротизации не имеет места.
В противном случае, как утверждает H.Tucker A977), парализованная часть
круговой мышцы рта должна быть реиннервирована за счет интактной, однако
этого не происходит. По нашему мнению, аналогичным примером является ге-
миатрофия языка после пересечения подъязычного нерва с одной стороны.
При нервной невротизации (нейроневротизация) аксоны проксимальной
культи перерезанного моторного нерва в результате своего роста образуют
новые моторные волокна. Этот факт доказан Н. Tucker A977), W. Trojborg A977),
S. Mackinnon A989), R. Bein и соавт. A992). Операцию осуществляют с
помощью нервных трансплантатов, расщепленные концы которых
имплантируют внутрь денервированной мышцы.
Наша собственная практика показала, что методика нейроневротизации
имеет большие возможности. Ее можно применять при парезах мышц
большой давности с целью устранения XIII симптома Бехтерева (восстановление
непроизвольных движений), усиления эффекта сокращения свободных
мышечных аутотрансплантатов и др. [Шургая Ц. М. и др., 1995].
Рис. 23.23. Транспозиция веточек лицевого
нерва (перекрещивание интактных ветвей с
поврежденными ветвями) (схема).
/ — участки дефектов нерва; 2 — участки
транспозиции интактных ветвей неба; 3 — лобные ветви;
4— скуловые ветви; 5— щечные ветви; 6— краевые
ветви; 7— шейные ветви.
172
СПИСОК ЛИТЕРАТУРЫ
Альперович П. М. Паралич Белла: этиология, патогенез, клиника, течение, исход //
Журн. невропатол. и психиатр. — 1978. — Т. 78, № 6. — С. 836—846.
Альперович Я. М., Билак В. Д., Корнейчук А. Г. Лечение и профилактика невритов
лицевого нерва и их последствий // Методические рекомендации. — Винница. —
1981. - 19 с.
Брусова Л. А. Восстановительные операции на лице с применением силоксановых
композиций (клинико-экспериментальное исследование): Дис. ... докт. мед.
наук. - М., 1996. - 175 с.
Горбач И. Н. Критерии диагностики в невропатологии. Синдроматика. — Минск: Вы-
шейшая школа, 1995. — 319 с.
Гречко В. Е., Степаненко Н. В., Шенгелия Н. Ш. Черепные нервы. — Тбилиси: Мец-
ниереба, 1990. — 285 с.
Емиленко П. И. Устранение Рубцовых деформаций век при сочетанной ожоговой
травме лица: Дис. ... канд. мед. наук. — М., 1980. — 179 с.
Золтан Я. Пересадка кожи. — Будапешт, 1984. — 334 с.
Лобзин В. С, Ласков В. Б., Жулев Н. М. Травмы нервов. — Воронеж, 1989. — 257 с.
Мамонов А. Г. Контурная пластика // Клиническая оперативная челюстно-лицевая
хирургия / Под ред. Н. М. Александрова. — Л.: Медицина, 1985. — С. 88—95.
Пщук Я. И. Невриты лицевого нерва в пожилом и старческом возрасте (этиология,
патогенез, клиника, лечение): Автореф. ... дис. канд. мед. наук — Винница. — 1979. — 25 с.
Фарбер М. Л., Кучковская Е. М., Козлова К Н. Отдаленные результаты лечения
больных с невритом лицевого нерва // Здравоохр. Казахстана. — 1976. — Т.6. — С. 59.
Шургая Ц. М., Неробеев А. И., Караян А. С., Мясковская Е. М. Возможности невроти-
зации при лечении больных с лицевыми параличами // Стоматология, 1995. —
Т. 74, № 4. - С. 33-39.
Aviv Ε. J., Urken L. Μ. Management of the paralyzed face with microneirovasciilar free muscle
transfer // Arch. Otolaringol. Head Nee. Surg. — 1992. — Vol. 113, N 9. — P. 909—912.
Baker D. C. Complications of cervicofacial Rhytidectomy // Clin, plast. Surg. — 1983. —
Vol. 10, N 3. - P. 543 - 562.
Bein J. R., McKinnon S., Hudson A. R. et al. The peripheral nerve alloggraft in the primate
immunosuppessed with electrophysiologic assessment // Plast. Rec. Surg. — 1992. —
Vol. 90, N 6. - P. 1036-1052.
Best T. J., McKinnon S. E., Bain J. R. et al. Verification of a Free vascularized nerve graft
model in the Rat with application to the peripheral nerve allograft // Plast. Reconstr.
Surg. - 1993. - Vol. 92, N 3. - P. 516-526.
Cutting С. В., Brookstein F. L., Grayson B. et al. Three dimensional computer assisted design
of craniofacial surgery procedures: Optimization and interactions with cephaJometrics
and CT based models // Plast. reconstr. Surg. — 1986. — Vol.77. — P.877.
Fisch U. Extratemporal facial nerve grafting and radiotheraphy // Arch. Otolaryngol. — 1979. —
Vol. 105, N 8. - P. 441-446.
Fujii M., Coto M. Nerve Firen analisis of the facial nerve // Ann. Otol. Rhinol. Laryngol. —
1989. - Vol. 98. - P. 732-735.
Fukutura K., Jackson /. Т., McEwan C. N., Neland N. B. Three dimensional emaging in
craniofacial surgery: A review of the role of mirror image production // Eur. J. plast.
Surg. - 1990. - Vol. 13. - P. 209-217.
Glasby Μ. Α., Sharp J. F. New possibilites for facial nerve repair // Fac. plast. Surg. — 1992. —
Vol. 8, N 2. — P. 100—108.
Gary-Bobo Α., Fuentes J. M., Guerrie B. Cross-Facial nerve anastomosis in the treatment of
facial paralysis: A preliminary report on 10 Gases // Brit, plast. Surg. — 1980. — Vol. 33,
N 7. — P. 195-201.
Holmstrom Η., Blomgren I. Simple adaptation of Muller's muscle to the tarsal plate in congenital
blepharoptosis // Scand. J. plast. reconstr. Surg. — 1986. — Vol. 20, N 2. — P. 197—200.
Lee К KfTerzis J. Management of acuta extratemporal facial nerve palsy // Clin, plast. Surg. —
1984. —Vol. II. - P. 203-215.
Luce E. A. Analysis of complex post extirpative deformity // Clin, plast. Surg. — 1995. —
Vol. 22, N 1. - P. 1-8.
173
McKinon S. Ε., Dellon Л. L. Surgical algorithm for the management of facial palsy //
Microsurgery. - 1988. - Vol. 9, N 1. - P. 30-35.
McKinnon S E. Technical considerations of the latissimus dorsi muscle flap: A segmental
innervated muscle transfer for facial reanimations // Microsurgery. — 1988. — Vol. 9, N 1. —
P. 36-45.
McKinnon S. E. New directions in pheripheral nerve surgery//Ann. in Plast. Surg. — 1989. —
Vol. 22, N 3. - P. 257-272.
Mario S. L. Facial nerve suturing and grafting // Operative Surgery Head and Nek. Part 2.
London—Boston: Butterwortst. — 1993. — P. 867—885.
Marsh J. L., Vanider M. W. The "third" dimension in craniofacial surgery // Plast, reconstr.
Surg. - 1983. - Vol. 71, N 6. - P. 759-767.
Marsh /. L., Vanider M. W.y Bresina S. B. et al. Applications of computer grafics in
craniofacial surgery // Clin, plast. Surg. - 1986. - Vol. 13, N 3. - P. 441-448.
Medinaceli L., Seaber A. V. Experimental nerve reconstruction of inital repair//
Microsurgery. - 1989. - Vol. 10, N 1. - P. 56-70.
Miehlke Α., Stennert E., Reinhard С. New Aspects in facial nerve surgery // Clin, plast. Surg. —
1979. -Vol. 6, N 1. - P. 45-50.
Millesi H., Berger A. Furthe experience with interfascicular grafting of the medial, ulnar and
radial nerves // J. Bone Jt Surg. — 1976. — Vol. 58. — P. 209—216.
Millesi H. Facial nerve surgery // Facial nerve surgery / Ed. U. Fich. — Birmingham: Ala,
Aesculapus Publ. - 1977. - P. 209-215.
Millesi H. Nerve suture and grafting to restore the extratemporal facial nerves // Clin, plast.
Surg. - 1979. - Vol. 6, N 3. - P. 333-346.
Nicolai J. P. Irreaversible facial paralisis and ins treatment. — Amsterdam. — 1985. — 279 p.
Podvinek M. Facial Nerve disorders. Anatomic, histological and clinical aspects //Adv. Oto-
Rhino-Laringol. - 1984. -Vol. 32, N 3. - P. 124-129.
Pribaz J. J·, Cheffer С #., Barrall D. T. The extended V—Y-flap // Plast. reconstr. Surg. —
1992. - Vol. 90, N 2. - P. 275-280.
Pribaz «/· J-, Stephens W., Crespo L., Gifford G A new intraoral flap: facial artery
musculomucosal flap // Plast. reconstr. Surg. — 1992. — Vol 90, N 3. — P. 421—429.
PribazJ. J., Morris D. J., Mulliken J. B. Three-dimensional foldes free-flap reconstruction of
complex facial defects using intraoperative modeling // Plast. reconstr. Surg. — 1994. —
Vol. 93, N 2. - P. 285-293.
Sunderland S Nerve and Nerve injuries. — Edinburgh: Churhill-Livinston, 1972. — P. 9—15.
Taylor G. /., Palmer J. H. The vascular territories (angiosomes) of the body: Experimental
study and clinical applications // Brit. J. plast. Surg. — 1987. — Vol. 40, N 2. —
P. 113-114.
Terzis J. K., Fee W. E. Current Issues in nerve repair // Arch. Otolaring. Head Neck Surg. —
1993. - Vol. 119, N 7. - P. 725-731.
The Facial Nerve / Ed. M. May. — New York: Tieme. — Stratlon, 1986.
Tucker H. M. Muscle-nerve blok transplantats // 1-th Facial Nerve Simp. — Pittsburg, 1977. —
P. 60.
Tucker H. M. The management of facial paralysis due to exracranial injuries // Laryngoscope. —
1978. - Vol. 88, N 4. - P. 348-354.
Глава 24
КОСТНАЯ ПЛАСТИКА
НИЖНЕЙ ЧЕЛЮСТИ
Замещение либо восстановление костных структур при различных
патологических процессах — одна из основных проблем современной челюстно-лице-
вой хирургии. Значительное место в восстановительной хирургии занимают
костно-пластические операции при дефектах нижней челюсти, возникающих
как в военное, так и в мирное время. Последствия огнестрельных ранений и
оперативных вмешательств по поводу опухолей, травм, остеомиелитов и др.
вызывают значительные нарушения функций и обезображивание лица.
Именно поэтому, на протяжении последнего столетия поиск новых
эффективных методов хирургического лечения является предметом внимания как
отечественных, так и зарубежных хирургов. Наиболее полно развитие
костной ауто- и аллопластики в историческом аспекте описано Н. А.
Плотниковым A979).
24.1. Историческая справка
Начало костно-пластическим операциям на нижней челюсти было положено
в конце XIX столетия. На первом этапе костные аутотрансплантаты, взятые
из края нижней челюсти или соседних областей, пересаживали в дефект
нижней челюсти на длинных питающих ножках. Последние выкраивали из кожно-
мышечного лоскута, связанного с костным трансплантатом. Впервые такую
операцию осуществил А. Bardenheuer A892). Дефект нижней челюсти,
образовавшийся после резекции по поводу саркомы, он заместил костным
трансплантатом, взятым из лобной области. В это же время A. Wildt A892) произвел
остеопластику нижней челюсти трансплантатами из ключицы на ножке из
мягких тканей; результаты операции неизвестны. А. Wolfler A892) для
замещения дефекта нижней челюсти использовал трансплантат на длинной
ножке, взятый из лопатки. Трансплантат некротизировался и был удален.
Восстановить непрерывность нижней челюсти не удалось. Несколько позднее для
восстановления непрерывности кости при небольших послеоперационных
дефектах нижней челюсти применяли трансплантаты на ножке, взятые из
нижней челюсти [Дьяконов П. И., 1897; Дешин Α. Α., 1897; Bardenheuer, 1896;
Krause, 1904].
В начале XX века аутоостеопластика нижней челюсти получила новое
направление: была доказана возможность замещать дефекты нижней
челюсти по способу свободной пересадки кости. В. М. Зыков в 1900 г. в асепти-
175
ческих условиях устранил дефект подбородочного отдела аутотранспланта-
том длиной 4 см, выпиленным с противоположной стороны нижней челюсти.
Трансплантат успешно прижил, результаты прослежены в течение 11 лет.
Необходимо отметить, что В. М. Зыков произвел "вторичную" остеопластику и
особо подчеркивал важность сохранения асептичности операционного поля
и трансплантата.
Вскоре после этого некоторым хирургам удалось выполнить вторичную
костную аутопластику нижней челюсти свободно пересаженными
трансплантатами из большеберцовой кости и ребра. Однако первичная костная пластика
никому не удавалась из-за нагноения и отторжения. В связи с этим сложилось
мнение, что свободную аутопластику нижней челюсти следует применять
только вторично. При этом большое значение придавали иммобилизации
отломков и целесообразности использования для аутопластики ребра и гребня
подвздошной кости [Петров Н. Н., 1913].
Этот период остеопластики охватывает 25 лет. В основном применяли
два способа костной пластики нижней челюсти аутогенным трансплантатом:
одномоментную свободную пересадку кости и двухэтапную пересадку
биологически подготовленного трансплантата. Значительному успеху в развитии
костной пластики нижней челюсти способствовало предложение С. С. Ти-
герштедта A916) использовать для фиксации отломков назубные
алюминиевые шины, которые в дальнейшем были усовершенствованы [Лимберг Α. Α.,
1923; Ванкевич М. М., 1924; Рауэр А. Э., 1932].
Широкое развитие костная пластика нижней челюсти получила в годы
Великой Отечественной войны и послевоенные годы. Большое внимание
уделялось надежным методам иммобилизации отломков. Появление различных
паяных и штампованных лабораторных шин, съемной верхнечелюстной шины
Ванкевич A945) позволили значительно улучшить результаты операций.
Широкое распространение получили внеротовые аппараты [Рудько В. Ф., 1945;
Penn J., Brown L., 1943], которые в дальнейшем были модифицированы
[Вернадский Ю. И., 1957; Збарж Я. М., 1957; Уваров В. М., 1958]. Кроме того,
были предложены накостные пластины для местной фиксации отломков
[Павлов Б. Л., 1959].
Появление более современных способов фиксации отломков нижней
челюсти позволило упростить костную пластику и за счет обеспечения
неподвижности трансплантата с использованием ранней функциональной
нагрузки улучшить ее результаты. Стало возможным использование
расщепленного ауторебра [Лимберг Α. Α., 1944; Наумов П. В., 1949; Панчоха В. П.,
1959]. Положительные результаты наблюдались более чем в 90 % случаев.
Однако осложнения, связанные со взятием ауторебра (пневмо- и гемоторакс), и
переломы аутотрансплантата в отдаленные сроки заставили изменить тактику.
А. И. Евдокимов A950), Н. М. Михельсон, А. Э. Рауэр, Т. Blocker,
L. Weis A946) для замещения дефектов нижней челюсти использовали
трансплантаты из гребешка подвздошной кости. В дальнейшем свободная ауто-
остеопластика не претерпела значительных изменений и методики в
описании различных авторов отличались лишь изменением размеров и формы
аутотрансплантата. Лишь в последнее время для замещения дефектов нижней
челюсти стали более широко использовать свободные аутотрансплантаты со
свода черепа — расщепленные и полнослойные (рис. 24.1).
Следует отметить, что покровные кости подвержены резорбции в
меньшей степени, чем другие трансплантаты и пересадка их в большем проценте
случаев дает положительный результат.
Анализ основных методов костной аутопластики нижней челюсти
позволил прийти к заключению, что практически всем видам аутотрансплан-
176
Рис. 24.1. Замещение дефекта тела
нижней челюсти послойным аутотрансплан-
татом со свода черепа (схема).
татов, несмотря на их положительные
остеопластические свойства, присущ
ряд недостатков: 1) взятие
трансплантата сопряжено с дополнительной
травмой; 2) не всегда удается
получить трансплантат желаемой формы и
добиться хорошего эстетического
результата.
Вопрос о поиске пластического
материала, с помощью которого
можно было бы легко устранять дефекты,
возник практически одновременно с
разработкой методов аутопластики.
В начале XX века для замещения
дефектов нижней челюсти рядом
авторов были использованы неденатуриро-
ванные и вываренные костные ал-
лотрансплантаты, взятые у здоровых
людей [Петров Н. Н., 1911; Lexer E.,
1908; МсЕѵеп W., 1909]. Однако
практически во всех странах пересадка
костного аутотрансплантата в условиях
первичной или вторичной пластики не
давала положительных результатов вследствие нагноения или отторжения.
Даже несмотря на появление антибиотиков, применение свежих ал-
лотрансплантатов не получило в то время широкого клинического
распространения из-за отсутствия возможности длительного хранения и
надежных средств борьбы с инфекцией [Симельсон Е. Б., 1945; Петров В. И.,
1964; Camera, 1954]. Развитие аллопластики невозможно без заготовки
тканей впрок и без консервации их на длительное время, указывали
авторы.
Начиная с 1951 г. в челюстно-лицевой хирургии стали использовать ал-
лотрансплантаты, консервированные методом лиофилизации [Kreis S. F. et al.,
1951]. Лиофилизированной костной тканью замещали полостные дефекты
после удаления радикулярных кист, ретинированных зубов [Загубелюк Н. К.,
1979]. В таких случаях удобнее применять измельченные трансплантаты, так
как регенерация костной ткани, а следовательно, рассасывание и замещение
трансплантатов новообразованной костью, в основном зависят от скорости
прорастания в них кровеносных сосудов со стороны воспринимающего
костного ложа и окружающих мягких тканей реципиента. Чем больше контактная
поверхность, тем интенсивнее протекает этот процесс. Наиболее
выраженными остеогенетическими свойствами обладают трансплантаты,
измельченные до состояния порошка (костная мука). По данным Н. К. Загубелюк
A979), отрицательные результаты при подобном оперативном вмешательстве
составили около 10 %. Однако костная мука, несмотря на хорошие остеоге-
нетические свойства, может быть использована лишь при заполнении
костных полостей, поскольку такому материалу очень трудно придать
необходимую форму.
Описаны результаты костной пластики лиофилизированными ал-
лотрансплантатами при замещении дефектов нижней челюсти с нарушением
ее непрерывности [Горячева Т. Н., 1972; Пузанов В. И., 1973], для контурной
пластики [Nasteff, 1966]. Названные авторы использовали трансплантаты как
из кортикального слоя, так и из губчатой кости.
12-1263
177
При экспериментальных исследованиях и клинических наблюдениях,
проведенных под руководством Н. А. Плотникова, установлены хорошие
пластические свойства лиофилизированных ортотопических трансплантатов
из нижней челюсти. Они являются незаменимым пластическим материалом,
особенно при замещении обширных дефектов нижней челюсти и артропла-
стике височно-нижнечелюстного сустава. По данным П. В. Наумова A965),
А. А. Колесова и соавт. A972), Н. К. Загубелюк A971), В. И. Пузанова A973),
Mellonigh J. и соавт. A976), более чем в 90 % случаев получены хорошие
функциональные и эстетические результаты.
Группе исследователей во главе с Н. А. Плотниковым присуждена
Государственная премия СССР за разработку методов реконструктивной
хирургии челюсти и височно-нижнечелюстного сустава с целью восстановления
анатомической целости и функции жевательного аппарата. Предложен ряд
методик взятия, стерилизации, лиофилизации, хранения и транспортировки
биопластического материала. Разработаны новые методики первичного и
вторичного восполнения дефектов нижней челюсти различной протяженности и
локализации лиофилизированными аллотрансплантатами. По мнению этих
исследователей, биологическая структура и однотипность ортотопических
трансплантатов создают наилучшие условия для развития регенерата. В то же
время В. И. Говалло A979) считает, что васкуляризация трансплантатов не
зависит от того, пересажена ли кость орто- или гетеротопно.
Кроме того, как отмечают А. А. Колесов и соавт. A980), ортотопические
трансплантаты мало пригодны для замещения дефектов челюстей у детей
младшего возраста, так как моделирование трансплантата приводит к
нарушению механической прочности, что впоследствии ведет к более ранней и
неравномерной его резорбции, в результате чего не происходит полноценного
развития регенерата.
Опыт применения в качестве аллотрансплантатов лиофилизированной
зрелой кости свидетельствует о том, что в послеоперационном периоде, хотя
и у небольшого числа больных, трансплантаты могут подвергаться
отторжению [Паникаровский В. В. и др., 1983]. Вторичная перестройка
трансплантатов из лиофилизированной зрелой кости происходит очень долго (от 6 мес
до 1,5 года). В связи с этим остаются актуальными поиски такого материала,
который бы утилизировался в организме в возможно кратчайшие сроки с
восстановлением первичной для кости органной структуры.
Другим интересным направлением в решении проблемы замещения
дефектов челюстей является пластика брефокостью. Известно, что
эмбриональные ткани обладают высокой стимулирующей способностью процессов
регенерации, у них отсутствуют выраженные антигенные свойства и по времени
перестройки кость не уступает аутотрансплантатам [Констандян Л. И. и др.,
1976; Сысолятин П. Г., 1979; Рузин Г. П., Захаров Ю. 3., 1975; Рузин Г. П.,
1979; Мамедов Г. Г., 1978; Crouse Α., 1959].
В стоматологии кость плода с успехом применяется для заполнения
костных полостей после удаления кист, пластики небольших дефектов
альвеолярного отростка и тела челюсти, стимуляции остеогенеза при переломах
челюстей и ложных суставах. Однако из-за малых размеров трубчатых костей
плода, обычно применяемых для трансплантации, их трудно использовать для
замещения значительных по объему дефектов челюстей. Антигенные свойства
трансплантатов из брефокости зависят от возраста плода, так как у эмбриона
в кости больше водорастворимых белков-антигенов, чем в кости взрослых лиц,
поэтому ткани, взятые в ранний эмбриональный период, очень быстро
рассасываются [Окулова А. Н., 1961]. Последнее в известной степени ограничивает
возможность использования такого трансплантационного материала.
178
В практике хирургической стоматологии широко используются форма-
линизированные трансплантаты. Н. Н. Бажанов и Г. П. Тер-Асатуров A979),
П. Г. Сысолятин A979) считают, что применение подобных трансплантатов
особенно оправдано при замещении дефектов, возникших в результате
остеомиелита и в других случаях инфицирования воспринимающего ложа. По
их мнению, в таких случаях важную роль играет антимикробное действие
формалина.
Другие авторы [Паникаровский В. В. и др., 1983] считают, что в настоящее
время применение формалинизированных трансплантатов имеет лишь
исторический интерес и подобные трансплантаты способны вызвать негативные
иммунные реакции организма реципиента. По данным Н. А. Плотникова
A979), в ранние сроки после операции формалинизированные трансплантаты
вызывают более сильный отек мягких тканей, чем лиофилизированные.
Трансплантаты, заготовленные перечисленными выше методами, могут быть
успешно использованы для замещения тотальных дефектов в виде стружек
для пломбирования полостей. Применение их для контурной пластики или
пластики альвеолярного отростка ограничено, так как им трудно придать
необходимую форму.
Возможность применения декальцинированного костного матрикса в
стоматологии доказана Н. И. Винниковой и соавт. A981), которые получили
хороший остеогенетический эффект при пломбировании им костных
полостей. Непосредственно для пластики альвеолярного отростка декальциниро-
ванный матрикс с успехом использовали Milier и Emmings A979).
Ксенотрансплантация — пересадка тканей от животного человеку, от
собаки — кролику. Данный метод устранения костного дефекта избавляет
больного от дополнительной операции, т. е. заимствования у него какого-либо
костного фрагмента. Однако от широкого применения ксенотрансплантации
пришлось отказаться из-за биологической несовместимости материала.
Многие виды консервации кости неспособны придать трансплантату
свойства, исключающие его конфликт с организмом реципиента.
Аллотрансплантация — пересадка тканей от одной особи другим
генетически различным организмам того же вида (от человека человеку).
В настоящее время используются различные способы консервации
костной ткани: замораживание при различных температурных режимах, лиофили-
зация, обработка химическими агентами, хранение в парафине, полиэфирных
смолах и др. Каждый из перечисленных способов имеет преимущества и
недостатки.
Как показали результаты экспериментальных исследований и
клинических наблюдений, для вторичной костной пластики аллотрансплантаты,
консервированные холодом, нельзя применять при замещении дефектов нижней
челюсти протяженностью более 2 см. Использование лиофилизированных
трансплантатов без сочетания с аутокостью при дефектах длиной более 4 см
не всегда приводит к образованию полноценного регенерата; иногда
наблюдается полная резорбция пересаженной кости.
Костные трансплантаты, консервированные в 0,5 % растворе формалина,
нередко вызывают осложнения в виде значительного отека, а в ряде случаев
остаются в организме как инородное тело либо через некоторое время
рассасываются без образования заместительного регенерата.
Вместе с тем ряд авторов считают целесообразным использовать для
восстановительных и реконструктивных операций на лице костную ткань,
консервированную различными способами. При этом отмечается хороший
клинический и косметический результат.
179
12*
24.2. Костная пластика аутотрансплантатом
Методы аутоостеопластики нижней челюсти детально разработаны и часто
применяются, так как не требуют специальных установок и средств для
консервации и в большом проценте случаев дают положительные результаты.
В отличие от 20—50-х годов в настоящее время обязательным условием
аутопластики нижней челюсти считается прочность фиксации отломков по
отношению к трансплантату.
Существующие способы фиксации отломков челюсти можно
разделить на две группы: внутриротовые (назубные, назубно-десневые,
накостные) и внеротовые (накостные с наружными приспособлениями для
фиксации, накостные без выступающих наружу приспособлений, внутри-
костные).
В последнее время шины Ванкевич, Ядровой, Бетельмана, Порта, а
также модификации этих аппаратов используют редко. С целью удержания
отломков нижней челюсти в основном применяют назубные шины Тигерштедта.
Для накостной фиксации в настоящее время широко используют
мини-пластины из титана, которые за рубежом были разработаны около 20 лет назад.
Благодаря наличию в арсенале хирургов титановых мини-пластин стало
возможным реже пользоваться проволочными швами для фиксации костных
отломков. При этом процент случаев успешной костной пластики значительно
повысился.
Выполнять операцию целесообразно двумя бригадами хирургов: одна
готовит воспринимающее ложе в области дефекта нижней челюсти, другая —
берет трансплантат из ребра, гребня подвздошной кости или другого участка,
после чего ушивает рану в этой области.
Правильное формирование воспринимающего ложа во многом
предопределяет успех оперативного вмешательства. Необходимо максимально
очистить рану от омертвевших и рубцовых тканей, инородных тел, склеро-
зированной костной ткани на концах отломков. При этом следует
сохранить достаточное количество хорошо кровоснабжаемых тканей как для
покрытия костного трансплантата, так и для того, чтобы изолировать ложе от
полости рта, если резекцию челюсти и остеопластику производят
одномоментно. Для отграничения от полости рта накладывают один ряд швов на
слизистую оболочку и как минимум один—два ряда на подслизистые мягкие
ткани.
После резекции фрагмента нижней челюсти на концах отломков
формируют воспринимающие площадки и отломки фиксируют в правильном
положении (по зубной дуге верхней челюсти). Размер трансплантата
определяют с помощью линейки.
Костный аутопластический материал выбирают, исходя из размеров и
формы дефекта. Для пластики подбородочной области целесообразнее
использовать гребень подвздошной кости, для тела нижней челюсти — прямой
участок гребня подвздошной кости, расщепленное ребро или трансплантат
со свода черепа, для угла и ветви нижней челюсти — гребень и крыло
подвздошной кости или кости свода черепа.
Взятие трансплантата из целого ребра. Операцию выполняют под
общей анестезией. После обработки операционного поля проводят
дугообразный разрез кожи и подкожной жировой клетчатки по ходу
соответствующего ребра (VII—IX). Кожный разрез делают на несколько сантиметров
длиннее, чем костный трансплантат. Широкий доступ значительно облегчает
и ускоряет операцию. По наружной поверхности ребра рассекают скальпелем
180
Рис. 24.2. Взятие расщепленного ребра
(схема).
мышцы и надкостницу на всем
протяжении раны. Надкостницу вместе с
мышцами распатором сдвигают с ребра
в межреберные промежутки так, чтобы
края ребра были освобождены от
мягких тканей.
Если трансплантат будет взят с
частью хряща, то в следующий момент
освобождают от мышц и надхрящницы
переднюю поверхность реберного хряща
на протяжении 2—3 см и осторожно,
чтобы не поранить внутренний листок
надхрящницы и париетальную плевру,
распатором выделяют хрящ
соответствующей величины. Если взято целое
ребро, то на протяжении 1—2 мм
надкостницу отделяют от внутренней
поверхности ребра и в это место вводят
реберный распатор для того, чтобы отделить надкостницу полностью. После
этого реберными кусачками или с помощью бормашины рассекают ребро в
заднем отделе и, поднимая отсеченную часть скальпелем, окончательно
отсекают мягкие ткани от хряща и отрезают соответствующую часть хряща.
Затем фрезой или кусачками скусывают острые края на оставшейся части ребра,
чтобы последние не поранили тонкую париетальную плевру.
После извлечения костного трансплантата из раны, следует
осуществить межреберную блокаду анестетиком для снятия болевого синдрома
после операции. В передний и задний отдел раны вводят резиновый выпускник
на 24—48 ч, накладывают швы на мышцы, подкожную жировую клетчатку
и кожу.
Если необходимо взять только наружную пластину ребра, то после
обнажения его передней поверхности с помощью дисковой пилы
проводятся распилы наружной пластины до губчатого вещества по верхнему и
нижнему краям ребра. Затем в переднем углу раны остеотомом,
поставленным на ребро под углом 45°, делают расщеп в ребре, проникая долотом в
губчатый слой. После этого желобоватым долотом с тонкими стенками
отделяют наружную кортикальную пластину необходимой длины (рис. 24.2).
Сглаживают острые костные края, осуществляют гемостаз. Послойно
ушивают рану.
Взятие трансплантата из гребня подвздошной кости. Операцию
выполняют под общей анестезией. После обработки операционного поля
проводят разрез кожи и подкожной жировой клетчатки над гребнем подвздошной
кости. Длина разреза зависит от размера трансплантата, который
необходимо взять. По верхнему краю гребня рассекают надкостницу и распатором
сдвигают ее на внутреннюю и наружную поверхность в глубину раны на
2,5—3 см. Если необходимо взять трансплантат для тела нижней челюсти,
то выбирают наиболее прямой участок кости и с помощью дисковой пилы
и фрез выпиливают необходимого размера костный фрагмент (рис. 24.3).
Затем, с помощью прямого тонкого долота рассекают нераспиленные
участки кости. Фрезой сглаживают острые костные края, осуществляют
гемостаз (иногда с помощью воска) и послойно ушивают рану, оставляя на 24—
48 ч резиновый выпускник.
Если для устранения дефектов нижней челюсти в области угла и ветви
необходимо взять трансплантат из гребня подвздошной кости с переходом на
181
Рис. 24.3. Замещение дефекта тела нижней челюсти аутотрансплантатом из гребня
подвздошной кости (схема).
крыльную часть, то обычно это делают при помощи шаблона, вырезанного
по размерам дефекта с запасом 1 — 1,5 см для площадок в местах закрепления
последнего с торцами отломков.
24.3. Костная пластика аллотрансплантатом
В последние годы значительное место среди методов аллопластики нижней
челюсти занимает применение лиофилизированных аллотрансплантатов,
особенно взятых из нижней челюсти трупа. Лиофилизированный
пластический материал можно длительное время хранить при комнатной температуре,
транспортировать и т. д.
Сущность метода лиофилизации заключается в сублимации воды из
предварительно замороженной ткани в условиях вакуума. Обезвоживание
ткани осуществляется за счет поддержания равновесия концентрации
водяных паров в тканях и окружающем пространстве. При таком высушивании
ткани в ней не происходит денатурации белков. Остаточная влажность
высушиваемого материала во многом зависит от способа лиофильной сушки и
аппаратуры и весьма существенно влияет на качество трансплантата, а
следовательно, и на исход пересадки.
Разносторонние клинико-экспериментальные исследования по
применению лиофилизированной кости для замещения костных дефектов нижней
челюсти провели Н. А. Плотников и сотр., обобщившие опыт 749 остеопла-
стических операций на нижней челюсти с применением лиофилизированных
аллотрансплантатов.
Пластика нижней челюсти лиофилизированной аллокостью.
Представляет собой одномоментную резекцию и остеопластику нижней челюсти лио-
филизированным аллотрансплантатом. Если резекцию или экзартикуляцию
челюсти производят по поводу доброкачественной опухоли, то следует
сохранить не измененную опухолевым процессом надкостницу и мениск ви-
сочно-нижнечелюстного сустава. При злокачественной опухоли удаляют не
только надкостницу, но и соседние с ней мягкие ткани и регионарные
лимфатические узлы. Образовавшееся сообщение раны с полостью рта
тщательно ушивают минимум двумя рядами кетгутовых швов. При помощи
циркулярной пилы, фрезы и долота на оставшемся фрагменте нижней челюсти с
наружной стороны (на расстоянии 1,5—2 см от свободного конца) снимают
костную пластинку вплоть до появления кровоточащих точек (это необходи-
182
мо для последующей васкуляризации трансплантата). На месте созданной
раневой площадки трепаном просверливают два отверстия для проволочного
шва. Затем в подготовленное ложе укладывают трансплантат, плотно
подгоняя его к концу фрагмента челюсти реципиента по типу русского замка
(трансплантат должен быть на 1,5—2 см длиннее удаляемого участка кости).
Для этого на конце трансплантата с внутренней стороны также создают
раневую поверхность и делают два отверстия. Трансплантат фиксируют к
фрагменту челюсти при помощи проволоки из нержавеющей стали, продетой в
перфорационные отверстия. Если резекция челюсти сопровождалась
отслойкой жевательных мышц, то под углом трансплантата соединяют швами
нижние концы отсепарованных жевательной и медиальной крыловидной мышц.
Окружающие мягкие ткани плотно ушивают, чтобы предупредить
образование в них полостей и гематомы. На кожу накладывают швы конским волосом
или синтетической нитью. Рану закрывают асептической повязкой. В угол
раны вводят узкий резиновый выпускник.
Если остеопластику производят после экзартикуляции половины челюсти,
то второй конец (головка нижней челюсти) аллотрансплантата помещают в
нижнечелюстную ямку.
Вторичная костная пластика нижней челюсти лиофилизированным ал-
лотрансплантатом. При частичных дефектах нижней челюсти костную
пластику производят после экономной резекции склерозированных концов кости.
С наружной стороны на концах обоих фрагментов создают раневые
площадки протяженностью 1,5—2 см. После появления кровоточащих точек костные
трансплантаты моделируют в виде буквы Т, вводят в качестве распорки
между костными фрагментами и одновременно накладывают на созданные
раневые площадки. Этим достигается контакт между трансплантатом и костью
реципиента, благодаря чему он быстрее приживляется.
При дефекте, возникшем вследствие остеомиелита, наблюдается рубцо-
вое изменение мягких тканей. В этих случаях при подготовке площадки для
височно-нижнечелюстного сустава удаляют дегенеративно перерожденный
суставной диск, а для проведения (укладки) ветви нижней челюсти (вместе
с головкой) формируют туннель в рубцово-измененных мягких тканях.
Наличие рубцово-измененных тканей, окружающих трансплантат и область
нижнечелюстной ямки, усложняет технику операции и отражается на
послеоперационной функции сустава. Для восполнения дефекта ветви и мыщел-
кового отростка автор рекомендует применять аллотрансплантат,
заготовленный из нижней челюсти вместе с головкой. Головку нижней челюсти вводят
во вновь образованную суставную полость, а другой конец трансплантата
соединяют с концом фрагмента челюсти реципиента по типу русского замка и
укрепляют швом. Необходимо избегать образования сообщения раны с
полостью рта. В ране на 24 ч оставляют выпускник.
Послеоперационный уход после обоих вариантов аллоостеопластики по
Плотникову предусматривает ежедневный туалет полости рта слабым
раствором антисептиков (ирригация, протирание), полноценное питание,
изоляцию наружной линии швов от загрязнения, контроль за состоянием
ортопедического фиксирующего приспособления и др. Первую перевязку делают на
следующий день после операции. Извлекают выпускник, а линию швов и
окружающую кожу обрабатывают этиловым спиртом. При возникновении
гематомы распускают 1—2 шва, удаляют скопившуюся кровь, в рану вводят
антибиотики и дренируют ее еще 2—3 дня. После этого дренаж извлекают.
Швы снимают на 7—8-й день. В течение 7—10 дней после операции с целью
профилактики проводят антибиотикотерапию, назначают поливитамины.
Пища для таких больных должна быть протертой или молотой, энергети-
183
чески ценной, витаминизированной. Кормить больных следует с помощью
поильника.
В случае наложения проволочных назубных шин нужно следить за их
фиксацией (подкручивать лигатуры, менять резиновые кольца). Через 1 — 1,5 мес
после операции межчелюстное крепление снимают, постепенно усиливают
нагрузку на нижнюю челюсть при механотерапии и назначают все более
жесткую пищу.
После костной пластики лиофилизированными аллотрансплантатами
возможны следующие осложнения: 1) рассасывание трансплантата без
последующего замещения новой костью; 2) нагноение с удалением
трансплантата; 3) образование ложного сустава; 4) поверхностное нагноение раны с
наружной стороны в области швов.
Самыми важными условиями, предупреждающими возникновение
осложнений при костно-пластических операциях, не обусловленных тканевой
несовместимостью, являются строго дифференцированный подбор
трансплантата по форме, качеству, способу консервации, максимальное
соблюдение асептики при оперативном вмешательстве, бережное обращение с
окружающими тканями, тщательное сопоставление концов трансплантата с
тканями реципиента, надежная фиксация и создание абсолютного покоя до
наступления консолидации.
Морфологические изменения в лиофилизированных алло- и аутотранс-
плантатах аналогичны. Разница заключается в скорости и полноценности
замещения трансплантата вновь образованной костью. Значительно быстрее и
полноценнее перестройка происходит в аутогенной костной ткани, где уже
на 16-й неделе после трансплантации процесс замещения в основном
завершается. В лиофилизированной кости ассимиляция протекает медленнее: на
24-й неделе в ней происходят такие же процессы, какие наблюдаются в ау-
токости на 16-й неделе.
При замещении дефекта ортотопическим лиофилизированным ал-
лотрансплантатом установлено, что к 12-й неделе трансплантат частично
замещается новообразованной пластинчатой костью, появляющейся по ходу
расширенных сосудистых каналов и на старых безостеоцитных костных
перекладинах. Через 26—35 нед после операции трансплантат почти полностью
замещается регенератором, а спустя 44—52 нед структура последнего
аналогична структуре челюсти реципиента [Никитин Α. Α., Золотарева Ю. Б.,
1979]. В лиофилизированном трансплантате антигенная активность костного
мозга, денатурирующегося во время лиофилизации, сравнительно низкая
[Плотников Η. Α., Троянский И. В., 1979], в то время как неконсервирован-
ные и консервированные при температуре —25°С аллотрансплантаты
проявляют активную антигенную способность, а потому подвергаются
интенсивной остеопластической резорбции, которая может опережать процесс репарации
ІОкунева Л. Μ., 1972]. Наряду с этим установлено, что сроки хранения лио-
филизированного аллотрансплантата не оказывают влияния на процессы
перестройки.
Широко используют также стерилизацию и консервирование аллокости
в слабом @,25 %) растворе формалина, в котором заготовленные в
нестерильных условиях костные аллотрансплантаты становятся стерильными
через 20 сут, а в 0,5 % растворе — через 10 сут [Бажанов Η. Η. и др., 1975].
После пересадки формализированной кости отмечается более значительный
отек мягких тканей, чем после пересадки лиофилизированной, но это не
должно служить препятствием к применению столь простого и широко
доступного метода консервирования аллокости.
184
24.4. Комбинированная костная пластика ауто-
и аллотрансплантатами
Результаты костнопластических операций при замещении дефектов нижней
челюсти в основном зависят от состояния воспринимающего ложа,
протяженности дефекта и вида трансплантата. При вторичной костной пластике
дефектов нижней челюсти большой протяженности практически всегда создаются
неблагоприятные условия для операции, особенно если ей предшествовала
лучевая терапия или воспринимающее ложе сформировано из тканей фила-
товского стебля. В этих случаях в области дефекта преобладает
неполноценная, бедная сосудами рубцовая ткань и заместительные процессы в ал-
лотрансплантате протекают медленно или отсутствуют. Ткань трансплантата
рассасывается быстрее, чем происходит его замещение новообразованной
костью. При больших дефектах нижней челюсти целесообразнее использовать
аутокость. Однако не всегда удается придать трансплантату необходимую
форму, сохранив достаточную прочность.
Ряд авторов для решения этой проблемы используют аллоаутопласти-
ку — комбинированную костную пластику ортотопическим аллотранс-
плантатом нижней челюсти в сочетании с губчатым аутогенным
трансплантатом. Аллокость выполняет роль каркаса и включается в процессы
регенерации позже аутотрансплантата. Однако такое сочетание позволяет
не только ауто-, но и аллотрансплантату перестроиться в полноценный
регенерат.
Н. А. Плотников, А. А. Никитин и П. Г. Сысолятин предложили
следующую методику операции. Комбинированную остеопластику нижней
челюсти аллотрансплантатом в сочетании с аутогенным трансплантатом лучше
производить под эндотрахеальным наркозом. Больной находится в
положении на спине с откинутой назад головой. После обработки кожи и полости
рта проводят разрез кожи в области дефекта по имеющемуся
послеоперационному рубцу или нижнему краю филатовского стебля с иссечением рубца.
Ткани рассекают послойно. При наличии оставшихся фрагментов челюсти
находят их свободные концы. Осторожно, чтобы не перфорировать
слизистую оболочку полости рта, выделяют их из рубцовой ткани, устанавливают
в правильном анатомическом соотношении и фиксируют с помощью внеро-
тового накостного аппарата. Накостные клеммы накладывают, отступя не
менее 2,5—3 см от свободного конца фрагментов с таким расчетом, чтобы
после снятия склерозированной костной ткани оставалась воспринимающая
площадка для трансплантата не менее 1,5—2 см.
Формирование ложа из мягких тканей осуществляют под контролем
введенных в полость рта пальцев. Нужно следить за тем, чтобы не
перфорировать слизистую оболочку полости рта. Не рекомендуется оставлять толстый
слой жировой клетчатки, поскольку при этом создаются неблагоприятные
условия для протезирования. В случае повреждения слизистой оболочки
полости рта ее необходимо изолировать от операционной раны двухрядными
кетгутовыми швами. При формировании воспринимающего ложа следует по
возможности удалить все рубцы из мягких тканей и провести тщательный
гемостаз. Мелкие кровеносные сосуды лучше коагулировать, более крупные —
изолированно без захвата мягких тканей перевязать тонким кетгутом. На
концах костных фрагментов нижней челюсти циркулярной пилой удаляют
склерозированную ткань до неизмененной кости. С наружной и
внутренней поверхностей снимают кортикальный слой кости длиной 1,5—2 см с
каждой культи до появления кровоточащих точек. В тех случаях, когда
сохранен только один фрагмент челюсти, в том числе и ее суставной конец, ложе
185
для трансплантата при подходе к
суставной площадке формируют тупым
путем. Создают туннель с учетом
расположения околоушной железы и
лицевого нерва.
Величину трансплантата
определяют в соответствии с размерами
дефекта после установления фрагментов
челюсти в правильном анатомическом
соотношении и удаления с их
концевых отделов участков склерозирован-
ной кости. Обычно берут трансплантат
на 3—4 см больше костного дефекта с
Рис. 24.4. Замещение дефекта тела ниж- таким расчетом, чтобы концы транс-
ней челюсти комбинированным ауто- (/) плантата соединялись с концами фраг-
и аллотрансплантатом B) (схема). ментов челюсти внакладку. В качестве
пластического материала в этих случаях
используют аллотрансплантат из лио-
филизированной нижней челюсти в сочетании с расщепленным аутотранс-
плантатом из ребра или гребня подвздошной кости. Для их соединения с
внутренней поверхности аллотрансплантата снимают кортикальный и
губчатый слои на всем протяжении, не доходя до нижнего края 0,5—0,6 мм. На
место удаленной части аллотрансплантата помещают расщепленный костный
аутотрансплантат в виде сплошной пластинки или нескольких отдельных
фрагментов с таким расчетом, чтобы они плотно соединялись не только
раневыми поверхностями, но и по нижнему краю, где аутокость входит в
желобок аллотрансплантата. Длина алло- и аутотрансплантатов должна быть
одинаковой, поскольку они соединяются с концами фрагментов челюсти.
Плотно соединенные трансплантаты фиксируют зажимами, делают в них ряд
сквозных отверстий, через которые соединяют их между собой П-образны-
ми швами из полиамидной нити. Алло- и аутотрансплантаты помещают в
сформированное ложе, где соединяют с фрагментами челюсти таким
образом, чтобы концы фрагментов челюсти с концами алло- и ауто кости можно
было фиксировать проволочными швами или титановыми мини-пластинами.
В тех случаях, когда для замещения дефекта суставного конца
аллотрансплантат взят из нижней челюсти с суставной головкой, в шейке суставного
отростка и в головке, не повреждая хрящевого покрытия, делают ряд
сквозных отверстий, которые заполняют аутогенным костным мозгом, взятым из
той же аутогенной кости (рис. 24.4). Для профилактики осложнений в рану
вводят антибиотики. Мягкие ткани послойно ушивают погружными кетгу-
товыми швами с таким расчетом, чтобы они плотно окутывали трансплантат
со всех сторон. В ране оставляют на 1—2 сут резиновый выпускник, на кожу
накладывают швы тонкой полиамидной нитью.
СПИСОК ЛИТЕРАТУРЫ
Бажанов И. #., Тер-Асатуров Г. П. Применение формализованных гомокостей при
костной пластике дефектов нижней челюсти; Метод, рекомендации. — М.,
1975.
Вернадский Ю. И. Аппарат для внеротового эластического вытяжения отломков в
нижней челюсти и последующей фиксации их // Стоматология. — 1957. — № 2 —
С. 40-41.
186
Вернадский Ю. И. Травматология и восстановительная хирургия челюстно-лицевой
области. — Киев: Вища школа, 1985.
Говалло В. И. Трансплантация тканей в клинике. — М.: Медицина, 1979.
Горячева Т. П. Применение лиофилизированного гомотрансплантата при первичной
костной пластике нижней челюсти в условиях предоперационной лучевой
терапии // Трансплантация органов и тканей. — Рига, 1972. — С. 379—380.
Дешин А. А. Костнопластическая операция по способу П. И. Дьяконова при
частичной резекции нижней челюсти и к вопросу о костной пластике вообще //
Хирургия. - 1897. - Т. 1. — С. 492-510.
Евдокимов А. И. Костная пластика нижней челюсти // Стоматология. — 1946. — № 3. —
С. 23-27.
Загубелюк Н. К. Отдаленные результаты остеопластики послеоперационных полостей
челюсти // Труды МОНИКИ им. М. Ф. Владимирского. — Т. 24. — М., 1979. —
С. 50-53.
Збарж Я. М.у Кабаков Б. Д. Некоторые вопросы современного лечения челюстно-ли-
цевых раненых // Воен.-мед. журн. — 1957. — № 7. — С. 13—18.
Кабаков Б. Д. Костная пластика нижней челюсти. — Л.: Медгиз, 1963.
Колесов Α. Α., Дьякова С. В.} Ерадзе Е. П. Использование консервированной гомоко-
сти при восстановительных операциях на нижней челюсти у детей //
Стоматология. - 1972. - № 4. - С. 49-52.
Къяндский А. А. Костная пластика нижней челюсти // Руководство по хирургической
стоматологии. — М.: Медицина, 1972. — С. 278—292.
Лаврищева Г. И., Оноприенко Г. А. Морфологические и клинические аспекты репа-
ративной регенерации опорных органов и тканей. — М.: Медицина, 1996. —
С. 207.
Лимберг А. А. Новый способ пластического удлинения горизонтальной ветви нижней
челюсти при односторонней микрогении и асимметрии лица //
Стоматологический сборник. — Л., 1927. — С. 142—158.
Наумов П. В. Замещение огнестрельных изъянов нижней челюсти свободной
пересадкой кости из наружной половины ребра: Автореф. дис. ... д-ра мед. наук. —
Л., 1950.
Никитин А. А. Аллопластика височно-нижнечелюстного сустава: Дис. ... д-ра мед.
наук. — М., 1987.
Павлов Б. Л. Накостный остеосинтез при переломах нижней челюсти //
Стоматология. - 1959. - № 4. - С. 29-32.
Паникаровский В. В., Григорян А. С, Борисов Г. П. Новые пути разработки алло- и ксе-
ногенных трансплантационных материалов для костной пластики челюстей //
Стоматология. — 1983. — № 2. — С. 4—10.
Панчоха В. П. Лечение переломов нижней челюсти с помощью внеротового аппарата
конструкции автора // Тр. Украинского ин-та стоматологии. — Т.9. — Одесса,
1959. - С. 227-234.
Плотников Н. А. Костная пластика нижней челюсти. - М.: Медицина, 1979.
Рауэр А. Э. Переломы челюстей и повреждения мягких тканей лица. — М.: Медгиз, 1932.
Рузин Г. П. и др. Костная брефопластика как метод стимуляции репаративного остеоге-
неза челюстей // Тр. МОНИКИ им. М. Ф. Владимирского. — Т. 24. — М., 1979. —
С. 53-56.
Семкин В. Α., Шамсудинов А. X. Одномоментное устранение фрагментарных дефектов
нижней челюсти при удалении нагноившихся доброкачественных образований //
Стоматология. Специальный выпуск. — 1996. — С. 76.
Симельсон Е. Б. К гомопластическому замещению дефектов нижней челюсти после
огнестрельных ранений // Сборник науч. трудов Ленинградского окружного
военного госпиталя. — 1945. — С. 109—111.
Сысолятин /7. Г. Применение эмбриональных костных гомотрансплантатов в
восстановительной хирургии челюстно-лицевой области: Дис. ... канд. мед. наук. —
Новосибирск, 1971.
Уваров В. М. Модифицированная модель шины для внеротовой фиксации отломков
нижней челюсти // Травматология и восстановительная хирургия
челюстно-лицевой области. — Л., Медгиз, 1959. — С. 339—341.
187
Шамсудинов Л. X. Сравнительная биохимическая и морфологическая оценка свойств
деминерализированного в различных растворах костного матрикса и его
применение для костной пластики: Дис. ... канд. мед. наук. — М., 1984.
Bardenheuer А. Unterkieferresektion und Oberkieferresektion //Arch. klin. Chir. — 1892. —
Bd44. - S. 604-611.
Blocker Т., Weiss L. Use of gancellous bone in the repair of defects about the jaws // Ann.
Surg. - 1946. - Vol. 123, N 4. - P. 622-639.
Kreis F., Hiat J., Tsotumer Т. The preservation and clinical use of freerendried bone // Bone
Jt Surg. - 1951. - Vol. 33. - P. 863-872.
Mellonigh J. et al. Clinical evaluation of freesedied bone allografts in periodontal osseous
defects //J. Periodont. - 1976. - Vol. 47. - P. 125-131.
Penn J.y Brown L. A new conception in extraoral splintage. — Johannesburg: Brenthursth
Paper, 1943. -Vol. 2. - P. 3-18.
Wildt A. Über partielle Unterkieferresektion mit Bildung einer naturlichen Prothese durch
Knochentransplantation // Zbl. Chir. - 1896. - Bd 50. - S. 1177-1182.
Wolfler A. Zur Kasuistik der medianen Gesichtsspalte // Zbl. Chir. — 1892. — Bd 10, N 21. —
S. 461-462.
Глава 25
АЛЛОПЛАСТИКА
ВИСОЧНО-НИЖНЕЧЕЛЮСТНОГО
СУСТАВА
25.1. Историческая справка
Хирургия височно-нижнечелюстного сустава (ВНЧС) — это один из
сложнейших разделов восстановительной челюстно-лицевой хирургии. Она
прошла длительный эволюционный путь от простого рассечения ветви нижней
челюсти на различных уровнях с целью создания примитивного "ложного
сустава" и обеспечения минимальной жевательной функции до сложных
реконструктивных операций с применением костных и хрящевых ауто- и ал-
лотрансплантатов, ортотопических костных аллотрансплантатов и
пересадкой искусственных полных ВНЧС — эндопротезов.
Весь арсенал хирургических методик направлен на обеспечение
нормальной физиологической функции ВНЧС, устранение нередко
сопутствующих недоразвития и деформации нижней челюсти. Сложность этой задачи
заключается в многообразии патологии ВНЧС, а также зависимости ее от
анатомо-структурных особенностей, физиологии и биомеханики височно-
нижнечелюстного сустава.
Начальным этапом в разработке методов восстановительной
костнопластической хирургии височно-нижнечелюстного сустава (ВНЧС) явилась
остеотомия с использованием аутотрансплантатов костей стопы [Bardenheimer G.,
1909; Klapp R. et al., 1927; Stuteville O., Lanfrauchi R., 1955; Stuteville O., 1957;
Brombergy G., Waiden R., 1963; Digmann O., Grabb W., 1964].
Однако, несмотря на положительные результаты этих операций, ауто-
трансплантаты из метатарзальных костей стопы имели ограниченное
применение из-за недостаточности их длины при замещении дефектов ветви и мы-
щелкового отростка нижней челюсти. Кроме того, использование в виде
аутотрансплантатов плюсневых костей значительно ослабляло стопу и
влияло на устойчивость при ходьбе.
Известно, что взятие аутотрансплантата всегда сопряжено с
дополнительной операционной травмой для больного, удлинением времени
операции и увеличением срока пребывания больного в стационаре. Это
обусловило необходимость поиска новых материалов и разработки новых методов
реконструктивной и восстановительной хирургии ВНЧС.
В начале 50-х годов появились сообщения о применении для
восстановления мыщелкового отростка нижней челюсти имплантатов. Применялись
материалы, не вызывающие реакции биологических тканей — виталлиум,
нержавеющая сталь, хромокобальтовые сплавы и др. [Freeman В., 1958; Byans L·,
189
ByaesC, 1948; Genest Α., 1956; Smith Α., Robinson Μ., 1956; Dewey Α., MookeT.,
1962; Habn G., Corgill D., 1969].
Наряду с металлическими протезами-имплантатами с учетом их
недостатков, применяли пластмассовые протезы, как более легкие и эластичные
[Михельсон Н. М., 1956; Вернадский Ю. И., Крумина О. Я., 1962; Неаіу Μ.
et al., 1954; Nasteff D., 1962].
Однако в дальнейшем названные авторы отметили развитие воспалений
пересаженного имплантата, образование свищей, отторжение. Причиной
таких исходов считали воздействие на ткани остаточного мономера метакри-
ловой кислоты, так называемый "акрилоз".
Для изготовления имплантатов с целью замещения дефектов суставного
конца нижней челюсти использовали и другие полимерные соединения,
такие, как тефлон — один из наиболее химически инертных материалов.
Недостатком имплантатов из тефлона является то, что костная ткань не врастает
в отверстия на тефлоновом протезе, поэтому область контакта с костным
ложем реципиента остается подвижной.
М. В. Мухин A955) отмечал, что аллопластические и металлические
вкладыши не могут обеспечить сращение с костными отломками и часто
вызывают осложнения в виде пролежней и свищей, вследствие чего их
приходится удалять. В связи с этим многие отечественные и зарубежные хирурги
наилучшим материалом для замещения дефектов мыщелкового отростка
нижней челюсти считают аутотрансплантаты.
Ряд хирургов при замещении различных дефектов ветви и мыщелкового
отростка нижней челюсти применяли метод Н. Gillies A917), предложившего
для образования мыщелкового отростка, ветви, а также части тела нижней
челюсти использовать реберный аутотрансплантат из VIII или IX ребра в месте
перехода его в хрящевую часть [Франкенберг Б. Е., 1936; Лимберг Α. Α., 1938;
Рауер А. Э., Михельсон Н. М., 1954; Львов П. П., 1950; Byaers L., 1948; Castro R.
et al., 1950; Brown G., Fryer Μ., 1953; Hinds Ε., Plasant G., 1955, и др.].
В последние два десятилетия для замещения дефектов ветви и
мыщелкового отростка нижней челюсти, а также при хирургическом лечении анкилоза
височно-нижнечелюстного сустава и микрогении стали широко использовать
костные аллотрансплантаты [Петерсон Б. Е., 1960; Мелехов В. Г., 1965; Иоан-
нидис Г. П., 1974].
Значительное развитие аллопластика ВНЧС получила в связи с
предложением Н. А. Плотникова A967) использовать для этих целей лиофилизиро-
ванный ортотопический аллотрансплантат из ветви нижней челюсти с мы-
щелковым отростком и нижнечелюстной головкой. Преимущество этого
костно-пластического материала перед другими видами аллотрансплантатов в
реконструктивной и восстановительной хирургии ВНЧС заключалось в
полной идентичности его по структуре, анатомической форме и функции
замещаемому или восстанавливаемому органу, а также в возможности точного
подбора и соответствия сочленяющихся поверхностей ВНЧС, что
значительно улучшило функциональные результаты хирургического лечения.
Использование ортотопических лиофилизированных аллотрансплантатов
из нижнечелюстной кости дало возможность разработать и внедрить в
клиническую практику новую методику хирургического лечения анкилозов ВНЧС
[Плотников Η. Α., Ткаченко А. М., 1967; Плотников Η. Α., Никитин Α. Α.,
1981; Никитин Α. Α., 1987], позволяющую создавать височно-нижнечелюст-
ной сустав по структуре и функции, приближающийся к нормальному
суставному сочленению. В связи с этим значительно сократилось количество
рецидивов заболевания, улучшились функциональные и косметические результаты
лечения.
190
Ортотопическая аллотрансплантация костной ткани открыла новые
перспективы в реконструктивной и восстановительной хирургии
височно-нижнечелюстного сустава в условиях первичной и отсроченной костной пластики
при различных патологических процессах, дефектах и деформациях нижней
челюсти и височно-нижнечелюстного сустава. Однако у специалистов,
занимающихся костнопластической хирургией челюстно-лицевой области нет
единого мнения об использовании ортотопических аллотрансплантатов в
восстановительной хирургии ВНЧС. Большинство хирургов считают наиболее
целесообразным использовать для аллопластики височно-нижнечелюстного
сустава консервированные ортотопические трансплантаты [Плотников Η. Α.,
1967, 1979; Никитин Α. Α., 1972-1987; Аржанцев П. 3., 1971; Сигал А. М.,
1972; Сысолятин П. Г., 1979—1984; Тер-Асатуров Г. П., 1981, и др.].
Исходя из данных литературы и собственного клинического опыта,
следует отметить, что ни одним из видов костных трансплантатов, кроме
ортотопических, невозможно полностью восстановить анатомические образования
ВНЧС и получить сочленение, функционирующее как нормальный сустав, а не
"приближающееся к суставному". От этого во многом зависят
функциональная активность и перестройка всего жевательного аппарата, так как анатомо-
функциональные условия, создающиеся после аллопластики ВНЧС и
перемещения нижней челюсти и жевательных мышц в новое положение,
несмотря на огромные адаптационные возможности жевательного аппарата,
вызывают дискоординацию всех групп мышц оперированной и здоровой стороны.
В связи с этим при хирургическом вмешательстве на ВНЧС следует
стремиться к сохранению или восстановлению нормальных анатомо-структур-
ных взаимоотношений элементов сустава и его биомеханики.
Наряду с клиническими исследованиями в последнее время активно
продолжается разработка новых методов хирургического восстановления
ВНЧС в эксперименте на животных. Учитывая сложность восстановления
анатомо-морфологического строения ВНЧС костными трансплантатами,
экспериментаторы стремятся создать эндопротез полного ВНЧС по аналогии
с пересадкой эндопротезов тазобедренного сустава в клиниках
травматологии и ортопедии.
25.2. Анатомо-физиологические особенности
и биомеханика височно-нижнечелюстного сустава
ВНЧС представляет собой сложную в функциональном отношении
биологическую систему, неразрывно связанную с организмом. В силу своего
анатомического строения он имеет много общего с другими суставами, а в силу
своеобразия функции обладает рядом специфических особенностей,
существенно отличающих его от них. Он образован головкой мыщелкового отростка
нижней челюсти и суставной ямкой височной кости.
По Б. Н. Бынину A947), элементами височно-нижнечелюстного сустава
являются: 1) суставная ямка с суставным бугорком и задним суставным
отростком; 2) головка нижней челюсти; 3) суставной диск (мениск); 4)
суставная капсула; 5) суставные связки.
Головка нижней челюсти представляет собой поперечно
лежащий эллипсовидной формы валик. В ней различают переднюю, заднюю и
верхнюю поверхности [Гинали В. Н., 1966]. Форма головки оказывает
огромное влияние на функцию жевательного аппарата и находится в зависимости
от работы височно-нижнечелюстного сустава. А. Аничкин A896), R. Fick
A904) указывали, что на форму головки нижней челюсти воздействуют мы-
191
щечная тяга и сила жевательного давления. Передняя поверхность головки
сферически вогнута и представляет собой ямку, которая служит для
прикрепления латеральной крыловидной мышцы. Задняя поверхность головки
напоминает треугольник, основанием которого является задний край ее верхней
поверхности. Стороны этого треугольника конвергируют книзу, переходя в
задний край ветви. На задней поверхности головки нижней челюсти имеется
фасетка — отпечаток позадисуставного отростка. По данным В. Н. Гинали
A966), головка нижней челюсти отклонена кзади в среднем на 107,3° от
места пересечения прямой, соединяющей эти точки на ветви нижней
челюсти. Верхняя поверхность нижнечелюстной головки напоминает эллипс,
продольный диаметр которого равен 20,06 мм, а поперечный — 8,52 мм.
Снаружи эта поверхность заканчивается наружным, а изнутри —
внутренним мыщелком головки. Продольная ось головки нижней челюсти
расположена под небольшим углом к горизонтальной плоскости, в результате чего
ее внутренний мыщелок находится несколько выше наружного. Головка
нижней челюсти как бы сдавлена в переднезаднем направлении и вытянута
в поперечном.
По сравнению с другими элементами ВНЧС головка нижней челюсти
представлена наиболее рыхлой костью. Она содержит 70,7 % губчатого
вещества и только 29,3 % компактного. Губчатое вещество головки представлено
костными балками пластинчатой формы, соединенными между собой мощными
спайками. Эти балки по ширине приближаются к диаметру ячеек губчатого
вещества и особенно широки в области шейки головки нижней челюсти. Они
играют исключительную роль в укреплении шейки нижнечелюстной головки.
Особенности строения костной ткани головки и шейки нижней челюсти
позволяют выдерживать значительные нагрузки при действии сил,
направленных в сагиттальной плоскости, в частности при ударе в подбородок.
Суставная ямка располагается ниже скуловой дуги и кпереди от
костной части наружного слухового прохода, имеет форму эллипса и по объему
почти в 3 раза превосходит головку, что дает возможность осуществлять
большой объем движений в суставе. Несоответствие размеров суставной ямки и
головки нижней челюсти позволяет некоторым авторам относить ВНЧС к
инконгруэнтным.
Суставная ямка ограничена спереди задней поверхностью суставного
бугорка, сзади — заднесуставным отростком и барабанной частью височной
кости отделяющими ее от наружного слухового прохода, вверху — тонким
слоем кости, отделяющим ее от средней черепной ямки, изнутри —
латеральным краем отростка основной кости и снаружи — гребнем скулового
отростка височной кости. В детском возрасте при тяжелых формах гнойного отита
близкая анатомическая связь суставной ямки с барабанной областью и
элементами среднего и внутреннего уха способствует переходу воспалительного
процесса на ВНЧС, что приводит к гибели элементов сустава и развитию
деформирующего артроза и анкилоза.
Барабанная часть височной кости, ограничивающая суставную ямку сзади,
представляет собой костную пластинку толщиной 0,45 мм. С возрастом
глубина суставной ямки индивидуально варьирует. У новорожденных ямка
плоская, в дальнейшем глубина ее увеличивается и к 6 годам устанавливается
индивидуально. С возрастом и особенно в связи с потерей зубов глубина
суставной ямки уменьшается вследствие ее атрофии.
Поперечный диаметр суставной ямки в среднем равен 26,6 мм,
сагиттальный — 17,2 мм [Гинали В. Н., 1966]. Мозговую полость черепа отделяет от
суставной ямки ее свод, состоящий из компактной кости, толщина которой
1,7 мм. Глубина суставной ямки при целом зубном ряде равняется 8,7 мм.
192
Заднесуставной отросток, являясь задней границей суставной ямки,
располагается впереди каменисто-барабанной щели. В норме у человека он
выражен слабо, однако достаточно, чтобы защитить сосудисто-нервный пучок,
выходящий из каменисто-барабанной щели, от ущемления головкой нижней
челюсти при ее движениях. При потере зубов особенно жевательной группы,
происходят уменьшение суставной высоты и дистальный сдвиг головки, в
результате чего могут возникнуть травма сосудисто-нервного пучка и боли в
суставе. Каменисто-барабанная щель делит суставную ямку на две части:
переднюю, интракапсулярную, лежащую в полости сустава, и заднюю, экстра-
капсулярную, находящуюся вне полости.
Суставной бугорок. Передняя часть суставной ямки представлена
суставным бугорком. Он образован утолщением кости заднего отдела
скулового отростка височной кости и имеет форму эллипса, сагиттальный диаметр
которого равен 8,5 мм, а поперечный —19,1 мм. Высота суставного бугорка
колеблется от 4 до 15 мм [Гинали В. Н., 1966]. По данным Н. А. Рабухиной
A966), высота суставного бугорка от 5 до 25 мм. Наклон его заднего ската к
горизонтальной плоскости составляет от 20 до 50°. На суставном бугорке
различают три поверхности: заднюю (скат суставного бугорка), по которой
совершает экскурсии головка нижней челюсти; горизонтальную,
представляющую собой вершину суставного бугорка, и переднюю, которая переходит в
подвисочную ямку. Суставной бугорок состоит из 55,5 % компактного
вещества кости и из 44,5 % губчатого.
Как и головка нижней челюсти, в течение жизни человека суставной
бугорок претерпевает сложные изменения. У новорожденных он отсутствует,
первые признаки его определяются к концу 1-го года жизни. Его развитие в
пределах индивидуальных размеров и формы завершается к 6—7 годам [Кас-
парова Н. Н. и др., 1981]. С возрастом и при потере жевательных зубов
суставной бугорок постепенно уплощается. Поданным В. Н. Гинали A966), при
двустороннем отсутствии моляров и премоляров глубина суставной ямки и
высота суставного бугорка уменьшаются на 3 мм и более. Суставной бугорок
является важнейшим элементом ВНЧС. Он играет существенную роль в его
эволюции и в значительной степени обусловливает его место в
сравнительной морфологии.
Суставной диск по форме напоминает двояковогнутую линзу,
которая как "колпачок" покрывает головку нижней челюсти, благодаря чему
устраняется инконгруэнтность суставных поверхностей и увеличивается
площадь их соприкосновения. Длинный диаметр его равен в среднем 21,3 мм,
короткий — 11,1 мм. Суставной диск (мениск) амортизирует жевательное
давление, действующее через головку нижней челюсти на суставную ямку.
Нижняя его поверхность образует как бы подвижную ямку для головки.
Суставной диск в центральной своей части как бы сдавлен снизу верхней
поверхностью головки нижней челюсти, а сверху — задним скатом суставного
бугорка. Толщина диска на этом участке 1,2 мм. Верхней поверхностью
заднего отдела диск располагается на дне суставной ямки, а самая выпуклая его
часть восполняет ее свод. Нижняя поверхность этого отдела диска является
верхней поверхностью головки нижней челюсти. Задний отдел суставного
диска имеет толщину 3,52 мм.
Гистологические исследования показали, что суставной диск с раннего
возраста до 25—30 лет состоит из коллагеновой соединительной ткани. После
30 лет он состоит из волокнистого хряща с войлокообразно идущими колла-
геновыми волокнами, местами переплетающимися с отдельными
эластическими волокнами [Гинали В. Н., 1966]. Между задним полюсом суставного
диска и капсулой находится рыхлая соединительнотканная прослойка — так
13-1263
193
называемая задисковая подушка, богатая сосудами и нервами, которая
связана с синовиальной оболочкой и принимает непосредственное участие в
питании тканей сустава. Суставной диск разделяет полость сустава на два
изолированных отдела. Верхний отдел ВНЧС (менисковисочный) по размерам
превосходит нижний (менискосуставной). Оба они выстланы изнутри
складчатой синовиальной оболочкой, богатой сосудами и нервными окончаниями.
По данным П. М. Егорова A979), объем верхнего отдела равен 1,5 мл,
а нижнего — 0,5 мл. При введении большего количества жидкости
наблюдается растяжение суставной капсулы, а при введении рентгеноконтрастных
веществ четкость изображения ухудшается.
Передним полюсом мениск прикрепляется к суставному бугорку,
суставной ямке, частично к головке, что имеет большое значение при
нарушении взаимного расположения суставного диска и головки нижней челюсти,
внутренним и наружным полюсами — к головке нижней челюсти. От
переднего отдела капсулы сустава и суставного диска отходят сухожильные
волокна верхнего пучка латеральной крыловидной мышцы.
Ряд авторов считают, что движение суставного диска вперед
осуществляется за счет латеральной крыловидной мышцы и головки нижней челюсти.
Однако Н. Sicher A955) утверждает, что латеральная крыловидная
мышца способствует удержанию мениска в определенном положении по
отношению к головке и суставной ямке, т. е. способствует как бы стабилизации
мениска, но не принимает участия в смещении его. Латеральная крыловидная
мышца предотвращает соскальзывание суставного диска (мениска) кзади при
пережевывании пищи и кпереди — при широком открывании рта. Движение
же мениска совершается за счет тяги головки нижней челюсти, без помощи
мышцы. Это обусловлено тем, что ход волокон латеральной крыловидной
мышцы не соответствует смещениям мениска. Одностороннее прикрепление
латеральной крыловидной мышцы к суставному диску создает благоприятные
условия для развития мышечного дисбаланса, который может привести к
постоянной микротравме тканей сустава, а при длительном существовании — к
развитию дегенеративных изменений в суставе.
Суставная капсула представляет собой эластичную
соединительнотканную оболочку, состоящую из двух слоев: наружного фиброзного и
внутреннего, образованного синовиальной оболочкой, состоящего из эндо-
телиальных клеток. Клетки синовиальной оболочки вырабатывают
синовиальную жидкость, способствующую уменьшению трения суставных поверхностей
и являющуюся иммунобиологической защитой от внедрения инфекции в
полость сустава.
Высказывается предположение о том, что синовиальная жидкость
вырабатывается в основном в заднем отделе сустава, там, где между задним
полюсом суставного диска и капсулой сустава имеется рыхлая соединительная
ткань, называемая "задисковой подушкой", или биламинарной зоной.
"Задисковая подушка" имеет форму трапеции, большее основание которой находится
у капсулы, меньшее — у диска. Верхние волокна ее идут от диска к височной
кости, нижние — к головке нижней челюсти, средние срастаются с капсулой
сустава при помощи связок, тормозящих движения головки нижней челюсти.
Травма "задисковой подушки" головкой нижней челюсти при адентии,
патологии прикуса или деформирующем артрозе ведет к нарушению питания и
дегенерации суставных тканей [Хватова В. Α., 1982]. "Задисковая подушка"
вместе с задним отделом мениска играет роль амортизатора при повышенной
функциональной нагрузке на сустав.
Капсула сустава очень прочна, эластична и не рвется даже при полных
вывихах сустава. Толщина суставной капсулы 0,4—1,7 мм. Наиболее тонки
194
передняя и внутренняя части капсулы. На височной кости капсула
прикрепляется спереди к переднему краю суставного бугорка и далее располагается
по внутреннему периметру суставной ямки до передней границы каменисто-
барабанной щели, тем самым значительно суживая суставную ямку. Внизу
суставная капсула прикрепляется к шейке мыщелкового отростка нижней
челюсти, причем на задней границе мыщелкового отростка ниже, чем на
передней, и имеет короткие плотно охватывающие шейку волокна. Самую
большую длину суставная капсула имеет спереди и снаружи. Видимо, поэтому
передние вывихи головки нижней челюсти наблюдаются значительно чаще,
чем задние.
Связки ВНЧС. Связочный аппарат состоит из вне- и внутрикапсу-
лярных связок. Они регулируют движения в суставе и, образуя своего рода
подвеску для нижней челюсти, поддерживают постоянный контакт
суставных поверхностей сочленяющихся костей. Связки сустава, особенно экстра-
капсулярные, препятствуют растяжению суставной капсулы и состоят из
фиброзной неэластичной соединительной ткани, которая не способна
восстанавливать свою длину после перерастяжения.
Из внутрикапсулярных, или собственно капсулярных, связок различают
две верхние (передняя и задняя) капсулярные связки, идущие от скуловой
дуги к верхнему краю суставного диска, и две нижние, прикрепляющиеся к
нижнему краю суставного диска и к шейке мыщелкового отростка нижней
челюсти с наружной и внутренней стороны на границе суставной капсулы.
В некапсул ярные связки ВНЧС более широкие и мощные. Их также четыре.
Самой широкой и мощной связкой, укрепляющей суставную капсулу
снаружи и ограничивающей боковые движения головки нижней челюсти,
является латеральная связка. Она берет начало от скулового отростка височной
кости и прикрепляется к шейке мыщелкового отростка. Другой не менее
важной связкой, ограничивающей выдвижение нижней челюсти вперед,
является шилонижнечелюстная. Она начинается от шиловидного отростка и
прикрепляется к углу нижней челюсти.
Клиновидно-нижнечелюстная связка ограничивает боковые движения
нижней челюсти, начинается от ости клиновидной кости и на внутренней
поверхности ветви нижней челюсти прикрепляется тремя пучками к шейке
мыщелкового отростка, язычку нижней челюсти и задневнутреннему краю ветви.
Последней экстракапсулярной связкой ВНЧС является медиальная,
также регулирующая боковые движения нижней челюсти. Она берет начало
от крючка крыловидного отростка и прикрепляется к язычку нижней
челюсти на внутренней поверхности ветви.
Следует отметить, что при воспалительных заболеваниях и
распространении воспаления на периартикулярные ткани связочный аппарат сустава теряет
эластичность, в результате чего наступает ограничение движений в ВНЧС.
При вторичном деформирующем артрозе и анкилозе ВНЧС рубцовые
изменения и оссификация связок приводят к ограничению движений или
полной неподвижности в суставе.
Особенно часто в патологический процесс вовлекаются расположенные
на внутренней поверхности ветви нижней челюсти медиальная и
крыловидно-нижнечелюстная связки. Сочленяющиеся поверхности ВНЧС покрыты
хрящом, о характере которого единого мнения нет.
W. Stouiis A954) описывает его как гиалиновый хрящ, П. Б. Балакирев
A914), А. Э. Рауэр A914), М. Zicher A955), R. Moss A959), Η. Ehoubas A980)
и др. — как волокнистый. Однако при тщательном изучении этого вопроса
на основании анатомо-гистологических исследований было выявлено
изменение характера хряща с возрастом [Несвижский С. С, 1950].
13*
195
До 25—30 лет сочлененная поверхность головок нижней челюсти
выстлана тонким слоем гиалинового хряща, покрытого надхрящницей с хорошо
выраженными камбиальным и фиброзным слоями. Суставные поверхности
суставной ямки и суставного бугорка височной кости не имеют хрящевого
покрытия и выстланы исключительно надкостницей с хорошо развитыми
камбиальным и фиброзным слоями. Надхрящница, покрывающая
поверхность головки нижней челюсти, переходит в надкостницу восходящей ветви.
Надхрящница, выстилающая поверхность суставной ямки и суставного
бугорка височной кости, является продолжением надкостницы височной кости
и основания черепа. Мениск состоит из плотной соединительной ткани.
В возрасте 25—30 лет на сочленовных поверхностях сустава обнаружен слой
типичного волокнистого хряща. В этом же возрасте центральная часть
мениска приобретает все свойства волокнистого хряща.
Кровоснабжение ВНЧС имеет огромное значение для
нормального функционирования сустава. Патогенез заболеваний височно-нижнече-
люстного сустава тесно связан с состоянием кровоснабжения его элементов.
В связи с этим изучению кровоснабжения ВНЧС были посвящены
многочисленные работы отечественных и зарубежных авторов [Воробьев В. П.,
1932; Уваров В. М., 1934; Александров Г. Н., 1935; Тонков В. Н., 1946;
Hankey С, 1954; Cohen W., Keller G., 1955; Sicher H., 1956, и др.].
Кровоснабжение височно-нижнечелюстного сустава осуществляется в
основном за счет двух конечных ветвей наружной сонной артерии —
поверхностной височной и внутренней челюстной артерий. Источником
кровоснабжения мыщелкового отростка является крыловидная артерия, ветви которой
проходят к мыщелковому отростку в области прикрепления латеральной
крыловидной мышцы. Кроме того, мыщелковый отросток кровоснабжается
за счет сосудов надкостницы.
Наиболее подробно кровоснабжение височно-нижнечелюстного сустава
и его элементов изучено Л. С. Измайловой A964). По ее данным от
поверхностной височной артерии в начальном ее отделе под углом в 100° отходит
средняя височная артерия, которая отдает височно-нижнечелюстному
суставу две артериальные ветви. Первая ветвь отходит на уровне задней
поверхности шейки мыщелкового отростка под углом 45° и направляется на
наружную поверхность ВНЧС, где вплетается в капсулу сустава и в дальнейшем
делится на три—пять мелких ветвей. Кроме того, она отдает веточку на
задней поверхности ВНЧС. Вторая артериальная ветвь, отходящая от средней
височной артерии, отдает на задней поверхности ВНЧС в его нижнем отделе
три—четыре сосудистые веточки, вплетающиеся в капсулу сустава.
От поверхностной височной артерии на уровне суставного диска
(мениска) и суставной ямки на задней поверхности ВНЧС под углом 45° отходят
две артериальные ветви, которые вплетаются также в капсулу сустава. Одна
из этих ветвей продолжается на наружную поверхность, принимая участие в
кровоснабжении суставной капсулы в этом отделе. Деление всех этих ветвей
осуществляется по магистральному типу. Кроме того, к задней поверхности
ВНЧС подходят ветви от внутренней челюстной артерии.
От ее ветвей (глубокая ушная и передняя барабанные артерии) к задней
и внутренней поверхности височно-нижнечелюстного сустава отходят одна—
три артериальные ветви, которые, достигнув ВНЧС, делятся по
магистральному типу.
В кровоснабжении передней поверхности сустава принимают участие
средняя менингеальная и крыловидная артерии. Последняя под углом 60°
отходит непосредственно от внутренней челюстной артерии. От средней ме-
нингеальной артерии отходит одна ветвь, которая, не доходя до ВНЧС, де-
196
лится на две веточки, которые направляются к суставу и вплетаются в его
капсулу на внутренней и передней поверхностях. Сосудистая сеть наиболее
выражена в верхнем отделе ВНЧС, где количество артериальных ветвей
достигает двадцати. В связи с этим Л. С. Измайлова считает, что
кровоснабжение головки нижней челюсти осуществляется в основном за счет внутрико-
стных артерий из системы внутренней челюстной артерии.
Суставной диск (мениск) имеет несколько зон кровоснабжения.
Зона крупных кровеносных сосудов расположена на границе
синовиальной оболочки и мениска. К мениску из суставной капсулы по задней
поверхности подходят два крупных артериальных ствола, которые идут по
магистральному типу и, не доходя 2 мм до края мениска, делятся на две артерии по
рассыпному типу. Эти сосуды принимают участие в питании мениска.
В краевой зоне мениска сосуды располагаются в два слоя
(поверхностный и глубокий). Здесь же имеется два типа краевой крупнопетлистой
сосудистой сети, петли которой образованы сосудами 3—4-го порядка. Эта
сосудистая сеть мениска по периферии образует "корону" вокруг центрального
бессосудистого участка.
В зоне сосудистых капилляров длинные сосуды, направляясь
непосредственно к центру диска, заканчиваются метелкообразными сосудами,
которые заходят в центральную зону мениска, не анастомозируя друг с другом.
Центральная зона мениска бессосудистая. В ней отсутствуют или изредка
встречаются отдельные конечные капилляры.
Задняя поверхность мениска имеет хорошо выраженную сосудистую сеть.
Передняя поверхность кровоснабжается значительно меньше. В старческом
возрасте кровоснабжение мениска намного беднее, чем у новорожденного.
Изучая сосудистую систему суставной ямки и головки нижней челюсти
на гистологических срезах, Л. С. Измайлова A964) установила, что
сосудистая система суставной ямки височной кости представлена расширенными
венозными каналами, между которыми проходит тончайшая артериальная
сеть. Суставная капсула обильно покрыта васкуляризованной тканью.
Синовиальная оболочка имеет сосудистую сеть, состоящую из тончайших сосудов,
которые идут параллельно капсуле сустава, анастомозируя с сосудами
капсулы. Там, где суставной диск (мениск) вплетается в капсулу сустава,
наблюдается переход сосудов с суставной капсулы непосредственно в мениск. Из
капсулы сустава сосуды проникают в надкостницу головки нижней челюсти
и питают наружные слои головки.
Важным моментом в кровоснабжении головки нижней челюсти
является перфорирование хрящевого покрытия веточками костных артерий в виде
отдельных конечных веточек.
Из сказанного выше очевидно, что ВНЧС очень хорошо
кровоснабжается. В связи с обилием сосудов, характером и расположением их нарушение
кровоснабжения, обмена, изменение окружающей среды, различного рода
инфекционные процессы, безусловно, отражаются на состоянии ВНЧС. Так,
нарушение кровоснабжения мениска или головки нижней челюсти может
вызвать развитие дистрофических процессов в элементах сустава с
формированием деформирующего артроза или анкилоза ВНЧС.
Иннервация ВНЧС, поданным М. А. Бубенновой A958) и У. Г. Ва-
лиева A970), осуществляется ушно-височным и жевательным нервами из
третьей ветви тройничного нерва, глубоким височным и лицевым нервами,
симпатическим сплетением поверхностной височной артерии, задним
глубоким височным и латеральным крыловидным нервами.
Ушно-височный нерв, проходя позади сустава, отдает три веточки,
которые иннервируют заднюю поверхность суставной капсулы.
197
У заднего края височной мышцы отходит суставная ветвь жевательного
нерва, иннервирующая переднюю поверхность суставной капсулы.
Симпатическое сплетение поверхностной височной артерии образуется за счет нервных
веточек, отходящих от начала височной артерии на уровне шейки мыщелко-
вого отростка. Эти веточки иннервируют наружную поверхность капсулы.
Кроме того, в диске, капсуле и связках сустава имеются чувствительные
и симпатические нервные волокна, идущие из верхнего шейного узла, от
которого получают иннервацию органы слуха и зрения. Этим объясняется
возникновение иногда ушных и глазных симптомов при патологии ВНЧС.
Лимфатическая система ВНЧС. В доступной литературе
исследований, посвященных описанию лимфатической системы, очень мало.
В. И. Ошкадеров A931) и А. Акилова A934), изучая лимфатические сосуды
ВНЧС, обнаружили, что они на всем протяжении анастомозируют с
лимфатическими узлами, собирающими лимфу от наружного и среднего уха. Вокруг
сустава имеется сеть лимфатических сосудов, связывающих поверхностные и
глубокие пути сустава. Наибольшее количество лимфатических сосудов
расположено в задней части капсулы ВНЧС.
Биомеханика ВНЧС. Изучение биомеханики сустава представляет
большой практический интерес в связи с тем, что от деятельности сустава во
многом зависят нормальные физиологические функции приема пищи,
мимики и речеобразования.
ВНЧС парные и представляют собой единую биологическую
кинематическую систему. Они построены симметрично по отношению друг к другу и
связаны непарной нижнечелюстной костью, поэтому движения в обоих
суставах осуществляются синхронно. Это является одной из анатомических
особенностей ВНЧС, которую необходимо учитывать при диагностике его
заболеваний.
Повреждение или заболевание одного из суставов создает
дополнительную функциональную нагрузку на другой сустав, что в конечном итоге
приводит к перегрузке здорового сустава и развитию в нем патологических
изменений. Это наглядно продемонстрировано нами в экспериментах на
животных, о чем будет сказано ниже.
Другой анатомо-функциональной особенностью ВНЧС, отличающей
его от других суставов человека, является комбинация поступательных и
вращательных движений. Эта особенность обусловлена инконгруэнтностью суставных
поверхностей и наличием в полости сустава суставного диска (мениска),
устраняющего несоответствие в суставе и разделяющего сустав на два
изолированных отдела — верхний и нижний. В верхнем отделе происходят в основном
поступательные движения головки нижней челюсти и скольжение мениска по
скату суставного бугорка. В нижнем отделе совершаются вращательные
движения головки вокруг горизонтальной оси. В обоих отделах движения
совершаются одновременно.
При сомкнутых в центральной окклюзии челюстях, а также при
положении нижней челюсти в покое головки нижней челюсти в обоих суставах
расположены у основания задней поверхности суставного бугорка. При этом
головки находятся на некотором расстоянии от дна суставной ямки и
кпереди от ее середины. При сокращении жевательных мышц головка нижней
челюсти не отходит в глубину суставной ямки и не оказывает давления на
тонкую верхнюю стенку. Это объясняется тем, что при закрывании рта
мышечный аппарат смещает нижнюю челюсть несколько вперед и удерживает
в определенном положении за счет своего тонуса.
В старческом возрасте вследствие отсутствия зубов, снижения
мышечного тонуса, атрофии суставного диска и суставной ямки головка нижней че-
198
люсти смещается дистально и в глубину суставной ямки, что может привести
к ущемлению сосудисто-нервного пучка, трофическим расстройствам в
мягких тканях сустава, воспалительным и дегенеративным процессам. При
открывании рта головки нижней челюсти в обоих суставах вместе с менисками
синхронно двигаются вперед и вниз по скату суставного бугорка.
В начальной фазе открывания рта происходят вращательные движения
в нижнем отделе сустава вокруг горизонтальной оси, а затем поступательные
движения в верхнем отделе сустава до вершины суставного бугорка.
При максимальном открывании рта суставные диски головки нижней
челюсти находятся на вершинах суставных бугорков. При попытке еще
больше открыть рот в нижнем отделе сустава опять происходят вращательные
движения головки, находящейся на вершине суставного бугорка.
Дальнейшему их перемещению препятствуют связки и жевательные мышцы. При
боковых движениях нижней челюсти на стороне, в направлении которой
смещается челюсть, происходит вращательное движение головки в нижнем
отделе сустава, а на противоположной — поступательное движение головки
в верхнем отделе сустава. Боковые движения нижней челюсти, связанные с
поступательным движением головок в верхнем отделе ВНЧС, осуществляются в
основном за счет сокращения латеральных крыловидных мышц. В связи с
этим большое значение при операциях на мыщелковом отростке нижней
челюсти или височно-нижнечелюстном суставе имеет восстановление не
только элементов сустава (суставная капсула, суставной диск), но и функции
латеральных крыловидных мышц.
При слабости или атрофии связочного аппарата и мышц происходят
дальнейшее смещение головки за вершину суставного бугорка и
односторонний или двусторонний вывих нижней челюсти. В. А. Хватова A982)
смещение головки нижней челюсти за вершину суставного бугорка при
максимальном открывании рта, определяемое на рентгенограмме, в отсутствие болей и
хруста в суставе рассматривает не как подвывих, а как индивидуальную
особенность функции данного сочленения. С этим следует согласиться, так как
особенности функции ВНЧС обусловливаются не только силой и тонусом
жевательной мускулатуры, но и конфигурацией суставных поверхностей,
особенностями суставной капсулы, суставного диска, связочного аппарата,
соотношением и сохранностью зубных рядов, видом прикуса и т. д. Очень
часто отроение височно-нижнечелюстного сустава, характерное для
определенного прикуса, трактуется как патология.
В настоящее время среди многочисленных вариантов сочленения
выделяют три основных типа строения ВНЧС, характеризующихся следующими
анатомо-функциональными особенностями.
Умеренно выпукло-вогнутый сустав характеризуется средней шириной
и глубиной суставной ямки, выпуклостью суставного бугорка,
выраженностью суставной поверхности головки нижней челюсти и небольшим
наклоном шейки мыщелкового отростка вперед. В нем сочетаются поступательные
и вращательные движения. Этот тип сустава характерен для ортогнатическо-
го прикуса.
Поверхностный, плоский сустав имеет уплощенную, как бы сошлифо-
ванную головку, невысокий плоский суставной бугорок, поверхностную и
широкую суставную ямку. Шейка мыщелкового отростка расположена почти
вертикально. Отмечается преобладание поступательных движений. Такое
строение сустава характерно для прямого прикуса.
Для выраженно выпукло-вогнутого сустава типичны глубокая и узкая
суставная ямка, высокий и выпуклый суставной бугорок. Головка нижней
челюсти под большим углом наклонена к шейке мыщелкового отростка, сус-
199
тавная поверхность ее сильно выпуклая. Сустав характеризуется
преобладанием вращательных движений и встречается при наличии глубокого резцового
перекрытия.
Несмотря на такое разделение, определенный тип анатомического
строения сустава, свойственный только данному виду прикуса, встречается
очень редко.
Еще одно своеобразие анатомо-функционального строения височно-
нижнечелюстного сустава заключается в том, что к суставному диску и
головке нижней челюсти прикрепляется латеральная крыловидная мышца.
Длительное время оставалась неясной функция этой мышцы. В последние
годы подтверждено предположение о том, что перемещение суставного диска
происходит механически одновременно с перемещением нижнечелюстной
головки в силу их анатомической связи в боковых отделах. Функция же
верхней части латеральной крыловидной мышцы, прикрепляющейся к суставному
диску, заключается в стабилизации его. A. Carlsoo A956), изучавший с
помощью игольчатых электродов биоэлектрическую активность этой мышцы,
обнаружил, что тонус ее постоянен при любых движениях нижней челюсти.
В связи с этим тонус и состояние латеральной крыловидной мышцы имеет
огромное значение для нормальной функции и расположения подвижного
комплекса головка нижней челюсти — суставной диск. Напряжение этой
мышцы не дает головке нижней челюсти смещаться вверх, удерживает ее в
определенном положении.
Таким образом, ВНЧС сформировался в филогенезе в зависимости от
характера прикуса и движения нижней челюсти, необходимых для
измельчения пищи, а также в тесной зависимости от эволюции лицевого и
мозгового отделов черепа. Он сложен не только по анатомическому строению, но
и по функции и является замкнутой кинематической системой, так как
движение в одном суставе вызывает движение и в другом. Он относится к
двухосным, так как движения в нем происходят по двум осям — горизонтальной и
вертикальной. Обладает тремя степенями свободы, так как движения в нем
осуществляются в вертикальном, сагиттальном и трансверсальном направлениях.
Большую роль в комбинации суставных движений имеет нейрогенный фактор.
Этот сустав инконгруэнтный. Следовательно, ВНЧС — это специфический
сустав, присущий только человеку.
25.3. Методы обследования и подготовка больных
к аллопластике височно-нижнечелюстного сустава
Важным звеном в общем комплексе реабилитационных мероприятий после
реконструктивных и восстановительных операций на височно-нижнечелюстном
суставе является догоспитальный период. Обследование и подготовку больных
к аллопластике височно-нижнечелюстного сустава следует начинать с
хирургического кабинета стоматологической поликлиники — начального этапа
медицинской реабилитации больных с челюстно-лицевой патологией.
В процессе обследования больных важное место занимает сбор
анамнестических данных. Необходимо выяснить у больного или его родственников
первые признаки и время появления заболевания, дату первоначального
обращения к врачу, а также то, какое обследование и лечение проводились по
поводу данного заболевания и каковы его результаты.
При травме нижней челюсти, сопровождающейся переломом ее на
различных уровнях, необходимо установить время и обстоятельства травмы,
наличие потери сознания, рвоты, тошноты, головокружения.
200
В большинстве случаев переломы мыщелкового отростка нижней
челюсти, особенно внутрисуставные и высокие, бывают закрытыми. При сочетан-
ных открытых переломах следует выяснить, вводилась ли противостолбнячная
сыворотка. Устанавливают характер травмирующего момента, направление
действующей силы и место ее приложения, наличие кровотечения изо рта, уха.
Кровотечение изо рта указывает на открытый перелом челюсти, а сукровичные
выделения из уха могут быть признаком перелома мыщелкового отростка с
повреждением костной или хрящевой части наружного слухового прохода.
При обследовании больных с заболеваниями ВНЧС (анкилозы,
деформирующие артрозы) выясняют, когда возникли и какой характер имели
проявления первых симптомов: болей, функциональных нарушений, признаков
недоразвития нижней челюсти.
Особо обращают внимание на наличие факторов, предрасполагающих к
возникновению заболевания суставов, таких, как охлаждение организма,
инфекционные заболевания, развитие общих суставных поражений,
повышенная нагрузка на сустав в результате патологии прикуса, травма сустава,
перенесенные гнойные процессы (гнойный средний отит, остеомиелит нижней
челюсти, сепсис и др.).
При выяснении характера болей обращают внимание на их
интенсивность, локализацию, частоту появления и продолжительность, время и условия
появления болей при движении нижней челюсти во время разговора, приеме
пищи, максимальном открывании рта. Выясняют, сопровождаются ли
движения нижней челюсти шумовыми симптомами (хруст, щелканье), тугопо-
движностью, блокированием движений в суставе.
Важным диагностическим признаком является нарушение функции
сустава, что клинически выражается в изменении объема и характера движений
нижней челюсти.
Осмотр ВНЧС, как правило, начинают с определения объема движений
нижней челюсти. Ограничение подвижности нижней челюсти может
возникнуть в результате воспалительной, мышечной или рубцовой контрактуры,
механического ограничения движений челюсти при переломах скуловой
дуги, развития опухоли ветви или венечного отростка нижней челюсти, свежих
или неправильно сросшихся переломов мыщелкового отростка,
деформирующего артроза и анкилоза ВНЧС. При изучении характера
функциональных нарушений определяют объем утраченной функции (отсутствие боковых
и сагиттальных движений нижней челюсти, степень ограничения
вертикальных движений).
Смещение нижней челюсти в одну сторону при ограниченных
вертикальных движениях свидетельствует о нарушении функции одного из суставов.
При переломе мыщелкового отростка или тугоподвижности одного из
суставов отмечается смещение (девиация) нижней челюсти в сторону
пораженного сустава. Смещение нижней челюсти в сторону, противоположную
поврежденному суставу, указывает на наличие вывиха или подвывиха одного из
суставов.
При высоком переломе мыщелкового отростка с вывихом головки
нижней челюсти отмечаются: хруст и боли в суставе, усиливающиеся при
движениях нижней челюсти, затрудненное открывание рта, нарушение прикуса,
резкая болезненность и западение мягких тканей в проекции нижней
челюсти, ограничение или отсутствие ее движений, определяемые пальпаторно;
отраженные боли в суставе при нагрузке на ветвь нижней челюсти в
продольном направлении кверху. Пальпация ВНЧС и всех отделов нижней
челюсти позволяет выявить дефект костной ткани, подвижность головки
нижней челюсти и ее форму, характер деформации нижней челюсти.
201
Для уточнения характера патологического процесса нижней челюсти и
ВНЧС наряду с клиническими проявлениями большое значение в
обследовании больного имеет рентгенологическое исследование.
В настоящее время наиболее распространенными являются методики
обследования по Пордессу в модификации Парма и по Шуллеру. Из
специальных методик применяют томографию, зонографию, ортопантомографию,
электрорентгенографию, рентгенкинематографию, артрографию, магниторе-
зонансную томографию [Дергилев А. П., 1997].
Одним из объективных методов оценки функционального состояния
жевательных мышц является электромиография с изучением
функциональной активности жевательных, височных и латеральных крыловидных мышц.
Большое значение имеют антропометрические исследования лица
больного. Их проводят не только для определения размеров нижней челюсти с
целью выявления ее недоразвития на стороне больного сустава, но и для
точного подбора ортотопического аллотрансплантата нижней челюсти, что
очень важно для получения хороших косметического и функционального
результатов хирургического лечения.
Методика ортотопической аллотрансплантации нижней челюсти
основана на тщательном подборе донорского аллотрансплантата путем наружных
измерений основных антропометрических параметров нижней челюсти
реципиента [Плотников Η. Α., 1979]. При аллопластике ВНЧС учитывают
следующие основные параметры: 1) длину половины нижней челюсти —
расстояние от средней линии подбородка до касательной к задним концам
головок нижней челюсти; 2) длину ветви — расстояние от нижнего края ветви
до верхнего края головки нижней челюсти.
Следует отметить важность тщательной предоперационной подготовки
больного, так как от этого в значительной степени зависит исход
хирургического лечения. Перед операцией, если возможно, проводят тщательную
санацию полости рта с целью ликвидации очагов хронической одонтогенной
инфекции. У всех без исключения больных из полости рта, зева или
преддверия полости рта следует брать мазок на микрофлору для определения ее
чувствительности к антибиотикам. Это позволяет в послеоперационном
периоде проводить целенаправленную антибиотикотерапию, а также создавать
в операционной ране депо нужного антибиотика, насыщая им ортотопиче-
ский аллотрансплантат при подготовке его к пересадке.
При замещении больших дефектов нижней челюсти ортотопическим ал-
лотрансплантатом очень важно правильно выбрать метод иммобилизации
нижней челюсти не только на весь послеоперационный период, но и до
момента назначения функциональных движений. При составлении плана
хирургического лечения еще в амбулаторных условиях целесообразно предусмотреть
и изготовить шинирующий внутри- или внеротовой ортопедический аппарат,
чтобы не откладывать надолго операцию.
Внутриротовые проволочные или ленточные (конструкции Васильева)
шины фиксируют к зубам больного накануне операции.
Проводят тщательное обследование больного: общие клиническое и
биохимическое исследования крови и мочи, определение группы крови и резус-
фактора, электрокардиографию, флюорографию или по показаниям
рентгенографию грудной клетки.
Для оценки возможностей эндоназальной интубации трахеи и
проведения назотрахеального наркоза больного накануне операции осматривают
оториноларинголог и анестезиолог и делают соответствующие назначения.
После полного и тщательного обследования и подготовки больного
обсуждают окончательный план и определяют объем предстоящей операции.
202
25.4. Методика заготовки и обработки костно-пластического
материала для аллопластики височно-нижнечелюстного сустава
Реконструктивные и восстановительные операции на височно-нижнечелю-
стном суставе в силу особенностей его анатомо-топографического строения
значительно отличаются от такого рода вмешательств на суставах
конечностей. Перед челюстно-лицевым хирургом стоит задача не только
восстановить непрерывность кости и создать новый сустав, но и обеспечить хорошие
функциональный и эстетический результаты костной аллопластики.
Необходимо подобрать такой биопластический материал, который бы
позволял с наименьшей травмой для больного получить наибольший эффект
хирургического лечения. Этот материал по структуре и функции должен быть
близок к замещаемому или воссоздаваемому органу, быстро перестраиваться и
замещаться новообразованной костью, способствуя восстановлению не только
анатомической формы, но и физиологической функции утраченного органа,
исключать дополнительную травму, связанную с получением трансплантата.
Наиболее полно этим требованиям соответствует орототопический аллотранс-
плантат из нижнечелюстной кости.
В клинической практике костно-пластический материал берут от свежих
трупов людей, Ьогибших в результате травмы или скоропостижно умерших в
связи с сердечно-сосудистыми заболеваниями в возрасте до 40—45 лет. Забор
костно-пластического материала осуществляют не позднее 13 ч после
смерти, если труп-донор хранится при температуре 20 ± 3 °С, и не позднее 22 ч,
если хранение осуществляется при 2—4 °С.
П. Г. Сысолятин A984) установил, что морфологическая структура
кости нижней челюсти сохраняется неизменной соответственно указанным
срокам хранения до 28 и 40 ч. Заготовленный в эти сроки костно-пластический
материал при стерилизации его химическими средствами и ортотопической
пересадке в дефекты нижней челюсти дает такие же результаты, как и взятый
сразу после смерти донора.
Впервые в практике челюстно-лицевой хирургии А. А. Никитиным и
Н. А. Плотниковым разработан метод заготовки интракраниальным
доступом ортотопического аллотрансплантата полного ВНЧС со всеми его
анатомическими образованиями — суставной ямкой височной кости, суставным
диском, головкой нижней челюсти с хрящевым покрытием, капсулой и ин-
тракапсулярными связками.
В условиях секционного зала судебно-медицинского морга соблюдать
правила стерильности трудно. Однако в какой-то степени можно
предупредить вторичное инфицирование костного материала при заготовке. Для этого
перед заготовкой кожу спецдонора в области предстоящих разрезов
обрабатывают 5 % раствором йода с целью исключения инфицирования подлежащих
тканей с поверхности кожи. Таким же раствором обрабатывают
электрическую дрель. Все инструменты хранят в этиловом спирте. Хирурги работают
в стерильных халатах и перчатках.
Методика заготовки ортотопического аллотрансплантата полного
височно-нижнечелюстного сустава (суставной блок) заключается в следующем.
На передней поверхности грудной клетки спецдонора, ниже ключиц, по
направлению к клювовидным отросткам лопаток проводят полуовальный разрез
кожи, который соединяют с двумя дополнительными разрезами,
проходящими по переднему краю трапециевидной мышцы до верхнего отдела
сосцевидных отростков. Оба последних разреза соединяют поперечным разрезом,
проходящим через волосистую часть головы в теменных областях. Кожный
лоскут вместе с подкожной мышцей отсепаровывают на всем протяжении до
203
нижнего края нижней челюсти и скуловой дуги и откидывают кверху. После
выделения тела и ветвей нижней челюсти с двух сторон пересекают скуловые
дуги, дисковой фрезой осуществляют горизонтальный распил альвеолярного
отростка нижней челюсти; затем откинутый кожный лоскут помещают на
прежнее место. Мозговой череп вскрывают по общепринятым правилам:
горизонтальным распилом по периметру отделяют крышу черепа, обнажают и
рассекают твердую мозговую оболочку, удаляют головной мозг. На
внутренней поверхности основания черепа по границам средней черепной ямки с
204
Рис. 25.1. Продолжение.
г — аллотрансплантат полного ВНЧС (суставной блок) с ветвью и боковым отделом нижней челюсти.
обеих сторон через основание пирамидки височной кости, теменной и
основной края ее чешуи наносят ряд часто расположенных перфораций кости,
который заканчивается у рваного отверстия. Соединяя эти отверстия долотом
и молотком, отделяют костный фрагмент дна средней черепной ямки от
основания черепа единым блоком вместе с тканями ВНЧС и нижней челюстью.
При необходимости можно получить блок ВНЧС (суставной блок) с любым
по размеру отрезком нижней челюсти.
После завершения всех этапов забора аллотрансплантата с помощью
проволочного каркаса или специального, заранее изготовленного
пластмассового протеза нижней челюсти восстанавливают анатомическую форму
нижней челюсти спецдонора. Кожные лоскуты укладывают на место и
ушивают (рис. 25.1).
Взятый костно-пластический материал помещают в стерильный
полиэтиленовый пакет, заворачивают в стерильную простыню или полотенце и
укладывают в стерильный бикс. Стерилизацию аллотрансплантатов суставных
блоков производят в растворах антисептиков либо после упаковки
аллотрансплантатов в полиэтиленовый пакет газообразной окисью этилена или гамма-
излучением, что позволяет осуществлять нестерильную заготовку
костнопластического материала. Консервацию ортотопических аллотрансплантатов
ВНЧС (суставные блоки) и нижней челюсти осуществляют методом
замедленной лиофилизации или в растворах формалина слабой концентрации.
Непосредственно перед операцией с целью отмывания клеток жирового
костного мозга и снижения антигенности аллотрансплантата методом вакуумиро-
вания насыщают ортотопические костные аллотрансплантаты ветви с головкой
нижней челюсти или суставного блока с ветвью и частью тела нижней
челюсти (в зависимости от клинической необходимости) стерильным
изотоническим раствором натрия хлорида с антибиотиками [Шумада И. В. и др., 1979].
Для этого за 30 мин до операции костно-пластический материал
помещают в стерильный эксикатор и заливают стерильным изотоническим
раствором натрия хлорида с антибиотиками (не менее 1 000 000 ЕД), к которым
чувствительна микрофлора полости рта или зева больного. Раствор должен
покрывать всю поверхность аллотрансплантата. Целесообразно использовать
антибиотики широкого спектра действия (оксациллин, метициллин, левоми-
205
цетин, линкомицин и др.) с учетом их индивидуальной переносимости больным.
Сведения об индивидуальной переносимости и чувствительности к
антибиотикам оперируемого больного вместе с антропометрическими размерами его
лица заносят в заявку на костно-пластический материал и передают в
лабораторию консервации тканей накануне операции.
Эксикатор с находящимся в нем биоматериалом помещают в вакуумную
камеру аппарата для лиофилизации тканей и создают отрицательное
давление до 1 атм. Через 15—20 мин начинают медленно (в течение 3 мин)
уравнивать отрицательное давление воздуха в камере с атмосферным. В это время
происходит заполнение пор и каналов кости изотоническим раствором
натрия хлорида с антибиотиками. Оптимальное насыщение аллотрансплантата
достигается после трехкратного проведения процедуры.
Насыщение лиофилизированного аллотрансплантата ВНЧС
антибиотиками в изотоническом растворе натрия хлорида не только делает его стойким к
инфекции, но и уменьшает вероятность воспалительных послеоперационных
осложнений. Это позволяет одновременно осуществлять его регидратацию, что
делает пластичными элементы сустава (суставная капсула, суставной диск, связки)
и исключает возможность их повреждения при механической обработке в
процессе операции.
Разработанные методики заготовки, консервации и обработки ортото-
пических костных аллотрансплантатов дают возможность получить
полноценный биопластический материал со сниженными антигенными и высокими
биологическими свойствами.
25.5. Основные принципы и особенности аллопластики
височно-нижнечелюстного сустава
Для восстановления правильных анатомических взаимоотношений всех
элементов ВНЧС, получения полноценного сочленения и нормализации его
функции после хирургического вмешательства очень важно подобрать орто-
топический аллотрансплантат по размеру удаленной головки и части нижней
челюсти. С этой целью в процессе подготовки больного к операции
тщательно измеряют основные параметры его нижней челюсти на здоровой стороне.
Измерения производят снаружи через кожу с учетом толщины мягких тканей
лица больного.
При концевых дефектах нижней челюсти различной этиологии,
внутрисуставных и высоких переломах мыщелкового отростка с вывихом
головки нижней челюсти и деформирующих артрозах
височно-нижнечелюстного сустава основными антропометрическими данными, на которые
ориентируется хирург при подборе ортотопического аллотрансплантата
суставного конца нижней челюсти, является длина ветви и размеры головки
нижней челюсти.
Длину ветви определяют при наружном измерении здоровой стороны
непосредственно на больном. Основными параметрами головки нижней
челюсти при измерении являются переднезадний размер и кондилярная
ширина (расстояние между наиболее выступающими точками внутреннего и
наружного мыщелков головки нижней челюсти).
Ширину суставной ямки (AB) и переднезадий размер головки (A]Bj)
определяют на боковых томограммах здорового сустава в положении (при
возможности) в центральной окклюзии по методике, разработанной Н. А. Рабухиной
A966), в модификации Н. Н. Каспаровой A981) (рис. 25.2). Кондилярную
ширину головки измеряют на прямых обзорных рентгенограммах нижней че-
206
Рис. 25.2. Анализ боковых томограмм ВНЧС
(схема) [Рабухина H.A., 1966].
AB — ширина суставной ямки; A,Bj — передне-
задний размер головки нижней челюсти.
люсти больного. Полученные данные
заносят в историю болезни и
учитывают при подборе ортотопического
аллотрансплантата перед
аллопластикой ВНЧС.
Соблюдение этих условий
необходимо для восстановления
полноценной функции ВНЧС.
Несоответствие размеров головки нижней
челюсти аллотрансплантата суставной
ямке реципиента не позволит
восстановить правильные анатомические
взаимоотношения сочленяющихся
суставных поверхностей и получить
полноценный сустав, что, безусловно,
отражается на восстановлении его
функции. Уменьшение головки
нижней челюсти аллотрансплантата во
время операции путем частичной
резекции ее мыщелков нежелательно, так как неизменно повреждаются
кортикальная пластинка (при этом обнажается губчатое вещество и хрящевое
покрытие головки, что в дальнейшем может привести к деформации и рассасыванию
головки нижней челюсти).
При аллопластике ВНЧС у больных с концевыми дефектами нижней
челюсти аллотрансплантат подбирают с учетом размеров не только головки и
ветви, но и тела нижней челюсти, а также величины угла. При замещении
субтотальных дефектов нижней челюсти и суставного конца учитывают
размеры не только ветви и тела челюсти, но и подбородка.
При переломах мыщелкового отростка и деформирующих артрозах
возможно проведение первичной пластики височно-нижнечелюстного сустава —
артропластики.
Существенное отличие и один из основных принципов артропластики
височно-нижнечелюстного сустава заключаются в обязательном
восстановлении имеющихся в этих случаях суставных элементов — суставной капсулы,
суставного диска и мышечно-связочного аппарата. Необходимым условием
при этом является восстановление правильного анатомического положения
латеральной крыловидной мышцы, играющей важную роль в поступательных
движениях головки и боковых смещениях нижней челюсти. С этой целью отделяют
латеральную крыловидную мышцу с кортикальной костной пластинкой в месте
прикрепления мышцы, формируя костно-мышечный декортикат, который
затем прочно фиксируют к костному ложу в области шейки мыщелкового
отростка ортотопического аллотрансплантата суставного конца. Суставную
капсулу плотно ушивают капроновой нитью вокруг шейки аллотрансплантата.
Это способствует созданию герметизма суставной полости, восстановлению
синовиальной оболочки и продукции синовиальной жидкости.
Как показали проведенные в нашей клинике экспериментальные
исследования по изучению васкуляризации ортотопического лиофилизированного
аллотрансплантата, замещающего дефект суставного конца нижней челюсти
[Золотарева Ю. Б., 1976], сосуды суставной капсулы и латеральной крыловидной
мышцы являются одним из основных источников васкуляризации головки
нижней челюсти аллотрансплантата и влияют на ее перестройку.
Экспериментальные и клинические исследования позволили обосновать
целесообразность остеопериостальной и костно-мышечной декортикации при
207
костно-пластических операциях на нижней челюсти [Троянский И. В., 1975;
Сысолятин П. Г. и др., 1979; Левенец А. А. и др., 1979, 1984; Сысолятин П. Г.,
1984, и др.].
При аллопластике ВНЧС мы не отслаиваем жевательные мышцы от кости,
а отделяем их вместе с кортикальной пластинкой соответственно месту их
прикрепления.
Сформированные костно-мышечные лоскуты образуют хорошо васку-
ляризованное трансплантационное ложе, в которое помещают ортотопиче-
ский аллотрансплантат ветви с головкой нижней челюсти, полный суставной
блок или нижней отдел сустава и фиксируют двумя-тремя проволочными
швами по краю декортиката. Прочность крепления мышц, которую
обеспечивает костно-мышечная пластика, делает возможным в ближайшие сроки
после операции выполнение свойственной им динамической функции, что
способствует ранней функциональной реабилитации не только ВНЧС, но и
всего жевательного аппарата. Обильная и постоянная васкуляризация
воспринимающего ложа обеспечивает интенсивную перестройку
аллотрансплантата, благодаря чему органотипический регенерат формируется в более
короткие сроки, чем при обычных способах костной пластики [Троянский
И. В., Никитин Α. Α., 1982].
Успешный исход аллопластики ВНЧС зависит от плотности контакта
ортотопического аллотрансплантата с воспринимающим ложем кости
реципиента на большом протяжении. Кроме того, положение головки нижней
челюсти ортотопического аллотрансплантата при аллопластике сустава зависит
от того, как сформировано воспринимающее костное ложе.
При формировании воспринимающих площадок следует удалять кость
на половину ее толщины как на нижней челюсти реципиента, так и на
трансплантате таким образом, чтобы после наложения трансплантат стал как бы
продолжением нижней челюсти реципиента без выступов с наружной и
внутренней стороны. Наружную кортикальную пластинку аллотрансплантата перед
наложением его на воспринимающее ложе целесообразно освежать костной
фрезой, не снижая, однако, его механической прочности. Эти мероприятия
способствуют более плотному прилеганию мягких тканей к трансплантату,
быстрому врастанию мягких тканей и сосудов в аллотрансплантат, улучшают
его васкуляризацию и перестройку.
Формируя костное ложе для аллотрансплантата на наружной
поверхности ветви нижней челюсти, как правило, удаляют кортикальную пластинку не
на всю ширину ветви. Ближе к венечному отростку в направлении от
полулунной вырезки к нижнему краю челюсти через всю длину ветви создают
ступеньку, являющуюся одновременно направляющей для введения суставного конца
аллотрансплантата в суставную ямку реципиента, а также ретенционным
уступом, препятствующим ротационным смещениям аллотрансплантата. При
недостаточной глубине воспринимающей площадки на ветви во время
наложения на нее ортотопического аллотрансплантата суставного конца может
оказаться, что головка нижней челюсти аллотрансплантата выходит из
суставной ямки и располагается кнаружи от нее, в результате чего нарушается
нормальное анатомическое соотношение суставных поверхностей, а
следовательно, и функция сустава. Однако при слишком большом заглублении
можно вскрыть и ранить сосудисто-нервный пучок.
При аллопластике сустава для получения полноценного сочленения важен
хороший контакт головки нижней челюсти аллотрансплантата с суставным
диском. Не следует удалять много костной ткани в области шейки
ортотопического аллотрансплантата, так как это снижает его механическую
прочность и может привести к перелому мыщелкового отростка аллотрансплантата.
208
Не меньшее значение в исходе аллопластики височно-нижнечелюстного
сустава имеют плотная посадка и прочность фиксации аллотрансплантата к
костному ложу реципиента.
Формирование костного ложа и наложение на него аллотрансплантата мы
считаем более целесообразным осуществлять "по плоскости", а не "встык".
Аллотрансплантат фиксируют проволочными швами, костными штифтами
или ультразвуковой сваркой [Никитин Α. Α., Волков С. М., 1977]. Наиболее
стабильную и прочную фиксацию дают проволочные швы из нержавеющей
стали марки ΙΧΙ8Η9Τ или титана. При хорошей подгонке аллотрансплантата
к костному ложу и плотной посадке его швы обеспечивают надежную
фиксацию аллотрансплантата с одновременной статической компрессией.
25.6. Клинические показания и противопоказания
к аллопластике височно-нижнечелюстного сустава
Аллопластика ВНЧС — это широкое понятие, в которое входят все
реконструктивные и восстановительные вмешательства на суставе с применением
костных аллотрансплантатов. В челюстно-лицевой хирургии под
аллопластикой ВНЧС следует понимать ортотопическую аллопластику сустава, т. е.
костную пластику сустава аналогичным по форме, структуре и топическому
положению аллотрансплантатами, в том числе пересадку аллотрансплантата
суставного конца или полного сустава.
Артропластика ВНЧС заключается в устранении дефекта суставного
конца нижней челюсти с восстановлением собственных элементов сустава —
суставной капсулы, суставного диска, латеральной крыловидной мышцы и
связочного аппарата сустава. Артропластика возможна только при первичной
костной пластике у больных с доброкачественными опухолями и диспласти-
ческими процессами; при внутрисуставных и высоких переломах мыщелко-
вого отростка нижней челюсти; в ряде случаев при деформирующих артрозах
и фиброзных анкилозах ВНЧС.
В случаях костного анкилоза ВНЧС и при отсроченной костной пластике,
если имеется послеоперационный дефект суставного конца нижней челюсти
или дефект суставного конца, связанный с огнестрельным ранением,
травмой, воспалительным процессом, а также если околосуставные ткани рубцово
изменены или отсутствуют, артропластику выполнить не удается, В таких
случаях можно лишь устранить или заместить дефект концевого отдела
нижней челюсти, а если это связано с пересадкой суставного конца ортотопиче-
ского аллотрансплантата, то осуществить аллопластику
височно-нижнечелюстного сустава ортотопическим аллотрансплантатом суставного конца.
Аллопластика ВНЧС ортотопическими аллотрансплантатами показана в
следующих случаях. Первичную аллопластику с восстановлением собственных
элементов височно-нижнечелюстного сустава (артропластика) выполняют
при: 1) резекции нижней челюсти с экзартикуляцией по поводу
доброкачественных новообразований и диспластических процессов; 2)
внутрисуставных и высоких переломах мыщелкового отростка с вывихом или
повреждением головки нижней челюсти; 3) деформирующих артрозах ВНЧС, если
выявляются умеренные изменения суставной капсулы и суставного диска;
4) начальных стадиях фиброзных анкилозов ВНЧС
Первичную аллопластику ВНЧС без восстановления собственных
элементов сустава производят при: 1) застарелых переломах мыщелкового
отростка с вывихом головки нижней челюсти или отрывом ее; 2) деформирующих
артрозах с грубыми дегенеративными изменениями всех элементов сустава;
14-1263
209
3) фиброзных анкилозах ВНЧС на стадии перехода в костную форму; 4)
костных анкилозах ВНЧС; 5) врожденных дефектах мыщелкового отростка и
ветви нижней челюсти.
Отсроченная аллопластика ВНЧС показана при концевых дефектах
нижней челюсти, возникших в результате операции, травмы, воспалительного
процесса.
Противопоказаниями к аллопластике ВНЧС ортотопическими аллотранс-
плантатами являются: 1) злокачественные новообразования нижней челюсти с
метастазами в регионарные и отдаленные лимфатические узлы; 2) резекция
нижней челюсти с экзартикуляцией по поводу злокачественных опухолей
после лучевой терапии в суммарной дозе свыше 40 Гр D000 рад); 3) обширные
дефекты мягких тканей в области ВНЧС или нижней челюсти; 4)
неудовлетворительный общесоматический статус больного.
25.7. Аллопластика височно-нижнечелюстного сустава
при деформирующих артрозах
Деформирующий артроз является конечной стадией функциональной патологии
ВНЧС, возникающей при нарушении равновесия между нагрузкой на сустав
и физиологической выносливостью его тканей, в результате мелкой, но
частой травмы сустава, воспалительных и инволютивных процессов, эндокринных
и обменных нарушений [Измайлова Л. С, 1964; Каспарова Н. Н., 1978;
Егоров П. М., Карапетян И. С, 1980; Хватова В. Α., 1982; Иванов А. С, 1985, и др.].
Изменения в зубочелюстной системе в виде дефектов в зубных рядах и
аномалий прикуса приводят к нарушению синхронной функции височно-
нижнечелюстных суставов и дисфункции жевательных мышц.
Причиной артроза может явиться нарушение функции жевательных
мышц, связанное с психоэмоциональными факторами, травмой, ошибками
в протезировании.
Нередкой причиной артроза ВНЧС являются эндогенные, гормональные
или обменные нарушения. Наблюдаются случаи деформирующего артроза,
вызванного внутрисуставным введением кортикостероидов при лечении
артритов ВНЧС.
В основе патологоанатомических изменений при артрозе лежат
прогрессирующие дистрофические и некробиотические процессы в суставном хряще и
суставном диске, приводящие к деструкции и деформации костной ткани
головки нижней челюсти. Поверхность ее становится неровной, как бы изъеденной с
острыми костными разрастаниями — экзостозами, которые при движениях
нижней челюсти травмируют мягкие ткани сустава, усугубляя их деструкцию.
Заболевание начинается с появления хруста, щелканья в ВНЧС, тугоподвижности,
скованности движений нижней челюсти, особенно по утрам. Боли в суставе в
начальной стадии могут отсутствовать или возникают после длительного
разговора, пережевывания твердой пищи, простуды. Это объясняется
первоначальным поражением суставного хряща, не имеющего сосудов и нервных
окончаний. Суставная капсула и ее синовиальная оболочка вовлекаются в
патологический процесс позднее.
В дальнейшем нарушается функция ВНЧС, что выражается в
ограничении объема движений на пораженной стороне и в увеличении — на здоровой.
Движения нижней челюсти теряют плавность, становятся ступенеобразными,
отмечаются хруст, крепитация, резкая болезненность в суставах.
Нередко при деформирующем артрозе боли иррадиируют в ухо и глаз на
стороне больного сустава, возникают головная боль, парестезии слизистой
210
Рис. 25.3. Аллотрансплантат нижнего отдела ВНЧС (полусустав).
оболочки полости рта, понижение слуха, глоссалгия [Хватова В. Α., 1982;
Петросов Ю. Α., 1985]. Больные деформирующим артрозом лишены
возможности нормально говорить, принимать пищу. Как правило, они
раздражительны, постоянно акцентируют внимание на своей болезни, теряют
трудоспособность.
Рентгенологически изменения при деформирующем артрозе
характеризуются значительным сужением суставной щели, деформацией головки
нижней челюсти с уплощением ее суставной поверхности и укорочением шейки
мыщелкового отростка, склерозом субхондральной замыкательной пластинки,
наличием костных разрастаний по передней суставной поверхности,
уплощением суставной ямки и сглаживанием суставного бугорка. В тяжелых случаях
головка нижней челюсти резко деформируется, приобретая булавовидную,
грибовидную, остроконечную форму или форму крючка с изъеденной
передней поверхностью и экзостозами.
В таких случаях единственно возможным методом лечения является
хирургическое, так как любая консервативная терапия неэффективна.
При деформирующем артрозе артропластику ВНЧС ортотопическим ал-
лотрансплантатом суставного конца применяют в основном в тех случаях,
когда имеются выраженные деструктивные изменения в самой головке
нижней челюсти при неизмененном или незначительно измененном суставном
диске (мениске). Операция заключается в удалении деформированной головки
нижней челюсти с одномоментным замещением дефекта ортотопическим
лиофилизированным аллотрансплантатом суставного конца с ветвью нижней
челюсти и восстановлением собственных суставной капсулы и латеральной
крыловидной мышцы.
Для успешного исхода хирургического лечения деформирующих артрозов
необходимо выполнить следующее основное условие: при проведении
операции с целью получения полноценного в анатомо-функциональном отношении
сочленения следует восстанавливать все анатомические образования ВНЧС.
Пластику суставного диска (мениска) следует осуществлять идентичной ему
тканью, способной противостоять повышенному жевательному давлению. Для
аллопластики височно-нижнечелюстного сустава при деформирующем артрозе
целесообразно использовать ортотопический аллотрансплантат, состоящий из
суставного диска, части суставной капсулы и головки нижней челюсти с
хрящевым покрытием, т. е. половину сустава (полусустав) (рис. 25.3).
14*
211
Методика операции. Для доступа к ВНЧС используют
модификацию предушного и зачелюстного разрезов. Разрез кожи начинают на
уровне верхнего края козелка уха, т. е. в проекции головки нижней челюсти, а
затем продолжают в зачелюстную область, огибая мочку уха и угол нижней
челюсти. Длина разреза 6—8 см. Такой доступ обеспечивает хороший обзор
сустава. Послойно рассекают ткани, не выходя на ствол лицевого нерва,
отводят его кверху вместе с мягкими тканями. По возможности формируют ко-
стно-мышечный декортикат жевательной мышцы. Обнажают ВНЧС, рассекают
его капсулу и отводят ее кверху. Верхний и нижний пучки латеральной
крыловидной мышцы отслаивают от шейки мыщелкового отростка, прошивают и
берут на лигатуру. Резецируют деформированный мыщелковый отросток на
уровне его основания. Иссекают измененный суставной диск (мениск) по его
периметру и удаляют. На наружной поверхности ветви нижней челюсти
реципиента формируют воспринимающую костную площадку для
аллотрансплантата. Ортотопический аллотрансплантат нижнего отдела сустава (полусустав),
представленный суставным диском, нижней частью капсулы сустава, головкой
и ветвью нижней челюсти, моделируют по размеру дефекта и профилю
воспринимающей костной площадки на ветви нижней челюсти. После
тщательной подгонки аллотрансплантата и удаления излишков мягких тканей в
области капсулы и суставного диска 4—6 длинными лигатурами из тонкого капрона
или лавсана прошивают суставной диск аллотрансплантата полусустава по
периметру. Затем, используя эти же лигатуры, прошивают суставную капсулу
больного в том месте, где к ней прикрепляется удаленный мениск (рис. 25.4).
212
Рис. 25.5. Этапы операции аллопластики ВНЧС при деформирующем артрозе.
а — погружение аллотрансплантата полусустава в рану; б — аллотрансплантат в ране перед
фиксацией его к костному ложу.
Одной из передних лигатур прошивают капсулу и верхний пучок
латеральной крыловидной мышцы, фиксируя его к суставному диску
аллотрансплантата. Используя лигатуры, верхний конец аллотрансплантата —
суставной диск погружают на место его естественного расположения и там
фиксируют, завязывая лигатуры. Нижнюю челюсть фиксируют в
правильном прикусе с помощью назубных шин или лигатурных повязок. Капсулу
сустава вместе с нижним пучком латеральной крыловидной мышцы
ушивают вокруг шейки мыщелкового отростка аллотрансплантата.
Окружающие сустав мягкие ткани плотно обшивают вокруг капсулы, создавая
мышечный футляр. Нижний конец аллотрансплантата помещают на
воспринимающую костную площадку (рис. 25.5). Излишки
аллотрансплантата срезают дисковой фрезой. Фиксацию аллотрансплантата к костному
ложу осуществляют проволочными швами. После завершения всех этапов
операции рану послойно ушивают. На 1—2 сут в ней оставляют резиновый
дренаж.
В 1-е сутки иммобилизацию нижней челюсти не выполняют, поскольку
213
Рис. 25.6. Томограмма правого (а) и левого (б) ВНЧС больного деформирующим
артрозом до операции. Недоразвитие и деформация головок нижней челюсти, суставная ямка
не выражена.
возможны рвота после наркоза и связанная с этим опасность аспирацион-
ной асфиксии, а затем снова осуществляют, но не более чем на 7—10 дней
(рис. 25.6, 25.7).
25.8. Аллопластика височно-нижнечелюстного сустава при анкилозах
Анкилозы ВНЧС характеризуются частичной или полной неподвижностью
нижней челюсти, обусловленной патологическими изменениями в суставе.
В зависимости от характера этих изменений анкилозы делят на фиброзные
и костные. Патологические изменения в суставе при фиброзном анкилозе
связаны с деструкцией хрящевой ткани суставных поверхностей и суставного
диска вплоть до полного исчезновения хряща и замещения суставного
пространства плотной фиброзной тканью, которая в дальнейшем может осси-
фицироваться. При костном анкилозе образуется костное сращение головки
нижней челюсти с суставной ямкой височной кости. При этом развивается
деформация головки нижней челюсти и мыщелкового отростка. Иногда мы-
щелковый и венечный отростки срастаются, образуя массивный костный
конгломерат, занимающий скуловую дугу, верхнюю челюсть, и
распространяющийся к основанию черепа. Происходит значительное уменьшение
полулунной вырезки или полное заращение ее.
Различают односторонние и двусторонние анкилозы ВНЧС в зависимости
от того, занимают ли костные разрастания всю суставную щель или только
часть ее (частичные и полные).
Патологические изменения в суставах могут возникнуть в результате
родовой травмы, инфекционных заболеваний, воспалительного процесса
среднего уха, остеомиелита и внутрисуставных и высоких внесуставных
переломов мыщелкового отростка.
В зависимости от того, в каком возрасте начал развиваться анкилоз,
появляются функциональные и косметические нарушения различной сте-
214
Рис. 25.7. Ортопантомограмма (а) нижней челюсти и внешний вид (б, в) больного
через 1 мес после операции.
а — мыщелковые отростки и анатомическая форма суставных головок нижней челюсти
восстановлены аллотрансплантатами полусустава; б — открывание рта без затруднений; в — проведено
функциональное протезирование.
пени. При возникновении анкилоза в раннем детском возрасте, помимо
нарушения функции приема пищи и речи, развиваются вторичные дефор-
мации всего костного скелета лица, приводящие к его обезображиванию.
Они заключаются в недоразвитии нижней челюсти (микрогнатия),
деформации прикуса и всей нижней трети лица (так называемый птичий
профиль). Такие больные становятся замкнутыми, сторонятся окружающих,
стесняются своего внешнего вида. Пищу в жидком виде они всасывают
через межзубные промежутки и дефекты зубного ряда или протирают ее
через зубы пальцами. Все это приводит к значительным изменениям
психики.
215
Успешное комплексное лечение гнойно-воспалительных и септических
процессов способствовало уменьшению количества осложнений,
приводящих к анкилозу ВНЧС. Однако в последние годы на фоне технического
прогресса, развития автомобилизма значительно увеличилось число
повреждений челюстно-лицевой области и сочетанных травм в результате дорожно-
транспортных происшествий, приводящих к различным осложнениям, в том
^сле к анкилозу ВНЧС.
; Проблема лечения анкилозов височно-нижнечелюстного сустава
является одной из наиболее сложных и актуальных проблем челюстно-лицевой
хирургии. Об этом свидетельствует тот факт, что разработкой методов
лечения этой патологии специалисты многих стран занимаются свыше 130 лет.
Первоначально хирургическое лечение анкилоза
височно-нижнечелюстного сустава заключалось в простом линейном рассечении или иссечении
участка кости в различных отделах нижней челюсти с целью восстановления
ее подвижности [Склифосовский Н. В., 1881; Сарычев И. Д., 1894; Березне-
говский Н. И., 1914;РауэрА. Э., 1928; Львов П. П., 1936; Rizolli Р., 1857; Bot-
tini J., 1872; Richet M., 1950, и др.]. Такие операции почти всегда
заканчивались рецидивом анкилоза. Они еще больше нарушали прикус и усугубляли
деформацию нижней челюсти.
Позднее для устранения анкилоза была использована идея интерпозиции
различных органических и неорганических материалов между фрагментами
кости после остеотомии: применяли жевательную мышцу на питающей
ножке, свободную пересадку жировой клетчатки, хряща, широкую фасцию
бедра, лоскут из ягодичной мышцы, надкостницу, биопластмассу, а также
прокладки и колпачки, которые плотно насаживали на нижний фрагмент ветви
нижней челюсти [Орлов Л. В., 1899; Мыш В. М, 1914; Рауэр А. Э., 1928;
ЛимбергА. Α., 1938; Михельсон Η. Η., 1950; Медведев П. М., 1953, 1957; Фи-
алковский В. В., 1956; Рудько В. Ф., Каспарова Н. Н., 1956; Семенченко Г. И.,
1956; Иванов А. Ф., 1959; КиняпинаИ. Д., 1960; Митрофанов Г. Г., 1961; Ве-
noit J., 1962; Palfer-Solliez Μ., 1968, и др.].
Однако анализ отдаленных результатов показал, что ни один из
предложенных пластических материалов и способов оперативного лечения не
отвечал в полной мере требованиям, предъявляемым к трансплантатам. Аутоткани
в биологическом отношении являются наиболее полноценными, но не
обладают необходимыми физическими свойствами. При движениях нижней
челюсти они разминались костными фрагментами, смещались, атрофировались,
превращались в рубцовую ткань. Металлические же и пластмассовые
прокладки и колпачки, являясь инородными материалами, не приживали и
вызывали бурное реактивное разрастание костной ткани, что приводило к рецидиву
анкилоза [Каспарова Н. Н., 1970; Плотников Η. Α., 1979; Каспарова Н. Н.
и др., 1981].
С целью подавления регенерации костной ткани и предупреждения
рецидивов анкилоза применяли методы химической и термической обработки
костных фрагментов [Великанова М. М., 1956; Алкалаева К. К., Петрова Т. Α.,
1959; Дмитриева В. С, Месина В. М., 1964; Вернадский Ю. Α., 1973]. Однако
все эти методы не избавляли от рецидивов анкилоза и были направлены лишь
на создание ложного сустава с целью восстановления подвижности нижней
челюсти любым путем. Устранению деформации нижней челюсти,
сопутствующей анкилозу, не придавали значения. Как правило, такие операции
проводили в том возрасте, когда заканчивался рост костей лицевого скелета.
По мере накопления практического опыта и усовершенствования
методов оперативного лечения анкилоза был сделан вывод о необходимости
раннего комплексного лечения анкилоза ВНЧС с одновременным исправлением
216
недоразвития нижней челюсти [Лимберг Α. Α., 1950; Медведев П. М., 1953;
Титова А. Т., 1961; Лукьяненко В. Α., 1963; Плотников Η. Α., 1967; Кузьмен-
ко В. Ф., 1967; Иоаннидис Г. П., 1970; Вернадский Ю. И., 1973; Бернадская-Ми-
хайлик Г. П., 1980; Каспарова Н. Н., 1981; Michelet F. etal., 1973; Delaire J., 1976],
В дальнейшем для замещения удаленной части кости стали применять
костные и хрящевые ауто- и аллотрансплантаты с суставной поверхностью [Пе-
терсон Б. Е., 1960; Мелехов В. Г., 1965; Плотников Η. Α., 1968; Савицкий В. Α.,
1968; Никандров А. М., 1969; Савицкий В. Α., Никитин Α. Α., 1971;
Каспарова Η. Η., 1978;TajimaS. etal., 1978; MatukasV. etal., 1980; TasanenA., 1985].
Это способствовало не только устранению недоразвития нижней челюсти и
созданию подвижности ее, но и формированию приближающегося к
суставному сочленения, что улучшало функциональные результаты.
Последнее десятилетие характеризуется разнообразием методов
хирургического лечения анкилозов: от иссечения участка кости с последующим
вытяжением и ранней функцией [Rajgopal Α. et al., 1983; Мегсіег J., Delaire J.,
1983; Kraszewski J. et al., 1985; Adekeue E., 1985], с интерпозицией между
костными фрагментами силиконовых и силастиковых имплантатов [Convers J.,
1979; lonsson Ε. et al., 1985], с применением колпачков из серебряно-палла-
диевого сплава [Максудов М. М., Драновский Г. Е,, 1981], дистракционных
аппаратов [Вернадский Ю. И. и др., 1985] до использования протезов мы-
щелкового отростка [Spiesse В., 1985; Heps Η. et al., 1985; Bjoraland J. et al,
1985] и тотальных протезов ВНЧС [Michelet F., 1973; Kumoona R., 1978; Son-
nenburg J., Sonnenburg M., 1980, и др.]. Такое разнообразие методик,
применяемых различными авторами при хирургическом лечении анкилозов ВНЧС,
свидетельствует о том, что эта проблема не решена. Продолжается разработка
новых, более эффективных методов хирургического лечения анкилозов.
Наиболее стабильные функциональные и косметические результаты у
больных анкилозом ВНЧС были получены после того, как Н. А. Плотников
и А. М. Ткаченко A966) предложили использовать для восстановления
подвижности нижней челюсти и устранения ее деформации ортотопический ал-
лотрансплантат ветви с головкой нижней челюсти, консервированный
методом лиофилизации. Операция заключается в пересадке суставного конца
вместе с частью ветви или тела ортотопического аллотрансплантата нижней
челюсти (в зависимости от степени микрогнатии) в дефект кости после
остеотомии костных фрагментов и максимального удаления костного
конгломерата с одновременным формированием суставной ямки в верхнем отделе
костного конгломерата на уровне ее естественного расположения (рис. 25.8).
Данная методика операции позволила: 1) отказаться от многоэтапных,
тяжелых хирургических вмешательств по устранению анкилоза и нижней
микрогнатии; 2) создать подвижное сочленение, приближающееся к
нормальному суставу на уровне его естественного расположения, что очень
важно для нормального функционирования здорового сустава при
односторонних анкилозах, а при двусторонних — получить хорошую дистальную опору
для нижней челюсти и мышечного комплекса всего жевательного аппарата;
3) улучшить функциональный и косметический результаты лечения,
уменьшить рецидивы анкилоза.
Однако, несмотря на бесспорные преимущества этого способа
хирургического лечения анкилоза, он не дает возможности получить оперативным
путем полноценный в анатомо-структурном и функциональном отношении
ВНЧС с восстановлением не только хрящевого покрытия головки нижней
челюсти, но и суставной ямки, целости суставной капсулы, суставного диска
и мышечно-связочного комплекса, что отражается на функции
новообразованного сустава и результатах хирургического лечения.
217
Рис. 25.8. Этапы пересадки ортотопического аллотрансплантата суставного конца
при анкилозе ВНЧС (а — е) (схема) [Плотников H.A., Ткаченко A.M., 1970].
Наиболее перспективным является другой способ хирургического
лечения анкилоза ВНЧС [Плотников Η. Α., Никитин Α. Α., 1981]. Он заключается
в том, что с целью получения стойкой и полноценной функции
новообразованного оперативным путем сустава и предотвращения рецидивов анкилоза
после остеотомии костных фрагментов и удаления костного конгломерата в
образовавшийся дефект на специально сформированные воспринимающие
костные площадки пересаживают ортотопический аллотрансплантат ВНЧС со
всеми его анатомическими образованиями — суставной ямкой с частью
височной кости и суставным покрытием, головкой нижней челюсти, суставным
диском, капсулой и интеркапсулярными связками (суставной блок).
Клиническими показаниями к применению методики аллотранспланта-
ции консервированных полных височно-нижнечелюстных суставов
являются костные и особенно многократно рецидивирующие анкилозы височно-
нижнечелюстного сустава.
Наличие, как правило, обширного костного конгломерата в области
сустава при этом виде анкилоза позволяет сформировать хорошую
воспринимающую костную площадку для верхнего отдела аллотрансплантата суставного
блока, представленного частью височной кости с суставной ямкой ВНЧС.
При фиброзных анкилозах, когда суставная ямка хорошо выражена, но
изменена структура суставного диска и головки нижней челюсти, пересадку
полного суставного блока производить нецелесообразно. В этих случаях
проводят аллотрансплантацию консервированного полусустава, включающего
нижний отдел сустава с суставным диском.
218
Хирургическое лечение анкилоза височно-нижнечелюстного сустава —
дело довольно сложное и травматичное. В связи с этим у больных с
анкилозом операции проводят, как правило, под общим обезболиванием.
Применяют эндотрахеальный наркоз с интубацией через нос. Если больной не
может открыть рот, то интубационную трубку вводят в трахею "вслепую" или,
чаще всего, с помощью эндоскопической аппаратуры.
Методика операции. Доступ к анкилозированному ВНЧС
осуществляют разрезом, который начинают на уровне верхнего козелка уха, ведут
впереди мочки, затем продолжают в зачелюстной области, окаймляя угол
нижней челюсти. Длина разреза 6—8 см. Послойно рассекают кожу,
подкожную жировую клетчатку, поверхностную мышцу шеи, обнажают задний и
нижний края нижней челюсти.
Восстановление функции жевательного аппарата зависит от состояния
жевательных мышц. С этой целью мышцы от кости целесообразно не отслаивать, а
отделять вместе с кортикальными пластинками (соответственно месту их
прикрепления), формируя таким образом костно-мышечные лоскуты (декортикаты).
Для этого по нижневнутреннему краю нижней челюсти в области
прикрепления жевательной и внутренней крыловидной мышц
сухожильно-мышечные волокна этих мышц вместе с надкостницей рассекают до кости и
осторожно отслаивают распатором только по краю нижней челюсти. Костной
фрезой с помощью бормашины распиливают кортикальный слой кости по
заднему и нижнему краям нижней челюсти, а также по передней границе
жевательной мышцы. Широким тонким долотом по линиям остеотомии
кортикальную костную пластинку вместе с жевательной мышцей отделяют и
отводят кверху. При этом избегают травмы мышечных волокон. Специальным
костным трепаном производят остеотомию ветви нижней челюсти в ее
верхней трети как можно ближе к месту естественного расположения сустава.
Уровень пересечения ветви зависит от характера и распространения
патологических изменений в кости. При фиброзных или костных сращениях
головки нижней челюсти с суставной ямкой остеотомию осуществляют на уровне
шейки или основания мыщелкового отростка нижней челюсти. При
распространении костных разрастаний на мыщелковый и венечный отростки
производят остеотомию ветви нижней челюсти в верхней ее трети. Ветвь нижней
челюсти после остеотомии смещают вниз и приступают к удалению костного
конгломерата (рис. 25.9).
Как правило, удаление его, особенно если он представлен мощной
костью компактного строения, осуществляют постепенно с помощью костной
фрезы и долота. Предел удаления патологически измененной кости зависит
от уровня естественного расположения сустава. Следует отметить, что
работать долотом близко к основанию черепа небезопасно, особенно у лиц
молодого возраста, так как можно вскрыть полость черепа — среднюю
черепную ямку. Об этом можно судить по истечению в рану цереброспинальной
жидкости, имеющей светло-желтый цвет. Выполнив остеотомию ветви и
удалив большую часть костного конгломерата, работают только костными
фрезами. Затем после максимально возможного удаления костного конгломерата
в оставшейся его части на уровне естественного расположения сустава и на
наружной поверхности оставшегося фрагмента ветви нижней челюсти
формируют воспринимающие костные площадки для аллотрансплантата полного
ВНЧС (суставной блок) со всеми его анатомическими образованиями.
Формируя костные площадки, фрезой снимают слой кости на толщину
аллотрансплантата, но обязательно до вскрытия губчатого вещества или
появления кровоточащих точек.
Необходимо тщательно сгладить все острые края кости, а также удалить
219
Рис. 25.9. Аллопластика ВНЧС при его анкилозе с вовлечением мыщелкового и
венечного отростков нижней челюсти аллотрансплантатом суставного блока с костно-
мышечной декортикацией (схема).
а — костный анкилоз; б — удален костный конгломерат, сформированы воспринимающие
площадки и костно-мышечный декортикат жевательной мышцы; в — положение аллотрансплантата
суставного блока ВНЧС; г — фиксация аллотрансплантата суставного блока и костно-мышечного
декортиката жевательной мышцы проволочными швами.
костные разрастания и шипы на внутренней поверхности фрагмента ветви
нижней челюсти, где нередко можно встретить костный тяж, представляющий
собой оссифицированные клиновидно-нижнечелюстную и шилонижнечелю-
стную связки. Только после пересечения этого костного тяжа становятся
возможны свободное перемещение нижней челюсти и открывание рта до нормы.
Затем аллотрансплантат полного височно-нижнечелюстного сустава с
ветвью или частью тела нижней челюсти (в зависимости от выраженности
микрогнатии), предварительно насыщенный антибиотиками и регидратиро-
ванный в вакууме, тщательно моделируют по размеру дефекта и профилю
воспринимающих костных площадок.
220
Рис. 25.10. Аллопластика ВНЧС при анкилозе в области мыщелкового отростка (схема).
а— костный анкилоз без распространения на венечный отросток; б — удален костный
конгломерат, сформирован костно-мышечный декорт и кат жевательной мышцы, отсечен венечный
отросток с височной мышцей; в — положение аллотрансплантата суставного блока (венечный
отросток с височной мышцей фиксированы); г — уложен и фиксирован костно-мышечный
декортикоит жевательной мышцы.
Верхний отдел его, представленный частью височной кости с суставной
ямкой, помещают на воспринимающую костную площадку так, чтобы он
точно и плотно совпадал с ней, а нижний — между костно-мышечными де-
кортикатами. Фиксацию ортотопического аллотрансплантата ВНЧС
осуществляют проволочными швами. При точной подгонке и плотной посадке на
воспринимающее ложе верхнего отдела аллотрансплантата сустава фиксацию
его к ложу проволочными швами мы не производим. Однако во всех случаях
обязательно подшивать окружающие мягкие ткани к суставной капсуле
аллотрансплантата так, чтобы создать хороший мышечный футляр, плотно
окружающий ее со всех сторон.
При наличии сопутствующей нижней микрогнатии перед фиксацией
аллотрансплантата нижнюю челюсть максимально выводят вперед и к средней
линии, затем под контролем прикуса фиксируют к вехней челюсти с помощью
заранее изогнутых бимаксиллярных шин и резиновых колец или лигатурных
221
Рис. 25.11. Рентгенограммы больного анкилозом правого ВНЧС до (а) и после (б)
операции.
а — томограмма правого ВНЧС. Костное сращение мыщелкового и венечного отростков с
основанием черепа; б — ортопантомограмма. Суставной блок и костно-мышечный декортикат
жевательной мышцы фиксированы проволочными швами.
повязок. У лиц молодого возраста в период незаконченного роста лицевого
скелета нижнюю челюсть устанавливают с некоторой гиперкоррекцией в
здоровую сторону, учитывая ее рост.
Важным моментом, особенно при устранении недоразвития нижней
челюсти являются перемещение и фиксация жевательных мышц в новом
положении, обеспечивающем их нормальное физиологическое натяжение. Для
этого выдвигают вперед нижнюю челюсть и фиксируют жевательные мышцы
ближе к заднему краю ветви, не изменяя их длины.
При анкилозе только мыщелкового отростка нижней челюсти очень
важно сохранить функцию височной мышцы, имеющей большое значение в
222
жевательной функции. С этой целью венечный отросток пересекают у
основания, а затем фиксируют к венечному отростку ортотопического
аллотрансплантата ВНЧС, взятого с ветвью и венечным отростком нижней челюсти.
Фиксацию венечного отростка реципиента с височной мышцей к аллотранс-
плантату осуществляют с учетом величины перемещения нижней челюсти
(рис. 25.10).
После завершения всех этапов операции рану послойно ушивают.
Антибиотик не вводят, так как предварительное насыщение аллотрансплантата
антибиотиками с учетом чувствительности к ним микрофлоры полости рта
больного позволяет создать в ране на длительное время антисептический фон
благодаря депонированию антибиотика в губчатом веществе
аллотрансплантата. Для профилактики образования гематомы на 1—2 дня оставляют в ране
резиновый дренаж.
Иммобилизацию нижней челюсти в послеоперационном периоде
осуществляют с помощью бимаксиллярных шин с резиновой тягой, лигатурных
повязок или внутриротовых ортопедических аппаратов. Специального
вытяжения нижней челюсти не требуется, так как она удерживается в нужном
положении за счет жесткости костной части аллотрансплантата.
Несмотря на наиболее благоприятные условия для перестройки костного
аллотрансплантата суставного блока и восстановления функции жевательных
мышц, не всегда удается произвести костно-мышечную пластику с
формированием костно-мышечных декортикатов. Это связано с тем, что при анкилозах,
особенно сопровождающихся недоразвитием нижней челюсти, в области
прикрепления жевательных мышц имеется характерная деформация угла нижней
челюсти в виде сапожка, или так называемой петушиной шпоры, не
позволяющая сформировать полноценный костно-мышечный декортикат. В таких
случаях осуществляют отслойку мышц от кости по известной методике.
При двусторонних анкилозах операцию производят одновременно с
обеих сторон. Если анкилоз сочетается с нижней микрогнатией или
открытым прикусом, то устранить эти деформации легче при оперативном
вмешательстве на обоих суставах.
При односторонних анкилозах, сочетающихся с резко выраженным
недоразвитием нижней челюсти, для устранения микрогнатии только
выдвижения нижней челюсти на стороне анкилозированного сустава иногда
недостаточно. В таких случаях, помимо аллопластики сустава и удлинения
ветви и тела нижней челюсти аллотрансплантатом на стороне операции, на
другой стороне выполняют плоскостную остеотомию нижней челюсти, что
позволяет максимально выдвинуть нижнюю челюсть вперед и полностью или
частично устранить нижнюю микрогнатию (рис. 25.11—25.15).
25.9. Аллопластика височно-нижнечелюстного сустава
при переломах мыщелкового отростка нижней челюсти
Переломы мыщелкового отростка нижней челюсти занимают значительное
место среди повреждений лицевого скелета и, по данным различных авторов,
составляют от 7,4 до 56 %.
Переломы мыщелкового отростка нижней челюсти неогнестрельного
происхождения в большинстве случаев являются отраженными, возникшими
в результате удара в область подбородка или тела нижней челюсти с
противоположной стороны. Прямые переломы мыщелкового отростка, связанные
непосредственно с приложением травмирующей силы, встречаются
значительно реже, так как мыщелковый отросток хорошо защищен костными об-
223
Рис. 25.12. Больной через 1 мес после устранения анкилоза и пересадки аллотранс-
плантата суставного блока ВНЧС.
а — открывание рта свободное; б— в поднижнечелюстной области послеоперационный рубец не виден.
Рис. 25.13. Больная с анкилозом правого ВНЧС и нижней микрогнатией до операции.
а — резкая асимметрия лица, открывание рта невозможно; б — недоразвитие нижней челюсти.
Рис. 25.14. Томограммы правого сустава больной с анкилозом ВНЧС до операции (о),
через 1 мес (б) и через 3 года после операции с закрытым (в) и открытом (г) ртом.
а — костное сращение в области сустава; б — аллотрансплантат суставного блока; в, г — томограммы
правого ВНЧС через 3 года после пересадки суставного блока, функция и анатомическая форма
сустава восстановлены полностью.
Рис. 25.15. Внешний вид (а, б) и открывание
рта (в) у больной через 3 года после артро-
пластики правого ВНЧС ортотопическим
аллотрансплантатом суставного блока.
а, б— деформация лица устранена; в —
открывание рта, движения в суставе восстановлены.
Рис. 25.16. Рентгенограмма. Двусторонний внутрисуставной перелом головок нижней
челюсти.
разованиями. Переломы мыщелкового отростка бывают в основном закрытыми,
реже — открытыми. При открытых переломах, как правило, повреждается
костная стенка наружного слухового прохода. Кроме того, переломы
мыщелкового отростка могут быть односторонними, двусторонними,
изолированными, а также в сочетании с повреждениями других отделов нижней челюсти и
костей лицевого скелета. В зависимости от направления линии перелома и
количества отломков они могут быть косыми, скользящими, оскольчатыми и др.
В клинической практике наиболее целесообразно пользоваться
классификацией, основанной на клинико-анатомической картине переломов
мыщелкового отростка нижней челюсти. В соответствии с этой классификацией
следует различать: 1) переломы головки нижней челюсти, или так
называемые внутрисуставные переломы; 2) переломы шейки мыщелкового отростка
нижней челюсти, или высокие внесуставные переломы; 3) переломы
основания мыщелкового отростка нижней челюсти.
Все перечисленные виды переломов мыщелкового отростка могут
сопровождаться разрывом суставной капсулы и вывихом головки нижней
челюсти, поэтому могут быть с вывихом и без вывиха головки.
Общими клиническими симптомами для всех видов переломов
мыщелкового отростка, особенно в случаях острой травмы, являются боли и хруст
в суставе, ограничение движений нижней челюсти, невозможность
нормального приема пищи. К наиболее трудно диагностируемым видам переломов
мыщелкового отростка относятся переломы собственно головки нижней
челюсти, или внутрисуставные переломы (рис. 25.16).
Чаще линия перелома проходит в косом направлении через основание
головки нижней челюсти и выходит за границу прикрепления суставной
капсулы. В этих случаях происходит разрыв суставной капсулы и малый
фрагмент под действием травмирующей силы и тяги латеральной крыловидной
мышцы выходит из суставной ямки и смещается за суставной бугорок, т. е.
возникает его вывих (рис. 25.17). Ветвь нижней челюсти укорачивается в
результате того, что больший фрагмент (ветвь нижней челюсти) за счет тяги
жевательных мышц смещается кзади и кверху и острыми краями травмирует
15*
227
Рис. 25.17. Рентгенограмма. Перелом
головки нижней челюсти с вывихом малого
фрагмента.
суставной диск. Прикус в этих
случаях почти не нарушается. При
открывании рта девиация нижней
челюсти в больную сторону также
незначительна.
При внутрисуставных
переломах, когда линия перелома проходит
через средний или верхний отделы
головки нижней челюсти,
образуется очень маленький фрагмент,
который под действием травмирующей
силы смещается в полость сустава и
остается в ней. Больные могут
предъявлять жалобы только на некоторое
ограничение открывания рта и хруст
в суставе. Прикус не нарушается,
боковые движения нижней челюсти
сохранены.
Переломы шейки мыщелкового
отростка в верхнем ее отделе, на
границе или несколько ниже
прикрепления суставной капсулы и
латеральной крыловидной мышцы
называются высокими внесуставны-
ми переломами мыщелкового
отростка и сопровождаются разрывом
суставной капсулы,
травмированием волокон латеральной
крыловидной мышцы, вывихом головки
нижней челюсти из суставной ямки и
смещением ее за суставной бугорок
(рис. 25.18). Нередко малый
фрагмент (головка нижней челюсти)
располагается почти перпендикулярно
большому фрагменту и ущемляется
между ним и основанием черепа.
Переломы в среднем и нижнем
отделах шейки мыщелкового
отростка также могут сопровождаться
разрывом суставной капсулы и вывихом
головки нижней челюсти из
суставной ямки. Клиническая
симптоматика этого вида переломов
складывается из жалоб больного на боли и
хруст в области сустава, нарушение
прикуса, затруднение открывания
рта, выраженное смещение нижней
челюсти в больную сторону при
открывании рта. При вывихе головки
нижней челюсти пальпаторно
определяется западение мягких тканей в
области сустава, движение головки
отсутствует. При двустороннем пе-
Рис. 25.18. Рентгенограмма. Перелом шейки
мыщелкового отростка с вывихом головки
нижней челюсти.
228
Рис. 25.19. Рентгенограмма. Перелом шейки мыщелкового отростка (я, б) с вывихом
головки нижней челюсти (Т-образный перелом).
реломе шейки мыщелкового отростка с вывихом головок отмечаются открытый
прикус в области фронтальной группы зубов, невозможность боковых движений
нижней челюсти в связи с полным выключением из функции обеих
латеральных крыловидных мышц. Положение малого фрагмента — головки нижней
челюсти зависит от силы травмирующего момента и степени сокращения
латеральной крыловидной мышцы. В некоторых случаях головка нижней
челюсти может сместиться кнутри от суставной поверхности, а линия излома —
кнаружи и вместе с большим фрагментом, ветвью нижней челюсти
составлять букву Т. В таких случаях впереди козелка уха пальпаторно определяется
край излома малого фрагмента (рис. 25.19).
При переломах основания мыщелкового отростка нижней челюсти
линия перелома проходит через его основание от полулунной вырезки к
заднему краю ветви нижней челюсти. В зависимости от направления линии
перелома различают поперечные, косые и скользящие переломы мыщелкового
отростка. Кроме того, они могут сопровождаться разрывом суставной
капсулы и вывихом головки нижней челюсти (рис. 25.20).
Больные предъявляют жалобы на боли, крепитацию в суставе, затруднение
открывания рта, невозможность приема пищи. Характерно нарушение прикуса
вследствие укорочения высоты ветви нижней челюсти — разобщение на
здоровой стороне на величину смещения костных фрагментов и плотный контакт
на стороне перелома, а также двухмоментное смыкание зубов-антагонистов (на
стороне повреждения раньше, чем на здоровой). При открывании рта
нижняя челюсть отклоняется в сторону перелома, боковые движения в здоровую
229
сторону резко ограничены или
невозможны. При двусторонних переломах
основания мыщелкового отростка
жевательная функция значительно
нарушается вследствие дистального
смещения нижней челюсти и
образования открытого прикуса во
фронтальном отделе.
В своевременной диагностике
переломов мыщелкового отростка
наряду со знанием клинической
симптоматики большое значение имеет
рентгенологическое исследование,
которое необходимо проводить в
двух взаимно перпендикулярных
проекциях — прямой и боковой.
В связи с тем что традиционные
рентгенограммы по Шуллеру и
Парма сложны для расшифровки из-за
наложения теней соседних отделов
костей черепа, при переломах
мыщелкового отростка наиболее
целесообразным следует считать
томографическое исследование или зонографию
ВНЧС. Смещение малого отломка
Рис. 25.20. Рентгенограмма. Перелом ос- кнутри или кнаружи от линии пе-
нования мыщелкового отростка с выви- релома более отчетливо определя-
хом и ротацией малого фрагмента. ется на обзорных рентгенограммах
нижней челюсти в прямой
проекции.
В настоящее время в лечении больных с переломами мыщелкового
отростка, сопровождающимися вывихом или повреждением головки нижней
челюсти, определились два основных направления —
консервативно-ортопедическое и хирургическое. Сущность первого направления заключается в том,
чтобы с помощью различных назубных шин и ортопедических аппаратов ре-
понировать отломки в правильное положение и удержать их в таком
соотношении до образования костной мозоли.
При свежих переломах основания шейки мыщелкового отростка нижней
челюсти возможно проведение остеосинтеза костным штифтом из аллотранс-
плантата кортикальной пластинки малоберцовой кости [Чернус Л. Α., 1978;
Плотников Н. А. и др., 1979] (рис. 25.21, 25.22). Если остеосинтез выполнить
невозможно, то осуществляют артропластику ВНЧС.
При выборе показаний к хирургическому лечению переломов
мыщелкового отростка методом артропластики учитывают вариабельность и
сложность клинической симптоматики, а также данные рентгенологического
обследования.
Артропластика ВНЧС ортотопическим аллотрансплантатом суставного
конца и ветви нижней челюсти показана при:
1) внутрисуставных переломах мыщелкового отростка с вывихом
головки нижней челюсти;
2) высоких внесуставных переломах шейки мыщелкового отростка с
вывихом головки нижней челюсти;
230
Рис. 25.21. Остеосинтез костным штифтом перелома мыщелкового отростка с
вывихом головки нижней челюсти (схема).
а — перелом шейки мыщелкового отростка с вывихом малого фрагмента; б — отломки фиксированы
костным штифтом.
3) косых и оскольчатых переломах шейки мыщелкового отростка с
повреждением головки нижней челюсти;
4) застарелых переломах мыщелкового отростка с вывихом головки
нижней челюсти.
Методика операции. Артропластика ВНЧС ортотопическим ал-
лотрансплантатом суставного конца технически не сложна и выполняется
следующим образом.
• б
Рис. 25.22. Рентгенограмма. Перелом мыщелкового отростка до (а) и после (б) остео-
синтеза костным штифтом.
231
Доступ к ВНЧС осуществляют из зачелюстного разреза, который
начинают от мочки уха и продолжают в зачелюстной области, окаймляя угол
челюсти, отступая 1,5 см от заднего и нижнего края нижней челюсти. Длина
разреза 5—6 см.
Ткани рассекают послойно. Обнажают задний край и угол нижней
челюсти вместе с прикрепляющимися жевательной и внутренней крыловидной
мышцами. Разрезами по заднему и нижнему краям челюсти острым
скальпелем рассекают сухожилия этих мышц и надкостницу и отделяют их
распатором только в области края челюсти.
Костной фрезой распиливают кортикальную пластинку по краю нижней
челюсти, а также по передней и задней границам жевательной мышцы.
Широким тонким долотом и молотком разделяют наружную и внутреннюю
кортикальные пластинки по линиям распила, формируя таким образом костно-
мышечный декортикат жевательной мышцы, который берут на лигатуры и
отводят кверху. Внутреннюю крыловидную мышцу не отделяют. В случае
невозможности сформировать костно-мышечный декортикат жевательной мышцы
в связи с анатомическими особенностями ветви нижней челюсти в этой
области (слишком тонкая или изогнутая ветвь, выраженная бугристость в области
прикрепления жевательной мышцы и др.) распатором отслаивают
жевательную мышцу вместе с надкостницей до линии перелома мыщелкового отростка.
Если перелом внутрисуставной и малый фрагмент находится в полости
сустава и целость капсулы не нарушена, что бывает крайне редко (за много
лет мы наблюдали всего один случай), то капсулу сустава рассекают, берут
на лигатуры и отводят кверху. Малый фрагмент (осколок головки нижней
челюсти) удаляют из полости сустава. Если есть возможность, то формируют
костно-мышечный декортикат латеральной крыловидной мышцы или
отслаивают ее и берут на лигатуры. Производят резекцию оставшегося
фрагмента мыщелкового отростка с вывихом головки на уровне его основания,
после чего приступают к формированию воспринимающей костной площадки
на наружной поверхности ветви нижней челюсти.
При высоких внесуставных переломах шейки мыщелкового отростка с
вывихом головки нижней челюсти после обнажения линии перелома
первоначально производят резекцию оставшейся части мыщелкового отростка на
уровне его основания, так как это значительно облегчает поиск вывихнутой
головки нижней челюсти, которая бывает смещена кнутри или кпереди от
ветви или при застарелых переломах замурована рубцовой тканью.
Найденную головку нижней челюсти захватывают специальным фиксатором или
зажимом, выделяют из рубцов, отделяют латеральную крыловидную мышцу и
удаляют головку. Все это следует делать осторожно, избегая травмы
суставного диска. При разрывах и рубцовых изменениях суставного диска его удаляют.
В последнем случае дефект мыщелкового отростка замещают ортотопическим
аллотрансплантатом нижнего отдела сустава (полусустава), включающего
суставной диск, нижнюю часть капсулы сустава, головку нижней челюсти с мы-
щелковым отростком и ветвью по описанной выше методике.
После формирования воспринимающего костного ложа на наружной
поверхности ветви нижней челюсти приступают к моделированию ортотопи-
ческого аллотрансплантата в соответствии с величиной дефекта и профилем
костного ложа. Подбор аллотрансплантата и подготовка его к операции
подробно описаны в разделе 25.4. В области шейки мыщелкового отростка
аллотрансплантата снимают кортикальный слой, формируя воспринимающую
площадку для декортиката латеральной крыловидной мышцы. Головку
аллотрансплантата подводят к суставному диску, вокруг шейки его кисетным
швом плотно обшивают суставную капсулу, обеспечивая герметизм сустав-
232
Рис. 25.23. Артропластика ВНЧС при высоких и внутрисуставных переломах мыщел-
кового отростка нижней челюсти (схема).
а — высокий перелом шейки мыщелкового отростка; б — сформированы костное ложе и декор-
ти кат латеральной крыловидной мышцы; в — ортотопичсский аллотрансплантат суставного конца,
подготовленный к замещению головки нижней челюсти; г — заключительный этап операции.
ной полости, фиксируют латеральную крыловидную мышцу. Прсле этого при
помощи бимаксиллярных шин и резиновой тяги иммобилизуют нижнюю
челюсть в правильном прикусе.
Нижний отдел аллотрансплантата, представленный частью ветви
нижней челюсти, помещают внакладку на воспринимающее костное ложе на
наружной поверхности ветви нижней челюсти реципиента и прочно фиксируют
233
проволочными швами. Излишки аллотрансплантата срезают дисковой
фрезой (рис. 25.23).
После завершения всех этапов операции рану обильно орошают
стерильным раствором фурацилина в стандартном разведении A:5000) для
вымывания костных опилок и кровяных сгустков, затем послойно ушивают. На
1—2 сут в ране оставляют резиновый дренаж. Перед экстубацией и
выведением больного из наркоза на 1 сут снимают резиновую тягу с целью
профилактики посленаркозных осложнений (аспирации). В дальнейшем
иммобилизацию нижней челюсти осуществляют на 7—10 дней до снятия швов и
контрольного рентгенологического исследования, при котором определяют
положение аллотрансплантата (рис. 25.24).
25.10. Аллопластика височно-нижнечелюстного сустава
при удалении опухолей, диспластических процессах
и концевых дефектах нижней челюсти
Доброкачественные опухоли и диспластические процессы могут поражать
любой участок нижней челюсти, в том числе восходящую ветвь, мыщелковый
отросток и головку нижней челюсти. Хирургическое лечение таких
патологических процессов заключается в радикальном удалении опухоли —
резекции того или иного участка нижней челюсти, а в случае распространения на
сустав — в резекции с экзартикуляцией в ВНЧС. После этого остается
значительный дефект костных тканей нижней челюсти и ВНЧС.
В этом случае необходимо не только устранить костный дефект нижней
челюсти, но и восстановить анатомо-структурную целость и утраченную
функцию ВНЧС. Если возможно одновременно удалить опухоль и заместить
образовавшийся дефект, то производят первичную артропластику ВНЧС
(рис. 25.25, 25.26).
Крайне неблагоприятные условия возникают после обширной резекции
нижней челюсти и окружающих мягких тканей при злокачественных
опухолях с последующей лучевой терапией, а также тогда, когда
трансплантационное ложе сформировано из филатовского стебля. В таких случаях сразу
после резекции устранить дефект костных тканей невозможно, поэтому
производят отсроченную аллопластику ВНЧС.
Перестройка ортотопического аллотрансплантата, пересаженного в руб-
цовую недостаточно кровоснабжаемую ткань, происходит замедленно, по
типу несовершенного остеогенеза с образованием неполноценного костного
регенерата, в связи с тем, что в таких условиях процессы рассасывания
аллотрансплантата преобладают над процессами замещения его
новообразованной костью. При замещении таких дефектов наиболее целесообразно
применять костные аутотрансплантаты, которые быстрее, чем аллотранс-
плантаты, перестраиваются и ассимилируются в организме больного.
Замещение же обширных дефектов нижней челюсти, включающих суставной
конец и подбородочный отдел челюсти, только одним аутотранспланта-
том чрезвычайно сложно. В условиях рубцово-измененного, аваскуляр-
ного ложа аутотрансплантат также рассасывается без образования новой
кости. В таких случаях целесообразно проводить комбинированную алло-
ауто пластику.
Комбинированная аллоаутопластика обширных дефектов нижней
челюсти при неблагоприятных условиях воспринимающего ложа заключается в
234
Рис. 25.24. Томограммы левого и правого ВНЧС. Артропластика ортотопическим ал-
лотрансплантатом суставного конца при двустороннем переломе головок нижней
челюсти.
а, б — до операции; в, г — после операции.
замещении дефектов в различных отделах нижней челюсти и ее суставного
конца ортотопическим аллотрансшіантатом нижнечелюстнои кости в
сочетании с аутотрансплантатом, который в виде сплошной пластинки или
отдельных фрагментов помещают с внутренней стороны аллотрансплантата на
специально сформированное ложе и через ряд сквозных отверстий
фиксируют кетгутом или полиамидной нитью. В области головки нижней челюсти
аллотрансплантата делают ряд отверстий, которые заполняют кусочками
аутогенной кости.
235
Рис. 25.25. Артропластика ВНЧС по Плотникову при резекции нижней челюсти с
экзартикуляцией по поводу опухолей и диспластических процессов (схема).
В качестве аутотрансплантата используют наружную пластинку гребешка
подвздошной кости или аутогенный костный мозг, взятый щадящим способом
из подвздошной или большеберцовой кости [Плотников Η. Α., 1967, 1979; Сы-
солятин П. Г., 1979; Соловьев М. М. и др., 1977, 1979; Водолацкий М. П.,
1982, и др.].
С целью улучшения остеопластических свойств и снижения антигенно-
сти аллотрансплантата эта методика модифицирована нами [Никитин Α. Α.,
1987]. В области шейки аллотрансплантата суставного конца
цилиндрической фрезой формируют полость, которую продолжают в головку. Затем из
головки и шейки мыщелкового отростка аллотрансплантата фрезой
тщательно удаляют всю губчатую кость, стараясь не повредить суставную
поверхность и хрящевое покрытие головки и не уменьшить механическую
прочность аллотрансплантата. Образовавшуюся костную полость в головке и
шейке мыщелкового отростка ортотопического аллотрансплантата суставного
конца заполняют аутогенным костным мозгом или аутогенной щебенкой из
гребешка подвздошной кости (рис. 25.27).
Методика замещения дефектов суставного конца и ветви нижней
челюсти (концевых дефектов) ортотопическим аллотрансплантатом нижнего
отдела сустава (полусустава), состоящего из суставного диска, нижнего отдела
суставной капсулы, головки с хрящевым покрытием и ветви нижней
челюсти, разработана в нашей клинике и применяется при первичной и
отсроченной аллопластике ВНЧС у больных с концевыми дефектами нижней
челюсти, фиброзными анкилозами и деформирующими артрозами ВНЧС. Она
позволяет создать полноценное в анатомо-функциональном отношении
суставное сочленение, улучшить условия перестройки суставного конца
ортотопического аллотрансплантата и уменьшить вероятность рассасывания
головки нижней челюсти аллотрансплантата.
При замещении дефектов ветви и бокового отдела нижней челюсти эта
методика усовершенствована нами — предложен комбинированный ортото-
пический аллоаутотрансплантат полусустава [Никитин Α. Α., 1981].
Методика отсроченной костной пластики комбинированным
ортотопическим трансплантатом полусустава заключается в том, что после рассечения
236
jlLaJ
Рис. 25.26. Первичная артропластика после резекции нижней челюсти справа по
поводу амелобластомы.
а, б — рентгенограмма до операции Амелобластома нижней челюсти справа: в, г —
рентгенограмма после операции. Опухоль удалена, дефект замещен ортотопическим аллотрансплантатом.
рубцов и формирования путем туннелирования мягкотканного
трансплантационного ложа костный дефект суставного конца и ветви нижней челюсти в
зависимости от его размера замещают ортотопическим аллоаутотранспланта-
том полусустава с ветвью или частью тела нижней челюсти (рис. 25.28).
При рубцовом перерождении суставной диск больного без ущерба для
исхода аллопластики иссекают и на его место фиксируют суставной диск
комбинированного трансплантата, прошивая его по периметру 3—4
капроновыми лигатурами. Вокруг шейки комбинированного трансплантата к ниж-
Рис. 25.27. Комбинированный орготопический
трансплантат для замещения дефектов
суставного конца нижней челюсти (схема).
/— ортотопический аллотрансплантатсуставного
конца; 2 — аутотрансплантат, заполняющий
полость в головке и шейке аллотрансплантата.
237
Рис. 25.28. Аллопластика ВНЧС комбинированным ортотопическим трансплантатом
полусустава (схема).
а — послеоперационный дефект мыщелкового отростка и ветви нижней челюсти; б —
комбинированный ортотопический трансплантат (аллоаутотрансплантат); / — аллотрансплантат
полусустава; 2 — аутотрансплантат из гребешка подвздошной кости.
ней части суставной капсулы подшивают окружающие мягкие ткани так,
чтобы они плотно охватывали капсулу, создавая мышечный футляр — основной
источник васкуляризации. Комбинированный трансплантат фиксируют к
фрагменту нижней челюсти больного по известному принципу. Операцию
заканчивают послойным ушиванием тканей по обычной методике.
Иммобилизацию нижней челюсти в послеоперационном периоде осуществляют в
течение 6 нед, после чего постепенно начинают разработку новообразованного
суставного сочленения.
25.11. Лечебно-профилактические мероприятия
после аллопластики височно-нижнечелюстного сустава
Одной из важнейших задач после костно-пластических и реконструктивных
операций на нижней челюсти и ВНЧС является как можно более раннее
восстановление утраченной функции нормального приема пищи и речи, что
имеет не только медицинское, но и социальное значение. От течения
послеоперационного периода зависит результат хирургического лечения. Блестяще
технически проведенная операция может иметь неблагоприятный исход,
если не учесть особенностей всех мероприятий, проводимых в
послеоперационном периоде, в зависимости от характера заболеваний и методики
хирургического лечения.
Лечение должно быть комплексным и заключаться в лекарственной
терапии, физиотерапии, миогимнастике, массаже или самомассаже, лечебной
физкультуре, ортопедических и ортодонтических мероприятиях, а в ряде
случаев — в ультрафонотерапии.
После операции не менее 7—10 дней применяют обезболивающие
препараты, остеотропные антибиотики. Необходимо парентеральное питание с
использованием белковых препаратов, глюкозы, витаминов, добавлением
диуретических средств. В дальнейшем выбор фармпрепаратов зависит от
клинической картины и стоящих перед врачом задач.
После любого хирургического вмешательства закономерно развивается
асептическое воспаление, проявляющееся нарушением микроциркуляции и
238
лимфостазом, реакцией напряжения мышц, болевым синдромом и отеком
мягких тканей, который бывает максимальным на 3—4-е сутки. В связи с
этим одним из наиболее адекватных физиофакторов является электрическое
поле УВЧ, применяемое в строго атермической дозе при мощности 15—20 Вт.
На фоне активизации крово- и лимфообращения, клеточных и тканевых
защитных механизмов этот фактор оказывает дегидратирующее,
противовоспалительное и обезболивающее действие. Курс не должен превышать 5—6
процедур, проводимых ежедневно. Его удлинение нецелесообразно в связи с
возможностью избыточного образования соединительной ткани. Одним из
эффективных дегидратирующих факторов, восстанавливающих венозно-
лимфатический отток и проводимость по нервным волокнам, а также
ускоряющих остеорегенерацию, является переменное магнитное поле, которое
можно назначать на 2-е сутки после операции (до 10 ежедневных процедур).
Перспективно сочетание воздействия инфракрасным и красным лазером в
раннем послеоперационном периоде, но дозы необходимо уточнить.
Раннее назначение флюктуирующих токов по поперечной методике приводит
к активизации микроциркуляции и двигательной активности жевательной
мышцы, что в дальнейшем способствует улучшению функционального
результата.
Для санации бронхолегочной системы и повышения дыхательной
функции после эндотрахеального наркоза назначают ингаляции с травами,
минеральными водами, муколитическими препаратами. Рекомендуется
гидромассаж десен для улучшения гигиенического состояния полости рта.
С целью уменьшения выраженности болевого синдрома после операции
проводят иглорефлексотерапию, индивидуально подбирая методику и
рецепт точек.
Одним из наиболее важных периодов в реабилитационном комплексе
является восстановление двигательной активности жевательной группы мышц.
Применяют синусоидальные модулированные токи, диадинамические токи по
методике электростимуляции. Импульсные токи повышают микроциркуляцию
жевательных мышц, способствуют сохранению их двигательной активности с
адекватной перестройкой их функциональной активности при новых
взаимоотношениях с костными структурами. Кроме того, под влиянием импульсных
токов уменьшается венозно-лимфатический отек, что способствует
регрессированию послеоперационного инфильтрата мягких тканей.
Наиболее адекватно сочетание указаных методик с ультразвуковой
терапией, которая оказывает выраженное влияние на трофику тканей, повышает
проводимость по нервным волокнам, препятствует соединительнотканному
перерождению жевательной группы мышц, работающих в новых анатомо-
функциональных соотношениях с костными структурами, а также уменьшает
выраженность иммуноконфликтных реакций и усиливает остеорепаративные
процессы. Ультразвук необходимо назначать в малых дозах при интенсивности
не более 0,2 Вт/см . Курс лечения состоит из 10—12 ежедневных процедур. Для
повышения рассасывающего действия ультразвука, образования мягкого
эластичного послеоперационного рубца можно назначать ультрафонофорез
лидазы или ронидазы области ВНЧС и подчелюстной области F4 У Ε
растворяют в 5 мл вазелинового масла и используют по мере необходимости).
Интенсивность ультразвука более 0,2 Вт/см2 отрицательно сказывается на ос-
теорегенерации и может активизировать распад лидазы.
Через 2—3 мес на амбулаторном этапе лечения желательно повторить курс
ультразвуковой терапии и электростимуляции, что повышает эффективность
реабилитационного комплекса. Можно также рекомендовать
парафинотерапию по салфетно-аппликационной методике, грязелечение в сочетании с им-
239
пульсными токами или электрофорезом послеоперационной области. Выбор
лекарственного вещества при электрофорезе зависит от стоящей перед врачом
на данном этапе задачей. Если наблюдается рубцовая деформация,
затрудненное открывание рта, остаточный послеоперационный инфильтрат, то
наиболее адекватно назначение лидазы, ронидазы, коллализина, йода. При
ухудшении остеорепаративных процессов, нарушениях микроциркуляции
назначают спазмолитические и сосудорасширяющие препараты (например,
никотиновая кислота, папаверин, но-шпа, кавинтон), а также
микроэлементы — ионы кальция (из 5—10 % раствора СаСІ), цинка и меди (из 2 %
раствора ZnC04 и CuS04) или полный набор микроэлементов из раствора гу-
мизоля, пеллоидина.
Если на сроки назначения физиотерапии вид оперативного
вмешательства влияет незначительно, за исключением больных после устранения
дефекта костной ткани при онкологических процессах (первичная и
отсроченная костная пластика), то выбор методики и сроков начала механотерапии,
миогимнастики и массажа зависит от патологии и вида оперативного
вмешательства.
После снятия швов всем больным, кроме онкологических,
рекомендуется массаж лица и воротниковой зоны, что способствует восстановлению
двигательной функции ВНЧС и жевательной группы мышц, улучшению
трофики мягких и костных тканей. Затем больного обучают приемам
самомассажа — бимануальному массажу жевательной группы мышц, который
проводят по 5—7 мин 2—4 раза в сутки. Больной производит поглаживания,
легкие постукивания, разминания мышц жевательной группы, проекции
ВНЧС с двух сторон, а также поглаживания и постукивания кончиками
пальцев по ходу кожных линий лица для активизации кровообращения.
Целесообразно обучить больного самомассажу мышц шеи с использованием
элементов поглаживания и разминания.
Выбор методики функциональной терапии, сроки ее начала,
продолжительность и дозы во многом зависят от метода хирургического лечения
анкилоза. При аллопластике ВНЧС с костно-мышечной декортикацией, когда
травма, наносимая жевательным мышцам в результате операции, минимальна,
пассивные движения нижней челюсти начинают на 2—3-й сутки. Можно
дополнительно проводить самомассаж жевательных мышц в виде легкого
поглаживания кончиками пальцев по ходу лимфооттока, начиная с 3—4-х суток
после операции E—7 мин 2—3 раза в сутки). При сильной болезненности
массаж назначают на 1—2 дня позднее.
При аллопластике ВНЧС по обычной методике с отслойкой жевательных
мышц от кости нижней челюсти, массаж, миогимнастику, пассивные
движения в новообразованном суставе назначают на 6—8-е сутки после операции.
Для разработки функциональных возможностей ВНЧС следует
придерживаться строго индивидуально дозированной механотерапии. Грубые
насильственные движения приводят к развитию микрогематом в жевательных
мышцах, которые потом организуются в рубцовую ткань. Образуется
порочный круг: сокращение двигательной активости мышцы за счет
соединительнотканного перерождения миофибрилл требует дополнительных мышечных
усилий, что в свою очередь приводит к гиперфункции с развитием рубцовых
изменений и прогрессированием патологии. Принудительную механотерапию
с помощью различных аппаратов и роторасширителей мы считаем
нецелесообразной, так как это приводит к излишней нагрузке на аллотрансплантат и
суставные хрящи пересаженного суставного блока. Лучше назначать жевание
резинки (ученический ластик) на молярах, опускание нижней челюсти с
помощью пальцев рук, наложенных на зубы или альвеолярные отростки (при
240
беззубой челюсти). Сначала больные занимаются под руководством
инструктора ЛФК, а затем самостоятельно 3—5 раз в день до появления усталости или
легких болевых ощущений. Кроме того, рекомендуются мимические движения,
движения языком, сжимание челюстей с напряжением мышц жевательной
группы.
Реабилитационные мероприятия, проводимые после пластики ВНЧС ор-
тотопическим аллотрансплантатом суставного конца по поводу переломов мы-
щелкового отростка с вывихом головки нижней челюсти, имеют особенности.
После снятия швов назначают пассивные, а затем активные движения в
оперированном суставе, так как при данной методике операции нет
необходимости в иммобилизации челюстей. Большее значение придают восстановлению
функции латеральных крыловидных мышц, поэтому обязательно добавляют
боковые и сагиттальные движения нижней челюсти. Кроме того, можно
использовать поперечные методики флюктуоризации, воздействие диадинамиче-
скими и синусоидальными модулированными токами, располагая один
электрод площадью 100 см2 на жевательной мышце и в проекции ВНЧС, а другой
(ротовой электрод с активной боковой поверхностью) — на слизистой
оболочке щеки. На амбулаторном этапе предпочтительнее назначать
электрофорез кальция, гумизоля, пеллоидина на послеоперационную область.
При замещении субтотальных и половинных дефектов нижней челюсти с
аллопластикой ВНЧС по поводу концевых дефектов нижней челюсти
особенности реабилитационного комплекса зависят от характера и протяженности
дефекта, объема и вида хирургического лечения. У таких больных
иммобилизацию осуществляют в течение 4 нед, за исключением случаев
хирургического замещения дефекта ветви и мыщелкового отростка, когда
функциональную терапию можно назначать на 10—12-е сутки после операции. В случаях
отсроченной комбинированной и некомбинированной костной пластики
дефектов нижней челюсти иммобилизацию продолжают до 6 нед независимо от
протяженности дефекта. Только после рентгенологического контроля,
первичного заживления операционной раны, отсутствия (или стихания)
воспалительных явлений, не связанных с отторжением аллотрансплантата, можно назначать
поэтапно функциональную терапию.
После снятия иммобилизации могут быть рекомендованы пассивные
движения нижней челюстью с постепенным увеличением амплитуды.
Механотерапию следует проводить только в щадящем режиме с использованием резинки
(ученический ластик), постепенно увеличивая ее высоту и используя разные
грани. Активные движения в суставах с помощью рук может выполнять сам
больной до появления субъективных болевых ощущений в мышцах
оперированной области. Миогимнастику мимических мышц лица, языка, жевательных
мышц можно проводить сразу после снятия швов. Массаж, тепловые
процедуры не показаны. В послеоперационном периоде на 2—3-й сутки может быть
назначена магнитотерапия A5—20 ежедневных процедур). Этот фактор
широко используется при комплексном лечении больных со злокачественными
новообразованиями и разрешен к применению Минздравом РФ и ВОЗ.
Всем больным при комплексном лечении целесообразно назначать
лечебную гимнастику, проводимую под руководством методиста лечебной
физкультуры и включающую в себя дыхательные упражнения, упражнения для
мышц шеи, верхних и нижних конечностей с поэтапным расширением объема
движений и нагрузки. В первые дни после операции для профилактики
пневмонии необходимо выполнять дыхательные упражнения, а также движения
кистями, стопами и по возможности головой.
У ряда больных после операции могут выявляться изменения речи,
поэтому для ускорения адаптации речевого аппарата к новым функциональным
16-1263
241
условиям назначают фонопедические упражнения, выполняемые под
руководством логопеда или фониатра. Как правило, необходимо несколько
занятий для закрепления полученных навыков.
Одним из обязательных условий реабилитации больных является
правильное питание с исключением приема жесткой пищи в первые дни и
повышением ее калорийности за счет включения белков, обязательным набором
минеральных компонентов и витаминов. В дальнейшем до полной
перестройки сустава ограничивают прием жесткой грубой пищи. В рацион
включают молочнокислые продукты, творог, морепродукты, рыбу, свежие овощи
и фрукты (при щадящей жевательной нагрузке). До полной перестройки
ВНЧС необходимо избегать резких движений в суставе, травм, тяжелой
физической работы, охлаждения, сквозняков. Больной находится под
наблюдением 1—2 года. Повторные осмотры проводят в первый квартал ежемесячно,
затем 1—2 раза в полгода.
Ортопедическое лечение при условии благоприятного течения
послеоперационного периода можно начинать в среднем через 2—3 мес
после костной пластики. К этому времени исчезает послеоперационный отек
мягких тканей, больной достаточно широко открывает рот и в области
соединения трансплантата с нижней челюстью отмечается костное сращение.
При замещении половинных и субтотальных дефектов нижней челюсти
протезирование необходимо начинать через 3—4 мес, после костной
пластики концевого дефекта нижней челюсти, связанного с оперативным
лечением злокачественных новообразований, — не ранее 1 года после
операции.
Ортопедическое лечение и коррекция окклюзии у больных после
аллопластики ВНЧС имеют следующие особенности: 1) при наличии
суперконтактов в центральной окклюзии должна быть проведена лечебная сошлифовка
зубов; 2) для устранения феномена Попова следует отдавать предпочтение
сошлифовыванию зубов с предварительным их депульпированием; 3) в
период до 1 года после операции ортодонтическая перестройка не показана во
избежание перегрузки трансплантата.
При наличии показаний целесообразно изготавливать несъемные мос-
товидные и опорные шинирующие протезы. Съемные пластиночные протезы
с обычными проволочными удерживающими кламмерами при
значительных дефектах зубных рядов без дистальных опор могут быть использованы
только как временные. При постоянном применении они вызывают
атрофию и травму альвеолярного отростка, пародонта оставшихся зубов,
снижение окклюзионной высоты нижнего отдела лица, травму тканей
ВНЧС.
Необходимо стремиться к раннему воздействию на трансплантат с
помощью физиологической жевательной нагрузки с целью наилучшего его
приживления и перестройки. В то же время следует избегать чрезмерных нагрузок
на костный саженец, чтобы не нарушить связь трансплантата с костью
реципиента, т. е. необходима дозированная нагрузка.
В первые месяцы интенсивно происходят процессы перестройки
костного аллотрансплантата. В результате наступают изменения конфигурации
костного аллотрансплантата и как следствие этого — изменение рельефа
протезного поля, что приводит к несоответствию рельефа базиса протеза и
протезного ложа.
В сроки от 1 до 1,5 года после операции можно приступать к изготовлению
постоянного протеза. В это время процесс перестройки костного
аллотрансплантата, как правило, уже закончен. Наиболее удовлетворяют требованиям
разнообразные конструкции цельнолитых шинирующих бюгельных протезов.
242
Опирающиеся элементы таких протезов позволяют рационально
распределить жевательное давление на оставшиеся зубы и протезное ложе. В таких
конструкциях нежелательно применять разгружающие пружины,
поскольку это приводит к дополнительной нагрузке на трансплантат. Снизить
нагрузку можно за счет максимального расширения границ базиса съемного
протеза.
Значительная перспектива в решении проблем ортопедического лечения
больных после костно-реконструктивных операций на нижней челюсти и
ВНЧС появилась в связи с распространением за рубежом, а в последнее
десятилетие и в нашей стране методики дентальной имплантации.
Использование дентальных имплантатов различных типов позволяет изготовить наиболее
рациональные ортопедические конструкции зубных протезов, восстановить
прикус и полноценную жевательную функцию у больных после костно-пла-
стического замещения обширных дефектов нижней челюсти, несмотря на
неблагоприятные условия протезного ложа, представленного костным
трансплантатом.
СПИСОК ЛИТЕРАТУРЫ
Аржанцев П. 3. О хирургических вмешательствах в области височно-нижнечелюстного
сустава//Воен.-мед. журнал. — 1971. — № 11. — С. 23—27.
Вернадский Ю. И., Крумина О. Я. Ближайшие и отдаленные результаты аллопласти-
ческих восстановительных операций в челюсти о-лицевой области//Стоматоло-
гия. - 1962. - № 2. - С. 52-55.
Гинали В. Н. Изменения височно-нижнечелюстного сустава при потере зубов. —
Ташкент: Медицина, 1966. — 61 с.
Дергилев А. П. Оптимизация диагностики внутренних нарушений
височно-нижнечелюстного сустава с помощью магнитно-резонансной томографии: Дис. ... канд.
мед. наук. — Новосибирск, 1997.
Егоров П. М.у Карапетян И. С. Лечение болевого синдрома височно-нижнечелюстного
сустава//Стоматология. — 1980. — № 3. — С. 38—40.
Золотарева Ю. Б. Васкуляризация аллотрансплантатаизлиофилизированной кости,
замещающего дефект суставного конца нижней челюсти: Дис. ... канд. мед. наук. —
М., 1976. - 176 с.
Иванов А. С. Профилактика и лечение артритов и артрозов височно-нижнечелюстного
сустава: Методические рекомендации. — Л., 1985. — 16 с.
Измайлова Л. С. Клиника и лечение артритов и артрозов височно-нижнечелюстного
сустава: Дис. ... канд. мед. наук. — М., 1964. — 182 с.
Иоаннидис Г. Я. Анкилоз височно-нижнечелюстного сустава и микрогения. —
Ташкент, 1974. — 42 с.
Каспарова Н. Н. Вторичный деформирующий остеоартроз и костный анкилоз
височно-нижнечелюстного сустава у детей: Автореф. дис. ... докт. мед. наук. — М.,
1978. - 423 с.
Каспарова Н. Н., Колесов А. А.у Воробьев Ю. И. Заболевания височно-нижнечелюстного
сустава у детей и подростков. — М.: Медицина, 1981. — 159 с.
Каспарова И. И., Богдашевская В. Б., Овчинников Ä М. Травма мыщелкового отростка
нижней челюсти и ее исход в детском возрасте//Тезисы докладов 7-го Всесоюзн.
съезда стоматологов. — Ташкент, 1981. — С. 138—140.
Левенец Α. Α., Прахина О. В., Панова 3. В. Костная пластика нижней челюсти в
различных условиях воспринимающего ложа//Труды ЦНИИС. — Т. 13. — 1984. —
С. 191.
Лимберг А. А. Учебник хирургической стоматологии. — М.: Медгиз, 1938. — 479 с.
Михельсон Η. Μ. Резекция половины нижней челюсти с одномоментной
имплантацией пластмассы/УСтоматология. — 1956. — № I. — С. 20—21.
Мухин М. В. Применение консервированной трупной кости в челюстно-лицевой
хирургии. — Л., 1955. — С. 166-167.
243
16*
Никитин А. А. Аллопластика височно-нижнечелюстного сустава (экспериментально-
клиническое исследование): Дис. ... докт. мед. наук. — М., 1987.
Петросов Ю. А. Клиника, диагностика и лечение функциональных синдромов
височно-нижнечелюстного сустава: Методические рекомендации. — М., 1985. — 32 с.
Плотников Η. Α., Ткаченко А. М. Новая методика хирургического лечения анкилозов
височно-нижнечелюстного сустава//Успехи клинической и экспериментальной
медицины. — М., 1967. — С. 566—567.
Плотников Η. Α., Ткаченко А. М. Артропластика височно-нижнечелюстыого сустава
при его анкилозе: Методическое письмо. — М., 1970. — 12 с.
Плотников Н. А.} Никитин Α. Α., ЧернусЛ. А. Хирургическое лечение травматических
повреждений суставного отростка нижней челюсти: Методические
рекомендации. — М., 1979.
Плотников Η. Α., Никитин А. А. Ультразвуковая сварка и резка кости при костно-пла-
стических операциях на верхней и нижней челюстях//Сборник науч. трудов Все-
союзн. науч.-техн. конференции "Проблемы технической медицины". —
Таганрог, 1979.
Плотников Я. Α., Никитин А. А. Новый способ хирургического лечения анкилоза
височно-нижнечелюстного сустава//Тезисы докладов 7-го Всесоюзн. съезда
стоматологов. — М., 1981. — С. 306—307.
Рабухина Н. А. Заболевания височно-нижнечелюстного сустава и их
рентгенологическое распознавание. — М.: Медицина, 1966. — 75 с.
Pay эр А. Э., Михельсон Н. М. Пластические операции на лице. — М.: Медгиз, 1954.
Савицкий В. А. Пластика реберным аутотрансплантатом и хрящевой частью у детей с
анкилозом височно-нижнечелюстного сустава//Материалы докладов 5-го
Всесоюзн. съезда стоматологов. — М., 1968. — С. 195—198.
Сигал А. М. Гомопластика височно-нижнечелюстного сустава и дефекта нижней
челюсти формалинизированными трансплантатами: Дис. ... канд. мед. наук. — М.,
1972. - 157 с.
Сысолятин П. Г., Железный П. Α., Ищенко Н. А. Артропластика консервированной ал-
локостыо при переломах мыщелкового отростка нижней челюсти с вывихом го-
ловки//Сборник науч. трудов МОНИКИ. - Т. 24. - М., 1979. - С. 79-81.
Сысолятин П. Г. Костная аллопластика нижней челюсти: Дис. ... докт. мед. наук. —
Новосибирск, 1984. — 421 с.
Тер-Асатуров Г. П. Пластика опорных тканей лица формалинизированными ал-
лотрансплантатами: Автореф. дис. ... докт. мед. наук. — М., 1981. — 46 с.
Троянский И. В. Костно-мышечная пластика при частичной резекции нижней
челюсти с использованием гомотрансплантата из лиофилизированной кости:
Автореф. дис. ... канд. мед. наук. — М., 1975. — 154 с.
Троянский И. В., Никитин А. А. Костно-мышечная пластика при восстановительных и
реконструктивных операциях нижней челюсти: Методические рекомендации. —
М., 1982. - 19 с.
Франкенберг Б. Е. Вопросы хирургии лииа. — Л., 1936. — С. 172—175.
Хватова В. А. Заболевания височно-нижнечелюстного сустава. — М.: Медицина,
1982. - 159 с.
Шумада И. В., Скрипнюк П. Α., Кривенко В. М. Способ насыщения костных
трансплантатов медикаментами//Ортопед., травматол. — 1979. — № 11. — С. 65—66.
Bardenheimer G. (цит. по: Digmann R., Crabb W. Plast. Reconstr. Surg. — 1964. — Vol. 34,
Ν 5. - P. 441-450).
Bell W. Η. Current concepts of bone grafting//.!, oral Surg. — 1968. — Vol. 26, N 2. —
P. 118-124.
Byars L. Preservation and restoration of mandibular function and vontour//Ann. Surg. —
1948. - Vol. 127, N 5. - P. 863-878.
Christensen R. W. The correction of inandidular anxylosis by artroplasty and the insertion of
a cast Vitallium glenoid fosse//J. South Calif. State Dent. Ass. — 1963. — Vol. 31. N 4.
Digmann O., Grabb W. Reconstraction of both mandibular condyles with metatursal bone
grafts//Reconstr. Surg. - 1964. - Vol. 34, N 5. - P. 441-451.
Genest A. Witallium jaw emplacement//Amer. J. Surg. - 1956. - Vol. 92, N 6. - P. 904—907.
244
Hahn G., Corgill D. Chrome cobalt mosh mandibular prothesitis//J. oral Surg. — 1969. —
Vol. 27, N 1. - P. 5-10.
Healy M., Sudday G., Niebel H. Use of acrylic methyl-methacrylate implants in of mandi-
bulare//Surg. Gynec. Obstet. - 1954. - Vol. 98, N 4. - P. 375-378.
Kummoona R. Functional rehabilitation of ankylosed temporo-mandibular jonts//J. oral Surg. —
1978. - Vol. 46, N 4. - P. 495-505.
Nasteff D. Infraoperative Implantation von Kunststoff korpern bei Unterkieferektionen//Dt-
sch. Stomat. - 1962. - N 7. - S. 494-502.
Sarnat R. G., Engel Μ. Β. A serial study of mandibulare growth after removal of the condule
in the macaca-rhesus monkey//Plast. Reconstr. Surg. — 1951. — Vol. 7. — P. 364—380.
Smith Α., Robinson M. A new surgical technic for the replacement of lost mandidiilar bone//
Amer. J. Surg. - 1956. - Vol. 92, N 6. - P. 857-862.
Sonnenburg /., Sonnenburg Μ. Totalersatz des Kiefergelenks durch alloplastisches Material//J.
Mitteilung Stomat. DDR. - 1978. - Bd 28. - S. 238-240.
Stiiteville O., Laufranchi R. Surgical reconstruction of the temporo-mandibular joint//Amer.
J. Surg. - 1955. - Vol. 90. - P. 940-950.
Глава 26
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
АНОМАЛИЙ И ДЕФОРМАЦИЙ
ЧЕЛЮСТЕЙ
26.1. Особенности хирургической анатомии лицевого черепа
у больных с аномалиями и деформациями
У больных с деформациями челюстей, лицевого и мозгового черепа резко
изменены топографические взаимоотношения между различными
анатомическими органами, а также нарушено нормальное анатомическое строение
каждого из них. Знание хирургической анатомии при различных видах
деформаций лицевого черепа позволяет хирургу чувствовать себя уверенно при
выполнении костно-реконструктивной операции, сокращает ее время, а
главное, дает возможность избежать опасных осложнений.
При верхней прогнатии корни фронтальных зубов расположены в
непосредственной близости к наружной компактной пластинке. В зависимости
от особенностей деформации верхней челюсти верхушки корней зубов
располагаются на различном расстоянии от дна полости носа. При верхней
прогнатии в сочетании с открытым прикусом они располагаются в 2—3 мм от дна
носа, а при верхней прогнатии, осложненной глубоким прикусом, это
расстояние может составить от 5 до 10—12 мм. Изменение формы неба, а именно
его углубление, значительно затрудняет выполнение остеотомии на уровне
малых коренных зубов. В зоне перехода альвеолярного отростка верхней
челюсти в небный отросток объем костной ткани значительно превышает
нормальную величину.
При нижней микрогнатии ветвь нижней челюсти становится на 3—5 мм
шире, а толщина ее уменьшается. На многих участках ветви губчатое
вещество истончено, что вызывает значительные трудности при плоскостной
остеотомии. Возрастает также возможность повреждения сосудисто-нервного
пучка нижней челюсти. Подбородочный отдел нижней челюсти скошен кзади.
Верхушки корней фронтальных зубов нижней челюсти расположены в толще
губчатого вещества и отстоят от нижнего края челюсти на 6—13 мм.
При верхней микрогнатии характерны уменьшение верхней челюсти во
всех плоскостях, уплощение клыковой ямки, скуловых костей. Передняя
носовая ость увеличена, резко выступает вперед, превышая значение нормы в
1,5—2 раза. В связи с отсутствием полноценной функциональной нагрузки
костная ткань истончается, особенно вне контрфорсов.
При верхней макрогнатии резко увеличена высота альвеолярного отростка.
Вертикальные размеры верхней челюсти также увеличены. Ширина
грушевидного отверстия значительно уменьшена, а высота увеличена.
246
У больных с нижней ретрогнатией высота подбородочного отдела на 5—
6 мм больше по сравнению с нормой. У больных с нижней макрогнатией или
нижней прогнатией на 3—5 мм уменьшена ширина ветви нижней челюсти и
на 4—5 мм увеличена высота подбородочного отдела.
26.2. Частота аномалий и деформаций лицевого черепа
В отечественной и зарубежной литературе приводятся разноречивые данные
о частоте аномалий и зубочелюстных деформаций у детей и взрослых. Это
связано с применением различных методик эпидемиологического
исследования, отсутствием общих четких критериев оценки деформации,
использованием различных классификаций. Многочисленные исследования,
проведенные отечественными и зарубежными авторами, показали, что зубочелюстные
деформации встречаются у 33,1—95,3 % обследованных. Четкие критерии
оценки различных видов деформаций и аномалий, детальное обследование и
регистрация выявленных отклонений позволяют получить объективно
сопоставимые данные эпидемиологических исследований. Подобные качества,
отражающие нужды челюстно-лицевых хирургов и ортодонтов, в настоящее
время имеет методика обследования больных с деформациями, предложенная
В. М. Безруковым и соавт. A979), которая, по рекомендации ВОЗ, проходит
проверку в различных регионах мира.
Высокий процент зубочелюстных аномалий у детей 5—15 лет еще не
свидетельствует о том, что такая же частота деформаций зубочелюстной
системы будет наблюдаться и у взрослых. Прежде всего часть деформаций
обусловлена диспропорциями роста и развития зубочелюстной системы и в
дальнейшем происходит саморегуляция прикуса. Кроме того, среди выявленных
аномалий зубочелюстной системы значительное место занимают аномалии
положения и формы отдельных зубов или их групп, деформации зубных рядов,
которые, как правило, исправляют в процессе ортодонтического лечения.
Несомненно, что на частоту деформаций челюстей у взрослых существенное
влияние оказывает ортодонтическое лечение детей. Установлено, что 41,6—
62,2 % детей, находящихся на ортодонтическом лечении, не заканчивают его
по различным причинам.
Эпидемиологические исследования не позволяют сделать
аргументированный вывод о потребности в хирургическом лечении при аномалиях и
деформациях лицевого черепа и зубочелюстной системы в частности. О частоте
зубочелюстных аномалий у взрослых можно судить по данным ряда
отечественных и зарубежных исследователей, проводивших эпидемиологические
исследования в возрастной группе от 15 лет до 21 года, когда рост лицевого
черепа фактически уже завершен. Частота выявленных деформаций
колебалась от 41,1 до 95,3 %.
Клинические наблюдения и экспериментальные исследования
показали, что ортодонтическими методами можно исправить форму зубных дуг,
положение отдельных зубов или целых групп зубов, устранить дистальное
смещение нижней челюсти. После окончания роста лицевого черепа добиться
увеличения или замедления роста челюстных костей, используя ортодонти-
ческие методы лечения, чрезвычайно трудно или невозможно.
В соответствии с изложенным выше многие клиницисты считают, что
после окончания роста лицевого черепа изолированное ортодонтическое
лечение скелетных форм деформаций челюстей, которые проявляются
формированием прогенического, прогнатического, открытого или глубокого
прикуса, бесперспективно. Нерациональное применение ортодонтических
247
аппаратов при лечении скелетных форм деформаций челюстей приводит к
изменению наклона фронтальных зубов, сопровождается патологическими
процессами в тканях пародонта, расшатыванием зубов или резорбцией их
корней.
Следовательно, для специалистов, занимающихся костно-реконструктив-
ными операциями, более ценны те данные эпидемиологических исследований,
которые отражают частоту аномалий и деформаций лицевого черепа и
аномалий прикуса, характеризующихся прогеническим и прогнатическим
соотношением зубных рядов, открытым или глубоким прикусом. При зубочелюстных
деформациях прогеническое соотношение зубных рядов выявлено у 1,1—8,7 %,
прогнатическое — у 12,4 %, открытый прикус — у 3 %, глубокий — у 11,2 %
пациентов.
В хирургическом лечении по поводу аномалий прикуса нуждаются 4,45 %
взрослых больных. Представленные данные наиболее полно характеризуют ту
категорию больных, которым показаны костно-реконструктивные
вмешательства на челюстных костях с обязательным использованием ортодонтических
методов лечения на всех этапах медицинской реабилитации. При
исследованиях, проведенных в США, установлено, что только по поводу нижней про-
гнатии и прогенического соотношения зубных рядов более 340 000 человек
нуждаются в ортодонтическом и хирургическом лечении. По данным
специальной рабочей группы Национального института стоматологии США, у 35 %
населения наблюдаются аномалии и деформации лицевого черепа, а также зу-
бочелюстные деформации, причем 5—15 % из них необходимо хирургическое
лечение.
К сожалению, ни в отечественной, ни в зарубежной литературе нет
систематизированных исчерпывающих данных о частоте как изолированных,
так и сочетанных деформаций челюстей. Поданным В. М. Безрукова A981),
изучавшего деформации верхней челюсти (верхняя микро- или ретрогнатия),
сочетанные деформации челюстей отмечались у 42 % взрослых больных с
деформациями. Еще раньше мнение о том, что изолированные аномалии
развития челюстей и особенно верхней встречаются редко, высказал X. А. Ка-
ламкаров A972).
Косвенным подтверждением сказанного являются клинические и
рентгенологические изменения в лицевом черепе по типу гипо- или
гиперплазии у больных с односторонними деформациями нижней челюсти.
Установлено, что первичные изменения в зонах роста нижней челюсти ведут
к развитию вторичных деформаций в прилежащих и отдаленных участках
лицевого черепа.
Представленные данные были бы неполными без учета частоты
врожденных пороков развития лица и челюстей, известных в литературе как
врожденные односторонние и двусторонние расщелины губы и неба, синдромы
первой и второй жаберных дуг. По данным различных исследователей,
частота врожденных расщелин составляет один случай на 600—800 рождений.
Пороки развития под названием синдром первой и второй жаберных дуг
встречаются у одного из 4000—5642 новорожденных. Пороки развития
лицевого и мозгового черепа, известные под названием синдром Крузона и
синдром Аперта, наблюдаются еще реже — у одного из 4000—160 000
новорожденных. Следует подчеркнуть, что большинство аномалий и деформаций
лицевого черепа встречаются одинаково часто у мужчин и женщин.
Приведенные выше данные о частоте зубочелюстных деформаций и аномалий
лицевого черепа свидетельствуют о важности и актуальности проблемы для
практического здравоохранения и многообразии проявлений аномалий и
деформаций в челюстно-лицевой области.
248
26.3. Этиология, патогенез, классификация,
клиническая картина, диагностика врожденных аномалий
и деформаций зубочелюстной системы
Этиология. Врожденные аномалии и деформации зубочелюстной
системы, как правило, являются проявлением нарушений развития лицевого и
мозгового черепа. Форма и размеры челюстей в значительной степени зависят
от индивидуальных особенностей формы и размеров черепа. Нарушение роста
или развития челюстей приводит к развитию деформации или аномалии,
причем это может наблюдаться как в процессе эмбриогенеза, так и после
рождения в период формирования временного или постоянного прикуса. В связи
с этим становится понятным, какое многообразие аномалий или деформаций
может наблюдаться, причем тяжесть их проявления находится в прямой
зависимости от сроков возникновения.
Этиология зубочелюстно-лицевых аномалий и деформаций чрезвычайно
разнообразна. Органо- и морфогенез челюстей, лицевого черепа может быть
нарушен в результате наследственного воздействия на эмбрион перенесенных
родителями заболеваний (эндокринные и обменные нарушения в организме
матери, инфекционные болезни), радиоактивного облучения, а также
физиологических и анатомических изменений половых органов матери и
неправильного положения плода.
В раннем детском возрасте развитие зубочелюстной системы может быть
нарушено под влиянием эндогенных факторов (наследственность, эндокринные
нарушения, различные инфекционные болезни, нарушения обмена веществ) и
экзогенных причин (воспаление в зонах роста челюстей, травма, в том числе
родовая, лучевое поражение, механическое давление, вредные привычки,
дисфункция жевательного аппарата, нарушение акта глотания, носового
дыхания и др.).
Большинство деформаций в детском и юношеском возрасте является
следствием заболеваний в период развития лицевого черепа (остеомиелит,
рахит, артрит височно-нижнечелюстного сустава), травмы, нарушения
прикуса в связи с потерей зубов, ранних и травматичных операций по поводу
расщелин губы и неба, удаления аденоидов, неправильного и
некачественного ортодонтического лечения.
Деформация одной челюсти в процессе роста и развития организма более
или менее резко отражается на строении всего лицевого черепа. О деформации
одной или обеих челюстей речь может идти лишь при резком отклонении их
параметров от условных средних величин, наиболее соответствующих
остальным отделам лицевого и мозгового черепа данного индивидуума. Вторым
критерием наличия деформации челюсти является нарушение функции
жевания или речи.
Патогенез. В основе патогенетических механизмов развития
аномалий лицевого черепа и деформаций зубочелюстной системы лежат угнетение
или частичное прекращение роста основания и свода черепа, а также
челюстных костей, убыль костного вещества, выключение функции жевания или
открывания рта. Значительную роль в патогенезе деформаций челюстей и
лицевого черепа играют эндокринные расстройства в растущем организме.
Аномалии и деформации лицевого черепа, в том числе деформации
челюстей, у детей и взрослых встречаются весьма часто и в разнообразных формах,
сопровождаясь выраженными эстетическими и функциональными
нарушениями. Большинство больных сосредоточивают внимание на нарушении
пропорций лица, изменении внешнего вида. Эстетический недостаток в свою
очередь отрицательно сказывается на эмоциональном состоянии больных,
249
делает их замкнутыми, малообщительными, подозрительными.
Неправильное отношение окружающих и самого больного к аномалии или деформации
лица приводит к развитию мучительного чувства внешней неполноценности,
оказывающего существенное влияние на весь уклад жизни больного.
Реакция личности на эстетический недостаток выражается в развитии
вторичной невротической реакции, патохарактерологических и
интеллектуальных расстройств, которые, по данным различных авторов, наблюдаются
в 45—50 % случаев. Многие клиницисты отмечают, что перечисленные
нарушения чаще встречаются у женщин, объясняя это более высокой
лабильностью женской психики.
Наряду с эстетическими нарушениями и психоэмоциональными
расстройствами у больных с аномалиями и деформациями лицевого черепа
наблюдаются и другие функциональные расстройства, которые оказывают
существенное влияние на жизнедеятельность организма. В связи с затруднениями
при откусывании и пережевывании пищи страдает функция органов
пищеварения, что приводит к развитию хронических заболеваний
желудочно-кишечного тракта. Образуется своеобразный порочный круг: аномалии прикуса
вызывают патологические сдвиги в нервной и пищеварительной системах,
органах дыхания, ЛОР-органах, а взаимосвязь между этими органами и
системами способствует прогрессированию функциональных отклонений вплоть до
возникновения структурных изменений в органе.
У части больных с аномалиями и деформациями зубочелюстной системы
отмечены нарушение речи, хронические воспалительные процессы в
воздухоносных путях и связанные с этим нарушения дыхания. При этом страдает
произношение преимущественно зубных и ряда других звуков вследствие
неправильного соотношения зубных рядов, наличия открытого прикуса,
деформации твердого и мягкого неба, сужения носовых ходов, нарушения
артикуляции языка.
Существенные изменения при деформациях челюстей происходят в
окружающих зубы тканях и височно-нижнечелюстных суставах. При этом в
слизистой оболочке десны у отдельных зубов и их групп развиваются
воспалительные изменения с переходом на пародонт и возникновением в дальнейшем
симптомов пародонтита, а нарушение объема движений нижней челюсти ведет
к дисфункциональным изменениям в височно-нижнечелюстных суставах.
Все изложенное свидетельствует об огромном спектре нарушений,
возникающих при деформациях зубочелюстной системы, существенных изменениях
функций ряда органов и систем, их тесной взаимосвязи и взаимодействии.
Устранение имеющихся анатомических изменений в развитии лицевого
черепа ведет к ликвидации ряда функциональных нарушений и в целом
способствует полноценной психосоциальной реабилитации больных с аномалиями и
деформациями лицевого черепа и возвращению их к активной
производственной и общественной деятельности.
Многообразие функциональных расстройств различных органов и
систем организма у больного с деформацией зубочелюстной системы
свидетельствует о важности целенаправленного комплексного лечения в процессе
медицинской реабилитации пациента. С организационной точки зрения большое
значение имеют эпидемиологические исследования, позволяющие определить,
насколько часто встречаются больные с аномалиями и деформациями лицевого
черепа и зубочелюстной системы. Прежде чем обсуждать вопрос о частоте
проявления различных аномалий и деформаций, необходимо определить понятие
нормы.
По мнению многих .специалистов, занимающихся лечением больных с
аномалиями и деформациями лицевого черепа и зубочелюстной системы,
250
под нормой следует понимать такие соотношения различных отделов
лицевого черепа, форму и взаимоотношение зубных рядов, которые: 1) по
внешним признакам сходны с наиболее часто встречающимися
физиологическими разновидностями (эстетический фактор), 2) обеспечивают оптимальную
жевательную эффективность (функциональный фактор), 3) обладают
максимальной устойчивостью в процессе развития и формирования жевательного
аппарата (онтогенетический фактор). В связи с этим нормой соотношения
зубных рядов верхней и нижней челюстей в клинической практике принято
считать ортогнатический прикус как наиболее часто встречающийся.
Отклонения от ортогнатического прикуса, за исключением его физиологических
разновидностей (прямой, бипрогнатический, прогенический), которые
характеризуются множественными контактами между зубами-антагонистами,
расцениваются как деформации.
Классификация. В отечественной и зарубежной литературе нет
единой классификации аномалий и деформаций лицевого черепа и зубоче-
люстной системы. Отечественные и зарубежные специалисты наиболее часто
используют классификацию Энгля, в основу которой положен симптом
соотношения первых постоянных больших коренных зубов верхней и нижней
челюстей. Недостатком классификации является то, что деформацию
оценивают только в переднезаднем направлении в пределах зубного ряда. При
определении соотношения зубных рядов невозможно получить представление
о строении лицевого и мозгового черепа в целом и выявить истинную
причину нарушения прикуса.
Внедрение в клиническую практику новых, более современных методов
исследования, особенно телерентгенографии, позволило реально оценить
морфологические нарушения у больного с аномалией или деформацией
лицевого черепа. Следует иметь в виду, что одни и те же нарушения прикуса
могут быть вызваны различными морфологическими изменениями в зубоче-
люстной системе и лицевом черепе. Точная регистрация их может иметь
решающее значение при разработке рационального плана лечения.
Предлагаемые различными авторами классификационные схемы аномалий лицевого
черепа и деформаций челюстей основаны на эмбриологических,
патогенетических, морфологических и других признаках.
Многообразие терминов, обозначающих деформацию или аномалию,
затрудняет диагностику и планирование лечения. Как правило, применение
каждой из классификационных схем ограничено узкой специальностью (ор-
тодонтия, ортопедия, челюстно-лицевая хирургия, эмбриология). Такие
схемы не отражают сущности аномалии или деформации, морфологических
изменений при них и не позволяют составить четкий план лечения на всех
этапах медицинской реабилитации.
В настоящее время наиболее полной является рабочая классификация
аномалий лицевого черепа, челюстей и зубов, а также их деформаций,
предложенная X. А. Каламкаровым A972) и усовершенствованная В. М.
Безруковым A981) и В. И. Гунько A986).
I. Аномалии развития зубов
1. Аномалии количества зубов: а) адентия (частичная, полная); б)
сверхкомплектные зубы.
2. Аномалии положения зубов (вестибулярные, оральные, медиальные, дис-
тальные, поворот зубов по оси, высокое или низкое положение зубов,
транспозиция).
3. Аномалии величины и формы зубов.
4. Аномалии прорезывания зубов (преждевременное, позднее, ретенция).
5. Аномалии структуры зубов.
251
IL Деформации челюстей.
1. Макрогнатия (верхняя, нижняя, симметричная, несимметричная,
различных отделов или всей челюсти).
2. Микрогнатия (верхняя, нижняя, симметричная, несимметричная,
различных отделов или всей челюсти).
3. Прогнатия (верхняя, нижняя, функциональная, морфологическая).
4. Ретрогнатия (верхняя, нижняя, функциональная, морфологическая).
III. Сочетанные деформации челюстей (симметричные, несимметричные).
1. Верхняя микро- и ретрогнатия, нижняя макро- и прогнатия.
2. Верхняя макро- и прогнатия, нижняя микро- и ретрогнатия.
3. Верхняя и нижняя микрогнатия.
4. Верхняя и нижняя макрогнатия.
IV. Сочетанные аномалии зубов и деформации челюстей.
V. Сочетанные аномалии и деформации лицевого и мозгового черепа и зубо-
челюстной системы.
1. Симметричные: а) челюстно-лицевые дизостозы (синдром Тричера —
Колинза — Франческети); б) краниостенозы (синдром Аперта, Крузона);
в) гипертелоризм I—III степени.
2. Несимметричные: а) гемифациальная микросомия I—III степени
(синдром Гольденхара); б) гипертелоризм I—III степени.
При формировании диагноза, помимо отражения морфологических
характеристик аномалии или деформации, приведенных в классификации,
целесообразно указать соотношение зубных рядов и вид прикуса (прогеническое,
прогнатическое, ортогнатическое соотношение зубных рядов; глубокий,
открытый, перекрестный прикус). Аномалии и деформации лицевого и мозгового
черепа характеризуются нарушением размеров в трех взаимно перпендикулярных
плоскостях, поэтому, формулируя диагноз, следует указать, какие размеры
преимущественно нарушены (сагиттальные, трансверсальные, вертикальные).
Использование данной классификационной схемы позволяет
обеспечить преемственность в работе узких специалистов (ортодонты, ортопеды,
челюстно-лицевые хирурги, нейрохирурги, логопеды) при медицинской
реабилитации больных с аномалиями и деформациями лицевого черепа и зубо-
челюстной системы.
Клиническая картина. При всех перечисленных видах аномалий
и деформаций лицевого черепа и зубочелюстной системы больные, как
правило, жалуются на эстетический недостаток — нарушение правильных
пропорций лица за счет недоразвития или чрезмерного развития различных отделов
лицевого черепа и функциональных нарушений, связанных с
неполноценным откусыванием и пережевыванием пищи, неправильным и нечетким
произношением ряда звуков, нарушением дыхания, артикуляции.
Следует обратить особое внимание на тот факт, что изолированные
деформации могут иметь место только в период роста и развития лицевого и
мозгового черепа. В возрасте старше 16 лет, когда рост и развитие мозгового
черепа и верхних челюстей завершаются, происходит формирование соче-
танных деформаций челюстей и аномалий лицевого черепа.
Клиническая картина у больных с верхней прогнатией или макрогнати-
ей характеризуется нарушением пропорций средней зоны лица: средняя
треть лица укорочена по сравнению с нижней, ширина ее больше; верхняя
губа выступает вперед, несколько приподнята. Носогубной угол либо
увеличивается, либо уменьшается. Носогубные складки сглажены. При данном виде
деформации наблюдается прогнатическое соотношение зубных рядов.
Сагиттальная щель между центральными зубами верхней и нижней челюстей
может иметь различные значения, что зависит от степени деформации. Прикус
может быть глубоким, глубоким травмирующим, когда фронтальная группа
252
нижних зубов упирается в слизистую оболочку твердого неба, и открытым.
Размеры зубной дуги верхней челюсти нарушены в трансверсальной и
сагиттальной плоскостях. В большинстве случаев уменьшается ширина верхнего
зубного ряда на уровне первых премоляров и увеличивается длина переднего
отдела верхней челюсти, фронтальные зубы выступают вперед. В состоянии
физиологического покоя верхняя губа не закрывает зубы на верхней челюсти.
В отдельных наблюдениях зубы верхней челюсти выступают из-под верхней
губы на 2/з высоты коронки или даже больше. При улыбке верхняя губа,
смещаясь кверху, обнажает и слизистую оболочку альвеолярного отростка
верхней челюсти.
Клиническая картина при нижней микрогнатии или ретрогнатии
характеризуется уменьшением размеров нижней зоны лица в сагиттальной
плоскости, а вертикальные размеры нижней зоны лица, как правило, увеличены.
Нижняя челюсть недоразвита, уменьшена в размерах либо смещена кзади
при сохранении нормальных параметров. У большинства больных с этим
видом деформации подбородочный отдел лица скошен кзади,
губоподбородочный угол не выражен, губоподбородочная борозда сглажена, мягкие ткани
подбородочной области смещены кзади по отношению к нижней губе. Шей-
но-подбородочный угол плохо выражен, расстояние между подбородком и
подъязычной костью уменьшено.
У части больных губоподбородочный угол и губоподбородочная борозда,
наоборот, резко выражены и сильны выделяются. Подбородочный отдел
выглядит как бы укороченным при сохранении его нормальных параметров.
Нижняя губа развернута вперед, слизистой оболочкой красной каймы
упирается в режущие поверхности верхних зубов. Шейно-подбородочный угол
выражен хорошо, а расстояние между подбородком и подъязычной костью
лишь незначительно короче.
У всех больных с нижней микро- или ретрогнатией отмечается
прогнатическое соотношение зубных рядов с различной величиной сагиттальной
щели между центральными резцами верхней и нижней челюстей, что зависит
от степени деформации. Прогнатическое соотношение зубов сопровождается
глубоким, глубоким травмирующим или открытым прикусом. У больных с
нижней микро- или ретрогнатией наблюдается нарушение трансверсальных
'и сагиттальных размеров зубного ряда нижней челюсти, которое выражается
в сужении ее на уровне первых премоляров и укорочении длины ее переднего
отдела. У многих больных выявляются скученность зубов на нижней
челюсти, вестибулярный наклон фронтальных зубов и смещение их кверху по
отношению к окклюзионной плоскости.
У больных с верхней микро- или ретрогнатией уплощена и западает
средняя треть лица. Это особенно четко проявляется при сравнении наиболее
выступающих точек в области лба, верхней челюсти и подбородка. Рельеф
скуловых и подглазничных областей симметрично сглажен и уплощен. Основание
хрящевого отдела носа западает, носовые ходы сужены вследствие уменьшения
грушевидного отверстия. Носовое дыхание затруднено. На границе перехода
костного отдела носа в хрящевой определяется горбинка. Верхняя губа,
особенно ее основание, западает. Носогубной угол меньше 90°. Носогубные
складки резко выражены, глубокие. Нижняя губа, несмотря на правильные размеры
нижней челюсти, перекрывает верхнюю. Подбородок выступает вперед.
У больных с данным видом деформации наблюдается прогеническое
соотношение зубных рядов. Это сопровождается формированием прогенического
или открытого прикуса, выраженность которого зависит от степени
деформации. При верхней ретрогнатии, как правило, размеры зубной дуги верхней
челюсти в трансверсальной и сагиттальной плоскостях не отличаются от нор-
253
мальных. У больных с верхней микрогнатией выявляются ретенция и дистопия
зубов, их скученность, сужение зубного ряда верхней челюсти. Свод твердого
неба резко выражен, глубокий, носит название готического.
У больных с верхней микрогнатией после хейло- и уранопластики по
поводу врожденных расщелин губы и неба, помимо всего перечисленного,
отмечается смещение костного остова носа в здоровую сторону. Хрящевой отдел
носа также смещен в здоровую сторону, крыло носа на стороне расщелины
деформировано, уплощено. Перегородка носа укорочена. Основание
грушевидного отверстия на стороне расщелины недоразвито, уплощено, западает.
Вход в нижний носовой ход на стороне расщелины расположен ниже по
сравнению со здоровой стороной. Костная и хрящевая перегородки носа
искривлены, носовые раковины на стороне расщелины гипертрофированы.
У всех больных с расщелинами нарушено носовое дыхание.
Верхняя губа укорочена, уплощена, рубцово деформирована.
Подвижность ее несколько ограничена из-за рубцовой деформации и наличия
Рубцовых спаек по верхнему своду преддверия полости рта. Носогубной угол
меньше 90°. Верхний зубной ряд значительно деформирован, в зоне
расщелины могут отсутствовать постоянные зубы. Верхний свод преддверия рта
неглубокий за счет рубцовых изменений тканей после ранее проведенных
операций хейло- и уранопластики. Слизистая оболочка твердого и мягкого неба
рубцово изменена, мягкое небо малоподвижное, укороченное. Нередко у части
больных данной группы выявляются остаточные дефекты твердого неба и ро-
тоносовое соустье в области верхнего свода преддверия рта.
У больных с нижней макро- или прогнатией имеется деформация нижней
трети лица за счет ее выступания вперед. При этом создается впечатление, что
верхняя губа западает. Носогубные складки резко выражены, глубокие. Нижняя
губа перекрывает верхнюю. Подбородок выступает вперед. При нижней мак-
рогнатии размеры тела и ветви нижней челюсти увеличены. У больных с
нижней прогнатией отмечается увеличение нижнечелюстного угла (в норме 127°).
При нижней макро- или прогнатии выявляется прогеническое
соотношение зубных рядов. Прикус прогенический, открытый либо глубокий.
Сагиттальное несоответствие между центральными резцами верхней и нижней
челюсти определяется степенью деформации. У больных с нижней макро-
гнатией увеличены трансверсальные и сагиттальные размеры зубной дуги.
При нижней прогнатии размеры зубной дуги не изменены. Артикуляция языка
нарушена, при разговоре кончик его упирается во фронтальные зубы нижней
челюсти.
У больных с несимметричными аномалиями лицевого черепа и
деформациями зубочелюстной системы клиническая картина характеризуется теми
морфологическими изменениями, которые присущи конкретной
деформации, и тесно связана с топографией патологических изменений, а также
^степенью их выраженности.
Клиническая картина деформации обусловлена односторонним
поражением верхней или нижней челюсти в виде макро- или микрогнатии. У
больных с гемифациальной микросомией II и III степени, помимо односторонней
деформации лицевого черепа, имеются и дефекты его, что сопровождается
значительными функциональными и эстетическими нарушениями.
Диагностика. При обследовании больных с аномалиями лицевого и
мозгового черепа и деформациями зубочелюстной системы большое значение
приобретает изучение анамнеза жизни, перенесенных заболеваний и
операций, семейного анамнеза, наследственности. Особенности клинического
обследования больных с аномалиями и деформациями лицевого черепа
заключаются в детальном анализе местного статуса, изучении фотографий лица в
254
Рис. 26.1. Анализ пропорций лица в фас (а, б, в) и профиль (г, д, ё) (схема).
различных проекциях, моделей челюстей, рентгенологическом исследовании
черепа и зубочелюстной системы. При опросе больных особое внимание
следует уделить выяснению жалоб, оценить их значимость в свете объективного
анализа функциональных и эстетических нарушений.
Изучение местного статуса рекомендуется проводить в следующей
последовательности: 1) оценить положение головы; 2) проанализировать
контуры лица в фас и профиль, определить его пропорции, симметрию (рис. 26.1);
3) выяснить соотношение зубных рядов, их форму, размеры,
взаимоотношение зубов верхней и нижней челюстей, положение отдельных зубов,
состояние пародонта; 4) оценить состояние полости носа, функцию носового
дыхания; 5) выяснить характер и объем движений нижней челюсти; 6) определить
размеры языка, его положение, артикуляцию, характер наршений речи; 7)
изучить особенности строения и функцию твердого и мягкого неба; 8) оценить
состояние слюнных желез, жевательных и мимических мышц,
функциональное состояние черепных нервов.
Изучать местный статус надо строго последовательно, целесообразнее
всего сверху вниз. Анализируя положение головы больного, необходимо
учитывать, что в течение многих лет пациент выбирал такое оптимальное ее
расположение, при котором аномалия или деформация менее всего видна окружающим.
Можно наблюдать изгиб шейного отдела позвоночника, вынужденное
положение нижней челюсти, наклон головы с поворотом по оси при
несимметричных деформациях. В связи с этим, проводя клиническое обследование,
255
необходимо постоянно следить за правильным положением головы больного
в пространстве.
Первоначально изучают контуры лица в трех взаимно перпендикулярных
проекциях с учетом его симметричности, пропорциональности верхней,
средней и нижней зон. Следует отметить, что абсолютная симметрия различных
отделов лица не встречается, а незначительные отклонения не могут служить
поводом для хирургического вмешательства. Разделяя лицо на области
условными линиями по вертикали и горизонтали, проводят детальный анализ
симметричных участков, определяя деформированные отделы.
Обследуя анатомические образования средней зоны лица (глазницы,
нос, верхняя челюсть, скуловые кости), оценивают их симметричность и
пропорциональность с учетом общей формы лица. Изучают функцию слезоот-
водящих путей, характер носового дыхания, форму костного и хрящевого
отделов носа, их расположение по отношению к другим отделам лица.
При анализе нижней зоны лица акцентируют внимание на положении
и характере смыкания верхней и нижней губ, особенности строения носо-
губных складок, выраженности подбородочного отдела нижней челюсти.
При функциональном покое верхняя и нижняя губы находятся в состоянии
смыкания либо между ними может быть диастаз до 3,5 мм. При активной
улыбке верхняя губа, приподнимаясь, может обнажать слизистую оболочку
альвеолярного отростка верхней челюсти не более чем на 2 мм от зубодесневого
края. Увеличение указанных параметров может свидетельствовать либо об
укорочении верхней губы, либо о чрезмерном развитии верхней челюсти по
вертикали. При оценке пропорции лица в профиль большое значение имеют
данные о положении основания хрящевого отдела носа. Правильный профиль
лица характеризуется расположением на одной линии трех основных точек
(наиболее выступающая точка лба, основание перегородки и наиболее
выступающая точка подбородка). С эстетических позиций важно оценить положение
костно-хрящевого отдела носа, носогубной и подбородочно-шейный углы,
степень выраженности подбородочно-губной складки. Особое внимание
обращают на форму и размеры углов нижней челюсти, форму ушных раковин.
Оценивая состояние височно-нижнечелюстных суставов, детально
анализируют объем и характер движений нижней челюсти. При осмотре полости рта
обращают внимание на соотношение зубных рядов, форму зубных дуг,
положение отдельных зубов, их форму и размеры. Анализируют состояние слизистой
оболочки полости рта, оценивают форму неба, функцию мягкого неба и языка.
После полного клинического обследования больного с аномалией или
деформацией лицевого черепа и зубочелюстной системы приступают к
объективной оценке состояния мягких тканей лица, костного остова лица и
зубочелюстной системы при помощи дополнительных методов: 1) изучения
диагностических моделей челюстей; 2) рентгенологического обследования;
3) анализа фотографий лица больного в прямой и боковой проекциях; 4)
функциональных исследований (электромиография, электроэнцефалография, рео-
полярография, ринопневмометрия, фоторегистрация движений нижней
челюсти).
Для каждого больного целесообразно изготовить две пары гипсовых
моделей челюстей, одну из них используют для планирования хирургического
лечения, другую для измерения. На моделях определяют размеры зубов и угол
их наклона, ширину зубной дуги, глубину неба, длину переднего отрезка зубных
дуг, а также форму зубного ряда, симметричность правой и левой его
половины. Измерение ширины зубных рядов в области первых малых коренных зубов
и первых больших коренных зубов проводят по методу Понта, а длины
переднего отрезка зубной дуги — по методу Коркхауза. Изучение взаимоотношения
256
зубных рядов проводят в трех плоскостях после фиксации гипсовых моделей
в положении центральной окклюзии в окклюдаторе.
В схему рентгенологического обследования больных с аномалиями и
деформациями лицевого черепа и зубочелюстной системы включают терелерентгено-
графию в прямой и боковой проекциях, ортопантомографию, рентгенографию
в полуаксиальной проекции, томографию височно-нижнечелюстных суставов
при открытом и закрытом рте, зонографию, панорамную рентгенографию.
Краниометрическое рентгенографическое исследование в трех проекциях
(прямая, боковая и полуаксиальная) нашло широкое применение в ортодонтии
и челюстно-лицевой хирургии. Следует отметить, что данные
телерентгенографического исследования характеризуются значительной вариабельностью и
зависят от пола, возраста, этнических особенностей и индивидуальных черт
строения лицевого и мозгового черепа. Кроме того, на полученные результаты
существенное влияние оказывают технические условия съемки, ошибки в ее
проведении, а также субъективные погрешности при разметке и измерении
линейных и угловых показателей на телерентгенограммах. Основными
достоинствами телерентгенографии являются: широкая возможность прижизненного
анализа основных параметров лицевого и мозгового черепа в различных
проекциях, определение точной локализации деформации и оценка характера
нарушений, регистрация их изменений в процессе роста и лечения.
При расшифровке телерентгенограмм в прямой и боковой проекциях
следует использовать определенные ориентиры, измерять ряд линейных и
угловых параметров (рис. 26.2, 26.3, 26.4). Детальное изучение линейных
размеров и угловых параметров на телерентгенограммах в прямой и боковой
проекциях позволяет получить цифровые данные и на их основании
провести анализ взаимного расположения отделов лицевого черепа, а также мягких
тканей лица. При телерентгенографическом исследовании можно установить
положение верхней челюсти по отношению к основанию черепа, положение
нижней челюсти по отношению к основанию черепа, их расположение по
отношению друг к другу и к основанию черепа, размеры базисов верхней и
нижней челюстей, локализацию зубных рядов по отношению к базисам
челюстей, определить идентичность размеров правой и левой половины лица
или их несоответствие.
На полуаксиальных снимках и ортопантомограммах оценивают
состояние околоносовых пазух носа. О состоянии височно-нижнечелюстных
суставов судят по данным ортопантомографии, томографии при открытом и
закрытом рте, зонографии. Структуру костной ткани челюстей, альвеолярных
отростков изучают на увеличенных панорамных рентгенограммах или
прицельных внутриротовых рентгенограммах.
Функциональные методы исследования используют для оценки
состояния мимических и жевательных мышц, кровоснабжения мягких и костных
тканей челюстно-лицевой области.
Дифференциальная диагностика деформаций челюстей
представляет значительные трудности. Она основывается на данных клинического
обследования больных с деформациями, результатах телерентгенографического
исследования, анализе биометрических показателей измерения моделей
челюстей. Следует дифференцировать микро- и макрогнатию, микро- и ретрогнатию,
макро- и прогнатию, а также верхнюю микро- или ретрогнатию и нижнюю
макро- или прогнатию, верхнюю макро- или прогнатию и нижнюю микро-
ил и ретрогнатию. Необходимо подчеркнуть, что у взрослых больных с
аномалиями и деформациями лицевого черепа и зубочелюстной системы, как
правило, встречаются сочетанные деформации челюстей, причем степень каждой
из них может быть определена в процессе дифференциальной диагностики.
257
17- 1263
Рис. 26.2. Расположение основных
ориентиров и измерение линейных
показателей на телерентгенограмах
в прямой проекции (схема).
R0— R0 — надглазничная плоскость;
Or—Or — глазничная плоскость; Мх—
Мх — плоскость базиса верхней
челюсти; ОС|—ОС| — окклюзионная
плоскость; Jo — Jo — нижнечелюстная
плоскость; RO|— ОС|— Jo( — точки
пересечения перпендикуляра,
опушенного на плоскость через наружный
край орбиты; Μ—Μ — расстояние
между медиальными стенками глазниц
Рис. 26.3. Расположение основных ориентиров и измерение линейных показателей
на телерентгенограммах в боковой проекции (схема).
NS — размер базиса основания черепа; Sna—Snp — размер базиса верхней челюсти; МТ| — размер
тела нижней челюсти; МТ2 — размер ветви нижней челюсти; А — наиболее глубокая точка
переднего контура верхней челюсти; В — наиболее глубокая точка переднего контура нижней
челюсти; J η — наиболее выступающая точка подбородка; Me — наиболее низкая точка тела нижней
челюсти; Ва — передняя точка большого затылочного отверстия; At — верхнепередняя точка I
шейного позвонка; N(—Ме, — проекция точек N и Me; Sj—Jof — проекция точек S и Jo; Jo —
угол нижней челюсти; Aj — точка пересечения перпендикуляра, опущенного из точки N с
базисом нижней челюсти; Snp—At — сагиттальный размер носоглотки; Je—Ph — сагиттальный
размер ротоглотки; ПЛВ — передняя лицевая высота; ПВЛВ — передневерхняя лицевая высота,
ПНЛ В — передненижняя лицевая высота; ЗЛВ — задняя лицевая высота; ЗВЛВ — задневерхняя
лицевая высота; ЗНЛВ — заднейижняя лицевая высота.
Рис. 26.4. Измерение угловых показателей на телерентгенограммах в боковой проекции.
N — точка назион; S — точка середины входа в турецкое седло; С — верхняя точка мыщелка
нижней челюсти; Ва — передняя точка большого затылочного отверстия; At — передневерхняя
точка контура I шейного позвонка; Jo — угол нижней челюсти; В — самая глубокая точка на
переднем контуре нижней челюсти; А — самая глубокая точка на переднем контуре верхней челюсти;
Snp — вершина задней носовой ости.
26.4. Показания к хирургическому лечению
и принципы его планирования
Больные с аномалиями лицевого черепа и деформациями зубочелюстной сие-
темы в первую очередь отмечают эстетические нарушения, которые нередко
приводят к развитию вторичных психических реакций. Многие исследователи
подчеркивают, что эти нарушения носят обратимый характер. Вовремя про-
веденное эффективное хирургическое лечение позволяет добиться полной
психосоциальной реабилитации больных с аномалиями и деформациями
лицевого черепа и зубочелюстной системы.
Не менее важны при деформациях зубочелюстной системы и
функциональные расстройства функций различных органов и систем. Пациенты
предъявляют жалобы на затрудненное откусывание и пережевывание пищи
вследствие нарушения правильных взаимоотношений зубных рядов верхней
и нижней челюстей и отсутствия множественного фиссурно-бугоркового
контакта между зубами-антагонистами. Кроме того, возможны нарушение речи,
дыхания, функций органов желудочно-кишечного тракта. У пациентов с
дефектами и деформациями зубочелюстной системы образуется своеобразный
порочный круг: аномалии прикуса вызывают патологические сдвиги в
нервной и пищеварительной системах, органах дыхания, а взаимосвязь между
этими органами и системами способствует дальнейшему прогрессированию
функциональных отклонений вплоть до структурных изменений органов.
При наличии зубочелюстных аномалий встречается поражение тканей па-
родонта зубов различных групп из-за их недогрузки или, наоборот, перегрузки.
В конечном счете это ведет к изменению функции жевательных мышц,
нарушению нормальных анатомо-топографических соотношений, а затем к
дисфункции височно-нижнечелюстного сустава.
Следовательно, устранение или предупреждение перечисленных
функциональных нарушений является важным показанием к медицинской
реабилитации больных с аномалиями и деформациями лицевого черепа и
зубочелюстной системы.
Успешная медицинская реабилитация больных с врожденными и
приобретенными деформациями лицевого черепа зависит от точности диагностики
нарушений, оптимального планирования консервативного и хирургического
лечения с привлечением смежных специалистов (ортодонт, психоневролог,
ортопед, логопед, оториноларинголог, челюстно-лицевой хирург, а при
необходимости невропатолог и нейрохирург) и квалифицированного
послеоперационного ведения больных.
Детальное изучение клинической картины у больных с аномалиями и
деформациями лицевого черепа и зубочелюстной системы, анализ
рентгенологических данных, оценка фотографий, расчет моделей челюстей позволяют
получить исчерпывающие данные о нарушениях у конкретного пациента.
Планирование лечения начинают с определения порядка и
последовательности лечебных мероприятий, их объема и сроков выполнения.
Существенным моментом является активное участие в нем самого больного.
Подробное ознакомление пациента с выявленными нарушениями, доступное
объяснение плана лечения на всех этапах медицинской реабилитации с учетом
последних достижений медицинской науки значительно повышают
эффективность лечения, так как больной выступает в роли целеустремленного
помощника врача. Однако мнение больного не является решающим при
определении объекта хирургического вмешательства и степени перемещения
остеотомированных фрагментов. Вопросы лечебной стратегии и тактики на
основании объективных данных, полученных при обследовании, обязан ре-
259
17*
шать врач, который в разумных пределах учитывает пожелания пациента.
В плане лечения должно быть предусмотрено не только устранение
эстетических нарушений, но также исправление функциональных недостатков.
При скелетных формах деформации ведущую роль в планировании
лечения должен играть челюстно-лицевой хирург, который совместно с другими
специалистами определяет необходимость подготовительного лечения перед
операцией, выбирает метод хирургического лечения и объект для
вмешательства. В случае необходимости на фотоснимках, копиях телерентгенограмм,
моделях челюстей моделируют предполагаемое оперативное вмешательство и
воспроизводят ожидаемые результаты хирургического лечения.
При лечении больных ,с аномалиями и деформациями лицевого черепа
и зубочелюстной системы рекомендуется соблюдать такую
последовательность реабилитационных мероприятий: предоперационная подготовка
(рациональное ортодонтическое лечение в детском и подростковом возрасте), ко-
стно-реконструктивная операция на лицевом черепе, в возрасте старше 16 лет,
завершающее ортодонтическое и ортопедическое лечение, корригирующие и
пластические операции на мягких тканях лица для устранения остаточных
послеоперационных деформаций.
Цель предоперационного ортодонтического лечения заключается в
исправлении положения отдельных зубов, улучшении формы зубных дуг с
учетом послеоперационного положения челюстей. Ортодонтическое лечение,
проводимое на этом этапе медицинской реабилитации, должно обеспечить
множественный фиссурно-бугорковый контакт зубов-антагонистов.
Большое значение в предоперационной подготовке больных с
аномалиями и деформациями лицевого черепа и зубочелюстной системы имеет
ортопедическое лечение. Его основная задача состоит в замещении дефектов
зубных рядов зубными протезами различной конструкции, обеспечивающими
множественные контакты между зубами-антагонистами. При этом следует
учитывать послеоперационное положение челюстей.
Существуют две точки зрения на сроки проведения хирургического
лечения. Одни специалисты считают, что при аномалиях и деформациях
лицевого черепа и зубочелюстной системы оперативное вмешательство
следует проводить в раннем детском возрасте. По их мнению, раннее
хирургическое лечение позволяет избежать или значительно уменьшить
выраженность вторичных деформаций. Другая точка зрения заключается в
том, что успешное лечение больных хирургическими методами возможно
лишь после завершения роста и развития лицевого и мозгового черепа, т. е.
в возрасте 16—18 лет. По мнению сторонников данной точки зрения,
раннее оперативное вмешательство вызывает повреждение зон роста, что в
свою очередь ведет к развитию тяжелых вторичных деформаций лицевого
и мозгового черепа.
Все изложенное выше свидетельствует о том, что к хирургическому
лечению больных с аномалиями и деформациями лицевого черепа и
зубочелюстной системы следует подходить дифференцированно: на верхней челюсти
оперативное вмешательство можно производить в возрасте 15—16 лет, когда
завершается ее рост и развитие, а на нижней — в возрасте 18—20 лет.
Особенности предоперационной подготовки и анестезиологического
обеспечения. Поступивший на лечение больной с аномалией или деформацией
лицевого черепа и зубочелюстной системы должен быть детально ознакомлен
с результатами обследования, планом операции, видом обезболивания,
особенностями предполагаемого хирургического лечения, особенностями
клинического течения послеоперационного периода, предупрежден о возможных
осложнениях.
260
Помимо общепринятой клинико-лабораторной оценки состояния
организма больного, которого в плановом порядке подготавливают к
оперативному вмешательству, необходимо учитывать ряд особенностей.
При выполнении костно-реконструктивных операций на лицевом
черепе необходимо обеспечить надежное обезболивание с блокадой
отрицательных нейровегетативных реакций. Для качественного хирургического
лечения, связанного с перемещением остеотомированных костных фрагментов
челюстей, и точного их сопоставления и фиксации в правильном положении
необходимо обеспечить интубацию трахеи через нос.
В период подготовки больного к операции из полости рта, носоглотки, зева,
уха берут материал для определения вида микрофлоры и ее чувствительности
к антибиотикам. Послеоперационную антибиотикотерапию проводят с учетом
антибиотикограмм, используя препараты широкого спектра действия.
Накануне операции фиксируют в полости рта гнутые проволочные
стальные шины с зацепными петлями, а также изготовленные зубные
протезы или ретенционно-шинирующие аппараты. Нередко в связи с
невозможностью адаптации к этим конструкциям в условиях деформации
изготовленные аппараты и протезы фиксируют непосредственно перед операцией.
При необходимости на основании данных, полученных при изучении
моделей челюстей, пришлифовывают бугры зубов-антагонистов для
получения множественного фиссурно-бугоркового контакта в послеоперационном
периоде.
После перемещения костных фрагментов при костно-реконструктивных
операциях на лицевом черепе, как правило, образуются дефекты, которые
необходимо заполнить костными трансплантатами. В процессе подготовки к
операции хирург должен определить, какой вид костных трансплантатов (ауто-
или аллотрансплантаты) будет применен и соответствующим образом
подготовить пациента.
За бугры верхних челюстей наиболее целесообразно помещать
аллотрансплантаты из компактной кости, которые, длительное время перестраиваясь,
обеспечивают надежную фиксацию верхнечелюстного комплекса в новом
положении. Ортотопические костные аллотрансплантаты следует использовать
при возмещении сложных по форме анатомических образований средней и
нижней зон лицевого черепа (особенно у больных с сочетанными
несимметричными деформациями лицевого и мозгового черепа), дублируя их ауто-
трансплантатами (реберный, гребешок подвздошной кости) или наполняя их
губчатым веществом из гребешка подвздошной кости.
26.5. Принципы хирургического лечения больных с аномалиями
и деформациями лицевого черепа и зубочелюстной системы
В основу хирургического лечения больных с верхней прогнатией или макро-
гнатией положен метод сегментарной остеотомии фронтального отдела
верхней челюсти, позволяющий устранить эстетический недостаток и добиться
множественного контакта между зубами антагонистами (рис. 26.5). Операция
сегментарной остеотомии фронтального отдела верхней челюсти состоит в
следующем.
Под эндотрахеальным наркозом проводят Г-образные разрезы
слизистой оболочки и надкостницы с вестибулярной стороны альвеолярного
отростка верхней челюсти на уровне 5]_5 до верхнего свода преддверия полости
рта. Слизисто-надкостничные лоскуты с обеих сторон отслаивают до уровня
313 зубов и свободные их концы берут на держалки. Удаляют 4J4 зубы и через
261
Рис. 26.5. Основные этапы сегментарной остеотомии фронтального отдела верхней
челюсти а — г (схема).
лунки удаленных зубов производят остеотомию и остэктомию на
планируемую величину, начиная от гребня альвеолярного отростка вертикально вверх
до уровня, располагающегося на 5 мм выше проекции верхушек корней
фронтальных зубов. Затем на данном уровне формируют мягкотканный
туннель до края грушевидного отверстия на уровне дна носового хода. Отводя
мобилизованные мягкие ткани, выполняют остеотомию и остэктомию,
соединяя вершину вертикального распила кости с дном нижнего носового хода.
Аналогичные манипуляции осуществляют и на противоположной стороне.
Затем отслаивают слизисто-надкостничные лоскуты и со стороны твердого
неба по направлению к средней линии в проекции удаленных 4[4 зубов.
После введения в сформированный туннель специальных защитных лопаток
производят остеотомию и остэктомию в области небных пластинок верхних
челюстей и небной кости. Через вертикальный разрез слизистой оболочки по
уздечке верхней губы скелетируют дно носа в переднем отделе и нижние
отделы перегородки носа. Остеотомом пересекают перегородку носа до того
262
уровня, на котором произведена остеотомия неба. При необходимости
резецируют нижний отдел хрящевой перегородки носа на нужную величину.
Размеры остэктомированных участков на уровне удаленных 4]4 зубов и
дна нижнего носового хода, а также резецированного участка твердого неба
и нижнего отдела хрящевой перегородки носа зависят от расстояния и
направления, в котором перемещают остеотомированный сегмент
фронтального отдела верхней челюсти. В правильном по прикусу положении костный
фрагмент фиксируют проволочными швами или мини-пластинками по
краям грушевидного отверстия. Слизисто-надкостничные лоскуты укладывают
на место и фиксируют кетгутом. Для обеспечения надежной и жесткой
фиксации остеотомированного сегмента на зубы верхней челюсти целесообразно
наложить гладкую шину-скобу. Нижние носовые ходы тампонируют на 1 —
2 сут для остановки кровотечения.
Усовершенствованная методика сегментарной остеотомии фронтального
отдела верхней челюсти обеспечивает: 1) хорошее кровоснабжение
остеотомированного сегмента и жизнеспособность зубов за счет мягкотканных
питающих лоскутов с вестибулярной стороны и со стороны твердого неба; 2)
проведение остеотомии и остэктомии под визуальным контролем на удалении от
верхушек зубов, чем объясняются их высокая жизнеспособность и
устойчивое положение; 3) условия для значительного перемещения
остеотомированного сегмента (вверх, вниз, кзади); 4) хороший операционный доступ и обзор
операционного поля, что позволяет избежать повреждения корней зубов и
питающих сосудов; 5) оптимальные условия для течения процессов репара-
тивной регенерации за счет создания плотного контакта костных фрагментов
и их надежной фиксации.
При лечении больных с нижней микро- или ретрогнатией выполняют
такие оперативные вмешательства, которые позволяют увеличить размеры
нижней челюсти либо изменить ее положение путем перемещения кпереди,
восстанавливая тем самым оптимальные эстетические пропорции лицевого черепа.
В настоящее время наиболее широкое распространение в клинической
практике получили операции в области угла и ветви нижней челюсти. Это
связано с тем, что их производят вне зубного ряда и формируют большие
контактирующие костные поверхности, обеспечивая тем самым
значительный диапазон перемещенных костных фрагментов. Кроме того, в процессе
операции можно переместить точки прикрепления жевательных мышц.
Чаще всего плоскостную остеотомию нижней челюсти в области ветвей
производят внутриротовым (по Обвегезеру) и наружным (по Митрофанову и
Рудько) доступами.
При внутриротовом доступе методика хирургического лечения состоит
в следующем. Под эндотрахеальным наркозом проводят разрез слизистой
оболочки по крыловидно-нижнечелюстной складке с переходом на
наружную поверхность тела нижней челюсти до уровня нижнего свода преддверия
полости рта. Затем рассекают надкостницу по переднему краю ветви нижней
челюсти. Распатором скелетируют наружную поверхность ветви нижней
челюсти до заднего края, который также скелетируют изогнутым распатором.
В рану вводят специальный крючок, который, будучи фиксирован за задний
край ветви, позволяет отвести в сторону мягкие ткани щеки, что
обеспечивает хороший обзор операционного поля.
С внутренней стороны ветви нижней челюсти выше проекции
сосудисто-нервного пучка нижней челюсти поднадкостнично отслаивают мягкие
ткани в виде туннеля до заднего края ветви нижней челюсти. В
образовавшийся туннель вводят другой специальный крючок, который также
фиксируют за задний край ветви нижней челюсти выше первого.
263
Затем при помощи бора пропиливают внутреннюю компактную
пластинку ветви нижней челюсти выше места вхождения сосудисто-нервного
пучка по проекции внутреннего крючка. Линию остеотомии продолжают по
переднему краю ветви нижней челюсти, переходя на наружную поверхность
ветви. Завершают пропил наружной компактной пластинки у нижнего края
челюсти. Тонким остеотомом, располагая его ближе к наружной компактной
пластинке ветви нижней челюсти, расщепляют ветвь нижней челюсти по
плоскости. Фиксируя крючки за задний край ветви, предупреждают
проникновение остеотома за пределы ветви нижней челюсти. Аналогичную
операцию проводят и с противоположной стороны. Центральный фрагмент
нижней челюсти перемещают вперед в правильное по прикусу положение и
фиксируют межчелюстной резиновой тягой. Костные фрагменты фиксируют
винтами или проволочными швами. Затем через контрапертуры в
подчелюстных областях в рану вводят трубчатые силиконовые дренажи диаметром
5 мм. Рану со стороны слизистой оболочки наглухо зашивают кетгутом.
Плоскостную остеотомию нижней челюсти в области ветвей наружным
доступом по Митрофанову и Рудько осуществляют следующим образом.
Под эндотрахеальным наркозом в подчелюстной области проводят
разрез кожи длиной 6—7 см, окаймляющий угол нижней челюсти. Послойно
рассекают кожу, подкожную жировую клетчатку и подкожную мышцу шеи.
Скальпелем рассекают надкостницу на протяжении 3 см, начиная от угла
нижней челюсти по ее нижнему краю. Распатором скелетируют наружную
поверхность ветви нижней челюсти до полулунной вырезки. Затем обнажают
передний и задний края ветви нижней челюсти. Отступя книзу 0,5—0,7 см от
полулунной вырезки по переднему и заднему краям ветви нижней челюсти,
бором выпиливают насечки, на уровне которых иглой Дешана отслаивают
надкостницу с внутренней стороны ветви выше сосудисто-нервного пучка
нижней челюсти. Затем, начиная с насечки по переднему краю ветви нижней
челюсти, бором производят параболической формы пропил кости до
губчатого вещества с переходом на наружную поверхность тела челюсти, нижний
край и заднюю поверхность ветви до насечки. При помощи иглы Дешана с
внутренней поверхности ветви проводят лавсановую лигатуру, при помощи
которой вводят пилу Джигли и пропиливают ею внутреннюю компактную
пластинку ветви на уровне насечек. При помощи лопатки Буяльского и
остеотома расщепляют ветвь нижней челюсти по плоскости (рис. 26.6).
Аналогичную операцию выполняют с другой стороны. Центральный фрагмент
перемещают вперед, фиксируют в правильном по прикусу положении и в
области ветвей производят остеосинтез проволочными швами, винтами или
накостными мини-пластинками. Рану послойно ушивают кетгутом, на кожу
накладывают швы полиамидной нитью. Между швами вводят выпускники из
перчаточной резины.
Для восстановления правильного и эстетически полноценного контура
нижней зоны лица разработана методика ступенчатой гениопластики. Этот
способ гениопластики показан при достаточной высоте подбородочного
отдела нижней челюсти.
Под эндотрахеальным наркозом на нижнюю губу на уровне углов рта
накладывают две держалки из лавсановой нити. Зубы верхней и нижней
челюстей покрывают салфеткой, смоченной раствором антибиотика, для изоляции
их от операционного поля. После инфильтрации мягких тканей
подбородочной области и нижней губы раствором новокаина проводят разрез длиной 6—
7 см слизистой оболочки нижней губы на 1 — 1,5 см выше нижнего свода
преддверия полости рта и параллельно ему. Рассекают ткани до мышечного
слоя, достигают переднего края тела нижней челюсти, пересекают надкост-
264
ницу и скелетируют
подбородочный отдел нижней челюсти до
уровня вторых малых коренных зубов
нижней челюсти.
Бором и циркулярной пилой
производят горизонтальную
остеотомию нижнего отдела подбородка,
пересекают нижние пучки
двубрюшных мышц и перемещают вперед ос-
теотомированный подковообразный
фрагмент на мягкотканной
питающей ножке. В новом положении ос-
теотомированный фрагмент
фиксируют тремя проволочными швами
либо мини-пластинками (рис. 26.7,
26.8). Рану со стороны полости рта в
три слоя зашивают кетгутом. Через
контрапертуру в подподбородочной
области в рану вводят выпускник из
перчаточной резины. Накладывают
формирующую бинтовую повязку.
В основу лечения больных с
верхней микрогнатией или ретрогна-
тией положен принцип
перемещения остеотомированного фрагмента
верхнечелюстного комплекса
кпереди в правильное по прикусу
положение.
Сущность оперативного
лечения состоит в следующем. Под эн-
дотрахеальным наркозом проводят
разрез слизистой оболочки и
надкостницы выше на 0,5 см верхнего
свода преддверия полости рта от 7|
до [7 зуба. Распатором скелетируют
передние поверхности верхних челюстей до уровня нижнеглазничных
отверстий, края грушевидного отверстия, нижние отделы скуловых костей и бугры
верхних челюстей — до крыловидных отростков основной кости. Затем
скелетируют дно носа, латеральные стенки носа и перегородку на уровне
нижних носовых ходов. При помощи бора производят остеотомию верхней
челюсти, начиная от основания грушевидного отверстия, под углом 45—60°
кверху до уровня нижнеглазничного отверстия. Линию остеотомии
продолжают горизонтально, огибая нижнеглазничное отверстие, до скуловерхнече-
люстного шва и захватывают нижние отделы скуловой кости, направляясь к
ее нижнему краю.
В области скуловерхнечелюстного шва формируют костное окно, через
которое тонким остеотомом производят остеотомию бугра верхней челюсти до
крыловидных отростков основной кости. Бугор верхней челюсти отделяют от
крыловидных отростков специально изогнутым остеотомом. Тонким
остеотомом от вершины сформированного треугольника вниз рассекают медиальную
стенку верхнечелюстной пазухи до дна носа, а затем линию остеотомии
продолжают горизонтально на уровне дна носа до крыловидных отростков. В
последнюю очередь на уровне дна носа пересекают хрящевую и костную части
Рис. 26.6. Плоскостная остеотомия в области
ветви нижней челюсти (я, б) (схема).
265
un^ Hn -wfiax веохней челюсти фиксируют лигатуру-держалку.
Рис 76 9 Остеотомия верхнечелюстного комплекса (схема).
а - вил снаружи; о- вид изнутри со стороны полости носа.
266
Рис. 26.10. Фиксация остеотомированного
фрагмента верхнечелюстного комплекса (схема).
У — линия остеотомии; 2— костный проволочный
шов; 3 — костный аллотрансплантат.
отростками основной кости фор-
малинизированных аллотранс-
плантатов необходимой
толщины из компактной кости и
наложением двух проволочных
швов по краям грушевидного
отверстия либо осуществляют
остеосинтез мини-пластинками
(рис. 26.10).
Сформированные в
процессе остеотомии костные
треугольные выступы обеспечивают
надежную фиксацию костного
фрагмента, предупреждают
смещение остеотомированного
фрагмента кзади.
Костно-реконструктивные
операции, применяемые при
лечении больных с нижней мак-
рогнатией или прогнатией,
основаны на смещении нижней
челюсти кзади. При этом
наиболее часто выполняют
остеотомии нижней челюсти в области
ветвей, которые описаны выше.
Следует отметить, что
плоскостная остеотомия ветвей нижней челюсти вызывает изменение элементов ви-
сочно-нижнечелюстного сустава, что может неблагоприятно отразиться на
его функции.
Более приемлема вертикальная субкондилярная остеотомия ветви нижней
челюсти, которая позволяет сохранить правильные взаимоотношения в височ-
но-нижнечелюстном суставе. Остеотомия выполняется следующим образом.
Под эндотрахеальным наркозом производят разрез кожи в
подчелюстной области длиной 4—5 см, окаймляющий угол нижней челюсти и
отстоящий от нижнего края челюсти на 2 см. Послойно рассекают кожу,
подкожную жировую клетчатку, подкожную мышцу шеи. По нижнему краю челюсти
в области угла рассекают надкостницу и скелетируют наружную поверхность
ветви нижней челюсти до полулунной вырезки. Освобождают от мягких
тканей задний край ветви и ее внутреннюю поверхность в дистальных отделах.
Затем бором производят вертикальную остеотомию ветви, начиная от
основания мыщелкового отростка до угла нижней челюсти. Параллельно первому
распилу производят второй в пределах наружной компактной пластинки.
Ширина удачяемой наружной компактной пластинки соответствует
планируемому смещению нижней челюсти кзади. Фрезой производят декортикацию
малого фрагмента с внутренней поверхности. Центральный фрагмент смещают
кзади и фиксируют в правильном положении. Костные фрагменты фиксируют
проволочными швами, винтами либо мини-пластинками (рис. 26.11). Рану
послойно ушивают кетгутом. На кожу накладывают швы из полиамидной нити.
В рану вводят выпускники из перчаточной резины.
У взрослых больных, как правило, диагностируют сочетанные
деформации челюстей, при устранении которых комбинируют описанные выше
методы хирургического лечения. Выбор того или иного вида оперативного
вмешательства зависит от характера морфологических нарушений при деформации.
267
При хирургическом лечении
больных с верхней и нижней мак-
рогнатией и увеличением
преимущественно вертикальных размеров
лицевого черепа следует
использовать двухэтапную методику лечения.
Под эндотрахеальным наркозом
проводят разрез слизистой оболочки
и надкостницы на 0,5 см выше
верхнего свода преддверия полости рта
от 7] до [7 зуба. Слизисто-надкост-
ничный лоскут отслаивают кверху
до уровня нижнеглазничных
отверстий, обнажая передние стенки
верхних челюстей, скулоальвеолярные
гребни, нижний отдел скуловых
костей, бугры верхних челюстей до
крыловидных отростков основной кости,
дно и латеральные стенки полости
носа, а также нижние отделы
перегородки носа. В зависимости от
величины, на которую необходимо
переместить остеотомированный нижний
отдел верхнечелюстного комплекса
вверх и кзади, производят
остеотомию бором и остэктомию фрезой
необходимого диаметра по всей
линии остеотомии, начиная от
основания нижнего носового хода
горизонтально до скулоальвеолярного гребня
и затем кзади до крыловидных
отростков. Затем специальным изогнутым
остеотомом бугор верхней челюсти
отсоединяют от крыловидных
отростков. Латеральные стенки носа и
перегородку носа пересекают на уровне
дна носа специальными тонкими ос-
теотомами с ограничителями.
Аналогичную операцию производят на другой верхней челюсти. Остеотомированный
нижний отдел верхнечелюстного комплекса смещают вниз и вперед. Фрезой
заканчивают остэктомию в области медиальных стенок верхних челюстей,
нижних отделах костной перегородки носа и дистальных отделах бугров верхних
челюстей. Ножницами резецируют на необходимую величину нижний отдел
хрящевой перегородки носа. Нижние носовые раковины также удаляют.
Нижний отдел верхнечелюстного комплекса поднимают кверху, смещают
назад и, установив в правильное положение, фиксируют четырьмя
проволочными швами по краям грушевидного отверстия и по скулоальвеолярным
гребням (рис. 26.12, 26.13). Слизисто-надкостничные лоскуты укладывают на
место и фиксируют кетгутовыми швами. Производят плотную тампонаду
носовых ходов на 2—3 сут. Через 4—6 мес после первого этапа выполняют
операцию на подбородочном отделе нижней челюсти.
Тяжелые несимметричные сочетанные деформации лицевого черепа
характеризуются нарушением положения и размеров костей лица в трех взаимно
б
Рис. 26.11. Вертикальная субкондилярная
остеотомия ветви нижней челюсти (схема).
а — линия распила ветви нижней челюсти; о—
фиксация костных фрагментов.
268
Рис. 26.12. Остеотомия и остэктомия при деформациях лицевого черепа с увеличением
вертикальных размеров (схема).
а — вид в профиль при остеотомии и остэктомии; б — вид в фас при остеотомии.
перпендикулярных плоскостях (вертикальной, сагиттальной и трансверсаль-
ной). Хирургическое лечение осуществляют в один этап.
Для исправления положения верхнечелюстного комплекса производят
его остеотомию на уровне нижнего носового хода. На увеличенной стороне
лица по всей линии остеотомии верхнечелюстного комплекса осуществляют
остэктомию фрезой на величину, равную половине разницы в размерах
между окклюзионной и надглазничной плоскостями справа и слева. Нижний
отдел верхнечелюстного комплекса после остэктомии на больной стороне
разворачивают с опорой на костно-хрящевую перегородку носа до
положения, обеспечивающего параллельное расположение окклюзионной и
надглазничной плоскостей.
На малой стороне между костными фрагментами образуется диастаз, в
который помещают костный аллотрансплантат или аутотрансплантат, взятый
из резецированного нижнего края тела нижней челюсти. Аутотрансплантат
следует располагать губчатым слоем в сторону покрывающих его мягких тканей.
Фиксацию остеотомированного фрагмента осуществляют четырьмя
проволочными швами по краям грушевидного отверстия и по скулоальвеолярным
гребням либо мини-пластинками.
На нижней челюсти с малой стороны производят вертикальную
остеотомию ветви нижней челюсти по методике Рудько, смещая центральный
фрагмент нижней челюсти вниз на необходимое расстояние. Костные фрагменты
в новом положении фиксируют двумя проволочными швами. На большой
стороне также производят вертикальную остеотомию ветви нижней челюсти.
Затем увеличенный в размерах мыщелок нижней челюсти выделяют вместе
с дистальным краем ветви, резецируют, а из оставшегося участка заднего края
ветви нижней челюсти формируют новую головку. Сформированный новый
269
Рис. 26.13. Фиксация костных
фрагментов после устранения
вертикальной деформации лицевого
черепа (схема).
а — вид в профиль; б — вид в фас.
мыщелок реплантируют и
после перемещения заднего края
ветви кверху фиксируют двумя
проволочными лигатурами.
Часть увеличенного тела
нижней челюсти иссекают таким
образом, чтобы
нижнечелюстная плоскость располагалась
параллельно надглазничной
плоскости. При этом нередко
приходится выделять
сосудисто-нервный пучок нижней
челюсти из нижнечелюстного
канала (рис. 26.14, 26.15).
Операцию заканчивают
послойным зашиванием ран в
подчелюстных областях и по
верхнему своду преддверия
полости рта.
При лечении больных с
тяжелыми несимметричными
деформациями лицевого
черепа, вызванными гемифациаль-
ной микросомией II и III
степени, необходимо большое
количество костно-пластиче-
ского материала. При
использовании с этой целью аутотранс-
плантатов костной ткани время
и тяжесть операции
значительно увеличиваются (рис. 26.16).
С учетом описанных выше недостатков существующих методов
хирургического лечения больных с гемифациальной микросомией, разработан
новый способ оперативного лечения, основанный на использовании ортотопи-
ческих аллотрансплантатов.
Под эндотрахеальным наркозом в подчелюстной области на стороне
поражения, отступя от края нижней челюсти, проводят разрез кожи, учитывая
диапазон перемещения нижней челюсти вниз. Скелетируют наружную
поверхность тела и ветви нижней челюсти. Часть рудимента ветви нижней
челюсти удаляют. На наружной поверхности тела и ветви нижней челюсти и на
нижней поверхности височной кости создают воспринимающее ложе для ор-
тотопического аллотрансплантата. Затем через разрез в подчелюстной
области на здоровой стороне скелетируют ветвь нижней челюсти и производят
вертикальную скользящую остеотомию ветви нижней челюсти. Выше верхнего
свода преддверия полости рта на 0,5 см проводят разрез слизистой оболочки
270
Рис. 26.14. Остеотомия при сочетанных несимметричных деформациях (а — в)
(схема).
Рис. 26.15. Фиксация костных фрагментов при сочетанных несимметричных
деформациях лицевого черепа (о-в) (схема).
Рис. 26.16. Реконструкция лицевого черепа при гемифациальной микросомии II (а)
и III (б) степени по Обвегезеру (схема).
и надкостницы от 7J до |7 зуба.
Мягкие ткани отслаивают до уровня
нижнеглазничного отверстия,
обнажая передние поверхности верхних
челюстей, нижние отделы скуловых
костей, бугры верхних челюстей до
крыловидных отростков основной
кости. Затем скелетируют дно,
латеральные стенки и нижние
отделы перегородки носа на уровне
нижних носовых ходов. Для
исправления положения окклюзион-
ной плоскости производят
остеотомию верхнечелюстного комплекса
на уровне дна нижнего носового
хода с остэктомией на здоровой
стороне (рис. 26.17).
Остеотомированный фрагмент
верхнечелюстного комплекса
разворачивают и устанавливают
параллельно надглазничной плоскости, а
образовавшийся диастаз на стороне
деформации закрывают
трансплантатом, сформированным из
удаленного рудимента ветви нижней
челюсти, или аллотрансплантатом.
Остеотомированный нижний отдел
верхнечелюстного комплекса в
правильном положении
фиксируют четырьмя проволочными швами
по краям грушевидного отверстия
и по скулоальвеолярным гребням.
По направлению к височно-ниж-
нечелюстному суставу на стороне
деформации из скуловой области
формируют мягкотканный
туннель, через который проводят
недостающий участок скуловой
кости и скуловую дугу аллотрансплантата, введенного в рану подчелюстной
области на стороне аномалии. Височно-нижнечелюстной сустав
аллотрансплантата располагают в сформированном ложе на нижней поверхности
височной кости и фиксируют проволочными швами у рудимента скуловой
кости и дуги, а тело нижней челюсти аллотрансплантата фиксируют к
недоразвитой нижней челюсти после ее перемещения на необходимую
величину вниз и вперед. Центральный фрагмент нижней челюсти на здоровой
стороне перемещают вверх и фиксируют проволочными швами (рис. 26.18).
Раны послойно зашивают, оставляя выпускники из перчаточной резины.
Таким образом удается устранить нарушения и восполнить недостающие
анатомические образования при помощи сложного ортотопического
аллотрансплантата, состоящего из части скуловой кости, дуги, всего височно-нижнече-
люстного сустава, ветви и тела нижней челюсти.
Особенности послеоперационного ведения больных. После остеотомии
верхней челюсти производят тампонаду носа на 2—3 сут. В течение 4—5 сут по-
Рис. 26.17. Остеотомия (а) и остэктомия (б)
при гемифациальной микросомии III
степени (схема).
274
еле операции больные
нуждаются в интенсивной терапии,
направленной на корреляцию
дыхательных, гемодинамиче-
ских и метаболических
нарушений. В первые часы после
одноэтапных обширных
операций на верхнечелюстном
комплексе и нижней челюсти
нарушение адекватного
дыхания связано с изменением
привычных анатомических
взаимоотношений в области
носо- и ротоглотки, дна
полости рта, а также
продолжающимся незначительным
кровотечением из
операционной раны в полость рта.
Кровотечение спонтанно
прекращается через 2—4 ч после
завершения операции.
Для предупреждения
воспалительных осложнений с
профилактической целью в
течение 5—6 сут применяют
антибиотики и
сульфаниламиды широкого спектра
действия в терапевтических дозах.
Большое значение в
предупреждении воспалительных
осложнений имеет уход за
послеоперационной раной.
После операций на
нижней челюсти межчелюстную
фиксацию осуществляют на
следующие сутки, а после
операций на верхней
челюсти — на 6—7-е сутки после
восстановления
полноценного носового дыхания.
Фиксация костных фрагментов при
гемифациальной микросомии III степени (я, б)
(схема).
Для обеспечения оптимальных условий течения репаративнои
регенерации в зоне оперативного лечения используют широко известные принципы —
надежную иммобилизацию костных фрагментов и медикаментозное лечение
(витамины, кальция глицерофосфат, неробол). Применяют также
физические методы лечения — магнитотерапию, УВЧ-терапию. Электрофорез
кальция хлорида.
Продолжительность межчелюстной фиксации при операциях на нижней
челюсти составляет 35—45 сут, после операций на верхней челюсти — 50—60 сут.
18,:
275
СПИСОК ЛИТЕРАТУРЫ
Аболмасов Я. Г. Этиология, патогенез, диагностика и лечение прогении: Дис. ... д-ра
мед. наук. — Калинин, 1982. — 378 с.
Александров Н. М. Клиническая оперативная челюстно-лицевая хирургия. — Л.:
Медицина, 1985. — 448 с.
Безруков В. М. Клиника, диагностика и лечение врожденных деформаций лицевого
скелета: Дис. ... д-ра мед. наук. — М., 1981. — 329 с.
Гунько В. И. Клиника, диагностика и лечение больных с сочетанными деформациями
челюстей: Дис. ... д-ра мед. наук. — М., 1986. — 525 с.
Каламкаров X. А. Клиника и лечение зубочелюстных аномалий у детей. — Ташкент:
Медицина, 1978. — 268 с.
Каламкаров Χ. Α., Рабухина Η. Α., Безруков В. Λ/. Деформации лицевого черепа. — М.:
Медицина, 1981. — 239 с.
Сукачев В. А. Атлас реконструктивных операций на челюстях. — М.: Медицина, 1984. —
118 с.
Bell W. Η., Profflt W. P., White R. P. Surgical correction of dentofacial deformities. —
Vol. 1—2. — Philadelphia — London — Toronto: W. B. Saunders Company, 1980. —
1785 p.
Bell W. #., Proffit W. P., White R. P. Surgical correction of dentofacial deformities. — Vol. 3. —
Philadelphia — London — Toronto: W. B. Saunders Company, 1985. — P. 783.
Moore J. R. Surgery of the mouth and Jaws//Blackwell Scientific Publications. — Oxford,
1985. - 854 p.
Глава 27
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ
ПОСТТРАВМАТИЧЕСКИХ
ДЕФОРМАЦИЙ ЛИЦЕВОГО ЧЕРЕПА
Реабилитация больных с посттравматическими деформациями средней зоны
лица является одной из актуальных проблем хирургической стоматологии.
Наряду с повышением числа травм челюстно-лицевой области,
особенно сочетанных, увеличивается их тяжесть. Сложность анатомо-физиологиче-
ских связей костей средней зоны лица и основания черепа затрудняет
диагностику травматических повреждений. Недооценка этого, как правило,
влечет за собой тяжелые ошибки в лечении больных с сочетанной травмой,
что впоследствии приводит к грубым деформациям средней зоны лица и
функциональным нарушениям. Возникают диплопия, затруднение дыхания
через нос, развиваются дакриоцистит, ринит, снижается качество
пережевывания пищи.
Доказано преимущество ранней специализированной помощи по
сравнению с отсроченной, так как при своевременной помощи снижается
процент деформации костей средней зоны лица и функциональных нарушений
в этой области. Немаловажную роль играют методы репонирования костных
фрагментов, их иммобилизация [Александров Н. М., Аржанцев П. 3., 1996;
Бажанов Н. Н., Тер-Асатуров Г. П., 1991; Takaka N. et al., 1994].
27.1. Диагностика посттравматических деформаций
средней зоны лицевого черепа
Диагностика патологических изменений средней зоны лица затруднена, что
обусловлено разнообразными анатомо-физиологическими особенностями
функционирования органов зрения, дыхания, пищеварения, а также
обоняния. Учитывая локализацию в этом регионе жизненно важных органов лица,
необходимо привлечь смежных специалистов —- нейрохирурга,
оториноларинголога, офтальмолога, стоматолога [Безруков В. М. и др., 1995]. Для
решения всех этих проблем больных с посттравматическими деформациями
средней зоны лица обследуют с учетом трех взаимосвязанных видов
реабилитации — медицинской, профессиональной и социальной [Ипполитов В. П.,
1986].
При обследовании больных используют следующие методы диагностики:
общее клиническое обследование, лабораторные методы, анализ местного
статуса, изучение диагностических моделей лица и челюстей, фотографирование
лица, рентгенологическое исследование черепа и зубочелюстной системы, изу-
277
чение функционального состояния верхних дыхательных путей, зрения,
степени подвижности глазных яблок, слезоотделения и состояния слезопрово-
дящих путей, характера прикуса и состояния зубов [Ипполитов В. П. и др.,
1979; Бельченко В. А. и др., 1989].
На основании анализа клинико-рентгенологических данных
предложена рабочая классификация посттравматических деформаций средней зоны
лицевого черепа [Ипполитов В. П., 1986J.
I. Посттравматическая деформация скулоглазничной области:
1) скуловой области, нижнего края глазницы;
2) скуловой области, нижнего края и дна глазницы;
3) скуловой области и наружного края глазницы;
4) скуловой области, наружного края и боковых стенок глазницы.
И. Посттравматическая деформация носоглазничной области:
1) внутреннего угла глазницы, основания корня носа (одно- и двусторонняя);
2) нижнего края глазницы, костного отдела носа (одно- и двусторонняя);
3) нижнего края, дна глазницы, костно-хрящевого отдела носа (одно- и
двусторонняя);
4) нижнего края, дна и внутренней стенки глазницы, корня носа (одно- и
двусторонняя).
III. Посттравматическая деформация лобно-носоглазничной области:
1) костного отдела носа, передней стенки лобной пазухи, внутренней
стенки глазницы (одно- и двусторонняя);
2) основания корня носа, передней стенки лобной пазухи, внутренней и
нижней стенки глазницы (одно- и двусторонняя);
3) основания края носа, передней стенки лобной пазухи, внутренней
нижней и наружной стенки глазницы (одно- и двусторонняя).
IV. Нососкулоглазничная деформация.
V. Посттравматическая деформация максиллярно-лобно-нососкулоглазнич-
ной области:
1) верхней челюсти (одно- и двусторонняя);
2) верхней челюсти, скуловой области (одно- и двусторонняя);
3) верхней челюсти, костей носа (одно- и двусторонняя);
4) верхней челюсти, скуловых и носовых костей (одно- и двусторонняя);
5) верхней челюсти, скуловых и носовых костей, передней стенки лобной
пазухи (одно- и двусторонняя).
При составлении плана операции надо определить причину и степень
повреждения покровов лица и костей лицевого скелета, оценить состояние
рубцовой ткани, ее подвижность, эластичность, толщину, форму,
рельефность. Особое внимание необходимо обратить на наличие келоидных рубцов,
состояние кожных покровов, расположенных вблизи деформаций. Очень
важно, чтобы кожа в области операции была не мацерирована и без
гнойничковых поражений [Gniss Т. et al., 199Ö; Giudice Μ. et al., 1994].
При планировании костно-пластических операций следует клинически
и рентгенологически оценить состояние повреждений кости, локализацию
дефекта, исключить хронический травматический остеомиелит, оценить
наличие тканей без создания костного воспринимающего ложа, определить
способ фиксации пересаженной кости и иммобилизации костных
фрагментов, необходимость в ортопедических аппаратах, план дальнейшего общего
и местного лечения больного. Для устранения указанных деформаций всем
больным показано хирургическое лечение. При ревизии операционного поля
у больных с посттравматическими деформациями скулоглазничной области
отмечаются диастазы между крупными костными фрагментами,
заполненные рубцовой тканью, разрушения дна глазницы, рубцовые изменения в
окологлазничной клетчатке и нижней прямой мышце глазного яблока, рубцовое
сращение измененной окологлазничной клетчатки с височной мышцей, при-
278
водящее к подвижности глаза при акте жевания [Ипполитов В. П., 1986; Бель-
ченко В. Α., 1996].
У больных с энофтальмом возникают деформации и смещение глазницы,
рубцовые изменения в окологлазничной клетчатке, рубцовая контрактура
нижней косой мышцы глаза [Кузнецов И. Α., Бельченко В. Α., 1997].
При значительном смещении скуловой кости наблюдается разрушение
нижнего глазничного канала с развитием рубцовых изменений в области
сосудисто-нервного пучка, чем и объясняется стойкое снижение
чувствительности в зоне иннервации подглазничного нерва. Ограничение подвижности
нижней челюсти обусловлено смещением скуловой кости вниз. При ревизии
верхнечелюстной пазухи обнаруживают изменения слизистой оболочки в
виде гиперплазии, а также мелкие костные фрагменты [Ипполитов В. П., 1986].
Выявленные во время оперативного вмешательства топографо-анатоми-
ческие особенности позволяют разработать тактику плановой реабилитации
больных. План хирургического лечения должен соответствовать рабочей
классификации посттравматических деформаций средней зоны лицевого скелета.
27.2. Хирургическое лечение посттравматических деформаций
Репозиция при деформациях костей скулоглазничной области. Данная
методика показана при деформациях костей скулоглазничной области в
различных направлениях смещения скуловых костей и костей дна глазницы с
сохранением их анатомической формы. Оперативная репозиция необходима для
восстановления измененной формы лица, функционирования собственно
жевательных, мимических мышц и устранения диплопии. В случае отсутствия
глазного яблока необходимость оперативной репозиции костей
скулоглазничной области обусловлена созданием оптимальных условий для эктопротезиро-
вания и функционирования глазного протеза.
Методика операции (рис. 27.1). Проводят разрез кожи в области
наружного угла глазницы, подглазничной и скуловой дуги. Острым и тупым
путем отсепаровывают ткани до надкостницы и рассекают ее в области краев
костных фрагментов. Полностью иссекают фиброзную соединительную ткань,
находящуюся между костными фрагментами. В случаях фиксации глазного
яблока рубцовой тканью к височной мышце освобождают его от рубцов и
устраняют контрактуру в этой области. Аналогичную операцию проводят в
области нижнего края и дна глазницы.
Во время иммобилизации костей с помощью проволочного шва создают
плотный контакт между краями костных фрагментов. Затем между краями
сближенных фрагментов в момент скручивания проволочного шва фиссур-
ным бором №1 производят дополнительный пропил, что позволяет
увеличить площадь контакта между костными фрагментами и способствует
регенерации. Вторым фактором, важным для создания целости скуловой дуги,
является применение остеотомии. Только продольный костный распил
скуловой дуги по всей ее длине дает возможность переместить фрагменты
относительно друг друга, удлинить ее и сохранить ее целость как в продольном,
так и в вертикальном направлении.
Для удержания скуловой кости в заданном положении немаловажное
значение имеет использование стальной или титановой проволоки
определенного диаметра. Для прочного закрепления костных фрагментов в области
скулолобного соединения необходима проволока диаметром 0,5 мм, так как в
этой области толщина костной ткани наибольшая. При укреплении тонких,
хрупких костных фрагментов в области нижнеглазничного края и скуловой ду-
279
Рис. 27.1. Оперативная репозиция скуловой кости с помощью элеватора при полном
ее отрыве (схема).
а — положение скуловой кости после травмы; б — репозиция скуловой кости элеватором Ка-
рапетяна; в — послойное рассечение тканей височной области; г — оперативный доступ к
внутренней поверхности скуловой кости; д — репозиция скуловой кости в правильное положение.
ги применяют проволоку диаметром 0,1 мм, которая в момент скручивания не
разрушает их тонкие края [Macleod S., Bainton R., 1992].
Для устранения рецидива смещения скуловой кости рассекают рубцовую
ткань в местах прикрепления собственно жевательных мышц к скуловым
костям.
Перечисленные методические приемы оперативной репозиции костей ску-
логлазничной области значительно улучшают результаты оперативного лечения
больных с посттравматическими деформациями скулоглазничной области [Ма-
ланчук В. Н., 1984; Медведев Ю. А. и др., 1989; Лимберг Α. Α., Фрегатов И. Д.,
1995; Randall D., Bernstein P., 1996].
Репозиция скуловых костей с одномоментной пластикой скулоальвеоляр-
ного гребня формализированной аллогенной костью. Методика применяется в
случаях значительного смещения скуловых костей и при отсутствии скуло-
альвеолярных гребней. Смещение скуловых костей наблюдается не только от
силы травмирующего агента, но и при значительных усилиях от собственно
жевательных мышц, которые при своем сокращении смещают скуловые
кости вниз и кзади. В отсутствие скулоальвеолярного гребня рецидив деформации
возникает в 100 % случаев. При воссоздании целости этого анатомического
образования по описанной ниже методике с использованием
формализированной аллогенной кости рецидив не наступает.
Основанием для применения формализированного трансплантата
является то, что у всех больных с патологией скулоглазничной области
верхнечелюстная пазуха сообщается с внешней средой. Перемещение скуловой
кости в первоначальное положение приводит к образованию сообщения с
верхнечелюстной пазухой, что в послеоперационном периоде может вызвать
инфицирование раны. В связи с этим пластику скулоальвеолярного гребня
следует производить формализированной аллогенной костью, которая
выделяет формальдегид и обеспечивает асептическое состояние в
послеоперационной зоне до 21-го дня. За этот период происходит восстановление целости
верхнечелюстной пазухи.
Методика операции (рис. 27.2). Костные фрагменты
скулоглазничной области перемещают по описанной выше методике. Особенность
операции заключается в том, что со стороны полости рта проводят
дополнительный разрез через слизистую оболочку до кости от вторых резцов до вторых
моляров. Осуществляют ревизию передней стенки верхнечелюстной пазухи
в области отсутствующего скулоальвеолярного гребня. Иссекают рубцово-из-
мененные ткани, освежают края костных тканей скуловой кости и верхней
челюсти. После репозиции скуловых костей в образовавшийся дефект
скулоальвеолярного гребня вводят предварительно подготовленный фигурный
формализированный трансплантат, полностью заполняющий этот дефект.
Скуловые кости и трансплантат скрепляют между собой и фиксируют
проволочными швами к верхней челюсти.
Для лечения больных с оскольчатыми переломами данной области V. Zic-
cardi и соавт. A993), В. А. Бельченко и И. А. Кузнецовым A997) предложен
способ репозиции и фиксации скуловой кости.
Методика операции (рис. 27.3). Используют трансвенечный
оперативный доступ. После скелетирования костей скулоглазничной области и
мобилизации передней части височной мышцы хирург собирает все
фрагменты скуловой кости воедино, скрепляет их между собой и восстановленную
таким образом скуловую кость фиксирует в области скуловой дуги и скулолоб-
ного шва. Третьей точкой фиксации является Π-образная пластина, введенная
в подвисочную ямку [Бельченко В. Α., 1995; Westermark Α. et al., 1992; Reher P.,
Duarte G., 1994]. Такой способ позволяет свободно осмотреть операционное
281
a
б
поле, без дополнительных
разрезов на лице
восстановить целость скуловой
кости и дуги, прочно
фиксировать костные
фрагменты.
Пластика дна
глазницы скулыітурно-моделиро-
ванным силиконовым им-
плантатом. Показанием к
применению этого метода
является частичный
дефект дна глазницы, при
котором клинически
выявляют смещение глазного
яблока вниз и кзади. Его
используют во всех
случаях, когда после
оперативной репозиции костей ску-
лоорбитальной области
наблюдаются диплопия и
энофтальм [Брусова Л. Α.,
Ипполитов В. П., 1984].
Метод и ка
операции (рис. 27.4).
Проводят разрез
подглазничной области, скелетируют
нижний край глазницы и
передний отдел дна
глазницы. Смещенную в
верхнечелюстную пазуху пара-
офтальную клетчатку и
нижнюю прямую мышцу
глаза тщательно высепа-
ровывают, рубцово-изме-
ненную ткань в ретро-
бульбарной области иссекают и тугой тампонадой перемещают глазное
яблоко вперед и вверх до нормального анатомо-физиологического уровня.
После гемостаза в образовавшееся ложе вводят заранее изготовленный
скульптурно-моделированный фигурный силиконовый имплантат, который
двумя-тремя П-образными швами из хромированного кетгута фиксируют к
нижнеглазничному краю. Рану послойно ушивают кетгутом, на кожу
накладывают швы полиамидной нитью и тугую асептическую повязку.
Предложенная методика надежна и позволяет корригировать положение
глазного яблока в деформированном его ложе путем перемещения глаза вверх
и вперед; при этом создается ложе для удержания глазного яблока в заданном
положении. Имплантат препятствует формированию рубцовой контрактуры
дна глаза за счет разобщения верхнечелюстной пазухи и параофтальной
клетчатки. Эффективен метод пластики нижней стенки глазницы с применением
Ф-образной мини-пластины из титана, который отличается от ранее
известных методов тем, что дает возможность более надежно фиксировать костные
отломки, замещать дефект нижней стенки глазницы и одновременно
устранять диплопию и энофтальм (рис. 27.5) [Бельченко В. Α., 1996].
Рис. 27.2. Оперативная репозиция скуловой кости с
одномоментной пластикой скулоальвеолярного
гребня формализированной аллокостью (схема).
а — положение скуловой кости после травмы; б— репозиция
скуловой кости и фиксация костным швом; в, г— фиксация
аллотрансплантата в участок дефекта.
282
Рис. 27.3. Фиксация скуловой кости с помощью П-образно изогнутой перфорироБ
титановой конструкции (схема).
а — вид сбоку; б — вид снизу.
A^-^/;
Рис. 27.4. Пластика дна глазницы скульптурно-моделированным силиконовым имплан-
татом (схема).
а — силиконовый имплантат; б, в — фиксация имплантата на дне глазницы; г — фиксация
имплантата на дне глазницы, подглазничной области.
Рис. 27.5. Реконструкция нижней стенки глазницы Ф-образной титановой пластинкой
с использованием трансантрального оперативного доступа (схема).
а — виды Ф-образных титановых имплантатов; б — внешний вид деформации; в — вид деформации
сбоку; г — положение имплантата в лицевом черепе.
Устранение посттравматических деформаций скулоглазничной области
скульптурно-моделированным имплантатом из силикона. Показаниями к
лечению этим методом являются посттравматические и послеоперационные
остаточные деформации скулоглазничных, подглазничных областей, края и
дна глазниц. Его используют также при значительных деструктивных
изменениях костей скулоглазничных областей, если костные реконструктивные
операции ранее не проводились.
Цель операции состоит в устранении единым сложным скульптурно-мо-
делированным силиконовым имплантатом деформации скуловой,
подглазничной областей и дна глазницы с одновременным поднятием глазного
яблока вверх до уровня анатомо-физиологической нормы. Для этого заранее
приготовленный силиконовый имплантат вводят в указанные области по
методике, разработанной Л. А. Брусовой A996).
Методика операции. Проводят разрез в подглазничной области по
нижней складке века размером 3,5—4 см. Остро-тупым путем кожу отпрепаро-
вывают от круговой мышцы нижнего века до уровня нижнеглазничного края.
Скальпелем рассекают надкостницу нижнеглазничного края, затем распатором
скелетируют подглазничноскуловые области на величину ранее изготовленного
силиконового имплантата, равного величине посттравматической деформации,
и туго тампонируют марлевыми тампонами, смоченными фурацилином.
Скелетируют дно глазницы. Проводят гемостаз тугой тампонадой марлевым тампоном,
смоченным 3 % раствором перекиси водорода со спиртовым раствором йода.
После удаления марлевых тампонов вводят скульптурно-моделированный
силиконовый имплантат в созданное ложе. Проводят фиксацию имплантата
двумя П-образными швами через перфорационные каналы к нижнему глазничному
краю. Рану послойно ушивают кетгутом. На кожные края раны накладывают
швы из полиамидной нити и асептическую повязку.
Устранение посттравматических деформаций носоглазничной области.
При грубых симметричных посттравматических деформациях костей носо-
285
Рис. 27.6. Устранение несимметричных посттравматических деформаций носоглаз-
ничной области (схема).
а — вид дефекта; б — фиксация перемещенных и поставленных в правильное положение костных
фрагментов.
Рис. 27.7. Устранение костей верхней зоны лица с использованием послойного
костного аутотрансплантата свода черепа с учетом кривизны поверхности
восстанавливаемого участка лобной кости и свода глазницы (схема).
а — свободные костные трансплантаты с лобной кости; б — костный дефект, подготовленный для
замещения лобной области трансплантатом.
глазничной области весь смещенный костный комплекс (кости носа, лобные
отростки верхних челюстей, слезные кости и часть решетчатой кости) остео-
томируют и перемещают в правильное анатомическое положение (рис. 27.6).
Предварительно проводят Η-образный разрез кожи в области носа. Скелетируют
смещенные кости носа, лобные отростки верхних челюстей, слезные кости и
внутренние стенки глазницы. По линии перелома между лобной костью с одной
стороны и костями носа, лобными отростками, слезными костями — с другой
фиссурным бором разъединяют фиброзно-костные спайки. Затем двумя
лопаточками Буяльского, введенными в носовые ходы, устанавливают весь костный
комплекс в анатомически правильное положение. Все вправленные кости
четырьмя проволочными швами фиксируют к юбной кости и нижним глазничным
краям. Рану послойно ушивают кетгутом, на кожные края ее накладывают швы
полиамидной нитью. Носовые ходы туго тампонируют турундой, смоченной йо-
доформной жидкостью, с вазелином [Ипполитов В. П., 1986].
Применение указанных методик позволяет достигнуть высокого
косметического эффекта в отдаленном посттравматическом периоде. Для устранения
дефектов и деформаций костей верхней зоны лица В. А. Бельченко и соавт.
A993) разработана оперативная методика с использованием полнослойного
костного аутотрансплантата свода черепа с учетом кривизны поверхности
восстанавливаемого участка лобной кости и свода глазницы (рис. 27.7).
287
Рис. 27.8. Опорно-контурная пластика скулоглазничной области свободным полно-
слойным костным лоскутом (схема).
а — взятие трансплантата со свода черепа и расщепление костных пластин; б— замещение дефекта
костным трансплантатом и фиксация его.
Для устранения дефектов и деформаций костей скулоглазничного
комплекса В. А. Бельченко и др. A993) разработана оперативная методика с
использованием полнослойного костного аутотрансплантата свода черепа с учетом
кривизны поверхности восстанавливаемого и донорского участка (рис. 27.8).
Устранение посттравматических деформаций носоглазничной области с
одномоментной каналикулоцистостомией. Данная методика находит применение
при грубых посттравматических деформациях носоглазничной области,
сочетающихся с дакриоциститами, эффективна, дает хорошие косметические и
функциональные результаты. Для устранения посттравматических
деформаций носоглазничной области выполняют оперативную репозицию и канали-
кулоцисториностомию с обязательным последующим дренированием слезо-
отводящих путей [Ипполитов В. П., 1986; Бельченко В. Α., 1996].
Операция делится на два этапа (рис. 27.9). На первом этапе проводят Н-
образной формы разрез в области корня носа. Скелетируют кости носа,
лобные отростки верхних челюстей, слезные кости, внутреннюю стенку
глазницы. Осуществляют гемостаз, оценивают состояние и положение костных
фрагментов, в операционной ране — состояние слезоотводящих путей.
Затем разъединяют смещенные костные фрагменты, иссекают или смещают
соединительную ткань, создают перфорационные отверстия в костных
фрагментах, через которые иммобилизуют костные фрагменты и
фиксируют их проволочными швами к лобной кости. На втором этапе операции
рассекают или иссекают деформированный слезный мешок, в котором
делают устье через нижнебоковую стенку носового хода. Через верхнюю и
288
Рис. 27.9. Устранение несимметричных посттравматических деформаций костей
носоглазничной области с одномоментной пластикой слезоотводящих путей (схема).
а, б — деформация носоглазничной области;
Рис. 27.9.
в — костный трансплантат; г — пластика дна глазницы костным трансплантатом; д — пластика
слезоотводящих путей.
нижнюю слезные точки проводят полихлорвиниловые трубки.
Оперативное вмешательство завершают тугой тампонадой верхнего и нижнего
носовых ходов турундами, смоченными йодоформенной жидкостью, а в нижний
носовой ход вводят полихлорвиниловую трубку для носового дыхания.
Рану послойно ушивают кетгутом. На кожу накладывают швы
полиамидной нитью.
290
Для больных с разрушенным слезно-носовым каналом и деформацией
внутреннего угла глазной щели В. А. Бельченко разработан способ устранения
деформации внутреннего угла глазной щели путем перемещения треугольного
кожно-мышечного лоскута с верхнего века на нижнее, фиксации внутреннего
угла глазной щели к внутренней стенке глазницы, высепаровывания слезного
мешка и проведения дакриоцисториностомии через отверстие в устье слезно-
носового канала. Этот способ позволяет одновременно устранить деформацию
внутренних углов глазных щелей и слезотечение (рис. 27.10). Для больных с
дистопией слезного мешка и отрывом его от слезно-носового канала
предложена оперативная методика его удлинения и репозиции (рис. 27.11).
С целью устранения дефектов и деформаций костей носа, а также
повышения его спинки В. А. Бельченко разработана оперативная методика с
использованием полнослойного костного аутотрансплантата с теменной кости
(рис. 27.12).
Для пластики дефектов внутренней выстилки воспринимающего ложа
В. А. Бельченко предложена оперативная методика с использованием
дублированного надкостничного лоскута со свода черепа (рис. 27.13).
Для устранения посттравматической деформации костно-хрящевого
отдела носа, проявляющейся значительным укорочением и снижением высоты
спинки носа, Л. А. Кауровой A998) предложен способ круговой остеотомии
пирамидки носа с пластикой дефектов, образовавшихся в области корня
носа, аутотрансплантатами с верхнеглазничных краев (рис. 27.14). При более
значительных костных дефектах используют полнослойные или
расщепленные аутотрансплантаты с теменной кости.
Для лечения пациентов с посттравматической деформацией носоверх-
нечелюстного комплекса, заключающейся в западении основания верхней
губы и крыльев носа, уменьшении высоты спинки носа, Л. А. Кауровой
A998) предложен способ контурной пластики основания грушевидного
отверстия полнослойным аутотрансплантатом с теменной кости, боковых краев
грушевидного отверстия — аутотрансплантатами с верхнеглазничных краев,
опорно-контурной пластики спинки носа — расщепленным
аутотрансплантатом с теменной кости. Методика в ряде случаев позволяет избежать такой
травматичной операции, как остеотомия верхней челюсти (рис. 27.15). Для
устранения деформации внутреннего угла глазной щели предложен способ
трансназальной кантопексии, которым можно устранить смещение
внутреннего угла глазной щели как во фронтальной, так и в сагиттальной плоскости.
Устранение посттравматических деформаций лобно-носоглазничной
области. Показанием к операции является поражение лобно-носоглазничной
области с переломом передней стенки лобной пазухи, костей носа, стенок
глазниц [Безруков В. М. и др., 1995].
При костной реконструкции с использованием наружной кортикальной
пластинки расщепленного аутотрансплантата покровных костей применяют
следующие методики:
1) оперативную репозицию передней стенки лобной пазухи и костей носа
с одномоментной санацией лобной пазухи;
2) оперативную репозицию вдавленного перелома передней стенки
лобной пазухи и костей носа единым блоком;
3) пластическое закрытие дефекта лобной кости с использованием
кортикальной пластинки покровных костей;
4) реконструкцию лобно-носовой области у больных с
посттравматическими дефектами лобной кости и костей носа;
5) реконструкцию супраорбитального края при его дефекте с
использованием ротационного аутотрансплантата лобно-теменной области.
291
19*
Рис. 27.10. Одномоментное устранение деформации внутреннего угла глазной щели
и дакриоцистита (схема).
а — патология внутреннего угла глаза; б — разрез внутреннего угла глаза; в — вскрытие слезного
мешка; г — введение силиконовой трубки в слезный мешок; д, е, ж, з — положение силиконовой
трубки в слезоотводящих каналах и слезном мешке; и — перемещение треугольных кожных лоскутов
внутреннего угла глаза.
Рис. 27.11. Дакриоцисториностомия при дистопированном слезном мешке (схема).
а — слезный мешок в дистопированном положении; б — рассечение слезного мешка; в, г, д —
положение силиконовой трубки в слезных канальцах и слезном мешке; е — слезный мешок с
силиконовыми трубками; ж — положение слезовыводящих путей.
Оперативную репозицию передней стенки лобной пазухи и костей носа
с одномоментной его санацией используют при реконструктивных
операциях у больных с вдавленным переломом передней стенки лобной пазухи,
костей носа и сопутствующим хроническим фронтитом.
Методика операции. Проводят коронарный разрез, скелетируют
лобную кость, кости носа. Остеотомированную переднюю стенку лобной па-
293
Рис. 27.12. Опорно-контурная пластика спинки носа полнослойным костным лоскутом
(схема).
а — взятие костного трансплантата в теменной области; б — расщепление аутотрансплантата; в —
положение аутотрансплантата в области носа.
зухи распиливают на фрагменты, которые скрепляют между собой
проволочными швами таким образом, чтобы достигнуть правильной анатомической
формы. Производят санацию лобной пазухи, остеотомию и репозицию
костей носа. Репонированную переднюю стенку лобной пазухи укладывают на
место послеоперационного дефекта и фиксируют к лобной кости
проволочными швами и мини-пластиной с шурупами (рис. 27.16).
Показанием к оперативной репозиции передней стенки лобной пазухи
и костей носа единым блоком является посттравматическая деформация костей
лобно-носовой области, а именно передней стенки лобной пазухи и костей
носа без латерального смещения фрагментов костей носа.
Операция заключается в остеотомии костей носа и передней стенки
лобной пазухи единым блоком. После санации пазухи переднюю стенку и кости
носа репонируют в анатомически правильное положение (рис. 27.17).
Пластическое закрытие дефекта лобной кости кортикальной пластинкой
покровных костей с использованием васкуляризованных надкостничных лоскутов
осуществляют при дефектах передней стенки лобной пазухи и сквозных
дефектах чешуи лобной кости.
При данном способе операции вдвое сокращаются сроки
нетрудоспособности пациентов за счет одноэтапного проведения санации лобной пазухи
и закрытия дефекта лобной кости аутотрансплантатом покровных костей.
Другим преимуществом является то, что благодаря использованию
васкуляризованных надкостничных лоскутов аутотрансплантат изолируется от
лобной пазухи и получает дополнительное питание, что расширяет показания к
294
Рис. 27.13. Пластическое восстановление внутренней выстилки воспринимающего ложа
на спинке носа дублированным надкостничным лоскутом.
а, б— выпрепаровка надкостничного лоскута в лобной области; в, г, д— перемещение, дублирование,
фиксация надкостничного лоскута в область дефекта корня носа.
применению указанного способа при атрофичной и рубцово-измененной
коже лба над костным дефектом.
Методика операции. Выше дефекта формируют два
надкостничных лоскута с питающими ножками на правой и левой височных областях.
Одним из надкостничных лоскутов покрывают дефект. Сформированный ау-
тотрансплантат покровных костей укладывают на дефект и сверху накрывают
вторым надкостничным лоскутом (рис. 27.18).
295
Рис. 27.14. Круговая остеотомия пирамиды носа и пластическое устранение дефекта
в области корня носа аутотрансплантатами с верхнеглазничных краев (схема).
а — остеотомия надбровной дуги, теменной области; б— костная пластика остеотомированными
аутотрансплантатами из надбровных дуг.
У больных с посттравматическими дефектами лобной кости, как
правило, отмечается неправильно сросшийся вколоченный перелом с частичным
дефектом носовых костей и лобных отростков верхней челюсти. Для
получения хороших косметических результатов в этих случаях недостаточно
остеотомии костей носа и их репозиции, так как из-за дефектов лобных отро-
296
стков и костей носа после
операции сохраняется
уплощение спинки носа. При
данных видах деформации
производят пластическое
закрытие сквозного дефекта
лобной кости и
реконструкцию костей носа с
использованием расщепленного
аутотрансплантата
покровных костей.
Забор расщепленного
аутотрансплантата
черепной кости производят в
лобно-теменной области в
соответствии с формой
дефекта лобной кости и
костей носа. Аутотрансплан-
таты, выполняющие зоны
дефекта и деформации
костей носа и лобной
кости, скрепляют друг с
другом проволочными швами
и мини-пластинами с
шурупами. При этом на кости
носа аутотрансплантат
помещают внакладку, а в
области дефекта лобной
кости — встык с краями
дефекта (рис. 27.19).
Реконструкцию суп-
раорбитального края при
его дефекте с
использованием ротационного
расщепленного
аутотрансплантата покровных костей
производят у больных с
деформацией или дефектом
лобной кости в области
верхнелатеральной части
орбиты.
Отличительной
особенностью этого метода
является то, что латераль-
нее и выше деформации
или дефекта лобной кости формируют костный аутотрансплантат из
наружной пластинки покровных костей, состоящий из двух ножек, повторяющих
контуры зоны деформации или дефекта, и основания, располагающегося ла-
теральнее. При ротации аутотрансплантата медиальная ножка заполняет
участок деформации или дефекта лобной кости, а латеральная занимает место
медиальной (рис. 27.20).
Отдаленные результаты лечения больных с деформациями и дефектами
костей верхней зоны лицевого черепа свидетельствуют о том, что примененное
Рис. 27.15. Устранение деформации внутреннего угла
глазной щели (а, б) (схема).
297
по показаниям хирургическое лечение высокоэффективно и способствует
достижению оптимальных анатомических и функциональных результатов
лечения.
Устранение одно- и двусторонних посттравматических деформаций ску-
лоносоглазничных областей. Показаниями к проведению оперативных
вмешательств являются обширные одно- и двусторонние посттравматические
деформации скулоносоглазничных областей. При этом отмечаются
значительные разрушения и деформации в области 2/з глазниц (наружная, нижняя
и внутренняя стенки), скуловых костей и костей носового комплекса.
В этих областях находятся жизненно важные органы, повреждение
которых при травме приводит к грубым функциональным нарушениям зрения,
дыхания, речи, жевания и обоняния. Поэтому всем больным, имеющим
посттравматические деформации этих областей, необходимо восстановить
анатомическую целостность пораженных органов и тканей для обеспечения
нормальных условий функционирования пораженных органов и тканей
челюстно-лицевой области и последующей психосоциальной реабилитации
больных.
Для устранения посттравматических деформаций необходимо
комплексное хирургическое лечение, заключающееся в репозиции всех костей
скулоносоглазничной области с последующей коррекцией остаточных
деформаций в случае необходимости.
Устранение посттравматических деформаций всей средней зоны лица.
Показаниями к операции являются обширные, обезображивающие больного
деформации всех костей средней зоны лица.
Методика операции (рис. 27.21). Под эндотрахеальным наркозом
проводят разрезы в области наружных углов глаз длиной до 3 см, в области
корня носа — Η-образный разрез, а также в полости рта — разрез по
переходной складке верхней челюсти от 6J до [6 . Скелетируют скуловые, носовые
кости и обе верхние челюсти. Выявляют патологическое положение костей
всей средней зоны. Фиссурным бором и долотом рассекают фиброзно-кост-
ное соединение по линиям переломов, затем долотом и крючком Лимберга
кости иммобилизуют, устанавливают в анатомически правильное положение.
Фиссурным бором создают перфорационные отверстия на костях, отступя
0,3—0,4 см от их краев, и последовательно фиксируют проволокой вначале
скуловые кости к лобным костям, затем верхнюю челюсть к скуловым костям
в области скулоальвеолярных гребней. Последним этапом является
иммобилизация и фиксация лобных отростков верхних челюстей, костей носа и
слезных костей, которые тонкой проволокой укрепляют между собой, а затем
фиксируют к лобной кости. Раны послойно зашивают кетгутом, на кожные края
ран накладывают швы из полиамидной нити. Края ран слизистой оболочки
полости рта сближают и ушивают хромированным кетгутом. Носовые ходы
тампонируют турундой, смоченной йодоформной жидкостью, на 8 дней.
При описанном методе оперативной репозиции костей всей средней
зоны лица более выраженные положительные результаты удается получить у
больных с грубой посттравматической деформацией при наличии всех
смещенных костных фрагментов челюстно-лицевой области, которые поступили
Рис. 27.16. Оперативная репозиция передней стенки лобной пазухи.
а — деформация передней стенки лобной пазухи; б— остеотомия передней стенки лобной пазухи;
в — лобная пазуха после выделения передней стенки; г — воссоздание передней стенки лобной
пазухи из костных фрагментов; д, е, ж — восстановленная передняя стенка лобной пазухи.
299
'lvv /Ж
Рис. 27.17. Оперативная репозиция передней стенки лобной пазухи и костей носа
единым блоком (схема).
а, б — посттравматическая деформация лобно-носоглазничной области; в, г, д — боковая
резекция смещенного костного фрагмента лобно-носовой области и постановка костного фрагмента в
правильное анатомическое положение.
Рис. 27.18. Пластическое закрытие дефекта передней стенки лобной пазухи с
использованием надкостничных лоскутов (схема).
а — дефект лобной пазухи; б — скальпирование, выкраивание надкостничного лоскута; в —
дефект передней стенки лобной пазухи; выкраивание костного трансплантата; г, д, в — постановка
костного трансплантата в дефект; ж, з, и — послойное ушивание раны.
Рис. 27.19. Пластическое устранение дефекта лобной кости и костей носа с
использованием расщепленных трансплантатов покровных костей (схема).
а — дефект лобно-носовых костей; б, в — выкраивание костных трансплантатов из верхнего отдела
лобной кости и его моделирование; г — фиксация аутотрансплантата и устранение дефекта.
Рис. 27.20. Устранение дефекта лобной кости в области супраорбитального края с
использованием ротационного костного лоскута (схема).
а — дефект кости лобно-орбитальной области, выкраивание костного лоскута; б, в —
перемещение костного лоскута в область дефекта и фиксация его.
Рис. 27.21. Устранение посттравматических деформаций костей всей средней зоны
лица (схема).
а — дефект, деформация костей средней зоны лица; б — е — последовательное перемещение и
фиксация костных фрагментов.
вскоре после травмы. Если посттравматический период был длительным, то
необходимо производить оперативную репозицию с последующими
корригирующими операциями. Это объясняется тем, что структура, форма и
функции костных и мягких тканей, длительно находившихся в деформированном
и смещенном состоянии, изменяются. Все это затрудняет выбор радикальных
методов лечения больных с этой патологией. Лечение больных с
посттравматическими деформациями всей средней зоны лица должно быть
направлено на полную реабилитацию больных этой группы. Правильно
организованная специализированная помощь (создание комплексных бригад, раннее
специализированное лечение с последующей реабилитацией больных,
нуждающихся в восстановительных корригирующих операциях, и пребывание
под наблюдением специалистов по профилю) в кабинете реабилитации
способствует успешному решению проблемы социальной, трудовой и
медицинской реабилитации.
СПИСОК ЛИТЕРАТУРЫ
Александров Я. М., Лржанцев П. 3. Травмы челюстно-лицевой области. — М.:
Медицина, 1986. — 447 с.
Безруков В. М., Ипполитов В. П., Лурье Т. М. и др. Восстановительная хирургия
челюстно-лицевой области//Сборник трудов ЦНИИС. — М., 1995. — 208 с.
Баженов Я. Н., Тер-Асатуров Г. П. Совершенствование тактики лечения и
реабилитации пострадавших с повреждениями скулоорбитального комплекса//Специа-
лизированная помощь пострадавшим с повреждениями лица при сочетанной
травме. - СПб, 1991. - С. 174-178.
Вернадский Ю. И. Травматология и восстановительная хирургия челюстно-лицевой
области. — Киев: Вища школа, 1985.
Бельченко В. А. Реконструкция верхней и средней зон лица у больных с
посттравматическими дефектами и деформациями лицевого скелета с использованием ау-
тотрансплантатов мембранозного происхождения и металлоконструкций из
титана: Дис. ... д-ра мед. наук. — ML: ЦНИИС, 1996. — 310 с.
Бельченко В. Α., Ипполитов В. П., Ростокин Ю. Н. Использование покровных костей
черепа при опорно-контурной пластике верхней и средней зон лица//Наследие
А. И. Евдокимова. - М: ММСИ, 1993. - С. 132-134.
Бельченко В. Α., Ипполитов В. Я., Кузнецов И. А. и др. Рконструкция мозгового и
лицевого черепа у больных с посттравматическими дефектами и деформациями//
Актуальные проблемы комплексного лечения и реабилитации детей с
врожденной краниофациальной и нейропатологией: Материалы 1-го Международного
симпозиума 19—21 ноября. — М., 1996.
Бельченко В. Α., Рабухина Я Α., Ипполитов В. П., Безруков В. М. Сопоставление
клинических, рентгенологических и операционных данных при посттравматических
деформациях носоглазничного комплекса//Стоматология. — 1989. — №5. —
С. 40-42.
Ипполитов В. П., Гунько В. //., Жибицкая Э. И. Клинико-рентгенологическая
характеристика неправильно сросшихся переломов костей средней зоны лица//Экспе-
риментальная и клиническая стоматология. — Т. 9, ч. 2. — М., 1979. — С. 106—110.
Кузнецов И. Α., Бельченко В. А. Лечение больных с оскольчатыми переломами костей
скулоглазничной области//Стоматология. — 1997. — №2. — С. 36—37.
Лимберг Α. Α., Фрегатов И. Д. Переломы скуловой дуги и их место в современной че-
репно-лицевой травме//Актуальные вопросы челюстно-лицевой хирургии:
Сборник научных трудов. — СПб, 1995. — С. 161 — 173.
Медведев Ю. Α., Темерханов Ф. Т., Малков Я. В., Колобовников С. С. Реконструктивная
хирургия челюстно-лицевой области//Сборник научных трудов Красноярского
гос. мед. ин-та. — Красноярск, 1989. — С. 72—74.
305
20-1263
Маланчук В. А. Хирургическое лечение переломов скулового комплекса в зависимости
от давности травмы: Автореф. канд. мед. наук. — Киев, 1984. — 24 с.
Giudice Μ., Colella G., Marra A. Complicanze ed esiti delle fracture del complesso orbito-
maxillo-zygomatico//Minerva stomatol. — 1994. — Vol. 38. — N 1—2. — P. 37—41.
Gruss J. S., Van Wyck L.f Phillips J. H., Antonyshyn O. The importance of the zigomatic arch
in complex midfacial fracture and correction of posttraumatic orbitozygomatic deform-
ities//Plast. Reconstr. Surg. — 1990. — Vol. 85, N 6.
Macleod S. P., Bainton R. Extrusion of microplate complication of osteosynthesis//.!. Crani-
omaxillofac. Surg. - 1992. - Vol. 20 G). - P. 303-304.
Randall D. A.y Bernstein P. E. Epistaxis balloon catheter stabilization of zygomatic arch frac-
tures//Ann. Otol. Rhinol. Laryngol. - 1996. - Vol. 105 A). - P. 68-69.
Reher P., Ditarte G C. Mini plates in the frontozygomatic region. An anatomic stydy//Int.
J. oral. Maxillofac. Surg. - 1994. - Vol. 23 E). - P. 273-275.
Tanaka N., Tomitsuka K., Shoinoya K. Aetiology of maxillofacial fracture//Brit. J. oral
Maxillofac. Surg. - 1994. - Vol. 32 A). - P. 19-23.
Westermark Α., Jensen J., Sindet-Pedersen A. Zygomatic fractures and infraorbital nerve
disturbances. Mini plate osteosynthesis vs. other treatment modalities//Oral. Surg. Oral.
Diagn. - 1992. - Vol. 3. - P. 27-30.
Ziccardi V В., Patterson G Т., Ravassastry S., Sotereanos G C. Management of a severe
zygomaticoorbital fracture with dislocation of the globe into the antrum//.!. Craniofac.
Surg. - 1993. - Vol. 4 B). - P. 95-101.
Глава 28
КОМПРЕССИОННО-ДИСТРАКЦИОННЫЕ
МЕТОДЫ ЛЕЧЕНИЯ
ПРИ РЕКОНСТРУКЦИИ ВЕРХНЕЙ
И НИЖНЕЙ ЧЕЛЮСТЕЙ
Устранение деформаций, как врожденного, так и приобретенного генеза
всегда являлось одной из сложных задач восстановительной и реконструктивной
хирургии. Проблема еще больше усложняется, если деформация
несимметрична и диспропорции сильно выражены. Во время оперативного
вмешательства не всегда возможно сразу правильно выбрать расстояние, на которое
должен быть перемещен костный фрагмент. В результате возникает
необходимость корригирующих операций.
Возможно поэтому работы последних лет свидетельствуют о все более
возрастающем интересе к компрессионно-дистракционному методу,
который позволяет длительное время после операции вносить коррективы в
результат лечения и добиваться хорошего эстетического эффекта.
28.1. Исторические аспекты компрессионно-дистракционного
остеогенеза
Компрессионно-дистракционный остеогенез — это метод выращивания
новой костной ткани путем компрессии и последующего вытяжения кости.
Хирурги-ортопеды широко используют этот метод для удлинения конечностей
и устранения ложных суставов.
А. Codivüla в 1905 г. впервые опубликовал работу по этой теме, где
описал 26 случаев удлинения конечностей. Он проводил остеотомию бедренной
кости и затем накладывал гипсовую повязку для ее вытяжения и
выравнивания. Благодаря этому методу конечность удлинялась на 3—8 см.
Первый внешний фиксатор для удлинения конечностей был описан
V. Putti в 1921 г. Он представлял собой напряженную пружину, которая
обеспечивала постоянное натяжение между двумя закрепленными штырями.
Вслед за этим было разработано множество методов удлинения конечностей,
однако ни один из них не обеспечивал равномерного образования костной
ткани и вызывал большое количество осложнений. Начиная с 50-х годов,
Г. А. Илизаров стал производить дистракционный остеогенез при лечении
тысяч больных, однако по ряду причин этот метод лишь в последнее
десятилетие привлек внимание медиков на Западе.
20*
307
28.2. Теоретическое обоснование и принципы
компрессионно-дистракционного остеогенеза
Компрессионно-дистракционный остеогенез, выполняемый Г. А. Илизаро-
вым, можно разделить на четыре этапа: остеотомию, период скрытого
восстановления или период компрессии, период вытяжения или дистракции, ре-
тенционный период.
Остеотомия (механическая травма) является пусковым механизмом
регенерации. При этом интенсифицируется остеокластическая резорбция,
выделяются неколлагеновые белки, которые регулируют репаративные процессы в
костной ткани.
Белки-регуляторы оказывают короткодистантное действие D00—500 нм).
Этим может быть обусловлена целесообразность компрессии, приводящей к
сближению отломков и дополнительной травме кости на втором этапе. В
период скрытого восстановления костной ткани торцы отломков плотно
прилежат друг к другу, что обеспечивает образование хорошо васкуляризованной
грануляционной ткани. Под влиянием белков-регуляторов при участии
перицитов образуется первичная костная мозоль.
Существуют различные мнения относительно оптимального периода
компрессии. Как правило, в клинической практике он составляет от 5 до 15
дней. Большинство авторов согласны с тем, что для скрытого заживления
требуется определенное время, а немедленный дистракционный остеогенез
(без периода компрессии) приводит к образованию фиброзной ткани при
минимальном росте кости [White S., Kenwright J., 1991].
На следующем этапе (период вытяжения) с помощью дозированной
дистракции новообразованной костной мозоли в области остеотомии
осуществляется поддержка остеогенеза до образования костного регенерата
необходимой величины. При этом постоянная микротравма костной мозоли
приводит к высвобождению новых порций белков — регуляторов остеогенеза,
которые влияют на репаративные процессы. На этом этапе особенно важно
при постоянной дистракции сохранять прочную фиксацию отломков,
которая способствует оптимальному расположению коллагеновых волокон, ос-
теогенных клеток и сосудов [Илизаров Г. А. и др., 1976].
Г. А. Илизаров установил, что вытяжение со скоростью менее 0,5 мм в
сутки может приводить к преждевременной консолидации, а более 1,5 мм —
вызывать образование "ложного сустава". Кроме того, большое значение
имеет не только скорость, но и частота приложения силы. Оптимальным считают
вытяжение 1 мм в сутки за четыре приема. Кратковременные, но частые
интервалы способствуют увеличению скорости образования костной ткани.
Ретенционный период является завершающим этапом дистракционного
остеогенеза и, по мнению многих авторов, должен быть сопоставим по
времени с периодом дистракции (не менее 4 нед). По данным Y. Komuro и соавт.
A994), уже через 8—10 нед после окончания вытяжения новая кость по
структуре не отличается от нормального кортикального вещества.
28.3. Использование компрессионно-дистракционных методов лечения
в челюстно-лицевой хирургии
Работы Г. А. Илизарова в 60—70-х годах привлекли внимание различных
специалистов к компрессионно-дистракционному остеогенезу. Ряд авторов
использовали этот метод при лечении больных с переломами нижней челюсти
308
[Соловьев Μ. Μ., Магарилл Е. С,
1966; Каганович С. И., 1967;
Локтев Н. И., 1967; Колмакова Α. Α.,
1970; Воупе Р., Morgan F., 1972;
Kline S., 1973].
В дальнейшем были
предложены компрессионно-дистракционные
аппараты (КДА) для лечения
переломов нижней челюсти и устранения
небольших (от 0,6 до 2 см) дефектов
после удаления секвестров
[Ермолаев И. И., Кулагов С. И., 1979;
Соловьев М. М. и др., 1981; Осипян Э. М.,
1982; Мелкий В. И., 1983;
Чудаков О. П., Бармуцкая А. 3., 1984].
Использовать компрессионно-
дистракционный метод для
устранения деформаций верхней и нижней
челюсти также предложили
отечественные авторы в 80-х годах. КДА
для верхней челюсти с фиксацией на
зубах и спице Киршнера в области
скуловых костей применяли В. А.
Сукачев, В. И. Гунько и У. Т. Таиров.
Лечение больных с
несимметричными деформациями нижней
челюсти описано В. И. Куцевляком
и соавт. A985). КДА фиксировались
на зубах, и дистракция
осуществлялась после кортикальной
остеотомии тела нижней челюсти со
скоростью 0,2 мм в сутки. Но автору
удавалось увеличить размер
челюсти только на 0,6—0,8 см.
Учитывая изложенное выше, а
также невозможность устранять
большие дефекты челюстей, в 1982 г.
М. Б. Швырков и соавт. предложили
КДА наружной фиксации и
способы остеопластики и несвободной
остеопластики местными
тканями.
В основу предлагаемого
способа устранения дефекта тела нижней
челюсти положен метод Илизарова,
трансформированный с учетом
анатомических особенностей челюстно-
лицевой области и кривизны
нижней челюсти. Сущность его состоит в активизации остеогенеза путем
кратковременного сдавливания (компрессии) двух свежих костных раневых
поверхностей (рис. 28.1, а, б) и последующем длительном поддержании активности
этого процесса с помощью дозированного растяжения (дистракции)
возникшей костной мозоли до образования регенерата необходимой величины
в
Рис. 28.1. Компрессия и дистракция при
переломе нижней челюсти,
сопровождающемся формированием большого костного
дефекта (схема).
а — костный дефект и встречный "маршрут"
костных отломков; б — положения отломков в
период компрессии; в — конечный результат после
прекращения дистракции вслед за образованием
костного регенерата необходимой величины.
309
(рис. 28.1, в). Этот метод
замещения костного дефекта называется
остеопластикой местными
тканями.
При больших дефектах прямой
контакт концов отломков в ране
невозможен, поэтому необходимо с
помощью закрытой остеотомии
создать мобильный костный
фрагмент, который был бы связан с
мягкими тканями и хорошо снабжался
кровью (рис. 28.2, а). Операция,
выполненная с использованием
такого костного фрагмента,
называется несвободной остеопластикой. На
месте остеотомии создается
компрессия свежих костных ран, что
резко активизирует остеогенез.
Спустя 10—12 дней приступают к
дистракции костной мозоли,
перемещая костный фрагмент в сторону
дефекта до контакта с другим
отломком (рис. 28.2, б). При этом
происходит микроскопическая деструкция
костного регенерата, что вызывает
постоянное выделение белков —
регуляторов остеогенеза и постоянную
трансформацию перицитов в
остеобласты. Дистракция положительно
влияет также на регенерацию мягких
тканей. Вместе с костным
фрагментом в сторону дефекта перемещаются
регенерирующие слизистая
оболочка, мышцы, нервы, сосуды, кожа и
другие ткани. Одновременно
замещается комбинированный дефект
тканей.
КДА, разработанный М. Б. Швырковым и соавт., позволил: 1)
перемещать отломки и фрагменты нижней челюсти на любое заданное расстояние;
2) прочно фиксировать отломки и фрагменты нижней челюсти.
КДА (рис. 28.3) состоит из спиц с винтовой нарезкой диаметром 2,5 мм,
которые укрепляют в нижней челюсти, планок различной формы,
объединяющих спицы в группы, гаек, с помощью которых происходит
соединение спиц и планок, муфт и гаек, которыми муфты крепят к планкам,
винтовой штанги, объединяющей муфты. При помощи элементов аппарата
отломки челюстей крепят к штанге и производят компрессию и дистрак-
цию отломков и фрагментов нижней челюсти. Для введения спиц в кость
используют специальный переходник и прямой стоматологический
наконечник.
Опыт лечения больных, особенно с огнестрельной травмой, позволил
широко применять КДА наружной фиксации. Однако сложность конструкции
и техники его наложения вынудила продолжать поиски новых видов фиксации,
в том числе внутриротовых.
Рис. 28.2. Закрытая остеотомия с созданием
мобильного костного фрагмента и его
стыковка с отломком нижней челюсти (схема).
а — костный дефект тела нижней челюсти, место
остеотомии, маршрут фрагмента челюсти; б—
конечный результат после стыковки фрагмента и
отломка. Заполнение дефекта костным регенератом.
310
Рис. 28.3. Компрессионно-дистракционный аппарат для нижней челюсти.
/ — гайка для крепления муфт; 2— гайка спицы; 3 — спицы; 4— планки; 5 — качающаяся муфта;
6— гайка винтовой штанги; 7— винтовая штанга.
В последнее десятилетие компрессионно-дистракционный остеогенез и
различные варианты аппаратов дали возможность в ряде случаев значительно
улучшить результаты лечения больных с деформациями средней и нижней
зон лица, устранять дефекты костной ткани [McCarthy J. et al., 1992; Klein С,
Howaldt Η.-P., 1995; Losken Η. et al., 1995; Sawaki Y. et al, 1996; Sawaki Y. et
al., 1998|.
Нами разработаны и усовершенствованы КДА для устранения
деформаций нижней челюсти (рис. 28.4), которые позволяют перемещать костные
отломки по кривой на расстояние до 2,5 см; их устанавливают внутриротовым
доступом. После остеотомии тела нижней челюсти КДА крепят к отломкам
с помощью мини-винтов. Создают режим компрессии на 7—10 дней.
Впоследствии с помощью дистракции удается получить новообразованный
костный регенерат длиной до 2,5 см (рис. 28.5, 28.6). На всех этапах лечения
функция нижней челюсти не страдает (рис. 28.7).
Для перемещения верхней челюсти мы используем аппарат оригинальной
конструкции с фиксацией на скуловой кости и скулоальвеолярном гребне (рис.
28.8). После горизонтальной остеотомии с помощью КДА создают режим
компрессии. Это позволяет довольно плотно сопоставить остеотомирован-
ные фрагменты и ликвидировать кровотечение. Через 7—10 дней начинают
дистракцию по 1 мм в сутки за четыре приема. После достижения желаемого
положения остеотомированного фрагмента его фиксируют мини-пластинами.
Этот этап осуществляют одновременно со снятием аппарата и под местной
анестезией. В результате лечения фрагмент верхней челюсти удается
переместить более чем на 1 см за 10 дней (рис. 28.9) и изменить профиль лица
больного и прикус (рис. 28.10).
Компрессионно-дистракционный метод позволяет наряду с костной
пластикой и реконструктивной хирургией устранить дефекты и деформации
челюстей, а в ряде случаев может быть альтернативой обширному
оперативному вмешательству. Кроме того, он может быть использован как один из
311
Рис. 28.4. Усовершенствованные КДА для устранения деформаций нижней челюсти.
Рис. 28.5. Рентгенограмма. Дистракция Рис. 28.6. Рентгенограмма. Образование
нижней челюсти. костного регенерата с помощью КДА.
Рис. 28.7. Аппараты в полости закрытого (а) и открытого (б) рта.
этапов ортодонтического лечения при малой эффективности последнего.
Компрессионно-дистракционный метод целесообразно использовать при
лечении выраженных нижних микрогнатий, чтобы избежать костной пластики.
Операции с использованием КДА менее травматичны и опасны, а их
результат можно корригировать в течение всего срока лечения больного.
Рис. 28.8. Фиксация оригинального КДА на скуловой кости и скулоальвеолярном гребне.
Рис. 28.9. Рентгенограмма. Перемещение фрагмента верхней челюсти
и его взаимоотношение с нижней челюстью.
Рис. 28.10. Устранение деформации верхней челюсти при помощи КДА.
а — больная до лечения; б — после дистракции.
СПИСОК ЛИТЕРАТУРЫ
Ермолаев И. И., Кулагов С. И. Внеочаговый компрессионно-дистракционный аппарат
БК//Остеосинтез нижней челюсти: Сборник трудов/Под ред. С. И. Кагановича. —
Ставрополь, 1979. — С. 54—57.
Илизаров Г. Α., Хелимский Г. М., Барабаш А. 77. Морфологическая картина репаратив-
ной регенерации костной ткани при удлиняющем артродезе коленного сустава в
эксперименте//Реконструктивная компрессия, дистракционный и
компрессионно-дистракционный остеосинтез в травматологии и ортопедии: Сборник науч.
трудов Курганского НИИЭКОТ. — Челябинск, 1976. — Вып. 2. — С. 36—42.
Каганович С. И. Компрессионный остеосинтез при лечении повреждений нижней че-
люсти//Отчетная науч. конф. Ставропольского мед. ин-та. — Ставрополь, 1967. —
С. 284-285.
Колмакова А. А. Наружный внеочаговый компрессионный остеопороз при переломах
нижней челюсти (Экспериментально-клиническое исследование): Дис. ... д-ра
мед. наук. — Ростов-на-Дону, 1970. — 401 с.
Куцевляк В. //., Сукачев В. А. Дистракция нижней челюсти в эксперименте//Стома-
тология. — 1984. — №4. — С. 13—15.
Локтев Н. И. Компрессионный остеосинтез при переломах нижней челюсти: Авто-
реф. дис. ... канд. мед. наук. — Калинин, 1967.
Мелкий В. И. Лечение больных с переломами нижней челюсти при помощи компрес-
сионно-дистракционного аппарата//Стоматология. — 1983. — №5. — С. 57—59.
Осипян Э. М. Компрессионный и дистракционный метод лечения больных с
переломами нижней челюсти (Клинико-экспериментальное исследование): Дис. ...
канд. мед. наук. — Ставрополь. — 1982. — 236 с.
315
Соловьев Μ. Л/., Магарил Ε. Ш. Компрессионный остеосинтез с помощью
модифицированного аппарата Рудько//Стоматология. — 1966. — №4. — С. 100—10і.
Соловьев М. А/., Мелкий В. И.} Колтун Р. К. Компрессионно-дистракционный
остеосинтез при переломах верхней и нижней челюсти//Всесоюз. съезд стоматологов,
7-й: Труды. - М., 1981. - С. 204-206.
Чудаков О. П., Бармуцкая А. 3. Компрессионно-дистракционный метод остеосинтеза
в лечении осложненных переломов нижней челюсти//Стоматологическая
помощь сельскому населению. — Рига, 1984. — С. 204—205.
Швырков М. Б. Остеопластика местными тканями и несвободная остеопластика
огнестрельных дефектов нижней челюсти и методы профилактики огнестрельного
остеомиелита: Дис. ... д-ра мед. наук. — М., 1988. — 404 с.
Швырков М. Б., Шамсудинов А. X. Остеопластика местными тканями дефектов
нижней челюсти//Воен.-мед. журн. — 1988. — №3. — С. 47—49.
Швырков М. Б., Шамсудинов А. X. Способы одновременного устранения дефектов
нижней челюсти и прилегающих мягких тканей//Acta chir. plast. — 1989. —
Vol. 31, N4. - P. 211-219.
Codivilia A. On the means of lengthening, in the lower limbs, the muscles and tissues which are
shortened through deformity//Amer. J. orthop. Surg. — 1905. — Vol. 2. — P. 353—369.
Kline S. H. Lateral compression in treatment of mandibular fractures//! oral Surg. — 1973. —
Vol. 3. - P. 182-187.
Komuro Y.} Takato Т., Kiyonoh #., Yonemara Y. The histologic analysis of distraction
osteogenesis of the mandible in rabbits//Plast. Reconstr. Surg. — 1994. — Vol. 94. —
P. 152-159.
Losken H. W.. Patterson G. Т., Lazarou S. Α., Whitney T. Planning mandibular distraction:
Preliminary report//Cleft. Palate J. — 1995. — Vol. 32. — P. 71—76.
McCarthy J. G, Schreiber J., Korp N. et al. Lengthening the human mandible by gradual dis-
traciion//Plast. Reconstr. Surg. — 1992. — Vol. 89. — P. I —10.
Putti V. The classic. The operative lengthening of the femur//CHn. Orthop. — 1990. —
Vol. 250. - P. 4-7.
Sawaki Y, Hagiro H., Yamamoto #., öeda M. Trifocal distraction osteogenesis for segmental
mandibular defect: a technical innovation//.!. Cranio-Maxillofac. Surg. — 1997. —
Vol. 25, N 6. - P. 310-315.
Sawaki Y, Ohkubo #., Hibi H., Ueda M. Mandibular lengthening by distraction osteogenesis
using osseointegrated implants and an intraoral device: a preliminary report//J. oral.
Maxillofac. Surg. - 1996. - Vol. 54. - P. 594-600.
Sawaki Y, Ohkubo H., Yamamoto, Ueda Y. Mandibular lengthening by intraoral distraction
using osseointegrated implants//Int. J. oral Maxillofac. Implants. — 1996. — Vol. 11. —
P. 186-193.
Shvyrkov M. В., Sumarokov D. D., Shamsudinov A. H. Osteoplasty of the mandible by local
tissues//! Cranio-Maxillofac. Surg. - 1995. - Vol. 23. - P. 377—381.
White S. #., KenwrightJ. The importance of delay in distraction of osteotomies//Ortop. Clin.
North Amer. - 1991. — Vol. 22. - P. 569-579.
Глава 29
ОСНОВЫ
ЭСТЕТИЧЕСКОЙ ХИРУРГИИ
ЛИЦА И ШЕИ
Эстетическая хирургия лица и шеи представляет собой один из разделов
общей пластической хирургии, основной задачей которой является устранение
дефектов внешности врожденного или приобретенного характера,
гармонизация различных изменений в тканях и отдельных органов лица с
окружающими тканями, определяющими естественность вида лица и шеи.
В эстетической хирургии применяются методы общей пластической
хирургии: иссечение рубцов и закрытие раневых дефектов поверхностных тканей
прямым соединением краев ран, местная пластика, перемещение лоскутов на
питающих ножках и свободная трансплантация кожных или
комбинированных лоскутов. Кроме того, при определенных показаниях могут быть
использованы восстановительно-реконструктивные вмешательства: хрящевая и
костная пластика, пластика различными ауто- и аллотрансплантатами и др.
Эстетическую хирургию лица и шеи можно рассматривать двояко: как
завершающие хирургические мероприятия после крупных реконструктивно-
восстановительных операций и как самостоятельную область со своими
специфическими проблемами и задачами, указанными выше. В области
эстетической хирургии лица и шеи приходится решать проблемы анатомического,
функционального, физиологического, топографического, общесоматического
и патологического характера. Вследствие этого к выполнению эстетических
вмешательств должны допускаться хирурги, обладающие определенными
знаниями и высокой оперативной техникой и, кроме того, художественным
вкусом, позволяющим грамотно и ответственно оценить недостаток
внешности с позиций эстетики и применить все доступное ему с целью
эстетической реабилитации обратившихся к нему пациентов.
Качественный профессиональный рост и повышение мастерства хирургов,
работающих в области эстетической хирургии, происходят благодаря тесной связи
и комплексному решению задач совместно со специалистами других профессий.
29.1. Общие проблемы отбора пациентов для эстетических операций
К помощи эстетических хирургов прибегают здоровые люди, желающие
улучшить свою внешность. При этом оценка нарушения ее самим пациентом
и хирургом может иметь различный характер, имеющий в своей основе
различное представление о красоте и естественности внешности — комплексе
культурных, социальных, этнических, профессиональных и других факторов,
входящих в индивидуально-субъективные представления. В человеческом
317
обществе такие представления могут формироваться соревнованиями по
бодибилдингу, конкурсами красоты, средствами массовой информации.
Во всех случаях явный или мнимый дефект внешности отражается на
психоэмоциональной сфере, приводя к замкнутости, угнетенности настроения,
резкому снижению результативности семейных, профессиональных,
общественных функций.
Подобная специфическая особенность пациентов с косметическими
недостатками и дефектами требует от хирурга определенных знаний и владения
приемами отбора пациентов для операций с учетом состояния
психоэмоциональной сферы, грамотной ориентации при разборе причин обращения к
врачу, умения найти и укрепить доверительные отношения при решении
вопросов межчеловеческих отношений с пациентами, имеющими различный
культурный и социальный уровень развития личности.
Общеизвестно, что многие пациенты неадекватно реагируют на
имеющийся у них или кажущийся эстетический недостаток. В первом случае
пациент может подвергаться оперативному вмешательству при всех прочих
положительных условиях, во втором — в основе могут лежать изменения в
психоэмоциональной сфере, требующие компетентного заключения и
соответствующей поддержки психоневрологом.
Опыт работы в эстетической хирургии позволяет подразделять всех
обращающихся в специализированные косметологические учреждения на
несколько групп.
1. Пациенты с пониженым или нормальным эстетическим представлением
о внешности — люди, ведущие обычный образ жизни и спокойно
относящиеся к дефектам своей внешности, которые не мешают им вести
полноценную жизнь. Обращение за хирургической консультацией может
иметь случайный характер, например после прочтения статей в журналах
и газетах, телепередач или бесед с оперированными людьми. Таких
пациентов интересует, можно ли вообще улучшить вид лица и тела.
Отрицательное заключение хирурга не вносит в их жизнь никаких изменений.
Их мотивировка необходимости проведения операции всегда
убедительна и реальна. Подобным пациентам можно производить эстетические
операции, так как они полностью доверяют врачу и спокойно
воспринимают все действия и мероприятия по улучшению состояния здоровья,
в том числе при возникновении послеоперационных осложнений.
2. Пациенты с недостаточно развитым эстетическим чувством обычно
страдают нарушениями в психоэмоциональной сфере. Их переживания
и поведение необычны и часто не соответствуют выраженности
косметического недостатка. Их состояние подчас вызывает тревогу у
родственников и друзей, так как близкий им человек замыкается в себе, угрожает
самоубийством и т. д. Сосредоточенность этих пациентов на имеющемся
у них недостатке не позволяет получить ожидаемые результаты, даже если
технически операция выполнена безукоризненно. Агрессивность
некоторых пациентов этой группы свидетельствует о нецелесообразности
проведения вмешательства. Характерно, что отказ от операции вызывает у них
нежелательные реакции, жалобы в вышестоящие организации с
требованиями наказать "некомпетентного" хирурга и т. д. Более тяжелые
ситуации могут возникать в тех случаях, когда операция уже произведена.
3. Пациенты с извращенным эстетическим чувством практически всегда
являются больными, сосредоточенными, как правило, на
несуществующих дефектах, которые они приписывают себе сами или после
замечаний окружающих. Психическое состояние пациента можно оце-
318
нить даже на основании некоторых внешних факторов (неряшливость
в одежде, болтливость, перебивание врача или, наоборот,
монотонность речи, фиксирование взгляда в одной точке или, напротив,
бегающий взгляд). Такие пациенты часто пренебрегают предоперационными
инструкциями о режиме, лекарственной подготовке,
фотографировании. Часто они несобранны, теряют регистрационные талоны и
мелкие вещи (книги, номерки из гардероба, ключи и др.).
Следует избегать пациентов, которые уже перенесли эстетические
операции и критикуют других врачей за то, что те якобы изуродовали их или
ухудшили их внешность. Такие пациенты льстят хирургу, хвалят его "золотые
руки", утверждают, что спасти их может только он.
Люди с нестабильной психикой, потерпевшие неудачу в
профессиональной деятельности или личной жизни, все надежды возлагают на эстетическую
хирургию. Такие пациенты настойчивы, переходят от одного хирурга к
другому до тех пор, пока кто-то по незнанию не произведет вмешательство,
которое будет безуспешным.
Не следует делать операции пациентам, у которых временное
психическое напряжение или угнетение связано с психическими травмами (смерть
родственника или близкого человека, неприятности на работе или в семье).
В этих случаях хирургическое лечение должно быть отсрочено до того
момента, когда внутреннее состояние пациента будет стабилизировано.
Некоторые поведенческие факторы помогают хирургу в какой-то мере
прогнозировать будущий контакт с пациентом. Так, откровенная грубость,
раздражительность, вызванная задержкой операции, обычно подсказывает, что
послеоперационный период будет протекать тяжело, что в отношениях
больного с обслуживающим персоналом может возникнуть конфликтная ситуация.
Принято считать, что нельзя производить эстетические операции
пациентам, приносящим с собой фотографии артистов, знаменитых людей с
просьбой "сделать" их похожими на них. Хотя пациенты правы по-своему,
т. е. имеют реальные основания желать улучшения внешнего вида, они не
осознают в полной мере того, что изменение внешности имеет пределы. Речь
может идти о сохранении индивидуальных особенностей, а стремление
добиться с каким-то идеалом противоестественно и практически невозможно.
Мотивы обращения пациента к хирургу-косметологу имеют
особенности временного и типового характера. Эстетические операции целесообразно
проводить при деформациях большой давности. Если изменения внешности
возникли вследствие недавно перенесенного заболевания или травмы, то
хирургическое лечение нежелательно по многим причинам. Чем больше
времени прошло от момента возникновения деформации до операции, тем
больше вероятность избежать нежелательных хирургических и психологических
проблем. У ряда пациентов со временем отпадает желание оперироваться, так
как человек адаптируется к своему косметическому недостатку.
Основным мотивом обращения пациента к врачу является естественное
желание нравиться другим людям и себе. Нередко родители, заботясь о
будущем своих детей, заставляют их изменить внешность (чаще всего нос),
особенно если в прошлом кто-то из родителей перенес подобное лечение с
хорошим результатом. Это не исключает таких ситуаций, когда давление на
пациента обусловлено отклонениями в психическом статусе самих родителей,
когда имеются налицо внутрисемейные конфликты.
Одним из важных типовых факторов, под влиянием которых возникает
желание оперироваться, может явиться проблема карьеры, налаживания
семейных или производственных отношений. В этих случаях хирургу следует
319
чрезвычайно осторожно оценивать показания к оперативному вмешательству,
поскольку нет гарантии того, что только изменение внешности, а не деловые
качества и характер пациента могут способствовать разрешению проблем.
К внутренним мотивам обращения к хирургу-косметологу относится
депрессия, возникающая у пациентов старше 50 лет в связи с увяданием тканей
лица и шеи. Желание приостановить каким-то образом наступление
старости, особенно при сохранности высокой активности в деловой и
общественной сфере, следует расценивать как достаточно обоснованное. Однако у лиц
этой возрастной группы часто возникает инволютивный психоз. Врачебные
ошибки возможны вследствие того, что это состояние обнаруживается не до
операции, а вскоре после нее, что выражается в эмоциональной депрессии.
Оценивая мотивы обращения пациентов, хирург определяет истинность,
обоснованность и реальность их жалоб. Главным при этом является
собственное (а не принужденное) желание пациента подвергнуться
хирургическому лечению. Правильность поведения врача при этом заключается в
определении возможностей и прогноза предполагаемой операции, ни в коем случае
не заставляя пациента сделать это. Не следует давать советы по изменению
внешности и оказывать давление на его психику, поскольку он еще не
пришел к твердому самостоятельному решению.
Предупреждение возможных конфликтов хирургического обслуживания
ставит перед хирургом задачи подробного объяснения того, что ожидает
пациента перед операцией, во время и сразу после нее. Нельзя считать, что пациент
сразу запомнил все инструкции, так как после первой беседы с врачом
сохраняется состояние неизвестности в отношении проблемы изменения
внешности. Опыт работы многих хирургов показывает, что пациенту необходимо дать
специальные памятки с описанием основных положений эстетической
хирургии вообще и особенностей намеченной операции в частности, предупредить
о возможных изменениях и осложнениях, поведении в косметологическом
учреждении, методах послеоперационного лечения и т. д. Необходимо
подписание договора между учреждением и пациентом на проведение операции с
перечислением лечебных и юридических обязанностей <? обеих сторон.
Таковы некоторые особенности отбора пациентов для эстетической
хирургии по психическому статусу и отношений между хирургом и пациентом,
от чего зависят результаты хирургического лечения. В первую очередь все
это должен делать хирург, но не исключается необходимость решения всех
допросов с психоневрологом, который должен иметь высокую
квалификацию и понимание особенностей эстетической хирургии. Хирург должен
определить также противопоказания к операции соматического характера,
которые делятся на местные и общие. К местным противопоказаниям
относятся острые воспалительные заболевания носа, век, полости рта, кожи и
других систем организма.
К общим противопоказаниям относятся заболевания центральной нервной
системы, гипертоническая болезнь и ее осложнения, заболевания
сердечнососудистой, эндокринной, дыхательной систем, обострение хронических
заболеваний (гепатит, бронхоэктатическая болезнь, туберкулез, бронхиальная
астма), а также болезни органов кроветворения.
Эстетические операции в области лица и шеи являются столь же
важными мероприятиями, как и другие операции. Для объективного анализа ср-
стояния здоровья пациента необходимо комплексное обследование:
клиническое и биохимическое исследование крови с оценкой гемостазиограммы,
на носительство вируса гепатита, ВИЧ-инфекции, реакцию Вассермана,
анализ мочи, электрокардиография, консультации специалистов — терапевтов,
оториноларинголога, гинеколога.
320
29.2. Особенности техники выполнения эстетических операций
В эстетической хирургии лица и шеи при планировании и выполнении
вмешательств следует применять определенные приемы, направленные на
достижение эстетического послеоперационного рубца, который иногда является
единственным следствием произведенного вмешательства. При операциях на
кожных покровах лица и шеи хорошим в эстетическом отношении следует
считать тонкий рубец, расположенный на одном уровне с окружающими
тканями, не отличающийся практически от них по цвету, плотности и не
приводящий к смещениям близлежащих образований.
Течение процесса заживления, от которого зависит вид рубца, в каждом
конкретном случае обусловлено многими факторами внешнего и
внутреннего характера, но принципиально определяется тремя общими моментами —
хирургической техникой, применяемыми инструментами и шовными
материалами, а также состоянием тканей в области раны (локальное отображение
состояния всего организма).
Сила напряжения кожи зависит от состояния ее структур, в первую
очередь коллагеновых и эластических волокон собственно дермы. При
рассечении кожи эти напряжения формируют вид раны и степень ее зияния,
"сопротивляются" при послойном ушивании краев раневого дефекта. Все эти
тяги и противотяги непосредственно влияют на ориентацию коллагеновых и
эластических волокон в зоне рубца и на его последующий вид.
При эстетических вмешательствах разрезы следует проводить в
соответствии с ориентацией коллагеновых волокон в коже, сообразно ходу линий
натяжения Лангера, которые отражают действие соматических сил. Более
качественные рубцы получаются при расположении разрезов по ходу
естественных борозд или складок, которые являются в основном результатом действия
динамических сил, приложенных к коже за счет действия подкожной
мышечной тяги. Такие линии, определяющие топографию кожного разреза,
названные линиями расслабления, могут в принципе соответствовать ходу морщин,
но далеко не всегда, так как расположение морщин и естественных складок
кожи зависит от направления действия подкожных мышц и движений в суставах,
что не всегда совпадает с направлением линий расслабления кожи в покое. Это
относится к вертикальным складкам и морщинам лба, косым линиям на
спинке носа, у наружных углов глаз, на виске и т. д. (рис. 29.1). Линии расслабления
кожи определяют путем сдавливания кожи пальцами. Если такая компрессия
осуществляется перпендикулярно к направлению действия подкожных мышц,
то между пальцами образуются равномерные параллельные кожные складки.
В противном случае складки кожи располагаются неравномерно. Характерно,
что у детей и во многих областях лица у взрослых кожа имеет невыраженный
рисунок, и в этих случаях для выявления линий расслабления рекомендуется
перед сжатием посыпать ее тонко измельченным тальком.
Эстетический вид послеоперационного рубца определяется и зональными
признаками. Так, на него может значительно влиять рельеф подлежащих тканей.
На выпуклых поверхностях (лоб, скулы, подбородок) рубцы более заметны,
чем в складках. Редко бывают удовлетворительными L- и U-образные рубцы
вследствие того, что при сокращении рубца происходит его втягивание, а
окружающая кожа выпячивается. Примерно то же наблюдается и в тех случаях,
когда ткани рассечены не под прямым углом, и края раны оказываются
скошенными. Следует обратить внимание на то, что соотношение линий
расслабления и направления кожного разреза имеет большее значение для толстой
кожи, чем для тонкой, где рубец меньше зависит от количества коллагеновых
волокон и их ориентации.
321
21 - 1263
Принцип
физиологического оперирования —
основа эстетической
хирургии — предъявляет большие
требования к
инструментарию и шовному материалу.
Для целей таких
вмешательств следует
использовать инструменты для
рассечения покровных тканей
с высокой режущей
способностью (глазные
скальпели, алмазные,
сапфировые, бритвенные лезвия),
сосудистые ножницы,
наиболее атравматические
пинцеты Адсона — Брауна,
крючки и подъемники
краев раны и применение
самых современных
шовных материалов на атрав-
матических иглах.
В задачи
физиологического оперирования входят
рассечение кожи под
прямым углом к поверхности
(это создает одинаковое
сокращение слоев в ране),
тщательное удаление со дна
раны травмированных
тканей (вымывание, ручное или
инструментальное
очищение), гемостаз (чаще всего
диатермокоагуляция
сосудов) и своеобразная техника наложения шовного материала для соединения
краев раны.
В эстетической хирургии условием для нормального заживления
особенно важно ушивание раны со дна кнаружи без оставления "мертвого
пространства".
Учитывая биомеханические свойства кетгута, для наложения глубоких
швов следует по возможности использовать не его, а ареактивные
синтетические нити типа вайкрила, дексона и др.
В настоящее время в эстетической хирургии из всего арсенала
существующих шовных материалов предпочтение отдают синтетическим нитям,
обладающим самыми высокими медико-биологическими, физическими
(прочностными) и другими характеристиками шовного материала. Это производные
полиамидов (нейлон, капрон), полиэфиров (терилен, дакрон), полиуретанов
(перлон), полиолифинов (полиэтилен, полипропилен). Большинство нитей
импрегнируют другими материалами (они обеспечивают более гладкую
поверхность волокон), биологически активными веществами или
антибиотиками, окрашивают в различные цвета для наилучшего обнаружения их в ране.
Более глубокие швы логично накладывать крученой или плетеной нитью
(№ 00, 000) как в виде единичных узлов, так и непрерывно. При поверхност-
Рис. 29.1. Линии натяжения (сплошная линия) и
линии расслабления кожи (пунктир) (схема).
322
ных швах в условиях
незначительного зияния ран предпочтительны
моноволокнистые (жилка) нити.
В эстетических целях
наложение поверхностных швов имеет
принципиальное значение. Узло- а
вой одинарный шов циркулярно
зажимает сосудистые и нервные
окончания, что приводит к ане-
мизации тканей внутри стежков и
вблизи них на микроуровне. Все
это, несомненно, оказывает
существенное влияние на процесс
заживления и, следовательно, на
вид рубца.
Наиболее рациональными в
эстетической хирургии являются Рис. 29.2. Внутренний шов по Холстеду (а)
линейные (незамкнутые) швы. и подкожно-внутрикожный шов по Эдвар-
Они не оказывают анемизирующе- дсу (б) (схема),
го влияния, и кровообращение
сохраняется даже в сосудах,
находящихся вблизи шва. При наложении таких швов невозможно развитие некроза
кожи. Рубцовые шовные каналы находятся глубоко под поверхностью кожи
и не влияют на косметическое состояние послеоперационных рубцов.
Другими словами, все явления, сопровождающие процесс заживления,
происходят в глубине кожи, а не на ее поверхности, где остается лишь след от разреза.
Из различных швов в эстетической хирургии наиболее популярными
являются внутрикожные швы по Холстеду (рис. 29.2), Тлатову и Эдвардсу.
Внутрикожно шов накладывают в горизонтальной плоскости раны. В
зависимости от уровня наложения различают интрадермальный и субкутику-
лярный швы. По форме внутрикожный шов напоминает гофрированную
линию. Интрадермальный шов накладывают в местах, где кожа утолщена за
счет дермального слоя (лоб, переднебоковая поверхность шеи), субкутику-
лярный — где кожа тонкая.
Наложение внутрикожного шва удобно начинать с вкола иглы в просвет
раны у любого конца, снаружи оставляют свободный конец нити длиной
около 1,5 см, за который впоследствии шовный материал будет удален из
раны. Этот конец нити может быть закреплен (пуговица, валик, трубочка). При
наложении внутрикожного шва следует обращать внимание на то, чтобы
вкол и выкол иглы располагались в одном слое по высоте раны относительно
поверхности кожи. Если это правило не соблюдается, то один край раны
будет выступать или, наоборот, западать над поверхностью кожи. Вкол и выкол
иглы должны располагаться в ране строго друг против друга, а стежки
захватывать одинаковые участки дермы (рис. 29.3), так как иначе будет
происходить сморщивание ткани. Оптимальной шириной стежка в области раны
лица и шеи является 3—4 мм.
Вследствие тканевой реакции на гладкую моноволокнистую
синтетическую нить, вокруг которой формируется капсула из соединительной ткани,
длинную по размеру нить не всегда удается извлечь полностью и легко после
заживления раны. При ушивании раны большой длины нить в виде петли
следует выводить наружу (ее укрепляют на валиках, пуговицах и т. п.), а затем
вновь погружать в рану. Расстояние между наружными петлями зависит от
толщины шовного материала. Так, оптимальным для супрамида, нейлона,
323
21'
капрона № 4-0 является расстояние 6—7 см,
для нитей № 6-0 — в 1,5—2 раза меньше. В
другом конце раны оставляют такой же
свободный конец, как и в начале раны. На последнем
этапе ушивания раны рекомендуется с силой
подтянуть нить за оба конца, чтобы
обеспечить хорошую адаптацию краев раны.
Внутрикожно расположенную нить после
рассечения промежуточных петель следует
удалять отдельными участками осторожным
непрерывным подтягиванием за любой из ее
концов. Быстрая или неравномерная тяга
может привести к обрыву нити и, кроме того,
болезненна для пациента. Оставление
внутрикожно наложенной нити безвредно, но темные
полоски окрашенного материала могут быть
видны под эпидермисом. При разрыве субку-
тикулярного шва нить может выталкиваться и
обнажаться со временем, и тогда удаление ее
не представляет никакой трудности.
Вторым из наиболее часто применяемых
видов шва в эстетической хирургии является
непрерывный наружный. Его высокие
медико-биологические свойства также
заключаются в незамкнутости петель. Возможное зияние
краев раны у поверхности уменьшают
наложением наружных, а зияние дна раны —
внутренних полупетель. Наружный непрерывный
шов можно применять при зашивании всех
кожных ран, но предпочтительнее накладывать его в тех случаях, когда для
соединения краев раны требуется более 3—4 стежков. Выраженное
натяжение краев раны в определенной степени служит противопоказанием к
применению этого вида шва, так как в связи с послеоперационным местным
отеком края раны между стежками могут расходиться. Натяжение следует
уменьшать, предварительно накладывая глубокие или разгружающие швы.
Непрерывный наружный шов начинают с закрепления (петля, узел,
пуговица, валики) нити у любого конца раны. При небольшом натяжении в ране
(операции в области век, заушной складке) его можно заменить вколом на
расстоянии 0,5—1 см со стороны кожи в углу раны, оставив свободный конец
нити длиной в 1,5 см. Последующие стежки накладывают на расстоянии 2—
3 мм от края раны для вкола и выкола иглы; расстояние между стежками
составляет 4—5 мм. При этом наружная полупетля шва расположена либо
поперек, либо косо по отношению к длиннику раны. Поперечное
расположение наружной полупетли более предпочтительно, так как след от давления
нити на кожу (шовные знаки) менее заметный и более короткий.
Специальными исследованиями на разрыв ран, на которые наложены
швы различных видов [Фришберг И. Α., 1984], было показано, что разрывная
нагрузка внутрикожного и наружного непрерывного швов выше, чем
одиночного узлового в одинаковых условиях эксперимента, т. е. в
удерживающем отношении они лучше последнего.
Применение указанных выше видов хирургического шва имеет
принципиальное значение для времени снятия швов после эстетических операций.
Многочисленными исследованиями и наблюдениями убедительно доказано,
Рис. 29.3. Условия наложения
косметического шва (схема).
а — одинаковая ширина петель по
горизонтали; б — одинаковая высота
вкола и выкола иглы по вертикали.
324
что практически накожные швы оставляют так называемые шовные знаки —
перемычки, являющиеся своеобразной атрофией кожи, если шовную нить не
удаляют в течение первых 7 дней. В худшем положении находится
непрерывный шов, снятие которого в ранние сроки возможно только при наложении
глубоких удерживающих швов. Снятие же внутрикожного шва по
изложенным выше соображениям возможно через довольно длительное время без
нарушения эстетического вида рубца.
Общие принципы шовной техники при эстетических операциях на
основании научных экспериментов и клинических наблюдений можно
сформулировать в виде следующих положений:
1. Длительное пребывание шовного материала в ране для удержания ее
краев бессмысленно, так как через 2 нед она становится достаточно
прочной, чтобы существовать без этих швов.
2. Широкие атрофические рубцы в ближайшем послеоперационном
периоде объясняются меньшей степенью прочности тканей в шве по
сравнению с окружающей интактной кожей в течение
продолжительного времени (около 1 года). Бороться с этими явлениями путем
длительного сохранения в тканях шовного материала нецелесообразно.
3. Удержание краев бывшей раны в течение длительного времени без
ухудшения косметического состояния рубцов возможно только при
использовании внутрикожного косметического шва.
29.3. Удаление доброкачественных образований
и коррекция простых рубцов
Доброкачественные новообразования в области лица и шеи могут быть
накожными, внутрикожными и исходящими из более глубоких тканей
(жировая, фасциальная, мышечная). Характер опухолей должен быть определен
после консультации с онкологом даже в тех случаях, когда диагноз ясен для
клинициста. Обязательным является и клиническое обследование пациента.
В любых случаях наружное новообразование (невусы, фибромы)
округлой формы следует иссекать в пределах здоровых тканей, ориентируя
будущую рану в виде веретена по существующим в данной области линиям
расслабления кожи. Примечательно, что продолговатые поверхностные невусы
обычно располагаются изначально по этим линиям, что дает хирургу
возможность определять линии кожных разрезов.
При более глубоко расположенных опухолях (атеромы, липомы, невромы
и др.) можно проводить линейный разрез над ними или с иссечением узкого
веретенообразного участка, ширина которого увеличивается в зависимости
от величины опухоли. Это необходимо для удаления избытка растянутой
кожи, вызванного выбуханием опухоли.
Удаление глубоко расположенных новообразований вызывает
необходимость ушивания раны в несколько слоев, начиная со дна. Затем
накладывают непрерывный внутрикожный косметический шов.
Весь удаляемый материал независимо от его происхождения в
обязательном порядке направляют для гистологического исследования.
Небольшие по величине рубцовые участки кожи можно иссекать
одномоментно с последующим сшиванием краев раны в один-два слоя. В
различных участках кожи лица и шеи при непосредственном прямом сшивании краев
раны существует предельно допустимая степень их скольжения. Для
создания оптимальных условий заживления края раны обычно мобилизуют. При
325
этом происходит не истинное растяжение кожи, а скольжение ее над под-
кожной жировой клетчаткой. Чем шире границы отслойки, чем более
рыхлым является подкожный жир, тем легче происходит сближение краев раны.
В тех случаях, когда неизвестно, удастся ли прямо сблизить края раны,
можно отслоить кожу с одной стороны рубца и, подтягивая к центру
крючком или пинцетом, определить ее пластические свойства. Затем отслаивают
другой край раны и также натягивают его. Если оба края сходятся в центре,
то сближение швом не будет проблематичным. На этом этапе рубец может
быть иссечен полностью или частично. В противном случае дефект кожи
после иссечения рубца закрывают одним из методов местной пластики или
трансплантацией свободных кожных лоскутов. Следует подчеркнуть, что
даже небольшим рубцам, расположенным поперек или под углом к линиям
расслабления кожи, необходимо придавать зигзагообразную форму в
соответствии с ориентацией этих линий (Z-пластика).
29.4. Натяжение кожи лба
Показаниями к натяжению кожи лба являются горизонтальные складки,
обусловленные фиброзом мышц данной области (лобной, мышцей гордецов,
мышцей, сдвигающей брови), или низкое положение (птоз) бровей при
гладкой коже. При планировании операции обращают внимание на высоту лба,
составляющую Уз высоты лица. При увеличении указанного размера разрез
проводят перед линией волос, при меньшем размере — в волосах. В
последнем случае пациента следует предупредить о том, что линия волос будет
смещена кверху на 1,5—2 см.
Лучше проводить внутривенный наркоз в сочетании с применением ме-
стноанестезирующих растворов, обеспечивающих, кроме того,
гидравлическую отслойку. Если операция направлена на выключение действия лобной
мышцы, то это предполагает проведение гидравлической отслойки подкожно
над апоневрозом мышцы и под нею. При правильном введении
анестезирующего раствора происходит четкое разглаживание кожи с исчезновением
борозд.
Независимо от места кожный разрез должен повторять форму линии волос,
т. е. иметь естественную выпуклость в центре и изгибы кверху в области висков.
Концы разреза обычно достигают вертикали, проведенной мысленно за
наружный конец брови.
Кожный лоскут отслаивают книзу до бровей и отворачивают книзу. При
этом правильность отслойки можно определить по краю лоскута: в него
должны входить кожа и плотная жировая клетчатка, пронизанная
вертикальными дольками с включением волосяных луковиц, наподобие частокола.
Дном раны является белесоватый и блестящий передний листок апоневроза
лобной мышцы.
Затем из мышцы с апоневрозом иссекают полосу параллельно кожному
разрезу и производят отслойку мышцы между задней стенкой апоневроза и
надкостницей. Наибольшее расслабление и опускание мышцы происходят
при проведении вертикальных сечений от концов разреза к концам бровей.
Кожу лба натягивают с соблюдением симметрии поднятия бровей и иссекают
возникающий избыток (рис. 29.4). Рану в волосистой части лба можно
ушивать узловыми швами или наружным непрерывным швом, перед линией
волос — внутрикожным косметическим швом.
На 7—10 дней накладывают давящую асептическую повязку, после
чего возможны мытье головы и парикмахерские манипуляции. Из послеопе-
326
Рис. 29.4. Операция в области лба (схема).
а — разрез и зона отслойки кожи; б — рассечение лобной мышцы с апоневрозом; в -
кожи и иссечение ее избытка.
натяжение
рационных изменений в первые дни в орбитальной области и щеках
отмечаются кровоподтеки, онемение кожи лба и теменных областей в течение
1 — 1,5 мес и (иногда) выпадение волос при расчесывании далеко от линии
волос (рефлекторная реакция, не
требующая специального лечения).
Полного выключения лобной
мышцы не происходит, и при ее
сокращении на коже могут быть лишь
очень пологие волны, эстетически
более приемлемые, чем бывшие
ранее борозды и резкие складки
(рис. 29.5).
В последние несколько лет в
зарубежной литературе широко
рекламируется эндоскопическая техника
при возрастных изменениях в области
лба. Она заключается в том, что через
один или два разреза длиной
несколько сантиметров в волосистой части
лба производят широкую
подкожную отслойку. Затем под контролем
оптики пересекаются волокна лобной
мышцы, мышцы гордецов и мышцы,
сдвигающей брови. Несомненно, что
подобные операции менее
травматичны и более эстетичны в отношении
послеоперационных рубцов, но они
не позволяют решить проблему
натяжения кожи и поднятия бровей, что
требуется при увядающих мягких тка- Рис. 29.5. Натяжение кожи лба до (а) и
нях лица. после {б) операции.
327
29.5. Коррекция бровей при птозе
По эстетическим показаниям коррекцию бровей проводят при опущении
(птоз) и связанной с этим их горизонтальной форме. В последние
десятилетия установлен так называемый голливудский стандарт формы и положения
брови, придающий лицу естественный вид. Вертикаль от головки брови
должна проходить через основание крыльев носа и в этой же точке должна
соприкоснуться с линией, идущей от наружного угла глаза (рис. 29.6). В
средней части бровь плавно изгибается кверху. Следует отметить, что в настоящее
время в соответствии со стандартами эстетической внешности не
рекомендуется подбривать или выщипывать волосы бровей.
Опущенные брови встречаются довольно часто и не всегда являются
признаком старения мягких тканей лица. При небольшом глазном яблоке, его
западении в глубокой орбите, узком входе в полость орбиты с рельефным
острым и выступающим вперед надбровьем прямое расстояние между бровью и
глазной щелью становится небольшим и положение брови воспринимается
зрительно как низкое. Такая картина может наблюдаться даже у детей
вследствие генетической зависимости.
Устранение птоза бровей можно проводить изолированно или в
сочетании с другими операциями (например, в области лба, верхних век). При
изолированном поднятии бровей проводят кожный разрез по краю роста волос.
Послеоперационный рубец менее виден у пациентов с темноволосыми и
широкими бровями. При тонких и светловолосых бровях рубцы практически
всегда заметны, и в этих случаях логичнее проводить натяжение кожи лба.
Форма иссекаемого участка кожи над бровями варьирует в зависимости
от необходимости подъема всей брови или только ее участков — головки,
тела, хвоста. Разрез кожи над бровями очень похож на запятую (правильный
полулунный разрез приводит к крутой изогнутости бровей). Кроме того,
брови более эстетичны, если их наружная часть слегка приподнята. Ширину
иссекаемого участка кожи устанавливают до операции. Она зависит от того,
на какую высоту необходимо поднимать бровь. В пределах намеченного
участка иссекают мягкие ткани. Большая осторожность необходима на
границе головки и средней трети, где располагается верхнеорбитальный нерв.
В начальной трети брови иссечение
идет только в кожном слое, в
остальных 2/з брови — вплоть до
надкостницы. Гемостаз осуществляют с помощью
электрокоагуляции. Вдоль верхнего
края раны дополнительно иссекают
полоску лобной мышцы шириной δ-
10 мм, что в ближайшем
послеоперационном периоде способствует
наилучшей иммобилизации брови в новом
положении. Затем подкожные ткани
нижнего края раны подшивают нерас-
сасывающейся нитью к надкостнице у
верхнего края раны (собственно
поднятие брови). Рану ушивают в два слоя
(поверхностный — внутрикожный
косметический шов). Давящая
асептическая повязка необходима в первые
дни. Швы снимают через 8—10 дней
(рис. 29.7).
Рис. 29.6. Эстетический стандарт
положения брови (схема).
328
Как вариант, обеспечивающий только один кожный рубец по
естественной складке верхних век, возможно сочетанное вмешательство при
проведении верхней эстетической блефаропластики. После иссечения намеченного
участка кожи отслаивают кожу до брови или несколько выше (следует
помнить о топографии верхнеорбитального нерва). Затем пальцами определяют
необходимую степень подъема брови и с внутренней стороны лоскута
подшивают бровь на новом уровне.
Осложнения при данной операции практически отсутствуют, и
эффективность ее улучшает эстетический результат за счет уменьшения наплыва
тканей кожи в области верхних век. Иногда поднятие бровей устраняет
необходимость проведения верхней блефаропластики.
29.6. Эстетическая верхняя блефаропластика
Хотя основными жалобами пациентов с увядающими тканями в области верхних
век являются избыток,кожи, в проблемы, решаемые при верхней
эстетической блефаропластике, может входить манипулирование на более глубоких
тканях (удаление жировых грыж, создание отсутствующей или недоразвитой
естественной складки и др.).
Изменения тканей в области верхних век не всегда являются возрастной
патологией и могут встречаться даже у детей в связи с генетической
предрасположенностью, гипертрофией круговой мышцы глаза или быть признаком
329
аллергии, заболеваний почек или сердечно-сосудистой системы. Любые
отеки век, возникающие при заболеваниях, интоксикациях, физиологических
циклических процессах (менструации), способствуют растяжению кожи,
ослаблению ее связей с подлежащими образованиями и появлению провисаний
и складчатости.
Возрастные изменения в области век характеризуются истончением
кожи, ее складчатостью с нависанием над ресничным краем (иногда с
перекрытием его). Естественная борозда прячется глубоко в этих складках и не
видна даже при сомкнутых веках. При надавливании на глазное яблоко в
средней части верхнего века и внутреннем отделе его увеличивается
выбухание тканей (симптом определения жировых грыж). Прогностическим
признаком эффекта оперативного вмешательства является состояние кожи: чем
больше она покрыта сеткой морщин, чем больше они распространяются к
внутреннему углу глаза, тем менее эффективна операция, так как у
внутреннего угла глаза невозможно иссечь столько же кожи, сколько в среднем иди
наружном участке верхнего века.
Планирование операции проводят при спокойно сомкнутых веках,
т. е. тогда, когда кожа находится в состоянии максимального
естественного расправления в положении пациента стоя или сидя. Точность
определения избытков кожи зависит также от степени натяжения тканей
вокруг орбитальной области (положение бровей, натянутость кожи нижних
век, висков).
Нижняя граница разреза кожи проходит по естественной (пальпебраль-
ной) складке от одного угла глаза до другого, которая соответствует верхнему
краю хряща века. При маркировке этой линии разреза краской важно, чтобы
она находилась на 7—9 мм выше ресничного края, если собственная складка
расположена низко. Это касается лиц с европейским строением век. У лиц
же с монголоидным строением естественная складка расположена более низко
и горизонтально. Верхняя граница разреза проходит по основанию складки от
взятия избытка кожи браншами атравматичного пинцета. При этом край века
не должен смещаться кверху и обнажать склеру. Форма иссекаемого участка
напоминает запятую (для левого глаза) с сужающимся краем у внутреннего угла
глаза (здесь избыток кожи всегда меньше) и расширением у наружного угла.
Рассечение тканей верхних век, удаление намеченного краской участка
кожи и другие хирургические манипуляции следует выполнять крайне
осторожно, учитывая тонкость покровов и высокую функциональную значимость
век. При утолщенном веке иссечение надо проводить через все слои (кожа,
круговая мышца, подлежащая клетчатка) вплоть до апоневроза леватора
верхнего века.
Кровотечение из раны обычно незначительное. Его останавливают
электрокоагуляцией сосудов или прикладыванием салфеток, смоченных ледяным
изотоническим раствором натрия хлорида. Последнее предпочтительнее, так
как в дальнейшем заживление будет происходить без очагов некроза от
электроприжигания или механического сдавления в лигатуре.
При наличии жировых грыж волокна круговой мышцы глаза
расслаивают тупым путем в среднем и внутреннем отделах, надсекают орбитальную
фасцию. После этого окологлазничный жир свободно выходит в рану и
избыток его строго по дну раны может быть иссечен с обработкой культи
грыжи (лигатура, электрокоагуляция и др.). Подтягивание жира наружу опасно
из-за возможности разрыва ткани с кровотечением в полость глазницы.
Особое внимание требуется при удалении жира во внутреннем отделе — в
зоне блокового нерва, где травма и даже глубокая анестезия могут вызвать
диплопию.
330
Рис. 29.8. Этапы операции на
верхних веках и варианты
иссечения кожи у внутренних
углов глаз (а — в).
На кожу накладывают наружные или внутрикожные швы. Края раны
должны сводиться свободно. Возможно незначительное обнажение
склеры, быстро проходящее по мере уменьшения послеоперационного отека
тканей.
При выраженном увядании тканей верхнего века особую трудность
представляет коррекция внутреннего угла глаза, где часто остается
некоторый избыток кожи, мало поддающийся удалению по стандартной
методике. Частичное улучшение ситуации возможно при вариантном
создании внутреннего края раны по методу Сильвера, Бурова и др.
(рис. 29.8).
Недоразвитие или отсутствие естественной складки кожи верхних век
корригируют созданием мышечно-апоневротического соединения
аналогично природному сращению апоневроза леватора с кожей по линии хряща
верхнего века. С этой целью ткани рассекают вплоть до апоневроза леватора
(его диагностируют при появлении блестящего листка на дне раны и
подвижности при подъеме верхнего века кверху). Затем край круговой мышцы
по нижней границе раны симметрично по центру и бокам подшивают к
апоневрозу кетгутовой нитью. Наложение швов контролируют движениями века.
Местоположение швов можно менять для достижения необходимой формы
и высоты складки.
Линию швов на 1 сут закрывают асептической повязкой, поверх которой
в течение суток на несколько минут с перерывом в 40—45 мин накладывают
пузыри со льдом. Рекомендуется прием болеутоляющих (анальгин) и
кровоостанавливающих (кальция глюконат, натрия этамзилат, дицинон и т. д.)
средств. По мере исчезновения видимой отечности швы удаляют через 4—5
дней. Длительное сохранение наружных швов не рекомендуется из-за
быстрого слипания краев раны и возникновении точечных знаков в местах вкола
и выкола иглы, что объясняется ускоренным врастанием эпидермиса в
шовный канал.
331
29.7. Эстетическая нижняя блефаропластика
Операции в области нижних век требуют повышенной внимательности,
поскольку даже небольшая ошибка в планировании и проведении его может
привести к вывороту нижнего века, исправить который крайне трудно.
Клиническая картина увядания мягких тканей нижних век типична: кожа
вялая, тонкая, легко смещается и собирается в складки, под ней выбухает
окологлазничный жир (жировые грыжи) в виде "мешков". При легком
надавливании на глазное яблоко эти выбухания увеличиваются.
Кожный разрез проводят отступя 2—3 мм от ресничного края и по ходу
края века от внутреннего угла (кнаружи от слезной точки) до вертикали,
проходящей через наружный угол глаза. От этой точки разрез ведут косо к
горизонтали через наружный угол таким образом, чтобы место изгиба находилось
около 5 мм от самого угла глаза. Это необходимо для того, чтобы
предупредить деформацию угла глаза послеоперационным рубцом (запаянность угла,
образование эпикантуса и др.)· Изгиб рубца можно располагать и по линии
одной из "гусиных лапок".
В области нижних век ткани можно отслаивать в подкожном или
подмышечном слоях. Выделение кожного лоскута показано при истонченной и
растянутой коже, а кожно-мышечного — при более упругой коже. Выделение
кожного лоскута до нижнего края глазницы сопровождается большей
кровоточивостью и травмой круговой мышцы. Кожно-мышечный лоскут
выделяют над рыхлой клетчаткой; кровоточивость при этом минимальная.
При раздвигании волокон мышцы (при кожной отслойке) выявляются
грыжи в среднем и внутреннем отделах (реже в наружных). Их удаляют таким
же образом, как при описанной выше верхней блефаропластике.
Особенно важно иссекать избыток кожи нижних век. При открытых
глазах и взгляде вверх кожу следует расправить кверху и кнаружи, но ни в коем
случае не тянуть ее инструментами. Избытком кожи считают участки
лоскута, расположенные выше линии кожного разреза. Избыток тканей иссекают
и рану ушивают наружным или внутрикожным швом (рис. 29.9).
Удаление жировых грыж возможно и в отсутствие избытка кожи. При
этом узким глазным скальпелем с шириной полотна 3—4 мм делают
небольшие проколы-разрезы через кожу и мышцы непосредственно над жировыми
"пакетами" строго по линиям расслабления кожи. В рану вводят концы
зажима-москита и вытягивают наружу глазную клетчатку. Это
малотравматичное вмешательство дает высокий эстетический эффект, хотя имеет
ограниченное применение (только у молодых людей без избытка кожи).
В последние годы отмечается высокая эффективность коррекции грыж
нижних век без их иссечения, что резко снижает количество осложнений и
рецидивов. Сущность операции заключается в обнажении жировых комков,
покрытых орбитальной фасцией. Затем накладывают непрерывный съемный
шов, нить которого (моноволокнистая синтетика) захватывает надкостницу
края глазницы и орбитальную фасцию по верхнему краю грыжевого мешка.
Таким образом, происходит инвагинация жировых масс с одновременным
укреплением стенки века. Шов удаляют через 5—6 дней.
Для профилактики образования выворота нижних век эффективны
различные хирургические приемы, особенно целесообразные при вялых тканях
и выраженной слабости стенки нижних век: укорочение века клиновидным
иссечением всех тканей по высоте, подшивание участка пальпебральной
части круговой мышцы к боковой наружной связке век, выделение треугольного
мышечного лоскута с вшиванием его под кожу у наружного угла глаз и др.
332
a — линии разрезов и площадь ί
отслоения тканей; б — иссечение
клетчатки; в — ушивание раны. в
Послеоперационное ведение пациентов аналогично таковому после
операций в области верхних век. Из-за отечности слезной точки и отхождения
ее от глазного яблока в течение нескольких дней может наблюдаться
слезотечение, проходящее самопроизвольно. Степень отечности уменьшается после
прикладывания в течение нескольких дней холодных примочек из крепкого чая,
отвара ромашки или шалфея. Такие примочки полезно делать и в дальнейшем
с целью дубления кожи и уменьшения ее отечности, вызывающей припухлость
под веками и в скуловой области. Через 7—10 дней можно проводить
мероприятия по уходу за кожей (тени, маски, краски, кремы и т. п.) (рис. 29.10).
Осложнения. После эстетической блефаропластики в
послеоперационном периоде отмечаются временные осложнения и длительные, требующие
активных мероприятий.
Ретробульбарная гематома и кровотечение в полость
орбиты — наиболее опасные осложнения, объясняемые травмой сосудов.
При кровотечении спустя 1,5—2 ч после операции может наступить потеря
зрения от сдавления центральной артерии сетчатки. Клинически глазное
яблоко не баллотирует, наблюдаются плотность и выбухание конъюнктивы,
инъецирование конъюнктивальных капилляров. Внутри глаза пациенты
ощущают боль, свободные движения глаза ограничены вследствие экзофтальма.
При тонометрии отмечается давление до 100 мм рт.ст. (норма 15,5 мм рт.ст.).
Слепота при ретробульбарном кровотечении имеет временый характер, так
как кровяные сгустки постепенно рассасываются. Тем не менее в литературе
описано более 70 случаев стойкой слепоты после блефаропластики. Лечение
заключается во внутривенном введении гипертонических растворов D0 %
раствор глюкозы, маннитол) с целью дегидратации, применении
диуретических средств, холодных компрессов. Параллельно следует проводить гемо-
статическую терапию A0 % раствор кальция хлорида, 5 % раствор аминока-
333
Рис. 29.10. Больная с избытком кожи и жировыми грыжами до (а) и после (б) операции.
проновой кислоты, дицинон). Использование парацентеза в настоящее время
не рекомендуется из-за возможности развития грыжи радужной оболочки.
Наилучшей профилактикой этого осложнения являются тщательный гемостаз
во время операции и отказ от применения ацетилсалициловой кислоты и
антикоагулянтов в течение 3—4 нед до вмешательства.
Подкожную гематому диагностируют при выявлении синюшности и
выбухания кожи с флюктуацией в центре. Удаление гематомы в 1-е сутки
нецелесообразно, если кожные покровы не поражены. Следует подождать, пока
произойдет стабилизация процесса и через 5—7 дней опорожнить полость через
небольшой штыковой разрез, а затем выдавить содержимое. При неудаленных
гематомах наблюдаются длительное уплотнение тканей век, медленное
рассасывание узлов под кожей и др. Ликвидации изменений в тканях вследствие гематомы
в значительной мере способствуют физиотерапевтические процедуры, массаж.
334
Слезоточивость возникает в результате отека тканей и проходит по
мере стихания его. Длительная слезоточивость (несколько недель) может быть
связана с сужением слезных канальцев или слезного мешка рубцами.
Профилактическими мерами являются бережное отношение к круговой мышце глаза,
являющейся своеобразным насосом для слезовыделительной системы глаза.
Кожные разрезы не следует доводить до слезной точки, чтобы не вовлечь ее
в рубцовый процесс. Лечение заключается в активной рассасывающей терапии,
массаже, бужировании слезно-носового канала (в сложных случаях).
Сухой кератоконъюнктивит может обнаруживаться после бле-
фаропластики, хотя и не является прямым следствием операции. Скорее всего
это является результатом того, что плохо был собран анамнез перед
операцией (глазные заболевания), недооценена слабость нижнего века с
обнажением склеры под радужкой или недостаточно тщательно проведены
манипуляции на тканях век. Во всех случаях перед операциями на нижних веках
следует использовать специальные тесты для определения продукции слезы.
Лечение сухого кератоконъюнктивита заключается в длительном
применении специальных глазных капель ("искусственные слезы").
Диплопия — двоение зрения. Может проявиться в первые несколько
часов после операции и быть связанной с нарушением функции глазных
мышц (например, нижней косой мышцы, разделяющей средний и
внутренний пакеты жировой клетчатки) или с вовлечением в процесс блокового
нерва при удалении грыж из внутреннего отдела верхних век. Если это состояние
сохраняется в течение недели, необходима консультация офтальмолога.
Блефарит. Необходимо лечение и наблюдения у офтальмолога.
Потеря ресниц может происходить самопроизвольно. Однако при
стойком выпадении ресниц их восстановление возможно путем тончайших
вмешательств с целью пересадки кожной полоски с волосом или единичным
вкраплением ресниц, лучше удающейся окулистам.
Μ ел кие кожные кисты возникают по линии рубца вследствие
врастания эпидермиса в шовный канал при наложении наружных швов уже
в первые 48 ч. Профилактика заключается в наложении внутрикожных швов,
раннем снятии наружных швов. Ликвидацию (вскрытие кист) лучше
проводить не ранее чем через месяц после операции.
Выворот нижних век клинически выражается в некотором
прилегании века к глазному яблоку (легкая степень) или выворачивании века с
обнажением гиперемированной слезной точки, конъюнктивы, а также в слезотечении
(тяжелая степень). Причины выворота нижних век разнообразны: чрезмерное
иссечение кожи, укорочение орбитальной фасции швом, парез круговой мышцы
глаза, чрезмерное удаление жировой клетчатки, гематома и др. При легкой
степени выворота успешными могут оказаться такие мероприятия, как наложение
поддерживающих швов на 72 ч, подтягивание нижних век пластырем кверху для
расслабления тканей, активная гимнастика для повышения тонуса круговой
мышцы. При выраженном и стойком вывороте прибегают к свободной кожной
пластинке полнослойным лоскутом в период от 48 ч до 4—6 мес после
первичного вмешательства. Для этих целей наилучшими донорскими участками
являются верхние веки, сосцевидная или надключичная область.
29.8. Коррекция деформаций носа
При анализе врожденных и приобретенных деформаций наружного носа
приходится учитывать не только его форму и размеры, но и отношение к
близлежащим образованиям и лицу в целом. В связи с этим при оценке вида
335
1 Рис. 29.11. Основные параметры
и размеры носа (схема).
I — расстояние между наружными
углами век (85—100 мм); 2 —
расстояние между внутренними углами век
C0—40 мм); ЗА — ширина спинки
носа у корня (8—15 мм); ЗБ — в
костном отделе A2—15 мм); ЗВ — у
кончика носа A0—12 мм); 4 — ширина
кожной перегородки носа F—10 мм);
5 — высота кожной перегородки носа
F—17 мм); 6 — расстояние между
основаниями крыльев носа B1—30 мм).
и степени деформации носа
необходимо учитывать: 1)
соотношение размеров
хрящевого, костного и концевого
отделов; 2) расположение
срединной вертикальной оси;
3) вид профильной линии с
учетом носолобного и носогуб-
ного углов; 4) степень
нарушения дыхательной функции.
Кроме того, следует
обращать внимание на
симметричность и конфигурацию носовых
ходов, на параметры,
определяющие положение и основные
размеры носа (рис. 29.11).
Нос составляет около у3
длины лица. Угол,
образованный линией, соединяющей
плоскость лба и подбородка, и
линией спинки носа
(профильный угол) в норме составляет 30°. При величине этого угла более 40° нос
кажется вздернутым, меньше 30° — уплощенным. Носогубной угол равен
примерно 90° (при более остром угле нос выглядит удлиненным, при более
тупом — укороченным).
Мягкие и плотные ткани наружного носа имеют специфические
анатомические взаимоотношения, которые отражаются на технике эстетической
ринопластики и конечном результате лечения. Прежде всего кожа носа
утолщается от корня до кончика носа; она смещается над костями и плотно
сращена с хрящами. Кровоснабжение кожи осуществляется поверхностными
субдермальными сплетениями, что следует учитывать при отслойке кожи.
Надкостница не только покрывает кости носа, но и внедряется между
ними. При ее мобилизации возможны разрывы у гребня спинки, приводящие
в послеоперационном периоде к возникновению грануляций под кожей,
неровностям спинки и др.
Верхние боковые хрящи (треугольные) перемычкой из плотной
соединительной ткани соединяются с большими (нижними) крыльными хрящами
таким образом, что в наружных отделах нижние хрящи накладываются на
верхние, как черепица. Благодаря этому хрящи могут смещаться по
отношению друг к другу, ноздри сужаются и расширяются, участвуя в дыхании и ми-
336
мике. Такое же соединение имеется между наружными отделами верхних
боковых хрящей и костями, где перекрытие хрящом достигает 1 см и отмечается
плотное сращение между надкостницей и надхрящницей.
Различия в высоте и ширине боковых отделов больших крыльных
хрящей и отстоянии их нижних краев от края крыла заставляют тщательно
планировать внутриносовые разрезы с целью сохранения правильной анатомии
кончика носа и его опорной системы.
Нижняя часть крыла носа имеет трехслойное строение (кожа, слизистая
оболочка и плотная фиброзная ткань между ними). Коллагеновые волокна
этой ткани ориентированы по длиннику хряща и носового хода, что
способствует сохранению формы крыла.
Наконец, важной структурой является кожная часть перегородки носа.
Ее основу составляют медиальные ножки больших крыльных хрящей. Она
должна быть достаточной длины для обеспечения выстояния кончика носа
над линией спинки, образовывать тупой угол с губой и располагаться на 2—
3 мм ниже прямой линии, проведенной через край крыльев носа.
Для эстетической ринопластики оптимальным считается возраст 17—25 лет,
так как в более позднем фиксация пациентом внимания на своей внешности
усиливается, а это в свою очередь значительно затрудняет ее изменение
посредством операции.
В дооперационный анализ деформации входит оценка анатомических
особенностей лица и гармонических соотношений (тип лица, его размеры,
степень утолщения костей носа, выраженность надпереносья, строение
перегородочного отдела и кожи). Обязательны анализ состояния слизистой
оболочки, определение размера раковин, положения хрящевой и костной
перегородок и др. Для оценки функционального состояния носа целесообразно
проводить специальное тестирование (ринопневмография и др.).
Длительное время фотография пациента была единственно достоверным
доказательством эффективности лечения. Снимки делают в трех проекциях:
в фас, профиль и с поднятым подбородком. При совместном с пациентом
просмотре фотографий можно показать ему (очертить) будущую форму носа,
продемонстрировать асимметрию в основании крыльев носа, спинке,
концевом отделе.
В последнее время в практику пластической и эстетической хирургии
лица входит ЭВМ-анализ: в присутствии пациента на экране происходит
поэтапное преображение внешности, и сам пациент как бы видит конечный
результат предполагаемого лечения. Однако компьютерный образ не всегда
может быть достигнут в реальности, когда начинают действовать многие
причины.
Оперативные доступы при эстетической ринопластике делятся на
наружные и внутренние. Последние по своей локализации делятся на:
1) передний эндоназальный доступ — по нижнему краю больших
крыльных хрящей и перед медиальными ножками их. Он позволяет
подойти к любому отделу крыльных хрящей, что особенно необходимо
при деформациях кончика носа и крыльев. Однако в
послеоперационном периоде может возникнуть рубцовая деформация края ноздри,
теряющей хрящевую опору;
2) средний эндоназальный доступ (чресхрящевой) — приблизительно
посредине боковой ножки большого крыльного хряща и позади
медиальных ножек его. При этом доступе достаточно хорошая
обозримость хрящевых и костных образований носа позволяет сохранить
архитектонику крыльев и кончика его;
337
22-1263
3) задний эндоназальный доступ (межхрящевой) — между нижним
краем верхних боковых (треугольных) хрящей и верхним краем нижних
боковых хрящей (крыльных). Он наиболее удобен для манипуляций
в костном отделе.
Несмотря на популярность эндоназальных доступов, за рубежом вновь
приобретают ценность наружные доступы с разрезом ткани типа "птички",
основание которого находится на кожной части перегородки носа.
Практически наружный послеоперационный рубец очень быстро становится
малозаметным, но нельзя недооценивать преимущество широкого доступа ко
всем структурам носа, возможность под контролем глаза с большой степенью
точности создать симметрию крыльев, гладкость контура спинки носа и
многое другое, представляемое наружным доступом ринопластики.
Частными задачами эстетической ринопластики являются
выравнивание спинки носа и сужение ее; укорочение, сужение и изменение
конфигурации кончика. Эти основные этапы эстетической ринопластики можно
осуществлять в той или иной последовательности, сочетанно или изолированно,
но почти всегда взаимосвязанно.
Выпрямление и сужение спинки носа. Необходимость выпрямления
спинки носа возникает при ее чрезмерной высоте (горб носа), выраженном
понижении (запавшая, седловидная спинка) и смещении по отношению к
срединной вертикали лица (искривленный нос). Все виды ринопластики
обычно выполняют под местным обезболиванием с премедикацией.
Понижение спинки носа. В зависимости от задач понижения
спинки носа проводят один из эндоназальных разрезов, симметрично с обеих
сторон. На протяжении крыльных хрящей отслойку следует вести очень
близко к хрящу, а не к коже. Вдоль края грушевидного отверстия скальпелем
делают насечку до появления ощущения костной поверхности. В
дальнейшем отслойку ведут поднадкостнично распатором, что обеспечивает
незначительную кровоточивость раны. На боковых скатах костной пирамидки носа
отслойка несложна, но ближе к гребню надкостница ощутимо истончается.
Вследствие этого при переходе с одной стороны на другую необходимо очень
осторожно производить движения распатором. В отдаленном
послеоперационном периоде сохранность надкостницы в области гребня спинки
обусловливает плавность перехода одного отдела спинки в другой. Отслойку
надкостницы продолжают у основания костей носа, а затем переходят на носовой
отросток верхней челюсти. Правильность отслойки определяют по весьма
характерному ощущению костной поверхности при поскребывании.
При уменьшении спинки носа по всей линии гребня в хрящевом отделе
по обеим сторонам перегородочного хряща рассекают слизистую оболочку и
верхние боковые хрящи, обнажая передний край перегородочного хряща.
Скальпелем или острыми ножницами иссекают небольшую полоску
перегородочного хряща и узкие полоски по переднему краю верхних боковых
хрящей. Костную часть удаляют остеотомом. Поверхность спила обрабатывают
рашпилем с различной насечкой. Костные опилки, обрывки надкостницы
удаляют маленькой ложкой. Для образования естественной линии спинки
носа производят боковую остеотомию.
При боковой остеотомии пользуются долотом, имеющим правый и
левый изгибы. Инструментом следует нащупать край грушевидного отверстия,
сделать первый надлом, а затем постепенно поворачивать долото
соответственно профилю боковой стенки. Линия остеотомии должна проходить
достаточно низко, чтобы можно было полностью отделить носовой отросток
верхней челюсти и в дальнейшем избежать образования ступенеобразной бо-
338
Рис. 29.12. Этапы операции
понижения спинки носа
(удаление горба носа) (схема).
а — устранение горба спинки носа;
б — обработка корневой костной
поверхности рашпилем; в —
боковая остеотомия.
ковой стенки за счет перепадов высоты костных фрагментов. Боковые
участки пирамидки сужают пальцами (рис. 29.12).
Одним из методов предупреждения вторичных изменений является
операция Руденко, в основу которой положен принцип уменьшения спинки
носа за счет его общего снижения без нарушения основных взаимоотношений
между его отделами (метод вдавления). Операцию начинают с проведения
промежуточного разреза слизистой оболочки (между медиальными ножками
больших крыльных хрящей и нижним краем перегородочного хряща), из
которого производят поднадхрящную отслойку хряща с одной стороны. Затем,
отступя 0,5 см от свода носа, двумя разрезами хряща до слизистой оболочки
на другой стороне иссекают из перегородочного хряща горизонтальную
полоску шириной 1—2 мм (чаще 4—6 мм). Затем выполняют двустороннюю
боковую остеотомию для получения единого блока, который раскачивают и
вдавливают пальцами в верхнюю челюсть так, чтобы сомкнулись края
дефекта в перегородочном хряще, а пирамида носа сместилась под основание
носовых отростков верхней челюсти (рис. 29.13). Врожденные пологие и даже
достаточно выраженные горбы при вдавлении спинки носа распрямляются
наподобие дуги лука, лишенной стягивания в конечных точках. Горбы,
возникшие вследствие травмы, особенно при деформации перегородки, не
подлежат такой коррекции. Их следует удалять описанным выше стандартным
способом.
Повышение спинки носа представляет собой ряд оперативных
методов восстановительного характера. В качестве пластического опорного
материала наиболее часто применяют аллохрящ из VII—VIII ребра, взятого от
трупов мужчин (женские хрящи более мягкие) в первые 24 ч после смерти.
Использование этого материала возможно только при полной безопасности для
здоровья пациента (проверка трупной крови на бактерицидность и др.). Хрящи
хранят в очищенном виде (без травмированных мягких тканей) в растворе
Рингера — Локка или фурацилина с добавлением антибиотиков при
температуре 4°С. Растворы обновляют один раз в неделю. Возможно использование
лиофилизированного хряща, высушенного в вакууме при температуре —
70°С. Такой хрящ перед моделированием и использованием выдерживают для
разбухания в изотоническом растворе натрия хлорида в течение 24 ч.
Консервация реберного хряща возможна в формалине, замачивание — в натрия мер-
тиолате (антисептик на основе ртути). Применение трупного реберного хряща
примечательно уже тем, что хирург располагает практически неограниченным
количеством пластического опорного материала для коррекции спинки носа.
При обычном сплошном западении операция заключается в
формировании подкожного туннеля и введении в него смоделированного хрящевого
или силиконового имплантата. В отсутствие между медиальными ножками
четырехугольного хряща дополнительно вводят аллохрящевую "стропилку",
339
22*
после чего имплантат, введенный
в область спинки, становится
менее подвижным и имеет две точки
опоры — в кончике носа и в
переносье.
При небольшом западении в
хрящевом отделе носа, выстоящем
кончике и нормальной высоте
костного отдела целесообразно
выполнить частичную резекцию
латеральных ножек больших крыльных
хрящей, сшить иссеченные
фрагменты и восполнить ими
западающий участок спинки носа.
Сочетай ную деформацию в виде
костного горба и западения
хрящевого отдела можно
корригировать снятием горба, боковой
остеотомией и смещением горба,
обработанного до
соответствующих размеров, в область
западения (рис. 29.14).
Наибольшую трудность для коррекции представляют искривленные носы,
при которых деформация может локализоваться в костном, хрящевом отделах
или быть комбинированной. В отличие от других деформаций последние, как
правило, сопровождаются нарушениями функции дыхания, что существенно
Рис. 29.13. Операция понижения спинки
носа по способу Руденко (схема).
Рис. 29.14. Больной с западением спинки носа до (а) и после (б) операции.
340
Рис. 29.15. Больной с искривленным носом до (а) и после (б) операции.
влияет на характер планируемой операции. Искривления в костном отделе
характеризуются смещением костей носа в той или иной степени
относительно срединной линии. Они делятся на односторонний горб,
одностороннее вдавление и двустороннее искривление скатов, искривление корня носа.
Искривления в хрящевом отделе возникают из-за смещения
четырехугольного хряща относительно носовой ости верхней челюсти. При этом его
свободный край выступает в полость носа, "выталкивает" одну из медиальных
ножек больших крыльных хрящей, а кончик носа, лишенный опоры,
поворачивается в сторону.
Коррекция искривленного носа заключается в различных манипуляциях
в зависимости от клинической картины. Всегда необходимо проводить сеп-
топластику: выделение и перемещение в правильное положение хрящевой и
костной перегородок носа, иссечение участков хряща, препятствующих
дыханию. Наконец, одним из методов септопластики является выделение
хрящевой перегородки, ее выравнивание вне носа и установка исправленной
пластинки на прежнее место. В случае необходимости (необратимая
деформация) перегородка полностью удаляется (желательно без повреждения
слизистой оболочки), а на ее место помещают пластину из реберного аллохряща.
Коррекция костного отдела при искривленном носе заключается в
мобилизации одного или двух скатов (остеотомия). Во многих случаях
целесообразно выполнять срединную остеотомию, разделяющую по шву носовые
кости, и фрагментацию — проведение нескольких линий остеотомии по
местам наибольшего выбухания или западения (иногда до 5—7) (рис. 29.15).
341
а б в
Рис. 29.16. Варианты укорочения носа за счет резекции перегородочного хряща (а — в).
4 k
а б
4 4
в г
Рис. 29.17. Варианты частичной резекции крыльного хряща при укорочении кончика
носа (а — г).
Коррекция деформаций концевого отдела носа.
Деформации кончика носа характеризуются изменением положения и размеров
крыльных хрящей за счет их гипертрофии, нарушения положения
относительно костно-хрящевой спинки и относительно друг друга. Одним из
способов укорочения носа является иссечение дистального отдела
перегородочного хряща вместе со слизистой оболочкой. Величина этой полоски колеблется
в широких пределах и индивидуальна в каждом конкретном случае (рис. 29.16).
Этот прием должен использоваться нечасто, после чего кожная часть
перегородки носа может втягиваться, а кончик носа лишается опоры. Скорее
342
всего это оправдано только при
истинной гипертрофии
перегородочного хряща.
Чаще всего укорочение носа
осуществляется за счет иссечения
полосок больших крыльных
хрящей. Форма и размеры иссекаемого
участка зависят от конкретных
задач. В этих случаях проводят чрес-
хрящевой эндоназальный разрез и
остроконечными ножницами
отслаивают крыльные хрящи от кожи
и слизистой оболочки. Во всех
случаях после иссечения намеченного
участка хряща вдоль края ноздри
обязательно оставлять узкую
хрящевую полоску шириной 2—3 мм,
обеспечивающую сохранность
формы крыла и служащую рессорой для
кончика носа (рис. 29.17).
Укорочения носа можно
добиться путем выдвижения кпереди
колумеллы (изменение носогуб-
ного угла), что достигается введе- рис. 29.18. Операция уменьшения высоты
нием между медиальными ножка- носа (схема),
ми больших крыльных хрящей
или перед носовой остью верхней
челюсти имплантатов — "стропилок", фигурных вкладышей и т. д.
Как вариант укорочения носа можно рассматривать выделение
изогнутых нижних частей медиальных ножек больших крыльных хрящей, сшивание
их и установление впереди ости верхней челюсти, что позволяет не только
удлинить кожную часть перегородки носа, но и увеличить носогубныи угол с
75 до 95°.
С целью уменьшения высоты концевого отдела носа производят
передний и межхрящевой разрезы, соединяют их поперечным сечением
ниже соединения латеральных и медиальных отделов больших крыльных
хрящей. Слизисто-хрящевой лоскут отделяют от кожи и выводят наружу
в рану. На его поверхности делают насечки хряща, сохраняя слизистую
выстилку. Из медиальных ножек иссекают небольшие полоски хряща со
слизистой оболочкой. Применение такой техники позволяет
одномоментно проводить моделирование кончика носа и уменьшать его высоту
(рис. 29.18).
После коррекции спинки носа и кончика края раны сшивают кетгутом
в полости носа и полиамидной нитью при наружном доступе. Тампонаду
носовых ходов можно производить перед наложением гипсовой повязки на
область носа в случае фрагментации костей. В остальных случаях на спинку
носа сначала накладывают гипсовую или коллодийную повязку, а после этого
тампонируют носовые ходы.
Переднюю тампонаду обычно осуществляют не туго йодоформными
тампонами или тампонами с синтомициновой эмульсией для придания
нужного положения костным отломкам со стороны полости носа и
профилактики образования подкожной гематомы в области кончика носа. Тампоны
343
^i
удаляют на 3—4-е сутки после
ринопластики.
Гипсовую повязку изготав-
ливаютлз 6 слоев гипсового
бинта^ІСэтой процедуре следует
относиться не менее
ответственно, чем к самой операции,
поскольку успех ринопластики в
значительной мере зависит от
правильного наложения повязки.
Следует перекрыть гипсом все
линии остеотомии и тщательно
сформировать корень, спинку и
кончик носа. После
вмешательства на мягких тканях
гипсовую повязку можно снимать
на 6—7-е, а после операции на
костно-хрящевом отделе — на
10—12-е сутки.
После ринопластики
рекомендуются покой в течение
2—3 дней, прикладывание
пузырей со льдом,
физиотерапевтические процедуры. После удаления
тампонов возможно
закапывание в нос растворов
сосудосуживающих средств или
персикового, абрикосового и других
растительных масел. Для
облегчения отхождения корочек
полезно увлажнять воздух в
помещении, где находится пациент,
устанавливая бытовые
увлажнители или помещая под шкаф,
кровать банки с водой. Отечность
носа может сохраняться в
течение 6—8 мес и дольше.
Кровоподтеки вокруг носа обычно
наблюдаются в течение 2—4 нед и
проходят самостоятельно. Более
быстрому рассасыванию
кровоподтеков способствуют
отбеливающие маски с перекисью
водорода и бодягой, гепариновая
мазь и т. д. (рис. 29.19).
Осложнения.
Кровотечение сопровождается характерной клинической картиной: промоканием
повязки кровью, заглатыванием и сплевыванием крови, истечением ее в виде
струйки из-под повязки. При кровотечении из наружных разрезов проводят
плотную тампонаду полости носа и по скатам носа накладывают поверх
коллоидной повязки марлевые валики, фиксируя их пластырем. При
кровотечении из полости носа может оказаться необходимой передняя или задняя
тампонада. При показаниях проводят обычные мероприятия по ликвидации
4
Рис. 29.19. Больная с деформацией кончика
носа до (о) и после (б) операции.
344
t
Рис. 29.20. Взаимоотношение ушной раковины и головы (а, б).
кровотечения: строгий постельный режим, холод местно, переливание крови
и кровезаменителей, аминокапроновои кислоты, контроль за показателями
периферического кровообращения и др.
Подкожная гематома иногда обнаруживается только на 10—11-й
день после удаления повязки. Ограниченные гематомы представляют
собой флюктуирующие припухлости. Чаще всего они располагаются по
скатам носа, иногда — у корня. Рекомендуется скальпелем со стороны
слизистой оболочки сделать надрез, пройти зондом в полость и выдавить
содержимое. Следует промыть полость растворами антисептиков и
антибиотиков, ввести дренаж и вновь наложить повязку или марлевые валики
по скатам.
Нагноение возникает часто при нераспознанных гематомах и
характеризуется плотной инфильтрацией тканей, гиперемией кожных покровов,
повышением температуры тела, чувством распирания в области носа и
болями. Мероприятия аналогичны таковым при лечении. Однако
целесообразнее наложение контрапертуры, постоянное промывание и санация полости,
применение перорально и внутримышечно антибиотиков широкого спектра
действия.
Некроз кожи происходит от чрезмерного сдавливания мягких
тканей повязками. Профилактика заключается в раннем отодвигании краев
повязки. При некрозе повязку удаляют и проводят соответствующее лечение ра-
345
невой поверхности. Образующийся изредка кожный рубец на месте некроза
требует дальнейшей коррекции через год в виде дермабразии, иссечения и др.
29.9. Эстетическая отопластика
В эстетической хирургии лица чаще всего требуют коррекции торчащие
ушные раковины. Хирургическая коррекция более сложных дефектов и
деформаций, требующих многоэтапных операций восстановительного
характера, использования пластических опорных материалов биологического или
синтетического происхождения, представляет самостоятельный раздел
пластической хирургии и здесь не рассматривается.
При отборе пациентов для отопластики важно учитывать, что в возрасте
6—7 лет размеры ушной раковины соответствуют размерам уха взрослого
человека. При дооперационном анализе деформаций имеют значение не только
отклонения их размеров от средних величин, но и угловые соотношения
между различными частями ушной раковины и головы. Необходимо иметь в виду
следующие показатели: 1) длину — 65,5—65,9 мм у мужчин, 61,5—62,9 мм
у женщин; 2) ширину — 39,2 мм у мужчин, 36,2 мм у женщин; 3) ширину
углубления — 25,6 мм у мужчин, 24 мм у женщин; 4) ушно-головной угол,
образованный плоскостью ушной раковины и поверхностью головы C0°);
5) скафоконхальный угол (между плоскостью возвышения κοήχη и противо-
завитковой частью
раковины) — 90°; 6) расстояние от
поверхности сосцевидного
отростка до завитка — 2 см
(рис. 29.20).
Увеличенные уши.
Хирургическая
коррекция увеличенных ушных
раковин заключается в
сквозном иссечении
определенных участков ее. При
этом форма и
расположение иссекаемых полосок
находятся в прямой
зависимости от задач
коррекции. Так, при
уменьшении поперечного размера
ушных раковин возможны
серповидные иссечения
вдоль завитка, а при
уменьшении продольного
размера — клиновидные
иссечения. На практике
приходится применять
чаше комбинированные
рассечения, что
позволяет уменьшить оба
размера. Это связано с тем, что
в плотность тканей ракови-
Рис. 29.21. Варианты уменьшения ушной раковины ны затрудняет сведение
(а — г). краев раны при простом
346
рассечении без образования
наплывов ткани ("стоячие конусы")
(рис. 29.21).
Для сужения широкой
ладьевидной ямки производят
серповидные иссечения под завитком с
образованием малозаметного рубца.
Такие операции могут быть
изолированными или их выполняют
вместе с коррекцией торчащих ушей из
доступа на внутренней
поверхности ушных раковин.
Деформация завитка уха. При
часто встречающемся
остроконечном ухе ("ухо сатира") наиболее
простым методом исправления
деформации является клиновидное
иссечение вовлеченных в
деформацию тканей.
Клиновидным иссечением
устраняют также деформацию
нисходящего отдела завитка в виде угло-
образного уха ("ухо макаки").
Утолщение тканей на границе
горизонтальной и нисходящей
частей завитка (бугорок Дарвина)
удаляют клиновидным иссечением
только при выраженной деформации,
так как недоразвитый бугорок
относится к естественной
характеристике ушной раковины.
Уплощенный край завитка
развернут, край раковины
становится остроконечным. Обычно
отмечается и определенная сглаженность
ладьевидной ямки. Хирургическая
коррекция состоит в обнажении
хряща уха на его внутренней
поверхности и нанесении 3—4
параллельных краю завитка сквозных
рассечений по всей длине уха на расстоянии примерно 0,3—0,4 см от его
свободного края. На ближайшей к завитку полоске в одном-двух местах
производят клиновидные иссечения, а саму полоску хряща полностью отделяют от
подлежащей кожи. В местах иссечения хрящевой ткани накладывают
одиночные швы, что приводит к укорочению хряща завитка и выталкиванию его
кпереди. Созданная хрящевая конструкция должна быть иммобилизована
валиками, пропитанными вазелиновым маслом.
Деформация мочек. Из деформаций мочек наиболее часто встречаются их
увеличение и расщепление. При раздвоенной мочке производят освежение
краев дефекта с образованием "замка" и последующим наложением узловых
швов на подкожные ткани и кожу.
Уменьшение мочек ушных раковин осуществляют различными путями:
клиновидной резекцией или с помощью фигурных разрезов (рис. 29.22).
Рис. 29.22. Операции при деформациях
мочек ушей (а — е).
347
При чрезмерно
развитой нижней части
углубления уха часто наблюдается
отставание мочки, которое
корригируют иссечением
части углубления и проти-
возавитка или сшиванием
кожи мочки с кожей
сосцевидного отростка для
уменьшения щели между
мочкой и заушным
пространством.
Торчащие уши. При
коррекции торчащих
ушных раковин следует
добиваться естественной
формы и положения ушной
раковины с соблюдением
некоторых анатомических
и гармонических соотно-
Рис. 29.23. Коррекция торчащих ушей I и II степени. шений: 1) следует устра-
а — линии разрезов кожи и хряща; б — отслаивание кожи НИТЬ торчание ушной ра-
и моделирование хряща. ковины, особенно верхней
ее трети; 2) в плоскости уха
завиток всегда должен быть
ниже (позади) противозавитка; 3) необходимо сохранить достаточную глубину и
правильное положение заушной складки; 4) ухо не должно быть плотно
прижато к голове, особенно у мальчиков; 5) положение ушей должно быть
симметричным; разница в измерениях в одинаковых точках не должна превышать
3 мм; 6) мочка уха не должна выходить за проекцию края завитка; 7) верхняя
часть завитка должна быть на 5 мм ближе к голове, чем средняя часть уха.
При систематизации деформации наиболее рациональна следующая
классификация торчащих ушей, что важно учитывать при выборе техники
исправления: I степень — увеличение высоты углубления; II степень —
недоразвитие верхней ножки и тела противозавитка; III степень — сочетание
двух указанных деформаций.
Оперативный доступ осуществляют рассечением кожи по внутренней
(задней) поверхности ушной раковины, отступя от края завитка около 1,5 см.
Разрез начинают в области верхнего полюса и продолжают книзу в проекции
противозавитка до начала мочки. Отслойку кожи производят на расстоянии
1 — 1,5 см в обе стороны от кожного разреза. Затем осуществляются
тщательный гемостаз электрокоагуляцией и этапы отопластики в зависимости от
вида и степени деформации.
При I степени торчащих ушей двумя или тремя иглами отмечают границу
углубления с телом противозавитка, рассекают хрящ в области верхней границы
углубления и проводят отслойку кожи хряща углубления на передней
поверхности для лучшего ее перераспределения. Далее иссекают серповидный участок
хряща шириной, соответствующей размеру избыточной высоты углубления.
При II степени для ориентации вводят три иглы: первая располагается
на нижней границе верхней ножки противозавитка, вторая — в месте
соединения верхней и нижней ножек противозавитка, третья — на границе между про-
тивозавитком и углублением ушной раковины. Через эти три точки проходит
линия нижнего сквозного разреза хряща. Второй сквозной разрез проводят
348
Рис. 29.24. Больная с торчащими ушами до (а) и после (б) операции.
вдоль завитка, отступя 0,5 см. Края хряща отслаивают от кожи передней
поверхности ушной раковины на небольшом протяжении и сшивают
непрерывным матрацным швом полиамидной нитью с образованием желоба. При
необходимости сформированные противозавиток и его верхнюю ножку
подшивают к хрящу углубления. На кожные края раны накладывают
непрерывный кетгутовый шов (рис. 29.23).
В послеоперационном периоде для сохранения формы уха и
предупреждения гематом накладывают формирующие валики, которые изготавливают
во время операции из стерильной марлевой салфетки, пропитанной
масляным раствором. Валики укладывают в области углубления, ладьевидную и
треугольную ямки. Местно применяют пузыри со льдом. Медикаментозная
терапия заключается в назначении анальгетиков, антигистаминных и
кровоостанавливающих средств. Асептическую повязку накладывают в течение
7 дней, сменяя через 2—3 дня. Затем в течение 1—2 мес желательно
фиксировать уши на ночь повязкой или платком (рис. 29.24).
Осложнения. При эстетической отопластике наиболее часто
встречаются следующие осложнения.
349
Подкожная гематома характеризуется выраженными давящими
или пульсирующими болями, отеком, синюшностью и напряженностью
тканей, выделением крови или сгустков по линии шва. Лечение заключается в
ревизии раны, удалении сгустков, окончательной остановке кровотечения.
Рекомендуются также давящая повязка, холод местно,
кровоостанавливающие и противовоспалительные средства для предупреждения перихондрита.
Эпидермальные пузыри не рекомендуется вскрывать, так как
они самостоятельно исчезают по мере рассасывания экссудата. Для
улучшения кровообращения в коже необходимо удалять валики.
Гипертрофические и келоидные рубцы часто встречаются
при избыточном иссечении кожи заушной области. Лечение их всегда носит
комплексный характер: местно применяют кортикостероидные препараты и
неспецифические средства, проводят физиотерапию, инъекции пирогенала,
букки-терапию и др.
Лигатурные свищи диагностируют при длительном выделении се-
розно-гнойного отделяемого из одной или нескольких точек по линии рубца
вследствие фитильности шовного материала или пролежней в местах тесного
соприкосновения узла нити с тонкой кожей ушной раковины. Лечение
состоит в удалении шовного материала из тканей и борьбе с местным
воспалительным процессом.
29.10. Иссечение избытков кожи лица и шеи
Патофизиологические процессы, захватывающие все слои тканей лица и
действие внешних сил тяжести, приводят к характерной картине стареющего
лица в виде наличия складок кожи (избыток), патологической смещаемости
ее при незначительно выраженной инфильтрации подкожной жировой
клетчатки. Расправление кожи с иссечением ее избытка приводит к устранению
мелких морщин только в иссекаемой коже, а в остальных отделах они лишь
немного расправляются. В связи с этим при старческих изменениях в виде
избытка кожи и многочисленных морщин необходимо сочетание нескольких
видов операций, включая дермабразию.
Учитывая большую площадь отслойки кожи, болевой раздражитель,
связанный с инфильтрацией 0,25 % раствором новокаина или тримекаина,
устраняют дополнительным внутривенным введением калипсола с седуксеном
или реланиумом.
Разрез кожи при ее избытке начинают на виске, отступя 2,5—3 см кзади
от границы волос, затем проводят его книзу и параллельно восходящей
ножке завитка ушной раковины, отступя кпереди 0,3—0,5 см от ее края. По дуге,
открытой кпереди, плавно огибают козелок, сохраняя его форму. После этого
разрез продолжают по основанию мочки ушной раковины, сгибая ее по
заушной борозде до уровня слияния верхней и нижней ножек противозавитка
уха и далее под углом 90° или чуть больше — в затылочной области. Кожу
ножницами Купера отслаивают в подкожном жировом слое, избегая травмы
глубжележащих тканей и истончения кожи.
Площадь отслоения зависит от выраженности избытка кожи, в среднем
же ее граница проходит на висках от верхней (височной) точки кожного
разреза до наружного угла глаза, затем до носогубной складки, от нее вниз до
половины переднебоковой поверхности шеи и далее до пограничной точки
разреза в затылочной области.
После мобилизации кожи производят тщательный гемостаз диатермо-
коагуляцией сосудов. Отслоенный кожный лоскут подтягивают равномер-
350
Рис. 29.25. Операция иссечения избытка кожи лица и шеи (схема).
а — границы отслойки кожи; б — наложение укрепляющих швов на клетчатку; в — натяжение
кожи и иссечение избытка ее: 1, 2, 3 — точки фиксирующих швов.
но кверху и кзади. Векторы тяги целесообразно распределять по трем
направлениям с одновременной фиксацией мобилизованного лоскута провизорными
швами в трех точках: 1) над верхним полюсом ушной раковины; 2) над
сосцевидным отростком в области перехода разреза с заушной области на шею;
3) отступя 2—2,5 см от предыдущей точки к затылку. В третьей точке кожу
следует подтягивать сильнее, чем в предыдущей, что позволяет более
равномерно распределить избыток кожи и способствует сохранению
достаточного кровотока в более тонкой коже заушной области во избежание
развития ее некроза.
Затем иссекают избыток кожи в височных и затылочной областях. После
освобождения мочки ее вшивают тесно в разрез и иссекают избыток кожи
впереди и позади ушной раковины. Края раны соединяют непрерывным
внутрикожным швом. На висках и шее между стежками вводят резиновые
выпускники (рис. 29.25).
С целью достижения наибольшей косметичности послеоперационного
рубца разрез кожи в пределах козелка ведут по его ребру или несколько кнутри.
Это может способствовать деформации козелка в дальнейшем, поэтому
избытки кожи данной области иссекают неполностью, с напуском и даже
иногда истончают смещающуюся сюда кожу щек, что рискованно.
351
В настоящее время описанная выше стандартная методика дополнена
рядом оперативных приемов, направленных на повышение эффекта операции.
1. Укрепление подкожных мягких тканей осуществляют собиранием
подкожной жировой клетчатки в складки. Первый ряд швов из не-
рассасывающей нити накладывают под скуловой дугой, второй — на
клетчатку щек от скулового возвышения по направлению к передней
поверхности уха. Изменяя направление швов, можно влиять на
форму овала лица. Собирание клетчатки целесообразно по следующим
соображениям: уменьшается область отслойки (а следовательно,
полость для накопления жидкости и крови), укорачиваются кожные
лоскуты, кожу можно уложить без натяжения, особенно перед ухом,
где нежелателен неэстетичный послеоперационный рубец.
2. Выделение и натяжение поверхностной мышечно-апоневротической
системы (SMAS), т. е. перемещение структуры, простирающейся от
височной области до шеи и являющейся растяжкой для мышц лица,
от лобной в верхнем отделе до подкожной на шее. После
стандартного разреза кожу отслаивают на 3—4 см кпереди. В области виска,
где между SMAS и височной фасцией имеется пространство,
отслойку осуществляют пальцем до места слипания этих двух фасциальных
образований (на 1—2 см выше скуловой дуги). Отступя 1—2 см вниз
от скуловой дуги, в 1—2 см от козелка рассекают фиброзный листок
примерно до угла нижней челюсти, но не доходя до него 1 см. Край
листка поднимают на зажимах и выделяют SMAS над околоушной
железой до ее переднего края. Для профилактики повреждений
нервных стволиков предпочтительнее тугая отслойка под контролем глаза
с дополнительным освещением раны. Над кивательной мышцей и в
области сосцевидного отростка на шее вследствие очень тесного
спаяния фасций со SMAS возможно только острое рассечение
тканей. Его производят под подкожной мышцей шеи на расстоянии 2 см
книзу от угла нижней челюсти до средней линии шеи. Выделение
SMAS вместе с подкожной мышцей облегчает смещение кзади тканей
щеки и шеи и натяжение спаянной с ними кожи практически без
выделения последней над подкожной жировой клетчаткой.
Возникающий при этом избыток SMAS может быть иссечен или ушит (с
подгибанием внутрь) впереди и позади уха.
3. Коррекция подбородочной области характеризуется выполнением
различных мышечных пластик: рассечения платизмы на небольшом
протяжении и Z-пластики в ее средней части, поперечного
рассечения краев подкожной мышцы шеи и натяжения двух образованных
лоскутов в направлении уха, простого иссечения передних краев
платизмы ножницами, наложения краев расслабленной подкожной
мышцы друг на друга внахлест.
4. Липосакцию избыточного жира подбородка производят при
соответствующих показаниях в подчелюстных и подбородочной областях с
помощью вакуум-системы. Лучше всего осуществлять это из
небольших кожных разрезов под ушными мочками и в подбородочной
борозде до начала общей отслойки кожи. Возможна обработка
подкожной жировой клетчатки вакуумным способом и в области носогубных
складок из доступов через нижнее веко и крыло носа. Условием
выполнения липосакции является туннелирование жировой ткани по
возможности в разных направлениях. В подбородочной области
жировые отложения следует удалять, оставляя небольшую прослойку
352
под кожей для более легкого смещения ее по отношению к мышцам
и предупреждения спаяния с ними, что нежелательно из-за видимых
перемещений и втяжений при глотании.
5. Коррекция носогубных складок — достижение эстетической
хирургии лица последних лет. Подход к решению этой проблемы
неоднозначен. Во-первых, необходима значительно большая отслойка кожи
лица по сравнению со стандартной. Во-вторых, расслабленная
жировая ткань может быть собрана (подтянута) в складку под прямым
углом к самой носогубной складке. В-третьих, толщина складки может
быть уменьшена с помощью липосакции. Наконец, необходимо
устранять носогубную борозду в основании носогубной складки. В
настоящее время этот вопрос можно удовлетворительно решать
введением в данную область биологических или синтетических материалов
(коллаген, гиалуроновая кислота, нити, гель и др.).
После операции иссечения избытка кожи лица и шеи в течение 1-х суток
рекомендуют локальную гипотермию и соблюдение постельного режима.
Положение головы возвышенное. На область щек и лба можно накладывать
пузыри со льдом попеременно на 20—25 мин с небольшими перерывами.
Назначают щадящую диету во избежание активных жевательных движений,
приводящих к появлению болей. С целью снижения интенсивности болевой
реакции рекомендуется вводить внутримышечно растворы анальгина, трамала,
баралгина с димедролом или реланиумом. Первую перевязку производят
обычно через сутки после операции: вновь накладывают умеренно давящую
повязку, которую уже можно держать дольше, а на 4—5-е сутки снять.
Отечность лица нарастает в течение 3—5 сут, а в последующие 2 нед постепенно
уменьшается. Кровоизлияния в кожу не требуют специального лечения и
полностью рассасываются самостоятельно через 2—2,5 нед. С целью
сокращения этого периода можно применять местно троксевазиновую или
гепариновую мазь, маски с бодягой (к смеси растительного масла и 3 % перекиси
водорода в равных пропорциях добавляют порошок бодяги до получения
сметанообразной массы, которую наносят на область кровоподтеков на 30—
40 мин). Восстановление чувствительности кожи в зоне отслойки происходит
медленно C—5 мес). Швы снимают на 10—12-е сутки (рис. 29.26).
Осложнения. Наиболее часто осложнением операций иссечения избытка
кожи лица и шеи является подкожная гематома. Ее можно обнаружить уже
на следующий день при появлении с одной или двух сторон "заплывших век".
После снятия повязки определяется флюктуирующая припухлость тканей без
четких границ. При нарастающей гематоме, как правило, в течение 1-х суток
необходима ревизия раны. Для этого в операционной снимают швы, разводят
края раны, осматривают ее и производят окончательную остановку
кровотечения, после чего вновь накладывают косметические швы и повязку. В
противном случае возможны перерастяжение кожи и трофические расстройства.
Лечение не требуется только при гематоме небольших размеров, если
отсутствует тенденция к ее нарастанию, а кожа над нею по цвету мало отличается
от окружающей. Ее опорожнение можно проводить на 8—10-е сутки через
отдельный разрез над местом флюктуации или туннель в линии шва в
зависимости от локализации.
Парезы лицевой мускулатуры возникают главным образом
вследствие глубокой инфильтрации анестезирующим раствором в височной
области и около угла рта, в результате сепарации тканей в подмышечной
области и электрокоагуляции, грубых захватов тканей инструментами,
наложения глубоких и грубых лигатур. Легкие парезы проходят самостоятельно, но ес-
353
23-1263
Рис. 29.26. Больная с избытком кожи лица и шеи до (а) и после (б) операции.
ли они не исчезают через 2—3 нед, то можно предполагать повреждение
нервных веточек. В течение 2—4 мес желательно проводить антипаретическую
противорубцовую терапию с привлечением невропатолога для консультации.
Расхождение краев раны всегда является следствием нарушения
трофики тканей по линии шва в результате сдавления нитями шовного
материала и других причин, связанных с техникой оперативного вмешательства.
Лечение заключается в очищении раневой поверхности и по возможности
наложении вторичного отсроченного шва.
Поредение и выпадение волос может происходить в области
висков и даже на темени вследствие нарушения трофики, происходящего при
отслойке и натяжении кожи. Как правило, выпадение волос
приостанавливается после соответствующего лечения у косметолога.
Рубцовые осложнения в виде гипертрофии и келоидов обычно
являются следствием общих и местных факторов, влияющих на процесс
заживления раны. Наиболее нежелательны гипертрофические и келоидные
рубцы вокруг уха. Создается впечатление, что их возникновение часто
связано с повышенным натяжением кожи, сшиванием различных по толщине
краев. Лечение заключается в проведении комплекса физио-, лазеро- и бук-
ки-терапии и др.
СПИСОК ЛИТЕРАТУРЫ
Виссарионов В. А. Некоторые аспекты косметической хирургии лица. — Екатеринбург,
1992.
Михельсон Н. М. Восстановительные операции челюстно-лицевой области. — М:
Медгиз, 1962.
Кручинский Г. В. Пластика ушной раковины. — М.: Медгиз, 1975.
Фришберг И. А. Косметические операции на лице. — М.: Медицина, 1984.
Фришберг И. А. Эстетические операции в области лица//Восстановительная хирургия
мягких тканей челюстно-лицевой области/Π од ред. А. И. Неробеева, Н. А.
Плотникова. — М.: Медицина, 1997. — С. 272—284.
Baker D. С. Lateral SMAS ectomy//Plast. Reconstr. Surg. - 1997. - Vol. 100, N 2. -
P. 509-513.
Hamra S. T. Composite rhytidectomy//Aesthetic Plastic Surgery. — Vol. 2 / Ed. T. D. Rees. —
1994. - P. 722-731.
Pina D. P. Aesthetic and safety considerations in composite rhytidectomy: a review of 145
patients over a 3-year period//PIast. Reconstr. Surg. — 1997. — Vol. 99, N 3. —
P. 670-678.
Teimourian В., Delia S., Wahrman A. The multiplane face lift//Plast. Reconstr. Surg. — 1994. —
Vol. 93, N 1. - P. 78-85.
23 *
Глава 30
ОСНОВЫ ЭНДОПРОТЕЗИРОВАНИЯ
И ЭКТОПРОТЕЗИРОВАНИЯ
ЛИЦА
ЗОЛ. Эндопротезирование лица
Эндопротезирование заключается в замещении имплантатами (эндопротезами)
элементов опорно-двигательного аппарата или частей органов, утративших
свою функцию в результате травмы или заболевания. В хирургии под им-
плантатом следует понимать предмет, изготовленный из небиологического
материала, который вводят в организм для выполнения каких-либо функций
в течение длительного времени. Главным требованием к имплантатам
является их биосовместимость, которая зависит в первую очередь от химических
свойств имплантируемого материала.
Историческая справка. Развитие восстановительной хирургии лица
непосредственно связано с поиском материалов для имплантации, которые
могли бы служить заменителями биотканей: костной, хрящевой, мышечной,
жировой и покровной (кожи). Имеются сведения об использовании в
древности различных материалов (пластинки из золота и серебра, слоновой кости,
янтаря и даже скорлупы кокосового ореха) для замещения дефектов черепа и
носа. В тот период инфицирование раны было скорее правилом, чем
исключением. Только с появлением антисептиков стало возможным
имплантировать в организм чужеродные материалы. С развитием химии полимеров
появились новые материалы, которые более подходили для использования в
качестве эндопротезов.
Разработанные в 40-х годах материалы на основе полиметилметакрилатов
(АКР-7, АКР-9, АКР-10, ЭГМАСС-12) сыграли важную роль в развитии
стоматологии. В челюстно-лицевой хирургии они нашли применение в качестве
интерпозиционного материала при операциях по поводу анкилоза височно-
нижнечелюстного сустава. С этой целью изготавливали колпачки из
пластмассы АКР-9, которые фиксировали на конце подвижного фрагмента
нижней челюсти. Эндопротезы из акриловой пластмассы широко использовали
для устранения деформации нижней челюсти, носа, закрытия дефектов свода
черепа. Однако при восстановлении контуров лица, особенно при
устранении обширных деформаций, требовался эластичный материал. Твердая
акриловая пластмасса не могла удовлетворить хирургов из-за трудностей
подгонки вкладышей к ложу во время операции, выступания краев имплантата
под кожей и возможной перфорации кожи при незначительном смещении
имплантата или несоответствия его формы, а также из-за раздражающего
действия выделяющегося из протеза мономера. Применявшиеся в тот период
356
модели имплантатов были несовершенной конструкции. Не были
разработаны методы оперативных вмешательств, что отражалось на результатах.
Важным этапом в восстановительной хирургии лица явились работы
Е. В. Груздковой A941 — 1969), посвященные применению
скульптурно-моделированных имплантатов из эластичной пластмассы ЭГМАСС-12. Такие
имплантаты сохраняли приданную им форму, но со временем теряли
пластификатор и отвердевали.
Необходимость устранения дефектов не только лицевого скелета, но и
мягких тканей лица требовала создания мягких и эластичных биосовместимых
материалов. В 50-х годах наряду с акрилатными полимерами в челюстно-ли-
цевой хирургии стали применять имплантаты из полиэтилена,
политетрафторэтилена (фторопласт-4), полисилоксанов. Наибольшее применение челю-
стно-лицевой хирургии получили операции с использованием силоксановых
имплантатов, так как они обладали высокой биосовместимостью и
биостабильностью, технология их изготовления была достаточно простой и
позволяла получать материалы с широким диапазоном твердости и эластичности.
В нашей стране экспериментально-клиническое исследование
возможности применения силоксановых материалов1 в восстановительной хирургии
лица было начато в 1964 г. под руководством Е. В. Груздковой. Результаты
дальнейших исследований показали, что силоксановые имплантаты
биологически инертны, сохраняют эластичность, прочность, не рассасываются в
тканях, не изменяют форму и процесс приживления можно рассматривать
как нормальную реакцию заживления стерильной раны. Хорошие результаты
при первом их применении сделали актуальной проблему
усовершенствования имевшихся имплантатов и разработку новых, более отвечающих
требованиям, предъявляемым к заменителям мягких тканей.
В результате экспериментально-клинических исследований для
исправления дефектов и деформаций костей лицевого скелета рекомендованы
монолитные резины марок CK 52-336/4 и CK 52-1194; для коррекции деформаций
мягких тканей — силоксановые резины марок ЦТ-9в, ЦТ-9г и гели из само-
отверждающихся в организме инъекционных силоксановых композиций эла-
стосил МИ и КС И.
В зависимости от локализации дефекта усовершенствованы методы
скульптурного моделирования индивидуальных имплантатов. Применение
силоксановых композиций позволило разработать новые методы
реконструктивных операций для улучшения результатов лечения больных с
дефектами и деформациями лица.
Наряду с силоксановыми композициями в восстановительной хирургии
лица все более широко использовали эндопротезы из нержавеющей стали,
титана, циркония, керамики и др.
В 70—80-х годах стали применять материалы, позволяющие не только
проводить контурную пластику, но и выполнять фиксирующую функцию
при костно-реконструктивных операциях. Внедрение в клинику тонких
перфорированных пластин из высоколегированного титана открыло новые
возможности в эндопротезировании костей мозгового и лицевого отделов черепа.
С появлением этого имплантационного материала были усовершенствованы
способы хирургического лечения и предложены новые эффективные методы
опорно-контурной пластики.
Силоксаны — химические соединения, содержащие силоксановую (==Si—О—) связь.
Силиконы — название силоксановых полимеров, содержащих атомы кремния,
принятое в США.
357
Начиная с 80-х годов, появлялись сообщения об использовании в кост-
но-реконструктивной хирургии пористой керамики, которая хорошо
переносится тканями организма и при определенной величине пор обеспечивает
врастание в них остеогенных структур, образуя прочное сращение с костью.
Однако слишком высокая твердость материала и сложность его обработки в
сочетании с низкой механической прочностью, склонностью к образованию
трещин ограничивают его применение.
В настоящее время внимание хирургов привлекают композитные угле-
родсодержащие материалы, которые также обладают высокой
биосовместимостью и даже способны ускорять заживление ран.
В качестве материала для эндопротезирования в челюстно-лицевой
хирургии начато применение углепластика «Остек» для восстановления тела и
ветви нижней челюсти, с формированием суставной головки из углеродной
керамики. Композитный материал на основе графита несомненно
представляет интерес, хотя сроки клинических наблюдений невелики и стабильность
таких имплантатов в живом организме мало изучена.
В последние годы эстетическую коррекцию небольших дефектов мягких
тканей лица проводят путем инъекции коллагена и полиакриламидного геля.
Хорошие результаты таких операций отмечены только на непродолжительных
сроках после операции.
Из всех рассмотренных материалов для эндопротезирования силоксано-
вые композиции не теряют значения со временем, позволяя устранять
деформацию как костных, так и мягких тканей лица. Простота технологии
изготовления эндопротезов из силоксана в отличие от других материалов дает
возможность делать имплантаты индивидуально для каждого больного. Для
их успешного применения разработана методика моделирования
индивидуальных имплантатов.
30.1.1. Моделирование эндопротезов
Цель моделирования — максимальное восполнение дефекта и точное
соответствие имплантата лицу больного. Плотное прилегание протеза к кости
способствует хорошей фиксации его в тканях и сокращению сроков вживления.
Кроме того, правильно определить расположение его на костной поверхности
в зоне дефекта во время операции помогает точно смоделированная
внутренняя поверхность имплантата. Если учтен рельеф деформированной кости и
бугорки, впадины точно соответствуют контрформам на имплантате, то это
способствует дополнительной фиксации последнего и уменьшению
количества фиксирующих швов, что сокращает время операции.
Индивидуальный имплантат изготавливают только после клинико-ла-
бораторного и рентгенологического обследования больного, изучения
деформации лица с учетом фотографий и гипсовой маски лица, которую
снимают в полусидячем положении больного в кресле. На гипсовой маске хирург
вместе со скульптором намечают границы деформации, затем скульптор
делает модель имплантата из зубоврачебного воска. Восковую модель
примеряют на больном, корригируя размеры и форму с учетом сохранения
функции мимической мускулатуры лица, а также сосудисто-нервных пучков и
слезоотводящих путей.
В зависимости от этиологии и локализации деформации применяют
различные способы моделирования имплантата.
У больных с гемиатрофией и липодистрофией лица при устранении
деформации лобных областей, если мягкие ткани истончены и рельеф дефор-
358
мированной кости не искажен покрывающими тканями, моделирование им-
плантата проводят по гипсовой маске.
При устранении деформации лобно-носоглазничной и скулоглазничной
областей, если мягкие ткани, покрывающие края глазницы, тонкие и
равномерной толщины, костные края глазницы хорошо пальпируются,
имплантаты моделируют по лицу больного.
При недоразвитии и деформации верхней и нижней челюстей, если слой
мягких тканей над дефектом неравномерный, моделирование имплантата
проводят по гипсовым моделям челюстей с хорошим оттиском
десневой поверхности и переходной складки, используя рентгенограммы
лицевого черепа в прямой и боковой проекциях с контурами мягких тканей, а
также зонограмму и ортопантомограмму.
Имплантаты для закрытия сквозного дефекта черепа
моделируют с учетом точного определения контура дефекта кости, используя
данные пальпаторного, рентгенологического обследования, так, чтобы имплантат
не оказывал давления на подлежащие ткани мозга. Для создания опоры и
фиксации имплантата наружные размеры его должны быть на 1,5—2 см
больше размеров закрываемого дефекта, а угол перехода лобного имплантата в
носовой отросток и верхний свод глазниц должны быть точно рассчитаны.
Для устранения наиболее типичных деформаций лица существуют
стандартные имплантаты из силиконовой резины. Такие имплантаты производят
фирмы "Koken" (Япония), "McGhan" (США), COX-UP-HOFT
(международная) и др. В России выпускается набор стандартных имплантатов для
устранения деформаций лица, отмеченный дипломом и золотой медалью на 44-м
Всемирном салоне изобретений "Брюссель — Эврика-95". Набор включает
лобно-носовой имплантат, имплантаты для коррекции подглазнично-скуло-
вой области (левый и правый), имплантаты для коррекции спинки носа D
размера), имплантаты для коррекции симметричного недоразвития нижней
члюсти C размера), имплантаты для коррекции одностороннего
недоразвития нижней челюсти (левый и правый), имплантаты для коррекции угла
нижней челюсти (левый и правый), блок для моделирования резанием
индивидуальных имплантатов (рис. 30.1).
30. L2. Клиническое применение имплантатов
По характеру дефектов и деформаций лица различают следующие
заболевания, при которых целесообразно применение имплантатов: врожденные и
посттравматические деформации, деформации лица после воспалительных
процессов и удаления опухолей, дефекты мягких тканей при липодистрофии
и гемиатрофии лица.
Основным показанием к применению силоксановых материалов в
восстановительной хирургии лица является невозможность устранения
деформации и достижения хорошего эстетического результата при использовании
костных, хрящевых, фасциальных и жировых трансплантатов, так как
недостаточные размеры биотрансплантатов, трудности моделирования во время
операции, последующие процессы резорбции, а также рубцовые деформации
кожи и подкожной жировой клетчатки над трансплантатом не позволяют
устранить дефект в полном объеме.
Преимущество силоксановых материалов обусловлено комплексом их
положительных свойств: биосовместимостью, возможностью коррекции не
только костных дефектов, но и мягких тканей лица, высокой стабильностью
формы и объема в условиях in vivo. Применение силоксановых материалов
359
Рис. ЗОЛ. Набор силоксановых имплантатов стандартных размеров для устранения
деформаций лица.
при контурной пластике лица является завершающей операцией. До
введения имплантата необходимо выполнить подготовительные костно-реконст-
руктивные и кожно-пластические операции с целью создания оптимальных
условий для приживления имплантатов.
Травмы. В результате транспортных катастроф, в быту, на производстве
возможны травмы, огнестрельные ранения и ожоги, которые чаще всего
приводят к повреждению нескольких областей лица. Развивающиеся в
травмированных тканях процессы рубцевания, а также сокращение разорванных
мышц и смещение раздробленных костей лицевого скелета вызывают грубые
деформации.
Наиболее сложный и тяжелый контингент составляют больные с
травмами свода черепа, л обно-носоглазнич ной области, так как у
них анамнез обычно отягощен ушибом, сотрясением мозга, переломом
основания черепа. Западение лобной кости, как правило, сочетается с
повреждением лобных пазух, дефектом костной ткани, деформацией
верхневнутренних краев орбит, уплощением корня носа. На коже лба обычно имеются
разнонаправленные рубцы. При сквозном дефекте лобной кости отмечается
пульсация мозга. Деформация верхневнутреннего края глазницы
сопровождается птозом верхнего века и смещением внутреннего угла глазной щели.
Смещение костных осколков в полость глазницы приводит к ограничению
верхнего поля зрения; иногда наблюдается частичная потеря зрения. У
больных с повреждением лобно-носовой области нередко отсутствует обоняние.,
На обзорных рентгенограммах, как правило, выявляется дефект костной
ткани лобной кости, верхнего края глазницы, нередко с множественными
отломками неправильной формы, сопровождающийся разрушением верхней
стенки носовой полости и верхнего края орбиты.
360
Методика операции. Перед имплантацией на коже раствором
бриллиантового зеленого намечают контуры имплантата и ориентиры.
Операцию проводят под эндотрахеальным наркозом. По типу инфильтрацион-
ной анестезии осуществляют гидропрепарирование 0,25 % раствором
новокаина или физиологическим раствором для облегчения рассепаровывания
рубцово-измененных тканей. Разрез кожи проводят по имеющимся рубцам,
по возможности с их иссечением. Края раны мобилизуют. Сохранившуюся
надкостницу рассекают по краю сквозного дефекта и распатором отслаивают
ее вместе с мягкими тканями по периферии от дефекта, ориентируясь на
контуры имплантата, намеченные на коже. Распатором скелетируют края дефекта,
сохраняя рубцово-измененные ткани над дефектом. В подготовленное ложе
вводят имплантат, тщательно следя за совпадением внутреннего контура
имплантата с краями дефекта. Имплантат закрывают отслоенной надкостницей
и фиксируют лавсановыми швами. Рану послойно ушивают (рис. 30.2, 30.3).
При деформации скул о глазничной области основными
клиническими симптомами являются: резкое уплощение скулоорбитальной области,
ано- или экзофтальм, опущение глазного яблока, диплопия. В результате
перелома медиальной стенки глазницы внутренний угол глаза округляется и
несколько выбухает, наружный угол глаза смещается вниз. На рентгенограммах
скуловая кость смещена внутрь и книзу, внедряясь в верхнечелюстную пазуху.
Отмечается разрушение скуловой кости по типу многооскольчатого перелома.
Восстановление рельефа скулоглазничной области, создание
нижнеглазничного края и нижней стенки глазницы проводят
индивидуальными моделированными силиконовыми имплантатами. Основной
особенностью восстановительных операций в скуло-глазничной области является
не только формирование рельефа области, но и создание дна глазницы
отдельным имплантатом (рис. 30.4, 30.5).
«Повреждения носа занимают второе место среди травм лица. Они
возникают вследствие ударов, укусов человека и животных, отрыва или
отсечения какой-либо части носа. Перелом костей носа приводит к его
уплощению, концевой отдел носа расширяется, приподнимается вверх вследствие
гематомы и искривления носовой перегородки и последующей рубцовой
деформации латеральных ножек крыльных хрящей — образуется
седловидная деформация носа. Нередко деформация усугубляется рубцами на коже,
которые приводят к укорочению крыльев носа и его асимметрии. При
седловидной деформации носа, если кожные покровы не изменены, для
восстановления формы носа достаточно ввести в область спинки носа скульптурно-
моделированный имплантат из силикона. Его вводят через эндоназальный
разрез или разрез на кончике носа по Рауэру.
Нередко травмы приводят к тотальным и субтотальным дефектам носа.
В таких случаях выполняют ряд подготовительных операций с целью
восстановления кожных покровов носа, создания его крыльев и перегородки.
При оперативных вмешательствах широко используют принципы
ринопластики по Хитрову.
Скрытые дефекты слизистой оболочки носа вызывают его укорочение.
Размер восстанавливается пластикой двумя горизонтально расположенными
лоскутами со щек с последующим созданием опоры для мягких тканей си-
локсановыми имплантатами. В зависимости от дефекта применяют метод
пластики носа лоскутом со лба по Конверсу. На боковой поверхности лба
выкраивают лоскут кожи, необходимый для формирования носа. Кожу в
области лба отслаивают от апоневроза так, чтобы не повредить мышцы и сосуды.
Лоскут перемещают в область носа и формируют из него перегородку, крылья
и кончик носа. При обширных дефектах прилежащих тканей предварительно
361
шяШ
\'а}\
-^мфч ^^fct «Я
4^ а
яи^ 11
^*\, 1|
\4
а
і:;і
ш
>і
ШШІ
Рис. 30.3. Больной с дефектом
лобной кости.
/ — до операции: a — в фас; б — в
профиль; β — рентгенограмма скуло-
глазничной области.
Рис. 30.2. Пластика сквозного дефекта теменно-височной области силоксановым им-
плантатом (схема). Художник этой и последующих схем И.П.Орловский.
о — линия разреза в височной области; б, в, г — создание ложа для имплантата; д, е, ж — фиксация
имплантата.
восстанавливают основание носа и верхнюю губу. Контурную пластику
выполняют с помощью каркасного имплантата из силоксана. Завершение ри-
нопластических операций введением индивидуально моделированных
фигурных и каркасных силоксановых имплантатов позволяет не только
восстановить форму носа, но и нормализовать функцию дыхания, так как
имплантат предотвращает втягивание крыльев носа при вдохе.
Деформации лица врожденной этиологии — это стойкие
морфологические изменения органа (органов), выходящие за пределы вариации их
строения, возникающие внутриутробно или после рождения ребенка.
364
Ч££££р0
Ж
Рис. 30.4. Пластика скулоглазничной области имплантатом из силоксана (схема).
а — дефект; б, <?, г — формирование ложа для имплантата; д — дефект после отслоения мягких
тканей; е, ж — имплантат и его фиксация.
Рис. 30.5. Больная с деформацией скулоглазнично-щечной области после травмы
/ — до операции: а — в фас, б — в профиль; //— после реконструктивных операций: β — в фас,
г — в профиль.
К трудно поддающимся хирургической коррекции деформациям
относятся такие пороки развития лица, как синдром Тричера—Коллинза, геми-
фациальная микросомия (отокраниостеноз), расщелины верхней губы и неба,
группа краниостенозов, в которую входят редко встречающиеся синдром
Крузона, Аперта, орбитальный гипертелоризм, брахи- и плагицефалия.
Синдром Трич ера—Ко л л и нза впервые описан Веіту A882), а
затем — Treacher и Collins A900). Изучая клинические проявления синдрома,
A. Francescetti, D. Klein A949) отметили, что недоразвитие мягких и костных
тканей средней зоны лица сочетается с деформацией нижней челюсти и
ушной раковины, в связи с чем они расценивали этот синдром как челюстно-
лицевой дизостоз. Он относится к редким врожденным заболеваниям.
При данной патологии клиническая картина характерна: в области
скуловых костей, наружно-нижних отделов глазниц отмечается резкое западе-
ние вследствие их недоразвития, глазные щели расположены в косом
направлении, наружные углы их опущены (антимонголоидный разрез глаз).
Нижние веки недоразвиты, ближе к наружному углу имеются колобомы,
ресницы частично или полностью отсутствуют. Отмечаются незначительный
птоз верхних век, резко выступающий нос с высоким переносьем, что
особенно подчеркивается недоразвитием подглазнично-скуловых областей.
Нередко вследствие искривления носа в костном отделе дыхание затруднено.
Ушные раковины недоразвиты и деформированы; иногда перед ними
расположены небольшие пучки волос в виде своеобразных выступов. Для всех
больных характерно снижение слуха, влекущее за собой нарушение развития речи.
В различной степени выражены недоразвитие верхней и нижней челюстей,
скошенность подбородка. Нижняя челюсть деформирована по типу
двусторонней микрогнатии. Деформация лицевого скелета при челюстно-лицевом
дизостозе, как правило, двусторонняя, но не симметричная. У всех больных
наблюдается истончение мягких тканей лица с недоразвитием подкожной
жировой клетчатки, особенно в подглазнично-скуловых областях.
При рентгенологическом исследовании черепа в прямой, боковой и
полуаксиальной проекциях, ортопантографии, томографии височно-нижнече-
люстных суставов выявляется, что глазницы вытянуты в вертикальном
направлении, скошены; создается впечатление, что они плоские. Нижнеглазничные
края не дифференцируются. Лобные пазухи хорошо выражены. Отмечается
недоразвитие скуловых костей и дуг, а у ряда больных — полное их отсутствие.
В ряде случаев верхнечелюстные пазухи имеют вид небольших
дополнительных ячеек, плотно прилегающих к клеткам решетчатого лабиринта. Высота
альвеолярного отростка верхней челюсти уменьшена. Нижняя челюсть
уменьшена в размерах, гониальные углы выражены, ветви значительно
укорочены. Мыщелковые отростки снижены за счет недоразвития, а в ряде
случаев вследствие полного отсутствия головок нижней челюсти и
укорочения шеек.
Хирургическое лечение больных с челюстно-лицевым дизостозом
многоэтапно. По данным литературы, нет единого мнения о сроках, методах и
последовательности оперативных вмешательств. Хирургическое лечение с
применением имплантатов проводят последовательно в три этапа.
В первую очередь выполняют костно-пластические операции с целью
уменьшения носа и устранения искривления. Через разрезы на слизистой
оболочке крыльев и перегородки носа отслаивают кожу с надкостницей,
производят двустороннюю остеотомию костей носа и иссечение сегмента
четырехугольного хряща с коррекцией хрящевого отдела носа. При резко
выраженной микрогнатии осуществляют костно-пластическое удлинение нижей
челюсти.
367
Рис. 30.6. Устранение
деформации при синдроме Тричера—
Коллинза с применением им-
плантатов из силоксана и
одномоментной пластикой нижних
век лоскутами на ножках с
верхних век (схема).
а — деформация; б — отслаивание и
перенос лоскута с верхнего века на
нижнее; в — расположение имплан-
татов.
Задача второго этапа заключается в восстановлении рельефа скулоорби-
тальных областей и наружно-нижних стенок глазиц с помощью имплантатов,
предварительно смоделированных и изготовленных из силоксана. При этом
для коррекции антимонголоидного разреза глазной щели и в связи с
недоразвитием кожи нижнего века одновременно производят пластику нижних
век лоскутом на ножке с верхнего века (рис. 30.6).
Пластику нижнего века целесообразно сочетать с подсадкой силоксано-
вого имплантата, так как при подготовке ложа для него ткани широко
мобилизуют, отслаивают надкостницу в области подглазничного края и
скуловой кости. При этом рассекают фиброзный тяж, идущий от наружнонижнего
угла глазницы к месту наибольшей деформации нижнего века, что позволяет
в
368
Рис. 30.7. Устранение деформации при синдроме Тричера—Коллинза с применением
имплантатов из силоксана с одномоментной пластикой подглазничных скуловых
областей артериализированным кожно-жировым лоскутом из лобной области.
а — деформация; б — отслаивание и перенос лоскута с верхнего века на нижнее; в — после операции.
устранить колобому. Кроме того, необходимо фиксировать лавсаном связку
наружного угла глазной щели. При резко выраженном недоразвитии кожных
покровов подглазнично-скуловых областей применяют методику их
пластики лоскутами на сосудистых ножках со лба (рис. 30.7).
На третьем этапе производят контурную пластику нижней зоны лица
индивидуально моделированным имплантатом из силоксана, устраняя тем
самым недоразвитие не только в подбородочном отделе, но и при
необходимости в области ветвей и углов нижней челюсти. При реконструктивных
операциях вводят по три имплантата: два в скулоорбитально-щечные области,
один — в область нижней челюсти.
Операция позволяет добиться хороших анатомических и
функциональных результатов. При этом одновременно восстанавливают рельеф скулоор-
битальных областей (имплантатами) и устраняют дефект мягких тканей
(кожно-жировыми лоскутами). Кроме того, корригируют деформацию
нижнего века, глазная щель приобретает правильное положение, перемещенный
кожно-жировой лоскут не сокращается и по цвету практически не отличается
от окружающих тканей (рис. 30.8).
Гемифациальная микросомия (отокраниостеноз)
относится к синдромам первой и второй жаберных дуг и выражается в односторонней
микротии, макростомии и недостаточном развитии ветви нижней челюсти.
Клиническая картина характеризуется резкой асимметрией лица из-за
уменьшения лицевого скелета с пораженной стороны и некоторого
увеличения — с другой. Выражена врожденная деформация ушной раковины, мягкие
ткани околоушной и щечной областей истончены, уменьшены в объеме.
Открывание рта не затруднено, прикус в большинстве случаев адаптирован,
несмотря на косое расположение окклюзионной плоскости. Асимметрия
нижней челюсти проявляется уже в раннем возрасте и, вероятно, играет
основную роль в прогрессирующем искривлении структуры на обеих
сторонах. На ортопантомограмме четко выявляется недоразвитие нижней челюсти:
ветвь не дифференцируется, тело резко сужено, уплощено, укорочено и
заканчивается закруглением, отдаленно напоминающим суставную головку,
подбородок смещен в сторону аномалии.
Хирургическое лечение зависит от клинической картины и степени
деформации.
При отокраниостенозе I степени достаточно выполнить корригирующие
операции на ушной раковине или восстановить имплантатом симметрию
подбородочного отдела. При гемифациальной микросомии II степени
сначала устраняют деформацию нижней челюсти имплантатом из силоксана,
затем корригируют скулоподглазнично-щечную область вторым
индивидуально изготовленным имплантатом. В заключение производят пластику ушной
раковины. Последовательность операций обусловлена тем, что после
устранения наиболее выраженной деформации нижней зоны лица легче
определить размеры и толщину имплантата, необходимого для коррекции скуло-
подглазнично-щечной области.
С целью коррекции деформации нижней зоны лица имплантат
моделируют индивидуально, так как нужно не только восстановить подбородочную
область, но и создать отсутствующий край и ветвь нижней челюсти.
Особенностью операции при контурной пластике нижней челюсти
является то, что вместо обычного разреза на коже в подчелюстной области,
оставляющего заметный рубец, делают два разреза: на слизистой оболочке
нижней губы и небольшой A — 1,5 см) разрез на коже за проекцией ветви нижней
челюсти. Это облегчает отслаивание надкостницы в области ветви и угла
нижней челюсти и позволяет проводить толстую лавсановую нить, помогаю-
370
Рис. 30.8. Больной с синдромом Тричера—Коллинза.
/ — до операции- а — в фас, б — в профиль; // — после операции: в — в фас, г — в профиль
Л ^ ^ч
Рис. 30.9. Больной с отокраниостенозом (гемифаииальной микросомией).
/ — до операции: а — в фас, б — в профиль; // — после операции: в — в фас, г — в профиль;
ѣ%
Рис. 30.9. Продолжение.
///— через 15 лет после операции: д — в фас, е — в профиль.
щую поместить большой гибкий имплантат в подготовленное ложе. Через
этот же разрез вводят дренажную трубку.
Деформацию скулоподглазнично-щечной области устраняют через
разрез под ресничным краем нижнего века и далее по линии морщин на уровне
наружного угла глаза на протяжении 1 см. Особенностью этой операции
является отслаивание надкостницы только в области подглазничного края и
скуловой кости, необходимое для введения имплантата под надкостницу и
фиксации его верхнего края. В щечной области ложе для имплантата
формируют под отслоенной подкожной жировой клетчаткой над мимическими
мышцами. При необходимости одновременно корригируют рубец после
поперечной расщелины лица.
При отокраниостенозе III степени предварительно производят костно-
реконструктивное вмешательство на лицевом скелете, позволяющее исправить
положение верхней и нижней челюстей путем их остеотомии, а также
восстановить недоразвитые или отсутствующие костные образования на стороне
аномалии сложным ортотопическим аллотрансплантатом. Эту предварительную
операцию производят по методике, разработанной группой авторов
[Плотников Н. А. и др., 1984; Безруков В. М. и др., 1988].
На следующем этапе восстанавливают рельеф и контуры лица силоксано-
выми имплантатами по методикам, описанным выше, поскольку костно-рекон-
структивными операциями не всегда можно полностью устранить деформацию.
Только применение имплантатов из силоксана при операциях по поводу
деформации при отокраниостенозе позволяет наиболее эффективно устранить
асимметрию лица и получить хороший эстетический результат (рис. 30.9).
373
Силоксановые имплантаты применяют также при восстановительных
операциях по поводу деформ аци и носа и верхней губы после
врожденной расщелины и хей л о π л асти к и. Ткани верхней губы,
слизисто-надкостничного и слизисто-надхрящичного лоскута в области
боковой поверхности и перегородки носа широко мобилизуют с целью
создания выстилки дна носового хода. Для закрытия ротоносового соустья
мышечный лоскут на питающей ножке выкраивают из круговой мышцы рта.
Одновременно имплантатами из силоксана корригируют западение основания
крыла носа на стороне расщелины и деформации спинки и кончика носа.
Операции с использованием таких имплантатов помогают восстановить рельеф
и контуры лица и получить хороший эстетический результат (рис. 30.10).
Деформации после воспалительных заболеваний. Дефекты и деформации
лица возникают вследствие перенесенных, особенно в раннем детстве, таких
воспалительных процессов, как фронтит, абсцессы, флегмоны, остеомиелит,
анкилоз височно-нижнечелюстного сустава.
Воспалительные процессы в носоверхнечелюстной области
(остеомиелит костей носа, абсцесс носовой перегородки) приводят к
недоразвитию всего носа и его основания по краю грушевидного отверстия.
Клинически это проявляется уплощением носовых костей, западением спинки
носа, втяжением кожной части перегородки, рубцовой деформацией и
укорочением кожных покровов носа.
При седловидной деформации носа, если кожные покровы не изменены
рубцами, для восстановления формы носа достаточно через эндоназальный
разрез или разрез на кончике носа по Рауеру ввести в область спинки носа
скульптурно-моделированные имплантаты из силоксановой резины. Если же
кожные покровы носа недостаточны, рубцово изменены, то необходимо
произвести ряд предварительных оперативных вмешательств для восполнения
объема мягких тканей.
Ринопластику дефектов носа производят путем перемещения встречных
разновеликих треугольных, трапециевидных лоскутов, одного или двух
лоскутов со щек или лба. Опору перемещенным тканям создают с помощью си-
локсановых имплантатов, формируя спинку, перегородку и основание носа.
Особенность индивидуального моделирования заключается в точном расчете
с помощью рентгенограмм высоты недостающих тканей верхней челюсти по
краю грушевидного отверстия и угла наклона отростка, восстанавливающего
концевой отдел четырехугольного хряща, что позволяет переместить кожную
часть перегородки носа в правильное положение. Второй имплантат
моделируют с учетом восстановления спинки, кончика и при необходимости крыльев
носа. Операцию проводят через два разреза: в области кончика носа и на
слизистой оболочке верхней губы. После широкой мобилизации тканей спинки,
перегородки, скелетирования основания носа по краю грушевидного
отверстия вводят и фиксируют имплантаты. Раны послойно ушивают (рис. 30.11).
Эластичные свойства силоксановых имплантатов, по консистенции
близких к хрящу, позволяют создать опору перемещенным тканям,
восстановить форму носа и дыхание (рис. 30.12).
Область нижней зоны лица. Наиболее часто причинами
развития деформации нижней части являются воспалительные процессы:
одонтогенный остеомиелит, артрит, анкилоз височно-нижнечелюстных
суставов. Односторонняя деформация нижней челюсти чаще всего
возникает после остеомиелита. При этом пораженная половина значительно
укорачивается, подбородок смещается в сторону поражения и назад. С другой
стороны тело нижней челюсти уплощается, ее край обычно развернут
внутрь и расположен ниже. В развитии двусторонней микрогнатии значи-
374
Рис. 30.10. Больной с деформацией верхней губы и носа при врожденной расщелине.
Дефект альвеолярного отростка верхней челюсти, ротоносовое соустье.
/ — до лечения: а — в фас, б — в профиль; // — после реконструктивных операций; β — в фас,
г — в профиль.
Рис. 30.11. Пластика носоверхнечелюстной области имплантатом из силоксана (схема).
а — дефект; б, в — линии разрезов в области наружного носа; г, д, е — деформирование ложа
для имплантата; ж, з — укладывание имплантата; и, к — фиксация имплантата.
Рис. 30.12. Больной со скрытым обширным дефектом носа вследствие абсцесса.
Состояние после пластики носа гомохрящом, проведенной 20 лет назад. Нос восстановлен
пластикой двумя трапециевидными лоскутами со щек и имплантатами из силоксана.
/ — до операции: а — в фас, б — в профиль; // — после операции: в — в фас, г — в профиль.
тельную роль играют инфекционные и воспалительные заболевания (корь,
скарлатина, отит), приводящие к нарушению зон роста, вследствие чего
нижняя челюсть уменьшается, подбородочный отдел скошен. Щеки
кажутся выпуклыми, нависающими над нижней челюстью, нижняя губа
отвисает.
377
Операцию контурной пластики нижней зоны лица производят внутри-
ротовым доступом через разрез на слизистой оболочке нижней губы. В
области нижней губы ближе к углу рта накладывают два шва-держалки, зубы
закрывают салфеткой, пропитанной фурацилином. На слизистой оболочке
нижней губы выше прикрепления уздечки проводят разрез длиной 3—3,5 см
так, чтобы в области нижней челюсти оставалась полоска тканей, состоящая
из части круговой мышцы рта и надкостницы. Мягкие ткани с надкостницей
отделяют распатором, обнажая подбородочный отдел, края нижней челюсти
от угла до угла и сохраняя стволы подбородочного нерва. В области
альвеолярного отростка надкостницу отслаивают распатором несколько выше
переходной складки. В подготовленное ложе вводят имплантат, концы
которого погружают в отслоенную надкостницу и m.masseter, что способствует
фиксации имплантата. После проверки правильности расположения им-
плантата по средней линии надкостницу в подбородочном отделе фиксируют
над имплантатом кетгутовыми или лавсановыми швами. На мышцу
накладывают швы кетгутом, слизистую оболочку нижней губы ушивают
непрерывным кетгутовым швом (рис. 30.13).
Применение силоксановых имплантатов при операциях после
воспалительных процессов не только помогает устранить деформацию лица, но и
показывает возможность использования полимеров при данной патологии, что
особенно важно при восстановлении нижней зоны лица после оперативного
лечения анкилоза (рис. 30.14).
Деформации мягких тканей лица после гемиатрофии и липодистрофии.
Дефекты и деформации мягких тканей лица, обусловленных
прогрессирующей гемиатрофией и липодистрофией (болезнь Барракера—Симонса), имеют
ряд сходных клинических признаков. В результате поражения гипоталами-
ческой области происходят дистрофические нарушения. Заболевание
наблюдается преимущественно у детей школьного возраста. В активной и
стационарной стадиях болезни развиваются дистрофические изменения в области
лица, а в дальнейшем грубые косметические дефекты [Гур Э. К., 1961;
Гусева Н. Г., 1993].
Особенностью клинического проявления прогрессирующей
гемиатрофии лица является нарастающее похудание всей половины лица,
обусловленное в основном дистрофическими изменениями подкожной жировой
клетчатки и кожи с вовлечением в процесс мышц, хрящей и костей лицевого
скелета.
Болезнь Бараккера—Симонса характеризуется нарушением жирового
обмена со своеобразным перераспределением подкожной жировой клетчатки
из области лица, рук и верхней половины туловиша в область ягодиц,
тазового пояса и проксимальных отделов ног.
Для устранения деформаций при гемиатрофии и липодистрофии
применяют только индивидуально смоделированные перфорированные имплан-
таты, так как под атрофированными и истонченными тканями видны любые
неровности имплантатов или трансплантатов. Разрезы проводят по
естественным складкам кожи, рубцам, в волосистой части лобной и височной
областей, на слизистой оболочке преддверия полости рта. Имплантаты
располагают под надкостницей и швами фиксируют к ней. При коррекции щечной
Рис. 30.13. Контурная пластика нижней зоны лица имплантатом из силоксана внут-
риротовым способом (схема).
а — дефект; б — линия разреза; в, г, д — отслаивание мягких тканей из нижней челюсти; е —
введение имплантатов в созданное ложе; ж — зашивание мягких тканей над имплантатом; з —
соотношение тканей после замещения дефекта имплантатом.
378
Рис. 30.14. Больная с деформацией и недоразвитием нижней челюсти.
/ — до операции: а — в фас, б — в профиль; // — после операции: β — в фас, г — в профиль.
Рис. ЗОЛ 5. Больная с липодмстрофией лица.
/, α — до операции; // — после операции: б — через I год; в — через 15 лет.
области поднадкостнично фиксируют только верхний край имплантата, а
нижнюю часть располагают в подкожном слое.
В связи с тем что имплантаты из силиконовой резины, несмотря на
гибкость и эластичность, все же достаточно плотны и при мимических
движениях края их могут контурироваться, целесообразно применять полимерные
материалы, по консистенции более соответствующие мягким тканям лица.
На основе силоксановых олигомеров разработаны инъецируемые самоотвер-
ждающиеся компаунды для коррекции дефектов лица — эластосил МИ
(медицинский инъекционный) и КСИ.
Применение инъекционных компаундов исключает необходимость
изготовления имплантатов in vitro. Хирург осуществляет моделирование
непосредственно во время инъекции. Отверждаясь, компаунды приобретают мягкоэла-
стическую консистенцию. КСИ используется при устранении деформации век,
губ, щек. Эстетические результаты хорошие, состояние восстановленных
тканей наиболее приближено к естественной эластичности мягких тканей лица.
При анализе отдаленных результатов A5 лет) применения силоксановых
самоотверждающихся компаундов отмечены стойкое восстановление
контуров мягких тканей лица, улучшение цвета кожных покровов, исчезновение
пигментации кожи, что, вероятно, связано с компенсаторным усилением
кожного кровообращения (рис. 30.15).
Многолетние C0 лет) наблюдения за оперированными больными
свидетельствуют о безопасности применения отечественных силоксановых
материалов в восстановительной хирургии лица. Ни в одном случае силокса-
новые имплантаты не являлись причиной осложнений. В челюстно-лицевой
хирургии осложнения после пластических операций с применением
силоксановых имплантатов могут быть связаны с одонтогенной инфекцией,
неточностью моделирования имплантата, рубцовой деформацией мягких
тканей и недостаточностью кожных покровов.
Метод объемной и контурной пластики силоксановыми композициями
применим практически во всех анатомических областях лица и является
наименее травматичным, позволяющим получить хорошие функциональные и
эстетические результаты, что ведет к социальной реабилитации больных.
30.2. Эктопротезирование лица
Наружные протезы лица называют также эктопротезами, эпипротезами, эпи-
тезами. Термин "эпитеза" происходит от греческого слова epitema и означает
"крышка", что помогает понять первичную задачу — скрыть дефект. Дефекты
лица, образовавшиеся вследствие удаления новообразований, огнестрельных
ранений, механических повреждений, могут быть исправлены с помощью
оперативных вмешательств или эктопротезирования. При обширных
дефектах лица, которые не могут быть устранены хирургическим путем,
эктопротезирование лица является важнейшим фактором для социальной
реабилитации пациента.
Историческая справка. Во все времена существовало стремление врачей
с помощью эктопротеза дать больному возможность вернуться в общество.
Изготовление искусственных частей лица было распространено уже в XVI в.
Для этого использовали металлы, кожу или папье-маше, причем на эстетику
обращали мало внимания. Первым пациентом, которому применили экто-
Термин, используемый в зарубежной литературе.
382
протез, был датский астроном Тихо Браге A546—1601). После ранения на
дуэли ему сделали нос из сплава меди, золота и серебра. В дальнейшем материалы
и методы совершенствовались. В XIX в. появились каучук, целлулоид,
желатиновые массы, которые позволили упростить изготовление эктопротеза и
сделали возможным эстетическое оформление лица. Однако литые протезы
из металла и каучука оказались тяжелыми, на них плохо удерживалась краска.
Протезы из желатиновой массы, имевшие естественный вид, плохо
фиксировались, высыхали и рвались. Протезы из целлулоида воспламенялись.
С 40-х годов XX в. стали применять полиметилметакрилат, что
значительно облегчило изготовление челюстно-лицевых протезов. Преимущество
акриловой пластмассы заключается в меньшем удельном весе, в возможности
окрашивания протеза под цвет кожи добавлением красителей, в простоте
гигиенической обработки без боязни изменения цвета. Эктопротезы из
пластмассы легко обрабатываются, не изменяют форму, хорошо соединяются с
оправой очков и другими фиксирующими приспособлениями, но со временем
все же изменяют цвет и вследствие твердости травмируют окружающие
дефект мягкие ткани.
В 40—50-х годах в нашей стране были разработаны эктопротезы лица,
изготавливаемые из полиметилметакрилата, сополимера хлорвинила и бути-
лакрилата. Фиксация этих протезов на лице осуществлялась с помощью
специального клея (раствор перхлорвиниловой смолы в органическом
растворителе). Аналогичные материалы и способ фиксации клеем не утратили
значения и в настоящее время. Однако эктопротезы из твердых материалов
или недолговечно эластичных материалов не имитируют естественные
мягкие ткани лица, поэтому поиск более совершенных эластичных материалов
продолжается.
Применение силоксановых композиций, разработка метода фиксации с
помощью титановых внутрикостных имплантатов открывают новые
возможности в эктопротезировании.
Одентология. При эктопротезировании дефектов лица наряду с
медицинскими проблемами на первом плане стоит проблема возврата пациенту
психического равновесия. Одной из первостепенных задач врача является
психическая стабильность пациента. Это может быть достигнуто только при
доверии к врачу. По возможности следует избегать всего, что может вызвать
разочарование больного. Во время первой беседы желательно участие супруга
(родственника). При этом можно обсудить варианты лечения, показать
фотографии больных с подобными поражениями и объяснить особенности эк-
топротезирования. Положительный момент заключается еще и в том, что
пациента посвящают в процесс лечения и знакомят с проблемами, стоящими
перед хирургом и ортопедом, и возможностями, которыми они располагают.
Врач должен оценить психоэмоциональное состояние пациента, внушить
ему уверенность в успехе лечения. При этом нужно идти навстречу
обоснованным желаниям больного относительно эстетического оформления и
надежной фиксации эктопротезов.
Функции эктопротеза. Эктопротез не может выполнять функции
утерянной части лица. С помощью него восстанавливают лицо лишь эстетически.
В связи с этим он выполняет социальную функцию, так как человек с
изуродованным лицом не может участвовать в общественной жизни, не
привлекая к себе внимания. Угроза социальной изоляции может быть устранена с
помощью эктопротеза.
Цель его применения состоит также в восстановлении возможности
приема пищи, глотания, так как дефекты мягких тканей приротовой области
вызывают выпадение пищи во время жевания и постоянное слюнотечение.
383
Кроме того, он помогает улучшить произношение, особенно при дефектах
верхней челюсти. Эктопротезы носа способствуют согреванию холодного
воздуха, что уменьшает возможность развития простудных заболеваний.
Защитная функция эктопротезов состоит также в том, что они предохраняют
рубцовые ткани и открытую слизистую оболочку от травм и физических
воздействий. Протезы, как маска, защищают легко ранимые ткани, что в
совокупности с косметическим эффектом повышает трудоспособность больных
и расширяет возможности общения в коллективе.
Этапы изготовления эктопротеза: 1) снятие слепка лица; 2) получение
гипсовой маски; 3) создание восковой модели протеза; 4) примерка модели;
5) подбор цвета; 6) гипсовка модели и замена воска на пластмассу; 7)
обработка протеза; 8) фиксация протеза.
Изготовление протеза необходимо начинать со снятия слепка всего лица
в полусидячем положении больного. Волосистые части лица смазывают
вазелином, волосы убирают под одноразовую шапочку. Раневую поверхность
дефекта закрывают двумя слоями марли или, лучше, адгезивной пленкой, в
носовые ходы или ротовую щель вставляют резиновые трубочки. Гипс сме-
танообразной консистенции слоем толщиной 1,5 см наносят сначала на
область дефекта глазниц (веки должны быть закрыты), а затем на другие
области лица. Больного необходимо предупредить о том, что во время снятия
слепка он будет испытывать чувство сдавления и тепла, выделяемого при
отверждении гипса. Слепок снимают через 10—15 мин. После замачивания его
в мыльной воде отливают гипсовую маску.
Для снятия слепка можно также применять эластические слепочные
массы.
На рубцово-измененные края дефекта и ретенционные пункты,
затрудняющие извлечение слепка, накладывают небольшое количество
эластической слепочной массы. На остальную поверхность лица и на эластическую
массу наносят гипс, создавая этим плотную основу для нее.
С целью уменьшения травматизации кожных покровов и раневых
поверхностей можно снимать слепок только эластической массой. Однако во
избежание деформации слепка необходима жесткая основа. Для решения
этой задачи В. А. Миняева предложила устройство в виде металлической
перфорированной формы. В результате сохранения слепка стало возможным
изготовление нескольких идентичных гипсовых масок лица, что необходимо
при эктопротезировании.
По гипсовой маске и лицу больного из зубоврачебного воска моделируют
недостающую часть лица, основываясь на антропометрических данных и
фотографии. В процессе моделировки скульптор вместе с врачом проводит примерки
с учетом пожеланий больного. Обращают внимание на плотность прилегания
модели к краям дефекта, определяют границы и пункты фиксации протеза,
осуществляют подбор цвета протеза, соответствующий оттенкам кожи лица. После
полимеризации пластмассы и обработки протеза проводят окончательную
припасовку эктопротеза, фиксацию его к очковой оправе, а также дополнительную
подкраску и крепление ресниц, бровей и усов, если это требуется.
С помощью эктопротеза возможно замещение дефекта носа, глазницы,
ушной раковины.
Особенно тяжелые дефекты лица появляются в результате
хирургического лечения злокачественных новообразований. При этом нередко
возникает необходимость в одновременном протезировании челюсти и тканей лица,
т. е. изготовлении комбинированного челюстно-лицевого протеза. Методы
сложного эктопротезирования онкологических больных описаны В. М. Чуч-
ковым A976). Комбинированные челюстно-лицевые протезы фиксируют на
384
Рис. 30.16. Больная с дефектом носа.
/ — до операции: а — в фас, б — в профиль; // — после замещения дефекта эктопротезом из
силикона: в — в фас, г — в профиль.
очковой оправе и протезе верхней челюсти, если он хорошо удерживается в
полости рта. В некоторых случаях Б. К. Костур рекомендует фиксировать эк-
топротез на цельнолитой съемной шине.
Эктопротез должен не только прикрывать дефект, но и отвечать
высоким эстетическим требованиям. Для фиксации существуют принципиально
разные, но связанные друг с другом возможности: 1) анатомическая
фиксация (закрепление без вспомогательных средств при использовании
благоприятных анатомических условий или опора, созданная хирургическим путем);
2) химическая фиксация (закрепление клеем); 3) механическая фиксация
(крепление эктопротеза к постоянной оправе для очков).
Анатомическая фиксация имеет ограниченные возможности и приводит
к успеху при использовании небольших эктопротезов. При длительном
использовании клея часто наблюдаются раздражение рубцово-измененных
кожных покровов и изменение цвета в области границ эктопротеза.
Крепление эктопротезов носа, глазниц к оправе очков не всегда позволяет хорошо
скрыть дефект лица, например при снятии очков или смещении эктопротеза
в сторону за счет его массы.
Разработка системы фиксации с помощью титановых внутрикостных
385
25- 1263
имплантатов открыла новые возможности для более стабильного крепления
эктопротезов. В 80-х годах появились сообщения о положительных
результатах применения титановых имплантатов в качестве средства фиксации при
эктопротезировании. Используют как внутри-, так и внеротовые титановые
имплантаты различной конструкции. Основу их составляет болт с внутренней
резьбой, в которую входит болт-замок в фазе заживления или основной болт
для фиксации опоры эктопротеза. Срок приживления имплантата 4—6 мес,
после чего устанавливают предварительно смоделированный эктопротез,
изготовленный из полиметилметакрплата или силикона. Пациента
информируют о необходимости гигиенической обработке протеза и регулярного
обследования.
Несмотря на расширившиеся возможности фиксации при
эктопротезировании, ранее применявшиеся простые методы фиксации на оправе очков
или с помощью клея не потеряли значения (рис. 30.16). Только активным
пациентам, готовым к совместной работе, можно проводить эктопротезирование
с использованием внутрикостных имплантатов.
Эктопротезирование наряду с реконструктивно-хирургическими
методами дает возможность реабилитировать пациента с дефектами лица. С
помощью удачно закрепленного эктопротеза можно не только восстановить
черты лица, но и возвратить человека в привычную социальную среду.
СПИСОК ЛИТЕРАТУРЫ
Безруков В. М. Клиника, диагностика и лечение врожденных деформаций средней
зоны лицевого скелета: Автореф. дис. ... д-ра мед. наук. — ML, 1981. — 46 с.
Безруков В. М., Гунько В. И., Баев В. Т. Устранение деформации подбородочного
отдела нижней челюсти // Стоматология. — 1986. — № 3. — С. 57—59.
Безруков В. М., Плотников Я. А, Гунько В. И. и др. Хирургическая коррекция
дефектов лицевого скелета у больных с гемифациальной микросомией // Acta chir.
plast. - 1988. - Vol. 30, № 4. - P. 185-196.
Безруков В. М. Восстановление функций; основные направления в пластической
хирургии Ф. М. Хитрова // Восстановительная хирургия челюстно-лицевой
области. - М., 1995. -С. 12-16.
Безруков В. М., Набиев Ф. Х.у Рабухина Я. А и др. Модифицированный метод
хирургического лечения больных с верхней ретро- и микрогнатией // Стоматология. —
1996. - Т.75, № 2. - С. 49-51.
Бельченко В. Α., Ипполитов В. П., Ростокин Ю. Я и др. Эндопротезирование
мозгового и лицевого черепа перфорированными пластинами из титана //
Стоматология. - 1996. - Т.75, № 2. - С. 52-54.
Брусова Л. А. Восстановительные операции на лице с применением силоксановых
композиций: Автореф. дис. ... д-ра мед. наук. — М., 1996. — 61 с.
Брусова Л. Α., Острецова Я И. Силоксановые материалы в реконструктивно-восстано-
вительной хирургии лица: Обзор литературы, клинический опыт и перспективы
// Ann. plast. reconstr. aesthet. Surg. — 1997. — № 2. — P. 52—64.
Вильяме Д. Р., Роуф Р. Имплантаты в хирургии / Пер. с англ. —М., 1978. — 558 с.
Гаврипов Е. И., Щербаков А. С. Ортопедическая стоматология. — М.: Медицина, 1984. —
С. 555-560.
Груздкова £. В., Брусова Л. А. Новые полимеры в восстановительной хирургии лица:
Тезисы науч.-практ. конф. Ин-та косметологии МЗ РСФСР. — М., 1969. —
С. 37-38.
Гунько В. И. Клиника, диагностика и лечение больных с сочетанными деформациями
челюстей: Автореф. дис. ... д-ра мед. наук. — М., 1987. — 44 с.
Гур Э. К. О патогенезе атрофии лица // Журн. невропатол. и психиатр. — 1961. — Т.62,
вып.6. - С. 820—824.
386
Гусева Η. П. Системная склеродермия и псевдосклеродермические синдромы. — М.,
1993. - 268 с.
Каламкаров Χ. Α., Рабухина Η. Α., Безруков В. М. Деформации лицевого черепа. — М.,
1981. - 235 с.
Костур Б. К., Миняева В. А. Челюстно-лицевое протезирование. — Л.: Медицина,
1985. - С. 67-133.
Краткая медицинская энциклопедия. — М, 1994.
Кручинский Г. В. Классификация синдромов первой и второй жаберных дуг // Acta
cliir. plast. - 1990. - Vol.32, № 3. - P. 166-176.
Лурье Т. М. Организация травматологической стоматологической помощи в мирное
время // Травмы челюстно-лицевой области. — М., 1986. — С. 387—394.
Маргазизов М. 3., Гюнтер В. Э., Итин В. И. и др. Сверхэластичные имплантаты и
конструкции из сплавов с памятью формы в стоматологии. —- М, 1993. — 231 с.
Медведев Ю. А. Возможности применения имплантатов из пористого никелида титана
в реконструкции травм нижней стенки глазницы // Восстановительная хирургия
челюстно-лицевой области. — М., 1995. — С. 87—89.
Плотников Н. А. Костная пластика нижней челюсти. — М.: Медицина, 1979. — 271 с.
Плотников Η. Α., Никитин Л. Α., Сергеев Ю. Н. 25-летний опыт МОНИКИ в
ортопедической аллотрансплантации костной ткани в челюстно-лицевой хирургии //
Проблемы аллопластики в стоматологии. — М., 1984. — С. 54.
Плотников Η. Α., Сысолятин Я. Г., Никитин Л. А. Актуальные проблемы лечения
заболеваний и повреждений височно-нижнечелюстного сустава// Заболевания ви-
сочно-нижнечелюстного сустава: Сборник научных трудов/ Под ред. Н. А.
Плотникова. - М., 1988. - С. 7-13.
Хитрое Ф. М. Атлас пластической хирургии лица и шеи. — М., 1988. — 208 с.
Чуйков В. М. Роль сложного челюстно-лицевого протезирования в реабилитации
онкологических больных: Дис. ... канд.мед.наук. — М., 1976. — 255 с.
Braley S. A. The use of silicone in plastic surgery // Plast. reconstr. Surg. — 1973. — Vol.51,
N 3. - P. 283-288.
Brauner Η., Lechner Κ. Η. Die Gesichtsmaske — Ein Hilfsmittel zur temporären Deckung
groserer Gesichtsdefekte // Quintessenz. — 1991. — N 2. — S. 309—315.
Bucher P., Yaguiery C, Lüscher N. Y, Prein Y. Grundlagen der Epithetik // Quintessenz. —
1996. - N 7/8. - S. 379-383.
Collins Ε. Τ. Case with symmetrical congenital notches in the outer part of each lower lid
and defective development of the malar bones // Trans. Ophtal. Sos. UK. — 1900. —
Vol. 20. - P. 190-193.
Convers J. M. Reconstructive plastic surgery. — Philadelphia — London — Toronto, 1986. —
1520 p.
Farkas L. G., Munro I. R. Antropometric facial proportions in medicin. — Illinois:
Springfield, 1987. - 344 p.
Francescett Α., Klein D. The mandibulo-facial dysostosis. A new hereditary syndrome //Acta
ophthalmol. - 1949. - N 27. - P. 143-147.
Gehl G. Optimization of fixation methods for epitheses // J. Cranio-Maxillofac. Surg. —
1996. -Vol. 24, N 1. - P. 135.
Laa S. M., Lange К. P., Thierfelder C, Kalz W. Implantologische
Verankerungsmöglichkeiten bei Defektprothesen und Epithesen // Quintessenz. — 1991. — N 11. —
S. 1725-1735.
Planas J., Del Cacho С Twenty years of experience with particulate silicone in plastic surgery
// Aesthetic Plast. Surg. - 1992. - Vol. 16, N 1. - P. 53-57.
Scheller H., Handel G Verankerung von Aiigenepithesen mit Hilf osseointegrierter Implantate
// Quintessenz. - 1989. - Ν 5. - S. 865-871.
Schonegg IV. D., Schonleber G Safety of silicone implants: Report of the congress of the
American society of plastic and reconstructive surgery (Seattle, 22—26 sept., 1991) //
Geburt, u. Frauenheilk. - 1992. - Bd 52, N 1. - S. 70-72.
Глава 31
ПРЕДПРОТЕЗНАЯ
ХИРУРГИЯ
ПОЛОСТИ РТА
Активное развитие предпротезной хирургии началось в конце 50-х годов,
хотя она была известна давно. Врачи, занимавшиеся протезированием зубов, с
большой неохотой прибегали к хирургии, хотя в большом проценте случаев
отмечали плохие условия для фиксации протезов. R. Hopkins A985)
установил, что у 80 % пациентов, носящих зубные протезы, нет хорошей опоры для
их фиксации и в полости рта наблюдаются патологические процессы,
создающие дискомфорт. Челюстно-лицевые хирурги долгое время не уделяли
внимания этим вопросам, как и возможностям хирургии для помощи
зубному протезированию.
Основой развития предпротезной хирургии в полости рта послужили
ранние работы таких выдающихся клиницистов-хирургов, как Е. Lexer
A909), P. Moure A923), W. Razanjian A924), Μ. Wassmund A938), П. Львов
A923), А. А. Лимберг A935), Α. Э. Рауэр A938), Η. Μ. Михельсон A943),
Α. И. Евдокимов A943), Г. А. Васильев A947). Отдельные методы
предпротезной хирургии были описаны в учебниках А. И. Евдокимова A950), Г. А.
Васильева A950, 1972), М. В. Мухина A972, 1998).
В настоящее время предпротезная хирургия стала достаточно
распространенным методом лечения заболеваний полости рта. Ей посвящены монографии,
главы в учебниках и руководствах [Guernsey L., 1973; Toma К., 1980; Laskiii D.,
1980; Bell W. et ab, 1988; Stoelinga P., 1984; Hopkins R., 1985; Fonseca R., 1993;
Krüger E., 1993; Tucker Μ., 1994].
Необходимость в предпротезной хирургии обусловлена рядом факторов,
в частности тем, что после потери естественных зубов происходит атрофия
альвеолярного отростка верхней челюсти и альвеолярной части нижней
челюсти. У отдельных пациентов процессы атрофии кости могут
прогрессировать в связи с сопутствующими заболеваниями и изменениями органов —
системными заболеваниями, остеопорозом костей, в том числе в
климактерическом и постклимактерическом периодах. На атрофию кости влияют
также местные факторы. Прежде всего — это травма при удалении зуба и частая
потеря одной из стенок альвеолы. Потере кости может способствовать также
ношение протезов, особенно в случае их плохой фиксации.
Кроме общеорганных и локальных факторов, вызывающих атрофию
кости при протезировании, трудности могут создавать анатомические
особенности челюстей. Они могут проявляться как в результате атрофических
процессов, так и в связи с особенностями, видом и развитием лицевых костей
скелета.
388
Ряд недостатков при протезировании может иметь сама костная ткань.
После удаления зубов альвеолярные возвышения могут чрезмерно выступать.
Кроме того, во время удаления зубов стенки зубных альвеол, чаще
вестибулярные, могут смещаться, образуя неровности кости. Плохие условия для
протезирования создают также атрофические процессы в кости,
происходящие чаще в вертикальном и переднезаднем направлениях, диспропорция
челюстей, увеличение расстояния между альвеолярными дугами и уменьшение
их ширины. Особенно часто протезирование усложняется из-за пародонтита,
пародонтоза, усугубляющих атрофические процессы в челюстях.
Определенные проблемы создают ретинированные зубы, особенно вызывающие
деформацию кости.
На верхней челюсти в месте соединения двух пластинок, образующих
твердое небо, может быть значительно выражен небный валик. Потеря
центральных зубов может привести к увеличению и неправильному окклюзион-
ному взаимоотношению альвеолярного отростка верхней челюсти с
аналогичным отделом нижней челюсти. При потере моляров верхней челюсти
могут создаваться неблагоприятные взаимоотношения с
зубами-антагонистами как по высоте, так и по окклюзии, в связи с чем может требоваться
уменьшение, увеличение или коррекция формы альвеолярного отростка.
На нижней челюсти трудности для протезирования создает сужение
альвеолярной части, ее атрофия, вследствие чего подбородочный бугорок, косая
линия, челюстно-подъязычная линия выступают, имеют острые края.
Помимо процессов атрофии кости, по мнению R. Popkins A985),
протезированию может препятствовать микростомия, возникающая за счет
хронических заболеваний зубов.
Протезирование может затруднить изменения мягкой ткани —
слизистой оболочки и надкостницы. После удаления зубов слизистая оболочка на
гребне альвеолярной дуги может рубцово изменяться. В некоторых случаях
эти изменения претерпевает и подлежащая надкостница. Большое значение
в гиперпластических изменениях имеет хроническая травма, в том числе
плохо фиксирующимися протезами. Последнее обстоятельство может быть
причиной папилломатоза, который чаще поражает твердое небо, преддверие рта,
гребень альвеолярной дуги. Такие изменения слизистой оболочки могут
усугубляться воспалительными изменениями пораженных тканей. Атрофия кости
может приводить к снижению сводов преддверия рта, выраженности уздечек
губ и языка, слизистых и мышечных тяжей, приближению их к альвеолярной
дуге. Челюстно-подъязычная, подбородочно-язычная и щечная мышцы
усугубляют трудности при фиксации зубных протезов.
Предоперационные манипуляции в полости рта направлены на устранение
изменений, которые могут касаться: 1) костных тканей челюстей; 2) мягких
тканей — слизистой оболочки, надкостницы, мышечных пучков,
присоединяющихся к челюстям; 3) переферических ветвей тройничного нерва.
На хирургическое лечение ортопед должен направлять пациентов с
такими патологическими изменениями, которые не позволяют полноценно
обеспечить изготовление протезов. При этом, помимо оценки условий для
протезирования, учитывают психологические факторы: адекватность жалоб
больного, понимание им необходимости оперативного вмешательства, а
также того, каких результатов в функциональном и эстетическом плане он
ожидает от ортопедического и хирургического лечения. Особенно важна
психологическая мотивация пациента в отношении его адаптации к временным и
постоянным зубным протезам.
Перед принятием решения о предпротезном оперативном вмешательстве
хирург должен детально изучить историю болезни пациента по всем прави-
389
лам, принятым в хирургической стоматологии, и определить возможную
связь изменений мягкой ткани и кости с общей патологией. Изменения
мягкой ткани, покрывающей альвеолярный отросток верхней челюсти и
альвеолярную часть нижней челюсти, следует оценивать с онкологической
настороженностью, а также с учетом возможных поражений слизистой оболочки
инфекционной, вирусной или другой природы.
При обследовании полости рта обязательно отмечают состояние уздечек
верхней и нижней губы, языка, наличие Рубцовых тяжей и складок слизистой
оболочки свода полости рта, мышечных тяжей. Особенно тщательно
оценивают воспалительные изменения свода преддверия полости рта, причиной
которых может быть травма краем протеза. В таких случаях нередко ставят
ошибочный диагноз дольчатой фибромы, тогда как имеют место
гипертрофия и рубцовые изменения слизистой оболочки.
Атрофия кости челюстей часто ведет к созданию избыточной подвижной
слизистой оболочки по альвеолярной дуге — так называемого болтающегося
гребня, который препятствует протезированию.
Оценку изменений мягких тканей дополняют обследованием кости
альвеолярного отростка верхней челюсти и альвеолярной части нижней
челюсти. Замеряют ширину и высоту кости, отмечают ее конфигурацию, наличие
выступов, неровностей, острых краев, экзостозов. На обеих челюстях
пальпируют те участки, где начинаются или прикрепляются мимические,
жевательные или другие мышцы. На верхней челюсти уточняют расположение
мышц, поднимающих верхнюю губу и крыло носа, а также щечной; на
нижней — челюстно-подъязычной, щечной, подбородочно-язычной и
подбородочной.
На альвеолярной части нижней челюсти пальпируют альвеолярную дугу,
неподвижную слизистую оболочку с целью обнаружения болезненности,
причиной которой из-за атрофии кости может быть поверхностное
расположение луночкового нерва или смещение кверху ментального отверстия.
31.1. Операции на костных тканях челюстей
(альвеолотомия и альвеолэктомия)
Пластика альвеол. Если при обработке раны после удаления зуба, а чаще
нескольких зубов, обнаруживают деформации альвеолярного отростка, то
производят пластику альвеол. Для этого слизисто-надкостничный лоскут
откидывают только для обнажения пораженного участка кости. Деформацию по
наружной и внутренней поверхности альвеолярной дуги устраняют при
помощи костных кусачек, костного напильника, бора или фрезы [Васильев Г. Α.,
1972]. При работе с бормашиной обязательно охлаждение операционного
поля путем ирригации изотоническим раствором натрия хлорида. После
удаления острых краев и их сглаживания слизисто-надкостничный лоскут
укладывают на место. Обращают внимание на сопоставление краев раны, и при
необходимости выравнивают ее края и иссекают излишек тканей.
Внутриперегородочная альвеолопластика. После удаления одного или
нескольких зубов в дальнейшем может потребоваться резекция
межальвеолярных перегородок [Dean О., 1941]. Рекомендуется произвести удаление
выступающей или неадекватной межальвеолярной перегородки (рис. 31.1) и
репозицию латеральной пластинки альвеолярного отростка верхней челюсти
или альвеолярной части нижней челюсти кнутри сильным давлением пальца
(следует иметь в виду, что возможно повреждение слизистой оболочки).
Такие действия позволяют устранить выступы с вестибулярной поверхности
390
Рис. 31.1. Резекция межальвеолярной перегородки.
а — откидывание слизисто-надкостничного лоскута; б — скусывание межальвеолярной
перегородки; в — зашивание раны (схема).
кости без уменьшения ее высоты и обеспечить сохранность прикрепленного
слизисто-надкостничного покрова. Кроме того, при такой методике альвео-
лопластики атрофия кости наименее выражена [Tuker M., 1994].
Уменьшение и коррекция неровной поверхности кости альвеолярного
отростка верхней челюсти и альвеолярной части нижней челюсти. Производят
при бугристости кости, препятствующей адекватному протезированию. Это
может быть обусловлено выступами кости, а также излишком, гипертрофией
покрывающих их тканей. Для создания нормальной альвеолярной дуги по
такой же методике, как при внутрипрегородочной альвеолопластике,
откидывают слизисто-надкостничный лоскут и обнажают с обеих сторон альвеолярный
отросток или альвеолярную часть челюсти. Выступы, неровности и другие
деформации кости удаляют костными кусачками, борами, фрезами. При
излишке мягких тканей их иссекают, на рану накладывают узловатые швы кетгутом
или полиамидной нитью. При операции на верхней челюсти необходимо
учитывать границы верхнечелюстной пазухи во избежание повреждения ее
дна. На нижней челюсти следует обратить внимание на расположение
подбородочного отверстия и выходящего из него сосудисто-нервного пучка.
Резекция участка альвеолярного отростка верхней челюсти и
альвеолярной части нижней челюсти. Показана в случае избытка тканей, деформации
кости, когда для зубов, в том числе для зубов-анатагонистов, в протезе нет
места. В зависимости от задач протезирования на моделях определяют
необходимый объем резекции кости. Рентгенологически оценивают расположение
носовой и верхнечелюстной пазух. Чтобы избежать их повреждения во время
операции, проводят линейный разрез по альвеолярной дуге и отсепаровывают
слизисто-надкостичный лоскут. Иногда делают дополнительно один или
несколько вертикальных разрезов, углообразно отсепаровывая трапециевидные
лоскуты. Избыток альвеолярной части удаляют костными кусачками, долотом,
а также борами, фрезами, позволяющими сгладить поверхность кости. В
соответствии с нужными для протезирования окклюзионными плоскостями
альвеолярных дуг оперируемому участку придают нужную форму. Избыток
мягких тканей удаляют с таким расчетом, чтобы края раны сближались без
натяжения. Лучше накладывать непрерывный шов из синтетической нити
[Daniel R., 1978; O'Ryan F., 1992].
391
Альвеолэктомию производят при диспропорции переднего отдела верхней
челюсти в случае ее адентии. Предложенные О. Dean A941), К. Kallenberger
A953), Η. Obwegeser A968) методики коррекции кости остаются
основополагающими, хотя отдельные авторы разработали их модификации [Keller Ε. et al.,
1987; Sailer Η., 1989; Richardson D., Cawood J., 1990].
Подготовка к немедленному протезированию. Подготовка альволярного
отростка верхней челюсти и альвеолярной части нижней челюсти
хирургическими действиями после множественного удаления зубов зависит от
возникшей ситуации. После удаления зубов остаются острые межальвеолярные
и межкорневые перегородки, которые особенно выражены при пародонтите
и пародонтозе. После обезболивания откидывают слизисто-надкостичный
лоскут, удаляют зубы и производят необходимые хирургические
манипуляции на кости. Перегородки убирают при помощи кусачек и производят
простейшую пластику альвеол, внутриперегородочную пластику. Выступы и
неровности кости сглаживают бором или фрезой. При помощи ножниц или
скальпеля иссекают межзубные сосочки и выравнивают край слизистой
оболочки с таким расчетом, чтобы имелось достаточно мягкой ткани для
закрытия кости, не было излишка слизистой оболочки и края раны хорошо
сопоставлялись. Рану зашивают наглухо.
Удаление экзостозов на верхней и нижней челюстях. Производят в тех
случаях, когда экзостозы имеют большие размеры и резко выражены. Разрез
делают по альвеолярной дуге; можно дополнять его вертикальными разрезами.
Откидывают лоскут углообразной или трапециевидной формы, обнажают
каждый участок деформированной кости. Экзостозы удаляют при помощи
кусачек, костного нашпиля, бора, фрезы. На мягкие ткани накладывают
узловатые или непрерывные швы.
При удалении экзостоза альвеолярного отростка верхней челюсти с
небной стороны и альвеолярной части нижней челюсти с язычной поверхности
обнажают кость через линейный разрез по альвеолярной дуге. Экзостозы
удаляют бором, фрезой, зубным нашпилем. Для хорошего обзора кости на нижней
челюсти следует отводить тупым крючком мягкие ткани, помня о близком
расположении язычного нерва, артерии, вены, а также протока поднижнечелю-
стной слюнной железы. При небольших экзостозах и недостаточной ширине
альвеолярного отростка по соответствующей поверхности делают один или
несколько разрезов слизистой оболочки и поднадкостнично формируют
туннель, в который вводят гидроксилапатит или другой биоматериал для создания
ровного и нужной толщины альвеолярного отростка. Рану на слизистой
оболочке зашивают. Желательно накладывать на альвеолярный отросток
формирующую пластинку или повязку.
Удаление экзостозов в области небного валика твердого неба. Нередко
при конструировании и оптимальном пользовании съемным зубным
протезом проблему создают экзостозы небного валика. Они могут быть разной
формы и конфигурации, иногда значительной величины, и, как правило,
деформируют небный свод. Удаление экзостозов проводят разрезом по средней
линии неба с послабляющими разрезами под углом 30—45° на переднем и
дистальном концах разреза. Слизисто-надкостичный лоскут отслаивают в
стороны, берут его по краям на лигатуры, обнажая основание костного выступа.
Выступ удаляют при помощи долота и молотка, бора или фрезы. Нередко
выступ приходится распиливать на несколько фрагментов и кусачками, долотом
удалять его по частям. Делать это следует с предельной осторожностью,
чтобы не перфорировать дно носовой полости. Поверхность кости сглаживают,
и слизисто-надкостничный лоскут укладывают на место, пальцем прижимая
мягкие ткани к поверхности кости (рис. 31.2). Избыток последних иссекают
392
Рис. 31.2. Удаление экзостозов в области небного валика твердого неба (а—г).
и на рану без натяжения ее краев накладывают узловатые швы. Для
профилактики гематомы на область неба с небольшим давлением накладывают
марлевую повязку, пропитанную йодоформной жидкостью или йодистой смесью,
маслом шиповника, облепихи и др. Такую повязку желательно фиксировать
шелковыми швами. Изготовленная защитная пластинка должна хорошо
фиксироваться, но не оказывать излишнего давления во избежание некроза мягких
тканей. В послеоперационном периоде проводят перевязки и гигиенические
процедуры в полости рта для профилактики воспалительных явлений.
Уменьшение и удаление челюстно-подъязычной линии. В зоне челюстно-
подъязычной линии нередко возникают трудности при фиксации протеза:
393
во-первых, гребень может быть острым, что становится причиной боли при
пользовании зубным протезом, во-вторых, нередко изъязвляется тонкая
слизистая оболочка, покрывающая его, в-третьих, прикрепляющиеся в этой
области мышечные волокна нередко являются препятствием при фиксации
ортопедической конструкции.
Уменьшение челюстно-подъязычной линии производят линейным
разрезом по вершине альвеолярного гребня с обеих сторон на уровне премоля-
ров, отслаивают слизистую оболочку и надкостницу. Мягкие ткани отсепа-
ровывают так, чтобы не повредить язычный нерв. Прикрепляющую мышцу
в месте выпячивания или острой поверхности линии отсекают, оставляя в
среднем отделе часть мышц, фасцию. Костными кусачками, бором и зубным
нашпилем снимают выступающую часть гребня, сглаживают кость. Протез
или шину желательно надеть сразу после зашивания раны узловатыми швами.
В соответствии с необходимым снижением дна полости рта увеличивают
оральный край протеза [Krüger E., 1993].
Уменьшение подбородочного бугорка и подбородочного выступа. При
атрофии нижней челюсти препятствием к адекватной фиксации зубного
протеза может быть выступающий подбородочный бугорок или выступ. Если
другого решения нет, то уменьшение бугорка или выступа осуществляют
разрезом по альвеолярной дуге на уровне резцов. С язычной стороны
отслаивают слизисто-надкостничный лоскут, отсекают часть пучков подбородочно-
язычной мышцы и обнаженный участок подбородочного бугорка или
выступа осторожно удаляют долотом или костными кусачками, а бором
сглаживают поверхность кости. Мышцу подшивают (или часть пучков
оставляют без фиксации) так, чтобы дно полости рта было снижено [Hopkins R.,
1985; Tucker M., 1994].
Удаление нижнечелюстного валика. На нижней челюсти небные валики
обычно располагаются на внутренней поверхности кости соответственно
малым коренным зубам. При наличии зубов они не создают проблем, но в
отсутствие их, особенно при атрофии кости, возможны затруднения при
конструировании протеза, нарушения речи, функции языка при еде. Чаще валики
увеличены с обеих сторон. При необходимости их удаления с обеих сторон
челюсти на уровне премоляров по гребню альвеолярной части делают разрез
длиной 1 — 1,5 см. С большой осторожностью отслаивают слизистую оболочку с
надкостницей, поскольку они часто бывают очень тонкими. В зону небного
валика можно поднадкостнично ввести раствор анестетика, удерживая мягкие
ткани тупым крючком. У верхней части небного валика бором делают желобок,
который потом удаляют при помощи долота и молотка. Сглаживают кость и,
уложив слизистую оболочку и надкостницу, проводят по их поверхности
пальцем, оценивая результат. Рану зашивают узловатыми или непрерывными
швами. В месте операции на подъязычную область на 12—24 ч накладывают
марлевый тампон, пропитанный йодоформной жидкостью, маслом облепихи,
шиповника и др. Это предохраняет от образования гематомы и действует как
противовоспалительное и противоотечное средство.
Оперативные вмешательства при оставлении корней зубов в альвеолах.
Для профилактики атрофии челюстей и сохранения оптимальных условий
для протезирования целесообразно оставлять корни зубов в альвеолах. После
тщательного клинико-рентгенологического обследования
запломбированные зубы и корни спиливают до поверхности кости так, чтобы глубина
кармана у десневого края была не более 3 мм. При наличии более глубокого
кармана и гипертрофии десны производят гингивэктомию. Мобилизуя ткани,
корни закрывают лоскутом слизистой оболочки и надкостницы и зашивают
наглухо. При нехватке тканей и необходимости реконструировать альвеоляр-
394
Рис. 31.3. Наращивание нижней челюсти (схема).
а — со стороны альвеолярной части; б — со стороны основания нижней челюсти.
ную дугу может быть применена пересадка ткани — свободного лоскута
слизистой оболочки.
В отдельных трудных случаях (при атрофии кости и нередко при полной
атрофии альвеолярной дуги и прилежащей базальной кости вследствие
потери зубов, ношения зубных протезов, общих заболеваний и др.) выполняют
более прогрессивные оперативные вмешательства.
Операция формирования высокой и широкой альвеолярной дуги. При
достаточной высоте и недостаточной ширине альвеолярной дуги, а также при
более глубоких нарушениях ее (наличие острого края, полного отсутствия
дуги до основания тела челюсти вследствие значительной атрофии последней)
выполняют сложные костно-пластические операции. Чаще производят
пластику аутокостью фрагментов челюстей или гребешком подвздошной кости,
ребром. Эти операции разработали в 50—60-х годах Н. М. Михельсон A945),
Ф. М. Хитров A945), Е. В. Грузкова A949), Л. М. Обухова A952), В. Д.
Кабаков A963), J. Lee и D. Downton A958), G. Howe A963), P. Boune и D. Cooksly
A965). В дальнейшем методики операций были усовершенствованы.
Широкое применение получила аллогенная кость благодаря исследованиям и
внедрению их результатов в клиническую практику Н. Н. Бажановым и соавт.
A972), Н. А. Плотниковым A969, 1979), А. Л. Никитиным A978), П. Г. Сысо-
лятиным A989), В. М. Безруковым A994), М. Bell и P. Barron A980), Μ. Block
A991), P. Gullane A991), Μ. Urken A991), Μ. Schusterman A992), W. Shockley
и Μ. Weissler A992), Ε. Keller A993). В последние годы высокую и широкую
альвеолярную дугу формируют, используя биоматериалы.
Наращивание нижней челюсти. Можно производить аутотранспланта-
том из ребра или гребешка подвздошной кости. Один из двух фрагментов
ауторебра длиной до 15 см укладывают на поверхность кости, придавая ему
форму зубной дуги, другой измельчают и обкладывают его частицами пер-
395
вый. Трансплантат фиксируют к остаточной кости нижней челюсти,
восполняя альвеолярную ее часть и закрепляют трансплантат окружающими
швами проволокой. Этот метод сложен. Перестройка кости занимает
длительное время до проведения функционального протезирования (рис.
31.3, а).
Опасность перелома нижней челюсти при значительной ее атрофии
делает иногда необходимым костную пластику со стороны ее основания. Ау-
тотрансплантат гребешка подвздошной кости фиксируют костным швом
проволокой или мини-пластинами и штифтами (рис. 31.3, б). Вместе с тем
эта методика, хотя и способствует предупреждению перелома нижней
челюсти, не улучшает условия для протезирования [Forneca R., Davis W.,
1993].
396
Рис. 31.5. Увеличение высоты и ширины альвеолярной дуги (схема).
а, б — нижней челюсти; в — верхней челюсти; г — реконструкция альвеолярного отростка и
поднятие верхнечелюстной пазухи: / — линия разреза мягких тканей; 2 — положение пазухи; 3 —
распатор для отделения слизистой оболочки от кости; 4— реконструкция альвеолярного отростка
и поднятие пазухи гидроксилапатитом; 5— шприц для введения биоматериала.
Описаны различные методики пластики нижней челюсти. По одной из них
нижнюю челюсть распиливают так, чтобы оральная ее часть осталась с
прилежащими тканями подъязычной области, а вестибулярная опустилась вниз.
Оставшееся слизисто-поднадкостничное пространство заполняют гидроксилапа-
титом, измельченной аутокостью гребешка подвздошной кости (рис. 31.4, а, б).
Увеличить нижнюю челюсть можно путем горизонтального распила кости,
поднятия верхнего фрагмента ее вверх и заполнения среднего пространства
измельченной аутокостью, аллокостью, гидроксилапатитом (рис. 31.4, в).
Наиболее простым методом наращивания кости является использование
гидроксилапатита. При значительной атрофии альвеолярной части нижней
челюсти делают симметричные разрезы слизистой оболочки по дуге
соответственно клыку или первому премоляру до кости. Создают поднадкост-
ничный туннель до ветви челюсти, который заполняют гидроксилапатитом
в таком количестве, чтобы обеспечить желаемые высоту, ширину и
конфигурацию альвеолярной части и дуги. Раны зашивают узловатыми швами
(рис. 31.5). Для сохранения формы альвеолярной части и формирования
397
Рис. 31.6. Остеотомия на верхней челюсти и пластика ауторебром (схема).
а — линия остеотомии по Ле Фор III; б— фиксация костного трансплантата металлической
проволокой.
преддверия полости рта рекомендуют ношение шины в течение 8—10 дней
после операции.
Проста и эффективна операция наращивания верхней челюсти при
помощи гидроксилапатита. Методика проведения ее такая же, как при пластике
гидроксилапатитом на нижней челюсти. Делают только один разрез по средней
линии альвеолярной дуги. Поднадкостничный туннель создают по передней
поверхности верхней челюсти. После введения в него достаточного количества
материала, формирования альвеолярного отростка достаточной высоты и
ширины (рис. 31.5, в) на 7—8 дней надевают шину и укрепляют ее проволочным
подвешиванием или при помощи небного шурупа. Для этого можно
использовать старый протез, приспособив его к новой форме альвеолярного отростка
[Block Μ., Goles Т., 1992; Block M., Kent J., 1993]. Увеличение альвеолярного
отростка верхней челюсти можно производить одновременно с поднятием
верхнечелюстной пазухи с помощью гидроксилапатата (рис. 31.5, г).
Наращивание верхней челюсти требуется не так часто, как нижней.
Однако при большой атрофии кости и в отсутствие адекватной формы небного
свода производят увеличение ее альвеолярного отростка. Можно
использовать аутотрансплантат из ребра. Эта операция аналогична таковой при
наращивании нижней челюсти: производят отсечение (остеотомию)
альвеолярного отростка по Ле Фор III и интерпозицию этого участка вниз, слизисто-
поднадкостное пространство заполняют измельченной аутогенной костью
(гребешок подвздошной кости или ребро). Трансплантат фиксируют на теле
челюсти и скуловой кости металлической проволокой, винтами,
мини-пластинами с винтами (рис. 31.6). Однако после этих операций наблюдаются
случаи послеоперационной резорбции кости и возникает необходимость в
повторной операции. В этих случаях больной не может долгое время
пользоваться протезом.
После атрофии альвеолярного отростка верхней челюсти, особенно при
недостаточной площади опоры зубного протеза в дистальной области,
производят пластику бугра верхней челюсти. Откинув слизисто-надкостичный
лоскут по альвеолярной дуге до верхней точки крылонебной складки,
обнажают бугор верхней челюсти, остеотомом отделяют лишнюю часть
латеральной пластинки крыловидного отростка и смещают ее кзади вместе с
крыловидным крючком. В образовавшееся углубление погружают конец лоскута.
398
Рис. 31.7. Остеотомия альвеолярных сегментов (схема).
а — линия распила кости и направления перемещения костного сегмента; б— положение костного
сегмента.
Раневую поверхность покрывают повязкой, смоченной йодоформной
жидкостью. Рана заживает вторичным натяжением. В результате этого создаются
условия для наилучшей фиксации зубного протеза [Ticker M., 1994].
Операция на альвеолярных сегментах. В отсутствие ряда зубов нередко
создается нехватка места для зубов-антагонистов. В таких случаях показана
остеотомия сегмента с перемещением его в нужном направлении. План
операции составляют на основании анализа клинических и рентгенологических
данных, а также моделей. На последних отмечают анатомические и
математические параметры операции. На моделях и в окклюдаторе ортопед
определяет задачу вмешательства. После рассечения слизистой оболочки и
надкостницы, отступя в стороны от места остеотомии, специальными пилками
остеотомируют зубочелюстной сегмент, ставят его в нужное положение и
фиксируют костным швом, винтами (рис. 31.7). Пространство,
образовавшееся между зубочелюстным сегментом и телом челюсти, заполняют гид-
роксилапатитом или другим биоматериалом. Слизисто-надкостничный
лоскут укладывают на место и фиксируют узловатыми швами [Shockley W.,
Weissler M., 1992].
Коррекцию костных деформаций беззубых челюстей проводят по
правилам остеотомии. Методика последней зависит от характера деформации и
планирования адекватного протезирования.
31.2. Операции на мягких тканях полости рта
После удаления зубов нередко происходят изменения мягких тканей.
Встречаются также врожденные нарушения отдельных анатомических
образований. Все это создает трудности для протезирования и требует хирургического
лечения. Наличие избытка мягких тканей всегда должно оцениваться с точки
зрения использования ее для увеличения кости.
Операции при укороченной уздечке языка. При протезировании иногда
требуется удлинить уздечку языка. Для этого делают длинный разрез через
уздечку, формируют два треугольных лоскута, которые взаимно перемещают и
фиксируют тонким кетгутом или синтетической нитью [Мухин М. В., 1973;
Александров Н. М., Балин В. В., 1998; Obwegeser Η., 1969; Forseca R., Davis Ν.,
1993]. Во время операции учитывают расположение подъязычных сосочков
во избежание их травмирования.
399
Рис. 31.8. Удаление уздечки губы перемещением встречных треугольных слизистых
лоскутов (схема).
а — линии рассечения уздечки и формирования треугольных лоскутов; б — перемещение лоскутов.
При значительном укорочении уздечки языка более целесообразно ее
горизонтальное рассечение. При полном освобождении языка рана
приобретает вид ромба, что позволяет, используя эластичность тканей, наложить
швы, сблизив края раны по вертикали [Мухин М. В., 1973; Ticker M., 1984;
Hopkins К., 1985].
При атрофии альвеолярной части нижней челюсти уздечка часто
прикрепляется прямо к дуге. В таких случаях ее иссекают углообразным
разрезом, обращенным вершиной к альвеолярной части нижней челюсти, а лоскут
на нижней поверхности языка отслаивают до полного освобождения.
Образовавшуюся рану зашивают наглухо.
Операции при укороченной уздечке губы. У пациентов с укороченной
уздечкой верхней и нижней губ фиксация зубных протезов затруднена.
Хирургическая тактика может быть различной. В случае прикрепления уздечки
губы к альвеолярной дуге широким основанием показано ее иссечение в этом
участке по эллипсу к периосту. Слизистую оболочку подшивают к периосту,
желательно на всю глубину десневой борозды. Образовавшуюся рану
ушивают по всей длине вместе с надкостницей.
Для удлинения уздечки губы производят пластику встречными
треугольными лоскутами так же, как при аналогичной операции на уздечке языка
(рис. 31.8). Удлинение уздечки при ее широком основании у альвеолярной
дуги, воспалительных изменениях вследствие травмы краем протеза
целесообразно путем углообразно сходящихся разрезов от десневой борозды к
альвеолярной части нижней челюсти. Отслаивают треугольный лоскут по
поверхности альвеолярного отростка и подшивают его концы к надкостнице на
уровне десневой борозды. Образовавшаяся раневая поверхность заживает
вторичным натяжением (рис. 31.9).
Рис. 31.9. Иссечение уздечки губы (схема).
а — линия разреза; б — подшивание слизистого лоскута к периосту у свода десневой борозды
400
Устранение мышечных и слизистых тяжей преддверия полости рта.
Одиночные рубцовые тяжи, складки слизистой оболочки преддверия полости рта
удлиняют по описанной выше методике: рассекают тяжи и складки, образуют
симметричные встречные треугольные лоскуты, мобилизуют их и перемещают.
При обширной зоне Рубцовых стяжений преддверия полости рта оперативное
вмешательство для создания достаточного свода заключается в рассечении
или иссечении их с некоторым увеличением величины свода преддверия
полости рта. На образовавшуюся раневую поверхность укладывают
расщепленный лоскут кожи размером 1,5—2 см, взятый в области живота, и фиксируют
его на вкладыше. Последний фиксируют шелком к краям раны слизистой
оболочки. Дополнительно можно накладывать несколько матрацных швов из
синтетической нити поверх вкладыша и вокруг тела нижней челюсти.
Вкладыш удаляют на 7—11-е сутки, а формирующий протез надевают в одних
случаях сразу, в других — через 4—5 сут. В последние годы производят пересадку
свободного лоскута слизистой оболочки, взятого с неба.
Удаление избытка воспалительно измененной ткани. При ношении плохо
фиксированных зубных протезов, их неадекватности нередко на
альвеолярной дуге, десневой борозде происходит изменение слизистой оболочки в виде
фиброзных разрастаний. При коррекции зубного протеза эти изменения
можно устранить. В других случаях необходима операция иссечения
патологической ткани. Наиболее простым методом является электрокоагуляция
или лазерное иссечение с последующим заживлением раны вторичным
натяжением под тампоном. При значительных размерах участка избыточной
воспаленной ткани проводят обычное иссечение до надкостницы с
ушиванием раны узловатым или непрерывным швом. При нехватке тканей для
ушивания раны без натяжения ее края пришивают к надкостнице;
образовавшийся дефект заживает вторичным натяжением. При всех
хирургических манипуляциях нужно предусматривать условия для будущего
протезирования, в том числе образование десневой борозды достаточной глубины.
Этому может способствовать фиксация формирующей шины или протеза на
мягкой подкладке, которые снимают при перевязках или гигиенических
процедурах.
Более сложно удаление папилломатозных разрастаний слизистой
оболочки твердого неба. Такие изменения обычно возникают при травме
зубными протезами, недостаточной гигиене полости рта, грибковой инфекции.
В случаях неэффективности консервативного лечения и коррекции протеза
необходимо оперативное вмешательство. Оно может заключаться в коагуляции,
лазерном иссечении, обработке жидким азотом, при помощи бора, а также
иссечении патологических тканей до надкостницы скальпелем. Обязательно
патологоанатомическое исследование тканей. При закрывании раневой
поверхности повязкой и защитной пластинкой (лучше на мягкой подкладке)
создаются благоприятные условия для заживления раны вторичным
натяжением, которое происходит около 4 нед.
Уменьшение бугристости слизистой оболочки и надкостницы, покрьюающей
альвеолярный отросток верхней челюсти и альвеолярную часть нижней челюсти.
Производят путем эллипсообразных сходящихся разрезов, окаймляющих
патологический участок. Мобилизуют слизисто-надкостничные лоскуты с
вестибулярной и оральной стороны до соприкосновения без натяжения, после чего
рану зашивают узловатыми или непрерывными швами. Если при сближении
краев раны остается участок обнаженной кости, то его прикрывают
марлевым тампоном. Рана заживает вторичным натяжением.
Уменьшение объема тканей ретромолярной области. В этой области
нередко наблюдается избыток ткани, чаще вследствие ее гипертрофии. Избыток
401
26-1263
Рис. 31.10. Иссечение избытка тканей по альвеолярной дуге верхней челюсти (схема).
а — линия иссечения тканей; б — линии иссечения тканей в поперечном разрезе; в —
альвеолярная дуга; г — наложение швов.
тканей удаляют эллипсообразным разрезом, истончают ткани по краям
дефекта и рану ушивают узловатыми или непрерывными швами.
Удаление избытка мягкой ткани в дистальном отделе неба. В дистальной
части небного свода нередко наблюдается избыток мягких тканей, что
обусловливает сужение его и создает трудности при протезировании. Во время
операции возможно повреждение передней небной артерии, петель
крыловидного венозного сплетения, поэтому рекомендуется неглубокое иссечение
тканей. Избыток мягких тканей иссекают острым тонким скальпелем по
касательной поверхности на глубину слизистой оболочки и подслизистого
слоя. Края раны сближают, накладывают швы и надевают на раневую
поверхность защитную пластинку.
Удаление избытка мягких тканей альвеолярной дуги. При атрофии кости,
ношении неадекватно фиксированных зубных протезов создается избыток
мягких тканей, не имеющих костной опоры. Если эта ткань не может быть
использована для увеличения высоты и ширины альвеолярного отростка или
альвеолярной части, то ее удаляют. Проводят два параллельных, сходящихся
на концах разреза до надкостницы, по ходу альвеолярной дуги, а рану
зашивают обычным способом (рис. 31.10). Нередко избыток мягких тканей имеет
402
Рис. 31.11. Иссечение избыточной подвижной
мягкой ткани по альвеолярной дуге нижней
челюсти (схема).
а — линии рассечения тканей; б — линия иссечения
тканей в поперечном разрезе.
форму "шнура", который излишне
подвижен. В таких случаях избыток мягких
тканей иссекают двумя эллипсообразными
сходящимися разрезами (рис. 31.11). При
Рубцовых изменениях тканей их иссекают
вместе с надкостницей. Необходимо
отметить, что такое иссечение часто приводит к
более выраженному изъяну преддверия
полости рта.
Пластика преддверия полости рта.
Эффективны оперативные вмешательства на
мягкой ткани для увеличения высоты
альвеолярной дуги нижней челюсти. Одним из
них является углубление преддверия
полости рта путем пластики лоскутом слизистой
оболочки, взятым с нижней поверхности
языка. Операция показана при
достаточной высоте центрального отдела
альвеолярной части нижней челюсти (не менее 15 мм),
достаточной глубине язычной стороны, но
недостаточной глубине преддверия
полости рта, в том числе за счет присоединения ѵ~
мышц и тяжей слизистой оболочки. Разре- б ^£^-^---
зом длиной 3—4 см параллельно альвеоляр- ^^1-^^ -
ной дуге формируют два лоскута слизистой
оболочки: один в области нижней губы,
другой по наружной поверхности альвеолярного отростка. Хорошо отсепаро-
ванный лоскут с альвеолярного отростка (на ножке) перемещают на участок
дефекта губы, лоскут с губы подшивают под десневой бороздой, углубляя
свод преддверия рта, а на открытую переднюю поверхность альвеолярного
отростка перекидывают лоскут, выкроенный на нижней поверхности языка,
и накладывают швы. Ткани фиксируют специально изготовленной шиной
или используют при этом старый протез, который корригируют для
формирования максимально глубокого преддверия полости рта. Протез должен
иметь мягкую подкладку. Через 3—4 нед можно приступать к
ортопедическому лечению.
При значительной атрофии альвеолярной части нижней челюсти, когда
преддверие полости рта, альвеолярная дуга и ткани с язычной стороны
находятся в одной плоскости и нет условий для фиксации протеза, используют
методику Обвегезера в различных модификациях. Операция заключается в
увеличении преддверия полости рта. Ширина альвеолярной части нижней
челюсти должна быть не менее 15 мм. Вначале заготавливают кожный лоскут
толщиной не менее 4 мм, взяв его с участка, где волосы отсутствуют. Делают
разрез по альвеолярной дуге, выкраивают слизисто-надкостничный лоскут
вместе с мягкими тканями и мышцами (обычно отделяют всю челюстно-
подъязычную и верхнюю часть подбородочно-язычной мышцы). Отсепаро-
403
26*
вывают его по вестибулярной и язычной поверхностям челюсти и подшивают
у ее основания. На обнаженный участок челюсти укладывают кожный
трансплантат, который укрепляют окружающими челюсть швами и удерживают
шиной. Следует обращать внимание на то, чтобы края шины достигали всех
участков свода преддверия нижней челюсти. Через 7 дней снимают
окружающие швы. Перевязки делают через день, гигиенические процедуры проводят
ежедневно. Протезирование начинают через 3—4 нед.
Пластика подслизистой ткани преддверия полости рта. Чтобы создать
необходимые условия для фиксации протеза при значительной атрофии
альвеолярного отростка и наличии тела верхней челюсти производят пластику
преддверия полости рта подслизистой тканью [Obwegeser Η., 1969].
Обязательным условием такой операции является достаточное количество
слизистой оболочки на верхней губе и в преддверии полости рта. В центре
преддверия делают вертикальный разрез слизистой оболочки и отделяют ее от
подслизистой ткани. Затем рассекают надкостницу в центре и по наружной
поверхности ее формируют поднадкостничный туннель (соответственно
туннелям по обе стороны преддверия полости рта). Иссекают подслизистую
ткань или перемещают ее вверх на ножке. Надевают на челюсть шину или
старый корригированный протез, укрепляя ее (его) небным шурупом или
путем подвешивания проволочными швами. Необходимо следить, чтобы была
хорошо зафиксирована глубина преддверия полости рта. Через 3 нед после
заживления раны приступают к протезированию.
Пластика преддверия верхней челюсти слизистым или кожными
трансплантатами. В тех случаях, когда преддверие полости рта недостаточно для
адекватной фиксации зубного протеза, недостает слизистой оболочки на
верхней губе, а пластика подслизистой тканью может привести к укорочению губы,
показана пластика свободным расщепленным кожным трансплантатом,
который помещают в рану, сформированную по своду преддверия полости рта.
Для увеличения преддверия полости рта в сформированное ложе может быть
помещен свободный лоскут в форме подковы, взятый с неба. Можно также
использовать лоскут на ножке с верхней губы. В таких случаях остается
непокрытым участок периоста, который заживает вторичным натяжением. Во
всех случаях накладывают шину или протез, которые фиксируют путем
подвешивания или с помощью небного винта. Через 4 нед приступают к
протезированию. При третьем способе пластики послеоперационный период
более длительный, поэтому протезирование производят в более поздние сроки.
Перемещение подбородочного нерва. При значительной атрофии нижней
челюсти сосудисто-нервный пучок, выходящий из подбородочного
отверстия, может находиться в области зубной дуги. В таких случаях ношение
зубного протеза часто вызывает боль. Если консервативные меры, коррекция
протеза не дают улучшения, то показано перемещение подбородочного нерва.
Разрез длиной 4 см делают по альвеолярной дуге, а иногда в переднем отделе
(вертикальный). Откидывают углообразной формы слизисто-надкостничный
лоскут. Отсепаровывают сосудисто-нервный пучок. При удалении кости в
вертикальном направлении нерв смещают вниз и укладывают в созданную
борозду. Нерв прикрывают удаленной кортикальной пластинкой кости. Для
прикрытия нерва можно пользоваться биоматериалами [Rosenqust В., 1992].
404
СПИСОК ЛИТЕРАТУРЫ
Васильев Г. А. Хирургия полости рта с курсом челюстно-лицевой травматологии. —
М.: Медицина, 1973.
Мухин М. В. Оперативная хирургия челюстно-лицевой области. — Л.: Медицина,
1963. - 359 с.
Оперативная хирургия челюстно-лицевой области/Под ред. В. В. Балина. — СПб, 1998.
Робустова Т. Г. Хирургическая подготовка полости рта к протезированию //
Хирургическая стоматология. — М., 1996. — С. 666.
Старобинский И. М. Операция на альвеолярных отростках // Руководство по
хирургической стоматологии. — М.: Медицина, 1972. — С. 73—117.
Archer Η. Oral surgery for dental prothesis // Oral and maxillofacial Surgery. — Toronto,
1975. - P. 438-476.
Davis H. Preprosthetic surgery// Forseca K., Davis H. Reconstructive preprosthetic oral and
maxillofacial surgery. — London: Mosby, 1995. — P. 733—742.
Georgiade G.t Rieflcohl R., Levin L. Plastic, maxillofacial and reconstructive Surgery. — New
York: Williams, Wilkins, 1998. - P. 670.
Kent J., Jarcum M. Ridge augmentation procedure with hydroxylapatite // Forseca K., Davis
H. Reconstructive preprosthetic oral and maxillofacial Surgery. — New York: Mosby,
1995. - P. 853-933.
Reitzin M. Autogenous bone for the reconstruction of the dentulous maxilla // Forseca K.,
Davis H. Reconstructive preprosthetic oral and maxillofacial Surgery. — New York:
Mosby, 1995. - P. 417.
Slaghter Τ Soft-tissue reconstruction // Forseca K., Davis H. Reconstructive preprosthetic
oral and maxillofacial Surgery. — New York: Mosby, 1995. — P. 498—510.
Starshak T. Corrective soft tissue surgery // Starshak Т., Sannders B. Preprosthetic oral and
maxillofacial Surgery. — New York: Mosby, 1980.
Tucker M. Advanced preprosthetic surgery // Peterson L. Contemporary oral and
maxillofacial Surgery. — New York: Mosby, 1994. — P. 331.
Tucker M. Basic preprosthetic surgery // Peterson L. Contemporary oral and maxillofacial
Surgery. — New York: Mosby, 1994. — P. 291.
Глава 32
ЗУБНАЯ
И ЧЕЛЮСТНО-ЛИЦЕВАЯ
ИМПЛАНТАЦИЯ
По ранее принятой Международной классификации имплантация относится
к аллотрансплантации, по новой — к эксплантации. В то же время в
зарубежной и отечественной литературе пользуются термином "имплантация",
особенно в отношении зубных конструкций.
В хирургической стоматологии принято различать зубную и челюстно-
лицевую имплантацию.
Развитие зубной имплантации связано с хирургическим разделом
зубоврачевания и челюстно-лицевой хирургией. С древних времен людей волновал
вопрос о замене утраченных или плохих зубов. Попытки вживления
искусственных зубов делались еще в древности, о чем свидетельствуют импланта-
ционные конструкции, найденные при раскопках в Египте, Центральной
Америке, Китае и других странах. По данным M.Arnaudow и U. Gerlich A972), в
1100 г. Spaniard Alabusasim первый выдвинул как медицинскую проблему рет-
ротрансплантацию (реплантацию) и трансплантацию зубов. Однако до
XVII—XIX вв. это не находило практического воплощения, а широкое
распространение таких инфекционных заболеваний, как сифилис, туберкулез, и
возможность их передачи при трансплантации зубов стали причиной критики
этого направления.
В конце XIX в. аллотрансплантация зубных конструкций получила
научную основу. Пионерами этого направления являются I. Magillo, Η. Edmunds
A886, 1887), Η. Η. Знаменский A891), Α.Hartmann A891), R. Payne A898). В
качестве материала они использовали золото, серебро, платину и другие
металлы, а также фарфор. Конструкции имели вид штифтов, капсул, трубок,
"корзин". К прообразам современного винтового имплантата следует
относить конструкции R. Adams и A. Strock. Первый в 1937 г. предложил имплан-
тат с винтовой нарезкой на его поверхности, а второй в 1939 г. изобрел им-
плантат из кобальта, хрома и молибдена. Большой вклад в развитие зубной
имплантации сделал P. Schercheve A940).
В России одонтопластика, в том числе реплантация, трансплантация и
аллотрансплантация зубов начали активно развиваться в 50-х годах. Это
предопределило попытки использовать пластмассу [Варес Э. Я., 1955; Брахман Г. Б.,
1956] и хромокобальтовые сплавы [Мудрый С. П., 1956] в качестве зубных и
челюстных имплантатов. В тот же период I. Scialom A952), L. Linkow A954),
S. Tramonte A965), G. Murratori A969), P. Paskialini A969) и др.
разрабатывали разнообразные конструкции зубных имплантатов. Однако многие
разработки энтузиастов не получали официальной поддержки и потому не на-
406
ходили широкого применения. В то же время эти новаторские работы
послужили основанием для создания двух видов внутрикостных имплантатов
(плоской формы и круглых в форме корня зуба) и внедрения имплантатов в
практику стоматологии.
Несмотря на значительный опыт зубной имплантации, накопленный в
60—70-х годах, участники Гарвардской конференции A978), специально
обсуждавшие этот метод лечения, посчитали необходимым установить для него
ряд ограничений. Только в 1987 г. Американским институтом здоровья и в
1988 г. на Международной конференции по имплантации, проходившей во
Франкфурте-на-Майне (Германия), методы зубной имплантации были
полностью признаны и одобрены.
Американскими и европейскими исследователями и клиницистами
накоплен 25—30-летний опыт зубной имплантации с результатами,
прослеженными в течение 10—15 лет и убедительно свидетельствующими об
эффективности этого метода лечения.
Различают зубные внутрикостные (эндодонто-эндооссальные и эндоос-
сальные), подслизистые, поднадкостничные, чрескостные и комбинированные
имплантаты. По функциям в зубочелюстной системе лицевом и мозговом
черепе имплантаты делятся на замещающие, опорные, опорно-замещающие, с
амортизационной системой или без нее. По биосовместимости материалы
могут быть биотолерантными (нержавеющая сталь, КХС), биоинертными (аллю-
минийоксидная керамика, углерод, титан, титана никелид) и биоактивными
(трикальцийфосфат, гидроксилапатит, стеклокерамика).
32.1. Внутрикостные зубные имплантаты
В зубной имплантологии чаще всего применяются внутрикостные имплантаты
плоской и круглой формы. Плоский имплантат был предложен в 1967 г.
L. Linkow. Разнообразные его варианты получили широкое распространение,
особенно при лечении пациентов с узким альвеолярным отростком. Р. Вгапе-
mark A967) разработал винтовой имплантат в форме корня зуба. Обе эти
новации стали прообразами всех последующих, применяющихся в настоящее
время видов зубных имплантатов. В качестве материала для них наилучшими
признаны титан и его сплавы, цирконий и керамика. У титана и его сплавов
отмечены антикоррозийные свойства, отсутствие изнашиваемости и
растворимости в тканях, высокая прочность. Большое значение имеет образование
окисного слоя на поверхности имплантатов из титана и его сплавов. Этот
слой, адекватно взаимодействуя с тканевыми жидкостями, способствует
интеграции титана с тканями. За рубежом на основе титана и его сплавов
производится много конструкций имплантатов, из которых в зубной
имплантологии наиболее широко применяются имплантаты системы Linkow,
Branemark, Bonefit, IMZ, Calsitec, Core-Vent, Frialit, Steri-Oss, Misch и др.
В нашей стране быстрое развитие дентальной имплантации началось в
80-х годах. Разработанные А. С. Черникисом, О. П. Суровым и др. плоские
имплантаты в 1983 г. были переданы для клинических испытаний в ЦНИИС
(В. М. Безруков, А. И. Матвеева и др.) и в ММСИ (Т. Г. Робустова, А. И.
Ушаков и др.). Полученные положительные результаты и изучение клинико-тео-
ретических вопросов при использовании плоских имплантатов нашли
отражение в диссертационных работах П. В. Балуды A990), В. А. Вигдерович
A991), Абу-Асали-Эяда A992), А. И. Сидельникова A992), А. И. Жусева
A995) и др. Официальное утверждение плоских конструкций, разработанных
В. М. Безруковым, О. Н. Суровым и А. С. Черникис и выпуск их ВНИИМТ
407
A986), а также монография О. Η. Сурова A994), способствовали внедрению
идей плоских имплантатов в практику стоматологических клиник и
поликлиник.
На основе концепции L. Linkow и P. Braiiemark в России приняты к
применению плоские имплантаты — ВНИИМТ, КВС-1 (В. Н. Лясников),
круглые в форме корня зуба — "Контраст" (А. С. Массарский, О. Н. Суров),
плоские, цилиндрические, винтовые, в том числе покрытые гидроксилапатитом
(КИВСТ—СИТУ 01) [Лясников В. Н. и др., 1996], а также запатентованы
винтовые (фирма "Лико"), винтовые из циркония (фирма "Дива"),
цилиндрические ("Комет") и плоские (МЭТЭМ) имплантаты, ряд оригинальных
конструкций фирмы "Radix".
В развитии зубной имплантации важную роль сыграли исследования,
проведенные P. Branemark, Т. Albrektsson, G. Heimke, J. Osborn, D. Buser, G. Zarb.
Они были связаны с применением в зубной имплантации титана и его сплавов,
исследованиями патоморфоза интеграции имплантатов, использованием алло-
пластических материалов на основе гидроксилапатита, коллагена, ауто- и алло-
кости при имплантации, а также метода направленной регенерации кости с
помощью мембран. Оригинальные исследования В. И. Итина и соавт. A975,
1985) и В. Э. Гюнтера и соавт. A979, 1989) никелид-титанового сплава
позволили М. 3. Миргазизову и соавт. A983, 1993) разработать зубные
имплантаты, в том числе с амортизационной системой.
Утвержден ряд авторских заявок на оригинальные имплантаты,
разработанные на стоматологических факультетах Московского,
Санкт-Петербургского, Пермского, Новосибирского и других медицинских институтов
России [Амарханов А. Г., 1986; Егорова И. П., 1986; Воробьев В. П., Дады-
кин В. П., Дадыкина В. Ф., 1987; Матвеева А. И., Вигдерович В. Α., 1988;
Суров О. Н., 1989; Трофимов В. В., 1989; Ушаков А. И., 1997; Иванов С. Ю.,
1998, и др.], а также созданные специалистами одноименных институтов и
университетов Республик Беларусь, Украина и других стран ближнего
зарубежья [Параскевич В., 1992, 1997].
Различными видами имплантатов, разными методиками операций,
функциональными нагрузками в зубных протезах создаются определенные
морфологические изменения в тканях челюсти, периосте и слизистой оболочке
полости рта. Характер сращения имплантата в тканях зависит от ряда факторов:
материала, формы, нагрузки в зубных протезах, особенностей
функционирования органов и систем организма, а также гигиены полости рта.
Морфологические исследования L. Linkow A967), R. Adell и соавт.
A981), Т. Albrektsson A984) и др. показали, что приживление внутрикостных
имплантатов может быть как фиброзным, так и костным, а также, по данным
С. Weiss A987), фиброкостным. Вместе с тем в участках соединения
имплантата и кости даже в случае остеоинтеграции, образуется зона аморфного
вещества, состоящего из частиц протео- и гликозаминогликанов размером от 10
до 300 нм [Buser D., 1990, 1995].
Одновременно с процессами, происходящими при имплантации в
кости, изменяются слизистая оболочка и надкостница в зоне, прилегающей к
имплантату и создающей механический барьер между ним и полостью рта.
От этого барьера во многом зависит функционирование имплантата.
Сохранность такого тканевого замка обусловливается хорошей гигиеной и
предотвращением образования зубной бляшки.
Интеграция имплантата с костью и мягкими тканями повышается при
напылении на его тело титана, гидроксилапатита, при наличии на теле
отверстий, желобков, прорезей, а также при высокой полировке его шейки. Такой
же эффект дает использование аллопластических материалов, которые воспол-
408
няют недостающую кость, устраняют ее дефекты, способствуют остеогенезу
и снижают выраженность резорбции после постановки имплантатов.
32.1.1. Показания и противопоказания к зубной имплантации
Показанием к имплантации является невозможность создать
функциональный и эстетический эффект зубочелюстной системы традиционными
методами ортопедического лечения. Показания определяются также общим
состоянием организма, в том числе полости рта — зубов и слизистой оболочки.
Для этого перед имплантацией проводят обследование пациента, оценивая
функциональное состояние организма с учетом возраста и сохранности систем
жизнеобеспечения. В имплантологии разработаны общемедицинские
показания к зубной имплантации и методы подготовки пациентов с учетом
сопутствующих заболеваний [Misch С, 1993]. Вместе с тем приводятся достаточно
широкие показания к имплантации, что не всегда оправдано. Т. Г. Робустовой
A987, 1996) установлены показания к имплантации с учетом сопутствующих
болезней.
Методом контроля обследования общими специалистами и стоматологами
служат иммунологические исследования, в том числе иммунограмма. Именно
с точки зрения состояния иммунной системы оценивают определенные группы
общих заболеваний, при которых происходят нарушения или дефекты
иммунитета и определяются показания и противопоказания к имплантации, а в
отдельных случаях подготовка к ней. Абсолютным противопоказанием к
имплантации являются заболевания, вызывающие аллергический, аутоиммунный,
иммунопролиферативный синдромы, и наследственные нарушения функций
иммунной системы. Инфекционный синдром также служит
противопоказанием к имплантации, но с учетом особенностей заболевания, после санации
инфекционного очага или очагов и предимплантационной подготовки
операция может быть разрешена. Особое внимание уделяют санации одонтоген-
ных очагов и ЛОР-органов.
Не рекомендуется производить имплантацию пациентам, употребляющим
наркотики, алкоголь, и злостным курильщикам. Особого внимания требуют
пациенты с системными и возрастными заболеваниями костей, женщины в
предклимактерическом и климактерическом периодах, когда наблюдается
остеопороз костей, в том числе челюстей. Важно изучить психическое
состояние больного, его мотивацию на имплантацию, а также возможность
хорошей адаптации к хирургическому и ортопедическому этапам лечения.
Т. Г. Робустова и А. И. Матвеева A992, 1996) разработали и утвердили
медико-юридические документы, которые должны оформляться перед
хирургическим этапом зубной имплантации и последующим протезированием.
Лечащий врач должен знать основные законы Российской Федерации,
относящиеся к правам пациента, и строго выполнять их. Пациента обязательно
информируют о положительных и отрицательных сторонах имплантации,
сообщают ему об альтернативных методах лечения. Имплантацию производят
после получения от пациента письменного подтверждения о согласии. В этом
документе, который является договором между пациентом и врачом,
указываются хирургические и ортопедические этапы лечения, их сроки и
особенности для данного пациента, фамилии врачей, ответственных за
хирургический и ортопедический этапы лечения. В документе также рассматриваются
экономические вопросы, связанные с лечением. Пациент должен быть
поставлен в известность о возможных побочных явлениях и осложнениях на
всех этапах лечения.
409
32.1.2. Местная диагностика
Перед имплантацией пациента обследуют по правилам, принятым в
стоматологии, в том числе хирург и ортопед.
Несмотря на желание пациента иметь протезы на зубных имплантатах и
положительную мотивацию этого, всегда уточняют возможную связь местных
жалоб с общими заболеваниями и системной патологией. Особое внимание
обращают на жалобы, связанные с нарушениями слюноотделения, болевыми
ощущениями при открывании рта и жевании, жалобами на кровоточивость
десен, нарушение чувствительности слизистой оболочки полости рта и др.
Уточняют анамнез заболеваний зубов и слизистой оболочки полости рта,
выясняют, какое лечение проходил пациент и каковы были результаты.
Внимание обращают на причину потери зубов и на то, как проходило их удаление,
на развитие последующих осложнений и на их последствия.
Для зубной имплантации важную роль играет установление изменений
конфигурации лица: значительная выраженность естественных складок лица,
западение ротовой щели или излишняя складчатость губ, диспропорция в
соотношении челюстей. Эстетические недостатки устраняют или уменьшают
при правильном выборе и адекватном применении имплантационных систем.
Однако выявленные изменения могут носить и аномальный характер, причем
как во всем организме, так и локализованно в зубочелюстной системе. Такого
рода отклонения учитывают при составлении плана лечения с
использованием имплантатов.
При местном обследовании преддверия полости рта особое внимание
обращают на цвет слизистой оболочки и ее увлажненность, глубину свода
преддверия полости рта, состояние прикрепленной и свободной десны,
выраженность уздечек верхней и нижней губы, наличие складок слизистой
оболочки и мышечных тяжей, а также уровень прикрепления ряда мимических
и других мышц. При осмотре альвеолярной части нижней челюсти с язычной
стороны можно судить о выраженности косой линии и состоянии челюстно-
подъязычных мышц, начинающихся на внутренней поверхности нижней
челюсти. Все это важно потому, что в некоторых случаях перед имплантацией
приходится прибегать к предварительному оперативному вмешательству:
пластике на уздечках языка и губы, рассечению слизистых и мышечных
тяжей, сглаживанию острого края косой линии.
Оценивают соотношение жевательных поверхностей зубов нижней и
верхней челюстей при закрытом рте в центральной окклюзии и вид прикуса.
Большую роль в определении показаний к имплантации играет аномальный
прикус (глубокий, открытый и перекрестный). На постановке имплантатов
отражаются также и физиологические разновидности прикуса (прогения,
прогнатия, бипрогнатия и прямой прикус). Все перечисленные особенности,
в том числе прикуса, должны быть изучены ортопедом с точки зрения
использования имплантатов в качестве опор зубных протезов.
Во время внешнего осмотра и при обследовании преддверия и
собственно полости рта ориентировочно судят о функциональных и эстетических
нарушениях, получают предварительную информацию о количестве кости и
конфигурации альвеолярных отростков, покрывающей их слизистой
оболочке, функции мимических, жевательных мышц, состоянии височно-нижнече-
люстных суставов и окклюзионных взаимоотношениях зубов верхней и
нижней челюстей.
На основании результатов обследования устанавливают показания и
противопоказания к зубной имплантации. Первоначально при клиническом
обследовании можно обнаружить убедительные противопоказания к зубной
410
имплантации в связи с наличием кариозных зубов и заболеваний периодонта,
болезнями пародонта, особенно генерализованными формами пародонтоза,
плохой гигиеной полости рта, а также поражениями слизистой оболочки
полости рта. В одних случаях обнаруженные патологические явления (кариес и
его осложнения, пародонтит, низкая гигиена полости рта) оказываются
относительными противопоказаниями к имплантации и могут исчезнуть после
санации полости рта, в других — остаются абсолютными, как, например,
генерализованный пародонтоз, заболевания слизистой оболочки рта и др.
Зубная имплантация может быть произведена при ортогнатическом или
других разновидностях физиологического прикуса. После детального
исследования стоматологического статуса с точки зрения этапов предстоящего
ортопедического лечения ортопед вместе с хирургом оценивает модели
челюстей в том числе, как рекомендует Н. Spiekermann A995), в окклюдаторе.
Комплексная оценка этих данных позволяет определить условия для
имплантации. В отдельных случаях выявляются скрытые нарушения жевательной
системы, в связи с чем возникают сомнения в целесообразности и
возможности зубной имплантации.
Клиническое обследование всегда дополняют рентгенологическими
данными. Наиболее часто применяют дентальные, панорамные снимки и зоно-
граммы челюстей, ортопантомограммы. В последние годы распространение
получила обычная и компьютерная томография. За рубежом в отдельных
случаях дополнительно к ней проводят магниторезонансное исследование.
Для первичного исследования используют ортопантомографию, которая
предоставляет больше информации о дистальной половине лицевого черепа.
Все эти исследования рекомендуется стандартизировать и проводить в
динамике имплантации [Рабухина Н. А. и др., 1993, 1999]. Все снимки следует
делать при одинаковом положении пациента и обрабатывать их одинаково.
Ортопантограмма дает возможность определить высоту кости и ее
качество, особенности дна верхнечелюстной пазухи и полости носа на верхней
челюсти, положение подбородочных отверстий и нижнечелюстных каналов на
нижней челюсти, а также особенности обеих альвеолярных дуг. Аналогичная
ортопантомограмма с маркировочными шариками определенного размера,
опирающимися на слизистую оболочку альвеолярной дуги и вмонтированными
в шаблоны или акриловую шину, позволяет судить об окклюзионной
плоскости и реальной высоте кости (рис. 32.1) [Misch С, 1993; Spiekerman Η., 1995].
Однако в 20—30 % случаев ортопантография не дает реальных сведений о
размере и качестве кости, расстоянии до канала нижней челюсти,
верхнечелюстных пазух [Shimura Μ. et al., 1990]. В связи с этим дополнительно делают прямые
и боковые панорамные снимки, по которым определяют такие параметры для
имплантации, как адекватная длина имплантата и необходимый его наклон.
Более детальные данные о зубоальвеолярных фрагментах челюстей, полости
носа и околоносовых пазухах получают при компьютерной томографии.
Компьютерная и магнитно-резонансная томография дает точные
изображения в трех измерениях. Определяют объемные и математические данные
о кости, топографию нижнечелюстных каналов и подбородочных отверстий,
верхнечелюстных синусов, а главное, особенности, толщину и качество кости.
Особое диагностическое значение компьютерная томография приобретает
при имплантации у пациентов, лишенных зубов. Томография с
использованием маркировочных шариков, расположенных в местах предстоящей
постановки имплантатов, позволяет судить о пространственном состоянии кости
и правильности выбора метода лечения. Первичная клинико-рентгенологиче-
ская диагностика дает возможность оценить состояние зубочелюстной системы,
подтвердить необходимость постановки имплантатов для устранения функ-
411
Рис. 32.1. Маркировочные шарики для планирования окклюзионных взаимоотношений
при имплантации.
циональных и эстетических нарушений, определить количество, качество и
конфигурацию кости, в которую предполагается поставить имплантаты.
На основании всех этих данных и обследования методами
ортопедической стоматологии, учитывая определенные анатомические особенности
челюстей и процессы, возникающие в костной ткани при утрате зуба или зубов,
степень и характер атрофии кости, ортопед дает окончательное заключение
о показаниях к конструированию зубных протезов с опорой на имплантат
или имплантаты, уточняет необходимое число имплантатов в зависимости от
будущей функциональной нагрузки.
При обследовании следует учитывать особенности строения челюстей и
изменения, произошедшие в них после утери зубов. На верхней челюсти
альвеолярный отросток имеет тонкий слой кортикального вещества, особенно
с вестибулярной стороны, а губчатое вещество отличается рыхлой
структурой. Вместе с тем на скелете верхней челюсти отражается реакция кости на
силы жевания. В. Ю. Курляндский A977) отметил напряжение в кости
верхней челюсти при нагрузке и показал на модели фотоупругости возможность
перемещения ее в зависимости от функционирования разных групп зубов.
U. Lekholm и G. Zarb A992) считают необходимым различать I—IV степени
плотности кости: при I степени кость наиболее плотная, при IV — самая
рыхлая. Эти же авторы альвеолярные гребни классифицируют по формам А, В,
С, D и Ε и диагностируют по цефалометрическим рентгеновским снимкам.
После удаления зубов на верхней челюсти атрофия альвеолярного
отростка наиболее выражена с вестибулярной стороны. Резорбтивные процессы
в альвеолярном отростке особенно усиливаются при потере верхних
центральных зубов — резцов и клыка, захватывая вестибулярную часть альвеол.
При этом небная поверхность остается выпуклой, а вестибулярная становится
плоской. Это отражается на строении альвеолярной дуги ("лезвие ножа").
Такая атрофия кости переднего отдела верхней челюсти обусловливает
вогнутый лицевой профиль и способствует выдвижению нижней челюсти.
412
В теле верхней челюсти располагается пазуха, которая в зависимости от
степени пневматизации может быть пневматической, склеротической и
комбинированной. Дно верхнечелюстной пазухи может находиться в различных
взаимоотношениях с корнями верхних зубов: они могут располагаться около
дна, проникать в нее или не доходить до ее дна.
Антропометрическими исследованиями, проведенными А. С. Ивановым
A991), установлено, что наибольшим является расстояние между дном
верхнечелюстной пазухи и верхушками корней первого малого коренного зуба и в
среднем равно 7,4 мм. Ближе всего к пазухе расположен первый коренной зуб.
Средняя величина костной ткани у щечных корней составляет 2,05—2,02 мм,
у небного корня — 2,02 мм.
На верхней челюсти принято ставить имплантаты в кость под
верхнечелюстной пазухой. Расстояние между имплантатом и пазухой должно быть не
менее 1—2 мм, но при потере зубов и атрофии кости она сближается с
альвеолярным отростком челюсти и их может разделять только тонкая пластинка
кости. Это затрудняет зубную имплантацию, и нередко от нее приходится
или отказываться или предварительно поднимать пазуху биоматериалами.
Постановка имплантатов в дистальном отделе верхней челюсти имеет ряд
особенностей. Во-первых, следует отметить близость и возможность
травмирования при имплантации, особенно при атрофии дистального отдела
альвеолярного отростка, внутренней челюстной артерии. Во-вторых, надо помнить,
что у бугра верхней челюсти расположено крыловидное венозное сплетение.
Как отмечает К. Hoffmann A995), хотя расстояние между артерией и
венозным сплетением отстоит от альвеолярного отростка, при постановке имплан-
тата в атрофированную кость это расстояние значительно уменьшается.
Индивидуальные особенности строения на нижней челюсти и атрофия
кости при адентии создают ряд проблем, которые надо учитывать при
имплантации. Прежде всего наклон альвеолярной части нижней челюсти может
быть как в вестибулярную, так и в оральную сторону. Наиболее часто зубы
отсутствуют в дистальном отделе нижней челюсти. Здесь кость может быть
различной как по форме, так и по качеству; большое значение имеет тяга
внутренней крыловидной мышцы. Если альвеолярная часть нижней челюсти
атрофирована и узкая, то при постановке имплантата может
перфорироваться или отломиться язычная стенка. Кроме того, в такой ситуации всегда есть
опасность повреждения язычного нерва.
На уровне альвеолярной части нижней челюсти соответственно молярам
и второму премоляру большое значение для постановки имплантатов имеет
расположение канала нижней челюсти и заключенного в нем сосудисто-
нервного пучка с нижним луночковым нервом. При атрофии альвеолярной
части нижней челюсти нижний альвеолярный нерв смещается'в язычную
сторону. Значительная атрофия кости альвеолярной части может привести к
такому обнажению нерва и смещению подбородочного отверстия, что они
окажутся на поверхности альвеолярной дуги. При их травмировании могут
развиться такие осложнения, как кровотечение или повреждение нерва. Кроме
того, перфорация нижнего луночкового нерва может влиять на приживление
имплантата и его будущую функцию в ортопедических конструкциях зубных
протезов. В других случаях такая ситуация делает имплантацию невозможной
без предварительной пластики альвеолярного отростка, репозиции нерва и
других дополнительных операций.
Атрофия альвеолярной части нижней челюсти происходит главным
образом за счет губчатого вещества. После удаления зубов вначале
атрофируется язычная сторона альвеолярной части. При этом альвеолярный гребень
часто приобретает форму лезвия ножа. В дальнейшем уменьшается по высоте
413
и делается более плоской альвеолярная часть гребня. В области симфиза
атрофия нередко создает плоскую поверхность с острым альвеолярным краем,
представленным чаще мягкой тканью. В местах отхождения подбородочно-
язычной и подбородочно-подъязычной мышц анатомические образования
могут пальпироваться у самого края атрофированной кости и выступать вверх.
Для оценки беззубой нижней челюсти предложено несколько
классификаций — Kennedy A928) с дополнениями A. Atwood A971, 1977) и для
зубной имплантации U. Linholm и G. Zarb A985), С.Misch и К. Judi A987).
Используют анатомические критерии челюстей по рентгеновским снимкам.
При диагностике и планировании зубной имплантации следует учитывать
антропометрические параметры челюстных костей и проводить
математическое моделирование на основании клинических, рентгенологических данных
и оценки моделей путем создания трехмерных образцов по РКТ и ЯМТ [Си-
дельников А. И., 1992; Робустова Т. Г., 2000].
На основании данных классификаций, в том числе различных
характеристик кости, выбирают способ остеотомии и постановки имплантата. Так,
при плотном компактном веществе кости надо проводить сверление
прерывисто, с охлаждением, но сохраняя достаточно высокую скорость вращения.
Если губчатое вещество кости рыхлое, особенно на верхней челюсти, то
сверлить кость следует с большой осторожностью, стараясь не применять
давление и не расширять ложе имплантата. В противном случае можно
перфорировать верхнечелюстную пазуху и травмировать нижний альвеолярный нерв.
Именно эти характеристики различных участков верхней и нижней
челюсти учтены в последней классификации, разработанной С.Misch A990).
По его данным, кость обладает высокими функциональными возможностями,
в том числе способностью адаптироваться к разным повреждениям и нагрузкам.
Они вызывают в ней перестройку и ремоделирование, но кость остается
физиологичной, если отсутствует излишняя перегрузка. По мнению автора,
этапность лечения при имплантации обеспечивает адаптацию кости. Всегда
можно достичь желаемых результатов правильным дозированием нагрузок на
кость: щадящей остеотомией, нетравматичной постановкой имплантатов,
обеспечением их первичной стабильности в кости и адекватной нагрузкой
после второго хирургического этапа в качестве опор зубных протезов.
Оценку клинического состояния альвеолярного отростка верхней челюсти
и альвеолярной части нижней челюсти дополняют замерами толщины
слизистой оболочки.
Комплексная оценка диагностических исследований позволяет
определить показания к имплантации, выбрать вид конструкции и число
имплантатов, разработать план хирургических действий и временного и постоянного
ортопедического лечения. Выбор имплантатов и их количества зависит от
условий в полости рта и будущей функции в качестве опор зубных протезов.
Учитывая большое количество конструкций имплантатов, следует
ориентироваться не на рекламные рекомендации изготовителей, а на результаты
лечения в различных клинических ситуациях.
32.1.3. Хирургические вмешательства при постановке
эндооссальных имплантатов плоской формы (пластиночные)
Плоские (пластиночные) имплантаты чаще представляют собой единую
конструкцию, иногда сборную. Имплантат состоит из внутрикостной части —
тела, шейки, и надальвеолярной — головки или головок (штифтов). Тело может
быть разнообразной конструкции и в поперечном разрезе имеет прямоуголь-
414
ную форму. Высота его от 8 до 15 мм, длина от 15 до 30 мм. Тело имплантата
имеет большое число прорезей, неровные края, а нижний край может быть
волнистым (рис. 32.2).
Плоские имплантаты имеют определенные преимущества, к которым
относятся: 1) возможность постановки плоской конструкции в узкую
альвеолярную дугу; 2) небольшая глубина погружения имплантата в кость, в связи
с чем уменьшается угроза повреждения верхнечелюстной пазухи, полости носа
и нижнего альвеолярного нерва; 3) небольшая ширина конструкции
уменьшает опасность отлома и перфорации наружной и внутренней стенок
альвеолярного отростка верхней челюсти и альвеолярной части нижней челюсти;
4) большая поверхность контакта имплантата с костью создает ему лучшую
фиксацию; 5) разнообразие форм имплантатов и наличие отверстий в их теле
способствует прорастанию кости, что улучшает его стабильность; 6)
имплантаты можно легко изогнуть и придать им форму, соответствующую изгибу
альвеолярной дуги, а опорным головкам — угол наклона, соответствующий
правильной окклюзии.
Кроме того, плоские имплантаты вместе с естественными зубами можно
включать в качестве опор в ортопедических конструкциях протезов. Это
позволяет уменьшать число имплантатов, что имеет особое значение при
включенных и дистальных дефектах зубов. По данным L. Linkow A993),
преимуществом плоских имплантатов является также возможность протезирования
уже на 3-—4-й неделе после операции.
Вместе с тем немало исследователей полагают, что плоские имплантаты
стабилизируются в кости путем фиброзной интеграции [Adell R. et al., 1981;
Albrektsson Т., Senneby L., 1990, и др.]. По мнению Т. Albrektsson A981), фиб-
роинтеграция является всего лишь фазой реакции хозяина на имплантат, что
в будущем не исключает его отторжения. Однако L. Linkow A968, 1983),
P. Schnitmann A985), С. Weiss и С. Misch A988, 1993) добились костной и фиб-
рокостной интеграции плоских имплантатов и отметили их долговечность в
течение 5—10 лет в 90—96 % случаев. Наиболее эффективны плоские
имплантаты при адентии и ширине альвеолярного гребня от 3 до 5 мм. Расстояние до
верхней границы канала нижней челюсти должно быть не менее 1 мм.
Операцию постановки имплантата производят после соответствующей
подготовки больного, премедикации и проводникового и инфильтрационного
обезболивания для выключения периферических ветвей тройничного нерва.
При имплантации должна быть соблюдена стерильность (техники операции,
стерилизации инструментов, материалов, имплантата, работа в перчатках).
Разрез проводят по альвеолярной дуге через слизистую оболочку и
надкостницу. Отслаивают слизисто-надкостничный лоскут по обе стороны
альвеолярного отростка верхней челюсти или альвеолярной части нижней челюсти. После
обнажения кость осматривают и отмечают ее конфигурацию, цвет,
консистенцию кортикального вещества. Скелетированную кость повторно замеряют
на разных уровнях альвеолярного отростка верхней челюсти и альвеолярной
части нижней челюсти. Обнаруженные при осмотре кости отдельные
неровности или выступы следует сгладить. Уплощение кости и ее сглаживание
осуществляют фрезой или круглым бором с внутренним или наружным
охлаждением. Если ставят несколько имплантатов, то расстояние между ними
должно быть не менее 3 мм, а расстояние до зуба, который будет служить
второй опорой зубного протеза, — не менее 2 мм.
На выбранных заранее и проверенных после скелетирования кости местах
для постановки имплантатов делают отметки на вестибулярной поверхности
альвеолярной дуги. Соответственно этим отметкам по центру альвеолярной
дуги в нескольких местах просверливают кортикальное вещество кости пре-
415
I
ä ä *
%. V rr rr
3 ?
V h V Ѵт
4TTF* <UXX> 'ѴЧГ' <*лл*>
<ттт> <тхт> ггіі) (ΤΙ Π1 ΓΤΤΤϊ*
<ΤϊΑτ> СПХІ* «ч^пАс* »Ar«**
Рис. 32.2. Виды внутрикостных имплантатов плоской формы.
а — одноэтапные; 5, β — двухэтапные.
рывисто, с внутренним или наружным охлаждением и проверяют прохождение
бора до губчатого вещества. Отверстия в кортикальном веществе, сделанные
соответственно телу имплантата, соединяют фиссурным бором, чтобы
образовалась борозда. Сверление в кортикальном веществе кости ведут с
постепенным увеличением диаметра сверлящих инструментов, также с наружным
и внутренним охлаждением. Правильность сверления контролируют аналогом
имплантата или измерительным прибором, а также по компьютерным
томограммам, сделанным в процессе остеотомии, для замеров каждого блока и
слоя костной ткани, а также по изображению на визиографе (рис. 32.3, а—г).
Костные опилки из туннеля убирают специальным инструментом.
Полость промывают стерильным изотоническим раствором натрия хлорида.
Кусочки кости и костные опилки помещают в стерильную емкость с
физиологическим раствором или в стерильную салфетку. После того как костное
ложе станет адекватным размеру конструкции, имплантат устанавливают в
него специальным плечепосадочным инструментом. Делают это легким
постукиванием молотком по краям плечепосадочного инструмента или по
специально затупленному долоту до тех пор, пока конструкция не встанет
плотно в кость (рис. 32.3, д). Однако некоторые исследователи полагают, что
имплантат должен входить в ложе свободно [Misch С, 1993]. В случае, если
он входит с трудом, постановку прекращают, его вынимают и углубляют
костное ложе. При этом убирают "навесы" и "выступы" кости. Затем имплантат
вновь вводят в ложе. Одновременно придают правильный угол наклону
опорной головки в соответствии с окклюзией. Плечи имплантата и основания
опорных головок должны быть заглублены на 2—3 мм ниже края кости. Если
делают примерки имплантата в костном ложе, то после каждой примерки его
временно помещают в стерильную емкость с изотоническим раствором
натрия хлорида. При постановке имплантата с гидроксилапатитным покрытием
все предварительные примерочные процедуры производят с аналогом.
Вводить такие имплантаты в ложе постукиванием и легким вколачиванием при
помощи молотка не следует.
В случае необходимости над плечами имплантата вокруг опорных
головок укладывают ранее извлеченные кусочки кости, костные опилки, а также
гранулы гидроксилапатита, иссекают слизистую оболочку соответственно
опорной головке имплантата и рану зашивают наглухо (рис. 32.3, е, ж). Через
3 нед—1 мес начинают протезирование. Если плоский имплантат разборный,
то на первом хирургическом этапе его устанавливают и мягкие ткани над ним
зашивают наглухо, а на втором — его вскрывают через 6 мес на верхней и
через 3—4 мес на нижней челюсти. Обнажив шейку имплантата, запорный винт
меняют на опорную головку и иссекают участок слизистой оболочки
соответственно этому отделу. Через 3 нед после вскрытия проводят
ортопедическое лечение (рис. 32.4).
32.1.4. Хирургические вмешательства при постановке
имплантатов в форме корня зуба (круглой формы)
Во всех странах используют преимущественно имплантаты в форме корня
зуба, как винтовые, так и цилиндрические, поскольку большинство
исследователей считают их более эффективными [Brauemark Р. I., Adell R. et al., 1981 —
1990; Kirsch Α., 1989; Niziiik G., 1982, 1994; Spiekermann H., 1995, и др.].
Имплантаты в форме зуба бывают погружными и непогружными и
соответственно требуют одноэтапного и двухэтапного оперативного вмешательства.
Одноэтапные непогружные имплантаты ставят в кость так, чтобы их надаль-
417
27- 1263
Рис. 32.3. Остеотомия при постановке
имплантатов плоской формы (схема).
а — линия рассечения слизистой оболочки
и надкостницы в области отсутствующих
моляров нижней челюсти; б— образование
шаровидным бором перфорационных
отверстий в кортикальном веществе кости
по ходу альвеолярной дуги; в — соединение
фиссурным бором перфорационных
отверстий; г — образование костного
туннеля соответственно глубине и ширине
имплантата и изгибу альвеолярной дуги;
д — постановка имплантата плечепоса-
дочным инструментом; е — иссечение
слизистой оболочки у основания опорной
головки имплантата; ж — глухое
зашивание раны.
Рис. 32.4. Рентгенограмма имплантата плоской формы в кости челюсти.
веолярная часть выступала в полость рта. Погружные имплантаты
применяют чаще. Они бывают винтовые и цилиндрические. На первом этапе
операции имплантаты ставят в кость, а слизистую оболочку и надкостницу над
ними зашивают наглухо. В ходе второго этапа имплантаты вскрывают и
ставят на них различные элементы супраструктуры. К наиболее
распространенным имплантатам двухэтапного хирургического лечения относятся системы
Branemark, Core Vent, Зі, Steri-Oss, Astra, Galsitec, IMZ и др., а также
отечественные конструкции "Контраст", "Плазма Поволжья". Одноэтапные непо-
гружньге имплантаты ставят в кость так, чтобы их надальвеолярная часть
выступала в полость рта. Среди них наиболее распространенными являются ІТІ,
Ledermann и отечественный "Комет" (рис. 32.5).
Имплантаты в форме корня зуба имеют следующие преимущества: 1) техника
остеотомии при создании ложа для имплантата отличается простотой, и
повреждение кости минимальное; 2) большое разнообразие размеров длины и диаметра
дает возможность подбирать имплантаты, наиболее соответствующие
конкретным условиям — ширине, высоте и качеству кости; 3) возможность с большой
точностью инструментально создавать костное ложе обеспечивает плотный
контакт имплантата с костью; 4) разнообразие шероховатых поверхностей тела
имплантатов, наличие резьбы и отверстий способствуют созданию плотного
механического соединения с костью и обеспечивают хорошую интеграцию с ней;
5) большое количество комплектующих элементов конструкции создает
наилучшие условия для эпителизации раны мягких тканей, и для создания
оптимальных углов наклона надальвеолярной части соответственно окклюзии.
Чаще применяют винтовые и цилиндрические погружные имплантаты для
двухэтапной операции. На первом этапе имплантат ставят в кость, а слизистую
оболочку и надкостницу зашивают над ним наглухо. На втором этапе
имплантаты вскрывают и на них ставят различные надальвеолярные компоненты.
Подготовку больного, премедикацию и обезболивание проводят по
общепринятым правилам, так же как при постановке плоских имплантатов. Хирур-
420
Щ '[УЩГЦ; 'Wß
Рис. 32.5. Виды внутрикостных имплантатов круглой формы.
гические действия начинаются с разрезов и откидывания слизисто-надкостнич-
ных лоскутов. Как отмечают Е. Krüger A982) и D. McGowan A990), чем больше
рассечения, тем лучше обзор раны, тем меньше при последующих действиях
опасность повреждения соседних анатомических структур, а также краев раны.
Способ создания костного ложа зависит от вида и конструкции имплантата.
Для внутрикостных имплантатов круглой формы особое значение имеет
методика подготовки костного ложа. Разнообразие форм и конструкций
имплантатов, выпускаемых большим числом фирм и компаний, требует для работы в
кости применения оригинальных инструментов для постановки каждого из них.
Имеются четыре принципиально важных инструмента для работы в
кортикальном и губчатом веществе кости. С их помощью последовательными
сверлениями соответственно длине и диаметру имплантата создают костное ложе.
Глубину сверления контролируют. При этом, как справедливо указывают
J. Lodos и J. Kent A995), Η. Spiekermann A995), решающую роль играет
оригинальный инструмент, режущий кость последним и окончательно
создающий ложе для имплантата (рис. 32.6).
В костное ложе имплантат можно вводить с помощью бормашины или
ручным способом. Сверление кости и вворачивание имплантата осуществляют
при специальных режимах вращения бормашины с внутренним и наружным
охлаждением. На завершающем этапе цилиндрический имплантат можно
заглублять легкими постукиваниями молотка. Глубина погружения имплантата
в кость зависит от его конструкции и взаимоотношений с мягкими тканями.
При одноэтапной операции с непогружаемыми имплантатами рану
зашивают вокруг ее надальвеолярной части. Особое внимание при этом обращают
на положение краев раны по отношению к трансмукозному удлинителю или
опорной головке. Принимают меры по предотвращению заворачивания
тканей внутрь и образования кармана (см. рис. 32.6).
Двухэтапные системы имплантатов круглой формы на нижней челюсти
вскрывают через 4 мес, на верхней — через 6 мес. Делают это путем короткого
рассечения над каждым из них или длинным над всеми конструкциями.
421
я
π
со
α
op
'•'О.:
ο i
61Ό
jo '
л·:
χ:
.*?υ·.ρ;
Рис. 32.6. Инструменты и этапы остеотомии для постановки имплантатов круглой
формы (схема).
а — этапы остеотомии для постановки винтовых имплантатов; б — этапы остеотомии для
постановки цилиндрических имплантатов;
Рис. 32.6. Продолжение.
в — этапы остеотомии для постановки винтовых одноэтапных имплантатов.
После вскрытия имплантата с большой осторожностью ручным способом
убирают излишки кости над запорным винтом. Затем последний
вывинчивают и проводят туалет внутренней части имплантата. Мягкие ткани вокруг
имплантата обрабатывают и, если необходимо, толстую слизистую оболочку
истончают. Зашивают слизистую оболочку и надкостницу так же, как при
погружных имплантатах, но при этом следят, чтобы не заворачивались края раны.
Для регенерации слизистой оболочки на 1,5—3 нед ставят винт заживления.
Вопрос возможности постановки временного протеза в период заживления
мягких тканей решает индивидуально врач-ортопед. Через 2—3 нед винт
заживления меняют на опорную головку или чресслизистый удлинитель и
начинают ортопедическое лечение (рис. 32.7).
32.2. Поднадкостничные имплантаты
Поднадкостничные имплантаты являются конструкцией, которая опирается
на альвеолярный отросток и тело челюсти. Такие имплантаты применяют
при значительной атрофии кости, когда нельзя создать полноценное жевание
съемными конструкциями протезов, а в кости нет места для постановки внут-
рикостных имплантатов для фиксации зубных протезов. Различают частичные
и полные субпериостальные имплантаты. Частичный имплантат ставят на
ограниченный участок челюсти, полный — на альвеолярный отросток и тело
всей челюсти. Имплантат состоит из головки, шейки и опорной части.
Последняя представляет собой вестибулярные и оральные ветви опорных пле-
чей, а также стабилизирующих и фиксирующих элементов. Опорная часть
имплантата, поставленная на кость и покрытая надкостницей и слизистой
оболочкой, постепенно соединяется с костью при помощи фиброзной ткани,
исходящей из периоста. Это происходит в течение 2—3 мес после постановки
имплантата. Трансдесневые штифты или головки проходят от опорной части
имплантата через надкостницу и слизистую оболочку и являются опорой
вначале капы, а затем съемного протеза, фиксируемого винтами, кнопочными
элементами, крючками.
423
Рис. 32.7. Имплантаты круглой формы.
а — рентгенограмма винтового непогружного имплантата в кости челюсти; б— цилиндрические
имплантаты в нижней челюсти с балочным устройством для фиксации зубного протеза.
В зубной имплантологии накоплен большой опыт применения поднад-
костничных конструкций [Суров О. Н., 1993; Кулаков Α. Α., 1996; Mentag P.,
1979; Weber S., 1979; Linkow L., 1986; Fallschüssel G., 1986; Misch C, 1993].
Оперативное вмешательство при постановке поднадкостничных им-
плантатов имеет особенности. После подготовки к операции и
проводниковой, инфильтрационной анестезии рассекают слизистую оболочку и
надкостницу путем линейных разрезов по гребню альвеолярной дуги, а также их
комбинации с вертикальными разрезами до свода преддверия полости рта.
Слизистую оболочку и надкостницу отслаивают с обеих сторон альвеолярного
отростка и тела челюсти. При скелетировании обращают внимание на
прикрепления к челюсти жевательных и мимических мышц, так как они могут
создавать трудности для фиксации опорной части имплантата. Осматривают кость
424
Рис. 32.8. Π од надкостничные конструкции имплантатов.
а — на верхней и нижней челюстях (рентгенограмма); б — с гидроксилапатитным покрытием.
челюсти, сглаживают отдельные выступы, острые края. Мешающие пучки
мышц отсекают, но при этом учитывают необходимость сохранения хорошего
кровоснабжения мягких тканей. Со скелетированной челюсти снимают слепок
и по изготовленной модели его вместе с ортопедом определяют конструкцию
имплантата, число и расположение опорных головок, особенности зубного
протеза и его крепления. Рану зашивают; через 4—6 ч швы, фиксирующие
слизисто-надкостничные лоскуты, снимают и надевают имплантат. Рану
зашивают наглухо, в участках опорных головок иссекают кусочки слизистой
оболочки и надкостницы. Обращают внимание на положение слизистой
оболочки по отношению к опорным головкам, чтобы мягкие ткани не
заворачивались внутрь. Затем надевают временный протез или каппу, а через 6—8 нед
ставят постоянный протез. При невозможности изготовить поднадкостничный
имплантат в день операции рану в полости рта зашивают наглухо (рис. 32.8).
425
Через 1 — 1,5 мес проводят повторную операцию скелетирования нижней
челюсти, ставят поднадкостничныи имплантат, по тем же правилам ушивают
рану и фиксируют временный протез на опорных головках. Через 2 мес
временный протез или каппа заменяются на постоянный протез. В
послеоперационном периоде проводят антибактериальную терапию, назначают
полоскания и ванночки с раствором хлоргексидина. До постановки постоянного
протеза рекомендуется прием жидкой пищи.
В нашей стране наибольшую трудность представляет изготовление
металлической конструкции поднадкостничного имплантата при помощи высокого
литья, поэтому на практике чаще осуществляют отсроченную постановку
имплантата. За рубежом продолжаются исследования для усовершенствования
поднадкостничных имплантатов. Применяют покрытия имплантатов
биоактивными материалами, в том числе гидроксилапатитом ("Calsitec"). При
помощи компьютерной томографии создают модель челюсти, по которой
изготавливают поднадкостничныи имплантат.
32.3. Внутрикостно-поднадкостничные имплантаты
Внутрикостно-поднадкостничные имплантаты были впервые предложены и
запатентованы J. Gerskovitz A974). Они представляли собой комбинацию
внутрикостной и поднадкостничной пластин. В дальнейшем их конструкции
совершенствовались многими исследователями [Суров О. Н., 1987; Yamane
Т., 1974; Linkow L., 1980]. Методика операции состоит в создании ложа для
внутрикостной части и скелетирования поверхности челюсти для помещения
накостной части конструкции. Такие имплантаты позволяют устранять
дефекты зубных рядов на ограниченных участках беззубой челюсти.
32.4. Чрескостные имплантаты
В отсутствие зубов и значительной атрофии кости нижней челюсти, при
которой остается лишь небольшой участок подбородочного отдела, применяют
чрескостные имплантаты [Дадыкина В. Ф., 1987; Higuchi К. et al., 1995]. Для
этого используют специальные чрескостные штифты, которые по краю
подбородочного отдела кости содиняют пластиной, а в полости рта скрепляют
соединяющими балками со специальными устройствами для крепления зубных
протезов. После традиционной подготовки и обезболивания делают разрез по
гребню остаточной кости нижней челюсти, обнажают кость по всему
периметру ее передней поверхности до подбородочного края. С помощью боров
и дрелей при наружном и внутреннем охлаждении сверлят сквозные
вертикальные отверстия в кортикальном и губчатом веществе кости. В полученные
костные каналы вводят внутрикостные штифты, соединяют и фиксируют их
по нижнему краю подбородочного отдела кости горизонтальной пластиной.
Слизисто-надкостничный лоскут укладывают на место, рану зашивают
наглухо. В области выступающих в полость рта штифтов иссекают кусочки
слизистой оболочки и устанавливают супраструктуру для фиксации протеза.
Временный протез надевают через 10—14 дней, постоянный — через 3—4
мес. Послеоперационное ведение больного аналогично таковому при
постановке поднадкостничных имплантатов. До постановки постоянных протезов
показан прием жидкой пищи.
Описаны и другие методики чрескостного введения таких имплантатов
[Дадыкина В. Ф. и др., 1988].
426
Рис. 32.9. Рамусный имплантат.
а — общий вид имплантата; б— рентгенограмма нижней челюсти с поставленным имплантатом.
32.5. Рамусные имплантаты
Рамусный имплантат представляет собой плоскую конструкцию, которую
фиксируют в трех местах кости нижней челюсти — в симфизе и обеих ветвях
[Streel Α., Roberts Η., 1983; Linkow L., 1987; Tatum Η., 1994; Tatum Η. et al.,
1995]. Постановка рамусного имплантата показана при прогрессирующей
атрофии нижней челюсти, когда применение внутрикостных и субпериостальных
имплантатов невозможно (рис. 32.9). По заранее снятому слепку и
изготовленной модели обеих челюстей, рентгеновским снимкам и расчетам,
проведенным по компьютерным томограммам, определяют места постановки
конструкции и участки рассечения тканей. Подготовка к операции традиционная,
как и обезболивание. Разрезы слизистой оболочки и надкостницы проводят
в ретромолярных ямках, по гребню альвеолярной дуги в области симфиза.
При помощи боров и фрез, с обязательным охлаждением проводят остеото-
427
мию для введения в ложе внутрикостных частей конструкции. Обязательны
примерочные процедуры на шаблоне и в полости рта для подгонки
конструкции к изгибу альвеолярной дуги и созданным ложам. Во все три ложа им-
плантат вставляют последовательно: вначале в одну и другую ветви, а затем
в симфиз. Мягкие ткани зашивают наглухо, без натяжения. После операции
ставят временный протез. В течение 8 дней показаны терапия антибиотиками,
прием анальгетиков и витаминов. Швы снимают через 2 нед. В течение 4 мес
рекомендуется употреблять жидкую и мягкую пищу. По истечении этого срока
ставят постоянный протез, хотя Н. Tatum A995) имеет положительный опыт
немедленного протезирования.
32.6. Внутрислизистые имплантаты
Внутрислизистые имплантаты представляют собой конструкцию, которую
вводят в съемный протез верхней челюсти. При значительной атрофии кости
и плохой фиксации протеза в слизистой оболочке неба и по альвеолярному
гребню делают перфорационные отверстия. Соответственно им на протезе
верхней челюсти создают углубления, в которые вставляют имплантаты.
Головка имплантата должна входить в перфорационное отверстие слизистой
оболочки. С. Weiss A992) рекомендует лабораторную работу с фиксацией им-
плантатов в протезе проводить одновременно с образованием отверстий в
слизистой оболочке и сразу же фиксировать протез. Болевые ощущения могут
наблюдаться в течение 3—4 нед, до полной эпителизации ран. В дальнейшем
рекомендуется тщательное соблюдение гигиены полости рта и протеза. Последний
С. Weiss A992) советует не снимать. Однако О. Н. Суров A993) считает
возможным снятие протеза, но не более чем на 6 ч.
32.7. Подслизистые имплантаты
Применение подслизистых имплантатов основано на помещении импланта-
тов-магнитов под слизистую оболочку для улучшения фиксации съемных
протезов на верхней и нижней челюстях [Попов Н., 1973; Марков Б. П., 1988]. В
нижнем отделе свода преддверия полости рта проводят разрез слизистой
оболочки до надкостницы, в который помещают специально изготовленные
магнитные имплантаты. Рану зашивают наглухо и через 6—7 дней надевают
протез с вмонтированными в него магнитами противоположной полярности. Их
расположение в протезе должно точно соответствовать помещенным под
слизистую оболочку магнитным имплантатам (рис. 32.10). В
послеоперационном периоде рекомендуются полоскания раствором хлоргексидина.
Соблюдение адекватной гигиены полости рта и протеза обязательно.
Остальные виды челюстно-лицевых имплантатов описаны в главах 21,27,28,30.
32.8. Дополнительные операции при зубной имплантации
Рассечение мягких тканей и остеотомию для имплантации начинают только
после того, как станет очевидно, что мягкой ткани или кости для постановки
имплантатов достаточно. Если же ткани недостаточно или ее объем
находится на пределе допустимой величины, то может возникнуть вопрос о ее
наращивании, что всегда требует дополнительных операций. В других случаях
могут потребоваться дополнительные операции на мягких и костных тканях
428
Рис. 32.10. Внутрислизистые имплантаты для фиксации полного съемного зубного
протеза верхней челюсти.
а - зубной протез с отверстиями для фиксации внутрислизистых имплантатов; б - ^отношение
имплантатов на зѵбном протезе с дефектами слизистой оболочки твердого неба: / - зубной протер
2 - ΖΖΙΖ^τΖκ3~ участок дефекта слизистой оболочки; 4- конструкция титанового
имплантата, вмонтированного в зубной протез (схема).
альвеолярного отростка верхней челюсти и на альвеолярной части^нижней
челюсти Такое случается, когда нет условий для постановки имплантата, не
хватает тканей для его закрытия или имеютсй дефекты кости.
УІловно дополнительные операции при зубной имплантации можно
разделить на две группы: вмешательства на костных тканях челюстей и на
429
мягких тканях полости рта
[Misch С, 1989, 1992, 1996;
Block M., Kent J., 1988, 1990,
1994]. На мягких тканях
полости рта осуществляют вес-
тибулопластику и
трансплантацию при помощи
свободных слизистых
лоскутов или лоскутов на
ножке, а также тонких,
расщепленных кожных лоскутов.
При нехватке кости
для зубной имплантации
применяют ауто- и алло-
кость (преимущественно де-
минерализированную),
искусственную кость —
трикальциофосфат, гидро-
ксилопатит, другие
биоматериалы, а также нерассасыва-
ющиеся и рассасывающиеся
мембраны [Zablotsky Μ. et
al., 1991; Buser D., 1996].
Мембраны могут быть
использованы при
обнаружении дефекта кости при
постановке имплантата, отломе
стенок созданного ложа,
плохом качестве кости в
пришеечной части
имплантата, расхождении швов и
обнажении погружных им-
плантатов или рецессии
слизистой оболочки вокруг
надальвеолярной части
непогружных конструкций, а
также при немедленной
имплантации после
удаления зуба и при развитии пе-
риимплантита.
Пластика аутогенными
костными трансплантатами.
Для увеличения кости проводится при затрудненной постановке импланта-
тов из-за атрофии костной ткани, особенно в дистальных отделах челюстей,
вблизи нижнего альвеолярного нерва и верхнечелюстной пазухи. В качестве
трансплантационного материала при зубной имплантации используют кость,
взятую вне полости рта (гребешок крыла подвздошной кости, фрагменты
малой берцовой кости, ребра), а также костную ткань челюстей — с симфиза;
ретромолярной области нижней челюсти, бугра верхней челюсти,
альвеолярных отростков (рис. 32.11). Самым важным условием успеха
комбинированной пластики аутогенным трансплантатом с одновременной постановкой
имплантата является достаточность мягких тканей для закрытия как
трансплантата, так и имплантата.
Рис. 32.11. Пластика аутокостью (схема).
а — пластика нижней челюсти гребешком подвздошной
кости и постановка имплантатов; б — пластика переднего
отдела альвеолярного отростка верхней челюсти
трансплантатом кости с симфиза нижней челюсти и постановка
имплантата.
430
Рис. 32.12. Репозиция подбородочного и нижнего альвеолярного нервов для
постановки имплантата (схема).
а — выделение подбородочного и нижнего альвеолярного нервов; б— репозиция нервов и
постановка имплантата; β — поперечный срез через нижнюю челюсть и взаимоотношение имплантата
и нервного ствола.
В качестве материала для трансплантации используют также
консервированные аллогенные костные трансплантаты и комбинацию ауто- и алло-
кости. Последние можно применять в комбинации с пластическими
материалами на основе гидроксилапатита и коллагена.
Одной из предимплантационных операций может быть репозиция нижнего
альвеолярного и подбородочного нерва (рис. 32.12). Одновременно с репозицией
нижнего альвеолярного нерва или перемещением подбородочного отверстия
рекомендуется использовать рассасывающиеся мембраны, аллогенную кость и др.
Пластика альвеолярного отростка верхней челюсти, поднятие дна носа,
верхнечелюстной пазухи — одна из распространенных операций при зубной
имплантации в тех случаях, когда альвеолярный отросток сильно атрофирован.
В результате операции дно носа или верхнечелюстная пазуха может быть
поднята, проведены их репозиция и увеличение верхней челюсти. Успех такой
операции может составлять от 94,4 % (рис. 32.13) [Block Μ., Kent J., 1993] до
100 % [Hall D., McKenney E., 1991].
При операциях на верхней челюсти для увеличения альвеолярного
отростка и поднятия пазухи применяют аутокость, деминерализированную ал-
локость [Block Μ., Kent J., 1993], их комбинацию с остеогеном [Whittaker et al.,
1989], комбинацию остеогена и коллагена [Smiler D. et al., 1992], остеогена и
крови [Wagner J., 1991], аутокости и гидроксилапатита [Tidwell J. et al., 1992].
Поскольку материала, как правило, недостаточно, D. Smiler и I. Holms A987),
J. Tidwell и соавт. A992), J. Kent и К. Block A993) стали использовать
аутокость в комбинации с пластическими материалами и керамикой,
преимущественно гидроксил апатитом.
При реконструкции верхней челюсти с поднятием верхнечелюстной пазухи
для имплантации должны соблюдаться следующие требования. Все
хирургические действия следует производить максимально щадяще. Трансплантируемый
материал при одновременной или отсроченной имплантации должен
образовывать кость, способную воспринять имплантат и плотно сращиваться с ним.
Резорбция вновь образованной кости не должна превышать 1,49 мм в первый
послеоперационный год и 0,1 мм в каждый последующий. Все оперативные
вмешательства не должны вызвать воспаления верхнечелюстной пазухи.
431
32.9. Осложнения при зубной имплантации
Зубная имплантация может привести ко всем осложнениям, развивающимся
при хирургических стоматологических операциях. Могут наблюдаться общие
и местные осложнения. К числу последних относятся отлом или перфорация
кортикальной стенки кости, вскрытие альвеолы соседнего зуба, вскрытие
верхнечелюстной пазухи, полости носа, нижнечелюстного канала, попадание
имплантата в мягкие ткани, верхнечелюстную пазуху, кровотечение, прозо-
палгия, воспалительные явления в области введенного имплантата в ранние
сроки после операции, а также поздние осложнения — мукозит, периим-
плантит, отторжение имплантата.
Перфорация или отлом кортикальной стенки кости. Чаще всего
необходимо лечение с помощью пластики аутокостью и консервированной аллоко-
стью (деминерализированной или лиофилизированной), различными
биоматериалами — колаполом, колапаном, мембраной. Во всех случаях
обязательно глухое зашивание раны (рис. 32.14).
При отломе кортикальной стенки и недостаточной фиксации имплантата
операцию прекращают, имплантат вынимают и выполняют пластику кости
так, как описано выше. Через 4—6 мес оценивают состояние кости и
возможность повторной постановки имплантата. В отдельных случаях
отказываются и от нее.
Вскрытие альвеолы соседнего зуба. Как правило, наблюдается при
неправильной технике операции и неадекватном расстоянии создаваемого ложа
имплантата от соседнего зуба. Целесообразно закрыть дефект боковой стенки
альвеолы биоматериалами — ауто- и аллокостью, гидроксилапатитом и др.
Имплантацию следует прекратить.
Вскрытие верхнечелюстной пазухи. Чаще наблюдается при
пневматическом типе ее строения. В одних случаях это происходит из-за неправильного
планирования и формирования костного ложа для имплантата, в других
перфорация возникает вследствие травматичного формирования ложа и большого
давления на тонкую стенку дна верхнечелюстной пазухи. Закрытие
перфорации можно проводить также пластическими материалами, если положение
имплантата в кости устойчиво.
В случае перфорации не только кости, но и слизистой оболочки
верхнечелюстной пазухи имплантацию прекращают, перфорацию закрывают
биоматериалом, рану ушивают наглухо.
Повреждение нижнего альвеолйрного нерва. При имплантации на
нижней челюсти, главным образом в дистальных отделах альвеолярной части, может
возникнуть перфорация нижнечелюстного канала. В таких случаях
имплантацию следует приостановить. Перфорация канала чревата развитием таких
осложнений, как кровотечение, повреждение нижнего луночкового нерва с
последующим развитием его поражения. В одних случаях после осмотра
перфорации следует выделить сосудисто-нервный пучок. Если перфорация
возникла в районе премоляров и первого моляра, то следует обнажить
подбородочное отверстие и выделить подбородочный нерв. После выделения сосудисто-
нервного пучка его отделяют от места перфорации биоматериалом —
рассасывающейся мембраной, колаполом, колапайом, а затем теми же материалами
прикрывают нерв снаружи.
При перфорации канала в районе второго моляра выпиливают фрагмент
кости соответственно передней стенке кости, выделяют срединную часть
сосудисто-нервного пучка и изолируют ее биоматериалом изнутри. Нерв
прикрывают снаружи. После хирургических манипуляций имплантат плотно
фиксируют в кости и рану зашивают наглухо.
432
Рис. 32.13. Пластика верхней челюсти (схема).
а — поднятие дна носа костным аутотрансплантатом и постановка имплантата в передний отдел
верхней челюсти; б — поднятие дна верхнечелюстной пазухи гребешком подвздошной кости и
постановка имплантатов; в — увеличение альвеолярного отростка верхней челюсти и поднятие
верхнечелюстного синуса гидроксилапатитом.
Кровотечение. Вблизи крупных артериальных или венозных сосудов при
имплантации может возникнуть кровотечение. Из нижней альвеолярной
артерии кровотечение может быть при перфорации канала нижней челюсти.
Его остановка возможна только путем локального наложения гемостатиче-
ской губки на кровоточащий участок. В других случаях, учитывая интимную
связь сосуда и нерва, образующего сосудисто-нервный ствол, выделяют со-
433
28-1263
Рис. 32.14. Устранение дефекта кости у имплантата.
а — аутокостью; б — мембраной; в — гид роке ил апатитом.
судисто-нервный пучок, отделяют и перевязывают артерию. При изоляции
сосудисто-нервного пучка с помощью биоматериалов используют гемостати-
ческую губку, в том числе с амбеном, фибринную пленку, желатиновую губку
"Кровостан", антисептическую губку с гентамицином или канамицином.
В случае длительного и обильного кровотечения имплантацию следует
прекратить, рану зашить наглухо и проводить общую гемостатическую терапию.
Ранние воспалительные осложнения. Одним из частых осложнений
имплантации являются воспалительные явления в первые 3 нед после операции.
Одной из причин такого осложнения может быть нестерильность имплантата
(изначальная или во время операции). Другой причиной развития ранних
воспалительных явлений является повреждение кости при перегреве или
травматичном воздействии на ее структуры во время остеотомии.
В одних случаях развиваются симптомы, схожие с таковыми при остром
периодонтите: боли в области имплантата, воспалительные изменения
прикрепленной слизистой оболочки, гнойный экссудат прорывает область швов и
содержимое выделяется из глубины тканей. В других случаях возникает
типичная картина острого гнойного периостита: выраженный отек околочелюстных
мягких тканей, регионарный лимфаденит, образование поднадкостничного
гнойника. В зависимости от выраженности воспалительных изменений
проводят общую и местную терапию. Однако некоторые исследователи
придерживаются мнения, что при перечисленных выше воспалительных явлениях
необходимо удалить имплантат [Orisim Α., 1987; Dougnerty S., 1988; Dougnerty S.,
Simmns R., 1989]. В то же время клинические наблюдения свидетельствуют
о том, что блокады с анестетиком и противовоспалительная терапия могут быть
эффективными. Стихание воспалительных явлений позволяет не удалять
имплантат [Робустова Т. Г., 1999; Bosker Η., Jordan R., 1991].
Поздние осложнения. При имплантации осложнения могут возникать в
поздние сроки. В 1988 г. Американская академия пародонтологии и в 1993 г.
Европейская федерация пародонтологии утвердили классификацию воспалений
при имплантации как болезни тканей вокруг имплантата. В зависимости от
патологоанатомических изменений в тканях вокруг имплантата различают
воспаление слизистой оболочки, прилегающей к имплантату, — мукозит и
одновременное воспаление мягкой и костной тканей в области имплантата — пе-
риимплантит.
434
Мукозит слизистой оболочки характеризуется появлением болей,
слизистая оболочка вокруг шейки или супраструктуры имплантата отечная, гипе-
ремированная. При зондировании возникает кровотечение, может выделяться
серозно-гнойный экссудат в небольшом количестве. Однако зонд погружают
неглубоко, определяя нормальную величину кармана. На рентгенограмме
патологических изменений в окружности имплантата не отмечается.
Периимплантит может начинаться так же и протекать с теми же
симптомами, что и мукозит. Но при зондировании инструмент погружается глубже
допустимых величин, обнаруживается кровотечение, налет под мягкой
тканью, который легко выдавливается наружу, серозно-гнойное отделяемое из
кармана, а также образование грануляций по периметру имплантата. D. Gam-
mage и соавт. A991) и D. Buser и соавт. A992) считают, что надо обращать
внимание на возрастающее с каждым посещением пациента увеличение
кармана и расценивают это как важный признак разрушения связки-замка, а
R. Brandes и соавт. A988) — как бесспорное разрушение кости.
В дальнейшем при зондировании кровоточивость усиливается,
появляются уже видимые глазом грануляции, а также рецессия слизистой оболочки
и обнажение шейки имплантата.
Согласно классификации, используемой американскими и европейскими
пародонтологами, различают четыре стадии периимплантита. В I стадии
наблюдается умеренная потеря кости по горизонтали и минимальная по
вертикали. Вторая стадия характеризуется умеренной или значительной потерей
кости по горизонтали и минимальной по вертикали. Третья стадия
отличается минимальной или умеренной потерей кости по горизонтали и
значительной по вертикали, причем часто можно наблюдать симметричную
резорбцию кости вокруг имплантата. В IV стадии отмечается значительная
потеря кости по вертикали и малая по горизонтали. Нередко кортикальное
вещество кости с вестибулярной и оральной стороны альвеолярной дуги на
месте имплантата полностью резорбировано.
Указанные выше изменения кости можно видеть на прицельных
рентгенограммах, зонограммах и ортопантограммах. Однако самые достоверные
количественные, качественные и анатомические данные о резорбции можно
получить только при компьютерной томографии.
Лечение мукозита осуществляют так же, как при начальных формах
заболеваний пародонта. При остром и хроническом течении заболевания
лечение начинают с гигиенических мероприятий: удаляют зубной налет,
обрабатывают карман 1 % раствором перекиси водорода и 0,06 % раствором
хлоргексидина. Одновременно обращают внимание на гигиеническое
состояние полости рта и обучают пациента правильной чистке зубов. Проводят
блокаду 5—10 мл 0,5 % раствора лидокаина по типу инфильтрационной
анестезии. При помощи пластикового инструмента удаляют зубной налет в
окружности имплантата, зубной налет и камень с супраструктуры имплантата.
После курса консервативной терапии оценивают состояние мягкой ткани
и рентгенологически определяют потерю кости. На основании этих
показателей планируют дальнейшее хирургическое лечение. R. Meffert A992)
считает, что для полноценного восстановления кости и адекватного
функционирования имплантата следует использовать аллогенные консервированные
и аутогенные костные трансплантаты, гранулированные формы гидроксила-
патита, направленную регенерацию при помощи рассасывающихся и нерас-
сасывающихся мембран [Dahlin С. et al., 1989; Jovanovic S., Spiekermann Η.,
1992; Jovanovic S. et al., 1993]. R. Adell и соавт. A991) в подобных ситуациях
с успехом выполняли резекцию участков воспаления и пластику местными
тканями.
435
28*
СПИСОК ЛИТЕРАТУРЫ
Абу-Асали-Эяд. Клинико-лабораторное обоснование применения имплантатов при
концевых дефектах зубного ряда нижней челюсти: Автореф. дис. ... канд.мед.
наук. - ML, 1992.
Вигдерович В. А. Прогнозирование результатов хирургического этапа дентальной
имплантации: Автореф. дис. ... канд.мед.наук. — М., 1991.
Гветадзе Р. Ш. Комплексная оценка отдаленных результатов дентальной
имплантации: Автореф. дис. ... канд.мед.наук. — М., 1996.
Жусев А. И. Микроциркуляция нарушений слизистой оболочки полости рта и их
коррекция при эндооссальной имплантации: Автореф. дис. ... канд.мед.наук. — М., 1995.
Кулаков А. А. Хирургические аспекты реабилитации больных с дефектами зубных
рядов при использовании различных систем зубных имплантатов: Автореф. дис. ...
докт. мед. наук. — М., 1997.
Лясников В. И., Лепилин А. В. Внутрикостные стоматологические имплантаты. —
Саратов: Изд. Саратовского ун-та, 1997. — 85 с.
Матвеева А. И., Кулаков Α. Α., Корнюшин В. И. и др. Применение отечественных
имплантатов в клинике ортопедической стоматологии. — М., 1991. — 19 с.
Матвеева А. И. Комплексный метод диагностики и прогнозирования в дентальной
имплантологии: Автореф. дис. ... д-ра мед.наук. —- М., 1993.
Робустова Т. Г. Зубная и челюстно-лицевая имплантация // Хирургическая
стоматология. — М.: Медицина, 1996. — С. 653—666.
Сидельников А. //. Планирование операции имплантации с учетом
антропометрических параметров лица: Автореф. дис. ... канд. мед. наук. — М., 1992. — IS с.
Суров О. Н. Зубное протезирование на имплантатах. — М.: Медицина, 1993. — 208 с.
Adell R., Lekholm U., Rockler В., Branemark P. A 15-year study of osseointegrated implants in
the treatment of the edentulous jaw // Int. J. oral Surg. — 1981. — N 10. — P. 387—416.
Anneroth G, Hedstrom K, Kjellman O. et al. Endosseous titanium implants in extraction sites
// Int. J. oral Surg. - 1985. - N 14. - P. 50-54.
Babbush C, Kirsch Α., Mentag P.} Hill B. Intramobile cylinder (IMZ) twostage osteointe-
grated implant system with the intramobile element (IME). Part 1. Its rationale and
procedure for use// Int. J. oral Maxillofac. Impl. - 1987. - Vol. 2, N 4. — P. 203-216.
Babbush С A. Surgical atlas of dental implant techniques. — Philadelphia: Saunders, 1980.
Babbush Ch. Dental Implants: priciples and practice. — Philadelphia: Saunders, 1991. — 384 p.
Block M., Kent J. Healing of mandibular ridge augmentation using hydroxylapatite with and
without autogenous bone in dogs // J. oral maxillofac. Surg. — 1985. — N 43. — P. 3—7.
Boyne P. Hydroxylapatite coatings on dental implants (bone response to hydroxylapatite) //
J. oral Implantol. - 1994. - Vol. 20, N 3. - P. 227-231.
Brunski J. Biomateriais and biomechanis in Dental implant design // Int. J. oral Maxillofac.
Impl. - 1988. - N 3. - P. 85-97.
Buser D., Dula K, Belser U. et al. Localized ridge augmentation using guided bone
regeneration. 2. Surgical procedure in the mandible // Int. J. Periodontol. Res. Dent. — 1995. —
N 15. - P. 11-29.
Cobb C, Eick /., Barker B. et al. Restoration of mandibular continuity defects using
combinations of hydroxylapatite and autogenous bone // J. oral Maxillofac. Surg. — 1990. —
N 48. - P. 268-275.
Dahlin C, Lekholm U., Becker W. et al. Treatment of fenestration and dehiscence bone
defects around oral implants using the guided tissue regeneration technique: a prospective
multicenter study// Int. J. oral Maxillofac. Impl. — 1995. — Vol. 10, N 3. — P. 312—318.
Jovanovic S., Schenk R., Orsini M., Kenney E. Supracrestal bone formation around dental
implants: an experimental dog study // Int. J. oral Maxillofac. Impl. — 1995. — Vol. 10,
N 1. - P. 23-31.
Kirsch A. Clinical use of the IMZ implant. Presentation at the Academy of periodontology. —
San Diego: Annual Meeting, 1989.
Lederman P. D., Mathys R., Frischherz R. Ein neues implantations-konzept fur den Einzel-
zahnersatz. Das ΗA-TlSchraubenimplantat // Ζ. Zahnärztl. Implantol. — 1986. — Ν 2. —
S. 111.
436
Ledermann P. D. Die neue Ledermann-Schraube. Beschreibung mit Bidserie // Swiss. Dent. —
1989. - Ν 10. - P. 31.
Linkow L. Clinical evaluation of the various designed endosseous implants // J. oral Impl. —
1966. - N 12. - P. 35.
Linkow L., Chercheve R. Theory and techniques of oral implantology. — St. Louis: Mosby,
1970.
Linkow L. The pess-fit anti-rotational vent-plant cylinder implant // J. oral Impl. — 1995. —
Vol. 21, N 1. - P. 40-45.
Matukas V. Medical risks associatd with dental implants // J. Dent. Educ. — 1988. — N 12. —
P. 745-749.
Misch С. Ε., Crawford Ε. Predictable mandibular nerve location. A clinical zone of safety //
Int. J. oral Impl. - 1990. - N 1. - P. 37-40.
Misch С. Ε. Medical evaluation of the implant candidate. Part 1: Vital signs and urinalysis //
J. oral Impl. - 1987. - P.,556-570.
Misch С. Ε., Judy К. Patient dental medical implant evaluation form // J. oral Maxillofac.
Surg. - 1987. - N 50 (Suppl. 2).
Misch С. M.f Misch С. Ε., Resnik R., Ismail Υ. Reconstruction of maxillary alveolar defects
with mandibular symphysis grafts for dental implants: a prelimenary procedural report
// Int. J. oral Maxillofac. Impl. - 1992. - Vol. 7, N 3. - P. 360-366.
Newman M., Flemmig T. Periodontal considerations of implants and implant associated
microbiota // J. Dent. Educ. — 1988. — N 12. - P. 738-743.
Niznick G The Core-Vent implant system //J. oral Impl. — 1982. — N 10. — P. 379—418.
Schenk R., Buser D., Hardwick W., Dahlin C. Healing pattern of bone regeneration in
membrane-protected defects: histologic study in the canine mandible // Int. J. oral
Maxillofac. Impl. - 1994. - Vol. 9, N 1. - P. 13-29.
SevorJ., Meffert R.f Block C. The immediate placement of dental implants into fresh maxillary
extraction sites // Pract. Periodont. Aesthet. Dent. — 1991. — N 3. — P. 55—59.
Spiekermann H., Jansen V., Richter Ε. A 10-year follow-up study of IMZ and TPS implants
in the edentulous mandible using bar-retained overdentures // Int. J. oral Maxillofac.
Impl. - 1995. - Vol. 10, N 2. - P. 231-243.
Tatum H. Maxillary and sinus implant reconstructions // Dent. Clin. N. Amer. — 1986. —
N 30. - P. 207-229.
Tatum #., Lebowitz M. Restoration of the atrophic, edentulous mandible // J. oral Impl. —
1994. - N 20. - P. 124-133.
Ulm С. W., Solar P., Krennmair G. et al. Incidence and suggested surgical management of
septa in sinus-lift procedures // Int. J. oral Maxillofac. Impl. — 1995. — N 10. —
P. 462-465.
Weiss C. Tissue integration of dental endosseous implants: Description and comparative
analysis of the fibro-osseous integration and osseous integration systems // Oral Impl. —
1986. - N 12. - P. 169-214.
Smiller D. G. Repositioning the interior alveolar nerve for placement of endosseous implsnts:
technical note // kit. J. oral Maxillofac. Impl. — 1993. — N 8. — P. 145.
Spiekermann H. Endossale implantate // Hupfauf L. Praxis der Zahnheilkunde. — Bd 7. —
München: Urban, Schwarzenberg, 1991. — S. 65.
Spiekermann H. Pre-surgical diagnosis in oral implantology // Yui J. Osseointegrated
implants: predictable clinical applications / Berlin: Quintessenz, 1993. — P. 14.
Sutter F., SchroederA., Buser D. Das neue ITI-Implanttatkonzept — Technische Aspekte und
Methodik // Quintessenz. - 1988. — N 39.
Tetsch P. Endossale Implantation in der Zahnheikunde. — München: Hanser, 1991.
Zarb G Α., Schmitt A. The longitudinal clinical effectiveness of osseointegrated implants: The
Toronto study. Part 1. Surgical results // J. Prosth. Dent. — 1990. — N 63. — P. 63.
Глава 33
ХИРУРГИЧЕСКИЕ МЕТОДЫ
ЛЕЧЕНИЯ
ЗАБОЛЕВАНИЙ ПАРОДОНТА
Пародонт — это комплекс тканей, окружающих зуб и обеспечивающих
фиксацию зуба в челюсти. В состав пародонта входят: десна, волоконный
аппарат периодонта, кость альвеолярных отростков и поверхностный слой
цемента корней зубов (рис. 33.1, 33.2).
Значение оперативных вмешательств на пародонте в общей
клинической стоматологической практике обусловливается двумя основными мо-
Рис. 33.1. Зоны десны (схема).
/ — краевая десна и межзубные сосочки; 2 — альвеолярная, или прикрепленная десна; 3 — нижняя
граница зоны прикрепленной десны с переходной складкой.
Рис. 33.2. Строение пародонта (схема).
/ — десневая борозда: пространство от десневого края до эмалево-цементной границы; 2 —
коронка зуба; 3 — зубодесневые, зубоальвеолярные и альвеолодесневые волокна, образующие
круговую связку зуба.
438
Рис. 33.3. Клинические формы состояния пародонта (схема).
а — интактный пародонт; б — хронический катаральный гингивит: вследствие скопления
микробных бляшек краевая десна воспалена, отечна; в — пародонтит (тяжелая форма). Альвеолярная
кость разрушена на з/4 длины корня с щечной и на і/г — с язычной стороны. Костный карман
с язычной стороны. Массивные отложения зубного камня, грануляций и детрита в пародонталь-
ном кармане. Выраженная воспалительная реакция в мягких тканях; г — рецессия десны с
щечной поверхности. С язычной стороны пародонт не изменен. Воспалительные изменения в десне
клинически не выражены.
ментами: распространенностью заболеваний пародонта и клинико-морфоло-
гической характеристикой поражений пародонта.
Распространенность заболеваний пародонта в различных регионах нашей
страны, как и в других странах, примерно одинакова и составляет от 85 до
98 % [Cripps S., 1984; Wilson Т. et al., 1992].
439
Различают следующие нозологические формы данной патологии: гингивит,
пародонтит, пародонтоз, опухолевые и опухолеподобные поражения — па-
родонтомы, идиопатические поражения пародонта и поражения пародонта
как симптомы общих заболеваний (рис. 33.3).
Среди перечисленных форм 92—95 % составляют воспалительные
поражения, причины, патогенез и клинические проявления которых хорошо
известны.
33.1. Этиология, патогенез, клиническая картина
и лечение заболеваний пародонта
Этиологическим фактором воспалительных поражений пародонта
является микробный. Выделяемые скапливающимися в придесневой области
микробами кислоты, ферменты и токсины до определенного времени успешно
нейтрализуются защитными клеточными и сывороточными компонентами
слюны и десневой жидкости.
По мере увеличения количества микробных бляшек, минерализации их
поверхностных слоев и выпадения неорганических солей из слюны,
активный микробный слой оказывается надежно закрытым сверху от защитного
действия слюны панцирем твердых зубных отложений. В его составе
появляются и интенсивно размножаются наиболее агрессивные по своему
токсическому действию на окружающие ткани микроорганизмы, которые
оцениваются как пародонтопатогенные. Как только их повреждающий
потенциал начинает превосходить возможности защитных тканевых
механизмов, клеточных и сывороточных компонентов крови, возникает
клинически определяемая воспалительная реакция.
Патогенез. Наличие микроорганизмов необходимо для
инициирования и развития воспалительной реакции. Однако имеется ряд факторов,
которые влияют на ее ход. Во-первых, это антимикробные компоненты слюны:
лизоцим, ß-лизины, во-вторых — защитные клеточные элементы ткани и
межтканевой жидкости, сывороточные и клеточные компоненты крови.
Индивидуальна структура кости и соединительнотканных образований
пародонта, активность метаболических процессов в них. Не случайно изучение
возможных причин возникновения и развития патологического процесса в
пародонте породило большое количество теорий, в частности микробную,
механическую, сосудистую, нервно-трофическую, генетическую, иммунную.
Общие заболевания существенно изменяют способность пародонтальных
структур противостоять действию микробных токсинов и ферментов,
снижают активность остео- и коллагеногенеза, подавляют защитные функции
клеточных элементов. В частности, при диабете нарушается проницаемость
сосудистых стенок, подавляется активность нейтрофилов и снижается их
хемотаксис. При нарушениях метаболизма кальция резко снижен остеогенез
и активизируется остеокластическая резорбция.
У лиц, подверженных стрессам, с неуравновешенными
психоэмоциональными реакциями обычно нарушается слюноотделение, а вследствие
этого — очищение полости рта и содержание в слюне антимикробных
компонентов. Кроме того, у таких пациентов отмечается трипсинемия,
повышена инфильтрация тканей десны активированными лейкоцитами,
выделяющими токсичный супероксиданион в ткани.
При заболеваниях желудочно-кишечного тракта часто обнаруживается
перенасыщение мягких тканей пародонта гистамином, усиливающим
воспалительную реакцию.
440
Такие физиологические состояния, как половое созревание,
беременность, характеризуются повышенным содержанием ряда гормонов, в частности
гормона роста, прогестерона, эстрогена, которые стимулируют активность
фиброцитов и оказываются хорошей питательной средой для пародонтопатоген-
ных микроорганизмов.
Нарушения иммунной системы, как первичные, так и возникающие в
результате общих заболеваний и нервно-психических расстройств, резко
сказываются на всех элементах общей и местной защиты и либо усиливают
местный воспалительный ответ, либо ответственны за быстропрогрессирующий
распад тканей, который неадекватен клиническим проявлением воспаления.
Клиническая картина. Первые воспалительные изменения
ограничиваются мягкими тканями десны и проявляются гингивитом —
покраснением, отечностью десневого края, его кровоточивостью. На этом уровне
процесс может сохраняться достаточно долго. Причиной является то, что зу-
бодесневое соединение представляет собой мощный тканевой барьер,
который надежно защищает нижележащие, непосредственно опорные структуры
пародонта — волокнистый аппарат периодонтальнои щели и кость альвеолярных
отростков. Пока это соединение сохраняется, процесс может быть успешно
излечен. Но если происходит его повреждение, то поток микроорганизмов, их
токсинов и ферментов устремляется в глубь волокнистых структур периодонта,
где они вызывают деструктивные изменения связочного аппарата зубов и
кости альвеолярных отростков. В этом случае речь идет о пародонтите.
Формирование вдродонтального кармана — это кардинальный признак па-
родонтита. Именно карман является резервуаром микробных и токсических
скоплений и обусловливает прогрессирующую деструкцию пародонта (рис. 33.4).
В этих условиях изменяется характер действия механической нагрузки,
которая в норме не только привычна, но даже необходима для
сбалансированных трофических процессов в пародонте. Ослабленные опорные структуры
становятся чувствительными к нагрузке, даже если она распределяется
равномерно на все зубы. В тех же случаях, когда на определенных участках
механические усилия оказываются более интенсивными (так называемые
травматические узлы), они уже не компенсируются эластичными и резистентными
свойствами пародонтальных тканей. В итоге происходит разрушение и пе-
риодонтальных волокон, и альвеолярной кости чисто травматического
характера. Травматический эффект возникает довольно часто (у 25—30 % пациентов)
с возрастом, если эмалевые бугры не стираются, так как после 25 лет буферные
свойства пародонта снижаются.
При определенной степени деструкции кости возникает подвижность
зубов. С этого момента процесс приобретает новые черты, так как любая
механическая нагрузка становится травматичной. В совокупности с постоянно
присутствующим микробным фактором она оказывает мощный
деструктивный эффект. Травматические узлы или супраконтакты усиливают его, их
влияние выражается в появлении дополнительных очагов вертикального
разрушения пародонта.
В связи с этим хирург должен учитывать действие механического
фактора и принимать меры для исключения локальных перегрузок и
стабилизации подвижных зубов с помощью избирательного пришлифовывания,
временного и постоянного шинирования.
В силу общих воздействий воспалительный процесс в пародонте протекает
неравномерно: для него характерны периоды активизации и
самопроизвольной ремиссии при одном и том же микробном и механическом потенциале.
Врач должен анализировать соотношение местных и общих факторов не только
с цельір выбора рцтищл£*нрй тактики ц реального прогнозирования возможных
441
результатов, но иногда и для решения
основного вопроса — о целесообразности
самого хирургического вмешательства в
конкретном случае.
Необходимо четко сознавать, что
хронический генерализованный гингивит или
пародонтит —- это местная воспалительная
реакция на действие микробных
скоплений. Все остальные местные и общие
факторы важны, но все же оказывают только
модифицирующее влияние на течение
местного воспалительного процесса.
В ответ на действие токсинов паро-
донтальные структуры разрушаются, в
карманах образуются некротические массы,
обильно разрастаются грануляции.
Отделяемое из пародонтальных карманов
(экссудат) является специфической
особенностью пародонтита. Его количество и
характер (серозное, гнойное, с запахом
или без него) помогают определить
течение заболевания либо оценить
результаты лечения. По расширенным
костномозговым пространствам микробные
скопления (тем более их легко пенетри-
рующие продукты — ферменты,
токсины, кислоты) проникают в мягкие ткани
и костные структуры, пропитывают
поверхностный слой цемента корней зуба.
Объем пораженной ткани очень большой:
площадь внутренних стенок карманов колеблется от 15 до 30 см2, поэтому
значительно и токсическое действие этого очага на организм; неизбежны не
только местные, но и общие явления сенсибилизации,
иммунопатологические нарушения клеточного и гуморального характера. Поскольку микробная
обсемененность полости рта постоянная и высокая, в ткани пародонта
микроорганизмы и их токсины поступают постоянно, поддерживая воспаление.
Указанные механизмы возникновения и развития типичных форм
хронического воспалительного процесса в пародонте диктуют характер и
последовательность лечебных вмешательств при гингивите и пародонтите. Эти
две клинически очень разные формы заболевания по сути представляют
собой только последовательные стадии развития единого процесса,
особенность которого заключается в том, что он течет по принципу сверху вниз.
Общим причинным фактором гингивита и пародонтита является
микробный. Клинически его присутствие и выраженность врачи обоснованно
определяют по количеству бляшек зубного налета и зубного камня.
Лечение. Независимо от формы и тяжести воспалительного процесса
первыми лечебными мероприятиями являются снятие зубного камня и
местная антимикробная обработка. При начальных изменениях это основной
метод лечения, при пародонтите — первый, но обязательный этап независимо
от того, какие хирургические вмешательства затем проводятся.
Второй обязательный шаг при лечении заболеваний пародонта —
устранение фактора механической перегрузки путем функционального
избирательного пришлифовывания по методу Дженкельсона. Таким путем уст-
Рис. 33.4. Пародонтальный карман.
Отложение зубного камня. Глубину
кармана измеряют с помощью
градуированного зонда: от эмапево-
цементной границы до дна кармана
(схема).
442
раняются супраконтакты и травматические узлы. Если пришлифовывание
проводят при гингивите, то этим можно предупредить очаговую деструкцию кости.
При развившейся деструкции после пришлифовывания и равномерного
распределения механической нагрузки скорость разрушения пародонтальных
структур снижается, а если метод применяют вкупе с другими лечебными
вмешательствами, то это позволяет добиться устойчивой ремиссии процесса.
Оперативные вмешательства на пародонте многочисленны и преследуют
конкретные задачи, которые различаются в зависимости от тяжести процесса
и ряда анатомических особенностей пародонта.
При гингивите хирургическое вмешательство используют фактически в
одном случае: для удаления разросшихся тканей десневого края в случае
гипертрофического гингивита или фиброматоза десен.
Гингивэктомия. При развившихся деструктивных изменениях в пародонте
(пародонтите) целью лечения являются удаление кармана — резервуара
повреждающих микробных и токсических веществ — и создание условий для
регенерации связочного аппарата и альвеолярной кости. Самый простой способ —
иссечение десневых стенок кармана. Достигается это при гингивэктомии.
Методика операции. Предварительно медикаментозно устраняют
воспаление, снимают зубные отложения. Непосредственно перед операцией
после антисептической обработки и анестезии определяют проекцию дна
карманов. Обычно для этого применяют зонд либо специальный пинцет. На
щечную и язычную стороны с помощью либо проколов, либо красящего
вещества наносят точки, соединяют их линией. Это линия разреза. Затем
скальпелем под углом 45° от десневого края иссекают мягкие стенки.
Дополнительно обрабатывают обнаженные поверхности корней зубов. На рану
накладывают десневую повязку (Periodontal-Pack) или пленку "Диплен" с
хлоргексидином или трихополом. Это простое вмешательство дает стойкий
эффект, но имеет значительные недостатки. Во-первых, не удается должным
образом обработать альвеолярную кость. Во-вторых, обнажаются корни
зубов, что зачастую сопровождается болезненностью при воздействии
термических и химических раздражителей и требует соответствующего лечения.
Тем не менее в области жевательных зубов при незначительной костной
деструкции эта операция в ряде случаев приемлема. Во фронтальном же участке
именно в связи с косметическим дефектом операция гингивэктомии
практически не проводится.
Исключением является только такая ситуация, когда наблюдаются
гипертрофический гингивит, фиброматоз десен. В таких случаях удаление
разросшихся тканей десны — обеспечивает косметический результат и является
основным методом лечения.
Что касается пародонтита, то решение перечисленных задач
(формирование зубодесневого соединения, приостановление разрушения
альвеолярной кости и по возможности хотя бы частичное ее восстановление) достигается
иным путем. Очевидно, что необходимо тщательно убрать из пародонтальных
карманов скопления микробных масс, зубного камня, тканевый детрит,
грануляционную ткань и пласты эпителия, выстилающего стенки карманов.
Другими словами, следует тщательно провести выскабливание пародонтальных
карманов. Технически кюретаж не отличается особой сложностью.
Наибольшие трудности представляет комплекс вмешательств, предшествующих
хирургическому лечению и завершающих его. Характер подготовительных мер и их
последовательность зависят от патогенетических механизмов пародонтита.
Оперативные вмешательства нельзя проводить пациентам с
неудовлетворительным гигиеническим состоянием полости рта. Гигиеническое обучение,
неоднократный контроль качества ухода за полостью рта перед операцией не-
443
обходимы. Полноценное лечение процесса в пародонте всегда комплексное.
Попытки упростить его за счет невыполнения какого-либо элемента
неминуемо сводят почти на нет все потраченные усилия. Может потому среди
населения и специалистов пародонтит и получил репутацию неизлечимого
заболевания. Мы не случайно подчеркиваем это: хирургический этап — один
из самых сложных и трудоемких в лечебном комплексе. Именно поэтому
хирург должен максимально контролировать выполнение всех других этапов.
Вмешательство можно планировать только после купирования
клинических признаков воспаления; в противном случае оно будет дополнительной
тяжелой травмой. Предварительно надо максимально убрать микробные
скопления и зубные отложения из карманов, провести их полноценную
антимикробную обработку.
Особое внимание при этом следует уделить лечению кариеса,
пломбированию полостей в придесневой области и восстановлению межзубных
контактов, чтобы предупредить интенсивное скопление микробных масс на этих
участках и рецидив воспаления. Послеоперационная регенерация тканей
происходит в основном за счет сформировавшегося кровяного сгустка.
Процесс этот длительный, и требуется долгое время обеспечивать сохранение
сгустка. Если зубы устойчивы, то задача решается легче. Поскольку для паро-
донтита характерна подвижность зубов, которая усиливается после
хирургической травмы, требуется максимально исключить имеющуюся и предупредить
дополнительную механическую травму зубов. После местного
противовоспалительного лечения необходимо провести функциональное избирательное
пришлифорывание. Дополнительную стабилизацию зубов осуществляют
предварительно изготовленной шиной или с помощью временного
шинирования композиционными материалами, пластмассой, Fiber-Splint сразу
после операции.
Закрытый кюретаж. Основное условие качественного выполнения кю-
ретажа состоит в том, чтобы специалист имел возможность контролировать
тщательность удаления распада из кармана, обработки корней и стенок
карманов. В зависимости от конкретной клинической картины: глубины кармана,
степени разрушения кости, вида деструкции — равномерной (горизонтальной)
или неравномерной (когда горизонтальная убыль кости сочетается с очагами
вертикальной деструкции и имеются костные карманы) врач выбирает способ
хирургической обработки (кюретажа).
Если есть уверенность в том, что можно надежно обработать карман без
предварительного раскрытия его с помощью разрезов, т. е. вслепую, то показан
закрытый кюретаж. Его проводят при небольшой глубине карманов. Однако
полноценность обработки с учетом тактильных ощущений сомнительна.
Следовательно, качество выполнения закрытого кюретажа в значительной
степени зависит от практических навыков врача (рис. 33.5).
Противопоказаниями к закрытому кюретажу являются ситуации, в
которых врач не может качественно провести обработку карманов: карманы
глубиной более 4 мм, наличие костных карманов, вовлечение в процесс зоны
расхождения корней — бифуркаций, трифуркаций.
Имеет значение толщина десны. Поскольку закрытый кюретаж —
травматичная процедура, истонченные стенки кармана являются абсолютным
противопоказанием к его проведению. В любом случае, проводя закрытый
кюретаж, врач должен сознавать, что качество обработки етенок карманов и
корневых поверхностей при этом очень посредственное, поэтому нельзя
рассчитывать на формирование зубодесневой связки. В лучшем случае можно
добиться приостановления процесса и образования мощного эпителиального
соединения^ что тоже неплохо.
444
Необходимо подготовить пациента к
проведению закрытого кюретажа и
устранить выраженные явления воспаления в
пародонте, в том числе медикаментозно.
Методика кюретажа. Область
вмешательства обезболивают,
обрабатывают антисептиком (слабый раствор фура-
цилина или 0,1 % раствор хлоргексидина).
Сначала снимают зубные отложения. Если
они обильные, то на первом этапе можно
их удалять с помощью ультразвуковых
аппаратов — скалера или ультрадента. Затем
острыми экскаваторами, крючками,
скребками и другими инструментами, входящими
в пародонтологический набор, удаляют
поддесневой камень со всех поверхностей
корней. Учитывая, что поверхность корня,
выступающая в карман, пропитана
токсинами, поверхностный слой цемента
некротически изменен, его снимают до видимо
(или ощутимо) здоровой ткани,
поверхность полируют. Если карманы достаточно
широки для полирования, то можно
применить ультразвуковые аппараты.
Стенки карманов обрабатывают с
помощью кюреток и специальных острых
крючков. Для этого (и с целью тактильного
контроля) врач прижимает обрабатываемую
стенку снаружи пальцем. Внутреннюю
поверхность обработанного кармана снова
промывают раствором антисептика, вымывают остатки детрита и
грануляций. Если кровоточивость отсутствует, надо слегка снова провести кюреткой
по стенкам, чтобы полость кармана заполнилась кровяным сгустком. Стенки
карманов не слишком плотно прижимают к поверхностям корней. Затем
накладывают десневую повязку. Таких повязок имеется значительное количество.
Наиболее доступны самоотвердеющие и оказывающие слабое антисептическое
действие повязки ("Periodontal-Pack" фирмы "Септодент", "Воко"), светоотвер-
ждаемые — типа "Баррикэйдер".
В настоящее время конкуренцию перечисленным зарубежным повязкам
составляют отечественные дипленовые пленки с различными лекарственными
наполнителями — в связи с удобством их применения и отсутствием
дискомфорта у пациентов.
Основные ошибки при проведении кюретажа объясняются тем, что врачи
обычно неоправданно упрощенно подходят к нему, забывая, что кюретаж —
самая настоящая операция, поэтому не всегда или недостаточно тщательно
проводят предварительное противовоспалительное лечение. Кюретаж
осуществляют без обезболивания либо после поверхностного обезболивания с
помощью шпрей-анестезии. При использовании тупых инструментов не
следует рассчитывать на удовлетворительное удаление камня, не говоря уже о
тонкой обработке поверхностей корней, а тем более об удалении грануляций
и эпителиальных пластов. Недостаточное внимание уделяют ведению
послеоперационного периода: наряду с хорошей индивидуальной гигиеной на
протяжении нескольких дней требуются медикаментозная обработка полости
Рис. 33.5. Состояние пародонта
после закрытого кюретажа. После
удаления зубного камня и
обработки стенок карман ликвидируется
за счет рецессии мягких тканей,
обнажается корневая поверхность
(схема).
445
рта с помощью антисептиков и использование лечебных повязок, чтобы
создать условия для успешного хода репарационных процессов.
Дискуссии об объеме вмешательства в одно посещение при нынешних
новациях в организации приема не совсем оправданы. При хорошем
обезболивании и выделении достаточного времени для приема пациента объем
операции может быть значительным. Основную роль играет то, как долго
пациент может выдержать это вмешательство.
Недостатки закрытого кюретажа определяются тем, что его проводят
вслепую. Даже при работе опытного специалиста в 50—70 % случаев остаются
неснятые зубные отложения, неудаленные грануляции. Начинающие же
хирурги оставляют их практически всегда. Не случайно в большинстве случаев
эффект достаточно кратковременный, хотя и закономерный: значительная
часть патогенных масс и микробных скоплений удаляется, и пока их
количество не достигнет определенного повреждающего потенциала, сохраняется
ремиссия. Сказанное объясняет, почему появились различные модификации
кюретажа. Их много, но общая их суть в том, чтобы расширить возможность
контролировать тщательность механической обработки карманов.
Открытый кюретаж. Заключается в том, что путем рассечения
межзубных сосочков раскрывают карман, чтобы под контролем зрения полностью
убрать грануляции, зубные отложения и качественно обработать корневые
поверхности. Межзубные сосочки рассекают, стенки карманов с щечной и
язычной сторон раздвигают (без отслаивания надкостницы). Врач имеет
возможность более тщательно обработать не только карманы, но и
альвеолярную кость (рис. 33.6).
Завершают операцию наложением твердеющей повязки или клеящейся
пленки (рис. 37.7). Ведение пациента в послеоперационном периоде
фактически такое же, как и при закрытом, или обычном, кюретаже [Лемецкая Т. И.,
Козловская А. Н., 1981].
Уместно сказать о продолжающейся дискуссии в отношении
правомерности терминов "закрытый" и "открытый" кюретаж, поскольку любой из них
является инвазивным вмешательством и всегда открытым. С другой стороны,
терминами "открытый" и "закрытый" кюретаж обозначают конкретную
методику.
Лоскутные операции изначально отнесены к сугубо оперативным
вмешательствам и входят в компетенцию весьма ограниченного круга хирур-
гов-пародонтологов. Базовой лоскутной операцией принято считать операцию
Цещинского—Видмана— Неймана, которые именно в такой
хронологической последовательности предложили ее соответственно в 1914, 1918 и
1920 гг.
Необходимость разработки этой операции была обусловлена
невозможностью перечисленными видами кюретажа обеспечить хороший доступ к
операционному полю, провести обработку карманов, пораженной кости
альвеолярных отростков при значительной костной деструкции. Фактически — это
совершенствование кюретажа. Дополнительные вертикальные разрезы по
краям оперируемого участка до переходной складки, отслаивание слизисто-
надкостничного лоскута с обеих сторон зубного ряда предоставляют врачу
новые возможности.
Методика операции. Предварительно проводят лечение зубов,
тщательную противовоспалительную терапию, избирательное пришлифовы-
вание (рис. 33.8). Местное медикаментозное лечение дополняют
назначением антибиотиков внутрь после предварительного определения
чувствительности микрофлоры пародонтальных карманов. Гигиеническое обучение
пациента и неоднократный гигиенический контроль обязательны.
446
Рис. 33.6. Открытый кюретаж (схема).
а — до лечения: деструкция кости, пародонтальный карман, отложения зубного камня; б— после
рассечения межзубных сосочков стенки кармана откидывают, проводят обработку кармана; в —
стенки кармана укладывают на место, фиксируют межзубными швами.
'%&
Рис. 33.7. Использование лечебных повязок после закрытого, открытого кюретажа
и лоскутной операции.
а — самоотвердеющая повязка типа Воко—ПАК или Септо—ПАК; б — клеющаяся пленка.
Рис. 33.8. Определение супра-
контактов в области жевательных
и центральных зубов (схема).
После обезболивания по границам
оперируемого участка, который определяют
заранее, отступив в сторону от межзубных
сосочков, проводят два вертикальных разреза
до переходной складки. Затем на расстоянии
1,5—2 мм от края десны делают
горизонтальные разрезы с щечной и язычной сторон.
Удаляют измененные полоски краевой
десны. Рассекают межзубные сосочки.
Распатором отслаивают ел изисто-надкостничный
лоскут до переходной складки со щечной и
на 4—5 мм — с язычной поверхности. Врач
получает возможность тщательно удалить
грануляции из альвеолярной кости и в
должной мере обработать костные карманы,
используя наряду с кюретками и крючками
методы лазерного и радиоактивного воздействия.
Затем повторяют медикаментозную
обработку. Иногда требуется дополнительная
механическая травма кости и надкостницы,
чтобы раневая поверхность не была сухой. Затем лоскуты укладывают на
место.
Чтобы предупредить послеоперационное обнажение шеек зубов,
применяют различные методики мобилизации лоскутов: рассекают надкостницу у
основания альвеолярных отростков, проводят дополнительные горизонтальные
или косые разрезы по краям лоскута, используют расщепленный или
частично расщепленный лоскут. После этого лоскуты максимально поднимают к
шейкам зубов, фиксируют их сначала по линиям вертикальных разрезов,
затем в области каждого межзубного промежутка (рис. 33.9). Для повышения
вероятности формирования соединительнотканного зубодесневого
соединения и регенерации связочного аппарата периодонта и костной ткани (что
достигается путем предупреждения прорастания ротового эпителия) около
каждого зуба накладывают манжетные швы [Гольбрайх В. В., 1964], особенно
на фронтальном участке.
С учетом того, что лоскутные операции производят при значительной
костной деструкции, которая обычно сопровождается подвижностью зубов,
усиливающейся после операции, зубы в участке операции временно
шинируют с помощью пластмассы, эвикрола или светоотверждаемых масс. Иногда
шинирующие конструкции планируют и изготавливают до операции, чтобы
сразу после нее иммобилизовать зубы (рис. 33.10).
Нет необходимости описывать модификации лоскутных операций. Следует
помнить, что все они продиктованы желанием повысить эффект за счет
устранения, а точнее, сведения к минимуму недостатков, присущих известным
вмешательствам. В ряде случаев появление модификации связано с
возможностями воздействовать на механизмы тканевой репарации и регенерации,
разработкой новых технических устройств, которые позволяют уменьшить
травматичность самих операций и обеспечить более спокойное течение
послеоперационного периода. Это касается применения лазерного скальпеля и
лазерных методик, радиоскальпеля.
Основной генератор новых идей — это устойчивые недостатки
вмешательства. Главным из них являлось то, что так и не удавалось добиться
гарантированной репарации периодонтальных структур. Первичный
косметический эффект снижается или сводится на нет в результате последующей
448
Рис. 33.9. Лоскутная операция (схема).
а — до операции; б — проведены вертикальные разрезы, рассечены межзубные сосочки; в — сли-
зисто-надкостничный лоскут отслоен. Удалены некротизированные ткани, обработаны корневые
поверхности и альвеолярная кость, иссечена полоска краевой десны, диэпителизирована
внутренняя поверхность лоскута; г — лоскут уложен на место, коронарно смещен за счет
мобилизации, фиксирован швами.
ретракции тканей. Основная причина кроется в том, что пародонтит — это
хронический воспалительный процесс, и даже после устранения воспаления
в мягких тканях, периодонтальных структурах и самой кости сохраняются
последствия дистрофических изменений. Кроме того, самые скрупулезные
расчеты успеха терпят крах, потому что не учитывается факт банальных воз-
449
29- 1263
Рис. 33.10. Виды шинирующих бюгелъных конструкций (а — г).
растных инволютивных изменений. Между тем степень деструкции, возраст
и сниженные возможности регенерации всех тканей тесно связаны. На
результатах операций сказывается существенная разница регенераторного
потенциала пародонтальных структур: периодонта, кости и эпителия — и то,
какая из перечисленных тканей начнет регенерировать раньше и интенсивнее.
450
вчЛш.
Ι ι
έι
4<%В
'Vi
Рис. 33.10. Продолжение.
Если первым прорастает эпителий (а его регенераторный потенциал
наибольший), то пародонтальный карман восстанавливается, хотя и в меньших
размерах, если же кость, то формируется соединение по типу кость — кость
(анкилоз). Идеально, если первыми регенерируют периодонтальные волокна:
только в этом случае формируется полноценное соединение. К сожалению,
этот вариант наиболее редкий [Schröder W., Ϊ982]. Важную роль играет
состояние поверхности обнаженных корней зубов внутри кармана: глубокая их
пенетрация микробными токсинами, белковыми патологическими
комплексами не позволяет периодонтальным волокнам сформировать соединение со
структурами поверхностного слоя цемента.
Для максимального восполнения утраченной кости рекомендованы
органические и неорганические вещества и тканевые подсадки. С целью
повышения вероятности формирования зубодесневого соединения апробированы
различные средства обработки корневых поверхностей. Чтобы повысить
активность трофических процессов в пародонтальных структурах, предложены
многочисленные физические и фармакологические средства,
дополнительные оперативные вмешательства (в частности, формирование поднадкостно-
го туннеля и заполнение его тканевыми подсадками).
Результаты лечения зависят от характера костной деструкции и формы
костных карманов. Если костные дефекты ограничены с трех сторон
альвеолярной костью и с одной — корневой поверхностью, то их называют четырех-
стеночными дефектами. Когда две стенки кармана состоят из альвеолярной
кости и одна представляет собой поверхность корня, это — трехстеночные
дефекты. Лечение трех- и четырехстеночных дефектов наиболее успешное.
Если имеются двухстеночные дефекты, обнажена область межкорневого
соединения (би-, трифуркаций), очаги вертикальной деструкции сочетаются с
равномерной горизонтальной убылью кости, то задача хирурга усложняется.
К тому же при равноценности клинических изменений и адекватной
операции эффективность ее варьирует у разных людей. Именно по указанным
причинам трудно использовать единый метод не только у разных пациентов, но
даже на разных участках пародонта у одного пациента. В связи с этим ученые
и практические врачи вынуждены постоянно модифицировать базовые
методики. Из модификаций эффективны применение остеопластических
материалов, направленная регенерация тканей пародонта с помощью мембран, а
также химическая обработка корней зубов.
33.2. Лечение заболеваний пародонта с использованием
остеопластических материалов
Для восполнения утраченных костных тканей при заболеваниях пародонта
применяют тканевые трансплантаты.
Аутокость. Нативные губчатые аутотрансплантаты, биологическая
совместимость которых способствует более ранней адаптации и васкуляриза-
ции. по сравнению с другими видами остеопластики (кортикальная аутокость,
аллотрансплантаты), обладают выраженными остеогенными свойствами.
В них рано начинается интенсивное костеобразование, в котором участвуют
клетки аутологичного костного мозга, обладающего высоким остеогенным
потенциалом. Однако метод аутопластики остается слишком травматичным,
требует дополнительной операционной травмы, которая превышает объем
оперативного вмешательства, поэтому при лечении пародонтита этот метод
не следует использовать. Кроме того, как отмечали Б. Д. Архипов и соавт.
A985), аутотрансплантаты не гарантируют надежности функциональных,
анатомических и косметических результатов.
452
Лиофилизированная формалинизированная и деми-
нерализированная аллокость. Этому пластическому материалу
авторы отдают предпочтение в связи с тем, что он хорошо поддается обработке
и способен обеспечить хорошие условия для последующего протезирования.
Однако пересадка данных трансплантатов нежелательна в инфицированное
ложе реципиента, так как нередко заканчивается его отторжением. Ю. А.
Петрович и соавт. A992), описывая преимущества лиофилизированных
трансплантатов, отмечали, что в заведомо инфицированных дефектах, каковыми
всегда являются пародонтальные карманы, их использование исключается,
поэтому следует отдавать предпочтение формалинизированным и частично де-
минерализированным трансплантатам.
A. П. Безрукова A978) дала высокую оценку формалинизированному
аллотрансплантату, указав на его высокие остеопластические свойства при
хирургическом лечении пародонтита. Противомикробный эффект
обеспечивается за счет отщепления молекул формальдегида.
Для потенцирования противомикробного эффекта формалинизированной
кости рекомендуется проводить УЗ-кавитацию через серебряную воду, что
способствует уменьшению отека, очищению раны, усилению фагоцитоза и
повышению неспецифической резистентности организма [Мухсинов М. 3.,
Таиров У. Т., 1985]. Однако лиофилизация костных трансплантатов в
известной степени приводит к потере их остеопластических свойств. При
сравнительном изучении биопластических свойств аллотрансплантатов оказалось,
что наиболее резко их пластическая активность снижается при консервации
в растворе диоцида. В формалине эффективная регенерация происходит
только в 40 %, при лиофилизации — в 75 % случаев. Иммуногенность больше
снижается при лиофильной сушке, меньше — при формалинизации.
B. И. Савельев A981) утверждает, что при консервации даже в слабых
растворах формалина жизнеспособность тканей не сохраняется. М. Ю. На-
заренко A989) показал довольно медленную динамику перестройки формали-
низированного трансплантата у взрослых больных. По данным Н. И. Локтева
A985), если костеобразование при пересадке губчатого костного аутотранс-
плантата принять за 100 %, то при использовании формалинизированного
аллотрансплантата оно составит 68,7 %, а кильского (депротеинизированная
и обезжиренная кость) — только 45,3 %. Приведенные факты указывают на
недостаточную эффективность данных видов трансплантатов при
хирургическом лечении заболеваний пародонта.
Наличие выраженных остеоиндуктивных свойств у деминерализирован-
ного костного трансплантата проявляется более быстрым восстановлением
дефектов костной ткани по сравнению с другими видами аллокости.
Местные регуляторы остеогенеза, такие как костный морфогенетический протеин
и скелетный фактор роста, содержащиеся в деминерализированной
аллокости, могут оказывать взаимодополняющее действие, вызывая дифференци-
ровку новых клеточных элементов и регулируя их общее количество. Это
является преимуществом остеогенного потенциала деминералйзированного
костного трансплантата перед замороженной и формалинизированной ал-
локостью. Кроме того, технологические условия позволяют насыщать
трансплантат растворами антибиотиков, ферментов, что делает его
устойчивым к инфекции и пригодным для пластики в воспалительно измененных
тканях.
Общим недостатком перечисленных трансплантатов является их
иммуногенность, выраженная в той или иной степени. В некоторых случаях в
результате этого развиваются воспалительные явления в тканях, окружающих
трансплантат.
453
Брефокость. Материалы на основе костной ткани эмбрионов
человека максимально снижают риск иммунного конфликта между тканями
эмбриона-донора и реципиента, обменные процессы активизируются быстрее,
чем при использовании других видов трансплантатов.
Эмбриопласт является активным стимулятором репаративного остеоге-
неза, а также проявляет низкую иммуногенность за счет упрощенной
антигенной структуры.
Однако некоторые авторы отрицательно относятся к использованию эм-
бриопласта в клинической практике, так как за 3 мес внутриутробного
развития полноценный костный материал не успевает сформироваться. В связи
с этим рекомендуется использовать брефопласт из костной ткани
5—7-месячных плодов. На основе брефощебенки и хряща разработан
трансплантационный материал, который получил название "брефоостеопласт". Он отличается
пластичностью, что позволяет идеально восполнить утраченный объем
костной ткани и оптимизировать процессы репаративной регенерации. Однако
брефоостеопласт имеет низкую биомеханическую прочность и довольно
быстро рассасывается в кости. Отсутствие синхронизации процессов резорбции
материала и формирования костной ткани является недостатком препарата.
Коллагенсодержащие материалы. Повышенный интерес
проявляется к использованию животного солюбилизированного коллагена из
дермы крупного рогатого скота. В процессе обработки снижаются его
антигенные свойства, которые в основном обусловливаются теплопептидами (но
не исчезают полностью, что не исключает развития реакций повышенной
чувствительности). В. С. Иванов A987) отмечал, что остеопластические
материалы на основе коллагена (коллаост, гидроксиапол, коллапол, гапкол,
линко-гап, синтост, колап) хорошо моделируются в костных полостях,
плотно их заполняют, осуществляя тесный контакт с воспринимающим ложем,
и сохраняют при этом свою пористую структуру, что обеспечивает их гемо-
статическую функцию.
Высокая гигроскопичность материала позволяет насыщать его
структуры антибиотиками, антиоксидантами, препаратами противовоспалительного
действия, тем самым понижая риск возникновения осложнений.
Однако в условиях выраженного воспаления и протеолиза, что имеет
место при пародонтите, препараты нативного коллагена быстро рассасываются,
не оказывая длительного противовоспалительного и стимулирующего
репарацию действия. В связи с этим для большей стабильности коллагена в
биологической среде используют комбинацию коллагена с гидроксилапатитом (ГА).
Например, материал "Avitene" на основе микрокристаллического коллагена
содержит кальций-фосфатную керамику. Для увеличения прочности
добавляли синтетические волокна (нейлон). Данный биоматериал D. Lew и соавт.
A986), Е. Nery и соавт. A978) использовали вместе с аутокостью и ГА для
восстановления гребня атрофированного альвеолярного отростка. Комплекс
коллаген—ГА применяли W. J. Spitzer и R. Mehlish A988).
Интересны данные об использовании в пародонтологической практике
комплекса кальций-фосфатной керамики с коллагеном.
Гидроксилапатит. Исследования по использованию
кальций-фосфатной керамики с целью стимулирования репаративного остеогенеза в месте
имплантации проводятся с 1920 г. Однако при применении данных
препаратов с высокой удельной площадью поверхности порошка в клинической
практике установлено незначительное ускорение процесса костного
заживления либо отсутствие такового. В силу данного обстоятельства возобладал
подход использовать для клинических целей образцы твердой
кальций-фосфатной керамики в качестве имплантатов.
454
Материалы на основе гидроксилапатита условно делятся на два
основных типа: 1) неотожженный (резорбируемый) гидроксилапатит, который
подразделяется на мелкодисперсные порошки, например остим-100, и
порошки резорбируемого ГА, в частности ГА-100; 2) высокотемпературная
керамика (нерезорбируемая), в состав которой входят порошки (гидроксиа-
пол), грануляты и блоковые керамики. Резорбируемый ГА синтезируется в
жидкофазной реакции при комнатной температуре и характеризуется низкой
кристалличностью, высокой сорбционной способностью, относительно
высокой резорбируемостью в биологической среде. Нерезорбируемый ГА
получается после нагревания при 800—1000 °С, при которой происходит фазовый
переход в конденсационно-кристаллическую форму, химически стабильную,
практически нерастворимую в воде. Мелкодисперсный ГА получают при
включении криогенного этапа в процесс изготовления.
Основным преимуществом ГА-керамики является ее способность
образовывать прочную химическую связь с костью. ГА интенсивно используется
для замещения костных дефектов тканей пародонта в ходе проведения
лоскутных операций. При этом уменьшается подвижность зубов, отсутствуют
рецидивы обострений воспалительного процесса, оптимизируются процессы
остео- и цементогенеза и образование зубодесневого прикрепления,
уменьшается глубина пародонтальных карманов, что коррелирует с
рентгенологическими данными. При лоскутных операциях без использования
гидроксилапатита улучшение достигается только в 44 % случаев. Существенной
разницы между различными формами ГА (в виде блоков или гранул) не
выявлено.
Биоситаллы. Появляются сообщения о разработке новых групп
материалов на основе бинарных или поликомпонентных смесей, содержащих
более широкий спектр микро- и макроэлементов в комплексе со
структурирующими твердеющими гелями природных полимеров (протеин, хондрои-
тин-сульфат, хитин, гиалуроновая кислота и др.). На основании природного
полимера, получаемого путем экстракции из водорослей, разработана
композиция для заполнения пародонтальных карманов. Воздействие материала
на рану заключается в способности абсорбировать, термоизолировать,
сохранять влагу в ране и оказывать гемостатическое действие. Новым материалом
для пластики является биополимер биоситалл. Он представляет собой
композицию ГА с альгигелем, в которой содержание ГА достигает 30 %.
Применяется в виде пористых или спеченных блоков, содержащих водные растворы
антисептиков и противовоспалительных препаратов. Используется при ос-
теопластических операциях.
При сравнении эффективности остеопластических материалов следует
отметить, что в настоящее время наилучшими являются коллагенсодержащие
препараты, биоситаллы, гидроксиапатит и их сочетания с мембранами
направленной регенерации тканей. Использование коллагенсодержащих
материалов обусловлено включением ксеногенного коллагена в строящийся
костный матрикс, а ГА усиливает регенерацию и минерализацию костной
ткани. Сочетание с мембранами повышает регенеративные возможности
перечисленных материалов. Кроме того, мембраны препятствуют прорастанию
эпителия в глубь тканей.
Однако успех вмешательства зависит не только от самого материала.
При анализе данных литературы нельзя не обратить внимание на тот
факт, что в наблюдениях разных авторов один и тот же материал давал
различные результаты. Эта разница могла бы натолкнуть на мысль об
индивидуальной восприимчивости пациентов к тому или иному препарату,
если бы группы больных, находившихся под наблюдением, не были дос-
455
таточно велики. Изложенное выше служит доказательством того, что успех
хирургического лечения во многом обусловлен эффективностью
проведения всех его этапов.
Поскольку важным моментом, влияющим на исход лечения, является
формирование и удержание кровяного сгустка, который служит источником
репарации, а иногда и регенерации связочного аппарата зуба, способность
остеопластического материала удерживать образующийся кровяной сгусток
может быть одним из главных факторов, определяющих его регенераторный
потенциал.
Искусственные мембраны для направленной
регенерации тканей π ар о д о нта. Впервые входе лоскутных операций на па-
родонте мембранный барьер применили S. Nyman и соавт. A982). Они
использовали миллипорный фильтр, поместив его между тканями десны и
поверхностью корней зубов. Этим было обеспечено препятствие для
сцепления клеток десневого лоскута с поверхностью обнаженных корней,
прорастания эпителия и одновременно созданы условия для роста тканей,
образующих периодонтальную связку. Значение их обусловлено тем, что только
периодонтальные ткани могут трансформироваться в цементобласты и
блокировать клеточный рост других тканей и в итоге обеспечить формирование
нового зубодесневого соединения.
Экспериментальные исследования показали, что полная регенерация
соединительнотканного аппарата зубов возможна только при полном
исключении прорастания эпителия десны. Вместе с тем ни кость, ни десна не
способны обеспечить образование нового соединительнотканного соединения
на лишенных периодонтальной связки поверхностях корней зубов. Более
того, при непосредственном контакте тканей десны с поверхностью корня даже
без прорастания эпителия происходит резорбция корневой поверхности или
же формируется соединение по типу костного анкилоза [Andreasen J., Kris-
terson L., 1976, 1981], возможно, по причине накопления токсинов в
обнаженных поверхностях зубов [Aleo J. et al., 1975].
В то же время предполагается, что и клетки костномозгового вещества
могут участвовать в формировании зубодесневой связки через напластовы-
вание новых Клеток цемента на поверхностях корней. По данным A. Nojima
и соавт. A980), ткань периодонтальной связки содержит прародительские
клетки типа остеобластов, которые дифференцируются в остеобласты и
цементобласты. Это является фактом в пользу предположения, что в результате
лечебных вмешательств клетки периодонтальной связки формируют новую
соединительнотканную связку со вновь образованным цементом корней.
Экспериментальные данные наряду с результатами клинических
исследований, проведенных S. Nyman и соавт. A982), J. Gottlow и соавт. A984),
R. Caffesse и соавт. A988), позволили разработать мембраны на основе "МШі-
роге" и политетрафлюорэтилена. Их использование обеспечивает
оптимальные условия для активной репопуляции клеток периодонтальной связки в
пространстве между внутренней стенкой мембраны и поверхностями корней
зубов. Специально для этих целей был разработан материал "Gore-Tex" (рис.
33.11), изготавливаемый из политетрафлюорэтилена в различных формовых
модификациях. Недостатком материала является то, что он не резорбируется,
поэтому через 4—6 нед необходимо повторное оперативное вмешательство,
чтобы удалить его после достигнутой регенерации соединительной связки.
Особый интерес представляют мембраны из резорбирующегося коллаге-
нового материала — биодеградирующие мембраны, которые оказались более
эффективными в экспериментальных условиях [Blumenthal N., 1988; Magnus-
son I. et al., 1988; Pitaru S. et al., 1987, 1988]. Преимущество их неоспоримо, так
456
Рис. 33.11. Мембраны "Gore-Tex" различной
конфигурации (а—д).
^=^^Л
Су
П
£9
как отпадает необходимость в повторном
оперативном вмешательстве.
Предоперационная подготовка
стандартная.
Особенности вмешательств с
использованием мембран заключаются во
введении их на место дефекта и
закреплении. Если применяют нерезорбирую-
щиеся мембраны, то через 6—8 нед
проводят повторные операции по их удалению:
после рассечения межзубных сосочков и
небольших вертикальных разрезов часть
краевой десны отодвигают, мембрану
убирают, отслоенные ткани укладывают
на место и фиксируют швами.
Одномоментно операцию проводят в
области не более двух рядом стоящих
зубов, чтобы обеспечить достаточное
кровоснабжение.
Методика операции. После
анестезии и вертикальных пограничных
разрезов лоскут откидывают. Корни и
внутреннюю поверхность лоскута
обрабатывают традиционно (механически,
химически).
В зависимости от того, какой вид
дефекта планируют устранить, выбирают
форму и размер мембран. На расстоянии
2 мм от края с помощью специального
шовного материала их фиксируют около
шейки зуба на уровне, до которого
планируют поднять уровень соединения.
После этого лоскут укладывают на место и фиксируют швами в межзубных
промежутках. На рис. 33.12 представлены этапы этого хирургического
вмешательства.
Применяют также резорбируемые мембраны на основе коллагена.
Тканевые ферменты человека вполне активны в отношении таких
коллагеновых структур. Хемотаксические свойства экзогенных коллагенов в
отношении фибробластов обусловливают формирование вокруг них
пространственных фибриллярных структур. К тому же эти коллагены стимулируют
распад тромбоцитарных пластинок, одновременно ускоряя сцепление в
кровяных сгустках [Lowenberg В. F. et al., 1985; Pitaru S. et al.3 1987; Blumenthal N.,
Steinberg J., 1990; Dowell P. et al., 1995].
Такие мембраны рассасываются в течение 30 дней, тогда как их корон-
ковая часть — через 10 дней. Видимо, уже через 10 дней после операции можно
определить степень эпителиальной миграции. Учитывая, что причина
недостаточной клинической эффективности коллагеновых мембран заключается в
30-1263
457
Рис. 33.12. Операция
направленной регенерации с
применением нерезорбируемой
мембраны (схема).
а — зубные отложения (исходное
состояние после откидывания
елизисто-надкостничного лоскута);
б — зубные отложения сняты,
грануляционная ткань удалена
Обнаженные корневые
поверхности обработаны путем
аппликации 18 % раствора лимонной
кислоты в течение 1 мин; в, г —
выбор мембраны для закрытия
фуркации. Фиксация мембраны
по линии эмалево-цементного
соединения. Полоска мембраны на
2 мм выше эмалево-цементной
границы; д — мембрана
зафиксирована; в секторе представлен вид
сверху после фиксации мембраны;
е — слизисто-надкостничный
лоскут уложен на место. По
линиям вертикальных разрезов и в
межзубных промежутках
наложены швы; ж — через 8 нед
повторная операция по удалению
мембраны. Десна в межзубных
промежутках рассечена.
Слизисто-надкостничный лоскут слегка
отодвинут; з — разрезают швы,
фиксирующие мембрану; и —
удаление мембраны; к — лоскут
укладывают на место. В
межзубных промежутках накладывают
швы кетгутом.
Рис. 33.12. Продолжение.
их подверженности действию тканевых ферментов, в 1991 г. S. Pitaru и соавт.
изготовили двухслойные мембраны. Их наружный слой состоял из коллагена,
а внутренний был обработан фактором роста I, гепарина сульфатом и
фибрином, которые стимулировали размножение клеток, образующих периодон-
тальную связку. В результате использования таких мембран эффективность
лечения возросла с 65 до 95 %.
При сочетанном применении коллагеновых мембран и костных
трансплантатов N. Blumenthal и J. Steinberg A990) в 93 % случаев наблюдали не
только формирование соединительнотканных образований, но и заполнение
костью исходных дефектов более чем 50 %.
Последние сообщения касаются применения коллагеновых мембран,
изготовленных на основе "Collistat", при лечении пациентов с
бифуркационными поражениями II класса [Anderegg С. et al., 1995]. В. Paul и соавт. A992)
не выявили различий в отношении степени костного заполнения дефекта.
К. Chung и соавт. A990), Н. Anderson A991), Μ. Tanner и соавт. A988), J.
Pfeifer A989), S. Garrett и соавт. A988) также показали ненадежность
улучшения пародонтальных параметров с помощью "Avitene", твердой мозговой
оболочки и однослойных коллагеновых мембран. Более того, результаты
использования искусственных подсадок в сочетании с операцией коронарного
смещения лоскута без применения мембран были даже лучше и стабильнее.
Вместе с тем многие авторы сдержанно оценивают эффективность
коллагеновых мембран и считают, что она обусловливается в основном
предупреждением прорастания эпителия, тогда как стимулирование роста клеток пе-
риодонта при этом не происходит. Вопрос о перспективности применения
мембран на основе коллагена требует дальнейшего изучения.
Оксидированную целлюлозу в виде гомогенной массы
применил Р. Galgut A990) для лечения межзубных и бифуркационных дефектов.
При контакте с кровью эта масса превращается в желатиноподобную, а в
дальнейшем рассасывается без выделения токсических продуктов.
Результаты использования этого материала успешны, но малочисленны. Необходимы
дальнейшие наработки для окончательного заключения о целесообразности
его широкого применения на практике.
Хрящевые (коллагеноподобные) мембраны изучали только
S. Card и соавт. A989). Материал получают из оболочки слепой кишки быков
и после хромирования используют в качестве шовного. В эксперименте такие
мембраны распадались в сроки от 4 до 8 нед, препятствовали прорастанию
эпителиального пласта. Однако не отмечено явных преимуществ
применения этих мембран по сравнению с контрольными исследованиями.
Сложность заготовки и хранения материала ставит под сомнение
целесообразность его применения.
Гидролизирующийся полиэфир изучали R. Caffesse и С. Nasjleti
A992) в эксперименте на собаках. Мембраны начинали рассасываться только
через 3 мес, были абсолютно толерантны. Их применение обеспечило
двойной эффект в отношении объема зубодесневого соединения и новой кости.
Материал заслуживает дополнительного экспериментального и клинического
изучения.
Полимолочную кислоту (биодеградирующий полиэфир)
первоначально применяли в общей ортопедии I. Magnusson и соавт. A990). Уже
через 1 мес после операции формировалось новое прикрепление, через 3
мес — кость. Сама мембрана рассасывалась через 6 мес. Данные S. Yamada
и соавт. A991), J. Gottow и соавт. A992), L. Laurell и соавт. A992),
полученные в эксперименте и в клинической практике, совпадают. Особенно
важно полное замещение бифуркационных поражений и угловых костных
460
дефектов. Необходимо уточнять показания и прогноз результатов при
различных видах операций.
Викриловая Macca(Polyglactin910) — синтетический продукт,
состоящий из гликолида и лактида в соотношении 9:1. Используется в
качестве шовного материала в нейрохирургии. В эксперименте и клинической
практике применяется для лечения локализованных рецессии десны и
костных дефектов, в том числе поражений в области бифуркаций. Полная
регенерация мягких тканей достигается в 4 раза чаще, чем в контрольных
наблюдениях. Межкорневые дефекты значительно уменьшаются, хотя полностью
не ликвидируются [Quinones С. et al., 1991]. Эффект существенно
повышается в тех случаях, когда викриловые мембраны применяют с искусственными
костными подсадками.
При сравнении эффективности рассасывающихся и нерезорбирующихся
мембран не выявлено четкого превосходства одних над другими. Более того,
даже при использовании мембран одного вида эффект на разных участках
вмешательства был различным и, очевидно, зависел от объема и формы
дефектов. Что касается резорбирующихся мембран, то наибольшим
регенераторным потенциалом в отношении клеток, образующих периодонтальную
связку, обладают (в порядке убывания) викриловая смесь, полимолочная
кислота и коллагеновые производные. Наряду с нерезорбирующимися
материалами такие мембраны дают возможность в 2—3 раза увеличить объем
соединительнотканного соединения и кости. При поражениях в области
бифуркации ни один вид мембран не позволяет добиться полного
восстановления кости.
I. Magniisson и соавт. A990), N. Claffey и соавт. A989), U. Wikesjö и соавт.
A991) считают, что эффект мембран всех видов обусловливается не их
специфичностью, а способностью в конкретном случае создать условия для
успешного формирования, надежного сохранения и нормальной
трансформации кровяного сгустка. В частности, для достижения необходимой зрелости
фибринного сгустка требуется 2 мес. Поскольку большинство
резорбирующихся мембран сохраняется не менее 6 нед, очевидно, что они выполняют
защитную функцию в самый критический период. Таким образом, эффект
всех мембран, видимо, в первую очередь зависит от этого свойства, а
специфическое влияние на генерацию клеток периодонтальной связки играет не
самую важную роль [Card S. et al., 1989; Pitaru S. et al., 1989; U. Wikesjö et al,
1992]. Тем не менее бесспорно, что в совокупности с совершенствованием
методов обработки поверхностей корней, использованием стимуляторов
роста клеток и искусственными подсадками применение мембран позволит
повысить клинический эффект и вероятность его предсказания [Poison Α., 1994;
Trombelli L. et al., 1994; Shin S., Allen Ε., 1994].
Лекарственные препараты для химической
биомодификации корней зубов. Необходимость в обработке корневых
поверхностей внутри пародонтальных карманов или обнаженных вследствие рецессии
десны вызвана тем, что в результате инфицирования обнаженных корневых
поверхностей даже путем тщательного механического очищения не удается
удалить из цемента микробные токсины и белковые агрегаты. В результате после
закрытия этих участков слизисто-надкостничным лоскутом не образуется
плотное соединение между поверхностью корней и мягкими тканями, поэтому
через короткое время достигаемый в ходе операции эффект существенно
снижается или полностью исчезает.
Коллагеновые волокна должны прорасти в глубь дентинных канальцев
или в пространства между клетками цемента, чтобы зубодесневое соединение
сформировалось на новом уровне, но патогенные включения препятствуют
461
этому. В случае рецессии десны поверхность корней представляется
полированной, устья дентинных канальцев плотно замурованы солевыми
отложениями. Чтобы обеспечить устойчивую связь перемещенных мягких тканей с
поверхностью корня, необходимо, во-первых, раскрыть устья, а во-вторых,
удалить из них патогенные включения. Для этих целей были апробированы
различные препараты. В настоящее время лучшие результаты дают лимонная
кислота, тетрациклин и фибронектин.
Лимонная кислота применяется в виде 18 % раствора (pH 1,0)
путем аппликаций на 0,5—1 мин. При этом ее токсическое воздействие на
окружающие ткани минимально. Что касается корневых поверхностей, то
после аппликации происходит полное удаление белковых конгломератов, устья
дентинных канальцев не только раскрываются, но и становятся шире
(эффект "раструба"), наблюдаются репарационные процессы в поверхностном
цементе: образуются так называемые цементные гвозди, обнажаются колла-
геновые фибриллы. После удаления инфицированного поверхностного слоя
и деминерализации даже оставшихся зубных отложений создается надежная
связь между поверхностью корня и лоскутом.
Тетрациклина гидрохлорид вызывает подобные, хотя и не
столь выраженные изменения при аппликации увлажненного порошка на 4—
5 мин. Дополнительным плюсом является антимикробное влияние
впитанного поверхностными твердыми и коллагеновыми структурами препарата.
Может быть, именно поэтому данный способ привлекает клиницистов. Ведь
в первые несколько суток после операции такой антимикробный эффект
значит очень много для сохранения кровяного сгустка и успешного начала
репарационных процессов.
Фибронектин в виде раствора после аппликации на поверхности
корней улучшает фиксацию лоскута за счет сильной клейкости, стимулирует
рост фиброцитов и сохраняет образовавшийся сгусток. Чтобы
компенсировать не очень высокий деминерализирующий эффект фибронектина, его
применяют после предварительной обработки тетрациклином или (чаще)
лимонной кислотой [Poison Α., 1995; Cohen W., 1996].
Обширный арсенал материалов для костной пластики наряду с
очевидным технологическим прогрессом в данной области свидетельствует и об
отсутствии абсолютно эффективного материала. Возможно, дальнейшие
разработки будут отмечены новыми достижениями. Результат их использования
может быть улучшен только при условии совершенствования способов и
средств, обеспечивающих более активную регенерацию связочного аппарата
зуба. Лишь в этом случае объем и восполнение костного дефекта могут
оставаться на стабильном уровне. Вопрос об использовании искусственных
мембран занимает центральное место среди перечисленных проблем паро-
донтальной хирургии.
Операции на мягких тканях преддверия полости рта. Воспалительные
поражения пародонта являются наиболее распространенными. Тем не менее
разнообразная клиническая картина поражений пародонта объясняется тем, что
ряд деструктивных изменений пародонта возникает в результате не только
хронического воспаления, но и действия нарушений мягких тканей преддверия
полости рта. В частности, очаговая деструкция альвеолярной кости,
обнажение шеек зубов различной степени (вплоть до такой степени, что это не
только вызывает значительный косметический дефект, но и влечет за собой
необходимость удаления зубов) обусловлены безобидными, на первый взгляд,
факторами: высоким прикреплением уздечки нижней (особенно часто) и
верхней губы, мелким преддверием полости рта, мощными тяжами слизистой
оболочки переходной складки, короткой уздечкой языка.
462
Механизм деструктивного действия перечисленных факторов на паро-
донт иной, нежели воспалительного процесса, причем он срабатывает тогда,
когда отсутствует зона прикрепленной десны, которая гасит мышечные силы
и не позволяет им передаваться непосредственно на краевую десну. В таких
случаях при каждом напряжении (движение губ, языка, мышц подбородка)
в местах прикрепления тяжей происходит ишемизация, т. е. нарушается
питание слизистой оболочки, надкостницы и определенных участков кости
альвеолярных отростков. Кроме того, механическая тяга передается
непосредственно на десневой край, фактически отрывая его от подлежащей кости.
Постоянно присутствующие в полости рта микроорганизмы именно на
участках ишемии наиболее активны, поэтому фактически сочетается действие
двух повреждающих факторов — механического и микробного, что
обусловливает суммарный повреждающий эффект.
Перечисленные анатомические нарушения выявляются в подростковом
и даже в детском возрасте, но разрушительный эффект их обнаруживается в
основном только у взрослых. Это объясняется значительными резервными
возможностями тканей пародонта в молодом возрасте, которые обусловлены
в первую очередь высокой эластичностью тканей. С возрастом уменьшается
количество эластичных волокон, снижаются амортизирующие свойства
всех тканей пародонта, в том числе периодонта и кости, и тогда
механические локальные перегрузки начинают полностью проявлять себя
клинически и морфологически.
Нарушения строения мягких тканей преддверия полости рта
ликвидируют только хирургическим путем. Мелкое преддверие полости рта устраняют
в ходе вести було пластики. Нарушение прикрепления уздечек губ
корригируют методом френулопластики. Если патологическое действие
оказывают уздечка языка или тяжи слизистой оболочки переходных складок,
то производят их рассечение — френулотомию.
У пациента может быть несколько из числа отмеченных нарушений,
поэтому по возможности в ходе одного оперативного вмешательства устраняют
либо несколько, либо все. В связи с тем что при этих операциях предполагается
коррекция слизистой оболочки, их объединяют под обшим названием
мукопластики. Однако, поскольку зачастую эти нарушения вызывают
повреждение тканей и десны, и кости, в чистом виде мукопластические операции
проводят до того, как нарушения вызовут деструкцию. Если же необходимо
устранить и деструктивные последствия данных нарушений, то в
зависимости от того, на каких тканях пародонта они уже отразились, осуществляют
мукогингиво- либо мукоостеогингивопластику.
Частота нарушений строения слизистой оболочки преддверия полости
рта достаточно высока: нами они отмечены у 22—25 % обследованных. В
амбулаторной практике хирургов-стоматологов с целью предупреждения
деструктивных изменений пародонта эти вмешательства следует чаще выполнять
у детей и подростков.
При хирургическом лечении пародонтита обязательно следует
предусмотреть коррекцию данного вида нарушений. В противном случае самые
сложные лоскутные операции могут оказаться неэффективными. В связи с этим
зачастую, планируя лоскутные операции, предполагают дополнительно муко- и
гингивопластику (в зависимости от конкретной клинической ситуации), чаще
всего остеомукогингивопластические вмешательства.
Если исходить из сказанного, то деление методов хирургического
лечения пародонтита на основные (кюретаж, лоскутные операции) и
вспомогательные (муко- и/или гингивопластика) не совсем оправдано. Мы придаем
всем им равное значение.
463
При заболеваниях пародонта
следует устранять нарушения
прикрепления уздечек губ.
Самым простым методом
коррекции при высоком прикреплении
нижней или низком — верхней
губы является рассечение
уздечки. Его выполняют в тех
случаях, когда уздечка длинная,
тонкая, а прикрепленная десна
достаточно широкая, толстая и
можно предполагать, что после
рассечения уздечки не
возникнут сильное рубцевание и
рецидив повреждающего натяжения
уздечки.
Если же уздечка мощная и
сильно натягивает краевую десну,
то либо прибегают к ее
иссечению с последующим
закрытием дефекта слизистой
оболочки (рис. 33.13), либо
производят френулопла-
с τ и к у: отсекают уздечку,
удаляют тяжи вместе с надкостницей;
отсепарованную уздечку
смещают к основанию отростка десны.
Дефект закрывают, переместив
треугольные лоскуты по Лимбергу
(рис. 33.14) либо мобилизовав
уздечку путем сепарации по
краям разреза. После операции
накладывают швы из кетгута.
Рекомендуют антисептическую обработку раствором фурацилина или калия
перманганата.
Могут потребоваться также рассечение уздечки языка и
иссечение тяжей слизистой оболочки переходных складок.
Применяют разные методы в зависимости от мощности и расположения тяжей.
Если тяж одиночный, то операция не отличается от таковой при рассечении
уздечки губы. Если же рядом расположено несколько тяжей, то на этом участке
целесообразно выполнить одномоментно вестибулопластическую операцию.
Очаговое обнажение корней зубов, или Ѵ-образный
дефект, — следствие действия тяжей переходных складок либо результат
индивидуального дефекта формирования тканей пародонта: чрезмерно тонкой
слизистой оболочки, надкостницы и альвеолярной кости с губной поверхности
зуба (или ряда зубов).
Для закрытия этого дефекта используют методику, предложенную R. Griipe
и Н. Warren A956), при которой дефект закрывают с помощью латерального
лоскута (рис. 33.15). Можно выкроить лоскуты с обеих сторон дефекта,
мобилизовать их и фиксировать друг к другу. При коронарной репозиции
лоскута (рис. 33.16) отслаивают сохранившуюся десну. С помощью
вертикальных разрезов ограничивают ширину лоскута, затем мобилизуют его, рассекая
надкостницу в области подвижной слизистой оболочки. Следует предусмот-
Рис. 33.13. Низкое прикрепление широкой
уздечки верхней губы (а—в).
464
реть как возможность
достаточной мобилизации лоскута, так и
обеспечение его трофики, а
также предупредить последующую
деформацию преддверия в
области вмешательства (иногда
выполняют повторную
корригирующую операцию). Существует
большое количество
модификаций этого вмешательства (как и
описанных выше). В частности,
применяют искусственные
мембраны. При проведении данной
операции следует строго
соблюдать правила механической и
химической обработки обнаженной
поверхности корней.
Обязательно прекращение курения не
менее чем за 1 мес до операции, так
как, кроме механического
закрытия дефекта, необходимо
добиться формирования
надежного соединения перемещенного
лоскута с поверхностью корня и
обеспечить сохранение
результата. Не случайно до сих пор успех
при этих вмешательствах не
гарантирован.
Операция вестибу-
лопластики производится
довольно часто и относится к разряду
пародонтологических. При
мелком преддверии полости рта
пациента беспокоит
косметический дефект или повышенная
чувствительность обнаженных
шеек зубов. Однако именно данная патология мягких тканей приводит к
резкой деструкции тканей пародонта на довольно большом протяжении (как
правило, от клыка до клыка нижней челюсти).
В зависимости от того, какие изменения в пародонте произошли при
мелком преддверии полости рта (деструкция кости, обнажение шеек зубов)
или клинически данная патология еще не проявляется, применяют
различные модификации вестибулопластики. Наиболее широко используется
вестибулопластика по Эдлану— Мейхару (рис. 33.17).
Перед операцией устраняют явления воспаления, проводят
избирательное пришлифовывание, пациента обучают правилам гигиенического ухода за
полостью рта.
Полость рта обрабатывают раствором антисептика. После инфильтра-
ционной анестезии осуществляют повторную инфильтрационную анестезию
поднадкостнично. Разрез проводят по слизистой оболочке губы на глубину
поверхностного слизистого слоя. Протяженность разреза планируют в
зависимости от того, на какую величину и в каких пределах требуется углубить
преддверие полости рта. Затем острыми краями ножниц отсепаровывают соб-
Рис. 33.14. Френулопластика с использованием
треугольных лоскутов (схема).
а — планирование линий разреза и направления
перемещения лоскутов; б— после завершения пластики
и наложения швов.
465
Рис. 33.15. Локализованная рецессия десны (схема).
а — планируемые разрезы по краям дефекта и разрез для последующего латерального перемещения
лоскута на обнаженную поверхность корня; б — лоскут после мобилизации перемешен на место
дефекта, фиксирован швами с одной стороны. Рана на месте забора лоскута открыта; в, г — второй
вариант разрезов с целью закрытия Ѵ-образного дефекта с помощью мобилизованного лоскута.
ственно слизистую оболочку на глубину, которая на 2—3 мм больше
планируемого увеличения ширины прикрепленной десны. Мягкие ткани рассекают
до надкостницы на границе планируемой нижней зоны прикрепленной десны.
Распатором отслаивают мышечные пучки от кости до основания
альвеолярного отростка. Отслоенный слизистый лоскут кетгутом подшивают к
надкостнице (первый шов посредине, последующие — через каждые 5—6 мм). Отсепа-
рованные мышечные пучки и мягкие ткани также фиксируют к надкостнице.
На обнаженную кость и слизистую оболочку губы накладывают клеящиеся
пленки "Диплен". Рана заживает вторичным натяжением.
Послеоперационное ведение заключается в регулярной
антисептической обработке, замене лечебных пленок через день в течение первых 3 сут.
Обычно через 6 сут используют повязки с каким-либо маслом. Клеящиеся
пленки "Диплен" выпускаются с лекарственными препаратами — дексамета-
зоном, хлоргексидином, трихополом. Модификации данной операции имеют
целью либо снижение травматичности (для этого отсепарировывают ткани
через единственный срединный разрез), либо использование подсадок
(слизистых лоскутов с неба или щеки либо консервированных тканей) для
замещения дефекта.
Как отмечено выше, в значительном проценте случаев воспалительная
деструкция пародонта сочетается с нарушениями строения мягких тканей
преддверия полости рта, поэтому при планировании оперативных вмеша-
466
д ^У/ лоскута; д — после операции.
тельств необходимо определить их очередность. Идеально такое положение,
когда хирург владеет навыками одномоментного проведения лоскутной
операции и коррекции нарушений мягких тканей преддверия полости рта, но в
таких случаях следует помнить о возможных осложнениях — последующей
ретракции мягких тканей и обнажении корней зубов, которые весьма
вероятны и могут значительно снизить эффект операции, особенно в
эстетическом отношении. Имеет смысл проводить лоскутную операцию не раньше
чем через 3—4 нед после предварительной мукопластики (вестибуло-, фре-
нул о пластика). Только в этом случае можно более надежно прогнозировать
эффект лоскутной операции.
Перечисленные методы позволяют добиться максимального эффекта.
Именно с хирургией связаны надежды пародонтологов. Тем не менее
специалисты должны учитывать показания и противопоказания к проведению
этих сложных вмешательств. В частности, при деструкции кости более чем
на половину длины корня прогноз очень сомнительный. Нецелесообразно
проводить хирургическое вмешательство, если изначальную подвижность
зубов не удалось полностью устранить на подготовительном этапе с помощью
467
Рис. 33.17. Операция вестибул on ластики по Эдлану— Мейхару.
а — определение линии разреза на слизистой оболочке губы; б — острыми краями ножниц
отделяют поверхностный слой слизистой оболочки губы. Около альвеолярного отростка проводят
разрез до кости, отслаивают слизисто-надкостничный лоскут; в — тупым путем с помощью
распатора отслаиваются мышечные пучки от кости альвеолярного отростка до его основания; г —
отслоенный лоскут укладывают на место и фиксируют к надкостнице. Новое преддверие полости
рта сформировано. Рану на губе закрывают с помощью дипленовых пленок, содержащих хлор-
гексидин или дексаметазон.
противовоспалительной терапии, избирательного пришлифовывания и
временного шинирования. Надо помнить, что даже наиболее объективное —
рентгенологическое исследование не всегда надежно, так как позволяет
суммарно оценить лишь картину кости с щечной и язычной поверхностей, а на
самом деле деструкция на одной из поверхностей может быть крайне
глубокой. В таких случаях решение об удалении зуба нередко является
единственно правильным.
468
Сложно решить вопрос о проведении вмешательств по устранению
косметических дефектов вследствие рецессии десны. Необходимо детально оценить
толщину слизистой оболочки и подлежащей кости, а также интенсивность
кровоснабжения. Иногда перед операцией можно стимулировать
надкостницу методом проколов под анестезией. Если через 3—4 нед после этого
клинически состояние десны не улучшается, то нереально рассчитывать на
стойкий результат.
Послеоперационное рубцевание может свести на нет первоначально
достигнутый эффект вестибулопластических вмешательств. В связи с этим до
их проведения необходимо по возможности выяснить, нет ли у пациента
склонности к образованию грубых келоидных рубцов. Если они уже
сформировались, то показаны механогимнастика и массаж, лекарственные
средства, физические методы лечения, способствующие их рассасыванию. Очень
ответственно надо подходить к ведению пациентов в послеоперационном
периоде, особенно после операций с применением мембран.
Следует отметить, что все перечисленные моменты относятся к разряду
сугубо профессиональных, а значит, в конечном счете, вполне решаемы.
В области пародонтологии наибольшие трудности для специалистов связаны
с проблемами, относящимися к специфике этой патологии. При изложении
материала перед описанием каждой методики мы подчеркивали важность
предоперационной подготовки и послеоперационного ведения пациентов с
акцентом на роль гигиены полости рта. Это не случайно: при кажущейся
элементарности адекватного гигиенического ухода за полостью рта именно данная
процедура является камнем преткновения. Пациенты либо не чистят зубы,
либо чистят недостаточно хорошо. Именно поэтому проблема болезней па-
родонта (по сути проблема грязного рта) до сих пор не решена во всем мире.
Хирургическое вмешательство на фоне недостаточной гигиены обречено
на провал. Хирург-стоматолог обязан знать правила чистки зубов и на
протяжении не менее 4 нед до операции и 6 мес после нее контролировать
качество гигиены полости рта пациента. При неудовлетворительном уровне
гигиены хирург не должен производить операцию. Если после
операции гигиена соблюдается плохо, то неминуем рецидив воспаления.
Лица с заболеваниями пародонта должны чистить зубы не менее 3 раз в день:
перед завтраком, после него и перед сном. Длительность чистки не менее
3 мин. Особенно тщательно следует чистить зубы, рядом с которыми
открываются протоки слюнных желез: щечную поверхность верхних моляров и
язычную поверхность фронтальной группы нижней челюсти. После чистки
межзубные промежутки необходимо очищать с помощью нитей (флоссы).
В случае, если невозможно использовать нити (при наличии мостовидных
протезов), необходимо дополнительно очищать межзубные промежутки с
помощью зубочисток. Щетки должны быть с жесткой щетиной; только на
протяжении недели после операции во избежание травмы рекомендуется
пользоваться щетками с мягкой щетиной. Первые движения щетки должны быть
направлены от десны к коронке зуба: на нижней челюсти — снизу вверх, на
верхней — сверху вниз. Если пациент имеет возможность чистить зубы и
после обеда, то это следует делать.
Чистка языка и твердого неба должна быть обязательным компонентом
гигиены полости рта, так как на этих участках микроорганизмы содержатся
даже в большем количестве, чем предполагается. Применяют ту же щетку.
Достаточно 6—8 движений, а усилия пациент должен регулировать сам.
Ориентиром является отсутствие болей и травматического эффекта.
Вторая проблема также специфична для пародонтологии. Лечение
хронического воспаления — длительный процесс, доставляющий пациенту мно-
469
го неприятных и болевых ощущений. Конечный клинический эффект
является результатом сотрудничества пациента и врача. Следовательно, фактор
психологической совместимости врача и пациента играет важную роль.
Отбор на лечение — едва ли не самый важный этап. Выяснение анамнеза,
беседа с пациентом не должны быть формальными. Если врач изначально
выявляет психическую неуравновешенность пациента, то он не должен
планировать сложные оперативные вмешательства, а вынужден ограничиваться
консервативным лечением.
Нужно выяснить, каких результатов пациент ждет от операции. Часто
требования и ожидания завышены, поэтому хирург обязан указать
недостатки косметического характера, которые могут возникнуть вследствие рецессии
десны, предупредить о повышении чувствительности шеек зубов и
необходимости соответствующего лечения. Оперировать можно только тех
пациентов, которые согласны с прогнозируемыми результатами.
Наиболее часто пациенты обращаются с просьбой или требованием
произвести операцию, сохранить и укрепить зубы, вмешательство в области
которых изначально не позволяет рассчитывать на сколько-нибудь
значительный и длительный эффект. Такие пациенты согласны дать расписку о
согласии на "условное" лечение. В этой ситуации врач обязан максимально
корректно и критически оценить психоэмоциональное состояние пациента.
Если эта сфера неустойчива, то врач должен руководствоваться только
строгими показаниями или противопоказаниями.
СПИСОК ЛИТЕРАТУРЫ
Архипов Б. Д., Зотов В. М., Вьюнышева М. А. и др. Остеопластика дефектов нижней
челюсти ауто- и аллогенными трансплантатами // Конструктивные и
реконструктивные операции в челюстно-лицевой области. — М., 1985. — С. 38—44.
Безрукова А. П. Хирургическое лечение заболеваний пародонта. — М, Медицина, 1978.
Иванов В. С Болезни пародонта. — М.: Медицина, 1981. — 192 с.
Локтев Я. И. Морфологическая оценка регенерата в костных трансплантатах при
пластике дефектов нижней челюсти // Стоматология. — 1985. — № 5. — С. 19—22.
Мухсинов М. Е., Таиров У. Т. Опыт применения костных ауто- и
алл©трансплантационных материалов при реконструктивных и оперативных вмешательствах на
лицевом черепе // Конструктивные и реконструктивные операции в
челюстно-лицевой области. — М., 1985. — С. 48—52.
Назаренко М. Ю. Обоснование выбора аллотрансплантата для замещения дефектов
нижней челюсти у детей (клинико-экспериментальное исследование): Дис. ...
канд.мед.наук. — М., 1989. — 191 с.
Петрович Ю. Α., Плотников Н. А.} Героев В. //., Киченко С. М. Минеральный обмен в
ортопедических аллотрансплантатах, консервированных различными способами
// Стоматология. — 1992. — № 2. — С. 26—28.
Савельев В. И. К вопросу о жизнеспособности формалинизированных
биотрансплантатов // Ортопед, травматол. — 1981. — № 11. — С. 55—57.
Aleo J. J., DeRenzis F. Α., Farber P. A. In vitro attachment of human gingival fibroblasts to
root surfaces // J. Periodontol. — 1975. — Vol. 46. — P. 639—645.
Anderegg С. R., Metrler D. G., Nicoll Ε. Κ. Gingiva thickness in guided tissue regeneration
and associated recession at facial furcation defects // J. Periodontol. — 1995. — Vol. 66
E). - P. 397-402.
Anderson Η. Η. The effectiveness of collagen membrane barrier in achieving new attachment
in class 11 furcation // J. Periodontol. - 1991. - Vol. 62. - P. 718.
Andreasen J. O. Histometric study of healing of periodontal tissues in rats after surgical injury.
Healing events of alveolar bone, periodontal ligament and cementum // Odontol. Rev. —
1976. -Vol. 27. - P. 131-144.
470
Andreasen J. О., Kristerson L. The effect of limited drying or removal of the periodontal
ligament. Periodontal healing after replantation of mature permanent incisors in monkeys
// Acta odontol. scand. - 1981. - Vol. 39. - P. 1-13.
Björn Я Experimental studies on reattachment // Dent. Pract. — 1961. — Vol. 11. —
P. 351-354.
Björn Я, Hollender L., Lindhe J. Tissue regeneration in patients with periodontal disease //
Odontol. Rev. - 1965. - Vol. 16. - P. 317-326.
Blumenthal Ν. Μ. The use of collagen membranes to guide regeneration of new connective
tissue attachment in dogs // J. Periodontol. — 1988. — Vol. 59. — P. 830—836.
Blumenthal Ν. Μ., Steinberg J. The use of collagen membrane barriers in conjunction with
combined demineralized bone collagen gel implants in human intrabone defects // J.
Periodontol. - 1990. - Vol. 61. - P. 319-327.
Caffesse R. G, Smith Β. Α., Castelfi W. Α., Nasjleti С. Ε. New attachment achieved by guided
tissue regeneration in beagle dogs //J. Periodontol. — 1988. — Vol. 59. — P. 589—594.
Caffesse R. G, Nasjleti С Е. Response to an absorbable membrane for guided tissue
regeneration in dogs // J. Dent. Res. — 1992. — Vol. 71. — P. 297.
Claffey N., Mostinger S., Ambruster J., Egelberg L. Placement of a porous membrane
underneath the mucoperiosteal flap and its effect on periodontal wound healing in dogs. //
J. clin. Periodontol. - 1989. - Vol. 16. - P. 12-16.
Card S. J., Caffesse R. G., Smith В., Nasjleti С New attachment following the use of a
resorbable membrane in treating periodontitis in beagle dogs // Int. J. Periodont. Res.
Dent. - 1989. - Vol. 9. - P. 59-69.
Chung K. M., Salkin L. M., Stein M. D., Freedman A. L. Clinical evaluation of a
biodegradable collagen membrane in guided tissue regeneration // J. Periodontol. — 1990. —
Vol. 61. - P. 732-736.
Gripps S. Periodontal Disease; Recognition, Interseption and Prevention. — Berlin:
Quintessence Publ. Co. Inc., 1984. - 109 p.
Dowell P., Al-Arrayed F., Adam S., Moran J. A comparative clinical study; the use of human type
1 collagen with and without the addition of metronidazole in the GTR method of
treatment of periodontal disease//J. clin. Periodontol. — 1995. — Vol. 22G). — P. 543—549.
Galgut P. N. Oxidized cellulose mesh used as a biodegradable barrier membrane in the technique
of guided tissue regeneration. A case report // J. Periodontol. — 1990. — Vol. 61. —
P. 766-768.
Garrett S., Loose В., Chamberlain D., Egelberg J. Treatment of intraosseous periodontal
defects with a combined adjunctive therapy of citric acid conditioning, bone graffiting, and
placement of collagenous membranes // J. clin. Periodontol. — 1988. — Vol. 15. —
P. 383-389.
Gottlow J., Nyman S., Laurell L. et al. Clinical result of GTR-therapy using a bioabsorbable
device (Guidor) // J. Dent. Res. - 1992. - Vol. 71. - P. 298.
Laurell L., Gottlow J., Nyman S. et al. Gingival response to Guidor, a biodegradable device
in GTR-therapy // J. Dent. Res. - 1992. - Vol. 71. - P. 298.
Lew D. Α., Clark R. J., Jimenez F. Autogenous Rid graft hydroxylapatite augmentation of the
severely atrophic mandible: Preliminary report // J. oral Maxillofac. Surg. — 1986. —
Vol. 44, N 8. - P. 606-608.
Lowenberg B. F., Aubin J. E., Deporter D. A. et al. Attachment, migration and orientation of
human gingival fibroblasts to collagen coated, surface demineralized and untreated root
slices // J. Dent. Res. - 1985. - Vol. 64. - P. 56-61.
Lukna R. A. Osseous defect responses to hydroxyapatite grafting versus open flap depridement
// J. clin. Periodontol. - 1989. - Vol. 16. - P. 398-402.
Magnusson f., Batich С, Collins В. R. New attachment formation following controlled tissue
regeneration using biodegradable membranes // J. Periodontol. — 1988. — Vol. 59. —
P. 1-7.
Magnusson /., Stenberg W. V.y Batich C, Egelberg J. Connective tissue repair in
circumferential periodontal defects in clogs following use of a biodegradable membrane // J. clin.
Periodontol. - 1990. - Vol. 17. - P. 243-248.
Mehlish D. R., Taylor T. D., Leibold D. G et al. Collagen/hydroxylapatite implant for augmenting
deficient alveolar ridges; Twelvemonth clinical data // J. oral Maxillofac. surg. — 1988. —
Vol. 46, N 10. - P. 839-843.
471
Nery Ε. В., Lynch К. L., Roomy G Ε. Alveolar ridje augmentation with tricalcium phosphate
ceramic // J. Prosthet. Dent. - 1978. - Vol. 40. — P. 668-673.
Nyman S., Gottlow /., Karring T, Lindhe /. The regenerative potential of the periodontal
ligament. An experimental study in the monkey // J. clin. Periodontol. — 1982. — Vol. 9. —
P. 257-265.
Paul В., Mellonig /. Т., Towle H. /., Gray J. S. Use of a collagen barrier to enhance healing
in human periodontal furcation defects // Int. J. Periodontol. Res. Dent. — 1992. —
Vol. 12. - P. 123-131.
Pfeifer J., Van Swot R., Ellinger R. Epithelial exclusion and tissue regeneration using a collagen
membrane barrier in chronic periodontal defects. A histologic study // Int. J.
Periodontol. Res. Dent. - 1989. - Vol. 9. - P. 263-^-274.
Pitaru S., Tal Η., Soldinger Μ. et al. Collagen membrane prevents the apical migration of
epithelium during periodontal wound healing // J. Periodontol. Res. — 1987. — Vol. 22. —
P. 331-333.
Pitaru S., Tal Η., Soldinger Μ. et al. Partial regeneration of periodontal tissues using collagen
barriers. Initial observations in the canine // J. Periodontol. — 1988. — Vol. 59. —
P. 380-386.
Pitaru S., Tal Η., Soldinger Μ., NoffM. Collagen membrane prevent apical migration of
epithelium and support new connective tissue during periodontal wound healing in dogs //
J. Periodont. Res. - 1989. - Vol. 24. - P. 247~-254.
Piani S., NoffM., Grosskopf A. et al. Heparin sulfate and fibronectin — improve the capacity
of collagen barriers to prevent apical migration of the junctional epithelium // J.
Periodontol. - 1991. - Vol. 628. - P. 597-601.
Poison A. M. Periodontal regeneration: current status and directions. — Berlin: Quintessence
Publ. Co. Inc., 1994. - 221 p.
Quinones C. R., Caton J. G., Poison A. M. et al. Evaluation of synthetic biodegradable barriers
to facilitate guided tissue regeneration // J. Periodontol. Res. — 1990. — Vol. 69. —
P. 275.
Quinones C. R., Caton J. G, Poison A. Metal. Evaluation of synthetic biodegradable barriers
to facilitate guided tissue regeneration in interproximal sites // J. Periodontol. — 1991. —
Vol. 62. - P. 86.
Shin S. D., Allen E. P. Use of guided tissue regeneration to treat a mucogingival defect
associated with interdental bone loss: a case report // Int. J. Periodont. Res. Dent. — 1994. —
Vol. 14F). - P. 552-561.
Spitzer W. J., Dumbach J. Aufbau des atrrophischem Kierkammes mit vorgeformteen
Implantaten aus hydroxylapatite-granulat und kollagennrste ergebnisse // Dtsch. Zahnarztl
Z. - 1988. - Bd 43, N 1. - S. 74-77.
Tanner M., Solt C. W., Vudhakanok S. An evaluation of new attachment formation using a
microfibrillar collagen barrier// J. Periodontol. — 1988. — Vol. 59. — P. 524—530.
Trombelli L., Schincaglia G, Checchi L., Calura G. Combined guided tissue regeneration, root
conditioning, and fibrinfibronectin system application in the treatment of gingival
recession. A 15-case report // J. Periodontol. - 1994. - Vol. 65(8). - P. 796-803.
Wikesjo U. M. E., Claffey N., Egelberg J. Periodontal repair in dogs: effect of heparin
treatment on the root surface // J. clin. Periodontol. — 1991. — Vol. 18. — P. 60—64.
Wikesjo U. M. E.} Nilveus R. E., Selvig K. A. Significance of early healing events in
periodontal repair: a review // J. Periodontol. — 1992. — Vol. 63. — P. 158—165.
Wilson Т., Kenneth J., Kormann K. Advances in Periodontics. — New York: Quintessence
Publ. Co. Inc., 1992. - 382 p.
Yamada S., Takahashi Y., Matsumoto Y. et al. The use of polylactic acid membrane in guided
tissue regeneration in dogs //J. Dent. Res. — 1991. — Vol. 70. — P. 507 (abstr. no. 1928).
ПРЕДМЕТНЫЙ УКАЗАТЕЛЬ1
Абсцесс(ы) внутрикостный 1, 334
— головного мозга одонтогенные
1, 456
— и флегмона(ы) глазницы 1, 260
лица и шеи 1, 245
диагностика 1, 233, 279
клиническая картина
1, 248
лечение 1, 280
патогенез 1, 246
патологическая
анатомия 1, 247
профилактика 1, 287
этиология 1, 245
области околоушно-жеватель-
ной 1, 265
подглазничной 1, 254
поднижнечелюстной 1, 262
подподбородочной 1, 264
подъязычной 1, 271
скуловой 1, 259
щечной 1, 255
послеинъекционные 1, 115
пространств жевательных
околоушных см. Абсцесс и флегмона
области околоушно-жевательной
клетчаточных щеки см.
Абсцесс и флегмона области щечной
пространства клетчаточного
подглазничного см. Абсцесс и
флегмона области подглазничной
крыловидно-нижнечелюстного 1, 267
окологлоточного 1, 269
поднижнечелюстного
Прямым шрифтом указаны страницы,
номера рисунков.
см. Абсцесс и флегмона области
поднижнечелюстной
подподбородочного
см. Абсцесс и флегмона области
подподбородочной
скулового см. Абсцесс
и флегмона области скуловой
подъязычного см. Абсцесс
и флегмона области подъязычной
языка 1, 277
— подвисочной ямки 1, 256
Адгезия губная 2, 17
Аденоамелобластома см. Опухоль
одонтогенная аденоматоидная
Аденокарцинома слюнных желез
1,691
Аденолимфома слюнных желез 1, 685
Аденома слюнных желез 1, 684
плеоморфная 1, 686; 27.75;
27.76
Аденофлегмона 1, 297
Актиномикоз 1, 327
— верхнечелюстной пазухи 1, 337
— лимфатических узлов 1, 332
— миндалин 1, 336
— органов полости рта 1, 335
— периоста челюсти 1, 333
— слизистой оболочки полости рта
1, 330
— слюнных желез 1, 336
— форма кожная 1, 329
подкожная 1, 329
подкожно-подмышечная 1, 331
подслизистая 1, 330
— челюстей 1, 333
полужирным — номер тома, курсивом —
31-1263
473
— языка 1, 335
Аллокость 2, 453
Аллотрансплантация зуба 1, 200
Альвеолит 1, 159
Альвеолопластика внутриперегоро-
дочная 2, 390
Амелобластома 1, 716; 21.29; 21.30
Ампутация корня 1, 203
Аналгезия 1, 83
Анальгетики 1, 126
Анамнез болезни 1, 56
— жизни 1, 57
Анатомия кожи лица и шеи 1, 578
— лица 2, 94
Анестезия 1, 80
— внутривенная 1, 80
— внутрисвязочная 1, 107
— инфраорбитальная 1, 97
— мандибулярная 1, 100
— местная кожи 1, 92
осложнения неспецифические
1, 109
при беременности 1, 111
— назопалатинальная 1, 99
— палатинальная 1, 97
— проводниковое 1, 95
по Егорову 1, 95, 103
— регионарная 1, 91
— стволовая (центральная) ветвей
тройничного нерва у основания
черепа 1, 105
— торусальсная 1, 102
— туберальная, способы 1, 96
Анкилоз ВНЧС 1, 630; 19.8; 19.9; 19.14
Аномалии ВНЧС врожденные 1, 637
Антисептика 1, 51
— биологическая 1, 52
— физическая 1, 51
— химическая 1, 52
Аплазия слюнных желез 1, 389
Аппарат(ы) Брагина 1, 17.70
— Бургонской—Ходоровича 1, 494
— внеочаговые 1, 17.36
— внеротовые 1, 17.35
— компрессионно-дистракционные
2, 310; 28.3; 28.4; 28.8
— компрессионные 1, 17.37
— Маланчука и Ходоровича 1, 543;
17.71
— Орлова 1, 17.50
— Петрова 1, 17.49
— стандартизованный Збаржа 1, 17.47
— стерилизационные 1, 47
— сшивающий Жадовского 1, 17.34
Карапетяна 1, 17.33
Артриты височно-нижнечелюстного
сустава 1, 621
Асептика 1, 41
Асфиксия 1, 550
Атарактики 1, 125
Атрофия лица прогрессирующая
1, 610
Аутокость 2, 452
Аутотрансплантация 2, 101, 121
— зуба 1, 200
Биоситаллы 2, 455
Блефаропластика эстетическая
верхняя 2, 329; 29.8
нижняя 2, 332
осложнения 2, 333
Болезнь Бараккера—Симонса см.
Деформация мягких тканей лица после
гемиатрофии и липодистрофии
— Микулича 1, 400, 409
— Рандю—Вебера—Ослера 1, 680
— слюннокаменная 1, 429
— солдатская см. Паротит
эпидемический
— Шегрена 1, 401
Боль(и) 1, 81
— лицевые 1, 599
— механизмы физиологические 1, 81
— определение 1, 83
— послеинъекционные 1, 114
— психогенная 1, 82
— физическая, виды 1, 82
Брефокость 2, 454
Бруксизм 1, 637
Бупивакаин 1, 86
Вазоконстрикторы 1, 87
Вентиляция легких искусственная
1, 131
Вестибулопластика по Эддану—Мейхару
2,465; 33.17
Виды костных швов 1, 511
— огнестрельных переломов нижней
челюсти 1, /7.5*7
— повязок при переломах 1, 506—509
474
Височно-нижнечелюстной сустав,
аллопластика, лечение
послеоперационное 2, 238
ортопедическое 2, 242
основные принципы 2, 206
показания 2, 209
при анкилозах 2, 214, 25.8—
25.1 а, 25.13
деформирующих артрозах
2, 210; 25.4- 25.5
переломах мыщелкового
отростка нижней челюсти 2, 223;
25.16~25.22
удалении опухолей и
концевых дефектах нижней челюсти
2, 234; 25.25; 25.27
противопоказания 2, 210
развитие метода 2, 189
анатомия и биомеханика 2, 191
заготовка аллотрансплантата
2, 203; 25J
подготовка больных к
аллопластике 2, 200
ВИЧ-инфекция 1, 366
— диагностика 1, 371
— клиническая картина 1, 367
— поражения оральные 1, 368
Вмешательства оперативные при
оставлении корней зубов в альвеолах
2, 394
Волчанка туберкулезная 1, 345
Воспаление верхнечелюстной пазухи
одонтогенное 1, 312
хроническое 1, 318
Вправление скуловой кости 1, 539;
17.57, 17.64; 17.65; 17.72
Выведение из наркоза 1, 118
Вывих ВНЧС первичный 1, 626
хронический 1, 626
— головки нижней челюсти
хронический с подвывихом суставного диска
1, 624
— зуба 1, 488
— нижней челюсти 1, 490
кзади 1, 495
передний двусторонний
1,491
двусторонний свежий 1, 492
застарелый 1, 493
односторонний 1, 491
привычный 1, 494
— суставной головки нижней челюсти
кнаружи или внутрь 1, 496
— суставного диска ВНЧС задний
хронический 1, 627
рецидивирующий 1, 626
хронический 1, 627
Выпрямление и сужение спинки носа
2, 338
Гайморит травматический 1, 556
Гексенал 1, 121
Гемангиома 1, 676, 707; 21.25
Гемангиоматоз системный 1, 680
Гематома как осложнение
пластических операций 2, 111
Гемиатрофия лица 2, 23.1
Гемисекция зуба 1, 203
Гидроксилапатит 2, 454
Гингивэктомия 2, 443
Гиперплазия слюнной железы 1, 391
Гиперсаливация 1, 398
Гипертелоризм 2 , 14
— орбитальный 2, 75
способы коррекции 2, 76; 22.45—
22.47; 22.49
Гипномидат 1, 123
Гипосаливация 1, 399
Гипосиалия см. Гипосаливация
Гистиоцитома фиброзная
злокачественная 1, 755; 21.54
Гонорея 1, 350
Гранулема актиномикозная
одонтогенная 1, 331
— эозинофильная 1, 736; 21.40
Гранулематоз Вегенера 1, 372
Дефекты бровей 2, 138
устранение 2, 139
— век 2, 142
— и деформации губ 2, 145, 147
— лица, устранение 2, 113, 134, 144;
23.7-23.12
— лобно-височной области сквозные
2, 135
— нижней зоны лица 2, 144
устранение 2, 147
— областей лба, виска и глазницы,
устранение 2, 134
— средней зоны лица, виды 2, 115
31"
475
комбинированные 2, 115,
133; 23.5
несквозные 2, 115; 23.2
сквозные 2, 115; 23.3; 23.4;
23.Ц ж; 23.12
устранение 2, 113; 23.7—
23.12
Деформации(я) век послеожоговые,
классификация 2, 141
устранение 2, 142
— краниофациальные 2, 60
диагностика 2, 61
осложнения после операций 2, 72
— лица после воспалительных
заболеваний 2, 374; 30.12
— мягких тканей лица после гемиат-
рофии и липодистрофии 2, 378
— ушной раковины врожденная 2, 63
Диагностика радионуклидная 1, 71
Дипидолор 1, 129
Дисплазия фиброзная монооссальная
1 , 724; 21.33
полиоссальная 1, 728
Жалобы больных 1, 54
Железы слюнные, анатомия 1, 376
заболевания дистрофические
1, 398
пороки развития выводных
протоков 1, 389
сцинтиграфия 1, 387
"Жирная шея" Маделунга 1, 672; 21.9
Заболевания воспалительные системы
лимфатической лица и шеи 1, 291
клиническая картина
1, 296
патогенез 1, 294
патологическая
анатомия 1, 295
этиология 1, 294
— гнойно-некротические 1, 360
— лица и шеи гнойные, осложнения
внутричерепные вторичные 1, 449
— пародонта 2, 440
клиническая картина 2, 441
лечение 2, 442
с использованием остеопла-
стических материалов 2, 452
патогенез 2, 440
— слюнных желез, методы диагностики
1, 377
— сопутствующие 1, 58
— челюстно-лицевой области
воспалительные 1, 162—164
инфекционные 1, 168
типы 1, 180
одонтогенные 1, 172
патогенез 1, J 78
этиология 1, 176
Закись азота 1, 120
Зарашение слюнного протока 1, 395
Заушница см. Паротит
эпидемический
Зуб ретинированный 1, 160
Иммобилизация лечебная 1, 529
— нижней челюсти временная 1, 17.87
— транспортная 1, 506, 528; 17.43
при повреждениях лица 1, 17.88
— фрагментов нижней челюсти
1, 17.9Q, 17.91
Имплантаты внутрикостно-поднадкост-
ничные 2, 426
— внутрислизистые 2, 428; 32.10
— ВНЧС титановые 1, 19.13
— в форме корня зуба (круглой
формы) 2,417; 32.5; 32.7
преимущества 2, 420
— зубные внутрикостные 2, 407
плоские (пластиночные)
2, 414; 32.2
преимущества 2, 415
-лица 2, 359; 30.1
клиническое применение 2, 360
— поднадкостничные 2, 423; 32.8
— подслизистые 2, 428
— рамусные 2 , 427; 32.9
— чрескостные 2, 426
Имплантация 2, 406
— зуба 1, 200
— зубная 2, 406
диагностика местная 2, 410
дополнительные операции 2, 428
осложнения 2, 432
поздние 2, 434
ранние воспалительные 2, 434
показания и противопоказания
2,409
476
— челюстно-лицевая 2, 406, 426, 431
Инфекция перекрестная 1, 45
— раневая 1, 46
Инъектор безыгольный 1, 90
Иссечение избытков кожи лица и шеи
2, 350; 29.25; 29.26
осложнения 2, 353
приемы оперативные
2, 352
Исследование лазерное 1, 73
— ультразвуковое 1, 73
Исследования иммунологические
1, 75
— лабораторные 1, 74
— цитологические 1, 77
Кабинет реабилитации, организация
1,31
Карбункул 1, 353
— злокачественный см. Язва сибирская
Карцинома слюнных желез
ацинозно-клеточная 1, 689
мукоэпидермальная 1, 690
цистаденоидная 1, 690
Кетамин 1, 129
Кислота полимолочная 2, 460
Кисты(а) дермоидные дна полости рта
2, 58
носа 2, 58; 22.29
— десневая 1, 656
— зубосодержащая (фолликулярная)
1, 654; 20.4
— корневая (радикулярная) 1, 647
— корня языка 2, 55
— носогубная 1, 657
— одонтогенная кальцифицирующая
1, 721
— первичная (кератокиста) 1, 653
— позадичелюстной области (около-
ушно-зачелюстные) 2, 54
— прорезывания 1, 309, 654
— резцового (носонебного) канала
1, 656
— слюнной железы травматическая
1, 395
— челюстей одонтогенные 1, 646
неодонтогенные 1, 655
— шеи боковые 2, 55
Классификация опухолей полости рта
и ротоглотки международная 1, 665
Коллапс 1, 108
Консолидация замедленная 1, 555
Контрактура челюстей 1, 555
Контрактуры жевательных мышц
1, 642
Коррекция бровей при птозе 2, 328;
29.7
— деформация завитка уха 2, 347
концевого отдела носа 2, 342;
29.17-29.19
мочек ушей 2, 347; 29.22
носа 2, 335
осложнения 2, 344
— искривленного носа 2, 341; 29.15
— неровной поверхности кости
альвеолярного отростка верхней челюсти
и альвеолярной части нижней
челюсти 2, 391
— торчащих ушей 2, 348; 29.23) 29.24
— увеличенных ушей 2, 346; 29.21
Краниостеноз, лечение 2, 14, 65;
22.33-22.35
Кровотечение луночковое 1, 156
Кровотечения 1, 551
Ксикаин 1, 85
Ксилонор 1, 89
Кюремат закрытый 2, 444
-~ открытый 2, 446; 33.6
Лейкоплакия волосяная слизистой
оболочки рта 1, 369
Лейшманиоз 1, 363
Лепра 1, 362
Лидокаина гидрохлорид 1, 85
Лимфаденит острый гнойный 1, 297
серозный 1, 296
— туберкулезный вторичный 1, 344
— хронический 1, 298
Лимфангиома 1, 681; 21.12
Лимфангит острый сетчатый,
или ретикулярный 1, 296
транкулярный, или стволовый
1, 296
— хронический 1, 296
Лимфография 1, 70
Липома 1, 672; 21.5-21.7
Масса викриловая (Polyglactin 910) 2, 461
Массаж сердца 1, 131
477
наружный 1, 132
прямой 1, 131
Материалы коллагенсодержащие
2, 454
Медиастинит контактный
одонтогенный 1, 441
признаки 1, 447
частота возникновения 1, 442
Мезенхимома 1, 694
Мембраны биодеградирующие 2, 456
— хрящевые 2, 460
Мепивакаин 1, 86
Метод(ы) Блехмана 1, 493
— Гиппократа 1, 492
— Илизарова устранения дефекта
нижней челюсти 2, 309; 28.1
— исследования дополнительные 1, 69
основные 1, 54
функциональные 1, 72
— Линдемана 1, 495
— фиксации ортопедические 1, 531;
17.53
Микросомия гемифациальная
(отокраниостеноз) 2, 370; 30.9
Миксома 1, 701; 21.23
Моделирование компьютерное
пластических операций 2, 109
— эндопротезов лица 2, 358
Морадол 1, 128
Нагноение костной раны 1, 552
Наращивание челюсти верхней 2, 398;
31.5, в\ 31.6
нижней 2, 395; 31.3—31.5, а, б
Наркоз ингаляционный 1, 118
— неингаляционный 1, 121
Нарушения функций ВНЧС
внутренние 1, 624
Натрия оксибутират (ГОМК) 1, 123
Натяжение кожи лба 2, 326; 29.5
Невралгия коленчатого узла лицевого
нерва 1, 608
— нерва барабанного 1, 608
видиева 1, 608
гортанного верхнего 1, 608
тройничного 1, 600
языкоглоточного 1, 607
Неврилеммома 1, 711; 21.26
Невринома см. Неврилеммома
Невролиз 2, 166
Невропатия нерва тройничного 1, 604
Невротизация 2, 172
Нейролептаналгезия 1, 125
Нейрорафия прямая 2, 166
Некрозы послеинъекционные 1, 115
Нерв лицевой, анатомия 2, 23.18
варианты дефектов 2, 23.22
,_ замещение нервными
аутовставками 2, 169
классификация повреждений
2, 160
параличи 2, 157
методы обследования при них
2, 158, 159
травматические 2, 157, 159
устранение хирургическое
2, 157, 162
Новокаин 1, 84
Нома 1, 360
Обезболивание аппликационное
1, 88
— внутрипериодонтальное 1, 107
— в области подбородочного нерва
1, 103
— инфильтрационное 1, 93
— инъекционное 1, 90
— местное 1, 84
осложнения местные 1, 114
общие 1, 108
— нерва язычного 1, 105
— нервов щечного и жевательного
1, 104
— общее 1, 116
Обоснование диагноза 1, 77
Обработка операционного поля 1, 45
— рук врача 1, 44
Обследование больного 1, 60
— пальпаторное 1, 62
— полости рта 1, 65
— челюстно-лицевой области 1, 61
Одонтома 1, 712; 21.27
Ожоги термические 1, 578
классификация 1, 17.92
клиническая картина 1, 579
лечение местное 1, 585
хирургическое 1, 586
— химические 1, 590
Олигоптиализм см. Гипосаливация
Олигосиалия см. Гипосаливация
478
Операция(и) на альвеолярных
сегментах 2, 399; 31.7
мягких тканях преддверия
полости рта 2, 462
— пластические на лице и шее,
принципы планирования 2, 100
— при небно-глоточной
недостаточности 2, 47; 22.20-22.24
укороченной уздечке губы 2, 400;
31.8; 31.9
языка 2, 399
— формирования высокой и широкой
альвеолярной дуги 2, 395
— Цещинского—Видмана—Неймана
2, 446; 33.9
— эстетические, виды швов 2, 323;
29.2; 29.3
особенности техники 2, 321
отбор пациентов 2, 318
шовный материал 2, 322
Опухоли ВНЧС 1, 637
— лицевого скелета у детей
доброкачественные, классификация 1, 692
— полости рта и челюстей
эпителиальные злокачественные
1,740
классификация
клиническая TN Μ Ι, 741
— слюнных желез 1, 683; 21.14
— сосудистые 1, 675
Опухоль Кюттнера см. Сиаладенит
интерстициальный
— младенцев нейроэктодермальная
меланотическая 1, 719
— одонтогенная аденоматоидная
1, 723
Ортопантомография 1, 70
Осмотр больного 1,61
— зубов 1, 66
Остеоартроз 1, 628
— вторичный 1, 627
Остеобластокластома 1, 697; 21.18',
21.21\ 21.22
Остеогенез компрессионно-дистракци-
онный, принципы 2, 308
Остеоид-остеом а 1, 696
Остеома 1, 695
Остеомиелит лунки ограниченный
1, 159
— травматический 1, 553
— челюсти 1, 220
диагностика 1, 233
клиническая картина 1, 225
осложнения 1, 242
патогенез 1, 220
патологическая анатомия 1, 223
стадия острая 1, 226
лечение 1, 234
подострая 1, 229
хронический 1, 230
лечение 1, 239
Остеотомия по Ле Фор 2, 63, 70
— челюсти верхней 2, 261; 26.5
нижней 2, 263; 26.6— 26.9; 26.11;
26.12; 26.14; 26.17
Отделение хирургическое, оснащение
1, 31
Отморожения 1, 592
Отопластика эстетическая 2, 346
осложнения 2, 349
Пальфиум 1, 128
Пантомоспалография 1, 382
Папиллома 1, 667
Папилломатоз 1, 667
— лицевого нерва 1, 18.2; 18.3
— мимических мышц 1, 608
Парез мимической мускулатуры 1,115
Парестезии 1, 116
Пародонт 2, 438; 33.1; 33.2
Пародонтит 2, 443
Паротит эпидемический 1, 410
Пентран 1, 120
Перелом(ы) 1, 496
— альвеолярного отростка челюстей
1,497
— верхней челюсти огнестрельные
1, 563; 17.80-, 17.81
— зуба 1, 489
— костей лица огнестрельные 1, 562
носа 1, 544
— скуловой кости и дуги 1, 536
лечение хирургическое 1, 539
— челюсти верхней 1, 521
классификации 1, 523
по Вассмунду 1, 17.41
Лефору—Герену 1, 524; 17.40
нижней 1, 497
диагностика 1, 504
клиническая картина 1, 503
лечение 1, 505
479
методы ортопедические
1, 506
хирургическое 1, 515
Перемещение подбородочного нерва
2, 404
Перикоронит гнойный 1, 305
— острый 1, 305
— хронический 1, 306
Перилен-ультра 1, 89
Период введения в наркоз 1, 116
— поддержания общей анестезии
1, 117
— постреанимационный 1, 133
Периодонтит 1, 185
— гранулематозный 1, 196
— гранулирующий 1, 193
— острый 1, 186
диагностика 1, 190
исход 1, 192
клиническая картина 1, 189
лечение 1, 191
патологическая анатомия 1, 187
— фиброзный 1, 197
— хронический 1, 192
профилактика 1, 209
Периостит позадимолярный 1, 307
— челюсти острый 1, 28, 210
диагностика 1,215
' клиническая картина 1, 213
лечение 1, 216
патогенез 1,211
патологическая анатомия
1, 212
этиология 1, 211
Перкуссия зубов 1, 67
Пиромекаин 1, 88
Плагиоцефалия лобная 2, 66
Пластика альвеол 2, 390
— дефекта(ов) дна полости рта
2, 147
губ и мягких тканей подбородка
2, 148
тотальных 2, 149
— дна глазницы скульптурно-модели-
рованным силиконовым импланта-
том 2, 282; 27.4
— костная нижней челюсти, развитие
метода 2, 175
аллотрансплантатом 2, 182
аутотрансплантатом
2, 180; 243
комбинированная
2, 185; 24.4
— подслизистой ткани преддверия
полости рта 2, 404
— преддверия полости рта 2, 403
— челюстей аутогенными костными
трансплантатами 2, 430; 32.11\ 32.12
Повреждения лица и полости рта
радиационные 1, 593
лечение 1, 596
— сосудов инъекционной иглой 1, 115
— челюстно-лицевой области лучевые
у онкологических больных 1, 757
лечение 1, 766
признаки 1, 760
профилактика 1, 765
огнестрельные 1, 557
классификация 1, 559
легкие 1, 558
средней тяжести 1, 558
тяжелые 1, 559
Повышение спинки носа
2, 339; 29.14
Подвывих суставного диска ВНЧС
1, 624
Подготовка альвеолярного отростка
верхней челюсти и альвеолярной
части нижней челюсти к
немедленному протезированию 2, 392
Поликлиники стоматологические,
организация 1, 30
Полиэфир гидролизирующий 2, 460
Положение о враче челюстно-лицевой
хирургии 1, 37
Полярография 1, 73
Помощь раненным в челюстно-лице-
вую область 1, 566
врачебная первая 1, 570
доврачебная 1, 570
медицинская
квалифицированная 1, 570
первая 1, 570
специализированная
1,574
— стоматологическая
квалифицированная 1, 29
специализированная 1, 29
узкоспециализированная 1, 29
хирургическая в поликлинике
1, 30
стационаре 1, 33
480
Понижение спинки носа 2, 338; 29.72;
29.13
Поражение туберкулезом
лимфатических узлов первичное 1, 343
слюнных желез 1, 344
Пороки развития губы и неба
врожденные, классификация 2, 13
— черепно-лицевой области и шеи
врожденные 2, 7
данные статистические
2,7
патогенез 2, 8
программа
реабилитации детей 2, 11
типы 2, 10
Премедикация 1, 112
Принципы пластической хирургии
2, 111
Прозалгии 1, 599
Прорезывание затрудненное
премоляров, клыков, верхнего
третьего коренного зуба 1, 310
Птиализм см. Гиперсаливация
Пульпанест 1, 89
Радиосиалография 1, 385
Рак водяной см. Нома
— губы 1, 742
— нижней челюсти 1, 751
— придаточных пазух носа 1, 750
— слизистой оболочки полости рта
1, 743
— форма папиллярная 1, 743
Ранения мягких тканей лица 1, 561
— челюстно-лицевой области
огнестрельные, особенности
1, 560
Раны лица 1, 481
Резекция верхушки корня 1, 205
— участка альвеолярного отростка
верхней челюсти и альвеолярной
части нижней челюсти 2, 391
Рентгенография внеротовая 1, 69
— контрастная 1, 70
— окклюзионная 1, 69
Реография 1, 72
Реплантация зуба 1, 198
Репозиция при деформациях костей
области скулоглазничной 2, 279;
27.7
— скуловых костей с одномоментной
пластикой скулоальвеолярного
гребня формализированной
аллогенной костью 2, 281; 27.2
Рожа 1, 358
Рубцы келоидные 2, 146
— послеожоговые 2, 146
Саркома Капоши 1, 370
— остеогенная 1, 753; 27.57
— ретикулярная 1, 757
— Юинга 1, 756
Свинка см. Паротит эпидемический
Свищ слюнной 1, 393
— слюнной железы см. Свищ слюнной
Свищи носа 2, 58; 22.28
— предушные 2, 54; 22.25
— шеи срединные 2, 55; 22.26
Секвестрэктомия 1, 240
Сепсис острый 1, 434
лечение хирургическое 1, 466
недостаточность дыхательная
при нем 1, 438
поражения печени и почек
при нем 1, 439
прогноз 1, 476
терапия антибактериальная
1,467
детоксикационная 1, 469
Септокаин 1, 87
Сиаладенит, вызванный внедрением
инородных тел в выводные протоки
желез 1, 415
— гриппозный 1, 412
— интерстициальный 1, 417
— калькулезный см. Болезнь слюнно-
каменная
— контактный 1, 415
— лимфогенный 1, 414
— острый 1, 413
— паренхиматозный 1, 420
— протоковый см. Сиалодохит
хронический
Сиаладеноз саркоидный 1, 409
Сиалография 1, 71
Сиалодохит хронический 1, 423
Сиалолитиаз см. Болезнь слюннокамен-
ная
Сиалорея см. Гиперсаливация
Сиалосонография 1, 387
481
Сиалотомография 1, 383
— компьютерная 1, 384
Силиконы 2, 357
Силоксаны 2, 357
Симптом Венсана 1, 66
— Герке 1, 448
— Иванова 1, 448
— Равич-Щербо 1, 446
— Штейнберга 1, 446
Синдром ауриколотемпоральный
1, 611
— дисфункции ВНЧС болевой 1, 637
— Кюттнера 1, 400
— Олбрайта 1, 729
— Рейхерта см. Невралгия нерва
барабанного
— Тричера—Коллинза 2, 367; 30.8
— Файля см. Невралгия нерва видиева
— Фрея см. Синдром
ауриколотемпоральный
— Ханта см. Невралгия коленчатого
узла лицевого нерва
— Хеерфордта 1, 400
— Шегрена 1, 388, 400, 401
Сифилис 1, 347
— поражение надкостницы челюсти
1, 348
Скандикаин 1, 86
Скрофулодерма см. Туберкулез кожи
первичный
Смерть биологическая 1, 130
"Смерть гипоксическая" 1, 130
— клиническая 1, 130
"Смерть наркозная" 1, 130
Сомбревин 1, 122
Состояние терминальное 1, 130
Сотрясение мозга 1, 549
СПИД 1, 368
— диагностика 1, 371
Средства седативные см. Атарактики
— стерилизационные 1, 47, 49
Ссадины лица 1, 481
Стереорентгенография протоков
слюнных желез 1, 383
Стерилизация инструментов 1, 46, 47
— материалов 1, 49
Сужение слюнного протока 1, 394
Сустав височно-нижнечелюстной,
анатомия 1, 613
заболевания воспалительные
1, 621
классификация 1, 620
невоспалительные 1, 623
механика движения 1, 618
патогенез дисфункции 1, 640
— ложный 1, 555
Схема Онгрена 1, 750; 21.50
Телерентгенография 1, 70
Термовизиография 1, 72
Тесты иммунологические 1, 76
Тиопентал-натрий 1, 121
Томография компьютерная 1, 71
— резонансная 1, 71
Травмы челюстно-лицевой области
1, 548
осложнения поздние 1, 551
ранние 1, 549
Трамал 1, 127
Трансплантаты тканевые 2, 452
Транспозиция ветвей лицевого нерва
2, 171; 23.23
Тримекаин 1, 84
Тромбоз кавернозного синуса 1, 455
Туберкулез кожи первичный 1, 343
— челюстей 1, 345
Туляремия 1, 365
Удаление зуба(ов) временных,
показания 1, 138
заживление раны 1, 152
методика 1, 141
методы обезболивания 1, 140
обработка раны 1, 151
осложнения местные 1, 152
постоянного показания
абсолютные 1, 138
противопоказания местные
1, 140
общие 1, 139
относительные 1, 139
при помощи бормашины, молотка
и долота 1, 149
щипцами, приемы 1, 144
элеватором 1, 147
— избытка воспалительно
измененной ткани 2, 401
мягких тканей альвеолярной дуги
2, 402; 31.Щ 31.11
— нижнечелюстного валика 2, 394
482
— образований доброкачественных
2, 325
— экзостозов в области небного
валика твердого неба 2, 392; 31.2
на верхней и нижней челюстях
2, 392
— щипцами клыков верхних 1, 145
нижних 1, 146
моляров верхних 1, 145
нижних 1, 147
третьего моляра 1, 147
премоляров верхних 1, 145
нижних 1, 147
резцов верхних 1, 145
нижних 1, 146
Узлы лимфатические лица и шеи
1, 291-293
Уменьшение и удаление челюстно-
подъязычной линии 2, 393
— объема ткани ретромолярной
области 2, 401
— подбородочного бугорка
и подбородочного выступа 2, 394
Уранопластика 2, 37; 22.14—22.19
Устранение дефектов глотки
и шейного отдела пищевода 2, 154
— деформаций посттравматических
всей средней зоны лица 2, 299; 27.21
области лобно-носоглазничной
2, 291; 27.16-27.20
носоглазничной 2, 285; 27.6
носоглазничной с
одномоментной каналикулоцистостомией
2, 288; 279-27.15
скулоглазничной скульп-
турно-моделированным импланта-
том из силикона 2, 285
— мышечных и слизистых тяжей
преддверия полости рта 2, 401
Уход за раненными в лицо 1, 577
Ушиб зуба 1, 488
— лица 1, 480
— мозга 1, 549
Фиброма 1, 668; 21.3
— амелобластическая 1, 722
— десмопластическая 1, 704; 21.24
— одонтогенная 1, 722
— оссифицирующая 1, 706
Фиброматоз десен 1, 670; 21.4
Фибронектин 2, 462
Фиброостеома см. Фиброма
оссифицирующая
Флегмона(ы) области(ей) височной
1,259
входящих в дно полости рта
1,273
позадичелюстной 1, 276
— пространств шеи передних 1, 277
— ямки позадичелюстной см.
Флегмона области позадичелюстной
— ямок подвисочной и
крыловидно-небной 1, 256
Фортрал 1, 126
Фторотан 1, 119
Фурункул 1, 353
Хейлопластика, варианты 2, 22.1
— двусторонняя 2, 30
— линейная 2, 15
— лоскутная 2, J 7
Хейлоринопластика первичная
2, 28; 22.7
Херувизм 1, 732; 21.38
Хирургия предпротезная 2, 388
— эстетическая лица и шеи 2, 317
Хламидиоз 1, 351
Хондродисплазия экзостозная 1, 739
Хондрома 1, 697
Хондросаркома 1, 754; 21.53
Целлюлоза оксидированная 2, 460
Цементома 1, 714; 21.28
Цистотомия 1, 659
— ороназальная 1, 662
— пластическая 1, 662
Цистэктомия 1, 657
— ороназальная 1, 662
Череп лицевой, аномалии и
деформации, анатомия хирургическая 2, 246
диагностика 2, 254
классификации 2, 251
клиническая картина 2, 252
лечение хирургическое,
показания 2, 259
принципы 2, 261
483
патогенез 2, 249
частота 2, 247
этиология 2, 249
деформации средней зоны
посттравматические, диагностика
2, 277
классификация 2, 278
Шваннома см. Неврилеммома
Шок анафилактический 1, 108
— септический 1, 437
— токсикоинфекционный 1, 452
— травматический 1, 550
Щипцы для удаления зубов верхней
челюсти 1, 142
корней зубов верхней челюсти
1, 143
— способы удержания в руке 1, 141,
143
— Ходоровича—Баринова 1, 17.63
Эктопротезирование лица 2, 382
Эктопротезы 2, 382
— функции 2, 383
— этапы изготовления 2, 384
Элеватор(ы) прямой(ые) 1, 147
— штыковидный Леклюза 1, 149
— угловые 1, 149
Электромиография 1, 73
Электронейромиография 1, 73
— стимуляционная 1, 74
Электроожоги 1, 588
— лечение хирургическое 1, 590
Электротермометрия 1, 72
Эмфизема 1, 115
Эндопротезирование лица 2, 356
ЭНКАД 1, 400
Эпитезы 2, 382
Язва сибирская 1, 356
ОГЛАВЛЕНИЕ
Врожденные пороки черепно-лицевой области и
шеи. В. В. Рогинский, В. М. Безруков, В. П.
Ипполитов 7
Статистические данные 7
Патогенез 8
Основные типы пороков развития черепно-
лицевой области и шеи 10
Предоперационная подготовка 14
Хейлопластика 15
Уранопластика 37
Врожденные кисты и свищи мягких тканей
челюстно-лицевой области 53
Краниофациальные деформации 60
Хирургическое лечение черепно-лицевых
деформаций 63
Орбитальный гипертелоризм 75
Восстановительные операции на мягких тканях
лица и шеи. Л. И. Неробеев, В. И. Малаховская,
Ц. М. Шургая 94
Анатомия и физиология лица и шеи 94
Принципы планирования пластических операций
на лице и шее. Особенности операций на мягких
тканях І00
Методы компьютерного моделирования .... 107
Основные принципы пластической хирургии . . 111
Устранение дефектов и Рубцовых деформаций
средней зоны лица 113
23.6. Устранение дефектов областей лба, виска
и глазницы 134
23.7. Устранение дефектов и деформаций нижней
зоны лица 144
23.8. Устранение дефектов глотки и шейного отдела
пищевода 154
23.9. Устранение лицевых параличей 157
Глава 24. Костная пластика нижней челюсти. В. М.
Безруков, В. Л. Сукачев, Л. X. Шамсутдинов 175
24.1. Историческая справка 175
Г
г
лава 22.
22.1.
22.2.
22.3.
22.4.
22.5.
22.6.
22.7.
22.8.
22.9.
22.10,
лава 23.
23.1.
23.2.
23.3.
23.4.
23.5.
485
24.2. Костная пластика аутотрансплантатом 180
24.3. Костная пластика аллотрансплантатом 182
24.4. Комбинированная костная пластика ауто-
и аллотрансплантатами 185
Глава 25. Аллопластика височно-нижнечелюстного сустава.
А. А. Никитин 189
25.1. Историческая справка 189
25.2. Анатомо-физиологические особенности и
биомеханика височно-нижнечелюстного сустава 191
25.3. Методы обследования и подготовка больных
к аллопластике височно-нижнечелюстного
сустава 200
25.4. Методика заготовки и обработки костно-пласти-
ческого материала для аллопластики височно-
нижнечелюстного сустава 203
25.5. Основные принципы и особенности
аллопластики височно-нижнечелюстного сустава 206
25.6. Клинические показания и противопоказания
к аллопластике височно-нижнечелюстного
сустава 209
25.7. Аллопластика височно-нижнечелюстного
сустава при деформирующих артрозах 210
25.8. Аллопластика височно-нижнечелюстного
сустава при анкилозах 214
25.9. Аллопластика височно-нижнечелюстного
сустава при переломах мыщелкового отростка
нижней челюсти 223
25.10. Аллопластика височно-нижнечелюстного
сустава при удалении опухолей,
диспластических процессах и концевых
дефектах нижней челюсти 234
25.11. Лечебно-профилактические мероприятия
после аллопластики височно-
нижнечелюстного сустава 238
Глава 26. Хирургическое лечение аномалий и деформаций
челюстей. В. М. Безруков, В. И. Гунько 246
26.1. Особенности хирургической анатомии
лицевого черепа у больных с аномалиями
и деформациями 246
26.2. Частота аномалий и деформаций лицевого
черепа 247
26.3. Этиология, патогенез, классификация,
клиническая картина, диагностика
врожденных аномалий и деформаций
зубочелюстной системы 249
26.4. Показания к хирургическому лечению
и принципы его планирования 259
26.5. Принципы хирургического лечения больных
с аномалиями и деформациями лицевого
черепа и зубочелюстной системы 261
486
32.4. Чрескостные имплантаты 426
32.5. Рамусные имплантаты 427
32.6. Внутрислизистые имплантаты 428
32.7. Подслизистые имплантаты 428
32.8. Дополнительные операции
при зубной имплантации 428
32.9. Осложнения при зубной имплантации 432
Глава 33. Хирургические методы лечения заболеваний
пародонта. А. И. Грудянов 438
33.1. Этиология, патогенез, клиническая картина
и лечение заболеваний пародонта 440
33.2. Лечение заболеваний пародонта
с использованием остеопластических
материалов 452
Предметный указатель 473
Руководство по хирургической стоматологии
и челюстно-лицевой хирургии
В 2 томах
Том 2
Зав. редакцией Т. П. Осокина
Редактор Л. Д. Иванова. Художественный редактор Т. С. Тихомирова
Технический редактор Г. Н. Жильцова. Корректор Л. В. Петрова
ЛР № 010215 от 29.04.97. Сдано в набор 11.02.2000. Подписано к печати 27.04.2000.
Формат бумаги 70х100,/|6. Бумага офсетная № 1. Гарнитура Тайме. Печать
офсетная. Усл. печ. л. 39,65. Усл. кр.-отт. 39,65. Уч.-изд. л. 39,60. Тираж 5000 экз.
Заказ № 1263.
Ордена Трудового Красного Знамени издательство «Медицина».
101000, Москва, Петроверигский пер., 6/8.
Диапозитивы изготовлены в ООО фирма Аким.
121609, Москва, Рублевское ш., д. 42, корп. 2.
Отпечатано в полном соответствии
с качеством предоставленных диапозитивов
в ОАО «Можайский полиграфический комбинат».
143200, г. Можайск, ул. Мира, 93.